Изобретение относится к новым химическим соединениям, применяемым для борьбы с нежелательной растительностью, в частности с однолетними и многолетними однодольными сорными растениями семейства Злаковые в посевах сельскохозяйственных культур.
Известны производные хлорфенолов, применяемые в качестве фунгицидов, протравителей семян [Н.Н. Мельников. Химия и технология пестицидов. -М.: Химия, 1974, C.148].
Однако указанные производные хлорфенолов обладают слабой гербицидной активностью.
Ближайшим аналогом по структуре и гербицидным свойствам является производное 2,4-дихлорфенола-2,4-дихлорфеноксиуксусная кислота (2,4-D кислота) [Там же, С.274].
Вместе с тем недостатком 2,4-D кислоты является слабая гербицидная активность в отношении сорных растений семейства Злаковых.
Задача изобретения - создание новых гидроксиалкильных производных хлорфенолов, обладающих высокой гербицидной активностью.
Нами созданы новые химические соединения - O-(2,3-дигидроксипроп-1-ил)-хлорфенолы структурной формулы
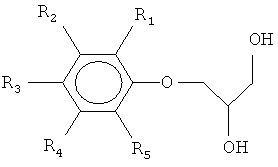
где R1=Cl, R2, R3, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-2-хлорфенол;
R3=Cl, R1, R2, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-4-хлорфенол;
R1, R3=Cl, R2, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-2,4-дихлорфенол;
R1, R4=Cl, R2, R3, R5=Н O-(2,3-дигидроксипроп-1-ил)-2,5-дихлорфенол;
R1=СН3, R3=Cl, R2, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-2-метил-4-хлорфенол;
R1, R3, R5=Cl, R2, R4=H O-(2,3-дигидроксипроп-1-ил)-2,4,6-трихлорфенол;
R1, R3, R4=Cl, R2, R5=H O-(2,3-дигидроксипроп-1-ил)-2,4,5-трихлорфенол;
R1, R2, R3, R4, R5=Cl, O-(2,3-дигидроксипроп-1-ил)-пентахлорфенол.
Методика синтеза O-(2,3-дигидроксипроп-1-ил)-хлорфенолов.
O-(2,3-дигидроксипропил)-хлорфенолы получают по следующей методике. 0,0061 моля хлорфенола и 0,3 г NaOH (0.075 моль) растворяют в 10 мл изопропилового спирта, затем при перемешивании постепенно добавляют 0,54 г (0,007 моля) аллила хлористого, поддерживая температуру смеси на уровне 25°C. После добавления всего реагента перемешивание продолжают в течение 3 часов. Реакционную смесь разбавляют хлористым метиленом, отделяют образующийся NaCl и отгоняют растворитель. Полученный O-(2,3-дигидроксипропил)-хлорфенол растворяют в 10 мл смеси ацетон: вода (85:15) и добавляют 1,2 г (0,007 моль) порошка КМnО4 в течение 30 мин. Перемешивание продолжают еще 3-4 часа.
O-(2,3-дигидроксипроп-1-ил)-2-хлорфенол (9). Выход 0.95 г (95.0%) продукта (1). Т.кип. 101-3° (1 мм рт.ст.). ИК-спектр (v, см-1): 3390, 3400 (ОН). Спектр ЯМР 1Н (CDCl3, δ/м.д.): 2.14 (с, 2Н, ОН); 3.86 (д, 2Н, J=10.8 Гц); 4.0 (м, 1Н); 4.8 (д, 2Н, J=10.5 Гц); 6.80-7.45 (с, 4Н, Аг-Н). Спектр ЯМР 13С: (CDCl3, δ/м.д.): 70.6 (СН); 76.7 (СН); 77.5 (СН2); 115.2, 123.8, 125.5, 126.7, 129.8, 152.4 (С-аром.).
Найдено (%): С 53.30; Н 5.45; Cl 17.45; О 23.60. C9H10O2Cl.
Вычислено (%):С 53.35; Н 5.47; Cl 17.50; О 23.69.
O-(2,3-дигидроксипроп-1-ил)-4-хлорфенол (10). Выход 0.96 г (96.0%) продукта (1). Т.кип. 101-3° (1 мм рт.ст.). ИК-спектр (v, см-1): 3390, 3400 (ОН). Спектр ЯМР 1Н (CDCl3, δ/м.д.): 2.14 (с, 2Н, ОН); 3.86 (д, 2Н, J=10.8 Гц); 4.0 (м, 1Н); 4.8 (д, 2Н, J=10.5 Гц); 6.80-7.45 (с, 4Н, Аг-Н). Спектр ЯМР 13С: (CDCl3, δ/м.д.): 70.6 (СН); 76.7 (СН); 77.5 (СН2); 115.2, 123.8, 125.5, 126.7, 129.8, 152.4 (С-аром.).
Найдено (%): С 53.30; Н 5.45; Cl 17.45; О 23.60. C9H10O2Cl.
Вычислено (%):С 53.35; Н 5.47; Cl 17.50; О 23.69.
O-(2,3-дигидроксипроп-1-ил)-2,4-дихлорфенола (11). Выход 0.93 г (92.0%) продукта (1). Т.кип. 102-3° (1 мм рт.ст.). ИК-спектр (v, см-1): 3391, 3404 (ОН). Спектр ЯМР 1Н (CDCl3, δ/м.д.): 2.15 (с, 2Н, ОН); 3.85 (д, 2Н, J=10.8 Гц); 4.1 (м, 1Н); 4.7 (д, 2Н, J=10.5 Гц); 6.85-7.35 (с, 3Н, Аг-Н). Спектр ЯМР 13C: (CDCl3, δ/м.д.): 70.6 (СН); 76.7 (СН); 77.5 (СН2); 115.1, 123.7, 125.8, 126.5, 129.6, 152.2 (С-аром.).
Найдено (%): С 45.58; Н 4.20; Cl 29.90; O 20.25. C9H10Cl2O3.
Вычислено (%):С 45.60; Н 4.25; Cl 29.91; О 20.25.
O-(2,3-дигидроксипроп-1-ил)-2,5-дихлорфенола (13). Выход 0.935 г (93.0%) продукта (1). Т.кип. 103-3° (1 мм рт.ст.). ИК-спектр (v, см-1): 3391, 3404 (ОН). Спектр ЯМР 1Н (CDCl3, δ/м.д.): 2.15 (с, 2Н, ОН); 3.85 (д, 2Н, J=10.8 Гц); 4.1 (м, 1Н); 4.7 (д, 2Н, J=10.5 Гц); 6.85-7.35 (с, 3Н, Аг-Н). Спектр ЯМР 13С: (CDCl3, δ/м.д.): 70.6 (СН2); 76.7 (СН2); 77.5 (СН); 115.1, 123.7, 125.8, 126.5, 129.6, 152.2 (С-аром.).
Найдено (%): С 45.58; Н 4.20; Cl 29.90; O 20.25. C9H10Cl2O3.
Вычислено (%):С 45.60; Н 4.25; Cl 29.91; O 20.25
O-(2,3-дигидроксипроп-1-ил)-2-метил-4-хлорфенола (12). Выход 0.929 г (93.0%) продукта (1). Т.кип. 104-3° (1 мм рт.ст.). ИК-спектр (v, см-1): 3391, 3404 (ОН). Спектр ЯМР 1Н (CDCl3, δ/м.д.): 2.15 (с, 2Н, ОН); 3.85 (д, 2Н, J=10.8 Гц); 4.1 (м, 1Н); 4.7 (д, 2Н, J=10.5 Гц); 6.85-7.35 (с, 3Н, Аг-Н). Спектр ЯМР 13С: (CDCl3, δ/м.д.): 70.6 (СН2); 76.7 (СН2); 77.5 (СН); 115.1, 123.7, 125.8, 126.5, 129.6, 152.2 (С-аром.).
Найдено (%): С 55.40; Н 4.20; Cl 29.86; O 20.25. C10H13ClO3.
Вычислено (%):С 55.44; Н 4.25; Cl 29.91; О 20.25.
O-(2,3-дигидроксипроп-1-ил)-2,4,6-трихлорфенола (15). Выход 0.829 г (78.0%). Т.кип. 114-3° (1 мм рт.ст.). ИК-спектр (v, см-1): 3391, 3404 (ОН). Спектр ЯМР 1Н (CDCl3, δ/м.д.): 2.15 (с, 2Н, ОН); 3.85 (д, 2Н, J=10.8 Гц); 4.1 (м, 1Н); 4.7 (д, 2Н, J=10.5 Гц); 6.85-7.35 (с, 3Н, Аг-Н). Спектр ЯМР 13С: (CDCl3, δ/м.д.): 70.6 (СН); 76.7 (СН); 77.5 (СН2); 115.1, 123.7, 125.8, 126.5, 129.6, 152.2 (С-аром.).
Найдено (%): С 45.58; Н 4.20; Cl 29.90; О 20.25. C9H10Cl2O3.
Вычислено (%):С 45.60; Н 4.25; Cl 29.91; О 20.25.
O-(2,3-дигидроксипроп-1-ил)-2,4,5-трихлорфенола (14). Выход 0.829 г (76.0%). Т.кип. 115-3° (1 мм рт.ст.). ИК-спектр (v, см-1): 3390, 3401 (ОН). Спектр ЯМР 1Н (CDCl3, d/м.д.): 2.15 (с, 2Н, ОН); 3.85 (д, 2Н, J=10.8 Гц); 4.1 (м, 1Н); 4.7 (д, 2Н, J=10.5 Гц); 6.85-7.35 (с, 2Н, Аг-Н). Спектр ЯМР 13С: (CDCl3, d/м.д.): 70.6 (СН); 76.7 (СН); 77.5 (СН2); 115.3, 123.9, 125.6, 126.4, 129.3, 152.0 (С-аром.). Найдено (%): С 41.90; Н 4.18; Cl 37.09; O 16.69. C10H12Cl3O3. Вычислено (%):С 41.91; Н 4.22; Cl 37.12; O 16.75.
O-(2,3-дигидроксипроп-1-ил)-2,3,4,5,6-пентахлорфенола (16). Выход 0.829 г (66.0%). Т.кип. 135-3° (1 мм рт. ст.). Найдено (%): С 31.70; Н 2.05; Cl 52.05; О 14.05. C10H12Cl3O3. Вычислено (%):С 31.75; Н 2.07; Cl 52.07; О 14.10. М+340.41 ИК-спектр (v, см-1): 3388, 3408 (ОН). Спектр ЯМР 1Н (CDCl3, d/м.д.): 2.15 (с, 2Н, ОН); 3.85 (д, 2Н, J=10.8 Гц); 4.1 (м, 1Н); 4.7 (д, 2Н, J=10.5 Гц); Спектр ЯМР 13С: (CDCl3, d/м.д.): 70.6 (СН2); 76.7 (СН2); 77.5 (СН); 115.0, 123.5, 125.3, 126.2, 129.3, 152.1 (С-аром.).
Найдено (%): С 31.70; Н 2.05; Cl 52.05; O 14.05. C10H12Cl3O3.
Вычислено (%):С 31.75; Н 2.07; Cl 52.07; O 14.10.
Испытания гербицидной активности O-(2,3-дигидроксипроп-1-ил)-хлорфенолов проводили по методике первичного скрининга новых продуктов органического синтеза на основе экспресс-тестирования в лабораторных условиях [Ю.Я. Спиридонов, Г.Е. Ларина, В.Г. Шестаков. Методическое руководство по изучению гербицидов, применяемых в растениеводстве. М.: Печатный Город, 2009, С.75].
В качестве тест-растения использовали пшеницу как злаковый сорняк в посевах овощных, технических и зернобобовых культур (Захаренко В.А., Захаренко А.В. Борьба с сорняками. Журнал «Защита и карантин растений». №4, 2004, С.63(3).
Представленные в таблице данные свидетельствуют о том, что предлагаемые замещенные фенолы превосходят по гербицидной активности 2,4-дихлорфеноксиуксусную кислоту. Ингибирование роста побегов под действием заявляемых соединений составляет 34,9-67,6%, при использовании прототипа - 2,4-дихлорфеноксиуксусной кислоты - 12,9-15,5%; ингибирование массы побегов соответственно 31,9-76,9% и 11,0-14,3%.
вание, %
| название | год | авторы | номер документа |
|---|---|---|---|
| ХЛОРЗАМЕЩЕННЫЕ 2-ГИДРОКСИФЕНИЛЬНЫЕ ПРОИЗВОДНЫЕ ПРОПАНДИОЛА, ПРОЯВЛЯЮЩИЕ ГЕРБИЦИДНУЮ АКТИВНОСТЬ | 2015 |
|
RU2605208C1 |
| Четвертичные аммониевые соли на основе производных витамина В6 | 2015 |
|
RU2607522C1 |
| ГИПОГЛИКЕМИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ПРОИЗВОДНЫЕ ПИРАЗИНА, НОВЫЕ ПРОИЗВОДНЫЕ ПИРАЗИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2194703C2 |
| 2-ГЕТАРИЛЗАМЕЩЕННЫЕ 1,3-ТРОПОЛОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНТИМИКРОБНОГО ДЕЙСТВИЯ | 2006 |
|
RU2314295C2 |
| ПРОИЗВОДНЫЕ 2-ТИОУРАЦИЛА, ОБЛАДАЮЩИЕ ПРОТИВОАДЕНОВИРУСНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2670204C1 |
| ПРОИЗВОДНЫЕ 1,2,3,4-ТЕТРАГИДРОПИРИДО[4,3-b]ИНДОЛСОДЕРЖАЩИХ ФЕНОТИАЗИНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ ХОЛИНЭСТЕРАЗ И БЛОКАТОРОВ СЕРОТОНИНОВЫХ РЕЦЕПТОРОВ 5-HT, СПОСОБЫ ПОЛУЧЕНИЯ ИХ ХЛОРГИДРАТОВ И ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2013 |
|
RU2530881C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЯ, СОЕДИНЕНИЯ, КОМПЛЕКСНЫЙ МЕТАЛЛООРГАНИЧЕСКИЙ КАТАЛИЗАТОР | 2012 |
|
RU2652807C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСАЗОЛОВ КОНДЕНСАЦИЕЙ АРОМАТИЧЕСКИХ АЛЬДЕГИДОВ С АЛЬФА-КЕТОКСИМАМИ С ОБРАЗОВАНИЕМ N-ОКСИДОВ И ПОСЛЕДУЮЩИМ ВЗАИМОДЕЙСТВИЕМ С АКТИВИРОВАННЫМИ ПРОИЗВОДНЫМИ КИСЛОТ | 2005 |
|
RU2402537C2 |
| ПРОИЗВОДНЫЕ 5H-ДИБЕНЗО[b, e][1, 4]ДИАЗЕПИНА И ИХ ПРИМЕНЕНИЕ | 2010 |
|
RU2441867C2 |
| ФТОРСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ ТЕВИНОЛА И ОРВИНОЛА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2012 |
|
RU2506265C1 |
Настоящее изобретение относится к новым соединениям структурной формулы
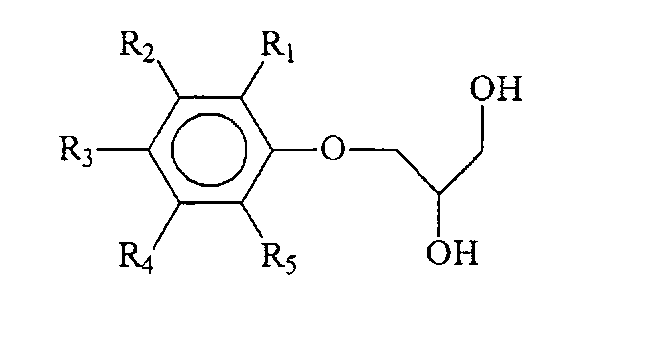
где R1=Cl, R2, R3, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-2-хлорфенол;
R3=Cl, R1, R2, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-4-хлорфенол;
R1, R4=Cl, R2, R3, R5=H O-(2,3-дигидроксипроп-1-ил)-2,5-дихлорфенол;
R1=CH3, R3=Cl, R2, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-2-метил-4-хлорфенол;
R1, R3 ,R5=Cl, R2, R4=H O-(2,3-дигидроксипроп-1-ил)-2,4,6-трихлорфенол;
R1, R3, R4=Cl, R2, R5=H O-(2,3-дигидроксипроп-1-ил)-2,4,5-трихлорфенол,
применяемым для борьбы с сорными растениями семейства Злаковые. 1 з.п.ф-лы, 1 табл.
1. Химическое соединение структурной формулы

где R1=Cl, R2, R3, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-2-хлорфенол;
R3=Cl, R1, R2, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-4-хлорфенол;
R1, R4=Cl, R2, R3, R5=H O-(2,3-дигидроксипроп-1-ил)-2,5-дихлорфенол;
R1=CH3, R3=Cl, R2, R4, R5=H O-(2,3-дигидроксипроп-1-ил)-2-метил-4-хлорфенол;
R1, R3 ,R5=Cl, R2, R4=H O-(2,3-дигидроксипроп-1-ил)-2,4,6-трихлорфенол;
R1, R3, R4=Cl, R2, R5=H O-(2,3-дигидроксипроп-1-ил)-2,4,5-трихлорфенол.
2. Химическое соединение по п.1, которое проявляет гербицидную активность.
| Хонинговальная головка | 1988 |
|
SU1604577A1 |
| Chemical Abstracts on STN, 60:5837 Original Reference N 60:1047d-e Herbicidal selectivity of some derivatives of 2,4-D due to differences in plant metabolism | |||
| Sudi, Janos et al, Antal Kiserletugyi Kozlemenyek, A Kotet: Novenytermesztes, 52(2), 73-92, 1959 | |||
| Устройство для синхронизации | 1932 |
|
SU34646A1 |
| Н.Н | |||
| Мельников | |||
| Химия и технология пестицидов | |||
| М.: Химия, 1974, стр | |||
| ТЕЛЕФОННЫЙ АППАРАТ, ОТЗЫВАЮЩИЙСЯ ТОЛЬКО НА ВХОДЯЩИЕ ТОКИ | 1920 |
|
SU274A1 |
Авторы
Даты
2014-08-10—Публикация
2013-03-19—Подача