Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения сложного эфира N-замещенной карбаминовой кислоты и способу получения изоцианата, в котором используют сложный эфир N-замещенной карбаминовой кислоты.
Уровень техники
Изоцианаты широко используются в качестве сырья при производстве таких продуктов, как пенополиуретан, краски и адгезивы. Несмотря на то что для промышленного получения изоцианатов может быть предложено множество реакций, основной способ промышленного производства включает реакцию амина с фосгеном (фосгеновый способ), описываемую следующей схемой (i), и практически весь объем производимых в мире изоцианатов получают на основе фосгенового способа. Однако фосгеновый способ имеет множество недостатков.
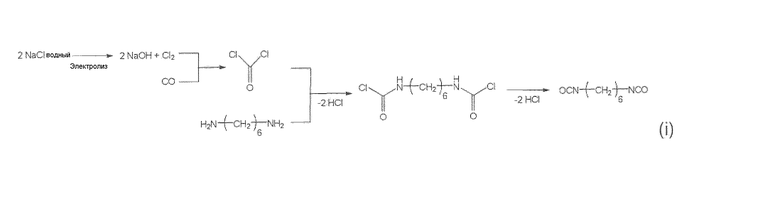
Во-первых, этот способ требует использования в качестве сырья большого количества фосгена. Фосген является исключительно ядовитым веществом, и для предотвращения воздействия фосгена на тех, кто с ним работает, требуются специальные меры предосторожности и, кроме того, необходимы специальные установки для обезвреживания ядовитых отходов.
Во-вторых, так как в качестве побочного продукта фосгенового способа образуются большие количества чрезвычайно коррозионно-агрессивного хлористого водорода, то дополнительно требуется применение способа обезвреживания хлористого водорода, во многих случаях в получаемых изоцианатах содержится гидролитический хлор, который может оказывать неблагоприятное воздействие на стойкость к атмосферным воздействиям и термостойкость полиуретановых продуктов в случае использования изоцианатов, полученных фосгеновым способом.
Таким образом, исходя из существующего на настоящий момент уровня техники, необходим способ получения соединений изоцианата, в котором не используется фосген.
Хотя примеры таких способов могут включать способ синтеза алифатического изоцианата из алифатического нитросоединения и монооксида углерода и способ превращения алифатического амидного соединения в изоцианат путем способа разложения Хоффмана, но оба эти способа дают низкий выход и не подходят для промышленного применения.
Уже давно известны способы получения изоцианата и гидроксильного соединения путем термического разложения соединения N-замещенной карбаминовой кислоты-O-алкилового эфира, примером которых является способ A.В. Хоффмана (см. Непатентный документ 1). Этот способ позволяет более легко достигать высокого выхода, чем в случае описанных выше способов, и основную реакцию, используемую в этом способе, можно изобразить следующей схемой (ii)

Термическое разложение, представленное выше общим уравнением реакции, является обратимым, и его равновесие при низких температурах смещено в левую сторону в направление исходного N-замещенной карбаминовой кислоты-O-алкилового эфира, а при высоких температурах равновесие смещается в сторону образования изоцианата и спирта. Поэтому способы получения изоцианата термическим разложением N-замещенной карбаминовой кислоты-O-алкилового эфира осуществляют при высоких температурах (см., например, примеры 12 и 13 Патентного документа 1). При этом, будучи зависимой от природы эфирной группы N-замещенной карбаминовой кислоты-O-алкилового эфира, температура кипения N-замещенной карбаминовой кислоты-O-метилового эфира составляет, например, 110°C (при пониженном давлении около 2 кПа) (строка 9 верхней правой колонки Непатетного документа 2). С другой стороны, температура кипения гексаметилендиизоцианата, который образуется по соответствующей реакции термического разложения, составляет от 130 до 140°C (при пониженном давлении около 2 кПа) (Непатентный документ 3). То есть, это указывает на то, что N-замещенной карбаминовой кислоты-O-метиловый эфир имеет более низкую температуру кипения, чем продукт в форме гексаметилендиизоцианата. Хотя подробные сведения по поводу температуры термического разложения N-замещенной карбаминовой кислоты-O-метилового эфира не приведены, термическое разложение происходит при 200°C или выше. Если реакцию термического разложения проводить при приведенной температуре 250°C при пониженном давлении, то, так как эти условия превышают температуру кипения N-замещенной карбаминовой кислоты-O-метилового эфира, реакция термического разложения протекает в газовой фазе. Так как в газовой фазе также присутствуют сырье в виде N-замещенной карбаминовой кислоты-O-метилового эфира вместе с продуктом в виде гексаметилендиизоцианата и побочным продуктом в виде метанола, то возникает сложности не только с осуществлением контроля протекания реакции, но и с тем, что также протекают и различные необратимые побочные реакции. Как указано в упомянутой выше публикации H. Schiff (Непатентный документ 4) и в исследовании E. Dyer и G.C. Wright (Непатентный документ 5), примерами таких побочных реакций являются образование замещенных мочевин, биуретов, уретодионов, карбодиимидов и изоциануратов. В случае газофазного термического разложения N-замещенной карбаминовой кислоты-O-алкиловых эфиров, в силу высоких концентраций изоцианата и N-замещенной карбаминовой кислоты-O-алкилового эфира в газовой фазе, легко образуются соединения аллофаната, как показано на следующей схеме реакции (iii). Температуры кипения этих соединений аллофаната являются высокими, так как они образуются в результате реакции сшивания, и эти соединения аллофаната тут же после образования в реакторе переходят в жидкое состояние. Кроме того, даже когда соединения аллофаната находятся в этом жидком состоянии, между ними легко происходит сшивание вследствие термического разложения групп N-замещенной карбаминовой кислоты-O-алкилового эфира. В результате, аллофанаты постепенно отвердевают, что приводит к забивке реактора.
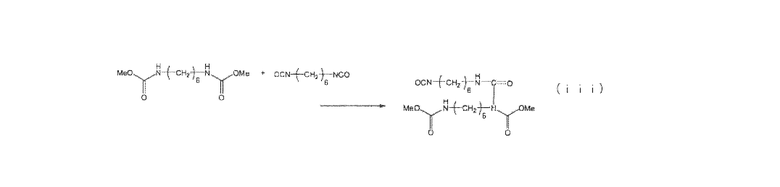
В случае использования N-замещенной карбаминовой кислоты-O-алкилового эфира в качестве сырья для реакции термического разложения эти побочные реакции не только приводят к снижению выхода и селективности по целевому изоцианату, но также вызывают в процессе производства образование полимеров, в частности полиизоцианата, и в зависимости от случая, могут приводить к ситуации, при которой затрудняется длительная эксплуатация реактора, например, к забивке реактора в результате осаждения твердых полимерных частиц.
Кроме того, уже в течение длительного времени проводятся исследования по способам получения описанных выше N-замещенной карбаминовой кислоты-O-алкиловых эфиров. Способ, описанный в Патентном документе 2, включает получение алифатической карбаминовой кислоты-O-алкилового эфира без использования фосгена. На первой стадии этого способа алифатической карбаминовой кислоты-O-алкиловый эфир получают из алифатического первичного амина и мочевины путем реакции N,N'-диалкилмочевины с гидроксисоединением, после чего образовавшийся первичный амин выделяют в качестве побочного продукта, извлекают и возвращают на первую стадию. Так как этот способ не только характеризуется низким выходом образующегося эфира карбаминовой кислоты, но и требует оборудования для рециркуляции первичного амина, он является слишком сложным и не подходит для промышленного применения.
В качестве альтернативных способов получения N-замещенной карбаминовой кислоты-O-алкилового эфира были предложены способы с использованием мочевины или производной угольной кислоты (такой как эфир угольной кислоты или эфир карбаминовой кислоты).
Способ, описанный в Патентном документе 3, включает взаимодействие первичного диамина и спирта с мочевиной или производной угольной кислоты в присутствии катализатора с последующей конверсией в N-замещенной карбаминовой кислоты-O-алкиловый эфир. В способе, описанном в Патентном документе 4, N-замещенной карбаминовой кислоты-O-алкиловый эфир получают после получения сначала бис-мочевины из алифатического первичного амина, мочевины и спирта, в то время как способ, описанный в Патентном документе 5, включает неполную реакцию мочевины и спирта на первой стадии с последующим введением диамина для получения N-замещенной карбаминовой кислоты-O-алкилового эфира на второй стадии. В Патентном документе 6 описан способ получения N-замещенной карбаминовой кислоты-O-алкилового эфира путем взаимодействия первичного амина и не-N-замещенной карбаминовой кислоты-O-алкилового эфира в присутствии спирта при отношении NH2 групп к карбамату и к спирту 1 : (от 0,8 до 10,0) : (от 0,25 до 50), при температуре от 160 до 300°C и в присутствии или в отсутствие катализатора, и затем удаления аммиака, если в этом есть необходимость. В способе, описанном в Патентном документе 7, получают ароматический диизоцианат и/или полиизоцианат с помощью следующих двух стадий. На первой стадии ароматический первичный амин и не-N-замещенной карбаминовой кислоты-O-алкиловый эфир подвергают взаимодействию в присутствии или в отсутствие катализатора и в присутствии или в отсутствие мочевины и спирта с получением N-арилкарбаминовой кислоты-O-алкилового эфира при удалении образующегося в качестве побочного продукта аммиака, если в этом есть необходимость, в то время как на второй стадии N-арилкарбаминовой кислоты-O-алкиловый эфир подвергают термическому разложению с получением ароматического изоцианата. Способ, описанный в Патентном документе 8, включает получение N-алкилкарбаминовой кислоты-O-алкилового эфира после получения сначала бис-мочевины из алифатического первичного полиамина, мочевины и спирта. В Патентном документе 9 описан способ получения алифатического O-алкилмоноуретана взаимодействием алифатического первичного амина и мочевины с алифатическим спиртом.
Однако, как уже было описано ранее, эти реакции термического разложения для получения изоцианатов из N-замещенной карбаминовой кислоты-O-алкиловых эфиров требуют высоких температур и приводят к образованию полимерных соединений, которые являются следствием протекания нежелательных побочных реакций, приведенных, например, в упомянутой выше схеме (iii).
Большинство нежелательных побочных реакций легко протекают при высоких температурах. Кроме того, изоцианаты, образовавшиеся в реакциях термического разложения, могут увеличивать продолжительность контакта с непрореагировавшим N-замещенной карбаминовой кислоты-O-алкиловым эфиром и другими компонентами реакций (включая те, в которых часть эфиров карбаминовой кислоты превратилась в изоцианатные группы в случае реакции термического разложения, для которой сырьем является поли(N-замещенной карбаминовой кислоты-O-алкиловый эфир)). Были предложены различные способы для достижения благоприятного выхода изоцианата путем предотвращения образования продуктов нежелательных побочных реакций в процессе термического разложения N-замещенной карбаминовой кислоты-O-алкиловых эфиров.
Среди N-замещенной карбаминовой кислоты-O-эфиров (N-замещенной карбаминовой кислоты-O-эфиры относятся к эфирам карбаминовой кислоты, содержащим группу карбаминовой кислоты и органическую группу, и в интерпретации настоящего изобретения обозначают N-замещенной карбаминовой кислоты-O-ариловые эфиры, в которых органическая группа является производной ароматической гидроксигруппы, и/или N-замещенной карбаминовой кислоты-O-алкиловыми эфирами, в которых органическая группа является производной спирта), N-замещенной карбаминовой кислоты-O-ариловые эфиры, в которых эфирная группа, которая составляет N-замещенной карбаминовой кислоты-O-эфир, является ароматической группой (то есть, сложноэфирной группой карбаминовой кислоты, полученной из ароматической гидроксигруппы) обладают преимуществом, связанным с возможностью применения более низкой температуры для реакции термического разложения по сравнению с N-замещенной карбаминовой кислоты-O-алкиловыми эфирами, в которых сложноэфирной группой является алкильная группа (см., например, Патентный документ 10). Другими словами, можно предотвратить образование продуктов в результате протекания упомянутых выше нежелательных побочных реакций, если возможно проводить реакцию термического разложения при более низкой температуре.
С другой стороны, получение таких N-замещенной карбаминовой кислоты-O-ариловых эфиров является более трудной задачей, чем получение N-замещенной карбаминовой кислоты-O-алкиловых эфиров. Это объясняется реакционной способностью спирта и ароматического гидроксисоединения, используемых в качестве сырья для их соответствующих реакций этерификации. Первой причиной является то, что ароматические гидроксисоединения имеют более низкую нуклеофильность, чем спирты. Вторая причина заключается в том, что с трудом идет реакция этерификации вследствие слабых кислотных свойств ароматических гидроксисоединений.
В Патентном документе 11 описан способ получения алифатической N-замещенной карбаминовой кислоты-O-арилового эфира без использования фосгена. В этом способе N-замещенной карбаминовой кислоты-O-ариловый эфир получают окислением из первичного амина, монооксида углерода и алифатического спирта или ароматического гидроксисоединения с использованием катализатора из благородного металла. Однако у этого способа есть недостатки, связанные со сложностью технологии и значительными затратами. Эти недостатки относятся к использованию высокотоксичного монооксида углерода и необходимости извлекать катализатор из продукта в виде N-замещенной карбаминовой кислоты-O-арилового эфира вследствие использования дорогого катализатора из благородного металла. В Патентном документе 12 описан способ получения N-замещенной карбаминовой кислоты-O-арилового эфира путем взаимодействия N-алкил-N,N'-диалкилмочевины, ароматического гидроксисоединения и газообразного хлористого водорода. Однако этот способ также имеет сложную технологию и требует значительных затрат. А именно, в этом способе используется коррозионно-агрессивный газообразный хлористый водород, расходуется дорогое и редкое соединение мочевины, и возникают сложности с извлечением N-замещенной карбаминовой кислоты-O-арилового эфира из гидрохлорида N,N'-диалкиламина, образующегося в качестве побочного продукта. В способе, описанном в Патентном документе 13, N-замещенной карбаминовой кислоты-O-ариловый эфир получают в одну стадию путем реакции между мочевиной, ароматическим гидроксисоединением и алифатическим первичный амином. В способе, описанном в Патентном документе 14, на первой стадии подвергают взаимодействию мочевину и ароматическое гидроксисоединение, и на следующей второй стадии получают путем реакции с первичным амином N-замещенной карбаминовой кислоты-O-ариловый эфир.
Были также раскрыты технологические методы повышения низкой нуклеофильности ароматических гидроксисоединений и преодоления сложности сдвига равновесия. В Патентном документе 15 и Патентном документе 16 раскрыты способы получения алифатического O-арилуретана в одну стадию путем реакции мочевины и/или O-арилкарбамата (не-N-замещенной карбаминовой кислоты-O-арилового эфира), ароматического гидроксисоединения и алифатического первичного амина. В этих способах разработано значительное усовершенствование в отношении удаления аммиака, например, путем реакционной дистилляции или введения большого количества инертного газа. В Патентном документе 17 раскрыт способ непрерывного получения уретана при непрерывной подаче в реакционную колонну первичного полиамина, мочевины и/или не-N-замещенной карбаминовой кислоты сложного эфира и органического гидроксисоединения с образованием соответствующего уретана и непрерывном выводе образовавшегося в реакционной колонне аммиака из реакционной колонны. С другой стороны, в Патентном документе 18 описан способ, в котором не используют описанное выше ароматическое гидроксисоединение с низкой нуклеофильностью. Этот способ позволяет получать соответствующий N-алкилкарбаминовой кислоты-O-ариловый эфир с выходом от 90 до 95% путем реакции первичного алкиламина с диарилкарбонатом в присутствие растворителя, такого как бензол, диоксан и четыреххлористый углерод. Этот способ имеет преимущество, связанное с возможностью получения N-замещенной карбаминовой кислоты-O-арилового эфира при низкой температуре и с высокой селективностью. Однако в настоящее время применению этого способа в промышленности препятствует высокая стоимость диарилкарбоната.
В случае способов, в которых применяют безопасное и недорогое сырье в виде мочевины и производных угольной кислоты, для того чтобы повысить выход по отношению к относительно дорогому первичному амину, необходимо использовать избыток мочевины или производной угольной кислоты по отношению к аминогруппе первичного амина. Однако это не означает, что в этих способах были успешно решены проблемы подавления побочных реакций или повышения селективности относительно первичного амина.
Способ, описанный в Патентном документе 19, включает извлечение не-N-замещенной карбаминовой кислоты-O-арилового эфира из полученной реакционной жидкости и его рециркуляцию для использования в качестве сырья для реакции при получении N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции алифатического первичного полиамина, ароматического гидроксисоединения, мочевины и/или не-N-замещенной карбаминовой кислоты-O-арилового эфира. А именно, этот способ позволяет снизить используемое количество мочевины и/или не-N-замещенной карбаминовой кислоты-O-арилового эфира. В этом способе после получения ароматического гидроксисоединения и изоциановой кислоты в результате термического разложения не-N-замещенной карбаминовой кислоты-O-арилового эфира, содержащегося в реакционной жидкости, и отгонки ароматического гидроксисоединения при низкой температуре, изоциановую кислоту снова подвергают взаимодействию с отогнанным ароматическим гидроксисоединением и извлекают в виде не-N-замещенной карбаминовой кислоты-O-арилового эфира. Однако, кроме того, что этот способ характеризуется сложной технологией, является неудовлетворительной степень извлечения не-N-замещенной карбаминовой кислоты-O-арилового эфира.
Таким образом, еще не описан способ получения N-замещенной карбаминовой кислоты-O-арилового эфира с использованием безопасной мочевины или производной угольной кислоты, в котором количества мочевины или производной угольной кислоты соответствуют количеству первичного амина. Как было ранее описано, это является следствием как низкой нуклеофильности ароматических гидроксисоединений, так и низкой катионности карбонильных углеродов мочевины и производной угольной кислоты.
Несмотря на упомянутые выше проблемы, так как с промышленной точки зрения было бы чрезвычайно важным получать изоцианаты без использования фосгена, в дополнение к уже описанным выше способам были предложены различные подходы для усовершенствования способов производства изоцианатов с использованием N-замещенной карбаминовой кислоты-O-эфиров. Предложены способы, которые осуществляют в газовой фазе при высоких температурах, так же как и способы, которые реализуют в жидкой фазе при относительно низких температурах. Однако, как уже было описано выше, так как в ряде случаев в процессе термического разложения N-замещенной карбаминовой кислоты-O-алкиловых эфиров протекают побочные реакции с образованием осадков, полимерных веществ, в результате чего происходит забивка реактора и установок для разделения, или с образованием веществ, прилипающих к стенкам реактора, то в случае производства изоцианатов в течение продолжительного периода времени экономическая эффективность таких процессов является низкой. Таким образом, несмотря на то, что были предложены методы повышения выхода в процессе термического разложения N-замещенной карбаминовой кислоты-O-алкиловых эфиров, например, применение химических методов, таких как использование специального катализатора (см. Патентный документ 20 или Патентный документ 21), или катализатора в комбинации с инертным растворителем (см. Патентный документ 22), проблемы, с которыми сталкиваются при производстве N-замещенной карбаминовой кислоты-O-ариловых эфиров, еще не решены. Например, способ, описанный в Патентном документе 23, является способом получения гексаметилендиизоцианата. Этот способ включает термическое разложение гексаметилендикарбаминовой кислоты-O-этилового эфира в присутствии каталитической смеси, содержащей метилтолуолсульфонат и дихлорид дифенилолова при использовании дибензилтолуола в качестве растворителя. Однако, подробно не описано получение и выделение исходных компонентов, так же как очистка и извлечение каким-либо способом растворителя и каталитической смеси, и экономическая эффективность этого способа является чрезвычайно низкой.
В способе, описанном в Патентном документе 24, N-замещенной карбаминовой кислоты-O-алкиловый эфир легко разлагают до изоцианата и спирта без использования катализатора в псевдоожиженном слое, содержащем частицы углерода. Однако, выход изоцианата, достигаемый в реакции термического разложения, составляет приблизительно от 83,8 до 98,7%, и хотя побочные продукты реакции и другие подобные продукты не описаны, так как N-замещенной карбаминовой кислоты-O-алкиловый эфир все-таки подвергают термическому разложению и получающиеся соединения включают изоцианат и спирт, которые аналогичным образом подвержены протеканию обратимых реакций, как и в способах предшествующего уровня техники, нельзя утверждать, что были подавлены упомянутые выше реакции. В способе, описанном в Патентном документе 25, предложен способ с циркуляцией для получения алициклического диизоцианата путем реакции алициклического первичного диамина, мочевины и спирта с получением алициклической дикарбаминовой кислоты-O-алкилового эфира с последующим термическим разложением алициклической дикарбаминовой кислоты-O-алкилового эфира. Этот способ осуществляют при снижении количества используемых материалов в результате извлечения непрореагировавшего спирта, не-N-замещенной карбаминовой кислоты-O-эфира и диалкилкарбонатов и рециркуляции части реакционной смеси со стадии термического разложения вместе с побочными продуктами на начальную стадию. Однако, этот способ требует отгонки алициклической дикарбаминовой кислоты-O-алкилового эфира при высокой температуре около 230°C для удаления остатка, который нельзя использовать в данном способе получения. Так как эта высокая температура отгонки находится в температурном интервале, при котором карбаминовой кислоты-O-алкиловые эфиры подвергаются термическому разложению, изоцианатные группы, образовавшиеся в процессе отгонки, перестают реагировать с алициклической дикарбаминовой кислоты-O-алкиловым эфиром, что приводит к возможности образования твердых полимеров. Хотя в примерах указано, что выход сохраняется постоянным на протяжении длительного периода эксплуатации, ничего не упоминается относительно наличия накопления полимеров или забивки установок вследствие протекания побочных реакций.
Кроме того, способ, описанный в Патентном документе 26, включает частичное удаление бесполезных побочных продуктов перед термическим разложением N-замещенной карбаминовой кислоты-O-алкилового эфира. Однако, в этом способе, вследствие того, что N-замещенной карбаминовой кислоты-O-алкиловый эфир также удаляют вместе с частично удаляемыми побочными продуктами, выход изоцианата в расчете на первичный амин и производную карбоновой кислоты, в конечном счете, понижается. Кроме того, из остающихся в реакторе побочных продуктов образуются полимерные соединения, которые не выводят из реактора при нагревании, и так как эти соединения прилипают к стенкам реактора, то затруднительно осуществлять непрерывную эксплуатацию реактора в течение длительного периода времени.
В реакциях получения N-замещенной карбаминовой кислоты-O-(алкилового или арилового)эфира путем взаимодействия мочевины и производной угольной кислоты (или производной карбаминовой кислоты) с первичным амином и спиртом или ароматическим гидроксисоединением, для повышения селективности по дорогому первичному амину, мочевину и производную угольной кислоты (или производную карбаминовой кислоты) используют в избытке.
Уравнение реакции N-замещенной карбаминовой кислоты-O-алкилового эфира в случае использования в качестве сырья первичного амина и мочевины приведено на следующей схеме реакции (iv). Несмотря на то, что в начальной стадии реакции присутствует соответствующее количество мочевины относительно первичного амина, по мере того как реакция входит в заключительную стадию, концентрации обоих (первичного амина и мочевины) понижаются, в результате чего N-замещенной карбаминовой кислоты-O-алкиловый эфир присутствует при высокой концентрации. Как уже было описано ранее, катионность мочевины и карбонильных углеродов производных угольной кислоты является низкой (вследствие принятия свободного электрона группами NH2 и алкоксильными группами), и разница в реакционной способности между карбонильными углеродами продукта в форме N-замещенной карбаминовой кислоты-O-алкилового эфира и первичным амином является незначительной. Таким образом, если количество мочевины присутствует не в избытке относительно первичного амина, то реакция происходит так, как указано в уравнении реакции (v) для последней фазы реакции. А именно, первичный амин реагирует с продуктом в форме N-замещенной карбаминовой кислоты-O-(алкилового или арилового) эфира, что приводит к превращению его в соединение, имеющего денатурированные связи N,N-дизамещенной мочевины. В случае использования полиамина, так как каждая аминогруппа реагирует последовательно, то образуются различные нежелательные формы в дополнение к тем, которые приведены в следующем уравнении реакции (v). Кроме того, также протекают реакции в соответствии со следующим уравнением реакции (vii), включая реакцию с изоцианатом, образовавшимся по следующему уравнению реакции (vi), и на основе знаний по органической химии и скоростей реакций можно без труда предположить, что по мере того как накапливается N-замещенной карбаминовой кислоты-O-(алкиловый или ариловый) эфир и снижается концентрация мочевины, резко возрастает образование этих продуктов денатурации. Обычно дополнительно образуются полимеризованные высокомолекулярные вещества в соответствии с уравнениями реакций (v), (vi) и (vii). Так как соединения, имеющие связи N,N-дизамещенной мочевины вследствие этой денатурации, имеют низкие уровни реакционной способности, становится затруднительным повторное добавление диссоциированного спирта. Такие реакции протекают при высоких температурах, но так как при высоких температурах также начинает протекать образование изоцианатов в результате термического разложения N-замещенной карбаминовой кислоты-O-(алкилового или арилового) эфира, то это приводит к протеканию набора разнообразных побочных реакций.
(Начальная реакция)
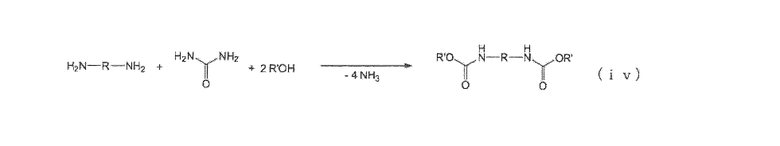
(Последующая реакция: реакция с N-замещенной карбаминовой кислоты-O-(алкиловым или ариловым)эфиром
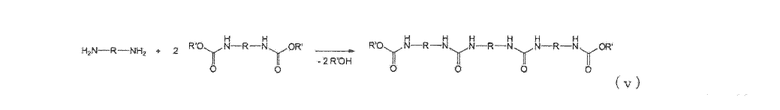
(Последующая реакция: реакция с изоцианатом)
Образование изоцианата
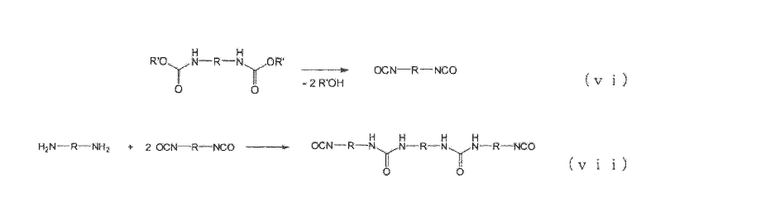
Так как полимерные вещества, образующиеся в соответствии с упомянутыми выше реакциями, имеют чрезвычайно низкую растворимость в растворителях и другие подобные свойства, они часто слипаются и становятся твердыми в реакторе, что делает такие способы неудовлетворительными с точки зрения их применения в промышленности. Для решения таких проблем уже были рассмотрены описанные ранее способы (см. Патентный документ 4) получения N-замещенной карбаминовой кислоты-O-алкилового эфира путем получения бис-мочевины из первичного амина, мочевины и спирта и затем взаимодействия бис-мочевины со спиртом, но эти способы относятся к реакции с высоконуклеофильным спиртом, и их не применяют для решения проблемы, возникающей при термическом разложении N-замещенной карбаминовой кислоты-O-алкилового эфира, что не позволяет решать проблемы с помощью таких способов, которые возникают в описанном выше процессе термического разложения N-замещенной карбаминовой кислоты-O-алкилового эфира. Кроме того, был предложен способ получения бис-мочевины, включающий реакцию расплавленной мочевины и амина в отсутствие растворителя (см. например, Непатентный документ 6), но вследствие высокой температуры плавления мочевины (около 135°C) во многих случаях реакция протекает неселективно, позволяя в результате протекать реакциям денатурации мочевины и реакциям, приводящим к образованию соединений, имеющих связи N,N-дизамещенной мочевины, что в результате не позволяет решать упомянутые выше проблемы.
Кроме того, был также разработан способ очистки таких полимерных веществ путем кристаллизации (Патентный документ 27). В этом способе также представляет сложность проведение селективной кристаллизации с высоким выходом соединений, имеющих аналогичные структуры, в то время как, с другой стороны, расходуется энергия для разделения жидких и твердых веществ, а также для извлечения растворителя кристаллизации.
Документы известного уровня техники
Патентные документы
Патентный документ 1: U.S. Patent No. 7122697
Патентный документ 2: U.S. Patent No. 2677698
Патентный документ 3: U.S. Patent No. 4713476
Патентный документ 4: EP Application No. 0568782
Патентный документ 5: EP Application No. 0657420
Патентный документ 6: U.S. Patent No. 4497963
Патентный документ 7: U.S. Patent No. 4290970
Патентный документ 8: Japanese Patent Application Laid-open No. H6-41045
Патентный документ 9: U.S. Patent No. 2409701
Патентный документ 10 : U.S. Patent No. 3992430
Патентный документ 11: U.S. Patent No. 4297501
Патентный документ 12: U.S. Patent No. 3873553
Патентный документ 13: U.S. Patent No. 4925971
Патентный документ 14: Japanese Patent Application Laid-open No. H4-164060
Патентный документ 15 : Japanese Patent Application Laid-open No. H2-759
Патентный документ 16 : Japanese Patent Application Laid-open No. H3-20254
Патентный документ 17: Japanese Patent Application Laid-open No. H8-277255
Патентный документ 18: Japanese Patent Application Laid-open No. S52-71443
Патентный документ 19: Japanese Patent Application Laid-open No. H7-157463
Патентный документ 20: U.S. Patent No. 2692275
Патентный документ 21: U.S. Patent No. 3734941
Патентный документ 22: U.S. Patent No. 4081472
Патентный документ 23: U.S. Patent No. 4388426
Патентный документ 24: U.S. Patent No. 4482499
Патентный документ 25: EP Application No. 0355443
Патентный документ 26: Japanese Patent No. 3382289
Патентный документ 27: Japanese Patent No. 2804132
Непатентные документы
Непатентный документ 1: Berchte der Deutechen Chemischen Gesellschaft, Vol. 3, p. 653, 1870
Непатентный документ 2: Journal of American Chemical Society, Vol. 73, p. 1831, 1951, line 9 from the top of the right column
Непатентный документ 3: Journal of American Chemical Society, Perkin Transactions 1: Organic and Bio-Organic Chemistry (1972-1999), pp. 141-143, 1976
Непатентный документ 4: Berchte der Deutechen Chemischen Gesellschaft, Vol. 3, p. 649, 1870
Непатентный документ 5: Journal of American Chemical Society, Vol. 81, p. 2138, 1959
Непатентный документ 6: Polymer, Vol. 35, p. 3766, 1994
Описание изобретения
Задачи, решаемые изобретением
Как было описано выше, даже с помощью любого из апробированных до настоящего времени способов при использовании в качестве сырья мочевины и не-N-замещенной карбаминовой кислоты-O-эфиров все же трудно получить N-замещенной карбаминовой кислоты-O-(алкиловые или ариловые) эфиры с высоким выходом, и обычно продукты их реакций практически во всех случаях включают соединения, имеющие связи мочевины (-NHCONH-), соединения, имеющие мочевинные концевые группы (-NHCONH2), соединения, имеющие аминные концевые группы (-NH2), или соединения, имеющие аллофанатные связи, и другие подобные соединения. Так для способов, в которых используют наименее дорогое и самое безопасное сырье в виде мочевины, все еще находится на стадии решения проблема предотвращения увеличения используемых количеств мочевины и первичного амина, связанная с их побочными реакциями, и вследствие забивки и других относящихся к способу проблем, а также высоких издержек производства изоцианатов, то необходимо разработать способ, альтернативный способу с использованием фосгена.
Таким образом, все еще остается множество нерешенных проблем, включая получение предшественников изоцианата в виде N-замещенной карбаминовой кислоты-O-(алкиловых или ариловых) эфиров, и существует срочная необходимость в решении этих проблем.
Как уже было описано ранее, были предложены различные способы в качестве способов получения N-замещенной карбаминовой кислоты-O-(алкилового или арилового) эфира при использовании мочевины или производных угольной кислот. Известно, что соответствующие изоцианаты могут быть получены термическим разложением N-замещенной карбаминовой кислоты-O-(алкиловых или ариловых)эфиров.
Однако, в случае использования N-замещенной карбаминовой кислоты-O-арилового эфира в качестве предшественника изоцианата, образующийся изоцианат и сырье в виде N-замещенной карбаминовой кислоты-O-арилового эфира реагируют вследствие высокой температуры термического разложения, что приводит к повышенной склонности к денатурированию. Кроме того, в реакции термического разложения как спирт, так и изоцианат, присутствуют в газовой фазе. Так как реакция между спиртом и изоцианатом протекает быстро, в результате обратимой реакции в газовой фазе происходит реакция, в которой изоцианат превращается обратно в N-замещенной карбаминовой кислоты-O-ариловый эфир, что приводит к повышенной склонности к возникновению забивки линий, таких как линия извлечения изоцианата из реактора.
С другой стороны, в случае использования N-замещенной карбаминовой кислоты-O-арилового эфира в качестве предшественника, возникают проблемы с получением N-замещенной карбаминовой кислоты-O-арилового эфира. Они являются следствием низкой нуклеофильности ароматических гидроксисоединений и сложности повышения селективности реакции получения N-замещенной карбаминовой кислоты-O-ариловых эфиров из первичных аминов. Причиной снижения селективности является низкая скорость этерификации и то, что скорости других нежелательных побочных реакций являются более высокими, чем скорость этерификации, вследствие низкой нуклеофильности ароматических гидроксисоединений.
Кроме того, для повышения выхода по относительно дорогому первичному амину, раскрытые способы требуют использования избытка мочевины или производной угольной кислоты относительно аминогрупп первичного амина. Однако, еще не был описан способ эффективного извлечения и повторного использования избытка мочевины или производной угольной кислоты, и отсутствует возможность предотвращения увеличения расходных коэффициентов по мочевине или производной угольной кислоты.
Авторы настоящего изобретения ранее раскрыли способ подавления реакций термического денатурирования N-замещенной карбаминовой кислоты-O-алкиловых эфиров путем использования специального ароматического гидроксисоединения в качестве реакционного растворителя (International Patent Publication WO 2008/120645), и также раскрыли способ повышения термической стабильности ароматических гидроксисоединений путем наличия следового количества производной угольной кислоты, присутствующей в процессе термического разложения N-замещенной карбаминовой кислоты-O-алкилового эфира, который получают путем реакции эфира угольной кислоты и первичного амина в присутствии ароматического гидроксисоединения (International Patent Publication WO 2008/084824).
В результате исследований, проведенных авторами настоящего изобретения, было четко определено, что если в реакционной жидкости N-замещенной карбаминовой кислоты-O-арилового эфира, полученного при использовании мочевины или производной угольной кислоты, присутствует определенное количество или более мочевины или производной угольной кислоты, то наблюдается склеивание и/или накопление нерастворимых твердых частиц, которые, как предполагается, являются продуктами взаимодействия мочевины и/или производной угольной кислоты и изоцианата в процессе получения изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира, что в результате приводит к возможности возникновения проблем, включающих проблемы, относящиеся к возможности длительной эксплуатации производственного оборудования.
Задачей настоящего изобретения является разработка способа получения N-замещенной карбаминовой кислоты-O-арилового эфира, при осуществлении которого не возникают различные обсужденные выше проблемы, и разработка способа получения изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира.
На основании вышеизложенного и в результате проведения обширных исследований по упомянутым выше проблемам авторы настоящего изобретения обнаружили, что эти проблемы решаются в результате того, что получаемый из соединения, имеющего уреидные группы, и ароматического гидроксисоединения N-замещенной карбаминовой кислоты-O-арилового эфира, получают из соединения, имеющего уреидные группы, и специальной ароматической гидроксикомпозиции, и затем путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира получают изоцианат, в результате чего и реализуется настоящее изобретение.
А именно, в первом своем аспекте настоящее изобретение предлагает
[1] Способ получения по меньшей мере одного N-замещенной карбаминовой кислоты-O-арилового эфира (где N-замещенной карбаминовой кислоты-O-ариловый эфир относится к эфиру N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с ароматическим кольцом), получаемого из соединения, имеющего уреидную группу, представленного следующей формулой (1), и ароматической гидроксикомпозиции, включающей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2), где способ включает стадию проведения этерификации, или этерификации и переэтерификации соединения, имеющего уреидную группу, и ароматической гидроксикомпозиции:
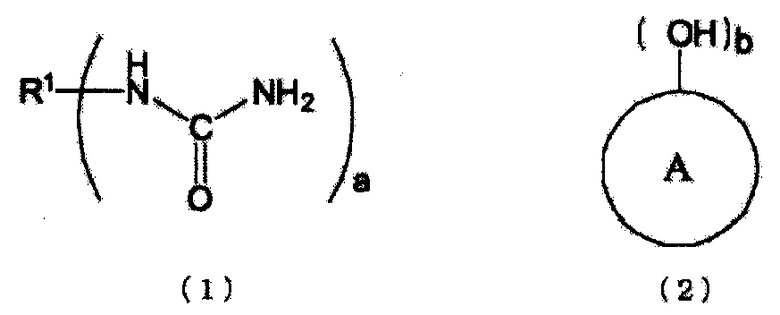
(где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена а раз уреидными группами (уреидной группой), и a представляет целое число от 1 до 10, и
кольцо A представляет органическую группу, которая содержит ароматическую группу, замещенную b раз гидроксильнми группами (гидроксильной группой) в произвольном месте (местах), которое сохраняет ароматические свойства, и которая содержит целое число углеродных атомов в интервале от 6 до 50, может являться одним или множеством гетероциклических колец, и может быть замещено другими заместителями, и b представляет целое число от 1 до 6).
[2] Способ получения по приведенному выше пункту [1], где соединением, имеющим уреидную группу, является соединение, имеющее уреидную группу, полученное с помощью способа, включающего следующую стадию A:
стадия (A): стадия получения по меньшей мере одного типа соединения, имеющего уреидную группу, получаемого из органического первичного амина, представленного следующей формулой (3), и мочевины, путем проведения реакции образования уреидов из органического первичного амина и мочевины в жидкой фазе и выделения или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта при реакции образования уреидов:
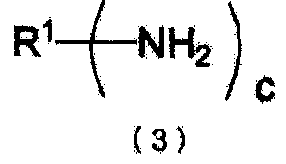
(где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена c раз группами (группой) NH2, и c представляет целое число от 1 до 10).
[3] Способ получения по приведенному выше пункту [2], где органическим первичным амином является органический первичный моноамин или органический первичный диамин.
[4] Способ получения по приведенному выше пункту [2], где стадию (A) проводят в присутствии воды, и/или спирта, и/или ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения.
[5] Способ получения по приведенному выше пункту [2], где стадию (A) проводят в присутствии ароматической гидроксикомпозиции, включающей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2):
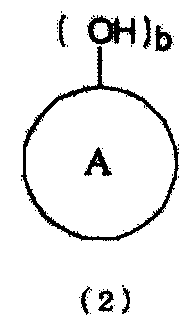
(где
кольцо A представляет органическую группу, которая содержит ароматическую группу, замещенную b раз гидроксильными группами (гидроксильной группой) в произвольном месте (местах), которая сохраняет ароматические свойства и которая содержит целое число углеродных атомов в интервале от 6 до 50, может являться одним или множеством гетероциклических колец и может быть замещена другими заместителями, и b представляет целое число от 1 до 6).
[6] Способ получения по приведенному выше пункту [2], где стадию (A) проводят в присутствии спирта, представленного следующей формулой (4):
R 2 OH (4)
(где
R2 представляет алифатическую группу или алифатическую группу, с которой связана ароматическая группа, которая содержит целое число углеродных атомов в интервале от 1 до 14, и OH группа спирта, представленного формулой (4), является OH группой, которая не связана с ароматическим кольцом).
Кроме того, во втором своем аспекте настоящее изобретение предлагает
[7] Композицию для транспортировки и хранения соединения, имеющего уреидную группу, где число молекул по меньшей мере одного типа ароматического гидроксисоединения, представленного следующей формулой (2), в ароматической гидроксикомпозиции, которая включает ароматическое гидроксисоединение, относительно числа уреидных групп, содержащихся в соединении, имеющем уреидную группу, представленным следующей формулой (1), в композиции составляет целое число от 1 до 100:

(где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена a раз уреидными группами (уреидной группой), и a представляет целое число от 1 до 10), и
кольцо A представляет органическую группу, которая содержит ароматическую группу, замещенную b раз гидроксильными группами (гидроксильной группой) в произвольном месте (местах), которая сохраняет ароматические свойства и которая содержит целое число углеродных атомов в интервале от 6 до 50, может являться одним или множеством гетероциклических колец и может быть замещена другими заместителями, и b представляет целое число от 1 до 6).
[8] Способ получения по приведенному выше пункту [1], дополнительно включающий следующие стадии (A) и (B):
стадия (A): стадия получения по меньшей мере одного типа соединения, имеющего уреидную группу, получаемого из органического первичного амина, представленного следующей формулой (3), и мочевины, путем проведения реакции образования уреидов из органического первичного амина и мочевины в жидкой фазе, и выделения или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта при реакции образования уреидов, и
стадия (B): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции, по меньшей мере, одного типа соединения, имеющего уреидную группу, и ароматической гидроксикомпозиции, включающей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2), в жидкой фазе, и извлечения аммиака, образующегося в качестве побочного продукта, в газовую фазу:
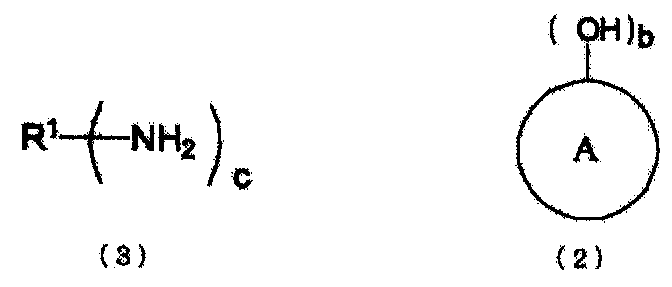
(где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена c раз группами (группой) NH2, и c представляет целое число от 1 до 10, и
кольцо A представляет органическую группу, которая содержит ароматическую группу, замещенную b раз гидроксильными группами (гидроксильной группой) в произвольном месте (местах), которая сохраняет ароматические свойства и которая содержит целое число углеродных атомов в интервале от 6 до 50, может являться одним или множеством гетероциклических колец и может быть замещена другими заместителями, и b представляет целое число от 1 до 6).
[9] Способ получения по приведенному выше пункту [1], дополнительно включающий следующие стадии (A), (R) и (P):
стадия (A): стадия получения по меньшей мере одного типа соединения, имеющего уреидную группу, получаемого из органического первичного амина, представленного следующей формулой (3), и мочевины, путем проведения реакции образования уреидов из органического первичного амина и мочевины в жидкой фазе и выделения или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта при реакции образования уреидов,
стадия (R): стадия получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции по меньшей мере одного типа соединения, имеющего уреидную группу, и спирта, представленного следующей формулой (4), в жидкой фазе, и извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта (где N-замещенной карбаминовой кислоты-O-R2 эфир представляет сложный эфир N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с группой R2, полученной из спирта), и
стадия (P): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции, включающей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2), в жидкой фазе и извлечения спирта, образующегося в качестве побочного продукта, в газовую фазу:
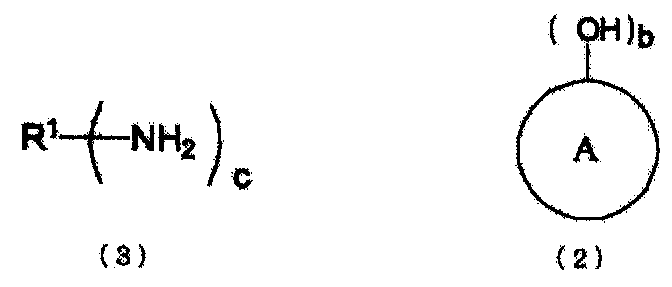
R 2 OH (4)
(где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена c раз группами (группой) NH2, и c представляет целое число от 1 до 10,
кольцо A представляет органическую группу, которая содержит ароматическую группу, замещенную b раз гидроксильными группами (гидроксильной группой) в произвольном месте (местах), которая сохраняет ароматические свойства и которая содержит целое число углеродных атомов в интервале от 6 до 50, может являться одним или множеством гетероциклических колец и может быть замещена другими заместителями, и b представляет целое число от 1 до 6, и
R2 представляет алифатическую группу или алифатическую группу, с которой связана ароматическая группа, которая содержит целое число углеродных атомов в интервале от 1 до 14, и OH группа спирта, представленного формулой (4), является OH группой, которая не связана с ароматическим кольцом).
[10] Способ получения по приведенному выше пункту [8] или [9], где органическим первичным амином является ароматический органический первичный моноамин, представленный следующей формулой (5), следующую стадию (C) проводят после стадии (B), после стадии (R) или после стадии (P), и N-замещенной карбаминовой кислоты-O-(R2 или ариловый) эфир, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира сшиты с помощью метиленовой группы (-CH2-), получают из N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира, полученного на стадии (B), стадии (R) или стадии (P):
стадия (C): стадия получения N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира сшиты с помощью метиленовой группы (-CH2-) путем реакции N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира с формальдегидом или сшивающим агентом с метиленовыми группами и сшивающими ароматическими группами, полученными из ароматического органического первичного моноамина, содержавшегося в N-замещенной карбаминовой кислоты-O-(R2 или ариловом) эфире с метиленовой группой (-CH2-) (где N-замещенной карбаминовой кислоты-O-(R2 или ариловый) эфир представляет N-замещенной карбаминовой кислоты-O-R2 эфир или N-замещенной карбаминовой кислоты-O-ариловый эфир):
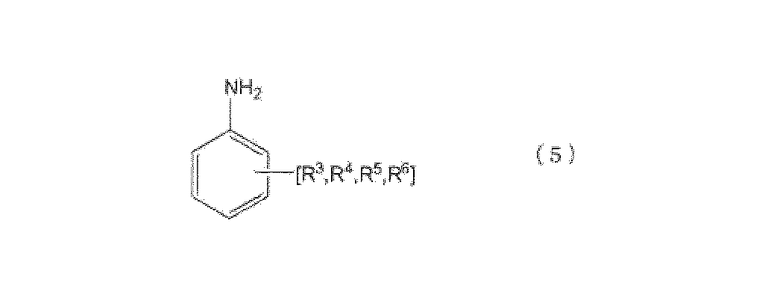
(где
по меньшей мере, одно место в орто-положении и/или пара-положении NH2 группы ароматического органического первичного моноамина, представленного формулой (5), не замещено, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут быть соединены с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из группы, состоящей из групп, в которых группу выбирают из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, соединенную насыщенными алифатическим связями и/или эфирными связями, число углеродных атомов в группах R3-R6 составляет целое число в интервале от 0-7, и суммарное целое число углеродных атомов, которые образуют ароматический органический первичный моноамин, представленный формулой (5), является целым числом от 6 до 13).
[11] Способ получения по приведенному выше пункту [8] или [9], включающий стадию извлечения мочевины путем проведения следующей стадии (D) перед стадией (B) или стадией (P), и/или одновременно со стадией (B) или стадией (P):
стадия (D): стадия извлечения мочевины путем ректификации или сублимации.
[12] Способ получения по приведенному выше пункту [8] или [9], включающий следующую стадию (E) рециркуляции извлеченной мочевины на стадию (A):
стадия (E): стадия рециркуляции мочевины, извлеченной на стадии (D), на стадию (A).
[13] Способ получения по приведенному выше пункту [1], включающий стадию получения изоцианата, представленного следующей формулой (6), который получают из N-замещенной карбаминовой кислоты-O-арилового эфира и ароматической гидроксикомпозиции путем проведения термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира на следующей стадии (F):
стадия (F): стадия получения изоцианата и ароматического гидроксисоединения из N-замещенной карбаминовой кислоты-O-арилового эфира:
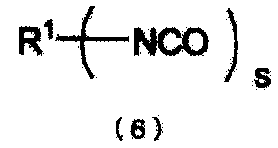
(где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена s NCO групп (группой), и s представляет целое число от 1 до 10).
[14] Способ получения по приведенному выше пункту [8] или [9], включающий стадию отделения ароматической гидроксикомпозиции, полученной на стадии (F), от изоцианата, и рециркуляцию ароматической гидроксикомпозиции на стадию (A) и/или стадию (B), или на стадию (A), и/или стадию (R), и/или стадию (P).
[15] Способ получения по любому одному из пунктов [1], [8] и [9], где ароматическое гидроксисоединение, которое входит в ароматическую гидроксикомпозицию, является по меньшей мере одним типом ароматического гидроксисоединения, представленного следующей формулой (7):
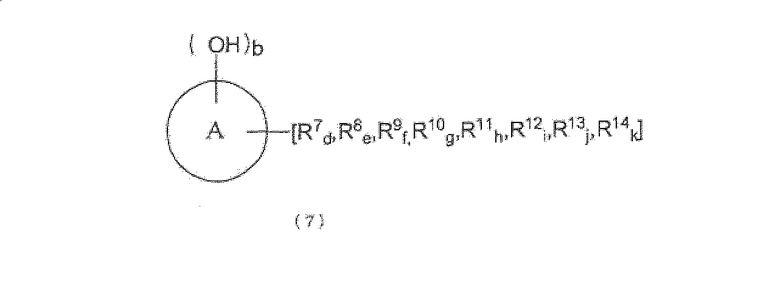
(где
кольцо A представляет ароматическое кольцо, выбранное из бензольного кольца, нафталинового кольца и антраценового кольца, OH группы и группы R7-R14 соответственно представляют группы, замещенные в произвольном месте (местах), которые сохраняют ароматические свойства кольца A, группы R7-R14 могут соответственно и независимо замещать кольцо A, группы R7-R14 могут быть соединены вместе с образованием кольца с ароматическим кольцом путем связывания с кольцом A, группы R7-R14 соответственно и независимо представляют атом водорода, атом галогена или группу, выбранную из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы, арильной группы, имеющей гидроксильную группу, аралкильной группы и эфирной группы (замещенной и/или незамещенной алкиловой эфирной и/или замещенной и/или незамещенной ариловой эфирной и/или замещенной и/или незамещенной аралкиловой группы), и/или группы, к которой один или более типов групп, выбранных из группы, присоединены, и/или группы, к которой один или более типов групп, выбранных из группы, присоединены с помощью насыщенных алифатических связей и/или эфирных связей, и кольцо A и группы R7-R14 состоят суммарно из целого числа углеродных атомов в интервале от 6 до 50,
b представляет целое число от 1 до 6, d, e, f, g, h, i, j и k представляют целые числа от 0 до 5, величина d + e + f + g + h + i + j + k представляет целое число, равное 6-b , в случае когда кольцо A является бензольным кольцом, представляет целое число, равное 8-b , в случае когда кольцо A является нафталиновым кольцом, или представляет целое число, равное 10-b , в случае когда кольцо A является антраценовым кольцом, и группа, выбранная из описанных выше групп R7-R14, может быть циклически связана с кольцом A с помощью связей углерод-углерод и/или эфирных связей).
[16] Композиция для транспортировки и хранения соединения, имеющего уреидную группу, по приведенному выше пункту [7], где ароматическое гидроксисоединение, которое входит в ароматическую гидроксикомпозицию, является по меньшей мере одним типом ароматического гидроксисоединения, представленного следующей формулой (7):

(где
кольцо A представляет ароматическое кольцо, выбранное из бензольного кольца, нафталинового кольца и антраценового кольца, OH группы и группы R7-R14 соответственно представляют группы, замещенные в произвольном месте (местах), которые сохраняют ароматические свойства кольца A, группы R7-R14 могут соответственно и независимо замещать кольцо A, группы R7-R14 могут быть соединены вместе с образованием кольца с ароматическим кольцом путем связывания с кольцом A, группы R7-R14 соответственно и независимо представляют атом водорода, атом галогена или группу, выбранную из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы, арильной группы, имеющей гидроксильную группу, аралкильной группы и эфирной группы (замещенной и/или незамещенной алкиловой эфирной, и/или замещенной и/или незамещенной ариловой эфирной, и/или замещенной и/или незамещенной аралкиловой группы), и/или группы, к которой один или более типов групп, выбранных из группы, присоединены, и/или группы, к которой один или более типов групп, выбранных из группы, присоединены с помощью насыщенных алифатических связей и/или эфирных связей, и кольцо A и группы R7-R14 состоят из целого числа углеродных атомов в интервале от 6 до 50,
b представляет целое число от 1 до 6, d, e, f, g, h, i, j и k представляют целые числа от 0 до 5, величина d + e + f + g + h + i + j + k представляет целое число, равное 6-b , в случае когда кольцо A является бензольным кольцом, представляет целое число, равное 8-b , в случае когда кольцо A является нафталиновым кольцом, или представляет целое число, равное 10-b , в случае когда кольцо A является антраценовым кольцом, и группа, выбранная из описанных выше R7-R14, может быть циклически связана с кольцом A с помощью связей углерод-углерод и/или эфирных связей).
[17] Способ получения по любому одному из пунктов [2], [8] и [9], где ароматическое гидроксисоединение, которое входит в ароматическую гидроксикомпозицию, имеет стандартную температуру кипения, которая отличается на 10°C или более от стандартной температуры кипения изоцианата, имеющего структуру, в которой все аминогруппы органического первичного амина (первичные аминогруппы) превращены в изоцианатные группы.
[18] Способ получения по любому одному из пунктов [1], [8] и [9], где ароматическое гидроксисоединение, содержащееся в ароматической гидроксикомпозиции, является одновалентным и/или двухвалентным ароматическим гидроксисоединением (то есть, ароматическим соединением, в котором b равно 1 и/или 2).
[19] Композиция для транспортировки и хранения соединения, имеющего уреидную группу, по приведенному выше пункту [7], где ароматическое гидроксисоединение, содержащееся в ароматической гидроксикомпозиции, является одновалентным и/или двухвалентным ароматическим гидроксисоединением (то есть, ароматическим соединением, в котором b равно 1 и/или 2).
[20] Способ получения по приведенному выше пункту [18], включающий рециркулирование непрореагировавшего N-замещенной карбаминовой кислоты-O-арилового эфира, который не был термически разложен на стадии (F), на стадию (A), и/или стадию (B), и/или стадию (R), и/или стадию (P), и/или стадию (F).
[21] Способ получения по приведенному выше пункту [8] или [9], дополнительно включающий следующую стадию (G) извлечения аммиака, образующегося в качестве побочного продукта на стадии (A), и/или стадии (B), и/или стадии (R); регенерации мочевины путем реакции аммиака с диоксидом углерода; и рецикла мочевины на стадию (A):
стадия (G): стадия извлечения аммиака, образующегося в качестве побочного продукта, регенерации мочевины путем реакции аммиака с диоксидом углерода и рецикла мочевины на стадию (A).
Положительные эффекты изобретения
Согласно способу получения N-замещенной карбаминовой кислоты-O-арилового эфира настоящего изобретения путем получения N-замещенной карбаминовой кислоты-O-арилового эфира из соединения, имеющего уреидную группу, и ароматической гидроксикомпозиции, при подавлении побочных реакций и эффективном извлечении и повторном использовании мочевины и других подобных веществ, используемых в реакции в избытке, может быть получен N-замещенной карбаминовой кислоты-O-ариловый эфир без каких-либо потерь используемых количеств мочевины и органического первичного амина. Кроме того, так как может быть предотвращено образование продуктов по различным побочным реакциям и продукты различных побочных реакций могут быть растворены с помощью ароматического гидроксисоединения и удалены из системы, возможно осуществление этого способа в течение длительного времени. Кроме того, предпочтительно, чтобы композиция для транспортировки и хранения соединения, имеющего уреидную группу, могла быть использована в качестве сырья для получения N-замещенной карбаминовой кислоты-O-арилового эфира.
Краткое описание чертежей
На фигуре 1 изображена принципиальная схема способа получения соединения, имеющего уреидную группу (группы) в соответствии со стадией (A) варианта настоящего осуществления.
На фигуре 2 изображена принципиальная схема стадии (B) варианта настоящего осуществления.
На фигуре 3 изображена принципиальная схема стадии (R) варианта настоящего осуществления.
На фигуре 4 изображена принципиальная схема стадии (P) варианта настоящего осуществления.
На фигуре 5 изображена принципиальная схема стадии (P) варианта настоящего осуществления.
На фигуре 6 изображена принципиальная схема стадии (P) варианта настоящего осуществления.
На фигуре 7 изображена принципиальная схема способа получения сложного эфира N-замещенной карбаминовой кислоты, в котором используют ароматическую гидроксикомпозицию, включающую активное ароматическое гидроксисоединение и неактивное ароматическое гидроксисоединение варианта настоящего осуществления.
На фигуре 8 изображена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 1) со стадиями (D), (E), (F) и (G).
На фигуре 9 изображена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 2) со стадиями (D), (E), (F) и (G).
На фигуре 10 изображена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 3) со стадиями (D), (E), (F) и (G).
На фигуре 11 изображена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 4) со стадиями (D), (E), (F) и (G).
На фигуре 12 изображена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 5) со стадиями (D), (E), (F) и (G).
На фигуре 13 изображена принципиальная схема производственной установки для получения сложного эфира N-замещенной карбаминовой кислоты в примере варианта настоящего осуществления.
На фигуре 14 изображена принципиальная схема производственной установки для получения сложного эфира N-замещенной карбаминовой кислоты в примере варианта настоящего осуществления.
На фигуре 15 изображена принципиальная схема производственной установки для получения сложного эфира N-замещенной карбаминовой кислоты в примере варианта настоящего осуществления.
На фигуре 16 изображена принципиальная схема производственной установки для проведения реакции переэтерификации в примере варианта настоящего осуществления.
На фигуре 17 изображена принципиальная схема производственной установки для получения изоцианата в примере варианта настоящего осуществления.
На фигуре 18 изображена принципиальная схема производственной установки для получения изоцианата в примере варианта настоящего осуществления.
На фигуре 19 изображена принципиальная схема производственной установки для получения соединения, имеющего уреидные группы, в примере варианта настоящего осуществления.
На фигуре 20 изображена принципиальная схема производственной установки для получения сложного эфира N-замещенной карбаминовой кислоты в сравнительном примере варианта настоящего осуществления.
На фигуре 21 изображена принципиальная схема производственной установки для получения сложного эфира N-замещенной карбаминовой кислоты в примере варианта настоящего осуществления.
На фигуре 22 изображена принципиальная схема производственной установки для получения мочевины в примере варианта настоящего осуществления.
На фигуре 23 приведен 1H-ЯМР спектр композиции для транспортировки и хранения соединения, имеющего уреидные группы, примера 97 варианта настоящего осуществления.
На фигуре 24 приведен 1H-ЯМР спектр композиции для транспортировки и хранения соединения, имеющего уреидные группы, примера 106 варианта настоящего осуществления.
На фигуре 25 приведен 1H-ЯМР спектр композиции для транспортировки и хранения соединения, имеющего уреидные группы, примера 122 варианта настоящего осуществления.
На фигуре 26 приведен 1H-ЯМР спектр композиции для транспортировки и хранения соединения, имеющего уреидные группы, примера 142 варианта настоящего осуществления.
Способ осуществления изобретения
Далее приводится подробное объяснение предпочтительного способа осуществления настоящего изобретения (называемого "вариантом настоящего осуществления"). Кроме того, настоящее изобретение не ограничивается следующим вариантом настоящего осуществления, и более того, оно может быть модифицировано различными путями в объеме его сущности.
Сначала приводится объяснение композиции для транспортировки и хранения соединения, имеющего уреидные группы, в варианте настоящего осуществления. Прежде всего, приводится объяснение соотношений для композиций и подобных соединений, содержащихся в композиции для транспортировки и хранения соединения, имеющего уреидные группы, и затем приводится подробное объяснение соединений, содержащихся в композиции для транспортировки и хранения соединения, имеющего уреидные группы.
Композиция для транспортировки и хранения соединения, имеющего уреидные группы, в варианте настоящего осуществления относится к композиции для транспортировки и хранения соединений, имеющих уреидные группы, в которых число молекул ароматического гидроксисоединения в ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)) относительно числа уреидных групп, содержащихся в соединении, имеющем уреидные группы, представленном следующей формулой (1), в композиции составляет целое число от 1 до 100:

(где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена a раз уреидными группами (уреидной группой), и a представляет целое число от 1 до 10), и
кольцо A представляет органическую группу, которая содержит ароматическую группу, замещенную b гидроксильных групп (гидроксильной группой) в произвольном месте (местах), которая сохраняет ароматические свойства, и которая содержит целое число углеродных атомов в интервале от 6 до 50, может являться одним или множеством гетероциклических колец, и может быть замещена другими заместителями, и b представляет целое число от 1 до 6).
Далее будут последовательно подробно объяснено соединение, имеющее уреидные группы, представленное формулой (1), и ароматическое гидроксисоединение, представленное формулой (2).
Так как соединение, имеющее уреидные группы, используемое в варианте настоящего осуществления, легко образует водородные связи между его молекулами за счет уреидных групп, которые составляют соединение, имеющее уреидные группы, во многих случаях оно имеет высокую температуру плавления. При транспортировке такого соединения, имеющего уреидные группы, транспортировку проводят, например, путем измельчения твердого соединения, имеющего уреидные группы, или формования, например, путем формования в гранулы. В качестве варианта, используют также способы, в которых соединение, имеющее уреидные группы, нагревают до температуры выше его температуры плавления, для того чтобы осуществлять транспортировку соединения, имеющего уреидные группы, в виде жидкости. Однако, в случае транспортировки твердого соединения, имеющего уреидные группы, которое было подвергнуто процессу формования, может происходить забивка трубопровода для транспортировки, так как существует значительный разброс по форме и размерам для частиц соединения, имеющего уреидные группы. Следовательно, во многих случаях требуются сложные установки для стабильной транспортировки фиксированного количества соединения, имеющего уреидные группы, или требуется стадия для усреднения в определенном интервале форм и размеров частиц соединения, имеющего уреидные группы. С другой стороны, в случае нагревания соединения, имеющего уреидные группы, и его транспортировки в виде жидкости, необходимо нагревать соединение, имеющее уреидные группы, до температуры выше, чем его температура плавления (например, 150°C), для того чтобы предотвратить его отверждение в процессе транспортировки. При нахождении соединения, имеющего уреидные группы, при таких высоких температурах, во многих случаях может образовываться изоцианат в нежелательных местах вследствие протекания реакции термического разложения соединения, имеющего уреидные группы, или протекания реакции термического денатурирования соединения, имеющего уреидные группы. Композиция варианта настоящего осуществления обладает способностью сохранять стабильность соединения, имеющего уреидные группы, в результате подавления термического денатурирования соединения, имеющего уреидные группы, в композиции при транспортировке или хранении композиции. Механизм, в результате которого проявляется эффект подавления термического денатурирования соединения, имеющего уреидные группы, не ясен, но авторы настоящего изобретения предположили, что ароматическое гидроксисоединение, которое составляет композицию, создает такие условия, при которых затрудняется образование уретановых связей вследствие образования водородных связей между уреидными связями (-NHCONH2) соединения, имеющего уреидные группы, и слабокислым ароматическим гидроксисоединением, в результате чего затруднено протекание реакции, которая приводит к образованию соединений, имеющих уреиленовые (-NHCONH-) группы.
Кроме того, при объяснении варианта настоящего осуществления уреиленовые группы (-NHCONH-) могут называть уреиновыми группами.
Предпочтительно, чтобы композицию для транспортировки и хранения можно было использовать, в частности, для получения N-замещенной карбаминовой кислоты-O-арилового эфира (в силу того, что в следующих объяснениях часто используют термин «N-замещенной карбаминовой кислоты-O-ариловый эфир», то термин «N-замещенной карбаминовой кислоты-O-ариловый эфир» относится к сложному эфиру N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с ароматическим кольцом, при этом ароматическое кольцо относится к ароматическому кольцу, в котором группа связана с ароматической группой, при этом указанную группу выбирают из группы, состоящей из ароматических групп и/или алифатических групп, и при этом ароматическое кольцо образуют путем связывания целого числа указанных групп, по меньшей мере, 0, с ароматической группой, что более подробно будет описано далее). Более конкретно, способ включает транспортировку композиции для транспортировки и хранения на стадию синтеза N-замещенной карбаминовой кислоты-O-арилового эфира, применяя соединение, имеющее уреидные группы, содержащееся в композиции, для реакции этерификации, и извлекая образующийся N-замещенной карбаминовой кислоты-O-ариловый эфир. Обычно, стадию синтеза N-замещенной карбаминовой кислоты-O-арилового эфира проводят при высокой температуре, и если соединения, имеющие уреидные группы, подают в состоянии наличия водородных связей между его молекулами, то для соединений, имеющих термически стабильные уреиленовые группы, реакция денатурирования является термодинамически благоприятной. Соединение, имеющее уреиленовые группы, является конденсированной формой соединения, имеющего уреидные группы, и является высокомолекулярным соединением. Таким образом, во многих случаях возникают проблемы образования полимеров, которые слипаются или отверждаются в реакторе. Кроме того, во многих случаях соединение, имеющее уреидные группы, включает такие соединения, как аммиак или мочевина. Эти соединения, и особенно мочевина, часто термически разлагаются до изоциановой кислоты и аммиака в интервале температур стадии синтеза N-замещенной карбаминовой кислоты-O-арилового эфира, и при взаимодействии изоциановой кислоты с соединением, имеющим уреидные группы, происходит денатурирование до соединений, имеющих биуретные связи. Соединения, имеющие биуретные связи, имеют высокую температуру термического разложения, и вследствие их реакции с ароматическми гидроксисоединениями возникают сложности при образовании N-замещенной карбаминовой кислоты-O-арилового эфира. Однако авторы настоящего изобретения обнаружили, что денатурирование соединений, имеющих уреидные группы, при транспортировке и хранении композиции для транспортировки и хранения подавляется даже в том случае, если композиция для транспортировки и хранения содержит конкретные количества этого аммиака и мочевины. Данный эффект особенно заметен в процессе длительного хранения, и во многих случаях денатурирование не происходило даже во время проведения ускоренных испытаний. Этот вывод до этого был неизвестен и является неожиданным. Механизм, на основании которого проявляется этот эффект, не ясен, но авторы настоящего изобретения предположили, что в процессе транспортировки и хранения композиции ароматическое гидроксисоединение подавляет денатурирование соединений аммиака и мочевины или других подобных соединений и соединений, имеющих уреидные группы, в результате улавливания присутствующих в следовых количествах воды и кислорода, и затем при получении N-замещенной карбаминовой кислоты-O-арилового эфира с использованием этой композиции, ароматическое гидроксисоединение действует также как катализатор этерификации N-замещенной карбаминовой кислоты-O-арилового эфира.
В композиции для транспортировки и хранения отношение числа молекул ( y ) ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию, к числу уреидных групп ( x ), которые составляют соединение (или которые содержатся в соединении), имеющее уреидные группы, находится в интервале от 1 до 100. Предпочтительно, чтобы y являлся избытком по отношению к x в случае описанного выше предполагаемого механизма, но с другой стороны, принимая во внимание эффективность транспортировки соединения, имеющего уреидные группы, и размер емкости для хранения, предпочтительно, чтобы отношение y к x находилось в интервале больше, чем 2, но меньше, чем 50, и более предпочтительно, в интервале больше, чем 3, но меньше, чем 20.
Предпочтительно, чтобы в композиции для транспортировки и хранения соединение, имеющее уреидные группы, содержащееся в композиции, являлось соединением, имеющим уреидные группы, которое получают реакцией органического первичного амина, мочевины и/или производной угольной кислоты (которые будут далее подробно объяснены), и/или изоциановой кислоты, и/или не-N-замещенной карбаминовой кислоты. С точки зрения доступности для промышленности, более предпочтительно, чтобы соединением, имеющим уреидные группы, являлось соединение, имеющее уреидные группы, которое получают реакцией органического первичного амина и мочевины.
Композиция для транспортировки и хранения может также содержать компоненты, не являющиеся соединением, имеющим уреидные группы, и ароматическим гидроксисоединением. Примеры таких компонентов могут включать упомянутые выше аммиак, мочевину, производную угольной кислоты (производная угольной кислоты, указанная в варианте настоящего осуществления, будет подробно объяснена далее), не-N-замещенную карбаминовую кислоту, соединение, имеющее биуретную связь, соединение, имеющее уреиленовую группу, воду, спирт, инертный газ (такой как газообразный азот, газообразный диоксид углерода, газообразный аргон или газообразный аммиак) и N-замещенной карбаминовой кислоты-O-эфир, такой как N-замещенной карбаминовой кислоты-O-(алкиловый или ариловый)эфир, полученный в результате реакции композиции для транспортировки и хранения с ароматической гидроксикомпозицией (которая будет подробно объяснена далее). Несмотря на то, что нет конкретных ограничений на содержащиеся количества этих компонентов, но если очевидно, что происходят ненужные побочные реакции, вызываемые температурой хранения и другими подобными факторами, предпочтительно, чтобы их количества корректировали, исходя из обстоятельств. Компонентами, особенно заслуживающими внимания являются кислород, аммиак, вода, окислители и восстановители. Во многих случаях композиция для транспортировки и хранения включает соединения, содержащие атомы азота, или ароматическая гидроксикомпозиция может быть денатурирована в результате окисления кислородом, что приводит к проявлению такого явления как окрашивание. Кроме того, так как композиция практически во всех случаях является легковоспламеняющейся композицией, следует регулировать содержание газообразного кислорода с использованием известных методов, которые обычно используют в этой области техники при хранении органических химических веществ. Например, концентрацию кислорода в газовой фазе в емкости для хранения регулируют путем продувки азотом, так чтобы концентрация кислорода составляла 10% или менее, предпочтительно, 1% или менее, и более предпочтительно, 100 ppm (м.д.) или менее. В случае пропускания инертного газа, такого как азот, через газовую фазу, концентрацию кислорода во вводимом газе регулируют до 10 ppm или менее. Концентрацию растворенного в композиции аммиака поддерживают до 1% по массе или менее и, предпочтительно, до 0,1% по массе или менее. Методом регулирования может являться известный метод, такой как продувка жидкой фазы инертным газом, таким как газообразный азот. Так как в ряде случаев большие количества воды могут приводить к образованию негомогенной композиции, концентрация воды в композиции составляет 10% по массе или менее, и, предпочтительно, 1% по массе или менее, при этом она зависит от компонентов композиции, и в случае использования композиции в качестве сырья для получения N-замещенной карбаминовой кислоты-O-арилового эфира, более предпочтительно, чтобы концентрация воды составляла 100 ppm или менее, так как большое количество присутствующей воды может вызывать протекание побочных реакций, вызываемых водой. Концентрация воды может регулироваться известным методом, таким как использование обезвоживающего вещества или осушителя, отгонка при пониженном давлении, повышенном давлении или нормальном давлении, или продувка жидкой фазы инертным газом для удаления воды вместе с инертным газом. Так как присутствие окислителя или восстановителя может вызывать денатурирование ароматического гидроксисоединения, содержание этих веществ регулируют с использованием известного метода контроля ароматических гидроксисоединений. Окислители относятся к кислотам Брэнстеда, таким как органические кислоты или неорганические кислоты и кислоты Льюиса, в то время как восстановители относятся к основаниям Брэнстеда, таким как органические основания или неорганические основания, основания Льюиса и газообразный водород. К восстановителям не относятся соединения, получаемые из композиции, такие как упомянутые выше аммиак, мочевина, производная угольной кислоты, или соединения, которые составляют композицию (например, N-замещенной карбаминовой кислоты-O-эфиры, такие как N-замещенной карбаминовой кислоты-O-ариловый эфир, N-замещенной карбаминовой кислоты-O-алкиловый эфир или N-замещенной карбаминовой кислоты-O-R2 эфир (N-замещенной карбаминовой кислоты-O-R2 эфир далее будет описан подробно)). Несмотря на то, что нет конкретных ограничений на содержание N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира (N-замещенной карбаминовой кислоты-O-R2 эфир далее будет описан подробно), полученного в способе получения N-замещенной карбаминовой кислоты-O-арилового эфира из композиции для транспортировки и хранения и ароматической гидроксикомпозиции (будет описана подробно далее), так как есть случаи, в которых соединение, имеющее уреидные группы, и N-замещенной карбаминовой кислоты-O-(R2 или ариловый)эфир реагируют в процессе хранения, что приводит к образованию деалкоголизированного или деароматического гидроксилированного соединения, которое конденсируется в результате образования уреиленовых связей, то его количество относительно соединения, имеющего уреидные группы, содержащегося в композиции для транспортировки и хранения, регулируют до 10 мольных эквивалентов или менее и, предпочтительно, до 1 мольного эквивалента или менее. Примеры других возможных содержащихся компонентов могут включать мочевину и спирт. Нет конкретных ограничения для содержания ни для одного из этих компонентов. Композиция для транспортировки и хранения может находиться в форме суспензии или в форме твердого вещества. Предпочтительно, чтобы она находилась в форме суспензии, и более предпочтительно, в форме жидкости. Так как мочевина имеет тенденцию легко затвердевать, для сохранения текучести ее содержание регулируют до 20 мольных эквивалентов или менее, и, предпочтительно, до 10 мольных эквивалентов или менее относительно соединения, имеющего уреидные группы, содержащегося в композиции для транспортировки и хранения. Несмотря на то, что нет также ограничений для спирта, его содержание могут регулировать в связи с необходимостью отгонки спирта после транспортировки. Например, регулируют количество спирта до 100 мольных эквивалентов или менее и, предпочтительно, до 10 мольных эквивалентов или менее относительно соединения, имеющего уреидные группы, содержащегося в композиции для транспортировки и хранения.
В настоящем описании часто используют термин «N-замещенной карбаминовой кислоты-O-(R2 или ариловый) эфир», и он относится к N-замещенной карбаминовой кислоты-O-R2 эфиру или N-замещенной карбаминовой кислоты-O-ариловому эфиру.
Нет конкретных ограничений на условия хранения и транспортировки композиции, но существуют условия, при которых исключительно легко при высоких температурах протекает реакция термического разложения соединения, имеющего уреидные группы. В зависимости от периода хранения, который может изменяться, хранение проводят в интервале температур от -40 до 280°C, и в случаях, при которых наблюдается отрицательное влияние процесса хранения на текучесть и стабильность композиции, предпочтительно, от 0 до 260°C, и более предпочтительно, от 40 до 260°C. Температура хранения может регулироваться на основе таких факторов, как применение композиции, период хранения композиции и легкость обращения с композицией. Несмотря на то, что транспортировку проводят также при температуре, которая соответствует температурному интервалу хранения, тем не менее, при использовании композиции в качестве сырья для получения N-замещенной карбаминовой кислоты-O-арилового эфира и при транспортировке на стадию синтеза N-замещенной карбаминовой кислоты-O-арилового эфира транспортировка может проводиться только после подтверждения того, что она может быть проведена безопасно в соответствии с условиями реакционной стадии и оборудованием, используемым на реакционной стадии, так как транспортировку в реактор на стадию синтеза обычно проводят после подогрева до температуры реакции. Обычно транспортировку проводят в интервале температур от -40 до 280°C, и в случаях, при которых наблюдается отрицательное влияние на текучесть и стабильность композиции, предпочтительно, от 0 до 260°C, и более предпочтительно, от 40 до 260°C. Транспортировка может подвергаться регулированию в зависимости от применения композиции, времени транспортировки композиции и легкости обращения с композицией, как это уже было описано ранее. Нет конкретных ограничений для давления в процессе транспортировки, и хранение может проводиться при условиях от пониженного давления до повышенного давления. При хранении в условиях пониженного давления, так как ароматическая гидроксикомпозиция может подвергаться ректификации, регулируют отношение соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции в композиции так, чтобы оно находилось в описанном выше интервале. Нет конкретных ограничений для емкостей хранения, технологических линий и другого подобного оборудования в процессе хранения и транспортировки. Емкость выбирают в соответствии с надлежащими нормами работы, принимая во внимание правила обращения с легковоспламеняющимся органическим веществом, учитывая при этом температуру вспышки композиции, с которой проводят работу. Нет также конкретных ограничений для материала, из которого изготовлено технологическое оборудование, и может быть использован один из известных материалов. Примеры материалов могут включать стекло, нержавеющую сталь, углеродистую сталь, сплав Хастелой, эмалированные материалы и материалы с нанесенным покрытием из тефлона (торговая марка). В связи с этим, в случае необходимости, в качестве оборудования для хранения и транспортировки композиции может быть предусмотрено известное оборудование, такое как насосы, оборудование для регулирования температуры или измерительные приборы.
Для составления описанной ранее композиции указанная выше композиция для транспортировки и хранения соединения, имеющего уреидные группы, может быть получена путем смешения описанных выше соединения, имеющего уреидные группы, ароматической гидроксикомпозиции, аммиака, N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира, мочевины, спирта, производной угольной кислоты и других компонентов, или для составления описанной ранее композиции она может быть получена на основе композиции, содержащей соединение, имеющее уреидные группы, полученное при получении соединения, имеющего уреидные группы, путем добавления и/или удаления ароматической гидроксикомпозиции, мочевины, спирта, аммиака или производной угольной кислоты и других подобных компонентов. Предпочтительно, чтобы способ получения соединения, имеющего уреидные группы, мог быть проведен описанным далее образом.
Далее приводится объяснение способа получения N-замещенной карбаминовой кислоты-O-арилового эфира варианта настоящего осуществления. Вариант настоящего осуществления относится к способу получения по меньшей мере одного N-замещенной карбаминовой кислоты-O-арилового эфира (где N-замещенной карбаминовой кислоты-O-ариловый эфир относится к сложному эфиру N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с ароматическим кольцом), получаемого из соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, а именно, из соединения, имеющего уреидные группы, представленные формулой (1), и ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2), который включает стадию проведения реакции этерификации или реакции этерификации и реакции переэтерификации. (Упомянутые выше формулы (1) и (2) будут подробно объяснены далее).
А именно, способом получения варианта настоящего осуществления является способ получения N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого из соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, из соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции (обозначающей группу ароматических гидроксисоединений, включающих по меньшей мере один тип ароматического гидроксисоединения) (и далее описанный подробно способ получения N-замещенной карбаминовой кислоты-O-арилового эфира и побочного продукта аммиака путем взаимодействия соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, так же, как и способ получения N-замещенной карбаминовой кислоты-O-R2 эфира и побочного продукта спирта (R2OH) путем получения N-замещенной карбаминовой кислоты-O-R2 эфира и побочного продукта аммиака путем этерификации соединения, имеющего уреидные группы, и спирта (несмотря на то, что далее объясняемый спирт относится к спирту, представленному R2OH в следующей формуле (4)) с последующей переэтерификацией N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции, также являются вариантами настоящего осуществления). А именно, способом получения варианта настоящего осуществления является способ получения N-замещенной карбаминовой кислоты-O-арилового эфира на стадии, включающей реакцию этерификации соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции. Более конкретно, способом получения варианта настоящего осуществления является способ получения N-замещенной карбаминовой кислоты-O-арилового эфира на стадии, включающей реакцию этерификации, или реакцию этерификации и реакцию переэтерификации. Реакция этерификации относится к реакции, в которой уреидные группы (-NHCONH2) в соединении, имеющем уреидные группы, превращаются в группы карбаминовой кислоты, и в качестве побочного продукта образуется аммиак. Более конкретно, эта реакция этерификации включает реакцию, в которой уреидные группы (-NHCONH2) превращаются в группы карбаминовой кислоты-O-арилового эфира (-NHCOOAr), получаемые из уреидных групп соединения, имеющего уреидные группы, и ароматического гидроксисоединения, при этом образуется аммиак в качестве побочного продукта реакции, или реакцию, в которой уреидные группы (-NHCONH2) превращаются в группы карбаминовой кислоты-O-R2 эфира (-NHCOOR2), получаемые из уреидных групп в соединении, имеющем уреидные группы, и спирта (R2OH), при этом образуется аммиак в качестве побочного продукта реакции. Ar, указанный для упомянутых выше групп карбаминовой кислоты-O-арилового эфира, относится к остатку, в котором один атом водорода гидроксильной группы, непосредственно связанной с ароматическим углеводородным кольцом, был удален из ароматического гидроксисоединения. Для более подробного объяснения реакции этерификации, реакция этерификации относится к реакции, в которой N-замещенной карбаминовой кислоты-O-ариловый эфир, представленный формулой (43), получают из соединения, имеющего уреидные группы, представленного формулой (1), которое будет далее указано, и ароматического гидроксисоединения, представленного формулой (2), при этом образуется аммиак в качестве побочного продукта реакции, и реакции, в которой N-замещенной карбаминовой кислоты-O-R2 эфир, представленный формулой (49), получают из соединения, имеющего уреидные группы, представленного формулой (1), и спирта, представленного формулой (4), при этом образуется аммиак в качестве побочного продукта реакции. Кроме того, упомянутая выше реакция переэтерификации конкретно относится к реакции, в которой N-замещенной карбаминовой кислоты-O-R2 эфир, представленный формулой (49), и ароматическое гидроксисоединение реагируют с превращением групп карбаминовой кислоты-O-эфира (-NHCOOR2) в N-замещенной карбаминовой кислоты-O-R2 эфире в группы карбаминовой кислоты-O-арилового эфира (-NHCOOAr), при этом в качестве побочного продукта реакции образуется спирт (R2OH). Ar определяется так же, как он уже был определен выше. (Это тоже будет далее описано подробно).
А именно, вариант настоящего осуществления включает случай получения N-замещенной карбаминовой кислоты-O-арилового эфира путем непосредственного проведения реакции этерификации соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения), и случай получения N-замещенной карбаминовой кислоты-O-арилового эфира путем проведения реакции этерификации соединения, имеющего уреидные группы, и спирта, и затем проведения реакции переэтерификации ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения).
Кроме того, несмотря на то, что способом получения соединения, имеющего уреидные группы, может являться известный способ, и оно может быть получено, например, путем реакции органического первичного амина, мочевины и/или производной угольной кислоты (которые будут далее описаны подробно), и/или изоциановой кислоты, и/или не-N-замещенной карбаминовой кислоты, тем не менее, предпочтительно получать по меньшей мере один тип соединения, имеющего уреидные группы, получаемого из органического первичного амина и мочевины, с помощью способа получения, в котором реагируют органический первичный амин и мочевина по реакции образования уреидов.
Далее приводится объяснение соединений, используемых в способе получения варианта настоящего осуществления, и соединений, которые составляют композицию для транспортировки и хранения соединений, имеющих уреидные группы.
<Органический первичный амин>
Органическим первичным амином, используемым в варианте настоящего осуществления (где органический первичный амин относится к "первичному амину" (первичным моноаминам и первичным полиаминам), определенным в правиле C-8 номенклатуры (номенклатуры Международного союза теоретической и прикладной химии (IUPAC) по органической химии), принятой Международным союзом теоретической и прикладной химии (IUPAC), является органический первичный амин, представленный следующей формулой (3). Это правило основано на рекомендациях по органической и биохимической номенклатуре. В дальнейшем, в случае ссылки на правила IUPAC в настоящем описании, а также в дальнейшем на указанные правила номенклатуры, определенные IUPAC (за исключением случаев, в которых специально цитируют рекомендации IUPAC других лет), такие рекомендации цитируются по изданию "Yukikagaku•Seikagaku Meimeihou" (Номенклатура по органической химии и биохимии) (2-ая измененная редакция, изданная в Японии в 1992 году фирмой Nankodo Co., Ltd.), которое основано на издании, содержащим все правила органической химии и биохимии, наряду с правилами транслитерации на японском языке, опубликованное в качестве приложения к "Chemical Fields" в 1980 году на основе рекомендаций 1979 года, так же, как и на всех последующих изменениях и рекомендациях. Термин "органические" относится в целом к группе соединений, рассматриваемых в качестве объекта для номенклатуры, раскрытой в приведенных выше публикациях. Объектами могут являться объекты, описанные в рекомендациях, опубликованных в 1993 году. Объектами могут являться объекты, описанные в рекомендациях, опубликованных в 1993 году (в случае, когда трудно найти упомянутые выше публикации, опубликованные в Японии, могут быть ссылки на рекомендации 1979 года и рекомендации 1993 года). Однако, "органические" соединения, охватываемые описанной выше номенклатурой, включают металлорганические соединения и комплексы металлов. В настоящем изобретении, несмотря на то, что далее приводится объяснение терминов "органический" и/или "органические группы" и/или "заместители" и других подобных терминов, так же, как и соединений, используемых в варианте настоящего осуществления, тем не менее, когда это специально не объяснено, они состоят из атомов, которые не включают атомы металлов и/или полуметаллов. Более предпочтительно, чтобы в варианте настоящего осуществления использовали "органические соединения", "органические группы" и "заместители", состоящие из атомов, выбранных из H (атомов водорода), C (атомов углерода), N (атомов азота), O (атомов кислорода), S (атомов серы), Cl (атомов хлора), Br (атомов брома) и I (атомов йода).
Кроме того, в идущих далее объяснениях часто используют в качестве признака для ограничения термины "алифатический" и "ароматический". Согласно упомянутым выше правилам IUPAC, органические соединения описывают как подразделяемые на алифатические и ароматические. Алифатические соединения имеют отношение к определению групп в соответствии с алифатическими соединениями на основе рекомендаций IUPAC 1995 года. Алифатические соединения определяют в этих рекомендациях как "ациклические или циклические насыщенные или ненасыщенные соединения углерода, исключая ароматические соединения". Алифатические группы, которые часто используют в настоящем описании, относятся к группам, состоящим из алифатических соединений. Эти группы являются такими, что фрагмент R, в котором атом водорода был удален из алифатического соединения в форме RH, например, определяют в качестве одновалентной алифатической группы. Кроме того, алифатические соединения и алифатические группы, используемые при объяснении настоящего изобретения, включают насыщенные и ненасыщенные, также как линейные и циклические алифатические соединения, и относятся к "органическим соединениям", "органическим группам" и "заместителям", состоящим из атомов, выбранных из упомянутых выше H (атомов водорода); C (атомов углерода); N (атомов азота); O (атомов кислорода); S (атомов серы); Si (атомов кремния); и атомов галогена, выбранных из Cl (атомов хлора), Br (атомов брома) и I (атомов йода). Кроме того, в случае ароматической группы, такой как аралкильная, группа связана с алифатической группой, такие группы часто обозначают как "алифатическая группа, замещенная с помощью ароматической группы" или "группа, состоящая из алифатической группы, соединенной с ароматической группой". Это связано с реакционной способностью в варианте настоящего осуществления, и с тем, что свойства, относящиеся к реакциям групп, подобным аралкильным группам, в точности похожи на реакционную способность алифатических групп, а не ароматических групп. Кроме того, неароматические реакционноспособные группы, включающие такие группы, как аралкильные группы и алкильные группы, часто обозначают как "алифатические группы, необязательно замещенные с помощью ароматической группы", "алифатическая группа, замещенная с помощью ароматической группы" или "алифатическая группа, связанная с ароматической группой" и другими подобными вариантами. Кроме того, несмотря на то, что описанные выше определения в соответствии с правилами номенклатуры, определенными IUPAC, используют при объяснении общих формул соединений, используемых в настоящем описании, тем не менее, также используют такие термины, как "органический первичный амин" или "N-замещенной карбаминовой кислоты-O-ариловый эфир", также часто используют тривиальные названия для наименования конкретных групп и наименования примеров соединений.
Кроме того, несмотря на то, что в настоящем описании часто описывают число молекул, число заместителей и самостоятельные числа, тем не менее, они все представляют ноль или положительное целое число (и также часто имеются случаи, в которых ноль рассматривается как положительное целое число).
Первичный амин относится к соединению, имеющему аминогруппу (-NH2), с которой являются связанными алифатическое соединение, и/или ароматическое соединение, и/или алифатическая группа и ароматическая группа. А именно, органический первичный амин, согласно изложенному в настоящей заявке, обозначает "первичный амин", который классифицируют как описанный выше "органический".
Предпочтительно, чтобы органический первичный амин, используемый в варианте настоящего осуществления, являлся органическим первичным амином, представленным следующей формулой (3):
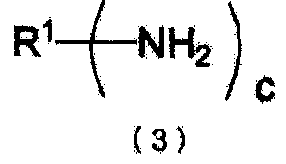
(где
R1 представляет органическую группу, которая содержит углеродные атомы в интервале от 1 до 85 и которая замещена c раз NH2 группами, и c представляет целое число от 1 до 10).
В приведенной выше формуле (3) R1 является органической группой, классифицированной как описанная выше "органическая", и органический первичный амин в варианте настоящего осуществления относится к органическому первичному амину, в котором число c групп NH2 связаны с органической группой, содержащей углеродные атомы в интервале от 1 до 85.
R1 представляет алифатическую группу, ароматическую группу или группу, связанную с алифатической группой и ароматической группой, и представляет группу, состоящую из ациклической углеводородной группы или циклической углеводородной группы (такой как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа, циклическая углеводородная группа, имеющая боковую цепь, гетероциклическая группа, гетероциклическая спирогруппа, гетеросшитая кольцевая группа или соединение кольцевой группы), группу, связанную с одним или более типов групп, выбранных из упомянутых выше ациклических углеводородных групп и циклических углеводородных групп, и группы, в которых упомянутые выше группы связаны с помощью ковалентной связи с конкретным атомом неметалла (углеродом, кислородом, азотом, серой или кремнием). Кроме того, ковалентная связь с конкретным описанным выше атомом неметалла (углеродом, кислородом, азотом, серой или кремнием) находится в состоянии, при котором упомянутые выше группы связаны с помощью ковалентной связи, например, с группами, представленными следующими формулами (8)-(16).
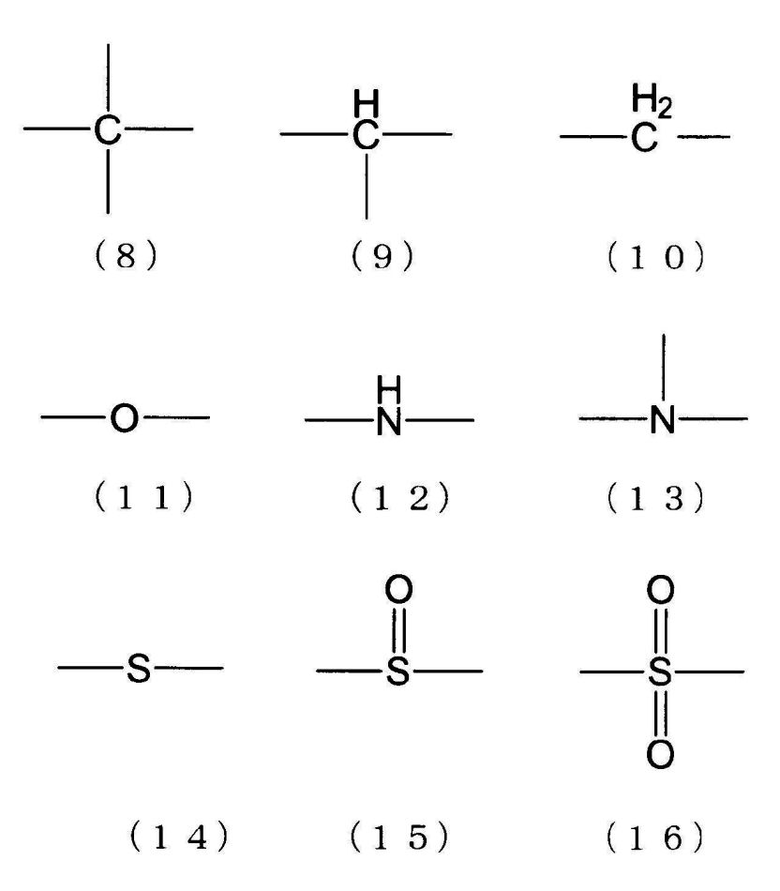
Среди этих групп R1 группы R1, которые могут быть предпочтительно использованы в варианте настоящего осуществления с точки зрения их меньшей склонности к протеканию побочных реакций, включают группы, выбранные из группы, состоящей из ациклических углеводородных групп и циклических углеводородных групп, выбранных из алифатических групп, ароматических групп и групп, связанных с алифатическими группами и ароматическими группами (таких как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа или циклическая углеводородная группа, имеющая боковую цепь), и групп, связанных по меньшей мере с одним типом групп, выбранных из этой группы (взаимно замещенные группы), имеющие углеродные атомы в интервале от 1 до 85 . Принимая во внимание текучесть и другие подобные параметры, предпочтительно, чтобы число углеродных атомов в группах находилось в интервале от 1 до 70, и более предпочтительно, в интервале от 1 до 13.
Предпочтительные примеры органических аминов, образуемых группой R1, могут включать
1) необязательно алифатически и/или ароматически замещенные ароматические органические первичные моноамины, в которых группа R1 имеет от 6 до 85 углеродных атомов и включает один или более типов ароматического кольца, необязательно замещенного с помощью алифатической группы и/или ароматической группы, ароматическая группа в группе R1 замещена с помощью группы NH2, и c равняется 1,
2) ароматические органические первичные полиамины, в которых группа R1 имеет от 6 до 85 углеродных атомов и включает один или более типов ароматического кольца, необязательно замещенного с помощью алифатической группы и/или ароматической группы, ароматическая группа в группе R1 замещена с помощью группы NH2, и c равняется 2 или более, и
3) алифатические органические первичные полиамины, в которых группой R1 является алифатическая группа, имеющая от 1 до 85 углеродных атомов, необязательно замещенная с помощью ароматической группы, и c равняется 2 или 3. В приведенных выше описаниях атомы, связанные с группой NH2 (и предпочтительно углеродные атомы), которые содержатся в ароматическом кольце, обозначаются в качестве ароматических органических аминов, в то время как случаи связывания с атомами не в ароматическом кольце (главным образом углерод) обозначаются в качестве алифатических органических аминов. Более предпочтительными алифатическими группами являются линейные углеводородные группы, циклические углеводородные группы и по меньшей мере один тип группы, выбранный из линейных углеводородных групп и циклических углеводородных групп (относящихся, например, к циклическим углеводородным группам, замещенным с помощью линейной углеводородной группы, или линейным углеводородным группам, замещенным с помощью циклической углеводородной группы), имеющих от 6 до 70 углеродных атомов.
Далее приводится перечень конкретных примеров предпочтительных органических первичных аминов.
1) Ароматические органические первичные моноамины
Необязательно алифатически и/или ароматически замещенные ароматические органические первичные моноамины, в которых группа R1 является группой, имеющей от 6 до 85 углеродных атомов, и включает один или более типов ароматического кольца, необязательно замещенного с помощью алифатической группы и/или ароматической группы, ароматическая группа в группе R1 замещена с помощью группы NH2 и c равняется 1, предпочтительно, ароматические органические первичные моноамины, в которых группа R1 является группой, имеющей от 6 до 70 углеродных атомов, и c равняется 1, и более предпочтительно, принимая во внимание текучесть и другие подобные параметры, ароматические органические первичные моноамины, в которых группа R1 имеет от 6 до 13 углеродных атомов и c равняется 1, которые являются ароматическими органическими первичными моноаминами, представленными следующей формулой (5).
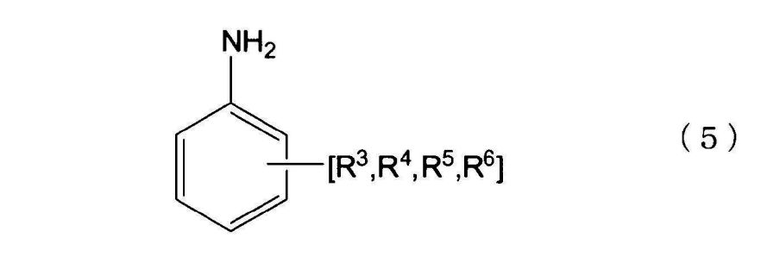
(где
по меньшей мере одно место в орто-положении и/или пара-положении NH2 группы в ароматическом органическом первичном моноамине, представленном формулой (5), не замещено, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца,
группы R3-R6 могут соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут быть соединены вместе с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, образуемыми из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью насыщенных алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 составляет целое число в интервале от 0 до 7, и суммарное число углеродных атомов, которые образуют ароматический органический первичный моноамин, представленный формулой (5), составляет целое число от 6 до 13).
Предпочтительные примеры ароматических органических первичных моноаминов, представленных формулой (5), могут включать примеры, в которых группы R3-R6 являются атомами водорода или группами, выбранными из алкильных групп, таких как метильная группа или этильная группа, и примеры таких ароматических органических первичных моноаминов могут включать анилин, аминотолуол (включая изомеры), диметиланилин (включая изомеры), диэтиланилин (включая изомеры), дипропиланилин (включая изомеры), аминонафталин (включая изомеры), аминометилнафталин (включая изомеры), диметилнафтиламин (включая изомеры) и триметилнафтиламин (включая изомеры), при этом использование анилина является более предпочтительным.
2) Ароматические органические первичные полиамины
Ароматические органические первичные полиамины, в которых группа R1 является группой, имеющей от 6 до 85 углеродных атомов и содержащей одно или более ароматических колец, необязательно замещенных с помощью алифатической группы и/или ароматической группы, ароматическая группа в группе R1 замещена с помощью группы NH2 и c равняется 2 или более, предпочтительными являются ароматические органические первичные полиамины, в которых группа R1 является группой, имеющей от 6 до 70 углеродных атомов, и c равняется 2 или более, и более предпочтительно, принимая во внимание текучесть и другие подобные параметры, ароматические органические первичные полиамины, в которых группа R1 содержит одно или более ароматических колец, ароматическим кольцом являются группы с количеством углеродных атомов от 6 до 13, которые могут быть дополнительно замещены с помощью алкильной группы, арильной группы или аралкильной группы, группа NH2 связана с ароматической группой, содержащейся в группе R1, и c равняется 2 или более. Примеры таких ароматических органических полиаминов могут включать диаминобензол (включая изомеры), диаминотолуол (включая изомеры), метилендианилин (включая изомеры), диаминомезитилен (включая изомеры), диаминобифенил (включая изомеры), диаминодибензил (включая изомеры), бис(аминофенил)метан (включая изомеры), бис(аминофенил)пропан (включая изомеры), бис(аминофениловый)эфир (включая изомеры), бис(аминофеноксиэтан) (включая изомеры), α,α'-диаминоксилол (включая изомеры), диаминоанизол (включая изомеры), диаминофенетол (включая изомеры), диаминонафталин (включая изомеры), диаминометилбензол (включая изомеры), диаминометилпиридин (включая изомеры), диаминометилнафталин (включая изомеры) и полиметиленполифенилполиамины, представленные следующей формулой (17).
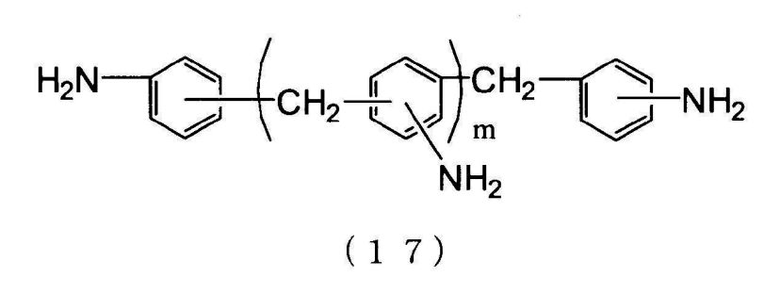
(где
m является целым числом от 0 до 6).
3) Алифатические органические первичные полиамины
Алифатические органические первичные полиамины, в которых группа R1 органического амина, представленного формулой (3), является алифатической группой, в которой число углеродных атомов является целым числом в интервале от 1 до 85 и которая может быть замещена с помощью ароматической группы, и c равняется 2 или 3.
Более предпочтительными органическими аминами являются алифатические органические первичные амины, в которых алифатическая группа является линейной углеводородной группой, циклической углеводородной группой или группой, к которой присоединен по меньшей мере один тип группы, выбранной из линейных углеводородных групп и циклических углеводородных групп (таких как циклическая углеводородная группа, замещенная с помощью линейной углеводородной группы, или линейная углеводородная группа, замещенная с помощью циклической углеводородной группы). Более предпочтительно, чтобы органическим амином являлся алифатический органический первичный полиамин, в котором группа R1 является алифатической группой, которая является ациклической углеводородной группой, циклической углеводородной группой или группой, с которой связан по меньшей мере один тип группы, выбранный из ациклических углеводородных групп и циклических углеводородных групп (таких как циклическая углеводородная группа, замещенная с помощью ациклической углеводородной группы, или ациклическая углеводородная группа, замещенная с помощью циклической углеводородной группы), имеющий от 1 до 70 углеродных атомов, и c равняется 2 или 3. Принимая во внимание текучесть и другие подобные параметры в процессе крупнотоннажного промышленного производства, более предпочтительным органическим амином является алифатический органический первичный полиамин, в котором группа R1 является ациклической углеводородной группой, циклической углеводородной группой или группой, с которой связан по меньшей мере один тип группы, выбранной из ациклических углеводородных групп и циклических углеводородных групп (таких как циклическая углеводородная группа, замещенная с помощью ациклической углеводородной группы, или ациклическая углеводородная группа, замещенная с помощью циклической углеводородной группы), имеющей от 6 до 13 углеродных атомов и состоящей из углеродных атомов и атомов водорода. А именно, это относится к случаю, в котором группа R1 является линейной и/или разветвленной алкильной группой, циклоалкильной группой или группой, состоящей из алкильных групп и циклоалкильных групп. Примеры этих органических аминов могут включать алифатические первичные диамины, такие как этилендиамин, диаминопропан (включая изомеры), диаминобутан (включая изомеры), диаминопентан (включая изомеры), диаминогексан (включая изомеры) или диаминодекан (включая изомеры); алифатические триамины, такие как триаминогексан (включая изомеры), триаминононан (включая изомеры) или триаминодекан (включая изомеры); и замещенные циклические алифатические полиамины, такие как диаминоциклобутан (включая изомеры), диаминоциклогексан (включая изомеры), 3-аминометил-3,5,5-триметилциклогексиламин (цис и/или транс-формы) или метиленбис(циклогексиламин) (включая изомеры). Их примеры могут включать первичные алкилдиамины, такие как этилендиамин, диаминопропан (включая изомеры), диаминобутан (включая изомеры), диаминопентан (включая изомеры), диаминогексан (включая изомеры), диаминогептан (включая изомеры), диаминооктан (включая изомеры), диаминононан (включая изомеры) или диаминодекан (включая изомеры); первичные алкилтриамины, такие как триаминогексан (включая изомеры), триаминогептан (включая изомеры), триаминооктан (включая изомеры), триаминононан (включая изомеры) или триаминодекан (включая изомеры); первичные циклоалкиламины, такие как диаминоциклобутан (включая изомеры), диаминоциклопентан (включая изомеры) или диаминоциклогексан (включая изомеры); и первичные циклогексилполиамины, замещенные с помощью алкильной группы, такие как 3-аминометил-3,5,5-триметилциклогексиламин (цис и/или транс-форма) или метиленбис(циклогексиламин) (включая изомеры).
Предпочтительно использовать органические первичные амины, описанные выше в пунктах 1), 2) и 3), и в частности более предпочтительно, чтобы органическим первичным амином являлся органический первичный моноамин, органический первичный диамин или органический первичный триамин (в котором c в приведенной выше формуле (3) является целым числом 1, 2 или 3).
<Соединение, имеющее уреидные группы>
Соединение, имеющее уреидные группы, используемое при получении N-замещенной карбаминовой кислоты-O-арилового эфира из композиции для транспортировки и хранения соединения, имеющего уреидные группы, варианта настоящего осуществления, и/или ароматической гидроксикомпозиции, является соединением, представленным следующей формулой (1):
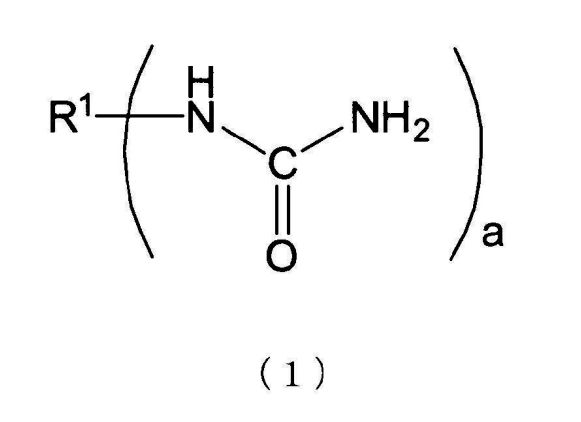
(где
R1 представляет органическую группу, которая содержит целое число углеродных атомов в интервале от 1 до 85 и которая замещена a раз уреидными группами, и a представляет целое число от 1 до 10).
Соединение, имеющее уреидные группы, представленное выше формулой (1), является соединением, имеющим "уреидные группы", определенное в правиле номенклатуры C-971, принятом IUPAC. В формуле (1) выше R1 является органической группой, классифицируемой как описанная выше “органическая”, и соединение, имеющее уреидные группы, согласно варианту настоящего осуществления является соединением, имеющим уреидные группы, связанным с числом a уреидных групп (-NH-CONH2), включающим углеродные атомы в интервале от 1 до 85. R1 представляет алифатическую группу, ароматическую группу или группу, связанную с алифатической группой и ароматической группой, и представляет группу, состоящую из ациклической углеводородной группы или циклической углеводородной группы (такой как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа, циклическая углеводородная группа, имеющая боковую цепь, гетероциклическая группа, гетероциклическая спирогруппа, гетеро-сшитая кольцевая группа или гетероциклическая группа), группы, связанной с одним или более типов групп, выбранных из упомянутых выше ациклических углеводородных групп и циклических углеводородных групп, и групп, в которых упомянутые выше группы связаны через ковалентную связь с конкретным атомом неметалла (углеродом, кислородом, азотом, серой или кремнием). Кроме того, описанная выше ковалентная связь с конкретным атомом неметалла (углеродом, кислородом, азотом, серой или кремнием) находится в состоянии, при котором упомянутые выше группы связаны ковалентной связью, например, с группами, представленными следующими формулами (8)-(16).
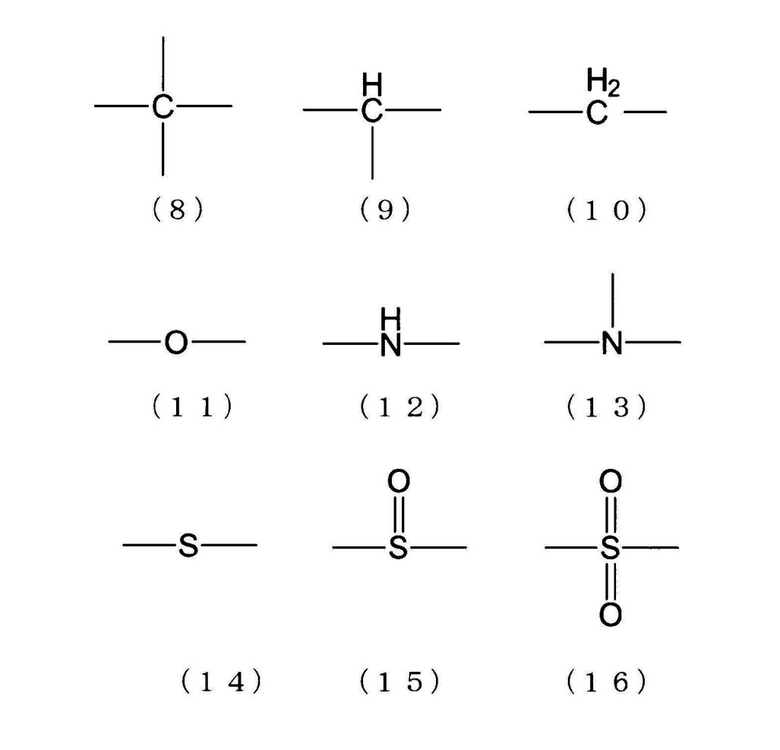
Среди этих групп R1 группы R1, которые могут быть предпочтительно использованы в варианте настоящего осуществления, принимая во внимание меньшую склонность к протеканию побочных реакций, включают группы, выбранные из группы, состоящей из ациклических углеводородных групп и циклических углеводородных групп, выбранных из алифатических групп и ароматических групп (таких как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа или циклическая углеводородная группа, имеющая боковую цепь), и группы, связанные по меньшей мере с одним типом группы, выбранным из этой группы (взаимно замещенные группы), содержащие от 1 до 85 углеродных атомов. Принимая во внимание текучесть и другие подобные параметры композиции для транспортировки и хранения, предпочтительно, чтобы число углеродных атомов составляло от 1 до 70, и более предпочтительно, от 1 до 13.
Предпочтительные примеры соединений, имеющих уреидную группу, образованных группой R1, могут включать 1) N-замещенные ароматические органические мономочевины, в которых группа R1 имеет от 6 до 85 углеродных атомов и содержит один или более типов ароматического кольца, необязательно замещенного с помощью алифатической группы и/или ароматической группы, ароматическая группа в группе R1 замещена с помощью уреидной группы, и c равно 1, 2) N-замещенные ароматические органические полимочевины, в которых группа R1 имеет от 6 до 85 углеродных атомов и содержит один или более типов ароматического кольца, необязательно замещенного с помощью алифатической группы и/или ароматической группы, ароматическая группа в группе R1 замещена с помощью уреидной группы, и c равняется 2 или более, и 3) N-замещенные алифатические органические полимочевины, в которых группа R1 является алифатической группой, имеющей от 1 до 85 углеродных атомов, необязательно замещенных с помощью ароматической группы, и c равно 2 или 3. В приведенных выше описаниях соединения, в которых атомы, связанные с уреидной группой (главным образом, углеродные атомы), которые содержатся в ароматическом кольце, обозначаются как N-замещенные ароматические органические мочевины, в то время как в случаях связывания с атомами не в ароматическом кольце (главным образом, углеродными атомами) обозначаются как N-замещенные алифатические органические мочевины. Более предпочтительно, чтобы алифатическая группа являлась линейной углеводородной группой, циклической углеводородной группой и по меньшей мере одним типом группы, связанной с группой, выбранной из линейных углеводородных групп и циклических углеводородных групп (относящихся, например, к циклическим углеводородным группам, замещенным с помощью линейной углеводородной группы, или линейным углеводородным группам, замещенным с помощью циклической углеводородной группы), имеющей от 6 до 70 углеродных атомов.
Несмотря на то, что способ получения соединения, имеющего уреидные группы, может являться известным способом и может быть осуществлен, например, в результате реакции органического первичного амина, мочевины, и/или производной угольной кислоты (будет далее описана подробно), и/или изоциановой кислоты, и/или не-N-замещенной карбаминовой кислоты, тем не менее по меньшей мере один тип соединения, имеющего уреидные группы, полученный из органического первичного амина и мочевины, предпочтительно получать путем способа получения, в котором реагирует органический первичный амин и мочевина в реакции образования уреидов, и в варианте настоящего осуществления, соединение, имеющее уреидные группы, предпочтительно использует соединение, имеющее уреидные группы, полученное в способе, который включает следующую стадию A:
стадия (A): стадия получения по меньшей мере одного типа соединения, имеющего уреидные группы, полученного из органического первичного амина, представленного следующей формулой (3), и мочевины, путем проведения реакции образования уреидов из органического первичного амина и мочевины в жидкой фазе и удаления или извлечения в газовую фазу аммиака, образовавшегося в качестве побочного продукта в реакции образования уреидов:
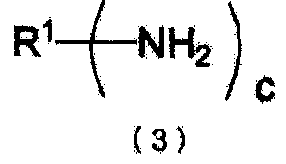
(где
R1 представляет органическую группу, которая содержит целое число углеродных атомов в интервале от 1 до 85 и которая замещена c раз группами NH2, и c представляет целое число от 1 до 10).
Соединение, имеющее уреидные группы, полученное на приведенной выше стадии (A), является соединением, имеющим уреидные группы, которое имеет органическую группу, полученную из упомянутого выше органического первичного амина. А именно, эта стадия включает реакцию органических первичных аминогрупп (-NH2) органического первичного амина с мочевиной с образованием уреидных групп (в варианте настоящего осуществления эту реакцию часто называют реакцией образования уреидных групп). Группы (-CONH2) внутри уреидных групп (-NHCONH2) образуются из мочевины, участвующей в реакции. Кроме того, обозначенное в формуле (1) a является целым числом, равным или меньшим чем c, обозначенное в формуле (3), и, предпочтительно, чтобы a являлось таким целым числом, чтобы a = c .
Часто применяемый в настоящем описании термин "получаемый" подразумевает приобретение группы, принадлежащей исходному сырью, в процессе обмена функциональной группы исходного соединения сырья в реакции. Например, в описанной выше реакции, в которой соединение, имеющее уреидные группы, получают из органического первичного амина, соединение, имеющее уреидные группы, имеет структуру, которая приобрела органические первичные аминогруппы (-NH2) органического первичного амина, в то время как группы (-CONH2) внутри уреидных групп относятся к группам (-CONH2), содержащимся в реагирующей мочевине (NH2CONH2). Таким образом, в упомянутых выше формулах (1) и (3), a является целым числом, равным или меньшим, чем c , и, предпочтительно, чтобы a и c были одинаковыми целыми числами.
Далее приводятся конкретные примеры предпочтительных соединений, имеющих уреидные группы. Уреидная группа является одним и тем же заместителем, и в настоящем описании ее описывают в названии соединения как "N-замещенная (название заместителя) мочевина". Для того чтобы однозначно указать, что атом азота (N) мочевины замещен (то есть, что атом азота не относится к группе -NH2), его однозначно обозначают как "N-замещенный", заместитель однозначно обозначают как ароматическую группу или алифатическую группу, и термин "органический" также специально однозначно используют в том смысле, что соединение является органическим соединением. Соединение называют "мономочевиной" в случае наличия одной уреидной группы в ее молекулы, или называют "полимочевиной" в случае наличия множества уреидных групп в ее молекуле. Так как соединение является N-замещенной мочевиной, даже в случаях наличия в нем множества уреидных групп, уреидные группы, содержащиеся в соединении, имеющем уреидные группы, которое объясняется ниже, для того, чтобы их было легче различать, обозначают путем применения префикса "поли", "ди" или "три" и других подобных префиксов непосредственно перед обозначенным выше термином "мочевина".
На протяжении всего описания настоящей заявки наименования "моно""замещенный" не используют, а в качестве названий примеров конкретных соединений приводят наименования в соответствии с номенклатурой IUPAC или тривиальные названия.
1) N-замещенная ароматическая органическая мономочевина
N-замещенная ароматическая органическая мономочевина относится к мочевине, в которой группа R1 имеет от 6 до 85 углеродных атомов и содержит один или более типов ароматического кольца, необязательно замещенного с помощью алифатической группы и/или ароматической группы, ароматическая группа в группе R1 замещена с помощью уреидной группы, и c равно 1, и, предпочтительно, чтобы она относилась к ароматической органической мономочевине, в которой группа R1 является группой, имеющей от 6 до 70 углеродных атомов, и c равняется 1, и, принимая во внимание текучесть и другие подобные параметры, более предпочтительно, чтобы она относилась к N-замещенной ароматической органической мономочевине, в которой группа R1 является группой, имеющей от 6 до 13 углеродных атомов, и c равно 1, и она является N-замещенной ароматической органической мономочевиной, представленной следующей формулой (41):
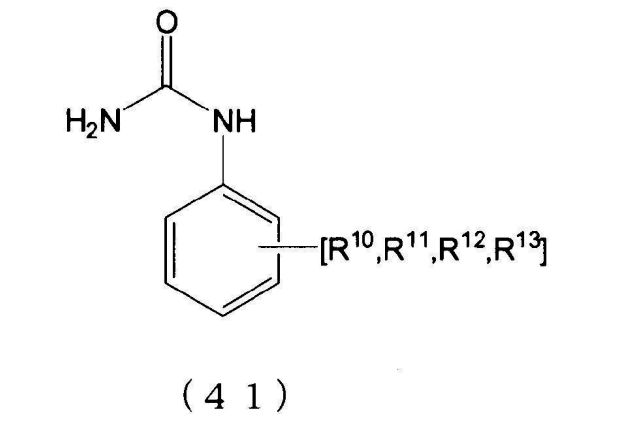
(где
по меньшей мере одно место в орто-положении и/или пара-положении уреидной группы N-замещенной ароматической органической мономочевины, представленной формулой (41), не замещено, группы R10-R13 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R10-R13 могут соответственно и независимо замещать ароматическое кольцо, или группы R10-R13 могут быть вместе связаны с образованием кольца с ароматическим кольцом, группы R10-R13 являются атомами водорода или группами, выбранными из групп, состоящих из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью насыщенных алифатических связей и/или эфирных связей, число углеродных атомов является целым числом в интервале от 0 до 7, и суммарное число углеродных атомов, которые образуют N-замещенную ароматическую органическую мономочевину, представленную формулой (41), исключая уреидные группы (-NH-CO-NH2), составляет целое число от 6 до 13).
Предпочтительные примеры таких N-замещенных ароматических органических мономочевин, представленных формулой (41), могут включать примеры, в которых группы R10-R13 являются атомами водорода или группами, выбранными из алкильных групп, таких как метильная группа или этильная группа, и примеры таких N-замещенных ароматических органических мономочевин могут включать N-фенилмочевину, N-толилмочевину (включая изомеры), N-диметилфенилмочевину (включая изомеры), N-диэтилфенилмочевину (включая изомеры), N-дипропилфенилмочевину (включая изомеры), N-нафталинилмочевину (включая изомеры), N-метилнафталинилмочевину (включая изомеры), N-диметилнафталинилмочевину (включая изомеры) и N-триметилнафталинилмочевину (включая изомеры). В частности, более предпочтительно использовать N-фенилмочевину.
2) N-замещенная ароматическая органическая полимочевина
N-замещенная ароматическая органическая полимочевина относится к соединению, в котором группа R1 является группой, имеющей от 6 до 85 углеродных атомов, которая содержит одно или более ароматических колец, необязательно замещенных с помощью алифатической группы и/или ароматической группы, ароматическая группа в группе R1 замещена с помощью уреидной группы, и c равняется 2 или более, предпочтительной является N-замещенная ароматическая органическая полимочевина, в которой группа R1 является группой, имеющей от 6 до 70 углеродных атомов, и c равняется 2 или более, и более предпочтительной, принимая во внимание текучесть и другие подобные параметры, является N-замещенная ароматическая органическая полимочевина, в которой группа R1 содержит один или более типов ароматических колец, ароматическое кольцо имеет от 6 до 13 углеродных атомов и может быть дополнительно замещено с помощью алкильной группы, арильной группы или аралкильной группы, уреидная группа связана с ароматической группой, содержащейся в группе R1, и c равняется 2 или более. Примеры таких N-замещенных ароматических органических полимочевин могут включать N,N'-фенилендимочевину (включая изомеры), N,N'-метилфенилендимочевину (включая изомеры), N,N'-мезитилендифенилендимочевину (включая изомеры), N,N'-мезитилендимочевину (включая изомеры), N,N'-бифенилендимочевину (включая изомеры), N,N'-дибензилдимочевину (включая изомеры), N,N'-пропандиилфенилендимочевину (включая изомеры), N,N'-оксидифенилендимочевину (включая изомеры), N,N'-дифенилдиилдипропандиилдимочевину (включая изомеры), N,N'-фенилендиметилендимочевину (включая изомеры), N,N'-метоксифенилендимочевину (включая изомеры), N,N'-этоксифенилендимочевину (включая изомеры), N,N'-нафталиндиилмочевину (включая изомеры), N,N'-пиридиндиилдиметилендимочевину (включая изомеры), N,N'-нафталиндиилдиметилендимочевину (включая изомеры), и полиметиленполифениленполиамины, представленные следующей формулой (42).
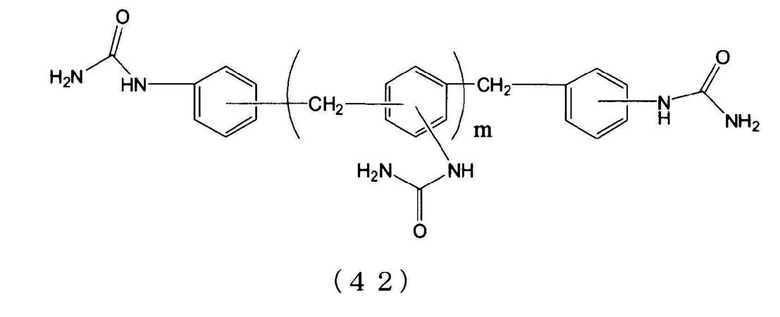
(где
m является целым числом от 0 до 6).
3) N-замещенная алифатическая органическая полимочевина
N-замещенная алифатическая органическая полимочевина является соединением, в котором группа R1 является алифатической группой, имеющей от 1 до 85 углеродных атомов, которая необязательно замещена ароматической группой, и c равно 2 или 3. Предпочтительными N-замещенными алифатическими органическими полимочевинами являются N-замещенные алифатические органические полимочевины, в которых алифатическая группа является линейной углеводородной группой, циклической углеводородной группой (включая ароматические группы) или группой, с которой связан, по меньшей мере, один тип группы, выбранной из линейных углеводородных групп и циклических углеводородных групп (таких как циклическая углеводородная группа, замещенная с помощью линейной углеводородной группы, или линейная углеводородная группа, замещенная с помощью циклической углеводородной группы). Более предпочтительно, чтобы N-замещенная алифатическая органическая полимочевина являлась N-замещенной алифатической органической полимочевиной, в которой группа R1 является алифатической группой, которая является ациклической углеводородной группой, циклической углеводородной группой или группой, которая связана по меньшей мере с одним типом группы, выбранной из ациклических углеводородных групп и циклических углеводородных групп (таких как циклическая углеводородная группа, замещенная с помощью ациклической углеводородной группы, или ациклическая углеводородная группа, замещенная с помощью циклической углеводородной группы), имеющей от 1 до 70 углеродных атомов, и c равняется 2 или 3. Принимая во внимание текучесть и другие подобные параметры в процессе крупнотоннажного промышленного производства, более предпочтительно, чтобы N-замещенная алифатическая органическая полимочевина являлась N-замещенной алифатической органической полимочевиной, в которой группа R1 является ациклической углеводородной группой, циклической углеводородной группой или группой, с которой связан по меньшей мере один тип группы, выбранной из ациклических углеводородных групп и циклических углеводородных групп (таких как циклическая углеводородная группа, замещенная с помощью ациклической углеводородной группы, или ациклическая углеводородная группа, замещенная с помощью циклической углеводородной группы), имеющей от 6 до 13 углеродных атомов, которая образована из углеродных атомов и атомов водорода. А именно, это относится к случаю, в котором группа R1 является линейной или разветвленной алкильной группой, циклоалкильной группой или группой, состоящей из алкильных групп и циклоалкильных групп. Их примеры могут включать N-замещенные алифатические органические полимочевины, такие как метилендимочевина, 1,2-диметилендимочевина, 1,3-триметилендимочевина, 1,4-тетраметилендимочевина, 1,5-пентаметилендимочевина, 1,6-гексаметилендимочевина, 1,8-октаметилендимочевина, циклопентандимочевина (включая изомеры), циклогександимочевина (включая изомеры), циклогептандимочевина (включая изомеры), циклооктандимочевина (включая изомеры), метилциклопентандимочевина (включая изомеры), этилциклопентандимочевина (включая изомеры), метилциклогександимочевина (включая изомеры), этилциклогександимочевина (включая изомеры), пропилциклогександимочевина (включая изомеры), бутилциклогександимочевина (включая изомеры), пентилциклогександимочевина (включая изомеры), гексилциклогександимочевина (включая изомеры), диметилциклогександимочевина (включая изомеры), диэтилциклогександимочевина (включая изомеры), дибутилциклогександимочевина (включая изомеры), 1,5,5-триметилциклогександимочевина (включая изомеры), 1,5,5-триэтилциклогександимочевина (включая изомеры), 1,5,5-трибутилциклогександимочевина (включая изомеры) или 3-уреидометил-3,5,5-триметилциклогексилмочевина.
Далее приводится объяснение спирта, используемого в варианте настоящего осуществления.
<Спирт>
Стадия (A), которая будет описана подробно позже, может быть проведена в присутствии воды, и/или спирта, и/или ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения) в дополнение к органическому первичному амину и мочевине.
В случае проведения стадии (A) в присутствии ароматической гидроксикомпозиции предпочтительно проводить стадию (A) в присутствии упомянутой выше ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)).
Кроме того, одним аспектом варианта настоящего осуществления является способ получения N-замещенной карбаминовой кислоты-O-арилового эфира, который включает стадию (A), следующую за ней стадию (R) и затем стадию (P), путем проведения стадии (R) (стадии реакции этерификации) с получением N-замещенной карбаминовой кислоты-O-R2 эфира (подробности которой будут описаны далее) и затем проведения стадии (P) (стадии реакции переэтерификации) с получением N-замещенной карбаминовой кислоты-O-арилового эфира, после того как проведена стадия (A). В качестве спирта, используемого в данном случае, также используют спирт, представленный следующей формулой (4). Ароматическая гидроксикомпозиция, используемая на следующей стадии (P) (композиция, содержащая по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)), будет подробно описана далее:
стадия (R): стадия получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции по меньшей мере одного типа соединения, имеющего уреидные группы, и спирта, представленного следующей формулой (4), в жидкой фазе и извлечения аммиака, образовавшегося в качестве побочного продукта в газовую фазу (где N-замещенной карбаминовой кислоты-O-R2 эфир представляет сложный эфир N-замещенной карбаминовой кислоты, в которой атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с группой R2, полученной из спирта), и
стадия (P): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции (содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)) в жидкой фазе и извлечения спирта, образовавшегося в качестве побочного продукта в газовую фазу:
Спирт, представленный следующей формулой (4), предпочтительно использовать в качестве спирта, используемого в варианте настоящего осуществления.
R 2 OH (4)
(где
R2 представляет группу, состоящую из алифатической группы или алифатической группы, с которой связана ароматическая группа, которая содержит целое число углеродных атомов в интервале от 1 до 14, и группа OH спирта, представленного формулой (4), является группой OH, которая не связана с ароматическим кольцом).
Предпочтительным спиртом, представленным формулой (4), является спирт, в котором группой R2 является группа, состоящая из алифатической группы или алифатической группой, с которой связана ароматическая группа и в которой группа OH спирта, представленного формулой (4), является группой OH, которая не связана с ароматическим кольцом. Группа R2 представляет группу, состоящую из ациклической углеводородной группы или циклической углеводородной группы (такой как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа, циклическая углеводородная группа, имеющая боковую цепь, гетероциклическая группа, гетероциклическая спирогруппа, гетеро-сшитая кольцевая группа или гетероциклическая группа), группу, связанную с одним или более типов групп, выбранных из упомянутых выше ациклических углеводородных групп и циклических углеводородных групп, и группу, в которой упомянутые выше группы связаны через ковалентную связь с конкретным атомом неметалла (углеродом, кислородом, азотом, серой или кремнием). Кроме того, ковалентная связь с конкретным описанным выше атомом неметалла (углеродом, кислородом, азотом, серой или кремнием) находится в состоянии, при котором упомянутые выше группы связаны ковалентной связью, например, с группами, представленными следующими формулами (8)-(16).
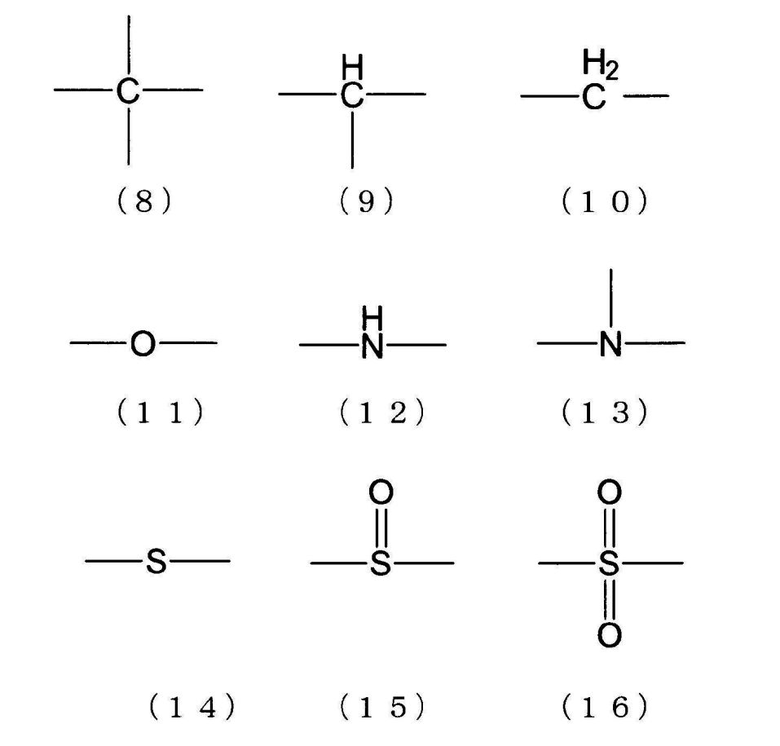
Среди этих групп R2 группы R2, которые могут быть предпочтительно использованы в варианте настоящего осуществления, принимая во внимание меньшую склонность к протеканию побочных реакций, содержат группы, выбранные из группы, состоящей из ациклических углеводородных групп и циклических углеводородных групп, выбранных из алифатических групп и/или алифатических групп, с которыми связаны ароматические группы (такие как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа или циклическая углеводородная группа, имеющая боковую цепь), группы, связанные по меньшей мере с одним типом группы, выбранной из этой группы (взаимно замещенные группы), и группы, в которых упомянутые выше группы замещены с помощью ароматической группы, и которые содержат число углеродных атомов в интервале от 1 до 14. На стадии (P) варианта настоящего осуществления N-замещенной карбаминовой кислоты-O-R2 эфир предпочтительно переэтерифицируют с помощью ароматической гидроксикомпозиции, и побочный продукт спирт удаляют из системы. Таким образом, предпочтительно, чтобы спирт, используемый на стадии (A) и/или стадии (R), имел температуру кипения, которая ниже температуры кипения ароматического гидроксисоединения, содержащегося в ароматической гидроксикомпозиции, и, более предпочтительно, чтобы группой R2 являлась группа, содержащая число углеродных атомов в интервале от 1 до 10. Более предпочтительно, чтобы группа R2 содержала число углеродных атомов в интервале от 1 до 8. Еще более предпочтительно, чтобы R2 являлась алкильной группой, группой, в которой связаны циклоалкильная группа и алкильная группа, или аралкильной группой. Предпочтительный примеры таких спиртов могут включать метанол, этанол, пропанол (включая изомеры), бутанол (включая изомеры), пентанол (включая изомеры), гексанол (включая изомеры), гептанол (включая изомеры), октанол (включая изомеры), бензиловый спирт, толилметанол (включая изомеры), ксилилметанол (включая изомеры) и фенилэтиловый спирт (включая изомеры). Еще более предпочтительные примеры спиртов могут включать приведенные выше спирты, в которых R2 является алкильной группой, и среди углеродных атомов, которые составляют алкильную группу, углеродный атом в α положении гидроксильной группы (углеродный атом, который составляет алкильную группу, с которым связана OH) является вторичным углеродным атомом (-CH2-).
Далее приводится объяснение ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)), используемой в варианте настоящего осуществления.
<Ароматическая гидроксикомпозиция>
В варианте настоящего осуществления присутствуют различные способы и стадии, в которых используется ароматическая гидроксикомпозиция. Ароматическую гидроксикомпозицию используют в качестве соединения, которое составляет композицию для транспортировки и хранения описанного выше соединения, имеющего уреидные группы. Кроме того, стадию (A) предпочтительно проводить в присутствии ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)). Кроме того, ароматическую гидроксикомпозицию (композицию, содержащую по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)), используют на стадии (P), описанной выше при объяснении спирта. Кроме того, примером другого аспекта варианта настоящего осуществления является способ получения N-замещенной карбаминовой кислоты-O-арилового эфира путем способа, который включает стадию (A) (стадию реакции образования уреидов), и следующую за ней стадию (B) (стадию реакции этерификации), и на стадии (B) также используют ароматическую гидроксикомпозицию (композицию, содержащую по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)):
стадия (B): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции по меньшей мере одного типа соединения, имеющего уреидные группы, с ароматической гидроксикомпозицией (композицией, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)), в жидкой фазе и извлечения аммиака, образующегося в качестве побочного продукта, в газообразную фазу.
Даже в случаях, когда ароматическую гидроксикомпозицию (композицию, содержащую по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)) используют, помимо указанных выше стадий, ароматическая гидроксикомпозиция, используемая в варианте настоящего осуществления, является ароматической гидроксикомпозицией, которая содержит по меньшей мере один тип описанного выше ароматического гидроксисоединения, представленного формулой (2).
Ароматическая гидроксикомпозиция в варианте настоящего осуществления относится к композиции, которая содержит один тип ароматического гидроксисоединения или множество типов ароматических гидроксисоединений. Далее приводится объяснение ароматических гидроксисоединений, предпочтительно используемых в качестве ароматических гидроксисоединений, которые составляют ароматическую гидроксикомпозицию.
Ароматические гидроксисоединения, которые составляют ароматическую гидроксикомпозицию (или которые содержатся в ароматической гидроксикомпозиции), являются по меньшей мере одним типом ароматического гидроксисоединения, представленного следующей формулой (2):
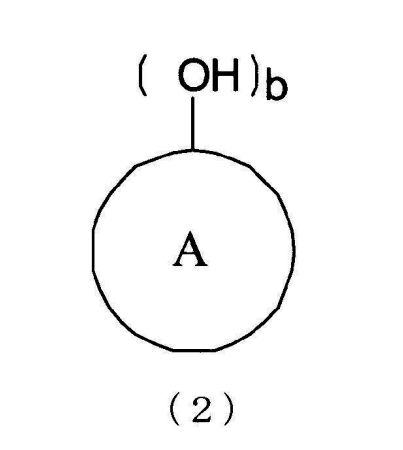
(где
кольцо A представляет органическую группу, которая содержит от 6 до 50 углеродных атомов и которая содержит ароматическую группу, замещенную b раз гидроксильными группами в произвольном положении, которая сохраняет ароматические свойства, и может являться одним кольцом или множеством колец, может являться гетероциклическим кольцом или может быть замещено другими заместителями, и b является целым числом от 1 до 6).
Примеры заместителей, которые замещают ароматическую группу ароматического гидроксисоединения, представленного формулой (2) выше, могут включать группы, выбранные из атома водорода, атома галогена, алифатических групп и ароматических групп, и групп, в которых упомянутые выше группы связаны, которые состоят из ациклических углеводородных групп или циклических углеводородных групп (таких как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа, циклическая углеводородная группа, имеющая боковую цепь, гетероциклическая группа, гетероциклическая спирогруппа, гетеро-сшитая кольцевая группа или гетероциклическая группа), групп, связанных с одним или более типов групп, выбранных из ациклических углеводородных групп и циклических углеводородных групп, и групп, в которых упомянутые выше группы связаны через ковалентную связь с конкретным атомом неметалла (атомом углерода, кислорода, азота, серы или кремния). Кроме того, ковалентная связь с описанным выше конкретным атомом неметалла (атомом углерода, кислорода, азота, серы или кремния) относится к состоянию, в котором, например, группа, представленная следующими формулами (8)-(11) и формулами (13)-(16), и упомянутые выше группы связаны с помощью ковалентной связи.
Кольцо A имеет структуру, которая содержит по меньшей мере одну структуру, выбранную из группы, состоящей из бензольного кольца, нафталинового кольца и антраценового кольца, предпочтительно, чтобы кольцо A имело структуру, которая содержит по меньшей мере одну структуру, выбранную из группы, состоящей из бензольного кольца, нафталинового кольца, антраценового кольца, и более предпочтительно, чтобы кольцо A имело структуру, которая содержит только одно бензольное кольцо.
Гидроксильные группы, связанные с ароматической группой кольца A, являются гидроксильными группами, которые связаны с атомом углерода ароматической группы кольца A, и, предпочтительно, чтобы число гидроксильных групп составляло целое число от 1 до 6, более предпочтительно, целое число от 1 до 3, еще более предпочтительно, целое число от 1 до 2, и еще более предпочтительно, 1 (а именно, b =1).
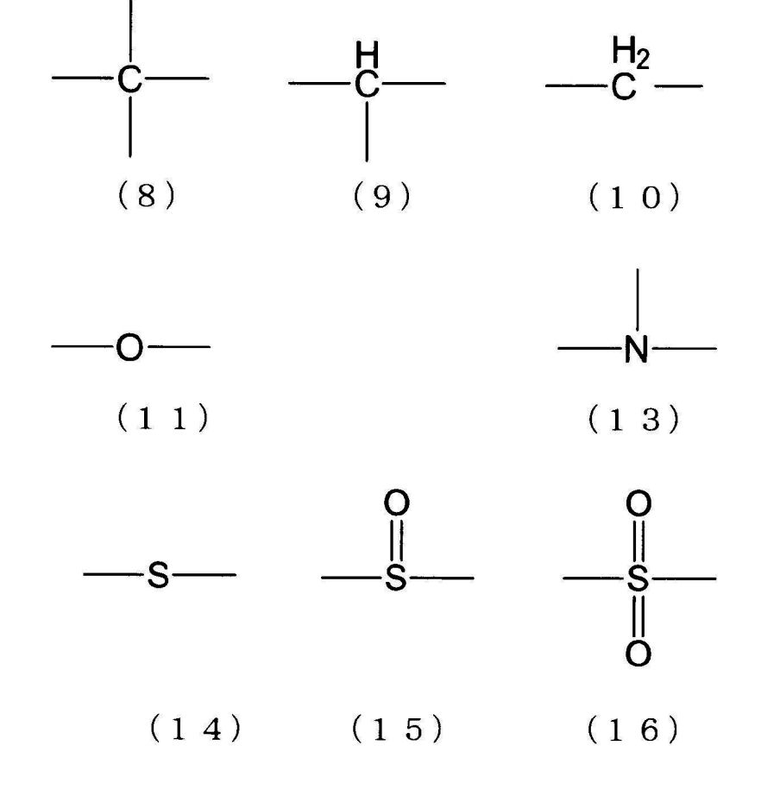
Среди таких заместителей заместители, которые могут быть предпочтительно использованы в варианте настоящего осуществления, принимая во внимание меньшую склонность к протеканию побочных реакций, содержат группы, выбранные из группы, состоящей из ациклических углеводородных групп и циклических углеводородных групп (таких как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа или циклическая углеводородная группа, имеющая боковую цепь), и групп, связанных по меньшей мере с одним типом группы, выбранной из этой группы (взаимно замещенные группы группы).
Кроме того, в случае транспортировки при высокой температуре композиции для транспортировки и хранения соединения, имеющего уреидные группы, или в случае реакции при высокой температуре соединения, имеющего уреидные группы, и/или N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции с получением N-замещенной карбаминовой кислоты-O-арилового эфира, предпочтительно, чтобы кольцо A ароматического гидроксисоединения являлось ароматическим гидроксисоединением, состоящим из группы, имеющей по меньшей мере один неактивный заместитель (включая атомы водорода), помимо ароматической группы и гидроксильных групп, связанных с ароматической группой (здесь, неактивный заместитель относится, например, к заместителю, который не имеет активного водорода, при котором величина pKa соединения, в котором неактивный заместитель связан с фенильной группой, составляет 30 или меньше, несмотря на то, что он может иметь ароматическую гидроксильную группу).
Если более подробно давать объяснения для заместителя, то ароматическое гидроксисоединение, представленное формулой (2), является ароматическим гидроксисоединением, имеющим помимо ароматической группы и гидроксильной группы, связанной с ароматической группой по меньшей мере один заместитель, выбранный из групп заместителей, указанных ниже:
(i) атом водорода,
(ii) группа, состоящая из углеродных атомов и атомов водорода (которые могут также образовывать кольцевую структуру путем связывания с кольцом A),
(iii) группа, состоящая из углеродных атомов, атомов водорода и атомов кислорода (представляющая, например, эфирную группу, состоящую из алифатических групп, эфирную группу, состоящую из ароматических групп или эфирную группу, состоящую из алифатических групп и ароматических групп, но исключая группы, содержащие активный водород, такие как карбонильная группа, эфирная группа, терминальная метиновая группа и спиртовая OH группа, карбоксильная группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа),
(iv) атом галогена, и
(v) группа, состоящая из атомов, выбранных из углеродных атомов, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена (но исключая группы, содержащие активный водород, такие как карбонильная группа, эфирная группа, терминальная метиновая группа и спиртовая OH группа, карбоксильная группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа).
Активный водород относится к атому водорода, связанному с кислородом, серой или азотом (но исключая ароматические гидроксильные группы). Несмотря на то, что ароматические гидроксильные группы (OH группы, непосредственно связанные с ароматической группой) включают в упомянутое выше определение активного водорода, так как ароматические гидроксильные группы также содержатся в композиции варианта настоящего осуществления и в сырье для реакции и, в частности, не оказывают негативного воздействия, ароматические гидроксильные группы не включают в группы, содержащие активный водород, если специально не указано иное. Даже если описание "групп, содержащих активный водород" часто приводится в других местах изобретения настоящей заявки, упомянутое выше определение также применяется к таким группам.
Кроме того, кольцо A является структурой, которая содержит по меньшей мере одну структуру, выбранную из группы, состоящей из бензольного кольца, нафталинового кольца и антраценового кольца, и предпочтительно, чтобы оно являлось ароматическим гидроксисоединением, представленным следующей формулой (7):
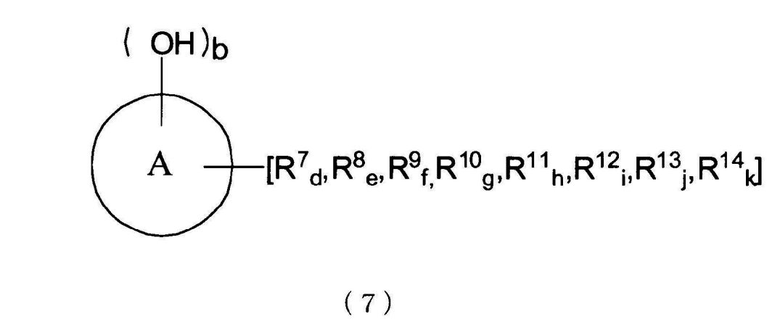
(где
кольцо A представляет ароматическое кольцо, выбранное из бензольного кольца, нафталинового кольца и антраценового кольца; OH группы и группы R7-R14 соответственно представляют группы, замещенные в произвольных местах, которые сохраняют ароматические свойства кольца A, группы R7-R14 могут соответственно и независимо замещать кольцо A, группы R7-R14 могут быть связаны вместе с образованием кольца с кольцом A, группы R7-R14 соответственно и независимо представляют атом водорода, атом галогена или группу, выбранную из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы, арильной группы, имеющей гидроксильную группу, аралкильной группы и эфирной группы (замещенной и/или незамещенной алкиловой эфирной и/или ариловой эфирной и/или аралкиловой эфирной группы), и/или группу, к которой один или более типов групп, выбранных из группы, связаны, и/или группу, к которой один или более типов групп, выбранных из группы, связаны с помощью насыщенных алифатических связей и/или эфирных связей, и кольцо A и группы R7-R14 состоят из суммарного целого числа углеродных атомов в интервале от 6 до 50,
b представляет целое число от 1 до 6, d, e, f, g, h, i, j и k представляют целые числа от 0 до 5, величина d + e + f + g + h + i + j + k представляет целое число, равное 6-b в случае, когда кольцо A является бензольным кольцом, представляет целое число, равное 8-b в случае, когда кольцо A является нафталиновым кольцом, или представляет целое число, равное 10-b в случае, когда кольцо A является антраценовым кольцом, и группа, выбранная из описанных выше групп R7-R14, может быть циклически связана с кольцом A связями углерод-углерод и/или эфирными связями).
С точки зрения возможности промышленного использования, предпочтительно, чтобы ароматическое гидроксисоединение, представленное упомянутой выше формулой (7) являлось ароматическим гидроксисоединением, в котором одна или две ароматические гидроксильные группы связаны с кольцом A (а именно, b =1 или 2), и более предпочтительно, ароматическим моногидроксисоединением, в котором одна ароматическая гидроксильная группа связана с кольцом A, так как в этом случае они обычно имеют низкую вязкость.
Кроме того, так как ароматическое гидроксисоединение является соединением, которое имеет уреидные группы, путем проведения стадии (B) и осуществления этерификации, оно образует N-замещенной карбаминовой кислоты-O-ариловый эфир, полученный из уреидных групп и ароматического гидроксисоединения (а именно, N-замещенной карбаминовой кислоты-O-ариловый эфир, в котором O-арильная группа, которая образует карбаминовой кислоты-O-ариловый эфир, образуется из ароматического гидроксисоединения, а фрагмент группы N-замещенной карбаминовой кислоты образуется из соединения, имеющего уреидные группы), в то время как в случае проведения стадии (P), N-замещенной карбаминовой кислоты-O-R2 эфир, образованный из N-замещенной карбаминовой кислоты-O-R2 эфира и ароматического гидроксисоединения, образуется из N-замещенной карбаминовой кислоты-O-R2 эфира путем проведения реакции переэтерификации (а именно, N-замещенной карбаминовой кислоты-O-ариловый эфир является N-замещенной карбаминовой кислоты-O-R2 эфиром, в котором O-алкиловую эфирную группу N-замещенной карбаминовой кислоты-O-R2 эфира подвергли переэтерификации с ароматическим гидроксисоединением). N-замещенной карбаминовой кислоты-O-ариловый эфир используют в качестве предшественника изоцианата. Способ получения изоцианата, получаемого из N-замещенной карбаминовой кислоты-O-арилового эфира, будет подробно описан далее, и предпочтительно, чтобы N-замещенной карбаминовой кислоты-O-ариловый эфир, полученный способом варианта настоящего осуществления, подвергали термическому разложению на следующей стадии (F) с получением изоцианата, представленного следующей формулой (6), который получают из N-замещенной карбаминовой кислоты-O-арилового эфира, и ароматической гидроксикомпозиции:
стадия (F): стадия получения изоцианата и ароматической гидроксикомпозиции из N-замещенной карбаминовой кислоты-O-арилового эфира:
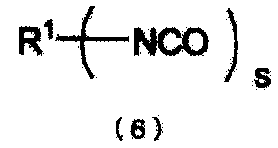
(где
R1 представляет органическую группу, которая содержит целое число углеродных атомов в интервале от 1 до 85, и которая замещена s группами NCO, и s представляет целое число от 1 до 10).
Способ получения включает термическое разложение N-замещенной карбаминовой кислоты-O-арилового эфира с получением ароматического гидроксисоединения и изоцианата, получаемого из N-замещенной карбаминовой кислоты-O-арилового эфира. Здесь, изоцианат, полученный из N-замещенной карбаминовой кислоты-O-арилового эфира, относится к соединению изоцианата, в котором O-арильная группа карбаминовой кислоты (-NHCOOAr, где Ar представляет арильную группу, полученную из ароматического гидроксисоединения) N-замещенной карбаминовой кислоты-O-арилового эфира превращается в изоцианатную группу (-NCO). Принимая во внимание уравнение реакции, ароматическое гидроксисоединение, образующееся в данном случае, является ароматическим гидроксисоединением, содержащимся в ароматической гидроксикомпозиции, реагирующей с соединением, имеющим уреидные группы, при получении N-замещенной карбаминовой кислоты-O-арилового эфира. А именно, ароматическое гидроксисоединение, представленное формулой (2) и, предпочтительно, формулой (7), образуется в качестве побочного продукта вместе с изоцианатом в процессе термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира. В одном аспекте варианта настоящего осуществления, в зависимости от конкретного случая, ароматическое гидроксисоединение и изоцианат разделяют путем отгонки после стадии термического разложения, и отделенное ароматическое гидроксисоединение может быть рециркулировано в виде ароматической гидроксикомпозиции, которая реагирует с соединением, имеющим уреидные группы. А именно, этот аспект варианта настоящего осуществления является предпочтительным аспектом, в котором ароматическую гидроксикомпозицию, полученную на стадии (F), отделяют от изоцианата и затем используют в результате рециркуляции на стадии (A), и/или стадии (B), или на стадии (A), и/или стадии (R), и/или стадии (P).
Таким образом, принимая во внимание способ со стадией производства изоцианата, в котором проводят стадию (F), необходимо принимать во внимание возможность отделения ароматического гидроксисоединения, служащего в качестве сырья, от N-замещенной карбаминовой кислоты-O-арилового эфира и изоцианата, образующегося из N-замещенной карбаминовой кислоты-O-арилового эфира. Обычно трудно предсказать возможность разделения веществ, но можно руководствоваться следующим правилом, что обычно два компонента, которые нужно разделить, могут быть соответствующим образом разделены в промышленности путем ректификации, если их стандартные температуры кипения различаются на 10°C или более. Таким образом, это определение относится к значению, которое ограничено известными на настоящий момент способами разделения, и не предполагается, что оно служит в качестве основы для варианта настоящего осуществления.
В следующей таблице (1) приведены стандартные температуры кипения ароматических гидроксисоединений или температуры кипения при пониженном давлении, в случае если их трудно измерить при нормальном давлении. Несмотря на то, что реакционная способность ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию, используемую в варианте настоящего осуществления, по отношению к соединению, содержащему уреидную группу, и/или к N-замещенной карбаминовой кислоты-O-R2 эфиру (подробности относительно этого N-замещенной карбаминовой кислоты-O-R2 эфира будут описаны далее), и/или к мочевине является важным критерием, стандартная температура кипения также является важным критерием для отбора с точки зрения возможности отделения каждого компонента. Как показано в следующей таблице (1), типы и число заместителей, положения заместителей и другие подобные параметры имеют значительное влияние на температуру кипения ароматического гидроксисоединения. Температура кипения является физическим свойством, которое также зависит от внутримолекулярных сил, и для обычных специалистов в этой области является общеизвестным, что температуру кипения невозможно определить, исходя только из структуры единичной молекулы. Таким образом, выбор ароматического гидроксисоединения, согласно важному аспекту настоящего изобретения, на основе его стандартной температуры кипения проводят путем измерения или исследования структуры и свойств (стандартной температуры кипения) требуемого N-замещенной карбаминовой кислоты-O-Ar эфира (который подробно будет описан далее) и/или изоцианата. Измерение стандартной температуры кипения может быть проведено известными методами, и может быть выполнено обычным путем исследователем с обычной квалификацией в соответствующей области техники. Как уже было описано выше, трудно предсказать возможность разделения ароматических гидроксисоединений, используемых в настоящем изобретении, на основе структуры, такой как общая формула, и предполагаемый способ варианта настоящего осуществления не является способом предсказания стандартной температуры кипения ароматического гидроксисоединения. Таким образом, обычный специалист в этой области способен осуществить вариант настоящего осуществления путем ссылки на стандартную температуру кипения или измерения стандартной температуры кипения, соответствующей описанному выше используемому соединению.
При объяснении с использованием одного из вариантов настоящего осуществления в качестве примера органический первичный амин, представленный упомянутой выше формулой (3), и упомянутую выше мочевину, подвергнутую реакции образования уреидов на стадии (A) для получения соединения, имеющего уреидные группы, обозначенного в формуле (1), соединение, имеющее уреидные группы, и ароматическую гидроксикомпозицию (композицию, содержащую по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2) (и, предпочтительно, формулой (7)) подвергают реакции этерификации путем проведения стадии (B) для получения соединения, имеющего группу N-замещенной карбаминовой кислоты-O-арилового эфира, и проводят стадию (F) с использованием N-замещенной карбаминовой кислоты-O-арилового эфира для получения ароматического гидроксисоединения и изоцианата, получаемых из N-замещенной карбаминовой кислоты-O-ариловый эфира. В качестве варианта, ароматическое гидроксисоединение и изоцианат, получаемые из N-замещенной карбаминовой кислоты-O-арилового эфира, получают с помощью способа, который включает стадии (A), (R), (P) и (F). В качестве варианта, в случае, когда органическим первичным амином является ароматический органический первичный моноамин, представленный следующей формулой (5), проводят следующую стадию (C) после стадии (B) или стадии (P) (стадия (C) будет подробно описана далее), и N-замещенной карбаминовой кислоты-O-ариловый эфир, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-арилового эфира сшиты с помощью метиленовых групп (-CH2-), получают из N-замещенной карбаминовой кислоты-O-арилового эфира, полученного на стадии (B) или стадии (P), с последующим проведением стадии (F) для получения ароматического гидроксисоединения и изоцианата, получаемых из N-замещенной карбаминовой кислоты-O-арилового эфира:
стадия (C): стадия получения N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира являются сшитыми с помощью метиленовых групп (-CH2-), путем реакции N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира с формальдегидом или сшивающим агентом с метиленовыми группами и сшивания ароматических групп, получаемых из ароматического органического первичного моноамина, содержащихся в N-замещенной карбаминовой кислоты-O-(R2 или ариловом)эфире, с помощью метиленовых групп (-CH2-):
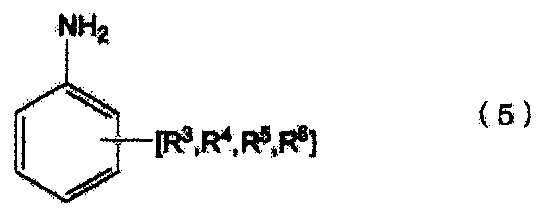
(где
по меньшей мере одно место в орто-положении и/или пара-положении группы NH2 ароматического органического первичного моноамина, представленного формулой (5), не замещено, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут быть связаны вместе с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из групп, состоящих из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 составляет целое число в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют ароматический органический первичный моноамин, представленный формулой (5), составляет целое число от 6 до 13).
Часто используемый в настоящем описании термин "N-замещенной карбаминовой кислоты-O-(R2 или ариловый) эфир" относится к "N-замещенной карбаминовой кислоты-O-R2 эфиру или N-замещенной карбаминовой кислоты-O-ариловому эфиру".
Таким образом, структуры ароматического гидроксисоединения и изоцианата, которые разделяют после реакции термического разложения, являются такими структурами, что ароматическое гидроксисоединение является ароматическим гидроксисоединением, которое составляет ароматическую гидроксикомпозицию (или содержится в ароматической гидроксикомпозиции), используемую при превращении соединения, имеющего уреидные группы, в N-замещенной карбаминовой кислоты-O-ариловый эфир, в то время как другой продукт в форме изоцианата получают из соединения, имеющего уреидные группы, представленного формулой (1), или органического первичного амина, представленного формулой (3) (а именно, получают изоцианат, имеющий структуру, в которой уреидную группу (-NHCONH2) соединения, имеющего уреидные группы, превращают в изоцианатную группу (-NCO), или первичную аминогруппу (-NH2) органического первичного амина превращают в изоцианатную группу (-NCO)).
А именно, если стандартные температуры кипения ароматического гидроксисоединения, представленного формулой (2), или, предпочтительно, формулой (7), и изоцианата, представленного формулой (6), различаются на 10°C или более, ароматическое гидроксисоединение и изоцианат могут быть разделены с помощью известных на настоящий момент методов. Как уже было описано ранее, так как изоцианат, представленный формулой (6), полученный способом варианта настоящего осуществления, получают путем использования в качестве сырья соединения, имеющего уреидные группы, или органического первичного амина, стандартная температура кипения получаемого изоцианата может являться стандартной температурой кипения изоцианата, в котором все уреидные группы или все первичные аминогруппы соединения, имеющего уреидные группы, или органического первичного амина превращены в изоцианатные группы. В предпочтительном аспекте соединение, имеющее уреидные группы, является соединением, имеющим уреидные группы, которое получают путем проведения стадии (A). А именно, предпочтительным является ароматическое гидроксисоединение, в котором стандартная температура кипения ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию, отличается на 10°C или более от стандартной температуры кипения изоцианата, имеющего структуру, в которой все аминогруппы (первичные аминогруппы) органического первичного амина превращены в изоцианатные группы.
Более того, принимая во внимание возможность промышленного использования, предпочтительным ароматическим моногидроксисоединением, имеющим бензольное кольцо, является легко доступное ароматическое моногидроксисоединение. Предпочтительные примеры такого ароматического моногидроксисоединения могут включать ароматические моногидроксисоединения, представленные следующей формулой (31):
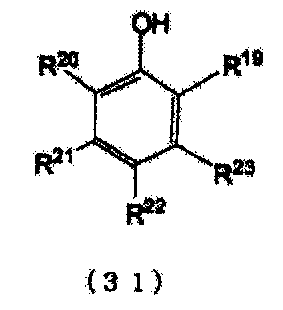
(где
R19, R20, R21, R22 и R23 являются группами, независимо выбранными из упомянутых выше групп R7-R14 (исключая арильные группы, имеющие гидроксильную группу), и ароматическое гидроксисоединение, представленное формулой (31), является ароматическим моногидроксисоединением, в котором число углеродных атомов составляет целое число от 6 до 50, а именно, суммарное число углеродных атомов групп R19, R20, R21, R22 и R23 составляет целое число от 0 до 44).
Среди ароматических моногидроксисоединений, представленных упомянутой выше формулой (31), предпочтительно, чтобы группы R19, R20, R21, R22 и R23 являлись атомами водорода и/или группами, соответственно и независимо выбранными из групп, указанных в следующих пунктах (i)-(iii):
(i): группа, в которой атом в α положении (атом, связанный с ароматическим кольцом) является углеродным атомом, число углеродных атомов составляет от 1 до 44, группа, связанная с углеродным атомом в α положении является атомом водорода, алкильной группой, имеющей от 1 до 43 углеродных атомов, циклоалкильной группой, имеющей от 1 до 44 углеродных атомов, алкоксильной группой, имеющей от 1 до 44 углеродных атомов, группой полиоксиалкиленалкилового эфира, имеющего от 2 до 44 углеродных атомов, но не имеющих OH группы на ее конце, арильной группой, имеющей от 6 до 43 углеродных атомов, аралкильной группой, имеющей от 7 до 43 углеродных атомов или аралкилоксильной группой, имеющей от 7 до 19 углеродных атомов, и тремя группами, выбранными из групп, в которых один или более типов приведенных выше групп связаны с атомом углерода,
(ii) арильная группа, в которой число углеродных атомов составляет от 1 до 44, арильная группа замещена с помощью заместителей, и заместителями являются арильные группы, которые могут быть замещены с помощью целого числа от 1 до 5 следующих заместителей, при этом заместители выбирают из атома водорода, алкильной группы, имеющей от 1 до 38 углеродных атомов, циклоалкильной группы, имеющей от 4 до 38 углеродных атомов, алкоксильной группы, имеющей от 1 до 38 углеродных атомов, группы полиоксиалкиленалкилового эфира, имеющего от 2 до 38 углеродных атомов, но не имеющих OH группы на ее конце, арильной группы, имеющей от 6 до 38 углеродных атомов, аралкильной группы, имеющей от 7 до 38 углеродных атомов, аралкилоксильной группы, имеющей от 7 до 38 углеродных атомов, и группы, в которой связаны один или более типов приведенных выше групп,
(iii) группа, в которой атом в α положении (атом, связанный с ароматическим кольцом) является атомом кислорода, число углеродных атомов составляет от 1 до 44, и группа, связанная с атомом кислорода в α положении, является группой, выбранной из алкильной группы, имеющей от 1 до 43 углеродных атомов, циклоалкильной группы, имеющей от 4 до 44 углеродных атомов, алкоксигруппы, имеющей от 1 до 44 углеродных атомов, группы полиоксиалкиленалкилового эфира, имеющего от 2 до 44 углеродных атомов, но не имеющих OH группы на ее конце, арильной группы, имеющей от 6 до 43 углеродных атомов, аралкильной группы, имеющей от 7 до 43 углеродных атомов и группы, в которой связаны один или более типов приведенных выше групп.
Используемый в упомянутой выше формуле (31) термин "атом в α положении" относится к атому, который составляет группы R19, R20, R21, R22 и R23 и который расположен рядом с углеродным атомом на ароматическом углеводородном кольце, с которым связаны группы R19, R20, R21, R22 и R23. Примеры этих групп R19, R20, R21, R22 и R23 могут включать атомы водорода, алкильные группы, и/или циклоалкильные группы, и/или циклоалкильные группы, замещенные с помощью алкильной группы, и/или алкильные группы, замещенные с помощью циклоалкильной группы, такие как метильная группа, этильная группа, пропильная группа (включая изомеры), бутильная группа (включая изомеры), пентильная группа (включая изомеры), гексильная группа (включая изомеры), гептильная группа (включая изомеры), октильная группа (включая изомеры), нонильная группа (включая изомеры), децильная группа (включая изомеры), додецильная группа (включая изомеры), октадецильная группа (включая изомеры), циклопентильная группа, циклогексильная группа, циклогептильная группа, циклооктильная группа, бис(циклогексил)алкан, метилциклопентильная группа (включая изомеры), этилциклопентильная группа (включая изомеры), метилциклогексильная группа (включая изомеры), этилциклогексильная группа (включая изомеры), пропилциклогексильная группа (включая изомеры), бутилциклогексильная группа (включая изомеры), пентилциклогексильная группа (включая изомеры), гексилциклогексильная группа (включая изомеры), диметилциклогексильная группа (включая изомеры), диэтилциклогексильная группа (включая изомеры) или дибутилциклогексильная группа (включая изомеры); алкоксильные группы и/или циклоалкоксильные группы и/или циклоалкоксильные группы, замещенные с помощью алкоксильной группы, и/или алкоксильные группы, замещенные с помощью циклоалкоксильной группы, такие как метоксильная группа, этоксильная группа, пропоксильная группа (включая изомеры), бутилоксильная группа (включая изомеры), пентилоксильная группа (включая изомеры), гексилоксильная группа (включая изомеры), гептилоксильная группа (включая изомеры), октилоксильная группа (включая изомеры), нонилоксильная группа (включая изомеры), децилоксильная группа (включая изомеры), додецилоксильная группа (включая изомеры), октадецилоксильная группа (включая изомеры), циклопентилоксильная группа (включая изомеры), циклогексилоксильная группа (включая изомеры), циклогептилоксильная группа (включая изомеры), циклооктилоксильная группа (включая изомеры), метилциклопентилоксильная группа (включая изомеры), этилциклопентилоксильная группа (включая изомеры), метилциклогексилоксильная группа (включая изомеры), этилциклогексилоксильная группа (включая изомеры), пропилциклогексилоксильная группа (включая изомеры), бутилциклогексилоксильная группа (включая изомеры), пентилциклогексилоксильная группа (включая изомеры), гексилциклогексилоксильная группа (включая изомеры), диметилциклогексилоксильная группа (включая изомеры), диэтилциклогексилоксильная группа (включая изомеры) или дибутилциклогексилоксильная группа (включая изомеры); замещенные или незамещенные арильные группы, такие как фенильная группа, метилфенильная группа (включая изомеры), этилфенильная группа (включая изомеры), пропилфенильная группа (включая изомеры), бутилфенильная группа (включая изомеры), пентилфенильная группа (включая изомеры), гексилфенильная группа (включая изомеры), гептилфенильная группа (включая изомеры), октилфенильная группа (включая изомеры), нонилфенильная группа (включая изомеры), децилфенильная группа (включая изомеры), бифенильная группа (включая изомеры), диметилфенильная группа (включая изомеры), диэтилфенильная группа (включая изомеры), дипропилфенильная группа (включая изомеры), дибутилфенильная группа (включая изомеры), дипентилфенильная группа (включая изомеры), дигексилфенильная группа (включая изомеры), дигептилфенильная группа (включая изомеры), терфенильная группа (включая изомеры), триметилфенильная группа (включая изомеры), триэтилфенильная группа (включая изомеры), трипропилфенильная группа (включая изомеры) или трибутилфенильная группа (включая изомеры); замещенные или незамещенные арилоксильные группы, такие как феноксильная группа, метилфеноксильная группа (включая изомеры), этилфеноксильная группа (включая изомеры), пропилфеноксильная группа (включая изомеры), бутилфеноксильная группа (включая изомеры), пентилфеноксильная группа (включая изомеры), гексилфеноксильная группа (включая изомеры), гептилфеноксильная группа (включая изомеры), октилфеноксильная группа (включая изомеры), нонилфеноксильная группа (включая изомеры), децилфеноксильная группа (включая изомеры), фенилфеноксильная группа (включая изомеры), диметилфеноксильная группа (включая изомеры), диэтилфеноксильная группа (включая изомеры), дипропилфеноксильная группа (включая изомеры), дибутилфеноксильная группа (включая изомеры), дипентилфеноксильная группа (включая изомеры), дигексилфеноксильная группа (включая изомеры), дигептилфеноксильная группа (включая изомеры), дифенилфеноксильная группа (включая изомеры), триметилфеноксильная группа (включая изомеры), триэтилфеноксильная группа (включая изомеры), трипропилфеноксильная группа (включая изомеры) или трибутилфеноксильная группа (включая изомеры); замещенные или незамещенные аралкильные группы, такие как фенилметильная группа, фенилэтильная группа (включая изомеры), фенилпропильная группа (включая изомеры), фенилбутильная группа (включая изомеры), фенилпентильная группа (включая изомеры), фенилгексильная группа (включая изомеры), фенилгептильная группа (включая изомеры), фенилоктильная группа (включая изомеры) или фенилнонильная группа (включая изомеры); аралкилоксильные группы, такие как фенилметоксильная группа, фенилэтоксильная группа (включая изомеры), фенилпропилоксильная группа (включая изомеры), фенилбутилоксильная группа (включая изомеры), фенилпентилоксильная группа (включая изомеры), фенилгексилоксильная группа (включая изомеры), фенилгептилоксильная группа (включая изомеры), фенилоктилоксильная группа (включая изомеры) или фенилнонилоксильная группа (включая изомеры), и группы, состоящие из гидроксиарильных групп и алкильных групп, такие как гидроксифенильная группа (включая изомеры), гидроксифеноксильная группа (включая изомеры), гидроксифенилметильная группа (включая изомеры), гидроксифенилэтильная группа (включая изомеры) или гидроксифенилпропильная группа (включая изомеры).
Предпочтительные примеры ароматических моногидроксисоединений, представленных упомянутой выше формулой (30), могут включать следующие соединения: фенол, метилфенол (включая изомеры), этилфенол (включая изомеры), пропилфенол (включая изомеры), бутилфенол (включая изомеры), пентилфенол (включая изомеры), гексилфенол (включая изомеры), гептилфенол (включая изомеры), октилфенол (включая изомеры), нонилфенол (включая изомеры), децилфенол (включая изомеры), додецилфенол (включая изомеры), октадецилфенол (включая изомеры), диметилфенол (включая изомеры), диэтилфенол (включая изомеры), дипропилфенол (включая изомеры), дибутилфенол (включая изомеры), дипентилфенол (включая изомеры), дигексилфенол (включая изомеры), дигептилфенол (включая изомеры), диоктилфенол (включая изомеры), динонилфенол (включая изомеры), дидецилфенол (включая изомеры), дидодецилфенол (включая изомеры), диоктадецилфенол (включая изомеры), триметилфенол (включая изомеры), триэтилфенол (включая изомеры), трипропилфенол (включая изомеры), трибутилфенол (включая изомеры), трипентилфенол (включая изомеры), тригексилфенол (включая изомеры), тригептилфенол (включая изомеры), триоктилфенол (включая изомеры), тринонилфенол (включая изомеры), тридецилфенол (включая изомеры), тридодецилфенол (включая изомеры), триоктадецилфенол (включая изомеры), (метоксиметил)фенол (включая изомеры), (этоксиметил)фенол (включая изомеры), (пропоксиметил)фенол (включая изомеры), (бутилоксиметил)фенол (включая изомеры), (пентилоксиметил)фенол (включая изомеры), (гексилоксиметил)фенол (включая изомеры), (гептилоксиметил)фенол (включая изомеры), (октилоксиметил)фенол (включая изомеры), (нонилоксиметил)фенол (включая изомеры), (децилоксиметил)фенол (включая изомеры), (додецилоксиметил)фенол (включая изомеры), (октадецилоксиметил)фенол (включая изомеры), (циклопентилоксиметил)фенол (включая изомеры), (циклогексилоксиметил)фенол (включая изомеры), (циклогептилоксиметил)фенол (включая изомеры), (циклооктилоксиметил)фенол (включая изомеры), (метилциклопентилоксиметил)фенол (включая изомеры), (этилциклопентилоксиметил)фенол (включая изомеры), (метилциклогексилоксиметил)фенол (включая изомеры), (этилциклогексилоксиметил)фенол (включая изомеры), (пропилциклогексилоксиметил)фенол (включая изомеры), (бутилциклогексилоксиметил)фенол (включая изомеры), (пентилциклогексилоксиметил)фенол (включая изомеры), (гексилциклогексилоксиметил)фенол (включая изомеры), (диметилциклогексилоксиметил)фенол (включая изомеры), (диэтилциклогексилоксиметил)фенол (включая изомеры), (дибутилциклогексилоксиметил)фенол (включая изомеры), (феноксиметил)фенол, (метилфеноксиметил)фенол (включая изомеры), (этилфеноксиметил)фенол (включая изомеры), (пропилфеноксиметил)фенол (включая изомеры), (бутилфеноксиметил)фенол (включая изомеры), (пентилфеноксиметил)фенол (включая изомеры), (гексилфеноксиметил)фенол (включая изомеры), (гептилфеноксиметил)фенол (включая изомеры), (октилфеноксиметил)фенол (включая изомеры), (нонилфеноксиметил)фенол (включая изомеры), (децилфеноксиметил)фенол (включая изомеры), (фенилфеноксиметил)фенол (включая изомеры), (диметилфеноксиметил)фенол (включая изомеры), (диэтилфеноксиметил)фенол (включая изомеры), (дипропилфеноксиметил)фенол (включая изомеры), (дибутилфеноксиметил)фенол (включая изомеры), (дипентилфеноксиметил)фенол (включая изомеры), (дигексилфеноксиметил)фенол (включая изомеры), (дигептилфеноксиметил)фенол (включая изомеры), (дифенилфеноксиметил)фенол (включая изомеры), (триметилфеноксиметил)фенол (включая изомеры), (триэтилфеноксиметил)фенол (включая изомеры), (трипропилфеноксиметил)фенол (включая изомеры), (трибутилфеноксиметил)фенол (включая изомеры), (фенилметоксиметил)фенол (включая изомеры), (фенилэтоксиметил)фенол (включая изомеры), (фенилпропилоксиметил)фенол (включая изомеры), (фенилбутилоксиметил)фенол (включая изомеры), (фенилпентилоксиметил)фенол (включая изомеры), (фенилгексилоксиметил)фенол (включая изомеры), (фенилгептилоксиметил)фенол (включая изомеры), (фенилоктилоксиметил)фенол (включая изомеры), (фенилнонилоксиметил)фенол (включая изомеры), ди(метоксиметил)фенол, ди(этоксиметил)фенол, ди(пропоксиметил)фенол (включая изомеры), ди(бутилоксиметил)фенол (включая изомеры), ди(пентилоксиметил)фенол (включая изомеры), ди(гексилоксиметил)фенол (включая изомеры), ди(гептилоксиметил)фенол (включая изомеры), ди(октилоксиметил)фенол (включая изомеры), ди(нонилоксиметил)фенол (включая изомеры), ди(децилоксиметил)фенол (включая изомеры), ди(додецилоксиметил)фенол (включая изомеры), ди(октадецилоксиметил)фенол (включая изомеры), ди(циклопентилоксиметил)фенол (включая изомеры), ди(циклогексилоксиметил)фенол (включая изомеры), ди(циклогептилоксиметил)фенол (включая изомеры), ди(циклооктилоксиметил)фенол (включая изомеры), ди(метилциклопентилоксиметил)фенол (включая изомеры), ди(этилциклопентилоксиметил)фенол (включая изомеры), ди(метилциклогексилоксиметил)фенол (включая изомеры), ди(этилциклогексилоксиметил)фенол (включая изомеры), ди(пропилциклогексилоксиметил)фенол (включая изомеры), ди(бутилциклогексилоксиметил)фенол (включая изомеры), ди(пентилциклогексилоксиметил)фенол (включая изомеры), ди(гексилциклогексилоксиметил)фенол (включая изомеры), бис(диметилциклогексилоксиметил)фенол (включая изомеры), бис(диэтилциклогексилоксиметил)фенол (включая изомеры), бис(дибутилциклогексилоксиметил)фенол (включая изомеры), ди(феноксиметил)фенол, ди(метилфеноксиметил)фенол (включая изомеры), ди(этилфеноксиметил)фенол (включая изомеры), ди(пропилфеноксиметил)фенол (включая изомеры), ди(бутилфеноксиметил)фенол (включая изомеры), ди(пентилфеноксиметил)фенол (включая изомеры), ди(гексилфеноксиметил)фенол (включая изомеры), ди(гептилфеноксиметил)фенол (включая изомеры), ди(октилфеноксиметил)фенол (включая изомеры), ди(нонилфеноксиметил)фенол (включая изомеры), ди(децилфеноксиметил)фенол (включая изомеры), ди(фенилфеноксиметил)фенол (включая изомеры), бис(диметилфеноксиметил)фенол (включая изомеры), бис(диэтилфеноксиметил)фенол (включая изомеры), бис(дипропилфеноксиметил)фенол (включая изомеры), бис(дибутилфеноксиметил)фенол (включая изомеры), бис(дипентилфеноксиметил)фенол (включая изомеры), бис(дигексилфеноксиметил)фенол (включая изомеры), бис(дигептилфеноксиметил)фенол (включая изомеры), бис(дифенилфеноксиметил)фенол (включая изомеры), ди(триметилфеноксиметил)фенол (включая изомеры), ди(триэтилфеноксиметил)фенол (включая изомеры), ди(трипропилфеноксиметил)фенол (включая изомеры), ди(трибутилфеноксиметил)фенол (включая изомеры), (фенилметоксиметил)фенол (включая изомеры), ди(фенилэтоксиметил)фенол (включая изомеры), ди(фенилпропилоксиметил)фенол (включая изомеры), ди(фенилбутилоксиметил)фенол (включая изомеры), ди(фенилпентилоксиметил)фенол (включая изомеры), ди(фенилгексилоксиметил)фенол (включая изомеры), ди(фенилгептилоксиметил)фенол (включая изомеры), ди(фенилоктилоксиметил)фенол (включая изомеры), ди(фенилнонилоксиметил)фенол (включая изомеры), три(метоксиметил)фенол, три(этоксиметил)фенол, три(пропоксиметил)фенол (включая изомеры), три(бутилоксиметил)фенол (включая изомеры), три(пентилоксиметил)фенол (включая изомеры), три(гексилоксиметил)фенол (включая изомеры), три(гептилоксиметил)фенол (включая изомеры), три(октилоксиметил)фенол (включая изомеры), три(нонилоксиметил)фенол (включая изомеры), три(децилоксиметил)фенол (включая изомеры), три(додецилоксиметил)фенол (включая изомеры), три(октадецилоксиметил)фенол (включая изомеры), три(циклопентилоксиметил)фенол (включая изомеры), три(циклогексилоксиметил)фенол (включая изомеры), три(циклогептилоксиметил)фенол (включая изомеры), три(циклооктилоксиметил)фенол (включая изомеры), три(метилциклопентилоксиметил)фенол (включая изомеры), три(этилциклопентилоксиметил)фенол (включая изомеры), три(метилциклогексилоксиметил)фенол (включая изомеры), три(этилциклогексилоксиметил)фенол (включая изомеры), три(пропилциклогексилоксиметил)фенол (включая изомеры), три(бутилциклогексилоксиметил)фенол (включая изомеры), три(пентилциклогексилоксиметил)фенол (включая изомеры), три(гексилциклогексилоксиметил)фенол (включая изомеры), бис(диметилциклогексилоксиметил)фенол (включая изомеры), бис(диэтилциклогексилоксиметил)фенол (включая изомеры), бис(дибутилциклогексилоксиметил)фенол (включая изомеры), три(феноксиметил)фенол, три(метилфеноксиметил)фенол (включая изомеры), три(этилфеноксиметил)фенол (включая изомеры), три(пропилфеноксиметил)фенол (включая изомеры), три(бутилфеноксиметил)фенол (включая изомеры), три(пентилфеноксиметил)фенол (включая изомеры), три(гексилфеноксиметил)фенол (включая изомеры), три(гептилфеноксиметил)фенол (включая изомеры), три(октилфеноксиметил)фенол (включая изомеры), три(нонилфеноксиметил)фенол (включая изомеры), три(децилфеноксиметил)фенол (включая изомеры), три(фенилфеноксиметил)фенол (включая изомеры), бис(диметилфеноксиметил)фенол (включая изомеры), бис(диэтилфеноксиметил)фенол (включая изомеры), бис(дипропилфеноксиметил)фенол (включая изомеры), бис(дибутилфеноксиметил)фенол (включая изомеры), бис(дипентилфеноксиметил)фенол (включая изомеры), бис(дигексилфеноксиметил)фенол (включая изомеры), бис(дигептилфеноксиметил)фенол (включая изомеры), бис(дифенилфеноксиметил)фенол (включая изомеры), три(триметилфеноксиметил)фенол (включая изомеры), три(триэтилфеноксиметил)фенол (включая изомеры), три(трипропилфеноксиметил)фенол (включая изомеры), три(трибутилфеноксиметил)фенол (включая изомеры), три(фенилметоксиметил)фенол, три(фенилэтоксиметил)фенол (включая изомеры), три(фенилпропилоксиметил)фенол (включая изомеры), три(фенилбутилоксиметил)фенол (включая изомеры), три(фенилпентилоксиметил)фенол (включая изомеры), три(фенилгексилоксиметил)фенол (включая изомеры), три(фенилгептилоксиметил)фенол (включая изомеры), три(фенилоктилоксиметил)фенол (включая изомеры), три(фенилнонилоксиметил)фенол (включая изомеры), (фенилметил)фенол (включая изомеры), ((метилфенил)метил)фенол (включая изомеры), ((этилфенил)метил)фенол (включая изомеры), ((пропилфенил)метил)фенол (включая изомеры), ((бутилфенил)метил)фенол (включая изомеры), ((пентилфенил)метил)фенол (включая изомеры), ((гексилфенил)метил)фенол (включая изомеры), ((гептилфенил)метил)фенол (включая изомеры), ((октилфенил)метил)фенол (включая изомеры), ((нонилфенил)метил)фенол (включая изомеры), ((децилфенил)метил)фенол (включая изомеры), ((бифенил)метил)фенол (включая изомеры), ((диметилфенил)метил)фенол (включая изомеры), ((диэтилфенил)метил)фенол (включая изомеры), ((дипропилфенил)метил)фенол (включая изомеры), ((дибутилфенил)метил)фенол (включая изомеры), ((дипентилфенил)метил)фенол (включая изомеры), ((дигексилфенил)метил)фенол (включая изомеры), ((дигептилфенил)метил)фенол (включая изомеры), ((терфенил)метил)фенол (включая изомеры), ((триметилфенил)метил)фенол (включая изомеры), ((триэтилфенил)метил)фенол (включая изомеры), ((трипропилфенил)метил)фенол (включая изомеры), ((трибутилфенил)метил)фенол (включая изомеры), ди(фенилметил)фенол (включая изомеры), ди((метилфенил)метил)фенол (включая изомеры), ди((этилфенил)метил)фенол (включая изомеры), ди((пропилфенил)метил)фенол (включая изомеры), ди((бутилфенил)метил)фенол (включая изомеры), ди((пентилфенил)метил)фенол (включая изомеры), ди((гексилфенил)метил)фенол (включая изомеры), ди((гептилфенил)метил)фенол (включая изомеры), ди((октилфенил)метил)фенол (включая изомеры), ди((нонилфенил)метил)фенол (включая изомеры), ди((децилфенил)метил)фенол (включая изомеры), ди((бифенил)метил)фенол (включая изомеры), ди((диметилфенил)метил)фенол (включая изомеры), ди((диэтилфенил)метил)фенол (включая изомеры), ди((дипропилфенил)метил)фенол (включая изомеры), ди((дибутилфенил)метил)фенол (включая изомеры), ди((дипентилфенил)метил)фенол (включая изомеры), ди((дигексилфенил)метил)фенол (включая изомеры), ди((дигептилфенил)метил)фенол (включая изомеры), ди((терфенил)метил)фенол (включая изомеры), ди((триметилфенил)метил)фенол (включая изомеры), ди((триэтилфенил)метил)фенол (включая изомеры), ди((трипропилфенил)метил)фенол (включая изомеры), ди((трибутилфенил)метил)фенол (включая изомеры), три(фенилметил)фенол (включая изомеры), три((метилфенил)метил)фенол (включая изомеры), три((этилфенил)метил)фенол (включая изомеры), три((пропилфенил)метил)фенол (включая изомеры), три((бутилфенил)метил)фенол (включая изомеры), три((пентилфенил)метил)фенол (включая изомеры), три((гексилфенил)метил)фенол (включая изомеры), три((гептилфенил)метил)фенол (включая изомеры), три((октилфенил)метил)фенол (включая изомеры), три((нонилфенил)метил)фенол (включая изомеры), три((децилфенил)метил)фенол (включая изомеры), три((бифенил)метил)фенол (включая изомеры), три((диметилфенил)метил)фенол (включая изомеры), три((диэтилфенил)метил)фенол (включая изомеры), три((дипропилфенил)метил)фенол (включая изомеры), три((дибутилфенил)метил)фенол (включая изомеры), три((дипентилфенил)метил)фенол (включая изомеры), три((дигексилфенил)метил)фенол (включая изомеры), три((дигептилфенил)метил)фенол (включая изомеры), три((терфенил)метил)фенол (включая изомеры), три((триметилфенил)метил)фенол (включая изомеры), три((триэтилфенил)метил)фенол (включая изомеры), три((трипропилфенил)метил)фенол (включая изомеры), три((трибутилфенил)метил)фенол (включая изомеры), фенилэтилфенол (включая изомеры), фенил-н-пропилфенол (включая изомеры), фенил-н-бутилфенол (включая изомеры), фенил-н-пентилфенол (включая изомеры), фенил-н-гексилфенол (включая изомеры), фенил-н-гептилфенол (включая изомеры), фенил-н-октилфенол (включая изомеры), фенил-н-нонилфенол (включая изомеры), метоксифенол (включая изомеры), этоксифенол (включая изомеры), пропилоксифенол (включая изомеры), бутилоксифенол (включая изомеры), пентилоксифенол (включая изомеры), гексилоксифенол (включая изомеры), гептилоксифенол (включая изомеры), октилоксифенол (включая изомеры), нонилоксифенол (включая изомеры), децилоксифенол (включая изомеры), додецилоксифенол (включая изомеры), октадецилоксифенол (включая изомеры), циклопентилоксифенол (включая изомеры), циклогексилоксифенол (включая изомеры), циклогептилоксифенол (включая изомеры), циклооктилоксифенол (включая изомеры), (метилциклопентилокси)фенол (включая изомеры), (этилциклопентилокси)фенол (включая изомеры), (метилциклогексилокси)фенол (включая изомеры), (этилциклогексилокси)фенол (включая изомеры), (пропилциклогексилокси)фенол (включая изомеры), (бутилциклогексилокси)фенол (включая изомеры), (пентилциклогексилокси)фенол (включая изомеры), (гексилциклогексилокси)фенол (включая изомеры), (диметилциклогексилокси)фенол (включая изомеры), (диэтилциклогексилокси)фенол (включая изомеры), (дибутилциклогексилокси)фенол (включая изомеры), феноксифенол, (метилфенилокси)фенол (включая изомеры), (этилфенилокси)фенол (включая изомеры), (пропилфенилокси)фенол (включая изомеры), (бутилфенилокси)фенол (включая изомеры), (пентилфенилокси)фенол (включая изомеры), (гексилфенилокси)фенол (включая изомеры), (гептилфенилокси)фенол (включая изомеры), (октилфенилокси)фенол (включая изомеры), (нонилфенилокси)фенол (включая изомеры), (децилфенилокси)фенол (включая изомеры), бифенилоксифенол (включая изомеры), (диметилфенилокси)фенол (включая изомеры), (диэтилфенилокси)фенол (включая изомеры), (дипропилфенилокси)фенол (включая изомеры), (дибутилфенилокси)фенол (включая изомеры), (дипентилфенилокси)фенол (включая изомеры), (дигексилфенилокси)фенол (включая изомеры), (дигептилфенилокси)фенол (включая изомеры), терфенилоксифенол (включая изомеры), (триметилфенилокси)фенол (включая изомеры), (триэтилфенилокси)фенол (включая изомеры), (трипропилфенилокси)фенол (включая изомеры), (трибутилфенилокси)фенол (включая изомеры), (фенилметилокси)фенол, (фенилэтилокси)фенол (включая изомеры), (фенилпропилокси)фенол (включая изомеры), (фенилбутилокси)фенол (включая изомеры), (фенилпентилокси)фенол (включая изомеры), (фенилгексилокси)фенол (включая изомеры), (фенилгептилокси)фенол (включая изомеры), (фенилоктилокси)фенол (включая изомеры), (фенилнонилокси)фенол (включая изомеры), диметоксифенол (включая изомеры), диэтоксифенол (включая изомеры), дипропилоксифенол (включая изомеры), дибутилоксифенол (включая изомеры), дипентилоксифенол (включая изомеры), дигексилоксифенол (включая изомеры), дигептилоксифенол (включая изомеры), диоктилоксифенол (включая изомеры), динонилоксифенол (включая изомеры), дидецилоксифенол (включая изомеры), дидодецилоксифенол (включая изомеры), диоктадецилоксифенол (включая изомеры), дициклопентилоксифенол (включая изомеры), дициклогексилоксифенол (включая изомеры), дициклогептилоксифенол (включая изомеры), дициклооктилоксифенол (включая изомеры), ди(метилциклопентилокси)фенол (включая изомеры), ди(этилциклопентилокси)фенол (включая изомеры), ди(метилциклогексилокси)фенол (включая изомеры), ди(этилциклогексилокси)фенол (включая изомеры), ди(пропилциклогексилокси)фенол (включая изомеры), ди(бутилциклогексилокси)фенол (включая изомеры), ди(пентилциклогексилокси)фенол (включая изомеры), ди(гексилциклогексилокси)фенол (включая изомеры), бис(диметилциклогексилокси)фенол (включая изомеры), бис(диэтилциклогексилокси)фенол (включая изомеры), бис(дибутилциклогексилокси)фенол (включая изомеры), фенилоксифенол, ди(метилфенилокси)фенол (включая изомеры), ди(этилфенилокси)фенол (включая изомеры), ди(пропилфенилокси)фенол (включая изомеры), ди(бутилфенилокси)фенол (включая изомеры), ди(пентилфенилокси)фенол (включая изомеры), ди(гексилфенилокси)фенол (включая изомеры), ди(гептилфенилокси)фенол (включая изомеры), ди(октилфенилокси)фенол (включая изомеры), ди(нонилфенилокси)фенол (включая изомеры), ди(децилфенилокси)фенол (включая изомеры), дибифенилоксифенол (включая изомеры), бис(диметилфенилокси)фенол (включая изомеры), бис(диэтилфенилокси)фенол (включая изомеры), бис(дипропилфенилокси)фенол (включая изомеры), бис(дибутилфенилокси)фенол (включая изомеры), бис(дипентилфенилокси)фенол (включая изомеры), бис(дигексилфенилокси)фенол (включая изомеры), бис(дигептилфенилокси)фенол (включая изомеры), дитерфенилоксифенол (включая изомеры), ди(триметилфенилокси)фенол (включая изомеры), ди(триэтилфенилокси)фенол (включая изомеры), ди(трипропилфенилокси)фенол (включая изомеры), ди(трибутилфенилокси)фенол (включая изомеры), (фенилметилокси)фенол, ди(фенилэтилокси)фенол (включая изомеры), ди(фенилпропилокси)фенол (включая изомеры), ди(фенилбутилокси)фенол (включая изомеры), ди(фенилпентилокси)фенол (включая изомеры), ди(фенилгексилокси)фенол (включая изомеры), ди(фенилгептилокси)фенол (включая изомеры), ди(фенилоктилокси)фенол (включая изомеры), ди(фенилнонилокси)фенол (включая изомеры), триметоксифенол (включая изомеры), триэтоксифенол (включая изомеры), трипропилоксифенол (включая изомеры), трибутилоксифенол (включая изомеры), трипентилоксифенол (включая изомеры), тригексилоксифенол (включая изомеры), тригептилоксифенол (включая изомеры), триоктилоксифенол (включая изомеры), тринонилоксифенол (включая изомеры), тридецилоксифенол (включая изомеры), тридодецилоксифенол (включая изомеры), триоктадецилоксифенол (включая изомеры), трициклопентилоксифенол (включая изомеры), трициклогексилоксифенол (включая изомеры), трициклогептилоксифенол (включая изомеры), трициклооктилоксифенол (включая изомеры), три(метилциклопентилокси)фенол (включая изомеры), три(этилциклопентилокси)фенол (включая изомеры), три(метилциклогексилокси)фенол (включая изомеры), три(этилциклогексилокси)фенол (включая изомеры), три(пропилциклогексилокси)фенол (включая изомеры), три(бутилциклогексилокси)фенол (включая изомеры), три(пентилциклогексилокси)фенол (включая изомеры), три(гексилциклогексилокси)фенол (включая изомеры), три(диметилциклогексилокси)фенол (включая изомеры), три(диэтилциклогексилокси)фенол (включая изомеры), три(дибутилциклогексилокси)фенол (включая изомеры), фенилоксифенол, три(метилфенилокси)фенол (включая изомеры), три(этилфенилокси)фенол (включая изомеры), три(пропилфенилокси)фенол (включая изомеры), три(бутилфенилокси)фенол (включая изомеры), три(пентилфенилокси)фенол (включая изомеры), три(гексилфенилокси)фенол (включая изомеры), три(гептилфенилокси)фенол (включая изомеры), три(октилфенилокси)фенол (включая изомеры), три(нонилфенилокси)фенол (включая изомеры), три(децилфенилокси)фенол (включая изомеры), трибифенилоксифенол (включая изомеры), три(диметилфенилокси)фенол (включая изомеры), три(диэтилфенилокси)фенол (включая изомеры), три(дипропилфенилокси)фенол (включая изомеры), три(дибутилфенилокси)фенол (включая изомеры), три(дипентилфенилокси)фенол (включая изомеры), три(дигексилфенилокси)фенол (включая изомеры), три(дигептилфенилокси)фенол (включая изомеры), тритерфенилоксифенол (включая изомеры), три(триметилфенилокси)фенол (включая изомеры), три(триэтилфенилокси)фенол (включая изомеры), три(трипропилфенилокси)фенол (включая изомеры), три(трибутилфенилокси)фенол (включая изомеры), (фенилметилокси)фенол, три(фенилэтилокси)фенол (включая изомеры), три(фенилпропилокси)фенол (включая изомеры), три(фенилбутилокси)фенол (включая изомеры), три(фенилпентилокси)фенол (включая изомеры), три(фенилгексилокси)фенол (включая изомеры), три(фенилгептилокси)фенол (включая изомеры), три(фенилоктилокси)фенол (включая изомеры), три(фенилнонилокси)фенол (включая изомеры), фенилфенол (включая изомеры), гидроксифенилфенол (включая изомеры), гидроксифеноксифенол (включая изомеры), гидроксифенилметилфенол (включая изомеры), гидроксифенилэтилфенол (включая изомеры), гидроксифенилпропилфенол, нафтол (включая изомеры), феноксифенол (включая изомеры) и дифеноксифенол (включая изомеры).
Предпочтительные примеры, с точки зрения легкости транспортировки упомянутых выше ароматических моногидроксисоединений, могут включать примеры, в которых по меньшей мере две из групп R19, R20, R21, R22 и R23 являются атомами водорода, и более предпочтительно, чтобы число углеродных атомов, которые составляют группы R19, R20, R21, R22 и R23, находилось в интервале от 0 до 13. Еще более предпочтительно, чтобы ароматическое моногидроксисоединение являлось ароматическим моногидроксисоединением, в котором группы R20, R21, R22 и R23 являются группами, имеющими от 0 до 9 углеродных атомов, которые выбирают из атомов водорода, линейных или разветвленных алкильных групп, циклоалкильных групп, замещенных или незамещенных арильных групп, линейных или разветвленных алкоксильных групп, замещенных или незамещенных арилоксильных групп и замещенных или незамещенных аралкильных групп.
Далее приводится объяснение активного ароматического моногидроксисоединения. Ароматическое гидроксисоединение, представленное упомянутой выше формулой (2), и/или формулой (7), и/или формулой (31), может предпочтительно использоваться в качестве ароматического гидроксисоединения, которое составляет ароматическую композицию, используемую в композиции для транспортировки и хранения соединения, имеющего уреидные группы. Кроме того, оно может также предпочтительно использоваться в качестве ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию, используемую в процессе получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидные группы, и/или N-замещенной карбаминовой кислоты-O-R2 эфира. Однако, последнее ароматическое гидроксисоединение, которое составляет ароматическую гидроксикомпозицию, используемую при получении N-замещенной карбаминовой кислоты-O-арилового эфира, является соединением, которое составляет группу -O-арилового эфира в N-замещенной карбаминовой кислоты-O-ариловом эфире, образующуюся в результате реакции с соединением, имеющим уреидные группы, и/или N-замещенной карбаминовой кислоты-O-R2 эфиром. В случае использования композиции для транспортировки и хранения соединения, имеющего уреидные группы, в качестве сырья для получения N-замещенной карбаминовой кислоты-O-арилового эфира, в случае получения N-замещенной карбаминовой кислоты-O-арилового эфира путем использования в качестве сырья соединения, имеющего уреидные группы, или при использовании в качестве сырья N-замещенной карбаминовой кислоты-O-R2 эфира с последующим получением N-замещенной карбаминовой кислоты-O-арилового эфира, несмотря на то, что ароматическое гидроксисоединение входит в объем упомянутой выше формулы (2), и/или формулы (7), и/или формулы (31), особенно предпочтительно использовать ароматическое гидроксисоединение, представленное следующей формулой (32) (ароматическое гидроксисоединение, представленное формулой (32), часто называют в настоящем описании "активным ароматическим гидроксисоединением", с точки зрения легкости протекания реакции). Активное ароматическое гидроксисоединение, представленное следующей формулой (32), может быть использовано само по себе в качестве ароматической гидроксикомпозиции, используемой в композиции для транспортировки и хранения соединения, имеющего уреидные группы, или может быть использовано в качестве одного типа ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию. Кроме того, ароматическое гидроксисоединение, представленное следующей формулой (32), может быть использовано само по себе в качестве ароматической гидроксикомпозиции для получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции с соединением, имеющим уреидные группы, и/или N-замещенной карбаминовой кислоты-O-R2 эфиром, или может быть использовано в качестве одного типа ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию. Разумеется, что в каждом из описанных выше случаев может также быть использовано множество активных ароматических гидроксисоединений, представленных следующей формулой (32).
Активное ароматическое моногидроксисоединение представлено следующей формулой (32):
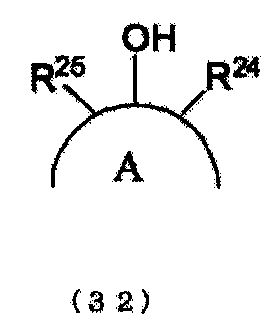
(где
кольцо A представляет органическую группу, которая содержит ароматическую группу, замещенную b раз гидроксильными группами в произвольных местах, которая сохраняет ароматические свойства, может быть одним или множеством гетероциклических колец и может быть замещена другими заместителями, и целое число от 1 до 6 OH групп, представленных формулой (32), замещены на ароматическом кольце, содержащемся в кольце A (а именно, формула (32) составляет часть кольца A, и на кольце A присутствуют целое число от 1 до 6 структур, к которым примыкают упомянутые выше группа R24, группа OH и группа R25, соответственно).
R24 и R25 являются группами, связанными с ароматическим кольцом, с которым связана гидроксильная группа и которые связаны с углеродным атомом, расположенным рядом с углеродным атомом, с которым связана гидроксигруппа. С кольцом A связано целое число от 1 до 6 гидроксигрупп, и, таким образом, с кольцом A связано целое число от 1 до 6 групп R24 и R25, соответственно. Ароматическое гидроксисоединение, представленное формулой (32), является ароматическим гидроксисоединением, которое содержит целое число углеродных атомов в интервале от 6 до 50.
Заместитель, который замещает ароматическую группу ароматического гидроксисоединения, представленного выше формулой (32) (группы R24 и R25 будут подробно объяснены далее) выбирают из группы, состоящей из атома водорода, атома галогена, алифатической группы, ароматической группы и алифатической группы, в которой связана ароматическая группа, и является группой, состоящей из ациклической углеводородной группы или циклической углеводородной группы (такой как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа, циклическая углеводородная группа, имеющая боковую цепь, гетероциклическая группа, гетероциклическая спирогруппа, гетеро-сшитая кольцевая группа или гетероциклическая группа), группой, связанной из одного или более типов групп, выбранных из упомянутых выше ациклических углеводородных групп и циклических углеводородных групп и групп, в которых упомянутые выше группы связаны с помощью ковалентной связи с конкретным атомом неметалла (углеродом, кислородом, азотом, серой или кремнием). Кроме того, ковалентная связь с конкретным описанным выше атомом неметалла (углеродом, кислородом, азотом, серой или кремнием) находится в состоянии, при котором упомянутые выше группы связаны ковалентной связью, например, с группами, представленными упомянутыми выше формулами (8)-(11) и (13)-(16).
Среди таких заместителей примеры заместителей, которые могут быть предпочтительно использованы в варианте настоящего осуществления, принимая во внимание меньшую склонность к протеканию побочных реакций, могут включать группы, выбранные из группы, состоящей из ациклических углеводородных групп и циклических углеводородных групп (таких как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа или циклическая углеводородная группа, имеющая боковую цепь), и группы, связанные по меньшей мере с одним типом группы, выбранной из этой группы (взаимно замещенные группы).
Кроме того, в случае транспортировки при высокой температуре композиции, содержащей соединение, имеющее уреидные группы, или в случае проведения при высокой температуре реакции для получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидные группы, и/или N-замещенной карбаминовой кислоты O-R2 эфира и ароматической гидроксикомпозиции, предпочтительно, чтобы кольцо A ароматического гидроксисоединения составляла группа, имеющая по меньшей мере один неактивный заместитель (включая атомы водорода), помимо ароматической группы и гидроксильной группы, связанной с ароматической группой (здесь, неактивный заместитель относится к группе, в которой неактивный заместитель не содержит ранее описанного активного водорода, несмотря на то, что он может иметь ароматическую гидроксильную группу).
Для более подробного объяснения заместителя, ароматическое гидроксисоединение, представленное формулой (32), является ароматическим гидроксисоединением, имеющим, помимо ароматической группы и гидроксильной группы, связанной с ароматической группой (R24 и R25 будут подробно объяснены далее), по меньшей мере один заместитель, выбранный из группы заместителей, описанных в следующих пунктах (i)-(v).
(i) атом водорода,
(ii) группа, состоящая из углеродных атомов и атомов водорода (которая может также образовывать конденсированную кольцевую структуру путем связывания с кольцом A),
(iii) группа, состоящая из углеродных атомов, атомов водорода и атомов кислорода (представляя, например, эфирную группу, состоящую из алифатических групп, эфирную группу, состоящую из ароматических групп, или эфирную группу, состоящую из алифатических групп и ароматических групп, но исключая группы, содержащие активный водород, такие как карбонильная группа, эфирная группа, терминальная метиновая группа и спиртовая OH группа, карбоксильная группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа),
(iv) атом галогена, и
(v) группа, состоящая из атомов, выбранных из углеродных атомов, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена (но исключая группы, содержащие активный водород, такие как карбонильная группа, эфирная группа, концевая метиновая группа и спиртовая OH группа, карбоксильная группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа).
R24 и R25 соответственно и независимо представляют любые из групп, определенных в следующих пунктах (i)-(v), и R24 и R25 могут дополнительно образовывать конденсированную кольцевую структуру путем связывания с кольцом A. Случаем связи между кольцом A и гидроксильной группой в упомянутой выше формуле (32), например, является структура, показанная в следующей формуле (33) или формуле (34), несмотря на то, что число групп R24 и R25, связанных с углеродом, находящимся рядом с OH группой, связанной с ароматической группой, которая составляет кольцо A, может часто не совпадать с числом OH групп в структуре, представленной следующей формулой (33), кольцо A может являться кольцевым фрагментом, показанным с правой стороны следующей формулы (35), в то время как R25 может образовывать кольцевую структуру путем связывания с кольцом A. В случае формулы (34), ароматическая гидроксильная группа, связанная с кольцом A, является центральной OH группой, в то время как расположенные рядом OH группы могут являться группами R24 и R25, соответственно:

(i) атом водорода,
(ii) группа, состоящая из углеродных атомов и атомов водорода (которая может также образовывать конденсированную кольцевую структуру путем связывания с кольцом A), в которой атом в α положении (атом, который образует R24 и R25, которые связаны с ароматическим кольцом кольца A) является углеродным атомом, и углеродный атом является первичным или вторичным углеродным атомом (а именно, представляя углеродный атом метильной группы или углеродный атом, который образует -CH2- связь), при условии, что в случае когда R24 и/или R25 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом A, и конденсированное кольцо имеет шесть членов или менее, углерод в α положении может являться третичным или четвертичным углеродным атомом как, например, в случае следующей формулы (36) или формулы (37), и в случае, когда углеродный атом в α положении образует двойную связь или тройную связь с атомом в β положении (находящимся рядом с атомом, который образует R24 и R25, который также связан с ароматическим кольцом кольца A), углерод в α положении может являться третичным или четвертичным углеродным атомом,
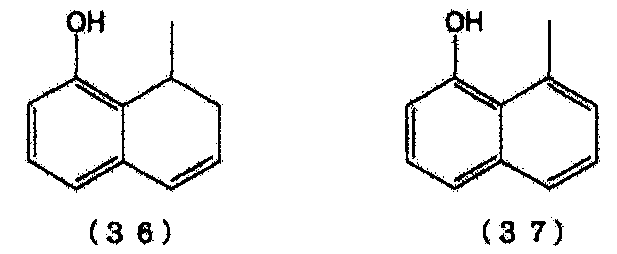
(iii) группа, состоящая из углеродных атомов, атомов водорода и атомов кислорода (представляя, например, эфирную группу, состоящую из алифатических групп, эфирную группу, состоящую из ароматических групп, эфирную группу, состоящую из алифатических групп и ароматических групп, но не имеющих спиртовых OH групп, карбонильную группу, эфирную группу, карбоксильную группу или метиновую группу на ее конце), в которой атом в α положении (атом, который образует R24 и R25, который связан с ароматическим кольцом кольца A) является углеродным атомом или атомом кислорода, и в случае углеродного атома, углеродный атом является первичным или вторичным углеродным атомом (а именно, углеродный атом метильной группы или углеродный атом, который образует -CH2- связь), при условии, что в случае когда R24 и/или R25 образует насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом A, и конденсированное кольцо имеет шесть членов или менее, углерод в α положении может являться третичным или четвертичным углеродным атомом, и в случае, когда углеродный атом в α положении также образует двойную связь или тройную связь с атомом в β положении (находящимся рядом с атомом, который образует R24 и R25, который связан с ароматическим кольцом кольца A), углерод в α положении может являться третичным или четвертичным углеродным атомом,
(iv) атом галогена,
(v) группа, состоящая из атомов, выбранных из углеродных атомов, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена (но исключая группы, содержащие активный водород, такие как спиртовая OH группа, карбонильная группа, эфирная группа, карбоксильная группа, концевая метиновая группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа), в которой атом в α положении (атом, который образует R24 и R25, который связан с ароматическим кольцом кольца A) является углеродным атомом, атомом кислорода или атомом серы, в случае углеродного атома, углеродный атом является первичным или вторичным углеродным атомом (а именно, углеродный атом метильной группы или углеродный атом, который образует -CH2-связь), и в случае атома серы, атом серы является атомом двухвалентной серы (а именно, атом серы, который образует -S-связь), при условии, что в случае, если R24 и/или R25 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом A и конденсированное кольцо имеет шесть членов или менее, углерод в α положении может являться третичным или четвертичным углеродным атомом, и в случае, если углеродный атом в α положении также образует двойную связь или тройную связь с атомом в β положении (находящимся рядом с атомом, который образует R24 и R25, который связан с ароматическим кольцом кольца A), углерод в α положении может являться третичным или четвертичным углеродным атомом.
При использовании термина "активный водород" активный водород относят к атому водорода, связанному с кислородом, серой или азотом. Однако, ароматические гидроксильные группы исключаются. Хотя ароматические гидроксильные группы (OH группы, непосредственно связанные с ароматической группой) также относятся к активному водороду, так как ароматические гидроксильные группы также содержатся в композиции варианта настоящего осуществления и исходном сырье для реакции и не обладают негативным воздействием, ароматические гидроксильные группы не включают в группы, содержащие активный водород, если специально не указано иное. "Группы, содержащие активный водород" часто встречаются и в других местах описания варианта настоящего осуществления, и к таким группам также применяется упомянутое выше определение. Такой активный водород является высоко реакционноспособным и реагирует с органическим первичным амином, соединением мочевины и другими подобными веществами, используемыми в варианте настоящего осуществления, так же, как и с соединениями, имеющими уреидные группы, N-замещенной карбаминовой кислоты-O-(R2 и ариловым)эфирами и другими подобными соединениями, образующимися в варианте настоящего осуществления, приводя к образованию побочных продуктов реакции, что является нежелательным.
Кроме того, предпочтительно, чтобы кольцо A являлось структурой, которая содержит по меньшей мере одну структуру, выбранную из группы, состоящей из бензольного кольца, нафталинового кольца и антраценового кольца. Принимая во внимание возможность использования в промышленности, предпочтительно, чтобы активное ароматическое гидроксисоединение, представленное упомянутой выше формулой (32), являлось ароматическим моногидроксисоединением, в котором одна или две ароматические гидроксильные группы связаны с кольцом A (а именно, b =1 или 2), и более предпочтительно, чтобы оно являлось ароматическим моногидроксисоединением, в котором одна ароматическая гидроксильная группа связана с кольцом A, так как в этом случае ароматические гидроксисоединения обычно имеют низкую вязкость.
Как было описано ранее, ароматическое гидроксисоединение, представленное формулой (2), (7), (31) или (32), образуется в качестве побочного продукта вместе с изоцианатом в процессе термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира при проведении стадии (F) (часто называемой стадией термического разложения, термическим разложением или процессом термического разложения). В одном аспекте варианта настоящего осуществления, в зависимости от случая, ароматическое гидроксисоединение и изоцианат разделяют путем ректификации после стадии термического разложения, и отделенное ароматическое гидроксисоединение может быть рециркулировано в виде ароматической гидроксикомпозиции варианта настоящего осуществления. Разделение проводят, используя в качестве индикатора стандартную температуру кипения, и метод выбирают в соответствии с ранее описанным определением.
Кроме того, принимая во внимание возможность использования в промышленности, предпочтительно, чтобы активное ароматическое гидроксисоединение являлось легко доступным ароматическим моногидроксисоединением. Предпочтительным примером такого ароматического моногидроксисоединения является ароматическое моногидроксисоединение, представленное следующей формулой (38):
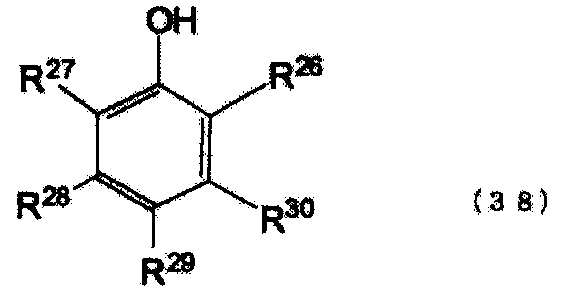
(где
R28, R29 и R30 являются группами, соответственно и независимо выбранными из упомянутых выше групп R7-R14 (исключая арильные группы, имеющие гидроксильную группу), группы R26 и R27 являются группами, соответственно и независимо выбранными из упомянутых выше групп R24 и R25, и ароматическое гидроксисоединение, представленное формулой (38), является ароматическим моногидроксисоединением, имеющим целое число от 6 до 50 углеродных атомов, при условии, что суммарное число углеродных атомов групп R26, R27, R28, R29 и R30 составляет целое число от 0 до 44, и R26 и R27 являются соответственно и независимо любой группой, определенной в следующих пунктах (i)-(iii).
R26 и R27 являются группами, соответственно и независимо выбранными из упомянутых выше групп R24 и R25, и являются соответственно и независимо любой группой, определенной в следующих пунктах (i)-(iii):
(i) атом водорода,
(ii) группа, состоящая из углеродных атомов и атомов водорода (которые могут также образовывать кольцевую структуру путем связывания с кольцом A), в которой атом в α положении (атом, который образует R26 и R27, который связан с ароматическим кольцом кольца A) является углеродным атомом, и углеродный атом является первичным или вторичным углеродным атомом (а именно, представляя углеродный атом метильной группы или углеродный атом, который образует -CH2-связь), при условии, что в случае R26 и/или R27 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с ароматическим кольцом и конденсированное кольцо имеет шесть членов или менее, углерод в α положении может являться третичным или четвертичным углеродным атомом как, например, в случае следующей формулы (36) или формулы (37), и в случае, если углеродный атом в α положении также образует двойную или тройную связь с атомом в β положении (расположенным рядом с атомом, который образует R26 и R27, который связан в ароматическим кольцом кольца A), углерод в α положении может являться третичным или четвертичным углеродным атомом,

(iii) группа, состоящая из углеродных атомов, атомов водорода и атомов кислорода (представляя, например, эфирную группу, состоящую из алифатических групп, эфирную группу, состоящую из ароматических групп, эфирную группу, состоящую из алифатических групп и ароматических групп, но не имеющих спиртовую OH группу, карбонильную группу, эфирную группу, карбоксильную группу или метиновую группу на ее конце), в которой атом в α положении (атом, который образует R26 и R27, который связан с ароматическим кольцом кольца A) является углеродным атомом или атомом кислорода, и в случае углеродного атома, углеродный атом является первичным или вторичным углеродным атомом (а именно, углеродный атом метильной группы или углеродный атом, который образует -CH2-связь), при условии, что в случае R26 и/или R27 образует насыщенную и/или ненасыщенную конденсированную кольцевую структуру и конденсированное кольцо имеет шесть членов или менее, углерод в α положении может являться третичным или четвертичным углеродным атомом, и в случае когда углеродный атом в α положении также образует двойную связь или тройную связь с атомом в β положении (находящимся рядом с атомом, который образует R26 и R27, который связан с ароматическим кольцом кольца A), углерод в α положении может являться третичным или четвертичным углеродным атомом.
Предпочтительными являются активные ароматические моногидроксисоединения, в которых R26 и R27 являются атомами водорода, и примеры таких ароматических моногидроксисоединений могут включать фенол, метилфенол (включая изомеры), этилфенол (включая изомеры), 2-н-пропилфенол (включая изомеры), 2-н-бутилфенол (включая изомеры), 2-н-пентилфенол (включая изомеры), 2-н-гексилфенол (включая изомеры), 2-н-гептилфенол (включая изомеры), 2-н-октилфенол (включая изомеры), 2-н-нонилфенол (включая изомеры), 2-н-децилфенол (включая изомеры), 2-н-додецилфенол (включая изомеры), 2-н-октадецилфенол (включая изомеры), 3-пропилфенол (включая изомеры), 3-бутилфенол (включая изомеры), 3-пентилфенол (включая изомеры), 3-гексилфенол (включая изомеры), 3-гептилфенол (включая изомеры), 3-октилфенол (включая изомеры), 3-нонилфенол (включая изомеры), 3-децилфенол (включая изомеры), 3-додецилфенол (включая изомеры), 3-октадецилфенол (включая изомеры), 4-пропилфенол (включая изомеры), 4-бутилфенол (включая изомеры), 4-пентилфенол (включая изомеры), 4-гексилфенол (включая изомеры), 4-гептилфенол (включая изомеры), 4-октилфенол (включая изомеры), 4-нонилфенол (включая изомеры), 4-децилфенол (включая изомеры), 4-додецилфенол (включая изомеры), 4-октадецилфенол (включая изомеры), диметилфенол (включая изомеры), диэтилфенол (включая изомеры), ди(н-пропил)фенол (включая изомеры), ди(н-бутил)фенол (включая изомеры), ди(н-пентил)фенол (включая изомеры), ди(н-гексил)фенол (включая изомеры), ди(н-гептил)фенол (включая изомеры), ди(н-октил)фенол (включая изомеры), ди(н-нонил)фенол (включая изомеры), ди(н-децил)фенол (включая изомеры), ди(н-додецил)фенол (включая изомеры), ди(н-октадецил)фенол (включая изомеры), триметилфенол (включая изомеры), триэтилфенол (включая изомеры), три(н-пропил)фенол (включая изомеры), три(н-бутил)фенол (включая изомеры), три(н-пентил)фенол (включая изомеры), три(н-гексил)фенол (включая изомеры), три(н-гептил)фенол (включая изомеры), три(н-октил)фенол (включая изомеры), три(н-нонил)фенол (включая изомеры), три(н-децил)фенол (включая изомеры), три(н-додецил)фенол (включая изомеры), три(н-октадецил)фенол (включая изомеры), (метоксиметил)фенол, (этоксиметил)фенол, (пропоксиметил)фенол (включая изомеры), (бутилоксиметил)фенол (включая изомеры), (пентилоксиметил)фенол (включая изомеры), (гексилоксиметил)фенол (включая изомеры), (гептилоксиметил)фенол (включая изомеры), (октилоксиметил)фенол (включая изомеры), (нонилоксиметил)фенол (включая изомеры), (децилоксиметил)фенол (включая изомеры), (додецилоксиметил)фенол (включая изомеры), (октадецилоксиметил)фенол (включая изомеры), (циклопентилоксиметил)фенол, (циклогексилоксиметил)фенол, (циклогептилоксиметил)фенол, (циклооктилоксиметил)фенол, (метилциклопентилоксиметил)фенол (включая изомеры), (этилциклопентилоксиметил)фенол (включая изомеры), (метилциклогексилоксиметил)фенол (включая изомеры), (этилциклогексилоксиметил)фенол (включая изомеры), (пропилциклогексилоксиметил)фенол (включая изомеры), (бутилциклогексилоксиметил)фенол (включая изомеры), (пентилциклогексилоксиметил)фенол (включая изомеры), (гексилциклогексилоксиметил)фенол (включая изомеры), (диметилциклогексилоксиметил)фенол (включая изомеры), (диэтилциклогексилоксиметил)фенол (включая изомеры), (дибутилциклогексилоксиметил)фенол (включая изомеры), (феноксиметил)фенол, (метилфеноксиметил)фенол (включая изомеры), (этилфеноксиметил)фенол (включая изомеры), (пропилфеноксиметил)фенол (включая изомеры), (бутилфеноксиметил)фенол (включая изомеры), (пентилфеноксиметил)фенол (включая изомеры), (гексилфеноксиметил)фенол (включая изомеры), (гептилфеноксиметил)фенол (включая изомеры), (октилфеноксиметил)фенол (включая изомеры), (нонилфеноксиметил)фенол (включая изомеры), (децилфеноксиметил)фенол (включая изомеры), (фенилфеноксиметил)фенол (включая изомеры), (диметилфеноксиметил)фенол (включая изомеры), (диэтилфеноксиметил)фенол (включая изомеры), (дипропилфеноксиметил)фенол (включая изомеры), (дибутилфеноксиметил)фенол (включая изомеры), (дипентилфеноксиметил)фенол (включая изомеры), (дигексилфеноксиметил)фенол (включая изомеры), (дигептилфеноксиметил)фенол (включая изомеры), (дифенилфеноксиметил)фенол (включая изомеры), (триметилфеноксиметил)фенол (включая изомеры), (триэтилфеноксиметил)фенол (включая изомеры), (трипропилфеноксиметил)фенол (включая изомеры), (трибутилфеноксиметил)фенол (включая изомеры), (фенилметоксиметил)фенол (включая изомеры), (фенилэтоксиметил)фенол (включая изомеры), (фенилпропилоксиметил)фенол (включая изомеры), (фенилбутилоксиметил)фенол (включая изомеры), (фенилпентилоксиметил)фенол (включая изомеры), (фенилгексилоксиметил)фенол (включая изомеры), (фенилгептилоксиметил)фенол (включая изомеры), (фенилоктилоксиметил)фенол (включая изомеры), (фенилнонилоксиметил)фенол (включая изомеры), ди(метоксиметил)фенол, ди(этоксиметил)фенол, ди(пропоксиметил)фенол (включая изомеры), ди(бутилоксиметил)фенол (включая изомеры), ди(пентилоксиметил)фенол (включая изомеры), ди(гексилоксиметил)фенол (включая изомеры), ди(гептилоксиметил)фенол (включая изомеры), ди(октилоксиметил)фенол (включая изомеры), ди(нонилоксиметил)фенол (включая изомеры), ди(децилоксиметил)фенол (включая изомеры), ди(додецилоксиметил)фенол (включая изомеры), ди(октадецилоксиметил)фенол (включая изомеры), ди(циклопентилоксиметил)фенол (включая изомеры), ди(циклогексилоксиметил)фенол (включая изомеры), ди(циклогептилоксиметил)фенол (включая изомеры), ди(циклооктилоксиметил)фенол (включая изомеры), ди(метилциклопентилоксиметил)фенол (включая изомеры), ди(этилциклопентилоксиметил)фенол (включая изомеры), ди(метилциклогексилоксиметил)фенол (включая изомеры), ди(этилциклогексилоксиметил)фенол (включая изомеры), ди(пропилциклогексилоксиметил)фенол (включая изомеры), ди(бутилциклогексилоксиметил)фенол (включая изомеры), ди(пентилциклогексилоксиметил)фенол (включая изомеры), ди(гексилциклогексилоксиметил)фенол (включая изомеры), бис(диметилциклогексилоксиметил)фенол (включая изомеры), бис(диэтилциклогексилоксиметил)фенол (включая изомеры), бис(дибутилциклогексилоксиметил)фенол (включая изомеры), ди(феноксиметил)фенол, ди(метилфеноксиметил)фенол (включая изомеры), ди(этилфеноксиметил)фенол (включая изомеры), ди(пропилфеноксиметил)фенол (включая изомеры), ди(бутилфеноксиметил)фенол (включая изомеры), ди(пентилфеноксиметил)фенол (включая изомеры), ди(гексилфеноксиметил)фенол (включая изомеры), ди(гептилфеноксиметил)фенол (включая изомеры), ди(октилфеноксиметил)фенол (включая изомеры), ди(нонилфеноксиметил)фенол (включая изомеры), ди(децилфеноксиметил)фенол (включая изомеры), ди(фенилфеноксиметил)фенол (включая изомеры), бис(диметилфеноксиметил)фенол (включая изомеры), бис(диэтилфеноксиметил)фенол (включая изомеры), бис(дипропилфеноксиметил)фенол (включая изомеры), бис(дибутилфеноксиметил)фенол (включая изомеры), бис(дипентилфеноксиметил)фенол (включая изомеры), бис(дигексилфеноксиметил)фенол (включая изомеры), бис(дигептилфеноксиметил)фенол (включая изомеры), бис(дифенилфеноксиметил)фенол (включая изомеры), ди(триметилфеноксиметил)фенол (включая изомеры), ди(триэтилфеноксиметил)фенол (включая изомеры), ди(трипропилфеноксиметил)фенол (включая изомеры), ди(трибутилфеноксиметил)фенол (включая изомеры), (фенилметоксиметил)фенол, ди(фенилэтоксиметил)фенол (включая изомеры), ди(фенилпропилоксиметил)фенол (включая изомеры), ди(фенилбутилоксиметил)фенол (включая изомеры), ди(фенилпентилоксиметил)фенол (включая изомеры), ди(фенилгексилоксиметил)фенол (включая изомеры), ди(фенилгептилоксиметил)фенол (включая изомеры), ди(фенилоктилоксиметил)фенол (включая изомеры), ди(фенилнонилоксиметил)фенол (включая изомеры), три(метоксиметил)фенол, три(этоксиметил)фенол, три(пропоксиметил)фенол (включая изомеры), три(бутилоксиметил)фенол (включая изомеры), три(пентилоксиметил)фенол (включая изомеры), три(гексилоксиметил)фенол (включая изомеры), три(гептилоксиметил)фенол (включая изомеры), три(октилоксиметил)фенол (включая изомеры), три(нонилоксиметил)фенол (включая изомеры), три(децилоксиметил)фенол (включая изомеры), три(додецилоксиметил)фенол (включая изомеры), три(октадецилоксиметил)фенол (включая изомеры), три(циклопентилоксиметил)фенол (включая изомеры), три(циклогексилоксиметил)фенол (включая изомеры), три(циклогептилоксиметил)фенол (включая изомеры), три(циклооктилоксиметил)фенол (включая изомеры), три(метилциклопентилоксиметил)фенол (включая изомеры), три(этилциклопентилоксиметил)фенол (включая изомеры), три(метилциклогексилоксиметил)фенол (включая изомеры), три(этилциклогексилоксиметил)фенол (включая изомеры), три(пропилциклогексилоксиметил)фенол (включая изомеры), три(бутилциклогексилоксиметил)фенол (включая изомеры), три(пентилциклогексилоксиметил)фенол (включая изомеры), три(гексилциклогексилоксиметил)фенол (включая изомеры), бис(диметилциклогексилоксиметил)фенол (включая изомеры), бис(диэтилциклогексилоксиметил)фенол (включая изомеры), бис(дибутилциклогексилоксиметил)фенол (включая изомеры), три(феноксиметил)фенол, три(метилфеноксиметил)фенол (включая изомеры), три(этилфеноксиметил)фенол (включая изомеры), три(пропилфеноксиметил)фенол (включая изомеры), три(бутилфеноксиметил)фенол (включая изомеры), три(пентилфеноксиметил)фенол (включая изомеры), три(гексилфеноксиметил)фенол (включая изомеры), три(гептилфеноксиметил)фенол (включая изомеры), три(октилфеноксиметил)фенол (включая изомеры), три(нонилфеноксиметил)фенол (включая изомеры), три(децилфеноксиметил)фенол (включая изомеры), три(фенилфеноксиметил)фенол (включая изомеры), бис(диметилфеноксиметил)фенол (включая изомеры), бис(диэтилфеноксиметил)фенол (включая изомеры), бис(дипропилфеноксиметил)фенол (включая изомеры), бис(дибутилфеноксиметил)фенол (включая изомеры), бис(дипентилфеноксиметил)фенол (включая изомеры), бис(дигексилфеноксиметил)фенол (включая изомеры), бис(дигептилфеноксиметил)фенол (включая изомеры), бис(дифенилфеноксиметил)фенол (включая изомеры), три(триметилфеноксиметил)фенол (включая изомеры), три(триэтилфеноксиметил)фенол (включая изомеры), три(трипропилфеноксиметил)фенол (включая изомеры), три(трибутилфеноксиметил)фенол (включая изомеры), три(фенилметоксиметил)фенол, три(фенилэтоксиметил)фенол (включая изомеры), три(фенилпропилоксиметил)фенол (включая изомеры), три(фенилбутилоксиметил)фенол (включая изомеры), три(фенилпентилоксиметил)фенол (включая изомеры), три(фенилгексилоксиметил)фенол (включая изомеры), три(фенилгептилоксиметил)фенол (включая изомеры), три(фенилоктилоксиметил)фенол (включая изомеры), три(фенилнонилоксиметил)фенол (включая изомеры), (фенилметил)фенол (включая изомеры), ((метилфенил)метил)фенол (включая изомеры), ((этилфенил)метил)фенол (включая изомеры), ((пропилфенил)метил)фенол (включая изомеры), ((бутилфенил)метил)фенол (включая изомеры), ((пентилфенил)метил)фенол (включая изомеры), ((гексилфенил)метил)фенол (включая изомеры), ((гептилфенил)метил)фенол (включая изомеры), ((октилфенил)метил)фенол (включая изомеры), ((нонилфенил)метил)фенол (включая изомеры), ((децилфенил)метил)фенол (включая изомеры), ((бифенил)метил)фенол (включая изомеры), ((диметилфенил)метил)фенол (включая изомеры), ((диэтилфенил)метил)фенол (включая изомеры), ((дипропилфенил)метил)фенол (включая изомеры), ((дибутилфенил)метил)фенол (включая изомеры), ((дипентилфенил)метил)фенол (включая изомеры), ((дигексилфенил)метил)фенол (включая изомеры), ((дигептилфенил)метил)фенол (включая изомеры), ((терфенил)метил)фенол (включая изомеры), ((триметилфенил)метил)фенол (включая изомеры), ((триэтилфенил)метил)фенол (включая изомеры), ((трипропилфенил)метил)фенол (включая изомеры), ((трибутилфенил)метил)фенол (включая изомеры), ди(фенилметил)фенол (включая изомеры), ди((метилфенил)метил)фенол (включая изомеры), ди((этилфенил)метил)фенол (включая изомеры), ди((пропилфенил)метил)фенол (включая изомеры), ди((бутилфенил)метил)фенол (включая изомеры), ди((пентилфенил)метил)фенол (включая изомеры), ди((гексилфенил)метил)фенол (включая изомеры), ди((гептилфенил)метил)фенол (включая изомеры), ди((октилфенил)метил)фенол (включая изомеры), ди((нонилфенил)метил)фенол (включая изомеры), ди((децилфенил)метил)фенол (включая изомеры), ди((бифенил)метил)фенол (включая изомеры), ди((диметилфенил)метил)фенол (включая изомеры), ди((диэтилфенил)метил)фенол (включая изомеры), ди((дипропилфенил)метил)фенол (включая изомеры), ди((дибутилфенил)метил)фенол (включая изомеры), ди((дипентилфенил)метил)фенол (включая изомеры), ди((дигексилфенил)метил)фенол (включая изомеры), ди((дигептилфенил)метил)фенол (включая изомеры), ди((терфенил)метил)фенол (включая изомеры), ди((триметилфенил)метил)фенол (включая изомеры), ди((триэтилфенил)метил)фенол (включая изомеры), ди((трипропилфенил)метил)фенол (включая изомеры), ди((трибутилфенил)метил)фенол (включая изомеры), три(фенилметил)фенол (включая изомеры), три((метилфенил)метил)фенол (включая изомеры), три((этилфенил)метил)фенол (включая изомеры), три((пропилфенил)метил)фенол (включая изомеры), три((бутилфенил)метил)фенол (включая изомеры), три((пентилфенил)метил)фенол (включая изомеры), три((гексилфенил)метил)фенол (включая изомеры), три((гептилфенил)метил)фенол (включая изомеры), три((октилфенил)метил)фенол (включая изомеры), три((нонилфенил)метил)фенол (включая изомеры), три((децилфенил)метил)фенол (включая изомеры), три((бифенил)метил)фенол (включая изомеры), три((диметилфенил)метил)фенол (включая изомеры), три((диэтилфенил)метил)фенол (включая изомеры), три((дипропилфенил)метил)фенол (включая изомеры), три((дибутилфенил)метил)фенол (включая изомеры), три((дипентилфенил)метил)фенол (включая изомеры), три((дигексилфенил)метил)фенол (включая изомеры), три((дигептилфенил)метил)фенол (включая изомеры), три((терфенил)метил)фенол (включая изомеры), три((триметилфенил)метил)фенол (включая изомеры), три((триэтилфенил)метил)фенол (включая изомеры), три((трипропилфенил)метил)фенол (включая изомеры), три((трибутилфенил)метил)фенол (включая изомеры), фенилэтилфенол (включая изомеры), фенил-н-пропилфенол (включая изомеры), фенил-н-бутилфенол (включая изомеры), фенил-н-пентилфенол (включая изомеры), фенил-н-гексилфенол (включая изомеры), фенил-н-гептилфенол (включая изомеры), фенил-н-октилфенол (включая изомеры), фенил-н-нонилфенол (включая изомеры), метоксифенол (включая изомеры), этоксифенол (включая изомеры), пропилоксифенол (включая изомеры), бутилоксифенол (включая изомеры), пентилоксифенол (включая изомеры), гексилоксифенол (включая изомеры), гептилоксифенол (включая изомеры), октилоксифенол (включая изомеры), нонилоксифенол (включая изомеры), децилоксифенол (включая изомеры), додецилоксифенол (включая изомеры), октадецилоксифенол (включая изомеры), циклопентилоксифенол (включая изомеры), циклогексилоксифенол (включая изомеры), циклогептилоксифенол (включая изомеры), циклооктилоксифенол (включая изомеры), (метилциклопентилокси)фенол (включая изомеры), (этилциклопентилокси)фенол (включая изомеры), (метилциклогексилокси)фенол (включая изомеры), (этилциклогексилокси)фенол (включая изомеры), (пропилциклогексилокси)фенол (включая изомеры), (бутилциклогексилокси)фенол (включая изомеры), (пентилциклогексилокси)фенол (включая изомеры), (гексилциклогексилокси)фенол (включая изомеры), (диметилциклогексилокси)фенол (включая изомеры), (диэтилциклогексилокси)фенол (включая изомеры), (дибутилциклогексилокси)фенол (включая изомеры), фенилоксифенол, (метилфенилокси)фенол (включая изомеры), (этилфенилокси)фенол (включая изомеры), (пропилфенилокси)фенол (включая изомеры), (бутилфенилокси)фенол (включая изомеры), (пентилфенилокси)фенол (включая изомеры), (гексилфенилокси)фенол (включая изомеры), (гептилфенилокси)фенол (включая изомеры), (октилфенилокси)фенол (включая изомеры), (нонилфенилокси)фенол (включая изомеры), (децилфенилокси)фенол (включая изомеры), бифенилоксифенол (включая изомеры), (диметилфенилокси)фенол (включая изомеры), (диэтилфенилокси)фенол (включая изомеры), (дипропилфенилокси)фенол (включая изомеры), (дибутилфенилокси)фенол (включая изомеры), (дипентилфенилокси)фенол (включая изомеры), (дигексилфенилокси)фенол (включая изомеры), (дигептилфенилокси)фенол (включая изомеры), терфенилоксифенол (включая изомеры), (триметилфенилокси)фенол (включая изомеры), (триэтилфенилокси)фенол (включая изомеры), (трипропилфенилокси)фенол (включая изомеры), (трибутилфенилокси)фенол (включая изомеры), (фенилметилокси)фенол, (фенилэтилокси)фенол (включая изомеры), (фенилпропилокси)фенол (включая изомеры), (фенилбутилокси)фенол (включая изомеры), (фенилпентилокси)фенол (включая изомеры), (фенилгексилокси)фенол (включая изомеры), (фенилгептилокси)фенол (включая изомеры), (фенилоктилокси)фенол (включая изомеры), (фенилнонилокси)фенол (включая изомеры), диметоксифенол (включая изомеры), диэтоксифенол (включая изомеры), дипропилоксифенол (включая изомеры), дибутилоксифенол (включая изомеры), дипентилоксифенол (включая изомеры), дигексилоксифенол (включая изомеры), дигептилоксифенол (включая изомеры), диоктилоксифенол (включая изомеры), динонилоксифенол (включая изомеры), дидецилоксифенол (включая изомеры), дидодецилоксифенол (включая изомеры), диоктадецилоксифенол (включая изомеры), дициклопентилоксифенол (включая изомеры), дициклогексилоксифенол (включая изомеры), дициклогептилоксифенол (включая изомеры), дициклооктилоксифенол (включая изомеры), ди(метилциклопентилокси)фенол (включая изомеры), ди(этилциклопентилокси)фенол (включая изомеры), ди(метилциклогексилокси)фенол (включая изомеры), ди(этилциклогексилокси)фенол (включая изомеры), ди(пропилциклогексилокси)фенол (включая изомеры), ди(бутилциклогексилокси)фенол (включая изомеры), ди(пентилциклогексилокси)фенол (включая изомеры), ди(гексилциклогексилокси)фенол (включая изомеры), бис(диметилциклогексилокси)фенол (включая изомеры), бис(диэтилциклогексилокси)фенол (включая изомеры), бис(дибутилциклогексилокси)фенол (включая изомеры), фенилоксифенол, ди(метилфенилокси)фенол (включая изомеры), ди(этилфенилокси)фенол (включая изомеры), ди(пропилфенилокси)фенол (включая изомеры), ди(бутилфенилокси)фенол (включая изомеры), ди(пентилфенилокси)фенол (включая изомеры), ди(гексилфенилокси)фенол (включая изомеры), ди(гептилфенилокси)фенол (включая изомеры), ди(октилфенилокси)фенол (включая изомеры), ди(нонилфенилокси)фенол (включая изомеры), ди(децилфенилокси)фенол (включая изомеры), дибифенилоксифенол (включая изомеры), бис(диметилфенилокси)фенол (включая изомеры), бис(диэтилфенилокси)фенол (включая изомеры), бис(дипропилфенилокси)фенол (включая изомеры), бис(дибутилфенилокси)фенол (включая изомеры), бис(дипентилфенилокси)фенол (включая изомеры), бис(дигексилфенилокси)фенол (включая изомеры), бис(дигептилфенилокси)фенол (включая изомеры), дитерфенилоксифенол (включая изомеры), ди(триметилфенилокси)фенол (включая изомеры), ди(триэтилфенилокси)фенол (включая изомеры), ди(трипропилфенилокси)фенол (включая изомеры), ди(трибутилфенилокси)фенол (включая изомеры), (фенилметилокси)фенол, ди(фенилэтилокси)фенол (включая изомеры), ди(фенилпропилокси)фенол (включая изомеры), ди(фенилбутилокси)фенол (включая изомеры), ди(фенилпентилокси)фенол (включая изомеры), ди(фенилгексилокси)фенол (включая изомеры), ди(фенилгептилокси)фенол (включая изомеры), ди(фенилоктилокси)фенол (включая изомеры), ди(фенилнонилокси)фенол (включая изомеры), триметоксифенол (включая изомеры), триэтоксифенол (включая изомеры), трипропилоксифенол (включая изомеры), трибутилоксифенол (включая изомеры), трипентилоксифенол (включая изомеры), тригексилоксифенол (включая изомеры), тригептилоксифенол (включая изомеры), триоктилоксифенол (включая изомеры), тринонилоксифенол (включая изомеры), тридецилоксифенол (включая изомеры), тридодецилоксифенол (включая изомеры), триоктадецилоксифенол (включая изомеры), трициклопентилоксифенол (включая изомеры), трициклогексилоксифенол (включая изомеры), трициклогептилоксифенол (включая изомеры), трициклооктилоксифенол (включая изомеры), три(метилциклопентилокси)фенол (включая изомеры), три(этилциклопентилокси)фенол (включая изомеры), три(метилциклогексилокси)фенол (включая изомеры), три(этилциклогексилокси)фенол (включая изомеры), три(пропилциклогексилокси)фенол (включая изомеры), три(бутилциклогексилокси)фенол (включая изомеры), три(пентилциклогексилокси)фенол (включая изомеры), три(гексилциклогексилокси)фенол (включая изомеры), три(диметилциклогексилокси)фенол (включая изомеры), три(диэтилциклогексилокси)фенол (включая изомеры), три(дибутилциклогексилокси)фенол (включая изомеры), фенилоксифенол, три(метилфенилокси)фенол (включая изомеры), три(этилфенилокси)фенол (включая изомеры), три(пропилфенилокси)фенол (включая изомеры), три(бутилфенилокси)фенол (включая изомеры), три(пентилфенилокси)фенол (включая изомеры), три(гексилфенилокси)фенол (включая изомеры), три(гептилфенилокси)фенол (включая изомеры), три(октилфенилокси)фенол (включая изомеры), три(нонилфенилокси)фенол (включая изомеры), три(децилфенилокси)фенол (включая изомеры), трибифенилоксифенол (включая изомеры), три(диметилфенилокси)фенол (включая изомеры), три(диэтилфенилокси)фенол (включая изомеры), три(дипропилфенилокси)фенол (включая изомеры), три(дибутилфенилокси)фенол (включая изомеры), три(дипентилфенилокси)фенол (включая изомеры), три(дигексилфенилокси)фенол (включая изомеры), три(дигептилфенилокси)фенол (включая изомеры), тритерфенилоксифенол (включая изомеры), три(триметилфенилокси)фенол (включая изомеры), три(триэтилфенилокси)фенол (включая изомеры), три(трипропилфенилокси)фенол (включая изомеры), три(трибутилфенилокси)фенол (включая изомеры), (фенилметилокси)фенол, три(фенилэтилокси)фенол (включая изомеры), три(фенилпропилокси)фенол (включая изомеры), три(фенилбутилокси)фенол (включая изомеры), три(фенилпентилокси)фенол (включая изомеры), три(фенилгексилокси)фенол (включая изомеры), три(фенилгептилокси)фенол (включая изомеры), три(фенилоктилокси)фенол (включая изомеры), три(фенилнонилокси)фенол (включая изомеры), нафтол (включая изомеры), феноксифенол (включая изомеры), и дифеноксифенол (включая изомеры). Особенно предпочтительные примеры включают ароматические моногидроксисоединения, в которых R26 и R27 являются атомами водорода, в то время как другими заместителями являются линейные и/или циклические насыщенные алкильные группы, нафтол (включая изомеры), феноксифенол (включая изомеры) и дифеноксифенол (включая изомеры).
Как уже было описано ранее, с точки зрения реакционной способности в реакции между соединением, имеющим уреидные группы, и/или N-замещенной карбаминовой кислоты-O-R2 эфиром и ароматической гидроксикомпозицией (а именно, в реакции этерификации или реакции переэтерификации) предпочтительно использовать ароматическое гидроксисоединение, имеющее конкретную структуру.
С другой стороны, авторы настоящего изобретения обнаружили, что в случае, когда группа, связанная с атомом в α положении заместителя по меньшей мере в одном орто-положении ароматического гидроксисоединения, является объемным заместителем, скорость образования N-замещенной карбаминовой кислоты-O-арилового эфира значительно снижается. Более конкретно, это относится к ароматическому гидроксисоединению, где заместитель, в котором атом в α положении является третичным или четвертичным углеродным атомом или атомом третичного азота, связан по меньшей мере с одним орто-положением относительно гидроксильной группы ароматического гидроксисоединения. Проявление такого эффекта ароматическим гидроксисоединением также не обнаружено в известном уровне техники. Далее, ароматическое гидроксисоединение, для которого является низкой скорость образования N-замещенной карбаминовой кислоты-O-Ar эфира, часто называется ароматическим гидроксисоединением с низкой активностью.
Более того, в результате придания большого значения тому факту, что скорость образования N-замещенной карбаминовой кислоты-O-арилового эфира различается в зависимости от типа описанного выше ароматического гидроксисоединения, авторы настоящего изобретения придумали и осуществили способ получения N-замещенной карбаминовой кислоты-O-арилового эфира, в котором используют ароматическую гидроксикомпозицию, содержащую множество типов ароматических гидроксисоединений.
Объясняемое ниже ароматическое гидроксисоединение является ароматическим гидроксисоединением с низкой активностью, которое используют в способе получения N-замещенной карбаминовой кислоты-O-арилового эфира, в котором используют ароматическую гидроксикомпозицию, содержащую множество типов ароматических гидроксисоединений, и в котором используют ароматическую гидроксикомпозицию, которая содержит активное ароматическое гидроксисоединение и гидроксисоединение с низкой активностью. А именно, способом получения является способ получения N-замещенной карбаминовой кислоты-O-эфира, в котором используют ароматическую гидроксикомпозицию, содержащую ароматическое гидроксисоединение, имеющее высокую скорость образования указанного выше N-замещенной карбаминовой кислоты-O-арилового эфира (упомянутое выше активное ароматическое гидроксисоединение), и ароматическое гидроксисоединение, имеющее низкую скорость образования N-замещенной карбаминовой кислоты-O-эфира (часто называемое ароматическим гидроксисоединением с низкой активностью).
Описанное выше ароматическое гидроксисоединение с низкой активностью представлено следующей формулой (39):
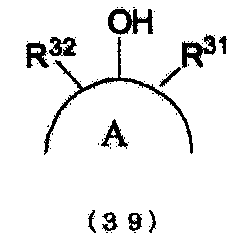
(где
кольцо А представляет органическую группу, которая содержит ароматическую группу, замещенную b раз гидроксильными группами в произвольных местах, которая сохраняет ароматические свойства, может являться одним или множеством гетероциклических колец и может быть замещена другими заместителями, и целое число от 1 до 6 OH групп, представленных формулой (39), замещены на ароматическом кольце, содержащемся в кольце А (а именно, формула (39) составляет часть кольца А, и целое число от 1 до 6 структур, с которыми упомянутая выше группа R31, группа OH и группа R32 находятся рядом, соответственно присутствуют на кольце А).
R31 и R32 являются группами, которые замещают ароматическое кольцо, с которым связана гидроксильная группа, и которые связаны с углеродным атомом, расположенным рядом с углеродным атомом, с которым связана гидроксильная группа. Целое число от 1 до 6 гидроксильных групп связаны с кольцом А, и, таким образом, максимальное целое число от 1 до 6 групп R31 и R32 соответственно связаны с кольцом А. Ароматическое гидроксисоединение, представленное формулой (39), является ароматическим гидроксисоединением, которое содержит суммарно целое число углеродных атомов в интервале от 6 до 50.
Примеры заместителей, которые замещают ароматическую группу ароматического гидроксисоединения, представленного выше формулой (39) (группы R31 и R32 будут подробно объяснены далее), могут включать группы, выбранные из атома водорода, атома галогена, алифатической группы и ароматической группы, которая состоит из ациклической углеводородной группы или циклической углеводородной группы (такой как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа, циклическая углеводородная группа, имеющая боковую цепь, гетероциклическая группа, гетероциклическая спирогруппа, гетеро-сшитая кольцевая группа или гетероциклическая группа), группы, связанной с одним или более типов групп, выбранных из упомянутых выше ациклических углеводородных групп и циклических углеводородных групп, и групп, в которых упомянутые выше группы связаны с помощью ковалентной связи с конкретным атомом неметалла (углеродом, кислородом, азотом, серой или кремнием). Кроме того, описанная выше ковалентная связь с конкретным атомом неметалла (углеродом, кислородом, азотом, серой или кремнием) находится в состоянии, в котором упомянутые выше группы связаны ковалентной связью, например, с группами, представленными упомянутыми выше формулами (8)-(11) и (13)-(16).
Среди этих заместителей, примеры заместителей, которые могут быть предпочтительно использованы в варианте настоящего осуществления, принимая во внимание меньшую склонность к протеканию побочных реакций, включают группы, выбранные из группы, состоящей из ациклических углеводородных групп и циклических углеводородных групп (таких как моноциклическая углеводородная группа, конденсированная полициклическая углеводородная группа, сшитая циклическая углеводородная группа, спироуглеводородная группа, связывающая в кольцо углеводородная группа или циклическая углеводородная группа, имеющая боковую цепь), и группы, связанные по меньшей мере с одним типом группы, выбранной из этой группы (взаимно замещенные группы).
Кроме того, в случае транспортировки при высокой температуре композиции, содержащей соединение, имеющее уреидные группы, или в случае реакции при высокой температуре соединения, имеющего уреидные группы, и/или N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции с получением N-замещенной карбаминовой кислоты-O-арилового эфира, предпочтительно, чтобы кольцо А ароматического гидроксисоединения являлось ароматическим гидроксисоединением, состоящим из группы, имеющей по меньшей мере один неактивный заместитель (включая атомы водорода) помимо ароматической группы и гидроксигрупп, связанных с ароматической группой (здесь неактивный заместитель относится к группе, в которой неактивный заместитель не содержит описанный выше активный водород, несмотря на то, что эта группа может иметь ароматическую гидроксильную группу).
Для более подробного объяснения заместителя, ароматическое гидроксисоединение, представленное формулой (39), является ароматическим гидроксисоединением, имеющим по меньшей мере один заместитель, выбранный из групп заместителей, объясняемых в следующих пунктах (i)-(v), помимо ароматической группы и гидроксигруппы, связанной с ароматической группой (группы R31 и R32 будут подробно объяснены далее):
(i) атом водорода,
(ii) группа, состоящая из углеродных атомов и атомов водорода (которая может также образовывать кольцевую структуру путем связывания с кольцом А),
(iii) группа, состоящая из углеродных атомов, атомов водорода и атомов кислорода (представляющая, например, эфирную группу, состоящую из алифатических групп, эфирную группу, состоящую из ароматических групп или эфирную группу, состоящую из алифатических групп и ароматических групп, но исключая группы, содержащие активный водород, такие как карбонильная группа, эфирная группа, концевая метиновая группа и спиртовая OH группа, карбоксильная группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа),
(iv) атом галогена, и
(v) группа, состоящая из атомов, выбранных из углеродных атомов, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена (но исключая группы, содержащие активный водород, такие как карбонильная группа, эфирная группа, концевая метиновая группа и спиртовая OH группа, карбоксильная группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа).
R31 и R32 соответственно и независимо представляют любую из групп, представленных в пунктах (i)-(viii), по меньшей мере одна из которых является группой, определенной в следующих пунктах (vi)-(viii), и R31 и R32 могут дополнительно образовывать конденсированную кольцевую структуру путем связывания с кольцом А. Для зависимости между кольцом А и гидроксильной группой в упомянутой выше формуле (39), например, во многих случаях число групп R31 и R32, связанных с углеродом, расположенным рядом с OH группой, не совпадает с числом OH групп (объясненных в упомянутой выше формуле (32)), и такие случаи являются допустимыми, при условии, что либо R31, либо R32 является группой, определенной в следующих пунктах (vi)-(viii):
(i) атом водорода,
(ii) группа, состоящая из углеродных атомов и атомов водорода (которая может также образовывать кольцевую структуру путем связывания с кольцом А), в которой атом в α положении (атом, который образует R31 и R32, который связан с ароматическим кольцом кольца А) является углеродным атомом, и углеродный атом является первичным или вторичным углеродным атомом (а именно, представляющим углеродный атом метильной группы или углеродный атом, который образует -CH2-связь), при условии, что в случае, если R31 и/или R31 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом А и конденсированное кольцо имеет шесть членов или менее, углерод в α положении может являться третичным или четвертичным углеродным атомом, и в случае, когда углеродный атом в α положении также образует двойную или тройную связь с атомом в β положении (расположенным рядом с атомом, который образует R31 и R32, который связан с ароматическим кольцом кольца А), углерод в α положении может являться третичным или четвертичным углеродным атомом,
(iii) группа, состоящая из углеродных атомов, атомов водорода и атомов кислорода (представляющая, например, эфирную группу, состоящую из алифатических групп, эфирную группу, состоящую из ароматических групп, или эфирную группу, состоящую из алифатических групп и ароматических групп, но не имеющих спиртовой OH группы, карбонильной группы, эфирной группы, карбоксильной группы или метиновой группы на их конце), в которой атом в α положении (атом, который образует R31 и R32, который связан с ароматическим кольцом кольца А) является углеродным атомом или атомом кислорода, и в случае углеродного атома, углеродный атом является первичным или вторичным углеродным атомом (а именно, углеродным атомом метильной группы или углеродным атомом, который образует -CH2-связь), при условии, что в случае, когда R31 или R32 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом А и конденсированное кольцо имеет шесть членов или менее, углерод в α положении может являться третичным или четвертичным углеродным атомом, и в случае, когда углеродный атом в α положении также образует двойную или тройную связь с атомом в β положении (расположенным рядом с атомом, который образует R31 и R32, который связан с ароматическим кольцом кольца А), углерод в α положении может являться третичным или четвертичным углеродным атомом,
(iv) атом галогена,
(v) группа, состоящая из атомов, выбранных из углеродных атомов, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена (но исключая группы, содержащие активный водород, такие как спиртовая OH группа, карбонильная группа, эфирная группа, карбоксильная группа, концевая метиновая группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа), в которой атом в α положении (атом, который образует R31 и R32, который связан с ароматическим кольцом кольца А) является углеродным атомом, атомом кислорода или атомом серы, в случае углеродного атома, углеродный атом является первичным или вторичным углеродным атомом (а именно, углеродным атомом метильной группы или углеродным атомом, который образует -CH2-связь), и в случае атома серы, атом серы является атомом двухвалентной серы (а именно, атомом серы, который образует -S-связь), при условии, что в случае R31 или R32 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом А, и конденсированное кольцо имеет шесть членов или менее, углерод в α положении может являться третичным или четвертичным углеродным атомом, и в случае, если углеродный атом в α положении также образует двойную или тройную связь с атомом в β положении (расположенным рядом с атомом, который образует R31 и R32, который связан с ароматическим кольцом кольца А), углерод в α положении может являться третичным или четвертичным углеродным атомом,
(vi) группа, состоящая из углеродных атомов и атомов водорода (которые могут также образовывать кольцевую структуру путем связывания с кольцом А), в которой атом в α положении (атом, который образует R31 и R32, который связан с ароматическим кольцом кольца А) является углеродным атомом, и углеродный атом является третичным или четвертичным углеродным атомом (а именно, углеродным атомом, который образует -CH-связь или углеродным атомом, не связанным с помощью водорода), при условии, что в случае R31 и/или R31 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом А, конденсированное кольцо может иметь семь членов или более, и в случае, если углеродный атом в α положении образует двойную связь с атомом в β положении (расположенным рядом с атомом, который образует R31 и R32, который связан с ароматическим кольцом кольца А), углерод в α положении может являться четвертичным углеродным атомом, но исключая углерод в α положении, образующий тройную связь с атомом в β положении,
(vii) группа, состоящая из углеродных атомов, атомов водорода и атомов кислорода (представляющая, например, эфирную группу, состоящую из алифатических групп, эфирную группу, состоящую из ароматических групп, или эфирную группу, состоящую из алифатических групп и ароматических групп, но не имеющую спиртовую OH группу, карбонильную группу, эфирную группу, карбоксильную группу или метиновую группу на ее конце), в которой атом в α положении (атом, который образует R31 и R32, который связан с ароматическим кольцом кольца А) является углеродным атомом, и углеродный атом является третичным или четвертичным углеродным атомом (а именно, углеродным атомом, который образует -CH-связь, или углеродным атомом, не связанным с помощью водорода), при условии, что в случае, когда R31 и/или R32 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом А, конденсированное кольцо может иметь семь членов или более, и в случае, когда углеродный атом в α положении образует двойную связь с атомом в β положении (расположенным рядом с атомом, который образует R31 и R32, который связан с ароматическим кольцом кольца А), углерод в α положении может являться четвертичным углеродным атомом, но исключая углерод в α положении, образующий тройную связь с атомом в β положении, и
(viii) группа, состоящая из атомов, выбранных из углеродных атомов, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена (но исключая группы, содержащие активный водород, такие как спиртовая OH группа, карбонильная группа, эфирная группа, карбоксильная группа, концевая метиновая группа, NH2 группа, NH группа, NOH группа, SH группа, SO3H группа или SOH группа), в которой атом в α положении (атом, который образует R31 и R32, который связан с ароматическим кольцом кольца А) является углеродным атомом или атомом азота, в случае углеродного атома, углеродный атом является третичным или четвертичным углеродным атомом (а именно, углеродным атомом, который образует -CH-связь, или углеродным атомом, не связанным с помощью водорода), при условии, что в случае, если R31 и/или R32 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом А, конденсированное кольцо может иметь семь членов или более, и в случае, если углеродный атом в α положении образует двойную связь с атомом в β положении (расположенным рядом с атомом, который образует R31 и R32, который связан с ароматическим кольцом кольца А), углерод в α положении может являться четвертичным углеродным атомом, но исключая углерод в α положении, образующий тройную связь с атомом в β положении, в то время как в случае атома азота, атом азота может являться третичным атомом азота, которые образует связь с атомом в β положении с помощью одинарной связи.
Кроме того, предпочтительно, чтобы кольцо А являлось структурой, которая содержит по меньшей мере одну структуру, выбранную из группы, состоящей из бензольного кольца, нафталинового кольца и антраценового кольца. Принимая во внимание возможность использования в промышленности, предпочтительно, чтобы неактивное ароматическое гидроксисоединение, представленное упомянутой выше формулой (39), являлось ароматическим моногидроксисоединением, в котором одна или две ароматических гидроксильных группы связаны с кольцом А (а именно, b =1 или 2), и более предпочтительно, являлось ароматическим моногидроксисоединением, в котором одна ароматическая гидроксильная группа связана с кольцом А, так как такие ароматические гидроксисоединения обычно имеют низкую вязкость.
Несмотря на то, что объяснение способа использования неактивного ароматического гидроксисоединения варианта настоящего осуществления будет приведено позже, тем не менее, в одном аспекте варианта настоящего осуществления ароматическое гидроксисоединение и изоцианат разделяют путем ректификации, и отделенное ароматическое гидроксисоединение может быть рециркулировано в виде ароматической гидроксикомпозиции, которая реагирует с соединением, имеющим уреидные группы. Разделение проводят на основе использования в качестве индикатора стандартной температуры кипения, и способ выбирают в соответствии с ранее описанным определением.
Кроме того, когда упомянутое выше активное ароматическое гидроксисоединение и неактивное ароматическое гидроксисоединение используют в качестве ароматической гидроксикомпозиции, несмотря на то, что легко разделить и очистить два компонента, если ароматическое гидроксисоединение выбирают так, что существует соотношение, при котором стандартная температура кипения активного ароматического гидроксисоединения составляет 10°C или выше, чем стандартная температура кипения неактивного ароматического гидроксисоединения, но, тем не менее, этого не требуется. В случае использования множества активных ароматических гидроксисоединений и множества неактивных ароматических гидроксисоединений, ароматические гидроксисоединения выбирают так, чтобы существовало соотношение, при котором стандартная температура кипения активного ароматического гидроксисоединения, имеющего самую низкую стандартную температуру кипения, была выше на 10°C или более, чем стандартная температура кипения неактивного ароматического гидроксисоединения, имеющего самую высокую стандартную температуру кипения. С точки зрения проведения разделения и очистки, число типов использования активных и малоактивных ароматических гидроксисоединений должно быть как можно меньшим, и, например, предпочтительно использовать только по одному из каждого типа ароматических гидроксисоединений.
Более того, принимая во внимание возможность использования в промышленности, предпочтительно, чтобы неактивным ароматическим гидроксисоединением являлось легко доступное ароматическое моногидроксисоединение. Предпочтительным примером такого ароматического моногидроксисоединения является ароматическое моногидроксисоединение, представленное следующей формулой (40):
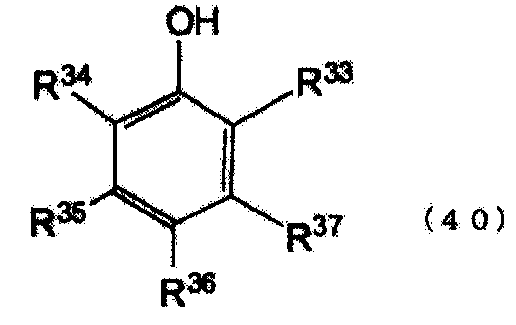
(где
R35, R36 и R37 являются группами, соответственно и независимо выбранными из упомянутых выше групп R7-R14 (исключая арильные группы, имеющие гидроксигруппу), группы R33 и R34 являются группами, соответственно и независимо выбранными из упомянутых выше групп R31 и R32, и ароматическое гидроксисоединение, представленное формулой (40), является ароматическим моногидроксисоединением, имеющим целое число от 6 до 50 углеродных атомов, при условии что суммарное число углеродных атомов групп R33, R34, R35, R36 и R37 составляет целое число от 0 до 44, и R33 и R34 являются соответственно и независимо любой группой, определенной в следующих пунктах (i)-(ii):
(i) группа, состоящая из углеродных атомов и атомов водорода (которые могут также образовывать кольцевую структуру путем связывания с кольцом А), в которой атом в α положении (атом, который образует R33 и R34, который связан с ароматическим кольцом кольца А) является углеродным атомом, и углеродный атом является третичным или четвертичным углеродным атомом (а именно, углеродным атомом, который образует -CH-связь, или углеродным атомом, не связанным с помощью водорода), при условии, что в случае, когда R33 и/или R34 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом А, конденсированное кольцо может иметь семь членов или более, и в случае, когда углеродный атом в α положении образует двойную связь с атомом в β положении (расположенным рядом с атомом, который образует R33 и R34, который связан с ароматическим кольцом кольца А), углерод в α положении может являться четвертичным углеродным атомом, но исключая углерод в α положении, образующий тройную связь с атомом в β положении, и
(ii) группа, состоящая из углеродных атомов, атомов водорода и атомов кислорода (представляющая, например, эфирную группу, состоящую из алифатических групп, эфирную группу, состоящую из ароматических групп, или эфирную группу, состоящую из алифатических групп и ароматических групп, но не имеющих спиртовой OH группы, карбонильной группы, эфирной группы, карбоксильной группы или метиновой группы на ее конце), в которой атом в α положении (атом, который образует R33 и R34, который связан с ароматическим кольцом кольца А) является углеродным атомом, и углеродный атом является третичным или четвертичным углеродным атомом (а именно, углеродным атомом, который образует -CH-связь, или углеродным атомом, не связанным с помощью водорода), при условии, что в случае, когда R33 и/или R34 образуют насыщенную и/или ненасыщенную конденсированную кольцевую структуру с кольцом А, конденсированное кольцо может иметь семь членов или более, и в случае, когда углеродный атом в α положении образует двойную связь с атомом в β положении (расположенным рядом с атомом, который образует R33 и R34, который связан с ароматическим кольцом кольца А), углерод в α положении может являться четвертичным углеродным атомом, но исключая углерод в α положении, образующий тройную связь с атомом в β положении.
Предпочтительные примеры таких ароматических моногидроксисоединений, представленных формулой (40), могут включать 2-трет-пропилфенол (включая изомеры), 2-трет-бутилфенол (включая изомеры), 2-трет-пентилфенол (включая изомеры), 2-трет-гексилфенол (включая изомеры), 2-трет-гептилфенол (включая изомеры), 2-трет-октилфенол (включая изомеры), 2-трет-нонилфенол (включая изомеры), 2-трет-децилфенол (включая изомеры), 2-трет-додецилфенол (включая изомеры), 2-трет-октадецилфенол (включая изомеры), 2-втор-пропилфенол (включая изомеры), 2-втор-бутилфенол (включая изомеры), 2-втор-пентилфенол (включая изомеры), 2-втор-гексилфенол (включая изомеры), 2-втор-гептилфенол (включая изомеры), 2-втор-октилфенол (включая изомеры), 2-втор-нонилфенол (включая изомеры), 2-втор-децилфенол (включая изомеры), 2-втор-додецилфенол (включая изомеры), 2-втор-октадецилфенол (включая изомеры), 2,4-ди-трет-пропилфенол (включая изомеры), 2,4-ди-трет-бутилфенол (включая изомеры), 2,4-ди-трет-пентилфенол (включая изомеры), 2,4-ди-трет-гексилфенол (включая изомеры), 2,4-ди-трет-гептилфенол (включая изомеры), 2,4-ди-трет-октилфенол (включая изомеры), 2,4-ди-трет-нонилфенол (включая изомеры), 2,4-ди-трет-децилфенол (включая изомеры), 2,4-ди-трет-додецилфенол (включая изомеры), 2,4-ди-трет-октадецилфенол (включая изомеры), 2,4-ди-втор-пропилфенол (включая изомеры), 2,4-ди-втор-бутилфенол (включая изомеры), 2,4-ди-втор-пентилфенол (включая изомеры), 2,4-ди-втор-гексилфенол (включая изомеры), 2,4-ди-втор-гептилфенол (включая изомеры), 2,4-ди-втор-октилфенол (включая изомеры), 2,4-ди-втор-нонилфенол (включая изомеры), 2,4-ди-втор-децилфенол (включая изомеры), 2,4-ди-втор-додецилфенол (включая изомеры), 2,4-ди-втор-октадецилфенол (включая изомеры), 2,6-ди-трет-пропилфенол (включая изомеры), 2,6-ди-трет-бутилфенол (включая изомеры), 2,6-ди-трет-пентилфенол (включая изомеры), 2,6-ди-трет-гексилфенол (включая изомеры), 2,6-ди-трет-гептилфенол (включая изомеры), 2,6-ди-трет-октилфенол (включая изомеры), 2,6-ди-трет-нонилфенол (включая изомеры), 2,6-ди-трет-децилфенол (включая изомеры), 2,6-ди-трет-додецилфенол (включая изомеры), 2,6-ди-трет-октадецилфенол (включая изомеры), 2,6-ди-втор-пропилфенол (включая изомеры), 2,6-ди-втор-бутилфенол (включая изомеры), 2,6-ди-втор-пентилфенол (включая изомеры), 2,6-ди-втор-гексилфенол (включая изомеры), 2,6-ди-втор-гептилфенол (включая изомеры), 2,6-ди-втор-октилфенол (включая изомеры), 2,6-ди-втор-нонилфенол (включая изомеры), 2,6-ди-втор-децилфенол (включая изомеры), 2,6-ди-втор-додецилфенол (включая изомеры), 2,6-ди-втор-октадецилфенол (включая изомеры), 2,4,6-три-трет-пропилфенол (включая изомеры), 2,4,6-три-трет-бутилфенол (включая изомеры), 2,4,6-три-трет-пентилфенол (включая изомеры), 2,4,6-три-трет-гексилфенол (включая изомеры), 2,4,6-три-трет-гептилфенол (включая изомеры), 2,4,6-три-трет-октилфенол (включая изомеры), 2,4,6-три-трет-нонилфенол (включая изомеры), 2,4,6-три-трет-децилфенол (включая изомеры), 2,4,6-три-трет-додецилфенол (включая изомеры), 2,4,6-три-трет-октадецилфенол (включая изомеры), 2,4,6-три-втор-пропилфенол (включая изомеры), 2,4,6-три-втор-бутилфенол (включая изомеры), 2,4,6-три-втор-пентилфенол (включая изомеры), 2,4,6-три-втор-гексилфенол (включая изомеры), 2,4,6-три-втор-гептилфенол (включая изомеры), 2,4,6-три-втор-октилфенол (включая изомеры), 2,4,6-три-втор-нонилфенол (включая изомеры), 2,4,6-три-втор-децилфенол (включая изомеры), 2,4,6-три-втор-додецилфенол (включая изомеры), 2,4,6-три-втор-октадецилфенол (включая изомеры), (2-метокси-2-метилэтил)фенол, (2-этокси-2-метилэтил)фенол, (2-пропокси-2-метилэтил)фенол (включая изомеры), (2-бутилокси-2-метилэтил)фенол (включая изомеры), (2-пентилокси-2-метилэтил)фенол (включая изомеры), (2-гексилокси-2-метилэтил)фенол (включая изомеры), (2-гептилокси-2-метилэтил)фенол (включая изомеры), (2-октилокси-2-метилэтил)фенол (включая изомеры), (2-нонилокси-2-метилэтил)фенол (включая изомеры), (2-децилокси-2-метилэтил)фенол (включая изомеры), (2-додецилокси-2-метилэтил)фенол (включая изомеры), (2-октадецилокси-2-метилэтил)фенол (включая изомеры), (2-циклопентилокси-2-метилэтил)фенол (включая изомеры), (2-циклогексилокси-2-метилэтил)фенол (включая изомеры), (2-циклогептилокси-2-метилэтил)фенол (включая изомеры), (2-циклооктилокси-2-метилэтил)фенол (включая изомеры), (2-(метилциклопентилокси)-2-метилэтил)фенол (включая изомеры), (2-(этилциклопентилокси)-2-метилэтил)фенол (включая изомеры), (2-(метилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-(этилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-(пропилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-(бутилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-(пентилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-(гексилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-(диметилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-(диэтилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-(дибутилциклогексилокси)-2-метилэтил)фенол (включая изомеры), (2-фенокси-2-метилэтил)фенол (включая изомеры), (2-(метилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(этилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(пропилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(бутилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(пентилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(гексилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(гептилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(октилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(нонилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(децилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(диметилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(диэтилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(дипропилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(дибутилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(дипентилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(дигексилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(дигептилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(дифенилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(триметилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(триэтилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(трипропилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(трибутилфенокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилметокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилэтокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилпропилокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилбутилокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилпентилокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилгексилокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилгептилокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилоктилокси)-2-метилэтил)фенол (включая изомеры), (2-(фенилнонилокси)-2-метилэтил)фенол (включая изомеры), (2-метокси-2-метилпропил)фенол, (2-этокси-2-метилпропил)фенол, (2-пропокси-2-метилпропил)фенол (включая изомеры), (2-бутилокси-2-метилпропил)фенол (включая изомеры), (2-пентилокси-2-метилпропил)фенол (включая изомеры), (2-гексилокси-2-метилпропил)фенол (включая изомеры), (2-гептилокси-2-метилпропил)фенол (включая изомеры), (2-октилокси-2-метилпропил)фенол (включая изомеры), (2-нонилокси-2-метилпропил)фенол (включая изомеры), (2-децилокси-2-метилпропил)фенол (включая изомеры), (2-додецилокси-2-метилпропил)фенол (включая изомеры), (2-октадецилокси-2-метилпропил)фенол (включая изомеры), (2-циклопентилокси-2-метилпропил)фенол (включая изомеры), (2-циклогексилокси-2-метилпропил)фенол (включая изомеры), (2-циклогептилокси-2-метилпропил)фенол (включая изомеры), (2-циклооктилокси-2-метилпропил)фенол (включая изомеры), (2-(метилциклопентилокси)-2-метилпропил)фенол (включая изомеры), (2-(этилциклопентилокси)-2-метилпропил)фенол (включая изомеры), (2-(метилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-(этилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-(пропилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-(бутилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-(пентилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-(гексилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-(диметилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-(диэтилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-(дибутилциклогексилокси)-2-метилпропил)фенол (включая изомеры), (2-фенокси-2-метилпропил)фенол (включая изомеры), (2-(метилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(этилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(пропилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(бутилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(пентилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(гексилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(гептилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(октилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(нонилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(децилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(диметилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(диэтилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(дипропилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(дибутилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(дипентилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(дигексилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(дигептилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(дифенилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(триметилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(триэтилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(трипропилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(трибутилфенокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилметокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилэтокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилпропилокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилбутилокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилпентилокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилгексилокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилгептилокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилоктилокси)-2-метилпропил)фенол (включая изомеры), (2-(фенилнонилокси)-2-метилпропил)фенол (включая изомеры), ди(2-метокси-2-метилэтил)фенол (включая изомеры), ди(2-этокси-2-метилэтил)фенол (включая изомеры), ди(2-пропокси-2-метилэтил)фенол (включая изомеры), ди(2-бутилокси-2-метилэтил)фенол (включая изомеры), ди(2-пентилокси-2-метилэтил)фенол (включая изомеры), ди(2-гексилокси-2-метилэтил)фенол (включая изомеры), ди(2-гептилокси-2-метилэтил)фенол (включая изомеры), ди(2-октилокси-2-метилэтил)фенол (включая изомеры), ди(2-нонилокси-2-метилэтил)фенол (включая изомеры), ди(2-децилокси-2-метилэтил)фенол (включая изомеры), ди(2-додецилокси-2-метилэтил)фенол (включая изомеры), ди(2-октадецилокси-2-метилэтил)фенол (включая изомеры), ди(2-циклопентилокси-2-метилэтил)фенол (включая изомеры), ди(2-циклогексилокси-2-метилэтил)фенол (включая изомеры), ди(2-циклогептилокси-2-метилэтил)фенол (включая изомеры), ди(2-циклооктилокси-2-метилэтил)фенол (включая изомеры), ди(2-(метилциклопентилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(этилциклопентилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(метилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(этилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(пропилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(бутилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(пентилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(гексилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(диметилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(диэтилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(дибутилциклогексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-фенокси-2-метилэтил)фенол (включая изомеры), ди(2-(метилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(этилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(пропилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(бутилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(пентилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(гексилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(гептилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(октилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(нонилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(децилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(диметилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(диэтилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(дипропилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(дибутилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(дипентилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(дигексилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(дигептилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(дифенилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(триметилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(триэтилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(трипропилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(трибутилфенокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилметокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилэтокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилпропилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилбутилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилпентилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилгексилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилгептилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилоктилокси)-2-метилэтил)фенол (включая изомеры), ди(2-(фенилнонилокси)-2-метилэтил)фенол (включая изомеры), ди(2-метокси-2-метилпропил)фенол (включая изомеры), ди(2-этокси-2-метилпропил)фенол (включая изомеры), ди(2-пропокси-2-метилпропил)фенол (включая изомеры), ди(2-бутилокси-2-метилпропил)фенол (включая изомеры), ди(2-пентилокси-2-метилпропил)фенол (включая изомеры), ди(2-гексилокси-2-метилпропил)фенол (включая изомеры), ди(2-гептилокси-2-метилпропил)фенол (включая изомеры), ди(2-октилокси-2-метилпропил)фенол (включая изомеры), ди(2-нонилокси-2-метилпропил)фенол (включая изомеры), ди(2-децилокси-2-метилпропил)фенол (включая изомеры), ди(2-додецилокси-2-метилпропил)фенол (включая изомеры), ди(2-октадецилокси-2-метилпропил)фенол (включая изомеры), ди(2-циклопентилокси-2-метилпропил)фенол (включая изомеры), ди(2-циклогексилокси-2-метилпропил)фенол (включая изомеры), ди(2-циклогептилокси-2-метилпропил)фенол (включая изомеры), ди(2-циклооктилокси-2-метилпропил)фенол (включая изомеры), ди(2-(метилциклопентилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(этилциклопентилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(метилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(этилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(пропилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(бутилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(пентилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(гексилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(диметилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(диэтилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(дибутилциклогексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-фенокси-2-метилпропил)фенол (включая изомеры), ди(2-(метилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(этилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(пропилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(бутилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(пентилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(гексилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(гептилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(октилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(нонилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(децилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(диметилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(диэтилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(дипропилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(дибутилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(дипентилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(дигексилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(дигептилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(дифенилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(триметилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(триэтилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(трипропилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(трибутилфенокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилметокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилэтокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилпропилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилбутилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилпентилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилгексилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилгептилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилоктилокси)-2-метилпропил)фенол (включая изомеры), ди(2-(фенилнонилокси)-2-метилпропил)фенол (включая изомеры), три(2-метокси-2-метилэтил)фенол (включая изомеры), три(2-этокси-2-метилэтил)фенол (включая изомеры), три(2-пропокси-2-метилэтил)фенол (включая изомеры), три(2-бутилокси-2-метилэтил)фенол (включая изомеры), три(2-пентилокси-2-метилэтил)фенол (включая изомеры), три(2-гексилокси-2-метилэтил)фенол (включая изомеры), три(2-гептилокси-2-метилэтил)фенол (включая изомеры), три(2-октилокси-2-метилэтил)фенол (включая изомеры), три(2-нонилокси-2-метилэтил)фенол (включая изомеры), три(2-децилокси-2-метилэтил)фенол (включая изомеры), три(2-додецилокси-2-метилэтил)фенол (включая изомеры), три(2-октадецилокси-2-метилэтил)фенол (включая изомеры), три(2-циклопентилокси-2-метилэтил)фенол (включая изомеры), три(2-циклогексилокси-2-метилэтил)фенол (включая изомеры), три(2-циклогептилокси-2-метилэтил)фенол (включая изомеры), три(2-циклооктилокси-2-метилэтил)фенол (включая изомеры), три(2-(метилциклопентилокси)-2-метилэтил)фенол (включая изомеры), три(2-(этилциклопентилокси)-2-метилэтил)фенол (включая изомеры), три(2-(метилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(этилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(пропилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(бутилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(пентилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(гексилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(триметилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(триэтилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(трибутилциклогексилокси)-2-метилэтил)фенол (включая изомеры), три(2-фенокси-2-метилэтил)фенол (включая изомеры), три(2-(метилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(этилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(пропилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(бутилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(пентилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(гексилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(гептилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(октилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(нонилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(децилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(триметилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(триэтилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(трипропилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(трибутилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(трипентилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(тригексилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(тригептилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(трифенилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(триметилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(триэтилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(трипропилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(трибутилфенокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилметокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилэтокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилпропилокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилбутилокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилпентилокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилгексилокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилгептилокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилоктилокси)-2-метилэтил)фенол (включая изомеры), три(2-(фенилнонилокси)-2-метилэтил)фенол (включая изомеры), три(2-метокси-2-метилпропил)фенол (включая изомеры), три(2-этокси-2-метилпропил)фенол (включая изомеры), три(2-пропокси-2-метилпропил)фенол (включая изомеры), три(2-бутилокси-2-метилпропил)фенол (включая изомеры), три(2-пентилокси-2-метилпропил)фенол (включая изомеры), три(2-гексилокси-2-метилпропил)фенол (включая изомеры), три(2-гептилокси-2-метилпропил)фенол (включая изомеры), три(2-октилокси-2-метилпропил)фенол (включая изомеры), три(2-нонилокси-2-метилпропил)фенол (включая изомеры), три(2-децилокси-2-метилпропил)фенол (включая изомеры), три(2-додецилокси-2-метилпропил)фенол (включая изомеры), три(2-октадецилокси-2-метилпропил)фенол (включая изомеры), три(2-циклопентилокси-2-метилпропил)фенол (включая изомеры), три(2-циклогексилокси-2-метилпропил)фенол (включая изомеры), три(2-циклогептилокси-2-метилпропил)фенол (включая изомеры), три(2-циклооктилокси-2-метилпропил)фенол (включая изомеры), три(2-(метилциклопентилокси)-2-метилпропил)фенол (включая изомеры), три(2-(этилциклопентилокси)-2-метилпропил)фенол (включая изомеры), три(2-(метилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(этилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(пропилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(бутилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(пентилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(гексилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(триметилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(триэтилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(трибутилциклогексилокси)-2-метилпропил)фенол (включая изомеры), три(2-фенокси-2-метилпропил)фенол (включая изомеры), три(2-(метилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(этилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(пропилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(бутилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(пентилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(гексилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(гептилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(октилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(нонилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(децилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(триметилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(триэтилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(трипропилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(трибутилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(трипентилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(тригексилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(тригептилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(трифенилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(триметилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(триэтилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(трипропилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(трибутилфенокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилметокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилэтокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилпропилокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилбутилокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилпентилокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилгексилокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилгептилокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилоктилокси)-2-метилпропил)фенол (включая изомеры), три(2-(фенилнонилокси)-2-метилпропил)фенол (включая изомеры), (диметиламино)фенол, (диэтиламино)фенол, (дипропиламино)фенол (включая изомеры), (дибутиламино)фенол (включая изомеры), (дипентиламино)фенол (включая изомеры), (дигексиламино)фенол (включая изомеры), (дигептиламино)фенол (включая изомеры), (диоктиламино)фенол (включая изомеры), (динониламино)фенол (включая изомеры), (дидециламино)фенол (включая изомеры), (дидодециламино)фенол (включая изомеры), (диоктадециламино)фенол (включая изомеры), (2-фенилизопропил)фенол (включая изомеры), (2-(метилфенил)изопропил)фенол (включая изомеры), (2-(этилфенил)изопропил)фенол (включая изомеры), (2-(пропилфенил)изопропил)фенол (включая изомеры), (2-(бутилфенил)изопропил)фенол (включая изомеры), (2-(пентилфенил)изопропил)фенол (включая изомеры), (2-(гексилфенил)изопропил)фенол (включая изомеры), (2-(гептилфенил)изопропил)фенол (включая изомеры), (2-(октилфенил)изопропил)фенол (включая изомеры), (2-(нонилфенил)изопропил)фенол (включая изомеры), (2-(децилфенил)изопропил)фенол (включая изомеры), (2-(бифенил)изопропил)фенол (включая изомеры), (2-(диметилфенил)изопропил)фенол (включая изомеры), (2-(диэтилфенил)изопропил)фенол (включая изомеры), (2-(дипропилфенил)изопропил)фенол (включая изомеры), (2-(дибутилфенил)изопропил)фенол (включая изомеры), (2-(дипентилфенил)изопропил)фенол (включая изомеры), (2-(дигексилфенил)изопропил)фенол (включая изомеры), (2-(дигептилфенил)изопропил)фенол (включая изомеры), (2-(терфенил)изопропил)фенол, (2-(триметилфенил)изопропил)фенол (включая изомеры), (2-(триэтилфенил)изопропил)фенол (включая изомеры), (2-(трипропилфенил)изопропил)фенол (включая изомеры), (2-(трибутилфенил)изопропил)фенол (включая изомеры), ди(2-фенилизопропил)фенол (включая изомеры), ди(2-(метилфенил)изопропил)фенол (включая изомеры), ди(2-(этилфенил)изопропил)фенол (включая изомеры), ди(2-(пропилфенил)изопропил)фенол (включая изомеры), ди(2-(бутилфенил)изопропил)фенол (включая изомеры), ди(2-(пентилфенил)изопропил)фенол (включая изомеры), ди(2-(гексилфенил)изопропил)фенол (включая изомеры), ди(2-(гептилфенил)изопропил)фенол (включая изомеры), ди(2-(октилфенил)изопропил)фенол (включая изомеры), ди(2-(нонилфенил)изопропил)фенол (включая изомеры), ди(2-(децилфенил)изопропил)фенол (включая изомеры), ди(2-(бифенил)изопропил)фенол (включая изомеры), ди(2-(диметилфенил)изопропил)фенол (включая изомеры), ди(2-(диэтилфенил)изопропил)фенол (включая изомеры), ди(2-(дипропилфенил)изопропил)фенол (включая изомеры), ди(2-(дибутилфенил)изопропил)фенол (включая изомеры), ди(2-(дипентилфенил)изопропил)фенол (включая изомеры), ди(2-(дигексилфенил)изопропил)фенол (включая изомеры), ди(2-(дигептилфенил)изопропил)фенол (включая изомеры), ди(2-(терфенил)изопропил)фенол, ди(2-(триметилфенил)изопропил)фенол (включая изомеры), ди(2-(триэтилфенил)изопропил)фенол (включая изомеры), ди(2-(трипропилфенил)изопропил)фенол (включая изомеры), ди(2-(трибутилфенил)изопропил)фенол (включая изомеры), три(2-фенилизопропил)фенол (включая изомеры), три(2-(метилфенил)изопропил)фенол (включая изомеры), три(2-(этилфенил)изопропил)фенол (включая изомеры), три(2-(пропилфенил)изопропил)фенол (включая изомеры), три(2-(бутилфенил)изопропил)фенол (включая изомеры), три(2-(пентилфенил)изопропил)фенол (включая изомеры), три(2-(гексилфенил)изопропил)фенол (включая изомеры), три(2-(гептилфенил)изопропил)фенол (включая изомеры), три(2-(октилфенил)изопропил)фенол (включая изомеры), три(2-(нонилфенил)изопропил)фенол (включая изомеры), три(2-(децилфенил)изопропил)фенол (включая изомеры), три(2-(бифенил)изопропил)фенол (включая изомеры), три(2-(диметилфенил)изопропил)фенол (включая изомеры), три(2-(диэтилфенил)изопропил)фенол (включая изомеры), три(2-(дипропилфенил)изопропил)фенол (включая изомеры), три(2-(дибутилфенил)изопропил)фенол (включая изомеры), три(2-(дипентилфенил)изопропил)фенол (включая изомеры), три(2-(дигексилфенил)изопропил)фенол (включая изомеры), три(2-(дигептилфенил)изопропил)фенол (включая изомеры), три(2-(терфенил)изопропил)фенол, три(2-(триметилфенил)изопропил)фенол (включая изомеры), три(2-(триэтилфенил)изопропил)фенол (включая изомеры), три(2-(трипропилфенил)изопропил)фенол (включая изомеры), три(2-(трибутилфенил)изопропил)фенол (включая изомеры), (2-фенил-втор-бутил)фенол (включая изомеры), (2-(метилфенил)-втор-бутил)фенол (включая изомеры), (2-(этилфенил)-втор-бутил)фенол (включая изомеры), (2-(пропилфенил)-втор-бутил)фенол (включая изомеры), (2-(бутилфенил)-втор-бутил)фенол (включая изомеры), (2-(пентилфенил)-втор-бутил)фенол (включая изомеры), (2-(гексилфенил)-втор-бутил)фенол (включая изомеры), (2-(гептилфенил)-втор-бутил)фенол (включая изомеры), (2-(октилфенил)-втор-бутил)фенол (включая изомеры), (2-(нонилфенил)-втор-бутил)фенол (включая изомеры), (2-(децилфенил)-втор-бутил)фенол (включая изомеры), (2-(бифенил)-втор-бутил)фенол (включая изомеры), (2-(диметилфенил)-втор-бутил)фенол (включая изомеры), (2-(диэтилфенил)-втор-бутил)фенол (включая изомеры), (2-(дипропилфенил)-втор-бутил)фенол (включая изомеры), (2-(дибутилфенил)-втор-бутил)фенол (включая изомеры), (2-(дипентилфенил)-втор-бутил)фенол (включая изомеры), (2-(дигексилфенил)-втор-бутил)фенол (включая изомеры), (2-(дигептилфенил)-втор-бутил)фенол (включая изомеры), (2-(терфенил)-втор-бутил)фенол, (2-(триметилфенил)-втор-бутил)фенол (включая изомеры), (2-(триэтилфенил)-втор-бутил)фенол (включая изомеры), (2-(трипропилфенил)-втор-бутил)фенол (включая изомеры), (2-(трибутилфенил)-втор-бутил)фенол (включая изомеры), ди(2-фенил-втор-бутил)фенол (включая изомеры), ди(2-(метилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(этилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(пропилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(бутилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(пентилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(гексилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(гептилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(октилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(нонилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(децилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(бифенил)-втор-бутил)фенол (включая изомеры), ди(2-(диметилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(диэтилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(дипропилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(дибутилфенил)изопропил)фенол (включая изомеры), ди(2-(дипентилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(дигексилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(дигептилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(терфенил)-втор-бутил)фенол, ди(2-(триметилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(триэтилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(трипропилфенил)-втор-бутил)фенол (включая изомеры), ди(2-(трибутилфенил)-втор-бутил)фенол (включая изомеры), три(2-фенил-втор-бутил)фенол (включая изомеры), три(2-(метилфенил)-втор-бутил)фенол (включая изомеры), три(2-(этилфенил)-втор-бутил)фенол (включая изомеры), три(2-(пропилфенил)-втор-бутил)фенол (включая изомеры), три(2-(бутилфенил)-втор-бутил)фенол (включая изомеры), три(2-(пентилфенил)-втор-бутил)фенол (включая изомеры), три(2-(гексилфенил)-втор-бутил)фенол (включая изомеры), три(2-(гептилфенил)-втор-бутил)фенол (включая изомеры), три(2-(октилфенил)-втор-бутил)фенол (включая изомеры), три(2-(нонилфенил)-втор-бутил)фенол (включая изомеры), три(2-(децилфенил)-втор-бутил)фенол (включая изомеры), три(2-(бифенил)изопропил)фенол (включая изомеры), три(2-(диметилфенил)изопропил)фенол (включая изомеры), три(2-(диэтилфенил)-втор-бутил)фенол (включая изомеры), три(2-(дипропилфенил)-втор-бутил)фенол (включая изомеры), три(2-(дибутилфенил)-втор-бутил)фенол (включая изомеры), три(2-(дипентилфенил)-втор-бутил)фенол (включая изомеры), три(2-(дигексилфенил)-втор-бутил)фенол (включая изомеры), три(2-(дигептилфенил)-втор-бутил)фенол (включая изомеры), три(2-(терфенил)-втор-бутил)фенол, три(2-(триметилфенил)-втор-бутил)фенол (включая изомеры), три(2-(триэтилфенил)-втор-бутил)фенол (включая изомеры), три(2-(трипропилфенил)-втор-бутил)фенол (включая изомеры), и три(2-(трибутилфенил)-втор-бутил)фенол (включая изомеры).
Более предпочтительные их примеры могут включать ароматические моногидроксисоединения, в которых группы R33, R34, R35, R36 и R37 являются линейными и/или циклическими насыщенными алкильными группами, и в которых по меньшей мере одна из групп R33 и R34 имеет третичный или четвертичный углеродный атом для углеродного атома в α положении.
<Производная угольной кислоты>
Производная угольной кислоты в варианте настоящего осуществления относится к соединению, представленному следующей формулой (19). В случае использования композиции для транспортировки и хранения соединения, имеющего уреидные группы, на стадии производства N-замещенной карбаминовой кислоты-O-R2 эфира или на стадии производства N-замещенной карбаминовой кислоты-O-арилового эфира, а именно на упомянутый выше стадии (R), стадии (P) или стадии (B), или в случае использования компонента, рециркулируемого с этих стадий производства при получении соединения, имеющего уреидные группы, производная угольной кислоты является компонентом, который может содержаться в композиции для транспортировки и хранения соединения, имеющего уреидные группы. Кроме того, производная угольной кислоты является компонентом, который также служит в качестве сырья соединения, имеющего уреидные группы.

(где
X и Y представляют органические группы или аминогруппы (-NH2), имеющие от 1 до 50 углеродных атомов, при условии, что X и Y не являются одновременно аминогруппами, и значение числа углеродных атомов является целым числом).
Примеры соединений, представленных упомянутой выше формулой (19), которые используют в варианте настоящего осуществления, могут включать не-N-замещенной карбаминовой кислоты-O-ариловые эфиры, не-N-замещенной карбаминовой кислоты-O-R2 эфиры и эфиры угольной кислоты. При использовании выражения терминов "не-N-замещенные карбаминовые кислоты", "не-N-замещенной карбаминовой кислоты-O-ариловые эфиры" и "не-N-замещенной карбаминовой кислоты-O-R2 эфиры" при объяснении варианта настоящего осуществления и в качестве названий общей формулы соединений, термин "не-N-замещенная карбаминовая кислота" используют здесь в смысле того, что NH2 группа карбамоильной группы (NH2-CO-) не замещена с помощью заместителя. А именно, NH2 группа карбамоильной группы (NH2-CO-) не-N-замещенной карбаминовой кислоты является NH2 группой.
Предпочтительно, чтобы не-N-замещенной карбаминовой кислоты-O-R2 эфир, представленный следующей формулой (21), использовали в качестве не-N-замещенной карбаминовой кислоты-O-R2 эфира:
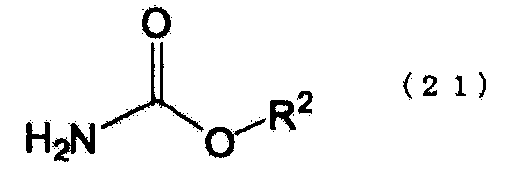
(где
R2 группа является такой же, как R2 группа спирта, представленного формулой (4), и представляет группу, состоящую из алифатической группы, с которой связана алифатическая группа или ароматическая группа, содержащая целое число углеродных атомов в интервале от 1 до 14, и -O-R2 группа не-N-замещенной карбаминовой кислоты-O-R2 эфира, представленного формулой (21), является R2O группа R2OH спирта, представленного формулой (4)).
Не-N-замещенной карбаминовой кислоты-O-R2 эфир может образовываться в качестве побочного продукта в процессе получения N-замещенной карбаминовой кислоты-O-арилового эфира в способе, включающем стадию (A) и/или стадию (R), на которых используется спирт (а именно, в способе, в котором используют спирт), или может являться не-N-замещенной карбаминовой кислоты-O-R2 эфиром, полученным известным способом. Предпочтительно, чтобы известным способом являлся способ получения не-N-замещенной карбаминовой кислоты-O-R2 эфира из мочевины и спирта, показанный в следующем уравнении реакции (23), путем реакции изоциановой кислоты (HNCO) и спирта, как показано в следующем уравнении реакции (22), и не-N-замещенной карбаминовой кислоты-O-R2 эфир, представленный выше формулой (21), может быть получен путем использования спирта, представленного формулой (4), для спирта, используемого в настоящее время.
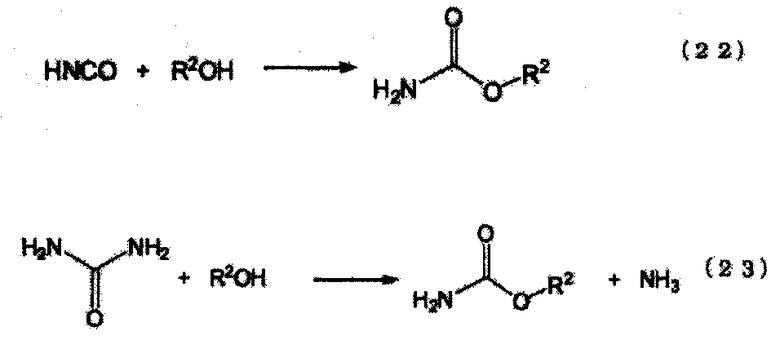
R2 группы, приведенные в качестве примеров при объяснении спирта, представленного формулой (4), могут быть предпочтительно использованы в качестве R2 группы.
Примеры таких не-N-замещенной карбаминовой кислоты-O-R2 эфиров, представленных формулой (21), могут включать метилкарбамат, этилкарбамат, пропилкарбамат (включая изомеры), бутилкарбамат (включая изомеры), пентилкарбамат (включая изомеры), гексилкарбамат (включая изомеры), гептилкарбамат (включая изомеры), октилкарбамат (включая изомеры), нонилкарбамат (включая изомеры), децилкарбамат (включая изомеры), ундецилкарбамат (включая изомеры), додецилкарбамат (включая изомеры), тридецилкарбамат (включая изомеры), тетрадецилкарбамат (включая изомеры), пентадецилкарбамат (включая изомеры), гексадецилкарбамат (включая изомеры), гептадецилкарбамат (включая изомеры), октадецилкарбамат (включая изомеры), нонадецилкарбамат (включая изомеры), бензилкарбамат, (метилбензил)карбамат (включая изомеры), (диметилбензил)карбамат (включая изомеры), (фенилэтил)карбамат (включая изомеры), (фенилпропил)карбамат (включая изомеры), (фенилбутил)карбамат (включая изомеры), (фенилпентил)карбамат (включая изомеры), (фенилгексил)карбамат (включая изомеры), (фенилгептил)карбамат (включая изомеры), (фенилоктил)карбамат (включая изомеры) и (фенилнонил)карбамат (включая изомеры). Более предпочтительные примеры включают не-N-замещенной карбаминовой кислоты алкиловые эфиры и не-N-замещенной карбаминовой кислоты аралкиловые эфиры.
Соединения, имеющие уреидные группы, могут быть получены из упомянутых выше не-N-замещенной карбаминовой кислоты-O-R2 эфиров путем реакции с органическим первичным амином с помощью известного способа. Уравнение реакции показано в виде следующего уравнения (24). В уравнении (24) структура моноамина приведена для структуры органического первичного амина, но структурой может также являться структура органического первичного полиамина.
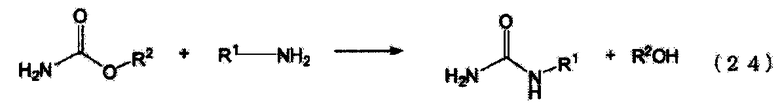
В варианте настоящего осуществления соединение, имеющее уреидные группы, предпочтительно получать путем проведения стадии (A), на которой реагируют органический первичный амин и мочевина, но одновременно в дополнение к ним может также проводиться реакции в соответствии с уравнением (24). Кроме того, этот способ является предпочтительным, так как он позволяет эффективно использовать побочные продукты реакции.
Не-N-замещенной карбаминовой кислоты-O-ариловый эфир, представленный следующей формулой (25), предпочтительно использовать в качестве не-N-замещенной карбаминовой кислоты-O-арилового эфира:
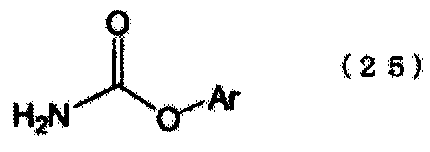
(где
Ar представляет группу, полученную из ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию, и Ar-O-группа представляет остаток, в котором атом водорода гидроксильной группы, непосредственно связанной с ароматическим углеводородным кольцом, был удален из ароматического гидроксисоединения).
Соединение, представленное формулой (25), может являться не-N-замещенной карбаминовой кислоты-O-ариловым эфиром, который либо образуется в качестве побочного продукта в процессе получения N-замещенной карбаминовой кислоты-O-арилового эфира способом, включающим любую из стадии (A), стадии (P) или стадии (B) с помощью ароматической гидроксикомпозиции, либо который получают с помощью известного способа. Предпочтительно, чтобы известный способ являлся способом, в котором не-N-замещенной карбаминовой кислоты-O-ариловый эфир получают из мочевины и ароматического гидроксисоединения, как показано в следующем уравнении реакции (27), по реакции между изоциановой кислотой (HNCO) и ароматическим гидроксисоединением, как показано в следующем уравнении реакции (26), и путем использования ароматического гидроксисоединения, представленного формулой (2), в качестве используемого в данном случае ароматического гидроксисоединения, не-N-замещенной карбаминовой кислоты-O-ариловый эфир, представленный выше формулой (25), может быть получен:
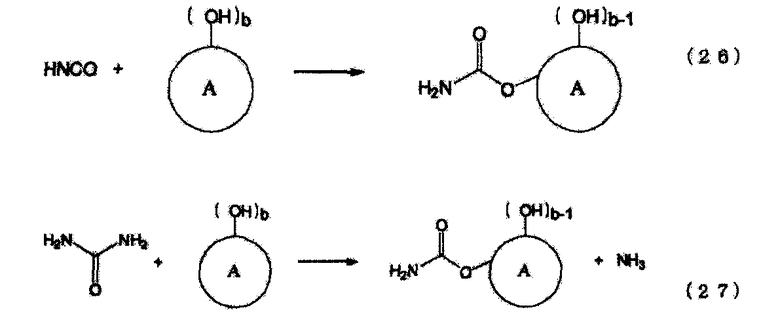
(где
кольцо A и b являются такими же, как они были определены для ароматического гидроксисоединения, представленного формулой (2), и фрагмент кислород-кольцо A, связанный с карбамоильной группой (NH2-CO-), содержащийся в структуре не-N-замещенной карбаминовой кислоты-O-арилового эфира, представленного в формулах (26) и (27), представляет остаток, в котором атом водорода был удален из гидроксильной группы, связанной с ароматическим кольцом ароматического гидроксисоединения).
В приведенном выше описании показана структура, в которой реагирует только одна гидроксильная группа ароматического гидроксисоединения, но может быть образован и поливалентный не-N-замещенной карбаминовой кислоты-O-ариловый эфир, имеющий структуру отличающуюся от той, которая приведена выше.
Так как в варианте настоящего осуществления ароматическое гидроксисоединение обычно используют в избытке, структура является такой, что отношение между группами карбаминовой кислоты в не-N-замещенной карбаминовой кислоты-O-ариловом эфире и группами, полученными из ароматического гидроксиостатка, полученного из формулы (2), составляет обычно 1:1.
Соединение, имеющее уреидные группы, может быть получено из упомянутого выше не-N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции с органическим первичным амином при помощи известного способа. Уравнение реакции приведено в виде следующего уравнения (28):

(где
Ar определен так же, как и Ar в упомянутой выше формуле (25)).
В варианте настоящего осуществления соединение, имеющее уреидные группы, предпочтительно получать путем проведения стадии (A), включающей реакцию органического первичного амина и мочевины, но одновременно с ней может также быть проведена реакция, приведенная выше в уравнении реакции (28). В уравнении (28), оба и не-N-замещенной карбаминовой кислоты-O-ариловый эфир и органический первичный амин представлены как одновалентные (имеющие одно реакционное место), но они могут также являться поливалентными не-N-замещенной карбаминовой кислоты-O-ариловым эфиром и органическим первичным полиамином, соответственно.
Кроме того, этот способ является предпочтительным, так как он позволяет эффективно использовать побочные продукты реакции. Кроме того, на стадии (A) могут также быть проведены одновременно реакция по уравнению (24), исходя из упомянутого выше не-N-замещенной карбаминовой кислоты-O-R2 эфира, и реакция по уравнению (28), исходя из не-N-замещенной карбаминовой кислоты-O-арилового эфира.
Для Ar группы может быть предпочтительно использована структура, в которой была удалена одна или более гидроксильных групп, связанных с ароматическим кольцом, содержащимся в ароматическом гидроксисоединении, приведенном в качестве примера при объяснении ароматического гидроксисоединения, представленного формулой (2). А именно, остаток, в котором атом водорода гидроксильной группы, непосредственно связанный с ароматическим углеводородным кольцом, был удален из ароматического гидроксисоединения, представленного формулой (2), может быть предпочтительно использован для -O-Ar группы не-N-замещенной карбаминовой кислоты-O-арилового эфира упомянутой выше формулы (25). Кроме того, среди ароматических гидроксисоединений, представленных формулой (2), ароматическое моногидроксисоединение, представленное формулой (31) или формулой (32), является предпочтительным, а активное ароматическое моногидроксисоединение, представленное формулой (38), является более предпочтительным. Естественно, что могут быть использованы один тип или два или более типов.
Примеры такого не-N-замещенной карбаминовой кислоты-O-арилового эфира, представленного формулой (21), могут включать фенилкарбамат, (метилфенил)карбамат (включая изомеры), (этилфенил)карбамат (включая изомеры), (пропилфенил)карбамат (включая изомеры), (бутилфенил)карбамат (включая изомеры), (пентилфенил)карбамат (включая изомеры), (гексилфенил)карбамат (включая изомеры), (гептилфенил)карбамат (включая изомеры), (октилфенил)карбамат (включая изомеры), (нонилфенил)карбамат (включая изомеры), (децилфенил)карбамат (включая изомеры), (бифенил)карбамат (включая изомеры), (диметилфенил)карбамат (включая изомеры), (диэтилфенил)карбамат (включая изомеры), (дипропилфенил)карбамат (включая изомеры), (дибутилфенил)карбамат (включая изомеры), (дипентилфенил)карбамат (включая изомеры), (дигексилфенил)карбамат (включая изомеры), (дигептилфенил)карбамат (включая изомеры), (терфенил)карбамат (включая изомеры), (триметилфенил)карбамат (включая изомеры), (триэтилфенил)карбамат (включая изомеры), (трипропилфенил)карбамат (включая изомеры) и (трибутилфенил)карбамат (включая изомеры). Его предпочтительные примеры могут включать не-N-замещенной карбаминовой кислоты-O-ариловые эфиры, в которых арильная группа -O-арилового эфира является фенильной группой, замещенной с помощью алкильной группы или фенильной группой.
Как уже было описано выше, не-N-замещенной карбаминовой кислоты-O-(R2 или ариловый)эфир, представленный формулой (21) или формулой (25), может быть эффективно использован в качестве сырья для синтеза соединения, имеющего уреидные группы. Во многих случаях в качестве производной угольной кислоты могут также одновременно присутствовать сложнозамещенный мономер или полимер соединения мочевины, биурета или нурата и другие подобные соединения, помимо ранее описанной мочевины, спирта, аммиака, сложного эфира N-замещенной карбаминовой кислоты и объясняемого далее эфира угольной кислоты и других подобных соединений, но присутствие таких соединений не вызывают никаких проблем. Кроме того, в ряде случаев при объяснении настоящего патентного описания используют термин "не-N-замещенной карбаминовой кислоты-O-(R2 или ариловый) эфир", и он относится к "N-замещенной карбаминовой кислоты-O-R2 эфиру или N-замещенной карбаминовой кислоты-O-ариловому эфиру".
<N-замещенной карбаминовой кислоты-O-ариловый эфир>
N-замещенной карбаминовой кислоты-O-ариловый эфир, полученный способом варианта настоящего осуществления, является соединением, представленным следующей формулой (43). Далее объясняемый подробно вариант настоящего осуществления относится к способу этерификации соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, или к способу получения N-замещенной карбаминовой кислоты-O-R2 эфира путем этерификации соединения, имеющего уреидные группы, и спирта с последующей переэтерификацией N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции с получением N-замещенной карбаминовой кислоты-O-арилового эфира (и N-замещенной карбаминовой кислоты-O-ариловый эфир относится к сложному эфиру N-замещенной карбаминовой кислоты, в котором атом кислорода группы карбаминовой кислоты (-NHCOO-) связан с ароматическим кольцом). Объясняя более подробно, O-арильная группа в группе карбаминовой кислоты-O-арилового эфира N-замещенной карбаминовой кислоты-O-арилового эфира является остатком, в котором атом водорода был удален из единственной гидроксильной группы (OH группы), связанной с углеродным атомом ароматического кольца ароматического гидроксисоединения. А именно, описанный выше первый способ является способом этерификации уреидной группы (-NHCONH2) и ароматического гидроксисоединения с получением карбаминовой кислоты-O-арильной группы (-NHCOOAr), в то время как описанный выше второй способ является способом этерификации уреидной группы (-NHCONH2) и спирта с получением карбаминовой кислоты-O-R2 группы (-NHCOOR2) с последующей переэтерификацией с ароматическим гидроксисоединением с получением карбаминовой кислоты-O-арильной группы (-NHCOOAr):
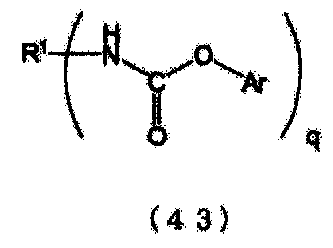
(где
R1 представляет группу, полученную из органического первичного амина или ранее определенного соединения, имеющего уреидные группы,
Ar представляет группу, полученную из ароматического гидроксисоединения, представленного формулой (2), которое составляет ароматическую гидроксикомпозицию, и Ar-O-группа представляет остаток, в котором атом водорода единственной гидроксильной группы, связанной непосредственно с ароматическим углеводородным кольцом, был удален из ароматического гидроксисоединения, и
q представляет целое число от 1 до a , или целое число от 1 до c , и a и c определены ранее).
Конкретная структура N-замещенной карбаминовой кислоты-O-арилового эфира, представленного выше формулой (43), определяется используемыми органическим первичным амином и/или соединением, имеющим уреидные группы, и ароматической гидроксикомпозицией. Например, в случае использования соединения, имеющего уреидные группы, представленного формулой (1), и/или органического первичного амина, представленного формулой (3), и использования ароматического гидроксисоединения, представленного формулой (2), в качестве ароматической гидроксикомпозиции, получают N-замещенной карбаминовой кислоты-O-ариловый эфир, представленный следующей формулой (44), в случае использования органического первичного амина, представленного формулой (5), и ароматического гидроксисоединения, представленного формулой (2), в качестве ароматической гидроксикомпозиции (и в случае b =1), получают N-замещенной карбаминовой кислоты-O-ариловый эфир, представленный следующей формулой (45), в случае использования соединения, имеющего уреидные группы, представленного формулой (1), и/или органического первичного амина, представленного формулой (3), и использования ароматического гидроксисоединения, представленного формулой (7), в качестве ароматической гидроксикомпозиции, получают N-замещенной карбаминовой кислоты-O-ариловый эфир, представленный следующей формулой (46), и в случае использования органического первичного амина, представленного формулой (5), и ароматического гидроксисоединения, представленного формулой (2), в качестве ароматической гидроксикомпозиции (и в случае b =1) и осуществления способа, который включает стадию (C), получают N-замещенной поли(карбаминовой кислоты-O-ариловый эфир), представленный следующей формулой (47) (упомянутый выше N-замещенной поли(карбаминовой кислоты-O-ариловый эфир) относится к N-замещенной карбаминовой кислоты-O-алкиловому эфиру, имеющему в его молекуле множество групп карбаминовой кислоты-O-арилового эфира). Таким образом, способом получения варианта настоящего осуществления может быть получен разнообразный спектр N-замещенной карбаминовой кислоты-O-ариловых эфиров, и они могут быть обычно представлены упомянутой выше формулой (43). (Термин "арил", согласно правилам номенклатуры, определенным IUPAC, относится к одновалентному ароматическому кольцу, и в варианте настоящего осуществления используют термин "арил", так как не удалось найти подходящего термина, который бы в целом относился к соединениям в варианте настоящего осуществления группа, относящаяся к N-замещенной карбаминовой кислоты-O-ариловому эфиру варианта настоящего осуществления содержит указанные выше N-замещенной карбаминовой кислоты-O-ариловые эфиры. В качестве варианта, N-замещенной карбаминовой кислоты-O-ариловый эфир в варианте настоящего осуществления может также быть назван как N-замещенной карбаминовой кислоты-O-Ar эфир, или другими словами, Ar имеет такое же значение, как описанное ранее:
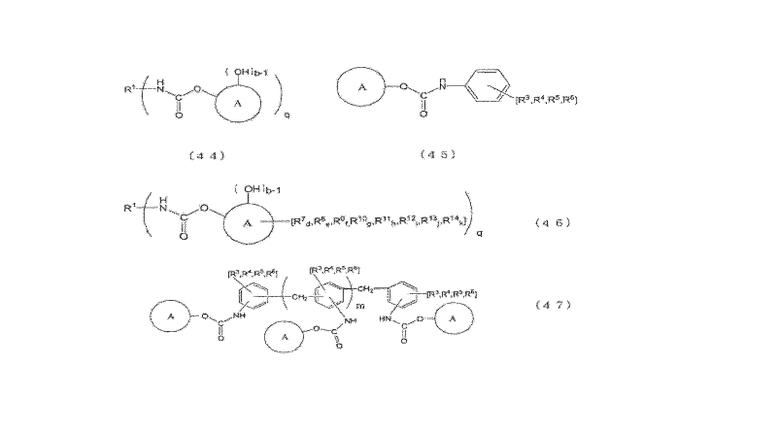
(где
R1 представляет группу, полученную из определенного ранее органического первичного амина,
кольцо A представляет ранее определенную группу, полученную из ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию, которая является остатком, в котором единственный атом водорода гидроксильной группы, непосредственно связанной с ароматическим углеводородным кольцом, был удален из ароматического гидроксисоединения,
R3-R14 представляют группы, определенные ранее,
b, d, e, f, g, h, i, j, k, m и q являются целыми числами, определенными ранее, и
q представляет целое число от 1 до a, или целое число от 1 до c , и a и c определены ранее).
В случае использования поливалентного ароматического гидроксисоединения, вследствие множества гидроксильных групп на ароматической группе может быть получен полимер, имеющий сложную структуру, так как в варианте настоящего осуществления используют избыток ароматического гидроксисоединения и обычно получают N-замещенной карбаминовой кислоты-O-ариловый эфир, представленный выше формулой (43).
Так как способ получения варианта настоящего осуществления может быть применен к широкому спектру описанных ранее соединений, имеющих уреидные группы, органическим первичным аминам, спиртам и ароматическим гидроксисоединениям, то все возможные примеры конкретных соединений не могут быть приведены, но примеры таких конкретных соединений могут включать N,N'-гександиилди(карбаминовой кислоты фениловый эфир), N,N'-гександиилди(карбаминовой кислоты (метилфениловый) эфир) (включая изомеры), N,N'-гександиилди(карбаминовой кислоты (этилфениловый) эфир) (включая изомеры), N,N'-гександиилди(карбаминовой кислоты (пропилфениловый) эфир) (включая изомеры), N,N'-гександиилди(карбаминовой кислоты (бутилфениловый) эфир) (включая изомеры), N,N'-гександиилди(карбаминовой кислоты (пентилфениловый) эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты фениловый эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты (метилфениловый) эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты (этилфениловый) эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты (пропилфениловый) эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты (бутилфениловый) эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты (пентилфениловый) эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты (гексилфениловый) эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты (гептилфениловый) эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты (октилфениловый) эфир) (включая изомеры), 3-(феноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты фениловый эфир, 3-(метилфеноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (метилфениловый) эфир (включая изомеры), 3-(этилфеноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (этилфениловый) эфир (включая изомеры), 3-(пропилфеноксикарбониламинометил)-3,5,5-триметилциклогексил-карбаминовой кислоты (пропилфениловый)эфир (включая изомеры), 3-(бутилфеноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (бутилфениловый) эфир (включая изомеры), 3-(пентилфеноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (пентилфениловый) эфир (включая изомеры), 3-(гексилфеноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (гексилфениловый) эфир (включая изомеры), 3-(гептилфеноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (гептилфениловый) эфир (включая изомеры), 3-(октилфеноксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (октилфениловый) эфир (включая изомеры), толуолди(карбаминовой кислоты фениловый эфир) (включая изомеры), толуолди(карбаминовой кислоты (метилфениловый) эфир) (включая изомеры), толуолди(карбаминовой кислоты (этилфениловый) эфир) (включая изомеры), толуолди(карбаминовой кислоты (пропилфениловый) эфир) (включая изомеры), толуолди(карбаминовой кислоты (бутилфениловый) эфир) (включая изомеры), толуолди(карбаминовой кислоты (пентилфениловый)эфир) (включая изомеры), толуолди(карбаминовой кислоты (гексилфениловый) эфир) (включая изомеры), толуолди(карбаминовой кислоты (гептилфениловый) эфир) (включая изомеры), толуолди(карбаминовой кислоты (октилфениловый) эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты фениловый эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты (метилфениловый) эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты (этилфениловый) эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты (пропилфениловый) эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты (бутилфениловый) эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты (пентилфениловый) эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты (гексилфениловый) эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты (гептилфениловый) эфир) (включая изомеры) и N,N'-(метандиилдифенил)ди(карбаминовой кислоты (октилфениловый)эфир) (включая изомеры). Предпочтительные N-замещенной карбаминовой кислоты-O-ариловые эфиры содержат N-замещенной карбаминовой кислоты-O-ариловые эфиры, полученные с помощью предпочтительных соединений, ранее объясненных для упомянутых выше органических первичных аминов, ароматических гидроксисоединений и соединений, имеющих уреидные группы, примеры которых могут включать N-замещенной карбаминовой кислоты-O-ариловые эфиры, полученные реакцией активного ароматического моногидроксисоединения с N-замещенной ароматической органической мономочевиной, N-замещенной ароматической органической полимочевиной или N-замещенной алифатической органической полимочевиной, и N-замещенной карбаминовой кислоты-O-ариловые эфиры, полученные конденсацией N-замещенной карбаминовой кислоты-O-арилового эфира, полученного из активного ароматического моногидроксисоединения и N-замещенной ароматической органической мономочевины с конденсирующим реагентом. Кроме того, предпочтительными также являются N-замещенной карбаминовой кислоты-O-ариловые эфиры, в которых все уреидные группы или первичные аминогруппы, содержащиеся в соединении, имеющем уреидные группы, или органический первичный амин замещены с помощью группы карбаминовой кислоты-O-арилового эфира (а именно, a = q или c = q ).
<N-замещенной карбаминовой кислоты-O-R2 эфир>
N-замещенной карбаминовой кислоты O-R2 эфир, полученный способом получения варианта настоящего осуществления, является соединением, представленным следующей формулой (49). Далее будет объяснено подробно соединение, которое относится к настоящему изобретению, получаемое при получении N-замещенной карбаминовой кислоты-O-арилового эфира способом, который включает упомянутую выше стадию (R). Оно является соединением, получаемое этерификацией соединения, имеющего уреидные группы, и спирта, представленного формулой (4), с превращением уреидных групп (-NHCONH2) в группы карбаминовой кислоты-O-R2 эфира (-NHCOOR2). А именно, оно является N-замещенной карбаминовой кислоты-O-R2 эфиром, который получают реакцией по меньшей мере одного типа соединений, имеющих уреидные группы, со спиртом, представленным формулой (4), в жидкой фазе с последующим извлечением аммиака, образующегося в качестве побочного продукта, в газовую фазу, и N-замещенной карбаминовой кислоты-O-R2 эфир относится к сложному эфиру N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с группой R2, полученной из спирта. Для более подробного объяснения, группа OR2 в группе карбаминовой кислоты-O-R2 эфира (-NHCOOR2) N-замещенной карбаминовой кислоты-O-R2 эфира является остатком, в котором атом водорода был удален из единственной гидроксильной группы (OH группы), связанной с углеродным атомом спирта:
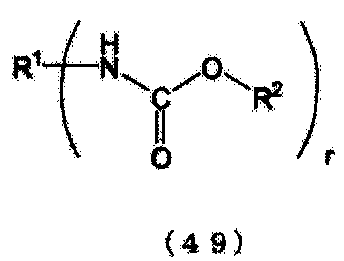
(где
R1 представляет ранее определенную группу, полученную из органического первичного амина,
R2 представляет ранее определенную группу, полученную из спирта,
r является целым числом от 1 до a , или от 1 до c , и a и c определены ранее).
Так как способ получения варианта настоящего осуществления может быть применен к широкому спектру описанных ранее соединений, имеющих уреидные группы, органическим первичным аминам, и спиртам, то все возможные примеры конкретных соединений не могут быть приведены, но примеры таких конкретных соединений могут включать N,N'-гександиилди(карбаминовой кислоты метиловый эфир), N,N'-гександиилди(карбаминовой кислоты этиловый эфир), N,N'-гександиилди(карбаминовой кислоты пропиловый эфир) (включая изомеры), N,N'-гександиилди(карбаминовой кислоты бутиловый эфир) (включая изомеры), N,N'-гександиилди(карбаминовой кислоты пентиловый эфир) (включая изомеры), N,N'-гександиилди(карбаминовой кислоты гексиловый эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты метиловый эфир), метиленди(циклогексилкарбаминовой кислоты этиловый эфир), метиленди(циклогексилкарбаминовой кислоты пропиловый эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты бутиловый эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты пентиловый эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты гексиловый эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты гептиловый эфир) (включая изомеры), метиленди(циклогексилкарбаминовой кислоты октиловый эфир) (включая изомеры), 3-(метоксикарбониламинометил)-3,5,5-триметилциклогексил карбаминовой кислоты метиловый эфир, 3-(этоксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты этиловый эфир (включая изомеры), 3-(пропилоксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты пропиловый эфир (включая изомеры), 3-(бутилоксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты бутиловый эфир (включая изомеры), 3-(пентилоксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты пентиловый эфир (включая изомеры), 3-(гексилоксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты гексиловый эфир (включая изомеры), 3-(гептилоксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты гептиловый эфир (включая изомеры), 3-(октилоксикарбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты октиловый эфир (включая изомеры), толуолди(карбаминовой кислоты метиловый эфир) (включая изомеры), толуолди(карбаминовой кислоты этиловый эфир) (включая изомеры), толуолди(карбаминовой кислоты пропиловый эфир) (включая изомеры), толуолди(карбаминовой кислоты бутиловый эфир) (включая изомеры), толуолди(карбаминовой кислоты пентиловый эфир) (включая изомеры), толуолди(карбаминовой кислоты гексиловый эфир) (включая изомеры), толуолди(карбаминовой кислоты гептиловый эфир) (включая изомеры), толуолди(карбаминовой кислоты октиловый эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты метиловый эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты этиловый эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты пропиловый эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты бутиловый эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты пентиловый эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты гексиловый эфир) (включая изомеры), N,N'-(метандиилдифенил)ди(карбаминовой кислоты гептиловый эфир) (включая изомеры) и N,N'-(метандиилдифенил)ди(карбаминовой кислоты октиловый эфир) (включая изомеры). Предпочтительные N-замещенной карбаминовой кислоты-O-R2 эфиры содержат N-замещенной карбаминовой кислоты-O-R2 эфиры, получаемые путем использования предпочтительных соединений, ранее объясненных для упомянутых выше органических первичных аминов, спиртов и соединений, имеющих уреидные группы, примеры которых могут включать N-замещенной карбаминовой кислоты-O-R2 эфиры, полученные реакцией спирта с N-замещенной ароматической органической мономочевиной, N-замещенной ароматической органической полимочевиной или N-замещенной алифатической органической полимочевиной, и N-замещенной карбаминовой кислоты-O-R2 эфиры, полученные конденсацией N-замещенной карбаминовой кислоты-O-R2 эфира, полученного из спирта и N-замещенной ароматической органической мономочевины, с конденсирующим реагентом. Кроме того, также предпочтительными являются N-замещенной карбаминовой кислоты-O-R2 эфиры, в которых все уреидные группы или первичные аминогруппы, содержащиеся в соединении, имеющем уреидные группы, или органическом первичном амине, замещены с помощью группы карбаминовой кислоты-O-алкилового эфира (а именно, a = r ).
<Эфир угольной кислоты>
Эфир угольной кислоты является компонентом, который предпочтительно содержится в конкретном количестве в композиции для транспортировки и хранения варианта настоящего осуществления.
Эфир угольной кислоты относится к соединению, в котором один или оба из двух атомов водорода угольной кислоты (CO(OH)2) замещены с помощью алифатической группы или ароматической группы. В варианте настоящего осуществления предпочтительно использовать соединение, представленное следующей формулой (20):
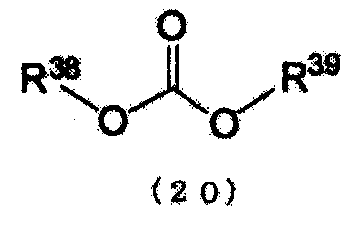
(где
R38 и R39 являются группами, которые соответственно и независимо выбирают из упомянутых выше R2 и Ar групп).
Упомянутый выше эфир угольной кислоты образуется в результате реакции между мочевиной и спиртом и/или ароматическим гидроксисоединением, реакции между N-замещенной карбаминовой кислоты-O-(R2 или ариловым)эфиром и спиртом и/или ароматическим гидроксисоединением, или реакции диспропорционирования образовавшегося эфира угольной кислоты.
Примеры групп R2 и Ar могут включать группы R2 и Ar, объсненные для N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира.
Примеры эфира угольной кислоты, представленного формулой (20), могут включать диметилкарбонат, диэтилкарбонат, дипропилкарбонат (включая изомеры), дибутилкарбонат (включая изомеры), дипентилкарбонат (включая изомеры), дигексилкарбонат (включая изомеры), дигептилкарбонат (включая изомеры), диоктилкарбонат (включая изомеры), динонилкарбонат (включая изомеры), дидецилкарбонат (включая изомеры), диундецилкарбонат (включая изомеры), дидодецилкарбонат (включая изомеры), дитридецилкарбонат (включая изомеры), дитетрадецилкарбонат (включая изомеры), дипентадецилкарбонат (включая изомеры), дигексадецилкарбонат (включая изомеры), дигептадецилкарбонат (включая изомеры), диоктадецилкарбонат (включая изомеры), динонадецилкарбонат (включая изомеры), дифенилкарбонат (включая изомеры), ди(метилфенил)карбонат (включая изомеры), ди(этилфенил)карбонат (включая изомеры), ди(пропилфенил)карбонат (включая изомеры), ди(бутилфенил)карбонат (включая изомеры), ди(пентилфенил)карбонат (включая изомеры), ди(гексилфенил)карбонат (включая изомеры), ди(гептилфенил)карбонат (включая изомеры), ди(октилфенил)карбонат (включая изомеры), ди(нонилфенил)карбонат (включая изомеры), ди(децилфенил)карбонат (включая изомеры), ди(бифенил)карбонат (включая изомеры), ди(диметилфенил)карбонат (включая изомеры), ди(диэтилфенил)карбонат (включая изомеры), ди(дипропилфенил)карбонат (включая изомеры), ди(дибутилфенил)карбонат (включая изомеры), ди(дипентилфенил)карбонат (включая изомеры), ди(дигексилфенил)карбонат (включая изомеры), ди(дигептилфенил)карбонат (включая изомеры), ди(фенилфенил)карбонат (включая изомеры), ди(триметилфенил)карбонат (включая изомеры), ди(триэтилфенил)карбонат (включая изомеры), ди(трипропилфенил)карбонат (включая изомеры), ди(трибутилфенил)карбонат (включая изомеры), ди(фенилметил)карбонат (включая изомеры), ди(фенилэтил)карбонат (включая изомеры), ди(фенилпропил)карбонат (включая изомеры), ди(фенилбутил)карбонат (включая изомеры), ди(фенилпентил)карбонат (включая изомеры), ди(фенилгексил)карбонат (включая изомеры), ди(фенилгептил)карбонат (включая изомеры), ди(фенилоктил)карбонат (включая изомеры) ди(фенилнонил)карбонат (включая изомеры), (метил)(этил)карбонат, (метил)(пропил)карбонат (включая изомеры), (метил)(бутил)карбонат (включая изомеры), (метил)(пентил)карбонат (включая изомеры), (метил)(гексил)карбонат (включая изомеры), (метил)(гептил)карбонат (включая изомеры), (метил)(октил)карбонат (включая изомеры), (метил)(нонил)карбонат (включая изомеры), (метил)(децил)карбонат (включая изомеры), (метил)(ундецил)карбонат (включая изомеры), (метил)(додецил)карбонат (включая изомеры), (метил)(тридецил)карбонат (включая изомеры), (метил)(тетрадецил)карбонат (включая изомеры), (метил)(пентадецил)карбонат (включая изомеры), (метил)(гексадецил)карбонат (включая изомеры), (метил)(гептадецил)карбонат (включая изомеры), (метил)(октадецил)карбонат (включая изомеры), (метил)(нонадецил)карбонат (включая изомеры), (метил)(фенил)карбонат (включая изомеры), (метил)(метилфенил)карбонат (включая изомеры), (метил)(этилфенил)карбонат (включая изомеры), (метил)(пропилфенил)карбонат (включая изомеры), (метил)(бутилфенил)карбонат (включая изомеры), (метил)(пентилфенил)карбонат (включая изомеры), (метил)(гексилфенил)карбонат (включая изомеры), (метил)(гептилфенил)карбонат (включая изомеры), (метил)(октилфенил)карбонат (включая изомеры), (метил)(нонилфенил)карбонат (включая изомеры), (метил)(децилфенил) карбонат (включая изомеры), (метил)(бифенил)карбонат (включая изомеры), (метил)(диметилфенил)карбонат (включая изомеры), (метил)(диэтилфенил)карбонат (включая изомеры), (метил)(дипропилфенил)карбонат (включая изомеры), (метил)(дибутилфенил)карбонат (включая изомеры), (метил)(дипентилфенил)карбонат (включая изомеры), (метил)(дигексилфенил)карбонат (включая изомеры), (метил)(дигептилфенил)карбонат (включая изомеры), (метил)(фенилфенил)карбонат (включая изомеры), (метил)(триметилфенил)карбонат (включая изомеры), (метил)(триэтилфенил)карбонат (включая изомеры), (метил)(трипропилфенил)карбонат (включая изомеры), (метил)(трибутилфенил)карбонат (включая изомеры), (метил)(фенилметил)карбонат (включая изомеры), (метил)(фенилэтил)карбонат (включая изомеры), (метил)(фенилпропил)карбонат (включая изомеры), (метил)(фенилбутил)карбонат (включая изомеры), (метил)(фенилпентил)карбонат (включая изомеры), (метил)(фенилгексил)карбонат (включая изомеры), (метил)(фенилгептил)карбонат (включая изомеры), (метил)(фенилоктил)карбонат (включая изомеры), (метил)(фенилнонил)карбонат (включая изомеры), (этил)(пропил)карбонат (включая изомеры), (этил)(бутил)карбонат (включая изомеры), (этил)(пентил)карбонат (включая изомеры), (этил)(гексил)карбонат (включая изомеры), (этил)(гептил)карбонат (включая изомеры), (этил)(октил)карбонат (включая изомеры), (этил)(нонил)карбонат (включая изомеры), (этил)(децил)карбонат (включая изомеры), (этил)(ундецил)карбонат (включая изомеры), (этил)(додецил)карбонат (включая изомеры), (этил)(тридецил)карбонат (включая изомеры), (этил)(тетрадецил)карбонат (включая изомеры), (этил)(пентадецил)карбонат (включая изомеры), (этил)(гексадецил)карбонат (включая изомеры), (этил)(гептадецил)карбонат (включая изомеры), (этил)(октадецил)карбонат (включая изомеры), (этил)(нонадецил)карбонат (включая изомеры), (этил)(фенил)карбонат (включая изомеры), (этил)(метилфенил)карбонат (включая изомеры), (этил)(этилфенил)карбонат (включая изомеры), (этил)(пропилфенил)карбонат (включая изомеры), (этил)(бутилфенил)карбонат (включая изомеры), (этил)(пентилфенил)карбонат (включая изомеры), (этил)(гексилфенил)карбонат (включая изомеры), (этил)(гептилфенил)карбонат (включая изомеры), (этил)(октилфенил)карбонат (включая изомеры), (этил)(нонилфенил)карбонат (включая изомеры), (этил)(децилфенил)карбонат (включая изомеры), (этил)(бифенил)карбонат (включая изомеры), (этил)(диметилфенил)карбонат (включая изомеры), (этил)(диэтилфенил)карбонат (включая изомеры), (этил)(дипропилфенил)карбонат (включая изомеры), (этил)(дибутилфенил)карбонат (включая изомеры), (этил)(дипентилфенил)карбонат (включая изомеры), (этил)(дигексилфенил)карбонат (включая изомеры), (этил)(дигептилфенил)карбонат (включая изомеры), (этил)(фенилфенил)карбонат (включая изомеры), (этил)(триметилфенил)карбонат (включая изомеры), (этил)(триэтилфенил)карбонат (включая изомеры), (этил)(трипропилфенил)карбонат (включая изомеры), (этил)(трибутилфенил)карбонат (включая изомеры), (этил)(фенилметил)карбонат (включая изомеры), (этил)(фенилэтил)карбонат (включая изомеры), (этил)(фенилпропил)карбонат (включая изомеры), (этил)(фенилбутил)карбонат (включая изомеры), (этил)(фенилпентил)карбонат (включая изомеры), (этил)(фенилгексил)карбонат (включая изомеры), (этил)(фенилгептил)карбонат (включая изомеры), (этил)(фенилоктил)карбонат (включая изомеры), (этил)(фенилнонил)карбонат (включая изомеры), (пропил)(бутил)карбонат (включая изомеры), (пропил)(пентил)карбонат (включая изомеры), (пропил)(гексил)карбонат (включая изомеры), (пропил)(гептил)карбонат (включая изомеры), (пропил)(октил)карбонат (включая изомеры), (пропил)(нонил)карбонат (включая изомеры), (пропил)(децил)карбонат (включая изомеры), (пропил)(ундецил)карбонат (включая изомеры), (пропил)(додецил)карбонат (включая изомеры), (пропил)(тридецил)карбонат (включая изомеры), (пропил)(тетрадецил)карбонат (включая изомеры), (пропил)(пентадецил)карбонат (включая изомеры), (пропил)(гексадецил)карбонат (включая изомеры), (пропил)(гептадецил)карбонат (включая изомеры), (пропил)(октадецил)карбонат (включая изомеры), (пропил)(нонадецил)карбонат (включая изомеры), (пропил)(фенил)карбонат (включая изомеры), (пропил)(метилфенил)карбонат (включая изомеры), (пропил)(этилфенил)карбонат (включая изомеры), (пропил)(пропилфенил)карбонат (включая изомеры), (пропил)(бутилфенил)карбонат (включая изомеры), (пропил)(пентилфенил)карбонат (включая изомеры), (пропил)(гексилфенил)карбонат (включая изомеры), (пропил)(гептилфенил)карбонат (включая изомеры), (пропил)(октилфенил)карбонат (включая изомеры), (пропил)(нонилфенил)карбонат (включая изомеры), (пропил)(децилфенил)карбонат (включая изомеры), (пропил)(бифенил)карбонат (включая изомеры), (пропил)(диметилфенил)карбонат (включая изомеры), (пропил)(диэтилфенил)карбонат (включая изомеры), (пропил)(дипропилфенил)карбонат (включая изомеры), (пропил)(дибутилфенил)карбонат (включая изомеры), (пропил)(дипентилфенил)карбонат (включая изомеры), (пропил)(дигексилфенил)карбонат (включая изомеры), (пропил)(дигептилфенил)карбонат (включая изомеры), (пропил)(фенилфенил)карбонат (включая изомеры), (пропил)(триметилфенил)карбонат (включая изомеры), (пропил)(триэтилфенил)карбонат (включая изомеры), (пропил)(трипропилфенил)карбонат (включая изомеры), (пропил)(трибутилфенил)карбонат (включая изомеры), (пропил)(фенилметил)карбонат (включая изомеры), (пропил)(фенилэтил)карбонат (включая изомеры), (пропил)(фенилпропил)карбонат (включая изомеры), (пропил)(фенилбутил)карбонат (включая изомеры), (пропил)(фенилпентил)карбонат (включая изомеры), (пропил)(фенилгексил)карбонат (включая изомеры), (пропил)(фенилгептил)карбонат (включая изомеры), (пропил)(фенилоктил)карбонат (включая изомеры), (пропил)(фенилнонил)карбонат (включая изомеры), (бутил)(пентил)карбонат (включая изомеры), (бутил)(гексил)карбонат (включая изомеры), (бутил)(гептил)карбонат (включая изомеры), (бутил)(октил)карбонат (включая изомеры), (бутил)(нонил)карбонат (включая изомеры), (бутил)(децил)карбонат (включая изомеры), (бутил)(ундецил)карбонат (включая изомеры), (бутил)(додецил)карбонат (включая изомеры), (бутил)(тридецил)карбонат (включая изомеры), (бутил)(тетрадецил)карбонат (включая изомеры), (бутил)(пентадецил)карбонат (включая изомеры), (бутил)(гексадецил)карбонат (включая изомеры), (бутил)(гептадецил)карбонат (включая изомеры), (бутил)(октадецил)карбонат (включая изомеры), (бутил)(нонадецил)карбонат (включая изомеры), (бутил)(фенил)карбонат (включая изомеры), (бутил)(метилфенил)карбонат (включая изомеры), (бутил)(этилфенил)карбонат (включая изомеры), (бутил)(пропилфенил)карбонат (включая изомеры), (бутил)(бутилфенил)карбонат (включая изомеры), (бутил)(пентилфенил)карбонат (включая изомеры), (бутил)(гексилфенил)карбонат (включая изомеры), (бутил)(гептилфенил)карбонат (включая изомеры), (бутил)(октилфенил)карбонат (включая изомеры), (бутил)(нонилфенил)карбонат (включая изомеры), (бутил)(децилфенил)карбонат (включая изомеры), (бутил)(бифенил)карбонат (включая изомеры), (бутил)(диметилфенил)карбонат (включая изомеры), (бутил)(диэтилфенил)карбонат (включая изомеры), (бутил)(дипропилфенил)карбонат (включая изомеры), (бутил)(дибутилфенил)карбонат (включая изомеры), (бутил)(дипентилфенил)карбонат (включая изомеры), (бутил)(дигексилфенил)карбонат (включая изомеры), (бутил)(дигептилфенил)карбонат (включая изомеры), (бутил)(фенилфенил)карбонат (включая изомеры), (бутил)(триметилфенил)карбонат (включая изомеры), (бутил)(триэтилфенил)карбонат (включая изомеры), (бутил)(трипропилфенил)карбонат (включая изомеры), (бутил)(трибутилфенил)карбонат (включая изомеры), (бутил)(фенилметил)карбонат (включая изомеры), (бутил)(фенилэтил)карбонат (включая изомеры), (бутил)(фенилпропил)карбонат (включая изомеры), (бутил)(фенилбутил)карбонат (включая изомеры), (бутил)(фенилпентил)карбонат (включая изомеры), (бутил)(фенилгексил)карбонат (включая изомеры), (бутил)(фенилгептил)карбонат (включая изомеры), (бутил)(фенилоктил)карбонат (включая изомеры), (бутил)(фенилнонил)карбонат (включая изомеры), (пентил)(гексил)карбонат (включая изомеры), (пентил)(гептил)карбонат (включая изомеры), (пентил)(октил)карбонат (включая изомеры), (пентил)(нонил)карбонат (включая изомеры), (пентил)(децил)карбонат (включая изомеры), (пентил)(ундецил)карбонат (включая изомеры), (пентил)(додецил)карбонат (включая изомеры), (пентил)(тридецил)карбонат (включая изомеры), (пентил)(тетрадецил)карбонат (включая изомеры), (пентил)(пентадецил)карбонат (включая изомеры), (пентил)(гексадецил)карбонат (включая изомеры), (пентил)(гептадецил)карбонат (включая изомеры), (пентил)(октадецил)карбонат (включая изомеры), (пентил)(нонадецил) карбонат (включая изомеры), (пентил)(фенил)карбонат (включая изомеры), (пентил)(метилфенил)карбонат (включая изомеры), (пентил)(этилфенил)карбонат (включая изомеры), (пентил)(пропилфенил)карбонат (включая изомеры), (пентил)(бутилфенил)карбонат (включая изомеры), (пентил)(пентилфенил)карбонат (включая изомеры), (пентил)(гексилфенил)карбонат (включая изомеры), (пентил)(гептилфенил)карбонат (включая изомеры), (пентил)(октилфенил)карбонат (включая изомеры), (пентил)(нонилфенил)карбонат (включая изомеры), (пентил)(децилфенил)карбонат (включая изомеры), (пентил)(бифенил)карбонат (включая изомеры), (пентил)(диметилфенил)карбонат (включая изомеры), (пентил)(диэтилфенил)карбонат (включая изомеры), (пентил)(дипропилфенил)карбонат (включая изомеры), (пентил)(дибутилфенил)карбонат (включая изомеры), (пентил)(дипентилфенил)карбонат (включая изомеры), (пентил)(дигексилфенил)карбонат (включая изомеры), (пентил)(дигептилфенил)карбонат (включая изомеры), (пентил)(фенилфенил)карбонат (включая изомеры), (пентил)(триметилфенил)карбонат (включая изомеры), (пентил)(триэтилфенил)карбонат (включая изомеры), (пентил)(трипропилфенил)карбонат (включая изомеры), (пентил)(трибутилфенил)карбонат (включая изомеры), (пентил)(фенилметил)карбонат (включая изомеры), (пентил)(фенилэтил)карбонат (включая изомеры), (пентил)(фенилпропил)карбонат (включая изомеры), (пентил)(фенилбутил)карбонат (включая изомеры), (пентил)(фенилпентил)карбонат (включая изомеры), (пентил)(фенилгексил)карбонат (включая изомеры), (пентил)(фенилгептил)карбонат (включая изомеры), (пентил)(фенилоктил)карбонат (включая изомеры), (пентил)(фенилнонил)карбонат (включая изомеры), (гексил)(гептил)карбонат (включая изомеры), (гексил)(октил)карбонат (включая изомеры), (гексил)(нонил)карбонат (включая изомеры), (гексил)(децил)карбонат (включая изомеры), (гексил)(ундецил)карбонат (включая изомеры), (гексил)(додецил)карбонат (включая изомеры), (гексил)(тридецил)карбонат (включая изомеры), (гексил)(тетрадецил)карбонат (включая изомеры), (гексил)(пентадецил)карбонат (включая изомеры), (гексил)(гексадецил)карбонат (включая изомеры), (гексил)(гептадецил)карбонат (включая изомеры), (гексил)(октадецил)карбонат (включая изомеры), (гексил)(нонадецил)карбонат (включая изомеры), (гексил)(фенил)карбонат (включая изомеры), (гексил)(метилфенил)карбонат (включая изомеры), (гексил)(этилфенил)карбонат (включая изомеры), (гексил)(пропилфенил)карбонат (включая изомеры), (гексил)(бутилфенил)карбонат (включая изомеры), (гексил)(пентилфенил)карбонат (включая изомеры), (гексил)(гексилфенил)карбонат (включая изомеры), (гексил)(гептилфенил)карбонат (включая изомеры), (гексил)(октилфенил)карбонат (включая изомеры), (гексил)(нонилфенил)карбонат (включая изомеры), (гексил)(децилфенил)карбонат (включая изомеры), (гексил)(бифенил)карбонат (включая изомеры), (гексил)(диметилфенил)карбонат (включая изомеры), (гексил)(диэтилфенил)карбонат (включая изомеры), (гексил)(дипропилфенил)карбонат (включая изомеры), (гексил)(дибутилфенил)карбонат (включая изомеры), (гексил)(дипентилфенил)карбонат (включая изомеры), (гексил)(дигексилфенил)карбонат (включая изомеры), (гексил)(дигептилфенил)карбонат (включая изомеры), (гексил)(фенилфенил)карбонат (включая изомеры), (гексил)(триметилфенил)карбонат (включая изомеры), (гексил)(триэтилфенил)карбонат (включая изомеры), (гексил)(трипропилфенил)карбонат (включая изомеры), (гексил)(трибутилфенил)карбонат (включая изомеры), (гексил)(фенилметил)карбонат (включая изомеры), (гексил)(фенилэтил)карбонат (включая изомеры), (гексил)(фенилпропил)карбонат (включая изомеры), (гексил)(фенилбутил)карбонат (включая изомеры), (гексил)(фенилпентил)карбонат (включая изомеры), (гексил)(фенилгексил)карбонат (включая изомеры), (гексил)(фенилгептил)карбонат (включая изомеры), (гексил)(фенилоктил)карбонат (включая изомеры), (гексил)(фенилнонил)карбонат (включая изомеры), (гептил)(октил)карбонат (включая изомеры), (гептил)(нонил)карбонат (включая изомеры), (гептил)(децил)карбонат (включая изомеры), (гептил)(ундецил)карбонат (включая изомеры), (гептил)(додецил)карбонат (включая изомеры), (гептил)(тридецил)карбонат (включая изомеры), (гептил)(тетрадецил)карбонат (включая изомеры), (гептил)(пентадецил)карбонат (включая изомеры), (гептил)(гексадецил)карбонат (включая изомеры), (гептил)(гептадецил)карбонат (включая изомеры), (гептил)(октадецил)карбонат (включая изомеры), (гептил)(нонадецил)карбонат (включая изомеры), (гептил)(фенил)карбонат (включая изомеры), (гептил)(метилфенил)карбонат (включая изомеры), (гептил)(этилфенил)карбонат (включая изомеры), (гептил)(пропилфенил)карбонат (включая изомеры), (гептил)(бутилфенил)карбонат (включая изомеры), (гептил)(пентилфенил)карбонат (включая изомеры), (гептил)(гексилфенил)карбонат (включая изомеры), (гептил)(гептилфенил)карбонат (включая изомеры), (гептил)(октилфенил)карбонат (включая изомеры), (гептил)(нонилфенил)карбонат (включая изомеры), (гептил)(децилфенил)карбонат (включая изомеры), (гептил)(бифенил)карбонат (включая изомеры), (гептил)(диметилфенил)карбонат (включая изомеры), (гептил)(диэтилфенил)карбонат (включая изомеры), (гептил)(дипропилфенил)карбонат (включая изомеры), (гептил)(дибутилфенил)карбонат (включая изомеры), (гептил)(дипентилфенил)карбонат (включая изомеры), (гептил)(дигексилфенил)карбонат (включая изомеры), (гептил)(дигептилфенил)карбонат (включая изомеры), (гептил)(фенилфенил)карбонат (включая изомеры), (гептил)(триметилфенил)карбонат (включая изомеры), (гептил)(триэтилфенил)карбонат (включая изомеры), (гептил)(трипропилфенил)карбонат (включая изомеры), (гептил)(трибутилфенил)карбонат (включая изомеры), (гептил)(фенилметил)карбонат (включая изомеры), (гептил)(фенилэтил)карбонат (включая изомеры), (гептил)(фенилпропил)карбонат (включая изомеры), (гептил)(фенилбутил)карбонат (включая изомеры), (гептил)(фенилпентил)карбонат (включая изомеры), (гептил)(фенилгексил)карбонат (включая изомеры), (гептил)(фенилгептил)карбонат (включая изомеры), (гептил)(фенилоктил)карбонат (включая изомеры), (гептил)(фенилнонил)карбонат (включая изомеры), (октил)(нонил)карбонат (включая изомеры), (октил)(децил)карбонат (включая изомеры), (октил)(ундецил)карбонат (включая изомеры), (октил)(додецил)карбонат (включая изомеры), (октил)(тридецил)карбонат (включая изомеры), (октил)(тетрадецил)карбонат (включая изомеры), (октил)(пентадецил)карбонат (включая изомеры), (октил)(гексадецил)карбонат (включая изомеры), (октил)(гептадецил)карбонат (включая изомеры), (октил)(октадецил)карбонат (включая изомеры), (октил)(нонадецил)карбонат (включая изомеры), (октил)(фенил)карбонат (включая изомеры), (октил)(метилфенил)карбонат (включая изомеры), (октил)(этилфенил)карбонат (включая изомеры), (октил)(пропилфенил)карбонат (включая изомеры), (октил)(бутилфенил)карбонат (включая изомеры), (октил)(пентилфенил)карбонат (включая изомеры), (октил)(гексилфенил)карбонат (включая изомеры), (октил)(гептилфенил)карбонат (включая изомеры), (октил)(октилфенил)карбонат (включая изомеры), (октил)(нонилфенил)карбонат (включая изомеры), (октил)(децилфенил)карбонат (включая изомеры), (октил)(бифенил)карбонат (включая изомеры), (октил)(диметилфенил)карбонат (включая изомеры), (октил)(диэтилфенил)карбонат (включая изомеры), (октил)(дипропилфенил)карбонат (включая изомеры), (октил)(дибутилфенил)карбонат (включая изомеры), (октил)(дипентилфенил)карбонат (включая изомеры), (октил)(дигексилфенил)карбонат (включая изомеры), (октил)(дигептилфенил)карбонат (включая изомеры), (октил)(фенилфенил)карбонат (включая изомеры), (октил)(триметилфенил)карбонат (включая изомеры), (октил)(триэтилфенил)карбонат (включая изомеры), (октил)(трипропилфенил)карбонат (включая изомеры), (октил)(трибутилфенил)карбонат (включая изомеры), (октил)(фенилметил)карбонат (включая изомеры), (октил)(фенилэтил)карбонат (включая изомеры), (октил)(фенилпропил)карбонат (включая изомеры), (октил)(фенилбутил)карбонат (включая изомеры), (октил)(фенилпентил)карбонат (включая изомеры), (октил)(фенилгексил)карбонат (включая изомеры), (октил)(фенилгептил)карбонат (включая изомеры), (октил)(фенилоктил)карбонат (включая изомеры), (октил)(фенилнонил)карбонат (включая изомеры), (метилфенил)(этилфенил)карбонат (включая изомеры), (метилфенил)(пропилфенил)карбонат (включая изомеры), (метилфенил)(бутилфенил)карбонат (включая изомеры), (метилфенил)(пентилфенил)карбонат (включая изомеры), (метилфенил)(гексилфенил)карбонат (включая изомеры), (метилфенил)(гептилфенил)карбонат (включая изомеры), (метилфенил)(октилфенил)карбонат (включая изомеры), (метилфенил)(нонилфенил)карбонат (включая изомеры), (метилфенил)(децилфенил)карбонат (включая изомеры), (метилфенил)(бифенил)карбонат (включая изомеры), (метилфенил)(диметилфенил)карбонат (включая изомеры), (метилфенил)(диэтилфенил)карбонат (включая изомеры), (метилфенил)(дипропилфенил)карбонат (включая изомеры), (метилфенил)(дибутилфенил)карбонат (включая изомеры), (метилфенил)(дипентилфенил)карбонат (включая изомеры), (метилфенил)(дигексилфенил)карбонат (включая изомеры), (метилфенил)(дигептилфенил)карбонат (включая изомеры), (метилфенил)(фенилфенил)карбонат (включая изомеры), (метилфенил)(триметилфенил)карбонат (включая изомеры), (метилфенил)(триэтилфенил)карбонат (включая изомеры), (метилфенил)(трипропилфенил)карбонат (включая изомеры), (метилфенил)(трибутилфенил)карбонат (включая изомеры), (метилфенил)(фенилметил)карбонат (включая изомеры), (метилфенил)(фенилэтил)карбонат (включая изомеры), (метилфенил)(фенилпропил)карбонат (включая изомеры), (метилфенил)(фенилбутил)карбонат (включая изомеры), (метилфенил)(фенилпентил)карбонат (включая изомеры), (метилфенил)(фенилгексил)карбонат (включая изомеры), (метилфенил)(фенилгептил)карбонат (включая изомеры), (метилфенил)(фенилоктил)карбонат (включая изомеры), (метилфенил)(фенилнонил)карбонат (включая изомеры), (этилфенил)(пропилфенил)карбонат (включая изомеры), (этилфенил)(бутилфенил)карбонат (включая изомеры), (этилфенил)(пентилфенил)карбонат (включая изомеры), (этилфенил)(гексилфенил)карбонат (включая изомеры), (этилфенил)(гептилфенил)карбонат (включая изомеры), (этилфенил)(октилфенил)карбонат (включая изомеры), (этилфенил)(нонилфенил)карбонат (включая изомеры), (этилфенил)(децилфенил)карбонат (включая изомеры), (этилфенил)(бифенил)карбонат (включая изомеры), (этилфенил)(диметилфенил)карбонат (включая изомеры), (этилфенил)(диэтилфенил)карбонат (включая изомеры), (этилфенил)(дипропилфенил)карбонат (включая изомеры), (этилфенил)(дибутилфенил)карбонат (включая изомеры), (этилфенил)(дипентилфенил)карбонат (включая изомеры), (этилфенил)(дигексилфенил)карбонат (включая изомеры), (этилфенил)(дигептилфенил)карбонат (включая изомеры), (этилфенил)(фенилфенил)карбонат (включая изомеры), (этилфенил)(триметилфенил)карбонат (включая изомеры), (этилфенил)(триэтилфенил)карбонат (включая изомеры), (этилфенил)(трипропилфенил)карбонат (включая изомеры), (этилфенил)(трибутилфенил)карбонат (включая изомеры), (этилфенил)(фенилметил)карбонат, (этилфенил)(фенилэтил)карбонат (включая изомеры), (этилфенил)(фенилпропил)карбонат (включая изомеры), (этилфенил)(фенилбутил)карбонат (включая изомеры), (этилфенил)(фенилпентил)карбонат (включая изомеры), (этилфенил)(фенилгексил)карбонат (включая изомеры), (этилфенил)(фенилгептил)карбонат (включая изомеры), (этилфенил)(фенилоктил)карбонат (включая изомеры), (этилфенил)(фенилнонил)карбонат (включая изомеры), (пропилфенил)(пропилфенил)карбонат (включая изомеры), (пропилфенил)(бутилфенил)карбонат (включая изомеры), (пропилфенил)(пентилфенил)карбонат (включая изомеры), (пропилфенил)(гексилфенил)карбонат (включая изомеры), (пропилфенил)(гептилфенил)карбонат (включая изомеры), (пропилфенил)(октилфенил)карбонат (включая изомеры), (пропилфенил)(нонилфенил)карбонат (включая изомеры), (пропилфенил)(децилфенил)карбонат (включая изомеры), (пропилфенил)(бифенил)карбонат (включая изомеры), (пропилфенил)(диметилфенил)карбонат (включая изомеры), (пропилфенил)(диэтилфенил)карбонат (включая изомеры), (пропилфенил)(дипропилфенил)карбонат (включая изомеры), (пропилфенил)(дибутилфенил)карбонат (включая изомеры), (пропилфенил)(дипентилфенил)карбонат (включая изомеры), (пропилфенил)(дигексилфенил)карбонат (включая изомеры), (пропилфенил)(дигептилфенил)карбонат (включая изомеры), (пропилфенил)(фенилфенил)карбонат (включая изомеры), (пропилфенил)(триметилфенил)карбонат (включая изомеры), (пропилфенил)(триэтилфенил)карбонат (включая изомеры), (пропилфенил)(трипропилфенил)карбонат (включая изомеры), (пропилфенил)(трибутилфенил)карбонат (включая изомеры), (пропилфенил)(фенилметил)карбонат (включая изомеры), (пропилфенил)(фенилэтил)карбонат (включая изомеры), (пропилфенил)(фенилпропил)карбонат (включая изомеры), (пропилфенил)(фенилбутил)карбонат (включая изомеры), (пропилфенил)(фенилпентил)карбонат (включая изомеры), (пропилфенил)(фенилгексил)карбонат (включая изомеры), (пропилфенил)(фенилгептил)карбонат (включая изомеры), (пропилфенил)(фенилоктил)карбонат (включая изомеры), (пропилфенил)(фенилнонил)карбонат (включая изомеры), (бутилфенил)(пентилфенил)карбонат (включая изомеры), (бутилфенил)(гексилфенил)карбонат (включая изомеры), (бутилфенил)(гептилфенил)карбонат (включая изомеры), (бутилфенил)(октилфенил)карбонат (включая изомеры), (бутилфенил)(нонилфенил)карбонат (включая изомеры), (бутилфенил)(децилфенил)карбонат (включая изомеры), (бутилфенил)(бифенил)карбонат (включая изомеры), (бутилфенил)(диметилфенил)карбонат (включая изомеры), (бутилфенил)(диэтилфенил)карбонат (включая изомеры), (бутилфенил)(дипропилфенил)карбонат (включая изомеры), (бутилфенил)(дибутилфенил)карбонат (включая изомеры), (бутилфенил)(дипентилфенил)карбонат (включая изомеры), (бутилфенил)(дигексилфенил)карбонат (включая изомеры), (бутилфенил)(дигептилфенил)карбонат (включая изомеры), (бутилфенил)(фенилфенил)карбонат (включая изомеры), (бутилфенил)(триметилфенил)карбонат (включая изомеры), (бутилфенил)(триэтилфенил)карбонат (включая изомеры), (бутилфенил)(трипропилфенил)карбонат (включая изомеры), (бутилфенил)(трибутилфенил)карбонат (включая изомеры), (бутилфенил)(фенилметил)карбонат (включая изомеры), (бутилфенил)(фенилэтил)карбонат (включая изомеры), (бутилфенил)(фенилпропил)карбонат (включая изомеры), (бутилфенил)(фенилбутил)карбонат (включая изомеры), (бутилфенил)(фенилпентил)карбонат (включая изомеры), (бутилфенил)(фенилгексил)карбонат (включая изомеры), (бутилфенил)(фенилгептил)карбонат (включая изомеры), (бутилфенил)(фенилоктил)карбонат (включая изомеры), (бутилфенил)(фенилнонил)карбонат (включая изомеры), (пентилфенил)(гексилфенил)карбонат (включая изомеры), (пентилфенил)(гептилфенил)карбонат (включая изомеры), (пентилфенил)(октилфенил)карбонат (включая изомеры), (пентилфенил)(нонилфенил)карбонат (включая изомеры), (пентилфенил)(децилфенил)карбонат (включая изомеры), (пентилфенил)(бифенил)карбонат (включая изомеры), (пентилфенил)(диметилфенил)карбонат (включая изомеры), (пентилфенил)(диэтилфенил)карбонат (включая изомеры), (пентилфенил)(дипропилфенил)карбонат (включая изомеры), (пентилфенил)(дибутилфенил)карбонат (включая изомеры), (пентилфенил)(дипентилфенил)карбонат (включая изомеры), (пентилфенил)(дигексилфенил)карбонат (включая изомеры), (пентилфенил)(дигептилфенил)карбонат (включая изомеры), (пентилфенил)(фенилфенил)карбонат (включая изомеры), (пентилфенил)(триметилфенил)карбонат (включая изомеры), (пентилфенил)(триэтилфенил)карбонат (включая изомеры), (пентилфенил)(трипропилфенил)карбонат (включая изомеры), (пентилфенил)(трибутилфенил)карбонат (включая изомеры), (пентилфенил)(фенилметил)карбонат (включая изомеры), (пентилфенил)(фенилэтил)карбонат (включая изомеры), (пентилфенил)(фенилпропил)карбонат (включая изомеры), (пентилфенил)(фенилбутил)карбонат (включая изомеры), (пентилфенил)(фенилпентил)карбонат (включая изомеры), (пентилфенил)(фенилгексил)карбонат (включая изомеры), (пентилфенил)(фенилгептил)карбонат (включая изомеры), (пентилфенил)(фенилоктил)карбонат (включая изомеры), (пентилфенил)(фенилнонил)карбонат (включая изомеры), (гексилфенил)(гептилфенил)карбонат (включая изомеры), (гексилфенил)(октилфенил)карбонат (включая изомеры), (гексилфенил)(нонилфенил)карбонат (включая изомеры), (гексилфенил)(децилфенил)карбонат (включая изомеры), (гексилфенил)(бифенил)карбонат (включая изомеры), (гексилфенил)(диметилфенил)карбонат (включая изомеры), (гексилфенил)(диэтилфенил)карбонат (включая изомеры), (гексилфенил)(дипропилфенил)карбонат (включая изомеры), (гексилфенил)(дибутилфенил)карбонат (включая изомеры), (гексилфенил)(дипентилфенил)карбонат (включая изомеры), (гексилфенил)(дигексилфенил)карбонат (включая изомеры), (гексилфенил)(дигептилфенил)карбонат (включая изомеры), (гексилфенил)(фенилфенил)карбонат (включая изомеры), (гексилфенил)(триметилфенил)карбонат (включая изомеры), (гексилфенил)(триэтилфенил)карбонат (включая изомеры), (гексилфенил)(трипропилфенил)карбонат (включая изомеры), (гексилфенил)(трибутилфенил)карбонат (включая изомеры), (гексилфенил)(фенилметил)карбонат (включая изомеры), (гексилфенил)(фенилэтил)карбонат (включая изомеры), (гексилфенил)(фенилпропил)карбонат (включая изомеры), (гексилфенил)(фенилбутил)карбонат (включая изомеры), (гексилфенил)(фенилпентил)карбонат (включая изомеры), (гексилфенил)(фенилгексил)карбонат (включая изомеры), (гексилфенил)(фенилгептил)карбонат (включая изомеры), (гексилфенил)(фенилоктил)карбонат (включая изомеры), (гексилфенил)(фенилнонил)карбонат (включая изомеры), (диметилфенил)(диэтилфенил)карбонат (включая изомеры), (диметилфенил)(дипропилфенил)карбонат (включая изомеры), (диметилфенил)(дибутилфенил)карбонат (включая изомеры), (диметилфенил)(дипентилфенил)карбонат (включая изомеры), (диметилфенил)(дигексилфенил)карбонат (включая изомеры), (диметилфенил)(дигептилфенил)карбонат (включая изомеры), (диметилфенил)(фенилфенил)карбонат (включая изомеры), (диметилфенил)(триметилфенил)карбонат (включая изомеры), (диметилфенил)(триэтилфенил)карбонат (включая изомеры), (диметилфенил)(трипропилфенил)карбонат (включая изомеры), (диметилфенил)(трибутилфенил)карбонат (включая изомеры), (диметилфенил)(фенилметил)карбонат (включая изомеры), (диметилфенил)(фенилэтил)карбонат (включая изомеры), (диметилфенил)(фенилпропил)карбонат (включая изомеры), (диметилфенил)(фенилбутил)карбонат (включая изомеры), (диметилфенил)(фенилпентил)карбонат (включая изомеры), (диметилфенил)(фенилгексил)карбонат (включая изомеры), (диметилфенил)(фенилгептил)карбонат (включая изомеры), (диметилфенил)(фенилоктил)карбонат (включая изомеры), (диметилфенил)(фенилнонил)карбонат (включая изомеры), (диэтилфенил)(дипропилфенил)карбонат (включая изомеры), (диэтилфенил)(дибутилфенил)карбонат (включая изомеры), (диэтилфенил)(дипентилфенил)карбонат (включая изомеры), (диэтилфенил)(дигексилфенил)карбонат (включая изомеры), (диэтилфенил)(дигептилфенил)карбонат (включая изомеры), (диэтилфенил)(фенилфенил)карбонат (включая изомеры), (диэтилфенил)(триметилфенил)карбонат (включая изомеры), (диэтилфенил)(триэтилфенил)карбонат (включая изомеры), (диэтилфенил)(трипропилфенил)карбонат (включая изомеры), (диэтилфенил)(трибутилфенил)карбонат (включая изомеры), (диэтилфенил)(фенилметил)карбонат (включая изомеры), (диэтилфенил)(фенилэтил)карбонат (включая изомеры), (диэтилфенил)(фенилпропил)карбонат (включая изомеры), (диэтилфенил)(фенилбутил)карбонат (включая изомеры), (диэтилфенил)(фенилпентил)карбонат (включая изомеры), (диэтилфенил)(фенилгексил)карбонат (включая изомеры), (диэтилфенил)(фенилгептил)карбонат (включая изомеры), (диэтилфенил)(фенилоктил)карбонат (включая изомеры), (диэтилфенил)(фенилнонил)карбонат (включая изомеры), (дипропилфенил)(дибутилфенил)карбонат (включая изомеры), (дипропилфенил)(дипентилфенил)карбонат (включая изомеры), (дипропилфенил)(дигексилфенил)карбонат (включая изомеры), (дипропилфенил)(дигептилфенил)карбонат (включая изомеры), (дипропилфенил)(фенилфенил)карбонат (включая изомеры), (дипропилфенил)(триметилфенил)карбонат (включая изомеры), (дипропилфенил)(триэтилфенил)карбонат (включая изомеры), (дипропилфенил)(трипропилфенил)карбонат (включая изомеры), (дипропилфенил)(трибутилфенил)карбонат (включая изомеры), (дипропилфенил)(фенилметил)карбонат (включая изомеры), (дипропилфенил)(фенилэтил)карбонат (включая изомеры), (дипропилфенил)(фенилпропил)карбонат (включая изомеры), (дипропилфенил)(фенилбутил)карбонат (включая изомеры), (дипропилфенил)(фенилпентил)карбонат (включая изомеры), (дипропилфенил)(фенилгексил)карбонат (включая изомеры), (дипропилфенил)(фенилгептил)карбонат (включая изомеры), (дипропилфенил)(фенилоктил)карбонат (включая изомеры), (дипропилфенил)(фенилнонил)карбонат (включая изомеры), (дибутилфенил)(дипентилфенил)карбонат (включая изомеры), (дибутилфенил)(дигексилфенил)карбонат (включая изомеры), (дибутилфенил)(дигептилфенил)карбонат (включая изомеры), (дибутилфенил)(фенилфенил)карбонат (включая изомеры), (дибутилфенил)(триметилфенил)карбонат (включая изомеры), (дибутилфенил)(триэтилфенил)карбонат (включая изомеры), (дибутилфенил)(трипропилфенил)карбонат (включая изомеры), (дибутилфенил)(трибутилфенил)карбонат (включая изомеры), (дибутилфенил)(фенилметил)карбонат (включая изомеры), (дибутилфенил)(фенилэтил)карбонат (включая изомеры), (дибутилфенил)(фенилпропил)карбонат (включая изомеры), (дибутилфенил)(фенилбутил)карбонат (включая изомеры), (дибутилфенил)(фенилпентил)карбонат (включая изомеры), (дибутилфенил)(фенилгексил)карбонат (включая изомеры), (дибутилфенил)(фенилгептил)карбонат (включая изомеры), (дибутилфенил)(фенилоктил)карбонат (включая изомеры), (дибутилфенил)(фенилнонил)карбонат (включая изомеры), (дипентилфенил)(дигексилфенил)карбонат (включая изомеры), (дипентилфенил)(дигептилфенил)карбонат (включая изомеры), (дипентилфенил)(фенилфенил)карбонат (включая изомеры), (дипентилфенил)(триметилфенил)карбонат (включая изомеры), (дипентилфенил)(триэтилфенил)карбонат (включая изомеры), (дипентилфенил)(трипропилфенил)карбонат (включая изомеры), (дипентилфенил)(трибутилфенил)карбонат (включая изомеры), (дипентилфенил)(фенилметил)карбонат (включая изомеры), (дипентилфенил)(фенилэтил)карбонат (включая изомеры), (дипентилфенил)(фенилпропил)карбонат (включая изомеры), (дипентилфенил)(фенилбутил)карбонат (включая изомеры), (дипентилфенил)(фенилпентил)карбонат (включая изомеры), (дипентилфенил)(фенилгексил)карбонат (включая изомеры), (дипентилфенил)(фенилгептил)карбонат (включая изомеры), (дипентилфенил)(фенилоктил)карбонат (включая изомеры), (дипентилфенил)(фенилнонил)карбонат (включая изомеры), (триметилфенил)(триэтилфенил)карбонат (включая изомеры), (триметилфенил)(трипропилфенил)карбонат (включая изомеры), (триметилфенил)(трибутилфенил)карбонат (включая изомеры), (триметилфенил)(фенилметил)карбонат (включая изомеры), (триметилфенил)(фенилэтил)карбонат (включая изомеры), (триметилфенил)(фенилпропил)карбонат (включая изомеры), (триметилфенил)(фенилбутил)карбонат (включая изомеры), (триметилфенил)(фенилпентил)карбонат (включая изомеры), (триметилфенил)(фенилгексил)карбонат (включая изомеры), (триметилфенил)(фенилгептил)карбонат (включая изомеры), (триметилфенил)(фенилоктил)карбонат (включая изомеры) и (триметилфенил)(фенилнонил)карбонат (включая изомеры).
В процессе получения N-замещенной карбаминовой кислоты-O-арилового эфира из композиции для транспортировки и хранения соединения, имеющего уреидные группы, варианта настоящего осуществления, и ароматического гидроксисоединения, и/или в процессе получения N-замещенной карбаминовой кислоты-O-R2 эфира из описанных выше соединения, имеющего уреидные группы, и спирта, в качестве побочного продукта образуется следовое количество эфира угольной кислоты. Предпочтительный аспект включает получение N-замещенной карбаминовой кислоты-O-арилового эфира с последующей рециркуляцией соединений, используемых на каждой стадии получения изоцианата термическим разложением N-замещенной карбаминовой кислоты-O-арилового эфира. Эфир угольной кислоты может присутствовать при получении композиции для транспортировки и хранения соединения, имеющего уреидные группы, в результате извлечения эфира угольной кислоты вместе с ароматическим гидроксисоединением. Эфир угольной кислоты, образующийся в качестве побочного продукта, является эфиром угольной кислоты, полученным из ароматического гидроксисоединения и/или спирта, используемых при получении N-замещенной карбаминовой кислоты-O-арилового эфира, а именно, эфиром угольной кислоты, где R38OH и R39OH, в которых гидроксильные группы были добавлены к R38 и R39 упомянутой выше формулы (20), соответствуют упомянутым выше ароматическому гидроксисоединению и/или спирту. При получении N-замещенной карбаминовой кислоты-O-арилового эфира с использованием соединения для транспортировки и хранения соединения, имеющего уреидные группы, которое содержит эфир угольной кислоты, существует также механизм, с помощью которого регенерируют N-замещенной карбаминовой кислоты-O-(R2 или ариловый) эфир путем его добавления к нежелательному соединению, имеющему уреиленовые группы, которое образуется вследствие конденсации N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира, в силу чего этот аспект становится предпочтительным. Кроме того, несмотря на то, что во многих случаях, помимо соединения мочевины, эфира карбаминовой кислоты и эфира угольной кислоты, могут содержаться сложнозамещенные мономеры или полимеры соединений мочевины, биуретов или нуратов и другие подобные соединения, тем не менее, содержание таких соединений не вызывает проблем.
Вкратце уже было дано объяснение нескольким стадиям при объяснении соединений, используемых в описанном выше варианте настоящего осуществления. Далее приводится подробное объяснение способа получения N-замещенной карбаминовой кислоты-O-арилового эфира из соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, так же, как и подробное объяснение каждой стадии, входящей в способ получения изоцианата из N-замещенной карбаминовой кислоты-O-арилового эфира. Способ получения N-замещенной карбаминовой кислоты-O-арилового эфира варианта настоящего осуществления является способом получения по меньшей мере одного N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого из соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, включающим стадию проведения реакции этерификации или стадий проведения реакции этерификации и реакции переэтерификации из соединения, имеющего уреидные группы, представленного формулой (1), и ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2) (здесь N-замещенной карбаминовой кислоты-O-ариловый эфир относится к сложному эфиру N-замещенной карбаминовой кислоты, в котором атом кислорода группы карбаминовой кислоты (-NHCOO-) связан с ароматическим кольцом, или, другими словами, N-замещенной карбаминовой кислоты-O-эфиру, полученному из соединения, имеющего уреидные группы, и ароматического гидроксисоединения). Более конкретно, способ получения является способом получения N-замещенной карбаминовой кислоты-O-арилового эфира, включающим стадию этерификации соединения, имеющего уреидные группы, и по меньшей мере одного типа ароматического гидроксисоединения, представленного формулой (2), или способом получения N-замещенной карбаминовой кислоты-O-арилового эфира, включающим стадию этерификации соединения, имеющего уреидные группы, и спирта, представленного формулой (4), с получением N-замещенной карбаминовой кислоты-O-R2 эфира, и стадию переэтерификации N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции. Более конкретно, способ получения является способом получения N-замещенной карбаминовой кислоты-O-арилового эфира из соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, который включает стадию (B), или способом получения N-замещенной карбаминовой кислоты-O-арилового эфира из соединения, имеющего уреидные группы, ароматической гидроксикомпозиции и спирта, представленного формулой (4), который включает стадию (R) и стадию (P). Предпочтительно, чтобы соединение, имеющее уреидные группы, являлось соединением, имеющим уреидные группы, полученным на стадии (A), и упомянутые выше способы получения, соответственно, включали способ получения, который включает стадию (A) и стадию (B), и способ получения, который включает стадию (A), стадию (R) и стадию (P). Упомянутый выше N-замещенной карбаминовой кислоты-O-R2 эфир относится к N-замещенной карбаминовой кислоты-O-эфиру, получаемому из соединения, имеющего уреидные группы, и R2 группы спирта, представленного формулой (4).
Сначала приводится краткое объяснение ранее упомянутых стадий (A), (B), (C), (R), (P) и (F) наряду с следующими стадиями (D), (E) и (G), которые также включены в способ получения варианта настоящего осуществления.
<Стадия (D)>
Следующую стадию (D) проводят для извлечения мочевины перед стадией (B), стадией (R) или стадией (P), или одновременно со стадией (B), стадией (R) или стадией (P):
стадия (D): стадия удаления мочевины ректификацией или сублимацией.
<Стадия (E)>
Стадия (E): стадия рециркуляции мочевины, извлеченной на стадии (D), на стадию (A).
<Стадия (G)>
Следующую стадию (G) проводят для извлечения аммиака, образующегося в качестве побочного продукта на стадии (A), и/или стадии (B), и/или стадии (R), реакции аммиака с диоксидом углерода для регенерации мочевины, и рециркуляции мочевины на стадию (A):
стадия (G): стадия извлечения аммиака, образующегося в качестве побочного продукта, реакции аммиака с диоксидом углерода для регенерации мочевины и рециркуляции мочевины на стадию (A).
Далее упомянутые выше стадии (D), (E) и (G) будут описаны подробно.
Способ получения N-замещенной карбаминовой кислоты-O-арилового эфира варианта настоящего осуществления позволяет получать разнообразные N-замещенной карбаминовой кислоты-O-ариловые эфиры путем выбора используемых соединений, таких как органический первичный амин, ароматическая гидроксикомпозиция и дополнительно спирт и другие подобные соединения, вместе с выбором и объединением упомянутых выше стадий (A)-(G), и, кроме того, позволяет получать изоцианат из N-замещенной карбаминовой кислоты-O-арилового эфира.
<Способ получения соединения, имеющего уреидные группы>
Как уже было описано ранее, соединение, имеющее уреидные группы, используемое в варианте настоящего осуществления, может являться соединением, имеющим уреидные группы, которое получают известным способом. Предпочтительно, чтобы оно являлось соединением, имеющим уреидные группы, которое получают с использованием следующей стадии (A):
стадия (A): стадия получения по меньшей мере одного типа соединения, имеющего уреидные группы, получаемого из органического первичного амина, представленного следующей формулой (3), и мочевины, путем проведения реакции образования уреидов из органического первичного амина и мочевины в жидкой фазе и удаления или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта при реакции образования уреидов.
Термин "удаленный" не относится к аммиаку в прямом смысле, а относится к растворенному и/или диспергированному аммиаку в жидкой фазе.
На фигуре 1 приведена принципиальная схема стадии (A) в варианте настоящего осуществления. Кроме того, упомянутая выше реакция образования уреидов обозначает реакцию между аминогруппой органического первичного амина и уреидной группой, а именно, реакцию, в которой органический первичный амин превращается в соединение, имеющее уреидные группы.
В результате обширных исследований, проведенных авторами настоящего изобретения, авторы настоящего изобретения предложили механизм реакции, по которому образуется соединение, имеющее уреидные группы, из органического первичного амина и мочевины, и который будет описан ниже, несмотря на то, что он до конца еще не ясен. Кроме того, для того чтобы упростить дальнейшее объяснение, органический первичный амин, имеющий две аминогруппы, показан как органический первичный амин. Естественно, что случаи использования органического первичного амина, отличающегося от того, который здесь показан, могут быть рассмотрены аналогичным образом.
По-видимому, реакция образования соединения, имеющего уреидные группы, из органического первичного амина и мочевины, может быть описана следующим уравнением реакции (111), и она протекает с образованием аммиака в качестве побочного продукта:
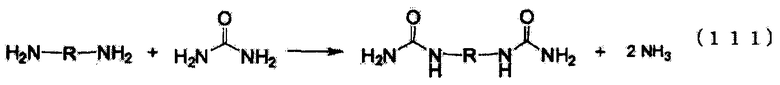
(где
R представляет органическую группу, замещенную с помощью двух заместителей).
При реакции образования соединения, имеющего уреидные группы, по приведенному выше уравнению (111), могут протекать параллельно побочная реакция, в которой, например, соединение, имеющее уреиленовые группы, образуется из соединения, имеющего уреидные группы, и органического первичного амина, представленная следующим уравнением (113), или, например, побочная реакция, в которой соединение, имеющее биуретные группы, образуется путем конденсации соединения, имеющего уреидные группы, представленная следующим уравнением (114) (уравнения реакций, используемые для объяснения в варианте настоящего осуществления, приводятся для отображения общих представлений о реакциях (являются ли соединения исходными реагентами или продуктами), и часто не отражают стехиометрию реакции):
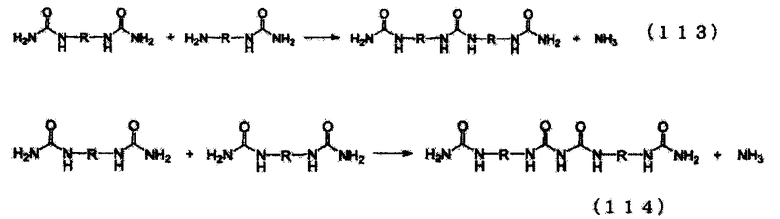
(где
R представляет двухвалентную органическую группу).
Далее приводится объяснение количеств органического первичного амина и мочевины, используемых в качестве сырья на стадии (A). Количество мочевины находится в интервале мольных отношений от 1 до 100 относительно аминогрупп органического первичного амина. Как уже было объяснено ранее в случае эфира не-N-замещенной карбаминовой кислоты, в случае не-N-замещенной карбаминовой кислоты-O-R2 эфира и/или N-замещенной карбаминовой кислоты-O-арилового эфира, соединение, имеющее уреидные группы, также может быть получено путем реакции с органическим первичным амином таким же образом, как и с мочевиной. А именно, количества мочевины, указанные ранее и указанные далее, являются суммарными мольными количествами мочевины, не-N-замещенной карбаминовой кислоты-O-R2 эфира и не-N-замещенной карбаминовой кислоты O-арилового эфира. В случае, когда количество используемой мочевины (и не-N-замещенной карбаминовой кислоты эфира) является низким, легко образуются сложнозамещенные карбонильные соединения и другие подобные соединения по приведенному выше уравнению (113), и поэтому предпочтительно использовать избыток мочевины и не-N-замещенной карбаминовой кислоты эфира.
Кроме того, предполагается, что мочевина и не-N-замещенной карбаминовой кислоты эфир, присутствующие в избытке в реакционной системе стадии (A), стабилизируют образующееся соединение, имеющее уреидные группы (не-N-замещенной карбаминовой кислоты-O-R2 эфир и/или не-N-замещенной карбаминовой кислоты-O-ариловый эфир часто вместе называют не-N-замещенной карбаминовой кислоты эфиром). Согласно исследованиям, проведенным авторами настоящего изобретения, в ряде случаев в процессе получения соединения, имеющего уреидные группы, в зависимости от условий реакции образуются соединения, имеющие биуретную связь (такие как соединение в правой части следующего уравнения (125)), или соединения, имеющие биуретную концевую группу (соединение в правой части следующего уравнения (126)). Для того чтобы селективно образовывалось целевое соединение, имеющее уреидные группы, важно подавить образование таких соединений. В результате обширных исследований, проведенных авторами настоящего изобретения, было неожиданно обнаружено, что существует тесная взаимосвязь между количеством мочевины (и количеством не-N-замещенной карбаминовой кислоты эфира) в реакционной системе и количествами таких образующихся соединений, и что количества таких соединений уменьшаются с увеличением количества присутствующей мочевины (и не-N-замещенной карбаминовой кислоты эфира). Несмотря на то, что механизм, на основании которого присутствующая в реакционной системе мочевина проявляет этот эффект, не ясен, авторы настоящего изобретения сделали предположения относительно этого механизма, которые приведены ниже.
Сначала, рассматривается механизм, на основании которого образуются соединения, имеющие биуретную связь, и соединения, имеющие биуретную концевую группу. Соединение, имеющее уреидные группы, образует в зависимости от условий реакции соединение, имеющее изоцианатную концевую группу (-NCO группу), и аммиак вследствие термического разложения уреидных групп (согласно следующему уравнению (124), например):
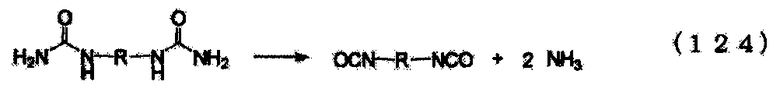
(где
R представляет двухвалентную органическую группу).
Предполагается, что в ряде случаев соединение, имеющее изоцианатную концевую группу, реагирует с мочевиной (и не-N-замещенной карбаминовой кислоты эфиром) (как, например, в следующих уравнениях (125) и (126) объясняется использование мочевины) с образованием соединения, имеющего биуретную связь, или соединения, имеющего биуретную концевую группу:
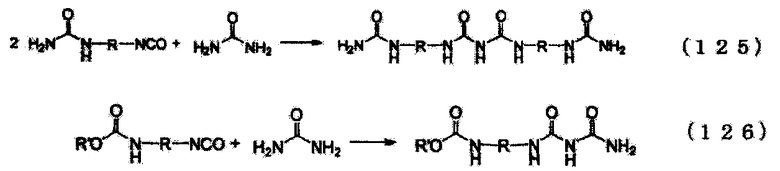
(где
R представляет двухвалентную органическую группу).
Предполагается, что мочевина (и не-N-замещенной карбаминовой кислоты эфир) стабилизирует в реакционной жидкости уреидные группы путем взаимодействия с уреидными группами с образованием водородной связи, и подавляет, в частности, первую реакцию (а именно, реакцию, представленную выше уравнением (124)) из этой последовательности реакций.
Таким образом, для селективного образования соединения, имеющего уреидные группы, важным моментом является использование избыточного количества мочевины (и не-N-замещенной карбаминовой кислоты эфира). Однако, использование мочевины в слишком большом избытке (и не-N-замещенной карбаминовой кислоты эфира) приводит к увеличению размера реактора, что нежелательно с точки зрения возможности промышленного использования, или, как будет описано позже, может усложнять отделение и извлечение мочевины (и не-N-замещенной карбаминовой кислоты эфира). Таким образом, предпочтительно, чтобы количество используемой мочевины, выраженное через мольное отношение к аминогруппам органического первичного амина, находилось в интервале от 1 до 100, более предпочтительно, в интервале от 1,1 до 10, и наиболее предпочтительно, в интервале от 1,5 до 5.
Кроме того, необходимо также обратить внимание на методику проведения реакции, принимая во внимание описанную выше роль мочевины (и не-N-замещенной карбаминовой кислоты эфира). А именно, предпочтительно осуществлять способ, в котором, например, все количество используемой мочевины (и не-N-замещенной карбаминовой кислоты эфира) растворяют заранее в реакционном растворителе (которой будет подробно описан далее) с последующим добавлением к этому перемешанному раствору органического первичного амина, так чтобы постоянно поддерживать число молекул мочевины (и не-N-замещенной карбаминовой кислоты эфира) в реакционной системе в избытке (и, если это возможно, в большом избытке) относительно числа аминогрупп органического первичного амина.
Далее приводится объяснение относительно концентрации аммиака в системе. Кроме того, описываемый здесь предпочтительный интервал концентрации аммиака относится к концентрации аммиака в реакционной жидкости после того, как образовалось, в определенной степени, соединение, имеющее уреидные группы (например, при выходе не меньше, чем 5%, по органическому амину), и не относится к концентрации в начале реакции.
Реакция, в которой образуется N-замещенной карбаминовой кислоты-O-(R2 и/или ариловый) эфир (такая как реакция согласно следующему уравнению (118)), является обратимой реакцией, и ее равновесие значительно сдвинуто в сторону исходных реагентов. Однако, в результате исследований, проведенных авторами настоящего изобретения, было определено, что реакция, в которой образуется соединение, имеющее уреидные группы (реакция согласно упомянутому выше уравнению (117)), является реакцией, в которой равновесие в значительной степени сдвинуто в сторону продуктов реакции, или которая является необратимой реакцией, и которая фактически не зависит от концентрации аммиака в системе. Такой вывод был до настоящего времени неизвестен и является неожиданным. Таким образом, было обнаружено, что соединение, имеющее уреидные группы, может селективно образовываться при поддержании на определенном уровне или выше концентрации аммиака в реакционной жидкости стадии (A), и может быть предотвращено образование N-замещенной карбаминовой кислоты эфира путем реакции между образовавшимся соединением, имеющим уреидные группы, и ароматическим гидроксисоединением (реакция по упомянутому выше уравнению (118)), и было дополнительно обнаружено, что соединение, имеющее уреидные группы, может быть получено с высокой селективностью в результате подавления побочных реакций путем поддержания концентрации аммиака на определенном уровне или выше. В ранее раскрытых способах получения соединений, имеющих уреидные группы, при получении соединения, имеющего уреидные группы, легко образовывались продукты побочных реакций в соответствии с упомянутой выше реакцией, и они содержались в таком количестве, при котором одновременно образовывался в больших количествах N-замещенной карбаминовой кислоты-O-алкиловый эфир, образующийся в соответствии со следующим уравнением реакции (118), что в результате приводило к серьезной проблеме протекания сопутствующих побочных реакций, связанных с N-замещенной карбаминовой кислоты-O-алкиловым эфиром. Для решения этой проблемы являются важными количество используемой мочевины (и не-N-замещенной карбаминовой кислоты эфира) и/или концентрация аммиака. Предпочтительной концентрацией аммиака для проявления этого эффекта является концентрация выше, чем 10 ppm, более предпочтительно, выше, чем 100 ppm, еще более предпочтительно, выше, чем 300 ppm, и наиболее предпочтительно, выше, чем 1000 ppm.
Кроме того, при использовании термина "N-замещенной карбаминовой кислоты-O-(R2 и/или ариловый) эфир" для объяснения настоящего описания изобретения, он относится к "N-замещенной карбаминовой кислоты-O-R2 эфиру и/или N-замещенной карбаминовой кислоты-O-ариловому эфиру":
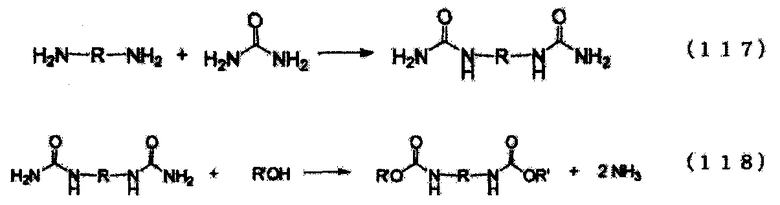
(где
R представляет органическую группу, замещенную с помощью двух заместителей, и
R'OH представляет одновалентное гидроксисоединение (спирт или ароматическое гидроксисоединение)).
Стадия (A) может быть проведена при температуре реакции в интервале от 30 до 250°C. Несмотря на то, что высокая температура является предпочтительной для увеличения скорости реакции, с другой стороны, так как при высоких температурах протекают нежелательные реакции (такие как разложение производной угольной кислоты), приводя к образованию сложнозамещенных соединений мочевины и карбонильных соединений, предпочтительно, чтобы температура реакции находилась в интервале от 50 до 200°C, и более предпочтительно, в интервале от 70 до 180°C. Для поддержания постоянной температуры реакции в реакторе для проведения стадии (A) может быть установлено известное оборудование для охлаждения или оборудование для нагрева.
В зависимости от типов используемых соединений, композиции реакционной системы, температуры реакции, реакционных аппаратов и других подобных параметров обычно предпочтительно проводить реакцию при давлении в интервале от 0,01 кПа до 10 МПа (абсолютное давление), и, принимая во внимание возможность промышленного использования, предпочтительно проводить реакцию при давлении в интервале от 0,1 кПа до 5 МПа (абсолютное давление).
Нет конкретных ограничений для времени реакции (времени пребывания в случае непрерывного способа) на стадии (A), и время реакции обычно составляет от 0,001 до 100 часов, предпочтительно, от 0,01 до 80 часов, и более предпочтительно, от 0,1 до 50 часов. Кроме того, реакция может быть остановлена после подтверждения того, что образовалось требуемое количество соединения, имеющего уреидные группы, путем взятия пробы реакционной жидкости и определения количества соединения, имеющего уреидные группы, с помощью, например, жидкостной хроматографии. Стадия (A) является стадией получения соединения, имеющего уреидные группы, на стадии (A), но если присутствует большое количество аминогрупп, полученных из непрореагировавшего органического амина, то в процессе хранения при использовании в форме композиции для транспортировки и хранения соединения, имеющего уреидные группы, или на стадии (B), или стадии (R), на которых используется реакционная жидкость после стадии (A), образуются соединения, имеющие уреиленовые группы, и другие подобные соединения, что часто не только вызывает снижение количества образующегося N-замещенной карбаминовой кислоты-O-эфира, но также вызывает явление слипания и затвердевания в реакторе. Таким образом, на стадии (A) предпочтительно снижать количество аминогрупп, полученных из органического первичного амина, путем образования соединения, имеющего уреидные группы, как можно с более высоким выходом. Более конкретно, реакцию предпочтительно проводить до тех пор, пока отношение числа аминогрупп, полученных из органического первичного амина, к числу уреидных групп, составляющих соединение, имеющее уреидные группы, не станет составлять 0,25 или менее, более предпочтительно, 0,1 или менее, и еще более предпочтительно, 0,05 или менее.
В варианте настоящего осуществления в случае необходимости может быть использован катализатор, и примеры катализаторов, которые могут быть использованы, включают органические соединения металлов и неорганические соединения металлов олова, свинца, меди или титана, и основные катализаторы, такие как алкоголяты щелочных металлов или щелочноземельных металлов в виде метилатов, этилатов и бутиратов (включая изомеры) лития, натрия, калия, кальция или бария. Если добавляют катализатор, то во многих случаях катализатор затем необходимо удалять, и поэтому предпочтительно проводить реакцию без добавления катализатора. В случае использования катализатора катализатор может быть удален после реакции. Так как в ряде случаев на стадиях варианта настоящего осуществления катализатор оказывает отрицательное действие на соединения, то в процессе получения изоцианата термическим разложением N-замещенной карбаминовой кислоты-O-арилового эфира и очистки изоцианата катализатор предпочтительно отделять или удалять. В случае хранения изоцианата в присутствии катализатора может происходить изменение цвета и другие нежелательные явления. Для удаления катализатора может быть использован известный способ, и могут быть использованы такие способы, как мембранное разделение, ректификационное разделение или кристаллизация. Катализатор предпочтительно удалять по причинам, описанным выше, без накладывания ограничений для стадии (A). Более предпочтительно, чтобы катализатор удаляли при завершении стадии, на которой он используется. Для удаления катализатора могут предпочтительно использоваться ранее описанные известные способы.
С точки зрения снижения вязкости реакционной жидкости и/или поддержания реакционной системы в гомогенном состоянии предпочтительно проводить реакцию стадии (A) в жидкой фазе в присутствии растворителя. Примеры растворителей, которые могут быть предпочтительно использованы в качестве реакционных растворителей могут включать алканы, такие как пентан (включая изомеры), гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; нитрильные соединения, такие как ацетонитрил или бензонитрил; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; сложные эфиры, такие как дибутилфталат, дигексилфталат, диоктилфталат или бензилбутилфталат; простые эфиры и тиоэфиры, такие как тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, дифениловый эфир или дифенилсульфид; кетоновые соединения, такие как ацетон или метилэтилкетон; эфирные соединения, такие как этилацетат или этилбензоат; сульфоксиды, такие как диметилсульфоксид или дифенилсульфоксид, и гидроксисоединения, такие как вода, спирты или ароматические гидроксисоединения. Однако, с точки зрения растворимости продукта в форме соединения, имеющего уреидные группы, предпочтительно, чтобы реакционным растворителем являлась вода или гидроксикомпозиция (композиция, содержащая спирт и/или ароматическое гидроксисоединение), и более предпочтительно, гидроксикомпозиция (при этом гидроксикомпозиция является гидроксикомпозицией, состоящей из одного типа или множества типов гидроксисоединений (спирта, представленного формулой (4), и/или ароматического гидроксисоединения, представленного формулой (2)), и гидроксикомпозицию, предпочтительно используемую в качестве реакционного растворителя на стадии (A), далее называют "гидроксикомпозицией a"). Кроме того, эти растворители могут быть использованы сами по себе или в виде смеси двух или более их типов.
Гидроксисоединения, которые составляют гидроксикомпозицию, могут быть абсолютно одинаковыми, частично похожими или отличаться от гидроксикомпозиции, используемой на стадии (B), стадии (R) или стадии (P) (композиции, состоящей из ароматического гидроксисоединения и/или спирта, которые составляют ароматическую гидроксикомпозицию), но для того чтобы облегчить методику, предпочтительно, чтобы гидроксикомпозиция либо являлась аналогичной гидроксикомпозиции, используемой на стадии (B) или стадии (P), либо являлась композицией, состоящей из той гидроксикомпозиции. Далее будет приведено объяснение этому, но более предпочтительно или проводить реакцию стадии (A) в присутствии ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)), или проводить реакцию стадии (A) в присутствии спирта или ароматической гидроксикомпозиции с последующим добавлением ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)). Стадию (A) более предпочтительно проводить в присутствии ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)). В случае проведения стадии (R) после стадии (A) может быть использован только спирт, и в этом случае ароматическую гидроксикомпозицию (композицию, содержащую по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)) добавляют после проведения реакции стадии (A).
Указанные здесь реакционные растворители могут быть использованы в произвольном количестве, но в случае использования спирта в качестве реакционного растворителя, он может быть использован при мольном отношении в интервале от больше, чем 1 до меньше, чем 100 относительно аминогрупп органического первичного амина. Для улучшения текучести реакционной жидкости и более эффективного проведения реакции предпочтительно использовать избыток спирта относительно аминогрупп органического первичного амина, но так как могут возникать проблемы, такие как увеличение размера реактора, при использовании чрезмерного избытка спирта, то более предпочтительно использовать спирт при мольном отношении в интервале от больше, чем 5 до меньше, чем 50, и еще более предпочтительно, в интервале от больше, чем 8 до меньше, чем 20 относительно аминогрупп органического первичного амина.
Кроме того, в случае использования ароматической гидроксикомпозиции в качестве реакционного растворителя стадии (A), она может быть использована при мольном отношении в интервале от больше, чем 1 до меньше, чем 100 относительно аминогрупп органического первичного амина. Для улучшения текучести реакционной жидкости и более эффективного проведения реакции предпочтительно использовать избыток спирта относительно аминогрупп органического первичного амина, но так как могут возникать проблемы, такие как увеличение размера реактора, при использовании чрезмерного избытка спирта, то более предпочтительно использовать спирт при мольном отношении в интервале от больше, чем 2 до меньше, чем 50, и еще более предпочтительно, в интервале от больше, чем 3 до меньше, чем 20 относительно аминогрупп органического первичного амина.
Среди гидроксисоединений, представленных соединениями, выбранными из спиртов, представленных упомянутой выше формулой (4), и ароматических гидроксисоединений, представленных формулой (2), с точки зрения растворимости образующегося соединения, имеющего уреидные группы, предпочтительно использовать ароматическое гидроксисоединение. Например, в патентном документе Japanese Examined Patent Publication No. H2-48539 описано, что соединение, имеющее уреидные группы, плохо растворимо в н-бутаноле, но что касается ароматического гидроксисоединения, то оно часто обеспечивают более высокую растворимость для соединений, имеющих уреидные группы. Кроме того, ароматические гидроксисоединения часто оказывают промотирующее действие на реакции между органическим первичным амином и мочевиной (и не-N-замещенной карбаминовой кислоты эфиром). Несмотря на то, что механизм, на основании которого проявляется этот эффект, неясен, тем не менее, авторы настоящего изобретения предположили, что мочевина (и не-N-замещенной карбаминовой кислоты эфир) обычно имеет тенденцию образовывать ассоциаты вследствие наличия водородной связи, но ароматические гидроксисоединения имеют кислотные гидроксильные группы, и эти гидроксильные группы предотвращают ассоциацию между молекулами мочевины (и не-N-замещенной карбаминовой кислоты эфиром), тем самым облегчая аминам достижение реакционных центров мочевины (и не-N-замещенной карбаминовой кислоты эфира) (которыми, как предполагается, являются углеродные атомы, которые составляют карбонильные группы мочевины (и не-N-замещенной карбаминовой кислоты эфира)).
В случае использования ароматической гидроксикомпозиции в качестве реакционного растворителя ароматическое гидроксисоединение может быть использовано само по себе или в виде смеси с другими растворителями, но количество используемого ароматического гидроксисоединения находится в интервале ранее описанных значений. В случае добавления ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)) после проведения стадии (A) также в присутствии спирта, ароматическую гидроксикомпозицию используют в ранее описанных интервалах. В данном случае количество спирта, используемого во время реакции на стадии (A), также используют при ранее описанном мольном отношении, указанном для ароматического гидроксисоединения относительно органического первичного амина. В случае использования воды на стадии (A) воду предпочтительно использовать вместе с ароматической гидроксикомпозицией и/или спиртом. Вода сама по себе может быть использована в качестве растворителя, но может возникнуть необходимость в удалении воды после завершения стадии (A). При добавлении ароматического гидроксисоединения в описанном выше количестве для получения композиция для транспортировки и хранения соединения, имеющего уреидные группы, путем использования соединения, имеющего уреидные группы, полученного на стадии (A), в ряде случаев реакционная жидкость расслаивается на водную фазу и органическую фазу, или ароматическое гидроксисоединение и соединение, имеющее уреидные группы, затвердевают. Кроме того, при проведении стадии (R) или стадии (B) после добавления ароматического гидроксисоединения в описанном выше количестве после завершения стадии (A), нельзя получить гомогенную жидкость для транспортировки, и в силу описанных выше причин насосы и линии для перекачки могут забиваться. Таким образом, в случае использования только воды в качестве растворителя на стадии (A), воду удаляют перед добавлением или после добавления ароматического гидроксисоединения. В зависимости от используемых соединений и композиции воду удаляют до тех пор, пока количество воды в реакционной жидкости (или смешанной жидкости) после ее удаления не будет находиться в интервале от 10 ppm до 10% по массе, предпочтительно, от 10 ppm до 5% по массе, и более предпочтительно, от 10 ppm до 2% по массе. В качестве способа удаления воды может быть использован известный способ удаления воды, и примеры способов, которые могут быть использованы, предпочтительно включают удаление ректификацией при пониженном давлении или нормальном давлении, использование адсорбента, такого как цеолит, добавление гидролизуемого соединения, такого как ацеталь с последующим удалением воды в результате реакции гидролиза, и удаление воды с помощью соединения, которое реагирует с водой, такого как N,N-дициклогексилкарбодиимид. Более предпочтительно удалять воду ректификацией. В случае использования воды вместе с ароматической гидроксикомпозицией и/или спиртом в качестве растворителя на стадии (A) количество воды в реакционной среде находится в интервале от 10 ppm до 10% по массе, предпочтительно, от 10 ppm до 5% по массе, и более предпочтительно, от 10 ppm до 2% по массе. Авторы настоящего изобретения неожиданно обнаружили, что вследствие присутствия воды происходит повышение скорости реакции на стадии (A). Таким образом, предпочтительным способом является наличие воды в процессе реакции. Несмотря на то, что подробно это явление не было изучено, предполагается, что вода усиливает нуклеофильность органического первичного амина.
Нет конкретных ограничений для реакционного аппарата, используемого при проведении реакции, и может быть использован известный реактор. Например, могут быть соответствующим образом подсоединены известные обычные реакторы, такие как реактор с мешалкой, работающий при повышенном давлении реактор с мешалкой, работающий при пониженном давлении реактор с мешалкой, реактор колонного типа, ректификационная колонна, насадочная колонна или пленочный дистилляционный аппарат. Предпочтительно использовать реактор типа резервуара, снабженного мешалкой. Нет конкретных ограничений для материала реакторов, и могут быть использованы известные материалы. Их примеры могут включать стекло, нержавеющую сталь, углеродистую сталь, сплав Хастелой, эмалированные материалы и материалы с тефлоновым покрытием. Материалы, такие как SUS304, SUS316 или SUS316L, являются недорогими, и их предпочтительно использовать. Могут быть добавлены при необходимости известные технологические устройства, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства, для нагревания может быть использован такой известный способ, как пар или нагреватель, и для охлаждения может быть использован такой известный способ, как воздушное охлаждение, охлаждение водой или рассолом. Могут также быть добавлены стадии, в случае необходимости. Например, могут быть добавлены стадии и установки, которые являются известными для обычного специалиста в этой области, такие как стадия удаления образующегося аммиака, стадия очистки органического первичного амина, стадия растворения мочевины в ароматическом гидроксисоединении, стадия растворения ароматического гидроксисоединения, стадия отделения спирта, стадия отделения и/или очистки ароматического гидроксисоединения, стадия очистки соединения, имеющего уреидные группы, от образующейся реакционной жидкости, или стадия сжигания или вывода побочных продуктов и другие подобные стадии.
В случае использования реакционного растворителя на стадии (A) реакционный растворитель может быть удален из реакционной жидкости стадии (A) при получении композиции для транспортировки и хранения соединения, имеющего уреидные группы, до требуемого содержания, или перед проведением стадии (B) или стадии (R), или композиция может быть приготовлена без удаления реакционного растворителя, или стадия может быть проведена без удаления реакционного растворителя. В частности, гидроксисоединение, используемое в качестве реакционного растворителя на стадии (A), предпочтительно использовать в качестве части гидроксикомпозиции стадии (B) или стадии (R).
Аммиак, образующийся в качестве побочного продукта на стадии (A), может быть извлечен в форме газообразного аммиака путем введения в конденсатор, предусмотренный в реакторе, при пониженном давлении или нормальном давлении, и конденсации всей или части гидроксикомпозиции, используемой на стадии (A), с соединением, имеющим карбонильные группы, полученным из мочевины.
В варианте настоящего осуществления, который является осуществлением способа, включающего стадию этерификации, или этерификации и переэтерификации, соединения, имеющего уреидные группы (и, предпочтительно, соединения, имеющего N-замещенные уреидные группы), и ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2) (а именно, способа, включающего стадию (B) или стадию (R) и стадию (P)), примеры аспектов способа получения по меньшей мере одного N-замещенной карбаминовой кислоты-O-ариловый эфира, полученного из соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции (где N-замещенной карбаминовой кислоты-O-ариловый эфир относится к эфиру N-замещенной карбаминовой кислоты, в котором атом кислорода группы карбаминовой кислоты (-NHCOO-) связан с ароматическим кольцом) включают пять указанных ниже аспектов, если способ дополнительно включает способ проведения стадии (C). Другие аспекты также являются возможными на основе варианта настоящего осуществления, и вариант настоящего осуществления не ограничивается пятью указанными ниже аспектами.
Примеры аспектов варианта настоящего осуществления могут включать следующие пять направлений, которые осуществляют после получения соединения, имеющего уреидные группы, или после получения по меньшей мере одного типа соединения, имеющего уреидные группы (или реакционной жидкости, содержащей соединение, имеющее уреидные группы), путем проведения стадии (A):
направление 1) способ проведения стадии (B);
направление 2) способ проведения стадии (B) и затем стадии (C);
направление 3) способ проведения стадии (R) и затем стадии (P)
направление 4) способ проведения стадии (R), стадии (P) и затем стадии (C); и
направление 5) способ проведения стадии (R), стадии (C) и затем стадии (P).
Способ, который включает стадию (B), является способом получения N-замещенной карбаминовой кислоты-O-арилового эфира из соединения, имеющего уреидные группы (или реакционной жидкости, содержащей соединение, имеющее уреидные группы), и ароматической гидроксикомпозиции путем реакции этерификации, в то время как способ, который включает стадию (R), является способом получения N-замещенной карбаминовой кислоты-O-арилового эфира путем этерификации соединения, имеющего уреидные группы, и спирта с получением N-замещенной карбаминовой кислоты-O-R2 эфира, и затем путем переэтерификации N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции на стадии, которая включает стадию (P).
В первом из упомянутых выше способов, N-замещенной карбаминовой кислоты-O-ариловый эфир получают из соединения, имеющего уреидные группы (или после его получения), и ароматической гидроксикомпозиции.
Сначала приводится объяснение направления 1).
<Направление 1)>
Направление 1) включает способ осуществления стадии (B).
Направление 1) является способом получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, или из композиции для транспортировки и хранения соединения, имеющего уреидные группы.
<Стадия (B)>
Стадия (B): Стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции по меньшей мере одного типа соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)) в жидкой фазе и затем извлечения аммиака, образующегося в качестве побочного продукта, в газовую фазу (реакцией является реакция этерификации).
По меньшей мере один тип соединения, имеющего уреидные группы, может являться соединением, имеющим уреидные группы, полученным с помощью известного способа, при условии, что оно является соединением, имеющим уреидные группы, представленным формулой (1). Предпочтительно, чтобы оно являлось по меньшей мере одним типом соединения, имеющего уреидные группы, полученным на стадии (A), или реакционной жидкостью, содержащей по меньшей мере один тип соединения, имеющего уреидные группы, полученной на стадии (A). Реакционная жидкость относится к жидкости, получающейся вследствие завершения реакции стадии (A), и/или к реакционной жидкости, к которой была добавлена ароматическая гидроксикомпозиция (композиция, содержащая по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2)) после проведения реакции стадии (A) в присутствии спирта или ароматической гидроксикомпозиции, и представляет реакционную жидкость, содержащую по меньшей мере один тип соединения, имеющего уреидные группы, и гидроксикомпозицию. В качестве варианта, ранее объясненная композиция для транспортировки и хранения соединения, имеющего уреидные группы, может быть использована вместо реакционной жидкости, содержащей по меньшей мере один тип соединения, имеющего уреидные группы, полученной на упомянутой выше стадии (A), и этот способ является также одним аспектом варианта настоящего осуществления.
Стадия (B) может являться стадией получения N-замещенной карбаминовой кислоты-O-арилового эфира путем этерификации соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции, и она является предпочтительным аспектом. На фигуре 2 приведена принципиальная схема стадии (B).
Органический первичный амин, используемый в этом направлении, является органическим первичным амином, представленным формулой (3), соединение, имеющее уреидные группы, полученное на стадии (A) этого направления, является соединением, имеющим уреидные группы, представленным формулой (1), полученным из органического первичного амина, и N-замещенной карбаминовой кислоты-O-ариловый эфир, полученный на стадии (B) этого направления, является N-замещенной карбаминовой кислоты-O-ариловым эфиром, представленным формулой (43), полученным из соединения, имеющего уреидные группы. Иллюстрации конкретных примеров каждого из этих соединений соответственно содержатся в ранее приведенных для них объяснениях.
Как было описано ранее, в случае, когда гидроксикомпозиция, используемая в качестве реакционного растворителя на стадии (A), является такой же, как гидроксикомпозиция стадии (B) (а именно, композиция, содержащая спирт, представленный формулой (4), и/или ароматическое гидроксисоединение, представленное формулой (2), которые содержит ароматическая гидроксикомпозиция, используемая на стадии (B)), стадия (B) может быть проведена, как есть, путем использования реакционной жидкости, полученной на стадии (A). Кроме того, в случае, когда гидроксикомпозиция, используемая в качестве реакционного растворителя на стадии (A), отличается от гидроксикомпозиции стадии (B), стадия (B) может быть проведена после добавления заново гидроксисоединения к реакционной жидкости, полученной на стадии (A), могут быть добавлены заново один или множество типов гидроксисоединений к реакционной жидкости, полученной на стадии (A), вслед за проведением стадии (B) после отделения всей или части гидроксикомпозиции, используемой в качестве реакционного растворителя стадии (A), или стадия (B) может быть проведена после удаления всей или части гидроксикомпозиции, используемой в качестве реакционного растворителя на стадии (A) вслед за добавлением заново одного или множества типов гидроксисоединений. Здесь, добавляемое заново гидроксисоединение является ароматической гидроксикомпозицией, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного упомянутой выше формулой (2).
Среди них, предпочтительно, чтобы ароматическая гидроксикомпозиция, используемая на стадии (B), являлась ароматической гидроксикомпозицией для проведения стадии (B), содержащей ароматическое гидроксисоединение, представленное формулой (7) или формулой (31), и более предпочтительно, ароматической гидроксикомпозицией, содержащей активное ароматическое гидроксисоединение, и еще более предпочтительно, ароматической гидроксикомпозицией, представленной формулой (32), и еще более предпочтительно, формулой (38). Как уже было описано ранее, способ получения N-замещенной карбаминовой кислоты-O-алкилового эфира путем использования соединения, имеющего уреидные группы, и реакции со спиртом раскрыт в патентном документе Japanese Patent Application Laid-open No. H6-41045. Как было ранее объяснено, этот N-замещенной карбаминовой кислоты-O-алкиловый эфир склонен к термическому денатурированию и легко образует соединение, имеющее уреиленовые группы. Кроме того, если N-замещенной карбаминовой кислоты-O-алкиловый эфир подвергают термическому разложению при попытке получить изоцианат, температура термического разложения становится высокой, и легко протекает обратная реакция реакции термического разложения. В результате исследований, проведенных авторами настоящего изобретения, в случае получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидные группы, и ароматического гидроксисоединения, было обнаружено, что N-замещенной карбаминовой кислоты-O-ариловый эфир может быть получен с высоким выходом без протекания реакции термического денатурирования.
Нет конкретных ограничений для способа отделения реакционного растворителя, используемого на стадии (A), и может быть использован известный способ, такой как ректификационное разделение, мембранное разделение или экстракционное разделение, но предпочтительным является ректификационное разделение. При проведении стадии (B) после проведения стадии (A) в ряде случаев предпочтительно проводить стадию (A) в присутствии ароматической гидроксикомпозиции, но в других случаях предпочтительно проводить стадию (A) в отсутствие спирта и в присутствии ароматической гидроксикомпозиции. Как уже было также описано ранее, в случае использования в качестве сырья соединения, имеющего уреидные группы, во многих случаях N-замещенной карбаминовой кислоты-O-алкиловый эфир склонен к термической денатурации. В результате исследований, проведенных авторами настоящего изобретения, было обнаружено, что даже если на стадии (A) используют спирт и на стадии (B) образуется следовое количество N-замещенной карбаминовой кислоты-O-R2 эфира, то, тем не менее, денатурирование значительно подавляется даже в присутствии ароматической гидроксикомпозиции.
При проведении стадии (B) в присутствии спирта, в ряде случаев образуется следовое количество N-замещенной карбаминовой кислоты-O-R2 эфира вместе с N-замещенной карбаминовой кислоты-O-ариловым эфиром, поэтому перед проведением стадии (B) или одновременно с проведением стадии (B) предпочтительно спирт удалять. Так как при проведении стадии (F) N-замещенной карбаминовой кислоты-O-R2 эфир является соединением, которое имеет высокую температуру термического разложения по сравнению с N-замещенной карбаминовой кислоты-O-ариловым эфиром, то в случае направления 1) или направления 2), которое включает стадию (B), предпочтительно не использовать по возможности спирт на стадии (A) (а именно, спирт не используют на протяжении всей стадии) для подавления образования количества N-замещенной карбаминовой кислоты-O-R2 эфира.
В зависимости от реагирующих соединений, условия реакции для получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции стадии (B) являются такими, что количество ароматического гидроксисоединения в используемой ароматической гидроксикомпозиции имеет мольное отношение в интервале от 1 до 500 относительно уреидных групп используемого соединения, имеющего уреидные группы. Предпочтительно использовать избыток ароматического гидроксисоединения, так как если его мольное отношение составляет величину менее, чем 1, то легко образуются сложнозамещенные карбонильные соединения и высокомолекулярные соединения, имеющие карбонильные связи в их молекулах, но принимая во внимание размер реактора, предпочтительно, чтобы мольное отношение находилось в интервале от 1 до 100, более предпочтительно, в интервале от 2 до 50, и еще более предпочтительно, в интервале от 3 до 20.
В зависимости от используемых соединений, предпочтительно, чтобы температура реакции находилась в интервале от 100 до 350°C. Если температура составляет ниже 100°C, реакция замедляется, или реакция практически вообще не идет, или увеличивается образование сложнозамещенных карбонильных соединений, что является нежелательным. С другой стороны, при температурах выше чем 350°C, либо N-замещенной карбаминовой кислоты-O-ариловый эфир остается на стадии (A), разлагается мочевина (и не-N-замещенной карбаминовой кислоты эфир), образовавшаяся в системе на стадии (B), гидроксикомпозиция подвергается денатурации в результате дегидрирования, либо легко протекают реакции разложения и денатурации продукта в форме N-замещенной карбаминовой кислоты-O-арилового эфира, что является нежелательным. С этой точки зрения более предпочтительно, чтобы температура реакции находилась в интервале от 120 до 320°C, и еще более предпочтительно, в интервале от 140 до 300°C.
Как уже было описано ранее, реакция, в результате которой образуется N-замещенной карбаминовой кислоты-O-ариловый эфир, является обратимой реакцией, и так как равновесие сдвинуто в сторону исходных реагентов, то предпочтительно проводить реакцию при удалении из системы как можно большего количества аммиака, образующегося в качестве побочного продукта. Предпочтительно удалять аммиак так, чтобы концентрация аммиака в реакционной жидкости составляла предпочтительно 1000 ppm или менее, более предпочтительно, 300 ppm или менее, еще более предпочтительно, 100 ppm или менее, и наиболее предпочтительно, 30 ppm или менее (содержание в реакционной жидкости относится к содержанию в жидкой фазе при проведении стадии (B)). Аммиак может быть удален с использованием таких способов, как реакционная дистилляция, использование инертного газа, мембранное разделение и адсорбционное разделение. Например, реакционная дистилляция относится к способу отделения непрерывно образующегося аммиака во время реакции путем дистилляции в форме газа. Для того чтобы повысить эффективность дистилляции аммиака, она может быть проведена при кипячении ароматического гидроксисоединения, растворителя или гидроксикомпозиции. Кроме того, способ, в котором используют инертный газ, относится к способу отделения непрерывно образующегося во время реакции аммиака от реакционной системы в форме газа вместе с инертным газом. Примеры используемых инертных газов могут включать азот, гелий, аргон, диоксид углерода, метан, этан и пропан, они могут быть использованы сами по себе или в виде смеси, и способ, в котором инертный газ вводят в реакционную систему, является предпочтительным. Примеры адсорбентов, используемых в способах адсорбционного разделения, могут включать адсорбенты, которые можно применять при температурных условиях проведения реакции, такие как оксид кремния, оксид алюминия, различные типы цеолита и диатомовая земля. Эти способы удаления аммиака из системы могут осуществляться в отдельности, или могут быть осуществлены множество типов способов в комбинации.
С целью повышения скорости реакции может быть использован в реакции, например, катализатор. Примеры используемых катализаторов могут предпочтительно включать основные катализаторы, такие как метилаты, этилаты или бутираты (включая изомеры) лития, натрия, калия, кальция или бария, редкоземельные элементы, сурьму или висмут сами по себе или в виде оксидов, сульфидов и их солей, бор сам по себе или соединения бора, металлы группы меди, группы цинка, группы алюминия, группы углерода и группы титана таблицы периодической системы элементов, так же, как оксиды металлов и их сульфиды, и карбиды и нитриды элементов группы углерода, исключая углерод, группы титана, группы ванадия и группы хрома таблицы периодической системы элементов. В случае использования катализатора нет конкретных ограничений для количества используемого катализатора, но катализатор может быть использован в интервале мольного отношения от 0,0001 до 100 относительно уреидных групп соединения, имеющего уреидные группы. Так как во многих случаях необходимо затем удалять катализатор, если катализатор используют, то реакцию предпочтительно проводить без добавления катализатора.
В зависимости от композиции реакционной системы, температуры реакции, используемого способа удаления аммиака, реакционного аппарата и других подобных параметров, обычно используют реакционное давление в интервале от 0,01 Па до 10 МПа (абсолютное давление), и с точки зрения возможности промышленного использования, более предпочтительно, чтобы реакционное давление находилось в интервале от 0,1 Па до 5 МПа (абсолютное давление), и принимая во внимание необходимость удаления газообразного аммиака из системы, еще более предпочтительно, от 0,1 Па до 1,5 МПа (абсолютное давление).
В зависимости от композиции реакционной системы, температуры реакции, используемого способа удаления аммиака, реакционного аппарата, реакционного давления и других подобных параметров, время реакции (время пребывания в случае непрерывного способа) обычно составляет от 0,01 до 100 часов. Время реакции может также быть определено исходя из образовавшегося количества целевого соединения в форме N-замещенной карбаминовой кислоты-O-арилового эфира (и в зависимости от случая, суммарного количества, обусловленного добавлением количества N-замещенной карбаминовой кислоты-O-R2 эфира). Например, реакция может быть остановлена после взятия образца реакционной жидкости, определения содержания в реакционной жидкости N-замещенной карбаминовой кислоты-O-арилового эфира (и в зависимости от случая, суммарного количества, обусловленного добавлением количества N-замещенной карбаминовой кислоты-O-R2 эфира) и подтверждения образования N-замещенной карбаминовой кислоты-O-ариловый эфир с выходом 10% или более относительно соединения, имеющего уреидные группы, или реакция может быть остановлена после подтверждения того, что выход составляет 90% или более. Изоцианат получают путем использования реакционной жидкости, содержащей N-замещенной карбаминовой кислоты-O-ариловый эфир на стадии (B), для реакции термического разложения на стадии (F). В данном случае, если содержание N-замещенной карбаминовой кислоты-O-арилового эфира на стадии (B) является низким (а именно, выход является низким), то следствием этого может быть снижение выхода изоцианата. Таким образом, предпочтительно, чтобы выход составлял 50% или более, более предпочтительно, 80% или более, и еще более предпочтительно, 90% или более.
Обязательное использование в реакции реакционного растворителя не требуется, но с целью облегчения осуществления реакции предпочтительно использовать подходящий растворитель в качестве реакционного растворителя, примеры которого включают алканы, такие как пентан (включая изомеры), гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; нитрильные соединения, такие как ацетонитрил или бензонитрил; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; сложные эфиры, такие как дибутилфталат, дигексилфталат, диоктилфталат или бензилбутилфталат; простые эфиры и тиоэфиры, такие как тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, дифениловый эфир или дифенилсульфид; кетоновые соединения, такие как ацетон или метилэтилкетон; эфирные соединения, такие как этилацетат или этилбензоат; и сульфоксиды, такие как диметилсульфоксид или дифенилсульфоксид. Естественно, что гидроксикомпозицию, используемую в избытке в реакции, также предпочтительно использовать в качестве реакционного растворителя.
Реакцию проводят в системе, имеющей газовую фазу, содержащую гидроксикомпозицию, соединение, имеющее карбонильные группы, полученное из мочевины (соединение, которое приобретает карбонильную группу, которой владела мочевина, такое как не-N-замещенной карбаминовой кислоты эфир или биурет, который относится к соединению, исключая N-замещенной карбаминовой кислоты-O-эфиры) и аммиак, получаемый в качестве побочного продукта в реакции; и жидкую фазу, в которой протекает реакция. Большую часть реакции проводят в жидкой фазе, но в зависимости от реакционных условий ее можно также проводить в газовой фазе. В данном случае предпочтительно, чтобы объемная доля жидкой фазы в реакционной смеси, в которой проводят реакцию, составляла 50% или менее. В случае непрерывного проведения реакции в течение длительного периода времени, вследствие колебаний параметров рабочих режимов (таких как температура и давление) и других подобных параметров могут образовываться полимерные побочные продукты, и если объемное содержание жидкой фазы в реакторе является высоким, то могут быть предотвращены слипание и накопление таких полимерных побочных продуктов в реакторе. Однако, так как при избыточно высокой объемной доле жидкой фазы может снизиться эффективность удаления побочного продукта аммиака и выход N-замещенной карбаминовой кислоты-O-арилового эфира, то предпочтительно, чтобы объемная доля жидкой фазы относительно газовой фазы составляла 50% или менее, более предпочтительно, 30% или менее, и еще более предпочтительно, 20% или менее (объемная доля жидкой фазы относится к отношению объема жидкой фазы к объему реакционной емкости в случае реактора типа емкости, объему ступени ниже ступени подачи сырья (не включая днище колонны и ребойлер) в случае реактора типа колонны, объему пленочного дистилляционного аппарата в случае пленочного дистилляционного аппарата).
Нет конкретных ограничений для используемого реакционного аппарата при проведении реакции, и может быть использован известный реактор, но предпочтительно использовать реактор типа емкости и/или реактор типа колонны. Предпочтительно, чтобы используемый реактор был оборудован конденсатором.
Как уже было описано ранее, реакцию предпочтительно проводить в системе, включающей газовую фазу, содержащую гидроксикомпозицию, соединение, имеющее карбонильные группы, полученные из мочевины, и аммиак, получаемый в качестве побочного продукта в реакции; и жидкую фазу, в которой проводят реакцию при таких условиях, что объемная доля жидкой фазы в реакторе, в котором проводят реакцию, составляет 50% или менее, и реактор, который удовлетворяет этим условиям, выбирают в качестве реактора, в котором проводят реакцию.
Более конкретно, могут быть соответствующим образом подсоединены и использованы традиционно известные реакторы, примеры которых могут включать реактор с мешалкой; работающий при повышенном давлении реактор с мешалкой; работающий при пониженном давлении реактор с мешалкой; реактор колонного типа, ректификационная колонна, насадочная колонна или пленочный дистилляционный аппарат.
Нет конкретных ограничений для типа конденсатора, устанавливаемого в реакторе, и может быть использован известный конденсатор. Например, могут быть соответствующим образом подсоединены и использованы известные традиционные конденсаторы, такие как трубчатый цилиндрический конденсатор, двухтрубный конденсатор, однотрубный конденсатор или конденсатор с воздушным охлаждением. Конденсатор может быть установлен внутри реактора или снаружи реактора, или он может быть соединен с реактором с помощью линии, и, принимая во внимание формы реактора и конденсатора, способ, с помощью которого сконденсированную жидкость транспортируют, и другие подобные параметры, могут быть использованы различные типы конденсаторов.
Нет конкретных ограничений для материалов реактора и конденсатора, и могут быть использованы известные материалы. Примеры материалов, которые могут быть использованы, могут включать стекло, нержавеющую сталь, углеродистую сталь, сплав Хастелой, эмалированные материалы и материалы с тефлоновым покрытием. Такие материалы как SUS304, SUS316 или SUS316L являются недорогими и могут быть предпочтительно использованы. Известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства могут быть добавлены при необходимости, для нагревания могут быть использованы такие известные способы, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. Могут также быть добавлены стадии, в случае необходимости. Например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области, такие как стадия растворения соединения, имеющего уреидные группы, в ароматической гидроксикомпозиции, стадия растворения ароматического гидроксисоединения, стадия отделения спирта, стадия отделения и/или очистки ароматического гидроксисоединения, стадия очистки N-замещенной карбаминовой кислоты-O-арилового эфира от образующейся реакционной жидкости, или стадия сжигания или вывода побочных продуктов и другие подобные стадии.
Стадия (B) является стадией получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции в жидкой фазе с использованием реактора (оборудованного конденсатором). Газообразный компонент, образующийся на стадии (B), содержащий соединение, имеющее карбонильные группы, полученные из мочевины, и аммиак, образующийся в качестве побочного продукта в реакции, вводят в конденсатор, установленный в реакторе, и всю или часть ароматической гидроксикомпозиции и соединение, имеющее карбонильные группы, полученное из мочевины, конденсируют с последующим извлечением аммиака в форме газа. В данном случае присутствует в определенном количестве или менее соединение, имеющее карбонильные группы, полученное из мочевины, которое содержится в аммиаке, извлекаемом в виде газа из конденсатора. А именно, отношение числа карбонильных групп (-C(=O)-), имеющихся в соединении, содержащем карбонильные группы, полученном из мочевины, присутствующем в аммиаке, к числу молекул аммиака составляет 1 или менее, предпочтительно, 0,5 или менее, более предпочтительно, 0,1 или менее, и еще более предпочтительно, 0,01 или менее. Причиной поддержания в конкретном интервале количества соединения, имеющего карбонильные группы, полученного из мочевины, содержащегося в аммиаке, является предотвращение слипания и накопления твердых компонентов в линиях для транспортировки аммиака из конденсатора.
Все твердые компоненты, которые прилипают и накапливаются в линии для транспортировки аммиака, не могут быть идентифицированы, но в результате исследований, проведенных авторами настоящего изобретения, было определено, что их большая часть является соединениями, имеющими карбонильные группы. Один возможный способ предотвращения слипания и накопления таких твердых компонентов включает нагревание линии для транспортировки аммиака для разложения соединений, имеющих карбонильные группы, но согласно исследованиям, проведенным авторами настоящего изобретения, во многих случаях нагревание само по себе вызывает полимеризацию продуктов разложения (таких как изоциановая кислота) или реакцию с другими соединениями, имеющими карбонильные группы, что затрудняет полное предотвращение слипания и накопления твердых компонентов. Кроме того, в случае простого нагревания линии, было обнаружено, что соединения, имеющие карбонильные группы, содержащиеся в аммиаке, и продукты их разложения затвердевают в результате их быстрого охлаждения на выходе линии для транспортировки аммиака (например, часть при контакте с атмосферой), что тем самым часто приводит к заметному слипанию и накоплению твердых компонентов. В результате проведения обширных исследований по этой проблеме авторы настоящего изобретения неожиданно обнаружили, что проблема слипания и накопления твердых компонентов может быть решена путем поддержания количества соединения, имеющего карбонильные группы, полученного из производной угольной кислоты, содержащейся в аммиаке, равным или меньшим, чем описанное выше конкретное количество. Несмотря на то, что механизм, на основании которого этот эффект проявляется, является неясным, авторы настоящего изобретения предположили, что слипание и накопление в линии вызывается самим по себе соединением, имеющим карбонильные группы, получаемым из производной угольной кислоты, так же, как и продуктами разложения и/или полимеризации соединения, имеющего карбонильные группы, получаемого из производной угольной кислоты, и что путем поддержания количества карбонильных групп, содержащихся в соединении, имеющем карбонильные группы, получаемом из производной угольной кислоты, равным или меньшим, чем конкретная концентрация, значительно снижаются слипание самого по себе соединения, имеющего карбонильные группы, получаемого из производной угольной кислоты, так же, как и скорости реакций разложения и/или полимеризации этого соединения.
С другой стороны, конденсацию ароматической гидроксикомпозиции и соединения, имеющего карбонильные группы, получаемого из мочевины, осуществляют таким образом, что мольное отношение сконденсированной ароматической гидроксикомпозиции к сконденсированному соединению, имеющему карбонильные группы, получаемому из мочевины, составляет 1 или более, предпочтительно, 2 или более, и более предпочтительно, 3 или более. Причиной определения таких интервалов является желание получить смесь ароматической гидроксикомпозиции и соединения, имеющего карбонильные группы, получаемого из мочевины, сконденсированных в конденсаторе, в форме гомогенной жидкой смеси. В результате, не только облегчается транспортировка смеси, но и может быть предотвращено возникновение проблем, таких как слипание и накопление твердых компонентов в конденсаторе.
Кроме того, на стадии (B) смесь ароматической гидроксикомпозиции и соединения, имеющего карбонильные группы, получаемого из мочевины, сконденсированных с помощью конденсатора, может быть рециркулирована в реактор и повторно использована в реакции стадии (A). В данном случае, предпочтительно, чтобы концентрация аммиака, содержащегося в смеси, составляла 5000 ppm или менее, более предпочтительно, 3000 ppm или менее, и еще более предпочтительно, 2000 ppm или менее.
Как уже было описано выше, различные соединения извлекают в форме соединений, имеющих карбонильные группы, получаемых из мочевины, но для повторного использования этих соединений нет конкретных ограничений.
<Направление 2)>
Направление 2) является способом проведения стадии (B), за которой следует проведение стадии (C). Направление 2) является одним аспектом способа, указанного в направлении 1).
Способ направления 2) является способом получения N-замещенной карбаминовой кислоты-O-арилового эфира из N-замещенной карбаминовой кислоты-O-арилового эфира стадии (B), в котором органический первичный амин является ароматическим органическим первичным моноамином, представленным следующей формулой (5), следующую стадию (C) проводят после стадии (B), и, по меньшей мере, две молекулы N-замещенной карбаминовой кислоты-O-арилового эфира являются сшитыми с помощью метиленовых групп (-CH2-). Предпочтительно, чтобы ароматическим гидроксисоединением, составляющим ароматическую гидроксикомпозицию, используемую на стадии (A) и/или стадии (B), являлось ароматическое моногидроксисоединение.
Стадия (C): стадия получения N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира являются сшитыми с помощью метиленовых групп (-CH2-) путем реакции N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира с формальдегидом или сшивающим агентом, образующим метиленовые связи, и сшивания с помощью метиленовых групп (-CH2-) ароматических групп, получаемых из ароматического органического первичного моноамина, содержащихся в N-замещенной карбаминовой кислоты-O-(R2 или ариловом) эфире.
N-замещенной карбаминовой кислоты-O-R2 эфир в направлении 2) представляет N-замещенной карбаминовой кислоты-O-R2 эфир, образующийся в качестве побочного продукта в случае использования спирта на стадии (A) и/или стадии (B).
В этом направлении, проводят стадию (A), используя органический первичный амин, представленный следующей формулой, и используют в качестве органического первичного амина для получения соединения, имеющего уреидные группы, получаемого из органического первичного амина, после чего проводят стадию (B) с получением N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого из соединения, имеющего уреидные группы, за которой следует проведение стадии (C). А именно, органический первичный амин, используемый в этом направлении, является органическим первичным амином, представленным формулой (5), соединение, имеющее уреидные группы, получаемое на стадии (A) этого направления, является соединением, имеющим уреидные группы, представленным формулой (41), получаемым из органического первичного амина, и, более конкретно, соединением, имеющим уреидные группы, представленным формулой (148), и N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (B) этого направления, является N-замещенной карбаминовой кислоты-O-ариловым эфиром, представленным формулой (43), получаемым из соединения, имеющего уреидные группы, и, более конкретно, N-замещенной карбаминовой кислоты-O-ариловым эфиром, представленным следующей формулой (149). Указания конкретных примеров каждого из этих соединений соответственно содержатся в ранее приведенных для них объяснениях.
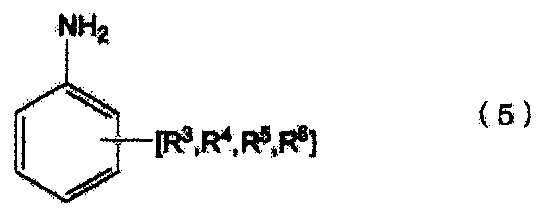
(где
по меньшей мере одно место в орто-положении и/или пара-положении NH2 группы ароматического органического первичного моноамина, представленного формулой (5), является незамещенным, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут быть соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут вместе быть связаны с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из групп, состоящих из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 составляет целое число в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют ароматический органический первичный моноамин, представленный формулой (5), составляет целое число от 6 до 13).
В этом случае соединение, имеющее уреидные группы, получаемое на стадии (A), является по меньшей мере одним типом соединения, имеющего уреидные группы, представленного следующей формулой (148). Кроме того, группы R3, R4, R5 и R6 в следующей формуле (148) выбирают из групп R3, R4, R5 и R6 органического первичного амина, представленного упомянутой выше формулой (5), и соединение, имеющее уреидные группы, является соединением, в котором аминогруппы (-NH2 группы) органического первичного амина, представленного формулой (5), находятся в форме уреидных групп (-NH-CO-NH2):
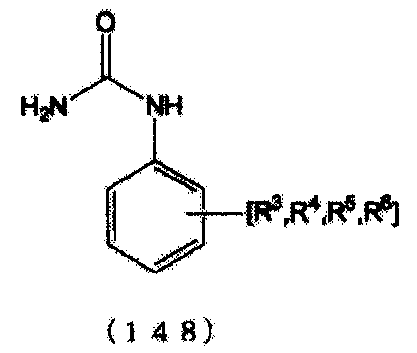
(где
по меньшей мере одно место в орто-положении и/или пара-положении уреидной группы N-замещенной ароматической органической мономочевины, представленной формулой (148), является незамещенным, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут быть соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут вместе быть связаны с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из групп, состоящих из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 составляет целое число в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют N-замещенную ароматическую органическую мономочевину, представленную формулой (148), исключая уреидные группы (-NH-CO-NH2), составляет целое число от 6 до 13).
В этом случае N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (B), является по меньшей мере одним типом N-замещенной карбаминовой кислоты-O-арилового эфира, представленного следующей формулой (149). Кроме того, группы R3, R4, R5 и R6 в следующей формуле (149) выбирают из групп R3, R4, R5 и R6 органического первичного амина, представленного упомянутой выше формулой (5), и соединение является соединением, в котором уреидные группы (-NH-CO-NH2) соединения, имеющего уреидные группы, представленного формулой (148), находятся в форме групп карбаминовой кислоты-O-арилового эфира:
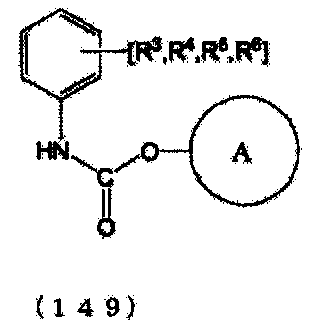
(где
группы R3-R6 являются группами, указанными выше).
На стадиях (A) и (B) этого направления используемый органический первичный амин является органическим первичным амином, представленным формулой (5), и стадии (A) и (B) этого направления проводят при условиях стадий (A) и (B) направления 1).
Стадия (C) является стадией получения N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира являются сшитыми с помощью метиленовых групп (-CH2-), путем сшивания по меньшей мере одного типа N-замещенной карбаминовой кислоты-O-арилового эфира (или реакционной жидкости, содержащей его), получаемого на стадии (B), с помощью метиленовых групп (-CH2-). В результате проведения стадии (C) получают N-замещенной карбаминовой кислоты-O-ариловый эфир, в котором по меньшей мере две молекулы по меньшей мере одного типа N-замещенной карбаминовой кислоты-O-арилового эфира, представленного следующей формулой (150), являются сшитыми с помощью метиленовых групп (-CH2-). Здесь, при проведении направления 2), ароматическую гидроксикомпозицию, содержащую ароматическое моногидроксисоединение, предпочтительно использовать для ранее описанного ароматического гидроксисоединения, используемого на стадии (A) и/или стадии (B) (а именно, ароматического гидроксисоединения, в котором b =1, в ароматическом гидроксисоединении, представленном формулой (2)). Может быть использовано поливалентное ароматическое гидроксисоединение, но в данном случае сшивание может происходить в местах, в которых это не требуется. В следующей формуле (150), в случае использования упомянутого выше ароматического моногидроксисоединения (а именно, в случае b =1), кольцо A следующей формулы не имеет других ароматических гидроксильных групп или спиртовых гидроксильных групп. Ароматическое гидроксисоединение, представленное упомянутой выше формулой (31), является предпочтительным в качестве ароматического моногидроксисоединения, более предпочтительным является случай использования активного ароматического гидроксисоединения, активных ароматических гидроксисоединений, представленных формулой (38), и еще более предпочтительным является случай использования ароматического гидроксисоединения, представленного формулой (38), в котором группы R26 и R27 являются атомами водорода, в то время как другие заместители являются линейными и/или циклическими насыщенными алкильными группами, или случай, в котором они являются нафтолом (включая изомеры), феноксифенолом (включая изомеры) или дифеноксифенолом (включая изомеры), в котором не замещено орто-положение или пара-положение гидроксильной группы.
Соединения, в которых m является целым числом от 0 до 6, представлены формулой (150), но эта величина может быть скорректирована в соответствии с используемым количеством и скоростью реакции реагирующего сшивающего реагента, образующего метиленовые связи (будет объяснен далее, и его часто будут называть агентом, образующим метиленовые группы):
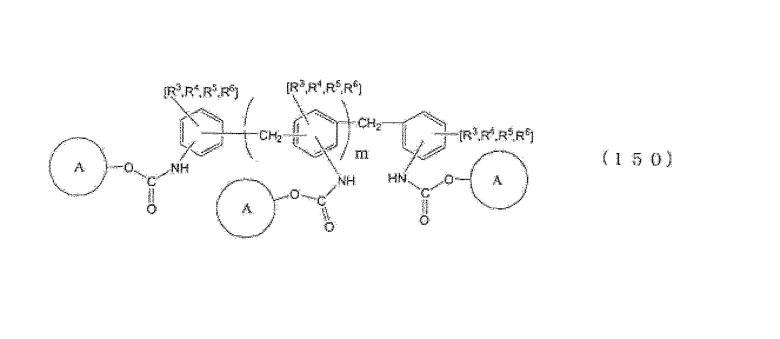
(где
R1 представляет группу, получаемую из ранее определенного органического первичного амина,
кольцо A представляет группу, получаемую из ароматического гидроксисоединения, которая образует ранее определенную ароматическую гидроксикомпозицию, и которая представляет остаток, в котором один атом водорода гидроксильных групп, непосредственно связанных с ароматическим углеводородным кольцом, был удален из ароматического гидроксисоединения,
группы R3-R6 представляют ранее определенные группы, и
m представляет целое число от 0 до 6).
В случае обычного использования изоцианатов в таких областях применения, как краска и полиуретан, может быть получен моноизоцианат путем использования для реакции термического разложения самого по себе N-замещенной карбаминовой кислоты-O-моно(арилового эфира), представленного упомянутой выше формулой (149), но, предпочтительно, чтобы изоцианатом являлся полифункциональный изоцианат. Таким образом, может быть осуществлен способ, в котором после предварительной полимеризации N-замещенной карбаминовой кислоты моно(арилового эфира) с помощью упомянутой выше стадии (C) полимер подвергают реакции термического разложения с получением полифункционального изоцианата. Упомянутый выше N-замещенной карбаминовой кислоты-O-моно(ариловый эфир) относится к N-замещенной карбаминовой кислоты-O-ариловому эфиру, имеющему в его молекуле одну группу карбаминовой кислоты-O-арилового эфира.
Далее приводится объяснение стадии (C). В следующем объяснении, N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (B) направления 2), часто обозначают как N-замещенной карбаминовой кислоты-O-моно(ариловый эфир) или N-замещенной карбаминовой кислоты моноариловый эфир.
Для стадии (C) может быть использован известный способ (см., например, патентный документ Federal Republic of Germany Patent No. 1042891).
Перед тем как проводить стадию (C), ароматическую гидроксикомпозицию, получаемую на стадии (B), отделяют от реакционной жидкости, содержащей образующийся N-замещенной карбаминовой кислоты-O-ариловый эфир. Стадия (C) может быть проведена в присутствии ароматического гидроксисоединения, но так как ароматическое гидроксисоединение может подвергаться сшиванию с помощью сшивающего реагента, образующего метиленовые связи, приводящему к образованию побочных продуктов, таких как полиароматические гидроксисоединения, или может увеличиваться количество используемого сшивающего реагента, образующего метиленовые связи, то предпочтительно отделять ароматические гидроксисоединения. Для способа разделения может быть использован известный способ, и в зависимости от используемых соединений, примеры способов разделения, которые могут быть использованы, могут включать способ ректификации, способ экстракционного разделения, в котором используется разница в растворимости между N-замещенной карбаминовой кислоты-O-ариловым эфиром и ароматическим гидроксисоединением, и способ фильтрации, проводимый путем отверждения либо N-замещенной карбаминовой кислоты-O-арилового эфира, либо ароматического гидроксисоединения. Эти способы не могут быть указаны конкретно, так как они зависят от соответствующих физических свойств используемых соединений, но способ и условия его осуществления могут быть соответствующим образом выбраны на основе знаний обычного специалиста в этой области.
При проведении стадии (C) ароматическое гидроксисоединение удаляют до тех пор, пока количество присутствующего ароматического гидроксисоединения после применения упомянутого выше способа разделения не составит мольное отношение 1 или меньше, предпочтительно, 0,5, и более предпочтительно, 0,1 относительно N-замещенной карбаминовой кислоты-O-арилового эфира. В данном случае ароматическое гидроксисоединение может быть удалено в присутствии растворителя, используемого на стадии (C), который будет объяснен далее.
Примеры сшивающих реагентов, образующих миетиленовые связи, предпочтительно используемых на стадии (C), могут включать формальдегид, параформальдегид, триоксан, диалкоксиметаны, имеющие низшие алкильные группы с количеством углеродных атомов от 1 до 6 (такие как диметоксиметан, диэтоксиметан, дипропоксиметан, дипентаноксиметан или дигексилоксиметан), и диацилоксиметаны, имеющие низшую карбоксильную группу, такие как диацетооксиметан или дипропиоксиметан. Они могут быть использованы сами по себе, или два или более типов могут быть использованы в виде смеси. Среди них особенно предпочтительными сшивающими реагентами, образующими метиленовые связи, являются водные растворы формальдегида, с точки зрения возможности промышленного применения, легкости транспортировки сшивающего реагента, образующего метиленовые связи, и других подобных факторов.
При проведении реакции стадии (C) нет конкретных ограничений для отношения N-замещенной карбаминовой кислоты-O-моно(арилового эфира) к сшивающему агенту, образующему метиленовые связи, но предпочтительно использовать N-замещенной карбаминовой кислоты-O-моноариловый эфир при мольном отношении от 2 до 20 к сшивающему агенту, образующему метиленовые связи. Образование полиядерных форм (относящихся к N-замещенной карбаминовой кислоты-O-ариловым эфирам, в которых три или более ароматических колец (ароматических колец, получаемых из органического первичного амина) связаны с помощью метиленовой сшивающей структуры, или другими словами, соединениям, в которых m является целым числами от 1 или более в упомянутой выше формуле (150)) подавляют путем использования большего количества N-замещенной карбаминовой кислоты-моноарилового эфира, но если используют чрезмерно избыточное количество N-замещенной карбаминовой кислоты-O-моноарилового эфира, то во многих случаях повышается остаточное количество исходного N-замещенной карбаминовой кислоты-O-моно(арилового эфира). Таким образом, более предпочтительно, чтобы используемое количество N-замещенной карбаминовой кислоты-O-моноарилового эфира, выраженное в мольном отношении к сшивающему реагенту, образующему метиленовые связи, находилось в интервале от 3 до 15, и еще более предпочтительно, в интервале от 5 до 10.
В качестве катализатора реакции конденсации предпочтительно использовать кислотный катализатор. Примеры кислотных катализаторов могут включать неорганические кислоты, такие как хлористоводородная кислота, серная кислота, фосфорная кислота или борная кислота, и органические кислоты, такие как муравьиная кислота, уксусная кислота, щавелевая кислота или толуолсульфоновая кислота. Кроме того, могут быть также эффективными кислоты, которые относят к очень сильным кислотам, таким как бромистоводородная кислота, перхлорная кислота, хлорсульфоновая кислота или трифторметансульфоновая кислота. Кроме того, эффективными являются также ионообменные смолы, имеющие кислотные группы, такие как карбоксильные группы или сульфонатные группы, а также кислоты, относящиеся к кислотам Льюиса, такие как трифторборная кислота, хлорид железа, хлорид алюминия, хлорид цинка или хлорид титана.
В случае протонной кислоты, такой как упомянутые выше неорганические кислоты, органические кислоты или очень сильные кислоты, используемое количество этих кислот находится в интервале мольного отношения от 0,001 до 10, и, предпочтительно, в интервале от 0,01 до 5 относительно исходного сырья эфира N-замещенной карбаминовой кислоты. Кроме того, в случае, когда эти кислоты используют в форме водных растворов, они могут быть использованы при концентрации в интервале от 10 до 95% по массе и, предпочтительно, в интервале от 20 до 80% по массе относительно количества воды в реакционной системе. Если концентрация составляет меньше, чем 10% по массе, скорость реакции конденсации становится чрезвычайно низкой, в то время как если концентрация превышает 95% по массе, могут протекать гидролиз сырья и другие нежелательные побочные реакции.
Реакция конденсации может быть проведена в присутствии или в отсутствие растворителя. Примеры используемых растворителей могут предпочтительно включать линейные, разветвленные или циклические углеводороды, такие как пентан, гексан, гептан, октан, нонан, декан, гексадекан, циклопентан или циклогексан; ароматические углеводороды, такие как бензол, толуол или ксилол и их алкил-, галоген- и нитрозамещенные формы; галогенированные углеводороды, такие как хлороформ, метиленхлорид, четыреххлористый углерод, дихлорэтан, трихлорэтан или тетрахлорэтан; алифатические алкиловые эфиры, такие как метилацетат или этилацетат; и простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, диоксан или тетрагидрофуран. Кроме того, предпочтительно использовать тиоацетали, ацетали или ацилали, так как они не образуют свободного формальдегида при условиях реакции и практически не образуют воду в результате реакции с водой, образующейся в качестве побочного продукта в реакции. Особенно предпочтительно использовать ацетали и ацилали. Кроме того, упомянутые выше кислоты предпочтительно использовать сами по себе в качестве растворителей. Эти растворители могут быть использованы само по себе, или два или более типов могут быть использованы в виде смеси.
Эти растворители могут быть использованы при массовом отношении в интервале от 0,1 до 100, и, предпочтительно, в интервале от 0,2 до 50 относительно сырья N-замещенной карбаминовой кислоты-O-моноарилового эфира.
Предпочтительно, чтобы температура реакции составляла от 10 до 160°C, более предпочтительно, от 20 до 140°C, и еще более предпочтительно, от 50 до 120°C. Реакцию предпочтительно проводить при высокой температуре, для того чтобы повысить скорость реакции и быстро закончить реакцию, но слишком высокая температура может вызывать нежелательные побочные реакции, такие как гидролиз.
В зависимости от способа реакции, используемых соединений и реакционных условий время реакции может находиться в интервале от 1 минуты до 20 часов. Кроме того, реакция может быть остановлена, при снижении количества сырья N-замещенной карбаминовой кислоты-O-моноарилового эфира достигнет определенного уровня, который определяется путем взятия пробы реакционной жидкости и использования известного аналитического метода, такого как жидкостная хроматография, или реакция может быть остановлена при достижении определенного уровня средней молекулярной массы продукта в форме N-замещенной карбаминовой кислоты-O-арилового эфира, который определяется путем использования известного аналитического метода, такого как гельпроникающая хроматография.
N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый описанным выше способом, является N-замещенной карбаминовой кислоты-O-ариловым эфиром, представленным упомянутой выше формулой (150). С точки зрения легкости транспортировки и, особенно, вязкости раствора и других подобных параметров предпочтительными являются N-замещенной карбаминовой кислоты-O-ариловые эфиры, в которых m равно 0, но не существуют проблем и в случае присутствия трехъядерных или более крупных полиядерных форм (а именно, соединений, представленных формулой (150), в которых m равняется 1 или более), при условии, что они не противоречат сути варианта настоящего осуществления.
N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (C), предпочтительно использовать на стадии (F).
Соединения, остающиеся в реакционной жидкости стадии (C), могут быть удалены из реакционной жидкости (такие, как используемые на стадии (C) реагент, образующий метиленовые связи, реакционный растворитель или катализатор). В качестве способа удаления может быть использован известный способ, и примеры таких способов могут включать мембранное разделение, ректификационное разделение и кристаллизацию, но предпочтительным является ректификационное разделение. В случае удаления соединения, остающегося в реакционной жидкости стадии (C), с помощью ректификационного разделения путем добавления ароматической гидроксикомпозиции, используемой на следующей стадии (F), к реакционной жидкости стадии (C) с получением смешанной жидкости и с последующим удалением соединений, остающихся в реакционной жидкости стадии (C) (таких, как используемые на стадии (C) реагент, образующий метиленовые связи, реакционный растворитель или катализатор) из смешанной жидкости, ректификационное разделение может быть проведено без выпадения в осадок сложного эфира N-замещенной карбаминовой кислоты, что делает этот способ предпочтительным.
При выборе материалов для реактора и конденсатора требуется определенная предосторожность, так как на стадии (C) используется кислота, но для материалов нет конкретных ограничений, при условии, что не возникает таких проблем как коррозия, вызываемая соединениями, используемыми на стадии (C), и могут быть использованы известные материалы. Примеры используемых материалов могут включать стекло, нержавеющую сталь, углеродистую сталь, сплав Хастелой, эмалированные материалы и материалы с тефлоновым покрытием. Известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства могут быть добавлены в случае необходимости. Для нагрева могут быть использованы известные способы, такие как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии, и например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области.
<Направление 3)>
Направление 3) является направлением, которое включает способ проведения стадии (R) после проведения стадии (P).
Сначала, получают N-замещенной карбаминовой кислоты-O-R2 эфир на стадии (R), используя соединение, имеющее уреидные группы, после чего N-замещенной карбаминовой кислоты-O-R2 эфир и ароматическая гидроксикомпозиция реагируют на стадии (P) с получением N-замещенной карбаминовой кислоты-O-арилового эфира. В качестве варианта, соединение, имеющее уреидные группы (или реакционную жидкость, содержащую его) получают на стадии (A), и стадию (R) проводят, используя соединение имеющее уреидные группы (или реакционную жидкость, содержащую его) после проведения стадии (P), с получением N-замещенной карбаминовой кислоты-O-арилового эфира.
<Стадия (R)> Стадия получения N-замещенной карбаминовой кислоты-O-R2 эфира
Стадия (R) является стадией получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции соединения, имеющего уреидные группы, со спиртом. В качестве варианта, N-замещенной карбаминовой кислоты-O-R2 эфир получают путем реакции (этерификации) соединения, имеющего уреидные группы (или реакционной жидкости, содержащей его), получаемого на стадии (A), со спиртом.
На фигуре 3 приведена принципиальная схема стадии (R).
Соединение, имеющее уреидные группы, получаемое на стадии (A) этого направления, является соединением, имеющим уреидные группы, представленным формулой (1), которое получают из органического первичного амина, N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (R) этого направления, является N-замещенной карбаминовой кислоты-O-R2 эфиром, представленным формулой (49), который получают из соединения, имеющего уреидные группы, и спирта, и N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (P) этого направления, является N-замещенной карбаминовой кислоты-O-ариловым эфиром, представленным формулой (43), который получают из N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции.
Как уже было заявлено ранее, в случае, когда гидроксикомпозиция, используемая в качестве реакционного растворителя на стадии (A), является такой же, как гидроксикомпозиция стадии (R) (а именно, композиция, содержащая спирт, представленный формулой (4), включая спирт, представленный формулой (4), используемый на стадии (R), и/или ароматическое гидроксисоединение, представленное формулой (2)), стадия (R) может быть проведена путем непосредственного использования реакционной жидкости, получаемой на стадии (A). Кроме того, в случае, когда гидроксикомпозиция, используемая в качестве реакционного растворителя на стадии (A), отличается от гидроксикомпозиции стадии (R), стадия (R) может быть проведена после добавления вновь гидроксисоединения (спирта, представленного формулой (4), и/или ароматического гидроксисоединения, представленного формулой (2)) к реакционной жидкости, получаемой на стадии (A), одно или множество типов гидроксисоединений могут быть вновь добавлены к реакционной жидкости, получаемой на стадии (A), за которой следует проведение стадии (R) после отделения всей или части гидроксикомпозиции, используемой в качестве реакционного растворителя стадии (A), или стадия (R) может быть проведена после удаления всей или части гидроксикомпозиции, используемой в качестве реакционного растворителя на стадии (A), за которой следует вновь добавление одного или множества типов гидроксисоединений. Здесь, добавляемое вновь гидроксисоединение является спиртом, представленным формулой (4), и/или ароматической гидроксикомпозицией. Нет конкретных ограничений для способа отделения реакционного растворителя, используемого на стадии (A), и может быть использован известный способ, такой как ректификационное разделение, мембранное разделение или экстракционное разделение, но предпочтительным является ректификационное разделение. В случае проведения стадии (R) после проведения стадии (A), в ряде случаев предпочтительно проводить стадию (A) в присутствии спирта, и также в ряде случаев предпочтительно проводить стадию (A) в отсутствие ароматической гидроксикомпозиции и в присутствии спирта. В случае проведения стадии (R) в присутствии ароматического гидроксисоединения, в ряде случаев в способе получения N-замещенной карбаминовой кислоты-O-арилового эфира варианта настоящего осуществления образуется следовое количество N-замещенной карбаминовой кислоты-O-арилового эфира вместе с N-замещенной карбаминовой кислоты-O-R2 эфиром, но после проведения стадии (R) это не должно вызывать какой-либо проблемы, так как N-замещенной карбаминовой кислоты-O-R2 эфир превращается в N-замещенной карбаминовой кислоты-O-ариловый эфир в результате проведения стадии (P), которая будет объяснена далее.
Как уже было описано ранее в отношении способа получения N-замещенной карбаминовой кислоты-O-алкилового эфира путем использования соединения, имеющего уреидные группы, и реакции со спиртом, в патентном документе Japanese Patent Application Laid-open No. H6-41045 раскрыт способ, который также ставит своей целью получение соответствующего изоцианата и спирта путем термического разложения N-замещенной карбаминовой кислоты-O-алкилового эфира. Как было объяснено ранее, при получении этим способом соединения, имеющего уреидные группы, возможно образование побочных продуктов, и при определенных условиях одновременно образуется большое количество N-замещенной карбаминовой кислоты-O-алкилового эфира, а N-замещенной карбаминовой кислоты-O-алкиловый эфир склонен к термической денатурации, в результате которой легко образуются соединения, имеющие уреиленовые группы. Кроме того, если изоцианат пытаются получать термическим разложением N-замещенной карбаминовой кислоты-O-алкилового эфира, приходится использовать более высокую температуру термического разложения, что приводит к повышению вероятности протекания обратной реакции термического разложения и возникновению забивки реактора термического разложения. В результате исследований, проведенных авторами настоящего изобретения, в случае получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидные группы, и ароматического гидроксисоединения, было обнаружено, что N-замещенной карбаминовой кислоты-O-ариловый эфир может быть получен с высоким выходом при незначительной термической денатурации.
С другой стороны, во многих случаях соединения, имеющие уреиленовые группы, и другие подобные соединения образуются в качестве побочных продуктов даже при получении N-замещенной карбаминовой кислоты-O-R2 эфира из соединения, имеющего уреидные группы, и спирта, но было обнаружено, что если при получении N-замещенной карбаминовой кислоты-O-R2 эфира из соединения, имеющего уреидные группы, и спирта присутствует ароматическое гидроксисоединение, то образование побочных продуктов может быть значительно подавлено. Предполагается, что этот эффект является следствием того, что ароматическое гидроксисоединение предотвращает ассоциацию соединения, имеющего уреидные группы, в результате чего подавляются побочные реакции, но такой вывод отсутствует в прототипе, и этот эффект был впервые обнаружен авторами настоящего изобретения. Таким образом, в зависимости от конкретного случая, при проведении стадии (R), стадию (R) также предпочтительно проводить в присутствии ароматической гидроксикомпозиции или ароматического гидроксисоединения. В этом случае, ароматическую гидроксикомпозицию или ароматическое гидроксисоединение выбирают из ароматических гидроксисоединений, представленных формулой (2), и предпочтительным является ароматическое гидроксисоединение, представленный формулой (7), и более предпочтительным, ароматическое гидроксисоединение, представленное формулой (31). Предпочтительный способ для использования множества типов ароматических гидроксисоединений будет объяснен далее, но ароматическое гидроксисоединение или ароматическую гидроксикомпозицию предпочтительно выбирать в соответствии с объясняемыми здесь критериями.
В зависимости от реагирующих соединений, условия реакции получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции соединения, имеющего уреидные группы, и спирта стадии (R) являются такими, что используемое количество спирта имеет мольное отношение в интервале от 1 до 500 относительно уреидных групп используемого соединения, имеющего уреидные группы. Предпочтительно использовать избыток спирта, так как если мольное отношение является меньшим, чем 1, то легко образуются сложнозамещенные карбонильные соединения и высокомолекулярные соединения, имеющие в их молекулах карбонильные связи, но принимая во внимание размер реактора, предпочтительно, чтобы мольное отношение находилось в интервале от 1 до 100, более предпочтительно, в интервале от 5 до 50, и, еще более предпочтительно, в интервале от 8 до 20.
В зависимости от используемых соединений, предпочтительно, чтобы температура реакции находилась в интервале от 100 до 350°C. Если температура составляет величину ниже, чем 100°C, реакция замедляется, или реакция вообще практически не идет, или увеличивается образование сложнозамещенных карбонильных соединений, что является нежелательным. С другой стороны, при температурах выше, чем 350°C, N-замещенной карбаминовой кислоты-O-R2 эфир также остается на стадии (A), разлагается мочевина (и не-N-замещенной карбаминовой кислоты эфир), образующаяся в системе стадии (R), гидроксикомпозиция подвергается денатурации в результате дегидрирования, или легко протекают реакции разложения и денатурации продукта в форме N-замещенной карбаминовой кислоты-O-R2 эфира, что является нежелательным. С этих точек зрения, более предпочтительно, чтобы температура реакции находилась в интервале от 120 до 320°C, и еще более предпочтительно, в интервале от 140 до 300°C.
Как уже было описано выше, реакция, по которой образуется N-замещенной карбаминовой кислоты-O-R2 эфир, является обратимой реакцией, и так как реакция сдвинута в сторону реагирующих веществ, реакцию предпочтительно проводить при удалении из системы образующегося в качестве побочного продукта аммиака как можно в большей степени. Аммиак предпочтительно удалять так, чтобы концентрация аммиака в реакционной жидкости составляла, предпочтительно, 1000 ppm или менее, более предпочтительно, 300 ppm или менее, еще более предпочтительно, 100 ppm или менее, и наиболее предпочтительно, 30 ppm или менее (содержание в реакционной жидкости относится к содержанию в жидкой фазе при проведении стадии (R)). Аммиак может быть удален с помощью таких способов, как реакционная дистилляция, использование инертного газа, мембранное разделение и адсорбционное разделение. Например, реакционная дистилляция относится к способу отделения непрерывно образующегося аммиака в процессе реакции путем его дистилляции в форме газа. Для того чтобы повысить эффективность дистилляции аммиака, она может быть проведена при кипячении спирта, растворителя или гидроксикомпозиции. Кроме того, способ, использующий инертный газ, относится к способу отделения непрерывно образующегося в процессе реакции аммиака от реакционной системы в форме газа вместе с инертным газом. Примеры используемых инертных газов могут включать азот, гелий, аргон, диоксид углерода, метан, этан и пропан, они могут быть использованы сами по себе, или в виде смеси, и предпочтительным является способ, в котором инертный газ вводят в реакционную систему. Примеры адсорбентов, используемых в способах адсорбционного разделения, могут включать адсорбенты, которые можно использовать при температурных условиях проведения реакции, такие как оксид кремния, оксид алюминия, различные типы цеолита или диатомовая земля. Эти способы удаления аммиака из системы могут быть проведены сами по себе, или могут быть проведены множество типов способов в комбинации.
В целях повышения скорости реакции может быть использован, например, катализатор. Примеры используемых катализаторов могут предпочтительно включать основные катализаторы, такие как метилаты, этилаты или бутираты (включая изомеры) лития, натрия, калия, кальция или бария, редкоземельные элементы, сурьма или висмут сами по себе или их оксиды, сульфиды и их соли, бор сам по себе или соединения бора, металлы группы меди, группы цинка, группы алюминия, группы углерода и группы титана периодической системы элементов, а также оксиды и сульфиды металлов, и карбиды и нитриды элементов группы углерода, исключая углерод, группы титана, группы ванадия и группы хрома периодической системы элементов. В случае использования катализатора нет конкретных ограничений для количества используемого катализатора, но катализатор может быть использован в интервале мольного отношения от 0,0001 до 100 относительно уреидных групп соединения, имеющих уреидные группы. Так как при использовании катализатора во многих случаях затем необходимо удалять катализатор, то реакцию предпочтительно проводить без добавления катализатора.
В зависимости от композиции реакционной системы, температуры реакции, способа, используемого для удаления аммиака, реакционного аппарата и других подобных параметров обычно применяют реакционное давление в интервале от 0,01 Па до 10 МПа (абсолютное давление), и принимая во внимание возможность промышленного использования, более предпочтительно, чтобы реакционное давление находилось в интервале от 0,1 Па до 5 МПа (абсолютное давление), и принимая во внимание необходимость удаления газообразного аммиака из системы, еще более предпочтительно, от 1,5 МПа (абсолютное давление).
В зависимости от композиции реакционной системы, температуры реакции, способа, используемого для удаления аммиака, реакционного аппарата, реакционного давления и других подобных параметров время реакции (время пребывания в случае непрерывной реакции) обычно составляет от 0,01 до 100 часов. Время реакции может также быть определено по количеству образовавшегося целевого соединения в форме N-замещенной карбаминовой кислоты-O-R2 эфира (и в зависимости от случая, по суммарному количеству, образующемуся вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира). Например, реакция может быть остановлена на основании взятия пробы реакционной жидкости, определения содержания сложного эфира N-замещенной карбаминовой кислоты в реакционной жидкости (и, в зависимости от случая, суммарного количества, образующегося вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира) и подтверждения, что образовался N-замещенной карбаминовой кислоты-O-R2 эфир с выходом 10% или более относительно соединения, имеющего уреидные группы, или реакция может быть остановлена после подтверждения того, что выход составляет 90% или более. Реакционную жидкость, содержащую N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (R), превращают в N-замещенной карбаминовой кислоты-O-ариловый эфир в способе, который включает стадию (P), которая будет описана далее, за которой следует получение изоцианата на стадии (F). В данном случае, если содержание N-замещенной карбаминовой кислоты-O-R2 эфира на стадии (R) является низким (его выход является низким), то в ряде случаев это может приводить к понижению выхода изоцианата. Таким образом, предпочтительно, чтобы выход N-замещенной карбаминовой кислоты-O-R2 эфира составлял 50% или более, более предпочтительно, 80% или более, и еще более предпочтительно, 90% или более.
Использование реакционного растворителя в реакции не является обязательным требованием, но с целью облегчения осуществления реакции предпочтительно использовать подходящий растворитель в качестве реакционного растворителя, примеры которого включают алканы, такие как пентан (включая изомеры), гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; нитрильные соединения, такие как ацетонитрил или бензонитрил; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; сложные эфиры, такие как дибутилфталат, дигексилфталат, диоктилфталат или бензилбутилфталат; простые эфиры и тиоэфиры, такие как тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, дифениловый эфир или дифенилсульфид; кетоновые соединения, такие как ацетон или метилэтилкетон; эфирные соединения, такие как этилацетат или этилбензоат; и сульфоксиды, такие как диметилсульфоксид или дифенилсульфоксид. Естественно, гидроксикомпозицию, используемую в реакции в избытке, также предпочтительно использовать в качестве реакционного растворителя.
Реакцию проводят в системе, включающей газовую фазу, содержащую гидроксикомпозицию, соединение, имеющее карбонильные группы, получаемое из мочевины (соединение, которое обретает карбонильную группу, которую имела мочевина, такое как не-N-замещенной карбаминовой кислоты эфир или биурет, которое относится к соединению, не включающему N-замещенной карбаминовой кислоты-O-эфиры), и аммиак, получаемый в реакции в качестве побочного продукта, и жидкую фазу, в которой проводят реакцию. Большую часть реакции проводят в жидкой фазе, но в зависимости от реакционных условий она может быть также проведена в газовой фазе. В данном случае предпочтительно, чтобы объемная доля жидкой фазы, в которой реакцию проводят, в реакционной смеси составляла 50% или менее. В случае проведения реакции непрерывно в течение длительного периода времени, вследствие колебаний технологических условий (таких как температура или давление) и других подобных параметров могут образовываться полимерные побочные продукты, но если объемная доля жидкой фазы в реакторе является высокой, то может быть предотвращено слипание и накопление таких полимерных побочных продуктов в реакторе. Однако, так как может стать низкой эффективность удаления побочного продукта аммиака и может понизиться выход N-замещенной карбаминовой кислоты-O-R2 эфира (и в зависимости от случая, суммарного количества, образующегося вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира), в случае, если объемная доля жидкой фазы является избыточно высокой, то предпочтительно, чтобы объемная доля жидкой фазы относительно газовой фазы составляла 50% или менее, более предпочтительно, 30% или менее, и еще более предпочтительно, 20% или менее (объемная доля жидкой фазы относится к объемному отношению жидкой фазы относительно объема реакционной емкости в случае реактора типа емкости, объема ступени, ниже ступени ввода сырья (не включая днище колонны и ребойлер) в случае колонного типа реактора, или объема пленочного дистилляционного аппарата в случае пленочного дистилляционного аппарата).
При проведении реакции нет конкретных ограничений для используемого реакционного аппарата, и может быть использован известный реактор, предпочтительно использовать реактор типа емкости и/или реактор колонного типа. Предпочтительно, чтобы используемый реактор был снабжен конденсатором.
Как было описано ранее, реакцию предпочтительно проводить в системе, включающей газовую фазу, содержащую гидроксикомпозицию, соединение, имеющее карбонильные группы, получаемое из мочевины, и аммиак, получаемый в качестве побочного продукта в реакции, и жидкую фазу, в которой проводят реакцию при таких условиях, что объемная доля жидкой фазы в реакторе составляет 50% или менее, и реактор, который удовлетворяет этим условиям, выбирают в качестве реактора, в котором проводят реакцию.
Более конкретно, могут быть соответствующим образом подсоединены и использованы традиционно известные реакторы, примеры которых могут включать реактор с мешалкой, работающий под повышенным давлением реактор с мешалкой, работающий под пониженным давлением реактор с мешалкой, реактор колонного типа, ректификационную колонну, насадочную колонну или пленочный дистилляционный аппарат.
Нет конкретных ограничений для типа конденсатора, устанавливаемого в реакторе, и может быть использован известный конденсатор. Например, могут быть соответствующим образом подсоединены и использованы известные традиционные конденсаторы, такие как трубчатый цилиндрический конденсатор, двухтрубный конденсатор, однотрубный конденсатор или конденсатор с воздушным охлаждением. Конденсатор может быть установлен внутри реактора или снаружи реактора, или он может быть соединен с реактором с помощью линии, и могут быть использованы различные типы, принимая во внимание формы реактора и конденсатора, способ, с помощью которого сконденсированную жидкость транспортируют, и другие подобные параметры. Нет конкретных ограничений для материалов реактора и конденсатора, и могут быть использованы известные материалы. Примеры используемых материалов могут включать стекло, нержавеющую сталь, углеродистую сталь, сплав Хастелой, эмалированные материалы и материалы с тефлоновым покрытием. Такие материалы как SUS304, SUS316 или SUS316L являются недорогими и могут быть предпочтительно использованы. Известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства могут быть добавлены при необходимости, для нагревания может быть использован такой известный способ, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии. Например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области, такие как стадия растворении мочевины в ароматическом гидроксисоединении, стадия растворения ароматического гидроксисоединения, стадия отделения спирта, стадия отделения и/или очистки ароматического гидроксисоединения, стадия очистки N-замещенной карбаминовой кислоты-O-R2 эфира от образующейся реакционной жидкости или стадия сжигания или вывода побочных продуктов и другие подобные стадии.
Стадия (R) является стадией получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции соединения, имеющего уреидные группы, и спирта в жидкой фазе с использованием реактора (оборудованного конденсатором). Газообразный компонент, образующийся на стадии (R), содержащий соединение, имеющее карбонильные группы, получаемое из мочевины, и аммиак, образующийся в реакции в качестве побочного продукта, вводят в конденсатор, установленный в реакторе, и весь или часть спирта и соединения, имеющего карбонильные группы, получаемого из мочевины, конденсируются, после чего следует извлечение аммиака в форме газа.
В данном случае, соединение, имеющее карбонильные группы, получаемое из мочевины, которое содержится в аммиаке, извлекаемом в виде газа из конденсатора, присутствует в конкретном количестве или менее. А именно, отношение числа карбонильных групп (-C(=O)-), содержавшихся в соединении, имеющем карбонильные группы, получаемом из мочевины, содержащемся в аммиаке, к числу молекул аммиака составляет 1 или менее, предпочтительно, 0,5 или менее, более предпочтительно, 0,1 или менее, и еще более предпочтительно, 0,01 или менее. Причиной поддержания в конкретном интервале количества соединения, имеющего карбонильные группы, получаемого из мочевины, содержавшегося в аммиаке, является предотвращение слипания и накопления твердых компонентов в линии для транспортировки аммиака из конденсатора.
Все твердые компоненты, которые слипаются и накапливаются в линии для транспортировки аммиака, не могут быть идентифицированы, но в результате исследований, проведенных авторами настоящего изобретения, было определено, что большая часть из них является соединениями, имеющими карбонильные группы. Один возможный способ предотвращения слипания и накопления таких твердых компонентов включает нагревание линии для транспортировки аммиака с целью разложения соединений, имеющих карбонильные группы, но согласно исследованиям, проведенным авторами настоящего изобретения, во многих случаях нагревание само по себе вызывает полимеризацию продуктов распада (таких как изоциановая кислота) или реакцию продуктов распада с другими соединениями, имеющими карбонильные группы, что затрудняет полностью предотвратить слипание и накопление твердых компонентов. Кроме того, в случае простого нагревания линии, было определено, что соединения, имеющие карбонильные группы, содержащиеся в аммиаке, и их продукты распада отверждаются в результате быстрого охлаждения на выходе из линии для транспортировки аммиака (например, часть при контакте с атмосферой), что часто приводит к значительному слипанию и накоплению твердых компонентов. В результате проведения обширных исследований по этой проблеме, авторы настоящего изобретения неожиданно обнаружили, что проблема слипания и накопления твердых компонентов может быть решена путем поддержания количества соединения, имеющего карбонильные группы, получаемого из производной угольной кислоты, содержавшегося в аммиаке, равным или меньшим, чем описанное выше конкретное количество. Механизм, на основании которого проявляется этот эффект, остается неясным, но авторы настоящего изобретения предположили, что слипание и накопление в линии вызывается самим по себе соединением, имеющим карбонильные группы, получаемым из производной угольной кислоты, а также продуктами разложения и/или полимеризации соединения, имеющего карбонильные группы, получаемого из производной угольной кислоты, и что в результате поддержания количества карбонильных групп, содержащихся в соединении, имеющем карбонильные группы, получаемом из производной угольной кислоты, на уровне, равном или меньшем, чем конкретная концентрация, значительно понижается слипание самого по себе соединения, имеющего карбонильные группы, полученного из производной угольной кислоты, так же как и снижаются скорости реакций разложения и/или полимеризации этого соединения.
С другой стороны, гидроксикомпозицию и соединение, имеющее карбонильные группы, получаемое из мочевины, конденсируют таким образом, чтобы мольное отношение сконденсированной гидроксикомпозиции к сконденсированному соединению, имеющему карбонильные группы, получаемому из мочевины, составляло 1 или более, предпочтительно, 2 или более, и более предпочтительно, 3 или более. Причиной для определения таких интервалов является желание получить смесь гидроксикомпозиции и соединения, имеющего карбонильные группы, получаемого из мочевины, сконденсированных в конденсаторе, в форме гомогенной жидкой смеси. В результате, не только облегчается транспортировка смеси, но и может быть предотвращено возникновение таких проблем, как слипание и накопление твердых компонентов в конденсаторе.
Кроме того, смесь гидроксикомпозиции и соединения, имеющего карбонильные группы, полученного из мочевины, сконденсированная конденсатором на стадии (R), может быть рециркулирована в реактор и повторно использована в реакторе стадии (A). В данном случае, предпочтительно, чтобы количество аммиака, содержащееся в смеси, составляло 5000 ppm или менее, более предпочтительно, 3000 ppm или менее, и еще более предпочтительно, 2000 ppm или менее.
Как уже было описано выше, извлекают различные соединения в форме соединений, имеющих карбонильные группы, получаемых из мочевины, но нет конкретных ограничений для повторного использования этих соединений.
<Стадия(P)> Стадия переэтерификации
Получаемый согласно стадии (R) N-замещенной карбаминовой кислоты-O-R2 эфир также позволяет получать изоцианат термическим разложением N-замещенной карбаминовой кислоты-O-R2 эфира, но более предпочтительным для использования эфиром N-замещенной карбаминовой кислоты является N-замещенной карбаминовой кислоты-O-ариловый эфир.
Обычно, N-замещенной карбаминовой кислоты-O-ариловые эфиры более склонны к термическому разложению, чем N-замещенной карбаминовой кислоты-O-R2 эфиры, и известно, что они легко разлагаются на соответствующий изоцианат и ароматическое гидроксисоединение.
После превращения термически легкоразлагаемого N-замещенной карбаминовой кислоты-O-арилового эфира в результате реакции переэтерификации согласно стадии (P), получаемый N-замещенной карбаминовой кислоты-O-ариловый эфир может быть использован в реакции получения изоцианата. Кроме того, так как эта стадия является стадией превращения эфирной группы N-замещенной карбаминовой кислоты-O-R2 эфира, в варианте настоящего осуществления ее также обычно называют "стадией переэтерификации".
Стадия (P): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции (композиции, содержащей, по меньшей мере, один тип ароматического гидроксисоединения, представленного следующей формулой (2)) в жидкой фазе и извлечения спирта, образующегося в качестве побочного продукта, в газовую фазу.
На фигуре 4 приведена принципиальная схема стадии (P).
Кроме того, спирт, получаемый из N-замещенной карбаминовой кислоты-O-R2 эфира, образуется на стадии (P). Далее приводится объяснение стадии (P).
Здесь, целевой N-замещенной карбаминовой кислоты-O-R2 эфир относится к N-замещенной карбаминовой кислоты-O-R2 эфиру, представленному упомянутой выше формулой (49).
Ароматическое гидроксисоединение в реагирующей ароматической гидроксикомпозиции может являться любым из ароматических гидроксисоединений, представленных упомянутой выше формулой (2), формулой (7), формулой (31), формулой (32), формулой (38), формулой (39) или формулой (40). Предпочтительным является случай, в котором используют ароматическое гидроксисоединение, представленное формулой (7) или формулой (31), более предпочтительным является случай, в котором используют ароматическую гидроксикомпозицию, которая содержит активное ароматическое гидроксисоединение, представленное формулой (32), и еще более предпочтительным является случай, в котором используют ароматическую гидроксикомпозицию, которая содержит активное ароматическое гидроксисоединение, представленное формулой (38).
Различные способы могут быть осуществлены для стадии (P) в соответствии с используемыми соединениями и другими подобными параметрами с ссылкой на известные способы (см., например, патентный документ WO 2008/059953).
В зависимости от реагирующих соединений, реакционные условия стадии (P) являются такими, что количество ароматического гидроксисоединения в используемой ароматической гидроксикомпозиции имеет мольное отношение в интервале от 2 до 1000 относительно эфирных групп, которые составляют сырье N-замещенной карбаминовой кислоты-O-R2 эфир. Для того чтобы быстро закончить реакцию, предпочтительно использовать избыток ароматического гидроксисоединения относительно эфирных групп, которые составляют сырье N-замещенной карбаминовой кислоты-O-R2 эфир, но принимая во внимание размер реактора, предпочтительно, чтобы мольное отношение находилось в интервале от 2 до 100, и более предпочтительно, в интервале от 5 до 50.
Температура реакции обычно находится в интервале от 100 до 300°C, и для повышения скорости реакции предпочтительной является высокая температура, но так как при высоких температурах могут легко протекать побочные реакции, предпочтительно, чтобы температура реакции находилась в интервале от 150 до 250°C. Для поддержания постоянной температуры в реакторе могут быть установлены в реакторе известный охлаждающий аппарат или нагревающий аппарат. Кроме того, в зависимости от типов используемых соединений и температуры реакции, реакция может проводиться при пониженном давлении, нормальном давлении или повышенном давлении, но обычно ее проводят при реакционном давлении в интервале от 20 до 1×106 Па. Нет конкретных ограничений для времени реакции (времени пребывания в случае непрерывного способа), и оно обычно составляет от 0,001 до 100 часов, предпочтительно, от 0,01 до 50 часов, и более предпочтительно, от 0,1 до 30 часов. Кроме того, реакция может быть остановлена после подтверждения того, что получено требуемое количество целевого N-замещенной карбаминовой кислоты-O-арилового эфира путем отбора пробы реакционной жидкости и определения образовавшегося количества, например, с помощью жидкостной хроматографии.
На стадии (P) не требуется в обязательном порядке применение катализатора, но для понижения температуры реакции или более быстрого завершения реакции может быть без проблем использован катализатор. Катализатор используют при концентрации от 0,01 до 30% по массе, и, предпочтительно, от 0,5 до 20% по массе относительно массы N-замещенной карбаминовой кислоты-O-R2 эфира. Примеры катализаторов могут включать кислоты Льюиса, а также соединения переходных металлов, которые образуют кислоту Льюиса, органические соединения олова, соединения металлов группы меди, соединения цинка или соединения группы железа, и более конкретно, кислоты Льюиса и соединения переходных металлов, которые образуют кислоту Льюиса, представленные AlX3, TiX3, TiX4, VOX3, VX5, ZnX2, FeX3 или SnX4 (где X представляет галоген, ацетоксильную группу, алкоксильную группу или арилоксильную группу); органические соединения олова, представленные (CH3)3SnOCHCH3, (C2H5)SnOCOC6H5, Bu3SnOCOCH3, Ph3SnOCOCH3, Bu2Sn(OCOCH3)2, Bu2Sn(OCOC11H23)2, Ph3SnOCH3, (C2H5)3SnOPh, Bu2Sn(OCH3)2, Bu2Sn(OC2H5)2, Bu2Sn(OPh)2, Ph2Sn(CH3)2, (C2H5)3SnOH, PhSnOH, Bu2SnO, (C8H17)2SnO, Bu2SnCl2 или BuSnO(OH); соединения металлов группы меди, представленные CuCl, CuCl2, CuBr, CuBr2, CuI, CuI2, Cu(OAc)2, Cu(acac)2, олефинатом меди, Bu2Cu, (CH3O)2Cu, AgNO3, AgBr, пикратом серебра или AgC6H6ClO4; соединения цинка, представленные Zn(acac)2; и соединения металлов группы железа, представленные Fe(C10H8)(CO)5, Fe(CO)5, Fe(C4H6)(CO)3, Co(мезитилен)2(PEt2Ph2), CoC5F5(CO)7 или ферроценом. (В приведенных выше примерах, Bu обозначает бутильную группу, Ph обозначает фенильную группу, и acac обозначает ацетилацетонатный хелатный лиганд). Амины, такие как 1,4-диазабицикло- [2,2,2]октан, триэтилендиамин или триэтиламин являются подходящими для использования в качестве катализаторов, в то время как металлорганические катализаторы, такие как дибутилоловодилаурат, октоат свинца или октоат двухвалентного олова являются особенно предпочтительными. Эти соединения могут быть использованы сами по себе или два или более типов могут быть использованы в виде смеси.
В варианте настоящего осуществления не требуется обязательное использование реакционного растворителя, но с целью облегчения осуществления реакции и для других подобных целей может быть предпочтительно использован подходящий инертный растворитель в качестве реакционного растворителя, примеры которого могут включать алканы, такие как гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; сложные эфиры, такие как дибутилфталат, дигексилфталат, диоктилфталат или бензилбутилфталат; простые эфиры и тиоэфиры, такие как дифениловый эфир или дифенилсульфид; сульфоксиды, такие как диметилсульфоксид или дифенилсульфоксид; и силиконовое масло. Эти растворители могут быть использованы сами по себе, или два или более типов могут быть использованы в виде смеси.
Реакция переэтерификации в варианте настоящего осуществления является обратимой реакцией. Таким образом, для того чтобы эффективно проводить переэтерификацию, предпочтительно проводить реакции при удалении продукта в форме спирта (спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира) из реакционной системы. Таким образом, если ароматическое гидроксисоединение выбирают так, что стандартная температура кипения ароматического гидроксисоединения, используемого в переэтерификации, является выше, чем стандартная температура кипения спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, то соединением, имеющим самую низкую стандартную температуру кипения в реакционной системе, становится спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, в силу чего облегчается удаление продуктов из реакционной системы. Основываясь на выводе, что обычно соответствующее ректификационное разделение в промышленных условиях является возможным, если стандартные температуры кипения двух компонентов, подвергаемых разделению, отличаются на 10°C или более, предпочтительно использовать ароматическое гидроксисоединение таким образом, чтобы в ароматической гидроксикомпозиции стандартная температура кипения соединения, имеющего самую низкую стандартную температуру кипения (на основе сравнения стандартных температур кипения) была выше на 10°C или более, чем стандартная температура кипения спирта.
Кроме того, переэтерификацию предпочтительно проводить с помощью непрерывного способа, который позволяет эффективно осуществлять переэтерификацию. А именно, сырье N-замещенной карбаминовой кислоты-O-R2 эфир и ароматическую гидроксикомпозицию непрерывно подают в реактор, проводят переэтерификацию, образующийся спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, извлекают из реактора в форме газообразного компонента, и реакционную жидкость, содержащую образовавшийся N-замещенной карбаминовой кислоты-O-ариловый эфир и ароматическую гидроксикомпозицию, непрерывно извлекают из нижней части реактора.
Материалы реактора и линий, используемых для проведения переэтерификации, могут являться известными материалами, при условии, что они не оказывают отрицательного действия на исходные вещества и реагирующие вещества, но такие материалы как SUS304, SUS316 или SUS316L являются недорогими и могут быть предпочтительно использованы. Известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства могут быть добавлены, в случае необходимости, для нагревания может быть использован такой известный способ, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии. Например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области, такие как стадия растворения ароматического гидроксисоединения, стадия отделения спирта, стадия отделения и/или очистки ароматического гидроксисоединения, стадия очистки N-замещенной карбаминовой кислоты-O-арилового эфира от образовавшейся реакционной жидкости или стадия сжигания или вывода побочных продуктов и другие подобные стадии.
Нет конкретных ограничений для типа реактора, и может быть использован известный реактор типа емкости или реактор колонного типа. Различные известные методы используют в качестве такого реактора, примеры которого могут включать типы используемых реакторов, содержащие реактор с мешалкой, многоступенчатый реактор с мешалкой, ректификационную колонну, многоступенчатую ректификационную колонну, трубчатый реактор, многоступенчатую ректификационную колонну непрерывного действия, насадочную колонну, пленочный испаритель, реактор, снабженный внутри средством поддержки, реактор с принудительной циркуляцией, испаритель с падающей пленкой, испаритель с падающей каплей, капельный проточный реактор или барботажную колонну, и типы, использующие их комбинации. Методы, использующие пленочный испаритель или реактор колонного типа, являются предпочтительными с точки зрения эффективного сдвига равновесия в сторону продуктов, в то время как структура, имеющая большую площадь контакта газ-жидкость является предпочтительной, для того, чтобы быстро осуществлять перенос образовавшегося спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, в газовую фазу.
Многоступенчатая ректификационная колонна относится к ректификационной колонне, имеющей множество ступеней, в которой число теоретических тарелок дистилляции составляет 2 или более, и может быть использована любая многоступенчатая ректификационная колонна, при условии что она позволяет осуществлять непрерывную ректификацию. Любая многоступенчатая ректификационная колонна может быть использована в качестве многоступенчатой ректификационной колонны, при условии, что она обычно используется в качестве многоступенчатой ректификационной колонны, примеры которой могут включать типы тарельчатой колонны, использующей такую тарелку, как колпачковая тарелка, пористая плоская тарелка, клапанная тарелка или противоточная тарелка, и типы насадочной колонны, заполненной различными типами таких насадочных материалов, как кольца Рашига, кольца Лессинга, полюсные кольца, седловидная насадка Берля, седловидная насадка Interlock, насадка Диксона, насадка МакМэна, насадка Helipack, насадка типа "Зульцер" или насадка Меллапак. Может быть использована любая насадочная колонна при условии, что колонна заполнена описанной выше известной насадкой. Кроме того, предпочтительно также использовать колонну с комбинацией "тарелки-насадки", в которой объединяется часть тарелок с частью насадок.
Может быть отдельно подсоединена линия подачи инертного газа и/или жидкого инертного растворителя к нижней части реактора, и в случае когда смесь целевого N-замещенной карбаминовой кислоты-O-арилового эфира и ароматического гидроксисоединения содержит сырье N-замещенной карбаминовой кислоты-O-R2 эфир, может быть подсоединена линия для рециркуляции всей или части смеси в реактор. Кроме того, в случае использования упомянутого выше инертного растворителя, инертный растворитель может находиться в форме газа и/или жидкости.
Предпочтительно, чтобы извлеченный из реактора газообразный компонент, содержащий спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, подвергали очистке с помощью известного метода, такого как метод, в котором используется ректификационная колонна, и он может быть повторно использован в качестве спирта стадии (A) и/или стадии (R).
<Направление 4)>
Направление 4) является способом проведения стадии (R), за которой следует проведение стадии (P) и стадия (C). Направление 4) является одним аспектом способа, указанного в направлении 2).
Способ направления 4) является способом получения N-замещенной карбаминовой кислоты-O-арилового эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-арилового эфира являются сшитыми с помощью метиленовых (-CH2-) групп, из N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого на стадии (P) путем проведения следующей стадии (C) после стадии (P), в котором органический первичный амин, используемый на стадии (A), является ароматическим органическим первичным моноамином, представленным следующей формулой (5). Ароматическое моногидроксисоединение предпочтительно использовать в качестве ароматического гидроксисоединения, которое составляет ароматическую гидроксикомпозицию, используемую на стадии (A), и/или стадии(R), и/или стадии (P).
Стадия (C): стадия получения N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира являются сшитыми с помощью метиленовых групп (-CH2-) путем реакции N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира с формальдегидом или сшивающим реагентом, образующим метиленовые связи, и сшивания ароматических групп, получаемых из ароматического органического первичного моноамина, содержащихся в N-замещенной карбаминовой кислоты-O-(R2 или ариловом)эфире, с помощью метиленовых групп (-CH2-).
N-замещенной карбаминовой кислоты-O-R2 эфир этого направления 4) относится к непрореагировавшему N-замещенной карбаминовой кислоты-O-R2 эфиру на стадии (P).
В этом направлении, стадию (A) проводят с использованием органического первичного амина, представленного следующей формулой, в качестве органического первичного амина с получением соединения, имеющего уреидные группы, представленного формулой (1), получаемого из органического первичного амина, за которой следует проведение стадии (R) с получением N-замещенной карбаминовой кислоты-O-R2 эфира, получаемого из соединения, имеющего уреидные группы, проведение стадии (P) с получением N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого из соединения, имеющего уреидные группы, и наконец проведение стадии (C). А именно, органический первичный амин, используемый в этом направлении, является органическим первичным амином, представленным формулой (5), соединение, имеющее уреидные группы, получаемое на стадии (A) этого направления, является соединением, имеющим уреидные группы, представленным формулой (41), получаемым из органического первичного амина, N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (R) этого направления, является N-замещенной карбаминовой кислоты-O-R2 эфиром, в котором r =1, который представлен формулой (49) и который получают из уреидных групп и спирта, и более конкретно, N-замещенной карбаминовой кислоты-O-R2 эфиром, представленным следующей формулой (146), и N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (P) в этом направлении, является N-замещенной карбаминовой кислоты-O-ариловым эфиром, в котором q =1, который представлен формулой (43) и который получают из N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции, и более конкретно, N-замещенной карбаминовой кислоты-O-ариловым эфиром, представленным следующей формулой (149). Указания конкретных примеров каждого из этих соединений соответственно содержатся в приведенных выше их объяснениях.
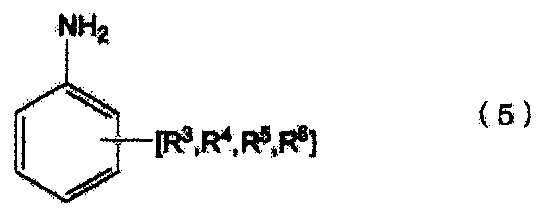
(где
по меньшей мере одно место в орто-положении и/или пара-положении NH2 группы ароматического органического первичного моноамина, представленного формулой (5), является незамещенным, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут быть соединены вместе с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из групп, состоящих из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью насыщенных алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 является целым числом в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют ароматический органический первичный моноамин, представленный формулой (5), является целым числом от 6 до 13).
В этом случае, соединение имеющее уреидные группы, получаемое на стадии (A), является по меньшей мере одним типом соединения, имеющего уреидные группы, представленного следующей формулой (148). Кроме того, группы R3, R4, R5 и R6 в следующей формуле (148) выбирают из групп R3, R4, R5 и R6 органического первичного амина, представленного упомянутой выше формулой (5), и он является соединением, в котором аминогруппы (-NH2 группы) органического первичного амина, представленного формулой (5), находится в форме уреидных групп (-NH-CO-NH2):

(где
по меньшей мере одно место в орто-положении и/или пара-положении уреидной группы N-замещенной ароматической органической мономочевины, представленной формулой (148), является незамещенным, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут быть связаны вместе с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из групп, состоящих из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью насыщенных алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 является целым числом в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют N-замещенную ароматическую органическую мономочевину, представленную формулой (148), исключая уреидные группы (-NH-CO-NH2), является целым числом от 6 до 13).
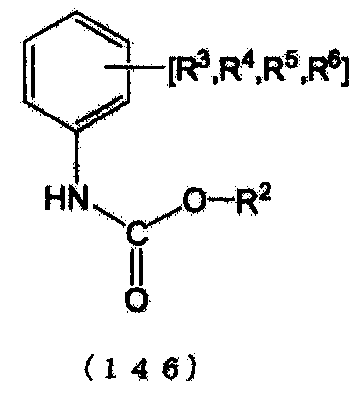
(где
группы R2-R6 являются группами, указанными выше).
В этом случае N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (P) путем проведении стадии (R), является по меньшей мере одним типом N-замещенной карбаминовой кислоты-O-арилового эфира, представленным следующей формулой (149). Кроме того, группы R3, R4, R5 и R6 в следующей формуле (149) выбирают из групп R3, R4, R5 и R6 органического первичного амина, представленного упомянутой выше формулой (5), и соединение является соединением, в котором уреидные группы (-NH-CO-NH2) соединения, имеющего уреидные группы, представленного формулой (148), находятся в форме групп карбаминовой кислоты-O-арилового эфира:

(где
группы R3-R6 являются группами, указанными выше).
На стадиях (A), (R) и (P) этого направления используемый органический первичный амин является органическим первичным амином, представленным формулой (5), и стадии (A), (R) и (P) этого направления проводят при условиях стадий (A), (R) и (P) направления 3).
В зависимости от реагируемых соединений, условия реакции для получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции соединения, имеющего уреидные группы, и спирта стадии (R) являются такими, что количество используемого спирта имеет мольное отношение в интервале от 1 до 500 относительно уреидных групп используемого соединения, имеющего уреидные группы. Предпочтительно использовать избыток спирта, так как если мольное отношение составляет меньше, чем 1, то легко образуются сложнозамещенные карбонильные соединения и высокомолекулярные соединения, имеющие в их молекулах карбонильные связи, но принимая во внимание размер реактора, предпочтительно, чтобы мольное отношение назодилось в интервале от 1 до 200, более предпочтительно, в интервале от 1,5 до 100, и еще более предпочтительно, в интервале от 2 до 50.
В зависимости от используемых соединений, предпочтительно, чтобы температура реакции находилась в интервале от 100 до 350°C. Если значение температуры составляет ниже, чем 100°C, реакция замедляется, или реакция вообще практически не идет, или увеличиваются образование сложнозамещенных карбонильных соединений, что является нежелательным. С другой стороны, при температурах выше чем 350°C, либо на стадии (A) остается N-замещенной карбаминовой кислоты-O-R2 эфир, разлагается мочевина (и не-N-замещенной карбаминовой кислоты эфир), образующаяся в системе стадии (R), гидроксикомпозиция подвергается денатурации в результате дегидрирования, либо легко протекают реакции разложения и денатурации продукта в форме N-замещенной карбаминовой кислоты-O-R2 эфира, что является нежелательным. С этой точки зрения, более предпочтительно, чтобы температура реакции находилась в интервале от 120 до 320°C, и еще более предпочтительно, в интервале от 140 до 300°C.
Как уже было описано выше, реакция, по которой образуется N-замещенной карбаминовой кислоты-O-R2 эфир, является обратимой реакцией, и так как равновесие сдвинуто в сторону реагирующих веществ, то реакцию предпочтительно проводить при удалении из системы аммиака, образующегося в качестве побочного продукта, как можно в большей степени. Аммиак предпочтительно удалять так, чтобы концентрация аммиака в реакционной жидкости составляла, предпочтительно, 1000 ppm или менее, более предпочтительно, 300 ppm или менее, еще более предпочтительно, 100 ppm или менее, и наиболее предпочтительно, 30 ppm или менее (содержание в реакционной жидкости относится к содержанию в жидкой фазе при проведении стадии (R)). Аммиак может быть удален с помощью таких способов, как реакционная дистилляция, использование инертного газа, мембранное разделение и адсорбционное разделение. Например, реакционная дистилляция относится к способу отделения непрерывно образующегося аммиака в процессе реакции путем дистилляции в форме газа. Для того чтобы повысить эффективность дистилляции аммиака, она может быть проведена при кипячении спирта, растворителя или гидроксикомпозиции. Кроме того, способ, использующий инертный газ, относится к способу отделения непрерывно образующегося аммиака в процессе реакции от реакционной системы в форме газа вместе с инертным газом. Примеры используемых инертных газов могут включать азот, гелий, аргон, диоксид углерод, метан, этан и пропан, они могут быть использованы сами по себе, или в виде смеси, и предпочтительным является способ, в котором инертный газ вводят в реакционную систему. Примеры адсорбентов, используемых в способах адсорбционного разделения, могут включать адсорбенты, которые можно использовать при температурных условиях, при которых проводят реакцию, такие как оксид кремния, оксид алюминия, различные типы цеолита или диатомовая земля. Эти способы удаления аммиака из системы могут быть проведены сами по себе, или множество типов способов могут быть проведены в комбинации.
В целях повышения скорости реакции может быть использован, например, катализатор. Примеры используемых катализаторов могут предпочтительно включать основные катализаторы, такие как метилаты, этилаты или бутираты (включая изомеры) лития, натрия, калия, кальция или бария, редкоземельные элементы, сурьма или висмут сами по себе или их оксиды, сульфиды и их соли, бор сам по себе или соединения бора, металлы группы меди, группы цинка, группы алюминия, группы углерод и группы титана периодической системы элементов, а также оксиды и сульфиды металлов, и карбиды и нитриды элементов группы углерода, исключая углерод, группы титана, группы ванадия и группы хрома периодической системы элементов. В случае использования катализатора нет конкретных ограничений для количества используемого катализатора, но катализатор может быть использован в интервале мольного отношения от 0,0001 до 100 относительно уреидных групп соединения, имеющих уреидные группы.
В зависимости от композиции реакционной системы, температуры реакции, способа, используемого для удаления аммиака, реакционного аппарата и других подобных параметров, обычно применяют реакционное давление в интервале от 0,01 Па до 10 МПа (абсолютное давление), и принимая во внимание возможность промышленного использования, более предпочтительно, чтобы реакционное давление находилось в интервале от 0,1 Па до 5 МПа (абсолютное давление), и принимая во внимание необходимость удаление газообразного аммиака из системы, еще более предпочтительно, от 1,5 МПа (абсолютное давление).
В зависимости от композиции реакционной системы, температуры реакции, способа, используемого для удаления аммиака, реакционного аппарата, реакционного давления и других подобных параметров, время реакции (время пребывания в случае непрерывной реакции) обычно составляет от 0,01 до 100 часов. Время реакции может также быть определено на основании количества образовавшегося целевого соединения в форме N-замещенной карбаминовой кислоты-O-R2 эфира (и в зависимости от случая, суммарного количества, образовавшегося вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира). Например, реакция может быть остановлена после взятия пробы реакционной жидкости, определения содержания эфира N-замещенной карбаминовой кислоты в реакционной жидкости (и, в зависимости от случая, суммарного количества, образующегося вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира) и подтверждения, что N-замещенной карбаминовой кислоты-O-R2 эфир образовался с выходом 10% или более относительно соединения, имеющего уреидные группы, или реакция может быть остановлена после подтверждения того, что выход составляет 90% или более. Реакционную жидкость, содержащую N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (R), превращают в N-замещенной карбаминовой кислоты-O-ариловый эфир в способе, который включает стадию (P), которая будет описана далее, за которой следует получение изоцианата на стадии (F). В данном случае, если содержание N-замещенной карбаминовой кислоты-O-R2 эфира на стадии (R) является низким (его выход является низким), то в ряде случаев это может приводить к понижению выхода изоцианата. Таким образом, предпочтительно, чтобы выход N-замещенной карбаминовой кислоты-O-R2 эфира составлял 50% или более, более предпочтительно, 80% или более, и еще более предпочтительно, 90% или более.
Использование в реакции реакционного растворителя не является обязательным условием, но с целью облегчения осуществления реакции предпочтительно использовать подходящий растворитель в качестве реакционного растворителя, примеры которого включают алканы, такие как пентан (включая изомеры), гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; нитрильные соединения, такие как ацетонитрил или бензонитрил; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; сложные эфиры, такие как дибутилфталат, дигексилфталат, диоктилфталат или бензилбутилфталат; простые эфиры и тиоэфиры, такие как тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, дифениловый эфир или дифенилсульфид; кетоновые соединения, такие как ацетон или метилэтилкетон; эфирные соединения, такие как этилацетат или этилбензоат; и сульфоксиды, такие как диметилсульфоксид или дифенилсульфоксид. Естественно, что также предпочтительно использовать в качестве реакционного растворителя гидроксикомпозицию, используемую в избытке в реакции.
Реакцию проводят в системе, включающей газовую фазу, содержащую гидроксикомпозицию, соединение, имеющее карбонильные группы, получаемое из мочевины (соединение, которое обретает карбонильную группу, которую имела мочевина, такое как не-N-замещенной карбаминовой кислоты эфир или биурет, которое относится к соединению, не включающему N-замещенной карбаминовой кислоты-O-эфиры), и аммиак, получаемый в качестве побочного продукта в реакции, и жидкую фазу, в которой проводят реакцию. Большую часть реакции проводят в жидкой фазе, но в зависимости от реакционных условий она может быть также проведена и в газовой фазе. В данном случае, предпочтительно, чтобы объемная доля жидкой фазы в реакционной смеси, в которой реакцию проводят, составляла 50% или менее. В случае проведения реакции непрерывно в течение длительного периода времени, вследствие колебания технологических условий (таких как температура или давление) и других подобных параметров могут образовываться полимерные побочные продукты, но если объемная доля жидкой фазы в реакторе является высокой, то может быть предотвращено слипание и накопление таких полимерных побочных продуктов в реакторе. Однако, если объемная доля жидкой фазы является чрезмерно высокой, то может снизиться эффективность удаления побочного продукта аммиака и может понизиться выход N-замещенной карбаминовой кислоты-O-R2 эфира (и в зависимости от случая, суммарного количества, образующегося вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира), поэтому, предпочтительно, чтобы объемная доля жидкой фазы относительно газовой фазы составляла 50% или менее, более предпочтительно, 30% или менее, и еще более предпочтительно, 20% или менее (объемная доля жидкой фазы относится к объемному отношению жидкой фазы относительно объема реакционной емкости в случае реактора типа емкости, объема ступени, ниже ступени ввода сырья (не включая днище колонны и ребойлер), в случае колонного типа реактора, или объема пленочного дистилляционного аппарата в случае пленочного дистилляционного аппарата).
При проведении реакции нет конкретных ограничений для используемого реакционного аппарата, и может быть использован известный реактор, но предпочтительно использовать реактор типа емкости и/или реактор колонного типа. Предпочтительно, чтобы используемый реактор был снабжен конденсатором.
Как было описано ранее, реакцию предпочтительно проводить в системе, включающей газовую фазу, содержащую гидроксикомпозицию, соединение, имеющее карбонильные группы, получаемое из мочевины, и аммиак, получаемый в качестве побочного продукта в реакции, и жидкую фазу, в которой проводят реакцию при таких условиях, что объемная доля жидкой фазы в реакторе составляет 50% или менее, и реактор, который удовлетворяет этим условиям, выбирают в качестве реактора, в котором проводят реакцию.
Более конкретно, могут быть соответствующим образом подсоединены и использованы известные традиционные реакторы, примеры которых могут включать реактор с мешалкой, работающий под повышенным давлением реактор с мешалкой, работающий под пониженным давлением реактор с мешалкой, реактор колонного типа, ректификационную колонну, насадочную колонну или пленочный дистилляционный аппарат.
Нет конкретных ограничений для типа конденсатора, устанавливаемого в реакторе, и может быть использован известный конденсатор. Например, могут быть соответствующим образом подсоединены и использованы традиционно известные конденсаторы, такие как трубчатый цилиндрический конденсатор, двухтрубный конденсатор, однотрубный конденсатор или конденсатор с воздушным охлаждением. Конденсатор может быть установлен внутри реактора или снаружи реактора, или он может быть соединен с реактором с помощью линии, и могут быть использованы различные типы конденсаторов, принимая во внимание формы реактора и конденсатора, способ, с помощью которого сконденсированную жидкость транспортируют, и другие подобные параметры.
Нет конкретных ограничений для материалов реактора и конденсатора, и могут быть использованы известные материалы. Примеры используемых материалов могут включать стекло, нержавеющую сталь, углеродистую сталь, сплав Хастелой, эмалированные материалы и материалы с тефлоновым покрытием. Такие материалы как SUS304, SUS316 или SUS316L являются недорогими и могут быть предпочтительно использованы. При необходимости, могут быть добавлены известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства, для нагревания может быть использован такой известный способ, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии. Например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области, такие как стадия растворения соединения, имеющего уреидные группы, в ароматической гидроксикомпозиции, стадия растворения ароматического гидроксисоединения, стадия отделения спирта, стадия отделения и/или очистки ароматического гидроксисоединения, стадия очистки N-замещенной карбаминовой кислоты-O-R2 эфира от образующейся реакционной жидкости или стадия сжигания или вывода побочных продуктов и другие подобные стадии.
Стадия (R) является стадией получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции (этерификации) соединения, имеющего уреидные группы, и спирта в жидкой фазе с использованием реактора (оборудованного конденсатором). Газообразный компонент, образующийся на стадии (R), содержащий соединение, имеющее карбонильные группы, получаемое из мочевины, и аммиак, образующийся в реакции в качестве побочного продукта, вводят в конденсатор, установленный в реакторе, и конденсируют весь или часть спирта и соединения, имеющего карбонильные группы, получаемого из мочевины, после чего следует извлечение аммиака в форме газа.
В данном случае присутствует в конкретном количестве или менее соединение, имеющее карбонильные группы, получаемое из мочевины, которое содержится в аммиаке, извлекаемом в виде газа из конденсатора. А именно, отношение числа карбонильных групп (-C(=O)-), содержавшихся в соединении, имеющем карбонильные группы, получаемом из мочевины, присутствующем в аммиаке, к числу молекул аммиака составляет 1 или менее, предпочтительно, 0,5 или менее, более предпочтительно, 0,1 или менее, и еще более предпочтительно, 0,01 или менее. Причиной для поддержания в конкретном интервале количества соединения, имеющего карбонильные группы, получаемого из мочевины, присутствующего в аммиаке, является предотвращение слипания и накопления твердых компонентов в линии для транспортировки аммиака из конденсатора.
Все твердые компоненты, которые слипаются и накапливаются в линии для транспортировки аммиака, не могут быть идентифицированы, но в результате исследований, проведенных авторами настоящего изобретения, было определено, что большая их часть является соединениями, имеющими карбонильные группы. Один возможный способ предотвращения слипания и накопления таких твердых компонентов включает нагревание линии для транспортировки аммиака с целью разложения соединений, имеющих карбонильные группы, но согласно исследованиям, проведенным авторами настоящего изобретения, во многих случаях нагревание само по себе вызывает полимеризацию продуктов распада (таких как изоциановая кислота) или реакцию продуктов распада с другими соединениями, имеющими карбонильные группы, что затрудняет полное предотвращение слипания и накопления твердых компонентов. Кроме того, было определено, что в случае простого нагревания линии, соединения, имеющие карбонильные группы, содержащиеся в аммиаке, и их продукты распада отверждаются в результате быстрого охлаждения на выходе из линии для транспортировки аммиака (например, часть при контакте с атмосферой), что часто приводит к значительному слипанию и накоплению твердых компонентов. В результате проведения обширных исследований этой проблемы, авторы настоящего изобретения неожиданно обнаружили, что проблема слипания и накопления твердых компонентов может быть решена путем поддержания количества соединения, имеющего карбонильные группы, получаемого из производной угольной кислоты, содержавшегося в аммиаке, на уровне, равном или меньшем, чем описанное выше конкретное количество. Механизм, на основании которого проявляется этот эффект, остается неясным, но авторы настоящего изобретения предположили, что слипание и накопление в линии вызывается самим по себе соединением, имеющим карбонильные группы, получаемым из производной угольной кислоты, а также продуктами разложения и/или полимеризации соединения, имеющего карбонильные группы, получаемого из производной угольной кислоты, и что путем поддержания количества карбонильных групп, содержащихся в соединении, имеющем карбонильные группы, получаемом из производной угольной кислоты, на уровне, равном или меньшем, чем конкретная концентрация, значительно уменьшается слипание самого по себе соединения, имеющего карбонильные группы, полученного из производной угольной кислоты, так же как и скорости реакций разложения и/или полимеризации этого соединения.
С другой стороны, гидроксикомпозицию и соединение, имеющее карбонильные группы, получаемое из мочевины, конденсируют таким образом, что мольное отношение сконденсированной гидроксикомпозиции к сконденсированному соединению, имеющему карбонильные группы, получаемому из мочевины, составляет 1 или более, предпочтительно, 2 или более, и более предпочтительно, 3 или более. Причиной для определения таких интервалов является желание получить смесь гидроксикомпозиции и соединения, имеющего карбонильные группы, получаемого из мочевины, сконденсированную в конденсаторе, в форме гомогенной жидкой смеси. В результате, не только облегчается транспортировка смеси, но и может быть предотвращено возникновение таких проблем, как слипание и накопление твердых компонентов в конденсаторе.
Кроме того, смесь гидроксикомпозиции и соединения, имеющего карбонильные группы, полученного из мочевины, сконденсированная в конденсаторе на стадии (R), может быть рециркулирована в реактор и повторно использована в реакторе стадии (A). В данном случае, предпочтительно, чтобы количество аммиака, содержащееся в смеси, составляло 5000 ppm или менее, более предпочтительно, 3000 ppm или менее, и еще более предпочтительно, 2000 ppm или менее.
Как уже было описано выше, различные соединения извлекают в форме соединений, имеющих карбонильные группы, получаемых из мочевины, но нет конкретных ограничений для повторного использования этих соединений.
<Стадия(P)> Стадия этерификации
Так как эта стадия является стадией превращения эфирной группы N-замещенной карбаминовой кислоты-O-R2 эфира, то в варианте настоящего осуществления ее также обычно называют "стадией этерификации".
На фигуре 5 приведена принципиальная схема стадии (P).
Кроме того, на стадии (P) образуется спирт, получаемый из N-замещенной карбаминовой кислоты-O-R2 эфира. Далее приводится объяснение стадии (P).
Ароматическое гидроксисоединение в реагирующей ароматической гидроксикомпозиции может являться любым из ароматических гидроксисоединений, представленных упомянутый выше формулой (2), формулой (7), формулой (31), формулой (32), формулой (38), формулой (39) или формулой (40). Предпочтительным является случай, в котором содержится ароматическое гидроксисоединение, представленное формулой (7) или формулой (31), более предпочтительным является случай, в котором используют ароматическую гидроксикомпозицию, которая содержит активное ароматическое гидроксисоединение, представленное формулой (32), и еще более предпочтительным является случай, в котором используют ароматическую гидроксикомпозицию, которая содержит активное ароматическое гидроксисоединение, представленное формулой (38).
В соответствии с используемыми соединениями и другими подобными параметрами для стадии (P) могут быть осуществлены различные способы с ссылкой на известные способы (см., например, патентный документ WO 2008/059953).
В зависимости от реагирующих соединений, реакционные условия стадии (P) являются такими, что количество ароматического гидроксисоединения в используемой ароматической гидроксикомпозиции имеет мольное отношение в интервале от 2 до 1000 относительно эфирных групп, которые составляют сырье N-замещенной карбаминовой кислоты-O-R2 эфир. Для того чтобы быстро закончить реакцию, предпочтительно использовать избыток ароматического гидроксисоединения относительно эфирных групп, которые составляют сырье N-замещенной карбаминовой кислоты-O-R2 эфир, но принимая во внимание размер реактора, предпочтительно, чтобы мольное отношение находилось в интервале от 2 до 100, и более предпочтительно, в интервале от 5 до 50.
Температура реакции обычно находится в интервале от 100 до 300°C, и для повышения скорости реакции является предпочтительной высокая температура, но так как при высоких температурах могут легко протекать побочные реакции, предпочтительно, чтобы температура реакции находилась в интервале от 150 до 250°C. Для поддержания постоянной температуры в реакторе могут быть установлены известный охлаждающий аппарат или нагревающий аппарат. Кроме того, в зависимости от типов используемых соединений и температуры реакции, реакция может проводиться при пониженном давлении, нормальном давлении или повышенном давлении, и обычно при реакционном давлении в интервале от 20 до 1×106 Па. Нет конкретных ограничений для времени реакции (времени пребывания в случае непрерывного способа), и оно обычно составляет от 0,001 до 100 часов, предпочтительно, от 0,01 до 50 часов, и более предпочтительно, от 0,1 до 30 часов. Кроме того, реакция может быть остановлена после подтверждения того, что получено требуемое количество целевого N-замещенной карбаминовой кислоты-O-арилового эфира, путем отбора пробы реакционной жидкости и определения образовавшегося количества с помощью, например, жидкостной хроматографии.
Применение катализатора на стадии (P) не является обязательным, но для понижения температуры реакции или более быстрого завершения реакции может быть использован без проблем катализатор. Катализатор используют при концентрации от 0,01 до 30% по массе, и, предпочтительно, от 0,5 до 20% по массе относительно массы N-замещенной карбаминовой кислоты-O-R2 эфира. Примеры катализаторов могут включать кислоты Льюиса, а также соединения переходных металлов, которые образуют кислоту Льюиса, органические соединения олова, соединения металлов группы меди, соединения цинка или соединения группы железа, и более конкретно, кислоты Льюиса и соединения переходных металлов, которые образуют кислоту Льюиса, представленные AlX3, TiX3, TiX4, VOX3, VX5, ZnX2, FeX3 или SnX4 (где X представляет галоген, ацетоксильную группу, алкоксильную группу или арилоксильную группу); органические соединения олова, представленные (CH3)3SnOCHCH3, (C2H5)SnOCOC6H5, Bu3SnOCOCH3, Ph3SnOCOCH3, Bu2Sn(OCOCH3)2, Bu2Sn(OCOC11H23)2, Ph3SnOCH3, (C2H5)3SnOPh, Bu2Sn(OCH3)2, Bu2Sn(OC2H5)2, Bu2Sn(OPh)2, Ph2Sn(CH3)2, (C2H5)3SnOH, PhSnOH, Bu2SnO, (C8H17)2SnO, Bu2SnCl2 или BuSnO(OH); соединения металлов группы меди, представленные CuCl, CuCl2, CuBr, CuBr2, CuI, CuI2, Cu(OAc)2, Cu(acac)2, олефинатом меди, Bu2Cu, (CH3O)2Cu, AgNO3, AgBr, пикратом серебра или AgC6H6ClO4; соединения цинка, представленные Zn(acac)2; и соединения металлов группы железа, представленные Fe(C10H8)(CO)5, Fe(CO)5, Fe(C4H6)(CO)3, Co(мезитилен)2(PEt2Ph2), CoC5F5(CO)7 или ферроценом. (В приведенных выше примерах, Bu обозначает бутильную группу, Ph обозначает фенильную группу, и acac обозначает ацетилацетонатный хелатный лиганд). Амины, такие как 1,4-диазабицикло-[2,2,2]октан, триэтилендиамин или триэтиламин являются подходящими для использования в качестве катализаторов, в то время как металлорганические катализаторы, такие как дибутилоловодилаурат, октоат свинца или октоат двухвалентного олова являются особенно предпочтительными. Эти соединения могут быть использованы сами по себе или два или более типов могут быть использованы в виде смеси.
В варианте настоящего осуществления использование реакционного растворителя не является обязательным, но с целью облегчения осуществления реакции и других подобных целей может быть предпочтительно использован подходящий инертный растворитель в качестве реакционного растворителя, примеры которого могут включать алканы, такие как гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; сложные эфиры, такие как дибутилфталат, дигексилфталат, диоктилфталат или бензилбутилфталат; простые эфиры и тиоэфиры, такие как дифениловый эфир или дифенилсульфид; сульфоксиды, такие как диметилсульфоксид или дифенилсульфоксид; и силиконовое масло. Эти растворители могут быть использованы сами по себе, или два или более типов могут быть использованы в виде смеси.
Реакция переэтерификации в варианте настоящего осуществления является обратимой реакцией. Поэтому для того, чтобы эффективно проводить переэтерификацию, предпочтительно проводить реакции при удалении продукта в форме спирта (спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира) из реакционной системы. Таким образом, если ароматическое гидроксисоединение выбирают так, что стандартная температура кипения ароматического гидроксисоединения, используемого в переэтерификации, является выше, чем стандартная температура кипения спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, то соединением, имеющим самую низкую стандартную температуру кипения в реакционной системе, становится спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, что облегчает удаление продуктов из реакционной системы. Исходя из того, что обычно соответствующее ректификационное разделение при применении в промышленности является возможным, если стандартные температуры кипения двух компонентов, подвергаемых разделению, отличаются на 10°C или более, ароматическое гидроксисоединение предпочтительно использовать так, чтобы стандартная температура кипения соединения, имеющего самую низкую стандартную температуру кипения в ароматической гидроксикомпозиции (на основе сравнения стандартных температур кипения), была выше на 10°C или более, чем стандартная температура кипения спирта.
Кроме того, переэтерификацию предпочтительно проводить с помощью непрерывного способа, что позволяет эффективно осуществлять переэтерификацию. А именно, сырье N-замещенной карбаминовой кислоты-O-R2 эфир и ароматическую гидроксикомпозицию непрерывно подают в реактор, проводят переэтерификацию, спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, который образуется, извлекают из реактора в форме газообразного компонента, и реакционную жидкость, содержащую образовавшийся N-замещенной карбаминовой кислоты-O-ариловый эфир и ароматическую гидроксикомпозицию непрерывно извлекают из нижней части реактора.
Материалы реактора и линий, используемых для проведения переэтерификации, могут являться известными материалами, при условии, что они не оказывают отрицательного действия на исходные вещества и реагирующие вещества, но такие материалы как SUS304, SUS316 или SUS316L являются недорогими и могут быть предпочтительно использованы. В случае необходимости могут быть добавлены известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства, для нагревания может быть использован такой известный способ, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии. Например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области, такие как стадия растворения ароматического гидроксисоединения, стадия отделения спирта, стадия отделения и/или очистки ароматического гидроксисоединения, стадия очистки N-замещенной карбаминовой кислоты-O-арилового эфира от образовавшейся реакционной жидкости или стадия сжигания или вывода побочных продуктов и другие подобные стадии. Нет конкретных ограничений для типа реактора, и может быть использован известный реактор типа емкости или реактор колонного типа. В качестве такого реактора используют различные известные методы, примеры которого могут включать используемые типы реакторов, содержащие реактор с мешалкой, многоступенчатый реактор с мешалкой, ректификационную колонну, многоступенчатую ректификационную колонну, трубчатый реактор, многоступенчатую ректификационную колонну непрерывного действия, насадочную колонну, пленочный дистилляционный аппарат, реактор, снабженный внутри средством поддержки, реактор с принудительной циркуляцией, испаритель с падающей пленкой, испаритель с падающей каплей, капельный проточный реактор или барботажную колонну, и типы, использующие их комбинации. С точки зрения эффективности сдвига равновесия в сторону продуктов предпочтительными являются способы, использующие пленочный дистилляционный аппарат или реактор колонного типа, в то время как структура, имеющая большую площадь контакта газ-жидкость является предпочтительной для быстрого осуществления переноса образовавшегося спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, в газовую фазу.
Многоступенчатая ректификационная колонна относится к ректификационной колонне, имеющей множество ступеней, в которой число теоретических тарелок дистилляции составляет 2 или более, и любая многоступенчатая ректификационная колонна может быть использована, при условии что она позволяет осуществлять непрерывную ректификацию. Любая многоступенчатая ректификационная колонна может быть использована в качестве многоступенчатой ректификационной колонны, при условии, что она обычно используется в качестве многоступенчатой ректификационной колонны, примеры которой могут включать типы тарельчатой колонны, использующей такую тарелку, как колпачковая тарелка, пористая плоская тарелка, клапанная тарелка или противоточная тарелка, и типы насадочной колонны, заполненной различными типами насадочных материалов, таких как кольца Рашига, кольца Лессинга, полюсные кольца, седловидная насадка Берля, седловидная насадка Interlock, насадка Диксона, насадка МакМэна, насадка Helipack, насадка типа "Зульцер" или насадка Меллапак. Любая насадочная колонна может быть использована при условии, что колонна заполнена описанной выше известной насадкой. Кроме того, предпочтительно также использовать колонну с комбинацией "тарелки-насадки", в которой объединяется часть тарелок с частью насадок.
Может быть отдельно подсоединена линия подачи инертного газа и/или жидкого инертного растворителя в нижней части реактора, и в случае когда смесь целевого N-замещенной карбаминовой кислоты-O-арилового эфира и ароматического гидроксисоединения содержит сырье N-замещенной карбаминовой кислоты-O-R2 эфир, может быть подсоединена линия для рециркуляции всей или части смеси в реактор. Кроме того, в случае использования упомянутого выше инертного растворителя, инертный растворитель может находиться в форме газа и/или жидкости.
Газообразный компонент, извлеченный из реактора, содержащий спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, предпочтительно очищать с помощью известного метода, такого как метод, в котором используется ректификационная колонна, и он может быть повторно использован в качестве спирта стадии (A) и/или стадии (R).
Стадия (C) является стадией получения N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира являются сшитыми с помощью метиленовых групп (-CH2-), путем сшивания по меньшей мере одного типа N-замещенной карбаминовой кислоты-O-арилового эфира (или реакционной жидкости, содержащей его), получаемого на стадии (Р), с помощью метиленовых групп (-CH2-). В результате проведения стадии (C), получают N-замещенной карбаминовой кислоты-O-ариловый эфир, в котором по меньшей мере две молекулы по меньшей мере одного типа N-замещенной карбаминовой кислоты-O-арилового эфира, представленного следующей формулой (150), являются сшитыми с помощью метиленовых групп (-CH2-). Здесь, при проведении направления 2), ароматическую гидроксикомпозицию, содержащую ароматическое моногидроксисоединение, предпочтительно использовать в качестве ранее описанного ароматического гидроксисоединения, используемого на стадии (A) и/или стадии (R) и/или стадии (P) (а именно, ароматического гидроксисоединения, в котором b =1, в ароматическом гидроксисоединении, представленном формулой (2)). Может быть использовано поливалентное ароматическое гидроксисоединение, но в этом случае сшивание может происходить в местах, в которых это не требуется. В следующей формуле (150), в случае использования упомянутого выше ароматического моногидроксисоединения (а именно, в случае b =1), кольцо A следующей формулы не имеет других ароматических гидроксильных групп или спиртовых гидроксильных групп. Ароматическое гидроксисоединение, представленное упомянутой выше формулой (31), является предпочтительным в качестве ароматического моногидроксисоединения, более предпочтительным является случай использования активного ароматического гидроксисоединения, активных ароматических гидроксисоединений, представленных формулой (38), и еще более предпочтительным является случай использования ароматического гидроксисоединения, представленного формулой (38), в котором группы R26 и R27 являются атомами водорода, в то время как другие заместители являются линейными и/или циклическими насыщенными алкильными группами, или случай, в котором они являются нафтолом (включая изомеры), феноксифенолом (включая изомеры) или дифеноксифенолом (включая изомеры), в котором незамещено орто-положение или пара-положение гидроксильной группы.
Соединения, в которых m является целым числом от 0 до 6, представлены формулой (150), но эта величина может быть скорректирована в соответствии с используемым количеством и скоростью реакции реагирующего сшивающего реагента, образующего метиленовые связи (будет объяснен далее и его часто будут называть реагентом, образующим метиленовые связи).

(где
R1 представляет группу, получаемую из ранее определенного органического первичного амина,
кольцо A представляет группу, получаемую из ароматического гидроксисоединения, которое образует ранее определенную ароматическую гидроксикомпозицию, и которая представляет остаток, в котором один атом водорода гидроксильных групп, непосредственно связанных с ароматическим углеводородным кольцом, был удален из ароматического гидроксисоединения,
группы R3-R6 представляют ранее определенные группы, и
m представляет целое число от 0 до 6).
Моноизоцианат может быть получен путем использования в реакции термического разложения самого по себе N-замещенной карбаминовой кислоты-O-моно(арилового эфира), представленного упомянутой выше формулой (149), но с учетом того, какие изоцианаты обычно используют в таких областях применения как получение краски и полиуретана, предпочтительно, чтобы изоцианатом являлся полифункциональный изоцианат.
Далее приводится объяснение стадии (C). В следующем объяснении N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (P) направления 4), часто обозначают как N-замещенной карбаминовой кислоты-O-моно(ариловый эфир) или N-замещенной карбаминовой кислоты моноариловый эфир.
Для стадии (C) может быть использован известный способ (см., например, патентный документ Federal Republic of Germany Patent No. 1042891).
Перед тем как проводить стадию (C), ароматическую гидроксикомпозицию, получаемую на стадии (P), отделяют от реакционной жидкости, содержащей образующийся N-замещенной карбаминовой кислоты-O-ариловый эфир. Стадия (C) может быть проведена в присутствии ароматического гидроксисоединения, но так как ароматическое гидроксисоединение может подвергаться сшиванию с помощью сшивающего реагента, образующего метиленовые связи, приводящему к образованию побочных продуктов, таких как полиароматические гидроксисоединения, или может увеличиваться количество используемого сшивающего реагента, образующего метиленовые связи, то предпочтительно отделять ароматические гидроксисоединения. Для способа разделения может быть использован известный способ, и в зависимости от используемых соединений, примеры используемых способов разделения могут включать способ ректификации, способ экстракционного разделения, в котором используется разница в растворимости между N-замещенной карбаминовой кислоты-O-ариловым эфиром и ароматическим гидроксисоединением, и способ фильтрации, проводимый путем отверждения либо N-замещенной карбаминовой кислоты-O-арилового эфира, либо ароматического гидроксисоединения. Эти способы не могут быть указаны конкретно, так как они зависят от соответствующих физических свойств используемых соединений, но способ и условия его осуществления могут быть соответствующим образом выбраны на основании знаний обычного специалиста в этой области.
При проведении стадии (C) ароматическое гидроксисоединение удаляют до тех пор, пока количество присутствующего ароматического гидроксисоединения после упомянутого выше способа разделения не составит мольное отношение 1 или меньше, предпочтительно, 0,5, и более предпочтительно, 0,1 относительно N-замещенной карбаминовой кислоты-O-арилового эфира. В данном случае ароматическое гидроксисоединение может быть удалено в присутствии растворителя, используемого на стадии (C), который будет объяснен далее.
Примеры предпочтительно используемых на стадии (C) сшивающих реагентов, образующих метиленовые связи, могут включать формальдегид, параформальдегид, триоксан, диалкоксиметаны, имеющие низшие алкильные группы, с числом углеродных атомов от 1 до 6 (такие как диметоксиметан, диэтоксиметан, дипропоксиметан, дипентаноксиметан или дигексилоксиметан), и диацилоксиметаны, имеющие низшую карбоксильную группу, такие как диацетооксиметан или дипропиоксиметан. Они могут быть использованы сами по себе, или два или более типов могут быть использованы в виде смеси. Среди них особенно предпочтительными сшивающими реагентами, образующими метиленовые связи, принимая во внимание возможность промышленного применения, легкость транспортировки сшивающего реагента, образующего метиленовые связи, и другие подобные факторы, являются водные растворы формальдегида.
При проведении реакции стадии (C) нет конкретных ограничений для отношения N-замещенной карбаминовой кислоты-O-моно(арилового эфира) к сшивающему реагенту, образующему метиленовые связи, но N-замещенной карбаминовой кислоты-O-моноариловый эфир предпочтительно использовать при мольном отношении от 2 до 20 к сшивающему реагенту, образующему метиленовые связи. Образование полиядерных форм (относящихся к N-замещенной карбаминовой кислоты-O-ариловым эфирам, в которых три или более ароматических колец (ароматических колец, получаемых из органического первичного амина) связаны с помощью метиленовой сшивающей структуры, или, другими словами, соединениям, в которых m является целым числом от 1 или более, в упомянутой выше формуле (150)) подавляется путем использования большего количества N-замещенной карбаминовой кислоты-моноарилового эфира, но если используют чрезмерно избыточное количество N-замещенной карбаминовой кислоты-O-моноарилового эфира, то во многих случаях повышается остаточное количество исходного N-замещенной карбаминовой кислоты-O-моно(арилового эфира). Поэтому, более предпочтительно, чтобы используемое количество N-замещенной карбаминовой кислоты-O-моноарилового эфира, выраженное в мольном отношении к сшивающему реагенту, образующему метиленовые связи, находилось в интервале от 3 до 15, и еще более предпочтительно, в интервале от 5 до 10.
В качестве катализатора реакции конденсации предпочтительно использовать кислотный катализатор. Примеры кислотных катализаторов могут включать неорганические кислоты, такие как хлористоводородная кислота, серная кислота, фосфорная кислота или борная кислота, и органические кислоты, такие как муравьиная кислота, уксусная кислота, щавелевая кислота или толуолсульфоновая кислота. Кроме того, могут быть также эффективными кислоты, которые относят к очень сильным кислотам, таким как бромистоводородная кислота, перхлорная кислота, хлорсульфоновая кислота или трифторметансульфоновая кислота. Кроме того, являются также эффективными ионообменные смолы, имеющие такие кислотные группы, как карбоксильные группы или сульфонатные группы, а также кислоты, относящиеся к кислотам Льюиса, такие как трифторборная кислота, хлорид железа, хлорид алюминия, хлорид цинка или хлорид титана.
В случае протонной кислоты, такой как упомянутые выше неорганические кислоты, органические кислоты или очень сильные кислоты, используемое количество этих кислот находится в интервале мольного отношения от 0,001 до 10, и, предпочтительно, в интервале от 0,01 до 5 относительно исходного сырья сложного эфира N-замещенной карбаминовой кислоты. Кроме того, в случае, когда эти кислоты используют в форме водных растворов, они могут быть использованы при концентрации в интервале от 10 до 95% по массе и, предпочтительно, в интервале от 20 до 80% по массе относительно количества воды в реакционной системе. Если концентрация составляет меньше чем 10% по массе, то становится чрезвычайно низкой скорость реакции конденсации, в то время как если концентрация превышает 95% по массе, могут протекать гидролиз сырья и другие нежелательные побочные реакции.
Реакция конденсации может быть проведена в присутствии или в отсутствие растворителя. Примеры используемых растворителей, могут предпочтительно включать линейные, разветвленные или циклические углеводороды, такие как пентан, гексан, гептан, октан, нонан, декан, гексадекан, циклопентан или циклогексан; ароматические углеводороды, такие как бензол, толуол или ксилол и их алкил-, галоген- и нитрозамещенные формы; галогенированные углеводороды, такие как хлороформ, метиленхлорид, четыреххлористый углерод, дихлорэтан, трихлорэтан или тетрахлорэтан; алифатические алкиловые эфиры, такие как метилацетат или этилацетат; и простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, диоксан или тетрагидрофуран. Кроме того, предпочтительно использовать тиоацетали, ацетали или ацилали, так как они не образуют свободный формальдегид при условиях реакции и практически не образуют воду в результате реакции с водой, образующейся в качестве побочного продукта в реакции. Особенно предпочтительно использовать ацетали и ацилали. Кроме того, упомянутые выше кислоты сами по себе предпочтительно использовать в качестве растворителей. Эти растворители могут быть использованы сами по себе, или два или более типов могут быть использованы в виде смеси.
Эти растворители могут быть использованы при массовом отношении в интервале от 0,1 до 100 и, предпочтительно, в интервале от 0,2 до 50 относительно сырья N-замещенной карбаминовой кислоты-O-моноарилового эфира.
Предпочтительно, чтобы температура реакции составляла от 10 до 160°C, более предпочтительно, от 20 до 140°C, и еще более предпочтительно, от 50 до 120°C. Для того чтобы повысить скорость реакции и быстро закончить реакцию, реакцию предпочтительно проводить при высокой температуре, но избыточно высокая температура может вызывать нежелательные побочные реакции, такие как гидролиз.
В зависимости от способа реакции, используемых соединений и реакционных условий время реакции может находиться в интервале от 1 минуты до 20 часов. Кроме того, реакция может быть остановлена при снижении до определенного уровня количества сырья N-замещенной карбаминовой кислоты-O-моноарилового эфира, которое определяют путем взятия пробы реакционной жидкости и использования известного аналитического метода, такого как жидкостная хроматография, или реакция может быть остановлена при достижении определенного уровня средней молекулярной массы продукта в форме N-замещенной карбаминовой кислоты-O-арилового эфира, определяемой путем использования известного аналитического метода, такого как гельпроникающая хроматография.
N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый описанным выше способом, является N-замещенной карбаминовой кислоты-O-ариловым эфиром, представленным упомянутой выше формулой (150). Предпочтительными являются N-замещенной карбаминовой кислоты-O-ариловые эфиры, в которых m равно 0, но с точки зрения легкости транспортировки и, особенно, вязкости раствора, и других подобных параметров, не существуют проблем в случае присутствия трехъядерных или более крупных полиядерных форм (а именно, соединений, представленных формулой (150), в которых m равняется 1 или более), при условии, что они не противоречат сути варианта настоящего осуществления.
N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (C), предпочтительно использовать на стадии (F).
Соединения, остающиеся в реакционной жидкости стадии (C) (такие как, используемые на стадии (C) реагент, образующий метиленовые связи, реакционный растворитель или катализатор), могут быть удалены из реакционной жидкости. Может быть использован известный способ в качестве способа удаления, и примеры таких способов могут включать мембранное разделение, ректификационное разделение и кристаллизацию, но предпочтительным является ректификационное разделение. В случае удаления соединения, остающегося в реакционной жидкости стадии (C), с помощью ректификационного разделения, путем добавления ароматической гидроксикомпозиции, используемой на следующей стадии (F), к реакционной жидкости стадии (C) с получением смешанной жидкости, с последующим удалением соединений, остающихся в реакционной жидкости стадии (C) (таких, как используемые на стадии (C) реагент, образующий метиленовые связи, реакционный растворитель или катализатор) из смешанной жидкости, ректификационное разделение может быть проведено без выпадения в осадок сложного эфира N-замещенной карбаминовой кислоты, что делает этот способ предпочтительным.
Так как на стадии (C) используется кислота, то это надо учитывать при выборе материалов реактора и конденсатора, но для материалов нет конкретных ограничений, при условии, что они не вызывают таких проблем, как коррозия в результате воздействия соединений, используемых на стадии (C), и могут быть использованы известные материалы. Примеры используемых материалов могут включать стекло, нержавеющую сталь, углеродистую сталь, сплав Хастелой (Hastelloy), эмалированные материалы и материалы с тефлоновым покрытием. В случае необходимости могут быть добавлены известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства, для нагревания может быть использован такой известный способ, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии, и например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области.
<Направление 5)>
Направление 5) является способом проведения стадии (R), проведения стадии (C) и проведения стадии (P). Направление 5) является одним аспектом способа, указанного в направлении 3).
Способ направления 5) является способом получения N-замещенной карбаминовой кислоты-O-R2 эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-R2 эфира являются сшитыми с помощью метиленовых (-CH2-) групп, из N-замещенной карбаминовой кислоты-O-R2 эфира, получаемого на стадии (R) путем проведения следующей стадии (C) после стадии (R), в котором органический первичный амин, используемый на стадии (A), является ароматическим органическим первичным моноамином, представленным следующей формулой (5), и затем проведения стадии (P) с получением N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого из N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-R2 эфира являются сшитыми с помощью метиленовых групп (-CH2-), путем реакции N-замещенной карбаминовой кислоты-O-R2 эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-R2 эфира являются сшитыми с помощью метиленовых групп (-CH2-), и ароматической гидроксикомпозиции.
Стадия (C): стадия получения N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира являются сшитыми с помощью метиленовых групп (-CH2-) путем реакции N-замещенной карбаминовой кислоты-O-(R2 или арилового)эфира с формальдегидом или сшивающим реагентом, образующим метиленовые связи, и сшивания ароматических групп, получаемых из ароматического органического первичного моноамина, содержащихся в N-замещенной карбаминовой кислоты-O-(R2 или ариловом) эфире, с помощью метиленовых групп (-CH2-).
N-замещенной карбаминовой кислоты-O-ариловый эфир этого направления 5) относится к N-замещенной карбаминовой кислоты-O-ариловому эфиру, образующемуся в следовых количествах при использовании ароматической гидроксикомпозиции на стадии (A) и/или стадии (R).
В этом направлении, стадию (A) проводят, используя органический первичный амин, представленный следующей формулой (5), в качестве органического первичного амина, с получением соединения, имеющего уреидные группы, представленного формулой (1), получаемого из органического первичного амина, за которой следует проведение стадии (R) с получением N-замещенной карбаминовой кислоты-O-R2 эфира, получаемого из соединения, имеющего уреидные группы, проводя стадию (C) с получением N-замещенной карбаминовой кислоты-O-R2 эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-R2 эфира являются сшитыми с помощью метиленовых групп (-CH2-), и, наконец, проводя стадию (P) с получением N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого из N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции, в котором N-замещенной карбаминовой кислоты-O-R2 эфир является сшитым с помощью метиленовых групп (-CH2-).
А именно, органический первичный амин, используемый в этом направлении, является органическим первичным амином, представленным формулой (5), соединение, имеющее уреидные группы, получаемое на стадии (A) этого направления, является соединением, имеющим уреидные группы, представленным формулой (41), получаемым из органического первичного амина, и, более конкретно, соединением, имеющим уреидные группы, представленным формулой (148), N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (R) этого направления, является N-замещенной карбаминовой кислоты-O-R2 эфиром, в котором r =1, который представлен формулой (49) и который получают из уреидных групп и спирта, и, более конкретно, N-замещенной карбаминовой кислоты-O-R2 эфиром, представленным следующей формулой (146), N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (C) этого направления, является N-замещенной карбаминовой кислоты-O-R2 эфиром, представленным следующей формулой (151), получаемым из N-замещенной карбаминовой кислоты-O-R2 эфира, и N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (P) этого направления, является N-замещенной карбаминовой кислоты-O-ариловым эфиром, представленным формулой (150), получаемым из N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции. Указания конкретных примеров каждого из этих соединений соответственно содержатся в ранее приведенных их объяснениях.
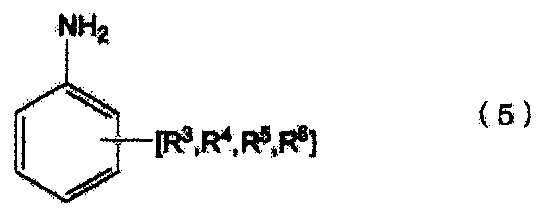
(где
по меньшей мере одно место в орто-положении и/или пара-положении NH2 группы ароматического органического первичного моноамина, представленного формулой (5), является незамещенным, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут быть соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут вместе быть связаны с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из групп, состоящих из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 составляет целое число в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют ароматический органический первичный моноамин, представленный формулой (5), составляет целое число от 6 до 13).
В этом случае соединение, имеющее уреидные группы, получаемое на стадии (A), является по меньшей мере одним типом соединения, имеющего уреидные группы, представленного следующий формулой (148). Кроме того, группы R3, R4, R5 и R6 в следующей формуле (148) выбирают из групп R3, R4, R5 и R6 органического первичного амина, представленного упомянутой выше формулой (5), и соединение, имеющее уреидные группы, является соединением, в котором аминогруппы (-NH2 группы) органического первичного амина, представленного формулой (5), находятся в форме уреидных групп (-NH-CO-NH2):

(где
по меньшей мере одно место в орто-положении и/или пара-положении уреидной группы N-замещенной ароматической органической мономочевины, представленной формулой (148), является незамещенным, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут быть соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут вместе быть связаны с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из групп, состоящих из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 составляет целое число в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют N-замещенную ароматическую органическую мономочевину, представленную формулой (148), исключая уреидные группы (-NH-CO-NH2), составляет целое число от 6 до 13).
В этом случае N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (R), путем проведения стадии (A) является по меньшей мере одним типом N-замещенной карбаминовой кислоты-O-R2 эфира, представленного следующей формулой (146). Кроме того, группы R3, R4, R5 и R6 в следующей формуле (146) выбирают из групп R3, R4, R5 и R6 соединения, имеющего уреидные группы, представленного упомянутой выше формулой (148), и является соединением, в котором уреидные группы (-NH-CO-NH2) соединения, имеющего уреидные группы, представленного формулой (148), находятся в форме групп карбаминовой кислоты-O-R2 эфира группы R2, получающейся из спирта:

(где
группы R2-R6 являются группами, указанными выше).
В этом случае N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (C) путем проведения стадии (R), является по меньшей мере одним типом N-замещенной карбаминовой кислоты-O-R2 эфира, представленного следующей формулой (151). Кроме того, R3, R4, R5 и R6 в следующей формуле (151) выбирают из групп R3, R4, R5 и R6 органического первичного амина, представленного упомянутой выше формулой (5):
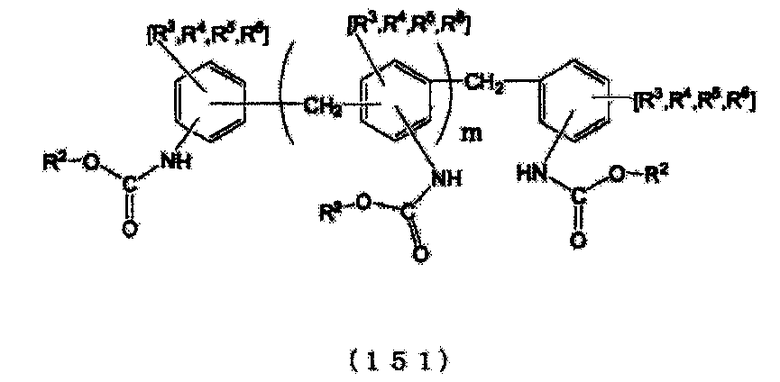
(где
группы R2-R6 являются группами, указанными выше, и m является целым числом от 0 до 6).
Используемый на стадиях (A) и (R) этого направления органический первичный амин является органическим первичным амином, представленным формулой (5), и стадии (A), (R) и (P) этого направления проводят при условиях стадий (A) и (R) направления 4). Кроме того, стадию (C) этого направления проводят при условиях стадии (C) направления 4), за исключением того, что реагирующим сырьем является N-замещенной карбаминовой кислоты-O-R2 эфир. Кроме того, в отличие от сырья, используемого в направлении 4), которым является N-замещенной карбаминовой кислоты-O-моно(R2 или ариловый) эфир, стадию (P) этого направления проводят при условиях стадии (P), описанных в направлении 4), за исключением того, что используемым сырьем является N-замещенной карбаминовой кислоты-O-R2 эфир, N-замещенной карбаминовой кислоты-O-R2 эфир является сшитым с помощью метиленовых групп (-CH2-).
В зависимости от реагируемых соединений, условия реакции получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции соединения, имеющего уреидные группы, и спирта стадии (R) являются такими, что используемое количество спирта имеет мольное отношение в интервале от 1 до 500 относительно уреидных групп используемого соединения, имеющего уреидные группы. Предпочтительно использовать избыток спирта, так как если мольное отношение является меньшим, чем 1, то легко образуются сложнозамещенные карбонильные соединения и высокомолекулярные соединения, имеющие в их молекулах карбонильные связи, но принимая во внимание размер реактора, предпочтительно, чтобы мольное отношение находилось в интервале от 1 до 200, более предпочтительно, в интервале от 1,5 до 100, и, еще более предпочтительно, в интервале от 2 до 50.
В зависимости от используемых соединений, предпочтительно, чтобы температура реакции находилась в интервале от 100 до 350°C. Если температура составляет величину ниже, чем 100°C, реакция замедляется, или реакция вообще практически не идет, или увеличивается образование сложнозамещенных карбонильных соединений, что является нежелательным. С другой стороны, при температурах выше чем 350°C, на стадии (A) также остается N-замещенной карбаминовой кислоты-O-R2 эфир, разлагается мочевина (и не-N-замещенной карбаминовой кислоты эфир), образующаяся в системе стадии (R), гидроксикомпозиция подвергается денатурации в результате реакции дегидрирования, или легко протекают реакции разложения и денатурации продукта в форме N-замещенной карбаминовой кислоты-O-R2 эфира, что является нежелательным. С этой точки зрения, более предпочтительно, чтобы температура реакции находилась в интервале от 120 до 320°C, и еще более предпочтительно, в интервале от 140 до 300°C.
Как уже было описано выше, реакция, по которой образуется N-замещенной карбаминовой кислоты-O-R2 эфир, является обратимой реакцией, и так как равновесие сдвинуто в сторону реагирующих веществ, реакцию предпочтительно проводить при удалении из системы как можно в большей степени аммиака, образующегося в качестве побочного продукта. Аммиак предпочтительно удалять так, чтобы концентрация аммиака в реакционной жидкости составляла, предпочтительно, 1000 ppm или менее, более предпочтительно, 300 ppm или менее, еще более предпочтительно, 100 ppm или менее, и наиболее предпочтительно, 30 ppm или менее (содержание в реакционной жидкости относится к содержанию в жидкой фазе при проведении стадии (R)). Аммиак может быть удален с помощью таких способов, как реакционная дистилляция, использование инертного газа, мембранное разделение и адсорбционное разделение. Например, реакционная дистилляция относится к способу отделения непрерывно образующегося аммиака в процессе реакции путем дистилляции в форме газа. Для того чтобы повысить эффективность дистилляции аммиака, она может быть проведена при кипячении спирта, растворителя или гидроксикомпозиции. Кроме того, способ, в котором используют инертный газ, относится к способу отделения непрерывно образующегося аммиака в процессе реакции от реакционной системы в форме газа вместе с инертным газом. Примеры используемых инертных газов могут включать азот, гелий, аргон, диоксид углерод, метан, этан и пропан, они могут быть использованы сами по себе, или в виде смеси, и предпочтительным является способ, в котором в реакционную систему вводят инертный газ. Примеры адсорбентов, используемых в способах адсорбционного разделения, могут включать адсорбенты, которые можно использовать при температурах проведения реакции, такие как оксид кремния, оксид алюминия, различные типы цеолита или диатомовая земля. Эти способы удаления аммиака из системы могут быть проведены сами по себе, или множество их типов могут быть проведены в комбинации.
В целях повышения скорости реакции может быть использован, например, катализатор. Примеры используемых катализаторов могут предпочтительно включать основные катализаторы, такие как метилаты, этилаты или бутираты (включая изомеры) лития, натрия, калия, кальция или бария, редкоземельные элементы, сурьма или висмут сами по себе или их оксиды, сульфиды и их соли, бор сам по себе или соединения бора, металлы группы меди, группы цинка, группы алюминия, группы углерода и группы титана периодической системы элементов, а также оксиды и сульфиды металлов, и карбиды и нитриды элементов группы углерода, исключая углерод, группы титана, группы ванадия и группы хрома периодической системы элементов. В случае использования катализатора нет конкретных ограничений для количества используемого катализатора, но катализатор может быть использован в интервале мольного отношения от 0,0001 до 100 относительно уреидных групп соединения, имеющего уреидные группы.
В зависимости от композиции реакционной системы, температуры реакции, используемого способа для удаления аммиака, реакционного аппарата и других подобных параметров, реакционное давление обычно находится в интервале от 0,01 Па до 10 МПа (абсолютное давление), но с точки зрения возможности промышленного применения, более предпочтительно, чтобы реакционное давление находилось в интервале от 0,1 Па до 5 МПа (абсолютное давление), и принимая во внимание необходимость удаления газообразного аммиака из системы, еще более предпочтительно, применять давление от 1,5 МПа (абсолютное давление).
В зависимости от композиции реакционной системы, температуры реакции, используемого способа для удаления аммиака, реакционного аппарата, реакционного давления и других подобных параметров, время реакции (время пребывания в случае непрерывной реакции) обычно составляет от 0,01 до 100 часов. Время реакции может также быть определено на основе количества образовавшегося целевого соединения в форме N-замещенной карбаминовой кислоты-O-R2 эфира (и в зависимости от случая, суммарного количества, образовавшегося вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира). Например, реакция может быть остановлена после взятия пробы реакционной жидкости, определения содержания эфира N-замещенной карбаминовой кислоты в реакционной жидкости (и, в зависимости от случая, суммарного количества, образующегося вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира) и подтверждения того, что N-замещенной карбаминовой кислоты-O-R2 эфир образовался с выходом 10% или более относительно соединения, имеющего уреидные группы, или реакция может быть остановлена после подтверждения того, что выход составляет 90% или более. Реакционную жидкость, содержащую N-замещенной карбаминовой кислоты-O-R2 эфир, получаемую на стадии (R), превращают в N-замещенной карбаминовой кислоты-O-ариловый эфир в способе, который включает стадию (P), которая будет описана далее, за которой следует получение изоцианата на стадии (F). В данном случае, если содержание N-замещенной карбаминовой кислоты-O-R2 эфира на стадии (R) является низким (его выход является низким), то в ряде случаев это может приводить к понижению выхода изоцианата. Поэтому, предпочтительно, чтобы выход N-замещенной карбаминовой кислоты-O-R2 эфира составлял 50% или более, более предпочтительно, 80% или более, и еще более предпочтительно, 90% или более.
Использование реакционного растворителя в реакции не является необходимым, но с целью облегчения осуществления реакции предпочтительно использовать подходящий растворитель в качестве реакционного растворителя, примеры которого включают алканы, такие как пентан (включая изомеры), гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; нитрильные соединения, такие как ацетонитрил или бензонитрил; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; сложные эфиры, такие как дибутилфталат, дигексилфталат, диоктилфталат или бензилбутилфталат; простые эфиры и тиоэфиры, такие как тетрагидрофуран, 1,4-диоксан, 1,2-диметоксиэтан, дифениловый эфир или дифенилсульфид; кетоновые соединения, такие как ацетон или метилэтилкетон; эфирные соединения, такие как этилацетат или этилбензоат; и сульфоксиды, такие как диметилсульфоксид или дифенилсульфоксид. Естественно, что в качестве реакционного растворителя также предпочтительно использовать гидроксикомпозицию, используемую в реакции в избытке.
Реакцию проводят в системе, включающей газовую фазу, содержащую гидроксикомпозицию, соединение, имеющее карбонильные группы, получаемое из мочевины (соединение, которое обретает карбонильную группу, которую имела мочевина, такое как не-N-замещенной карбаминовой кислоты эфир или биурет, которое относится к соединению, не включающему N-замещенной карбаминовой кислоты-O-эфиры), и аммиак, получаемый в качестве побочного продукта в реакции, и жидкую фазу, в которой проводят реакцию. Большую часть реакции проводят в жидкой фазе, но в зависимости от реакционных условий она может быть также проведена в газовой фазе. В данном случае, предпочтительно, чтобы объемная доля жидкой фазы в реакционной смеси, в которой реакцию проводят, составляла 50% или менее. В случае проведения реакции непрерывно в течение длительного периода времени, вследствие колебаний технологических условий (таких как температура или давление) и других подобных параметров могут образовываться полимерные побочные продукты, но если объемное содержание жидкой фазы в реакторе является высоким, то слипание и накопление таких полимерных побочных продуктов в реакторе может быть предотвращено. Однако, если объемное содержание жидкой фазы является избыточно высоким, то, так как может снизиться эффективность удаления побочного продукта аммиака и уменьшиться выход N-замещенной карбаминовой кислоты-O-R2 эфира (и в зависимости от случая, суммарного количества, образующегося вследствие добавления количества N-замещенной карбаминовой кислоты-O-арилового эфира), предпочтительно, чтобы объемная доля жидкой фазы относительно газовой фазы составляла 50% или менее, более предпочтительно, 30% или менее, и еще более предпочтительно, 20% или менее (объемная доля жидкой фазы относится к объемному отношению жидкой фазы относительно объема реакционной емкости в случае реактора типа емкости, объема ступени, ниже ступени ввода сырья (не включая днище колонны и ребойлер) в случае колонного типа реактора, или объема пленочного дистилляционного аппарата в случае пленочного дистилляционного аппарата).
При проведении реакции нет конкретных ограничений для используемого реакционного аппарата, и может быть использован известный реактор, но предпочтительно использовать реактор типа емкости и/или реактор колонного типа. Предпочтительно, чтобы используемый реактор был снабжен конденсатором.
Как было описано ранее, реакцию предпочтительно проводить в системе, включающей газовую фазу, содержащую гидроксикомпозицию, соединение, имеющее карбонильные группы, получаемое из мочевины, и аммиак, получаемый в качестве побочного продукта в реакции, и жидкую фазу, в которой проводят реакцию при таких условиях, что объемная доля жидкой фазы в реакторе составляет 50% или менее, и реактор, который удовлетворяет этим условиям, выбирают в качестве реактора, в котором проводят реакцию.
Более конкретно, могут быть соответствующим образом подсоединены и использованы известные традиционные реакторы, примеры которых могут включать реактор с мешалкой, работающий под повышенным давлением реактор с мешалкой, работающий под пониженным давлением реактор с мешалкой, реактор колонного типа, ректификационную колонну, насадочную колонну или пленочный дистилляционный аппарат.
Нет конкретных ограничений для типа конденсатора, устанавливаемого в реакторе, и может быть использован известный конденсатор. Например, могут быть соответствующим образом подсоединены и использованы традиционно известные конденсаторы, такие как трубчатый цилиндрический конденсатор, двухтрубный конденсатор, однотрубный конденсатор или конденсатор с воздушным охлаждением. Конденсатор может быть установлен внутри реактора или снаружи реактора, или он может быть соединен с реактором с помощью линии, и могут быть использованы различные типы конденсаторов, принимая во внимание формы реактора и конденсатора, способ транспортирования сконденсированной жидкости и другие подобные параметры.
Нет конкретных ограничений для материалов реактора и конденсатора, и могут быть использованы известные материалы. Примеры используемых материалов могут включать стекло, нержавеющую сталь, углеродистую сталь, сплав Хастелой, эмалированные материалы и материалы с тефлоновым покрытием. Такие материалы как SUS304, SUS316 или SUS316L являются недорогими и могут быть предпочтительно использованы. Могут быть добавлены при необходимости известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства, для нагревания может быть использован такой известный способ, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии. Например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области, такие как стадия растворения соединения, имеющего уреидные группы, в ароматической гидроксикомпозиции, стадия растворения ароматического гидроксисоединения, стадия отделения спирта, стадия отделения и/или очистки ароматического гидроксисоединения, стадия очистки N-замещенной карбаминовой кислоты-O-R2 эфира от образующейся реакционной жидкости или стадия сжигания или вывода побочных продуктов и другие подобные стадии.
Образующийся на стадии (R) газообразный компонент, содержащий соединение, имеющее карбонильные группы, получаемое из мочевины, и аммиак, образующийся в реакции в качестве побочного продукта, вводят в установленный в реакторе конденсатор, и конденсируют весь или часть спирта и соединения, имеющего карбонильные группы, получаемого из мочевины, после чего следует извлечение аммиака в форме газа.
В данном случае соединение, имеющее карбонильные группы, получаемое из мочевины, которое содержится в аммиаке, извлекаемом в виде газа из конденсатора, присутствует в конкретном количестве или менее. А именно, отношение числа карбонильных групп (-C(=O)-), содержавшихся в соединении, имеющем карбонильные группы, получаемом из мочевины, содержащемся в аммиаке, к числу молекул аммиака составляет 1 или менее, предпочтительно, 0,5 или менее, более предпочтительно, 0,1 или менее, и еще более предпочтительно, 0,01 или менее. Причиной поддержания в конкретном интервале количества соединения, имеющего карбонильные группы, получаемого из мочевины, содержавшегося в аммиаке, является предотвращение слипания и накопления твердых компонентов в линии для транспортировки аммиака из конденсатора.
Все твердые компоненты, которые слипаются и накапливаются в линии для транспортировки аммиака, не могут быть идентифицированы, но в результате исследований, проведенных авторами настоящего изобретения, было определено, что их большая часть является соединениями, имеющими карбонильные группы. Один возможный способ предотвращения адгезии и накопления таких твердых компонентов включает нагревание линии для транспортировки аммиака для разложения соединений, имеющих карбонильные группы, но, согласно исследованиям, проведенным авторами настоящего изобретения, во многих случаях нагревание само по себе вызывает полимеризацию продуктов распада (таких как изоциановая кислота) или реакцию продуктов распада с другими соединениями, имеющими карбонильные группы, что затрудняет полное предотвращение слипания и накопление твердых компонентов. Кроме того, в случае простого нагревания линии, было обнаружено, что соединения, имеющие карбонильные группы, содержащиеся в аммиаке, и их продукты распада отверждаются в результате быстрого охлаждения на выходе из линии для транспортировки аммиака (например, часть при контакте с атмосферой), что часто приводит к значительному слипанию и накоплению твердых компонентов. В результате проведения обширных исследований этой проблемы авторы настоящего изобретения неожиданно обнаружили, что проблема слипания и накопления твердых компонентов может быть решена путем поддержания на определенном уровне количества соединения, имеющего карбонильные группы, получаемого из производной угольной кислоты, содержавшегося в аммиаке, которое равно или меньше, чем описанное выше конкретное количество. Механизм, на основании которого этот эффект проявляется, остается неясным, но авторы настоящего изобретения предположили, что слипание и накопление в трубопроводе вызывается самим по себе соединением, имеющим карбонильные группы, получаемым из производной угольной кислоты, а также продуктами разложения и/или полимеризации соединения, имеющего карбонильные группы, получаемого из производной угольной кислоты, и что в результате поддержания на определенном уровне количества карбонильных групп, содержащихся в соединении, имеющем карбонильные группы, получаемом из производной угольной кислоты, который равен или меньше, чем конкретная концентрация, значительно уменьшается слипание самого по себе соединения, имеющего карбонильные группы, полученного из производной угольной кислоты, так же как и скорости реакций разложения и/или полимеризации этого соединения.
С другой стороны, гидроксикомпозицию и соединение, имеющее карбонильные группы, получаемое из мочевины, конденсируют таким образом, что мольное отношение сконденсированной гидроксикомпозиции к сконденсированному соединению, имеющему карбонильные группы, получаемому из мочевины, составляет 1 или более, предпочтительно, 2 или более, и более предпочтительно, 3 или более. Причиной для определения таких интервалов является желание получить смесь гидроксикомпозиции и соединения, имеющего карбонильные группы, получаемого из мочевины, сконденсированных в конденсаторе, в форме гомогенной жидкой смеси. В результате, не только облегчается транспортировка смеси, но и может быть предотвращено возникновение таких проблем, как слипание и накопление твердых компонентов в конденсаторе.
Кроме того, смесь гидроксикомпозиции и соединения, имеющего карбонильные группы, полученного из мочевины, сконденсированная в конденсаторе на стадии (R), может быть рециркулирована в реактор и повторно использована в реакторе стадии (A). В данном случае, предпочтительно, чтобы количество аммиака, содержащееся в смеси, составляло 5000 ppm или менее, более предпочтительно, 3000 ppm или менее, и еще более предпочтительно, 2000 ppm или менее.
Как уже было описано выше, извлекают различные соединения в форме соединений, имеющих карбонильные группы, получаемых из мочевины, но нет конкретных ограничений для повторного использования этих соединений.
Стадия (C) этого направления является стадией получения N-замещенной карбаминовой кислоты-O-R2 эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-R2 эфира являются сшитыми с помощью метиленовых групп (-CH2-), путем сшивания по меньшей мере одного типа N-замещенной карбаминовой кислоты-O-R2 эфира (или реакционной жидкости, содержащей его), получаемого на стадии (R), с помощью метиленовых групп (-CH2-). В результате проведения стадии (C) получают N-замещенной карбаминовой кислоты-O-ариловый эфир, в котором по меньшей мере две молекулы по меньшей мере одного типа N-замещенной карбаминовой кислоты-O-арилового эфира, представленного упомянутой выше формулой (151), являются сшитыми с помощью метиленовых групп (-CH2-).
Здесь, при проведении направления 5), предпочтительно, чтобы ароматическое гидроксисоединение, представленное формулой (2), и, более предпочтительно, ароматическое гидроксисоединение, представленное формулой (7), использовалось в качестве ароматического гидроксисоединения, которое составляет описанную ранее ароматическую гидроксикомпозицию, используемую на стадии (A) и/или стадии (R). Более предпочтительно, чтобы ароматическое гидроксисоединение являлось ароматическим гидроксисоединением, представленным формулой (31), нафтолом (включая изомеры), феноксифенолом (включая изомеры) или дифеноксифенолом (включая изомеры), в котором орто-положение или пара-положение гидроксильной группы не является замещенным, или ароматическим моногидроксисоединением, в котором группы R19 и R23 ароматического гидроксисоединения, представленного формулой (31), являются линейными и/или циклическими насыщенными алкильными группами. Предпочтительно, чтобы ароматическое гидроксисоединение, которое составляет ароматическую гидроксикомпозицию, используемую на стадии (P) направления 5), являлось активным ароматическим гидроксисоединением, ароматическим гидроксисоединением, выбранным из ароматических гидроксисоединений, представленных формулой (32), и более предпочтительно, ароматическим гидроксисоединением, представленным формулой (38).
Соединения, в которых m является целым числом от 0 до 6, представлены формулами (151) и (150), но эта величина может быть скорректирована в соответствии с используемым количеством и скоростью реакции реагирующего сшивающего реагента, образующего метиленовые связи (будет объяснен далее и часто будет обозначаться как реагент, образующий метиленовые связи):

(где
R1 представляет группу, получаемую из ранее определенного органического первичного амина,
кольцо A представляет группу, получаемую из ароматического гидроксисоединения, которое составляет ранее определенную ароматическую гидроксикомпозицию, и которая представляет остаток, в котором один атом водорода гидроксильных групп, непосредственно связанных с ароматическим углеводородным кольцом, был удален из ароматического гидроксисоединения, и
R3-R6 представляют ранее определенные группы, и
m представляет целое число от 0 до 6).
Далее приводится объяснение стадии (C). В следующем объяснении, N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (R) направления 5), часто обозначают как N-замещенной карбаминовой кислоты-O-моно(R2 эфир) или N-замещенной карбаминовой кислоты моно-R2 эфир.
Для стадии (C) может быть использован известный способ (см., например, патентный документ Federal Republic of Germany Patent No. 1042891).
Перед проведением стадии (C), в случае использования ароматической гидроксикомпозиции на стадии (R), ароматическую гидроксикомпозицию, получаемую на стадии (R), отделяют от реакционной жидкости, содержащей образующийся N-замещенной карбаминовой кислоты-O-R2 эфир. Стадия (C) может быть проведена в присутствии ароматического гидроксисоединения, но так как ароматическое гидроксисоединение может подвергаться сшиванию с помощью сшивающего реагента, образующего метиленовые связи, приводящему к образованию побочных продуктов, таких как полиароматические гидроксисоединения, или может увеличиваться количество используемого сшивающего реагента, образующего метиленовые связи, ароматические гидроксисоединения предпочтительно отделять. Для способа разделения может быть использован известный способ, и в зависимости от используемых соединений, примеры используемых способов разделения могут включать способ ректификации, способ экстракционного разделения, в котором используется разница в растворимости между N-замещенной карбаминовой кислоты-O-R2 эфиром и ароматическим гидроксисоединением, и способ фильтрации, проводимый путем отверждения либо N-замещенной карбаминовой кислоты-O-R2 эфира, либо ароматического гидроксисоединения. Эти способы не могут быть указаны конкретно, так как они зависят от соответствующих физических свойств используемых соединений, но способ и условия его осуществления могут быть соответствующим образом выбраны на основании знаний обычного специалиста в этой области.
При проведении стадии (C) ароматическое гидроксисоединение удаляют до тех пор, пока количество присутствующего ароматического гидроксисоединения после применения упомянутого выше способа разделения не составит мольное отношение 1 или меньше, предпочтительно, 0,5, и более предпочтительно, 0,1 относительно N-замещенной карбаминовой кислоты-O-R2 эфира. В данном случае ароматическое гидроксисоединение может быть удалено в присутствии растворителя, используемого на стадии (C), который будет объяснен далее.
Примеры сшивающих реагентов, образующих метиленовые связи, предпочтительно используемых на стадии (C), могут включать формальдегид, параформальдегид, триоксан, диалкоксиметаны, имеющие низшие алкильные группы, с числом углеродных атомов от 1 до 6 (такие как диметоксиметан, диэтоксиметан, дипропоксиметан, дипентаноксиметан или дигексилоксиметан), и диацилоксиметаны, имеющие низшую карбоксильную группу, такие как диацетооксиметан или дипропиоксиметан. Они могут быть использованы сами по себе, или два или более типов могут быть использованы в виде смеси. Среди них особенно предпочтительными сшивающими реагентами, образующими метиленовые связи, являются водные растворы формальдегида, принимая во внимание возможность промышленного применения, легкость транспортировки сшивающего реагента, образующего метиленовые связи, и другие подобные факторы.
При проведении реакции стадии (C), нет конкретных ограничений для отношения N-замещенной карбаминовой кислоты-O-моно(R2 эфира) к сшивающему реагенту, образующему метиленовые связи, но N-замещенной карбаминовой кислоты-O-моно(R2 эфир) предпочтительно использовать при мольном отношении от 2 до 20 к сшивающему реагенту, образующему метиленовые связи. Образование полиядерных форм (относящихся к N-замещенной карбаминовой кислоты-O-R2 эфирам, в которых три или более ароматических колец (ароматических колец, получаемых из органического первичного амина) связаны с помощью метиленовой сшивающей структуры, или другими словами, соединениям, в которых m является целым числами от 1 или более в упомянутой выше формуле (151)) предотвращают путем использования большего количества N-замещенной карбаминовой кислоты-моно(R2 эфира), но если используют чрезмерно избыточное количество N-замещенной карбаминовой кислоты-O-моно(R2 эфира), то во многих случаях повышается остаточное количество исходного N-замещенной карбаминовой кислоты-O-моно(R2 эфира). Таким образом, более предпочтительно, чтобы используемое количество N-замещенной карбаминовой кислоты-O-моно(R2 эфира), выраженное в мольном отношении к сшивающему реагенту, образующему метиленовые группы, находилось в интервале от 3 до 15, и еще более предпочтительно, в интервале от 5 до 10.
В качестве катализатора реакции конденсации предпочтительно использовать кислотный катализатор. Примеры кислотных катализаторов могут включать неорганические кислоты, такие как хлористоводородная кислота, серная кислота, фосфорная кислота или борная кислота, и органические кислоты, такие как муравьиная кислота, уксусная кислота, щавелевая кислота или толуолсульфоновая кислота. Кроме того, могут быть также эффективными кислоты, которые относят к очень сильным кислотам, таким как бромистоводородная кислота, хлорная кислота, хлорсульфоновая кислота или трифторметансульфоновая кислота. Кроме того, являются также эффективными ионообменные смолы, имеющие кислотные группы, такие как карбоксильные группы или сульфонатные группы, а также кислоты, относящиеся к кислотам Льюиса, такие как трифторборная кислота, хлорид железа, хлорид алюминия, хлорид цинка или хлорид титана.
В случае протонной кислоты, такой как упомянутые выше неорганические кислоты, органические кислоты или очень сильные кислоты, используемое количество этих кислот находится в интервале мольного отношения от 0,001 до 10, и, предпочтительно, в интервале от 0,01 до 5 относительно исходного сырья эфира N-замещенной карбаминовой кислоты. Кроме того, в случае, когда эти кислоты используют в форме водных растворов, они могут быть использованы при концентрации в интервале от 10 до 95% по массе и, предпочтительно, в интервале от 20 до 80% по массе относительно количества воды в реакционной системе. Если концентрация составляет меньше, чем 10% по массе, то становится чрезвычайно низкой скорость реакции конденсации, в то время как если концентрация превышает 95% по массе, могут протекать гидролиз сырья и другие нежелательные побочные реакции.
Реакция конденсации может быть проведена в присутствии или в отсутствие растворителя. Примеры используемых растворителей могут предпочтительно включать линейные, разветвленные или циклические углеводороды, такие как пентан, гексан, гептан, октан, нонан, декан, гексадекан, циклопентан или циклогексан; ароматические углеводороды, такие как бензол, толуол или ксилол и их алкил-, галоген- и нитрозамещенные формы; галогенированные углеводороды, такие как хлороформ, метиленхлорид, четыреххлористый углерод, дихлорэтан, трихлорпентан или тетрахлорпентан; алифатические алкиловые эфиры, такие как метилацетат или этилацетат; и простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, диоксан или тетрагидрофуран. Кроме того, предпочтительно использовать тиоацетали, ацетали или ацилали, так как они не образуют свободный формальдегид при условиях реакции и практически не образуют воду путем реакции с водой, образующейся в качестве побочного продукта в реакции. Особенно предпочтительно использовать ацетали и ацилали. Кроме того, упомянутые выше кислоты сами по себе предпочтительно использовать в качестве растворителей. Эти растворители могут быть использованы само по себе, или два или более типов могут быть использованы в виде смеси.
Эти растворители могут быть использованы при массовом отношении в интервале от 0,1 до 100 и, предпочтительно, в интервале от 0,2 до 50 относительно сырья N-замещенной карбаминовой кислоты-O-моно(R2 эфира).
Предпочтительно, чтобы температура реакции составляла от 10 до 160°C, более предпочтительно, от 20 до 140°C, и еще более предпочтительно, от 50 до 120°C. Для того чтобы повысить скорость реакции и быстро закончить реакцию, реакцию предпочтительно проводить при высокой температуре, но избыточно высокая температура может вызывать нежелательные побочные реакции, такие как гидролиз.
В зависимости от способа реакции, используемых соединений и реакционных условий, время реакции может находиться в интервале от 1 минуты до 20 часов. Кроме того, реакция может быть остановлена, когда снижение количества сырья N-замещенной карбаминовой кислоты-O-моно(R2 эфира) достигнет определенного уровня, определяемого путем взятия пробы реакционной жидкости и использования известного аналитического метода, такого как жидкостная хроматография, или реакция может быть остановлена, когда средняя молекулярная масса продукта в форме N-замещенной карбаминовой кислоты-O-арилового эфира достигнет определенного уровня, определяемого путем использования известного аналитического метода, такого как гельпроникающая хроматография.
N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый описанным выше способом, является N-замещенной карбаминовой кислоты-O-R2 эфиром, представленным упомянутой выше формулой (151). N-замещенной карбаминовой кислоты-O-R2 эфиры, в которых m равно 0, являются предпочтительными, но с точки зрения легкости транспортировки и, особенно, вязкости раствора и других подобных параметров, не существует проблем с присутствием трехъядерных или более крупных полиядерных форм (а именно, соединений, представленных формулой (151), в которых m равняется 1 или более), при условии, что они не противоречат сущности варианта настоящего осуществления.
N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (C), предпочтительно использовать на стадии (P).
Соединения, остающиеся в реакционной жидкости стадии (C) (такие как, используемые на стадии (C) реагент, образующий метиленовые связи, реакционный растворитель или катализатор), могут быть удалены из реакционной жидкости. В качестве способа удаления может быть использован известный способ, и примеры таких способов могут включать мембранное разделение, ректификационное разделение и кристаллизацию, но предпочтительным является ректификационное разделение. В случае удаления соединения, остающегося в реакционной жидкости стадии (C), с помощью ректификационного разделения, путем добавления ароматической гидроксикомпозиции, используемой на следующей стадии (P), к реакционной жидкости стадии (C) с получением смешанной жидкости, с последующим удалением соединений, остающихся в реакционной жидкости стадии (C) (таких, как используемые на стадии (C) реагент, образующий метиленовые связи, реакционный растворитель или катализатор), из смешанной жидкости, ректификационное разделение может быть проведено без выпадения в осадок сложного эфира N-замещенной карбаминовой кислоты, что делает этот способ предпочтительным.
Так как на стадии (C) используется кислота, то это надо учитывать при выборе материалов реактора и конденсатора, но для материалов нет конкретных ограничений, при условии, что они не вызывают таких проблем, как коррозия в результате воздействия соединений, используемым на стадии (C), и могут быть использованы известные материалы. Примеры используемых материалов могут включать стекло, нержавеющую сталь, углеродистую сталь, Сплав Хастелой, эмалированные материалы и материалы с тефлоновым покрытием. В случае необходимости могут быть добавлены известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства, для нагревания может быть использован такой известный способ, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии, и например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области.
<Стадия(P)> Стадия переэтерификации
Так как эта стадия является стадией превращения эфирной группы N-замещенной карбаминовой кислоты-O-R2 эфира, то в варианте настоящего осуществления ее также обычно называют "стадией переэтерификации".
Стадия (P): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции N-замещенной карбаминовой кислоты-O-R2 эфира и ароматической гидроксикомпозиции (композиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2)) в жидкой фазе и извлечения спирта, образующегося в качестве побочного продукта, в газовую фазу.
На фигуре 6 представлена принципиальная схема стадии (P).
Кроме того, на стадии (P) образуется спирт, получаемый из N-замещенной карбаминовой кислоты-O-R2 эфира. Далее приводится объяснение стадии (P).
Ароматическое гидроксисоединение в реагирующей ароматической гидроксикомпозиции может являться любым из ароматических гидроксисоединений, представленных упомянутый выше формулой (2), формулой (7), формулой (31), формулой (32), формулой (38), формулой (39) или формулой (40). Предпочтительным является случай, в котором содержится ароматическое гидроксисоединение, представленное формулой (7) или формулой (31), более предпочтительным является случай, в котором используют ароматическую гидроксикомпозицию, которая содержит активное ароматическое гидроксисоединение, представленное формулой (32), и еще более предпочтительным является случай, в котором используют ароматическую гидроксикомпозицию, которая содержит активное ароматическое гидроксисоединение, представленное формулой (38).
В соответствии с используемыми соединениями и другими подобными параметрами для стадии (P) могут быть осуществлены различные способы с ссылкой на известные способы (см., например, патентный документ WO 2008/059953).
В зависимости от реагирующих соединений, реакционные условия стадии (P) являются такими, что количество ароматического гидроксисоединения в используемой ароматической гидроксикомпозиции имеет мольное отношение в интервале от 2 до 1000 относительно эфирных групп, которые составляют сырье N-замещенной карбаминовой кислоты-O-R2 эфир. Для того чтобы быстро закончить реакцию, предпочтительно использовать избыток ароматического гидроксисоединения относительно эфирных групп, которые составляют сырье N-замещенной карбаминовой кислоты-O-R2 эфир, но принимая во внимание размер реактора, предпочтительно, чтобы мольное отношение находилось в интервале от 2 до 100, и более предпочтительно, в интервале от 5 до 50.
Температура реакции обычно находится в интервале от 100 до 300°C, и для повышения скорости реакции является предпочтительной высокая температура, но так как при высоких температурах могут легко протекать побочные реакции, предпочтительно, чтобы температура реакции находилась в интервале от 150 до 250°C. Для поддержания постоянной температуры в реакторе могут быть установлены известный охлаждающий аппарат или нагревающий аппарат. Кроме того, в зависимости от типов используемых соединений и температуры реакции, реакция может проводиться при пониженном давлении, нормальном давлении или повышенном давлении, и обычно при реакционном давлении в интервале от 20 до 1×106 Па. Нет конкретных ограничений для времени реакции (времени пребывания в случае непрерывного способа), и оно обычно составляет от 0,001 до 100 часов, предпочтительно, от 0,01 до 50 часов, и более предпочтительно, от 0,1 до 30 часов. Кроме того, реакция может быть остановлена после подтверждения того, что получено требуемое количество целевого N-замещенной карбаминовой кислоты-O-арилового эфира, путем отбора пробы реакционной жидкости и определения образовавшегося количества с помощью, например, жидкостной хроматографии.
Применение катализатора на стадии (P) не является обязательным, но для понижения температуры реакции или более быстрого завершения реакции может быть использован без проблем катализатор. Катализатор используют при концентрации от 0,01 до 30% по массе, и, предпочтительно, от 0,5 до 20% по массе относительно массы N-замещенной карбаминовой кислоты-O-R2 эфира. Примеры катализаторов могут включать кислоты Льюиса, а также соединения переходных металлов, которые образуют кислоту Льюиса, органические соединения олова, соединения металлов группы меди, соединения цинка или соединения группы железа, и более конкретно, кислоты Льюиса и соединения переходных металлов, которые образуют кислоту Льюиса, представленные AlX3, TiX3, TiX4, VOX3, VX5, ZnX2, FeX3 или SnX4 (где X представляет галоген, ацетоксильную группу, алкоксильную группу или арилоксильную группу); органические соединения олова, представленные (CH3)3SnOCHCH3, (C2H5)SnOCOC6H5, Bu3SnOCOCH3, Ph3SnOCOCH3, Bu2Sn(OCOCH3)2, Bu2Sn(OCOC11H23)2, Ph3SnOCH3, (C2H5)3SnOPh, Bu2Sn(OCH3)2, Bu2Sn(OC2H5)2, Bu2Sn(OPh)2, Ph2Sn(CH3)2, (C2H5)3SnOH, PhSnOH, Bu2SnO, (C8H17)2SnO, Bu2SnCl2 или BuSnO(OH); соединения металлов группы меди, представленные CuCl, CuCl2, CuBr, CuBr2, CuI, CuI2, Cu(OAc)2, Cu(acac)2, олефинатом меди, Bu2Cu, (CH3O)2Cu, AgNO3, AgBr, пикраптом серебра или AgC6H6ClO4; соединения цинка, представленные Zn(acac)2; и соединения металлов группы железа, представленные Fe(C10H8)(CO)5, Fe(CO)5, Fe(C4H6)(CO)3, Co(мезитилен)2(PEt2Ph2), CoC5F5(CO)7 или ферроценом. (В приведенных выше примерах, Bu обозначает бутильную группу, Ph обозначает фенильную группу, и acac обозначает ацетилацетонатный хелатный лиганд). Амины, такие как 1,4-диазабицикло-[2,2,2]октан, триэтилендиамин или триэтиламин являются подходящими для использования в качестве катализаторов, в то время как металлорганические катализаторы, такие как дибутилоловодилаурат, октоат свинца или октоат двухвалентного олова являются особенно предпочтительными. Эти соединения могут быть использованы сами по себе или два или более типов могут быть использованы в виде смеси.
В варианте настоящего осуществления, использование реакционного растворителя не является обязательным, но с целью облегчения осуществления реакции и других подобных целей может быть предпочтительно использован подходящий инертный растворитель в качестве реакционного растворителя, примеры которого могут включать алканы, такие как гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; сложные эфиры, такие как дибутилфталат, дигексилфталат, диоктилфталат или бензилбутилфталат; простые эфиры и тиоэфиры, такие как дифениловый эфир или дифенилсульфид; сульфоксиды, такие как диметилсульфоксид или дифенилсульфоксид; и силиконовое масло. Эти растворители могут быть использованы сами по себе, или два или более типов могут быть использованы в виде смеси.
Реакция переэтерификации в варианте настоящего осуществления является обратимой реакцией. Поэтому для того чтобы эффективно проводить переэтерификацию, предпочтительно проводить реакции при удалении продукта в форме спирта (спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира) из реакционной системы. Таким образом, если ароматическое гидроксисоединение выбирают так, что стандартная температура кипения ароматического гидроксисоединения, используемого в переэтерификации, является выше, чем стандартная температура кипения спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, то соединением, имеющим самую низкую стандартную температуру кипения в реакционной системе, становится спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, что облегчает удаление продуктов из реакционной системы. Исходя из того, что обычно соответствующее ректификационное разделение при применении в промышленности является возможным, если стандартные температуры кипения двух компонентов, подвергаемых разделению, отличаются на 10°C или более, ароматическое гидроксисоединение предпочтительно использовать так, чтобы стандартная температура кипения соединения, имеющего самую низкую стандартную температуру кипения в ароматической гидроксикомпозиции (на основе сравнения стандартных температур кипения) была выше на 10°C или более, чем стандартная температура кипения спирта.
Кроме того, переэтерификацию предпочтительно проводить с помощью непрерывного способа, что позволяет эффективно осуществлять переэтерификацию. А именно, сырье N-замещенной карбаминовой кислоты-O-R2 эфир и ароматическую гидроксикомпозицию непрерывно подают в реактор, проводят переэтерификацию, спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, который образуется, извлекают из реактора в форме газообразного компонента, и реакционную жидкость, содержащую образовавшийся N-замещенной карбаминовой кислоты-O-ариловый эфир и ароматическую гидроксикомпозицию непрерывно извлекают из нижней части реактора.
Материалы реактора и линий, используемых для проведения переэтерификации, могут являться известными материалами, при условии, что они не оказывают отрицательного действия на исходные вещества и реагирующие вещества, но такие материалы как SUS304, SUS316 или SUS316L являются недорогими и могут быть предпочтительно использованы. В случае необходимости могут быть добавлены известные технологические приборы, такие как расходомер, термометр и другие измерительные приборы, или ребойлер, насос или конденсатор и другие подобные устройства, для нагревания может быть использован такой известный способ, как применение пара или нагревателя, и для охлаждения может быть использован такой известный способ, как применение воздушного охлаждения, охлаждения водой или рассолом. В случае необходимости могут быть также добавлены стадии. Например, могут быть добавлены стадии и аппараты, которые являются известными для обычного специалиста в этой области, такие как стадия растворения ароматического гидроксисоединения, стадия отделения спирта, стадия отделения и/или очистки ароматического гидроксисоединения, стадия очистки N-замещенной карбаминовой кислоты-O-арилового эфира от образовавшейся реакционной жидкости или стадия сжигания или вывода побочных продуктов и другие подобные стадии. Нет конкретных ограничений для типа реактора, и может быть использован известный реактор типа емкости или реактор колонного типа. В качестве такого реактора используют различные известные методы, примеры которого могут включать используемые типы реакторов, содержащие реактор с мешалкой, многоступенчатый реактор с мешалкой, ректификационную колонну, многоступенчатую ректификационную колонну, трубчатый реактор, многоступенчатую ректификационную колонну непрерывного действия, насадочную колонну, пленочный дистилляционный аппарат, реактор, снабженный внутри средством поддержки, реактор с принудительной циркуляцией, испаритель с падающей пленкой, испаритель с падающей каплей, капельный проточный реактор или барботажную колонну, и типы, использующие их комбинации. С точки зрения эффективности сдвига равновесия в сторону продуктов предпочтительными являются способы, использующие пленочный дистилляционный аппарат или реактор колонного типа, в то время как структура, имеющая большую площадь контакта газ-жидкость является предпочтительной для быстрого осуществления переноса образовавшегося спирта, получаемого из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, в газовую фазу.
Многоступенчатая ректификационная колонна относится к ректификационной колонне, имеющей множество ступеней, в которой число теоретических тарелок дистилляции составляет 2 или более, и любая многоступенчатая ректификационная колонна может быть использована, при условии что она позволяет осуществлять непрерывную ректификацию. Любая многоступенчатая ректификационная колонна может быть использована в качестве многоступенчатой ректификационной колонны, при условии, что она обычно используется в качестве многоступенчатой ректификационной колонны, примеры которой могут включать типы тарельчатой колонны, использующей такую тарелку, как колпачковая тарелка, пористая плоская тарелка, клапанная тарелка или противоточная тарелка, и типы насадочной колонны, заполненной различными типами насадочных материалов, таких как кольца Рашига, кольца Лессинга, полюсные кольца, седловидная насадка Берля, седловидная насадка Interlock, насадка Диксона, насадка МакМэна, насадка Helipack, насадка типа "Зульцер" или насадка Меллапак. Любая насадочная колонна может быть использована при условии, что колонна заполнена описанной выше известной насадкой. Кроме того, предпочтительно также использовать колонну с комбинацией "тарелки-насадки", в которой объединяется часть тарелок с частью насадок.
Может быть отдельно подсоединена линия подачи инертного газа и/или жидкого инертного растворителя в нижней части реактора, и в случае когда смесь целевого N-замещенной карбаминовой кислоты-O-арилового эфира и ароматического гидроксисоединения содержит сырье N-замещенной карбаминовой кислоты-O-R2 эфир, может быть подсоединена линия для рециркуляции всей или части смеси в реактор. Кроме того, в случае использования упомянутого выше инертного растворителя, инертный растворитель может находиться в форме газа и/или жидкости.
Газообразный компонент, извлеченный из реактора, содержащий спирт, получаемый из сырья N-замещенной карбаминовой кислоты-O-R2 эфира, предпочтительно очищать с помощью известного метода, такого как метод, в котором используется ректификационная колонна, и он может быть повторно использован в качестве спирта стадии (A) и/или стадии (R).
Далее приводится объяснение стадии (F) для получения изоцианата термическим разложением N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого в упомянутых выше направлениях 1)-5).
<Стадия (F): стадия получения изоцианата реакций термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира>
Стадия (F) является способом получения изоцианата, представленного следующей формулой (6), получаемого из N-замещенной карбаминовой кислоты-O-арилового эфира, и ароматической гидроксикомпозиции путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира на следующей стадии (F).
Стадия (F): стадия получения изоцианата и ароматической гидроксикомпозиции из N-замещенной карбаминовой кислоты-O-арилового эфира:
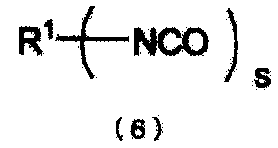
(где
R1 представляет органическую группу, которая имеет целое число углеродных атомов в интервале от 1 до 85 и которая замещена s NCO группами, и s представляет целое число от 1 до 10).
N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый согласно описанному выше способу, предпочтительно использовать для получения изоцианата. Далее приводится объяснение стадии получения изоцианата путем использования N-замещенной карбаминовой кислоты-O-арилового эфира в реакции термического разложения (называемой стадией (F)).
На стадии (F) может использоваться или может не использоваться растворитель, но ее предпочтительно проводить в присутствии ароматической гидроксикомпозиции. Так как ароматическую гидроксикомпозицию используют в направлениях 1), 3) и 5) при проведении стадии (B) или стадии (P), стадия (F) может быть проведена с использованием реакционной жидкости, получаемой на этих стадиях, или стадия (F) может быть проведена путем корректировки количества ароматической гидроксикомпозиции, если в этом есть необходимость. В качестве варианта, так как ароматическую гидроксикомпозицию используют на стадии (C) направлений 2) и 4), то стадия (F) может быть проведена путем повторного использования отделенной ароматической гидроксикомпозиции, количество используемой ароматической гидроксикомпозиции может быть скорректировано, или ароматическая гидроксикомпозиция может быть заново приготовлена и использована. Растворитель, используемый на стадии (C), может быть отделен от N-замещенной карбаминовой кислоты-O-арилового эфира или может быть использован с ароматической гидроксикомпозицией.
Корректировка количества ароматической гидроксикомпозиции или приготовление новой ароматической гидроксикомпозиции уже были описаны выше, и ее количество является таким, что отношение числа ароматических гидроксисоединений в ароматической гидроксикомпозиции к суммарному числу эфирных групп-O-арилового эфира, содержащихся в N-замещенной карбаминовой кислоты-O-ариловом эфире, составляет от 0,2 до 50, но, принимая во внимание эффективность транспортировки N-замещенной карбаминовой кислоты-O-арилового эфира и размер емкости для хранения во время хранения, предпочтительно, чтобы оно составляло от 0,3 до 30, и более предпочтительно, от 1 до 20. Примеры других растворителей, которые могут быть добавлены с целью облегчения протекания реакции и с другими подобными целями, могут включать подходящие инертные растворители, включающие алканы, такие как гексан (включая изомеры), гептан (включая изомеры), октан (включая изомеры), нонан (включая изомеры) или декан (включая изомеры); ароматические углеводороды и алкилзамещенные ароматические углеводороды, такие как бензол, толуол, ксилол (включая изомеры), этилбензол, диизопропилбензол (включая изомеры), дибутилбензол (включая изомеры) или нафталин; ароматические соединения, замещенные с помощью галогена или нитрогруппы, такие как хлорбензол, дихлорбензол (включая изомеры), бромбензол, дибромбензол (включая изомеры), хлорнафталин, бромнафталин, нитробензол или нитронафталин; полициклические углеводородные соединения, такие как дифенил, замещенный дифенил, дифенилметан, терфенил, антрацен или дибензилтолуол (включая изомеры); алифатические углеводороды, такие как циклогексан, циклопентан, циклооктан или этилциклогексан; кетоны, такие как метилэтилкетон или ацетофенон; и дибутилфталат, дигексилфталат или диоктилфталат.
Температура реакции термического разложения, проводимой на стадии (F), обычно находится в интервале от 100 до 300°C, и высокая температура является предпочтительной для повышения скорости реакции, но так как при высоких температурах могут протекать описанные выше побочные реакции с участием N-замещенной карбаминовой кислоты-O-арилового эфира и/или с участием продукта в форме изоцианата, предпочтительно, чтобы температура реакции находилась в интервале от 150 до 250°C. Для поддержания постоянной температуры реакции в реакторе могут быть установлены известные устройства для охлаждения или нагревания. Кроме того, в зависимости от типов используемых соединений и температуры реакции, реакция может проводиться при пониженном давлении, нормальном давлении или повышенном давлении и, обычно, при реакционном давлении в интервале от 20 до 1×106 Па. Нет конкретных ограничений для времени реакции (времени пребывания в случае непрерывного способа), но оно обычно составляет от 0,001 до 100 часов, предпочтительно, от 0,005 до 50 часов и, более предпочтительно, от 0,01 до 10 часов.
В варианте настоящего осуществления предпочтительно не использовать катализатор, но в случае использования катализатора на любой из стадий при получении N-замещенной карбаминовой кислоты-O-арилового эфира остаток катализатора может быть подан на стадию термического разложения, так как присутствие остатка такого катализатора не представляет проблемы.
При хранения N-замещенной карбаминовой кислоты-O-арилового эфира при высокой температуре в течение длительного периода времени в ряде случаев протекают побочные реакции, такие как реакция образования соединений, содержащих мочевинные связи, в результате реакции эфирного декарбоксилирования двух молекул N-замещенной карбаминовой кислоты-O-арилового эфира, или реакция образования аллофанатных групп в результате реакции и изоцианатом, образующимся в результате термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира. Поэтому предпочтительно, чтобы период времени, в течение которого N-замещенной карбаминовой кислоты-O-ариловый эфир и изоцианат находятся при высокой температуре, мог бы быть как можно короче. Поэтому реакцию термического разложения предпочтительно проводить в непрерывном режиме. Непрерывный способ относится к способу, в котором смесь, содержащую N-замещенной карбаминовой кислоты-O-ариловый эфир, непрерывно подают в реактор, где она подвергается реакции термического разложения, и образующиеся изоцианат и ароматическое гидроксисоединение непрерывно выводятся из реактора термического разложения. В этом непрерывном способе, компоненты с низкой температурой кипения, образующиеся при термическом разложении уретана, предпочтительно извлекать из верхней части реактора термического разложения в форме газофазных компонентов, в то время как остаток извлекают из нижней части реактора термического разложения в форме жидкофазных компонентов. Все соединения, присутствующие в реакторе термического разложения, могут быть извлечены в виде газофазных компонентов, но присутствие жидкофазных компонентов в реакторе термического разложения позволяет растворять полимерные вещества, образующиеся в результате побочных реакций с участием N-замещенной карбаминовой кислоты-O-арилового эфира и/или изоцианата, что предотвращает слипание и отвердевание полимерных веществ в реакторе термического разложения. Изоцианат и ароматическое гидроксисоединение образуются путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира, и по меньшей мере одно из этих соединений извлекают в форме газофазного компонента. Какое соединение извлекать в виде газофазного компонента зависит от таких факторов, как условия реакции термического разложения.
Используемый здесь термин "компонент с низкой температурой кипения, образующийся в результате термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира" в варианте настоящего осуществления равнозначен ароматическому гидроксисоединению и/или изоцианату, образующимся в результате термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира, но конкретно он относится к соединению, которое способно присутствовать в форме газа в условиях, при которых проводят реакцию термического разложения.
Например, может быть использован способ, в котором изоцианат и ароматическое гидроксисоединение, образующиеся в результате реакции термического разложения, могут быть извлечены в форме газообразных компонентов, в то время как извлекают жидкофазный компонент, который содержит N-замещенной карбаминовой кислоты-O-ариловый эфир. В этом способе изоцианат и ароматическое гидроксисоединение могут быть извлечены раздельно в реакторе термического разложения. Извлеченный жидкофазный компонент, который содержит изоцианат, предпочтительно направлять в ректификационную колонну для отделения и очистки изоцианата в газовой фазе. Извлеченный газообразный компонент, который содержит изоцианат, может быть направлен в ректификационную колонну после превращения в жидкую фазу с помощью конденсатора и других подобных устройств, но во многих случаях это приводит к усложнению конструкции установки и увеличению энергетических затрат, что является нежелательным. В случае, когда компонент жидкой фазы содержит N-замещенной карбаминовой кислоты-O-ариловый эфир, весь или часть компонента жидкой фазы предпочтительно направлять в верхнюю часть реактора термического разложения, где N-замещенной карбаминовой кислоты-O-ариловый эфир опять подвергают реакции термического разложения. Называемая здесь верхняя часть реактора термического разложения относится к двум или более ступеням выше нижней части колонны, выраженным в виде числа теоретических тарелок, в случае когда реактор термического разложения является ректификационной колонной, в то время как в случае, когда реактор термического разложения является пленочным дистилляционным аппаратом, верхняя часть реактора относится к части, расположенной выше нагреваемой части поверхности массообмена. При подаче всего или части жидкофазного компонента в верхнюю часть реактора термического разложения предпочтительно транспортировать жидкофазный компонент при поддержании температуры от 50 до 180°C, более предпочтительно, от 70 до 170°C, и еще более предпочтительно, от 100 до 150°C.
Кроме того, может быть также использован способ, в котором, например, изоцианат и ароматическое гидроксисоединение, образующиеся в результате реакции термического разложения извлекают в форме газообразных компонентов, в то время как жидкофазный компонент, содержащий N-замещенной карбаминовой кислоты-O-ариловый эфир, извлекают из нижней части реактора термического разложения. Кроме того, в этом способе, извлекаемый газофазный компонент, который содержит изоцианат, предпочтительно направлять в ректификационную колонну для отделения и очистки изоцианата в газовой фазе. С другой стороны, весь или часть жидкофазного компонента, который содержит N-замещенной карбаминовой кислоты-O-ариловый эфир, подают в верхнюю часть реактора термического разложения, где N-замещенной карбаминовой кислоты-O-ариловый эфир опять подвергают реакции термического разложения. При подачи всего или части жидкофазного компонента в верхнюю часть реактора термического разложения, предпочтительно транспортировать жидкофазный компонент при поддержании температуры от 50 до 180°C, более предпочтительно, от 70 до 170°C, и еще более предпочтительно, от 100 до 150°C.
Кроме того, может быть также использован способ, в котором, например, ароматическое гидроксисоединение из смеси изоцианата и ароматического гидроксисоединения, образующихся в результате реакции термического разложения, извлекают в форме газофазного компонента, в то время как смесь, содержащую изоцианат, извлекают в форме жидкофазного компонента из нижней части реактора термического разложения. В этом случае жидкофазный компонент подают в ректификационную колонну для извлечения изоцианата. В случае, когда N-замещенной карбаминовой кислоты-O-ариловый эфир содержится в жидкофазном компоненте, всю или часть смеси, содержащей N-замещенной карбаминовой кислоты-O-ариловый эфир, предпочтительно подавать в верхнюю часть реактора термического разложения, и N-замещенной карбаминовой кислоты-O-ариловый эфир опять подвергать реакции термического разложения. При подачи всего или части жидкофазного компонента в реактор термического разложения предпочтительно транспортировать жидкофазный компонент при поддержании температуры от 50 до 180°C, более предпочтительно, от 70 до 170°C, и еще более предпочтительно, от 100 до 150°C.
Ранее было описано, что при реакции термического разложения жидкофазный компонент предпочтительно извлекать из нижней части реактора термического разложения. Причина состоит в том, что присутствие жидкофазного компонента в реакторе термического разложения позволяет растворять полимерные вещества, образующиеся в результате описанных ранее побочных реакций с участием N-замещенной карбаминовой кислоты-O-арилового эфира и/или изоцианата, в результате чего появляется возможность выводить полимерные вещества из реактора термического разложения и предотвращать слипание и отверждение полимерных веществ в реакторе термического разложения.
В случае, когда компонент жидкой фазы содержит N-замещенной карбаминовой кислоты-O-ариловый эфир, весь или часть жидкофазного компонента подают в верхнюю часть реактора термического разложения, где N-замещенной карбаминовой кислоты-O-ариловый эфир опять подвергают реакции термического разложения, но если эту стадию повторяют, то в жидкофазном компоненте могут накапливаться полимерные побочные продукты. В этом случае, для того чтобы снизить накопление полимерных побочных продуктов, весь или часть жидкофазного компонента могут быть удалены из реакционной системы или поддерживаться при заданной концентрации.
Для типа реактора термического разложения нет конкретных ограничений, но для того чтобы эффективно извлекать газофазные компоненты, предпочтительно использовать известную ректификационную установку. Различные известные методы используют для такого реактора, примеры которого могут включать используемые типы реакторов, включающие ректификационную колонну, многоступенчатую ректификационную колонну, трубчатый реактор, многоступенчатую ректификационную колонну непрерывного действия, насадочную колонну, пленочный дистилляционный аппарат, реактор, снабженный внутри средством поддержки, реактор с принудительной циркуляцией, испаритель с падающей пленкой, испаритель с падающей каплей, и типы, использующие их комбинации. С точки зрения быстрого удаления компонентов с низкой температурой кипения из реакционной системы, предпочтительным является способ, использующий трубчатый реактор, в то время как способ, использующий такой реактор, как трубчатый пленочный испаритель или трубчатый испаритель с падающей пленкой, является более предпочтительным, и для обеспечения быстрого переноса образующихся компонентов с низкой температурой кипения в газовую фазу является предпочтительной структура, имеющая большую поверхность контакта газ-жидкость.
Для реактора термического разложения и линий в качестве материала может быть использован известный материал, при условии, что он не оказывает отрицательного действия на уретан или продукты в форме ароматического гидроксисоединения и изоцианата, и материалы SUS304, SUS316 или SUS316L являются недорогими и могут быть предпочтительно использованы.
Ароматические гидроксисоединения, содержащиеся в описанных выше газофазных компонентах и/или жидкофазном компоненте, получаемых при реакции термического разложения, каждое, могут быть отделены, извлечены и повторно использованы. Более конкретно, ароматические гидроксисоединения могут быть повторно использованы в качестве ароматических гидроксисоединений, используемых на стадии (A), и/или стадии (A), и/или стадии (B), и/или стадии (R), и/или стадии (P). Другими словами, предпочтительно, чтобы ароматическую гидроксикомпозицию, получаемую на стадии (F), отделяли от изоцианата и затем использовали путем рециркуляции на стадию (A) и/или стадию (B), описанные в направлении 1), или на стадию (A), и/или стадию (R), и/или стадию (P), описанные в направлении 3).
Кроме того, в предпочтительном аспекте варианта настоящего осуществления непрореагировавший N-замещенной карбаминовой кислоты-O-ариловый эфир, который не подвергся термическому разложению на стадии (F), предпочтительно использовать путем рециркуляции на упомянутую выше стадию (A), и/или стадию (B), и/или стадию (R), и/или стадию (P), и/или стадию (F).
<Очистка реактора>
При получении N-замещенной карбаминовой кислоты-O-арилового эфира и при получении изоцианата с использованием N-замещенной карбаминовой кислоты-O-арилового эфира варианта настоящего осуществления в ряде случаев могут образовываться полимерные побочные продукты, хотя и в незначительном количестве. Так как эти полимерные побочные продукты имеют высокую растворимость в ароматической гидроксикомпозиции, используемой в варианте настоящего осуществления, они удаляются из реактора в форме раствора ароматической гидроксикомпозиции. Однако, в случаях колебаний в реакционном аппарате рабочих режимов и случаях продолжительной эксплуатации, полимерные побочные продукты могут прилипать к реактору.
В таких случаях, для того чтобы сохранять внутренность реактора чистой, внутренность (и особенно внутренние стенки) реактора могут быть очищены с помощью кислоты, которая является хорошим растворителем полимерных побочных продуктов.
Нет конкретных ограничений для кислоты для очистки, при условии, что она растворяет полимерные побочные продукты, и могут быть использованы и органические кислоты, и неорганические кислоты, но предпочтительно использовать органические кислоты. Примеры используемых органических кислот могут включать карбоновую кислоту, сульфоновую кислоту, сульфиновую кислоту, фенолы, енолы, тиофенолы, имиды, оксимы и ароматические сульфонамиды, предпочтительно использовать карбоновую кислоту и фенолы. Примеры таких соединений могут включать насыщенные или ненасыщенные алифатические монокарбоновые кислоты, такие как муравьиная кислота, уксусная кислота, пропионовая кислота, н-масляная кислота, изомасляная кислота, валериановая кислота, изовалериановая кислота, 2-метилбутановая кислота, триметилуксусная кислота, капроновая кислота, изокапроновая кислота, 2-этилбутановая кислота, 2,2-диметилбутановая кислота, энантовая кислота (включая изомеры), каприловая кислота (включая изомеры), нонановая кислота (включая изомеры), декановая кислота (включая изомеры), ундекановая кислота (включая изомеры), лауриновая кислота (включая изомеры), миристиновая кислота (включая изомеры), пальмитиновая кислота (включая изомеры), акриловая кислота, бета-метилакриловая кислота, изо-бета-метилакриловая кислота, винилуксусная кислота, метакриловая кислота, ангеликовая кислота, тиглиновая кислота, арилацетат или ундеценовая кислота (включая изомеры); насыщенные или ненасыщенные алифатические дикарбоновые кислоты, такие как щавелевая кислота, малоновая кислота, янтарная кислота, глутаровая кислота, адипиновая кислота, пимелиновая кислота (включая изомеры), октандикарбоновая кислота (включая изомеры), азелаиновая кислота (включая изомеры), себациновая кислота (включая изомеры), малеиновая кислота, фумаровая кислота, метилмалеиновая кислота, метилфумаровая кислота, глутаровая кислота (включая изомеры), итаконовая кислота или аллилмалоновая кислота; насыщенные или ненасыщенные алифатические трикарбоновые кислоты, такие как 1,2,3-пропантрикарбоновая кислота, 1,2,3-пропентрикарбоновая кислота или 2,3-диметилбутан-1,2,3-трикарбоновая кислота; ароматические карбоновые кислоты, такие как бензойная кислота, метилбензойная кислота (включая изомеры), этилбензойная кислота (включая изомеры), пропилбензойная кислота (включая изомеры), диметилбензойная кислота (включая изомеры) или триметилбензойная кислота (включая изомеры); ароматические дикарбоновые кислоты, такие как фталиевая кислота, изофталевая кислота, терефталевая кислота или метилизофталевая кислота; ароматические трикарбоновые кислоты, такие как гемимеллитовая кислота, тримеллитовая кислота или тримезиновая кислота; фенол; монозамещенные фенолы, такие как метилфенол (включая изомеры), этилфенол (включая изомеры), пропилфенол (включая изомеры), бутилфенол (включая изомеры), пентилфенол (включая изомеры), гексилфенол (включая изомеры), гептилфенол (включая изомеры), октилфенол (включая изомеры), нонилфенол (включая изомеры), децилфенол (включая изомеры), додецилфенол (включая изомеры), фенилфенол (включая изомеры), феноксифенол (включая изомеры) или кумилфенол (включая изомеры); и диметилфенол (включая изомеры), диэтилфенол (включая изомеры), дипропилфенол (включая изомеры), дибутилфенол (включая изомеры), дипентилфенол (включая изомеры), дигексилфенол (включая изомеры), дигептилфенол (включая изомеры), диоктилфенол (включая изомеры), динонилфенол (включая изомеры), дидецилфенол (включая изомеры), дидодецилфенол (включая изомеры), дифенилфенол (включая изомеры), дифеноксифенол (включая изомеры) или дикумилфенол (включая изомеры). Принимая во внимание воздействия растворителя для очистки, которые могут возникать в случае присутствия его остаточного количества в реакторе термического разложения после его очистки, более предпочтительные примеры этих органических кислот могут включать ароматические гидроксисоединения, в то время как еще более предпочтительные примеры могут включать соединения, аналогичные ароматическим гидроксисоединениям, образующимся в способе получения N-замещенной карбаминовой кислоты-O-арилового эфира и/или в реакции термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира варианта настоящего осуществления.
Кроме того, в случае использования ароматического гидроксисоединения в качестве кислоты для очистки, предпочтительно, с точки зрения очищающего действия, чтобы стандартная температура кипения ароматического гидроксисоединения имела разницу в температуре кипения 10°C или более относительно стандартной температуры кипения изоцианата, образующегося в результате реакции термического разложения описанного выше N-замещенной карбаминовой кислоты-O-арилового эфира.
Различные методы могут быть использованы для очистки реактора с использованием упомянутого выше растворителя для очистки, примеры которых могут включать метод, в котором реактор очищают путем введения растворителя для очистки через верхнюю часть реактора, и метод, в котором внутренность реактора очищают путем введения реагента для очистки в нижнюю часть реактора и затем кипячения реагента для очистки во всем объеме реактора.
Необходимо проводить процедуру очистки реактора каждый раз при проведении реакции, но предпочтительная периодичность очистки может быть определена произвольно с учетом используемых соединений, степени загрузки и других подобных параметров, и предпочтительно проводить процедуру очистки один раз в течение периода работы от 1 до 20000 часов, более предпочтительно, один раз в течение периода работы от одного дня до одного года, и еще более предпочтительно, один раз в течение периода работы от одного месяца до одного года. Реактор может быть оборудован линией для введения реагента для очистки.
Стадии (D), (E) и (G), объясняемые ниже, проводят в дополнении к упомянутому выше способу.
<Стадия (D)>
Мочевину извлекают путем проведения следующей стадии (D) перед стадией (B), стадией (R) или стадией (P) и/или одновременно со стадией (B), стадией (R) или стадией (P):
стадия (D): стадия удаления мочевины ректификацией или сублимацией.
При получении соединения, имеющего уреидные группы, описанного на стадии (A), мочевину предпочтительно использовать в избытке относительно органического первичного амина. В данном случае, так как соединения, имеющие уреиленовые группы, могут образовываться в качестве побочных продуктов при присутствии избыточного количества непрореагировавшей мочевины на стадии (B), и стадия (R) или стадия (P) все еще содержат избыток мочевины, то мочевину отделяют путем ректификации или сублимации. Для метода отделения может быть использован известный метод, и в зависимости от используемых соединений, может быть использован такой метод, как фильтрация, ректификация или сублимация. Метод, который проводят одновременно со стадией (B), стадией (R) или стадией (P), является предпочтительным.
А именно, в реакции, проводимой на стадии (B), стадии (R) или стадии (P), газ, содержащий гидроксикомпозицию (гидроксикомпозиция относится к композиции, содержащей по меньшей мере один тип ароматической гидроксикомпозиции, и/или ароматического гидроксисоединения, и/или спирт), соединение, имеющее карбонильные группы, получаемое из мочевины, и аммиак, образующийся в реакции в качестве побочного продукта, вводят в конденсатор, которым снабжен реактор, и конденсируют всю или часть гидроксикомпозиции и соединение, имеющее карбонильные группы, получаемое из мочевины.
В данном случае предпочтительно, чтобы сконденсированная гидроксикомпозиция присутствовала в мольном количестве 1 или более относительно сконденсированной мочевины и соединения, имеющего карбонильные группы, получаемого из мочевины.
В варианте настоящего осуществления "соединение, имеющее карбонильные группы, полученное из мочевины", которое сконденсировано в конденсаторе, включает соединения, имеющие карбонильные группы, получаемое из мочевины, используемой в реакции с органическим амином, мочевину и гидроксикомпозицию, саму по себе мочевину, используемую в качестве сырья (включающая непрореагировавшую мочевину и/или избыточную часть в случае использования ее в избытке относительно органического амина), соединения, получаемые реакцией между мочевиной и гидроксикомпозицией, и соединения, получаемые реакцией между одинаковыми или различными типами производных угольной кислоты. Трудно идентифицировать все соединения, имеющие карбонильные группы, получаемые из мочевины, но конкретные примеры могут включать изоциановую кислоту, мочевину, соединения мочевины, такие как биуреты или нураты, не-N-замещенной карбаминовой кислоты-O-эфиры, в которых эфирные группы являются группами, получаемыми из гидроксикомпозиции, и эфиры угольной кислоты, в которых эфирные группы являются группами, получаемыми из гидроксикомпозиции. Соединения, имеющие карбонильные группы, получаемые из производной угольной кислоты, могут быть количественно определены с помощью метода, который обнаруживает карбонильные группы, содержащиеся в соединении, такого как инфракрасная спектроскопия, ближняя инфракрасная спектроскопия, спектроскопия комбинационного рассеяния или ультрафиолетовая спектроскопия, или с помощью метода, который непосредственно определяет образующиеся соединения, такого как газовая хроматография, жидкостная хроматография или ЯМР. Многие из этих соединений, имеющих карбонильные группы, получаемые из мочевины, имеют высокую температуру плавления и склонны выпадать в осадок. Среди упомянутых выше соединений, имеющих карбонильные группы, получаемые из мочевины, сама мочевина, в частности, требует к себе наибольшего внимания, так как она образуется в больших количествах (обнаруживаемых количествах) и имеет температуру плавления 135°C.
В результате использования мольного отношения сконденсированной гидроксикомпозиции,Ю равной 1 или более, относительно сконденсированного соединения, имеющего карбонильные группы, получаемые из мочевины, в процессе конденсации, их смесь может быть получена в конденсаторе в форме гомогенной жидкой смеси. Таким образом, это не только облегчает транспортировку смеси, но также позволяет предотвратить возникновение таких проблем, как слипание и накопление твердых компонентов в конденсаторе. Кроме того, как будет описано далее, это также позволяет эффективно снижать количества соединений, имеющих карбонильные группы, получаемые из мочевины, содержавшихся в аммиаке, извлекаемом из конденсатора, до уровня, который равен или меньше, чем конкретное количество. Более предпочтительно, чтобы количество сконденсированной гидроксикомпозиции относительно количества сконденсированного соединения, имеющего карбонильные группы, получаемые из мочевины, выраженное через мольное отношение, составляло 2 или более, и еще более предпочтительно, 3 или более. Для того чтобы обеспечить количество сконденсированной гидроксикомпозиции относительно сконденсированного соединения, имеющего карбонильные группы, получаемые из мочевины, в приведенных выше интервалах, температуру в конденсаторе предпочтительно поддерживать, по меньшей мере, на 90°C ниже, чем стандартная температура кипения гидроксикомпозиции.
<Способ получения N-замещенной карбаминовой кислоты-O-арилового эфира с использованием ароматической гидроксикомпозиции, содержащей множество типов ароматических гидроксисоединений>
N-замещенной карбаминовой кислоты-O-ариловый эфир может быть получен на упомянутых выше стадиях 1)-5) с использованием ароматической гидроксикомпозиции, содержащей множество типов ароматических гидроксисоединений.
Кроме того, в случае проведения стадии (D) в направлении 1) или направлении 2), газ, содержащий ароматическую гидроксикомпозицию, мочевину и соединение, имеющее карбонильные группы, получаемое из мочевины, конденсируют в конденсаторе, для того чтобы извлечь мочевину и соединение, имеющее карбонильные группы, получаемые из мочевины, в форме гомогенного раствора. Следовательно, предпочтительно, чтобы ароматическая гидроксикомпозиция содержала ароматическое гидроксисоединение, которое при условиях реакции легко испаряется до определенной степени. С другой стороны, так как соединение, имеющее уреидные группы, и ароматическая гидроксикомпозиция реагируют главным образом в жидкой фазе с образованием N-замещенной карбаминовой кислоты-O-арилового эфира, предпочтительно, чтобы ароматическая гидроксикомпозиция содержала ароматическое гидроксисоединение, которое при условиях реакции присутствует в виде жидкости. Таким образом, ароматическая гидроксикомпозиция, которая содержит множество типов ароматических гидроксисоединений, имеющих различные стандартные температуры кипения, может предпочтительно использоваться в качестве ароматической гидроксикомпозиции.
В этом случае, во многих случаях все множество типов ароматических гидроксисоединений, имеющих различные стандартные температуры кипения, образуют эфир N-замещенной карбаминовой кислоты путем реакции с соединением, имеющим уреидные группы, множество типов ароматических гидроксисоединений образуются вместе с изоцианатом во время получения изоцианата путем термического разложения эфира N-замещенной карбаминовой кислоты, что усложняет отделение ароматических гидроксисоединений. Поэтому способ получения N-замещенной карбаминовой кислоты-O-арилового эфира, имеющего эфирные группы, получаемого из активного ароматического гидроксисоединения с высокой селективностью, предпочтительно проводить путем использования комбинации активного ароматического гидроксисоединения и неактивного ароматического гидроксисоединения. Кроме того, если ароматические гидроксисоединения выбирают так, что стандартная температура кипения активного ароматического гидроксисоединения является самой высокой в ароматической гидроксикомпозиции, то повышается концентрация активного ароматического гидроксисоединения в жидкой фазе, в которой главным образом происходит реакция образования N-замещенной карбаминовой кислоты-O-арилового эфира, что приводит к образованию N-замещенной карбаминовой кислоты-O-эфира, получаемого из активного ароматического гидроксисоединения с высокой селективностью. Неактивное ароматическое гидроксисоединение, имеющее стандартную температуру кипения ниже чем стандартная температура кипения активного ароматического гидроксисоединения, предпочтительно вводить в конденсатор в форме газофазного компонента и конденсировать в конденсаторе вместе с соединением, имеющим карбонильные группы, получаемым из производной угольной кислоты.
На фигуре 7 приведена принципиальная схема способа получения эфира N-замещенной карбаминовой кислоты, в котором используют ароматическую гидроксикомпозицию, состоящую из множества типов описанных выше ароматических гидроксисоединений (здесь, для простоты объяснения, описывают ароматическое гидроксисоединение, которое содержит два типа ароматических гидроксисоединений, включающих активное ароматическое гидроксисоединение и неактивное ароматическое гидроксисоединение).
Примером активного ароматического гидроксисоединения этого типа является ароматическое гидроксисоединение, представленное формулой (32), и, предпочтительно, ароматическое гидроксисоединение, представленное формулой (38). Кроме того, примером неактивного ароматического гидроксисоединения является ароматическое гидроксисоединение, представленное формулой (39), и более предпочтительно, ароматическое гидроксисоединение, представленное формулой (40). Обычно трудно определить возможность разделения, исходя из того, что обычно два компонента, подвергаемые разделению, могут быть в достаточной степени разделены с помощью промышленной ректификации, если их стандартные температуры кипения различаются на 10°C или более, но предпочтительно, чтобы разница между стандартными температурами кипения активного ароматического гидроксисоединении и неактивного ароматического гидроксисоединения являлась такой, чтобы соединением, имеющим самую высокую стандартную температуру кипения, являлось активное ароматическое гидроксисоединение, в то время как соединением, имеющим самую низкую стандартную температуру кипения, являлось неактивное ароматическое гидроксисоединение, и их предпочтительно выбирать так, чтобы стандартная температура кипения была на 10°C или выше, и более предпочтительно, на 20°C или выше, относительно соединения, имеющего самую высокую температуру кипения, а также выбирать, принимая во внимание разницу со стандартной температурой кипения ранее описанного образующегося изоцианата. В этом случае выбирают активное ароматическое гидроксисоединение, имеющее стандартную температуру кипения, которая отличается на 10°C или более от стандартной температуры кипения образующегося изоцианата. В случае использования ароматического гидроксисоединения, имеющего стандартную температуру кипения выше, чем стандартная температура кипения изоцианата, выбирают активное ароматическое гидроксисоединение, которое имеет стандартную температуру кипения выше на 10°C или более, чем стандартная температура кипения изоцианата, и в случае использования ароматического гидроксисоединения, имеющего стандартную температуру кипения ниже, чем стандартная температура кипения изоцианата, выбирают активное ароматическое гидроксисоединение, которое имеет стандартную температуру кипения ниже на 10°C или более, чем стандартная температура кипения изоцианата.
<Стадия (E)>
Стадия (E): стадия рециркуляции мочевины, извлекаемой на стадии (D), на стадию (A).
Стадия (E) является стадией рециркуляции мочевины, извлекаемой на описанной выше стадии (D), на стадию (A). Использование рециркуляции является предпочтительным, так как она позволяет уменьшить количество используемой мочевины. На стадии (E) смесь, извлеченная на стадии (D), может быть рециркулирована непосредственно на стадию (A), или может быть рециркулирована только мочевина. Рециркулируемые компоненты могут быть разделены, если в этом есть необходимость, или компоненты могут быть добавлены перед рециркулированием на стадию (A). Разделение и добавление могут быть проведены с использованием известных методов, и мочевину, соединение, имеющее карбонильные группы, получаемое из мочевины, и гидроксикомпозицию и другие подобные соединения подвергают анализу и затем соответствующим образом рециркулируют.
<Стадия (G)>
Следующую стадию (G) проводят для извлечения аммиака, образующегося в качестве побочного продукта на стадии (A), и/или стадии (B), и/или стадии (R), и аммиак подвергают реакции с диоксидом углерода для регенерации мочевины, за которой следует рециркуляция мочевины на стадию (A):
Стадия (G): стадия извлечения аммиака, образующегося в качестве побочного продукта, регенерации мочевины путем реакции аммиака с диоксидом углерода, и рециркуляции мочевины на стадию (A).
В варианте настоящего осуществления аммиак, выводимый из конденсатора на упомянутой выше стадии (A), стадии (B) и/или стадии (R), поглощает воду, что приводит к образованию водного раствора аммиака, и он может быть использован в холодильных агентах аммиачных абсорбционных холодильников, тканевых маслоочистителях, коагулянтах сырого каучука, производстве различных типов аммиачных солей, при обработке оксидов азота, образуемых теплоэлектростанциями, и для других подобных целей, или получении фотографических эмульсий или так далее, или при применении такого метода разделения, как глубокое охлаждение, он может быть использован в форме жидкого аммиака в качестве сырья для азотных удобрений, сырья для синтетических волокон (такого как капролактам или акрилонитрил), при обработке оксидов азота, образуемых теплоэлектростанциями, и для других подобных целей, или в качестве холодильных агентов, но его предпочтительно использовать для синтеза мочевины. Далее приводится объяснение этой стадии синтеза мочевины (называемой стадией (G)).
Для получения мочевины путем реакции аммиака и диоксида углерода может быть использован известный традиционный метод, пример которого может включать реакцию аммиака и диоксида углерода при давлении в интервале от 20 до 40 МПа и температуре в интервале от 190 до 200°C при мольном отношении аммиака к диоксиду углерода в интервале от 3 до 5.
Полученная таким методом мочевина может быть использована в реакции стадии (A).
Далее приводится пример предпочтительного аспекта, который объединяет упомянутый выше метод, но нет конкретных ограничений для других аспектов, при условии, что они основываются на упомянутом выше методе. Дополнительные стадии (такие как стадии (D), (E), (F) или (G)) могут не проводиться, или дополнительные стадии могут быть соответствующим образом выбраны и проведены. Стадию (F) проводят при получении изоцианата из N-замещенной карбаминовой кислоты-O-арилового эфира. В следующем аспекте гидроксикомпозиция относится к композиции, содержащей по меньшей мере один тип компонента, выбранного из ароматической гидроксикомпозиции, и/или ароматического гидроксисоединения, и/или спирта. В случае, когда наблюдается накопление побочного продукта на каждой стадии, побочный продукт предпочтительно соответствующим образом удалять из рециркулируемой композиции или вместе с рециркулируемой композицией из системы, и он может быть удален с использованием известного метода. Метод удаления может быть соответствующим образом определен обычным специалистом в этой области. Примеры используемых методов могут включать метод частичного удаления из системы жидкофазного компонента и/или газофазного компонента, и метод удаления твердого компонента фильтрацией и другие подобные методы.
На фигуре 8 приведена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 1) со стадиями (D), (E), (F) и (G).
Сначала, получают на стадии (A) соединение, имеющее уреидные группы, путем реакции органического первичного амина и мочевины. На этой стадии (A) ароматическая гидроксикомпозиция действует в основном в качестве реакционного растворителя. В реакции стадии (A) аммиак, образующийся в качестве побочного продукта, может быть извлечен из реакционной жидкости, до тех пор пока концентрация аммиака в реакционной жидкости не будет находиться в описанных ранее предпочтительных интервалах. Реакционная жидкость, получаемая на стадии (A), содержит соединение, имеющее уреидные группы, и ароматическую гидроксикомпозицию, и, в зависимости от используемого сырья, соотношения компонентов в сырье, условий реакции стадии (A) и других подобных параметров, реакционная жидкость может являться композицией для транспортировки и хранения соединения, имеющего уреидные группы, варианта настоящего осуществления. На последующей стадии (B) получают N-замещенной карбаминовой кислоты-O-ариловый эфир путем реакции соединения, имеющего уреидные группы, и ароматического гидроксисоединения. Аммиак, образующийся в качестве побочного продукта в реакции стадии (B), извлекают из реакционной жидкости, до тех пор пока концентрация аммиака не будет находиться в описанных ранее предпочтительных интервалах, и используют на стадии (G) вместе с аммиаком, извлеченным на стадии (A). Мочевину, получаемую на стадии (G), повторно используют в качестве сырья стадии (A). Кроме того, стадию (D) проводят одновременно со стадией (B). А именно, непрореагировавшую избыточную мочевину удаляют путем ректификации или сублимации. В данном случае мочевину отгоняют вместе с частью ароматической гидроксикомпозиции, и, предпочтительно, удаляют и извлекают в форме смеси с ароматической гидроксикомпозицией. Мочевину, извлекаемую на стадии (D), повторно используют в качестве сырья стадии (A) путем проведения стадии (E).
N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (B), подвергают термическому разложению на последующей стадии (F), что приводит к образованию соответствующего изоцианата и ароматической гидроксикомпозиции. Ароматическую гидроксикомпозицию, отделяемую от изоцианата на стадии (F), повторно используют в качестве сырья стадии (A).
На фигуре 9 приведена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 2) со стадиями (D), (E), (F) и (G).
Это направление 2) является примером предпочтительного аспекта в случае использования моноариламина в качестве органического первичного амина.
Сначала органический первичный амин (моноариламин) и мочевина реагируют на стадии (A) с образованием соединения, имеющего уреидные группы. На этой стадии (A) ароматическая гидроксикомпозиция действует главным образом как реакционный растворитель. В реакции стадии (A) аммиак, образующийся в качестве побочного продукта, может быть извлечен из реакционной жидкости, до тех пор пока концентрация аммиака в реакционной жидкости не будет находиться в описанных ранее предпочтительных интервалах. Реакционная жидкость, получаемая на стадии (A), содержит соединение, имеющее уреидные группы, и ароматическую гидроксикомпозицию, и, в зависимости от используемого сырья, соотношения компонентов в сырье, условий реакции стадии (A) и других подобных параметров, реакционная жидкость может являться композицией для транспортировки и хранения соединения, имеющего уреидные группы, варианта настоящего осуществления. На последующей стадии (B) получают N-замещенной карбаминовой кислоты-O-моно(ариловый эфир) путем реакции соединения, имеющего уреидные группы, и ароматического гидроксисоединения. Аммиак, образующийся в качестве побочного продукта в реакции стадии (B), извлекают из реакционной жидкости, до тех пор пока концентрация аммиака не будет находиться в описанных ранее предпочтительных интервалах, и используют на стадии (G) вместе с аммиаком, извлеченным на стадии (A). Мочевину, получаемую на стадии (G), повторно используют в качестве сырья стадии (A). Кроме того, стадию (D) проводят одновременно со стадией (B). А именно, непрореагировавшую избыточную мочевину удаляют путем ректификации или сублимации. В данном случае мочевину отгоняют вместе с частью ароматической гидроксикомпозиции, и, предпочтительно, удаляют и извлекают в форме смеси с ароматической гидроксикомпозицией. Мочевину, извлекаемую на стадии (D), повторно используют в качестве сырья стадии (A) путем проведения стадии (E).
N-замещенной карбаминовой кислоты-O-моно(ариловый эфир), получаемый на стадии (B), используют для получения N-замещенной карбаминовой кислоты-O-арилового эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-моно(арилового эфира) являются сшитыми с помощью метиленовых (-CH2-) групп путем сшивания с помощью метиленовых групп на следующей стадии (C). При проведении стадии (C) ароматическую гидроксикомпозицию, используемую на стадии (B), отделяют от реакционной жидкости, содержащей N-замещенной карбаминовой кислоты-O-моно(ариловый эфир). После проведения стадии (C) предпочтительно, чтобы ароматическую гидроксикомпозицию добавляли к получаемому N-замещенной карбаминовой кислоты-O-ариловому эфиру и затем подвергали N-замещенной карбаминовой кислоты-O-ариловый эфир реакции термического разложения на стадии (F). На стадии (F) N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (C), подвергают термическому разложению с образованием соответствующего изоцианата и ароматической гидроксикомпозиции. Ароматическую гидроксикомпозицию, отделяемую от изоцианата на стадии (F), повторно используют в качестве сырья стадии (A).
На фигуре 10 приведена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 3) со стадиями (D), (E), (F) и (G).
Сначала органический первичный амин и мочевина реагируют на стадии (A) с образованием соединения, имеющего уреидные группы. Спирт и/или ароматическую гидроксикомпозицию предпочтительно использовать как реакционный растворитель на этой стадии (A). В реакции стадии (A) аммиак, образующийся в качестве побочного продукта, может быть извлечен из реакционной жидкости, до тех пор пока концентрация аммиака в реакционной жидкости не будет находиться в описанных ранее предпочтительных интервалах. В данном случае часть непрореагировавшей избыточной мочевины может быть извлечена в качестве газофазного компонента. Реакционная жидкость, получаемая на стадии (A), в зависимости от используемого сырья, соотношения компонентов в сырье, условий реакции стадии (A) и других подобных параметров, может являться композицией для транспортировки и хранения соединения, имеющего уреидные группы, варианта настоящего осуществления. На последующей стадии (R) получают N-замещенной карбаминовой кислоты-O-R2 эфир путем реакции соединения, имеющего уреидные группы, и спирта. Аммиак, образующийся в качестве побочного продукта в реакции стадии (R), извлекают из реакционной жидкости, до тех пор пока концентрация аммиака не будет находиться в описанных ранее предпочтительных интервалах, и используют на стадии (G) вместе с аммиаком, извлеченным на стадии (A). Мочевину, получаемую на стадии (G), повторно используют в качестве сырья стадии (A). Кроме того, стадию (D) проводят одновременно со стадией (R). А именно, непрореагировавшую избыточную мочевину удаляют путем ректификации или сублимации. В данном случае мочевину отгоняют вместе с частью ароматической гидроксикомпозиции (спиртом и/или ароматическим гидроксисоединением), и, предпочтительно, удаляют и извлекают в форме смеси с ароматической гидроксикомпозицией. Мочевину, извлекаемую на стадии (D), повторно используют в качестве сырья стадии (A) путем проведения стадии (E).
Далее, N-замещенной карбаминовой кислоты-O-R2 эфир, получаемый на стадии (R), превращают в N-замещенной карбаминовой кислоты-O-ариловый эфир путем реакции с ароматической гидроксикомпозицией на стадии (P). Спирт, получаемый из N-замещенной карбаминовой кислоты-O-R2 эфира, который получают в качестве побочного продукта по этой реакции, повторно используют на стадии (A). Кроме того, в случае, когда удаление мочевины является недостаточным на стадии (D), которую проводят одновременно со стадией (R), стадия (D) может также быть проведена одновременно со стадией (P) для удаления мочевины из реакционной жидкости. Мочевину, извлекаемую на стадии (D), также повторно используют в качестве сырья стадии (A) путем аналогичного проведения стадии (E).
N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (P), подвергают термическому разложению на последующей стадии (F) с образованием соответствующего изоцианата и ароматической гидроксикомпозиции. Ароматическую гидроксикомпозицию, отделяемую от изоцианата на стадии (F), повторно используют в качестве сырья стадии (A).
На фигуре 11 приведена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 4) со стадиями (D), (E), (F) и (G).
Это направление 4) является примером предпочтительного аспекта в случае использования моноариламина в качестве органического первичного амина.
Сначала органический первичный амин (моноариламин) и мочевина реагируют на стадии (A) с образованием соединения, имеющего уреидные группы. На этой стадии (A) спирт и/или ароматическую гидроксикомпозицию предпочтительно использовать как реакционный растворитель. В реакции стадии (A) аммиак, образующийся в качестве побочного продукта, может быть извлечен из реакционной жидкости, до тех пор пока концентрация аммиака в реакционной жидкости не будет находиться в описанных ранее предпочтительных интервалах. В данном случае часть непрореагировавшей или избыточной мочевины может также быть извлечена в качестве газофазного компонента. Реакционная жидкость, получаемая на стадии (A), в зависимости от используемого сырья, соотношения компонентов в сырье, условий реакции стадии (A) и других подобных параметров, может являться композицией для транспортировки и хранения соединения, имеющего уреидные группы, варианта настоящего осуществления. На последующей стадии (R) получают N-замещенной карбаминовой кислоты-O-моно(R2 эфир) путем реакции соединения, имеющего уреидные группы, и спирта. Аммиак, образующийся в качестве побочного продукта в реакции стадии (R), извлекают из реакционной жидкости, до тех пор пока концентрация аммиака не будет находиться в описанных ранее предпочтительных интервалах, и используют на стадии (G) вместе с аммиаком, извлеченным на стадии (A). Мочевину, получаемую на стадии (G), повторно используют в качестве сырья стадии (A). Кроме того, стадию (D) проводят одновременно со стадией (R). А именно, непрореагировавшую или избыточную мочевину удаляют путем ректификации или сублимации. В данном случае мочевину отгоняют вместе с частью ароматической гидроксикомпозиции (спиртом и/или ароматическим гидроксисоединением), и, предпочтительно, удаляют и извлекают в форме смеси с ароматической гидроксикомпозицией. Мочевину, извлекаемую на стадии (D), повторно используют в качестве сырья стадии (A) путем проведения стадии (E).
Далее, N-замещенной карбаминовой кислоты-O-моно(R2 эфир), получаемый на стадии (R), превращают в N-замещенной карбаминовой кислоты-O-моно(ариловый эфир) путем реакции с ароматической гидроксикомпозицией на стадии (P). Спирт, получаемый из N-замещенной карбаминовой кислоты-O-моно(R2 эфира), который получают в качестве побочного продукта по этой реакции, повторно используют на стадии (A). Кроме того, в случае, когда удаление мочевины является недостаточным на стадии (D), которую проводят одновременно со стадией (R), стадия (D) может также быть проведена одновременно со стадией (P) для удаления мочевины в реакционной жидкости. Мочевину, извлекаемую на стадии (D), также повторно используют в качестве сырья стадии (A) путем аналогичного проведения стадии (E).
N-замещенной карбаминовой кислоты-O-моно(ариловый эфир), получаемый на стадии (P), используют для получения N-замещенной карбаминовой кислоты-O-арилового эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-моно(арилового эфира) являются сшитыми с помощью метиленовых (-CH2-) групп путем сшивания с помощью метиленовыз групп на последующей стадии (C). При проведении стадии (C) ароматическую гидроксикомпозицию, остающуюся в реакционной жидкости стадии (P), отделяют от реакционной жидкости, содержащей N-замещенной карбаминовой кислоты-O-моно(ариловый эфир). После проведения стадии (C), предпочтительно, чтобы ароматическую гидроксикомпозицию добавляли к получаемому N-замещенной карбаминовой кислоты-O-ариловому эфиру и затем подвергали N-замещенной карбаминовой кислоты-O-ариловый эфир реакции термического разложения на стадии (F).
На стадии (F) N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (C), подвергают термическому разложению с образованием соответствующего изоцианата и ароматической гидроксикомпозиции. Ароматическую гидроксикомпозицию, отделяемую от изоцианата на стадии (F), повторно используют в качестве сырья стадии (A).
На фигуре 12 приведена принципиальная схема одного аспекта варианта настоящего осуществления, который объединяет направление 5) со стадиями (D), (E), (F) и (G).
Это направление 5) является примером предпочтительного аспекта в случае использования моноариламина в качестве органического первичного амина.
Сначала органический первичный амин (моноариламин) и мочевина реагируют на стадии (A) с образованием соединения, имеющего уреидные группы. На этой стадии (A) спирт и/или ароматическую гидроксикомпозицию предпочтительно использовать как реакционный растворитель. В реакции стадии (A) аммиак, образующийся в качестве побочного продукта, может быть извлечен из реакционной жидкости, до тех пор пока концентрация аммиака в реакционной жидкости не будет находиться в описанных ранее предпочтительных интервалах. В данном случае часть непрореагировавшей или избыточной мочевины может быть извлечена в качестве компонента газовой фазы. Реакционная жидкость, получаемая на стадии (A), в зависимости от используемого сырья, соотношения компонентов в сырье, условий реакции стадии (A) и других подобных параметров может являться композицией для транспортировки и хранения соединения, имеющего уреидные группы, варианта настоящего осуществления. На последующей стадии (R) получают N-замещенной карбаминовой кислоты-O-моно(R2 эфир) путем реакции соединения, имеющего уреидные группы, и спирта. Аммиак, образующийся в качестве побочного продукта в реакции стадии (R), извлекают из реакционной жидкости, до тех пор пока концентрация аммиака не будет находиться в описанных ранее предпочтительных интервалах, и используют на стадии (G) вместе с аммиаком, извлеченным на стадии (A). Мочевину, получаемую на стадии (G), повторно используют в качестве сырья стадии (A). Кроме того, стадию (D) проводят одновременно со стадией (R). А именно, непрореагировавшую или избыточную мочевину удаляют путем ректификации или сублимации. В данном случае мочевину отгоняют вместе с частью ароматической гидроксикомпозиции (спиртом и/или ароматическим гидроксисоединением), и, предпочтительно, удаляют и извлекают в форме смеси с ароматической гидроксикомпозицией. Мочевину, извлекаемую на стадии (D), повторно используют в качестве сырья стадии (A) путем проведения стадии (E).
Далее, N-замещенной карбаминовой кислоты-O-моно(R2 эфир), получаемый на стадии (R), используют для получения N-замещенной карбаминовой кислоты-O-R2 эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-моно(R2 эфира) являются сшитыми с помощью метиленовых (-CH2-) групп путем сшивания с помощью метиленовых групп на стадии (C). При проведении стадии (C) ароматическую гидроксикомпозицию, остающуюся в реакционной жидкости стадии (R), отделяют от реакционной жидкости, содержащей N-замещенной карбаминовой кислоты-O-моно(R2 эфир). Кроме того, в случае, когда удаление мочевины является недостаточным на стадии (D), которую проводят одновременно со стадией (R), стадия (D) может также быть проведена одновременно с отделением гидроксикомпозиции, остающейся в реакционной жидкости стадии (R), от реакционной жидкости, за которой следует извлечение мочевины и гидроксикомпозиции. Извлеченные мочевину и гидроксикомпозицию повторно используют в качестве сырья стадии (A) путем проведения стадии (E).
После проведения стадии (C) получаемый N-замещенной карбаминовой кислоты-O-R2 эфир подвергают реакции переэтерификации на стадии (P). Спирт, получаемый из N-замещенной карбаминовой кислоты-O-R2 эфира, который образуется в качестве побочного продукта в этой реакции, повторно используют на стадии (A).
N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый на стадии (P), подвергают реакции термического разложения на стадии (F) с образованием соответствующего изоцианата и ароматической гидроксикомпозиции. Ароматическую гидроксикомпозицию, отделенную от изоцианата на стадии (F), повторно используют в качестве ароматической гидроксикомпозиции стадии (P).
ПРИМЕРЫ
Далее приводится подробное объяснение настоящего изобретения на основе его примеров, но объем настоящего изобретения не ограничивается этими примерами.
<Аналитические методы>
1) ЯМР анализ
Прибор: система JNM-A400 FT-ЯМР, фирма JEOL Ltd., Japan
(1) Приготовление образцов для 1H-ЯМР и 13C-ЯМР анализа
Взвешивали около 0,3 г образца раствора, затем добавляли около 0,7 г дейтерированного хлороформа (99,8%, фирмы Aldrich Corp., USA) и 0,05 г внутреннего стандарта в форме тетраметилолова (гарантированный реагент, фирмы Wako Pure Chemical Industries, Ltd., Japan) и смешивали до гомогенного состояния с получением растворов, используемых в качестве образцов для ЯМР анализа.
(2) Количественный анализ
Проводили анализ каждого стандарта и проводили количественные определения образцов анализируемых растворов на основе полученной калибровочной кривой.
2) Жидкостная хроматография
Прибор: система LC-10AT, фирмы Shimadzu Corp., Japan
Колонка: колонка Inertsil-ODS, фирмы GL Sciences Inc., Japan, две колонки, соединенные последовательно
Проявляющий растворитель: смешанная жидкость 5 ммоль/л водного раствора ацетата аммония (раствор A) и ацетонитрила (раствор B)
Расход проявляющего растворителя: 2 мл/мин
Температура колонки: 35°C
Детектор: детектор показателя преломления (рефрактометр) и PDA детектор (детектор на фотодиодной матрице, измеряющей в диапазоне длин волн: 200-300 нм)
(1) Анализ образцов с помощью жидкостной хроматографии
Взвешивали около 0,1 г образца, затем добавляли около 1 г тетрагидрофурана (обезвоженного, фирмы Wako Pure Chemical Industries, Ltd., Japan) и около 0,02 г внутреннего стандарта в форме 1,1-диэтилмочевины (фирмы Tokyo Chemical Industry Co., Ltd., Japan) и смешивали до гомогенного состояния с получением растворов, используемых в качестве образцов для анализа с помощью жидкостной хроматографии.
(2) Количественный анализ
Проводили анализ каждого стандарта и проводили количественные определения образцов анализируемых растворов на основе полученной калибровочной кривой.
3) Анализ воды
Прибор: Анализатор для определения микросодержания воды Model CA-21, фирмы Mitsubishi Chemical Analytech Co., Ltd., Japan
(1) Количественный анализ
Для определения содержания воды в образце взвешивали около 1 г образца и вводили в анализатор для определения микросодержания воды.
4) Анализ содержания аммиака в жидких и твердых веществах
Прибор: ионный хроматограф IC2001 (фирмы Tosoh Corp., Japan)
Колонка: SuperIC-CR
Проявляющий раствор: раствор, получаемый смешением 1 л воды и около 0,25 г 18-краун-6 (фирмы Wako Pure Chemical Industries, Ltd., Japan) и около 2,1 мл 2 моль/л метансульфоновой кислоты (фирмы Wako Pure Chemical Industries, Ltd., Japan).
(1) Анализ образцов с помощью ионной хроматографии
Взвешивали около 0,15 г образца и затем добавляли около 1 г толуола и около 15 г 2 ммоль/л водного раствора азотной кислоты, хорошо перемешивали и давали возможность постоять в течение приблизительно 2 часов. Затем отделяли водный слой и использовали его в качестве образца для анализа с помощью ионной хроматографии.
(2) Количественный анализ
Получали калибровочную кривую с использованием стандартной смеси катионов Cation Mixed Standard II (фирмы Kanto Chemical Co., Inc., Japan), и определяли количества аммиака в анализируемых образцах растворов на основе калибровочной кривой.
Кроме того, названия используемых соединений в следующих примерах приводятся в соответствии с правилами номенклатуры, определенными IUPAC, а также с использованием тривиальных названий.
[ПРИМЕР 1] ПОЛУЧЕНИЕ N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ-O-АРИЛОВОГО ЭФИРА С ПОМОЩЬЮ НАПРАВЛЕНИЯ 1)
Стадия (A): Получение соединения, имеющего уреидные группы
Использовали установку, приведенную на фигуре 13.
41,84 кг п-гептилфенола (фирмы Schenectady Chemicals, USA) и 3,10 кг мочевины смешивали в емкости для хранения 101, нагретой до 120°C, при перекрытой линии 13, с полученной смеси при использовании в качестве ароматической гидроксикомпозиции. Концентрация воды в смеси составляла около 15 ppm. Смесь транспортировали в реактор с мешалкой 103 (с перегородками), нагретый до 120°C. Затем подавали 1,50 кг органического амина в форме гексаметилендиамина со скоростью около 20 г/мин (скорость подачи органического амина) из емкости для хранения 102 в реактор с мешалкой 103 через линию 12 при перемешивании в реакторе с мешалкой 103. Образование аммиака подтверждали с помощью анализа проб, отбираемых через линию 19. После завершения подачи гексаметилендиамина перемешивание продолжали в течение около 2 часов и отбирали пробу реакционной жидкости. В результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что реакционная жидкость содержит 6,3% по массе соединения, имеющего уреидные группы, в форме 6-гексаметилендимочевины. Кроме того, концентрация аммиака в растворе составляла 6300 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были. Отношение числа молекул п-гептилфенола к числу уреидных групп в реакционной жидкости составляло 7,5.
Открывали линию 13, и реакционную жидкость транспортировали в емкость для хранения 104 через линию 13.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Продолжали использовать установку, показанную на фигуре 13.
Насадочную колонну 105, заполненную насадкой (Helipack No. 3), нагревали до 240°C и создавали давление внутри колонны 26 кПа. Реакционную жидкость, получаемую на стадии (A), подавали по линии 14, подсоединенной к насадочной колонне 105, при скорости около 1,5 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, вводимой после того как реакция достигала стационарного состояния, составляло около 35,1 кг. Реакционную жидкость извлекали в емкость для хранения 110 через линию 16, подсоединенную к нижней части насадочной колонны 105. Газофазный компонент через линию 15, подсоединенную к верхней части насадочной колонны 105, подавали в конденсатор 106 и подвергали конденсации, и полученный с помощью газо-жидкостного сепаратора 108 жидкофазный компонент извлекали в емкость для хранения 109. При анализе реакционной жидкости, извлеченной в емкость для хранения 109, с помощью 1H-ЯМР было обнаружено, что сконденсированный компонент содержит мочевину и п-гептилфенол. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 23,0 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты(п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты(п-гептилфенилового)эфира) относительно гексаметилендиамина составлял около 97%. Содержание мочевины в реакционной жидкости составляло ниже предела обнаружения. Кроме того, N,N'-бис(6-(п-гептилфеноксикарбамино-гексил)мочевину не обнаруживали. Концентрация аммиака в реакционной жидкости составляла 9,0 ppm.
С другой стороны, количество смеси, извлекаемой в емкость для хранения 109, составляло 13,5 кг. Эта смесь содержала ароматическое гидроксисоединение (п-гептилфенол) и мочевину, и содержание ароматического гидроксисоединения (п-гептилфенола) в смеси составляло 85,4% по массе, в то время как содержание мочевины составляло 10,2% по массе.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 17.
Пленочный дистилляционный аппарат 602 (фирмы Kobelco Eco-Solutions Co., Ltd., Japan), имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в пленочном дистилляционном аппарате около 1,3 КПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в пленочный дистилляционный аппарат при скорости около 1800 г/час по линии 60. Жидкий компонент извлекали через линию 62, подсоединенную к нижней части пленочного дистилляционного аппарата 602, и извлекали в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в пленочный дистилляционный аппарат 602 через линию 63. Газообразный компонент, содержащий гексаметилендиизоцианат и п-гептилфенол, извлекали через линию 61, подсоединенную к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и дополнительно подвергали ректификационному разделению. Газофазный компонент, подаваемый по линии 69 в конденсатор 610, подвергали конденсации и извлекали с помощью газо-жидкостного сепаратора 611 в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно органического амина стадии (A) (гексаметилендиамина) составлял около 90%. Смесь, содержащую п-гептилфенол, получали в емкости для хранения 614.
Стадия (E): Получение эфира N-замещенной карбаминовой кислоты путем повторного использования смеси, получаемой в конденсаторе
Концентрация аммиака в смеси, извлеченной в емкость для хранения 109, на стадии (B) примера 1 составляла 820 ppm. Добавляли в смесь 12,8 кг п-гептилфенола и 0,578 кг мочевины, затем транспортировали в реактор с мешалкой 103 и осуществляли такой же способ, как на стадии (A), используя 0,92 кг гексаметилендиамина. Получали раствор, содержащий 6,3% по массе 1,6-гександимочевины. Осуществляли такой же способ, как на стадии (B), используя этот раствор вместо раствора стадии (A). Реакционная жидкость, извлекаемая в емкость для хранения 610, содержала N,N'-гександиилди(карбаминовой кислоты(п-гептилфениловый) эфир), и выход N,N'-гександиилди(карбаминовой кислоты(п-гептилфенилового) эфира) относительно гексаметилендиамина составлял около 97%.
[ПРИМЕР 2] ПОЛУЧЕНИЕ N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ-O-АРИЛОВОГО ЭФИРА С ПОМОЩЬЮ НАПРАВЛЕНИЯ 1)
Стадия (A): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 14.
Смесь 1,92 кг мочевины и 11,9 кг растворителя (1-бутанола) транспортировали из емкости для хранения 200 в реактор с мешалкой 203, нагретый до 120°C, при закрытой линии 23. Затем подавали 0,930 кг органического амина в форме гексаметилендиамина при скорости около 5 г/мин (скорости подачи органического амина) из емкости для хранения 201 в реактор с мешалкой 103 через линию 21 при перемешивании в реакторе с мешалкой 203. После завершения подачи гексаметилендиамина перемешивание продолжали в течение около 1 часа. При анализе реакционной жидкости с помощью жидкостной хроматографии, было обнаружено, что она содержит 11,2% по массе 1,1'-(гексан-1,6-диил)димочевины. Кроме того, концентрация аммиака в растворе составляла 7500 ppm. Отношение непрореагировавших аминогрупп к уреидным группам составляло 0,001. Транспортировали 23,1 кг ароматического гидроксисоединения в форме п-гептилфенола из емкости для хранения 202 в реактор с мешалкой 203, затем после получения гомогенного раствора транспортировали в емкость для хранения 204.
Стадия (D): Отделение и извлечение мочевины
Продолжали использовать установку, показанную на фигуре 14. Насадочную колонну 205, заполненную насадкой (Helipack No. 3) нагревали до температуры около 120°C и создавали давление внутри колонны 10 кПа. Реакционную жидкость, получаемую на стадии (A), подавали в насадочную колонну 205 при скорости около 8,2 г/мин по линии 24, подсоединенной к насадочной колонне 205. Газообразный компонент извлекали по линии 25 и после конденсации в конденсаторе 206 извлекали в емкость для хранения 208. Извлекаемая жидкость, получаемая в емкости для хранения 208, являлась смешанной жидкостью, содержащей 1-бутанол и мочевину. Остаточная жидкость, извлекаемая в емкость для хранения 209 из нижней части насадочной колонны 205 через линию 26, являлась смешанной жидкостью, содержащей 1,1'-(гексан-1,6-диил)димочевину и п-гептилфенол. Извлекаемое количество остаточной жидкости составляло около 13,5 кг. Концентрация 1,1'-(гексан-1,6-диил)димочевины в остаточной жидкости составляла 12,0% по массе, и отношение числа молекул п-гептилфенола к числу уреидных групп составляло около 2,9.
С другой стороны, около 9,8 кг смеси 1-бутанола и мочевины извлекали в емкость для хранения 208. Количество 1-бутанола, содержавшегося в смеси, составляло 92,5% по массе, в то время как количество мочевина составляло 7,1% по массе.
Стадия (B): Получение N-замещенной карбаминовой кислоты-O-арилового эфира
Продолжали использовать установку, показанную на фигуре 14. Насадочную колонну 210, заполненную насадкой (Helipack No. 3), нагревали до 250°C и создавали давление внутри колонны 26 кПа. Остаточную жидкость, извлекаемую в емкость для хранения 209 на стадии (D), подавали по линии 28, подсоединенной к насадочной колонне 210, при скорости около 3,8 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 8,95 кг. Реакционную жидкость извлекали в емкость для хранения 216 через линию 31, подсоединенную к нижней части насадочной колонны 210. Газофазный компонент извлекали по линии 29, подсоединенной к верхней части насадочной колонны 210, и конденсировали с помощью конденсатора 211, и полученный с помощью газо-жидкостного сепаратора 212 жидкофазный компонент извлекали в емкость для хранения 213 и рециркулировали в насадочную колонну 210. С другой стороны, аммиак выводили в форме газообразного компонента по линии 31. Аммиак абсорбировали водой и извлекали в форме водного раствора аммиака. При анализе реакционной жидкости, извлекаемой в емкость для хранения 216, с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты(п-гептилфениловый) эфир), и выход N,N'-гександиилди(карбаминовой кислоты(п-гептилфенилового) эфира) относительно гексаметилендиамина составлял около 95%. Кроме того, концентрация аммиака в реакционной жидкости составляла 8,0 ppm.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 17.
Пленочный дистилляционный аппарат 602, имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в пленочном дистилляционном аппарате около 1,3 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в пленочный дистилляционный аппарат при скорости около 1500 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части пленочного дистилляционного аппарата 602, и извлекали в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в пленочный дистилляционный аппарат 602 по линии 63. Газообразный компонент, содержащий гексаметилендиизоцианат и п-гептилфенол, извлекали по линии 61, подсоединенной к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и дополнительно подвергали ректификационному разделению. Газофазный компонент через линию 69 подавали в конденсаторе 610 и подвергали конденсации и с помощью газо-жидкостного сепаратора 611 извлекали в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии, было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно органического амина (гексаметилендиамина) составлял около 90%.
Стадия (E): Получение эфира N-замещенной карбаминовой кислоты путем повторного использования смеси, получаемой в конденсаторе
Концентрация аммиака в смеси, извлекаемой в емкость для хранения 109 на стадии (D) примера 2, составляла 550 ppm. Добавляли к смеси 0,962 кг мочевины (без добавления растворителя), затем транспортировали в реактор с мешалкой 103 и осуществляли такой же способ, как на стадии (A), используя 0,930 кг гексаметилендиамина. Получали раствор, содержащий 14,1% по массе 1,6-гексан-бис-мочевины. Осуществляли такой же способ, как на стадии (B), используя этот раствор вместо раствора стадии (A). Реакционная жидкость, извлекаемая в емкость для хранения 610, содержала N,N'-гександиилди(карбаминовой кислоты(п-гептилфениловый) эфир), и выход N,N'-гександиилди(карбаминовой кислоты(п-гептилфенилового) эфира) относительно гексаметилендиамина составлял около 95%.
[ПРИМЕР 3]
Стадия (A): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 13.
Смешивали 13,6 кг 1-бутанола в качестве гидроксисоединения и 2,49 кг мочевины в емкости для хранения 101, нагретой до 120°C, с перекрытой линией 13, с получением смеси. Смесь транспортировали в реактор с мешалкой 103 (с перегородками), нагретый до 120°C. Затем подавали 1,07 кг органического амина в форме гексаметилендиамина при скорости около 20 г/мин (скорости подачи органического амина) из емкости для хранения 102 в реактор с мешалкой 103 через линию 12 при перемешивании в реакторе с мешалкой 103. После завершения подачи гексаметилендиамина, перемешивание продолжали в течение около 2 часов, и отбирали пробу реакционной жидкости. В результате анализа реакционной жидкости с помощью жидкостной хроматографии, было обнаружено, что реакционная жидкость содержит 10,9% по массе соединения, имеющего уреидные группы, в форме 1,1'-(гексан-1,6-диил)димочевины. Кроме того, концентрация аммиака в растворе составляла 4300 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были. К реакционной жидкости добавляли 26,6 кг гидроксисоединения в форме п-гептилфенола с получением гомогенного раствора. Отношение числа молекул п-гептилфенола к числу уреидных групп в реакционной жидкости составляло 7,6. Открывали линию 13, и транспортировали реакционную жидкость в емкость для хранения 104 через линию 13.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Продолжали использовать установку, изображенную на фигуре 13.
Насадочную колонну 105, заполненную насадкой (Helipack No. 3), нагревали до 240°C и создавали давление внутри колонны 50 кПа. Реакционную жидкость, получаемую на стадии (A), подавали по линии 14, подсоединенной к насадочной колонне 105, при скорости около 3,8 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 37,8 кг. Реакционную жидкость извлекали в емкость для хранения 110 по линии 16, подсоединенной к нижней части насадочной колонны 105. Газофазный компонент подавали по линии 15, подсоединенной к верхней части насадочной колонны 105, в конденсатор 106 и подвергали конденсации, и образующийся жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 108 в емкость для хранения 109. Количество сконденсированного компонента, извлекаемого в емкость для хранения 109, составляло 13,3 кг, и при анализе сконденсированного компонента с помощью 1H-ЯМР было обнаружено, что сконденсированный компонент содержит мочевину и 1-бутанол. Содержание мочевины составляло 9,09% по массе и содержание 1-бутанола составляло 89,1% по массе. При анализе реакционной жидкости, извлеченной в емкость для хранения 110, с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты(п-гептилфениловый) эфир), и выход N,N'-гександиилди(карбаминовой кислоты(п-гептилфенилового) эфира) относительно гексаметилендиамина составлял около 94%. Мочевину в реакционной жидкости не обнаруживали. Количество аммиака, содержащегося в реакционной жидкости, составляло 8,1 ppm.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 17.
Пленочный дистилляционный аппарат 602, имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в пленочном дистилляционном аппарате около 1,3 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в пленочный дистилляционный аппарат при скорости около 1800 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части пленочного дистилляционного аппарата 602, и извлекали в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в пленочный дистилляционный аппарат 602 по линии 63. Газообразный компонент, содержащий гексаметилендиизоцианат и п-гептилфенол, извлекали по линии 61, подсоединенной к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Газофазный компонент подавали по линии 69 в конденсатор 610 и подвергали конденсации и с помощью газо-жидкостного сепаратора 611 извлекали в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии, было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно органического амина (гексаметилендиамина) составлял около 90%.
[ПРИМЕР 4] ПОЛУЧЕНИЕ N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ-O-АРИЛОВОГО ЭФИРА ПУТЕМ НАПРАВЛЕНИЯ 2)
Стадия (A): Получение соединение, имеющее уреидные группы
Использовали установку, показанную на фигуре 13.
Смешивали 43,5 кг ароматического гидроксисоединения в форме 4-трет-амилфенола и 3,61 кг мочевины в емкости для хранения 101, нагретой до 80°C, с перекрытой линией 13, и смесь транспортировали в реактор с мешалкой 103, нагретой до 80°C. Затем подавали 1,12 кг анилина при скорости около 10 г/мин (скорости подачи анилина) из емкости для хранения 102 в реактор с мешалкой 603 по линии 12 при перемешивании в реакторе с мешалкой 103. После завершения подачи гексаметилендиамина, перемешивание продолжали в течение около 28 часов и отбирали пробу реакционной жидкости. В результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что реакционная жидкость содержит 4,5% по массе N-фенилмочевины. Отношение числа молекул 4-трет-амилфенола к числу уреидных групп в реакционной жидкости составляло 11. Количество аммиака, содержащегося в реакционной жидкости, составляло 3800 ppm.
Открывали линию 63 и реакционную жидкость транспортировали в емкость для хранения 604 по линии 63.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты моно(O-арилового эфира)
Продолжали использовать установку, показанную на фигуре 13.
Насадочную колонну 105, заполненную насадкой (Helipack No. 3), нагревали до 200°C и создавали давление внутри колонны 8 кПа. Реакционную жидкость, получаемую на стадии (A), подавали по линии 14, подсоединенной к насадочной колонне 105, при скорости около 1,6 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 8,95 кг. Реакционную жидкость извлекали в емкость для хранения 110 по линии 16, подсоединенной к нижней части насадочной колонны 105. Газофазный компонент вводили в конденсатор 106 по линии 15, подсоединенной к верхней части насадочной колонны 105, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 108 в емкость для хранения 109. При анализе сконденсированного компонента, извлекаемого в емкость для хранения 109, с помощью 1H-ЯМР было обнаружено, что сконденсированный компонент содержит мочевину и 4-трет-амилфенол. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 8,72 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N-фенилкарбаминовой кислоты (4-трет-амилфениловый) эфир, и выход N-фенилкарбаминовой кислоты (4-трет-амилфенилового)эфира относительно анилина составлял около 93%. Количество аммиака, содержавшегося в реакционной жидкости, составляло 5,6 ppm.
Стадия (C): Конденсация N-замещенной карбаминовой кислоты моно(-O-арилового эфира)
Использовали установку, показанную на фигуре 15.
Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в реактор с мешалкой 408. Реактор с мешалкой 408 нагревали до 160°C и создавали внутри него давление 2 кПа, затем отгоняли ароматическое гидроксисоединение. Ароматическое гидроксисоединение в форме 4-трет-амилфенола подавали через линию 44 в конденсаторе 405 и подвергали конденсации и извлекали в емкость для хранения 407. Затем 1,14 кг метилаля (формальдегид диметил ацеталя) из емкости для хранения 400, 4,70 кг нитробензола из емкости для хранения 401 и 5,6 кг серной кислоты из емкости для хранения 402 добавляли в реактор с мешалкой 408, затем нагревали в течение 10 часов при 100°C при перемешивании в реакторе с мешалкой 408. Затем отгоняли растворитель и непрореагировавшие вещества путем поддержания температуры внутри реактора с мешалкой 408 при 100°C и снижения давления внутри до 1 кПа. При анализе образовавшегося соединения с помощью жидкостной хроматографии, было обнаружено, что оно является смесью, содержащей около 55% по массе N,N'-(метандиилдифенил)ди(карбаминовой кислоты (4-трет-амилфенилового) эфира). К смеси добавляли около 5,1 кг ароматического гидроксисоединения (4-трет-амилфенола) с получением гомогенного раствора, который затем транспортировали в емкость для хранения 404.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 18.
Пленочный дистилляционный аппарат 1002 (фирмы Kobelco Eco-Solutions Co., Ltd., Japan), имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 260°C и создавали давление в пленочном дистилляционном аппарате около 1,5 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 404 на стадии (C), помещали в емкость для хранения 1001 и подавали в пленочный дистилляционный аппарат при скорости около 1200 г/час по линии A1. Жидкий компонент извлекали по линии A4, подсоединенной к нижней части пленочного дистилляционного аппарата 1002, и извлекали в емкость для хранения 1003. Жидкий компонент, извлекаемый в емкость для хранения 1003, опять подавали в пленочный дистилляционный аппарат 1002 по линии A3. Газообразный компонент извлекали по линии A4, подсоединенной к верхней части пленочного дистилляционного аппарата 1002. Газообразный компонент вводили в ректификационную колонну 1004, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 1009 по линии A8, подсоединенной к части ректификационной колонны 1004 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Жидкофазный компонент подавали в ректификационную колонну 1014 по линии A12, подсоединенной к части ректификационной колонны 1009 ниже линии подачи сырья, и затем подвергали ректификационному разделению.
Газофазный компонент извлекали по линии A13, подсоединенной к верхней части ректификационной колонны 1014, и конденсировали в конденсаторе 1015, и конденсат извлекали в емкость для хранения 1019. При анализе конденсата с помощью 1H-ЯМР, было обнаружено, что он является раствором, содержащим около 99% по массе 4,4'-дифенилметан диизоцианата (MDI). Выход относительно анилина составлял около 50%.
Стадия (E): Получение сложного эфира N-замещенной карбаминовой кислоты путем повторного использования смеси, получаемой в конденсаторе
При анализе содержания аммиака в смеси, извлекаемой в емкость для хранения 109 на стадии (B) примера 3, было обнаружено, что оно составляет 1800 ppm. Добавляли 19,0 кг 4-трет-амилфенола и 0,690 кг мочевины к 14,7 кг смеси, затем транспортировали в реактор с мешалкой 603, и осуществляли такой же способ, как на стадии (A), используя 0,820 кг анилина. Получали раствор, содержащий 4,5% по массе фенилмочевины. Осуществляли такой же способ, как на стадии (B), используя этот раствор вместо раствора стадии (A). Выход N-фенилкарбаминовой кислоты (4-трет-амилфенилового) эфира в реакционной жидкости, извлекаемой в емкость для хранения 110, относительно анилина составлял около 93%.
[ПРИМЕР 5] ПОЛУЧЕНИЕ N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ-O-АРИЛОВОГО ЭФИРА ПО НАПРАВЛЕНИЮ 3)
Стадия (A): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 13.
Смешивали 14,6 кг растворителя (1-октанол, фирмы Wako Pure Chemical Industries, Ltd., Japan) и 1,47 кг мочевины в емкости для хранения 101, нагретой до 120°C, с перекрытой линией 13, и смесь транспортировали в реактор с мешалкой 103 (внутренний объем: 80 л, снабженный перегородками), нагретый до 120°C. Затем подавали 0,87 кг органического амина в форме 3-аминометил-3,5,5-триметилциклогексиламина при скорости около 10 г/мин из емкости для хранения 102 в реактор с мешалкой 103 по линии 12 при перемешивании в реакторе с мешалкой 103. После завершения подачи 3-аминометил-3,5,5-три-метилциклогексиламина, перемешивание продолжали в течение около 2 часов и отбирали пробу реакционной жидкости. В результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что реакционная жидкость содержит около 7,87% по массе 3-(уреидометил)-3,5,5-триметилциклогексилмочевины. Кроме того, концентрация аммиака в реакционной жидкости составляла 7300 ppm. Добавляли 13,4 кг ароматического гидроксисоединения в форме п-додецилфенола из емкости для хранения 101 с получением гомогенного раствора. Открывали линию 13 и раствор транспортировали в емкость для хранения 104 по линии 13.
Стадии (R) и (D): Получение N-замещенной карбаминовой кислоты-O-алкилового эфира и извлечение мочевины
Продолжали использовать установку, показанную на фигуре 13.
Насадочную колонну 105, заполненную насадкой (Helipack No. 3), нагревали до 190°C. Реакционную жидкость, получаемую на стадии (A), подавали по линии 14, подсоединенной к насадочной колонне 105, при скорости около 1,1 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 15,1 кг. Реакционную жидкость извлекали в емкость для хранения 110 по линии 16, подсоединенной к нижней части насадочной колонны 105. Газофазный компонент подавали по линии 15, подсоединенной к верхней части насадочной колонны 105, в конденсатор 106 и подвергали конденсации, и образующийся жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 108 в емкость для хранения 109. При проведении анализа сконденсированного компонента, извлекаемого в емкость для хранения 109, с помощью 1H-ЯМР, было обнаружено, что сконденсированный компонент содержит 1-октанол и мочевину. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 8,80 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит 3-((1-октилокси)карбониламидометил)-3,5,5-три-метилциклогексилкарбаминовой кислоты (1-октиловый) эфир, и выход относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял около 95%. Концентрация аммиака в реакционной жидкости составляла 5,8 ppm.
Стадия (P): Реакция переэтерификации
Использовали установку, показанную на фигуре 16.
К реакционной жидкости, получаемой на описанной выше стадии, добавляли 0,5% по массе катализатора в форме дилаурата дибутилолова, и полученный раствор помещали в емкость для хранения 501. Насадочную колонну 502, заполненную насадкой (Helipack No. 3), нагревали до 260°C и создавали давление внутри колонны 26 кПа. Смесь в емкости для хранения 501 подавали по линии 51, подсоединенной к насадочной колонне 502, при скорости около 1,9 г/мин. Реакционную жидкость извлекали в емкость для хранения 505 по линии 54, подсоединенной к нижней части насадочной колонны 502. Газофазный компонент вводили в конденсатор 503 по линии 52, подсоединенной к верхней части насадочной колонны 502, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 507 в емкость для хранения 504. Количество реакционной жидкости, извлекаемой в емкость для хранения 505, составляло 18,2 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость является раствором, содержащим 3-((п-додецилфенилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (п-додецилфениловый) эфир, и выход относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял 89%.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 17.
Пленочный дистилляционный аппарат 602 (фирмы Kobelco Eco-Solutions Co., Ltd., Japan), имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в пленочном дистилляционном аппарате около 1,3 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в пленочный дистилляционный аппарат при скорости около 1080 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части пленочного дистилляционного аппарата 602, и извлекали в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в пленочный дистилляционный аппарат 602 по линии 63. Газообразный компонент, содержащий изофорон диизоцианат и п-додецилфенол, извлекали по линии 61, подсоединенной к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Газофазный компонент подавали по линии 69 в конденсатор 610 и подвергали конденсации и извлекали с помощью газо-жидкостного сепаратора 611 в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии, было обнаружено, что конденсат содержит около 99% по массе изофорон диизоцианата. Выход относительно органического амина (3-аминометил-3,5,5-триметилциклогексиламина) составлял около 83%.
Стадия (E): Получение эфира N-замещенной карбаминовой кислоты путем повторного использования смеси, получаемой в конденсаторе
При анализе концентрации аммиака в смеси, извлекаемой в емкость для хранения 109 на стадии (B) примера 4, было обнаружено, что она составляет 1300 ppm. Добавляли 7,57 кг 1-октанола и 0,70 кг мочевины к 9,4 кг смеси, затем транспортировали в реактор с мешалкой 103, и осуществляли такой же способ, как на стадии (A), используя 0,87 кг 3-аминометил-3,5,5-триметилциклогексиламина. Получали раствор, содержащий 6,3% по массе 3-(уреидометил)-3,5,5-триметилциклогексилмочевины. Осуществляли такой же способ, как на стадии (B, используя этот раствор вместо раствора стадии (A). Реакционная жидкость, извлекаемая в емкость для хранения 110, содержала 3-((3-метилбутилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (3-метилбутиловый) эфир, и выход 3-((3-метилбутилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (3-метилбутилового) эфира относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял около 95%.
[ПРИМЕР 6] ПОЛУЧЕНИЕ N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ-O-АРИЛОВОГО ЭФИРА С ПОМОЩЬЮ НАПРАВЛЕНИЯ 4)
Стадия (A): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 13.
Смешивали 33,5 кг растворителя (1-нонанола) и 3,34 кг мочевины в емкости для хранения 101, нагретой до 90°C, при перекрытой линии 13, и смесь транспортировали в реактор с мешалкой 103, нагретый до 90°C. Затем подавали 1,08 кг анилина при скорости около 12 г/мин из емкости для хранения 102 в реактор с мешалкой 603 по линии 12 при перемешивании в реакторе с мешалкой 103. После завершения подачи анилина перемешивание продолжали в течение около 28 часов и отбирали пробу реакционной жидкости. В результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что реакционная жидкость содержит около 5,6% по массе фенилмочевины. Концентрация аммиака в реакционной жидкости составляла 7900 ppm. Непрореагировавшие аминогруппы обнаружены не были. После реакции добавляли 25,9 кг ароматического гидроксисоединения в форме 2-фенилфенола с получением смеси. Отношение числа молекул спирта к числу уреидных групп в смеси составляло 10,1. Открывали линию 63, и смесь транспортировали в емкость для хранения 604 по линии 63.
Стадии (R) и (D): Получение N-замещенной карбаминовой кислоты моно(-O-R 2 эфира)
Насадочную колонну 105, заполненную насадкой (Helipack No. 3), нагревали до 210°C и создавали давление внутри колонны 50 кПа. Реакционную жидкость, получаемую на стадии (A), подавали по линии 14, подсоединенной к насадочной колонне 105, при скорости около 1,2 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 35,8 кг. Реакционную жидкость извлекали в емкость для хранения 110 по линии 16, подсоединенной к нижней части насадочной колонны 105. Газофазный компонент вводили в конденсатор 106 по линии 15, подсоединенной к верхней части насадочной колонны 105, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 108 в емкость для хранения 109. При анализе сконденсированного компонента, извлекаемого в емкость для хранения 109, с помощью 1H-ЯМР было обнаружено, что сконденсированный компонент содержит мочевину и 1-нонанол. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 18,9 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N-фенилкарбаминовой кислоты (нониловый эфир), и выход N-фенилкарбаминовой кислоты (нониловый эфир) относительно анилина составлял около 91%.
Стадия (P): Получение N-замещенной карбаминовой кислоты моно(-O-арилового эфира) путем реакции переэтерификации
Использовали установку, показанную на фигуре 16.
К смеси, получаемой на стадии (B), добавляли 0,5% по массе катализатора в форме дилаурата дибутилолова и помещали в емкость для хранения 501. Насадочную колонну 502, заполненную насадкой (Helipack No. 3) и имеющую внутренний диаметр 20 мм, нагревали до 260°C и создавали давление внутри колонны 26 кПа. Реакционную жидкость, получаемую на стадии (A), подавали по линии 51, подсоединенной к насадочной колонне 105, при скорости около 1,9 г/мин. Реакционную жидкость извлекали в емкость для хранения 505 по линии 54, подсоединенной к нижней части насадочной колонны 502. Газофазный компонент вводили в конденсатор 503 по линии 52, подсоединенной к верхней части насадочной колонны 502, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 507 в емкость для хранения 504. Количество реакционной жидкости, извлекаемой в емкость для хранения 505, составляло 26,4 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость является раствором, содержащим N-фенилкарбаминовой кислоты (2-фенилфениловый) эфир, и выход N-фенилкарбаминовой кислоты (2-фенилфенилового) эфира относительно анилина составлял около 89%.
Стадия (C): Конденсация N-замещенной карбаминовой кислоты моно(-O-арилового эфира)
Использовали установку, показанную на фигуре 15.
Реакционную жидкость, извлекаемую в емкость для хранения 505 на стадии (B), помещали в реактор с мешалкой 408. Реактор с мешалкой 408 нагревали до 160°C и создавали внутри давление 1 кПа, затем отгоняли 2-фенилфенол. Подавали 2-фенилфенол по линии 44 в конденсатор 405 и подвергали конденсации и извлекали в емкость для хранения 407. Затем добавляли 2,04 кг метилаля из емкости для хранения 400, 1,94 кг нитробензола из емкости для хранения 401 и 1,02 кг серной кислоты из емкости для хранения 402 в реактор с мешалкой 408, затем нагревали в течение 24 часов при 90°C при перемешивании в реакторе с мешалкой 408. Затем отгоняли растворитель и непрореагировавшие вещества путем поддержания температуры реактора с мешалкой 408 при 90°C и снижения внутри давления до 1 кПа. При анализе образовавшегося соединения с помощью жидкостной хроматографии, было обнаружено, что оно является смесью, содержащей около 53% по массе N,N'-(метандиилдифенил)-бис(карбаминовой кислоты (2-фенилфенилового) эфира).
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 18.
Пленочный дистилляционный аппарат 1002 (фирмы Kobelco Eco-Solutions Co., Ltd., Japan), имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 260°C и создавали давление в пленочном дистилляционном аппарате около 1,5 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 404 на стадии (C), помещали в емкость для хранения 1001 и направляли в пленочный дистилляционный аппарат при скорости около 1200 г/час по линии A1. Жидкий компонент извлекали по линии A4, подсоединенной к нижней части пленочного дистилляционного аппарата 1002, в емкость для хранения 1003. Жидкий компонент, извлекаемый в емкость для хранения 1003, опять подавали в пленочный дистилляционный аппарат 1002 по линии A3. Газообразный компонент извлекали по линии A4, подсоединенной к верхней части пленочного дистилляционного аппарата 1002. Газообразный компонент вводили в ректификационную колонну 1004, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 1009 по линии A8, подсоединенной к части ректификационной колонны 1004 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Жидкофазный компонент подавали в ректификационную колонну 1014 по линии A12, подсоединенной к части ректификационной колонны 1009 ниже линии подачи сырья, и затем подвергали ректификационному разделению.
Газофазный компонент извлекали по линии A13, подсоединенной к верхней части ректификационной колонны 1014, и конденсировали в конденсаторе 1015, и конденсат извлекали в емкость для хранения 1019. При анализе конденсата с помощью 1H-ЯМР, было обнаружено, что он является раствором, содержащим около 99% по массе 4,4'-дифенилметан диизоцианата (MDI). Выход относительно анилина составлял около 54%.
Стадия (E): Получение эфира N-замещенной карбаминовой кислоты путем повторного использования смеси, получаемой в конденсаторе
При анализе содержания аммиака в смеси, извлекаемой в емкость для хранения 109 на стадии (R) примера 5, было обнаружено, что оно составляет 1500 ppm. Добавляли 11,4 кг 1-нонанола и 1,47 кг мочевины к 14,7 кг смеси, затем транспортировали в реактор с мешалкой 603, и осуществляли такой же способ, как на стадии (A), используя 1,08 кг анилина. Получали раствор, содержащий около 6,8% по массе фенилмочевины. Осуществляли такой же способ, как на стадии (B), с использованием этого раствора вместо раствора стадии (A). Выход N-фенилкарбаминовой кислоты (нонилового эфира) в реакционной жидкости, извлекаемой в емкость для хранения 110, относительно анилина составлял около 91%.
[ПРИМЕР 7] ПОЛУЧЕНИЕ N-ЗАМЕЩЕННОЙ КАРБАМИНОВОЙ КИСЛОТЫ-O-АРИЛОВОГО ЭФИРА С ПОМОЩЬЮ НАПРАВЛЕНИЯ 5)
Стадия (A): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 13.
Смешивали 25,4 кг растворителя (1-гептанола) и 3,50 кг мочевины в емкости для хранения 101, нагретой до 90°C, при перекрытой линии 13, и смесь транспортировали в реактор с мешалкой 103, нагретый до 90°C. Затем подавали 1,13 кг анилина при скорости около 18 г/мин из емкости для хранения 102 в реактор с мешалкой 103 по линии 12 при перемешивании в реакторе с мешалкой 603. После завершения подачи анилина перемешивание продолжали в течение 28 часов и отбирали пробу реакционной жидкости. В результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что реакционная жидкость содержит около 7,4% по массе фенилмочевины. Концентрация аммиака в реакционной жидкости составляла 8300 ppm. Непрореагировавшие аминогруппы обнаружены не были. Добавляли к реакционной жидкости 24,2 кг гидроксисоединения в форме 2,4-ди-трет-амилфенола (фирмы Tokyo Chemical Industry Co., Ltd., Japan) с получением смеси. Отношение числа молекул спирта к числу уреидных групп в смеси составляло 9,0.
Открывали линию 63 и смесь транспортировали в емкость для хранения 604 по линии 63.
Стадии (R) и (D): Получение N-замещенной карбаминовой кислоты моно(-O-алкилового эфира)
Насадочную колонну 105, заполненную насадкой (Helipack No. 3) и имеющую диаметр 40 мм, нагревали до 190°C и создавали давление внутри колонны 50 кПа. Реакционную жидкость, получаемую на стадии (A), подавали по линии 14, подсоединенной к насадочной колонне 105, при скорости около 1,0 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 28,0 кг. Реакционную жидкость извлекали в емкость для хранения 110 по линии 16, подсоединенной к нижней части насадочной колонны 105. Газофазный компонент подавали по линии 15, подсоединенной к верхней части насадочной колонны 105, в конденсатор 106 и подвергали конденсации, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 108 в емкость для хранения 109. При анализе сконденсированного компонента, извлекаемого в емкость для хранения 109, с помощью 1H-ЯМР было обнаружено, что сконденсированный компонент содержит мочевину и 1-гептанол. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 13,8 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N-фенилкарбаминовой кислоты (1-гептиловый) эфир, и выход относительно анилина составлял около 90%.
Стадия (C): Конденсация N-замещенной карбаминовой кислоты моно(-O-алкилового эфира)
Использовали установку, показанную на фигуре 15.
Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (R), помещали в реактор с мешалкой 408. Реактор с мешалкой 408 нагревали до 160°C и создавали внутри давление 1 кПа, затем отгоняли 1-гептанол. Подавали 1-гептанол по линии 44 в конденсатор 405 и подвергали конденсации и извлекали в емкость для хранения 407. Затем добавляли 1,30 кг метилаля из емкости для хранения 400, 7,34 кг нитробензола из емкости для хранения 401 и 1,33 кг серной кислоты из емкости для хранения 402 в реактор с мешалкой 408, затем нагревали в течение 10 часов при 100°C при перемешивании в реакторе с мешалкой 408. Затем отгоняли растворитель и непрореагировавшие вещества путем поддержания температуры реактора с мешалкой 408 при 100°C и снижения внутри давления до приблизительно 1 кПа. При анализе образовавшегося соединения с помощью жидкостной хроматографии было обнаружено, что оно является смесью, содержащей около 63% по массе N,N'-(метандиилдифенил)-бис(карбаминовой кислоты октилового эфира). Затем добавляли в эту смесь 24,2 кг ароматического гидроксисоединения в форме 2,4-ди-трет-амилфенола с получением смеси.
Стадия (P): Получение N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции переэтерификации
Применяли установку, показанную на фигуре 16.
Добавляли 0,5% по массе катализатора в форме дилаурата дибутилолова к смеси, получаемой на стадии (C), и помещали в емкость для хранения 501. Насадочную колонну 502, заполненную насадкой (Helipack No. 3) и имеющую внутренний диаметр 20 мм, нагревали до 250°C и создавали давление внутри колонны 20 кПа. Реакционную жидкость, получаемую на стадии (A), подавали по линии 51, подсоединенной к насадочной колонне 502, при скорости около 1,3 г/мин. Реакционную жидкость извлекали в емкость для хранения 505 по линии 54, подсоединенной к нижней части насадочной колонны 502. Газофазный компонент вводили в конденсатор 503 по линии 52, подсоединенной к верхней части насадочной колонны 502, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 507 в емкость для хранения 504. Количество реакционной жидкости, извлекаемой в емкость для хранения 505, составляло 25,0 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость является раствором, содержащим N,N'-(метандиилдифенил)-бис(карбаминовой кислоты (2,4-ди-трет-амилфениловый) эфир).
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 18.
Пленочный дистилляционный аппарат 1002 (фирмы Kobelco Eco-Solutions Co., Ltd., Japan), имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 260°C и создавали давление в пленочном дистилляционном аппарате около 1,5 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 404 на стадии (C), помещали в емкость для хранения 1001 и подавали в пленочный дистилляционный аппарат при скорости около 1200 г/час по линии A1. Жидкий компонент извлекали по линии A4, подсоединенной к нижней части пленочного дистилляционного аппарата 1002, в емкость для хранения 1003. Жидкий компонент, извлекаемый в емкость для хранения 1003, опять подавали в пленочный дистилляционный аппарат 1002 по линии A3. Газообразный компонент извлекали по линии A4, подсоединенной к верхней части пленочного дистилляционного аппарата 1002. Газообразный компонент вводили в ректификационную колонну 1004, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 1009 по линии A8, подсоединенной к части ректификационной колонны 1004 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Жидкофазный компонент подавали в ректификационную колонну 1014 по линии A12, подсоединенной к части ректификационной колонны 1009 ниже линии подачи сырья, и затем подвергали ректификационному разделению.
Газофазный компонент извлекали по линии A13, подсоединенной к верхней части ректификационной колонны 1014, и конденсировали в конденсаторе 1015, и конденсат извлекали в емкость для хранения 1019. При анализе конденсата с помощью 1H-ЯМР было обнаружено, что он является раствором, содержащим около 99% по массе 4,4'-дифенилметан диизоцианата (MDI). Выход относительно анилина составлял около 47%.
Стадия (E): Получение эфира N-замещенной карбаминовой кислоты путем повторного использования смеси, получаемой в конденсаторе
При анализе содержания аммиака с смеси, извлекаемой в емкость для хранения 109 на стадии (B) примера 6, было обнаружено, что оно составляет 900 ppm. Добавляли к смеси 9,48 кг 1-гептанола и 1,54 кг мочевины, затем транспортировали в реактор с мешалкой 603 и осуществляли такой ж способ, как на стадии (A), используя 1,12 кг анилина. Получали раствор, содержащий около 7,4% по массе фенилмочевины. Осуществляли такой же способ, как на стадии (B), используя этот раствор вместо раствора стадии (A). Выход N-фенилкарбаминовой кислоты (гептилового эфира) в реакционной жидкости, извлекаемой в емкость для хранения 110, относительно анилина составлял около 90%.
[ПРИМЕРЫ 8-30]
Осуществляли такой же способ, как в примере 1, но изменяя используемые соединения и условия реакции. Соединения и условия реакции, используемые на стадии (A) примеров 8-30, вместе с результатами приведены в таблицах 2 и 3. Кроме того, соединения и условия реакции, используемые на стадиях (B) и (D) примеров 8-30, вместе с результатами приведены в таблицах 4 и 5. Кроме того, соединения и условия реакции, используемые на стадии (F) примеров 8-30, вместе с результатами приведены в таблицах 6 и 7. Несмотря на то, что "фигура 17" и "фигура 18" указаны в колонке "чертеж установки" в таблице 12 для стадии (F), "фигура 17" указывает, что был осуществлен такой же способ, как на стадии (F) примера 1, но с использованием установки, показанной на фигуре 17. С другой стороны, "фигура 18" указывает, что был осуществлен такой же способ, как на стадии (F) примера 4, но с использованием установки, показанной на фигуре 18. Кроме того, соединения и условия реакции, используемые на стадии (E) примеров 8-30, вместе с результатами приведены в таблицах 8 и 9. Кроме того, условия реакции и результаты для примера 1 также приведены в таблицах 2-9 для разъяснения соответствия с описанием примера 1.
Кроме того, в таблицах примеров используются следующие сокращения.
HDA: гексаметилендиамин
IPDA: 3-аминометил-3,5,5-триметилциклогексиламин
TDA: 2,4-толуолдиамин
MDA: 4,4'-метилендианилин
H-MDA: 4,4'-метиленди(циклогексиламин)
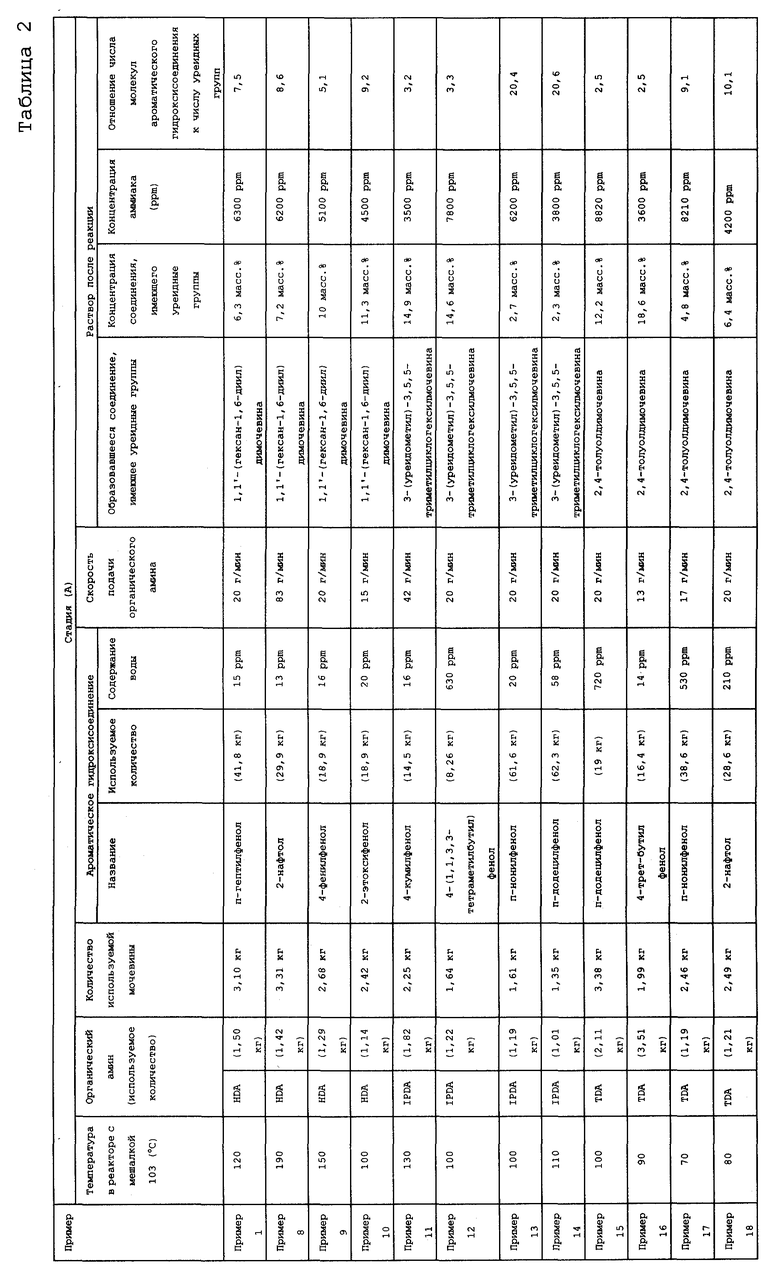
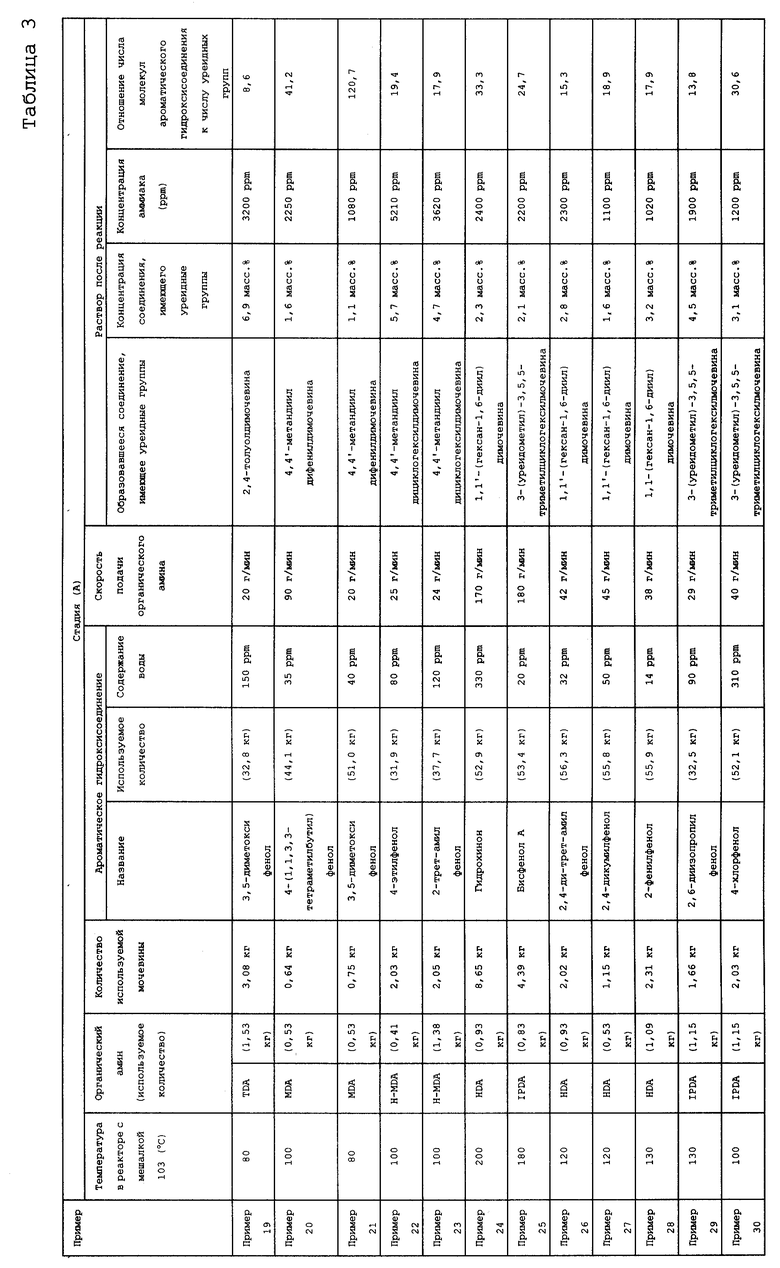
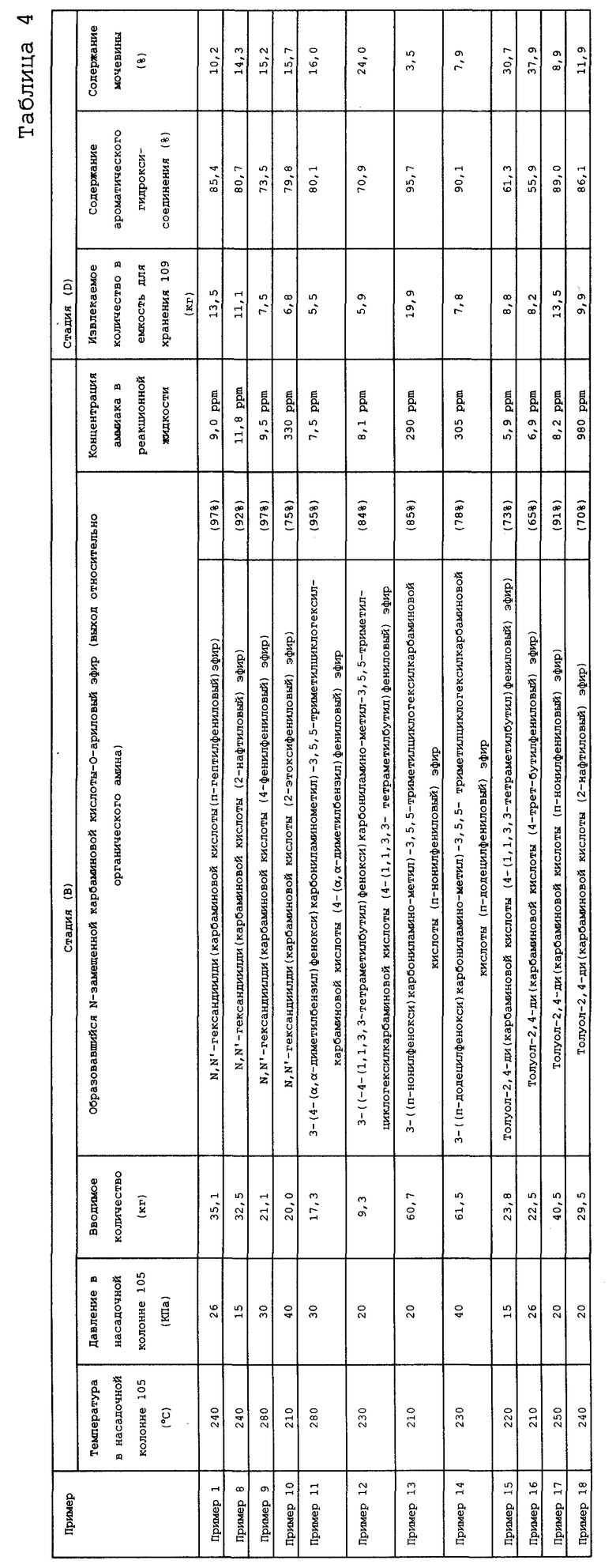
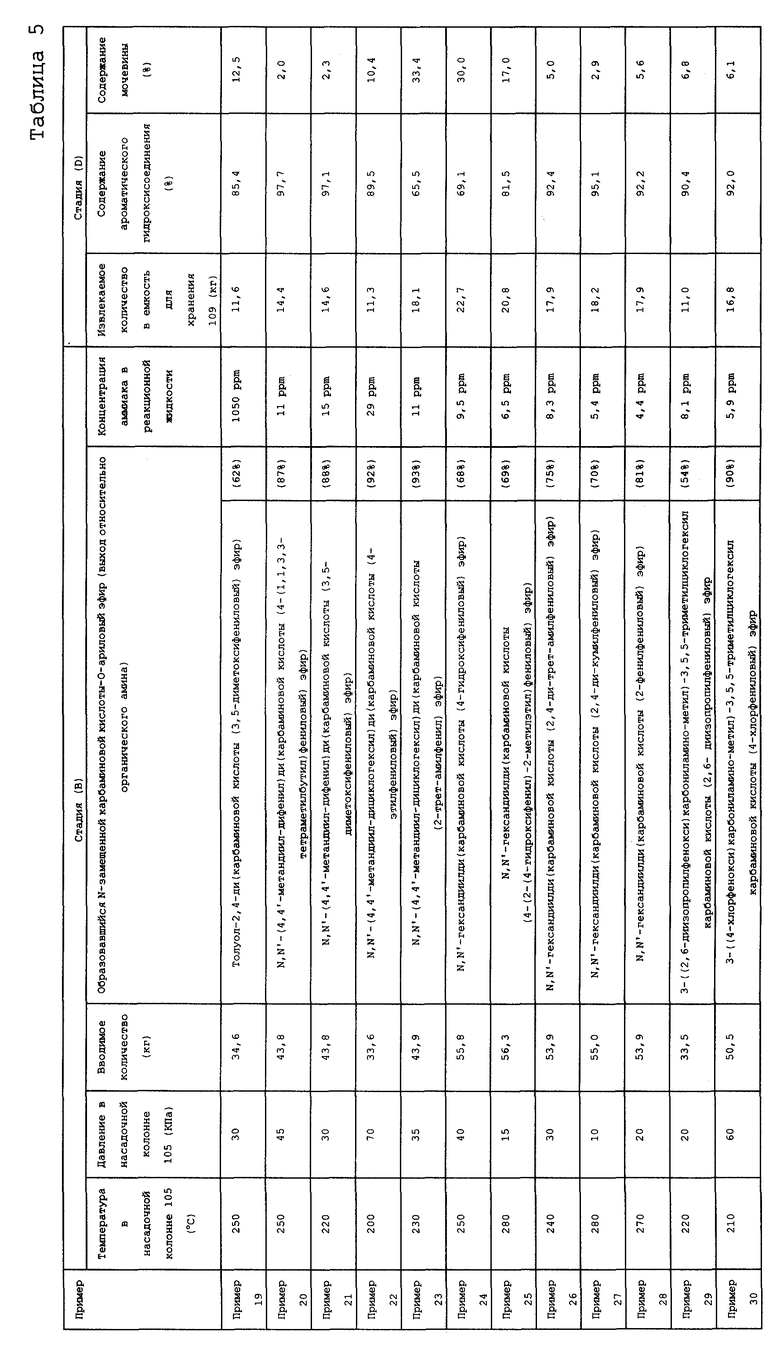
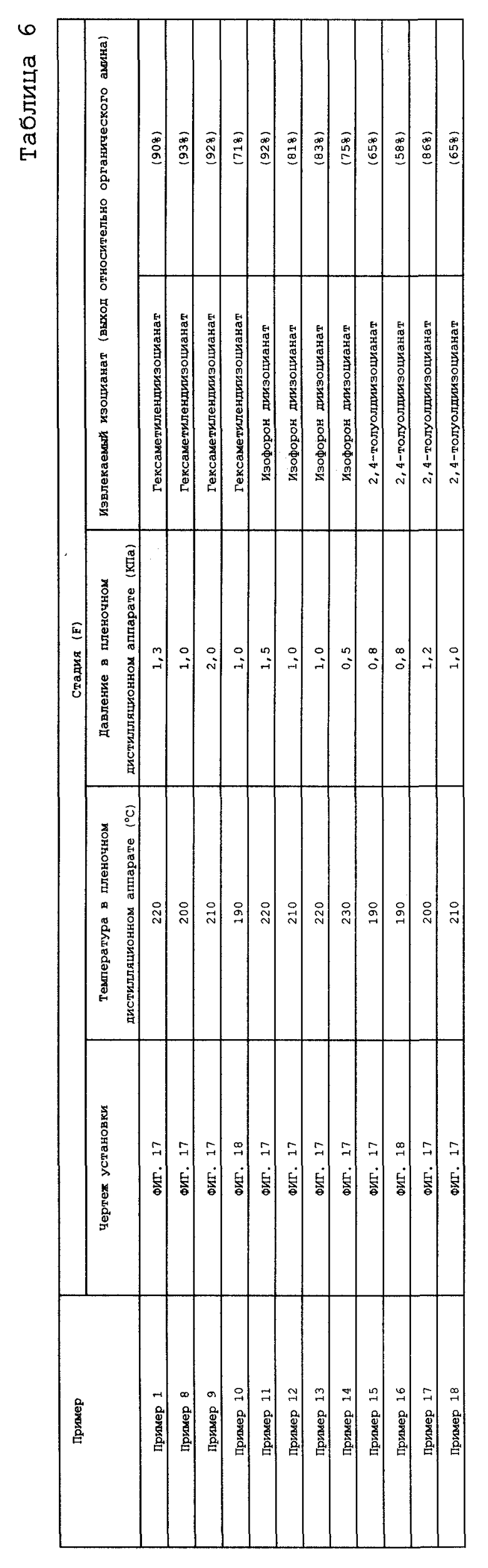
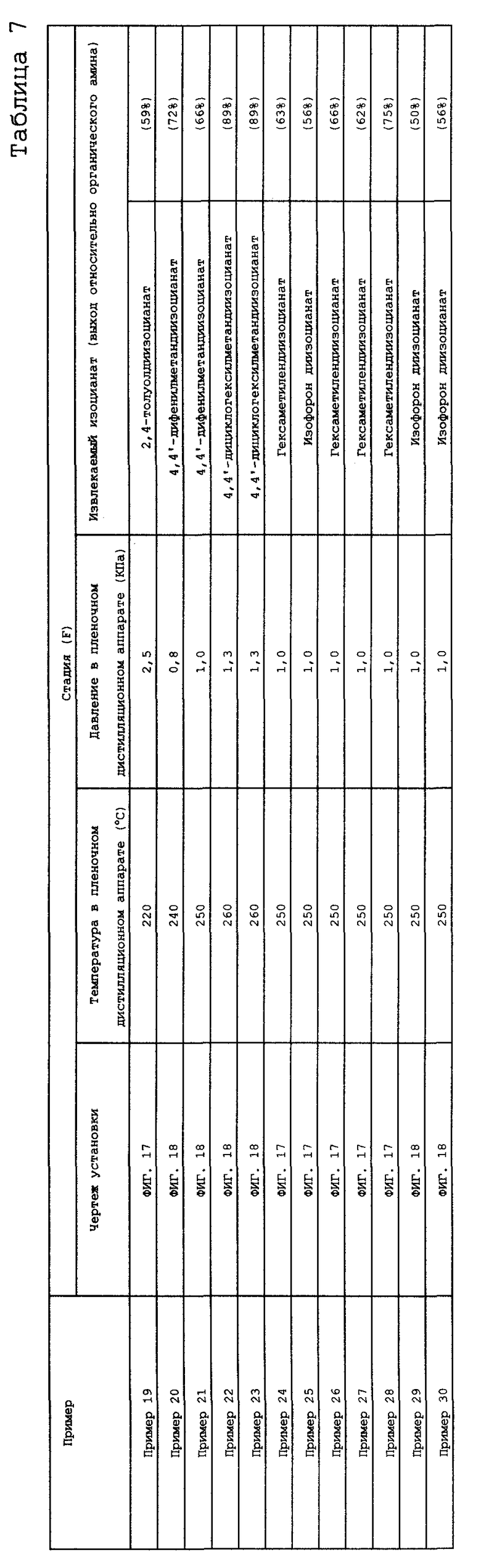
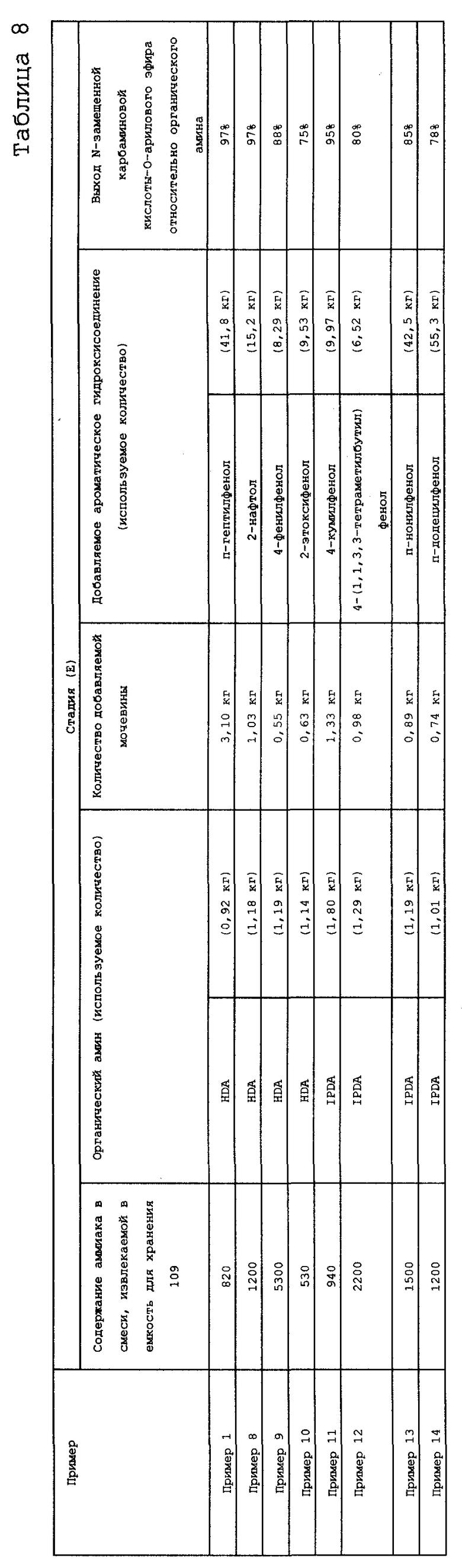
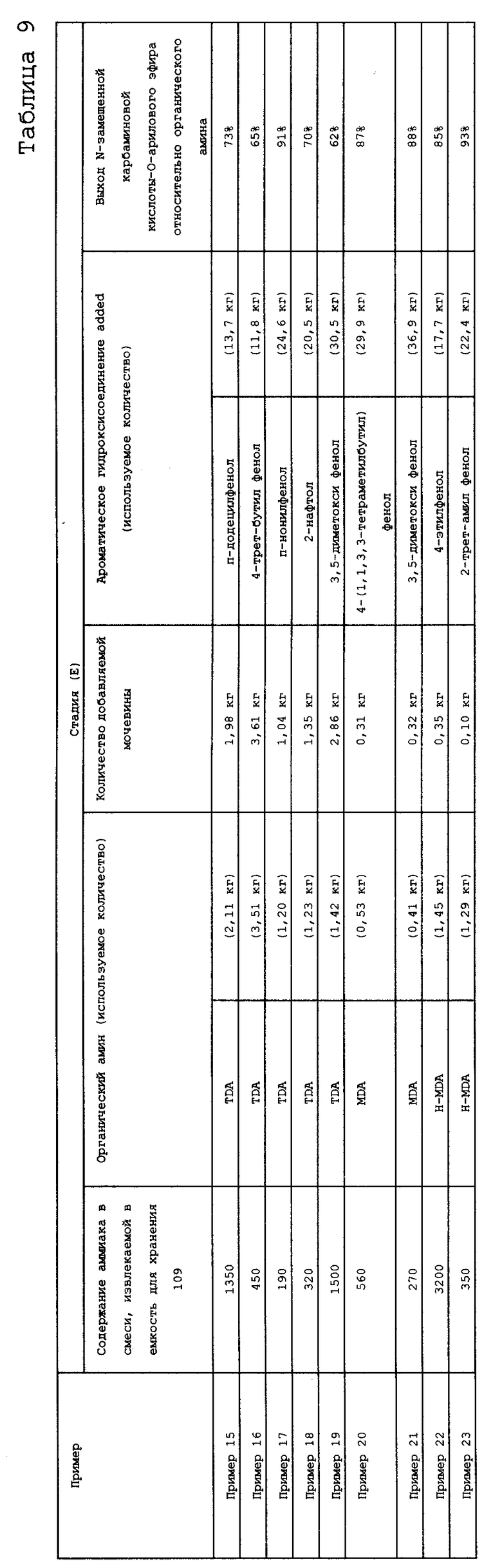
[ПРИМЕРЫ 31-42]
Осуществляли такой же способ, как в примере 2, но изменяя используемые соединения и условия реакции. Соединения и условия реакции, используемые на стадии (A) примеров 31-42, вместе с результатами приведены в таблице 10. Кроме того, соединения и условия реакции, используемые на стадии (D) примеров 21-32, вместе с результатами приведены в таблице 11. Соединения и условия реакции, используемые на стадиях (B) и (F) примеров 26-37, вместе с результатами приведены в таблице 12. Несмотря на то, что "фигура 17" и "фигура 18" указаны в колонке "чертеж установки" для стадии (F), "фигура 17" указывает, что был осуществлен такой же способ, как на стадии (F) примера 1, с использованием установки, показанной на фигуре 17. С другой стороны, "фигура 18" указывает, что был осуществлен такой же способ, как на стадии (F) примера 4, с использованием установки, показанной на фигуре 18. Кроме того, соединения и условия реакции, используемые на стадии (E) примеров 31-42, вместе с результатами приведены в таблице 13.
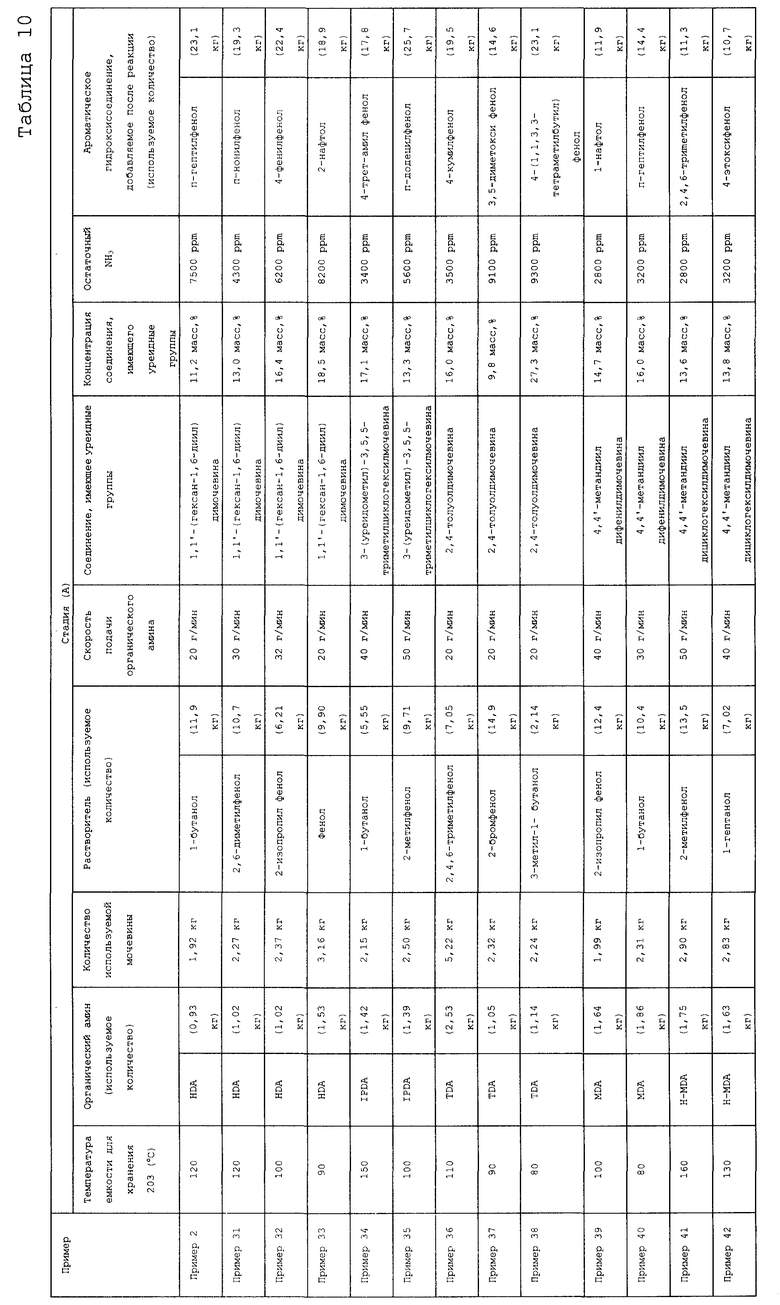
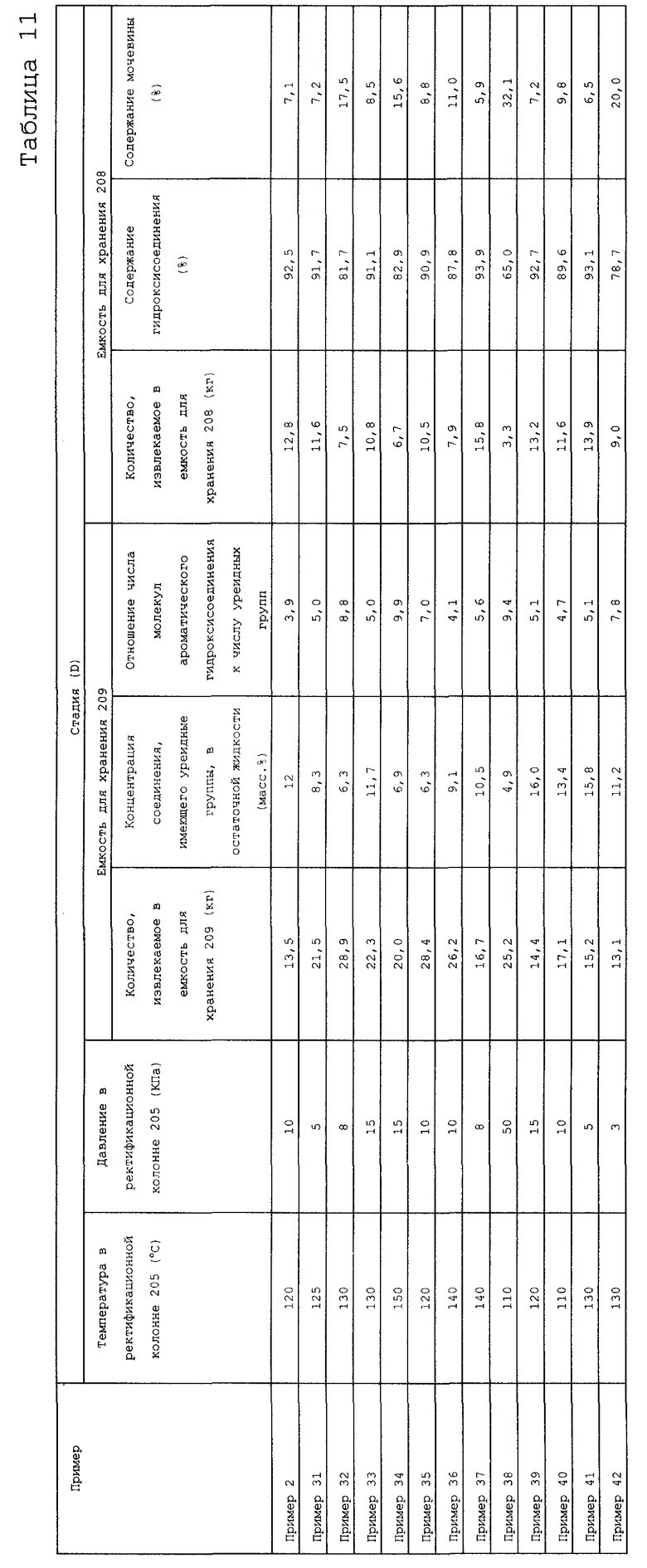
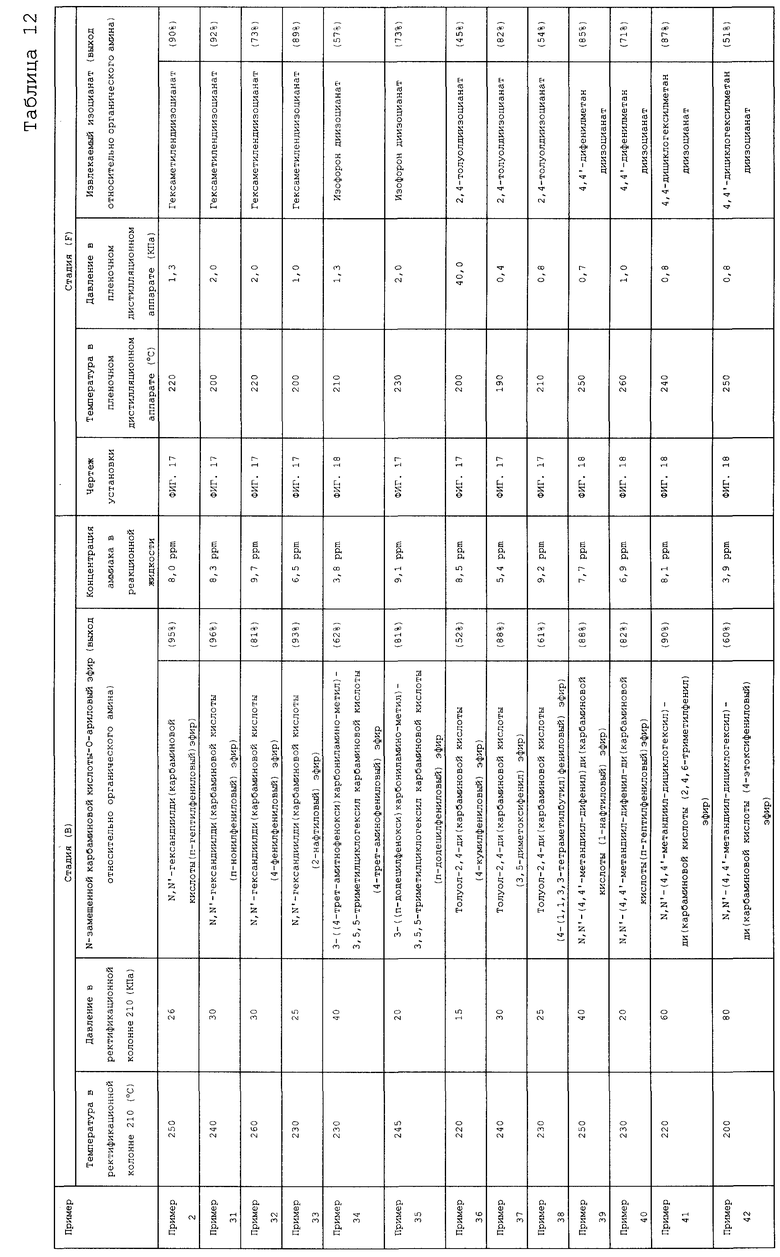
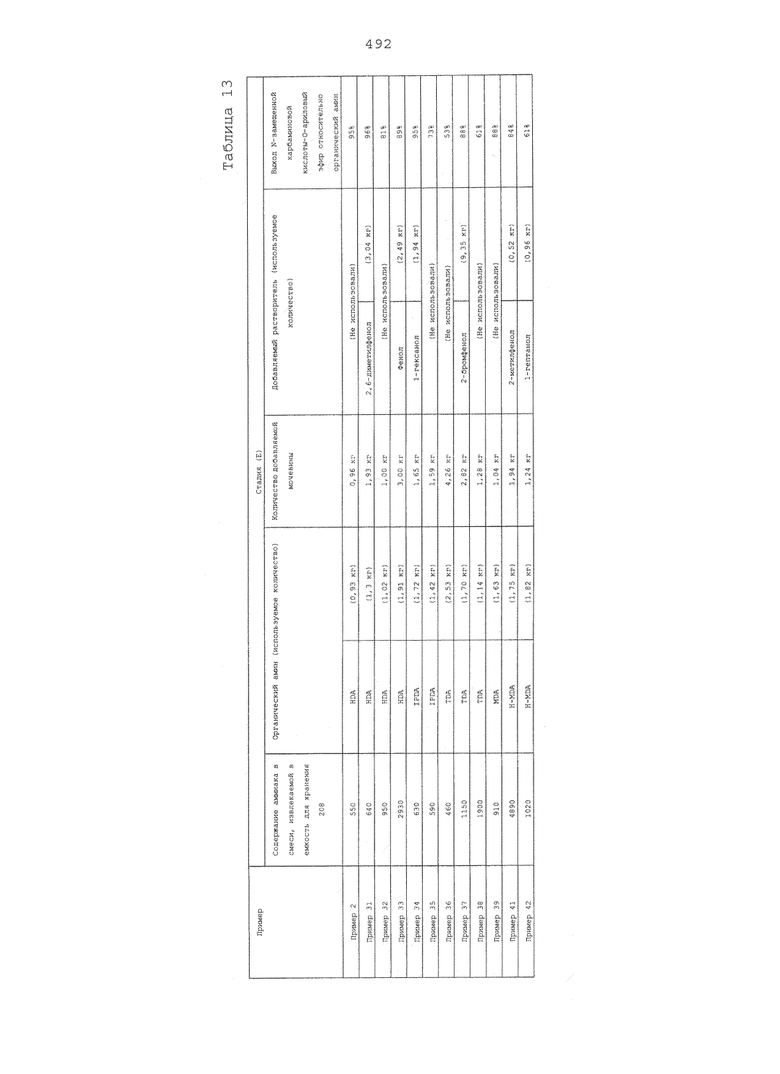
[ПРИМЕРЫ 43-49]
Осуществляли такой же способ, как в примере 3, но изменяя используемые соединения и условия реакции. Соединения и условия реакции, используемые на стадии (A) примеров 43-49, вместе с результатами приведены в таблице 14. Кроме того, соединения и условия реакции, используемые на стадиях (B) и (D) примеров 43-49, вместе с результатами приведены в таблице 15. Несмотря на то, что "фигура 17" и "фигура 18" указаны в колонке "чертеж установки" в таблице 15 для стадии (F), "фигура 17" указывает, что был осуществлен такой же способ, как на стадии (F) примера 1, с использованием установки, показанной на фигуре 17. С другой стороны, "фигура 18" указывает, что был осуществлен такой же способ, как на стадии (F) примера 4, с использованием установки, показанной на фигуре 18. Кроме того, соединения и условия реакции, используемые на стадии (E) примеров 43-49, вместе с результатами приведены в таблице 16.
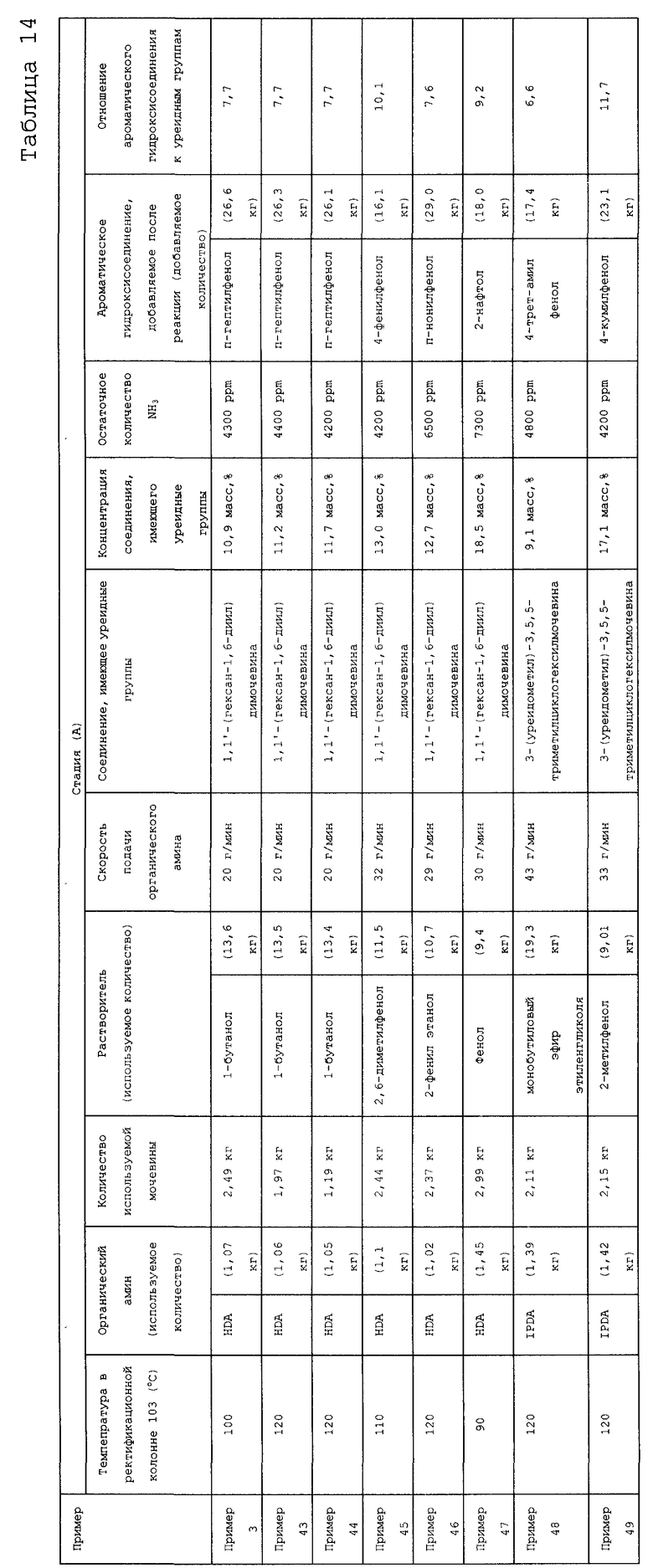
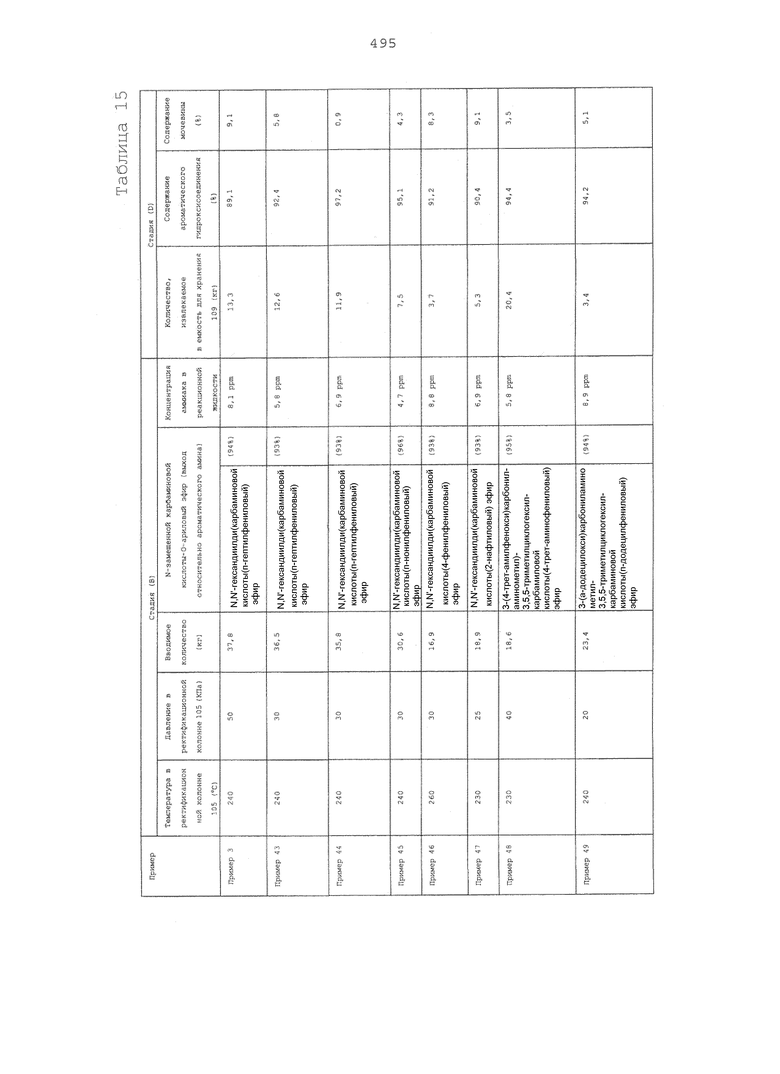
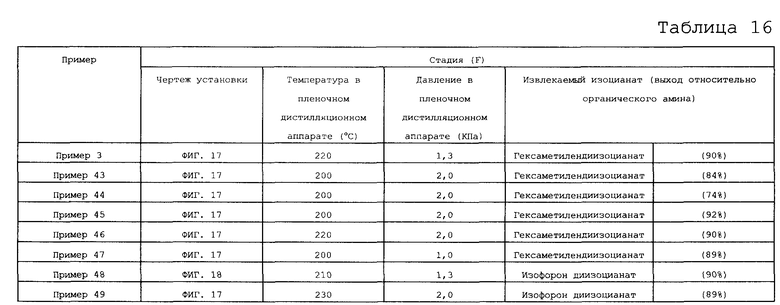
[ПРИМЕРЫ 50-52]
Осуществляли такой же способ, как в примере 4, но изменяя используемые соединения и условия реакции. Соединения и условия реакции, используемые на стадии (A) примеров 50-52, вместе с результатами приведены в таблице 17. Кроме того, соединения и условия реакции, используемые на стадиях (B) и (D) примеров 50-52, вместе с результатами приведены в таблице 18. Соединения и условия реакции, используемые на стадии (C) примеров 50-52, вместе с результатами приведены в таблице 19. Условия реакции стадии (F) примеров 50-52 приведены в таблице 20. Кроме того, описание "фигуры 18" в колонке "чертеж установки" в таблице 20 указывает, что установку, показанную на фигуре 18, использовали для стадии (F).


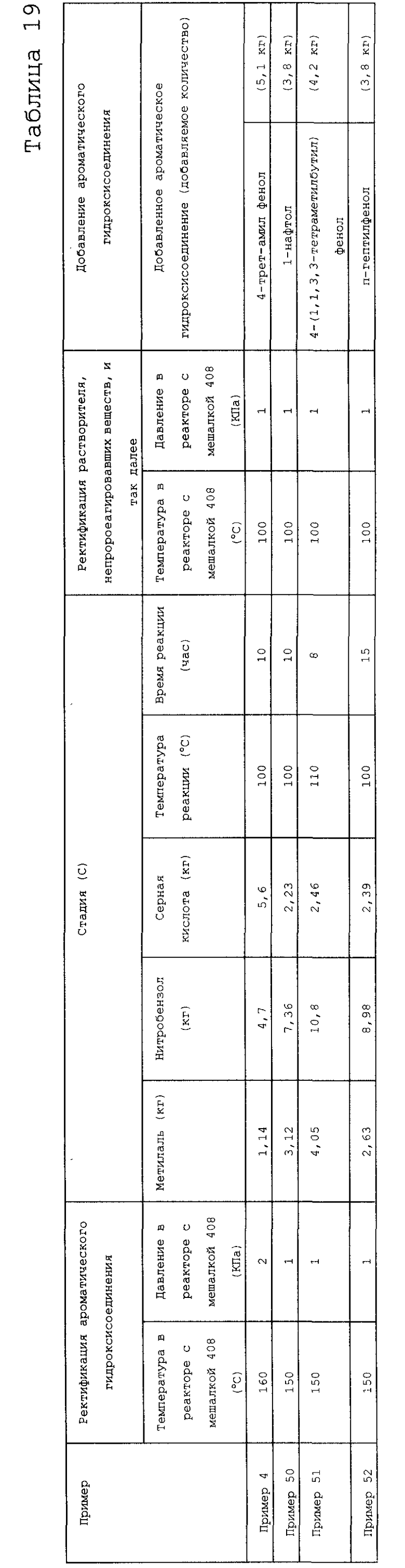
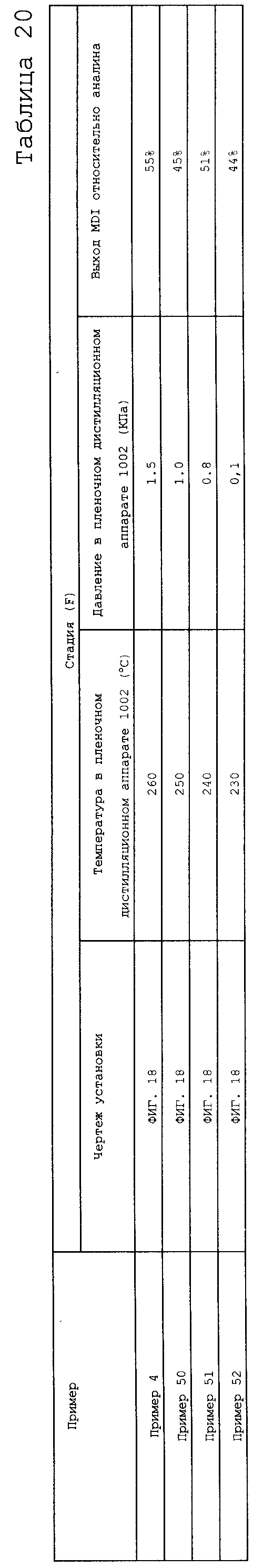
[ПРИМЕРЫ 53-67]
Осуществляли такой же способ, как в примере 5, но изменяя используемые соединения и условия реакции. Соединения и условия реакции, используемые на стадии (A) примеров 53-67, вместе с результатами приведены в таблицах 21 и 22. Кроме того, соединения и условия реакции, используемые на стадиях (R) и (D) примеров 53-67, вместе с результатами приведены в таблицах 23 и 24. Соединения и условия реакции, используемые на стадиях (P) и (F) примеров 53-67, вместе с результатами приведены в таблицах 25 и 26. Несмотря на то, что "фигура 17" и "фигура 18" указаны в колонке "чертеж установки" в таблицах 25 и 26 для стадии (F), "фигура 17" указывает, что был осуществлен такой же способ, как на стадии (F) примера 1 с использованием установки, показанной на фигуре 17. С другой стороны, "фигура 18" указывает, что был осуществлен такой же способ, как на стадии (F) примера 4, с использованием установки, показанной на фигуре 18. Кроме того, соединения и условия реакции, используемые на стадии (E) примеров 53-67, вместе с результатами приведены в таблице 27.
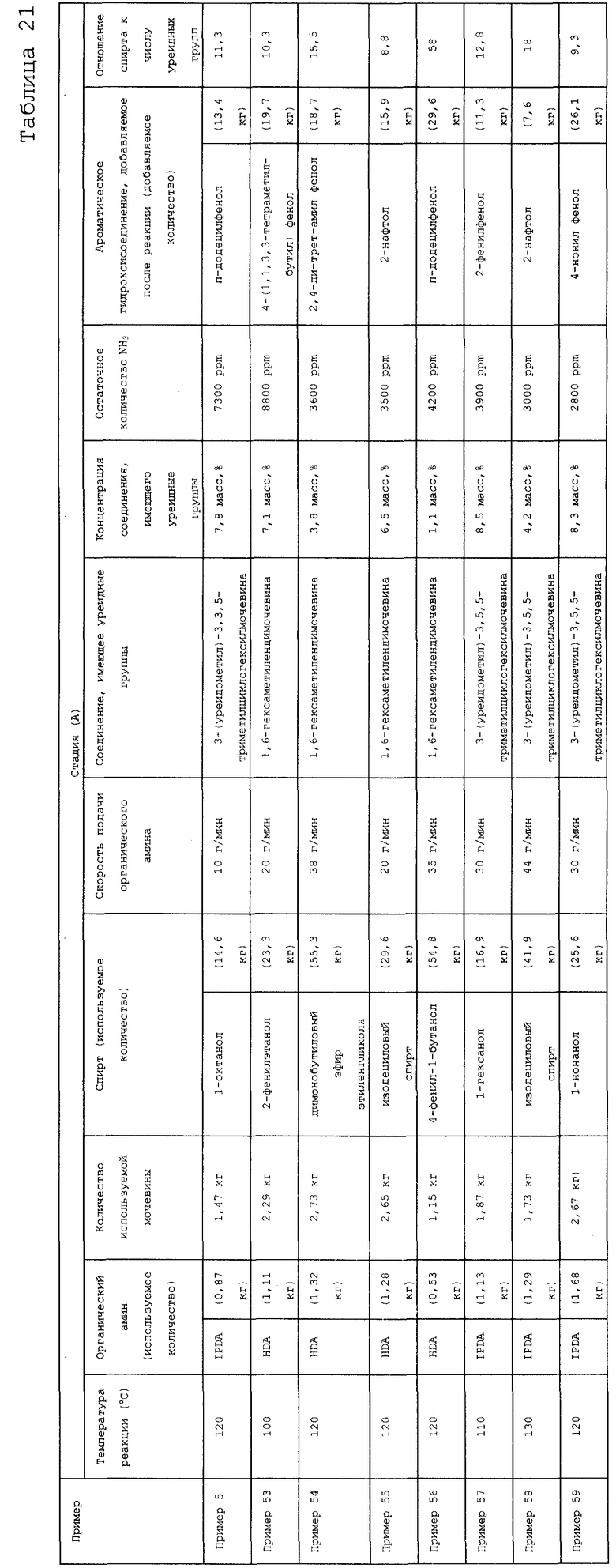
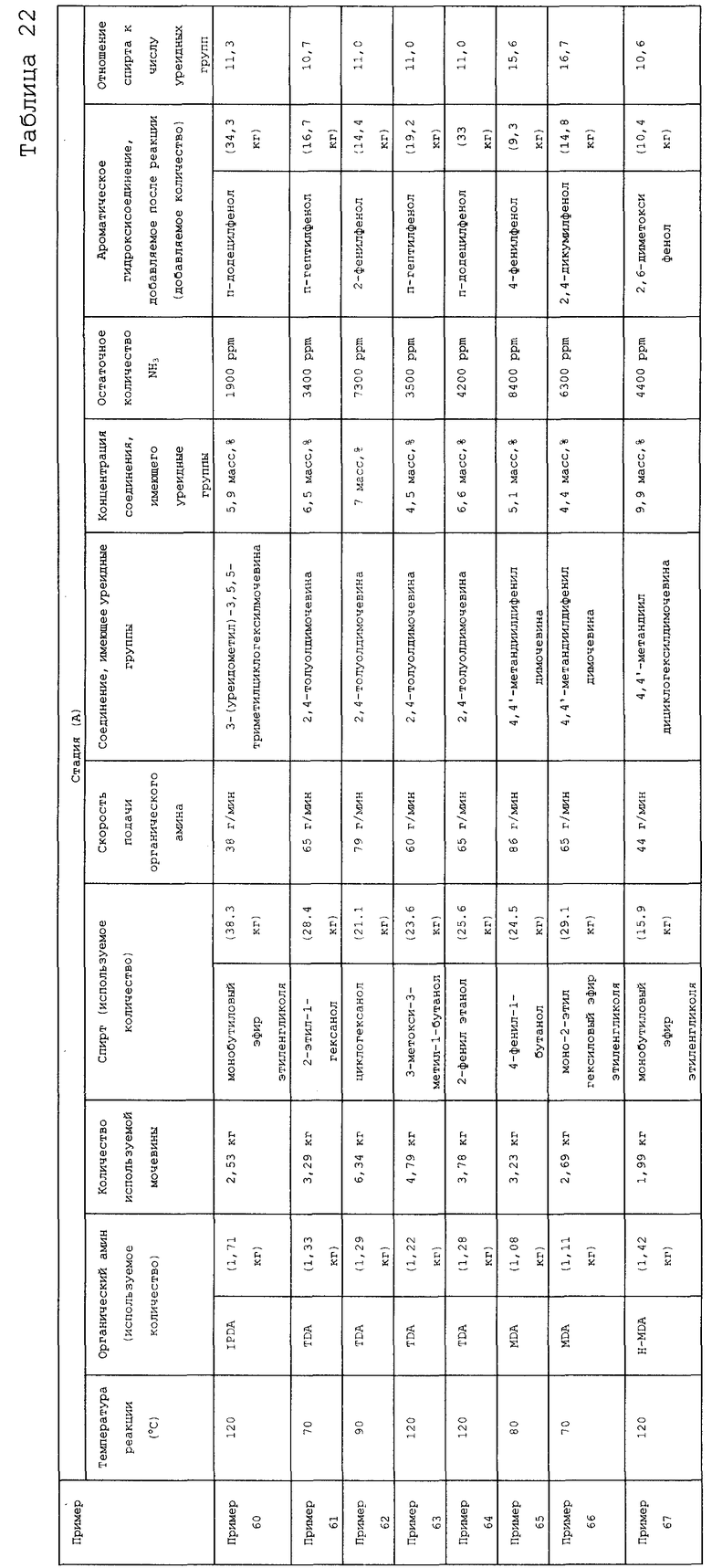
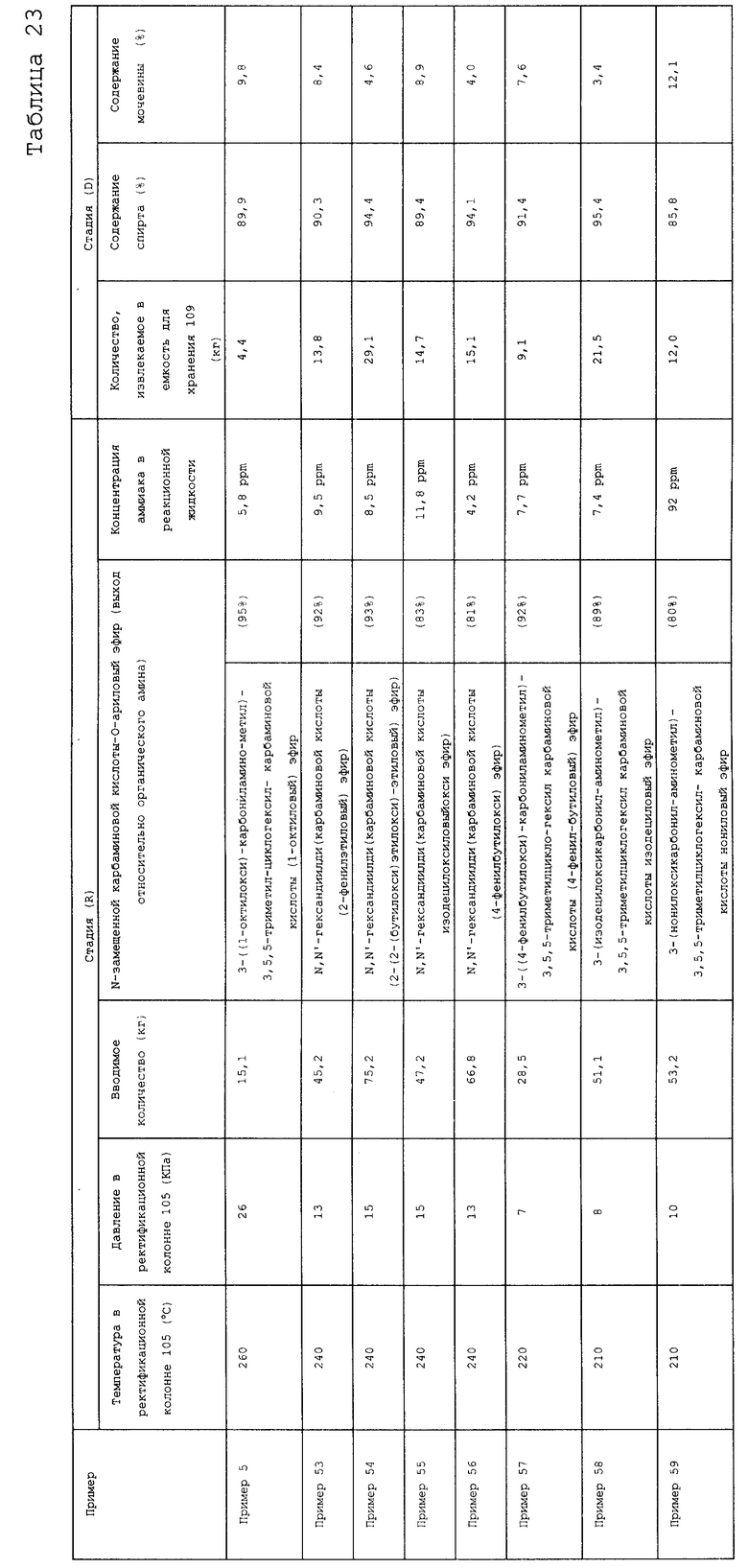
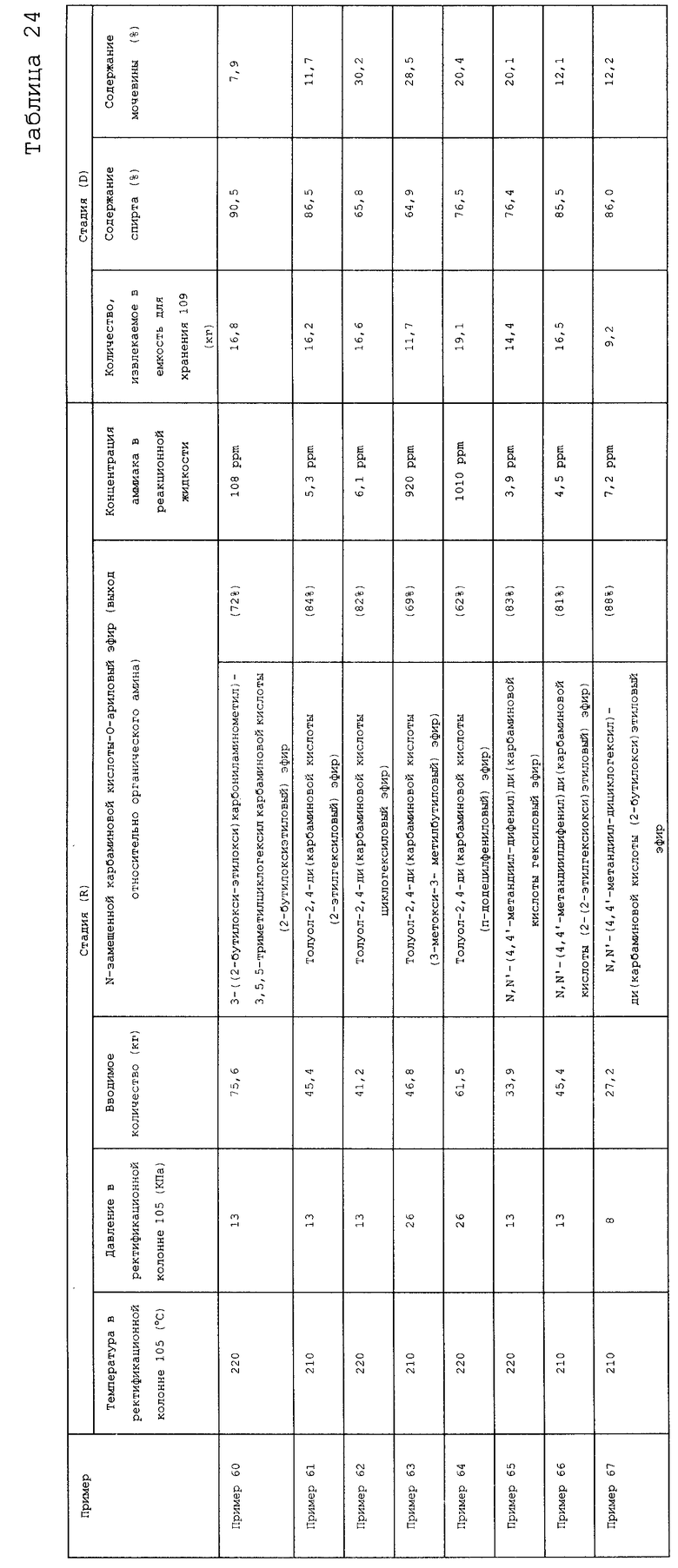
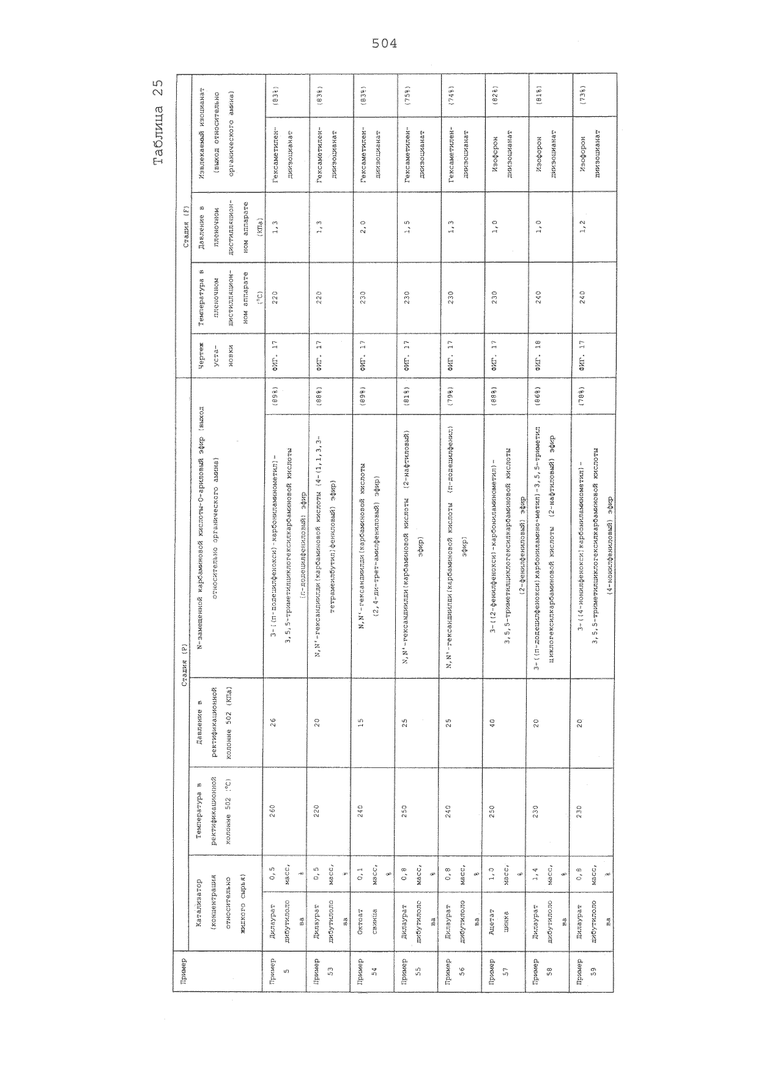
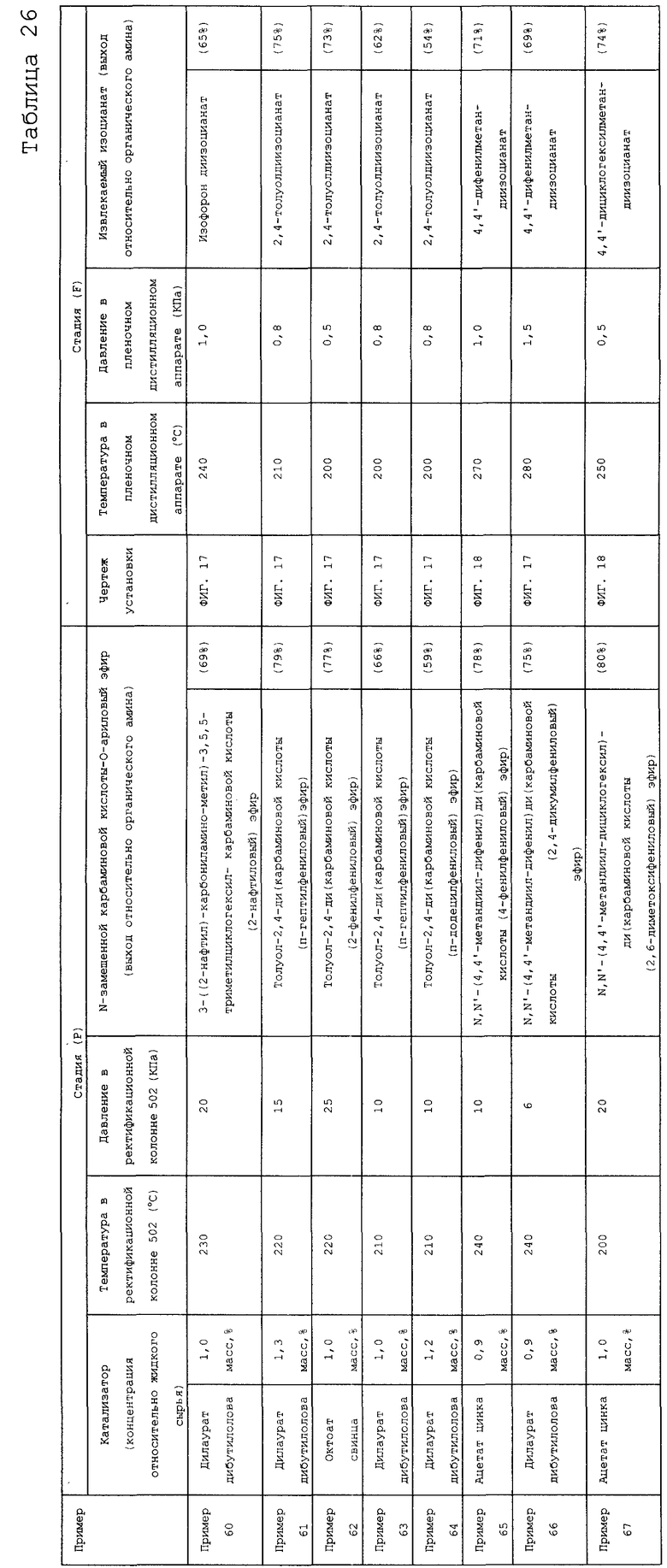
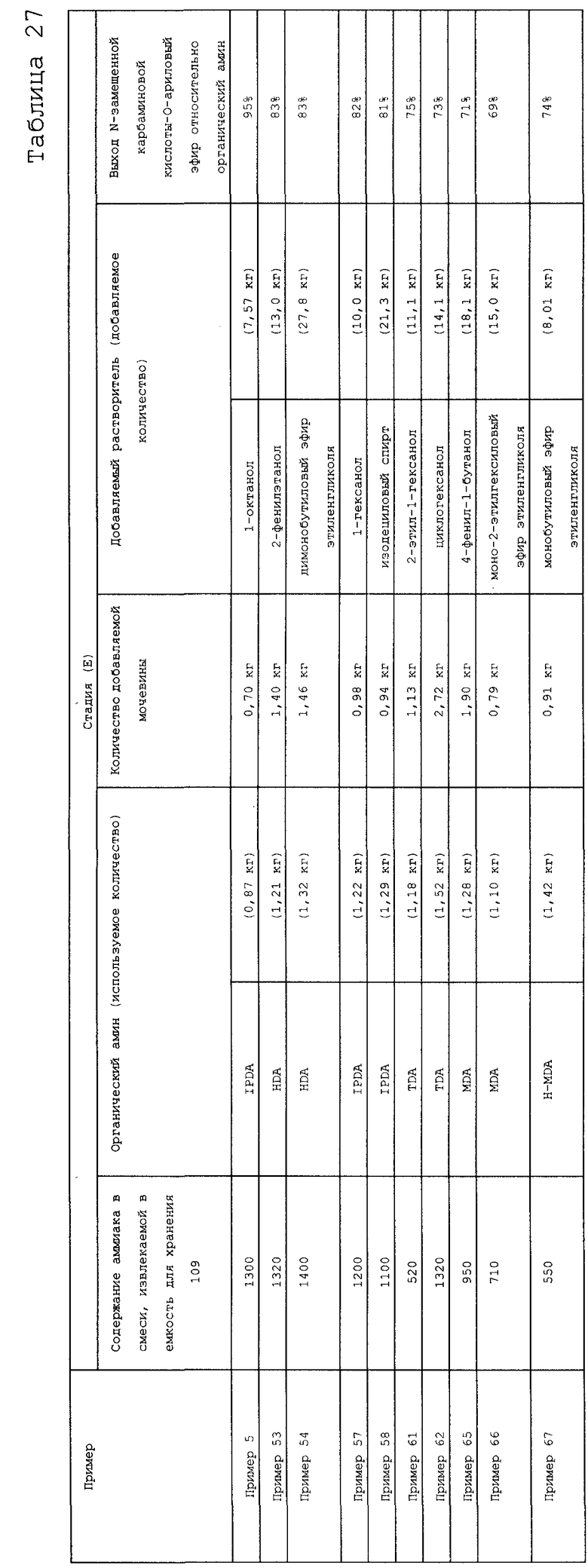
[ПРИМЕРЫ 68-70]
Осуществляли такой же способ, как в примере 6, но изменяя используемые соединения и условия реакции. Соединения и условия реакции, используемые на стадии (A) примеров 68-70, вместе с результатами приведены в таблице 28. Кроме того, соединения и условия реакции, используемые на стадиях (R) и (D) примеров 68-70, вместе с результатами приведены в таблице 29. Соединения и условия реакции, используемые на стадии (P) примеров 68-70, вместе с результатами приведены в таблице 30. Соединения и условия реакции, используемые на стадии (C) примеров 68-70, вместе с результатами приведены в таблице 31. Соединения и условия реакции, используемые на стадии (F) примеров 68-70, вместе с результатами приведены в таблице 32. Несмотря на то, что "фигура 17" и "фигура 18" указаны в колонке "чертеж установки" в таблице 32 для стадии (F), "фигура 17" указывает, что был осуществлен такой же способ, как на стадии (F) примера 1 с использованием установки, показанной на фигуре 17. С другой стороны, "фигура 18" указывает, что был осуществлен такой же способ, как на стадии (F) примера 4, с использованием установки, показанной на фигуре 18.
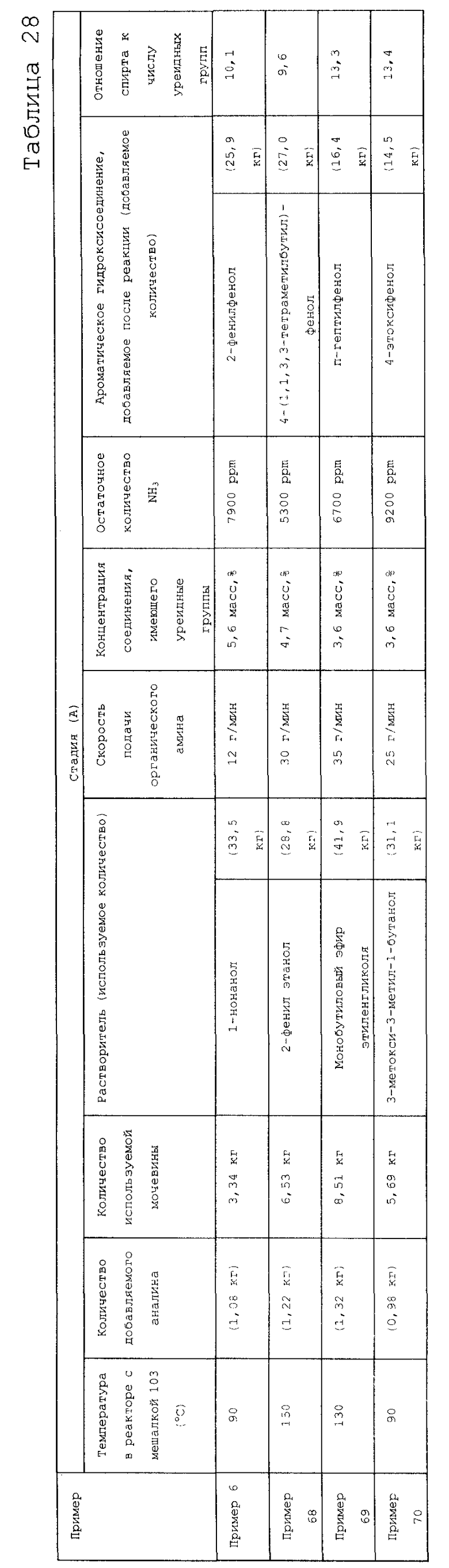

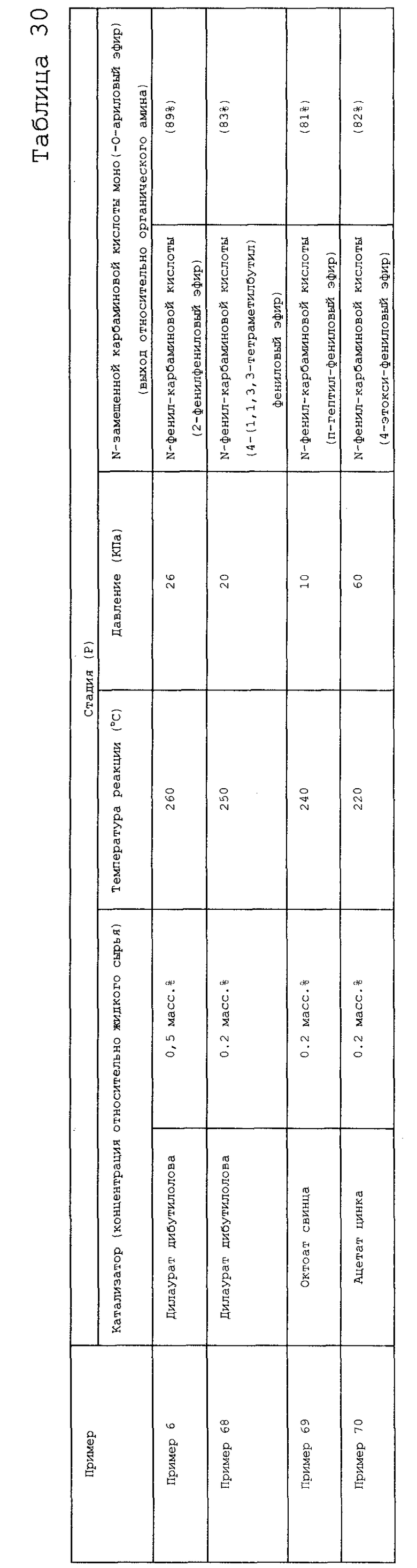
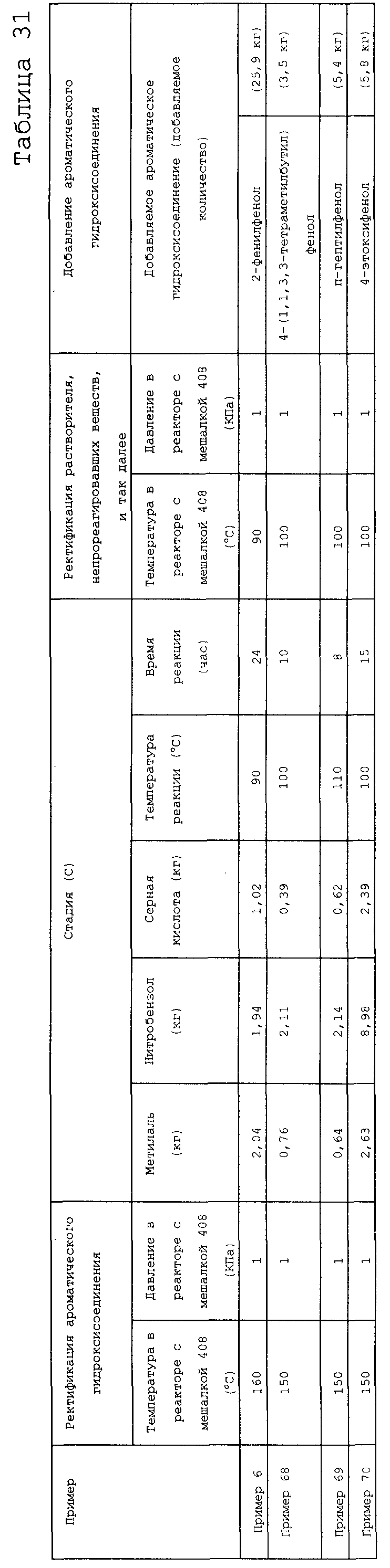
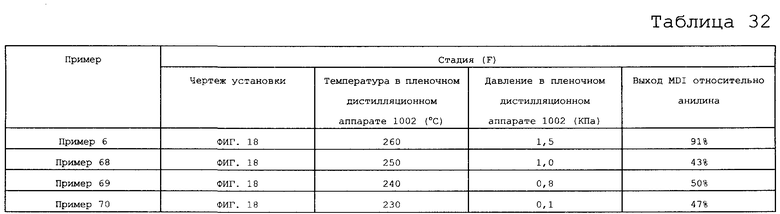
[ПРИМЕРЫ 71-73]
Осуществляли такой же способ, как в примере 7, но изменяя используемые соединения и условия реакции. Соединения и условия реакции, используемые на стадии (A) примеров 71-73, вместе с результатами приведены в таблице 33. Кроме того, соединения и условия реакции, используемые на стадиях (R) и (D) примеров 71-73, вместе с результатами приведены в таблице 34. Соединения и условия реакции, используемые на стадии (C) примеров 71-73, вместе с результатами приведены в таблице 35. Условия реакции, используемые на стадиях (P) и (F) примеров 71-73, вместе с результатами приведены в таблице 36. Несмотря на то, что "фигура 18" указана в колонке "чертеж установки" в таблице 36 для стадии (F), "фигура 18" указывает, что был осуществлен такой же способ, как на стадии (F) примера 4, с использованием установки, показанной на фигуре 18.
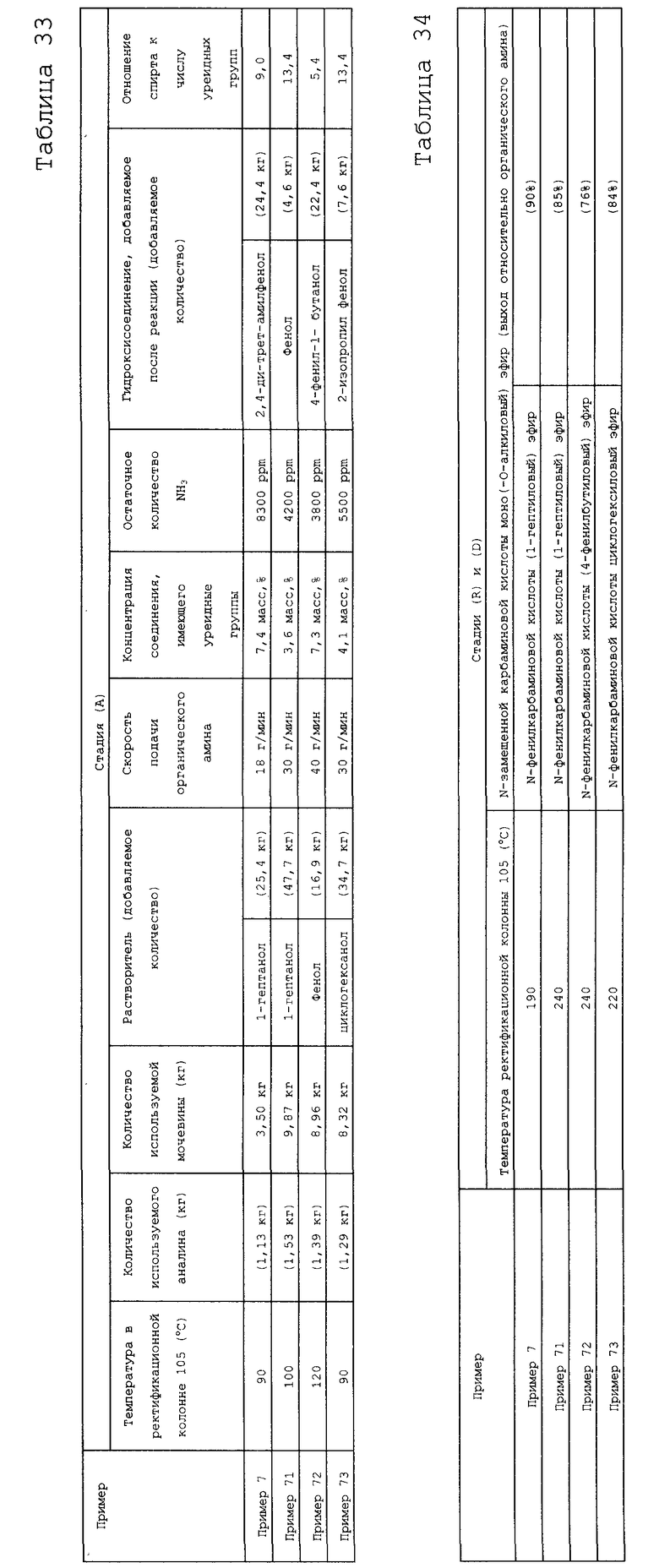
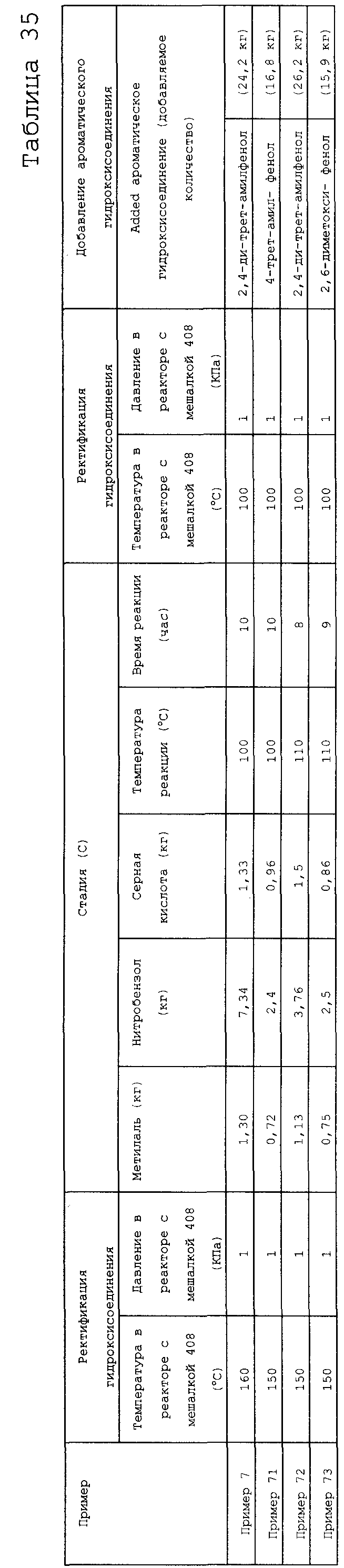

[Пример 74]
Стадия (74-1): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 19.
Транспортировали 2,54 кг мочевины из емкости для хранения 1100 в реактор с мешалкой 1103 при перекрытой линии B3. После плавления мочевины в результате нагревания реактора с мешалкой 1103 до 150°C, подавали 0,820 кг гексаметилендиамина при скорости около 10 г/мин из емкости для хранения 1101 в реактор с мешалкой 1103 по линии A1 при перемешивании в реакторе с мешалкой 1103. После завершения подачи гексаметилендиамина перемешивание продолжали в течение около 1 часа и помещали около 8,5 кг воды в реактор с мешалкой 1103 из емкости для хранения 1102 с получением раствора типа суспензии. Раствор типа суспензии подавали на напорную фильтровальную установку 1104 и твердый компонент отделяли фильтрацией. При анализе извлекаемого твердого компонента с помощью 1H-ЯМР было обнаружено, что он содержит соединение, имеющее уреиленовые группы. Добавляли к твердому компоненту около 50 кг воды при температуре около 80°C, затем перемешивали с получением дисперсии, и дисперсию фильтровали с получением фильтрата. Твердый компонент, который осаждался после охлаждения фильтрата, отделяли и извлекали. Извлекаемый твердый компонент нагревали до температуры около 100°C и сушили с помощью сушилки в атмосфере азота с получением 125 г твердого вещества. При анализе твердого вещества с помощью 1H-ЯМР было обнаружено, что оно является 1,1'-(гексан-1,6-диил)димочевиной. Затем упомянутую выше методику повторяли 10 раз с получением около 1270 г 1,1'-(гексан-1,6-диил)димочевины.
Стадия (B): Получение N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 20.
Смешивали 1,1'-(гексан-1,6-диил)димочевину, получаемую на стадии (74-1), и 25,9 кг 4-(1,1,3,3-тетраметилбутил)фенола с получением раствора исходного сырья, который помещали в емкость для хранения 1201.
Насадочную колонну 1202, заполненную насадкой (Helipack No. 3), нагревали до 240°C и создавали давление внутри колонны 26 кПа. Упомянутый выше раствор исходного сырья подавали при скорости около 3,5 г/мин по линии C1, подсоединенной к насадочной колонне 1202. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 23,2 кг. Реакционную жидкость извлекали в емкость для хранения 1205 по линии C4, подсоединенной к нижней части насадочной колонны 1202. Газофазный компонент извлекали по линии C2, подсоединенной к верхней части насадочной колонны 1202, и конденсировали с помощью конденсатора 1203, и полученный с помощью газо-жидкостного сепаратора 1204 жидкофазный компонент рециркулировали в насадочную колонну 1202. С другой стороны, из газо-жидкостного сепаратора 1204 извлекали аммиак в форме газообразного компонента. При анализе реакционной жидкости, извлекаемой в емкость для хранения 1205, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты (4-(1,1,3,3-тетраметилбутиловый)фениловый) эфир), и выход N,N'-гександиил-ди(карбаминовой кислоты (4-(1,1,3,3-тетраметилбутил)фенилового) эфира) относительно гексаметилендиамина составлял около 86%.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-ариловового эфира
Использовали установку, показанную на фигуре 17.
Пленочный дистилляционный аппарат 602, имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в пленочном дистилляционном аппарате около 1,3 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в пленочный дистилляционный аппарат при скорости около 1800 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части пленочного дистилляционного аппарата 602, и извлекали в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в пленочный дистилляционный аппарат 602 по линии 63. Газообразный компонент, содержащий гексаметилендиизоцианат и п-гептилфенол извлекали по линии 61, подсоединенной к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604 и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604, ниже линии подачи сырья, и затем подвергали ректификационному разделению. Газообразный компонент подавали по линии 69 в конденсатор 610 и подвергали конденсации и извлекали с помощью газо-жидкостного сепаратора 611 в емкость для хранения 612.
При анализе сконденсированной жидкости с помощью 1H-ЯМР и газовой хроматографии, было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 80%.
[ПРИМЕР 75]
Стадия (75-1): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (74-1) примера 74, за исключением того, что использовали 3,41 кг мочевины и 1,11 кг гексаметилендиамина. Затем аналогичную процедуру повторяли 10 раз, и полученную 1,1'-(гексан-1,6-диил)димочевину смешивали с приблизительно 25,6 кг 4-этоксифенола, и получали гомогенный раствор. При анализе раствора с помощью 1H-ЯМР было обнаружено, что он является раствором, содержащим 6,3% по массе 1,1'-(гексан-1,6-диил)димочевины и 7,7% по массе мочевины.
Стадия (B): Получение N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 20.
Раствор, получаемый на стадии (75-1), транспортировали в емкость для хранения 401.
Насадочную колонну 1202 нагревали до 240°C и создавали давление внутри колонны 26 кПа. Раствор, получаемый на стадии (75-1), подавали при скорости около 3,7 г/мин по линии 41, подсоединенной к насадочной колонне 1202. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 24,3 кг. Реакционную жидкость извлекали в емкость для хранения 1205 по линии 44, подсоединенной к нижней части насадочной колонны 1202. Газофазный компонент извлекали по линии C2, подсоединенной к верхней части насадочной колонны 1202, и конденсировали с помощью конденсатора 1203, поддерживаемого при температуре около 85°C, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 1204 в емкость для хранения 1207. С другой стороны, извлекали из газо-жидкостного сепаратора 1204 аммиак в форме газообразного компонента. При анализе реакционной жидкости, извлекаемой в емкость для хранения 1205, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты (4-этоксифениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (4-этоксифенилового) эфира) относительно гексаметилендиамина составлял около 93%. Количество раствора, извлекаемого в емкость для хранения 1207, составляло 16,1 кг, и при анализе раствора с помощью 1H-ЯМР было обнаружено, что он содержит 11,6% по массе мочевины.
[ПРИМЕР 76]
Стадия (76-1): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (74-1) примера 74, за исключением того, что использовали 3,33 кг мочевины и использовали 1,18 кг 3-аминометил-3,5,5-триметилциклогексиламина вместо гексаметилендиамина. Затем повторяли аналогичную методику 10 раз с получением 1,53 кг твердого вещества. При анализе твердого вещества с помощью 1H-ЯМР было обнаружено, что оно является 3-(уреидометил)-3,5,5-триметилциклогексилмочевиной.
Стадия (B): Получение N-замещенной карбаминовой кислоты-O-арилового эфира
Твердое вещество, получаемое на стадии (76-1), смешивали с 21,3 кг п-гептилфенола с получением раствора исходного сырья и помещали в емкость для хранения 401.
Осуществляли такую же методику, как в примере (56-2), за исключением того, что подавали раствор исходного сырья при скорости около 2,8 г/мин. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 19,7 кг. При анализе реакционной жидкости, извлекаемой в емкость для хранения 405, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость содержит 3-((п-гептилфенокси)карбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (п-гептилфениловый) эфир, и выход 3-((п-гептилфенокси)карбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (п-гептилфенилового) эфира относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял около 83%.
[ПРИМЕР 77]
Стадия (77-1): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 19.
Транспортировали 3,01 кг мочевины из емкости для хранения 1100 и 5,21 кг воды из емкости для хранения 1102 в реактор с мешалкой 1103 при перекрытой линии B3. Реактор с мешалкой 1103 нагревали до 90°C с получением гомогенного раствора, и подавали 0,970 кг гексаметилендиамина при скорости около 8 г/мин из емкости для хранения 1101 в реактор с мешалкой 1103 по линии B1 при перемешивании в реакторе с мешалкой 1103. После завершения подачи гексаметилендиамина перемешивание продолжали в течение около 1 часа. Получали раствор типа суспензии. Раствор типа суспензии подавали на напорную фильтровальную установку 1104, и твердый компонент отделяли фильтрацией. Извлекаемый фильтрат охлаждали до температуры около 20°C, и твердый компонент, который осаждался, отделяли фильтрацией и извлекали. Твердый компонент нагревали до температуры около 100°C и сушили с помощью сушилки в атмосфере азота с получением 0,32 кг твердого вещества. При анализе твердого вещества с помощью 1H-ЯМР было обнаружено, что оно является 1,1'-(гексан-1,6-диил)димочевиной. Затем упомянутую выше методику повторяли 5 раз с получением около 1,48 кг 1,1'-(гексан-1,6-диил)димочевины.
Стадия (B): Получение N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 20.
Смешивали 1,1'-(гексан-1,6-диил)димочевину, получаемую на стадии (77-1), и 15,6 кг 4-кумилфенола с получением раствора исходного сырья, который помещали в емкость для хранения 1201.
Насадочную колонну 1202 нагревали до 240°C и создавали давление внутри колонны 26 кПа. Упомянутый выше раствор исходного сырья подавали при скорости около 3,5 г/мин по линии C1, подсоединенной к насадочной колонне 1202. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 15,6 кг. Реакционную жидкость извлекали в емкость для хранения 406 по линии C4, подсоединенной к нижней части насадочной колонны 1202. Газофазный компонент извлекали по линии C2, подсоединенной к верхней части насадочной колонны 402, и конденсировали с помощью конденсатора 1203, и полученный с помощью газо-жидкостного сепаратора 1204 жидкофазный компонент рециркулировали в насадочную колонну 1202. С другой стороны, из газо-жидкостного сепаратора 1204 извлекали аммиак в форме газообразного компонента. При анализе реакционной жидкости, извлекаемой в емкость для хранения 1205, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты (4-кумилфениловый) эфир), и выход N,N'-гександиилди(карбаминовой кислоты (4-кумилфенилового) эфира) относительно гексаметилендиамина составлял около 83%.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-ариловового эфира
Использовали установку, показанную на фигуре 17.
Пленочный дистилляционный аппарат 602, имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в пленочном дистилляционном аппарате около 1,3 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в пленочный дистилляционный аппарат при скорости около 1800 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части пленочного дистилляционного аппарата 602, в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в пленочный дистилляционный аппарат 602 по линии 63. Газообразный компонент, содержащий гексаметилендиизоцианат и 4-кумилфенол извлекали по линии 61, подсоединенной к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и затем подвергали ректификационному разделению.
При анализе сконденсированной жидкости с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 80%.
[ПРИМЕР 78]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 1, за исключением того, что использовали 34,3 кг п-гептилфенола, 2,92 кг мочевины и 1,38 кг гексаметилендиамина. После завершения реакции, отбирали пробу реакционной жидкости, и в результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что она содержит 6,1% по массе соединения, имеющего уреидные группы, в форме 1,1'-(гексан-1,6-диил)димочевины. Кроме того, концентрация аммиака в растворе составляла 5500 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были. Отношение числа молекул п-гептилфенола к числу уреидных групп составляло 7,7.
Затем открывали линию 13, и реакционную жидкость транспортировали в емкость для хранения 104 по линии 13.
Стадия (B): Получение N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 13.
Насадочную колонну 105, заполненную насадкой (Helipack No. 3), нагревали до 240°C и создавали давление внутри колонны 26 кПа. Реакционную жидкость, получаемую на стадии (A), подавали при скорости около 1,5 г/мин по линии 14, подсоединенной к насадочной колонне 105. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 36,3 кг. Реакционную жидкость извлекали в емкость для хранения 110 по линии 16, подсоединенной к нижней части насадочной колонны 105. Газофазный компонент подавали по линии 15, подсоединенной к верхней части насадочной колонны 105, в конденсатор 106, поддерживаемый при температуре около 85°C, и подвергали конденсации, и получаемый с помощью газо-жидкостного сепаратора 108 жидкофазный компонент рециркулировали в насадочную колонну 105. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 35,9 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый) эфир) и мочевину. Выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового) эфира) относительно гексаметилендиамина составлял около 89%.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 17.
Тонкопленочный дистилляционный аппарат 602, имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в тонкопленочном дистилляционном аппарате около 1,3 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в тонкопленочный дистилляционный аппарат при скорости около 1800 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части тонкопленочного дистилляционного аппарата 602, и извлекали в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в тонкопленочный дистилляционный аппарат 602 по линии 63. Газообразный компонент, содержащий гексаметилендиизоцианат и п-гептилфенол, извлекали по линии 61, подсоединенной к верхней части тонкопленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Газофазный компонент подавали по линии 69 в конденсатор 610 и подвергали конденсации, и с помощью газо-жидкостного сепаратора 611 извлекали в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно органического амина (гексаметилендиамина) составлял около 79%.
[ПРИМЕР 79]
Стадии (A) и (B): Получение N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 21.
Смешивали 1,31 кг гексаметилендиамина и 3,39 кг мочевины в 3,5 кг воды с получением гомогенного водного раствора. Водный раствор помещали в емкость для хранения 1300. Часть ректификационной колонны 1302, заполненной насадкой (Helipack No. 3), выше линии D1 нагревали до 200°C, в то время как часть ректификационной колонны 1302 ниже линии D1 нагревали до 240°C, и подавали водный раствор в емкости для хранения 1300 при скорости около 1,6 г/мин по линии D0, в то время как газообразный азот подавали при скорости 0,1 нормальных литров/мин по линии D6. Кроме того, подавали 4-(1,1,3,3-тетраметилбутил)фенол по линии 1301 при скорости около 16,1 г/мин. При отборе пробы реакционной жидкости из пробоотборной линии D5, установленной выше линии D1, и анализе с помощью 1H-ЯМР и жидкостной хроматографии было обнаружено, что реакционная жидкость содержит 1,1'-(гексан-1,6-диил)димочевину. Кроме того, при анализе реакционной жидкости соединения, имеющие аминогруппы (такие как гексаметилендиамин или 6-уреидогексаметиленамин), обнаружены не были.
Реакционную жидкость извлекали в емкость для хранения 1305 по линии D4, подсоединенной к нижней части ректификационной колонны 1302. При анализе реакционной жидкости, извлекаемой в емкость для хранения 1305, с помощью 1H-ЯМР и жидкостной хроматографии было обнаружено, что реакционная жидкость является раствором, содержащим N,N'-гександиилди(карбаминовой кислоты (4-(1,1,3,3-тетраметилбутил)фениловый) эфир). Выход N,N'-гександиилди(карбаминовой кислоты (4-(1,1,3,3-тетраметилбутил)фенилового) эфира) относительно гексаметилендиамина составлял 78%.
[ПРИМЕР 80]
Стадии (A) и (R): Получение N-замещенной карбаминовой кислоты-O-алкилового эфира
Использовали установку, показанную на фигуре 21.
Смешивали 1,25 кг гексаметилендиамина и 3,23 кг мочевины в 3,3 кг воды с получением гомогенного водного раствора. Водный раствор помещали в емкость для хранения 1300. Часть ректификационной колонны 1302, заполненной насадкой (Helipack No. 3), выше линии D1 нагревали до 200°C, в то время как часть ректификационной колонны 1302 ниже линии D1 нагревали до 240°C, и подавали водный раствор в емкости для хранения 1300 при скорости около 1,55 г/мин по линии D0, в то время как газообразный азот подавали при скорости 0,1 нормальных литров/мин по линии D6. Кроме того, 2-фенилэтанол подавали по линии 1301 при скорости около 9,13 г/мин. При отборе пробы реакционной жидкости из пробоотборной линии D5, установленной выше линии D1, и анализе с помощью 1H-ЯМР и жидкостной хроматографии было обнаружено, что реакционная жидкость содержит 1,1'-(гексан-1,6-диил)димочевину. Кроме того, при анализе реакционной жидкости, соединения, имеющие аминогруппы (такие как гексаметилендиамин или 6-уреидогексаметиленамин), обнаружены не были.
Реакционную жидкость извлекали в емкость для хранения 1305 по линии D4, подсоединенной к нижней части ректификационной колонны 1302. При анализе реакционной жидкости, извлекаемой в емкость для хранения 1305, с помощью 1H-ЯМР и жидкостной хроматографии было обнаружено, что реакционная жидкость является раствором, содержащим N,N'-гександиилди(карбаминовой кислоты (2-фенилэтиловый) эфир). Выход N,N'-гександиилди(карбаминовой кислоты (2-фенилэтилового) эфира) относительно гексаметилендиамина составлял 75%.
Стадия (P): Получение N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции переэтерификации
Использовали установку, показанную на фигуре 16.
Добавляли 20,7 кг п-гептилфенола в реакционную жидкость, полученную на приведенной выше стадии, с получением гомогенного раствора, который помещали в емкость для хранения 501.
Насадочную колонну 502, заполненную насадкой (Helipack No. 3), нагревали до 260°C и создавали давление внутри колонны 26 кПа. Смесь в емкости для хранения 501 подавали при скорости около 2,3 г/мин по линии 51, подсоединенной к насадочной колонне 502. Реакционную жидкость извлекали в емкость для хранения 505 по линии 54, подсоединенной к нижней части насадочной колонны 502. Газофазный компонент вводили в конденсатор 503 по линии 52, подсоединенной к верхней части насадочной колонны 502, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 507 в емкость для хранения 504. При анализе реакционной жидкости, извлекаемой в емкость для хранения 505, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость является раствором, содержащим N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового) эфира) относительно гексаметилендиамина составлял 71%.
[ПРИМЕР 81]
Стадия (G): Стадия регенерации мочевины
Повторяли пример 1, и аммиак, получаемый по линиям 19 и 17 на стадиях (A) и (B) извлекали в форме жидкого аммиака, используя установку для сжижения.
Аммиак, сжатый под давлением 17,6 МПа, нагретый до 150°C и подаваемый при скорости 3,44 кг/час, диоксид углерода, сжатый под давлением 17,6 МПа и подаваемый при скорости 2,20 кг/час, и конденсат, который будет описан позже, подавали в реактор синтеза мочевины 1401 и проводили реакцию при 190°C.
Жидкость, образующуюся при синтезе мочевины, которая выходила из реактора синтеза мочевины, подавали в сепаратор высокого давления 1402, в то время как диоксид углерода, одновременно подаваемый по линии 21, контактировали с жидкостью, образующейся при синтезе мочевины, при скорости 2,20 кг/час для разложения непревращенных продуктов при 195°C, затем отделяли газовую смесь, содержащую аммиак при 4,26 кг/час, диоксид углерода при 2,43 кг/час и воду при 0,50 кг/час, от водного раствора мочевины, содержащего мочевину, при 6,0 кг/час, аммиак при 2,88 кг/час, диоксид углерода при 2,34 кг/час и воду при 3,01 кг/час. Понижали давление над водным раствором мочевины до 1,76 МПа и затем до 0,20 МПа для отделения остаточных неконвертированных продуктов и затем подвергали конечной обработке с получением мочевины при скорости 6,0 кг/час. Отделенные неконвертированные продукты абсорбировали водой с получением водного раствора карбамата аммония при 1,76 МПа, содержащего аммиак при 2,84 кг/час, диоксид углерода при 2,34 кг/час и воду при 1,21 кг/час.
Газовую смесь затем подавали в конденсатор 1403 для всасывания и сжатия под давлением водного раствора карбамата аммония, сжимаемого до 17,6 МПа. Получаемый конденсат рециркулировали в реактор синтеза мочевины 1401.
Стадия (A): Получение соединения, имеющего уреидные группы, с использованием мочевины, полученной на стадии (G)
Осуществляли такой же способ, как на стадии (A) примера 1, за исключением того, что использовали 40,0 кг п-гептилфенола, 3,33 кг мочевины, полученной на приведенной выше стадии (G), и 1,61 кг гексаметилендиамина. Реакционная жидкость содержала 6,3% по массе 1,1'-(гексан-1,6-диил)димочевины. Кроме того, концентрация аммиака в растворе составляла 6300 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадии (B) примера 1, за исключением того, что использовали раствор, получаемый на приведенной выше стадии (A), и затем извлекали реакционную жидкость в емкость для хранения 110. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый) эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового) эфира) относительно гексаметилендиамина составлял около 97%.
[ПРИМЕР 82]
Стадия (G): Стадия регенерации мочевины
Использовали установку, показанную на фигуре 22.
Повторяли пример 5, и аммиак, получаемый по линиям 19 и 17 на стадиях (A) и (R), извлекали в форме жидкого аммиака, используя установку для сжижения.
Аммиак, сжатый под давлением 17,6 МПа, нагретый до 150°C и подаваемый при скорости 3,44 кг/час, диоксид углерода, сжатый под давлением 17,6 МПа и подаваемый при скорости 2,20 кг/час, и конденсат, который будет описан позже, подавали в реактор синтеза мочевины 1401 и проводили реакцию при 190°C.
Жидкость, образующуюся при синтезе мочевины, которая выходила из реактора синтеза мочевины, подавали в сепаратор высокого давления 1402, в то время как диоксид углерода, одновременно подаваемый по линии 21, контактировали с жидкостью, образующейся при синтезе мочевины, при скорости 2,20 кг/час для разложения непревращенных продуктов при 195°C, затем отделяли газовую смесь, содержащую аммиак при 4,26 кг/час, диоксид углерода при 2,43 кг/час и воду при 0,50 кг/час, от водного раствора мочевины, содержащего мочевину при 6,0 кг/час, аммиак при 2,88 кг/час, диоксид углерода при 2,34 кг/час и воду при 3,01 кг/час. Понижали давление над водным раствором мочевины до 1,76 МПа и затем до 0,20 МПа для отделения остаточных неконвертированных продуктов, и затем подвергали конечной обработке с получением мочевины при скорости 6,0 кг/час. Отделенные неконвертированные продукты абсорбировали водой с получением водного раствора карбамата аммония при 1,76 МПа, содержащего аммиак при 2,84 кг/час, диоксид углерода при 2,34 кг/час и воду при 1,21 кг/час.
Газовую смесь затем подавали в конденсатор 1403 для всасывания и сжатия под давлением водного раствора карбамата аммония, сжимаемого до 17,6 МПа. Получаемый конденсат рециркулировали в реактор синтеза мочевины 1401.
Стадия (A): Получение сложного эфира N-замещенной карбаминовой кислоты с использованием мочевины, регенерированной на стадии (G)
Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 5, за исключением того, что использовали 14,6 кг 1-октанола, 1,47 кг мочевины, полученной на приведенной выше стадии (G), и 0,87 кг 3-аминометил-3,5,5-триметилциклогексиламина. В результате анализа полученной реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что она содержит около 7,8% по массе 3-(уреидометил)-3,5,5-триметилциклогексилмочевины. Кроме того, концентрация аммиака в растворе составляла 7300 ppm. Добавляли 13,4 кг ароматического гидроксисоединения в форме п-додецилфенола из емкости для хранения 101 с получением гомогенного раствора. Затем открывали линию 13, и раствор транспортировали в емкость для хранения 104 по линии 13.
Стадии (R) и (D): Получение N-замещенной карбаминовой кислоты-O-алкилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадиях (R) и (D) примера 4, за исключением того, что использовали реакционную жидкость, получаемую на стадии (A), которая использовала описанную выше регенерированную мочевину. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 8,80 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит 3-((1-октилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (1-октиловый) эфир, и выход относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял около 95%.
Стадия (P): Реакция переэтерификации
Осуществляли такой же способ, как на стадии (P) примера 4, за исключением того, что использовали реакционную жидкость, получаемую выше на стадиях (R) и (D). При анализе реакционной жидкости, извлекаемой в емкость для хранения 505, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость является раствором, содержащим 3-((п-(додецилфенокси)карбониламинометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (п-додецилфениловый) эфир, и выход относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял 89%.
[ПРИМЕР 83]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 1, за исключением того, что использовали 1,33 кг гексаметилендиамина, 3,09 кг мочевины, 28,1 кг 2-нафтола вместо п-гептилфенола, и нагревали емкость для хранения 103 до 120°C.
Получали реакционную жидкость, которая содержала 7,2% по массе 1,1'-(гексан-1,6-диил)димочевины и 6100 ppm аммиака.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира
Осуществляли такой же способ, как на стадиях (B) и (D) примера 1, за исключением того, что нагревали насадочную колонну 105 до 240°C, создавали внутреннее давление 15 кПа, и использовали реакционную жидкость, получаемую выше на стадии (A).
Получали реакционную жидкость, которая содержала N,N'-гександиилди(карбаминовой кислоты (2-нафтиловый) эфир), и выход N,N'-гександиилди(карбаминовой кислоты (2-нафтилового) эфира) относительно гексаметилендиамина составлял около 97%. Концентрация аммиака в реакционной жидкости составляла около 8 ppm.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-алкилового эфира
Использовали установку, показанную на фигуре 17.
Пленочный дистилляционный аппарат 602 нагревали до 220°C и создавали давление в пленочном дистилляционном аппарате около 1,0 кПа. Реакционную жидкость, получаемую выше на стадии (B), помещали в емкость для хранения 601 и подавали в пленочный дистилляционный аппарат при скорости около 1800 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части пленочного дистилляционного аппарата 602, и извлекали в емкость для хранения 603 (жидкий компонент, извлекаемый в емкость для хранения 603, не подавали в пленочный дистилляционный аппарат 602). В емкости для хранения 603 получали около 15,2 кг раствора. Газообразный компонент, содержащий гексаметилендиизоцианат и 2-нафтол, извлекали по линии 61, подсоединенной к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Газофазный компонент подавали по линии 69 в конденсатор 610 и подвергали конденсации и извлекали с помощью газо-жидкостного сепаратора 611 в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата.
Стадия (A-2): Повторное использование N-замещенной карбаминовой кислоты-O-арилового эфира, не подвергающегося термическому разложению
При анализе раствора, извлекаемого в емкость для хранения 603 на стадии (F) выше, с помощью жидкостной хроматографии было обнаружено, что он является смесью, содержащей N,N'-гександиилди(карбаминовой кислоты (2-нафтиловый) эфир) и 2-нафтол.
Осуществляли такой же способ, как выше на стадии (A), за исключением того, что использовали смесь около 5,9 кг смеси и 22,2 кг 2-нафтола вместо 2-нафтола, 1,33 кг гексаметилендиамина и 3,22 кг мочевины. Получали реакционную жидкость, которая содержала 7,2% по массе 1,1'-(гексан-1,6-диил)димочевины и 6300 ppm аммиака.
[ПРИМЕР 84]
Стадия (B-2): Повторное использование N-замещенной карбаминовой кислоты-O-арилового эфира, который не был подвергнут термическому разложению
Осуществляли такой же способ, как на стадии (A) примера 83, с получением около 32,1 кг раствора, содержащего 7,2% по массе 1,1'-(гексан-1,6-диил)димочевины.
Добавляли к этому раствору 6,0 кг смеси, извлекаемой в емкость для хранения 603 на стадии (F) выше, с получением смеси, затем осуществляли такой же способ, как выше на стадии (B), с использованием этой смеси. Получали реакционную жидкость, которая содержала N,N'-гександиилди(карбаминовой кислоты (2-нафтиловый) эфир), и выход N,N'-гександиилди(карбаминовой кислоты (2-нафтилового) эфира) относительно гексаметилендиамина составлял около 97%.
Кроме того, обозначенный здесь выход указывает выход N,N'-гександиилди(карбаминовой кислоты (2-нафтилового) эфира), образующегося на стадии (B). А именно, он относится к величине, получаемой делением количества, получаемого вычитанием количества N,N'-гександиилди(карбаминовой кислоты (2-нафтилового) эфира), содержащегося в смеси, извлекаемой в емкость для хранения 603, используемой на этой стадии, из количества N,N'-гександиилди(карбаминовой кислоты (2-нафтилового) эфира), содержащегося в реакционной жидкости, на количество гексаметилендиамина, используемого на стадии (A).
[ПРИМЕР 85]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 5, за исключением того, что использовали 11,7 кг 1-гексанола вместо 1-октанола, использовали 1,64 кг мочевины и 1,22 кг 3-аминометил-3,5,5-триметилциклогексиламина, и нагревали емкость для хранения 103 до 120°C. В результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что реакционная жидкость содержит около 7,8% по массе 3-(уреидометил)-3,5,5-триметилциклогексилмочевины. Кроме того, концентрация аммиака в растворе составляла 7500 ppm. Добавляли из емкости для хранения 101 12,2 кг ароматического гидроксисоединения в форме 4-фенилфенола с получением гомогенного раствора. Открывали линию 13, и раствор транспортировали в емкость для хранения 104 по линии 13.
Стадии (R) и (D): Получение N-замещенной карбаминовой кислоты-O-алкилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадиях (R) и (D) примера 4, за исключением того, что нагревали насадочную колонну 105 до 240°C, создавали давление в насадочной колонне 105 около 10 кПа. При анализе реакционной жидкости, извлекаемой в емкость для хранения 110, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость содержит 3-((1-гексилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (1-гексиловый) эфир, и выход относительно 3-аминометил-3,5,5-трициклогексиламина составлял около 92%. Концентрация аммиака в реакционной жидкости составляла около 10 ppm.
Стадия (P): Реакция переэтерификации
Осуществляли такой же способ, как на стадии (P) примера 4, за исключением того, что нагревали насадочную колонну 502 до 250°C и создавали внутреннее давление 15 кПа. При анализе реакционной жидкости, извлекаемой в емкость для хранения 505, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость является раствором, содержащим 3-((4-(фенилфенилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (4-фенилфениловый) эфир, и выход относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял 88%.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 17.
Тонкопленочный дистилляционный аппарат 602 нагревали до 230°C и создавали давление в тонкопленочном дистилляционном аппарате около 1,0 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 505 выше на стадии (P), помещали в емкость для хранения 601 и подавали в тонкопленочный дистилляционный аппарат при скорости около 1080 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части пленочного дистилляционного аппарата 602, и подавали в емкость для хранения 603 (жидкий компонент, извлекаемый в емкость для хранения 603, не подавали в пленочный дистилляционный аппарат 602). Газообразный компонент, содержащий изофорон диизоцианат и п-додецилфенол, извлекали по линии 61, подсоединенной к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Газофазный компонент подвергали конденсации в конденсаторе 610 по линии 69 и извлекали с помощью газо-жидкостного сепаратора 611 в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии, было обнаружено, что конденсат содержит около 99% по массе изофорон диизоцианата.
Стадия (R-2): Повторное использование смеси, содержащей непрореагировавший N-замещенной карбаминовой кислоты-O-ариловый эфир
При анализе смеси, извлекаемой в емкость для хранения 603 выше на стадии (F), с помощью жидкостной хроматографии было обнаружено, что смесь является смесью, содержащей 3-((4-фенилфенилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (4-фенилфениловый)эфир и 4-фенилфенол, и содержание 3-((4-фенилфенилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (4-фенилфенилового)эфира составляло около 42% по массе.
Осуществляли такой же способ, как выше на стадиях (R) и (D), за исключением того, что добавляли около 1,5 кг смеси, извлекаемой в емкость для хранения 603, к реакционной жидкости, получаемой путем осуществления такого же способа, как выше на стадии (A), с получением смеси, и использовали эту смесь. При анализе реакционной жидкости, извлекаемой в емкость для хранения 110, с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость содержит 3-((1-гексилокси)карбониламидометил)-3,5-5-триметилциклогексилкарбаминовой кислоты (1-гексиловый)эфир. Выход 3-((1-гексилокси)карбониламидометил)-3,5-5-триметилциклогексилкарбаминовой кислоты (1-гексилового)эфира, образовавшегося на этой стадии (R-2), относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял около 92%. Концентрация аммиака в реакционной жидкости составляла около 10 ppm.
[ПРИМЕР 86]
Стадия (P-2): Повторное использование смеси, содержащей непрореагировавший N-замещенной карбаминовой кислоты-O-ариловый эфир
Осуществляли такой же способ, как на стадиях (A) и (R) примера 85, с получением около 20,3 кг раствора, содержащего 3-((1-гексилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (1-гексилового)эфира. Около 2,5 кг смеси, извлекаемой в емкость для хранения 603, приведенной выше стадии (F), смешивали с этим раствором, затем осуществляли такой же способ, как выше на стадии (P), с получением раствора, содержащего 3-((4-фенилфенокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (4-фенилфениловый)эфир, в емкости для хранения 505. Выход 3-((4-фенилфенилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (4-фенилфенилового)эфира, исключая 3-((4-фенилфенилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (4-фенилфениловый)эфир, получаемый на стадии (P-2) и содержащийся в смеси, извлекаемой в емкость для хранения 603, которую добавляли, как описано выше, относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял 88%.
[ПРИМЕР 87]
Стадия (A-2): Повторное использование N-замещенной карбаминовой кислоты-O-арилового эфира, который не был подвергнут термическому разложению
Осуществляли такой же способ, как на стадиях (A) и (R) примера 85, с получением около 21,5 кг раствора, содержащего 3-((1-гексилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (1-гексилового)эфир.
Осуществляли такой же способ, как выше на стадии (A), за исключением того, что использовали смесь около 6,8 кг этого раствора и 16,9 кг 1-октанола вместо только одного 1-октанола, и использовали 1,41 кг гексаметилендиамина и 2,39 кг мочевины. Получали реакционный раствор, который содержал 7,6% по массе 1,1'-(гексан-1,6-диил)димочевины и 5300 ppm аммиака.
[ПРИМЕР 88]
Стадия (A): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 13.
Смешивали 30,5 кг п-гептилфенола и 2,54 кг мочевины в емкости для хранения 101, нагретой до 120°C, с перекрытой линией 13, с получением смеси. Смесь транспортировали в реактор с мешалкой 103 (с перегородками), нагретый до 120°C. Линию 19 соединяли с вакуумным насосом, и давление внутри реактора с мешалкой 103 снижали до приблизительно 70 кПа. Подавали 1,23 кг органического амина в форме гексаметилендиамина при скорости около 20 г/мин (скорость подачи органического амина) из емкости для хранения 102 в реактор с мешалкой 103 по линии 12 при перемешивании в реакторе с мешалкой 103. После завершения подачи гексаметилендиамина перемешивание продолжали в течение около 2 часов и отбирали пробу реакционной жидкости. В результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что образовывалась 1,1'-(гексан-1,6-диил)димочевина с выходом около 97% относительно гексаметилендиамина. Кроме того, концентрация аммиака в растворе составляла 1200 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Затем линию 13 открывали, и реакционную жидкость транспортировали в емкость для хранения 104 по линии 13.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Продолжали использовать установку, показанную на фигуре 13.
Насадочную колонну 105, заполненную насадкой (Helipack No. 3), нагревали до 240°C и создавали давление внутри колонны 26 кРа. Реакционную жидкость, получаемую на стадии (A), подавали по линии 14, подсоединенной к насадочной колонне 105, при скорости около 1,5 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 35,1 кг. Реакционную жидкость извлекали в емкость для хранения 110 по линии 16, подсоединенной к нижней части насадочной колонны 105. Газофазный компонент подавали по линии 15, подсоединенной к верхней части насадочной колонны 105, в конденсатор 106, поддерживаемый при температуре около 85°C, и подвергали конденсации, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 108 в емкость для хранения 109. При анализе реакционной жидкости, извлекаемой в емкость для хранения 109, с помощью 1H-ЯМР было обнаружено, что сконденсированный компонент содержит мочевину и п-гептилфенол. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 23,0 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР, было обнаружено, что реакционная жидкость содержит N,N'-гександиилди(карбаминовой кислоты(п-гептилфениловый)эфир). Выход N,N'-гександиилди(карбаминовой кислоты(п-гептилфенилового)эфира) относительно гексаметилендиамина составлял около 96%. Мочевину в реакционной жидкости не обнаруживали.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Использовали установку, показанную на фигуре 17.
Тонкопленочный дистилляционный аппарат 602, имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в тонкопленочном дистилляционном аппарате около 1,3 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в тонкопленочный дистилляционный аппарат при скорости около 1800 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части тонкопленочного дистилляционного аппарата 602, в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в тонкопленочный дистилляционный аппарат 602 по линии 63. Газообразный компонент, содержащий гексаметилендиизоцианат и п-гептилфенол, извлекали по линии 61, подсоединенной к верхней части тонкопленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Газофазный компонент подавали по линии 69 в конденсатор 610 и подвергали конденсации и извлекали с помощью газо-жидкостного сепаратора 611 в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно органического амина (гексаметилендиамина) составлял около 92%.
[ПРИМЕР 89]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 88, за исключением того, что использовали 29,5 кг п-гептилфенола и 2,46 кг мочевины, понижали давление в реакторе с мешалкой 103 до приблизительно 40 КПа, и использовали 1,19 кг гексаметилендиамина. При анализе реакционной жидкости было обнаружено, что образовалась 1,1'-(гексан-1,6-диил)димочевина с выходом около 91% относительно гексаметилендиамина. Кроме того, было обнаружено, что образовался N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир) с выходом около 0,5% относительно гексаметилендиамина. Концентрация аммиака составляла 820 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Затем открывали линию 13, и реакционную жидкость транспортировали в емкость для хранения 104 по линии 13.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадии (B) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (A). Было обнаружено, что реакционная жидкость, извлекаемая в емкость для хранения 110, содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового)эфира относительно гексаметилендиамина составлял около 91%. Мочевину в реакционной жидкости не обнаруживали.
Стадия (F): Получение изоцианата путем термического разложение N-замещенной карбаминовой кислоты-O-арилового эфира
Осуществляли такой же способ, как на стадии (F) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (B). При анализе конденсата, извлекаемого в емкость для хранения 612, с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 86%.
[ПРИМЕР 90]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 88, за исключением того, что использовали 30,3 кг п-гептилфенола и 2,52 кг мочевины, снижали давление в реакторе с мешалкой 103 приблизительно до 26 кПа, и использовали 1,22 кг гексаметилендиамина. При анализе реакционной жидкости было обнаружено, что образовывалась 1,1'-(гексан-1,6-диил)димочевина с выходом около 89% относительно гексаметилендиамина. Кроме того, было обнаружено, что образовывался N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир) с выходом около 0,7% относительно гексаметилендиамина. Концентрация аммиака составляла 350 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадии (B) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (A). Было обнаружено, что реакционная жидкость, извлекаемая в емкость для хранения 110, содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового)эфира) относительно гексаметилендиамина составлял около 90%. Мочевину в реакционной жидкости не обнаруживали.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Осуществляли такой же способ, как на стадии (F) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (B). При анализе конденсата, извлекаемого в емкость для хранения 612, с помощью 1H-ЯМР и газовой хроматография было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 85%.
[ПРИМЕР 91]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 88, за исключением того, что использовали 31,8 кг п-гептилфенола и 2,64 кг мочевины, понижали давление в реакторе с мешалкой 103 приблизительно до 20 кПа, и использовали 1,28 кг гексаметилендиамина. При анализе реакционной жидкости было обнаружено, что образовалась 1,1'-(гексан-1,6-диил)димочевина с выходом около 82% относительно гексаметилендиамина. Кроме того, было обнаружено, что образовывался N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир) с выходом 5,2% относительно гексаметилендиамина. Концентрация аммиака составляла 280 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадии (B) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (A). Было обнаружено, что реакционная жидкость, извлекаемая в емкость для хранения 110, содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового)эфира относительно гексаметилендиамина составлял около 85%. Мочевину в реакционной жидкости не обнаруживали.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Осуществляли такой же способ, как на стадии (F) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (B). При анализе конденсата, извлекаемого в емкость для хранения 612, с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 82%.
[ПРИМЕР 92]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 88, за исключением того, что использовали 29,5 кг п-гептилфенола и 2,46 кг мочевины, снижали давление а реакторе с мешалкой 103 приблизительно до 20 кПа и использовали 1,19 кг гексаметилендиамина. При анализе реакционной жидкости было обнаружено, что образовывалась 1,1'-(гексан-1,6-диил)димочевина с выходом около 77% относительно гексаметилендиамина. Кроме того, было обнаружено, что образовывался N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир) с выходом около 5,0% относительно гексаметилендиамина. Концентрация аммиака составляла 120 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадии (B) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (A). Было обнаружено, что реакционная жидкость, извлекаемая в емкость для хранения 110, содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового)эфира) относительно гексаметилендиамина составлял около 82%. Мочевину в реакционной жидкости не обнаруживали.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Осуществляли такой же способ, как на стадии (F) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (B). При анализе конденсата, извлекаемого в емкость для хранения 612, с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 79%.
[ПРИМЕР 93]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 88, за исключением того, что использовали 32,5 кг п-гептилфенола и 2,71 кг мочевины, понижали давление в реакторе с мешалкой 103 до приблизительно 20 кПа и использовали 1,31 кг гексаметилендиамина. При анализе реакционной жидкости было обнаружено, что образовалась 1,1'-(гексан-1,6-диил)димочевина с выходом около 68% относительно гексаметилендиамина. Кроме того, было обнаружено, что образовывался N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир) с выходом 9,1% относительно гексаметилендиамина. Концентрация аммиака составляла 90 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадии (B) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (A). Было обнаружено, что реакционная жидкость, извлекаемая в емкость для хранения 110, содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового)эфира относительно гексаметилендиамина составлял около 76%. Мочевину в реакционной жидкости не обнаруживали.
Стадия (F): Получение изоцианата путем термического разложение N-замещенной карбаминовой кислоты-O-арилового эфира
Осуществляли такой же способ, как на стадии (F) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (B). При анализе конденсата, извлекаемого в емкость для хранения 612, с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 71%.
[ПРИМЕР 94]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 88, за исключением того, что использовали 31,1 кг п-гептилфенола и 2,58 кг мочевины, снижали давление а реакторе с мешалкой 103 приблизительно до 20 кПа и использовали 1,25 кг гексаметилендиамина. При анализе реакционной жидкости было обнаружено, что образовывалась 1,1'-(гексан-1,6-диил)димочевина с выходом около 67% относительно гексаметилендиамина. Кроме того, было обнаружено, что образовывался N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир) с выходом около 10,3% относительно гексаметилендиамина. Концентрация аммиака составляла 17 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадии (B) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (A). Было обнаружено, что реакционная жидкость, извлекаемая в емкость для хранения 110, содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового)эфира) относительно гексаметилендиамина составлял около 74%. Мочевину в реакционной жидкости не обнаруживали.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Осуществляли такой же способ, как на стадии (F) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (B). При анализе конденсата, извлекаемого в емкость для хранения 612, с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 69%.
[ПРИМЕР 95]
Стадия (A): Получение соединения, имеющего уреидные группы
Осуществляли такой же способ, как на стадии (A) примера 88, за исключением того, что использовали 31,8 кг п-гептилфенола и 2,65 кг мочевины, понижали давление в реакторе с мешалкой 103 приблизительно до 20 кПа и использовали 1,28 кг гексаметилендиамина. При анализе реакционной жидкости было обнаружено, что образовалась 1,1'-(гексан-1,6-диил)димочевина с выходом около 52% относительно гексаметилендиамина. Кроме того, было обнаружено, что образовывался N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир) с выходом 16,1% относительно гексаметилендиамина. Концентрация аммиака составляла 8 ppm. Непрореагировавшие концевые аминогруппы обнаружены не были.
Стадии (B) и (D): Получение N-замещенной карбаминовой кислоты-O-арилового эфира и извлечение мочевины
Осуществляли такой же способ, как на стадии (B) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (A). Было обнаружено, что реакционная жидкость, извлекаемая в емкость для хранения 110, содержит N,N'-гександиилди(карбаминовой кислоты (п-гептилфениловый)эфир), и выход N,N'-гександиилди(карбаминовой кислоты (п-гептилфенилового)эфира относительно гексаметилендиамина составлял около 65%. Мочевину в реакционной жидкости не обнаруживали.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира
Осуществляли такой же способ, как на стадии (F) примера 74, за исключением того, что использовали реакционную жидкость приведенной выше стадии (B). При анализе конденсата, извлекаемого в емкость для хранения 612, с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 99% по массе гексаметилендиизоцианата. Выход относительно гексаметилендиамина составлял около 61%.
[СРАВНИТЕЛЬНЫЙ ПРИМЕР 1]
Использовали установку, показанную на фигуре 13.
Смешивали 1,21 кг гексаметилендиамина, 2,51 кг мочевины и 42,9 кг 4-(1,1,3,3-тетраметилбутил)фенола при 100°C с получением раствора сырья, который помещали в емкость для хранения 104. Раствор сырья подавали при скорости около 3,0 г/мин в ректификационную колонну 105, нагретую до 240°C и с внутренним давлением 30 кПа, и проводили реакцию. Газофазный компонент вводили в конденсатор 106 по линии 15, подсоединенной к верхней части ректификационной колонны 105, и конденсат извлекали в емкость для хранения 109. С другой стороны, реакционную жидкость извлекали по линии 16, подсоединенной к нижней части колонны, и извлекали в емкость для хранения 110. Во время реакции производили отбор пробы реакционной жидкости из пробоотборной линии 18, установленной между линией 14 и нижней частью колонны, и пробу жидкости анализировали с помощью 1H-ЯМР и жидкостной хроматографии. Было обнаружено, что проба жидкости является смесью, содержащей 0,12% по массе гексаметилендиамина, 0,42% по массе 6-уреидогексаметиленамина, 1,26% по массе 1,1'-(гексан-1,6-диил)димочевины, 3,49% по массе N-(6-уреидогексан-ил)карбаминовой кислоты (4-(1,1,3,3-тетраметилбутил)фенилового эфира), и 1,30% по массе N,N'-гександиилди(карбаминовой кислоты (4-(1,1,3,3-тетраметилбутил)фенилового эфира). Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 33,5 кг. При анализе реакционной жидкости с помощью 1H-ЯМР и жидкостной хроматографии было обнаружено, что она является реакционной жидкостью, которая содержит N,N'-гександиилди(карбаминовой кислоты (4-(1,1,3,3-тетраметилбутил)фениловый эфир). Выход N,N'-гександиилди(карбаминовой кислоты (4-(1,1,3,3-тетраметилбутил)фенилового эфира) относительно гексаметилендиамина составлял 53%. Кроме того, реакционная жидкость содержала около 13 моль.% N,N'-бис(6-(4-(1,1,3,3-тетраметилбутил)феноксикарбаминогексил)-мочевины относительно N,N'-гександиилди(карбаминовой кислоты (4-(1,1,3,3-тетраметилбутил)фенилового эфира).
[СРАВНИТЕЛЬНЫЙ ПРИМЕР 2]
Стадия (A): Получение соединения, имеющего уреидные группы
Использовали установку, показанную на фигуре 13.
Смешивали 22,5 кг 1-октанола и 2,27 кг мочевины в емкости для хранения 101, нагретой до 120°C, с перекрытой линией 13, и смесь транспортировали в реактор с мешалкой 103, нагретый до 120°C. Затем подавали 1,34 кг органического амина в форме 3-аминометил-3,5,5-триметилциклогексиламина при скорости около 10 г/мин из емкости для хранения 102 в реактор с мешалкой 103 по линии 12 при перемешивании в реакторе с мешалкой 103. После завершения подачи 3-аминометил-3,5,5-триметилциклогексиламина, перемешивание продолжали в течение около 2 часов и отбирали пробу реакционной жидкости. В результате анализа реакционной жидкости с помощью жидкостной хроматографии было обнаружено, что реакционная жидкость содержит около 7,8% по массе 3-(уреидометил)-3,5,5-триметилциклогексилмочевины. Концентрация аммиака в реакционной жидкости составляла 6800 ppm. Открывали линию 13 и раствор транспортировали в емкость для хранения 104 по линии 13.
Стадии (R) и (D): Получение N-замещенной карбаминовой кислоты-O-алкилового эфира и извлечение мочевины
Продолжали использовать установку, показанную на фигуре 13.
Насадочную колонну 105, заполненную насадкой (Helipack No. 3), нагревали до 190°C. Реакционную жидкость, получаемую на стадии (A), подавали по линии 14, подсоединенной к насадочной колонне 105, при скорости около 1,1 г/мин. Так как реакция в начальной стадии протекает в нестационарном режиме, пробу в данном случае отбрасывали. Количество реакционной жидкости, подаваемой после того, как реакция достигала стационарного состояния, составляло около 23,4 кг. Реакционную жидкость извлекали в емкость для хранения 110 по линии 16, подсоединенной к нижней части насадочной колонны 105. Газофазный компонент вводили в конденсатор 106 по линии 15, подсоединенной к верхней части насадочной колонны 105, и полученный жидкофазный компонент извлекали с помощью газо-жидкостного сепаратора 108 в емкость для хранения 109. При анализе конденсированного компонента, извлекаемого в емкость для хранения 109, с помощью 1H-ЯМР было обнаружено, что сконденсированный компонент содержит 1-октанол и мочевину. Количество реакционной жидкости, извлекаемой в емкость для хранения 110, составляло 8,80 кг. При анализе реакционной жидкости с помощью жидкостной хроматографии и 1H-ЯМР было обнаружено, что реакционная жидкость содержит 3-((1-октилокси)карбониламидо-метил)-3,5,5-триметилциклогексилкарбаминовой кислоты (1-октиловый)эфир, и выход относительно 3-аминометил-3,5,5-триметилциклогексиламина составлял около 90%.
Стадия (F): Получение изоцианата путем термического разложения N-замещенной карбаминовой кислоты-O-алкилового эфира
Использовали установку, показанную на фигуре 17.
Тонколеночный дистилляционный аппарат 602, имеющий площадь теплопроводящей поверхности 0,2 м2, нагревали до 220°C и создавали давление в пленочном дистилляционном аппарате около 1,3 кПа. Реакционную жидкость, извлекаемую в емкость для хранения 110 на стадии (B), помещали в емкость для хранения 601 и подавали в пленочный дистилляционный аппарат при скорости около 1800 г/час по линии 60. Жидкий компонент извлекали по линии 62, подсоединенной к нижней части пленочного дистилляционного аппарата 602, и извлекали в емкость для хранения 603. Жидкий компонент, извлекаемый в емкость для хранения 603, опять подавали в пленочный дистилляционный аппарат 602 по линии 63. Газообразный компонент, содержащий гексаметилендиизоцианат и п-гептилфенол, извлекали по линии 61, подсоединенной к верхней части пленочного дистилляционного аппарата 602. Газообразный компонент вводили в ректификационную колонну 604, и компонент с низкой температурой кипения отделяли ректификацией. Жидкофазный компонент подавали в ректификационную колонну 609 по линии 68, подсоединенной к части ректификационной колонны 604 ниже линии подачи сырья, и затем подвергали ректификационному разделению. Газообразный компонент подавали по линии 69 в конденсатор 610 и подвергали конденсации и извлекали с помощью газо-жидкостного сепаратора 611 в емкость для хранения 612.
При анализе конденсата с помощью 1H-ЯМР и газовой хроматографии было обнаружено, что конденсат содержит около 93% по массе изофорон диизоцианата и около 4% по массе 3-((1-октилокси)карбониламидометил)-3,5,5-триметилциклогексилкарбаминовой кислоты (1-октилового)эфира. Выход относительно органического амина (3-аминометил-3,5,5-триметилциклогексиламина) составлял около 53%.
[ПРИМЕР 96]
Композицию, содержащую 9% по массе соединения, имеющего уреидные группы в форме 1,1'-(гексан-1,6-диил)димочевины, 89% по массе ароматической гидроксикомпозиции в форме 4-(2,4,4-триметилпентан-2-ил)фенола, 0,01% по массе аммиака и мочевины при соотношении 0,1 (обозначающем отношение числа молекул мочевины к числу уреидных групп, которые составляют соединение (или содержатся в соединении), имеющее уреидные группы, или, другими словами, 0,1 обозначает 0,2 мольных эквивалента, так как соединение, имеющее уреидные группы, имеет две уреидные группы в своей молекуле), помещали в емкость для хранения из нержавеющей стали объемом 100 л приблизительно на 1/2 ее объема, затем заполняли емкость для хранения азотом и хранили в течение 1095 дней при окружающих условиях во время хранения, характерных для района Коджима (Kojima district) города Курашики (Kurashiki city) префектуры Окаяма (Okayama prefecture) в Японии. Композиция также содержала другие компоненты, структура которых была неизвестна (такие как соединения, содержащие уреиленовые группы, и соединения, содержащие концевые биуретовые связи). Во время периода хранения емкость обогревали с помощью водяной рубашки с циркулирующей горячей водой при 40°C (регулируемой от приблизительно 30 до 50°C). Во время периода хранения температура временами падала приблизительно до 0°C и поднималась приблизительно до 50°C вследствие перебоев с подачей воды, отключений электроэнергии и регламентных работ по обслуживанию инженерных коммуникаций предприятия. Кроме того, температура однажды поднималась приблизительно до 80°C вследствие неполадок. При анализе композиции после хранения содержание в композиции 1,1'-(гексан-1,6-диил)димочевины составляло 92 моль.% по сравнению с содержанием до хранения. После периода хранения композицию нагревали до 180°C и вводили через подогреватель (устройство для подогрева композиции до 230°C) вблизи от середины ректификационной колонны с ситчатыми тарелками, имеющей внутренний диаметр 2,5 дюйма и 40 теоретических тарелок (ректификационную колонну эксплуатировали при снижении давления от нормального давления до пониженного давления в интервале температур жидкой фазы в нижней части ректификационной колонны от 150 до 300°C и поддержании рабочих условий; минимальное давление во время работы составляло около 0,3 КПа). N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый из 1,1'-(гексан-1,6-диил)димочевины и ароматической гидроксикомпозиции, в форме бис(4-(2,4,4-триметилпентан-2-ил)фенил)гексан-1,6-диил карбамата получали из нижней части ректификационной колонны. Аммиак, образующийся в качестве побочного продукта в реакции этерификации, небольшое количество ароматической гидроксикомпозиции и компонент, имеющий более низкую температуру кипения, чем ароматическая гидроксикомпозиция, извлекали из верхней части ректификационной колонны (включая побочный продукт в форме соединения, имеющего молекулярную массу 178 или менее и имеющего карбонильную группу, структуру которого идентифицировать не удалось). Выход изменялся от начала до конца работы вследствие колебаний рабочих условий, но при самом высоком уровне функционирования во время периода работы выход бис-(4-(2,4,4-триметилпентан-2-ил)фенил)гексан-1,6-диил)дикарбамата относительно 1,1'-(гексан-1,6-диил)димочевины в начале периода хранения составлял 87 моль.%. Не происходило забивки линий как во время хранения, так и в процессе транспортировки, и не наблюдалось образования твердого вещества внутри ректификационной колонны.
[ПРИМЕРЫ 97-144 И СРАВНИТЕЛЬНЫЕ ПРИМЕРЫ 3-6]
Хранение и этерификацию (реакцию получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции уреидных групп с ароматическим гидроксисоединением) осуществляли с использованием 1,1'-(гексан-1,6-диил)димочевины в качестве соединения, имеющего уреидные группы, при таких же условиях, как в примере 96, за исключением соотношений соединения, имеющего уреидные группы, ароматической гидроксикомпозиции, аммиака, производной угольной кислоты и других подобных соединений в композициях, и результаты ректификации приведены в таблицах 37-44. Выходы N-замещенной карбаминовой кислоты-O-арилового эфира указаны как значения, полученные путем анализа жидкофазного компонента из нижней части ректификационной колонны с ситчатыми тарелками.
В таблицах ArOH представляет ароматическое гидроксисоединение, которое составляет ароматическую гидроксикомпозицию. Содержание каждого компонента в композиции представлено в массовых процентах (масс.%), получаемых путем округления содержаний соединения, имеющего уреидные группы, ароматической гидроксикомпозиции, воды и аммиака до числа значащих цифр аналитического прибора или менее, металлические компоненты выражаются в ppm, в то время как другие компоненты (такие как производная угольной кислоты) указаны как отношение числа их молекул к числу уреидных групп, которые составляют соединение (или содержатся в соединении), имеющее уреидные группы. (Если не указано иначе, то такие явления как забивка или образование твердого вещества не происходят во время хранения и транспортировки).
Спектры 1H-ЯМР композиций для транспортировки и хранения соединения, имеющего уреидные группы, примеров 97, 106, 122 и 142 приведены на фигурах 23, 24, 25 и 26, соответственно.
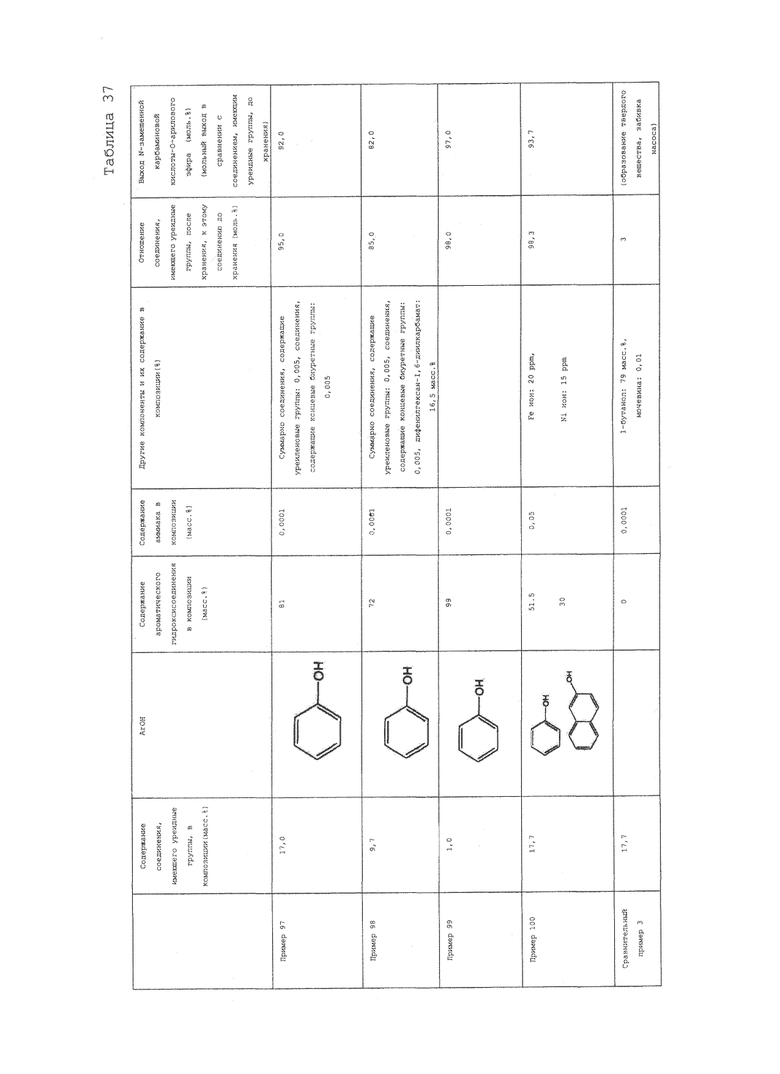
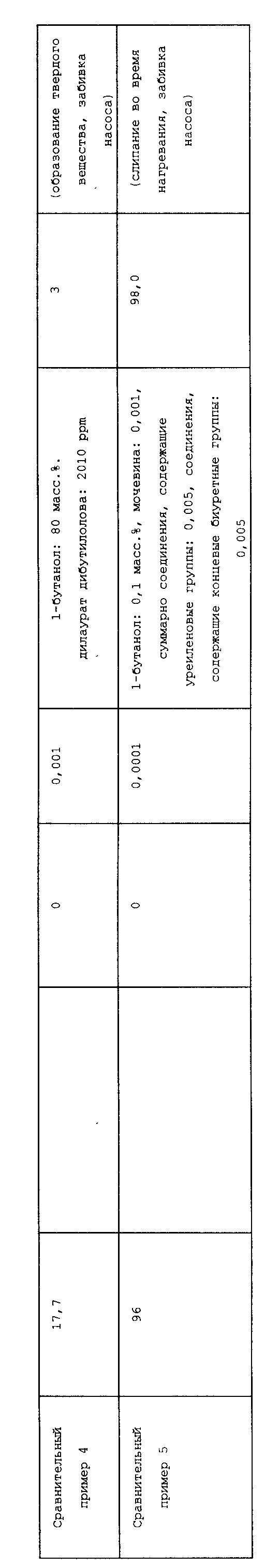
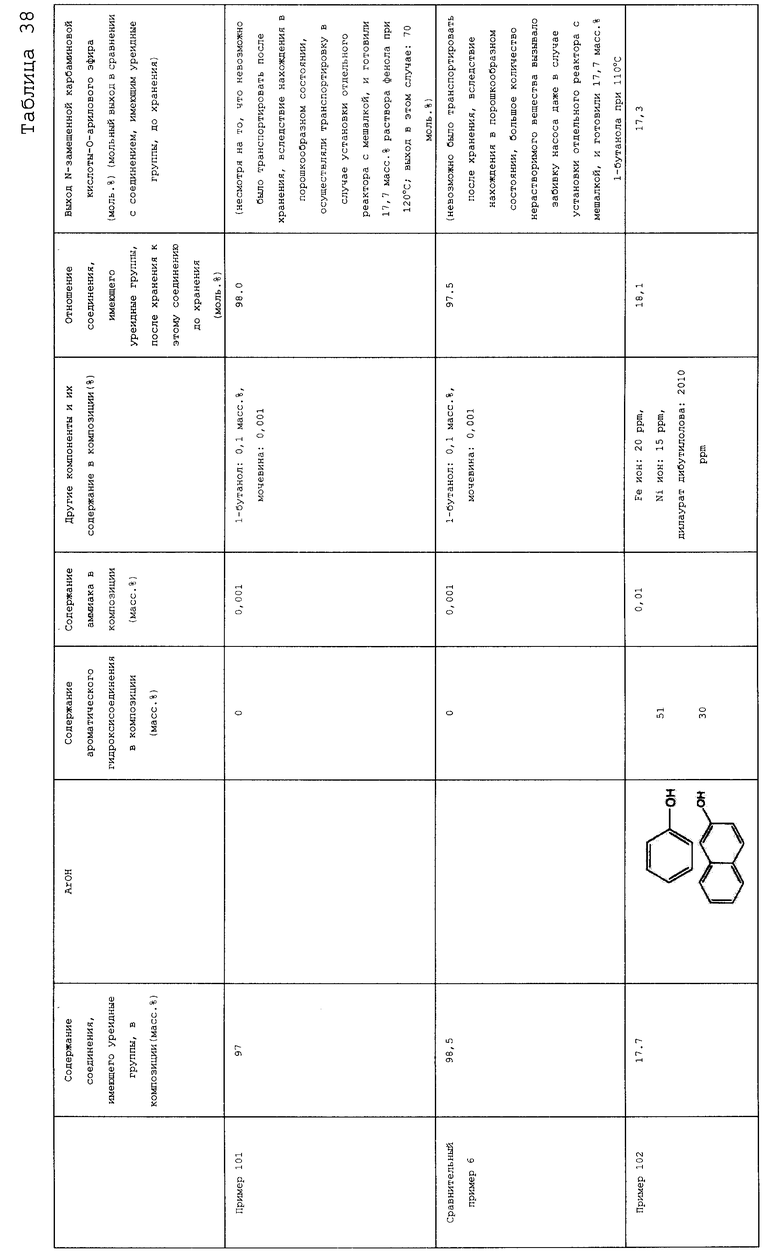
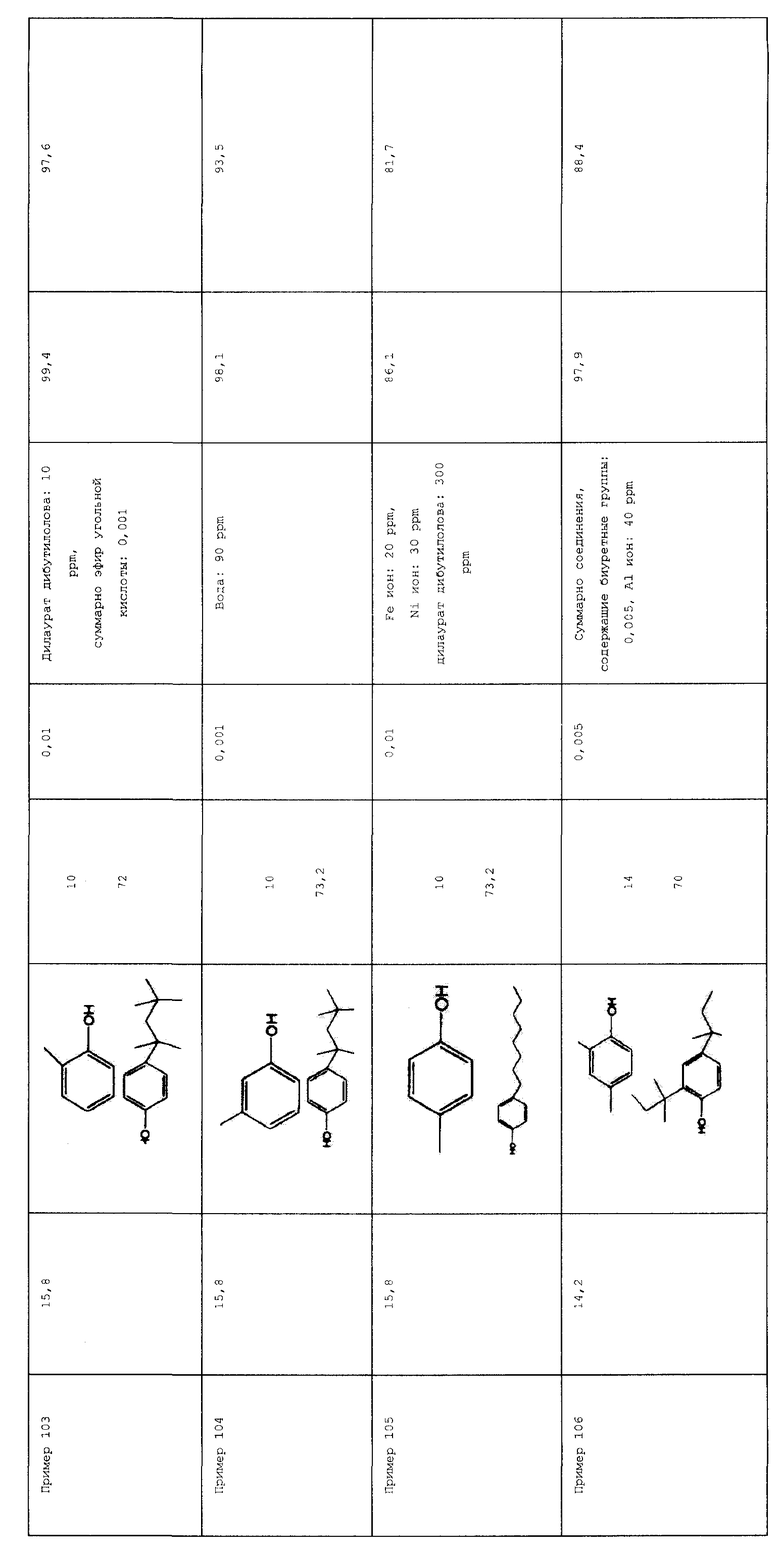
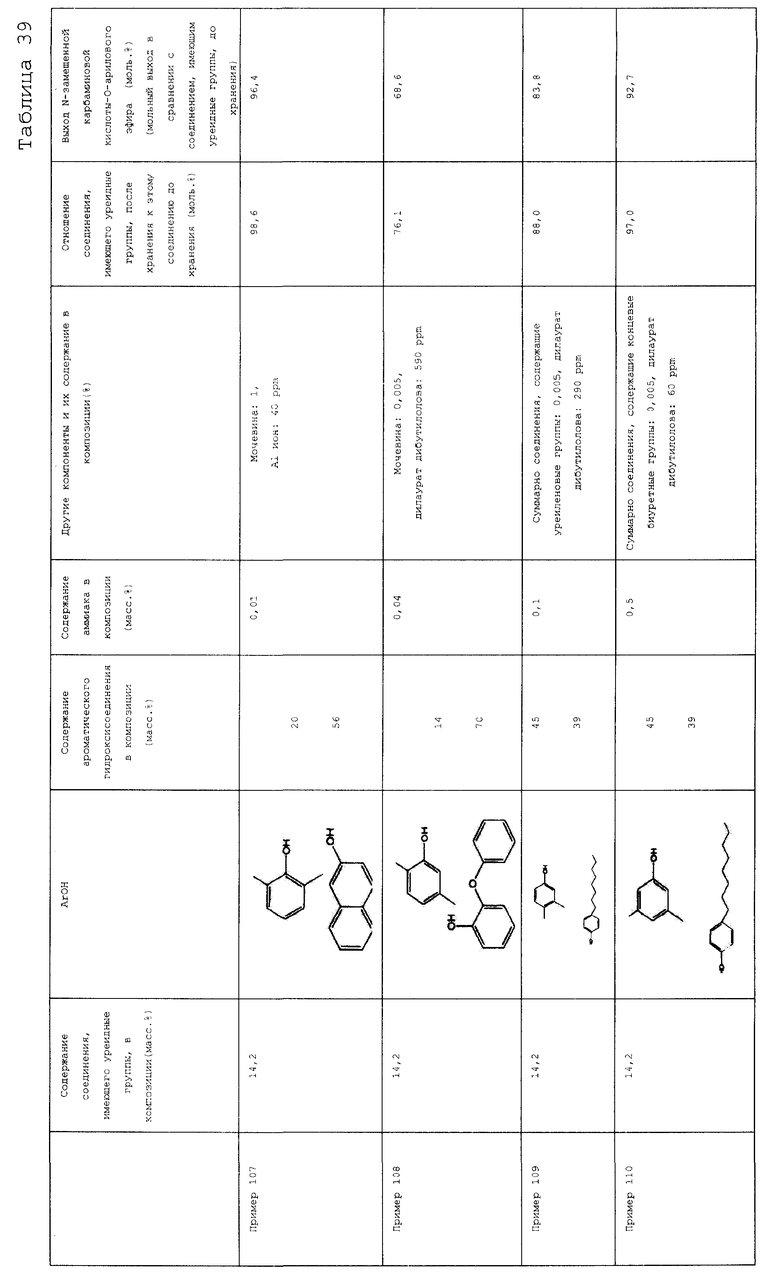
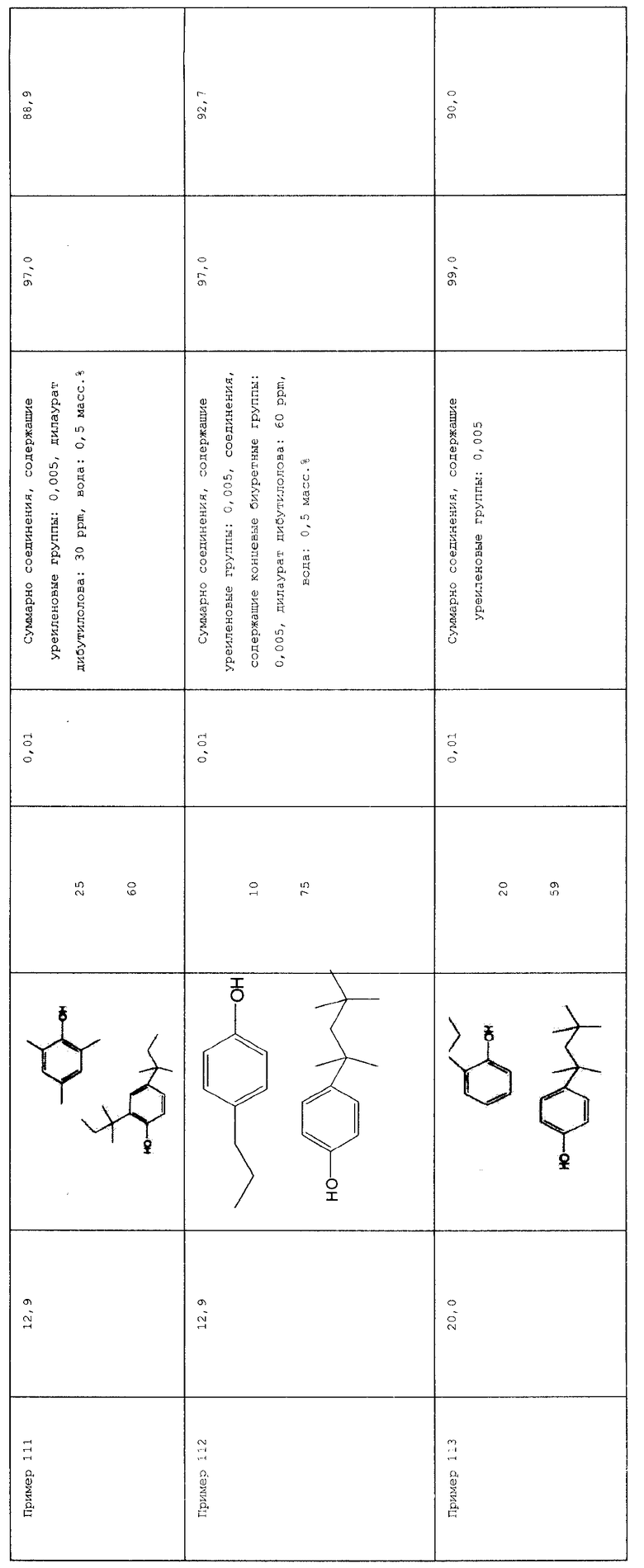
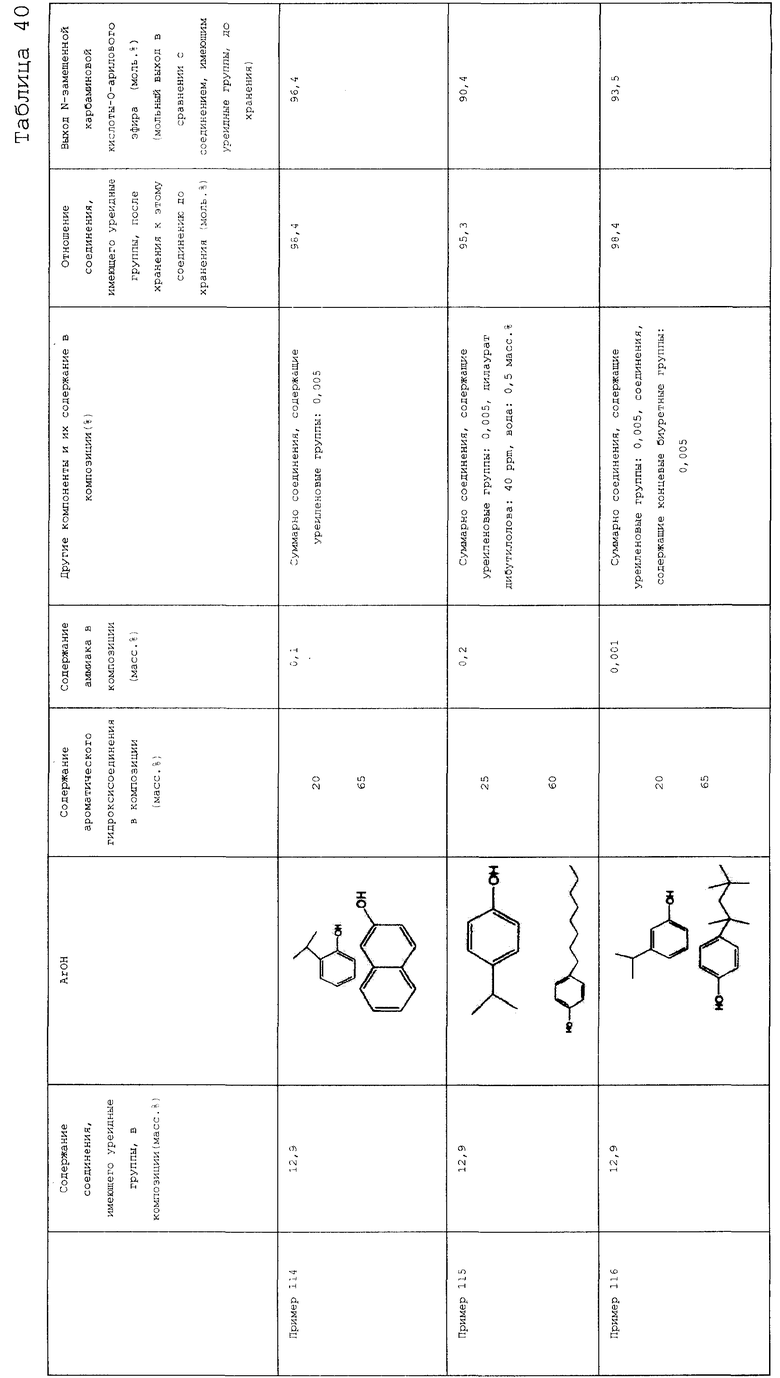
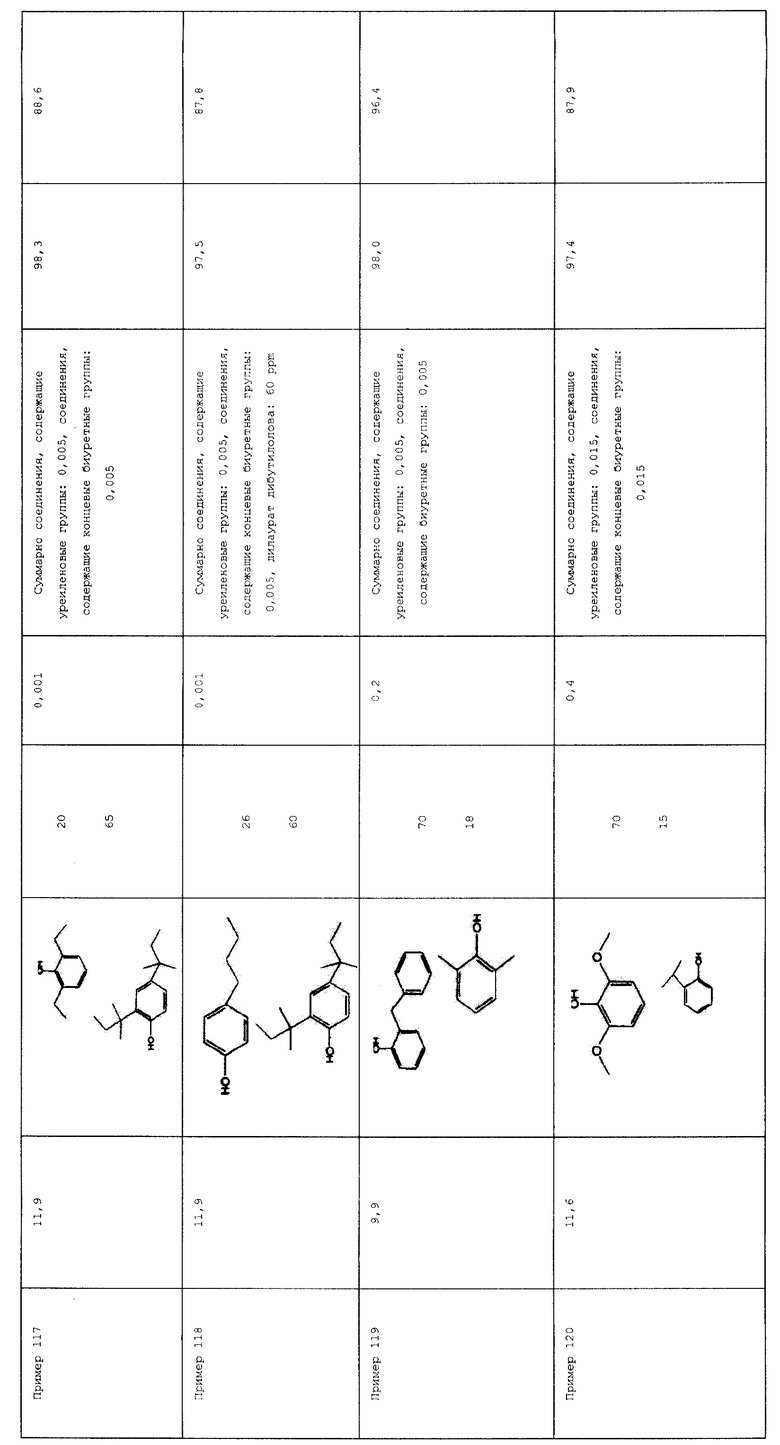
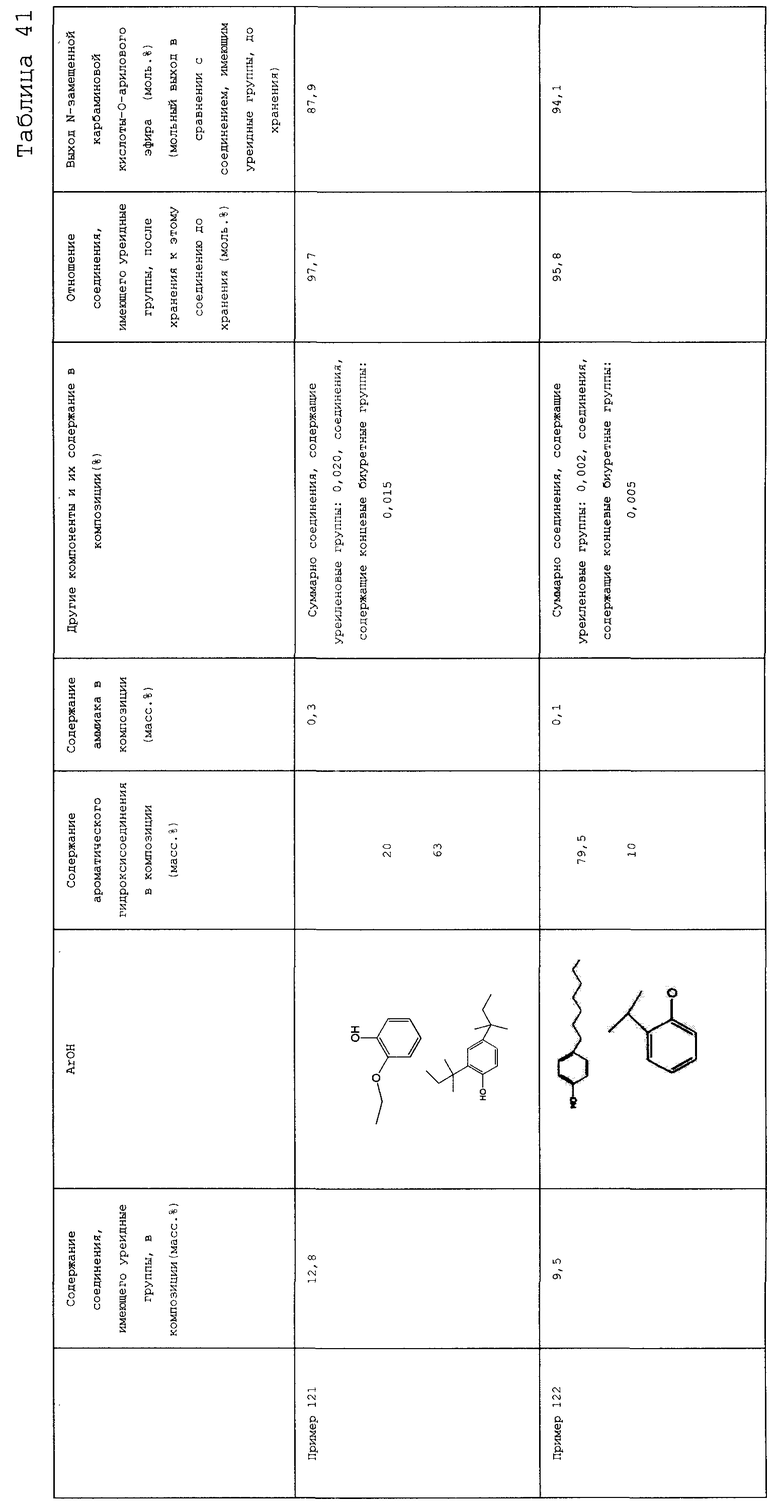
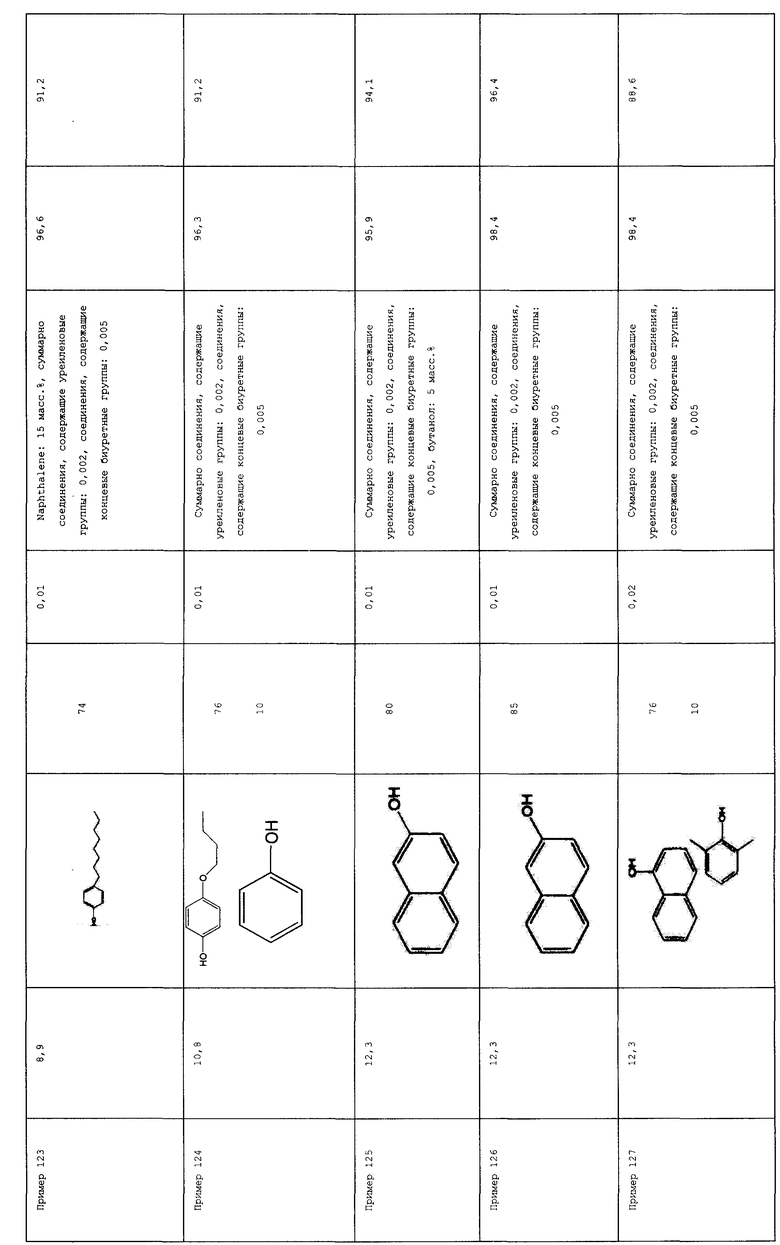
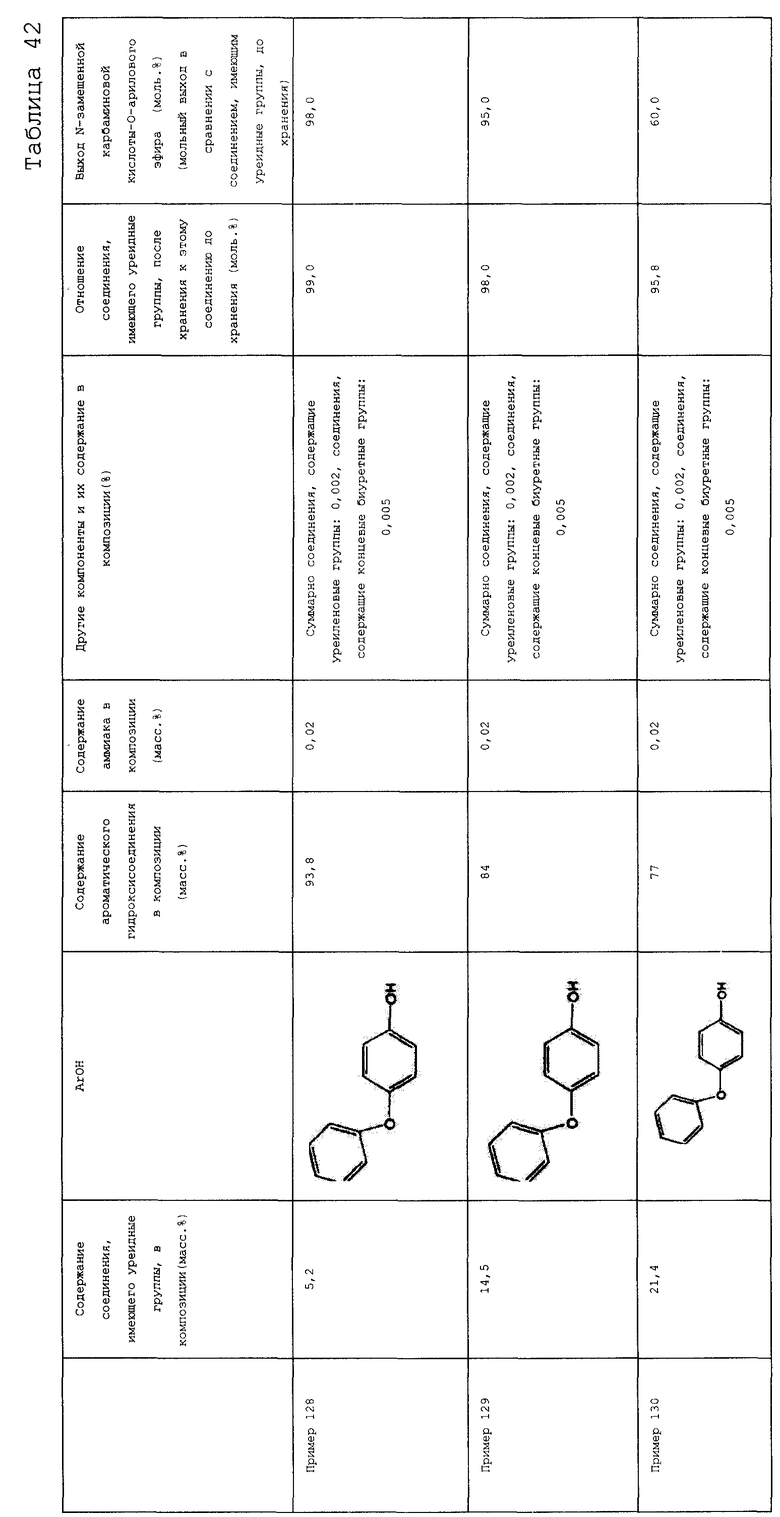
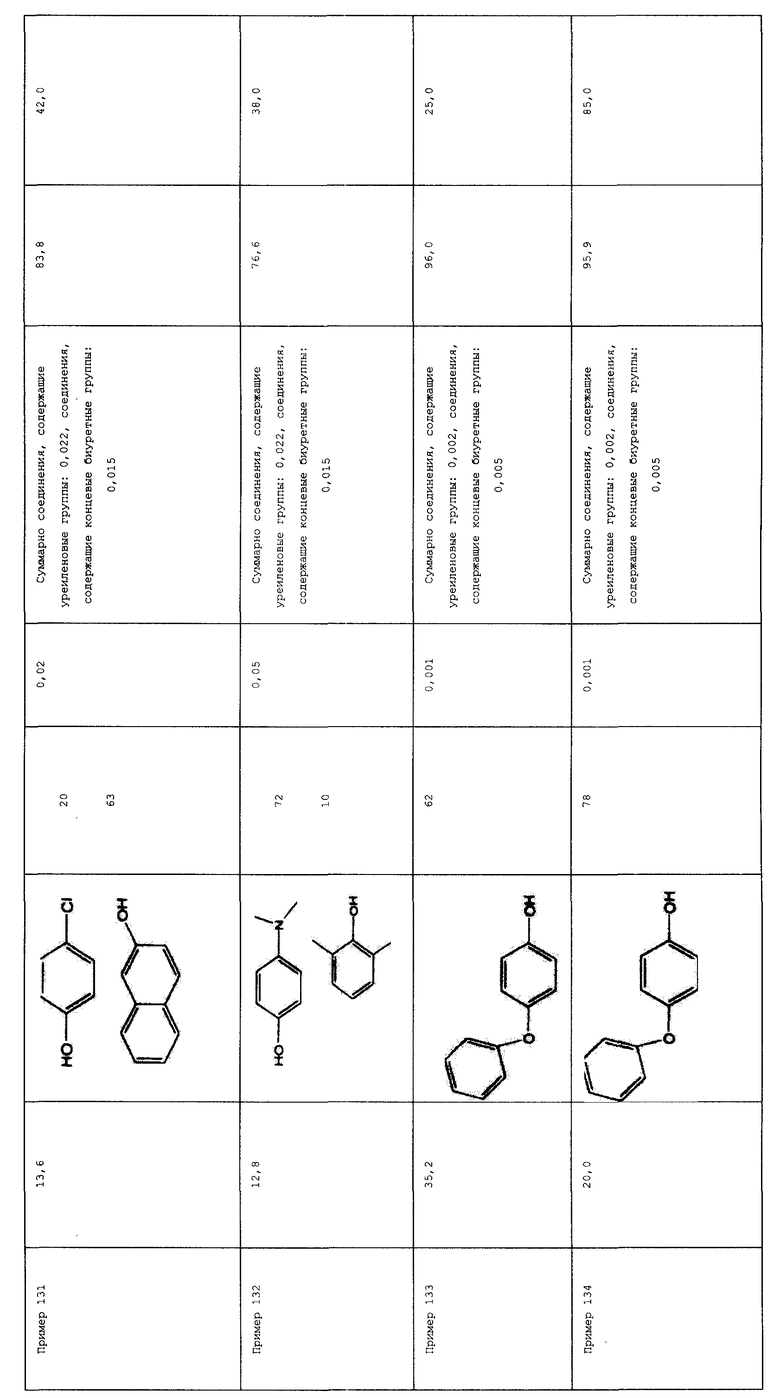
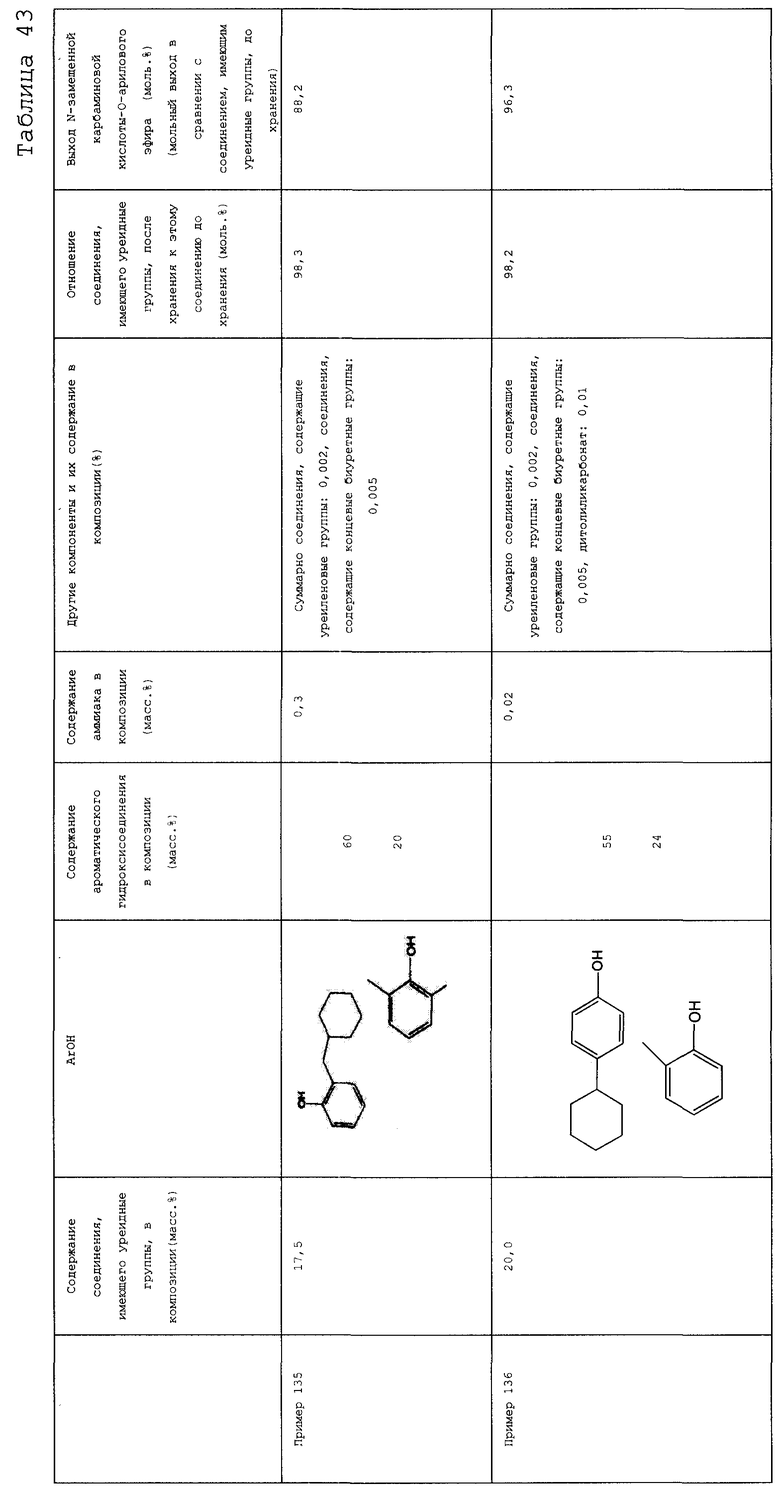
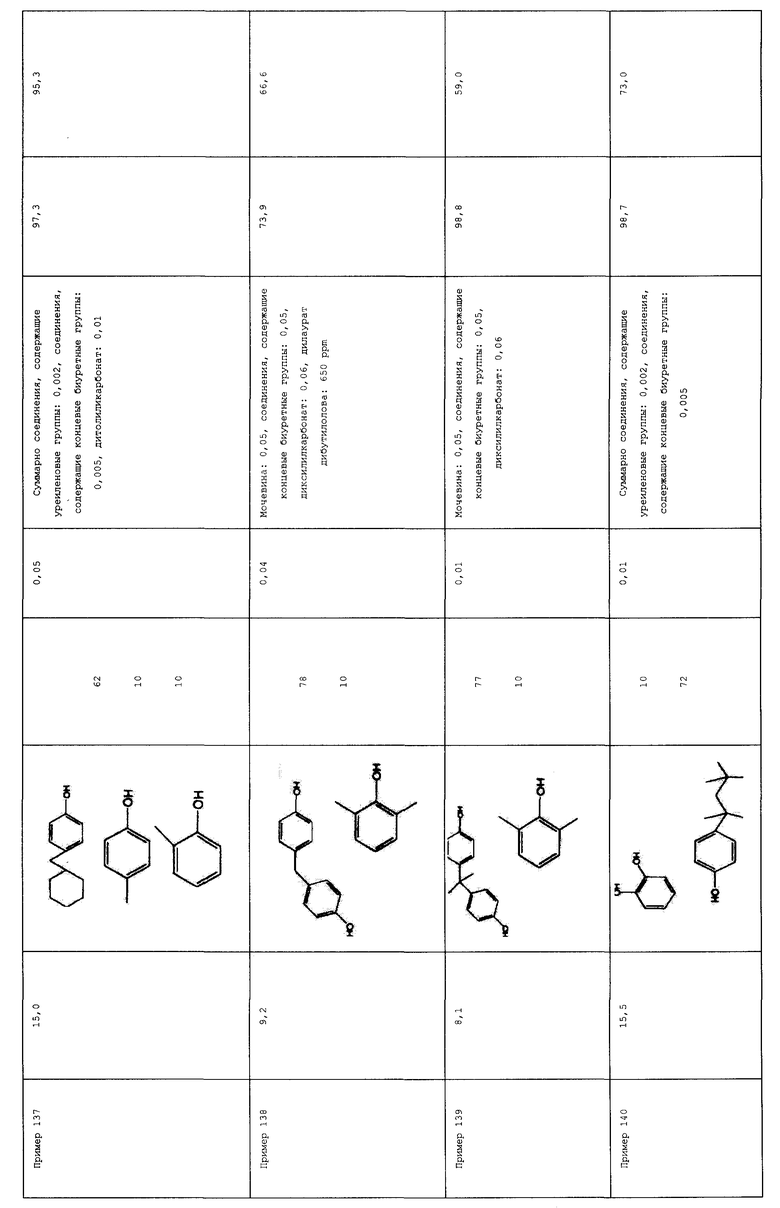
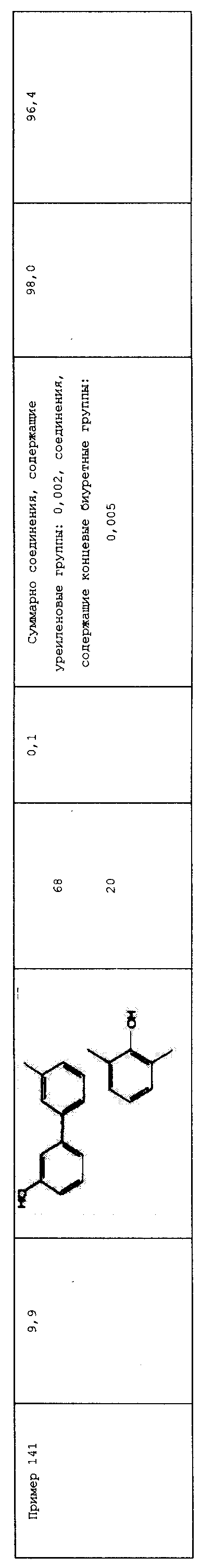
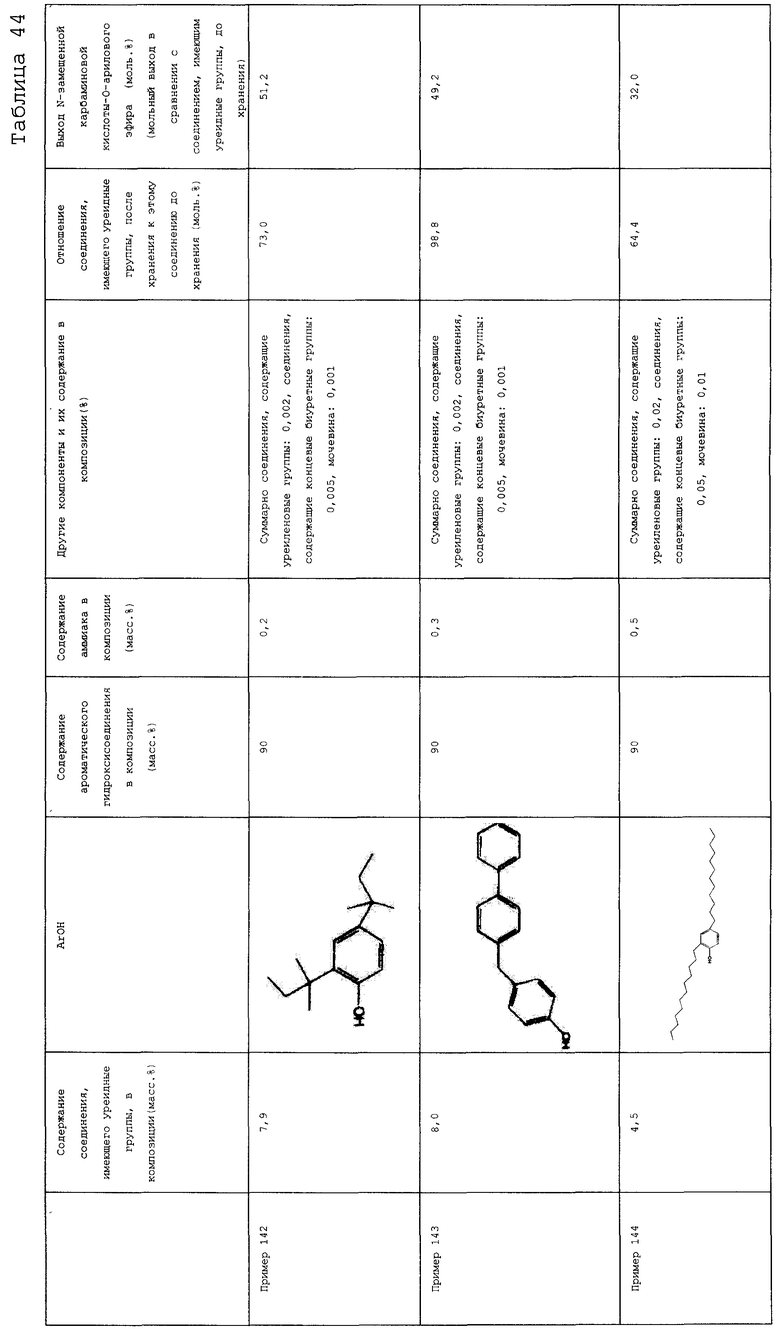
[ПРИМЕР 145]
Композицию, содержащую 21% по массе соединения, имеющего уреидные группы, представленную следующей формулой (200), 77% по массе ароматической гидроксикомпозиции в форме фенола, 0,01% по массе аммиака и мочевины при соотношении 0,01 (обозначающим отношение числа молекул мочевины к числу уреидных групп, которые составляют (или содержатся в) соединение, имеющее уреидные группы, или, другими словами, 0,01 обозначает 0,02 мольных эквивалентов, так как соединение, имеющее уреидные группы, имеет две уреидные группы в своей молекуле) помещали в емкость для хранения из нержавеющей стали объемом 100 л приблизительно на 1/2 ее объема, затем заполняли емкость для хранения азотом и хранили в течение 1095 дней при окружающих условиях во время хранения, характерных для района Коджима (Kojima district) города Курашики (Kurashiki city) префектуры Окаяма (Okayama prefecture) в Японии. Композиция также содержала другие компоненты, структура которых была неизвестна (такие как соединения, содержащие уреиленовые группы, и соединения, содержащие концевые биуретовые связи). Во время периода хранения емкость обогревали с помощью водяной рубашки с циркулирующей горячей водой при 40°C (регулируемой от приблизительно 30 до 50°C). Во время периода хранения температура временами падала приблизительно до 0°C и поднималась приблизительно до 50°C вследствие перебоев с подачей воды, отключений электроэнергии и регламентных работ по обслуживанию инженерных коммуникаций предприятия. Кроме того, температура однажды поднималась приблизительно до 80°C вследствие неполадок. При анализе композиции после хранения содержание соединения, имеющего уреидные группы, в композиции составляло около 93 моль.% по сравнению с содержанием до хранения. После периода хранения композицию нагревали до 180°C и вводили через подогреватель (устройство для подогрева композиции до 230°C) вблизи от середины ректификационной колонны с ситчатыми тарелками, имеющей внутренний диаметр 2,5 дюйма и 40 теоретических тарелок (ректификационную колонну эксплуатировали при снижении давления от нормального давления до пониженного давления при интервале температур жидкой фазы в нижней части ректификационной колонны от 150 до 300°C и поддержании рабочих условий; минимальное давление во время работы составляло около 0,3 КПа). N-замещенной карбаминовой кислоты-O-ариловый эфир, получаемый из соединения, имеющего уреидные группы, и ароматической гидроксикомпозиции получали из нижней части ректификационной колонны. Аммиак, образующийся в качестве побочного продукта в реакции этерификации, небольшое количество ароматической гидроксикомпозиции, и компонент, имеющий более низкую температуру кипения, чем ароматическая гидроксикомпозиция, извлекали из верхней части ректификационной колонны (включая побочный продукт в форме соединения, имеющего молекулярную массу 178 или менее и имеющего карбонильную группу, структуру которого идентифицировать не удалось). Выход изменялся от начала до конца работы вследствие колебаний рабочих условий, но при самом высоком уровне функционирования во время периода работы выход N-замещенной карбаминовой кислоты-O-арилового эфира относительно соединения, имеющего уреидные группы, в начале периода хранения составлял 87 моль.%. Не происходило забивки линий как во время хранения, так и в процессе транспортировки, и не наблюдалось образования твердого вещества внутри ректификационной колонны.
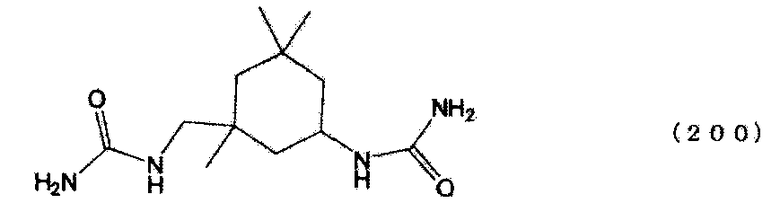
[ПРИМЕРЫ 146-186 И СРАВНИТЕЛЬНЫЕ ПРИМЕРЫ 7-10]
Хранение и этерификацию (реакцию получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции уреидных групп с ароматическим гидроксисоединением) осуществляли с использованием соединения, имеющего уреидные группы, представленного формулой (200) в пример 145, при таких же условиях, как в примере 145, за исключением соотношений соединения, имеющего уреидные группы, ароматической гидроксикомпозиции, аммиака, производной угольной кислоты и других подобных соединений в композициях, и результаты ректификации приведены в таблицах 45-50. Выходы N-замещенной карбаминовой кислоты-O-арилового эфира указаны как значения, полученные путем анализа жидкофазного компонента из нижней части ректификационной колонны с ситчатыми тарелками.
В таблицах ArOH представляет ароматическое гидроксисоединение, которое составляет ароматическую гидроксикомпозицию. Содержание каждого компонента в композиции представлено в массовых процентах (масс.%), получаемых путем округления содержаний соединения, имеющего уреидные группы, ароматической гидроксикомпозиции, воды и аммиака до числа значащих цифр аналитического прибора или менее, металлические компоненты выражаются в ppm, в то время как другие компоненты (такие как производная угольной кислоты) указаны как отношение числа их молекул к числу уреидных групп, которые составляют (или содержатся в) соединение, имеющее уреидные группы. (Если не указано иначе, то такие явления как забивка или образование твердого вещества не происходят во время хранения и транспортировки).
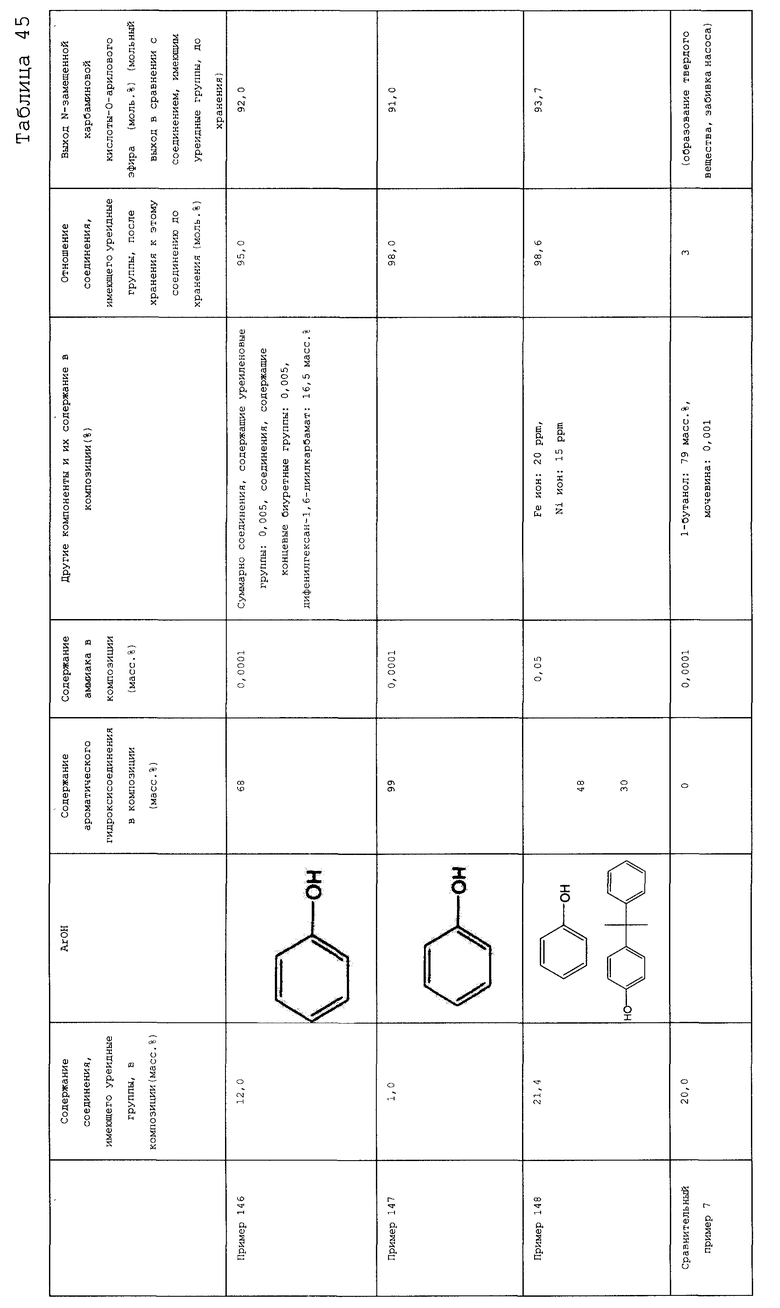
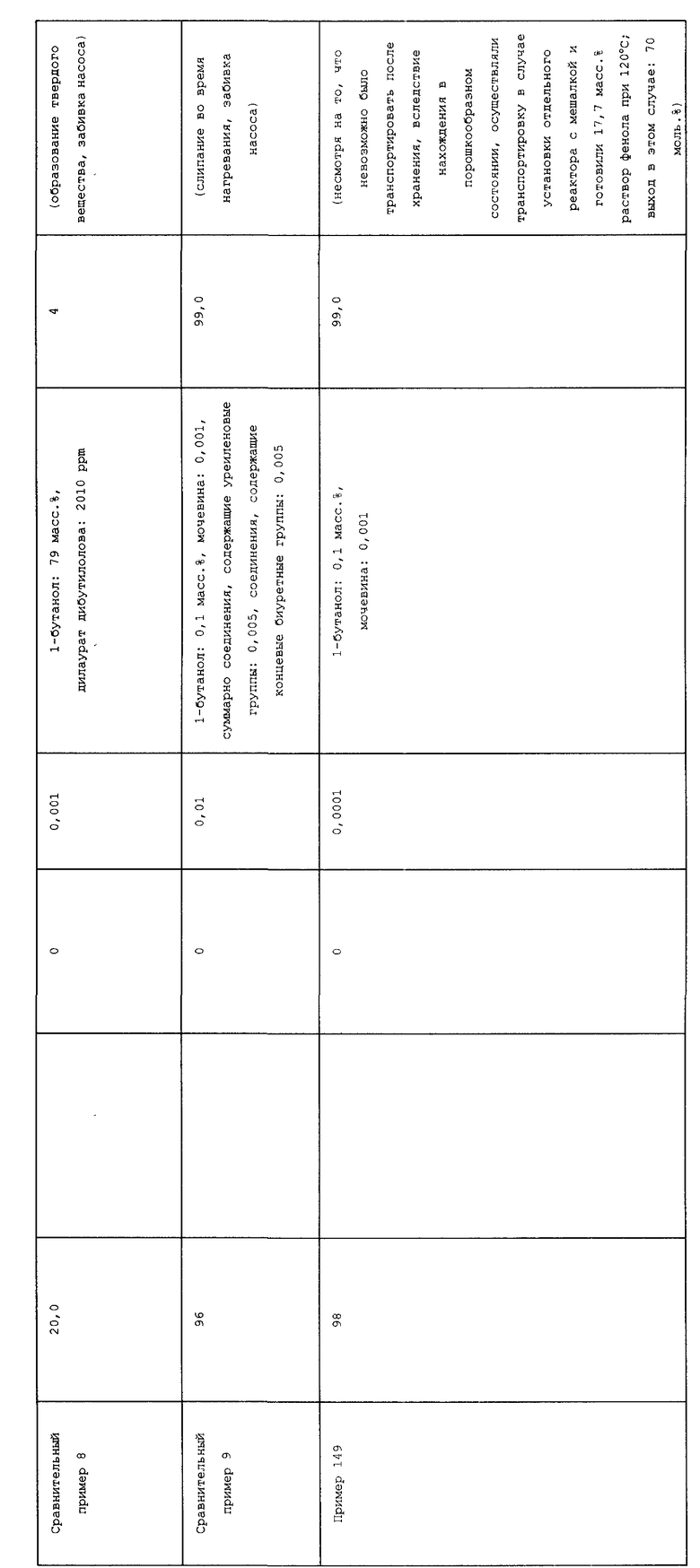
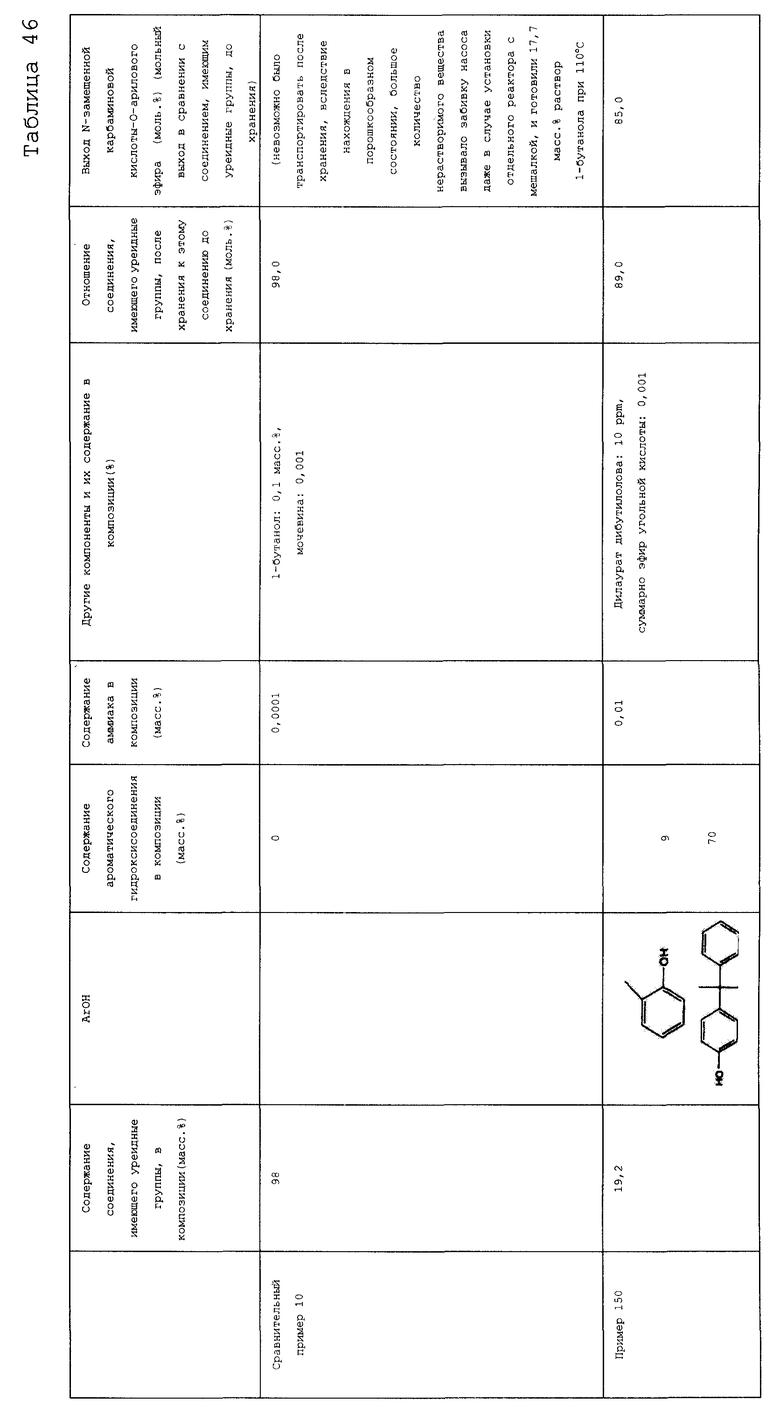
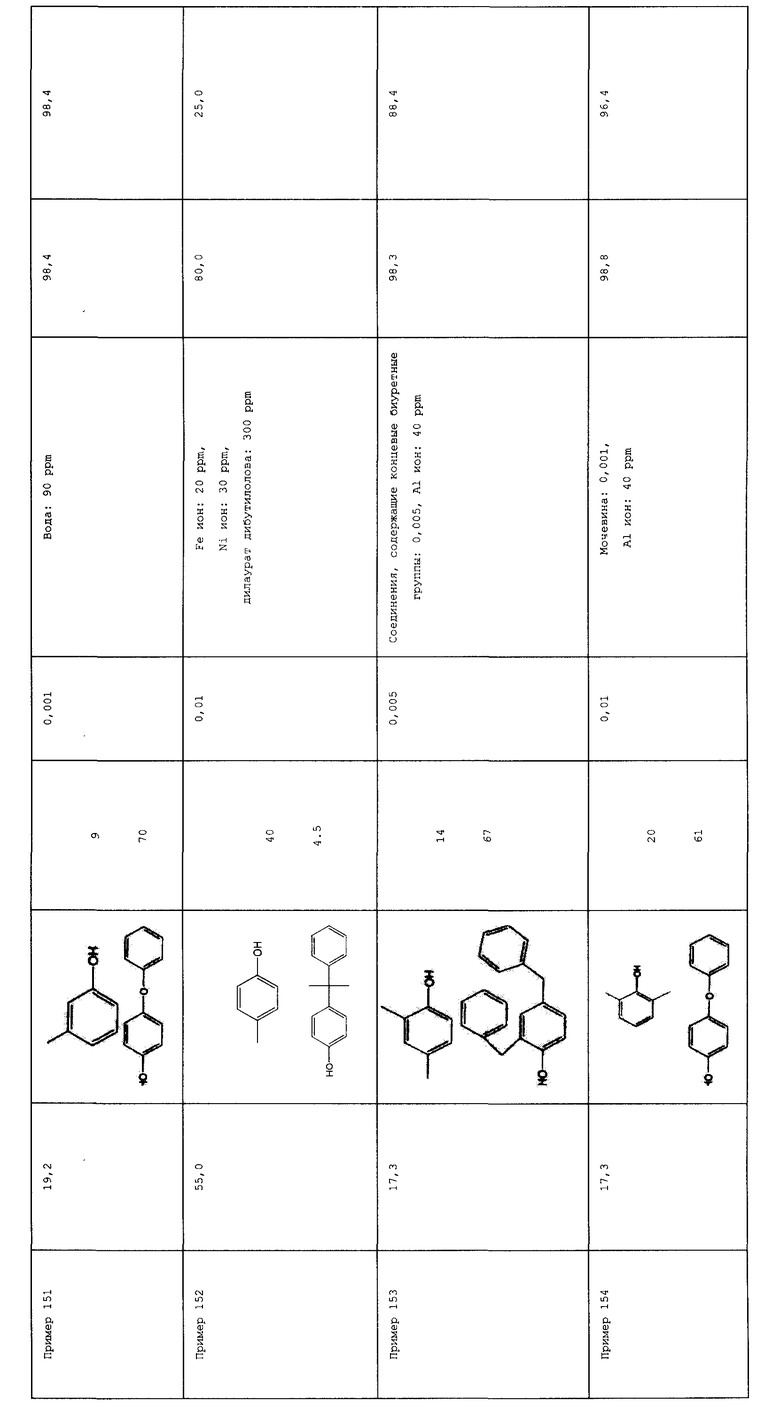
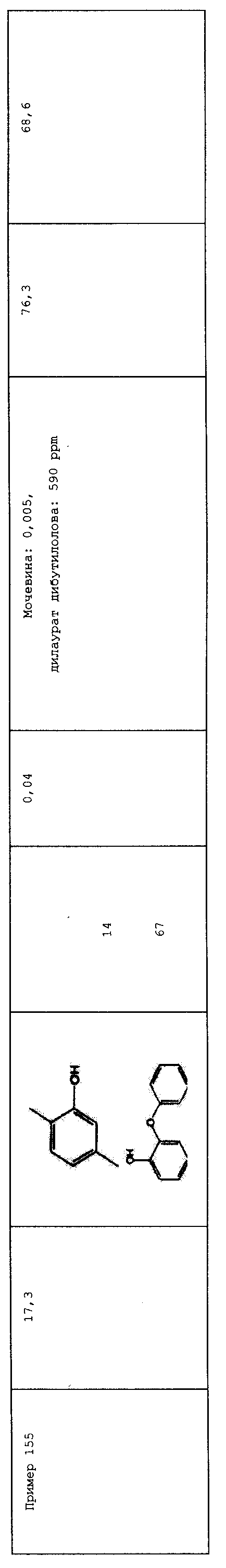
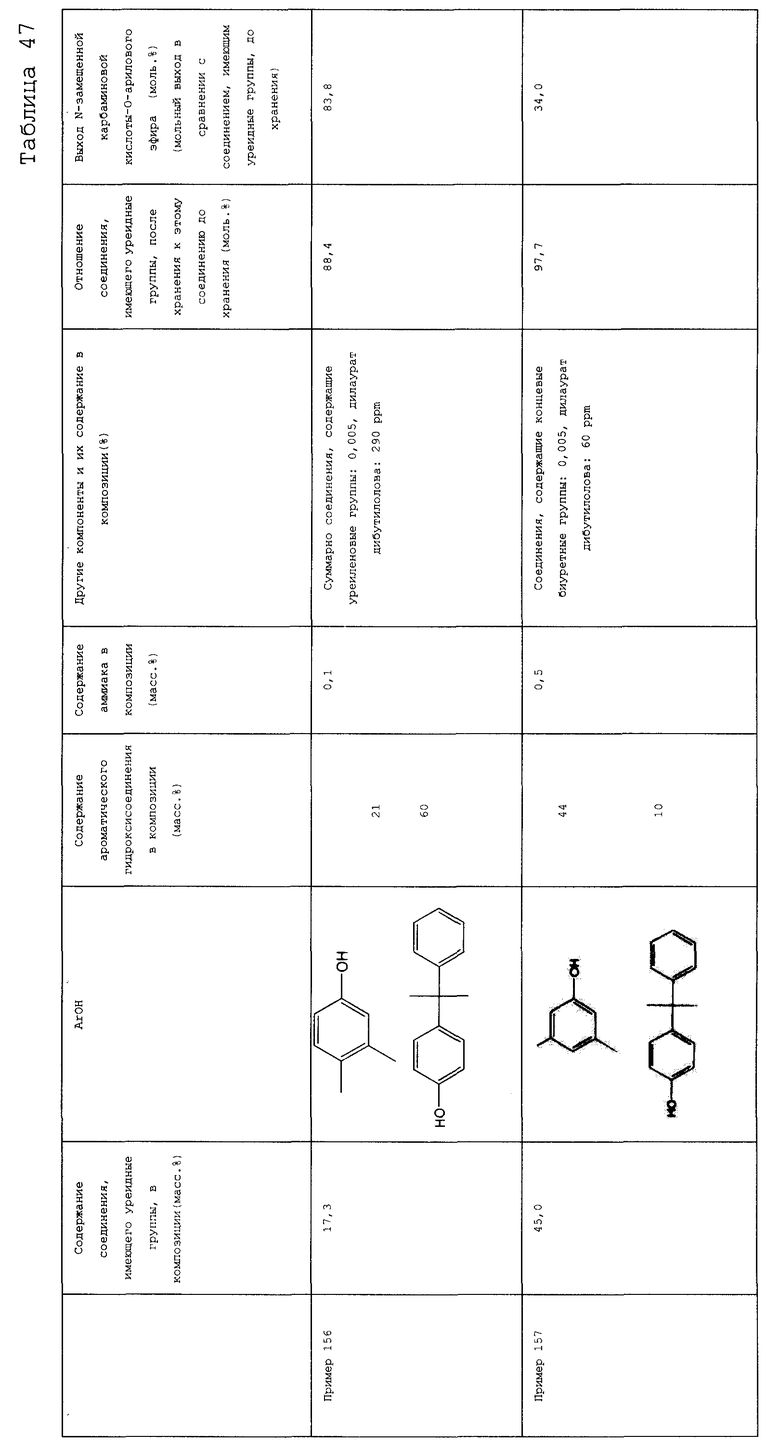
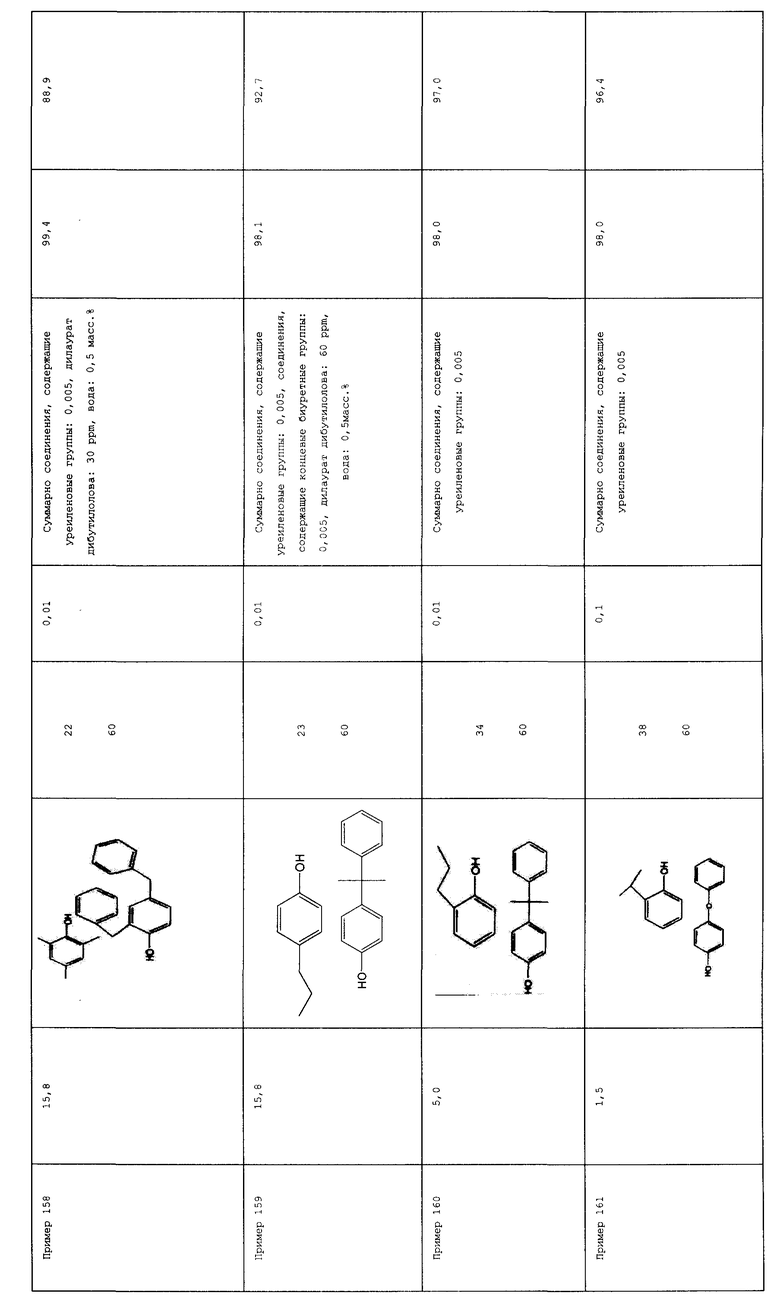
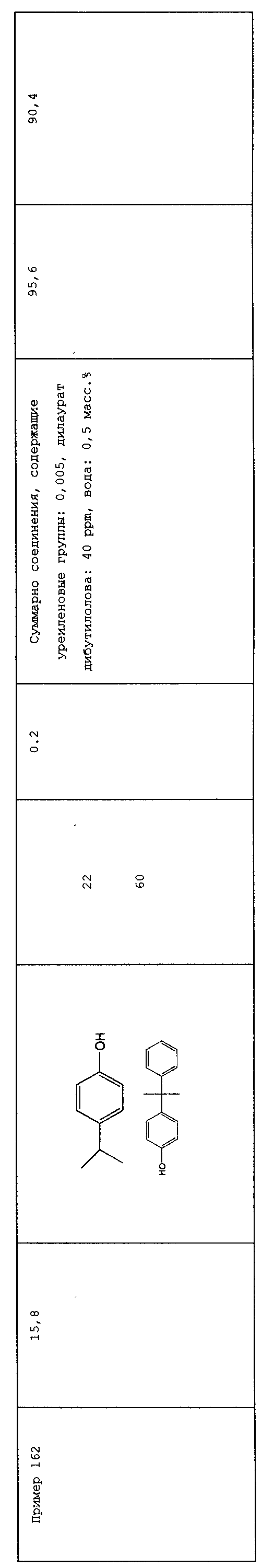

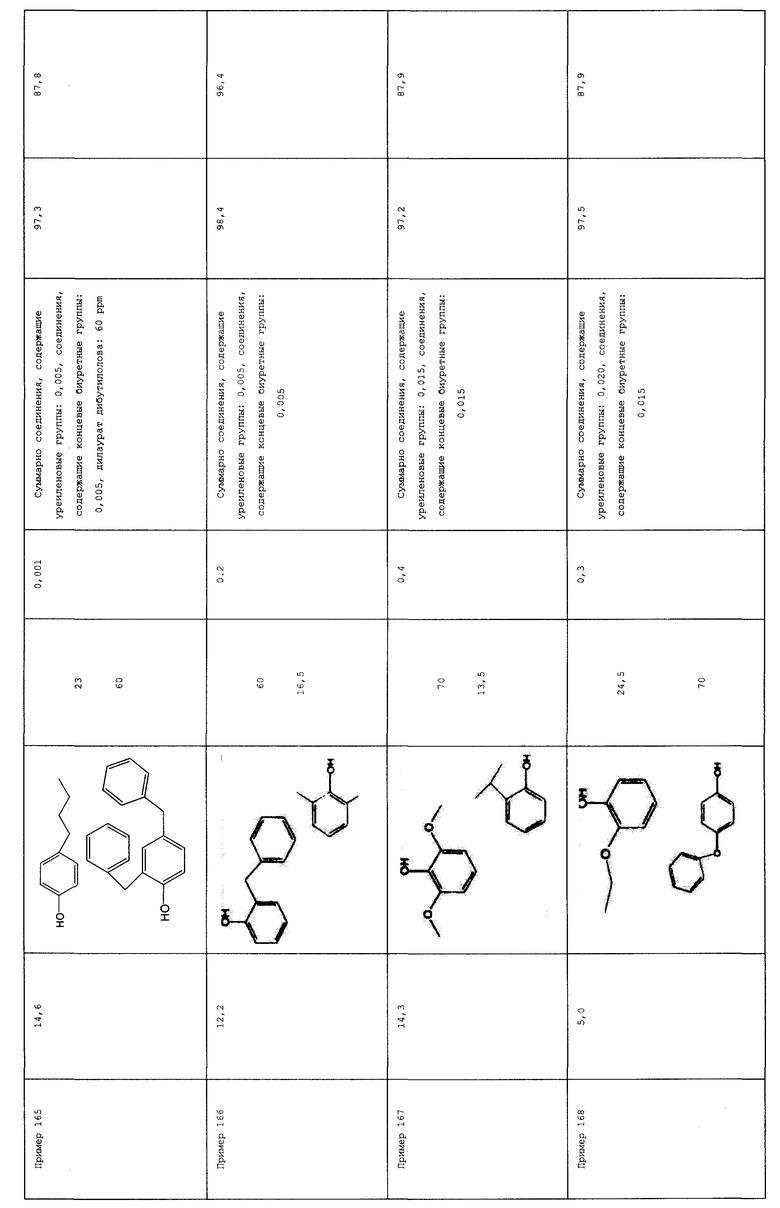
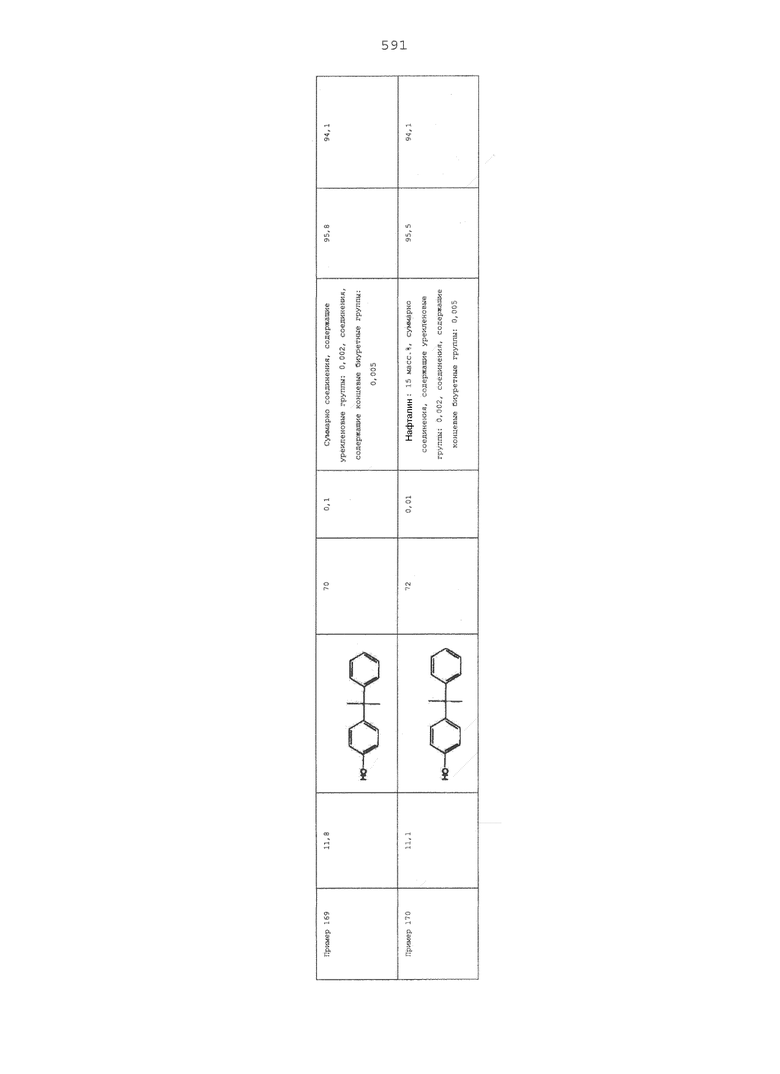
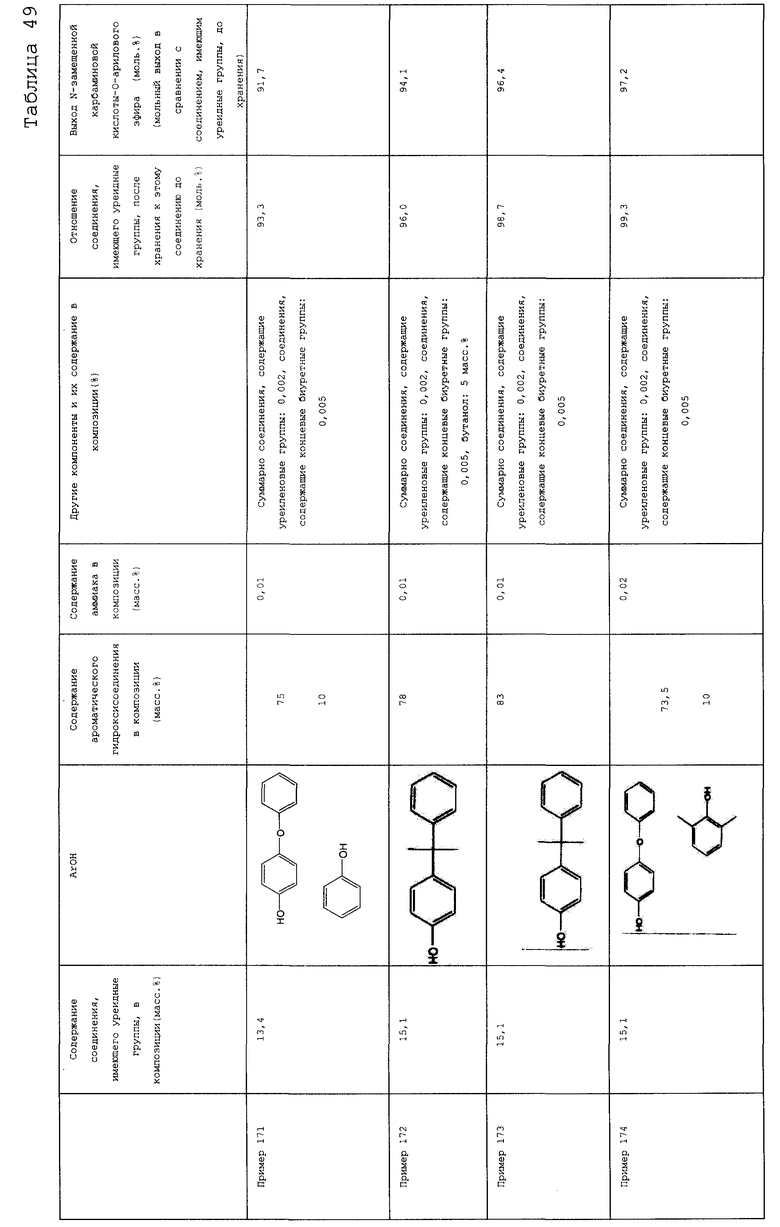
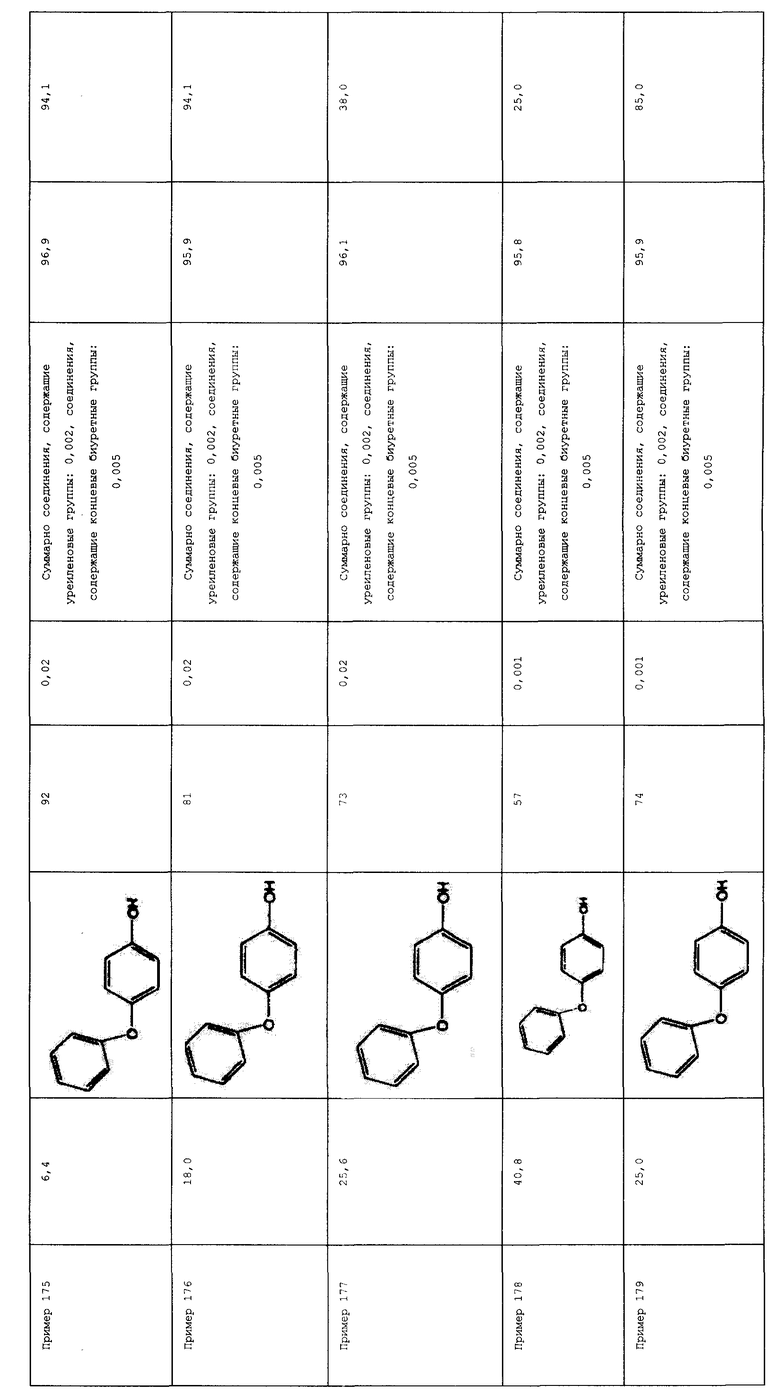
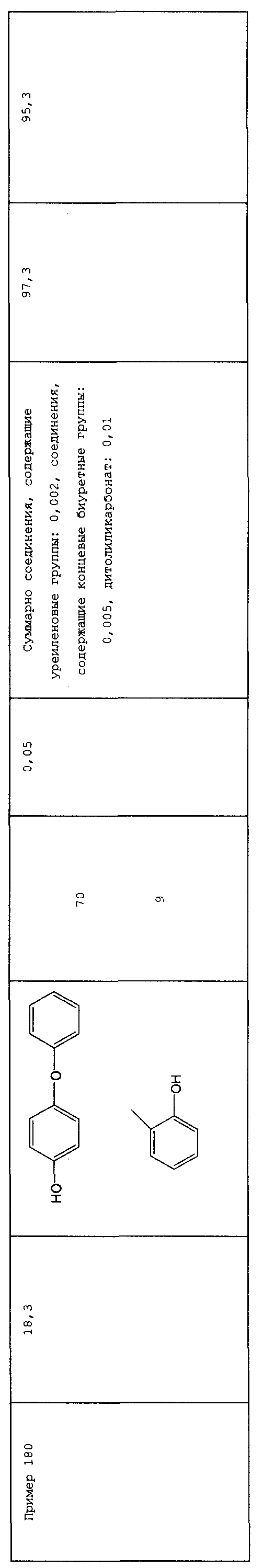
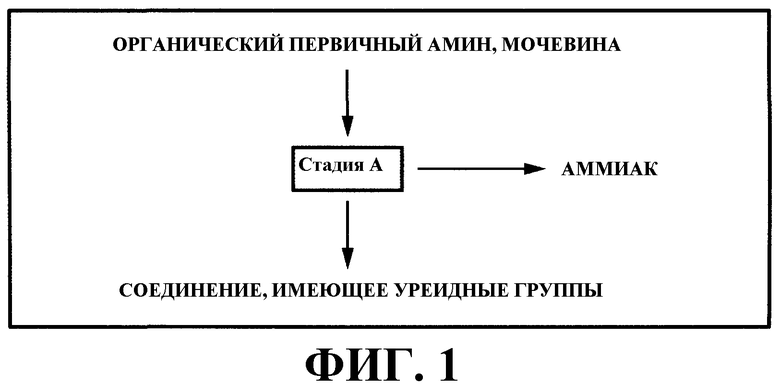
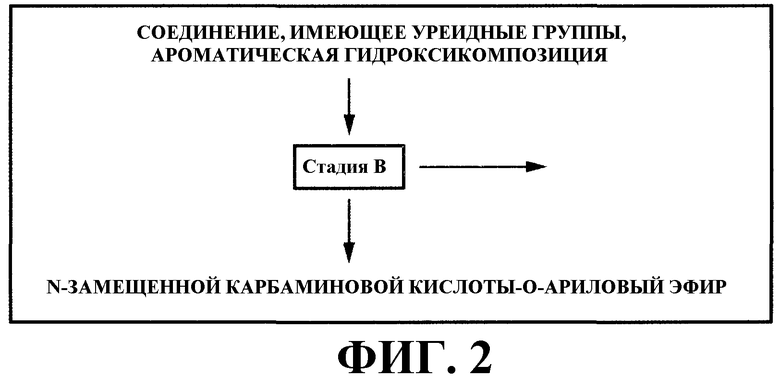
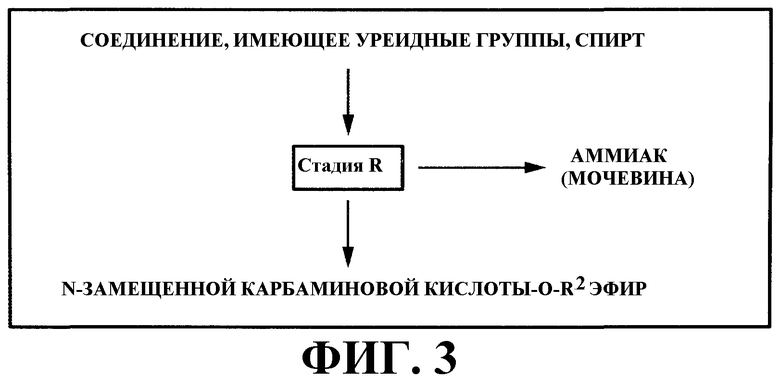
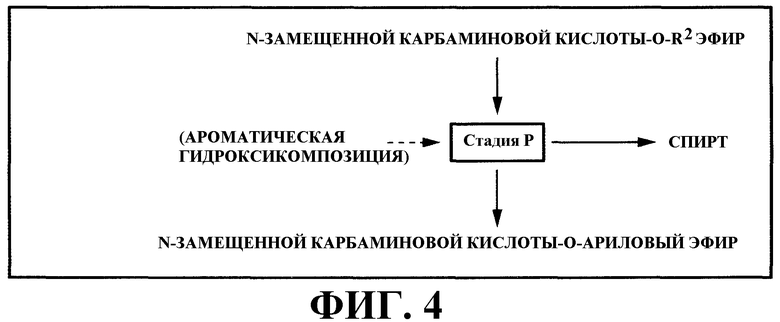
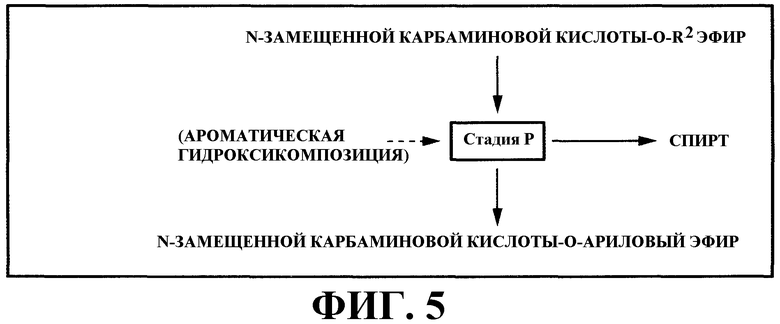
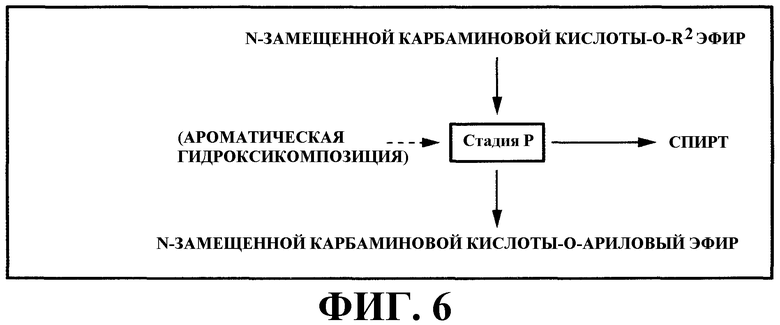
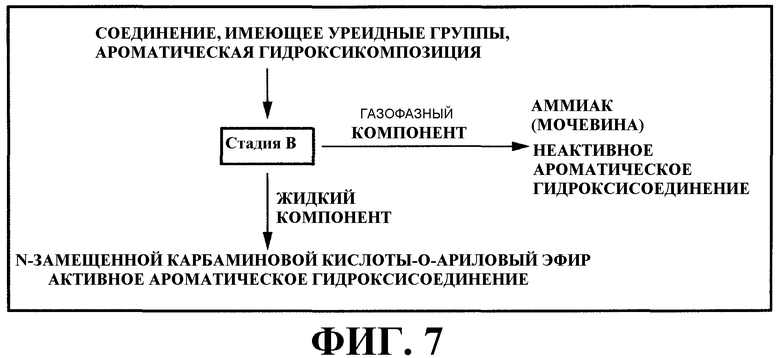
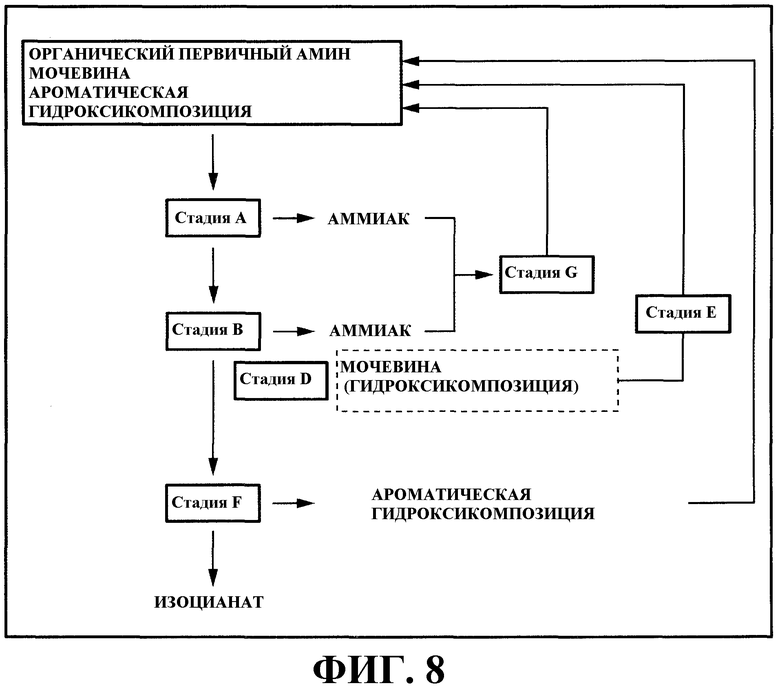
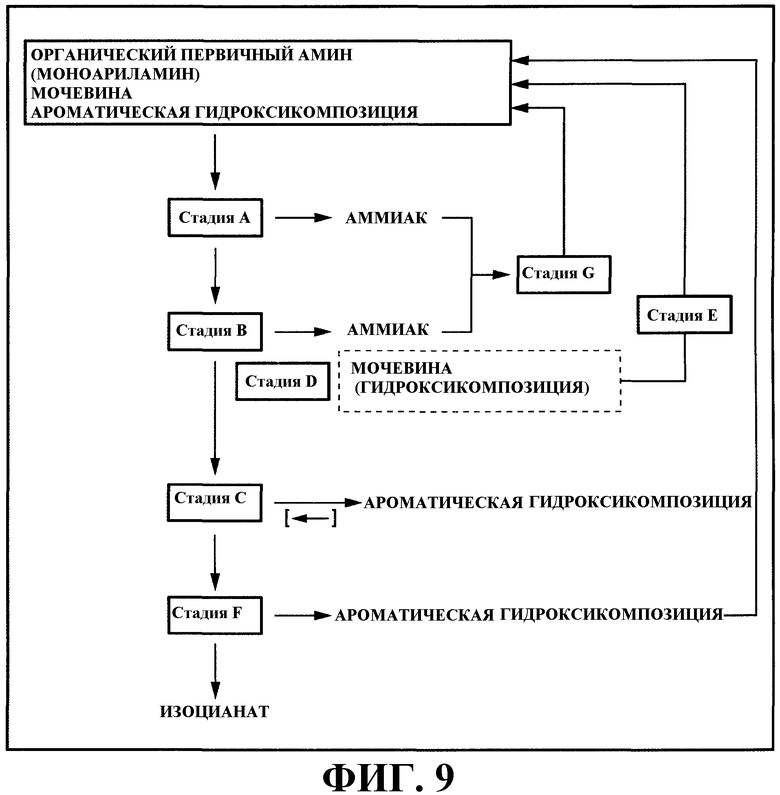
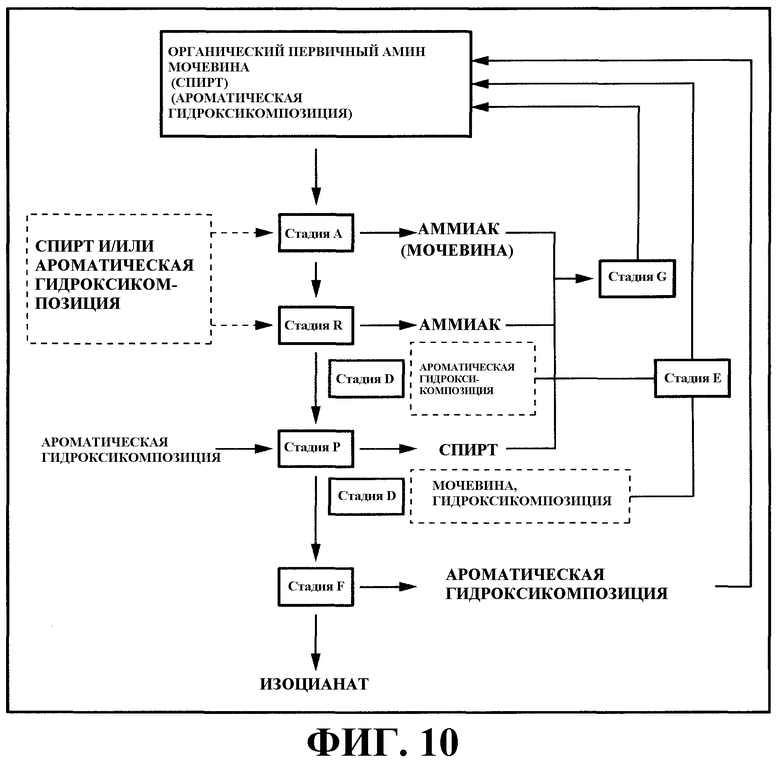
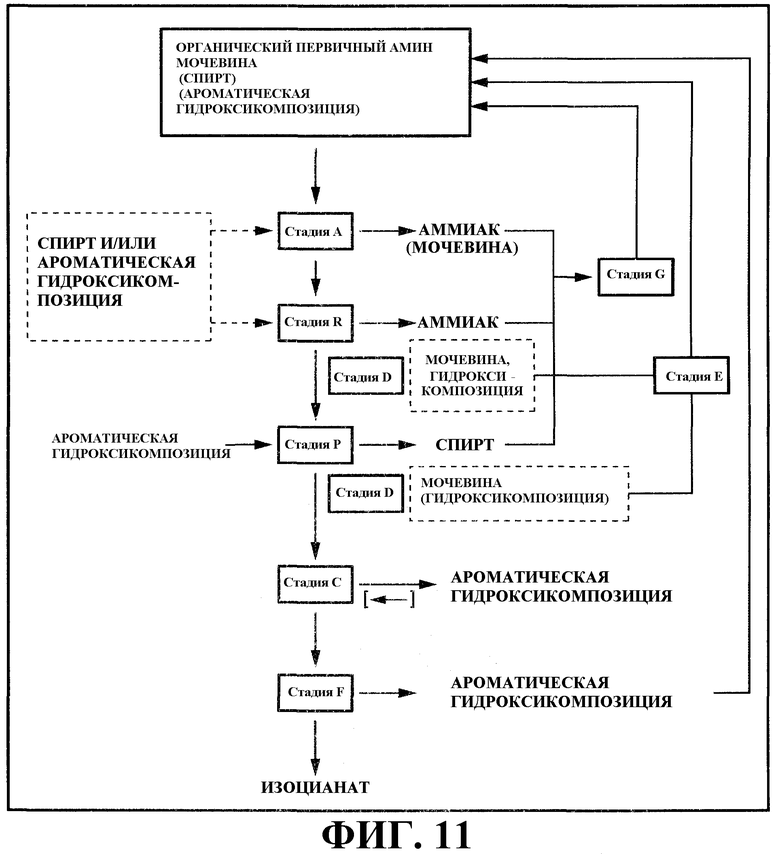
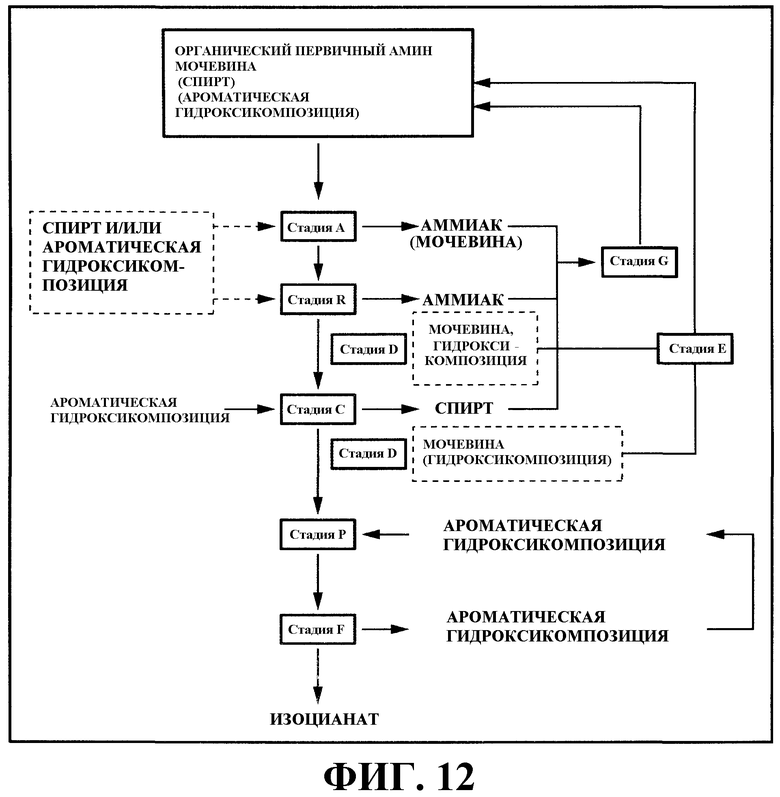
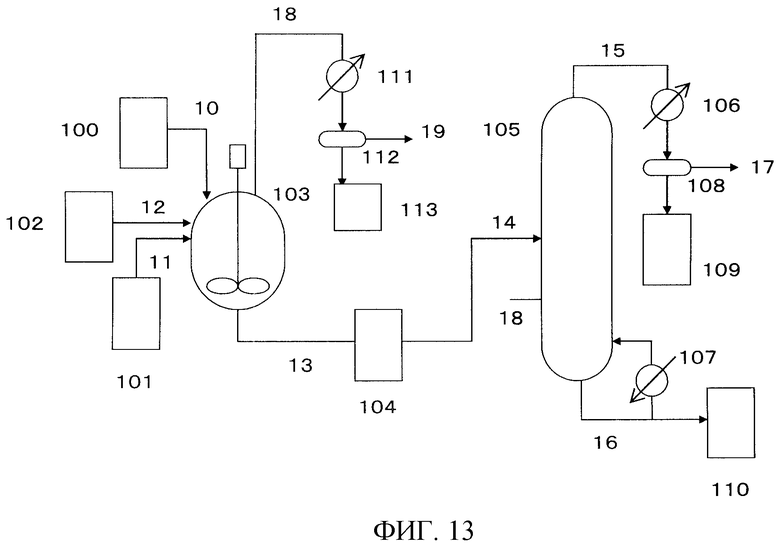
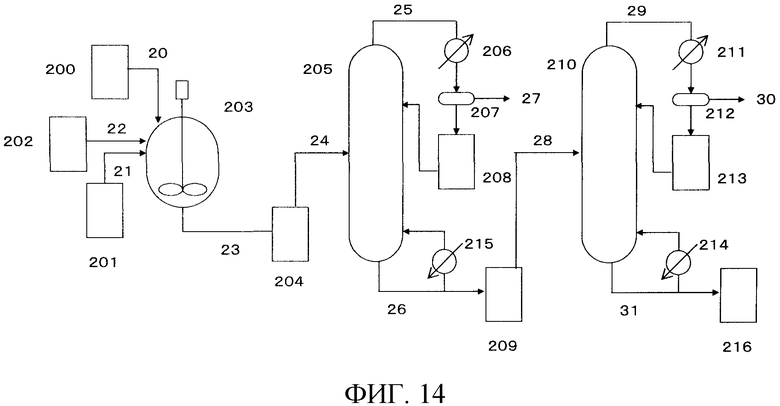
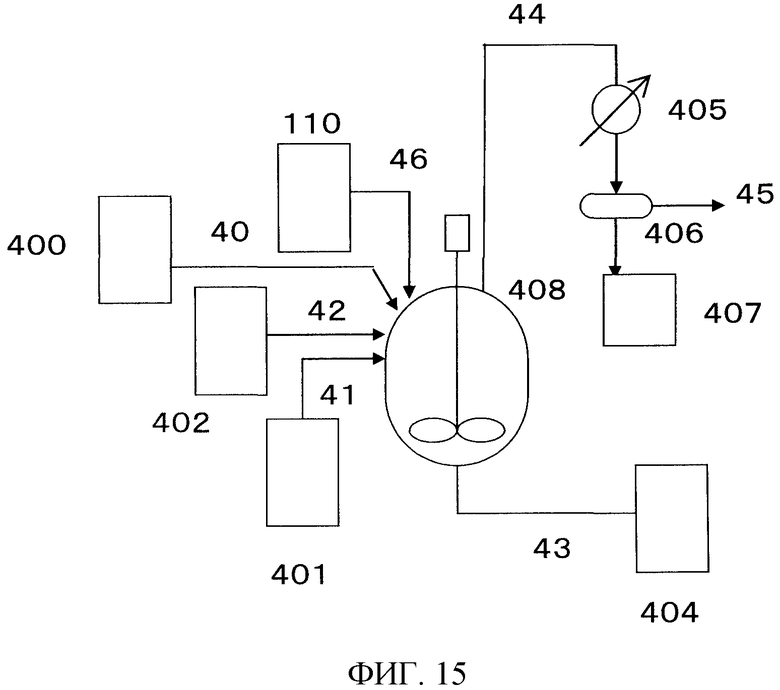
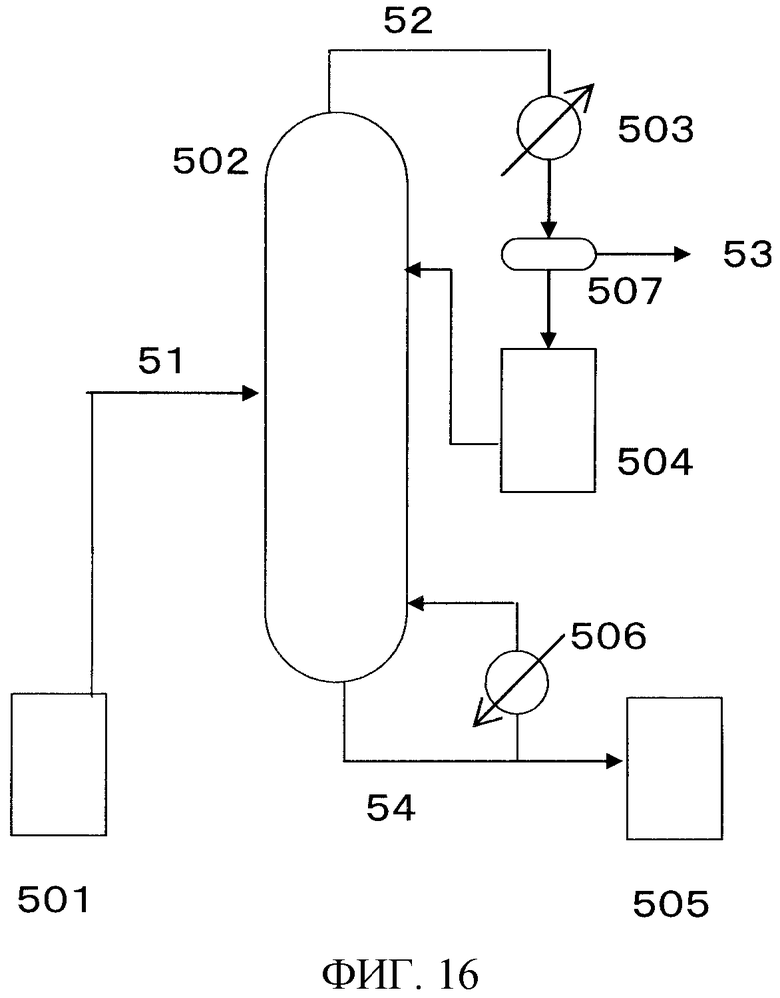
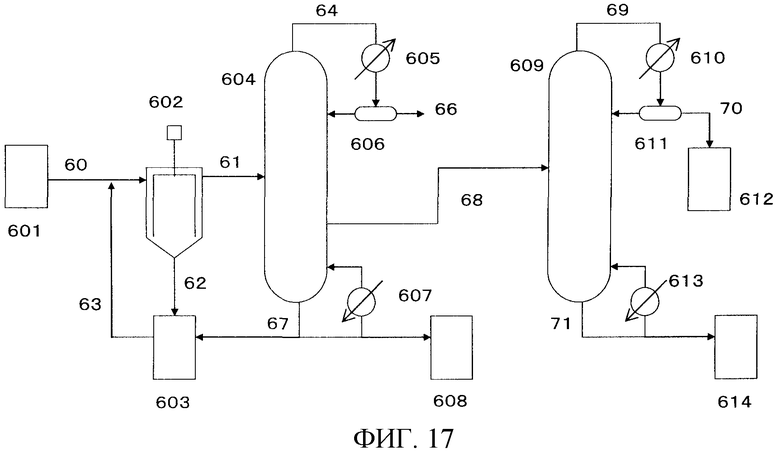
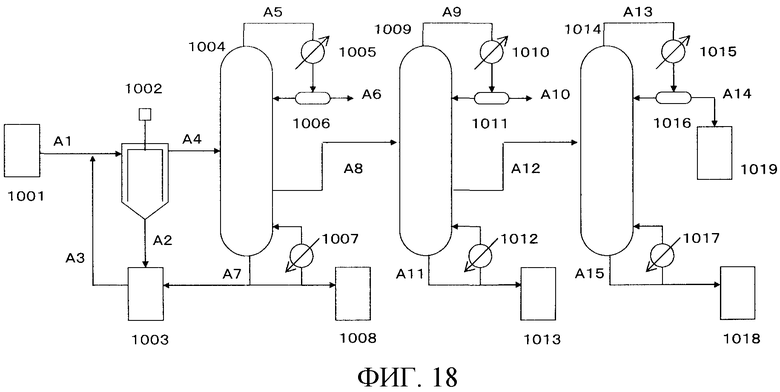
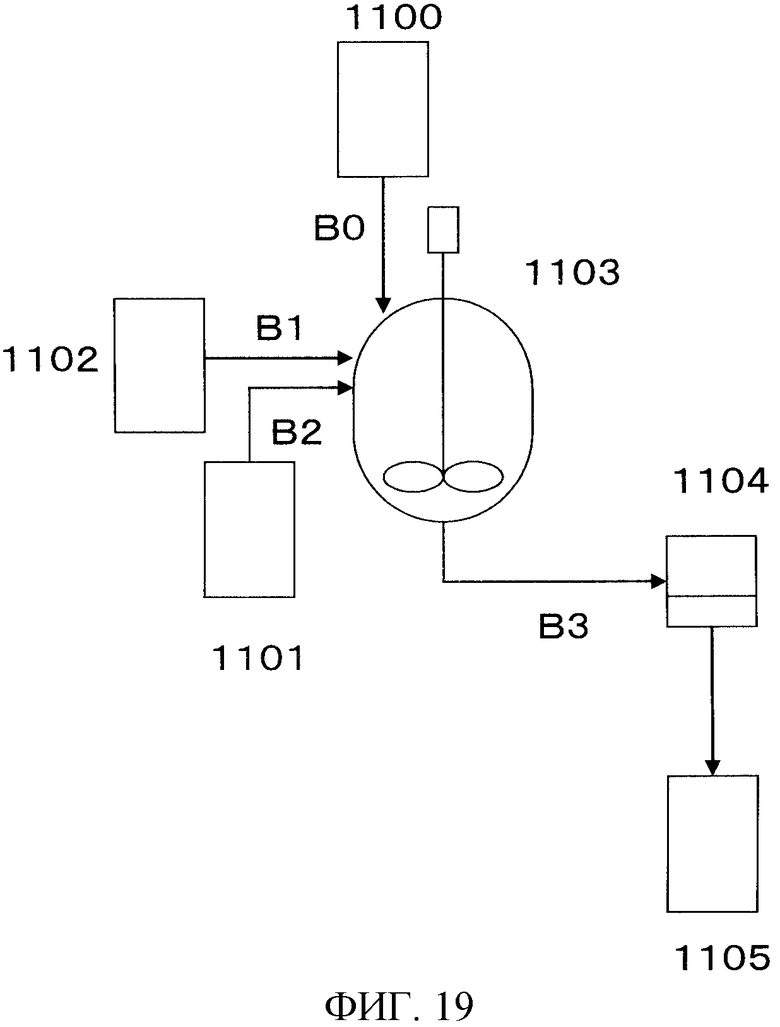
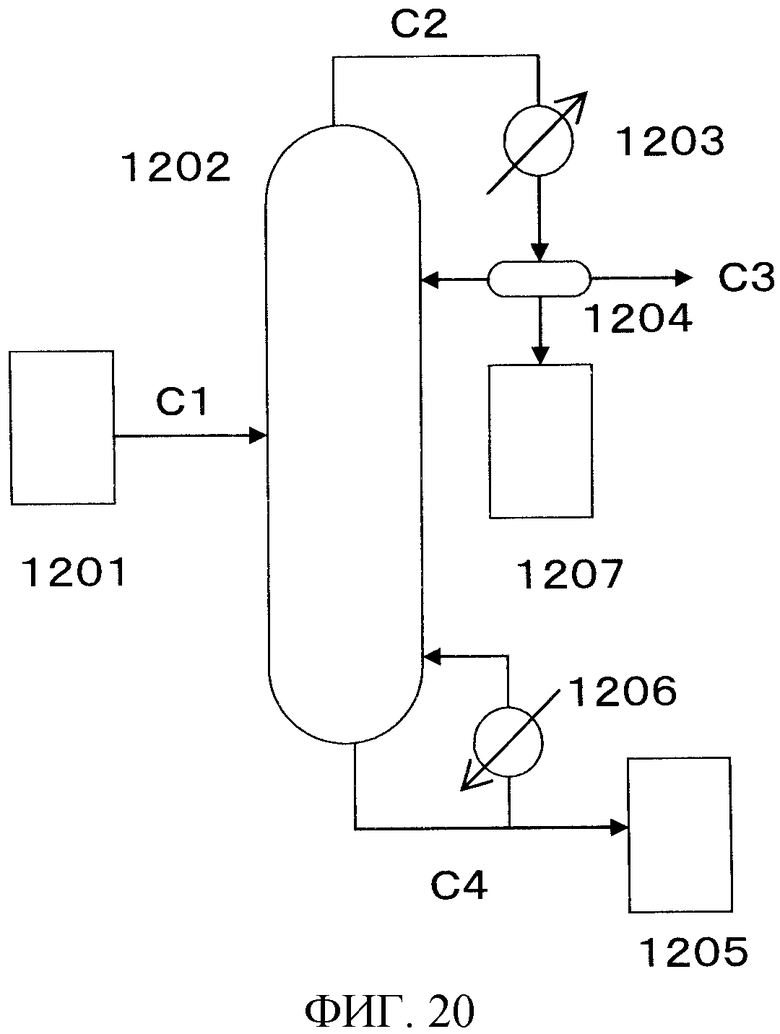
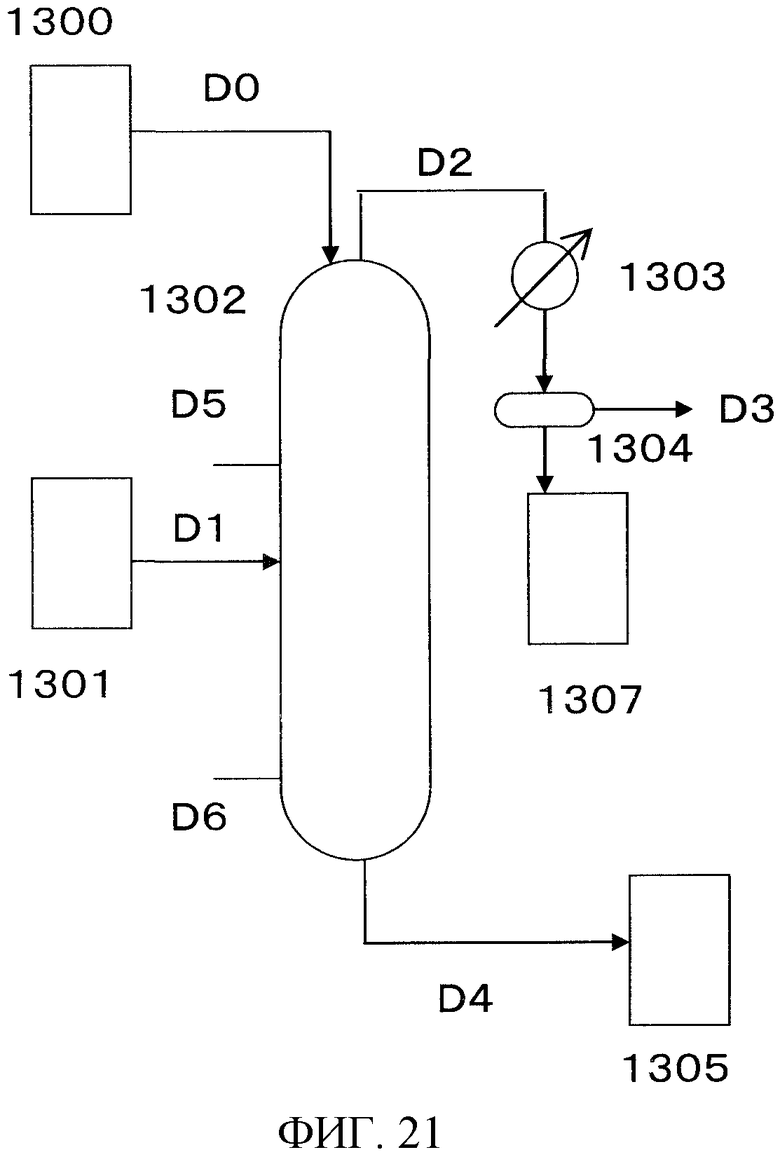
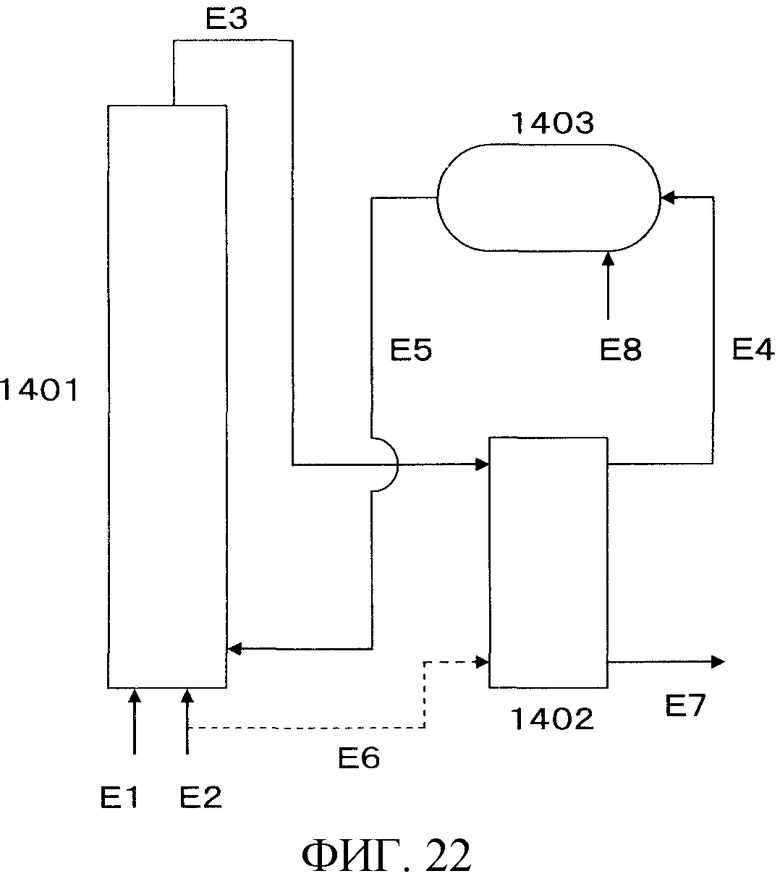
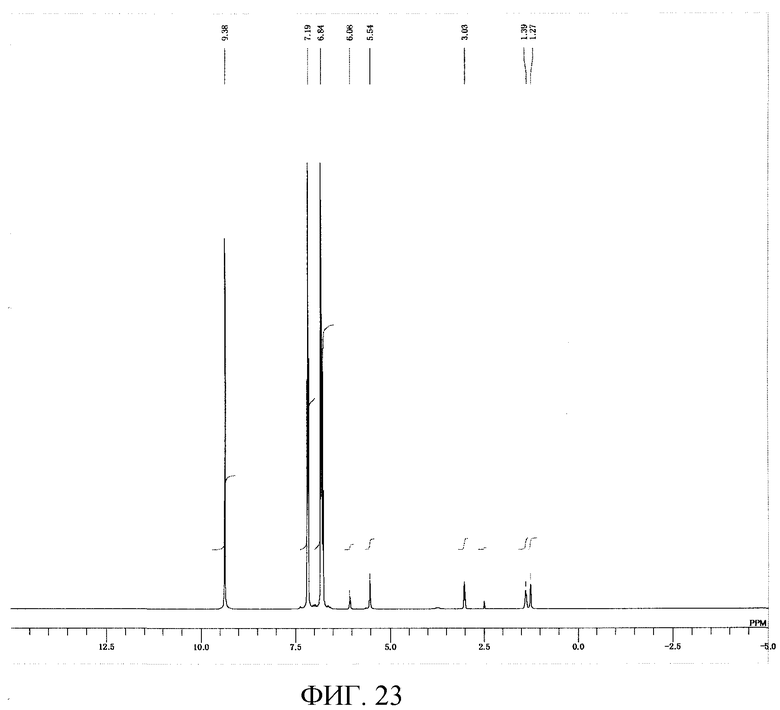
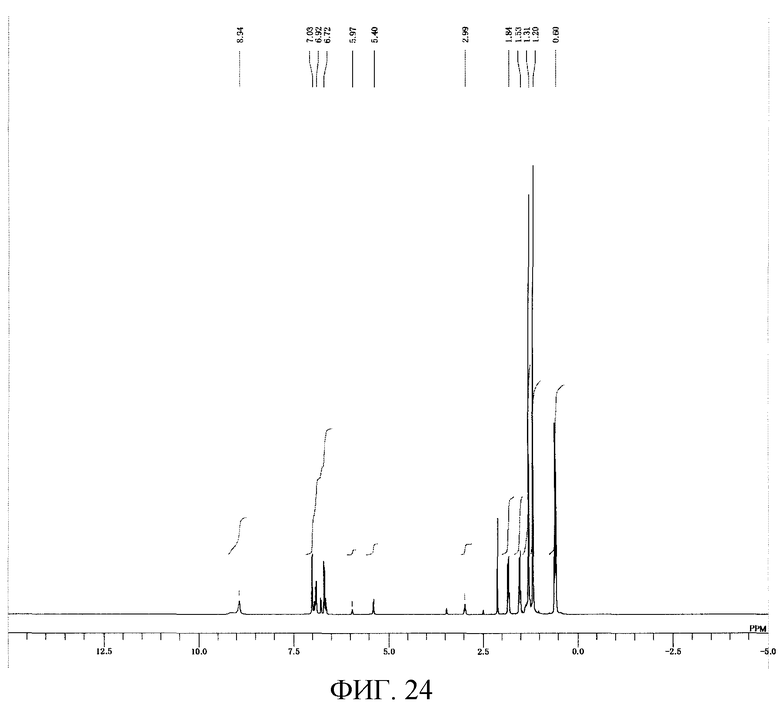
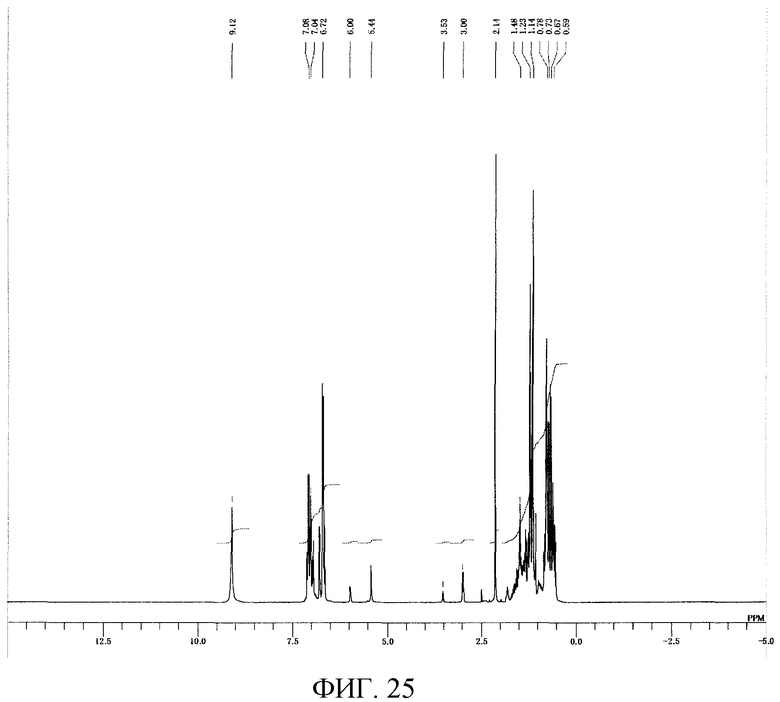
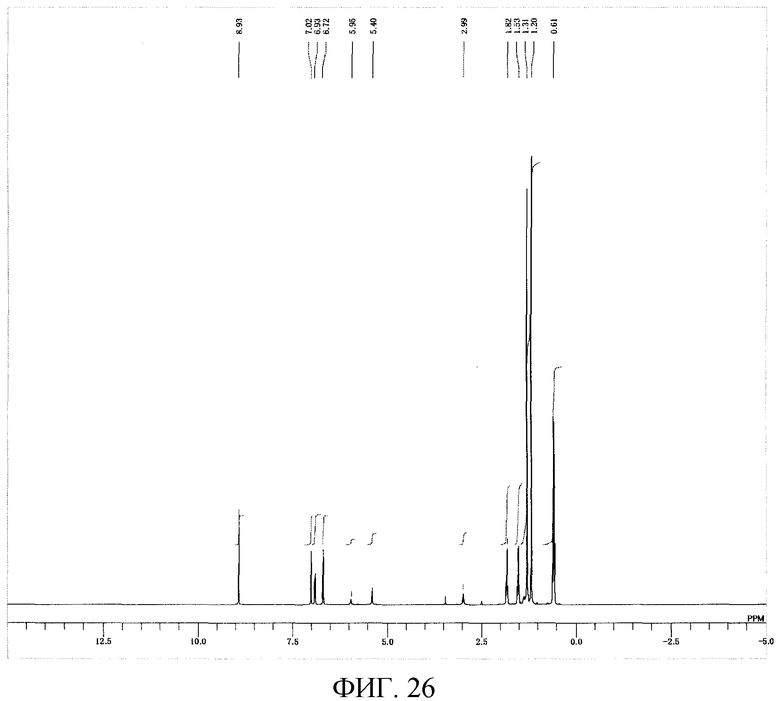
Изобретение относится к способу получения по меньшей мере одного N-замещенной карбаминовой кислоты-О-арилового эфира (где указанный эфир обозначает сложный эфир N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с ароматическим кольцом) из соединения формулы (1), имеющего уреидную группу, и ароматического гидроксисоединения формулы (2) или ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного формулой (2). Способ включает стадию этерификации или этерификации и переэтерификации соединения формулы (1) и ароматического гидроксисоединения или ароматической гидроксикомпозиции формулы (2). В формуле (1) R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена а раз уреидной(ыми) группой(ами), а представляет целое число от 1 до 10. В формуле (2) кольцо А представляет ароматическую группу, выбранную из бензольного или нафталинового кольца, замещенную b раз OH-группами, и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей (i)-(v), которые сохраняют ароматические свойства кольца А, кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, b представляет целое число от 1 до 2. Группы заместителей (i)-(v) обозначают (i) атом водорода; (ii) группу, состоящую из атомов углерода и водорода, которые могут также образовывать кольцевую структуру связыванием с кольцом А; (iii) группу, состоящую из атомов углерода, водорода и кислорода; (iv) атом галогена; (v) группу, состоящую из атомов, выбранных из атомов углерода, водорода, кислорода, азота, серы и галогена, исключая группы, содержащие карбонильную, сложноэфирную, карбоксильную, концевую метиновую и спиртовую OH-группы, NH2-, NH-, NOH-, SH-, SO3H- и SOH-группы. Способ позволяет предотвратить образование побочных продуктов и повторно использовать исходные вещества. Кроме того, изобретение относится к различным вариантам предлагаемого способа, композиции для транспортировки и хранения соединения, имеющего уреидную группу, а также к способу получения изоцианата термическим разложением N-замещенной карбаминовой кислоты-О-арилового эфира. 7 н. и 15 з.п. ф-лы, 26 ил., 67 табл., 306 пр.
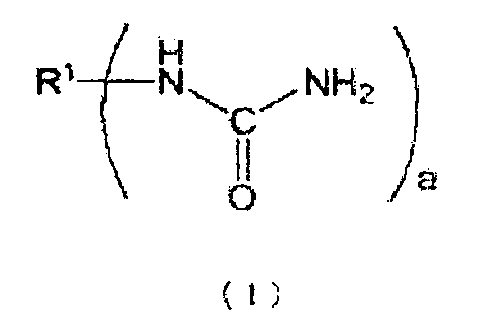
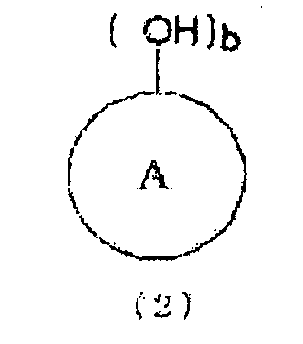
1. Способ получения по меньшей мере одного N-замещенной карбаминовой кислоты-О-арилового эфира (где N-замещенной карбаминовой кислоты-О-ариловый эфир обозначает сложный эфир N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с ароматическим кольцом), получаемого из соединения, имеющего уреидную группу, представленного следующей формулой (1), и ароматического гидроксисоединения, представленного следующей формулой (2), или ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2), где способ включает стадию проведения этерификации или этерификации и переэтерификации соединения, имеющего уреидную группу, и ароматического гидроксисоединения, представленного следующей формулой (2), или ароматической гидроксикомпозиции:

 ,
,
где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена а раз уреидной(ыми) группой(ами), и а представляет целое число от 1 до 10, и
кольцо А представляет ароматическую группу, выбранную из бензольного кольца или нафталинового кольца, замещенную b раз гидроксильными группами в произвольном положении(ях), и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей, указанных ниже (i)-(v), которые сохраняют ароматические свойства кольца А, и кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, и b представляет целое число от 1 до 2:
(i) атом водорода;
(ii) группа, состоящая из атомов углерода и атомов водорода, которые могут также образовывать кольцевую структуру посредством связывания с кольцом А;
(iii) группа, состоящая из атомов углерода, атомов водорода и атомов кислорода, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу;
(iv) атом галогена;
(v) группа, состоящая из атомов, выбранных из атомов углерода, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу, NH2-группу, NH-группу, NOH-группу, SH-группу, SO3H-группу, SOH-группу.
2. Способ получения по п.1, где соединение, имеющее уреидную группу, является соединением, имеющим уреидную группу, получаемым способом, включающим следующую стадию А:
стадия (А): стадия получения соединения, имеющего уреидную группу, полученного из органического первичного амина, представленного следующей формулой (3), и мочевины, путем проведения реакции образования уреидов из органического первичного амина и мочевины в жидкой фазе и удаления или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта в реакции образования уреидов:
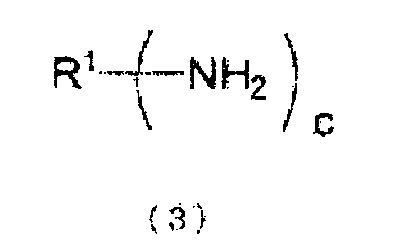 ,
,
где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена с раз NH2-группой(ами), и с представляет целое число от 1 до 10.
3. Способ получения по п.2, где органический первичный амин является органическим первичным моноамином или органическим первичным диамином.
4. Способ получения по п.2, где стадию (А) проводят в присутствии воды, и/или спирта, и/или ароматического гидроксисоединения, представленного следующей формулой (2), и/или ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2):
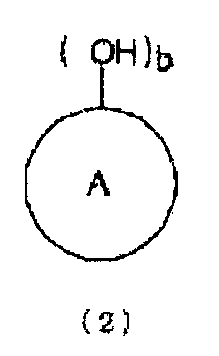 ,
,
где кольцо А представляет ароматическую группу, выбранную из бензольного кольца или нафталинового кольца, замещенную b раз гидроксильными группами в произвольном положении(ях), и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей, указанных ниже (i)-(v), которые сохраняют ароматические свойства кольца А, и кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, и b представляет целое число от 1 до 2:
(i) атом водорода;
(ii) группа, состоящая из атомов углерода и атомов водорода, которые могут также образовывать кольцевую структуру посредством связывания с кольцом А;
(iii) группа, состоящая из атомов углерода, атомов водорода и атомов кислорода, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу;
(iv) атом галогена;
(v) группа, состоящая из атомов, выбранных из атомов углерода, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу, NH2-группу, NH-группу, NOH-группу, SH-группу, SO3H-группу, SOH-группу.
5. Способ получения по п.2, где стадию (А) проводят в присутствии ароматической гидроксикомпозиции, представленной следующей формулой (2), или ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2):
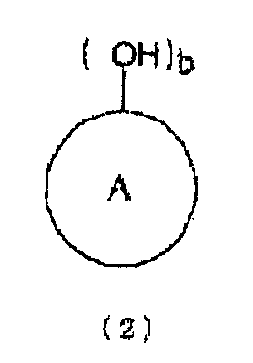 ,
,
где кольцо А представляет ароматическую группу, выбранную из бензольного кольца или нафталинового кольца, замещенную b раз гидроксильными группами в произвольном положении(ях), и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей, указанных ниже (i)-(v), которые сохраняют ароматические свойства кольца А, и кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, и b представляет целое число от 1 до 2:
(i) атом водорода;
(ii) группа, состоящая из атомов углерода и атомов водорода, которые могут также образовывать кольцевую структуру посредством связывания с кольцом А;
(iii) группа, состоящая из атомов углерода, атомов водорода и атомов кислорода, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу;
(iv) атом галогена;
(v) группа, состоящая из атомов, выбранных из атомов углерода, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу, NH2-группу, NH-группу, NOH-группу, SH-группу, SO3H-группу, SOH-группу.
6. Способ получения по п.2, где стадию (А) проводят в присутствии спирта, представленного следующей формулой (4):
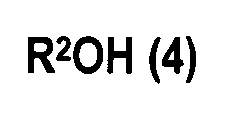 ,
,
где
R2 представляет алкильную группу, циклоалкильную группу, фенилалкильную группу или алкоксиалкильную группу, которая содержит целое число углеродных атомов в интервале от 1 до 14, и ОН-группа спирта, представленного формулой (4), является ОН-группой, которая не связана с ароматическим кольцом.
7. Композиция для транспортировки и хранения соединения, имеющего уреидную группу, где число молекул ароматического гидроксисоединения, представленного следующей формулой (2), относительно числа уреидных групп, содержащихся в соединении, имеющем уреидную группу, представленном следующей формулой (1), в композиции является целым числом от 1 до 100:
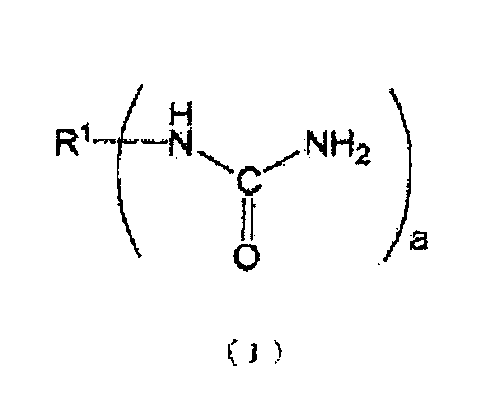
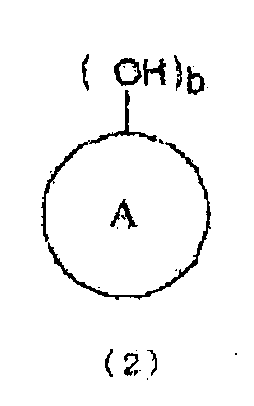 ,
,
где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена а раз уреидной(ыми) группой(ами), и а представляет целое число от 1 до 10, и
кольцо А представляет ароматическую группу, выбранную из бензольного кольца или нафталинового кольца, замещенную b раз гидроксильными группами в произвольном положении(ях), и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей, указанных ниже (i)-(v), которые сохраняют ароматические свойства кольца А, и кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, и b представляет целое число от 1 до 2:
(i) атом водорода;
(ii) группа, состоящая из атомов углерода и атомов водорода, которые могут также образовывать кольцевую структуру посредством связывания с кольцом А;
(iii) группа, состоящая из атомов углерода, атомов водорода и атомов кислорода, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу;
(iv) атом галогена;
(v) группа, состоящая из атомов, выбранных из атомов углерода, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу, NH2-группу, NH-группу, NOH-группу, SH-группу, SO3H-группу, SOH-группу.
8. Способ получения N-замещенной карбаминовой кислоты-O-арилового эфира, включающий следующие стадии (А) и (В):
стадия (А): стадия получения соединения, имеющего уреидную группу, полученного из органического первичного амина, представленного следующей формулой (3), и мочевины, путем проведения реакции образования уреидов из органического первичного амина и мочевины в жидкой фазе и удаления или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта в реакции образования уреидов, и
стадия (В): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидную группу, и ароматического гидроксисоединения, представленного следующей формулой (2), или ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2), в жидкой фазе и удаления или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта:
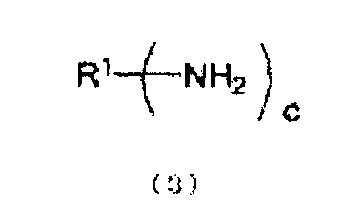
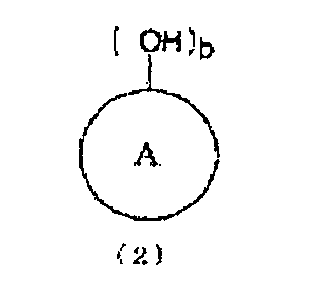 ,
,
где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена с раз группой(ами) NH2, и с представляет целое число от 1 до 10, и
кольцо А представляет ароматическую группу, выбранную из бензольного кольца или нафталинового кольца, замещенную b раз гидроксильными группами в произвольном положении(ях), и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей, указанных ниже (i)-(v), которые сохраняют ароматические свойства кольца А, и кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, и b представляет целое число от 1 до 2:
(i) атом водорода;
(ii) группа, состоящая из атомов углерода и атомов водорода, которые могут также образовывать кольцевую структуру посредством связывания с кольцом А;
(iii) группа, состоящая из атомов углерода, атомов водорода и атомов кислорода, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу;
(iv) атом галогена;
(v) группа, состоящая из атомов, выбранных из атомов углерода, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу, NH2-группу, NH-группу, NOH-группу, SH-группу, SO3H-группу, SOH-группу.
9. Способ получения N-замещенной карбаминовой кислоты-O-арилового эфира, включающий следующие стадии (A), (R) и (Р):
стадия (А): стадия получения соединения, имеющего уреидную группу, полученного из органического первичного амина, представленного следующей формулой (3), и мочевины, путем проведения реакции образования уреидов из органического первичного амина и мочевины в жидкой фазе и удаления или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта в реакции образования уреидов,
стадия (R): стадия получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции соединения, имеющего уреидную группу, и спирта, представленного следующей формулой (4), в жидкой фазе и извлечения аммиака, образующегося в качестве побочного продукта, в газовую фазу, где N-замещенной карбаминовой кислоты-O-R2 эфир представляет сложный эфир N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с R2 группой, получаемой из спирта, и
стадия (Р): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции N-замещенной карбаминовой кислоты-O-R2 эфира и ароматического гидроксисоединения, представленного следующей формулой (2), или ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2), в жидкой фазе и извлечения спирта, образующегося в качестве побочного продукта, в газовую фазу:
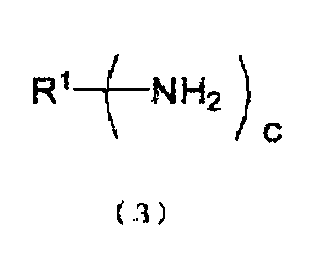
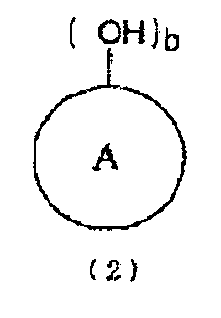
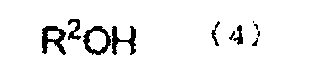 ,
,
где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена с раз NH2-группой(ами), и с представляет целое число от 1 до 10,
кольцо А представляет ароматическую группу, выбранную из бензольного кольца или нафталинового кольца, замещенную b раз гидроксильными группами в произвольном положении(ях), и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей, указанных ниже (i)-(v), которые сохраняют ароматические свойства кольца А, и кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, и b представляет целое число от 1 до 2:
(i) атом водорода;
(ii) группа, состоящая из атомов углерода и атомов водорода, которые могут также образовывать кольцевую структуру посредством связывания с кольцом А;
(iii) группа, состоящая из атомов углерода, атомов водорода и атомов кислорода, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу;
(iv) атом галогена;
(v) группа, состоящая из атомов, выбранных из атомов углерода, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу, NH2-группу, NH-группу, NOH-группу, SH-группу, SO3H-группу, SOH-группу, и
R2 представляет алкильную группу, циклоалкильную группу или алкоксиалкильную группу, которая содержит целое число углеродных атомов в интервале от 1 до 14, и ОН-группа спирта, представленного формулой (4), является ОН-группой, которая не связана с ароматическим кольцом.
10. Способ получения по меньшей мере одного N-замещенной карбаминовой кислоты-O-арилового эфира, включающий следующие стадии (А), (В) и (С), где следующую стадию (С) проводят после стадии (В), и N-замещенной карбаминовой кислоты-O-ариловый эфир, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-арилового эфира являются сшитыми с помощью метиленовой группы (-CH2-), получают из N-замещенной карбаминовой кислоты-O-арилового эфира, получаемого на стадии (В):
стадия (А): стадия получения соединения, имеющего уреидную группу, получаемого из ароматического первичного моноамина, представленного следующей формулой (5), и мочевины, путем проведения реакции образования уреидов из органического первичного моноамина и мочевины в жидкой фазе и выделения или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта при реакции образования уреидов;
стадия (В): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира путем реакции соединения, имеющего уреидную группу, и ароматического гидроксисоединения, представленного следующей формулой (2), или ароматической гидроксикомпозиции, включающей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2), в жидкой фазе и извлечения аммиака, образующегося в качестве побочного продукта, в газовую фазу;
стадия (С): стадия получения N-замещенной карбаминовой кислоты-O-арилового эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-арилового эфира являются сшитыми с помощью метиленовой группы (-CH2-), путем реакции N-замещенной карбаминовой кислоты-O-арилового эфира с формальдегидом или сшивающим реагентом, образующим метиленовые связи, и сшивания ароматических групп, получаемых из ароматического органического первичного моноамина, содержащихся в N-замещенной карбаминовой кислоты-O-ариловом эфире, с помощью метиленовой группы (-СН2-):
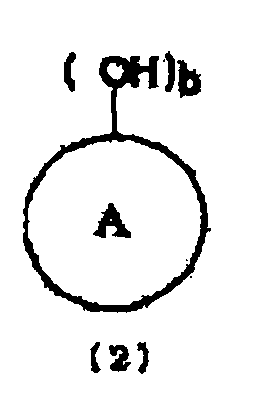
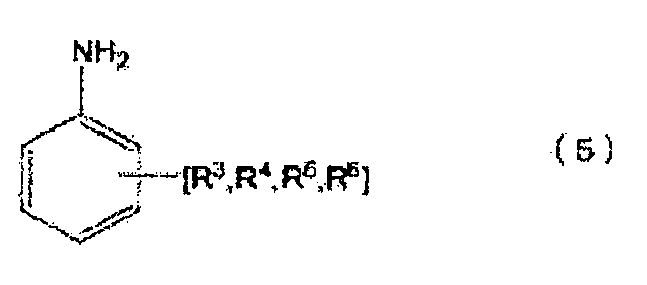 ,
,
где по меньшей мере одно место в орто-положении и/или пара-положении NH2-группы ароматического органического первичного моноамина, представленного формулой (5), является незамещенным, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут быть связаны вместе с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из группы, состоящей из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 является целым числом в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют ароматический органический первичный моноамин, представленный формулой (5), является целым числом от 6 до 13,
кольцо А представляет ароматическую группу, выбранную из бензольного кольца или нафталинового кольца, замещенную b раз гидроксильными группами в произвольном положении(ях), и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей, указанных ниже (i)-(v), которые сохраняют ароматические свойства кольца А, и кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, и b представляет целое число от 1 до 2:
(i) атом водорода;
(ii) группа, состоящая из атомов углерода и атомов водорода, которые могут также образовывать кольцевую структуру посредством связывания с кольцом А;
(iii) группа, состоящая из атомов углерода, атомов водорода и атомов кислорода, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу;
(iv) атом галогена;
(v) группа, состоящая из атомов, выбранных из атомов углерода, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу, NH2-группу, NH-группу, NOH-группу, SH-группу, SO3H-группу, SOH-группу.
11. Способ получения по меньшей мере одного N-замещенной карбаминовой кислоты-О-арилового эфира, включающий следующие стадии (A), (R), (Р) и (С), где стадию (С) проводят после стадии (R) или после стадии (Р), и N-замещенной карбаминовой кислоты-O-(R2 или ариловый) эфир, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира являются сшитыми с помощью метиленовой группы (-CH2-), получают из N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира, получаемого на стадии (R) или стадии (Р):
стадия (А): стадия получения соединения, имеющего уреидную группу, получаемого из ароматического первичного моноамина, представленного следующей формулой (5), и мочевины, путем проведения реакции образования уреидов из органического первичного моноамина и мочевины в жидкой фазе и выделения или извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта при реакции образования уреидов;
стадия (R): стадия получения N-замещенной карбаминовой кислоты-O-R2 эфира путем реакции соединения, имеющего уреидную группу, и спирта, представленного следующей формулой (4), в жидкой фазе и извлечения в газовую фазу аммиака, образующегося в качестве побочного продукта (где N-замещенной карбаминовой кислоты-O-R2 эфир представляет сложный эфир N-замещенной карбаминовой кислоты, в котором атомы кислорода группы карбаминовой кислоты (-NHCOO-) связаны с группой R2, полученной из спирта), и
стадия (Р): стадия получения N-замещенной карбаминовой кислоты-О-арилового эфира путем реакции N-замещенной карбаминовой кислоты-O-R2 эфира и ароматического гидроксисоединения, представленного следующей формулой (2), или ароматической гидроксикомпозиции, содержащей по меньшей мере один тип ароматического гидроксисоединения, представленного следующей формулой (2), в жидкой фазе и извлечения спирта, образовавшегося в качестве побочного продукта, в газовую фазу;
стадия (С): стадия получения N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира, в котором по меньшей мере две молекулы N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира являются сшитыми с помощью метиленовой группы (-CH2-), путем реакции N-замещенной карбаминовой кислоты-O-(R2 или арилового) эфира с формальдегидом или сшивающим реагентом, образующим метиленовые связи, и сшивания ароматических групп, получаемых из ароматического органического первичного моноамина, содержащихся в N-замещенной карбаминовой кислоты-O-(R2 или ариловом) эфире, с помощью метиленовой группы СН2-) (где N-замещенной карбаминовой кислоты-O-(R2 или ариловый) эфир представляет N-замещенной карбаминовой кислоты-O-R2 эфир или N-замещенной карбаминовой кислоты-О-ариловый эфир):
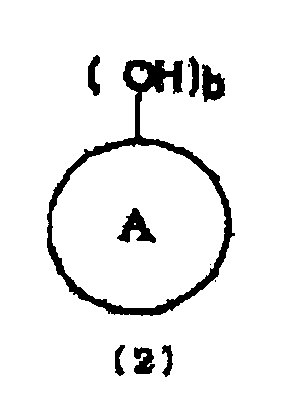
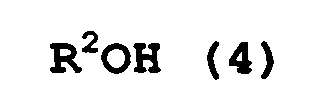
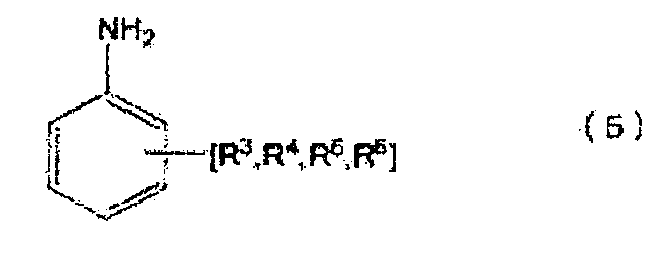 ,
,
где по меньшей мере одно место в орто-положении и/или пара-положении NH2-группы ароматического органического первичного моноамина, представленного формулой (5), является незамещенным, группы R3-R6 соответственно представляют группу, замещенную в произвольном месте, которая сохраняет ароматические свойства кольца, группы R3-R6 могут соответственно и независимо замещать ароматическое кольцо, или группы R3-R6 могут быть связаны вместе с образованием кольца с ароматическим кольцом, группы R3-R6 являются атомами водорода или группами, выбранными из группы, состоящей из групп, в которых группа, выбранная из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы и арильной группы, имеющей гидроксильную группу, связана с помощью алифатических связей и/или эфирных связей, число углеродных атомов групп R3-R6 является целым числом в интервале от 0 до 7, и суммарное число углеродных атомов, которые составляют ароматический органический первичный моноамин, представленный формулой (5), является целым числом от 6 до 13,
кольцо А представляет ароматическую группу, выбранную из бензольного кольца или нафталинового кольца, замещенную b раз гидроксильными группами в произвольном положении(ях), и может быть замещено по меньшей мере одним заместителем, выбранным из групп заместителей, указанных ниже (i)-(v), которые сохраняют ароматические свойства кольца А, и кольцо А и по меньшей мере один заместитель содержат целое число углеродных атомов в интервале от 6 до 50, и b представляет целое число от 1 до 2:
(i) атом водорода;
(ii) группа, состоящая из атомов углерода и атомов водорода, которые могут также образовывать кольцевую структуру посредством связывания с кольцом А;
(iii) группа, состоящая из атомов углерода, атомов водорода и атомов кислорода, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу;
(iv) атом галогена;
(v) группа, состоящая из атомов, выбранных из атомов углерода, атомов водорода, атомов кислорода, атомов азота, атомов серы и атомов галогена, исключая группы, содержащие карбонильную группу, сложноэфирную группу, концевую метиновую группу и спиртовую OH-группу, карбоксильную группу, NH2-группу, NH-группу, NOH-группу, SH-группу, SO3H-группу, SOH-группу.
12. Способ получения по п.8 или 9, дополнительно включающий стадию извлечения мочевины путем проведения следующей стадии (D) перед стадией (В) или стадией (Р) и/или одновременно со стадией (В) или стадией (Р):
стадия (D): стадия удаления мочевины путем ректификации или сублимации.
13. Способ получения по п.12, дополнительно включающий следующую стадию (Е) рециркуляции извлекаемой мочевины на стадию (А):
стадия (Е): стадия рециркуляции мочевины, извлекаемой на стадии (D), на стадию (А).
14. Способ получения изоцианата, представленного следующей формулой (6)
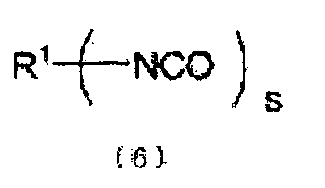 ,
,
где
R1 представляет органическую группу, содержащую целое число углеродных атомов в интервале от 1 до 85, которая замещена s раз группой(ами) NCO, и s представляет целое число от 1 до 10,
путем проведения термического разложения N-замещенной карбаминовой кислоты-O-арилового эфира, полученного на следующей стадии (F):
стадия (F): стадия получения изоцианата и ароматической гидроксикомпозиции из N-замещенной карбаминовой кислоты-O-арилового эфира.
15. Способ получения по п.14, дополнительно включающий стадию отделения ароматической гидроксикомпозиции, получаемой на стадии (F) в качестве побочного продукта, от изоцианата и рециркуляцию ароматической гидроксикомпозиции на стадию (А) и/или стадию (В) по п.8, или на стадию (А) и/или стадию (R) и/или стадию (Р) по п.9.
16. Способ получения по любому из пп.1, 8 и 9, где ароматическое гидроксисоединение является по меньшей мере одним типом ароматического гидроксисоединения, представленного следующей формулой (7):
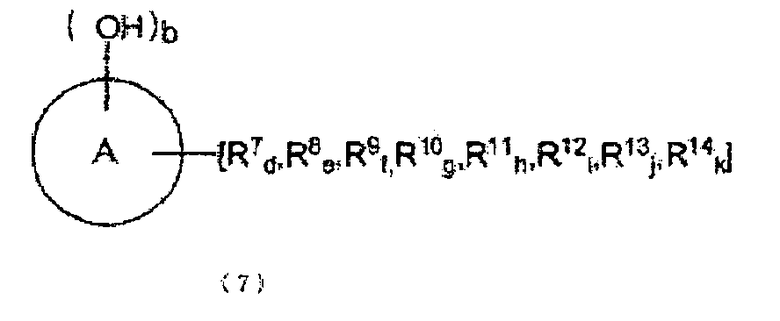 ,
,
где
кольцо А представляет ароматическое кольцо, выбранное из бензольного кольца или нафталинового кольца, и группы R7-R14 соответственно представляют группы, замещенные в произвольном месте(ах), которые сохраняют ароматические свойства кольца А, группы R7-R14 могут соответственно и независимо замещать кольцо А, группы R7-R14 могут быть связаны вместе с образованием кольца с ароматическим кольцом путем связывания с кольцом A, группы R7-R14 соответственно и независимо представляют атом водорода, атом галогена или группу, выбранную из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы, арильной группы, имеющей гидроксильную группу, аралкильной группы и эфирной группы (замещенной и/или незамещенной алкиловой эфирной группы и/или замещенной и/или незамещенной ариловой эфирной группы и/или замещенной и/или незамещенной аралкиловой эфирной группы), и/или группу, с которой один или более типов групп, выбранных из указанной группы, связаны, и/или группу, с которой один или более типов групп, выбранных из указанной группы, связаны с помощью насыщенных алифатических связей и/или эфирных связей, и кольцо A и группы R7-R14 состоят из суммарного общего числа углеродных атомов в интервале от 6 до 50, значение d+e+f+g+h+i+j+k представляет целое число, равное от 0 до 6-b, в случае, когда кольцо A является бензольным кольцом, представляет целое число, равное от 0 до 8-b, в случае, когда кольцо A является нафталиновым кольцом, и группа, выбранная из описанных выше групп R7-R14, может быть циклически связана с кольцом А с помощью связей углерод-углерод и/или эфирных связей.
17. Композиция для транспортировки и хранения соединения, имеющего уреидную группу, по п.7, где ароматическое гидроксисоединение является по меньшей мере одним типом ароматического гидроксисоединения, представленного следующей формулой (7):
 ,
,
где
кольцо А представляет ароматическое кольцо, выбранное из бензольного кольца, нафталинового кольца, и группы R7-R14 соответственно представляют группы, замещенные в произвольном месте(ах), которые сохраняют ароматические свойства кольца А, группы R7-R14 могут соответственно и независимо замещать кольцо А, группы R7-R14 могут быть связаны вместе с образованием кольца с ароматическим кольцом путем связывания с кольцом А, группы R7-R14 соответственно и независимо представляют атом водорода, атом галогена или группу, выбранную из группы, состоящей из алкильной группы, циклоалкильной группы, арильной группы, арильной группы, имеющей гидроксильную группу, аралкильной группы и эфирной группы (замещенной и/или незамещенной алкиловой эфирной группы и/или замещенной и/или незамещенной ариловой эфирной группы и/или замещенной и/или незамещенной аралкиловой эфирной группы), и/или группу, с которой один или более типов групп, выбранных из указанной группы, связаны, и/или группу, с которой один или более типов групп, выбранных из указанной группы, связаны с помощью насыщенных алифатических связей и/или эфирных связей, и кольцо А и группы R7-R14 состоят из суммарного общего числа углеродных атомов в интервале от 6 до 50,
значение d+e+f+g+h+i+j+k представляет целое число, равное от 0 до 6-b, в случае, когда кольцо А является бензольным кольцом, представляет целое число, равное от 0 до 8-b, в случае, когда кольцо А является нафталиновым кольцом, и группа, выбранная из описанных выше групп R7-R14, может быть циклически связана с кольцом А с помощью связей углерод-углерод и/или эфирных связей.
18. Способ получения по любому из пп.2, 8 и 9, где ароматическое гидроксисоединение имеет стандартную температуру кипения, которая отличается на 10°C или более от стандартной температуры кипения изоцианата, имеющего структуру, в которой все аминогруппы органического первичного амина (первичные аминогруппы) превращены в изоцианатные группы.
19. Способ получения по любому из пп.1, 8 и 9, где ароматическое гидроксисоединение является одновалентным и/или двухвалентным ароматическим гидроксисоединением (а именно, в котором b является равным 1 и/или 2).
20. Композиция для транспортировки и хранения соединения, имеющего уреидную группу, по п.7, где ароматическое гидроксисоединение, содержащееся в ароматической гидроксикомпозиции, является одновалентным и/или двухвалентным ароматическим гидроксисоединением (а именно, в котором b является равным 1 и/или 2).
21. Способ получения по п.14, дополнительно включающий рециркуляцию непрореагировавшего N-замещенной карбаминовой кислоты-O-арилового эфира, который не был термически разложен на стадии (F), на стадию (А) и/или стадию (В) по п.8, и/или стадию (R) и/или стадию (Р) по п.9, и/или стадию (F).
22. Способ получения по п.8 или 9, дополнительно включающий следующую стадию (G) извлечения аммиака, образующегося в качестве побочного продукта на стадии (А) и/или стадии (В) и/или стадии (R), регенерации мочевины путем реакции аммиака с диоксидом углерода и рециркуляции мочевины на стадию (А):
стадия (G): стадия извлечения аммиака, образующегося в качестве побочного продукта, регенерации мочевины путем реакции аммиака с диоксидом углерода, рециркуляции мочевины на стадию (А).
| E | |||
| STEDMAN et al, The Methylurethanes of the Isomeric α-Hydroxyphenylethyldimethylamines and their Miotic Activity, J | |||
| CHEM | |||
| SOC., 1929, 609-617 |
Авторы
Даты
2014-09-20—Публикация
2009-09-29—Подача