Изобретение относится к способу получения α-гидроксикарбоновых кислот, в частности к новому способу получения 2-гидрокси-2-карбоксиалкиладамантанов общей формулы
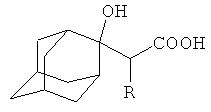
где R=Н, СН3,
которые находят применение в качестве полупродуктов в синтезе адамантилсодержащих аминокислот и гетероциклических соединений.
Известен способ получения 2-гидрокси-2-(2-пиридил)метиладамантана с выходом 93% по реакции адамантанона-2 с 2-метилпиридином в присутствии эквимолярного количества н-бутиллития при -20°С [Setaki D., Tataridis D., Stamatiou G., Kolocouris A., Foscolos G.В., Fytas G., Kolocouris N., Padaiko E., Neyts J., De Clercq E. // Bioorganic Chemistry, vol. 34, nb. 5, (2006), p.248-273].
Недостатком данного способа является применение низких температур и труднодоступного н-бутиллития. Данным способом не были получены соединения заявляемой структурной формулы.
Известен способ получения 2-гидрокси-2-адамантилацетонитрила по реакции ацетонитрила с н-бутиллитием в тетрагидрофуране при -80°С, дальнейшим взаимодействием литиевого интермедиата с адамантаноном-2 и последующим гидролизом промежуточного соединения. Целевой продукт получен с выходом 97% [Zoidis G., Kolocouris N., Kelly J.M., Prathalingam S.R., Naesens L., De Clercq E. // European Journal of Medicinal Chemistry, vol. 45, nb. 11, (2010), p.5022-5030]. Аналогичный продукт получен по реакции адамантанона-2 с ацетонитрилом в присутствии гидрида натрия в диметилсульфоксиде с выходом 60% [Скоморохов М.Ю., Леонова М.В., Ширяев А.К., Климочкин Ю.Н. // ЖОрХ, 2003. - Т. 36, Вып.9, - с.1432-1433].
Недостатками данных методов являются необходимость использования низких температур и труднодоступного н-бутиллития в первом случае и невысокий выход продукта во втором. Данными способами невозможно получение соединений заявляемой структурной формулы.
Известен способ получения метилового эфира 2-гидрокси-2-адамантанкарбоновой кислоты с выходом 51% по реакции адамантанона-2 с 2,5-дигидро-2,2-диметокси-5,5-диметил-1,3,4-оксадиазолом в толуоле [Romanski. Jaroslaw, Mioston. Grzegorz, Heimgartner. Heinz, Helvetica Chimica Acta, vol. 90, nb. 7, (2007), p.1279-1283].
Недостатком данного метода является использование труднодоступного 2,5-дигидро-2,2-диметокси-5,5-диметил-1,3,4-оксадиазола. Данным способом не могут быть получены соединения заявляемой структурной формулы.
Известен способ получения этилового эфира 2-гидроксиадамантил-2-уксусной кислоты по реакции адамантанона-2 с этил бромацетатом триметилхлорсиланом и цинком в диэтиловом эфире [Zhao Mei-Xin, Wang Mei-Xi-ang, Yu Chu-Yi, Huang Zhi-Tang, Fleet George W.J. // Journal of Organic Chemistry, vol. 69, nb. 3, (2004), p.997-1000].
Недостатком данного способа является то, что с его помощью возможно получить только эфиры 2-гидрокси-2-карбоксиалкиладамантанов, получение самих кислот данным способом невозможно.
Известен способ получения 2-гидрокси-2-адамантил-(2,2-диметил)уксусной кислоты по реакции адамантанона-2 с изомасляной кислотой и двумя эквивалентами диизопропиламина и н-бутиллития в смеси н-гептан - абсолютный тетрагидрофуран при 0°C с выходом 75% [Moersch G.W., Burkett A.R. // Journal of Organic Cnemistry, vol. 36, (1971), - p.1149-1151].
Недостатками данного способа являются использование в большом количестве дорогих н-бутиллития и диизопропиламина, необходимость захолаживания реакционной смеси.
Задачей заявляемого способа является разработка технологичного способа получения 2-гидрокси-2-карбоксиалкиладамантанов из легкодоступных реагентов в мягких условиях.
Техническим результатом является расширение ряда соединений заявляемой структурной формулы и получение продуктов с высокими выходами и высокой степенью чистоты.
Поставленный результат достигается в способе получения 2-гидрокси-2-карбоксиалкиладамантанов общей формулы

где R=Н, СН3,
заключающемся во взаимодействии адамантанона-2 с дилитиевыми солями уксусной или пропионовой кислоты, полученными in situ по реакции ацетата или пропионата лития с гексаметилдисилиламидом лития, предварительно полученным из гексаметилдисилазана и фениллития, в среде осушенного тетрагидрофурана при температуре 20-45°С и мольном соотношении гексаметилдисилазан : ацетат или пропионат лития : адамантанон-2, равном 1.3-1.4:1.8-2.1:1.
Сущность изобретения заключается в получении литиевых солей 2-гидрокси-2-карбоксиалкиладамантанов путем взаимодействия адамантанона-2 с дилитиевыми солями уксусной или пропионовой кислоты. Дилитиевые соли уксусной или пропионовой кислоты синтезируются in situ по реакции ацетата или пропионата лития с гексаметилдисилиламидом лития. При этом гексаметилдисилиламид лития получают из фениллития и гексаметилдисилазана. Весь процесс синтеза протекает в одном реакторе в среде осушенного тетрагидрофурана при температуре 20-45°С в течение 5 часов при последовательном прибавлении лития, бромбензола, гексаметилдисилазана, ацетата или пропионата лития и адамантанона-2 в мольных соотношениях 2.5:1.2:1.3-1.4:1.8-2.1:1.
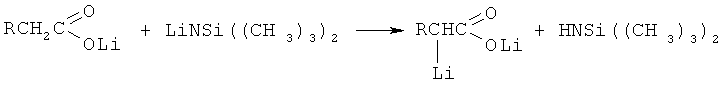


R=H, CH3
Способ осуществляется следующим образом. К смеси мелконарезанного металлического лития в безводном тетрагидрофуране при 20-25°С порциями прибавляется раствор бромбензола в тетрагидрофуране со скоростью, не допускающей нагрева реакционной массы выше 40°С, на что затрачивается 1 час. После образования раствора фениллития к нему порционно прибавляют гексаметилдисилазан и выдерживают реакционную массу 2 часа. Затем в реакционную массу прибавляют ацетат или пропионат лития. Далее (или одновременно с ацетатом или пропионатом лития) прибавляют адамантанон-2. Реакционную смесь выдерживают 2 часа, после чего приливают избыток воды, при этом соли целевых продуктов переходят в водную фазу. Нижний водный слой подкисляют разбавленной серной кислотой до слабокислой реакции, при этом осаждаются 2-гидрокси-2-карбоксиалкиладамантаны, которые отфильтровывают и сушат.
Реакция протекает в одном реакционном объеме при последовательном прибавлении доступных реагентов без использования низких температур. Выделение целевых 2-гидрокси-2-карбоксиалкиладамантанов производится в результате разложения реакционной массы водой, при этом литиевые соли 2-гидрокси-2-карбоксиалкиладамантанов переходят в водную фазу, а все органические примеси остаются в органическом слое. Действием разбавленной серной кислоты на водный раствор литиевых солей 2-гидрокси-2-карбоксиалкиладамантанов выделяются соответствующие 2-гидрокси-2-карбоксиалкиладамантаны. Таким образом, предлагаемый способ характеризуется простотой в проведении синтеза и выделении продуктов реакции. Выход 2-гидрокси-2-карбоксиалкиладамантанов составляет 76 и 87% соответственно.
Как показали наши исследования, наиболее удобным способом проведения реакции является ее осуществление при избытке гексаметилдисилазана по отношению к бромбензолу для увеличения скорости и полноты реакции переметаллирования. В противном случае активно происходит побочное взаимодействие не прореагировавшего фениллития с другими компонентами реакционной массы. Одна из этих реакций, связанная с образованием алкоголята 2-фениладамантанола-2, влечет снижение выхода 2-гидрокси-2-карбоксиалкиладамантанов.
Рационально добавление избыточного количества ацетата (пропионата) лития относительно гексаметилдисилазана и адамантанона-2 (мольное соотношение 1.8-2.1:1.3-1.4:1 соответственно), так как в этом случае протекает более полная конверсия адамантанона-2. Дальнейшее увеличение избытка ацетата (пропионата) лития не приводит к росту выхода 2-гидрокси-2-карбоксиалкиладамантанов.
Обнаружено, что применение вместо уксусной и пропионовой других карбоновых кислот из ряда: масляная, изомасляная, валериановая не приводит к образованию соответствующих гидроксипроизводных. По всей видимости, это обусловлено стерическими препятствиями, возникающими при атаке литийорганическими соединениями адамантанона-2.
Изобретение иллюстрируется следующими примерами.
Пример 1.
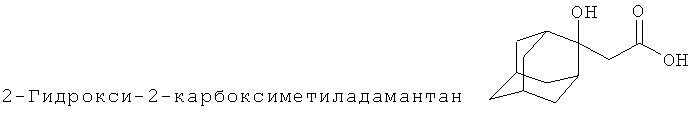
К 0.58 г (0.083 моль) интенсивно перемешиваемого мелконарезанного металлического лития в 20 мл осушенного тетрагидрофурана порционно прибавляют 6.3 г (0.04 моль) бромбензола с такой скоростью, чтобы не допустить сильного повышения температуры. Затем перемешиваемую смесь нагревают до 45°С в течение 30-40 минут, охлаждают до комнатной температуры и порциями приливают 7.5 г (0.047 моль) гексаметилдисилазана. Смесь выдерживают 2 часа, после чего добавляют 4.4 г (0.067 моль) ацетата лития, затем к ней приливают раствор 5 г (0.033 моль) адамантанона-2 в 20 мл тетрагидрофурана. При перемешивании смесь нагревают при 45°С в течение 2 часов. После ее охлаждения литийорганические соединения разлагают 25 мл воды. Смесь разделяют на слои. Водный экстракт обрабатывают разбавленной серной кислотой до слабо кислой реакции. Выпавший осадок фильтруют. После осушки получают 5.3 г (0,025 моль) 2-гидрокси-2-карбоксиметиладамантана. Выход 76%, т. пл. 124-127°С. Спектр ЯМР 1Н, δ, м.д.: 1.32-2.15 м (14Н, 2,2-Ad); 2.50 с (2Н, -СН2).
Пример 2.

К 0.35 г (0.05 моль) интенсивно перемешиваемого мелконарезанного металлического лития в 15 мл осушенного тетрагидрофурана порционно прибавляют 3.77 г (0.024 моль) бромбензола с такой скоростью, чтобы не допустить сильного повышения температуры. Затем перемешиваемую смесь нагревают до 45°С в течение 30-40 минут, охлаждают до комнатной температуры и порциями приливают 4.2 г (0.026 моль) гексаметилдисилазана. Смесь выдерживают 2 часа, после чего добавляют 2.9 г (0.036 моль) пропионата лития и приливают раствор 3 г (0.02 моль) адамантанона-2 в 10 мл тетрагидро- фурана. При перемешивании смесь нагревают при 45°С в течение 2 часов. После ее охлаждения литийорганические соединения разлагают 25 мл воды. Смесь разделяют на слои, водный экстракт обрабатывают разбавленной серной кислотой до слабо кислой реакции. Выпавший осадок фильтруют. После осушки получают 3.9 г (0.017 моль) продукта. Выход 87%, т. пл. 138-141°С. Спектр ЯМР 1Н, δ, м.д.: 0.91д (ЗН, -СН3); (1.31-2.18 м 14Н, 2,2-Ad); 2.87к (1Н, -СНС(О)).
Таким образом, разработан новый способ синтеза 2-гидрокси-2-карбоксиалкиладамантанов, заключающийся в реакции адамантанона-2 с дилитиевыми солями уксусной или пропионовой кислоты, протекающий в одном реакторе при температуре 20-45°С в течение 5 часов.
Изобретение относится к способу получения α-гидроксикарбоновых кислот, в частности к новому способу получения 2-гидрокси-2-карбоксиалкиладамантанов общей формулы 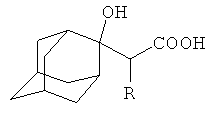 где R=Н, СН3, которые находят применение в качестве полупродуктов в синтезе адамантилсодержащих аминокислот и гетероциклических соединений. Способ заключается во взаимодействии адамантанона-2 с дилитиевыми солями уксусной или пропионовой кислоты, полученными in situ по реакции ацетата или пропионата лития с гексаметилдисилиламидом лития, предварительно полученным из гексаметилдисилазана и фениллития, в среде осушенного тетрагидрофурана при температуре 20-45°С и мольном соотношении гексаметилдисилазан : ацетат или пропионат лития : адамантанон-2, равном 1.3-1.4:1.8-2.1:1. Техническим результатом является расширение ряда соединений заявляемой структурной формулы и получение продуктов с высокими выходами и высокой степенью чистоты. 2 пр.
где R=Н, СН3, которые находят применение в качестве полупродуктов в синтезе адамантилсодержащих аминокислот и гетероциклических соединений. Способ заключается во взаимодействии адамантанона-2 с дилитиевыми солями уксусной или пропионовой кислоты, полученными in situ по реакции ацетата или пропионата лития с гексаметилдисилиламидом лития, предварительно полученным из гексаметилдисилазана и фениллития, в среде осушенного тетрагидрофурана при температуре 20-45°С и мольном соотношении гексаметилдисилазан : ацетат или пропионат лития : адамантанон-2, равном 1.3-1.4:1.8-2.1:1. Техническим результатом является расширение ряда соединений заявляемой структурной формулы и получение продуктов с высокими выходами и высокой степенью чистоты. 2 пр.
Способ получения 2-гидрокси-2-карбоксиалкиладамантанов общей формулы
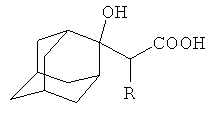
где R=Н, СН3,
заключающийся во взаимодействии адамантанона-2 с дилитиевыми солями уксусной или пропионовой кислоты, полученными in situ по реакции ацетата или пропионата лития с гексаметилдисилиламидом лития, предварительно полученным из гексаметилдисилазана и фениллития, в среде осушенного тетрагидрофурана при температуре 20-45°С и мольном соотношении гексаметилдисилазан : ацетат или пропионат лития : адамантанон-2, равном 1.3-1.4:1.8-2.1:1.
| JP 2008268743 A, 06.11.200 | |||
| JP 2000241977 A, 08.09.2000 | |||
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛАТОВ И МЕТАКРИЛАТОВ ТРЕТИЧНЫХ АДАМАНТАНОВЫХ СПИРТОВ | 2001 |
|
RU2213727C2 |
| Mei-Xin Zhao et al | |||
| "A Direct Retro-Reformatsky Fragmentation: Formal Ring Enlargement of Cyclic Ketones for Novel and Practical Synthesis of Heterocyclic Enamines", J | |||
| Org | |||
| Chem., 2004, 69 (3), pp 997-1000 | |||
| . | |||
Авторы
Даты
2014-09-27—Публикация
2013-04-23—Подача