РОДСТВЕННЫЕ ЗАЯВКИ
В соответствии с разделом 35, § 119(e) Свода законов США для настоящей заявки испрашивается приоритет предварительной заявки США номер 61/095757, поданной 10 сентября 2008; предварительной заявки США номер 61/103502, поданной 7 октября 2008; и предварительной заявки США номер 61/234519, поданной 17 августа 2009, содержание которых включено в данное описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится, главным образом, к композициям и способам, которые можно использовать для лечения состояний и заболеваний, ассоциированных с ангиогенезом. В частности, настоящее изобретение относится к антагонистам тетраспанина 12 (TSPAN12) и норрина.
УРОВЕНЬ ТЕХНИКИ
В настоящее время точно установлено, что ангиогенез представляет собой важный фактор патогенеза большого числа расстройств. К ним относятся солидные опухоли и метастазирование, внутриглазные неоваскулярные заболевания, такие как пролиферативные ретинопатии, например, диабетическая ретинопатия, окклюзия ретинальной вены (RVO), влажная возрастная дегенерация желтого пятна (AMD), неоваскулярная глаукома, иммунное отторжение трансплантированной роговичной ткани и других тканей и ревматоидный артрит. Duda et al. J. Clin. Oncology 25(26): 4033-42 (2007); Kesisis et al. Curr. Pharm. Des. 13: 2795-809 (2007); Zhang & Ma Prog. Ret. & Eye Res. 26: 1-37 (2007).
Сетчатка получает свое кровоснабжение из ретинальных сосудов, которые снабжают внутреннюю часть сетчатки, и хориоидальных сосудов, которые снабжают наружную часть. Повреждение ретинальных сосудов наблюдается при некоторых патологических процессах, включающих диабетическую ретинопатию, ретинопатию недоношенных и окклюзии центральной вены сетчатки и ее ветвей (ишемические ретинопатии). Ишемия сетчатки из-за данного повреждения приводит к нежелательной неоваскуляризации. Хориоидальная неоваскуляризация наблюдается при большом числе других патологических процессов, включая AMD. Напротив, неполная васкуляризация сетчатки характерна для пациентов, страдающих некоторыми генетическими заболеваниями, например, семейной экссудативной витреоретинопатией (FEVR) и болезнью Норри, обусловленной мутацией Wnt-рецептора Frizzled4 (Fzd4), корецептора LRP5 или секретируемого лиганда норрина (Berger et al. Nature Genet. 1:199-203 (1992); Chen et al. Nature Genet. 1:204-208 (1992); Robitaille et al. Nature Genet. 32:326-30 (2002); Toomes et al. Am. J. Hum. Genet. 74:721-30 (2004)). Модели этих генетических заболеваний доступны на мышах с нокаутом соответствующих гомологичных генов.
Несмотря на большое число достижений в области ангиогенеза глаз, сохраняется потребность в идентификации мишеней и разработке средств, которые могут дополнить или усилить эффективность существующих способов лечения.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение основано, по меньшей мере отчасти, на обнаружении того, что TSPAN12 представляет собой компонент пути сигнальной трансдукции, индуцируемого норрином и опосредуемого Frizzled4 и LRP5, и необходим для развития патологического ангиогенеза. Поэтому норрин и TSPAN12 представляют собой мишени лекарственных средств, ингибирующих аномальный ангиогенез глаз, включающий состояния, при которых не существует генетических мутаций в генах норрина, TSPAN12, Frizzled-4 или LRP5. Соответственно, настоящее изобретение относится к новым способам лечения глазных болезней, ассоциированных с ангиогенезом, используя реагенты, которые блокируют активность норрина или TSPAN12.
В одном из аспектов изобретение относится к способу снижения или ингибирования ангиогенеза у индивидуума, страдающего заболеванием глаз или состоянием, ассоциированным с ангиогенезом, предусматривающему введение индивидууму антагониста TSPAN12. В некоторых вариантах осуществления антагонист TSPAN12 представляет собой антитело против TSPAN12. В некоторых вариантах осуществления антагонист TSPAN12 содержит полипептидный фрагмент TSPAN12, включающий внеклеточный домен, такой как вторая внеклеточная петля. В некоторых вариантах осуществления антагонист дополнительно содержит константный регион иммуноглобулина, например, Fc-регион IgG. В некоторых вариантах осуществления заболевание или состояние глаз выбирают из группы, состоящей из: диабетической ретинопатии, хориоидальной неоваскуляризации (CNV), возрастной дегенерации желтого пятна (AMD), диабетического отека желтого пятна (DME), патологической миопии, болезни Фон Хиппеля-Линдау, гистоплазмоза глаз, окклюзии центральной вены сетчатки (CRVO), окклюзии ветвей центральной вены сетчатки (BRVO), неоваскуляризации роговицы, неоваскуляризации сетчатки, ретинопатии недоношенных (ROP), субконъюнктивального кровоизлияния и гипертензивной ретинопатии.
В некоторых вариантах осуществления способ дополнительно предусматривает введение второго антиангиогенного агента. В некоторых вариантах осуществления второй ангиогенный агент вводят до или после введения антагониста TSPAN12. В других вариантах осуществления, второй антиангиогенный агент вводят одновременно с антагонистом TSPAN12. В некоторых вариантах осуществления второй антиангиогенный агент представляет собой антагонист норрина или фактора роста клеток эндотелия сосудов (VEGF). В некоторых вариантах осуществления антагонист норрина или антагонист VEGF представляет собой антитело против норрина или антитело против VEGF (например, ранибизумаб).
В другом аспекте изобретение относится к способу снижения или ингибирования ангиогенеза у индивидуума, страдающего заболеванием или состоянием глаз, ассоциированным с ангиогенезом, содержащему введение индивидууму антагониста норрина. В некоторых вариантах осуществления антагонист норрина представляет собой антитело против норрина. В некоторых вариантах осуществления заболевание или состояние глаз выбирают из группы, состоящей из: диабетической ретинопатии, CNV, AMD, DME, патологической миопии, болезни фон Хиппеля-Линдау, гистоплазмоза глаз, CRVO, BRVO, неоваскуляризации роговицы, неоваскуляризации сетчатки, ROP, субконъюнктивального кровоизлияния и гипертензивной ретинопатии.
В некоторых вариантах осуществления способ дополнительно предусматривает введение второго антиангиогенного агента. В некоторых вариантах осуществления второй антиангиогенный агент вводят до или после введения антагониста норрина. В других вариантах осуществления второй антиангиогенный агент вводят одновременно с антагонистом норрина. В некоторых вариантах осуществления второй антиангиогенный агент представляет собой антагонист VEGF, например, антитело против VEGF, такое как ранибизумаб.
В другом аспекте изобретение относится к способу лечения заболевания или состояния глаз, ассоциированного с нежелательным ангиогенезом у индивидуума, предусматривающему введение индивидууму антагониста TSPAN12. В некоторых вариантах осуществления антагонист TSPAN12 представляет собой антитело против TSPAN12. В некоторых вариантах осуществления антагонист TSPAN12 содержит полипептидный фрагмент TSPAN12, включающий внеклеточный домен, такой как вторая внеклеточная петля. В некоторых вариантах осуществления антагонист дополнительно содержит константный регион иммуноглобулина, например, Fc-регион IgG. В некоторых вариантах осуществления заболевание или состояние глаз выбирают из группы, состоящей из: пролиферативных ретинопатий, включающих пролиферативную диабетическую ретинопатию, CNV, AMD, диабетической или других ишемических ретинопатий, DME, патологической миопии, болезни фон Хиппеля-Линдау, гистоплазмоза глаз, CRVO, BRVO, неоваскуляризации роговицы, неоваскуляризации сетчатки, ROP, субконъюнктивального кровоизлияния и гипертензивной ретинопатии.
В некоторых вариантах осуществления способ дополнительно предусматривает введение второго антиангиогенного агента. В некоторых вариантах осуществления второй антиангиогенный агент вводят до или после введения антагониста TSPAN12. В других вариантах осуществления второй антиангиогенный агент вводят одновременно с антагонистом TSPAN12. В некоторых вариантах осуществления второй антиангиогенный агент представляет собой антагонист норрина или VEGF. В некоторых вариантах осуществления антагонист норрина или антагонист VEGF представляет собой антитело против норрина или антитело против VEGF (например, ранибизумаб).
В другом аспекте изобретение относится к способу лечения заболевания или состояния глаз, ассоциированного с нежелательным ангиогенезом у индивидуума, содержащему введение индивидууму антагониста норрина. В некоторых вариантах осуществления антагонист норрина представляет собой антитело против норрина. В некоторых вариантах осуществления заболевание или состояние глаз выбирают из группы, состоящей из: пролиферативных ретинопатий, включающих пролиферативную диабетическую ретинопатию, CNV, AMD, диабетической или других ишемических ретинопатий, DME, патологической миопии, болезни Фон Хиппеля-Линдау, гистоплазмоза глаз, CRVO, BRVO, неоваскуляризации роговицы, неоваскуляризации сетчатки, ROP, субконъюнктивального кровоизлияния и гипертензивной ретинопатии.
В некоторых вариантах осуществления способ дополнительно предусматривает введение второго антиангиогенного агента. В некоторых вариантах осуществления второй антиангиогенный агент вводят до или после введения антагониста норрина. В других вариантах осуществления второй антиангиогенный агент вводят одновременно с антагонистом норрина. В некоторых вариантах осуществления второй антиангиогенный агент представляет собой антагонист VEGF, например, антитело против VEGF, такое как ранибизумаб.
В другом аспекте изобретение относится к способу получения антитела, используя пептид, состоящий по существу из аминокислот CRREPGTDQMMSLK (SEQ ID NO: 5). В некоторых вариантах осуществления способ предусматривает иммунизацию животного пептидом. В некоторых вариантах осуществления способ содержит скрининг библиотеки (например, библиотеки Fab) для идентификации антитела или фрагмента антитела, который связывается с пептидом. В некоторых вариантах осуществления изобретение относится к антителам, полученным любым из таких способов. В некоторых вариантах осуществления изобретение относится к способу определения TSPAN12, используя любое из таких антител.
В другом аспекте изобретение относится к in vitro и in vivo способам ингибирования образования мультимера FZD4, предусматривающим введение антагониста TSPAN12. В другом аспекте изобретение относится к in vitro и in vivo способам ингибирования передачи сигнала, опосредованной норрином, предусматривающим введение антагониста TSPAN12. В некоторых вариантах осуществления антагонист TSPAN12 представляет собой антитело против TSPAN12. В некоторых вариантах осуществления антагонист TSPAN12 содержит полипептидный фрагмент TSPAN12, включающий внеклеточный домен, такой как вторая внеклеточная петля. В некоторых вариантах осуществления антагонист дополнительно содержит константный регион иммуноглобулина, например, Fc-регион IgG.
В другом аспекте изобретение относится к способу лечения индивидуума, страдающего врожденным заболеванием глаз, обусловленным генетической мутацией в каком-либо из генов норрина, TSPAN12, FZD4 или LRP5, содержащему введение индивидууму агента, который усиливает образование мультимера FZD4. В некоторых вариантах осуществления заболевание представляет собой FEVR, болезнь Норри или болезнь Коатса. В некоторых вариантах осуществления агент, который повышает образование мультимера FZD4, выбирают из группы, состоящей из: норрина, антитела против FZD4, антитела против LRP5 и биспецифического антитела против FZD4/против LRP5. В некоторых вариантах осуществления генетическая мутация повреждает передачу сигнала, опосредованную FZD4. В некоторых вариантах осуществления генетическая мутация у индивидуума продуцирует аномальный белковый продукт у индивидуума, выбранный из группы, состоящей из: норрин-C95R, FZD4-M105V и FZD4-M157V. В некоторых вариантах осуществления наличие мутации у индивидуума определяют до лечения индивидуума.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На ФИГУРЕ 1 представлены типичные срезы сетчатки при ретинопатии недоношенных (ROP) мышей дикого типа (верх) и с нокаутом (КО) гена TSPAN12 (низ).
На ФИГУРЕ 2 представлены количественные результаты по числу зон неоваскуляризации, обнаруженных в срезах сетчатки при ROP мышей дикого типа (WT; слева) и с КО TSPAN12 (Hom; справа).
На ФИГУРЕ 3 показано, что TSPAN12 усиливает через Fzd4/LRP5 сигнальную трансдукцию, опосредованную норрином.
На ФИГУРЕ 4 показано, что усиление TSPAN12 сигнальной трансдукции, опосредованной норрином, специфично для Fzd4.
На ФИГУРЕ 5 показано, что TSPAN12 не усиливает сигнальную трансдукцию, опосредованную Wnt3a.
На ФИГУРЕ 6 показано, что норрин связывается с Fzd4, но не с LRP5 или TSPAN12.
На ФИГУРЕ 7 показано, что норрин связывается с клетками, экспрессирующими Fzd4, но не с клетками, экспрессирующими Fzd5, LRP5 или TSPAN12, и что норрин не иммунопреципитирует совместно с TSPAN12.
На ФИГУРЕ 8 показано, что TSPAN12 не ассоциирует с LRP5.
На ФИГУРЕ 9 показано, что TSPAN12 не усиливает связывание норрина с Fzd4.
На ФИГУРЕ 10 показано, что коэкспрессия TSPAN12 не изменяет экспрессию Fzd4 на плазматической мембране.
На ФИГУРЕ 11 показаны структуры высокого порядка, образованные норрином дикого типа и мутантным норрином C95R.
На ФИГУРЕ 12 показано, что сверхэкспрессия TSPAN12 может компенсировать дефекты в мономерном норрине C95R.
На ФИГУРЕ 13 показано, что TSPAN12 регулирует кластеризацию FZD4 в процессе передачи сигнала.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Определения
Если иначе не определено, технические и научные термины, использованные в данном документе, имеют то же значение, что и обычно понимаемое специалистами в данной области, к которым настоящее изобретение относится. См., например, руководства Singleton et al., Dictionary of Microbiology and Molecular Biology 2nd ed., J.Wiley & Sons (New York, NY 1994); Sambrook et al., Molecular Cloning, A Laboratory Manual, Cold Spring Harbor Press (Cold Spring Harbor, NY 1989). Для целей настоящего изобретения некоторые термины определяются ниже.
Под используемыми в данном документе терминами «TSPAN12», «полипептид TSPAN12», «норрин» и «полипептид норрина» понимают полипептид, имеющий аминокислотную последовательность природного полипептида TSPAN12 или норрина, независимо от способа его получения или вида. Таким образом, такие полипептиды могут иметь аминокислотную последовательность природного TSPAN12 или норрина человека, мыши или любого другого вида. Полноразмерная аминокислотная последовательность TSPAN12 человека представляет собой:

(SEQ ID NO: 1).
Полноразмерная аминокислотная последовательность TSPAN12 мыши представляет собой:
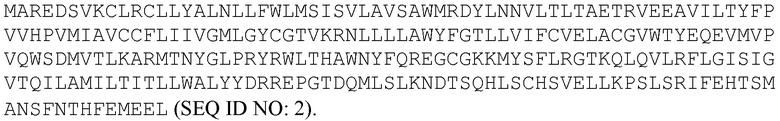 .
.
Полноразмерная аминокислотная последовательность норрина человека представляет собой:
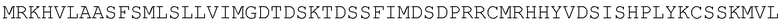
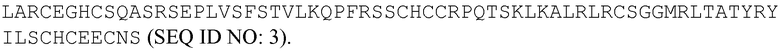
Полноразмерная аминокислотная последовательность норрина мыши представляет собой:

Такие полипептиды TSPAN12 или норрина могут быть выделены из природного материала или получены рекомбинантными и/или синтетическими способами.
«Выделенный» в отношении полипептида означает, что он был очищен из природного источника или получен рекомбинантными или синтетическими способами и очищен. «Очищенный» полипептид по существу свободен от других полипептидов или пептидов. «По существу свободен» в данном случае означает меньше чем около 5%, предпочтительно меньше чем около 2%, более предпочтительно меньше чем около 1%, еще более предпочтительно меньше чем около 0,5%, самое предпочтительное, меньше чем около 0,1% контаминации другими белками источника.
Термин «антагонист» используется в широком смысле и включает любую молекулу, которая частично или полностью блокирует, ингибирует или нейтрализует биологическую активность полипептида. Например, антагонист TSPAN12 или норрина частично или полностью блокировал бы, ингибировал или нейтрализовал способность TSPAN12 или норрина трансдуцировать или инициировать индуцированную норрином передачу сигнала или давать возможность патологического образования сосудов в глазе. Подходящие молекулы антагонистов включают, в частности, антагонистические антитела или фрагменты антител, фрагменты или варианты аминокислотной последовательности нативного полипептида TSPAN12 или норрина, пептиды, растворимые фрагменты корецептора(ов) TSPAN12 или норрина, антисмысловые РНК, рибозимы, РНКи, небольшие органические молекулы и т.д. Способы идентификации антагонистов полипептида TSPAN12 или норрина могут предусматривать приведение в контакт полипептида TSPAN12 или норрина с молекулой кандидатного антагониста и измерение детектируемого изменения одной или нескольких биологических активностей, обычно ассоциируемых с полипептидом.
«Активный» или «активность» для целей данного документа относится к форме(ам) TSPAN12 или норрина, которая(ые) сохраняет(ют) биологическую и/или иммунологическую активность, где под «биологической» активностью понимают биологическую функцию, обусловленную TSPAN12 или норрином, отличную от способности индуцировать продукцию антитела, и под «иммунологической» активностью понимают способность индуцировать продукцию антитела против антигенного эпитопа, содержащегося в TSPAN12 или норрине. Основными биологическими активностями TSPAN12 и норрина являются трансдукция или инициация передачи сигнала, индуцированной норрином, и индуцирование патологического образования сосудов в глазу.
Под «корецептором TSPAN12» или «корецептором норрина» понимают молекулы, с которыми TSPAN12 или норрин связывается и которые опосредуют биологическую активность TSPAN12 или норрина.
Термин «антитело» в данном документе используется в широком смысле и включает в частности моноклональные антитела человека, отличные от человеческих (например, мышиные) и гуманизированные (включая полноразмерные моноклональные антитела), поликлональные антитела, мультиспецифические антитела (например, биспецифические антитела) и фрагменты антител при условии, что у них наблюдается желаемая биологическая активность.
«Нативные антитела» обычно представляют собой гетеротетрамерные гликопротеины размером около 150000 дальтон, состоящие из двух идентичных легких (L) цепей и двух идентичных тяжелых (Н) цепей. Каждая легкая цепь соединена с тяжелой цепью одной ковалентной дисульфидной связью, тогда как число дисульфидных связей между тяжелыми цепями различных изотипов иммуноглобулинов варьирует. Каждая тяжелая и легкая цепь также имеет расположенные на равном расстоянии друг от друга внутрицепочечные дисульфидные мостики. Каждая тяжелая цепь имеет на одном конце вариабельный домен (VH) с последующим большим числом константных доменов. Каждая легкая цепь имеет вариабельный домен на одном конце (VL) и константный домен на другом своем конце; константный домен легкой цепи соответствует первому константному домену тяжелой цепи, и вариабельный домен легкой цепи соответствует вариабельному домену тяжелой цепи. Полагают, что определенные аминокислотные остатки образуют поверхность контакта между вариабельными доменами легкой и тяжелой цепей.
Расщепление антител папаином приводит к образованию двух идентичных антигенсвязывающих фрагментов, называемых “Fab”-фрагментами, каждый из которых имеет один антигенсвязывающий сайт, и остаточного “Fc”-фрагмента, название которого отражает его способность легко кристаллизоваться. Обработка пепсином приводит к получению F(ab')2-фрагмента, который имеет два антигенсвязывающих сайта и все еще способен перекрестно связывать антиген.
«Fv» представляет собой минимальный фрагмент антитела, который содержит полный сайт распознавания и связывания антигена. Этот регион состоит из димера вариабельного домена одной тяжелой цепи и одной легкой цепи в плотной нековалентной ассоциации.
Fab-фрагмент также содержит константный домен легкой цепи и первый константный домен (СН1) тяжелой цепи. Fab'-фрагменты отличаются от Fab-фрагментов добавлением нескольких остатков на карбоксильном конце домена СН1 тяжелой цепи, включающих один или несколько цистеин(ов) из шарнирного региона антитела. Fab'-SH представляет собой обозначение в данном документе Fab', в котором цистеиновый(е) остаток(ки) константных доменов несет(ут) свободную тиольную группу. F(ab')2-фрагменты антитела исходно получали в виде пар Fab'-фрагментов, которые имеют между собой шарнирные цистеины. Также известны и другие химические сочетания фрагментов антител.
«Легкие цепи» антител (иммуноглобулинов) любого вида позвоночных могут быть отнесены к одному из двух четко различающихся типов, называемых каппа (κ) и лямбда (λ) исходя из аминокислотных последовательностей их константных доменов.
В зависимости от аминокислотной последовательности константного домена их тяжелых цепей иммуноглобулины могут быть отнесены к различным классам. Существует пять основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM, и некоторые из них могут быть дополнительно разделены на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные домены тяжелых цепей, которые соответствуют различным классам иммуноглобулинов, называются α, δ, ε, γ и μ соответственно. Структуры субъединиц и трехмерные конфигурации различных классов иммуноглобулинов хорошо известны.
«Фрагменты антитела» содержат часть полноразмерного антитела, как правило, его антигенсвязывающий или вариабельный домен. К примерам фрагментов антител относятся Fab, Fab', F(ab')2 и Fv-фрагменты.
Под используемым в данном документе термином «моноклональное антитело» понимают антитело, полученное из популяции по существу гомогенных антител, т.е. отдельные антитела, составляющие популяцию, идентичны за исключением возможных природных мутаций, которые могут присутствовать в незначительных количествах. Моноклональные антитела высокоспецифичны, они направлены против одного антигенного сайта. Более того, в противоположность препаратам традиционных (поликлональных) антител, которые обычно включают различные антитела, направленные против различных детерминант (эпитопов), каждое моноклональное антитело направлено против одной детерминанты на антигене. Определение «моноклональное» указывает на природу антитела, как полученного из по существу гомогенной популяции антител, и не должно быть истолковано, как требующее получения антитела каким-либо конкретным способом. Например, моноклональные антитела, используемые по настоящему изобретению, могут быть созданы гибридомным способом, впервые описанным в статье Kohler et al., Nature 256:495 (1975), или могут быть созданы способами рекомбинантных ДНК (см., например, патент США 4816567). «Моноклональные антитела» также могут быть выделены из библиотек фаговых антител, используя техники, описанные, например, в статьях Clackson et al., Nature 352:624-628 (1991) и Marks et al., J. Mol. Biol. 222:581-597 (1991).
К моноклональным антителам в данном документе относятся, в частности, «химерные» антитела, в которых часть тяжелой и/или легкой цепи идентична или гомологична соответствующим последовательностям в антителах, полученных от конкретного вида или относящихся к определенному классу или подклассу антител, тогда как остальная часть цепи(ей) идентична или гомологична соответствующим последовательностям в антителах, полученных из другого вида или относящихся к другому классу или подклассу антител, а также фрагменты таких антител при условии, что у них наблюдается желаемая биологическая активность (патент США 4816567; и статья Morrison et al., Proc. Natl. Acad. Sci. USA 81:6851-6855 (1984)).
«Гуманизированные» формы антител, отличных от человеческих (например, мышиных), представляют собой химерные антитела, которые содержат минимальную последовательность, происходящую из иммуноглобулина, отличного от человеческого. Преимущественно, гуманизированные антитела представляют собой иммуноглобулины человека (реципиентное антитело), в которых остатки гипервариабельного региона реципиента замещены остатками гипервариабельного региона вида, отличного от человека (донорное антитело), такого как мышь, крыса, кролик или примат, отличный от человека, обладающие желаемой специфичностью, аффинностью и активностью. В некоторых случаях остатки каркасного региона (FR) иммуноглобулина человека замещены соответствующими остатками, отличными от человеческих. Более того, гуманизированные антитела могут содержать остатки, которых не находят в реципиентном антителе или в донорном антителе. Эти модификации создают для осуществления дополнительного улучшения антитела. В целом гуманизированное антитело должно содержать, по существу, все из по меньшей мере одного и обычно два вариабельных домена, в которых все или по существу все гипервариабельные регионы соответствуют гипервариабельным регионам иммуноглобулина, отличного от человеческого, и все или по существу все регионы FR представляют собой FR последовательности иммуноглобулина человека. Гуманизированное антитело необязательно также будет содержать по меньшей мере часть константного региона иммуноглобулина (Fc), обычно иммуноглобулина человека. Более подробно см. статьи Jones et al. Nature 321:522-525 (1986); Reichmann et al. Nature 332:323-329 (1988); и Presta Curr. Op. Struct. Biol. 2:593-596 (1992).
Под используемым в данном документе термином «лечение» понимают подход для получения благоприятных или желательных клинических результатов. Для целей настоящего изобретения к благоприятным или желательным клиническим результатам относятся, но не ограничиваясь ими, облегчение симптомов, уменьшение степени заболевания, стабилизированное (т.е. не ухудшающееся) состояние заболевания, задержка или замедление прогрессирования заболевания, улучшение состояния или временное облегчение заболевания и ремиссия (либо частичная, либо полная), либо детектируемые, либо недетектируемые. «Лечение» представляет собой вмешательство, осуществляемое с целью предотвращения развития или изменения патологии расстройства. Соответственно, под «лечением» может пониматься терапевтическое лечение или профилактическое или способы упреждения. К нуждающимся в лечении относятся индивидуумы, уже страдающие расстройством, а также индивидуумы, у которых расстройство должно быть предотвращено. Конкретно, лечение может непосредственно предотвращать, замедлять или иным образом уменьшать патологию клеточной дегенерации или повреждения, такую как патология опухолевых клеток при лечении рака, или может делать клетки более чувствительными к лечению другими терапевтическими агентами.
Под «длительным» применением понимают введение агента(ов) продолжительно, в противоположность экстренному введению, чтобы поддерживать начальный терапевтический эффект (активность) в течение длительного периода времени. «Дробное» введение представляет собой лечение, которое осуществляют не последовательно без перерыва, а скорее периодически по характеру.
«Внутриглазное неоваскулярное заболевание» представляет собой заболевание, отличающееся неоваскуляризацией глаза. К примерам внутриглазных неоваскулярных заболеваний относятся, но не ограничиваясь ими, пролиферативные ретинопатии, включающие пролиферативную диабетическую ретинопатию, хориоидальная неоваскуляризация (CNV), возрастная дегенерация желтого пятна (AMD), диабетическая и другие ишемические ретинопатии, диабетический отек желтого пятна (DME), патологическая миопия, болезнь Фон Хиппеля-Линдау, гистоплазмоз глаз, окклюзия центральной вены сетчатки (CRVO), окклюзия ветвей центральной вены сетчатки (BRVO), неоваскуляризация роговицы, неоваскуляризация сетчатки, ретинопатия недоношенных (ROP), субконъюнктивальное кровоизлияние и гипертензивная ретинопатия. Предпочтительно, чтобы внутриглазное неоваскулярное заболевание исключало состояния, которые являются следствием генетических мутаций в каком-либо из генов норрина, TSPAN12, Frizzled-4 или LRP5. Например, внутриглазное неоваскулярное заболевание по изобретению предпочтительно исключает FEVR и болезнь Норри.
К «патологии» заболевания относятся все явления, которые подвергают опасности здоровье пациента.
К введению «в сочетании с» одним или несколькими дополнительными терапевтическими агентами относятся одновременное и последовательное введение в любом порядке.
К «носителям», используемым в данном документе, относятся фармацевтически приемлемые носители, эксципиенты или стабилизаторы, которые нетоксичны для клетки или млекопитающего, подвергаемым их воздействию, в используемых дозах и концентрациях. Часто физиологически приемлемый носитель представляет собой водный рН забуференный раствор. К примерам физиологически приемлемых носителей относятся буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту; низкомолекулярный (меньше чем из около 10 остатков) полипептид; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелирующие агенты, такие как EDTA; сахарные спирты, такие как маннитол или сорбитол; солеобразующие противоионы, такие как натрий; и/или неионные поверхностно-активные вещества, такие как TWEENTM, полиэтиленгликоль (PEG) и PLURONICSTM.
«Малая молекула» определяется в данном документе как имеющая молекулярную массу ниже около 500 дальтон.
Способы осуществления изобретения
Получение и идентификация антагонистов активности TSPAN12 или норрина
Для идентификации соединений, которые связываются или образуют комплекс с полипептидами TSPAN12 или норрина или иным образом влияют на их активность и/или взаимодействие с другими клеточными белками, разрабатывают скрининговые анализы на кандидатные лекарственные средства-антагонисты.
В качестве антагонистов TSPAN12 или норрина могут действовать малые молекулы и, таким образом, быть терапевтически используемыми. К таким малым молекулам могут относиться природные малые молекулы, синтетические органические или неорганические соединения и пептиды. Тем не менее, малые молекулы по настоящему изобретению не ограничиваются этими формами. Обширные библиотеки малых молекул коммерчески доступны, и для скрининга этих молекул в отношении желаемой активности в данном документе представлен или хорошо известен в данной области широкий спектр анализов.
В некоторых вариантах осуществления малые молекулы-антагонисты TSPAN12 или норрина идентифицируют по их способности ингибировать одну или несколько биологических активностей TSPAN12 или норрина. Таким образом, кандидатное соединение приводят в контакт с TSPAN12 или норрином и затем анализируют биологическую активность TSPAN12 или норрина. В одном из вариантов осуществления оценивают способность TSPAN12 или норрина трансдуцировать или инициировать передачу сигнала, опосредованную норрином. При ингибировании биологической активности TSPAN12 или норрина соединение идентифицируют как антагониста.
Соединения, идентифицированные в качестве антагонистов TSPAN12 или норрина, могут быть использованы в способах по настоящему изобретению. Например, антагонисты TSPAN12 или норрина могут быть использованы для лечения внутриглазного неоваскулярного заболевания.
Для дальнейшего понимания значения TSPAN12 или норрина в развитии и патогенезе внутриглазного неоваскулярного заболевания и тестирования эффективности кандидатных терапевтических агентов, включающих антитела и другие антагонисты нативных полипептидов TSPAN12 или норрина, такие как малые молекулы-антагонисты, может быть использовано большое число хорошо известных моделей животных (включая, например, модели ретинопатии недоношенных и индуцированную лазером хориоидальную неоваскуляризацию; Ruiz-Edera & Verkman Invest. Ophthalmol. & Vis. Sci. 48(10): 4802-10 (2007), Yu et al. Invest. Ophthalmol. & Vis. Sci. 49(6): 2599-605 (2007)). In vivo природа таких моделей делает их особенно предсказуемыми в отношении ответов у пациентов-людей.
Исследования связывания антител
Тестируют способность антител связывать и ингибировать влияние TSPAN12 или норрина на репортерные клетки, передающие сигнал Wnt. Типичные способы представлены в примере 2, но специалисту в данной области будут без труда понятны и другие способы. К типичным антителам относятся поликлональные, моноклональные, гуманизированные, биспецифические и гетероконъюгированные антитела, получение которых описано в данном документе.
Исследования связывания антител могут быть осуществлены любым известным способом анализа, таким как анализы конкурентного связывания, прямые и непрямые сэндвич-анализы и анализы иммунопреципитации. Zola, Monoclonal Antibodies: A Manual of Techniques (CRC Press, Inc., 1987), pp.147-158.
Анализы конкурентного связывания основаны на способности меченого стандарта конкурировать с аналитом испытываемого образца за связывание с ограниченным количеством антитела. Количество белка-мишени в испытываемом образце обратно пропорционально количеству стандарта, который становится связанным с антителами. Для содействия определению количества стандарта, становящегося связанным, предпочтительно понижают растворимость антител до или после конкуренции, так что стандарт и аналит, которые связываются с антителами, можно удобно отделить от стандарта и аналита, которые остаются несвязанными.
Сэндвич-анализы включают в себя применение двух антител, каждое из которых способно связываться с отличным иммуногенным участком, или эпитопом, детектируемого белка. В сэндвич-анализе аналит испытываемого образца связывается первичным антителом, которое иммобилизуют на твердой подложке, и после этого вторичное антитело связывается с аналитом, таким образом формируя нерастворимый комплекс, состоящий из трех частей. См., например, патент США 4376110. Вторичное антитело само может являться меченным с помощью детектируемого фрагмента (прямые сэндвич-анализы) или его можно измерить, используя антитело против иммуноглобулина, которое метят с помощью детектируемого фрагмента (непрямой сэндвич-анализ). Например, один из видов сэндвич-анализа представляет собой анализ ELISA, в этом случае детектируемый фрагмент представляет собой фермент.
Для иммуногистохимии образец ткани может быть свежим или замороженным или может быть залит в парафин и фиксирован с помощью консерванта, такого как формалин.
К соединениям, используемым в лечении сердечно-сосудистых, эндотелиальных и ангиогенных расстройств, относятся, без ограничения, антитела, малые органические и неорганические молекулы, пептиды, фосфопептиды, антисмысловая, малая интерферирующая РНК и молекулы рибозимов, трехспиральные молекулы и т.д., которые ингибируют экспрессию и/или активность генного продукта-мишени.
К более конкретным примерам потенциальных антагонистов относятся полипептид, который связывается с TSPAN12 или норрином, и, в частности, антитела, включая, без ограничения, поли- и моноклональные антитела и фрагменты антител, одноцепочечные антитела, антиидиотипические антитела и химерные или гуманизированные варианты таких антител или фрагментов, а также антитела и фрагменты антител человека. В отношении TSPAN12 в качестве антагонистов также может(гут) служить некоторый(е) внеклеточный(е) домен(ы) (см., например, статьи Ho et al. J. Virol. 80(13): 6487-96 (2006); Hemler Nature Rev. Drug Discovery 7: 747-58 (2008)). Альтернативно, потенциальный антагонист может представлять собой близкородственный белок, например, мутированную форму TSPAN12 или норрина, которая взаимодействует с корецептором(ами), но без эффекта, таким образом, конкурентно ингибируя действие TSPAN12 или норрина.
Другой потенциальный антагонист TSPAN12 или норрина представляет собой конструкцию антисмысловой РНК или ДНК, полученную, используя антисенс-технологию, где, например, молекула антисмысловой РНК или ДНК непосредственно блокирует трансляцию мРНК за счет гибридизации с мРНК-мишенью и предотвращения трансляции белка. Антисенс-технология может быть использована для контролирования экспрессии гена через образование тройной спирали или антисмысловую ДНК или РНК, оба этих способа основаны на связывании полинуклеотида с ДНК или РНК. Например, 5'-кодирующий участок последовательности полинуклеотида, которая кодирует зрелые полипептиды TSPAN12 и норрина в данном документе, используют для создания антисмыслового РНК-олигонуклеотида длиной от около 10 до 40 пар оснований. ДНК-олигонуклеотид создают так, чтобы он был комплементарен региону гена, включенному в транскрипцию (тройная спираль - см. статьи Lee et al., Nucl. Acids Res. 6:3073 (1979); Cooney et al., Science 241:456 (1988); Dervan et al., Science 251:1360 (1991)), таким образом, предотвращая транскрипцию и продукцию TSPAN12 или норрина. Под последовательностью, «комплементарной» участку РНК, как обозначается в данном документе, понимают последовательность, обладающую достаточной комплементарностью, чтобы быть способной гибридизоваться с РНК, образуя устойчивый дуплекс; в случае двухцепочечных антисмысловых нуклеиновых кислот, таким образом может быть протестирована одна из цепей дуплексной ДНК или может быть проанализировано образование тройной спирали. Способность гибридизоваться будет зависеть как от степени комплементарности, так и от длины антисмысловой нуклеиновой кислоты. Как правило, чем длиннее гибридизирующаяся нуклеиновая кислота, тем больше несоответствий оснований с РНК она может содержать, при этом все-таки образуя устойчивый дуплекс (или может быть триплекс). Специалист в данной области может установить приемлемую степень несоответствия, используя стандартные процедуры определения точки плавления гибридизовавшегося комплекса. Антисмысловой РНК-олигонуклеотид гибридизуется с мРНК in vivo и блокирует трансляцию молекулы мРНК в TSPAN12 (антисенс - Okano, Neurochem. 56:560 (1991); Oligodeoxynucleotides as Antisense Inhibitors of Gene Expression (CRC Press: Boca Reton, FL, 1988).
Антисмысловые олигонуклеотиды могут представлять собой ДНК или РНК или химерные смеси или их производные или модифицированные версии, одноцепочечные или двухцепочечные. Олигонуклеотид может быть модифицирован по фрагменту основания, фрагменту сахара или фосфатному остову, например, для улучшения устойчивости молекулы, гибридизации и т.д. Олигонуклеотид может включать другие присоединенные группы, такие как пептиды (например, для нацеливания рецепторов клетки-хозяина in vivo) или агенты, облегчающие транспорт через клеточную мембрану (см., например, статьи Letsinger, et al., Proc. Natl. Acad. Sci. U.S.A. 86:6553-6556 (1989); Lemaitre, et al., Proc. Natl. Acad. Sci. U.S.A. 84:648-652 (1987); публикацию РСТ WO88/09810, опубликованную 15 декабря 1988), или гематоэнцефалический барьер (См., например, публикацию РСТ WO89/10134, опубликованную 25 апреля 1988), расщепляющие агенты, запускающие гибридизацию (См., например, статью Krol et al., BioTechniques 6:958-976 (1988) или интеркалирующие агенты (См., например, Zon, Pharm. Res. 5:539-549 (1988)). Для этого олигонуклеотид может быть конъюгирован с другой молекулой, например, пептидом, перекрестно-сшивающим агентом, запускающим гибридизацию, транспортным агентом, расщепляющим агентом, запускающим гибридизацию и т.д.
Антисмысловой олигонуклеотид может содержать по меньшей мере один модифицированный фрагмент основания, который выбирают из группы, включающей, но не ограничиваясь ими, 5-фторурацил, 5-бромурацил, 5-хлорурацил, 5-йодурацил, гипоксантин, ксантин, 4-ацетилцитозин, 5-(карбоксигидроксилметил) урацил, 5-карбоксиметиламинометил-2-тиоуридин, 5-карбоксиметиламинометилурацил, дигидроурацил, бета-D-галактозилквеозин, инозин, N6-изопентениладенин, 1-метилгуанин, 1-метилинозин, 2,2-диметилгуанин, 2-метиладенин, 2-метилгуанин, 3-метилцитозин, 5-метилцитозин, N6-аденин, 7-метилгуанин, 5-метиламинометилурацил, 5-метоксиаминометил-2-тиоурацил, бета-D-маннозилквеозин, 5'-метоксикарбоксиметилурацил, 5-метоксиурацил, 2-метилтио-N6-изопентениладенин, урацил-5-оксиуксусная кислота (v), вибутоксозин, псевдоурацил, квеозин, 2-тиоцитозин, 5-метил-2-тиоурацил, 2-тиоурацил, 4-тиоурацил, 5-метилурацил, метиловый эфир урацил-5-оксиуксусной кислоты, урацил-5-оксиуксусная кислота (v), 5-метил-2-тиоурацил, 3-(3-амино-3-N-2-карбоксипропил) урацил, (аср3)w и 2,6-диаминопурин.
Антисмысловой олигонуклеотид также может содержать, по меньшей мере, один модифицированный фрагмент сахара, выбранного из группы, включающей, но не ограничиваясь ими, арабинозу, 2-фторарабинозу, ксилулозу и гексозу.
В еще одном варианте осуществления антисмысловой олигонуклеотид содержит по меньшей мере один модифицированный фосфатный остов, выбранный из группы, состоящей из фосфоротиоата, фосфородитиоата, фосфорамидотиоата, фосфорамидата, фосфордиамидата, метилфосфоната, алкилфосфотриэфира и формацеталя или их аналога.
В еще одном варианте осуществления антисмысловой олигонуклеотид представляет собой аномерный олигонуклеотид. Аномерный олигонуклеотид образует специфические двуцепочечные гибриды с комплементарной РНК, в которых, в противоположность обычным составляющим, цепи идут параллельно друг другу (Gautier, et al., Nucl. Acids Res. 15:6625-6641 (1987)). Олигонуклеотид представляет собой 2'-0-метилрибонуклеотид (Inoue, et al., Nucl. Acids Res. 15:6131-6148 (1987)) или химерный РНК-ДНК-аналог (Inoue, et al., FEBS Lett. 215:327-330 (1987)).
В некоторых вариантах осуществления антагонисты представляют собой ингибиторные дуплексные РНК, например, siРНК, shРНК и т.д.
Олигонуклеотиды по изобретению могут быть синтезированы стандартными способами, известными в данной области, например, используя автоматический ДНК-синтезатор (такой как коммерчески доступные ДНК-синтезаторы фирм Biosearch, Applied Biosystems и т.д.). Например, фосфоротиоатные олигонуклеотиды могут быть синтезированы способом Stein, et al. (Nucl. Acids Res.16:3209 (1988)), метилфосфонатные олигонуклеотиды могут быть получены, используя подложки на основе полимера и стекла с контролируемым размером пор (Sarin, et al., Proc. Natl. Acad. Sci. U.S.A. 85:7448-7451 (1988)) и т.д.
Олигонуклеотиды, описанные выше, также могут быть доставлены к клеткам так, что антисмысловая РНК или ДНК может быть экспрессирована in vivo для ингибирования продукции TSPAN12 или норрина. При использовании антисмысловой ДНК предпочтительны олигодезоксирибонуклеотиды, полученные из сайта инициации трансляции, например, между около -10 и +10 позициями нуклеотидной последовательности гена-мишени.
К потенциальным антагонистам дополнительно относятся малые молекулы, которые связываются с TSPAN12 или норрином, таким образом блокируя его активность. К примерам малых молекул относятся, но не ограничиваясь ими, малые пептиды или пептидоподобные молекулы, предпочтительно растворимые пептиды, и синтетические непептидильные органические или неорганические соединения.
Дополнительные потенциальные антагонисты представляют собой рибозимы, которые являются энзиматическими молекулами РНК, способными катализировать специфическое расщепление РНК. Рибозимы действуют путем гибридизации, специфичной для последовательности, с комплементарной РНК-мишенью с последующим эндонуклеолитическим расщеплением. Специфические сайты расщепления для рибозимов в потенциальной РНК-мишени могут быть идентифицированы известными техниками. Более подробно см., например, статью Rossi, Current Biology 4:469-471 (1994) и публикацию РСТ WO 97/33551 (опубликованную 18 сентября 1997).
Тогда как рибозимы, которые расщепляют мРНК по последовательностям сайт-специфического распознавания, могут быть использованы для разрушения мРНК генов-мишеней, предпочтительно применение рибозимов типа головки молотка. Рибозимы типа головки молотка расщепляют мРНК по сайтам, определяемым фланкирующими регионами, которые образуют комплементарные пары нуклеотидов с мРНК-мишенью. Единственное условие заключается в том, что мРНК-мишень должна иметь следующую последовательность из двух оснований: 5'-UG-3'. Конструкция и получение рибозимов типа головки молотка хорошо известны в данной области и более полно описаны в руководстве Myers, Molecular Biology and Biotechnology: A Comprehensive Desk Reference, VCH Publishers, New York (1995), (смотри конкретно фигуру 4, страница 833) и статье Haseloff and Gerlach, Nature, 334:585-591 (1988), которая приводится в данном документе в качестве ссылки в полном объеме.
Предпочтительно, рибозим создают так, чтобы сайт распознавания и расщепления был расположен вблизи 5'-конца мРНК гена-мишени, т.е. для повышения эффективности и минимизации внутриклеточной аккумуляции нефункциональных мРНК-транскриптов.
К рибозимам по настоящему изобретению также относятся РНК-эндорибонуклеазы (далее в данном документе «рибозимы типа Cech»), такие как эндорибонуклеаза, которая встречается в природе в Tetrahymena thermophila (известная как IVS или РНК L-19 IVS) и которая была подробно описана Thomas Cech и соавторами (Zaug, et al., Science, 224:574-578 (1984); Zaug and Cech, Science, 231:470-475 (1986); Zaug, et al., Nature, 324:429-433 (1986); опубликованная международная патентная заявка WO 88/04300 Университетом патентов Inc.; Been and Cech, Cell, 47:207-216 (1986)). Рибозимы типа Cech имеют активный сайт из восьми пар нуклеотидов, который гибридизуется с последовательностью РНК-мишени, после чего происходит расщепление РНК-мишени. Изобретение охватывает такие рибозимы типа Cech, которые нацеливают последовательности активного сайта из восьми пар нуклеотидов, которые присутствуют в гене-мишени.
Как и в антисенс-подходе, рибозимы могут быть составлены из модифицированных олигонуклеотидов (например, для улучшения устойчивости, нацеливания и т.д.) и должны быть доставлены к клеткам, которые экспрессируют ген-мишень in vivo. Предпочтительный способ доставки включает применение ДНК-конструкции, «кодирующей» рибозим под контролем сильного конститутивного промотора pol III или pol II, так что трансфицированные клетки будут продуцировать достаточные количества рибозима, чтобы разрушить эндогенные месседжеры гена-мишени и ингибировать трансляцию. Поскольку рибозимы в отличие от антисмысловых молекул каталитически активны, для получения результата нужна более низкая внутриклеточная концентрация.
Молекулы нуклеиновых кислот при образовании тройной спирали, используемые для ингибирования транскрипции, должны быть одноцепочечными и состоять из дезоксинуклеотидов. Комбинацию оснований этих олигонуклеотидов задают так, чтобы она способствовала образованию тройной спирали по правилам спаривания оснований Хугстэна, что обычно требует протяженных участков пуринов или пиримидинов на одной из цепей дуплекса. Более подробно см., например, публикацию РСТ WO 97/33551, выше.
Антагонисты TSPAN12 или норрина также могут быть использованы в лечении внутриглазных заболеваний, к которым относятся, но не ограничиваясь ими, пролиферативные ретинопатии, включающие пролиферативную диабетическую ретинопатию, хориоидальная неоваскуляризация (CNV), возрастная дегенерация желтого пятна (AMD), диабетическая и другие ишемические ретинопатии, диабетический отек желтого пятна (DME), патологическая миопия, болезнь Фон Хиппеля-Линдау, гистоплазмоз глаз, окклюзия центральной вены сетчатки (CRVO), окклюзия ветвей центральной вены сетчатки (BRVO), неоваскуляризация роговицы, неоваскуляризация сетчатки, ретинопатия недоношенных (ROP), субконъюнктивальное кровоизлияние и гипертензивная ретинопатия.
Протоколы введения, схемы приема, дозы и составы
Антагонисты TSPAN12 или норрина можно использовать в фармацевтических целях в качестве профилактического и терапевтического агента для лечения большого числа расстройств и заболеваний, приведенных выше.
Терапевтические композиции антагонистов получают для хранения в форме лиофилизированных препаративных форм или водных растворов путем смешивания желаемой молекулы, обладающей подходящей степенью чистоты, с необязательными фармацевтически приемлемыми носителями, эксципиентами или стабилизаторами (Remington's Pharmaceutical Sciences, 16th edition, Osol, A. Ed. (1980)). Приемлемые носители, эксципиенты или стабилизаторы нетоксичны для реципиентов в используемых дозах и концентрациях, и к ним относятся буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как хлорид октадецилдиметилбензиламмония; хлорид гексаметония; хлорид бензалкония, хлорид бензетония; фенол, бутиловый или бензиловый спирт; алкилпарабены, такие как метил- или пропилпарабен; катехол; резорцинол; циклогексанол; 3-пентанол; и мета-крезол); низкомолекулярные (меньше чем около 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин, или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелирующие агенты, такие как EDTA; сахара, такие как сахароза, маннитол, трегалоза или сорбитол; солеобразующие противоионы, такие как натрий; комплексы с металлами (например, комплексы Zn-белок); и/или неионные поверхностно-активные вещества, такие как TWEENTM, PLURONICSTM или полиэтиленгликоль (PEG).
К дополнительным примерам таких носителей относятся ионообменники, оксид алюминия, стеарат алюминия, лецитин, белки сыворотки, такие как сывороточный альбумин человека, забуферивающие вещества, такие как фосфаты, глицин, сорбиновая кислота, сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, вода, соли или электролиты, такие как протаминсульфат, вторичный кислый фосфат натрия, вторичный кислый фосфат калия, хлорид натрия, соли цинка, коллоидная окись кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы и полиэтиленгликоль. К носителям антагониста для форм местного нанесения или гелевых форм относятся полисахариды, такие как натрий-карбоксиметилцеллюлоза или метилцеллюлоза, поливинилпирролидон, полиакрилаты, блочные полимеры полиоксиэтилен-полиоксипропилен, полиэтиленгликоль и спирты из древесного воска. Для всех введений подходящим образом используются принятые формы депонирования. К таким формам относятся, например, микрокапсулы, нанокапсулы, липосомы, пластыри, формы для ингаляции, назальные спреи, таблетки под язык и препараты с замедленным высвобождением. Антагонисты TSPAN12 или норрина обычно должны быть смешаны в таких носителях в концентрации от около 0,1 мг/мл до 100 мг/мл.
Другой состав содержит встраивание антагониста TSPAN12 или норрина в сформированные препараты. Такие препараты могут быть использованы в модуляции эндотелиального клеточного роста и ангиогенеза. Кроме того, с помощью этих препаратов могут модулироваться опухолевая инвазия и метастазирование.
Антагонисты TSPAN12 или норрина, используемые для введения in vivo, должны быть стерильными. Это легко осуществляют фильтрацией через стерильные фильтрующие мембраны до или после лиофилизации и восстановления. Для лиофилизованной формы антагонист TSPAN12 или норрина обычно смешивают в момент использования вместе с другими ингредиентами для восстановления с подходящим разбавителем. Примером жидкого состава антагониста TSPAN12 или норрина является стерильный прозрачный бесцветный, не содержащий консервантов раствор, разлитый в емкость с одной дозой для подкожного введения. Консервированные фармацевтические композиции, подходящие для повторного применения, могут содержать, например, в зависимости главным образом от показания и типа полипептида:
антагонист TSPAN12 или норрина;
буфер, способный поддерживать рН в диапазоне максимальной стабильности полипептида или другой молекулы в растворе, предпочтительно около 4-8;
детергент/поверхностно-активное вещество, главным образом, для стабилизации полипептида или молекулы против агрегации, индуцированной встряхиванием;
агент для поддержания изотоничности;
консервант, выбранный из группы, состоящей из фенола, бензилового спирта и галогенида бензетония, например, хлорида; и
воду.
При использовании неионного детергента он может представлять собой, например, полисорбаты (например, POLYSORBATETM (TWEENTM 20, 80 и т.д.) или полоксамеры (например, POLOXAMERTM 188). Применение неионных поверхностно-активных веществ дает возможность подвергать состав воздействию нагрузок поверхности раздела, не вызывая денатурации полипептида. Кроме того, такие составы, содержащие поверхностно-активные вещества, могут быть использованы в аэрозольных устройствах, таких как устройства, используемые для дозированного введения лекарственных средств через легкие, и безыгольных шприцах (См., например, ЕР 257956).
Агент для поддержания изотоничности может присутствовать для обеспечения изотоничности жидкой композиции антагониста TSPAN12 или норрина и включает многоатомные сахарные спирты, предпочтительно трехатомные или выше сахарные спирты, такие как глицерин, эритритол, арабитол, ксилитол, сорбитол и маннитол. Эти сахарные спирты могут использоваться самостоятельно или в комбинации. Альтернативно, для доведения растворов до изотоничности могут быть использованы хлорид натрия или другие подходящие неорганические соли.
Буфер может представлять собой, например, ацетатный, цитратный, сукцинатный или фосфатный буфер в зависимости от желаемой величины рН. Величина рН одного из видов жидкой препаративной формы по настоящему изобретению находится в диапазоне от около 4 до 8, предпочтительно около физиологической рН.
Консерванты фенол, бензиловый спирт и галогениды бензетония, например хлорид, представляют собой известные антимикробные агенты, которые могут быть использованы.
Терапевтические композиции полипептидов, описанные в данном документе, как правило, помещают в контейнер, имеющий стерильное отверстие, например, упаковку или пузырек для внутривенного раствора, имеющий пробку, поддающуюся прокалыванию иглой для подкожных инъекций. Составы могут быть введены в виде повторных внутривенных (i.v.), подкожных (s.c.) или внутримышечных (i.m.) инъекций или в виде аэрозольных составов, подходящих для интраназальной или внутрилегочной доставки (в отношении внутрилегочной доставки см., например, ЕР 257956). Составы предпочтительно вводят в виде интравитреальной (IVT) или субконъюнктивальной доставки.
Терапевтические полипептиды также могут быть введены в форме составов замедленного высвобождения. К подходящим примерам составов замедленного высвобождения относятся полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие белок, эти матрицы существуют в форме профилированных изделий, например, пленок или микрокапсул. К примерам матриц замедленного высвобождения относятся сложные полиэфиры, гидрогели (например, поли (2-гидроксиэтилметакрилат), описанные в статьях Langer et al., J. Biomed. Mater. Res. 15:167-277 (1981) и Langer, Chem. Tech. 12:98-105 (1982) или поли (виниловый спирт)), полилактиды (патент США 3773919, ЕР 58481), сополимеры L-глутаминовой кислоты и гамма этил-L-глутамата (Sidman et al., Biopolymers 22:547-556 (1983)), неразлагаемый этиленвинилацетат (Langer et al., выше), разлагаемые сополимеры молочная кислота-гликолевая кислота, такие как Lupron Depot® (инъекционные микросферы, составленные из сополимера молочная кислота-гликолевая кислота и лейпролидацетата) и поли-D-(-)-3-гидроксимасляная кислота (ЕР 133988).
В то время как полимеры, такие как этиленвинилацетат и молочная кислота - гликолевая кислота, способны высвобождать молекулы в течение более 100 дней, некоторые гидрогели высвобождают белки в течение более коротких периодов времени. При сохранении инкапсулированных белков в организме в течение длительного времени они могут денатурироваться или агрегироваться в результате воздействия влажности при 37°С, что приводит к потере биологической активности и возможным изменениям иммуногенности. Для стабилизации белков могут быть разработаны разумные стратегии в зависимости от вовлеченного механизма. Например, при обнаружении механизма агрегации с образованием межмолекулярной S-S-связи путем тио-дисульфидного обмена стабилизация может быть получена модификацией сульфгидрильных остатков, лиофилизацией из кислых растворов, контролем содержания влаги, применением подходящих добавок и разработкой композиций специфических полимерных матриц.
К композициям антагониста TSPAN12 или норрина замедленного высвобождения также относятся антагонисты, включенные в липосомы. Такие липосомы получают способами, по существу известными: DE 3218121; Epstein et al., Proc. Natl. Acad. Sci. USA 82:3688-3692 (1985); Hwang et al., Proc. Natl. Acad. Sci. USA 77:4030-4034 (1980); EP 52322; EP 36676; EP 88046; EP 143949; EP 142641; японская патентная заявка 83-118008; патенты США 4485045 и 4544545; и ЕР 102324. Обычно липосомы небольшие (около 200-800 ангстрем), однослойные, содержание в них липидов составляет больше чем около 30% мол. холестерина, выбранная пропорция доводится для оптимального лечения.
Терапевтически эффективная доза антагониста TSPAN12 или норрина будет, конечно, варьировать в зависимости от таких факторов, как патологическое состояние, подвергаемое лечению (включая профилактику), способ введения, тип соединения, используемого для лечения, любая включенная сопутствующая терапия, возраст пациента, вес, общее состояние, анамнез заболевания и т.д. и ее определение хорошо известно лечащему врачу. Соответственно, врачу необходимо определить дозу и модифицировать путь введения, как требуется для получения максимального терапевтического эффекта.
Согласно рекомендациям, указанным выше, эффективная доза, как правило, находится в диапазоне от около 0,001 до около 1,0 мг/кг, более предпочтительно около 0,01-1,0 мг/кг, самое предпочтительное около 0,01-0,1 мг/кг.
Путь введения антагониста TSPAN12 или норрина соответствует известным способам, например, с помощью инъекции или инфузии посредством внутривенного, внутримышечного, внутримозгового, внутрибрюшинного, интрацереброспинального, подкожного, внутриглазного (включая внутрь стекловидного тела), внутрисуставного, интрасиновиального, интратекального, перорального, местного или ингаляторного введений, или с помощью указанных систем замедленного высвобождения.
При использовании в качестве антагониста пептида или малой молекулы его(ее) вводят млекопитающим предпочтительно перорально или путем, отличным от перорального, в виде жидкости или твердого вещества.
К примерам фармакологически приемлемых солей молекул, которые образуют соли и в силу этого могут использоваться, относятся соли щелочных металлов (например, натриевая соль, калиевая соль), соли щелочно-земельных металлов (например, кальциевая соль, магниевая соль), соли аммония, органические основные соли (например, соль пиридиния, триэтиламиновая соль), неорганические кислые соли (например, гидрохлорид, сульфат, нитрат) и соли органической кислоты (например, ацетат, оксалат, пара-толуолсульфонат).
Комбинированные способы лечения
Эффективность антагонистов TSPAN12 или норрина в профилактике или лечении рассматриваемого расстройства может быть повышена за счет введения активного агента периодически или в сочетании с другим агентом, который эффективен для этих целей либо в той же композиции, либо в виде отдельных композиций.
Например, антагонисты TSPAN12 или норрина, используемые для лечения состояний, ассоциированных с ангиогенезом, таких как глазные болезни, могут быть скомбинированы с другими агентами. В частности, желательно применение антагонистов TSPAN12 или норрина в сочетании друг с другом или с другим антиангиогенным агентом. В некоторых вариантах осуществления антагонист TSPAN12 или норрина используют в сочетании с антагонистом VEGF, например, антителом, например, ранибизумабом.
Эффективные количества терапевтических агентов, вводимых в сочетании с антагонистом TSPAN12 или норрина, должны выбираться лечащим врачом или ветеринаром. Введение и подбор дозы осуществляют так, чтобы получить максимальный эффект лечения состояний, подвергаемых лечению. Доза будет дополнительно зависеть от таких факторов, как тип используемого терапевтического агента и конкретный пациент, получающий лечение. Как правило, используемое количество будет представлять собой ту же дозу, которую используют при введении данного терапевтического агента в отсутствие TSPAN12 или норрина.
Антитела против TSPAN12 или норрина
Некоторые из самых перспективных кандидатных лекарственных средств по настоящему изобретению представляют собой антитела и фрагменты антител, которые могут ингибировать продукцию TSPAN12 или норрина и/или снижать активность TSPAN12 или норрина.
Поликлональные антитела
Способы получения поликлональных антител известны специалистам в данной области. Поликлональные антитела могут быть индуцированы в млекопитающем, например, одной или несколькими инъекциями иммунизирующего агента и при желании наполнителя. Как правило, иммунизирующий агент и/или наполнитель должен быть введен в млекопитающего большим числом подкожных или внутрибрюшинных инъекций. Иммунизирующий агент может включать полипептид TSPAN12 или норрина или слитый с ним белок. Может быть полезным конъюгировать иммунизирующий агент с белком, как известно, являющимся иммуногенным в иммунизируемом млекопитающем. К примерам таких иммуногенных белков относятся, но не ограничиваясь ими, гемоцианин лимфы улитки, сывороточный альбумин, бычий тиреоглобулин и соевый ингибитор трипсина. К примерам наполнителей, которые могут быть использованы, относятся полный адъювант Фрейнда и наполнитель MPL-TDM (монофосфорил липид А или синтетический дикориномиколат трегалозы). Протокол иммунизации может быть выбран специалистом в данной области без излишних экспериментов.
Моноклональные антитела
Антитела против TSPAN12 или норрина альтернативно могут представлять собой моноклональные антитела. Моноклональные антитела могут быть получены, используя способы гибридомы, такие как описанные в статье Kohler and Milstein, Nature 256:495 (1975). В способе гибридомы мышь, хомяка или другое подходящее животное-хозяин обычно иммунизируют иммунизирующим агентом для получения лимфоцитов, которые продуцируют или способны продуцировать антитела, которые будут специфически связываться с иммунизирующим агентом. Альтернативно, лимфоциты могут быть иммунизированы in vitro.
Иммунизирующий агент обычно должен включать полипептид TSPAN12 или норрина или слитый с ним белок. Как правило, используют либо лимфоциты периферической крови («PBL»), если желательны клетки человека, либо клетки селезенки или клетки лимфатического узла, если желательны источники из не относящихся к человеку млекопитающих. Лимфоциты затем сливают с иммортализованной линией клеток, используя подходящий агент для слияния, такой как полиэтиленгликоль, для образования клетки гибридомы. Goding, Monoclonal Antibodies: Principles and Practice (New York: Academic Press, 1986), pp. 59-103. Иммортализованные линии клеток обычно представляют собой трансформированные клетки млекопитающих, в частности клетки миеломы, полученные от грызуна, быка и человека. Обычно используют линии клеток миеломы крысы или мыши. Клетки гибридомы могут быть культивированы в подходящей культуральной среде, которая предпочтительно содержит одно или несколько веществ, которые ингибируют рост или жизнеспособность неслившихся иммортализованных клеток. Например, при недостаточности у родительских клеток фермента гипоксантингуанинфосфорибозилтрансферазы (HGPRT или HPRT) культуральная среда для гибридом обычно будет включать гипоксантин, аминоптерин и тимидин («среда НАТ»), эти вещества предотвращают рост HGPRT-дефицитных клеток.
Предпочтительные иммортализованные линии клеток представляют собой такие линии, которые эффективно сливаются, поддерживают устойчивую экспрессию антитела на высоком уровне за счет отобранных антителопродуцирующих клеток и чувствительны к среде, такой как среда НАТ. Более предпочтительные иммортализованные линии клеток представляют собой миеломные линии мыши, которые могут быть получены, например, из Salk Institute Cell Distribution Center, San Diego, California и American Type Culture Collection, Manassas, Virginia. С целью получения моноклональных антител также были описаны линии клеток миеломы человека и гетеромиеломы мыши-человека. Kozbor, J. Immunol. 133:3001 (1984); Brodeur et al., Monoclonal Antibody Production Techniques and Applications (Marcel Dekker, Inc.: New York, 1987) pp. 51-63.
Культуральная среда, в которой культивируют клетки гибридомы, затем может быть исследована на наличие моноклональных антител, направленных против полипептида TSPAN12 или норрина. Предпочтительно, чтобы специфичность связывания моноклональных антител, продуцируемых клетками гибридомы, определяли путем иммунопреципитации или анализом связывания in vitro, таким как радиоиммуноанализ (RIA) или ферментный иммуноабсорбентный анализ (ELISA). Такие техники и анализы известны в данной области. Сродство связывания моноклонального антитела может быть определено, например, анализом Скетчарда Munson and Pollard, Anal. Biochem. 107:220 (1980).
После идентификации желаемых клеток гибридомы клоны могут быть субклонированы процедурами предельных разведений и подращены стандартными способами. Goding, выше. К подходящим культуральным средам для этой цели относятся, например, среда Дульбеско, модифицированная Иглом, и среда RPMI-1640. Альтернативно, клетки гибридомы могут быть подращены in vivo в виде асцитов в млекопитающем.
Моноклональные антитела, секретированные субклонами, могут быть выделены или очищены из культуральной среды или жидкости асцитов с помощью принятых процедур очистки иммуноглобулинов, таких как, например, белок А-сефароза, хроматография на гидроксилапатите, гель-электрофорез, диализ или аффинная хроматография.
Моноклональные антитела также могут быть получены способами рекомбинантных ДНК, такими как описанные в патенте США 4816567. ДНК, кодирующая моноклональные антитела по изобретению, может быть без труда выделена и секвенирована, используя принятые процедуры (например, используя олигонуклеотидные зонды, которые способны специфически связываться с генами, кодирующими тяжелую и легкую цепи антител мыши). Клетки гибридомы по изобретению служат в качестве предпочтительного источника такой ДНК. После выделения ДНК может быть встроена в экспрессирующие векторы, которые затем трансфицируют в клетки-хозяева, такие как клетки обезьян COS, клетки яичника китайского хомячка (СНО) или клетки миеломы, которые без этого не продуцируют белок иммуноглобулина, для синтеза моноклональных антител в рекомбинантных клетках-хозяевах. ДНК также может быть модифицирована, например, путем замещения кодирующей последовательностью константных доменов тяжелой и легкой цепей человека гомологичных последовательностей мыши (патент США 4816567; Morrison et al., выше) или путем ковалентного присоединения к кодирующей последовательности иммуноглобулина всей или части кодирующей последовательности полипептида, отличного от иммуноглобулинового. Такой полипептид, отличный от иммуноглобулинового, может быть замещен на константные домены антитела по изобретению или может быть замещен на вариабельные домены одного антигенсвязывающего сайта антитела по изобретению для создания химерного бивалентного антитела.
Антитела могут представлять собой моновалентные антитела. Способы получения моновалентных антител хорошо известны в данной области. Например, один из способов включает рекомбинантную экспрессию легкой цепи и модифицированной тяжелой цепи иммуноглобулина. Тяжелую цепь усекают, как правило, в какой-либо точке в Fc-регионе, чтобы предотвратить сшивание тяжелых цепей. Альтернативно, для предотвращения сшивания соответствующие цистеиновые остатки замещают другим аминокислотным остатком или удаляют.
Для получения моновалентных антител также подходят in vitro способы. Расщепление антител для получения их фрагментов, в частности Fab-фрагментов, может быть осуществлено, используя принятые техники, известные в данной области.
Антитела человека и гуманизированные антитела
Антитела против TSPAN12 или норрина дополнительно могут содержать гуманизированные антитела или антитела человека. Гуманизированные формы антител, отличных от человеческих (например, мышиных), представляют собой химерные иммуноглобулины, иммуноглобулиновые цепи или их фрагменты (такие как Fv, Fab, Fab', F(ab')2, или другие антигенсвязывающие субпоследовательности антител), которые содержат минимальную последовательность, полученную из иммуноглобулина, отличного от человеческого. К гуманизированным антителам относятся иммуноглобулины человека (реципиентное антитело), в которых остатки CDR реципиента замещаются остатками CDR вида, отличного от человека (донорное антитело), такого как мышь, крыса или кролик, обладающими желаемой специфичностью, аффинностью и активностью. В некоторых случаях каркасные остатки Fv иммуноглобулина человека замещаются соответствующими остатками, отличными от человеческих. Гуманизированные антитела также могут содержать остатки, которые не обнаруживаются ни в реципиентом антителе, ни в импортированных CDR или каркасных последовательностях. В целом, гуманизированное антитело будет содержать по существу все из по меньшей мере одного и обычно два вариабельных домена, в которых все или по существу все CDR-регионы соответствуют CDR-регионам иммуноглобулина, отличного от человеческого, и все или по существу все FR-регионы представляют собой FR-регионы консенсусной последовательности иммуноглобулина человека. Гуманизированное антитело предпочтительно также будет содержать по меньшей мере часть константного региона (Fc) иммуноглобулина, обычно иммуноглобулина человека. Jones et al., Nature 321:522-525 (1986); Riechmann et al., Nature 332:323-329 (1988); Presta, Curr. Op. Struct. Biol. 2:593-596 (1992).
Способы гуманизации антител, отличных от человеческих, хорошо известны в данной области. Как правило, гуманизированное антитело имеет один или несколько аминокислотных остатков, встроенных в него из источника, отличного от человека. Эти аминокислотные остатки, отличные от человеческих, часто обозначают как «импортные» остатки, которые обычно получают из «импортного» вариабельного домена. Гуманизация по существу может быть осуществлена, следуя способу Winter и соавторов (Jones et al., Nature 321:522-525 (1986); Riechmann et al., Nature 332:323-327 (1988); Verhoeyen et al., Science 239:1534-1536 (1988)), посредством замещения CDR-регионов или CDR-последовательностей грызунов соответствующими последовательностями антитела человека. Соответственно, такие «гуманизированные» антитела представляют собой химерные антитела (патент США 4816567), в которых по существу меньше чем один интактный вариабельный домен человека замещен соответствующей последовательностью вида, отличного от человека. На практике гуманизированные антитела обычно представляют собой антитела человека, в которых некоторые остатки CDR и возможно некоторые остатки FR замещены остатками из аналогичных сайтов антител грызунов.
Антитела человека также могут быть получены, используя большое число техник, известных в данной области, включая библиотеки фаговых дисплеев. Hoogenboom and Winter, J. Mol. Biol. 227:381 (1991); Marks et al., J. Mol. Biol. 222:581 (1991). Для получения моноклональных антител человека также доступны техники Cole et al. и Boerner et al. Cole et al., Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, p.77 (1985) и Boerner et al., J. Immunol. 147(1):86-95 (1991). Аналогично, антитела человека могут быть получены введением локусов иммуноглобулина человека в трансгенных животных, например, мышей, у которых эндогенные гены иммуноглобулина были частично или полностью инактивированы. При заражении наблюдается продукция антител человека, которая близко совпадает с наблюдаемой у людей во всех отношениях, включая перестройку генов, сборку и набор антител. Этот подход описан, например, в патентах США 5545807; 5545806; 5569825; 5625126; 5633425 и 5661016 и в следующих научных публикациях: Marks et al, Bio/Technology 10:779-783 (1992); Lonberg et al, Nature 368:856-859 (1994); Morrison, Nature, 368:812-813 (1994); Fishwild et al, Nature Biotechnology 14:845-851 (1996); Neuberger, Nature Biotechnology 14:826 (1996); Lonberg and Huszar, Intern. Rev.
Биспецифические антитела
Биспецифические антитела представляют собой моноклональные, предпочтительно человеческие или гуманизированные антитела, которые обладают специфичностями связывания по меньшей мере для двух различных антигенов. В настоящем случае одна из специфичностей связывания относится к полипептиду TSPAN12 или норрина, другая - к полипептиду или любому другому антигену. К примерам относятся белок или рецептор или субъединица рецептора клеточной поверхности.
Способы создания биспецифических антител известны в данной области. Традиционно рекомбинантное получение биспецифических антител основано на коэкспрессии двух пар тяжелая цепь/легкая цепь иммуноглобулина, где две тяжелых цепи обладают отличными специфичностями. Milstein & Cuello, Nature 305:537-539 (1983). Вследствие случайного набора тяжелых и легких цепей иммуноглобулинов эти гибридомы (квадромы) продуцируют потенциальную смесь десяти различных молекул антител, из которых лишь одна имеет правильную биспецифическую структуру. Очистку правильной молекулы обычно осуществляют с помощью стадий аффинной хроматографии. Подобные процедуры описаны в патенте WO 93/08829, опубликованном 13 мая 1993, и в статье Traunecker et al., EMBO J. 10:3655-3659 (1991).
Вариабельные домены антител с желательными специфичностями связывания (сайты объединения антитело-антиген) могут быть слиты с последовательностями константных доменов иммуноглобулинов. Слияние предпочтительно проводят с константным доменом тяжелой цепи иммуноглобулина, содержащим по меньшей мере часть шарнира, регионы СН2 и СН3. Предпочтительно, чтобы по меньшей мере в одном из слияний присутствовал первый константный регион тяжелой цепи (СН1), содержащий сайт, необходимый для связывания легкой цепи. ДНК, кодирующие слитые тяжелые цепи иммуноглобулина и, если желательно, легкую цепь иммуноглобулина, встраивают в раздельные экспрессирующие векторы и совместно трансфицируют в подходящий организм-хозяин. Более подробно о получении биспецифических антител См., например, статью Suresh et al., Methods in Enzymology 121:210 (1986).
Гетероконъюгированные антитела
Гетероконъюгированные антитела состоят из двух ковалентно соединенных антител. Такие антитела были предложены, например, для нацеливания клеток иммунной системы на нежелательные клетки (патент США 4676980) и для лечения ВИЧ-инфекции. WO 91/00360; WO 92/200373; EP 03089. Полагают, что антитела могут быть получены in vitro, используя известные способы химии синтеза белков, к которым относятся способы, включающие сшивающие агенты. Например, иммунотоксины могут быть созданы, используя реакцию дисульфидного обмена или путем образования тиоэфирной связи. К примерам подходящих реагентов для этой цели относятся иминотиолат и метил-4-меркаптобутиримидат и реагенты, описанные, например, в патенте США 4676980.
Иммунолипосомы
Антитела, описанные в данном документе, также могут находиться в смеси в виде иммунолипосом. Липосомы, содержащие антитело, получают способами, известными в данной области, такими как описанные в статьях Epstein et al., Proc. Natl. Acad. Sci. USA 82:3688 (1985); Hwang et al., Proc. Natl. Acad. Sci. USA 77:4030 (1980) и патентах США 4485045 и 4544545. Липосомы с увеличенным временем циркуляции описаны в патенте США 5013556.
Особенно пригодные липосомы могут быть получены способом обратнофазового выпаривания с липидной композицией, содержащей фосфатидилхолин, холестерин и PEG-дериватизированный фосфатидилэтаноламин (PEG-PE). Липосомы экструдируют через фильтры с определенным размером пор для получения липосом желаемого диаметра. Fab'-фрагменты антитела по настоящему изобретению могут быть конъюгированы с липосомами, как описано в статье Martin et al., J. Biol. Chem. 257:286-288 (1982) посредством реакции дисульфидного обмена. В липосоме необязательно содержится химиотерапевтический агент (такой как доксорубицин). См. статью Gabizon et al., J. National Cancer Inst. 81(19):1484 (1989).
Фармацевтические композиции антител
Антитела, специфически связывающие полипептид TSPAN12 или норрина, идентифицированный в данном документе, а также другие молекулы, идентифицированные скрининговыми анализами, описанными в данном документе, могут быть введены для лечения большого числа расстройств, отмеченных выше и ниже, в виде фармацевтических композиций.
Препаративная форма в данном документе также может содержать более чем одно активное соединение при необходимости для конкретного симптома, подвергаемого лечению, предпочтительно с дополняющими активностями, которые не влияют друг на друга негативно. Альтернативно, или в дополнение, композиция может содержать агент, который усиливает ее функцию. Такие молекулы подходящим образом присутствуют в комбинации в количествах, которые эффективны для намеченной цели.
Активные ингредиенты также могут быть заключены в микрокапсулы, полученные, например, техниками коацервации или пограничной полимеризацией, например, гидроксиметилцеллюлозные или желатиновые микрокапсулы и поли-(метилметацилат) микрокапсулы, соответственно, в коллоидных системах доставки лекарственных средств (например, липосомах, микрочастицах альбумина, микроэмульсиях, наночастицах и нанокапсулах) или в макроэмульсиях. Такие техники описаны в руководстве Remington's Pharmaceutical Sciences, выше.
Препаративные формы, используемые для введения in vivo, должны быть стерильными. Это легко осуществляют путем фильтрации через стерильные фильтрующие мембраны.
Могут быть получены препараты замедленного высвобождения. К подходящим примерам препаратов замедленного высвобождения относятся полупроницаемые матрицы твердых гидрофобных полимеров, содержащие антитело, эти матрицы существуют в форме профилированных изделий, например, пленок или микрокапсул. К примерам матриц с замедленным высвобождением относятся полиэфиры, гидрогели (например, поли (2-гидроксиэтилметакрилат) или поли (виниловый спирт)), полиактиды (патент США 3773919), сополимеры L-глутаминовой кислоты и γ-этил-L-глутамата, неразлагаемый этиленвинилацетат, разлагаемые сополимеры молочная кислота-гликолевая кислота, такие как LUPRON DEPOT® (инъецируемые микрочастицы, составленные из сополимера молочная кислота-гликолевая кислота и лейпролидацетата) и поли-D-(-)-3-гидроксимасляная кислота. Тогда как полимеры, такие как этиленвинилацетат и молочная кислота-гликолевая кислота, способны высвобождать молекулы в течение свыше 100 дней, некоторые гидрогели высвобождают белки в течение более коротких периодов времени. Если инкапсулированные антитела сохраняются в организме в течение длительного времени, они могут денатурировать или агрегироваться в результате воздействия влажности при 37°С, что приводит к потере биологической активности и возможным изменениям иммуногенности. Для стабилизации могут быть разработаны разумные стратегии в зависимости от вовлеченного механизма. Например, при обнаружении механизма агрегации с образованием межмолекулярной S-S-связи путем тио-дисульфидного обмена стабилизация может быть получена модификацией сульфгидрильных остатков, лиофилизацией из кислых растворов, контролем содержания влаги, применением подходящих добавок и разработкой композиций специфических полимерных матриц.
Способы лечения с применением антитела
Полагают, что антитела против TSPAN12 или норрина могут быть использованы для лечения большого числа состояний, ассоциированных с ангиогенезом, отмеченных выше.
Антитела вводят млекопитающему, предпочтительно человеку, в соответствии с известными способами, такими как внутривенное введение в виде болюса или путем непрерывной инфузии в течение периода времени, посредством интравитреального, внутримышечного, внутрибрюшинного, интрацереброспинального, подкожного, внутрисуставного, интрасиновиального, интратекального, перорального, местного или ингаляторного путей. Предпочтительно введение антитела через стекловидное тело.
В одном из вариантов осуществления на патологическую неоваскуляризацию глаза воздействуют комбинированной терапией. Антитело против TSPAN12 и/или норрина и другое антитело (например, против VEGF) вводят пациентам в терапевтически эффективных дозах.
Например, в зависимости от типа и тяжести расстройства исходная кандидатная доза для введения пациенту составляет от около 1 мкг/кг до 50 мг/кг (например, 0,1-20 мг/кг) антитела, либо, например, одним или несколькими раздельными введениями, либо путем непрерывной инфузии. Обычная ежедневная или еженедельная доза может находиться в диапазоне от около 1 мкг/кг до 100 мг/кг или больше в зависимости от факторов, указанных выше. Для повторных введений в течение нескольких дней или дольше в зависимости от состояния лечение повторяют или продолжают до появления желаемой супрессии симптомов расстройства. Тем не менее, могут быть использованы и другие схемы приема. Прогресс этой терапии легко контролируется принятыми техниками и анализами, к которым относится, например, радиографическое изображение опухоли.
Последующие примеры предлагаются лишь с целью иллюстрации и не предназначены ограничить каким-либо образом объем настоящего изобретения.
Описания всех патентных и литературных ссылок, перечисленных в настоящем описании, приводятся, таким образом, в качестве ссылок в полном объеме.
ПРИМЕРЫ
Коммерчески доступные реагенты, обозначенные в примерах, использовались согласно инструкциям производителя, если не указано другого. Все ссылки, перечисленные в данном документе, приводятся, таким образом, в качестве ссылок.
ПРИМЕР 1. TSPAN12 вовлечен в нормальный и патологический ангиогенез
Несмотря на то что регион, кодирующий TSPAN12, известен у нескольких организмов, включая людей и мышей (См., например, GenBank® номера доступа NM_012338 для hTSPAN12 и NM_173007 для mTSPAN12), его функции идентифицированы не были. Чтобы приступить к выяснению его функции, получали мышей с нокаутом (КО) TSPAN12, используя принятые способы. При этом целевую конструкцию электропорировали в ES клетки 129/SvEvBrd (Lex-2) и целевые клоны идентифицировали, используя анализ саузерн-блот. Клетки целевого клона вводили в бластоцисты C57BL/6 (albino). Полученные химеры скрещивали с самками C57BL/6 (albino) для получения мышей, гетерозиготных по мутации, и затем возвратно скрещивали с родителем C57BL/6 (>N3) и использовали для фенотипического анализа и других экспериментов. Мыши TSPAN12-/- оказались жизнеспособными и фертильными.
Авторы получили кроличью поликлональную сыворотку, обозначаемую αTSPAN12-Anaspec-C, против с-концевого внутриклеточного пептида CRREPGTDQMMSLK (SEQ ID NO:5) и очистили ее аффинным способом. Авторы также получили вторую поликлональную сыворотку, обозначаемую α-TSPAN12-Josman-B, против his-меченого фрагмента TSPAN12, соответствующего аминокислотам 116-221 (аа116-221-His6), экспрессированного в бактериях и очищенного. Направленное изменение у мутантных мышей подтверждали саузерн-блотом, ПЦР и вестерн-блотом лизатов голов в Р1, которые обогащали TSPAN12 за счет иммунопреципитации, используя αTSPAN12-Anaspec-C.
Авторы вначале проанализировали экспрессию TSPAN12 в большом числе тканей и обнаружили, что он экспрессировался при развитии сосудистой сети сетчатки в Р15 и в оболочках мозга в Р1. В сосудистой сети, не относящейся к CNS, детектировали незначительную экспрессию либо ее отсутствие. Тем не менее, авторы не наблюдали широкомасштабного морфологического изменения сосудистой сети NFL в тотальных препаратах сетчатки, окрашенных изолектином, мышей TSPAN12 КО, которых обрабатывали согласно опубликованным процедурам (Gerhardt et al., J. Cell. Biol. 161(6):1163-77 (2003)). Соответственно, авторы анализируют мышей, мутантных по TSPAN12, в отношении фенотипов на большом числе моделей глазных болезней.
Детенышей мышей от восьми скрещиваний het x het TSPAN12 (C57BL/6) получали и использовали в модели на мышах ретинопатии недоношенных (ROP). Шесть выводков вместе с их кормящими матерями помещали в атмосферу 75% кислорода (гипероксия) в течение периода пяти дней, начиная с Р7. На Р12 животных возвращали в условия комнатного воздуха (нормоксия) и оставляли в течение последующих пяти дней (Р17). Для генотипирования использовали биопсии хвостов, и 37 животных классифицировали согласно следующему: гомозиготные дикого типа n=8, гетерозиготные n=21, гомозиготные мутантные n=8.
На Р17 правый глаз помещали в 4% PFA и левый глаз помещали в фиксатор Давидсона. Роговицу и хрусталик удаляли из левых глаз для обработки парафином и приготовления срезов. Глазные бокалы помещали в камеру радужной оболочкой вниз, поворачивая поверхностью среза. Получали срезы толщиной 16 микрон и анализировали в отношении неоваскуляризации, используя сканер Aperio ScanScope®, оснащенный специально разработанным алгоритмом подсчета зон неоваскуляризации. Вкратце, в качестве интересующих регионов для алгоритма количественной оценки идентифицировали неоваскулярные пучки, непосредственно ассоциированные со слоем нервных волокон (NFL). Для анализа неоваскуляризации сетчатки количественно оценивали минимум 30 срезов на животное, содержащих зоны неоваскуляризации.
У животных дикого типа, полученных при условиях, заданных для модели ROP, зоны неоваскуляризации идентифицировали на поверхности раздела сетчатка/стекловидное тело (фиг.1). Для сравнения, у гомозиготных мутантных мышей TSPAN12 имелось заметно меньшее количество зон неоваскуляризации (фиг.2). Эти данные указывают на то, что в этой модели ROP TSPAN12 необходим для патологической неоваскуляризации.
После обнаружения этого фенотипа на модели ROP авторы проанализировали развитие сосудистой сети сетчатки в мелком масштабе. В сетчатке мышей поверхностное сосудистое сплетение в NFL формируется из диска зрительного нерва посредством сочетания спраутинга, миграции и ремоделирования между днями жизни Р0-Р10. Затем сосуды прорастают во внешний сетчатый слой (OPL) и во внутренний сетчатый слой (IPL), где формируются два капиллярных русла, образуя трехслойную сосудистую архитектуру. На Р8 авторы обнаружили, что в тотальных препаратах сетчатки мышей TSPAN12-/- развитие сосудистой сети NFL оказалось незначительно измененным. В поперечных срезах авторы обнаружили, что образование капилляров в OPL началось на Р11 у мышей TSPAN12+/+, тогда как у мышей TSPAN12-/- спраутинг полностью отсутствовал. Тот факт, что экспрессия TSPAN12 детектировалась в сосудистой сети, но не в других тканях сетчатки, вместе с обнаружением того, что при окраске гематоксилином и эозином гистология сетчатки оказалась нормальной, указывает на то, что первичен дефект сосудов. У взрослых мышей TSPAN12-/- OPL также не васкуляризовался, подтверждая, что дефект не является временным. Вместо организованного капиллярного русла в IPL у мышей TSPAN12-/- наблюдались несколько расширенные и извитые капилляры в пространстве между NFL и IPL. Толщина внутреннего и наружного ядерных слоев в сетчатках TSPAN12-/- неуклонно снижалась у взрослых, но недоразвитых мышей, указывая на то, что на нервные клетки вторично влияют дефекты васкуляризации.
Вместе с тем, фенотип мышей TSPAN12-/- отличался в основном нормальным развитием поверхностного сосудистого пучка и недостаточностью капилляров в OPL, фенотип, который, по всей видимости, очень похож на фенотипы, описанные для мышей, мутантных по Fzd4, (Xu et al. Cell 116: 883-95 (2004)) и мышей, мутантных по норрину (Luhmann et al. Invest. Ophthalmol. Vis. Sci. 46(9): 3372-82 (2005)). Авторы поэтому протестировали, наблюдались ли у мышей TSPAN12-/- дополнительные отличительные особенности, которые обусловлены разрушением Fzd4 или его лиганда норрина. У мышей, мутантных по норрину, наблюдались очень характерные микроаневризмы, которые на Р15 простирались от NFL к внутреннему ядерному слою. Удивительно, что анализ сетчаток мышей TSPAN12-/- на Р16 посредством конфокальной микроскопии выявил мальформации сосудов, подобные микроаневризмам, которые оказались крайне схожи с дефектами, описанными у мышей, мутантных по норрину. Схожесть этих очень характерных дефектов подтверждалась тем фактом, что как у мышей, мутантных по норрину, так и у мышей TSPAN12-/- дефекты развились в практически одинаковые точки времени. Дополнительное сходство включило нарушенную экспрессию Meca-32 в сосудах сетчатки мышей TSPAN12-/-, маркера фенестрированных сосудов, который в норме не экспрессируется в сосудистом русле сетчатки, но повышается у мышей, мутантных по Fzd4. Поскольку норрин и Fzd4 представляют собой пару лиганд/рецептор, которая наравне с корецептором LRP5 активирует канонический путь Wnt и усиливает аккумуляцию цитоплазматического β-катенина, фенотипическая характеристика мышей TSPAN12-/-, данная авторами, указывает, что TSPAN12 также может быть необходим для передачи сигнала норрин/β-катенин.
ПРИМЕР 2. TSPAN12 ВОВЛЕЧЕН В ПЕРЕДАЧУ СИГНАЛА ЧЕРЕЗ Wnt
На основании сходства между фенотипами, обнаруженными у мышей с КО по TSPAN12, Fzd4 и норрину, авторы осуществили анализы репортерной конструкции Topflash для определения, вовлечен ли TSPAN12 в индуцированную норрином передачу сигнала Wnt на β-катенин через Fzd4. Конструкция Topflash состоит из люциферазы светлячка под контролем промотора, содержащего консенсусные сайты LEF/TCF, которая поэтому отвечает на каноническую передачу сигнала через β-катенин. В качестве внутреннего контроля используется конструкция, экспрессирующая люциферазу кишечнополостного Renilla под контролем конститутивного промотора. Клетки, трансфицированные репортерными конструкциями и рецепторами, активировали с помощью 10 нМ рекомбинантного норрина при наличии экзогенного TSPAN12 или контроля вектора. Спустя 16-18 часов определяли репортерную активность (активность светлячка, деленная на активность Renilla). Опосредованная норрином передача сигнала оказалась приблизительно в 4 раза выше в клетках, сверхэкспрессирующих TSPAN12, чем в контрольных клетках (фиг.3, левая панель - правая панель показывает, что контрольная экспрессия люциферазы Renilla оказалась одинаковой при всех условиях). Авторы осуществили аналогичные эксперименты на клетках, у которых снижали уровень мРНК TSPAN12 дикого типа, используя siРНК (экспрессия оказалась немного ниже одной пятой уровней контроля), и обнаружили, что индуцированная норрином опосредованная Fzd4/LRP5 экспрессия существенно снижалась после нокаута TSPAN12.
Для дополнительного изучения специфичности влияния TSPAN12 авторы осуществили несколько экспериментов, в которых они изменяли конструкции frizzled и/или лиганд. Сначала авторы осуществили эксперименты, используя клетки, трансфицированные тем же вектором, экспрессирующим другие конструкции frizzled (Fzd1, Fzd2, Fzd7, Fzd10), а также Fzd4. Как показано на фиг.4, основное влияние TSPAN12 на каноническую сигнальную трансдукцию Wnt/β-катенин, опосредованную норрином, специфично для Fzd4 с гораздо меньшим влиянием на передачу сигнала, опосредованную Fzd10. Затем авторы проанализировали передачу сигнала в этом анализе, используя Wnt3a в качестве лиганда для индукции передачи сигнала. В данном случае авторы обнаружили, что TSPAN12 не повысил существенно какую-либо передачу сигнала, опосредованную FZD (фиг.5). Авторы обнаружили аналогичные результаты, используя в качестве лиганда Wnt5a.
ПРИМЕР 3. TSPAN12 представляет собой часть Fzd4-рецепторного комплекса
Если TSPAN12 в самом деле действует в процессе инициации передачи сигнала норрин/β-катенин, предполагается, что он колокализовал бы и взаимодействовал с компонентами рецепторного комплекса. Для тестирования этой возможности авторы трансфицировали клетки Hela с помощью flag-Fzd4 (метка расположена внеклеточно) и НА-TSPAN12. Fzd4 в плазматической мембране детектировали с помощью анти-flag-антитела на непроницаемых жизнеспособных клетках на льду, и TSPAN12 детектировали после фиксации и повышения проницаемости. С помощью этой схемы окрашивания обнаружили обильную экспрессию Fzd4 на поверхности клеток Hela. Fzd4 не распределялся гомогенно в плазматической мембране, а вместо этого обнаруживался сконденсированным в многочисленных пористых областях. TSPAN12 колокализовался на большом протяжении с Fzd4-положительными порами и, кроме того, появился во внутриклеточных структурах, которые не окрашивались анти-flag-антителом, поскольку окрашивание анти-flag проходило на клеточной поверхности без повышения проницаемости клеток. Напротив, CD9 и Fzd4 не колокализовались. При замещении Fzd4 на Fzd5 и коэкспрессии с TSPAN12 авторы обнаружили, что TSPAN12 и Fzd5 локализовались, главным образом, раздельно (сегрегация отчасти преодолевалась лишь в редких клетках с повышенной экспрессией обоих белков).
Для изучения взаимодействий норрин-рецептор была использована кондиционированная среда, содержащая N-терминальные слияния норрина и щелочной фосфатазы (АР-норрин), (Xu et al. выше). Авторы трансфицировали клетки HeLa либо Fzd4, LRP5, либо TSPAN12 и проанализировали эти клетки с помощью кондиционированной среды, содержащей flag-АР-норрин. В соответствии с ранее опубликованными сообщениями, авторы обнаружили, что flag-АР-норрин эффективно связывается с клетками, экспрессирующими Fzd4, но не LRP5. Важно, что норрин также не связался с клетками, экспрессирующими один TSPAN12 (фиг.6). Для изучения взаимодействий TSPAN12 с рецепторным комплексом авторы коэкспрессировали Fzd4, LRP5 и TSPAN12 в клетках 293 и использовали Fzd5 в качестве альтернативного Frizzled и CD9 в качестве альтернативного тетраспанина в соответствующих контролях. После инкубации этих клеток с кондиционированной средой, содержащей flag-АР-норрин, на льду (для предотвращения случаев интернализации) и расширенной отмывки белки мембраны, ассоциированные с норрином, слабо сшивали и затем иммунопреципитировали с помощью анти-flag-антитела. Норрин эффективно преципитировал Fzd4, но не Fzd5. Более того, TSPAN12 копреципитировался норрином с Fzd4, но не Fzd5 и не преципитировался при отсутствии Frizzled. Напротив, CD9, хотя и экспрессировался до аналогичного TSPAN12 уровня, не копреципитировал с Fzd4 при участии норрина (фиг.7). Таким образом, TSPAN12 физически ассоциируется с Fzd4-рецепторным комплексом. TSPAN12 также копреципитировался норрином с Fzd4 в отсутствие LRP5 из экстрактов детергента (1% NP-40 + 0,1% N-додецил-бета-D-мальтозид), когда не использовался кросслинкер (данные не представлены). При коэкспрессии TSPAN12 и LRP5 и иммунопреципитации TSPAN12 ассоциации с LRP5 не детектировалось (фиг.8).
Принимая во внимание значительное усиление передачи сигнала норрин/β-катенин посредством TSPAN12, авторы проанализировали, может ли TSPAN12 повышать связывание норрина с Fzd4. С этой целью клетки Hela трансфицировали flag-Fzd4, LRP5, TSPAN12 или контролем вектора и затем проанализировали с помощью нескольких разведений кондиционированной flag-АР-норрином среды. Связывание flag-АР-норрина с клетками было аналогичным при наличии или в отсутствие TSPAN12 при всех протестированных концентрациях норрина (фиг.9). Чтобы исключить вероятность того, что TSPAN12 снижал уровни экспрессии Fzd4, но в то же время повышал связывание норрина, авторы непосредственно определили экспрессию Fzd4 с помощью HRP-связанного антитела, направленного против flag-пептида. Коэкспрессия TSPAN12 не изменила экспрессию Fzd4 на плазматической мембране (фиг.10). Вместе с тем, обнаружение того, что TSPAN12 не коиммунопреципитирует с норрином (кроме случаев наличия Fzd4) (фиг.7) и не усиливает связывание норрина с Fzd4 (фиг.9), указывает на то, что TSPAN12 усиливает передачу сигнала уникальным образом. Это согласуется с функциями некоторых других тетраспанинов, которые обычно не связываются непосредственно с лигандами, но вместе с тем полагают, что они организуют микродомены, которые содействуют передаче сигнала вовлеченных рецепторов. Поэтому авторы далее оценили возможность того, что TSPAN12 содействует взаимодействию между компонентами рецепторного комплекса.
ПРИМЕР 4. Дефекты мономерного норрина C95R нивелируются с помощью TSPAN12
Норрин принадлежит подгруппе белков с цистеиновым узлом, которые образуют димеры посредством межмолекулярных дисульфидных связей (Vitt et al. Mol. Endocrinol. 15(5): 681-94 (2001)), и было предположено, что димеры норрина могут дополнительно собираться в высокомолекулярные структуры (Perez-Vilar et al. J. Biol. Chem. 272(52): 33410-15 (1997)). Норрин в значительной степени ассоциируется внеклеточным матриксом (ЕСМ), если норрин не сливают с АР (Xu et al. выше). Посредством ослабления межмолекулярных дисульфидных связей норрин может быть полностью превращен в мономеры, альтернативно, предполагается, что мутация цистеина в положении 95 уничтожает межмолекулярные дисульфидные связи. Авторы экспрессировали V5-меченый норрин дикого типа и V5-меченый мутантный норрин C95R в клетках 293 и экстрагировали норрин из ЕСМ. С помощью SDS-PAGE при восстанавливающих условиях выявили мономеры норрина дикого типа и мутантного, которые оказались практически неразличимыми. В соответствии с ранее опубликованными сообщениями анализ в невосстанавливающих условиях выявил, что норрин дикого типа образовал димеры и высокомолекулярные группировки. Напротив, мутантный норрин C95R оказался в основном мономерным и не образовывал больших группировок (фиг.11). Небольшая фракция всего норрина C95R образовала димеры, возможно, за счет нековалентной ассоциации или межмолекулярных дисульфидов в положении, отличном от C95.
Авторы предположили, что группировки норрина большие, чем мономеры, обладают способностью переносить большое число молекул Fzd4 ближе друг к другу в мембране и усиливать передачу сигнала норрин/β-катенин, тогда как мономерный норрин-C95R этого не может. Для проверки этого предположения авторы трансфицировали клетки 293 увеличивающимися количествами кДНК норрина дикого типа или норрина C95R вместе с рецепторами для индукции активности Topflash при наличии или в отсутствие TSPAN12. Экспрессия норрина дикого типа эффективно индуцировала передачу сигнала норрин/β-катенин при котрансфекции 5-100 нг плазмиды, кодирующей норрин, с FZD4 и LRP5, и добавление TSPAN12 в значительной степени повысило эту активность (фиг.12). Мономерный мутантный норрин C95R, тем не менее, практически инактивировался в клетках, не сверхэкспрессирующих TSPAN12, даже при самой высокой дозе плазмиды, кодирующей норрин, 100 нг. В соответствии с предположением, что TSPAN12 может переносить рецепторы в микродомены и давать им возможность располагаться близко друг к другу, TSPAN12 в значительной степени восстановил дефект передачи сигнала мутантного норрина C95R. Более того, добавление TSPAN12 повысило передачу сигнала норрина дикого типа (фиг.12). Вместе с тем, эти данные показали, что мультимеры норрина и TSPAN12 предоставляют различные способы переноса большого числа молекул FZD4 близко друг к другу, и оба эти механизма действуют вместе, приводя к максимальной передаче сигнала.
ПРИМЕР 5. TSPAN12 усиливает кластеризацию рецептора
Авторы осуществили биохимический анализ кластеризации рецептора, используя ранее описанную мутацию FZD4-M157V, которая значительно повреждает передачу сигнала норрин/β-катенин, но сохраняет способность связываться с норрином (Xu et al., выше). Изучив сведения о структуре (Dann et al. Nature 412;86-90 (2001)), было предположено, что мутация M157V влияет на индуцированную норрином димеризацию FZD4 и, следовательно, мультимеризацию (Dann et al., выше Toomes et al., выше; Xu et al., выше). В соответствии с ранее опубликованными сообщениями (Xu et al., выше) авторы обнаружили, что передача сигнала, опосредованная FZD4-M157V, существенно нарушалась. Интересно, что коэкспрессия TSPAN12 полностью восстановила дефект передачи сигнала, обусловленный FZD4-M157V (фиг.13А).
Авторы затем использовали FZD4-M157V для непосредственного изучения значения TSPAN12 в мультимеризации FZD4. Клетки 293 трансфицировали TSPAN12 или контрольным вектором и котрансфицировали FLAGTM-FZD4 и gD-FZD4 или FLAG-FZD4-M157V и gD-FZD4-M157V. Клетки инкубировали на льду со средой, содержащей норрин или не содержащей лиганда. Лизаты клеток иммунопреципитировали с анти-FLAG-антителом и анализировали в отношении коиммунопреципитации gD-FZD4. Чтобы количественно оценить белок-белковые взаимодействия, в этом эксперименте не использовали сшивающего реагента. Детектировали схожие исходные уровни ассоциации между gD-FZD4 и FLAG-FZD4 или gD-FZD4-M157V и FLAG-FZD4-M157V (фиг.13В и не представленные данные). И норрин, и TSPAN12 повысили количество gD-FZD4, сниженное за счет FLAG-FZD4, и сочетание норрина и TSPAN12 дополнительно повысило кластеризацию FZD4 (фиг.13В, левые панели; 13С, пустые столбцы). Важно, что мутация M157V существенно повредила способность норрина кластеризовать gD-FZD4 с FLAG-FZD4, тогда как коэкспрессия TSPAN12 компенсировала этот дефект (фиг.13В, правые панели; 13С, закрашенные столбцы). Вместе с тем, эти данные указывают на то, что как TSPAN12, так и норрин усиливают мультимеризацию FZD4 и полагают, что для инициации передачи сигнала норрин/β-катенин необходимы i) факторы, которые усиливают мультимеризацию FZD4 и ii) активация FZD4 за счет связывания лиганда.
Авторы далее проверили, могло ли добавление антител, которые усиливают кластеризацию рецептора FZD4, восстановить активность FZD4-M157V. В 24-луночных планшетах трансфицировали 1,6×105 клеток/лунка смесью ДНК, содержащей репортерную смесь для передачи сигнала через β-катенин (Topflash, pRL-CMV и pCan-myc-lef-1), LRP5 и либо FZD4, либо FZD4-M157V. Через двадцать четыре часа после трансфекции в указанные лунки добавили 1 мкг/мл антитела против LRP5/6. Через один час в указанные лунки добавили 125 нг/мл рекомбинантного норрина. После дополнительной 16-часовой инкубации при 37°С клетки лизировали и экспрессию люциферазы светлячка и Renilla измеряли, используя реагенты Dual-Glo®, продукция фирмы Promega. Величины люциферазы светлячка нормализовали к экспрессии Renilla. Результаты представлены в таблице 1. В клетках, экспрессирующих FZD4, репортерная активность активируется в ~6 раз при наличии норрина. При экспрессии FZD4-M157V активация норрина существенно нарушается до лишь ~2-кратной. Добавление антитела LRP5 частично восстанавливает дефект передачи сигнала в FZD4-M157V приблизительно в 2 раза.
ПРИМЕР 6. Получение антител против TSPAN12 и против норрина
Авторы получают антитела против TSPAN12 и против норрина, используя большое число способов. Например, авторы получают антитела иммунизацией и технологией гибридомы. Авторы также используют синтетические фаговые библиотеки антител, построенные на одной каркасной области (гуманизированное антитело против ErbB2, 4D5) за счет внесения вариабельности в определяющие комплементарность регионы (регионы CDR) тяжелых и легких цепей (Lee, et al. J. Mol. Biol. 340: 1073-93 (2004); Liang et al. J. Biol. Chem. 281: 951-61 (2006)). Пэннинг на планшетах с помощью наивных библиотек осуществляют против His-меченого TSPAN12 человека, иммобилизованного на иммунопланшетах MaxiSorpTM. После четырех раундов обогащения случайным образом отбирают клоны, и специфические связи идентифицируют, используя ELISA фагов. Для идентификации межвидовых клонов полученные клоны, связывающиеся с hTSPAN12, дополнительно скринируют с помощью His-меченого белка TSPAN12 мыши. Для каждого положительного фагового клона субклонируют вариабельные регионы тяжелой и легкой цепей в экспрессирующие векторы pRK, которые создают для экспрессии полноразмерных цепей IgG. Конструкции тяжелой цепи и легкой цепи котрансфицируют в клетки 293 или СНО, и экспрессированные антитела очищают из бессывороточной среды, используя колонку для аффинной хроматографии с белком А. Очищенные антитела тестируют с помощью ELISA в отношении связывания с рекомбинантным TSPAN12 или норрином и с помощью FACS в отношении связывания с устойчивыми линиями клеток, экспрессирующими либо полноразмерный TSPAN12 человека, либо полноразмерный TSPAN12 мыши наряду с FZD4 или экспрессирующими норрин человека или мыши. Антитела затем тестируют посредством TSPAN12 в отношении блокирования усиления репортерной активности Wnt, опосредованной норрином и FZD4/LRP5 (антитела против TSPAN12) или в отношении блокирования передачи сигнала, индуцированной норрином (антитела против норрина). Для созревания аффинности с помощью стратегии частичной рандомизации создают фаговые библиотеки с тремя различными сочетаниями CDR-петель (CDR-L3, -H1 и -H2), полученные из исходного интересующего клона, так чтобы каждая выбранная позиция мутировала к остатку, отличному от дикого типа, или сохранялась в виде дикого типа с частотой около 50:50 (Liang et al., 2006, выше). Высокоаффинные клоны затем идентифицируют посредством четырех раундов пэннинга фазы раствора против His-меченых белков TSPAN12 как человека, так и мыши с постепенно увеличивающейся жесткостью.
ПРИМЕР 7. Модели заболевания глаз на мышах
Авторы тестируют антитела или полипептиды TSPAN12 на моделях мышей. Для мышиной модели ROP детенышей помещают в атмосферу 75% кислорода (гипероксия) в течение периода пяти дней, начиная с Р7. На Р12 животных возвращают в условия комнатного воздуха (нормоксия) и поддерживают в течение последующих пяти дней (Р17). В стекловидное тело животных в возрасте Р12 вводят антитело против TSPAN12, против норрина или большую внеклеточную петлю TSPAN12 (например, Ho et al. выше). Осуществляют большое число уровней и частот введения дозы, основываясь на прогнозах, определяемых аффинностью и стабильностью антагониста. На Р17 правый глаз помещают в 4% PFA и левый глаз помещали в фиксатор Давидсона. Роговицу и хрусталик удаляют из левых глаз для обработки парафином и приготовления срезов. Глазные бокалы помещают в камеру радужной оболочкой вниз, поворачивая поверхностью среза. Получают срезы толщиной 16 микрон и анализируют в отношении неоваскуляризации, используя сканер Aperio ScanScope®, оснащенный специально разработанным алгоритмом подсчета зон неоваскуляризации. В качестве интересующих регионов для алгоритма количественной оценки идентифицируют неоваскулярные пучки, непосредственно ассоциированные с NFL. Для анализа неоваскуляризации сетчатки количественно оценивают минимум 30 срезов на животное, содержащих зоны неоваскуляризации.
Авторы также тестируют антитела и полипептиды на модели хориоидальной неоваскуляризации мышей, индуцированной лазером.
Предполагается, что вышеуказанное описание должно быть достаточным, чтобы дать возможность специалисту в данной области осуществить изобретение. Тем не менее, из вышеуказанного описания специалистам в данной области будет очевидно большое число модификаций по изобретению помимо представленных и описанных в данном документе, и они входят в объем прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ИНГИБИРОВАНИЯ АНГИОГЕНЕЗА С ПОМОЩЬЮ АНТАГОНИСТОВ EGFL8 | 2009 |
|
RU2486200C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ ПУТИ КОМПЛЕМЕНТА ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ | 2006 |
|
RU2417099C2 |
| КОМПОЗИЦИИ И СПОСОБЫ СВЯЗЫВАНИЯ СФИНГОЗИН-1-ФОСФАТА | 2007 |
|
RU2460541C2 |
| АНТАГОНИСТЫ РЕЦЕПТОРА И ЛИГАНДОВ ALK1 И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2559532C2 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ ПУТИ КОМПЛЕМЕНТА ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ | 2010 |
|
RU2583927C2 |
| ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ ГЛАЗ, ВЫЗВАННЫХ КОМПЛЕМЕНТОМ | 2008 |
|
RU2522976C2 |
| НОВЫЕ АНТИТЕЛА | 2008 |
|
RU2490277C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ С ИСПОЛЬЗОВАНИЕМ АНТАГОНИСТОВ АЛЬФА5БЕТА1 | 2007 |
|
RU2465282C2 |
| АНТАГОНИСТЫ ИЛ-6 И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2670943C9 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ ЛИГАНДЫ, И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2699007C2 |




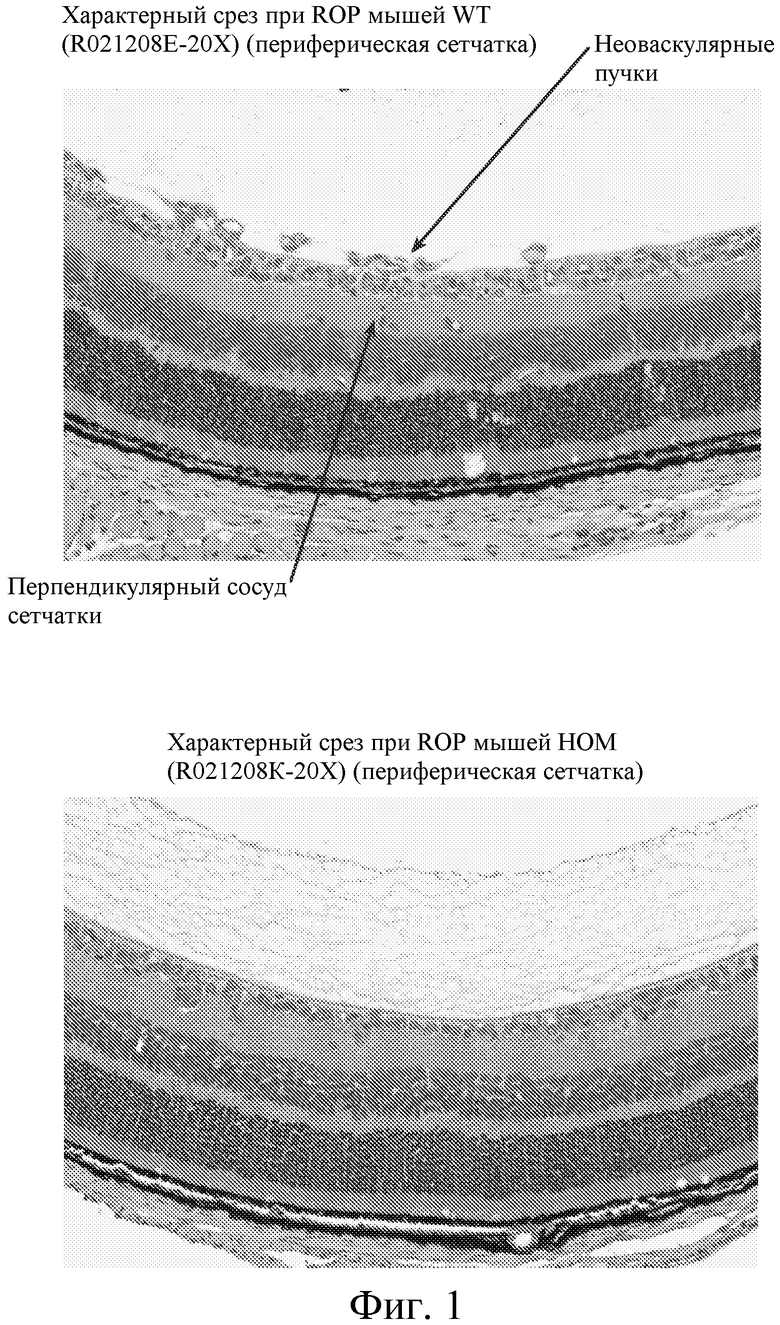
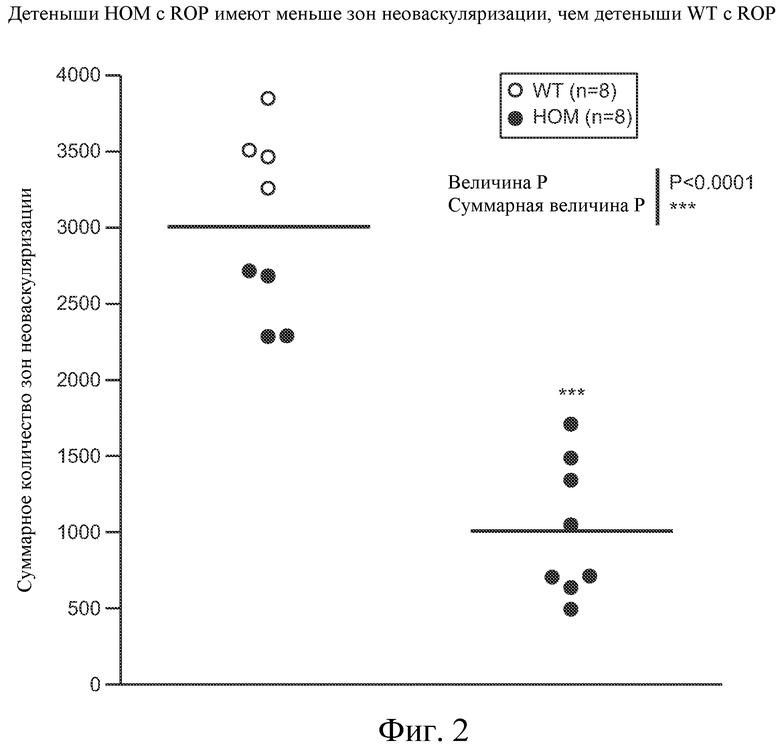
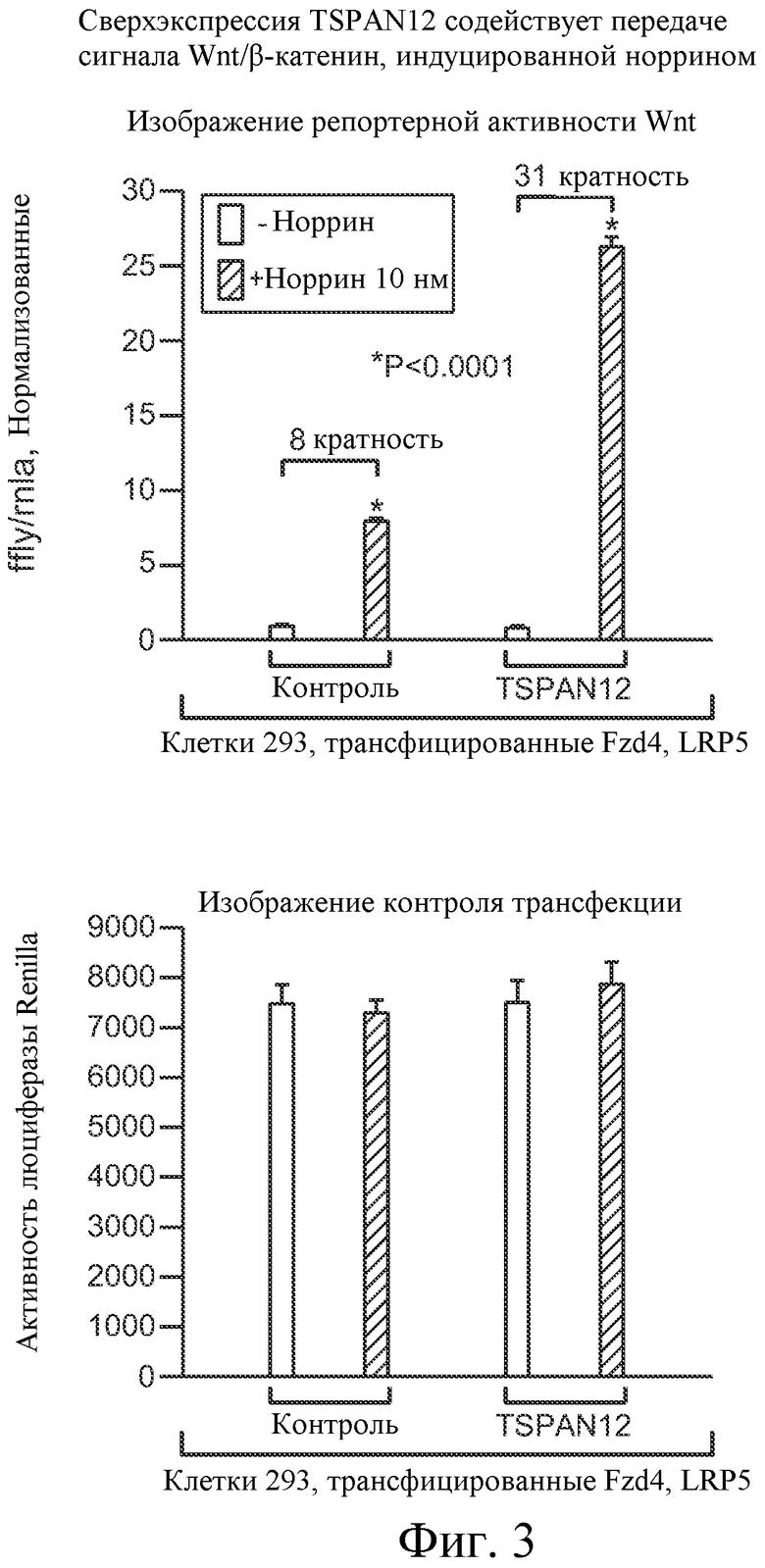
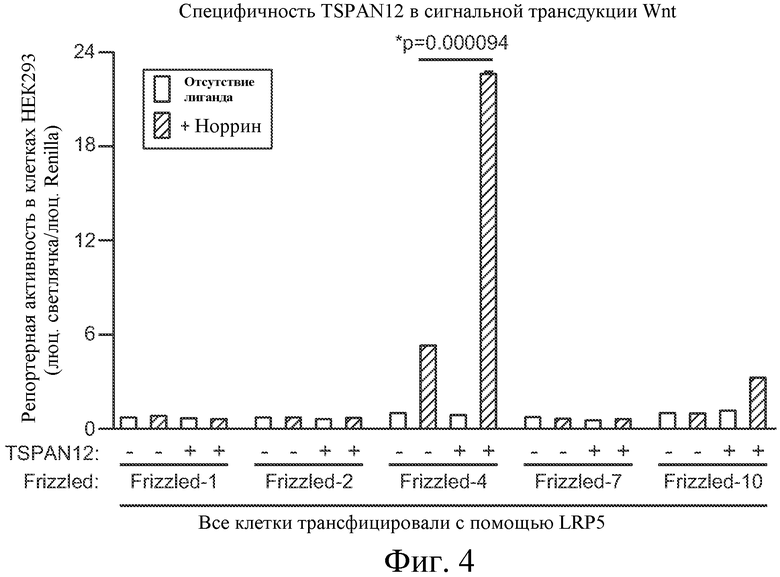
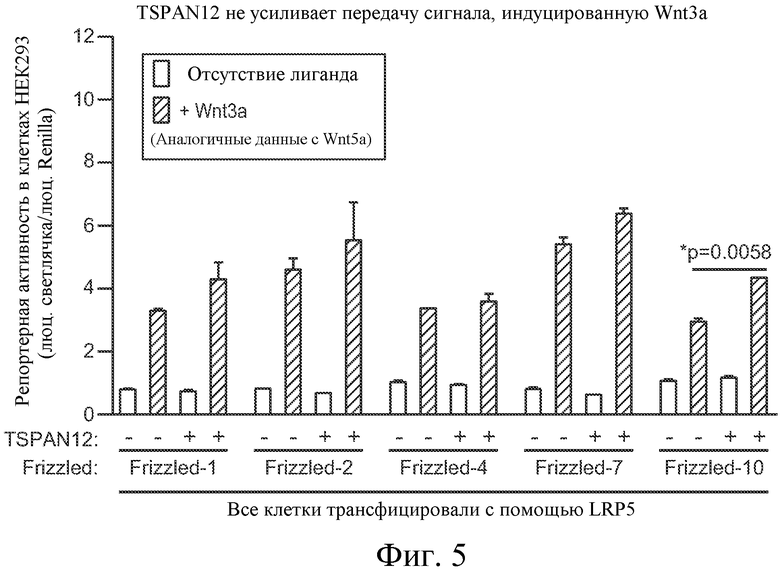
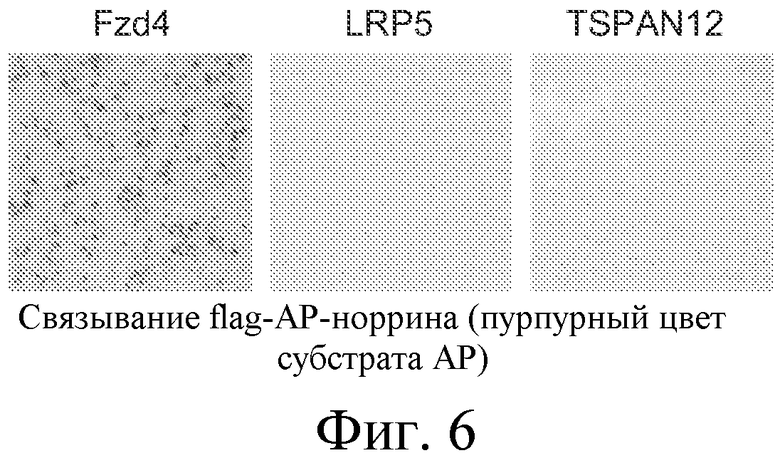
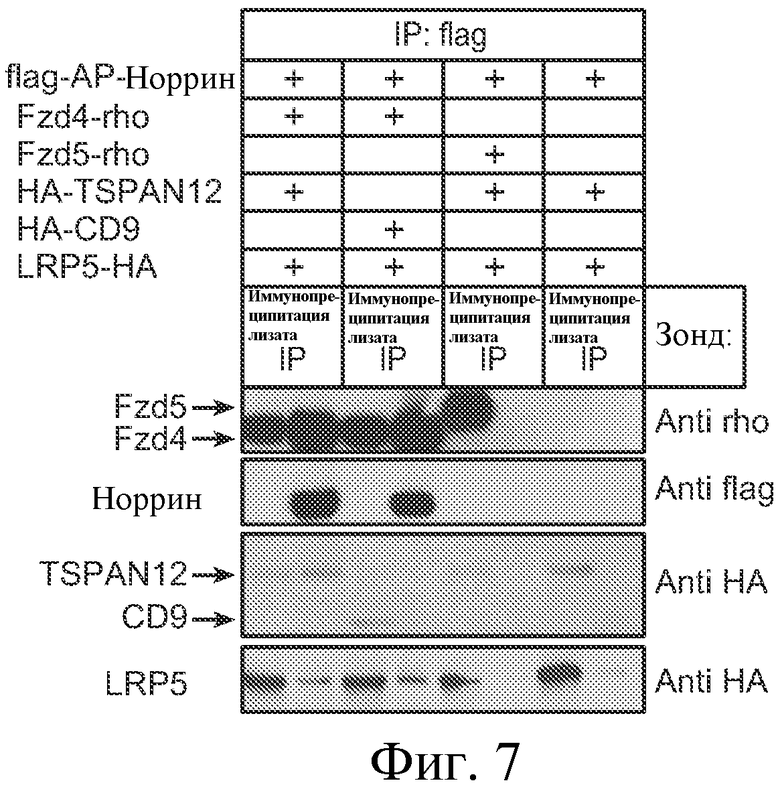
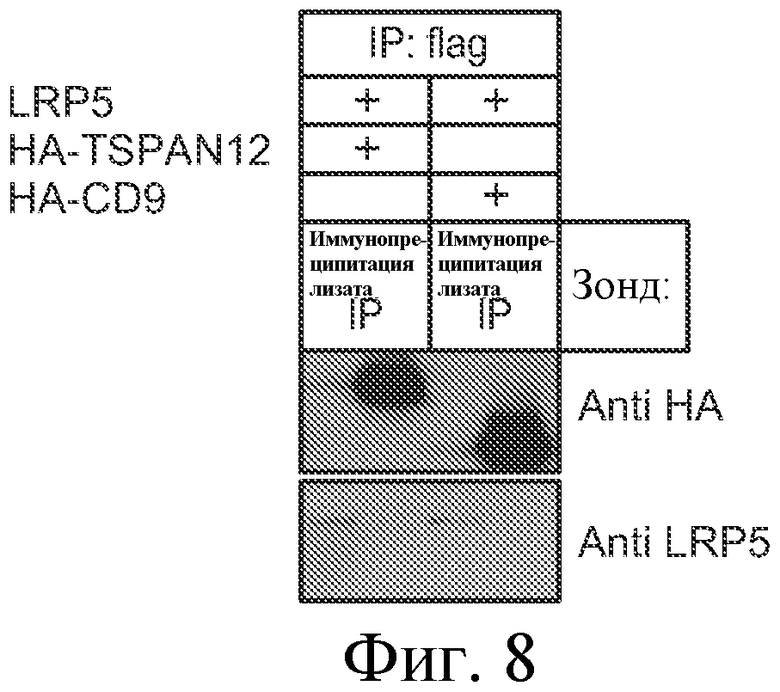
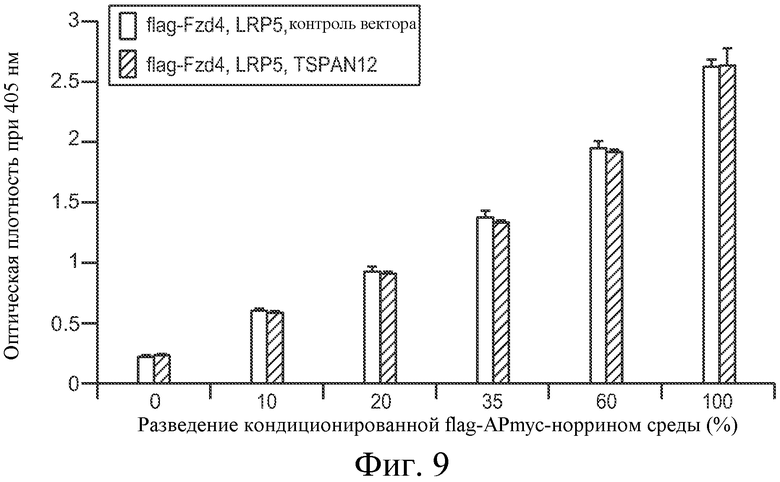

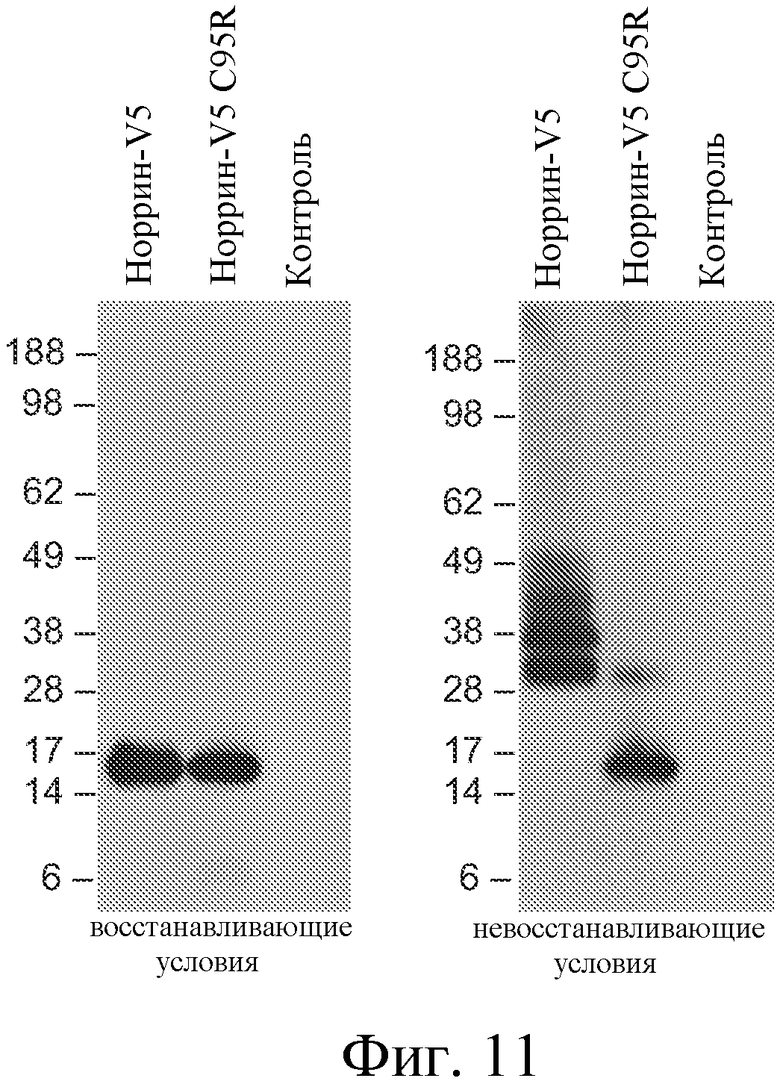
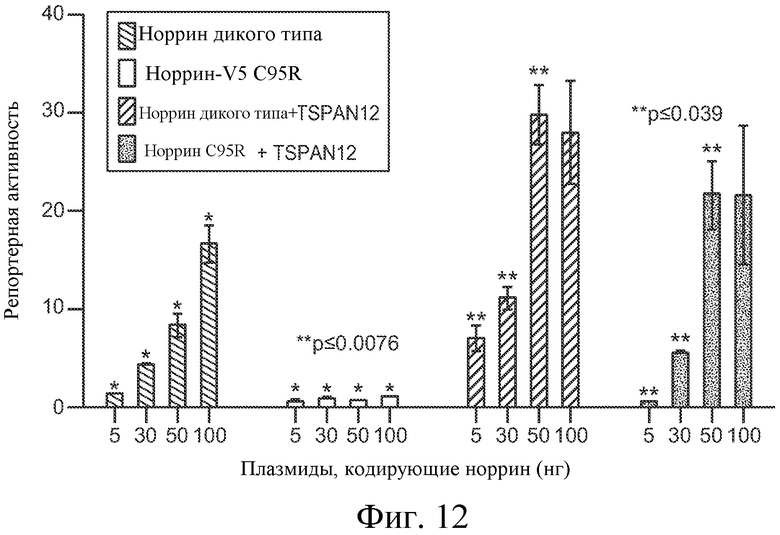
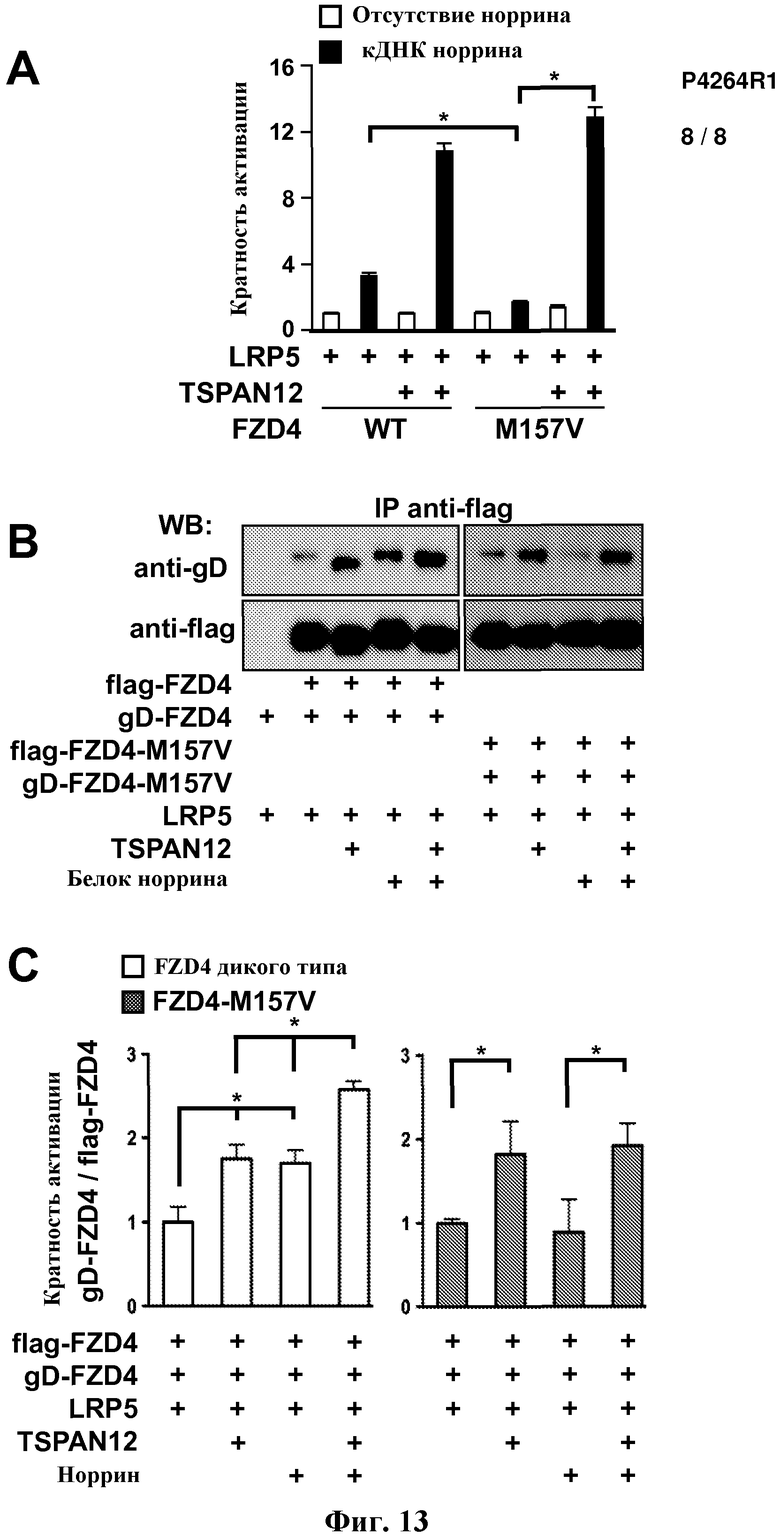
Группа изобретений относится к медицине, а именно к офтальмологии, и может быть использована для снижения или ингибирования ангиогенеза у индивидуума, страдающего заболеванием глаз, или состояния, ассоциированного с ангиогенезом. Для этого индивидууму вводят антагонист TSPAN12. Также предложен способ лечения заболевания или состояния глаз, ассоциированного с нежелательным агиогенезом. Группа изобретений обеспечивает снижение ангиогенеза сосудов наружного плексиформного слоя (OPL), связанного со слоем нервных волокон (NFL) зрительного нерва. 2 н. и 28 з.п. ф-лы, 13 ил., 1 табл., 7 пр.
1. Способ снижения или ингибирования ангиогенеза у индивидуума, страдающего заболеванием глаз или состоянием, ассоциированным с ангиогенезом, предусматривающий введение индивидууму антагониста TSPAN12.
2. Способ по п.1, в котором антагонист TSPAN12 представляет собой антитело против TSPAN12.
3. Способ по п.1, в котором антагонист TSPAN12 содержит фрагмент полипептида TSPAN12.
4. Способ по п.3, в котором фрагмент полипептида TSPAN12 содержит внеклеточный домен TSPAN12.
5. Способ по п.3 или 4, в котором антагонист TSPAN12 дополнительно содержит константный регион иммуноглобулина.
6. Способ по п.5, в котором константный регион иммуноглобулина представляет собой Fc-фрагмент IgG.
7. Способ по п.1, в котором заболевание или состояние глаз выбрано из группы, состоящей из: диабетической ретинопатии, хориоидальной неоваскуляризации (CNV), возрастной дегенерации желтого пятна (AMD), диабетического отека желтого пятна (DME), патологической миопии, болезни фон Хиппеля-Линдау, гистоплазмоза глаз, окклюзии центральной вены сетчатки (CRVO), окклюзии ветвей центральной вены сетчатки (BRVO), неоваскуляризации роговицы, неоваскуляризации сетчатки, ретинопатии недоношенных (ROP), субконъюнктивального кровоизлияния и гипертензивной ретинопатии.
8. Способ по п.7, в котором заболевание или состояние глаз выбрано из группы, состоящей из диабетической ретинопатии, AMD, DME, CRVO и BRVO.
9. Способ по п.1, дополнительно предусматривающий введение индивидууму второго антиангиогенного агента.
10. Способ по п.9, в котором второй антиангиогенный агент вводят до или после введения антагониста TSPAN12.
11. Способ по п.9, в котором второй антиангиогенный агент вводят одновременно с антагонистом TSPAN12.
12. Способ по п.9, в котором второй антиангиогенный агент представляет собой антагонист норрина или фактора роста эндотелиальных клеток сосудов (VEGF).
13. Способ по п.12, в котором антагонист норрина представляет собой антитело против норрина.
14. Способ по п.12, в котором антагонист VEGF представляет собой антитело против VEGF.
15. Способ по п.14, в котором антитело против VEGF представляет собой ранибизумаб.
16. Способ лечения заболевания или состояния глаз, ассоциированного с нежелательным ангиогенезом, у индивидуума, предусматривающий введение индивидууму антагониста TSPAN12.
17. Способ по п.16, в котором антагонист TSPAN12 представляет собой антитело против TSPAN12.
18. Способ по п.16, в котором антагонист TSPAN12 содержит полипептидный фрагмент TSPAN12.
19. Способ по п.17, в котором фрагмент полипептида TSPAN12 содержит внеклеточный домен TSPAN12.
20. Способ по п.18 или 19, в котором антагонист TSPAN12 дополнительно содержит константный регион иммуноглобулина.
21. Способ по п.20, в котором константный регион иммуноглобулина представляет собой Fc-фрагмент IgG.
22. Способ по п.16, в котором заболевание или состояние глаз выбрано из группы, состоящей из: пролиферативных ретинопатий, включая пролиферативную диабетическую ретинопатию, CNV, AMD, диабетической и других ишемических ретинопатий, DME, патологической миопии, болезни фон Хиппеля-Линдау, гистоплазмоза глаз, CRVO, BRVO, неоваскуляризации роговицы, неоваскуляризации сетчатки, ROP, субконъюнктивального кровоизлияния и гипертензивной ретинопатии.
23. Способ по п.22, в котором заболевание или состояние глаз выбирают из группы, состоящей из диабетической ретинопатии, AMD, DME, CRVO и BRVO.
24. Способ по п.16, дополнительно содержащий введение индивидууму второго антиангиогенного агента.
25. Способ по п.24, в котором второй антиангиогенный агент вводят до или после введения антагониста TSPAN12.
26. Способ по п.24, в котором второй антиангиогенный агент вводят одновременно с антагонистом TSPAN12.
27. Способ по п.24, в котором второй антиангиогенный агент представляет собой антагонист норрина или VEGF.
28. Способ по п.27, в котором антагонист норрина представляет собой антитело против норрина.
29. Способ по п.27, в котором антагонист VEGF представляет собой антитело против VEGF.
30. Способ по п.29, в котором антитело против VEGF представляет собой ранибизумаб.
| WO 2008019144 A2, 14.02.2008 | |||
| RU 2004127577 A, 27.05.2005 | |||
| WO2006132788 A2, 14.09.2006 | |||
| MARTIN E.HEMLER Targeting of tetraspanin proteins- potential benefits and strategies // Nature Reviews/ Drug Discovery | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ULRICH F.O | |||
| LUHMANN et al | |||
| Role of the Norrie Disease Pseudoglioma Gene in Sprouting Angiogenesis during | |||
Авторы
Даты
2014-10-10—Публикация
2009-09-10—Подача