Уровень техники изобретения
[0001] Многие воспалительные заболевания кожи часто приводят к некрасивым и болезненным высыпаниям, угрям, постоянно красным венам и угреподобным кожным сыпям, таким как пятна, узелки и пустулы, которые могут мокнуть или покрываться коркой. Например, розацеа обычно поражает щеки, нос, подбородок и лоб, и типичный возраст появления соответствует 30-60 годам. См., например, Zuber T. J., Rosacea: Beyond First Blush 32 H OSP. P RACT. 188-189 (1997); THE MERCK MANUAL 813-814 (Keryn A. G. Lane et al. eds. 17th ed. 2001). Многие люди с розацеа неверно полагают, что страдают угрями взрослых, от солнца, или обветренности, или нормальных эффектов старения. Симптомы розацеа включают частое покраснение и частое раздражение кожи лица, и эритему возрастающей тяжести (аномальное покраснение кожи), и телеангиэктазию (видимые красные линии из-за аномального расширения капиллярных сосудов и мелких артерий). Могут появляться прыщеобразные высыпания, которые могут быть плотными (под названием папулы или узелки) или заполненными гноем (так называемые пустулы). Такие сыпи часто выглядят как угри, но белоголовые угри или черноголовые угри (открытые и закрытые угри, соответственно) обычно не присутствуют. Более тяжелые симптомы розацеа включают симптомы, характеризующиеся ринофимой (утолщенным, мелкодольчатым разрастанием сальных желез и эпителиальной соединительной ткани носа). Если не лечить, розацеа может прогрессировать до неизгладимого обезображивания лица. Симптомы розацеа часто усиливаются под действием солнца, изменений или экстремальных значений температуры, ветра и при употреблении некоторых продуктов питания, таких как острая пища, кофеин и алкоголь.
[0002] Не существует никакого известного метода лечения многих воспалительных заболеваний кожи, включая воспалительные дерматологические заболевания лица, такие как розацеа. Современные терапии, направленные на контроль покраснения, воспаления и кожных сыпей, обладают ограниченной эффективностью для многих пациентов и обычно могут использоваться в течение ограниченного срока. Стандартные терапии включают избегание триггерных факторов, таких как воздействие солнца, воздействие ветра, употребление алкоголя, острой пищи и раздражающих очищающих средств для лица, лосьонов и косметики. Антибиотики являются традиционной первой линией терапии. Длительное лечение (от 5 до 8 недель или более) пероральными антибиотиками, такими как тетрациклин, миноциклин, доксициклин или кларитромицин, позволяет контролировать кожные сыпи. Альтернативные пероральные терапии включают лекарственные препараты с витамином A, такие как изоретиноин, и противогрибковые лекарственные препараты. К сожалению, такие пероральные лекарственные препараты часто вызывают побочные эффекты и для многих людей обладают ограниченной переносимостью. Местные терапии, такие как местное нанесение метронидазола, изоретиноина, стероидов, азелаиновой кислоты, ретиноевой кислоты или ретинальдегида, или препаратов с витамином C, могут быть использованы, но имеют ограниченную эффективность и не могут лечить все симптомы. Например, изоретиноин имеет серьезные тератогенные побочные эффекты, и пациентки детородного возраста должны использовать эффективные противозачаточные меры либо избегать терапии. Хирургия, такая как лазерное удаление кровеносных сосудов, как правило, является крайней мерой и может быть предписана, если другое лечение неэффективно. У пациентов с гиперплазией носа хирургическое восстановление может улучшить косметическую внешность пациента, но не лечит само заболевание. Терапия пульсирующего смешанного света (фотодермальная) оказалась до некоторой степени эффективной в отношении симптомов, связанных с определенными воспалительными заболеваниями кожи, такими как розацеа, для некоторых пациентов.
[0003] Агонисты α2-адренорецепторов нашли терапевтическое применение для ряда состояний, включая такие состояния, как гипертензия, застойная сердечная недостаточность, стенокардия, спастичность, глаукома, диарея, и для ослабления симптомов отмены опиатов (J. P. Heible and R. R. Ruffolo Therapeutic Applications of Agents Interacting with α-Adrenoceptors, pp.180-206 in Progress in Basic and Clinical Pharmacology Vol.8, P. Lomax and E. S. Vesell Ed., Karger, 1991). Агонисты адренорецепторов, такие как клонидин, первоначально использовались перорально, хотя известна лекарственная форма в виде пластыря.
[0004] Системные побочные эффекты связаны с применением агонистов α2-адренорецепторов. Побочные эффекты включают, например, такие как кардиопульмональные эффекты β-блокаторов типа тимолола; сухость во рту, прилив, лихорадка, тахикардия, задержка мочи, судорога и возбудимость под влиянием атропина; гипертензия под влиянием фенилэфрина; повышенное слюноотделение, тошнота, рвота, диарея, желудочные колики, бронхиальная секреция, бронхоконстрикция, астма, брадикардия, парестезия под влиянием миотиков; гипотензия под влиянием клонидина; и ксеростомия, утомляемость и сонливость под влиянием апраклонидина и бримонидина. См. патент Канады № CA2326690.
[0005] Опубликованная патентная заявка США US20050276830 описывает агонисты α2-адренергических рецепторов и применение указанных агонистов для лечения или предупреждения воспалительных заболеваний кожи.
[0006] Нестероидные противовоспалительные средства (НПВС) используются для уменьшения воспаления и в качестве анальгетиков. Однако НПВС связаны с широким спектром нежелательных побочных эффектов. Например, использование НПВС может вызывать прямое и косвенное раздражение желудочно-кишечного тракта (ЖКТ), приводящее ко многим нежелательным лекарственным реакциям (НЛР), таким как тошнота, диспепсия, желудочное изъязвление/кровотечение и диарея. Риск изъязвления возрастает с длительностью приема и увеличением доз НПВС. НПВС также связаны с относительно высокой частотой возникновения почечных НЛР, таких как задержка солей и жидкости и гипертензия, и, в редких случаях, более тяжелых почечных заболеваний, таких как интерстициальный нефрит, нефротический синдром, острая почечная недостаточность и острый тубулярный некроз. Мета-анализ исследований, сопоставляющих НПВС, показал, что, за исключением напроксена, как селективный ингибитор Cox-2, так и традиционные НПВС связаны с повышением риска сердечно-сосудистых заболеваний (Kearney et al., BMJ 332: 1302-1308 (2006)).
[0007] Следовательно, остается потребность в новых способах и композициях, улучшающих состояние при воспалительных заболеваниях кожи, таких как розацеа и соответствующих симптомах, без побочного эффекта или при очень незначительных побочных эффектах. Такие способы и композиции описаны в настоящей заявке.
Краткое описание изобретения
[0008] В настоящее время установлено, что комбинация агониста α2-адренергических рецепторов и нестероидного противовоспалительного средства приводит к существенному усовершенствованию в лечении воспалительных заболеваний кожи, без побочного эффекта или при незначительных побочных эффектах.
[0009] Согласно одному из основных аспектов, варианты осуществления настоящего изобретения касаются способа лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, у субъекта. Способ включает местное нанесение на участок кожи субъекта композиции для местного применения, включающей терапевтически эффективное количество агониста α2-адренергических рецепторов, терапевтически эффективное количество нестероидного противовоспалительного средства и фармацевтически приемлемый носитель, где участок кожи подвержен или может быть поражен воспалительным заболеванием кожи или проявляется симптом, связанный с указанным заболеванием.
[0010] Согласно другому основному аспекту, варианты осуществления настоящего изобретения касаются местного введения композиции для лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, у субъекта. Композиция включает терапевтически эффективное количество агониста α2-адренергических рецепторов, терапевтически эффективное количество нестероидного противовоспалительного средства и фармацевтически приемлемый носитель.
[0011] Согласно еще одному основному аспекту, варианты осуществления настоящего изобретения касаются набора для лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, у субъекта. Набор включает:
(1) первую местно вводимую композицию, включающую терапевтически эффективное количество агониста α2-адренергических рецепторов и фармацевтически приемлемый носитель;
(2) вторую местно вводимую композицию, включающую терапевтически эффективное количество нестероидного противовоспалительного средства и фармацевтически приемлемый носитель; и
(3) инструкции по местному нанесению первой местно вводимой композиции и второй местно вводимой композиции на участок кожи субъекта, где участок кожи подвержен или может быть поражен воспалительным заболеванием кожи или проявляются признаки и/или симптомы, связанные с указанным заболеванием.
Другие аспекты, особенности и преимущества изобретения будут очевидны из следующего раскрытия сущности, включающего подробное описание изобретения и предпочтительные варианты осуществления и приложенную формулу изобретения.
Краткое описание чертежей
[0012] Предшествующее краткое описание, равно как следующее подробное описание изобретения, будет лучше понято при рассмотрении вместе с приложенными чертежами. С целью иллюстрации изобретения, варианты осуществления изобретения представлены диаграммами. Следует понимать, однако, что изобретение не ограничивается приведенными точными схемами и техническими средствами.
[0013] На чертежах:
[0014] фиг.1 иллюстрирует влияние бримонидина и диклофенака, как таковых или в комбинации, на снижение вызванного TPA отека уха у мышей: толщину уха измеряют через 6 часов после местного нанесения соединений на ухо; ось y представляет среднюю толщину уха, измеренную для каждой группы из 5 мышей, и ось x представляет концентрацию соединений; и
[0015] фиг.2 иллюстрирует влияние бримонидина и диклофенака, как таковых или в комбинации, на снижение вызванного арахидоновой кислотой отека уха у мышей: толщину уха измеряют через 1 час после местного нанесения соединений на ухо; ось y представляет среднюю толщину уха, измеренную для каждой группы из 5 мышей, и ось x представляет концентрацию соединений.
Подробное описание изобретения
[0016] Различные публикации, статьи и патенты цитируются или упоминаются в обосновании и во всем описании; каждый такой противопоставленный материал полностью включен здесь в качестве ссылки. Рассмотрение документов, актов, материалов, устройств, статей и т.п. включено в настоящее описание с целью определения контекста данного изобретения. Такое рассмотрение не является признанием того, что часть либо все упомянутые материалы входят в состав известного уровня техники в отношении любых изобретений, раскрытых или заявленных.
[0017] Если не указано иное, все технические и научные термины, используемые здесь, имеют то же значение, в каком обычно понимаются средним специалистом в области техники, к которой относится данное изобретение. В противоположном случае, отдельные используемые здесь термины имеют значения, указанные в описании. Все цитируемые патенты, опубликованные патентные заявки и публикации полностью включены здесь в качестве ссылок. Следует отметить, что, как использовано здесь и в приложенной формуле изобретения, формы единственного числа включают ссылку на форму множественного числа, если контекст явно не диктует иное.
[0018] Термины "воспалительное заболевание кожи или признак и/или симптом, связанный с указанным заболеванием" и "воспалительное дерматологическое заболевание" означают любое заболевание или патологическое состояние, связанное с кожей, ногтями или мембранами слизистой оболочки, с проявлением таких признаков и/или симптомов, как покраснение, прилив, жжение, шелушение, угри (прыщи, папулы, пустулы (в особенности, при отсутствии белоголовых угрей или черноголовых угрей)), телеангиэктазия, открытые поражения кожи, поверхностное раздражение или боль, зуд и/или воспаление. Степень или тяжесть заболевания или патологического состояния может изменяться. Характерные примеры воспалительных заболеваний кожи или признаков и/или симптомов, связанных с указанным заболеванием, включают, но не в порядке ограничения, дерматит, такой как контактный дерматит, атопический дерматит, себорейный дерматит, нуммулярный дерматит, генерализованный эксфолиативный дерматит, статис дерматит, простой хронический лишай; поражения волосяных фолликулов и сальных желез, такие как угри, розацеа и ринофима, периоральный дерматит и псевдофолликулит волос бороды; и воспалительные реакции, такие как лекарственная сыпь, полиморфная эритема, нодозная эритема и анулярная гранулема. В предпочтительном варианте осуществления лекарственные составы для местного применения по изобретению используют для лечения или предупреждения воспалительных дерматологических заболеваний лица, таких как розацеа.
[0019] Существует четыре подтипа розацеа: подтип I: эритематознотелеангиэктатическая розацеа (ETR): подтип II: папулопустулезная розацеа (PPR); подтип III: фиматозная розацеа (PR) и подтип IV: окулярная розацеа. Каждый подтип затем подразделяют на классы по степени тяжести заболевания. См. Wilkin J. et al., 2004, J Am Acad Dermatol. 2004 Jun; 50(6):907-12 и Wilkin J. et al., 2002, J Am Acad Dermatol. 2002 Apr; 46(4):584-7). Такая классификация и система градации, основанная на клиническом диагнозе, способствует уяснению различных компонентов розацеа и помогает клиницистам в выборе терапии. Но неизвестно, представляют ли различные подтипы розацеа различные последовательные стадии развития заболевания или представляют различные болезни. Подразумевается, что термин "воспалительное заболевание кожи или признак и/или симптом, связанный с указанным заболеванием" охватывает все четыре подтипа розацеа.
[0020] Термин "агонист α2-адренергических рецепторов" или "агонист α2-адренорецептора" означает соединение, которое связывает и селективно стимулирует подкласс α2 альфа-адренергических рецепторов. Такие соединения могут обладать мощными эффектами вазоконстрикции при введении в организм млекопитающих, в особенности людей.
[0021] Термин "нестероидное противовоспалительное средство" или "НПВС" означает нестероидное противовоспалительное соединение, которое ингибирует продуцирование простагландинов (PG), действующих (помимо всего прочего) как молекулы мессенджера в процессе воспаления. Большинство НПВС действуют как неселективные ингибиторы фермента циклооксигеназы (COX), включая COX-1, COX-2 и, возможно, другие изоферменты COX. COX катализирует образование PG и тромбоксана, прежде всего, из арахидоновой кислоты.
[0022] Термин "алкил" означает насыщенную, одновалентную, неразветвленную или разветвленную углеводородную цепь. Примеры алкильных групп включают, но не в порядке ограничения, (C1-C3)-алкильные группы, такие как метил, этил, пропил, изопропил, и (C4-C8)-алкильные группы, такие как 2-метил-1-пропил, 2-метил-2-пропил, 2-метил-1-бутил, 3-метил-1-бутил, 2-метил-3-бутил, 2,2-диметил-1-пропил, 2-метилпентил, 3-метил-1-пентил, 4-метил-1-пентил, 2-метил-2-пентил, 3-метил-2-пентил, 4-метил-2-пентил, 2,2-диметил-1-бутил, 3,3-диметил-1-бутил, 2-этил-1-бутил, бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, гексил, гептил, октил и тому подобное. Алкильная группа может быть незамещенной или замещенной одним или несколькими подходящими заместителями.
[0023] Термин "алкокси" означает кислородсодержащий простой эфирный радикал алкила. Примеры алкокси включают, но не в порядке ограничения, метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси и тому подобное. Алкоксигруппа может быть незамещенной или замещенной одним или несколькими подходящими заместителями.
[0024] Когда отдельная группа является "замещенной" (например, алкил, алкокси), такая группа может содержать один или несколько заместителей, предпочтительно, от одного до пяти заместителей, более предпочтительно, от одного до трех заместителей, наиболее предпочтительно, от одного до двух заместителей, независимо выбираемых из перечня заместителей.
[0025] В отношении заместителей, термин "независимо" означает, что когда возможно несколько таких заместителей, указанные заместители могут быть одинаковыми или отличными друг от друга.
[0026] Термин "галоген" означает фтор, хлор, бром или йод.
[0100] В данном контексте предполагается, что название соединения охватывает все возможные существующие изомерные формы (например, оптический изомер, энантиомер, диастереомер, рацемат или рацемическую смесь), сложные эфиры, пролекарства, метаболитные формы или фармацевтически приемлемые соли соединения. Например, "бримонидин" может означать соединение (5-бромхиноксалин-6-ил)-(4,5-дигидро-1H-имидазол-2-ил)амин и любую фармацевтически приемлемую соль соединения, такую как тартрат бримонидина; "диклофенак" может означать соединение 2-[2-(2,6-дихлорфениламино)фенил]уксусную кислоту и любую фармацевтически приемлемую соль соединения, такую как натриевая или калиевая соль диклофенака.
[0027] Фраза "фармацевтически приемлемая соль (соли)", как использована здесь, означает те соли рассматриваемого соединения, которые являются безопасными и эффективными для местного применения млекопитающими и которые обладают требуемой биологической активностью. Фармацевтически приемлемые соли включают соли кислотных или основных групп, присутствующих в указанных соединениях. Фармацевтически приемлемые кислотно-аддитивные соли включают, но не в порядке ограничения, такие соли, как гидрохлорид, гидробромид, гидройодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, изоникотинат, ацетат, лактат, салицилат, цитрат, тартрат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкаронат, сахарат, формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат и памоат (т.е. 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)). Некоторые соединения, используемые в данном изобретении, могут образовывать фармацевтически приемлемые соли с различными аминокислотами. Подходящие основные соли включают, но не в порядке ограничения, соли алюминия, кальция, лития, магния, калия, натрия, цинка и диэтаноламина. В отношении обзора по фармацевтически приемлемым солям см. BERGE ET AL., 66 J. PHARM. SCI. 1-19 (1977), включенный здесь в качестве ссылки.
[0028] Термин "гидрат" означает рассматриваемое соединение или фармацевтически приемлемую соль такого соединения, дополнительно включающее (включающую) стехиометрическое или нестехиометрическое количество воды, связанной нековалентными межмолекулярными силами.
[0029] Термин "местно вводимая композиция", "композиция для местного применения" или "состав для местного применения", как использован здесь, означает любой состав или композицию, фармацевтически и/или косметически приемлемый (приемлемую) для местной доставки указанных соединений по изобретению. Характерные формы составов, которые могут быть использованы для местного введения, включают, но не в порядке ограничения, спреи, туман-аэрозоли, аэрозоли, растворы, лосьоны, гели, кремы, притирания, пасты, мази, эмульсии и суспензии. Выбор местно вводимой композиции зависит от ряда факторов, включающих характер излечиваемых или предупреждаемых симптомов, физико-химические характеристики конкретного вводимого соединения и других присутствующих наполнителей, стабильность указанных соединений в составе, имеющееся производственное оборудование и ограничения по стоимости.
[0030] Подразумевается, что термин "композиция" охватывает продукт, включающий указанные ингредиенты в указанных количествах, равно как любой продукт, образующийся, прямо или косвенно, из комбинаций указанных ингредиентов в указанных количествах.
[0031] "Карбомер" согласно фармакопее США обозначает различные полимерные кислоты, диспергируемые, но не растворимые, в воде. Когда кислотную дисперсию нейтрализуют основанием, образуется прозрачный, устойчивый гель. Карбомер 934P физиологически инертен и не является первичным раздражителем или сенсибилизатором. Другие карбомеры включают 910, 940, 941 и 1342.
[0032] Термин "субъект" означает любое животное, преимущественно млекопитающее, наиболее предпочтительно, человека, которому будут вводиться, или были введены, соединения или составы для наружного применения согласно вариантам осуществления изобретения. Термин "млекопитающее", как использован здесь, включает любое млекопитающее. Примеры млекопитающих включают, но не в порядке ограничения, таких млекопитающих, как коровы, лошади, овцы, свиньи, кошки, собаки, мыши, крысы, кролики, морские свинки, обезьяны, люди и т.д., более предпочтителен человек. Предпочтительно, субъект нуждается в лечении или профилактике воспалительного заболевания кожи и связанных с ним симптомов, либо является объектом наблюдения или эксперимента.
[0033] Термин "инструкции", когда используется в контексте набора, включает сборник информации, протокол, схему или средство выражения, которое может быть использовано для доведения до сведения применимости набора согласно целевому назначению. Инструкции могут быть, например, прикреплены к контейнеру или содержаться внутри контейнера для набора.
[0034] "Терапия" или "лечение" означает уменьшение интенсивности, профилактику или купирование болезни или поражения или по меньшей мере одного из явных симптомов, например лечение воспалительного поражения кожи (например, розацеа) путем уменьшения покраснения кожи. В другом варианте осуществления "терапия" или "лечение" означает уменьшение интенсивности, профилактику или реверсирование по крайней мере одного из измеряемых физических параметров, связанных с излечиваемой болезнью или поражением, не обязательно различимого или воспринимаемого млекопитающим. В еще одном варианте осуществления "терапия" или "лечение" означает ингибирование или замедление прогрессирования заболевания или поражения физически, например стабилизацию явного симптома, физиологически, например стабилизацию физического параметра, либо то и другое. В еще одном варианте осуществления "терапия" или "лечение" означает задержку наступления заболевания или поражения.
[0035] В некоторых вариантах осуществления рассматриваемые соединения вводят в качестве профилактической меры. "Профилактика" или "предупреждение" относится к снижению риска приобретения данного заболевания или поражения. В предпочтительном способе воплощения указанные соединения вводят в качестве профилактической меры субъекту с предрасположенностью к воспалительному поражению кожи, такому как розацеа, даже если симптомы поражения отсутствуют или минимальные.
[0036] "Терапевтически эффективное количество агониста α2-адренергических рецепторов" означает количество агониста α2-адренергических рецепторов, вызывающее биологический или лекарственный отклик в системе тканей, организме животного или человека, которого добивается исследователь, ветеринар, лечащий врач или другой клиницист, что включает частичное снятие симптомов излечиваемой болезни или поражения. В предпочтительном варианте осуществления терапевтически эффективное количество агониста α2-адренергических рецепторов является эффективным для лечения, усиления терапии или профилактического предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием.
[0037] "Терапевтически эффективное количество нестероидного противовоспалительного средства" означает количество нестероидного противовоспалительного средства, вызывающее биологический или лекарственный отклик в системе тканей, организме животного или человека, которого добивается исследователь, ветеринар, лечащий врач или другой клиницист, что включает частичное снятие симптомов излечиваемой болезни или поражения. В предпочтительном варианте осуществления терапевтически эффективное количество нестероидного противовоспалительного средства является эффективным для лечения, усиления терапии или профилактического предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием.
[0038] В одном из основных аспектов, настоящее изобретение касается способа лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, у субъекта. Способ включает местное нанесение на участок кожи субъекта композиции, включающей фармацевтически приемлемый носитель, терапевтически эффективное количество агониста α2-адренергических рецепторов и терапевтически эффективное количество нестероидного противовоспалительного средства, где участок кожи подвержен или может быть поражен воспалительным поражением кожи или проявляется симптом, связанный с указанным заболеванием.
[0039] Другие аспекты настоящего изобретения включают композиции, например местно вводимые композиции, и наборы, которые могут быть использованы для лечения или профилактики воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, у субъекта. Композиция или набор согласно вариантам осуществления изобретения включает терапевтически эффективное количество агониста α2-адренергических рецепторов и терапевтически эффективное количество нестероидного противовоспалительного средства.
[0040] Способы и композиции по настоящему изобретению могут применяться для лечения или профилактики воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, примеры которого включают, но не в порядке ограничения, состояния, связанные с пролиферацией клеток, такие как псориаз, экзема и дерматит (например, экзематозный дерматит, топический, атопический или себорейный дерматит, аллергический или ирритативный контактный дерматит, нуммулярный дерматит, генерализованный эксфолиативный дерматит, экзема craquelee, фотоаллергический дерматит, фототоксический дерматит, фитофотодерматит, радиационный дерматит и застойный дерматит, простой хронический лишай); склеродермия, язвы и эрозии, возникающие в результате травмы, ожогов, буллезных поражений или ишемии кожи или слизистых оболочек; некоторые формы ихтиозов, буллезных эпидермозов, гипертрофических рубцов, келоидов; кожные изменения по причине старения от воздействия внутренних факторов, воздействия ультрафиолетовых лучей; возникновение волдырей при трении, вызванное механическим сдвигом кожи, и атрофия кожи в результате местного применения кортикостероидов, воспаление слизистых оболочек, такое как хейлит, потрескавшиеся губы, раздражение носа, мукозит и вульвовагинит.
[0041] Примеры воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, которое может быть излечено или предупреждено способами, соответствующими вариантам осуществления настоящего изобретения, также включают, но не в порядке ограничения, поражения волосяных фолликулов и сальных желез, такие как угри, розацеа и ринофима, периоральный дерматит и псевдофолликулит волос бороды; и воспалительные реакции, такие как лекарственная сыпь, полиморфная эритема, нодозная эритема и анулярная гранулема.
[0042] В предпочтительном варианте осуществления способ, соответствующий вариантам осуществления настоящего изобретения, применяют для лечения или профилактики воспалительных дерматологических заболеваний лица, таких как розацеа или признак и/или симптом, сопутствующий розацеа, например эритема при розацеа. Другие предпочтительные примеры воспалительных поражений кожи, которые могут излечены или предупреждены способами, соответствующими вариантам осуществления настоящего изобретения, также включают, но не в порядке ограничения, псориаз, топический дерматит и угри.
[0101] Согласно варианту осуществления настоящего изобретения, агонисты α2-адренергических рецепторов включают, но не в порядке ограничения, агонисты α2-адренергических рецепторов, описанные в опубликованной патентной заявке США US20050276830, которая полностью включена здесь в качестве ссылки.
[0102] В одном из вариантов осуществления изобретения агонистом α2-адренергических рецепторов является соединение формулы (I):

где каждый из R1, R2 и R3 независимо означает водород, галоген, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси; каждый из R4 и R5 независимо означает водород, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси; и каждый из R6 и R7 независимо означает водород, нитро, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси.
[0103] В предпочтительном варианте осуществления R6 и R7 оба означают водород в формуле (I).
[0104] В другом предпочтительном варианте осуществления R4 и R5 оба означают водород в формуле (I).
[0105] В одном из вариантов осуществления настоящего изобретения агонистом α2-адренергических рецепторов является соединение формулы (Ia):

где каждый из R1, R2 и R3 независимо означает водород, галоген, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси; каждый из R4 и R5 независимо означает водород, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси; и каждый из R6 и R7 независимо означает водород, нитро, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси.
[0106] В предпочтительном варианте осуществления R6 и R7 оба означают водород в формуле (Ia).
[0107] В другом предпочтительном варианте осуществления R4 и R5 оба означают водород в формуле (Ia).
[0108] В еще одном предпочтительном варианте осуществления R2 и R3 оба означают водород, и R1 означает галоген, предпочтительно бром, в формуле (Ia).
[0109] В одном из вариантов осуществления настоящего изобретения агонистом α2-адренергических рецепторов является соединение формулы (Ib):

где каждый из R1, R2 и R3 независимо означает водород, галоген, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси.
[0110] В предпочтительном варианте осуществления R2 и R3 оба означают водород, и R1 означает галоген, предпочтительно бром, в формуле (Ib).
[0111] В одном из вариантов осуществления настоящего изобретения агонистом α2-адренергических рецепторов является соединение формулы (Ic):
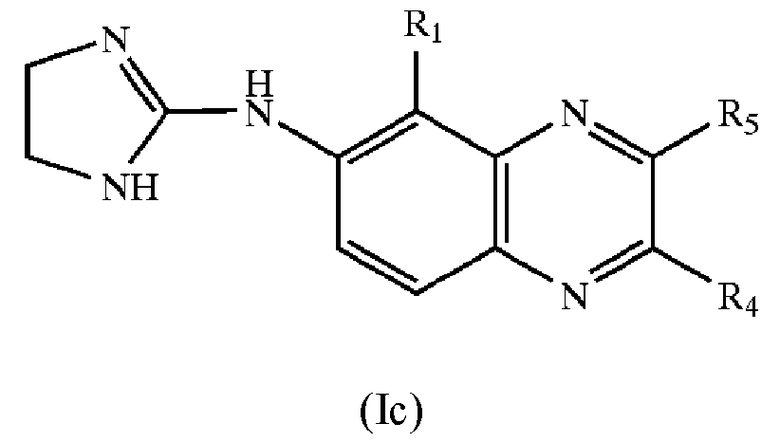
где R1 означает водород, галоген, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси.
[0112] В предпочтительном варианте осуществления R1 означает галоген, более предпочтительно бром; и каждый из R4 и R5 независимо означает водород, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси, в формуле (Ic).
[0113] В предпочтительном варианте осуществления по меньшей мере один из R4 и R5 означает водород в формуле (Ic).
[0114] В одном из вариантов осуществления настоящего изобретения агонистом α2-адренергических рецепторов является соединение формулы (Id):
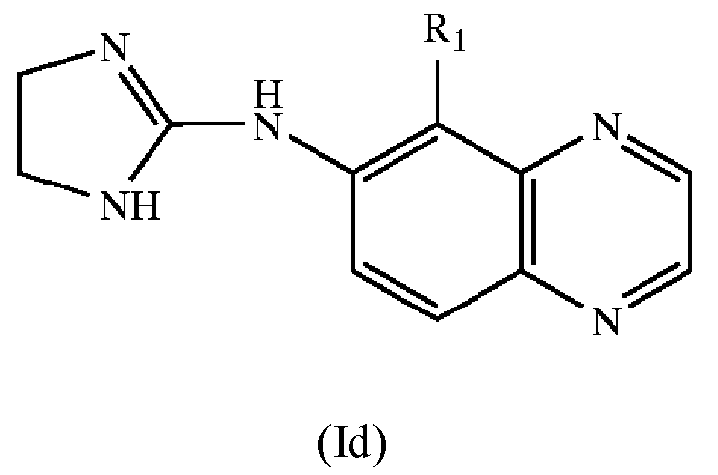
где R1 означает водород, галоген, алкил, предпочтительно незамещенный алкил, или алкокси, предпочтительно незамещенный алкокси.
[0115] В другом предпочтительном варианте осуществления R1 означает галоген, более предпочтительно бром, в формуле (Id).
[0116] В другом варианте осуществления настоящего изобретения агонистом α2-адренергических рецепторов является соединение формулы (II):

где каждый из A1, A3 и A4 независимо означает водород или алкил и A2 независимо означает водород или гидрокси.
[0117] В еще одном варианте осуществления настоящего изобретения агонистом α2-адренергических рецепторов является соединение формулы (III):

где каждый из B1, B2 и B3 независимо означает водород, гидрокси или алкокси, предпочтительно метокси; и каждый из B4 и B5 независимо означает водород или алкил.
[0118] Типичные представители агонистов α2-адренергических рецепторов, которые могут применяться в настоящем изобретении, включают, но не в порядке ограничения, агонисты, перечисленные в таблице 1.
[0119]
Типичные представители агонистов α2-адренергических рецепторов
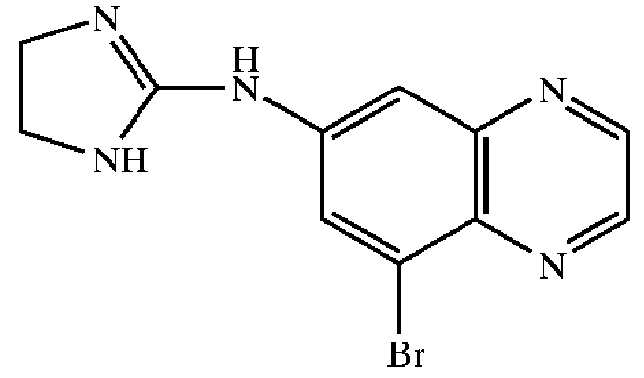
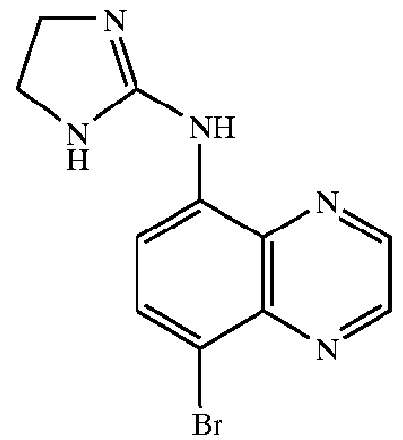

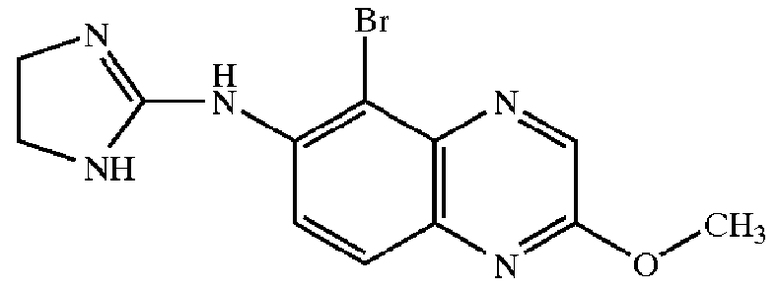



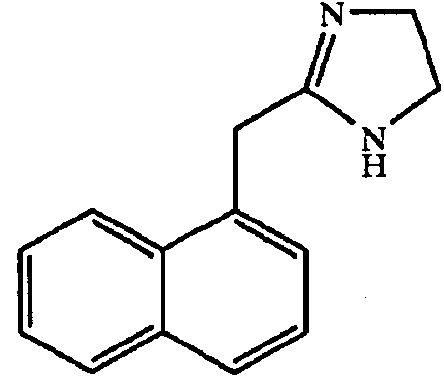
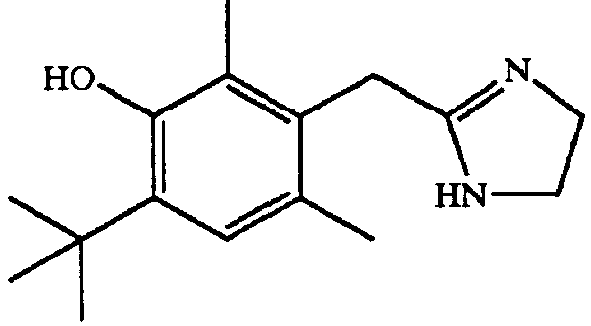




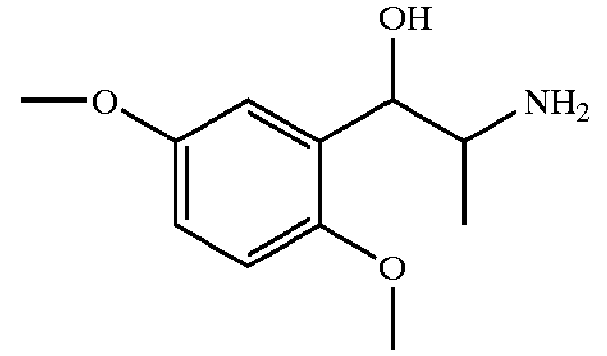
[0120] Наиболее предпочтительным агонистом α2-адренергических рецепторов является бримонидин, (5-бромхиноксалин-6-ил)-(4,5-дигидро-1H-имидазол-2-ил)амин, и фармацевтически приемлемые соли указанного соединения, такие как тартратная соль бримонидина.
[0121] Другие примеры α2-адренергических рецепторов, которые могут применяться в настоящем изобретении, включают, но не в порядке ограничения, дексмедетомидин, медетомидин, ромифидин, клонидин, детомидин, лофексидин, ксилазин, тизанидин, гуанфацин и амитраз.
[0122] Согласно варианту осуществления настоящего изобретения, нестероидное противовоспалительное средство выбирают из группы, состоящей из диклофенака, аспирина, ибупрофена, кетопрофена, пироксикама, напроксена, сулиндака, холина субсалицилата, дифлунизала, фенопрофена, индометацина, меклофенамата, салсалата, толметина и салицилата магния.
[0123] Предпочтительно, НПВС представляет собой диклофенак, 2-[2-(2,6-дихлорфениламино)фенил]уксусную кислоту, и фармацевтически приемлемые соли указанного соединения, такие как натриевая или калиевая соль диклофенака.
[0124] В предпочтительном варианте осуществления способ по настоящему изобретению включает местное нанесение на кожу субъекта композиции, включающей терапевтически эффективное количество бримонидина, терапевтически эффективное количество диклофенака и фармацевтически приемлемый носитель.
[0125] Специалисту в данной области понятно, что терапевтически эффективное количество агониста α2-адренергических рецепторов и терапевтически эффективное количество НПВС, применяемое в настоящем изобретении, может изменяться в зависимости от факторов, таких как конкретный субъект, например возраст, диета, состояние здоровья и т.д., тяжесть и осложнения воспалительного поражения кожи, которое стремятся излечить или предупредить, используемые составы и прочее. В свете настоящего описания могут быть выполнены стандартные процедуры для оценки влияния введения композиции для местного применения субъекту, что таким образом позволяет специалисту в данной области определить терапевтически эффективное количество агониста α2-адренергических рецепторов и терапевтически эффективное количество НПВС для введения субъекту. Например, клинически заметное благоприятное воздействие комбинации агониста α2-адренергических рецепторов и НПВС при лечении воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, можно наблюдать или отслеживать непосредственно мониторингом субъекта.
[0126] Клинически заметное благоприятное воздействие быть такой ситуацией, при которой, если композицию по настоящему изобретению вводят субъекту после обнаружения признаков и/или симптомов, связанных с воспалительным заболеванием кожи, то предотвращается дальнейшее развитие или обострение признаков и/или симптомов или развитие происходит в меньшей степени, чем без введения указанной композиции согласно вариантам осуществления настоящего изобретения. Клинически заметное благоприятное воздействие может также состоять в том, что когда композицию по настоящему изобретению вводят субъекту до заметного проявления признаков и/или симптомов, связанных с указанным заболеванием, то предотвращается возникновение признаков и/или симптомов или последующее развитие происходит в меньшей степени, чем без введения указанной композиции согласно вариантам осуществления настоящего изобретения.
[0127] В одном из вариантов осуществления терапевтически эффективное количество агониста α2-адренергических рецепторов в комбинации с терапевтически эффективным количеством НПВС ослабляет синдром или состояние дискомфорта у субъекта, связанное с воспалительным заболеванием кожи, или признак и/или симптом, связанный с указанным заболеванием, по меньшей мере примерно на 20%, например, по меньшей мере примерно на 30%, примерно на 40%, примерно на 50%, примерно на 60%, примерно на 70%, примерно на 80%, примерно на 90%, примерно на 100%.
[0128] В другом варианте осуществления терапевтически эффективное количество агониста α2-адренергических рецепторов в комбинации с терапевтически эффективным количеством НПВС предупреждает развитие синдрома или состояния дискомфорта у субъекта, связанного с воспалительным заболеванием кожи, или признака и/или симптома, связанного с указанным заболеванием, или снижает вероятность их наступления по меньшей мере примерно на 20%, например, по меньшей мере примерно на 30%, примерно на 40%, примерно на 50%, примерно на 60%, примерно на 70%, примерно на 80%, примерно на 90% или примерно на 100%.
[0129] Способы по настоящему изобретению могут быть использованы в сочетании с одной или несколькими другими терапиями и лекарственными препаратами от воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, такими, как описаны в публикации THE MERCK MANUAL 811-830 (Keryn A. G. Lane et al. eds. 17th ed. 2001), включенной здесь в качестве ссылки.
[0130] Другой лекарственный препарат или другое лечение можно назначать субъекту одновременно или последовательно и в пределах временного интервала, с комбинированной терапией агонистом α2-адренергических рецепторов и НПВС, так чтобы активные ингредиенты или средства могли оказывать совместное действие по лечению или предупреждению воспалительных заболеваний кожи (например, розацеа) и признаков и/или симптомов, связанных с указанным заболеванием. Например, другой лекарственный препарат или другое лечение, агонист α2-адренергических рецепторов и НПВС, могут быть введены в одной и той же или в раздельных лекарственных формах в то же самое или в различное время.
[0131] Любой подходящий способ введения может быть использован для обеспечения дополнительного лечения или доставки лекарственного препарата, включая, но не в порядке ограничения, пероральный, интраоральный, ректальный, парентеральный, местный, накожный, трансдермальный, подкожный, внутримышечный, интраназальный, сублингвальный, буккальный, интрадуральный, интраокулярный, интрареспираторный способ или назальную ингаляцию.
[0132] В одном из вариантов осуществления лекарственные формы для местного применения по изобретению используют в комбинации с системным введением антибиотиков или ретиноидов, включая, но не в порядке ограничения, перорально дозируемые антибиотики, такие как тетрациклин, миноцин, миноциклин, эритромицин и доксициклин, и перорально дозируемые ретиноиды, такие как изотретиноины (например, аккутан или роаккутан).
[0133] В другом варианте осуществления лекарственные формы для местного применения по изобретению используют в комбинации с другими местными терапиями, включающими, но не в порядке ограничения, лекарственные формы для местного применения, содержащие метронидазол, перекись водорода, бензоилпероксид, липоевую кислоту и азелаиновую кислоту и серные препараты; местно дозируемые антибиотики, такие как метронидазол, клиндамицин и эритромицин; местные ретиноиды, такие как третиноин, адапален, тазаротен; или местные стероиды.
[0134] В другом варианте осуществления составы для местного применения по изобретению используют в комбинации с терапией пульсирующим смешанным светом (фотодермальной), импульсным лазером на красителе или электрохирургией.
[0135] Местно вводимая композиция согласно вариантам осуществления настоящего изобретения включает фармацевтически приемлемый носитель, терапевтически эффективное количество агониста α2-адренергических рецепторов и терапевтически эффективное количество нестероидного противовоспалительного средства. Носители, используемые для местной доставки указанных соединений согласно вариантам осуществления изобретения, могут представлять собой любой носитель, известный из уровня техники для фармацевтических препаратов местного введения, включающий, но не в порядке ограничения, фармацевтически приемлемые растворители, такие как полиспирт или воду; эмульсии (эмульсии либо масло-в-воде, либо вода-в-масле), такие как кремы или лосьоны; микрокапсулированные эмульсии; гели; притирания; липосомы; порошки и водные растворы или суспензии. Фармацевтически приемлемый носитель содержит необходимые и инертные фармацевтические наполнители, включающие, но не в порядке ограничения, связующие вещества, суспендирующие средства, смазывающие вещества, корригенты, консерванты, красители и вещества для нанесения оболочки.
[0136] Местно вводимую композицию согласно вариантам осуществления настоящего изобретения получают смешением фармацевтически приемлемого носителя с терапевтически эффективным количеством агониста α2-адренергических рецепторов и терапевтически эффективным количеством нестероидного противовоспалительного средства известными из уровня техники способами, например способами, приведенными в стандартных справочниках, таких как REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY 1577-1591, 1672-1673, 866-885 (Alfonso R. Gennaro ed. 19th ed. 1995); Ghosh, T. K.; et al. TRANSDERMAL AND TOPICAL DRUG DELIVERY SYSTEMS (1997), которые оба включены здесь в качестве ссылки.
[0137] В одном из вариантов осуществления местно вводимая композиция по изобретению находится в форме эмульсии. Эмульсии, такие как кремы и лосьоны, являются удобными лекарственными формами для местного применения по изобретению. Эмульсия представляет собой дисперсную систему, включающую по меньшей мере две несмешивающиеся фазы, одна фаза диспергирована в другой в виде капель с диаметром в диапазоне от 0,1 мкм до 100 мкм. Эмульгирующие средства обычно включают для улучшения стабильности. Когда вода является диспергированной фазой и масло является диспергирующей средой, эмульсия носит название эмульсии вода-в-масле. Когда масло диспергировано в виде капель в водной фазе в виде капель, эмульсия носит название эмульсии масло-в-воде. Эмульсии, такие как кремы и лосьоны, которые могут использоваться в качестве носителей для местного применения, и получение таких эмульсий описано в REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY 282-291 (Alfonso R. Gennaro ed. 19th ed. 1995), включенном здесь в качестве ссылки.
[0138] В другом варианте осуществления местно вводимая композиция по изобретению находится в форме геля, например двухфазного геля или однофазного геля. Гели являются полутвердыми системами, содержащими суспензии мелких неорганических частиц или крупных органических молекул, глубоко пропитанные жидкостью. Гелевая масса, содержащая сеть мелких дискретных неорганических частиц, классифицируется как двухфазный гель. Однофазные гели состоят из органических макромолекул, однородно распределенных в жидкости, таким образом, что никакие явные границы не существуют между диспергированными макромолекулами и жидкостью. Подходящие для применения по изобретению гели описаны в REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY 1517-1518 (Alfonso R. Gennaro ed. 19th ed. 1995), включенном здесь в качестве ссылки. Другие подходящие для применения по изобретению гели описаны в патенте США № 6387383 (опубликованном 14 мая, 2002); патенте США № 6517847 (опубликованном 11 февраля, 2003) и патенте США № 6468989 (опубликованном 22 октября, 2002), каждый из упомянутых патентов включен здесь в качестве ссылки.
[0139] Согласно варианту осуществления, местно вводимая композиция дополнительно содержит водный гель, включающий воду и водо-загеливающее количество фармацевтически приемлемого гелеобразующего агента, выбираемого из группы, включающей карбомеры, глицерин полиакрилат и смеси указанных агентов, и местно вводимая композиция имеет физиологически приемлемый pH.
[0140] Полимерные загустители (гелеобразующие агенты), которые могут быть использованы в композициях согласно вариантам осуществления настоящего изобретения, включают загустители, известные специалистам в данной области, такие как гидрофильные и водно-спиртовые гелеобразующие агенты, часто используемые в косметической и фармацевтической промышленностях. Предпочтительно, гидрофильный или водно-спиртовый гелеобразующий агент включает "CARBOPOL®" (B.F. Goodrich, Cleveland, Ohio), "HYPAN®" (Kingston Technologies, Dayton, N.J.), "NATROSOL®" (Aqualon, Wilmington, Del), "KLUCEL®" (Aqualon, Wilmington, Del) или "STABILEZE®" (ISP Technologies, Wayne, N.J.). Предпочтительно, гелеобразующий агент составляет приблизительно от 0,2 до 4 масс.% от композиции. Конкретнее, предпочтительный диапазон композиционного состава в массовых процентах для "CARBOPOL®" примерно соответствует 0,5-2%, тогда как предпочтительный диапазон композиционного состава в массовых процентах для "NATROLSOL®" и "KLUCEL®" примерно соответствует 0,5-4%. Предпочтительный диапазон композиционного состава в массовых процентах как для "HYPAN®", так и для "STABILEZE®" примерно соответствует 0,5-4%.
[0141] "CARBOPOL®" является одним из многочисленных сшитых полимеров акриловой кислоты, имеющих общее, официально присвоенное название карбомер. Такие полимеры растворяются в воде и образуют прозрачный или слегка опалесцирующий гель после нейтрализации щелочным веществом, таким как гидроксид натрия, гидроксид калия, триэтаноламин или другими аминовыми основаниями. "KLUCEL®" представляет собой полимер целлюлозы, который диспергирован в воде и образует однородный гель после полной гидратации. Другие предпочтительные гелеобразующие полимеры включают гидроксиэтилцеллюлозу, целлюлозную камедь, декадиеновый кроссполимер MVE/MA, сополимер PVM/MA или комбинацию указанных веществ.
[0142] В другом предпочтительном варианте осуществления местно вводимая композиция по изобретению находится в форме притирания. Притирания представляют собой маслянистые, полутвердые массы, содержащие незначительное количество, если есть, воды. Предпочтительно притирания имеют углеводородную основу, такую как воск, вазелин или гелеобразное минеральное масло. Подходящие притирания для применения по изобретению хорошо известны в данной области и описаны в REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY 1585-1591 (Alfonso R. Gennaro ed. 19th ed. 1995), включенном здесь в качестве ссылки.
[0143] Согласно варианту осуществления настоящего изобретения, местно вводимая композиция по изобретению содержит по крайней мере один из компонентов, выбираемых из крема и притирания, каждый из которых содержит агент, выбираемый из группы, включающей стеариновую кислоту, стеариловый спирт, цетиловый спирт, глицерин, воду и смеси указанных веществ, и композиция для местного применения имеет физиологически приемлемый pH.
[0144] В другом варианте осуществления местно вводимая композиция по изобретению находится в форме водного раствора или суспензии, предпочтительно в форме водного раствора. Подходящие водные составы для местного применения по изобретению включают составы, описанные в REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY 1563-1576 (Alfonso R. Gennaro ed. 19th ed. 1995), включенном здесь в качестве ссылки. Другие подходящие водные системы носителей для местного применения включают системы, описанные в патенте США № 5424078 (опубликованном 13 июня, 1995); патенте США № 5736165 (опубликованном 7 апреля, 1998); патенте США № 6194415 (опубликованном 27 февраля, 2001); патенте США № 6248741 (опубликованном 19 июня, 2001); № 6465464 (опубликованном 15 октября, 2002), все указанные патенты включены здесь в качестве ссылок.
[0145] pH составов для местного применения по изобретению предпочтительно находится в диапазоне физиологически приемлемого pH, например приблизительно в диапазоне от 6 до 8, более предпочтительно, приблизительно от 6,3 до 6,5. Для стабилизации pH предпочтительно включают эффективное количество буферного раствора. В одном из вариантов осуществления буферный агент присутствует в водном составе для местного применения в количестве приблизительно от 0,05 до 1 масс.% от состава. По необходимости, кислоты или основания могут быть использованы для доведения pH до требуемой величины.
[0146] Регулирующие тоничность вещества могут быть включены в водные составы для местного применения по изобретению. Примеры подходящих регулирующих тоничность веществ включают, но не в порядке ограничения, хлорид натрия, хлорид калия, маннит, декстрозу, глицерин и пропиленгликоль. Количество регулирующего тоничность вещества может изменяться в широких пределах, в зависимости от заданных свойств состава. В одном из вариантов осуществления регулирующее тоничность вещество присутствует в водном составе для местного применения в количестве приблизительно от 0,5 до 0,9 масс.% от состава.
[0147] Предпочтительно, водные составы для местного применения по изобретению имеют вязкость в диапазоне приблизительно от 15 спз до 25 сП. Вязкость водных растворов по изобретению может быть доведена до требуемого значения добавлением регулирующих вязкость веществ, например, но не в порядке ограничения, таких как поливиниловый спирт, повидон, гидроксипропилметилцеллюлоза, полоксамеры, карбоксиметилцеллюлоза или гидроксиэтилцеллюлоза.
[0148] В предпочтительном варианте осуществления водный состав для местного применения по изобретению является изотоническим солевым раствором, содержащим консервант, такой как хлорид бензалкония или диоксид хлора, регулирующее вязкость вещество, такое как поливиниловый спирт, и буферную систему, такую как цитрат натрия и лимонная кислота.
[0149] Местно вводимая композиция согласно вариантам осуществления настоящего изобретения может содержать фармацевтически приемлемые наполнители, такие как наполнители, перечисленные в REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY 866-885 (Alfonso R. Gennaro ed. 19th ed. 1995; Ghosh, T. K.; et al. TRANSDERMAL AND TOPICAL DRUG DELIVERY SYSTEMS (1997), включенных здесь в качестве ссылки, включая, но не в порядке ограничения, защитные вещества, адсорбенты, уменьшающие раздражение средства, мягчители, консерванты, антиоксиданты, увлажнители, буферные вещества, солюбилизирующие средства, улучшающие проникновение через кожу вещества и поверхностно-активные вещества.
[0150] Подходящие защитные вещества и адсорбенты включают, но не в порядке ограничения, присыпки, стеарат цинка, коллодий, диметикон, силиконы, карбонат цинка, гель алоэ вера и другие продукты алоэ, масляный витамин E, аллантоин, глицерин, петролатум и оксид цинка.
[0151] Подходящие, уменьшающие раздражение средства включают, но не в порядке ограничения, бензоин, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу и поливиниловый спирт.
[0152] Подходящие мягчители включают, но не в порядке ограничения, животные и растительные жиры и масла, миристиловый спирт, квасцы и ацетат алюминия.
[0153] Согласно варианту осуществления, местно вводимая композиция по изобретению дополнительно содержит один или несколько агентов, выбираемых из группы, включающей консервант, местный анестетик и увлажнитель кожи.
[0154] Подходящие консерванты включают, но не в порядке ограничения, соединения четвертичного аммония, такие как хлорид бензалкония, хлорид бензетония, цетримид, хлорид деквалиния и хлорид цетилпиридиния; содержащие ртуть вещества, такие как фенилртутьнитрат, фенилртутьацетат и тимеросал; спиртовые вещества, например хлорбутанол, фенилэтиловый спирт и бензиловый спирт; антибактериальные сложные эфиры, например эфиры парагидроксибензойной кислоты; и другие противомикробные средства, такие как хлоргексидин, хлоркрезол, бензойная кислота и полимиксин.
[0155] Диоксид хлора (ClO2), преимущественно, стабилизированный диоксид хлора, является предпочтительным консервантом для использования с составами для местного применения по изобретению. Термин "стабилизированный диоксид хлора" хорошо известен в промышленности и специалистам в данной области. Стабилизированный диоксид хлора включает один или несколько предшественников диоксида хлора, таких как один или несколько комплексов, содержащих диоксид хлора, и/или один или несколько компонентов, содержащих хлорит, и/или одно или несколько других веществ, способных к разложению или разлагаемых в водной среде с образованием диоксида хлора. Патент США № 5424078 (опубликованный 13 июня, 1995), включенный здесь в качестве ссылки, описывает форму стабилизированного диоксида хлора и способ получения указанной формы, которая может быть использована в качестве консерванта для водных офтальмологических растворов и полезна в составах для местного применения по изобретению. Промышленное изготовление или получение некоторых стабилизированных продуктов с диоксидом хлора описано в патенте США № 3278447, включенном здесь в качестве ссылки. Коммерчески доступным стабилизированным диоксидом хлора, который может быть применен при практическом осуществлении настоящего изобретения, является патентованный стабилизированный диоксид хлора фирмы BioCide International, Inc. of Norman, Okla., выпускаемый под торговой маркой Purogene® или Purite®. Другие подходящие стабилизированные продукты с диоксидом хлора включают продукты, выпускаемые под торговой маркой DuraKlor фирмой Rio Linda Chemical Company, Inc., и продукты, выпускаемые под торговой маркой Antheium Dioxide фирмой International Dioxide, Inc.
[0156] Подходящие антиоксиданты включают, но не в порядке ограничения, аскорбиновую кислоту и эфиры указанной кислоты, бисульфит натрия, бутилированный гидрокситолуол, бутилированный гидроксианизол, токоферолы и хелатообразующие вещества, типа EDTA и лимонной кислоты.
[0157] Подходящие увлажнители включают, но не в порядке ограничения, глицерин, сорбит, полиэтиленгликоли, мочевину и пропиленгликоль.
[0158] Подходящие буферные вещества для применения по изобретению включают, но не в порядке ограничения, ацетатные буферы, цитратные буферы, фосфатные буферы, буферы с молочной кислотой и боратные буферы.
[0159] Подходящие солюбилизирующие средства включают, но не в порядке ограничения, хлориды четвертичного аммония, циклодекстрины, бензилбензоат, лецитин и полисорбаты.
[0160] Подходящие, улучшающие проникновение через кожу вещества включают, но не в порядке ограничения, этиловый спирт, изопропиловый спирт, октилфенилполиэтиленгликоль, олеиновую кислоту, полиэтиленгликоль 400, пропиленгликоль, N-децилметилсульфоксид, эфиры жирных кислот (например, изопропилмиристат, метиллаурат, глицеролмоноолеат и пропиленгликольмоноолеат) и N-метилпирролидон.
[0161] Местно вводимая композиция согласно вариантам осуществления настоящего изобретения может включать фармацевтические средства или фармацевтически приемлемые соли указанных средств, такие как агонист α2-адренергических рецепторов и нестероидное противовоспалительное средство, и, необязательно, один или несколько других фармацевтически активных ингредиентов, включая, но не в порядке ограничения, кортикостероиды и другие противовоспалительные средства, такие как бетаметазон, дифлоразон, амцинонид, флуоцинолон, мометазон, гидрокортизон, преднизон и триамцинолон; местные анестетики и анальгетики, такие как камфора, ментол, лидокаин и дибукаин и прамоксин; противогрибковые средства, такие как циклопирокс, хлорксиленол, триацетин, сулконазол, нистатин, ундециленовая кислота, толнафтат, миконизол, клотримазол, оксиконазол, гризеофульвин, эконазол, кетоконазол и амфотерицин B; антибиотики и препараты для лечения инфекций, такие как мупироцин, эритромицин, клиндамицин, гентамицин, полимиксин, бацитрацин и сульфадиазин серебра; и антисептики, такие как йод, повидин-йод, хлорид бензалкония, бензойная кислота, хлоргексидин, нитрофуразин, пероксид бензоила, перекись водорода, гексахлорофен, фенол, резорцин и хлорид цетилпиридиния.
[0162] В предпочтительном варианте осуществления местно вводимая композиция согласно вариантам осуществления изобретения дополнительно включает диоксид титана (TiO2), предпочтительно в количестве, достаточном, чтобы замаскировать цвет бримонидина или другого окрашенного ингредиента в составе, но не вызывающем раздражения кожи. TiO2 может вызывать умеренное раздражение и покраснение глаз, таким образом, следует избегать контакта глаз с TiO2-содержащей местно вводимой композицией.
[0163] Дозировки и частота дозирования определяются специалистом-медиком в зависимости от активности используемых соединений, характеристик конкретного состава для местного применения и идентичности и тяжести излечиваемого или предупреждаемого дерматологического поражения.
[0164] Согласно варианту осуществления настоящего изобретения, местно вводимая композиция содержит от 0,01% до 5 масс.% агониста α2-адренергических рецепторов и от 0,01% до 5 масс.% нестероидного противовоспалительного средства. Например, композиция может содержать 0,01%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,8%, 0,9%, 1%, 2%, 3%, 4% или 5 масс.% агониста α2-адренергических рецепторов и 0,01%, 0,05%, 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,8%, 0,9%, 1%, 2%, 3%, 4% или 5 масс.% нестероидного противовоспалительного средства.
[0165] В предпочтительном варианте осуществления местно вводимая композиция содержит 0,05-0,5%, 0,07%-0,7% или 0,1-0,6 масс.% агониста α2-адренергических рецепторов и 0,05%-0,5%, 0,1%-1% или 0,5%-2 масс.% нестероидного противовоспалительного средства.
[0166] Для лечения или профилактики воспалительных поражений кожи (например, розацеа), с учетом настоящего описания, например, местно вводимые композиции по изобретению наносят местно, непосредственно на пораженный участок любым общепринятым способом, хорошо известным из уровня техники, например, пипеткой или палочкой-аппликатором, в виде аэрозоля через аппликатор аэрозольного баллона, посредством интрадермального или трансдермального пластыря, или просто намазывая состав по изобретению на пораженный участок пальцами. Обычно количество состава для местного применения по изобретению, наносимое на пораженный участок кожи, изменяется в диапазоне приблизительно от 0,1 г/см2 площади поверхности кожи до 5 г/см2, предпочтительно, приблизительно от 0,2 г/см2 до 0,5 г/см2 площади поверхности кожи. Как правило, рекомендуют одну-четыре аппликации в день в течение срока лечения.
[0167] Другой аспект изобретения касается набора, который содержит один или несколько составов для местного применения согласно вариантам осуществления изобретения, в одном или нескольких подходящих контейнерах с этикетками и инструкциями по применению для лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием. Набор включает:
(1) первую местно вводимую композицию, включающую терапевтически эффективное количество агониста α2-адренергических рецепторов и фармацевтически приемлемый носитель;
(2) вторую местно вводимую композицию, включающую терапевтически эффективное количество нестероидного противовоспалительного средства и фармацевтически приемлемый носитель; и
(3) инструкции по местному нанесению первой местно вводимой композиции и второй местно вводимой композиции на участок кожи субъекта, где участок кожи подвержен или может быть поражен воспалительным заболеванием кожи или проявляются признаки и/или симптомы, связанные с указанным заболеванием.
[0168] В одном из вариантов осуществления изобретения первая и вторая местно вводимые композиции представляют собой одну и ту же единую местно вводимую композицию, содержащую как терапевтически эффективное количество агониста α2-адренергических рецепторов, так и терапевтически эффективное количество нестероидного противовоспалительного средства. Единая местно вводимая композиция содержится в едином подходящем контейнере, таком как пипетка, баночка или туба с подходящим небольшим размером отверстия, такая как туба длительного использования, изготовленная из любого фармацевтически подходящего материала.
[0169] В другом варианте осуществления первая и вторая местно вводимые композиции представляют собой две отдельные, индивидуальные, местно вводимые композиции, каждая из которых содержит терапевтически эффективное количество агониста α2-адренергических рецепторов или терапевтически эффективное количество нестероидного противовоспалительного средства, соответственно. Две отдельные местно вводимые композиции содержатся в двух подходящих отдельных контейнерах, таких как пипетка, баночка или туба с подходящим небольшим размером отверстия, такая как туба длительного использования, изготовленная из любого фармацевтически подходящего материала.
[0170] Составы для местного применения по изобретению могут быть наполнены и упакованы в пластмассовую бутылку-пульверизатор или тубу. Подходящие системы упаковки/укупорки составов для местного применения по изобретению коммерчески доступны, например, от Wheaton Plastic Products, 1101 Wheaton Avenue, Millville, N.J. 08332.
[0171] Предпочтительно, инструкции упаковывают вместе с составами по изобретению, например инструкция по применению или упаковочная этикетка. Маркировки-инструкции поясняют, как вводить составы для местного применения по изобретению, в каком количестве и в течение какого периода времени, достаточного для лечения или предупреждения воспалительного заболевания кожи (например, розацеа) и признаков и/или симптомов, связанных с указанным заболеванием, например инструкции по местному применению первой местно вводимой композиции и второй местно вводимой композиции субъекту, либо вводимых в одной композиции в одно время, либо в двух композициях, вводимых в одно и то же время или в различные моменты времени. Предпочтительно, этикетка включает инструкцию по дозированию и введению, состав лекарственной формы для местного применения, клиническую фармакологию, устойчивость к лекарственному средству, фармакокинетику, всасывание, биологическую доступность и противопоказания.
[0172] Настоящее изобретение будет лучше понято при обращении к следующим неограничивающим примерам, но для специалиста в данной области очевидно, что примеры только иллюстрируют изобретение, более полно раскрытое в приложенной формуле изобретения.
ПРИМЕР 1
Гелевый состав
[0173] Характерный гелевый состав получают, используя известные из уровня техники способы, например, смешением следующих ингредиентов в указанных концентрациях:
ПРИМЕР 2
Улучшенная противовоспалительная активность комбинации бримонидина и диклофенака в модели вызванного TPA отека у животных
[0174] Модель отека, вызванного 12-O-тетрадеканоилфорбол-13-ацетатом (TPA) у животных, используют для демонстрации улучшенного противовоспалительного влияния бримонидина и диклофенака.
[0175] Все процедуры с вовлечением животных проводят в полностью гарантирующем качество виварии и в соответствии с предварительно одобренными протоколами.
[0176] Стимулятор отека, TPA, растворяют в этаноле при концентрации 0,01 масс.%, получая раствор TPA ("TPA-раствор"). Испытуемые соединения, бримонидин (CD07805) и диклофенак (CD08100/02), растворяют в TPA-растворе как таковые или в комбинации при заданных концентрациях. Соединение положительного контроля, бетаметазона валерат (CD0153), растворяют в TPA-растворе при концентрации 0,01 масс.%.
[0177] TPA-раствор (отрицательный контроль), испытуемое соединение, растворенное в TPA-растворе, или положительный контроль, растворенный в TPA-растворе, по двадцать (20) мкл каждого, наносят местно на ухо интактных самок мышей (BALB/c ByJ Rj), возрастом 8-9-недель. Различные соединения при различных дозировках исследуют на 10 группах животных, где каждая группа содержит 5 мышей (см. таблицу 2).
[0178]
Группы животных, используемые в эксперименте на TPA-вызванном отеке
[0179] Толщину уха каждого из 50 животных измеряют через 6 часов после нанесения соединений. После измерения животных умерщвляют диоксидом углерода согласно предварительно одобренному протоколу.
[0180] Рассчитывают среднюю толщину уха, измеренную для 5 животных в каждой из 10 групп. Противовоспалительную активность испытуемого соединения оценивают по способности уменьшать вызванный TPA отек уха, т.е. как процент уменьшения толщины уха животных, обработанных как испытуемым соединением, так и TPA, по сравнению с соответствующей величиной для обработанных только TPA.
[0181] Как показано в таблице 3 и на фиг.1, после однократного местного нанесения 0,2% бримонидин (CD07805), как таковой, снижает TPA-вызванный отек уха у мышей на 46,3%, демонстрируя умеренное противовоспалительное действие. Диклофенак (CD08100/02), как таковой, при 0,1%, 0,3% и 1% снижает TPA-вызванный отек уха у мышей на 63,8%, 60,0% и 70,0%, соответственно, демонстрируя противовоспалительное действие от умеренного до сильного. Неожиданно, комбинация 0,2% бримонидина (CD07805) с диклофенаком (CD08100/02) при 0,1%, 0,3% и 1% полностью устраняет вызванный TPA отек уха у мышей, т.е. на 100%, при всех трех исследуемых концентрациях диклофенака.
[0182]
Результаты эксперимента по ТРА-вызванному отеку
[0183] Полное противовоспалительное действие комбинации бримонидина и диклофенака сопоставлено с соответствующим действием 0,01% бетаметазона валерата (CD0153), который снижает вызванный TPA отек уха у мышей на 97,5% в тех же условиях испытания.
[0184] Приведенные результаты демонстрируют, что местное введение комбинации агониста α2-адренергических рецепторов и нестероидного противовоспалительного средства приводит к улучшенному лечению воспалительного поражения кожи.
ПРИМЕР 3
Улучшенная противовоспалительная активность комбинации бримонидина и диклофенака в модели вызванного арахидоновой кислотой острого отека у животных
[0185] Модель острого отека, вызванного арахидоновой кислотой (AA) у животных, используют для дальнейшей демонстрации улучшенного противовоспалительного влияния бримонидина и диклофенака.
[0186] Все процедуры с вовлечением животных проводят в полностью гарантирующем качество виварии и в соответствии с предварительно одобренными протоколами.
[0187] Стимулятор отека, арахидоновую кислоту, растворяют в растворе из смеси тетрагидрофуран (ТГФ):метанол (1:1) при 4 масс.%, получая раствор арахидоновой кислоты (AA-раствор). Испытуемые соединения, бримонидин (CD07805) и диклофенак (CD08100/02), растворяют в AA-растворе как таковые или в комбинации при заданных концентрациях. Соединение положительного контроля, индометацин (CD0016), растворяют в AA-растворе при концентрации 5 масс.%.
[0188] AA-раствор (отрицательный контроль), испытуемое соединение, растворенное в AA-растворе, или положительный контроль, растворенный в AA-растворе, по двадцать (20) мкл каждого, наносят на внутреннюю сторону правого уха интактных самок мышей (BALB/c ByJ Rj), возрастом 8-9-недель. Различные соединения при различных дозировках исследуют на 10 группах животных, где каждая группа содержит 5 мышей (см. таблицу 4).
[0189]
Группы животных, используемые в эксперименте на AA-вызванном отеке
[0190] Толщину уха каждого из 50 животных измеряют спустя 0, 1, 2 и 4 часа после нанесения соединения. После последнего измерения животных умерщвляют диоксидом углерода согласно предварительно одобренному протоколу.
[0191] Рассчитывают среднюю толщину уха, измеренную для 5 животных в каждой из 10 групп. Противовоспалительную активность испытуемого соединения оценивают по способности уменьшать вызванный AA отек уха, т.е. как процент уменьшения толщины уха животных, обработанных как испытуемым соединением, так и AA, по сравнению с соответствующей величиной для обработанных только AA.
[0192] Как показано в таблице 5 и на фиг.2, после однократного местного нанесения 0,2% бримонидин (CD07805), как таковой, снижает AA-вызванный отек уха у мышей до 80,8%, демонстрируя противовоспалительное действие от умеренного до сильного. Диклофенак (CD08100/02), как таковой, при 0,1%, 0,3% и 1% снижает AA-вызванный отек уха у мышей до 71,2%, 80,6% и 83,9%, соответственно, демонстрируя противовоспалительное действие от умеренного до сильного. Неожиданно, комбинация 0,2% бримонидина (CD07805) с диклофенаком (CD08100/02) при 0,1%, 0,3% и 1% полностью устраняет вызванный AA отек уха у мышей, т.е. на 100%, при всех трех исследуемых концентрациях диклофенака.
[0193] Противовоспалительное действие комбинации бримонидина и диклофенака сильнее, чем 5% индометацина (CD0016), который снижает AA-вызванный отек уха у мышей до 94,2% в тех же условиях испытания.
[0194] Как показано в таблице 6, комбинация бримонидина и диклофенака существенно улучшает противовоспалительное действие диклофенака при всех трех испытуемых концентрациях и всех трех временах измерений.
[0195] Приведенные результаты подтверждают результаты, полученные при изучении TPA-вызванного отека уха. Приведенные результаты также демонстрируют, что местное введение комбинации агониста α2-адренергических рецепторов и нестероидного противовоспалительного средства приводит к улучшенному лечению воспалительного поражения кожи.
[0196] Специалисту в данной области понятно, что могут быть произведены изменения описанных выше вариантов осуществления, не выходящие за широкий объем охраны идеи изобретения. Таким образом, ясно, что настоящее изобретение не ограничивается описанными конкретными вариантами осуществления, а, как подразумевается, охватывает модификации в рамках сущности и объема настоящего изобретения, определенного приложенной формулой изобретения.
Результаты эксперимента на АА-вызванном отеке (I)
Отек уха и ингибирование против арахидоновой кислоты при 4%
Результаты эксперимента на АА-вызванном отеке (II)
Отек уха и ингибирование против диклофенака, как такового


Представлена группа изобретений: способ лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, у субъекта, композиция и набор. Группа изобретений относится к медицине, а именно к дерматологии, и может быть использована при лечении таких заболеваний, как розацеа, псориаз, топический дерматит или угри. Для этого используют местное нанесение на участок кожи субъекта композиции для местного применения, которая может быть в составе набора, включающей терапевтически эффективное количество агониста α2-адренергических рецепторов, где агонист α2-адренергических рецепторов выбирают из группы, включающей:

где каждый из R1, R2 и R3 независимо означает водород, галоген, (C1-C8)алкил или алкокси; каждый из R4 и R5 независимо означает водород, (C1-C8)алкил или алкокси; и каждый из R6 и R7 независимо означает водород, нитро, (C1-C8)алкил или алкокси; алкокси выбран из метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси; и терапевтически эффективное количество нестероидного противовоспалительного средства диклофенака и фармацевтически приемлемый носитель, где участок кожи подвержен или может быть поражен воспалительным заболеванием кожи или симптомом, связанным с указанным заболеванием. В качестве агониста α2-адренергических рецепторов может, например, применятся бримонидин. Группа изобретений обеспечивает синергетический эффект при использовании заявленной комбинации, которая проявляет синергетический эффект, улучшая противовоспалительное действие диклофенака, приводя к полному уменьшению симптомов воспалительного заболевания. 4 н. и 17 з.п. ф-лы, 3 пр., 6 табл., 2 ил.
1. Способ лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, у субъекта, включающий местное нанесение на участок кожи субъекта композиции для местного применения, включающей терапевтически эффективное количество агониста α2-адренергических рецепторов, где агонист α2-адренергических рецепторов выбирают из группы, включающей:

где каждый из R1, R2 и R3 независимо означает водород, галоген, (C1-C8)алкил или алкокси; каждый из R4 и R5 независимо означает водород, (C1-C8)алкил или алкокси; и каждый из R6 и R7 независимо означает водород, нитро, (C1-C8)алкил или алкокси; алкокси выбран из метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси; и
терапевтически эффективное количество нестероидного противовоспалительного средства диклофенака и фармацевтически приемлемый носитель, где участок кожи подвержен или может быть поражен воспалительным заболеванием кожи или симптомом, связанным с указанным заболеванием.
2. Способ по п.1, где агонист α2-адренергических рецепторов выбирают из группы, состоящей из бримонидина, (8-бромхиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (5-бром-3-метилхиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (5-бром-2-метоксихиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (4,5-дигидро-1Н-имидазол-2-ил)-(8-метилхиноксалин-6-ил)амина, (4,5-дигидро-1Н-имидазол-2-ил)хиноксалин-6-иламина.
3. Способ по п.2, в котором агонистом α2-адренергических рецепторов является бримонидин.
4. Способ по п.1, в котором композиция включает 0,01-5 мас.% агониста α2-адренергических рецепторов и 0,01-5 мас.% диклофенака.
5. Способ по п.1, в котором воспалительным заболеванием кожи является розацеа, псориаз, топический дерматит или угри.
6. Способ по п.1, дополнительно включающий назначение субъекту одной или нескольких других терапий и лекарственных препаратов от воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием.
7. Местно вводимая композиция для лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, у субъекта, где композиция включает терапевтически эффективное количество агониста α2-адренергических рецепторов, где агонист α2-адренергических рецепторов выбирают из группы, включающей:


где каждый из R1, R2 и R3 независимо означает водород, галоген, (C1-C8)алкил или алкокси; каждый из R4 и R5 независимо означает водород, (C1-C8)алкил или алкокси; и каждый из R6 и R7 независимо означает водород, нитро, (C1-C8)алкил или алкокси; алкокси выбран из метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси; и
терапевтически эффективное количество нестероидного противовоспалительного средства диклофенака и фармацевтически приемлемый носитель.
8. Местно вводимая композиция по п.7, где агонист α2-адренергических рецепторов выбирают из группы, состоящей из бримонидина, (8-бромхиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (5-бром-3-метилхиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (5-бром-2-метоксихиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (4,5-дигидро-1Н-имидазол-2-ил)-(8-метилхиноксалин-6-ил)амина, (4,5-дигидро-1Н-имидазол-2-ил)хиноксалин-6-иламина.
9. Местно вводимая композиция по п.8, в которой агонистом α2-адренергических рецепторов является бримонидин.
10. Местно вводимая композиция по п.7, где композиция находится в форме, выбираемой из группы, состоящей из спреев, туман-аэрозолей, аэрозолей, растворов, лосьонов, гелей, кремов, притираний, паст, мазей, эмульсий и суспензий.
11. Местно вводимая композиция по п.7, включающая 0,01-5 мас.% агониста α2-адренергических рецепторов и 0,01-5 мас.% диклофенака.
12. Местно вводимая композиция по п.7, дополнительно содержащая водный гель, включающий воду и водо-загеливающее количество фармацевтически приемлемого гелеобразующего агента, выбираемого из группы, состоящей из карбомеров, глицерин полиакрилата и смеси указанных агентов, и местно вводимая композиция имеет физиологически приемлемый pH.
13. Местно вводимая композиция по п.7, дополнительно содержащая по меньшей мере один из компонентов, выбираемых из крема и притирания, каждый из которых содержит агент, выбираемый из группы, состоящей из стеариновой кислоты, стеарилового спирта, цетилового спирта, глицерина, воды и смеси указанных веществ, и композиция имеет физиологически приемлемый pH.
14. Местно вводимая композиция по п.7, дополнительно содержащая один или несколько агентов, выбираемых из группы, состоящей из дополнительного фармацевтически активного ингредиента для лечения или предупреждения воспалительного поражения кожи или симптома, связанного с указанным поражением, консервант, местный анестетик и увлажнитель кожи.
15. Местно вводимая композиция по п.7, дополнительно включающая диоксид титана.
16. Набор для лечения или предупреждения воспалительного заболевания кожи или признака и/или симптома, связанного с указанным заболеванием, где набор включает:
(1) первую местно вводимую композицию, включающую терапевтически эффективное количество агониста α2-адренергических рецепторов, где агонист α2-адренергических рецепторов выбирают из группы, включающей:

где каждый из R1, R2 и R3 независимо означает водород, галоген, (C1-C8)алкил или алкокси; каждый из R4 и R5 независимо означает водород, (C1-C8)алкил или алкокси; и каждый из R6 и R7 независимо означает водород, нитро, (C1-C8)алкил или алкокси; алкокси выбран из метокси, этокси, н-пропокси, втор-бутокси, трет-бутокси, н-гексилокси; и фармацевтически приемлемый носитель;
(2) вторую местно вводимую композицию, включающую терапевтически эффективное количество нестероидного противовоспалительного средства диклофенака и фармацевтически приемлемый носитель; и
(3) инструкции по местному нанесению первой местно вводимой композиции и второй местно вводимой композиции на участок кожи субъекта, где участок кожи подвержен или может быть поражен воспалительным заболеванием кожи или проявляются признаки и/или симптомы, связанные с указанным заболеванием.
17. Набор по п.16, где агонист α2-адренергических рецепторов выбирают из группы, состоящей из бримонидина, (8-бромхиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (5-бром-3-метилхиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (5-бром-2-метоксихиноксалин-6-ил)-(4,5-дигидро-1Н-имидазол-2-ил)амина, (4,5-дигидро-1Н-имидазол-2-ил)-(8-метилхиноксалин-6-ил)амина, (4,5-дигидро-1Н-имидазол-2-ил) хиноксалин-6-иламина.
18. Набор по п.17, где агонистом α2-адренергических рецепторов является бримонидин.
19. Местно вводимая композиция для лечения или предупреждения воспалительного заболевания кожи у субъекта, включающая 0,07-0,7 мас.% бримонидина, 0,1-1 мас.% диклофенака и фармацевтически приемлемый носитель.
20. Местно вводимая композиция по п.19, включающая 0,2 мас.% бримонидина, 0,1-1 мас.% диклофенака.
21. Местно вводимая композиция по любому из пп.7, 10-15 и 19-20, где воспалительным заболеванием кожи является розацеа, псориаз, топический дерматит или угри.
| WO2004105703 A2 09.12.2004 | |||
| WO2007103555 A2 13.09.2007 | |||
| WO2009129147 A2 22.10.2009 | |||
| ARTIGUES-VARIN C | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Fundam Clin Pharmacol | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| TUTTLE JL | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Am J Physiol Heart Circ Physiol | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
Авторы
Даты
2014-11-10—Публикация
2010-11-18—Подача