Изобретение относится к области ветеринарной вирусологии и биотехнологии, в частности к гибридомной технологии, и касается способа получения моноклональных антител к VP30 вируса африканской чумы свиней с помощью слияния клеток миеломы и лимфоцитов мыши, иммунизированной сочетанным введением плазмидной ДНК со встройкой гена, кодирующего p30 вируса африканской чумы свиней (АЧС) и рекомбинантного белка p30 в смеси с адъювантом. Изобретение может быть использовано при получении моноклональных антител (МКА) к определенным белкам, отдельным эпитопам, белкам, обладающим низким иммуногенной (антигенной) активностью, а также минорным белкам микроорганизмов.
Африканская чума свиней (АЧС) - вирусная болезнь, характеризующаяся высокой контагиозностью и летальностью, получила в настоящее время широкое распространение на европейской территории Российской Федерации. Важнейшей эпизоотологической особенностью («коварством») африканской чумы свиней является чрезвычайно быстрое изменение форм течения инфекции среди домашних свиней от острого со 100% летальностью до хронического и бессимптомного носительства и непредсказуемого распространения. Одним из иммунодоминантных диагностически значимых белков вируса АЧС является фосфопротеин p30 (30 кДа), который располагается во внутренней мембране инфицированных клеток [1], обладает антигенностью и синтезируется на всех этапах инфекционного цикла, начиная с 12-16 часов после инфицирования, накапливаясь в цитоплазме, что позволяет выявлять вирусный антиген в первые сутки после заражения. После выхода вирусных частиц во внеклеточное пространство, большая часть p30 также остается в клетках [2].
Иммунизация плазмидной ДНК, несущей ген целевого белка, индуцирует образование специфических антител и активацию Т-лимфоцитов, имеющих рецепторы обоих типов молекул гистосовместимости (МНС), необходимых для индукции полноценного гуморального и клеточного иммунного ответа. Mazumder S. et al. (2011) [3] при изучении индукции и длительности иммунного ответа против лейшманиоза у мышей линии BALB/c при различных комбинациях ДНК/ДНК, ДНК/белок и белок/белок показали преимущество иммунизации с праймированием плазмидной ДНК и последующим введением белка в растворимой форме.
В плазмиде pTT9/ASFVp30 штамма клеток E.coli BL21(DE3)plysS [4], использованной для праймирования при иммунизации мышей, присутствует ген CBD, кодирующий в структуре рекомбинантного белка целлюлозо-связывающий домен, с помощью которого рекомбинантный сплит-белок p30 способен связываться с целлюлозными матрицами. Повышение уровня гуморального и клеточного иммунного ответа осуществляется путем связывания со специфическими углеводородными рецепторами (лектинами), экспрессируемыми на антиген-презентирующих клетках, чем усиливают антиген-специфичный T- и B-клеточный ответ [6].
Наиболее близкими аналогами изобретения являются получение МКА к основным структурным белкам вируса АЧС: vp73, vp30 [7], штамм 2F2 гибридных клеток животных, продуцирующий МКА к Vp72, но эффективность взаимодействия этих антител с соединениями антигенного комплекса не известна [10]. В отечественной литературе описано получение МКА к полипептидам АЧС. [13, 14]
Все перечисленные методы получения МКА к полипептидам АЧС использовали вирусный антиген той или иной степени очистки и концентрации. Однако даже при глубокой очистке в препарате, предназначенном для иммунизации, направленной на получение МКА к белку p30, присутствуют примесные белки 14, 31 и 73 кDа [13].
Близким по принципу получения МКА заданной специфичности является «Способ получения гибридом, продуцирующих моноклональные антитела к рекомбинантным белкам» [15].
Целью изобретения является совершенствование способа получения гибридом - продуцентов моноклональных антител заданной специфичности.
Задачей изобретения является разработка способа получения стабильных высокопродуктивных линий гибридных клеток, секретирующих МКА, специфичные к Vp30 вируса АЧС и его рекомбинантному аналогу с использованием метода ДНК-иммунизации и введения соответствующего рекомбинантного белка. Для последующего конструирования на основе полученных МКА высокоспецифичных и стандартных отечественных тест-систем выявления Vp30 в инфицированных вирусом АЧС биологических жидкостях и тканях животных, в клещах, пищевых продуктах и продовольственном сырье.
Поставленная цель достигается за счет праймирования реципиента плазмидной ДНК, кодирующей ген нужного белка. Синтез закодированного в плазмиде белка in vivo обеспечивает его дальнейший процессинг для презентации в комплексе с антигенами МНС I и II классов иммунокомпетентным клеткам. Последующее введение соответствующего рекомбинантного белка обеспечивает синтез специфических антител к вводимому иммуногену.
Этот метод доставки генетического материала имеет ряд преимуществ перед обычной белковой иммунизацией. Наиболее важное из них - запуск обеих путей иммунного ответа. В отличие от белковых антигенов, синтез антигена in vivo обеспечивает правильный фолдинг и посттрансляционное модифицирование белковой молекулы. Снижается риск побочных эффектов, связанных с введением в организм чужеродных, балластных белков и т.п. К тому же ДНК-плазмида, несущая ген целевого белка, вызывает продолжительную экпрессию антигена и, соответственно, иммунный ответ. Синергизм праймирования и бустер эффекта обеспечивают высокую авидность CD4+ и CD8+ T-клеток и, как следствие, аффинность и авидность полученных антител.
Технический результат изобретения: повышается процент выхода гибридом, продуцирующих МКА к искомому антигену, уменьшается время получения доноров иммунных лимфоцитов и клонов гибридом, продуцирующих МКА к антигенным детерминантам целевого белка, в данном случае белка p30 вируса АЧС.
Сущность изобретения заключается в следующем.
Мышь линии BALB/c иммунизируют препаратом плазмиды pTT9/ASFVp30/2 и в последующем рекомбинантным белком p30, проводят слияние клеток мышиной миеломной линии Sp2/0-Ag14.1 с лимфоцитами иммунизированной мыши. Получают гибридомы, иммунохимически тестируют супернатанты полученных гибридом, отбирают клоны гибридом, продуцирующие моноклональные антитела, обладающие специфичностью и сродством к эпитопам Vp30 вируса АЧС. Это в свою очередь дает возможность изучать цикл и особенности репродукции данного белка и вируса в целом, а также определять Vp30 в инфицированных вирусом АЧС биологических жидкостях и тканях животных, в клещах, пищевых продуктах и продовольственном сырье животного происхождения.
Способ получения моноклональных антител к Vp30 вируса АЧС с использованием рекомбинантных конструкций осуществляется следующим образом.
Иммунизацию мышей проводят с использованием этапа праймирования плазмидной ДНК, с последующим введением рекомбинантного белка p30 с адъювантами. Гибридомы получают путем слияния в соотношении 10:1 спленоцитов иммунных мышей линии BALB/c и клеток мышиной миеломной линии SP2/0-Ag14.1. в присутствии 50% раствора ПЭГ-4000 (Sigma) и последующих этапов скринирования, трех кратного клонирования и стабилизации полученных линий гибридом.
Изобретение иллюстрируется, но не ограничивается следующими примерами.
Пример 1. Специфический иммунный ответ у мышей, иммунизированных рекомбинантными конструкциями p30 вируса АЧС.
Схема иммунизации мышей линии BALB/c и определение титров специфических антител
Из представленных в таблице данных видно, что иммунизация мышей по данной схеме может быть использована для индукции специфического иммунного ответа и, следовательно, получения МКА к белку p30 вируса АЧС.
Пример 2. Получение гибридом, продуцирующих моноклональные антитела к белку p30 вируса АЧС с использованием рекомбинантных конструкций.
Мышей линии BALB/c иммунизировали, как показано в примере 1. В опыте по гибридизации использовали мышей, имеющих титр специфических антител в непрямом ТФ ИФА не менее 6-7 log2. Гибридомы получали путем слияния в присутствии 50% раствора ПЭГ-4000 (Sigma) спленоцитов иммунных мышей линии BALB/c и тестированной на отсутствие ревертантов клеток мышиной миеломной линии SP2/0-Ag14.1. в соотношении 10:1. Полученные клетки высевали в 96-луночные культуральные планшеты на слой фидерных перитонеальных макрофагов и культивировали при температуре 37°C в атмосфере, содержащей 5% CO2. Селекцию клонов гибридом проводили на среде HAT и HT с последующим культивированием в среде ДМЕМ (Sigma) с 15% ФСТ, L-глютамином, пируватом натрия, глюкозой, амфотерицином-B.
Скрининг антителопродукции клонами гибридом проводили по стандартной методике непрямым ТФ ИФА, реакцией латексагглютинации на основе рекомбинантного белка p30, дот-блот ИФА, используя в качестве специфических антигенов рекомбинантный белок p30, нативный культуральный антиген вируса АЧС и методом иммунохимического окрашивания клеток линии CV-1 и ППК-66б, инфицированных вирусом АЧС.
Клонирование антителопродуцирующих гибридом проводили методом лимитирующих разведений по стандартной методике в 96-луночных культуральных планшетах на слое фидерных перитонеальных макрофагов, начиная с 7-10 суток культивирования.
С целью определения стабильности полученного клона гибридом и для длительного хранения клоны криоконсервировали на среде, состоящей из 90% эмбриональной телячьей сыворотки и 10% диметилсульфоксида. Клоны гибридом хранили в сосудах Дьюара с жидким азотом (минус 196°C).
За 24 часа до замораживания клетки гибридомы пассировали с кратностью рассева 1:2. Осажденные центрифугированием (1500 об/мин, 10 мин) клетки ресуспендировали в криозащитной среде (90% ФСТ, 10% DMSO) и разливали по ампулам в концентрации 3-5 млн/мл, по 2 см3. Выдерживали час при 4°C, 24 часа при -70°C, затем переносили в жидкий азот (минус 196°С).
Быстрое размораживание клеток проводили при 37-39°С. Гибридомные клетки разводили в 10 раз ростовой средой без сыворотки эмбрионов коров, осаждали центрифугированием при 1500 об/мин 10 мин, осадок ресуспендировали в ростовой среде, содержащей 20% эмбриональной сыворотки коров, до концентрации 3-4×105 клеток/см3. Жизнеспособность восстановленных клеток устанавливали по дифференциальной окраске клеток с использованием 0,4% раствора трипанового синего, pH 7,2-7,3, которая составляла 70-80%.
Получение асцитических жидкостей, содержащих МКА. За 14 дней до введения клеток гибридомы мышей линии BALB/c предварительно обрабатывали внутрибрюшинно 2,6,10,14-тетраметилпентадеканом (Pristane, «Sigma», США) в дозе 0,3-0,5 см3/животное. Далее праймированным животным вводили в брюшную полость гибридные клетки одного клона в дозе (5-10)·106 клеток. Асцитические жидкости, содержащие МКА, получали через 7-15 дней после введения.
Характеристика продуцируемых МКА:
- мишень - основной конформационный эпитоп структурного белка vp30 вируса АЧС;
- специфичность связывания с конформационным эпитопом vp30 вируса АЧС - 100% в ТФ ИФА;
- перекрестная иммунореактивность к конформационному эпитопу рекомбинантного белка, взятого для иммунизации - 100%;
- изотип продуцируемых иммуноглобулинов - IgG1 (ИФА, тест-система «Mouse-Hybridoma-Subtyping Kit» («Sigma», США).
Пример 3. Использование МКА к p30 вируса АЧС, полученных методом иммунизации генно-инженерными конструкциями, для выявления антигенов вируса АЧС методом непрямой иммунофлуоресценции (РНИФ).
Для постановки РНИФ использовали стандартную методику. В качестве антивидового конъюгата использовали ФИТЦ-конъюгат IgG козы к IgG мыши в рабочем разведении.
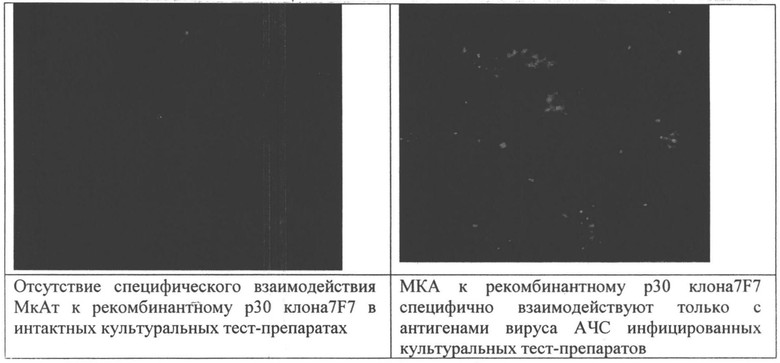
Результат реакции учитывали по уровню специфического свечения в отраженном синем свете на люминесцентном микроскопе при увеличении 1×90. МКА к рекомбинантному p30 клонов 1С2, 7F7, 2В7 и 5D11 специфично взаимодействовали только с антигенами вируса АЧС инфицированных культуральных тест-препаратов, вызывая в цитоплазме инфицированных клеток характерную специфическую гранулярную флуоресценцию. Не взаимодействовали с антигенами тест-препаратов интактной культуры клеток CV-1 и препаратами вируса болезни Тешена, классической чумы свиней и болезни Ауески - отсутствие подобного свечения. Возможно незначительное присутствие фона диффузного окрашивания. Активность МкАт в РНИФ составила 1:256-1:512.
Литература
1. Andres, G. Characterization of two african swine fever virus 220-kDa proteins: a precursor of the major structural protein p150 and an oligomer of phosphoprotein p32 / G. Andres, C. Simon-Mateo, E. Vinuela // Virology. - 1993. - Vol.194. - P.284-293.
2. Neutralizing antibodies to different proteins of African swine fever virus inhibit both virus attachment and internalization / P. Gomez-Puertas, F. Rodriguez, J.M. Oviedo [et al.] // J. Virol. - 1996. - Vol.70. - P.5689-5694.
3. Mazumder S. Potency, Efficacy and Durability of DNA/DNA, DNA/Protein and Protein/Protein Based Vaccination Using gp63 Against Leishmania donovani in BALB/c Mice [text] / S. Mazumder, M. Maji, A. Das, N. Ali // PLoS ONE - 2011. - №6(2): e14644.
4. Пат. 2463343 RU 2463343 C1. Штамм клеток E.coli BL21(DE3)pLysS, клон pTT9/ASFVp30, содержащий рекомбинантную плазмиду со встройкой участка гена CP204L вируса африканской чумы свиней, кодирующего конформационный эпитоп белка p30, пригодный для изготовления диагностических препаратов / В.О. Копытов, С.Ж. Цыбанов, А.С. Казакова, Т.Э. Южук, С.А. Белянин, А.Г. Гузалова, Н.Н. Власова, Д.В. Колбасов (RU). - №2011141517/10; заявлено 13.10.2011; опубл. 10.10.2012, Бюл. №28. - 8 с.
5. Petrovsky N. Carbohydrate-based immune adjuvants [text]. / N. Petrovsky, P.D. Cooper // Expert. Rev. Vaccines. - 2011. - №10(4). - P.523-537.
6. Maurice S., Dekel M., Shoseyov O. et al. Cellulose beads bound to cellulose binding domain-fused recombinant proteins; an adjuvant system for parenteral vaccination of fish // Vaccine. - 2003. - №21. - P. 3200-3207.
7. A solid-phase enzyme linked immunosorbent assay using monoclonal antibodies, for the detection of african swine fever virus antigens and antibodies / M.I. Vidal, M. Stiene, J. Henkel, U. Bilitewski, J.V. Costa, A.G. Oliva // J. Virol. Methods. - 1997. - Vol.66, №2. - P. 211-218.
8. High level expression of the major antigenic African swine fever virus proteins p54 and p30 in baculovirus and their potencial use as diagnosis reagents / J.M. Oviedo, F. Rodriguez, P. Gomez-Puertas [et al.] // J. Virol. Methods. - 1997. - Vol.64. - P.27-35.
9. Serodiagnosis of african swine fever using the recombinant protein p30 expressed in insect larvae / M.G. Barderas, A. Wigdorovitz, F. Merelo [et al.] // J. Virol. Methods. - 2000. - Vol.89. - P.129-136.
10. Патент CN №101261272, A, 10.09.2008.
11. Патент CA №2039541, опубл. 06.10.1991.
12. Копытов, В.О. Клонирование и экспрессия генов структурных белков p30 и р72 вируса африканской чумы свиней: дис. … канд. биол. наук: 03.00.06: защищена 23.12.04 / Копытов Валерий Олегович. - Покров, 2004. - 140 с.
13. Пиря А.А., Устин А.В., Колонцов А.А., Реутова Е.Г., Макаров В.В., Митин Н.И. Получение и характеристика моноклональных антител к полипептидам АЧС // Тезисы научн. конфер. - Покров, 1991, т.3, с.494.
14. Митин Н.И., Сидоров С.И., Реутова Е.Г.
15. «Способ получения гибридом, продуцирующих моноклональные антитела к рекомбинантным белкам». Патент SU 1733470, A1.
Изобретение относится к области биотехнологиии и может быть использовано в гибридомной технологии для получения антител заданной специфичности против рекомбинантных антигенов, экспрессированных в клетках мыши. Изобретение состоит в праймировании мышей плазмидной ДНК, кодирующей ген белка, интересующего исследователя, которое обеспечивает in vivo экспрессию, процессинг, соответствующую посттрансляционную 3D конформацию и индуцирует иммунный ответ, подобный сывороточному на инфекционный агент. Синергизм праймирования ДНК-плазмидой и бустер эффекта введения рекомбинантного белка в растворимой форме обеспечивают высокую авидность CD4+ и CD8+ T-клеток и, как следствие, аффинность и авидность полученных моноклональных антител. Повышается выход гибридом продуцирующих МКА к искомому антигену и уменьшается время получения доноров иммунных лимфоцитов и линий гибридом, продуцирующих специфические МКА. Применение метода ДНК-иммунизации и последующего введения рекомбинантного белка расширяет арсенал способов получения гибридом, продуцирующих специфические МКА к различным антигенам. Способ апробирован при получении моноклональных антител к эпитопам фосфопрротеина vp30 вируса африканской чумы свиней Полученные таким образом моноклональные антитела способны распознавать антигеные детеминанты фосфопрротеина vp30 вируса африканской чумы свиней с перекрестной иммунореактивностью к рекомбинантному белку, продуцируемому в E.coli клоном PTT9/ASFVp30/2. 2 ил., 2 табл., 3 пр.
Способ получения гибридом, продуцирующих моноклональные антитела к структурному белку p30 вируса африканской чумы свиней, включающий иммунизацию мышей и получение клонов гибридом, отличающийся тем, что для праймирования иммунной системы реципиента используют плазмидную ДНК, несущую ген целевого белка с последующим усилением иммунного ответа введением соответствующего рекомбинантного белка.
| Способ получения гибридом, продуцирующих моноклональные антитела к рекомбинантным белкам | 1989 |
|
SU1733470A1 |
| ШТАММ КЛЕТОК E.coli BL21(DE3)pLysS, КЛОН pTT9/ASFVp30, СОДЕРЖАЩИЙ РЕКОМБИНАНТНУЮ ПЛАЗМИДУ СО ВСТРОЙКОЙ УЧАСТКА ГЕНА СР204L ВИРУСА АФРИКАНСКОЙ ЧУМЫ СВИНЕЙ, КОДИРУЮЩЕГО КОНФОРМАЦИОННЫЙ ЭПИТОП БЕЛКА p30, ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2011 |
|
RU2463343C1 |
| GOMEZ-PUERTAS P | |||
| et al., "The African swine fever virus proteins p54 and p30 are involved in two distinct steps of virus attachment and both contribute to the antibody-mediated protective immune response", Virology | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| NEILAN G.G | |||
| et al., "Neutralizing antibodies to | |||
Авторы
Даты
2014-11-27—Публикация
2013-09-02—Подача