Область изобретения
Изобретение относится к области химии полициклических конденсированных гетероциклических соединений, более конкретно к области химии производных азепина, в которых азепиновый цикл конденсирован с тремя 1,2,5-оксадиазольными циклами, а именно к способу синтеза 7R-замещенных производных 7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]-азепина (1). Предлагаемые соединения могут найти применение в качестве компонентов взрывчатых составов, твердых ракетных топлив и в энергоемких составоах различного назначения, эксплуатируемых при повышенных температурах. Также соединения (1) путем известных в органической химии типичных трансформаций функциональных групп, входящих в состав 7R заместителей боковой цепи, могут служить полупродуктами для синтеза ряда прочих производных 7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина и могут найти применение в органическом синтезе.
Описание известного уровня техники
Известно значительное число конденсированных с различными гетероциклическими системами производных азепина, однако из возможных четырех типов сочленения 1,2,5-оксадиазольного и азепинового циклов описаны только немногочисленные производные 1,2,5-оксадиазоло[3,4-с]азепина [А.Б. Шереметев. Усп. химии, 1999, 68 (2), 154-166]. Взаимодействием β-дикарбонильных соединений с 3,4-диаминофуразаном получен ряд производных 4H-фуразано[3,4-b][1,4]диазепина [A. Gasco, G. Rua, E. Menziani, G.М. Nano, G. Tappi. J. Heterocycl. Chem., 7 (1), p.131-133, 1970]. Информация о синтезе азепиновых гетероциклических систем, содержащих несколько аннелированных с азепиновым циклом 1,2,5-оксадиазольных цикла, в настоящее время отсутствует.
С точки зрения специалиста в области создания перспективных энергоемких соединений производные 1,2,5-оксидиазола представляют явный интерес [J.P. Agraval, R.D. Hodgson. Organic Chemistry of Explosives, John Wiley & Sons Ltd, Chippenham, Wiltshire 2006, p.297-302], обусловленный не только связанной с ароматическим характером рассматриваемой гетероциклической системы повышенной термической устойчивостью, но и наличием в ее структуре атома «активного кислорода», который не связан с атомами углерода или водорода, а следовательно, способен к их окислению с высвобождением энергии [см., например, Philip F. Pagoria, Gregory S. Lee, Alexander R. Mitchell, Robert D. Schmidt. - A review of energetic materials synthesis // Thermochimica Acta, 384, 187-204 (2002)]. Также было показано, что замена нитрогруппы на фуразановое кольцо приводит к увеличению плотности энергоемкого соединения на 0,06-0,08 г·см-3 и к увеличению в свою очередь скорости детонации на 300 м·с-1 [Sheremetev А.В., Kulagina V.O., Batog L.V., Lebedev O.V., Yudin I.L., Pivina T.S., Andrianov V.G., Starchenkov I.B. Furazan derivatives: high energetic materials from diaminofurazan // Proc. 22th International Pyrotechnics Seminar, Fort Collins, Colorado, USA, 15-19 July, 1996, p.377-388; Ou Y.X. Synthesing Chemistry of Modern Explosivives, Weapon Industry Publishing, Beijing, 1998, p.192]. Использование в химическом дизайне новых высокоэнергетических соединений конденсированных гетероциклических систем приводит к прогнозируемому увеличению их плотности [Котомин А.А., Козлов А.С. Метод расчета плотности органических соединений по вкладам фрагментов молекул // Журнал прикладной химии, 79 (6), 966-977 (2009)] и, следовательно, к увеличению их мощности.
Ближайшими структурными аналогами простейшего представителя предлагаемых в настоящей публикации четырехядерных конденсированных гетероциклических систем - 7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]-азепина являются следующие производные 1,2,5-оксадиазола:
- производные 7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]оксепин-1-оксида (представляет собой аналог указанного выше соединения, отличающийся от последнего заменой азепинового цикла на оксепиновый, а также наличием N-оксидной группы при центральном 1,2,5-оксадиазольном цикле) [Zhou Y., Wang В., Wang X., Zhou С., Huo Н., Zhang Y. Synthesis of Bifurazano[3,4-b:3′,4-f]furoxano[3″,4″-d]oxacyclohetpatriene // Chinese Journal of Energetic Materials (CJEM), 20 (1), 137-138 (2012); Zhou Yan-shui, Wang Bo-zhou, Wang Xi-jie, Zhou Cheng, Ning Yan-li, Lian Peng, Li Jian-kang, Zhang Ye-gao. Synthesis and Quantum Chemistry Study of Novel Bifurazano [3,4-b□3′,4′-f]furoxano[3″,4″-d]oxacyclo-hetpatriene // Chinese Journal of Synthetic Chemistry, 20 (2), 147-152 (2012)], для которого заявлены следующие энергетические характеристики: Тпл. 93,5°C; ρ 1,866 г/см3 (·H2O); VD 8256 м/с (1,850); Qвзp. 6162 Дж/г (1,870); ΔH0 f+275,2 кДж/моль; чувствительность к механическим воздействиям: к удару 12% (10 кг, 25 см); к трению 4600 кг/см2; 0% (3,92 МПа, 90°);
- 3,4-бис(4-аминофуразан-3-ил)фуроксан (представляет собой аналог указанного выше соединения линейного строения, отличающийся от последнего отсутствием сочленения двух боковых 1,2,5-оксадиазольных циклов мостиковой аминогруппой, а также наличием N-оксидной группы при центральном из 1,2,5-оксадиазольном цикле) [Wang J., Li J., Liang Q., Huang Y., Dong, H. A Novel Insensitive High Explosive 3,4-Bis(Aminofurazano)Furoxan // Propellants, Explosives, Pyrotechnics, 33, 347-352 (2008)], для которого заявлены следующие энергетические характеристики: Тпл 168,2°C; ρ 1,794 г/см3; VD 8100 м/с; Qвзр. 6162 Дж/г; чувствительность к механическим воздействиям: к удару 24% (10 кг, 25 см); к трению 4300 кг/см2; 8% (3,92 МПа, 90°), рассматриваются для использования в качестве мощных термостойких энергоемких соединений с температурами начала интенсивного разложения 280°C и 230°C, соответственно.
Сущность изобретения
Предложены гетероциклические соединения - производные 7R-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина общей формулы (1)
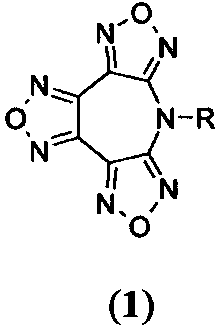 ,
,
где R представляет собой H, NH2 группу, алкильный заместитель: метил, замещенный алкильный заместитель: 2-гидроксиэтил, бензил, фурфурил, тетрагидрофурфурил, гомовератрил.
Предложен способ получения производных 7R-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина формулы (1) путем взаимодействия 3,4-бис(4-нитрофуразан-3-ил)фуразана с соединением, выбранным из группы: аммиак, гидразин, соединение, содержащее первичную аминогруппу: метиламин, 2-гидроксиэтиламин, бензиламин, фурфуриламин, тетрагидрофурфуриламин, гомовератриламин.
3,4-Бис(4-нитрофуразан-3-ил)фуразан (2) легко вступает в реакции нуклеофильного замещения нитрогрупп на N- и O-содержащие нуклеофильные агенты.
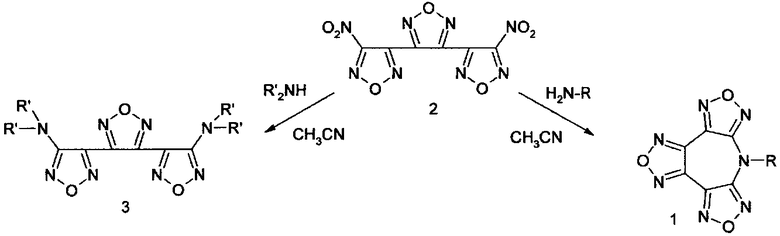
Результат реакции (2) с соединениями, содержащими аминогруппу, зависит от строения используемого амина. В случае использования вторичных аминов (диметиламина, диэтиламина, морфолина, пиперидина, 4-метилпиперазина и т.п.) образуются дизамещенные производные тримера фуразана, описываемые структурной формулой (3). Реакция (2) с первичными аминами, аммиаком и гидразином приводит к формированию аннелированной азепиновой гетероциклической системы, описываемой структурной формулой (1).
Необходимое для синтеза соединение (2) может быть получено окислением известного соединения 3,4-бис(3-аминофуразан-4-ил)-фуразана (3,4-бис(4-амино-1,2,5-оксадиазол-3-ил)-1,2,5-оксадиазола)) [П.B. Анокина, Т.В. Романова, С.Ф. Мельникова, И.В. Целинский. - Журн. Орг. Химии, 2011, 47 (10), 1575-1575] пероксидом водорода в кислой среде согласно общему методу синтеза нитрозамещенных производных фуразана [Novikova T.S., Mel'nikova Т.М., Kharitonova O.V., Kulagina V.O., Aleksandrova N.S., Sheremetev A.V., Pivina T.S., Khmel'nitskii L.I. and Novikov S.S. - Mendeleev Commun., 1994, 4, 138-140].
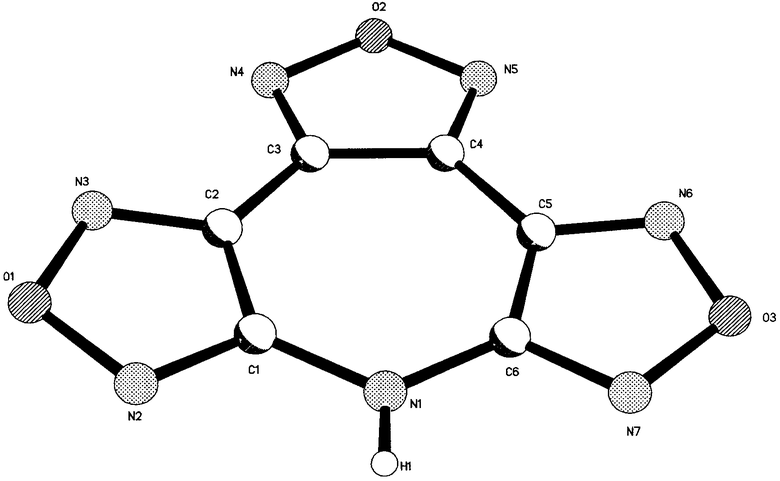
Структура предлагаемых соединений (1) доказана методами физико-химического анализа, а также рентгеноструктурным анализом соединения (1), где R=H (фиг.1).
Заявленные соединения структурной формулой (1) обладают высокой потенциальной энергоемкостью, что подтверждается следующими взрывчатыми характеристиками:
а) R=H
Тпл. 192°C; ρ 1,87 г/см3; ΔH0 f+600,0 кДж/моль; чувствительность к механическим воздействиям - к удару 0% (10 кг, 25 см), к трению 4840 кг/см2;
б)R=NH2
Тпл. 214°C; ρ 1,85 г/см3; ΔH0 f+721,9 кДж/моль; чувствительность к механическим воздействиям - удару 60% (10 кг, 25 см), трению 2500 кг/см2, и, с этой точки зрения, представляют собой высокоплотные термостойкие энергоемкие соединения с расчетными скоростями детонации VD=8200-8300 м/с.
Производные, полученные с другими заместителями, также имеют высокую температуру плавления в диапазоне от 125 до 222°C, расчетную плотность выше 1,5 г/см3, низкую чувствительность к механическим воздействиям и трению, что позволяет их рассматривать в качестве потенциальных компонентов энергетических материалов.
Специалисту в данной области техники должно быть понятным, что энергонасыщенность соединений структурной формулы (1) может быть увеличена за счет введения в боковую цепь типичных эксплозофорных групп, например нитрогрупп, нитроэфирных групп, а также азидогрупп.
Примеры конкретного исполнения
Для иллюстрации предлагаемых в изобретении методов нами были включены следующие примеры. Приведенные примеры иллюстрируют типичные синтетические приемы в лабораторной практике. В свете настоящего раскрытия предмета изобретения следует иметь в виду, что изложенные ниже примеры предназначены служить только образцами и что многочисленные изменения, модификации и внесение изменений возможно использовать без отклонения за рамки изобретения.
Пример 1
Соединение 4-бис(4-нитрофуразан-3-ил)фуразан (2) (0.01 моль, 2.96 г) растворяют в 20 мл ацетонитрила. Полученный раствор охлаждают до 5-10°C и при этой температуре прибавляют при перемешивании по каплям раствор 0.04 моль морфолина в 10 мл ацетонитрила. По окончании дозировки амина смесь нагревают до 30-40°C и перемешивают 2-3 часа. Полученный раствор выливают в 150 мл холодной воды и экстрагируют метиленхлоридом (2×25 мл). Органический слой отделяют, промывают несколько раз водой и сушат над Na2SO4. После отгонки растворителя в вакууме остаток перекристаллизовывают из CCl4. Выход 4,4″-диморфолино[3,3′,4′,3″]трис[[1,2,5]оксадиазола] (3,R',R'=морфолин) 50-70%. tпл. 87°C.
ЯМР-1Н (ДМСО-d6), δ, м.д., 3,20-3,17, t, (8H, C1, C6-N(CH2)2); 3,63-3,60, t, (8H, 2 O(CH2)2). ЯМР13C (ДМСО-d6), δ, м.д.: 159.5; 144.1; 137.2. Масс-спектр, m/z: M 376(1,6); 359(17), (M-OH); 346(4), (M-NO); 233(12); 86(44), O(CH2CH2)2N; 66(26); 56(98); 45(100). Найдено, %: C 44,83; H 4,41; N 29,54. C14H16N8O5. Вычисл., %: C 44,68; H 4,25; N 29,79.
Пример 2
Соединение (2) (2.96 г, 0.01 моль) растворяют в 20 мл ацетонитрила. Полученный раствор охлаждают до 5-10°C и при этой температуре прибавляют при перемешивании по каплям раствор не менее 0.03 моль гидразингидрата в 10 мл ацетонитрила. По окончании дозировки амина смесь нагревают до 30-40°C и перемешивают 2-3 часа. Полученный раствор разбавляют в 2-3 раза водой. Выпавший осадок отфильтровывают и перекристаллизовывают из уксусной кислоты.
Выход 7-амино-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина (1, R=NH2) 1,5 г (66%), tпл. 214°C (ДМФА-изопропанол).
ЯМР1H (ДМСО-d6), δ, м.д., 6,0 (2H, с., NH2). ЯМР13C (ДМСО-d6), δ, м.д.: 157,0; 155,8; 144,6; 136,2. Масс-спектр, m/z: [M]+ 234(100); 219(0,8), [M-NH]+; 204(26), [M-NO]+; 189(2), [M-NO-NH]+; 174(9), [M-2NO]+; 147(11), [М-2NO-HCN]+; 68(68) [C2N2O]+; 38(37), [C2N2O-NO]+. ИК- спектр, см-1: 3310 (νasNH2); 3260 (νsNH2); 1620; 1580; 1490; 1360; 1210; 1000; 990; 970; 790. Найдено, %: C 28,65; H 1,05; N 44,46. C6H2N8O3. Вычисл., %: С 28,80; Н 0,80; N 44,71.
Пример 3
Соединение (2) (2.96 г, 0.01 моль) растворяют в 20 мл ацетонитрила. Полученный раствор охлаждают до 5-10°C и при этой температуре прибавляют при перемешивании по каплям 3 мл (0.04 моль) 28%-го водного раствора аммиака. По окончании дозировки амина смесь перемешивают 2-3 часа. Полученный раствор разбавляют в 2-3 раза водой и отгоняют ацетонитрил в вакууме. Выпавший осадок отфильтровывают и перекристаллизовывают из уксусной кислоты.
Выход 7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина (1, R=Н) 1,3 г (60%), tпл. 192°C (H2O).
ЯМР1Н (ДМСО-d6), δ, м.д., 12,4 (с, NH). ЯМР13С (ДМСО-d6), δ, м.д.: 152,8; 144,9; 137,7. Масс-спектр, m/z: [M] 219(100); 189(56), [М-NO]+; 159(7), [М-2NO]+; 129(0,5), [M-3NO]+; 121(18); 69(37); 53(35), [C2HN2]+, 41(53), [HNCN]+. ИК спектр, см-1: 3300, 3190, 3080, 2940, 2760 (ассоц. NH); 1620, 1600, 1500, 1470 (фуразан); 1340; 1270; 1000; 970; 900; 870. Найдено, %: C 32,61; H 0,65; N 44,51. C6H1N7O3. Вычисл., %: С 32,88; H 0,46; N 44,75.
Пример 4
Соединение (2) (2.96 г, 0.01 моль) растворяют в 20 мл ацетонитрила. Полученный раствор охлаждают до 5-10°C и при этой температуре прибавляют при перемешивании по каплям 3.5 мл (0.04 моль) 40%-го водного раствора метиламина. По окончании дозировки амина смесь перемешивают 2-3 часа. Полученный раствор разбавляют в 2-3 раза водой и отгоняют ацетонитрил в вакууме. Выпавший осадок отфильтровывают и перекристаллизовывают из уксусной кислоты.
Выход 7-метил-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина (1, R=CH3) 1,5 г (65%), tпл. 161°C (EtOH-ДМФА).
ЯМР1Н (ДМСО-d6), δ, м.д., 3,72 (с., CH3). ЯМР13C (ДМСО-d6), δ, м.д.: 150,7; 144,5; 139,5; 22,9 (CH3). Масс-спектр, m/z: [М] 233(100); 203(25), [М-NO]+; 173(1), [M-2NO]+; 143(2,5), [M-3NO]+; 83(28); 67(30). ИК-спектр, см-1: 3430; 1590; 1550; 1500; 1420; 1200; 1000; 980; 900; 880. Найдено, %: C 35,95; H 1,34; N 41,88. C7H3N7O3. Вычисл. %: C 36,05; H 1,29; N 42,06.
Пример 5
Соединение (2) (0.01 моль, 2.96 г) растворяют в 20 мл ацетонитрила. Полученный раствор охлаждают до 5-10°C и при этой температуре прибавляют при перемешивании по каплям 0,03 моль бензиламина. По окончании дозировки амина смесь нагревают до 30-40°C и перемешивают 2-3 часа. Полученный раствор разбавляют в 2-3 раза водой и отгоняют большую часть ацетонитрила под уменьшенным давлением. Выпавший осадок отфильтровывают и перекристаллизовывают из смеси этанол-уксусная кислота 1:1 по объему.
Выход 7-бензил-7-H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина, (1, R=CH2Ph), 2,3 г (75%), tпл. 144°C (EtOH-ДМФА).
ЯМР-1H (ДМСО-d6), δ, м.д., 7,53-7,51 и 7,38-7,27m (5H, C6H5); 5,41s (2H, CH2). ЯМР13С (ДМСО-d6), δ, м.д., атомы фуразановых циклов: 154.4; 144.5; 137.1; Ar: 134.4(C1′); 128.9(C3′); 128.2(C4′); 127.6(C2′); 55.16(CH2). Масс-спектр, m/z: [M] 309(6); 91(100), [PhCH2]+; 65(26). ИК спектр, см-1: 3070; 3020 (Ar-H); 2990; 2920 (CH2); 1630 (N→O); 1600; 1590; 1570; 1520; 1480; 1430; 1370; 1220; 1160; 1000; 980; 900; 600. Найдено, %: C 50,27; H 2,48; N 31,53. C13H7N7O3. Вычисл., %: C 50,48; H 2,26; N 31,71.
Пример 6
Синтез проведен аналогично Примеру 5, но второй компонент 2-амино-этанол(2-гидроксиэтиламин) (0,03 моль).
Выход 7-(2-гидроксиэтил)-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина, (1, R=CH2CH2OH), 1,8 г (69%), tпл. 139°C (МеОН).
ЯМР-1H (ДМСО-d6), δ, м.д., 6.66 (s, 1H, OH); 4.86 (m, 2H, т., Het-CH2); 4.72 (m, 2H, CH2). ЯМР13C (ДМСО-d6), δ, м.д., сигналы атомов углерода гетероциклической системы: 154.4; 144.5; 137.1; заместитель: 58.91; 50.01. Масс-спектр, m/z: [M] 263(3); 246(5), M-OH; 232(6), M-NO-H; 68(5); 55(7); 54(7); 53(6); 45(7), [CH2CH2OH]+; 44(19), [CH2CH2O]+; 43(13); 42(7); 41(5); 31(6); 30(100); 29(8). ИК- спектр, см-1: 3550 (OH); 2980 (νasCH2); 2920 ((νsCH2); 1610; 1590; 1570; 1520; 1480; 1350; 1200; 1160; 1070 (νasC-C-O); 1020; 980; 970; 900; 840. Найдено, %: C 36,08; H 2,92; N 37,04. C8H5N7O4. Вычисл., %: C 36,50; H 2,6; N 37,26.
Пример 7
Синтез проведен аналогично Примеру 5, но второй компонент - фурфуриламин.
Выход 7-фурфурил-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]-азепина, (1, R=CH3C4H3O), 1,1 г (35%), tпл. 125-126°C (этанол), реакция протекает с образованием смол, продукт дополнительно осветляли углем.
ЯМР-1H (ДМСО-d6), δ, м.д., 7.68 (m, 1H, C4′H); 6.61 (m, 1H, C3′H); 6.47 (m, 1H, C4′H), 5.39 (s, 2H, CH2). ЯМР13C (ДМСО-d6), δ, м.д.: 154.1; 144.8; 137.3 (атомы гетероциклической системы); 148.0 (C5′); 111.1 (C3′); 111.0 (C4′); 48.00 (CH2)) (атомы бокового заместителя). Масс-спектр, m/z: 299(0.5)[M]+; 82(6); 81(100)[C4H3OCH2]+; 53(35)[C2HN2]+; 52(7); 51(8); 39(6); 32(16); 30(32).
Пример 8
Синтез проведен аналогично Примеру 5, но второй компонент - тетрагидрофурфуриламин (0,03 моль).
Выход 7-(тетрагидрофуран-2-ил-метил)-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина, (1, R=CH2C4H7O, тетрагидрофурфурил), 1,9 г (65%), очень вязкое масло, температура стеклования минус 20°C.
ЯМР-1H (ДМСО-d6), δ, м.д., 4.45 (m, 1H, C2′H); 4.38-4.31, 4.21-4.16 (m, 2xH, С5′H); 3.85, 3.70 (m, 2H, N-CH2); 2.07-1.95 (2H), 1.91-1.88 (1H), 1.80-1.76 (m, 2:1:1H, C3′-H, C4′H). Масс-спектр, m/z: 303(1.00) [M]+; 71(100) [C4H7O]+; 43(57) [CH2CHO]+; 41(30) [CH2CH=CH2]+; 39(11) [CH2C≡CH]+; 32(11); 30(39) [NO]+; 29(20) [CHO]+.
Пример 9
Синтез проведен аналогично Примеру 5, но второй компонент - гомовератриламин (0,03 моль).
Выход 7-(2-(3,4-диметоксифенил)-этил)-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3″,4″-f]азепина, (1, R=CH2C6H3(2,4-OCH3)2, гомовератрил), 2,5 г (60%), tпл. 221-222°C (этанол).
ЯМР-1H (ДМСО-d6), δ, м.д., Ar: 6.94 (s, 1H, C2′H+d, J9Hz, 0.5H, C5′H); 6.92 d, J9Hz, 0.5H, C5′H), 6.89, 6.87 (d, 1H, J9Hz, C6′H); 4.31 (t, 2H, J8Hz, NCH2); 3.03 (t, 2H, J8Hz, ArCH2); 3.79, 3.74 (2s, 6H, 2OCH3). Масс-спектр, m/z: 384(3.8)[M+1]+; 383(20.02)[M]+; 164(30); 152(11); 151(100) [CH2C6H3(OCH3)2]+; 107(9); 91(7); 78(6); 77(9); 65(6); 32(21); 30(19).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 4Н-БИС[1,2,5]ОКСАДИАЗОЛО[3,4-b:3',4'-f]АЗЕПИН-8,9-ДИАМИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2499799C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3, 4-БИС(3-АМИНОФУРАЗАН-4-ИЛ)-ФУРАЗАНА И ЕГО N, N'-ДИАЦИЛЬНЫХ ПРОИЗВОДНЫХ | 2012 |
|
RU2489428C1 |
| Способ получения дибензо[f,h]фуразано[3,4-b]хиноксалина и его замещенных производных, обладающих зарядотранспортными полупроводниковыми свойствами | 2019 |
|
RU2723014C1 |
| Производные 3-(5-нитратометил-1Н-1,2,3-триазол-1-ил)-4-нитро-1,2,5-оксадиазола и способ их получения | 2023 |
|
RU2817968C1 |
| 3-(4-Нитратометил-1Н-1,2,3-триазол-1-ил)-4-нитро-1,2,5-оксадиазол и способ его получения | 2023 |
|
RU2813466C1 |
| 3,4-БИС(4-НИТРОФУРАЗАН-3-ИЛ)-ФУРАЗАН | 2012 |
|
RU2496779C1 |
| ПРОИЗВОДНЫЕ ТЕТРАФУРАЗАНО[3,4-b:3',4'-f:3",4"-j:3'",4'"-N][1,4,5,8,9,12,13,16]ОКТААЗАБ ИЦИКЛО[14.2.2]ЭЙКОЗА-4,8,12-ТРИЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2000 |
|
RU2167161C1 |
| 3-(ТРИНИТРОМЕТИЛ-ONN-АЗОКСИ)-4-НИТРАМИНОФУРАЗАНЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2485108C1 |
| НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ BRD4 | 2016 |
|
RU2721120C2 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДРАЗОНОВ 4-R-1,2,5-ОКСАДИАЗОЛ-3-КАРБОНОВОЙ КИСЛОТЫ | 2014 |
|
RU2557659C1 |
Изобретение относится к области химии полициклических конденсированных гетероциклических соединений, более конкретно к 7R-замещенным производным трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3′′,4′′-f]-азепина общей формулы (1), где R - H, NH2 группа, алкильный заместитель: метил, замещенный алкильный заместитель: 2-гидроксиэтил, бензил, фурфурил, тетрагидрофурфурил, гомовератрил. Соединения получают путем взаимодействия с 3,4-бис(4-нитрофуразан-3-ил)фуразана с соединением, соответственно выбранным из группы: аммиак, гидразин, соединение, содержащее первичную аминогруппу: метиламин, 2-гидроксиэтиламин, бензиламин, фурфуриламин, тетрагидрофурфуриламин, гомовератриламин. Технический результат - 7R-замещенные производные трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3′′,4′′-f]-азепина, пригодные в качестве компонента взрывчатых составов, твердых ракетных топлив и энергоемких составов различного назначения, эксплуатируемых при повышенных температурах. 2 н.п. ф-лы, 1 ил., 9 пр.
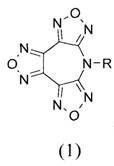
1. Гетероциклические соединения - производные 7R-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3”,4”-f]азепина общей формулы (1)
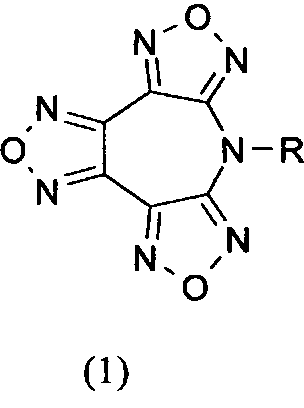 ,
,
где R - Н, NH2 группа, алкильный заместитель: метил, замещенный алкильный заместитель: 2-гидроксиэтил, бензил, фурфурил, тетрагидрофурфурил, гомовератрил.
2. Способ получения производных 7R-7H-трис[1,2,5]оксадиазоло[3,4-b:3′,4′-d:3”,4”-f]азепина общей формулы (1) по п.1, где R - Н, NH2, алкильный заместитель: метил, 2-гидроксиэтил, бензил, фурфурил, тетрагидрофурфурил, гомовератрил, путем взаимодействия 3,4-бис(4-нитрофуразан-3-ил)фуразана с соединением, соответственно выбранным из группы: аммиак, гидразин, соединение, содержащее первичную аминогруппу: метиламин, 2-гидроксиэтиламин, бензиламин, фурфуриламин, тетрагидрофурфуриламин, гомовератриламин.
| СТЕПАНОВ А.И | |||
| и др.: "Синтез линейных и циклических соединений, включающих 3,4-бис(фуразан-3-ил)фуроксановый фрагмент", Известия Академии наук | |||
| Серия химическая, 2012, N5, с.1019-1034 | |||
| ШЕРЕМЕТЬЕВ А.Б.: "Химия фуразанов, конденсированных с шести- и семичленными гетероциклами с одним гетероатомом", Успехи химии, 1999, том 68, N2, с.154-166 | |||
| ZHOU Y. |
Авторы
Даты
2014-12-10—Публикация
2013-05-31—Подача