Изобретение относится к области химии и медицины, конкретно к новому 4-изопропил-7-метокси-2a1-метил-2,2a,2a1,3,5a,9b-гексагидрофлуорено[9,1-bc]фуран-8-олу общей формулы 1 (включая его пространственные изомеры, в том числе оптически активные формы):

обладающему противоопухолевой активностью.
Химическая терапия онкологических заболеваний является одной из основных проблем современной медицины, что связано как с недостаточной эффективностью многих препаратов, так и с сопутствующими их применению побочными эффектами. Кроме того, опухолевые клетки, пережившие химиотерапию, нередко проявляют лекарственную устойчивость к широкому спектру препаратов. Таким образом, поиск лекарственных средств новых структурных типов остается важной и актуальной задачей.
Многие противораковые средства, применяющиеся в химиотерапии, являются природными соединениями, их производными или аналогами благодаря высокой активности и умеренным побочным эффектам (G.M. Cragg, P.G. Grothaus, D.J. Newman. Impact of Natural Products on Developing New Anti-Cancer Agents. Chem. Rev., 2009, 109, 3012-3043) [1], (D.G.I. Kingston. Tubulin-Interactive Natural Products as Anticancer Agents. J. Nat. Prod., 2009, 72, 507-515) [2]. Существенную проблему представляет малая доступность многих из этих соединений, как правило, являющихся минорными метаболитами растительного или животного происхождения, или их производными.
Задачей изобретения является создание нового эффективного средства, обладающего противоопухолевым действием, которое может быть синтезировано из доступных монотерпеноидов.
Поставленная задача решается 4-изопропил-7-метокси-2a1-метил-2,2a,2a1,3,5a,9b-гексагидрофлуорено[9,1-bc]фуран-8-олом общей формулы 1,

включая его пространственные изомеры, в том числе оптически активные формы.
Соединение 1 не было ранее описано в литературе, оно может быть синтезировано в соответствии со схемой 1 взаимодействием 4-гидроксиметил-2 карена 2 с изованилином в присутствии кислотного катализатора, предпочтительно монтмориллонитовой глины. Соединение 2, в свою очередь, может быть синтезировано из 3-карена, одного из основных компонентов скипидара, взаимодействием с формальдегидом и последующим омылением образующегося эфира по известной методике (G. Ohloff, H. Farnow, W. Philipp Zur Kenntnis homologer Alkohole der Terpen- und Sesquiterpenreihe X. Synthese Des (+)-3-Hydroxymethyl-Δ4-Carens. Justus Liebigs Ann. Chem., 1958, 613 43-55) [3]. Таким образом, соединение 1 может быть получено в три стадии из распространенного монотерпена 3-карена с использованием доступных и недорогих реагентов.
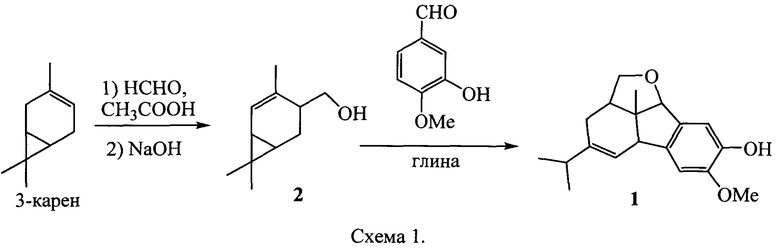
Было исследовано влияние заявляемого соединения 1 на жизнеспособность различных опухолевых клеток человека. В результате было показано, что заявляемое соединение 1 проявляет высокую противоопухолевую активность по отношению к опухолевым клеточным культурам U-937 и МТ-4.
Значения CD50 (концентрация соединений, при которой наблюдается гибель 50% клеток) составляют 50 мкМ для U-937 и 0.9 мкМ для МТ-4. Соединение 1 является умеренно токсичным по отношению к опухолевой клеточной культуре СЕМ-13, что говорит о высокой избирательности его действия.
Показано, что механизм противоопухолевого действия соединения 1 связан с индукцией апоптоза в опухолевых клетках моноцитов человека U-937 (процент клеток с апоптозом составляет 24% на 48 часов инкубации) и в опухолевых лимфоидных клетках МТ-4 (процент клеток с апоптозом составляет 49% на 72 час инкубации).
Полученные данные позволяют рассматривать это соединение как перспективное для создания лекарственных средств, применимых в клинической практике.
Изобретение иллюстрируется следующими примерами:
Пример 1. Синтез 4-изопропил-7-метокси-2al-метил-2,2a,2al,3,5a,9b-гексагидрофлуорено[9,1-bc]фуран-8-ола 1
К суспензии 0.35 г глины К10, прокаленной в течение 3 ч при 105°C, в 4 мл CH2Cl2 последовательно добавили раствор 0.120 г изованилина (3-гидрокси-4-метоксибензальдегида) в 1 мл CH2Cl2 и раствор 0.100 г 4-гидроксиметил-2 карена 2 в 1 мл CH2Cl2. Смесь перемешивали в течение 3 ч при комнатной температуре, затем добавили 2 мл этилацетата и 2 мл ацетона, катализатор отфильтровали, растворитель отогнали. Остаток делили колоночной хроматографией на силикагеле. Получили 0.075 г (41%) соединения 1.
 Спектр ЯМР 1H (CDCl3), δ, м.д.: 1.96 и 1.97 (2д, J(17, 16)=J(18, 16)=6.7 Гц, по 3H, Me(17) и Me(18)); 1.33 (с, 3H, Me(19)); (дд, J(10а, 10е)=16.5 Гц, J(10а, 1)=3.2 Гц, 1H, Ha-C(10)); 2.17 (дддд, J(10е, 10а)=16.5 Гц, J(10е, 1)=5.7 Гц, J(10е, 7)=2.6 Гц, J(10е, 8)=2.0 Гц, 1Н, Не-С(10)); 2.22 (ушир. септет, J(16, 17(18))=6.7 Гц, 1Н, Н-С(16)); 2.24 (дддд, J(1, 2)=10 Гц, J(1, 2′)=6.7 Гц, J(1, 10е)=5.7 Гц, 1Н, H-C(1)); 3.17 (ушир. дд, J(7, 8)=3.3 Гц, J(7, 10е)=2.6 Гц, 1Н, Н-С(7)); 3.19 (дд, J(2, 1)=10.0 Гц, J(2, 2′)=8.2 Гц, 1Н, Н-С(2)); 3.76 (дд, J(2′, 2)=8.2 Гц, J(2′, 1)=6.7 Гц, 1Н, Н′-C(2)); 3.88 (с, 3Н, OMe-С(14)); 4.97 (с, 1Н, Н-С(4)); 5.62 (ш.с., OH-C(13)); 5.63 (ушир. дд, J(8, 7)=3.3 Гц, J(8, 10е)=2.0 Гц, 1Н, Н-С(8)); 6.66 (с, 1Н, Н-С(12)); 6.89 (с, 1Н, Н-С(15)).
Спектр ЯМР 1H (CDCl3), δ, м.д.: 1.96 и 1.97 (2д, J(17, 16)=J(18, 16)=6.7 Гц, по 3H, Me(17) и Me(18)); 1.33 (с, 3H, Me(19)); (дд, J(10а, 10е)=16.5 Гц, J(10а, 1)=3.2 Гц, 1H, Ha-C(10)); 2.17 (дддд, J(10е, 10а)=16.5 Гц, J(10е, 1)=5.7 Гц, J(10е, 7)=2.6 Гц, J(10е, 8)=2.0 Гц, 1Н, Не-С(10)); 2.22 (ушир. септет, J(16, 17(18))=6.7 Гц, 1Н, Н-С(16)); 2.24 (дддд, J(1, 2)=10 Гц, J(1, 2′)=6.7 Гц, J(1, 10е)=5.7 Гц, 1Н, H-C(1)); 3.17 (ушир. дд, J(7, 8)=3.3 Гц, J(7, 10е)=2.6 Гц, 1Н, Н-С(7)); 3.19 (дд, J(2, 1)=10.0 Гц, J(2, 2′)=8.2 Гц, 1Н, Н-С(2)); 3.76 (дд, J(2′, 2)=8.2 Гц, J(2′, 1)=6.7 Гц, 1Н, Н′-C(2)); 3.88 (с, 3Н, OMe-С(14)); 4.97 (с, 1Н, Н-С(4)); 5.62 (ш.с., OH-C(13)); 5.63 (ушир. дд, J(8, 7)=3.3 Гц, J(8, 10е)=2.0 Гц, 1Н, Н-С(8)); 6.66 (с, 1Н, Н-С(12)); 6.89 (с, 1Н, Н-С(15)).
Спектр ЯМР 1C (CDCl2), δ, м.д: 45.38 (д, С(1)); 70.93 (т, С(2)); 94.12 (д, С(4)); 132.80 и 138.07 (2 с, С(5) и C(6)); 50.09 (д, С(7)); 120.18 (д, С(8)); 140.17 (с, С(9)); 23.28 (т, С(10)); 50.02 (с, С(11)); 105.02 (д С(12)); 145.30 (с, С(13)); 147.93 (с, С(14)); 110.86 (д, С(15)); 34.95 (д, С(16)); 20.72 и 20.90 (2к, С(17) и С(18)); 26.72 (к, С(19)); 55.89 (к, С(20)).
Пример 2.
Влияние соединения 1 на жизнеспособность опухолевых клеток Т-клеточного лейкоза человека МТ-4 Клетки линии МТ-4 (клетки Т-клеточного лейкоза человека) культивировали в среде RPMI 1640, содержащей 10%-ную эмбриональную телячью сыворотку, антибиотики (100 ед./мл пенициллина и 0.1 мг/мл стрептомицина), в атмосфере 5%-ного CO2 при 37°C.
Жизнеспособность клеток после инкубации с соединением 1 определяли с помощью МТТ теста, который основан на способности живых клеток превращать соединения на основе тетразола (МТТ) в ярко окрашенные кристаллы формазана, что позволяет спектрофотометрически оценивать количество живых клеток в препарате. Для этого клетки высаживали в 96-луночные планшеты (100 мкл клеток с концентрацией 500 тыс. клеток/мл). Затем к клеткам добавляли раствор соединения 1 в ДМСО до конечной концентрации в среде от 0.1 до 100 мкг/мл. Клетки инкубировали в присутствии соединения 1 в течение 3-х суток в тех же условиях. По окончании инкубации, без смены среды, к клеткам добавляли раствор МТТ (5 мг/мл) в фосфатно-солевом буфере до концентрации 0.5 мг/мл и инкубировали в течение 3 ч в тех же условиях. Среду удаляли, к клеткам добавляли по 100 мкл ДМСО, в котором происходит растворение образовавшихся в клетках кристаллов формазана, и измеряли оптическую плотность на многоканальном спектрофотометре на длинах волн 570 и 630 нм, где A570 - поглощение формазана, а A630 - фон клеток.
Данные представляли в виде количества живых клеток относительно контроля. За 100% принимали количество клеток в контроле, где клетки инкубировали в отсутствие соединения, но в присутствии растворителя ДМСО.
Значения CD50 - концентрация соединения 1, при которой наблюдается гибель 50% клеток, а также CD80 и CD90 (концентрации, при которых наблюдается гибель 80 и 90% клеток соответственно) приведены в таблице 1. Из этих данных видно, что обработка клеток линии МТ-4 соединением 1 вызывает 50%-ную гибель при концентрации соединения 0.9 мкМ и 80%-ную гибель при концентрации 96 мкМ.
Пример 3. Влияние соединения 1 на жизнеспособность опухолевых клеток человека U-937.
Клетки линии U-937 (опухолевая линия моноцитов человека) культивировали в среде RPMI 1640, содержащей 10%-ную эмбриональную телячью сыворотку, антибиотики (100 ед./мл пенициллина и 0.1 мг/мл стрептомицина), в атмосфере 5%-ного CO2 при 37°C.
Жизнеспособность клеток после инкубации с соединением 1 определяли с помощью МТТ теста, который основан на способности живых клеток превращать соединения на основе тетразола (МТТ) в ярко окрашенные кристаллы формазана, что позволяет спектрофотометрически оценивать количество живых клеток в препарате. Для этого клетки высаживали в 96-луночные планшеты (100 мкл клеток с концентрацией 500 тыс. клеток/мл). Затем к клеткам добавляли раствор соединения 1 в ДМСО до конечной концентрации в среде от 0.1 до 100 мкг/мл. Клетки инкубировали в присутствии соединения 1 в течение 3-х суток в тех же условиях. По окончании инкубации, без смены среды, к клеткам добавляли раствор МТТ (5 мг/мл) в фосфатно-солевом буфере до концентрации 0.5 мг/мл и инкубировали в течение 3 ч в тех же условиях. Среду удаляли, к клеткам добавляли по 100 мкл ДМСО, в котором происходит растворение образовавшихся в клетках кристаллов формазана, и измеряли оптическую плотность на многоканальном спектрофотометре на длинах волн 570 и 630 нм, где A570 - поглощение формазана, а A630 - фон клеток.
Данные представляли в виде количества живых клеток относительно контроля. За 100% принимали количество клеток в контроле, где клетки инкубировали в отсутствие соединения, но в присутствии растворителя ДМСО.
Значения CD50 - концентрация соединения 1, при которой наблюдается гибель 50% клеток, а также CD80 и CD90 (концентрации, при которых наблюдается гибель 80 и 90% клеток соответственно) приведены в таблице 2. Из этих данных видно, что обработка клеток линии U-937 соединением 1 вызывает 50%-ную гибель при концентрации соединения 0.9 мкМ.
Пример 4. Влияние соединения 1 на жизнеспособность опухолевых клеток Т-клеточного лейкоза человека СЕМ-13.
Клетки линии СЕМ-13 культивировали в среде RPMI 1640, содержащей 10%-ную эмбриональную телячью сыворотку, антибиотики (100 ед./мл пенициллина и 0.1 мг/мл стрептомицина), в атмосфере 5%-ного CO2 при 37°C.
Жизнеспособность клеток после инкубации с соединением 1 определяли с помощью МТТ теста, который основан на способности живых клеток превращать соединения на основе тетразола (МТТ) в ярко окрашенные кристаллы формазана, что позволяет спектрофотометрически оценивать количество живых клеток в препарате. Для этого клетки высаживали в 96-луночные планшеты (100 мкл клеток с концентрацией 500 тыс. клеток/мл). Затем к клеткам добавляли раствор соединения 1 в ДМСО до конечной концентрации в среде от 0.1 до 100 мкг/мл. Клетки инкубировали в присутствии соединения 1 в течение 3-х суток в тех же условиях. По окончании инкубации, без смены среды, к клеткам добавляли раствор МТТ (5 мг/мл) в фосфатно-солевом буфере до концентрации 0.5 мг/мл и инкубировали в течение 3 ч в тех же условиях. Среду удаляли, к клеткам добавляли по 100 мкл ДМСО, в котором происходит растворение образовавшихся в клетках кристаллов формазана, и измеряли оптическую плотность на многоканальном спектрофотометре на длинах волн 570 и 630 нм, где A570 - поглощение формазана, а A630 - фон клеток.
Данные представляли в виде количества живых клеток относительно контроля. За 100% принимали количество клеток в контроле, где клетки инкубировали в отсутствие соединения, но в присутствии растворителя ДМСО.
Значения CD50 - концентрация соединения 1, при которой наблюдается гибель 50% клеток, а также CD80 и CD90 (концентрации, при которых наблюдается гибель 80 и 90% клеток соответственно) приведены в таблице 3. Из этих данных видно, что обработка клеток линии СЕМ-13 соединением 1 вызывает 50%-ную гибель при концентрации соединения 93 мкМ.
Пример 5. Влияние соединения 1 на индукцию апоптоза в опухолевых клетках человека U-937.
В результате активации апоптоза происходит фрагментация ДНК за счет активации эндонуклеаз. Для определения фрагментированной ДНК клетки окрашивают красителем пропидиум йодид и затем определяют процент фрагментированной ДНК с использованием проточного цитофлюориметра.
Фиксируют клетки в суспензии в 70%-ном этаноле путем добавления 1 мл клеток, суспендированных в фосфатно-солевом буфере (ФСБ) (1-5×106 клеток), к 9 мл 70%-ного этанола в пробирке на льду. Далее клетки центрифугируют при 200 g в течение 3 мин, этанол удаляют, клетки суспендируют в 10 мл PBS и центрифугируют при 300 g в течение 5 мин. Затем клетки суспендируют в 0,5 мл PBS и инкубируют при комнатной температуре в течение 5 мин. После центрифугирования при 300 g в течение 5 мин осадок клеток суспендируют в 1 мл в растворе для окрашивания ДНК. Раствор для окрашивания ДНК готовят следующим образом: растворяют 200 мкг пропидиум йодида в 10 мл ФСБ, а затем добавляют 10 мкл Triton Х-100 и 2 мг РНКазы. Полученный раствор инкубируют 15 мин при 70°C. Для окрашивания клетки инкубируют в течение 30 мин при комнатной температуре.
Анализ клеток проводят методом проточной цитометрии на проточном цитофлюориметре Canto FACS. Для возбуждения флюоресценции используют лазер (длина волны 488 нм), измеряют флуоресценцию при длине 600 нм и светорассеяние. Производят подсчет 10000 клеток. Количество клеток, в которых наблюдается апоптоз, соответствует области SubG1. Полученные результаты приведены на рис.1 и таблице 4. Использовали концентрацию соединения 1, вызывающую гибель 50% клеток. Из этих данных видно, что обработка клеток линии U-937 приводит к индукции апоптоза через 24 часа в 13-15% клеток, а через 48 часов - в 22-25% клеток. В таблице приведены данные двух независимых экспериментов, в каждом было просчитано 10 тысяч клеток.
Пример 6. Влияние соединения 1 на индукцию апоптоза в опухолевых клетках человека МТ-4.
В результате активации апоптоза происходит фрагментация ДНК за счет активации эндонуклеаз. Для определения фрагментированной ДНК клетки окрашивают красителем пропидиум йодид и затем определяют процент фрагметированной ДНК, с использованием проточного цитофлюориметра.
Фиксируют клетки в суспензии в 70%-ном этаноле путем добавления 1 мл клеток, суспендированных в фосфатно-солевом буфере (ФСБ) (1-5×106 клеток), к 9 мл 70% этанола в пробирке на льду. Далее клетки центрифугируют при 200 g в течение 3 мин, этанол удаляют, клетки суспендируют в 10 мл PBS и центрифугируют при 300 g в течение 5 мин. Затем клетки суспендируют в 0,5 мл PBS и инкубируют при комнатной температуре в течение 5 мин. После центрифугирования при 300 g в течение 5 мин осадок клеток суспендируют в 1 мл в растворе для окрашивания ДНК. Раствор для окрашивания ДНК готовят следующим образом: растворяют 200 мкг пропидиум йодида в 10 мл ФСБ, а затем добавляют 10 мкл Triton Х-100 и 2 мг РНКазы. Полученный раствор инкубируют 15 мин при 70°C. Для окрашивания клетки инкубируют в течение 30 мин при комнатной температуре.
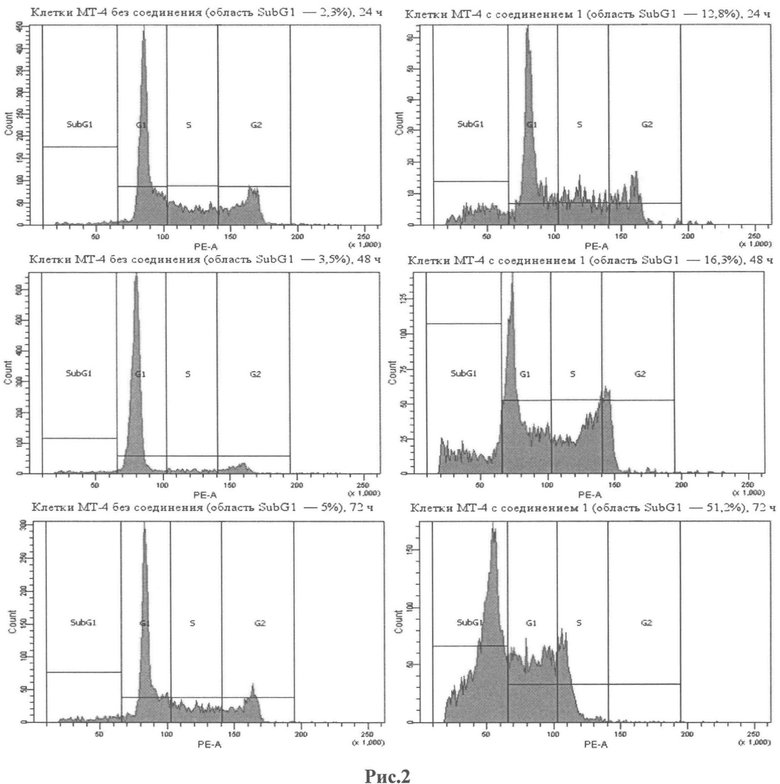
Анализ клеток проводят методом проточной цитометрии на проточном цитофлюориметре Canto FACS. Для возбуждения флюоресценции используют лазер (длина волны 488 нм), измеряют флуоресценцию при длине 600 нм и светорассеяние. Производят подсчет 10000 клеток. Количество клеток, в которых наблюдается апоптоз, соответствует области SubG1. Полученные результаты приведены на рис.2 и таблице 5. Из этих данных видно, что обработка клеток линии МТ-4 приводит к индукции апоптоза через 24 часа в 7-12% клеток, через 48 часов - в 16-19% клеток, а через 72 час - в 47-51% клеток. В таблице приведены данные двух независимых экспериментов, в каждом было просчитано 10 тысяч клеток.
Источники информации
1. G.M. Cragg, P.G. Grothaus, D.J. Newman. Impact of Natural Products on Developing New Anti-Cancer Agents. Chem. Rev., 2009, 109, 3012-3043.
2. D.G.I. Kingston. Tubulin-Interactive Natural Products as Anticancer Agents. J. Nat. Prod., 2009, 72, 507-515.
3. G. Ohloff, H. Farnow, W. Philipp Zur Kenntnis homologer Alkohole der Terpen- und Sesquiterpenreihe X. Synthese Des (+)-3-Hydroxymethyl-Δ4-Carens. Justus Liebigs Ann. Chem., 1958, 613 43-55.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ УСНИНОВОЙ КИСЛОТЫ КАК ПРОТИВООПУХОЛЕВЫЕ АГЕНТЫ | 2013 |
|
RU2536873C1 |
| N-ЭТИЛПИПЕРАЗИЛАМИД БЕТУЛОНОВОЙ КИСЛОТЫ КАК ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО ТРИТЕРПЕНОВОЙ ПРИРОДЫ | 2010 |
|
RU2445317C1 |
| ГИДРИРОВАННАЯ БЕТУЛОНОВАЯ КИСЛОТА И ЕЕ АМИДЫ КАК ПРОТИВООПУХОЛЕВЫЕ СРЕДСТВА ТРИТЕРПЕНОВОЙ ПРИРОДЫ | 2010 |
|
RU2448115C1 |
| N-[3-ОКСОЛУП-20(29)-ЕН-28-ОИЛ]-2,2,6,6-ТЕТРАМЕТИЛПИПЕРИДИН-4-ИЛАМИН, ОБЛАДАЮЩИЙ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ОПУХОЛЕВЫХ КЛЕТОК ЧЕЛОВЕКА | 2017 |
|
RU2641900C1 |
| 6-ГИДРОКСИНАФТОХИНОНЫ ЛАБДАНОВОГО ТИПА, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К ОПУХОЛЕВЫМ КЛЕТКАМ ЧЕЛОВЕКА | 2012 |
|
RU2479582C1 |
| 16-(1,2,4-ОКСАДИАЗОЛ-3-ИЛ)-15,16-ЭПОКСИЛАБДАНОИДЫ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К ОПУХОЛЕВЫМ КЛЕТКАМ ЧЕЛОВЕКА | 2011 |
|
RU2473550C1 |
| N,N'-(АЛКАНДИИЛ)БИС[ЛАБДА-7(9),13,14-ТРИЕН-4-КАРБОКСАМИДЫ], ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2654201C1 |
| Лекарственное средство, обладающее противовоспалительной активностью | 2016 |
|
RU2617123C1 |
| ПРОИЗВОДНЫЕ ТИАКАЛИКСАРЕНОВ КАК СРЕДСТВО ДОСТАВКИ ДНК В КЛЕТКИ | 2014 |
|
RU2551277C1 |
| ПРОИЗВОДНЫЕ АЛКИЛАММОНИЙНОГО ГЕМИНАЛЬНОГО ПОВЕРХНОСТНО-АКТИВНОГО ВЕЩЕСТВА, ОБЕСПЕЧИВАЮЩИЕ ЭФФЕКТИВНУЮ ДОСТАВКУ ДНК В КЛЕТКИ | 2012 |
|
RU2513726C2 |

Изобретение относится к новому соединению, а именно 2,2a,2al,3,5a,9b-гексагидрофлуорено[9,1-bc]фуран-8-олу формулы 1
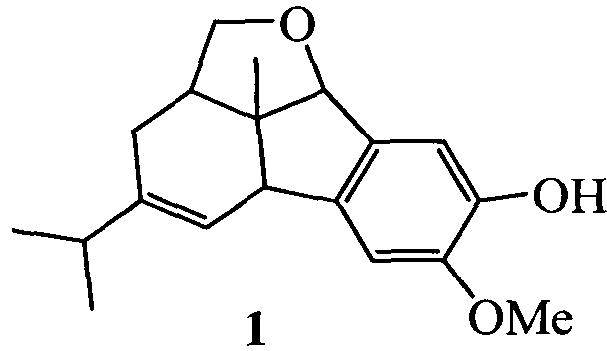 , который обладает противоопухолевой активностью. 2 ил., 5 табл., 1 пр.
, который обладает противоопухолевой активностью. 2 ил., 5 табл., 1 пр.
4-Изопропил-7-метокси-2а1-метил-2,2a,2al,3,5a,9b-гексагидрофлуорено[9,1-bc]фуран-8-ол общей формулы 1,
 , обладающий противоопухолевой активностью.
, обладающий противоопухолевой активностью.
| G.M.Cragg et al, Chem.Rev.,2009,v.109,no.7,p.1012-3043 | |||
| US 20120165556 A1 28.06.2012 | |||
| RU 2009122411 A 20.12.2010 |
Авторы
Даты
2014-12-20—Публикация
2013-09-30—Подача