Настоящее изобретение относится к способу снижения и/или удаления FXI и FXIa из растворов, содержащих указанные факторы свертывания, концентрату, содержащему FXI и FXIa, получаемому способом по изобретению, и фармацевтической композиции, содержащей FXI и FXIa, получаемой способом по изобретению.
Хорошо известно, что фактор свертывания XI (FXI) представляет собой участвующий в свертывании крови белок и отражает одну из сторон внутреннего пути системы свертывания. FXI является предшественником активированного FXI (FXIa), который представляет собой активное соединение при свертывании. Таким образом необходимо удалять FXIa из фармацевтических препаратов, предназначенных для внутривенного введения пациентам, т.к. указанный FXIa может непреднамеренно активировать свертывание, приводящее к опасным для жизни тромбическим нарушениям. С другой стороны, концентрат FXI и/или FXIa может быть благоприятным для пациентов, страдающих заболеванием, связанным с дефицитом или недостаточной активностью FXI, или для пациентов, перенесших большую потерю крови, при которой жизненно важным является быстрое и эффективное свертывание. Такой концентрат также может быть благоприятным для пациентов, имеющих ингибиторные антитела к факторам свертывания, таким как при гемофилии A и B. Такие ингибиторы могут провоцировать случаи кровотечения, таким образом, пациентам необходимы средства для поддержания свертывания и закрытия раны.
Таким образом, целью настоящего изобретения является удаление или по меньшей мере снижение FXI и/или FXIa в растворах, которые содержат FXI и/или FXIa. Другой целью настоящего изобретения является получение предоставленным способом терапевтически применимого концентрата FXI, FXIa или терапевтически применимого концентрата, содержащего смесь FXI и FXIa.
Известно несколько способов получения концентрата FXI. Bouma и Griffin опубликовали в The Journal of Biological Chemistry, 1977, vol. 252, no. 18, pp. 6432-6437 способ очистки FXI из плазмы человека хроматографией в пять этапов. Хроматографические вещества, используемые в хронологическом порядке, представляют собой DEAE-Sephadex®, QAE-Sephadex®, SP-Sephadex® (дважды) и в заключении Concanavalin A, связанный с Sepharose®. Все используемые буферы содержат Polybrene® и бензамидин.
M. Burnouf-Radosevich и T. Burnouf опубликовали в Transfusion, 1992, 32, pp. 861-867, получение лиофилизата FXI фильтрацией криосупернатантной плазмы через отрицательно заряженный фильтр (Zeta plus 50S), который адсорбирует FXI, элюированием адсорбированного FXI и хроматографией элюата на катионообменной смоле (Sulfate-Sepharose® Fast Flow). Элюат FXI формулировали с антитромбином и гепарином до лиофилизации.
Hiroshi Mashiko и Hidenobu Takahashi описали в Biol. Chem. Hoppe Seyler., 1994, vol. 375, pp. 481-484, способ получения FXI и FXIa свиньи аффинной хроматографией на основе высокомолекулярного кининогена и хроматографией на Q-Sepharose®. Для предотвращения контактной активации и решения проблемы протеолитического расщепления они добавляли Polybrene® и бензамидин к используемым буферам. Они также опубликовали, что им не удалось очистить FXI аффинной хроматографией на Heparin-Sepharose®.
В другой статье Hiroshi Mashiko и Hidenobu Takahashi в Agents and actions supplements,(Birkhaeuser Verlag, Bfse, CH), 1992, vol. 38, part 2, pp. 249-256, описали способ получения FXI и FXIa свиньи на основе хроматографии с содержащимися в буферах высокомолекулярным кининогеном, Q-Sepharose® и Protein A-Superose® с Polybrene® и бензамидином.
Tait и Fujikawa в Journal of Biological Chemistry, 1981, vol. 262, no. 24, pp. 11651-11656, описали способ очистки FXI и прекалликреина из плазмы человека хроматографией в три этапа и с использованием Polybrene® и бензамидина в буферах. Синтетический пептид, представляющий собой один участок легкой цепи высокомолекулярного кининогена, иммобилизовали на носителе и использовали для выделения прекалликреина, FXI и некоторого переноса IgG из плазмы. Затем прекалликреин и FXI разделяли хроматографией на гепарине-агарозе и в дальнейшем обрабатывали CM-Sephadex® с получением практически чистых фракций FXI и прекалликреина.
Saito et al. в The Journal of Clinical Investigation, vol. 52, pp. 850-861, 1973, описали способ очистки FXI, состоящий из адсорбции плазмы на Ca3(PO4)2, многократного фракционирования сульфата аммония и последующей хроматографии на QAE-Sephadex® (дважды), Sephadex®-G150 и SP-Sephadex® с Polyprene®, содержащимся для предотвращения активации FXI.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу снижения содержания FXI, FXIa или их смеси в растворе, содержащем указанные белки и иммуноглобулины в качестве основного компонента. Это получают адсорбцией указанных белков на адсорбирующем веществе, выбранном из силикатов (в частности диоксида кремния, перлитов, цеолитов или диатомовой земли), гидроксида алюминия (Al2(OH)3), оксигидроксида алюминия (AlO(OH)), оксида алюминия (Al2O3) или веществ, подходящих для аффинной хроматографии. Указанные подходящие для аффинной хроматографии вещества состоят из полисахаридов, например декстрана, гепарина или гепарана, связанных с веществом матрицы (например, цеолитов или полимеров, таких как акрилаты и сахариды), в частности геля, используемого для аффинной хроматографии на гепарине, такого как, например, Heparin Sepharose(TM) FF или Toyopearl AF Heparin 650 M(TM).
Содержащие источник растворы могут представлять собой любые жидкости, содержащие FXI и/или FXIa, получаемые из крови или плазмы крови, или жидкости, получаемые биотехнологическими способами. Известные, но неограничивающие примеры таких растворов представляют собой криосупернатантную плазму, промежуточные соединения способа по Коэну (например, восстановленную пасту I+II+III) и их производные, промежуточные соединения способа по Кистлер-Нитшман (например, восстановленный осадок A) и их производные или растворы, получаемые в результате экспрессии рекомбинантного белка, а также растворы, которые преимущественно состоят из других белков, где FXI или FXIa содержатся в виде примеси, что может быть в случае растворов иммуноглобулина гамма (IgG).
Способ снижения и/или удаления FXI и FXIa из растворов, содержащих указанные факторы свертывания и иммуноглобулины в качестве основного компонента, включает следующие этапы:
a) контактирование раствора, содержащего FXI и/или FXIa, с аффинным хроматографическим гелем, где гепарин или гепаран связаны с веществом матрицы;
b) обеспечение адсорбции FXI и/или FXIa и
c) выделение обедненной по FXI и/или FXIa жидкости из адсорбирующей среды.
Также возможно модифицировать этап a) таким образом, что активные центры матрицы или геля являются уже насыщенными или их насыщают антитромбином во время нагрузки матрицы или геля FXI и/или FXIa.
Адсорбцию можно проводить как статическую адсорбцию, где раствор источника смешивают с адсорбентом, перемешивают и нагруженные на адсорбент FXI и/или FXIa удаляют из супернатанта известными способами, такими как седиментация, фильтрация или центрифугирование. Альтернативный способ представляет собой помещение адсорбирующего материала в хроматографическую колонку и применение раствора источника для нагрузки адсорбента FXI и/или FXIa.
В одном из вариантов осуществления изобретения силикаты, выбранные из группы из диоксида кремния, перлитов, цеолитов или диатомовой земли, можно дополнительно использовать в качестве адсорбентов FXI и/или FXIa.
В дополнительном варианте осуществления можно использовать дополнительную адсорбционную среду, выбранную из группы из гидроксида алюминия, оксигидроксида алюминия или оксида алюминия.
Также возможно комбинировать адсорбцию, проводимую в статической режиме, например, с диатомовой землей или гидроксидом алюминия в качестве адсорбирующего вещества, с адсорбцией, проводимой на хроматографической колонке с Heparin Sepharose(TM) в качестве адсорбента.
В другом варианте осуществления изобретения одну адсорбцию на гепарине или гепаране, связанных с веществом матрицы, проводят после предварительной обработки хроматографического вещества антитромбином III.
Нагруженный адсорбент тщательно промывают промывочным буфером для предотвращения десорбции FXI и/или FXIa и получаемый промывной раствор можно добавлять к фильтрату и/или супернатанту для дополнительной обработки и для оптимизации выхода других представляющих интерес соединений, таких как иммуноглобулины, в частности IgG, в этом обедненном FXI/FXIa растворе. Обработанный Heparin Sepharose(TM) обедненный FXI/FXIa раствор, как правило, содержит менее 0,15 МЕд/мл FXI, в частности менее 0,1 МЕд/мл FXI, даже более предпочтительно от 0,00 до 0,05 МЕд/мл FXI. Выраженное в международных единицах (МЕд) содержание FXIa такого обедненного раствора, как правило, составляет менее 10 мЕд/мл FXIa, в частности менее 5 мЕд/мл FXIa, даже более предпочтительно от 0,0 до 1,0 мЕд/мл FXIa.
Дополнительную обработку обедненного по FXI/FXIa раствора можно включать в один или более этапов инактивации вирусов, где приводимые примеры представляют собой обработку растворителем/детергентом (обработку S/D), УФ-облучение, пастеризацию, инкубацию при низком pH, осаждение или нанофильтрацию каприлатами. Другие этапы включают этапы хроматографии, концентрирования для получения концентрата фармацевтически активного соединения, формулирование и наполнение, которые известны из способов получения различных белков, таких как иммуноглобулины, в частности IgG, альбумина, фибриногена, антитромбина или альфа-1-антитрипсина, и являются обязательными для получения фармацевтических композиций и зависят от продукта, который необходимо получать.
FXI и/или FXIa можно элюировать из нагруженного адсорбента, в частности, если адсорбент представляет собой аффинный хроматографический гель с гепарином или гепараном, связанным с матрицей. Элюирование FXI и/или FXIa из аффинного хроматографического геля проводят элюирующим буфером, состоящим из 0,2-1,4 M NaCl, в частности 0,25-1,0 M NaCl, даже более конкретно 0,25-0,5 M NaCl и 0,003-0,03 M фосфата, или эквивалентной ионной силы. Получаемый таким образом раствор, содержащий FXI и/или FXIa, также можно подвергать инактивации вирусов указанными выше способами и концентрировать ультрафильтрацией/диафильтрацией с получением концентрата, содержащего FXI, FXIa или оба белка. Указанный концентрат можно дополнительно формулировать с адъювантами для получения фармацевтической композиции, обеспечивающей лечение заболеваний, связанных с дефицитом или недостаточной активностью FXI или FXIa.
Неожиданно было обнаружено, что уровни FXI и FXIa элюата хроматографического геля на основе гепарина ниже предела детекции указанных белков, несмотря на то что антитромбин проходил. Ожидалось, что FXI и FXIa будут замещены антитромбином, в частности изоформой антитромбин-β, т.к. известно, что он прочно связывается с аффинными гелями на основе гепарина и гепарана. Даже более удивительным было то, что удалось избирательно элюировать FXI и FXIa из насыщенного антитромбином аффинного геля на основе гепарина элюирующими буферами с от низкой до средней ионной силой, в основном содержащими 0,2-1,4 M NaCl, или буферами эквивалентной ионной силы, в то время как антитромбин III (AT-III) необходимо элюировать буферами с высокой ионной силой, в основном содержащими более 1,5 M NaCl, в частности приблизительно 2,0 M NaCl. Это свойство позволяет даже избирательно элюировать FXI/FXIa с последующим элюированием AT-III или совместно элюировать смесь, содержащую FXI, FXIa и AT-III при элюировании буфером с достаточно высокой ионной силой также для элюирования AT-III.
Даже более удивительным было обнаружить, что добавление Polybrene® и бензамидина к буферам не является необходимым, как обычно указано в литературе известного уровня техники для предотвращения контактной активации и решения проблемы протеолитического расщепления.
Одну из целей настоящего изобретения с наиболее значительным преимуществом осуществляют путем предварительной обработки аффинных хроматографических гелей декстраном, гепарином или гепараном, связанными с матрицей вещества антитромбином III (AT-III). Предварительную обработку можно проводить до такой степени, что активные центры хроматографического вещества являются насыщенными AT-III. Этот способ является особенно эффективным, т.к. связывающая способность аффинного геля в отношении FXI и FXIa является улучшенной, а связывание других факторов свертывания предотвращено или по меньшей мере в значительной степени пространственно затрудненно. Таким образом возможно избирательно удалять FXI и FXIa из сопутствующих белков и получать раствор FXI и FXIa, не содержащий другие факторы свертывания после элюирования из аффинного геля.
Также объектом изобретения является концентрат фармацевтически активного компонента, получаемый способом по изобретению, а также получаемая, как указано выше, фармацевтическая композиция.
В концентрате фармацевтически активный компонент по изобретению или фармацевтически активный компонент фармацевтической композиции по изобретению представляет собой IgG.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способу снижения содержания FXI, FXIa или смеси обоих белков в растворе, содержащем указанные белки и иммуноглобулины в качестве активного компонента. Это получают адсорбцией указанных белков на адсорбирующем веществе, выбранном из силикатов (в частности, диатомовой земли) или подходящих для аффинной хроматографии веществ, в частности геля, используемого для аффинной хроматографии на гепарине или гепаране, такого как, например, Heparin Sepharose (TM) FF или Toyo-pearl AF Heparin 650 M(TM).
Содержащий источник раствор может представлять собой любую жидкость, содержащую FXI и/или FXIa, полученную из крови или плазмы крови или жидкости, полученные биотехнологическими способами. Известные, но неограничивающие примеры таких растворов представляют собой криосупернатантную плазму, промежуточные соединения способа по Коэну (например, восстановленную пасту I+II+III) и их производные, промежуточные соединения способа по Кистлер-Нитшман (например, восстановленный осадок A) и их производные или растворы, получаемые в результате экспрессии рекомбинантного белка, а также растворы, которые преимущественно состоят из других белков, где FXI или FXIa содержатся в виде примеси, что может быть в случае растворов иммуноглобулина гамма (IgG).
Способ снижения и/или удаления FXI и FXIa из растворов, содержащих указанные факторы свертывания и иммуноглобулины в качестве основного компонента, включает следующие этапы:
a) контактирование раствора, содержащего FXI и/или FXIa, с аффинным хроматографическим гелем, где гепарин или гепаран связаны с веществом матрицы;
b) обеспечение адсорбции FXI и/или FXIa и
c) выделение обедненной по FXI и/или FXIa жидкости из адсорбирующей среды.
Также возможно модифицировать этап a) таким образом, что активные центры матрицы или геля являются уже насыщенными или их насыщают антитромбином во время нагрузки матрицы или геля FXI и/или FXIa.
Альтернативный способ представляет собой помещение адсорбирующего вещества в хроматографическую колонку и применение раствора источника для нагрузки адсорбента FXI и/или FXIa.
Этапы a) и b) проводят, нагружая белками в буфере с электропроводностью 10-18 мС, в частности с электропроводностью 14-17 мС, хроматографическую смолу (Heparin-Sepharose™ FF). Нагруженный адсорбент тщательно промывают промывающим буфером аналогичной электропроводности для предотвращения десорбции FXI и/или FXIa и получаемый промывной раствор можно добавлять к фильтрату и/или к супернатанту для дополнительной обработки и оптимизации выхода IgG, содержащегося в фильтрате в качестве обедненного по FXI/FXIa раствора. Обработанный Heparin Sepharose™ обедненный по FXI/FXIa раствор, как правило, содержит менее 0,1 МЕд/мл FXI, даже более конкретно от 0,00 до 0,05 МЕд/мл FXI. Выраженное в международных единицах (МЕд) содержание FXIa такого обедненного раствора, как правило, составляет менее 5 мЕд/мл FXIa, даже более конкретно от 0,0 до 1,0 мЕд./мл FXIa.
Дополнительную обработку обедненного FXI/FXIa раствора можно включать в один или более этапов инактивации вирусов, где приводимые примеры представляют собой обработку растворителем/детергентом (обработку S/D), как описано в EP-A-131740, включенной посредством ссылки, УФ-облучение, пастеризацию, инкубацию при низком pH, осаждение или нанофильтрацию каприлатами. Другие этапы включают этапы хроматографии, концентрирования для получения концентрата фармацевтически активного соединения, формулирование и наполнение, которые известны из способов получения различных белков, таких как иммуноглобулины, в частности IgG, альбумина, фибриногена, антитромбина или альфа-1-антитрипсина, и являются обязательными для получения фармацевтических композиций и зависят от продукта, который необходимо получать.
FXI и/или FXIa можно элюировать из нагруженного адсорбента элюирующим буфером, состоящим из 0,36 M NaCl и 0,01M фосфата, или эквивалентной ионной силы. Получаемый таким образом раствор, содержащий FXI и/или FXIa, также можно подвергать инактивации вирусов указанными выше способами и концентрировать ультрафильтрацией/диафильтрацией с получением концентрата, содержащего FXI, FXIa или оба белка. Указанный концентрат можно дополнительно формулировать с адъювантами для получения фармацевтической композиции, обеспечивающей лечение заболеваний, связанных с дефицитом или недостаточной активностью FXI или FXIa.
ПРИМЕРЫ
Анализ активности фактора XIa
Рекомбинант фактор свертывания IX (без FIXa) активировался до FIXa содержащимся в образце FXIa. В присутствии фосфолипидов и ионов кальция FIXa образует ферментный комплекс с активированным тромбином FVIII:C, который в избытке содержится в анализируемом растворе. Затем этот ферментный комплекс активирует FX, который также содержится в анализируемом образце, до фактора Xa (FXa). Образуемое количество FXa измеримо коммерчески доступными субстратами и прямо пропорционально концентрации FXIa в образце. Количественное определение проводили посредством сравнения с калибровочной кривой.
Стоит отметить, что этот анализ показывает активности FIXa и FXa, когда образцы измеряют на ранних стадиях процесса фракционирования плазмы, такого как криосупернатантная плазма. Таким образом понятно, что для таких образцов указаны суммарные активности FXIa, FIXa и FXa с условием, что в образце содержатся FIXa и Fxa.
Пример 1
Исходное вещество обрабатывали Heparin Sepharose FF, помещенным в колонку, для обеспечения адсорбции FXI и FXIa на хроматографическом веществе. Содержащий IgG фильтрат приводили в контакт с Hyflo, т.е. диатомовой землей, центрифугировали для удаления нагруженного Hyflo, а затем содержащий IgG супернатант обрабатывали промежуточной пастой I+II+III. Восстановлением таким образом полученного промежуточного вещества было выявлено 0,02 МЕд/мл FXI и менее 1 мЕд/мл FXIa.
Пример 2
Пасту I+II+III получали аналогичным образом, как в примере 1, за исключением связывания FXI/FXIa диатомовой землей. Определением FXI и FXIa выявлено содержание 0,05 МЕд/мл FXI и 3,5 мЕд/мл FXIa.
В таблицах 1-3 представлены аналитические данные образцов до и после хроматографии, где измерения 2-5 проводили при уменьшенной нагрузке исходного материала для геля на основе гепарина по сравнению с измерением 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ СНИЖЕНИЯ И/ИЛИ УДАЛЕНИЯ FXI и FXIa ИЗ РАСТВОРОВ, СОДЕРЖАЩИХ УКАЗАННЫЕ ФАКТОРЫ СВЕРТЫВАНИЯ | 2011 |
|
RU2649363C2 |
| ПОЛУЧЕНИЕ ИММУНОГЛОБУЛИНОВ С ПОНИЖЕННЫМ СОДЕРЖАНИЕМ ТРОМБОГЕННЫХ АГЕНТОВ И ИММУНОГЛОБУЛИНОВАЯ КОМПОЗИЦИЯ | 2012 |
|
RU2627162C2 |
| ОЧИСТКА И ПРИМЕНЕНИЕ ФАКТОРА, СПОСОБСТВУЮЩЕГО ЗАЖИВЛЕНИЮ РАН | 2007 |
|
RU2520817C2 |
| АНТИТЕЛА К ФАКТОРУ XI И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2739946C2 |
| НОВЫЕ ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА К ФАКТОРУ XI С АНТИТРОМБОТИЧЕСКИМ И ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2817219C2 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ ЦЕЛЕВОГО БЕЛКА БЕЗ ПРИМЕСИ ПРИОНОВОГО БЕЛКА PrP | 2008 |
|
RU2491292C2 |
| СПОСОБ ОЧИСТКИ РАСТВОРА АЛЬФА-1-АНТИТРИПСИНА | 2004 |
|
RU2370500C2 |
| СПОСОБ ОЧИСТКИ ВИТАМИН К-ЗАВИСИМЫХ БЕЛКОВ, ТАКИХ КАК КОАГУЛЯЦИОННЫЙ ФАКТОР VII | 2011 |
|
RU2731720C2 |
| СПОСОБ ОЧИСТКИ ВИТАМИН К-ЗАВИСИМЫХ БЕЛКОВ, ТАКИХ КАК КОАГУЛЯЦИОННЫЙ ФАКТОР IX | 2011 |
|
RU2590726C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООЧИЩЕННОГО РЕКОМБИНАНТНОГО ИНГИБИТОРА С1-ЭСТЕРАЗЫ ЧЕЛОВЕКА ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ | 2020 |
|
RU2769201C2 |
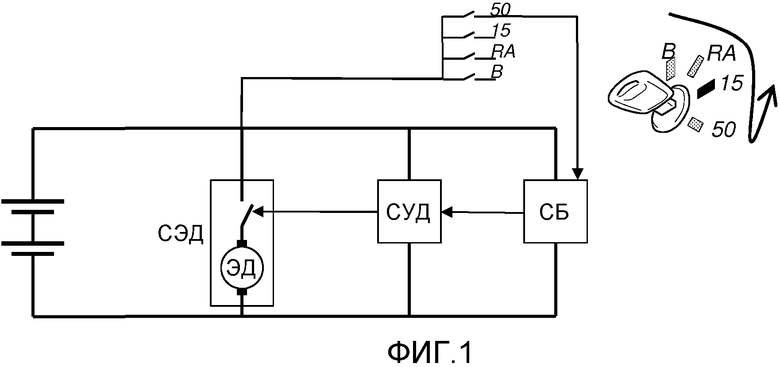
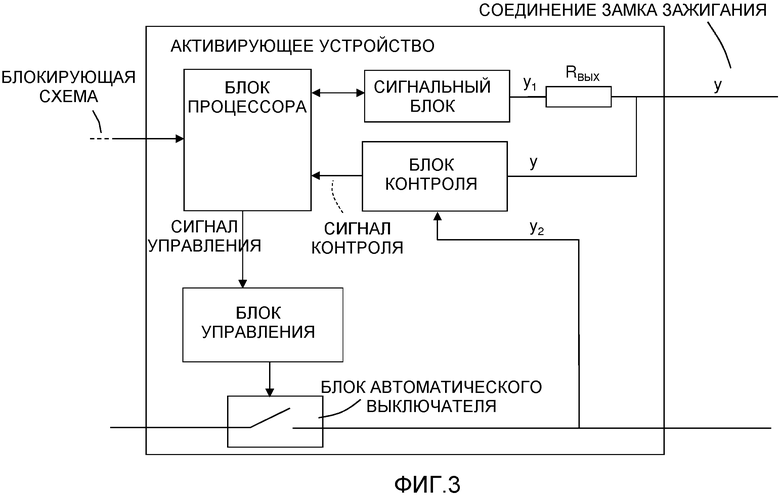
Изобретение относится к активирующему устройству с блоком автоматического выключателя для сдвоенной батарейной системы, которая содержит систему батарей питания, соединенную с электрической системой, содержащей стартерный двигатель и схему замка зажигания для транспортного средства, и систему стартерных батарей, выполненную с возможностью параллельного соединения с системой батарей питания посредством блока автоматического выключателя, который выполнен с возможностью переключения между разомкнутым состоянием и замкнутым состоянием, при этом в последнем состоянии система стартерных батарей способна питать электрическую систему энергией. Активирующее устройство содержит блок управления, сигнальный блок, выполненный с возможностью генерирования сигнала yi напряжения и передачи сигнала у напряжения в схему замка зажигания, блок контроля, выполненный с возможностью контроля сигнала у напряжения от соединения замка зажигания и с возможностью генерирования сигнала контроля на основании контролируемого сигнала у напряжения, и блок процессора, выполненный с возможностью сравнения сигнала контроля по меньшей мере с одним заранее определенным критерием детектирования и с возможностью генерирования на основе этого сравнения сигнала управления, который передается в
блок
управления. Изобретение также содержит способ активации блока автоматического выключателя в сдвоенной батарейной системе. Повышение надежности активирования устройства является техническим результатом изобретения 3 н. и 11 з.п.ф-лы, 5 ил., 3 табл.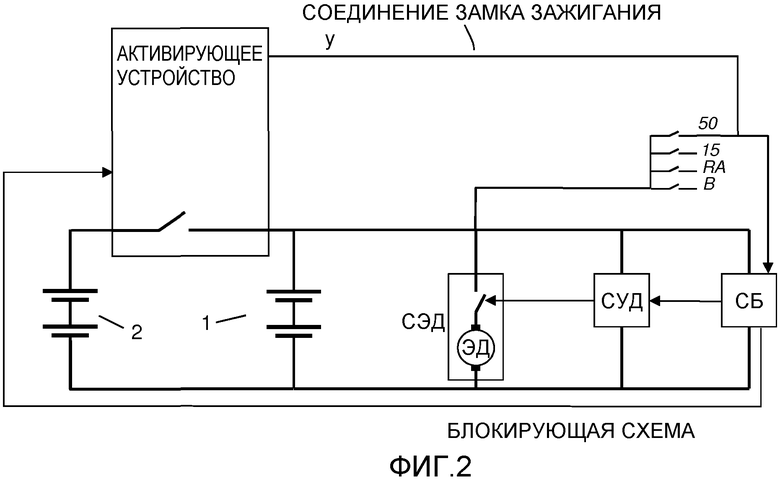
1. Активирующее устройство с блоком автоматического выключателя для сдвоенной батарейной системы, содержащей
систему батарей питания, соединенную с электрической системой, содержащей стартерный двигатель и схему замка зажигания для транспортного средства, и
систему стартерных батарей, выполненную с возможностью параллельного соединения с системой батарей питания посредством блока автоматического выключателя, который выполнен с возможностью переключения между разомкнутым состоянием и замкнутым состоянием, причем в последнем состоянии система стартерных батарей выполнена с возможностью питать электрическую систему энергией, причем активирующее устройство содержит
блок управления, выполненный с возможностью переключать автоматический выключатель между разомкнутым и замкнутым состояниями, и отличается тем, что содержит:
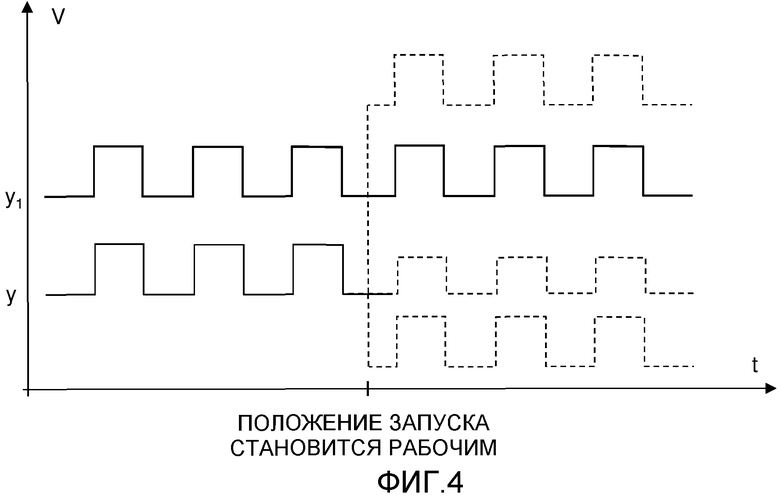
сигнальный блок, выполненный с возможностью генерировать сигнал y1 напряжения и передавать сигнал y напряжения через соединение замка зажигания в схеме замка зажигания,
блок контроля, выполненный с возможностью контролировать сигнал y напряжения от соединения замка зажигания и с возможностью генерировать сигнал контроля на основании контролируемого сигнала y напряжения, и
блок процессора, выполненный с возможностью сравнивать сигнал контроля по меньшей мере с одним заранее определенным критерием детектирования и с возможностью генерировать на основе этого сравнения сигнал управления, который передается в блок управления, выполненный с возможностью переключать блок автоматического выключателя на основе сигнала управления, причем активирующее устройство выполнено с возможностью запитываться от системы стартерных батарей.
2. Активирующее устройство по п.1, в котором критерий детектирования представляет собой сигнал контроля, отличающийся от заранее определенного значения сигнала, и если критерий детектирования удовлетворяется, то блок процессора переходит к генерированию сигнала управления для замыкания блока автоматического выключателя.
3. Активирующее устройство по пп.1 и 2, в котором сигнал y1 напряжения содержит напряжение переменного тока.
4. Активирующее устройство по п.3, в котором сигнал y напряжения имеет амплитуду между 0,1 мВ и 30% максимального напряжения системы батарей питания.
5. Активирующее устройство по п.1, в котором блок контроля выполнен с возможностью контролировать сигнал у2 напряжения от системы батарей питания, а блок процессора выполнен с возможностью сравнивать сигнал y2 напряжения с заранее определенным пороговым значением Ty2, и, если сигнал y2 напряжения больше порогового значения Ty2 или равен ему, деактивировать сигнальный блок таким образом, что первый сигнал y1 напряжения не генерируется.
6. Активирующее устройство по п.1, содержащее выходное сопротивление.
7. Активирующее устройство по п.6, в котором контроль сигнала y напряжения осуществляется где-либо на соединении замка зажигания между выходным сопротивлением и схемой замка зажигания.
8. Активирующее устройство по п.1, в котором блок управления содержит блок таймера, выполненный с возможностью измерять период времени t, в течение которого блок автоматического выключателя замкнут, и, когда время t превышает заранее определенное пороговое значение T1, переключать блок автоматического выключателя в разомкнутое состояние.
9. Способ активации блока автоматического выключателя в сдвоенной батарейной системе, содержащей систему батарей питания, соединенную с электрической системой, содержащей стартерный двигатель и схему замка зажигания для транспортного средства, и систему стартерных батарей, выполненную с возможностью параллельно соединяться с системой батарей питания посредством блока автоматического выключателя, который выполнен с возможностью автоматически переключаться между разомкнутым состоянием и замкнутым состоянием, причем в последнем состоянии система стартерных батарей выполнена с возможностью питать электрическую систему энергией, причем способ отличается тем, что содержит этапы, на которых:
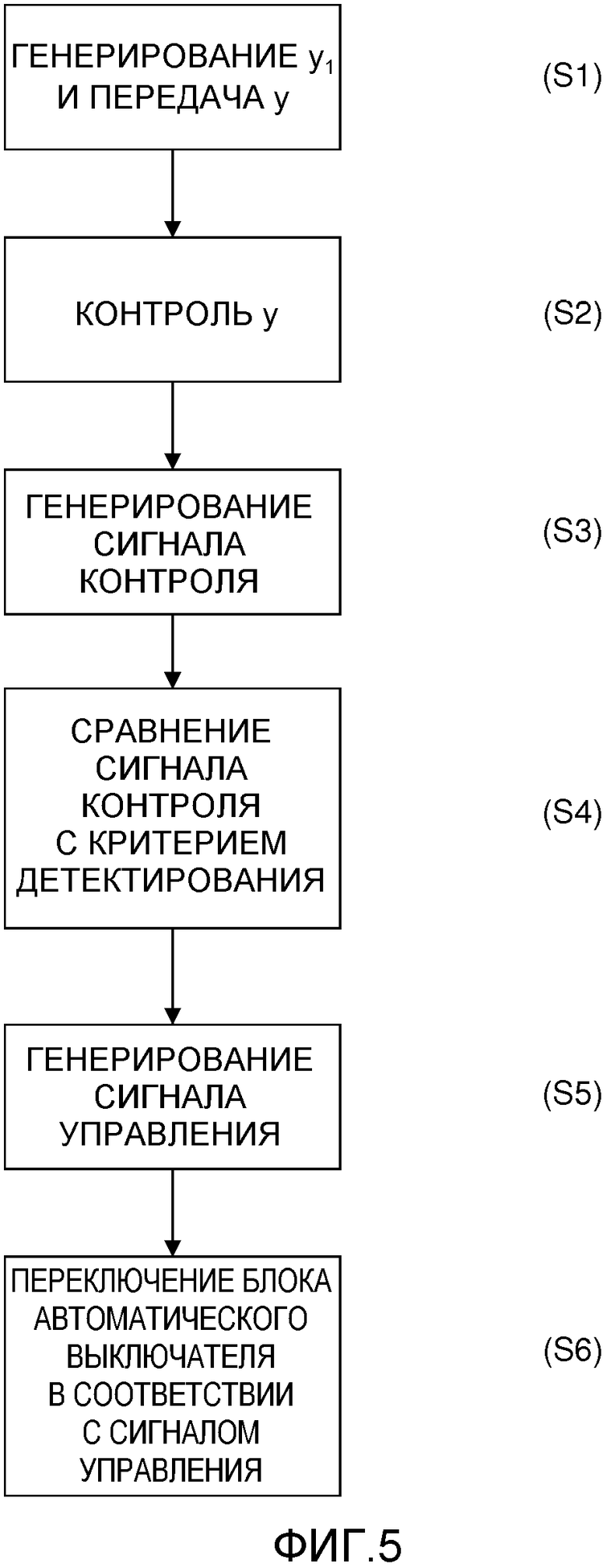
генерируют сигнал y1 напряжения и передают сигнал y напряжения через соединение замка зажигания в схеме замка зажигания;
осуществляют контроль сигнала y напряжения от соединения замка зажигания и генерирование сигнала контроля на основании контролируемого сигнала y напряжения;
сравнивают сигнал контроля по меньшей мере с одним заранее определенным критерием детектирования и генерируют сигнал управления на основе этого сравнения и
осуществляют переключение блока автоматического выключателя на основе сигнала управления.
10. Способ по п.9, в котором критерий детектирования представляет собой сигнал контроля, отличающийся от заранее определенного значения сигнала, и если критерий детектирования удовлетворяется, то блок автоматического выключателя переключают в замкнутое состояние.
11. Способ по п.9 или 10, в котором сигнал y1 напряжения содержит напряжение переменного тока.
12. Способ по п.9, содержащий этапы, на которых осуществляют контроль сигнала y2 напряжения от системы батарей питания, сравнивают этот сигнал с заранее определенным пороговым значением Ty2 и, если сигнал y2 напряжения больше порогового значения Ty2 или равен ему, деактивируют сигнальный блок таким образом, что первый сигнал y1 напряжения не генерируется.
13. Способ по п.9, содержащий этап, на котором измеряют период времени t, в течение которого блок автоматического выключателя замкнут, и переключают блок автоматического выключателя в разомкнутое состояние, когда время t превышает заранее определенное пороговое значение T1.
14. Машиночитаемый носитель, хранящий компьютерную программу с командами компьютерной программы, предписывающими компьютерной системе в транспортном средстве выполнять этапы в соответствии со способом по любому из пп.9-13, когда эти команды запущены на компьютерной системе.
| US 2006201724 A1, 14.09.2006 | |||
| US 2006097577 A1, 11.05.2006 | |||
| WO 2009099383 A1, 13.08.2009 | |||
| DE 102007016196 A1, 09.10.2008 | |||
| Система зажигания для двигателей внутреннего сгорания с электростартерным пуском | 1990 |
|
SU1821560A1 |
| . | |||
Авторы
Даты
2014-12-20—Публикация
2011-10-18—Подача