Предлагаемое изобретение относится к органической химии и медицине, а именно к смеси цис- и транс-изомеров 6-метил-1-(1-оксотиетан-3-ил)урацила, проявляющей гипотензивную активность.
Известными гипотензивным препаратами, которые широко применяются для лечения гипертензий, являются амлодипин, лизиноприл и небиволол.
Амлодипин производное дигидропиридина - антагонист кальция II поколения. Недостатками амлодипина являются отеки голеней и стоп. Вазодилатация приводит к повышению капиллярного гидростатического давления, что способствует фильтрации жидкости в ткани; процессы ауторегуляции капиллярного кровотока и дренажа лимфы являются кальцийзависимыми и поэтому ингибируются антагонистами кальция. Побочные эффекты амлодипина достаточно хорошо известны и изучены в длительных клинических исследованиях (Osterloh, 1989, 1991; Circo и сотр., 1992; Hofling и сотр., 1991; Heynen 1992). Амлодипин вызывает побочные эффекты со стороны сердечно-сосудистой системы и крови: гиперемия кожи лица, сердцебиение; редко - нарушения ритма (брадикардия, желудочковая тахикардия, трепетание предсердий), боль в грудной клетке; со стороны органов ЖКТ: запоры, тошнота, боль в животе; со стороны нервной системы и органов чувств: усталость, головная боль, головокружение, сонливость. Препарат имеет ряд ограничений к применению: нестабильная стенокардия, выраженный аортальный стеноз, сердечная недостаточность, нарушение функции печени, возраст до 18 лет (безопасность и эффективность применения не определены). Применение при беременности возможно, если ожидаемый эффект терапии превышает потенциальный риск для плода. По данным FDA амлодипин относится к категории C, то есть изучение репродукции на животных выявило неблагоприятное действие на плод, а адекватных и строго контролируемых исследований у беременных женщин не проводилось, однако потенциальная польза для беременной может оправдать его использование [Инструкция по медицинскому применению препарата «Амлодипин», Рег. номер: ЛСР-004932/07 от 17.12.2007 г.].
Лизиноприл относится к классу гипотензивных препаратов-ингибиторов АПФ. Лизиноприл обладает рядом побочных действий: со стороны сердечно-сосудистой системы: снижение АД, аритмии, боль в груди, редко - ортостатическая гипотензия, тахикардия; со стороны нервной системы: головокружение, головная боль, повышенная утомляемость, сонливость, подергивание мышц конечностей и губ, редко - астения, лабильность настроения, спутанность сознания; со стороны пищеварительной системы: тошнота, диспепсия, снижение аппетита, изменение вкуса, боль в животе, диарея, сухость во рту; со стороны органов кроветворения: лейкопения, тромбоцитопения, нейтропения, агранулоцитоз, анемия (снижение гемоглобина, эритроцитопения). Аллергические реакции: ангионевротический отек, кожные высыпания, зуд. Лабораторные показатели: гиперкалиемия, гиперурикемия; редко - повышение активности "печеночных" трансаминаз, гипербилирубинемия. Прочие: "сухой" кашель, снижение потенции; редко - острая почечная недостаточность, артралгия, миалгия, лихорадка, отек (языка, губ, конечностей), нарушение развития почек плода. В связи с побочными эффектами со стороны нервной системы необходимо с осторожностью применять лизиноприл людям, профессия которых связана с повышенной концентрацией внимания. Оценка соотношения риск-польза при применении лизиноприла необходима в следующих случаях: цереброваскулярные заболевания (в т.ч. недостаточность мозгового кровообращения), ИБС, коронарная недостаточность, коллагенозы (в т.ч. системная красная волчанка, склеродермия), угнетение костномозгового кроветворения, артериальная гипотензия, аортальный митральный стеноз или другие обструктивные изменения, затрудняющие отток крови из сердца; гиперкалиемия или высокий риск ее возникновения (сахарный диабет, выраженная почечная недостаточность, одновременное назначение диуретиков), азотемия, гипонатриемия или ограничение натрия в диете, двусторонний стеноз почечных артерий или стеноз артерии единственной почки, наличие пересаженной почки, первичный альдостеронизм, гиперурикемия, пожилой возраст, беременность [Инструкция по медицинскому применению препарата лизиноприл, Рег. номер: ЛС-000779].
Небиволол - селективный блокатор β1-адренорецепторов с сосудорасширяющим действием. Препарат обладает рядом противопоказаний: гиперчувствительность, синусовая брадикардия (менее 45-50 уд./мин), артериальная гипотензия, кардиогенный шок, синдром слабости синусного узла; AV блокада II-III степени, рефракторная к лечению тяжелая сердечная недостаточность; нарушение периферического кровообращения, синоатриальная блокада, нарушения функции печени, бронхиальная астма, бронхоспазм, беременность, кормление грудью, детский возраст. Небиволол имеет ограничение к применению при склонности к брадикардии, сахарном диабете, гиперфункции щитовидной железы, псориазе, отягощенном аллергологическом анамнезе, пожилом возрасте (старше 75 лет). Прекращать терапию небивололом рекомендуется постепенно (в течение 1-2 нед.). Урежение ЧСС до 55 уд./мин требует уменьшения дозы. На фоне сахарного диабета возможна маскировка признаков гипогликемии, при гиперфункции щитовидной железы - тахикардии. Препарат может усиливать реакции на пыльцу и другие аллергены. Небиволол следует отменить за 24 ч перед оперативным вмешательством с использованием общей анестезии (включая хирургическую стоматологию) или выбрать анестезирующее средство с наименьшим отрицательным инотропным действием. С осторожностью применять во время работы водителям транспортных средств и людям, профессия которых связана с повышенной концентрацией внимания. В двухгодичном исследовании небиволола на мышах наблюдалось статистически значимое увеличение частоты развития гиперплазии тестикулярной ткани и аденомы яичка при введении в дозе 40 мг/кг в сутки. По данным FDA небиволол относится к категории C - изучение репродукции на животных выявило неблагоприятное действие на плод. В исследованиях на крысах при введении небиволола на ранних сроках беременности в дозах 20-40 мг/кг в сутки, у детенышей наблюдалось снижение массы тела, временная задержка окостенения грудины и ребер, повышение резорбции костей. При введении небиволола кроликам в период беременности в дозе 20 мг/кг в сутки, негативных эффектов у потомства выявлено не было. Было также показано, что небиволол и его метаболиты способны проникать через гематоплацентарный барьер. При введении небиволола самкам крыс на поздних сроках беременности, во время родов и в период лактации в дозах 1,25 мг/кг и 2,5 мг/кг в сутки, у новорожденных детенышей отмечалось снижение массы тела. При введении в дозах 5 мг/кг в сутки и выше у крыс наблюдалась переношенная беременность, нарушение родовой деятельности, а также снижение заботы о потомстве, что сопровождалось повышением внутриутробной гибели плодов и мертворождением, рождением детенышей со сниженной массой тела и снижением выживаемости потомства. Оценить репродуктивную способность потомства не удалось, в связи с недостаточным количеством выживших детенышей. Небиволол и его метаболиты способны экскретироваться с грудным молоком. Однако неизвестно экскретируется ли небиволол с грудным молоком у человека. Тем не менее, учитывая потенциально возможные неблагоприятные эффекты β-блокаторов, которые могут возникнуть у новорожденного, в частности брадикардию, небиволол не рекомендован к применению у кормящих женщин [РЛС 2013 - Регистр лекарственных средств России. Энциклопедия лекарств. 21-й вып. 2013 г. Гл. ред: Г.Л. Вышковский. - М. РЛС - МЕДИА - 1612 с.].
Наиболее близким аналогом изобретения является препарат урапидил - 6-[[3-[4-(2-Метоксифенил)-1-пиперазинил]пропил]-амино]-1,3-диметил-урацил. Урапидил - антигипертензивный препарат, обладающий центральным и периферическим действием. Блокирует постсинаптические α1-адренорецепторы, благодаря чему снижается общее периферическое сосудистое сопротивление. Регулирует центральный механизм поддержания сосудистого тонуса за счет стимуляции серотониновых 5-НТ1А-рецепторов сосудодвигательного центра (предотвращает рефлекторное увеличение тонуса симпатической нервной системы). Обычно указанный препарат применяют для снижения артериального давления при гипертонических кризах [Патент US 4131678 A от 09.02.77].
Задачей изобретения является расширение арсенала биологически активных веществ, в том числе обладающих гипотензивной активностью.
Технический результат - получение биологически активного вещества с высокой гипотензивной активностью, малой токсичностью и превосходящего препараты сравнения по длительности действия.
Сущность изобретения: смесь цис- и транс-изомеров 6-метил-1-(1-оксотиетан-3-ил)урацила в мольном соотношении 10:1 общей формулы (I)
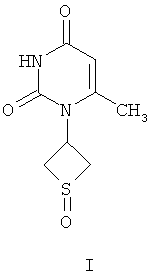
проявляющая гипотензивную активность.
Указанное соединение и его свойства в литературе не описаны.
Заявляемое соединение синтезируют следующим образом.
Взаимодействием 6-метилурацила с 2-хлорметилтиираном в присутствии гидроксида калия в воде получают 6-метил-1-(тиетан-3-ил)урацил [Катаев В.А., Мещерякова С.А., Лазарев В.В., Кузнецов В.В. // Синтез тиетанилзамещенных пиримидин-2,4(1H,3H)-дионов. - ЖорХ. - 2013. - Т.49. Вып.5. - с.760-762.], который окислением раствором перекиси водорода в среде уксусной кислоты превращают в смесь изомеров 6-метил-1-(1-оксотиетан-3-ил)урацила.
Пример 1.
Синтез заявляемого соединения.
6-Метил-1-(тиетан-3-ил)урацил 10,0 г (50 ммоль) растворяют при нагревании в 180 мл ледяной уксусной кислоты. После охлаждения к раствору добавляют 9 г (100 ммоль) 37,7%-ного раствора перекиси водорода. Через 1 ч реакционную смесь нейтрализуют концентрированным раствором аммиака до pH=7 при охлаждении льдом. Осадок отфильтровывают, сушат. Получают 7,49 г (70%) смеси цис- и транс-изомеров 6-метил-1-(1-оксотиетан-3-ил)урацила в мольном соотношении 10:1, очищают кристаллизацией из диметилформамида. Тпл.=234-235°C.
ИК спектр, ν, см-1: 2944 (N-H), 1737 (C2=O), 1639 (C4=O), 1607 (C=С), 1428 (C-N), 1089 (S=O), 706 [S(CH2)2].
Спектр ЯМР 1H (500 МГц, ДМСО-d6), δ, м.д.:
2,00 (3H, с, 6-CH3, транс); 2,01 (3H, с, 6-CH3, цис);
3,31-3,36 [2H, м, O=S(CH)2, цис]; 3,84-3,89 [2Н, м, O=S(CH)2, транс],
3,92-3,96 [2H, м, O=S(CH)2, цис], 4,16-4,21 [2H, м, O=S(CH)2, транс],
5,47 (1H, с, 5-H, транс); 5,49 с (1H, с, 5-H, цис);
5,12-5,19 (1H, м, NCH, транс); 6,18-6,22 (1H, м, NCH, цис);
11,25 (1H, уш. c, 3-NH).
Спектр ЯМР 13C (300 МГц, ДМСО-d6), δ, м.д.: 17,98 (6-CH3); 42,24 (NCH); 54,50 [S(CH2)2)]; 98,48 (C5); 150,87 (C6); 152,07 (C2); 162,37 (C4).
Количественный состав обоих изомеров определен путем сравнения интегральных интенсивностей сигналов соответствующих протонов цис-6-метил-1-(1-оксотиетан-3-ил)урацила и транс-6-метил-1-(1-оксотиетан-3-ил)урацила, подтверждающих мольное соотношение 10:1.
Элементный анализ.
Найдено, %: C 44,97; H 4,57; N 13,16 - C8H10N2O3S.
Вычислено, %: C 44,85; H 4,71; N 13,08.
Заявляемое соединение представляет собой белый с кремоватым оттенком кристаллический порошок, нерастворимый в воде, этаноле, хлороформе, диметилформамиде, растворимый в диметилсульфоксиде, растворах щелочей.
Пример 2. Изучение гипотензивного действия смеси цис- и транс-изомеров 6-метил-1-(1-оксотиетан-3-ил)урацила в мольном соотношении 10:1 (соединение Д-36) при внутривенном введении с использованием методики неинвазивного измерения артериального давления у бодрствующих крыс.
Данная методика является базисной моделью оценки гипотензивного действия исследуемых веществ (Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012. - 944 с.).
Влияние соединения Д-36 на систолическое артериальное давление (САД) и частоту сердечных сокращений (ЧСС) изучали на 2 группах бодрствующих крысах-самках, массой 280-320 г (по 6 животных в каждой группе). Исследуемое соединение растворялось в 50% растворе диметилсульфоксида (ДМСО) и вводилось в хвостовую вену в дозе 7,1 мг/кг. Контрольная группа животных получала 50% раствор ДМСО в эквивалентном объеме. Показатели САД и ЧСС регистрировали через 30, 60 и 90 минут после введения исследуемого соединения с хвоста животного при помощи прибора неинвазивного измерения артериального давления - IITC 29 (IITC Life Science Inc., США). За исходный уровень принимали значения САД и ЧСС, зафиксированные до введения исследуемых соединений. Для подготовки к неинвазивному измерению АД животные предварительно приучались к нахождению в пластиковых пеналах-держателях, для этого их в течение трех дней помещали в пеналы-держатели на 1 час для ознакомления с окружающей обстановкой. Метод измерения АД заключается в помещении животного в пенал-держатель, на хвост животного надевается манжета с интегрированным фотосенсером, в которую нагнетается воздух (на 10-15 мм рт.ст. выше предполагаемого АД) и затем медленно стравливается. Прибор автоматически фиксирует САД и ЧСС.
Установлено, что соединение Д-36 в дозе 7,1 мг/кг при внутривенном введении оказывает незначительное влияние на ЧСС и выраженное гипотензивное действие (Таблица 1).
Пример 3. Изучение зависимости «доза-гипотензивный эффект» и длительности действия соединения Д-36 с использованием препаратов сравнения при пероральном введении с помощью методики неинвазивного измерения артериального давления у бодрствующих крыс.
Влияние соединения Д-36 на систолическое артериальное давление (САД) и частоту сердечных сокращений (ЧСС) изучали на бодрствующих крысах-самках, массой 280-320 г (по 6 животных в каждой группе). Исследуемое соединение суспензировалось в 2% крахмальной слизи и вводилось перорально внутрижелудочно в дозах: 7,1 мг/кг, 14,2 мг/кг и 28,4 мг/кг. В качестве препаратов сравнения использовали небиволол (небилет, Berlin-Chemie AG, Германия) в дозе 2 мг/кг, лизиноприл (диротон, «Гедеон-Рихтер», Венгрия) в дозе 10 мг/кг и амлодипин (нормодипин, «Гедеон-Рихтер», Венгрия) в дозе 1 мг/кг. Контрольная группа животных получала 2% крахмальную слизь в эквивалентном объеме. Показатели САД и ЧСС регистрировали через час после введения исследуемого соединения с хвоста животного с интервалом в 1 час в течение 8 часов и через 24 часа. За исходный уровень принимали значения САД и ЧСС, зафиксированные до введения исследуемых соединений. Методика измерения артериального давления описана в примере 2.
Установлено, что соединение Д-36 оказывает гипотензивное действие наиболее выраженный эффект в дозе 14,2 мг/кг (Таблица 2), схожее с таковым у препаратов сравнения, но превосходит их по длительности действия.
Выполненное исследование свидетельствует о том, что соединение Д-36 обладает выраженной гипотензивной активностью. Эффект препарата наблюдается при его пероральном введении в дозе 14 мг/кг в экспериментальных исследованиях на животных. Достоинством вещества Д-36 является также и то, что оно может применяться один раз в сутки. По гипотензивной активности вещество Д-36 не уступает препаратам сравнения и превосходит их по длительности действия. Вещество Д-36 представляет интерес для дальнейшего изучения его гипотензивной активности и разработке на его основе гипотензивного препарата.
Пример 4. Изучение острой токсичности соединения Д-36.
Острую токсичность LD50 изучаемого соединения - Д-36 определяли на половозрелых мышах обоего пола массой 20-22,0 грамма по методу J. Litchfield и F. Wilcoxon в модификации В.Б. Прозоровского (Прозоровский В.Б. Использование метода наименьших квадратов для пробит-анализа кривых летальности. Фармакология и токсикология. - 1962. - №1 - с.115-119).
Изучаемое соединение предварительно суспензировали в Твин-80 и вводили однократно внутрибрюшинно и внутрижелудочно. Наблюдение за животными: - поведенческие реакции, активность, учет гибели проводили в течение 14 суток. Соединение Д-36 вводили в объеме 0,5 мл суспензии на 20,0 массы животных.
Таким образом были тестированы дозы, вводимые однократно per os и внутрибрюшинно: 1000 мг/кг массы белых мышей, 2500 мг/ кг и 4000 мг/кг массы животных, а внутрибрюшинно еще 5000 мг/кг.
При разведениях в дозах, превышающих указанные, введение взвеси соединения было затруднено. Дальнейшее повышение концентрации испытуемых соединений требовало увеличения объема вводимой суспензии, что превышало допустимые нормативы (Хабриев Р.У. (ред.) Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. Изд. II, перер., М. - 2005. - 832 с).
За время эксперимента не наблюдалось изменений в поведенческих реакциях, внешнего вида, не было симптомов интоксикации у мышей опытной группы по сравнению с животными контрольной группы.
Путь введения не оказал существенного влияния на показатели острой токсичности. Соединение при внутрибрюшном и внутрижелудочном введении отнесено к классу практически нетоксичных соединений по классификации К.К. Сидорова (Измеров Н.Ф., Саноукий И.В., Сидоров К.К. - Параметры токсикометрии промышленных ядов при однократном воздействии: Справочник., 1977).
Полученные данные свидетельствуют об отсутствии летальных исходов у животных при введении исследуемого соединения в дозах более 4000 мг/кг внутрибрюшинно и внутрижелудочно у лабораторных мышей в течение 14-30 дней.
| название | год | авторы | номер документа |
|---|---|---|---|
| (4-БРОМФЕНИЛ)ЭТИЛИДЕНГИДРАЗИД 2-[6-МЕТИЛ-1-(ТИЕТАН-3-ИЛ)УРАЦИЛ-3-ИЛ]УКСУСНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ГИПОТЕНЗИВНУЮ АКТИВНОСТЬ | 2013 |
|
RU2539301C1 |
| Способ оптимизации лечения мужчин кардиотропной терапией и заместительной гормональной терапией при андрогенодефиците с артериальной гипертензией | 2016 |
|
RU2632449C1 |
| Способ оптимизации лечения женщин кардиотропной терапией и заместительной гормональной терапией при эстрогенодефиците с артериальной гипертензией в позднем репродуктивном периоде | 2016 |
|
RU2648470C2 |
| ПРОЛОНГИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ГИПОТЕНЗИВНОГО ДЕЙСТВИЯ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 2012 |
|
RU2543637C2 |
| СПОСОБ ИНДИВИДУАЛЬНОГО ВЫБОРА ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ПРИ ТЕРАПИИ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ | 2011 |
|
RU2477974C2 |
| СПОСОБ ЛЕЧЕНИЯ ЭССЕНЦИАЛЬНОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ НА ФОНЕ ОЖИРЕНИЯ | 2013 |
|
RU2563832C2 |
| СПОСОБ КОРРЕКЦИИ БЕВАЦИЗУМАБ-ИНДУЦИРОВАННОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ НЕФИКСИРОВАННОЙ КОМБИНАЦИЕЙ ТЕЛМИСАРТАН И АМЛОДИПИН | 2024 |
|
RU2830480C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ МЕДИКО-СОЦИАЛЬНОЙ ЭФФЕКТИВНОСТИ КОМПЛЕКСНОГО ЛЕЧЕНИЯ БОЛЬНЫХ АРТЕРИАЛЬНОЙ ГИПЕРТОНИЕЙ | 2012 |
|
RU2522389C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ (ГБ) II СТАДИИ И ЕЕ ЛЕЧЕНИЯ | 2011 |
|
RU2481062C1 |
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ ПРОВЕДЕНИЯ УЛЬТРАБЫСТРОЙ ОПИОИДНОЙ ДЕТОКСИКАЦИИ | 2012 |
|
RU2524421C1 |
Предлагаемое изобретение относится к новому 6-метил-1-(1-оксотиетан-3-ил)урацилу в виде смеси цис- и транс-изомеров в мольном соотношении 10:1. Соединение проявляет гипотензивную активность и соответствует общей формуле
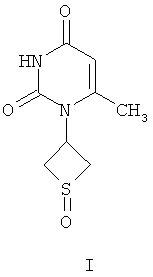
1 з.п. ф-лы, 2 табл., 4 пр.
1. Смесь цис- и транс-изомеров 6-метил-1-(1-оксотиетан-3-ил)урацила в мольном соотношении 10:1 общей формулы
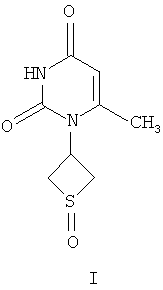
2. Соединение по п.1, проявляющее гипотензивную активность.
| 6-МЕТИЛ-1-(ТИЕТАНИЛ-3)УРАЦИЛ, СТИМУЛИРУЮЩИЙ ЗАЩИТНУЮ АКТИВНОСТЬ ФАГОЦИТОВ | 2012 |
|
RU2485118C1 |
| 5(6)-НИТРО-1-(1,1-ДИОКСОТИЕТАНИЛ-3)-2-ХЛОРБЕНЗИМИДАЗОЛ, ПРОЯВЛЯЮЩИЙ БИОЛОГИЧЕСКУЮ АКТИВНОСТЬ | 2002 |
|
RU2225401C1 |
| КАТАЕВ В.А.и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Прибор для выемки образцов подводного грунта | 1924 |
|
SU760A1 |
Авторы
Даты
2014-12-27—Публикация
2013-09-24—Подача