Изобретение относится к области биотехнологии и может быть использовано для повышения эффективности и достоверности определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях путем проведения твердофазного иммуноферментного анализа.
Из уровня техники известен способ проведения иммуноферментного анализа, включающий адсорбцию антигенов на твердой фазе физической сорбции, инкубацию тестируемых биологических образцов, инкубацию конъюгатсодержащего раствора, спектрофотометрический анализ реакции по экстинции раствора хромагента (RU 2014610 C1, G01N 33/53, 1994).
Также известен способ определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях путем проводимого в колонке тест-системы иммуноферментного анализа, включающий размещение в колонке носителя в виде слоя иммуноаффинного геля с привитыми антивидовыми антителами, зафиксированного между двумя пористыми мембранами, обработку носителя блокирующим раствором для закрытия на носителе оставшихся свободными мест неспецифического связывания, иммобилизацию на носителе специфических антител, внесение тестируемых образцов, обработку носителя конъюгатсодержащим раствором и анализ обработанного носителя на изменение окраски (RU 2374649 C1, G01N 33/53, 2009). Несмотря на достаточную простоту, точность визуального определения уровня токсикантов в данном способе недостаточно высокая.
Кроме того, известна тест-система для иммуноферментного определения токсикантов, включающая колонку, в которой установлен носитель в виде слоя иммуноаффинного геля с привитыми специфическими антителами, размещенного между двумя пористыми мембранами (RU 2374649 C1, G01N 33/53, 2009). Недостатком данного устройства является отсутствие средств, обеспечивающих измерение уровня токсикантов.
Технический результат, на получение которого направлено изобретение, заключается в повышении эффективности и достоверности иммуноферментного определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях, проводимого в колонке тест-системы.
Решение поставленной задачи с достижением заявленного технического результата обеспечивается тем, что в способе определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях путем проводимого в колонке тест-системы твердофазного иммуноферментного анализа, согласно изобретению в колонке тест-системы размещают носитель в виде зафиксированного между двумя пористыми мембранами слоя иммуноаффинного геля с привитыми - ковалентно связанными - молекулами токсиканта, производят обработку носителя - слоя геля - блокирующим раствором для закрытия на носителе оставшихся свободными мест неспецифического связывания, вносят тестируемые образцы, содержащие определенное количество предварительно введенных специфичных к токсиканту антител, производят обработку носителя конъюгатсодержащим раствором, в качестве которого используют раствор конъюгата антивидовых антител, химически связанных с люминесцентными квантовыми точками или с липосомами, содержащими люминесцентные квантовые точки, а уровень токсикантов определяют путем освещении обработанного носителя возбуждающим излучением по интенсивности люминесценции, возбужденной в квантовых точках.
При этом иммуноаффинный гель приготовляют в емкости с пористым дном путем обработки циан бром активированной сефарозы соляной кислотой и введения после набухания в полученный гель раствора антигена-токсиканта в карбонатном буфере.
Решение поставленной задачи обеспечивается также тем, что в тест-системе для способа определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях, включающей колонку, в которой установлен носитель в виде слоя иммуноаффинного геля, размещенного между двумя пористыми мембранами, согласно изобретению колонка снабжена устройством для измерения уровня люминесценции, включающим источник возбуждающего излучения и фотоприемник, причем перед фотоприемником дополнительно установлена фокусирующая оптическая система, а выход фотоприемника электрически подключен через усилитель сигнала и аналого-цифровой преобразователь к блоку управления - контроллеру, к выходу которого подключены блок индикации и через блок стабилизации источник возбуждающего излучения, при этом боковые стенки колонки выполнены из прозрачного для возбуждающего и люминесцентного излучения материала.
Кроме того, перед фокусирующей оптической системой может быть размещен светофильтр.
Благодаря наличию в растворе конъюгата люминесцентных квантовых точек (или липосом, содержащих люминесцентные квантовые точки), химически связанных с антивидовыми антителами (кроличьими антимышиными антителами), которые обладают способностью связываться со специфичными к токсиканту антителами, и при освещении возбуждающим излучением люминесцируют, в заявленном изобретении, реализующем непрямой конкурентный твердофазный иммуноферментный анализ, обеспечивается увеличение интенсивности полезного сигнала люминесценции, обратно пропорционального концентрации токсинов, что повышает чувствительность способа определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях. Кроме того, наличие в заявленной тест-системе устройства для измерения уровня люминесценции, включающего источник возбуждающего излучения и фотоприемник, которые подключены к блоку управления - контроллеру, позволяет в автоматическом режиме просто и достоверно определять уровень токсикантов по степени интенсивности люминесценции, возбужденной в квантовых точках.
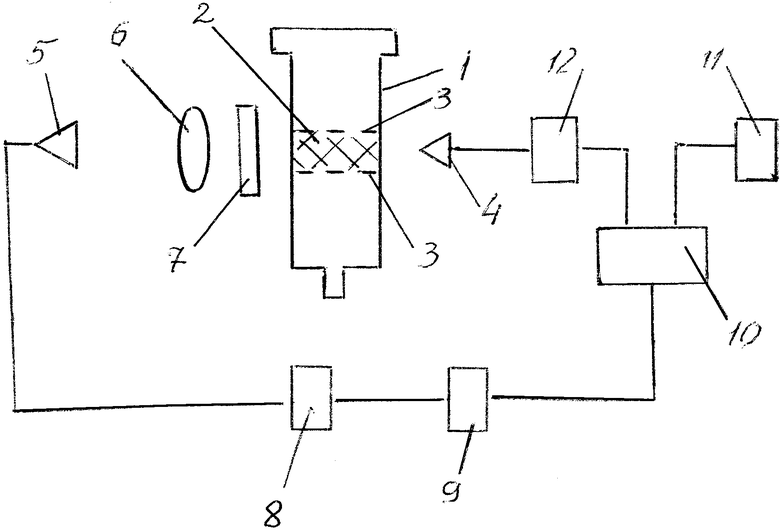
На чертеже схематично подставлен общий вид тест-системы.
Заявленная тест-система для определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях включает колонку 1 с боковыми стенками, выполненными из прозрачного для возбуждающего и люминесцентного излучения материала, в которой установлен носитель в виде слоя 2 иммуноаффинного геля с привитыми - ковалентно связанными - молекулами токсиканта-антигена, размещенного между двумя пористыми мембранами 3, и устройство для измерения уровня люминесценции, включающее источник 4 возбуждающего излучения, выполненный, например, в виде набора светодиодов с максимумами длин волн излучения в диапазоне 395÷500 нм, и фотоприемник 5 (фотодиод), спектральный диапазон чувствительности которого лежит в диапазоне 420÷675 нм, причем перед фотоприемником 5 установлена фокусирующая оптическая система 6 (например, собирающая линза F=5÷30 мм), перед которой дополнительно размещен светофильтр 7, спектр пропускания которого соответствуют спектру люминесценции. Выход фотоприемника 5 электрически подключен через усилитель 8 сигнала и аналого-цифровой преобразователь 9 к блоку 10 управления - контроллеру, к выходу которого подключены блок 11 индикации и через блок 12 стабилизации источник 4 возбуждающего излучения.
Заявленный способ определения уровня токсикантов реализуют следующим образом.
Для приготовления иммуноаффинного геля, например, 0,5 г циан бром активированной сефарозы 4В помещают в емкость с пористым дном и промывают в 100 мл 0,001 M соляной кислоты. После набухания геля раствор соляной кислоты сливают и добавляют 150 мкл раствора токсиканта-антигена с концентрацией 2,5 г/л и 450 мкл карбонатного буфера (pH 8,3), содержащего 0,1 М гидрокарбоната натрия и 0,1 M хлорида натрия, после чего смесь продолжительно встряхивают (в течение 2-х часов) при комнатной температуре. Остаток не связавшегося токсиканта-антигена удаляют с помощью промывания геля 5 мл карбонатного буфера (pH 8,3), содержащего 0,1 M гидрокарбоната натрия и 0,1 M хлорида натрия. Для закрытия оставшихся свободными мест неспецифического связывания (активных групп сефарозы) в полученный гель с привитыми - ковалентно связанными - молекулами токсиканта-антигена вносят блокирующий раствор, в качестве которого используют 0,2 M раствор глицина в карбонатном буфере (pH 8,3), содержащем 0,1 M гидрокарбоната натрия и 0,1 M хлорида натрия, и перемешивают в течение 2 часов при комнатной температуре. После процедуры блокирования гель трижды промывают последовательно пятикратным объемом ацетатного буфера (0,1 M ацетата натрия, 0,5 моль хлорида натрия, pH 4,0) и пятикратным объемом фосфатного буфера (pH 7.4÷7.6). Полученный иммуноафинный гель с привитыми - ковалентно связанными - молекулами токсиканта-антигена разводят в фосфатном буфере (pH 7.4÷7.6) в соотношении 1:3 и хранят при температуре 4°C.
Пример 1
Для определения уровня токсиканта, например концентрации зераленона, в анализируемой среде (природной воде) предварительно приготовляют - синтезируют раствор конъюгата антивидовых антител, химически связанных с люминесцентными квантовыми точками - полупроводниковые наночастицы CdSe/ZnS, следующим образом.
20 µл раствора антивидовых антител в карбонатном буфере (0,1 M гидрокарбоната натрия, 0,1 M хлорида натрия, pH 8,3) сливают с 800 µл раствора квантовых точек CdSe/ZnS (разведение 1/10 в карбонатном буфере (0,1 M гидрокарбоната натрия, 0,1 М хлорида натрия, pH 8,3), количество квантовых точек CdSe/ZnS равно 3.2×10-4 µmo1) и перемешивают в течение 12 часов при температуре 4°C.
Затем 200 мкл ранее приготовленного иммуноаффинного геля с привитыми - ковалентно связанными - молекулами токсиканта-антигена помещают в виде слоя 2 носителя на пористую полиэтиленовую мембрану 3 (фритт), установленную в пустую колонку 1 типа Bond Elut (V=1 мл), предварительно промытую фосфатным буфером (pH 7.4÷7.6) и хранившуюся при температуре 4°C. Затем сверху на слой 2 иммуноаффинного геля с привитыми - ковалентно связанными - молекулами токсиканта-антигена помещают вторую пористую полиэтиленовую мембрану 3 (фритт).
К 1 мл анализируемой среды добавляют 25 мкл раствора специфичных к токсиканту - зераленону моноклональных мышиных антител, перемешивают в течение 5 минут и пропускают через подготовленную выше указанным образом колонку 1, после чего промывают колонку 1 фосфатным буфером (рН 7.4÷7.6), содержащим 0,05% Tween 20.
Затем в колонку 1 вводят 100 мкл предварительно приготовленного раствора конъюгата антивидовых антител, химически связанных с люминесцентными квантовыми точками - полупроводниковые наночастицы CdSe/ZnS (разведение 1/30 в фосфатном буфере (pH 7.4÷7.6), содержащем 0,05% Tween 20 и 0,2% бычьего сывороточного альбумина), и инкубируют в течение 6 минут. Избыток конъюгата удаляют путем промывания колонки 1 фосфатным буфером (pH 7.4÷7.6), после чего осуществляют освещение носителя - слоя 2, содержащего люминесцентные квантовые точки - полупроводниковые наночастицы, световым потоком, поступающим от источника 4 возбуждающего излучения, и регистрируют возникший в результате возбуждающего излучения уровень люминесценция, величина которого обратно пропорциональна концентрации токсиканта - зераленона - в анализируемой среде.
При этом, если в анализируемой среде концентрация токсиканта - зераленона - превышает концентрацию специфических антител, добавленных к анализируемой пробе, которая соответствует, например, предельно допустимой концентрации токсиканта, то происходит связывание всех специфических антител с молекулами токсиканта - зераленона, а при пропускании через носитель - слой 2 - раствора конъюгата антивидовых антител с флуоресцентными метками - люминесцентными квантовыми точками - из-за отсутствия специфических антител, связанных с помощью молекул зераленона, сорбированных на носителе - слое 2, содержащиеся в конъюгате антивидовые антитела остаются несвязанными (свободными) и удаляются после промывки из колонки 1 вместе с люминесцентными квантовыми точками - полупроводниковыми наночастицами CdSe/ZnS. В результате при облучении носителя - слоя 2 - источником 4 возбуждающего излучения люминесценция не возникает.
В том случае если в анализируемой среде концентрация токсиканта - зераленона - не превышает концентрацию специфических антител, добавленных к анализируемой пробе, которая соответствует, например, предельно допустимой концентрации токсиканта, или токсикант - зераленон - в анализируемой среде отсутствует, то происходит связывание избыточных специфических антител с молекулами токсиканта - зераленона, сорбированного на носителе - слое 2 - и при пропускании через носитель - слой 2 раствора конъюгата антивидовых антител с флуоресцентными метками - люминесцентными квантовыми точками - происходит связывание специфических антител, связавшихся с молекулами зераленона, сорбированными на носителе-слое 2, с содержащимися в конъюгате антивидовыми антителами, содержащими люминесцентные квантовые точки - полупроводниковые наночастицы CdSe/ZnS. В результате при облучении носителя - слоя 2 - источником 4 возбуждающего излучения возникает люминесценция, уровень которой обратно пропорционален концентрации токсиканта - зераленона - в анализируемой среде.
При этом поступающий из носителя - слоя 2 - суммарный световой фронт, состоящий из полезного сигнала люминесценции и паразитного сигнала возбуждающего излучения, проходит через светофильтр 7, который ослабляет паразитный сигнал, и отфильтрованный суммарный световой фронт с выделенным полезным сигналом фокусируется оптической системой 6 на фотоприемник 5 (фотодиод). Выработанный на выходе фотоприемника 5 электрический сигнал (значение напряжения которого соответствует уровню люминесценции) усиливается усилителем сигнала 8, оцифровывается с помощью аналого-цифрового преобразователя 9, и в цифровом представлении передаются для регистрации на вход блока 10 управления - контроллера - для регистрации уровня люминесценции, где обрабатывается путем сопоставления с предварительно занесенными в память калибровочными постоянными, и количественное значение уровня люминесценции, пропорциональное концентрации токсиканта - зераленона, и/или соответствующее значение уровня (концентрации) токсиканта заносится в память блока 10 управления - контроллера - и отображается в блоке 11 индикации.
Кроме того, блок 10 управления - контроллер - в соответствии с заложенным программным алгоритмом в автоматическом режиме осуществляет программируемое управление работой светодиодов источника 4 возбуждающего излучения, нормируя посредством блока 12 стабилизации напряжение источника 1 возбуждающего излучения, и обеспечивает сохранение в памяти параметров калибровочных постоянных (калибровочной кривой), значения которых определяются в процессе предварительных тарировочных измерений с использованием стандартных источников возбуждающего излучения и предварительной калибровки колонки 1 с использованием образцов анализируемой среды, содержащей токсиканты, например зераленон, известной концентрации.
Пример 2
Для определения уровня токсиканта, например концентрации зераленона, в анализируемой среде (природной воде) предварительно приготовляют поэтапно раствор конъюгата антивидовых антител с липосомами, содержащими водорастворимые люминесцентными квантовые точки - полупроводниковые наночастицы CdSe/ZnS, следующим образом.
На первом этапе методом гидратирования тонких пленок готовят липосомы, содержащие водорастворимые люминесцентными квантовые точки - полупроводниковые наночастицы CdSe/ZnS. Для этого 70 мг (94 µмоль) фосфолипидов (Lipoid S75) растворяют в 1 мл хлороформа в круглодонной колбе (V=10 мл). Затем хлороформ выпаривают с помощью роторного испарителя до образования пленки фосфолипидов на стенках колбы. Образовавшуюся пленку фосфолипидов обрабатывают 6 мл воды, содержащей 5 µмоль квантовых точек CdSe/ZnS, и перемешивают в течение 30 минут при температуре 45°C. Затем раствор обрабатывают ультразвуком в течение 5 минут для достижения приемлемого размера частиц липосом (порядка 100 нм). Полученный раствор, содержащий липосомы с водорастворимыми квантовыми точками CdSe/ZnS, хранят при температуре 45°C.
На втором этапе синтезируют раствор конъюгата антивидовых антител с липосомами, содержащими квантовые точки.
Для этого к 0,4 мл раствора, содержащего липосомы с инкорпорированными квантовыми точками - полупроводниковыми наночастицами CdSe/ZnS, капельно при постоянном перемешивании добавляют 0,5 мл 2,5% раствора глутарового альдегида в воде, после чего образовавшийся раствор перемешивают в течение 4 часов при комнатной температуре. Избыток глутарового альдегида удаляют с помощью диализа в течение 2 дней при температуре 4°C. Затем капельно при постоянном перемешивании в течение 2 часов при комнатной температуре добавляют 20 µл раствора антивидовых антител в фосфатном буфере (pH 7.4-7.6). Затем добавляют 60 µл 3M глицина в растворе гидроксида натрия (pH 7,2) для блокирования оставшихся свободными альдегидных групп глутарового альдегида на поверхности липосом. Полученную смесь выдерживают при температуре 4°C при постоянном перемешивании. Избыток не прореагировавших компонентов удаляют с помощью диализа в течение 3 часов. Полученные конъюгаты хранят при температуре 4°C.
К 1 мл анализируемой среды добавляют 25 мкл раствора специфичных к токсиканту - зераленону - моноклональных мышиных антител, перемешивают в течение 5 минут и пропускают через подготовленную аналогично примеру 1 колонку 1, после чего промывают колонку 1 фосфатным буфером (pH 7.4÷7.6), содержащим 0,05% Tween 20.
Затем в колонку 1 вводят 100 мкл предварительно приготовленного раствора конъюгата антивидовых антител, химически связанных с липосомами, содержащими водорастворимые люминесцентные квантовые точки - полупроводниковые наночастицы CdSe/ZnS (разведение 1/30 в фосфатном буфере (pH 7.4÷7.6), и инкубируют в течение 6 минут. Избыток конъюгата удаляют путем промывания колонки 1 фосфатным буфером (pH 7.4÷7.6), после чего осуществляют освещение носителя - слоя 2, содержащего люминесцентные квантовые точки - полупроводниковые наночастицы, световым потоком, поступающим от источника 4 возбуждающего излучения, и регистрируют возникший в результате возбуждающего излучения уровень люминесценции, величина которого обратно пропорциональна концентрации токсиканта - зераленона - в анализируемой среде.
Пример 3
Для определения уровня токсиканта, например концентрации зераленона, в анализируемой среде (природной воде) предварительно приготовляют поэтапно раствор конъюгата зераленона с липосомами, содержащими гидрофобные люминесцентными квантовые точки - полупроводниковые наночастицы CdSe/ZnS, следующим образом.
На первом этапе 70 мг (94 µмоль) фосфолипидов (Lipoid S75) и 30 пмоль гидрофобных квантовых точек (λem = 577 nm) в толуоле (52 µл) растворяют в 1 мл хлороформа в круглодонной колбе (V=10 мл) при воздействии ультразвуком при температуре 4°C.
Затем в образовавшийся раствор добавляют 3 мл воды и хлороформ выпаривают с помощью роторного испарителя. После этого добавляют еще 3 мл воды и в течение 60 минут перемешивают раствор с образовавшимися липосомами при температуре 4°C.
Затем раствор обрабатывают ультразвуком в течение 5 минут для достижения приемлемого размера частиц липосом (порядка 100 нм). Полученный раствор, содержащий липосомы с гидрофобными квантовыми точками CdSe/ZnS, хранят при температуре 4°C.
На втором этапе осуществляют синтез конъюгата антивидовых антител с липосомами, содержащими гидрофобные квантовые точки.
Для этого к 0,4 мл раствора, содержащего липосомы с инкорпорированными квантовыми точками - полупроводниковыми наночастицами CdSe/ZnS, капельно при постоянном перемешивании добавляют 0,5 мл 2,5% раствора глутарового альдегида в воде, после чего образовавшийся раствор перемешивают в течение 3 часов при комнатной температуре. Избыток глутарового альдегида удаляют с помощью диализа в течение 2 дней при температуре 4°C. Затем капельно при постоянном перемешивании в течение 2 часов при комнатной температуре добавляют 20 µл раствора антивидовых антител в фосфатном буфере (pH 7.4-7.6). Затем добавляют 60 µл 3M глицина в растворе гидроксида натрия (pH 7,2) для блокирования оставшихся свободными альдегидных групп глутарового альдегида на поверхности липосом. Полученную смесь выдерживают при температуре 4°C при постоянном перемешивании. Избыток не прореагировавших компонентов удаляют с помощью диализа в течение 3 часов. Полученные конъюгаты хранят при температуре 4°C.
К 1 мл анализируемой среды добавляют 25 мкл раствора специфичных к токсиканту - зераленону - моноклональных мышиных антител, перемешивают в течение 5 минут и пропускают через подготовленную аналогично примеру 1 колонку 1, после чего промывают колонку 1 фосфатным буфером (pH 7.4÷7.6), содержащим 0,05% Tween 20.
Затем в колонку 1 вводят 100 мкл предварительно приготовленного раствора конъюгата антивидовых антител, химически связанных с липосомами, содержащими гидрофобные люминесцентные квантовые точки - полупроводниковые наночастицы CdSe/ZnS, (разведение 1/30 в фосфатном буфере (pH 7.4÷7.6), и инкубируют в течение 10 минут. Избыток конъюгата удаляют путем промывания колонки 1 фосфатным буфером (рН7.4÷7.6), после чего осуществляют освещение носителя - слоя 2, содержащего люминесцентные квантовые точки - полупроводниковые наночастицы, световым потоком, поступающим от источника 4 возбуждающего излучения, и регистрируют возникший в результате возбуждающего излучения уровень люминесценция, величина которого пропорциональна концентрации токсиканта - зераленона - в анализируемой среде.
Заявленное изобретение обеспечивает возможность определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях путем проводимого в колонке тест-системы непрямого конкурентного иммуноферментного анализа уровня токсиканта с пределом обнаружения (чувствительностью) 1÷3 нг/мл.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ УРОВНЯ ТОКСИКАНТОВ В ВОДЕ, ПРОДУКТАХ ПИТАНИЯ ИЛИ ФИЗИОЛОГИЧЕСКИХ ЖИДКОСТЯХ И ТЕСТ-СИСТЕМА | 2012 |
|
RU2508553C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ УРОВНЯ ТОКСИКАНТОВ В ВОДЕ, ПРОДУКТАХ ПИТАНИЯ ИЛИ ФИЗИОЛОГИЧЕСКИХ ЖИДКОСТЯХ И ТЕСТ-СИСТЕМА | 2012 |
|
RU2506586C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ УРОВНЯ ТОКСИКАНТОВ В ВОДЕ, ПРОДУКТАХ ПИТАНИЯ ИЛИ ФИЗИОЛОГИЧЕСКИХ ЖИДКОСТЯХ И ТЕСТ-СИСТЕМА | 2013 |
|
RU2547577C1 |
| НАНОКОМПОЗИЦИОННЫЙ МАТЕРИАЛ | 2007 |
|
RU2332352C1 |
| СПОСОБ УПРАВЛЕНИЯ ОПТИЧЕСКИМИ СВОЙСТВАМИ НАНОКОМПОЗИЦИОННЫХ МАТЕРИАЛОВ | 2007 |
|
RU2332697C1 |
| Способ диагностики вируса простого герпеса | 2018 |
|
RU2702000C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2008 |
|
RU2395268C2 |
| СПОСОБ МАРКИРОВКИ ОРГАНИЧЕСКИХ ТОПЛИВ С ПОМОЩЬЮ КВАНТОВЫХ ТОЧЕК | 2022 |
|
RU2780550C1 |
| Способ изготовления материала люминесцентного сенсора и устройство люминесцентного сенсора для анализа кислых и основных компонентов в газовой фазе | 2017 |
|
RU2758182C2 |
| АЛКИНИЛФОСФИНОВЫЕ ЗОЛОТОМЕДНЫЕ КОМПЛЕКСЫ КАК ЛЮМИНИСЦЕНТНЫЕ МЕТКИ ДЛЯ ФЛУОРЕСЦЕНТНОЙ МИКРОСКОПИИ | 2013 |
|
RU2541794C1 |
Группа изобретений относится к области биотехнологии. Более подробно группа изобретений относится к способу определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях и тест-системе. Группа изобретений основана на том, что в колонке тест-системы размещают носитель в виде зафиксированного между двумя пористыми мембранами слоя иммуноаффинного геля с привитыми - ковалентно связанными - молекулами токсиканта, производят обработку носителя - слоя геля - блокирующим раствором для закрытия на носителе оставшихся свободными мест неспецифического связывания, вносят тестируемые образцы, содержащие определенное количество предварительно введенных специфичных к токсиканту антител, производят обработку носителя конъюгатсодержащим раствором, в качестве которого используют раствор конъюгата антивидовых антител, химически связанных с люминесцентными квантовыми точками или с липосомами, содержащими люминесцентные квантовые точки, а уровень токсикантов определяют путем освещения обработанного носителя возбуждающим излучением по интенсивности люминесценции, возбужденной в квантовых точках. Группа изобретений позволяет эффективно и достоверно определить уровень токсикантов в воде, продуктах питания или физиологических жидкостях. 2 н. и 2 з.п. ф-лы, 1 ил., 3 пр.
1. Способ определения уровня токсикантов в воде, продуктах питания или физиологических жидкостях путем проводимого в колонке тест-системы твердофазного иммуноферментного анализа, характеризующийся тем, что в колонке тест-системы размещают носитель в виде зафиксированного между двумя пористыми мембранами слоя иммуноаффинного геля с привитыми - ковалентно связанными - молекулами токсиканта, производят обработку носителя - слоя геля - блокирующим раствором для закрытия на носителе оставшихся свободными мест неспецифического связывания, вносят тестируемые образцы, содержащие определенное количество предварительно введенных специфичных к токсиканту антител, производят обработку носителя конъюгатсодержащим раствором, в качестве которого используют раствор конъюгата антивидовых антител, химически связанных с люминесцентными квантовыми точками или с липосомами, содержащими люминесцентные квантовые точки, а уровень токсикантов определяют путем освещении обработанного носителя возбуждающим излучением по интенсивности люминесценции, возбужденной в квантовых точках.
2. Способ по п.1, характеризующийся тем, что иммуноаффинный гель приготовляют в емкости с пористым дном путем обработки циан бром активированной сефарозы соляной кислотой и введения после набухания в полученный гель раствора антигена - токсиканта - в карбонатном буфере.
3. Тест-система для способа определения уровня токсикантов в воде, продуктах питания или физиологических жидкостя по п.1, включающая колонку, в которой установлен носитель в виде слоя иммуноаффинного геля, размещенного между двумя пористыми мембранами, характеризующаяся тем, что колонка снабжена устройством для измерения уровня люминесценции, включающим источник возбуждающего излучения и фотоприемник, причем перед фотоприемником дополнительно установлена фокусирующая оптическая система, а выход фотоприемника электрически подключен через усилитель сигнала и аналого-цифровой преобразователь к блоку управления - контроллеру, к выходу которого подключены блок индикации и через блок стабилизации источник возбуждающего излучения, при этом боковые стенки колонки выполнены из прозрачного для возбуждающего и люминесцентного излучения материала.
4. Тест-система по п.3, характеризующаяся тем, что перед фокусирующей оптической системой размещен светофильтр.
| КОМПЛЕКСНАЯ ТЕСТ-СИСТЕМА ИММУНОФЕРМЕНТНОГО АНАЛИЗА (ИФА) ДЛЯ ОПРЕДЕЛЕНИЯ УРОВНЯ АНТИТЕЛ К ВИРУСНЫМ РЕСПИРАТОРНЫМ ЗАБОЛЕВАНИЯМ КРУПНОГО РОГАТОГО СКОТА | 2008 |
|
RU2371726C1 |
| ТЕСТ-СИСТЕМА ДЛЯ ИММУНОФЕРМЕНТНОГО ОПРЕДЕЛЕНИЯ ТОКСИКАНТОВ | 2008 |
|
RU2374649C1 |
| БИОСЕНСОР НА ОСНОВЕ КЛЕТОК МИКРОВОДОРОСЛЕЙ ДЛЯ ОПРЕДЕЛЕНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ И ГЕРБИЦИДОВ В ВОДНЫХ СИСТЕМАХ | 2009 |
|
RU2426779C1 |
| BALMAND S | |||
| et al | |||
| Whole | |||
Авторы
Даты
2015-01-10—Публикация
2013-08-21—Подача