Данная заявка претендует на приоритет временной заявки США №60/567294, поданной 30 апреля 2004 г., и временной заявки США №60/609424, поданной 13 сентября 2004 г.
Область изобретения
Изобретение относится к области биотехнологии или генной инженерии. Конкретнее, данное изобретение относится к области генной экспрессии. Более конкретно, данное изобретение относится к новым ядерным рецепторам, содержащим мутацию замещения, и их использованию в системе экспрессии индуцибельного гена на основе ядерного рецептора и способам модулирования экспрессии гена в клетке-хозяине с использованием данной системы экспрессии индуцибельного гена.
Известный уровень техники
В данной заявке цитируются различные публикации, описание которых целиком включается сюда в качестве ссылок. Однако цитирование тут любого источника не должно толковаться как допущение, что такой источник представляет собой "известный уровень техники" по отношению к данной заявке.
В области генной инженерии, точный контроль генной экспрессии является ценным инструментом для изучения, манипулирования и контроля развития и других физиологических процессов. Генная экспрессия представляет собой сложный биологический процесс, включающий ряд специфических белок-белковых взаимодействий. Для запуска генной экспрессии, чтобы при этом продуцировалась РНК, необходимая в качестве первой стадии синтеза белка, активатор транскрипции должен быть помещен в непосредственной близости от промотора, контролирующего генную транскрипцию. Типично, активатор транскрипции сам ассоциирован с белком, имеющим по меньшей мере один ДНК-связывающий домен, связывающийся с сайтами связывания ДНК, присутствующими в промоторных участках генов. Таким образом, для протекания генной экспрессии, белок, содержащий ДНК-связывающий домен и домен трансактивации, расположенный на соответствующем расстоянии от ДНК-связывающего домена, должен занять правильное положение по отношению к промоторному участку гена.
Традиционный трансгенный подход использует специфичный к клеточному типу промотор для осуществления экспрессии требуемого трансгена. Структурный элемент ДНК, содержащий трансген, сначала внедряется в геном хозяина. При запуске с помощью активатора транскрипции происходит экспрессия трансгена в данном типе клеток.
Другим средством регулирования экспрессии чужеродных генов в клетках является использование индуцибельных промоторов. Примеры использования таких индуцибельных промоторов включают промотор PR1-a, прокариотические системы репрессор-оператор, системы иммунодепрессивных иммунофилинов и системы активации транскрипции высших эукариотов, такие как системы рецептора экдистероидного гормона, и описаны ниже.
Промотор PR1-a табака индуцируется в процессе системной приобретенной резистентности после воздействия патогена. Использование PR1-a может быть ограничено, поскольку он часто реагирует на эндогенные материалы и внешние факторы, такие как патогены, облучение УФ-В и загрязняющие агенты. Были описаны системы генной регуляции, основанные на промоторах, индуцируемых тепловым шоком, интерфероне и тяжелых металлах (Wurn et al., 1986, Proc. Natl. Acad. Sci. USA 83: 5414-5418; Arnheiter et al., 1990, Cell 62:51-61; Fihnus et al., 1992, Nucleic Acids Research 20: 27550-27560). Однако эти системы имеют ограничения вследствие их влияния на экспрессию нецелевых генов. Эти системы также являются растекающимися.
Прокариотические системы репрессор-оператор используют бактериальные репрессорные белки и уникальные операторные ДНК-последовательности, с которыми они связываются. Как тетрациклиновая ("Tet"), так и лактозная ("Lac") системы репрессор-оператор из бактерии Escherichia coli использовались для контроля генной экспрессии в растениях и животных, В Tet-системе, тетрациклин связывается с репрессорным белком TetR, приводя к конформационным изменениям, освобождающим репрессорный белок от оператора, который в результате обеспечивает возможность протекания транскрипции. В Lac-системе, lac-оперон активируется в ответ на присутствие лактозы или ее синтетических аналогов, таких как изопропил-b-D-тиогалактозид. К сожалению, использование таких систем ограничено из-за нестабильной химии лигандов, т.е. тетрациклина и лактозы, их токсичности, их естественного присутствия или относительно высоких уровней, необходимых для индукции или репрессии. По аналогичным причинам, полезность таких систем для животных ограничена.
Иммунодепрессивные молекулы, такие как FK506, рапамицин и циклоспорин А, могут связываться с иммунофилинами FKBP12, циклофилином и т.д. С использованием этой информации, была разработана общая стратегия связывания любых двух белков простым введением FK506 в каждый из двух белков или введения FK506 в один из них и циклоспорина А - в другой. Синтетический гомодимер FK506 (FK1012) или соединение, образующееся в результате слияния РК506-циклоспорин (FKCsA), может затем быть использован для индуцирования димеризации этих молекул (Spencer et al., 1993, Science 262: 1019-24; Belshaw et al., 1996 Proc. Natl. Acad. Sci. USA93: 4604-7). Gal4 ДНК-связывающий домен, слитый с FKBP12, и VP16 активаторный домен, слитый с циклофилином, и соединение FKCsA были использованы для того, чтобы продемонстрировать гетеродимеризацию и активацию репортерного гена под контролем промотора, содержащего сайты связывания Gal4. К сожалению, эта система включает иммунодепрессанты, которые могут иметь нежелательные побочные эффекты и тем самым ограничивают ее использование для переключения разных генов млекопитающих.
Использовались также системы активации транскрипции высших эукариотов, такие как системы рецептора стероидного гормона. Рецепторы стероидного гормона являются членами суперсемейства ядерных рецепторов и присутствуют в клетках позвоночных и беспозвоночных. К сожалению, использование стероидных соединений, которые активируют рецепторы для регуляции генной экспрессии, особенно, в растениях и млекопитающих, ограничено вследствие их участия во многих других природных биологических путях в таких организмах. Для того чтобы преодолеть такие трудности, была разработана альтернативная система с использованием рецепторов экдизона насекомых (EcR).
Рост, линька и развитие насекомых регулируются стероидным гормоном экдизоном (гормон линьки) и ювенильными гормонами (Dhadialla, et al., 1998, Annu. Rev. Entomol. 43: 545-569). Молекулярная мишень экдизона у насекомых состоит из по меньшей мере рецептора экдизона (EcR) и белка ultraspiracle (USP). EcR является членом суперсемейства ядерных стероидных рецепторов, которое характеризуется сигнатурной ДНК и лигандсвязывающими доменами, и доменом активации (Koelle et al. 1991, Cell, 67:59-77). Рецепторы EcR восприимчивы к ряду экдистероидных соединений, таких как понастерон А и муристерон А. Недавно были описаны нестероидные соединения с активностью экдистероидных агонистов, включая коммерчески доступные инсектициды тебуфенозид и метоксифенозид, которые продаются во всем мире фирмой Rohm and Haas Company (см. международную патентную заявку № РСТ/ЕР96/00686 и патент США №5530028). Оба аналога имеют исключительные профили безопасности для других организмов.
Рецептор экдизона насекомых (EcR) гетеродимеризуется с белком ultraspiracle (USP), встречающимся у насекомых гомологом RXR (Х-ретиноидного рецептора) млекопитающих, связывает экдистероиды и элементы ответа рецептора экдизона и активирует транскрипцию генов-респондеров экдизона (Riddiford et al., 2000). Комплексы EcR/USP/лиганд играют важную роль в развитии и размножении насекомых. EcR является членом суперсемейства рецепторов стероидного гормона и имеет пять модульных доменов - А/В (трансактивация), С (ДНК связывание, гетеродимеризация), D (шарнирный, гетеродимеризация), Е (лигандсвязывающий, гетеродимеризация и трансактивация) и F (трансактивация) домены. Некоторые из этих доменов, такие как А/В, С и Е, сохраняют свои функции после слияния с другими белками.
Строго регулируемая система экспрессии индуцибельных генов или "генные переключатели" является полезной в различных областях применения, таких как генная терапия, крупномасштабное производство белков в клетках, высокопроизводительные скрининг-анализы на основе клеток, функциональная геномика и регулирование признаков у трансгенных растений и животных.
Первая версия генного переключателя на основе EcR использовала EcR Drosophila melanogaster (DmEcR) и RXR Mus musculus (MmRXR) и показала, что эти рецепторы в присутствии экдистероида понастерона А трансактивируют репортерные гены в клеточных линиях млекопитающих и у трансгенных мышей (Christopherson et al., 1992; No et al., 1996). Позднее, Suhr et al., 1998, показали, что неэкдистероидный экдизоновый агонист тебуфенозид индуцирует высокий уровень трансактивации репортерных генов в клетках млекопитающих посредством EcR Bombyx mori (BmEcR) в отсутствие экзогенного гетеродимерного партнера.
Международные патентные заявки №№ PCT/US97/05330 (WO 97/38117) и PCT/US99/08381 (WO 99/58155) раскрывают способы модулирования экспрессии экзогенного гена, в которых структурный элемент ДНК, включающий экзогенный ген и экдизоновый элемент ответа, активируется вторым структурным элементом ДНК, включающим рецептор экдизона, который, в присутствии своего лиганда и, необязательно, в присутствии рецептора, способного выступать в роли молчащего партнера, связывается с экдизоновым элементом ответа для индуцирования генной экспрессии. Предпочтительный рецептор экдизона изолировали из Drosophila melanogaster. Типично, такие системы требуют присутствия молчащего партнера, предпочтительно, ретиноидного Х-рецептора (RXR), для обеспечения оптимальной активации. В клетках млекопитающих, рецептор экдизона насекомых (EcR) гетеродимеризуется с ретиноидным X-рецептором (RXR) и регулирует экспрессию целевых генов лиганд-зависимым образом. Международная патентная заявка № PCT/US98/14215 (WO 99/02683) раскрывает, что рецептор экдизона, выделенный из тутового шелкопряда Bombyx mori, является функциональным в системах млекопитающих без необходимости в экзогенном партнере димеризации.
Патент США №6265173 В1 раскрывает, что разные члены суперсемейства стероидных/тиреоидных рецепторов могут связываться с рецептором белка ultraspiracle (USP) Drosophila melanogaster или его фрагментами, включающими по меньшей мере домен димеризации USP для использования в системе генной экспрессии. Патент США №5880333 раскрывает EcR Drosophila melanogaster и систему гетеродимера ultraspiracle (USP), используемую в растениях, в которой домен трансактивации и ДНК-связывающий домен расположены на двух разных гибридных белках. К сожалению, эти системы на основе USP являются конститутивными в клетках животных и потому не могут эффективно регулировать экспрессию гена-репортера.
В каждом из этих случаев, домен трансактивации и ДНК-связывающий домен (в виде нативного EcR, как в международной патентной заявке № PCT/US98/14215, или модифицированного EcR, как в международной патентной заявке № PCT/US97/05330) вводили в состав одной молекулы, а другие гетеродимерные партнеры, будь то USP или RXR, были использованы в своем нативном состоянии.
Недостатки описанных выше систем генной регуляции на основе EcR включают значительную фоновую активность в отсутствие лигандов и неприменимость этих систем для использования как в растениях, так и в животных (см. патент США №5880333). Поэтому в известном уровне техники существует потребность в усовершенствовании систем на основе EcR для точного модулирования экспрессии экзогенных генов как в растениях, так и в животных. Такие усовершенствованные системы были бы полезны в таких областях применения, как генная терапия, крупномасштабное производство белков и антител, системы высокопроизводительного скрининг-анализа на основе клеток, функциональная геномика и регулирование признаков у трансгенных животных. Для некоторых областей применения, таких как генная терапия, может быть желательным иметь систему экспрессии индуцибельного гена, которая хорошо взаимодействовала бы с синтетическими неэкдистероидными лигандами и в то же время была нечувствительной к природным экдистероидам. Таким образом, усовершенствованные системы, которые были бы простыми, компактными и зависящими от относительно недорогих лигандов, легко доступными и низкотоксичными для хозяина, были бы полезными для регулирования биологических систем.
Ранее, заявители показали, что система экспрессии индуцибельного гена на основе рецептора экдизона, в которой трансактивирующий и ДНК-связывающий домены разделены друг от друга путем их помещения на два разные белка, приводит к значительно сниженной фоновой активности в отсутствие лиганда и значительно повышенной активности по сравнению с фоновой в присутствии лиганда (находящаяся на рассмотрении заявка PCT/US01/09050, которая целиком включена сюда по ссылке). Эта двухгибридная система представляет собой значительно усовершенствованную систему модулирования индуцибельной генной экспрессии по сравнению с двумя системами, раскрытыми в заявках PCT/US97/05330 и PCT/US98/14215. Двухгибридная система использует способность пары взаимодействующих белков приводить домен активации транскрипции в более благоприятное положение по отношению к ДНК-связывающему домену таким образом, что когда ДНК-связывающий домен связывается с сайтом связывания ДНК гена, домен трансактивации более эффективно активирует промотор (см., например, патент США №5283173). Вкратце говоря, двухгибридная система генной экспрессии включает две кассеты генной экспрессии; первая кодирует ДНК-связывающий домен, слитый с полипептидом ядерного рецептора, и вторая кодирует домен трансактивации, слитый с другим полипептидом ядерного рецептора. В присутствии лиганда, взаимодействие первого полипептида со вторым полипептидом эффективно сцепляет ДНК-связывающий домен с доменом трансактивации. Поскольку домены связывания ДНК и трансактивации находятся в двух разных молекулах, фоновая активность в отсутствие лиганда значительно уменьшается.
Двухгибридная система также обеспечивает улучшенную чувствительность к неэкдистероидным лигандам, например диацилгидразинам, по сравнению с экдистероидными лигандами, например понастероном А ("PonA") или муристероном A ("MurA"). Это означает, что, по сравнению с экдистероидами, неэкдистероидные лиганды обеспечивают более высокую активность при меньших концентрациях. Кроме того, поскольку трансактивация на основе EcR генных переключателей часто является зависимой от клеточной линии, становится легче смоделировать системы переключения для достижения максимальной трансактивационной способности для каждой области применения. Более того, двухгибридная система позволяет избежать некоторых побочных эффектов благодаря сверхэкспрессии RXR, которая часто происходит при использовании немодифицированного RXR в качестве партнера переключения. В предпочтительной двухгибридной системе, нативный ДНК-связывающий и трансактивирующий домены EcR или RXR удалены, в результате чего эти гибридные молекулы имеют меньше возможностей взаимодействия с другими присутствующими в клетке рецепторами стероидных гормонов, приводя к уменьшению побочных эффектов.
EcR являются членами суперсемейства ядерных рецепторов и делятся на подсемейство 1, группа Н (которая называется тут "группа Н ядерных рецепторов"). Члены каждой группы имеют 40-60% аминокислотной идентичности в Е (лигандсвязывающем) домене (Laudet et al., A Unified Nomenclature System for the Nuclear Receptor Subfamily, 1999; Cell 97: 161-163). Кроме рецептора экдизона, другие члены этого подсемейства ядерных рецепторов 1, группа Н, включают: вездесущий рецептор (UR), рецептор-сирота 1 (OR-1), ядерный рецептор стероидного гормона 1 (NER-1), RXR-взаимодействующий белок-15 (RIP-15), х-рецептор печени β (LXRβ), белок, подобный рецептору стероидного гормона (RLD-й), х-рецептор печени (LXR), х-рецептор печени α (LXRα), фарнезоидный х-рецептор (FXR), рецептор-взаимодействующий белок 14 (RJP-14) и рецептор фарнезола (HRR-1).
Для разработки усовершенствованной системы экспрессии индуцибельного гена на основе ядерного рецептора группы Н с модифицированной лигандсвязывающей способностью или лигандспецифичностью, заявители создали субституционный мутант EcRs, который включает замещенные аминокислотные остатки в лигандсвязывающем домене (LBD). Был использован метод гомологического моделирования и стыковки для предсказания критических остатков, оторые медиируют связывание экдистероидов и неэкдистероидов с EcR LBD. Эти субституционные мутантные EcRs оценивали путем проведения лигандсвязывающих и трансактивационных анализов. Как описывается тут, полученные заявителями новые субституционне мутантные ядерные рецепторы и их использование в системе экспрессии индуцибельного гена на основе ядерного рецептора обеспечивают усовершенствованную систему экспрессии индуцибельного гена для прокариотических и эукариотических клеток-хозяев, в которой чувствительность к лигандам и степень трансактивации могут быть выбраны по желанию, в зависимости от области применения.
Детальное описание изобретения
Заявители описали тут конструирование ядерных рецепторов группы Н, которые включают субституционные мутации (которые называются тут "субституционными мутантами") по аминокислотным остаткам, участвующим в связывании лиганда с лигандсвязывающим доменом ядерного рецептора группы Н, которые влияют на чувствительность к лигандам и степень индукции ядерного рецептора группы Н, и продемонстрировали, что эти субституционные мутантные ядерные рецепторы пригодны для использования в способах модулирования генной экспрессии.
Конкретнее, заявители разработали новую систему экспрессии индуцибельного гена на основе ядерного рецептора, включающую лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения. Заявители показали, что такие субституционные мутации могут повышать или понижать лигандсвязывающую активность или чувствительность к лигандам, причем лиганд может быть специфичным по отношению к экдистероидам или не-экдистероидам. Таким образом, созданное заявителями изобретение предлагает систему экспрессии индуцибельного гена на основе ядерного рецептора группы Н, пригодную для модулирования экспрессии гена, представляющего интерес в клетке-хозяине. В особенно предпочтительном варианте исполнения, созданное заявителями изобретение предусматривает систему экспрессии индуцибельного гена на основе рецептора экдизона, которая реагирует только на экдистероидные лиганды или не-экдистероидные лиганды. Кроме того, настоящее изобретение также предусматривает систему экспрессии индуцибельного гена на основе рецептора экдизона, чувствительную к усовершенствованному не-экдистероидному лиганду. Таким образом, предложенная заявителями новая система экспрессии индуцибельного гена и ее использование в способах модулирования генной экспрессии в клетке-хозяине преодолевают ограничения имеющихся в настоящее время индуцибельных систем экспрессии и дают квалифицированному специалисту эффективные средства для контроля генной экспрессии.
Настоящее изобретение пригодно для использования в таких областях, как генная терапия, крупномасштабное производство белков и антител, системы высокопроизводительного скрининг-анализа на основе клеток, скрининг-анализ ортогональных лигандов, функциональная геномика, протеомика, метаболомика и регулирование признаков у трансгенных организмов, где является желательным контроль уровней генной экспрессии. Преимуществом изобретения заявителей является то, что оно обеспечивает средства регулирования генной экспрессии и приведения уровней экспрессии в соответствии с требованиями пользователя.
Определения
В данном описании используется ряд терминов и аббревиатур. Приведем следующие определения, которые должны помочь пониманию объема и практики настоящего изобретения.
В конкретном варианте исполнения, термин "около" или "приблизительно" означает в пределах 20%, предпочтительно, в пределах 10%, более предпочтительно, в пределах 5%, и еще более предпочтительно, в пределах 1% от указанного значения или интервала значений.
Термин "по существу не содержит" означает, что композиция, включающая "А" (где "А" обозначает отдельный белок, молекула ДНК, вектор, рекомбинантная клетка-хозяин и т.д.), по существу не содержит "В" (где "В" включает один или больше загрязняющих белков, молекул ДНК, векторов и т.д.), когда по меньшей мере около 75% мас. белков, ДНК, векторов (в зависимости от категории компонентов, к которым принадлежат А и В) в композиции составляет "А". Предпочтительно, "А" включает по меньшей мере около 90% мас. А+В компонентов в композиции, наиболее предпочтительно, по меньшей мере около 99% мас. Также предпочтительно, чтобы композиция, по существу не содержащая загрязнений, содержала только компоненты одного молекулярного веса, обладающие активностью или характеристиками компонентов, представляющих интерес.
Термин "изолированный" в целях настоящего изобретения обозначает биологический материал (нуклеиновую кислоту или белок), извлеченный из его исходной среды (среды, в которой он находится в природных условиях). Например, полинуклеотид, присутствующий в природном состоянии в растении или животном, не является изолированным, однако тот же полинуклеотид, отделенный от граничащих с ним нуклеиновых кислот, в которых он находится в природных условиях, считается "изолированным". Термин "очищенный" не требует, чтобы материал находился в форме, обладающей абсолютной чистотой, исключающей присутствие других соединений. Это скорее относительное определение.
Полинуклеотид находится в "очищенном" состоянии после очистки исходного материала или природного материала по меньшей мере на один порядок величины, предпочтительно, 2 или 3, и предпочтительнее, 4 или 5 порядков величины.
"Нуклеиновая кислота" представляет собой полимерное соединение, состоящее из ковалентно связанных субъединиц, называемых нуклеотидами. Нуклеиновая кислота включает полирибонуклеиновую кислоту (РНК) и полидезоксирибонуклеиновую кислоту (ДНК), которые обе могут быть одноцепочечными или двухцепочечными. ДНК включает, без ограничений, кДНК, геномную ДНК, плазмидную ДНК, синтетическую ДНК и полусинтетическую ДНК. ДНК может быть линейной, кольцевой или сверхскрученной.
"Молекула нуклеиновой кислоты" относится к полимерной форме фосфатного сложного эфира рибонуклеозидов (аденозин, гуанозин, уридин или цитидин; "молекулы РНК") или дезоксирибонуклеозидов (дезоксиаденозин, дезоксигуанозин, дезокситимидин или дезоксицитидин; "молекулы ДНК") или любым их фосфоэфирным аналогам, таким как фосфоротиоаты и тиоэфиры, в одноцепочечной форме или в форме двухцепочечной спирали. Возможны двухцепочечные спирали ДНК-ДНК, ДНК-РНК и РНК-РНК. Термин молекула нуклеиновой кислоты, в частности молекула ДНК или РНК, относится только к первичной и вторичной структуре молекулы и не ограничивает ее какими-либо конкретными третичными формами. Таким образом, этот термин включает двухцепочечные ДНК, присутствующие, в том числе, в линейных или кольцевых молекулах ДНК (например, рестрикционные фрагменты), плазмиды и хромосомы. При обсуждении структуры конкретных двухцепочечных молекул ДНК, последовательности могут быть описаны тут в соответствии с обычной конвенцией с указанием только последовательности в направлении от 5'- к 3'-концу вдоль нетранскрибированной цепи ДНК (т.е. цепи, имеющей последовательность, гомологичную мРНК). "Рекомбинантная молекула ДНК" представляет собой молекулу ДНК, подвергнутую молекулярным биологическим манипуляциям.
Термин "фрагмент" следует понимать как обозначающий нуклеотидную последовательность уменьшенной длины по сравнению с эталонной нуклеиновой кислотой, включающей, на общем участке, нуклеотидную последовательность, идентичную эталонной нуклеиновой кислоте. Такой фрагмент нуклеиновой кислоты в соответствии с изобретением может, в соответствующих случаях, входить в состав большего по размеру полинуклеотида, составной частью которого он является. Такие фрагменты включают или, альтернативно, состоят из олигонуклеотидов, имеющих в длину от по меньшей мере 6, 8, 9, 10, 12, 15, 18, 20, 21, 22, 23, 24, 25, 30, 39, 40, 42, 45, 48, 50, 51, 54, 57, 60, 63, 66, 70, 75, 78, 80, 90, 100, 105, 120, 135, 150, 200, 300, 500, 720, 900, 1000 или 1500 последовательных нуклеотидов нуклеиновой кислоты в соответствии с изобретением.
В используемом тут значении, "изолированный фрагмент нуклеиновой кислоты" представляет собой полимер РНК или ДНК, который является одно- или двухцепочечным, необязательно содержащим синтетические, неприродные или измененные нуклеотидные основания. Изолированный фрагмент нуклеиновой кислоты в форме полимера ДНК может состоять из одного или больше сегментов кДНК, геномной ДНК или синтетической ДНК.
"Ген" относится к набору нуклеотидов, кодирующих полипептид, и включает нуклеиновые кислоты кДНК и геномной ДНК. "Ген" также относится к фрагменту нуклеиновой кислоты, который экспрессирует специфический белок или полипептид, включая регуляторные последовательности, предшествующие (5'-некодирующие последовательности) и следующие за (3'-некодирующие последовательности) кодирующей последовательностью. "Нативный ген" относится к гену в том виде, в каком он встречается в природе, со своими собственными регуляторными последовательностями. "Химерный ген" относится к любому гену, не являющемуся нативным геном, включающему регуляторные и/или кодирующие последовательности, которые не встречаются вместе в природе. Соответственно, химерный ген может включать регуляторные последовательности и кодирующие последовательности, полученные из разных источников, или регуляторные последовательности и кодирующие последовательности, полученные из одного источника, но имеющие взаимное расположение, отличное от встречающегося в природе. Химерный ген может включать кодирующие последовательности, полученные из разных источников и/или регуляторные последовательности, полученные из разных источников. "Эндогенный ген" относится к нативному гену в его природном положении в геноме организма. "Чужеродный" ген или "гетерологичный" ген относится к гену, который нормально не присутствует в организме хозяина, но был введен в организм хозяина путем переноса гена. Чужеродные гены могут включать нативные гены, введенные в ненативный организм, или химерные гены. "Трансген" представляет собой ген, который был введен в геном посредством процедуры трансформации.
"Гетерологичная" ДНК относится к ДНК, которая в природных условиях не присутствует в клетке или в хромосомной области клетки. Предпочтительно, гетерологичная ДНК включает ген, чужеродный по отношению к клетке.
Термин "геном" включает хромосомную, а также митохондриальную, хлоропластовую и вирусную ДНК или РНК.
Молекула нуклеиновой кислоты "гибридизуется" с другой молекулой нуклеиновой кислоты, такой как кДНК, геномная ДНК или РНК, если одноцепочечная форма молекулы нуклеиновой кислоты может соединяться с другой молекулой нуклеиновой кислоты в соответствующих условиях температуры и ионной силы раствора (см. Sambrook et al., 1989, infra). Условия гибридизации и промывки хорошо известны и описаны в Sambrook, J., Fritsch, E.F. и Maniatis, T. Molecular Cloning: A Laboratory Manual, Second Edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor (1989), особенно, Глава 11 и Таблица 11,1 данного источника (который целиком включен сюда по ссылке). Условия температуры и ионной силы определяют "суровость" гибридизации.
Суровость условий может быть отрегулирована для отбора от умеренно подобных фрагментов, таких как гомологичные последовательности из отдаленно родственных организмов, до сильно подобных фрагментов, таких как гены, дуплицирующие функциональные ферменты из близко родственных организмов. Для предварительного скрининга гомологичных нуклеиновых кислот, могут быть использованы условия гибридизации низкой суровости, соответствующие, например, Tm 55°, 5×SSC, 0,1% ДСН, 0,25% молока, без формамида; или 30% формамида, 5×SSC, 0,5% ДСН. Условия гибридизации умеренной суровости соответствуют, например, более высокой Tm, 40% формамида, с 5× или 6×SCC. Условия гибридизации высокой суровости соответствуют, например, самым высоким значениям Tm, 50% формамида, 5× или 6×SCC.
Гибридизация требует, чтобы две нуклеиновые кислоты содержали комплементарные последовательности, хотя в зависимости от суровости гибридизации, возможны ошибки спаривания оснований. Термин "комплементарный" используется для описания соотношения между нуклеотидными основаниями, способными гибридизоваться друг с другом. Например, по отношению к ДНК, аденозин является комплементарным тимину, а цитозин является комплементарным гуанину. Соответственно, настоящее изобретение также включает изолированные фрагменты нуклеиновой кислоты, которые являются комплементарными к целой последовательности, раскрытой или используемой тут, а также существенно подобные последовательности нуклеиновой кислоты.
В конкретном варианте исполнения изобретения, полинуклеотиды детектируют с использованием условий гибридизации, включающих стадию гибридизации при Tm 55°С, и описанных выше условиях. В предпочтительном варианте исполнения, Tm равна 60°С; в более предпочтительном варианте исполнения, Tm равна 63°С; в еще более предпочтительном варианте исполнения, Tm равна 65°С.
Постгибридизационная промывка также определяет условия суровости. Один набор предпочтительных условий использует серию промывок, начиная с 6×SSC, 0,5% ДСН при комнатной температуре в течение 15 минут (мин), затем повторяют процедуру, используя 2×SSC, 0,5% ДСН при 45°С в течение 30 минут, и затем повторяют дважды, используя 0,2×SSC, 0,5% ДСН при 50°С в течение 30 минут. Более предпочтительный набор суворых условий использует более высокие температуры с идентичными указанным выше промывными жидкостями, за исключением того, что температура последних двух 30-минутных промывок в 0,2×SSC, 0,5% ДСН, повышена до 60°С. Другой предпочтительный набор очень суворых условий использует две последние промывки в 0,1×SSC, 0,1% ДСН при 65°С. Гибридизация требует, чтобы две нуклеиновые кислоты включали комплементарные последовательности, хотя в зависимости от суровости гибридизации, возможны ошибки спаривания оснований.
Соответствующая суворость гибридизации нуклеиновых кислот зависит от длины нуклеиновых кислот и степени комплементарности, причем эти факторы хорошо известны специалистам. Чем больше степень подобия или гомология между двумя нуклеотидными последовательностями, тем больше значение Tm для гибридных нуклеиновых кислот, содержащих эти последовательности. Относительная стабильность (соответствующая более высокой Tm) гибридизации нуклеиновых кислот уменьшается в следующем порядке: РНК:РНК, ДНК:РНК, ДНК:ДНК. Для гибридов, имеющих более 100 нуклеотидов в длину, были выведены уравнения для расчета Tm (см. Sambrook et al., supra, 9,50-0,51). Для гибридизации с более короткими нуклеиновыми кислотами, т.е. олигонуклеотидами, положение ошибок спаривания становится более важным, и длина олигонуклеотида определяет его специфичность (см. Sambrook et al., supra, 11,7-11,8).
В конкретном варианте исполнения изобретения, полинуклеотиды детектируют путем использования условий гибридизации, включающих стадию гибридизации в менее чем 500 мМ соли и по меньшей мере 37°С и стадию промывки в 2×SSPE при по меньшей мере 63°С. В предпочтительном варианте исполнения, условия гибридизации включают менее чем 200 мМ соли и по меньшей мере 37°С для стадии гибридизации. В более предпочтительном варианте исполнения, условия гибридизации включают 2×SSPE и 63°С для обоих стадий гибридизации и промывки.
В одном варианте исполнения, длина гибридизуемой нуклеиновой кислоты составляет по меньшей мере около 10 нуклеотидов. Предпочтительно, минимальная длина гибридизуемой нуклеиновой кислоты составляет по меньшей мере около 15 нуклеотидов; более предпочтительно, по меньшей мере около 20 нуклеотидов; и наиболее предпочтительно, длина составляет по меньшей мере 30 нуклеотидов. Кроме того, квалифицированному специалисту понятно, что температура и концентрация соли промывного раствора могут быть отрегулированы в зависимости от необходимости с учетом таких факторов, как длина зонда.
Термин "зонд" относится к одноцепочечной молекуле нуклеиновой кислоты, которая может спариваться с комплементарной одноцепочечной нуклеиновой кислотой-мишенью с образованием двухцепочечной молекулы.
В используемом тут значении, термин "олигонуклеотид" относится к нуклеиновой кислоте, состоящей в общем из по меньшей мере 18 нуклеотидов, которая способна гибридизироваться с молекулой геномной ДНК, молекулой кДНК, плазмидной ДНК или молекулой мРНК. Олигонуклеотиды могут быть помечены, например, 32Р-нуклеотидами или нуклеотидами, ковалентно конъюгированными с меткой, такой как биотин. Меченый олигонуклеотид может быть использован в качестве зонда для детектирования присутствия нуклеиновой кислоты. Олигонуклеотиды (один или оба из которых могут быть мечеными) могут быть использованы в качестве праймеров ПЦР, для клонирования полной нуклеиновой кислоты или ее фрагмента или для детектирования присутствия нуклеиновой кислоты. Олигонуклеотид также может быть использован для образования тройной спирали с молекулой ДНК. Обычно, олигонуклеотиды получают синтетически, предпочтительно, с помощью синтезатора нуклеиновых кислот. Соответственно, олигонуклеотиды могут быть получены с неприродными аналогами фосфоэфирных связей, такими как тиоэфирные связи и т.д.
"Праймер" является олигонуклеотидом, который гибридизуется с последовательностью нуклеиновой кислоты-мишени с образованием участка двухцепочечной нуклеиновой кислоты, который может служить сайтом инициации для синтеза ДНК в пригодных условиях. Такие праймеры могут быть использованы в полимеразной цепной реакции.
"Полимеразная цепная реакция" сокращенно обозначается ПЦР и обозначает in vitro метод ферментативной амплификации специфических последовательностей нуклеиновой кислоты. ПЦР включает повторяющуюся серию температурных циклов, каждый из которых включает три стадии: денатурирование матричной нуклеиновой кислоты для разделения цепей молекулы-мишени, отжиг одноцепочечного олигонуклеотидного праймера ПЦР с матричной нуклеиновой кислотой и удлинение отожженного праймера (праймеров) ДНК полимеразой. ПЦР обеспечивает средства детектирования присутствия целевой молекулы и, в количественных или полуколичественных условиях, определения относительного количества данной молекулы-мишени в исходном пуле нуклеиновых кислот.
"Полимеразная цепная реакция с обратной транскриптазой" сокращенно обозначается ОТ-ПЦР и обозначает in vitro метод ферментативного синтеза целевой молекулы или молекул кДНК из молекулы или молекул РНК, с последующей ферментативной амплификацией специфической последовательности или последовательностей нуклеиновой кислоты в целевой молекуле или молекулах кДНК, как описано выше. ОТ-ПЦР также обеспечивает средства детектирования присутствия целевой молекулы и, в количественных или полуколичественных условиях, определения относительного количества данной целевой молекулы в исходном пуле нуклеиновых кислот.
"Кодирующая последовательность" ДНК представляет собой двухцепочечную последовательность ДНК, которую подвергают транскрипции и трансляции в полипептид в клетке in vitro или in vivo под контролем соответствующих регуляторных последовательностей. "Пригодные регуляторные последовательности" относятся к нуклеотидным последовательностям, предшествующим (5' некодирующие последовательности), расположенным внутри или следующим (3' некодирующие последовательности) за кодирующей последовательностью, которые влияют на транскрипцию, процессинг или стабильность РНК или трансляцию ассоциированной кодирующей последовательности. Регуляторные последовательности могут включать промоторы, лидерные последовательности трансляции, интроны, последовательности узнавания полиаденилирования, сайт процессинга РНК, сайт связывания эффектора и структуру стебель-петля. Границы кодирующей последовательности определяются старт-кодоном на 5' (амино) конце и кодоном терминации трансляции на 3' (карбоксильном) конце. Кодирующая последовательность может включать, без ограничений, прокариотические последовательности, кДНК из мРНК, геномные ДНК-последовательности и даже синтетические ДНК-последовательности. Если кодирующая последовательность предназначена для экспрессии в эукариотической клетке, то сигнал полиаденилирования и последовательность терминации транскрипции будут обычно расположены со стороны 3'-конца от кодирующей последовательности.
"Открытая рамка считывания" сокращенно обозначается ОРС и обозначает участок последовательности нуклеиновой кислоты, будь то ДНК, кДНК или РНК, который включает сигнал начала трансляции или инициирующий кодон, такой как ATG или AUG, и терминирующий кодон и может быть потенциально транслирован в полипептидную последовательность.
Термин "головой-к-голове" используется тут для описания ориентации двух полинуклеотидных последовательностей по отношению друг к другу. Два полинуклеотида расположены с ориентацией головой-к-голове, если 5'-конец кодирующей цепи одного полинуклеотида прилегает к 5'-концу кодирующей цепи другого полинуклеотида, вследствие чего направление транскрипции каждого полинуклеотида направлено прочь от 5'-конца другого полинуклеотида. Термин "головой-к-голове" может быть сокращенно обозначен (5')-к-(5') и также может быть указан символами (← →) или (3'←5' 5'→3').
Термин "хвостом-к-хвосту" используется тут для описания ориентации двух полинуклеотидных последовательностей по отношению друг к другу. Два полинуклеотида расположены с ориентацией хвостом-к-хвосту, если 3'-конец кодирующей цепи одного полинуклеотида прилегает к 3'-концу кодирующей цепи другого полинуклеотида, причем направление транскрипции каждого полинуклеотида направлено в сторону к другому полинуклеотиду. Термин "хвостом-к-хвосту" может быть сокращенно обозначен (3')-к-(3') и также может быть указан символами (→ ←) или (5'→3' 3'←5').
Термин "головой-к-хвосту" используется тут для описания ориентации двух полинуклеотидных последовательностей по отношению друг к другу. Два полинуклеотида расположены с ориентацией головой-к-хвосту, если 5'-конец кодирующей цепи одного полинуклеотида прилегает к 3'-концу кодирующей цепи другого полинуклеотида, причем транскрипция каждого из полинуклеотидов происходит в том же направлении, что и другого полинуклеотида. Термин "головой-к-хвосту" может быть сокращенно обозначен (5')-к-(3') и также может буть указан символами (→ →) или (5'→3' 5'→3').
Термин "следующий за" (также "последующий", "справа") относится к нуклеотидной последовательности, расположенной со стороны 3'-конца от рассматриваемой нуклеотидной последовательности. В частности, последующие нуклеотидные последовательности обычно относятся к последовательностям, которые следуют за начальной точкой транскрипции. Например, кодон инициации трансляции гена расположен справа сайта начала транскрипции.
Термин "предшествующий" (также "слева") относится к нуклеотидной последовательности, которая расположена со стороны 5'-конца от рассматриваемой нуклеотидной последовательности. В частности, предшествующие нуклеотидные последовательности обычно относятся к последовательностям, расположенным со стороны 5'-конца от кодирующей последовательности или точки начала транскрипции. Например, большинство промоторов расположены слева от сайта начала транскрипции.
Термины "эндонуклеаза рестрикции" и "рестриктаза" относятся к ферменту, который связывается и расщепляет специфическую нуклеотидную последовательность в двухцепочечной ДНК.
"Гомологичная рекомбинация" относится к вставке чужеродной ДНК-последовательности в другую молекулу ДНК, например вставке вектора в хромосому. Предпочтительно, вектор нацелен на специфический участок хромосомы для гомологичной рекомбинации. Для специфической гомологичной рекомбинации, вектор должен содержать достаточно длинные участки гомологии с последовательностями хромосомы для обеспечения возможности комплементарного связывания и включения вектора в хромосому. Более длинные участки гомологии и большие степени подобности последовательностей могут увеличивать эффективность гомологичной рекомбинации.
Несколько известных специалистам методов могут быть использованы для репродуцирования полинуклеотида в соответствии с изобретением. После определения пригодной системы хозяина и условий роста, векторы рекомбинантной экспрессии могут быть репродуцированы и получены в значительном количестве. Как было описано выше, векторы экспрессии, которые могут быть использованы, включают, без ограничения, в качестве нескольких примеров, следующие векторы или их производные: вирусы человека или животных, такие как вирус коровьей оспы или аденовирус; вирусы насекомых, такие как бакуловирус; векторы дрожжей; векторы бактериофаги (например, лямбда) и плазмидные и космидные ДНК-векторы.
"Вектор" представляет собой любое средство клонирования и/или переноса нуклеиновой кислоты в клетку-хозяина. Вектор может быть репликоном, к которому может быть присоединен другой сегмент ДНК для того, чтобы вызвать репликацию присоединенного сегмента. "Репликон" представляет собой любой генетический элемент (например, плазмиду, фаг, космиду, хромосому, вирус), который функционирует в качестве автономной единицы репликации ДНК in vivo, т.е. способен к репликации под своим собственным контролем. Термин "вектор" включает как вирусные, так и невирусные средства введения нуклеиновой кислоты в клетку in vitro, ex vivo или in vivo. Большое число известных специалистам векторов может быть использовано для манипулирования нуклеиновыми кислотами, включения в гены элементов ответа и промоторов и т.д. Возможные векторы включают, например, плазмиды или модифицированные вирусы, включая, например, бактериофаги, такие как производные лямбда, или плазмиды, такие как производные плазмид pBR322 или pUC, или вектор Bluescript. Например, инсерция фрагментов ДНК, соответствующих элементам ответа и промоторам, в пригодный вектор, может быть осуществлена путем лигирования соответствующих фрагментов ДНК в выбранный вектор, имеющий комплементарные липкие концы. Альтернативно, концы молекул ДНК могут быть ферментативно модифицированы, или любой сайт может быть получен, путем лигирования нуклеотидных последовательностей (линкеров) в концы ДНК. Такие векторы могут быть сконструированы таким образом, чтобы они содержали селектируемые маркерные гены, обеспечивающие селектирование клеток, имеющих маркер, включенный в клеточный геном. Такие маркеры позволяют проводить идентификацию и/или селектирование клеток-хозяев, которые включают и экспрессируют белки, кодируемые маркером.
Вирусные векторы, и особенно ретровирусные векторы, использовались в различных целях для доставки генов в клетки, а также в живых животных. Вирусные векторы, которые могут быть использованы, включают, без ограничения, векторы на основе ретровируса, адено-ассоциированного вируса, вируса оспы, бакуловируса, вирусов коровьей оспы, простого герпеса, Эпштейна-Барр, аденовируса, геминивируса и колимовируса. Невирусные векторы включают плазмиды, липосомы, электрически заряженные липиды (цитофектины), комплексы ДНК-белок и биополимеры. Помимо нуклеиновой кислоты, вектор может также включать один или больше регуляторных участков и/или селектируемых маркеров, пргодных для селектирования, измерения и контроля результатов переноса нуклеиновой кислоты (в какие ткани, продолжительность экспрессии и т.д.).
Термин "плазмида" относится к внехромосомному элементу, часто несущему ген, не являющийся частью центрального метаболизма клетки, и обычно имеющему форму кольцевых двухцепочечных молекул ДНК. Такие элементы могут быть автономно реплицирующимися последовательностями, интегрируемыми в геном последовательностями, фаговыми или нуклеотидными последовательностями, линейными, кольцевыми или сверхскрученными, одно- или двухцепочечных ДНК или РНК, выделенными из любого источника, в которых ряд нуклеотидных последовательностей были соединены или рекомбинированы в уникальную конструкцию, способную вводить в клетку промоторный фрагмент и ДНК последовательность выбранного генного продукта вместе с соответствующей 3' нетранслированной последовательностью.
"Клонирующий вектор" представляет собой "репликон", который является единичным фрагментом нуклеиновой кислоты, предпочтительно ДНК, который последовательно реплицируется и включает начало репликации, такое как плазмида, фаг или космида, к которому может быть присоединен другой сегмент нуклеиновой кислоты для того, чтобы вызвать репликацию присоединенного сегмента. Клонирующие векторы могут быть способны к репликации в одном типе клеток и к экспрессии - в другом ("челночный вектор").
Векторы могут быть введены в требуемые клетки-хозяева известными специалистам методами, например трансфекцией, электропорацией, микроинъекцией, трансдукцией, слиянием клеток, с использованием DEAE-декстрана, кальций-фосфатным осаждением, липофекцией (слиянием лизосом), с использованием генной пушки или переносчика ДНК вектора (см., например, Wu et al., 1992, J. Biol. Chem. 267: 963-967; Wu and Wu, 1988, J. Biol. Chem. 263: 14621-14624; и Hartmut et al., патентная заявка Канады №2012311, подана 15 марта 1990 г.).
Полинуклеотид в соответствии с изобретением может также быть введен in vivo методом липофекции. В прошедшее десятилетие наблюдалось увеличение использования липосом для инкапсулирования и трансфекции нуклеиновых кислот in vitro. Синтетические катионные липиды, предназначенные для уменьшения сложностей и опасностей, наблюдающихся при медиируемой липосомами трансфекции, могут быть использованы для получения липосом для in vivo трансфекции гена, кодирующего маркер (Feigner et al., 1987, Proc. Natl. Acad. Sci. U.S.A. 84: 7413; Mackey, et al., 1988, Proc. Natl. Acad. Sci. U.S.A. 85:8027-8031; и Ulmer et al., 1993, Science 259: 1745-1748). Использование катионных липидов может промотировать инкапсулирование отрицательно заряженных нуклеиновых кислот и также промотировать слияние с отрицательно заряженными клеточными мембранами (Feigner and Ringold, 1989, Science 337:387-388). Особенно полезные липидные соединения и композиции для переноса нуклеиновых кислот описаны в международных патентных публикациях WO 95/18863 и WO 96/17823 и в патенте США №5459127. Использование липофекции для введения экзогенных генов в конкретные органы in vivo имеет определенные практические преимущества. Молекулярное нацеливание липосом на специфические клетки является одной из полезных областей применения. Ясно, что нацеливание трансфекции на определенный тип клеток было бы особенно предпочтительным в ткани с клеточной гетерогенностью, такой как поджелудочная железа, печень, почка и мозг. Липиды могут быть химически связаны с другими молекулами для нацеливания (Mackey, et al., 1988, supra). Нацеленные пептиды, например гормоны или нейротрансмиттеры, и белки, такие как антитела, или непептидные молекулы могут быть химически связаны с липосомами.
Другие молекулы также являются полезными для облегчения трансфекции нуклеиновой кислоты in vivo, такие как катионный олигопептид (например, WO 95/21931), пептиды, выделенные из ДНК-связывающих белков (например, WO 96/25508), или катионный полимер (например, WO 95/21931).
Можно также ввести вектор in vivo в виде плазмиды депротеинизированной ДНК (см. патенты США 5693622, 5589466 и 5580859). Могут также быть использованы рецептор-медиируемые подходы к доставке ДНК (Curiel et al., 1992, Hum. Gene Ther. 3: 147-154; и Wu and Wu, 1987, J. Biol. Chem. 262: 4429-4432).
Термин "трансфекция" означает поглощение экзогенной или гетерологичной РНК или ДНК клеткой. Клетка была подвергнута "трансфекции" экзогенной или гетерологичной РНК или ДНК, если такая РНК или ДНК была введена внутрь клетки. Клетка была "трансформирована" экзогенной или гетерологичной РНК или ДНК, если введенная РНК или ДНК вызывает фенотипическое изменение. Трансформирующая РНК или ДНК может быть интегрирована (ковалентно связана) в хромосомную ДНК, входя в геном клетки.
"Трансформация" относится к переносу фрагмента нуклеиновой кислоты в геном организма-хозяина, приводящему к генетически стабильной наследственности. Организмы-хозяева, содержащие трансформированные фрагменты нуклеиновой кислоты, называются "трансгенными", или "рекомбинантными", или "трансформированными" организмами.
Термин "генетическая область" относится к участку молекулы нуклеиновой кислоты или нуклеотидной последовательности, включающему ген, который кодирует полипептид.
Кроме того, рекомбинантный вектор, включающий полинуклеотид в соответствии с изобретением, может включать одно или больше начал репликации в клеточных хозяевах, в которых требуется провести их амплификацию или экспрессию, маркеры или селектируемые маркеры.
Термин "селектируемый маркер" обозначает идентифицирующий фактор, обычно, ген стойкости к антибиотику или химическому агенту, который может быть выбран на основе эффекта маркерного гена, т.е. стойкости к антибиотику, стойкости к гербициду, колориметрических маркеров, ферментов, флуоресцентных маркеров и т.п., где эффект используется для отслеживания наследственности представляющей интерес нуклеиновой кислоты и/или для идентификации клетки или организма, который унаследовал представляющую интерес нуклеиновую кислоту. Примеры селектируемых маркерных генов, известных и используемых в технике, включают: гены, обеспечивающие стойкость к ампициллину, стрептомицину, гентамицину, канамицину, гигромицину, гербициду биалафос, сульфонамиду и т.п.; и гены, используемые в качестве фенотипических маркеров, т.е. гены, регулирующие антоцианин, ген изопентанилтрансферазы и т.п.
Термин "репортерный ген" означает нуклеиновую кислоту, кодирующую идентифицирующий фактор, который может быть идентифицирован на основе эффекта репортерного гена, где эффект используется для отслеживания наследственности представляющей интерес нуклеиновой кислоты, для идентификации клетки или организма, которые унаследовали представляющую интерес нуклеиновую кислоту, и/или для измерения генной экспрессии, индукции или транскрипции. Примеры репортерных генов, известных и используемых в технике, включают: люциферазу (Luc), зеленый флуоресцентный белок (GFP), хлорамфениколацетилтрансферазу (CAT), β-галактозидазу (LacZ), β-глюкуронидазу (Gus) и т.п. Селектируемые маркерные гены могут также считаться репортерными генами.
"Промотор" относится к ДНК последовательности, способной контролировать экспрессию кодирующей последовательности или функциональной РНК. В общем, кодирующая последовательность расположена со стороны 3'-конца от промоторной последовательности. Промоторы могут быть выделены целиком из нативного гена или могут быть составлены из разных элементов, выделенных из разных промоторов, встречающихся в природе, или даже включать синтетические сегменты ДНК. Специалистам в данной области техники понятно, что разные промоторы могут направлять экспрессию гена в разных тканях или типах клеток, или на разных стадиях развития, или в ответ на разные окружающие или физиологические условия. Промоторы, вызывающие экспрессию гена в большинстве типов клеток, в большинстве случаев обычно называются "конститутивными промоторами". Промоторы, вызывающие экспрессию гена в специфическом типе клеток, обычно называются "клетка-специфическими промоторами" или "ткань-специфическими промоторами". Промоторы, вызывающие экспрессию гена на определенной стадии развития или дифференцировки клеток, обычно называются "развитие-специфическими промоторами" или "дифференцировка клеток-специфическими промоторами". Индуцируемые промоторы, вызывающие экспрессию гена после воздействия или обработки клетки агентом, биологической молекулой, химикатом, лигандом, светом и т.п., которые индуцируют промотор, обычно называются "индуцибельными промоторами" или "регулируемыми промоторами". Принято считать, что, поскольку в большинстве случаев точные границы регуляторных последовательностей не были полностью определены, фрагменты ДНК разной длины могут обладать идентичной промоторной активностью.
"Промоторная последовательность" представляет собой регуляторный участок ДНК, способный связывать РНК-полимеразу в клетке и инициировать транскрипцию следующей за ней (в направлении к 3'-концу) кодирующей последовательности. В целях определения настоящего изобретения, промоторная последовательность ограничена на ее 3'-конце сайтом инициации транскрипции и простирается влево (в направлении к 5'-концу), включая минимальное число оснований или элементов, необходимых для инициации транскрипции на уровнях, детектируемых выше фонового. Внутри промоторной последовательности находится сайт инициации транскрипции (удобно определяемый, например, путем картирования нуклеазой S1), а также белок-связывающие домены (консенсусные последовательности), ответственные за связывание РНК-полимеразы.
Кодирующая последовательность находится "под контролем" транскрипционной и трансляционной контрольной последовательности в клетке, если РНК-полимераза транскрибирует кодирующую последовательность в мРНК, которая затем сплайсируется транс-РНК (если кодирующая последовательность содержит интроны) и транслируется в белок, кодируемый кодирующей последовательностью.
"Транскрипционные и трансляционные контрольные последовательности" являются регуляторными ДНК-последовательностями, такими как промоторы, энхансеры, терминаторы и т.п., обеспечивающими экспрессию кодирующей последовательности в клетке-хозяине. В эукариотических клетках контрольными последовательностями являются сигналы полиаденилирования.
Термин "элемент ответа" означает один или больше действующий в цис-положении элемент ДНК, который придает чувствительность промотору, медиируемому посредством взаимодействия с ДНК-связывающими доменами первого химерного гена. Этот элемент ДНК может быть палиндромным (совершенным или несовершенным) в своей последовательности или состоящим из мотивов последовательности или полусайтов, разделенных переменным числом нуклеотидов. Полусайты могут быть подобными или идентичными и могут быть расположены как прямые или обращенные повторы или как отдельно взятый полусайт или мультимеры прилегающих друг к другу полусайтов в тандеме. Элемент ответа может включать минимальный промотор, выделенный из разных организмов, в зависимости от природы клетки или организма, в который должен быть введен элемент ответа. ДНК-связывающий домен первого гибридного белка связывается, в присутствии или отсутствии лиганда, с ДНК последовательностью элемента ответа для инициации или подавления транскрипции следующего за ним гена (генов) под управлением этого элемента ответа. Примеры ДНК последовательностей элементов ответа природного рецептора экдизона включают: RRGGHTCANTGAC/ACYY (см. Cherbas L, et al., (1991), Gene Dev. 5, 120-131); AGGTCAN(n)AGGTCA, где N(n) может быть одним или больше спейсерным нуклеотидом (см. D'Avino P.P., et al. (1995), Mol. Cell. Endocrinol., 113, 1-9); и GGGTTGAATGAATTT (см. Antoniewski С., et al. (1994). Mol. Cell Biol., 14, 4465-4474).
Термин "функционально связанный" относится к ассоциации последовательностей нуклеиновой кислоты в одном фрагменте нуклеиновой кислоты таким образом, что одна из них влияет на функцию другой. Например, промотор функционально связан с кодирующей последовательностью, если он способен влиять на экспрессию этой кодирующей последовательности (т.е. эта кодирующая последовательность находится под транскрипционным контролем промотора). Кодирующие последовательности могут быть функционально связаны с регуляторными последовательностями в смысловой или антисмысловой ориентации.
Термин "экспрессия", в используемом тут значении, относится к транскрипции и стабильному накоплению смысловой (мРНК) или антисмысловой РНК, образующейся из нуклеиновой кислоты или полинуклеотида. Экспрессия может также относиться к трансляции мРНК в белок или полипептид.
Термины "кассета", "кассета экспрессии" и "генная кассета экспрессии" относятся к сегменту ДНК, который может быть вставлен в нуклеиновую кислоту или полинуклеотид по специфическим сайтам рестрикции или путем гомологичной рекомбинации. Сегмент ДНК включает полинуклеотид, который кодирует представляющий интерес полипептид, и кассета и сайты рестрикции рассчитаны на то, чтобы обеспечить инсерцию кассеты в соответствующую рамку считывания для транскрипции и трансляции. "Кассета трансформации" относится к специфическому вектору, включающему полинуклеотид, кодирующий представляющий интерес полипептид и содержащий, помимо полинуклеотида, элементы, способствующие трансформации определенной клетки-хозяина. Кассеты, кассеты экспрессии, кассеты генной экспрессии и кассеты трансформации по изобретению могут также включать элементы, позволяющие усиливать экспрессию полинуклеотида, кодирующего представляющий интерес полипептид, в клетке-хозяине. Эти элементы могут включать, без ограничения: промотор, минимальный промотор, энхансер, элемент ответа, терминирующую последовательность, полиаденилирующую последовательность и т.п.
В целях данного изобретения, термин "генный переключатель" относится к комбинации элемента ответа, ассоциированного с промотором, и системы на основе EcR, которая в присутствии одного или больше лигандов модулирует экспрессию гена, в который встроены элемент ответа и промотор.
Термины "модулировать" и "модулирует" означают индуцирование, ослабление или ингибирование экспрессии нуклеиновой кислоты или гена, приводящее к соответствующей индукции, уменьшению или ингибированию продуцирования белка или полипептида.
Плазмиды или векторы в соответствии с изобретением могут далее включать по меньшей мере один промотор, пригодный для управления экспрессией гена в клетке-хозяине. Термин "вектор экспрессии" означает вектор, плазмиду или средство транспорта, обеспечивающее возможность экспрессии вставленной последовательности нуклеиновой кислоты после трансформации в хозяина. Клонированный ген, т.е. инсерцированная последовательность нуклеиновой кислоты, обычно помещается под управление контрольных элементов, таких как промотор, минимальный промотор, энхансер и т.п. Имеются многочисленные участки контроля инициации или промоторы, пригодные для управления экспрессией нуклеиновой кислоты в требуемой клетке-хозяине, известные специалистам в данной области техники. Практически любой промотор, способный управлять этими генами, является пригодным для настоящего изобретения, включая, без ограничений: вирусные промоторы, бактериальные промоторы, промоторы животных, промоторы млекопитающих, синтетические промоторы, конститутивные промоторы, ткань-специфические промоторы, развитие-специфические промоторы, индуцибельные промоторы, светочувствительные промоторы; CYC1, HIS3, GAL1, GAL4, GAL10, ADH1, PGK, РНO5, GAPDH, ADC1, TRP1, URA3, LEU2, ENO, TPI, промоторы щелочной фосфатазы (пригодны для экспрессии в Saccharomyces); промотор АОХ1 (пригоден для экспрессии в Pichia); промоторы β-лактамазы, lac, ara, tet, trp, IPL, IPR, T7, tac и trc (пригодны для экспрессии в Eschenchia coil); светорегулируемые, семя-специфические, пыльца-специфические, яичник-специфические, патогенез- или болезнь-ассоциированные, вируса мозаики цветной капусты 35S, минимальный CMV 35S, вируса мозаики жилок маниоки (CsVMV), хлорофилл а/b связывающий белок, рибулозы 1, 5-бифосфаткарбоксилазы, росток-специфические, корень-специфические, хитиназы, стресс-индуцибельные, палочкообразного вируса tungro риса, суперпромотор растений, лейцинаминопептидазы картофеля, нитратредуктазы, маннопинсинтазы, нопалинсинтази, убиквитина, белка зеина и антоцианина промоторы (пригодны для экспрессии в растительных клетках); промоторы животных и млекопитающих, известные специалистам, включают, без ограничения, SV40 ранний (SV40e) промоторный участок, промотор, содержащийся в 3'-длинном терминальном повторе (LTR), вирус саркомы Рауса (RSV), промоторы EIA или большой поздний промотор (MLP) генов аденовирусов (Ad), ранний промотор цитомегаловируса (CMV), промотор тимидинкиназы (ТК) вируса простого герпеса (HSV), промотор IE1 абакуловируса, промотор фактора удлинения 1 альфа (EF1), промотор фосфоглицераткиназы (PGK), промотор убиквитина (Ubc), промотор альбумина, промотор и участки транскрипционного контроля регуляторных последовательностей металлотионеина-L мыши, вездесущие промоторы (HPRT, виментин, α-актин, тубулин и т.п.), промоторы промежуточных филаментов (десмин, нейрофиламенты, кератин, GFAP и т.п.), промоторы терапевтических генов (MDR, CFTR или типа фактора VIII и т.п.), патогенез- или болезнь-ассоциированные промоторы, и промоторы, проявляющие тканеспецифичность и используемые в трансгенных животных, такие как контрольный участок гена эластазы I, проявляющий активность в ацинарных клетках поджелудочной железы; контрольный участок гена инсулина, проявляющий активность в панкреатических бета-клетках, контрольный участок гена иммуноглобулина, проявляющий активность в лимфоидных клетках, контрольный участок вируса опухоли молочной железы мыши, проявляющий активность в тестикулярных клетках, клетках молочной железы, лимфоидных клетках и мастоцитах; контрольные участки гена альбумина, Аро AI и Аро AII, проявляющие активность в печени, контрольный участок гена альфа-фетопротеина, проявляющий активность в печени, контрольный участок гена альфа-1-антитрипсина, проявляющий активность в печени, контрольный участок гена бета-глобина, проявляющий активность в миелоидных клетках, контрольный участок гена основного белка миелина, проявляющий активность в олигодендроцитных клетках мозга, контрольный участок гена легкой цепи-2 миозина, проявляющий активность в скелетных мышцах, и контрольный участок гена гонадотропин-рилизинг-гормона, проявляющий активность в гипоталамусе, промотор пируваткиназы, промотор виллина, промотор кишечного белка связывания жирных кислот, промотор α-актина гладких мышечных клеток и т.п. Кроме того, эти последовательности экспрессии могут быть модифицированы путем добавления энхансерных или регуляторных последовательностей и т.п.
Энхансеры, которые могут быть использованы в вариантах исполнений изобретения включают, без ограничения: энхансер SV40, энхансер цитомегаловируса (CMV), энхансер фактора удлинения 1 (EF1), энхансеры дрожжей, энхансеры вирусных генов и т.п.
Контрольные участки терминации, т.е. терминаторные или полиаденилирующие последовательности, также могут быть выделены из различных генов, нативных для предпочтительных хозяев. Необязательно, сайт терминации может не быть необходимым, однако, более предпочтительно, он присутствует. В предпочтительном варианте исполнения изобретения, контрольный участок терминации может включать или быть выделенным из синтетической последовательности, синтетического сигнала полиаденилирования, позднего сигнала полиаденилирования SV40, сигнала полиаденилирования SV40, сигнала полиаденилирования гормона роста крупного рогатого скота (BGH), вирусные терминаторные последовательности и т.п.
Термины "3'-некодирующие последовательности" или "3'-нетранслированный участок (UTR)" относятся к ДНК-последовательности, расположенной справа (3') от кодирующей последовательности и могут включать последовательности распознавания полиаденилирования [поли(А)] и другие последовательности, кодирующие регуляторные сигналы, способные влиять на процессинг мРНК или экспрессию гена. Сигнал полиаденилирования обычно характеризуется влиянием на добавление хвостов полиадениловой кислоты к 3'-концу прекурсора мРНК.
"Регуляторный участок" означает последовательность нуклеиновой кислоты, которая регулирует экспрессию второй последовательности нуклеиновой кислоты. Регуляторный участок может включать последовательности, которые в природных условиях отвечают за экспрессию определенной нуклеиновой кислоты (гомологичный участок), или может включать последовательности другого происхождения, отвественные за экспрессию других белков или даже синтетических белков (гетерологичный участок). В частности, последовательности могут быть последовательностями прокариотическтх, эукариотических или вирусных генов или производными последовательностей, стимулирующих или подавляющих транскрипцию гена специфическим или неспецифическим образом и индуцибельным или неиндуцибельным образом. Регуляторные участки включают начала репликации, сайты сплайсинга РНК, промоторы, энхансеры, последовательности терминации транскрипции и сигнальные последовательности, которые направляют полипептид на секреторные пути целевой клетки.
Регуляторный участок из "гетерологичного источника" представляет собой регуляторный участок, который в природных условиях не ассоциирован с экспрессируемой нуклеиновой кислотой. Гетерологичные регуляторные участки включают регуляторные участки от разных видов, регуляторные участки из других генов, гибридные регуляторные последовательности и регуляторные последовательности, которые не встречаются в природе, а были сконструированы рядовым специалистом в данной области техники.
"РНК-транскрипт" относится к продукту, образующемуся в результате катализируемой РНК полимеразой транскрипции ДНК последовательности. Если РНК-транскрипт является полностью комплементарной копией ДНК-последовательности, то он называется первичным транскриптом, или же он может быть РНК-последовательностью, полученной в результате посттранскрипционного процессинга первичного транскрипта, и тогда называется зрелой РНК. "Информационная (матричная) РНК (мРНК)" относится к РНК, которая не содержит интронов и может быть транслирована в белок клеткой. "кДНК" относится к двухцепочечной ДНК, комплементарной по отношению к и полученной из мРНК. "Смысловая" РНК относится к РНК-транскрипту, который включает мРНК и потому может быть транслирован в белок клеткой. "Антисмысловая РНК" относится к РНК-транскрипту, который является комплементарным по отношению ко всему или части целевого первичного транскрипта или мРНК и блокирует экспрессию целевого гена. Комплементарность антисмысловой РНК может проявляться по отношению к любой части специфического генного транскрипта, т.е. 5'-некодирующей последовательности, 3'-некодирующей последовательности или кодирующей последовательности. "Функциональная РНК" относится к антисмысловой РНК, рибозимной РНК или другой РНК, которая еще не была транслирована, но оказывает влияние на клеточные процессы,
"Полипептид" представляет собой полимерное соединение, состоящее из ковалентно связанных аминокислотных остатков. Аминокислоты имеют следующую общую структуру:
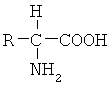
Аминокислоты классифицируются на семь групп на основании боковой цепи R: (1) алифатические боковые цепи, (2) боковые цепи, содержащие гидроксильную (ОН) группу, (3) боковые цепи, содержащие атомы серы, (4) боковые цепи, содержащие кислотную или амидную группу, (5) боковые цепи, содержащие основную группу, (6) боковые цепи, содержащие ароматическое кольцо, и (7) пролин, иминокислота, в которой боковая цепь слита с аминогруппой. Полипептид по изобретению предпочтительно включает по меньшей мере около 14 аминокислот.
"Белок" представляет собой полипептид, выполняющий структурную или функциональную роль в живой клетке.
"Изолированный полипептид" или "изолированный белок" представляет собой полипептид или белок, который по существу не содержит соединений, обычно ассоциированных с ним в его природном состоянии (например, других белков или полипептидов, нуклеиновых кислот, углеводов, липидов). "Изолированный" не исключает искусственные или синтетические смеси с другими соединениями или присутствие загрязнений, не влияющих на биологическую активность, которые могут присутствовать, например, вследствие неполной очистки, добавления стабилизаторов или составления фармацевтически приемлемого препарата.
"Субституционный мутантный полипептид" или "субституционный мутант" следует понимать как мутантный полипептид, включающий замещение по меньшей мере одной (1) аминокислоты дикого типа или природной аминокислоты на другую аминокислоту по отношению к полипептиду дикого типа или природному полипептиду. Субституционный мутантный полипептид может включать только одно (1) замещение аминокислоты дикого типа или природной и может быть назван "точковым мутантным" или "одноточковым мутантным" полипептидом. Альтернативно, субституционный мутантный полипептид может включать замещение двух (2) или более аминокислот дикого типа или природных на 2 или более аминокислоты по отношению к полипептиду дикого типа или природному. В соответствии с изобретением, полипептид лигандсвязывающего домена ядерного рецептора группы Н, содержащий мутацию замещения, включает замещение по меньшей мере одной (1) аминокислоты дикого типа или природной на другую аминокислоту по отношению к полипептиду дикого типа или природного лигандсвязывающего домена ядерного рецептора группы Н.
В тех случаях, когда субституционный мутантный полипептид включает замещение двух (2) или больше аминокислот дикого типа или природных, это замещение может включать эквивалентное число аминокислот дикого типа или природных, удаляемых при замещении, т.е. 2 аминокислоты дикого типа или природные, замещаются на 2 аминокислоты недикого типа или неприродные, или неэквивалентное число аминокислот дикого типа, удаляемых при замещении, т.е. 2 аминокислоты дикого типа, замещаются на 1 аминокислоту недикого типа (мутация замещение + делеция) или 2 аминокислоты дикого типа замещаются на 3 аминокислоты недикого типа (мутация замещение + инсерция). Субституционные мутанты могут быть описаны с помощью системы сокращенной номенклатуры, с указанием замещаемого аминокислотного остатка и его номера в исходной полипептидной последовательности и нового замещенного аминокислотного остатка. Например, субституционный мутант, в котором замещен двадцатый (20th) аминокислотный остаток полипептида, может быть сокращенно обозначен "x20z", где "х" обозначает замещаемую аминокислоту, "20" указывает положение аминокислотного остатка или его номер в полипептиде и "z" обозначает новую замещающую аминокислоту. Таким образом, субституционный мутант, сокращенно обозначенный взаимозаменяемо "Е20А" или "Glu20Ala", указывает, что мутант включает остаток аланина (обычно сокращенно обозначаемый специалистами "А" или "Ala") вместо глутаминовой кислоты (обычно сокращенно обозначаемой специалистами "Е" или "Glu") в положении 20 полипептида. Мутация или мутант могут быть любыми изменениями, включая, без ограничений, замещения, делеции, инсерции или любую их комбинацию.
Субституционная мутация может быть выполнена любым методом мутагенеза, известным специалистам, включая, без ограничений, in vitro сайт-специфический мутагенез (Hutchinson, С., et al., 1978, J. Biol. Chem. 253: 6551; Zoller and Smith, 1984, DNA 3: 479-488; Oliphant et al., 1986, ген 44: 177; Hutchinson et al., 1986, Proc. Natl. Acad. Sci. U.S.A. 83: 710), использование ТАВ®-линкеров (Pharmacia), расщепление эндонуклеазой рестрикции/делеция и замещение фрагмента, ПЦР-медиируемый/олигонуклеотид-направленный мутагенез и т.п. Методы на основе ПЦР являются предпочтительными для сайт-специфического мутагенеза (см. Higuchi, 1989, "Using PCR to Engineer DNA", in PCR Technology: Principles and Applications for DNA Amplification, H. Eriich, ed., Stockton Press, глава 6, с.61-70).
"Фрагмент" полипептида в соответствии с изобретением следует понимать как обозначающий полипептид, аминокислотная последовательность которого короче, чем полипептида сравнения, и включает, по всей длине участка, совпадающего с этими полипептидами сравнения, идентичную аминокислотную последовательность. Такие фрагменты могут, в соответствующих случаях, входить в состав большего по размеру полипептида, частью которого они являются. Такие фрагменты полипептида в соответствии с изобретением могут иметь длину по меньшей мере 2, 3, 4, 5, 6, 8, 10, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 25, 26, 30, 35, 40, 45, 50, 100, 200, 240 или 300 аминокислот.
"Вариант" полипептида или белка представляет собой любой аналог, фрагмент, производное или мутант, полученный из полипептида или белка и сохраняющий, по меньшей мере, одно биологическое свойство полипептида или белка. Разные варианты полипептида или белка могут существовать в природе. Эти варианты могут быть аллельными вариациями, характеризующимися различиями в нуклеотидных последовательностях структурного гена, кодирующего белок, или могут включать различные сплайсинговые или посттрансляционные модификации. Квалифицированный специалист может получить варианты, имеющие одиночные или множественные замещения, делеции, добавления или замены аминокислот. Эти варианты могут включать, в том числе: (а) варианты, в которых один или больше аминокислотных остатков замещены консервативными или неконсервативными аминокислотами, (b) варианты, в которых одна или больше аминокислот добавлены к полипептиду или белку, (с) варианты, в которых одна или больше аминокислот включают замещающую группу, и (а) варианты, в которых полипептид или белок слит с другим полипептидом, таким как сывороточный альбумин. Методики получения этих вариантов, включая генетические (супрессии, делеции, мутации и т.д.), химические и ферментативные методы, известны рядовым специалистам в данной области техники. Вариант полипептида предпочтительно включает по меньшей мере около 14 аминокислот.
"Гетерологичный белок" относится к белку, в природных условиях не вырабатываемому в клетке.
"Зрелый белок" относится к подвергнутому посттрансляционной обработке полипептиду; т.е. такому, из которого были удалены любые пре- или пропептиды, присутствующие в первичном продукте трансляции. "Прекурсорный" белок относится к первичному продукту трансляции мРНК; т.е. с присутствующими пре- и пропептидами. Пре- и пропептиды могут быть, без ограничения, внутриклеточными сигналами локализации.
Термин "сигнальный пептид" относится к аминотерминальному полипептиду, являющемуся предшественником секретируемого зрелого белка. Сигнальный пептид отщепляется от зрелого белка и потому не присутствует в нем. Сигнальные пептиды имеют функцию направления и транслокации секретируемых белков через клеточные мембраны. Сигнальный пептид также называется сигнальным белком.
"Сигнальная последовательность" находится в начале кодирующей последовательности экспрессируемого белка на поверхности клетки. Эта последовательность кодирует сигнальный пептид, N-терминальный по отношению к зрелому полипептиду, который указывает клетке-хозяину транслоцировать полипептид. Термин "последовательность сигнала транслокации" используется тут по отношению к этому виду сигнальной последовательности. Последовательности сигнала транслокации могут быть ассоциированы с различными белками, нативными для эукариотов и прокариотов, и часто являются функциональными в обоих типах организмов.
Термин "гомология" относится к проценту идентичности между двумя полинуклеотидными или двумя полипептидными фрагментами. Соответствие между одним и вторым фрагментами последовательностей может быть определено методами, известными специалистам. Например, гомология может быть определена прямым сравнением информации о последовательности для двух полипептидных молекул путем совмещения информации о последовательностях с использованием легко доступных компьютерных программ. Альтернативно, гомология может быть определена путем гибридизации полинуклеотидов в условиях образования стабильных дуплексов между гомологичными участками, с последующим расщеплением одноцепочечно-специфичной нуклеазой (нуклеазами) и определением размера отщепленных фрагментов.
В используемом тут значении, термин "гомологичный" во всех его грамматических формах и вариантах написания относится к соотношению между белками, имеющими "общее эволюционное происхождение", включая белки из суперсемейств (например, суперсемейство иммуноглобулинов) и гомологичные белки от разных видов (например, легкая цепь миозина и т.д.) (Reeck et al., 1987, Cell 50: 667). Такие белки (и кодируемые ими гены) имеют гомологию последовательностей, что отражается в высокой степени подобия последовательностей. Однако в практическом использовании и в данной заявке, термин "гомологичный", модифицированный прилагательным, таким как "высоко", может относиться к подобности последовательностей, а не к общему эволюционному происхождению.
Соответственно, термин "подобие последовательностей" во всех его грамматических формах относится к степени идентичности или соответствия между нуклеиновыми кислотами или аминокислотными последовательностями белков, которые могут иметь общее эволюционное происхождение или не иметь его (см. Reeck et al., 1987, Cell 50:667).
В конкретном варианте исполнения, две ДНК-последовательности являются "существенно гомологичными" или "существенно подобными", если по меньшей мере около 50% (предпочтительно, по меньшей мере около 75%, и наиболее предпочтительно, по меньшей мере около 90 или 95%) нуклеотидов совпадают на определенном отрезке ДНК-последовательности. Последовательности, являющиеся существенно гомологичными, могут быть идентифицированы путем сравнения последовательностей с использованием стандартного программного обеспечения, имеющегося в банках данных последовательностей, или с помощью эксперимента по саузерн-гибридизации, например, в суровых условиях, определенных для данной конкретной системы. Определение соответствующих условий гибридизации находится в пределах возможностей специалиста в данной области техники. См., например, Sambrook et al., 1989, supra.
В используемом тут значении, "существенно подобный" относится к фрагментам нуклеиновой кислоты, у которых изменения одного или больше нуклеотидных оснований приводят к замещению одной или больше аминокислот, но не влияют на функциональные свойства белка, кодируемого ДНК-последовательностью. "Существенно подобный" относится также к фрагментам нуклеиновой кислоты, в которых изменения одного или больше нуклеотидных оснований не влияют на способность фрагмента нуклеиновой кислоты медиировать изменение генной экспрессии по антисмысловой или ко-супрессорной технологии. "Существенно подобный" также относится к модификациям фрагментов нуклеиновой кислоты по настоящему изобретению, таким как делеция или инсерция одного или больше нуклеотидных оснований, которые существенно не влияют на функциональные свойства образующегося транскрипта. Поэтому следует понимать, что изобретение охватывает не только конкретные типичные последовательности. Каждая из предложенных модификаций является вполне доступной для специалистов в данной области техники, как и определение степени сохранения биологической активности кодируемых продуктов.
Кроме того, квалифицированному специалисту понятно, что существенно подобные последовательности, охватываемые настоящим изобретением, также определяются их способностью к гибридизации в суровых условиях (0,1×SSC, 0,1% ДСН, 65°С и промывка 2×SSC, 0,1% ДСН, а затем 0,1×SSC, 0,1% ДСН), с приведенными тут в качестве примера последовательностями. Существенно подобными фрагментами нуклеиновых кислот по настоящему изобретению являются такие фрагменты нуклеиновых кислот, у которых ДНК-последовательности являются по меньшей мере на 70% идентичными описанным тут ДНК-последовательностям фрагментов нуклеиновых кислот. Предпочтительными существенно подобными фрагментами нуклеиновых кислот по настоящему изобретению являются такие фрагменты нуклеиновых кислот, в которых ДНК-последовательности по меньшей мере на 80% идентичны описанным тут ДНК-последовательностям фрагментов нуклеиновых кислот. Более предпочтительные фрагменты нуклеиновых кислот по меньшей мере на 90% идентичны ДНК-последовательностям описанных тут фрагментов нуклеиновых кислот. Еще более предпочтительными являются фрагменты нуклеиновых кислот, которые по меньшей мере на 95% идентичны описанным тут ДНК-последовательностям фрагментов нуклеиновых кислот.
Две аминокислотные последовательности являются "существенно гомологичными" или "существенно подобными", если более чем примерно 40% аминокислот являются идентичными или более чем 60% являются подобными (функционально идентичными). Предпочтительно, подобные или гомологичные последовательности идентифицируют путем совмещения последовательностей с использованием, например, программы наложения GCG (Genetics Computer Group, Program Manual for the GCG Package, Version 7, Madison, Wisconsin).
Термин "соответствующий" используется тут по отношению к подобным или гомологичным последовательностям, независимо от того, является точное положение идентичным или отличным от молекулы, по отношению к которой измеряют подобие или гомологию. Совмещение последовательностей нуклеиновых кислот или аминокислот может включать пробелы. Таким образом, термин "соответствующий" относится к подобию последовательностей, а не к нумерации аминокислотных остатков или нуклеотидных оснований.
"Существенная часть" аминокислотной или нуклеотидной последовательности включает достаточную часть аминокислотной последовательности полипептида или нуклеотидной последовательности гена для того, чтобы предположительно идентифицировать этот полипептид или ген путем оценки последовательности вручную специалистом в данной области техники или путем автоматизированного компьютерного сравнения и идентификации последовательностей с использованием таких алгоритмов, как BLAST (Basic Local Alignment Search Tool; Altschul, S.F., et al. (1993) J. Mol. Biol. 215: 403-410; см. также www.ncbi.nlm.nih.gov/BLAST/). В общем, последовательность из десяти или более смежных аминокислот или тридцати или более нуклеотидов необходима для предположительной идентификации полипептида или последовательности нуклеиновой кислоты как гомологичной по отношению к известному белку или гену. Более того, что касается нуклеотидных последовательностей, то ген-специфические олигонуклеотидные зонды, включающие 20-30 последовательных нуклеотидов, могут быть использованы в последовательность-зависимых методах идентификации (например, саузерн-гибридизация) и выделения (например, in situ гибридизация бактериальных колоний или бляшек бактериофагов) гена. Кроме того, короткие олигонуклеотиды из 12-15 оснований могут быть использованы в качестве праймеров амплификации в ПЦР для получения определенного фрагмента нуклеиновой кислоты, содержащего праймеры. Соответственно, "существенная часть" нуклеотидной последовательности включает часть последовательности, достаточную для специфической идентификации и/или выделения фрагмента нуклеиновой кислоты, включающего эту последовательность.
Термин "процент идентичности", как известно специалистам, обозначает соотношение между двумя или более полипептидными последовательностями или двумя или более полинуклеотидными последовательностями, определенное путем сравнения последовательностей. В технике, "идентичность" также означает степень соответствия полипептидных или полинуклеотидных последовательностей, в зависимости от обстоятельств, определенную путем определения соответствия между цепочками таких последовательностей. "Идентичность" и "подобие" могут быть легко рассчитаны известными методами, включая, без ограничений, описанные в: Computational Molecular Biology (Lesk, A.M., ed.), Oxford University Press, New York (1988); Biocomputing: Informatics and Genome Projects (Smith, D.W., ed.), Academic Press, New York (1993); Computer Analysis of Sequence Data, Part I (Griffin, A.M., and Griffin, H.G., eds.), Humana Press, New Jersey (1994); Sequence Analysis in Molecular Biology (von Heinje, G., ed.), Academic Press (1987); и Sequence Analysis Primer (Gribskov, M. and Devereux, J., eds.), Stockton Press, New York (1991). Предпочтительные методы определения идентичности рассчитаны на достижения наилучшего совпадения между исследуемыми последовательностями. Методы определения идентичности и подобия кодифицированы в общедоступных компьютерных программах. Выравнивание последовательностей и расчеты процента идентичности могут быть выполнены с помощью программы Megalign из комплекта программ для биоинформатических вычислений LASERGENE (DNASTAR Inc., Madison, WI). Множественное выравнивание последовательностей может быть выполнено с помощью метода выравнивания Clustal (Higgins and Sharp (1989) CABIOS. 5:151-153) с параметрами по умолчанию (GAP PENALTY=10, GAP LENGTH PENALTY=10). Параметры по умолчанию для попарного выравнивания с использованием метода Clustal могут быть выбраны такими: KTUPLE 1, GAP PENALTY=3, WLNDOW=5 и DIAGONALS SAVED=5.
Термин "программное обеспечение для анализа последовательностей" относится к любому компьютерному алгоритму или прикладной компьютерной программе, пригодной для анализа нуклеотидной или аминокислотной последовательности. "Программное обеспечение для анализа последовательностей" может быть коммерчески доступным или разработано независимо. Типичное программное обеспечение для анализа последовательностей включает, без ограничений, комплект программ GCG (Wisconsin Package Version 9,0, Genetics Computer Group (GCG), Madison, WI), BLASTP, BLASTN, BLASTX (Altschul et al., J. Mol. Biol. 215: 403-410 (1990)) и DNASTAR (DNASTAR, Inc. 1228 S. Park St. Madison, WI53715 USA). В контексте данной заявки следует понимать, что в случаях использования для анализа программного обеспечения для анализа последовательностей, результаты анализа будут основаны на "принятых по умолчанию значениях" указанной программы, если не оговорено иное. В используемом тут значении "принятые по умолчанию значения" означают любой набор значений или параметров, которые прикладная программа первоначально загружает при первом запуске.
"Синтетические гены" могут быть собраны из олигонуклеотидных структурных блоков, которые химически синтезируются с использованием процедур, известных специалистам в данной области техники. Эти структурные блоки лигируют и отжигают с образованием сегментов гена, которые затем ферментативно собирают в целый ген. "Химически синтезированный", по отношению к ДНК-последовательности, означает, что составляющие ее нуклеотиды были собраны in vitro. Ручной химический синтез ДНК может быть осуществлен с помощью хорошо отработанных процедур, или же автоматизированный химический синтез может быть проведен с использованием одной из ряда коммерчески доступных машин. Соответственно, гены могут быть изменены для достижения оптимальной генной экспрессии на основе оптимизации нуклеотидной последовательности с учетом кодоновых особенностей клетки-хозяина. Квалифицированному специалисту понятно, что вероятность успешной экспрессии генов возрастает, если используются кодоны, предпочтительные для хозяина. Определение предпочтительных кодонов может быть основано на исследовании выделенных из клетки-хозяина генов, для которых имеется информация о последовательностях.
В используемом тут значении, две или более индивидуально функционирующие системы генной регуляции называются "ортогональными", если а) модуляция каждой из данных систем ее соответствующим лигандом, в выбранной концентрации, приводит к измеримому изменению величины экспрессии гена этой системой, и b) изменение является статистически значимо отличным от изменения экспрессии всех других систем, одновременно функционирующих в клетке, ткани или организме, независимо от одновременного или последовательного характера проведения фактической модуляции. Предпочтительно, модуляция каждой индивидуально функционирующей системы генной регуляции вызывает изменение генной экспрессии, по меньшей мере в 2 раза большее, чем для всех других функционирующих систем в клетке, ткани или организме. Более предпочтительно, изменение является по меньшей мере в 5 раз большим. Еще более предпочтительно, изменение является по меньшей мере в 10 раз большим. Еще более предпочтительно, изменение является по меньшей мере в 100 раз большим. Еще более предпочтительно, изменение является по меньшей мере в 500 раз большим. Идеально, модуляция каждой из данных систем ее соответствующим лигандом в выбранной концентрации приводит к измеримому изменению величины экспрессии гена этой системы при отсутствии измеримых изменений экспрессии во всех других системах, функционирующих в клетке, ткани или организме. В таких случаях, множественно индуцибельная система генной регуляции называется "полностью ортогональной". Настоящее изобретение полезно для поиска ортогональных лигандов и ортогональных систем генной экспрессии на основе рецепторов, таких как описанные в находящейся одновременно на рассмотрении заявке США №09/965697, которая целиком включена сюда по ссылке.
Система модулирования генной экспрессии по изобретению
Заявители идентифицировали тут аминокислотные остатки, принимающие участие в связывании лиганда с лигандсвязывающим доменом ядерного рецептора группы Н, которые влияют на чувствительность к лигандам и величину индукции в системе экспрессии индуцибельного гена на основе рецептора экдизона. Заявители описывают тут конструирование ядерных рецепторов группы Н, включающих субституционные мутации (которые называются тут "субституционные мутанты") по этим критическим остаткам и демонстрируют, что эти субституционные мутантные ядерные рецепторы пригодны для использования в способах модулирования генной экспрессии. Как представлено тут, предложенные заявителями новые субституционные мутантные ядерные рецепторы и их использование в системе экспрессии индуцибельного гена на основе ядерного рецептора обеспечивают получение усовершенствованной системы экспрессии индуцибельного гена в прокариотических и эукариотических клетках-хозяевах, в которой чувствительность к лигандам и степень трансактивации могут быть выбраны по желанию, в зависимости от области применения.
Таким образом, настоящее изобретение относится к новым субституционным мутантным полинуклеотидам и полипептидам ядерных рецепторов группы Н, системе экспрессии индуцибельного гена на основе ядерного рецептора, включающей такие мутированные полинуклеотиды и полипептиды ядерных рецепторов группы Н, и способам модулирования экспрессии гена в клетке-хозяине с использованием такой системы экспрессии индуцибельного гена на основе ядерного рецептора.
В частности, настоящее изобретение относится к системе модулирования генной экспрессии, включающей по меньшей мере одну кассету генной экспрессии, способную экспрессироваться в клетке-хозяине, содержащей полинуклеотид, кодирующий полипептид, включающий лигандсвязывающий домен ядерного рецептора группы Н, имеющий мутацию замещения. Предпочтительно, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, получают из рецептора экдизона, вездесущего рецептора, сиротского рецептора 1, NER-1, ядерного рецептора стероидного гормона 1, ретиноидного Х-рецептор-взаимодействующего белка 15, X-рецептора печени β, белка, подобного рецептору стероидного гормона, X-рецептора печени, Х-рецептора печени α, фарнезоидного Х-рецептора, рецептор-взаимодействующего белка 14 и рецептора фарнезола. Более предпочтительно, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, получают из рецептора экдизона.
В конкретном варианте исполнения, система модулирования генной экспрессии включает кассету генной экспрессии, содержащую полинуклеотид, который кодирует полипептид, включающий домен трансактивации, ДНК-связывающий домен, который распознает элемент ответа, ассоциированный с геном, экспрессия которого модулируется; и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения. Система модулирования генной экспрессии может дополнительно включать вторую кассету генной экспрессии, содержащую: i) элемент ответа, распознаваемый ДНК-связывающим доменом кодируемого полипептида первой кассеты генной экспрессии; ii) промотор, который активируется доменом трансактивации кодируемого полипептида первой кассеты генной экспрессии; и iii) ген, экспрессия которого модулируется.
В другом конкретном варианте исполнения, система модулирования генной экспрессии включает кассету генной экспрессии, содержащую а) полинуклеотид, который кодирует полипептид, включающий домен трансактивации, ДНК-связывающий домен, который распознает элемент ответа, ассоциированный с геном, экспрессия которого модулируется; и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, и b) лигандсвязывающий домен второго ядерного рецептора, выбранного из группы, состоящей из лигандсвязывающего домена ретиноидного Х-рецептора позвоночных, лигандсвязывающего домена ретиноидного Х-рецептора беспозвоночных, лигандсвязывающего домена белка ultraspiracle и химерного лигандсвязывающего домена, включающего два полипептидных фрагмента, где первый полипептидный фрагмент выделен из лигандсвязывающего домена ретиноидного Х-рецептора позвоночных, лигандсвязывающего домена ретиноидного Х-рецептора беспозвоночных или лигандсвязывающего домена белка ultraspiracle и второй полипептидный фрагмент получен из другого лигандсвязывающего домена ретиноидного Х-рецептора позвоночных, лигандсвязывающего домена ретиноидного Х-рецептора беспозвоночных или лигандсвязывающего домена белка ultraspiracle. Система модулирования генной экспрессии может дополнительно включать вторую кассету генной экспрессии, включающую: i) элемент ответа, распознаваемый ДНК-связывающим доменом кодируемого полипептида первой кассеты генной экспрессии; ii) промотор, который активируется доменом трансактивации кодируемого полипептида первой кассеты генной экспрессии; и iii) ген, экспрессия которого модулируется.
В другом конкретном варианте исполнения, система модулирования генной экспрессии включает первую кассету генной экспрессии, содержащую полинуклеотид, кодирующий первый полипептид, включающий ДНК-связывающий домен, который распознает элемент ответа, ассоциированный с геном, экспрессия которого модулируется, и лигандсвязывающий домен ядерного рецептора, и вторую кассету генной экспрессии, содержащую полинуклеотид, кодирующий второй полипептид, включающий домен трансактивации и лигандсвязывающий домен ядерного рецептора, где один из лигандсвязывающих доменов ядерного рецептора представляет собой лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения. В предпочтительном варианте исполнения, первый полипептид по существу не содержит домена трансактивации, а второй полипептид по существу не содержит ДНК-связывающего домена. В целях изобретения, "по существу не содержит" означает, что рассматриваемый белок не содержит последовательности рассматриваемого домена, достаточной для обеспечения активации или связывающей активности. Система модулирования генной экспрессии может дополнительно включать третью кассету генной экспрессии, содержащую: i) элемент ответа, распознаваемый ДНК-связывающим доменом первого полипептида первой кассеты генной экспрессии; ii) промотор, который активируется доменом трансактивации второго полипептида второй кассеты генной экспрессии; и iii) ген, экспрессия которого модулируется.
В тех случаях, когда только один лигандсвязывающий домен ядерного рецептора является лигандсвязывающим доменом группы Н, включающим мутацию замещения, другой лигандсвязывающий домен ядерного рецептора может быть получен из любого другого ядерного рецептора, образующего димер с лигандсвязывающим доменом группы Н, включающим мутацию замещения. Например, если лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является лигандсвязывающим доменом рецептора экдизона, включающим мутацию замещения, другой лигандсвязывающий домен ядерного рецептора ("партнер") может быть получен из рецептора экдизона, ретиноидного Х-рецептора (RXR) позвоночных, RXR беспозвоночных, белка ultraspiracle (USP) или химерного ядерного рецептора, содержащего по меньшей мере два разных полипептидных фрагмента лигандсвязывающих доменов ядерных рецепторов, выбранных из группы, состоящей из RXR позвоночных, RXR беспозвоночных и RXR (см. находящиеся одновременно на рассмотрении заявки PCT/US01/09050, US 60/294814 и US 60/294819, включенные сюда целиком в качестве ссылок). "Партнер" лигандсвязывающего домена ядерного рецептора может дополнительно включать мутацию усечения, мутацию делеции, субституционную мутацию или другую модификацию.
Предпочтительно, лигандсвязывающий домен RXR позвоночных получают из RXR человека Homo sapiens, мыши Mus musculus, крысы Rattus norvegicus, курицы Gallus gallus, свиньи Sus scrota domestica, лягушки Xenopus laevis, полосатого данио Danio rerio, оболочника Polyandrocarpa misakiensis или медузы Tripedalia cysophora.
Предпочтительно, лигандсвязывающий домен RXR беспозвоночных получают из полипептида RXR саранчи Locusta migratoria ("LmRXR"), гомолога RXR 1 иксоидного клеща Amblyomma americanum ("AmaRXRT"), гомолога RXR 2 иксоидного клеща Amblyomma americanum ("AmaRXR2"), гомолога RXR манящего краба Celuca pugilator ("CpRXR"), гомолога RXR жука Tenebn'o molitor ("TmRXR"), гомолога RXR пчелы Apis mellifera ("AmRXR"), гомолога RXR тли Myzuspersicae ("MpRXR") или гомолога RXR недвукрылого/нечешуекрылого насекомого.
Предпочтительно, лигандсвязывающий домен химерного RXR включает по меньшей мере два полипептидных фрагмента, выбранных из группы, состоящей из полипептидного фрагмента RXR видов позвоночных, полипептидного фрагмента RXR видов беспозвоночных и полипептидного фрагмента гомолога RXR видов недвукрылых/нечешуекрылых беспозвоночных. Лигандсвязывающий домен химерного RXR для использования в настоящем изобретении может включать по меньшей мере два полипептидных фрагмента RXR разных видов, или, если вид один и тот же, два или более полипептидных фрагмента могут быть получены из двух или более разных изоформ полипептидного фрагмента RXR данного вида.
В предпочтительном варианте исполнения, лигандсвязывающий домен химерного RXR включает по меньшей мере один полипептидный фрагмент RXR вида позвоночных и один полипептидный фрагмент RXR вида беспозвоночных.
В более предпочтительном варианте исполнения, лигандсвязывающий домен химерного RXR включает по меньшей мере один полипептидный фрагмент RXR вида позвоночных и один полипептидный фрагмент гомолога RXR вида недвукрылых/нечешуекрылых беспозвоночных.
В конкретном варианте исполнения, ген, экспрессия которого модулируется, является гомологичным геном по отношению к клетке-хозяину. В другом конкретном варианте исполнения, ген, экспрессия которого модулируется, является гетерологичным геном по отношению к клетке-хозяину.
Лиганды для использования в настоящем изобретении, описанные ниже, сцепленные с лигандсвязывающим доменом ядерного рецептора (рецепторов), который, в свою очередь, связывается с элементом ответа, связанным с геном, обеспечивают средство внешней временной регуляции экспрессии гена. Механизм связывания или порядок, в котором разные компоненты данного изобретения связываются друг с другом, то есть, например, лиганд с лигандсвязывающим доменом, ДНК-связывающий домен с элементом ответа, домен трансактивации с промотором и т.д., не является критическим.
В конкретном примере, связывание лиганда с лигандсвязывающим доменом ядерного рецептора группы Н и его партнером лигандсвязывающего домена ядерного рецептора обеспечивает возможность экспрессии или супрессии гена. Этот механизм не включает возможность связывания лиганда с ядерным рецептором группы Н (GHNR) или его партнером и образования в результате этого активных гомодимерных комплексов (например, GHNR+GHNR или партнер + партнер). Предпочтительно, один или больше доменов рецептора изменен с образованием гибридного генного переключателя. Типично, один или больше из трех доменов - DBD, LBD и домена трансактивации - может быть выбран из источника, отличного от источника других доменов, так что гибридные гены и образующиеся гибридные белки оптимизируются по трансактивирующей активности, комплементарному связыванию лиганда и распознаванию специфического элемента ответа в выбранной клетке или организме-хозяине. Кроме того, элемент ответа может быть сам модифицирован или замещен на элементы ответа для других доменов ДНК-связывающего белка, такого как белок GAL-4 дрожжей (см. Sadowski, et al. (1988), Nature, 335: 563-564) или белок LexA Escherichia coli (см. Brent and Ptashne (1985), Cell, 43: 729-736), или синтетические элементы ответа, специфические к целевым взаимодействиям с белками, спроектированными, модифицированными и выбранными для таких специфических взаимодействий (см., например, Kim, et al. (1997), Proc. Natl. Acad. Sci., USA, 94:3 616-3620) для взаимодействия с гибридными рецепторами. Другое преимущество двухгибридных систем заключается в том, что они позволяют выбрать промотор, используемый для управления генной экспрессей в соответствии с желательным конечным результатом. Такой двойной контроль может быть особенно важным в области генной терапии, особенно при получении цитотоксичных белков, потому что позволяет контролировать как время экспрессии, так и клетки, в которых происходит экспрессия. При введении в клетки субъекта генов, функционально связанных с пригодным промотором, экспрессия экзогенных генов контролируется за счет присутствия системы по настоящему изобретению. Промоторы могут быть конститутивно или индуцибельно регулируемыми или могут быть ткань-специфическими (то есть экспрессируемыми только в определенном типе клеток) или специфическими по отношению к определенной стадии развития организма.
Рецептор экдизона является членом суперсемейства ядерных рецепторов и относится к подсемейству 1, группа Н (которые называются тут "ядерными рецепторами группы Н"). Члены каждой группы обладают 40-60% аминокислотной идентичностью в Е (лигандсвязывающем) домене (Laudet et al., A Unified Nomenclature System for the Nuclear Receptor Subfamily, 1999; Cell 97: 161-163). Кроме рецептора экдизона, другие члены этой группы Н подсемейства 1 ядерных рецепторов включают: вездесущий рецептор (UR), сиротский рецептор 1 (OR-1), ядерный рецептор стероидного гормона 1 (NER-1), ретиноидный Х-рецептор-взаимодействующий белок 15 (RIP-15), Х-рецептор печени β (LXRβ), белок, подобный рецептору стероидного гормона (RLD-1), Х-рецептор печени (LXR), X-рецептор печени α (LXRα), фарнезоидный Х-рецептор (FXR), рецептор-взаимодействующий белок 14 (RDP-14) и рецептор фарнезола (HRR-1).
Заявители разработали модель гомологии CfEcR и использовали эту модель гомологии вместе с опубликованной моделью гомологии рецептора экдизона Chironomous tetans ("CtEcR") (Wurtz et al., 2000) для идентификации критических остатков, принимающих участие в связывании с экдистероидами и неэкдистероидами. Было показано, что синтетические неэкдистероиды диацилгидразины связывают лепидоптеран EcRs с высоким сродством и индуцируют преждевременную неполную линьку у этих насекомых (Wing et al., 1988), и несколько этих соединений в настоящее время продаются в качестве инсектицидов. Лигандсвязывающая полость или "карман" EcRs эволюционировал до размеров, позволяющих размещать длинные структуры цепей экдистероидов, таких как 20-гидроксиэкдизон (20Е). Диацилгидразины имеют компактную структуру по сравнению с экдистероидами и занимают только донную часть кармана связывания EcR. Благодаря этому, в верхней части кармана связывания остаются несколько критических остатков, которые входят в контакт с экдистероидами, но не с неэкдистероидами, такими как бисацилгидразины. Заявители описывают тут конструкцию мутантных рецепторов экдизона, включающих мутацию замещения, в этих карманах связывания остатков и идентифицировали несколько классов субституционных мутантных рецепторов экдизона с модифицированными лигандсвязывающими и трансактивационными характеристиками.
С учетом близкого родства рецептора экдизона с другими ядерными рецепторами группы Н, ожидается, что идентифицированные заявителями субституционные мутации лигандсвязывающего домена рецептора экдизона будут работать при введении в аналогичное положение лигандсвязывающих доменов других ядерных рецепторов группы Н для модификации их лигандсвязывающей способности или чувствительности к лигандам. Специалист в данной области техники может идентифицировать аналогичные положения аминокислот в последовательности и по функциям с использованием стандартных методов, таких как анализ последовательностей, анализ кармана связывания путем гомологического моделирования и анализ связывания. Предложенные заявителями новые полинуклеотиды и полипептиды ядерных рецепторов группы Н с мутацией замещения являются полезными в системе модулирования индуцибельного гена на основе ядерного рецептора для различных областей применения, включая генную терапию, экспрессию представляющих интерес белков в клетках-хозяевах, получение трансгенных организмов и методы анализа на основе клеток.
В частности, заявители описывают тут новую систему модулирования генной экспрессии, включающую лигандсвязывающий домен ядерного рецептора группы Н, имеющий мутацию замещения. Эта система генной экспрессии может быть системой генной экспрессии на основе "одного переключателя", в которой домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен находятся в одном кодируемом полипептиде. Альтернативно, система модулирования генной экспрессии может быть системой модулирования генной экспрессии на основе "двойного переключателя" или "двухгибридной", в которой домен трансактивации и ДНК-связывающий домен расположены на двух разных кодируемых полипептидах. Заявители впервые продемонстрировали, что мутированный замещением ядерный рецептор может быть использован как компонент системы экспрессии индуцибельного гена на основе ядерного рецептора для модификации лигандсвязывающей активности и/или лигандспецифичности как прокариотических, так и эукариотических клеток. Как обсуждается тут, полученные заявителями результаты являются неожиданными и удивительными.
Система модулирования генной экспрессии на основе рецептора экдизона по настоящему изобретению может быть гетеродимерной или гомодимерной. функциональный комплекс EcR обычно относится к гетеродимерному белковому комплексу, состоящему из двух членов семейства стероидных рецепторов - рецептора экдизона белка, полученного из различных насекомых, и белка ultraspiracle (USP) или встречающегося у позвоночных гомолога USP, белка ретиноидного Х-рецептора (см. Yao, et al. (1993) Nature 366: 476-479; Yao, et al. (1992) Cell 71: 63-72). Однако комплекс может также быть гомодимером, как описано ниже. Комплекс рецептора функционального экдистероида может также включать дополнительный белок (белки), такие как иммунофилины. Дополнительные члены семейства белков стероидных рецепторов, известные как транскрипционные факторы (такие как DHR38 или бета-FTZ-1), также могут быть лигандзависимыми или независимыми партнерами для EcR, USP и/или RXR. Дополнительно, могут быть необходимы другие кофакторы, такие как белки, обычно известные как коактиваторы (также называемые адаптеры или медиаторы). Эти белки не связываются последовательность-специфично с ДНК и не принимают участия в базовой транскрипции. Они могут проявлять свое воздействие на активацию транскрипции по различным механизмам, включая стимулирование ДНК-связывание активаторов, влияние на структуру хроматина или медиирование взаимодействий активатор-инициаторный комплекс. Примеры таких коактиваторов включают RTP140, TIF1, RAP46/Bag-1, ARA70, SRC-1/NCoA-1, TIF2/GRIP/NCoA-2, ACTR/AIB1/RAC3/pCIP, а также связывающий белок элемента ответа В смешанного коактиватора С, СВР/р300 (см. обзор в Glass et al., Curr. Opin. Cell Biol. 9:222-232, 1997). Кроме того, для эффективного ингибирования транскрипционной активации в отсутствие лиганда могут потребоваться белковые кофакторы, обычно известные как корепрессоры (также известны как репрессоры, глушители или медиаторы глушения). Эти корепрессоры могут взаимодействовать с несвязанным с лигандом рецептором экдизона для глушения активности элемента ответа. Современный уровень знаний позволяет предположить, что связывание с лигандом изменяет конформацию рецептора, что приводит к высвобождению корепрессора и рекрутменту описанных выше коактиваторов, тем самым подавляя их способность к глушению. Примеры корепрессоров включают N-CoR и SMRT (см. обзор в Horwitz et al., Mol. Endocrinol. 10: 1167-1177, 1996). Эти кофакторы могут быть эндогенными по отношению к клетке или организму или могут быть введены экзогенно в виде трансгенов для экспрессии регулируемым или нерегулируемым образом. Гомодимерные комплексы белка рецептора экдизона, USP или RXR также могут быть функциональными в некоторых условиях.
Комплекс рецептора экдизона типично включает белки, являющиеся членами суперсемейства ядерных рецепторов, все члены которого обычно характеризуются присутствием аминотерминального домена трансактивации, ДНК-связывающего домена ("DBD") и лигандсвязывающего домена ("LBD"), отделенного от DBD шарнирным участком. В используемом тут значении, термин "ДНК-связывающий домен" включает минимальную полипептидную последовательность ДНК-связывающего белка, до полной длины ДНК-связывающего белка, при условии, что ДНК-связывающий домен функционально обеспечивает связывание с определенным элементом ответа. Члены суперсемейства ядерных рецепторов также характеризуются наличием четырех или пяти доменов: А/В, С, D, Е, и у некоторых членов, F (см. патент США 4981784 и Evans, Science 240:889-895 (1988)). Домен "А/В" соответствует домену трансактивации, "С" соответствует ДНК-связывающему домену, "D" соответствует шарнирному участку, и "Е" соответствует лигандсвязывающему домену. Некоторые члены семейства могут также иметь еще один домен трансактивации с карбокситерминального конца LBD, соответствующий "F".
DBD характеризуются присутствием двух цистеиновых цинковых пальцев, между которыми находятся два аминокислотных мотива, Р-рамка и D-рамка, которые обеспечивают специфичность к элементам ответа экдизонв. Эти домены могут быть нативными, модифицированными или химерами разных доменов гетерологичных рецепторных белков. Рецептор EcR, как подмножество семейства стероидных рецепторов, также обладает менее четко выраженными участками, ответственными за способность к гетеродимеризации. Поскольку домены ядерных рецепторов в природе являются модульными, LBD, DBD и домен трансактивации могут меняться местами.
Известны системы генных переключателей, которые включают компоненты комплекса рецептора экдизона. Однако, при использовании EcR в этих известных системах, он ассоциирован с нативными или модифицированными ДНК-связывающими доменами и доменами трансактивации в той же молекуле. USP или RXR типично используются как молчащие партнеры. Заявители ранее показали, что, если ДНК-связывающие домены и домены трансактивации находятся в одной и той же молекуле, фоновая активность в отсутствие лиганда является высокой и что такая активность резко снижается, когда ДНК-связывающие домены и домены трансактивации находятся в разных молекулах, то есть на каждом из двух партнеров гетеродимерного или гомодимерного комплекса (см. PCT/US01/09050).
Кассеты генной экспрессии по изобретению
Новая система экспрессии индуцибельного гена на основе ядерного рецептора по изобретению включает по меньшей мере одну кассету генной экспрессии, способную экспрессироваться в клетке-хозяине, причем кассета генной экспрессии включает полинуклеотид, кодирующий полипептид, включающий лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения. Таким образом, созданное заявителями изобретение также предусматривает новые кассеты генной экспрессии для использования в системе генной экспрессии по изобретению.
В конкретном варианте исполнения, кассета генной экспрессии, способная экспрессироваться в клетке-хозяине, включает полинуклеотид, кодирующий полипептид, выбранный из группы, состоящей из а) полипептида, включающего домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения; b) полипептида, включающего ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения; и с) полипептида, включающего домен трансактивации и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения.
В другом конкретном варианте исполнения, настоящее изобретение предусматривает кассету генной экспрессии, способную экспрессироваться в клетке-хозяине, причем кассета генной экспрессии включает полинуклеотид, кодирующий гибридный полипептид, выбранный из группы, состоящей из а) гибридного полипептида, включающего домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения; b) гибридного полипептида, включающего ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения; и с) гибридного полипептида, включающего домен трансактивации и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения. Гибридный полипептид в соответствии с изобретением включает по меньшей мере два полипептидных фрагмента, причем все полипептидные фрагменты имеют разные источники происхождения, т.е. разные полипептиды, разные ядерные рецепторы, разные виды и т.д. Гибридный полипептид в соответствии с изобретением может включать по меньшей мере два полипептидных домена, причем все полипептидные домены имеют разные источники происхождения.
В конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, получают из рецептора экдизона, вездесущего рецептора, сиротского рецептора 1, NER-1, ядерного рецептора стероидного гормона 1, ретиноидного Х-рецептор-взаимодействующего белка-15, Х-рецептора печени β, рецептор стероидного гормона-подобного белка, Х-рецептора печени, Х-рецептора печени α, фарнезоидного Х-рецептора, рецептор-взаимодействующего белка 14 и рецептора фарнезола. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
Таким образом, настоящее изобретение также предусматривает кассету генной экспрессии, включающую полинуклеотид, кодирующий полипептид, выбранный из группы, состоящей из а) полипептида, включающего домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен рецептора экдизона, содержащий мутацию замещения; b) полипептида, включающего ДНК-связывающий домен и лигандсвязывающий домен рецептора экдизона, содержащий мутацию замещения; и с) полипептида, включающего домен трансактивации и лигандсвязывающий домен рецептора экдизона, содержащий мутацию замещения. Предпочтительно, кассета генной экспрессии включает полинуклеотид, кодирующий гибридный полипептид, выбранный из группы, состоящей из а) гибридного полипептида, включающего домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен рецептора экдизона, содержащий мутацию замещения; b) гибридного полипептида, включающего ДНК-связывающий домен и лигандсвязывающий домен рецептора экдизона, содержащий мутацию замещения; и с) гибридного полипептида, включающего домен трансактивации и лигандсвязывающий домен рецептора экдизона, содержащий мутацию замещения; где кодируемый гибридный полипептид включает по меньшей мере два полипептидных фрагмента, причем каждый полипептидный фрагмент имеет разный источник происхождения.
Лигандсвязывающий домен (LBD) рецептора экдизона (EcR) может быть получен из EcR беспозвоночных, предпочтительно выбранных из EcR класса Arthropod. Предпочтительно, EcR выбирают из группы, состоящей из EcR чешуекрылых, EcR двукрылых, EcR прямокрылых, EcR равнокрылых и EcR полужесткокрылых. Более предпочтительно, лигандсвязывающий домен EcR для использования в настоящем изобретении получают из EcR гусениц листовертки-почкоеда елового Chotistoneura fumiferana ("CfEcR"), EcR жука Tenebrio molitor ("TmEcR"), EcR Manduca sexta ("MsEcR"), EcR Hetiothies virescens ("HvEcR"), EcR мошки Chironomus tentans ("CtEcR"), EcR тутового шелкопряда Bombyx mori ("BmEcR"), EcR бархатницы (squinting bush brown) Bicyclus anynana ("BanEcR"), EcR Junonia coenia ("JcEcR"), EcR плодовой мушки Drosophila melanogaster ("DmEcR"), EcR москита Aedes aegypti ("AaEcR"), EcR мясной мухи Lucilia capitata ("LcEcR"), мясной мухи Lucilia cuprina EcR ("LucEcR"), EcR мясной мухи Calliphora vicinia ("CvEcR"), EcR средиземноморской плодовой мушки Ceratitis capitata ("CcEcR"), EcR саранчи Locusta migratolia ("LmEcR"), EcR тли Myzus persicae ("MpEcR"), EcR манящего краба Celuca pugilator ("CpEcR"), EcR иксоидного клеща Amblyomma americanum ("AniaEcR"), EcR белокрылки Bamecia argentifoli ("BaEcR") или EcR цикадки Nephotetix cincticeps ("NcEcR"). Более предпочтительно, LBD выбирают из CfEcR, DmEcR или AmaEcR.
В конкретном варианте исполнения, LBD представляет собой укороченный полипептид EcR. Усечение полипептида EcR приводит к делеции по меньшей мере 1, 2, 3, 4, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 105, 110, 115, 120, 125, 130, 135, 140, 145, 150, 155, 160, 165, 170, 175, 180, 185, 190, 195, 200, 205, 210, 215, 220, 225, 230, 235, 240, 245, 250, 255, 260 или 265 аминокислот. Предпочтительно, усечение полипептида EcR приводит к делеции по меньшей мере части полипептидного домена. Более предпочтительно, усечение полипептида EcR приводит к делеции по меньшей мере всего полипептидного домена. В конкретном варианте исполнения, усечение полипептида EcR приводит к делеции по меньшей мере А/В-домена, С-домена, D-домена, F-домена, А/В/С-доменов, А/В/1/2-С-доменов, A/B/C/D-доменов, А/В/С/D/F-доменов, A/B/F-доменов, A/B/C/F-доменов, части Е домена или части F домена. Также могут быть выполнены комбинации нескольких полных и/или частичных делеций доменов.
В конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н кодируется полинуклеотидом, включающим мутацию кодона, приводящую к замещению а) аминокислотного остатка 48, 51, 52, 54, 92, 95, 96, 109, 110, 119, 120, 125, 128, 132, 219, 223, 234 или 238 SEQ ID NO: 1, b) аминокислотных остатков 96 и 119 SEQ ID NO: 1, с) аминокислотных остатков 110 и 128 SEQ ID NO: 1, d) аминокислотных остатков 52 и 110 SEQ ID NO: 1, e) аминокислотных остатков 107, 110 и 127 SEQ ID NO: 1 или f) аминокислотных остатков 52, 107 и 127 SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н кодируется полинуклеотидом, включающим мутации кодонов, приводящие к замещению аминокислотных остатков 107 и 127 и инсерции аминокислоты 259 SEQ ID NO: 1. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н кодируется полинуклеотидом, включающим мутацию кодона, приводящую к замещению а) аспарагинового, аргининового, тирозинового, триптофанового, лейцинового или лизинового остатка в положении, эквивалентном аналогичному аминокислотному остатку 48 SEQ ID NO: 1, b) метионинового, аспарагинового или лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 51 SEQ ID NO: 1, с) лейцинового, пролинового, метионинового, аргининового, триптофанового, глицинового, глутаминового остатка или остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, d) триптофанового или треонинового остатка в положении, эквивалентном или аналогичном аминокислоте 54 SEQ ID NO: 1, e) лейцинового остатка или остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 92 SEQ ID NO: 1, f) гистидинового, метионинового или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 95 SEQ ID NO: 1, g) лейцинового, серинового, глутаминовой кислоты или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 96 SEQ ID NO: 1, h) триптофанового, пролинового, лейцинового, метионинового или аспарагинового в положении, эквивалентном или аналогичном аминокислоте 109 SEQ ID NO: 1, i) глутаминовой кислоты, триптофанового или аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, j) фенилаланинового в положении, эквивалентном или аналогичном аминокислоте 119 SEQ ID NO: 1, k) триптофанового или метионинового в положении, эквивалентном или аналогичном аминокислоте 120 SEQ ID NO: 1, l) глутаминовой кислоты, пролинового, лейцинового, цистеинового, триптофанового, глицинового, изолейцинового, аспарагинового, серинового, валинового или аргининового в положении, эквивалентном или аналогичном аминокислоте 125 SEQ ID NO: 1, m) фенилаланинового в положении, эквивалентном или аналогичном аминокислоте 128 SEQ ID NO: 1, n) метионинового, аспарагинового, глутаминовой кислоты или валинового в положении, эквивалентном или аналогичном аминокислоте 132 SEQ ID NO: 1, о) аланинового, лизинового, триптофанового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 SEQ ID NO: 1, р) лизинового, аргининового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 223 SEQ ID NO: 1, q) метионинового, аргининового, триптофанового или изолейцинового в положении, эквивалентном или аналогичном аминокислоте 234 SEQ ID NO: 1, r) пролинового, глутаминовой кислоты, лейцинового, метионинового или тирозинового в положении, эквивалентном или аналогичном аминокислоте 238 SEQ ID NO: 1, s) фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислоте 119 SEQ ID NO: 1, и треонинового в положении, эквивалентном или аналогичном аминокислоте 96 SEQ ID NO: 1, t) пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, и фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислоте 128 SEQ ID NO: 1, u) валинового остатка в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1, и пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, v) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, или w) изолейцинового в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и валинового в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н кодируется полинуклеотидом, включающим мутации кодонов, приводящие к замещению изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и инсерции глицинового остатка в положении, эквивалентном или аналогичном аминокислоте 259 SEQ ID NO: 1. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
В конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является лигандсвязывающим доменом рецептора экдизона, содержащим мутацию замещения, кодируемым полинуклеотидом, включающим мутацию кодона, приводящую к мутации замещения выбранной из группы, состоящей из мутаций замещения F48Y, F48W, F48L, F48N, F48R, F48K, 151М, 151N, 151L, T52M, T52V, T52L, Т52Е, Т52Р, T52R, T52W, T52G, T52Q, M54W, М54Т, M92L, М92Е, R95H, R95M, R95W, V96L, V96W, V96S, V96E, F109W, F109P, F109L, F109M, F109N, А110Е, A110N, A110W, N119F, Y120W, Y120M, М125Р, M125R, М125Е, M125L, М125С, M125W, M125G, М1251, M125N, M125S, M125V, V128F, L132M, L132N, L132V, L132E, М219К, M219W, M219Y, М219А, L223K, L223R, L223Y, L234M, L234I, L234R, L234W, W238P, W238E, W238Y, W238M, W238L, N119F/V96T, V128F/A110P, T52V/A110P, V107l/Y127En52V и V107I/Y127E/A110P SEQ ID NO: 1. В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является лигандсвязывающим доменом рецептора экдизона, содержащим мутацию замещения, кодируемым полинуклеотидом, включающим мутацию кодона, приводящую к мутации замещения V107I/Y127E SEQ ID NO: 1, который дополнительно включает мутацию инсерции G259 SEQ ID NO: 1 (V107I/Y127E/G259).
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является полипептидом лигандсвязывающего домена рецептора экдизона, включающим мутацию замещения, кодируемым полинуклеотидом, который гибридизуется с полинуклеотидом, включающим мутацию кодона, приводящую к мутации замещения, выбранной из группы, состоящей из F48Y, F48W, F48L, F48N, F48R, F48K, 151М, 151N, 151L, T52M, T52V, T52L, Т52Е, Т52Р, T52R, T52W, T52G, T52Q, M54W, М54Т, M92L, М92Е, R95H, R95M, R95W, V96L, V96W, V96S, V96E, F109W, F109P, F109L, F109M, F109N, А110Е, A110N, A110W, N119F, Y120W, Y120M, М125Р, M125R, М125Е, M125L, М125С, M125W, M125G, M125I, M125N, M125S, M125V, V128F, L132M, L132N, L132V, L132E, М219К, M219W, M219Y, М219А, L223K, L223R, L223Y, L234M, L234I, L234R, L234W, W238P, W238E, W238Y, W238M, W238L, N119F/V96T, V128F/A110P, T52V/A110P, V107l/Y127En52V и V107I/Y127E/A110P SEQ ID NO: 1 в условиях гибридизации, включающих стадию гибридизации в менее чем 500 мМ соли и по меньшей мере 37°С и стадию промывки в 2×SSPE при по меньшей мере 63°С. В предпочтительном варианте исполнения, условия гибридизации включают менее чем 200 мМ соли и по меньшей мере 37°С для стадии гибридизации. В другом предпочтительном варианте исполнения, условия гибридизации включают 2×SSPE и 63°С как для стадии гибридизации, так и для промывки.
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н включает мутацию замещения в положении, эквивалентном или аналогичном а) аминокислотному остатку 48, 51, 52, 54, 92, 95, 96, 109, 110, 119, 120, 125, 128, 132, 219, 223, 234 или 238 SEQ ID NO: 1, b) аминокислотным остаткам 96 и 119 SEQ ID NO: 1, с) аминокислотным остаткам 110 и 128 SEQ ID NO: 1, d) аминокислотным остаткам 52 и 110 SEQ ID NO: 1, e) аминокислотным остаткам 107, 110 и 127 SEQ ID NO: 1 или f) аминокислотным остаткам 52, 107 и 127 SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н включает субституционные мутации, приводящие к мутации замещения в положении, эквивалентном или аналогичном аминокислотным остаткам 107 и 127, и инсерции аминокислотного остатка 259 SEQ ID NO: 1. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
Предпочтительно, лигандсвязывающий домен ядерного рецептора группы Н включает замещение а) аспарагинового, аргининового, тирозинового, триптофанового, лейцинового или лизинового остатка в положении, эквивалентном аналогичному аминокислотному остатку 48 SEQ ID NO: 1, b) метионинового, аспарагинового или лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 51 SEQ ID NO: 1, с) лейцинового, пролинового, метионинового, аргининового, триптофанового, глицинового, глутаминового остатка или остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, d) триптофанового или треонинового остатка в положении, эквивалентном или аналогичном аминокислоте 54 SEQ ID NO: 1, е) лейцинового остатка или остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 92 SEQ ID NO: 1, f) гистидинового, метионинового или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 95 SEQ ID NO: 1, g) лейцинового, серинового, глутаминовой кислоты или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 96 SEQ ID NO: 1, h) триптофанового, пролинового, лейцинового, метионинового или аспарагинового в положении, эквивалентном или аналогичном аминокислоте 109 SEQ ID NO: 1, i) остатка глутаминовой кислоты, триптофанового или аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, j) фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислоте 119 SEQ ID NO: 1, k) триптофанового или метионинового остатка в положении, эквивалентном или аналогичном аминокислоте 120 SEQ ID NO: 1, l) остатка глутаминовой кислоты, пролинового, лейцинового, цистеинового, триптофанового, глицинового, изолейцинового, аспарагинового, серинового, валинового или аргининового остатка в положении, эквивалентном или аналогичном аминокислоте 125 SEQ ID NO: 1, m) фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислоте 128 SEQ ID NO: 1, n) метионинового, аспарагинового, глутаминовой кислоты или валинового остатка в положении, эквивалентном или аналогичном аминокислоте 132 SEQ ID NO: 1, о) аланинового, лизинового, триптофанового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 SEQ ID NO: 1, p) лизинового, аргининового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 223 SEQ ID NO: 1, q) метионинового, аргининового, триптофанового или изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 234 SEQ ID NO: 1, r) пролинового, глутаминовой кислоты, лейцинового, метионинового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислоте 238 SEQ ID NO: 1, s) фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислоте 119 SEQ ID NO: 1, и треонинового остатка в положении, эквивалентном или аналогичном аминокислоте 96 SEQ ID NO: 1, t) пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, и фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислоте 128 SEQ ID NO: 1, u) валинового остатка в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1, и пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, v) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, или w) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и валинового остатка в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н включает замещение изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и инсерцию глицинового остатка в положении, эквивалентном или аналогичном аминокислоте 259 SEQ ID NO: 1. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является полипептидом лигандсвязывающего домена рецептора экдизона, включающим мутацию замещения, где мутацию замещения выбирают из группы, состоящей из мутаций замещения F48Y, F48W, F48L, F48N, F48R, F48K, 151М, 151N, 151L, T52M, T52V, T52L, Т52Е, Т52Р, T52R, T52W, T52G, T52Q, M54W, М54Т, M92L, М92Е, R95H, R95M, R95W, V96L, V96W, V96S, V96E, F109W, F109P, F109L, F109M, F109N, А110Е, A110N, A110W, N119F, Y120W, Y120M, М125Р, M125R, М125Е, M125L, М125С, M125W, M125G, М1251, M125N, M125S, M125V, V128F, L132M, L132N, L132V, L132E, М219К, M219W, M219Y, М219А, L223K, L223R, L223Y, L234M, L234I, L234R, L234W, W238P, W238E, W238Y, W238M, W238L, N119F/V96T, T52V/A110P, V128F/A110P, V107I/Y127E/T52V и V107I/Y127E/A110P SEQ ID NO: 1. В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является полипептидом лигандсвязывающего домена рецептора экдизона, включающим мутацию замещения V107I/Y127E SEQ ID NO: 1, который дополнительно включает мутацию инсерции G259 SEQ ID NO: 1 (V107I/Y127E/G259).
ДНК-связывающий домен может быть любым ДНК-связывающим доменом с известным элементом ответа, включая синтетические и химерные ДНК-связывающие домены или их аналоги, комбинации или модификации. Предпочтительно, DBD представляет собой DBD GAL4, DBD LexA, DBD фактора транскрипции, DBD члена группы Н ядерных рецепторов, DBD члена суперсемейства ядерных рецепторов стероидных/тиреоидных гормонов или DBD бактериального LacZ. Более предпочтительно, DBD представляет собой DBD EcR [SEQ ID NO: 4 (полинуклеотид) или SEQ ID NO: 5 (полипептид)], DBD GAL4 [SEQ ID NO: 6 (полинуклеотид) или SEQ ID NO: 7 (полипептид)] или DBD LexA [(SEQ ID NO: 8 (полинуклеотид) или SEQ ID NO: 9 (полипептид)].
Домен трансактивации (сокращенно "AD" или "ТА") может быть любым AD члена группы Н ядерных рецепторов, AD ядерного рецептора стероидного/тиреоидного гормона, синтетическим или химерным AD, полиглутаминовым AD, AD основной или кислотной аминокислоты, AD VP16, AD GAL4, AD NF-kB, AD BP64, кислотным доменом активации В42 (B42AD), доменом трансактивации р65 (p65AD) или их аналогами, комбинациями или модификациями. В конкретном варианте исполнения, AD представляет собой синтетический или химерный AD или получается из AD EcR, глюкокортикоидного рецептора, VP16, GAL4, NF-kB или кислотного домена активации В42. Предпочтительно, AD представляет собой AD EcR [SEQ ID NO: 10 (полинуклеотид) или SEQ ID NO: 11 (полипептид)], AD VP16 [SEQ ID NO: 12 (полинуклеотид) или SEQ ID NO: 13 (полипептид)], AD B42 [SEQ ID NO: 14 (полинуклеотид) или SEQ ID NO: 15 (полипептид)] или AD p65 [SEQ ID NO: 16 (полинуклеотид) или SEQ ID NO: 17 (полипептид)].
В конкретном варианте исполнения, кассета генной экспрессии кодирует гибридный полипептид, включающий а) ДНК-связывающий домен, кодируемый полинуклеотидом, включающим последовательность нуклеиновой кислоты SEQ ID N0: 4, SEQ ID NO: 6 или SEQ ID NO: 8, или b) домен трансактивации, кодируемый полинуклеотидом, включающим последовательность нуклеиновой кислоты SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 14 или SEQ ID NO: 16; и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, кодируемый полинуклеотидом в соответствии с изобретением. Предпочтительно, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является лигандсвязывающим доменом рецептора экдизона, содержащим мутацию замещения, кодируемым полинуклеотидом в соответствии с изобретением.
В другом конкретном варианте исполнения, кассета генной экспрессии кодирует гибридный полипептид, включающий а) ДНК-связывающий домен, включающий аминокислотную последовательность SEQ ID NO: 5, SEQ ID NO: 7 или SEQ ID NO: 9, или b) домен трансактивации, включающий аминокислотную последовательность SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 15 или SEQ ID NO: 17; и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением. Предпочтительно, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является лигандсвязывающим доменом рецептора экдизона, содержащим мутацию замещения, в соответствии с изобретением.
Настоящее изобретение также предусматривает кассету генной экспрессии, включающую: i) элемент ответа, включающий домен, распознаваемый полипептидом, включающим ДНК-связывающий домен; ii) промотор, который активируется полипептидом, включающим домен трансактивации; и iii) ген, экспрессия которого модулируется.
Элемент ответа ("RE") может быть любым элементом ответа с известным ДНК-связывающим доменом или его аналогом, комбинациями или модификациями. Может быть использован один RE, или же в настоящем изобретении могут быть использованы многочисленные RE, которые являются множественными копиями одного и того же RE или двумя или более разными RE. В конкретном варианте исполнения, RE представляет собой RE GAL4 ("GAL4RE"), LexA, RE ядерного рецептора группы Н, RE ядерного рецептора стероидного/тиреоидного гормона или синтетический RE, который распознает синтетический ДНК-связывающий домен. Предпочтительно, RE является элементом ответа экдизона (EcRE), включающим полинуклеотидную последовательность SEQ ID NO: 18, GAL4RE, включающим полинуклеотидную последовательность SEQ ID NO: 19, или RE LexA (оперон, "ор"), включающим полинуклеотидную последовательность SEQ ID NO: 20 ("2XLexAopRE").
ДНК-связывающий домен, домен активации или элемент ответа ядерного рецептора стероидного/тиреоидного гормона в соответствии с изобретением могут быть получены из ядерного рецептора стероидного/тиреоидного гормона, выбранного из группы, состоящей из рецептора тиреоидного гормона α (TRα), тиреоидного рецептора 1 (c-erbA-1), рецептора тиреоидного гормона β (TRβ), рецептора ретиноевой кислоты α (RARα), рецептора ретиноевой кислоты β (RARβ, MAP), рецептора ретиноевой кислоты γ (RARγ), гамма-подобного рецептора ретиноевой кислоты (RARD), пролифератор пероксисом-активируемого рецептора α (PPARα), пролифератор пероксисом-активируемого рецептора β (PPAR-β), пролифератор пероксисом-активируемого рецептора δ (PPARδ, NUC-1), пролифератор пероксисом-активаторассоциированного рецептора (FFAR), пролифератор пероксисом-активируемого рецептора γ (PPARγ), сиротского рецептора, кодируемого некодирующей цепью рецептора тиреоидного гормона α (REVERBα), v-erb родственного рецептора (EAR-1), v-erb родственного рецептора (EAR-1A), γ), сиротского рецептора, кодируемого некодирующей цепью рецептора тиреоидного гормона β (REVERBβ), v-erb родственного рецептора (EAR-1β), сиротского ядерного рецептора BD73 (BD73), reverbA-родственного рецептора (RVR), белка цинкового пальца 126 (HZF2), экдизон-индуцибельного белка Е75 (Е75), экдизон-индуцибельного белка Е78 (Е78), рецептора Drosophila 78 (DR-78), ретиноид-родственного сиротского рецептора α (RORα), ретиноидного Z-рецептора α (RZRα), ретиноид-родственного сиротского рецептора β (RORβ), ретиноидного Z-рецептора β (RZRβ), ретиноид-родственного сиротского рецептора γ (RORγ), ретиноидного Z-рецептора γ (RZRγ), ретиноид-родственного сиротского рецептора (TOR), рецептора гормона 3 (HR-3), рецептора гормона Drosophila 3 (DHR-3), рецептора гормона Manduca (MHR-3), рецептора гормона Galleria 3 (GHR-3), ядерного рецептора С. elegans 3 (CNR-3), рецептора гормона Choristoneura 3 (CHR-3), ядерного рецептора С. elegans 14 (CNR-14), рецептора экдизона (ECR), вездесущего рецептора (UR), сиротского ядерного рецептора (OR-1), NER-1, рецептор-взаимодействующего белка 15 (RIP-15), Х-рецептора печени β (LXRβ), рецептора стероидного гормона-подобного белка (RLD-1), X-рецептора печени (LXR), Х-рецептора печени α (LXRα), фарнезоидного X-рецептора (FXR), рецептор-взаимодействующего белка 14 (RIP-14), HRR-1, рецептора витамина D (VDR), сиротского ядерного рецептора (ONR-1), X-рецептора прегнана (PXR), стероидного и ксенобиотического рецептора (SXR), X-рецептора бензоата (BXR), ядерного рецептора (МВ-67), конститутивного андростанового рецептора 1 (CAR-1), конститутивного андростанового рецептора α (CARα), конститутивного андростанового рецептора 2 (CAR-2), конститутивного андростанового рецептора β (CARβ), рецептора гормона Drosophila 96 (DHR-96), ядерного рецептора гормона 1 (NHR-1), ядерного фактора гепатоцитов 4 (HNF-4), ядерного фактора гепатоцитов 4G (HNF-4G), ядерного фактора гепатоцитов 4В (HNF-4B), ядерного фактора гепатоцитов 4D (HNF-4D, DHNF-4), ретиноидного X-рецептора α (RXRα), ретиноидного Х-рецептора β (RXRβ), H-2 участок II-связывающего белка (H-2RIIBP), ко-регулятора ядерного рецептора 1 (RCoR-1), ретиноидного Х-рецептора γ (RXRγ), Ultraspiracle (USP), ядерного рецептора 2С1, хорионического фактора 1 (CF-1), тестикулярного рецептора 2 (TR-2), тестикулярного рецептора 2-11 (TR2-11), тестикулярного рецептора 4 (TR4), ТАК-1, рецептора гормона Drosophila (DHR78), Tailless (TLL), гомолога tailless (TLX), XTLL, фактора транскрипции апстрим-промотора куриного овальбумина I (COUP-TF1), фактора транскрипции апстрим-промотора куриного овальбумина А (COUP-TFA), EAR-3, SVP-44, фактора транскрипции апстрим-промотора куриного овальбумина II (COUP-TFII), фактора транскрипции апстрим-промотора куриного овальбумина В (COUP-TFB), ARP-1, SVP-40, SVP, фактора транскрипции апстрим-промотора куриного овальбумина III (COUP-TFIII), фактора транскрипции апстрим-промотора куриного овальбумина G (COUP-TFG), SVP-46, EAR-2, эстрогенового рецептора α (ERα), эстрогенового рецептора β (ERβ), эстроген-родственного рецептора 1 (ERR1), эстроген-родственного рецептора α (ERRα), эстроген-родственного рецептора 2 (ERR2), эстроген-родственного рецептора β (ERRβ), глюкокортикоидного рецептора (GR), минералокортикоидного рецептора (MR), прогестеронового рецептора (PR), андрогенового рецептора (AR), фактор роста нервов-индуцируемого гена В (NGFI-B), ядерного рецептора, подобного Nur-77 (TRS), N10, сиротского рецептора (NUR-77), гена раннего ответа человека (NAK-1), Nurr-родственного фактора 1 (NURR-1), гена предраннего ответа человека (NOT), регенерирующего ядерного рецептора печени 1 (RNR-1), гематопоэтического цинкового пальца 3 (HZF-3), Nur-родственного белка-1 (TINOR), ядерного сиротского рецептора 1 (NOR-1), NOR1-родственного рецептора (MINOR), рецептора гормона Drosophila 38 (DHR-38), ядерного рецептора С. elegans 8 (CNR-8), C48D5, стероидогенного фактора 1 (SF1), эндозепин-подобного пептида (ELP), фактора fushi tarazu 1 (FTZ-FI), адреналового 4 связывающего белка (AD4BP), гомолога рецептора печени (LRH-1), Ftz-F1-родственного сиротского рецептора A (xFFrA), Ftz-F1-родственного сиротского рецептора В (xFFrB), ядерного рецептора, родственного LRH-1 (FFLR), ядерного рецептора, родственного LRH-1 (PHR), фактора транскрипции фетопротеина (FTF), ядерного фактора зародышевых клеток (GCNFM), ретиноидный рецептор-родственного яичко-ассоциированного рецептора (RTR), knirps (KNI), knirps-родственного (KNRL), эмбриональных гонад (EGON), гена лиганд-зависимого ядерного рецептора Drosophila (EAGLE), ядерного рецептора, подобного trithorax (ODR7), Trithorax, гена доза-чувствительного пол-трансформируемого врожденной гипоплазии надпочечника критического участка хромосомы Х (DAX-1), врожденной гипоплазии надпочечника и гипогонадотропного гипогонадизма (АНСН) и короткого гетеродимерного партнера (SHP).
В целях данного изобретения, ядерные рецепторы и ядерные рецепторы группы Н также включают синтетические и химерные ядерные рецепторы и ядерные рецепторы группы Н и их гомологи.
Гены, представляющие интерес для использования в предложенных заявителями кассетах генной экспрессии, могут быть эндогенными генами или гетерологичными генами. Информация о последовательности нуклеиновых кислот или аминокислотной последовательности для желательного гена или белка может быть размщена в одной из многих баз даных с публичным доступом, например GENBANK, EMBL, Swiss-Prot и PIR, или во многих журнальных публикациях биологической тематики. Таким образом, специалисты в данной области техники имеют доступ к информации о последовательностях нуклеиновых кислот практически для всех известных генов. Такая информация может быть затем использована для конструирования желательных структурных элементов для инсерции представляющего интерес гена в кассеты генной экспрессии, используемые в описанных тут заявителями методах.
Примеры генов, представляющих интерес для использования в описанных заявителями кассетах генной экспрессии, включают, без ограничения: гены, кодирующие терапевтически желательные полипептиды или продукты, которые могут быть использованы для лечения состояния, болезни, расстройства, дисфункции, генетического дефекта, такие как моноклональные антитела, ферменты, протеазы, цитокины, интерфероны, инсулин, эритропоэтин, факторы свертывания крови, другие факторы или компоненты крови, вирусные векторы для генной терапии, вирусы для вакцин, мишени для доставки лекарственных средств, анализов и применения в функциональной геномике и протеомике и т.п.
Полинуклеотиды по изобретению
Новая система экспрессии индуцибельного гена на основе ядерного рецептора по изобретению включает по меньшей мере одну кассету генной экспрессии, включающую полинуклеотид, кодирующий лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения. Эти кассеты генной экспрессии, входящие в их состав полинуклеотиды и кодируемые ими полипептиды пригодны для использования в качестве компонентов системы генной экспрессии на основе ядерного рецептора для модулирования экспрессии гена в клетке-хозяине.
Таким образом, настоящее изобретение предусматривает изолированный полинуклеотид, кодирующий лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения.
В конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н кодируется полинуклеотидом, включающим мутацию кодона, приводящую к замещению аминокислотного остатка в положении, эквивалентном или аналогичном а) аминокислотному остатку 48, 51, 52, 54, 92, 95, 96, 109, 110, 119, 120, 125, 128, 132, 219, 223, 234 или 238 SEQ ID NO: 1, b) аминокислотным остаткам 96 и 119 SEQ ID NO: 1, с) аминокислотным остаткам 110 и 128 SEQ ID NO: 1, d) аминокислотным остаткам 52 и 110 SEQ ID NO: 1, e) аминокислотным остаткам 107, 110 и 127 SEQ ID NO: 1 или f) аминокислотным остаткам 52, 107 и 127 SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н кодируется полинуклеотидом, включающим мутации кодонов, приводящие к замещению аминокислотных остатков в положениях, эквивалентных или аналогичных аминокислотным остаткам 107 и 127, и инсерции аминокислоты 259 SEQ ID NO: 1. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получен из рецептора экдизона.
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н кодируется полинуклеотидом, включающим мутацию кодона, приводящую к замещению а) аспарагинового, аргининового, тирозинового, триптофанового, лейцинового или лизинового остатка в положении, эквивалентном аналогичному аминокислотному остатку 48 SEQ ID NO: 1, b) метионинового, аспарагинового или лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 51 SEQ ID NO: 1, с) лейцинового, пролинового, метионинового, аргининового, триптофанового, глицинового, глутаминового остатка или остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, d) триптофанового или треонинового в положении, эквивалентном или аналогичном аминокислоте 54 SEQ ID NO: 1, е) лейцинового остатка или глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 92 SEQ ID NO: 1, f) гистидинового, метионинового или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 95 SEQ ID NO: 1, g) лейцинового, серинового, глутаминовой кислоты или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 96 SEQ ID NO: 1, h) триптофана, пролина, лейцина, метионина или аспарагина в положении, эквивалентном или аналогичном аминокислоте 109 SEQ ID NO: 1, i) остатка глутаминовой кислоты, триптофанового или аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, j) фенилаланина в положении, эквивалентном или аналогичном аминокислоте 119 SEQ ID NO: 1, k) триптофана или метионина в положении, эквивалентном или аналогичном аминокислоте 120 SEQ ID NO: 1, l) глутаминовой кислоты, пролина, лейцина, цистеина, триптофана, глицина, изолейцина, аспарагина, серина, валина или аргинина в положении, эквивалентном или аналогичном аминокислоте 125 SEQ ID NO: 1, m) фенилаланина в положении, эквивалентном или аналогичном аминокислоте 128 SEQ ID NO: 1, n) метионина, аспарагина, глутаминовой кислоты или валина в положении, эквивалентном или аналогичном аминокислоте 132 SEQ ID NO: 1, о) аланинового, лизинового, триптофанового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 SEQ ID NO: 1, р) лизинового, аргининового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 223 SEQ ID NO: 1, q) метионина, аргинина, триптофана или изолейцина в положении, эквивалентном или аналогичном аминокислоте 234 SEQ ID NO: 1, r) пролина, глутаминовой кислоты, лейцина, метионина или тирозина в положении, эквивалентном или аналогичном аминокислоте 238 SEQ ID NO: 1, s) фенилаланина в положении, эквивалентном или аналогичном аминокислоте 119 SEQ ID NO: 1, и треонина в положении, эквивалентном или аналогичном аминокислоте 96 SEQ ID NO: 1, t) пролина в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, и фенилаланина в положении, эквивалентном или аналогичном аминокислоте 128 SEQ ID NO: 1, u) валинового остатка в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1, и пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, v) изолейцина в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и пролина в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, или w) изолейцина в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и валина в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н кодируется полинуклеотидом, включающим мутации кодонов, приводящие к замещению изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и инсерции глицинового остатка в положении, эквивалентном или аналогичном аминокислоте 259 SEQ ID NO: 1. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является лигандсвязывающим доменом рецептора экдизона, содержащим мутацию замещения, кодируемым полинуклеотидом, включающим мутацию кодона, приводящую к мутации замещения, выбранной из группы, состоящей из мутаций замещения F48Y, F48W, F48L, F48N, F48R, F48K, 151М, 151N, 151L, T52M, T52V, T52L, Т52Е, Т52Р, T52R, T52W, T52G, T52Q, M54W, М54Т, M92L, М92Е, R95H, R95M, R95W, V96L, V96W, V96S, V96E, F109W, F109P, F109L, F109M, F109N, А110Е, A110N, A110W, N119F, Y120W, Y120M, М125Р, M125R, М125Е, M125L, М125С, M125W, M125G, М1251, M125N, M125S, M125V, V128F, L132M, L132N, L132V, L132E, М219К, M219W, M219Y, М219А, L223K, L223R, L223Y, L234M, L234I, L234R, L234W, W238P, W238E, W238Y, W238M, W238L, N119F/V96T, V128F/A110P, T52V/A110P, V107I/Y127E/T52V и V107I/Y127E/A110P SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является лигандсвязывающим доменом рецептора экдизона, содержащим мутацию замещения, кодируемым полинуклеотидом, включающим мутацию кодона, приводящую к мутации замещения V107I/Y127E SEQ ID NO: 1, который дополнительно включает мутацию инсерции G259 SEQ ID NO: 1 (V107I/Y127E/G259).
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является лигандсвязывающим доменом рецептора экдизона, содержащим мутацию замещения, кодируемым полинуклеотидом, который гибридизуется с полинуклеотидом, включающим мутацию кодона, приводящую к мутации замещения, выбранной из группы, состоящей из F48Y, F48W, F48L, F48N, F48R, F48K, 151М, 151N, 151L, T52M, T52V, T52L, Т52Е, Т52Р, T52R, T52W, T52G, T52Q, M54W, М54Т, M92L, М92Е, R95H, R95M, R95W, V96L, V96W, V96S, V96E, F109W, F109P, F109L, F109M, F109N, А110Е, A110N, A110W, N119F, Y120W, Y120M, М125Р, M125R, М125Е, M125L, М125С, M125W, M125G, М1251, M125N, M125S, M125V, V128F, L132M, L132N, L132V, L132E, М219К, M219W, M219Y, М219А, L223K, L223R, L223Y, L234M, L234I, L234R, L234W, W238P, W238E, W238Y, W238M, W238L, N119F/V96T, V128F/A110P, T52V/A110P, V107l/Y127En-52V и V107I/Y127E/A110P SEQ ID NO: 1, в условиях гибридизации, включающих стадию гибридизации в менее чем 500 мМ соли и при по меньшей мере 37°С и стадию промывки в 2×SSPE при по меньшей мере 63°С. В предпочтительном варианте исполнения, условия гибридизации включают менее чем 200 мМ соли и по меньшей мере 37°С для стадии гибридизации. В другом предпочтительном варианте исполнения, условия гибридизации включают 2×SSPE и 63°С для обеих стадий гибридизации и промывки.
Настоящее изобретение также предусматривает изолированный полинуклеотид, кодирующий полипептид, выбранный из группы, состоящей из а) полипептида, включающего домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением; b) полипептида, включающего ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением; и с) полипептида, включающего домен трансактивации и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением.
В конкретном варианте исполнения, изолированный полинуклеотид кодирует гибридный полипептид, выбранный из группы, состоящей из а) гибридного полипептида, включающего домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением; b) гибридного полипептида, включающего ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением; и с) гибридного полипептида, включающего домен трансактивации и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением.
Настоящее изобретение также относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения влияет на лигандсвязывающую активность или чувствительность к лигандам лигандсвязывающего домена ядерного рецептора группы Н.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения снижает активность связывания неэкдистероида диацилгидразина или чувствительность к неэкдистероиду диацилгидразину лигандсвязывающего домена ядерного рецептора группы Н. Предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению аминокислотного остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48, 51, 52, 54, 92, 95, 96, 109, 120, 125, 219, 223, 234 или 238 SEQ ID NO: 1. Более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48 или 109 SEQ ID NO: 1, b) лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 51, 92, 96 или 238 SEQ ID NO: 1, с) остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 52, 92, 96, 125 или 238 SEQ ID NO: 1, d) триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 54, 95, 96, 120, 219 или 234 SEQ ID NO: 1, е) метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 51, 52, 120, 234 или 238 SEQ ID NO: 1, f) аланинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 SEQ ID NO: 1, g) лизинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48, 219 или 223 SEQ ID NO: 1, h) изолейцинового, аргининового или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 234 SEQ ID NO: 1, i) тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 или 238 SEQ ID NO: 1, j) валинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 125 SEQ ID NO: 1, k) глицинового или глутаминового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, или l) аргининового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 или 223 SEQ ID NO: 1. Еще более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения F48N, F48K, 151L, 151М, Т52Е, Т52М, T52R, T52G, T52Q, M54W, M92L, М92Е, R95W, V96W, V96E, V96L, F109N, Y120M, Y120W, М125Е, M125V, М219А, М219К, M219W, M219Y, L223K, L223R, L234M, L234I, L234R, L234W, W238E, W238Y, W238L или W238M SEQ ID NO: 1.
Кроме того, настоящее изобретение также относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения усиливает лигандсвязывающую активность или чувствительность к лигандам лигандсвязывающего домена ядерного рецептора группы Н.
В конкретном варианте исполнения, настоящее изобретение относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения обычно усиливает активность связывания экдистероида или чувствительность к экдистероиду лигандсвязывающего домена ядерного рецептора группы Н. Предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению аминокислотного остатка в положении, эквивалентном или аналогичном а) аминокислотному остатку 96 SEQ ID NO: 1 или b) аминокислотным остаткам 96 и 119 SEQ ID NO: 1. Более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) серинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 96 SEQ ID NO: 1 или b) треонинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 96 SEQ ID NO: 1, и фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 119 SEQ ID NO: 1. Еще более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения V96T или N119F/V96T SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения обычно усиливает активность связывания неэкдистероида диацилгидразина или чувствительность к неэкдистероиду диацилгидразину лигандсвязывающего домена ядерного рецептора группы Н. Предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению аминокислотного остатка в положении, эквивалентном или аналогичном а) аминокислотному остатку 48, 52, 54, 109, 110, 125, 132 или 223 SEQ ID NO: 1 или b) аминокислотным остаткам 52 и 110 SEQ ID NO: 1. Более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) тирозинового, триптофанового, аргининового или лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48 SEQ ID NO: 1, b) лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, с) треонинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 54 SEQ ID NO: 1, d) метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 109 SEQ ID NO: 1, е) пролинового, глутаминовой кислоты или аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, f) изолейцинового, аспарагинового или глицинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 125 SEQ ID NO: 1, g) остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1, h) тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 223 SEQ ID NO: 1, или i) валинового остатка в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1, и пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1. Еще более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения F48Y, F48W, F48L, F48R, T52L, М54Т, F109M, А110Р, А110Е, A110N, М1251, M125G, M125N, L132E, L223Y или T52V/A110P SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы H, содержащий мутацию замещения, где мутация замещения обычно усиливает активность связывания неэкдистероида диацилгидразина и неэкдистероида тетрагидрохинолина или чувствительность к неэкдистероиду диацилгидразину и неэкдистероиду тетрагидрохинолину лигандсвязывающего домена ядерного рецептора группы H. Предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) аминокислотных остатков в положении, эквивалентном или аналогичном аминокислотным остаткам 107 и 127 SEQ ID NO: 1, или b) аминокислотных остатков 107, 110 и 127 SEQ ID NO: 1. Более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 107 SEQ ID NO: 1, и остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 127 SEQ ID NO: 1, или b) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 107 SEQ ID NO: 1, пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, и остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 127 SEQ ID NO: 1. Еще более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения V1071/Y127E или V107I/Y127E/A110P SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения обычно усиливает как активность связывания экдистероида или чувствительность к экдистероиду, так и активность связывания неэкдистероида диацилгидразина или чувствительность к неэкдистероиду диацилгидразину лигандсвязывающего домена группы Н. Предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению аминокислотного остатка в положении, эквивалентном или аналогичном а) аминокислотному остатку 109, 132 или W238P SEQ ID NO: 1, b) аминокислотным остаткам 52, 107 и 127 SEQ ID NO: 1 или с) аминокислотным остаткам 107 и 127 SEQ ID NO: 1, и инсерции аминокислоты 259 SEQ ID NO: 1. Более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 109 SEQ ID NO: 1, b) валинового или метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1, с) пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 238 SEQ ID NO: 1, d) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 127 SEQ ID NO: 1, и валинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1, или е) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и инсерции глицинового остатка в положении, эквивалентном или аналогичном аминокислоте 259 SEQ ID NO: 1. Еще более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения F109W, L132M, L132V, W238P, V107I/Y127E/T52V или V1071/Y127E/259G SEQ ID NO: 1. В другом варианте исполнения, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения V107I/Y127E SEQ ID NO: 1, дополнительно включающую мутацию инсерции G259 SEQ ID NO: 1 (V10717Y127E/G259).
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения обычно усиливает активность связывания неэкдистероида тетрагидрохинолина или чувствительность к неэкдистероиду тетрагидрохинолину лигандсвязывающего домена ядерного рецептора группы Н. Предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) аминокислотного остатка в положении, эквивалентном или аналогичном аминокислотным остаткам 110 или 128 SEQ ID NO: 1, или b) аминокислотных остатков в положении, эквивалентном или аналогичном аминокислотным остаткам 110 и 128 SEQ ID NO: 1. Более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, b) фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 128 SEQ ID NO: 1, или с) пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, и фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 128 SEQ ID NO: 1. Еще более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения A110W, V128F или V128F/A110P SEQ ID NO:1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения дифференциально отвечает на лиганды неэкдистероида диацилгидразина. Предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению аминокислотного остатка в положении, эквивалентном или аналогичном аминокислотным остаткам 52, 95, 109, 125 или 132 SEQ ID NO: 1. Более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, b) гистидинового или метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 95 SEQ ID NO: 1, с) лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 109 SEQ ID NO: 1, d) лейцинового, триптофанового, аргининового, цистеинового или пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 125 SEQ ID NO: 1, или е) метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1. Еще более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения Т52Р, T52W, R95H, R95M, F109L, M125L, M125W, M125R, М125С, М125Р или L132M SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полинуклеотиду, кодирующему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения дифференциально отвечает на лиганды неэкдистероида диацилгидразина. Более предпочтительно изолированный полинуклеотид включает мутацию кодона, приводящую к замещению а) лизинового или аргининового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48 SEQ ID NO: 1, b) глицинового, глутаминового, метионинового, аргининового или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, с) изолейцинового, глицинового, аспарагинового, серинового или валинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 125 SEQ ID NO: 1, d) остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1, е) лизинового, триптофанового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 SEQ ID NO: 1, f) аргининового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 223 SEQ ID NO: 1, или g) лейцинового или метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 238 SEQ ID NO: 1. Еще более предпочтительно, изолированный полинуклеотид включает мутацию кодона, приводящую к мутации замещения F48K, F48R, T52G, T52Q, Т52М, T52R, T52W, М1251, M125G, M125N, M125S, M125V, L132E, М219К, M219W, M219Y, L223R, L223Y, W238L или W238M SEQ ID NO: 1.
Кроме того, настоящее изобретение относится к вектору экспрессии, включающему полинуклеотид в соответствии с изобретением, функционально связанный с регуляторным элементом транскрипции. Предпочтительно, полинуклеотид, кодирующий лигандсвязывающий домен ядерного рецептора, содержащий мутацию замещения, функционально связан с контрольной последовательностью экспрессии, позволяющей экспрессию лигандсвязывающего домена ядерного рецептора в экспрессионно компетентной клетке-хозяине. Контрольная последовательность экспрессии может включать промотор, функциональный в клетке-хозяине, в котором желательна экспрессия. Вектор может быть молекулой плазмидной ДНК или вирусным вектором. Предпочтительные вирусные векторы включают ретровирус, аденовирус, адено-ассоциированный вирус, герпесвирус и вирус коровьей оспы. Изобретение далее относится к репликация-дефектному рекомбинантному вирусу, в геном которого входит полинуклеотид, кодирующий лигандсвязывающий домен ядерного рецептора, содержащий мутацию замещения, как описано выше. Таким образом, настоящее изобретение также относится к изолированной клетке-хозяину, включающей такой вектор экспрессии, где регуляторный элемент транскрипции является функциональным в клетке-хозяине.
Настоящее изобретение также относится к изолированному полипептиду, кодируемому полинуклеотидом в соответствии с изобретением.
Полипептиды по изобретению
Новая система экспрессии индуцибельного гена на основе ядерного рецептора по изобретению включает по меньшей мере одну кассету генной экспрессии, включающую полинуклеотид, кодирующий полипептид, включающий лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения. Таким образом, настоящее изобретение также предусматривает изолированный полипептид, включающий лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением.
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н включает мутацию замещения в положении, эквивалентном или аналогичном а) аминокислотному остатку 48, 51, 52, 54, 92, 95, 96, 109, 110, 119, 120, 125, 128, 132, 219, 223, 234 или 238 SEQ ID NO: 1, b) аминокислотным остаткам 96 и 119 SEQ ID NO: 1, с) аминокислотным остаткам 110 и 128 SEQ ID NO: 1, d) аминокислотным остаткам 52 и 110 SEQ ID NO: 1, e) аминокислотным остаткам 107, 110 и 127 SEQ ID NO: 1 или f) аминокислотным остаткам 52, 107 и 127 SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н включает мутацию замещения в положениях, эквивалентных или аналогичных аминокислотным остаткам 107 и 127, и инсерцию аминокислоты 259 SEQ ID NO: 1. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
Предпочтительно, лигандсвязывающий домен ядерного рецептора группы Н включает замещение а) аспарагинового, аргининового, тирозинового, триптофанового, лейцинового или лизинового остатка в положении, эквивалентном аналогичному аминокислотному остатку 48 SEQ ID NO: 1, b) метионинового, аспарагинового или лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 51 SEQ ID NO: 1, с) лейцинового, пролинового, метионинового, аргининового, триптофанового, глицинового, глутаминового остатка или остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, d) триптофанового или треонинового в положении, эквивалентном или аналогичном аминокислоте 54 SEQ ID NO: 1, e) лейцина или глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 92 SEQ ID NO: 1, f) гистидинового, метионинового или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 95 SEQ ID NO: 1, g) лейцинового, серинового, глутаминовой кислоты или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 96 SEQ ID NO: 1, h) триптофана, пролина, лейцина, метионина или аспарагина в положении, эквивалентном или аналогичном аминокислоте 109 SEQ ID NO: 1, i) глутаминовой кислоты, триптофанового или аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, j) фенилаланинового в положении, эквивалентном или аналогичном аминокислоте 119 SEQ ID NO: 1, k) триптофана или метионина в положении, эквивалентном или аналогичном аминокислоте 120 SEQ ID NO: 1, l) глутаминовой кислоты, пролина, лейцина, цистеина, триптофана, глицина, изолейцина, аспарагина, серина, валина или аргинина в положении, эквивалентном или аналогичном аминокислоте 125 SEQ ID NO: 1, m) фенилаланина в положении, эквивалентном или аналогичном аминокислоте 128 SEQ ID NO: 1, n) метионина, аспарагина, глутаминовой кислоты или валина в положении, эквивалентном или аналогичном аминокислоте 132 SEQ ID NO: 1, о) аланинового, лизинового, триптофанового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 SEQ ID NO: 1, р) лизинового, аргининового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 223 SEQ ID NO: 1, q) метионина, аргинина, триптофана или изолейцина в положении, эквивалентном или аналогичном аминокислоте 234 SEQ ID NO: 1, r) пролина, глутаминовой кислоты, лейцина, метионина или тирозина в положении, эквивалентном или аналогичном аминокислоте 238 SEQ ID NO: 1, s) фенилаланина в положении, эквивалентном или аналогичном аминокислоте 119 SEQ ID NO: 1, и треонина в положении, эквивалентном или аналогичном аминокислоте 96 SEQ ID NO: 1, t) пролина в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, и фенилаланина в положении, эквивалентном или аналогичном аминокислоте 128 SEQ ID NO: 1, u) валинового остатка в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1 и пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, v) изолейцина в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и пролина в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, или w) изолейцина в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и валина в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н включает замещение изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и инсерцию глицинового остатка в положении, эквивалентном или аналогичном аминокислоте 259 SEQ ID NO: 1. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
В другом конкретном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является полипептидом лигандсвязывающего домена рецептора экдизона, включающим мутацию замещения, где мутацию замещения выбирают из группы, состоящей из мутаций замещения F48Y, F48W, F48L, F48N, F48R, F48K, 151М, 151N, 151L, T52M, T52V, T52L, Т52Е, Т52Р, T52R, T52W, T52G, T52Q, M54W, М54Т, M92L, М92Е, R95H, R95M, R95W, V96L, V96W, V96S, V96E, F109W, F109P, F109L, F109M, F109N, А110Е, A110N, A110W, N119F, Y120W, Y120M, М125Р, M125R, М125Е, M125L, М125С, M125W, M125G, М1251, M125N, M125S, M125V, V128F, L132M, L132N, L132V, L132E, М219К, M219W, M219Y, М219А, L223K, L223R, L223Y, L234M, L234I, L234R, L234W, W238P, W238E, W238Y, W238M, W238L,N119F/V96T, V128F/A110P, T52V/A110P, V107l/Y127En52V и V107I/Y127E/A110P SEQ ID NO: 1. В другом варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, является полипептидом лигандсвязывающего домена рецептора экдизона, включающим мутацию замещения V107I/Y127E SEQ ID NO: 1, который дополнительно включает мутацию инсерции G259 SEQ ID NO: 1 (V107I/Y127E/G259).
Настоящее изобретение также предусматривает изолированный полипептид, выбранный из группы, состоящей из а) изолированного полипептида, включающего домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением; b) изолированного полипептида, включающего ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением; и с) изолированного полипептида, включающего домен трансактивации и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
Настоящее изобретение также предусматривает изолированный гибридный полипептид, выбранный из группы, состоящей из а) изолированного гибридного полипептида, включающего домен трансактивации, ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением; b) изолированного гибридного полипептида, включающего ДНК-связывающий домен и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением; и с) изолированного гибридного полипептида, включающего домен трансактивации и лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, в соответствии с изобретением. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н получают из рецептора экдизона.
Настоящее изобретение также предусматривает изолированный полипептид, включающий лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, который влияет на лигандсвязывающую активность или чувствительность к лигандам лигандсвязывающего домена ядерного рецептора группы Н.
В частности, настоящее изобретение относится к изолированному полипептиду ядерного рецептора группы Н, включающему лигандсвязывающий домен, содержащий мутацию замещения, которая снижает лигандсвязывающую активность или чувствительность к лигандам лигандсвязывающего домена ядерного рецептора группы Н.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, которая снижает активность связывания неэкдистероида диацилгидразина или чувствительность к неэкдистероиду диацилгидразину ядерного рецептора группы Н лигандсвязывающего домена. Предпочтительно, изолированный полипептид включает замещение аминокислотного остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48, 51, 52, 54, 92, 95, 96, 109, 120, 125, 219, 223, 234 или 238 SEQ ID NO: 1. Более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению а) аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48 или 109 SEQ ID NO: 1, b) лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 51, 92, 96 или 238 SEQ ID NO: 1, с) остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 52, 92, 96, 125 или 238 SEQ ID NO: 1, d) триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 54, 95, 96, 120 или 219 SEQ ID NO: 1, e) метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 51, 52, 120, 234 или 238 SEQ ID NO: 1, f) аланинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 SEQ ID NO: 1, g) лизинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48, 219 или 223 SEQ ID NO: 1, h) изолейцинового, аргининового или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 234 SEQ ID NO: 1, i) тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 или 238 SEQ ID NO: 1, j) аргининового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 или 223 SEQ ID NO: 1, k) валинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 125 SEQ ID NO: 1, или l) глицинового или глутаминового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1. Еще более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к мутации замещения F48N, 151L, 151М, Т52Е, Т52М, T52R, T52G, T52Q, M54W, M92L, М92Е, R95W, V96W, V96E, V96L, F109N, Y120M, Y120W, М125Е, M125V, М219А, М219К, M219W, M219Y, L223K, L223R, L234M, L234I, L234W, L234R, W238E, W238L, W238M или W238Y SEQ ID NO: 1.
Кроме того, настоящее изобретение также относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы H, содержащий мутацию замещения, которая усиливает лигандсвязывающую активность или чувствительность к лигандам лигандсвязывающего домена ядерного рецептора группы H.
В конкретном варианте исполнения, настоящее изобретение относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы H, содержащий мутацию замещения, которая обычно усиливает активность связывания экдистероида или чувствительность к экдистероиду лигандсвязывающего домена ядерного рецептора группы Н. Предпочтительно, изолированный полипептид включает замещение аминокислотного остатка в положении, эквивалентном или аналогичном а) аминокислотному остатку 96 SEQ ID NO: 1 или b) аминокислотным остаткам 96 и 119 SEQ ID NO: 1. Более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению а) серинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 96 SEQ ID NO: 1, или b) треонинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 96 SEQ ID NO: 1, и фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 119 SEQ ID NO: 1. Еще более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к мутации замещения V96T или N119F/V96T SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, которая обычно усиливает активность связывания диацилгидразина или чувствительность к диацилгидразину лигандсвязывающего домена ядерного рецептора группы Н. Предпочтительно, изолированный полипептид включает замещение аминокислотного остатка в положении, эквивалентном или аналогичном а) аминокислотному остатку 48, 52, 54, 109, 110, 125, 132 или 223 SEQ ID NO: 1 или b) аминокислотным остаткам 52 и 110 SEQ ID NO: 1. Более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению а) тирозинового, триптофанового, аргининового или лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48 SEQ ID NO: 1, b) лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, d) треонинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 54 SEQ ID NO: 1, e) метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 109 SEQ ID NO: 1, f) пролинового, глутаминовой кислоты или аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, g) изолейцинового, глицинового или аспарагинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 125 SEQ ID NO: 1, h) валинового остатка в положении, эквивалентном или аналогичном аминокислоте 52 SEQ ID NO: 1, и пролинового остатка в положении, эквивалентном или аналогичном аминокислоте 110 SEQ ID NO: 1, i) остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1, или j) тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 223 SEQ ID NO: 1. Еще более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к мутации замещения F48Y, F48W, F48L, F48R, T52L, М54Т, F109M, А110Р, А110Е, A110N, М1251, M125G, M125N, L132E, L223Y или T52V/A110P SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы H, содержащий мутацию замещения, которая обычно усиливает как активность связывания экдистероида или чувствительность к экдистероиду, так и активность связывания неэкдистероида диацилгидразина или чувствительность к неэкдистероиду диацилгидразину лигандсвязывающего домена группы H. Предпочтительно, изолированный полипептид включает замещение аминокислотного остатка в положении, эквивалентном или аналогичном а) аминокислотному остатку 109, 132 или W238P SEQ ID NO: 1, b) аминокислотным остаткам 52, 107 и 127 SEQ ID NO: 1 или с) аминокислотным остаткам 107 и 127 SEQ ID NO: 1, и инсерцию аминокислоты 259 SEQ ID NO: 1. Более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению а) триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 109 SEQ ID NO: 1, b) валинового или метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1, с) пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 238 SEQ ID NO: 1, d) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 127 SEQ ID NO: 1, и валинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1, или е) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислоте 107 SEQ ID NO: 1, остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислоте 127 SEQ ID NO: 1, и инсерции глицинового остатка в положении, эквивалентном или аналогичном аминокислоте 259 SEQ ID NO: 1. Еще более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к мутации замещения F109W, L132M, L132V, W238P или V107I/Y127E/T52V SEQ ID NO: 1. В другом варианте исполнения, изолированный полипептид включает мутацию кодона, приводящую к мутации замещения V107I/Y127E SEQ ID NO: 1, который дополнительно включает мутацию инсерции G259 SEQ ID NO: 1 (V1071/Y127E/G259).
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения обычно усиливает активность связывания диацилгидразина и тетрагидрохинолина или чувствительность к диацилгидразину и тетрагидрохинолину лигандсвязывающего домена ядерного рецептора группы Н. Предпочтительно, изолированный полипептид включает мутацию замещения, приводящую к замещению а) аминокислотных остатков в положении, эквивалентном или аналогичном аминокислотным остаткам 107 и 127 SEQ ID NO: 1, или b) аминокислотных остатков 107, 110 и 127 SEQ ID NO: 1. Более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению а) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 107 SEQ ID NO: 1, и остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 127 SEQ ID NO: 1, или b) изолейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 107 SEQ ID NO: 1, пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, и остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 127 SEQ ID NO: 1. Еще более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к мутации замещения V107I/Y127E или V107I/Y127E/A110P SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения обычно усиливает активность связывания неэкдистероида тетрагидрохинолина или чувствительность к неэкдистероиду тетрагидрохинолину лигандсвязывающего домена ядерного рецептора группы Н. Предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению а) аминокислотного остатка в положении, эквивалентном или аналогичном аминокислотным остаткам 110 или 128 SEQ ID NO: 1, или b) аминокислотных остатков в положении, эквивалентном или аналогичном аминокислотным остаткам 110 и 128 SEQ ID NO: 1. Более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению а) триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, b) фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 128 SEQ ID NO: 1, или с) пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 110 SEQ ID NO: 1, и фенилаланинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 128 SEQ ID NO: 1. Еще более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к мутации замещения A110W, V128F или V128F/A110P SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения дифференциально отвечает на лиганды неэкдистероида диацилгидразина. Предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению аминокислотного остатка в положении, эквивалентном или аналогичном аминокислотным остаткам 52, 95, 109, 125 или 132 SEQ ID NO: 1. Более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к замещению а) пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, b) гистидинового или метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 95 SEQ ID NO: 1, с) лейцинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 109 SEQ ID NO: 1, d) лейцинового, триптофанового, аргининового, цистеинового или пролинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 125 SEQ ID NO: 1, или е) метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1. Еще более предпочтительно, изолированный полипептид включает мутацию кодона, приводящую к мутации замещения Т52Р, R95H, R95M, F109L, M125L, M125W, M125R, М125С, М125Р или L132M SEQ ID NO: 1.
В другом конкретном варианте исполнения, настоящее изобретение относится к изолированному полипептиду, включающему лигандсвязывающий домен ядерного рецептора группы Н, содержащий мутацию замещения, где мутация замещения дифференциально отвечает на лиганды неэкдистероида диацилгидразина. Более предпочтительно изолированный полипептид включает мутацию кодона, приводящую к замещению а) лизинового или аргининового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 48 SEQ ID NO: 1, b) глицинового, глутаминового, метионинового, аргининового или триптофанового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 52 SEQ ID NO: 1, с) изолейцинового, глицинового, аспарагинового, серинового или валинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 125 SEQ ID NO: 1, d) остатка глутаминовой кислоты в положении, эквивалентном или аналогичном аминокислотному остатку 132 SEQ ID NO: 1, е) лизинового, триптофанового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 219 SEQ ID NO: 1, f) аргининового или тирозинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 223 SEQ ID NO: 1, или g) лейцинового или метионинового остатка в положении, эквивалентном или аналогичном аминокислотному остатку 238 SEQ ID NO: 1. Еще более предпочтительно изолированный полипептид включает мутацию кодона, приводящую к мутации замещения F48K, F48R, T52G, T52Q, Т52М, T52R, T52W, М1251, M125G, M125N, M125S, M125V, L132E, М219К, M219W, M219Y, L223R, L223Y, W238L или W238M SEQ ID N0:1.
Настоящее изобретение также относится к композиции, включающей изолированный полипептид в соответствии с изобретением.
Способ модулирования генной экспрессии по изобретению
Предложенное заявителями изобретение также относится к способам модулирования генной экспрессии в клетке-хозяине с использованием системы модулирования генной экспрессии в соответствии с изобретением. Конкретно, предложенное заявителями изобретение предусматривает способ модулирования экспрессии гена в клетке-хозяине, включающий стадии: а) введение в клетку-хозяина системы модулирования генной экспрессии в соответствии с изобретением и b) введение в клетку-хозяина лиганда; где модулируемый ген является компонентом кассеты генной экспрессии, включающей: i) элемент ответа, включающий домен распознавания ДНК-связывающего домена системы генной экспрессии; ii) промотор, который активируется доменом трансактивации системы генной экспрессии; и iii) ген, экспрессия которого модулируется, причем при введении лиганда в клетку-хозяина, экспрессия гена модулируется.
Изобретение также предусматривает способ модулирования экспрессии гена в клетке-хозяине, включающий стадии: а) введения в клетку-хозяина системы модулирования генной экспрессии в соответствии с изобретением; b) введения в клетку-хозяина кассеты генной экспрессии в соответствии с изобретением, где кассета генной экспрессии включает i) элемент ответа, включающий домен, распознаваемый ДНК-связывающим доменом системы генной экспрессии; ii) промотор, который активируется доменом трансактивации системы генной экспрессии; и iii) ген, экспрессия которого модулируется; и с) введения в клетку-хозяина лиганда; причем при введении лиганда в клетку-хозяина, экспрессия гена модулируется.
Предложенное заявителями изобретение также предусматривает способ модулирования экспрессии гена в клетке-хозяине, включающий кассету генной экспрессии, содержащую элемент ответа, включающий домен, с которым связывается ДНК-связывающий домен первого гибридного полипептида системы модулирования генной экспрессии; промотор, который активируется доменом трансактивации второго гибридного полипептида системы модулирования генной экспрессии; и ген, экспрессия которого модулируется; в котором способ включает стадии: а) введения в клетку-хозяина системы модулирования генной экспрессии в соответствии с изобретением и b) введения в клетку-хозяина лиганда; причем при введении лиганда в хозяина, экспрессия гена модулируется.
Гены, представляющие интерес для экспрессии в клетке-хозяине с использованием предложенных заявителями способов, могут быть эндогенными генами или гетерологичными генами. Информация о последовательности нуклеиновых кислот или аминокислотной последовательности для желательного гена или белка может находиться в одной из многих баз данных с публичным доступом, например GENBANK, EMBL, Swiss-Prot и PIR, или во многих публикациях в журналах биологической тематики. Таким образом, специалисты в данной области техники имеют доступ к информации о последовательностях нуклеиновых кислот практически для всех известных генов. Такая информация может затем быть использована для конструирования желательных структурных элементов для инсерции представляющего интерес гена в кассеты генной экспрессии, используемые в предложенных заявителями способах, описанных тут.
Примеры генов, представляющих интерес для экспрессии в клетке-хозяине с использованием предложенных заявителями способов, включают, без ограничения: антигены, продуцируемые в растениях как вакцины, ферменты, такие как альфа-амилаза, фитаза, глюканы, ксилаза и ксиланаза, гены устойчивости к насекомым, нематодам, грибкам, бактериям, вирусам и абиотическим стрессам, нутрицевтики, фармацевтические средства, витамины, гены для модифицирования содержания аминокислот, устойчивости к гербицидам, холоду, засухе и повышенным температурам, промышленных продуктов, масел, белка, углеводов, антиоксидантов, мужских стерильных растений, цветов, топливных продуктов, других признаков, имеющих прикладное значение, гены, кодирующие терапевтически желательные полипептиды или продукты, которые могут быть использованы для лечения состояния, болезни, расстройства, дисфункции, генетического дефекта, такие как моноклональные антитела, ферменты, протеазы, цитокины, интерфероны, инсулин, эритропоэтин, факторы свертывания крови, другие факторы или компоненты крови, вирусные векторы для генной терапии, вирусы для вакцин, мишени для доставки лекарственных средств, аналитические реагенты для функциональной геномики и протеомики и т.п.
Приемлемыми лигандами являются любые лиганды, модулирующие экспрессию гена, когда связывание ДНК-связывающего домена системы генной экспрессии в соответствии с изобретением с элементом ответа в присутствии лиганда приводит к активация или супрессии экспрессии генов. Предпочтительные лиганды включают экдистероид, такой как экдизон, 20-гидроксиэкдизон, понастерон А, муристерон А и т.п., 9-цис-ретиноевую кислоту, синтетические аналоги ретиноевой кислоты, N,N'-диацилгидразины, такие как раскрытые в патентах США №№6013836; 5117057; 5530028; 5378726; и патентных заявках США №№10/775883 и 10/787906; дибензоилалкилцианогидразины, такие как раскрытые в европейской заявке №461809; N-алкил-N,N'-диароилгидразины, такие как раскрытые в патенте США №5225443; N-ацил-N-алкилкарбонилгидразины, такие как раскрытые в европейской заявке №234994; N-ароил-N-алкил-N'-ароилгидразины, такие как описанные в патенте США №4985461; тетрагидрохинолины, такие как раскрытые в международной заявке № PCT/US03/00915; которые все включены сюда в качестве ссылок, и другие подобные материалы, включая 3,5-ди-трет-бутил-4-гидрокси-N-изобутилбензамид, 8-O-ацетилгарпагид, оксистеролы, 22(R)-гидроксихолестерин, 24(S)-гидроксихолестерин, 25-эпоксихолестерин, Т0901317, 5-альфа-6-альфа-эпоксихолестерин-3-сульфат (ECHS), 7-кетохолестерин-3-сульфат, фарнезол, желчные кислоты, 1,1-бифосфонатные сложные эфиры, ювенильный гормон III и т.п.
В предпочтительном варианте исполнения, лиганд для использования в предложенном заявителями способе модулирования экспрессии гена является соединением формулы:
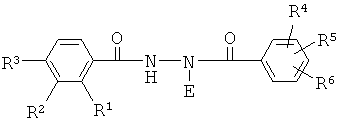
где:
Е является разветвленным (С4-С12)-алкилом или разветвленным (C4-C12)-алкенилом, содержащим третичный углерод, или циано-(С3-С12)-алкилом, содержащим третичный углерод;
R1 обозначает Н, Me, Et, i-Pr, F, формил, CF3, CHF2, CHCl2, CH2F, CH2Cl, CH2OH, CH2OMe, CH2CN, CN, С0СН, 1-пропинил, 2-пропинил, винил, ОН, ОМе, OEt, циклопропил, CF2CF3, CH=CHCN, аллил, азидо, SCN или SCHF2;
R2 обозначает Н, Me, Et, n-Pr, i-Pr, формил, CF3, CHF2, CHCl2, CH2F, CH2Cl, CH2OH, CH2OMe, CH2CN, CN, С0СН, 1-пропинил, 2-пропинил, винил, Ac, F, Cl, ОН, ОМе, OEt, O-n-Pr, ОАс, NMe2, NEt2, SMe, SEt, SOCF3, OCF2CF2H, COEt, циклопропил, CF2CF3, CH=CHCN, аллил, азидо, OCF3, OCHF2, O-i-Pr, SCN, SCHF2, SOMe, NH-CN или, связанный с R3 и атомами углерода фенила, к которым присоединены R2 и R3, образует этилендиокси, дигидрофурильное кольцо с атомом кислорода, прилегающим к углероду фенила, или дигидропирильное кольцо с атомом кислорода, прилегающим к углероду фенила;
R3 обозначает Н, Et или, связанный с R2 и атомами углерода фенила, к которым присоединены R2 и R3, образует этилендиокси, дигидрофурильное кольцо с атомом кислорода, прилегающим к углероду фенила, или дигидропирильное кольцо с атомом кислорода, прилегающим к углероду фенила;
R4, R5 и R6 независимо обозначают Н, Me, Et, F, Cl, Br, формил, CF3, CHF2, CHCl2, CH2F, CH2Cl, CH2OH, CN, С0СН, 1-пропинил, 2-пропинил, винил, ОМе, OEt, SMe или SEt.
В другом предпочтительном варианте исполнения, лиганд для использования в предложенном заявителями способе модулирования экспрессии гена является соединением формулы:
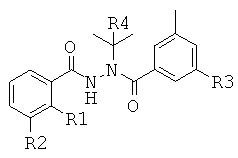
где:
В другом предпочтительном варианте исполнения, лиганд для использования в предложенном заявителями способе модулирования экспрессии гена является соединением формулы:
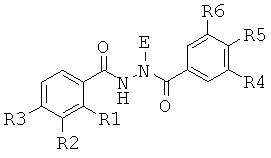
где:
В следующем предпочтительном варианте исполнения, лиганд для использования в предложенном заявителями способе модулирования экспрессии гена является соединением формулы:
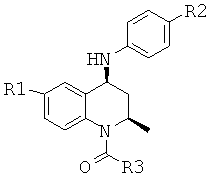
где:
В другом предпочтительном варианте исполнения, лиганд для использования в предложенном заявителями способе модулирования экспрессии гена является экдизоном, 20-гидроксиэкдизоном, понастероном А, муристероном А, оксистеролом, 22(R)-гидроксихолестерином, 24(S)-гидроксихолестерином, 25-эпоксихолестерином, Т0901317, 5-альфа-6-альфа-эпоксихолестерин-3-сульфатом (ECHS), 7-кетохолестерин-3-сульфатом, фарнезолом, желчными кислотами, 1,1-бифосфонатными сложными эфирами или ювенильным гормоном III.
В другом предпочтительном варианте исполнения, в предложенном заявителями способе модулирования экспрессии гена может быть использован второй лиганд, помимо первого лиганда, описанного выше. Предпочтительно, этот второй лиганд является 9-цис-ретиноевой кислотой или синтетическим аналогом ретиноевой кислоты.
Клетки- и организмы-хозяева, кроме человека, по изобретению
Как было описано выше, система модулирования генной экспрессии по настоящему изобретению может быть использована для модулирования генной экспрессии в клетке-хозяине. Экспрессия в трансгенных клетках-хозяевах может быть пригодна для экспрессии различных представляющих интерес генов. Предложенное заявителями изобретение предусматривает модуляцию генной экспрессии в прокариотических и эукариотических клетках-хозяевах. Экспрессия в трансгенных клетках-хозяевах пригодна для экспрессии различных полипептидов, представляющих интерес, включая, без ограничений, антигены, продуцируемые в растениях как вакцины, ферменты, такие как альфа-амилаза, фитаза, глюканы, ксилаза и ксиланаза, гены для придания устойчивости против насекомых, нематод, грибков, бактерий, вирусов и абиотических стрессов, антигены, нутрицевтики, фармацевтические средства, витамины, гены для модифицирования содержания аминокислот, устойчивости к гербицидам, холоду, засухе и повышенным температурам, промышленных продуктов, масел, белка, углеводов, антиоксидантов, мужских стерильных растений, цветов, топливных продуктов, других признаков, имеющих прикладное значение, терапевтических полипептидов, промежуточных соединений путей; для модуляции путей, уже существующих в хозяине, для синтеза новых продуктов, которые ранее нельзя было получить с использованием хозяина; анализов на основе клеток; функциональных геномных анализов, производства биотерапевтических белков, анализов в области протеомики и т.п. Дополнительно, генные продукты могут быть пригодны для придания хозяину способности к более высоким урожаям клеток или для обеспечения возможности использования альтернативного режима выращивания.
Таким образом, предложенное заявителями изобретение предусматривает изолированную клетку-хозяина, включающую систему генной экспрессии в соответствии с изобретением. Настоящее изобретение также предусматривает изолированную клетку-хозяина, включающую генную кассету экспрессии в соответствии с изобретением. Предложенное заявителями изобретение также предусматривает изолированную клетку-хозяина, включающую полинуклеотид или полипептид в соответствии с изобретением. Настоящее изобретение также относится к клетке-хозяину, трансформированной вектором экспрессии в соответствии с изобретением. Клетка-хозяин может быть бактериальной клеткой, грибковой клеткой, клеткой нематоды, клеткой насекомого, клеткой рыбы, растительной клеткой, клеткой птицы, клеткой животного или клеткой млекопитающего. В еще одном варианте исполнения, изобретение относится к способу продуцирования лигандсвязывающего домена ядерного рецептора, включающего мутацию замещения, в котором способ включает культивирование клетки-хозяина, как описано выше, в культуральной среде в условиях, позволяющих протекание экспрессии полинуклеотида, кодирующего лигандсвязывающий домен ядерного рецептора, включающий мутацию замещения, и выделение лигандсвязывающего домена ядерного рецептора, включающего мутацию замещения, из культуры.
В конкретном варианте исполнения, изолированная клетка-хозяин является прокариотической клеткой-хозяином или эукариотической клеткой-хозяином. В другом конкретном варианте исполнения, изолированная клетка-хозяин является клеткой-хозяином беспозвоночных или клеткой-хозяином позвоночных. Предпочтительно, клетку-хозяина выбирают из группы, состоящей из бактериальных клеток, грибковых клеток, дрожжевых клеток, клеток нематод, клеток насекомых, клеток рыб, растительных клеток, клеток птиц, клеток животных и клеток млекопитающих. Более предпочтительно, клетка-хозяин является дрожжевой клеткой, клеткой нематоды, клеткой насекомого, растительной клеткой, клеткой полосатого данио, куриной клеткой, клеткой хомячка, мышиной клеткой, клеткой крысы, клеткой кролика, кошачьей клеткой, собачьей клеткой, бычьей клеткой, козьей клеткой, коровьей клеткой, свиной клеткой, лошадиной клеткой, клеткой овцы, клеткой человекообразной обезьяны, клеткой мартышки, клеткой шимпанзе или клеткой человека. Примеры предпочтительных клеток-хозяев включают, без ограничения, клетки-хозяева грибковых или дрожжевых видов, таких как Aspergillus, Trichoderma, Saccbaromyces, Pichia, Candida, Hansenula, или бактериальных видов, таких как принадлежащие к родам Synechocystis, Synechococcus, Salmonella, Bacillus, Acinetobacter, Rhodococcus, Streptomyces, Escherichia, Pseudomonas, Methylomonas, Methylobacter, Alcaligenes, Synechocystis, Anabaena, Tuobacillus, Methanobacterium и Klebsiella; растительных видов, выбранных из группы, состоящей из яблока, Arabidopsis, проса посевного, банана, ячменя, бобов, свеклы, фасоли мунго, турецкого гороха, стручкового перца, огурца, баклажана, кормовых бобов, кукурузы, дыни, проса, фасоли золотистой, овса, бамии, Panicum, папайи, арахиса, гороха, перца, каянуса, ананаса, Phaseolus, картофеля, тыквы, риса, сорго, сои, тыквенных, сахарного тростника, сахарной свеклы, подсолнечника, батата, чая, томата, табака, арбуза и пшеницы; животных; и млекопитающих.
В конкретном варианте исполнения, клетка-хозяин является дрожжевой клеткой, выбранной из группы, состоящей из клеток-хозяев Saccharomyces, Pichia и Candida.
В другом конкретном варианте исполнения, клетка-хозяин является клеткой нематоды Caenorhabdus elegans.
В другом конкретном варианте исполнения, клетка-хозяин является клеткой насекомого.
В другом конкретном варианте исполнения, клетка-хозяин является растительной клеткой, выбранной из группы, состоящей из яблока, Arabidopsis, проса посевного, банана, ячменя, бобов, свеклы, фасоли мунго, турецкого гороха, стручкового перца, огурца, баклажана, кормовых бобов, кукурузы, дыни, проса, фасоли золотистой, овса, бамии, Panicum, папайи, арахиса, гороха, перца, каянуса, ананаса, Phaseolus, картофеля, тыквы, риса, сорго, сои, тыквенных, сахарного тростника, сахарной свеклы, подсолнечника, батата, чая, томата, табака, арбуза и пшеницы
В другом конкретном варианте исполнения, клетка-хозяин является клеткой полосатого данио.
В другом конкретном варианте исполнения, клетка-хозяин является куриной клеткой.
В другом конкретном варианте исполнения, клетка-хозяин является клеткой млекопитающего, выбранного из группы, состоящей из клетки хомяка, мышиной клетки, клетки крысы, клетки кролика, кошачьей клетки, собачьей клетки, бычьей клетки, козьей клетки, коровьей клетки, свиной клетки, лошадиной клетки, овечьей клетки, клетки обезьяны, клетки шимпанзе и клетки человека.
Трансформация клеток-хозяев хорошо известна специалистам и может быть осуществлена различными способами, включая, без ограничений, электропорацию, вирусную инфекцию, трансфекцию плазмидой/вектором, трансфекцию, медиируемую невирусным вектором, Agrobacterium-медиируемую трансформацию, бомбардировку частицами и т.п. Экспрессия желательных генных продуктов предусматривает культивирование трансформированных клеток-хозяев в пригодных условиях и индуцирование экспрессии трансформированного гена. Условия культивирования и протоколы генной экспрессии в прокариотических и эукариотических клетках хорошо известны специалистам (см. раздел Общие методы Примеров). Клетки могут быть собраны и генные продукты изолированы в соответствии с протоколами, специфическими для генного продукта.
Кроме того, может быть выбрана клетка-хозяин, которая модулирует экспрессию вставленного полинуклеотида или модифицирует и процессирует полипептидный продукт определенным желательным образом. Разные клетки-хозяева имеют характерные и специфические механизмы трансляционного и посттрансляционного процессинга и модификации [например, гликозилирование, отщепление (например, сигнальной последовательность)] белков. Соответствующие клеточные линии или системы хозяев могут быть выбраны для обеспечения желательной модификации и процессинга экспрессированного чужеродного белка. Например, экспрессия в бактериальной системе может быть использована для продуцирования негликозилированного корового белкового продукта. Однако полипептид, экспрессированный в бактериях, может иметь неправильную укладку. Экспрессия в дрожжах может дать гликозилированный продукт. Экспрессия в эукариотических клетках может повышать вероятность "нативного" гликозилирования и укладки гетерологичного белка. Кроме того, экспрессия в клетках млекопитающих может дать инструмент для реконституирования или конституирования активности полипептида. Кроме того, разные системы экспрессии вектор/хозяин могут в разной степени влиять на реакции процессинга, такие как протеолитическое расщепление.
Предложенное заявителями изобретение также относится к организмам, кроме человека, включающим изолированную клетку-хозяина в соответствии с изобретением. В конкретном варианте исполнения, организм, кроме человека, является прокариотическим организмом или эукариотическим организмом. В другом конкретном варианте исполнения, организм кроме человека является организмом беспозвоночных или организмом позвоночных.
Предпочтительно, организм, кроме человека, выбирают из группы, состоящей из бактерий, грибков, дрожжей, нематод, насекомых, рыб, растений, птиц, животных и млекопитающих. Более предпочтительно, организм, кроме человека, является дрожжами, нематодой, насекомым, растением, полосатым данио, курицей, хомячком, мышью, крысой, кроликом, кошкой, собакой, жвачным животным, козой, коровой, свиньей, лошадью, овцой, человекообразной обезьяной, обезьяной или шимпанзе.
В конкретном варианте исполнения, организм, кроме человека, является дрожжами, выбранными из группы, состоящей из Saccharomyces, Pichia и Candida.
В другом конкретном варианте исполнения, организм, кроме человека, является нематодой Caenorhabdus elegans.
В другом конкретном варианте исполнения, организм, кроме человека, является растением, выбранным из группы, состоящей из яблока, Arabidopsis, проса посевного, банана, ячменя, бобов, свеклы, фасоли мунго, турецкого гороха, стручкового перца, огурца, баклажана, кормовых бобов, кукурузы, дыни, проса, фасоли золотистой, овса, бамии, Panicum, папайи, арахиса, гороха, перца, каянуса, ананаса, Phaseolus, картофеля, тыквы, риса, сорго, сои, тыквенных, сахарного тростника, сахарной свеклы, подсолнечника, батата, чая, томата, табака, арбуза и пшеницы.
В другом конкретном варианте исполнения, организм, кроме человека, является мышью Mus musculus.
Измерение генной экспрессии/транскрипции
Одним пригодным измерением по изобретению из предложенных заявителями методов является измерение транскрипционного состояния клетки, включая идентификацию и относительное содержание РНК, предпочтительно видов мРНК. Такие измерения удобно проводить путем измерения относительного содержания кДНК несколькими существующими методами генной экспрессии.
Технология матриц нуклеиновых кислот является полезным способом для определения дифференциальной экспрессии мРНК. Такая технология включает, например, олигонуклеотидные микросхемы и микроматрицы ДНК. Эти методики основаны на использовании ДНК-фрагментов или олигонуклеотидов, которые соответствуют разным генам или кДНК, иммобилизованных на твердой подложке и гибридизуемых с зондами, приготовленными из пулов общей мРНК, экстрагированной из клеток, тканей или целых организмов и преобразованной в кДНК. Олигонуклеотидные микросхемы представляют собой матрицы олигонуклеотидов, синтезированных на субстрате с использованием фотолитографических методов. Были получены микросхемы, которые могут анализировать до 1700 генов. Микроматрицы ДНК представляют собой матрицы образцов ДНК, типично, продуктов ПЦР, которые роботизированно наносятся печатными методами на предметное стекло. Каждый ген анализируется с помощью полной или частичной целевой ДНК-последовательности. В настоящее время отработано промышленное изготовление микроматриц, содержащих до 10000 генов. Основная разница между этими двумя методиками заключается в том, что олигонуклеотидные микросхемы типично используют 25-мерные олигонуклеотиды, которые позволяют фракционировать короткие молекулы ДНК, в то время как большие по размеру ДНК-мишени микроматриц, приблизительно по 1000 пар оснований, могут обеспечить большую чувствительность при фракционировании сложных смесей ДНК.
Другим полезным измерением из предложенных заявителями способов по изобретению является определение трансляционного состояния клетки путем измерения относительного содержания составляющих белковых видов, присутствующих в клетке, с использованием процессов, хорошо известных специалистам.
В тех случаях, когда желательна идентификация генов, ассоциированных с разными физиологическими функциями, может быть использован метод анализа, в котором измеряют изменения таких функций, как клеточный рост, апоптоз, старение, дифференцировка, адгезия, связывание со специфическими молекулами, связывание с другими клетками, клеточная организация, органогенез, внутриклеточный транспорт, ускорение транспорта, преобразование энергии, метаболизм, миогенез, нейрогенез и/или гематопоэз.
Кроме того, селектируемый маркер или экспрессия гена-репортера могут быть использованы для измерения модуляции генной экспрессии с использованием предложенного заявителями изобретения.
Другие способы детектирования продуктов генной экспрессии хорошо известны специалистам и включают саузерн-блотирование (детектирование ДНК), дот- или слот-блоттинг (ДНК, РНК), нозерн-блоттинг (РНК), ОТ-ПЦР (РНК), вестерн-блоттинг (детектирование полипептидов) и иммуноферментные твердофазные (ELISA) анализы (полипептиды). Хотя и менее предпочтительно, меченые белки могут быть использованы для детектирования определенной последовательности нуклеиновой кислоты, с которой они гибридизуются.
В некоторых случаях, необходимо амплифицировать количество последовательности нуклеиновой кислоты. Это может быть сделано с использованием одного или нескольких из ряда пригодных способов, включая, например, полимеразную цепную реакцию ("ПЦР"), лигазную цепную реакцию ("LCR"), амплификацию с вытеснением цепи ("SDA"), транскрипции на основе амплификации и т.п. ПЦР проводится в соответствии с известными методиками, в которых, например, образец нуклеиновой кислоты обрабатывают в присутствии термостабильной ДНК полимеразы, в условиях гибридизации, с одной парой олигонуклеотидных праймеров, причем один праймер гибридизуется с одной цепью (матричной) специфической детектируемой последовательности. Праймеры являются в достаточной степени комплементарными по отношению к каждой матричной цепи специфической последовательности для гибридизации с ней. Синтезируют продукт наращивания каждого праймера, который является комплементарным к матричной цепи нуклеиновой кислоты, с которой он гибридизуется. Продукт наращивания, синтезированный с каждого праймера, также может использоваться в качестве матрицы для дальнейшего синтеза продуктов наращивания с использованием тех же праймеров. После достаточного числа циклов синтеза продуктов наращивания образец может быть проанализирован, как описано выше, для определения присутствия детектируемой последовательности или последовательностей.
Скрининг-анализы лигандов
Настоящее изобретение также относится к способам скрининга соединений, которые индуцируют или подавляют трансактивацию лигандсвязывающего домена ядерного рецептора, включающего мутацию замещения, в клетке путем введения в контакт лигандсвязывающего домена ядерного рецептора с молекулой-кандидатом и детектирования активности репортерного гена в присутствии лиганда. Соединения-кандидаты могут быть агонистами или антагонистами лигандсвязывающего домена ядерного рецептора. В предпочтительном варианте исполнения, лигандсвязывающий домен ядерного рецептора экспрессируется из полинуклеотида в клетке и проводятся измерения активности трансактивации (т.е. экспрессия или репрессия репортерного гена) или активность связывания соединения.
Соответственно, в дополнение к целесообразному конструированию агонистов и антагонистов на основе структуры лигандсвязывающего домена ядерного рецептора настоящее изобретение предусматривает альтернативный способ идентифицирования специфических лигандов лигандсвязывающего домена ядерного рецептора с использованием различных скрининг-анализов, известных специалистам.
Любая методика скрининга, известная специалистам, может быть использована для отбора агонистов или антагонистов лигандсвязывающего домена ядерного рецептора группы Н. Например, пригодная клеточная линия, включающая систему генной экспрессии на основе ядерного рецептора в соответствии с изобретением, может быть трансформирована кассетой генной экспрессии, кодирующей маркерный ген, функционально связанный с индуцибельным или репрессируемым промотором. Трансформированные клетки затем подвергают воздействию тестового раствора, содержащего соединение-кандидат агониста или антагониста, и затем проводят анализ на маркер генной экспрессии или репрессии. Присутствие большего количества маркера генной экспрессии по сравнению с контрольными клетками, не подвергнутыми воздействию тестового раствора, указывает на присутствие соединения-агониста в тестовом растворе. Наоборот, присутствие меньшего количества маркера генной экспрессии по сравнению с контрольными клетками, не подвергнутыми воздействию тестового раствора, указывает на присутствие в тестовом растворе соединения-антагониста.
Настоящее изобретение предусматривает скрининг малых молекул лигандов или аналогов и имитаторов лигандов, а также скрининг природных лигандов, которые in vivo связываются и агонизируют или антагонизируют лигандсвязывающий домен ядерного рецептора группы Н в соответствии с изобретением. Например, библиотеки природных продуктов могут быть подвергнуты скринингу с использованием методов анализа по изобретению на молекулы, агонизирующие или антагонизирующие активность системы генной экспрессии на основе ядерных рецепторов.
Идентификация и скрининг антагонистов дополнительно облегчаются путем определения структурных особенностей белка, например, с использованием рентгеновской кристаллографии, нейтронной дифракции, спектрометрии ядерного магнитного резонанса и других методик определения структуры. Эти методики обеспечивают целесообразное конструирование или идентификацию агонистов и антагонистов.
Другой подход использует рекомбинантный бактериофаг для продуцирования больших библиотек. С использованием "фагового способа" [Scott and Smith, 1990, Science 249: 386-390 (1990); Cwiria, et al., Proc. Natl. Acad. Scl, 87: 6378-6382 (1990); Devlin et al., Science, 249:404-406 (1990)], могут быть сконструированы очень большие библиотеки (106-108 химических объектов). Второй подход использует преимущественно химические способы, примерами которых являются способ Гейзена [Geysen et al., Molecular Immunology 23: 709-715 (1986); Geysen et al., J. Immunologic Method. 102: 259-274 (1987)] и способ Fodor et al. [Science 251: 767-773 (1991)]. Furka et al. [14th International Congress of Biochemistry, Volume 5, Abstract FR:013 (1988); Furka, Int. J. Peptide Protein Res. 37: 487-493 (1991)], Houghton [патент США №4631211, выданный в декабре 1986 г.] и Rutter et al. [патент США №5010175, выданный 23 апреля 1991 г.] описывают способы продуцирования смеси пептидов, которые могут тестироваться в качестве агонистов или антагонистов.
В другом аспекте, для скрининга лигандов-кандидатов в соответствии с настоящим изобретением могут быть использованы синтетические библиотеки [Needels et al., Proc. Natl. Acad. Sci. USA 90: 10700-4 (1993); Ohimeyer et al., Proc. Natl. Acad. Sci. USA 90: 10922-10926 (1993); Lam et al., международная патентная публикация № WO 92/00252; Kocis et al., международная патентная публикация №WO 9428028, которые все целиком включены сюда в качестве ссылок] и т.п.
Скрининг может быть осуществлен с помощью рекомбинантных клеток, которые экспрессируют лигандсвязывающий домен ядерного рецептора в соответствии с изобретением или, альтернативно, с использованием очищенного белка, например, полученного рекомбинантными методами, как описано выше. Например, меченый растворимый лигандсвязывающий домен ядерных рецепторов может быть использован для скрининга библиотек, как описано в приведенных выше ссылках.
В одном варианте исполнения, лигандсвязывающий домен ядерного рецептора группы Н в соответствии с изобретением может быть меченным непосредственно. В другом варианте исполнения, меченый вторичный реагент может быть использован для детектирования связывания лигандсвязывающего домена ядерного рецептора по изобретению с молекулой, представляющей интерес, например молекулой, связанной с твердой подложкой. Связывание может детектироваться in situ образованием хромофора ферментной меткой. Пригодные ферменты включают, без ограничения, щелочную фосфатазу и пероксидазу хрена. В другом варианте исполнения, может быть использован двухцветный анализ с использованием двух хромогенных субстратов с двумя ферментными метками на разные молекулы-акцепторы, представляющие интерес. С помощью двухцветного анализа могут быть идентифицированы кросс-реактивные и однореактивные лиганды.
Другие метки для использования по изобретению включают окрашенные латексные бусины, магнитные бусины, флуоресцентные метки (например, в качестве нескольких примеров флорофоров можно назвать флуоресцеинизотиоианат (FITC), фитоэритрин (РЕ), краситель Texas red (TR), родамин, свободные или хелатированные соли ряда лантанидов, особенно Eu3+), хемолюминесцентные молекулы, радиоизотопы или метки для магниторезонансной визуализации. Двухцветные анализы могут быть проведены с использованием двух или более окрашенных латексных бусин или флуорофоров, излучающих на разных длинах волн. Меченые молекулы или клетки могут быть детектированы визуально или с помощью механических/оптических средств. Механические/оптические средства включают сортировку с активацией флуоресценции, т.е. аналогично FACS, и средства выборки с помощью микроманипулятора.
Настоящее изобретение может быть лучше понято со ссылкой на следующие неограничивающие Примеры, которые приводятся как типичные для изобретения.
ПРИМЕРЫ
Заявители разработали модель гомологии CfEcR и использовали эту модель гомологии вместе с опубликованной моделью гомологии рецептора экдизона Chironomous tetans ("CtEcR") (Wurtz et al., 2000) для идентификации критических остатков, участвующих в связывании с экдистероидами и не-экдистероидами. Было показано, что синтетические нестероиды диацилгидразины связываются с EcR чешуекрылых с высоким сродством и индуцируют преждевременную неполную линьку этих насекомых (Wing et al., 1988), и несколько этих соединений с настоящее время продаются в качестве инсектицидов. Лигандсвязывающая полость EcR эволюционировала таким образом, чтобы помещать длинную структуру основной цепи экдистероидов, таких как 20Е. Диацилгидразины имеют компактную структуру по сравнению с экдистероидами и занимают только донную часть кармана связывания EcR. Это оставляет несколько критических остатков в верхней части кармана связывания, которые могут контактировать с экдистероидами, но не неэкдистероидами, такими как диацилгидразины. Заявители выполнили мутации замещения остатков, контактирующих с экдистероидами и/или неэкдистероидами, и определили эффект мутаций связывание лигандов. Заявители описывают тут субституционные мутации нескольких из этих остатков и идентифицируют несколько классов рецепторов субституционных мутантов на основе их характеристик связывания и трансактивации. Предложенные заявителями новые полинуклеотиды и полипептиды ядерных рецепторов с мутацией замещения пригодны для использования в системах модулирования индуцибельного гена на основе ядерного рецептора для различных областей применения, включая генную терапию, экспрессию представляющих интерес белков в клетках-хозяевах, продуцирование трансгенных организмов и системы для анализа на основе клеток.
Общие способы
Используемые тут стандартные методики рекомбинантных ДНК и молекулярного клонирования хорошо известны специалистам и описаны Sambrook, J., Fritsch, E.F., and Maniatis, Т. Molecular Cloninig: A Laboratory Manual; Cold Spring Harbor Laboratory Press: Cold Spring Harbor, N.Y. (1989) (Maniatis) и T.J.Silhavy, M.L.Bennan, and L.W.Enquist, Experiments with Gene Fusion, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y. (1984) и Ausubel, F.M. et al., Current Protocols in Molecular Biology, Greene Publishing Assoc. and Wiley-Interscience (1987).
Материалы и способы, пригодные для поддержания и роста бактериальных культур, хорошо известны специалистам. Методики, пригодные для использования в следующих примерах, можно найти в Manual of Methods for General Bacteriology (Phillipp Gerhardt, R.G.E. Murray, Ralph N.Costilow, Eugene W.Nester, Willis A.Wood, Noel R.Krieg and G.Briggs Phillips, eds), American Society for Microbiology, Washington, DC. (1994)) или Thomas D. Brock, Biotechnology: A Textbook of Industrial Microbiology, Second Edition, Sinauer Associates, Inc., Sunderland, MA (1989). Все реагенты, рестриктазы и материалы, используемые для выращивания и содержания клеток-хозяев, были получены от Aldrich Chemicals (Milwaukee, WI), DIFCO Laboratories (Detroit, MI), GIBCO/BRL (Gaithersburg, MD), или Sigma Chemical Company (St. Louis, МО), если не указано иное.
Манипуляции с генетическими последовательностями могут быть осуществлены с использованием комплекта программ, доступных от Genetics Computer Group Inc. (Wisconsin Package Version 9,0, Genetics Computer Group (GCG), Madison, WI). В тех случаях, когда использовалась программа GCG "Pileup", используется заданное по умолчанию значение параметра gap creation, равное 12, и может быть использовано заданное по умолчанию значение параметра gap extension, равное 4. В тех случаях, когда использовались программы GCG "Gap" или "Bestfit", могут быть использованы заданное по умолчанию значение параметра gap creation penalty, равное 50, и заданное по умолчанию значение параметра gap extension penalty, равное 3. В любом случае, если программа GCG не запрашивает значения параметров, то в этих или любых других программах GCG могут быть использованы принятые по умолчанию значения.
Аббревиатуры имеют следующие значения: "ч" обозначает час(ы), "мин" обозначает минуту (минуты), "с" обозначает секунду (секунды), "д." обозначает день (дни), "мкл" обозначает микролитр(ы), "мл" обозначает миллилитр(ы), "л" обозначает литр(ы), "мкМ" обозначает микромолярную концентрацию, "мМ" обозначает миллимолярную концентрацию, 'мкг" обозначает микрограмм(ы), "мг" обозначает миллиграмм(ы), "А" обозначает аденин или аденозин, "Т" обозначает тимин или тимидин, "G" обозначает гуанин или гуанозин, "С" обозначает цитидин или цитозин, "×g" обозначает кратность ускорения свободного падения, "nt" обозначает нуклеотид(ы), "аа" обозначает аминокислоту (аминокислоты), "п.о." обозначает пару оснований (пары оснований), "тыс.п.о." обозначает тысячу (тысячи) пар оснований, "к" обозначает кило, "мк" обозначает микро, и "°С" обозначает градус Цельсия.
Пример 1
Данный Пример описывает конструирование нескольких кассет генной экспрессии, включающих новые субституционные мутанты полинуклеотидов и полипептидов ядерных рецепторов группы Н по изобретению для использования в системе экспрессии индуцибельного гена на основе ядерного рецептора. Заявители сконструировали кассеты генной экспрессии на основе EcR гусеницы листовертки-почкоеда елового Choristoneura fumiferana ("CfEcR"). Полученные структурные элементы рецептора включают лигандсвязывающий домен EcR или химеры Homo sapiens RXR-LmRXR; и GAL4 ДНК-связывающий домен (DBD) или VP16 домен трансактивации (AD). Репортерные структурные продукты включают репортерный ген люциферазы, функционально связанный с синтетической конструкцией промотора, включающей GAL4 элемент ответа, с которым связывается Gal4 DBD. Разные комбинации этих рецепторных и репортерных конструкций были ко-трансформированы в клетки млекопитающих, как описано ниже в Примерах 2-5.
Кассеты генной экспрессии
На основе рецептора экдизона были сконструированы кассеты генной экспрессии (переключатели), как описано ниже, с использованием стандартных способов клонирования, известных специалистам. Далее приводятся краткое описание получения и композиция каждого переключателя, используемого в описанных тут Примерах.
1,1 - GAL4CfEcR-DEF/VP16-βRXREF-LmRXREF: Домены D, Е и F дикого типа EcR гусениц листовертки-почкоеда елового Choristoneura fumiferana ("CfEcR-DEF"; SEQ ID NO: 21) сливали с GAL4 ДНК-связывающим доменом ("GaI4DNABD" или "GaI4DBD"; SEQ ID NO: 6) и помещали под контроль промотора CMV (SEQ ID NO: 2). Спирали 1-8 доменов EF RXRβ Homo sapiens ("HsRXRβ-EF"; нуклеотиды 1-465 SEQ ID NO: 3) и спирали 9-12 доменов EF белка ultraspiracle Locusta migratoria ("LmRXR-EF"; нуклеотиды 403-630 SEQ ID NO: 23) сливали с доменом трансактивации VP16 ("VP16AD"; SEQ ID NO: 12) и помещали под контроль промотора SV40e (SEQ ID NO: 22). Пять консенсусных сайтов связывания элементов ответа GAL4 ("5×GAL4RE"; включающих 5 копий GAL4RE, содержащих SEQ ID NO: 19), сливали с синтетическим минимальжм промотором ТАТА (SEQ ID NO: 24) и помещали слева (upstream) от репортерного гена люциферазы (SEQ ID NO: 25).
1,2 - GAL4/мутантный CfEcR-DEF/VP16-βRXREF-LmRXREF: Эта конструкция была приготовлена таким же образом, как и описанный выше переключатель 1,1, за исключением того, что CfEcR-DEF дикого типа был замещен на мутант CfEcR-DEF, включающий лигандсвязывающий домен, содержащий мутацию замещения, выбраную из Таблицы 1 ниже.
Конструкция лигандсвязывающих доменов рецептора экдизона, содержащих мутацию замещения
В попытке модифицировать связывание лигандов EcR остатки в лигандсвязывающем домене EcR, которые были определены как важные для связывания лигандов на основе анализа методом молекулярного моделирования, были мутированы в EcR организмов трех разных классов. Таблица 1 указывает аминокислотные остатки внутри лигандсвязывающего домена CfEcR (EcR чешуекрылых) (SEQ ID NO: 1), которые были мутированы и исследованы на модификацию связывания экдистероида и не-экдистероида.
Все аминокислотные субституционные мутации, перечисленные в Таблице 1, были сконструированы в кДНК EcR методом ПЦР-медиируемого сайт-специфического мутагенеза. Помимо многих выполненных единичных точковых мутаций было также получено два разных двухточковых мутанта CfEcR: один, включающий замещения V128F и А110Р (V128F/A110P), и второй, включающий замещения N119F и V96T (N119F/V96T). Были также получены три разных трехточковых мутанта CfEcR: один, включающий замещения V107I, Y127E и А110Р (V107I/Y127E/A110P), второй, включающий замещения V107I, Y127E и T52V (V107I/Y127E/T52V), и третий, включающий замещения V107I и Y127E и инсерцию глицина (G) (V107I/Y127E/259G) (SEQ ID NO: 1).
ПЦР сайт-специфический мутагенез был осуществлен с использованием набора для сайт-специфического мутагенеза Quikchange (Stratagene, La Jolla, CA) с использованием следующих реакционных условий и параметров циклов. ПЦР сайт-специфический мутагенез проводили с использованием 1× реакционного буфера (поставляется производителем), 50 нг матриц dsДНК, 125 нг прямого праймера (FP), 125 нг обратного комплементарного праймера (RCP) и 1 мкл смеси dNTP (поставляется производителем) в конечном реакционном объеме 50 мкл. Прямой праймер и обратный комплементарный праймер, использованные для получения всех мутантов EcR, приведены в Таблице 2. Использованные параметры циклов заключались в одном цикле денатурации при 95°С в течение 30 секунд с последующими 16 циклами денатурирования при 95°С в течение 30 секунд, отжиге при 55°С в течение 1 минуты и синтезе при 68°С в течение 22 минут.
Полученные методом ПЦР продукты нуклеиновых кислот, кодирующие лигандсвязывающие домены мутантов EcR, были затем слиты с ДНК-связывающим доменом GAL4, как описано в Примере 1,2 выше. Конструкции GAI-4/мутантный рецептор EcR тестировались на активность путем их трансфекции в клетки NIH3T3 вместе с VP16/βRXREF-LmRXREF и pFRLuc в присутствии различных лигандов.
Мутант GaI4-CfEcR-DEF(VYG) был создан путем инсерции дополнительного глицина на С-терминальном конце субституционного мутанта EcR V107I/Y127E [CfECR(VY)] методом ПЦР. По существу, это делалось в две стадии: ПЦР-амплификация CfEcR-DEF(VYG) и замещение CfEcR(VY) в векторе GAL4-CfEcR DEF(VY) pBIND 1-9 на ПЦР-амплифицированный CfEcR-DEF(VYG). Участок CfEcR-DEF (с дополнительным глицином) амплифицировали с использованием вектора GAL4-CfEcR DEF(VY) pBIND 1-9 в качестве матрицы и следующих ПЦР-праймеров:
5EcR-wt
GGAATTCCCGGGGATCCGGCCTGAGTGCGTAGTACCC (SEQ ID NO: 175)
3EcR-gly
CTCTCTGCGGCCGCCTATCCGAGATTCGTGGGGGACTCGAGGATAG (SEQ ID NO: 176)
Продукт ПЦР изолировали и расщепляли Not I (расщепляет 3'-конец; входит в праймер 3' ПЦР) и Xma I (расщепляет 5'-конец; входит в праймер 5' ПЦР). Этот продукт лигируют в вектор, полученный следующим образом: GAL4-CfEcR DEF(VY) pBIND 1-9 расщепляют Xma I и Not I (расщепление удаляет из вектора CfEcR-DEF (VY)). Фрагменты выделяют на 1% агарозном геле и очищают медленнее мигрирующий вектор ДНК. После лигирования между вектором и описанным выше фрагментом CfEcR-DEF(VYG) реакцию лигирования трансформируют в бактерии. Положительные колонии выбирают методом ПЦР колоний с использованием указанных выше праймеров. Мутации VYG в выбранном клоне подтверждают секвенированием.
Пример 2
Этот Пример описывает идентификацию субституционных мутантов экдистероид-чувствительного лигандсвязывающего домена CfEcR, проявляющих повышенную активность в ответ на экдистероидный лиганд. В попытке идентификации субституционных мутаций в CfEcR, которые повышают активность экдистероидного лиганда, заявители провели мутации аминокислотных остатков, определенных как критические для связывания экдистероида, и создали кассеты генной экспрессии GAL4/мутантная CfEcR-DEF кДНК, как описано в Примере 1 выше, с использованием набора для ПЦР-медиируемого сайт-специфического мутагенеза. Были получены мутированные и WT (дикого типа) кДНК, соответствующие различным конструкциям переключателей, описанным в Примере выше, и протестированы методом анализа GAL4-контролируемого люциферазного репортера, как описано ниже.
Трансфекции
ДНК вводили трансфекцией в клетки NIH3T3 мыши (АТСС) следующим образом. Придерживались стандартных способов культивации и содержания клеток. Клетки собирали и засеивали 96-луночные планшеты по 2500 клеток на лунку в 50 мкл, среды для выращивания, содержащей 10% сыворотки плода коровы (FBS). Через двадцать четыре часа клетки обрабатывали 35 мкл небессывороточной питательной среды, содержащей диметилсульфоксид (ДМСО; контроль) или раствор лиганда в ДМСО. Клетки затем подвергали трансфекции с использованием реагента для трансфекции Superfect™ (Qiagen Inc.). Для каждой лунки 0,625 мкл Superfect™ смешивали с 14,2 мкл бессывороточной питательной среды. 0,16 мкг конструкции репортера и 0,04 мкг каждой конструкции рецептора добавляли в смесь реагента для трансфекции. Содержимое смеси для трансфекции перемешивали в вихревой мешалке и оставляли при комнатной температуре на 30 минут. В конце инкубации 15 мкл смеси для трансфекции прибавляли к клеткам. Клетки выдерживали при 37°С и 5% CO2 в течение 48 часов в 5% FBS.
Лиганды
Экдистероидные лиганды понастерон А и 20-гидроксиэкдизон были приобретены у фирм Sigma Chemical Company и Invitrogen. Неэкдистероидный диацилгидразиновый лиганд N-(2-этил-3-метоксибензоил)-N'-(3,5-диметилбензоил)-N'-трет-бутилгидразин (RG-102240, лиганд GS®-E) представляет собой синтетический стабильный экдистероидный лиганд, который был синтезирован фирмой Rohm and Haas Company. Неэкдистероидные диацилгидразиновые лиганды RG-101691, RG-102362, RG-115840, RG-115853, RG-115855, RG-115859 и RG-115898 были синтезированы фирмой RheoGene Inc. Синтез RG-101691, RG-102362, RG-115840, RG-115859 и RG-115898 описан ниже. Синтез RG-115853 и RG-115855 описан в находящейся одновременно на рассмотрении патентной заявке США №10/775883. Неэкдистероидные тетрагидрохинолиновый лиганды RG-120499 и RG-120500 были синтезированы фирмой RheoGene, Inc. и описаны в находящейся одновременно на рассмотрении патентной заявке США №10/460820. Все лиганды растворяли в ДМСО.
Синтез лигандов
Синтез N-трет-бутил-N'-(3-этил-2-метилбензоил)гидразида 3,5-диметилбензойной кислоты (RG-101691)
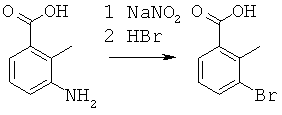
3-Амино-2-метилбензойную кислоту (6,16 г) нагревают при температуре кипения с обратным холодильником в течение 30 минут в концентрированной HBr. Смесь охлаждают до 0°С и обрабатывают раствором NaNO2 при 0°С (2,8 г в 5,6 мл H2O). Полученный раствор соли диазония медленно прибавляют к предварительно нагретому (60-70°С) раствору CuBr (3,8 г) в 3,2 мл концентрированной HBr. После прибавления смесь перемешивают в течение ночи при комнатной температуре и фильтруют. Полученный осадок на фильтре промывают сначала водой, а затем 10% HCl и высушивают на воздухе, получая 6,93 г 3-бром-2-метилбензойной кислоты в виде порошкообразного твердого вещества светло-лилового цвета. Этот материал растворяют в этилацетате, промывают дважды 5% HCl, осушают над NazSO4 и перекристаллизовывают из смеси 4:1 гексаны:этилацетат сначала при комнатной температуре, а затем при охлаждении. 1H ЯМР (ДМСО, 200 МГц), δ (млн-1): 7,72 (дд, 2Н), 7,2 (т, 1Н), 2,5 (с, 3Н).
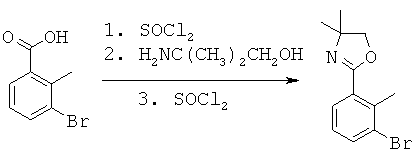
3-Бром-2-метилбензойную кислоту (7,03 г, 32,7 ммоль) нагревают при температуре кипения с обратным холодильником в 10 мл SOCl2 (98 ммоль) и капле ДМФ в течение 3 часов. Избыток SOCl2 удаляют под вакуумом. Остаток растворяют в 20 мл CH2Cl2 и прибавляют к охлажденному льдом раствору 2-амино-2-метилпропан-1-ола (8,74 г, 9,36 мл) в 20 мл CH2Cl2. Смесь перемешивают при комнатной температуре в течение 18 часов и растворитель удаляют под вакуумом, получая маслянистый остаток. К этому остатку прибавляют SOCl2 (7,4 мл, 100 мл, 3 экв.) в течение одного часа, смесь перемешивают еще 30 мин, а затем выливают в 150 мл эфира.
Образуется маслянистая несмешивающаяся фаза, а эфир отбрасывают. Маслянистую жидкость смешивают с 100 мл 20% NaOH и экстрагируют 3×150 мл порциями эфира. Эфирные экстракты объединяют, осушают над MgSO4 и растворитель удаляют под вакуумом, получая маслянистую жидкость желтого цвета. Хроматография на силикагеле с использованием смеси 4:1 гексан:эфир в качестве элюента дает 4,87 г 2-(3-бром-2-метилфенил)-4,4-диметил-4,5-дигидрооксазола в виде бесцветной маслянистой жидкости. (Rf = 0,25 (4:1 гексан:эфир). 1Н ЯМР (CDCl3, 200 МГц), δ (млн-1): 7,62 (м, 2Н), 7,1 (т, 1Н), 4,1 (с, 2Н), 2,6 (с, 3Н), 1,4 (с, 6Н).
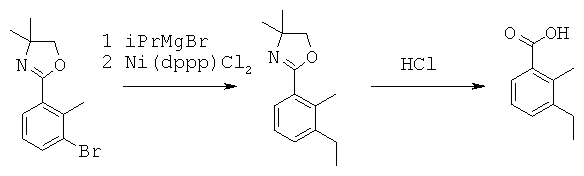
2-(3-Бром-2-метилфенил)-4,4-диметил-4,5-дигидрооксазол (3,4 г, 12,7 ммоль) растворяют в 30 мл этилового эфира под атмосферой азота в круглодонной колбе на 100 мл, оборудованной магнитной мешалкой, термометром и обратным холодильником. Прибавляют Ni(dppp)Cl2 (100 мг) и смесь охлаждают до 0°С на ледяной бане. Прибавляют магнийэтилбромид (5,5 мл, 3М в эфире), реакционную смесь перемешивают при 0°С в течение 30 минут, при комнатной температуре в течение 2,5 часов и, наконец, при температуре кипения с обратным холодильником в течение 2 часов. Смесь затем охлаждают до 0°С, гасят насыщенным водным NH4Cl. Органический слой удаляют и водный слой экстрагируют эфиром. Органические фазы объединяют и осушают над MgSO4. Растворитель удаляют под вакуумом, получая 2,84 г 2-(3-этил-2-метилфенил)-4,4-диметил-4,5-дигидрооксазола, 1H ЯМР (CDCl3, 200 МГц), δ (млн-1): 7,5 (д, 2Н), 7,2 (м, 2Н), 4,1 (с, 2Н), 2,7 (м, 2Н), 2,45 (с, 3Н), 1,4 (с, 6Н), 1,2 (т, 3Н), Rf = 0,25 (4:1 гексан:эфир), содержащего около 5% исходного арилбромида. Оксазолин суспендируют в 100 мл 6N HCl и кипятят с обратным холодильником 5 часов при энергичном перемешивании. Смеси позволяют остыть до комнатной температуры, после чего кристаллизуется 3-этил-2-метилбензойная кислота: 1,74 г, т.пл. 96-98°С, 1Н ЯМР (CDCl3, 200 МГц), δ (млн-1): 7,85 (д, 1Н), 7,4 (д, 1Н), 7,22 (т, 1Н), 2,7 (кв, 2Н), 2,6 (с, 3Н), 1,21 (т, 3Н). Еще 110 мг получают экстракцией эфиром из водной фазы.
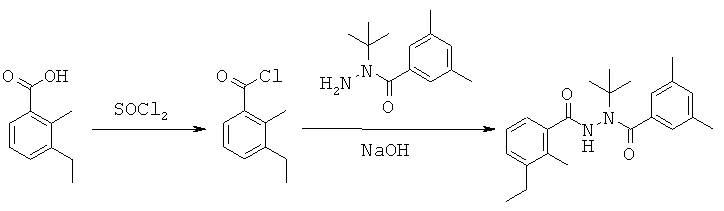
3-Этил-2-метилбензойную кислоту (0,517 г) нагревают при температуре кипения с обратным холодильником в 3 мл тионилхлорида с каплей ДМФ в течение нескольких часов. Тионилхлорид удаляют под вакуумом, получая 0,89 г (4,48 ммоль) 3-этил-2-метилбензоилхлорида. Хлорангидрид кислоты растворяют в 5 мл CH2Cl2 и прибавляют медленно и одновременно с, но отдельно от, 5 мл водного NaOH (0,30 г, 7,5 ммоль) к раствору N-трет-бутилгидразида 3,5-диметилбензойной кислоты (0,96 г, 4,36 ммоль), растворенного в 10 мл CH2Cl2, предварительно охлажденного до -5°С. Во время прибавления температуру поддерживают ниже 5°С. Смеси позволяют медленно нагреться до комнатной температуры и перемешивают в течение ночи. Органический слой удаляют и водный слой экстрагируют CH2Cl2. Органические экстракты объединяют, осушают и растворитель удаляют под вакуумом, получая 1,5 г сырого продукта. Этот остаток экстрагируют 100 мл гексанов при нагревании до кипения с обратным холодильником и горячий экстракт декантируют с маслянистого остатка и позволяют остыть до комнатной температуры, после чего кристаллизуется N-трет-бутил-N'-(3-этил-2-метилбензоил)гидразид 3,5-диметилбензойной кислоты (0,56 г, т.пл. 167-169°С, 1H ЯМР (CDCl3, 200 МГц), δ (млн-1): 7,43 (с, 1Н), 7,18 (м, 1Н), 7,1 (с, 2Н), 7,03 (с, 1Н), 7,0 (м, 1Н), 6,35 (д, 1Н), 2,58 (кв, 2Н), 2,3 (с, 6Н), 1,95 (с, 3Н), 1,6 (с, 9Н), 1,15 (т, 3Н). Растворение маслянистого остатка и кристаллизация дают вторую порцию менее чистого материала, 0,21 г.
Синтез N-трет-бутил-N'-(3-изопропил-2-метилбензоил)гидразида 3,5-диметилбензойной кислоты (RG-102362)
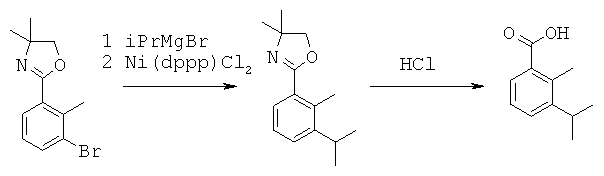
В сухую 3-горлую круглодонную колбу на 250 мл, оснащенную магнитной мешалкой и находящуюся под атмосферой азота, загружают 5,0 г 2-(3-бром-2-метилфенил)-4,4-диметил-4,5-дигидрооксазола, 60 мл безводного ТГФ и 100 мг Ni(dppp)Cl2. Смесь охлаждают до 15°С и прибавляют магнийизопропилхлорид (11 мл, 2М в этиловом эфире). Наблюдается слабый экзотермический эффект, и смесь немного темнеет. Реакцию перемешивают в течение ночи при комнатной температуре, после чего 1H ЯМР показывает степень завершения 50%. Прибавление около 75 мг Ni(dppp)Cl2 и нагрев до температуры кипения с обратным холодильником в течение 3 часов не привели к дальнейшему протеканию реакции. Смесь охлаждают до 15°С, прибавляют еще 13 мл магнийизопропилхлорида (2М в этиловом эфире) и 100 мг никелевого катализатора и смесь перемешивают в течение ночи при комнатной температуре. Реакцию гасят насыщенным водным NH4Cl, органический слой удаляют, водный слой экстрагируют и органические фазы объединяют и осушают. Растворитель удаляют под вакуумом, получая 3,84 г сырого продукта в виде маслянистой жидкости желтого цвета. Хроматография на колонке с силикагелем с использованием в качестве элюента смеси 4:1 гексаны:эфир дает 0,79 г 2-(3-изопропил-2-метилфенил)-4,4-диметил-4,5-дигидрооксазола в виде бесцветной маслянистой жидкости. 1Н ЯМР (CDCl3, 200 МГц), δ (млн-1): 7,5 (д, 1Н), 7,37 (д, 1Н), 7,22 (т, 1Н), 4,13 (с, 2Н), 3,23 (м, 1Н), 2,5 (с, 3Н), 1,45 (с, 6Н), 1,22 (д, 6Н). Оксазолин суспендируют в 34 мл 6N HCl и нагревают до кипения под обратным холодильником на масляной бане в течение 6 часов. Смесь охлаждают и экстрагируют CH2Cl2. Экстракт осушают над Na2SO4 и упаривают, получая 0,76 г 3-изопропил-2-метилбензойной кислоты, достаточно чистой для следующей стадии. 1H ЯМР (CDCl3, 300 МГц), δ (млн-1): 7,8 (д, 1Н), 7,48 (д, 1Н), 7,3 (т, 1Н), 3,3 (м, 1Н), 2,55 (с, 3Н), 1,2 (д, 6Н).
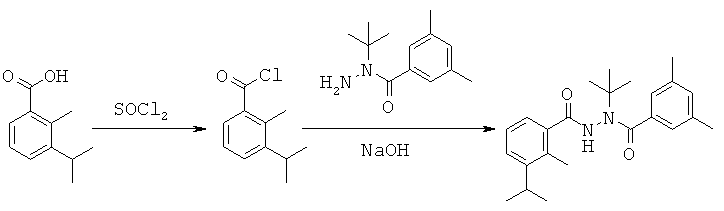
3-Изопропил-2-метилбензойную кислоту (0,75 г) нагревают при температуре кипения с обратным холодильником в примерно 3 мл тионилхлорида с каплей ДМФ в течение нескольких часов и тионилхлорид удаляют под вакуумом, получая 3-изопропил-2-метилбензоилхлорид. Хлорангидрид кислоты растворяют в 5 мл CH2Cl2 и прибавляют медленно и одновременно с, но отдельно от, 5 мл водного NaOH (0,265 г, 6,6 ммоль) к раствору N-трет-бутилгидразида 3,5-диметилбензойной кислоты (0,973 г, 4,4 ммоль), растворенного в 10 мл CH2Cl2, предварительно охлажденного до -5°С. Во время прибавления температуру поддерживают ниже 5°С. Смеси позволяют медленно нагреться до комнатной температуры и перемешивают в течение ночи. Органический слой удаляют и водный слой экстрагируют CH2Cl2. Органические экстракты объединяют, осушают и растворитель удаляют под вакуумом, получая 1,61 г сырого продукта в виде маслянистой жидкости желтого цвета. Этот материал хроматографируют на силикагеле с использованием в качестве элюента смеси 4:1 гексаны:этилацетат и затем тритурируют из смеси 1:1 гексан:эфир, получая N-трет-бутил-N'-(3-изопропил-2-метилбензоил)гидразид 3,5-диметилбензойной кислоты после энергичного удаления эфира в вакуумной печи при 60°С (0,35 г, т.пл. 182,5°С. 1H ЯМР (CDCl3, 200 МГц), δ (млн-1): 7,6 (с, 1Н), 7,25 (д, 1Н), 7,1 (с, 2Н), 7,05 (с, 1Н), 7,0 (м, 1Н), 6,3 (д, 1Н), 3,1 (м, 1Н), 2,3 (с, 6Н), 1,95 (с, 3Н), 1,6 (с, 9Н), 1,18 (м, 6Н).
Синтез N'-(5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонил)-N-(1-этил-2,2-диметилпропил)гидразида 3,5-диметилбензойной кислоты (RG-115858)
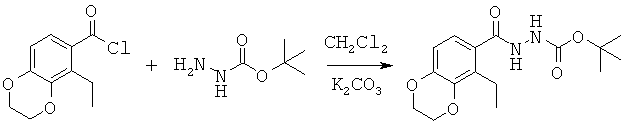
Растворяют 2,38 г (18 ммоль) т-бутилкарбазата в 50 мл CH2Cl2 в круглодонной колбе на 250 мл и охлаждают до 0°С. Готовят водный раствор К2СО3 (4,15 г К2СО3/35 мл H2O) и прибавляют к реакционной смеси, которую снова охлаждают до 0°С. Растворяют 3,63 г (16 ммоль) 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонилхлорида в 40 мл CH2Cl2 и прибавляют по каплям из делительной воронки в течение 15 мин. Реакционную смесь перемешивают при комнатной температуре в течение 3 дней. Реакционную смесь переносят в делительную воронку с помощью CH2Cl2 и H2O. Водную фазу тщательно экстрагируют CH2Cl2. CH2Cl2 экстракт затем экстрагируют 0,5N HCl, осушают и упаривают. Остаток далее высушивают в вакуумной печи, получая в виде твердого вещества желтовато-коричневого цвета 5,15 г трет-бутиловый сложный эфир N'-(5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонил)гидразинкарбоновой кислоты. ТСХ (1:1 этилацетат:гексан) дает одно пятно с Rf = 0,43 и ЯМР указывает на очень чистый продукт: 1H ЯМР (CDCl3, 500 МГц) δ (млн-1): 7,5 (шир., 1Н), 7,0 (шир., 1Н), 6,75 (д, 2Н), 4,28 (шир., 4Н), 2,76 (м, 2Н), 1,5 (с, 9Н), 1,18 (т, 3Н).
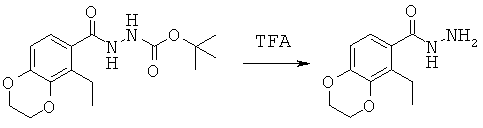
Помещают 5,15 г (16 ммоль) трет-бутилового сложного эфира N'-(5-этил-2,3-дигидро-бензо[1,4]диоксин-6-карбонил)гидразинкарбоновой кислоты в круглодонную колбу на 200 мл. Прибавляют около 20 мл трифторуксусной кислоты и реакционную смесь перемешивают при комнатной температуре в течение 24 часов. Затем прибавляют около 40 мл воды с последующим медленным прибавлением холодного 10% NaOH/H2O при перемешивании до нейтрализации кислоты (рН ~14). Реакционную смесь переносят в делительную воронку и экстрагируют этилацетатом, аккуратно встряхивая (осторожно: выделение газа). Этилацетатный экстракт осушают и упаривают, получая 5,51 г бледного, вязкого полутвердого вещества желтого цвета. Материал затем помещают в вакуумную печь при 50°С примерно на 1 час, получая 4,62 г гидразида 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты. Отщепление t-Boc лучше всего проводят в неразведенной трифторуксусной кислоте; использование вспомогательных растворителей всегда приводит к значительно более низким выходам. 1Н ЯМР (CDCl3, 500 МГц) δ (млн-1): 7,0 (шир., 1Н), 6,83 (м, 1Н), 6,71 (м, 1Н), 4,28 (шир.с, 4Н), 2,76 (м, 2Н), 1,6 (шир., 2Н), 1,17 (т, 3Н).
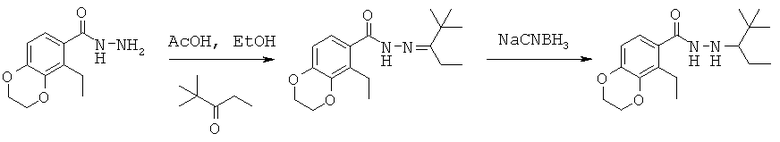
Кипятят с обратным холодильником 1,12 г (5,1 ммоль) гидразида 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты, 1,37 г (12 ммоль) 2,2-диметилпентанон-3, 30 мл этанола и 20 капель ледяной уксусной кислоты в течение 6 часов, получая (1-этил-2,2-диметилпропилиден)гидразид 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты, который используют in situ. К охлажденной реакционной смеси прибавляют 3 мл ледяной уксусной кислоты и 0,63 г (10 ммоль) NaCNBH3. Реакцию перемешивают при комнатной температуре в течение 24 часов. Прибавляют 25 мл воды и большую часть спирта удаляют на вращающемся испарителе. Затем прибавляют 10% NaOH/H2O до основной реакции реакционной смеси. Продукт экстрагируют этилацетатом, который затем осушают и упаривают, получая 1,61 г остатка. Чистый N'-(1-этил-2,2-диметилпропил)гидразид 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты (ок. 0,77 г) получают хроматографией на колонке с силикагелем, элюируя смесью 25% этилацетата/гексан. ТСХ: Rf = 0,53, 1:1 этилацетат:гексан). 1H ЯМР (CDCl3, 500 МГц) δ (млн-1): 7,1 (шир.с, 1Н), 6,8 (д, 1Н), 6,7 (д, 1Н), 4,27 (м, 4Н), 2,8 (м, 2Н), 2,4 (м, 1Н), 1,7 (м, 1Н), 1,3 (м, 1Н), 1,2 (т, 3Н), 1,15 (т, 3Н), 0,97 (с, 9Н).
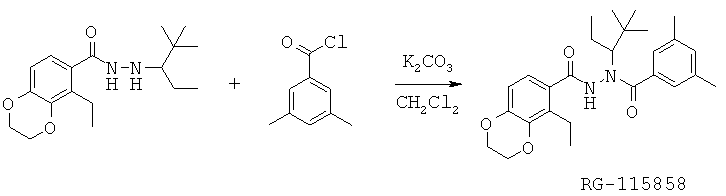
Помещают 0,214 г (0,70 ммоль) N'-(1-этил-2,2-диметилпропил)гидразида 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты, 151 мг (0,9 ммоль) 3,5-диметилбензоилхлорида, 7 мл 25% К2СО3/H2O и 7 мл CH2Cl2 во флакон на 20 мл и перемешивают при комнатной температуре в течение 24 часов. Реакционную смесь переносят в делительную воронку, разводят NaHCO3 и прибавляют CH2Cl2. Отделяют слой CH2Cl2 и водный слой экстрагируют дважды CH2Cl2. Экстракты CH2Cl2 осушают над MgSO4 и упаривают, получая 0,59 г белого остатка. Очистка хроматографией на колонке и элюирование 15 мл смеси 20% этилацетата/гексан дают около 350 мг N'-(5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонил)-N-(1-этил-2,2-диметилпропил)гидразида 3,5-диметилбензойной кислоты (чистота 95% по данным ТСХ: Rf = 0,56, 1:1 этилацетат:гексан). 1Н ЯМР (CDCl3, 500 МГц) δ (млн-1): 7,05 (с, 1Н), 7,0 (с, 2Н), 6,6 (д, 1Н), 6,27 (д, 1Н), 4,65 (д, 1Н), 4,25 (с, 4Н), 2,9 (м, 1Н), 2,3 (с, 6Н), 2,0 (м, 1Н), 1,55-1,7 (м, 2Н), 1,25 (м, 3Н), 0,9-1,2 (3с, 9Н), 0,9 (т, 3Н).
Синтез N-(1-трет-бутил-3,4,4-триметилпент-1-енил)-N'-(5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонил)гидразид 3,5-диметокси-4-метилбензойной кислоты (RG115898)
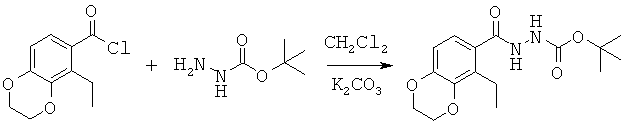
Растворяют 2,38 г (18 ммоль) т-бутилкарбазата в 50 мл CH2Cl2 в круглодонной колбе на 250 мл и охлаждают до 0°С. Готовят водный раствор К2СО3 (4,15 г К2СО3/35 мл H2O) и прибавляют к реакционной смеси, которую снова охлаждают до 0°С. Растворяют 3,63 г (16 ммоль) 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонилхлорида в 40 мл CH2Cl2 и прибавляют из делительной воронки по каплям на протяжении 15 мин. Реакционную смесь перемешивают при комнатной температуре в течение 3 дней. Реакционную смесь переносят в делительную воронку с помощью CH2Cl2 и H2O. Водную фазу тщательно экстрагируют CH2Cl2. Экстракт CH2Cl2 затем экстрагируют 0,5N HCl, осушают и упаривают. Остаток далее высушивают в вакуумной печи, получая 5,15 г трет-бутилового сложного эфира N'-(5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонил)гидразинкарбоновой кислоты в виде твердого вещества желтовато-коричневого цвета. ТСХ (1:1 этилацетат:гексан) дает одно пятно с Rf = 0,43, а ЯМР указывает на очень чистый продукт: 1H ЯМР (CDCl3, 500 МГц) δ (млн-1): 7,5 (шир., 1Н), 7,0 (шир., 1Н), 6,75 (д, 2Н), 4,28 (шир., 4Н), 2,76 (м, 2Н), 1,5 (с, 9Н), 1,18 (т, 3Н).

Помещают 5,15 г (16 ммоль) трет-бутилового сложного эфира N'-(5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонил)гидразинкарбоновой кислоты в круглодонную колбу на 200 мл. Прибавляют около 20 мл трифторуксусной кислоты и реакционную смесь перемешивают при комнатной температуре в течение 24 часов. Затем прибавляют около 40 мл воды с последующим медленным прибавлением холодного 10% NaOH/H2O при перемешивании до нейтрализации кислоты (рН ~14). Реакционную смесь переносят в делительную воронку и экстрагируют этилацетатом при аккуратном встряхивании (осторожно: выделение газа). Этилацетатный экстракт осушают и упаривают, получая 5,51 г бледного вязкого полутвердого вещества желтого цвета. Материал затем помещают при 50°С в вакуумную печь на примерно 1 час, получая 4,62 г гидразида 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты. Отщепление t-Boc лучше всего проводят в неразведенной трифторуксусной кислоте; использование вспомогательных растворителей всегда приводит к значительно меньшим выходам. 1H ЯМР (CDCl3, 500 МГц) δ (млн-1): 7,0 (шир., 1Н), 6,83 (м, 1Н), 6,71 (м, 1Н), 4,28 (шир.с, 4Н), 2,76 (м, 2Н), 1,6 (шир., 2Н), 1,17 (т, 3Н).
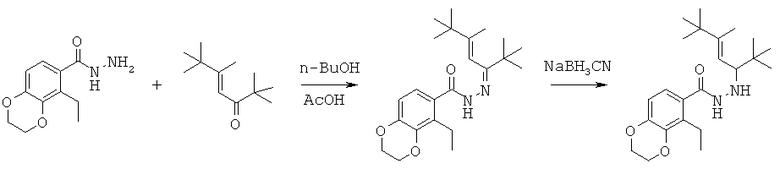
2,2,5,6,6-Пентаметилгепт-4-ен-3-он (1,48 г, 8,1 ммоль) растворяют в н-бутиловом спирте (20 мл). Затем прибавляют гидразид 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты (1,80 г, 8,1 ммоль) и 10 капель ледяной уксусной кислоты. Реакционную смесь нагревают при температуре кипения с обратным холодильником в течение 20 часов (необходимо для завершения реакции), контролируя методом ТСХ. К раствору промежуточного соединения (1 -трет-бутил-3,4,4-триметилпент-2-енилиден)гидразида 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты прибавляют 1,8 мл ледяной уксусной кислоты и 1,02 г (16,2 ммоль) цианоборгидрида натрия. Реакцию нагревают при температуре кипения с обратным холодильником в течение трех часов. Реакцию охлаждают и прибавляют 50 мл воды и 10% водного NaOH до щелочной реакции (рН ~14). Большую часть спирта удаляют на вращающемся испарителе и остаток экстрагируют EtOAc. Водный экстракт осушают и концентрируют до постоянного веса, получая 4 г вязкого материала. Получают 2,3 г чистого N'-(1-трет-бутил-3,4,4-триметилпент-2-енил)гидразида 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты (желтая маслянистая жидкость, Rf = 0,30 в 25% EtOAc в н-гексане, выход 73%) хроматографией на колонке с силикагелем. 1Н ЯМР (400 МГц, CDCl3) δ (млн-1): 7,42 (шир., 1Н), 6,80 (д, J=8,4 Гц, 1Н), 6,71 (д, J=8,4 Гц, 1Н), 6,17 (шир., 1Н), 5,30 (дд, J=0,8, 10 Гц, 1Н), 4,33-4,29 (м, 4Н), 3,68 (д, J=10 Гц, 1Н), 2,80 (м, 2Н), 1,72 (с, 3Н), 1,21 (с, 3Н), 1,12 (с, 9Н), 1,05 (с, 9Н).
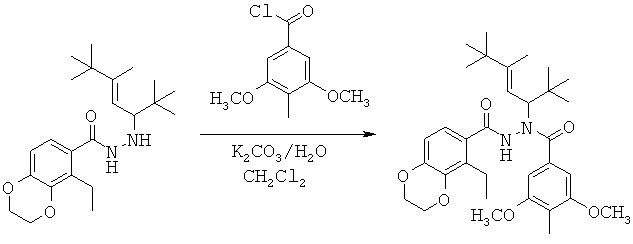
Растворяют N'-(1-трет-бутил-3,4,4-триметилпент-2-енил)гидразид 5-этил-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты (150 мг, 0,39 ммоль) и 3,5-диметокси-4-метилбензоилхлорида (83 мг, 0,39 ммоль) в 5 мл CH2Cl2. Прибавляют 5 мл 25% К2СО3 и реакционную смесь перемешивают при комнатной температуре в течение ночи. Реакцию контролируют методом ТСХ. Фазы разделяют, при необходимости добавляя дополнительно CH2Cl2 и/или воду для облегчения манипуляции. Слой CH2Cl2 осушают и растворитель удаляют под вакуумом, получая 210 мг сырого продукта. Этот материал очищают хроматографией на колонке с силикагелем, элюируя ступенчатым градиентом 10-25% этилацетата в гексане, получая N-(1-трет-бутил-3,4,4-триметилпент-2-енил)-N'-(5-этил-2,3-дигидробензо[1,4]диоксин-6-карбонил)гидразид 3,5-диметокси-4-метилбензойной кислоты RG115898 (83 мг, Rf = 0,19 в 25% этилацетате в н-гексане, выход 38 %). 1H ЯМР (400 МГц, ДМСО-d6) δ (млн-1): 10,19 (с, 1Н), 6,75 (д, J=8,0 Гц, 1Н), 6,69 (с, 2Н), 6,61 (д, J=8,0 Гц, 1Н), 5,43 (д, J=10,0 Гц, 1Н), 5,41 (д, 14,4 Гц, 1Н), 4,30-4,20 (м, 4Н), 3,80 (с, 6Н), 2,21-2,15 (м, 1Н), 2,01 (с, 3Н), 1,81 (м, 1Н), 1,76-1,64 (м, 1Н), 1,06 (с, 9Н), 1,00 (с, 9Н), 0,70 (т, J=7,6 Гц, 3Н).
Синтез N-(1-трет-бутилпентил)-N'-(4-этилбензоил)гидразида 3,5-диметилбензойной кислоты (RG-115840)
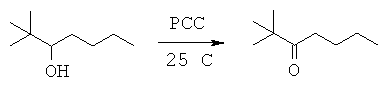
2,2-Диметилгептан-3-ол (0,23 моль) растворяют в 350 мл CH2Cl2 в круглодонной колбе на 500 мл с помощью магнитной мешалки. Колбу частично охлаждают с помощью льда. Прибавляют при энергичном перемешивании 76,6 г (0,355 моль) хлорхромата пиридиния. Реакция чернеет и немного нагревается. Реакционную смесь перемешивают при комнатной температуре в течение 24 часов. Раствор декантируют с черного осадка, который промывают гексаном. Органические экстракты объединяют и хроматографируют непосредственно на силикагеле. (Примечание: было обнаружено, что только силикагель связывает и удаляет непрореагировавшие соединения хрома). Продукт, 2,2-диметилгептан-3-он, элюируют смесью CH2Cl2/гексан, а затем фракцией 10% этилацетат/гексан, получая 29,19 г продукта с выходом 88%. 1H ЯМР (CDCl3, 500 МГц) δ (млн-1): 2,48 (т, 2Н), 1,54 (м, 2Н), 1,28 (м, 2Н), 1,13 (с, 9Н), 0,90 (м, 3Н).
Синтез N'-(1-трет-бутилпентил)гидразида 4-этилбензойной кислоты
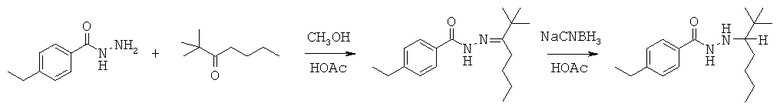
Гидразид 4-этилбензойной кислоты (1,64 г, 10 ммоль) растворяют в 12,5 мл метанола. Затем прибавляют одну каплю уксусной кислоты, а затем 1,55 г 2,2-диметилгептан-3-она. Смесь перемешивают при комнатной температуре в течение нескольких дней, после чего прибавляют 2,1 мл уксусной кислоты и 667 мг NaBH3CN. После перемешивания в течение около 7 часов метанол удаляют под вакуумом. Остаточный продукт разводят около 20 мл воды и экстрагируют метиленхлоридом. Экстракты осушают над MgSO4, отделяют на фильтре твердые вещества и растворитель удаляют под вакуумом, получая 1,8 г сырого продукта. Этот материал очищают хроматографией на колонке с силикагелем, элюируя градиентом 100% гексанов - 100% этилового эфира. Получают N'-(1-трет-бутилпентил)гидразид 4-этилбензойной кислоты с выходом 45% (1,32 г).
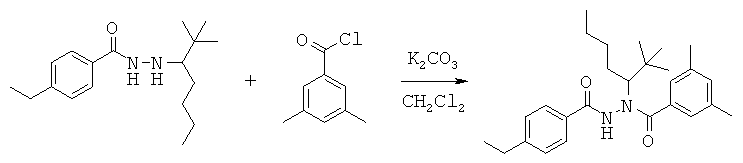
Растворяют N'-(1-трет-бутилпентил)гидразид 4-этилбензойной кислоты (145,2 мг, 0,5 ммоль) в 5 мл метиленхлорида и прибавляют 1,5 ммоль PS-NMM (804 мг, -SO2NH(СН2)3-морфолин функционализованная полистирольная смола производства фирмы Argonaut Technologies, San Carlos, CA). Смесь разводят 3 мл метиленхлорида для получения пригодной для перемешивания суспензию. Прибавляют 3,5-диметилбензоилхлорид (0,5 ммоль, 74 мл) и смесь перемешивают в течение ночи. На следующий день прибавляют 1 ммоль (775 мг) смолы AP-NCO resin (изоцианат-функционализованная смола производства фирмы Argonaut Technologies, San Carlos, CA) и 1 ммоль (401,6 мг) АР-trisamine (полистирол-CH2NHCH2CH2NH(CH2CH2NH2)2 смола производства фирмы Argonaut Technologies, San Carlos, CA) с 3 мл метиленхлорида для удаления остатка исходного материала. Смесь перемешивают в течение 4 часов, смолы отфильтровают и фильтрат осушают, получая 191 мг сырого продукта, который дает одно пятно при анализе методом ТСХ. Этот материал очищают флеш-хроматографией на силикагеле с использованием градиента 100% гексана -100% этилового эфира. Выход: 50 мг (ок. 23%) N-(1-трет-бутилпентил)-N'-(4-этилбензоил)гидразида 3,5-диметилбензойной кислоты. 1H ЯМР (CDCl3, 400 МГц) δ (млн-1): 7,8+7,5 (шир./шир., 1Н), 7,4-6,9 (м, 7Н), 4,7+3,6 (м/м, 1Н), 2,65 (м, 2Н), 2,38+2,28 (с/с, 6Н), 1,9+1,75 (шир„ 2Н), 1,4-1,2 (шир., м, 7Н), 1,1 (шир.с, 9Н), 0,95 (шир.с, 3Н).
Репортерные анализы
Клетки собирают через 40 часов после прибавления лигандов. Прибавляют к каждой лунке 24-луночного планшета 125 мкл пассивного буфера для лизиса (часть системы для репортерного анализа Dual-luciferase™ фирмы Promega Corporation). Планшеты помещают на ротационный встряхиватель на 15 минут. Анализируют двадцать мкл лизата. Активность люциферазы измеряют с использованием системы для репортерного анализа Dual-luciferase™ фирмы Promega Corporation в соответствии с инструкциями производителя. Индукцию укладки (FI) рассчитывают путем деления относительных световых единиц ("RLU") для клеток, обработанных лигандом, на RLU для клеток, обработанных ДМСО (необработанный контроль).
ПРИМЕР 3
Этот пример описывает идентификацию субституционных мутантов лигандсвязывающего домена CfEcR, которые обычно являются экдистероид-чувствительными и проявляют повышенную активность в ответ на экдистероиды. В попытке идентифировать субституционные мутации в CfEcR, которые повышают экдистероидную активность, заявители провели мутации аминокислотных остатков и создали кассеты генной экспрессии кДНК GAL4/мутантный CfEcR-DEF, как описано в Примере 1 выше, с использованием набора для ПЦР-медиируемого сайт-специфического мутагенеза. Были изготовлены мутированные и дикого типа (WT) кДНК, соответствующие различным конструкциям переключателя, описанным выше в Примере 1.1 и 1.2, и испытаны методом анализа GAL4-управляемого люциферазного репортера, как описано в Примере 2.
Были идентифицированы специфические аминокислотные остатки, которые в случае их замещения дают мутантный рецептор экдизона, проявляющий повышенную активность в ответ на экдистероидный лиганд. Влияние аминокислотного замещения аминокислотного остатка 119 SEQ ID NO: 1 на активность мутированного рецептора CfEcR-DEF представлено в Таблице 3а как кратность увеличения активности переключателя по сравнению с Gal4/CfEcR-DEF дикого типа (WT). Эффект аминокислотного замещения аминокислотного остатка 96 SEQ ID NO: 1 и двойного аминокислотного замещения аминокислотных остатков 96 и 119 на активность мутированного рецептора CfEcR-DEF представлен в Таблице 3b как ЕС50 и относительный максимум индуцирования укладки. Значения EC50 рассчитывали по данным дозовой зависимости с использованием трехпараметрической логистической модели. Относительный Max FI определяют как отношение максимума индуцирования укладки тестируемого лиганда (вариант исполнения изобретения), наблюдающийся при любой концентрации, к максимуму индукцирования укладки лиганда GS®-E (RG-102240; N-трет-бутил-N'-(2-этил-3-метоксибензоил)гидразида 3,5-диметилбензойной кислоты, наблюдающемуся при любой концентрации.
Как видно из Таблиц 3а и 3b, активность экдистероидов значительно возрастала при проведении мутации лигандсвязывающего домена CfEcR по аминокислотным остаткам 96 или 119 SEQ ID NO: 1 и двойной мутации по аминокислотным остаткам 96 и 119 SEQ ID NO: 1, что указывает на важную роль этих остатков в лигандсвязывающем кармане CfEcR.
ПРИМЕР 4
Этот Пример описывает идентификацию дополнительных субституционных мутантов лигандсвязывающего домена CfEcR, которые обычно являются чувствительными к неэкдистероиду диацилгидразину и проявляют повышенную активность в ответ на диацилгидразиновые лиганды. Для идентификации субституционных мутаций CfEcR, которые повышают активность диацилгидразиновых лигандов, заявители провели мутации аминокислотных остатков, которые были предсказаны как критические для связывания экдистероидов, и создали кДНК кассет генной экспрессии GAL4/мутантный CfEcR-DEF, как описано в Примере 1 выше, с использованием набора для ПЦР-медиируемого сайт-специфического мутагенеза. Были получены мутированные и дикого типа (WT) кДНК, соответствующие различным конструкциям переключателя, описанным выше в Примере 1.1 и 1.2, и протестированы методом анализа GAL4-управляемого люциферазного репортера, как описано в Примере 2.
Были идентифицированы специфические аминокислотные остатки, при замещении которых образуются мутантные рецепторы экдизона, проявляющие повышенную активность в ответ на лиганды неэкдистероида диацилгидразина. Влияние аминокислотного замещения аминокислотных остатков 48, 52, 54, 109, 110, 125, 132 и 223 SEQ ID NO: 1 и двойного замещения аминокислотных остатков 52 и 110 SEQ ID NO: 1 на активность мутированного рецептора CfEcR-DEF показано в Таблицах 4а и 4b как EC50 и относительный максимум индуцирования укладки. Значения ЕС50 рассчитывали по данным дозовой зависимости с использованием трехпараметрической логистической модели. Относительный Max FI определяли как отношение максимума индуцирования укладки тестируемого лиганда (вариант исполнения изобретения), наблюдающегося при любой концентрации, к максимуму индуцирования укладки лиганда GS®-E (N-трет-бутил-N'-(2-этил-3-метоксибензоил)гидразид 3,5-диметилбензойной кислоты), наблюдающемуся при любой концентрации.
Как видно из Таблиц 4а и 4b, активность диацилгидразинов была значительно повышенной, когда лигандсвязывающий домен CfEcR был подвергнут мутациям аминокислотных остатков 48, 52, 54, 109, 110, 125, 132 и 223 SEQ ID NO: 1 и двойным мутациям аминокислотных остатков 52 и 110 SEQ ID NO: 1, что указывает на важную роль этих остатков в лигандсвязывающем кармане CfEcR.
ПРИМЕР 5
Этот Пример описывает идентификацию дополнительных субституционных мутантов лигандсвязывающего домена CfEcR, которые обычно являются чувствительными к диацилгидразину и экдистероидам и проявляют активность в ответ на диацилгидразиновый лиганд и экдистероид. Для идентификации субституционных мутаций CfEcR, которые повышают активность диацилгидразиновых лигандов и активность экдистероидных лигандов, заявители провели мутации аминокислотных остатков и создали кДНК кассет генной экспрессии GAL4/мутантный CfEcR-DEF, как описано в Примере 1 выше, с использованием набора для ПЦР-медиируемого сайт-специфического мутагенеза. Были получены мутированные и дикого типа (WT) кДНК, соответствующие различным конструкциям переключателя, описанным выше в Примере 1.1 и 1.2, и протестированы методом анализа GAL4-управляемого люциферазного репортера, как описано в Примере 2. Влияние аминокислотного замещения аминокислотного остатка 109, 132, 238 SEQ ID NO: 1 или замещения аминокислотных остатков 52, 107 и 127 SEQ ID NO: 1 или 107, 127 и добавления глицина в конце SEQ ID NO: 1 на активность мутированного рецептора CfEcR-DEF приведено в Таблице 5.
Как видно из Таблицы 5, активность по отношению как к диацилгидразину, так и к экдистероиду возрастала, когда лигандсвязывающий домен CfEcR подвергали мутации аминокислотных остатков 48, 51, 52, 54, 96, 120, 125, 128, 132, 234 и 238, что указывает на важную роль этих остатков в лигандсвязывающем кармане CfEcR.
ПРИМЕР 6
Этот Пример описывает идентификацию дополнительных субституционных мутантов лигандсвязывающего домена CfEcR, которые обычно являются чувствительными к диацилгидразину и тетрагидрохинолину и проявляют повышенную активность в ответ на диацилгидразиновые и тетрагидрохинолиновые лиганды. Для идентификации субституционных мутаций CfEcR, которые повышают активность диацилгидразинового лиганда и активность тетрагидрохинолинового лиганда, заявители провели мутации предсказанных аминокислотных остатков и создали кДНК кассет генной экспрессии GAL4/мутантный CfEcR-DEF, как описано в Примере 1, с использованием набора для ПЦР-медиируемого сайт-специфического мутагенеза. Были получены мутированные и дикого типа (WT) кДНК, соответствующие различным конструкциям переключателя, описанным выше в Примере 1.1 и 1.2, и протестированы методом анализа GAL4-управляемого люциферазного репортера, как описано в Примере 2. Эффект тройной мутации аминокислотных остатков 107, 110 и 127 SEQ ID NO: 1 и двойной мутации 107 и 127 SEQ ID NO: 1 на активность мутированного рецептора CfEcR-DEF представлен в Таблице 6.
Как видно из Таблицы 6, активности неэкдистероида диацилгидразина и тетрагидрохинолина возрастали при мутировании аминокислотных остатков 107, 110 и 127 и 107 и 127 лигандсвязывающего домена CfEcR, что указывает на важную роль этих остатков в лигандсвязывающем кармане CfEcR.
ПРИМЕР 7
Таблица 7 описывает влияние диацилгидразинового лиганда GS™-E по сравнению с контролем ДМСО в разных концентрациях на максимум индуцирования укладки различных мутантов CfEcR.
ПРИМЕР 8
Этот Пример описывает идентификацию дополнительных субституционных мутантов лигандсвязывающего домена CfEcR, которые проявляют пониженную активность в ответ на диацилгидразиновые лиганды. Для идентификации субституционных мутаций CfEcR, которые уменьшают активность диацилгидразинового лиганда, заявители провели мутацию аминокислотных остатков, предсказанных как критические при связывании диацилгидразина, и создали кДНК кассет генной экспрессии GAL4/мутантный CfEcR-DEF, как описано в Примере 1, с использованием набора для ПЦР-медиируемого сайт-специфического мутагенеза. Были приготовлены мутированные и дикого типа (WT) кДНК, соответствующие различным конструкциям переключателя, описанным выше в Примере 1.1 и 1.2, и протестированы методом анализа GAL4-управляемого люциферазного репортера, как описано в Примере 2. Эффект аминокислотного замещения аминокислотного остатка 48, 51, 52, 54, 92, 95, 96, 109, 120, 125, 219, 223, 234 или 238 SEQ ID NO: 1 на активность мутированного рецептора CfEcR-DEF представлен в Таблицах 8а и 8b.
Как видно из Таблиц 8а и 8b, активность диацилгидразинов значительно уменьшалась при мутации в лигандсвязывающем домене CfEcR аминокислотных остатков 48, 51, 52, 54, 92, 95, 96, 109, 120, 125, 219, 223, 234 или 238 SEQ ID NO: 1, что указывает на важную роль этих остатков в лигандсвязывающем кармане CfEcR.
ПРИМЕР 9
Этот Пример описывает идентификацию дополнительных субституционных мутантов лигандсвязывающего домена CfEcR, которые обычно являются чувствительными к тетрагидрохинолину и проявляют повышенную активность в ответ на тетрагидрохинолиновые лиганды. Для идентификации субституционных мутаций CfEcR, которые повышают активность тетрагидрохинолинового лиганда, заявители провели мутации специфических аминокислотных остатков и создали кДНК кассет генной экспрессии GAL4/мутантный CfEcR-DEF, как описано в Примере 1, с использованием набора для ПЦР-медиируемого сайт-специфического мутагенеза. Были получены мутированные и дикого типа (WT) кДНК, соответствующие различным конструкциям переключателя, описанным выше в Примере 1.1 и 1.2, и протестированы методом анализа GAL4-управляемого люциферазного репортера, как описано в Примере 2. Эффект аминокислотного замещения аминокислотного остатка 110 или 128 SEQ ID NO: 1 или двойного аминокислотного замещения аминокислотных остатков 110 и 128 SEQ ID NO: 1 на активность мутированного рецептора CfEcR-DEF представлена в Таблице 9.
Как видно из Таблицы 9, активность тетрагидрохинолинов была значительно повышенной, когда в лигандсвязывающем домене CfEcR была проведена мутация аминокислотных остатков 110 или 128 SEQ ID NO: 1 или двойная мутация аминокислотных остатков 110 и 128 SEQ ID NO: 1, что указывает на важную роль этих остатков в лигандсвязывающем кармане CfEcR.
ПРИМЕР 10
Этот Пример описывает идентификацию дополнительных субституционных мутантов лигандсвязывающего домена CfEcR, являющихся дифференцированно чувствительными к диацилгидразиновым лигандам. Эти мутанты проявляют общее снижение диацилгидразиновой активности; однако они селективно чувствительны к специфическому диацилгидразиновому лиганду. Для идентификации субституционных мутаций CfEcR заявители выполнили мутации специфических аминокислотных остатков и создали кДНК кассет генной экспрессии GAL-4/мутантный CfEcR-DEF, как описано в Примере 1, с использованием набора для ПЦР-медиируемого сайт-специфического мутагенеза. Были получены мутированные и дикого типа (WT) кДНК, соответствующие различным конструкциям переключателя, описанным выше в Примере 1.1 и 1.2, и протестированы методом анализа GAL-4-управляемого люциферазного репортера, как описано в Примере 2. Эффект аминокислотного замещения аминокислотного остатка 52, 95, 109, 125 или 132 SEQ ID NO: 1 на активность мутированного рецептора CfEcR-DEF представлен в Таблицах 10а и 10b.
Как видно из Таблиц 10а и 10b, мутации аминокислотных остатков 52, 95, 109, 125 или 132 SEQ ID NO: 1 лигандсвязывающего домена CfEcR дифференциально влияли на активность диацилгидразинов, что указывает на важную роль этих остатков в лигандсвязывающем кармане CfEcR.
Объем настоящего изобретения не ограничен описанными тут конкретными вариантами исполнения. Действительно, разные модификации изобретения, помимо описанных тут, будут очевидными для специалистов в данной области техники из приведенного выше описания и сопровождающих фигур. Такие модификации должны считаться входящими в объем приложенной формулы изобретения.
Следует также понимать, что все размеры оснований или размеры аминокислот и все значения молекулярных весов или молекулярной массы, указанные для нуклеиновых кислот или полипептидов, являются приближенными и приведены в целях описания.


























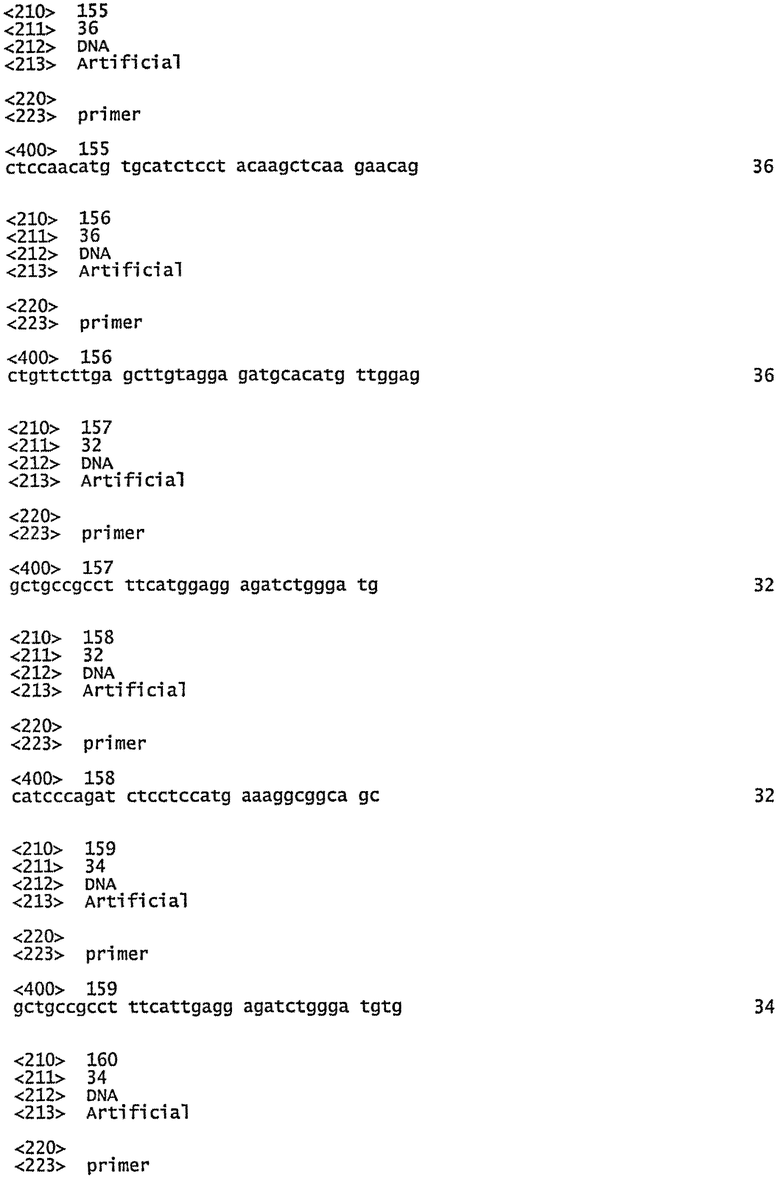

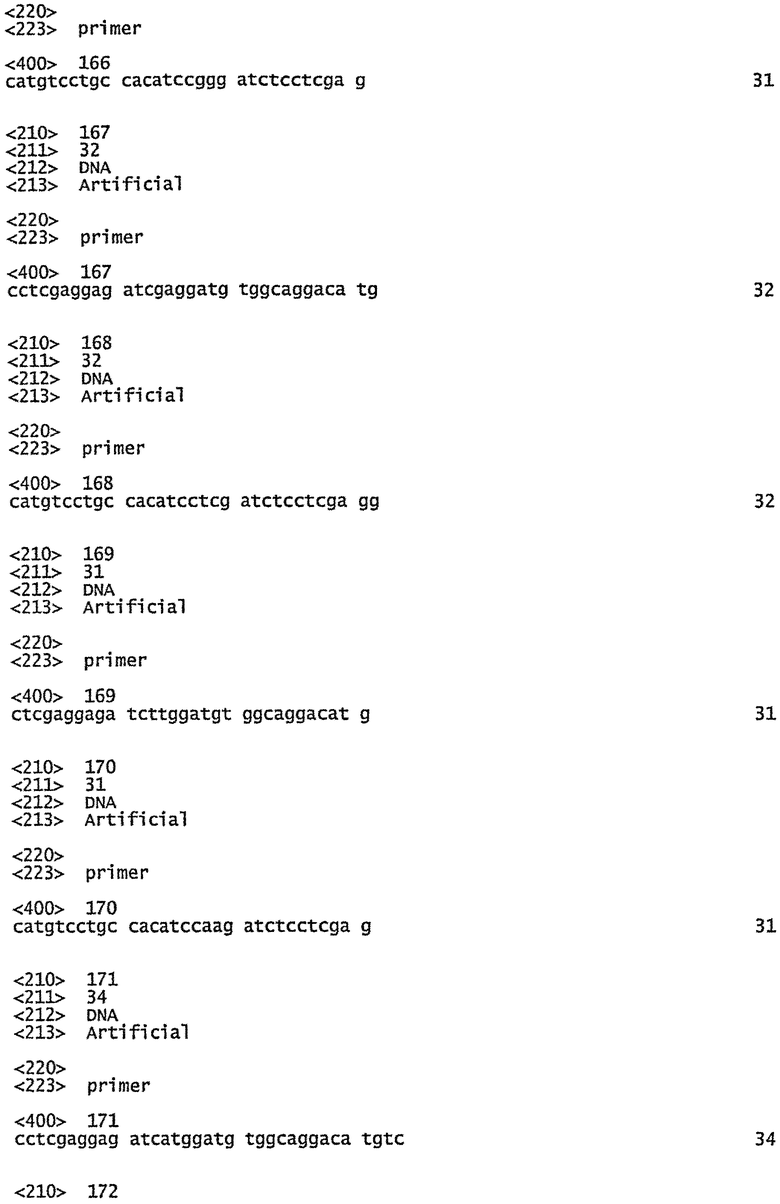

Изобретение относится к области биотехнологии или генной инженерии. Описана система модулирования экспрессии рекомбинантного гена, вектор экспрессии и клетка-хозяин. Изобретение расширяет арсенал методов модулирования экспрессии гена. 3 н. и 9 з.п. ф-лы, 14 табл., 10 пр.
1. Система модулирования экспрессии рекомбинантного гена, содержащая:
а) первую кассету экспрессии рекомбинантного гена, способного к экспрессии в клетке-хозяине, содержащую полинуклеотид, кодирующий первый полипептид, содержащий:
i) ДНК-связывающий домен, распознающий элемент ответа, ассоциированный с геном, экспрессия которого должна быть модулирована, причем ДНК-связывающий домен выбран из группы, содержащей домен рецептора экдизона, ДНК-связывающий домен GAL4 и ДНК-связывающий домен LexA, и
ii) первый лигансвязывающий домен ядерного рецептора, и
б) вторую кассету экспрессии рекомбинантного гена, способного к экспрессии в клетке-хозяине, содержащую полинуклеотид, кодирующий второй полипептид, который содержит:
i) домен трансактивации, выбранный из группы, состоящей из домена трансактивации рецептора экдизона, домена трансактивации VP16, домена трансактивации кислотного активатора В42 и домена трансактивации р 65; и
ii) второй лигандсвязывающий домен ядерного рецептора, причем один из первого и второго лигандсвязывающих доменов ядерного рецептора является лигандсвязывающим доменом рецептора экдизона, который дополнительно содержит:
(1) заместительную мутацию в позиции, эквивалентной или аналогичной аминокислотному остатку 110 SEQ ID NO: 1, и
(2) заместительную мутацию в позиции, эквивалентной или аналогичной аминокислоте 128 SEQ ID NO: 1 или аминокислотам 107 и 127 SEQ ID NO: 1 и необязательно аминокислотному остатку 52 SEQ ID NO: 1, причем указанные мутации обеспечивают повышение чувствительности указанного лигандсвязывающего домена к диацилгидразиновому лиганду и тетрагидрохинолиновому лиганду, и
при этом другой из указанных первого и второго лигансвязывающих доменов ядерного рецептора способен димеризоваться с лигандсвязывающим доменом рецептора экдизона, содержащим указанную мутацию.
2. Система модулирования экспрессии рекомбинантного гена по п.1, в которой заместительная мутация в позиции, эквивалентной или аналогичной аминокислотному остатку 110, представляет собой А110Е, A110N, А110Р или A110W.
3. Система модулирования экспрессии рекомбинантного гена по п.1, в которой лигандсвязывающий домен рецептора экдизона дополнительно содержит заместительную мутацию в позиции, эквивалентной или аналогичной аминокислотному остатку 52 SEQ ID NO: 1.
4. Система модулирования экспрессии рекомбинантного гена по п.3, в которой заместительные мутации представляют собой T53V и А110Р.
5. Система модулирования экспрессии рекомбинантного гена по п.1, в которой лигандсвязывающий домен рецептора экдизона содержит заместительные мутации в позиции, эквивалентной или аналогичной аминокислотному остатку 107 и аминокислотному остатку 127 SEQ ID NO: 1.
6. Система модулирования экспрессии рекомбинантного гена по п.5, в которой мутации представляют собой V107I, Y127E и А110Р.
7. Система модулирования экспрессии рекомбинантного гена по п.1, в которой лигандсвязывающий домен рецептора экдизона содержит заместительную мутацию в позиции, эквивалентной или аналогичной аминокислотному остатку 128 SEQ ID NO: 1.
8. Система модулирования экспрессии рекомбинантного гена по п.7, в которой заместительные мутации представляют собой V128F и А110Р.
9. Вектор экспрессии, содержащий систему модулирования экспрессии рекомбинантного гена по п.1.
10. Экспрессирующая клетка-хозяин, содержащая вектор экспрессии по п.9, которая содержит систему модулирования экспрессии рекомбинантного гена по п.1, обеспечивающую повышение чувствительности лигандсвязывающего домена к диацилгидразину и тетрагидрохинолину.
11. Система модулирования экспрессии рекомбинантного гена по п.1, в которой другой лигансвязывающий домен ядерного рецептора является ретиноидным Х-рецептором лигансвязывающего домена.
12. Система модулирования экспрессии рекомбинантного гена по п.11, в которой ретиноидный Х-рецептор лигансвязывающего домена является химерным.
| WO200170816, 27.09.2001 | |||
| M | |||
| B | |||
| Kumar, A single point mutation inecdysone receptor leads to increased ligand specificity: Implications for gene switch applications, Proc Natl Acad Sci USA 2002 Nov 12; 99(23):14710-5 | |||
| РТУТНОЕ РЕЛЕ ДЛЯ ТЕРМОСТАТОВ | 1926 |
|
SU4062A1 |
Авторы
Даты
2015-01-10—Публикация
2005-05-02—Подача