Изобретение относится к области химико-фармацевтической промышленности и может использоваться для получения биологически активных веществ, лечебных и профилактических средств.
Магний и калий относятся к основным микроэлементам организма человека. Магний активирует около трехсот ферментов, все ферментные системы, в которых в качестве субстрата принимает участие АТФ, который необходим для самых разных энергетических процессов при углеводном, белковом и липидном обменах, а также при синтезе нуклеиновых кислот.
Основная роль калия в организме - поддержание функционирования клеточных стенок. Кроме того, он способствует сохранению концентрации магния и его физиологических функций.
Преимуществами оротатов калия и магния по сравнению с другими препаратами - простыми солями органических кислот (например, аспаргинатов калия и магния, входящих в состав аспаркама и панангина), заключается в том, что фармакологическое действие препарата определяется не только катионами металла, но и оротат-анионом.
Оротовая кислота не только принимает участие в магниевом обмене, но и обладает самостоятельным метаболическим действием. Оротовая кислота является непосредственным предшественником пиримидиновых оснований - одного из составляющих нуклеиновых кислот (ДНК и РНК). Установлено, что оротовая кислота является кардиопротектором: ускоряет регенерацию миокарда, увеличивает устойчивость к ишемии и выживаемость при инфаркте. Именно оротовая кислота необходима для фиксации магния на АТФ в клетке.
Известно средство, включающее в качестве активного начала эффективное количество калия оротата и целевые добавки в количестве от 45 до 55% от массы действующего вещества (RU 2173998). В качестве целевых добавок использованы сахар молочный, крахмал картофельный или кукурузный, желатин пищевой, кислота стеариновая.
Известен препарат Магнерот в виде таблеток, содержащий магния оротат фирмы Worwag Pharma, Германия (Справочник Видаль, Астра Фарм Сервис, 2006, с. 695).
Недостатками известных препаратов являются недостаточная эффективность и низкая скорость усвоения магния, что приводит к необходимости более длительного приема препаратов и увеличению медикаментозной нагрузки на организм.
Известна фармацевтическая композиция (патент RU 2225713), объединяющая два действующих вещества - оротат калия и магния. Одновременный прием таблетированных препаратов «магнерот» и «оротат калия» приведет к такому же действию на организм человека, что и прием препарата «орокамаг».
Эффективность действия известных препаратов на основе оротатов калия и магния ограничивается плохой растворимостью. В результате для получения эффекта лечения необходимы относительно высокие дозы и длительный курс лечения.
Повышение растворимости может достигаться за счет сокристаллизации с хорошо растворимым компонентом [Душкин А.В., Сунцова Л.П., Халиков С.С. Механохимическая технология для повышения растворимости лекарственных веществ. Фундаментальные исследования №1, 2013, стр. 450]. Сокристаллизация осуществляется путем механохимической реакции. В результате получается фактически новое вещество с новой химической формулой: «за счет перевода ЛВ в их водорастворимые соли (если ЛВ имеет выраженные кислотно-основные свойства), а также за счет включения молекул ЛВ в супрамолекулярные водорастворимые образования (межмолекулярные комплексы, мицеллы) со специально подобранными «вспомогательными» веществами». К числу недостатков данного способа можно отнести необходимость проведения полноценных клинических испытаний, выявление возможных побочных действий полученного нового вещества.
Известно, что биологические свойства лекарственных препаратов зависят от кристаллической структуры (аморфная или кристаллическая), полиморфной модификации кристаллической структуры, а также от изомерной структуры молекул. Поэтому перспективным путем является изменение структуры известных препаратов с целью повышения их терапевтической эффективности.
Скорость растворения зависит от площади поверхности соприкосновения воды с твердым веществом, поэтому повышение дисперсности приводит к увеличению скорости растворении. Аморфизация также, как правило, приводит к повышению скорости растворения. При этом величина растворенного вещества (растворимость) не изменяется.
Известен способ получения фармацевтической композиции (RU 2452480), выбранный в качестве прототипа, который осуществляется совместной механической обработкой глицина, обогащенной гамма-кристаллической модификацией глицина, в количестве 90-98% и добавку нетоксичных органических кислот в количестве 2-10%, в вибрационной мельнице компонентов композиции в течение 6-60 минут. Растворимость композиции повышается за счет изменения pH среды желудка при использовании органических кислот, а скорость растворения - за счет диспергирования порошка и изменения кристаллической модификации глицина в результате механической обработки. Недостатком данного способа является то, что указанные воздействия на выбранные компоненты оказывают слабое влияние на биологическую доступность действующего вещества, которая определяется механизмом взаимодействия молекулы этого вещества с липидным слоем из желудочно-кишечного тракта и механизмом взаимодействия молекулы действующего вещества с мембранами клеток. Диспергирование ускоряет скорость растворения вещества, практически не изменяя его растворимости (количества растворенного вещества), изменение кристаллической модификации влияет на процесс абсорбции из желудочно-кишечного тракта. Однако оба эти фактора не влияют на механизм взаимодействия молекулы растворенного действующего вещества с мембраной клетки. Этот механизм определяется стерическими факторами - доступностью определенных функциональных групп и электронным строением молекулы. При осуществлении способа не контролируют дозу переданной энергии при механоактивации.
В настоящем изобретении предлагается использовать механоактивацию оротатов в смеси с вспомогательными веществами в шаровой планетарной мельнице. Механоактивация приводит к изменению изомерной структуры оротата - таутомерному превращению. Для оротат-аниона известно три таутомера-, оксо-, гидрокси- и дигидрокси-формы. Различие электронного строения таутомерных форм заключается в следующем.
Оксо-форма содержит два пиррольных атома азота (-NH-)e карбонильных группы (>C=O). Гидрокси-форма имеет один пиррольный и один пиридиновый (-N=) атом азота, одни карбонильную и одну гидроксильную (-С-ОН) группу. Диокси-форма имеет два пиридиновых атома азота и две гидроксильных группы.
Пиридиновый атом азота имеет неподеленную пару электронов и проявляет основные свойства. Неподеленная пара электронов пиррольного атома азота является частью ароматической системы и атом азота может служить центром кислотности. Тригональный sp2-гибридизованный атом углерода карбонильной группы образует три σ-связи, лежащие в одной плоскости и п-связь с кислородом за счет негибридизованной р-орбитали. Вследствие различия в электроотрицательности атомов углерода и кислорода п-связь между ними сильно поляризована. В результате на атоме углерода карбонильной группы возникает эффективный положительный заряд, а на атоме кислорода - отрицательный заряд. Электронодефицитный атом углерода становится центром нуклеофильной реакции. Гидроксильная группа, присоединенная к гетероциклу, проявляет мезомерный эффект, в результате чего водород приобретает подвижность и способность диссоциировать в водных растворах. Гидроксильная группа менее гидрофильна, чем карбонильная.
Различие электронного строения оротат-аниона приводит к различной растворимости в воде, водных растворах и липидах. Самым важным является различие механизмов взаимодействия разных таутомеров с белками клеточной мембраны.
Техническим результатом настоящего изобретения является создание препаратов на основе солей оротовой кислоты, характеризующихся повышенной растворимостью, скоростью растворения и усваиваемостью (биологической доступностью).
Техническим результатом настоящего изобретения является создание препаратов на основе солей оротовой кислоты, характеризующихся повышенной растворимостью и скоростью растворения в воде, липофильностью и биологической доступностью.
Технический результат достигается в способе получения препарата, содержащего аморфные или аморфно-кристаллические соли оротовой кислоты с повышенным содержанием гидрокси-формы (лактимного изомера) оротатов, включающем термообработку кристаллических оротата калия и/или оротата магния, с последующим измельчением в измельчительном активаторном устройстве. Термообработка заключается в термостатировании при температуре 115-125°C в течение 40-60 мин для удаления кристаллогидратной воды. В качестве измельчительного активаторного устройства используют шаровую планетарную мельницу, измельчение проводится в течение времени, необходимого для подвода удельной энергии 7-10 кДж/г.
Обработка в измельчительном активаторном устройстве приводит к изменению структурного состояния оротат-анионов - таутомерного превращения оксо- в гидрокси- и дигидрокси-форму. Гидрокси-форма имеет наиболее высокую биологическую активность благодаря повышенной липофильности, обуславливающей абсорбцию из желудочно-кишечного тракта, наличию двух двойных связей C=C и механизму взаимодействия оротат-аниона с карбонильной и гидрофильной группами с белками мембраны клетки. Диспергирование, частичная или полная аморфизация смеси в результате механообработки приводит к повышению скорости растворения смеси.
О полученных веществах судят по данным эмиссионной спектроскопии, рентгеновской дифракции, ИК-, РФЭС спектроскопии.
Согласно данным анализа методом эмиссионной спектроскопии с индуктивно связанной (аргоновой) плазмой (спектрометр Spectroflame) в составе механоактивированных оротатов калия и магния отсутствуют какие-либо неорганические примеси, источником которых могут быть шары и стенки сосудов для измельчения.
Методы рентгеновской дифракции, рентгеноэлектронной спепктроскопии и ИК-спектроскопии свидетельствуют, что в результате механоактивации не наблюдается изменения химического состава смесей, деструкции или образования новых веществ.
Изобретение поясняется чертежами.
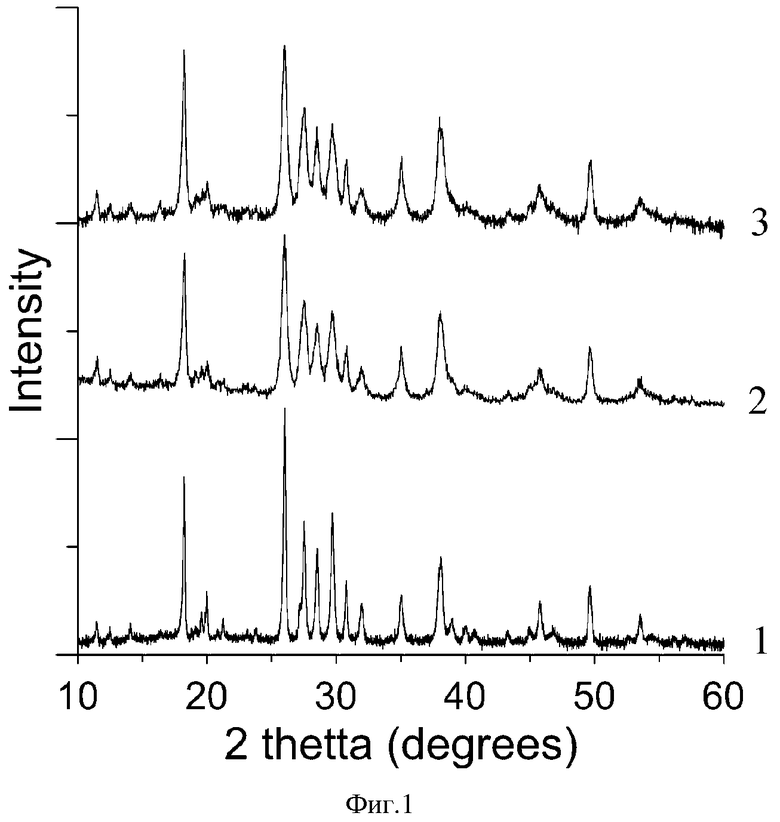
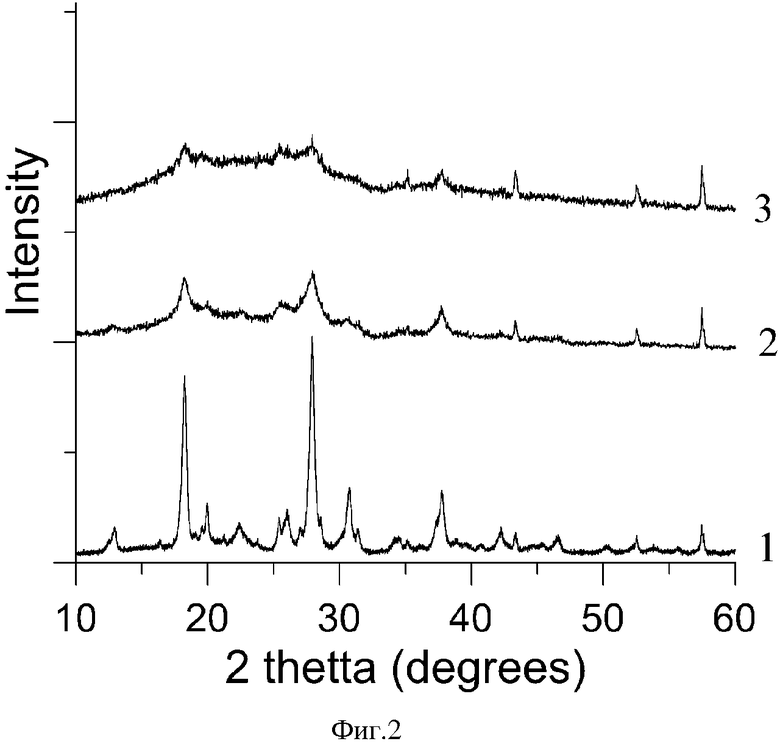
фиг. 1-2 - Рентгеновские дифрактограммы исходных (1) и механоактивированных (2-7 кДж/г; 3-42 кДж/г) оротатов магния и калия соответственно;
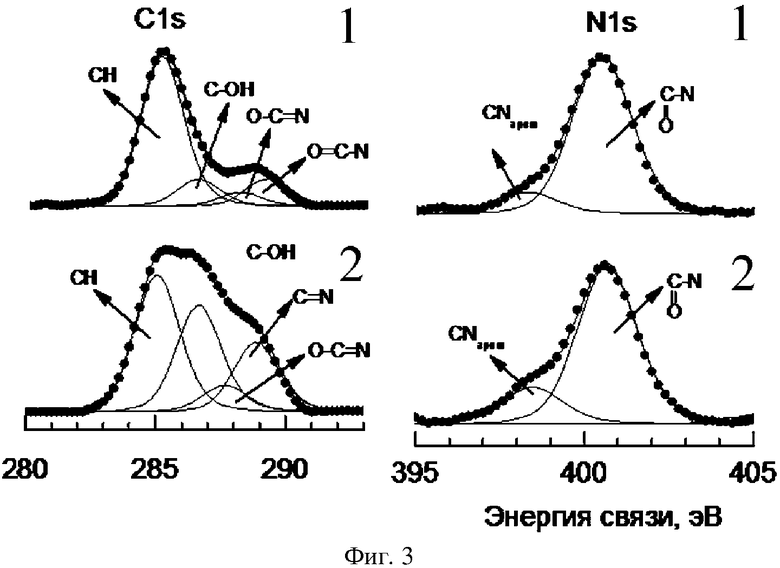
фиг. 3 - Рентгеноэлектронные C1s- и N1s-спектры оротата калия: 1 - исходный; 2 - механоактивированный (7 кДж/г);
фиг. 4 - Рентгеноэлектронные C1s- и N1s-спектры оротата магния: 1 - исходный; 2 - механоактивированный (7 кДж/г);
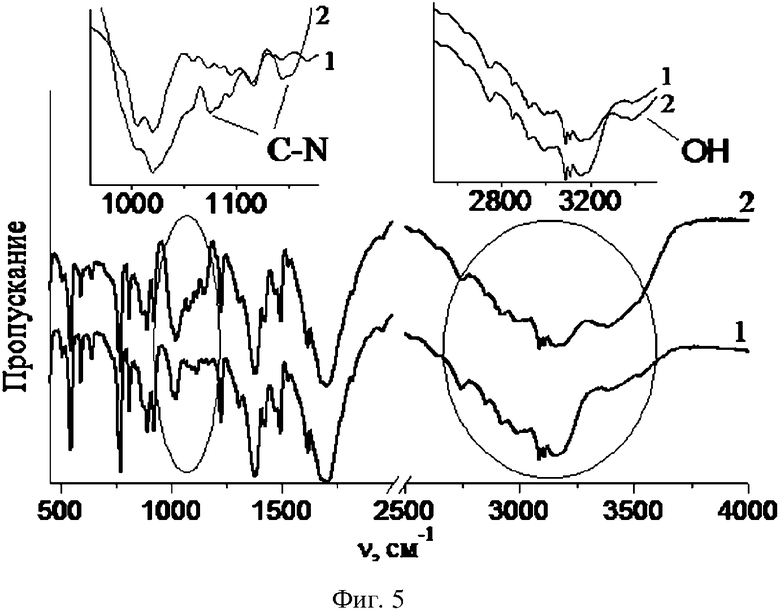
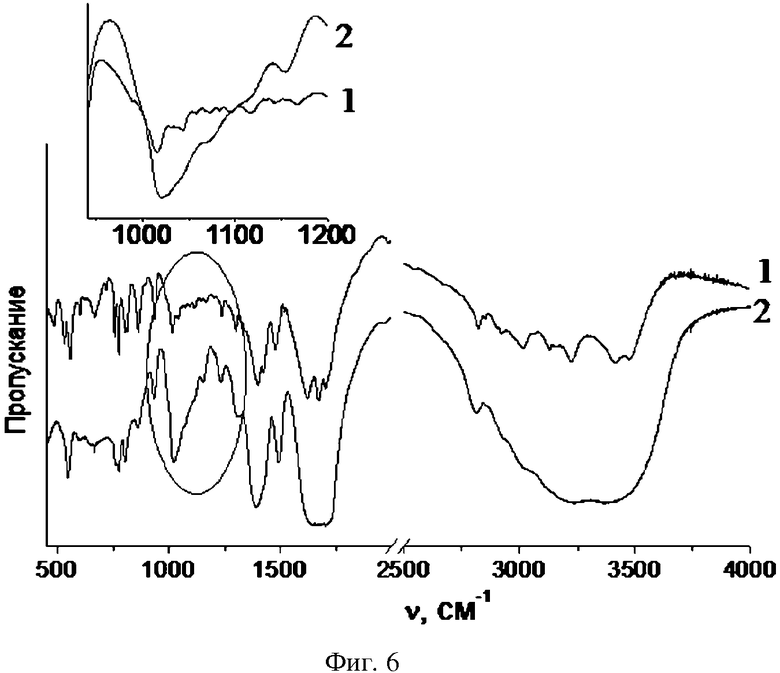
фиг. 5-6 ИК-спектры оротатов калия и магния соответственно: 1 - исходный; 2 - механоактивированный (7 кДж/г).
Способ получения препарата, содержащего аморфные или аморфно-кристаллические соли оротовой кислоты, включает термообработку кристаллических оротата калия и/или оротата магния с последующим измельчением в измельчительном активаторном устройстве.
Термообработка заключается в термостатировании при температуре 115-125°C в течение 40-60 мин для удаления кристаллогидратной воды. Удаление кристаллогидратной воды необходимо, поскольку таутомерное превращение оксо-формы в гидрокси- или дигидрокси-форму в зависимости от количества гидратной воды оказывается или невозможным, или проходит в малой степени: кристаллогидратная вода связана с гидрофильными карбонильными (>С=O) группами оротат-аниона, и препятствует переходу атома водорода от - NH- группы к кислороду карбонильной группы. Кроме того, термообработка позволяет ускорить процесс таутомерного превращения. Без предварительной термообработки результат достигается не через 1 ч, а через несколько часов (примерно 3.5 ч).
В качестве измельчительного активаторного устройства используют шаровую планетарную мельницу, измельчение проводится в течение времени, необходимого для подвода удельной энергии 7-10 кДж/г. Подведенная энергия может быть определана как энергонапряженность мельницы (Вт/г) × масса вещества (г) × время обработки (с), например, методом тест-объектов, когда обрабатывают вещество или несколько веществ до формирования определенной структуры или нового вещества. Из термодинамики определяют, сколько необходимо потратить энергии на такой процесс. В нашем эксперименте скорость вращения мельницы составляла 890 об/мин, время обработки - 2-2.5 ч.
На фиг. 1-2 приведены дифрактограммы образцов смесей исходных и механоактивированных оротатов. Видно, что в исходном состоянии оротаты имеют кристаллическую структуру (дифрактограммы 1 на фиг. 1-2). После 1 ч (7 кДж/г) механоактивации структура оротата магния становится аморфно-кристаллической: об этом свидетельствует размытие рефлексов рентгеновской дифрактограммы (дифрактограмма 2 на фиг. 2), а через 6 ч (42 кДж/г) механоактивации оротат магния полностью аморфизуется (дифрактограмма 3 на фиг. 2). Структура оротата калия через 1 ч (7 кДж/г) механоактивации становится аморфно-кристаллической и практически не меняется даже через 6 ч (42 кДж/г) механоактивации (дифрактограммы 2 и 3 на фиг. 1).
На фиг. 3 приведены РФЭС спектры оротатов калия и магния до и после механоактивации (7 кДж/г)). Анализ спектров свидетельствует об изменении атомной структуры оротатов - превращении лактамной формы в лактимную, в результате которого в азотсодержащем гетероцикле формируется ароматическая система связей:
в C1s- и N1s-спектрах оротатов после механоактивации не появляется составляющих, свидетельствующих об образовании новых химических соединений;
в C1s- и N1s-спектрах механоактивированного оротата калия возрастает интенсивность составляющих от атомов углерода и азота в составе ароматического гетероцикла (связь C=N); в O1s-спектре увеличилась интенсивность составляющей от ОН-групп;
в C1s-спектрах механоактивированного оротата магния интенсивность составляющей от атомов углерода в составе O=C-N остается относительно высокой, а относительный вклад составляющей от атомов углерода в связи С-ОН ниже, чем в спектрах оротата калия.
В ИК-спектре (фиг. 5-6) механоактивированного образца оротата калия (7 кДж/г) появляется полоса поглощения при ~3390 см-1, отвечающая за валентные колебания ОН-группы. Отмечаются изменения в области спектра 950-1100 см-1, которые могут быть обусловлены «дышащими» колебаниям (N-C) пиримидинового кольца, а также валентными колебаниями группы C-O. Эти эффекты свидетельствуют о таутомерном превращении оротат-аниона с образованием ароматического кольца.
После механоактивации в ИК-спектре образца оротата магния (фиг. 4) исчезает тонкая структура полос поглощения 950-1100, 1500-1800 и 2800-3700 см-1, что может быть следствием уменьшения индуцированного дипольного взаимодействия с увеличением межмолекулярного расстояния в результате аморфизации. Изменения, связанные с образованием ароматического кольца в спектре механоактивированного оротата магия, мало заметны на фоне изменений, связанных с аморфизацией.
Биологический ответ организма на лекарство, прежде всего, зависит от его растворимости, которая обусловливает распределение вещества в этом организме и во многом определяет фармакокинетические свойства лекарственного препарата. Растворимость оказывает существенное влияние на проникновение препарата из кишечника в кровь, то есть на такие процессы, как всасывание, фильтрация, диффузия и др.
В табл. 1 приведены растворимости исходных и механоактивированных оротатов в зависимости от кислотности (pH) среды. Кислотность выбрана в соответствии с кислотностью среды различных отделов желудка и кишечника.
Растворимость механоактивированных оротатов калия и магния выше, чем исходных, и при этом зависит от кислотности среды (pH). Причиной повышения растворимости оротатов является формирование ароматического гетероцикла, что способствует повышению растворимости в полярных растворителях, к которым относится вода.
Скорость растворения в воде (pH 6.5) механоактивированного оротата калия выше, чем исходного: так, в первые 20 минут скорость растворения составляет 4.9 мг/л·мин и 6.6 мг/л·мин для исходного и механоактивированного (3 ч) образцов, соответственно.
Скорость растворения механоактивированного оротата магния в воде (pH 6.5) такая же, как исходного.
Повышение скорости растворения оротатов обусловлено аморфизацией образцов в результате механоактивации.
Не наблюдается взаимодействия вспомогательных веществ (крахмал, лактоза, микроцеллюлоза) с оротатами калия и магния при механоактивация. Данные вещества вводятся для облегчения таблетирования механоактивированных препаратов. Введение вспомогательных веществ перед процессом механоактивации обеспечивает равномерное их смешивание с оротатами.
Изменение физико-химических свойств механоактивированных оротатов по сравнению с исходными свидетельствует об увеличении биологической доступности в результате механоактивации. Эта характеристика была исследована методом микроэлектрофореза. Исследуемые эпителиоциты помещали в водные растворы оротатов калия и магния и с помощью устройства, описанного, например, в патенте RU 2168176, создавали многовекторные, симметричные, знакопеременные электрические поля. Под микроскопом определяли реакции клеток на воздействия электрических полей по возвратно-поступательным движениям клеток или их ядер, цитолеммы.
Результаты исследования биологической активности оротатов калия и магния методом микроэлектрофореза исследовано на клетках крови и буккальных эпителиоцитов (табл. 2 и 3).
Повышение биологической активности оротатов калия и магния после механоактивации обусловлено следующими моментами:
- диспергирование и формирование аморфной (для оротата магния) и аморфно-кристаллической (для оротата калия) структуры, приводящие к увеличению скорости растворения в воде;
- формированием ароматического гетероцикла дигироксоформы оротата калия, которое способствует повышению растворимости в полярных растворителях (воде) и улучшению абсорбции из желудочно-кишечного тракта;
- образованием OH-групп взамен C=O в результате формирования гидроксо-формы оротата магния и дигидроксо-формы оротата калия, которое приводит к увеличению гидрофобности молекул оротатов, т.е. увеличению липофильности способствующей улучшению усвоения механоактивированных оротатов организмом.
Использование механоактивированных оротатов калия и магния влияет на прижизненные свойства клеток: активируется плазмолемма и ядра клеток, наблюдается активация лимфоцитов.
Повышение биологической активности наблюдается для оротатов, механоактивированных при дозе механической энергии в диапазоне 7-10 кДж/г.
Пример
На паре несмешивающихся жидкостей вода-1-октанол была смоделирована мембрана кишечно-желудочного тракта. Из водных растворов гидрокси-формы в октанол перешло почти в 2 раза больше оротата калия и в 1,7 раза больше оротата магния. Это свидетельствует о большем количестве гидрокси-форм оротатов калия и магния, перешедшем из желудочно-кишечного тракта в организм. Вывод подтверждается исследованиями на лабораторных крысах.
Для исследований на лабораторных крысах на модели гипомагниемии (ГМЕ) на основании данных микроэлектрофореза была выбрана наиболее активная гидрокси-форма и одна из менее активных - оксо-форма оротата магния. Гипомагниемия достигалась введением крысам в течение 14 дней внутрибрюшинно диуретика фуросемида (Furosemidi 1%) в дозе 30 мг/кг. В состоянии ГМЕ содержание магния в крови понижалось почти в 2 раза по сравнению с исходным состоянием крыс. При приеме оксо-формы продолжалось последействие фуресемида и содержание магния продолжало уменьшаться. При приеме гидрокси-формы наблюдалась положительная тенденция - восстановление концентрации магния в сыворотке крови.
| название | год | авторы | номер документа |
|---|---|---|---|
| МЕХАНОАКТИВИРОВАННЫЕ АМОРФНЫЕ И АМОРФНО-КРИСТАЛЛИЧЕСКИЕ КАЛЬЦИЕВЫЕ СОЛИ ГЛЮКОНОВОЙ КИСЛОТЫ, КОМПОЗИЦИИ, СПОСОБЫ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ И СПОСОБ ЛЕЧЕНИЯ НА ИХ ОСНОВЕ | 2007 |
|
RU2373185C2 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ДИПРОПИОНАТА БЕТУЛИНА | 2013 |
|
RU2541153C1 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ДИАЦЕТАТА БЕТУЛИНА | 2013 |
|
RU2517157C1 |
| СОЛЬ АЛИСКИРЕНА И ОРОТОВОЙ КИСЛОТЫ | 2007 |
|
RU2456267C2 |
| ФАРМАКОЛОГИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПОВЫШЕНИЯ АДАПТАЦИОННЫХ ВОЗМОЖНОСТЕЙ ОРГАНИЗМА В УСЛОВИЯХ ФИЗИЧЕСКИХ НАГРУЗОК | 2014 |
|
RU2564949C1 |
| НОВЫЕ КОМПОЗИЦИИ И СПОСОБЫ ПОЛУЧЕНИЯ 5-АМИНО- ИЛИ ЗАМЕЩЕННЫХ АМИНО-1,2,3-ТРИАЗОЛОВ И ТРИАЗОЛ-ОРОТАТНЫХ КОМПОЗИЦИЙ | 2010 |
|
RU2594155C2 |
| АДДУКТЫ ОРОТОВОЙ КИСЛОТЫ С АМИНОКИСЛОТАМИ ИЛИ АМИНАМИ, ПРОЯВЛЯЮЩИЕ ГЕПАТОЗАЩИТНЫЙ ЭФФЕКТ | 1993 |
|
RU2047606C1 |
| Способ получения аморфных водорастворимых солей цитрата магния | 2020 |
|
RU2756322C1 |
| 2-Этил-6-метил-3-гидроксипиридина оротата дигидрат и способ его получения | 2017 |
|
RU2690674C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИАНГИНАЛЬНЫМ, АНТИИШЕМИЧЕСКИМ И НООТРОПНЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2225713C1 |

Изобретение относится к области химико-фармацевтической промышленности и представляет собой способ получения препарата, содержащего аморфные или аморфно-кристаллические соли оротовой кислоты, включающий термообработку кристаллических оротата калия и/или оротата магния с последующим измельчением в измельчительном активаторном устройстве, термообработка заключается в термостатировании при температуре 115-125°C в течение 40-60 мин, а в качестве измельчительного активаторного устройства используют шаровую планетарную мельницу, измельчение проводится в течение времени, необходимого для подвода удельной энергии 7-10 кДж/г. Изобретение обеспечивает создание препаратов на основе солей оротовой кислоты, характеризующихся повышенной растворимостью, скоростью растворения и биологической доступностью. 6 ил., 4 табл.
Способ получения препарата, содержащего аморфные или аморфно-кристаллические соли оротовой кислоты, включающий термообработку кристаллических оротата калия и/или оротата магния с последующим измельчением в измельчительном активаторном устройстве, термообработка заключается в термостатировании при температуре 115-125°C в течение 40-60 мин, а в качестве измельчительного активаторного устройства используют шаровую планетарную мельницу, измельчение проводится в течение времени, необходимого для подвода удельной энергии 7-10 кДж/г.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИАНГИНАЛЬНЫМ, АНТИИШЕМИЧЕСКИМ И НООТРОПНЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2225713C1 |
| МЕХАНОАКТИВИРОВАННЫЕ АМОРФНЫЕ И АМОРФНО-КРИСТАЛЛИЧЕСКИЕ КАЛЬЦИЕВЫЕ СОЛИ ГЛЮКОНОВОЙ КИСЛОТЫ, КОМПОЗИЦИИ, СПОСОБЫ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ И СПОСОБ ЛЕЧЕНИЯ НА ИХ ОСНОВЕ | 2007 |
|
RU2373185C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ГЛИЦИНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2452480C2 |
| 1996 |
|
RU2167649C2 | |
| 2000 |
|
RU2173998C | |
| Душкин А.В., Сунцова Л.П., Халиков С.С | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2015-02-20—Публикация
2013-10-16—Подача