Область техники, к которой относится изобретение
Изобретение относится к созданию клеточных моделей болезни Альцгеймера, предназначенных для тестирования лекарственной эффективности химических веществ с целью их дальнейшего использования в медицине, более конкретно в сфере лечения нейродегенеративных заболеваний человека, обусловленных нейротоксическими эффектами бета-амилоидных агрегатов.
Уровень техники
Болезнь Альцгеймера (БА) является смертельной нейродегенеративной патологией, клиническое протекание которой сопровождается неуклонным упадком психомоторных функций пациента на протяжении длительного периода (7). В России число таких больных составляет около полутора миллионов человек (2). Лекарственных средств, способных остановить течение данной патологии, в настоящее время не существует нигде в мире, однако их поиску придается колоссальное значение во всех развитых странах, где с ростом числа лиц пожилого возраста увеличивается и число страдающих от болезни Альцгеймера.
Характерным молекулярным процессом болезни Альцгеймера является конформационное превращение небольшого (39-43 аминокислотных остатка) белка, бета-амилоида (3). Этот белок является нормальным компонентом крови, где присутствует в виде мономера, однако образует олигомеры и надмолекулярные агрегаты (амилоидные бляшки) у пациентов с клинически диагностированной болезнью Альцгеймера (4). Согласно широко принятой амилоидной гипотезе именно полимеризация бета-амилоида, которая приводит к церебральному амилоидозу, является ключевым событием, запускающим весь патогенный каскад болезни Альцгеймера (5).
Молекулярный механизм патогенного действия агрегированных форм бета-амилоида не установлен, однако хорошо известно, что присутствие агрегатов бета-амилоида в тканях организма вызывает явно выраженный цитотоксический эффект (6). В настоящее время для скринирования потенциальных лекарственных средств широко используются клеточные модели болезни Альцгеймера (7-8). При этом используются как экзогенные, так и эндогенные клеточные модели, в которых патология обусловлена избыточным производством бета-амилоида или тау-белка человека.
В патенте США US 5,994,084 описаны трансгенные клеточные модели, которые наряду с перепроизводством тау-белка характеризуются содержанием киназ, ответственных за гиперфосфорилирование тау белка, что вызывает его повышенную агрегацию. В патентной заявке США US 2009/0280110 описана методика контроля ранних клеточных явлений при болезни Альцгеймера, в которой клетки, содержащие белки тау и тубулин, непосредственно контактируют с бета-амилоидом. В патенте США US 6,803,233 описана экзогенно-индуцируемая клеточная модель болезни Альцгеймера, в которой первичная культура клеток из мозга грызунов подвергается действию различных агентов, в том числе бета-амилоида, для индукции в них таких явлений, ассоциированных с БА, как образование нейрофибриллярных клубков, гиперфосфорилирование и/или фрагментация тау-белка и выработка цитокинов TGF-бета, IL-1b или TNF. B патентной заявке WO 2010/112737 описана человеческая нейронная модель, полученная на основе плюропатентных стволовых клеток, содержащих геном пациентов с диагнозом болезнь Альцгеймера. В патентной заявке (США) US 2005/0172344 описана клеточная модель, полученная на основе клеток гиппокампа, выделенных из животной модели БА, содержащих мутации в гене, кодирующем АРР и PS1. B патенте США US 6,548,261 описана методика тестирования препаратов, которые способны ингибировать клеточные явления, ассоциированные с БА, на основе трансфецированных нейрональных клеточных линий млекопитающих. В то же время не было обнаружено никаких сведений о создании и применении экзогенно-индуцируемых клеточных моделей болезни Альцгеймера с использованием модифицированных форм бета-амилоида.
Ранее авторами данного изобретения было показано, что изомеризация остатка аспарагиновой кислоты в положении 7 ведет к цинк-зависимой олигомеризации металлсвязывающего домена 1-16 бета-амилоида (9). Так как амилоидные бляшки содержат до 75% изомеризованного бета-амилоида и избыток ионов цинка, то нами было предположено, что именно цинковые комплексы этой изоформы бета-амилоида могут являться молекулярным агентом, вызывающим олигомеризацию и последующую агрегацию растворимых форм бета-амилоида, то есть тех самых процессов, которые абсолютным большинством исследователей считаются пусковыми механизмами патогенеза болезни Альцгеймера.
Сущность изобретения
Настоящее изобретение относится к способу создания клеточных моделей болезни Альцгеймера, в которых цитотоксический эффект индуцируется посредством введения в культуральную среду синтетического аналога изомеризованного по остатку аспарагиновой кислоты в положении 7 человеческого бета-амилоида 1-42. Преимуществом таких клеточных моделей болезни Альцгеймера по сравнению с существующими в настоящее время экзогенно-индуцируемыми моделями, в которых цитотоксические эффекты вызываются немодифицированной формой бета-амилоида, является более высокая способность изомеризованного бета-амилоида индуцировать клеточную гибель как по некротическому, так и по апоптозному механизмам. Дополнительным преимуществом данного изобретения является возможность использования в качестве моделей болезни Альцгеймера первичных клеточных культур.
Технический результат
Технический результат, достигаемый при использовании патентуемого изобретения, заключается в создании экзогенно-индуцируемых клеточных моделей болезни Альцгеймера.
Пример осуществления изобретения
В качестве клеточной линии была использована иммортализованная культура нейральных стволовых клеток человека NSC-hTERT (10). Клетки NSC-hTERT были получены с помощью иммортализации введением гена каталитической субъединицы теломеразы (hTERT) в клетки первичной культуры. Первичные культуры нейральных стволовых клеток человека (NSC) были предоставлены И.Н. Сабуриной (Институт биологии гена РАН). Клетки были получены из переднего отдела мозга эмбриона человека (медицинского абортуса) в возрасте 9 недель. Мозг эмбриона механически измельчали, обрабатывали растворами трипсина и Версена, пипетировали и переносили в культуральную среду. Клетки культивировали при 3% кислорода в ростовой среде, состоящей из следующих компонентов: среда DMEM/F12, 2% FetalClone III (Hyclone, США), 10 нг/мл FGF2, 10 нг/мл EGF, 0,11 мг/мл пирувата натрия, 0,32 мг/мл глутамина, однократная концентрация N2supplement (Invitrogen, США) и 40 ед./мл гентамицина. При ведении клеток на такой среде они растут как обычная пластик-адгезивная культура. Пересев осуществляли по достижении монослоя с помощью растворов Версена и трипсин-Версена. При уменьшении концентрации FetalClone III клетки способны переходить к росту в виде нейросфер. Первичные культуры NSC обладают ограниченным пролиферативным потенциалом и в наших условиях были способны достигать уровня около 42 удвоений популяции на сроках около полугода. Трансфекция клеток была осуществлена лентивирусной конструкцией, содержащей кДНКhTERT под CMV-промотором. Конструкция pLA-CMV-hTERT (9645 пар оснований) была любезно предоставлена П.М. Чумаковым (ИМБ РАН). Вирусный концентрат (с титром 108/мл) разводили в два раза полной ростовой средой, добавляли 5 мкг/мл полибрена и добавляли к растущим NSC. Клонирования не производили. Эффективность лентивирусной трансфекции (по параллельному введению GFP) составляла около 75%. Возраст клеток на момент трансфекции был около 9 удвоений популяции. В непрерывном эксперименте длительностью 560 дней было показано, что NSC-hTERT не меняют скорости роста и пролиферировали свыше 100 удвоений популяции. Эти клетки обладают теломеразной активностью, экспрессируют hTERT (определяли с помощью антител) и содержат несколько удлиненные теломеры. В них сохраняется диплоидный кариотип. Они способны образовывать нейросферы. В них экспрессируются гены, связанные со стволовым состоянием (нестин, определен по РНК и белку), нейрональной дифференцировкой (бета-III-тубулин, определен по РНК и белку), нейрон-специфическая енолаза, тирозингидроксилаза, холин-ацетил-трансфераза (определены по РНК) и глиальной дифференцировкой (глиальный фибриллярный кислый белок, определен по РНК и белку) и липофилин (определен по РНК).
Синтетические пептиды Аβ: [H2N]-DAEFRHDSGYEVHHQKLVFFAEDVGSNKGAIIGLMVGGVVIA-[COOH] и isoAβ: [H2N]-DAEFRH[isoD]SGYEVHHQKLVFFAEDVGSNKGAIIGLMVGGVVIA-[COOH] были получены от Biopeptide (СА, USA). Все эксперименты и приготовления проводились в стерильных условиях. Синтетические пептиды были растворены в диметилсульфоксиде до конечной концентрации стока 10 мМ. Затем 1 мкл стока был растворен в 5 мкл деионизованной воды. Полученный раствор был добавлен к 500 мкл среды до конечной концентрации пептида 20 мкМ. В эксперименте были использованы дифференцированные нервные клетки, сыворотка в среду не добавлялась. Клетки культивировались в 500 мкл среды в 12-луночных планшетах. В ячейках среда, в которой культивировались клетки, была заменена на среду, содержащую 1 мкл диметилсульфоксида и 5 мкл деионизованной воды (три контрольных ячейки), пептид Αβ (три ячейки) и пептид isoAβ (три ячейки). Затем планшет помещался в термостат при 37°С на 24 часа.
Для снятие клеток использовался следующий протокол: отобрали ростовую среду;1 раз промыли клетки раствором Версена (~120 мкл на 1,9 см2); залили монослой раствором для снятия клеток (0,25% стерильный раствор Трипсина с солями Хенкса (без Са и Mg))(~120 мкл на 1,9 см2); инкубировали при 37°С, периодически аккуратно покачивая, ~1-2 мин; когда клетки полностью отделились от субстрата, добавили полной среды 500 мкл и тщательно диспергировали клетки; провели подсчет количества клеток в счетной камере Горяева под инвертированным микроскопом с предварительным окрашиванием трипановым синим.
Цитометрический анализ клеток проводили на проточном цитофлуориметре GALLIOS (BeckmanCoulter).
Определение процента клеток с поврежденной мембраной. Клетки, обладающие поврежденной мембраной, определяли с помощью пропидиййодида (PI) («Sigma», США) (Ex/Em 535/617 нм). Для этого за 1 минуту до начала измерений к клеточной суспензии добавляли пропидиййодид до конечной концентрации 10 мкг/мл. Регистрировали процент клеток, обладающих флуоресценцией в красной области спектра, при возбуждении лазером с длиной волны 488 нм.
Определение процента апоптических клеток. Определение процента апоптических клеток проводили с помощью Аннексина V, позволяющего детектировать выход фосфатидилсерина на поверхность клеток. Для определения процента апоптических клеток суспензию клеток центрифугировали (800 об/мин, 7 мин), отбирали супернатант и ресуспендировали в буфере для связывания Аннексина V (10 мМ HEPES, 140 мМ NaCl и 2.5 мМ CaCl2, рН 7.4). Затем к 100 мкл суспензии клеток с концентрацией 106 клеток/мл добавляли 5 мкл раствора Аннексина V, меченного флуоресцеином FITC (Invitrogen), длины волн возбуждения и эмиссии Ex/Em которого составляют 494 и 518 нм соответственно. Таким образом, флуоресценцию аннексин-положительных клеток регистрировали в зеленой области спектра при возбуждении лазером с длиной волны 488 нм. Инкубацию проводили в течение 15 минут в темноте при комнатной температуре, после чего добавляли 300 мкл холодного буфера для связывания Аннексина и ставили в лед. Жизнеспособные клетки не окрашивались ни аннексином, ни пропидиййодидом. Окрашенные Аннексином и неокрашенные PI клетки характеризовали как раннеапоптические. Окрашенные PI и Аннексином клетки определяли как позднеапоптические или некротические. Клетки, окрашенные только пропидиййодидом, характеризовали как некротические.
Определение процента гибнущих клеток. К гибнущим клеткам относят клетки с измененной морфологией, характеризующейся снижением размера клеток и возрастанием их гранулярности. Данные параметры при проточной цитометрии оценивают с помощью параметров малоуглового и бокового рассеяния. Таким образом, определение процента гибнущих клеток в популяции проводили, оценивая процент клеток с малым размером и высокой гранулярностью.
Определение процента клеток со сниженным митохондриальным потенциалом
Процент клеток со сниженным митохондриальным потенциалом определяли с помощью красителя DilC1 (5) (Invitrogen), длины волн возбуждения и эмиссии Ex/Em которого составляют 638 и 658 нм соответственно. Таким образом, флуоресценцию окрашенных DilC1 (5) клеток регистрировали в красной области спектра при возбуждении лазером с длиной волны 638 нм. Для окрашивания клетки ресуспендировали в 100 мкл среды до концентрации 1×106 клеток/мл и добавляли к ним 0,5 мкл 10 мкМ DilC1 (5) до конечной концентрации 50 нМ, после чего инкубировали в течение 20 минут в СО2 инкубаторе при 37°С. Краситель проникает в цитозоль клеток и накапливается в митохондриях. За 1 минуту до измерения добавляли пропидиййодид, как описано выше. Процент клеток со сниженным митохондриальным потенциалом регистрировали как процент клеток с неповрежденной мембраной, обладающих сниженной интенсивностью флуоресценции митохондриального красителя. Спектральные характеристики используемых красителей: Аннексин-FITC, DilC1 (5), пропидиййодид позволяют использовать их для одновременного окрашивания и анализа клеток на проточном цитофлуориметре. При этом сначала проводится окрашивание DilC1 (5), а затем окрашивание Аннексином, меченным FITC. PI добавляется к клеткам за 1 минуту до измерения, как описано выше.
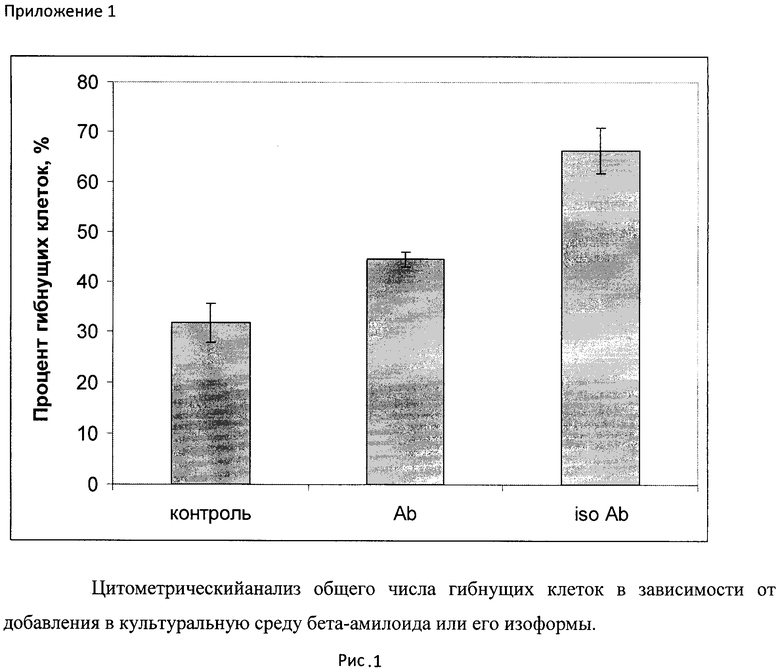
Цитофлуометрическое исследование апоптических изменений и морфологических характеристик клеток под действием бета-амилоида и его изоформы позволило установить, что изоформа обладает большим цитотоксическим эффектом по отношению к нейрональным клеткам, чем бета амилоид. Эффект проявляется при культивировании клеток с интактным бета-амилоидом (Ab) и его изомеризованной по остатку аспарагиновой кислоты в положении 7 изоформы (isoAb) в течение 24 часов (Рисунки 1, 2). На рисунке 1 показан процент гибнущих клеток, оцененный как процент клеток с малым размером и высокой гранулярностью. Из представленных данных видно, что доля гибнущих клеток под действием изоформы бета-амилоида возрастает и составляет более 65%.
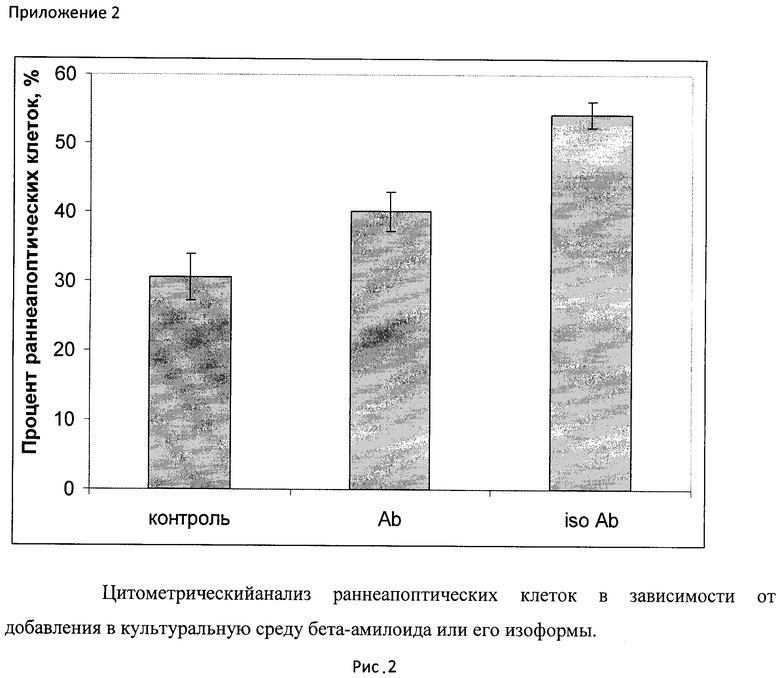
На рисунке 2 представлен процент раннеапоптических клеток, то есть клеток, находящихся в стадии раннего апоптоза, через 24 часа инкубации с бета-амилоидом и его изоформой. Как следует из приведенных данных, под действием изоформы бета-амилоида происходит значительное возрастание процента раннеапоптических клеток до 55%.
Таким образом, изомеризованный по остатку аспарагиновой кислоты в положении 7 человеческий бета-амилоид 1-42 (isoAb) гораздо эффективнее, чем немодифицированный бета-амилоид 1-42 (Ab), индуцирует как некроз, так и апоптознейральных клеток. Так как клеточная гибель под воздействием различных форм бета-амилоида играет одну из ключевых ролей при болезни Альцгеймера, то очевидно, что isoAb является более сильнодействующим, чем Ab патогенным агентом, а клеточные модели болезни Альцгеймера на основе использования isoAbB качестве экзогенного фактора индукции клеточной гибели представляются более адекватными.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭКЗОГЕННО-ИНДУЦИРУЕМАЯ ЖИВОТНАЯ МОДЕЛЬ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2012 |
|
RU2532525C2 |
| ПЕПТИД И СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2018 |
|
RU2679059C1 |
| Животная модель цинк-зависимого амилоидогенеза при болезни Альцгеймера | 2021 |
|
RU2781331C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНДУЦИРОВАННЫХ ПЛЮРИПОТЕНТНЫХ СТВОЛОВЫХ КЛЕТОК ПАЦИЕНТОВ С СИНДРОМОМ ДАУНА | 2012 |
|
RU2492233C1 |
| СРЕДСТВО ДЛЯ СЕЛЕКТИВНОЙ АПОПТОТИЧЕСКОЙ ЭЛИМИНАЦИИ ОПУХОЛЕВЫХ КЛЕТОК | 2014 |
|
RU2567670C2 |
| СИНТЕТИЧЕСКИЙ ТЕТРАПЕПТИД HAEE И ЕГО ПРОИЗВОДНЫЕ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ВОССТАНОВЛЕНИЯ ФУНКЦИИ НЕЙРОНОВ ЧЕЛОВЕКА | 2023 |
|
RU2822603C1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ АМИЛОИДНЫХ ОТЛОЖЕНИЙ | 2013 |
|
RU2673484C2 |
| СИНТЕТИЧЕСКИЙ ТЕТРАПЕПТИД HAEE И ЕГО ПРОИЗВОДНЫЕ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЗАЩИТЫ ФУНКЦИИ НЕЙРОНОВ ЧЕЛОВЕКА | 2023 |
|
RU2822602C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ ИЗОМЕРИЗОВАННОГО АСПАРТАТА В БЕТА-АМИЛОИДЕ | 2009 |
|
RU2431143C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ НАРУШЕНИЙ | 2005 |
|
RU2387453C2 |
Изобретение относится к способу создания клеточных моделей болезни Альцгеймера, предназначенных для тестирования лекарственной эффективности химических веществ с целью их дальнейшего использования в медицине, более конкретно в сфере лечения нейродегенеративных заболеваний человека, обусловленных нейротоксическими эффектами бета-амилоидных агрегатов. В качестве молекулярного агента цитотоксического действия используется синтетический аналог изомеризованного по остатку аспарагиновой кислоты в положении 7 ([isoD]) человеческого бета-амилоида 1-42 (аминокислотная последовательность: DAEFRH[isoD]SGYEVHHQKLVFFAEDVGSNKGAIIGLMVGGVVIA). Преимуществом таких клеточных моделей болезни Альцгеймера по сравнению с существующими в настоящее время экзогенно-индуцируемыми моделями, в которых цитотоксические эффекты вызываются немодифицированной формой бета-амилоида, является более высокая способность изомеризованного бета-амилоида индуцировать клеточную гибель как по некротическому, так и по апоптозному механизмам. Дополнительным преимуществом данного изобретения является возможность использования в качестве моделей болезни Альцгеймера первичных клеточных культур. 2 ил.
Способ создания клеточных моделей болезни Альцгеймера, отличающийся тем, что цитотоксический эффект вызывается добавлением в культуральную среду синтетического аналога изомеризованного по остатку аспарагиновой кислоты в положении 7 ([isoD]) человеческого бета-амилоида 1-42 (аминокислотная последовательность: DAEFRH[isoD]SGYEVHHQKLVFFAEDVGSNKGAIIGLMVGGVVIA).
| US 2005172344 A1, 04.08.2005 | |||
| СПОСОБ ИДЕНТИФИКАЦИИ ИЗОМЕРИЗОВАННОГО АСПАРТАТА В БЕТА-АМИЛОИДЕ | 2009 |
|
RU2431143C2 |
| TSVETKOV P.O | |||
| et al., "Isomerization of the Asp7 residue results in zinc-induced oligomerization of Alzheimer's disease amyloid beta(1-16) peptide", Chembiochem | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| US 6548261 B1, 15.04.2003 | |||
Авторы
Даты
2015-03-20—Публикация
2013-04-17—Подача