Изобретение относится к области нефтехимии и разработки катализатора для получения синтез-газа в процессе парциального окисления метана.
Известен способ и катализатор получения синтез-газа методом парциального окисления метана, описанный в патенте RU 2144844, согласно которому синтез-газ получают путем селективного каталитического окисления метана кислородом при температуре 700-850°C. Указанный способ имеет недостаток, заключающийся в необходимости одновременной подачи сырья (метана) и окислителя (кислорода) в реактор, что приводит к повышенной взрывоопасности процесса вследствие образования смесей метана с кислородом. Еще одним недостатком данного способа является высокая стоимость получения кислорода.
Известен способ получения синтез-газа, описанный в патенте US 2665199 A, опубл. 05.01.1954, кл. C01B 3/30, C01B 3/44, согласно которому синтез-газ получают из газообразных углеводородов в установке, состоящей из реактора и регенератора, в присутствии твердых частиц оксида металла, находящихся в псевдоожиженном состоянии. В реакторе протекает окисление углеводородов кислородом, содержащимся в твердых частицах, в регенераторе происходит окисление твердых частиц до оксида металла. Реакция окисления углеводородов проводится в псевдоожиженном слое, имеющем следующие недостатки:
- неравномерность времени пребывания сырья в зоне реакции, в результате некоторая часть сырья подвергается чрезмерному превращению до образования сажи, а другая часть не достигает полной конверсии;
- среднее фиктивное время пребывания сырья в зоне реакции недостаточно малое, чтобы обеспечить максимально высокую селективность процесса.
В качестве оксида металла применяют оксид железа. Применение оксида металла без носителя может привести к спеканию или агломерации частиц. Для предотвращения агломерации и обеспечения высокой площади контакта активной фазы и реагентов применяют нанесение активного компонента катализатора на какой-либо малоактивный или инертный материал [Дж. Андерсон. Структура металлических катализаторов. / М.: Мир, 1978].
Наиболее близким к заявленному по технической сущности и достигаемому эффекту являются катализатор и способ получения синтез-газа, описанный в патенте US 6833013 B1, опубл. 21.12.2004, кл. C01B 3/32, согласно которому синтез-газ получают парциальным окислением низших алканов кислородом, содержащимся в твердых частицах, содержащих оксид металла и подвергающихся окислительно-восстановительным циклам. Низшие алканы окисляются в реакторе при температуре 800-1100°C и давлении 0,5-5 МПа, твердые частицы окисляются в регенераторе при температуре 750-1050°C. Полученный синтез-газ содержит 60,2% H2 и 30,6% CO, т.е. мольное отношение H2/CO в нем составляет 1,97, что хорошо подходит для получения из синтез-газа метанола, продуктов синтеза Фишера-Тропша. Согласно примеру в описываемом способе получения синтез-газа катализатор содержит 20 мас.% оксида хрома (VI). Во время реакции с углеводородами с образованием водорода и монооксида углерода оксид хрома (VI) восстанавливается до оксида хрома (III). Таким образом, оксид хрома (VI) выступает в виде донора «активного кислорода», участвующего в реакции парциального окисления углеводородов. Именно от его содержания в катализаторе зависит эффективность описанного способа получения синтез-газа: чем больше активного кислорода может запасать катализатор, тем большее количество сырья можно конвертировать в его присутствии. Исходя из данных, представленных в рассматриваемом патенте, содержание активного кислорода на оксидно-хромовом катализаторе составляет 4,8 мас. %.
Однако недостатком описанного способа является применение катализатора на основе оксида хрома. Хром и его соединения являются токсичными веществами [Плющев В.Е. Справочник по редким металлам / М.: Мир, 1978], поэтому использование предлагаемого способа получения синтез-газа существенно повышает требования к уровню техники безопасности и охраны окружающей среды. Еще одним недостатком описанного способа является проведение реакции окисления углеводородов и регенерации твердых частиц в псевдоожиженном слое, в результате чего обеспечивается весьма низкий удельный съем продукта, а именно 0,159 кг синтез-газа с килограмма катализатора в час, что оказывает отрицательное влияние на производительность реактора. Удельным съемом называется количество продукта, полученное при осуществлении процесса на катализаторе определенной массы за единицу времени [Мельников Е.Я. Справочник азотчика. / М.: Химия, 1967, 492 C.]. Удельный съем продукта в наиболее близком аналоге был рассчитан исходя из количества катализатора в реакторе - 1400 г и выхода продукта - 516 л/ч.
Задача настоящего изобретения заключается в создании оксидно-металлического катализатора получения синтез-газа путем парциального окисления метана, не содержащего хрома и его соединений и способного к многократным окислительно-восстановительным переходам, а также в увеличении удельного съема продукта при сохранении преимуществ наиболее близкого аналога - исключении образования взрывоопасных смесей и низких энергозатратах с возможностью получения синтез-газа с отношением Н2/СО в пределах 1,5-2,5.
Решение поставленной задачи достигается тем, что катализатор получения синтез-газа в процессе парциального окисления метана представляет собой микросферический носитель, в качестве которого используют частицы диаметром от 50 до 160 мкм оксида алюминия и/или алюмосиликата, а в качестве активного компонента - оксид Со, или Ni, или Fe, или Mn, или Cu, или Ce, или смесь оксидов NiO, Co3O4 и Ce2O3, при следующем соотношении компонентов, % мас:
Катализатор получают нанесением предшественника активного компонента - растворов солей указанных металлов - на микросферический носитель с диаметром частиц от 50 до 160 мкм путем пропитки по влагопоглощению, сушки при температуре от 90 до 120°C в течение 1-5 часов и прокаливания при температуре от 500 до 1200°C в течение 2-8 часов.
Синтез-газ получают окислительной конверсией метансодержащего газа при температуре более 750°C в реакторе с использованием в качестве окислителя катализатора - микросферического носителя с нанесенным активным компонентом на основе оксидов металлов - и регенерацией восстановленного катализатора путем его окисления в регенераторе, из которого регенерированный катализатор поступает в реактор, причем используют указанный катализатор, окислительную конверсию проводят в сквознопоточном лифт-реакторе, через который катализатор непрерывно проходит снизу вверх в потоке метансодержащего газа при времени пребывания сырья в зоне реакции 0,1-10 с, затем выходящий из реактора восстановленный катализатор отделяют от продукта - синтез-газа - и направляют в регенератор.
Окислительную конверсию предпочтительно проводят при температуре от более 750 до 1100°C, наиболее предпочтительно - 850°C.
Регенерацию катализатора предпочтительно проводят в псевдоожиженном, или форсированном псевдоожиженном, или полусквозном потоке путем окисления кислородсодержащим агентом.
В качестве кислородсодержащего агента предпочтительно используют воздух или кислород.
Принято считать, что псевдоожиженный слой присутствует при скоростях газового потока до 0,8 м/с. При скоростях газа 0,8-1,5 м/с система характеризуется состоянием форсированного псевдоожиженного слоя. Системы, в которых перемещение твердых частиц осуществляется при скоростях газа, достигающих 1,5-3,0 м/с, называются полусквозным потоком. Скорости газового потока выше 3-4 м/с соответствуют перемещению твердых частиц в потоке газа в режиме сквозного потока [Хаджиев С.Н. Крекинг нефтяных фракций на цеолитсодержащих катализаторах / М.: Химия, 1982. - 280 С.].
Реакторы, работающие в двух последних режимах, называют сквознопоточными (лифт-реакторы).
Процесс является непрерывным, и его проводят в двух пространственно разделенных аппаратах: реакторе и регенераторе. В такой системе «реактор-регенератор» катализатор по мере истирания и разрушения выводят из системы в виде пыли и заменяют свежим.
Полученный синтез-газ и восстановленный катализатор выводят из реактора и поток отработанного (восстановленного) катализатора отделяют от потока целевого продукта. Поток восстановленного катализатора по транспортной линии подают в блок регенерации, где происходит окисление катализатора в потоке кислородсодержащего агента (воздух, кислород). Затем катализатор отделяют от газов регенерации и по транспортным линиям снова подают в реактор конверсии, как описано выше.
Процесс является непрерывным и состоит из следующих стадий:
- конверсия углеводородного сырья в синтез-газ (с восстановлением катализатора до металлического состояния);
- регенерация катализатора (с окислением его металлических компонентов).
Стадии окисления и восстановления катализатора проходят параллельно и непрерывно.
Таким образом, осуществляется непрерывная циркуляция катализатора, и обеспечивается перенос кислорода из зоны регенерации в зону реакции, а также сводятся материальный и тепловой балансы.
В качестве носителя катализатора используют микросферический оксид алюминия и/или алюмосиликат. Диаметр частиц носителя от 50 до 160 мкм, удельная площадь поверхности - от 10 до 330 м2/г.
Достигаемый технический результат заключается:
- в повышении удельного съема продукта;
- в возможности использования углеводородного сырья, содержащего диоксид углерода;
- в снижении опасности взрыва и возгорания, низких энергозатратах, получении синтез-газа с отношением Н2/СО в пределах 1,5-2,5.
- в использовании катализаторов, содержащих менее токсичные вещества, чем соединения хрома;
- в возможности получения побочного продукта - технического азота.
Сущность предлагаемого изобретения иллюстрируется следующими примерами.
Пример 1
Готовят микросферический алюмосиликатный носитель путем смешения водных суспензий силиката натрия и сульфата алюминия в таких пропорциях, чтобы композиция алюмосиликата имела состав Na2O(Al2O3·nSiO2), где n является мольным отношение SiO2/Al2O3 и равно 2,3, с последующим получением микросферической формы методом распылительной сушки и прокаливанием при 800°C в течение 3 ч. 100 г микросферического алюмосиликатного носителя пропитывают по влагопоглощению водным раствором, полученным смешением 57,9 г Ni(NO3)2·6H2O, 53,9 г Co(NO3)2·6H2O, 41,0 г Al(NO3)3·9H2O, и 4,7 г Ce(NO3)3·6H2O при температуре 90°C. Образец сушат при температуре 100°C и затем прокаливают в печи при температуре 500-900°C в течение 3-5 часов. Полученный катализатор содержит 10,8 мас. % NiO, 10,8 мас. % Co3O4,
4,1 мас.% Al2O3, 1,4 мас.% CeO2, остальное (70,2 мас.%) - алюмосиликатный носитель. Количество активного кислорода в катализаторе составляет 5,2 мас.%, диаметр микросфер от 50 до 160 мкм. Катализатор испытан в реакции парциального окисления метана.
В нижнюю часть лифт-реактора подают метан, который контактирует с микросферическим катализатором, поступающим из регенератора. Катализатор, подхваченный восходящим потоком метана, движется по реактору снизу вверх в режиме сквозного потока, при этом происходит окисление метана кислородом, содержащимся в катализаторе, в монооксид углерода и водород по реакции
CH4+[O]→CO+2H2.
Метан подают с такой скоростью, чтобы поддерживать время пребывания сырья в лифт-реакторе 2,1 с. Температуру в зоне реакции держат 850°C. Пары продуктов отделяют от катализатора, катализатор направляют в регенератор. В регенераторе катализатор подвергают окислению воздухом в режиме псевдоожиженного слоя. Температуру в зоне регенерации держат 600°C. Окисленный катализатор из регенератора вновь направляют в нижнюю часть реактора.
Конверсию сырья рассчитывают как отношение количества превращенного сырья к исходному, выраженное в %:
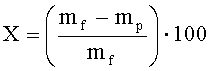
где X - конверсия сырья, мас.%,
mf - масса сырья, кг,
mp - масса углеводородов в продуктах, кг.
Удельный съем синтез-газа рассчитывают как количество синтез-газа, полученное с одного килограмма катализатора в час:
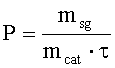
где P - удельный съем синтез-газа, кг/(кг кат.·ч),
msg - масса синтез-газа, полученного за время τ, л,
mcat - масса катализатора, находящегося в реакторе, кг,
τ - время, с.
Мольное отношение H2/CO рассчитывают как отношение количества водорода к количеству монооксида углерода в продуктах реакции:
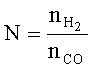
Показатели процесса приведены в таблице 1.
Как видно из таблицы, существенно возрастает удельный съем синтез-газа (по сравнению с удельным съемом синтез-газа по прототипу - 0,159 кг/(кг кат. · ч) при высоком значении конверсии сырья.
Пример 2
Опыт проводят, как в примере 1, но процесс проводят при температуре в зоне реакции, равной 750°C, в присутствии катализатора, полученного путем пропитки по влагопоглощению 100 г микросферического оксида алюминия (полученного путем распылительной сушки суспензии гидроксида алюминия) водным раствором 88,6 г Fe(NO3)3·9H2O, при температуре 90°C. Катализатор содержит 14,5 мас.% Fe3O4, остальное (85,5) алюмооксидный носитель.
Конверсия сырья согласно примеру составляет 60,3%.
Удельный съем синтез-газа согласно примеру составляет 2,180 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 3
Опыт проводят, как в примере 1, но температуру в зоне реакции поддерживают равной 950°C.
Конверсия сырья согласно примеру составляет 99,4%.
Удельный съем синтез-газа согласно примеру составляет 3,649 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 4
Опыт проводят, как в примере 1, но температуру в зоне реакции поддерживают равной 1000°C.
Конверсия сырья согласно примеру составляет 99,6%.
Удельный съем синтез-газа согласно примеру составляет 3,649 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 5
Опыт проводят, как в примере 1, но процесс проводят при температуре в зоне регенерации, равной 800°C, в присутствии катализатора, содержащего оксид кобальта, нанесенного на алюмосиликатный носитель, полученный путем пропитки по влагопоглощению 100 г микросферического алюмосиликатного носителя водным раствором 64,2 г Co(NO3)2·6H2O, при температуре 90°C. Катализатор содержит 15,1 мас.% Co3O4, остальное (84,9) алюмосиликатный носитель.
Конверсия сырья согласно примеру составляет 95,1%.
Удельный съем синтез-газа согласно примеру составляет 3,460 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 6
Опыт проводят, как в примере 5, но температуру в зоне регенерации держат равной 1100°C.
Конверсия сырья согласно примеру составляет 95,1%.
Удельный съем синтез-газа согласно примеру составляет 3,460 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 7
Опыт проводят, как в примере 1, но процесс проводят при температуре в зоне реакции, равной 1100°C, и времени пребывания сырья в зоне реакции 0,1 с в присутствии катализатора, полученного путем пропитки по влагопоглощению 100 г микросферического оксида алюминия (полученного путем распылительной сушки суспензии гидроксида алюминия) 89,4 г Ni(NO3)2·6H2O, при температуре 90°C. Катализатор содержит 18,7 мас.% NiO, остальное (81,3) алюмооксидный носитель.
Конверсия сырья согласно примеру составляет 20,4%.
Удельный съем синтез-газа согласно примеру составляет 19,147 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 8
Опыт проводят, как в примере 7 при времени пребывания сырья в зоне реакции, равном 5,0 с, и температуре в реакторе 850°C.
Конверсия сырья согласно примеру составляет 99,4%.
Удельный съем синтез-газа согласно примеру составляет 1,374 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 9
Опыт проводят, как в примере 8, при времени пребывания сырья в зоне реакции, равном 10,0 с.
Конверсия сырья согласно примеру составляет 99,2%.
Удельный съем синтез-газа согласно примеру составляет 0,711 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 10
Опыт проводят, как в примере 1, но в качестве метансодержащего сырья в лифт-реактор подают газовую смесь, состоящую из метана и этана с концентрацией последнего 20 об.%, а катализатор содержит оксид марганца, нанесенный на алюмосиликатный носитель, и получен путем пропитки по влагопоглощению 100 г микросферического алюмосиликатного носителя водным раствором 40,3 г Mn(NO3)2·6H2O, при температуре 90°C. Катализатор содержит 10,9 мас.% MnO2, остальное (89,1) алюмосиликатный носитель.
Конверсия сырья согласно примеру составляет 92,3%.
Удельный съем синтез-газа согласно примеру составляет 3,792 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 11
Опыт проводят, как в примере 1, но в лифт-реактор подают реакционную газовую смесь, состоящую из метана и диоксида углерода с концентрацией последнего 10 об.%, а катализатор содержит оксид меди, нанесенный на алюмосиликатный носитель и получен путем пропитки по влагопоглощению 100 г микросферического алюмосиликатного носителя водным раствором 92,3 г Cu(NO3)2·6H2O, при температуре 90°C. Катализатор содержит 19,9 мас.% CuO, остальное (80,1) алюмосиликатный носитель.
Конверсия сырья согласно примеру составляет 91,6%.
Удельный съем синтез-газа согласно примеру составляет 3,436 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
Пример 12
Опыт проводят, как в примере 1, но в лифт-реактор подают реакционную газовую смесь, состав которой приведен в таблице 2. Состав этой смеси соответствует усредненному составу попутных нефтяных газов (ПНГ) России и СНГ. Попутные газы - газообразные углеводороды, сопровождающие сырую нефть, в условиях пластового давления, растворенные в нефти и выделяющиеся в процессе ее добычи. Попутные газы содержат 30-80% метана, 10-26% этана, 7-22% пропана, 4-7% бутана и изобутана, 1-3% н-пентана и высших н-алканов. Также в этих газах содержатся сероводород, диоксид углерода, азот, инертные газы, меркаптаны. Средний газовый фактор нефтяных месторождений России - 95-112 куб. м/т (количество попутных газов в куб. м, приходящееся на 1 т добытой нефти) Для расчета усредненного состава модельной смеси (концентраций метана, этана, пропана и бутана) использовали данные состава попутных нефтяных газов некоторых нефтяных месторождений РФ и СНГ (таблица 3) [Лапидус А.Л., Голубева И.А., Жагфаров Ф.Г. Газохимия. М.: ЦентрЛитНефтеГаз, 2008].
Концентрацию каждого компонента в составе модельной смеси рассчитывали:
ccpi=100·Σ(cij·pj)/Σ(Σ( cij·pj)i),
где cij - концентрация i-го компонента в j-м месторождении,
pj - j-е месторождение.
Катализатор состоит из оксидов никеля, кобальта и церия, нанесенных на алюмосиликат и оксид алюминия.
Конверсия сырья согласно примеру составляет 97,6%.
Удельный съем синтез-газа согласно примеру составляет 4,739 кг/(кг кат.·ч).
Показатели процесса приведены в таблице 1.
Мольное отношение H2/CO в получаемом синтез-газе составляет 2,1.
Концентрация азота в газе регенерации составляет 99,1% об.
Как видно из таблицы 1, уменьшение времени пребывания сырья в зоне реакции ниже определенной величины (2 с) приводит к увеличению съема продукта, но снижению степени конверсии, что в свою очередь потребует разделения непрореагировавшего сырья от продуктов реакции. Увеличение времени пребывания сырья в зоне реакции до 10 с связано с уменьшением скорости потока, что может привести к переходу режима работы реактора из сквозного потока в полусквознопоточный и, соответственно, снижению съема продукта.
При снижении температуры реакции до 750°C падает конверсия и съем продукта.
Таким образом, предложен способ получения синтез-газа, позволяющий в оптимальных условиях при высоких значениях конверсии метансодержащего сырья увеличить удельный съем синтез-газа в 20-30 раз по сравнению с прототипом при соотношении H2/CO в пределах 1,5-2,5, при исключении опасности взрыва и возгорания и низких энергозатратах.
Пример 13
Опыт проводят, как в примере 1, но катализатор в регенераторе окисляют кислородом.
Конверсия сырья согласно примеру составляет 95,1%.
Удельный съем синтез-газа согласно примеру составляет 3,460 кг/(кг кат. · ч).
Показатели процесса приведены в таблице 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2012 |
|
RU2533731C2 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2013 |
|
RU2556941C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ОКСИДНО-ПОЛИМЕТАЛЛИЧЕСКИХ КАТАЛИЗАТОРОВ НА ОСНОВЕ ЖАРОПРОЧНЫХ СПЛАВОВ ДЛЯ ПАРЦИАЛЬНОГО ОКИСЛЕНИЯ УГЛЕВОДОРОДОВ В СИНТЕЗ-ГАЗ | 2013 |
|
RU2552639C1 |
| Наноструктурированный катализатор с целью получения синтез-газа путем углекислотной конверсии метана и способ его получения | 2017 |
|
RU2660648C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2012 |
|
RU2493912C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА | 2013 |
|
RU2528829C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОКИСЛИТЕЛЬНОЙ КОНДЕНСАЦИИ МЕТАНА, КАТАЛИЗАТОР, ПРИГОТОВЛЕННЫЙ ПО ЭТОМУ СПОСОБУ, И СПОСОБ ОКИСЛИТЕЛЬНОЙ КОНДЕНСАЦИИ МЕТАНА С ИСПОЛЬЗОВАНИЕМ ПОЛУЧЕННОГО КАТАЛИЗАТОРА | 2013 |
|
RU2515497C1 |
| СПОСОБ ДОБЫЧИ ПРИРОДНОГО ГАЗА ИЗ ГАЗОВЫХ ГИДРАТОВ | 2000 |
|
RU2169834C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА, КАТАЛИЗАТОР, ПРИГОТОВЛЕННЫЙ ПО ЭТОМУ СПОСОБУ, И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА С ЕГО ИСПОЛЬЗОВАНИЕМ | 2012 |
|
RU2491118C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2010 |
|
RU2429072C1 |
Изобретение относится к катализатору получения синтез-газа в процессе парциального окисления метана, представляющему собой микросферический носитель с нанесенным активным компонентом на основе оксидов металлов, при этом в качестве микросферического носителя используют частицы диаметром от 50 до 160 мкм оксида алюминия и/или алюмосиликата, а в качестве активного компонента - оксид Со или Ni, или Fe, или Mn, или Cu, или Се, или смесь оксидов NiO, Co3O4 и Се2О3, при следующем соотношении компонентов, мас.%: указанный активный компонент - 2-40, оксид алюминия и/или алюмосиликат - остальное. Изобретение также относится к способу получения катализатора и к способу получения синтез-газа в присутствии заявленного катализатора. Технический результат - повышение удельного съема продукта, исключение опасности взрыва и возгорания, низкие энергозатраты, получение синтез-газа с отношением Н2/СО в пределах 1,5-2,5, возможность получения побочного продукта - технического азота при высоких значениях конверсии метансодержащего сырья. 3 н. и 4 з.п. ф-лы, 3 табл., 13 пр.
1. Катализатор получения синтез-газа в процессе парциального окисления метана, представляющий собой микросферический носитель с нанесенным активным компонентом на основе оксидов металлов, отличающийся тем, что в качестве микросферического носителя используют частицы диаметром от 50 до 160 мкм оксида алюминия и/или алюмосиликата, а в качестве активного компонента - оксид Со или Ni, или Fe, или Mn, или Cu, или Се, или смесь оксидов NiO, Co3O4 и Се2О3, при следующем соотношении компонентов, % мас:
2. Способ получения катализатора по п. 1, включающий нанесение предшественника активного компонента - растворов солей указанных металлов - на микросферический носитель - оксид алюминия и/или алюмосиликат с диаметром частиц от 50 до 160 мкм путем пропитки по влагопоглощению, сушку при температуре от 90 до 120°C в течение 1-5 часов и прокаливание при температуре от 500 до 1200°C в течение 2-8 часов.
3. Способ получения синтез-газа, включающий окислительную конверсию метансодержащего газа при температуре более 750°C в реакторе с использованием в качестве окислителя катализатора - микросферического носителя с нанесенным активным компонентом на основе оксидов металлов - и регенерацию восстановленного катализатора путем его окисления в регенераторе, из которого регенерированный катализатор поступает в реактор, отличающийся тем, что используют катализатор по п. 1, окислительную конверсию проводят в сквознопоточном лифт-реакторе, через который катализатор непрерывно проходит снизу вверх в потоке метансодержащего газа при времени пребывания сырья в зоне реакции 0,1-10 с, затем выходящий из реактора восстановленный катализатор отделяют от продукта - синтез-газа - и направляют в регенератор.
4. Способ по п. 3, отличающийся тем, что окислительную конверсию проводят при температуре от более 750 до 1100°C.
5. Способ по п. 4, отличающийся тем, что окислительную конверсию проводят при температуре 850°C.
6. Способ по одному из пп. 3-5, отличающийся тем, что регенерацию катализатора проводят в псевдоожиженном, или форсированном псевдоожиженном, или полусквозном потоке путем его окисления кислородсодержащим агентом.
7. Способ по п. 6, отличающийся тем, что в качестве кислородсодержащего агента используют кислород или воздух.
| US 5780381 A, 14.07.1998 | |||
| КАТАЛИЗАТОР ДЛЯ ОКСИХЛОРИРОВАНИЯ ЭТИЛЕНА В 1,2-ДИХЛОРЭТАН И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2000 |
|
RU2183987C1 |
| US 0006833013 B1, 21.12.2004 | |||
| КАТАЛИЗАТОР (ЕГО ВАРИАНТЫ) И ПРОЦЕСС ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 1997 |
|
RU2144844C1 |
Авторы
Даты
2015-04-10—Публикация
2013-09-06—Подача