ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретению относится к новым агентам, фармацевтическим композициям и их применению в терапии, в частности в любой терапии, где желательно или выгодно уменьшать или предупреждать пролиферацию или рост клеток, например в лечении гиперпролиферативных заболеваний или фактически любого состояния, которое нуждается в цитостатической терапии или восприимчиво к ней. Изобретение основано на установлении новых взаимодействий между ядерным антигеном пролиферирующих клеток (PCNA) и различными белками, вовлеченными в репарацию ДНК, поддержании и регуляции клеточного цикла и последующей идентификации нового пентапептидного мотива, отвечающего за такие взаимодействия, который авторы изобретения назвали APIM. Таким образом, настоящее изобретение в частности относится к пептидам или их миметикам, содержащим такой мотив и способным взаимодействовать с PCNA, к фармацевтическим композициям, содержащим такие агенты, и к применению таких агентов в терапии, в частности в терапиях, включающих уменьшение или предупреждение клеточной пролиферации, как указано выше. Также предложены терапевтические способы, которые включают использование агента, содержащего мотив, связывающий PCNA, предпочтительно в комбинации с цитостатическим агентом.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Человеческие и животные клетки подвергаются воздействию ряда факторов, вызывающих повреждение ДНК, таких как активные формы кислорода, ультрафиолетовое излучение, рентгеновские лучи и эндогенные или экзогенные цитостатические агенты.
Цитостатические агенты представляют собой агенты, которые подавляют или замедляют клеточный рост и/или размножение (пролиферацию/репликацию), например путем повреждения ДНК или воздействуя на механизм клеточный репликации. Алкилирующие агенты представляют собой класс цитостатических агентов, некоторые из которых используют клинически или в исследовательских целях.
Алкилирующие агенты вызывают повреждения ДНК, модифицируя основания по атомам N или О. Тип повреждения зависит от типа агента, большинство агентов вызывают конкретную модификацию ДНК. Повреждения ДНК включают аддукты алкилирования и межнитевые сшивки, которые могут приводить к неправильному кодированию во время репликации и/или к блокировкам репликации с последующими двухнитевыми разрывами или транслезионным синтезом.
Человеческие и животные клетки имеют различные системы репарации ДНК, включая эксцизионную репарацию оснований, эксцизионную репарацию нуклеотидов и репарацию ошибочно спаренных нуклеотидов. Примером является окислительная ДНК-деметилаза человека, hABH2, которая превращает 3-метилцитозин (3meC) обратно в цитозин и 1-метиладенин (1meA) в аденин посредством окислительного деметилирования.
Тесная координация между репарацией ДНК и репликацией ДНК, регулируемой клеточным циклом, имеет большое значение для целостности генома. Важно, чтобы при наличии повреждения репликация ДНК прекращалась до исправления повреждения, в противном случае возникают и воспроизводятся мутации. Известен один белок, включенный как в репликацию ДНК, так и в репарацию ДНК представляющий собой ядерный антиген пролиферирующих клеток (PCNA).
PCNA является членом семейства белков скользящего захвата, которые функционально сохраняются от бактерий до высших эукариот, и основная функция которых состоит в предложении репликационных полимераз с высокой процессивностью, необходимой для копирования генома. В живых клетках S-фазы PCNA, меченный зеленым флуоресцентным белком (GFP), образует отчетливые фокусы, представляющие сайты репликации. Таким образом, его можно использовать как маркер S-фазы.
Многочисленные белки, вовлеченные в клеточные процессы, такие как репарация ДНК, сборка хроматина, эпигенетическое и хроматиновое ремоделирование, когезия сестринских хроматид, контроль клеточного цикла и выживаемость, локализованы в так называемых репликационных зонах, которые содержат более дюжины репликационных вилок. Многие из этих белков взаимодействуют с PCNA посредством консервативной пептидной последовательности, взаимодействующей с PCNA, называемой PIP-бокс (QxxL/I/MxxF/DF/Y), где х может представлять собой любую аминокислоту. Альтернативный мотив, связывающий PCNA, называемый КАх-бокс, идентифицировали, используя библиотеку пептидного дисплея, но важность данного мотива для взаимодействий с PCNA in vivo не была подтверждена.
Различные белки взаимодействуют с PCNA, и было доказано, что некоторые из данных белков, включая hABH2, локализованы вместе с PCNA в фокусах репликации. Однако совместная локализация сама по себе не означает, что между совместно локализованными белками происходит какое-либо прямое или непрямое взаимодействие. Действительно, отсутствие в hABH2 PCNA-связывающего мотива, такого как PIP-бокс или КАх бокс, предполагает, что hABH2 не взаимодействует с PCNA.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В работе, приводящей к настоящему изобретению, авторы изобретения неожиданно обнаружили, что различные белки взаимодействуют с PCNA посредством нового мотива, взаимодействующего с PCNA. В одном из таких белков, hABH2, данный мотив расположен на N-конце. Авторы изобретения установили, что данный мотив является и необходимым и достаточным для взаимодействия с PCNA (смотри Пример 1).
В Примерах ниже подробно объясняется, что для изучения функции данного мотива, взаимодействующего с PCNA, в репарации ДНК при повреждении алкилированием клеточные линии, экспрессирующие рекомбинантный пептид, содержащий этот мотив, подвергали воздействию различных доз MMS (метилметансульфоната), который представляет собой алкилирующий агент SN2, вызывающий образование 3-метилцитозина и 1-метиладенина. Было обнаружено, что экспрессия рекомбинантного пептида, содержащего мотив, повышала чувствительность клеток к повреждению ДНК, вызванному MMS, указывая на то, что рекомбинантный пептид, содержащий мотив, конкурентно ингибировал взаимодействие между PCNA и hABH2.
Также тестировали другие агенты, включающие BCNU (бис-этилхлорнитрозомочевина), темозоломид (TZM) и митомицин С (ММС), которые вызывают другие виды повреждения ДНК, и к своему большому удивлению, авторы изобретения обнаружили, что рекомбинантный пептид, содержащий мотив, также повышал чувствительность клеток к повреждениям, вызванным такими агентами. Это было совершенно неожиданно, так как BCNU представляет собой О6-хлорэтилирующий агент, который главным образом приводит к межнитевым поперечным связям, а также к некоторым одноосновным циклическим аддуктам (1,N(6)этаноаденин), сообщается, что TZM является O6G-метилирующим агентом, и ММС вызывает образование межнитевых поперечных связей посредством N-алкилирования гуанина в CpGs, и hABH2 не исправляет такие типы повреждения ДНК. Альтернативно, существуют другие ферменты, которые исправляют данный вид повреждения, например повреждения посредством TZM исправляют непосредственно O-метилгуанин-ДНК-трансферазой (MGMT). Полученные данные показывают, что рекомбинантный пептид, содержащий этот мотив, не только ингибирует взаимодействие между hABH2 и PCNA, и что могут быть вовлечены другие белки, то есть другие белки могут взаимодействовать с PCNA посредством нового мотива.
Авторы изобретения также обнаружили, что экспрессия рекомбинантного пептида, содержащего мотив, увеличивала цитотоксический эффект цитостатических агентов (особенно MMS) выше наблюдаемого в клеточных линиях от нокаутных мышей АВН2, то есть мышей, которые не имеют АВН2, это также указывало на то, что рекомбинантный пептид, содержащий мотив, имеет расширенный эффект, и возможно ингибирует другие белки в дополнение к hABH2.
Такие неожиданные данные позволили авторам изобретения предложить терапевтическое применение пептида, содержащего мотив, связывающий PCNA.
Новый PCNA-связывающий мотив по изобретению, названный APIM, был охарактеризован и может быть определен следующим образом:
X1X2X3X3'X1' (SEQ ID NO:1),
где X1 и Х1' независимо выбран из группы основных аминокислот, Х2 представляет собой липофильную аминокислоту, и Х3 и Х3' - независимо выбраны из группы незаряженных, предпочтительно неполярных аминокислот.
Пептид (или олигопептидное соединение), способный взаимодействовать с PCNA, может включать или содержать такой мотив пептида (или последовательности). Таким образом, олигопептидное соединение, способное взаимодействовать с PCNA и содержащее такой мотив, раскрыто в данном описании изобретения, и может представлять собой некоторые аспекты настоящего изобретения.
Например, в одном воплощении настоящего изобретения могут быть предложено олигопептидное соединение, которое способно к взаимодействию с PCNA, и которое содержит мотив X1X2X3X3'X1' (SEQ ID NO:1), где X1 и X1' независимо выбраны из группы основных аминокислот, Х3 представляет собой липофильную аминокислоту, и Х3 и Х3' - независимо выбраны из группы незаряженных, предпочтительно неполярных аминокислот, где олигопептидное соединение дополнительно отличается по меньшей мере одним из следующих:
(1) олигопептидное соединение содержит по меньшей мере 11 аминокислот или эквивалентных субъединиц;
(2) Х2 не является фенилаланином;
(3) олигопептидное соединение содержит по меньшей мере одну D-аминокислоту;
(4) олигопептидное соединение содержит по меньшей мере одну сигнальную последовательность, а именно последовательность, которая направляет олигопептидное соединение в конкретное место, например в клетку (например последовательность для проникновения в клетку, которая направляет олигопептидное соединение в клетку) и/или в особый клеточный компартмент (например сигнал ядерной локализации, который направляет олигопептидное соединение в ядро); и
(5) олигопептидное соединение содержит мотив [K/R]-F-[L/I/V]-[L/I/V]-[K/R] (SEQ ID NO:27).
В частности, в таком воплощении олигопептидное соединение содержит сигнальную последовательность ядерной локализации. В другом воплощении олигопептидное соединение содержит последовательность для проникновения в клетку (пептид проникновения в клетку). В еще одном воплощении олигопептидное соединение содержит последовательность проникновения в клетку и последовательность ядерной локализации.
Таким образом, можно видеть, что в таких воплощениях соединение по изобретение может принимать форму конструкции, содержащей (то есть включающей) олигопептидное соединение, которое содержит мотив, взаимодействующий с PCNA, как определено выше, вместе по меньшей мере с одной сигнальной последовательностью. В этом аспекте изобретение можно, таким образом, рассматривать как предложение конструкции, содержащей олигопептидное соединение, которое способно взаимодействовать с PCNA, и которое содержит мотив X1X2X3X3'X1' (SEQ ID NO:1), где X1 и Х1' независимо выбраны из группы основных аминокислот, Х2 представляет собой липофильную аминокислоту, и Х3 и Х3' независимо выбраны из группы незаряженных, предпочтительно неполярных аминокислот, вместе по меньшей мере с одной сигнальной последовательностью.
Как указано выше, было определено, что новый мотив по изобретению опосредует взаимодействие олигопептидного соединения (например пептида) или белка, содержащего такой мотив, с PCNA.
Взаимодействие может быть прямым или опосредованным, и может включать непосредственное связывание мотива с PCNA, или мотив может связываться опосредованно, например связывание может быть опосредовано другой молекулой. Указанная ссылка на «PCNA-взаимодействие» или «PCNA-связывание» может, таким образом, включать любую форму взаимодействия и как прямое, так и опосредованное связывание.
Любую ссылку в данном описании изобретения на «мотив» следует понимать как означающую Х1Х2Х3Х3'Х1', как определено в данном описании изобретения.
Предпочтительно, X1 и Х1' независимо выбраны из лизина (К), аргинина (R), гистидина (И), орнитина (Om), метиллизина (МеК) и ацетиллизина (АсК), и более предпочтительно К, R и Н, или К и R;
Х2 предпочтительно представляет собой ароматическую аминокислоту, более предпочтительно он выбран из фенилаланина (F), триптофана (W), тирозина (Y), трет-бутилглицина, циклогексилаланина, трет-бутилфенилаланина, бифенилаланина и три-трет-бутилтриптофана (в некоторых воплощениях этот перечень может исключать F), в частности F, W и Y, или W и Y, F и Y, или F и W, или в конкретных воплощениях Х2 может представлять собой F, или W, или Y;
Х3 и Х3' - предпочтительно представляют собой алифатические аминокислоты и могут, например, быть независимо выбраны из лейцина (L), изолейцина (I), валина (V), аланина (А) метионина (М) и норлейцина (Nor);
Предпочтительно, Х3 и Х3' не являются оба А, более предпочтительно Х3 и Х3' - выбраны из L, I, V и М, еще более предпочтительно из L, I и V.
Связывание мотива с PCNA может быть улучшено в некоторых воплощениях, когда Х2 представляет собой W или Y. Таким образом, в одном воплощении X2 не является F. Однако, как отмечено выше, в других воплощениях он может представлять собой F.
Таким образом, в изобретении может быть предложено олигопептидное соединение, содержащее мотив [K/R]-[F/Y/W]-[L/I/V/AM]-[L/I/V/A/M]-[K/R] (SEQ ID NO:28), где указанное олигопептидное соединение способно взаимодействовать с PCNA.
В другом воплощении мотив может быть определен как: [K/R]-[Y/W]-[L/I/V/A/M]-[L/I/V/A/M]-[K/R] (SEQ ID NO:29).
В другом воплощении мотив может быть определен как: [K/R]-[F/Y/W]-[L/I/V/A]-[L/I/V/A]-[K/R] (SEQ ID NO:30).
В другом воплощении мотив может быть определен как: [K/R]-[Y/W]-[L/I/V/A]-[L/I/V/A]-[K/R] (SEQ ID NO:31).
В другом воплощении мотив может быть определен как: [K/R]-[F/W]-[L/I/V/A/M]-[L/I/V/A/M]-[K/R] (SEQ ID NO:32).
В другом воплощении мотив может быть определен как: [K/R]-[F/W]-[L/I/V/A]-[L/I/V/A]-[K/R] (SEQ ID NO:33).
В другом воплощении мотив может быть определен как: [K/R]-[F/W]-[L/I/V]-[L/I/V]-[KR] (SEQ ID NO:34).
В другом воплощении мотив может быть определен как: [K/R]-[F/Y/W]-[L/I/V]-[L/I/V]-[K/R] (SEQ ID NO:35).
В еще одном воплощении мотив может быть определен как: [K/R]-[Y/W]-[L/I/V]-[L/I/V]-[K/R] (SEQ ID NO:36).
В еще одном воплощении мотив может быть определен как: [K/R]-F-[L/I/V]- [L/I/V]-[K/R] (SEQ ID NO:37).
Олигопептидное соединение предпочтительно представляет собой выделенное соединение.
В предпочтительном воплощении олигопептидное соединение имеет или содержит последовательность RFLVK (SEQ ID NO:2). В других предпочтительных воплощениях олигопептидное соединение имеет или содержит последовательность, выбранную из KFLLR (SEQ ID NO:3), KYLLR (SEQ ID NO: 4), KWLLR(SEQ ID NO: 5), KYILR (SEQ ID NO: 6), KYVLR (SEQ ID NO: 7), RFLLR (SEQ ID NO: 8), RYLLR (SEQ ID NO: 9), RWLLR (SEQ ID NO: 10), RYILR (SEQ ID NO: 11), RYVLR (SEQ ID NO: 12), RFLIR (SEQ ID NO: 13), RYLVR (SEQ ID NO: 14) RWLMR (SEQ ID NO: 15), RYVLR (SEQ ID NO: 16), RYVIR (SEQ ID NO: 17), RWLVK (SEQ ID NO: 18), RYLVK (SEQ ID NO: 19), RWLIK (SEQ ID NO: 20), RWIVK (SEQ ID NO: 21), RWVVK (SEQ ID NO: 22), RWAVK (SEQ ID NO: 23), RYVVK (SEQ ID NO: 24), RYLIK (SEQ ID NO: 25) или RYLMK (SEQ ID NO: 26). Эти конкретные последовательности перечислены в качестве примера, и их не предназначают для ограничения объема настоящего изобретения.
В одном предпочтительном воплощении олигопептидное соединение по изобретению также содержит сигнальную последовательность, которая нацеливает мотив на конкретный тип клеток, облегчает проникновение соединения в клетку, и/или локализует соединение в конкретном внутриклеточном компартменте, предпочтительно ядре.
Таким образом, сигнальную последовательность можно рассматривать как любую последовательности, которая влияет на локализацию, или иначе говоря, на направление, транслокацию или транспорт олигопептидного соединения в любое желательное положение, например в любое желательное клеточное или субклеточное положение. В предпочтительных воплощениях желательное положение представляет собой клетку (то есть внутреннее пространство клетки) и/или ядро клетки.
Таким образом, сигнальная последовательность может представлять собой последовательность, которая влияет на транспорт олигопептидного соединения в клетку, или через клеточную мембрану (то есть внутрь клетки). Это может быть, таким образом, так называемая последовательность «проникновения в клетку» (или более конкретно «пептид проникновения в клетку»), также известная в данной области техники как домен белковой трансдукции (PTD) или последовательность белковой трансдукции.
Таким образом, как указано выше, предпочтительное воплощение изобретения представляет собой конструкцию, содержащую (1) олигопептидное соединение, содержащее мотив APIM (то есть PCNA-взаимодействующий мотив), как определено в данном описании изобретения, и (2) последовательность проникновения в клетку (более конкретно пептид проникновения в клетку).
Технология пептидного проникновения в клетку (СРР) в последние годы развивалась в значительной степени, и известен большое множество пептидов проникновения в клетку, описанных в данной области техники, и конечно, ряд таких пептидов имеется в продаже. Пептиды проникновения в клетку могут широко варьироваться по размеру, последовательности и заряду, и конечно по механизму их действия (который в настоящее время неизвестен для некоторых пептидов и не полностью выяснен для других), но разделяют общую способность перемещаться через плазменную мембрану и доставлять прикрепленную или ассоциированную группировку (так называемый «груз») в цитоплазму, или даже в некоторых случаях в ядро, клетки. СРР представляют собой, таким образом, пептидные векторы доставки.
СРР могут быть произведены из имеющихся в природе белков, которые способны перемещаться через клеточные мембраны, такие как гомеобоксный белок антеннапедия Drosophila (транскрипционный фактор), вирусные белки, такие как HIV-1 (вирус иммунодефицита человека - 1), транскрипционный фактор ТАТ и капсидный белок VP22 из HSV-I (вирус простого герпеса - 1), и/или они могут быть произведены синтетически, например из химерных белков или синтетических полипептидов, таких как полиаргинин. Как указано выше, не существует одного механизма, отвечающего за эффект трансдукции, и, следовательно, конструирование СРР может быть основано на разных структурах и последовательностях. Пептиды проникновения в клетку рассмотрены в Jarver et al. 2006 Biochimica et Biophysica Acta 1758, pages 260-263, и в Таблице 2 ниже перечислены различные типичные пептиды. В US 6645501 дополнительно описаны различные пептиды проникновения в клетку, которые можно использовать.
СРР, произведенные от Антеннапедия (класс Antp), являются особенно интересным классом, основанным приблизительно на 16 аминокислотах последовательности пенетратина, как показано в Таблице 2, которые соответствуют третьей петле белка антеннапедия, и, как было показано, отвечают за транслокацию белка. Пенетратин активно разрабатывали в качестве носителя, включая в частности фармацевтическое использование, и был предложен и описан широкий ассортимент производных пенетратина и модифицированных последовательностей. Можно сделать ссылку в частности на WO 91/1891, WO 00/1417, WO 00/29427, WO 2004/069279 и US 6080724. Таким образом, 16-аминокислотная последовательность Пенетратина может быть модифицирована и/или укорочена, или пептид может быть химически модифицированным или могут быть получены ретро-, инверсные- или ретро-инверсные аналоги, все еще сохраняющие активность проникновения в клетку.
Другая группа пептидов проникновения в клетку, которые можно успешно использовать, основаны на последовательности HIV-TAT, и HIV-TAT и ее фрагменты представляют собой предпочтительный класс СРР для применения согласно настоящему изобретению. Различные СРР на основе ТАТ описаны в US 5656122. Типичный пептид HIV-TAT, который используют в Примерах ниже, представляет собой RKKRRQRRR (SEQ ID NO:71), но как нетрудно понять, можно использовать более длинные или более короткие фрагменты ТАТ.
Как упоминается выше, отсутствуют конкретные структурные признаки или мотивы последовательности, которые являются общими для всех СРР. Однако разные классы СРР можно идентифицировать по конкретным признакам, таким как, например, пептиды, которые являются амфипатическими и имеют положительный результирующий заряд. Другие группы СРР могут иметь структуру с высоким содержанием α-спиралей. Другая группа может представлять собой пептиды, отличающиеся высоким содержанием основных аминокислот. СРР могут, таким образом, представлять собой или могут содержать олигомеры основных аминокислот, таких как аргинин, например от 5 до 20, от 6 до 15 или от 6 до 12 R-остатков, например R7 (SEQ ID NO:70), R8 (SEQ ID NO:72), или R11 (SEQ ID NO:73), или QSR8 (SEQ ID NO:74).
Богатые пролином амфипатические пептиды являются еще одним классом СРР, и такие пептиды, отличающиеся присутствием пирролидиновых колец из пролинов, описаны в Pujals et al. 2008 Advanced Drug Delivery Reviews 60, pages 473-484.
Другие успешно разработанные СРР включают pVEC (Elmquist et al. 2003 Biol. Chem 384, pages 387-393; Holm et al. 2005 Febs Lett. 579, pages 5217-5222) и пептиды, произведенные из кальцитонина (Krauss et al. 2Q04 Bioorg. Med. Chem. Lett., 14, pages 51-54).
Имеющиеся в продаже СРР включают Chariot на основе пептида Рер-1 (Active Motif, France), векторы Syn-B на основе пептида протегрина PG-1 (Syntem, France) и Express-si Delivery на основе пептида MPG от Genospectra, USA.
В дополнение к общедоступным и описанным СРР, могут быть спроектированы и синтезированы новые пептиды или производные СРР на основе известных или описанных критериев (например известных последовательностей или признаков СРР, таких как содержание основных аминокислот, содержание α-спиралей и так далее, как обсуждалось выше). Кроме того, случайно сконструированные или другие пептиды могут быть подвергнуты скринингу на активность СРР, например путем присоединения или прикрепления такого пептида, содержащего репортерную молекулу, например определяемую метку или маркер, такую как флуоресцентную метку, к требуемому грузу (олигопептидному соединению по настоящему изобретению) и тестирования, чтобы убедиться в перемещении этой конструкции через клеточную мембрану, например путем добавления таких пептидов к живым клеткам с последующим изучением клеточного импорта, например с использованием конфокальной микроскопии.
Действительно, в то время как обычно СРР будет проникать или входить в практически любой тип клеток, в некоторых случаях можно наблюдать, что успешная или эффективная доставка может зависеть, или может варьироваться в зависимости от точной природы груза (например пептидной последовательности груза) и/или используемого СРР. В рамках обычной квалификации специалиста в данной области техники определить оптимальные пептидные последовательностями и комбинации и так далее, и протестировать и/или модифицировать груз и/или последовательность СРР или структуру и так далее.
Как упоминалось выше, сигнальная последовательность, которая может содержаться в олигопептидных соединениях (или конструкциях) по изобретению, может представлять собой сигнальный пептид, который направляет соединение (или конструкцию) в конкретный субклеточный компартмент, и в частности ядро. Сигналы ядерной локализации (NLS) также хорошо известны в данной области техники и широко описаны в литературе, и можно использовать любой известный или функциональный NLS.
Таким образом, еще одним предпочтительным воплощением изобретения является конструкция, содержащая (1) олигопептидное соединение, содержащее мотив APIM (то есть мотив, взаимодействующий с PCNA), как определено в данном описании изобретения, и (2) сигнал ядерной локализации.
NLS может варьироваться по длине и/или последовательности и был описан широкий ряд конкретных последовательностей NLS. В общем случае, однако, было обнаружено, что пептиды, содержащие положительно заряженные аминокислоты (в частности лизин (К), аргинин (R) и/или гистидин (Н)) могут функционировать в качестве NLS. Типичный NLS может, таким образом, представлять собой пептид, например из 4-20, более конкретно из 4-15, 4-12, 4-10 или 4-8 аминокислот, где по меньшей мере 4 аминокислоты (и более конкретно по меньшей мере 60, 70, 75, 80, 85 или 90% аминокислотных остатков в пептиде NLS) представляют собой положительно заряженные аминокислоты, предпочтительно выбранные из К, R или Н. Такой типичный NLS может, например, иметь или содержать последовательность RKRH (SEQ ID NO:75).
Сигналы ядерной локализации, включая как реальные экспериментально определенные, так и спрогнозированные или предложенные последовательности NLS, и стратегии идентификации NLS, описаны в Lange et a.l, J. Biol. Chem. 2007, 282 (8), 5101-5105 ; Makkerh et al., Current Biology 1996, 6 (8), 1025-1027; Leslie et al., Methods 2006, 39, 291-308; и Lusk et al. Nature Reviews MCB 2007, 8, 414-420.
Классический NLS состоит либо из одного (одинарный), либо из двух (двойной) участков основных аминокислот. Примером одинарного NLS может быть SV40 большой Т-антиген NLS (126PKKKRKV132 [SEQ ID NO:76]) и двойного - нуклеонеоплазмин NLS (155KRPAATKKAGOAKKKK170 [SEQ ID NO:77]). Была предложена консенсусная последовательность одинарного NLS K-[K/R]-X-[K/R] (SEQ ID NO:78), и, таким образом, NLS по настоящему изобретению может в одном воплощении содержать или состоять из такой консенсусной последовательность (где Х представляет собой любую аминокислоту).
Типичный двойной NLS по изобретению может иметь последовательность KR-[X]5-20-KKKK (SEQ ID NO:79), например KR-Х10-КККК (SEQ ID NO:80) (где Х представляет собой любую аминокислоту).
Альтернативный типичный двойной NLS может принимать форму RKRH-[Х]2-10-КК (SEQ ID NO:81), например RKRH-X2-KK (SEQ ID NO:82), например RKRH-II-KK (SEQ ID NO:83).
NLS онкобелка c-myc отличается от классических NLS тем, что только 3 из 9 аминокислотных остатков являются основными (PAAKRVKLD [SEQ ID NO:84]), указывая на то, что NLS не обязательно соответствует консенсусным или классическим последовательностям, приведенным выше. Makkerh et al. (выше) описывает последовательности NLS, в которых кластер основных аминокислот (например КККК [SEQ ID NO:85]) фланкирован нейтральными и кислыми остатками, например PAAKKKKLD (SEQ ID NO:86).
Другие возможные последовательности NLS, которые могут быть приведены в качестве примера, включают: PKKKRKVL (SEQ ID NO:87), KKKRK (SEQ ID NO:88), KKKRVK (SEQ ID NO:89), KKKRKVL (SEQ ID NO:90) и RKKRKVL (SEQ ID NO:91). Можно использовать любой NLS, который является производным известного NLS, например NLS для SV40, нуклеоплазмина, UNG2 или c-myc NLS.
Предполагаемую, предложенную или прогнозируемую последовательность NLS можно протестировать на активность NLS, используя принципы и анализы, известные и описанные в данной области техники. Например, кандидатную последовательность NLS можно прикреплять к желательному «грузу» (в данном случае олигопептиду по изобретению, как определено в данном описании изобретения), и конструкцию можно снабдить определяемой репортерной молекулой (например меткой или маркером, который можно визуализировать, например флуоресцентной меткой) и приводить в контакт с тестируемой клеткой. Затем можно определять распределение конструкции в клетке.
Таким образом, в качестве обобщения, специалист осведомлен о подходящих сигнальных последовательностях, но в качестве примера в данном описании изобретения упоминается следующее. Примеры пептидных последовательностей проникновения в клетку включают Пенетратин™, 16-аминокислотный пептид, соответствующий третьей спирали гомеодомена белка Антеннапедия, R-обогащенные метки, такие как Рб-Пенетратин (где остатки аргинина добавлены к N-концу Пенетратина) и производные белка HIV Tat, такие как GRKKRRQRRRPPQQ (SEQ ID NO:92). Примеры последовательностей ядерной локализации включают производное белка SV40 KKKRK (SEQ ID NO:93).
Предпочтительная конструкция по настоящему изобретению содержит (1) олигопептидное соединение, содержащее мотив APIM, как определено в данном описании изобретения, (2) сигнал ядерной локализации и (3) сигнальную последовательность проникновения в клетку.
Отдельные элементы или компоненты конструкции по настоящему изобретению могут содержаться или присутствовать в любом порядке, но предпочтительно в порядках, указных выше (например олигопептидное соединение APIM-CPP; олигопептидное соединение APIM-NLS; олигопептидное соединение APIM-NLS-CPP).
Кроме того, олигопептидное соединение или конструкция по изобретению может содержать более одного мотива, взаимодействующего с PCNA. Таким образом, альтернативно выражаясь, конструкция по настоящему изобретению может содержать более одного олигопептидного соединения, содержащего мотив, взаимодействующий с PCNA. Конструкция или олигопептидное соединение может, например, содержать, 1-10, например 1-6, или 1-4, или 1-3, или один или два мотива. В конструкции, также содержащей сигнальную последовательность, такие мотивы могут быть расположены или помещены по желанию, например они могут быть сгруппированы вместе, или они могут быть разделены элементами сигнальной последовательности, например мотив-NLS-мотив-СРР; или мотив-NLS-мотив-мотив-СРР; или мотив-мотив-NLS-CPP и так далее.
Компоненты или элементы конструкции по изобретению могут быть прикреплены или связаны друг с другом любым желательным или удобным путем методами, хорошо известными в данной области техники. Таким образом, компоненты или отдельные части могут быть связаны или конъюгированы химически, например с использованием известных методов химического связывания, или эти конструкции могут быть образованы в виде единого целого, с использованием методов генной инженерии, например способов образования слитых белков, или они могут быть просто синтезированы в виде целого, например с использованием методов синтеза пептидов.
Отдельные части или компоненты можно связывать непосредственно друг с другом, или их можно связывать опосредованно при помощи одной или более линкерных (или спейсерных) последовательностей. Таким образом, линкерная последовательность может заполнять промежутки или разделять две или более отдельные части конструкцию или разделять элементы мотива в олигопептидной конструкции. Точная природа линкерной последовательности не является критической, и она может иметь разную длину и/или последовательность, например она может иметь 0-40, более конкретно 0-20, 0-15, 0-12, 0-10, 0-8 или 0-6, 0-4 или 0-3 остатков, например 1, 2 или З или более остатка. В качестве типичного примера линкерная последовательность, если она присутствует, может иметь 1-15, 1-12, 1-10, 1-8, 1-6 или 1-4 остатка и так далее. Природа остатков не является критической, и они могут, например, представлять собой любую аминокислоту, например нейтральную аминокислоту, или алифатическую аминокислоту, или, альтернативно, они могут быть гидрофобными, или полярными, или заряженными, или структурообразующими, например пролином. Был показано, что применим ряд разных линкерных последовательностей, включая короткие (например 1-6) последовательности нейтральных и/или алифатических аминокислот.
Типичные линкерные последовательности, таким образом, включают любой единственный аминокислотный остаток, например A, I, L, V, G, R, Q, Т или W, или ди-, три-, тетра-, пента- или гексапептид, состоящий из таких остатков.
В качестве типичных линкеров можно упомянуть I, II, IL, R, W, WW, WWW, RIL, RIW, GAQ, GAW, VAT, IILVI (SEQ ID NO:94), IILVIII (SEQ ID NO:95) и так далее.
Линкеры между различными элементами могут быть одинаковыми или разными.
В одном воплощении предлагается олигопептидное соединение, имеющее или содержащее последовательность MDRWLVKRILVATK (SEQ ID N0: 96) или MDRWLVKRILKKKRKVATKG (SEQ ID NO:97).
Другие типичные соединения (или более конкретно конструкции) по изобретению включают
MDRWLVKGAQPKKKRKVLRQIKIWFQNRRMKWKK (SEQ ID NO:98),
MDRWLVKGAWKKKRVKIIRKKRRQRRRK (SEQ ID NO:99),
MDRWLVKGAWKKKRKIIRKKRRQRRRG (SEQ ID NO:100),
MDRWLVKGAWKKKRKIIRKKRRQRRRK (SEQ ID NO:101),
MDRWLVKJUWKKKRKIIRKKRRQRRRK (SEQ ID NO:102),
MDRWLVKWWWKKKRKIIRKKRRQRRRK (SEQ ID NO:103),
MDRWLVKWWRKRHIIKKRKKRRQRRRK (SEQ ID NO:104),
MDRWLVKillWKKKRKIIRRRRRRRRRRRK (SEQ ID NO:105),
MDRWLVKJirWKKKRKIIRQIKIWFQNRRMKWKK(SEQ ID NO:106),
MDRFLVKGAWRKRHIIKKRKKRRQRRRK (SEQ ID NO:107),
MDRWLVKWKKKRKIRRRRRRRRRRRK (SEQ ID NO:108),
MDRWLVKWKKKRKIRKKRRQRRRK (SEQ ID NO:109),
MDRWLVKWRKRHIRKKRRQRRRK (SEQ ID NO:110),
Ac-MDRWLVKGAWRKRHIRKKRRQRRRK (SEQ ID NO:111),
Ac-MDRWLVKWKKKRKIRRRRRRRRRRR (SEQ ID NO:112),
Ac-MDRALVKWKKKRKIRRRRRRRRRRR (SEQ ID NO; 113),
Ac-MDRWLVKKKKRKRRRRRRRRRRRK (SEQ ID NO:114),
Ac-MDRWLVKKKKRKRRRRRRRRRRR (SEQ ID NO:115),
MDRWLVKRIWKKKRKIIRWLVKWWWRKKRRQRRRK (SEQ ID NO:116),
KRRRQRRKKRIIKRKKKWWWKVLWRDM (SEQ ID NO:117).
Олигопептидные соединения, имеющие последовательности, как представлено в SEQ ID NO:98-117, показаны в Таблице 3 в Примере 6 ниже, которая показывает отдельные компоненты, составляющие конструкции (то есть мотив-содержащая последовательность, линкер, NLS, СРР и так далее) Таким образом, можно видеть, что SEQ ID NO:98-117 представляют собой конструкции, содержащие по меньшей мере одну мотив-содержащую последовательность, NLS и СРР, в некоторых случаях связанные линкерными последовательностями, которые могут варьироваться в последовательности, как указано. SEQ ID NO:117 (RI-MDR26-3) представляет собой ретро-инверсный пептид, состоящий из D-аминокислот. Используют NLS-последовательности на основе SV40 или UNG2 NLS-последовательности, и СРР-последовательности на основе Пенетратина, HIV-TAT или R-обогащенного пептида.
В еще одном аспекте изобретения предлагается молекула нуклеиновой кислоты, кодирующая пептид, имеющий или содержащий (например) SEQ ID NO:1, как определено выше. Также предлагается комплемент такой молекулы нуклеиновой кислоты. Предпочтительно молекула нуклеиновой кислоты содержит промоторную последовательность, функционально связанную с последовательностью, кодирующей пептид, имеющий или содержащий (например) SEQ ID NO:1. В предпочтительном воплощении молекула нуклеиновой кислоты также кодирует сигнальную последовательность, как определено выше.
Молекула нуклеиновой кислоты по изобретению содержит по меньшей мере 15 нуклеотидов и предпочтительно по более 800 нуклеотидов, более предпочтительно не более 700, 650, 600, 550, 500, 450, 400, 350, 300, 250, 200, 150, 100 или 50 нуклеотидов. Молекула нуклеиновой кислоты предпочтительно представляет собой выделенную молекулу.
Еще один аспект относится к вектору, содержащему молекулу нуклеиновой кислоты, как определено в данном описании изобретения. Вектор может также содержать дополнительные элементы, обычно находящиеся в векторе, такие как точка начала репликации, селектируемый маркер, например устойчивость к антибиотикам, и/или сайт множественного клонирования. Кроме того вектор может представлять собой вектор экспрессии и может содержать дополнительные элементы, например элементы транскрипционного и/или трансляционного контроля или регуляторные элементы для экспрессии молекул нуклеиновой кислоты. Такие контрольные элементы, например промоторы, сайты связывания рибосом, энхансеры, терминаторы и так далее, хорошо известны и широко описаны в данной области техники.
Вектор может, например, представлять собой плазмиду или вирус, предпочтительно он выбран из ретровируса, аденовируса и вируса, ассоциированного с аденовирусом.
В другом аспекте предлагается рекомбинантная клетка-хозяин, содержащая молекулу нуклеиновой кислоты и/или вектор, как описано выше. Клетка-хозяин представляет собой животную клетку, предпочтительно клетку млекопитающего, наиболее предпочтительно клетку крысы, мыши или человека.
Под «рекомбинантной» подразумевается молекула нуклеиновой кислоты и/или вектор, которые были введены в клетку-хозяина. Клетка-хозяин может естественным образом содержать или не содержать эндогенную копию молекулы нуклеиновой кислоты, но она является рекомбинантной, поскольку была введена экзогенная или дополнительная эндогенная копия молекулы нуклеиновой кислоты и/или вектор.
В еще одном аспекте предлагается фармацевтическая композиция, содержащая олигопептидное соединение, как определено в данном описании изобретения, молекулу нуклеиновой кислоты, как определено в данном описании изобретения, и/или вектор, как определено в данном описании изобретения, вместе с фармакологически (или фармацевтически) приемлемым эксципиентом.
Эксципиент может включать любые эксципиенты, известные в данной области техники, например любой носитель или разбавитель или любой другой ингредиент или агент, такой как буфер, антиоксидант, комплексообразующий агент, связывающее вещество, покрывающее вещество, разрыхлитель, наполнитель, ароматическое вещество, красящее вещество, скользящее вещество, смазывающее вещество, консервант, сорбент и/или подсластитель и так далее
Эксципиент может быть выбран, например, из молочной кислоты, декстрозы, метабисульфата натрия, бензилового спирта, полиэтиленгликоля, полипропиленгликоля, микрокристаллической целлюлозы, лактозы, крахмала, хитозана, предварительно желатинированного крахмала, карбоната кальция, сульфата кальция, декстратов, декстрина, декстрозы, дигидрата двухосновного фосфата кальция, трехосновного фосфата кальция, карбоната магния, оксида магния, мальтодекстрина, маннитола, порошковой целлюлозы, хлорида натрия, сорбита и/или талька.
Фармацевтическая композиция может быть предложена в любой форме, известной в данной области техники, например в виде таблетки, капсулы, покрытой оболочкой таблетки, жидкости, суспензии, пластинки, саше, имплантата, средства для ингаляции, порошка, драже, эмульсии, лиофилизата, шипучего напитка, спрея, целебной мази, эмульсии, бальзама, пластыря или любой их смеси. Она может быть предложена, например, в виде препарата, устойчивого к желудочной жидкости, и/или в форме для пролонгированного действия. Она может представлять собой форму, подходящую для перорального, парентерального, местного, ректального, генитального, подкожного, трансуретрального, трансдермального, интраназального, внутрибрюшинного, внутримышечного и/или внутривенного введения и/или для введения путем ингаляции.
В типичном воплощении фармацевтическая композиция находится в форме, подходящей для липосомального введения, так что предпочтительно предлагаются липосомы, содержащие фармацевтическую композицию. Если используют липосомы, может не требоваться включение дополнительного эксципиента, таким образом также предлагаются липосомы, содержащие олигопептидное соединение, как определено в данном описании изобретения, молекулу нуклеиновой кислоты, как определено в данном описании изобретения, и/или вектор, как определено в данном описании изобретения.
Используя поиск по базе данных, авторы изобретения обнаружили присутствие нового PCNA-связывающего мотива в более чем 200 других белках, многие из которых вовлечены в репарацию ДНК, поддержание и регуляцию клеточного цикла, например транскрипцию, репликацию, фосфорилирование, убиквитинирование, транслезионный синтез, когезию сестринских хроматид и регуляцию клеточного цикла (смотри Таблицу 1 и Пример 4). Такие белки включают следующие:
- белок с неизвестной функцией, который содержит консервативный домен I N-конца, обнаруженный в факторе элонгации TFIIS (транскрипционный фактор IIS), важный белок для развития остановленной транскрипции, так что авторы изобретения назвали его TFIIS-подобным белком. Такой белок содержит мотив в пределах его 7 N-концевых аминокислот.
- многофункциональный транскрипционный фактор TFII-I, который является критически важным для контроля клеточного цикла и пролиферации. Клетки, сверхэкспрессирующие TFII-I, обладают повышенной устойчивостью фокусов Y-H2AX (маркера двухнитевых разрывов ДНК), что предполагает роль TFII-I в репарации ДНК. Такой белок содержит 4 мотива.
- ДНК-топоизомераза II альфа (Торо II α), которая действует в пострепликационном разъединении ДНК и сегрегации ДНК. Такой белок содержит один мотив.
- ключевой белок эксцизионной репарации нуклеотидов ХРА, который распознает петли спирали. Такой белок содержит один мотив.
- RAD51 В, гомологичный рекомбинантный белок, который, как показано, является важным для правильного функционирования центросом и хромосомной сегрегации. Такой белок содержит один мотив.
- белок ядерного комплекса анемии Фанкони (FA), FANCC. Ядерный комплекс FA, как показано, вовлечен в сигнальный путь, активирующий повреждения ДНК, регулируя репарацию ДНК сшивающих агентов. Такой белок содержит один мотив.
Дополнительные белки, которые, как было обнаружено, содержат по меньшей мере один мотив, перечислены в Таблице 1.
Не желания быть связанными теорией, данные авторов изобретения указывают на то, что путем предотвращения взаимодействия PCNA по меньшей мере с одним из его обычных партнеров, можно повышать чувствительность клеток к действию цитостатических агентов. Таким образом, эффект цитостатического агента можно модулировать. Например, взаимодействие белка репарации с PCNA можно ингибировать (например hABH2), тем самым ингибируя репарацию ДНК, и вследствие этого увеличивая эффект цитостатического агента в повреждении ДНК.
Таким образом, в еще одном аспекте предлагается способ лечения расстройства или состояния, в частности расстройства или состояния, где желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или любого состояния, которое нуждается в цитостатической терапии или откликается на нее, включающий введение (в частности введение эффективного количества) олигопептидного соединения, как определено в данном описании изобретения, молекулы нуклеиновой кислоты, как определено в данном описании изобретения, и/или вектора, как определено в данном описании изобретения, субъекту, нуждающемуся в этом.
В другом аспекте предлагается олигопептидное соединение, как определено в данном описании изобретения, молекула нуклеиновой кислоты, как определено в данном описании изобретения, и/или вектор, как определено в данном описании изобретения, для применения в терапии, в частности для применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или в любом лечении, которое включает цитостатическую терапию (то есть использование цитостатического агента). Таким образом, соединение и так далее может использовать в лечении любого состояния, которое нуждается в цитостатической терапии или откликается на нее.
В другом аспекте предлагается применение олигопептидного соединения, как определено в данном описании изобретения, молекулы нуклеиновой кислоты, как определено в данном описании изобретения, и/или вектора, как определено в данном описании изобретения, в изготовлении лекарственного средства для применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или в лечении, которое включает цитостатическую терапию.
Как указано выше, одно неожиданное наблюдение, приводящее к данному изобретению, состоит в том, что действие ряда разных цитостатических лекарственных средств можно усилить или потенцировать путем применения пептида, имеющего мотив, взаимодействующий с PCNA, посредством этого ингибировать взаимодействие PCNA предположительно с широким рядом белков, например белков, вовлеченных в репарацию и репликацию ДНК и прохождение клеточного цикла и так далее. Это приводит к общему предположению о том, что любую молекулу, взаимодействующую с PCNA, можно использовать в комбинации с цитостатическим агентом для усиления эффекта такого цитостатического агента, или для повышения чувствительности клетки к его действию.
Таким образом, в еще одном аспекте предлагается способ лечения расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или способ лечения, который включает цитостатическую терапию, включающий введение олигопептидного соединения, способного взаимодействовать с PCNA, или молекулы нуклеиновой кислоты, которая содержит нуклеотидную последовательность, кодирующую олигопептидное соединение, способное взаимодействовать с PCNA, и раздельное, одновременное или поочередное введение цитостатического агента субъекту, нуждающемуся в этом.
Альтернативно, предлагается олигопептидное соединение, способное взаимодействовать с PCNA, или молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую указанное олигопептидное соединение, для применения в комбинации с цитостатическим агентом в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или в лечении, которое включает цитостатическую терапию.
Таким образом, предлагается использование олигопептидного соединения, способного взаимодействовать с PCNA, или молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, которая кодируют указанное олигопептидное соединение, в изготовлении лекарственного средства для применения в комбинации с цитостатическим агентом в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или в лечении, которое включает цитостатическую терапию.
Таким образом, в одном воплощении лекарственное средство может дополнительно содержать цитостатический агент.
Лекарственное средство может находиться в форме одной композиции, содержащей как олигопептидное соединение или молекулу нуклеиновой кислоты, так и цитостатический агент, или оно может находиться в форме набора или продукта, содержащего их для раздельного (например совместного или поочередного) введения.
Таким образом, также предлагается применение олигопептидного соединения, способного взаимодействовать с PCNA, или молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, которая кодирует указанное олигопептидное соединение, в изготовлении лекарственного средства для лечения расстройства клеток, например гиперпролиферативного расстройства, или в лечении, которое включает цитостатическую терапию, где лекарственное средство вводят раздельно, совместно или поочередно с цитостатическим агентом.
В другом аспекте изобретения предлагается продукт, содержащий олигопептидное соединение, способное взаимодействовать с PCNA, или молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, которая кодируют указанное олигопептидное соединение, вместе с цитостатическим агентом, в виде комбинированного препарата для раздельного, совместного или поочередного применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или в лечении, которое включает цитостатическую терапию.
Олигопептидное соединение, способное взаимодействовать с PCNA, предпочтительно олигопептидное соединение, содержащее или имеющее SEQ ID NO:1, можно использовать для модулирования или потенцирования действия цитостатического агента.
Олигопептидные соединения (включая конструкции) по изобретению, таким образом, терапевтически полезны в любом состоянии или клинической ситуации, где желательно (или где это может быть полезно) ингибировать рост клеток.
Термин «ингибировать» используется в широком смысле и включает любое снижение или уменьшение клеточного роста, а также предупреждение или ликвидация клеточного роста. «Ингибирование», таким образом, включает уменьшение или предупреждение клеточного роста. Его можно определять любыми подходящими или удобными способами, такими как определение или оценка количества клеток, размера (например размера ткани, в которой содержатся клетки), жизнеспособности клеткой и/или смерти клеток и так далее, а также можно определять способами, хорошо известными в данной области техники.
«Рост» клеток, как он упоминается в данном описании изобретения, также используют в широком смысле и он включает любой аспект клеточного роста, включая в частности пролиферацию клеток.
Олигопептидные соединения, таким образом, можно использовать в лечении любого состояния (используемого в данном описании изобретения в широком смысле и включающего любое расстройство или любую клиническую ситуацию), которое откликается на снижение клеточного роста (в частности клеточной пролиферации). Олигопептидные соединения, таким образом, находят применение в любой терапии (или лечении), которая нацелена на клеточный рост (или пролиферацию). Другими словами, соединения можно использовать в любом терапевтическом применении, в котором желательно или выгодно ингибировать клеточную пролиферацию.
Термин «лечение» при использовании в данном описании изобретения относится в широком смысле к любому действию или стадии (или вмешательству), благоприятному для контроля за клиническим состоянием, и, таким образом, включает как терапевтическое, так и профилактическое лечение. Лечение может включать снижение, облегчение, улучшение, замедление развития или ликвидацию состояния или одного или более его симптомов, которые подлежат лечению, по сравнению с состоянием или симптомом до лечения, или улучшение любым путем клинического статуса субъекта. Лечение может включать любую клиническую стадию или вмешательство, которые содействуют, или является частью лечебной программы или схемы. Профилактическое лечение может включать замедление, ограничение, уменьшение или предупреждение состояния или начала состояния, или одного или более его симптомов, например относительно состояния или симптома до профилактического лечения. Профилактика, таким образом, однозначно включает как абсолютное предупреждение возникновения или развития состояния, или его симптома, так и любое замедление в начале или развитии состояния или симптома, или уменьшение или ограничение развития или прогрессии состояния или симптома. Лечение по изобретению, таким образом, включает ликвидацию, ингибирование или замедление роста клеток, или увеличение размера организма или популяции клеток (например в ткани, опухоли или культуре), уменьшение количества клеток или предупреждение распространение клеток (например в другой анатомический участок), уменьшение величины клеточного роста и так далее. Термин «лечения» не предполагает исцеления или полного устранения или ликвидации клеточного роста, или роста клеток.
Так как терапевтические применения и использования по настоящему изобретению могут в общем случае включать ингибирование клеточной пролиферации, любая пролиферирующая клетка может быть целевой в терапиях и использованиях, раскрытых и включенных в данное описание изобретения. Такие пролиферирующие клетки могут включать здоровые или заболевшие клетки и клетки любой ткани, в которой имеет место пролиферация. Например, такие клетки могут включать, в частности, неопластические клетки, включая как злокачественные, так и незлокачественные неопластические клетки и клетки иммунной системы (иммунные клетки), клетки гематопоэтической системы вообще, или клетки кожи.
Расстройства или состояния, включающие аномальный или нежелательный рост клеток, можно лечить цитостатическими агентами, и цитостатические агентов можно использовать в любой ситуации, где желательно снижать или предупреждать клеточный рост и пролиферацию, включая ситуации, при которых желательно убивать или удалять клетки. Таким образом, как альтернативно сформулировано выше, олигопептидные соединения (включая конструкции) по настоящему изобретению можно использовать в любом способе лечения, который подразумевает (или включает) использование цитостатического агента. Он может включать лечение любого состояния, реагирующего на цитостатический агент, или любого состояния, которое можно лечить при помощи использования цитостатического агента или которое нуждается в этом применении.
Лечение гиперпролиферативных расстройств является особенно интересным аспектом. Термин «гиперпролиферативные расстройства» широко используется в данном описании изобретения и включает любое расстройство или состояние, которое включает повышенную, неблагоприятную или нежелательную пролиферацию клеток. Таким образом включены не только состояния, при которых пролиферация клеток увеличена, например относительно нормальных или здоровых клеток, или клетки в отсутствие состояния, о котором идет речь (например по сравнению с или относительно здорового или контрольного субъекта, или по сравнению с или относительно клеток, взятых из здоровой или неповрежденной ткани у того же самого субъекта), но также состояния, при которых клеточная пролиферация не увеличена (или незначительно или значительно увеличена) по сравнению с нормальной, но при которых имеющая место пролиферация, является неблагоприятной или нежелательной, либо в общем случае, либо в конкретном контексте. Оно может включать, например, неблагоприятную или нежелательную пролиферацию клеток, которая может иметь место при «нормальном» ответе, например иммунном ответе или воспалительном ответе и так далее (другими словами «нормальный» ответ, который может иметь место в конкретном (например нормальном) контексте, но который может, тем не менее, быть нежелательным). Такой нежелательный пролиферативный ответ может, например, представлять собой пролиферацию клеток, приводящую к нежелательному воспалительному ответу, или нежелательному иммунному ответу, такому как аутоиммунный ответ или аллергическая реакция и так далее.
Гиперпролиферативные расстройства, которые можно лечить согласно настоящему изобретению, таким образом, однозначно включают воспаление (более конкретно воспалительные расстройства или состояния, или состояния, включающие воспаление, или ассоциированные с воспалением, или характеризующиеся воспалением) и аутоиммунные расстройства или состояния, или расстройства или состояния, которые имеют аутоиммунный компонент.
Гиперпролиферативное расстройство может включать (без ограничения) пролиферацию клеток, которые имеют способность автономного роста, то есть клетки, которые существуют и репродуцируются независимо от нормальных регуляторных механизмов. Гиперпролиферативное расстройство может, таким образом, представлять собой неопластическое расстройство, и как указано выше, оно может являться злокачественным или незлокачественным расстройством.
Гиперпролиферативные клетки можно классифицировать как патологические (то есть имеющие отклонения от нормальных клеток и ассоциированные с болезненным состоянием) или непатологические (то есть имеющие отклонения от нормальных, но не ассоциированные с болезненным состоянием).
Патологические Гиперпролиферативные клетки могут быть ассоциированы с, или характеризоваться, следующими болезненными состояниями или расстройствами: рестеноз, диабетическая нефропатия, гиперплазия щитовидной железы, базедова болезнь, псориаз, доброкачественная гиперплазия предстательной железы, синдром Ли-Фроменти, и раковые заболевания (включая любые опухоли или злокачественные образования).
Примеры непатологических гиперпролиферативных клеток включают эпителиальные клетки протоков молочной железы во время развития лактации и также клетки, ассоциированные с заживлением ран.
Соединения по изобретению могут быть полезны в лечении таких расстройств и заболеваний и других, включая диабетическую ретинопатию и периферические сосудистые заболевания.
Гиперпролиферативные расстройства могут являться, как указано выше, злокачественными или незлокачественными неопластическими расстройствами. Также включены предраковые и ненеопластические расстройства. Примеры предраковых или ненеопластических или незлокачественных гиперпролиферативных расстройств включают миелодиспластические расстройства, цервикальную карциному in situ, семейный кишечный полипоз (например синдром Гарднера), оральную лейкоплакию, гистиоцитоз, келоиды, гемангиомы, гиперпролиферативный артериальный стеноз, воспалительный артрит, гиперкератоз и папулосквамозное высыпание, включая артрит. Также включены вызванные вирусом гиперпролиферативные заболевания, такие как бородавки и вызванное вирусом Эпштейна-Барр заболевание (например инфекционный мононуклеоз), образование рубцов и тому подобное.
Гиперпролиферативное расстройство может, таким образом, представлять собой любое Гиперпролиферативное расстройство, например выбранное из неопластических расстройств, таких как рак, псориатический артрит, ревматоидный артрит, гастральные гиперпролиферативные расстройства, такие как воспалительное заболевание кишечника, кожные расстройства, включая псориаз, синдром Рейтера, красный волосистый питириаз, и гиперпролиферативные варианты расстройств кератинизации.
Рак представляет собой особенно интересующее Гиперпролиферативное расстройство, и включены все типы рака, например, солидные опухоли и гематологические раковые заболевания. Типичные типы раковых заболеваний включают рак шейки матки, рак матки, рак яичников, рак поджелудочной железы, рак почек, рак желчного пузыря, рак печени, рак головы и шеи, плоскоклеточную карциному, желудочно-кишечный рак, рак молочной железы, рак предстательной железы, рак яичка, рак легкого, немелкоклеточный рак легкого, неходжкинскую лимфому, множественную миелому, лейкемию (такую как острый лимфоцитарный лейкоз, хронический лимфоцитарный лейкоз, острый миелогенный лейкоз, и хронический миелобластный лейкоз), рак головного мозга (например астроцитому, глиобластому, медуллобластому), нейробластому, саркому, рак ободочной кишки, рак прямой кишки, рак желудка, анальный рак, рак мочевого пузыря, рак поджелудочной железы, рак эндометрия, плазмоцитому, лимфому, ретинобластому, опухоль Вильмса, саркому Юинга, меланому и другие раковые заболевания кожи.
Также можно упомянуть опухоли синуса, раковые заболевания уретры и мочеполовой системы, рак пищевода, миелому, эндокринные раковые заболевания, остеосаркому, ангиосаркому и фибросаркому, и любую опухоль периферической или центральной нервной системы, злокачественную или доброкачественную, включая глиомы и нейробластомы.
Аутоиммунные расстройства или заболевания также являются особенно интересующими состояниями, и включают, например, ревматоидный артрит, рассеянный склероз, иммунные расстройства, такие как системная красная волчанка (SLE; волчанка) или ложный бульбарный паралич.
Также представляют интерес, в общем случае, гематологические расстройства, или заболевания крови или костного мозга, которые не обязательно являются злокачественными или раковыми (например различные дискразии, или дисплазии, незлокачественные гиперплазии, агранулома или MGUS (моноклональная гаммапатия неизвестной значимости). Таким образом, любое состояние, которое включает нежелательную, или неблагоприятную, или ненормальную пролиферацию клеток крови или костного мозга, или их предшественников, можно лечить согласно настоящему изобретению.
Другие состояния, которые можно особо упомянуть, включают неопластический менингит и миелопролиферативные заболевания, например истинную полицитемию (которая встречается при избыточном продуцировании красных кровяных клеток).
Различные состояния могут также возникать в результате воспаления или аутоиммунного заболевания, или могут быть иным образом ассоциированными с ними. Такие состояния также можно лечить согласно настоящему изобретению. Особенно можно упомянуть склеромикседерму и папулезный муциноз, амилоидоз и гранулематоз Вегенера.
Как указано выше, соединения по изобретению могут усиливать или потенцировать эффекты цитостатического агента. Таким образом, они могут находить применение в любом терапевтическом использовании, где можно использовать цитостатический агент. Оно может включать любую ситуацию, когда желательно убить или удалить клетки, которые могут включать не только больные клетки. В частности, такая ситуация возникает, когда желательно удалить костный мозг перед трансплантацией. Соединения по изобретению можно, таким образом, использовать в миелоабляции, и в частности миелоабляции, предшествующей пересадке, которая может, например, представлять собой пересадку костного мозга или, в более общем случае, пересадку гемопоэтических стволовых клеток (HSCT) (также как из костного мозга, гемопоэтические стволовые клетки можно получать или производить из крови, например периферической крови).
Трансплантацию стволовых клеток может применять в лечении заболеваний или состояний крови или костного мозга (то есть гематологических состояний или расстройств), которые могут быть злокачественными или незлокачественными, и некоторых других типов рака, включая солидные опухолевые раковые заболевания, такие как нейробластома, демопластический мелко-круглоклеточный рак, саркома Юинга и хориокарцинома. Гематологические злокачественные заболевания включают лейкозы, лимфомы (ходжкинская и неходжкинская) и миеломы. Незлокачественные гематологические расстройства включают фагоцитные расстройства (например миелодисплазию), анемии (например тяжелую аплазию или апластическую анемию), и миелопролиферативные расстройства (например истинную полицитемию и эссенциальный тромбоцитоз). Другие приобретенные состояния, которые можно лечить при помощи трансплантации стволовых клеток, включают метаболические расстройства, такие как амилоидоз, и заболевания, вызванные окружающей средой, такие как радиационное отравление. Пересадку стволовых клеток также можно использовать в лечении врожденных расстройств, включая различные лизосомные болезни накопления, иммунодефицитные состояния и незлокачественные гематологические расстройства, например анемии, цитопении, гемофагоцитные синдромы, гемоглобинопатии, серповидно-клеточное заболевание и большая β-талассемия.
Радиотерапию (также известную как радиационная терапия и радиационная онкология) можно использовать в лечении различных состояний, включая гиперпролиферативные расстройства, описанные выше. Под «радиотерапией» подразумевают применение ионизирующего излучения, которое способно повреждать ДНК клеток посредством прямой или непрямой ионизации атомов, которые образуют цепь ДНК. Непрямая ионизация происходит в результате ионизации воды, образования свободных радикалов, в частности гидроксильных радикалов, которые затем повреждают ДНК. В наиболее распространенных формах радиотерапии наибольший эффект от излучения достигается посредством свободных радикалов.
Радиотерапия полезна в лечении рака и для удаления патологических тканей из-за цитотоксических эффектов, которые вызываются стойкими двухнитевыми разрывами ДНК или активацией запрограммированной клеточной гибели. Ионизирующее излучение вызывает клеточную гибель гиперпролиферирующих клеток, таких как опухолевые и раковые клетки посредством апоптоза как in vivo, так и in vitro.
К сожалению, радиотерапия часто является неудачной для полной ликвидации раковых клеток пациента, так как часто она не способна доставлять достаточно высокую дозу местного излучения, чтобы убить опухолевые клетки без недопустимо высокого риска повреждения окружающей нормальной ткани. Также известно, что клетки демонстрируют широко варьирующиеся чувствительности к вызываемой излучением клеточной гибели, и ионизирующее излучение также может активировать механизм ответа выживаемости посредством путей сигнальной трансдукции фосфатидилинозитол-3-киназа/Akt (PI3K/Akt) и митоген-активированной протеинкиназы (МАРК). Таким образом, существует необходимость в усилении эффективности радиотерапии при помощи повышения чувствительности клеток к действиям ионизирующего излучения.
Таким образом, соединения по изобретению может использовать для получения такого эффекта сенсибилизации, другими словами, для усиления (или, альтернативно выражаясь, для увеличения, нарастания или потенцирования) эффектов радиотерапии, или чтобы сделать субъекта (или, более конкретно, клеток, которые могут присутствовать у субъекта) в более чувствительным к эффектам радиотерапии. Таким образом, они могут найти применение в любом терапевтическом лечении, где используется радиотерапия. Оно может включать любую ситуацию, когда желательно убить или ликвидировать клетки, которые могут включать не только больные клетки.
Таким образом, соединения по изобретению можно использовать в качестве сенсибилизатора клеток к ДНК-повреждающим эффектам ионизирующего излучения. Под «сенсибилизатором» подразумевается использование соединений по изобретению для усиления ДНК-повреждающего эффекта ионизирующего излучения на клетки. Его можно добиться ингибированием эндогенных механизмов репарации клеточной ДНК.
Таким образом, настоящее изобретение включает олигопептидное соединение, содержащее PCNA-взаимодействующий мотив (более конкретно, олигопептидное соединение, содержащее PCNA-взаимодействующий мотив, как определено в данном описании изобретения), или молекулу нуклеиновой кислоты, содержащей последовательность, кодирующую указанный PCNA-взаимодействующий мотив, для использования в комбинации с радиотерапией, где соединение вводят раздельно, совместно или последовательно с радиотерапией. Радиотерапию, вместе с соединением, можно вводить в лечение любого состояния, которое откликается на радиотерапию или которое нуждается в ней. Соединения или конструкции по изобретению можно, таким образом, использовать в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или в любом лечении, которое включает радиотерапию.
Альтернативно определяя, в изобретении предлагается олигопептидное соединение, содержащее PCNA-взаимодействующий мотив (более конкретно, олигопептидное соединение, содержащее PCNA-взаимодействующий мотив, как определено в данном описании изобретения), или молекулу нуклеиновой кислоты, содержащую последовательность, кодирующую указанный PCNA-взаимодействующий мотив, в качестве сенсибилизатора для радиотерапии, где соединение вводят раздельно, одновременно или последовательно с радиотерапией.
В данных аспектах изобретения также предложен способ сенсибилизации субъекта (или, более конкретно, клеток или ткани указанного субъекта) к радиотерапии, включающий введение указанному субъекту олигопептидного соединения по изобретению, как определено в данном описании изобретения, в частности такого количества указанного соединения, которое является эффективным для повышения чувствительности указанного субъекта (или указанных клеток или ткани) к радиотерапии.
Как можно заметить, в данном аспекте изобретения также предлагается способ лечения субъекта, включающий введение радиотерапии указанному субъекту вместе с олигопептидным соединением по изобретению, как определено в данном описании изобретения. Более конкретно, такой способ может представлять собой способ лечения расстройства или состояния, которое откликается на радиотерапию, или которое нуждается в ней, или расстройства или состояния, в котором желательно ингибировать рост клеток, или способ лечения, который включает радиотерапию.
Изобретение предполагает все типы радиотерапии, включая, но без ограничения ими, обычную дистанционную лучевую радиотерапию, стереотактическую радиотерапию, виртуальную симуляцию, 3-мерную конформную радиотерапию, регулируемую по интенсивности радиотерапию и радиоизотопную терапию (RIT).
Таким образом, в одном предпочтительном воплощении любого из аспектов, перечисленных в данном описании изобретения, олигопептидное соединение, молекула нуклеиновой кислоты и/или вектор, как определено в данном описании изобретения, используются вместе (совместно, раздельно или последователь) с радиотерапией.
В еще одном предпочтительном воплощении любого из аспектов, перечисленных в данном описании изобретения, олигопептидное соединение, молекула нуклеиновой кислоты и/или вектор, как определено в данном описании изобретения, используются вместе (совместно, раздельно или последовательно) с цитостатическим агентом.
Под «цитостатическим агентом» подразумевают агент, который способен ингибировать или замедлять рост и/или размножение (репликацию/пролиферацию) животных клеток.
Цитостатические агенты включают цитотоксические агенты, антинеопластические агенты и любой агент, который может быть показан для онкологического или гематологического использования. Таким образом, включены агенты, используемые в протоколах химиотерапевтического лечения («химиотерапевтические агенты»).
Цитостатические агенты обычно группируют в разные классы согласно их механизму действия, и все эти классы рассматриваются в данном описании изобретения. Таким образом, цитостатический агент может являться алкилирующим агентом, сшивающим агентом, интеркалирующим агентом, нуклеотидным аналогом, ингибитором образования веретена деления и/или ингибитором топоизомеразы I и/или II. Другие типы или классы агента включают антиметаболиты, растительные алкалоиды и терпеноиды или противоопухолевый антибиотик. Предпочтительно он представляет собой алкилирующий агент.
Алкилирующие агенты модифицируют ДНК при помощи алкилирующих нуклеозидов, которые приводят к предупреждению правильной репликации ДНК. Нуклеотидные аналоги включаются в ДНК в процессе репликации и ингибируют синтез ДНК. Ингибиторы образования веретена деления нарушают образование веретена деления, приводя к задержке митоза во время метафазы. Интеркалирующие агенты вставляются между основаниями ДНК, тем самым ингибируя синтез ДНК. Ингибиторы топоизомеразы 1 или II воздействуют на скручивание ДНК, тем самым препятствуя репликации ДНК.
Подходящие цитостатические агенты известны в данной области техники, но в качестве примера в данном описании изобретения указаны актиномицин D, BCNU (кармустин), карбоплатин, CCNU (1-(2-хлорэтил)-3-циклогексил-1-нитрозомочевина), кампотецин (СРТ), кантаридин, цисплатин, цисплофосфамид, цитарабин, дакарбазин, даунорубицин, доцетаксел, доксорубицин, DTIC ((диметилтриазеноимидазола карбоксамид), эпирубицин, этопозид, гефинитиб, гемцитабин, ифосамид, иринотекан, иономицин, мелфалан, метотрексат, митомицин С (ММС), митозантронмеркаптопурин, оксалиплатин, паклитаксел (таксол), ингибитор PARP-I (поли(АДФ-рибоза)-полимеразы), таксотер, темозоломид (TZM), тенипозид, топотекан, треосульфан, винорелбин, винкристин, винбластин, 5-азацитидин, 5,6-дигидро-5-азацитидин и 5-фторурацил. Специалист осведомлен о подходящих интервалах дозировок для любого такого цитостатического агента, и в одном воплощении цитостатический агент присутствует в фармацевтической композиции, или вводят субъекту, в типичном диапазоне доз.
В предпочтительном воплощении может присутствовать/использоваться более низкая доза цитостатического агента, так как олигопептидное соединение, молекула нуклеиновой кислоты или вектор по изобретению повышают чувствительность клетки к цитостатическим агентам, и поэтому при использовании в комбинации с олигопептидным соединением, молекулой нуклеиновой кислоты или вектором по изобретении более низкая доза цитостатического агента будет иметь такой же или сравнимый терапевтический эффект, как и более высокая доза цитостатического агента сама по себе. Олигопептидное соединение, молекула нуклеиновой кислоты или вектор по изобретению, таким образом, делают возможным лечение субъектов, которые имеют низкую, или ниже средней, переносимость цитостатических агентов, таких как пожилые люди, новорожденные или маленькие дети, или люди, ослабленные, например, вследствие заболевания, недостаточного питания и тому подобного.
Одна проблема, возникшая при использовании цитостатических агентов для лечения гиперпролиферативных расстройств, заключается в том, что обычно убивают не все пораженные клетки. Предполагается, что, когда цитостатический агент и олигопептидное соединение, молекула нуклеиновой кислоты или вектор по изобретению используют вместе, убивать более высокий процент пораженных клеток, и в одном воплощении используют дозу цитостатического агента выше обычной вместе с олигопептидным соединением, молекулой нуклеиновой кислоты или вектором по изобретению, чтобы добиться умерщвления очень большой части больных клеток, например по меньшей мере 50, 60 70 или 80%, предпочтительно по меньшей мере 85, 90 или 95%, наиболее предпочтительно убить по существу все больные клетки.
Как указано выше, когда олигопептидное соединение, молекулу нуклеиновой кислоты и/или вектор, как определено в данном описании изобретения, используют вместе с цитостатическим агентом, тогда два разных агента могут присутствовать в одной и той же фармацевтической композиции, или их можно вводить отдельно. Отдельное введение может включать введение по существу в одно и то же время, но при помощи различных путей введения или путем введения в разные участки. Раздельное введение может также включать введение в различные моменты времени, например с интервалом вплоть до 1, 2, 3, 4, 5, 6 или 12 часов.
Субъект представляет собой животное (то есть любого человека или животное, отличное от человека), предпочтительно млекопитающее, наиболее предпочтительно человека.
Специалисту хорошо известны подходящие способы введения олигопептидного соединения, молекулы нуклеиновой кислоты и/или вектора в клетки. В качестве примера несколько подходящих способов кратко обсуждаются ниже. Как подробно обсуждалось выше, можно использовать опосредованные пептидами способы доставки, в частности пептиды проникновения в клетку (СРР), которые, как обсуждалось выше, являются короткими, в некоторых случаях поликатионными, последовательностями, которые могут облегчать клеточный захват пептидов, белков или нуклеотидных молекул, которые содержат СРР или к которым присоединены СРР, например путем усиления захвата в эндосомы клеток млекопитающих. Микрокапсулирование обеспечивает простой и экономически эффективный способ включения биоактивных веществ в полупроницаемую полимерную мембрану с целью защиты биоактивных веществ и высвобождения включенных веществ или их продуктов контролируемым способом. При фотохимической интернализации (РС1) и представляющие интерес молекулы и фотосенсибилизирующее соединение захватываются клеткой в лизосому или эндосому. Затем клетки подвергают воздействию света с подходящими длинами волн для активации фотосенсибилизирующего соединения, заставляя фотосенсибилизирующее соединение разрушать мембрану лизосомы или эндосомы, тем самым высвобождая представляющую интерес молекулу в цитозоль клетки.
Другие способы включают микроинъекцию, слияние, опосредованное тенями эритроцитов, липосомное слияние, осмотический лизис пиносом, введение путем соскоба, электропорацию, трансфекцию, опосредованную фосфатом кальция и вирусом, и использование сополимерных носителей.
Хитозан и водорастворимые производные хитозана, в частности гликольхитозан, выступают в качестве предпочтительных носителей лекарственных средств из-за их биосовместимости и способности к биоразложению in vivo. Предпочтительным примером является гликольхитозан, гидрофобно модифицированный 5 β-холановой кислотой.
В данном описании изобретения используют стандартный аминокислотный однобуквенный код, таким образом, К означает лизин (Lys), I означает изолейцин (IIe) и тому подобное.
Олигопептидное соединение по изобретению может включать одну или более, например по меньшей мере 1, 2, 3, 4 или 5 аминокислот, которые имеют боковую цепь, которая не кодируется стандартным генетическим кодом, называемую в данном описании изобретения «некодируемыми аминокислотами». Они могут быть выбраны из аминокислот, которые образуются в метаболических процессах, таких как орнитин или таурин, и/или искусственно модифицированных аминокислот, таких как 9H-флуорен-9-илметоксикарбонил (Fmoc), (трет)-(б)утил(о)кси(к)арбонил (Вое), 2,2,5,7,8-пентаметилхроман-6-сульфонил (Pmc)-защищенных аминокислот, или аминокислот, имеющих бензилоксикарбонильную (Z) группу. Предпочтительно, когда присутствуют такие некодируемые аминокислоты, они не находятся в мотиве, но в одном воплощении одна или более некодируемых аминокислот присутствуют в мотиве.
Стабильность олигопептидного соединения по изобретению in vitro и/или in vivo можно улучшать или усиливать, используя стабилизирующие или защитные средства, известные в данной области техники, например добавление защитных или стабилизирующих групп, введением аминокислотных производных или аналогов или химическую модификацию аминокислот. Такие защитные или стабилизирующие группы можно, например, добавлять к N- и/или С-концу. Примером такой группы является ацетильная группы, но и другие защитные группы или группы, которые могут стабилизировать пептид, известны в данной области техники.
Олигопептидные соединения по изобретение обычно содержат только аминокислоты, имеющие L-конфигурацию, но может присутствовать одна или более аминокислот, имеющих D-конфигурацию. Предпочтительно олигопептидное соединение содержит по меньшей мере 1, 2, 3, 4 или 5 D-аминокислот и они предпочтительно находятся в мотиве, но в другом воплощении, D-аминокислоты присутствуют только вне мотива. Олигопептидное соединение может быть линейным или циклическим.
Таким образом, включены, в частности, инверсные олигопептидные соединения или инверсные аналоги олигопептидных соединений по изобретению (и более конкретно инверсные пептиды).
Также включены ретро-олигопептидные соединения (или ретро-пептиды), в которых остатки (например аминокислотные остатки) скомпонованы в противоположном направлении к родительскому или сравнительному соединению (например пептиду).
Ретро-инверсные олигопептидные соединения включают D-аминокислоты в обратном (противоположном) порядке к последовательности родительского или исходного соединения. Ретро-инверсный аналог, таким образом, имеет реверсированные концы и реверсированный порядок, например, пептидных связей, в то же время приблизительно поддерживая топологию боковых цепей как в родительской или сравнительной последовательности.
Соединения по изобретению могут включать частичные инверсные, ретро или ретро-инверсные последовательности.
Под «олигопептидным соединением» подразумевают соединение, которое состоит из аминокислот или эквивалентных субъединиц, которые связаны вместе пептидными или эквивалентными связями. Таким образом, термин «олигопептидное соединение» включает пептиды и пептидомиметики.
Под «эквивалентной субъединицей» подразумевают субъединицу, которая структурно и функционально аналогична аминокислоте. Скелетная группировка субъединицы может отличаться от стандартной аминокислоты, например, она может включать один или более атомов азота вместо одного или более атомов углерода.
Под «пептидомиметиком» подразумевают соединение, которое функционально эквивалентно или подобно пептиду, и которое может принимать трехмерную структуру, подобную его пептидным аналогам, но которое состоит не только из аминокислот, связанных пептидными связями. Предпочтительным классом пептидомиметиков являются пептоиды, то есть N-замещенные глицины. Пептоиды являются близкородственными их природным пептидным аналогам, но химически отличаются тем, что их боковые цепи присоединены к атомам азота вдоль скелета молекулы, а не к α-атомам углерода, как в аминокислотах.
В предпочтительном воплощении по меньшей мере часть мотива олигопептидного соединения содержит только пептидные связи и предпочтительно она образована только кодированными аминокислотами. Наиболее предпочтительно, олигопептидное соединение представляет собой пептид.
Олигопептидное соединение может включать ди-аминокислоты и/или β-аминокислоты, но по меньшей мере часть мотива предпочтительно образована только α-аминокислотами. Наиболее предпочтительно олигопептидное соединение состоит из α-аминокислот.
Приставку «олиго» используют для обозначения относительно небольшого числа субъединиц, таких как аминокислоты, то есть менее 200, предпочтительно менее 100, 90, 80, 70 60 или 50 субъединиц. Олигопептидное соединение по изобретению может, таким образом, содержать по меньшей мере 5 и не более 200 субъединиц. Предпочтительно оно содержит по меньшей мере 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 субъединиц. Согласно альтернативному определению, оно содержит не более 40, 35, 30, 29, 28, 27, 26 или 25 субъединиц. Типичные диапазоны субъединиц, таким образом, включают 5-40, 5-35, 5-30, 5-25, 5-20, 5-15, 5-12, 5-10 и так далее, предпочтительными являются 5-20 и 5-30.
Когда олигопептидное соединение содержит более 5 субъединиц, тогда природа субъединиц вне мотива не является критичной, то есть субъединицы вне мотива могут, например, представлять собой субъединицы, обнаруженные в нативном белке, таком как hABH2, или они могут представлять собой остатки аланина или любые другие подходящие остатки.
Пептидомиметики обычно имеют более длинный период полувыведения из организма человека, поэтому они предпочтительны в воплощениях, где желательно более длительное воздействие. Это может помочь уменьшить частоту, с которой композицию следует вводить повторно.
Однако в других воплощениях из соображений биологической безопасности может быть предпочтительным более короткий период полувыведения; в таких воплощениях предпочтительными являются пептиды.
Олигопептидное соединение по изобретение может образовывать часть более крупной единицы, например оно может быть слито с полипептидом с получением рекомбинантного слитого белка или прикреплено к матриксу с получением пептидного аптамера. Таким образом, слитые белки или аптамеры, включающие олигопептидное соединение по изобретение, образуют дополнительные аспекты настоящего изобретения. Еще одни аспекты включают фармацевтические композиции, содержащие такие слитые белки или аптамеры, и применение таких слитых белков или аптамеров в терапии или в способе лечения, как описано выше.
Не желая быть связанными теорией, представляется, что для оптимальной репарации ДНК, поддержания и/или регуляции клеточного цикла, некоторые белки должны взаимодействовать с PCNA, и что олигопептидные соединения по изобретению способны конкурировать с белками, которые имеют консенсусный мотив для взаимодействия с PCNA. Примеры белков, которые возможно должны взаимодействовать с PCNA посредством нового мотива для оптимальной репарации ДНК, поддержания и/или регуляции клеточного цикла, приведены в Таблице 1, так что белок может представлять собой ДНК-пол и меразу, ДНК-лигазу, топоизомеразу, белок репарации ДНК, белки, ассоциированные/взаимодействующие с репарацией ДНК, белок, вовлеченный в когезию сестринских хроматид, ремоделирование хроматина связывание ДНК, процессирование убиквитина или процессирование SUMO, убиквитин-лигазу Е3, транскрипционный фактор, регулятор клеточного цикла, протеинкиназу, метилтрансферазу, ацетил-трансферазу, антиген, ассоциированный с раком, структурный белок или центросомный кинезин.
Если в клетке присутствует достаточный уровень олигопептидного соединения по изобретению, тогда активность одного или более из этих белков снижается или даже исчезает вследствие такого конкурентного ингибирования.
Полагают, что олигопептидное соединение, молекула нуклеиновой кислоты или вектор, как определено в данном описании изобретения, сами по себе не имеют ферментной активности и нетоксичны для клеток (смотри Пример 2). Таким образом было показано, что экспрессия пептида по изобретению, содержащего PCNA-взаимодействующий мотив, как определено в данном описании изобретения, не оказывает воздействия или оказывает только незначительные воздействия на рост клетки, в которой он экспрессируется. Это может зависеть от уровня экспрессии. Однако в некоторых ситуациях, как полагают, олигопептидные соединения по изобретению могут быть цитотоксическими и таким образом их можно использовать в качестве цитотоксических (или цитостатических) агентов сами по себе. Таким образом, соединения по изобретению может использовать в качестве цитотоксических агентов в лечении состояний, как обсуждалось в данном описании изобретения, и необязательно всегда в комбинации с отдельным цитостатическим агентом или с радиотерапией.
Эксперименты показали, что олигопептидные соединения, введенные в клетки, могут обладать цитотоксическим воздействием на клетку.
Цитотоксический эффект может варьироваться в зависимости от точной природы соединения, например его последовательности или состава. В частности, цитотоксический эффект может быть получен при помощи конструкций, содержащих NLS и/или СРР, и, наблюдался с конструкциями, содержащими как NLS, так и СРР. Наблюдалось убедительное доказательство цитотоксичности в случае конструкций с ядерной локализацией.
Олигопептидные соединения, которые проявляют цитотоксический эффект, могут быть инверсными, ретро или ретро-инверсными и так далее
Более конкретно, было дополнительно отмечено, что усиленный цитотоксический эффект может быть получен для соединения или конструкций, которые содержат более одного PCNA-взаимодействующего мотива по настоящему изобретению.
В еще одном аспекте в данном описании изобретения предлагается набор, или фармацевтический продукт, содержащий
(1) олигопептидное соединение, как определено в данном описании изобретения, молекулу нуклеиновой кислоты, как определено в данном описании изобретения, и/или вектор, как определено в данном описании изобретения; и
(2) цитостатический агент.
В другом аспекте предлагается продукт, содержащий (1) олигопептидное соединение, как определено в данном описании изобретения, молекулу нуклеиновой кислоты, как определено в данном описании изобретения, и/или вектор, как определено в данном описании изобретения, и (2) цитостатический агент, в виде комбинированного препарата для совместного, последовательного или раздельного применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или в лечении, которое включает цитостатическую терапию.
Также предполагается in vitro введение олигопептидного соединения, молекулы нуклеиновой кислоты и/или вектора, как определено в данном описании изобретения, в клетку или клеточную культуру. Такие in vitro методы может использовать для изучения репарации ДНК, поддержания и/или регуляции клеточного цикла. В предпочтительном аспекте метод in vitro используют для идентификации новых цитостатических агентов. Он может обеспечить более быструю идентификацию цитостатических агентов, или идентификацию агентов, которые являются только слабыми цитостатиками, когда используются сами по себе, но которые имеют полезную цитостатическую активность при использовании в комбинации с олигопептидным соединением, молекулой нуклеиновой кислоты или вектором по изобретению.
Новый PCNA-взаимодействующий мотив, как определено в данном описании изобретения, можно использовать в диагностике или мониторинге расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, или лечения, которое включает цитостатическую терапию или радиотерапию.
Авторы изобретения обнаружили, что некоторые ассоциированные с раком антигены имеют мотив, связывающий PCNA (смотри Таблицу 1). Таким образом, представляется возможным, что гиперпролиферативное или другое расстройство, как обсуждалось выше, может быть диагностировано или за его развитием может наблюдать путем определения уровня экспрессии и/или локализации белка, содержащего мотив, где аберрантный уровень и/или локализация белка указывал на расстройство, например гиперпролиферативное расстройство.
Под «аберрантным уровнем» подразумевают повышенный уровень белка, например уровень выше 10, 20, 30 или 40% по сравнению с уровнем в здоровых клетках такого же клеточного типа, или пониженный уровень белка, например уровень ниже 10, 20, 30 или 40% по сравнению с уровнем в здоровых клетках аналогичного клеточного типа.
В предпочтительном воплощении повышенный уровень белка, содержащего мотив, указывает на расстройство, например гиперпролиферативное расстройство.
Уровень мотив-содержащего белка можно анализировать, используя любой известный способ обнаружения белка. Предпочтительно используют антитело, специфичное к этому мотиву. Антитело должно быть достаточно специфичным к мотиву (по сравнению с контрольным белком, таким как бычий сывороточный альбумин) для использования в диагностическом способе.
Антитело может представлять собой моноклональное или поликлональное антитело и может представлять собой целое антитело, например IgG, IgA, IgE, IgM или IgD, или фрагмент антитела, такой как Fab, Fab', F(ab')2, scFv, Fv, dsFv, ds-scFv, Fd, dAbs.
Анализ определения можно выполнять in vivo или in vitro, например в ткани, или клетке, или образце биологической жидкости, например клеточном лизате, сыворотке или крови.
Определение можно облегчить присоединением (то есть физическим связыванием) антитела к определяемому веществу (то есть введением метки в антитело). Примеры определяемых веществ включают различные ферменты, простетические группы, флуоресцентные вещества, люминесцентные вещества, биолюминесцентные вещества, контрастные агенты для ЯМР и радиоактивные вещества. Примеры подходящих ферментов включают пероксидазу хрена, щелочную фосфатазу, люциферазу, бета-галактозидазу, ацетилхолинэстеразу, глюкозооксидазу, лизоцим, малатдегирогеназу и тому подобное; примеры подходящих комплексов простетических групп включают стрептавидин/биотин и авидин/биотин; примеры подходящих флуоресцентных веществ включают умбеллиферон, флуоресцеин, флуоресцеина изотиоцианат, родамин, дихлортриазиниламина флуоресцеин, дансилхлорид или фикоэритрин; пример люминесцентного вещества включает люминол; примеры биолюминесцентных веществ включают люциферазу, люциферин и экворин, и примеры подходящих радиоактивных веществ включают 1251, 1311, 35S или 3H. В случае прямого визуального маркера, можно использовать коллоидную металлическую или неметаллическую частицу.
Предпочтительно предложен способ диагностики или мониторинга развития у субъекта расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства, включающий стадии:
(1) приведения тестируемого образца, взятого от указанного субъекта (например млекопитающего), в контакт с антителом, специфичным к мотиву, в условиях, которые допускают образование комплекса антитело-антиген;
(2) измерения количества комплекса антитело-антиген в тестируемом образце; и
(3) сравнения количества комплекса антитело-антиген в тестируемом образце с контролем.
Контролем может являться здоровая клетка, взятая от того же субъекта, например здоровая фибробластная клетка.
В другом аспекте изобретение относится к антителам, специфичным к мотиву.
Кроме того изобретение включает набор для диагностики или мониторинга расстройства или состояния, при котором желательно ингибировать рост клеток, например гиперпролиферативного расстройства,
где указанный набор содержит антитело, специфичное к мотиву, и инструкции для применения их для диагностики расстройства или состояния. Предпочтительно антитело присоединено к обнаруживаемому веществу, как описано выше, или набор включает такое обнаруживаемое вещество.
Альтернативный способ диагностики включает определение аберрантного уровня молекулы нуклеиновой кислоты, которая кодируют мотив. В данном способе за уровнем нуклеиновой кислоты наблюдают, используя подходящий метод определения, такой как полимеразная цепная реакция (PCR) или методы гибридизации с использованием подходящим образом меченых зондов. Далее изобретение дополнительно описано со ссылкой на следующие неограничивающие Примеры и графические материалы, где:
На Фиг. 1 показаны изображения, полученные с помощью конфокальной микроскопии, которые показывают, что hABH2 и PCNA локализованы совместно, и что 10 N-концевых аминокислот hABH2 являются необходимыми и достаточными для такой совместной локализации. Различные конструкции hABH2 (полноразмерный hAHB2, имеющий остатки 1-261, усеченный hABH2, имеющий остатки 11-261 и N-концевой фрагмент НАВН2, состоящий из остатков 1-10), меченные EYFP, испытывали в отношении совместной локализации с ECFP-меченным PCNA (смотри Пример 1). На полосе слева показаны клетки, трансфицированные одним hABH2, в то время как на трех остальных полосах показаны клетки, совместно трансфицированные конструкцией hABH2 и PCNA.
На Фиг. 2 представлена диаграмма, показывающая результаты анализа FRET (флуоресцентный резонансный перенос энергии). Нормализованные измерения FRET (NFREГ) показаны между EYFP (желтый флуоресцентный белок)/ЕСРР (голубой флуоресцентный белок) (полоса 1, фон из-за димеризации меток), EYFP-PCNA/ECFP-PCNA (полоса 2, положительный контроль, поскольку PCNA связывается с PCNA), hAHB2-EYFP/ECFP-PCNA (полоса 3) и 1-10N hABH2-EYFP/ECFP-PCNA (полоса 4).
На Фиг. 3 представлены диаграммы, показывающие эффект различных цитостатических агентов на клетках, экспрессирующих hABH21-10-EYFP, или экспрессирующих EYFP в качестве контроля. Обработанные клетки показаны слева, необработанные - справа. Обработки выполняли при помощи 10 мкМ MMS, 40 мкМ BCNU, 1 мкМ ММС или 600 мкМ TMZ в течение 4 суток (Фиг.3 a-d соответственно). Представлены данные одного типичного эксперимента по меньшей мере из 3 экспериментов, клеточный рост при различных дозах тестировали в 8 параллельных лунках.
На Фиг.4 показано выравнивание последовательностей 10 N-концевых аминокислот АВН2-гомологов от Homo sapiens (NP 001001655.1), Bos Taurus (NP 001019687.1), Rattus non/egicus (XP 222273.3), Mus musculus (NP 778181.2), Gallus gallus (XP 415188.2) и Strongylocentrotus purpuratus (XP 797704.1) с использованием Clustal W. Последовательности получали из общедоступной базы данных.
На Фиг.5 показано выравнивание последовательностей белков, идентифицированных в Примере 4, от разнообразных отличающихся видов.
На Фиг.6 представлены диаграммы, показывающие результаты анализа цитотоксичности с различными пептидами, как описано в Примере 7 (Фиг.6(А)-(Н)). Клетки HeLa высевали в 96-луночные планшеты (6000 клеток/лунка) и инкубировали в течение 3 часов. Различные дозы пептидов добавляли в лунки в присутствии (закрашенные ромбы) или в отсутствии сыворотки (закрашенный квадрат) в среде. Через 1 ч в лунки добавляли равный объем среды с 10% или 20% сыворотки (к среде, не содержащей сыворотку). Клетки инкубировали в течение 48 часов, затем измеряли клеточную выживаемость с помощью МТТ-анализа (анализ с использованием 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразола бромида). Графические материалы показывают клеточный рост (OD (оптическая плотность)750 нм) против концентрации пептида (мкМ).
Примеры
Методики экспериментов, использованные в Примерах
Конструкции экспрессии
Клонирование флуоресцентно меченых конструкций экспрессии ECFP-PCNA и hABH21-261-EYFP было описано ранее (Aas et al., 2003). Используя в качестве матрицы hABH21-261-EYFP, при помощи PCR генерировали hABH21-10-EYFP и hABH211-261-EYFP. Ампликоны клонировали в pEYFP-NI (Clonetech), используя /VcteI/AgeI и AgeI/EcoRI соответственно. Продукт PCR из EST (Image clone 5176979 (ВС035374) RZPD) клонировали в pEYFP-CI (HindIII/Acc65I) с получением EYFP-TFIIS-L. Конструкцию EYFP-XPA создавали путем переключения EYFP на EGFP (фрагмент NheI/BsrGI) в His9-HA-EGFP-XPA (Rademakers et al., 2003), великодушно предложенный Dr. Wim Vermeulen (Department of Cell Biology и Genetics, Rotterdam). TFII-I-EYFP генерировали PCR-ампликацией TFII-I из pI3CX-TFII-I (Roy et al., 1993), великодушно предложенного Dr. Robert G. Roeder (Laboratory of Biochemistry and Molecular Biology, The Rockefeller University, New York), и клонируя в EYFP-N1 (SacI/ApaI). EYFP-Topo-IIα создавали переключением метки EGFP (EcoRI blunt/NheI) на метку EYFP (XhoI blunt/NheI) в EGFP-Topo-IIα (pT104-1) (Mo и Beck, 1999), великодушно предложенной William Т. Beck (Division of Molecular Pharmacology, Department of Molecular Genetics, University of Illinois, Chicago). Конструкции hABH21-7-EYFP, включая мутанты F4, получали отжигом олиго с "липким" концом XhoI/EcoRI с последующим клонированием в EYFP-N1, мутированный в кодоне ATG. Все точечные мутации создавали с помощью сайт-направленного мутагенеза в соответствии с руководством QuickChange® II. Ферменты рестрикции и телячью кишечную щелочную фосфатазу (CIP) получали от England Biolabs® Inc. и олигонуклеотиды получали от MedProbe, Eurogentech (Oslo, Norway). Все конструкции подтверждали секвенированием.
Получение конфокальных изображений и измерения FRET Живые клетки HeLa изучали через 16-24 часа после транзиторной трансфекции (при помощи Fugene 6 (Roche Inc.) в соответствии с рекомендациями изготовителя) слитых конструкций ECFP и EYFP. Флуоресцентные изображения получали, используя лазерный сканирующий микроскоп Zeiss LSM 510 Meta, оборудованный масляно-иммерсионным объективом Plan-Apochromate 63х/1,4. Улучшенный голубой флуоресцентный белок (ECFP) возбуждали при λ=458 нм и определяли при λ=470-500 нм, и улучшенный желтый флуоресцентный белок (EYFP) возбуждали при λ=514 нм и определяли при λ=530-600 нм, используя непрерывное сканирование. Толщина среза составляла 1 мкм.
Флуоресцентный резонансный перенос энергии (FRET) происходит, если метки (EYFP и ECFP) находятся на расстоянии менее 100 Å (10 нм). Авторы изобретения определяли FRET, используя метод сенсибилизированной эмиссии, измеряя эмиссию акцептора (EYFP) после возбуждения донора (ECFP). Авторы изобретения получали FRET, когда интенсивность излучаемого света от EYFP после возбуждения ECFP-флуорохрома была сильнее, чем у света, излучаемого самими ECFP- или EYFP-меченными белками, после того как возбуждение EYFP- и ECFP-лазерами соответственно (просачивание), заданное уравнением: FRET=I2-I1(ID2/ID1)-I3(IA2/IA3) было >0. FRET нормализовали к уровням экспрессии, используя уравнение: NFRET=fret/(I1×b)1/2. NFREГ рассчитывали из средних интенсивностей (I) в интересующей области (ROI), содержащей более 25 пикселей, где все пиксели имели интенсивности ниже 250, и средние интенсивности равнялись 100-200 для конструкций как донора, так и акцептора. Канал 1 (ECFP) и 3 (EYFP) измеряли, как описано выше для получения изображения, и канал 2 (FRET) возбуждали при λ=458 нм и определяли при λ=530-600 нм. ID1, D2, D3 и IA1, А2, A3 определяли для клеток, трансфицированных только конструкциями ECFP и EYFP, с теми же параметрами настройки и такими же интенсивностями флуоресценции, как для совместно трансфицированных клеток (I1 и I3). ECFP-PCNA и EYFP-PCNA были включены в качестве положительных контролей, и вследствие димеризации совместно экспрессируемых меток, белки ECFP и EYFP, экспрессированные с пустых векторов, были включены в качестве отрицательных контролей во все эксперименты.
Культивирование клеточных линий и получение клеточных экстрактов
Клетки HeLa (рак шейки матки) и НаСаТ (спонтанно трансформированный кератиноцит), стабильно экспрессирующие интересующие конструкции, получали трансфекцией (при помощи Fugene 6) с последующей сортировкой клеток или клонированном посредством серийных разведений, и продолжительного культивирования в селективной (используя гентицин, G418, 400 мкг/мл, Invitrogen) модифицированной Дульбекко среде Игла с высоким содержанием глюкозы 4,5 г/л (DMEM) (BioWhittaker®) с добавлением 10% фетальной телячьей сывороткой (FCS), амфотерицина В (250 мкг/мл, Sigma-Aldrich), гентамицина (100 мкг/мл, Gibco) и глутамина (1 мМ, BioWhittaker®). Клетки культивировали при 37°С в 5% двуокиси углерода, влажной атмосфере. Фракционированные клеточные экстракты из HeLa получали ресуспендированием клеточного остатка в 1х гематокрите (PCV) в буфере I (10 мМ Трис-HCl, рН 8,0 и 50 мМ KCl) и 1х PCV в буфере II (10 мМ Трис-HCl, 100 мМ KCI, 20% глицерин, 0,5% Nonidet P-40, 10 мМ EGTA, 10 мМ MgCl2, 1 мМ DTT), 1х полном ингибиторе протеазы (Roche), смеси ингибиторов фосфатаз (PIC I и PIC II, Sigma). Клетки инкубировали при постоянном встряхивании в течение 30 мин при 4°С. Собирали надосадочную жидкость (растворимую фракцию). Осадок (содержащий ядра) ресуспендировали в 1х PCV с буфером III (10 мМ Трис-HCl, рН 8,0 и 100 мМ KCl) и 1x PCV буфере II, и в течение короткого времени обрабатывали ультразвуком вплоть до разрушения всех ядер. 750 мкг фракции, содержащей нуклеоли, центрифуговали, и осадок (хроматин-связывающую фракцию) ресуспендировали в буфере II и III. Хроматин-связывающую фракцию инкубировали со смесью ДНКаза/РНКаза (2 мкл эндонуклеазы Omnicleave® (200 Ед/мкл, Epicentre® Biotecnologies, WI), 2 мкл ДНКазы (10 Ед/мкл, Roche Inc.), 2 мкл бензоназы (250 Ед/мкл, Novagene, Ge), 2 мкл нуклеазы микрококков (100-300 Ед/мкл, Sigma- Aldrich) и 2 мкл РНКазы (10 мг/мл, Sigma-Aldrich) в течение 30 мин при комнатной температуре и 1 ч при 37°С. 750 мкг растворимой фракции инкубировали с дополнительными 2 мкл Omnicleave® в течение ночи при 4°С во время IP.
Совместная иммунопреципитация (co-IP) и вестерн-анализ (WB). Очищенные кроличьи поликлональные антитела с внутренней аффинностью, полученные против белка GFP, который также распознает белки EYFP и ECFP, ковалентно связывали с парамагнитными гранулами белка-А (Dynal®), согласно методике от New England Biolabs® Inc (всюду далее называемыми гранулами α-GFP). Каждую фракцию инкубировали с гранулами a-GFP (10 мкл) при постоянном вращении при 4°С в течение ночи (IP). После IP гранулы промывали 4 раза при помощи 200 мкл 10 мМ Трис-HCl, 50 мМ KCl (рН 7,5), с 5 мин инкубацией на льду в промежутках. Затем гранулы ресуспендировали в загрузочном буфере NuPAGE® (Invitrogen) и 1 мМ DTT, нагревали, и разделяли на гелях 10% или 4-12% бис-Трис-HCl (NuPAGE®) и переносили на мембраны PVDF (Immobilon®, Millipore). Мембраны блокировали в течение 1 ч в 5% сухом молоке с низким содержанием жира в PBST (PBS с 0,1% Tween®20). Первичные антитела, a-PCNA (PCIO, Santa Cruz biotechnology Inc.) и α-GFP разводили в 1% сухом молоке в PBST и инкубировали в течение 1 ч, с последующим 1 ч инкубации с вторичными антителами, поликлональными антителами кролика против мышиного IgG/HRP и поликлональными антителами свиньи против кроличьего IgG/HRP, соответственно (DakoCytomation, Denmark). Мембраны обрабатывали хемилюминесцентным реагентом (SuperSignal® West Femto Maximum, PIERCE), и белки визуализировали на Kodak Image Station 2000R.
Анализ последовательности
Для анализа исходной последовательности использовали базы данных Swiss-Prot и TrEMBL, чтобы обнаружить белки с суб-последовательностями, подобными последовательности интересующей области. В базах данных запрашивали мотивы в формате PROSITE. Для выравнивания интересующих последовательностей использовали Clustal W. Консервативные мотивы, перечисленные в дополнительном файле 1, идентифицировали путем сравнения ортологов генов. Файлы данных для версии Inparanoid 5.1 загружали с веб-сервера Inparanoid <http://inparanoid.sbc.su.se/> для типичной подгруппы организмов. Последовательности человека использовали в качестве сравнения, и искали обработанный Inparanoid fasta файл с регулярной экспрессией мотива APIM, используя локальный инструмент. Использовали слегка расширенное определение мотива, где Ala допускался в положении 3 или положении 4 мотива, в дополнение к lie, Val и Leu, но не в обоих положениях одновременно. Из общего количества 22218 белковых последовательностей, имелись 636 последовательности по меньшей мере с одним совпадением с мотивом APIM. Эти вводимые данные сопоставляли с экспериментальными и прогнозируемой субклеточной локализацией в базе данных eSLDB, загруженной с веб-сервера <http://gpcr.biocomp.unibo.it/esldb/>, и удаляли 349 вводимых данных без указания нацеливания на ядро. Для оставшихся 287 вводимых данных идентифицировали соответствующие Inpranoid ортологи, соответствующие последовательностями извлекали из fasta файлов, и полученные библиотеки последовательностей выравнивали при помощи Clustal W.
Вводимые данные 24 последовательностей без ортологов в Inparanoid исключали из анализа. Два различных способа использовали параллельно для идентификации консервативных участков. В первом методе (консенсусный) консенсусную последовательность устанавливали из множественного выравнивания для каждого совпадающего положения в последовательности человека. При определении консенсусные эквивалентные символы в консервативном мотиве APIM (без Ala) обрабатывали как эквивалентные символы для определения консенсуса, так что, например, Ile, Val и Leu обрабатывали как остатки одного типа. Нормальную экспрессию тестировали повторно на консенсус перед признанием совпадающего положения. В альтернативном методе (индивидуальный) нормальную экспрессию тестировали для каждой ортологической субпоследовательности, соответствующей совпадающему положению в последовательности человека, и были признаны только те положения, где по меньшей мере 50% ортологов совпадают по экспрессии. При такой оценке были исключены субпоследовательности, состоящие только из пробелов, полагая, что они могут представлять собой, например, альтернативные сплайс-варианты. Эти два метода давали почти идентичные результаты, и суммарный выход показан в Дополнительном файле 1. В итоге этим методом были исключены 37 вводимых данных, остающиеся 226 вводимых данных были упорядочены и проанализированы. Описания белков, использованные на выходе, были взяты из Inparanoid unprocessed human (необработанный, для человека) fasta файла и EnsembI release 45. Выходной файл представлен в формате html и может быть открыт при помощи стандартного веб-браузера.
Дот-блот анализ прогнозируемых PCNA-связывающих пептидов
Лист амино-PEG500-UC540 (кислотозащищенный с повышенной стабильностью), содержащий пятна 28 нмоль пептида (окрашенные понсо для визуализации пятен), получали в лаборатории пептидного синтеза в Центре биотехнологии Университета в Осло, Норвегия. Мембрану тестировали при помощи 1 мкг/мл PCNA в течение 2 ч, Затем тестировали с первичным антителом (α-PCNA, PCIO) и проявляли как описано выше для WB (вестерн-блоттинг).
Анализ выживаемости клеток
Клетки HeLa и НаСаТ сеяли в 96-луночные планшеты (4000 клеток/лунка) и инкубировали в течение 4 часов. В лунки добавляли различные дозы MMS (метилметансульфонат, Acros), BCNU (1,3-бис(2-хлорэтил)-1-нитрозомочевина, Sigma), темозоломида (4-метил-5-оксо-2,3,4,6,8-пентазабицикло-[4.3.0]-нона-2,7,9-триен-9-карбоксамида, TZM, Sigma) и митомицина С (6-амино-1,1 а,2,8,8а,8b-гексагидро-8-(гидроксиметил)-8а-метокси-5-метил-азирино[2',3',3,4]-пирроло[1,2-а]индол-4,7-дион-карбамат, ММС, Sigma). Клетки U20S подвергали воздействию только MMS и TMZ. Клетки подвергали воздействию непрерывно вплоть до сбора. Клетки собирали каждый день в течение 4 суток, используя МТТ-анализ (Mosmann, 1983). OD (оптическую плотность) измеряли при 570 нм, и среднее значение из по меньшей мере 6 лунок использовали для расчета выживаемости клеток. Представленные данные являются ростом в одном типичном эксперименте и были воспроизведены по меньшей мере 2 раза.
Пример 1
Данное исследование, описанное в этом Примере, изучает локализацию ПАВН2 в фокусе репликации и идентифицирует прямое взаимодействие между ПАВН2 и PCNA, и участок ПАВН2, отвечающий за такое взаимодействие.
В живых клетках S-фазы PCNA, меченый зеленым флуоресцентным белком (EGFP) образует четкий фокус, представляющий участки репликации и, таким образом, он может быть использован в качестве маркера S-фазы.
PCNA, меченый голубым флуоресцентным белком (ECFP) совместно экспрессировали с различными делеционными конструкциями hABH2, слитыми с желтым флуоресцентным белком (EYFP). Было обнаружено, что делеция 10 N-концевых аминокислот в ПАВН2 (hABH211-261-EYFP) полностью аннулировала совместную локализацию с PCNA в фокусе репликации. Неожиданно то, что если данные 10 аминокислот были слиты с EYFP (с получением конструкции, названной hABH21-10-EYFP), их было достаточно для совместной локализации с PCNA. (Фиг.1). В частности, совместная экспрессия ECFP-PCNA увеличивала локализацию полноразмерного ПАВН2 (hABH21-261-EYFP), а также hABH21-10-EYFP в фокусе ядра по сравнению с клетками, экспрессирующими только конструкции ПАВН2. Это свидетельствует о прямом взаимодействии между PCNA и hABH2, опосредованном 10 N-концевыми аминокислотами hABFO.
Для изучения степени близости hABH2 и PCNA измеряли флуоресцентный резонансный перенос энергии (FRET). Оба полноразмерные hABH2-EYFP и hABH21-10-EYFP создавали положительный FRET с ECFP-PCNA, демонстрируя, что расстояние между флуоресцентными метками составляет менее 100 Å. Это свидетельствует о том, что варианты hABH2 непосредственно взаимодействуют с таким же комплексом как ECFP-PCNA или находятся в нем (Фиг.2).
Для подтверждения прямого взаимодействия изучали совместную иммунопреципитацию, используя белковые экстракты из клеток, стабильно экспрессирующих hABH2-EYFP, hABH211-261-EYFP, hABH21-10-EYFP или EYFP. Анти-GFP антитела использовали для иммунопреципитации соответствующих слитых белков. Последующие вестерн-блоттинг анализы показали, что эндогенный PCNA ослабляли hABH21-216-EYFP и hABH21-10-EYFP, но не hABH211-261-EYFP или EYFP. Взятые вместе, эти результаты свидетельствуют о том, что hABH2 непосредственно взаимодействует с PCNA и что связывающая последовательность содержится в рамках 10 N-концевых аминокислот hABH2.
Пример 2
Тестировали способность hABH2i.io ингибировать hABH2.
Клеточные линии, экспрессирующие только hABH21-10-EYFP или EYFP, подвергали воздействию алкилирующих агентов: MMS (метилметансульфонат), BCNU (кармустин), темозоломида (TZM) или митомицина С (ММС). MMS представляет собой алкилирующий агент SN2, приводящий к 3-метилцитозину (3meC) и 1-метиладенину (1meA), которые репарируют при помощи hABH2, в то время как BCNU представляет собой О6-хлорэтилирующий агент, который главным образом приводит к межнитевым поперечным связям, а также к некоторым моноосновным циклическим аддуктам (1,N(6)этанаденин). Сообщают, что TZM представляет собой O6G-метилирующий агент, в то время как ММС инициирует межнитевые связи путем N-алкилирования гуанина в CpG.
Сверхэкспрессия hABH21-10-EYFP или EYFP не мешает скорости роста необработанных клеток; однако было обнаружено, что экспрессия hABH21-10-EYFP повышала чувствительность клеток HeLa к обработке при помощи MMS. Также неожиданно обнаружилось, что экспрессия hABH21-10-EYFP повышала чувствительность клеток HeLa ко всем другим испытанным цитостатическим агентам (Фиг.3). Это указывает на то, что повышенная чувствительность была вызвана не только ингибированием hABH2, который, как полагают, главным образом репарирует 3meC и 1meA.
Из предыдущего исследования известно, что мышиные клетки Abh2-/-, то есть нокаутные клетки АВН2, демонстрируют повышенную чувствительность к MMS, но не к BCNU. Таким образом, повышенная чувствительность клеток, экспрессирующих hABH21-10-EYFP, к цитостатическим агентам, таким как BCNU, не может быть объяснена только ингибированием hABH2.
Клетки НаСаТ (спонтанно трансформированный кератиноцит), стабильно экспрессирующие hABH21-10-EYFP, также были гиперчувствительными к MMS и TMZ.
Проточный и кометный анализ клеток после обработки разными алкилирующими агентами показал, что лекарственные средства воздействовали на клеточный цикл по-разному и индуцировали разные уровни и структуры промежуточных соединений в репарации ДНК (участки с удаленными азотистыми основаниями, SSB (однонитевые разрывы), DSB (двухнитевые разрывы)), как определено кометным анализом. MMS приводит к задержке S-фазы (1 сутки) и дает самые высокие уровни промежуточных соединений в репарации ДНК после 4 часов. Однако клетки, обработанные MMS, демонстрировали нормальное распределение клеточного цикла и отсутствие повышенных уровней промежуточных соединений репарации ДНК на 2 сутки. Подобно MMS, TMZ также приводит к самым высоким уровням промежуточных соединений репарации через 4 часов, однако клетки задерживались на G2/M вплоть до 3 суток, что указывало на другое повреждение и характер репарации. TMZ также индуцировал больше нитевых разрывов, чем все три другие испытанные агента. Это является неожиданным, так как предполагалось, что TMZ индуцирует главным образом O6метил-О, который репарируют механизмом прямой репарацией при помощи MGMT, не вовлекая удаление каких-либо оснований или разрывы нитей. Обработка BCNU приводит к временному торможению G2/M в 1 сутки и к очень низким уровням промежуточных соединений репарации, указывая на то, что большинство клеток, содержащих поперечные связи, погибли. Обработка ММС, с другой стороны, приводит к торможению S-фазы на 1 и 2 сутки, и это было более ярко выражено для клеток, экспрессирующих hABH21-10-EYFP, чем для контрольных клеток. Клетки по-прежнему были замедленными на G2/M на 3 сутки. В кометном анализе после обработки ММС не наблюдалось значительных различий между клеточными линиями, но количество промежуточных соединений репарации достигло верхней границы на 2 сутки.
В общем, при помощи кометного анализа было невозможно определить какие-либо значительные различия в количестве промежуточных соединений репарации между клетками, экспрессирующими EYFP и hABH21-10-EYFP. Кометный и проточный анализ показывают, что разные используемые агенты индуцируют как разные ответы от клеточного цикла, так и разные характеры репарации. Однако все агенты имели повышенную цитотоксичность в клетках, экспрессирующих APIM, по сравнению с клетками, экспрессирующими EYFP, таким образом подтверждая роль некоторых белков, содержащих APIM, в регуляции между репарацией или клеточной смертью.
Пример 3
Выравнивание последовательностей АВН2 от различных видов показало, что 7 N-концевых аминокислот являются высококонсервативными (Фиг. 4). Для идентификации связывающей последовательности изучали значимость этих аминокислот для взаимодействия пептид-PCNA, используя дот-блот анализ. Между прочим было обнаружено, что Arg3 и Lys7 могли заменять друг друга, и что Leu5 и Val6 могли быть заменены одна другой или другими алифатическими аминокислотами, такими как Не и Ala, без влияния на видимую аффинность к PCNA. Более того, полностью консервативная ароматическая аминокислота Phe4 могла быть заменена Tyr, тогда как Ala в данном положении значительно снижал связывание PCNA.
Замены аминокислот 1-2 и 8-10 на Ala не влияют на связывание PCNA, позволяя предположить, что пентапептид RFLVK (SEQ ID NO:2) является последовательностью, взаимодействующей с ядром.
Дальнейшие анализы показали, что данный пентапептид сам по себе был достаточным для связывания PCNA, но дополнительные фланкирующие аминокислоты усиливали взаимодействие.
Затем аминокислоты 1-7 в hABH2 и варианты данной последовательности, в которых Phe4 заменен на Tyr, Trp или Ala, экспрессировали в слиянии с EYFP и тестировали в отношении совместной локализации с PCNA in vivo. Подобно обнаруженному в дот-блот анализе, слитые белки, содержащие ароматическую аминокислоту в положении 4, были совместно локализованы с ECFP-PCNA, в то время как белки с Ala в этом положении не были совместно локализованы.
Пример 4
Базы данных Swiss-Prot и TrEMBL использовали для поиска белков с субпоследовательностями, аналогичными последовательности, которая была идентифицирована как ответственная за связывание hABH2 с PCNA. Используя консенсус [KR]-[FYW]-[LIVA]-[LIVA]-[KR] (SEQ ID NO:30) в качестве запроса, получили 226 совпадений (обобщенные результаты смотри в Таблице 1), из которых несколько человеческих белков были выбраны для дальнейшего анализа.
Первым был белок, который подобно hABH2 содержит вышеуказанную консенсусную последовательность в рамках ее 7 N-концевых аминокислот. Такой белок также содержит консервативный N-конечный домен I, обнаруженный в факторе элонгации TFIIS, важном белке для развития остановленной транскрипции. Авторы изобретения назвали данный белок TFIIS-подобным белком (TFIIS-L). Функция этого белка неизвестна.
Второй белок представлял собой многофункциональный транскрипционный фактор TFII-I, который содержит 4 консенсусные последовательности. TFII-I является критически важным для регулирования клеточного цикла и пролиферации, и клетки, сверхэкспрессирующие TFII-I, имеют повышенную устойчивость фокуса Y-H2AX (маркера двухнитевых разрывов ДНК), что подтверждает роль TFII-I в репарации ДНК.
Также изучали ДНК-топоизомеразу II альфа (Торо II α), содержащую одну консенсусную последовательность. Торо II α функционирует в пострепликационном расцеплении ДНК и сегрегации ДНК.
Консенсусную последовательность также обнаружили внутри ключевого белка эксцизионной репарации нуклеотидов (NER) XPA (Xeroderma pigmentosum группы А), который распознает спиральные изгибы.
Консенсусную последовательность обнаружили в RAD51B, гомологичном рекомбинантном белке, который, как было показано, является важным для правильного фукционирования центросом и сегрегации хромосом.
Другой белок представлял собой белок ядерного комплекса анемии Фанкони, FANCC, который, как было обнаружено, содержит одну консенсусную последовательность. Анемия Фанкони (FA) представляет собой редкое генетическое расстройство, характеризующееся апластической анемией, повышенной подверженностью к лейкемии и гиперчувствительностью к сшивающим агентам. Было показано, что ядерный комплекс FA включен в сигнальный путь, активирующий повреждение ДНК, регулируя репарацию ДНК сшивающими агентами.
Во всех этих белках было обнаружено, что предполагаемый PCNA-связывающий мотив является консервативным для разных видов (Фиг. 5). Сообщалось, что среди этих пяти белков только Торо II α и FANCC (после повреждения) локализуются совместно с BRCAI в фокусах ядра S-фазы, и Торо II α представляет собой единственный белок, содержащий потенциальный PIP-бокс (QttLaFkp, а.к. 1277-84). Теперь авторы изобретения доказали, что слитые с EYFP белки всех без исключения этих белков локализуются совместно с ECFP-PCNA в фокусах S-фазы.
Другие интересные обнаруженные APIM-содержащие белки являются членами семейства поли(АОР(аденозиндифосфат)-рибоз) (PARP-1, 2 и 4), вовлеченных в некоторые процессы сохранения ДНК, включающие репарацию ДНК, партнера PARP-1 и Тоpо II α изоформы ДНК-топоизомеразы II бета, вовлеченных в разрешение топологических проблем, вызванных репликационными вилками. Кроме того, APIM обнаружен в субъединице REV3L транслезионной полимеразы ζ, вовлеченной как в точечный мутагенез, так и в более крупномасштабную геномную стабильность, в ДНК-лигазе I и IV, вовлеченной как в репликацию, так и в репарацию ДНК, в четырех убиквитин-протеин-лигазах Е3 (UHRF1 и UHRF2/NIRF, UBR1 и 2), все из которых вовлечены в регуляцию клеточного цикла, сохранение генома и его целостности, а также в некоторых других убиквитин-лигазах Е3 (Таблица 1). Интересно, что убиквитин-лигаза ЕЗ часто была показана генетически и экспрессионно измененной при образовании опухоли молочной железы. Также содержащей APIM является N-ацетилтрансфераза ESC01/EF01, белок, чей дрожжевой ортолог связывает PCNA при помощи своего усеченного PIP-бокса, и который вовлечен в правильную когезию сестринских хроматид, и сохранение структурного хромосомного белка 5 человека, hSMC5, который, как показано, вовлечен в репарацию двухнитевых разрывов ДНК посредством HR и в сохранение теломеров в клетках ALT (альтернативное удлинение теломеров). Наконец, было обнаружено, что некоторые субъединицы основных транскрипционных факторов II и III, субъединицы РНК-полимеразы II и серин/треонин-протеинкиназ содержат мотив APIM (Таблица 1).
Жирный шрифт: белки, локализованные в фокусах репликации при нормальных условиях или после повреждения ДНК. Данное исследование* или в другом месте:
1G.L.Moldovan, В.Pfander, and S.Jentsch, Cell 129 (4), 665 (2007).
2Z.Lou, К. Minter-Dykhouse, and J. Chen, Nat Struct Mol В/о/12 (7), 589 (2005); A.Niimi, N.Suka, M.Harata et al., Chromosome 110 (2), 102 (2001).
3С.M.Simbulan-Rosenthal, D.S.Rosenthal, S.Iyer et al., Molecular and cellular biochemistry 193 (1-2), 137 (1999).
4С.Jacquemont and T.Taniguchi, BMC biochemistry Q SuppI I, SIO (2007).
5P.R.Potts, M.H.Porteus, and H.Yu, Embo J25 (14), 3377 (2006).
6P.L.Opresko, M.Otterlei, J.Graakjaer et al., Mol Cell 14 (6), 763 (2004).
Пример 5
Экспериментально изучали функцию консенсусной последовательности в белках, исследованных в Примере 4. Так как замена ароматической аминокислоты Phe в консенсусной последовательности на Ala аннулировала взаимодействие с PCNA in vitro и совместную локализацию с PCNA in vivo, изучали, оказывает ли соответствующая мутация подобный эффект на полноразмерные белки. Мутация Phe4 на Ala в полноразмерном hABH2 аннулировала совместную локализацию с PCNA. В TFII-I, содержащем 4 мотива, остатки Phe (F431A, F536A, F641 А и F803A) были замены отдельно и совместно на Ala. Одна мутация не уменьшала совместную локализацию с PCNA, но мутации во всех консенсусных последовательностях в TFII-I значительно уменьшали совместную локализацию с PCNA в фокусах репликации, это указывало на то, что некоторые мотивы консенсусной последовательности, присутствующие в том же белке, могут вносить вклад в оптимальное PCNA-взаимодействие.
Ссылки
Aas, PA, Otterlei, M., Falnes, P.O., Vagbo, C.B., Skorpen, F., Akbari, M., Sundheim, O., Bjoras, M., Slupphaug, G., Seeberg, E., and Krokan, H.E. (2003). Human and bacterial oxidative demethylases repair alkylation damage in both RNA and DNA. Nature 421, 859-863.
Mp, Y.Y., and Beck, W.T. (1999). Association of human DNA topoisomerase ll-alfa with mitotic chromosomes in mammalian cells is independent of its catalytic activity. Experimental cell research 252, 50-62.
Mosmann, Т. (1983). Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays. Journal of immunological methods 65, 55-63.
Rademakers, S., Volker, M., Hoogstraten, D., Nigg, A.L, Mone, M. J., Van Zeeland, A.A., Hoeijmakers, J.FL, Houtsmuller, A.B., and Vermeulen, W. (2003). Xeroderma pigmentosum group A protein loads as a separate factor onto DNA lesions. Mol Cell Biol 23, 5755-5767.
Roy, A.L., Malik, S., Meisterernst, M., and Roeder, R.G. (1993). An alternative pathway for transcription initiation involving TFII-I. Nature 365, 355-359.
Пример 6
Получение и испытание конструкций, содержащих мотив ("APIM") - содержащий пептид с сигнальными последовательностями
Пептиды SEQ ID NO:98-117 синтезировали, используя стандартные способы, и вводили флуоресцентные метки, где это указано, снова используя стандартные методы. Пептиды показаны в Таблице 3, где представлена аминокислотная последовательность для каждого пептида, а также отдельно перечислены индивидуальные компоненты, составляющие каждый пептид (мотив («АР1М»)-содержащий пептид), NLS, СРР и линкеры, когда целесообразно, и используемая метка, где она содержится). Пептиды SEQ ID NO:98-116 составлены из L-аминокислот. Пептид RI-MDR26-3 из SEQ ID NO:117 представляет собой ретро-инверсный пептид, составленный из D-аминокислот. Все пептиды, показанные в Таблице 3, имеют по меньшей мере один APIM-пептид, NLS и СРР.
Были выполнены различные исследования, чтобы продемонстрировать воздействие пептидов на клетки. Так, клетки инкубировали с пептидами для определения локализации пептидов в клетках, используя способы на основе способов, описанных в Примерах выше. В кратком изложении, пептиды, указанные как меченные флуоресцентными метками, инкубировали с клетками (клетки HeLa), и изучали клеточный импорт, используя конфокальную микроскопию.
Действия пептидов в сенсибилизированных клетках на эффекты цитостатических лекарственных средств изучали, используя МТТ-анализ и клоногенный анализ (CFU (анализ колониеобразующих единиц), как описано ниже.
Цитотоксичность пептидов изучали при помощи МТТ-анализа, как описано ниже, используя только пептид в отсутствии цитостатических лекарственных средств. Данные по цитотоксичности также получали от контролей, используемых в МТТ-анализах цитостатических лекарственных средств (контроли с пептидом, но без цитостатического лекарственного средства), где за контрольными пептидами следили в течение более продолжительного срока (4 суток).
Мембранную токсичность изучали снова, как описано ниже.
Стабильность пептидов изучали при помощи М8(масс-спектрометрический)-анализа пептидов после инкубации пептидов в среде, содержащей сыворотку.
МТТ-Анализ
Клетки HeLa высевали в 96-луночные планшеты (6000 клеток/лунка) и инкубировали в течение 3 часов. В лунки добавляли различные дозы MMS и цисплатина. Через 24 часа пептиды добавляли к клеткам в среде, не содержащей сыворотку, и инкубировали в течение 1 ч. Добавляли свежую среду с цитостатическими лекарственными средствами, и клетки собирали через еще 24, 48 и 72 часа. К клеткам добавляли МТТ (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромид), и OD измеряли при 570 нм [52], и среднее значение по меньшей мере из 6 лунок использовали для расчета выживаемости клеток. Данные представлены как рост в одном типичном эксперименте и были воспроизведены по меньшей мере 2 раза.
Клоногенный (CFU) анализ
750 HeLa клеток высевали в 10 см чашки для культивирования клеток в 11 мл ростовой среды, содержащей цитостатические лекарственные средства (MMS). На 2 сутки клетки обрабатывали пептидами в течение одного часа в условиях, не содержащих сыворотку. К клеткам добавляли свежую среду, содержащую свежие цитостатические лекарственные средства для дополнительной инкубации в течение 10 суток. Затем клетки фиксировали в 6% глутаральдегиде в PBS в течение 15 мин при комнатной температуре, промывали один раз в PBS, окрашивали кристаллическим фиолетовым и подсчитывали колониеобразующие единицы. Включали только колонии, состоящие по меньшей мере из 50 клеток.
Анализ цитотоксичности
Цитотоксичность пептидов измеряли через 48 часов, используя МТТ-анализ. Клетки HeLa высевали в 96-луночные планшеты (6000 клетки/лунка) и инкубировали в течение 3 часов. Различные дозы пептидов добавляли в лунки в присутствии или в отсутствие сыворотки в среде. Через 1 ч добавляли равный объем среды, 1Х или 2Х (к среде, не содержащей сыворотку), и клетки инкубировали в течение 48 часов перед добавлением МТТ (смотри выше)
Токсичность для мембран, определенная при помощи проточной цитометрии
Клетки обрабатывали разными концентрациями (2, 4 и 8 мкМ) пептида в течение 1 часа. Затем добавляли пропидия иодид (PI) (50 мкг/мл в PBS), который окрашивает ДНК, когда клеточные мембраны проницаемы. Анализ выполняли в пределах 10 минут на проточном цитометре FACS Canto (BD-Life Science).
Результаты показаны в Таблице 4, из которой видно, что все меченые маркером испытанные пептиды, которые представляют собой по существу конструкции APIM-содержащего пептида с СРР и NLS, локализованы в ядре. Этот эффект обнаружили у пептидов с разными линкерными последовательностями, связывающими отдельные компоненты конструкции, линкерами различной длины, и у пептидов без линкерных последовательностей. Это показывает, что присутствие линкерных последовательностей не является существенным, и линкерная последовательность может варьироваться.
Результаты МТТ- и CFU-экспериментов с цитостатическими агентами показывают эффект пептидов в увеличении ингибирующих рост эффектов цитостатических агентов. Таким образом, пептиды способны повышать чувствительность клеток к действиям цитостатических агентов. Данный эффект аналогичен тому, о котором сообщалось в Примере 2 выше для трансфицированных клеточных линий, экспрессирующих APIM-содержащий пептид.
В Таблице 4 также показан цитотоксический эффект ряда пептидов. Дополнительное экспериментальное исследование (данные не показаны) показало, что более высокий цитотоксический эффект наблюдается для пептидов, которые локализуются в ядре, по сравнению с теми, которые не локализуются в ядре. Эксперимент на мембранную токсичность, выполненный с одним пептидом (MDR2; SEQ ID NO:98), указывает на то, что мембранная токсичность является низкой, это может означать, что цитотоксический эффект, наблюдаемый для пептидов, не связан с мембранным эффектом. Было обнаружено, что в некоторых случаях цитотоксический эффект может наблюдаться только в случае повышенных концентраций пептида (например, при 1 мкМ пептида цитотоксичность может не наблюдаться (хотя наблюдается эффект сенсибилизации клеток к цитостатическому агенту), тогда как при 2 мкМ пептида наблюдается цитотоксический эффект пептид самого по себе, а также сенсибилизирующий эффект).
Результаты в Таблице 4 также показывают, что эффекты пептидов на вхождение в клетку и локализацию в ядре, на сенсибилизацию клеток к цитостатическим агентам и на цитотоксичность могут быть получены с разными последовательностями NLS и/или СРР и, хотя величина или распространение эффекта могут варьироваться, эффекты не зависят от конкретных последовательностей NLS и/или СРР.
В некоторые пептиды, как показано в Таблицах 3 и 4, на N-конце включена Ас-группа. Ее включали с целью стабилизации пептидов, как в сыворотке, так и в цитозоле. Пептид MDR26-72-0 (SEQ ID NO:112) показал хорошую стабильность и хорошую активность в CFU- и МТТ-анализах и испытаниях на цитотоксичность. MDR26-72-0 содержит R-богатую последовательность в качестве СРР. Считается, что одинаково хорошие результаты могут быть получены с эквивалентными пептидами, в которых СРР заменен на СРР, производный от пенетратина или HIV-TAT или основанный на них, где NLS может представлять собой SV40 или быть производной от UNG2).
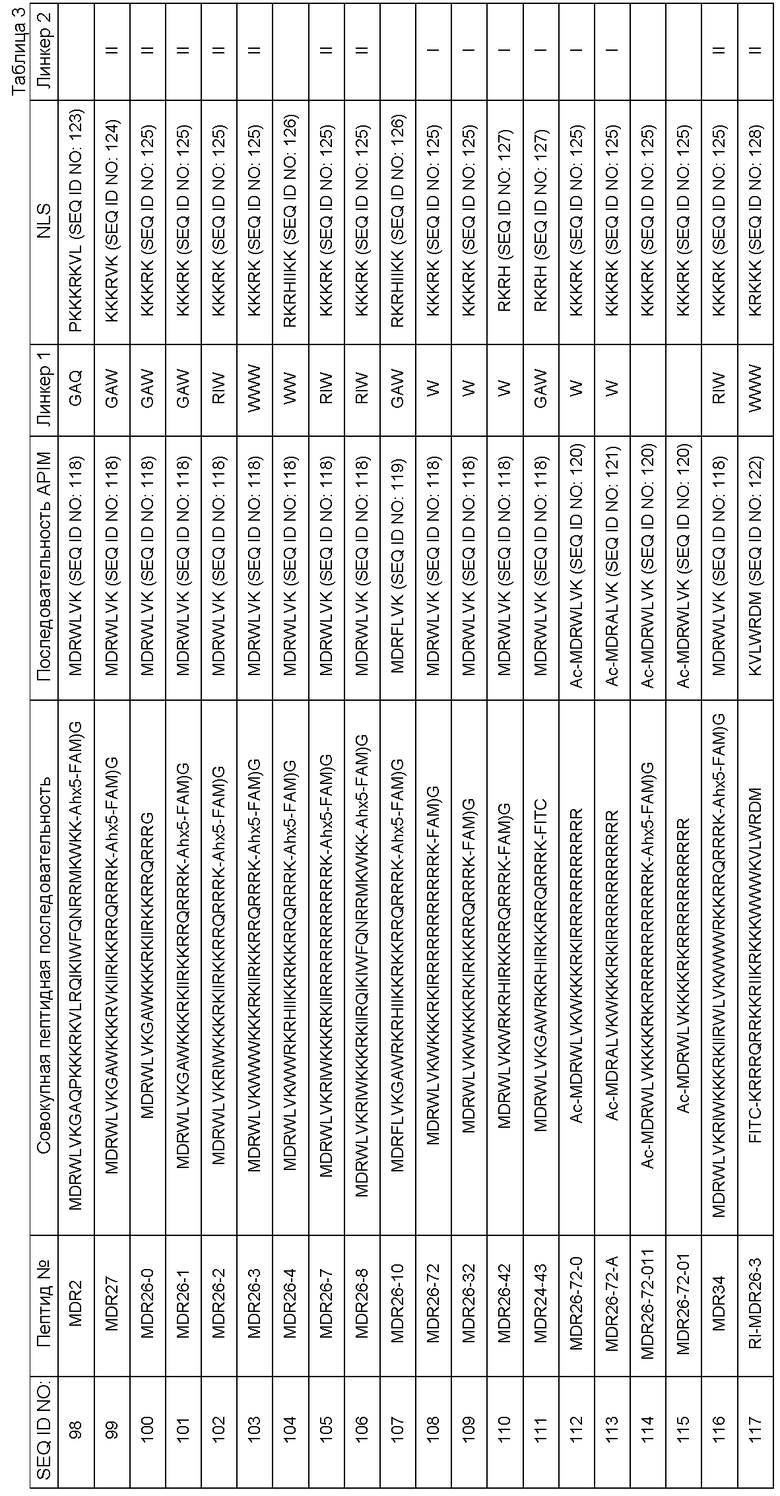
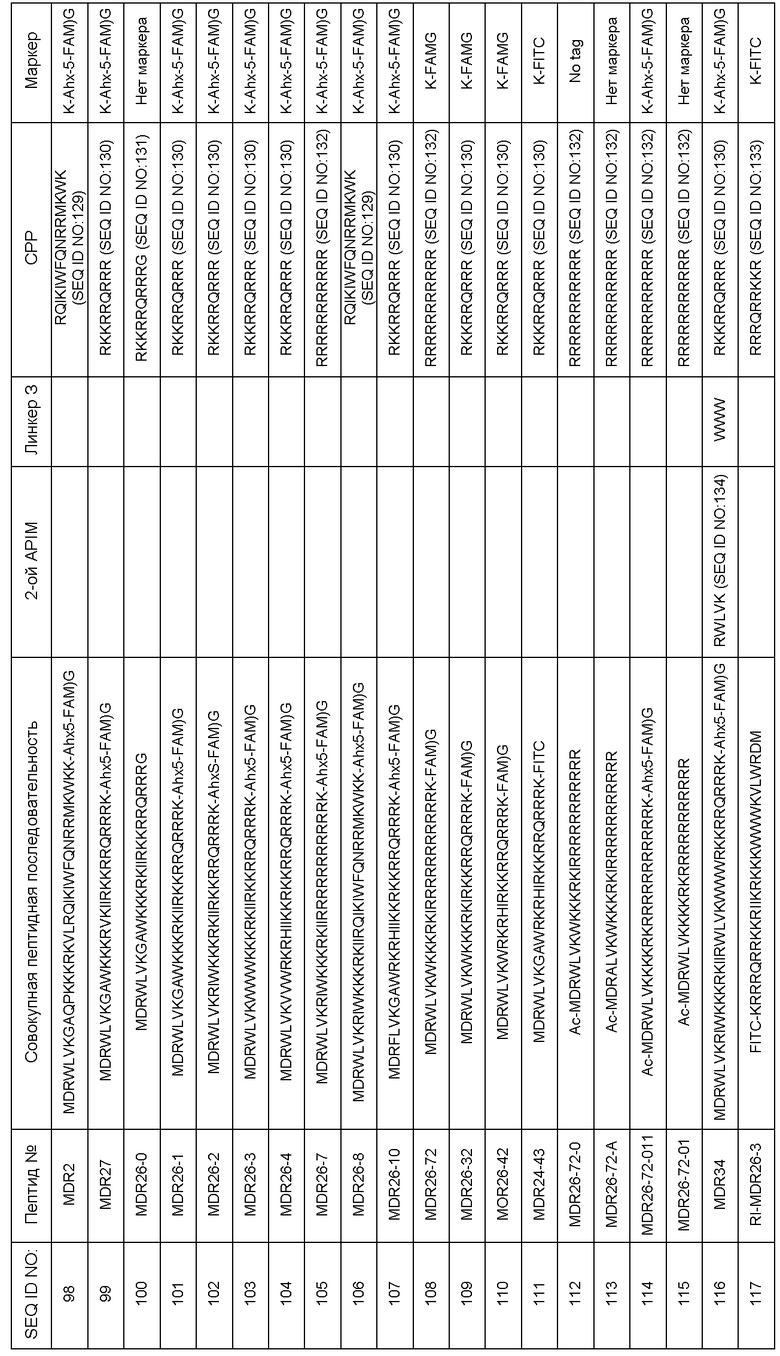

Пример 7
Дополнительные данные по цитоксичности
В этом Примере представлены более подробные данные тестов на цитотоксичность. Анализ на цитотоксичность выполняли, как описано в Примере 6 выше. Результаты представлены на Фиг. 6, где показаны результаты МТТ-анализа цитотоксичности для пептидов MDR26-0 (SEQ ID NO:100), MDR26-3 (SEQ ID NO:103), MDR26-4 (SEQ ID NO:104), MDR26-8 (SEQ ID NO:106), MDR26-7 (SEQ ID NO:105), MDR26-72-0 (SEQ ID NO:112), MDR26- 72-01 (SEQ ID NO:115) и MDR34 (SEQ ID NO:116).
Как можно видеть, может наблюдаться цитотоксичность пептидов, с более значительным эффектом, проявляющимся в отсутствие сыворотки. Цитотоксичность наблюдается для всех вариантных пептидов MDR26, которые имеют один APIM-мотив. Повышенная цитотоксичность наблюдается для вариантов MDR34, которые имеют два APIM-мотива. Аналогичные результаты, демонстрирующие цитотоксичность, получают для пептидов, соответствующих MDR34 (SEQ ID NO:116), которые не имеют метки (MDR34-0), или которые являются инверсными (I-MDR-34) или ретроинверсными (RI-MDR-34) эквивалентами MDR34. MDR34-2, который не имеет последовательности NLS, и который вместо этого имел удлиненную линкерную последовательность IILVIII (SEQ ID NO:95) в качестве линкера 2, показал пониженную цитотоксичность.
Пример 8
Были выполнены дополнительные эксперименты, которые подтверждают взаимодействие между PCNA и APIM-содержащими пептидами. В экспериментах по совместной иммунопреципитации (co-IP) было показано, что как эндогенный PCNA, так и EYFP-PCNA из клеток, стабильно экспрессирующих EYFP-PCNA, были способны понижать hABH2. Значительное взаимодействие, наблюдаемое между hABH2 и PCNA во фракциях, обогащенных хроматином, указывает на посттрансляционные модификации PCNA или hABH2. В данных экспериментах была продемонстрирована co-IP для hABH2 из клеток, стабильно экспрессирующих EYFP-PCNA, с использованием магнитных гранул, соединенных с антителам против α-EYFP. Мембрану зондировали с помощью α-hABH2 и повторно зондировали при помощи антитела α-PCNA. Также была продемонстрирована co-IP hABH2 из клеток, экспрессирующих только эндогенные белки, с использованием магнитных гранул, связанных с антителами против α-PCNA. Мембрану зондировали при помощи a-hABH2 и повторно зондировали с помощью α-PCNA антитела.
Дополнительные эксперименты, показывающие сшивание in vivo, подтверждают непосредственное связывание между АР1М и PCNA. Сшитые и сшитые в обратном направлении слитые белки FLAG из клеток, стабильно экспрессирующих hABH21-7-EYFP 3xFLAG и hABH21-7-F4A-EYFP 3xFLAG иммунопреципитировали, используя аффинный гель α-FLAG. IP (иммунопреципитированные) элюированные фракции анализировали при помощи вестерн-блоттинга, используя αa-PCNA или α-FLAG антитела.




































































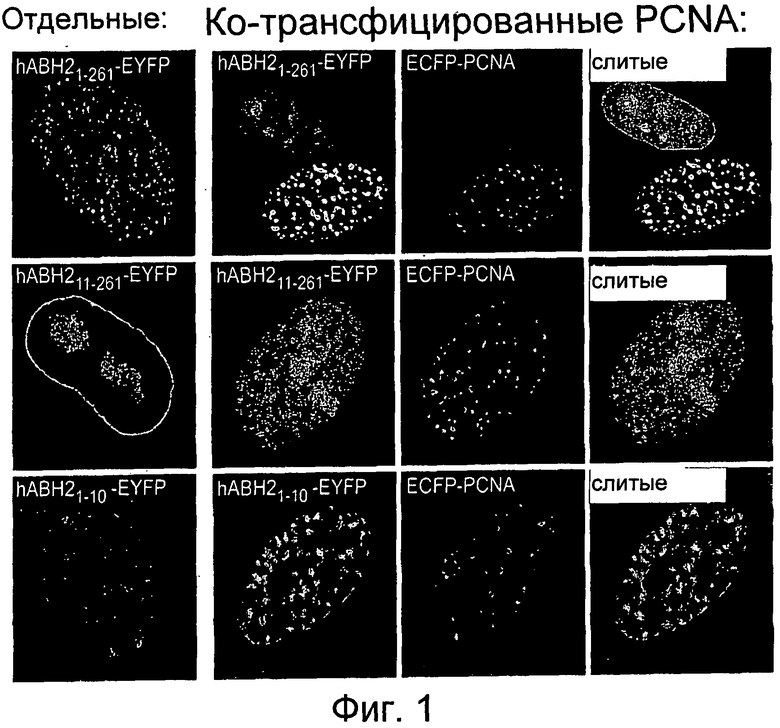
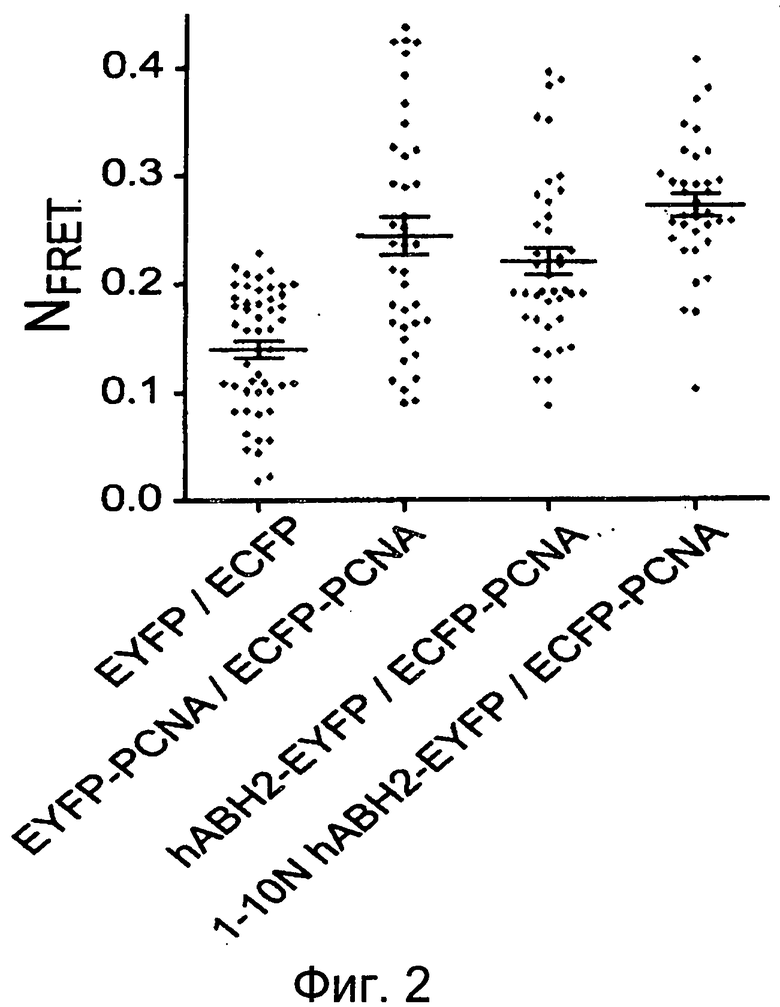

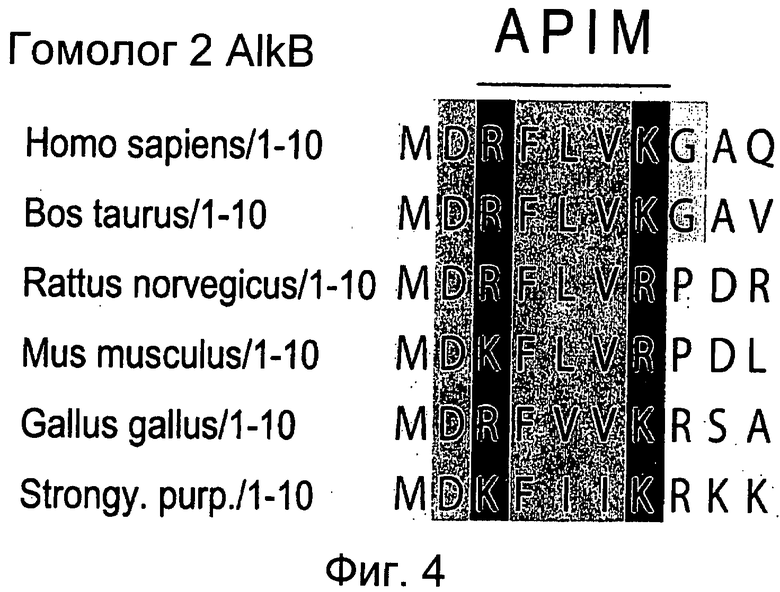

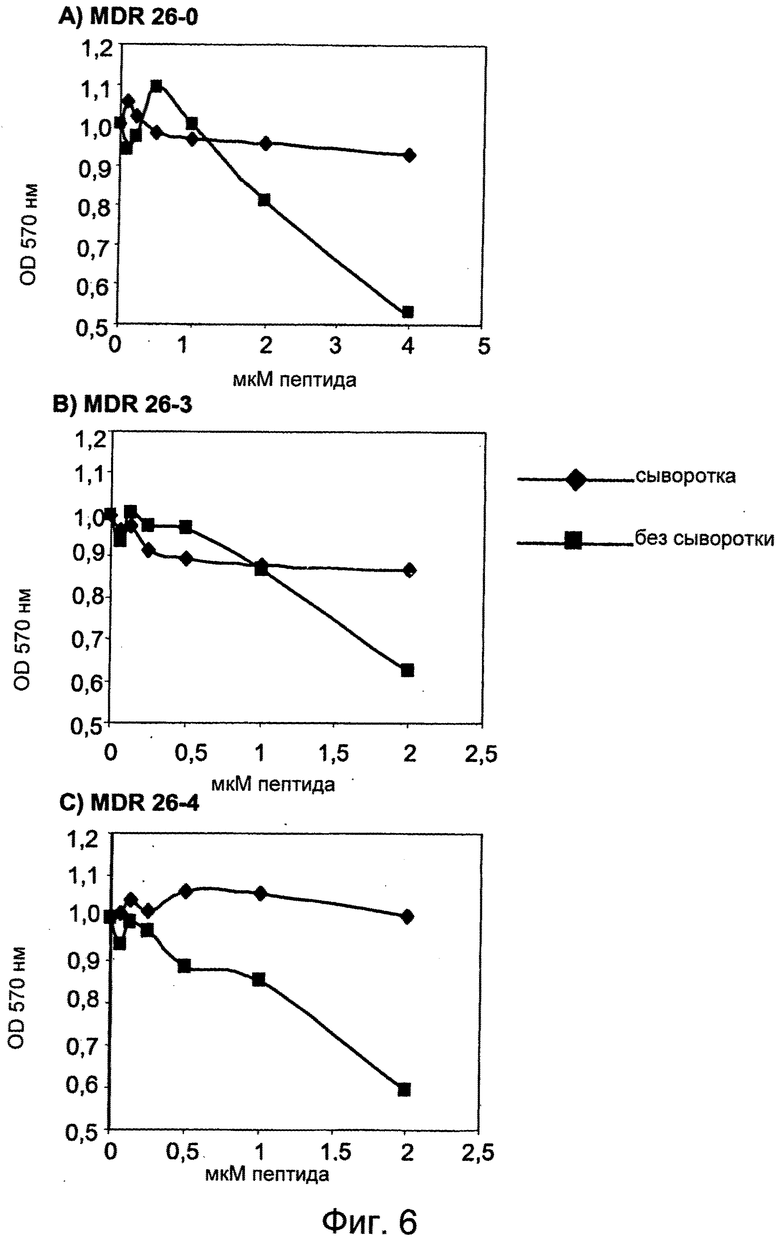
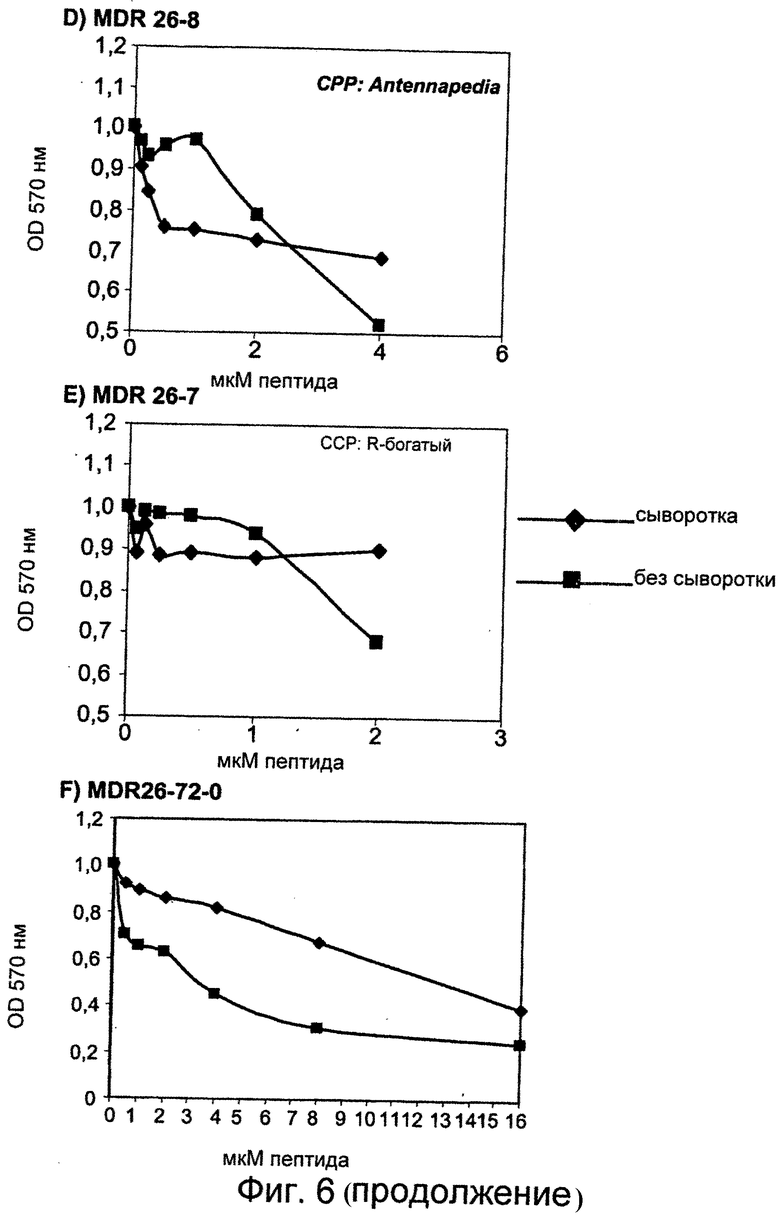
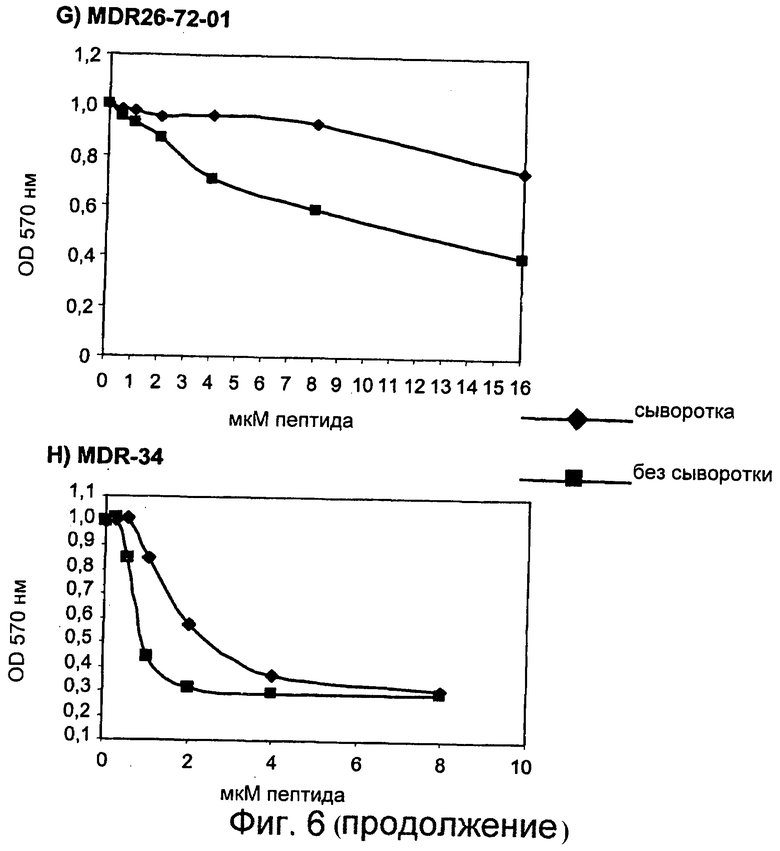
Изобретение относится к области биотехнологии, конкретно к получению олигопептидных соединений, содержащих мотив, взаимодействующий с ядерным антигеном пролиферирующих клеток (PCNA), и может быть использовано в медицине. Олигопептидное соединение состоит из 14-70 аминокислот и содержит PCNA-взаимодействующий мотив, представляющий собой [K/R]-[F/Y/W]-[L/I/V/A]-[L/I/V/A]-[K/R], по меньшей мере одну сигнальную последовательность ядерной локализации и по меньшей мере одну сигнальную последовательность проникновения в клетку, при этом PCNA-взаимодействующий мотив расположен в направлении к N-концу относительно сигнальной последовательности. Изобретение позволяет эффективно лечить гиперпролиферативные расстройства путем использования олигопептидного соединения в цитостатической терапии или в радиотерапии в качестве сенсибилизирующего вещества. 16 н. и 18 з.п. ф-лы, 6 ил., 4 табл., 8 пр.
1. Олигопептидное соединение, содержащее PCNA (ядерный антиген пролиферирующих клеток) - взаимодействующий мотив для применения в лечении, которое включает в себя цитостатическую терапию, или в качестве сенсибилизирующего вещества для радиотерапии,
где PCNA-взаимодействующий мотив представляет собой
 (SEQ ID NO: 30), и
(SEQ ID NO: 30), и
где олигопептидное соединение содержит 14-70 аминокислот и содержит по меньшей мере одну сигнальную последовательность ядерной локализации и по меньшей мере одну сигнальную последовательность проникновения в клетку, где в указанном соединении PCNA-взаимодействующий мотив расположен в направлении к N-концу относительно сигнальной последовательности.
2. Олигопептидное соединение по п. 1, где PCNA-взаимодействующий мотив представляет собой:
 (SEQ ID NO: 31);
(SEQ ID NO: 31);
 (SEQ ID NO: 33);
(SEQ ID NO: 33);
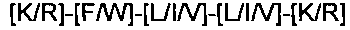 (SEQ ID NO: 34);
(SEQ ID NO: 34);
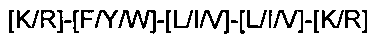 (SEQ ID NO: 35);
(SEQ ID NO: 35);
 (SEQ ID NO: 36); или
(SEQ ID NO: 36); или
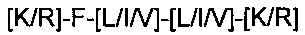 (SEQ ID NO: 37).
(SEQ ID NO: 37).
3. Олигопептидное соединение по п. 1, где PCNA-взаимодействующий мотив имеет последовательность, представленную в SEQ ID NO: 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25.
4. Олигопептидное соединение по п. 1, где сигнальная последовательность проникновения в клетку представляет собой HIV-TAT или пенетратин или их фрагмент или производное.
5. Олигопептидное соединение по п. 1, где цитостатическая терапия включает использование цитостатического агента и где указанное олигопептидное соединение используют вместе, одновременно, раздельно или последовательно с указанным цитостатическим агентом.
6. Олигопептидное соединение по п. 5, где указанный цитостатический агент выбран из MMS (метилметансульфонат), бис-хлорэтилнитрозомочевины, карбоплатина, CCNU (1-(2-хлорэтил)-3-циклогексил-1-нитрозомочевина), цисплатина, циклофосфамида, цитарабина, дакарбазина, доксорубицина, гемцитабина, иринотекана, мелфалана, митомицина C (MMC), оксалиплатина, темозоломида (TZM), треосульфана, 5-азацитидина, 5,6-дигидро-5-азацитидина и 5-фторурацила.
7. Олигопептидное соединение по п. 5, где указанный цитостатический агент представляет собой алкилирующий агент.
8. Олигопептидное соединение по п. 1 для применения в лечении гиперпролиферативного расстройства или в миелоабляции.
9. Олигопептидное соединение по п. 8, где указанное гиперпролиферативное расстройство выбрано из злокачественного, предзлокачественного или незлокачественного неопластического расстройства, воспаления, аутоиммунного расстройства, гематологического расстройства, кожного расстройства, вызванного вирусом гиперпролиферативного расстройства, миелодипластического расстройства или миелопролиферативного расстройства.
10. Олигопептидное соединение по п. 8, где указанное гиперпролиферативное расстройство выбрано из рака, доброкачественных опухолей, псориатического артрита, ревматоидного артрита, воспалительного заболевания кишечника, псориаза, синдрома Рейтера, красного волосистого питириаза, гиперпролиферативных вариантов расстройств кератинизации, рестеноза, диабетической нефропатии, гиперплазии щитовидной железы, базедовой болезни, доброкачественной гиперплазии предстательной железы, синдрома Ли-Фроменти, диабетической ретинопатии, периферического сосудистого заболевания, цервикальной карциномы-in-situ, семейного кишечного полипоза, оральной лейкоплакии, гистиоцитоза, келоидов, гемангиом, гиперпролиферативного артериального стеноза, воспалительного артрита, гиперкератоза, папулосквамозных высыпаний, включающих артрит, бородавки, и EBV (вирус Эпштейна-Барр) - индуцируемое заболевание, образования рубцов, рассеянного склероза, системной красной волчанки (SLE; волчанки), тяжелой псевдопаралитической миастении, незлокачественной гиперплазии, агранулемы, MGUS (моноклональная гаммапатия неясного значения), неопластического менингита, истинной полицитемии, склеромикседемы, папулезного муциноза, амилоидоза и гранулематоза Вегенера.
11. Олигопептидное соединение по п. 1, содержащее PCNA-взаимодействующий мотив, представленный в SEQ ID NO: 18, сигнальную последовательность ядерной локализации, представленную в SEQ ID NO: 125, и сигнальную последовательность проникновения в клетку, представленную в SEQ ID NO: 73.
12. Олигопептидное соединение по п. 11, содержащее последовательность, представленную в SEQ ID NO: 112.
13. Олигопептидное соединение, содержащее PCNA (ядерный антиген пролиферирующих клеток) - взаимодействующий мотив, сигнальную последовательность ядерной локализации и сигнальную последовательность проникновения в клетку, для применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, где соединение характеризуется последовательностью, представленной в любой из SEQ ID NO: 100, 103-106, 112 или 114-116.
14. Применение олигопептидного соединения по п. 13 в изготовлении лекарственного средства для применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток.
15. Применение олигопептидного соединения по любому из пп. 1-12 в изготовлении лекарственного средства для применения в лечении, которое включает в себя цитостатическую терапию.
16. Способ лечения расстройства или состояния, при котором желательно ингибировать рост клеток, включающий введение олигопептидного соединения по п. 13 субъекту, нуждающемуся в этом.
17. Способ лечения, включающий в себя цитостатическую терапию или радиотерапию, включающий введение олигопептидного соединения по любому из пп. 1-12 субъекту, нуждающемуся в этом.
18. Фармацевтическая композиция для применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, содержащая эффективное количество олигопептидного соединения по п. 13 вместе по меньшей мере с одним фармакологически приемлемым носителем или эксципиентом.
19. Фармацевтическая композиция для применения в лечении, включающем в себя цитостатическую терапию, или в качестве сенсибилизирующего вещества для радиотерапии, содержащая эффективное количество олигопептидного соединения по любому из пп. 1-12 вместе по меньшей мере с одним фармакологически приемлемым носителем или эксципиентом.
20. Фармацевтическая композиция по п. 18 или 19, предложенная в форме, подходящей для перорального, парентерального, местного, ректального, генитального, подкожного, трансуретрального, трансдермального, интраназального, внутрибрюшинного, внутримышечного и/или внутривенного введения и/или для введения посредством ингаляции.
21. Набор для применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, или в лечении, которое включает в себя цитостатическую терапию, или в качестве сенсибилизирующего вещества для радиотерапии, содержащий:
(1) олигопептидное соединение по п. 1 и
(2) цитостатический агент.
22. Набор по п. 21, где указанный цитостатический агент выбран из MMS (метилметансульфонат), бис-хлорэтилнитрозомочевины, карбоплатина, CCNU (1-(2-хлорэтил)-3-циклогексил-1-нитрозомочевина), цисплатина, циклофосфамида, цитарабина, дакарбазина, доксорубицина, гемцитабина, иринотекана, мелфалана, митомицина С (ММС), оксалиплатина, темозоломида (TZM), треосульфана, 5-азацитидина, 5,6-дигидро-5-азацитидина и 5-фторурацила.
23. Набор по п. 21, где указанный цитостатический агент представляет собой алкилирующий агент.
24. Фармацевтический комбинированный препарат для одновременного, последовательного или раздельного применения в лечении расстройства или состояния, при котором желательно ингибировать рост клеток, или в лечении, которое включает в себя цитостатическую терапию, содержащий:
(1) олигопептидное соединение по п. 1; и
(2) цитостатический агент
25. Фармацевтический комбинированный препарат по п. 24, где указанный цитостатический агент выбран из MMS (метилметансульфонат), бис-хлорэтилнитрозомочевины, карбоплатина, CCNU (1-(2-хлорэтил)-3-циклогексил-1-нитрозомочевина), цисплатина, циклофосфамида, цитарабина, дакарбазина, доксорубицина, гемцитабина, иринотекана, мелфалана, митомицина C (MMC), оксалиплатина, темозоломида (TZM), треосульфана, 5-азацитидина, 5,6-дигидро-5-азацитидина и 5-фторурацила.
26. Фармацевтический комбинированный препарат по п. 24, где указанный цитостатический агент представляет собой алкилирующий агент.
27. Молекула нуклеиновой кислоты, кодирующая олигопептидное соединение по п. 1.
28. Вектор экспрессии, содержащий молекулу нуклеиновой кислоты по п. 27.
29. Применение олигопептидного соединения по любому из пп. 11-13 или фармацевтического комбинированного препарата по любому из пп. 24-26 в изготовлении лекарственного средства для применения в лечении воспаления.
30. Применение олигопептидного соединения по любому из пп. 11-13 или фармацевтического комбинированного препарата по любому из пп. 24-26 в изготовлении лекарственного средства для лечения рака.
31. Применение по п. 30, где указанный рак выбран из рака мочевого пузыря, рака предстательной железы или гематологического рака, такого так множественная миелома или лейкемия.
32. Способ лечения воспаления, включающий введение олигопептидного соединения по любому из пп. 11-13 или фармацевтического комбинированного препарата по любому из пп. 24-26 субъекту, нуждающемуся в этом.
33. Способ лечения рака, включающий введение олигопептидного соединения по любому из пп. 11-13 или фармацевтического комбинированного препарата по любому из пп. 24-26 субъекту, нуждающемуся в этом.
34. Способ по п. 33, где указанный рак выбран из рака мочевого пузыря, рака предстательной железы или гематологического рака, такого так множественная миелома или лейкоз.
| WO 2004031768 A2, 15.04.2004 | |||
| НАВЕСНОЙ БРЕВНОТОЛКАТЕЛЬ | 0 |
|
SU164835A1 |
| KRAG D | |||
| N., Phage-displayed random peptide libraries in mice: toxicity after serial panning, 2002, v | |||
| Устройство для выпрямления многофазного тока | 1923 |
|
SU50A1 |
| Водяной двигатель | 1921 |
|
SU325A1 |
| WO 2004035732 A2, 29.04.2004 | |||
| 0 |
|
SU155367A1 | |
| FUNK J.O | |||
| et al, Inhibition of CDK activity and PCNA-dependent DNA replication by p21 is blocked by interaction with | |||
Авторы
Даты
2015-04-27—Публикация
2009-02-20—Подача