Изобретение относится к области диагностической медицины, а именно к молекулярно-генетической диагностике, и направлено на повышение диагностической эффективности аналитических систем, основанных на использовании циркулирующих внеклеточных нуклеиновых кислот (свободно циркулирующих в плазме и связанных с поверхностью клеток крови).
Актуальной задачей диагностической медицины является своевременное и точное выявление у пациентов специфических последовательностей нуклеиновых кислот, ассоциированных с различными заболеваниями. Особенно интенсивные исследования ведутся в области разработки тестов, основанных на анализе циркулирующих внеклеточных нуклеиновых кислот крови (внНК), поскольку кровь непосредственно контактирует со всеми органами/тканями, и ряд процессов, таких как беременность, нарушение функций клеток и тканей, развитие опухолей сопровождается изменением состава циркулирующих нуклеиновых кислот крови даже на самых ранних этапах развития этих процессов, в частности, когда опухоль трудно/невозможно локализовать физическими методами (1).
Ранее было показано, что использование в диагностике внНК, связанных с поверхностью клеток крови нуклеиновых кислот (спкНК), наряду с широко используемыми внНК, свободно циркулирующими в плазме крови (2), позволяет существенно повысить чувствительность диагностических систем (3).
Известен способ выделения внДНК, связанной с поверхностью клеток крови (4), включающий следующие стадии: сбор крови самотеком в пробирки с фосфатным буфером (10 мМ) и ЭДТА (50 мМ ЭДТА pH 7.5); разделение крови на плазму и клеточную фракцию при помощи центрифугирования (20 мин при 400 g); разделение клеточной фракции крови на эритроциты и лейкоциты; получение ДНК, связанной с поверхностью эритроцитов и ДНК, связанной с поверхностью лейкоцитов при помощи инкубации клеток с фосфатным элюирующим буфером (5 мин инкубация с последующим осаждением клеток центрифугированием 20 мин при 400 g); получение внДНК из эритроцитатрой и лейкоцитарной фракций при помощи инкубации клеток с раствором трипсина и затем ингибитора трипсина (5 мин инкубация с раствором трипсина, добавление ингибитора трипсина, перемешивание раствора, осаждение клеток центрифугированием 20 мин при 400 g). ВнДНК выделяли из плазмы крови и полученных элюатов с поверхности клеток крови при помощи мелкодисперсного стекла.
Недостатками известного способа являются трудоемкая процедура получения фракций, содержащих внДНК крови; а также использование трипсина в процессе получения внДНК, что требует тщательности при выполнении протоколов и контроля за активностью препарата.
Известен способ выделения внРНК, связанных с поверхностью клеток крови (5), включающий следующие стадии: сбор крови самотеком в пробирки с фосфатным буфером (10 мМ) и ЭДТА (50 мМЭДТА pH 7.5); разделение крови на плазму и клеточную фракцию при помощи центрифугирования (20 мин при 400 g); получение внРНК клеток крови при помощи инкубации клеток с фосфатным элюирующим буфером (5 мин инкубация с последующим центрифугированием 20 мин при 400 g); получение внРНК клеток крови при помощи инкубации клеток с раствором трипсина и затем ингибитором трипсина (5 мин инкубация с раствором трипсина, добавление ингибитора трипсина, перемешивание и осаждение клеток центрифугированием 20 мин при 400 g). Выделение внРНК из плазмы проводили на стекловолокнистых фильтрах.
Этому методу присущи ранее перечисленные недостатки, общее время получения фракций, содержащих внРНК составляет 2 часа 42 минуты (время рассчитано для обработки 2 образцов крови объемом 8 мл), метод не может быть автоматизирован.
Наиболее близким к заявленному способу - прототипом, является способ выделения внДНК из крови, включающий следующие стадии: сбор крови в вакутейнеры; разделение крови на плазму и клеточную фракцию при помощи центрифугирования (20 мин при 400 g); получение внДНК в результате последовательной обработки клеток крови фосфатным элюирующим буфером (5 мин инкубация с последующим центрифугированием 20 мин при 400 g); затем обработки клеток крови раствором трипсина (5 мин инкубация с раствором трипсина, добавление ингибитора трипсина, перемешивание и осаждение клеток центрифугированием 20 мин при 400 g). ВнДНК крови из полученных супернатантов выделяли на стекловолокнистых фильтрах при помощи набора «Blood DNA isolation Kit» (BioSilica Ltd, Россия) (6).
Недостатками способа являются трудоемкость и длительность получения фракций, содержащих внДНК крови: общее время получения фракций, содержащих внДНК составляет 2 часа 42 минуты. Кроме того, известный способ требует постоянного контроля эффективности протеазной обработки. Способ содержит много стадий, требует постоянного фиксирования объемов, его крайне сложно автоматизировать. При этом анализируются две фракции внДНК: отдельно - внДНК плазмы крови и отдельно внДНК из клеточной фракции крови, что увеличивает вдвое расходы на выделение внДНК и ПЦР-анализ образцов.
Задачей изобретения является разработка простого, быстрого и воспроизводимого способа получения суммарной фракции внНК крови, содержащей одновременно внНК из плазмы крови и внНК из клеточной фракции крови для последующего использования внНК в качестве диагностического материала.
Технический результат: упрощение, сокращение длительности способа и повышение выхода внНК.
Поставленная задача достигается предлагаемым способом, заключающимся в следующем.
Проводят сбор крови при помощи вакутейнера или других пробирок для сбора и консервирования крови (например, Cell-Free DNA BCT, Streck, США). К аликвоте крови добавляют равный объем элюирующего буфера (DDB), содержащего 1 М NaCl, 0,2 М NaHCO3 (pH 9,3), 20 мМ ЭДТА или буфера, содержащего 1 М NaCl, 20 мМ ЭДТА, инкубируют смесь при комнатной температуре в течение 4-6 минут, осторожно перемешивая. Далее смесь крови и элюирующего буфера DDB разделяют на супернатант и клеточную фракцию при помощи двукратного центрифугирования (5 мин при 1000 g и 5 минут при 1200 g). Полученный супернатант содержит суммарную фракцию внНК, включающую внНК плазмы и внНК клеточной фракции. Далее из супернатанта внНК выделяют любым пригодным методом выделения нуклеиновых кислот, а именно: методом, основанном на экстракции фенол-хлороформом; гуанидин-фенольным методом; методом выделения нуклеиновых кислот при помощи мелкодисперсного стекла или стекловолокнистых фильтров в присутствии хаотропных солей. Количественный анализ внНК крови также проводят любым известным методом исследования нуклеиновых кислот, как то: количественная ПЦР и ОТ-ПЦР; метил-специфичная количественная ПЦР, метод измерения концентрации НК при помощи флуоресцентных красителей (Hoechst 32258, SYBR Green II, DAPI и т.д.).
Определяющим отличием предлагаемого способа по сравнению с прототипом является то, что к образцу исследуемой крови добавляют равный объем элюирующего буфера, содержащего 1 М NaCl, 0,2 М NaHCO3 (pH 9,3), 20 мМ ЭДТА или буфера, содержащего 1 М NaCl, 20 мМ ЭДТА, инкубируют смесь при комнатной температуре в течение 4-6 минут при перемешивании, что обеспечивает получение суммарной фракции, содержащей внНК из плазмы крови и внНК из клеточной фракции крови, что в свою очередь позволяет упростить способ, сократить его длительность и повысить выход нуклеинового материала, позволяющего увеличить чувствительность детекции маркерных последовательностей ДНК и РНК.
Предлагаемый способ имеет следующие преимущества по сравнению с прототипом:
- обеспечивает лизис меньшего количества клеток крови, чем прототип, и устойчив к отклонениям от регламента не более чем на 20%, что делает его пригодным для применения в клинических лабораториях для выполнения рутинных исследований и позволяет автоматизировать процесс;
- позволяет сократить время получения суммарной фракции внНК более чем в 4 раза (с 2 часов 42 минут до 34 минут);
- позволяет почти в 4 раза снизить суммарный объем получаемой фракции (с 44,5 мл до 12 мл), что приводит к уменьшению трудоемкости, снижению расходов реактивов на выделение НК, что в свою очередь уменьшает стоимость тестов, основанных на использовании внНК крови.
Изобретение иллюстрируется следующими примерами конкретного выполнения способа.
Пример 1
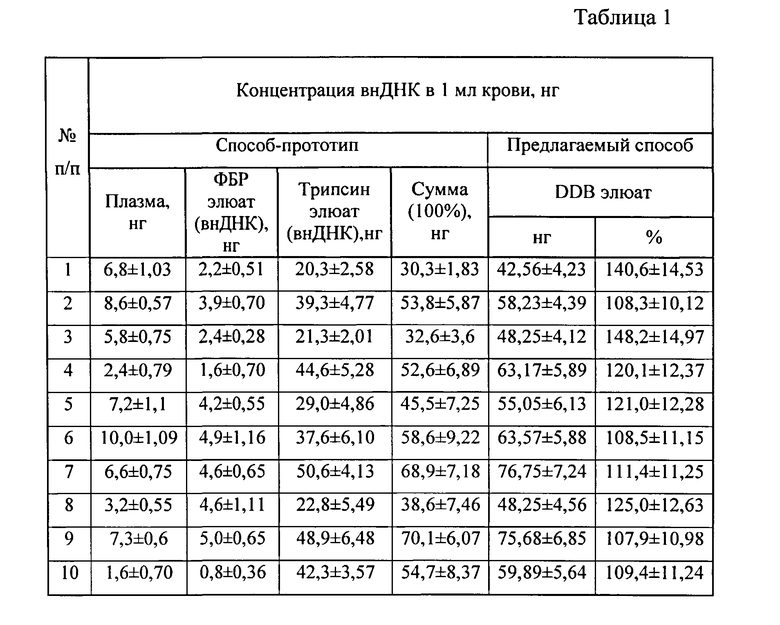
В группе здоровых доноров (n=10) было проведено выделение суммарной фракции внДНК, полученной способом-прототипом (6) и предлагаемым способом. У всех здоровых доноров-добровольцев была взята кровь при помощи вакутейнера с антикоагулянтом. Собранную кровь делили на 2 равные части, одну часть обрабатывали в три стадии по протоколу-прототипу, а оставшуюся часть обрабатывали в одну стадию заявляемым способом: к аликвоте крови добавляли равный объем элюирующего буфера (DDB), содержащего 1 М NaCl, 0,2 М NaHCO3 (pH 9,3), 20 мМ ЭДТА и инкубировали смесь при комнатной температуре в течение 4 минут, осторожно перемешивая, далее смесь крови и элюирующего буфера DDB разделяли на супернатант и клеточную фракцию при помощи двукратного центрифугирования (5 мин при 1000 g и 5 минут при 1200 g), а из полученного супернатанта внДНК выделяли с помощью мелкодисперсного стекла в присутствии хаотропных солей (4). Концентрацию ДНК определяли при помощи TaqMan-ПЦР на LINE-1 повторы (7).
Результаты исследования представлены в Таблице 1. Как видно из таблицы 1, использование предлагаемого способа получения суммарной фракции внДНК крови позволяет увеличить выход внДНК в среднем на 20,07%. При этом экономия времени составляет 2 часа 8 минут.
Данный пример иллюстрирует возможность использования разработанного способа в клинических лабораториях, применяющих поточные методы с высокой воспроизводимостью.
Пример 2
В группе больных раком легких (n=10) было проведено выделение суммарной фракции внДНК, полученной при помощи способа-прототипа (6) и предлагаемым способом. У всех принимающих в исследовании людей была взята кровь при помощи вакутейнера. Собранную кровь делили на 2 равные части, одну часть обрабатывали в три стадии по протоколу-прототипу, а вторую часть обрабатывали в одну стадию - с использованием предлагаемого способа, а именно: к аликвоте крови добавляли равный объем элюирующего буфера (DDB), содержащего 1 М NaCl, 20 мМ ЭДТА и инкубировали смесь при комнатной температуре в течение 6 минут, осторожно перемешивая, далее смесь крови и элюирующего буфера DDB разделяли на супернатант и клеточную фракцию при помощи двукратного центрифугирования (5 мин при 1000 g и 5 минут при 1200 g), а из полученного супернатанта внДНК выделяли с помощью наборов БиоСилика (ООО Биосилика, Россия). Концентрацию опухолеспецифичной ДНК определяли при помощи метил-специфической SYBR-Green ПЦР на метилированный фрагмент гена RARbeta2 (8).
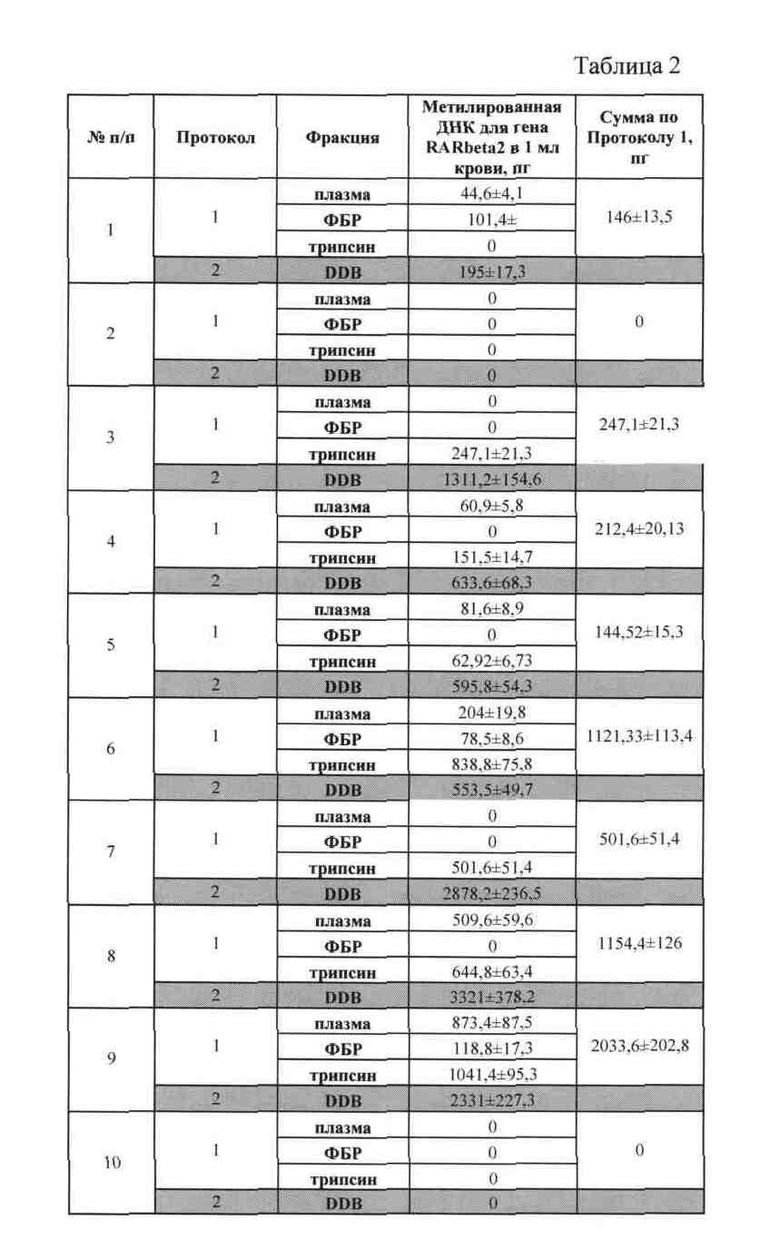
В Таблице 2 представлена концентрация метилированной формы гена RARβ2 в составе внДНК в крови больных раком легкого, где Протокол 1 - способ-прототип. Протокол 2 - предлагаемый способ.
Как видно из таблицы 2, использование предлагаемого способа получения суммарной фракции внДНК из крови онкологических больных позволяет значительно увеличить выход опухолеспецифичной внДНК в среднем на 58%, при этом время, затрачиваемое на выполнение предлагаемого способа, снижается более чем в 4 раза (с 2 часов 42 минут до 34 минут).
Пример 3
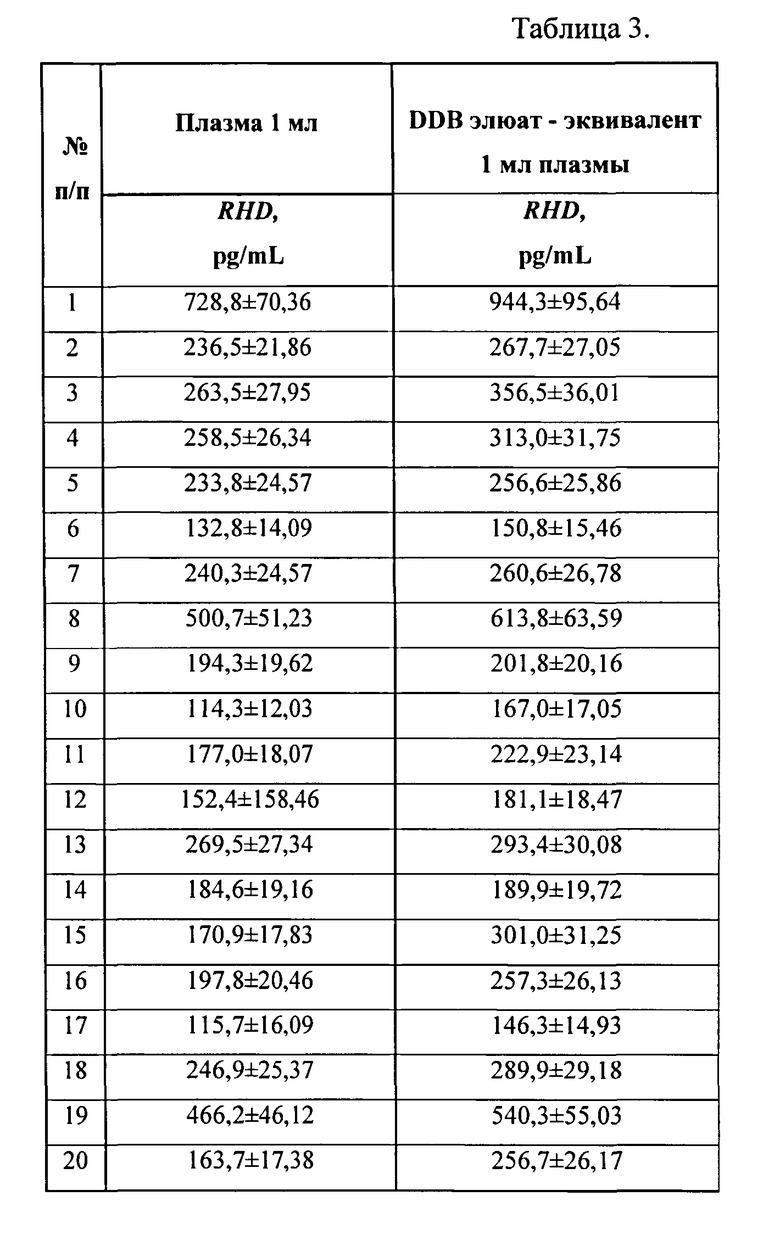
В группе беременных RhD-отрицательных женщин, ждущих RhD-положительного ребенка (n=20), было проведено сравнительное исследование концентраций суммарной фракции внДНК и генетического маркера резус-принадлежности (RHD) в образцах, полученных при помощи способа-прототипа (6) и предлагаемого способа аналогично примеру 1. У всех пациенток была взята кровь при помощи вакутейнера. Собранную кровь делили на 2 равные части, одну часть обрабатывали по протоколу-прототипу до стадии использования элюирующих буферов (получали только образцы плазмы крови), а вторую часть обрабатывали с использованием предлагаемого способа аналогично примеру 1, при этом внДНК из полученного супернатанта выделяли с помощью автоматической станции QIAsymphony (Qiagen, США). Концентрации ДНК были исследованы при помощи TaqMan-ПЦР для фрагмента гена домашнего хозяйства GAPDH и для генетического маркера резус-принадлежности RHD (9) (Таблица 3).
Как видно из таблицы 3, использование предлагаемого способа позволяет в среднем в 6,5 раз увеличить концентрацию внДНК. При этом концентрация плодной ДНК при использовании предлагаемого способа увеличивается в среднем на 18%. Этот факт может быть очень важен при анализе плодной ДНК у женщин с ранним сроком беременности, когда концентрация плодной ДНК очень мала. Использование предлагаемого способа обработки крови может позволить проводить RhD типирование плода на более ранних сроках беременности.
Пример 4
В группах больных раком легких (n=10) и здоровых доноров (n=10) был исследован уровень экспресии в крови циркулирующих микроРНК (миРНК) на примере миРНК-21 и 155, уровень экпрессии которых повышается при развитии онкопатологии (10). Получение фракций внРНК проводили при помощи способа-прототипа (6) и предлагаемым способом. У всех принимающих участие в исследовании людей была взята кровь при помощи вакутейнера. Собранную кровь делили на 2 равные части, одну часть обрабатывали в три стадии по протоколу-прототипу, а вторую часть обрабатывали в одну стадию аналогично примеру 1, при этом внРНК из полученного супернатанта выделяли с помощью гуанидин фенольной экстракции (11). Уровень экспрессии миРНК мишеней определяли при помощи количественной ОТ-ПЦР (12). Было показано, что использование предлагаемого способа получения суммарной фракции внРНК крови позволяет увеличить выход внРНК мишеней в среднем на 32%.
Использование предлагаемого способа позволит упростить и сократить длительность процедуры, а также повысить количество диагностического материла, что позволит повысить чувствительность детекции маркерных НК, специфичных для онкозаболеваний и патологий беременности.
Источники информации
1. Jung K., Fleischhacker M Rabien A. Cell-free DNA in the blood as a solid tumor biomarker-a critical appraisal of the literature // Clin Chim Acta. - 2010. - V. 411. P. 1611-1624.
2. Pinzani P., Salvianti F., Pazzagli M. et al. Circulating nucleic acids in cancer and pregnancy. // Methods. - 2010. - V. 50(4). P. 302-307.
3. Rykova E.Y., Morozkin E.S., Ponomaryova A.A. et al. Cell-free and cell-bound circulating nucleic acid complexes: mechanisms of generation, concentration and content // Expert Opin Biol Ther. - 2012. - V. 12. P. 141-153.
4. Skvortsova Т.Е., Rykova E.Y., Tamkovich S.N., et al. Cell-free and cell-bound circulating DNA in breast tumours: DNA quantification and analysis of tumour-related gene methylation // Br J Cancer. - 2006. - V. 94. P. 1492-1495.
5. Рыкова Е.Ю., Скворцова Т.Э., Хоффман А-Л. и др. // Циркулирующие внеклеточные ДНК и РНК крови в диагностике онкопатологий молочной железы. Биомедицинская химия. 2008, Том 54, Выпуск 1, С. 94-103.
6. Лактионов П.П., Тамкович С.Н., Рыкова Е.Ю. и др. Способ ранней диагностики и мониторинга онкологических заболеваний. Патент RU 2251696 С2, опубл. 10.05.2005 г.
7. Morozkin E.S., Babochkina T.I., Vlassov V.V., Laktionov P.P. The effect of protein transport inhibitors on the production of extracellular DNA // Ann N Y Acad Sci. - 2008. - V. 1137. - P. 31-35.
8. Ponomaryova A.A., Rykova E.Y., Cherdyntseva N.V. et al. / RARβ2 gene methylation level in the circulating DNA from lung cancer patient blood // Eur J Cancer Prev. - 2011 V. - 20, N. 6. - P. 453-455.
9. Clausen F.B., Jakobsen T.R., Rieneck K. et al. Pre-analytical conditions in non-invasive prenatal testing of cell-free fetal RHD // PLoS One. - 2013. - V. 8(10). e76990.
10. Jones K., Nourse J.P., Keane С. et al. Plasma microRNA are disease response biomarkers in classical Hodgkin lymphoma // Clin Cancer Res. - 2014. - V. 20. - P. 253-64.
11. Chomczynski P., Sacchi N. Single-step method of RNA isolation by acid guanidinium thiocyanate-phenol-chloroform extraction // Anal Biochem. - 1987. - V. 162. - P. 156-159.
12. Chen С., Ridzon D.A., Broomer A.J. et al. Real-time quantification of microRNAs by stem-loop RT-PCR // Nucleic Acids Res. - 2005. - V. 33. - P. e179.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЫДЕЛЕНИЯ ВНЕКЛЕТОЧНЫХ ДЕЗОКСИРИБОНУКЛЕИНОВЫХ КИСЛОТ ИЗ КРОВИ | 2008 |
|
RU2372405C1 |
| СПОСОБ ДИАГНОСТИКИ И МОНИТОРИНГА ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ С ИСПОЛЬЗОВАНИЕМ ЭКЗОСОМ КРОВИ | 2014 |
|
RU2571507C1 |
| СПОСОБ РАННЕГО ОПРЕДЕЛЕНИЯ ПОЛА БУДУЩЕГО РЕБЕНКА | 2006 |
|
RU2317334C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКЗОСОМ ИЗ КРОВИ | 2014 |
|
RU2556825C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКЗОСОМ ИЗ КРОВИ | 2016 |
|
RU2608509C1 |
| Малоинвазивный способ диагностики метастатического поражения регионарных лимфатических узлов у больных раком шейки матки на основании показателя копийности генов CCND1 и PPARGC1A | 2021 |
|
RU2766774C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С НАРУШЕНИЕМ ФУНКЦИОНИРОВАНИЯ ГЕНЕТИЧЕСКОГО АППАРАТА КЛЕТКИ | 2003 |
|
RU2249820C1 |
| Способ ранней диагностики опухолей предстательной железы | 2021 |
|
RU2756643C1 |
| Малоинвазивный способ диагностики рака легкого на основании изменения копийности локуса мтДНК HV2 | 2018 |
|
RU2678227C1 |
| СПОСОБ ВЫДЕЛЕНИЯ ДЕЗОКСИРИБОНУКЛЕИНОВЫХ КИСЛОТ | 2002 |
|
RU2232768C2 |
Изобретение относится к области биохимии и диагностической медицины. Способ включает сбор крови в антисвертывающий раствор, добавление равного объема элюирующего буфера, содержащего 1 М NaCl, 0,2 М NaHCO3 (pH 9,3), 20 мМ ЭДТА или буфера, содержащего 1 М NaCl, 20 мМ ЭДТА. Полученную смесь инкубируют при комнатной температуре в течение 4-6 минут при перемешивании с последующим разделением собранной крови на плазму и клеточную фракцию крови при помощи центрифугирования и сбором супернатанта, из которого выделяют суммарную фракцию внеклеточных нуклеиновых кислот (внНК). Использование изобретения позволяет сократить время получения суммарной фракции внНК, повысить выход внНК крови, повысить чувствительность детекции маркерных НК, специфичных для онкозаболеваний и патологий беременности. 2 з.п. ф-лы, 3 табл., 4 пр.
1. Способ выделения суммарной фракции внеклеточных нуклеиновых кислот из крови (внНК), включающий сбор крови в антисвертывающий раствор, разделение собранной крови на плазму и клеточную фракцию крови при помощи центрифугирования, выделение внНК из полученного супернатанта с последующим измерением концентрации внНК, отличающийся тем, что к образцу крови, перед разделением ее на фракции, добавляют равный объем элюирующего буфера, содержащего 1 М NaCl, 0,2 М NaHCO3 (pH 9,3), 20 мМ ЭДТА или буфера, содержащего 1 М NaCl, 20 мМ ЭДТА, полученную смесь инкубируют при комнатной температуре в течение 4-6 минут при перемешивании.
2. Способ по п. 1, отличающийся тем, что внНК выделяют из супернатанта методом, выбранным из: экстракция фенол-хлороформом; экстракция гуанидин-фенольным методом; выделение при помощи мелкодисперсного стекла или стекловолокнистых фильтров в присутствии хаотропных солей.
3. Способ по п. 1, отличающийся тем, что измерение концентрации внНК проводят методом, выбранным из: количественная ПЦР и ОТ-ПЦР, метил-специфичная количественная ПЦР, метод измерения концентрации НК при помощи флуоресцентных красителей.
Авторы
Даты
2015-06-27—Публикация
2014-05-21—Подача