Изобретение относится к области диагностической медицины, а именно к разработке неинвазивных способов диагностики онкологических заболеваний человека, а также мониторинга эффективности противораковой терапии и направлено на повышение эффективности аналитических систем путем анализа опухолеспецифических маркеров и белков в составе экзосом крови.
Экзосомы крови представляют собой микровезикулы размером 40-100 нм, активно секретируемые через каскад экзоцитоза, обычно используемый для разгрузки рецептора и внутриклеточных перекрестных сигналов. В дополнение к белкам главного комплекса гистосовместимости (МНС I, МНС II) и белкам, вовлеченным в представление антигена, экзосомы могут содержать мембранные и цитозольные белки, вовлеченные во множество клеточных функций. Экзосомы продуцируются всеми клетками организма человека и животных, а их состав и свойства зависят от функционального состояния клеток-продуцентов, что определяет уникальность экзосом каждой клетки (клеточной популяции) [1].
Раннее выявление в крови опухолеспецифических маркеров является важной проблемой в диагностической медицине. В то время как прямой анализ пораженных тканей бывает затруднен или недоступен (нет симптоматики), периферическая кровь является легкодоступным биологическим материалом для получения экзосом, которые могут быть удобным источником опухолеспецифичных мРНК [2], микроРНК [3] и белков [4].
Известен способ диагностики меланомы при помощи определения в сыворотке крови пациентов матричной опухолеспецифичной РНК (мРНК), включающий сбор крови самотеком с последующим разделением собранной крови на сывороточную и клеточную фракции и определением РНК в сыворотке крови. Данным способом мРНК обнаруживают лишь в 67% случаев у больных меланомой [5].
Недостатком данного способа являются трудоемкость, высокая вероятность получения ложноотрицательных результатов, низкая чувствительность и специфичность маркера для определенного вида рака.
Известен способ диагностики рака при помощи определения концентрации мРНК в плазме крови онкологических больных [6], включающий сбор крови самотеком с последующим разделением собранной крови на сыворотку и фракцию клеток крови и определением концентрации мРНК маммоглобина в сыворотке крови при помощи обратной транскрипции (ОТ) с последующей ПНР и детекцией амплифицированного продукта окрашиванием бромистым этидием в агарозном геле. Известный способ выявляет мРНК маммоглобина в сыворотке крови у здоровых доноров в 38% случаев, а у больных с раком молочной железы - 60% случаев.
Недостатками данного способа являются высокая вероятность получения ложноотрицательных результатов, поскольку данный способ не позволяет выявлять все виды онкологических заболеваний, высокая вероятность получения ложноположительных результатов, поскольку увеличение концентрации мРНК маммоглобина в плазме крови наблюдается также у здоровых женщин (44%) и мужчин (29%) [6].
Известен способ диагностики онкозаболеваний путем выявления опухолеспецифических микроРНК в плазме крови. Для анализа выделяют микроРНК одним из известных способов, а затем проводят ОТ с последующей количественной ПЦР [7]. Показано, что при раке легкого в плазме крови микроРНК-182 выявляется у 60,7% пациентов (17/28), а микроРНК-210 - 57,1% (16/28).
Недостатками данного способа являются низкая достоверность результатов диагностики раковых и особенно предраковых состояний из-за небольшого удельного содержания специфических последовательностей микроРНК, что затрудняет клиническое использование данного способа.
Известен способ диагностики рака при помощи выявления опухолеспецифических белков в плазме крови онкологических больных, включающий сбор крови самотеком с последующим разделением собранной крови на сыворотку и фракцию клеток крови и определением концентрации ракового эмбрионального антигена (РЭА) при помощи иммуноферментного анализа. В норме сывороточный уровень РЭА не превышает 3 нг/мл. Повышенная концентрация этого антигена в крови наблюдается у 30-50% больных при карциномах молочной железы, головы и шеи; у 50-90% больных с карциномой пищеварительного тракта и дыхательных путей, а также у 23% больных со злокачественными новообразованиями соединительнотканного происхождения [8].
Недостатками данного способа являются низкая специфичность и высокая вероятность получения ложноотрицательных результатов.
Ближайшим к заявленному способу - прототипом, является способ диагностики рака легкого при помощи определения концентрации микроРНК в составе экзосом из плазмы крови онкологических больных [9]. Способ заключается в выделении экзосом из плазмы крови путем ультрацентрифугирования и определении концентрации 9 микроРНК (miR-629, miR-379, miR-378a, miR-200b-5p, miR-154-3р, miR-151a-5p, miR-139-5p, miR-100 и miR-30a-3p) у онкологических больных после проведения обратной транскрипции (ОТ) и последующей количественной ПИР Данный способ обеспечивает чувствительность 91% и специфичность 60%.
Недостатками данного способа являются большая трудоемкость (анализ 9 микроРНК) и низкая специфичность.
Задачей изобретения является разработка более простого и достоверного способа для диагностики, оценки раковых состояний и мониторинга противораковой терапии.
Технический результат: уменьшение трудоемкости способа и повышение специфичности диагностики, при сохранении высокой чувствительности способа.
Поставленная техническая задача достигается предлагаемым способом, заключающимся в следующем.
Производят забор крови в вакутейнер или другие пробирки для сбора и консервирования крови (например, Cell-Free DNA ВСТ, Streck, США). Кровь разделяют на плазму и клеточную фракцию при помощи центрифугирования. Далее проводят выделение экзосом, связанных с поверхностью форменных элементов, из клеточной фракции. Для этого может быть использован любой пригодный метод. В преимущественном варианте, клетки обрабатывают буферным раствором PBS (10 мМ фосфатный буфер, 0,15 Μ NaCl, рН 7,5), содержащим 5 мМ ЭДТА (5 мин инкубация с последующим центрифугированием 20 минут при 300 g, сбор супернатанта), либо клетки обрабатывают равным объемом 0,15-0,35% раствора трипсина в PBS (5 минут инкубация, добавление ингибитора трипсина, перемешивание с последующим центрифугированием 20 минут при 300 g, сбор супернатанта), либо последовательно обрабатывают клетки буферным раствором PBS, содержащим 5 мМ ЭДТА, собирают первый супернатант, а затем обрабатывают клетки равным объемом 0,15-0,35% раствора трипсина в PBS, собирают второй супернатант.
Далее плазму и полученный супернатант из клеточной фракции объединяют, фильтруют через фильтры с диаметром пор 0,1 мкм и используют для выделения суммарного пула экзосом крови. Суммарный пул экзосом крови выделяют любым пригодным методом, а именно: путем последовательного удаления клеточного дебриса центрифугированием, а затем осаждением экзосом ультрацентрифугированием [10]; путем последовательного удаления клеточного дебриса фильтрацией, а затем отделением экзосом центрифугированием в градиенте сахарозы, отмывом экзосом PBS-ом и осаждением экзосом ультрацентрифугированием [11]; с помощью коммерческого набора ExoQuick™ Exosome Precipitation Solution (System Biosciences Inc., Mountain View, CA, USA) и др.
Далее в составе экзосом крови выявляют не менее 2-х известных опухолеспецифических белков или выделяют РНК либо микроРНК и, после проведения обратной транскрипции, определяют концентрацию не менее 2-х опухолеспецифических маркеров, ассоциированных с определенным онкологическим заболеванием, и при концентрации последних, превышающих концентрацию данных маркеров в контрольном образце, диагностируют наличие онкологического заболевания
Для выделения опухолеспецифических маркеров (мРНК или микроРНК) используют любой пригодный метод, например, метод, основанный на экстракции фенол-хлороформом [12]; гуанидин-фенольный метод [13]; метод выделения нуклеиновых кислот при помощи мелкодисперсного стекла или стекловолокнистых фильтров в присутствии хаотропных солей [14].
Определение концентрации опухолеспецифических маркеров также проводят любым известным методом исследования нуклеиновых кислот, как то: количественная ПЦР и ОТ-ПЦР, метод измерения концентрации нуклеиновых кислот при помощи флуоресцентных красителей (RiboGreen, SYBR Green II) и т.д.
Для выявления опухолеспецифических белков также могут быть использованы любые пригодные методы анализа белков, а именно: двумерный электрофорез с последующей оцифровкой; одномерный электрофорез с последующим выявлением опухолеспецифических белков путем окрашивания специфическими антителами после вестерн-блотинга; MALDI-анализ и др.
Определяющим отличием предлагаемого способа, по сравнению с прототипом, является использование в качестве диагностического объекта суммарного пула экзосом крови, включающего экзосомы из плазмы и экзосомы, связанные с поверхностью форменных элементов, выделенные из клеточной фракции крови, что позволяет значительно повысить достоверность выявления опухолеспецифических маркеров и белков уже на ранних стадиях заболевания. В прототипе анализируют опухолеспецифические маркеры (последовательности микроРНК), выделенные только из экзосом плазмы крови.
Использование нового диагностического объекта - экзосом, связанных с поверхностью форменных элементов крови (вкупе с экзосомами плазмы), позволяет увеличить специфичность детекции опухолеспецифических последовательностей РНК и белков за счет увеличения количества анализируемых экзосом крови без использования инвазивных методов диагностики, дифференцировать доброкачественные и злокачественные новообразования и осуществлять мониторинг эффективности противоопухолевой терапии.
Изобретение иллюстрируется следующими примерами конкретного выполнения способа.
Пример 1.
Проведена диагностика рака молочной железы путем определения концентрации двух опухолевых маркеров (мРНК RASSF8 и Ki-67) в составе экзосом плазмы (для сравнения) и экзосом крови (т.е. экзосом плазмы и экзосом, связанных с поверхностью клеток крови) у здоровых женщин (n=19), у пациентов с мастопатией (n=14) и у больных раком молочной железы (n=20) на I-II стадиях заболевания.
У всех женщин была взята кровь в вакутейнер с К3ЭДТА во время первично установленного диагноза. Собранную кровь разделили на плазму и фракцию клеток крови при помощи центрифугирования (10 мин, 400 g). Затем провели выделение экзосом плазмы и экзосом крови. В первом случае плазму фильтровали через фильтры с диаметром пор 0,1 мкм, экзосомы осаждали ультрацентрифугированием при 100000 g в течение 1,5 ч. Во втором случае (из клеточной фракции) экзосомы, связанные с поверхностью клеток крови, элюировали PBS, содержащим 5 мМ ЭДТА в течение 5 мин, затем клетки осаждали центрифугированием (5 мин, 400 g) и отбирали супернатант. Для получения суммарного пула экзосом крови плазму и супернатант объединяли, фильтровали через фильтры с диаметром пор 0,1 мкм, экзосомы осаждали ультрацентрифугированием (100000 g, 1,5 ч). Выделение РНК из экзосом плазмы и из экзосом крови проводили на стекловолокнистых фильтрах производства «Биосилика» по протоколу, рекомендованному производителем. Образцы выделенной РНК инкубировали с 2 единицами активности ДНКазы, не содержащей РНКаз (Fermentas, EN0531) в течение 1 ч при 37°С. Реакцию ОТ проводили с использованием гексамерных праймеров случайной последовательности и набора Superscript ТМ II Reverse Transcriptase kit (Invitrogen, USA), как описано в работе [15]. Праймеры и Taqman-пробы для мРНК RASSF8 и Ki-67 были разработаны и синтезированы, как описано в работе [15].
Средняя концентрация мРНК RASSF8 и Ki-67 в составе экзосом крови у больных раком молочной железы составила 4,8×103 и 5,78×104 копий/мл, соответственно. С помощью ROC-анализа было установлено, что чувствительность теста для опухолеспецифической мРНК Ki-67 (при пороговом уровне 4×104 копий/мл) составила 80%, специфичность 89%; для мРНК RASSF8 чувствительность теста при пороговом уровне 3×103 копий/мл составила 79%, специфичность 91%, что подтверждает высокую специфичность заявляемого способа с одновременным снижением количества анализируемых маркерных последовательностей (по сравнению с прототипом).
Данный пример иллюстрирует возможность использования разработанного способа для диагностики онкологических заболеваний у пациентов, являющихся группой риска, а также возможность дифференцировки доброкачественных и злокачественных новообразований с помощью измерения концентрации всего 2-х опухолеспецифических маркеров в составе экзосом крови.
Пример 2.
Была исследована концентрация двух микроРНК (miR-200a и miR-141) в составе экзосом, связанных с поверхностью клеток крови у пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ, являются группой риска) (n=15) и у больных раком предстательной железы на различных стадиях заболевания (n=19).
У всех пациентов была взята кровь во время первичного установления диагноза. Кровь была собрана в вакутейнеры и разделена центрифугированием на плазму и клеточную фракцию. Экзосомы, связанные с клетками крови, элюировали обработкой 0,25% раствором трипсина, с последующим ингибированием фермента, осаждали клетки центрифугированием и собирали супернатант. Плазму и супернатант объединяли и использовали для выделения суммарного пула экзосом крови коммерческим набором ExoQuick™ Exosome Precipitation Solution (System Biosciences Inc., Mountain View, CA, USA) по протоколу, рекомендованному производителем. МикроРНК из экзосом крови были выделены при помощи набора MirVana (США) по протоколу, рекомендованному производителем. ОТ проводили с помощью набора TaqMan MicroRNA Reverse Transcription Kit (США) по протоколу, рекомендованному производителем. Концентрация микроРНК в составе экзосом крови была определена при помощи количественного ПЦР с использованием специфических праймеров TaqMan MicroRNA assay (США) и TaqMan Universal PCR Master Mix (США).
Средняя концентрация miR-200a и miR-141 в составе экзосом крови у больных раком предстательной железы составила 483121 и 498158 копий/мл, соответственно. С помощью ROC-анализа было установлено, что чувствительность теста для опухолеспецифической miR-200a (количество правильно определенных пациентов со злокачественными опухолями) при пороговом уровне 105 копий/мл составила 86%, специфичность 88%; для miR-141 чувствительность теста при пороговом уровне 2,3×105 копий/мл составила 81%, специфичность 90%, что подтверждает высокую специфичность с одновременным снижением количества анализируемых маркерных последовательностей (по сравнению с прототипом).
Данный пример иллюстрирует возможность использования разработанного способа для дифференцировки неонкологических и онкологических заболеваний с помощью измерения концентрации всего двух опухолевых микроРНК в составе экзосом крови.
Пример 3.
У трех женщин, успешно прооперированных три года назад по поводу раковой опухоли груди и прошедших курс химиотерапии, были взяты образцы крови с профилактической целью, так как пациентки с раком груди входят в группу пациентов с высоким риском повторных новообразований.
Кровь была собрана в вакутейнеры и разделена центрифугированием на плазму и клеточную фракцию. Экзосомы плазмы выделяли аналогично примеру 1. Экзосомы, связанные с форменными элементами (клеточная фракция), элюировали в две стадии: сначала клетки обрабатывали PBS, содержащим 5 мМ ЭДТА, клетки осаждали центрифугированием и собирали супернатант №1, затем клетки обрабатывали 0,15% раствором трипсина, с последующим ингибированием фермента, осаждением клеток центрифугированием и сбором супернатанта №2. Для получения экзосом крови плазму и супернатанты №1 и №2 объединяли и выделяли суммарный пул экзосом крови аналогично примеру 1.
Для выявления опухолеспецифических белков, имеющих важное прогностическое значение при раке груди, провели двумерный электрофорез белков экзосом плазмы и экзосом крови с последующим оцифровыванием полиакриламидного геля.
Эффективность выявления опухолеспецифических белков в составе экзосом плазмы и экзосом крови у пациенток представлена в таблице 1.
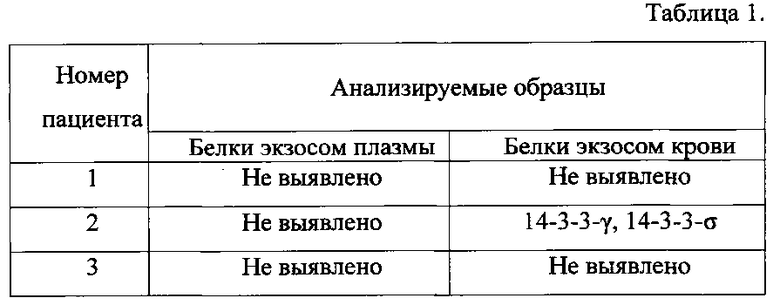
Из таблицы 1 видно, что анализ белков экзосом крови выявил у пациентки №2 наличие опухолеспецифических белков 14-3-3-γ и 14-3-3-σ, в то время как при анализе данных белков в составе экзосом только плазмы той же пациентки были получены отрицательные результаты. В течение последующего года у нее были клинически диагностированы повторные метастазы в регионарных лимфоузлах.
Данный пример иллюстрирует, что предлагаемый способ с использованием экзосом крови позволяет повысить эффективность диагностики онкологических заболеваний за счет увеличения специфичности выявления опухолеспецифических белков.
Использование предлагаемого способа позволит, по сравнению с прототипом:
- увеличить удельное содержание выявляемых специфических последовательностей в составе экзосом, связанных с клеточной поверхностью, по сравнению с содержанием специфических последовательностей в составе экзосом, выделенных из плазмы;
- увеличить и специфичность детекции специфических (маркерных) последовательностей нуклеиновых кислот и белков в составе экзосом, связанных с поверхностью клеток крови, при сохранении высокой чувствительности, что особенно важно на ранних стадиях развития патологий;
- исключить получение ложноположительных или ложноотрицательных результатов анализа;
- расширить область применения способа за счет возможности мониторинга антираковой терапии онкологических заболеваний.
Источники ирформации
1. Villarroya-Beltri С., Baixauli F., Gutiérrez-Vázquez С., Sánchez-Madrid F., Mittelbrunn M. Sorting it out: Regulation of exosome loading // Semin Cancer Biol. 2014. V. 28C. P. 3-13.
2. Pant S., Hilton H., Burczynski M.E. The multifaceted exosome: biogenesis, role in normal and aberrant cellular function, and frontiers for pharmacological and biomarker opportunities // Biochemical pharmacology. 2012. V. 83. P. 1484-1494.
3. Salido-Guadarrama I., Romero-Cordoba S., Peralta-Zaragoza O., Hidalgo-Miranda Α., Rodríguez-Dorantes M. MicroRNAs transported by exosomes in body fluids as mediators of intercellular communication in cancer // Onco Targets Ther. 2014. V. 7. P. 1327-1338.
4. Choi D.-S., Kim D.-K., Kim Y.-K., Gho Y.S. Proteomics, transcriptomics and lipidomics of exosomes and ectosomes // Proteomics. 2013. V. 13. P. 1554-1571.
5. Kopreski M., Benko F., Kwak L., Gocke C. Detection of tumor messenger RNA in the serum of patients with malignant melanoma // Clin. Cancer Res. 1999. V. 5. P. 1961-1965.
6. Gal S., Fidler C., Lo Y.M., Chin K., Moore J., Harris A.L., Wainscoat J.S. Detection of mammaglobin mRNA in the plasma of breast cancer patients // Ann. N.Y. Acad. Sci. 2001 V. 945. P. 192-194.
7. Shen J., Liu Z., Todd N.W., Zhang H., Liao J., Yu L., Guarnera M.A., Li R., Cai L., Zhan M., Jiang F. Diagnosis of lung cancer in individuals with solitary pulmonary nodules by plasma microRNA biomarkers // BMC Cancer. 2011. V. 11. P. 374.
8. Кушлинский H.E., Портный С.М., Лактионов К.П. 2005. Рак молочной железы. РАМН, М.
9. Cazzoli R., Buttitta F., Di Nicola Μ., Malatesta S., Marchetti Α., Rom W.N., Pass H.I. microRNAs derived from circulating exosomes as noninvasive biomarkers for screening and diagnosing lung cancer // J. Thorac. Oncol. 2013. V. 8. P. 1156-1162.
10. Gallo Α., Tandon M., Alevizos I., Illei G.G. The majority of microRNAs detectable in serum and saliva is concentrated in exosomes // PLoS ONE. 2012. V. 7. P. e30679.
11. Rupp A.-K., Rupp C., Keller S., Brase J.C., Ehehalt R., Fogel M., Moldenhauer G., Marmé F., Sültmann H., Altevogt P. Loss of EpCAM expression in breast cancer derived serum exosomes: role of proteolytic cleavage // Gynecologic Oncology. 2011. V. 122. P. 437-446.
12. Short protocols in molecular biology. Third edition. Wiley, 1995.
13. Chomezynski P., Mackey K. Single-step method of total RNA isolation by acid Guanidine-Phenol extraction // Organelles and cellular structures. 1996. V. 10. P. 221-224.
14. Boom R., Sol C.J.A. Rapid and simple method for purification nucleic acids // J. Clin. Microbiol. 1990. V. 28. P. 495-503.
15. Рыкова Е.Ю., Скворцова Т.Э., Хоффман А.Л., Тамкович С.Н., Стариков А.В., Брызгунова О.Е., Пермякова В.И., Варнеке Е., Шакиель Г., Власов В.В., Лактионов П.П. Циркулирующие внеклеточные ДНК и РНК крови в диагностике опухолей молочной железы. // Биомедицинская химия 2008. Т. 54. С. 94-103.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЭКЗОСОМ ИЗ КРОВИ | 2014 |
|
RU2556825C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА ЗЛОКАЧЕСТВЕННОЙ ТРАНСФОРМАЦИИ КЛЕТОК ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2022 |
|
RU2806518C1 |
| Способ диагностики меланомы с помощью экзосомальных микроРНК | 2020 |
|
RU2769927C2 |
| СПОСОБ ВЫДЕЛЕНИЯ ЭКЗОСОМ ИЗ ПЛАЗМЫ КРОВИ | 2020 |
|
RU2741776C1 |
| СПОСОБ ВЫДЕЛЕНИЯ МИКРОРНК ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 2013 |
|
RU2548816C1 |
| ВНЕКЛЕТОЧНЫЕ ВЕЗИКУЛЫ ДЛЯ ИНГАЛЯЦИИ | 2019 |
|
RU2799315C2 |
| НОВЫЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ И ОХАРАКТЕРИЗОВАНИЯ МИКРОВЕЗИКУЛ В ЖИДКОСТЯХ ОРГАНИЗМА ЧЕЛОВЕКА | 2009 |
|
RU2520741C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКЗОСОМ ИЗ КРОВИ | 2016 |
|
RU2608509C1 |
| ЭКЗОСОМАЛЬНЫЕ БИОМАРКЕРЫ | 2015 |
|
RU2712223C2 |
| Набор для выделения экзосом | 2023 |
|
RU2824663C1 |
Изобретение относится к области медицины и представляет собой способ диагностики и мониторинга онкологических заболеваний, включающий сбор крови, разделение крови на плазму и клеточную фракции, определение концентрации опухолевых маркеров в составе экзосом плазмы крови, отличающийся тем, что дополнительно осуществляют выделение экзосом из клеточной фракции крови, далее плазму и полученный супернатант из клеточной фракции объединяют и выделяют суммарный пул экзосом крови, а затем в составе экзосом крови выявляют не менее 2-х известных опухолеспецифических белков или выделяют РНК либо микроРНК и, после проведения обратной транскрипции определяют концентрацию не менее 2-х опухолеспецифических маркеров, ассоциированных с определенным онкологическим заболеванием, и при концентрации последних, превышающих концентрацию данных маркеров в контрольном образце, диагностируют наличие онкологического заболевания. Осуществление изобретения обеспечивает уменьшение трудоемкости и повышение специфичности диагностики. 4 з.п. ф-лы, 1 табл., 3 пр.
1. Способ диагностики и мониторинга онкологических заболеваний с использованием экзосом крови, включающий сбор крови, разделение крови на плазму и клеточную фракции с помощью центрифугирования, выделение экзосом из плазмы, определение концентрации опухолевых маркеров в составе экзосом плазмы крови с последующим составлением заключения о наличии онкологического заболевания, отличающийся тем, что дополнительно осуществляют выделение экзосом из клеточной фракции крови, далее плазму и полученный супернатант из клеточной фракции объединяют и выделяют суммарный пул экзосом крови, а затем в составе экзосом крови выявляют не менее 2-х известных опухолеспецифических белков или выделяют РНК либо микроРНК и, после проведения обратной транскрипции, определяют концентрацию не менее 2-х опухолеспецифических маркеров, ассоциированных с определенным онкологическим заболеванием, и при концентрации последних, превышающих концентрацию данных маркеров в контрольном образце, диагностируют наличие онкологического заболевания.
2. Способ по п. 1, отличающийся тем, что клеточную фракцию крови обрабатывают буферным раствором PBS, содержащим 5 мМ ЭДТА, 5 мин инкубируют с последующим центрифугированием 20 минут при 300 g и сбором супернатанта.
3. Способ по п. 1, отличающийся тем, что клеточную фракцию крови обрабатывают равным объемом 0,15-0,35% раствора трипсина в PBS, инкубируют 5 минут, добавляют ингибитор трипсина, перемешивают с последующим центрифугированием 20 минут при 300 g и сбором супернатанта.
4. Способ по п. 1, отличающийся тем, что клеточную фракцию крови последовательно обрабатывают буферным раствором PBS, содержащим 5 мМ ЭДТА, собирают первый супернатант, а затем обрабатывают клеткиравным объемом 0,15-0,35% раствора трипсина в PBS, собирают второй супернатант.
5. Способ по п. 1, отличающийся тем, что суммарный пул экзосом крови выделяют методом, выбранным из группы: путем удаления клеточного дебриса центрифугированием с последующим осаждением экзосом ультрацентрифугированием; путем удаления клеточного дебриса фильтрацией, отделением экзосом центрифугированием в градиенте сахарозы с последующим отмывом экзосом PBS и осаждением ультрацентрифугированием; с помощью готового коммерческого набора.
| УЗЕЛ ОТКЛОНЯЕМОГО НОСКА КРЫЛА | 1996 |
|
RU2181332C2 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Веникодробильный станок | 1921 |
|
SU53A1 |
Авторы
Даты
2015-12-20—Публикация
2014-10-09—Подача