Изобретение относится к области органической химии - химии гетероциклических соединений - и касается способа получения полугидрата 2-(1Н-имидазол-1-ил)пиридина, который является предшественником для синтеза азогетероарилфункционализированных карбеновых лигандов переходных металлов (Cu, Fe, Ru, Ag и др.), являющихся эффективными катализаторами изомеризации, полимеризации, гидрирования, образования С-С связи в реакциях ароматических галоидпроизводных [A. Raba, M. Cokoja, S. Ewald et al., Organometallics, V. 31, 2793-2800 (2012); X. Liu, W. Chen, J. Chem. Soc. Dalton Trans., V. 31, 599-608 (2012); В. Liu, Y. Zhang, D. Xu, J. Chem. Soc. Chem. Commun., N 47, 2883-2885 (2011)], ионных жидкостей, ускоряющих протекание реакций Сузуки, Хека и т.п. [С. Ye, J.-C. Xiao, В. Twamley et al., Eur. J. Org. Chem., 5095-5180 (2007)], различных билдинг-блоков получения фармпрепаратов для лечения онкологии (рак простаты) [WO 201116363 А2 (2011), 20111229 (2011)], болезни Альцгеймера и других заболеваний, связанных с нейропатологией [US 4826835 (1989)], как кардиотонические средства [WO 2011029537 А1 (2011), 20110317 (2011)].
Основной способ получения производных 2-(1Н-имидазол-1-ил)пиридина включает в себя взаимодействие имидазола с 2-галоидпиридинами [W. Chen, F. Liu, Ζ. Xi et al., Tetrahedron, V. 64, Ν 48, 4254-4259 (2008); R. Chandra, R. Chaudhary, V.K. Sankar et al., Tetrahedron Lett., V. 48, N 24, 4207-4210 (2007); B.M. Choudary, L.M. Kantam, B. Sreedhar et al., J. Am. Chem. Soc, V. 127, N 28, 9948-9949 (2005); M.R. Anneser, M. Cokoja, W.A. Herrmann et al., Tetrahedron Lett., V. 54, N 26, 3384-3387 (2013); S. Jennings, A. T. Londregan, L. Wei, Org. Lett., V. 13, N 7, 1840-1843 (2011); P. Khan, J. Chem. Soc, C, 85-88 (1970)]:
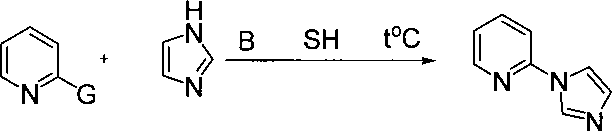
где G=F, Cl, Br, I, В - основание (карбонаты калия, цезия, трет-бутилат калия, едкое кали, N-этил-N,N-диизопропиламин, избыток имидазола), SH - растворитель (диметилсульфоксид, диметилформамид, без растворителя), t°C - температура проведения реакции (120-200°С). Использование окислов, солей или комплексов одновалентной меди, а также других активирующих добавок позволяет снижать температуру протекания реакции [S. Jennings, А.Т. Londregan, L. Wei, Org. Lett., V. 12, N 22, 5254-5257(2010); W. Zhang, J. Lan, R. Xie et al., J.Am. Chem. Soc., V. 129, N 45, 13879-13886 (2007)].
Выходы обычно высокие: 80-95%.
Недостатками указанного способа являются относительная «жесткость» условий протекания реакций, необходимость использования оснований, соединений меди в качестве катализаторов, других катализирующих добавок, различных апротонных растворителей, что ухудшает экологичность указанных процессов вследствие большого количества органических и неорганических отходов.
Другой способ получения 2-(1Н-имидазол-1-ил)пиридина включает в себя взаимодействие 2-бромпиридина с карбонилдиимидазолом [L. Ki, X.-D. Yang, H.-B. Zhang, Helv. Chim. Acta, V. 91, N 8, 1435-1442 (2008)]. Данная реакция осуществляется при 200°C, в присутствии карбоната калия, иодида одновалентной меди и тетраэтоксисилана, при микроволновом облучении. Выход целевого продукта равен 87%:
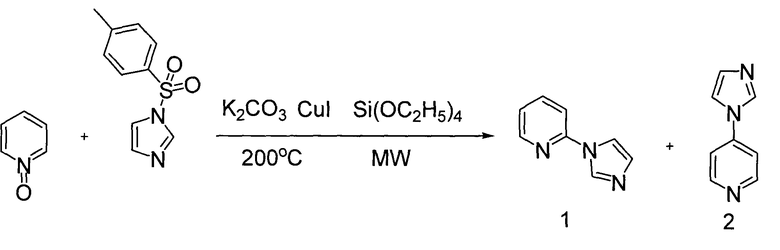
Недостатками указанного способа являются относительная «жесткость» условий протекания реакций, необходимость использования оснований, соединений меди, в качестве катализаторов, других катализирующих добавок. Уменьшают также синтетическую привлекательность данного способа необходимость использования ультразвукового облучения, вследствие чего снижается возможность масштабирования процесса, и образование смеси изомеров.
Наиболее близким аналогом предлагаемого нами способа является метод (прототип), описанный в [J.M. Keith, J. Org. Chem., V. 73, N 1, 327-330 (2008)]. Согласно этому способу для получения 2-(1Н-имидазол-1-ил)пиридина осуществляют взаимодействие эквимолярных количеств пиридин-N-оксида и 1,1′-сульфонилдиимидазола в кипящем толуоле в течение 4 час. После окончания реакции толуол отгоняют, остаток обрабатывают водным раствором едкого натра, экстрагируют хлористым метиленом. Целевой продукт - 2-(1Н-имидазол-1-ил)пиридин (1) - выделяют из реакционной смеси после отгонки растворителя с помощью колоночной хроматографии на силикагеле (элюент: смесь хлористого метилена и метанола). Выход соединения (1) - 78%:
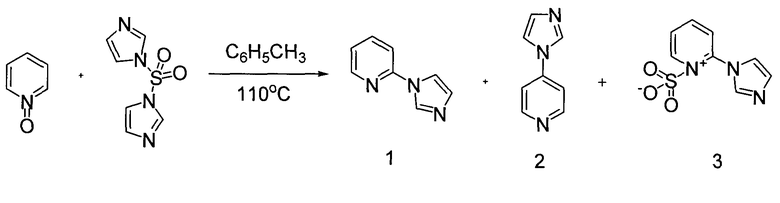
Недостатками способа являются:
- Использование дорогого реагента - 1,1′-сульфонилдиимидазола.
- Образование в реакции изомера целевого продукта - соединения (2) (содержание в смеси 12%), что затрудняет выделение 2-(1Н-имидазол-1-ил)пиридина (1) в чистом виде.
- Образование в реакции аддукта целевого продукта с трехокисью серы - соединение (3). Для превращения аддукта (3) в целевой продукт необходима специальная обработка его с использованием комплексов Родия и 7,8-бензохинолина [S. Chen, X. Li, G. Song, Tetrahedron Lett., V. 49, N 48, 6929-6932 (2002)].
- Необходимость обработки реакционной массы водной щелочью для перевода солей продуктов реакции в основную форму.
- Необходимость экстракции продуктов реакции органическими растворителями.
Настоящее изобретение направлено на достижение технического результата, заключающегося в удешевлении и упрощении процесса получения и выделения 2-(1Н-имидазол-1-ил)пиридина. Это достигается заменой 1,1′-сульфонилдиимидазола на более дешевый 1,1′-карбонилдиимидазол. Заявляемый способ включает в себя взаимодействие эквимолярных количеств пиридин-N-оксида и 1,1′-карбонилдиимидазола в кипящем толуоле в течение 10 час с последующим выделением целевого продукта с помощью колоночной хроматографии на силикагеле.
Нижеследующий пример иллюстрирует суть изобретения.
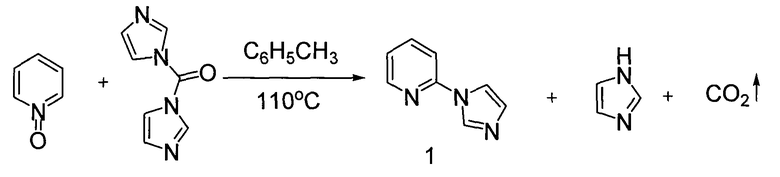
Пример 1. В круглодонную одногорлую стеклянную колбу емкостью 100 мл, снабженную обратным холодильником с водяным охлаждением, верхнее отверстие которой закрыто хлоркальциевой трубкой, загрузили 2.38 г (0.025 г-моля) пиридин-N-оксида, 4.25 г (0.026 г-моля) 1,1'-карбонилдиимидазола, 30 мл толуола. Полученную смесь кипятили в течение 10 час до полного расходования пиридин-N-оксида [контроль с помощью метода тонкослойной хроматографии на пластинах ″Silufol-U254″ элюент: хлороформ-метанол (9:1)]. Толуол отогнали в вакууме водоструйного насоса. Из остатка (~6 г) с помощью колоночной хроматографии на силикагеле [элюент: хлористый метилен-метанол (1%)] выделили 3.04 г (79 %) полугидрата 2-(1Н-имидазол-1-ил)пиридина в виде темно-желтого масла. Найдено (%): С, 62.49; Н, 5.31; N, 27.15. C8H7N3×0.5H2O. Вычислено (%): С, 62.32; Н, 5.23; N, 27.26. ИК-спектр (хлороформ), v/см-1: 1306, 1598, 1672, 2594, 3120. Спектр ЯМР 1Н (400 Мгц, CDCl3), δ, м.д., J/Гц: 7.21-7.29 (м., 2Н); 7.38 (д., J=8.2, 1H); 7.66 (с., 1H); 7.83 (т., J=8.6, 1H); 8.36 (с., 1H); 8.49 (м., 1H). Спектр ЯМР 13С (400 Мгц, CDCl3), δ, м.д.: 112.36, 116.25, 121.98, 130.76, 130.85, 134.91, 138.95, 149.14.
Образования 4-изомера - соединения (2) - зафиксировано не было.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ОКСИНДОЛОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1992 |
|
RU2073671C1 |
| АЗАИНДОЛОКСОУКСУСНЫЕ ПРОИЗВОДНЫЕ ПИПЕРАЗИНЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2303038C2 |
| АЗАИНДОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Xa | 2004 |
|
RU2330853C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛАМИДА 5-(4-ФТОРФЕНИЛ)-1-[2-((2R,4R)-4-ГИДРОКСИ-6-ОКСОТЕТРАГИДРОПИРАН-2-ИЛ)ЭТИЛ]-2-ИЗОПРОПИЛ-4-ФЕНИЛ-1H-ПИРРОЛ-3-КАРБОНОВОЙ КИСЛОТЫ | 2004 |
|
RU2337905C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ФЕНИЛПРОПАРГИЛОВОГО СПИРТА | 2012 |
|
RU2515241C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 1-О-АЦИЛ-2-ДЕЗОКСИ-2-ФТОР-4-ТИО-β-D-АРАБИНОФУРАНОЗ | 2010 |
|
RU2559364C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ (8↔8) ДИМЕРА КАТЕХИНА, И/ИЛИ ЭПИКАТЕХИНА, И/ИЛИ ЭПИКАТЕХИНГАЛЛАТА | 2000 |
|
RU2293081C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГЕНОЛ-3-АНГЕЛАТА | 2011 |
|
RU2586975C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ЛИПОЕВОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2233840C2 |
| ПРОИЗВОДНЫЕ 1-N-ФЕНИЛАМИНО-1Н-ИМИДАЗОЛА И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2004 |
|
RU2365586C2 |
Изобретение относится к области органической химии, а именно к способу получения полугидрата 2-(1Н-имидазол-1-ил)пиридина, заключающемуся во взаимодействии эквимолярных количеств пиридина-оксида и 1,1′-карбонилдиимидазола в кипящем толуоле в течение 10 час, последующей экстракции продуктов реакции органическими растворителями. Технический результат: разработан способ получения полугидрата 2-(1Н-имидазол-1-ил)пиридина, при этом процесс протекает без образования побочных веществ, затрудняющих выделение целевого продукта. 1 пр.
Способ получения полугидрата 2-(1H-имидазол-1-ил)пиридина взаимодействием эквимолярных количеств пиридина-оксида и 1,1′-карбонилдиимидазола в кипящем толуоле в течение 10 час, характеризующийся тем, что при выделении целевого продукта отсутствуют стадии обработки реакционной массы водной щелочью и экстракции продуктов реакции органическими растворителями; процесс протекает без образования побочных веществ, затрудняющих выделение целевого продукта.
| Yang, Xiao-Dong; Li, Liang; Zhang, Hong-Bin: "Ligand-free copper-catalyzed arylation of imidazole and N,N'-carbonyldiimidazole, and microwave-assisted synthesis of N-aryl-1H-imidazoles", Helvetica Chimica Acta, 91(8), 2008, pp.1435-1442 | |||
| J.M.Keith: "One step conversion of heteroaromatic-N-oxides to imidazolo-heteroarenes", J.Org.Chem., 2008, 73, pp.327-330 | |||
| RU 99119081 A, 27.07.2001 |
Авторы
Даты
2015-06-27—Публикация
2014-05-15—Подача