Данное изобретение относится к новым замещенным нитрокатехолам и их применению при лечении расстройств центральной и периферической нервной системы в соответствии с точно определенным режимом дозирования.
Объяснение для применения ингибиторов КОМТ (катехол-O-метилтрансферазы) в качестве вспомогательных средств при терапии с L-ДОПА/ингибитором декарбоксилазы ароматических L-аминокислот (ИДАА) основывается на их способности уменьшать метаболическое O-метилирование L-ДОПА до 3-O-метил-L-ДОПА (3-ОМД). Период вызванного L-ДОПА клинического улучшения непродолжителен как результат короткого времени полужизни in vivo L-ДОПА в отличие от длительного времени полужизни 3-ОМД. Кроме того, 3-ОМД конкурирует с L-ДОПА за перенос через гематоэнцефалический барьер (ВВВ, от - blood-brain barrier), что означает, что только очень ограниченное количество перорально введенной дозы L-ДОПА действительно достигает места действия, т.е. головного мозга. Обычно только через несколько лет после начальной L-ДОПА терапии с обычным режимом дозирования вызванное L-ДОПА клиническое улучшение снижается в конце каждого цикла дозировки, приводя к так называемому состоянию «изнашивания» двигательных флуктуации. Описана прямая взаимосвязь между феноменом «изнашивания» и накоплением 3-ОМД (Tohgi, H., et al., Neurosci. Letters, 132: 19-22, 1992). Предполагается, что это может быть следствием замедленного проникания L-ДОПА в мозг из-за конкуренции за транспортную систему через ВВВ с 3-ОМД (Reches, A. et al., Neurology, 32: 887-888, 1982) или, проще говоря, небольшое количество L-ДОПА способно достигнуть головного мозга (Mutt, J.G., Fellman, J.H., Clin. Neuropharmacol., 7: 35-49, 1984). В действительности ингибирование КОМТ защищает L-ДОПА от метаболического расщепления на периферии в ходе O-метилирования, так что при повторных дозах L-ДОПА средняя величина концентрации L-ДОПА в плазме повышается. В дополнение к пониженной конкуренции за перенос к головному мозгу значительно больший процент перорально введенной дозы L-ДОПА способен достигнуть места действия. Таким образом, ингибирование КОМТ способствует увеличению биодоступности L-ДОПА, и период антипаркинсонического действия удлиняется с однократными дозами L-ДОПА (Mutt, J.G., Lancet, 351: 1221-1222, 1998).
Наиболее эффективными ингибиторами КОМТ, описанными к настоящему времени, являются 3,4-дигидрокси-4'-метил-5-нитробензофенон (толкапон, Австралийский патент AU-B-69764/87) и (Б)-2-циано-N,N-диэтил-3-(3,4-дигидрокси-5-нитрофенил)акриламид (энтакапон, Германский патент DE 3740383 А1).
Имея по существу одинаковый фармакофор, толкапон отличается от энтакапона тем, что легко проникает в центральную нервную систему (ЦНС) и способен ингибировать церебральную КОМТ, а также периферическую КОМТ. Вскоре после его выпуска толкапон изъяли из продажи после того, как стало известно о нескольких случаях гепатотоксичности, включая три внезапных смерти от летального фульминантного гепатита. На сегодняшний день толкапон можно. использовать только для больных паркинсонизмом, которые не восприимчивы к другим способам лечения, и только при постоянном наблюдении за функцией печени, что дорого и неудобно для пациента. Хотя фактические механистические причины печеночной токсичности, связанной с толкапоном, понятны не полностью, in vitro изучения показали, что толкапон можно уменьшить метаболически до реакционно-способных промежуточных соединений, и предполагается, что они могут образовывать ковалентные аддукты с белками печени, вызывая гепатоцеллюлярное повреждение (Smith, K.S. et al., Chem. Res. Toxicol., 16: 123-128, 2003).
Энтакапон напротив, имея с толкапоном один и тот же нитрокатехоловый фармакофор, не связан с печеночной токсичностью и, как правило, рассматривается как безопасное лекарственное вещество. К сожалению, однако, энтакапон является значительно менее эффективным ингибитором КОМТ, чем толкапон, и обладает намного более коротким временем полужизни in-vivo. Это означает, что энтакапон имеет очень ограниченную продолжительность действия и, как следствие, лекарственно вещество следует вводить в очень больших дозах с каждой дозой L-ДОПА, принятой пациентом. В связи с этим клиническая эффективность энтакапона была подвергнута сомнению - действительно, недавнее исследование (Parashos, S.A. et al., Clin. Neuropharmacol., 27(3): 119-123, 2004) показало, что основной причиной для прекращения лечения энтакапоном пациентов с болезнью Паркинсона является ощутимая нехватка эффективности.
Кроме того, относительно короткое время полужизни in-vivo известных ингибиторов КОМТ требует продолжительных режимов лечения, обычно включающих введение нескольких доз в день, что многие пациенты находят обременительным. Например, толкапон следует вводить три раза в сутки. Поэтому данное обстоятельство может мешать соблюдению пациентом режима лечения и качеству жизни.
Таким образом, все еще существует потребность в ингибиторах КОМТ, проявляющих сбалансированные свойства биоактивности, биодоступности и безопасности. А именно, существует потребность в ингибиторах КОМТ, имеющих длительное время полужизни in-vivo и, таким образом, пролонгированное действие на КОМТ, что позволяет с меньшим количеством дозировок получать требуемый терапевтический эффект.
Нами неожиданно было обнаружено, что, несмотря на относительно короткое время полужизни, соединения общей формулы I представляют собой очень эффективные ингибиторы КОМТ, обеспечивающие исключительно длительную продолжительность действия по сравнению с ингибиторами КОМТ из предшествующего уровня техники.
Соединения общей формулы I также заметно повышают биодоступность L-ДОПА и увеличивают доставку L-ДОПА к головному мозгу. Соединения значительно повышают уровни дофамина в головном мозге в течение длительного периода времени.
Еще более неожиданно, что увеличенные уровни L-ДОПА поддерживаются постоянными в течение длительных периодов времени. Эти продолжительные влияния как на активность КОМТ, так и биодоступность L-ДОПА после введения соединений общей формулы I заметно больше чем те, что наблюдаются с толкапоном, единственным ингибитором КОМТ, до сих пор известным, который обеспечивает достаточно длительную продолжительность действия. (Толкапон имеет предельное время полужизни около 2 часов и должен вводиться около 3 раз в день). Кроме того, соединения общей формулы I вызывают постоянное увеличение доставки L-ДОПА к головному мозгу в течение длительных периодов времени, что отличается от того, что наблюдается с толкапоном, который склонен вызывать заметные колебания в доставке L-ДОПА к головному мозгу. Таким образом, соединения общей формулы I вероятнее всего будут наделены терапевтическими преимуществами вследствие продолжительного постоянного повышения уровней L-ДОПА, тогда как применение толкапона вероятно вызовет нежелательные побочные эффекты, такие как дискинезия, из-за внезапного увеличения и уменьшения в уровнях L-ДОПА.
Соединения общей формулы I являются соединениями, имеющими следующую формулу
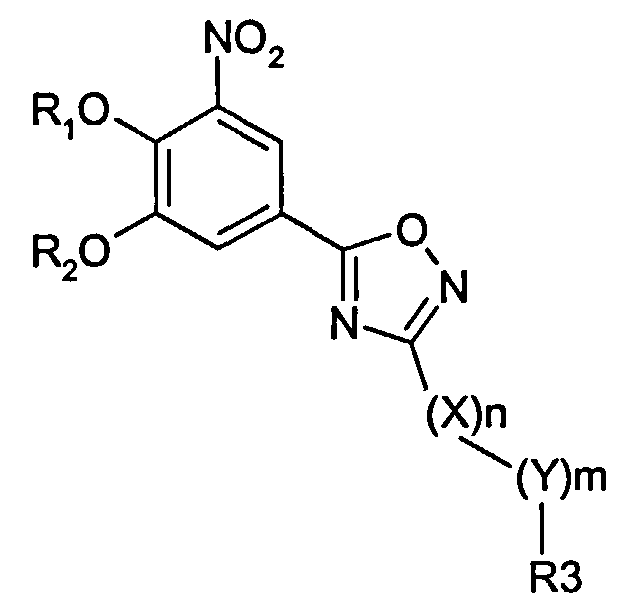
где R1 и R2 являются одинаковыми или разными и обозначают водород, группы, которые гидролизуются при физиологических условиях, или возможно замещенные алканоилы или ароилы; X обозначает метиленовую группу; Y представляет собой O, S или NH; n представляет собой 0, 1, 2 или 3; m представляет собой 0 или 1; R3 обозначает группу N-оксида пиридина согласно формуле А, Б или В, которая присоединяется, как показано неотмеченной связью:
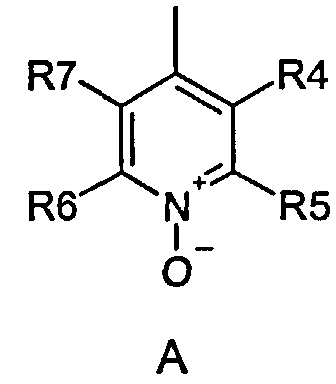
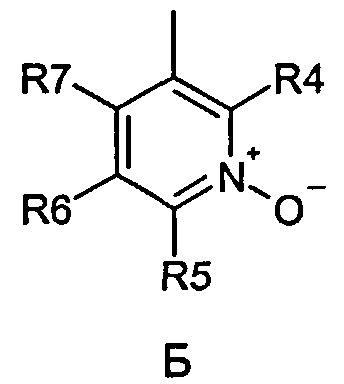
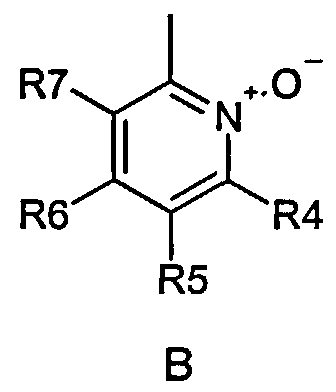
где R4, R5, R6 и R7 являются одинаковыми или разными и обозначают водород, алкил, тиоалкил, алкокси, арилокси, тиоарил, алканоил, ароил, арил, амино, алкиламино, диалкиламино, циклоалкиламино, гетероциклоалкиламино, алкилсульфонил, арилсульфонил, галоген, галоалкил, трифторметил, циано, нитро или гетероарил; или два или более взятых вместе R4, R5, R6 и R7 обозначают алифатические или гетероалифатические кольца или ароматические или гетероароматические кольца; термин «алкил», включая его вариант «алк-» в терминах, таких как «алкокси», «алканоил», означает углеродные остатки, неразветвленные или разветвленные, содержащие от одного до шести атомов углерода; термин «арил» означает фенильную или нафтильную группу; термин «гетероциклоалкил» представляет собой четырех-восьмичленное циклическое кольцо, возможно содержащее по меньшей мере один атом кислорода, серы или азота; термин «гетероарил» представляет собой пяти или шестичленное кольцо, содержащее по меньшей мере один атом серы, кислорода или азота; термин «галоген» представляет собой фтор, хлор, бром или йод; и если R4, R5, R6 и R7 представляют собой алкил или арил, то они возможно замещены одной или более чем одной гидрокси, алкокси группой или галогеном; или их фармацевтически приемлемая соль или эфир.
Предпочтительно R4, R5, R6 и R7 независимо друг от друга представляют собой водород, C1-C6-алкил, C1-C6-тиоалкил, C1-C6-алкокси, C6-C10-арилокси, C6-C10-тиоарил, C1-C6-алканоил, C7-C11-ароил, амино, C1-C6-алкиламино, ди-C1-C6-алкиламино, C3-C13-циклоалкиламино, C4-C8-гетероциклоалкиламино, C1-C6-алкилсульфонил, C6-C10-арилсульфонил, галоген, C1-C6-галоалкил, трифторметил, циано, нитро или гетероарил.
Когда R4, R5, R6 и/или R7 представляют собой C1-C6-алкильные остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил, пентил или гексил.
Когда R4, R5, R6 и/или R7 представляют собой C1-C6-тиоалкильные остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой тиометил, тиоэтил, тио-н-пропил, тио-изопропил, тио-н-бутил, тио-н-пентил или тио-н-гексил.
Когда R4, R5, R6 и/или R7 представляют собой C1-C6-алкокси остатки, то R4, R5, R7 и/или Ry предпочтительно представляют собой метокси, этокси, н-пропокси, изопропокси, н-бутокси, втор-бутокси или трет-бутокси.
Когда R4, R5, R6 и/или R7 представляют собой C6-C10-арилокси остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой фенокси или нафтокси.
Когда R4, R5, R6 и/или R7 представляют собой C6-C10-тиоарильные остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой тиофенил или тионафтил.
Когда R4, R5, R6 и/или R7 представляют собой C1-C6-алканоильные остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой метаноил, этаноил, пропаноил или бутаноил.
Когда R4, R5, R6 и/или R7 представляют собой C7-C11-ароильные остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой бензоил или нафтоил.
Когда R4, R5, R6 и/или R7 представляют собой C1-C6-алкиламино остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой метиламино, этиламино, н-пропиламино, изопропиламино или н-бутиламино.
Когда R4, R5, R6 и/или R7 представляют собой ди-C1-C6-алкиламино остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой диметиламино, диэтиламино, ди-н-пропиламино, ди-н-бутиламино, ди-изопропиламино, метилэтиламино, метилпропиламино или этилпропиламино.
Когда R4, R5, R6 и/или R7 представляют собой C3-C12-циклоалкиламино остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой пирролидино, пиперидино, циклогексиламино или дициклогексиламино.
Когда R4, R5, R6 и/или R7 представляют собой С4-С8-гетероциклоалкиламино остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой морфолино, 2,6-диметилморфолино, 3,5-диметилморфолино, пиперазино, N-метилпиперазино или N-этилпиперазино.
Когда R4, R5, R6 и/или R7 представляют собой C1-C6-алкилсульфонильные или C6-C10-арилсульфонильные остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой метилсульфонил, этилсульфонил, фенилсульфонил или толилсульфонил.
Когда R4, R5, R6 и/или R7 представляют собой остатки галогена, то R4, R5, R6 и/или R7 предпочтительно представляют собой хлор, бром, йод или фтор.
Когда R4, R5, R6 и/или R7 представляют собой C1-C6-галоалкильные остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой хлорметил, фторметил, дихлорметил, дифторметил, трихлорметил или трифторметил.
Когда R4, R5, R6 и/или R7 представляют собой гетероарильные остатки, то R4, R5, R6 и/или R7 предпочтительно представляют собой пиридил, пиримидил, изоксазолил, оксазолил, изоксадиазолил, оксадиазолил, триазолил или тетразолил.
Когда два или более взятых вместе остатка R4, R5, R6 и R7 представляют собой алифатические или гетероалифатические кольца или ароматические или гетероароматические кольца, то два или более остатка предпочтительно представляют собой алифатические или гетероалифатические кольца или ароматические или гетероароматические кольца. Предпочтительными объединенными остатками являются индолизинил, изоиндолил, индолил, индазолил, пуринил, хинолизинил, нафтиридинил, изохинолил и хинолил.
Когда они представляют собой арил или алкил, то вышеприведенные заместители R4, R5, R6 и R7 могут быть замещены один или более чем один раз гидрокси, алкокси группами или галогенами.
Подробности получения соединений общей формулы I можно найти в WO 2007/013830 A1.
Биодоступность, биоактивность, профиль безопасности и другие родственные свойства, известные в данной области (например, проницаемость гематоэнцефалического барьера), могут быть обычным способом оптимизированы квалифицированным специалистом на основе идеи настоящей заявки путем изменения заместителей R1-R7 вышеприведенной общей формулы I для получения желательного сбалансированного сочетания свойств.
Также соединения общей формулы I могут находиться в форме их фармакологически приемлемых солей или эфиров. Подходящие фармацевтически приемлемые противоионы известны в данной области.
Также возможно применять пролекарства соединений общей формулы I для изменения терапевтического профиля активного соединения.
В следующем описании медицинских показаний, методов лечения и режимов дозирования фармацевтических композиций, содержащих соединения согласно общей формуле I по изобретению, наиболее предпочтительным примером соединения согласно общей формуле 1 является 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол, далее обозначаемый как соединение А, и его фармакологически приемлемые соли и эфиры. Время полужизни соединения А является относительно коротким, учитывая его длительную продолжительность действия.
Другие предпочтительные соединения вышеприведенной общей формулы (I) для применения при последующих медицинских показаниях, методах лечения и режимах дозирования включают 3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-4-(трифторметил)пиридин-1-оксид, 2-хлор-3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-4,6-диметилпиридин-1 -оксид, 3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-2-метил-6-(трифторметил)пиридин-1 -оксид, 5-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-2-(трифт6рметил)пиридин-1-оксид, 5-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-2-метил-4-(трифторметил)пиридин-1-оксид, 3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-2,6-диметил-4-(трифторметил)пиридин-1-оксид, 3,5-дихлор-4-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)пиридин-1-оксид, 3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-6-метил-2-фенил-4-(трифторметил)пиридин-1-оксид, 2-бром-3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-4,5,6-триметилпиридин-1-оксид, 2-хлор-3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-4,5,6-триметилпиридин-1-оксид, 3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-2-(трифторметил)пиридин-1-оксид, 2,5-дихлор-3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-4,6-диметилпиридин-1 -оксид, 3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-5-(трифторметил)пиридин-1-оксид, 3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-2-фторпиридин-1-оксид, 4-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-2-фторпиридин-1-оксид, 2-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-6-ил)-6-фторпиридин-1-оксид, 2-хлор-3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-6-метилпиридин-1-оксид, 2-бром-3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-6-метилпиридин-1 -оксид и 2-бром-5-хлор-3-(3-(3,4-дигидрокси-5-нитрофенил)-1,2,4-оксадиазол-5-ил)-4,6-диметилпиридин-1-оксид и их фармакологически приемлемые соли или эфиры.
Настоящее изобретение относится к применению соединений общей формулы I, их фармацевтически приемлемых солей или эфиров для предотвращения или лечения определенных патологических состояний, особенно у людей (например, расстройств центральной и периферической нервной системы), и к получению фармацевтических композиций, содержащих их.
Для получения фармацевтических композиций соединений общей формулы I инертные фармацевтически приемлемые носители смешивают с активными соединениями. Фармацевтически приемлемые носители могут быть твердыми или жидкими. Препараты твердой формы включают порошки, таблетки, диспергируемые гранулы и капсулы. Твердый носитель может представлять собой одно или более чем одно вещество, которое также может действовать в качестве разбавителя, ароматизатора, солюбилизатора, смазывающего вещества, суспендирующего агента, связующего вещества, скользящего вещества или дезинтегрирующего вещества; он также может представлять собой инкапсулирующее вещество.
Предпочтительно фармацевтическая композиция находится в форме единичного дозирования, например упакованный препарат, упаковка содержит дискретные количества препарата, например упакованные таблетки, капсулы и порошки в пузырьках или ампулах.
Предпочтительно подвергаемые лечению патологические состояния представляют собой связанные с центральной и периферической нервной системой расстройства человека, а именно, те, которые получают пользу от введения ингибитора КОМТ. Предпочтительно расстройства представляют собой двигательные расстройства, включая расстройства, относящиеся к паркинсонизму, болезни Паркинсона и синдрому усталых ног. Наиболее предпочтительным расстройством, связанным с центральной и периферической нервной системой, является болезнь Паркинсона.
Как используется здесь, термин «лечение» и варианты, такие как «лечить» или «подвергаемый лечению», относятся к любому режиму, который может приносить пользу человеку или животному, не относящемуся к человеку. Лечение может быть в отношении существующего состояния или может быть профилактическим (предупреждающее лечение). Лечение может включать целебное действие, облегчение или профилактические эффекты, относящиеся к одному или более чем одному симптому, связанному с расстройствами, связанными с центральной и периферической нервной системой.
Соединения общей формулы I предпочтительно используются для получения лекарства для предотвращения или лечения расстройств, связанных с центральной и периферической нервной системой, в соответствии с точно определенным режимом дозирования.
Подходящие режимы дозирования включают режимы, имеющие периодичность дозирования в диапазоне от приблизительно двух раз в день до приблизительно одного раза в семь дней.
Предпочтительно периодичность дозирования выбрана от одного раза в три дня до одного раза в неделю, то есть введение приблизительно один раз каждый 3ий, 4ый, 5ый, 6ой или 7ой день.
Подходящие неограниченные начальные точки интервалов дозирования включают утро, середину дня, полдень, послеобеденное время, вечер и полночь.
Как используется здесь, термин «эффективная суточная доза» представляет собой эффективное ежедневное количество вводимого соединения при введении в соответствии с периодичностью дозирования.
В настоящем изобретении эффективные суточные дозы соединений общей формулы I находятся в диапазоне от приблизительно 1 до приблизительно 900 мг/сутки, более предпочтительно от приблизительно 5 до приблизительно 400 мг/сутки, еще более предпочтительно от приблизительно 25 до приблизительно 300 мг/сутки, еще более предпочтительно от приблизительно 70 до приблизительно 200 мг/сутки и наиболее предпочтительно от приблизительно 120 до приблизительно 150 мг/сутки.
Как используется здесь, термин «единица дозирования» относится к количеству соединения, вводимого с любой периодичностью дозирования.
Предпочтительно отдельные единицы дозирования соединений общей формулы I находятся в диапазоне от приблизительно 1 до приблизительно 2400 мг, более предпочтительно от приблизительно 10 до приблизительно 1200 мг, еще более предпочтительно от приблизительно 25 до приблизительно 800 мг, еще более предпочтительно от приблизительно 50 до приблизительно 400 мг и наиболее предпочтительно от приблизительно 100 до приблизительно 200 мг.
Предпочтительно объект, подвергаемый лечению с соединением общей формулы I, также получает лечение с предшественником дофамина (ДОПА) и/или ИДАА.
Типичные предшественники ДОПА включают L-ДОПА.
Подходящие ингибиторы декарбоксилазы ароматических L-аминокислот включают бенсеразид и карбидопу.
Соединения общей формулы I, предшественник ДОПА и ИДАА могут быть введены раздельно или в любом сочетании. Они могут быть введены параллельно (например, совместно) или последовательно и с одинаковой или разной периодичностью дозирования. Например, соединения общей формулы I могут быть параллельно или последовательно введены с предшественником ДОПА. В случае сопутствующего введения также возможно объединить оба или все активные ингредиенты в одной форме единичного дозирования.
Согласно другому аспекту настоящего изобретения разработан способ лечения по меньшей мере одного патологического состояния у пациента, нуждающегося в этом, согласно которому вводят пациенту от приблизительно одного раза в три дня до приблизительно одного раза в неделю фармакологически эффективную дозу соединения общей формулы I, как определено выше.
Согласно другому аспекту изобретения разработан способ уменьшения ингибирования КОМТ у объекта в течение 3-7 дней, согласно которому вводят объекту от приблизительно одного раза в три дня до приблизительно одного раза в неделю эффективную дозу соединения общей формулы I, как определено выше.
Согласно другому аспекту изобретения разработан способ увеличения уровней L-ДОПА в головном мозге объекта в течение 3-7 дней, согласно которому вводят объекту от приблизительно одного раза в три дня до приблизительно одного раза в неделю эффективную дозу соединения общей формулы I, как определено выше.
Согласно другому аспекту изобретения разработан способ увеличения уровней L-ДОПА в плазме объекта в течение 3-7 дней, согласно которому вводят объекту от приблизительно одного раза в три дня до приблизительно одного раза в неделю эффективную дозу соединения общей формулы I, как определено выше.
Согласно другому аспекту изобретения разработан способ уменьшения уровней 3-O-метил-L-ДОПА (3-ОМД) в головном мозге объекта в течение 3-7 дней, согласно которому вводят объекту от приблизительно одного раза в три дня до приблизительно одного раза в неделю эффективную дозу соединения общей формулы I, как определено выше.
Согласно другому аспекту изобретения разработан способ уменьшения уровней 3-ОМД в плазме объекта в течение 3-7 дней, согласно которому вводят объекту от приблизительно одного раза в три дня до приблизительно одного раза в неделю эффективную дозу соединения общей формулы I, как определено выше.
Согласно другому аспекту изобретения разработан способ увеличения биодоступности L-ДОПА в головном мозге объекта в течение 3-7 дней, согласно которому вводят объекту от приблизительно одного раза в три дня до приблизительно одного раза в неделю эффективную дозу соединения общей формулы I, как определено выше.
Согласно другому аспекту изобретения разработан способ увеличения биодоступности L-ДОПА в плазме объекта в течение 3-7 дней, согласно которому вводят объекту от приблизительно одного раза в три дня до приблизительно одного раза в неделю эффективную дозу соединения общей формулы I, как определено выше.
Объект, подвергаемый лечению с соединением общей формулы I, также может получать лечение с предшественником ДОПА и/или ингибитором декарбоксилазы ароматических L-аминокислот. Подобное лечение с предшественником ДОПА и/или ИДАА может предшествовать, следовать за или проходить одновременно или параллельно с лечением с соединением общей формулы I.
Настоящее изобретение также относится к упаковке, включающей фармацевтическую композицию соединения общей формулы 1 в сочетании с инструкциями по введению указанного препарата с режимом дозирования, имеющим периодичность дозирования в диапазоне от приблизительно одного раза в три дня до приблизительно одного раза в неделю.
Материалы и методы
В двойном слепом рандомизированном плацебо-контролируемом изучении, предназначенном для исследования переносимости, фармакокинетики и фармакодинамики соединений общей формулы I, группам по восемь молодых здоровых мужчин вводили плацебо, 5 мг, 10 мг, 20 мг или 30 мг соединения А по утрам натощак в течение 8 дней. В каждой группе (5 мг, 10 мг, 20 мг или 30 мг) 2 отдельных представителей случайным образом отбирали для введения плацебо, а 6 подвергали лечению.
Активность растворимой катехол-O-метилтранферазы (P-КОМТ) выражали как количество метанефрина (в пмоль), образуемого под воздействием Р-КОМТ отмытых эритроцитов на субстрат эпинефрина, на миллиграмм белка в образце за час.
Пробы крови были взяты в следующие периоды и использовались для получения отмытых эритроцитов:
День 1: до приема дозы, и через 0,25, 0,5, 0,75, 1, 1,5, 2, 3, 4, 6, 8, 10, 12 и 16 часов после приема дозы
Дни 2-7: только до приема дозы
День 8: до приема дозы, и через 0,25, 0,5, 0,75, 1, 1,5, 2, 3, 4, 6, 8, 10, 12, 16, 24, 36, 48, 72, 96, 120 и 144 часа после приема дозы
После центрифугирования и удаления плазмы супернатант (самый верхний слой эритроцитов) удаляли и пробирки помещали на лед. Затем добавляли холодный 0,9% раствор хлорида натрия объемом в два раза больше, чем объем эритроцитов. Эритроциты центрифугировали и промывали, используя данную процедуру три раза. Центрифугирование осуществляли при 4°С и при приблизительно 1500 g в течение 10 минут. Получали две точно по 500 мкл отмеренные пипеткой аликвоты отмытых эритроцитов и каждую аликвоту хранили в 2-мл пробирке при -70°С до использования в анализе.
Определение активности P-КОМТ осуществляли в соответствии с надлежащей лабораторной практикой (НЛП) с помощью ВЭЖХ с электрохимическим детектированием.
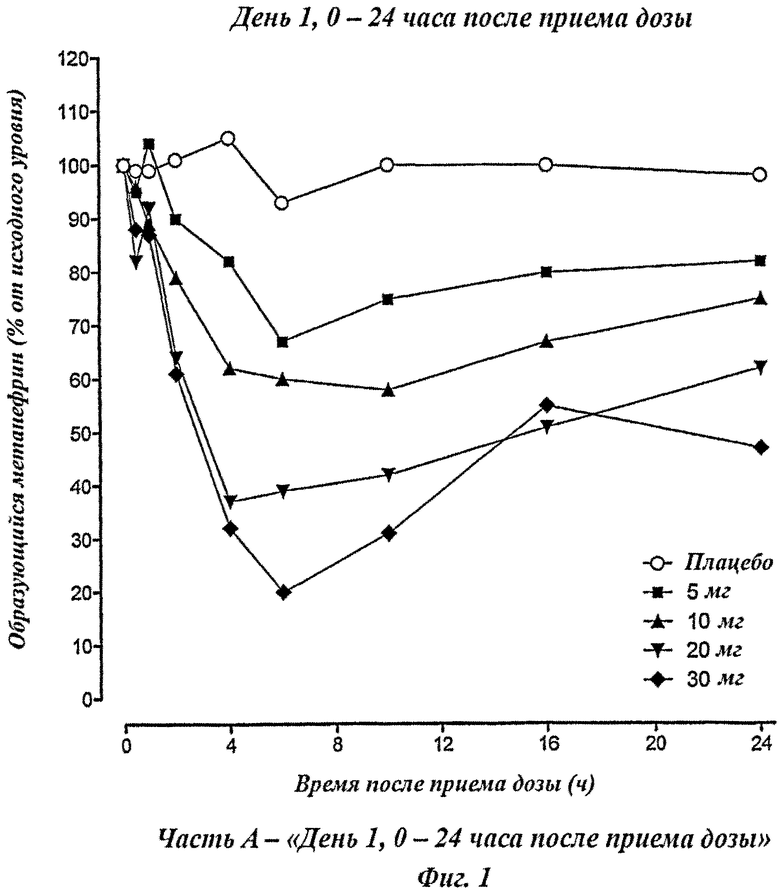
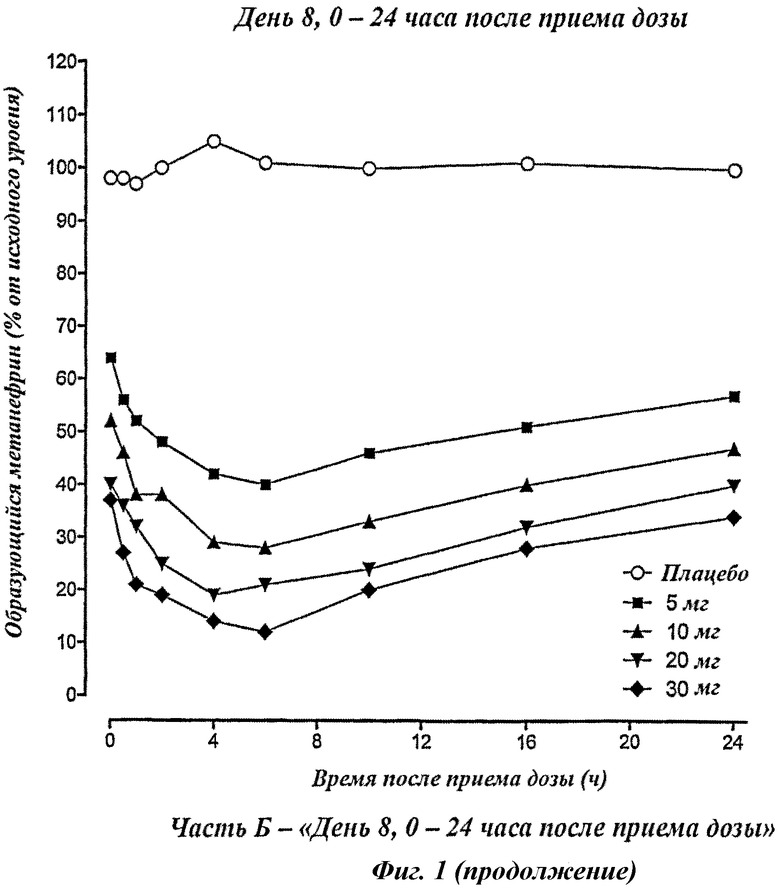
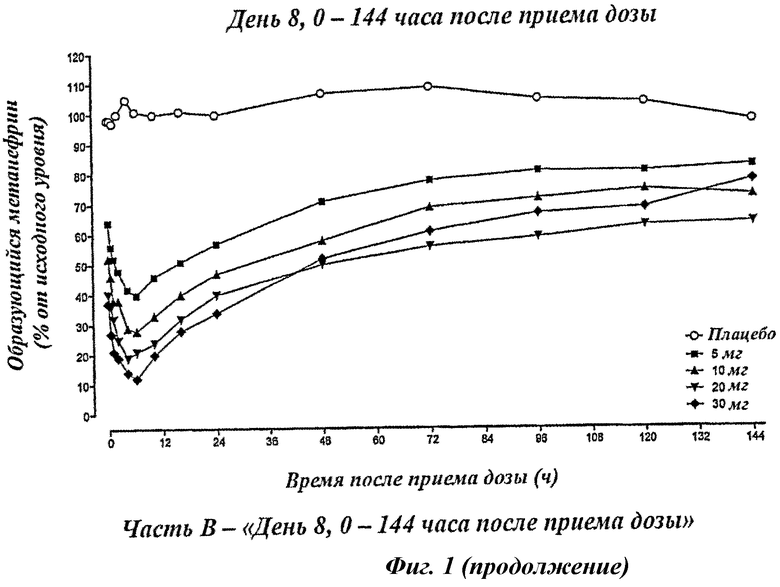
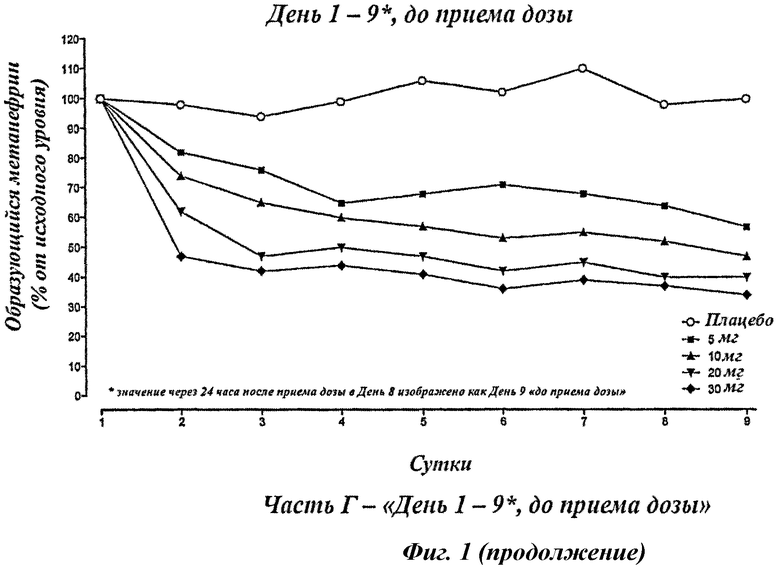
Описание фигур
Фигура 1 показывает значение активности P-КОМТ [выраженное как % изменения образующегося метанефрина относительно исходного уровня (до приема дозы в День 1)] в зависимости от времени после первой дозы (День 1) и последней дозы (День 8), и до приема дозы 8-дневного периода введения плацебо, 5 мг, 10 мг, 20 мг или 30 мг Соединения А (n=6 для каждой лечебной группы и n=8 для каждой контрольной группы).
Результаты
Фигура 1 показывает зависимость значение активности P-КОМТ - время после первой дозы (Фигура 1А) и последней дозы (Фигура 1Б и 1В), и до приема дозы (Фигура 1Г) 8-дневного режима введения один раз в сутки плацебо, 5 мг, 10 мг, 20 мг или 30 мг дозировки соединения А (n=6 для лечебной группы и n=8 для контрольной группы).
Заметное и продолжительное ингибирование P-КОМТ наблюдалось с первого введения, и через 5 дней (144 ч) после последней дозы значимое ингибирование КОМТ все еще было заметно, что подтверждает возможность режима введения один раз в неделю.
Теперь изобретение будет описано со ссылкой на следующий пример получения, который, как подразумевается, не ограничивает изобретение каким-либо образом.
Пример 1 - Получение соединения А
(5-[3-(2,5-Дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол)
а. К перемешиваемому раствору 3,4-дибензилокси-5-нитробензойной кислоты (0,50 г, 1,319 ммоль) в диметилформамиде (5 мл) при комнатной температуре добавляли 1,1-карбонилдиимидазол (0,24 г, 1,45 ммоль) за один раз. После перемешивания в течение девяноста минут одной порцией добавляли 2,5-дихлор-N'-гидрокси-4,6-диметилникотинамид (0,40 г, 1,45 ммоль). Полученную в результате смесь перемешивали при 135°С в течение пяти часов и затем при комнатной температуре в течение ночи. Реакционную смесь выливали в лед - 2 н. HCl (100 мл) и полученный в результате осадок отфильтровывали, промывали водой и высушивали на воздухе. Перекристаллизация из изопропанола давала бледно-желтое твердое вещество (0,55 г, 72%).
б. К перемешиваемому раствору полученного выше твердого вещества (0,50 г, 0,866 ммоль) в дихлорметане (20 мл) добавляли комплекс мочевина - перекись водорода (0,41 г, 4,33 ммоль) за один раз. Смесь охлаждали на бане с ледяной водой и по каплям добавляли трифторуксусный ангидрид (0,73 г, 3,46 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи, после чего нерастворимое вещество отфильтровывали. Фильтрат промывали водой и солевым раствором, высушивали над безводным сульфатом магния, фильтровали и выпаривали. Остаток кристаллизовали из изопропанола, что давало бледно-желтое твердое вещество (0,35 г, 68%).
в. К перемешиваемому раствору полученного выше твердого вещества (0,30 г, 0,5 ммоль) в дихлорметане (10 мл) при -78°С в атмосфере аргона по каплям добавляли трибромид бора (0,38 г, 1,5 ммоль). Полученную в результате фиолетовую суспензию перемешивали при комнатной температуре в течение одного часа, затем опять охлаждали до -78°С и осторожно гасили, добавляя воду. После перемешивания при комнатной температуре в течение одного часа осадок отфильтровывали, промывали водой и высушивали при 50°С в вакууме, что давало требуемое соединение в виде желтых кристаллов (0,18 г, 87%) с Tпл 237-240°С.
Пример 2 - Фармацевтический препарат
Фармацевтические препараты получают, как изложено ниже:
Капсула:
Капсула:
Таблетка:
Пример 3 - Режим дозирования
Пациентам дают один раз в неделю таблетки, содержащие 100 мг соединения общей формулы I, пациентам, которые страдают от болезни Паркинсона, и которые проходят L-ДОПА терапию. Наблюдается продолжительное ингибирование КОМТ и значительное улучшение клинической картины.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕЖИМ ДОЗИРОВАНИЯ ИНГИБИТОРОВ КОМТ | 2007 |
|
RU2518483C2 |
| Режим введения для нитрокатехолов | 2011 |
|
RU2639131C2 |
| ПРОИЗВОДНЫЕ НИТРОКАТЕХОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ СОМТ | 2006 |
|
RU2441001C2 |
| ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ, СОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ НИТРОКАТЕХИНА, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2701731C2 |
| ТАРТРАТНЫЕ ПРОИЗВОДНЫЕ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА СВЕРТЫВАНИЯ КРОВИ IXA | 2007 |
|
RU2446160C2 |
| АЛЛОСТЕРИЧЕСКИЕ МОДУЛЯТОРЫ МЕТАБОТРОПНЫХ ГЛУТАМАТНЫХ РЕЦЕПТОРОВ | 2004 |
|
RU2360902C2 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛА | 2006 |
|
RU2416605C2 |
| НОВОЕ ПРОИЗВОДНОЕ КАТЕХИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПРОИЗВОДНОЕ КАТЕХИНА, ПРИМЕНЕНИЕ ПРОИЗВОДНОГО КАТЕХИНА И ПРИМЕНЕНИЕ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ | 2008 |
|
RU2459812C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИРАЗОЛА | 2014 |
|
RU2682247C2 |
| ПРОИЗВОДНЫЕ БЕНЗАНИЛИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ АНТАГОНИЗМ К 5-HT РЕЦЕПТОРАМ | 1992 |
|
RU2077535C1 |
Настоящее изобретение относится к химико-фармацевтической промышленности и представляет собой применение замещенных нитрокатехолов формулы (I) для предотвращения или лечения расстройств, связанных с центральной и периферической нервной системой, которые получают пользу от ингибирования катехол-О-метилтранферазы (КОМТ), согласно режиму дозирования в диапазоне от одного раза в три дня до одного раза в неделю. 3 н. и 42 з.п. ф-лы, 1 ил., 3 пр.
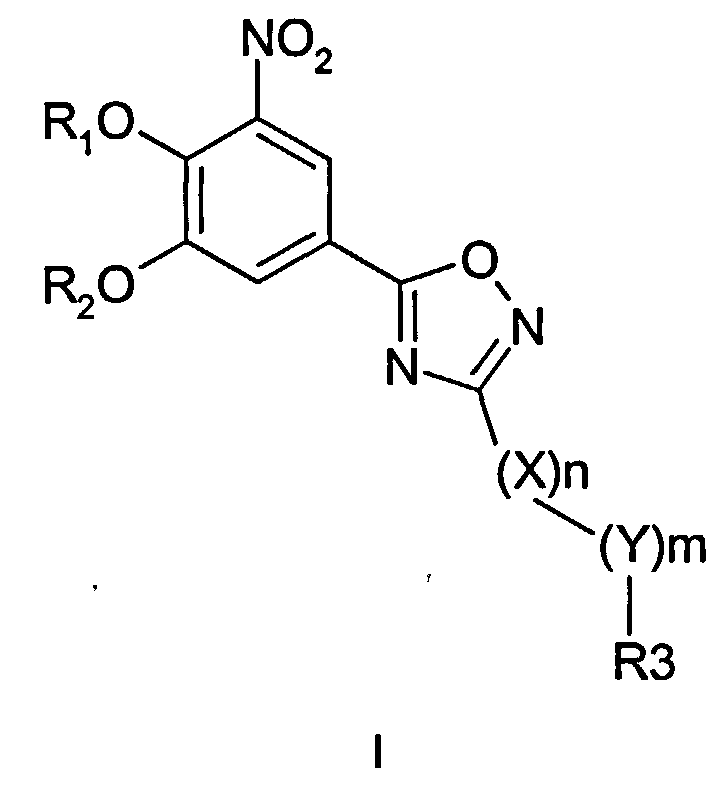
1. Применение соединения формулы I
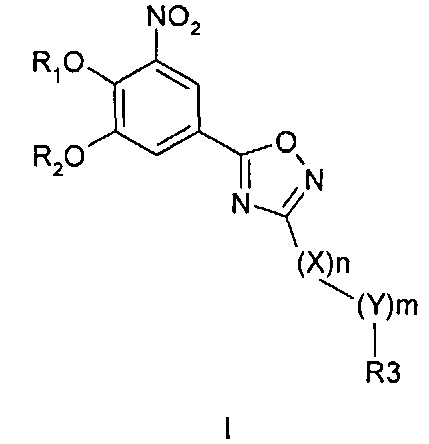
где R1 и R2 представляют собой водород, X обозначает метиленовую группу; Y представляет собой O; n представляет собой 0, 1, 2 или 3; m представляет собой 0 или 1; R3 обозначает группу N-оксида пиридина согласно формуле Б, которая присоединяется, как показано неотмеченной связью:
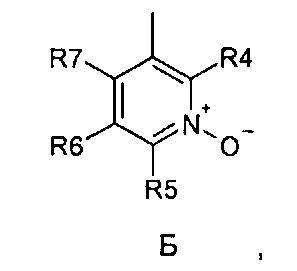
где R4, R5, R6 и R7 являются одинаковыми или разными и обозначают водород, низший алкил, галоген, галоалкил, трифторметил, причем термин «алкил», включая его вариант «алк-» в терминах, таких как «алкокси» и «алканоил», означает углеродные остатки, неразветвленные или разветвленные, содержащие от одного до шести атомов углерода; термин «галоген» представляет собой фтор, хлор, бром или йод; или его фармацевтически приемлемой соли или эфира для получения лекарства для предотвращения или лечения расстройств, связанных с центральной и периферической нервной системой, которые получают пользу от ингибирования катехол-О-метилтранферазы (КОМТ), где указанное лекарство вводят согласно режиму дозирования, имеющему периодичность дозирования в диапазоне от приблизительно одного раза в три дня до приблизительно одного раза в неделю.
2. Применение соединения формулы I
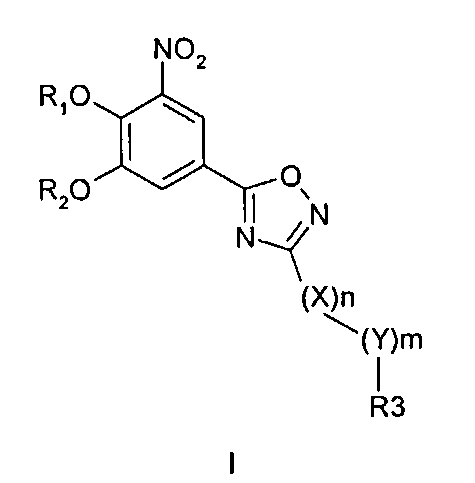
где R1 и R2 представляют собой водород; X обозначает метиленовую группу; Y представляет собой О; n представляет собой 0, 1, 2 или 3; m представляет собой 0 или 1; R3 обозначает группу N-оксида пиридина согласно формуле Б, которая присоединяется, как показано неотмеченной связью:
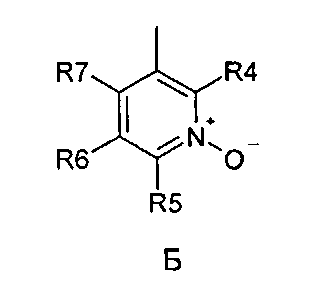
где R4, R5, R6 и R7 являются одинаковыми или разными и обозначают водород, низший алкил, галоген, галоалкил, трифторметил; термин «алкил», включая его вариант «алк-» в терминах, таких как «алкокси», «алканоил», означает углеродные остатки, неразветвленные или разветвленные, содержащие от одного до шести атомов углерода; термин «галоген» представляет собой фтор, хлор, бром или йод; или его фармацевтически приемлемой соли или эфира для предотвращения или лечения расстройств, связанных с центральной и периферической нервной системой, которые получают пользу от ингибирования КОМТ, где указанное соединение вводят согласно режиму дозирования, имеющему периодичность дозирования в диапазоне от приблизительно одного раза в три дня до приблизительно одного раза в неделю.
3. Применение по п.1 или 2, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
4. Применение по п.1 или 2, где режим дозирования составляет один раз в три дня.
5. Применение по п.4, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
6. Применение по п.1 или 2, где режим дозирования составляет один раз в четыре дня.
7. Применение по п.6, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
8. Применение по п.1 или 2, где режим дозирования составляет один раз в пять дней.
9. Применение по п.8, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
10. Применение по п.1 или 2, где режим дозирования составляет один раз в шесть дней.
11. Применение по п.10, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
12. Применение по п.1 или 2, где режим дозирования составляет один раз в семь дней.
13. Применение по п.12, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
14. Применение по п.1 или 2, где начальная точка интервала дозирования включает утро, середину дня, послеобеденное время и полночь.
15. Применение по п.1 или 2, где начальная точка интервала дозирования представляет собой вечер.
16. Применение по п.1 или 2, где расстройство, связанное с центральной и периферической нервной системой, подвергают лечению с терапией L-ДОПА / ингибитором декарбоксилазы ароматических L-аминокислот.
17. Применение по п.16, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
18. Применение по п.1 или 2, где расстройство, связанное с центральной и периферической нервной системой, представляет собой двигательное расстройство.
19. Применение по п.18, где двигательное расстройство представляет собой болезнь Паркинсона.
20. Применение по п.18, где двигательное расстройство представляет собой синдром усталых ног.
21. Применение по п.20, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
22. Применение по п.1 или 2, где соединение формулы I вводят последовательно или одновременно с L-ДОПА.
23. Применение по п.22, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
24. Применение по п.1 или 2, где соединение формулы I вводят последовательно или одновременно с ингибитором декарбоксилазы ароматических L-аминокислот.
25. Применение по п.24, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
26. Применение по п.24, где ингибитор декарбоксилазы ароматических L-аминокислот представляет собой карбидопу или бенсеразид.
27. Применение по п.1 или 2, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол и его применяют во вспомогательной терапии пациента, где пациент также принимает L-ДОПА и/или ингибитор декарбоксилазы ароматических L-аминокислот.
28. Применение по п.1 или 2, где единица дозирования представляет собой 5 мг, 10 мг, 20 мг, 30 мг или 100 мг.
29. Применение по п.1 или 2, где диапазон доз представляет собой от 50 мг до 400 мг, предпочтительно от 100 мг до 200 мг.
30. Способ предотвращения или лечения расстройств, связанных с центральной и периферической нервной системой, которые получают пользу от ингибирования КОМТ, у пациента, нуждающегося в этом, согласно которому вводят пациенту от приблизительно одного раза в три дня до приблизительно одного раза в семь дней фармакологически эффективную дозу соединения формулы I
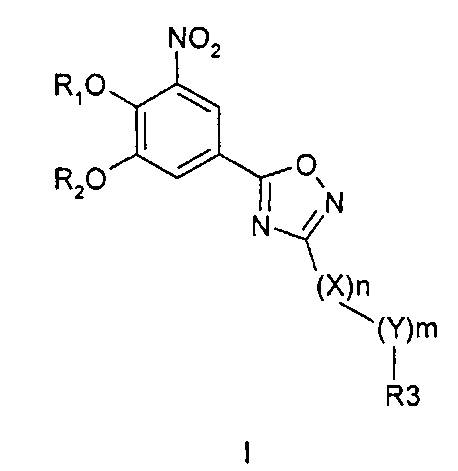
где R1 и R2 являются водородом; X обозначает метиленовую группу; Y представляет собой O; n представляет собой 0, 1, 2 или 3; m представляет собой 0 или 1; R3 обозначает группу N-оксида пиридина согласно формуле Б, которая присоединяется, как показано неотмеченной связью:
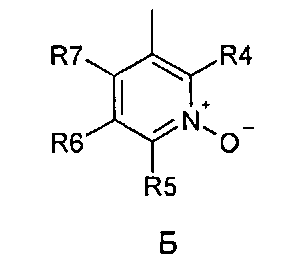
где R4, R5, R6 и R7 являются одинаковыми или разными и обозначают водород, низший алкил, галоген, галоалкил, трифторметил; термин «алкил», включая его вариант «алк-» в терминах, таких как «алкокси», «алканоил», означает углеродные остатки, неразветвленные или разветвленные, содержащие от одного до шести атомов углерода; термин «галоген» представляет собой фтор, хлор, бром или йод; или его фармацевтически приемлемой соли или эфира.
31. Способ по п.30, где введение осуществляют один раз в три дня.
32. Способ по п.30, где введение осуществляют один раз в четыре дня.
33. Способ по п.30, где введение осуществляют один раз в пять дней.
34. Способ по п.30, где введение осуществляют один раз в шесть дней.
35. Способ по п.30, где введение осуществляют один раз в семь дней.
36. Способ по любому из пп.30-35, где состояние или заболевание подвергают лечению с терапией L-ДОПА/ингибитором декарбоксилазы ароматических L-аминокислот.
37. Способ по п.36, где состояние или заболевание представляет собой двигательное расстройство.
38. Способ по п.37, где двигательное расстройство представляет собой болезнь Паркинсона.
39. Способ по п.37, где двигательное расстройство представляет собой синдром усталых ног.
40. Способ по любому из пп.30-35, 37, 38 и 39, где соединение формулы I представляет собой 5-[3-(2,5-дихлор-4,6-диметил-1-окси-пиридин-3-ил)-[1,2,4]оксадиазол-5-ил]-3-нитробензол-1,2-диол.
41. Способ по любому из пп.30-35, 37, 38 и 39, где способ дополнительно включает последовательное или сопутствующее введение L-ДОПА.
42. Способ по любому из пп.30-35, 37, 38 и 39, где способ дополнительно включает последовательное или сопутствующее введение ингибитора декарбоксилазы ароматических L-аминокислот.
43. Способ по п. 42, где ингибитор декарбоксилазы ароматических L-аминокислот представляет собой карбидопу или бенсеразид.
44. Способ по любому из пп.30-35, где единица дозирования представляет собой 5 мг, 10 мг, 20 мг, 30 мг или 100 мг.
45. Способ по любому из пп.30-35, где диапазон доз представляет собой от 50 мг до 400 мг, предпочтительно от 100 мг до 200 мг.
| WO 2007013830 A, 01.02.2007 | |||
| EA 200702469 A, 30.06.2008 | |||
| EP 1845097 A, 17.10.2007 |
Авторы
Даты
2015-07-20—Публикация
2009-07-29—Подача