По данной заявке испрашивается приоритет согласно предварительной заявке США №61/405,582, поданной 21 октября 2010, которая включена посредством отсылки во всей полноте.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Ряд насущных проблем противостоит индустрии здравоохранения. На декабрь 2009 зарегистрировано 105305 пациентов, как нуждающиеся в трансплантации органов Службой Обеспечения Донорскими Органами (UNOS). Между январем и сентябрем 2009 было проведено только 21423 трансплантации. Каждый год к списку UNOS добавляется больше пациентов, чем проводится трансплантаций, что приводит к суммарному увеличению числа пациентов, ожидающих трансплантацию. Например, в начале 2008 было зарегистрировано 75834 человека, как нуждающиеся в почке; к концу того года это число выросло до 80972. За тот год было проведено 16546 трансплантаций почек, но к списку добавились 33005 новых пациентов. Уровень трансплантации в 2008 для пациентов, зарегистрированных UNOS как нуждающихся в почке, составил 20%. Уровень смертности пациентов из списка ожидания составил 7%.
Дополнительно, стоимость исследования и разработки нового фармацевтического соединения составляет приблизительно 1,8 миллиардов долларов США. Смотри Paul, et al. (2010). How to improve R&D productivity: the pharmaceutical industry's grand challenge. Nature Reviews Drug Discovery 9(3):203-214. Поиск лекарственных средств - это процесс, при котором лекарственные средства находят и/или разрабатывают. Процесс поиска лекарственных средств обычно включает по меньшей мере стадии: идентификации кандидатов, синтеза, получения характеристик, скрининга и анализов на терапевтическую эффективность. Несмотря на успехи в технологии и понимании биологических систем, поиск лекарственных средств все еще является продолжительным, дорогим и неэффективным процессом с низкой степенью нового терапевтического открытия.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Существует необходимость в инструментах и методиках, которые ускоряют применение регенеративной медицины и технологий тканевой инженерии для облегчения острой потребности в тканях и органах. Также существует необходимость в инструментах и методиках, которые по существу увеличивают число и качество инновационных, экономически эффективных новых лекарственных препаратов без несения непосильных расходов на научно-исследовательские и опытные работы. В соответствии с этим изобретатели описывают в настоящем документе устройства, системы и способы изготовления тканей и органов.
Описанное в настоящем документе представляет собой биопринтеры, включающие: одну или более печатающую головку, где печатающая головка включает средство для приема и удерживания по меньшей мере одного картриджа, и где указанный картридж включает содержимое, выбранное из одного или более: биочернил и вспомогательного материала; средство для калибровки положения по меньшей мере одного картриджа; и средство для раздачи содержимого по меньшей мере одного картриджа. В одном варианте выполнения изобретения печатающая головка, описанная в настоящем документе, включает средство для приема и удерживания одного картриджа. В другом варианте выполнения изобретения печатающая головка, описанная в настоящем документе, включает средство для приема и удерживания более чем одного картриджа. В другом варианте выполнения изобретения биопринтер дополнительно включает печатную платформу. В другом варианте выполнения изобретения средство для приема и удерживания по меньшей мере одного картриджа выбирается из: магнитного притяжения, зажатия цанговым патроном, металлического обода, гайки, адаптера втулки или комбинации указанных. В еще другом варианте выполнения изобретения средство для приема и удерживания по меньшей мере одного картриджа представляет собой зажатие цанговым патроном. В еще другом варианте выполнения изобретения средство для калибровки положения по меньшей мере одного картриджа выбирается из: лазерной юстировки, оптической юстировки, механической юстировки, пьезоэлектрической юстировки, магнитной юстировки, электрического поля или емкостной юстировки, ультразвуковой юстировки или комбинации указанных. В еще другом варианте выполнения изобретения средство для калибровки положения по меньшей мере одного картриджа представляет собой лазерную юстировку. В другом варианте выполнения изобретения средство для раздачи содержимого по меньшей мере одного картриджа представляет собой применение поршня, применение давления, применение сжатого газа, гидравлику или комбинацию указанных. В еще другом варианте выполнения изобретения средство для раздачи содержимого по меньшей мере одного картриджа представляет собой применение поршня. В еще другом варианте выполнения изобретения диаметр поршня меньше, чем диаметр картриджа. В другом варианте выполнения изобретения биопринтер дополнительно включает средство для установления температуры. В еще другом варианте выполнения изобретения биопринтер дополнительно включает средство для установления температуры окружающей среды, температуры картриджа, температуры содержимого картриджа, температуры принимающей поверхности или комбинации указанных. В еще другом варианте выполнения изобретения средство для установления температуры представляет собой нагревательный элемент. В еще другом варианте выполнения изобретения средство для установления температуры представляет собой нагреватель. В еще другом варианте выполнения изобретения средство для установления температуры представляет собой радиантный нагреватель, конвективный нагреватель, кондукционный нагреватель, вентиляторный нагреватель, теплообменник или комбинацию указанных. В еще другом варианте выполнения изобретения средство для установления температуры представляет собой охлаждающий элемент. В еще другом варианте выполнения изобретения средство для установления температуры представляет собой контейнер с хладагентом, охлажденной жидкостью, льдом, радиантный охладитель, конвективный охладитель, кондукционный охладитель, вентиляторный охладитель или комбинацию указанных. В еще другом варианте выполнения изобретения температура устанавливается между около 40 и около 90°C. В еще другом варианте выполнения изобретения температура устанавливается между около 0 и около 10°C. В другом варианте выполнения изобретения биопринтер, описанный в настоящем документе, дополнительно включает средство для применения увлажняющего агента к одному или более: печатной платформе; принимающей поверхности, распределительному отверстию, биочернилам, вспомогательному материалу или отпечатанной конструкции.
Также описанное в настоящем документе представляет собой способы калибровки положения картриджа, включающего распределительное отверстие, где картридж прикреплен к биопринтеру, включающие: калибровку положения картриджа вдоль по меньшей мере одной оси; где ось выбирается из оси х, оси y, оси z; и где каждая калибровка проводится с использованием лазера. В одном варианте выполнения изобретения способы включают активацию лазера и генерирование по меньшей мере одного по существу стабильного и/или по существу стационарного лазерного луча, и где указанный лазерный луч является горизонтальным по отношению к земле. В другом варианте выполнения изобретения способы включают активацию лазера и генерирование по меньшей мере одного по существу стабильного и/или по существу стационарного лазерного луча, и где указанный лазерный луч является вертикальным по отношению к земле. В еще другом варианте выполнения изобретения каждая калибровка проводится с использованием первого и второго лазера. В еще другом варианте выполнения изобретения первый лазер является вертикальным по отношению к земле, и второй лазер является горизонтальным по отношению к земле. В другом варианте выполнения изобретения калибровка положения картриджа вдоль оси y с использованием горизонтального лазера включает: позиционирование картриджа таким образом, что картридж (i) расположен в первом октанте y, и (ii) распределяющее отверстие находится ниже верхнего порога лазерного луча; (а) перемещение картриджа по направлению к лазерному лучу и прекращение указанного передвижения, как только лазерный луч прерывается картриджем, где положение, при котором лазерный луч прерывается картриджем, является первым положением y; (b) изменение положения картриджа таким образом, что картридж расположен во втором октанте y, и распределяющее отверстие находится ниже верхнего порога лазерного луча; (с) перемещение картриджа по направлению к лазерному лучу и прекращение указанного передвижения, как только лазерный луч прерывается картриджем, где положение, при котором лазерный луч прерывается, является вторым положением y; (d) и расчет средней точки между первым положением у и вторым положением y. В другом варианте выполнения изобретения калибровка положения картриджа вдоль оси х с использованием горизонтального лазера включает: (а) позиционирование картриджа (i) в средней точке между первым положением y и вторым положением y и (ii) вне порога лазерного датчика; (b) перемещение картриджа по направлению к порогу датчика и прекращение указанного перемещения, как только картридж контактирует с порогом датчика; (с) где положение, при котором картридж контактирует с датчиком, увеличилось на половину ширины картриджа, является положением х. В другом варианте выполнения изобретения калибровка положения картриджа вдоль оси z с использованием горизонтального лазера включает: (а) позиционирование картриджа таким образом, что распределяющее отверстие располагается выше лазерного луча; (b) перемещение картриджа по направлению к лазерному лучу и прекращение указанного перемещения, как только лазерный луч прерывается картриджем, где положение, при котором лазерный луч прерывается картриджем, является положением z. В другом варианте выполнения изобретения калибровка положения картриджа вдоль оси y с использованием вертикального лазера включает: (а) позиционирование картриджа таким образом, что картридж (i) расположен в первом октанте y, и (ii) распределяющее отверстие находится вне порога датчика лазерного луча; (b) перемещение картриджа по направлению к лазерному лучу и прекращение указанного передвижения, как только лазерный луч прерывается картриджем, где положение, при котором лазерный луч прерывается картриджем, является первым положением y; (с) изменение положения картриджа таким образом, что картридж расположен во втором октанте y, и распределяющее отверстие находится вне порога датчика лазерного луча; (d) перемещение картриджа по направлению к лазерному лучу и прекращение указанного передвижения, как только лазерный луч прерывается картриджем, где положение, при котором лазерный луч прерывается, является вторым положением y; (е) расчет средней точки между первым положением у и вторым положением y; и (f), необязательно, повторение (а)-(е) и усреднение рассчитанных средних точек. В другом варианте выполнения изобретения калибровка положения картриджа вдоль оси х с использованием вертикального лазера включает: (а) позиционирование картриджа таким образом, что картридж (i) расположен в первом октанте х, и (ii) распределяющее отверстие находится вне порога датчика лазерного луча; (b) перемещение картриджа по направлению к лазерному лучу и прекращение указанного передвижения, как только лазерный луч прерывается картриджем, где положение, при котором лазерный луч прерывается картриджем, является первым положением х; (с) изменение положения картриджа таким образом, что картридж располагается во втором октанте х, и распределяющее отверстие находится вне порога датчика лазерного луча; (d) перемещение картриджа по направлению к лазерному лучу и прекращение указанного передвижения, как только лазерный луч прерывается картриджем, где положение, при котором лазерный луч прерывается, является вторым положением х; (е) расчет средней точки между первым положением х и вторым положением х; и (f), необязательно, повторение (а)-(е) и усреднение рассчитанных средних точек. В другом варианте выполнения изобретения калибровка положения картриджа вдоль оси z с использованием вертикального лазера включает: (а) позиционирование печатающей головки таким образом, что распределяющее отверстие располагается выше лазерного луча и вне порога дальности лазерного датчика; (b) перемещение печатающей головки вдоль оси z до достижения порога датчика; где положение z является положением, при котором достигается порог лазерного датчика; и, необязательно, повторение стадий (а) и (b) и расчет средних положений z. В другом варианте выполнения изобретения калибровка положения картриджа вдоль оси z включает: визуальное определение положения распределяющего отверстия.
Далее описанное в настоящем документе представляет собой системы для калибровки положения картриджа, включающего распределительное отверстие, где картридж прикреплен к биопринтеру, указанная система включает: средство для калибровки положения картриджа вдоль по меньшей мере одной оси, и где ось выбирается их оси y, оси х и оси z. В одном варианте выполнения изобретения средство для калибровки картриджа представляет собой лазерную юстировку, оптическую юстировку, механическую юстировку, пьезоэлектрическую юстировку, магнитную юстировку, электрическое поле или емкостную юстировку, ультразвуковую юстировку или комбинацию указанных. В другом варианте выполнения изобретения средство для калибровки картриджа представляет собой лазерную юстировку. В еще другом варианте выполнения изобретения средство лазерной юстировки включает по меньшей мере один лазер, выбранный из горизонтального лазера и вертикального лазера. В еще другом варианте выполнения изобретения средство лазерной юстировки включает горизонтальный лазер и вертикальный лазер. В еще другом варианте выполнения изобретения средство лазерной юстировки представляет собой точность до ±40 мкм по вертикальной оси и ±20 мкм по горизонтальной оси.
Далее описанное в настоящем документе представляет собой способы изготовления тканевых конструкций, включающие: компьютерный модуль, принимающий ввод визуального представления желаемой тканевой конструкции; компьютерный модуль, генерирующий серию команд, где команды основаны на визуальном представлении и читаются биопринтером; компьютерный модуль, обеспечивающий серии команд для биопринтера; и биопринтер, наносящий биочернила и материал подложки в соответствии с командами с формированием конструкции с определенной геометрией. В некоторых вариантах выполнения изобретения компьютерный модуль включает экран монитора. В дополнительных вариантах выполнения изобретения компьютерный модуль включает графический пользовательский интерфейс (ГИП). В еще дополнительных вариантах выполнения изобретения пользователь определяет содержание одного или более объектов для формирования визуального представления желаемой тканевой конструкции с использованием ГИП, обеспеченного компьютерным модулем. В одном варианте выполнения изобретения экран монитора состоит по существу из сетки, включающей множество объектов по существу одинаковой формы и по существу одинакового размера. В еще другом варианте выполнения изобретения каждый объект имеет форму круга. В еще другом варианте выполнения изобретения пользователь определяет содержание одного или более объектов для получения визуального представления желаемой тканевой конструкции. В еще другом варианте выполнения изобретения пользователь определенное пользователем содержание объекта выбирается из биочернил или вспомогательного материала. В дополнительных вариантах выполнения изобретения экран монитора состоит из трехмерного(ых) рендеринга(ов), которые вводятся пользователем электронно или вручную, тем самым различные компоненты трехмерного рендеринга могут быть установлены в любую подходящую плоскость или вектор до выполнения протокола биопечати на биопринтере.
Далее описанное в настоящем документе представляет собой способы прикрепления картриджа к биопринтеру, включающие: (а) вставку картриджа в цанговый патрон, где цанговый патрон прикрепляется к печатающей головке биопринтера; и (b) установку внешней втулки цангового патрона; где вставка и установка по существу не изменяют положение печатающей головки.
Далее описанное в настоящем документе представляет собой картриджи для использования с биопринтерами, описанными в настоящем документе, включающие по меньшей мере одно отверстие, где углы отверстия сглажены или по существу сглажены. В одном варианте выполнения изобретения картридж представляет собой капиллярную трубку или микропипетку. В другом варианте выполнения изобретения картридж включает биочернила. В еще другом варианте выполнения изобретения картридж включает материал подложки. В еще другом варианте выполнения изобретения отверстие является круглым или квадратным. В еще другом варианте выполнения изобретения картридж имеет внутренний диаметр от около 1 мкм до около 1000 мкм. В еще другом варианте выполнения изобретения картридж имеет внутренний диаметр около 500 мкм. В еще другом варианте выполнения изобретения картридж имеет объем от около 1 мкл до около 50 мкл. В еще другом варианте выполнения изобретения картридж имеет объем около 5 мкл. В еще другом варианте выполнения изобретения картридж имеет маркировку для индикации композиции биочернил. В еще другом варианте выполнения изобретения картридж имеет маркировку для индикации композиции вспомогательного материала. В некоторых вариантах выполнения изобретения биочернила и/или материал подложки подаются. В дополнительных вариантах выполнения изобретения биочернила подаются путем выдавливания биочернил до уровня распределяющего отверстия до запуска протокола биопринтера. В дополнительных вариантах выполнения изобретения материал подложки подается путем выдавливания вспомогательного материала до уровня распределяющего отверстия до запуска протокола биопринтера.
Далее описанное в настоящем документе представляет собой системы для прикрепления картриджа к биопринтеру, включающие: средство для приема и прикрепления картриджа к печатающей головке биопринтера; где использование средства для приема и прикрепления картриджа существенно не изменяет положение печатающей головки. В некоторых вариантах выполнения изобретения средство для приема и прикрепления картриджа к печатающей головке выбирается из: магнитного притяжения, зажатия цанговым патроном, металлического обода, гайки, адаптера втулки или комбинации указанных. В одном варианте выполнения изобретения средство для приема и прикрепления картриджа к печатающей головке представляет собой патрон.
Далее описанное в настоящем документе представляет собой принимающие поверхности для принятия одной или более структур, полученных из биопринтеров. В одном варианте выполнения изобретения принимающая поверхность является ровной или по существу ровной. В другом варианте выполнения изобретения принимающая поверхность является гладкой или по существу гладкой. В еще другом варианте выполнения изобретения принимающая поверхность является (а) ровной или по существу ровной и (b) гладкой или по существу гладкой или (с) определенной или по существу определенной. В другом варианте выполнения изобретения топография принимающей поверхности разработана для размещения или влияния на размер, форму, или текстуру, или геометрию одной или более полученных структур. В еще другом варианте выполнения изобретения принимающая поверхность включает твердый материал, полутвердый материал или комбинацию указанных. В еще другом варианте выполнения изобретения принимающая поверхность включает стекло, пластик, металл, сплав металлов или комбинацию указанных. В еще другом варианте выполнения изобретения принимающая поверхность включает гель. В еще другом варианте выполнения изобретения принимающая поверхность препятствует адгезии одной или более структур. В еще другом варианте выполнения изобретения принимающая поверхность включает полимеризованный NovoGel™.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1 иллюстрирует неограничивающий пример калибровки картриджа с использованием горизонтального лазера.
Фигура 2 иллюстрирует неограничивающий пример калибровки картриджа с использованием вертикального лазера.
Фигура 3 иллюстрирует неограничивающий пример процесса капиллярной подачи.
Фигура 4 иллюстрирует неограничивающий пример двумерного представления биоотпечатанной тканевой конструкции.
Фигура 5 иллюстрирует неограничивающий пример трехмерной конструкции, полученной путем непрерывного нанесения PF-127 с использованием биопринтера NovoGen MMX™, соединенного со шприцом с иглой 510 мкм; в этом случае конструкция имеет форму пирамиды.
Фигура 6 иллюстрирует неограничивающий пример трехмерной конструкции, полученной путем непрерывного нанесения PF-127 с использованием биопринтера NovoGen MMX™, соединенного со шприцом с иглой 510 мкм; в этом случае конструкция имеет форму куба (слева) и в форме полого куба (справа).
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Изобретение относится к областям регенеративной медицины, тканевой инженерии/культивированию органов, биологическому и медицинскому исследованию и поиску лекарственных средств. Более конкретно изобретение относится к устройствам для изготовления тканей и органов, системам и способам калибровки и использования таких устройств, и тканям и органам, изготовленным с помощью устройств, систем и способов, описанных в настоящем документе.
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой биопринтеры, включающие: одну или более печатающих головок, где печатающая головка включает средство для приема и удерживания по меньшей мере одного картриджа, и где указанный картридж включает содержимое, выбранное из одного или более: биочернил и вспомогательного материала; средство для калибровки положения по меньшей мере одного картриджа; и средство для раздачи содержимого по меньшей мере одного картриджа.
Также описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой способы калибровки положения картриджа, включающего отверстие для нанесения, где картридж прикреплен к биопринтеру, включающие: калибровку положения картриджа вдоль по меньшей мере одной оси; где ось выбирается из оси х, оси y и оси z; и где каждая калибровка проводится с использованием лазера.
Также описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой системы калибровки положения картриджа, включающего отверстие для нанесения, где картридж прикреплен к биопринтеру, причем указанная система включает: средство для калибровки положения картриджа вдоль по меньшей мере одной оси; где ось выбирается из оси х, оси y и оси z.
Также описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой способы изготовления тканевых конструкций, включающие: компьютерный модуль, принимающий ввод визуального представления желаемой тканевой конструкции; компьютерный модуль, генерирующий серию команд, где команды основаны на визуальном представлении и читаются биопринтером; компьютерный модуль, передающий серии команд биопринтеру; и биопринтер, размещающий биочернила и материал подложки в соответствии с командами с формированием конструкции определенной геометрии.
Далее описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой способы прикрепления картриджа к биопринтеру, включающие: (а) вставку картриджа в цанговый патрон, где цанговый патрон прикреплен к печатающей головке биопринтера; и (b) установку внешней втулки цангового патрона;
где вставка и установка по существу не изменяют положение печатающей головки.
Далее описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой системы прикрепления картриджа к биопринтеру, включающие: средство для приема и прикрепления картриджа к печатающей головке биопринтера; где использование средства для приема и прикрепления картриджа существенно не изменяет положение печатающей головки.
Некоторые определения
Если не определено иначе, все технические и научные термины, использованные в настоящем документе, имеют тоже значение, как обычно понимаются средним специалистом в данной области техники, к которой принадлежит это изобретение. Все публикации, патентные заявки, патенты и другие ссылки, упомянутые в настоящем документе, включаются посредством ссылки во всей своей полноте.
Как используется в этом описании и приложенной формуле изобретения формы единственного числа "a," "an," и "the" включают ссылки на множественное число, если по контексту явно не следует иное. Таким образом, например, ссылки на «нуклеиновую кислоту» включают одну или более нуклеиновых кислот и/или композиции такого типа, описанного в настоящем документе, которые будут очевидны специалистам в данной области техники вследствие прочтения этого описания и так далее. Любая ссылка на «или» в настоящем документе направлена на схватывание «и/или», если не указано иное.
Как используется в настоящем документе, «аллографт» означает орган или ткань, полученную от генетически неидентичного члена того же вида, что и реципиент.
Как используется в настоящем документе, «биочернила» означают жидкую, полутвердую или твердую композицию, включающую множество клеток. В некоторых вариантах выполнения изобретения биочернила включат клеточные растворы, клеточные агрегаты, содержащие клетки гели, многоклеточные тела или ткани. В некоторых вариантах выполнения изобретения биочернила дополнительно включают материал подложки. В некоторых вариантах выполнения изобретения биочернила дополнительно включают неклеточные материалы, которые обеспечивают специфические биомеханические свойства, которые дают возможность биопечати.
Как используется в настоящем документе, «биопечать» означает использование трехмерного точного нанесения клеток (напр., клеточных растворов, содержащих клетки гелей, клеточных суспензий, клеточных концентраций, многоклеточных агрегатов, многоклеточных тел и т.д.) посредством методики, которая совместима с автоматизированным, компьютеризированным, трехмерным опытным устройством (напр., биопринтером).
Как используется в настоящем документе, «картридж» означает любой объект, который способен принимать (и удерживать) биочернила или материал подложки.
Как используется в настоящем документе, «компьютерный модуль» означает компонент программного обеспечения (включая участок кода), который взаимодействует с большей компьютерной системой. В некоторых вариантах выполнения изобретения модуль программного обеспечения (или программный модуль) выражается в форме файла и, как правило, обрабатывает конкретное задание большей компьютерной системы. В некоторых вариантах выполнения изобретения модуль может быть включен в одну или более систему программного обеспечения. В других вариантах выполнения изобретения модуль может, как единое целое, быть интегрированным с одним или более модулем в одну или более систем программного обеспечения. Компьютерный модуль, необязательно, представляет собой обособленный участок кода или, необязательно, код, который отдельно не идентифицируется. Ключевой характеристикой компьютерного модуля является то, что он позволяет конечному пользователю использовать компьютер для проведения определенных функций.
Как используется в настоящем документе, «имплантабельный» означает биосовместимый и способный быть внедренным или пересаженным в или присоединенным к живому организму либо временно, либо по существу постоянно.
Как используется в настоящем документе, «орган» означает совокупность тканей, собранных в структурную единицу, выполняющих одинаковую функцию. Примеры органов включают, но не ограничиваясь, кожу, потовые железы, сальные железы, грудные железы, кость, мозг, гипоталамус, гипофиз, шишковидное тело, сердце, кровеносные сосуды, гортань, трахею, бронх, легкое, лимфатический сосуд, слюнные железы, слизистые железы, пищевод, желудок, желчный пузырь, печень, поджелудочную железу, тонкую кишку, толстую кишку, толстую кишку, уретру, почку, надпочечник, подвздошный канал, мочеточник, мочевой пузырь, фаллопиевую трубу, матку, яичники, яички, простату, щитовидную железу, паращитовидную железу, мейбомиевую железу, околоушную железу, миндалину, аденоид, тимус и селезенку.
Как используется в настоящем документе, «пациент» означает любой индивидуум. Термин является взаимозаменяемым с «субъектом», «реципиентом» и «донором». Ни один из этих терминов не должен рассматриваться как требующий наблюдения (постоянного или другого) медицинским работником (напр., лечащим врачом, сиделкой, фельдшером, помощником врача, санитаром, работником хосписа, социальным работником, специалистом по клиническим исследованиям и т.д.) или научным исследователем.
Как используется в настоящем документе, «стволовая клетка» означает клетку, которая проявляет активность и самообновление. Стволовые клетки включают, но не ограничиваясь, тотипотентные клетки, плюрипотентные клетки, мультипотентные клетки, олигопотентные клетки, унипотентные клетки и клетки-предшественники. Стволовые клетки могут быть зародышевыми стволовыми клетками, перинатальными стволовыми клетками, взросльми стволовыми клетками, амниотическими стволовьми клетками и индуцированными плюрипотентными стволовыми клетками.
Как используется в настоящем документе, «ткань» означает агрегат клеток. Примеры тканей включают, но не ограничиваясь, соединительную ткань (напр., ареолярную соединительную ткань, плотную соединительную ткань, эластичную ткань, ретикулярную соединительную ткань и жировую ткань), мышечную ткань (напр., скелетную мускулатуру, гладкую мускулатуру и сердечную мускулатуру), урогенитальную ткань, желудочно-кишечную ткань, легочную ткань, костную ткань, нервную ткань и эпителиальную ткань (напр., простой эпителий и многослойный эпителий), полученную из эндодермы ткань, полученную из мезодермы ткань и полученную из эктодермы ткань.
Как используется в настоящем документе, «ксенографт» означает орган или ткань, полученную от другого вида, нежели реципиент.
Существующие способы трансплантации органов
В настоящее время не существует надежного способа синтеза органов de novo. Органы получают только от живых доноров (напр., для донорства почки и печени), мертвых доноров (для донорства легкого и сердца) и в некоторых случаях животных (напр., сердечные клапаны свиньи). Таким образом, пациенты, нуждающиеся в трансплантации органов, должны ждать донорского органа, который станет доступен. Это приводит к уменьшению доступных органов. Кроме того, зависимость от органов, полученных от живого организма, увеличивает шанс отторжения трансплантата.
Отторжения трансплантата
В некоторых случаях пациент, получающий трансплантат органа, испытывает сверхострое отторжение. Как используется в настоящем документе, «сверхострое отторжение» означает опосредованную комплементом иммунную реакцию, возникающую вследствие существования у реципиента антител к донорскому органу. Сверхострое отторжение возникает в течение минут и характеризуется агглютинацией крови. Если трансплантированный орган немедленно не удалить, у пациента может развиться сепсис. Ксенографты будут приводить к сверхострому отторжению, за исключением случаев, когда реципиент сначала принимал иммуносупрессанты. В некоторых вариантах выполнения изобретения ткань или орган, изготовленные de novo, не будут включать какие-либо антигены и, таким образом, не могут быть распознаны антителами реципиента.
В некоторых случаях пациент, получающий трансплантат органа, испытывает острое отторжение. Как используется в настоящем документе, «острое отторжение» означает иммунную реакцию, которая начинается от около одной недели спустя после трансплантации до около одного года после трансплантации. Острое отторжение возникает вследствие наличия чужеродных молекул HLA в донорском органе. В некоторых случаях АРС распознают чужеродные HLA и активируют клетки Т-хелперы. В некоторых случаях клетки Т-хелперы активируют цитотоксические Т-клетки и макрофаги. В некоторых случаях наличие цитотоксических Т-клеток и макрофагов приводит к смерти клеток с чужеродными HLA и, таким образом, повреждают (или убивают) трансплантированный орган. Острое отторжение возникает в около 60-75% трансплантатов почек и 50-60% трансплантатов печени. В некоторых вариантах выполнения изобретения ткань или орган, изготовленные de novo, не будут включать какие-либо HLA и, таким образом, не приведут к активации клеток Т-хелперов.
В некоторых случаях пациент, получающий трансплантат органа, испытывает хроническое отторжение. Как используется в настоящем документе, «хроническое отторжение» означает отторжение трансплантата, возникающее вследствие хронического воспаления и иммунных реакций против трансплантированной ткани. В некоторых вариантах выполнения изобретения ткань или орган, изготовленные de novo, не будут включать какие-либо антигены или чужеродные HLA и, таким образом, не будут индуцировать воспаление или иммунные реакции.
В некоторых случаях пациент, получающий трансплантат органа, испытывает хроническую аллографтную васкулопатию (CAV). Как используется в настоящем документе, «хроническая аллографтная васкулопатия» означает потерю функции в трансплантированных органах, возникающую вследствие фиброза внутренних кровеносных сосудов трансплантированного органа. В некоторых случаях CAV является результатом продолжительных иммунных реакций на трансплантированный орган. В некоторых вариантах выполнения изобретения ткань или орган, изготовленные de novo, не будут включать какие-либо антигены или чужеродные HLA и, таким образом, не приведут к иммунной реакции.
Для того чтобы избежать отторжения трансплантата, реципиентам органов вводятся иммуносуппрессирующие лекарственные средства. Иммунносуппрессанты включают, но не ограничиваясь, кортикостероиды (напр., преднизон и гидрокортизон), ингибиторы кальциневрина (напр., циклоспорин и такролимус), антипролиферативные агенты (напр., азатиоприн и микофеноловую кислоту), антитела против специфических компонентов иммунной системы (напр., басиликсимаб, даклузимаб, антитимоцитарный глобулин (ATG) и антилимфоцитарный глобулин (ALG) и ингибиторы mTOR (напр., сиролимус и эверолимус). Однако иммуносуппрессанты имеют несколько негативных побочных эффектов, включающих, но не ограничиваясь, предрасположенность к инфецированию (напр., инфекцированию пневмоцитарной плазмоклеточной пневмонией (РСР), цитомегаловирусной пневмонией (CMV), вирусом простого герпеса и вирусом опоясывающего герпеса) и распространению злокачественных клеток, гипертензии, дислипидемии, гипергликемии, оптическим язвам, повреждению печени и почек и взаимодействию с другими лекарственными препаратами. В некоторых вариантах выполнения изобретения ткань или орган, изготовленные de novo, не приведут к иммунной реакции и, таким образом, не будет требоваться введение иммуносуппрессанта.
Инфекции
В конкретных случаях донорский орган может быть инфицирован инфекционным агентом. Вслед за трансплантатом инфицированного органа инфекционный агент способен распространиться по донору (отчасти вследствие применения иммуносуппрессирующих лекарственных средств). В качестве неограничивающего примера реципиенты заражались ВИЧ, вирусом Западного Нила, бешенствами, гепатитом С, вирусом лимфоцитарного хориоменингита (LCMV), туберкулезом, болезнью Чагаса и болезнью Крейтцфельда-Якоба от трансплантированных органов. Хотя такие инфекции редки, тем не менее, они могут возникнуть - социальные анамнезы мертвых доноров часто неточные, так как они в силу необходимости получены от ближайших родственников, серологические тесты могут давать ложноотрицательные результаты, если не произошла сероконверсия, или серологические тесты могут также давать ложноотрицательные результаты вследствие разбавления крови после переливания крови. Кроме того, множество нетипичных инфекционных агентов не обнаруживается из-за ограниченного времени жизнеспособности взятого органа. В некоторых вариантах выполнения изобретения ткань или орган, изготовленные de novo, не будут содержать какой-либо инфекционный агент.
Осложнения у донора
Живой донор также может испытывать осложнения в результате донорства органа. Эти осложнения включают внутрибольничные инфекции, аллергические реакции на анестезию и хирургические ошибки. Кроме того, донор органа может однажды оказаться нуждающимся в органе, который отдает. Например, оставшаяся почка у донора почки или оставшаяся доля печени донора могут быть повреждены. В некоторых вариантах выполнения изобретения ткань или орган, изготовленные de novo, устраняют необходимость в донорских органах и, таким образом, донор будет избегать негативных побочных эффектов.
В свете дефицита доступных органов и всех осложнений, которые сопровождают трансплантацию донорского органа, существует необходимость в способе de novo изготовления тканей и органов.
Тканевая инженерия
Тканевая инженерия представляет собой межотраслевую область, в которой применяются и соединяются принципы инжиниринга и наук о живой природе в направлении развития биологических заместителей, которые восстанавливают, сохраняют или улучшают тканевую функцию посредством наращивания, репарации или замещения органа или ткани. Основным подходом к классическому тканевому инжинирингу является посев живых клеток в биосовместимую и впоследствии биоразлагаемую среду (напр., подложку) и затем культивирование этой конструкции в биореакторе таким образом, чтобы исходная популяция клеток могла далее увеличиться и созреть до образования целевой ткани вследствие имплантации. С подходящей подложкой, которая имитирует биологический внеклеточный матрикс (ЕСМ), развивающаяся ткань может принимать как форму, так и функцию желаемого органа после in vitro и in vivo созревания. Однако достижение достаточно высокой плотности клеток со структурой, подобной естественной ткани, является сомнительным вследствие ограниченной возможности контролировать распространение и пространственное расположение клеток на подложке. Эти ограничения могут привести к тканям или органам с низкими механическими свойствами и/или недостаточной функцией. Дополнительные сомнения существуют в отношении биоразрушения подложки, захвата остаточного полимера и промышленного масштаба процесса производства. Осуществлялись попытки подходов без подложек. Существующие подходы без подложек являются предметом нескольких ограничений:
- Сложные геометрии, такие как многослойные структуры, где каждый слой включает различный тип клеток, могут требовать определенного высокочувствительного помещения типов клеток внутрь специфичной архитектуры для воспроизводимого достижения результата, подобного естественной ткани.
- Масштаб и геометрия ограничиваются диффузией и/или требованием функциональных сосудистых сетей для снабжения питательными веществами.
- Жизнеспособность тканей может быть снижена изолирующим материалом, который ограничивает диффузию и сдерживает доступ клеток к питательным веществам.
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой устройства, системы и способы, которые генерируют трехмерные тканевые конструкции. В устройствах, системах и способах, описанных в настоящем документе, используется трехфазный процесс: (i) препроцессинг или приготовление биочернил, (и) процессинг, т.е., фактическая автоматизированная доставка/печать биочернильных частиц на биобумаге с помощью биопринтера и (iii) постпроцессинг, т.е., созревание/инкубирование печатной конструкции в биореакторе. Формирование конечной структуры происходит в ходе постпроцессинга посредством слияния частиц биочернил. Устройства, системы и способы, описанные в настоящем документе, имеют следующие преимущества:
- Они способны производить содержащие клетки ткани и/или органы.
- Они воспроизводят условия окружающей среды процессов образования ткани в естественных условиях путем использования принципов онтогенетики.
- Они могут обеспечивать широкий ряд комплексных топологий (напр., многослойные структуры, повторяющиеся геометрические рисунки, сегменты, листы, трубки, мешочки и т.д.).
- Они совместимы с автоматизированными средствами изготовления и масштабируемы.
Биопечать делает доступными улучшенные способы создания включающих клетки имплантабельных тканей, которые пригодны для репарации ткани, наращивания ткани, замещения ткани и замещения органа. Кроме того, биопечать делает доступными улучшенные способы создания микромасштабных тканевых аналогов, включающих те, которые пригодны для анализов in vitro.
Биопечать
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой устройства, системы и способы изготовления тканей и органов. В некоторых вариантах выполнения изобретения устройства представляют собой биопринтеры. В некоторых вариантах выполнения изобретения способы включают использование биопринтерных методик. В дополнительных вариантах выполнения изобретения ткани и органы, изготовленные с использованием устройств, систем и способов, описанных в настоящем документе, являются биоотпечатанными.
В некоторых вариантах выполнения изобретения биоотпечатанные клеточные конструкции, ткани и органы сделаны способом, в котором используется технология быстрого прототипирования, основанная на трехмерном, автоматизированном, компьютеризированном размещении клеток, включая клеточные растворы, клеточные суспензии, включающие клетки гели или пасты, клеточные концентрации, многоклеточные тела (напр., цилиндры, сфероиды, полоски и т.д.), и вспомогательного материала на биосовместимой поверхности (напр., составленной из гидрогеля и/или пористой мембраны) с помощью трехмерного устройства доставки (напр., биопринтера). Как используется в настоящем документе в некоторых вариантах выполнения изобретения термин «сконструированный», когда используется в отношении тканей и/или органов, означает, что клетки, клеточные растворы, клеточные суспензии, включающие клетки гели или пасты, клеточные концентраты, многоклеточные агрегаты и слои указанных расположены таким образом, чтобы формировать трехмерные структуры с помощью компьютеризированного устройства (напр., биопринтера) в соответствии с компьютерным кодом. В дополнительных вариантах выполнения изобретения компьютерный сценарий представляет собой, например, одну или более компьютерную программу, компьютерное приложение или компьютерные модули. В еще дополнительных вариантах выполнения изобретения трехмерные тканевые структуры образуются посредством слияния после печати клеток или многоклеточных тел, подобно явлению самоорганизации при раннем морфогенезе.
В то время как ряд способов является доступным для организации клеток, многоклеточных агрегатов и/или слоев указанных на биосовместимой поверхности с образованием трехмерной структуры, включающих ручное размещение, позиционирование с помощью автоматизированной компьютеризированной машины, такой как биопринтер, является преимущественным. Преимущества доставки клеток или многоклеточных тел с помощью этой технологии включают быстрое, точное и воспроизводимое размещение клеток или многоклеточных тел с получением конструкций, проявляющих запланированные или заранее определенные ориентации или рисунки клеток, многоклеточных агрегатов и/или слоев указанных с различными композициями. Преимущества также включают гарантированную высокую плотность клеток при минимизации повреждения клеток.
В некоторых вариантах выполнения изобретения способы биопечати являются непрерывными или по существу непрерывными. Неограничивающий пример непрерывного способа биопечати представляет собой распределение биочернил из биопринтера посредством распределительного наконечника (напр., шприца, капиллярной трубки и т.д.), соединенного с резервуаром биочернил. В дополнительных неограничивающих вариантах выполнения изобретения непрерывный способ биопечати представляет собой распределение чернил в повторяющийся рисунок функциональных единиц. В различных вариантах выполнения изобретения повторяющаяся функциональная единица имеет любую подходящую форму, включая, например, круги, квадраты, прямоугольники, треугольники, полигоны и неправильные формы. В дополнительных вариантах выполнения изобретения повторяющийся рисунок биоотпечатанных функциональных единиц включает слой и множество слоев, биоотпечатанных рядом (напр., друг над другом) с формированием сконструированной ткани или органа. В различных вариантах выполнения изобретения 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или более слоев биоотпечатаны рядом (напр., друг над другом) с формированием сконструированной ткани или органа.
В некоторых вариантах выполнения изобретения биоотпечатанная функциональная единица повторяется в виде мозаичного рисунка. «Мозаичный рисунок» представляет собой плоскость с фигурами, которые заполняют плоскость без перекрытий и зазоров. Преимущество непрерывной и/или мозаичной биопечати может включать увеличенное производство биоотпечатанной ткани. Увеличенное производство может включать достижение повышенных масштабов, повышенной сложности или сниженного времени или стоимости производства. Другим неограничивающим потенциальным преимуществом может быть снижение числа калибровочных приемов, которые требуются для завершения биопечати трехмерной конструкции. Непрерывная биопечать может также способствовать печати больших тканей из большого резервуара биочернил, необязательно, с использованием шприцевого механизма.
Способы непрерывной биопечати могут включать оптимизацию и/или балансировку параметров, таких как высота принтера, скорость насоса, скорость робота или комбинации указанных независимо или в зависимости друг от друга. В одном примере скорость головки биопринтера для нанесения составляла 3 мм/с с высотой нанесения 0,5 мм для первого слоя, и высота нанесения была увеличена на 0,4 мм для каждого последующего слоя. В некоторых вариантах выполнения изобретения высота нанесения приблизительно равна диаметру распределительного наконечника биопринтера. Без ограничения подходящее и/или оптимальное распределительное расстояние не приводит к выравниванию или адгезии материала к распределяющей игле. В различных вариантах выполнения изобретения распределительный наконечник биопринтера имеет внутренний диаметр около 20, 50, 100, 150, 200, 250, 300, 350,400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000 мкм или более, включая промежуточные значения между ними. В различных вариантах выполнения изобретения резервуар биочернил биопринтера имеет объем около 5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 кубических сантиметров или более, включая промежуточные значения между ними. Скорость насоса может быть подходящей и/или оптимальной, когда остаточное давление, созданное в системе, низкое. Благоприятные скорости насоса могут зависеть от соотношения между площадями поперечного сечения резервуара и распределительной иглы, где для больших соотношений требуются более низкие скорости насоса. В некоторых вариантах выполнения изобретения подходящая и/или оптимальная скорость печати позволяет нанесение универсальной линии без влияния на механическую целостность материала.
Изобретения, описанные в настоящем документе, включают бизнес-методы. В некоторых вариантах выполнения изобретения скорость и возможность масштабирования устройств и способов, описанных в настоящем документе, используются для разработки, построения и управления промышленными и/или коммерческими возможностями для производства сконструированных тканей и/или органов. В дополнительных вариантах выполнения изобретения сконструированные ткани и/или органы производятся, хранятся, распространяются, выводятся на рынок, рекламируются и продаются как, например, материалы, инструменты и наборы для медицинского лечения повреждения ткани, заболевания ткани и/или повреждения органа, или материалы, инструменты и наборы для проведения биологических анализов и/или поиска лекарственных средств - в качестве вспомогательных устройств.
Биопринтер
Описанное с настоящем документе в конкретных вариантах выполнения изобретения представляет собой биопринтеры для изготовления тканей и органов. В некоторых вариантах выполнения изобретения биопринтер представляет собой любой инструмент, который автоматизирует процесс биопечати. В конкретных вариантах выполнения изобретения биопринтер, описанный в настоящем документе, включает: одну или более печатающую головку, где печатающая головка включает средство для приема и удерживания по меньшей мере одного картриджа, и где указанный картридж включает содержимое, выбранное из одного или более: биочернила и вспомогательного материала; средство для калибровки положения по меньшей мере одного картриджа; и средство для раздачи содержимого по меньшей мере одного картриджа.
В различных вариантах выполнения изобретения биопринтер распределяет биочернила и/или материал подложки в заранее определенной геометрии (напр., положениях, рисунках и т.д.) в двух или трех измерениях. В некоторых вариантах выполнения изобретения биопринтер достигает конкретной геометрии путем перемещения печатающей головки относительно печатной платформы или принимающей поверхности, адаптированной для приема биоотпечатанных материалов. В других вариантах выполнения изобретения биопринтер достигает конкретной геометрии путем перемещения печатной платформы или принимающей поверхности относительно печатающей головки. В конкретных вариантах выполнения изобретения биопринтер поддерживается в стерильной среде.
В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем документе, включает одну или более печатающую головку. В дополнительных вариантах выполнения изобретения печатающая головка включает средство для приема и удерживания по меньшей мере одного картриджа. В некоторых вариантах выполнения изобретения печатающая головка включает средство для приема и удерживания более чем одного картриджа. В некоторых вариантах выполнения изобретения средство для приема и удерживания по меньшей мере одного картриджа выбирается из: магнитного притяжения, зажатия цанговым патроном, металлического обода, гайки, адаптера втулки или комбинации указанных. В некоторых вариантах выполнения изобретения средство для приема и удерживания по меньшей мере одного картриджа представляет собой зажатие цанговым патроном.
В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем документе, включает средство для калибровки положения по меньшей мере одного картриджа. В некоторых вариантах выполнения изобретения средство для калибровки положения по меньшей мере одного картриджа выбирается из: лазерной юстировки, оптической юстировки, механической юстировки, пьезоэлектрической юстировки, магнитной юстировки, электрического поля или емкостной юстировки, ультразвуковой юстировки или комбинации указанных. В некоторых вариантах выполнения изобретения средство для калибровки положения по меньшей мере одного картриджа представляет собой лазерную юстировку.
В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем документе, включает средство для раздачи содержимого по меньшей мере одного картриджа. В некоторых вариантах выполнения изобретения средство для раздачи содержимого по меньшей мере одного картриджа представляет собой применение поршня, применение давления, применение сжатого газа, применение гидравлики или комбинацию указанных. В некоторых вариантах выполнения изобретения средство для раздачи содержимого по меньшей мере одного картриджа представляет собой применение поршня. В некоторых вариантах выполнения изобретения диаметр поршня меньше, чем диаметр картриджа.
В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем документе, дополнительно включает принимающую поверхность. В дополнительных вариантах выполнения изобретения принимающая поверхность является нецитотоксичной поверхностью, на которой биопринтер распределяет биочернила и/или материал подложки. В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем документе, дополнительно включает печатную платформу. В некоторых вариантах выполнения изобретения принимающая поверхность представляется собой поверхность печатной платформы. В других вариантах выполнения изобретения принимающая платформа является компонентом, отделенным от печатающей платформы, но прикрепленной к или поддерживаемой платформой. В некоторых вариантах выполнения изобретения принимающая поверхность является ровной или по существу ровной. В некоторых вариантах выполнения изобретения поверхность является гладкой или по существу гладкой. В других вариантах выполнения изобретения поверхность является как по существу ровной, так и по существу гладкой. В еще дополнительных вариантах выполнения изобретения принимающая поверхность разработана для размещения размера, формы, текстуры или геометрии биоотпечатанной структуры. В еще дополнительных вариантах выполнения изобретения принимающая поверхность контролирует или влияет на размер, форму, текстуру или геометрию биоотпечатанной конструкции.
В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем изобретении, дополнительно включает средство для установления температуры. В некоторых вариантах выполнения изобретения средство для установления температуры устанавливает и/или поддерживает температуру окружающей среды. В других различных вариантах выполнения изобретения средство установления температуры устанавливает и/или поддерживает температуру, в качестве неограничивающего примера, печатающей головки, картриджа, содержимого картриджа (напр., биочернил, вспомогательного материала и т.д.), печатной платформы и принимающей поверхности.
В некоторых вариантах выполнения изобретения средство для установления температуры представляет собой нагревательный элемент.В некоторых вариантах выполнения изобретения средство для установления температуры представляет собой нагреватель. В некоторых вариантах выполнения изобретения средство для установления температуры представляет собой радиантный нагреватель, конвективный нагреватель, кондукционный нагреватель, вентиляторный нагреватель, теплообменник или комбинацию указанных. В некоторых вариантах выполнения изобретения средство для установления температуры представляет собой охлаждающий элемент.В некоторых вариантах выполнения изобретения средство для установления температуры представляет собой контейнер с хладагентом, охлажденной жидкостью, льдом или комбинацию указанных. В некоторых вариантах выполнения изобретения средство для установления температуры представляет собой радиантный охладитель, конвективный охладитель, кондукционный охладитель, вентиляторный охладитель или комбинацию указанных.
В различных вариантах выполнения изобретения средством для установления температуры устанавливается температура до около 0, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85 или 90°C, включая промежуточные значения между ними. В некоторых вариантах выполнения изобретения температура устанавливается между около 40°C и около 90°C. В некоторых вариантах выполнения изобретения температура устанавливается между около 0°C и около 10°C.
В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем документе, дополнительно включает средство для применения увлажняющего агента к одному или более из: печатной платформы; принимающей поверхности, отверстия для нанесения, биочернил, вспомогательного материала или биоотпечатанной конструкции. В некоторых вариантах выполнения изобретения средство для применения увлажняющего агента представляет собой любой подходящий способ нанесения жидкости (напр., разбрызгивателем, пипеткой, соплом и т.д.). В некоторых вариантах выполнения изобретения увлажняющий агент представляет собой воду, тканевую культуральную среду, забуференные солевые растворы, сыворотку или комбинацию указанных. В дополнительных вариантах выполнения изобретения увлажняющий агент наносится после того, как биочернила или материал подложки распределяется биопринтером. В некоторых вариантах выполнения изобретения увлажняющий агент наносится одновременно или по существу одновременно с биочернилами или вспомогательным материалом, который распределяется биопринтером. В некоторых вариантах выполнения изобретения увлажняющий агент наносится перед тем, как биочернила или материал подложки распределяется биопринтером.
Печатающая Головка
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой биопринтеры для изготовления тканей и органов. В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем документе, включает одну или более печатающую головку. В некоторых вариантах выполнения изобретения биопринтер, описанный в настоящем документе, включает средства для получения и удерживания по меньшей мере одного картриджа. В еще дополнительных вариантах выполнения изобретения печатающая головка прикрепляет по меньшей мере один картридж к биопринтеру.
Многие средства для приема и удерживания по меньшей мере одного картриджа являются подходящими. Подходящие средства для приема и удерживания по меньшей мере одного картриджа включают те, которые надежно, точно и плотно прикрепляют по меньшей мере один картридж к биопринтеру. В различных вариантах выполнения изобретения средство для приема и удерживания по меньшей мере одного картриджа представляет собой, в качестве неограничивающего примера, магнитное притяжение, зажатие цанговым патроном, металлический обод, гайку, адаптер втулки или комбинацию указанных.
В некоторых вариантах выполнения изобретения печатающая головка, описанная в настоящем документе, принимает и удерживает один картридж. В различных других вариантах выполнения изобретения печатающая головка, описанная в настоящем документе, принимает и удерживает 2, 3, 4, 5, 6, 7, 8, 9, 10 или более картриджей одновременно. В дополнительных вариантах выполнения изобретения печатающая головка, описанная в настоящем документе, дополнительно включает средство для выбора картриджа, который будет применяться при биопечати, среди множества принятых и удержанных картриджей.
В некоторых вариантах выполнения изобретения печатающая головка, описанная в настоящем документе, дополнительно включает (или находится в жидкостной связи с) резервуар, который содержит биочернила и/или вспомогательные материалы сверх загрузки одного или более картриджей. В дополнительных вариантах выполнения изобретения резервуар поставляет биочернила и/или вспомогательные материалы к одному или более картриджу для распределения посредством распределяющего отверстия. Конфигурации печатающей головки, включающей резервуар, являются особенно пригодными для применения в непрерывной или по существу непрерывной биопечати. Многие объемы являются подходящими для резервуара, описанного в настоящем документе. В различных вариантах выполнения изобретения резервуар имеет внутренний объем, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350, 400, 450, 500 мл или более, включая промежуточные значения между ними.
В некоторых вариантах выполнения изобретения биопечать включает использование компьютера для конфигурации параметров, таких как высота печати, скорость насоса, скорость робота или комбинации указанных независимо или относительно друг друга. В дополнительных вариантах выполнения изобретения компьютерный код конкретизирует положение печатающей головки для конфигурации высоты печатающей головки над принимающей поверхностью. В дополнительных вариантах выполнения изобретения компьютерный код конкретизирует направление и скорость движения печатающей головки для конфигурации характеристик распределения биочернил и/или вспомогательного материала.
Картриджи
Описанное в настоящем документе в конкретных вариантах выполнение изобретения представляет собой биопринтеры для изготовления тканей и органов. В некоторых вариантах выполнения изобретения картридж, прикрепленный к биопринтеру, включает биочернила или материал подложки. В некоторых вариантах выполнения изобретения биопринтер распределяет биочернила или материал подложки в виде конкретного рисунка и в конкретных положениях для того, чтобы сформировать конкретную клеточную конструкцию, ткань или орган. Для того чтобы изготовить комплексные тканевые конструкции, биопринтер наносит биочернила или материал подложки при точных скоростях и в одинаковых количествах. Таким образом, существует необходимость в картридже с (а) распределяющим отверстием, который является гладким или по существу гладким, и (b) внутренней поверхностью, которая является гладкой или оп существу гладкой. Как используется в настоящем документе, «картридж» означает любой объект, который способен принимать (и удерживать) биочернила и/или материал подложки.
В некоторых вариантах выполнения изобретения картридж, описанный в настоящем документе, включает биочернила. В некоторых вариантах выполнения изобретения картридж, описанный в настоящем документе, включает комбинацию биочернил и вспомогательного материала.
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой картриджи для использования с биопринтером, описанным в настоящем документе, включающие по меньшей мере одно распределяющее отверстие. В некоторых вариантах выполнения изобретения картридж включает одно распределительное отверстие. В различных других вариантах выполнения изобретения картридж включает 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 20, 30, 40, 50, 60, 70, 80, 90, 100 или более распределительных отверстий. В дополнительном варианте выполнения изобретения изобретения углы распределительного отверстия являются гладкими или по существу гладкими.
Множество форм является подходящим для распределительных отверстий, описанных в настоящем документе. В различных вариантах выполнения изобретения подходящие формы для распределительных отверстий включают, в качестве неограничивающих примеров, круглую, овальную, треугольную, квадратную, прямоугольную, полигональную и неправильную. В некоторых вариантах выполнения изобретения отверстие является круглым. В других вариантах выполнения изобретения отверстие является квадратным. В еще других вариантах выполнения изобретения отверстие является овальным, удлиненным или прямоугольным и распределяет твердые или полутвердые биочернила и/или вспомогательные материалы в лентообразную форму.
В некоторых вариантах выполнения изобретения внутренняя поверхность картриджа является гладкой или по существу гладкой. В некоторых вариантах выполнения изобретения картридж составлен из жесткой структуры для облегчения калибровки. В некоторых вариантах выполнения изобретения стенки картриджа составлены из материала, который устойчив к прикреплению клеток. В некоторых вариантах выполнения изобретения картриджи составлены из материала, который является биосовместимым.
Многие типы картриджей являются подходящими для использования с биопринтерами, описанными в настоящем документе, и способами их использования. В некоторых вариантах выполнения изобретения картридж является совместимым с биопечатью, в которой используется экструдирование полутвердых или твердых биочернил или вспомогательного материала через одно или более распределительное отверстие. В некоторых вариантах выполнения изобретения картридж является совместимым с биопечатью, в которой используется распределение жидкого или полутвердого клеточного раствора, клеточной суспензии или клеточной концентрации через одно или более распределительное отверстие. В некоторых вариантах выполнения изобретения картридж является совместимым с периодической биопечатью. В некоторых вариантах выполнения изобретения картридж является совместимым с непрерывной и/или по существу непрерывной биопечатью.
В некоторых вариантах выполнения изобретения картридж представляет собой капиллярную трубку или микропипетку. В некоторых вариантах выполнения изобретения картридж представляет собой шприц или иглу. Многие внутренние диаметры являются подходящими для по существу круглых или цилиндрических картриджей. В различных вариантах выполнения изобретения подходящие внутренние диаметры включают, в качестве неограничивающих примеров, 1, 10, 50, 100, 200, 300,400, 500, 600, 700, 800, 900, 1000 или более мкм, включая промежуточные значения между ними. В других различных вариантах выполнения изобретения подходящие внутренние диаметры включают, в качестве неограничивающих примеров, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 или более мм, включая промежуточные значения между ними. В некоторых вариантах выполнения изобретения картридж имеет внутренний диаметр от около 1 мкм до около 1000 мкм. В конкретном варианте выполнения изобретения картридж имеет внутренний диаметр около 500 мкм. В другом конкретном варианте выполнения изобретения картридж имеет внутренний диаметр около 250 мкм. Многие внутренние объемы являются подходящими для картриджей, описанных в данном документе. В различных вариантах выполнения изобретения подходящие внутренние объемы включают, в качестве неограничивающих примеров, 1, 10, 20, 30, 40, 50, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000 или более мкл, включая промежуточные значения между ними. В других различных вариантах выполнения изобретения подходящие внутренние объемы включают, в качестве неограничивающих примеров, 1, 2, 3, 4, 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500 или более мл, включая промежуточные значения между ними. В некоторых вариантах выполнения изобретения картридж имеет объем от около 1 мкл до около 50 мкл. В конкретном варианте выполнения изобретения картридж имеет объем около 5 мкл.
В некоторых вариантах выполнения изобретения картридж является совместимым со струйной печатью биочернилами и/или вспомогательным материалом на принимающую поверхность, такую как описанная в Патенте США 7,051,654. В дополнительных вариантах выполнения изобретения картридж включает распределительные отверстия в форме потенциалзависимых выпускных отверстий или игл под управлением компьютерного кода, описанного в настоящем документе.
В некоторых вариантах выполнения изобретения картридж является заполненным. В некоторых вариантах выполнения изобретения заполнение картриджа повышает точность процесса распределения, нанесения или экструдирования. Как используется в настоящем документе, «заполненный» означает, что содержимое картриджа готовится для распределения, нанесения или экструдирования путем упаковки и перемещения содержимого картриджа до тех пор, пока материал, который необходимо распределить (биочернила или материал подложки), не будет расположен в месте контакта с распределительным отверстием. В некоторых вариантах выполнения изобретения картридж заправляется, когда содержимое упаковано или по существу упаковано и содержимое находится в физическом контакте с отверстием картриджа.
В некоторых вариантах выполнения изобретения картридж марикирован для индикации состава его содержимого. В дополнительных вариантах выполнения изобретения картридж маркирован для индикации состава биочернил и/или вспомогательного материала, содержащихся в нем. В некоторых вариантах выполнения изобретения поверхность картриджа является цветной. В некоторых вариантах выполнения изобретения внешняя поверхность картриджа окрашена, раскрашена, помечена ручкой, помечена стикером или комбинацией указанного.
В некоторых вариантах выполнения изобретения внешняя поверхность картриджа маркирована для увеличения непрозрачности поверхности картриджа (напр., для увеличения количества лазерного луча, который отражается от поверхности картриджа). В некоторых вариантах выполнения изобретения поверхность картриджа окрашена. В некоторых вариантах выполнения изобретения на внешней поверхности картриджа нанесены метки. Как используется в настоящем документе, «с нанесенной меткой» означает маркирование поверхности картриджа для уменьшения гладкости поверхности.
Любой подходящий способ используется для нанесения меток на поверхность картриджа (напр., применение кислотного вещества, применение едкого вещества, применение абразивного вещества и т.д.). В некоторых вариантах выполнения изобретения внешняя поверхность картриджа раскрашена, отполирована (напр., оплавлена), гравирована (напр., гравирована лазером), помечена ручкой, помечена стикером или комбинацией указанного.
Крепление
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой биопринтеры для изготовления тканей и органов. В некоторых вариантах выполнения изобретения картридж, прикрепленный к биопринтру, включает биочернила и/или материал подложки. В некоторых вариантах выполнения изобретения биопринтер распределяет биочернила и/или материал подложки в виде конкретного рисунка и в конкретных положениях для того, чтобы сформировать конкретную клеточную конструкцию, ткань или орган. В некоторых вариантах выполнения изобретения картридж, включающий биочернила, является одноразовым. В некоторых вариантах выполнения изобретения картридж вынимается из биопринтера после выдавливания содержимого. В некоторых вариантах выполнения изобретения новый картридж впоследствии прикрепляется к биопринтеру.
Для того чтобы изготовить комплексные структуры, биопринтеры, описанные в настоящем документе, распределяют биочернила и/или материал подложки из картриджа с подходящей воспроизводимой точностью. В различных вариантах выполнения изобретения подходящие воспроизводимые точности включают ±5, 10, 20, 30, 40 или 50 мкл по любой оси. В некоторых вариантах выполнения изобретения биопринтеры, описанные в настоящем документе, распределяют биочернила и/или материал подложки из картриджа с воспроизводимой точностью около±20 мкм. Однако неконтролируемое удаление и вставка картриджей может привести к изменениям положения печатающей головки (и таким образом, картриджей) в отношении тканевой конструкции, такому что точное расположение первой частицы биочернил, распределенной из нового картриджа, может варьироваться относительно последней частицы биочернил, распределенной из предыдущего картриджа. Таким образом, существует необходимость в способе прикрепления и закрепления картриджа к печатающей головке, в котором указанное прикрепление и закрепление приводит к минимальным изменениям положения печатающей головки.
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой способы прикрепления картриджа к биопринтеру, включающие: (а) вставку картриджа в цанговый патрон, где цанговый патрон прикреплен к печатающей головке биопринтера; и (b) установку внешней гайки цангового патрона; где вставка и установка по существу не изменяют положение печатающей головки.
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой системы для прикрепления картриджа к биопринтеру, включающие: средство для приема и закрепления картриджа к печатающей головке биопринтера; где применение средства для приема и закрепления картриджа по существу не изменяет положение печатающей головки. В некоторых вариантах выполнения изобретения средство для приема и закрепления картриджа к печатающей головке представляет собой зажим или втулку. Как используется в настоящем документе, «зажим» означает удерживающее устройство, состоящее из регулируемых тисок. В некоторых вариантах выполнения изобретения средством для приема и прикрепления картриджа к принтеру является головка цанги. Как используется в настоящем документе, «цанга» означает подтип зажима, который образует воротник вокруг объекта, который необходимо удержать, и оказывает сильное зажимное действие. Как используется в настоящем документе, «втулка» означает ленту (напр., металлическую ленту), используемую для защиты одного объекта от другого. В некоторых вариантах выполнения изобретения средством для приема и прикрепления картриджа к принтеру является адаптер втулки. Как используется в настоящем документе, «адаптер втулки» означает трубку с резьбой, используемую для защиты одного объекта от другого.
Принимающая поверхность
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой биопринтеры для изготовления тканей и органов. В некоторых вариантах выполнения изобретения биопринтер распределяет множество элементов, секций и/или областей биочернил и/или вспомогательного материала на принимающую поверхность. В дополнительных вариантах выполнения изобретения распределение происходит по конкретному рисунку и в определенных положениях. В еще дополнительных вариантах выполнения изобретения изобретения местоположения, в которых биопринтер наносит биочернила и/или материал подложки на принимающую поверхность, определяются путем пользовательского ввода и переводится в компьютерный код.
В некоторых вариантах выполнения изобретения каждый из элементов, секций и/или областей биочернил и/или вспомогательного материала имеет размеры менее, чем 300 мм × 300 мм × 160 мм. Только в качестве примера, размеры секции биочернил или вспомогательного материала могут быть 75 мм × 5,0 мм × 5,0 мм; 0,3 мм × 2,5 мм × 2,5 мм; 1 мм × 1 мм × 50 мм; или 150 мм × 150 мм × 80 мм. Из-за обычно маленького размера каждой секции и в некоторых случаях требуется высокая степень точности, незначительные дефекты в принимающей поверхности могут привести к дефектам (и, возможно, браку) клеточной конструкции, ткани или органа. Таким образом, существует необходимость в, по существу, гладкой и, по существу, ровной принимающей поверхности или определенной или, по существу, определенной поверхности, которая способна принимать секции биочернил и/или вспомогательного материала.
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой принимающие поверхности для приема одной или более структур, полученных с помощью биопринтера, описанного в настоящем документе. В некоторых вариантах выполнения изобретения принимающая поверхность является ровной или по существу ровной. В некоторых вариантах выполнения изобретения принимающая поверхность является гладкой или по существу гладкой. В некоторых вариантах выполнения изобретения принимающая поверхность является ровной или по существу ровной. В некоторых вариантах выполнения изобретения принимающая поверхность является определенной или по существу определенной. В других вариантах выполнения изобретения принимающая поверхность разработана специально для размещения формы, размера, текстуры или геометрии специфичной биоотпечатанной структуры. В дополнительных вариантах выполнения изобретения принимающая поверхность контролирует или влияет на размер, форму, текстуру или геометрию биоотпечатанной конструкции.
В некоторых вариантах выполнения изобретения принимающая поверхность включает твердый материал, полутвердый материал или комбинацию указанного. В некоторых вариантах выполнения изобретения принимающая поверхность включает стекло, покрытое стекло, пластик, покрытый пластик, металл, сплав металлов или комбинацию указанных. В некоторых вариантах выполнения изобретения принимающая поверхность включает гель. В некоторых вариантах выполнения изобретения принимающая поверхность и любые ее покрытия являются биосовместимыми. В различных вариантах выполнения изобретения принимающая поверхность включает любые вспомогательные материалы и/или защитные материалы, описанные в настоящем документе. В специальных вариантах выполнения изобретения принимающая поверхность включает полимеризованный NovoGel™ или полимеризованную агарозу, полимеризованный желатин, внеклеточный матрикс (или его компоненты), коллаген или комбинацию указанного.
Программное обеспечение
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой биопринтеры для изготовления тканей и органов. В некоторых вариантах выполнения изобретения один или более картриджей, прикрепленных к биопринтеру, включает биочернила и/или материал подложки. В некоторых вариантах выполнения изобретения биопринтер распределяет биочернила или материал подложки в виде конкретного рисунка и в конкретном положении для того, чтобы образовать конкретную клеточную конструкцию, ткань или орган.
Для того чтобы изготовить комплексный тканевый конструкт, биопринтер наносит биочернила или материал подложки в точные местоположения (в двух или трех измерениях) на принимающей поверхности. В некоторых вариантах выполнения изобретения местоположения, в которые биопринтер наносит биочернила и/или материал подложки, определяются путем пользовательского ввода и переводится в компьютерный код. В дополнительных вариантах выполнения изобретения компьютерный код включает последовательность инструкций, исполняемых в центральном процессоре (CPU) цифрового обрабатывающего устройства, написанных для исполнения конкретного задания. В некоторых вариантах выполнения изобретения дополнительные параметры биопечати, включающие, в качестве неограничивающих примеров, высоту печати, скорость насоса, скорость робота и/или контроль различных распределяющих отверстий, определяются путем пользовательского ввода и транслируются в компьютерный код. В других вариантах выполнения изобретения такие параметры биопечати непосредственно не определяются путем пользовательского ввода, но выводятся из других параметров и условий с помощью компьютерного кода, описанного в настоящем документе.
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой способы изготовления тканевых конструкций, тканей и органов, включающие: компьютерный модуль, принимающий ввод визуального представления желаемой тканевой конструкции; компьютерный модуль, генерирующий серии команд, где команды основаны на визуальном представлении и читаются биопринтером; компьютерный модуль, обеспечивающий серии команд биопринтеру; и биопринтер, наносящий биосернила и/или материал подложки в соответствии с командами с формированием конструкции с определенной геометрией.
Машиночитаемый носитель
В некоторых вариантах выполнения изобретения позиции, в которые биопринтер наносит биочернила и/или материал подложки, определяются пользовательским вводом и переводятся в машинный код. В некоторых вариантах выполнения изобретения устройства, системы и способы, описанные в настоящем документе, дополнительно включают машиночитаемый носитель или носитель, закодированный машиночитаемым программным кодом. В дополнительных вариантах выполнения изобретения машиночитаемый носитель представляет собой материальный компонент цифрового процессингового устройства, такого как биопринтер (или его компонент) или компьютер, подключенный к биопринтеру (или его компонент). В еще дополнительных вариантах выполнения изобретения машиночитаемый носитель представляет собой, необязательно, съемный с цифрового процессингового устройства. В некоторых вариантах выполнения изобретения машиночитаемый носитель включает, в качестве не ограничивающих примеров, CD-ROM, DVD, устройства флэш-памяти, твердотельную память, дисководы магнитных дисков, дисководы магнитных кассет, дисководы оптических дисков, системы и сервисы облачных вычислений и тому подобное.
Компьютерные модули
В некоторых вариантах выполнения изобретения устройства, системы и способы, описанные в настоящем документе, включают программное обеспечение, сервер и модули базы данных. В некоторых вариантах выполнения изобретения "компьютерный модуль" представляет собой программный компонент (в том числе часть кода), который взаимодействует с большей компьютерной системой. В дополнительных вариантах выполнения изобретения программный модуль (или модуль программы) поставляется в виде одного или нескольких файлов и обычно обрабатывает конкретную задачу в большей программной системе.
В некоторых вариантах выполнения изобретения модуль включен в одну или несколько программных систем. В других вариантах выполнения изобретения модуль интегрирован с одним или несколькими другими модулями в одну или несколько программных систем. Компьютерный модуль представляет собой, необязательно, автономную часть кода или, необязательно, код, который не является отдельно идентифицируемым. В некоторых вариантах выполнения изобретения модули находятся в одном приложении. В других вариантах выполнения изобретения модули представляют собой множество приложений. В некоторых вариантах выполнения изобретения модули размещаются на одной машине. В других вариантах выполнения изобретения модули размещаются на множестве машин. В некоторых вариантах выполнения изобретения модули размещаются на множестве машин в одном месте. В других вариантах выполнения изобретения модули размещаются на множестве машин более, чем в одном месте. Далее описанное в настоящем документе представляет собой форматирование расположения и позиционирование данных. В некоторых вариантах выполнения изобретения файлы данных, описанные в настоящем документе, отформатированы в любой подходящий формат сериализации данных, включая, в качестве не ограничивающих примеров, значениями, разделенные табуляцией, значения, разделенные запятыми, значения, разделенные знаками, значения, разделенные разделителями, XML, JSON, BSON и YAML. Ключевой особенностью компьютерного модуля является то, что он позволяет конечному пользователю использовать компьютер для выполнения определенных функций.
Графический пользовательский интерфейс
В некоторых вариантах выполнения изобретения компьютерный модуль содержит графический пользовательский интерфейс (ГИП). Как используется в настоящем документе, термин "графический пользовательский интерфейс" означает пользовательскую среду, использующую как изобразительное, так и текстовое представление входных и выходных приложений и иерархическую или другую структуру данных, в которой хранится информация. В некоторых вариантах выполнения изобретения компьютерный модуль содержит экран дисплея. В дополнительных вариантах выполнения изобретения компьютерный модуль представляет посредством экрана дисплея двумерный ГИП. В других вариантах выполнения изобретения компьютерный модуль представляет посредством экрана трехмерный ГИП, такой среда виртуальной реальности. В некоторых вариантах выполнения изобретения экран дисплея является сенсорным или мультисенсорным и представляет собой интерактивный ГИП.
В некоторых вариантах выполнения изобретения экран дисплея представляет собой ГИП, который состоит по существу из сетки, содержащей регулярно расположенные объекты по существу одинаковой формы и по существу одинакового размера. Представленные объекты имеют любую подходящую форму. В некоторых вариантах выполнения изобретения подходящие формы для объектов включают, в качестве неограничивающих примеров, круг, овал, квадрат, прямоугольник, треугольник, ромб, многоугольник или их комбинацию.
В некоторых вариантах выполнения изобретения пользователь определяет содержание одного или нескольких объектов, чтобы сформировать двумерное или трехмерное визуальное представление желаемой тканевой конструкции. Смотри, напр., на Фигуру 4. В некоторых вариантах выполнения изобретения определенное пользователем содержимое объекта, в качестве не ограничивающих примеров, представляет собой биочернила с различными составами или материал подложки с различными составами. В некоторых вариантах выполнения изобретения пользователь определяет содержимое объект, изменяя цвет ячейки или форму объекта.
Биочернила
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой устройства, системы и способы изготовления тканей и органов. В некоторых вариантах выполнения изобретения устройства включают одну или более печатающую головку для приема и удерживания по меньшей мере одного картриджа, который, необязательно, содержит биочернила. В некоторых вариантах выполнения изобретения способы включают использование биочернил. В дополнительных вариантах выполнения изобретения ткани и органы, изготовленные с использованием устройств, систем и способов, описанных в настоящем документе, включают биочернила во время изготовления или после.
В некоторых вариантах выполнения изобретения «биочернила» включают жидкие, полутвердые или твердые составы, включающие множество клеток. В некоторых вариантах выполнения изобретения биочернила включают жидкие или полутвердые клеточные растворы, клеточные суспензии или клеточные концентрации. В дополнительных вариантах выполнения изобретения клеточный раствор, суспензия или концентрация включает жидкий или полутвердый (напр., вязкий) носитель и множество клеток. В еще дополнительном варианте выполнения изобретения носитель представляет собой подходящую клеточную питательную среду, такую, как описана в настоящем документе. В некоторых вариантах выполнения изобретения биочернила включают полутвердые или твердые многоклеточные агрегаты или многоклеточные тела. В дополнительных вариантах выполнения изобретения биочернила производятся путем 1) смешивания множества клеток или клеточных агрегатов и биосовместимой жидкости или геля в заранее определенном соотношении с получением биочернил, и 2) уплотнения биочернил для получения биочернил с желаемой клеточной плотностью и вязкостью. В некоторых вариантах выполнения изобретения уплотнение биочернил достигается путем центрифугирования, фильтрования с тангенциальным потоком («TFF») или комбинацией указанных. В некоторых вариантах выполнения изобретения уплотнение биочернил приводит к композиции, которая является экструдируемой, позволяющей образование многоклеточных агрегатов или многоклеточных тел. В некоторых вариантах выполнения изобретения «экструдируемая» означает способность к формованию путем приложения усилия (напр., под давлением) через сопло или отверстие (напр., один или более канал или трубку). В некоторых вариантах выполнения изобретения уплотнение биочернил является результатом роста клеток до желаемой плотности. Плотность клеток, необходимая для биочернил, будет варьироваться в зависимости от используемых клеток и ткани и органа, который необходимо получить. В некоторых вариантах выполнения изобретения клетки биочернил сцепляются и/или адгезируются. В некоторых вариантах выполнения изобретения «сцепляться», «сцепленный» и «сцепление» относятся к свойствам клетка-клеточной адгезии, которая связывает клетки, многоклеточные агрегаты, многоклеточные тела и/или их слои. В дополнительных вариантах выполнения изобретения термины используются взаимозаменяемо с «сливаться», «слитый» и «слияние». В некоторых вариантах выполнения изобретения биочернила дополнительно включают материал подложки, клеточную культуральную среду, внеклеточный матрикс (или его компоненты), агенты клеточной адгезии, ингибиторы гибели клеток, антиапоптотические агенты, антиоксиданты, экструзионные соединения и комбинации указанных.
Клетки
Описанное в настоящем документе в различных вариантах выполнения представляет собой биочернила, которые включают жидкие, полутвердые или твердые составы, включающие множество клеток. В некоторых вариантах выполнения изобретения биочернила включают жидкие или полутвердые клеточные растворы, клеточные суспензии или клеточные концентрации. В некоторых вариантах выполнения изобретения любая клетка млекопитающих является подходящей для использования в биочернилах и в изготовлении тканей и органов с использованием устройств, систем и способов, описанных в настоящем документе. В различных вариантах выполнения изобретения клетки являются любыми подходящими клетками. В дополнительных различных вариантах выполнения изобретения клетки представляют собой клетки позвоночных, клетки млекопитающих, клетки человека или комбинации указанных. В некоторых вариантах выполнения изобретения тип клеток, использованных в способах, описанных в настоящем документе, зависит от типа клеточной конструкции, ткани или органа, которые получают. В некоторых вариантах выполнения изобретения биочернила включают один тип клеток (также называются «гомологичные чернила»). В некоторых вариантах выполнения изобретения биочернила включают более чем один тип клеток (также называются «гетерологичные чернила»).
В дополнительных ваирантах выполнения изобретения клетки представляют собой, в качестве неограничивающих примеров, сократительные или мышечные клетки (напр., клетки скелетной мышцы, кардиомициты, клетки гладкой мускулатуры и миобласты), клетки соединительной ткани (напр., клетки кости, клетки хряща, фибробласты и клетки, дифференцирующиеся в клетки формирования кости, хондроциты или ткани лимфы), клетки костного мозга, эндотелиальные клетки, клетки кожи, эпителиальные клетки, клетки молочной железы, сосудистые клетки, клетки крови, клетки лимфы, невральные клетки, клетки Шванна, желудочно-кишечные клетки, клетки печени, клетки поджелудочной железы, клетки легкого, трахеальные клетки, роговичные клетки, мочеполовые клетки, почечные клетки, половые клетки, жировые клетки, паренхиматозные клетки, перициты, мезотелиальные клетки, стромальные клетки, недифференцированные клетки (напр., эмбриональные клетки, стволовые клетки и клетки-предшественники), полученные из эндодермы клетки, полученные из мезодермы клетки, полученные из эктодермы клетки и комбинации указанных.
В некоторых вариантах выполнения изобретения клетки являются взрослыми дифференцированными клетками. В дополнительных вариантах выполнения изобретения «дифференцированные клетки» представляют собой клетки с ткань-специфичным фенотипом, указывающие, например, на клетку гладкой мускулатуры, фибробласт или эндотелиальную клетку во время выделения, где ткань-специфичный фенотип (или возможность проявить фенотип) сохраняется от времени выделения до времени использования. В других вариантах выполнения изобретения клетки являются взрослыми недифференцированными клетками. В дополнительных вариантах выполнения изобретения «недифференцированные клетки» представляют собой клетки, которые не обладают или потеряли определенные ткань-специфичные черты, например, клетки гладкой мускулатуры, фибробласты или эндотелиальные клетки. В некоторых вариантах выполнения изобретения недифференцированные клетки включают стволовые клетки. В дополнительных вариантах выполнения изобретения «стволовые клетки» представляют собой клетки, которые проявляют активность и самообновляются. Стволовые клетки включают, но не ограничиваясь, тотипотентные клетки, плюрипотентные клетки, мультипотентные клетки, олигопотентные клетки, унипотентные клетки и клетки-предшественники. Стволовые клетки могут быть эмбриональными стволовыми клетками, взрослыми стволовыми клетками, амниотическими стволовыми клетками и индуцированными плюрипотентными клетками. В еще других вариантах выполнения изобретения клетки представляют собой смесь взрослых дифференцированных клеток и взрослых недифференцированных клеток.
Клеточная культуральная среда
В некоторых вариантах выполнения изобретения биочернила включают клеточную культуральную среду. Клеточная культуральная среда включает любую подходящую среду. В различных вариантах выполнения изобретения подходящая клеточная среда включает, в качестве неограничивающих примеров, забуференный фосфатом физиологический раствор Дульбекко, сбалансированный солевой раствор Эрла, сбалансированный солевой раствор Хенкса, соли Тирода, раствор Олсвера, сбалансированный солевой раствор Гея, модифицированный буфер Креба-Хенселейта, бикарбонатный буфер Креба-Рингера, физиологический раствор Пака, модифицированную по способу Дульбекко среду Игла, модифицированную по способу Дульбекко среду Игла/питательную среду F-12 Хэма, питательную смесь F-10 Хэма (F-10 Хэма), среду 199, минимальную эссенциальную среду Игла, среду RPMI-1640, среду Эймса, среду BGJb (модификация Фиттона-Джексона), среду Клика, среду CMRL-1066, среду Фишера, минимальную эссенциальную среду Глазго (GMEM), среду Дульбекко, модифицированную по способу Исков, среду L-15 (Лейбовиц), модифицированную среду 5А Мак-Коя, среду NCTC, среду S-77 Свима, среду Вэймаус, среду Е Вильяма или комбинации указанных. В некоторых вариантах выполнения изобретения клеточная культуральная среда является модифицированной или с добавками. В некоторых вариантах выполнения изобретения клеточная культуральная среда дополнительно включает альбумин, селен, трансферрины, фетуины, сахара, аминокислоты, витамины, факторы роста, цитокины, гормоны, антибиотики, липиды, липидные носители, циклодекстрины или комбинации указанных.
Внеклеточный матрикс
В некоторых вариантах выполнения изобретения биочернила дополнительно включают один или более компонентов внеклеточного матрикса или его производных. В некоторых вариантах выполнения изобретения «внеклеточный матрикс» включает белки, которые производятся клетками и транспортируются из клеток во внеклеточное пространство, где они могут выступать в качестве вспомогательного материала для поддержания тканей вместе, для обеспечения прочности на разрыв и/или для облегчения клеточной сигнализации. Примеры компонентов внеклеточного матрикса включают, но не ограничиваясь, коллаген, фибронектин, ламинин, гиалуронаты, эластин и протеогликаны. Например, многоклеточные агрегаты могут содержать различные белки ЕСМ (напр., желатин, фибриноген, фибрин, коллаген, фибронектин, ламинин, эластин и/или протеогликаны). Компоненты ЕСМ или производные компонентов ЕСМ могут быть добавлены к клеточной пасте, используемой для получения многоклеточного агрегата. Компоненты ЕСМ или производные компонентов ЕСМ, добавленные к клеточной пасте, могут быть выделены из источника человеческого или животного происхождения или получены рекомбинантными способами, известными в данной области техники. В качестве альтернативы компоненты ЕСМ или производные компонентов ЕСМ могут быть естественным образом выделены клетками в удлиненном клеточном теле, или клетки, использованные для получения удлиненного клеточного тела, могут быть получены генетически с использованием любого подходящего способа, известного в данной области техники, для варьирования уровня экспрессии одного или более компонента ЕСМ или производных компонентов ЕСМ и/или одной или более молекул клеточной адгезии или молекул адгезии клетка-субстрат (напр., селектины, интегрины, иммуноглобулины и адгерины). Компоненты ЕСМ или производные компонентов ЕСМ могут ускорять сцепление клеток в многоклеточных агрегатах. Например, желатин и/или фибриноген могут быть подходящим образом добавлены к клеточной пасте, которая используется для образования многоклеточных агрегатов. Фибриноген может быть превращен в фибрин путем добавления тромбина.
В некоторых вариантах выполнения изобретения биочернила дополнительно включают агент, который способствует клеточной адгезии.
В некоторых вариантах выполнения изобретения биочернила дополнительно включают агент, который ингибирует гибель клеток (напр., некроз, апоптоз или аутофагоцитоз). В некоторых вариантах выполнения изобретения биочернила дополнительно включают антиапоптотический агент. Агенты, которые ингибируют гибель клеток, включают, но не ограничиваясь, маленькие молекулы, антитела, пептиды, пептитела или их комбинации. В некоторых вариантах выполнения изобретения агент, который ингибирует гибель клеток, выбирается из: агентов анти-TNF, агентов, которые ингибируют активность интерлейкина, агентов, которые ингибируют активность интерферона, агентов, которые ингибируют активность GCSF (колониесмулирующего фактора гранулоцитов), агентов, которые ингибируют активность воспалительного белка макрофагов, агентов, которые ингибируют активность TGF-B (трансформирующего фактора роста В), агентов, которые ингибируют активность ММР (матрикса металлопротеиназы), агентов, которые ингибируют активность каспазы, агентов, которые ингибируют активность сигнального каскада MAPK/JNK, агентов, которые ингибируют активность киназы Src, агентов, которые ингибируют активность JAK (Янус-киназы) или комбинации указанных. В некоторых вариантах выполнения изобретения биочернила включают антиоксидант.
Экструзионные соединения
В некоторых вариантах выполнения изобретения биочернила дополнительно включают экструзионное соединение (т.е. соединение, которое модифицирует экструзионные свойства биочернил). Примеры экструзионных соединений включают, но не ограничиваясь, гели, гидрогели, поврехностно-активные полиолы (напр., Pluronic F-127 или PF-127), термореактивные полимеры, гиалуронаты, альгинаты, компоненты внеклеточного матрикса (и их производные), коллагены, другие биосовместимые природные или синтетические полимеры, нановолокна и самоорганизующиеся нановолокна.
Гели, иногда называемые студнями, определяются различными путями. Например, Фармакопея США определяет глеи как полутвердые системы, состоящие из либо суспензий, полученных из маленьких неорганических частиц, либо больших органических молекул, взаимно проникнутых жидкостью. Гели включают однофазную или двухфазную систему. Однофазный гель состоит из органических макромолекул, равномерно распределенных по жидкости таким образом, что не существует видимых границ между распределенными макромолекулами и жидкостью. Некоторые однофазные гели готовятся из синтетических макромолекул (напр., карбомера) или из природных смол (напр., трагаканта). В некоторых вариантах выполнения изобретения однофазные гели обычно являются водными, но могут быть также получены с использованием спиртов и масел. Двухфазные гели состоят из сети маленьких дискретных частиц.
Гели также могут классифицироваться как гидрофобные или гидрофильные. В конкретных вариантах выполнения изобретения основание гидрофобного геля состоит из жидкого парафина с полиэтиленом или жирными маслами, загущенных с помощью коллоидного диоксида кремния или алюминиевых или цинковых мыл. В противоположность этому, основание гидрофобных гелей обычно состоит из воды, глицерина или пропиленгликоля, загущенных с помощью подходящего гелеобразующего агента (напр., трагаканта, крахмала, производных целлюлозы, карбоксивиниловых полимеров и силикатов магния-алюминия). В конкретных вариантах выполнения изобретения реология композиций или устройств, описанных в настоящем документе, является псевдопластичной, пластичной, тиксотропной или дилатантной.
Подходящие гидрогели включают полученные из коллагена, гиалуроната, фибрина, альгината, агарозы, хитозана и комбинаций указанных. В других вариантах выполнения изобретения подходящие гидрогели представляют собой синтетические полимеры. В дополнительных вариантах выполнения изобретения подходящие гидрогели включают полученные из поли(акриловой кислоты) и ее производных, поли (этиленоксида) и его сополимеров, поли(винилового спирта), полифосфазена и комбинаций указанных. В различных конкретных вариантах выполнения изобретения материал подложки выбирается из: гидрогеля, NovoGel™, агарозы, альгината, желатина, Matrigel™, гиалуронана, полоксамера, пептидного гидрогеля, поли(изопропил н-полиакриламида), полиэтиленгликоль диакрилата (ПЭГ-ДА), гидроксиэтилметакрилата, полидиметилсилоксана, полиакриламида, поли(молочной кислоты), силикона, шелка или комбинаций указанных.
В некоторых вариантах выполнения изобретения экструзионные соединения на основе гидрогеля представляют собой термообратимые гели (также известные как термореактивные гели или термогели). В некоторых вариантах выполнения изобретения подходящие термореактивный гель не является жидким при комнатной температуре. В конкретных вариантах выполнения изобретения температура гелеобразования (Тгел) подходящего гидрогеля составляет около 10°С, около 15°C, около 20°C, около 25°C, около 30°C, около 35°C и около 40°C, включая промежуточные значения между ними. В конкретных вариантах выполнения изобретения Тгел подходящего гидрогеля составляет от около 10°C до около 25°C. В некоторых вариантах выполнения изобретения биочернила (напр., включающие гидрогель, один или более тип клеток и другие добавки, и т.д.), описанные в настоящем документе, не являются жидкими при комнатной температуре. В конкретных вариантах выполнения изобретения температура гелирования (Тгел) биочернил, описанных в настоящем документе, составляет около 10°C, около 15°C, около 20°C, около 25°C, около 30°С, около 35°С и около 40°С, включая промежуточные значения между ними. В конкретных вариантах выполнения изобретения Тгел биочернил, описанных в настоящем документе, составляет от около 10°С до около 25°С.
Полимеры, составленные из полиоксипропилена и полиоксиэтилена, образуют термореактивные гели, когда включаются в водные растворы. Эти полимеры имеют способность изменяться от жидкого состояния до состояния геля при температурах, которые могут поддерживаться в аппаратах биопринтера. Фазовое превращение из жидкого состояния в состояние геля зависит от концентрации полимера и ингредиентов в растворе.
Полоксамер 407 (Pluronic F-127 или PF-127) представляет собой неионный поверхностно-активный агент, составленный из сополимеров полиоксиэтилена-полиоксипропилена. Другие полоксамеры включают 188 (категория F-68), 237 (категория F-87), 338 (категория F-108). Водные растворы полоксамеров являются стабильными в присутствии кислот, щелочей и ионов металлов. PF-127 представляет собой коммерчески доступный триблок сополимер полиоксиэтилена-полиоксипропилена общей формулы Е106 Р70 Е106 со средней молярной массой 13000. Полимер может быть дополнительно очищен подходящими способами, которые будут улучшать свойства гелирования полимера. Он содержит приблизительно 70% этиленоксида, который обуславливает его гидрофильность. Это один из серии полоксамерных блок-сополимеров АВА. PF-127 имеет хорошую солюбилизирующую способность, низкую токсичность и, тем самым, считается подходящим экструзионным соединением.
В некоторых вариантах выполнения изобретения вязкость гидрогелей и биочернил, представленных в настоящем документе, измеряется любыми описанными средствами. Например, в некоторых вариантах выполнения изобретения для расчета вязкости гидрогелей и биочернил используется LVDV-II+CP Cone Plate Viscometer и Cone Spindle CPE-40. В других вариантах выполнения изобретения для расчета вязкости гидрогелей и биочернил используется вискозиметр Брукфилда (конус и чаша). В некоторых вариантах выполнения изобретения диапазоны вязкости относятся к измеренным при комнатной температуре. В других вариантах выполнения изобретения диапазоны вязкости относятся к измеренным при температуре тела (напр., средней температуре тела здорового человека).
В дополнительных вариантах выполнения изобретения гидрогели и/или биочернила характеризуются как имеющие вязкость между около 500 и 1000000 сантипуаз, между около 750 и 1000000 сантипуаз; между около 1000 и 1000000 сантипуаз; между около 1000 и 400000 сантипуаз; между около 2000 и 100000 сантипуаз; между около 3000 и 50000 сантипуаз; между около 4000 и 25000 сантипуаз; между около 5000 и 20000 сантипуаз; или между около 6000 и 15000 сантипуаз.
В некоторых вариантах выполнения изобретения биочернила включают клетки и экструзионные соединения, подходящие для непрерывной биопечати. В конкретных вариантах выполнения изобретения биочернила имеют вязкость около 1500 мПа*с. Смесь Pluronic F-127 и клеточного материала может быть подходящей для непрерывной печати. Такие биочернила могут быть приготовлены путем растворения порошка Pluronic F-127 при непрерывном перемешивании в холодном (4°С) физиологическомй растворе с фосфатным буфером (PBS) в течение 48 часов до 30% (масс/об). Pluronic F-127 может также быть растворен в воде. Клетки могут быть культивированы и выращены с использованием стандартных методикстерильной клеточной культуры. Клетки могут быть пеллетированы при 200g, например, и ресуспендированы в 30% Pluronic F-127 и аспирированы в резервуар, прикрепленный к биопринтеру, где может происходить затвердение при температуре гелирования от около 10 до около 25°С. Возможно гелеобразование биочернил до биопечати. Биочернила, включая биочернила, включающие Pluronic F-127, могут быть распределены как жидкость.
В различных вариантах выполнения изобретения концентрация Pluronic F-127 может быть любого значения с подходящей вязкостью и/или цитотоксическими свойствами. Подходящая концентрация Pluronic F-127 может также быть способна поддерживать массу при сохранении ее формы, будучи биоотпечатанными. В некоторых вариантах выполнения изобретения концентрация Pluronic F-127 составляет около 10%, около 15%, около 20%, около 25%, около 30%, около 35%, около 40%, около 45% или около 50%. В некоторых вариантах выполнения изобретения концентрация Pluronic F-127 находится между около 30% и около 40% или между около 30% и около 35%.
Фигура 5 иллюстрирует трехмерную конструкцию в форме пирамиды, полученную путем непрерывного нанесения PF-127 с использованием биопринтера NovoGen MMX™, соединенного со шприцом с иглой 510 мкм.
Фигура 6 иллюстрирует трехмерные конструкции в форме куба (слева) и в форме полого куба (справа), полученные путем непрерывного нанесения PF-127 с использованием биопринтера NovoGen MMX™, соединенного со шприцом с иглой 510 мкм.
В некоторых вариантах выполнения изобретения неклеточные компоненты биочернил (напр., экструзионные соединения, и т.д.) удаляются перед использованием. В дополнительных вариантах выполнения изобретения неклеточные компоненты представляют собой, например, гидрогели, поверхностно-активные полиолы, термореактивные полимеры, гиалуронаты, альгинаты, коллагены или другие биосовместимые природные или синтетические полимеры. В еще дополнительных вариантах выполнения изобретения неклеточные компоненты удаляются с помощью физических, химических или ферментных средств. В некоторых вариантах выполнения изобретения часть неклеточных компонентов остается связанной с клеточными компонентами во время использования.
В некоторых вариантах выполнения изобретения клетки предварительно обрабатываются для увеличения клеточного взаимодействия. Например, клетки могут инкубироваться внутри центрифужной трубки после центрифугирования для того, чтобы увеличить клетка-клеточные взаимодействия до формования биочернил.
Материал подложки
Описанное в настоящем документе в конкретных вариантах выполнения изобретения представляет собой устройства, системы и способы для изготовления тканей и органов. В некоторых вариантах выполнения изобретения устройства содержат одну или более головок принтера для приема и удерживания по меньшей мере одного картриджа, который необязательно содержит материал подложки. В некоторых вариантах выполнения изобретения способы включают использование материала подложки. В дополнительных вариантах выполнения изобретения ткани и органы, изготовленные с использованием устройств, систем и способов, описанных в настоящем документе, включают материал подложки во время изготовления или после него.
В некоторых вариантах выполнения изобретения материал подложки способен исключать рост клеток или миграцию в клетки или адгезию к ним. В некоторых вариантах выполнения изобретения материал подложки является проницаемым для питательной среды.
В некоторых вариантах выполнения изобретения вязкость материала подложки является изменяемой. В некоторых вариантах выполнения изобретения вязкость материала подложки изменяют путем модифицирования температуры вспомогательного материала. В некоторых вариантах выполнения изобретения вязкость материала подложки изменяют путем модифицирования давления вспомогательного материала. В некоторых вариантах выполнения изобретения вязкость вспомогательного материала изменяют путем модифицирования концентрации вспомогательного материала. В некоторых вариантах выполнения изобретения вязкость вспомогательного материала изменяют перекрестным сшиванием (напр., с использованием химического сшивающего линкера) или фотоперекрестным сшиванием (напр., с использованием ультрафиолетового излучения).
В некоторых вариантах выполнения изобретения проницаемость вспомогательного материала является изменяемой. В некоторых вариантах выполнения изобретения проницаемость вспомогательного материала модифицируют путем изменения температуры вспомогательного материала или температуры, окружающей материал подложки. В некоторых вариантах выполнения изобретения проницаемость вспомогательного материала модифицируют путем контактирования вспомогательного материала с агентом, который модифицирует проницаемость.
В некоторых вариантах выполнения изобретения деформируемость (т.е. упругость или твердость) вспомогательного материала модифицируется. В некоторых вариантах выполнения изобретения деформируемость вспомогательного материала модифицируют путем изменения температуры вспомогательного материала или температуры, окружающей материал подложки. В некоторых вариантах выполнения изобретения деформируемость вспомогательного материала модифицируют путем контактирования вспомогательного материала с агентом, который модифицирует деформируемость.
Многие вспомогательные материалы являются подходящими для использования в способах, описанных в настоящем документе. В некоторых вариантах выполнения изобретения гидрогели являются примерными вспомогательными материалами, обладающими одним или более полезными свойствами, включая: отсутствие прилипания, биосовместимость, экструдируемость, способность к биопечати, неклеточность и подходящую прочность. В некоторых вариантах выполнения изобретения подходящие гидрогели представляют собой природные полимеры. В одном варианте выполнения изобретения изолирующий материал составлен из NovoGel™. В дополнительных вариантах выполнения изобретения подходящие гидрогели включают полученные из поверхностно-активных полиолов (напр., Pluronic F-127), коллагена, гиалуроната, фибрина, альгината, агарозы, хитозана, их производных или комбинаций. В дополнительных вариантах выполнения изобретения подходящие гидрогели представляют собой синтетические полимеры. В других вариантах выполнения изобретения подходящие гидрогели включают производные поли(акриловой кислоты) и ее производных, поли(этиленоксида) и его сополимеров, поли(винилового спирта), полифосфазена и их комбинаций. В различных конкретных вариантах выполнения изобретения изолирующий материал выбирают из гидрогеля, NovoGel™, агароз, альгината, желатина, Matrigel™, гиалуронана, полоксамера, пептидного гидрогеля, поли(изопропил н-полиакриламида), полиэтиленгликоль диакрилата (ПЭГ-ДА), гидроксиэтил метакрилата, полидиметилсилоксана, полиакриламида, поли(молочной кислоты), кремния, шелка или их комбинаций.
В некоторых вариантах выполнения изобретения материал подложки содержит клетки до нахождения в биопринтере. В некоторых вариантах выполнения изобретения материал подложки представляет собой гидрогель, содержащий суспензию клеток. В некоторых вариантах выполнения изобретения материал подложки представляет собой гидрогель, содержащий смесь из более чем одного типа клеток.
Примеры использования материалов подложки
В некоторых вариантах выполнения изобретения материал подложки используется в качестве строительных единиц для построения биологической конструкции (напр., клеточной конструкции, ткани, органа и т.д.). В дополнительных вариантах выполнения изобретения единицу вспомогательного материала используют для определения и поддержания доменов пустоты клеточного материала (напр., промежуточных клеточных единиц) требуемой конструкции. В некоторых вариантах выполнения изобретения материал подложки способен принимать любую форму или размер.
Например, в соответствии с одним вариантом выполнения изобретения раствор NovoGel™ (первоначально в виде порошковой фазы смешали с буфером и водой) может быть нагрет до снижения его вязкости и перенесен в микропипетку с требуемым измерением (или в камеру требуемой формы при отрицательном смещении поршня). Раствор NovoGel™ в пипетке (или камере) может быть охлажден до комнатной температуры, например, путем принудительной подачи воздуха на внешнюю сторону пипетки (или камеры) или погружением микропипетки в емкость с холодной жидкостью, таким образом, чтобы он мог затвердеть в гель требуемой формы, т.е. материал подложки. Полученный материал подложки может быть распределен из пипетки или камеры во время строительства конкретной клеточной конструкции, ткани или органа. Смотри, напр., Фигуру 4.
В некоторых вариантах выполнения изобретения материал подложки используется для повышения жизнеспособности сконструированной ткани или органа после биопечати. В дополнительных вариантах выполнения изобретения материал подложки обеспечивает непосредственный контакт между тканью или органом и питательной средой через временную или полупостоянную решетку изолирующего материала (напр., вспомогательного материала). В некоторых вариантах выполнения изобретени ткань ограничена пористым или содержащим зазоры материалом. Непосредственный доступ по меньшей мере некоторых клеток ткани или органа к питательным веществам повышает жизнеспособность ткани или органа.
В дополнительных вариантах выполнения изобретения описанные в настоящем документе способы включают дополнительные и необязательные этапы для повышения жизнеспособности сконструированной ткани или органа, включая: 1) необязательное распределение базового слоя изолирующего материала (напр., вспомогательного материала) до размещения слипшихся многоклеточных агрегатов; 2) необязательное распределение периметра изолирующего материала; 3) биопечать клеток ткани определенной геометрии; и 4) распределение вытянутых тел (напр., цилиндров, лент и т.д.) изолирующего материала с нанесением на возникающую ткань рисунка, который вводит зазоры в изолирующий материал, такие как решетка, сетка или грид.
В некоторых вариантах выполнения изобретения рисунок наносимых зазоров распределен равномерно или по существу равномерно по поверхности ткани или органа. В других вариантах выполнения изобретения зазоры распределены неравномерно, в результате чего клетки ткани или органа подвергаются воздействию питательных веществ неравномерно. В неуниверсальных вариантах выполнения изобретения дифференцированный доступ к питательным веществам может быть использован для влияния на одно или более свойств ткани или органа. Например, может требоваться иметь клетки на одной поверхности биоотпечатанной клеточной конструкции, ткани или органа, пролиферирующие быстрее, чем клетки на другой поверхности. В некоторых вариантах выполнения изобретения воздействие питательных веществ на различные части ткани или органа может быть изменено в различные моменты времени, чтобы влиять на развитие ткани или органа с требуемым результатом.
В некоторых вариантах выполнения изобретения изолирующий материал удаляют в любое удобное время, в том числе, но не ограничиваясь, сразу после биопечати (напр., в пределах 10 минут), после биопечати (напр., через 10 минут), прежде чем клетки существенно прилипнут друг к другу, после того, как клетки существенно прилипнут друг к другу, прежде чем клетки образуют внеклеточную матрицу, после того, как клетки образуют внеклеточную матрицу, непосредственно перед использованием и тому подобное. В различных вариантах выполнения изобретения изолирующий материал удаляют любым подходящим способом. Например, в некоторых вариантах выполнения изобретения изолирующий материал иссекают, снимают с клеток, расщепляют или растворяют.
Способы и системы для калибровки положения картриджа биопринтера
Описанное в настоящем документе в некоторых вариантах выполнения изобретения представляет собой биопринтеры для изготовления тканей и органов. В некоторых вариантах выполнения изобретения картридж, прикрепленный к биопринтеру, включает биочернила и/или материал подложки. В некоторых вариантах выполнения изобретения биопринтер наносит биочернила или материал подложки в определенном рисунке и в специфических положениях для того, чтобы сформировать специфическую тканевую конструкцию. В некоторых вариантах выполнения изобретения картридж, содержащий биочернила, является одноразовым. В некоторых вариантах выполнения изобретения картридж извлекается из биопринтера с последующей экструзией, распределением или размещением содержимого. В некоторых вариантах выполнения изобретения к биопринтеру прикрепляют новый картридж.
Для изготовления комплексных структур описанные в настоящем документе биопринтеры распределяют биочернила и/или материал подложки из картриджа с подходящей погрешностью. В различных вариантах выполнения изобретения подходящие погрешности включают погрешности около ±5, 10, 20, 30, 40 или 50 мкм по любой оси. В некоторых вариантах выполнения изобретения описанные в настоящем документе биопринтеры распределяют биочернила и/или материал подложки из картриджа с погрешностью около ±20 мкм. Тем не менее, в некоторых вариантах выполнения изобретения из-за удаления и вставки картриджей положение печатающей головки (и, следовательно, картриджей) по отношению к тканевой конструкции меняется. Таким образом, существует потребность в способе точной калибровки положения печатающей головки, картриджа и распределительного отверстия по отношению к этапу печати, принимающей поверхности, ткани или органу.
В некоторых вариантах выполнения изобретения способ калибровки положения печатающей головки включает использование по меньшей мере одного лазера. В других вариантах выполнения изобретения способ калибровки положения печатающей головки включает использование первого и второго лазера.
В некоторых вариантах выполнения изобретения способ калибровки положения печатающей головки включает ручную (напр., визуальную) калибровку.
В некоторых вариантах выполнения изобретения способ калибровки положения печатающей головки включает ручную калибровку и лазерную калибровку.
В некоторых вариантах выполнения изобретения положение печатающей головки откалибровано по одной оси, где ось выбирается из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения положение печатающей головки откалибровано по двум осям, где оси выбраны из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения положение печатающей головки откалибровано по трем осям, где оси выбраны из оси х, оси y и оси z.
В некоторых вариантах выполнения изобретения калибровку выполняют с использованием по меньшей мере одного лазера. В дополнительных вариантах выполнения изобретения калибровку выполняют с использованием первого и второго лазера.
Способ для калибровки с использованием горизонтального лазера
Описанное в настоящем документе в некоторых вариантах выполнения изобретения представляет собой способы калибровки положения печатающей головки, содержащей распределительное отверстие. В некоторых вариантах выполнения изобретения описанный в настоящем документе способ дополнительно включает активацию лазера и генерирование по меньшей мере одного по существу стабильного и/или по существу стационарного лазерного луча, и где указанный лазерный луч расположен горизонтально по отношению к земле. Смотри Фигуру 1.
В некоторых вариантах выполнения изобретения способы включают калибровку положения печатающей головки вдоль по меньшей мере одной оси, где ось выбирается из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения способы включают калибровку положения печатающей головки вдоль по меньшей мере двух осей, где оси выбираются из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения способы включают калибровку положения печатающей головки вдоль по меньшей мере трех осей, где оси выбираются из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения способы включают (а) калибровку положения печатающей головки по оси y;
(b) калибровку положения печатающей головки по оси х; и/или (с) калибровку положения печатающей головки по оси z, где каждая ось соответствует оси с одноименным названием в декартовой системе координат. В некоторых вариантах выполнения изобретения калибровку выполняют с использованием по меньшей мере одного лазера. В некоторых вариантах выполнения изобретения калибровку выполняют с использованием первого и второго лазера.
В некоторых вариантах выполнения изобретения калибровка положения печатающей головки вдоль оси y - включает: (а) позиционирование печатающей головки так, что печатающая головка является (i) расположенной в первом октанте y, и (ii) распределяющее отверстие расположено ниже верхнего порога лазерного луча, (b) перемещение печатающей головки в направлении лазерного луча и остановку указанного перемещения, как только лазерный луч прервется печатающей головкой, где положение, при котором лазерный луч прервется печатающей головкой, является первым положением y; (с) повторное позиционирование печатающей головки так, чтобы печатающая головка находилась во втором октанте y и распределительное отверстие было ниже верхнего порога лазерного луча, (d) перемещение печатающей головки в направлении лазерного луча и остановку указанного перемещения, как только лазерный луч прервется печатающей головкой, где положение, при котором лазерный луч прервется, является вторым положением y; (е) и расчета средней точки между первым положением у и вторым положением y.
В некоторых вариантах выполнения изобретения калибровка положения печатающей головки вдоль оси х включает: (а) позиционирование печатающей головки (i) в средней точке между первым положением y и вторым положением y и (ii) за пределами порога лазерного датчика, и (b) перемещение печатающей головки в направлении порога датчика и остановку указанного перемещения, как только печатающая головка войдет в контакт с порогом датчика; где положение, при котором печатающая головка входит в контакт с датчиком, увеличенное на половину ширины печатающей головки, является положением х.
В некоторых вариантах выполнения изобретения калибровки положение печатающей головки вдоль оси y - включает: (а) размещение печатающей головки так, что лазерный луч может измерить точное местоположение одной стороны печатающей головки; (b) позиционирование печатающей головки так, что лазерный луч может измерить точное местоположение противоположной стороны печатающей головки; (с) и расчет средней точки расположения печатающей головки в отношении позиции лазера во время каждого измерения и измеренных расстояний.
В некоторых вариантах выполнения изобретения калибровка положения печатающей головки вдоль оси х - включает: (а) позиционирование печатающей головки так, что лазерный луч может измерить точное местоположение одной стороны печатающей головки; (b) позиционирование печатающей головки так, что лазерный луч может измерить точное местоположение противоположной стороны печатающей головки;
(с) и расчет средней точки расположения печатающей головки в отношении позиции лазера во время каждого измерения и измеренных расстояний.
В некоторых вариантах выполнения изобретения калибровка положения печатающей головки вдоль оси z включает: (а) позиционирование печатающей головки так, чтобы распределительное отверстие было расположено над лазерным лучом; и (b) перемещение печатающей головки в направлении лазерного луча и остановку указанного перемещения, как только лазерный луч прервется печатающей головкой, где положение, при котором лазерный луч прервется, является положением z.
Способ для калибровки с использованием вертикального лазера Описанное в настоящем документе в некоторых вариантах выполнения изобретения является способами калибровки положения печатающей головки, содержащей распределительное отверстие. В некоторых вариантах выполнения изобретения описанный в настоящем документе способ дополнительно включает активацию лазера и генерирование по меньшей мере одного по существу стабильного и/или по существу стационарного лазерного луча, и где указанный лазерный луч расположен вертикально по отношению к земле. Смотри Фигуру 2.
В некоторых вариантах выполнения изобретения способы включают калибровку положения печатающей головки вдоль по меньшей мере одной оси, где ось выбирается из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения способы включают калибровку положения печатающей головки вдоль по меньшей мере двух осей, где оси выбираются из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения способы включают калибровку положения печатающей головки вдоль по меньшей мере трех осей, где оси выбираются из оси х, оси y и оси z.
В некоторых вариантах выполнения изобретения способы включают (а) калибровку положения печатающей головки по оси y; (b) калибровку положения печатающей головки по оси х; (с) калибровку положения печатающей головки по оси z-, где каждая ось соответствует оси с одноименным названием в декартовой системе координат.
В некоторых вариантах выполнения изобретения калибровка положения печатающей головки вдоль оси y включает: (а) позиционирование печатающей головки так, что печатающая головка является (i) расположенной в первом октанте y, и (И) распределяющее отверстие расположено вне порога лазерного датчика; (b) перемещение печатающей головки в направлении лазерного луча и остановку указанного перемещения, как только лазерный луч прервется печатающей головкой, где положение, при котором лазерный луч прервется печатающей головкой, является первым положением y; (с) повторное позиционирование печатающей головки так, чтобы печатающая головка находилась во втором октанте y, и распределительное отверстие было вне порога лазерного датчика; (d) перемещение печатающей головки в направлении лазерного луча и остановку указанного перемещения, как только лазерный луч прервется печатающей головкой, где положение, при котором лазерный луч прервется, является вторым положением y; (е) и расчет средней точки между первым положением y и вторым положением y.
В некоторых вариантах выполнения изобретения калибровка положения печатающей головки вдоль оси х - включает: (а) размещение печатающей головки (i) в средней точке между первым положением y и вторым положением y и (ii) за пределами порога лазерного датчика; и (b) перемещение печатающей головки в направлении порога датчика и остановку указанного перемещения, как только печатающая головка войдет в контакт с порогом датчика; где положение, при котором печатающая головка войдет в контакт с датчиком, увеличенное на половину ширины печатающей головки, является положением х.
В некоторых вариантах выполнения изобретения калибровка положения печатающей головки вдоль оси z включает: (а) позиционирование печатающей головки так, чтобы распределительное отверстие было расположено над лазерным лучом так, чтобы она была прямо за диапазоном порога лазерного датчика; и (b) снижение печатающей головки до достижения порога датчика, где положение, при котором достигается порог лазерного датчика, является положением z. В некоторых вариантах выполнения изобретения этапы (а) и (b) повторяются несколько во множестве точек печатающей головки и измеренные высоты усредняются для определения положения z.
В некоторых вариантах выполнения изобретения калибровка положения печатающей головки вдоль оси z включает: (а) позиционирование печатающей головки так, что лазерный луч может измерить точное местоположение одной или нескольких точек на нижней части печатающей головки; (b) вычисление абсолютного или среднего расположения печатающей головки на основе положения лазера и известного измеренного расстояния.
Способ для калибровки с использованием вертикального и горизонтального Лазеров
Описанное в настоящем документе в некоторых вариантах выполнения изобретения представляет собой способы калибровки положения печатающей головки, содержащей распределительное отверстие, где печатающая головка прикреплена к биопринтеру, включающие калибровку положения печатающей головки вдоль по меньшей мере одной оси, где ось выбирают из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения способ включает калибровку положения печатающей головки вдоль по меньшей мере двух осей, где оси выбирают из оси х, оси y и оси z. В некоторых вариантах выполнения изобретения способ включает калибровку положения печатающей головки вдоль по меньшей мере трех осей, где оси выбирают из оси х, оси y и оси z.
В некоторых вариантах выполнения изобретения способы включают (а) калибровку положения печатающей головки вдоль оси y, (b) калибровку положения печатающей головки вдоль оси х; и (с) калибровку положения печатающей головки вдоль оси z; где каждая оси соответствует оси с одноименным названием в декартовой системе координат.
В некоторых вариантах выполнения изобретения калибровка включает использование первого и второго лазера. В некоторых вариантах выполнения изобретения первый лазер представляет собой вертикальный лазера и второй лазер представляет собой горизонтальный лазер.
Система для калибровки с использованием лазера
Описанное в настоящем документе в некоторых вариантах выполнения изобретения представляет собой системы для калибровки положения картриджа, содержащего распределительное отверстие, где картридж прикреплен к биопринтеру, указанная система включает: средство для калибровки положения картриджа вдоль по меньшей мере одной оси, где ось выбирают из оси y, оси х и оси z.
Кроме того, описанное в настоящем документе в некоторых вариантах выполнения изобретения представляет собой системы для калибровки положения печатающей головки, содержащей распределительное отверстие, где печатающая головка прикреплена к биопринтеру, указанная система включает: средство для калибровки положения печатающей головки вдоль оси х, средство для калибровки положения печатающей головки вдоль оси y; и средство для калибровки положения печатающей головки вдоль оси z.
В некоторых вариантах выполнения изобретения система для калибровки положения печатающей головки содержит средство для калибровки печатающей головки вдоль оси х, оси y и оси z. В некоторых вариантах выполнения изобретения средство для калибровки печатающей головки вдоль оси х, оси y и оси z представляет собой лазерную юстировку, оптическую юстировку, механическую юстировку, пьезоэлектрическую юстировку, магнитную юстировку, юстировку электрическим полем или емкостную юстировку, ультразвуковую юстировку или их комбинации.
В некоторых вариантах выполнения изобретения система для калибровки положения печатающей головки содержит средство для калибровки печатающей головки вдоль оси х, оси y и оси z. В некоторых вариантах выполнения изобретения средство для калибровки печатающей головки вдоль оси х, оси y и оси z представляет собой лазерную юстировку. В некоторых вариантах выполнения изобретения средство лазерной юстировки содержит по меньшей мере один лазер. В некоторых вариантах выполнения изобретения средство лазерной юстировки содержит множество лазеров.
В некоторых вариантах выполнения изобретения средство лазерной юстировки означает, что оно имеет любую подходящую точностью. В различных вариантах выполнения изобретения подходящие точности включают около ±5, 10, 20, 30, 40 или 50 мкм по любой оси. В некоторых вариантах выполнения изобретения средство лазерной юстировки имеет точность до ±40 мкм по вертикальной оси и ±20 мкм по горизонтальной оси.
В некоторых вариантах выполнения изобретения траектория лазера не прерывается между источником лазера и точкой измерения. В некоторых вариантах выполнения изобретения траектория лазера изменяется на величину вплоть до 179° за счет использования отражающей поверхности или оптических линз. В некоторых вариантах выполнения изобретения траектория лазера меняется на 90°. В некоторых вариантах выполнения изобретения горизонтальный лазерный луч используется для измерения в вертикальной траектории отклонением с использованием отражающей поверхности. В некоторых вариантах выполнения изобретения вертикальной лазерный луч используется для измерения в горизонтальной траектории отклонением с использованием отражающей поверхности.
ПРИМЕРЫ
Следующие конкретные примеры следует рассматривать только как иллюстративные и не ограничивающие остальное описание каким-либо образом. Без дальнейших уточнений считается, что специалист в данной области техники может на основании приведенного здесь описания использовать настоящее изобретение в его наиболее полном объеме. Все публикации, процитированные здесь, включены в качестве отсылки во всей их полноте. Ссылки на них свидетельствуют о доступности и публичном распространении такой информации.
Пример 1: HASMC-HAEC смешанные клеточные цилиндры
Культура клеток
Клетки гладкой мускулатуры: Первичные клетки гладкой мускулатуры аорты человека (HASMC) выдерживали и выращивали в низко глюкозной модифицированной по способу Дульбекко среде Игла (DMEM; Invitrogen Corp., Carlsbad, CA) с добавлением 10% фетальной бычьей сыворотки (FBS), 100 ЕД/мл пенициллина, 0,1 мг/мл стрептомицина, 0,25 мкг/мл амфотерицина В, 0,01М HEPES (все от Invitrogen Corp., Carlsbad, CA), 50 мг/л пролина, 50 мг/л глицина, 20 мг/л аланина, 50 мг/л аскорбиновой кислоты и 3 мкг/л CuSO4 (все от Sigma, St. Louis, МО) при 37°C и 5% СО2. Во всех исследованиях использовали конфлюэнтные культуры HASMC между пассажами 4 и 8.
Эндотелиальные клетки: Первичные эндотелиальные клетки аорты человека (НАЕС) выдерживали и выращивали в Medium 200 с добавлением 2% FBS, 1 мкг/мл гидрокортизона, 10 нг/мл эпидермального фактора роста человека, 3 нг/мл основного фактора роста фибробластов, 10 мкг/мл гепарина, 100 ЕД/мл пенициллина, 0,1 мг/мл стрептомицина и 0,25 мкг/мл амфотерицина В (все от Invitrogen Corp., Carlsbad, CA). Клетки выращивали на обработанных культурой ткани, покрытой желатином, (из свиной сыворотки; Sigma, St. Louis, МО) колбах при 37°C и 5% СО2. Во всех исследованиях использовали конфлюэнтные культуры НАЕС между пассажами 4 и 8.
Форма из NovoGel™
Получение 2% масс/об раствора NovoGel™: 1 г NovoGel™ с низкой температурой плавления растворяли в 50 мл физиологического раствора, забуференного фосфатом Дульбекко (DPBS). Вкратце, DPBS и NovoGel™ нагревали до 85°C на горячей плитке при постоянном перемешивании до полного растворения NovoGel™. Раствор NovoGel™ стерилизовали паром при 125°C в течение 25 минут. Раствор NovoGel™ оставался в жидкой фазе тех пор, пока температура поддерживалась выше 66,5°C. Ниже этой температуры происходит фазовый переход, вязкость раствора NovoGel™ увеличивается, и NovoGel™ образует твердый гель.
Получение формы из NovoGel™: Форму из NovoGel™ для инкубации клеточных цилиндров изготавливали с использованием формы Teflon®, которая соответствует 10 см чашке Петри. Вкратце, форму Teflon® предварительно стерилизовали, используя 70%-ный раствор этанола, и подвергали форму ультрафиолетовому излучению в течение 45 минут. Стерилизованную форму помещали на верхнюю часть 10 см чашки Петри (VWR International LLC, West Chester, PA) и надежно закрепляли. Этот блок (форма Teflon® + чашка Петри) поддерживали вертикально и в пространство между формой Teflon® и чашкой Петри выливали 45 мл предварительно подогретого стерильного 2% раствора NovoGel™. Блок затем помещали горизонтально при комнатной температуре на 1 час для завершения полного превращения NovoGel™ в гель. После превращения в гель принт Teflon® удаляли и форму NovoGel™ дважды промывали DPBS. Затем добавляли к форме NovoGel™ 17,5 мл культуральной среды HASMC.
Цилиндры HASMC-HAEC
Изготовление смешанных клеточных цилиндров HASMC-HAEC: Для получения смешанных клеточных цилиндров HASMC и НАЕС собирали отдельно и затем смешивали в заранее определенных соотношениях. Вкратце, культуральную среду удаляли из колб с конфлюэнтной культурой и клетки промывали DPBS (1 мл/5 см2 области роста). Клетки отделяли от поверхности колб с культурой инкубированием в присутствии трипсина (1 мл/15 см2 области роста) в течение 10 минут.HASMC отделяли с использованием 0,15% трипсина, в то время как НАЕС отделяли с использованием 0,1% трипсина. После инкубирования в колбы добавляли подходящую культуральную среду (2Х объем относительно объема трипсина). Клеточную суспензию центрифугировали при 200g в течение 6 минут с последующим полным удалением надосадочной жидкости. Сгусток клеток ресуспендировали в соответствующей культуральной среде и подсчитывали с использованием гемоцитометра. Подходящие объемы HASMC и НАЕС объединяли, получая смешанные клеточные суспензии, содержащие 5, 7,5, 10, 12,5 и 15% НАЕС (в % от общего количества клеток). Смешанные клеточные суспензии центрифугировали при 200g в течение 5 минут с последующим полным удалением надосадочной жидкости. Смешанные сгустки клеток ресуспендировали в 6 мл культуральной среды HASMC и переносили в 20 мл стеклянные флаконы с последующим инкубированием на орбитальном шейкере со скоростью 150 об/мин в течение 60 минут и при 37°C и 5% CO2. Это позволяет клеткам агрегировать друг с другом и инициирует слипание клеток. После инкубирования клеточную суспензию переносили в 15 мл центрифужную пробирку и центрифугировали при 200g в течение 5 минут. После удаления надосадочной среды сгусток клеток ресуспендировали в 400 мкл культуральной среды HASMC и пипетировали вверх и вниз несколько раз, чтобы убедиться, что все кластеры клеток были сломаны. Клеточную суспензию переносили в 0,5 мл микроцентрифужную пробирку, помещенную внутрь 15 мл центрифужной пробирки, с последующим центрифугированием при 2000g в течение 4 минут для образования высокоплотного и компактного сгустка клеток. Надосадочную среду отсасывали и клетки переносили в капиллярные трубки (OD 1,0 мм, ID 0,5 мм, L 75 мм; Drummond Scientific Со, Broomall, PA) аспирацией так, чтобы получить клеточные цилиндры 50 мм в длину. Клеточную пасту внутри капилляров инкубировали в среде HASMC в течение 20 минут при 37°C и 5% СО2. Затем клеточные цилиндры из капиллярных трубок размещали в канавки формы NovoGel™ (покрытой средой HASMC), используя поршень, снабженный капиллярами. Клеточные цилиндры инкубировали в течение 24 и 48 часов при 37°C и 5% CO2 .
Пример 2: Многослойные сосудистые трубки
Культура клеток
Клетки гладкой мускулатуры: Первичные клетки гладкой мускулатуры аорты человека (HASMC; GIBCO) выдерживали и выращивали в низко глюкозной модифицированной по способу Дульбекко среде Игла (DMEM) с добавлением 10% фетальной бычьей сыворотки (FBS), 100 ЕД/мл пенициллина, 0,1 мг/мл стрептомицина, 0,25 мкг/мл амфотерицина В, 0,01М HEPES (все от Invitrogen Corp., Carlsbad, CA), 50 мг/л пролина, 50 мг/л глицина, 20 мг/л аланина, 50 мг/л аскорбиновой кислоты и 3 мкг/л CuSO4 (все от Sigma, St. Louis, МО) при 37°C и 5% СО2. Во всех исследованиях использовали конфлюэнтные культуры HASMC между пассажами 4 и 8.
Эндотелиальные клетки: Первичные эндотелиальные клетки аорты человека (НАЕС) выдерживали и выращивали в Medium 200 с добавлением 2% FBS, 1 мкг/мл гидрокортизона, 10 нг/мл эпидермального фактора роста человека, 3 нг/мл основного фактора роста фибробластов, 10 мкг/мл гепарина, 100 ЕД/мл пенициллина, 0,1 мг/мл стрептомицина и 0,25 мкг/мл амфотерицина В (все от Invitrogen Corp., Carlsbad, СА). Клетки выращивали на обработанных культурой тканей покрытых желатином (из свиной сыворотки) колбах при 37°C и 5% СО2. Во всех исследованиях использовали конфлюэнтные культуры НАЕС между пассажами 4 и 8.
Фибробласты: Первичные фибробласты кожи человека (HDF) выдерживали и выращивали в Medium 106 с добавлением 2% FBS, 1 мкг/мл гидрокортизона, 10 нг/мл эпидермального фактора роста человека, 3 нг/мл основного фактора роста фибробластов, 10 мкг/мл гепарина, 100 ЕД/мл пенициллина и 0,1 мг/мл стрептомицина (все от Invitrogen Corp., Carlsbad, CA) при 37°C и 5% СО2. Во всех исследованиях использовали конфлюэнтные культуры HDF между пассажами 4 и 8.
Растворы и форма NovoGel™
Получение 2% и 4% (масс/об) раствора NovoGel™: 1 г или 2 г (для 2% или 4% соответственно) NovoGel™ с низкой температурой плавления (Ultrapure LMP) растворяли в 50 мл физиологического раствора, забуференного фосфатом Дульбекко (DPBS). Вкратце, DPBS и NovoGel™ нагревали до 85°C на горячей плитке при постоянном перемешивании до полного растворения NovoGel™. Раствор NovoGel™ стерилизовали паром при 125°C в течение 25 минут. Раствор NovoGel™ остается в жидкой фазе тех пор, пока температура поддерживается выше 66,5°C. Ниже этой температуры происходит фазовый переход, вязкость раствора NovoGel™ увеличивается, и NovoGel™ образует твердый гель.
Получение формы из NovoGel™: форму из NovoGel™ изготовливали для инкубирования клеточных цилиндров с использованием формы Teflon®, которая соответствует 10 см чашке Петри. Вкратце, форму Teflon® предварительно стерилизовали, используя 70%-ный раствор этанола, и подвергали форму ультрафиолетовому излучению в течение 45 минут. Стерилизованную форму помещали на верхнюю часть 10 см чашки Петри и надежно закрепляли. Этот блок (форма Teflon® + чашка Петри) поддерживали вертикально и в пространство между формой Teflon® и чашкой Петри выливали 45 мл предварительно подогретого стерильного 2% раствора NovoGel™. Блок затем помещали горизонтально при комнатной температуре на 1 час для завершения полного превращения NovoGel™ в гель. После превращения в гель, принт Teflon® удаляли и форму NovoGel™ дважды промывали DPBS. Затем либо к форме NovoGel™ добавляли 17,5 мл культуральной среды HASMC для инкубирования смешанных клеточных цилиндров HASMC-HAEC, либо к форме NovoGel™ добавляли 17,5 мл культуральной среды HDF для инкубирования клеточных цилиндров HDF.
Клеточные цилиндры
Изготовление смешанных клеточных цилиндров HASMC-HAEC: Для получения смешанных клеточных цилиндров HASMC и НАЕС собирались отдельно и затем смешивались в заранее определенных соотношениях. Вкратце, культуральную среду удаляли из колб с конфлюэнтной культурой, и клетки промывали DPBS (1 мл/5 см2 области роста). Клетки отделяли от поверхности колб с культурой инкубированием в присутствии трипсина (1 мл/15 см области роста) в течение 10 минут. HASMC отделяли с использованием 0,15% трипсина, в то время как НАЕС отделяли с использованием 0,1% трипсина. После инкубирования в колбы добавляли соответствующую культуральную среду (2Х объем относительно объема трипсина). Суспензию клеток центрифугировали при 200g в течение 6 минут с последующим полным удалением надосадочной жидкости. Сгусток клеток ресуспендировали в соответствующей культуральной среде и подсчитывыали с использованием гемоцитометра. Соответствующие объемы HASMC и НАЕС объединяли, получая смешанные клеточные суспензии, содержащие 15% НАЕС и оставшиеся 85% HASMC (в % от общего количества клеток). Смешанную клетосную суспензию центрифугировали при 200g в течение 5 минут с последующим полным удалением надосадочной жидкости. Смешанные сгустки клеток ресуспендировали в 6 мл культуральной среды HASMC и переносили в 20 мл стеклянные флаконы с последующим инкубированием на орбитальном шейкере со скоростью 150 об/мин в течение 60 минут и при 37°C и 5% СО2. Это позволяет клеткам агрегировать друг с другом и инициирует слипание клеток. После инкубирования клеточную суспензию переносили в 15 мл центрифужную пробирку и центрифугировали при 200g в течение 5 минут. После удаления надосадочной среды сгусток клеток ресуспендировали в 400 мкл культуральной среды HASMC и пипетировали вверх и вниз несколько раз, чтобы убедиться, что все кластеры клеток были сломаны. Клеточную суспензию переносили в 0,5 мл микроцентрифужную пробирку, помещенную внутрь 15 мл центрифужной пробирки, с последующим центрифугированием при 2000g в течение 4 минут с образованием высокоплотного и компактного сгустка клеток. Надосадочную среду отсасывали, и клетки переносили в капиллярные трубки (OD 1,0 мм, ID 0,5 мм, L 75 мм) аспирацией так, чтобы получить клеточные цилиндры 50 мм в длину. Клеточную пасту внутри капилляров инкубировали в среде HASMC в течение 20 минут при 37°C и 5% СО2. Затем клеточные цилиндры из капиллярных трубок размещали в канавках формы NovoGel™ (покрытой средой HASMC), используя поршень, которым снабжены капилляры. Клеточные цилиндры инкубировали в течение 24 часов при 37°C и 5% CO2.
Изготовление клеточных цилиндров HDF: Цилиндры HDF получали, используя способ, аналогичный получению смешанных клеточных цилиндров HASMC-HAEC. Вкратце, культуральную среду удаляли из колб с конфлюэнтной культурой HDF, и клетки промывали DPBS (1 мл/5 см области роста). Клетки отделяли от поверхности колб с культурой инкубированием в присутствии трипсина (0,1%; 1 мл/15 см2 области роста) в течение 10 минут. После инкубирования в колбы добавляли культуральную среду HDF (2Х объем относительно объема трипсина). Суспензию клеток центрифугировали при 200g в течение 6 минут с последующим полным удалением надосадочной жидкости. Сгустки клеток ресуспендировали в 6 мл культуральной среды HDF и переносили в 20 мл стеклянные флаконы с последующим инкубированием на орбитальном шейкере со скоростью 150 об/мин в течение 75 минут и при 37°C и 5% СО2. После инкубирования клеточную суспензию переносили в 15 мл центрифужную пробирку и центрифугировали при 200g в течение 5 минут. После удаления надосадочной среды сгусток клеток ресуспендировали в 400 мкл культуральной среды HDF и пипетировали вверх и вниз несколько раз, чтобы убедиться, что все кластеры клеток были сломаны. Клеточную суспензию перенесли в 0,5 мл микроцентрифужную пробирку, помещенную внутрь 15 мл центрифужной пробирки, с последующим центрифугированием при 2000g в течение 4 минут с образованием высокоплотного и компактного сгустка клеток. Надосадочную среду отсасывали, и клетки переносили в капиллярные трубки (OD 1,0 мм, ID 0,5 мм, L 75 мм) аспирацией так, чтобы получить клеточные цилиндры 50 мм в длину. Клеточную пасту внутри капилляров инкубировали в среде HDF в течение 20 минут при 37°C и 5% CO2. Затем клеточные цилиндры из капиллярных трубок размещали в канавках формы NovoGel™ (покрытой средой HDF). Клеточные цилиндры инкубировали в течение 24 часов при 37°C и 5% CO2.
Изготовление многослойных сосудистых трубок
Получение основания NovoGel™: Основание NovoGel™ изготавливали путем распределения 10 мл предварительно нагретого (>40°C) NovoGel™ (2% масс/об) в 10 см чашку Петри. Сразу после распределения NovoGel™ был равномерно размещен таким образом, чтобы покрыть все основание чашки и образовать равномерный слой. Чашку Петри инкубировали при комнатной температуре в течение 20 минут, чтобы полностью дать NovoGel™ превратиться в гель.
Многослойная сосудистая трубка: Сосудистые трубки, состоящие из внешнего слоя HDF и внутреннего слоя HASMC-HAEC, изготавливали с использованием цилиндров HDF и смешанных клеточных цилиндров HASMC-HAEC. Применяли геометрическое расположение, как показано на Фигуре 4. Вкратце, в конце 24-часового периода инкубирования зрелые цилиндры HDF и HASMC-HAEC отсасывали назад в капиллярные трубки и помещали в подходящую культуральную среду до дальнейшего использования. Вспомогательную структуру, состоящую из стержней NovoGel™, получали следующим образом: предварительно нагретый 2% NovoGel™ всасывали в капиллярные трубки (L=50 мм) и быстро охлаждали в холодном растворе PBS (4°C). Гелевые цилиндры NovoGel™ длиной 5 см размещали из капилляра (используя поршень) и выкладывали прямо на основание NovoGel™. Второй цилиндр NovoGel™ присоединяли к первому, и процесс повторяли до тех пор, пока 10 цилиндров NovoGel™ не были размещены с формированием первого слоя. В этот момент над цилиндрами NovoGel™ распыляли 20 мкл PBS, чтобы поддерживать их влажными. Далее шесть цилиндров NovoGel™ были размещены на верхней части слоя 1 в положениях, как показано на Фигуре 4 (слой 2). Три цилиндра HDF затем были размещены в положениях 4, 5 и 6 для завершения слоя 2. После распределения каждого цилиндра HDF на верхнюю часть размещенного цилиндра распределяли 40 мкл культуральной среды HDF для облегчения размещения последующего цилиндра, а также чтобы предотвратить обезвоживание клеточных цилиндров. Следующие цилиндры NovoGel™ для слоя 3 размещали вслед за цилиндрами HDF в положениях 3 и 6. После повторного увлажнения структуры культуральной средой HDF, укладывали смешанные цилиндры HASMC-HAEC в положения 4 и 5. Затем на верхнюю часть клеточных цилиндров распределяли 40 мкл среды HASMC и 40 мкл среды HDF. Слой 4 был сформирован размещением цилиндров NovoGel™ в положения 1 и 7, цилиндров HDF в положения 2 и 6, смешанных цилиндров HASMC-HAEC в положения 3 и 5 и, наконец, 4% цилиндра NovoGel™ в положение 4. Слои 5, 6 и 7 были завершены аналогично укладкой цилиндров NovoGel™, затем цилиндров HDF и, наконец, цилиндров HASMC-HAEC в положения, показанные на Фигуре 4. Как только вся конструкция была завершена, над каждым концом конструкции распределили 0,5 мл теплого NovoGel™ и позволили превратиться в гель при комнатной температуре в течение 5 минут. После гелеобразования того NovoGel™ добавили в чашку Петри 30 мл среды HASMC (чтобы убедиться, что вся конструкция полностью погружена). Конструкцию инкубировали в течение 24 часов при 37°C и 5% CO2, чтобы обеспечить слияние между клеточными цилиндрами.
По истечении 24 часов из сплавленной многослойной сосудистой трубки удаляли окружающую вспомогательную структуру NovoGel™.
Пример 3: Биопринтер
Осуществляли сборку биопринтера. Биопринтер содержал печатную головку, имеющую захват цанговым патроном для удерживания картриджа, и поршень для распределения содержимого картриджа. Использованные картриджи представляли собой стеклянные микрокапиллярные трубки длиной 75-85 мм. Новую капиллярную трубку загружали каждый раз, как требовались биочернила или материал подложки.
Для печати структур требовалась распределительная позиция с воспроизводимостью±20 мкм во время процесса печати, т.е. когда новые капилляры загружались в печатающую головку. Для того чтобы сохранить воспроизводимость всех загруженных капиллярных трубок по отношению к одной и той же точке в направлениях х, y и z, биопринтер содержал лазерную систему калибровки для калибровки положения микрокапиллярной трубки. Система лазерной калибровки калибровала положение всех концов капилляров к единому исходному месту. Все шаги печати делались относительно этого исходного положения.
Все три оси (х, y и z-оси) калибровали посредством использования одиночного лазерного датчика измерения расстояния. Система состояла из лазерного датчика и лазерного луча. Порог чувствительности датчика являлся максимальным расстоянием обнаружения лазерного сенсора. Датчик был сконфигурирован так, чтобы игнорировать все сигналы, которые были дальше, чем предварительно определенный порог. Датчик использовал триангуляцию для определения расстояния до объекта (конца капилляра). Лазерный сенсор был ориентирован лучом, направленным вертикально вверх (+z-ось).
Калибровка вертикальным Лазером
Для калибровки по оси х: Конец капилляра перемещали в диапазоне лазерного датчика, концом влево (-х) от лазерного луча. Капилляр перемещали в направлении +х до тех пор, пока датчик не обнаружит край капилляра, и эту позицию записывали. Описанные выше этапы повторяли с противоположной стороны (т.е., конец позиционировали вправо (+х) от луча лазера и перемещали в направлении -х до тех пор, пока датчик не обнаружит край капилляра). Положения из обоих этапов усредняли для расчета средней точки капилляра. Необязательно, вышеуказанный процесс повторяли для различных положений y и усредняли рассчитанные средние точки.
Для калибровки по оси y: Приведенные выше процедуры (для оси х) повторяли для оси y.
Для калибровки по оси z: Конец капилляра перемещали над лучом датчика так, чтобы луч попадал на нижнюю поверхность капилляра, и конец был прямо за порогом диапазона датчика. Капилляр снижали до достижения порогового значения датчика, и это положение записывали как положение z. Необязательно, вышеуказанные этапы повторяли в нескольких точках на поверхности конца капилляра и усредняли измеренные высоты.
Калибровка горизонтальным лазером
Для калибровки по оси y: Капилляр перемещали так, чтобы конец был чуть ниже высоты лазерного луча, и капилляр был удален в одну сторону (в направлении y). Капилляр перемещали в направлении у по отношению к лазеру. Капилляр останавливали, когда лазерный датчик обнаруживал луч, отраженный от капилляра, и это положение записывали. Описанные выше этапы повторяли с капилляром на другой стороне лазера и перемещали в направлении -y). Среднюю точку из вышеуказанных этапов записывали как положение y.
Для калибровки по оси х: Используя результаты калибровки по оси y, ось y перемещали таким образом, чтобы лазер был отцентрирован на капилляре. Капилляр перемещали мимо порогового значения датчика и перемещали по направлению к датчику. Капилляр останавливали, как только капилляр пересекал пороговое значение датчика, и выходной сигнал датчика изменялся. Это положение, плюс 1/2 ширины капилляра (из калибровки y) записывали как положение х.
Для калибровки по оси z: Капилляр поднимали от положения х до тех пор, пока он не вышел из луча лазера. Конец капилляра перемещали вниз в направлении лазерного луча, и останавливали, как только луч лазера прерывался (с использованием того же процесса, что и для оси y). Эту позицию записывали как положение z.
Заправка капилляров
Перед печатью из капилляра, биочернила или материал подложки были заправлены внутрь капилляра так, что биочернила или материал подложки начинали бы печататься с самого кончика капилляра. Для заправки капилляра использовали лазер для калибровки. Конец капилляра перемещали непосредственно над лазерным лучом, с лучом, центрированным по оси y. Кончик был на 20-100 мкм выше лазерного луча. Поршень для распределения в печатающей головке снижали до тех пор, пока биочернила или материал подложки не начинали выходить из кончика капилляра и прерывать лазерный луч. Высвобожденные биочернила или материал подложки всасывали обратно в капиллярную трубку при движении поршня в обратном направлении (20-100 мкм). Капилляр затем заправляли и готовили к распределению.
Очистка капилляров с NovoGel™
В качестве вспомогательного материала использовали NovoGel™. Для удаления избытка NovoGel™, прилипшего к наружной поверхности капиллярной трубки, и для того, чтобы избежать влияния избыточного NovoGel™ на качество печати, избыток NovoGel™ удаляли. Функция стирки была интегрирована в объем сосуда с NovoGel™. Объем сосуда с NovoGel™ был снабжен стандартным медицинским флаконом с открытой крышкой для прикрепления мембраны. Мембрана была устроена со сквозным разрезом в центре силикона толщиной 1-2 мм. При погружении капилляра в готовый к использованию сосуд NovoGel™ через мембрану и отсасывании NovoGel™, избыток NovoGel™ стирался с капилляра по мере того, как он выходил из сосуда и оставался в объеме сосуда.
Печать сосудистой структуры
Осуществляли сборку биопринтера и картриджа как указано выше. Биопринтер имел платформу, имеющую чашку Петри для получения структур, создаванных биопринтером. Чашка Петри была покрыта NovoGel™.
Двумерное представление (смотри, напр., Фигуру 4) сосудистой структуры было введено пользователем в программное обеспечение в компьютер, который был соединен с биопринтером. Двумерное представление сосудистой структуры состояло из стержней смешанных клеточных цилиндров HASMC-HAEC, цилиндров HDF и стержней NovoGel™, определяющих пустоты сосудистой структуры и окружающих сосудистую структуру. Смешанные клеточные цилиндры HASMC-HAEC и клеточные цилиндры HDF получали, как в Примере 1, и всасывали в капиллярные трубки для вставки в цанговый патрон печатающей головки. Альтернативно, капиллярные трубки загружали в печатающую головку и погружали в объем сосуда с NovoGel™, и NovoGel™ всасывали в капиллярные трубки. Капиллярные трубки калибровали с использованием вертикальной лазерной системы калибровки.
Когда команды от программного обеспечения передавались биопринтеру, биопринтер печатал трехмерную структуру, чередуя стержни HASMC-HAEC, стержни HDF и стержни NovoGel™, на чашку Петри, в заранее определенных положениях. Смотри Пример 2. После того как каждый стержень укладывали на чашку Петри, стержень смачивали небольшим количеством культуральной среды. Как только вся конструкция была завершена, на каждый конец конструкции распределяли теплый NovoGel™ и позволяли превращаться в гель при комнатной температуре, и в чашку Петри добавляли клеточную культуральную среду для погружения всей конструкции. Конструкцию затем инкубировали при 37°C и 5% СО2, чтобы обеспечить слияние между клеточными цилиндрами. По истечении времени инкубирования окружающую вспомогательную структуру NovoGel™ удаляли из слитой многослойной сосудистой трубки.
Хотя изобретение было описано в связи с конкретными его вариантами, должно быть понятно, что изобретательская методология применима к дальнейшим модификациям. Эта патентная заявка охватывает любые вариации, применения или адаптации изобретения, следующие, в общем, принципам изобретения и включает такие отклонения от настоящего описания, которые находятся в пределах известной или обычной практики в данной области техники, к которой относится изобретение, и которые могут быть применены к существенным признакам, ранее здесь изложенным и следующим из объема прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЛАТФОРМА ДЛЯ ИНЖЕНЕРИИ ИМПЛАНТИРУЕМЫХ ТКАНЕЙ И ОРГАНОВ И СПОСОБЫ СОЗДАНИЯ (БИОФАБРИКАЦИИ) ЭТИХ ТКАНЕЙ И ОРГАНОВ | 2012 |
|
RU2623303C2 |
| ИСКУССТВЕННЫЕ ТКАНИ ПЕЧЕНИ, МАТРИКСЫ ИСКУССТВЕННЫХ ТКАНЕЙ И СПОСОБЫ ИХ ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2625016C2 |
| БИОПРИНТЕР | 2014 |
|
RU2558290C1 |
| Способ создания предполимеризационной морфогенетической матрицы | 2022 |
|
RU2791073C1 |
| Способ получения биочернил, обеспечивающих высокий уровень пористости в тканеинженерных конструкциях | 2021 |
|
RU2772734C2 |
| СИСТЕМА И СПОСОБ АДДИТИВНОГО ПРОИЗВОДСТВА ТРЕХМЕРНЫХ СТРУКТУР | 2014 |
|
RU2643138C2 |
| Роботизированная медицинская система и манипулятор для 3D-биопечати для полнослойного закрытия кожного дефекта | 2023 |
|
RU2814949C1 |
| Способ создания тканеинженерных конструкций методом биопечати биочернилами для регенерации хрящевой ткани в условиях организма | 2021 |
|
RU2770558C2 |
| МНОГОСЛОЙНЫЕ СОСУДИСТЫЕ ТРУБОЧКИ | 2011 |
|
RU2522966C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ТКАНЕЙ | 2013 |
|
RU2733838C2 |

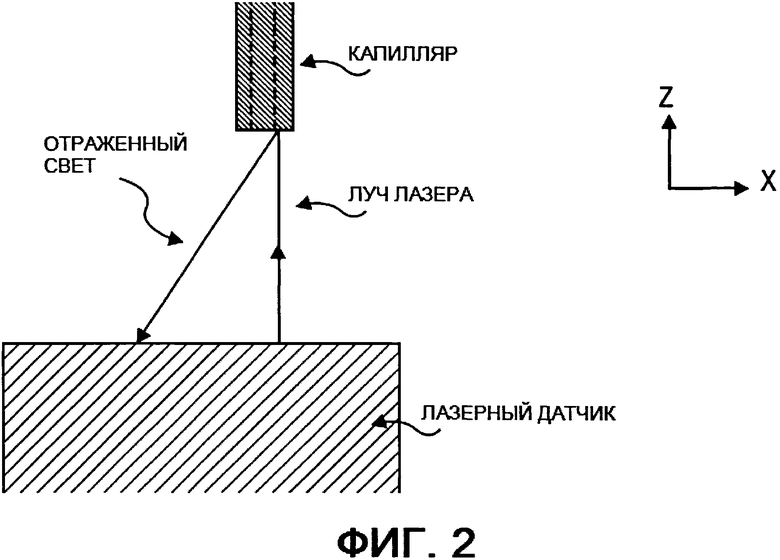




Изобретение относится к биопринтеру, способу калибровки положения картриджа, способу изготовления тканевой конструкции, при этом биопринтер включает одну или более печатающих головок, где печатающая головка включает средство для приема и удерживания по меньшей мере одного картриджа, и где указанный картридж включает содержимое, выбранное из одного или более: биочернил и материала подложки. Биопринтер также включает средства для калибровки положения по меньшей мере одного картриджа с использованием по меньшей мере одного лазерного луча, чтобы определить положение картриджа в пространстве, и средства для раздачи содержимого по меньшей мере одного картриджа. 6 н. и 10 з.п. ф-лы, 6 ил, 3 пр.
1. Биопринтер, включающий:
a. одну или более печатающих головок, где печатающая головка включает средство для приема и удерживания по меньшей мере одного картриджа, и где указанный картридж включает содержимое, выбранное из одного или более:
i. биочернил, и
ii. материала подложки;
b. средства для калибровки положения по меньшей мере одного картриджа с использованием по меньшей мере одного лазерного луча, чтобы определить положение картриджа в пространстве, и
c. средства для раздачи содержимого по меньшей мере одного картриджа.
2. Биопринтер по п. 1, где средство для раздачи содержимого по меньшей мере одного картриджа представляет собой применение поршня, применение давления, применение сжатого газа, гидравлику или комбинацию указанного.
3. Биопринтер по п. 1, дополнительно включающий средство для установления температуры.
4. Биопринтер по п. 3, дополнительно включающий средство для установления температуры окружающей среды, температуры картриджа, температуры содержимого картриджа, температуры принимающей поверхности или комбинации указанных.
5. Биопринтер по п. 4, где средство для установления температуры представляет собой нагревательный элемент.
6. Биопринтер по п. 5, где средство для установления температуры представляет собой радиационный нагреватель, конвективный нагреватель, кондукционный нагреватель, вентиляторный нагреватель, теплообменник или комбинацию указанного.
7. Биопринтер по п. 4, где средство для установления температуры представляет собой охлаждающий элемент.
8. Биопринтер по п. 7, где средство для установления температуры представляет собой контейнер с хладагентом, охлажденной жидкостью, льдом, радиационный охладитель, конвективный охладитель, кондукционный охладитель, вентиляторный охладитель или комбинацию указанного.
9. Биопринтер по п. 1, дополнительно включающий средство для нанесения увлажняющего агента на один или более из следующего:
a. печатная платформа;
b. принимающая поверхность;
c. распределительное отверстие;
d. биочернила;
e. материал подложки; и
f. отпечатанная конструкция,
где увлажняющий агент наносят в одной или более точке времени, выбранной из следующего: перед раздачей биопринтером биочернил или материала подложки, по существу, одновременно с раздачей и после раздачи биопринтером биочернил или вспомогательного материала.
10. Способ калибровки положения картриджа в пространстве, включающего распределительное отверстие, где картридж прикреплен к биопринтеру, включающий калибровку положения картриджа вдоль по меньшей мере одной оси; где ось выбирают из оси х, оси у и оси z; и где каждую калибровку проводят с использованием лазера.
11. Способ по п. 10, где калибровка положения картриджа вдоль по меньшей мере одной оси с использованием лазера включает:
a. позиционирование луча лазера вдоль оси;
b. перемещение картриджа вдоль оси, которая перпендикулярна оси лазерного луча, и остановку указанного перемещения, как только лазерный луч прервется картриджем, где положение, при котором лазерный луч прервется, записывают;
c. перемещение картриджа вдоль той же оси лазерного луча по пути лазерного луча и остановку указанного перемещения, как только будет достигнут порог датчика, где положение, при котором будет достигнут порог датчика, записывают;
d. позиционирование картриджа таким образом, чтобы лазерный луч мог измерять точное положение одной или более точек на картридже, и
е. повторение одного или более этапов (а), (b), (с) и (d) по одной или более осям и осуществление расчета по записанным положениям для определения положения картриджа в пространстве.
12. Система для калибровки положения картриджа, включающего распределительное отверстие, где картридж прикреплен к биопринтеру, причем указанная система включает средство для калибровки положения картриджа вдоль по меньшей мере одной оси, где ось выбирают из оси у, оси х и оси z, и где применяются средства для калибровки положения картриджа с использованием по меньшей мере одного лазерного луча.
13. Способ изготовления тканевой конструкции, включающий:
a. компьютерный модуль, представляющий собой графический пользовательский интерфейс, который сконфигурирован, чтобы получать ввод визуального представления желаемой тканевой конструкции с определенной трехмерной геометрией;
b. компьютерный модуль, генерирующий серию команд, где команды основаны на визуальном представлении и читаются биопринтером, и
c. компьютерный модуль, обеспечивающий серии команд для биопринтера, где биопринтер включает средства для приема и удерживания по меньшей мере одного картриджа, где по меньшей мере один картридж калибруется с использованием по меньшей мере одного лазерного луча, чтобы определить положение картриджа в пространстве, и
d. биопринтер, наносящий биочернила и материал подложки в соответствии с командами для формирования желаемой конструкции с определенной трехмерной геометрией.
14. Способ по п. 13, где визуальное представление включает идентификацию одного или более элементов желаемой тканевой конструкции как одного или более из следующего:
a. биочернила;
b. конкретная композиция биочернил;
c. материал подложки, и
d. конкретная композиция материала подложки.
15. Принимающая поверхность для приема одной или более структур, нанесенных из биопринтера по п. 1, где принимающая поверхность является, по существу, ровной или, по существу, гладкой.
16. Принимающая поверхность для приема одной или более структур, нанесенных из биопринтера по п. 1, где топография принимающей поверхности выполнена с возможностью размещения или влияния на размер, форму, или текстуру, или геометрию одной или более нанесенных структур.
| US 2008070304 A1, 20.03.2008 | |||
| Three-Dimensional BioAssembly Tool for Generating Viable Tissue-Engineered Constructs | |||
| Tissue Engineering, 2004, стр.1566-1576 | |||
| EP 1934288 A2, 25.06.2008 |
Авторы
Даты
2015-08-20—Публикация
2011-09-27—Подача