Изобретение относится к получению ранее неизвестных оксоацетатных соединений платины M2Pt2O(CH3COO)5, где M=Li, K, Na. Rb, Cs. Они могут быть использованы для приготовления гетерогенных платиновых катализаторов на носителях методом пропитки, а также для синтеза других соединений платины и в гомогенном катализе.
Для приготовления металлических нанесенных катализаторов используют пропитку носителей с развитой поверхностью типа силикагеля, окиси алюминия, двуокиси титана, сибунита и пр. растворами подходящих соединений этих металлов с последующими сушкой и восстановлением до металла. Основные требования к таким соединениям - доступность, хорошая растворимость (прежде всего в воде и полярных растворителях), устойчивость при хранении в сочетании со способностью легко восстанавливаться до металла. В составе таких соединений должны отсутствовать каталитические яды (галогены, сера, фосфор, мышьяк, ртуть и др.). Для получения гетерогенных платиновых катализаторов используют такие ионные соединения, как платинахлористоводородную кислоту H2PtCl6 и ее соли со щелочными металлами [И.П. Мухленов, Е.И. Добкина, В.И. Дерюжкина, В.Е. Сороко, Технология катализаторов, Л., Химия, 1989, с. 146; Симонов П.А., Романенко А.В., Бухтияров В.И., Воропаев И.Н., Собянин В.А., пат. РФ №2415707], аммиачные комплексы платины Pt(NH3)4Cl2 [И. Черкендорф, Х. Наймантсведрайт, Современный катализ и химическая кинетика, пер. с англ., Долгопрудный, Интеллект, 2010, с. 228], Pt(NH3)4(OH)2 [J.A.A. Van den Tilaart, J. Leyrer, S. Eckhoff, E.S. Lox, Appl. Catal., 1996, B10, p. 53] и Pt(NH3)6](NO3)4 [US Pat. 3 864284, РЖХим., 1975, 23Л215], основные нитраты четырехвалентной платины [А.В. Беляев, М.А. Федотов, C.H. Воробьева, Координационная химия, 2011, т. 37, №4, с. 278] и даже неустойчивые аллильные Pt(C3H5)2 и карбонильные комплексы 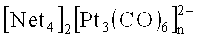
Ниже приводятся примеры известных из литературы синтезов ацетатов двух- и трехвалентной платины. Первая статья, в которой было описано получение ацетата двухвалентной платины последовательной обработкой Na2Pt(OH)6 азотной кислотой и смесью уксусной и муравьиной кислот, вышла еще в 1965 г. [Т.А Stephenson, S.M. Morehouse, A.R. Powell, J.P. Heffer, G. Wilkinson, Journal of Chemical Society, 1965, №6, p. 3652].
Недостатком этого метода является то, что реакция нередко завершается взрывом [J.M. Davidson, С. Triggs, Chemistry and Industry (London), 1966, N 2, p. 306], а в тех случаях, когда взрыва удается избежать, получают сложную смесь продуктов, из которой выделено нитрозильное производное Pt4(OAc)6(NO)2 [M.A.A.F. de С.Т. Carrondo, А.С. Scapski, Journal of Chemical Society, Chemical Communications, 1976, N 11, p. 410; Meester P., Skapski A.C., Journal of Chemical Society, Chemical Communications, 1972, № 18, p. 1039].
В патентной литературе описано получение ацетата платины реакцией хлорида четырехвалентной платины с избытком ацетата серебра в кипящей уксусной кислоте или в эфире с последующей обработкой выпавшего осадка смесью уксусной и муравьиной кислот. Выход технического продукта 73-75% [DE 1948837, 1970 (D. Wright, Chemical Abstracts, 1970, v. 72, 123514P)]:
PtCl4+CH3COOAg→Ag[PtCl4(CH3COO)2]→[Pt(CH3COO)2]n+Ag+AgCl+…
Качество продукта реакции вызывает сомнения: в патенте не приведены физико-химические характеристики продукта, а пурпурный цвет продукта слишком отличается от цвета чистого ацетата платины. При очистке технического продукта перекристаллизацией из ледяной уксусной кислоты получают желтый или коричневый ацетат платины Pt4(OAc)8 (выход не указан), строение двух кристаллических форм которого установлено рентгеноструктурным анализом [M.A.A.F. de С.Т. Carrondo, Skapski A.C. Acta Crystallogr. 1978, B34, N 6, p. 1857 и № 12, р. 3576]. Методом колоночной хроматографии из технического продукта выделяют чистый ацетат платины с выходом 20% [M. Basato, A. Biffis, G. Martinati, С. Tubaro, A. Venzo, P. Ganis, F. Benetollo, Inorganica Chimica Acta, 2003, v. 355, p. 399].
Недостатками метода являются невысокий выход ацетата платины, сложность его выделения и необходимость переработки отходов, содержащих как платину, так и серебро.
Более совершенный способ получения высших карбоксилатов платины [Th.H. Nappier, US Pat. 5149854 A, 1990 г.] основан на реакции хлорида четырехвалентной платины с солями щелочных или щелочноземельных металлов (М) и высших карбоновых кислот в органических растворителях, в которых образующиеся карбоксилаты платины растворимы, а хлориды щелочных и щелочноземельных металлов M нерастворимы:
PtCl4+M(RCOO)m→Pt(RCOO)2+MClm↓+…
m=1 или 2, алифатический остаток R содержит от 3 до 17 атомов углерода.
Однако этот метод не подходит для получения ацетата платины. Приготовленные растворы высших карбоксилатов платины используют непосредственно для пропитки носителей и приготовления катализаторов.
Известен метод получения ацетата платины [M. Basato, A. Biffis, G. Martinati, С. Tubaro, A. Venzo, P. Ganis, F. Benetollo, Inorganica Chimica Acta, 2003, v. 355, p. 399; T. Megues, S. Balint, I. Bako, T. Grosz, L. Kotai, G. Palinkas, Journal of Molecular Liquids, 2008, v. 143, № 1, p. 25], основанный на развитии подхода, изложенного в патенте [DE 1948837, 1970 (D. Wright, Chemical Abstracts, 1970, v. 72, 123514 P)], но для реакции обмена с ацетатом серебра используют хлорид двух-, а не четырехвалентной платины. При очистке продукта реакции выделены синие кристаллы состава Pt4(CH3COO)8·2CH3COOH, но сольват ацетата платины такого состава неизвестен - при кристаллизации из уксусной кислоты образуются две кристаллические формы Pt4(CH3COO)8 от желтого до коричневого цвета (см. выше). Скорее всего основной продукт Pt4(CH3COO)8 загрязнен смешанным олигомерным соединением двух- и трехвалентной платины [Pt(CH3COO)n]x (n~2,5, так называемой «платиновой синью»):
PtCl2+nAgOCOCH3→Pt4(CH3COO)8+[Pt(CH3COO)n]x+AgCl+Ag,
где x принимает значение свыше 100.
Выход продукта реакции составляет 45-55%, но содержание основного компонента не указано. Основные недостатки методики те же, что и в исходном патенте.
Реакцией нитритного комплекса K2Pt(NO2)4 с этанолом и уксусной кислотой получено кристаллическое производное ацетата двухвалентной платины Pt4(CH3COO)5(NO)(NO2)2 темноболотного цвета с выходом 50% [Г.Г. Александров, Г.Н. Кузнецова, Т.Н. Федотова, Журнал неорганической химии, 2006, т. 51, №12, с. 1989]. А при проведении реакции того же реагента K2Pt(NO2)4 с уксусной кислотой и водными растворами сильных кислот HX в отсутствие этанола получены с высоким выходом кристаллические биядерные ацетатные соединения трехвалентной платины [Pt2(CH3COO)4(H2O)2]X2 желтого и оранжевого цвета, где X=NO3, ClO4, CH3SO3. В ледяной уксусной кислоте при 20°C эти ионные соединения превращаются в неустойчивый биядерный ацетат трехвалентной платины [Pt2(CH3COO)4(H2O)2](CH3COO)2, самопроизвольно восстанавливающийся в растворе уже через 5 ч до «платиновой сини» [Appleton T.G., Byriel K.А., Garrett J.M., Hall J.R., Kennard C.H.L., Mathieson M.T., Stranger R., Inorg. Chem., 1995, v. 34, N 22, p. 5646]:
[Pt2(CH3COO)4(H2O)2]X2+CH3COOH→[Pt2(CH3COO)4(H2O)2](CH3COO)2+HX→Ptn(CH3COO)m, где m≈2,5 n.
Хотя, как сказано выше, в растворе ацетат трехвалентной платины неустойчив, описано его получение с выходом 50% в виде темнокоричневого с металлическим блеском порошка последовательной обработкой K2Pt(OH)6 уксусной и муравьиной кислотами при нагревании. Вещество с составом близким к Pt2(OAc)6 растворимо в воде, хлороформе, уксусной кислоте и диметилсульфоксиде и нерастворимо в эфире и углеводородах. [Р.И. Рудый, Н.В. Черкашина, Г.Я. Мазо, Я.В. Салынь, И.И. Моисеев, Изв. АН СССР, сер. Хим., 1980, №4, с. 754]. Растворимость в воде согласуется с ионной природой соединения и при условии устойчивости растворов могла бы служить достаточным основанием для его использования с целью получения гетерогенных катализаторов.
Недостаток методики - отсутствие гарантий чистоты получаемого продукта и сравнительно невысокий выход, связанные с тем, что ацетат трехвалентной платины в условиях синтеза является промежуточным неустойчивым продуктом в цепочке сложных химических превращений:
K2Pt(OH)6+CH3COOH+HCOOH→Pt2(CH3COO)6→Pt4(CH3COO)8→Ptn.
Однако решающим недостатком является доказанная неустойчивость растворов ацетата трехвалентной платины. Недавнее исследование этой реакции [N.V. Cherkashina, D.I. Kochubey, V.V. Kanazhevskiy, V.I. Zaikovsky, V.K. Ivanov, A.A. Markov, A.P. Klyagina, Zh.V. Dobrokhotova, N.Yu. Kozitsina, I.B. Baranovsky, O.G. Ellert, N.N. Efimov, S.E. Nefedov, M.N. Vargaftik, V.M. Novotortsev, I.I. Moiseev, Platinum Acetate Blue: Synthesis and Characterization, Inorganic Chemistry, 2014, v. 53, N 16, p. 8397-8406] показало, что при небольшом варьировании условий образуется не ацетат трехвалентной платины, а так называемые платиновые сини - олигомерные ацетатные соединения переменного состава, куда входят атомы двух- и трехвалентной платины, связанные между собой ацетатными мостиками. Это означает, что небольшие случайные отклонения от методики синтеза могут сильно сказываться на составе и свойствах продукта реакции.
Таким образом, все известные способы получения ацетатов платины имеют те или иные недостатки, препятствующие их практическому применению. В частности, ацетат двухвалентной платины нерастворим в воде, но может использоваться для пропитки носителей в виде растворов в органических растворителях. Нерастворимость в воде не мешает широкому использованию ацетата палладия, самого близкого по свойствам к платине металла платиновой группы, для приготовления гетерогенных катализаторов на основе палладия [Савостин Ю.А., Пчелякова Л.Е., Селицкий М.А., Троицкая И.Б., патент РФ №2050185, 1995] (прототип).
Недостатком ацетата палладия является то, что он растворяется лишь в полярных органических растворителях, но не в воде, что удорожает процессы изготовления гетерогенных катализаторов и делает их пожароопасными.
Среди растворимых в воде основных ацетатов платиновых металлов структурного типа 
Настоящее изобретение направлено на получение оксоацетататных соединений платины, растворимых в воде и пригодных для использования в качестве исходных для приготовления гетерогенных пропиточных катализаторов.
Технический результат достигается тем, что предложены новые оксоацетатные соединения платины для изготовления геторогенных катализаторов, характеризующиеся растворимостью в воде, образующиеся либо при взаимодействии свежеприготовленного тетрагидрата двуокиси платины PtO2·4H2O с ацетатами щелочных металлов, выбранных из ряда: литий, натрий, калий, рубидий, цезий; либо при взаимодействии гидроксоплатинатов указанных щелочных металлов M2Pt(OH)6 с уксусной кислотой в обоих случаях при температурах от 90 до 118°C с образованием темномалинового раствора, из которого затем удаляют уксусную кислоту в вакууме при температуре не выше 100°C и получают твердые гигроскопичные соединения темнофиолетового цвета, отвечающие формуле M2Pt2O(CH3COO)5, где M=Li, Na, K, Rb, Cs, с выходом 90-98%, устойчивые до температуры 150°C.
Сущность изобретения заключается в том, что для получения новых оксоацетататных соединений платины используют кислотно-основную реакцию гидроксоплатинатов щелочных металлов и/или тетрагидрата двуокиси платины с ледяной уксусной кислотой в присутствии ацетатов щелочных металлов, причем промежуточно образующиеся соединения четырехвалентной платины из-за неустойчивости при нагревании превращаются в ионные смешанные оксоацетатные соединения двух- и трехвалентной платины постоянного состава:
2PtO2·4H2O+2MOCOCH3+CH3COOH→M2Pt2O(CH3COO)5+H2O+(CH3)2СО+CO2+CH4+…
Наличие в реакционной смеси катионов щелочных металлов ускоряет термораспад промежуточных продуктов и обеспечивает получение устойчивых анионных оксоацетатных комплексов, растворимых в воде.
Оксоацетатные соединения платины получают в виде гигроскопичных твердых веществ фиолетового цвета. Они устойчивы при комнатной температуре и разлагаются при температурах выше 150°C. Растворяются в воде с образованием глубоко окрашенных растворов от фиолетового до коричневого цвета. Растворы устойчивы при комнатной температуре. Легко восстанавливаются в растворах водородом при комнатной температуре с образованием металлической платины.
M2Pt2O(CH3COO)5+Н2→2Pt+CH3COOH+Н2О+2MOCOCH3
Пропиткой растворами этих соединений платины неорганических носителей, таких как окись алюминия и сибунит, с последующим восстановлением водородом получены гетерогенные катализаторы (примеры 4 и 5). Их каталитические свойства в реакциях гидрирования тройных и двойных связей углерод-углерод и окислительной этерификации пропилена проиллюстрированы примерами 6 и 7.
Химический анализ полученных соединений проводили на CHN-анализаторе ЕА3000 фирмы EuroVector. Содержание платины определяли весовым методом после восстановления навески соединения борогидридом натрия в водном растворе. Данные приведены в Таблице 1 «Условия синтеза и данные химического анализа».
Электронные спектры поглощения регистрировали в среде уксусной кислоты на спектрофотометре Саrу 50 Scan фирмы Varian.
ИК-спектры регистрировали на ИК-Фурье спектрофотометре Nexus фирмы Nicolet методом нарушенного полного внутреннего отражения (НПВО) в диапазоне 4000-550 см-1. Образец твердого вещества наносили на алмазный кристалл. Данные приведены в Таблице 2: «Волновые числа колебаний карбоксильных групп в ИК-спектрах нарушенного полного внутреннего отражения (НПВО)».
Масс-спектры (электрораспыление в ацетонитриле) получали на жидкостном хроматографе с масс-спектральным детектором LCMS 2020 (LC/MS) фирмы Shimadzu. Реакции гидрирования и окисления ненасыщенных органических соединений в присутствии катализаторов исследовали методом газовой хроматографии (хроматограф GC-17A Shimadzu с капиллярной колонкой 0,2 мм × 25 м, ДИП, фаза ХЕ-60).
Используемые в синтезе реактивы: 1) гидроксоплатинат K2Pt(OH)6 получали согласно методике из книги "Синтез комплексных соединений металлов платиновой группы" под ред. акад. И.И. Черняева, Москва, Наука, 1964, стр. 102; 2) гидрат двуокиси платины PtO2·4H2O(H2Pt(OH)6) получали согласно «Руководству по неорганическому синтезу» под ред. Г. Брауэра, т. 5, М., Мир, 1986, с. 1820; 3) ледяную уксусную кислоту квалификации «хч» производства Химмед (РФ) использовали без какой-либо очистки; 4) ацетаты MOCOCH3, где M=Li, K, Na квалификации «хч» и «осч», ацетаты рубидия и цезия получали реакцией уксусной кислоты с соотв. гидроксидами МОН в воде до достижения pH 7 с последующим удалением воды в вакууме.
Достижение заявленного технического результата подтверждается примерами 1-3. Примеры иллюстрируют, но не ограничивают предложенное техническое решение.
Пример 1. Получение M2Pt2O(CH3COO)5, где M=Li, Na, K, Rb, Cs из тетрагидрата двуокиси платины и ацетатов щелочных металлов.
Осажденный из водного раствора гидрат двуокиси платины PtO2·4H2O(H2Pt(OH)6) тщательно промывали метилацетатом или ацетоном и высушивали в вакууме над гидроксидом калия. Свежеприготовленный гидрат двуокиси платины PtO2·4H2O (0,2991 г, 1 ммоль) и ацетат щелочного металла CH3COOM, где M=Na, Li, K, Rb, Cs (1 ммоль) нагревали при 90-118°C в круглодонной колбе с обратным холодильником при перемешивании с 15 мл ледяной уксусной кислоты. Белый осадок полностью растворился в течение 1,5 ч с образованием темномалинового раствора. Реакционную смесь профильтровали через стеклянный фильтр. Растворитель из фильтрата удалили в вакууме 30 Торр при температуре 60-100°C, полученную вязкую массу выдерживали в вакуум-эксикаторе над щелочью до полного застывания. Получили твердое темнофиолетовое гигроскопичное вещество состава M2Pt2O(CH3COO)5·nCH3COOH (0<n<1). После измельчения и длительного выдерживания в вакуум-эксикаторе над щелочью вещество теряет сольватные молекулы уксусной кислоты и соответствует формуле M2Pt2O(CH3COO)5. Выход продуктов 90-98%. Данные хим. анализа: % C 20,02, % H 2,94, % Pt 45,64 (расч. для % С 19,69, % H 2,93, % Pt 45,72). Данные хим. анализа приведены в Таблице 1. Данные масс-спектроскопии (электрораспыление в ацетонитриле MeCN): отрицательные ионы 



Пример 2. Получение оксоацетатного соединения K2Pt2O(CH3COO)5 из тетрагидрата двуокиси платины и гидроксоплатината калия.
Кристаллический гидроксоплатинат калия K2Pt(OH)6 (0,3753 г, 1 ммоль) и свежеприготовленный PtO2·4H2O (0,2991 г, 1 ммоль) нагревали при 100°C в круглодонной колбе с обратным холодильником при перемешивании с 30 мл ледяной уксусной кислоты. При комнатной температуре K2Pt(OH)6 реагирует с уксусной кислотой с образованием ацетата калия и PtO2·4H2O, таким образом реакция сводится к взаимодействию гидрата двуокиси платины PtO2·4H2O и ацетата щелочного металла, приведенному в примере 1. Белый осадок оксо- и гидроксосоединений платины полностью растворялся в течение 1,5 ч с образованием темномалинового раствора. Реакционную смесь профильтровали через пористый стеклянный фильтр. Растворитель удалили из фильтрата в вакууме 30 торр при 60-100°C, полученную темную вязкую массу выдерживали в вакуум-эксикаторе над щелочью до полного застывания с образованием темнофиолетового гигроскопичного вещества состава K2Pt2O(CH3COO)5··nCH3COOH (0<n<1). После измельчения и длительного выдерживания в вакуум-эксикаторе над щелочью вещество теряет сольватные молекулы уксусной кислоты и соответствует формуле K2Pt2O(CH3COO)5. Выход продукта 98%. Данные хим. анализа: % C 20,02, % H 2,94, % Pt 45,64 (расч. для % C 19,69, % H 2,93, % Pt 45,72). Электронный спектр поглощения в уксусной кислоте: λ 420 и 525 нм, ε 3539 и 3691 л·м-1·см-1 соответственно. Данные масс-спектроскопии (электрораспыление в ацетонитриле MeCN): отрицательные ионы 

Пример 3. Получение K2Pt2O(CH3COO)5 из гидроксоплатината калия.
Кристаллический гидроксоплатинат калия K2Pt(OH)6 (0,3753 г, 1 ммоль) нагревали при 100°C в круглодонной колбе с обратным холодильником с 10 мл ледяной уксусной кислоты. Осадок гидроксосоединения в ходе реакции полностью растворяется в течение 15-20 мин с образованием темномалинового раствора. Уксусную кислоту из раствора удаляли в вакууме при 60-100°C, полученную вязкую массу выдерживали в вакуум-эксикаторе над щелочью до полного застывания. Получили гигроскопичное темнофиолетовое вещество, состоящее из смеси ацетата калия и соединения K2Pt2O(CH3COO)5·nCH3COOH (0<n<1). Выход продукта 90%. Данные химического анализа для смеси: % С 17,22; % Н 2,68, % Pt 46,92 (расчет для смеси % С 17,29; % Н 2,16, % Pt 46,84). Для выделения оксоацетатного соединения смесь растворили в 3 мл ацетонитрила и осадили оксоацетат 15 мл эфира. Осадок отделили декантацией, промыли эфиром и высушили на воздухе. Получен фиолетовый порошок состава K2[Pt2O(CH3COO)5]·(C2H5)2О, выход 97%. Эфир из этого соединения удаляли вакууме 0,1 торр при 100°C. Данные хим. анализа полученного K2Pt2O(CH3COO)5 приведены в таблице №1. Состав и свойства те же, что у соединения, полученного по методике, описанной в примере 2.
Примеры 4 и 5 иллюстрируют промышленную применимость заявленного технического решения.
Пример 4. Приготовление гетерогенного катализатора 0,3% Pt/Al2O3
Раствор 0,0300 г соединения Li2Pt2O(CH3COO)5 в 3-4 мл дистиллированной воды добавляли к 5,00 г гранулированной гамма-окиси алюминия марки МОА-25 в фарфоровой чашке и осторожно при перемешивании удаляли воду при нагревании на электроплитке. Полученные фиолетовые гранулы помещали в кварцевую трубку и в течение 1 ч восстанавливали водородом при 200°C, после чего охлаждали до комнатной температуры в токе водорода. Готовый катализатор черного цвета, активная фаза (платина) находится на поверхности гранул.
Пример 5. Приготовление гетерогенного катализатора 0,3% Pt/сибунит
Раствор 0,0300 г соединения K2Pt2O(CH3COO)5 в 3-4 мл дистиллированной воды добавляли к 5,00 г гранулированного сибунита в фарфоровой чашке и осторожно при перемешивании удаляли воду при нагревании на электроплитке. Пропитанные гранулы помещали в кварцевую трубку и в течение 1 ч восстанавливали водородом при 200°C, после чего охлаждали до комнатной температуре в токе водорода.
Примеры 6 и 7 иллюстрируют эффективность гетерогенных катализаторов, полученных по примерам 4 и 5.
Пример 6. Гидрирование фенилацетилена в присутствии катализатора 0,3% Pt/Al2O3
В стеклянном реакторе с магнитной мешалкой перемешивали при комнатной температуре суспензию 1,00 г катализатора в растворе 0,20 мл фенилацетилена в 5,00 мл метилацетата в атмосфере водорода при давлении 1 атм, периодически отбирая пробу жидкости, для хроматографического анализа. Постепенно в растворе накапливаются продукты гидрирования: стирол и этилбензол. При конверсии фенилацетилена 97% селективность по стиролу составляет 83%.
Пример 7. Окислительное ацетоксилирование пропилена в присутствии катализатора 0,3% Pt/C (сибунит)
В стеклянном реакторе с магнитной мешалкой энергично перемешивали суспензию 1,00 г катализатора в 5,00 мл ледяной уксусной кислоты, в которой растворено 0,50 г ацетата калия, при пропускании через реактор смеси пропилена с кислородом (2:1), при температуре 90°C, периодически отбирая пробу жидкости для хроматографического анализа. Постепенно в растворе накапливаются продукты окисления пропилена: аллилацетат и вода. За 24 ч концентрация аллилацетата достигает 10 вес. %. Селективность по аллилацетату составляет 99%.
Таким образом, предлагаемое изобретение позволяет получить устойчивые оксоацетатные соединения платины с выходом 90-98%, растворимые в воде и пригодные для изготовления гетерогенных платиновых катализаторов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гетероядерных ацетатных комплексов двухвалентной платины | 2017 |
|
RU2647131C1 |
| КАТАЛИТИЧЕСКИ АКТИВНЫЕ ПЕРФТОРКАРБОКСИЛАТНЫЕ СОЕДИНЕНИЯ ЧЕТЫРЕХВАЛЕНТНОЙ ПЛАТИНЫ | 2014 |
|
RU2556219C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КАТАЛИЗАТОРА НА МЕТАЛЛИЧЕСКОЙ ПОДЛОЖКЕ | 2007 |
|
RU2391137C1 |
| СОЕДИНЕНИЕ, СОДЕРЖАЩЕЕ МУЛЬТИМЕТАЛЛИЧЕСКИЙ КОМПЛЕКС И КОМПЛЕКС МЕТАЛЛА, И СПОСОБЫ ИХ ИЗГОТОВЛЕНИЯ, И СПОСОБ ИЗГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ С ПРИМЕНЕНИЕМ ДАННЫХ КОМПЛЕКСОВ | 2007 |
|
RU2403086C2 |
| Способ получения платинового композита на носителе из термически обработанного оксида графена | 2024 |
|
RU2827645C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ ФРАКЦИИ АЛКАНОВ, ПРИГОДНОЙ ДЛЯ БЕНЗИНОВОГО И ДИЗЕЛЬНОГО ТОПЛИВА | 2015 |
|
RU2603967C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ПЛАТИНЫ (IV) | 2009 |
|
RU2415085C2 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2024 |
|
RU2834479C1 |
| КАТАЛИЗАТОР ИЗОМЕРИЗАЦИИ ПАРАФИНОВЫХ УГЛЕВОДОРОДОВ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2015 |
|
RU2595341C1 |
| Способ получения синего пигмента на основе силиката цинка, допированного никелем | 2024 |
|
RU2832843C1 |
Изобретение относится к получению ранее неизвестных оксоацетатных соединений трехвалентной платины M2Pt2O(CH3COO)5, где М=Li, K, Na, Rb, Cs. Они могут быть использованы для синтеза других соединений платины, в гомогенном и гетерогенном катализе в качестве предшественников катализаторов, а также в качестве исходных соединений для получения наноразмерных частиц платины. Соединения платины образуются либо при взаимодействии свежеприготовленного тетрагидрата двуокиси платины PtO2*4H2O с ацетатами щелочных металлов, выбранных из ряда: литий, натрий, калий, рубидий, цезий; либо при взаимодействии гидроксоплатинатов указанных щелочных металлов M2Pt(OH)6 с уксусной кислотой в обоих случаях при температурах от 90 до 118°C с образованием темномалинового раствора, из которого затем удаляют уксусную кислоту в вакууме при температуре не выше 100°C и получают твердые гигроскопичные соединения темнофиолетового цвета, отвечающие формуле M2Pt2O(CH3COO)5, где M=Li, Na, K, Rb, Cs. Предлагаемое изобретение позволяет получить устойчивые до температуры 150°C оксоацетатные соединения платины с выходом 90-98%, растворимые в воде и пригодные для изготовления гетерогенных платиновых катализаторов. 2 табл., 7 пр.
Оксоацетатные соединения платины для изготовления геторогенных катализаторов, характеризующиеся растворимостью в воде, образующиеся либо при взаимодействии свежеприготовленного тетрагидрата двуокиси платины PtO2·4H2O с ацетатами щелочных металлов, выбранных из ряда: литий, натрий, калий, рубидий, цезий; либо при взаимодействии гидроксоплатинатов указанных щелочных металлов M2Pt(OH)6 с уксусной кислотой в обоих случаях при температурах от 90 до 118°C с образованием темномалинового раствора, из которого затем удаляют уксусную кислоту в вакууме при температуре не выше 100°C и получают твердые гигроскопичные соединения темнофиолетового цвета, отвечающие формуле M2Pt2O(CH3COO)5, где M = Li, Na, K, Rb, Cs, с выходом 90-98%, устойчивые до температуры 150°C.
| КАРБОКСИЛАТНЫЕ СОЕДИНЕНИЯ БЛАГОРОДНЫХ МЕТАЛЛОВ Ir, Ru, Rh, Pd, Pt И Au, ОБЛАДАЮЩИЕ ВЫСОКОЙ КАТАЛИТИЧЕСКОЙ ЭФФЕКТИВНОСТЬЮ | 2008 |
|
RU2482916C2 |
| Способ получения нитроацетата платины | 1973 |
|
SU464596A1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ НАНЕСЕННЫХ ПАЛЛАДИЕВЫХ КАТАЛИЗАТОРОВ | 2004 |
|
RU2282498C2 |
| DE 102007014914 A1, 02.10.2008 | |||
| JP 2011032224 A, 17.02.2011 | |||
| CN 103113412 A, 22.05.2013 | |||
Авторы
Даты
2015-10-20—Публикация
2014-11-06—Подача