Заявленное техническое решение относится к способам получения катализаторов, представляющим собой наночастицы платины на носителе из термически обработанного оксида графена.
Предлагаемое изобретение может найти применение в ряде химических и электрохимических процессов, в частности, в протон-обменных топливных элементах, используемых в автомобилестроении/транспорте, и в качестве мобильного/стационарного источника электроэнергии в удаленных труднодоступных регионах, а также в реакциях химического синтеза.
На дату представления заявочных материалов стало актуально развитие водородной энергетики, в частности, за счёт широкого внедрения топливных элементов в качестве основного источника электроэнергии, который отличается высокой эффективностью, мощностью и экологичностью по сравнению с иными источниками электроэнергии, имеющими высокую долю в топливно-энергетическом секторе экономики [Об утверждении Концепции развития водородной энергетики в Российской Федерации: распоряжение Правительства РФ от 05 августа 2021 года №2162-р]. Серьёзным сдерживающим фактором в развитии данного направления является использование дорогостоящего платинового катализатора, изготавливаемого и предлагаемого на рынке такими иностранными компаниями как: «Tanaka Precious Metals» (Япония); Cataler Corporation (Япония); ENY - Mobility GmbH (Германия); HIAT (Германия); Johnson Matthey (Великобритания); Sainergy Fuel Cell India Private Limited (Индия); TFP Hydrogen Products (Великобритания); Umicore (Бельгия), и др.
Заявленное техническое решение направлено на создание отечественной производственной базы катализаторов, что входит в число приоритетных задач научно-технического развития РФ, и способно привести к замещению импортируемой продукции.
Данное техническое решение призвано решить вопрос уменьшения содержания дорогостоящей платины в катализаторах при сохранении или улучшении их эффективности.
Далее в тексте заявителем приведено пояснение терминов, которое необходимо для облегчения однозначного понимания сущности заявленных материалов и исключения противоречий и/или спорных трактовок при выполнении экспертизы по существу.
Прекурсор (предшественник) - химическое исходное вещество, участвующее в реакции, приводящей к образованию целевого вещества [Большая Российская энциклопедия: официальный сайт. - URL: https://bigenc.ru/c/prekursor-5522c6 (дата обращения: 19.10.2023. - Текст: электронный];
Композит - композиционный материал или композитный материал, сокращённо композит - многокомпонентный материал, изготовленный из двух или более компонентов с существенно различными физическими и/или химическими свойствами, которые, в сочетании, приводят к появлению нового материала с характеристиками, отличными от характеристик отдельных компонентов и не являющимися простой их суперпозицией [Карпинос Д. М. Композиционные материалы: справочник / Д.М. Карпинос; под ред. Л. Р. Вищнякова, Т.В. Грудиной [и др.] - Киев: Наукова думка, 1985. - 589с.];
Оксид графена - двумерный наноматериал, состоящий из атомов углерода, образующих гексагональную кристаллическую решётку с присоединёнными кислородсодержащими функциональными группами, такими как эпоксидные, гидроксильные и карбоксильные группы. [Dimiev A.M. Graphene Oxide: Fundamental and Applications / A.M. Dimiev, S. Eigler. - West Sussex: John Wiley & Sons, Ltd, 2017. - 454p.];
Термически обработанный оксид графена - двумерный углеродный материал, получаемый в ходе термического воздействия на оксид графена, в результате чего происходит частичная потеря кислородсодержащих функциональных групп и увеличение числа дефектов углеродной сети [Dimiev A.M. Graphene Oxide: Fundamental and Applications / A.M. Dimiev, S. Eigler. - West Sussex: John Wiley & Sons, Ltd, 2017. - 454p.];
Наночастицы - образования, состоящие из атомов или молекул с размерами от 1 до 100 нм [Таланов В.М. Основы нанохимии и нанотехнологий: учебное пособие / В.М. Таланов, Г.П. Ерейская. - Новочеркасск: ЮРГПУ (НПИ), 2014. - 524с.];
Катализатор - вещества, которые участвуют в химической реакции, но не входят в состав конечных продуктов. Главной функцией таких веществ является изменение скорости химической реакции [Крылов О.В. Гетерогенный катализ: учебное пособие для вузов / О.В. Крылов. - Москва: ИКЦ «Академкнига», 2004. - 15-18с.];
Гетерогенный катализ - катализатор и реагирующие вещества находятся в разных фазах, между которыми имеется граница раздела [Крылов О.В. Гетерогенный катализ: учебное пособие для вузов / О.В. Крылов. - Москва: ИКЦ «Академкнига», 2004. - 15-18с.];
Носитель - это вещества, которые неактивные или малоактивные, нанесение на них катализатора значительно повышает активность этого катализатора [Крылов О.В. Гетерогенный катализ: учебное пособие для вузов / О.В. Крылов. - Москва: ИКЦ «Академкнига», 2004. - 15-18с.].
В настоящее время проведение химических реакций преимущественно осуществляется с использованием платинового катализатора, который отличается от остальных металлических катализаторов высокой каталитической активностью. Небольшое содержание в земной коре и затраты на извлечение и обработку платины определяют её высокую стоимость. Несмотря на данную проблему платина остаётся одним из важных и популярных металлов в области гетерогенного катализа. В частности её применение в качестве катализатора может быть реализовано при очистке сточных вод от такого токсичного соединения, как 4-нитрофенол, для получения промежуточного продукта синтеза парацетамола - 4-аминофенола или в качестве материала анода и/или катода топливного элемента с протонообменной мембраной (ПОМТЭ) [Hughes A. E. Platinum Group Metals: A Review of Resources, Production and Usage with a Focus on Catalysts / A.E. Hughes, N. Haque, S.A. Northey, S. Giddey // Resources. - 2021. - V.10. - Is.93. - P.93].
На дату представления заявочных материалов Правительством Российской Федерации было поддержано решение по противодействию изменению климата, охране окружающей среды и рациональному природопользованию, что главным образом может быть реализовано за счёт развития водородной энергетики и следовательно благодаря широкому внедрению топливных элементов с протонообменной мембраной в качестве основного источника электроэнергии, который отличается высокой эффективностью, мощностью и экологичностью по сравнению с иными источниками электроэнергии, имеющими высокую долю в топливно-энергетическом секторе экономики [Об утверждении Концепции развития водородной энергетики в Российской Федерации: распоряжение Правительства РФ от 05 августа 2021 года №2162-р].
Серьёзным препятствие на пути масштабирования водородной энергетики в будущем стало использование дорогостоящего платинового катализатора, который в основном изготавливается иностранными производителями, такими как: «Tanaka Precious Metals» (Япония); Cataler Corporation (Япония); ENY - Mobility GmbH (Германия); HIAT (Германия); Johnson Matthey (Великобритания); Sainergy Fuel Cell India Private Limited (Индия); TFP Hydrogen Products (Великобритания); Umicore (Бельгия).
На дату подачи заявки на лицо необходимость создания отечественной производственной базы катализаторов. При этом снижение содержания дорогостоящей платины при сохранении эффективности остается важной научно-технической задачей. Снижение содержания дорогостоящей платины достигается повышением ее дисперстности (уменьшением размера наночастиц платины).
В электро-химических катализаторах в качестве носителей для платиновых наночастиц используют углеродные материалы. Популярность их использования при изготовлении гетерогенного катализатора обуславливается наличием таких свойств, как высокая площадь поверхности, высокая коррозионная устойчивость в окислительных условиях, хорошая электропроводность. Практически все коммерческие платиновые катализаторы, использующееся в топливных элементах с протонообменной мембраной синтезируются на таком углеродном материале, как «Carbon Black XC 72R». Однако данный носитель не может обеспечить плотное и равномерное распределение металлического компонента, так как не содержит на своей поверхности точек связывания. [Sakthivel M. An extensive study about influence of the carbon support morphology on Pt activity and stability for oxygen reduction reaction / M. Sakthivel, J. - F. Drillet // Applied Catalysis B: Environmental. - 2018. - №. 231. - p.62-72].
Следовательно появляется потребность в поиске иных углеродных носителей обеспечивающих равномерное распределение наночастиц платины по поврехности такого носителя.
Из уровня техники известно, что такой двумерный углеродный материал, как оксид графена обладает множеством кислородсодержащих функциональных групп, которые способны образовывать связи с переходными металлами по координационному механизму. Такие группы могут выполнять функцию центров связывания металлов с носителем, что позволяет добиться лучшего распределения металлического компонента катализатора по поверхности носителя по сравнению с дешёвым углеродным материалом «Carbon Black XC 72R» . [Amirov R.R. Analysis of competitive binding of several metal cations by graphene oxide reveals the quantity and spatial distribution of carboxyl groups on its surface / R. R. Amirov, J. Shayimova, Z. Nasirova, A. Solodov, A.M. Dimiev // Physical Chemisty Chemical Physics. -2018. - №.20.], [Solodov A. N. Binding modes of Fe(III) with graphene oxide in aqueous solutions. Competition with Sr2+, Cs+, Na+ ions and Fe(III) chelators / A. N. Solodov, J. Shayimova, R. R. Amirov, A. M. Dimiev // Journal of Molecular Liquids. - 2020. - №.302.].
Также известно, что оксид графена не обладает проводящими свойствами, однако его химическое восстановление или термообработка позволяет получить графеноподобный материал, который содержит большое количество вакансионных дефектов углеродной сетки а также значительное количество кислородсодержащих функциональных группб выполняющих роль центров связывания металлов с поверхностью носителя [Pei S. The reduction of graphene oxide / S. Pei, H. - M. Cheng // Carbon. -2012. - №.50.-p. 3210-3228].
Очень часто платиновые композиты на углеродных носителях, в том числе на носителе из оксида графена и его производных синтезируются с использованием платинохлористоводородной кислоты.
Так Li Y. и др. показали, что предварительный синтез наночастиц платины из платинохлористоводородной кислоты с их последующим нанесением на носитель из восстановленного оксида графена приводит к получению наночастиц платины со средним размером 5 нм, хорошо распределённых по поверхности носителя. Полученный композит был протестирован в лабораторных условиях в качестве катализатора для топливного элемента с протонообменной мембраной. [Li Y. Stabilization of High-Performance Oxygen Reduction Reaction Pt Electrocatalyst Supported on Reduced Graphene Oxide /Carbon Black Composite / Y. Li, Y. Li, E. Zhu [et al] // Journal of The American Chemical Society. -2012. - №.134. -p. 12326-12329];
В своём исследовании Zhanga Q.-L и др. также использовали платинохлористоводородную кислоту в качестве основного источника получения платиновых наночастиц на носителе из азот легированного оксида графена. В результате средние размеры образовавшихся на поверхности платиновых наночастиц составляли 4,3 нм, при этом многие из них образовывали небольшие нитевидные агломераты. [Zhanga Q.-L. Facile synthesis of uniform Pt nanoparticles on polydopamine-reduced graphene oxide and their electrochemical sensing / Q.-L. Zhanga, T.-Q. Xu, J. Weia [et al] // Electrochemica Acta. - 2013.- №.112. - p.127-132.];
Su Y. и др. использовали методику синтеза одновременного восстановления оксида графена и платинохлористоводородной кислоты в этиленгликоле с помощью автоклава при температуре 200°С. С помощью данной методики синтеза были получены платиновые наночастицы, средние размеры которых составили 5 нм. Они одиночно и равномерно располагались на поверхности восстановленного оксида графена. [Su Y. Upgrading of furans from in situ catalytic fast pyrolysis of xylan by reduced graphene oxide supported Pt nanoparticles / Y. Su, Y. Zhang, J. Qi [et al] // Renewable Energy. - 2020. - №.152. - p.94-101];
Dang C.L.T. получили наночастицы платины на носителе из восстановленного оксида графена путём совместного химического восстановления оксида графена в смеси платинохлористоводородной кислоты и этилового спирта. В результате средние платиновые наночастицы находили на поверхности восстановленного оксида графен в виде одиночных наночастиц с размерами от 10 до 25 нм или в виде крупных агломератов [Dang C.L.T. Effect of Synthesis Conditions of Platinum/Reduced Graphene Oxide Nanocomposites on the Electrochemical Behaviors of Cathodes in Dye-Sensitized Solar Cells / C.L.T. Dang, C. V. Le., T. D. Nguyen [et al] // Journal of Electronic Materials. - 2021. -№. 50. - p. 1425-1433].
Однако если такие композиты в дальнейшем использовать в качестве катализаторов, то даже следовые количества хлора в составе в скором времени могут дезактивировать их [Mendyka B. Effect of chlorine compounds on the deactivation of platinum catalysts / B. Mendyaka, A. Musialik-piotrowska, K. Syczewska // Catalysis Today. - 1992. - №.11. - p.597-610]. По этой причине выбор реагента крайне важен для синтеза каталитических систем.
Из уровня техники известны такие бесхлорные реактивы, как растворы нитрата платины (II) или (IV), которые редко используются в процессе изготовления катализаторов на носителях. Так, известно, что такой реагент был применён для синтеза катализатора на носителе из оксида алюминия. Однако использование носителя из оксида алюминия для катализаторов, использующихся в топливных элементах с протонообменной мембраной, невозможно вследствие низкой проводимости данного носителя [Hinz A. Platinum on alumina, titania, and magnesia supports for the combustion of methanol in a waste gas with trace amount of ammonia / A. Hinz, P.-O. Larsson, B. Skårman, A. Andersson // Applied Catalysis B: Environmental. - 2001. -№.34. - p. 161-178], [Nartova, A. V. Influence of a precursor solution on the characteristics of platinum on alumina catalysts / A.V. Nartova, L.M. Kovtunova, Y. V. Larichev [et al] // Mendeleev Communications. - 2017. - №.27.- p.70-71]. Кроме этого, известно, что синтез платинового катализатора с использованием прекурсора - нитрата платины (IV) был проведён на носителе из азотлегированного графена, полученном темплатным методом. В результате на таком носителе были получены наночастицы, содержащие платину, со средними размерами 12 нм, то есть использование такого прекурсора в сочетании с данным углеродным носителем не позволило получить мелкодисперсный катализатор. [Chesnokov V. V. Effect of Platinum Precursor on the Properties of Pt/N-Graphene Catalysts in Formic Acid Decomposition / V.V. Chesnakov, V.V. Kriventsov, I. P. Prosvirin, E. Y. Gerasimov // Catalysts. - 2022. - V.12. - №.9]. При этом заявителем не выявлены источники, в которой бы был использован данный прекурсор для синтеза композита на носителе из термически обработанного оксида графена.
Центральный атом нитрата платины (IV) имеет координационное число, равное четырём, с двумя свобоными вакансиями в аксиальном положении. В то же время, центральный атом платины в гексахлороплатиновой кислоте имеет максимальное координационное число, равное шести. Принимая вышеперечисленное во внимание, можно предположить, что в ходе синтеза композита с использованием нитрата платины (IV) атомы платины смогут более эффективно связываться с кислородсодержащими группами оксида графена за счет наличия двух свободных вакансий. В то же время атом платины в гексахлороплатиновой кислоте, напротив, будет менее активен в первую очередь за счет стерических препятствий. Соответственно у него меньше возможностей прочного связывания с носителем; поэтому в этом случае будет преобладать взаимодействие атомов платины друг с другом, нежели взаимодействие с подложкой. Таким образом, выбор прекурсора может влиять на дисперсность платины на углеродной подложке, что напрямую связано с эффективностью катализатора.
Из уровня техники известно, что контроль размера металлических наночастиц может быть произведён с помощью варьирования температуры синтеза. Так в работе Lushta V. и др. показано, что при увеличении температуры синтеза происходит увеличение диаметра наночастиц [Lushta V. Nanoscale Characterization of Ion Mobility by Temperature-Controlled Li-Nanoparticle Growth / V. Lushta, D. Dietzel, B. Roling, A. Schirmeisen // ACS Applied materials and interfaces. - 2019. - V.11. - №.5. - p. 5476-5483], [Mott D. Synthesis of Size-Controlled and Shaped Copper Nanoparticle / D. Mott, J. Galkowski [et al.] // Langmuir. - 2007. - №.23.-p.5740-5745]. Другим не мало важным параметром при проведении синтеза является выбор растворителя. Такой прекурсор, как нитрат платины (IV) подвергается гидролизу с образованием частиц PtO2, которые не имеют такой же каталитической активности, как частицы Pt [Chesnokov V.V. Effect of Platinum Precursor on the Properties of Pt/N-Graphene Catalysts in Formic Acid Decomposition / V. V. Chesnokov, V. V. Krieventsov, I. P. Prosvirin, E. Yu.]. Использование таких спиртов, как изопропанол и этиленгликоль, позволяет провести синтез при комнатной температуре, а также при повышенных температурах (до 82°С - температуры кипения изопропанола и до 197°С - температуры кипения этиленгликоля).
Заявителем проведён анализ патентной и научной литературы и выявлены аналоги заявленного технического решения.
Так, известно изобретение по патенту RU 2787270 «Катализатор, способ его приготовления и способ фотокаталитического получения водорода», сущностью является катализатор для процесса фотокаталитического получения водорода из щелочного раствора триэтаноламина под действием видимого излучения с нанесёнными на поверхность графитоподобного нитрида углерода g-C3N4 частицами платины, имеющий состав 0,5 мас.% Pt/g-C3N4 и характеризующийся следующими параметрами: удельная поверхность 66-80 м2/г, объем пор 0,27-0,33 см3/г, размер частиц 15-18 нм. Способ приготовления катализатора для процесса фотокаталитического получения водорода из щелочного раствора триэтаноламина под действием видимого излучения, который заключается в термолизе супрамолекулярного аддукта меламин-циануровая кислота в атмосфере воздуха при температуре 550°С в течение 2 ч с получением графитоподобного нитрида углерода g-C3N4, в пропитке g-C3N4 раствором нитрата платины в ацетоне с последующим восстановлением платины в токе водорода, в результате получают катализатор, имеющий состав 0,5 мас.% Pt/g-C3N4 и характеризующийся следующими параметрами: удельная поверхность 66-80 м2/г, объем пор 0,27-0,33 см3/г, размер частиц 15-18 нм. Способ фотокаталитического получения водорода из щелочного раствора триэтаноламина под действием видимого излучения при температуре 20°С в течение 1,5 ч, отличающийся тем, что процесс осуществляют в присутствии катализатора по п. 1 или приготовленного по п. 2.
Таким образом, в известном техническом решении также используется нитрат платины в качестве прекурсора (предшественника) заявленного композита, как и в заявленном техническом решении.
Недостатками известного технического решения являются:
- термолиз азотсодержащих органических соединений в атмосфере воздуха приводит к образованию токсичных и едких паров (по сравнению с отжигом оксида графена, в ходе которого не образуется токсичных и едких веществ, в заявленном техническом решении);
- графитоподобный нитрид углерода не обладает достаточным количеством центров закрепления и/или зародышеобразования наночастиц платины, так как его поверхность практически бездефектна, а функциональные группы, содержащие азот располагаются только на поверхности углеродной матрицы, а не дополнительно по краям и в зоне дефектов, как в случае термически обработанного оксида графена в заявленном техническом решении;
- графитоподобный нитрид углерода не обладает высокими значениями удельной поверхности, так как имеет трёхмерную структуру, в то время как оксид графена и термически обработанный оксид графена двумерны, следовательно их удельная поверхность выше;
- недостаточная дисперсность (размер частиц от 15 до 8 нм по сравнению с одиночными атомами/ионами, кластерами и наночастицами со средними размерами 1,4 - 2,8 нм в заявленном техническом решении).
Известно изобретение по патенту RU 2316394 «Способ приготовления моно- и биметаллического катализатора и процессы с участием кислорода и/или водорода», сущностью является способ приготовления моно- или биметаллического катализатора для процессов с участием кислорода и/или водорода, включающий пропитку углеродного носителя соединениями палладия и/или платины или палладия и, по крайней мере, одного из металлов I группы, отличающийся тем, что носитель предварительно обрабатывают в азотной кислоте с концентрацией от 3 до 15 М при температуре не выше 80°С, пропиточный раствор готовят из азотнокислых растворов безхлоридных соединений палладия и/или платины или палладия и, по крайней мере, одного из металлов I группы, их сушку и разложение осуществляют в токе инертного газа при температуре не выше 105°С и от 150 до 350°С соответственно, восстановление проводят в токе водорода при 110-350°С, при прочих условиях нанесения, сушки, разложения, восстановления и соотношении исходных компонентов, обеспечивающих получение дисперсных частиц металлов платиновой группы размером 1-10 нм, локализованных в порах размером 2-20 нм, при содержании нанесённых палладия и/или платины от 3 до 50 мас.% или палладия и/или платины и серебра от 0,1 до 1,4 мас.%. Способ по п.1, отличающийся тем, что используют углеродный носитель, получаемый термическим разложением углеводородов на гранулах сажи с последующей окислительной активацией или без неё и представляющий собой углеродный материал с объёмом пор 0,2-1,7 см/г, образованный слоями углерода толщиной 10-1000 нм с радиусом кривизны 10-1000 нм, истинной плотностью по гелию 1,80-2,1 г/см3, рентгеновской плотностью 2,112-2,236 г/см3 и распределением пор по размерам с максимумами в области 3-20 и 20-200 нм. Способ по п.1, отличающийся тем, что используют углеродный носитель, получаемый разложением метана или этилена при температурах от 600 до 700°С на катализаторе, содержащем нанесённые на окись алюминия металлические никель и железо или никель и медь и представляющий собой углеродный материал с удельной поверхностью по адсорбции азота от 105 до 260 м2/г, поверхностью мезопор от 95 до 240 м2/г, объемом микропор от 0,01 до 0,02 см3/г, суммарным объемом пор от 0,31 до 0,4 см3/г и средним диаметром пор от 6,2 до 17,5 нм.
Таким образом, в известном техническом решении также используется прекурсор -нитрат платины и углеродный носитель для изготовления катализатора
Недостатками известного технического решения являются:
- низкие значения удельной поверхности углеродных нановолокон, которые используются в качестве носителей для катализаторов по сравнению со значениями удельной поверхности двумерного оксида графена и его производных;
- неравномерное распределение активных металлических центров катализатора вследствие отсутствия большого числа равномерно распределённых функциональных групп и дефектов, которое может привести к потере каталитической эффективности в процессе эксплуатации катализатора;
- недостаточная степень дисперсии катализатора (размер частиц 1,6-6,3 нм, в среднем 3,95 нм, по сравнению с одиночными атомами/ионами, кластерами и наночастицами со средними размерами 1,4 - 2,8 нм в заявленном техническом решении);
- меньшая технологичность, так как отжиг в токе водорода при 250°С приводит к дополнительным энергетическим затратам, при этом повышаются экономические затраты, следовательно, стоимость готового продукта может увеличиться.
Известно изобретение по патенту CN116093350 «Графен, легированный азотом, нагруженный платиной, а также способ его получения и применения», сущностью является способ получения графена, легированного азотом, нагруженного платиной, который характеризуется тем, что включает следующие стадии: смешивают оксид графена, соль платины и растворитель с образованием смешанного раствора, а затем выполняют гидротермальную реакцию для получения композитного порошка оксида графена и соли платины; композитный порошок оксида графена и соли платины смешивают с аминосоединением и измельчают в шаровой мельнице с получением порошка модифицированного амином композита оксида графена и соли платины; и композиционный порошок аминомодифицированного оксида графена и соли платины подвергают микроволновому облучению для получения графена, легированного азотом и нагруженного платиной. Способ приготовления по п.1, отличающийся тем, что способ приготовления имеет по меньшей мере одну из следующих характеристик: 1) Платиновая соль включает платинохлористоводородную кислоту и/или ацетат платины; 2) Аминосоединение включает аммиак и/или мочевину. Способ получения по п.1, отличающийся тем, что количество слоев оксида графена составляет от 1 до 10, а содержание кислорода составляет от 30 ат% до 60 ат%. Способ получения по п.1, в котором массовое соотношение атомов углерода в оксиде графена к атомам платины в соли платины составляет (0,5-3):1. Способ получения по п.4, отличающийся тем, что массовое соотношение атомов углерода в порошке смеси оксида графена и соли платины к атомам азота в аминосоединении составляет (1-10):1. Способ получения по любому из пп.1-5, отличающийся тем, что температура гидротермальной реакции составляет от 80°С до 120°С, а время составляет от 0,5 часа до 3 часов. Способ приготовления по любому из пп.1-5, отличающийся тем, что мощность микроволнового облучения составляет от 1 кВт до 15 кВт, а время - от 5 с до 300 с. Способ приготовления по любому из пп.1-5, отличающийся тем, что скорость вращения шаровой мельницы составляет от 200 до 500 об/мин, а время составляет от 0,5 до 3 часов. Способ приготовления по любому из пп.1-5, отличающийся тем, что способ образования смешанной жидкости включает: диспергирование оксида графена в воде с образованием дисперсии оксида графена; соль платины растворяют в органическом растворителе с образованием раствора соли платины; и смешивают дисперсионную жидкость и раствор соли платины, чтобы получить смешанную жидкость; необязательно органический растворитель включает этанол и/или этиленгликоль. Графен, легированный азотом на носителе из платины, полученный способом получения по любому из пп.1-9.
Таким образом, в известном техническом решении также используется носитель, синтезированный из оксида графена, и нитрат платины в качестве прекурсора для изготовления катализатора.
Недостатками известного технического решения являются:
- недостаточная дисперсность катализатора (размер частиц 10 нм по сравнению с одиночными атомами/ионами, кластерами и наночастицами со средними размерами 1,4 - 2,8 нм в заявленном техническом решении);
- недостаточное связывание металла с носителем вследствие того, что легирование атомами азота углеродной сетки оксида графена происходит после получения промежуточного композита оксида графена с платиной, что не позволяет образовывать связи между азотсодержащими функциональными группами и платиной;
- меньшая экологичность, так как разложение мочевины при нагревании приводит к образованию токсичных соединений;
- недостаточная технологичность, так как синтез является многостадийным за счёт легирования, гидротермального восстановления и микроволнового облучения, следовательно, выход готового платинового композита может быть небольшим.
- высокие энергетические затраты из-за использования микроволного облучения высокой мощности приводит к повышению стоимости готового платинового композита;
Известна публикация «Влияние прекурсора платины на свойства Pt/N-графеновых катализаторов разложения муравьиной кислоты» [Chesnakov V.V. Effect of Platinum Precursor on the Properties of Pt/N-Graphene Catalysts in Formic Acid Decomposition / V.V. Chesnakov, V.V. Kriventsov, I.P. Prosvirin, E. Y. Gerasimov // Catalysts. - 2022. - №.12.], сущностью которой является получение графена, легированного атомами азота, нагруженного платиной, который характеризуется тем, что включает следующие стадии:
1. Для синтеза N-графена оксид магния нагревали в токе аргона до необходимой температуры (650-750°С). Затем отключали подачу аргона и открывали подачу питания. Оксид магния подвергали карбонизации 40%NH3-1%C2H2-C2H4. Смесь прекурсоров, содержащая азот (40%NH3-1%C2H2-C2H4), была использована для синтеза графена, легированного азотом (N-графена). Присутствующий в этой смеси аммиак внедрялся в углеродную цепь, и образовывался углеродный материал с легированными атомами азота. В дальнейшем N-графен был очищен от MgO. Удельная поверхность синтезированного N-графена составила 1300 м2/г.
2. Платину наносили на N-графен из водного раствора Pt(NO3)4 с концентрацией 250 г/мл. Рассчитанное количество раствора Pt(NO3)4 разбавляли 10-15 мл дистиллированной воды. Затем добавляли 1,0 г углеродного носителя при непрерывном перемешивании магнитной мешалкой. После выпаривания воды сухой остаток переносили в фарфоровую посуду и нагревали в муфельной печи при температуре 150°С в течение 30 мин. Концентрация платины в катализаторе варьировалась от 0,2 до 1 мас.%.
Таким образом, в известном техническом решении также используется нитрат платины в качестве прекурсора (предшественника) заявленного композита, как и в заявленном техническом решении.
Недостатками известного технического решения являются:
- низкие значения удельной поверхности носителя, так как из уровня техники известно, что использование в качестве катализатора оксида магния приводит к получению не графена, а аморфного углерода;
- невысокая дисперсность катализатора (размер частиц 12 нм по сравнению с одиночными атомами/ионами, кластерами и наночастицами со средними размерами 1,4 - 2,8 нм в заявленном техническом решении);
- отсутствие большого количества равномерно распределённых функциональных групп и дефектов, которые связываются металлические центры катализатора по сравнению с термически обработанным оксидом графена, который используется в качестве носителя в заявленном техническом решении;
- слабое взаимодействие металлического компонента с носителем вследствие внедрения атомов азота непосредственно в углеродную сеть, которое может привести к потере каталитической эффективности в процессе эксплуатации катализатора;
- использование воды в качестве растворителя прекурсора - нитрата платины приводит к его гидролизу, в отличие от использования изопропилового спирта, в котором образуются устойчивый раствор нитрата платины;
- высокие энергетические затраты вследствие выпаривания воды и отжига катализатора на последней стадии его синтеза, что может привести к повышению стоимости катализатора.
Выявленные аналоги совпадают с заявленным техническим решением по отдельным совпадающим признакам, поэтому прототип не выявлен и формула изобретения составлена без ограничительной части.
Таким образом, технической проблемой, решаемой заявленным техническим решением, является устранение недостатков аналогов:
- небольшая удельная поверхность носителей катализаторов;
- недостаточная дисперсность катализаторов;
- меньшая технологичность;
- меньшая экологичность процессов.
Техническим результатом заявленного технического решения является разработка способа получения платинового композита на носителе из термически обработанного оксида графена, позволяющего устранить недостатки выявленных аналогов, а именно:
- увеличение удельной поверхности, а также повышение числа дефектов в структуры графена благодаря введению стадии отжига оксида графена, при этом оставшиеся кислородсодержащие функциональные группы, а также терминированные такими группами образовавшиеся дефекты являются центрами связывания металла с носителем и позволяют провести плотное и равномерное засевание поверхности носителя наночастицами, что, в свою очередь, приводит к повышению каталитической эффективности композита.
- увеличение дисперсности катализатора благодаря использованию в качестве прекурсора нитрата платины (IV), которое позволяет провести синтез с образованием химических связей между кислородсодержащими функциональными группами носителя и платиной, а также способствует более равномерному распределению наночастиц платины на поверхности носителя, в отличие от использование гексахлороплатиновой кислоты в качестве основного источника платины;
- улучшение технологичности благодаря разработке заявленного способа, проводимого при температуре не выше 180°С по сравнению с 550°С, 250°С в токе водорода и микроволновым облучением в аналогах, а также включающего меньшее количество действий по сравнению с аналогами;
- повышение экологичности процессов благодаря тому, что в ходе проведения отжига не образуются токсичные соединения.
Сущностью заявленного технического решения является способ получения платинового композита на носителе из термически обработанного оксида графена, заключающийся в том, что проводят два этапа: на 1 этапе получают термически обработанный оксида графена, для чего 10 вес.ч. графита диспергируют в 1147 вес.ч. 96 мас.% серной кислоты, для чего графит и серную кислоту смешивают и перемешивают в течение 30 минут, затем добавляют порционно перманганат калия для окисления графита - четыре раза по 9 вес.ч., суммарно 36 вес.ч., при постоянном перемешивании, о завершении окисления судят по исчезновению зелёной окраски, затем полученную смесь разбавляют 1300 вес.ч. смеси лёд/вода в весовом соотношении 1:1, добавляют 18 вес.ч. 30 мас.% раствора пероксида водорода для превращения побочных продуктов марганца в растворимые бесцветные ионы Mn (II), затем смесь центрифугируют, полученный осадок растворяют в воде и перемешивают в течение 60 минут, затем вновь центрифугируют, затем выполняют последовательно циклы очистки: первый раз промывают дистиллированной водой, затем трижды промывают водным раствором 4 мас.% соляной кислоты, затем оксид графена сушат на воздухе и отжигают в токе инертного газа при температуре 600°С в течение 30 минут; на 2 этапе получают платиновый композит на носителе из термически обработанного оксида графена, для чего готовят 0,2 мас.% по Pt4+ изопропанольного раствора нитрата платины (IV), для чего берут 23,7 вес.ч. 15 мас.% по Pt4+ раствора нитрата платины (IV) и разбавляют 1572 вес.ч. изопропанола при перемешивании, затем берут 10 - 12 вес.ч. термически обработанного оксида графена, полученного на 1 этапе, и диспергируют его в 1600 вес.ч. изопропанола либо этиленгликоля с помощью ультразвуковой ванны в течение 60 - 120 минут, затем изопропанольный раствор нитрата платины (IV) добавляют к изопропанольной либо этиленгликольной дисперсии термически обработанного оксида графена при постоянном перемешивании в весовом соотношении: Pt4+ : термически обработанный оксид графена = 1 : 4, полученную смесь либо перемешивают при комнатной температуре в течение 24 часов до однородного состава, либо нагревают до 80°С и перемешивают в течение 6 часов до однородного состава - в случае использования в качестве растворителя изопропанола; либо нагревают до 80°С при постоянном перемешивании в течение 2 часов, затем температуру повышают до 180°С и перемешивают её при данной температуре в течение 2 часов до получения однородного состава - в случае использования в качестве растворителя этиленгликоля, затем смесь фильтруют и промывают изопропанолом, осадок сушат на воздухе.
Заявленное техническое решение иллюстрируется Фиг.1 - Фиг.5.
На Фиг. 1 представлены изображения, полученных методом просвечивающей электронной микроскопии в светлом поле (BF-TEM) для синтезированных композитов, а также гистограммы распределения наночастиц по размерам:
1а. BF-TEM изображение композита Pt/anGO-IPA, демонстрирующие морфологию и равномерное распределение наночастиц по поверхности носителя из термически обработанного оксида графена;
1б. Гистограмма распределения по размерам полученных платиновых наночастиц на носителе из термически обработанного оксида графена для композита Pt/anGO-IPA;
1в. BF-TEM изображение композита Pt/anGO-IPA_80, демонстрирующие морфологию и равномерное распределение наночастиц по поверхности носителя из термически обработанного оксида графена;
1г. Гистограмма распределения по размерам полученных платиновых наночастиц на носителе из термически обработанного оксида графена для композита Pt/anGO-IPA_80;
1д. BF-TEM изображение композита Pt/anGO-EG, демонстрирующие морфологию и равномерное распределение наночастиц по поверхности носителя из термически обработанного оксида графена;
1е. Гистограмма распределения по размерам полученных платиновых наночастиц на носителе из термически обработанного оксида графена для композита Pt/anGO-EG.
На Фиг.2 представлено изображение композита Pt/anGO-IPA, полученное методом сканирующей просвечивающей электронной микроскопии в тёмном поле с большим углом (HAADF-STEM), демонстрирующее нахождение платины в трёх состояниях,
где А (жёлтый кружок) - группа наночастиц, Б (фиолетовые кружки) - группа одиночных атомов/ионов или кластеров.
На Фиг. 3 представлены результаты, полученные в ходе тестирования композита Pt/anGO-EG и коммерческого катализатора «PM-20», изготовленного научно-производственным предприятием ООО «Прометей РД», в электрохимической реакции восстановления кислорода в виде серии линейных поляризационных кривых, зарегистрированных при разных скоростях вращения дискового электрода для электрохимической реакции восстановления кислорода, проводимой с использованием (3а) коммерческого катализатора «PM-20» и (3в) композита Pt/anGO-EG. Токи нормированы на площадь стеклоуглеродного рабочего электрода (0,071 см2); график зависимости Коутецкого-Левича, полученные для катализаторов (3б) «PM-20» и (3г) Pt/anGO-EG. Коммерческий катализатор «PM-20» используется в качестве образца сравнения каталитической эффективности:
3а. Серия линейных поляризационных кривых коммерческого катализатора «PM-20», зарегистрированных для электрохимической реакции восстановления кислорода в щелочной среде на установке с вращающимся дисковым электродом со скоростью вращения электрода от 400 до 2500 rpm (об/мин), со скоростью сканирования 5мВ/с; По оси Х указан диапазон значений потенциала относительно обратимого водородного электрода, измеряемый в В, по оси Y указана величина плотности тока, которая измеряется в мА/см2;
3б. График зависимостей Коутецкого-Левича (обратной зависимости величины измеряемой плотности тока от ω-0,5, где ω - скорость вращения дискового электрода в рад/с-0,5) при потенциалах 0,3В, 0,5В и 0,7В относительно обратимого водородного электрода сравнения для коммерческого катализатора «PM-20»; По оси Х указан обратно квадратичные значения величины скорости вращения дискового электрода в рад/с-0,5, по оси Y указаны обратные значения плотности тока в см2/мА;
3в. Серия линейных поляризационных кривых композита Pt/anGO-EG, зарегистрированных для электрохимической реакции восстановления кислорода в щелочной среде на установке с вращающимся дисковым электродом со скоростью вращения электрода от 400 до 2500 rpm (об/мин), со скоростью сканирования 5мВ/с; По оси Х указан диапазон значений потенциала относительно обратимого водородного электрода, измеряемый в В, по оси Y указана величина плотности тока, которая измеряется в мА/см2;
3г. График зависимостей Коутецкого-Левича (обратной зависимости величины измеряемой плотности тока от ω-0,5, где ω - скорость вращения дискового электрода в рад/с-0,5) при потенциалах 0,2В и 0,3В относительно обратимого водородного электрода сравнения для композита Pt/anGO-EG. По оси Х указан обратно квадратичные значения величины скорости вращения дискового электрода в рад/с-0,5, по оси Y указаны обратные значения плотности тока в см2/мА.
На Фиг. 4 представлены результаты, полученные в ходе тестирования композита Pt/anGO-EG и коммерческого катализатора «PM-20», изготовленного научно-производственным предприятием ООО «Прометей РД» в электрохимической реакции окисления водорода в виде серии линейных поляризационных кривых, зарегистрированных при разных скоростях вращения дискового электрода для электрохимической реакции окисления водорода, проводимой с использованием (4а) коммерческого катализатора «PM-20» и (4б) композита Pt/anGO-EG. Токи нормированы на площадь стеклоуглеродного рабочего электрода (0,071 см2). Коммерческий катализатора «PM-20» используется в качестве образца сравнения каталитической эффективности:
4а. Серия линейных поляризационных кривых коммерческого катализатора «PM-20», зарегистрированных для электрохимической реакции окисления водорода в кислой среде на установке с вращающимся дисковым электродом со скоростью вращения электрода от 650 до 2500 rpm (об/мин), со скоростью сканирования 5мВ/с. По оси Х указан диапазон значений потенциала относительно обратимого водородного электрода, измеряемый в В, по оси Y указана величина плотности тока, которая измеряется в мА/см2;
4б. Серия линейных поляризационных кривых композита Pt/anGO-EG, зарегистрированных для электрохимической реакции окисления водорода в кислой среде на установке с вращающимся дисковым электродом со скоростью вращения электрода от 650 до 2500 rpm (об/мин), со скоростью сканирования 5мВ/с. По оси Х указан диапазон значений потенциала относительно обратимого водородного электрода, измеряемый в В, по оси Y указана величина плотности тока, которая измеряется в мА/см2.
На Фиг.5 представлены серии УФ-видимых спектров поглощения, зарегистрированных для реакции восстановления 4 - нитрофенола до 4 - аминофенола в присутствии тетрагидробората натрия (5а) без использования катализатора и с использованием композитов (5б) Pt/anGO-IPA и (5в) Pt/anGO-EG. По оси Х указан диапазон длины волны в нанометрах, при котором регистрировался спектр поглощение в УФ-видимой области, по оси Y указана величина поглощения в относительных единицах. Кроме этого, на фигуре 5 представлены кинетические кривые для (5г) композита Pt/anGO-IPA и (5д) Pt/anGO-EG. По оси Х время в секундах, а по оси Y значения натурального логарифма отношения концентрации 4-нитрофенола в данный момент времени к концентрации 4-нитрофенола в начале реакции до добавления композита Pt/anGO-IPA
5а. Спектры поглощения, зарегистрированный в УФ-вид области для 4-нитрофенола в присутствии 50-кратного избытка тетрагидробората натрия в диапазоне длин волн от 475 до 300 нм;
5б. Серия спектров поглощения, зарегистрированных в УФ-вид области для реакции восстановления 4-нитрофенола в присутствии 50-кратного избытка тетрагидробората натрия и композита Pt/anGO-IPA;
5в. Серия спектров поглощения, зарегистрированных в УФ-вид области для реакции восстановления 4-нитрофенола в присутствии 50-кратного избытка тетрагидробората натрия и композита Pt/anGO-EG;
5г. Линеаризованная кинетическая кривая реакции восстановления 4-нитрофенола в присутствии 50-кратного избытка тетрагидробората натрия и композита Pt/anGO-IPA;
5д. Линеаризованная кинетическая кривая реакции восстановления 4-нитрофенола в присутствии 50-кратного избытка тетрагидробората натрия и композита Pt/anGO-IPA.
Далее заявителем представлено описание заявленного технического решения.
Выявленная техническая проблема решается и заявленный технический результат достигается разработкой способа получения платинового композита, полученного из прекурсора нитрата платины (IV) на носителе из восстановленного путём отжига оксида графена.
Структура и морфология полученного композита исследована с помощью физических методов исследования:
- методом светлопольной просвечивающей микроскопии (BF-TEM),
- методом сканирующей просвечивающей электронной микроскопии в тёмном поле с большим углом (HAADF-STEM).
Заявителем использованы следующие реагенты:
Серная кислота по ГОСТ 2184-2013;
Соляная кислота по ГОСТ 3118-77;
Гидроксид калия по ГОСТ 24363-80;
Перманганат калия по ГОСТ 20490-75;
Графит по ГОСТ 5279-74;
Нитрат платины (IV) по CAS 10102-09-7 [https://www.fishersci.com/shop/products/platinum-iv-nitrate-solution-pt-15-w-w-thermo-scientific/AAH3773703];
Пропанол - 2 (изопропанол) по ГОСТ 9805-84;
Этандиол - 1,2 (этиленгликоль) по ГОСТ 19710-83;
Тетрагидроборат натрия по ГОСТ 4199-76;
4-нитрофенол по ТУ 6-09-3973-75 [https://lenreactiv.ru/shop/himicheskaya/himicheskie_reaktivy/130653/?ysclid=lo765tgpqk451787007];
Сополимер тетрафторэтилена с перфтор-3,6-диокса-4-метил-7-октенсульфоновой кислотой (Нафион) по CAS 31175-20-9 [sigmaaldrich.com];
Катализатора «PM-20», изготовленный научно-производственным предприятием ООО «Прометей РД» [https://www.prometheusrd.com/products].
Заявителем использовано следующее оборудование:
Центрифуга Hettich Rotina 380, Германия;
Ультразвуковая ванна ПСБ - 5760 -05, Россия;
Печь трубчатая LOIP LF-50/500-1200 с модулем управления TS87B, Россия;
Просвечивающий (сканирующий) электронный микроскоп Titan Themis Z, TFS (ThermoFisherScientific), Нидерланды;
УФ-Вид спектрофотометр Hitachi U-2900, Япония;
Просвечивающий (сканирующий) электронный микроскоп Titan Themis Z, TFS (ThermoFisherScientific), Нидерланды;
RRDE-3A Apparatus Ver.3.0 BAS, Япония;
CS series electrochemical workstation, corrtest instruments, Китай;
Лазерный анализатор элементного состава LEA-S500, Республика Беларусь.
Из уровня техники известны платиновые композиты на носителях из различных углеродных материалов, синтез которых в основном проводится с использованием такого известного прекурсора, как гексахлороплатиновая кислота. Для достижения заявленного технического результата заявителем использован прекурсор - нитрат платины (IV), позволяющий получить большую дисперсность полученного композита.
Синтез платинового композита проводили при комнатной температуре или с нагреванием до 80°С или 180°C на носителе из термически обработанного оксида графена, что позволило достигнуть заявленный технический результат.
Далее заявителем приведена последовательность действий заявленного способа, состоящего из 2-х этапов:
1 этап. Получение термически обработанного оксида графена.
2 этап. Синтез заявленного композита.
Далее приведено подробное описание этапов заявленного способа.
1 этап. Получение термически обработанного оксида графена.
Оксид графена синтезируют модифицированным методом Хаммерса [Hummers, W.S.; Offeman, R.E., Preparation of graphite oxide. J. Amer. Chem. Soc. 1958, 80 (6), 1339-1339.].
Для этого 10 вес.ч. графита диспергируют в 1147 вес.ч. 96 мас.% серной кислоты, для чего графит и серную кислоту смешивают и перемешивают в течение 30 минут.
Затем добавляют порционно перманганат калия для окисления графита - четыре раза по 9 вес.ч. (суммарно 36 вес.ч.) при постоянном перемешивании, о завершении окисления судят по исчезновению зелёной окраски.
Затем полученную смесь разбавляют 1300 вес.ч. смеси лёд/вода в весовом соотношении 1:1.
Затем добавляют 18 вес.ч. 30 мас.% раствора пероксида водорода для превращения побочных продуктов марганца в растворимые бесцветные ионы Mn (II).
Затем смесь центрифугируют, например, в течение 40 минут при 5000 об/мин. для отделения оксида графена от кислоты.
Полученный осадок растворяют в воде и перемешивают в течение 60 минут. Затем вновь центрифугируют, например, в течение 40 минут при 5000 об/мин.
Следующие выполняют последовательно циклы очистки: первый раз промывают дистиллированной водой, затем трижды промывают водным раствором 4 мас.% соляной кислоты.
Затем оксид графена сушат на воздухе.
Затем оксид графена отжигают в токе инертного газа при температуре 600°С в течение 30 минут.
Получают термически обработанный оксид графена (anGO).
2 этап. Получение платинового композита на носителе из термически обработанного оксида графена.
Сначала готовят 0,2 мас.% по Pt4+ изопропанольного раствора нитрата платины (IV), для чего берут 23,7 вес.ч. 15 мас.% по Pt4+ раствора нитрата платины (IV) и разбавляют 1572 вес.ч. изопропанола при перемешивании.
Затем берут 10 - 12 вес.ч. термически обработанного оксида графена (anGO), полученного на 1 этапе, и диспергируют его в 1600 вес.ч. изопропанола либо этиленгликоля с помощью ультразвуковой ванны в течение 60 - 120 минут.
Затем изопропанольный раствор нитрата платины (IV) добавляют к изопропанольной либо этиленгликольной дисперсии термически обработанного оксида графена (anGO) при постоянном перемешивании в весовом соотношении: Pt4+ : термически обработанный оксид графена = 1 : 4.
Полученную смесь:
- либо перемешивают при комнатной температуре в течение 24 часов до однородного состава, либо нагревают до 80°С и перемешивают в течение 6 часов до однородного состава - в случае использования в качестве растворителя изопропанола,
- либо нагревают до 80°С при постоянном перемешивании в течение 2 часов, затем температуру повышают до 180°C и перемешивают её при данной температуре в течение 2 часов до получения однородного состава - в случае использования в качестве растворителя этиленгликоля.
Затем смесь фильтруют и промывают изопропанолом, осадок сушат на воздухе.
Получают платиновый композит на носителе из термически обработанного оксида графена.
Далее заявителем приведены примеры осуществления заявленного технического решения.
Пример 1. Проведение 1 этапа - получение термически обработанного оксида графена.
10 г графита (10 вес. ч) диспергируют в 625 мл 96 мас.% (1147 вес. ч.) серной кислоты с использованием, например, верхнеприводной мешалки, для чего графит и серную кислоту смешивают и перемешивают в течение 30 минут.
Затем добавляют порционно перманганат калия для окисления графита - четыре раза по 9 г (суммарно 36 г) при постоянном перемешивании, о завершении окисления судят по исчезновению зелёной окраски.
Затем полученную смесь разбавляют 1300 мл смеси лёд/вода в весовом соотношении 1:1.
Затем добавляют 16 мл 30 мас.% (18 вес. ч.) раствора пероксида водорода для превращения побочных продуктов марганца в растворимые бесцветные ионы Mn (II).
Затем смесь центрифугируют, например, в течение 40 минут при 5000 об/мин. для отделения оксида графена от кислоты.
Полученный осадок растворяют в воде и перемешивают, например, в течение 60 минут. Затем вновь центрифугируют, например, в течение 40 минут при 5000 об/мин.
Затем выполняют последовательно циклы очистки: первый раз промывают дистиллированной водой, затем трижды промывают водным раствором 4 мас.% соляной кислоты.
Затем оксид графена сушат на воздухе, получают 19,95 г оксида графена.
Затем оксид графена отжигают в токе инертного газа при температуре 600°С в течение 30 минут.
Для этого в термостойкую посуду, например, в фарфоровую лодочку, насыпают, например, 110 мг оксида графена. Затем помещают её в кварцевую трубу для отжига в трубчатой печи. Дают ток инертного газа, например, азота, повышают температуру до 600°С и выдерживают при данной температуре в течение 30 минут.
Получают 41,7 мг термически обработанного оксида графена (anGO).
Пример 2. Проведение 2-го этапа - синтез платинового композита на носителе из термически обработанного оксида графена при комнатной температуре.
Сначала готовят 0,2 мас.% по Pt4+ изопропанольного раствора нитрата платины (IV), для чего берут 23,7 мг (23,7 вес.ч.) 15 мас.% по Pt4+ раствора нитрата платины (IV) и разбавляют 1,572 г (1572 вес. ч.) изопропанола при перемешивании.
Затем берут 10 мг (10 вес.ч.) термически обработанного оксида графена полученного на 1 этапе, и диспергируют в 1,6 г (1600 вес.ч.) изопропанола с помощью ультразвуковой ванны в течение 60 минут.
Затем изопропанольный раствор нитрата платины (IV) добавляют к изопропанольной дисперсии термически обработанного оксида графена (anGO) при постоянном перемешивании в весовом соотношении: Pt4+ : термически обработанный оксид графена, мг = 2,5 : 10.
Полученную смесь перемешивают, например, с помощью магнитной мешалки, при комнатной температуре до однородного состава, например, в течение 24 часов.
Затем смесь фильтруют, например, через мембранный фильтр (Например, сyclopore track etched membrane , CYCLPR PCH 47 мм, Dia. 0,4мкм) и промывают, например, 20 мл изопропанола, затем осадок сушат на воздухе.
Получают платиновый композит на носителе из термически обработанного оксида графена Pt/anGO-IPA, в котором содержание платины составляет 14,95 мас.% (данные были получены с помощью лазерного анализатора элементного).
Пример 3. Проведение 2 этапа - синтез платинового композита на носителе из термически обработанного оксида графена при температуре 80°C.
Сначала готовят 0,2 мас.% по Pt4+ изопропанольного раствора нитрата платины (IV), для чего берут 23,7 мг 15 мас.% (23,7 вес.ч.) по Pt4+ раствора нитрата платины (IV) и разбавляют 1,572 г (1572 вес. ч.) изопропанола при перемешивании.
Затем берут 11 мг (11 вес.ч.) термически обработанного оксида графена полученного на 1 этапе, и диспергируют в 1,6 г (1600 вес.ч.) изопропанола с помощью ультразвуковой ванны в течение 90 минут.
Затем изопропанольный раствор нитрата платины (IV) добавляют к изопропанольной дисперсии термически обработанного оксида графена (anGO) при постоянном перемешивании в весовом соотношении: Pt4+ : термически обработанный оксид графена, мг = 2,75 : 11.
Полученную смесь нагревают до 80°С при постоянном перемешивании, например, с помощью магнитной мешалки, и перемешивают её при данной температуре в течение 6 часов до однородного состава.
Затем смесь фильтруют, например, через мембранный фильтр (Например, сyclopore track etched membrane, CYCLPR PCH 47 мм, Dia. 0,4мкм) и промывают, например, 20 мл изопропанола, затем осадок сушат на воздухе.
Получают платиновый композит на носителе из термически обработанного оксида графена Pt/anGO-IPA_80, в котором содержание платины составляет 12,38 мас.% (данные были получены с помощью лазерного анализатора элементного).
Пример 4. Проведение 2 этапа - синтез платинового композита на носителе из термически обработанного оксида графена при температуре 180°С.
Сначала готовят 0,2 мас.% по Pt4+ изопропанольного раствора нитрата платины (IV), для чего берут 23,7 мг 15 мас.% (23,7 вес.ч.) по Pt4+ раствора нитрата платины (IV) и разбавляют 1,572 г (1572 вес. ч.) изопропанола при перемешивании.
Затем берут 12 мг (12 вес.ч.) термически обработанного оксида графена полученного на 1 этапе, и диспергируют в 1,6 г (1600 вес.ч.) этиленгликоля с помощью ультразвуковой ванны в течение 120 минут.
Затем изопропанольный раствор нитрата платины (IV) добавляют к этиленгликольной дисперсии термически обработанного оксида графена (anGO) при постоянном перемешивании в весовом соотношении: Pt4+ : термически обработанный оксид графена, мг = 3 : 12.
Полученную смесь нагревают до 80°С при постоянном перемешивании, например, с помощью магнитной мешалки, в течение 2 часов, затем температуру повышают до 180°C и перемешивают её при данной температуре в течение 2 часов до получения однородного состава.
Затем смесь фильтруют, например, через мембранный фильтр (Например, сyclopore track etched membrane, CYCLPR PCH 47 мм, Dia. 0,4мкм) и промывают, например, 20 мл изопропанола, затем осадок сушат на воздухе.
Получают платиновый композит на носителе из термически обработанного оксида графена Pt/anGO-EG, в котором содержание платины составляет 10,07 мас.% (данные были получены с помощью лазерного анализатора элементного).
Далее приведены примеры 5, 6, 7, 8 и 9 исследования структуры и морфологии полученных композитов с помощью современных физических методов, а также изучение их каталитической способности по отношению к реакции электрохимического восстановления кислорода, электрохимического окисления водорода и восстановления 4-нитрофенола до 4-аминофенола в присутствии избытка тетрагидробората натрия.
Пример 5. Изучение полученных композитов методом светлопольной просвечивающей микроскопии (BF-TEM ) (Фиг.1).
На фигуре 1 представлены изображения композитов Pt/anGO-IPA, Pt/anGO-IPA_80 и Pt/anGO-EG, демонстрирующие равномерное распределение наночастиц с квазисферической формой по поверхности носителя из термически обработанного оксида графена.
На фигуре 1а продемонстрировано равномерное распределение наночастиц платины композита Pt/anGO-IPA на поверхности носителя из термически обработанного оксида графена. Полученные наночастицы располагаются по-отдельности, не образуя агломератов;
На фигуре 1б представлена гистограмма распределения платиновых наночастиц композита Pt/anGO-IPA по размерам. Согласно полученным данным средние размеры наночастиц составляют 1,4 нм;
На фигуре 1в продемонстрировано равномерное распределение наночастиц платины композита Pt/anGO-IPA_80 на поверхности носителя из термически обработанного оксида графена. В отличие от наночастиц композита Pt/anGO-IPA, платиновые наночастицы композита Pt/anGO-IPA_80 находятся на поверхности носителя в большинстве случаев в виде нитевидных скоплений;
На фигуре 1г представлена гистограмма распределения платиновых наночастиц композита Pt/anGO-IPA_80 по размерам. Согласно полученным данным средние размеры наночастиц составляют 2,4 нм;
На фигуре 1д продемонстрировано наличие платиновых наночастиц композита Pt/anGO-EG, равномерно распределённых по поверхности носителя из термически обработанного оксида графена. На фигуре 1д можно наблюдать, что большинство платиновых наночастиц находится на носителе по-отдельности, а не в виде агломератов;
На фигуре 1е представлена гистограмма распределения платиновых наночастиц композита Pt/anGO-EG по размерам. Согласно полученным данным средние размеры наночастиц составляют 2,8 нм.
Пример 6. Изучение Pt/anGO-IPA методом сканирующей просвечивающей электронной микроскопии в тёмном поле с большим углом (HAADF-STEM) (Фиг.2).
На фигуре 2 представлено HAADF-STEM изображение композита Pt/anGO-IPA, на котором видно, что платина на носителе из термически обработанного оксида графена находится в трёх состояниях: платиновые наночастицы со средними размерами 1,4 нм (выделены на фигуре 2 рамкой жёлтого цвета), одиночные атомы/ионы и кластеры (выделены на фигуре 2 рамкой фиолетового цвета).
Пример 7. Изучение каталитической активности полученного композита в электрохимической реакции восстановления кислорода
Каталитическая активность композита Pt/anGO-EG и коммерческого катализатора «PM-20», изготовленного научно-производственным предприятием ООО «Прометей РД» (используется в качестве образца сравнения каталитической эффективности в электрохимической реакции восстановления кислорода) была изучена в электрохимической реакции восстановления кислорода с использованием установки с вращающимся дисковым электродом.
На основании полученных линейных поляризационных кривых были построены зависимости Коутецкого-Левича, благодаря которым вычислено количество электронов, принимающих участие в электрохимической реакции восстановления кислорода, и установлен механизм реакции. В дальнейшем на основании установленных параметров сделан вывод о каталитической эффективности композита/катализатора при данной загрузке на поверхность рабочего электрода.
Электрохимическую реакцию восстановления кислорода проводят в трёхэлектродной ячейке, состоящей из ртутнооксидного электрода сравнения, графитового противоэлектрода, стеклоуглеродного вращающегося дискового электрода - рабочего электрода (RRDE-3A Apparatus Ver.3.0 BAS) с S = 0.071 см2 и электролита - раствора гидроксида калия с концентрацией 0,1 моль/л.
Электрохимическая ячейка подключается к бипотенциостату (Corrtest Instruments, CS2350).
Предварительно изготавливают чернила исследуемого материала следующим образом: 1. взвешивают 1,2 мг исследуемого материала и 2. диспергируют в 400 мкл изопропанола и 100 мкл изопропанольного раствора Нафиона с концентрацией 0,001 мас.% с помощью ультразвуковой мешалки в течение 60 минут при комнатной температуре.
По описанной выше процедуре приготавливаются чернила композита Pt/anGO-EG и коммерческого катализатора «PM-20», изготовленного научно-производственным предприятием ООО «Прометей РД».
2,95 мкл готовых чернил композита Pt/anGO-EG и катализатора «PM-20», в которых содержится 0,007 мг композита или катализатора, наносят с помощью микропипетки на стеклоуглеродную поверхность рабочего электрода и сушат на воздухе (загрузка катализатора на поверхность рабочего электрода составляет 0,1 мг/см2).
Рабочий электрод с нанесённым композитом или катализатором опускают в электролит и полностью собирают электрохимическую ячейку.
До начала непосредственного проведения электрохимической реакции восстановления кислорода через раствор гидроксида калия (V = 60 мл, Сm = 0,1 моль/л) в течение 30 минут барботируют газ - чистый кислород. Далее регистрируют серию линейных поляризационных кривых по следующей методике:
1. Скорость вращения дискового электрода - 400 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 1,15В до 0,2В относительно обратимого водородного электрода;
2. Скорость вращения дискового электрода - 650 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 1,15В до 0,2В относительно обратимого водородного электрода;
3. Скорость вращения дискового электрода - 980 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 1,15В до 0,2В относительно обратимого водородного электрода;
4. Скорость вращения дискового электрода - 1500 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 1,15В до 0,2В относительно обратимого водородного электрода;
5. Скорость вращения дискового электрода - 2000 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 1,15В до 0,2В относительно обратимого водородного электрода;
6. Скорость вращения дискового электрода - 2500 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 1,15В до 0,2В относительно обратимого водородного электрода;
Заданную шкалу потенциалов пересчитывают на шкалу обратимого водородного электрода сравнения по следующей формуле:
ERHE = EHg/HgO + E°Hg/HgO + 0.059pH (формула 1),
где ERHE - потенциал обратимого водородного электрода;
EHg/HgO - потенциал ртутнооксидного электрода сравнения, значение которого было задано для проведения электрохимической реакции восстановления кислорода;
E°Hg/HgO - номинальное значение потенциала ртутнооксидного электрода относительно стандартного водородного электрода при температуре 25°С;
pH - водородный показатель электролита, в котором проводится электрохимическая реакция восстановления кислорода.
После получения серии линейных поляризационных кривых (Фиг. 3а и 3в) строят зависимости Коутецкого - Левича (зависимости 1/i - 1/ω0,5, где ω - скорость вращения дискового электрода, рад/с) при потенциалах 0,3В, 0,5В и 0,7В относительно обратимого водородного электрода (Фиг. 3б и 3г). В дальнейшем определяют угол наклона полученных зависимостей, с помощью которого в дальнейшем рассчитывают количество электронов по формуле 2, участвующих в электрохимической реакции восстановления кислорода.
1/i = 1/iк + 1/iд (уравнение 1),
где i - плотность тока на дисковом электроде (мА/см2);
iк - плотность кинетического тока (мА/см2);
iд - плотность диффузионного тока (мА/см2).
Величина диффузионного тока описывается формулой
iд= 0.62nFD2/3υ -1/6cω0,5 (формула 2),
где iд - плотность диффузионного тока (мА/см2);
ω - скорость вращения дискового электрода (рад/с);
n - количество электронов, участвующих в реакции электровосстановления молекулы кислорода;
F - постоянная Фарадея (Кл/моль);
D - коэффициент диффузии (см2/с);
υ - кинематическая вязкость электролита (см2/с);
с - концентрация кислорода в растворе (моль/см3).
Согласно полученным результатам, представленным в приведенной ниже Таблице 1, можно сделать вывод о том, что в случае использования катализатора «PM-20» с загрузкой 0,1 мг/см2 реализуется 2-х электронный механизм реакции, который приводит к получению пероксид ионов. Для катализатора Pt/anGO-EG при той же загрузке наблюдается 4-х электронный механизм реакции, который приводит к образованию гидроксид ионов.
Электрохимическое восстановление кислорода по 4-х электронному механизму предпочтительнее, чем по 2-х электронному механизму, так как 4-х электронный механизм требуется для эффективного функционирования водородного топливного элемента. Следовательно, можно сделать вывод о том, что эффективность катализатора Pt/anGO-EG выше, чем катализатора «PM-20».
Таблица 1. Сводные результаты электрохимических исследований катализаторов «PM-20» и Pt/anGO-EG в реакции восстановления кислорода на вращающемся дисковом электроде
y = -0,051 + 5,333x (R2 = 0,969)
При 0,5В:
y = -0,054 + 5,722
(R2 = 0,961)
При 0,7В:
y = 0,007 + 6,258x (R2 = 0,959)
y = 0,054+2.933x
(R2 = 0,955)
При 0,5В:
y = 0,029+2.895x
(R2 = 0,961)
При 0,3В:
y = 0,019+2,797x
(R2 = 0,966)
Пример 8. Изучение каталитической активности полученного композита в электрохимической реакции окисления водорода
Каталитическая активность композита Pt/anGO-EG и коммерческого катализатора «PM-20», изготовленного научно-производственным предприятием ООО «Прометей РД» (используется в качестве образца сравнения каталитической эффективности в электрохимической реакции восстановления кислорода) была изучена в электрохимической реакции окисления водорода с использованием установки с вращающимся дисковым электродом. На основании полученных линейных поляризационных кривых были установлены значения диффузионного тока и плотности тока для композита/катализатора при скорости вращения дискового электрода 2500 rpm (об/мин). Полученные значение сравнили с теоретическим и сделали вывод о каталитической эффективности композита/катализатора при данной загрузке на поверхность рабочего электрода.
Электрохимическую реакцию окисления водорода проводят в трёхэлектродной ячейке, состоящей из хлоридсеребряного электрода сравнения, графитового противоэлектрода, стеклоуглеродного вращающегося дискового электрода - рабочего электрода (RRDE-3A Apparatus Ver.3.0 BAS) с S = 0.071 см2 и электролита - раствора серной кислоты с концентрацией 0,5 моль/л.
Электрохимическая ячейка подключается к бипотенциостату (Corrtest Instruments, CS2350).
Предварительно изготавливают чернила исследуемого материала следующим образом: 1. взвешивают 1,2 мг исследуемого материала и 2. диспергируют в 400 мкл изопропанола и 100 мкл изопропанольного раствора Нафиона с концентрацией 0,001 мас.% с помощью ультразвуковой мешалки в течение 60 минут при комнатной температуре.
По описанной выше процедуре приготавливаются чернила катализатора Pt/anGO-EG и коммерческого катализатора «PM-20», изготовленного научно-производственным предприятием ООО «Прометей РД». Последний используется в качестве образца сравнения каталитической эффективности в электрохимической реакции окисления водорода.
2,95 мкл готовых чернил, в которых содержится 0,007 мг катализатора, наносят на стеклоуглеродную поверхность рабочего электрода и сушат на воздухе (загрузка катализатора на поверхность рабочего электрода составила 0,1 мг/см2).
Рабочий электрод с нанесённым катализатором опускают в электролит и полностью собирают электрохимическую ячейку.
До начала непосредственного проведения электрохимической реакции окисления водорода через раствор серной кислоты в течение 30 минут барботируют газ - чистый водород. Далее регистрируют серию линейных поляризационных кривых по следующей методике:
1. Скорость вращения дискового электрода - 650 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 0 до 0,4В относительно обратимого водородного электрода;
2. Скорость вращения дискового электрода - 980 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 0 до 0,4В относительно обратимого водородного электрода;
3. Скорость вращения дискового электрода - 1500 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 0 до 0,4В относительно обратимого водородного электрода;
4. Скорость вращения дискового электрода - 2000 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 0 до 0,4В относительно обратимого водородного электрода;
5. Скорость вращения дискового электрода - 2500 rpm (об/мин), скорость сканирования 5мВ/с, интервал потенциалов от 0 до 0,4В относительно обратимого водородного электрода.
Заданную шкалу потенциалов пересчитывают на шкалу обратимого водородного электрода сравнения по следующей формуле:
ERHE = EAg/AgCl + EAg/AgCl+ 0,059pH (формула 3),
где ERHE - потенциал обратимого водородного электрода;
EAg/AgCl - потенциал хлоридсеребряного электрода сравнения, значение которого было задано для проведения электрохимической реакции восстановления кислорода;
E°Ag/AgCl - номинальное значение потенциала хлоридсеребряного электрода относительно стандартного водородного электрода при температуре 25°С;
pH - водородный показатель электролита, в котором проводится электрохимическая реакция восстановления кислорода.
Согласно полученным данным (фиг. 4а и 4б) катализатор Pt/anGO-EG показывает более высокие плотности тока по сравнению с «PM-20». Предельная плотность тока при максимальной скорости вращения дискового электрода (2500 rpm) была ниже рассчитанного значения на 34% для катализатора Pt/anGO-EG и на 66% для катализатора «PM-20» (при данной загрузке катализатора на поверхность рабочего электрода).
Теоретическую плотность тока рассчитывают по формуле 2 и получают значение равное 3,2 мА/см2.
Согласно полученным данным можно сделать вывод о том, что эффективность катализатора Pt/anGO-EG в электрохимической реакции окисления водорода, проводимой в кислой среде, выше по сравнению с каталитической эффективность катализатора «PM-20».
Пример 9. Изучение каталитической активности полученного композита в реакции восстановления 4-нитрофенола до 4-аминофенола
Демонстрация проявления каталитических свойств композитами Pt/anGO-IPA и Pt/anGO-EG была проведена в реакции восстановления 4-нитрофенола до 4-аминофенола в присутствии избытка тетрагидробората натрия, являющейся эталонной реакцией тестирования каталитической активности новых материалов.
Предварительно для проведения реакции восстановления нитроароматического соединения готовят водный раствор 4-нитрофенола в мерной колбе объёмом 100 мл, в которой содержится 1,39 мг 4-нитрофенола.
Затем отбирают аликвоту объёмом 20 мл полученного водного раствора 4-нитрофенола.
Затем взвешивают 13,9 мг тетрагидробората натрия и 1,2 мг композита Pt/anGO-IPA или Pt/anGO-EG.
В дальнейшем к водному раствору 4-нитрофенола добавляют тетрагидроборат, перемешивают для смешения этих реагентов с целью получения промежуточного соединения, 4-нитрофенолята натрия. Далее к полученному раствору добавляют композит Pt/anGO-IPA или Pt/anGO-EG при постоянном перемешивании раствора и отмечают начало проведения эксперимента.
Через некоторые промежутки времени отбирают порции раствора в кварцевую кювету толщиной 5 мм для их анализа с помощью УФ-вид (ультрафиолетовая и видимая область) спектроскопии, с помощью которой регистрируют спектры поглощения в диапазоне длин волн от 475 нм до 300 нм (раствором сравнения является дистиллированная вода, которая также находится в кварцевой кювете толщиной 5мм)
На фигуре 5а представлена серия спектров поглощения в УФ-видимой области для реакции восстановления 4-нитрофенола до 4-аминофенола в присутствии 50-кратного избытка тетрагидробората натрия. На фигуре видно, что высота пиков поглощения
4-нитрофенолят иона при 400 нм практически не изменяется в первые 12 часов после добавления к водному раствору 4-нитрофенола тетрагидробората натрия. Такие данные свидетельствуют о том, что реакция восстановления 4-нитрофенола до 4-аминофенола практически не идёт без катализатора.
На фигуре 5б представлена серия спектров поглощения в УФ-видимой области для реакции восстановления 4-нитрофенола до 4-аминофенола в присутствии 50-кратного избытка тетрагидробората натрия и композита Pt/anGO-IPA. На фигуре видно, что высота пиков поглощения 4-нитрофенолят иона при 400 нм значительно уменьшается в течение 45 минут после начала проведения эксперимента. Такие данные свидетельствуют о том, что в присутствии композита Pt/anGO-IPA проходит реакция восстановления 4-нитрофенола до 4-аминофенола. Следовательно композит Pt/anGO-IPA обладает каталитическими свойствами в этой реакции.
На фигуре 5в представлена серия спектров поглощения в уф-видимой области для реакции восстановления 4-нитрофенола до 4-аминофенола в присутствии 50 - кратного избытка тетрагидробората натрия и композита Pt/anGO-EG. На фигуре видно, что высота пиков поглощения 4-нитрофенолят иона при 400 нм значительно уменьшается в течение 41 минут после начала проведения эксперимента. Такие данные свидетельствуют о том, что в присутствии композита Pt/anGO-IPA проходит реакция восстановления
4-нитрофенола до 4-аминофенола. Следовательно композит Pt/anGO-IPA обладает каталитическими свойствами в этой реакции.
В дальнейшем для определения константы скорости реакции было принято допущение, что реакция восстановления 4-нитрофенола до 4-аминофенола является реакцией первого порядка, так как её проводят в присутствии 50-кратного избытка тетрагидробората натрия.
На фигуре 5г представлена линеаризованная кинетическая кривая композита Pt/anGO-IPA. На графике видно, что кривая имеет два участка. В течение 17 минут после добавления композита Pt/anGO-IPA к смеси 4-нитрофенола и тетрагидробората натрия, реакция проходит с достаточно высокой скоростью, о чём свидетельствует большой наклон кривой, при этом константа скорости реакции (k1) на данном участке составляет 5,819*10-4 c-1. Меньший наклон кривой, который ведёт после 17 минуты проведения реакции восстановления, может свидетельствовать о замедлении реакции восстановления в присутствии композита Pt/anGO-IPA. Константа скорости реакции (k2) на данном участке отличается от константы скорости реакции (k1) почти в два раза и составляет 2,435*10-4 с-1.
На фигуре 5д представлена линеаризованная кинетическая кривая композита Pt/anGO-EG. На графике видно, что кривая имеет два участка. В течение 9 минут после добавления композита Pt/anGO-EG к смеси 4-нитрофенола и тетрагидробората натрия, реакция проходит с достаточно высокой скоростью, о чём свидетельствует большой наклон кривой, при этом константа скорости реакции (k1) на данном участке составляет 5,029*10-4 c-1. Меньший наклон кривой, который ведёт после 9 минуты проведения реакции восстановления может свидетельствовать о замедлении реакции восстановления в присутствии композита Pt/anGO-EG. Константа скорости реакции (k2) на данном участке отличается от константы скорости реакции (k1) почти в два раза и составляет
2,370*10-4 с-1.
Для сравнения константы скорости реакции были рассчитаны коэффициенты активности композитов Pt/anGO-IPA и Pt/anGO-EG, как отношение констант скорости реакций к массе металла, который содержится в композите. Полученные данные представлены в таблице.
Таблица 2. Сводные результаты исследований каталитических свойств композитов Pt/anGO-IPA и Pt/anGO-EG в реакции восстановления 4-нитрофенола до 4-аминофенола в присутствии 50-кратного избытка тетрагидробората натрия.
Согласно полученным данным можно сделать вывод о том, что композиты Pt/anGO-IPA и Pt/anGO-EG обладают каталитическими свойствами в реакции восстановления 4-нитрофенола до 4-аминофенола в присутствии 50-кратного избытка тетрагидробората натрия.
Таким образом, из приведённых выше данных можно сделать вывод, что заявителем решена выявленная техническая проблема и достигнут заявленный технический результат, а именно: разработан способ получения платинового композита на носителе из термически обработанного оксида графена, позволивший устранить недостатки выявленных аналогов, а именно:
- повысить степень дисперсии катализатора (получены одиночные атомы/ионы, кластеры платины, а также наночастицы платины средний размер которых варьировался от 1,4 нм до 2,8 нм) благодаря использованию в качестве носителя термически обработанного оксида графена, который имеет большую удельную поверхность, достаточное количество кислородсодержащих функциональных групп на поверхности носителя, а также на краях дефектов, которые играют роль связывания металлического компонента с поверхностью носителя. Вследствие того, что данные функциональные группы плотно и равномерно располагаются на поверхности носителя, основной металлический компонент катализатора также равномерно и плотно распределяется по поверхности носителя;
- использовать в качестве прекурсора нитрат платины (IV), что позволяет получить более высокодисперсный катализатор по сравнению с использованием в качестве прекурсора гексахлороплатината (IV) калия. Кроме того, нитрат платины (IV) обеспечивает более равномерное распределение частиц платины на поверхности носителя из термически обработанного оксида графена;
- улучшить технологичность благодаря разработке заявленного способа получения платинового катализатора на носителе из термически обработанного оксида графена, последняя стадия синтеза которого осуществляется: 1 - при температуре не выше 180°С по сравнению с 550°С, 250°С в токе водорода, описанных в аналогах, 2 - без использования микроволного излучения высокой мощности в аналоге, и 3 - с использованием спиртового растворителя в качестве основной среды для проведения синтеза по сравнению с использованием дистиллированной воды в аналоге.
Таким образом, заявителем проведены исследования структуры и морфологии полученных композитов с помощью современных физических методов. В результате было установлено, что двумерная структура носителя сохраняется во время отжига исходного оксида графена. На поверхности полученного носителя были образованы платиновые наночастицы, которые в композите Pt/anGO-IPA имели средний размер 1,4 нм, в композите Pt/anGO-IPA_80 - 2,4 нм, а в композите Pt/anGO-EG - 2,8 нм. Помимо платиновых наночастиц в композите Pt/anGO-IPA содержались кластеры и одиночные атомы/ионы платины. В трёх композитах металлическая составляющая имела высокую степень дисперсности.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения биметаллического электрокатализатора на основе платиновых ядер | 2021 |
|
RU2778126C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРОВ С НАНОРАЗМЕРНЫМИ ЧАСТИЦАМИ ПЛАТИНЫ И ЕЕ СПЛАВОВ С МЕТАЛЛАМИ | 2018 |
|
RU2695999C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КАТАЛИТИЧЕСКОГО ЭЛЕКТРОДА НА ОСНОВЕ ГЕТЕРОПОЛИСОЕДИНЕНИЙ ДЛЯ ВОДОРОДНЫХ И МЕТАНОЛЬНЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2012 |
|
RU2561711C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ МЕТАЛЛ-ОКСИДНОГО КАТАЛИТИЧЕСКОГО ЭЛЕКТРОДА ДЛЯ НИЗКОТЕМПЕРАТУРНЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2012 |
|
RU2522979C2 |
| ГАЗОАНАЛИТИЧЕСКИЙ МУЛЬТИСЕНСОРНЫЙ ЧИП НА ОСНОВЕ ГРАФЕНА, МОДИФИЦИРОВАННОГО НАНОЧАСТИЦАМИ БЛАГОРОДНЫХ МЕТАЛЛОВ, И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2023 |
|
RU2814586C1 |
| ЭЛЕКТРОКАТАЛИЗАТОР ДЛЯ ТВЁРДОПОЛИМЕРНЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2022 |
|
RU2798434C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КАТАЛИТИЧЕСКОГО СЛОЯ ЭЛЕКТРОДОВ ДЛЯ ТВЕРДОПОЛИМЕРНОГО ТОПЛИВНОГО ЭЛЕМЕНТА | 2021 |
|
RU2781052C1 |
| КАТАЛИЗАТОР КОНВЕРСИИ УГЛЕВОДОРОДОВ, СПОСОБ КАТАЛИТИЧЕСКОГО РЕФОРМИНГА ИСХОДНОЙ НАФТЫ С ИСПОЛЬЗОВАНИЕМ КАТАЛИЗАТОРА | 1997 |
|
RU2186622C2 |
| КАТАЛИЗАТОР ДЛЯ ТВЁРДОПОЛИМЕРНЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2022 |
|
RU2802919C1 |
| Способ получения платиносодержащих катализаторов для топливных элементов и электролизеров | 2022 |
|
RU2775979C1 |
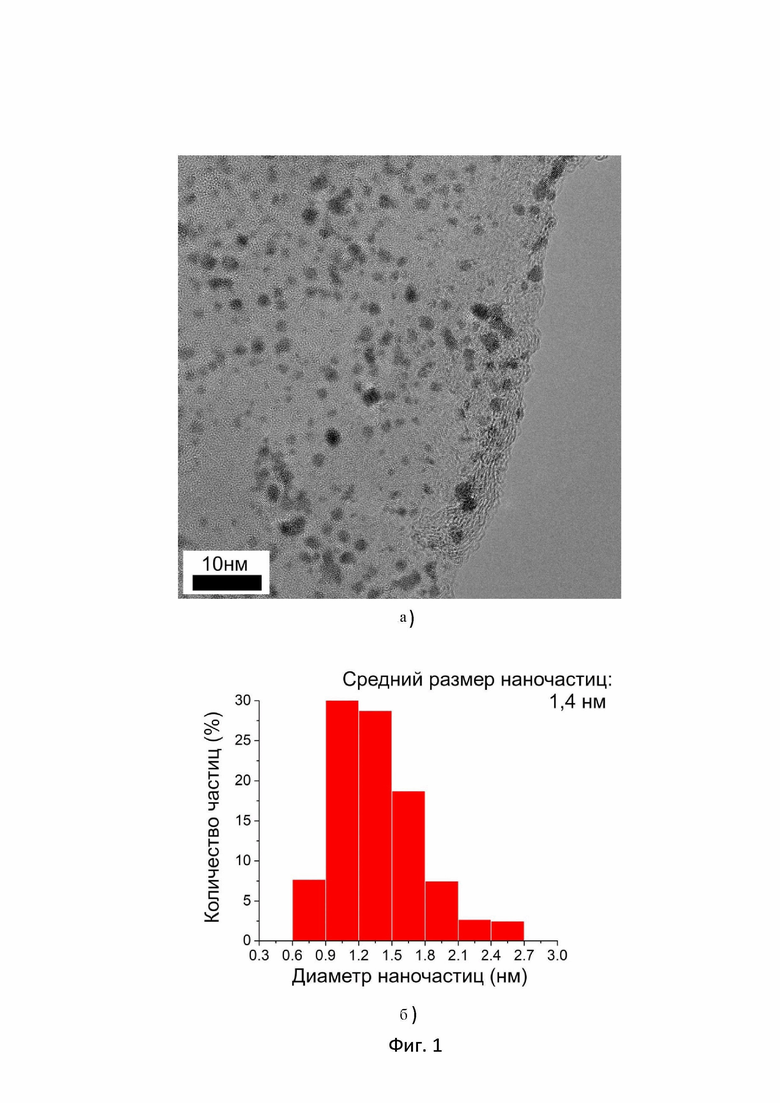
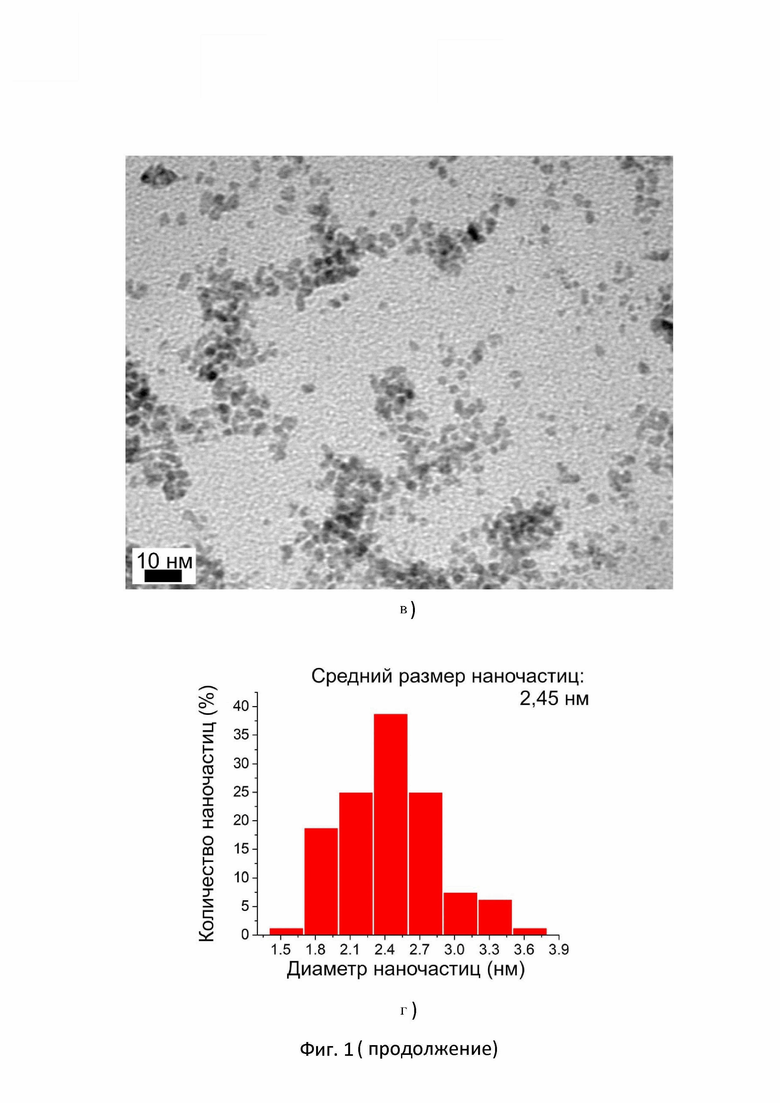
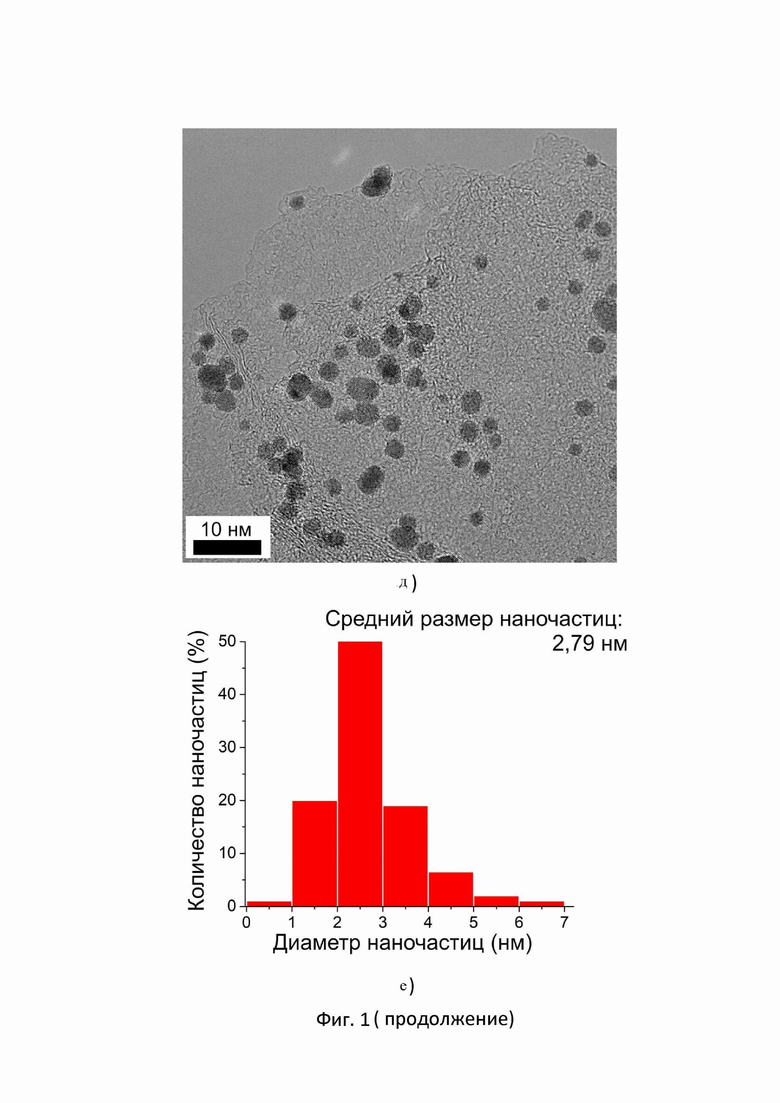


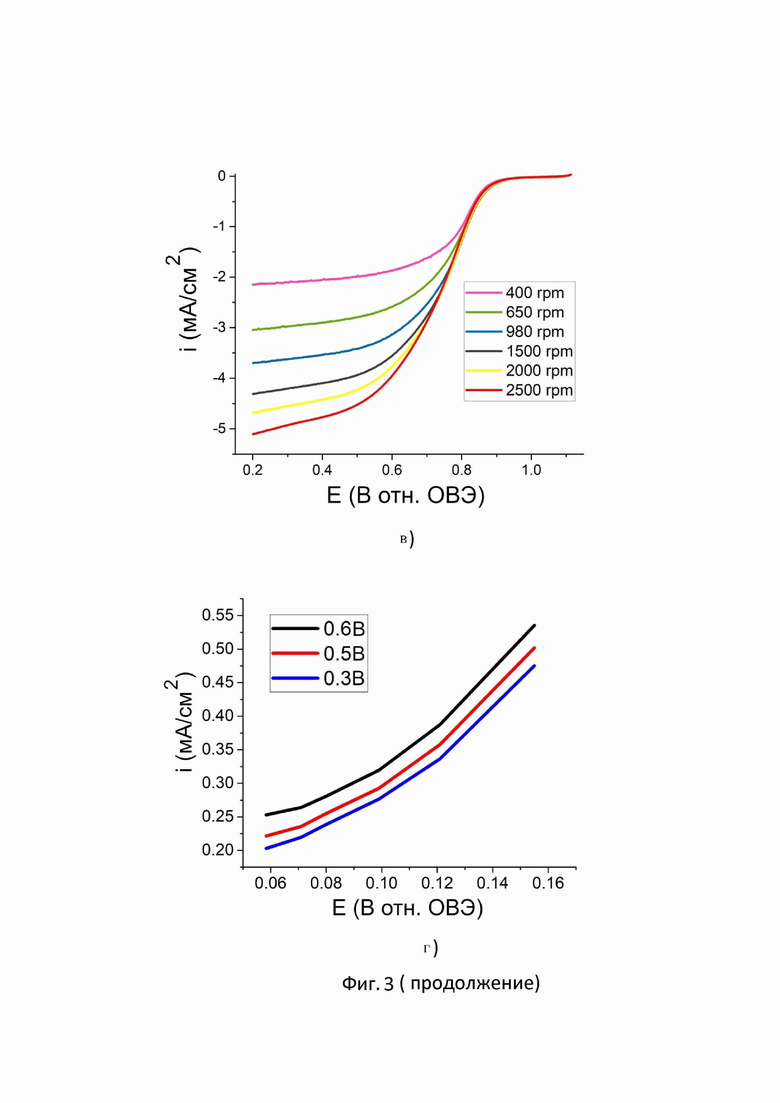
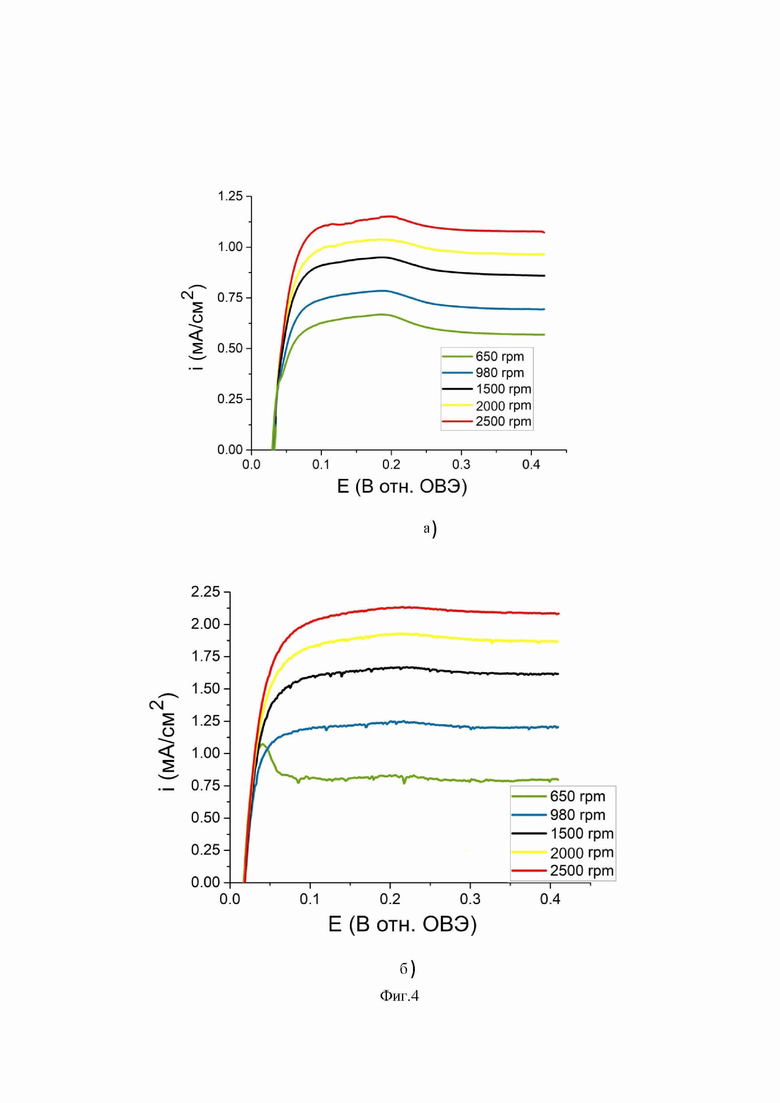
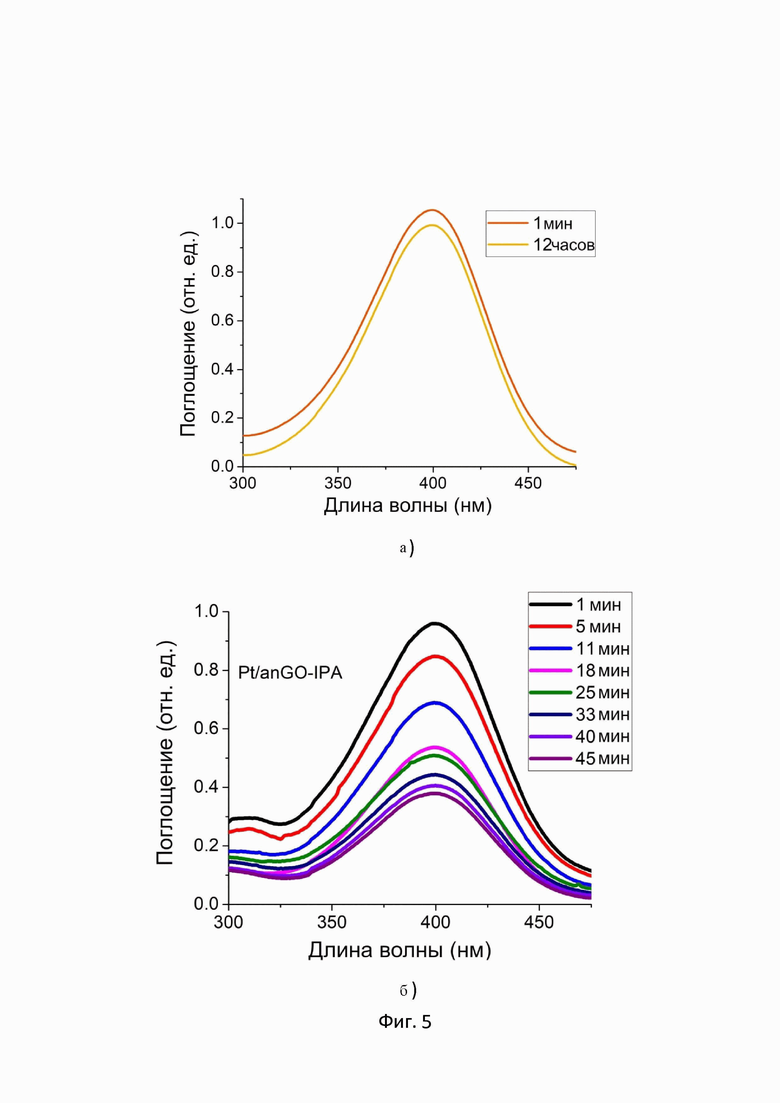
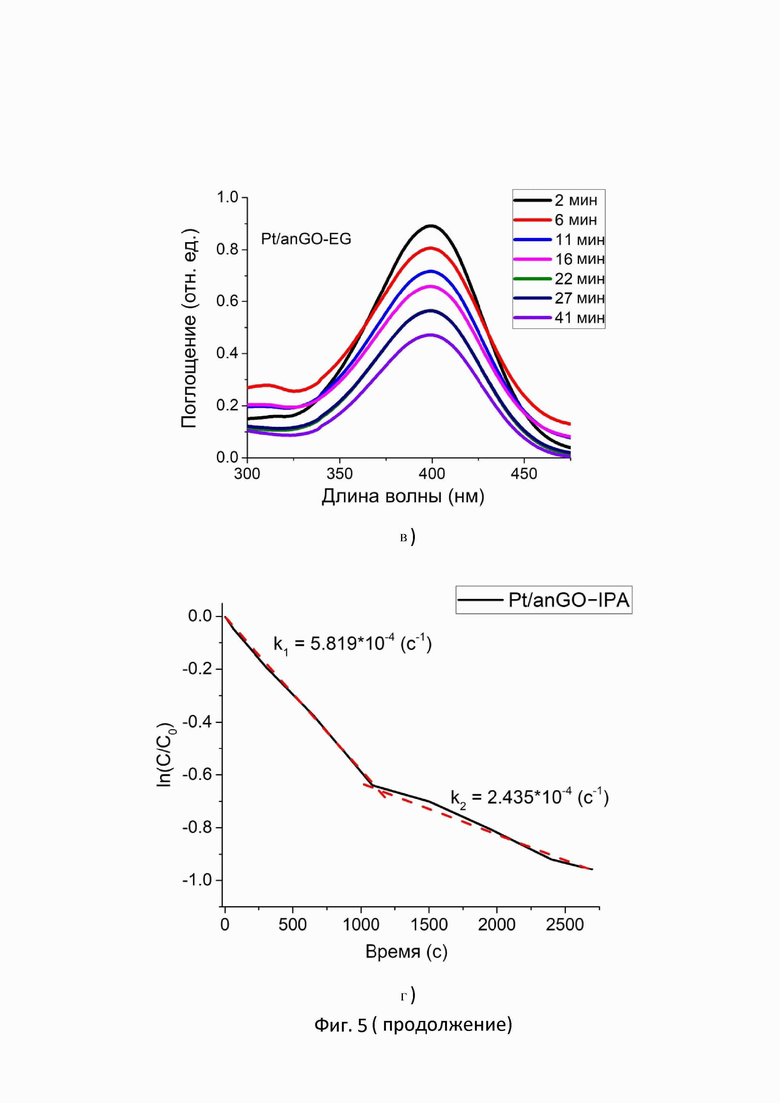
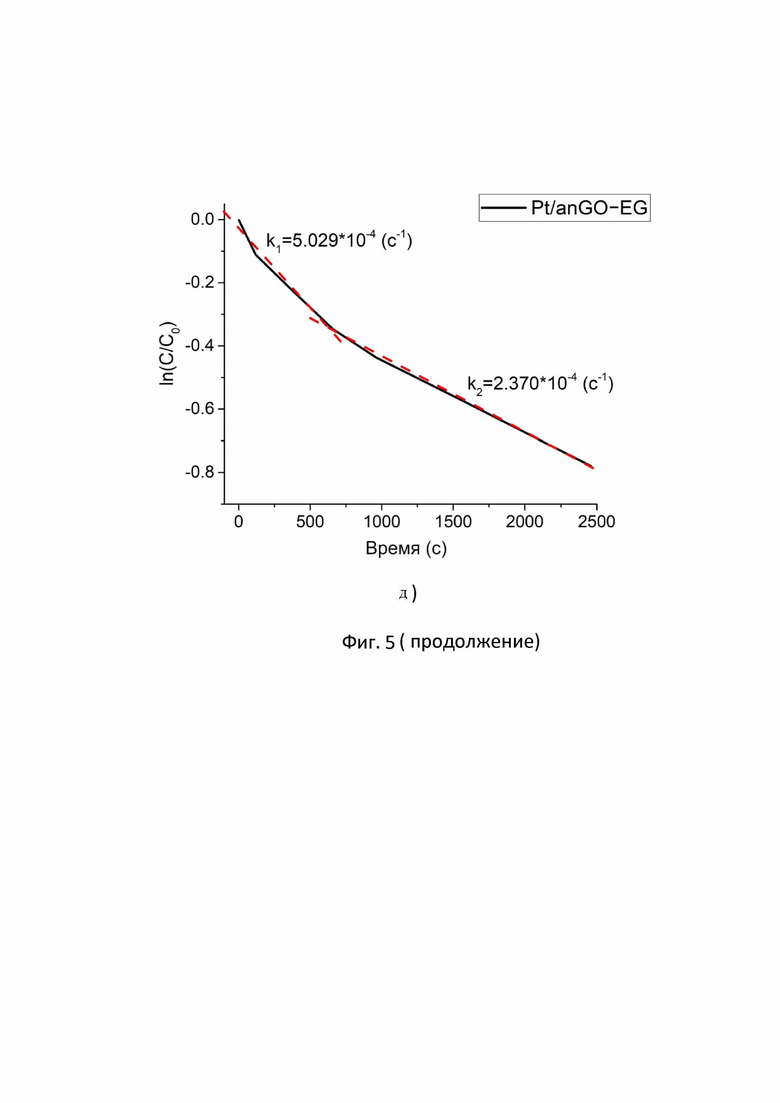
Настоящее изобретение относится к способу получения платинового композита на носителе из термически обработанного оксида графена, включающему два этапа. На 1 этапе получают термически обработанный оксида графена, для чего 10 вес.ч. графита диспергируют в 1147 вес.ч. 96 мас.% серной кислоты, для чего графит и серную кислоту смешивают и перемешивают в течение 30 минут, затем добавляют порционно перманганат калия для окисления графита – четыре раза по 9 вес.ч., суммарно 36 вес.ч., при постоянном перемешивании, о завершении окисления судят по исчезновению зелёной окраски, затем полученную смесь разбавляют 1300 вес.ч. смеси лёд/вода в весовом соотношении 1:1, добавляют 18 вес.ч. 30 мас.% раствора пероксида водорода для превращения побочных продуктов марганца в растворимые бесцветные ионы Mn (II), затем смесь центрифугируют, полученный осадок растворяют в воде и перемешивают в течение 60 минут, затем вновь центрифугируют, затем выполняют последовательно циклы очистки: первый раз промывают дистиллированной водой, затем трижды промывают водным раствором 4 мас.% соляной кислоты, затем оксид графена сушат на воздухе и отжигают в токе инертного газа при температуре 600°С в течение 30 минут. На 2 этапе получают платиновый композит на носителе из термически обработанного оксида графена, для чего готовят 0,2 мас.% по Pt4+ изопропанольного раствора нитрата платины (IV), для чего берут 23,7 вес.ч. 15 мас.% по Pt4+ раствора нитрата платины (IV) и разбавляют 1572 вес.ч. изопропанола при перемешивании, затем берут 10-12 вес.ч. термически обработанного оксида графена, полученного на 1 этапе, и диспергируют его в 1600 вес.ч. изопропанола либо этиленгликоля с помощью ультразвуковой ванны в течение 60-120 минут, затем изопропанольный раствор нитрата платины (IV) добавляют к изопропанольной либо этиленгликольной дисперсии термически обработанного оксида графена при постоянном перемешивании в весовом соотношении Pt4+:термически обработанный оксид графена=1:4, полученную смесь либо перемешивают при комнатной температуре в течение 24 часов до однородного состава, либо нагревают до 80°С и перемешивают в течение 6 часов до однородного состава – в случае использования в качестве растворителя изопропанола; либо нагревают до 80°С при постоянном перемешивании в течение 2 часов, затем температуру повышают до 180°С и перемешивают её при данной температуре в течение 2 часов до получения однородного состава – в случае использования в качестве растворителя этиленгликоля, затем смесь фильтруют и промывают изопропанолом, осадок сушат на воздухе. Изобретение позволяет повысить каталитическую эффективность композита, обеспечить равномерное распределение наночастиц платины, улучшить технологичность способа и его экологичность. 5 ил., 2 табл., 9 пр.
Способ получения платинового композита на носителе из термически обработанного оксида графена, заключающийся в том, что проводят два этапа:
на 1 этапе получают термически обработанный оксида графена, для чего
10 вес.ч. графита диспергируют в 1147 вес.ч. 96 мас.% серной кислоты, для чего графит и серную кислоту смешивают и перемешивают в течение 30 минут,
затем добавляют порционно перманганат калия для окисления графита – четыре раза по 9 вес.ч., суммарно 36 вес.ч., при постоянном перемешивании, о завершении окисления судят по исчезновению зелёной окраски,
затем полученную смесь разбавляют 1300 вес.ч. смеси лёд/вода в весовом соотношении 1:1, добавляют 18 вес.ч. 30 мас.% раствора пероксида водорода для превращения побочных продуктов марганца в растворимые бесцветные ионы Mn (II),
затем смесь центрифугируют, полученный осадок растворяют в воде и перемешивают в течение 60 минут, затем вновь центрифугируют,
затем выполняют последовательно циклы очистки: первый раз промывают дистиллированной водой, затем трижды промывают водным раствором 4 мас.% соляной кислоты, затем оксид графена сушат на воздухе и отжигают в токе инертного газа при температуре 600°С в течение 30 минут;
на 2 этапе получают платиновый композит на носителе из термически обработанного оксида графена, для чего
готовят 0,2 мас.% по Pt4+ изопропанольного раствора нитрата платины (IV), для чего берут 23,7 вес.ч. 15 мас.% по Pt4+ раствора нитрата платины (IV) и разбавляют 1572 вес.ч. изопропанола при перемешивании,
затем берут 10-12 вес.ч. термически обработанного оксида графена, полученного на 1 этапе, и диспергируют его в 1600 вес.ч. изопропанола либо этиленгликоля с помощью ультразвуковой ванны в течение 60-120 минут,
затем изопропанольный раствор нитрата платины (IV) добавляют к изопропанольной либо этиленгликольной дисперсии термически обработанного оксида графена при постоянном перемешивании в весовом соотношении Pt4+:термически обработанный оксид графена=1:4,
полученную смесь либо перемешивают при комнатной температуре в течение 24 часов до однородного состава, либо нагревают до 80°С и перемешивают в течение 6 часов до однородного состава – в случае использования в качестве растворителя изопропанола; либо нагревают до 80°С при постоянном перемешивании в течение 2 часов, затем температуру повышают до 180°С и перемешивают её при данной температуре в течение 2 часов до получения однородного состава – в случае использования в качестве растворителя этиленгликоля, затем смесь фильтруют и промывают изопропанолом, осадок сушат на воздухе.
| CN 116093350 A, 09.05.2023 | |||
| CHESNAKOV V.V | |||
| et al | |||
| Effect of Platinum Precursor on the Properties of Pt/N-Graphene Catalyst in Formic Acid Decomposition, Catalysts, 2022, v | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| ПРЕДОХРАНИТЕЛЬ ОТ ВЗРЫВА ХРАНИЛИЩ ЛЕГКО ВОСПЛАМЕНЯЮЩИХСЯ ЖИДКОСТЕЙ | 1923 |
|
SU1022A1 |
| CN 111342060 A, 26.06.2020 | |||
| SADROLHOSSEINI A.R | |||
| et al | |||
| Optical and Thermal Properties of Laser-Ablated Platinum Nanoparticles Graphene Oxide Composite, | |||
Авторы
Даты
2024-09-30—Публикация
2024-04-02—Подача