1. ЗАЯВЛЕНИЕ, КАСАЮЩЕЕСЯ ПРАВ НА ИЗОБРЕТЕНИЯ, СДЕЛАННЫЕ В ФЕДЕРАЛЬНО ФИНАНСИРУЕМОМ ИССЛЕДОВАНИИ ИЛИ ФЕДЕРАЛЬНО ФИНАНСИРОВАННОЙ РАЗРАБОТКЕ
Это исследование поддерживалось Грантом № EY08061 из Национальных Институтов здравоохранения (NIH). Правительство имеет определенные права в этом изобретении.
По данной заявке испрашивается приоритет предварительной заявки на патент США № 61/027625, поданной в патентном ведомстве Соединенных Штатов 11 февраля 2007 года.
2. УРОВЕНЬ ТЕХНИКИ
Пониженная острота зрения или полная потеря зрения могут происходить от ряда глазных болезней или нарушений, вызываемых дисфункцией ткани или структур в переднем сегменте глаза и/или заднем сегменте глаза. Для понимания, почему зрение человека снижается с возрастом, большое количество исследований фокусировалось на сетчатке, слое палочковидных и колбочковидных зрительных клеток-фоторецепторов, которые превращают свет в электрические сигналы. Исследования на мышах показали, что обусловленные возрастом уменьшения функции ретинальных (относящихся к сетчатке) палочковидных зрительных клеток не могут быть объяснены утратой палочковидных зрительных клеток, патологической ретинальной пластичностью или любыми признаками заболевания сетчатки (Jackson, G.R., Owsley, C. & McGwin, G., Jr. Vision research 39, 3975-3982 (1999); Gao, H. & Hollyfield, J.G. Investigative ophthalmology & visual science 33, 1-17 (1992); Jackson, G.R., Owsley, C, Cordle, E.P. & Finley, C.D. Vision research 38, 3655-3662 (1998)). Действительно, Jackson et al. сообщили разительное замедление опосредованной палочками сетчатки темновой адаптации после подвергания действию света, ассоциированное со старением человека, которое было связано с замедленной регенерацией родопсина (Jackson, G.R., Owsley, C. & McGwin, G., Jr. Vision research 39, 3975-3982 (1999)).
Обусловленная возрастом дегенерация желтого пятная (AMD) является одним из специфических заболеваний, ассоциированных с задней частью глазного яблока, и является главной причиной слепоты среди пожилых людей. AMD приводит к повреждению желтого пятна, небольшой круговой зоны в центре сетчатки. Поскольку желтое пятно является зоной, которая позволяет различать малые детали и читать или водить машину, его разрушение может вызывать уменьшенную остроту зрения и даже слепоту. Сетчатка содержит две формы воспринимающих свет клеток, палочковидные зрительные клетки (палочки сетчатки) и колбочковидные зрительные клетки (колбочки сетчатки), которые изменяют свет с образованием электрических сигналов. Затем головной мозг превращает эти сигналы в изображения. Желтое пятно является богатым колбочковидными зрительными клетками, что обеспечивает центральное зрение. Люди с AMD страдают от разрушения центрального зрения, но обычно сохраняют периферическое зрение.
Недостаточная доступность и/или процессинг витамина А в зрительный хромофор, 11-цис-ретиналь (11-цис-ретинальдегид, витамин А), может оказывать вредное действие на регенерацию родопсина и визуальную трансдукцию в позвоночных (обзор в McBee, J.K., Palczewski, K., Baehr, W. & Pepperberg, D.R. Prog Retin Eye Res 20, 469-529 (2001); Lamb, T.D. & Pugh, E.N., Jr. Prog Retin Eye Res 23, 307-380 (2004); и Travis, G.H., Golczak, M., Moise, A.R. & Palczewski, K. Annu Rev Pharmacol Toxicol (2006). Как и при старении, регенерация родопсина после светового воздействия является более замедленной у человека и мышей, лишенных витамина А вследствие либо режима питания, либо недостаточного кишечного поглощения (Lamb, T.D. & Pugh, E.N., Jr. Prog Retin Eye Res 23, 307-380 (2004)). Кроме того, лечение витамином А и его производными может иметь благоприятные действия при старении (Jacobson, S.G., et al. Nat Genet 11, 27-32 (1995)) и в случае ретинальных заболеваний, таких как дистрофия глазного дна Sorbsby fundus (Jacobson, S.G., et al. Nat Genet 11, 27-32 (1995) и пигментный ретинит (Berson, E.L., et al. Arch Ophthalmol 111, 761-772 (1993)).
Абсорбция, накапливание и рециркуляция ретиноидов после обесцвечивания пигментов сетчатки являются нарушенными в мышах, лишенных лецитин:ретинолацилтрансферазы (LRAT) (Imanishi, Y., Batten, M.L., Piston, D.W., Baehr, W. & Palczewski, K. J Cell Biol 164, 373-383 (2004); Batten, M.L., et al. PLoS medicine 2, e333 (2005); Batten, M.L., et al. J Biol Chem 279, 10422-10432 (2004); O'Byrne, S.M., et al. J Biol Chem 280, 35647-35657 (2005)), и нуль-мутация в гене LRAT человека приводит к раннему появлению дистрофии палочек и колбочек (Thompson, D.A., et al. Nat Genet 28, 123-124 (2001)). Последнее сходно с врожденным (наследственным) амаврозом Лебера (LCA), в котором лишающие трудоспособности мутации в специфическом для пигментного эпителия сетчатки гене 65 кДа (RPE65) также вызывают тяжелую дисфункцию палочковидных и колбочковидных фоторецепторов (Thompson, D.A., et al. Nat Genet 28, 123-124 (2001)). Пациенты с LCA, несущие мутации как в гене LRAT, так и в гене RPE65, могут, подобно мышам с Lrat-/- и Rpe65-/-нокаутом, быть лишены 11-цис-ретиналя и родопсина, иметь патологии в уровнях транс-ретиниловых сложных эфиров в клетках RPE, обнаруживать тяжелое нарушение функций палочковых и колбочковых фоторецепторов и проявлять дегенерацию сетчатки (ретинодистрофию) (Imanishi, Y., Batten, M.L., Piston, D.W., Baehr, W. & Palczewski, K. J Cell Biol 164, 373-383 (2004); Batten, M.L., et al. PLoS medicine 2, e333 (2005); Redmond, T.M., et al. Nat Genet 20, 344-351 (1998); Van Hooser, J.P., et al. Proceedings of the National Academy of Sciences of the United States of America 97, 8623-8628 (2000); Van Hooser, J.P., et al. J Biol Chem 277, 19173-19182 (2002)).
Биохимические дефекты, вызывающие LCA-подобные симптомы в мышах с Lrat-/- и Rpe65-/-нокаутом, могут быть исключены пероральным зондовым введением 9-цис-ретиналя. Эта обработка приводит к сохраненной морфологии сетчатки и восстановлению нормальной функции палочек сетчатки, оцениваемым как регистрацией отдельных клеток, так и измерениями ERG (Batten, M. L., et al. PLoS medicine 2, e333 (2005); Van Hooser, J.P., et al. Proceedings of the National Academy of Sciences of the United States of America 97, 8623-8628 (2000); Van Hooser, J.P., et al. J Biol Chem 277, 19173-19182 (2002)). 9-цис-ретиналь образует фотоактивный изородопсин, который, при обесцвечивании, подвергается конформационным изменениям через те же самые фотопродукты, через которые родопсин природно регенерируется из 11-цис-ретиналя (Yoshizawa, T. & Wald, G. Nature 214, 566-571 (1967)). Кроме того, 11-цис-ретиналь, предоставляемый внутрибрюшинной инъекцией, также улучшает зрение в Rpe65-/-мышах (Ablonczy, Z., et al. J Biol Chem 277, 40491-40498 (2002)). Кроме того, введение через желудочный зонд более химически стабильного соединения, чем 9-цис- или 11-цис-ретиналь, т.е. 9-цис-ретинилацетатом (9-cis-R-Ac), производит те же самые благоприятные эффекты, что и 9-цис-ретиналь в Lrat-/-мышах (Batten, M.L., et al. PLoS medicine 2, e333 (2005)). Другие синтетические производные ретиналя, которые могут быть использованы для восстановления и/или стабилизации фоторецепторной функции, были описаны, например, в WO 2006/002097 A2.
В настоящее время имеется мало способов лечения ретиноидной недостаточности. Один способ, комбинирование антиоксидантных витаминов и цинка, производит только небольшое восстанавливающее действие посредством замедления прогрессирования AMD. Таким образом, существует потребность в способах восстановления или стабилизации фоторецепторной функции у стареющих субъектов. Данное изобретение относится к неожиданному открытию, что продолжительное лечение синтетическим производным ретиноида значимо улучшает обусловленное старением разрушение фоторецепторной функции.
3. СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение обеспечивает способы лечения или предупреждения возрастного ухудшения зрения, включающие продолжительное введение одного или нескольких синтетических производных ретиналя (ретинальдегида).
В одном варианте осуществления данное изобретение обеспечивает способ лечения или предупреждения обусловленной возрастом дисфункции сетчатки у субъекта, включающий введение субъекту фармацевтически эффективного количества синтетического производного ретиналя, где это синтетическое производное ретиналя вводят этому субъекту в течение периода по меньшей мере трех месяцев.
В одном варианте осуществления это синтетическое производное ретиналя вводят этому субъекту приблизительно один раз каждые две недели - приблизительно один раз каждые шесть недель в течение периода по меньшей мере трех месяцев.
В одном варианте осуществления это производное ретиналя вводят этому субъекту приблизительно один раз в месяц в течение периода от приблизительно 6 до приблизительно 10 месяцев.
В другом варианте осуществления эта обусловленная возрастом дисфункция сетчатки проявляется одним или несколькими из следующих клинических состояний: ухудшение опосредуемой палочками сетчатки темновой адаптации после воздействия света, ухудшение ночного видения, ухудшение контрастной зрительной чувствительности и возрастной дегенерацией желтого пятна (AMD).
Еще в одном варианте осуществления данное изобретение обеспечивает способ улучшения степени регенерации родопсина у млекопитающего, включающий введение этому млекопитающему фармацевтически эффективного количества синтетического производного ретиналя, где это синтетическое производное ретиналя вводят этому млекопитающему в течение периода по меньшей мере трех месяцев.
4. КРАТКОЕ ОПИСАНИЕ ФИГУР
Фиг.1. Экспериментальная временная линия для лечения единичной дозой 9-cis-R-Ac 10-месячных мышей и экспериментальные протоколы для продолжительных (долгосрочных) способов введения. (A) Полностью адаптированным к темноте (48 ч) 10-месячным мышам вводили через желудочный зонд 9-cis-R-Ac (~80 мг/кг массы тела) или контрольный раствор носителя. Спустя один час после зондового введения мышей подвергали действию непрерывного сильного света при 500 канделах (кд)/м2 в течение 20 минут (~90% обесцвеченного родопсина) с последующей 16-часовой темновой адаптацией. Затем мышей испытывали при помощи ERG (электроретинографии) и анализировали на содержание родопсина и ретиноидов. ERG регистрировали также перед обработкой 9-cis-R-Ac. Количества мышей, используемых для каждого анализа, показаны в таблице 1. (B) Мышам вводили через желудочный зонд 9-cis-R-Ac (~80 мг/кг массы тела) или раствор носителя (растительного масла) один раз в месяц в течение 6 или 10 месяцев, как описано в разделе Способы. (C) Группу мышей испытывали спустя 2 недели после последнего зондового введения либо при помощи ERG, либо на содержание родопсина или ретиноидов, и на морфологию сетчатки. Количества мышей, используемые для каждого анализа, показаны в таблице 1.
Фиг.2. Характеристика очищенного родопсина/опсина из обработанных 9-cis-R-Ac мышей и контрольных мышей. Совместно элюируемые родопсин и опсин очищали, как описано в Способах, из мышей, обработанных, как описано на фиг.1. Уровень регенерации родопсина рассчитывали из отношения оптической плотности при 498 нм (опсин с хромофором)/280 нм (общий опсин). Вверху. Показаны репрезентативные спектры оптической плотности очищенного родопсина из 10-месячной обработанной 9-cis-R-Ac мыши (a) и контрольной мыши (b). Столбик ошибки указывает 0,02 AU. Внизу. Степень регенерации обработанной 9-cis-R-Ac группы была слегка более высокой, чем контрольной группы, показывая, что обработанная группа имела более низкий уровень не являющегося лигандом (свободного) опсина (а). Показаны средние величины ± стандартное отклонение (S.D.).
Фиг.3. Уровни ретиноидов в глазах из получающих 9-cis-R-Ac через желудочный зонд мышей, подвергнутых действию интенсивного света с последующей темновой адаптацией. (A) ВЭЖХ-разделение ретиноидов из обработанных 9-cis-R-Ac и контрольных мышей. Первыми элюировались полностью-транс-ретиниловые эфиры жирных кислот (пик 1), а затем оксим syn-11-cis-ретиналя (2), оксим полностью-транс-ретиналя (3), оксим 9-cis-ретиналя (4) и полностью-транс-ретинол (5). Оксимы syn-ретиналя являются минорными пиками на этой хроматограмме, и звездочка (*) указывает выброс (спайк), относящийся к смене растворителя. Вставка (а), удлиненная шкала этой хроматограммы показывает пики 3 и 4, соответствующие уровням syn-полностью-транс-ретиналя и оксимов syn-9-cis-ретиналя. On-line-спектры этих оксимов показаны ниже (3 и 4). Уровни ретиноидов в глазах из обработанных и контрольных мышей (фиг.1А) анализировали при помощи ВЭЖХ. Процедуры экстракции и дериватизация гидроксиламином для улучшения извлечения ретиналей описаны в разделе Способы. (В и С) Определение количества ретиналей и эфиров. Количества 11-cis-ретиналя и полностью-транс-ретиниловых эфиров были сходными в глазах обработанных и контрольных мышей, но 9-cis-ретиналь и 9-cis-ретиниловые эфиры детектировались только в глазах обработанных 9-cis-R-Ac мышей (n=3, P<0,0001). Уровни других неполярных ретиноидов были сходными у обработанных 9-cis-R-Ac и необработанных мышей. В пробе из обработанных мышей детектировали значимое количество 9-cis-ретиналя (пик 4). Показаны средние величины ± S.D.
Фиг.4. ERG-анализ контрольных и продолжительно обрабатываемых 9-cis-R-Ac мышей. (A) Скотопические и фотопические ERG-реакции 10-месячных мышей. Реакции обработанных 9-cis-R-Ac мышей увеличивались значимо при скотопических и фотопических условиях (P<0,01), за исключением амплитуд а-волн при фотопических условиях (нижняя левая панель). (В) Скотопические и фотопические ERG-реакции 14-месячных мышей, обработанных 9-cis-R-Ac с использованием двух разных режимов. Значимых различий между обработанной и необработанной группами 14-месячных мышей не наблюдали ни при скотопических, ни при фотопических условиях. Мышей адаптировали к темноте в течение 48 часов перед ERG (фиг.1C). Скотопические (верхние панели) и фотопические (нижние панели) ERG регистрировали, как описано в Способах. Амплитуды а- и b-волн строили в виде функции интенсивности света. Показаны столбики ошибок (n=10).
Фиг.5. Восстановление темновой адаптации в контрольных и продолжительно обрабатываемых 9-cis-R-Ac мышах после интенсивного светового обесцвечивания. (A) Восстановление 10-месячных мышей от интенсивного ретинального обесцвечивания. Различные группы адаптированных к темноте в течение 48 часов мышей обесцвечивали интенсивным постоянным освещением (500 кд/м2) в течение 3 минут и восстановление амплитуды а-волны подвергали мониторингу посредством регистрации ERG с единственными мгновенными импульсами (~0,2 log кд.с. м2) на протяжении периода 60 минут адаптации к темноте. Скорость восстановления была значимо более высокой в обработанных мышах (N1), чем в контрольных мышах (C1) при возрасте 10 месяцев. Кроме того, обработка 9-cis-R-Ac восстанавливала скорость восстановления относительно скорости, наблюдаемой в 4-месячных мышах. (В) Восстановление 14-месячных мышей от интенсивного обесцвечивания сетчатки. Значимо более высокая скорость восстановления имела место в обработанных (N2 и N3) мышах в сравнении с необработанными (C2) мышами (*, n=5; P<0,01 и Р<0,0001, соответственно). Опять обработанные мыши обнаруживали такую же реакцию, что и молодые 4-месячные мыши. Показаны столбики ошибок (n=5).
Фиг.6. Накапливание A2E в глазах контрольных и продолжительно обрабатываемых 9-cis-R-Ac мышей. (А) Показано хроматографическое разделение и спектры A2E и изо-A2E. Показана репрезентативная ВЭЖХ-хроматограмма элюированных A2E и изо-A2E из группы мышей N1 (левая панель в A). Вставка. Выделены увеличенные зоны элюции A2E и изо-A2E. Спектры этих пиков (I и II) представляют A2E и изо-A2E, соответственно (верхняя правая). (B) Показаны количества A2E (черные столбцы) и изо-A2E (серые столбцы) из различных экспериментальных групп. Количества A2E не отличаются значимо среди всех групп, за исключением N3, где они являются слегка более низкими (P<0,05). Уровни изо-A2E были сходными среди всех групп. Ни одно соединение не детектировали при значимых уровнях в молодых необработанных мышах (C0). Показаны средние величины ± S.D.
Фиг.7. Морфология сетчатки мышей с введением 9-cis-R-Ac через желудочный зонд. (A) Показан репрезентативный поперечный срез 4-месячной необработанной мыши (С0). RPE, пигментный эпителий сетчатки; PR, фоторецепторы, ROS, наружный сегмент палочки сетчатки; IS, внутренний сегмент; ONL, наружный зернистый слой (роговицы); OPL, наружный плексиформный (переплетенный) слой; INL, внутренний зернистый слой; IPL, внутренний плексиформный (переплетенный) слой, и GCL, слой ганглиозных клеток (ганглиоцитов). (B) Показаны толщина ROS и толщина IS и количество зерен ONL контрольных и обработанных мышей в возрасте 10 и 14 месяцев. Точки данных построены в виде функции расстояния от головки зрительного нерва (ONH). Длины ROS и IS молодых контрольных мышей (C0) были значимо большими, чем длины ROS и IS во всех других группах (*, n=5; P<0,01). Не были детектированы другие значимые различия. Показаны средние величины ± S.D.
Фиг.8. Анализы массивов (микрочипов) РНК контрольных и продолжительно обрабатываемых 9-cis-R-Ac мышей. Уровни экспрессии 37364 генов из глаза, печени и почки двух групп мышей, С2 и N2, исследовали при помощи кДНК-массивов (кДНК-микрочипов) (обеспечиваемых Nimblegen). Готовили две независимые пробы РНК для гибридизации с микромассивами (микрочипами). Нормализованные величины экспрессии мРНК строили (контроль vs. каждой обработанной 9-cis-R-Ac группы, Способы) в виде графиков разброса при помощи Sigma Plot v9.0. Гены, экспрессируемые более чем в 2,0-кратном размере или менее чем 0,5-кратном размере, указаны красным и синим цветом, соответственно. Дополнительная информация доступна из дополнительных таблиц S1 и S2. Иммуноблоты экстрактов глаз из разных групп мышей зондировали различными антителами, как описано в Способах.
5. ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данные способы направлены на лечение или предупреждение обусловленной возрастом дисфункции сетчатки у субъекта посредством продолжительного введения фармацевтически эффективного количества синтетического производного ретиналя.
В данном контексте термин "обусловленная возрастом дисфункция сетчатки" относится к возрастным уменьшениям фоторецепторной функции сетчатки. Предполагается, что этот термин включает обусловленные возрастом разрушения, связанные с недостаточностью электроретинограммы и смертью фоторецепторных клеток и структурными патологиями, которые наблюдали в исследованиях старения как на животных, так и на людях. В одном аспекте обусловленная возрастом дисфункция сетчатки включает замедление опосредуемой палочками сетчатки адаптации к темноте после воздействия светом, уменьшение ночного зрения и/или уменьшение контрастной зрительной чувствительности. В другом аспекте обусловленная возрастом дисфункция сетчатки включает возрастную дегенерацию желтого пятна (AMD). AMD может быть мокрой или сухой формы.
Термины "лечение", “обработка" и т.п. используются здесь обычно для обозначения желаемого фармакологического и физиологического действия. Более конкретно, синтетические производные ретиналя (ретинальдегида), описанные здесь, которые используют для лечения субъекта с обусловленной возрастом дисфункцией сетчатки, обеспечивают в терапевтически эффективном количестве для достижения улучшения в возрастной дисфункции сетчатки в системе зрения стареющего субъекта, в сравнении со сравнимой системой зрения, не получающей этого синтетического производного ретиналя. Улучшение в обусловленной возрастом дисфункции сетчатки включает продолжительное (например, измеряемое неделями или месяцами) улучшение или восстановление фоторецепторной функции в системе зрения, в сравнении со сравнимой системой зрения, не получающей этого синтетического производного ретиналя. Улучшение включает также стабилизацию системы зрения позвоночного животного или минимизацию дополнительной деградации в системе зрения позвоночного животного, в сравнении со сравнимой системой зрения позвоночного, не получающей этого синтетического производного ретиналя.
Термины "предупреждающий", "предупреждение" и т.п. используются обычно для обозначения предупреждения или ингибирования разрушения или дополнительного разрушения системы зрения стареющего субъекта, в сравнении со сравнимой системой зрения, не получающей этого синтетического производного ретиналя.
Термин "фармацевтически эффективное" относится в данном контексте к эффективности конкретной программы лечения или предупреждения. Фармацевтическая эффективность может быть измерена на основе такой характеристики, как, например, увеличенная или стабилизированная скорость адаптации к темноте, более высокое или стабилизированное отношение родопсин/опсин, более высокая или стабилизированная скорость регенерации родопсина или другие подобные улучшения электроретинографических (ERG) реакций.
В данных способах синтетическое производное ретиналя вводят субъекту. В данном контексте термин "субъект" или "пациент" относится к позвоночному, например, млекопитающему, такому как человек. В одном варианте осуществления этот субъект является стареющим субъектом, таким как человек, страдающий от обусловленной возрастом дисфункции сетчатки. В данном контексте стареющий субъект-человек имеет обычно возраст по меньшей мере 45, или по меньшей мере 50, или по меньшей мере 60, или по меньшей мере 65 лет. Этот субъект имеет стареющий глаз, который характеризуется как имеющий обусловленную возрастом дисфункцию сетчатки. Обусловленная возрастом дисфункция сетчатки может проявляться одним или несколькими из следующих клинических состояний: ухудшение опосредуемой палочками сетчатки темновой адаптации после воздействия света, ухудшение ночного видения, ухудшение контрастной зрительной чувствительности и возрастной дегенерацией желтого пятна (AMD).
Синтетическое производное ретиналя вводят с использованием продолжительных (долгосрочных) схем введения доз. В одном варианте осуществления синтетическое производное ретиналя вводят периодически в течение трех месяцев или дольше, и в другом варианте осуществления - в течение шести месяцев или дольше. В одном варианте осуществления это синтетическое производное ретиналя может вводиться, например, в течение периода приблизительно трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати или двенадцати месяцев или дольше. Это синтетическое производное ретиналя может вводиться с перерывами субъекту приблизительно один раз в день - приблизительно один раз каждые два месяца. Прерываемое введение включает введение этому субъекту приблизительно один раз через день; приблизительно четыре раза в неделю, три раза в неделю и два раза в неделю; приблизительно один раз каждые две, три, четыре, пять, шесть, семь, восемь и девять недель; и приблизительно один раз в месяц. В одном варианте осуществления это синтетическое производное ретиналя вводят приблизительно один раз каждые три недели - каждые шесть недель в течение периода приблизительно три месяца или дольше; и в другом варианте осуществления его вводят приблизительно один раз в месяц в течение приблизительно шести - десяти месяцев.
Количество синтетического производного ретиналя, вводимого на одну дозу, может увеличиваться по мере увеличения временного периода между дозами. Например, если синтетическое производное ретиналя вводят по меньшей мере один раз в день, доза на одно введение может быть большей, чем эффективная суточная доза. В данном контексте термин "эффективная суточная доза" относится к суточной дозе, эффективной для получения желаемого фармакологического и физиологического эффекта (т.е. суточной дозе, эффективной для "лечения" и/или "предупреждения" обусловленной возрастом дисфункции сетчатки в субъекте, как описано выше).
Кроме того, это синтетическое производное ретиналя может продолжительно высвобождаться из формы или устройства регулируемой доставки лекарственного средства в течение пролонгированного периода времени, например, в течение периода приблизительно шести месяцев или более. Большое разнообразие способов регулируемого высвобождения было разработано и известно квалифицированным в данной области специалистам, включая насосы, пластыри, таблетки, имплантаты, микрочипы (микропроцессоры) и полимерные системы.
Подходящие дозы синтетических производных ретиналя будут зависеть от клинического состояния, состояния и возраста пациента, активного агента, состава и дозированной формы, частоты введения дозы и т.п. Во многих случаях выбор подходящей дозы будет находиться в пределах квалификации соответствующего врача-практика, такого как врач-терапевт или медсестра. В случае глазных капель, синтетическое производное ретиналя может вводиться, например, от приблизительно 0,01 мг, приблизительно 0,1 мг или приблизительно 1 мг до приблизительно 25 мг, до приблизительно 50 мг или до приблизительно 90 мг на одну дозу. В случае инъекции, подходящими дозами являются приблизительно 0,0001 мг, приблизительно 0,001 мг, приблизительно 0,01 мг или приблизительно 0,1 мг - приблизительно 10 мг, приблизительно 25 мг, приблизительно 50 мг или приблизительно 500 мг синтетического производного ретиналя. Подходящие пероральные дозы находятся в диапазоне от приблизительно 0,1 до приблизительно 1000 мг синтетического производного ретиналя. В других вариантах осуществления могут вводиться приблизительно 1,0 - приблизительно 300 мг синтетического производного ретиналя на дозу.
В некоторых вариантах осуществления эта доза является пероральной дозой приблизительно 0,01 - приблизительно 10 мг/кг массы тела; приблизительно 0,05 - приблизительно 7,5 мг/кг массы тела; приблизительно 0,1 - приблизительно 5 мг/кг массы тела или приблизительно 0,5 - приблизительно 2,5 мг/кг массы тела. Например, синтетическое производное ретиналя может вводиться при пероральной дозе приблизительно 6,4 мг/кг массы тела (т.е. приблизительно 240 мг/м2 площади поверхности тела). В другом варианте осуществления эта доза является пероральной суточной дозой приблизительно 0,1 - приблизительно 1 мг/кг массы тела, такой как пероральная суточная доза приблизительно 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9 или 1 мг/кг массы тела.
Синтетические производные ретиналя, подходящие для способов данного изобретения, были описаны в международных публикациях WO 2004/082622 A2 и WO 2006/002097 A2 и в US 2004/0242704 A1.
Синтетическим производным ретиналя, подходящим для способов данного изобретения, является производное 9-cis-ретиналя или 11-cis-ретиналя, в котором альдегидная группа в полиеновой цепи является модифицированной. Это синтетическое производное ретиналя может превращаться прямо или опосредованно в ретиналь или синтетический аналог ретиналя. Таким образом, в некоторых аспектах соединения в соответствии с данным изобретением могут быть описаны как пролекарства, которые после метаболического превращения превращаются в 9-cis-ретиналь, 11-cis-ретиналь или их синтетический аналог. Метаболическое превращение может происходить, например, посредством гидролиза, эстеразной активности, ацетилтрансферазной активности, дегидрогеназной активности или т.п.
Это синтетическое производное ретиналя может быть заменителем ретиноида, дополняющим уровни эндогенного ретиноида. В некоторых вариантах осуществления синтетический ретиналь может связываться с опсином и функционировать в качестве агониста опсина. В данном контексте термин "агонист" относится к синтетическому ретиналю, который связывается с опсином и облегчает способность комплекса опсин/синтетический ретиналь реагировать на свет. В качестве агониста опсина, синтетический ретиналь может уменьшать потребность в эндогенном ретиноиде (например, 11-cis-ретинале). Синтетический ретиналь может также восстанавливать или улучшать функцию (например, фоторецепцию) опсина связыванием с опсином и образованием функционального комплекса опсин/синтетический ретиналь, посредством чего этот комплекс опсин/синтетический ретиналь может реагировать на фотоны, когда он является частью мембраны палочек или колбочек сетчатки.
Синтетические производные ретиналя могут вводиться для восстановления или стабилизации фоторецепторной функции и для ослабления эффектов недостаточности уровней ретиноидов. Фоторецепторная функция может восстанавливаться или стабилизироваться, например, обеспечением синтетического производного ретиналя в качестве заменителя 11-cis-ретиноида и/или агониста опсина. Это синтетическое производное ретиналя может также устранять эффекты ретиноидной недостаточности в системе зрения позвоночных. Это синтетическое производное ретиналя может вводиться профилактически или терапевтически позвоночному животному. Подходящие позвоночные животные включают, например, человека и позвоночных животных, не являющихся человеком. Подходящие позвоночные, не являющиеся человеком, включают, например, млекопитающих, таких как собаки (собачьи), кошки (кошачьи), лошади (лошадиные), и других домашних животных.
В одном аспекте этого изобретения синтетическими производными ретиналя являются 9-cis-ретиналь или 11-cis-ретиналь, в которых альдегидная группа в полиеновой цепи превращена в сложный эфир, простой эфир, спирт, гемиацеталь, ацеталь или оксим, описанные здесь далее. Такие синтетические производные ацеталя включают сложные 9-cis-ритиниловые эфиры, простые 9-cis-ретиниловые эфиры, 9-cis-ретинол, оксимы 9-cis-ретиналя, 9-cis-ретинилацетали, 9-cis-ретинилгемиацетали, сложные 11-cis-ритиниловые эфиры, простые 11-cis-ретиниловые эфиры, 11-cis-ретинол, 11-cis-ретинилоксимы, 11-cis-ретинилацетали и 11-cis-ретинилгемиацетали, описанные здесь далее. Это синтетическое производное ретиналя может метаболизироваться с высвобождением природного или синтетического ретиналя, такого как, например, 9-cis-ретиналь, 11-cis-ретиналь или синтетический аналог ретиналя, такой как синтетические аналоги, описанные здесь или в международных публикациях WO 2004/082622 A2 и WO 2006/002097 A2.
В одном аспекте синтетическим производным ретиналя является сложный ретиниловый эфир. В некоторых вариантах осуществления этот ретиниловый эфир является 9-cis-ретиниловым эфиром или 11-cis-ретиниловым эфиром. Этим эфирным заместителем может быть, например, карбоновая кислота, такая как моно- или поликарбоновая кислота. В данном контексте "поликарбоновой кислотой" является ди-, трикарбоновая кислота или карбоновая кислота более высокого порядка. В некоторых вариантах осуществления этой карбоновой кислотой является C1-C22, C2-C22, C3-C22, C1-C10, C2-C10, C3-C10, C4-C10, C4-C8, C4-C6 или C4-монокарбоновая кислота или поликарбоновая кислота.
Подходящие группы карбоновых кислот включают, например, уксусную кислоту, пропионовую кислоту, масляную кислоту, валериановую кислоту, капроновую кислоту, каприловую кислоту, пеларгоновую кислоту, каприновую кислоту, лауриновую кислоту, олеиновую кислоту, стеариновую кислоту, пальмитиновую кислоту, миристиновую кислоту или линолевую кислоту. Этой карбоновой кислотой может быть, например, щавелевая кислота (этандиовая кислота), малоновая кислота (пропандиовая кислота), янтарная кислота (бутандиовая кислота), фумаровая кислота (бутендиовая кислота), яблочная кислота (2-гидроксибутендиовая кислота), глутаровая кислота (пентандиовая кислота), адипиновая кислота (гександиовая кислота), пимелиновая кислота (гептандиовая кислота), субериновая кислота (октандиовая кислота), азелаиновая кислота (нонандиовая кислота), себациновая кислота (декандиовая кислота), лимонная кислота, щавелевоуксусная кислота, кетоглутаровая кислота или т.п.
В одном примерном варианте осуществления ретиниловым эфиром является сложный 9-cis-ретиниловый эфир или сложный 11-cis-ретиниловый эфир, включающий заместитель (группу) C3-C10-поликарбоновой кислоты. (В данном контексте термины "заместитель" или "группа" относятся к радикалу, ковалентно связанному с концевым кислородом в полиеновой цепи). В другом примерном варианте осуществления этим сложным ретиниловым эфиром является сложный 9-cis-ретиниловый эфир или сложный 11-cis-ретиниловый эфир, включающий заместитель (группу) C2-C22- или C3-C22-поликарбоновой кислоты. Этим заместителем поликарбоновой кислоты может быть, например, сукцинат, цитрат, кетоглутарат, фумарат, малат или оксалоацетат. В другом примерном варианте осуществления этим сложным ретиниловым эфиром является сложный 9-cis-ретиниловый эфир или сложный 11-cis-ретиниловый эфир, включающий заместитель C3-C22-дикарбоновой кислоты (дикислоты). В некоторых вариантах осуществления эта поликарбоновая кислота не является 9-cis-ретинилтартратом или 11-cis-ретинилтартратом. В некоторых вариантах осуществления этот сложный ретиниловый эфир не является природно-встречающимся сложным ретиниловым эфиром, обнаруживаемым в глазе. В некоторых вариантах осуществления этот сложный ретиниловый эфир является выделенным ретиниловым эфиром. В данном контексте "выделенная" относится к молекуле, которая существует отдельно от ее природного окружения и, следовательно, не является природным продуктом. Выделенная молекула может существовать в очищенной форме или может существовать в неприродном окружении.
В другом аспекте этим производным ретиналя может быть сложный или простой 9-cis-ретиниловый эфир следующей формулы I:
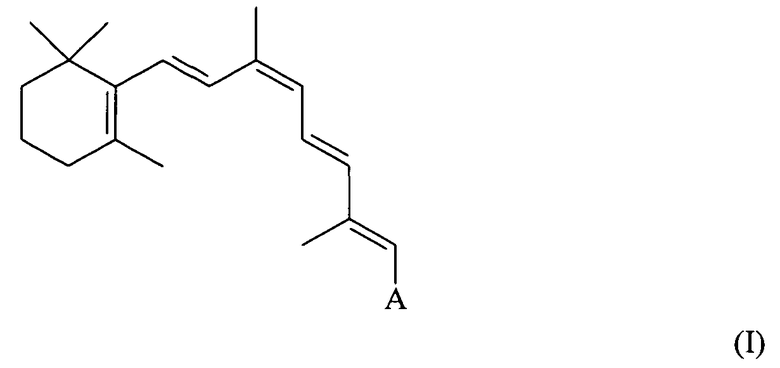
В некоторых вариантах осуществления A обозначает CH2OR, где R может быть альдегидной группой, для образования сложного ретинилового эфира. Подходящей альдегидной группой является C1-C24-альдегидная группа с прямой или разветвленной цепью. Этой альдегидной группой может быть также C1-C14-альдегидная группа с прямой или разветвленной цепью. Этой альдегидной группой может быть также C1-C12-альдегидная группа с прямой или разветвленной цепью, такая как, например, ацетальдегид, пропиональдегид, бутиральдегид, валеральдегид, гексаналь, гептаналь, октаналь, нонаналь, деканаль, ундеканаль, додеканаль. R может быть С1-С10-альдегидной группой с прямой или разветвленной цепью, С1-С8-альдегидной группой с прямой или разветвленной цепью или С1-С6-альдегидной группой с прямой или разветвленной цепью.
R может быть также карбоксилатной группой дикарбоновой кислоты или другой карбоновой кислоты (например, гидроксикислотой) для образования ретинилового эфира (некоторые из которых называют также сложными ретиноиловыми эфирами). Этой карбоновой кислотой может быть, например, щавелевая кислота (этандиовая кислота), малоновая кислота (пропандиовая кислота), янтарная кислота (бутандиовая кислота), фумаровая кислота (бутендиовая кислота), яблочная кислота (2-гидроксибутендиовая кислота), глутаровая кислота (пентандиовая кислота), адипиновая кислота (гександиовая кислота), пимелиновая кислота (гептандиовая кислота), субериновая кислота (октандиовая кислота), азелаиновая кислота (нонандиовая кислота), себациновая кислота (декандиовая кислота), лимонная кислота, щавелевоуксусная кислота, кетоглутаровая кислота или т.п.
R может быть также алкановой группой для образования простого ретинилалканового эфира. Подходящие алкановые группы включают, например, С1-С24-алкилы с прямой или разветвленной цепью, такие как, например, метан, этан, бутан, изобутан, пентан, изопентан, гексан, гептан, октан или т.п. Например, алкановой группой может быть линейный, изо-, втор-, трет- или другой низший алкил с прямой или разветвленной цепью в диапазоне С1-С6. Эта алкановая группа может быть также имеющим линейную, изо-, втор-, трет- или другую разветвленную цепь средней длины алкилом в диапазоне C8-C14. Эта алкановая группа может быть также имеющим линейную, изо-, втор-, трет- или другую разветвленную цепь средней длины алкилом в диапазоне C16-C24.
Кроме того, R может быть спиртовой группой, для образования простого ретинилового эфира спирта. Подходящими спиртовыми группами могут быть имеющие линейную, изо-, втор-, трет- или другую разветвленную цепь низшие спирты в диапазоне С1-С6, имеющие линейную, изо-, втор-, трет- или другую разветвленную цепь средней длины спирты в диапазоне C8-C14, или имеющий линейную изо-, втор-, трет- или другую разветвленную цепь большой длины алкил в диапазоне C16-C24. Этой спиртовой группой может быть, например, метанол, этанол, бутанол, изобутанол, пентанол, гексанол, гептанол, октанол или т.п.
R может быть также карбоновой кислотой для образования эфира ретинилкарбоновой кислоты. Подходящими группами карбоновых кислот могут быть имеющие линейную, изо-, втор-, трет- или другую разветвленную цепь низшие карбоновые кислоты в диапазоне С1-С6, имеющие линейную, изо-, втор-, трет- или другую разветвленную цепь средней длины карбоновые кислоты в диапазоне C8-C14, или имеющие линейную изо-, втор-, трет- или другую разветвленную цепь большой длины карбоновые кислоты в диапазоне C16-C24. Подходящие группы карбоновых кислот включают, например, уксусную кислоту, пропионовую кислоту, масляную кислоту, валериановую кислоту, капроновую кислоту, каприловую кислоту, пеларгоновую кислоту, каприновую кислоту, лауриновую кислоту, олеиновую кислоту, стеариновую кислоту, пальмитиновую кислоту, миристиновую кислоту, линолевую кислоту, янтарную кислоту, фумаровую кислоту или т.п.
Ретинилпроизводным может быть ретинилгемиацеталь, где А обозначает CH(OH)OR. R может быть любой из групп R, представленных выше в формуле I. R обозначает обычно низший алкан, такой как метильная или этильная группа, или насыщенный и ненасыщенный, циклический или ациклический С1-С7-алкан, с гетероатомами или без гетероатомов, как описано здесь.
Ретинилпроизводным может быть ретинилацеталь, где А обозначает CH(ORa)ORb. Каждый из Ra и Rb может быть независимо выбран из любой из групп R, представленных выше в формуле I. Ra и Rb обозначают обычно насыщенный и ненасыщенный, циклический или ациклический С1-С7-алкан, с гетероатомами или без гетероатомов, как описано здесь.
Ретинилпроизводным может быть также ретинилоксим, где А обозначает CH:NOH или CH:NOR. R может быть любой из групп R, представленных выше в формуле I. R обозначает обычно водород или алкан.
Примеры подходящих синтетических производных ретиналя включают, например, 9-cis-ретинилацетат, 9-cis-ретинилформиат, 9-cis-ретинилсукцинат, 9-cis-ретинилцитрат, 9-cis-ретинилкетоглутарат, 9-cis-ретинилфумарат, 9-cis-ретинилмалат, 9-cis-ретинилоксалоацетат, оксим 9-cis-ретиналя, О-метилоксимы 9-cis-ретиналя, О-этилоксимы 9-cis-ретиналя и метилацетали и гемиацетали 9-cis-ретиналя, простой 9-cis-ретинилметиловый эфир, простой 9-cis-ретинилэтиловый эфир и простой 9-cis-ретинилфениловый эфир.
В родственном аспекте производным ретиналя может быть сложный или простой 11-cis-ретиниловый эфир следующей формулы II:
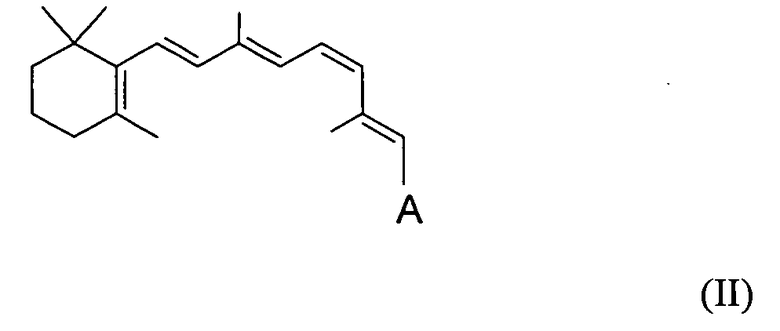
A может быть любой из групп, представленных выше в формуле I.
Примеры подходящих синтетических производных ретиналя включают, например, 11-cis-ретинилацетат, 11-cis-ретинилформиат, 11-cis-ретинилсукцинат, 11-cis-ретинилцитрат, 11-cis-ретинилкетоглутарат, 11-cis-ретинилфумарат, 11-cis-ретинилмалат, оксим 11-cis-ретиналя, О-метилоксим 11-cis-ретиналя, О-этилоксимы 11-cis-ретиналя и метилацетали и гемиацетали 11-cis-ретиналя, простой 11-cis-ретинилметиловый эфир, простой 11-cis-ретинилэтиловый эфир.
В дополнительных аспектах синтетическими производными ретиналя могут быть, например, производное сложного 9-cis-ретинилового эфира, простого 9-cis-ретинилового эфира или сложного 11-cis-ретинилового эфира или простых 11-cis-ретиниловых эфиров, таких как, например, ациклические ретиниловые сложный эфир или простые эфиры, сложный или простой ретиниловый эфир с модифицированной длиной полиеновой цепи, такие как триеновый или тетраеновый ретиниловый сложный или простой эфир; ретиниловый сложный или простой эфир с замещенной полиеновой цепью, такой как замещенные алкилом, галогеном или гетероатомом полиеновые цепи; ретиниловый сложный или простой эфир с модифицированной полиеновой цепью, такой как транс- или цис-замкнутая полиеновая цепь, или, например, с алленовыми или алкиновыми модификациями; ретиниловый сложный или простой эфир с модификациями в кольце, такими как гетероциклические, гетероароматические или замещенные циклоалкановые или циклоалкеновые кольца.
Синтетическим производным ретиналя может быть ретиниловый сложный или простой эфир следующей формулы III:
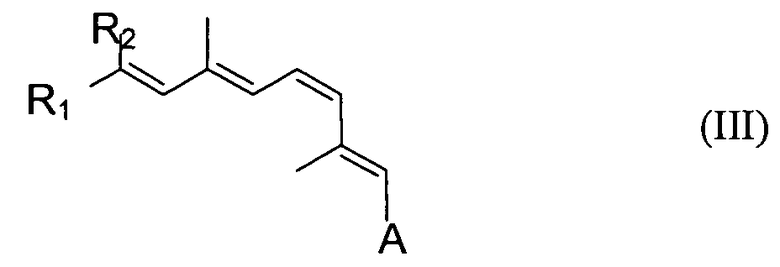
A может быть любой из групп, представленных выше для формулы (I). R1 и R2 могут быть независимо выбраны из линейных, изо-, втор- трет- и других разветвленных алкильных групп, а также замещенных алкильных групп, замещенного разветвленного алкила, гидроксила, гидроалкила, амина, амида или т.п. R1 и R2 могут быть независимо низшим алкилом, который является прямым или разветвленным алкилом с 1-6 атомами углерода, таким как метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, пентил, гексил или т.п. Подходящие замещенные алкилы и замещенные разветвленные алкилы включают, например, алкилы, разветвленные алкилы и циклоалкилы, замещенные кислородом, гидроксилом, азотом, амидом, амином, галогеном, гетероатомом или другими группами. Подходящие гетероатомы включают, например, серу, кремний и фтор- или бром-замещения.
R1 или R2 могут обозначать циклоалкил, такой как, например, гексан, циклогексен, бензол, а также замещенный циклоалкил. Подходящие замещенные циклоалкилы включают, например, циклоалкилы, замещенные кислородом, гидроксилом, азотом, амидом, амином, галогеном, гетероатомом или другими группами. Подходящие гетероатомы включают, например, серу, кремний и фтор- или бром-замещения.
Это синтетическое производное ретиналя может также иметь модифицированную длину полиеновой цепи, например, как следующая формула IV:
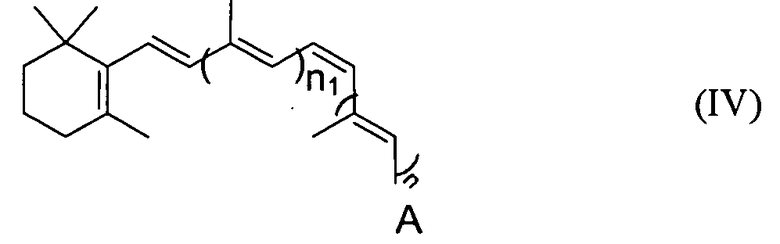
A может быть любой из групп, представленных выше для формулы (I). Длина полиеновой цепи может быть удлинена 1, 2 или 3 алкильными, алкеновыми или алкиленовыми группами. В соответствии с формулой (IV), каждый n и n1 может быть независимо выбран из 1, 2 или 3 алкильных, алкеновых или алкиленовых групп, при условии, что сумма n и n1 равна по меньшей мере 1.
Это синтетическое производное ретиналя может также иметь замещенную полиеновую цепь следующей формулы V:
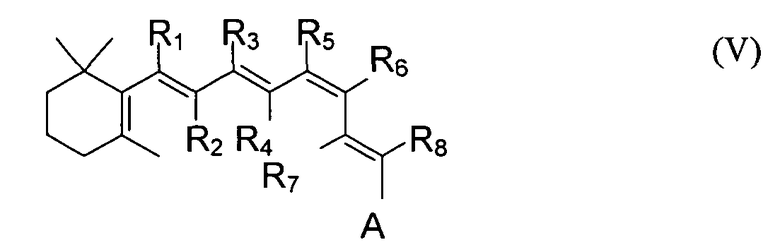
A может быть любой из групп, представленных выше для формулы (I). Каждый из R1 - R8 может быть независимо выбран из водорода, алкила, разветвленного алкила, циклоалкила, галогена, гетероатома или т.п. Подходящие алкилы включают, например, метил, этил, пропил, замещенный алкил (например, алкил с гидроксилом, гидроалкилом, амином, амидом) или т.п. Подходящие разветвленные алкилы могут быть, например, изопропилом, изобутилом, замещенным разветвленным алкилом или т.п. Подходящие циклоалкилы могут включать, например, циклогексан, циклогептан и другие циклические алканы, а также замещенные циклические алканы, такие как замещенный циклогексан или замещенный циклогептан. Подходящие галогены включают, например, бром, хлор, фтор или т.п. Подходящие гетероатомы включают, например, серу, кремний и фтор- или бром-замещения. Подходящие замещенные алкилы, замещенные разветвленные алкилы и замещенные циклоалкилы включают, например, алкилы, разветвленные алкилы и циклоалкилы, замещенные кислородом, гидроксилом, азотом, амидом, амином, галогеном, гетероатомом или другими группами.
Например, синтетическое производное ретиналя может быть выбрано из таких соединений, как 9-этил-11-цис-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 7-метил-11-цис-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 13-дезметил-11-цис-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-10-F-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-10-Cl-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-10-метилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-10-этилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-10-F-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-10-Cl-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-10-метилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-10-этилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-12-F-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-12-Cl-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-12-метилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-10-этилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-12-F-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-12-Cl-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-12-метилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-14-F-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-14-метилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 11-цис-14-этилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-14-F-ретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-14-метилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; 9-цис-14-этилретиниловый сложный эфир, простой эфир, оксим, ацеталь или гемиацеталь; или т.п.
Кроме того, это синтетическое производное ретиналя может иметь структуру с модифицированным кольцом. Подходящие примеры включают, например, производные, содержащие кольцевые модификации, ароматические аналоги и гетероароматические аналоги следующих формул VI, VII и VIII, соответственно:
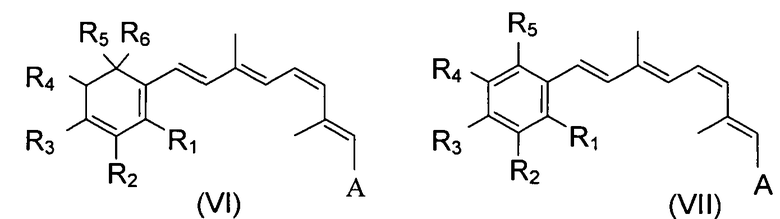
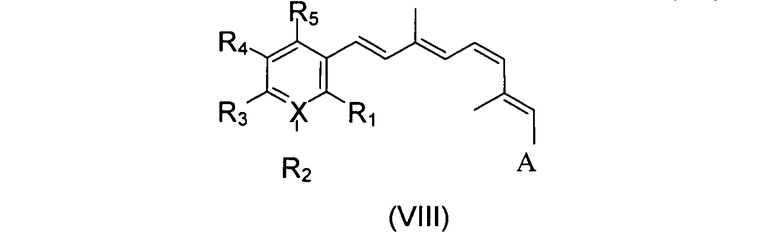
A может быть любой из групп, представленных выше для формулы (I). Каждый из R1 - R6, в случае их применения, может быть независимо выбран из водорода, алкила, замещенного алкила, гидроксила, гидроалкила, амина, амида, галогена, гетероатома или т.п. Подходящие алкилы включают, например, метил, этил, пропил, изопропил, бутил, изобутил или т.п. Подходящие галогены включают, например, бром, хлор, фтор или т.п. Подходящие гетероатомы включают, например, серу, кремний или азот. В формулах VIII, X может быть, например, замещениями в виде серы, кремния, азота, фтора или брома. Подобным образом, обсуждаются 9-cis-синтетические производные ретиналя, содержащие кольцевые модификации, ароматические аналоги и гетероароматические аналоги соединений, показанных в формулах VI, VII и VIII.
Синтетическое производное ретиналя может также иметь модифицированную полиеновую цепь. Подходящие производные включают, например, производные с транс/цис-замкнутой конфигурацией, 6s-замкнутые аналоги, а также модифицированные алленовые, алкеновые, алкиновые или алкиленовые группы в полиеновой цепи. В одном примере этим производным является 11-цис-замкнутый аналог следующей формулы IX:
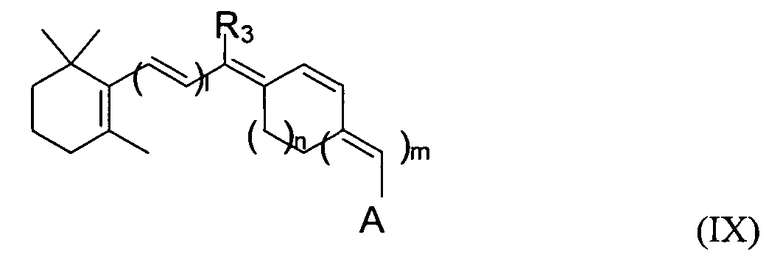
A может быть любой из групп, представленных выше для формулы (I). R3 может быть, например, водородом, метилом, или другим алканом или разветвленным алканом. n может быть равно 0-4. m плюс 1 равно 1, 2 или 3.
В одном варианте осуществления синтетическим производным ретиналя может быть 11-цис-замкнутый аналог следующей формулы Х:
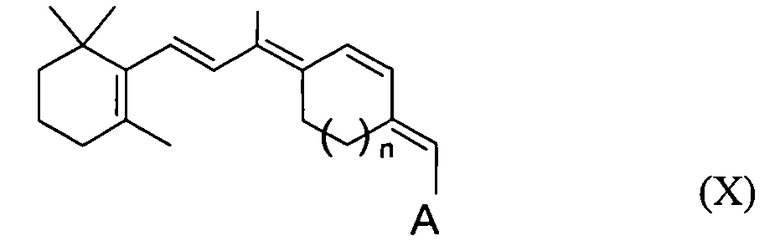
n может быть равно 1-4. A может быть любой из групп, представленных выше для формулы (I).
Синтетическим производным ретиналя является сложный или простой ретиниловый эфир 9,11,13-tri-cis-7-кольца, сложный или простой ретиниловый эфир 11,13-ди-цис-7-кольца, сложный или простой ретиниловый эфир 11-цис-7-кольца или сложный или простой ретиниловый эфир 9,11-ди-цис-7-кольца.
В другом примере синтетическим производным ретиналя является 6s-замкнутый аналог формулы XI. A может быть любой из групп, представленных выше для формулы (I). R1 и R2 могут быть независимо выбраны из водорода, метила и другого низшего алкила и замещенного низшего алкила. R3 может быть независимо выбран из алкеновой группы в любом из указанных положений.
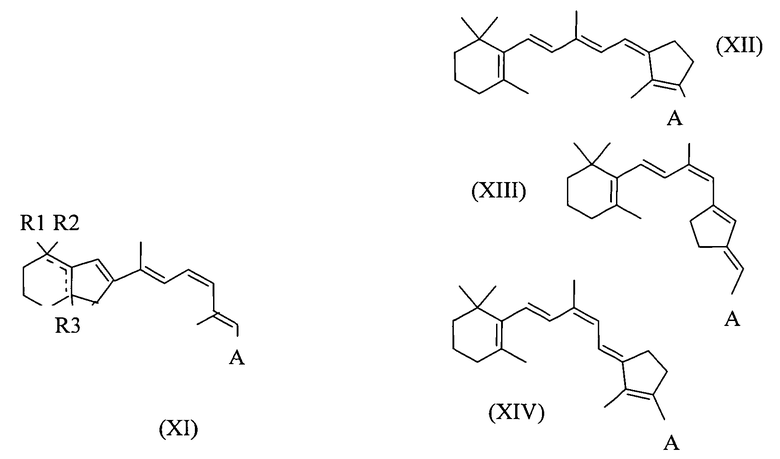
Синтетическим производным ретиналя может быть 9-cis-производное с конденсированными кольцами, такое как, например, производные, показанные в формулах XII-XIV. A может быть любой из групп, представленных выше для формулы (I).
Синтетическое производное ретиналя может также иметь следующую формулу XV или XVI.
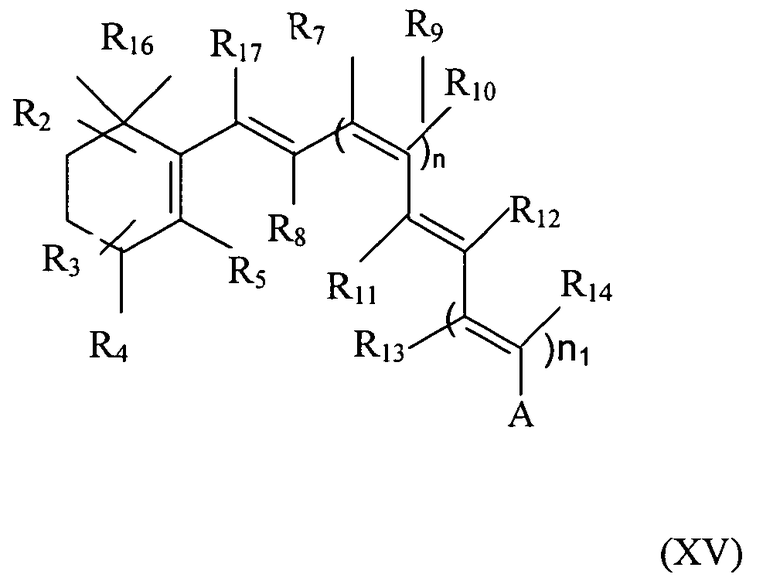
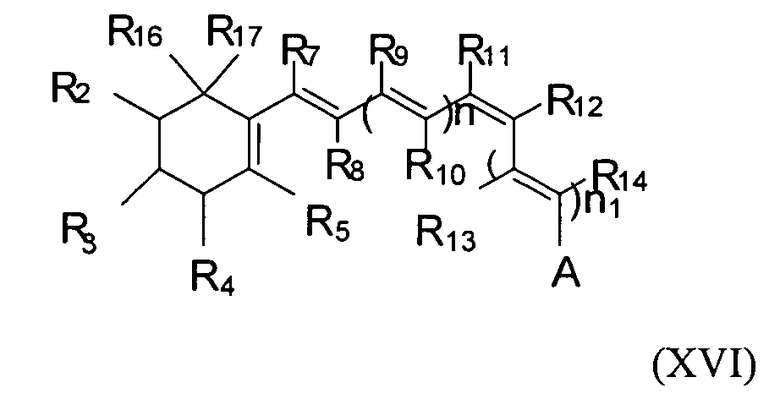
A может быть любой из групп, представленных выше для формулы (I). Каждый из R2 - R5, R7 - R14, R16 и R17 может отсутствовать или быть независимо выбран из водорода, алкила, разветвленного алкила, галогена, гидроксила, гидроалкила, амина, амида, гетероатома или т.п. Подходящие алкилы включают, например, метил, этил, пропил, замещенный алкил (например, алкил с гидроксилом, гидроалкилом, амином, амидом) или т.п. Подходящим разветвленным алкилом может быть, например, изопропил, изобутил, замещенный разветвленный алкил или т.п. Подходящие галогены включают, например, бром, хлор, фтор или т.п. Подходящие гетероатомы включают, например, серу, кремний и фтор- или бром-заместители. Подходящие замещенные алкилы и замещенные разветвленные алкилы включают, например, алкилы и разветвленные алкилы, замещенные кислородом, гидроксилом, азотом, амидом, амином, галогеном, гетероатомом или другими группами. Каждый из n и n1 может быть независимо выбран из 1, 2 или 3 алкильных, алкеновых или алкиленовых групп, при условии, что сумма n и n1 равна по меньшей мере 1. Кроме того, R3-R4 и/или R2-R16 может содержать алкеновую группу в циклическом углеродном кольце, и в этом случае R17 отсутствует. R10 и R13 вместе могут образовывать циклоалкил, такой как пяти-, шести-, семи- или восьмичленный циклоалкил, или замещенный циклоалкил, такие как циклоалкилы, показанные в формулах IX, X, XII, XIII и XIV.
Способы получения синтетических ретиналей и производных описаны, например, в следующих ссылках: Anal. Biochem. 272:232-42 (1999); Angew. Chem. 36:2089-93 (1997); Biochemistry 14:3933-41 (1975); Biochemistry 21:384-93 (1982); Biochemistry 28:2732-39 (1989); Biochemistry 33:408-16 (1994); Biochemistry 35:6257-62 (1996); Bioorganic Chemistry 27:372-82 (1999); Biophys. Chem. 56:31-39 (1995); Biophys. J. 56:1259-65 (1989); Biophys. J. 83:3460-69 (2002); Chemistry 7:4198-204 (2001); Chemistry (Europe) 5:1172-75 (1999); FEBS 158:1 (1983); J. Am. Chem. Soc. 104:3214-16 (1982); J. Am. Chem. Soc. 108:6077-78 (1986); J. Am. Chem. Soc. 109:6163 (1987); J. Am. Chem. Soc. 112:7779-82 (1990); J. Am. Chem. Soc. 119:5758-59 (1997); J. Am. Chem. Soc. 121:5803-04 (1999); J. American Chem. Soc. 123:10024-29 (2001); J. American Chem. Soc. 124:7294-302 (2002); J. Biol. Chem. 276:26148-53 (2001); J. Biol. Chem. 277:42315-24 (2004); J. Chem. Soc. - Perkin T. 1:1773-77 (1997); J. Chem. Soc. - Perkin T. 1:2430-39 (2001); J. Org. Chem. 49:649-52 (1984); J. Org. Chem. 58:3533-37 (1993); J. Physical Chemistry B 102:2787-806 (1998); Lipids 8:558-65; Photochem. Photobiol. 13:259-83 (1986); Photochem. Photobiol. 44:803-07 (1986); Photochem. Photobiol. 54:969-76 (1991); Photochem. Photobiol. 60:64-68 (1994); Photochem. Photobiol. 65:1047-55 (1991); Photochem. Photobiol. 70:111-15 (2002); Photochem. Photobiol. 76:606-615 (2002); Proc. Natl Acad. Sci. USA 88:9412-16 (1991); Proc. Natl Acad. Sci. USA 90:4072-76 (1993); Proc. Natl Acad. Sci. USA 94:13442-47 (1997); и Proc. R. Soc. Lond. Series B, Biol. Sci. 233 (1270): 55-76 1998) (описания которых включены здесь посредством ссылки).
Синтетические ретиноиды включают производные 9-cis-ретиналя или 11-cis-ретиналя, такие как, например, следующие ациклические ретинали; ретинали с модифицированной длиной полиеновой цепи, такие как триеновые или тетраеновые ретинали; ретинали замещенной полиеновой цепью, такой как замещенные алкилом, галогеном или гетероатомом полиеновые цепи; ретинали с модифицированной полиеновой цепью, такой как транс- или цис-замкнутая полиеновая цепь; и ретинали с алленовыми или алкиновыми модификациями; и ретинали с модификациями в кольце, такими как гетероциклические, гетероароматические или замещенные циклоалкановые или циклоалкеновые кольца.
В некоторых вариантах осуществления синтетический ретиноид может представлять собой ретиналь формулы XVII:
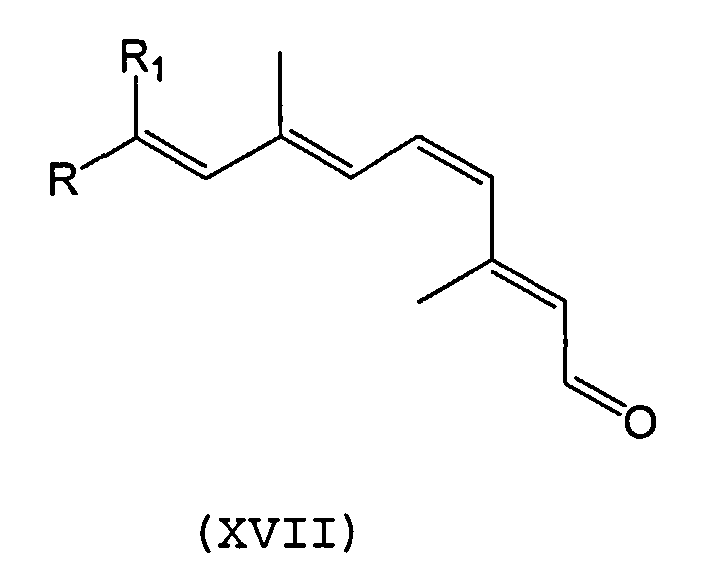
в котором R1 и R2 могут быть независимо выбраны из линейных, изо-, втор- трет- и других разветвленных алкильных групп, а также замещенных алкильных групп, замещенного разветвленного алкила, гидроксила, гидроалкила, амина, амида или т.п. R1 и R2 могут быть независимо низшим алкилом, который является прямым или разветвленным алкилом с 1-6 атомами углерода, таким как метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, пентил, гексил или т.п. Подходящие замещенные алкилы и замещенные разветвленные алкилы включают, например, алкилы, разветвленные алкилы и циклоалкилы, замещенные кислородом, гидроксилом, азотом, амидом, амином, галогеном, гетероатомом или другими группами. Подходящие гетероатомы включают, например, серу, кремний и фтор- или бром-замещения.
В некоторых вариантах осуществления R1 или R2 могут представлять собой циклоалкил, такой как, например, гексан, циклогексен, бензол, а также замещенный циклоалкил. Подходящие замещенные циклоалкилы включают, например, циклоалкилы, замещенные кислородом, гидроксилом, азотом, амидом, амином, галогеном, гетероатомом или другими группами. Подходящие гетероатомы включают, например, серу, кремний и фтор- или бром-замещения.
Синтетические ретиноиды могут также представлять собой производные 9-cis-ретиналя или 11-cis-ретиналя, которые имеют модифицированную длину полиеновой цепи, например, как соединение следующей формулы XVIII:
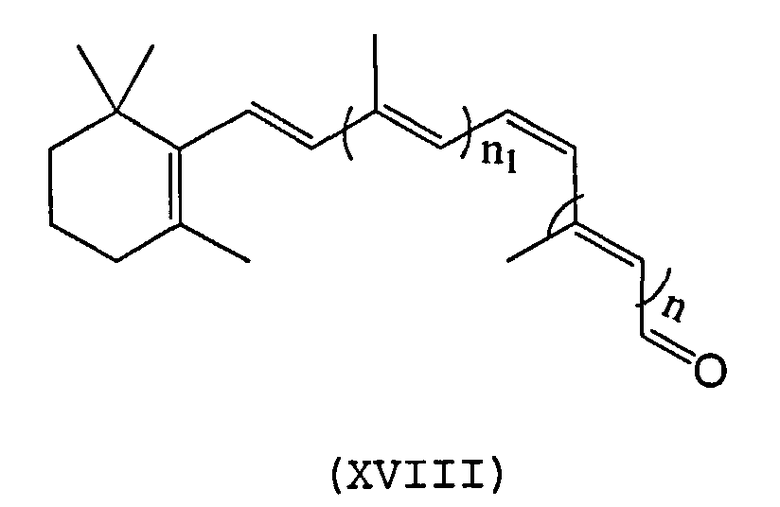
Длина полиеновой цепи может быть удлинена 1, 2 или 3 алкильными, алкеновыми или алкиленовыми группами. В соответствии с формулой (II), каждый n и n1 может быть независимо выбран из 1, 2 или 3 алкильных, алкеновых или алкиленовых групп, при условии, что сумма n и n1 равна по меньшей мере 1.
Синтетический ретиноид может также представлять собой производное 11-cis-ретиналя или 9-cis-ретиналя, которое имеет замещенную полиеновую цепь, следующей формулы XIX:
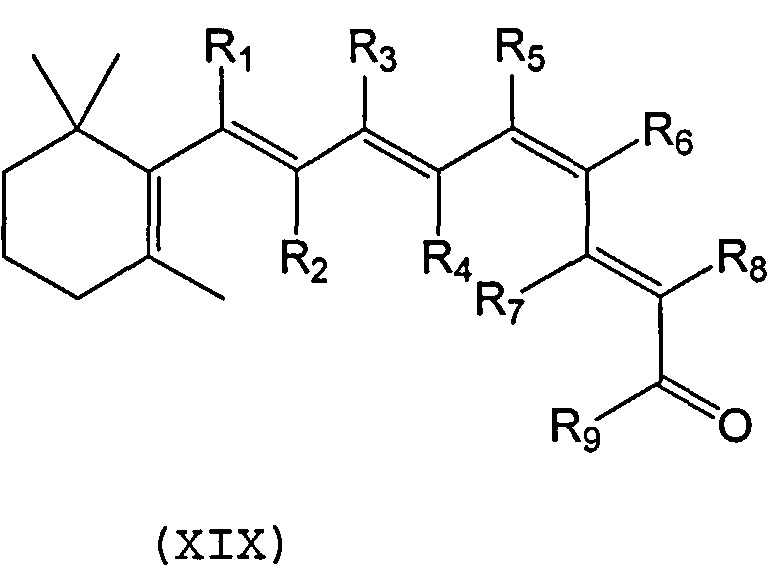
Каждый из R1-R8 может быть независимо выбран из водорода, алкила, разветвленного алкила, циклоалкила, галогена, гетероатома, гидроксила, гидроалкила, амина, амида или т.п. Подходящие алкилы включают, например, метил, этил, пропил, замещенный алкил (например, алкан с гидроксилом, гидроалкилом, амином, амидом) или т.п. Подходящие разветвленные алкилы могут быть, например, изопропилом, изобутилом, замещенным разветвленным алкилом или т.п. Подходящие циклоалкилы могут включать, например, циклогексан, циклогептан и другие циклические алканы, а также замещенные циклические алканы, такие как замещенный циклогексан или замещенный циклогептан. Подходящие галогены включают, например, бром, хлор, фтор или т.п. Подходящие гетероатомы включают, например, серу, кремний и фтор- или бром-замещения. Подходящие замещенные алкилы, замещенные разветвленные алкилы и замещенные циклоалкилы включают, например, алкилы, разветвленные алкилы и циклоалкилы, замещенные кислородом, гидроксилом, азотом, амидом, амином, галогеном, гетероатомом или другими группами.
В иллюстративных вариантах осуществления синтетический ретиноид представляет собой 9-этил-11-cis-ретиаль; 7-метил-11-cis-ретиналь; 13-дезметил-11-cis-ретиналь; 11-cis-10-F-ретиналь; 11-cis-10-Cl-ретиналь; 11-cis-10-метилретиналь; 11-cis-10-этилретиналь; 9-cis-10-F-ретиналь; 9-cis-10-Cl-ретиналь; 9-cis-10-метилретиналь; 9-cis-10-этилретиналь; 11-cis-12-F-ретиналь; 11-cis-12-Cl-ретиналь; 11-cis-12-метилретиналь; 11-cis-10-этилретиналь; 9-cis-12-F-ретиналь; 9-cis-12-Cl-ретиналь; 9-cis-12-метилретиналь; 11-cis-14-F-ретиналь; 11-cis-14-метилретиналь; 11-cis-14-этилретиналь; 9-cis-14-F-ретиналь; 9-cis-14-метилретиналь; 9-cis-14-этилретиналь; или т.п.
Синтетический ретиноид может также представлять собой производное 11-cis-ретиналя или 9-cis-ретиналя, которое имеет структуру с модифицированным кольцом. Подходящие примеры включают, например, производные, содержащие кольцевые модификации, ароматические аналоги и гетероароматические аналоги следующих формул XX, XXI и XXII, соответственно:
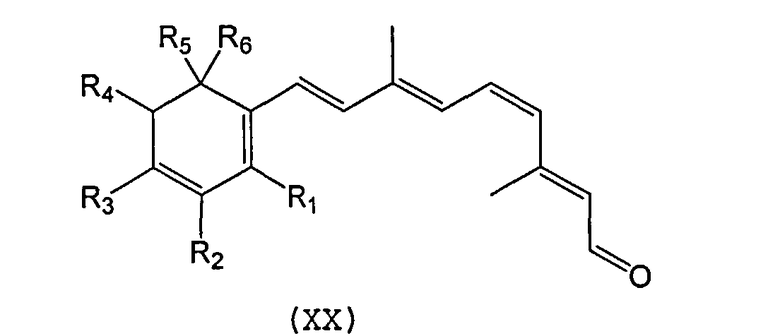
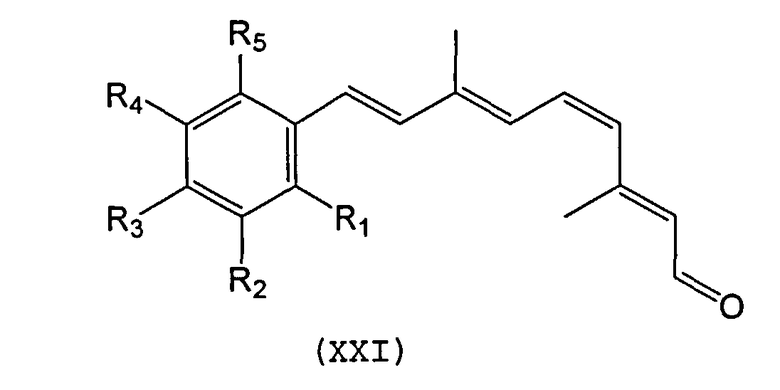
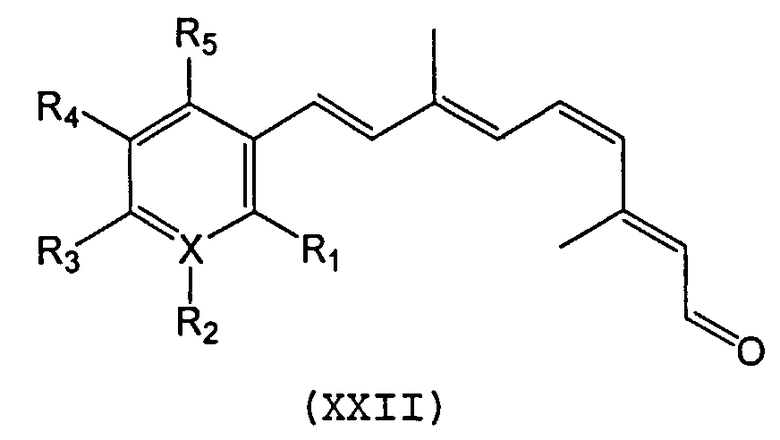
Каждый из R1-R2 или R6, в случае их применения, может быть независимо выбран из водорода, алкила, замещенного алкила, гидроксила, гидроалкила, амина, амида, галогена, гетероатома или т.п. Подходящие алкилы включают, например, метил, этил, пропил, изопропил, бутил, изобутил или т.п. Подходящие галогены включают, например, бром, хлор, фтор или т.п. Подходящие гетероатомы включают, например, серу, кремний или азот. Кроме того, X может быть гетероатомом, таким как сера, кремний или азот.
Синтетический ретиноид может также представлять собой производное 11-cis-ретиналя или 9-cis-ретиналя, которое имеет модифицированную полиеновую цепь. Подходящие производные включают, например, производные с транс/цис-замкнутой конфигурацией, 6s-замкнутые аналоги, а также модифицированные алленовые, алкеновые, алкиновые или алкиленовые группы в полиеновой цепи. В одном примере этим производным является 11-cis-замкнутый аналог следующей формулы XXIII;
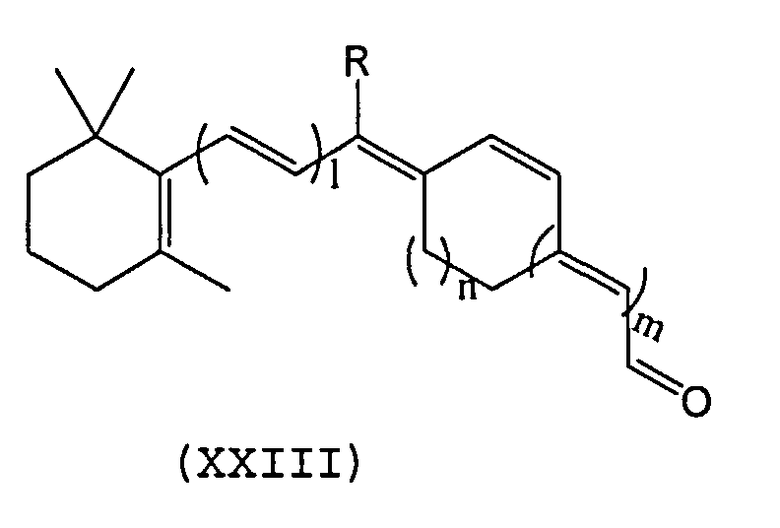
R может быть, например, водородом, метилом, или другим низшим алканом или разветвленным алканом, или гетероатомом, n может быть равно 0-4. m плюс 1 равно 1, 2 или 3.
В частных вариантах осуществления синтетический ретиноид представляет собой 11-cis замкнутый аналог следующей формулы XXIV:
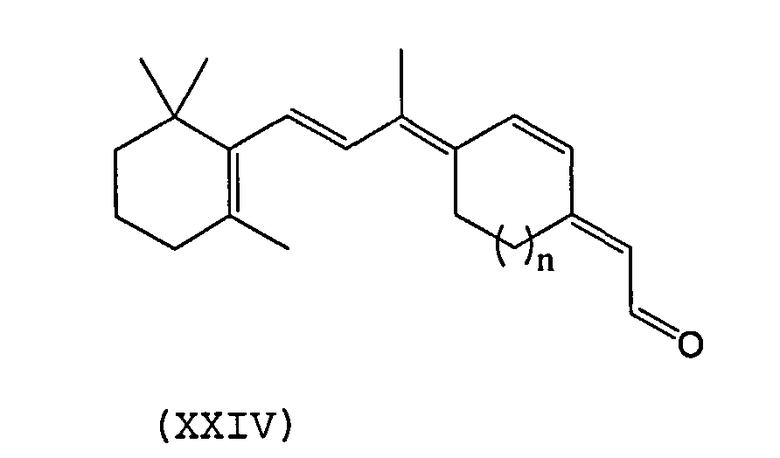
n может быть равно 1-4.
В некоторых иллюстративных вариантах осуществления синтетический ретиноид представляет собой 9,11,13-три-cis-7-кольцевой ретиналь, 11,13-ди-цис-7-кольцевой ретиналь, 11-цис-7-кольцевой ретиналь или 9,11-ди-цис-7-кольцевой ретиналь.
В другом варианте осуществления синтетический ретиноид представляет собой 6s-замкнутый аналог формулы XXV. R1 и R2 могут быть независимо выбраны из водорода, метила и другого низшего алкила и замещенного низшего алкила. R3 может быть независимо выбран из алкеновой группы в любом из указанных положений.
В другом варианте осуществления синтетический ретиноид может представлять собой 9-cis-производное с конденсированными кольцами, такое как, например, производные, показанные в формулах XXVI-XVIII:
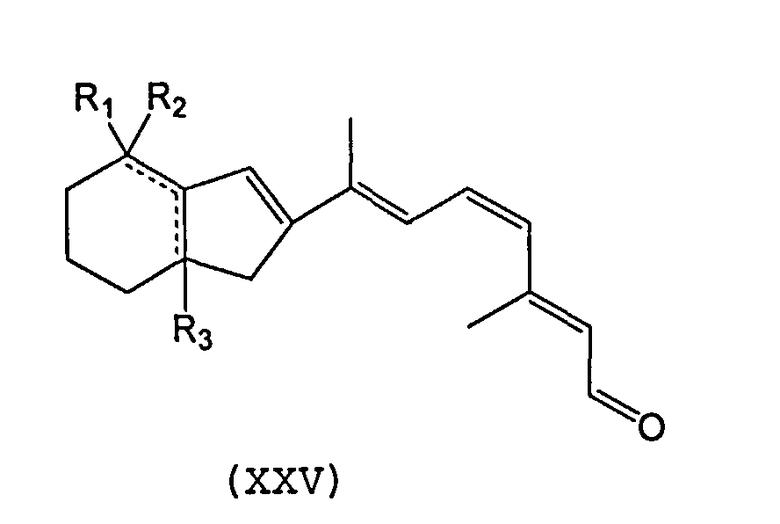
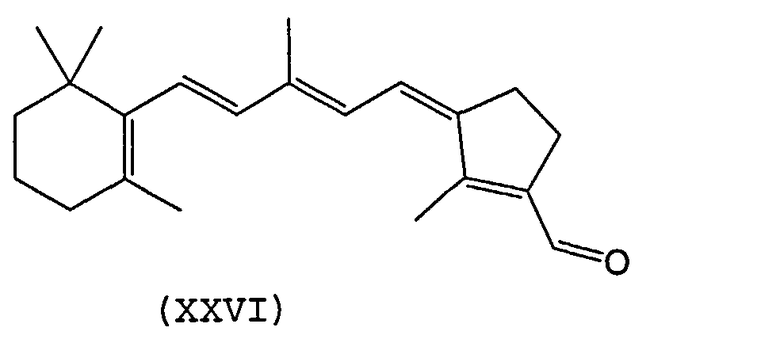
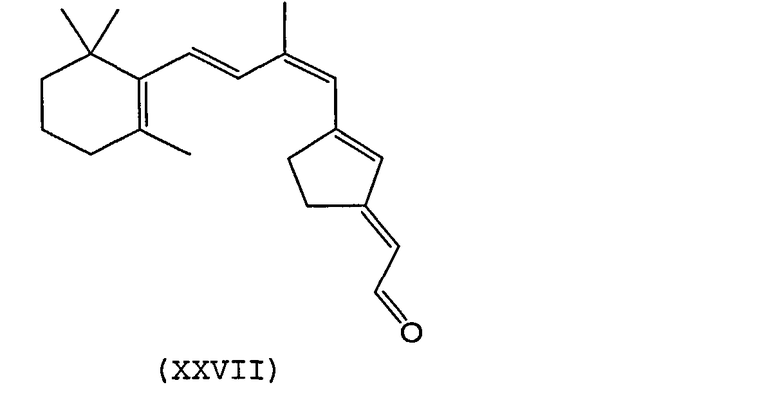
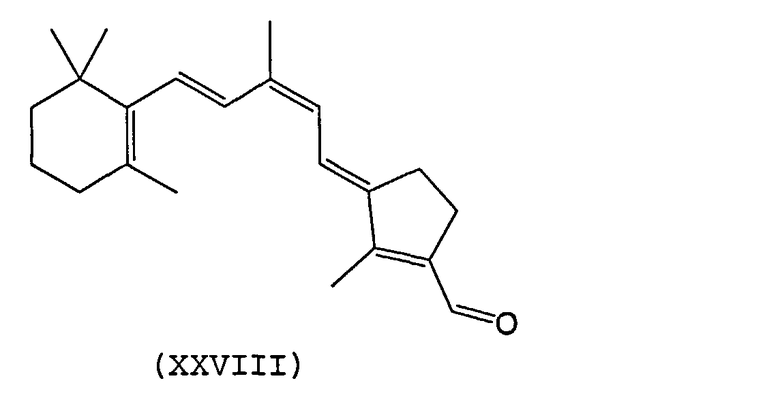
В еще одном варианте осуществления синтетический ретиноид представлять собой соединение формулы XXIX.
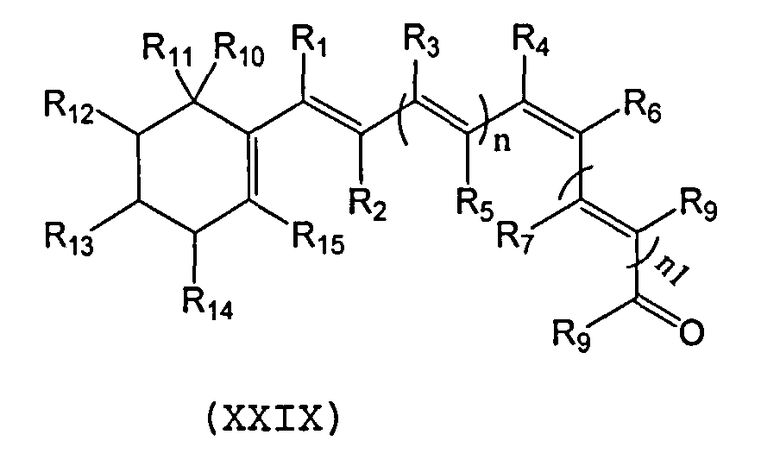
Каждый из R1-R15 может быть независимо выбран из водорода, алкила, разветвленного алкила, галогена, гидроксила, гидроалкила, амина, амида, гетероатома или т.п. Подходящие алкилы включают, например, метил, этил, пропил, замещенный алкил (например, алкил с гидроксилом, гидроалкилом, амином, амидом) или т.п. Подходящим разветвленным алкилом может быть, например, изопропил, изобутил, замещенный разветвленный алкил или т.п. Подходящие галогены включают, например, бром, хлор, фтор или т.п. Подходящие гетероатомы включают, например, серу, кремний и фтор- или бром-заместители. Подходящие замещенные алкилы и замещенные разветвленные алкилы включают, например, алкилы и разветвленные алкилы, замещенные кислородом, гидроксилом, азотом, амидом, амином, галогеном, гетероатомом или другими группами. Каждый из n и n1 может быть независимо выбран из 1, 2 или 3 алкильных, алкеновых или алкиленовых групп, при условии, что сумма n и n1 равна по меньшей мере 1. Кроме того, R11-R12 и/или R13-R14 может содержать алкеновую группу в циклическом углеродном кольце. В некоторых вариантах выполнений R5 и R7 вместе могут образовывать циклоалкил, такой как пяти-, шести-, семи- или восьмичленный циклоалкил, или замещенный циклоалкил, такие как циклоалкилы, показанные в формулах XXIII, XXIV, XXVI, XXVII и XXVIII.
В другом варианте осуществления синтетический ретиноид может представлять собой 9-cis-ретиналь. Альтернативно, может быть использован 11-cis-ретиналь.
Ретиниловые сложные эфиры могут быть образованы способами, известными в данной области, такими как, например, катализируемая кислотой этерификация ретинола карбоновой кислотой, реакцией ацилгалогенида с ретинолом, переэтерификацией ретинилового сложного эфира карбоновой кислотой, реакцией первичного галогенида с солью ретиноевой кислоты, катализируемой кислотой реакцией ангидрида с ретинолом, или т.п. В одном примере ретиниловые сложные эфиры могут быть образованы катализируемой кислотой этерификацией ретинола карбоновой кислотой, такой как уксусная кислота, пропионовая кислота, масляная кислота, валериановая кислота, капроновая кислота, каприловая кислота, пеларгоновая кислота, каприновая кислота, лауриновая кислота, олеиновая кислота, стеариновая кислота, пальмитиновая кислота, миристиновая кислота, линолевая кислота, янтарная кислота, фумаровая кислота или т.п. В другом примере ретиниловые сложные эфиры могут быть образованы реакцией ацилгалогенида с ретинолом (см., например. Van Hooser et al., Proc. Natl. Acad. Sci. USA, 97:8623-28 (2000)). Подходящие ацилгалогениды включают, например, ацетилхлорид, пальмитоилхлорид или т.п.
Ретиниловые простые эфиры могут быть образованы способами, известными в данной области, такими как, например, реакция ретинола с первичным алкилгалогенидом.
Транс-ретиноиды могут быть изомеризованы до цис-ретиноидов воздействием УФ-света. Например, полностью-транс-ретиналь, полностью-транс-ретинол, полностью-транс-ретиниловый сложный эфир или полностью-транс-ретиноевая кислота могут быть изомеризованы до 9-cis-ретиналя, 9-cis-ретинола, 9-cis-ретинилового сложного эфира или 9-cis-ретиноевой кислоты, соответственно. Транс-ретиноиды могут быть изомеризованы до 9-cis-ретиноидов, например, воздействием УФ-света, имеющего длину волны приблизительно 365 нм и по существу не содержащего более короткие длины волн, которые вызывают деградацию цис-ретиноидов, как описано здесь далее.
Ретинильацетали и гемиацетали могут быть получены, например, обработкой 9-cis- и 11-cis-ретиналей спиртами в присутствии кислотных катализаторов. Воду, образованную во время этой реакции, удаляют, например, при помощи Al2O3 молекулярного сита.
Ретинилоксимы могут быть получены, например, реакцией ретиналя с гидроксиламином, О-метил- или О-этилгидроксиламином, или т.п.
Это синтетическое производное ретиналя может быть по существу чистым, в том смысле, что оно содержит менее приблизительно 5%, или менее приблизительно 1%, или менее приблизительно 0,1% других ретиноидов. Может вводиться комбинация синтетических производных ретиналя.
Синтетические производные ретиналя могут доставляться в глаз любыми подходящими способами, включающими, например, пероральное, внутривенное, внутримышечное или местное введение. Способы местного введения могут включать, например, глазные капли, внутриглазную инъекцию или периорбитальную инъекцию или доставку через форму и/или устройство доставки лекарственного средства посредством контролируемого высвобождения. Периорбитальная инъекция обычно включает инъекцию синтетического производного ретиналя в конъюнктиву или в тенонову капсулу (фиброзную ткань, покрывающую глаз). Внутриглазная инъекция обычно включает инъекцию синтетического производного ретиналя в стекловидное тело. Это введение может быть неинвазивным, таким как глазные капли или пероральная дозированная форма.
Синтетические производные ретиналя могут быть приготовлены, например, в виде фармацевтических композиций для местного введения в глаз и/или для внутривенного, внутримышечного или перорального введения.
Синтетические производные ретиналя могут быть приготовлены для введения с использованием фармацевтически приемлемых носителей, а также способов, рутинно используемых в данной области. Носитель может быть выбран в соответствии с растворимостью синтетического производного ретиналя. Подходящие фармацевтические композиции включают композиции, которые могут вводиться локально в глаз, такие как глазные капли, инъекционный раствор или т.п. В случае глазных капель, эта готовая форма может необязательно включать, например, офтальмически совместимые агенты, такие как изотонизирующие агенты, такие как хлорид натрия, концентрированный глицерин, и т.п.; буферные агенты, такие как фосфат натрия, ацетат натрия и т.п.; поверхностно-активные вещества, такие как моноолеат полиоксиэтиленсорбитана (также называемый Полисорбатом 80), полиоксилстеарат 40, полиоксиэтилированное гидрогенизированное касторовое масло, и т.п.; стабилизирующие агенты, такие как цитрат натрия, эдентат натрия, и т.п.; консерванты, такие как хлорид бензалкония, парабены, и т.п.; и другие ингредиенты. Консерванты могут быть использованы, например, при уровне от приблизительно 0,001 до приблизительно 1,0% (масса/объем). рН этой готовой формы обычно находится в диапазоне, приемлемом для офтальмологических готовых форм, например, в пределах диапазона приблизительно рН 4-8.
Подходящие фармацевтические композиции включают также композиции, приготовленные для инъекции. Например, синтетическое производное ретиналя может быть обеспечено в солевом растворе категории растворов для инъекций, в форме инъекционного липосомного раствора или в других носителях или наполнителях. Внутриглазные и периорбитальные инъекции известны квалифицированным в данной области специалистам и описаны в многочисленных публикациях, включающих, например, Ophthalmic Surgery: Principles of Practice, Ed., G.L. Spaeth, W.B. Sanders Co., Philadelphia, Pa., U.S.A., pages 85-87 (1990).
Синтетическое производное ретиналя может также вводиться в форме и/или устройстве с высвобождением, зависимым от времени, например, в композиции, которая включает полимер с медленным высвобождением. Это синтетическое производное ретиналя может быть получено с носителем (носителями), которые будут защищать это соединение от быстрого высвобождения, например, в виде формы регулируемого высвобождения, включающей имплантаты и микроинкапсулированные системы доставки. Могут быть использованы биодеградируемые, биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры, полимолочная кислота и сополимеры полимолочной и полигликолевой кислот (PLG). Многие способы приготовления таких готовых форм известны квалифицированным в данной области специалистам.
Подходящие пероральные дозированные формы включают, например, таблетки, пилюли, пакетики (с порошком) или капсулы из твердого или мягкого желатина, метилцеллюлозы или другого подходящего материала, легко растворяющегося в пищеварительном тракте. Могут быть использованы подходящие нетоксичные твердые носители, которые включают, например, фармацевтические категории маннита, лактозы, крахмала, стеарата магния, натрий-сахарина, талька, целлюлозы, глюкозы, сахарозы, карбоната магния и т.п. (См., например, Remington "Pharmaceutical Sciences", 17 Ed., Gennaro (ed.), Mack Publishing Co., Easton, Pennsylvania (1985).
Следующие примеры обеспечены только в качестве иллюстрации различных аспектов этого изобретения и не должны рассматриваться как ограничение каким бы то ни было образом этого изобретения.
6. ПРИМЕРЫ
РЕЗУЛЬТАТЫ
Введение
Схемы введения как единичной дозы, так и продолжительного ежемесячного введения доз с 9-cis-R-Ac использовали для оценки действия увеличения искусственного хромофора на зрительную функцию мышей. Используемым хромофором был 9-cis-R-Ac, пролекарство, которое метаболизируется и превращается в 9-cis-ретиналь для образования изородопсина (Batten, M.L., et al. PLoS medicine 2, e333 (2005)). Для экспериментов с единичной дозой использовали двадцать мышей (фиг.1А, таблица 1), тогда как для продолжительного ежемесячного лечения использовали 210 мышей (фиг.1А, 1В, таблица 1). Мышам вводили через желудочный зонд полностью-транс-R-Ac (n=10) и его продолжительные эффекты оценивали при помощи выбранных анализов.
Аббревиатуры
9-cis-R-Ac, 9-cis-ретинилацетат; A2E, N-ретинилиден-N-ретинилэтаноламин; ERG, электроретинограмма; LRAT, лецитин:ретинол-ацилтрансфераза; ROS, наружные сегменты палочек сетчатки; RPE, ретинальный пигментный эпителий (пигментный эпителий сетчатки); RPE65, RPE-специфический белок 65 кДа.
Пример 1
Лечение единичной дозой самок мышей C57BL/6 с использованием 9-cis-R-Ac
Адаптированным в течение сорока восьми часов к темноте, 10-месячным мышам вводили через желудочный зонд единичную дозу (~80 мг/кг массы тела) 9-cis-R-Ac или контрольный носитель и подвергали действию сильного освещения в течение 20 минут (свет 500 кд/м2, который обесцвечивал ~90% родопсина). Затем мышей адаптировали к темноте в течение 16 часов, после чего выполняли различные анализы (фиг.1A). ERG с единичной вспышкой, проводимая на обработанных и необработанных мышах, показала, что функциональные амплитуды а- и b-волн обработанных мышей слегка увеличивались в сравнении с амплитудами в контрольных мышах (а-волны, P<0,01; данные не показаны). Для исследования, использовался ли 9-cis-ретиналь для образования изородопсина, и для оценки, какое количество не являющегося лигандом опсина присутствовало в глазах мышей, родопсин, изородопсин и опсин очищали иммуноаффинной хроматографией из обработанных и контрольных групп мышей. Коэффициент регенерации родопсина, рассчитанный по соотношению родопсина и изородопсина (оптическая плотность при 498 нм) к очищенному белку (оптическая плотность при 280) в каждой фракции, был значимо более высоким в глазах обработанных мышей, чем контрольных мышей, тогда как общее количество очищенного белка не различалось значимо (фиг. 2). При экстракции ретиноидов из очищенных белков для идентификации связанного хромофора, значительное количество 9-cis-ретиналя детектировали в пробах от обработанных мышей, что позволяет предполагать, что 9-cis-ретиналь использовался для регенерации опсина с образованием изородопсина (данные не показаны). Значительные количества 9-cis-ретиналя детектировали в глазах подвергнутых интенсивному свету и обработанных мышей (фиг.3А и 3В), в то время как не было значимого влияния на количества 11-cis-ретиналя и полностью-транс-ретиниловых сложных эфиров во всех группах мышей (фиг.3В и 3С). В этих обработанных и подвергнутых интенсивному свету мышах RPE также сохранял значительное количество 9-cis-ретиниловых сложных эфиров, предшественника ретиналя (фиг.3С). Только следовые количества 9-cis-ретиналя детектировали в глазах контрольных мышей и обесцвеченных глазах обработанных мышей (фиг.3В и С). Эти результаты ясно демонстрируют, что 9-cis-R-Ac метаболизирует его сложные эфиры с образованием 9-cis-ретиналя и в самках мышей C57BL/6 дикого типа. После обесцвечивания 9-cis-ретиналь связывается с опсином даже в присутствии функционального ретиноидного цикла, который производит 11-cis-ретиналь, для регенерации родопсина. Глаза из необесцвеченных или обесцвеченных и адаптированных к темноте необработанных мышей содержали малое количество свободного опсина.
Пример 2
Продолжительная обработка самок мышей C57BL/6 9-cis-R-Ac
Для продолжительных исследований (фиг.1В и 1С) самкам мышей C57BL6 вводили через желудочный зонд 9-cis-R-Ac, полностью-транс-R-Ac или контрольный носитель ежемесячно в течение 6 или 10 месяцев.
Пример 3
Анализы ERG c единичной вспышкой
Для оценки действий опосредуемых палочками и колбочками сетчатки световых реакций после продолжительных обработок 9-cis-R-Ac, мышей исследовали неинвазивными способами ERG. Первый набор анализов выполняли при возрасте 4 и 10 месяцев. При скотопических условиях амплитуды а-волн уменьшались с возрастом, особенно при высоких интенсивностях вспышек (группа C1 в сравнении с группой C0, фиг.4А, левая верхняя панель), тогда как изменения в b-волнах были менее очевидными (фиг.4А, правая верхняя панель). При фотопических условиях не наблюдали различий ни для а-, ни для b-волн (фиг.4А, нижние панели). При сравнении обработанных и необработанных групп (N1 в сравнении с С1) небольшое улучшение наблюдали для группы N1 относительно a- или b-волн при высоких интенсивностях вспышек (p<0,01, односторонний ANOVA) как при фотопических, так и при скотопических условиях, за исключением а-волн при фотопических условиях (фиг.4А, левые нижние панели).
Второй набор анализов выполняли при возрасте 14 месяцев. Не были обнаружены значимые различия в амплитудах а- и b-волны между контрольной группой (С2) и обработанными группами мышей (N2 и N3) ни при скотопических, ни при фотопических условиях (фиг.4В). Из максимальных реакций а-волны в адаптированных к темноте мышах оценивали чувствительности и максимальные амплитуды а-волн, и было обнаружено, что эти параметры также не были значимо различными (данные не показаны).
Пример 4
Изменения в темновой адаптации
Восстановление ERG-реакции (темновой адаптации) после обесцвечивания измеряли мониторингом амплитуды а-волн после подвергания сетчатки интенсивному постоянному освещению (500 кд/м2, на ~90% обесцвеченный родопсин) в течение 3 минут. Восстановление этих реакций было значимо более быстрым в обработанных 9-cis-R-Ac группах в сравнении с контрольными группами мышей как при 10-месячном (N1 против C1, фиг.5А), так и при 14-месячном возрасте (N2 и N3 vs. C2, фиг.5B) (p<0,001, односторонний ANOVA). Кинетики ретиноидов в глазах каждой группы оценивали количественно во время 60 минут темновой адаптации после 3 минут обесцвечивания при четырех последовательных временных точках темновой адаптации (0, 10, 30 и 60 мин). При возрасте 10 месяцев уровень регенерации 11-cis-ретиналя в обработанной группе (N1) был значимо более высоким, чем в контрольной группе (C1) (p<0,01) спустя 60 мин после обесцвечивания. Однако не было значимого различия в кинетике полностью-транс-ретиналя и полностью-транс-ретиниловых эфиров между этими группами и между обработанными и необработанными мышами при возрасте 14 месяцев. Ни 9-cis-ретиналь, ни 9-cis-ретиниловые сложные эфиры не обнаруживались в глазах из необработанных групп (данные не показаны).
Пример 5
Действия продолжительного введения полностью-транс-R-Ac на зрительную функцию
В дополнительных контрольных экспериментах мышам вводили через желудочный зонд неактивный изомер, полностью-транс-R-Ac (n=10) в течение 10 месяцев и оценивали при возрасте 14 месяцев. ERG-исследование не обнаруживало значимого различия в сравнении с контролем (C2) в анализах ERG с единичной вспышкой a- и b-волн или в восстановлении темновой адаптации (n=3). Эти результаты показали, что эффекты ERG являются специфическими в отношении 9-cis-изомера.
Пример 6
Анализы родопсина, А2Е и ретиноидных кислот в контрольных и обработанных 9-cis-R-Ac мышах
Коэффициенты регенерации (родопсин/опсин) и общие количества очищенного родопсина не обнаруживали значимых различий между контрольными и обработанными группами мышей как при возрасте 10 месяцев, так и при возрасте 14 месяцев. Количества очищенного белка, извлеченного из обработанных групп при возрасте 14 месяцев (N2 и N3), были значимо более низкими, чем количества очищенного белка из контрольных мышей (C2), тогда как это количество было лишь слегка уменьшенным в 10-месячных обработанных мышах (N1 против C1) (данные не показаны).
Для оценки безвредности продолжительного введения 9-cis-R-Ac, измеряли накапливание A2E (фиг.6A), поскольку ретинали спонтанно конденсируются с образованием этого соединения (Mata, N.L., Weng, J. & Travis, G.H. Proceedings of the National Academy of Sciences of the United States of America 97, 7154-7159 (2000); Parish, C.A., Hashimoto, M., Nakanishi, K., Dillon, J. & Sparrow, J. Proceedings of the National Academy of Sciences of the United States of America 95, 14609-14613 (1998)). A2E и изо-A2E детектировали при сходных уровнях в обработанных и контрольных мышах при возрасте как 10, так и 14 месяцев (фиг.6B). В контролях перед обработкой (C0, в возрасте 4 месяцев), накапливание A2E было ниже детектируемых уровней (фиг.6B). Хотя продолжительная обработка ретиниловыми сложными эфирами может вызывать повышенные уровни митогенной ретиноевой кислоты в печени, уровни ретиноида в виде кислоты в печени были ниже детектируемых уровней во всех группах (данные не показаны).
Пример 7
Состояние животных и морфология сетчаток из обработанных 9-cis-R-Ac мышей
Животных оценивали один раз в неделю в отношении активности и изменений во внешнем виде шерсти и кожи. Изменений в этих параметрах не наблюдали во время экспериментального периода, кроме изменений вследствие природного старения. Массы тела мышей, оцениваемые перед обработкой, при 10 месяцах и 14 месяцах, не обнаруживали значимых различий между контрольными (C1-2) и обработанными группами (N1-3) (данные не показаны).
Световая микроскопия не выявила больших отклонений от нормы в сетчатках обработанных носителем, 9-cis-R-Ac или полностью-транс-R-Ac (n=2) мышах при возрасте 10 и 14 месяцев, и сетчатки из этих двух обработанных групп были неотличимыми. Длины наружных сегментов палочек сетчатки (ROS) были сходными в контрольной и обработанной группах при возрасте 10 и 14 месяцев. (фиг.7В; n=5), но значимо уменьшались в сравнении с длинами ROS 4-месячных мышей (C0), гистология сетчатки которых показана на фиг.7А. Толщина каждого основного слоя в этой сетчатке также была сходной между контрольными и обработанными группами. EM-анализ наружной сетчатки и RPE-слоя не выявил макроскопических различий между контрольными и обработанными мышами. Более высокое разрешение пограничного слоя между RPE и ROS также не обнаруживало отклонений от нормы (данные не показаны).
Пример 8
Изменения в профилях экспрессии ДНК введением 9-cis-R-Ac
Анализы микромассивов (микрочипов) ДНК использовали для документации возможных изменений в профилях экспрессии генов после продолжительной обработки 9-cis-R-Ac. Уровни экспрессии мРНК в глазе, печени и почке определяли и сравнивали между обработанными (N2) и контрольными (C2) группами с использованием массива (чипа) 37364 генов, обеспечиваемого NimbleGen System Inc. В глазу обработка 9-cis-R-Ac повышала экспрессию 290 генов в 2 раза или более и ослабляла экспрессию более чем 1057 генов в 0,5 раз или менее (фиг.8; таблица S1). В печени обработанных мышей экспрессия только 7 генов увеличивалась в 2 раза или более и экспрессия только 20 генов подавлялась в 0,5 раз или менее (фиг.8; таблица S2). В почке обработанных мышей 90 генов увеличивали их экспрессию в 2 раза или более и 3 гена подавляли экспрессию в 0,5 раз или менее (фиг.8; таблица S2). Специфические для фототрансдукции, процессирующие ретиноиды и классифицированные по их функции гены, на экспрессию которых обнаруживалось влияние, перечислены в таблицах S2. Не было обнаружено действие на уровни белков трансдуцина (Gt), родопсинкиназы, активируемого гуанилатциклазой белка 1 и активируемого гуанилатциклазой белка 2, гуанилатциклазы 1, ретинолдигидрогеназы 12 и LRAT во всех группах мышей, в соответствии с оцениванием с использованием иммуноблоттинга (данные не показаны).
b Один глаз из мыши использовали для световой микроскопии, а другой для электронной микроскопии.
ОБСУЖДЕНИЕ
Как показано в этих исследованиях, обусловленное возрастом разрушение темновой адаптации у мышей ослаблялось лечением искусственным цис-ретиноидом. Это открытие является аналогичным обусловленным возрастом ухудшениям в зрении человека, проявляющимся разительным замедлением опосредуемой палочками сетчатки темновой адаптации, приписываемым замедленной регенерации родопсина (Jackson, G.R., Owsley, C. & McGwin, G., Jr. Vision Research 39, 3975-3982 (1999)). Выполнены два различных типа исследований. Исследования с единичной дозой выявили, что 9-cis-R-ретиноиды могут входить в глаз, а вторая серия экспериментов показала, что продолжительное введение 9-cis-R-Ac значимо улучшало разрушенную функцию сетчатки у стареющих мышей.
Эксперименты с единичной дозой
Эти эксперименты планировались для исследования, входят ли 9-cis-ретиноиды в глаза 10-месячных мышей и улучшают ли они зрительную функцию. ERG-реакция измеримо уменьшалась со старением, и малые, но измеримые количества свободного опсина присутствовали у этих старых мышей. 9-cis-ретиналь входил в глаз, когда подлежащих лечению мышей подвергали действию сильного света и исследовали их спустя 18 часов. Предшественники 9-cis-ретиналя, 9-cis-ретиниловые сложные эфиры, были легко детектируемыми в глазах этих мышей, а также улучшалось отношение родопсин/опсин.
Продолжительное лечение мышей 9-cis-R-Ac
ERG-реакции на единичную вспышку света значимо улучшались у 10-месячных мышей, которых лечили в течение 6 месяцев 9-cis-R-Ac, в сравнении с получавшими масло контролями (фиг.4А). Этот терапевтический результат в значительной степени исчезал у 14-месячных мышей, которых лечили в течение 10 месяцев (фиг.4В), возможно, вследствие маскирующего эффекта ухудшения здоровья у этих более старых мышей. Однако эти более старые мыши не обнаруживали значимого действия, включающего темновую адаптацию (фиг.5В, группы N2 и N3). То, что продолжительное введение через желудочный зонд 14-месячным мышам полностью-транс-R-Ac не влияло на измеряемые параметры ERG, не является удивительным, так как только cis-форма этого хромофора может рекомбинироваться с опсином (как обсуждается в обзоре Palczewski, K. Annual review of biochemistry 75, 743-767 (2006); Filipek, S., Stenkamp, R.E., Teller, D.C. & Palczewski, K. Annu Rev Physiol 65, 851-879 (2003)). Таким образом, полностью-транс-ретиноид мог только добавлять субстрат для реакции изомеризации, но не восполнять активный хромофор, если изомеризация ослаблялась. Важным является то, что мыши в неволе содержались на рационе с высоким содержанием витамина А, следовательно, наблюдаемые действия цис-ретиноидов выходят на первое место относительно дополнительного введения полностью-транс-ретиноидов.
Продолжительное лечение (6-10 месяцев) хорошо переносилось самками мышей C57BL/6. Лечение не влияло на обусловленные возрастом детектируемые морфологические изменения в сетчатке, наблюдаемые как у проходивших лечение, так и у контрольных мышей. Потенциальные токсичные побочные продукты лечения ретиноидами, A2E и ретиноевая кислота, не накапливались у этих мышей. В этом исследовании 9-cis-R-Ac включался в свободный опсин в сетчатке, приводя к увеличенному коэффициенту регенерации пигментов палочек сетчатки. Однако количество полностью-транс-ретиналя, индуцируемое физиологическими световыми условиями, является постоянным независимо от количеств пигментов палочек сетчатки и коэффициента регенерации. Таким образом, неудивительно, что введение 9-cis-R-Ac не влияло на уровни A2E. Таким образом, благоприятное действие добавления цис-ретиноидов кажется более предпочтительным с этой точки зрения, чем с точки зрения антиоксидантных свойств, обычно приписываемых ретиноидам (Maxwell, S. & Greig, L. Expert opinion on pharmacotherapy 2, 1737-1750 (2001)).
Авторы не детектировали никакого накапливания ретиноевых кислот. Кроме того, изменения экспрессии генов были минимальными в печени и почке, хотя несколько белков были нерегулируемыми в глазе. Детальный анализ этих генов авторами изобретения не выявил никаких особых распределений экспрессии.
Профилактическое применение 9-cis-ретиноидов
Люди начинают терять их способность к темновой адаптации с 3-его - 4-го десятка лет (Jackson, G.R., McGwin, G., Jr., Phillips, J.M., Klein, R. & Owsley, C. Vision research 46, 1422-1431 (2006)). Ухудшение зрительной функции проявляется функционально уменьшением способности выполнения некоторых активностей, таких как вождение машины ночью и чтение в затемненном окружении (Schilling, O.K. & Wahl, H.W. Psychology and aging 21, 703-714 (2006)). Такие симптомы становятся все более изнуряющими с возрастом и могут приводить к уменьшенной независимости и активности в пожилом возрасте. Эта проблема становится более острой, так как люди живут сейчас дольше. Результаты экспериментов авторов изобретения демонстрируют, что перорально вводимый 9-cis-ретиноид применим в качестве долгосрочного профилактического агента, а также терапевтического соединения.
Предпочтительные результаты и относительная безвредность 9-cis-ретиноидов распространяются на обусловленную возрастом дегенерацию желтого пятна, главную причину легальной слепоты в США и в Европе (Zack, D.J., et al. Mol Vis 5, 30 (1999)). Здесь авторы этого изобретения показали, что имеются биохимические изменения в цикле превращений родопсина в сетчатке, которые встречаются со старением, а именно, увеличение количества свободного опсина и отношения опсин/родопсин. Когда подобные биохимические изменения являются избыточными, они могут приводить к дегенерациям сетчатки, таким как наблюдаемые в LCA (Fan, J., Woodruff, M.L., Cilluffo, M.C., Crouch, R.K. & Fain, G.L. J Physiol 568, 83-95 (2005)). Кроме того, свободный опсин приводит к спонтанной инициации зрительного каскада в палочковых фоторецепторах (Lisman, J. & Fain, G. Nat Med 1, 1254-1255 (1995); Fain, G.L., Matthews, H.R., Cornwall, M.C. & Koutalos, Y. Physiol Rev 81, 117-151 (2001); Surya, A., Foster, K.W. & Knox, B.E. J Biol Chem 270, 5024-5031 (1995); Hofmann, K.P., Pulvermuller, A., Buczylko, J., Van Hooser, P. & Palczewski, K. J Biol Chem 267, 15701-15706 (1992); Palczewski, K., et al. Biochemistry 33, 13741-13750 (1994); Jager, S., Palczewski, K. & Hofmann, K.P. Biochemistry 35, 2901-2908 (1996)). Это приводит к уменьшенному отношению сигнал/шум в системе зрения, увеличенной метаболической перегрузке в RPE, что приводит к образованию большего количества продуктов выделения, свободных радикалов и, в конечном счете, друз. Таким образом, уменьшение свободного опсина при помощи 9-cis-ретиноидной терапии будет приводить к уменьшению предшественников, которые, как считается, инициируют AMD.
СПОСОБЫ
Животные
Имеющих пигментную ретинопатию подобранных по возрасту самок мышей C57BL/6, полученных из Charles River Laboratories, поддерживали на нормальном рационе в полной темноте или при цикле 12 ч свет/темнота. Все эксперименты на животных использовали процедуры, одобренные University of Washington и Case Western Reserve University Animal Care Committees и соответствующие рекомендациям American Veterinary Medical Association Panel on Euthanasia и the Association of Research for Vision and Ophthalmology.
Лечения единичной дозой и продолжительное лечение мышей 9-cis-R-Ac
9-cis-R-Ac готовили, как описано ранее (Batten, M.L., et al. PLoS medicine 2, e333 (2005); Batten, M.L., et al. J Biol Chem 279, 10422-10432 (2004)). Дозу ~80 мг/кг массы тела 9-cis-R-Ac в 150 мкл растительного масла вводили через желудочный зонд каждому получающему лечение животному. Перед экспериментами с единичной дозой (фиг.1А, таблица 1) 10-месячных мышей адаптировали к темноте в течение более чем 48 часов, вводили через желудочный зонд 9-cis-R-Ac или контрольный раствор носителя за 1 час перед обесцвечиванием, выдерживали на свету в течение 20 минут при 500 кд/м2 и адаптировали к темноте в течение 16 часов перед анализом.
Для продолжительного исследования (фиг.1В и 1С, таблица 1) мышей получали в возрасте 3 месяца и выращивали до возраста 4 месяца перед началом этих экспериментов. Затем мышам вводили через желудочный зонд 9-cis-R-Ac или раствор носителя один раз в месяц в течение различных периодов времени. Исследовали шесть групп мышей (фиг.1В). Первые 3 группы (C0, C1 и C2, всего n=35 для каждой группы) обрабатывали в качестве контролей и тестировали при возрасте 4, 10 и 14 месяцев. Другие 3 группы (N1, N2 и N3, n=35) получали через желудочный зонд 9-cis-R-Ac. Группе N1 вводили через зонд 9-cis-R-Ac в течение 6 месяцев и мышей тестировали при возрасте 10 месяцев. Группе N2 вводили через зонд 9-cis-R-Ac в течение 10 месяцев и мышей тестировали при возрасте 14 месяцев. Группе N3 вводили через зонд носитель до возраста 10 месяцев и затем им вводили 9-cis-R-Ac один раз в день до тестирования при возрасте 14 месяцев. В другой контрольной группе, не показанной на фиг.1В, мышам вводили через зонд ~80 мг/кг массы тела полностью-транс-R-Ac (Sigma-Aldrich, Corp.) в течение 10 месяцев и тестировали мышей в возрасте 14 месяцев.
Спустя две недели после последнего введения через зонд 9-cis-R-Ac, полностью-транс-R-Ac или носителя группы из адаптированных к темноте в течение 48 часов мышей анализировали на восстановление темновой адаптации, на отношение очищенный родопсин/опсин и ретиноиды в их глазах и на морфологию сетчатки (фиг.1C; Способы). Мышей подвергали действию света с интенсивностью 500 кд/м2, который обесцвечивал ~90% родопсина, анестезировали и подвергали мониторингу при помощи ERG в течение одного часа для оценки восстановления темновой адаптации. Родопсин очищали и определяли отношения родопсин/опсин. Анализы ретиноидов выполняли на иссеченных глазах, удаленных при 0, 10, 30 и 60 мин после воздействия одного и того же количества света. Мышей, используемых для оценки морфологии сетчатки, не подвергали фотообесцвечиванию перед анализом.
Электроретинография (ERG)
ERG-анестезированных мышей регистрировали, как сообщалось ранее 24,39.
Очистка родопсина
Очистку родопсина выполняли под слабым (тусклым) красным светом, как описано ранее (Zhu, L., et al. J Biol Chem 279, 53828-53839 (2004)). Очищенное антитело 1D4 против С-конца родопсина (MacKenzie, D., Arendt, A., Hargrave, P., McDowell, J.H. & Molday, R.S. Biochemistry 23, 6544-6549 (1984)) иммобилизовали на CNBr-активированной Сефарозе 4B и колонку 4,6×12 мм загружали 2 мг антитела 1D4/мл на гранулах Сефарозы. Целые глаза мыши гомогенизировали в 137 мМ NaCl, 5,4 мМ Na2HPO4, 2,7 мМ KCl и 1,8 мМ KH2PO4 (pH 7,5) с использованием полностью стеклянного гомогенизатора. Растворимые белки в супернатанте удаляли центрифугированием при 14000×g в течение 5 мин и осадок солюбилизировали в буфере, содержащем 1% додецил-β-мальтозид в 10 мМ Бис-Трис-пропане (pH 7,5), содержащем 500 мМ NaCl. Этот супернатант осветляли центрифугированием при 125000×g в течение 20 мин и наносили на упакованную антителом 1D4 иммунноаффинную колонку, которую затем тщательно промывали при скорости тока 0,5 мл/мин 10 мМ Бис-Трис-пропаном (pH 7,5), содержащим 500 мМ NaCl и 0,1% додецил-β-мальтозид. Очищенный родопсин мыши элюировали 100 мкМ нонапептидом (TETSQVAPA) в 10 мМ Бис-Трис-пропане (pH 7,5), содержащем 500 мМ NaCl и 0,1% додецил-β-мальтозид, при комнатной температуре. Концентрацию очищенного родопсина определяли при 500 нм и общее количество опсина и родопсина при 280 нм с использованием спектрофотометра Hewlett-Packard 8452A UV-visible spectrophotometer (Palczewski, K., Carruth, M.E., Adamus, G., McDowell, J.H. & Hargrave, P.A. Vision research 30, 1129-1137 (1990)).
Анализ ретиноидов
Все экспериментальные процедуры, связанные с экстракцией, дериватизацией и разделением ретиноидов, проводили при слабом красном свете, обеспечиваемом (фото) лабораторным фильтром Kodak No. 1 (коэффициент пропускания >560 нм), как описано ранее (Van Hooser, J.P., et al. Proceedings of the National Academy of Sciences of the United States of America 97, 8623-8628 (2000); Van Hooser, J.P., et al. J Biol Chem 277, 19173-19182 (2002); Maeda, A., et al. J Biol Chem 280, 18822-18832 (2005); Van Hooser, J.P., Garwin, G.G. & Saari, J.C. Methods Enzymol 316, 565-575 (2000)). Элюированные фракции очищенного родопсина из 6 глаз мышей объединяли (всего 3,0 мл) и смешивали с равным объемом 100% метанола. Эту смесь перемешивали на вортексе и инкубировали на льду в течение 15 минут. Ретиноиды экстрагировали дважды равным объемом 100% гексана (всего 6 мл). Объединенные экстракты сушили в атмосфере аргона и ретиноиды разделяли ВЭЖХ с нормальной фазой (Beckman, Ultrasphere-Si, 5 мкм, 4,6×250 мм) с использованием 10% этилацетата и 90% гексана при скорости тока 1,4 мл/мин и детектировали при 325 нм при помощи HP1100 ВЭЖХ с использованием диодного детектора и программного обеспечения HP Chemstation A.03.03. A2E анализировали, как описано ранее (Maeda, A., et al. J Biol Chem 280, 18822-18832 (2005)).
Анализ ретиноевой кислоты в печени проводили, как описано ранее (Batten, M.L., et al. PLoS medicine 2, e333 (2005)) при помощи Agilent 1100 HPLC с двумя тандемными колонками с нормальной фазой: колонкой Varian Microsorb Silica 3 мкм, 4,6×100 мм (Varian, Palo Alto, CA) и колонкой Ultrasphere-Si, 5 мкм, 4,6×250 мм. Использовали систему изократических растворителей 1000:4,3:0,675 гексан:2-пропанол:ледяная уксусная кислота (об./об.) при скорости тока 1 мл/мин при 20°C с детектированием при 355 нм. Калибровку выполняли со стандартами полностью-транс-R-Ac и 9-cis-R-Ac, приобретенными из Sigma-Aldrich.
Иммуноблоттинг
Иммуноблоттинг выполняли в соответствии со стандартными протоколами с использованием Immobilon-P для адсорбции белков (поливинилидендифторид; Millipore Corp.).
Моноклональное антитело против родопсина (1D4) получали от доктора R. Molday. Анти-LRAT (mAb) (Moise, A.R., Golczak, M., Imanishi, Y. & Palczewski, K. J Biol Chem (2006)), антитело против трансдуцина (Gt) (mAb) (неопубликованное), антитело против гуанилатциклазы 1 (1S4, mAb); Haire, S.E., et al. Investigative ophthalmology & visual science 47, 3745-3753 (2006)), антитело против активирующего гуанилатциклазу белка 1 (UW14 pAb) (Gorczyca, W.A., et al. J Biol Chem 270, 22029-22036 (1995)), антитело против активирующего гуанилатциклазу белка 2 (UW50 pAb) Otto-Bruc, A., et al. Proceedings of the National Academy of Sciences of the United States of America 94, 4727-4732 (1997)), антитело против родопсинкиназы (Zhao, X., Huang, J., Khani, S.C. & Palczewski, K. J Biol Chem 273, 5124-5131 (1998)) и антитело против ретинолдегидрогеназы 12 (pAb) (Maeda, A., et al J Biol Chem 281, 37697-37704 (2006)) генерировали в лаборатории авторов этого изобретения. Конъюгированное со щелочной фосфатазой козье антитело против мышиного IgG или козье антитело против кроличьего IgG (Promega) использовали в качестве вторичных антител. Полосы белков визуализировали с использованием развивающего окраску субстрата 5-бром-4-хлор-3-индолилфосфат/нитрокраситель тетразолиевый синий (Promega). Белки (30 мкг на каждую лунку) разделяли при помощи электрофореза в 12,5% ДСН-ПААГ.
Морфология сетчатки
Для световой микроскопии глазные бокалы мышей фиксировали 2,5% глутаровым альдегидом и 1,6% параформальдегидом в содержащем 0,08M 1,4-пиперазиндиэтансульфонат буфере (PIPES) (pH 7,4), содержащем 2% сахарозу, в течение ~1 часа при комнатной температуре с последующими 23 часами при 4°С. Затем глазные бокалы промывали 0,13M содержащим фосфат натрия буфером (pH 7,3) и дегидратировали проведением через серию CH3OH и заливали в гликольметакрилате JB4. Срезы (6 мкм) окрашивали иммерсией в 5% красителе Ричардсона в течение 1,5-2 минут при комнатной температуре и краситель удаляли в 0,13М фосфате натрия (рН 7,3), пока слои сетчатки не становились видимыми под световым микроскопом (приблизительно 8-15 минут). Для трансмиссионной электронной микроскопии глазные бокалы мышей анализировали, как описано ранее (Maeda, A., et al. J Biol Chem 280, 18822-18832 (2005); Maeda, T., Lem, J., Palczewski, K. & Haeseleer, F. Investigative ophthalmology & visual science 46, 4320-4327 (2005)).
Анализ с использованием ДНК-микромассива (ДНК-чипа, массива экспрессии генов)
РНК выделяли из 10 глаз, 100 мг печени или 100 мг почки из групп мышей С2 и N2 (фиг.1В) с применением набора RiboPure Kit (Ambion, Austin, TX). Качество препарата проверяли с использованием электрофореза РНК в агарозном геле и биоанализатора (Agilent Bioanalyzer). Аликвоты общей (тотальной) РНК, выделенной из различных тканей и из мышей, подвергающихся различным обработкам, метили детектируемой меткой и гибридизовали на геномном микромассиве (микрочипе) мыши с использованием службы NimbleGen System Inc. (Madison, WI). Этот микромассив (микрочип) содержал 37364 гена и охватывал весь транскрипт мыши, представленный базой данных Santa Cruz, University of California, (build HG 17) с минимальным количеством 11 зондов на один ген. Экспрессию генов нормализовали в соответствии с сигналом зондов, и средний сигнал для каждого гена нормализовали относительно каждой повторности пробы.
Результаты, полученные с ДНК-массивом для проб на протяжении всего исследования, нормализовали с использованием сервиса NimbleGen Systems Inc. (Madison, WI), который использовал признак твердого (не допускающего возражений) мультичип-анализа пакета анализа данных, содержащегося в открытом для доступа источнике Bioconductor и открытом проекте развития программ для анализа и понимания геномных данных. Таблицы твердого мультичип-анализа в рамках проекта экспортировали в MICROSOFT® EXEL® и коэффициенты уровней экспрессии рассчитывали для всех возможных парных сравнений, содержащих одну контрольную и одну обработанную пробу. Эти парные коэффициенты импортировали в Microsoft Access и исследовали на вероятные изменения в экспрессии генов. Изменения, превышающие 2-кратное увеличение или равные 2-кратному увеличению, или меньшие чем 0,5-кратное уменьшение или равные 0,5-кратному уменьшению, считали значимыми. Затем дифференциально экспрессируемые гены экспортировались из Access в виде Excel-файлов и им присваивались функциональные аннотации посредством программы LUCIDYX SEARCHER™ при помощи Lucidyx LLC.
Статистические анализы
Статистические анализы выполняли с использованием одностороннего дисперсионного анализа (ANOVA).
Предыдущие примеры представлены для иллюстрации, но не для ограничения объема притязаний. Другие варианты этих изобретений будут вполне очевидными для специалистов с обычной квалификацией в данной области и включены в прилагаемую формулу изобретения.
Все публикации, патенты, заявки на патенты и другие ссылки, цитируемые здесь, включены, тем самым, посредством ссылки.
Пример 9
Исследование по безопасности мультидозового режима введения
Рандомизированное, открытое, плацебо-контролируемое, параллельное исследование мультидозового режима введения было выполнено для оценки безопасности, переносимости и фармакокинетики композиции, содержащей 20 мг/мл 9 -cis-ретинилацетата ((2E,4E,6Z,8E)-3,7-диметил-9-(2,6,6-триметилциклогекс-1-ен-1-ил)нона-2,4,6,8-тетраен-1-ил ацетат), при пероральном приеме здоровыми добровольцами. В исследование было включено 35 субъектов. Исследование состояло из субъектов, получавших 4 (группа получавшая плацебо и группа, получавшая дозу 2 0 мг/м2) или 6 (группы, получавшие дозу 40 и 60 мг/м2) последовательные 28-дневные циклы дозирования/элиминации (7-дневное дозирование и 21-дневная элиминация). После заключительного цикла субъекты наблюдались в течение 2 месяцев. Во время каждого цикла субъекты получили или терапевтическую дозу, включающую суточную дозу композиции для перорального приема (9-cis-ретинилацетат), вводимую в дозах 2 0 мг/м2, 40 мг/м2, 60 мг/м2 или плацебо, в течение 7 дней, сопровождаемых 21-дневным периодом элиминации, во время которого не субъекты не получали лечения. Субъекты периодически проверялись во время цикла для контроля различных неблагоприятных событий, таких как головные боли, приливы к лицу и ощущение жжения на лице. Субъекты также проверялись на токсичность, связанную с лечением, такую как повышение уровня триглицеридов и снижение уровня липопротеинов высокой плотностей (ЛПВП). Наблюдаемые неблагоприятные события включали головную боль, фотофобию, тошноту, увеличение повышенные уровни ALT, увеличение уровня триглицеридов и повышенные уровни AST. Большинство этих параметров возвратилось к нормальному уровню у всех субъектов на 14 день или через 1 месяц.
В исследовании не наблюдались новые или неожиданные неблагоприятные события. До шести повторных циклов лечения композицией в дозах 20 мг/м2/день, 40 мг/м2/день и 60 мг/м2/день в течение семи дней, с последующим 21-дневным периодом элиминации, были в целом безопасны и хорошо перенесены. Профиль безопасности повторных циклов лечения был схож с профилем одного цикла лечения, с полной тенденцией к снижению тяжести неблагоприятных событий с каждым последующим циклом дозирования. Результаты безопасности этого исследования дополнительно поддерживают применение повторного дозирования фармацевтических композиций на основе 9- или 11-cis-ретиниловых эфиров, включая композицию 9-cis-ретинилацетата этого Примера, при нерегулярных циклах дозирования.
Фармакокинетические результаты исследования были получены на основании данных о концентрации 9-cis-ретинилацетата и его метаболитов в плазме. Измерения концентрации проводили в течение всего периода исследования в предписанных точках времени. Объем этого анализа РК охватывает пробы от группы 1, включая группы, получавшие плацебо (n=2), дозу 40 мг/м2 (n=б) и 60 мг/м2 (n=2) в циклах лечения 1, 2 и 3.
Пробы плазмы анализировали с помощью жидкостной хроматографии с двойной масс-спектрометрией (LC/MS/MS) для определения концентрации исходного лекарственного средства и потенциальных метаболитов. Были получены модельнонезависимые (NCA)
фармакокинетические (РК) параметры, такие как AUC, используя программное обеспечение WinNonlin, с наблюдаемыми значениями Cmax, tmax и продолжительности сохранения концентраций выше нормы (TD).
Концентрации 9-cis-ретинилацетата в плазме были низкими и кратковременными, указывая на быстрый первичный метаболизм с дополнительным метаболизмом до неполярных и полярных метаболитов. В группе, получавшей дозу 40 мг/м2 в периодических семидневных циклах, 9-cis-ретинол и метаболиты ретинилового эфира показали небольшое накопление при множественном дозировании с высоким значением AUC в День 7, в соответствии с ожиданиями со Дня 1. Для более долго живущих метаболитов имело место ежедневное повышение значения Cmin, соответствующее небольшому накоплению. Эти картины накопления и концентрации были схожи для Циклов 1, 2 и 3, без накопления, наблюдаемого от цикла к циклу.
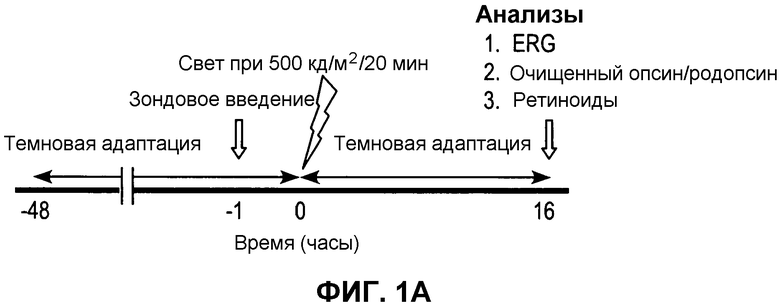
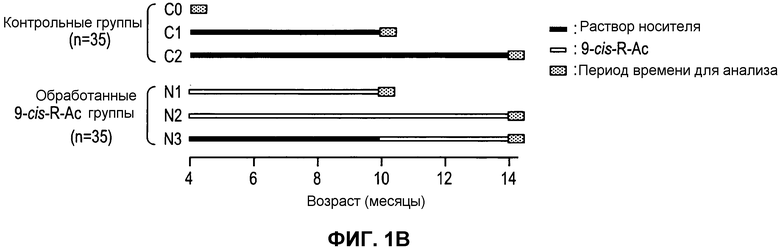
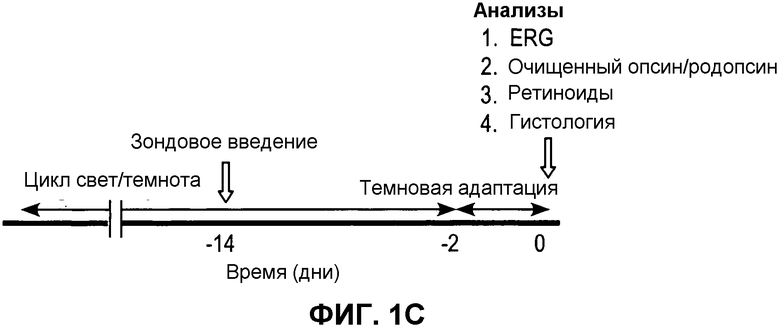
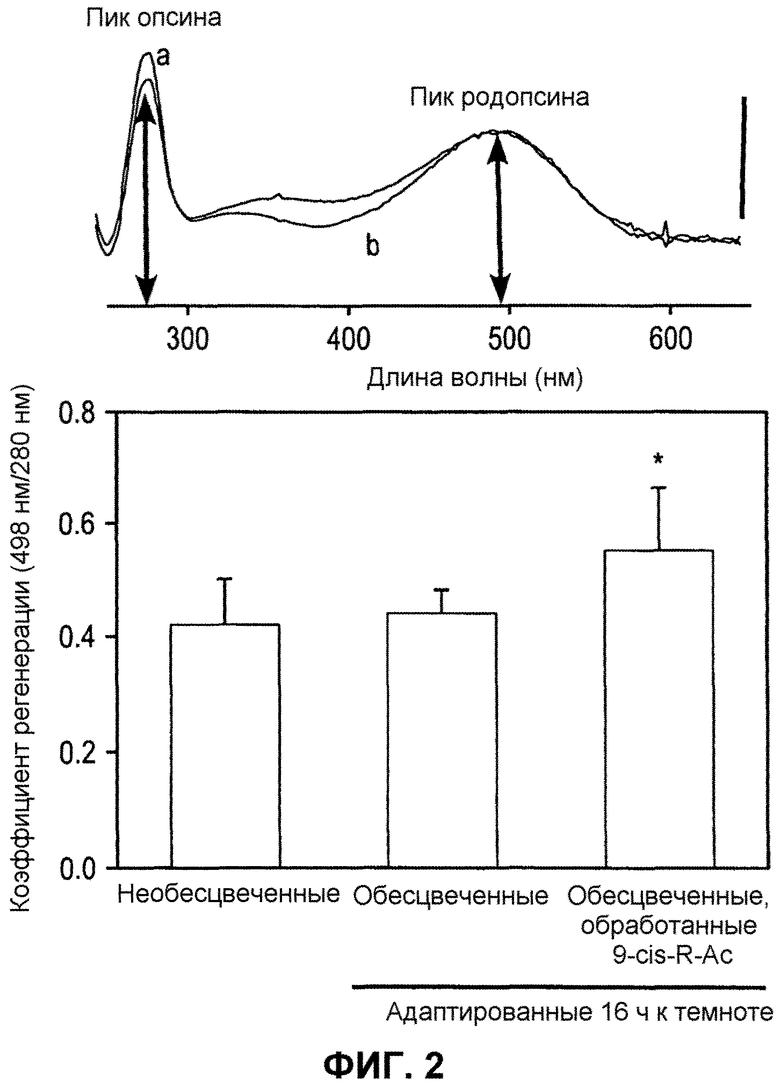
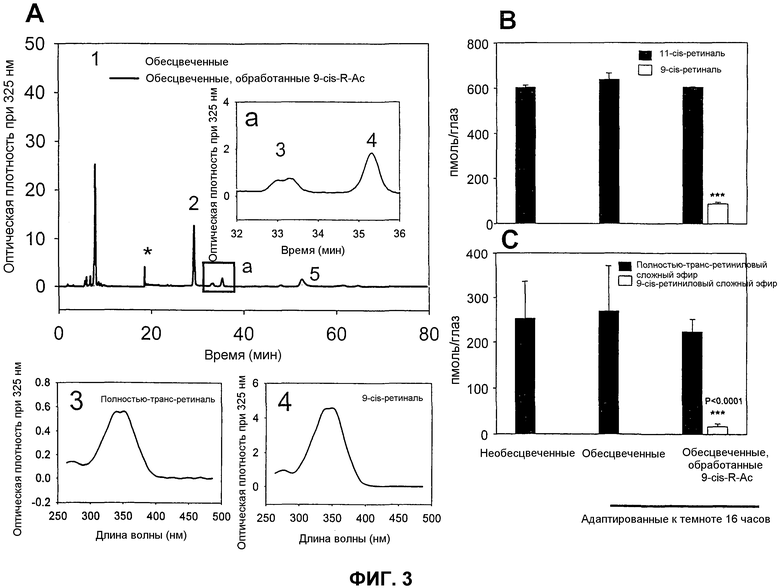
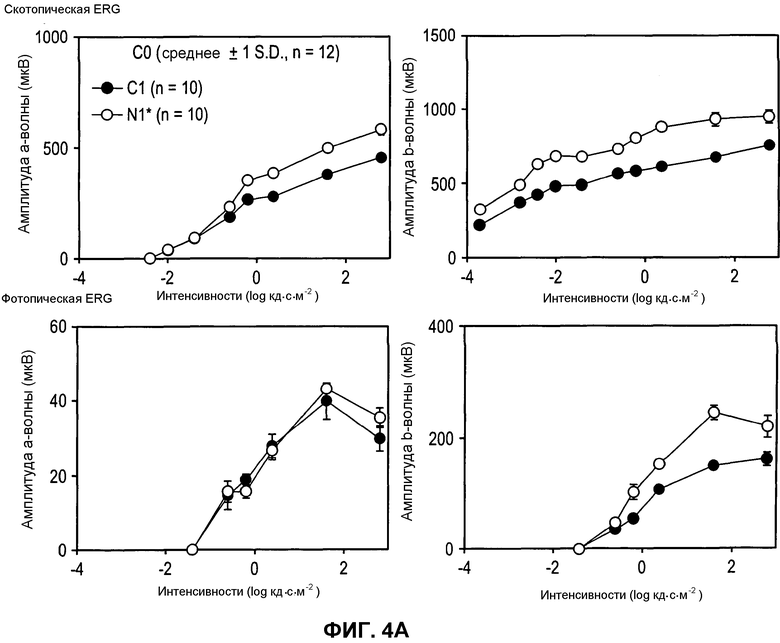
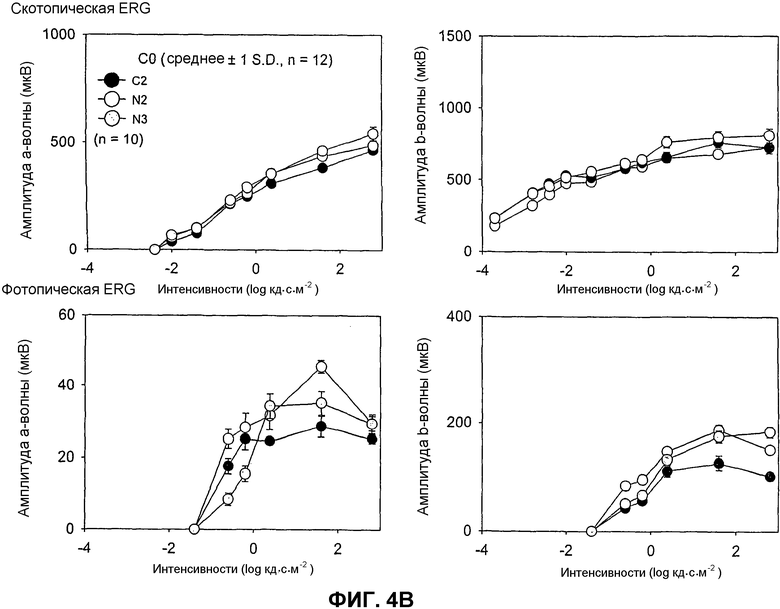
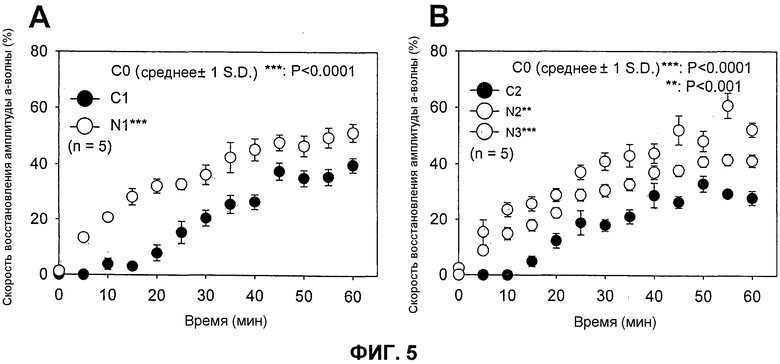
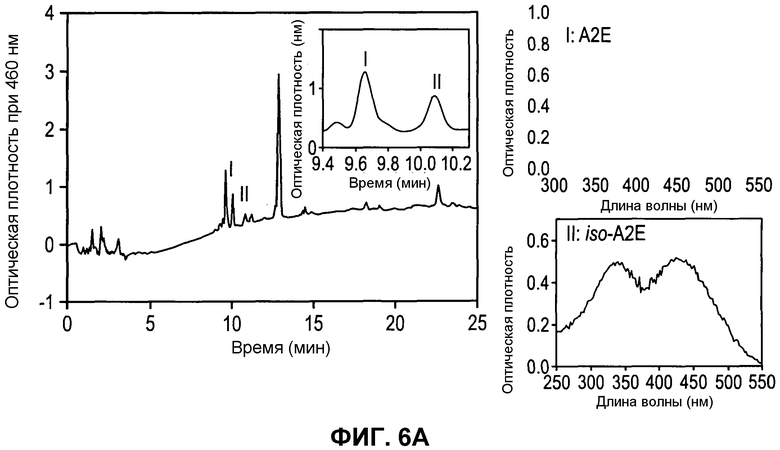
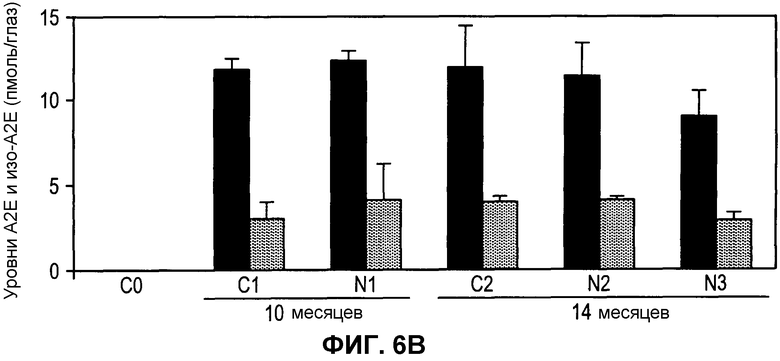
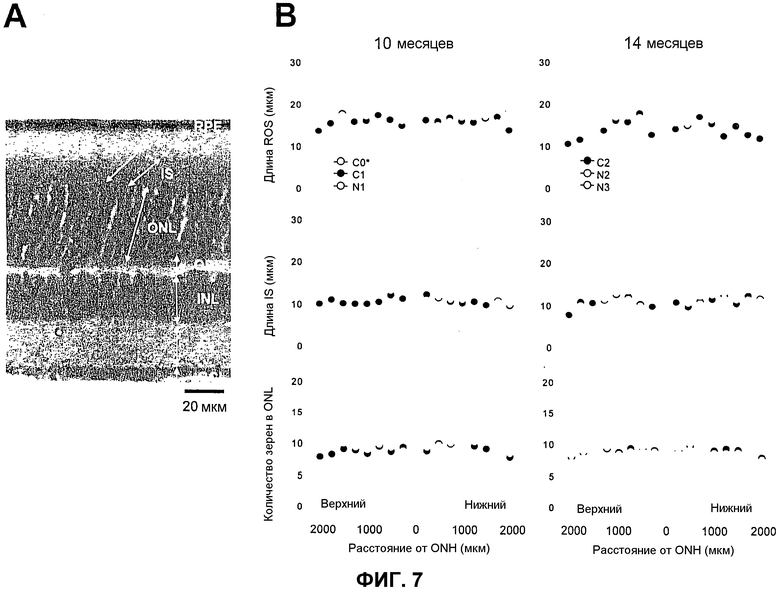
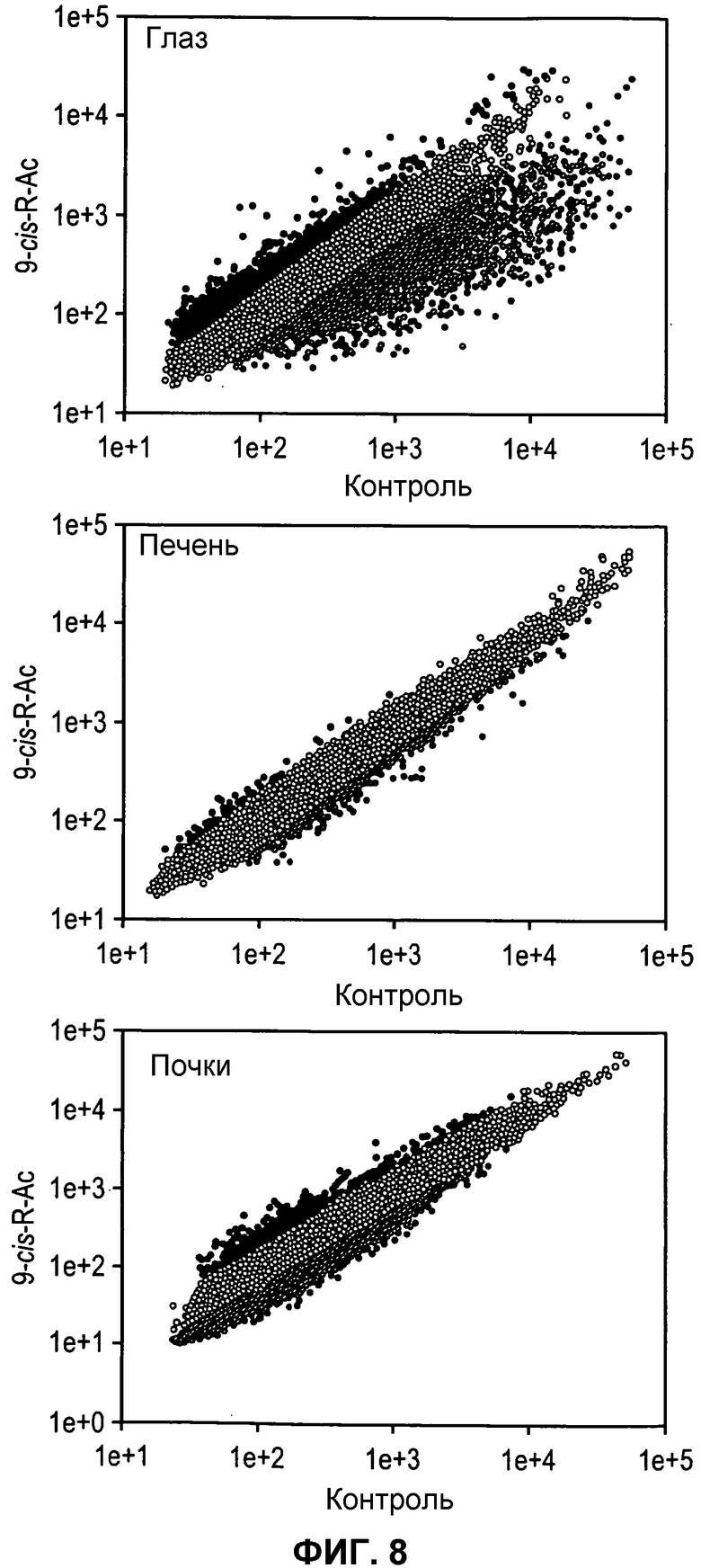
Изобретение относится к способам лечения или предупреждения обусловленной возрастом дисфункции сетчатки, возрастного ухудшения опосредуемой палочками сетчатки темновой адаптации после воздействия света, а также способу улучшения коэффициента регенерации родопсина. Указанные способы предполагают введение субъекту фармацевтически эффективного количества синтетического производного 11-cis-ретиналя или 9-cis-ретиналя периодически в течение по меньшей мере четырех месяцев. Изобретение обеспечивает значительное улучшение обусловленного старением разрушения фоторецептарной функции. 3 н. и 59 з.п. ф-лы, 1 табл., 9 пр., 8 ил.
1. Способ лечения или предупреждения обусловленной возрастом дисфункции сетчатки у субъекта, включающий введение указанному субъекту фармацевтически эффективного количества синтетического производного ретиналя, где указанное синтетическое производное ретиналя вводят указанному субъекту периодически в течение по меньшей мере четырех месяцев,
где указанное синтетическое производное ретиналя представляет собой 11-cis-ретиналь или 9-cis-ретиналь, имеющий структуру, представленную формулой I или формулой II;
формула I:
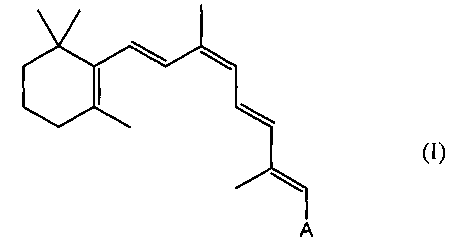
где А представляет собой CH2OR или А представляет собой CH(OH)OR и R выбирают из:
(i) альдегидной группы с прямой или разветвленной цепью, содержащей 1-24 атома(ов) углерода, для образования сложного эфира ретиналя;
(ii) образующей сложный эфир части C1-С10 монокарбоновой кислоты или С2-С22 поликарбоновой кислоты;
(iii) алкильной группы с прямой или разветвленной цепью, содержащей 1-24 атома(ов) углерода, для образования простого ретинилалканового эфира;
(iv) спиртовой группы с линейной цепью, изо-, втор-, трет- или другой разветвленной цепью, содержащей 1-6, 8-14 или 16-24 атома(ов) углерода, для образования простого ретинилового эфира спирта; и
(v) группы карбоновой кислоты с линейной цепью, изо-, втор-, трет- или другой разветвленной цепью, содержащей 1-6, 8-14 или 16-24 атома(ов) углерода, для образования простого ретинилового эфира карбоновой кислоты; или
где А представляет собой CH(ORa)ORb и каждый Ra и Rb независимо выбирают из группы, указанной выше для R; или
где А представляет собой CH=NOR, для образования оксима ретинила, и R выбирают из группы, указанной выше для R;
формула II:
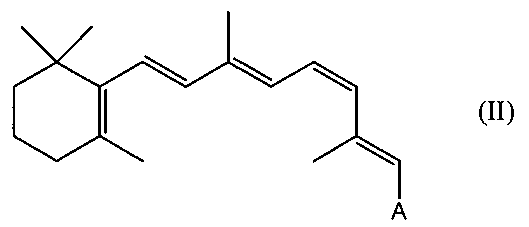
где А выбирают из группы, указанной выше для формулы I.
2. Способ по п. 1, где синтетическое производное ретиналя вводят указанному субъекту периодически один раз в месяц.
3. Способ по п. 1, где указанное синтетическое производное ретиналя вводят указанному субъекту в течение по меньшей мере шести месяцев.
4. Способ по п. 1, где указанное производное ретиналя вводят указанному субъекту один раз в месяц в течение по меньшей мере десяти месяцев.
5. Способ по п. 1, где указанная обусловленная возрастом дисфункция сетчатки проявляется одним или несколькими из следующих клинических состояний: ухудшение опосредуемой палочками сетчатки темновой адаптации после воздействия света, ухудшение ночного видения и ухудшение контрастной зрительной чувствительности.
6. Способ по п. 1, где указанная обусловленная возрастом дисфункция сетчатки представляет собой возрастную дегенерацию желтого пятна (AMD).
7. Способ по п. 1, где указанным субъектом является человек.
8. Способ по п. 1, где указанное синтетическое производное ретиналя вводят перорально.
9. Способ по п. 8, где указанное синтетическое производное ретиналя приготовлено в виде таблетки, пилюли, пакетика с порошком или капсулы.
10. Способ по п. 9, где указанная капсула представляет собой капсулу из твердого или мягкого желатина.
11. Способ по п. 8, где указанное синтетическое производное ретиналя вводят в дозе от 0,01 до 10 мг/кг массы тела.
12. Способ по п. 8, где указанное синтетическое производное ретиналя вводят в дозе от 0,1 до 1000 мг.
13. Способ по п. 8, где указанное синтетическое производное ретиналя вводят в дозе от 1,0 до 300 мг.
14. Способ по п. 1, где указанное синтетическое производное ретиналя вводят локально в глаз субъекта.
15. Способ по п. 14, где указанное синтетическое производное ретиналя вводят с использованием глазных капель, внутриглазного инъекционного раствора или периорбитального инъекционного раствора.
16. Способ по п. 15, где указанное синтетическое производное ретиналя вводят в дозе от 0,0001 до 500 мг.
17. Способ по п. 1, где доза указанного синтетического производного ретиналя на одно введение является большей, чем эффективная суточная доза.
18. Способ по любому из пп. 1-17, где возраст субъекта составляет по меньшей мере 45, по меньшей мере 50, по меньшей мере 60 или по меньшей мере 65 лет.
19. Способ улучшения коэффициента регенерации родопсина у субъекта с обусловленной возрастом дисфункцией сетчатки, включающий введение указанному субъекту фармацевтически эффективного количества синтетического производного ретиналя, где указанное синтетическое производное ретиналя вводят указанному субъекту периодически в течение по меньшей мере четырех месяцев, где указанное синтетическое производное ретиналя представляет собой 11-cis-ретиналь или 9-cis-ретиналь, имеющий структуру, представленную формулой I или формулой II;
формула I:
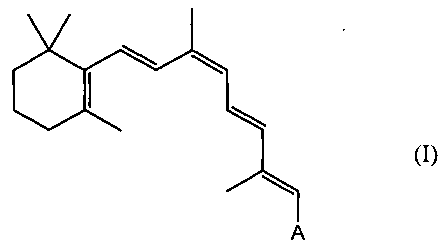
где А представляет собой CH2OR или А представляет собой CH(OH)OR и R выбирают из:
(i) альдегидной группы с прямой или разветвленной цепью, содержащей 1-24 атома(ов) углерода, для образования сложного эфира ретиналя;
(ii) образующей сложный эфир части C1-С10 монокарбоновой кислоты или С2-С22 поликарбоновой кислоты;
(iii) алкильной группы с прямой или разветвленной цепью, содержащей 1-24 атома(ов) углерода, для образования простого ретинилалканового эфира;
(iv) спиртовой группы с линейной цепью, изо-, втор-, трет- или другой разветвленной цепью, содержащей 1-6, 8-14 или 16-24 атома(ов) углерода, для образования простого ретинилового эфира спирта; и
(v) группы карбоновой кислоты с линейной цепью, изо-, втор-, трет- или другой разветвленной цепью, содержащей 1-6, 8-14 или 16-24 атома(ов) углерода, для образования простого ретинилового эфира карбоновой кислоты; или
где А представляет собой CH(ORa)ORb и каждый Ra и Rb независимо выбирают из группы, указанной выше для R; или
где А представляет собой CH=NOR, для образования оксима ретинила, и R выбирают из группы, указанной выше для R;
формула II:
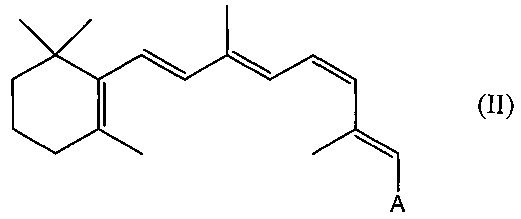
где А выбирают из группы, указанной выше для формулы I.
20. Способ по п. 19, где синтетическое производное ретиналя вводят указанному субъекту периодически один раз в месяц.
21. Способ по п. 19, где указанное синтетическое производное ретиналя вводят указанному субъекту в течение по меньшей мере шести месяцев.
22. Способ по п. 19, где указанное синтетическое производное ретиналя вводят указанному субъекту в течение по меньшей мере 10 месяцев.
23. Способ по п. 19, где указанная обусловленная возрастом дисфункция сетчатки проявляется одним или несколькими из следующих клинических состоянии: ухудшение опосредуемой палочками сетчатки темновой адаптации после воздействия света, ухудшение ночного видения и ухудшение контрастной зрительной чувствительности.
24. Способ по п. 19, где указанная обусловленная возрастом дисфункция сетчатки представляет собой возрастную дегенерацию желтого пятна (AMD).
25. Способ по п. 19, где указанным субъектом является человек.
26. Способ по п. 19, где указанное синтетическое производное ретиналя вводят перорально.
27. Способ по п. 26, где указанное синтетическое производное ретиналя приготовлено в виде таблетки, пилюли, пакетика с порошком или капсулы.
28. Способ по п. 27, где указанная капсула представляет собой капсулу из твердого или мягкого желатина.
29. Способ по п. 26, где указанное синтетическое производное ретиналя вводят в дозе от 0,01 до 10 мг/кг массы тела.
30. Способ по п. 26, где указанное синтетическое производное ретиналя вводят в дозе от 0,1 до 1000 мг.
31. Способ по п. 26, где указанное синтетическое производное ретиналя вводят в дозе от 1,0 до 300 мг.
32. Способ по п. 19, где указанное синтетическое производное ретиналя вводят локально в глаз субъекта.
33. Способ по п. 26, где указанное синтетическое производное ретиналя вводят с использованием глазных капель, внутриглазного инъекционного раствора или периорбитального инъекционного раствора.
34. Способ по п. 33, где указанное синтетическое производное ретиналя вводят в дозе от 0,0001 мг до 500 мг.
35. Способ по п. 19, где доза указанного синтетического производного ретиналя на одно введение является большей, чем эффективная суточная доза.
36. Способ по п. 1, где синтетическое производное ретиналя выбирают из группы, состоящей из 9-cis-ретинилацетата, 9-cis-ретинилсукцината, 9-cis-ретинилцитрата, 9-cis-ретинилкетоглутарата, 9-cis-ретинилфумарата, 9-cis-ретинилмалата и 9-cis-ретинилоксалоацетата.
37. Способ по п. 36, где синтетическое производное ретиналя представляет собой 9-cis-ретинилацетат.
38. Способ по п. 1, где синтетическое производное ретиналя выбирают из группы, состоящей из 11-cis-ретинилацетата, 11-cis-ретинилсукцината, 11-cis-ретинилцитрата, 11-cis-ретинилкетоглутарата, 11-cis-ретинилфумарата, 11-cis-ретинилмалата и 11-cis-ретинилоксалоацетата.
39. Способ по п. 38, где синтетическое производное ретиналя представляет собой 11-cis-ретинилацетат.
40. Способ по п. 19, где синтетическое производное ретиналя выбирают из группы, состоящей из 9-cis-ретинилацетата, 9-cis-ретинилсукцината, 9-cis-ретинилцитрата, 9-cis-ретинилкетоглутарата, 9-cis-ретинилфумарата, 9-cis-ретинилмалата и 9-cis-ретинилоксалоацетата.
41. Способ по п. 40, где синтетическое производное ретиналя представляет собой 9-cis-ретинилацетат.
42. Способ по п. 19, где синтетическое производное ретиналя выбирают из группы, состоящей из 11-cis-ретинилацетата, 11-cis-ретинилсукцината, 11-cis-ретинилцитрата, 11-cis-ретинилкетоглутарата, 11-cis-ретинилфумарата, 11-cis-ретинилмалата и 11-cis-ретинилоксалоацетата.
43. Способ по п. 42, где синтетическое производное ретиналя представляет собой 11-cis-ретинилацетат.
44. Способ лечения или предупреждения возрастного ухудшения опосредуемой палочками сетчатки темновой адаптации после воздействия света, где способ включает введение указанному субъекту фармацевтически эффективного количества синтетического производного ретиналя, где указанное синтетическое производное ретиналя вводят указанному субъекту периодически в течение по меньшей мере четырех месяцев, где указанное синтетическое производное ретиналя представляет собой 11-cis-ретиналь или 9-cis-ретиналь, имеющий структуру, представленную формулой I или формулой II; формула I:
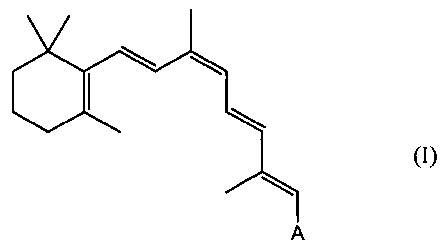
где А представляет собой CH2OR или А представляет собой CH(OH)OR и R выбирают из:
(i) альдегидной группы с прямой или разветвленной цепью, содержащей 1-24 атома(ов) углерода, для образования сложного эфира ретиналя;
(ii) образующей сложный эфир части C1-С10 монокарбоновой кислоты или С2-С22 поликарбоновой кислоты;
(iii) алкильной группы с прямой или разветвленной цепью, содержащей 1-24 атома(ов) углерода, для образования простого ретинилалканового эфира;
(iv) спиртовой группы с линейной цепью, изо-, втор-, трет- или другой разветвленной цепью, содержащей 1-6, 8-14 или 16-24 атома(ов) углерода, для образования простого ретинилового эфира спирта; и
(v) группы карбоновой кислоты с линейной цепью, изо-, втор-, трет- или другой разветвленной цепью, содержащей 1-6, 8-14 или 16-24 атома(ов) углерода, для образования простого ретинилового эфира карбоновой кислоты; или
где А представляет собой CH(ORa)ORb и каждый Ra и Rb независимо выбирают из группы, указанной выше для R; или
где А представляет собой CH=NOR, для образования оксима ретинила, и R выбирают из группы, указанной выше для R;
формула II:
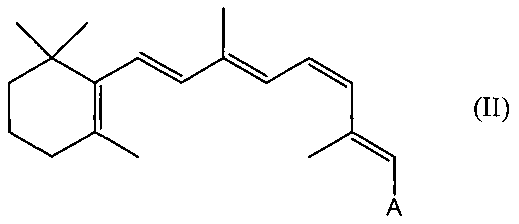
где А выбирают из группы, указанной выше для формулы I.
45. Способ по п. 44, где синтетическое производное ретиналя вводят указанному субъекту периодически один раз в месяц.
46. Способ по п. 44, где указанное синтетическое производное ретиналя вводят указанному субъекту в течение по меньшей мере шести месяцев.
47. Способ по п. 44, где указанное производное ретиналя вводят указанному субъекту один раз в месяц в течение по меньшей мере десяти месяцев.
48. Способ по п. 44, где указанным субъектом является человек.
49. Способ по п. 44, где указанное синтетическое производное ретиналя вводят перорально.
50. Способ по п. 49, где указанное синтетическое производное ретиналя приготовлено в виде таблетки, пилюли, пакетика с порошком или капсулы.
51. Способ по п. 50, где указанная капсула представляет собой капсулу из твердого или мягкого желатина.
52. Способ по п. 49, где указанное синтетическое производное ретиналя вводят в дозе от 0,01 до 10 мг/кг массы тела.
53. Способ по п. 49, где указанное синтетическое производное ретиналя вводят в дозе от 0,1 до 1000 мг.
54. Способ по п. 49, где указанное синтетическое производное ретиналя вводят в дозе от 1,0 до 300 мг.
55. Способ по п. 44, где указанное синтетическое производное ретиналя вводят локально в глаз субъекта.
56. Способ по п. 55, где указанное синтетическое производное ретиналя вводят с использованием глазных капель, внутриглазного инъекционного раствора или периорбитального инъекционного раствора.
57. Способ по п. 56, где указанное синтетическое производное ретиналя вводят в дозе от 0,0001 мг до 500 мг.
58. Способ по п. 44, где доза указанного синтетического производного ретиналя на одно введение является большей, чем эффективная суточная доза.
59. Способ по п. 44, где синтетическое производное ретиналя выбирают из группы, состоящей из 9-cis-ретинилацетата, 9-cis-ретинилсукцината, 9-cis-ретинилцитрата, 9-cis-ретинилкетоглутарата, 9-cis-ретинилфумарата, 9-cis-ретинилмалата и 9-cis-ретинилоксалоацетата.
60. Способ по п. 59, где синтетическое производное ретиналя представляет собой 9-cis-ретинилацетат.
61. Способ по п. 44, где синтетическое производное ретиналя выбирают из группы, состоящей из 11-cis-ретинилацетата, 11-cis-ретинилсукцината, 11-cis-ретинилцитрата, 11-cis-ретинилкетоглутарата, 11-cis-ретинилфумарата, 11-cis-ретинилмалата и 11-cis-ретинилоксалоацетата.
62. Способ по п. 61, где синтетическое производное ретиналя представляет собой 11-cis-ретинилацетат.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| PRESTON VAN HOOSER "Rapid restoration of visual pigment and function with oral retinoid in a mouse model of childhood blindness", PNAS, 2000, v.97, стр.8623 " 8628 | |||
Авторы
Даты
2015-10-20—Публикация
2009-02-10—Подача