Настоящая заявка испрашивает приоритет по предварительной заявке на патент США № 62/585237, поданной 13 ноября 2017 года, предварительной заявке на патент США № 62/589476, поданной 21 ноября 2017 года, и предварительной заявке на патент США № 62/641783, поданной 12 марта 2018 года, каждая из данных заявок включена в настоящий документ посредством ссылки во всей своей полноте.
Заявление об исследовании, финансируемом из федерального бюджета
Настоящее изобретение было выполнено при государственной поддержке в соответствии с EY018241, присужденным Национальными институтами здравоохранения. Правительство имеет определенные права на настоящее изобретение.
Введение
Наследственные и связанные с возрастом дегенеративные заболевания сетчатки вызывают прогрессирующую потерю фоторецепторов палочек и колбочек, что приводит к полной слепоте. Несмотря на потерю чувствительных к свету клеток, необходимых для зрения, нижестоящие нейроны внутренней сетчатки выживают в функциональном состоянии, обеспечивая цель для оптогенетической терапии. На сегодняшний день, оптогенетические подходы столкнулись с определенными ограничениями, включая: а) очень низкую светочувствительность бактериальных опсинов и химически сконструированных рецепторов млекопитающих; b) очень медленную кинетику в опсинах сетчатки; и c) отсутствие механизмов адаптации, обеспечивающих естественное зрение с высокой чувствительностью в очень широком диапазоне уровней окружающего освещения.
В данной области техники существует потребность в улучшенных подходах оптогенетики к лечению нарушений зрения.
Сущность изобретения
В настоящем изобретении предложен способ восстановления или улучшения зрительной функции у индивидуума, причем способ включает введение индивидууму нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую один или более средневолновых конопсинов (MW-опсин), длинноволновых конопсинов (LW-опсин) и коротковолновых конопсинов (SW-опсин). Один или более из MW-опсина, LW-опсина и SW-опсина экспрессируется в клетке сетчатки у индивидуума, тем самым восстанавливая или улучшая зрительную функцию.
Краткое описание графических материалов
На фиг. 1А-1С продемонстрировано, что активация светом MW-опсина или родопсина активирует каналы GIRK для получения внутреннего фототока при отрицательных исходных потенциалах в высоком уровне внешнего калия.
На фиг. 2A-2G продемонстрирована экспрессия белка и световые отклики в сетчатке, выделенной от мышей rd1, чьи палочки и колбочки дегенерировали. Продемонстрирована экспрессия MW-опсина в клетках сетчатки (фиг. 2A-2D), и продемонстрированы вызванные светом отклики, которые опосредованы MW-опсином (фиг. 2E-2G).
На фиг. 3A-3G изображено время светового отклика, размер и высокая чувствительность MW-опсина или родопсина в клетках сетчатки, выделенных от слепых мышей rd1.
На фиг. 4A-4I продемонстрированы поведенческие тесты, демонстрирующие одинаковую способность отличать свет от темноты, опосредованной MW-опсином и родопсином, в клетках сетчатки мышей rd1 (фиг. 4A-4C), но только MW-опсин позволяет животным различать мигающий и постоянный свет (фиг. 4D-4E), или различные световые пространственные паттерны (фиг. 4F-4G). MW-опсин также поддерживает дифференциацию линий на уровне массы между параллельными линиями с разным интервалом, которые отображаются как неподвижные изображения или в движении (фиг. 4H-4I).
На фиг. 5A-5F изображена опосредованная MW-опсином адаптация к свету у мышей rd1: в записях MEA на выделенной сетчатке (фиг. 5A-5C) и зрительно-опосредованное поведение (фиг. 5D-5F).
На фиг. 6 изображены поведенческие тесты, демонстрирующие восстановление способности различать параллельные линии на расстоянии 1 vs 6 см посредством MW-опсина, LW-опсина и SW-опсина.
На фиг. 7 изображен пороговый отклик оптогенетических систем в слепых сетчатках по сравнению с нормальным зрением.
На фиг. 8А-8Е изображены зависимые от интенсивности кинетические отклики, опосредованные MW-опсином.
На фиг. 9A-9G изображено поведение избегания света и наученного поведения распознавания паттернов.
На фиг. 10A-10G изображена адаптация к свету у мышей с удаленной сетчаткой и поведенческих мышей.
На фиг. 11 представлена таблица 1, в которой показана статистическая значимость избегания света и наученного зрительно-опосредованного поведения.
На фиг. 12A-12B изображено выравнивание аминокислотных последовательностей SW-опсина человека (SEQ ID NO: 5) и SW-опсина мыши (SEQ ID NO: 6), а также приведен пример аминокислотной последовательности химерного SW-опсина человека/мыши (SEQ ID NO: 7). Трансмембранные (TM) домены SW-опсина человека и химерный SW-опсин человека/мыши подчеркнуты; внутриклеточные домены SW-опсина мыши и химерного SW-опсина человека/мыши подчеркнуты дважды.
На фиг. 13A-13L изображено восстановление зрительно-опосредованного поведения с помощью MW-опсина.
На фиг. 14А-14В изображена экспрессия MW-опсина в сетчатке мыши rd1.
На фиг. 15А-15В изображена экспрессия родопсина в сетчатке мыши rd1.
На фиг. 16A-16D изображена эффективность трансдукции MW-опсина в сетчатке rd1.
На фиг. 17A-17D изображена характеристика медленного компонента светового отклика в сетчатке rd1, экспрессирующей MW-опсин.
На фиг. 18A-18C изображено обнаружение контраста в выделенной сетчатке мыши, экспрессирующей MW-опсин мыши rd1.
На фиг. 19А-19Е изображен световой отклик in vivo в V1 мыши rd1, экспрессирующей MW-опсин.
На фиг. 20А-20В изображено обнаружение контраста in vivo у мышей rd1, экспрессирующих MW-опсин.
На фиг. 21A-21C изображены временные свойства откликов V1 in vivo у мышей rd1, экспрессирующих MW-опсин.
На фиг. 22A-22B изображены предпочтения местоположения в заданиях на различение.
Определения
Термин «клетка сетчатки» может относиться в данном документе к любому из типов клеток, которые составляют сетчатку, таким как ганглиозные клетки сетчатки; амакринные клетки; горизонтальные клетки; биполярные клетки; и фоторецепторные клетки, включая палочки и колбочки.
«Функционально связанный» относится к сопоставлению генетических элементов, при этом элементы находятся во взаимосвязи, позволяющей им функционировать ожидаемым образом. Например, промотор функционально связан с кодирующей областью, если промотор способствует инициировать транскрипцию кодирующей последовательности. Между промотором и кодирующей областью могут присутствовать промежуточные остатки при условии сохранения этой функциональной взаимосвязи.
«Вектор экспрессии» представляет собой вектор, содержащий область, которая кодирует представляющий интерес полипептид, и используется для осуществления экспрессии белка в предполагаемой клетке-мишени. Вектор экспрессии также содержит контрольные элементы, функционально связанные с кодирующей областью для облегчения экспрессии белка в мишени. Комбинация контрольных элементов и гена, или генов, с которыми они функционально связаны для экспрессии, иногда упоминается как «экспрессионная кассета», большое количество которых известно и доступно в данной области техники, или может быть легко сконструировано из компонентов, доступных в данной области техники.
Термины «лечение», «процесс лечения» и тому подобное, в контексте данного документа, относится к получению желаемого фармакологического и/или физиологического эффекта. Эффект может быть профилактическим с точки зрения полного или частичного предотвращения заболевания или его симптома, и/или может быть терапевтическим с точки зрения частичного или полного излечения от заболевания и/или неблагоприятного воздействия, связанного с заболеванием. «Лечение», в контексте данного документа, охватывает любое лечение заболевания у млекопитающего, в частности у человека, и включает: (a) предотвращение возникновения заболевания у субъекта, который может быть предрасположен к заболеванию или подвержен риску приобретения заболевания, но еще не был диагностирован как имеющий заболевание; (b) подавление заболевания, то есть прекращение его развития; (c) облегчение заболевания, то есть вызывание регрессии заболевания; и (d) восполнение утраченной функции в результате заболевания.
Термины «индивидуум», «хозяин», «субъект» и «пациент» используются в данном документе взаимозаменяемо и относятся к млекопитающему, включая, но не ограничиваясь этим, человека и приматов, включая обезьян и людей; спортивные животные (например, лошади, верблюды и т.д.); сельскохозяйственные животные (например, овцы, козы, коровы и т.д.); домашние животные (собаки, кошки и т.д.); и грызуны (например, мыши, крысы и т.д.). В некоторых случаях индивидуум представляет собой человека.
Прежде чем настоящее изобретение будет дополнительно описано, следует понимать, что настоящее изобретение не ограничено конкретными описанными вариантами осуществления, поскольку они, как таковые, могут изменяться. Также следует понимать, что используемая в настоящем документе терминология предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения, поскольку объем настоящего изобретения будет ограничен только прилагаемой формулой изобретения.
Когда предоставляется диапазон значений, подразумевается, что каждое промежуточное значение, с точностью до десятой доли нижнего предела, если контекст явно не предписывает иное, между верхним и нижним пределом этого диапазона и любым другим указанным или промежуточным значением в указанном диапазоне, находится в пределах настоящего изобретения. Верхний и нижний пределы этих меньших диапазонов могут быть независимо включены в меньшие диапазоны и также охватываться настоящим изобретением, с учетом любого специально исключенного предела в указанном диапазоне. Если указанный диапазон включает одно или оба из пределов, диапазоны, исключающие один или оба из этих включенных пределов, также включаются в настоящее изобретение.
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимают специалисты в области техники, к которой относится настоящее изобретение. Хотя любые способы и материалы, подобные или эквивалентные тем, которые описаны в данном документе, также могут быть использованы при практическом применении или испытании настоящего изобретения, предпочтительные способы и материалы описываются далее. Все публикации, упомянутые в данном документе, включены в него посредством ссылки для раскрытия и описания способов и/или материалов, в связи с которыми цитируются публикации.
Следует отметить, что используемые в настоящем документе и в прилагаемой формуле изобретения формы единственного числа, также предполагают включение множественного числа, если контекст явно не предписывает иное. Таким образом, например, ссылка на «полипептид MW-опсин» включает множество таких полипептидов, а ссылка на «относящийся к сетчатке глаза» включает ссылку на одну или более клеток сетчатки и их эквиваленты, известные специалистам в данной области техники, и так далее. Кроме того, следует отметить, что формула изобретения может быть составлена таким образом, чтобы исключить любой необязательный признак. Как таковое, это утверждение предназначено для того, чтобы служить предшествующей основой для использования такой исключительной терминологии, как «только» и т.п., в связи с перечислением признаков формулы изобретения или использованием «отрицательного» ограничения.
Следует принимать во внимание, что определенные признаки изобретения, которые для ясности описаны в контексте отдельных вариантов осуществления, также могут быть предоставлены в качестве комбинации в одном варианте осуществления. И наоборот, различные признаки настоящего изобретения, которые для краткости описаны в контексте одного варианта осуществления, также могут быть предусмотрены отдельно или в любой подходящей комбинации. Все комбинации вариантов осуществления, принадлежащие настоящему изобретению, конкретно охватываются настоящим изобретением и раскрываются в данном документе так же, как если бы каждая комбинация была раскрыта индивидуально и в явном виде. Кроме того, все промежуточные комбинации различных вариантов осуществления и их элементов также конкретно охвачены настоящим изобретением и раскрыты в данном документе так же, как если бы каждое такое сочетание было индивидуально и явно раскрыто в данном документе.
Публикации, обсуждаемые в настоящем документе, предназначены исключительно для их раскрытия до даты подачи настоящей заявки. Ничто из содержащегося в настоящем документе не должно быть истолковано как признание того, что настоящее изобретение не имеет права предшествовать такой публикации в силу предшествующего изобретения. Кроме того, указанные даты публикации могут отличаться от фактических дат публикации, которые, возможно, потребуется подтвердить независимо.
Подробное описание сущности изобретения
В настоящем изобретении предложен способ восстановления или улучшения зрительной функции у индивидуума, причем способ включает введение индивидууму нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую один или более средневолновых конопсинов (MW-опсин), длинноволновых конопсинов (LW-опсин) и коротковолновых конопсинов (SW-опсин). Один или более из MW-опсина, LW-опсина и SW-опсина экспрессируется в клетке сетчатки у индивидуума, тем самым восстанавливая или улучшая зрительную функцию.
Полипептид MW-опсин может содержать аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% следующей аминокислотной последовательности MW-опсина человека:
maqqwslqrl agrhpqdsye dstqssifty tnsnstrgpf egpnyhiapr wvyhltsvwm ifvviasvft nglvlaatmk fkklrhplnw ilvnlavadl aetviastis vvnqvygyfv lghpmcvleg ytvslcgitg lwslaiiswe rwmvvckpfg nvrfdaklai vgiafswiwa avwtappifg wsrywphglk tscgpdvfsg ssypgvqsym ivlmvtccit plsiivlcyl qvwlairava kqqkesestq kaekevtrmv vvmvlafcfc wgpyaffacf aaanpgypfh plmaalpaff aksatiynpv iyvfmnrqfr ncilqlfgkk vddgselssa sktevssvss vspa (SEQ ID NO:1).
Полипептид MW-опсин может содержать аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% следующей аминокислотной последовательности MW-опсина мыши:
maqrltgeqt ldhyedstha siftytnsns tkgpfegpny hiaprwvyhl tstwmilvvv asvftnglvl aatmrfkklr hplnwilvnl avadlaetii astisvvnqi ygyfvlghpl cviegyivsl cgitglwsla iiswerwlvv ckpfgnvrfd aklatvgivf swvwaaiwta ppifgwsryw pyglktscgp dvfsgtsypg vqsymmvlmv tccifplsii vlcylqvwla iravakqqke sestqkaeke vtrmvvvmvf ayclcwgpyt ffacfatahp gyafhplvas lpsyfaksat iynpiiyvfm nrqfrncilh lfgkkvddss elsstsktev ssvssvspa (SEQ ID NO:8)
Полипептид родопсин может содержать аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или 100% следующей аминокислотной последовательности родопсина:
mngtegpnfy vpfsnatgvv rspfeypqyy laepwqfsml aaymfllivl gfpinfltly vtvqhkklrt plnyillnla vadlfmvlgg ftstlytslh gyfvfgptgc nlegffatlg geialwslvv laieryvvvc kpmsnfrfge nhaimgvaft wvmalacaap plagwsryip eglqcscgid yytlkpevnn esfviymfvv hftipmiiif fcygqlvftv keaaaqqqes attqkaekev trmviimvia flicwvpyas vafyifthqg snfgpifmti paffaksaai ynpviyimmn kqfrncmltt iccgknplgd deasatvskt etsqvapa (SEQ ID NO:2).
Полипептид канальный родопсин может содержать аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% следующей аминокислотной последовательности канального родопсина:
MDYGGALSAVGRELLFVTNPVVVNGSVLVPEDQCYCAGWIESRGTNGAQTASNVLQ WLAAGFSILLLMFYAYQTWKSTCGWEEIYVCAIEMVKVILEFFFEFKNPSMLYLATGHRVQW LRYAEWLLTCPVILIHLSNLTGLSNDYSRRTMGLLVSDIGTIVWGATSAMATGYVKVIFFCLG LCYGANTFFHAAKAYIEGYHTVPKGRCRQVVTGMAWLFFVSWGMFPILFILGPEGFGVLSVY GSTVGHTIIDLMSKNCWGLLGHYLRVLIHEHILIHGDIRKTTKLNIGGTEIEVETLVEDEAEAG AVP (SEQ ID NO:3).
LW-опсин может содержать аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% следующей аминокислотной последовательности LW-опсина человека:
maqqwslqrl agrhpqdsye dstqssifty tnsnstrgpf egpnyhiapr wvyhltsvwm ifvvtasvft nglvlaatmk fkklrhplnw ilvnlavadl aetviastis ivnqvsgyfv lghpmcvleg ytvslcgitg lwslaiiswe rwmvvckpfg nvrfdaklai vgiafswiwa avwtappifg wsrywphglk tscgpdvfsg ssypgvqsym ivlmvtccii plaiimlcyl qvwlairava kqqkesestq kaekevtrmv vvmifaycvc wgpytffacf aaanpgyafh plmaalpayf aksatiynpv iyvfmnrqfr ncilqlfgkk vddgselssa sktevssvss vspa (SEQ ID NO:4).
LW-опсин может содержать аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% следующей аминокислотной последовательности LW-опсина мыши:
mngtegpnfy vpfsnvtgvv rspfeqpqyy laepwqfsml aaymfllivl gfpinfltly vtvqhkklrt plnyillnla vadlfmvfgg ftttlytslh gyfvfgptgc nlegffatlg geialwslvv laieryvvvc kpmsnfrfge nhaimgvvft wimalacaap plvgwsryip egmqcscgid yytlkpevnn esfviymfvv hftipmivif fcygqlvftv keaaaqqqes attqkaekev trmviimvif flicwlpyas vafyifthqg snfgpifmtl paffaksssi ynpviyimln kqfrncmltt lccgknplgd ddasataskt etsqvapa (SEQ ID NO:9).
Полипептид SW-опсин может содержать аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или 100% следующей аминокислотной последовательности SW-опсина человека:
mrkmseeefy lfknissvgp wdgpqyhiap vwafylqaaf mgtvfligfp lnamvlvatl rykklrqpln yilvnvsfgg fllcifsvfp vfvascngyf vfgrhvcale gflgtvaglv tgwslaflaf eryivickpf gnfrfsskha ltvvlatwti gigvsippff gwsrfipegl qcscgpdwyt vgtkyrsesy twflfifcfi vplslicfsy tqllralkav aaqqqesatt qkaerevsrm vvvmvgsfcv cyvpyaafam ymvnnrnhgl dlrlvtipsf fsksaciynp iiycfmnkqf qacimkmvcg kamtdesdtc ssqktevstv sstqvgpn (SEQ ID NO:5).
В некоторых случаях SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или 100% аминокислотной последовательности SW-опсина человека (SEQ ID NO: 5), реагирующую на свет в видимом диапазоне и проявляющую возбуждающую активность.
Полипептид SW-опсин может содержать аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или 100% следующей аминокислотной последовательности SW-опсина мыши:
msgeddfylf qnissvgpwd gpqyhlapvw afrlqaafmg fvffvgtpln aivlvatlhy kklrqplnyi lvnvslggfl fcifsvftvf iaschgyflf grhvcaleaf lgsvaglvtg wslaflafer yvvickpfgs irfnskhalm vvlatwiigi gvsippffgw srfipeglqc scgpdwytvg tkyrseyytw flfifcfiip lslicfsysq llrtlravaa qqqesattqk aerevshmvv vmvgsfclcy vpyaalamym vnnrnhgldl rlvtipaffs ksscvynpii ycfmnkqfra cilemvcrkp madesdvsgs qktevstvss skvgph (SEQ ID NO:6). В некоторых случаях SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или 100% аминокислотной последовательности SW-опсина мыши (SEQ ID NO: 6), реагирующий на свет в ультрафиолетовом диапазоне и проявляющий ингибирующую активность.
В некоторых случаях как SW-опсин человека, так и SW-опсин мыши продуцируются в клетке сетчатки у индивидуума. В некоторых случаях как SW-опсин человека, так и SW-опсин мыши (но не LW-опсин или MW-опсин) продуцируются в клетке сетчатки у индивидуума. В некоторых случаях как SW-опсин человека, так и SW-опсин мыши, а также LW-опсин (но не MW-опсин) продуцируются в клетке сетчатки у индивидуума. В некоторых случаях как SW-опсин человека, так и SW-опсин мыши, а также MW-опсин (но не LW-опсин) продуцируются в клетке сетчатки у индивидуума. В некоторых случаях как SW-опсин человека, так и SW-опсин мыши, а также LW-опсин и MW-опсин продуцируются в клетке сетчатки у индивидуума. Например, в некоторых случаях первый рекомбинантный вектор экспрессии, содержащий нуклеотидную последовательность, кодирующую полипептид SW-опсин, содержащий аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности SW-опсина человека (SEQ ID NO: 5); и второй рекомбинантный вектор экспрессии, содержащий нуклеотидную последовательность, кодирующую полипептид SW-опсин, содержащий аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности SW-опсина мыши (SEQ ID NO: 6) вводят в клетку сетчатки.
В некоторых случаях и MW-опсин, и LW-опсин (но не SW-опсин) продуцируются в клетке сетчатки у индивидуума. В некоторых случаях и MW-опсин, и SW-опсин (но не LW-опсин) продуцируются в клетке сетчатки у индивидуума. В некоторых случаях MW-опсин, LW-опсин и SW-опсин экспрессируются в клетке сетчатки у индивидуума.
В некоторых случаях подходящим опсином является химерный опсин, например, опсин, который содержит аминокислотную последовательность (последовательности) от первого вида и аминокислотную последовательность (последовательности) от второго вида. Например, в некоторых случаях химерный опсин содержит внутриклеточные участки SW-опсина мыши и трансмембранные участки SW-опсина человека. Пример подходящего химерного SW-опсина показан на фиг.12A-12B.
В некоторых случаях подходящий химерный SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности химерного SW-опсина, изображенного на фиг. 12A-12B, причем химерный SW-опсин имеет следующую аминокислотную последовательность:
EDDFYLFQNISSVGPWDGPQYHLAPVWAFYLQAAFMGTVFLIGFPLNAMVLVATLHY KKLRQPLNYILVNVSFGGFLLCIFSVFPVFVASCNGYFVFGRHVCALEGFLGTVAGLVTGWSL AFLAFERYVVICKPFGSIRFNSKHALTVVLATWTIGIGVSIPPFFGWSRFIPEGLQCSCGPDWYT VGTKYRSESYTWFLFIFCFIVPLSLICFSYTQLLRALRAVAAQQQESATTQKAEREVSHMVVV MVGSFCVCYVPYAAFAMYMVNNRNHGLDLRLVTIPSFFSKSACIYNPIIYCFMNKQFRACILE MVCRKPMADESDVSGSQKTEVSTVSSSKVGPH (SEQ ID NO:7).
MW-опсин и/или LW-опсин, и/или SW-опсин может быть использован в комбинации с гетерологичным опсином, например, опсином, не принадлежащем млекопитающему, такому как опсин водорослей, опсин простейших или их вариант. Подходящие гетерологичные опсины включают деполяризующие опсины, например, каналородопсин ChR2 (Zhang et al. (2007) Nature 446:633; GenBank ABO64386.1), выделенный из Chlamydomonas reinhardtii; ступенчато-функциональный опсин (SFO) (Berndt et al. (2009) Nat. Neurosci. 12:229) или стабилизированный ступенчато-функциональный опсин (SSFO) (WO 2010/056970; Yizhar et al. (2011) Nature 477:171); катион-переносящий канальный опсин, выделенный из Volvox carteri (VChR1 - NCBI Gene ID: 9619570; U.S. Patent No. 9,249,200); химерный белок C1V1, производное белка VChR1 Volvox carteri и белок ChR1, выделенный из Chlamydomonas reinhardtii (U.S. Patent No. 9,175,095); химерный белок C1C2, производное белка ChR1 и белка ChR2, выделенных из Chlamydomonas reinhardtii (Lin et al. (2009) Biophys. J. 96:1803); сдвинутый в красную область деполяризующий светочувствительный полипептид, выделенный из Chlamydomonas reinhardtii, где такие светочувствительные полипептиды упоминаются как “ReaChR” (Lin et al. (2013) Nat. Neurosci. 16:1499); CnChR2 (Genbank Accession No.: AHH02139), выделенный из Chlamydomonas noctigama; химерный белок CsChrimson, выделенный из CsChR (Genbank Accession No.: AHH02144; Klapoetke et al. (2014) Nature Methods 11:338) белок Chloromonas subdivisa; ShChR1 (Genbank Accession No.: AHH02106), выделенный из Stigeoclonium helveticum; опсин “ChETA” Gunaydin et al. (2010 Nat. Neurosci. 13:387) белок “SwiChR” (WO 2015/148974); белок “bReaChes” (WO/2017/048808); и тому подобное. Другие подходящие деполяризующие опсины известны в данной области техники; см., например, Zhang et al. (2011) Cell 147:1446; Deisseroth (2015) Nature Neurosci. 18:1213; Berndt and Deisseroth (2015) Science 349:590; и тому подобное.
Экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает видение паттернов и распознавание изображения индивидуумом. Распознаваемое изображение может быть статическим изображением и/или движущимся изображением.
Экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает распознавание изображения при интенсивности света от около 10-4 Вт/см2 до около 10 Вт/см2. Например, в некоторых случаях экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает распознавание изображения при интенсивности света от около 10-2 Вт/см2 до около 10-4 Вт/см2, от около 10-4 Вт/см2 до около 1 Вт/см2, от около 10-4 Вт/см2 до около 10-1 Вт/см2 или от около 10-4 Вт/см2 до около 5×10-1 Вт/см2. В некоторых случаях экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает распознавание изображения при интенсивности света от около 10-4 Вт/см2 до около 10-3 Вт/см2, от около 10-3 Вт/см2 до около 10-2 Вт/см2, от около 10-2 Вт/см2 до около 10-1 Вт/см2 или от около 10-1 Вт/см2 до около 1 Вт/см2. В некоторых случаях экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает распознавание изображения при интенсивности света до 2 Вт/см2, до 3 Вт/см2, до 4 Вт/см2, до 5 Вт/см2 или до 10 Вт/см2. Экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает распознавание изображения при интенсивности света менее чем 5 Вт/см2, менее чем 4 Вт/см2, менее чем 3 Вт/см2 или менее чем 2 Вт/см2.
Экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает распознавание изображения индивидуумом при интенсивности света, которая по меньшей мере в 10 раз ниже, чем интенсивность света, необходимая для обеспечения распознавания изображения индивидуумом, экспрессирующим полипептид канальный родопсин (например, полипептид, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 3) в клетке сетчатки. Например, экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает распознавание изображения индивидуумом при интенсивности света, которая по меньшей мере в 10 ниже, по меньшей мере в 25 раз ниже, по меньшей мере в 50 раз ниже, по меньшей мере в 100 раз ниже, по меньшей мере в 150 раз ниже, по меньшей мере в 200 раз ниже, по меньшей мере в 300 раз ниже, по меньшей мере в 400 раз ниже или по меньшей мере в 500 раз ниже, чем интенсивность света, необходимая для обеспечения распознавания изображения индивидуумом, экспрессирующим полипептид канальный родопсин в клетке сетчатки.
Экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки обеспечивает кинетику, которая, по меньшей мере в 2 раза быстрее, чем кинетика, обеспечиваемая в клетке сетчатки родопсином (например, полипептид, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 2). Например, экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки обеспечивает кинетику, которая по меньшей мере в 2 раза, по меньшей мере в 5 раз, по меньшей мере в 10 раз, по меньшей мере в 15 раз, по меньшей мере в 20 раз, по меньшей мере в 25 раз, по меньшей мере в 30 раз, по меньшей мере в 50 раз, по меньшей мере в 100 раз или более чем в 100 раз быстрее кинетики, обеспечиваемой в клетке сетчатки полипептидом родопсином.
Способ по настоящему изобретению включает доставку в глаз индивидуума нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или SW-опсин. В некоторых случаях нуклеотидная последовательность функционально связана с элементом контроля транскрипции, который функционирует в клетке млекопитающего. В некоторых случаях нуклеотидная последовательность функционально связана с элементом контроля транскрипции, который обеспечивает экспрессию в клетке сетчатки, например, которая обеспечивает селективную экспрессию в клетке сетчатки. В некоторых случаях нуклеотидная последовательность функционально связана с промотором, который обеспечивает экспрессию в клетке сетчатки, например, который обеспечивает селективную экспрессию в клетке сетчатки. В некоторых случаях нуклеотидная последовательность функционально связана с промотором, который обычно обеспечивает экспрессию в клетке эукариот или клетке млекопитающего.
Подходящие промоторы включают, но не ограничиваются этим, промотор CAG (Miyazaki et al. (1989) Gene 79:269); промотор цитомегаловируса (CMV); промотор метаботропного глутаматного рецептора 6 (grm6) (Cronin et al. (2014) EMBO Mol. Med. 6:1175); промотор Pleiades (Portales-Casamar et al. (2010) Proc. Natl. Acad. Sci. USA 107:16589); промотор холинацетилтрансферазы (ChAT) (Misawa et al. (1992) J. Biol. Chem. 267:20392); промотор везикулярного глутаматного переносчика (V-glut) (Zhang et al. (2011) Brain Res. 1377:1); промотор глутаматдекарбоксилазы (GAD) (Rasmussen et al. (2007) Brain Res. 1144:19; Ritter et al. (2016) J. Gene Med. 18:27); промотор холецистокинина (CCK) (Ritter et al. (2016) J. Gene Med. 18:27); промотор парвальбумина (PV); промотор соматостатина (SST); промотор нейропептида Y (NPY); и промотор вазоактивного интестинального пептида (VIP). Подходящие промоторы включают, но не ограничиваются ими, промотор чувствительного к красному свету конопсина, промотор родопсина, промотор родопсинкиназы и промотор GluR (например, промотор GluR6; также упоминается как grm6). Подходящие промоторы включают, но не ограничиваются ими, промотор гена вителлиформной макулярной дистрофии 2 (VMD2) или промотор гена межфоторецепторного ретинол-связывающего белка (IRBP). Также подходящим для использования является промотор L7 (Oberdick et al. (1990) Science 248:223), промотор thy-1, промотор рековерина (Wiechmann and Howard (2003) Curr. Eye Res. 26:25); промотор кальбиндина; и промотор бета-актина. Подходящие промоторы включают синтетические (не встречающиеся в природе) комбинации промотор/энхансер.
В некоторых случаях нуклеиновая кислота, содержащая нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, находится в рекомбинантном векторе экспрессии. Подходящие векторы экспрессии включают, но не ограничиваются ими, лентивирусный вектор, вектор вируса простого герпеса (HSV), вектор аденовируса, ретровирусный вектор, вектор аденоассоциированного вируса (AAV) и тому подобное. Таким образом, в некоторых случаях нуклеиновая кислота, содержащая нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, представляет собой рекомбинантный лентивирусный вектор, рекомбинантный вектор HSV, рекомбинантный вектор аденовируса, рекомбинантный ретровирусный вектор или рекомбинантный вектор AAV.
В некоторых случаях нуклеиновая кислота (например, рекомбинантный вектор экспрессии), содержащая нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, находится в комплексе с наночастицей.
В некоторых случаях нуклеиновая кислота, содержащая нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или SW-опсин, представляет собой рекомбинантный вектор AAV (rAAV). В некоторых случаях вектор rAAV содержит нуклеотидную последовательность, кодирующую вариантный белок капсида AAV, где вариантный белок капсида AAV обеспечивает инфекционность по отношению к клеткам сетчатки и/или способность пересекать внутреннюю ограничивающую мембрану (ILM) в глазу. See, e.g., Day et al. (2014) Adv. Exp. Med. Biol. 801:687; Boye et al. (2016) J. Virol. 90:4215; Vandenberghe and Auricchio (2012) Gene Therapy 19:162; Klimczak et al. (2009) PLoS One 4:e7467; патентная публикация США № 2012/0164106; и патентная публикация США № 2016/0017295.
Клетки сетчатки включают ганглиозные клетки сетчатки; амакринные клетки; горизонтальные клетки; биполярные клетки; и фоторецепторные клетки, включая палочки и колбочки.
В некоторых случаях способ по настоящему изобретению включает введение нуждающемуся в этом индивидууму, фармацевтической композиции, содержащей: а) нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или полипептид SW-опсин; и b) фармацевтически приемлемое вспомогательное вещество.
Фармацевтическая композиция, содержащую нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, может быть введена пациенту отдельно или в комбинации с другими дополнительными активными веществами. Фармацевтические композиции могут быть изготовлены с использованием любого из множества способов, включая, без ограничения, обычное смешивание, растворение, гранулирование, дражирование, растирание в порошок, эмульгирование, капсулирование, захватывание и лиофилизацию. Фармацевтическая композиция может принимать любую из множества форм, включая, без ограничения, стерильный раствор, суспензию, эмульсию, лиофилизат, таблетку, пилюлю, пеллету, капсулу, порошок, сироп, эликсир или любую другую лекарственную форму, подходящую для введения.
Фармацевтическая композиция, содержащая нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, может необязательно включать фармацевтически приемлемый носитель(и), который облегчает переработку активного ингредиента в фармацевтически приемлемые композиции. Термин «фармакологически приемлемый носитель», в контексте данного документа, относится к любому носителю, который практически не оказывает длительного или постоянного негативного воздействия при введении, и охватывает такие термины, как «фармакологически приемлемый носитель, стабилизатор, разбавитель, вспомогательное вещество или наполнитель». Такой носитель обычно смешивают с активным соединением (например, нуклеиновой кислотой по настоящему изобретению) или разбавляют, или заключают в него активное соединение, и такой носитель может быть твердым, полутвердым или жидким агентом. Понятно, что активные ингредиенты могут быть растворимыми или могут быть доставлены в виде суспензии в желаемом носителе или разбавителе. Может быть использован любой из множества фармацевтически приемлемых носителей, включая, без ограничения, водную среду, такую как, например, дистиллированная, деионизированная вода, физиологический раствор; растворители; дисперсионные среды; покрытия; антибактериальные и противогрибковые средства; изотонические и задерживающие абсорбцию агенты; или любое другое вспомогательное вещество. Выбор фармакологически приемлемого носителя может зависеть от способа введения. За исключением случаев, когда какой-либо фармакологически приемлемый носитель несовместим с активным ингредиентом, предполагается его использование в фармацевтически приемлемых композициях. Неограничивающие примеры конкретного использования таких фармацевтических носителей можно найти в “Pharmaceutical Dosage Forms and Drug Delivery Systems” (Howard C. Ansel et al., eds., Lippincott Williams & Wilkins Publishers, 7th ed. 1999); “Remington: The Science and Practice of Pharmacy” (Alfonso R. Gennaro ed., Lippincott, Williams & Wilkins, 20th 2000); “Goodman & Gilman’s The Pharmacological Basis of Therapeutics” Joel G. Hardman et al., eds., McGraw-Hill Professional, 10.sup.th ed. 2001); и “Handbook of Pharmaceutical Excipients” (Raymond C. Rowe et al., APhA Publications, 4th edition 2003).
Фармацевтическая композиция может необязательно содержать, без ограничения, другие фармацевтически приемлемые компоненты, включая, без ограничения, буферы, консерванты, агенты, регулирующие тоничность, соли, антиоксиданты, физиологические растворы, вещества, влияющие на фармакологические свойства, наполнители, эмульгирующие агенты, смачивающие агенты, подсластители или ароматизаторы, и тому подобное. Различные буферные растворы и средства для регуляции рН могут быть использованы для приготовления фармацевтической композиции при условии, что полученный препарат является фармацевтически приемлемым. Такие буферы включают, без ограничения, ацетатные буферы, цитратные буферы, фосфатные буферы, нейтральный солевой буферный раствор, фосфатно-солевой буферный раствор и боратный буфер. Понятно, что кислоты или основания могут быть использованы для регуляции рН композиции по мере необходимости. Фармацевтически приемлемые антиоксиданты включают, без ограничения, метабисульфит натрия, тиосульфат натрия, ацетилцистеин, бутилированный гидроксианизол и бутилированный гидрокситолуол. Пригодные консерванты включают, без ограничения, хлорид бензалкония, хлорбутанол, тимеросал, ацетат фенилртути, нитрат фенилртути и стабилизированный оксихлор-комплекс, например, PURITE™. Агенты, регулирующие тоничность, подходящие для включения в фармацевтическую композицию, включают, без ограничения, соли, такие как, например, хлорид натрия, хлорид калия, маннит или глицерин, и другие фармацевтически приемлемые агенты, регулирующие тоничность. Понятно, что эти и другие вещества, известные в области фармакологии, могут быть включены в фармацевтическую композицию.
Некоторые примеры веществ, которые могут выступать как фармацевтически приемлемые носители, включают (1) сахара, такие как лактоза, глюкоза и сахароза; (2) крахмал, такой как кукурузный крахмал и картофельный крахмал; (3) целлюлоза и ее производные, такие как натрийкарбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; (4) порошкообразный трагакант; (5) солод; (6) желатин; (7) тальк; (8) наполнители, такие как масло какао и воски для суппозиториев; (9) масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; (10) гликоли, такие как пропиленгликоль; (11) полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; (12) сложные эфиры, такие как этилолеат и этиллаурат; (13) агар; (14) буферные агенты, такие как гидроксид магния и гидроксид алюминия; (15) альгиновая кислота; (16) апирогенная вода; (17) изотонический солевой раствор; (18) раствор Рингера; (19) этиловый спирт; (20) рН-регулирующие буферные растворы; (21) сложные полиэфиры, поликарбонаты и/или полиангидриды; и (22) другие нетоксичные совместимые вещества, используемые в фармацевтических композициях.
В некоторых случаях нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, составляют с одним или более биосовместимыми полимерами. Подходящие биосовместимые полимеры включают, но не ограничиваются ими, полиамиды, поликарбонаты, полиалкилены, полиалкиленгликоли, полиалкиленоксиды, полиалкилентерефталаты, поливиниловые спирты, поливиниловые эфиры, поливиниловые эфиры, поливинилгалогениды, поли(винилпирролидон), полигликолиды, полисилоксаны, полиуретаны и их сополимеры, алкилцеллюлоза, гидроксиалкилцеллюлозы, простые эфиры целлюлозы, сложные эфиры целлюлозы, нитроцеллюлозы, полимеры акриловых и метакриловых эфиров, метилцеллюлоза, этилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксибутилметилцеллюлоза, ацетат целлюлозы, пропионат целлюлозы, ацетатбутират целлюлозы, ацетатфталат целлюлозы, карбоксилэтилцеллюлоза, триацетат целлюлозы, натриевая соль сульфата целлюлозы, полиметилметакрилат), поли(этилметакрилат), поли(бутилметакрилат), поли(изобутилметакрилат\поли(гексилметакрилат), поли(изодецилметакрилат), поли(лаурилметакрилат), поли(фенилметакрилат), поли(метилакрилат), поли(изопропилакрилат), поли(изобутилакрилат), поли(октадецилакрилат), полиэтилен, полипропилен поли(этиленгликоль), поли(этиленоксид), поли(этилентерефталат), поливиниловые спирты, поливинилацетат, поливинилхлорид полистирол, поли(винилпирролидон), полигиалуроновые кислоты, казеин, желатин, глютин, полиангидриды, полиакриловая кислота, альгинат, хитозан, поли(метилметакрилаты), поли(этилметакрилаты), поли(бутилметакрилат), поли(изобутилметакрилат), поли(гексилметакрилат) поли(изодецилметакрилат), поли(лаурилметакрилат), поли(фенилметакрилат), поли(метилакрилат), поли(изопропилакрилат), поли(изобутилакрилат), поли(октадецилакрилат) и комбинации любого из вышеизложенного.
В некоторых случаях нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, формулируют в липосому. См., например, патентную публикацию США № 2017/0119666. В некоторых случаях нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, формулируют в наночастицу. Наночастицы включают, например, наночастицы полиалкилцианоакрилата, наночастицы, содержащие поли(молочную кислоту), наночастицы, включающие наночастицы сополимера молочной кислоты и гликолевой кислоты (PLGA), и тому подобное. В некоторых случаях нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, формулируют в липосому. Подходящие компоненты гидрогеля включают, но не ограничиваются ими, шелк (см., например, публикацию патента США № 2017/0173161), поли(молочную кислоту) (PLA), поли(гликолевую кислоту) (PGA), сополимер лактида с гликолидом (PLGA), сложные полиэфиры, поли(ортоэфир), поли(фосфазин), поли(фосфатный эфир), поликапролактон, желатин, коллаген, целлюлоза, гиалуронан, поли(этиленгликоль) (PEG), триблочные сополимеры, полилизин, поли(этиленоксид), поли(винилпирролидон), гиалуроновую кислоту, акрилированную гиалуроновую кислоту, поли(N-изопропилакриламид) и тому подобное.
В некоторых случаях композиция, содержащая нуклеиновую кислоту (например, вектор рекомбинантной экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, находится в солевом буферном растворе. В некоторых случаях композиция, содержащая рекомбинантный вектор экспрессии на основе вируса, содержащий нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, находится в солевом буферном растворе в количестве от около 108 до около 1015 вирусных геномов (вг) в объеме от около 50 мкл до около 1000 мкл. Например, в некоторых случаях композиция, содержащая рекомбинантный вектор экспрессии на основе вируса, содержащий нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, находится в солевом буферном растворе в количестве от около 108 вг до около 109 вг, от около 109 вг до около 1010 вг, от около 1010 вг до около 1011 вг, от около 1011 вг до около 1012 вг, от около 1012 вг до около 1013 вг, от около 1013 вг до около 1014 вг, или от около 1014 вг до около 1015 вг, в объеме от около 50 мкл до около 75 мкл, от около 75 мкл до около 100 мкл, от около 100 мкл до около 150 мкл, от около 150 мкл до около 200 мкл, от около 200 мкл до около 300 мкл, от около 300 мкл до около 400 мкл, от около 400 мкл до около 500 мкл, от около 500 мкл до около 600 мкл, от около 600 мкл до около 700 мкл, от около 800 до 900 мкл или от около 900 до около 1000 мкл. В некоторых случаях композиция, содержащая нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, находится в солевом буферном растворе, содержащем неионный детергент в концентрации около 0,001%. Подходящие неионные детергенты включают, например, Pluronic F68®. В некоторых случаях композиция, содержащая рекомбинантный вирусный вектор экспрессии, содержащий нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, находится в солевом буферном растворе в количестве от около 108 вг до около 109 вг, от около 109 вг до около 1010 вг, от около 1010 вг до около 1011 вг, от около 1011 вг до около 1012 вг, от около 1012 вг до около 1013 вг, от около 1013 вг до около 1014 вг, или от около 1014 вг до около 1015 вг, в объеме от около 50 мкл до около 75 мкл, от около 75 мкл до около 100 мкл, от около 100 мкл до около 150 мкл, от около 150 мкл до около 200 мкл, от около 200 мкл до около 300 мкл, от около 300 мкл до около 400 мкл, от около 400 мкл до около 500 мкл, от около 500 мкл до около 600 мкл, от около 600 мкл до около 700 мкл, от около 800 до около 900 мкл или от около 900 до около 1000 мкл, причем солевой буферный раствор содержит неионный детергент в концентрации около 0,001%. Солевой раствор может содержать 0,9% NaCl.
Нуклеиновая кислота (например, рекомбинантный вектор экспрессии, такой как рекомбинантный вирусный вектор), содержащая нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, может быть введена нуждающемуся в этом индивидууму согласно любому из множества способов введения. Подходящие пути введения включают, например, периокулярный, интраокулярный, интравитреальный, субконъюнктивный, ретробульбарный, в склеру и межкамерный. В некоторых случаях нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, доставляют путем интравитреальной инъекции. В некоторых случаях нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащая нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, доставляют внутриглазным способом. В некоторых случаях нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, доставляют посредством субретинальной инъекции.
В некоторых случаях способ по настоящему изобретению включает однократное введение нуждающемуся в этом индивидууму (на глаз) композиции, содержащей нуклеиновую кислоту (например, рекомбинантный вектор экспрессии, такой как рекомбинантный вирусный вектор), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин.
В некоторых случаях индивидууму вводят множественные дозы нуклеиновой кислоты (например, рекомбинантного вектора экспрессии), содержащей нуклеотидную последовательность, кодирующую MW-опсин и/или LW-опсин. Например, в некоторых случаях нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, вводят один раз в месяц, два раза в месяц, три раза в месяц, каждую вторую неделю (qow), один раз в неделю (qw), два раза в неделю (biw), три раза в неделю (tiw), четыре раза в неделю, пять раз в неделю, шесть раз в неделю, через день (qod), ежедневно (qd), два раза в день (qid) или три раза в день (tid).
Нуклеиновая кислота (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, может быть введена индивидууму в течение периода времени от около 1 день до около 1 года или более 1 года. Например, нуклеиновая кислота (например, рекомбинантный вектор экспрессии), содержащая нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, может быть введена индивидууму в течение периода времени от 1 недели до 2 недель, от 2 недель до 1 месяца, от 1 месяца до 4 месяцев, от 4 месяцев до 6 месяцев, от 6 месяцев до 1 года или более 1 года.
Когда нуклеиновая кислота, содержащая нуклеотидную последовательность, представляет собой рекомбинантный вектор экспрессии на основе вируса, содержащий нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, рекомбинантный вирусный вектор может быть введен в количестве от около 108 вг до около 109 вг, от около 109 вг до около 1010 вг, от около 1010 вг до около 1011 вг, от около 1011 до около 1012 вг, от около 1012 вг до около 1013 вг, от около 1013 вг до около 1014 вг или от около 1014 вг до около 1015 вг на дозу.
Нуклеиновую кислоту (например, рекомбинантный вектор экспрессии), содержащую нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, вводят в количестве, эффективном для улучшения зрительной функции у индивидуума по меньшей мене на 10%, по меньшей мене на 15%, по меньшей мене на 20%, по меньшей мене на 25%, по меньшей мене на 30%, по меньшей мене на 40%, по меньшей мене на 50%, по меньшей мене в 2 раза, по меньшей мене в 5 раз, по меньшей мене в 10 раз или более чем в 10 раз по сравнению со зрительной функцией до введения нуклеиновой кислоты. Испытания зрительной функции известны в данной области техники, и любое испытание может применяться для оценки зрительной функции.
Индивидуумы, подходящие для лечения способом по настоящему изобретению, включают индивидуумов, имеющих сниженную зрительную функцию из-за потери фоторецепторов палочек и колбочек. В некоторых случаях индивидуум имеет наследственное дегенеративное заболевание сетчатки, такое как пигментный ретинит, ретиношизис или врожденный амавроз Лебера. В некоторых случаях индивидуум имеет заболевание глаз (например, наследственное заболевание глаз), выбранное из пигментного ретинита, макулярной дегенерации, возрастной макулярной дегенерации, ретиношизиса и врожденного амавроза Лебера, а также диабетической ретинопатии. Индивидуумы, подходящие для лечения способом по настоящему изобретению, включают индивидуумов, имеющих состояние дегенерации сетчатки, при котором снижается чувствительность к естественному свету и, следовательно, нарушается зрение, но где нейроны находятся в конце цепи сетчатки (например, биполярные клетки или амакринные интернейроны, или ганглиозные клетки, которые выводятся в мозг) защищены и могут быть осуществлены непосредственно чувствительными к свету путем введения конопсина (ов).
Индивидуумы, подходящие для лечения способом по настоящему изобретению, включают индивидуумов, имеющих поражение сетчатки, которое является травматической или острой, без генетической или наследственной основы. Например, в некоторых случаях у индивидуума имело место отслоение сетчатки вследствие тупой травмы, такой как поражение ударной волной (например, в военном сражении), или в результате удара по голове, например, в ходе автокатастрофы, или другого несчастного случая, приводящего к удару в голову. В некоторых случаях фоторецепторы гибнут из-за травматического отслоения сетчатки от основного RPE, но внутренние нейроны сетчатки не повреждены. Индивидуумы, подходящие для лечения способом по настоящему изобретению, включают индивидуумов, имеющих потерю фоторецептора из-за острого светового повреждения, воздействия лазера или химического токсического действия.
Композиции
В настоящем изобретении предлагается композиция, содержащая один или более рекомбинантных векторов нуклеиновой кислоты, содержащей одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов. В случае, если композицию вводят нуждающемуся в этом индивидууму, одна или более нуклеотидных последовательностей, кодирующих один или более конопсинов, экспрессируются в глазу нуждающегося в этом субъекта, так что один или более конопсинов продуцируются в глазу субъекта, что приводит к одному или более положительным клиническим результатам. Например, когда композицию вводят в глаз нуждающегося в этом индивидуума, одна или более нуклеотидных последовательностей, кодирующих один или более конопсинов, экспрессируются в глазу нуждающегося в этом субъекта, так что один или более конопсинов продуцируются в глазу субъекта, что приводит к одному или более положительным клиническим результатам. Когда одна или более нуклеотидных последовательностей, кодирующих один или более конопсинов, экспрессируются в глазу нуждающегося в этом субъекта, так что один или более конопсинов продуцируются в глазу субъекта, это приводит к одному или более положительным клиническим результатам. Положительные клинические результаты включают: 1) субъект может различать между изображением, содержащим вертикальную линию, и изображением, содержащим горизонтальную линию, в анализе распознавания пространственного паттерна; 2) субъект может различать между изображением, содержащим статическую линию, и изображением, содержащим движущуюся линию, в анализе распознавания пространственного паттерна; 3) субъект может различать между мигающим светом и постоянным светом в анализе временного светового паттерна; 4) субъект может распознавать изображение при интенсивности света от около 10-4 Вт/см2 до около 10 Вт/см2 в анализе распознавания изображения; и 5) субъект может различать между областью с белым светом и областью без белого света в анализе избегания света.
Предоставляет ли композиция один или более из указанных выше положительных клинических результатов, можно определить с помощью испытаний, известных в данной области техники. См., например, Leinonen and Tanila (2017) Behavioural Brain Research pii: S0166-4328(17)30870-7; Caporale et al. (2011). Molecular Therapy 19, 1212-9; Gaub et al. (2014) Proc. Natl. Acad. Sci. USA 111, E5574-83; Gaub et al. (2015) Molecular Therapy 23:1562; and Berry et al. (2017) Nat. Commun. 8:1862.
В настоящем документе предлагается композиция, содержащая один или более рекомбинантных векторов нуклеиновой кислоты, содержащей одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда: i) композицию вводят индивидууму, нуждающемуся в этом; или ii) композицию вводят в глаз нуждающегося в этом индивидуума таким образом, что одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта (так что один или более опсинов продуцируются в глазу субъекта), субъект может различать между изображением, содержащим вертикальную линию, и изображением, содержащим горизонтальную линию, в анализе распознавания пространственного паттерна. Композиция по настоящему изобретению, содержащая один или более рекомбинантных векторов нуклеиновой кислоты, содержащей одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта, (так, что один или более опсинов продуцируются в глазу субъекта), субъект может различать между изображением, содержащим вертикальную линию, и изображением, содержащим горизонтальную линию, в анализе распознавания пространственного паттерна.
Композиция по настоящему изобретению, содержащая один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда: i) композицию вводят нуждающемуся в этом индивидууму; или ii) композицию вводят в глаз нуждающегося в этом индивидуума таким образом, что одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта (так что один или более опсинов продуцируются в глазу субъекта), субъект может различать между изображением, содержащим статическую линию, и изображением, содержащим движущуюся линию, в анализе распознавания пространственного паттерна. Настоящее изобретение относится к композиции, содержащей один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда указанные одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта(так, что один или более опсинов продуцируются в глазу субъекта), субъект может различать между изображением, содержащим статическую линию, и изображением, содержащим движущуюся линию, в анализе распознавания пространственного паттерна.
Композиция по настоящему изобретению, содержащая один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда: i) композицию вводят нуждающемуся в этом индивидууму, ; или ii) композицию вводят в глаз нуждающегося в этом индивидуума таким образом, что одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта (так, что один или более опсинов продуцируются в глазу субъекта), субъект может различать между мигающим светом и постоянным светом в анализе временного светового паттерна. Настоящее изобретение относится к композиции, содержащей один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда указанные одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта (так, что один или более опсинов продуцируются в глазу субъекта), субъект может различать между мигающим светом и постоянным светом в анализе временного светового паттерна.
Композиция по настоящему изобретению, содержащая один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда: i) композицию вводят индивидууму, нуждающемуся в этом; или ii) композицию вводят в глаз нуждающегося в этом индивидуума таким образом, что одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта (так, что один или более опсинов продуцируются в глазу субъекта), субъект может распознавать изображение с интенсивностью света от около 10-4 Вт/см2 до около 10 Вт/см2 в анализе распознавания изображений. Настоящее изобретение относится к композиции, содержащей один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда указанные одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта (так, что один или более опсинов образуются в глазу субъекта), субъект может распознавать изображение при интенсивности света от около 10-4 Вт/см2 до около 10 Вт/см2 (например, интенсивность света от около 10-4 Вт/см2 до около 10-3 Вт/см2, от около 10-3 Вт/см2 до около 10-2 Вт/см2, от около 10-2 Вт/см2 до около 10-1 Вт/см2 или от около 10-1 Вт/см2до около 1 Вт/см2. В некоторых случаях экспрессия полипептида MW-опсина, и/или полипептида LW-опсина, и/или полипептида SW-опсина в клетке сетчатки у индивидуума обеспечивает распознавание изображения при интенсивности света до 2 Вт/см2 до 3 Вт/см2, до 4 Вт/см2, до 5 Вт/см2 или до 10 Вт/см2) в анализе распознавания изображений.
Композиция по настоящему изобретению, содержащая один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда: i) композицию вводят нуждающемуся в этом индивидууму; или ii) композицию вводят в глаз нуждающегося в этом индивидуума таким образом, что одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта (так что один или более опсинов продуцируются в глазу субъекта), субъект может различать между областью с белым светом и областью без белого света в анализе избегания света. Настоящее изобретение относится к композиции, содержащей один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда указанные одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта (так, что один или более опсинов продуцируются в глазу субъекта), субъект может различать между областью с белым светом и областью без белого света в анализе избегания света.
Конопсины, которые могут кодироваться одной или более рекомбинантными нуклеиновыми кислотами, присутствующими в композиции по настоящему изобретению, описаны выше и включают, например, MW-опсин, LW-опсин, SW-опсин, химерный опсин и тому подобное.
В некоторых случаях один или более конопсинов, кодируемых одной или более рекомбинантными нуклеиновыми кислотами, присутствующими в композиции по настоящему изобретению, выбраны из группы, состоящей из:
a) MW-опсина, содержащего аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 1;
b) LW-опсина, содержащего аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 4;
c) SW-опсина, содержащего аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 5; и
d) химерного SW-опсина, содержащего: i) внутриклеточные участки SW-опсина мыши, содержащие аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 6; и ii) трансмембранные участки SW-опсина человека, содержащие аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 5.
В некоторых случаях композиция по настоящему изобретению содержит рекомбинантную нуклеиновую кислоту, содержащую нуклеотидную последовательность, которая кодирует один конопсин. В некоторых случаях один или более рекомбинантных векторов нуклеиновой кислоты, присутствующих в композиции по настоящему изобретению, содержат одну или более нуклеотидных последовательностей, кодирующих 2 разных конопсина. Например, в некоторых случаях один или более рекомбинантных векторов нуклеиновой кислоты, присутствующих в композиции по настоящему изобретению, содержат одну или более нуклеотидных последовательностей, кодирующих MW-опсин и LW-опсин. В качестве еще одного примера, в некоторых случаях один или более рекомбинантных векторов нуклеиновой кислоты, присутствующих в композиции по настоящему изобретению, содержат одну или более нуклеотидных последовательностей, кодирующих MW-опсин и SW-опсин. В качестве еще одного примера, в некоторых случаях один или более рекомбинантных векторов нуклеиновой кислоты, присутствующих в композиции по настоящему изобретению, содержат одну или более нуклеотидных последовательностей, кодирующих LW-опсин и SW-опсин. 2 разных конопсина могут кодироваться в одной рекомбинантной нуклеиновой кислоте. 2 разных конопсина могут кодироваться в 2 отдельных рекомбинантных нуклеиновых кислотах.
В некоторых случаях один или более рекомбинантных векторов нуклеиновой кислоты, присутствующих в композиции по настоящему изобретению, содержат одну или более нуклеотидных последовательностей, кодирующих 3 разных конопсина. Например, в некоторых случаях один или более рекомбинантных векторов нуклеиновой кислоты, присутствующих в композиции по настоящему изобретению, содержат одну или более нуклеотидных последовательностей, кодирующих MW-опсин, SW-опсин и LW-опсин. 3 разных конопсина могут кодироваться на одной рекомбинантной нуклеиновой кислоте. 3 разных конопсина могут кодироваться в 3 отдельных рекомбинантных нуклеиновых кислотах.
Подходящие рекомбинантные векторы нуклеиновых кислот включают вектор на основе аденоассоциированного вируса, рекомбинантный лентивирусный вектор, рекомбинантный вектор на основе вируса простого герпеса и рекомбинантный ретровирусный вектор. В некоторых случаях один или более рекомбинантных векторов нуклеиновой кислоты является/являются рекомбинантными векторами на основе аденоассоциированного вируса. В некоторых случаях рекомбинантный вектор AAV содержит нуклеотидную последовательность, кодирующую вариантный полипептид капсида, который придает повышенную инфекционность по отношению к клеткам сетчатки и/или придает повышенную способность пересекать внутреннюю ограничивающую мембрану по сравнению с капсидом AAV дикого типа.
Нуклеотидная последовательность, кодирующая конопсин, может быть функционально связана с одним или более элементами транскрипционного контроля. Например, нуклеотидная последовательность, кодирующая конопсин, может быть функционально связана с промотором. Примеры подходящих промоторов включают, но не ограничиваются ими, промотор синапсина, промотор CAG, промотор CMV, промотор grm6, промотор Pleiades, промотор ChAT, промотор V-glut, промотор GAD, промотор PV, промотор соматостатина (SST), промотор нейропептида Y (NPY), промотор VIP, промотор чувствительного к красному свету конопсина, промотор родопсина, промотор родопсинкиназы, промотор гена вителлиформной макулярной дистрофии 2 (VMD2) и промотор гена межфоторецепторного ретинол-связывающего белка (IRBP).
Композиция по настоящему изобретению вводится нуждающемуся в этом индивидууму. В некоторых случаях композицию вводят непосредственно в глаз индивидуума, например, в глаз с нарушением зрительной функции. В некоторых случаях субъект имеет заболевание глаз, выбранное из пигментного ретинита, макулярной дегенерации, ретиношизиса и врожденного амавроза Лебера, а также диабетической ретинопатии. В некоторых случаях у субъекта имело место отслоение сетчатки или потеря фоторецептора вследствие травмы или повреждения головы. В некоторых случаях, субъект имеет состояние дегенерации сетчатки, при котором снижается чувствительность к естественному свету и, следовательно, нарушается зрение, но при этом нейроны, находящиеся на конце сетчатки (например, биполярные клетки или амакринные интернейроны, или ганглиозные клетки, идущие к мозгу), остаются неповрежденными и путем введения конопсина(ов) могут проявлять чувствительность к свету.
Композиция по настоящему изобретению может содержать, помимо одной или более рекомбинантных нуклеиновых кислот, фармацевтически приемлемое вспомогательное вещество. Подходящие фармацевтически приемлемые вспомогательные вещества известны в данной области техники и описаны в другом месте настоящего документа. В некоторых случаях композиция по настоящему изобретению является подходящей для введения человеку; например, в некоторых случаях композиция является стерильной и не содержит пирогенов, загрязнений и тому подобного.
Рекомбинантный вирусный вектор
Настоящее изобретение относится к рекомбинантному вирусному вектору, содержащему нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин. Подходящие вектор экспрессии на основе вируса включают, но не ограничиваются ими, лентивирусный вектор, вектор вируса простого герпеса (HSV), вектор аденовируса, вектор ретровируса, вектор на основе аденоассоциированного вируса (AAV) и тому подобное. Таким образом, в некоторых случаях рекомбинантный вирусный вектор, содержащий нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или полипептид LW-опсин, и/или полипептид SW-опсин, представляет собой рекомбинантный лентивирусный вектор, рекомбинантный вектор HSV, рекомбинантный вектор аденовируса, рекомбинантный вектор ретровируса или рекомбинантный вектор AAV.
В некоторых случаях нуклеотидная последовательность, кодирующая MW-опсин и/или LW-опсин, и/или SW-опсин, функционально связана с промотором, который обеспечивает экспрессию в клетке сетчатки. В некоторых случаях нуклеотидная последовательность функционально связана с промотором, который обычно обеспечивает экспрессию в клетке эукариот или клетке млекопитающего.
Подходящие промоторы включают, но не ограничиваются этим, промотор CAG (Miyazaki et al. (1989) Gene 79:269); промотор цитомегаловируса (CMV); промотор метаботропного глутаматного рецептора 6 (grm6) (Cronin et al. (2014) EMBO Mol. Med. 6:1175); промотор Pleiades (Portales-Casamar et al. (2010) Proc. Natl. Acad. Sci. USA 107:16589); промотор холинацетилтрансферазы (ChAT) (Misawa et al. (1992) J. Biol. Chem. 267:20392); промотор везикулярного глутаматного переносчика (V-glut) (Zhang et al. (2011) Brain Res. 1377:1); промотор глутаматдекарбоксилазы (GAD) (Rasmussen et al. (2007) Brain Res. 1144:19; Ritter et al. (2016) J. Gene Med. 18:27); промотор холецистокинина (CCK) (Ritter et al. (2016) J. Gene Med. 18:27); промотор парвальбумина (PV); промотор соматостатина (SST); промотор нейропептида Y (NPY); и промотор вазоактивного интестинального пептида (VIP). Подходящие промоторы включают, но не ограничиваются ими, промотор чувствительного к красному свету конопсина, промотор родопсина, промотор родопсинкиназы и промотор GluR (например, промотор GluR6). Подходящие промоторы включают, но не ограничиваются ими, промотор гена вителлиформной макулярной дистрофии 2 (VMD2) или промотор гена межфоторецепторного ретинол-связывающего белка (IRBP). Также подходящим для использования является промотор L7 (Oberdick et al. (1990) Science 248:223), промотор thy-1, промотор рековерина (Wiechmann and Howard (2003) Curr. Eye Res. 26:25); промотор кальбиндина; и промотор бета-актина.
В некоторых случаях рекомбинантный вирусный вектор по настоящему изобретению содержит нуклеотидные последовательности, кодирующие MW-опсин, LW-опсин и SW-опсин. В некоторых случаях нуклеотидные последовательности, кодирующие MW-опсин, LW-опсин и SW-опсин, функционально связаны с одним промотором. В некоторых случаях рекомбинантный вирусный вектор содержит внутренний участок посадки рибосомы (IRES) между нуклеотидными последовательностями, кодирующими MW-опсин и LW-опсин, и между нуклеотидными последовательностями, кодирующими LW-опсин и SW-опсин.
В некоторых случаях рекомбинантный вирусный вектор, содержащий нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин, представляет собой рекомбинантный вектор AAV (rAAV). В некоторых случаях вектор rAAV содержит: i) нуклеотидную последовательность, кодирующую полипептид MW-опсин и/или LW-опсин, и/или SW-опсин; и ii) нуклеотидная последовательность, кодирующая вариантный капсидний белок AAV, где вариантный белок капсида AAV обеспечивает инфекционность по отношению к клеткам сетчатки и/или повышенную способность пересекать внутреннюю ограничивающую мембрану (ILM) в глазу по сравнению с исходным диким типом AAV. See, e.g., Day et al. (2014) Adv. Exp. Med. Biol. 801:687; Boye et al. (2016) J. Virol. 90:4215; Vandenberghe and Auricchio (2012) Gene Therapy 19:162; Klimczak et al. (2009) PLoS One 4:e7467; патентная публикация США № 2012/0164106; и патентная публикация США № 2016/0017295.
Например, вариантный белок капсида AAV может содержать аминокислотную замену при аминокислоте 451 капсида AAV6 или при соответствующем положении в другом серотипе AAV. В некоторых случаях аминокислотная замена при аминокислоте 451 капсида AAV6 или соответствующем положении в другом серотипе AAV представляет собой замену аспарагина на аспарагиновую кислоту. В качестве другого примера, вариантный белок капсида AAV может содержать аминокислотную замену при аминокислоте 532 капсида AAV6 или соответствующем положении в другом серотипе AAV. В некоторых случаях аминокислотная замена в аминокислоте 532 капсида AAV6 или соответствующая позиция в другом серотипе AAV представляет собой замену аспарагиновой кислоты на аспарагин.
Капсид AAV6 может иметь следующую аминокислотную последовательность: MAADGYLPDWLEDNLSEGIREWWDLKPGAPKPKANQQKQDDGRGLVLPGYKYLGPFNGLD KGEPVNAADAAALEHDKAYDQQLKAGDNPYLRYNHADAEFQERLQEDTSFGGNLGRAVFQ AKKRVLEPFGLVEEGAKTAPGKKRPVEQSPQEPDSSSGIGKTGQQPAKKRLNFGQTGDSESVP DPQPLGEPPATPAAVGPTTMASGGGAPMADNNEGADGVGNASGNWHCDSTWLGDRVITTST RTWALPTYNNHLYKQISSASTGASNDNHYFGYSTPWGYFDFNRFHCHFSPRDWQRLINNNW GFRPKRLNFKLFNIQVKEVTTNDGVTTIANNLTSTVQVFSDSEYQLPYVLGSAHQGCLPPFPA DVFMIPQYGYLTLNNGSQAVGRSSFYCLEYFPSQMLRTGNNFTFSYTFEDVPFHSSYAHSQSL DRLMNPLIDQYLYYLNRTQ QSGSAQNKDLLFSRGSPAGMSVQPKNWLPGPCYRQQRVSKT KTDNNNSNFTWTGASKYNLNGRESIINPGTAMASHKDDK
QSGSAQNKDLLFSRGSPAGMSVQPKNWLPGPCYRQQRVSKT KTDNNNSNFTWTGASKYNLNGRESIINPGTAMASHKDDK FFPMSGVMIFGKESAGASNTA LDNVMITDEEEIKATNPVATERFGTVAVNLQSSSTDPATGDVHVMGALPGMVWQDRDVYLQ GPIWAKIPHTDGHFHPSPLMGGFGLKHPPPQILIKNTPVPANPPAEFSATKFASFITQYSTGQVS VEIEWELQKENSKRWNPEVQYTSNYAKSANVDFTVDNNGLYTEPRPIGTRYLTRPL (SEQ ID NO:10), где Asn-451 и Asp-532 выделены жирным шрифтом и подчеркнуты.
FFPMSGVMIFGKESAGASNTA LDNVMITDEEEIKATNPVATERFGTVAVNLQSSSTDPATGDVHVMGALPGMVWQDRDVYLQ GPIWAKIPHTDGHFHPSPLMGGFGLKHPPPQILIKNTPVPANPPAEFSATKFASFITQYSTGQVS VEIEWELQKENSKRWNPEVQYTSNYAKSANVDFTVDNNGLYTEPRPIGTRYLTRPL (SEQ ID NO:10), где Asn-451 и Asp-532 выделены жирным шрифтом и подчеркнуты.
В некоторых случаях белок капсида AAV содержит следующую аминокислотную последовательность: MAADGYLPDWLEDNLSEGIREWWDLKPGAPKPKANQQKQDDGRGLVLPGYKYLGPFNGLD KGEPVNAADAAALEHDKAYDQQLKAGDNPYLRYNHADAEFQERLQEDTSFGGNLGRAVFQ AKKRVLEPFGLVEEGAKTAPGKKRPVEQSPQEPDSSSGIGKTGQQPAKKRLNFGQTGDSESVP DPQPLGEPPATPAAVGPTTMASGGGAPMADNNEGADGVGNASGNWHCDSTWLGDRVITTST RTWALPTYNNHLYKQISSASTGASNDNHYFGYSTPWGYFDFNRFHCHFSPRDWQRLINNNW GFRPKRLNFKLFNVQVKEVTTNDGVTTIANNLTSTVQVFSDSEYQLPYVLGSAHQGCLPPFPA DVFMIPQYGYLTLNNGSQAVGRSSFYCLEYFPSQMLRTGNNFTFSYTFEDVPFHSSYAHSQSL DRLMNPLIDQYLYYLNRTQDQSGSAQNKDLLFSRGSPAGMSVQPKNWLPGPCYRQQRVSKT KTDNNNSNFTWTGASKYNLNGRESIINPGTAMASHKDDKNKFFPMSGVMIFGKESAGASNT ALDNVMITDEEEIKATNPVATERFGTVAVNLQSSSTDPATGDVHVMGALPGMVWQDRDVYL QGPIWAKIPHTDGHFHPSPLMGGFGLKNPPPQILIKNTPVPANPPAEFSATKFASFITQYSTGQV SVEIEWELQKENSKRWNPEVQYTSNYAKSANVDFTVDNNGLYTEPRPIGTRYLTRPL (SEQ ID NO:11).
Настоящее изобретение относится к способу доставки MW-опсина, и/или LW-опсина, и/или SW-опсина в клетку сетчатки, включающему введение рекомбинантного вирусного вектора по настоящему изобретению (или вирусной частицы, содержащей рекомбинантный вирусный вектор) в глаз индивидуума. После введения рекомбинантного вирусного вектора (или вирусной частицы, содержащей рекомбинантный вирусный вектор), MW-опсин продуцируется в клетке сетчатки.
В настоящем раскрытии предложен способ улучшения или восстановления зрительной функции у индивидуума, причем способ включает введение рекомбинантного вирусного вектора по настоящему изобретению (или вирусной частицы, содержащей рекомбинантный вирусный вектор) в глаз индивидуума. После введения рекомбинантного вирусного вектора (или вирусной частицы, содержащей рекомбинантный вирусный вектор), MW-опсин и/или LW-опсин, и/или SW-опсин продуцируются в клетке сетчатки. Выработка MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает усиленную или восстановленную зрительную функцию у индивидуума.
В настоящем раскрытии предлагается фармацевтическая композиция, содержащая: а) рекомбинантный вирусный вектор по настоящему изобретению или вирусную частицу, содержащую рекомбинантный вирусный вектор; и b) фармацевтически приемлемое вспомогательное вещество. Подходящие фармацевтически приемлемые вещества описаны выше.
В настоящем раскрытии предлагается способ доставки MW-опсина, и/или LW-опсина, и/или SW-опсина в клетку сетчатки, включающему введение фармацевтической композиции, содержащей рекомбинантный вирусный вектор (или вирусную частицу, содержащую рекомбинантный вирусный вектор) в глаз индивидуума. После введения рекомбинантного вирусного вектора (или вирусной частицы, содержащей рекомбинантный вирусный вектор), MW-опсин и/или LW-опсин, и/или SW-опсин продуцируются в клетке сетчатки.
В настоящем раскрытии предложен способ улучшения или восстановления зрительной функции у индивидуума, причем способ включает введение фармацевтической композиции, содержащей рекомбинантный вирусный вектор по настоящему раскрытию (или вирусную частицу, содержащую рекомбинантный вирусный вектор), в глаз индивидуума. После введения рекомбинантного вирусного вектора (или вирусной частицы, содержащей рекомбинантный вирусный вектор), MW-опсин и/или LW-опсин, и/или SW-опсин продуцируются в клетке сетчатки. Продуцирование MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает улучшение или восстановление зрительной функции у индивидуума.
Рекомбинантный вектор экспрессии по настоящему изобретению (или вирусная частица, содержащая рекомбинантный вирусный вектор) может быть введен нуждающемуся в этом индивидууму любым из множества способов введения. Подходящие пути введения включают, например, периокулярный, интраокулярный, интравитреальный, субконъюнктивный, ретробульбарный, в склеру и межкамерный. В некоторых случаях рекомбинантный вектор экспрессии по настоящему изобретению (или вирусная частица, содержащая рекомбинантный вирусный вектор) доставляется путем интравитреальной инъекции. В некоторых случаях рекомбинантный вектор экспрессии по настоящему изобретению (или вирусная частица, содержащая рекомбинантный вирусный вектор) доставляется внутриглазно. В некоторых случаях рекомбинантный вектор экспрессии по настоящему изобретению (или вирусная частица, содержащая рекомбинантный вирусный вектор) доставляется посредством субретинальной инъекции.
Индивидуумы, подходящие для лечения способом по настоящему изобретению, включают индивидуумов, имеющих сниженную зрительную функцию из-за потери фоторецепторов палочек и колбочек. В некоторых случаях индивидуум имеет наследственное дегенеративное заболевание сетчатки. В некоторых случаях индивидуум имеет глазное заболевание, выбранное из пигментного ретинита, макулярной дегенерации, ретиношизиса и врожденного амавроза Лебера, а также диабетической ретинопатии. В некоторых случаях индивидуум имеет возрастное дегенеративное заболевание сетчатки. В некоторых случаях у индивидуума наблюдается возрастная макулярная дегенерация.
Примеры неограничивающих аспектов настоящего изобретения
Аспекты, включая варианты осуществления, объекта настоящего изобретения, описанного выше, могут быть полезными отдельно или в комбинации с одним или более другими аспектами или вариантами осуществления. Не ограничивая вышеприведенное описание, некоторые неограничивающие аспекты настоящего изобретения, пронумерованные 1-54, представлены ниже. Как будет понятно специалистам в данной области техники после прочтения этого раскрытия, каждый из отдельно пронумерованных аспектов может использоваться или комбинироваться с любым из предыдущих или следующих отдельно пронумерованных аспектов. Это предназначено для обеспечения поддержки всех таких комбинаций аспектов и не ограничивается комбинациями аспектов, которые явно предоставлены ниже:
Аспект 1. Способ восстановления или улучшения зрительной функции у индивидуума, включающий введение индивидууму нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую средневолновый опсин (MW-опсин) и/или длинноволновый опсин (LW-опсин), и/или коротковолновый опсин (SW-опсин), причем указанное введение обеспечивает экспрессию MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки у индивидуума и восстановление, или улучшение зрительной функции.
Аспект 2. Способ по аспекту 1, в котором MW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 1; причем LW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 4, и при этом SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 5.
Аспект 3. Способ по аспекту 1, в котором SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности SW-опсина человека, представленной в SEQ ID NO: 5, или идентичную по меньшей мере на 87% аминокислотной последовательности SW-опсина мыши, представленной в SEQ ID NO: 6.
Аспект 4. Способ по аспекту 1, включающий введение индивидууму: i) первой нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую SW-опсин, содержащий аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности SW-опсина человека, представленной в SEQ ID NO: 5; и ii) вторую нуклеиновую кислоту, содержащую нуклеотидную последовательность, кодирующую SW-опсин, содержащий аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности SW-опсина мыши, представленной в SEQ ID NO: 6.
Аспект 5. Способ по аспекту 1, в котором SW-опсин представляет собой химерный SW-опсин, содержащий внутриклеточные домены SW-опсина мыши и трансмембранные домены SW-опсина человека.
Аспект 6. Способ по аспекту 5, в котором химерный SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности химерного SW-опсина, представленной в SEQ ID NO: 7.
Аспект 7. Способ по любому из аспектов 1-6, в котором экспрессия MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает видение паттернов и распознавание изображения индивидуумом.
Аспект 8. Способ по аспекту 7, в котором распознавание изображения представляет собой распознавание статического изображения или паттерна.
Аспект 9. Способ по аспекту 7, в котором распознавание изображения представляет собой распознавание движущегося изображения или паттерна.
Аспект 10. Способ по любому из аспектов 1-9, в котором экспрессия MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает распознавание изображения при интенсивности света от около 10-4 Вт/см2 до около 1 Вт/см2.
Аспект 11. Способ по любому из аспектов 1-9, в котором экспрессия MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает распознавание изображения при интенсивности света, которая по меньшей мере в 10 раз ниже, чем интенсивность света, необходимая для распознавания изображения индивидуумом, у которого экспрессируется полипептид канальный родопсин в клетке сетчатки.
Аспект 12. Способ по любому из аспектов 1-9, в котором экспрессия MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает кинетику, которая по меньшей мере в 2 раза быстрее, чем кинетика в клетке сетчатки, вызванная полипептидом родопсином.
Аспект 13. Способ по любому из аспектов 1-12, в котором нуклеиновая кислота представляет собой рекомбинантный вектор экспрессии.
Аспект 14. Способ по аспекту 13, в котором рекомбинантный вектор экспрессии представляет собой рекомбинантный вирусный вектор.
Аспект 15. Способ по аспекту 14, в котором рекомбинантный вирусный вектор представляет собой вектор на основе аденоассоциированного вируса, лентивирусный вектор, вектор вируса простого герпеса или вектор ретровируса.
Аспект 16. Способ по любому из аспектов 1-15, в котором нуклеотидная последовательность функционально связана с элементом контроля транскрипции, который функционирует в клетке сетчатки.
Аспект 17. Способ по аспекту 16, в котором элемент контроля транскрипции представляет собой специфичный для клеток сетчатки промотор.
Аспект 18. Способ по аспекту 17, в котором промотор представляет собой промотор синапсина, промотор CAG, промотор CMV, промотор grm6, промотор Pleiades, промотор ChAT, промотор V-glut, промотор GAD, промотор PV, соматостатин (SST) промотор, нейропептидный Y (NPY) промотор, промотор VIP, промотор чувствительного к красному свету конопсина, промотор родопсина, промотор родопсинкиназы, промотор гена вителлиформной макулярной дистрофии 2 (VMD2) или промотор гена межфоторецепторного ретинол-связывающего белка (IRBP).
Аспект 19. Способ по любому из аспектов 1-18, в котором указанное введение осуществляется посредством внутриглазной инъекции.
Аспект 20. Способ по любому из аспектов 1-18, в котором указанное введение осуществляется посредством интравитреальной инъекции.
Аспект 21. Способ по любому из аспектов 1-18, в котором указанное введение осуществляется посредством субретинальной инъекции.
Аспект 22. Способ по любому из аспектов 1-21, в котором индивидуум имеет глазное заболевание, выбранное из пигментного ретинита, макулярной дегенерации, ретиношизиса и врожденного амавроза Лебера, а также диабетической ретинопатии.
Аспект 23. Способ по любому из аспектов 1-21, в котором у индивидуума имело место отслоение сетчатки или потеря фоторецептора вследствие травмы или повреждения головы.
Аспект 24. Способ по любому из аспектов 1-23, в котором нуклеиновая кислота находится в комплексе с наночастицей.
Аспект 25. Рекомбинантный вирусный вектор, содержащий нуклеотидную последовательность, кодирующую средневолновый опсин (MW-опсин) и/или длинноволновый опсин (LW-опсин), и/или коротковолновый опсин (SW-опсин).
Аспект 26. Рекомбинантный вирусный вектор по аспекту 25, причем вирусный вектор представляет собой вектор аденоассоциированного вируса.
Аспект 27. Рекомбинантный вирусный вектор по аспекту 25 или аспекту 26, причем MW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 1; при этом LW-опсин содержит аминокислотную последовательность, идентичную аминокислотной последовательности по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 4, и при этом SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в одной из SEQ ID NO: 5-7.
Аспект 28. Рекомбинантный вирусный вектор по любому из аспектов 25-27, в котором нуклеотидная последовательность функционально связана с промотором.
Аспект 29. Рекомбинантный вирусный вектор по аспекту 28, в котором промотор представляет собой промотор синапсина, промотор CAG, промотор CMV, промотор grm6, промотор Pleiades, промотор ChAT, промотор V-glut, промотор GAD, промотор PV, промотор соматостатина (SST), промотор нейропептида Y (NPY), промотор VIP, промотор чувствительного к красному свету конопсина, промотор родопсина, промотор родопсинкиназы, промотор гена вителлиформной макулярной дистрофии 2 (VMD2) или промотор гена межфоторецепторного ретинол-связывающего белка (IRBP).
Аспект 30. Рекомбинантный вирусный вектор по любому из аспектов 25-29, в котором рекомбинантный вирусный вектор представляет собой рекомбинантный вектор AAV, причем рекомбинантный вектор AAV содержит нуклеотидную последовательность, кодирующую вариантный полипептид капсида, который придает повышенную инфекционность по отношению к клеткам сетчатки и/или придает повышенную способность пересекать внутреннюю ограничивающую мембрану по сравнению с AAV капсидом дикого типа.
Аспект 31. Фармацевтическая композиция, содержащая:
a) рекомбинантный вирусный вектор по любому из аспектов 25-30; и
b) фармацевтически приемлемое вспомогательное вещество.
Аспект 32. Способ восстановления или улучшения зрительной функции у индивидуума, причем способ включает введение индивидууму рекомбинантного вирусного вектора по любому из аспектов 25-30 или фармацевтической композиции по аспекту 31, при этом указанное введение обеспечивает экспрессию MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки у индивидуума и восстановление, или улучшение зрительной функции.
Аспект 33. Химерный SW-опсин, содержащий внутриклеточные области SW-опсина мыши, содержащего аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 6 и содержащий трансмембранные области SW-опсина человека, содержащего аминокислотную последовательность, идентичную по меньшей мере на 87%, по меньшей мере на 90%, по меньшей мере на 95%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% аминокислотной последовательности, представленной в SEQ ID NO: 5.
Аспект 34. Химерный SW-опсин по аспекту 33, содержащий аминокислотную последовательность, идентичную по меньшей мере на 90% аминокислотной последовательности, представленной в SEQ ID NO: 7.
Аспект 35. Рекомбинантный вектор экспрессии, содержащий нуклеотидную последовательность, кодирующую химерный SW-опсин по аспекту 33 или аспекту 34.
Аспект 36. Композиция, содержащая:
а) рекомбинантный вектор экспрессии по аспекту 35; и
b) фармацевтически приемлемое вспомогательное вещество.
Аспект 37. Композиция, содержащая один или более рекомбинантных векторов нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем, когда указанные одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта, указанный субъект может различать между изображением, содержащим вертикальную линию, и изображением, содержащим горизонтальную линию, в анализе распознавания пространственного паттерна.
Аспект 38. Композиция, содержащая один или более векторов рекомбинантной нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем в случае, когда указанные одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта, указанный субъект может различать между изображением, содержащим статическую линию, и изображением, содержащим движущуюся линию, в анализе распознавания пространственного паттерна.
Аспект 39. Композиция, содержащая один или более векторов рекомбинантной нуклеиновой кислоты, содержащих одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем в случае, когда указанная одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта, указанный субъект может различать между мигающим светом и постоянным светом в анализе временного светового паттерна.
Аспект 40. Композиция, содержащая один или более векторов рекомбинантной нуклеиновой кислоты, содержащей одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем в случае, если указанная одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта, указанный субъект может распознавать изображение при интенсивности света от около 10-4 Вт/см2 до около 10 Вт/см2 в анализе распознавания изображения.
Аспект 41. Композиция, содержащая один или более векторов рекомбинантной нуклеиновой кислоты, содержащей одну или более нуклеотидных последовательностей, кодирующих один или более конопсинов, причем в случае, когда указанная одна или более нуклеотидных последовательностей экспрессируются в глазу нуждающегося в этом субъекта, указанный субъект может различать между областью с белым светом и областью без белого света в анализе избегания света.
Аспект 42. Композиция по любому из аспектов 37-41, в котором один или более конопсинов выбраны из группы, состоящей из: а) MW-опсина, содержащего аминокислотную последовательность, идентичную по меньшей мере на 85% аминокислотной последовательности, представленной в SEQ ID NO: 1; b) LW-опсина, содержащего аминокислотную последовательность, идентичную по меньшей мере на 85% аминокислотной последовательности, представленной в SEQ ID NO: 4; c) SW-опсина, содержащего аминокислотную последовательность, идентичную по меньшей мере на 85% аминокислотной последовательности, представленной в SEQ ID NO: 5; и d) химерного SW-опсина, содержащего: i) внутриклеточные области SW-опсина мыши, содержащего аминокислотную последовательность, идентичную по меньшей мере на 87% аминокислотной последовательности, представленной в SEQ ID NO: 6; и ii) трансмембранные области SW-опсина человека, содержащего аминокислотную последовательность, идентичную по меньшей мере на 87% аминокислотной последовательности, представленной в SEQ ID NO: 5.
Аспект 43. Композиция по любому из аспектов 37-41, в котором один или более рекомбинантных векторов нуклеиновой кислоты содержат одну или более нуклеотидных последовательностей, кодирующих 2 разных конопсина.
Аспект 44. Композиция по любому из аспектов 37-41, в котором один или более рекомбинантных векторов нуклеиновой кислоты содержат одну или более нуклеотидных последовательностей, кодирующих 3 разных конопсина.
Аспект 45. Композиция по любому из аспектов 37-44, в котором один или более рекомбинантных векторов нуклеиновой кислоты представляют собой аденоассоциированный вирусный вектор, лентивирусный вектор, вектор вируса простого герпеса или ретровирусный вектор.
Аспект 46. Композиция по любому из аспектов 37-44, в котором один или более рекомбинантных векторов нуклеиновой кислоты представляют собой рекомбинантные аденоассоциированные вирусные векторы.
Аспект 47. Композиция по аспекту 46, в котором рекомбинантный вектор AAV содержит нуклеотидную последовательность, кодирующую вариантный полипептид капсида, который придает повышенную инфекционность по отношению к клеткам сетчатки и/или придает повышенную способность пересекать внутреннюю ограничивающую мембрану по сравнению с капсидом AAV дикого типа.
Аспект 48. Композиция по любому из аспектов 37-47, в котором один или более нуклеотидных последовательностей функционально связаны с промотором.
Аспект 49. Композиция по аспекту 48, в котором промотор представляет собой промотор синапсина, промотор CAG, промотор CMV, промотор grm6, промотор Pleiades, промотор ChAT, промотор V-glut, промотор GAD, промотор PV, промотор соматостатина (SST), нейропептидный Y (NPY) промотор, промотор VIP , промотор чувствительного к красному свету конопсина, промотор родопсина, промотор родопсинкиназы, промотор гена вителлиформной макулярной дистрофии 2 (VMD2) или промотор гена межфоторецепторного ретинол-связывающего белка (IRBP).
Аспект 50. Композиция по любому из аспектов 37-49, в котором у субъекта имеется глазное заболевание, выбранное из пигментного ретинита, макулярной дегенерации, ретиношизиса, врожденного амавроза Лебера и диабетической ретинопатии.
Аспект 51. Композиция по любому из аспектов 37-49, в котором у субъекта имело место отслоение сетчатки или потеря фоторецептора вследствие травмы или повреждения головы.
Аспект 52. Композиция по любому из аспектов 37-51, в котором композиция содержит фармацевтически приемлемое вспомогательное вещество.
Аспект 53. Композиция по аспекту 52, в котором фармацевтически приемлемое вспомогательное вещество содержит физиологический раствор.
Аспект 54. Композиция по любому из аспектов 37-53, в котором композиция является стерильной.
Примеры
Следующие примеры приведены для того, чтобы предоставить специалистам в данной области техники полное раскрытие и описание того, как создать и использовать настоящее изобретение, и не предназначены для ограничения объема того, что изобретатели считают своим изобретением, и приведенные ниже эксперименты не являются всеми или единственными проведенными экспериментами. Были предприняты усилия для обеспечения точности в отношении используемых чисел (например, количества, температуры и т.д.), но следует учитывать некоторые экспериментальные ошибки и отклонения. Если не указано иное, части представляют собой части по массе, молекулярная масса представляет собой средневесовую молекулярную массу, температура приведена в градусах Цельсия, а давление равно атмосферному или близко к нему. Можно использовать стандартные сокращения, например, п.о., пара(ы) оснований; т.п.о., тысяча(и) пар оснований; пл, пиколитр(ы); с, секунда(ы); мин, минута(ы); ч, час(ы); аа, аминокислота(ы); т.п.о., тысяча(и) пар оснований; п.о., пара(ы) оснований; нт, нуклеотид(ы); в/м внутримышечно; в/б внутрибрюшинно; п/к подкожно; и тому подобное.
Пример 1. Влияние экспрессии MW-опсина в клетках сетчатки in vitro и in vivo
Наследственные и связанные с возрастом дегенеративные заболевания сетчатки вызывают прогрессирующую потерю фоторецепторов палочек и колбочек, что приводит к полной слепоте. Несмотря на потерю чувствительных к свету клеток, необходимых для зрения, нижестоящие нейроны внутренней сетчатки выживают в функциональном состоянии, обеспечивая цель для оптогенетической терапии. На сегодняшний день, оптогенетические подходы столкнулись с двумя основными ограничениями: очень низкая чувствительность к свету у микробных опсинов и очень медленная кинетика у опсинов сетчатки. Данные, представленные ниже, показывают, что конопсин сред длины волны позвоночных (MW-опсин) преодолевает эти ограничения и поддерживает структурированное зрение при слабом освещении. Экспрессия MW-опсина в ганглиозных клетках сетчатки (RGC) слепых мышей rd1 вводит переходный световой отклик ON, который является высокочувствительным к свету и имеет быструю кинетику. MW-опсин восстанавливает фото-избегание при той же светочувствительности, что и у диких животных, на три порядка ниже уровня, необходимого для микробных опсинов, и на уровне родопсина. MW-опсин позволяет животным rd1 различать как разные временные световые паттерны, так и разные пространственные световые паттерны, даже когда пространственные паттерны находятся в движении. Напротив, животные rd1 с родопсином в RGC не способны ни к временной, ни к пространственной дискриминации. Поразительно, что световой отклик MW-опсина адаптируется к окружающему свету в ~1000-кратном диапазоне. Таким образом, MW-опсин сочетает в себе скорость, чувствительность и адаптацию для восстановления регулируемого узорного зрения при реалистичной интенсивности света. LW-опсин и SW-опсин также поддерживают различение зрения между статическими визуальными паттернами, предполагая, что конопсины могут индивидуально восстанавливать естественное монохроматическое зрение и что, в сочетании, они могут восстанавливать цветовое зрение.
Материалы и способы
Животные и AAV
Эксперименты на мышах проводились с согласия Комитета по уходу и использованию животных при Калифорнийском университете. Мыши wt (C57BL/6J) и мыши rd1 (C3H) были приобретены в лаборатории Джексона и помещены в 12-часовой цикл свет/темнота с пищей и водой ad libitum. кДНК, кодирующая средневолновый конопсин или родопсин позвоночных, была связана с геном желтого флуоресцентного белка (YFP) на С-конце и вставлена в установленную вирусную кассету под контролем промотора синапсина человека (hsyn-1). Ген и промотор были фланкированы инвертированными концевыми повторными доменами, стабилизированы сигнальной последовательностью полиаденилирования (polyA) с посттранскрипционным регуляторным элементом (WPRE) гепатита сурка и упакованы в капсид AAV 2/2-4YF. Титр AAV определяли с помощью КПЦР по отношению к стандарту инвертированных повторных доменов и, как сообщалось, содержали 1010–1012 вирусных геномов. AAV получали, как описано ранее 15. Вектор доставлялся в объеме 2 мкл в стекловидное тело глаза мыши rd1 с помощью микроинъекции с использованием тупого шприца Гамильтона 32-го калибра, хотя разрез выполнялся позади ora serrata с помощью острой иглы 30-го калибра. Инъекции rAAV проводили при p30 – p60, а эксперименты in vivo и in vitro - при p90 – p160. Мышей анестезировали в/б кетамином (72 мг/кг) и ксилазином (64 мг/кг). Глаза были анестезированы пропаракаином (0,5%), а зрачки были расширены фенилэфрином (2,5%) и тропикамидом (1%).
Электрофизиология и светостимуляция
Регистрацию клеток HEK проводили, как было описано ранее 15,51,52. Вкратце, клетки фиксировали в режиме целых клеток в растворе с высоким содержанием внешнего калия (50 мМ) и выдерживали при VH = -80 мВ, чтобы обеспечить внутреннюю движущую силу для калия. 5-10 с импульсы света подавались с низкой интенсивностью (1 мВт/см-2) при 535 нм (для MW-опсина) или 500 нм (для родопсина).
Записи MEA выполняли на мышах wt (C57BL/6J), и у необработанных и обработанных мышах rd1 при> p90, через 6-10 недель после инъекции AAV вырезали экспериментальную сетчатку из глаза при тусклом красном свете, устанавливали на мембраны клеток 4 мкм и помещали в инкубатор (35°С) в течение 30 мин и перфузировали экзогенным хромофором 9-цис ретиналя. Ткань сетчатки помещали стороной ганглиозных клеток вниз 53 в камеру записи (pMEA 100/30iR-Tpr; многоканальные системы) 60-канальной системы MEA с постоянной перфузией носителя записи Эймса (32°C). Вес сетки Multi Channel Systems (Scientific Instruments - Slice grids) был помещен на сетчатку для предотвращения движения, и вакуум был приложен к сетчатке с помощью насоса (перфорированная система MEA1060 с CVP; Multi Channel Systems), улучшая контакт электрода с тканью и обеспечивая согласованное отношение сигнал/шум на сетчатке. Кроме того, сухой кристалл экзогенного хромофора 9-цис-ретиналя растворяли в мкл 100% этаноле в темноте. Растворенный ретиналь затем добавляли к 100 мкл матригеля на льду и добавляли в верхнюю часть сетки, чуть выше сетчатки, чтобы обеспечить непрерывное поступление хромофора. Кроме того, 9-цис-ретиналь растворяли в растворе для записи и постоянно перфузировали в камеру для записи. Более подробная информация о способах MEA ранее подробно описана в Gaub. et al. (2015)15. Освещение in vitro осуществлялось ртутной дуговой лампой мощностью 300 Вт (DG-4; Sutter Instruments) с полосовым фильтром 535/50 нм для MW-опсина или полосовым фильтром 510/89 нм для родопсина. Интенсивность света контролировали путем изменения рабочего цикла источника света или с использованием фильтров нейтральной плотности и варьировалась от 0,038 мкВт см-2 до 38,2 мВт/см2. Относительные сравнения с интенсивностью естественного света были получены в различных средах с использованием прямого измерения света с помощью измерителя мощности (Thorlabs). Спектральная составляющая белого света измерялась с помощью CCD спектрометра с программным обеспечением для анализа оптического спектра с преобразованием Фурье (Thorlabs).
MEA Сбор и анализ данных
Активность сетчатки на MEA отбирали при 25 кГц, фильтровали между 100 и 2000 Гц и регистрировали с использованием программного обеспечения MC_rack (многоканальные системы). Следы напряжения были преобразованы в последовательности пичков в автономном режиме, и пики, записанные на каждом электроде, были отсортированы в отдельные единицы, которые определены как «ячейки», посредством анализа основных компонентов с использованием автономного сортировщика (Plexon-64bit), где каждый электрод обычно идентифицирует 1-3 ячейки. Одиночные спайк-кластеры были экспортированы в MATLAB (MathWorks) и были проанализированы и графически представлены с помощью специального программного обеспечения. Все частоты пульсаций были извлечены из следов, усредненных за 3-10 циклов светового отклика, если не указано иное, подробности которых указаны в условных обозначениях на фигурах. Отклики между клетками и сетчаткой были нормализованы с использованием индекса светового отклика (LRI), взятого у Tochitsky, I., et al. (2014) 37 и Gaub et al. (2014) 47 (LRI =(пиковая частота пульсаций на свету - средняя скорость отклика в темноте)/пиковая частота пульсаций на свету + средняя частота пульсаций в темноте). В экспериментах, в которых изменялись условия в сетчатке (светочувствительность, чувствительность к свету и темноте и зависимость отклика от длительности вспышки), отклики были нормализованы по отношению к пику с наибольшим откликом от базовой линии, и каналы отслеживались по всем параметрам записи. Подгонка всех кривых и кинетический анализ проводились в Clampfit 10.6 (Molecular Devices). Клетки были определены как «отвечающие», если LRI удовлетворял условию LRI> 0,1 или LRI <-0,1. Ширина отклика на половине максимума пика от базовой линии была определена с помощью специального программного обеспечения для анализа MATLAB (MathWorks), которое интерполировало следы отдельных ячеек и применялось сглаживание до определения FWHM. Отношения интенсивность-отклик соответствовали одному Больцмановскому распределению и нормировались для соответствия между 0 и 1.
Сравнение светочувствительности оптогенетических зондов
Естественная чувствительность зрения человека охватывает широкий диапазон, от скотопической (тусклый 104 - 1011 фотонов −2 с−1) до фотопической полосы (яркий 1010 – 1017 фотонов см−2 с−1), приводя к восприятию в условиях динамического освещения. Чтобы связать чувствительность MW-опсина с чувствительностью других оптогенетических систем и нормальным зрением, были проведены эксперименты, в которых измеряли интенсивность естественного света при различных внешних и внутренних условиях с использованием портативного измерителя мощности (Thorlabs), сравнивая их с экспериментальными парадигмами и порогами чувствительности света (наименьшие измеримые световые реакции), описанными в литературе с использованием монохроматических длин волн света при максимальных функциональных максимумах или около них для эксплантов сетчатки, полученных от мышей rd1, которым оптогенетический зонд был доставлен посредством трансфекции AAV (фиг. 7).
Электрофизиология и световая стимуляция для записи мозга in vivo
Записи in vivo выполняли, как описано ранее Veit et. al. (2017)58. Мышей анестезировали изофлураном (концентрация пара 2,5%). Скальп был удален, фасция втянута, а череп слегка протравлен иглой 27 калибра. После нанесения Vetbond на поверхность черепа, специальная пластина из нержавеющей стали была прикреплена к черепу с помощью зубного цемента (Metabond). Мышам позволяли восстанавливаться после операции в течение не менее 2 д. Затем мышей приучали в течение 2–5 д. к фиксации головы на свободно вращающейся круговой беговой дорожке. В день записи мышей ненадолго анестезировали изофлураном (2%), череп над V1 истончен и небольшая (<250 мкм) краниотомия была открыта по первичной зрительной зоне коры головного мозга тонкой иглой. 16-канальная линейная электродная матрица с интервалом 25 микрон (NeuroNexus, A1x16-5mm-25-177-A16) вводилась в мозг с использованием микроманипулятора (Sensapex) и стереомикроскопа (Leica). Электрическая активность усиливалась и оцифровывалась при частоте 30 кГц (Spike Gadgets) и сохранялась на жестком диске компьютера. Глубина коры каждого электрического контакта определялась путем обнуления нижнего контакта с поверхностью мозга. Электрод вставляли близко к перпендикуляру к поверхности мозга.
Визуальные стимулы генерировались с помощью Psychophysics Toolbox59, работающего на Apple Mac Mini, и были представлены на 23-дюймовом ЖК-дисплее Eizo FORIS FS2333 с гамма-коррекцией и частотой обновления 60 Гц. Монитор был расположен в 15 см от правого глаза мыши, охватывая примерно 108 на 61 градус угла обзора. Мышей адаптировали к темноте за 7-10 мин перед каждым блоком записей. Были использованы две разные парадигмы стимуляции: 1) Контрастность: Мышам показывали полноэкранные вспышки 500 мс при 0,5 Гц четырех разных уровнях яркости (15, 25, 50 и 100% от максимальной яркости), которые повторялись 10 раз в разных случайных порядках. 2) Мерцание: Мышам показывали 20 500 мс полноэкранных вспышек (максимальная яркость 116 мкВт см-2) при 0,0167 Гц (одна в мину) или 100 вспышек при 0,5, 1, 2 и 4 Гц в отдельных блоках.
In vivo кортикальная запись данных, сбор и анализ
Пиковую активность извлекали путем фильтрации необработанного сигнала между 800 и 7000 Гц. Обнаружение всплеска проводилось с использованием пакета UltraMega Sort60. Обнаруженные пики сигналов были отсортированы с использованием пакета MClust (http://redishlab.neuroscience.umn.edu/MClust/MClust.html). Формы сигналов сначала автоматически группировались с помощью KlustaKwik, а затем вручную корректировались для соответствия критериям для дальнейшего анализа. Единицы с более чем 2% их отдельных форм волны, нарушающих рефрактерный период 2 мс, были классифицированы как мульти-единицы. Глубина каждого блока была назначена на основе вычисленной глубины электрода на матрице, которая показала свою самую большую амплитуду отсортированного сигнала. Частоты пульсаций рассчитывали путем подсчета пиков в двухсекундном окне, начинающемся через 250 мс после появления визуального стимула для фиг. 20b, и в окне 5 с, начинающемся непосредственно после появления стимула для фиг. 21c. Значения для гистограмм перистимульного времени (PSTH) были сгенерированы путем разбивки отклика на скачки либо на 20 мс (фиг. 19), либо на 50 мс (фиг. 20), либо на 25 мс (фиг. 21), и сглаживания полученных значений с помощью фильтра скользящих средних. Для фиг. 21 амплитуда модуляции была рассчитана по усредненным пробным откликам пика, которые были сгруппированы через 25 мс в окне 2, 1, 0,5 или 0,25 с для мерцания 0,5, 1, 2 и 4 Гц соответственно. Соответствующие базовые амплитуды модуляции были получены из испытания, усредняющего такое же количество окон одинаковой длины до начала первого визуального стимула (в течение периода адаптации темноты). Локальные потенциалы поля были извлечены с помощью низкочастотной фильтрации необработанного сигнала, дискретизированного при 30 кГц, ниже 200 Гц и последующей понижающей дискретизации до 1 кГц.
Статистика
Чтобы оценить статистическую значимость записей МЭА, применяли непараметрические двусторонние U-критерии Манна-Уитни. Для наученного поведения избегания темноты и наученного поведения распознавания паттернов значимость определялась двумя способами. (1) Значимость поведенческих характеристик была рассчитана с использованием двусторонних непарных критериев Стьюдента с коррекцией Бонферрони, когда это применимо. Значение было также определено путем расчета доли успешных выступлений (2). Успех был определен как большее, чем сумма среднего значения в контрольной группе и одного S.D, а неудача - это любое значение, которое не достигло этого критерия. Коэффициенты успеха были затем рассчитаны для каждого условия. Для определения значимости различий между условиями была построена таблица попарных сопряженностей, и первоначально был проведен двусторонний тест хи-квадрат Пирсона. Чтобы исправить условия с малым n, был также проведен точный односторонний тест Фишера. Фиг. 11 (таблица 1).
Подготовка тканей и иммуногистохимия
Мышей> через 4-6 недель после лечения AAV2/2-hsyn-MW-конопсин-YFP умерщвляли, глаза фиксировали в 4% параформальдегиде (Ted Pella) (30 мин), сетчатки удаляли и тщательно промывали с использованием PBS и монтировали на плоской поверхности на предметных стеклах с использованием среды Vectashield (Vector Laboratories), пропитанной DAPI (окрашивание ядер клеток - синий). Для срезов сетчатки целые крепления были встроены в агарозу (Sigma) и разрезаны поперечно с использованием вибратома (Leica Microsystems) со сред скоростью, максимальной вибрацией и толщиной 180 мкм. Ткани сетчатки, используемые для иммуногистохимии при криосекции сетчатки или тотальных препаратах, обрабатывали и исследовали с помощью конфокальной микроскопии (Leica TCS SP5; Leica Microsystems).
Пассивное избегание - тест в открытом поле
Тест на открытом поле был выполнен, как описано ранее 16,47. Вкратце, двухместная (светлая и темная) челночная коробка (Colbourn Instruments) позволяет мыши свободно перемещаться через небольшое отверстие, соединяющее два отсека. Светлый отсек освещался ЖК-панелью над отсеком. Белый свет, а также длины волн 535 нм и 460 нм использовали при интенсивности света ~100 мкВт см-2 (белый свет) и 0,5-25 мкВт см-2 (синий и зеленый свет), которые были равномерно распределены по полу. День 1 - мышей переносили в коробку для испытаний и им давали привыкать к новой среде со своими однопометниками в течение 45 мин. Затем мышей возвращали в их домашнюю клетку и затем тестировали индивидуально. День 2 - Мышей помещали в светлый отсек и давали максимум 3 мин, чтобы обнаружить, что есть второй отсек. 15-минное испытание начиналось, когда они вошли в темный отсек, и время, проведенное на свету, было записано. Мыши, которые пересекли отверстие только один раз и оставались в темном отсеке в течение всего времени, были дисквалифицированы. Для экспериментов по адаптации мышей предварительно подвергали воздействию белого света в течение 1 часа (1 мВт/см-2) или условий темноты, а затем сразу же проводили тест в открытом поле. Движения животных отслеживались с помощью ИК-датчиков на челночной коробке. Время, проведенное с обеих сторон, было записано и проанализировано с использованием программ Graphic State и RT Graphic State (Colbourn Instruments).
Визуально настроенная парадигма формирования страха
Эксперименты по формированию страха проводились с использованием ударных камер Colbourn - камера Colbourn Habitest с испытательной клеткой (Coulbourn Instruments, PA) со светодиодным экраном, прикрепленным к потолку. В 1-й день животных доставляли в комнату для испытаний в домашних клетках, а затем индивидуально акклиматизировали в течение 30 мин для очистки ударных камер Colbourn. На 2-3-й день животных подвергали парному или непарному формированию страха в легкой форме, состоящему из 5-мин привыкания к камере (темнота) с последующими тремя испытаниями с ударом током при 0,7 мА в течение 15 мин. Для парных испытаний переход от статического или мигающего (2 Гц) света на ЖК-дисплее совпал с коротким ударом током по ноге с интервалом между скачками 2 с (в течение 10 с). Для непарных испытаний животные также получали удары током, но не зависели от перехода стимула. Эти короткие, слабые удары током обеспечили минимальные неприятные стимулы, чтобы создать память страха, связанную с узорным светом. На 4-й день настил коробки был заменен пластиком вместо ударной решетки. Мышей приучали к камере в течение 5 мин и подвергали тому же протоколу светостимуляции, что и на 2 и 3 д., но без удара током. Замораживающее поведение в ожидании удара током регистрировалось программным обеспечением Colbourn FreezeFrame и нормализовалось к поведению движения, полученному до стимуляции. Затем результаты сравнивали между парными и непарными когортами, чтобы определить, был ли отклик страха обусловлен переходом стимула.
Модифицированный протокол активного избегания
Протоколы избегания выполнялись с использованием челночной коробки Colbourn (H10-11M-SC) Colbourn Habitest Isolation Cubicle (H10-24) и программного обеспечения Graphic State и Graphic State RT (Colbourn Instruments, PA). В 1-й день животные акклиматизировались в затемненной процедурной комнате в течение 30 мин в своих домашних клетках с последующей индивидуальной адаптацией к затемненной челночной коробке до тех пор, пока животные не перестали бояться и проводить примерно одинаковое количество времени с каждой стороны челночной коробки (исследовательское поведение). На 2-3-й день экраны iPad были установлены в стене клеточного челнока и отображали два разных изображения одинаковой формы, размера и интенсивности света. Каждый забег начинался, когда животное перемещалось на другую сторону челночной коробки от того места, где оно было размещено. Каждый прогон длился 15 мин. Отвращающая сторона изображения была спарена с ударом током ноги 0,7 мА с интервалами в 5 секунд, пока животное не вернулось в «безопасную» сторону. Любое животное, остававшееся на аверсивной стороне более 60 секунд, было удалено из клетки, и этот ход был отброшен. На 4-й день световые паттерны поменялись местами (таким образом, отвращающий экран находился там, где раньше была «безопасная» сторона), чтобы избежать смещения местоположения, а не паттерна. Кроме того, настил клетки заменен на пластиковый вместо ударной решетки. Это гарантирует, что единственная связь с тренировочным днем - это световые стимулы. Опять же, животные бегали в течение 15 мин, и время, проведенное на каждой стороне, регистрировали. В экспериментах по адаптации к свету применялся тот же протокол, за исключением того, что на 4-й день фазе воспоминания предшествовала либо светлая (белая лампочка 65 Вт), либо темная фаза адаптации в течение одного часа. Расчеты оптического угла визуальной дискриминации проводились с использованием параметров поведенческой челночной клетки (15,24 × 36 см), расстояния от точки принятия решения (делителя), центрального положения ЖК-панели (18,85 см) и параметров паттерна стимула (расстояние между параллельными линиями 1 - 6 см) с использованием уравнения оптического (физического) угла. Угол обзора = V = 2tan-1((D/2)/(L)) = 18 град = 0,33 - 0,49 рад. Циклы на градус = 1/V ~0,056 ц/град. Это примерно в 9 раз ниже, чем у визуально интактных мышей wt (~0,3-0,5 ц/град), как указано в других исследованиях 39,54,55,56.
Для исследовательского анализа поведения два объекта были помещены в поле размером 50 см × 50 см. Животных помещали в пустую коробку и позволяли свободно исследовать ее в течение 10 мин. На следующий день два новых объекта были помещены в коробку, и животные были снова размещены вдоль стены коробки и им было позволено свободно исследовать ее в течение 10 мин, пока арена непрерывно снималась. Используя технологию Noldus Ethosvision XT v13.5, видео анализировали на предмет задержки, чтобы достичь и исследовать каждый объект, скорости перемещения (см/с) и пройденного расстояния (см).
Результаты
Характеристика MW-опсина в клетках HEK293
Недавние исследования показали, что родопсин позвоночных, обнаруженный в наружных сегментах палочек, может быть эктопически использован для контроля передачи сигналов Gi/o в культивируемых клетках при низкой интенсивности света 25, но снижается при повторной стимуляции и имеет медленную дезактивацию 24,26. Медленная кинетика также наблюдается, когда родопсин экспрессируется в ON-биполярных клетках слепой сетчатки 14,15, что вызывает обеспокоенность тем, что он может не поддерживать видение естественных сцен из-за движения наблюдателя и окружающих объектов. Был задан вопрос, будет ли другой опсин позвоночных обладать высокой чувствительностью родопсина, но иметь более быструю кинетику. Меланопсин и экстраретинальные опсины были измерены за пределами фоторецепторных клеток в различных типах клеток, в том числе в нефоторецепторных клетках сетчатки, и все они оказались медленными или медленнее, чем родопсин 14-16,27-29. Опсины из клеток фоторецепторов колбочек млекопитающих были выбраны потому, что они дезактивируются быстрее в колбочках, чем родопсин в палочках 30. Среди опсинов колбочек был выбран MW-опсин, который действует в центре видимого спектра. MW-опсин или родопсин экспрессировался в клетках HEK293T с GIRK1 (F137S), версией калиевого канала, связанного с внутренним выпрямителем G, который образует гомотетрамер, который активируется Gβγ после активации связанного с Gαi рецептора 31 (фиг. 1). В присутствии 9-цис-ретиналя (функционально стабильного аналога природного хромофора 11-цис-ретиналя) клетки, экспрессирующие MW-опсин и родопсин, демонстрировали большие внутренние фототоки при отрицательных потенциалах удержания при высоком внешнем уровне калия, которые были вызваны вспышками света низкой интенсивности (1 мВт см-2) при 535 нм (для MW-опсина) или 500 нм (для родопсина) (фиг. 1a,b). После освещения ток, вызванный MW-опсином, затухал в ~8 раз быстрее, чем ток, вызываемый родопсином, и восстанавливался более полно, обеспечивая воспроизводимые отклики при повторных вспышках освещения (фиг. 1a,c), как показано ранее в гетерологичных клетках для конопсинов короткой и длинной волны 24. Это предполагает, что более высокая скорость может быть свойственной передаче сигналов MW-опсина, а не специализацией колбочек. MW-опсин затем тестировали в не фоторецепторных ретинальных нейронах.
Фиг. 1а-1c. Активация MW-опсином и родопсином каналов GIRK в клетках HEK293. (a, b). Репрезентативные следы активации каналов гомотетрамера GIRK (F137S) путем фотостимуляции родопсина (a) или MW-опсина (b), измеренные в слое целых клеток в 50 мМ [K+]вн при VH = -80 мВ в отклик на импульсы света низкой интенсивности (1 мВт см-2) при 535 нм (для MW-опсина) или 500 нм (для родопсина). (c) Затухание фотоотклика (Tau OFF) для родопсина (синий) и MW-опсина (зеленый). Значения средние + СОС; n = 6 (Rho), 8 (MW-опсин) клеток.
MW-опсин восстанавливается быстрые и вызывает чувствительные световые реакции в слепой сетчатке
MW-опсин был протестирован на сетчатке мыши rd1, которая имеет мутацию в гене PDE-6-β, что приводит к прогрессирующей потере клеток фоторецепторов палочек и колбочек. MW-опсин под контролем синапсинового промотора человека (hSyn-1) с желтой флуоресцентной (YFP) C-концевой меткой для отслеживания экспрессии был упакован в AAV2/2 (4YF) и инъецирован интравитреально в постнатальный день 45 (фиг. 2а, b). Сетчатки были выделены через 4-8 нед. Было обнаружено, что экспрессия является панретинальной с уровнем трансфекции 45% + 19% (SD), ограниченной слоем RGC и локализованной в соме и дендритах как ON-, так и OFF-RGC (фиг. 2c, d и 14), четко определенный профиль экспрессии, согласуется с ранее показанным нацеливанием 32 и сходен с экспрессией родопсина при идентичных параметрах (фиг. 15). Сетчатки были установлены на многоэлектродной матрице (МЭА) со слоем RGC, контактирующим с электродами, для проверки активности, вызванной светом. Из-за полной дегенерации фоторецепторов у животных > 3 месяцев 33 не было выявлено вызванного светом отклика в сетчатке контрольных однопометных особей rd1 (фиг. 2e), за исключением нескольких RGC, которые демонстрировали медленные отклики, характерные для собственно фоточувствительных RGC 57. Напротив, сетчатки от животных, которым инъецировали MW-опсин, кодирующий AAV, демонстрировали сильное вызванное светом увеличение потенциального воздействия, состоящее из большого быстрого переходного компонента и небольшого (размером ~ 30%) медленного компонента (фиг. 2f, g, 3a, 16 и 17). Световые реакции снижались при повторных приступах световой стимуляции, как и следовало ожидать после удаления пигментного эпителия сетчатки, источника 11-цис. Сокращение было уменьшено добавлением 9-цис-ретиналя (стабильного аналога 11-цис-ретиналя) к регистрирующему раствору (фиг. 2g).
Фиг. 2a-2g. Экспрессия и функция MW-опсина в RGC сетчатки мыши rd1. (а). Вирусная ДНК-экспрессионная кассета. MW-опсин с YFP (зеленый) под контролем промотора hSyn-1, фланкированный доменами инвертированного концевого повтора (ITR), стабилизированный сигнальной последовательностью полиаденилирования (полиА) и посттранскрипционным регуляторным элементом гепатита сурка (WPRE). (b) Схема дегенерированной сетчатки мыши rd1 с выделенными целевыми RGC (зеленый). ONL: внешний ядерный слой. IPL: внутренний плексиформный слой. Фоторецепторная дегенерация обозначена светло-серым. (c,d) En face изображение плоского крепления (c) и поперечного среза (d) конфокальных изображений экспрессии MW-опсина сетчатки rd1 мыши через 4 недели после интравитреального введения AAV2/2-hSyn- MW-опсина-YFP. Изображения YFP, слитые с C-концом MW-опсина (зеленый), показывают пан-ретинальное распределение (c) в слое RGC по отношению к окрашиванию DAPI ядер (d, синий). Весы 60 мкм (с) и 20 мкм (d). (e,f) Записи MEA из неинъецированного контроля (e) и MW-опсина, экспрессирующего (f) rd1 сетчатки мыши. (Вверху) Растровый график с пичками для каждого RGC (e: n = 75 ячеек; g: n = 84 единицы). (Внизу) Гистограмма перистимульного времени (PSTH). Протокол световой стимуляции: 4 световых импульса длительностью 1 с (λ = 535 нм, зеленые полосы), разделенных темными интервалами 30 с. (g) Нормализованный индекс световой реакции (LRI) для сетчатки rd1 без (серый) и с экспрессией MW-опсина (зеленый) (серый: N = 3 сетчатки, n = 190 клеток; зеленый: N = 6 сетчатки, n = 273 клетки). LRI для 1-й и 5-й вспышки света без (светло-зеленый; N = 3 сетчатки, n = 106 клеток) и с (темно-зеленый; N = 3 сетчатки, n = 167 клеток) 9-цис ретиналем. Интенсивность света 3,38 мВт см-2. Длина волны: λ = 535 нм (MW-O), значения являются средними + СОС. Все клетки относятся к отсортированным единицам. Статистическую значимость оценивали с использованием U-критерия Манна-Уитни (* p <0,001).
Фиг. 14а-14b. MW-опсин экспрессируется в сетчатке мыши rd1. Конфокальные изображения плоского монтирования (а) и среза (b) MW-опсин-YFP в RGC сетчатке rd1 мыши через 4-6 недель после интравитреального введения AAV2/2-hSyn-MW-опсин-YFP. Флуоресценция YFP (зеленый) и окрашивание ядер DAPI (синий). INL = внутренний ядерный слой, RGC = слой ганглиозных клеток сетчатки. Масштаб 40 мкм (а) и 20 мкм (b).
Фиг. 15а-15b. Родопсин экспрессируется в сетчатке мыши rd1. Конфокальные изображения плоского монтирования (а) и среза (b) родопсина-YFP в RGC сетчатке rd1 мыши через 4-6 недель после интравитреального введения AAV2/2-hSyn-родопсин-YFP. Флуоресценция YFP (зеленый) и окрашивание ядер DAPI (синий). INL = внутренний ядерный слой, RGC = слой ганглиозных клеток сетчатки. Масштаб 40 мкм (а) и 20 мкм (b).
Фиг. 16а-16d. Эффективность трансдукции MW-опсина в сетчатке rd1. (а) Средний процент каналов, идентифицированных в сетчатке мышей rd1, экспрессирующих MW-опсин, которые показывают чувствительность к свету в записях МЭА. Светочувствительность, определяемая как Светочувствительный индекс (LRI)> 0,1, параметры которые установлены в Tochitsky et al. (2014)37, Gaub. et al (2014)47 и Berry et al. (2017)62. (LRI = пиковая частота пульсаций в темноте - средняя частота пульсаций в темноте/пиковая частота пульсаций в темноте + средняя частота пульсаций в темноте). (b) Средний нормализованный отклик по сетчатке). (a,b) N = 8 rd1 сетчаток, N = 5 wt сетчаток. (c) Средние значения взаимной корреляции в MW-опсине rd1 (n = 370 клеток, N = 3 сетчатки) и в диком типе (n = 237 клеток, N = 3 сетчатки). Взаимная корреляция всех светочувствительных единиц за период от 1 с до 2 с после светового импульса. (d) Распределение корреляционных значений для светочувствительных единиц в одной и той же сетчатке для MW-опсина (n = 370 клеток, N = 3 сетчатки) и wt сетчатке (n = 237 клеток, N = 3 сетчатки).
Фиг. 17a-17d. Характеристика медленного компонента светового отклика в сетчатке rd1, экспрессирующей MW-опсин. (a) Репрезентативная кривая среднего отклика популяции RGC для rd1, экспрессирующей MW-опсин (λ = 510 нм; длительность импульса 1 секунда; 5 вспышек, усредненных с интервалом 30 секунд), показывает быстрый переходный компонент и медленный компонент светового отклика (СОС в сером цвете). (b) Сравнение LRI быстрого переходного (зеленый) и медленного (стальной-серый) компонентов светового отклика и их соотношение (черный) быстрый/медленный) (n = 122 канала, N = 3 сетчатки). (c) Кинетика медленного компонента: время до пика (T. - пик) и постоянная времени распада (тау-распад). (d) LRI быстрого (зеленого) и медленного (стально-серого) компонентов в темных (слева) и светлых (справа) условиях.
Одним из потенциальных преимуществ опсинов сетчатки является их высокая чувствительность к свету в их нормальных клеточных средах. Родопсин и меланопсин остаются очень чувствительными при эктопической экспрессии 25, в том числе в сетчатке, как показано для родопсина в ON-BC и RGC и меланопсина в RGC 14-17. В соответствии с этим, MW-опсин в RGC в сетчатке мыши rd1 был высокочувствительным к свету до степени, неотличимой от родопсина (фиг. 3b, c). Эта чувствительность около в 1000 раз выше, чем у канального родопсина 8,13 или галородопсина 11,12, и находится в диапазоне нормальных интенсивностей внутреннего освещения. Фиг. 7. Несмотря на схожесть по чувствительности к родопсину, MW-опсин продемонстрировал кинетику: ~3,5-кратное ускорение нарастания и ~4-кратное ускорение до пика в начале светового импульса и ~7-кратное ускорение затухания после окончания светового потока импульс (фиг. 3d,e), приводящие к импульсному отклику длительностью 270 + 21 мс при половинной амплитуде, ~10 раз короче, чем длительность 2,61 + 0,21 с при половинной амплитуде импульсного отклика родопсина. Tau ON, время до пика и tau OFF незначительно изменялись с уменьшением интенсивности света, сохраняя преимущество в скорости перед родопсином (фиг. 8a-c) 14,15. Кинетика нарастания и затухания отклика в RGC сетчатки rd1, экспрессирующей MW-опсин, напоминала таковую у переходного ON-отклика RGC, наблюдаемого в wt сетчатке глаза, за исключением того, что первый имел более длительную латентность (фиг. 3e и 8d, e). Кинетика быстрого отклика и чувствительность MW-опсина позволили предположить, что он будет реагировать на короткие вспышки света. Действительно, импульсы освещения, короткие до 25 мс, по-прежнему вызывали отклики, которые достигали ~60% от максимального пикового отклика (фиг. 3f, g), аналогично тому, что наблюдается в wt сетчатки 34.
Контрастная чувствительность в удаленной сетчатке и в первичной зрительной зоне коры головного мозга была исследована in vivo путем измерения отклика на полные полутоновые шаги. В вырезанной сетчатке rd1, экспрессирующей MW-опсин, активность RGC изменялась в ответ на изменения яркости всего лишь на 25% (фиг. 18а, b), приближаясь, но не являясь эквивалентно контрастной чувствительности сетчатки дикого типа (фиг. 18с). В дополнительных экспериментах in vivo на животных rd1, экспрессирующих MW-опсин в RGC, эксперименты включали измерение единичных ответных реакций и визуально вызванных потенциалов через слои первичной зрительной зоне коры головного мозга у бодрствующих, свободно бегущих животных (фиг. 19) и наблюдение аналогичной контрастной чувствительности с использованием стандартного монитора компьютера (фиг. 20). Корковые реакции следовали за частотой вспышки, по крайней мере, до 4 Гц (фиг. 21). Чувствительность и кинетика световых реакций, передаваемых MW-опсином в RGC, позволяют предположить, что он может поддерживать зрительно-опосредованное поведение.
Фиг. 3a-3g. Световой отклик в выделенной сетчатке мыши rd1 с MW-опсином в RGC. (a) (Вверху) Средний отклик на 1-секундную вспышку света популяции RGC, экспрессирующей MW-опсин (зеленый) или родопсин (синий) в RGC сетчатки мыши rd1. (Внизу) График растрового среднего отклика RGC сетчатки мыши rd1 на 5 вспышек света длительностью 1 с при 535 нм для MW-опсина (n = 88 клеток) и 510 нм для родопсина (n = 54 клеток), экспрессирующего в RGC. (b, c) Светочувствительность для MW-опсина (N = 2 сетчатки, n = 127 клеток) и родопсина (N = 2 сетчатки, n = 95 клеток) в RGC сетчатки мыши rd1. Пиковая частота пульсаций нормализуется до максимума при максимальной интенсивности. (d, e) Время реакции на свет. Средние значения популяции прослеживаются во времени от появления света до максимального возбуждения (время до пика: 355 + 21 мс), экспоненциальными подгонками для фазы возбуждения (Tau ON: 112 + 25 мс) и затухания (Tau OFF: 260 + 31 мс) и полной шириной на половине максимума (FWHM: 183 + 85 мс) (e) для MW-опсина (d; e, зеленый; N = 3 сетчатки, n = 95 клеток) и родопсина (e, синий; N = 2 сетчатки, n = 67 клетки). (f, g) Зависимость светового отклика MW-опсина от длительности вспышки. (f) Репрезентативный световой отклик сетчатки (n = 117 клеток): средняя частота пульсаций среди популяции (вверху) и растровый график единичных откликов (внизу). (h) Нормализованные пиковые отклики для различной продолжительности стимуляции (N = 2 сетчатки, n = 183 клетки). Интенсивность света 3,82 × 10-1 мВт см-2, если не указано иное, длина волны: λ = 535 нм (MW-опсин) или 510 нм (родопсин). N = количество сетчатки, n = количество клеток/единиц. Все клетки относятся к отсортированным единицам. Значения означают + СОС. Статистическую значимость оценивали с использованием U-критерия Манна-Уитни (* p <0,001).
Фиг. 7. Пороговый отклик оптогенетических систем в слепых сетчатках по сравнению с нормальным зрением. Сравнение пороговой чувствительности естественного зрения (вверху) с чувствительностью различных оптогенетических систем, введенных в определенный набор выживших нейронов в сетчатке после дегенерации фоторецепторных клеток (внизу). Млекопитающие MW-опсин (зеленый), родопсин (синий) и меланопсин (циан) в ~1000 раз более чувствительны, чем микробный канальный родопсин2 и галородопсин. Порог для альтернативных оптогенетических подходов от Bi et al. (2006)8, Zhang et al (2009)12, Sengupta et al. (2016)13, Doroudchi et al. (2011)45, Gaub et al. (2014)47, Cronin et al (2014)65, Berry et al. (2017)66 De Silva et al. (2017)17. (8) Bi et al. (2006) Каналородопсин, экспрессированный с промотором AAV2-CAG, стимулировали при 460 нм, у мыши rd1 с пределом чувствительности в RGC = 2,2 × 1015 фотонов см−2 с−1 ~1 мВт см-2. (12) Zhang et al (2009) Галородопсин экспрессированный с промотором AAV2-CMV , стимулировали при 555 – 575 нм при полосе пропускания rd1 у мыши rd1 с пределом чувствительности в RGC = 5.8 × 1016 фотонов см−2 с−1 ~20 мВт см-2. (13) Sengupta et al. (2016) - Сдвинутый к красному цвету каналородопсин экспрессированный с промотором AAV2-hSyn стимулировали при 595 нм у мыши rd1 с пределом чувствительности в RGC = 2.5 × 1015 фотонов см−2 с−1 ~1 мВт см-2. (45) Doroudchi et al. (2011) Канальный родопсин экспрессированный с промотором AAV8-Y733F & SV-40 стимулировали при 450–490 нм при полосе пропускания у rd10 мыши с пределом чувствительности в ON-BC = 4 × 1016 фотонов см−2 с−1 ~ 17 мВт см-2. (47) Gaub et al. (2014) LiGluR-MAG460 экспрессированный с промотором AAV2-hSyn и AAV2-4xGrm6 стимулировали при 445/20 нм у rd1 мыши с пределом чувствительности в RGC и ON-BC = 7,1 × 1014 фотонов см−2 с−1 ~0.3 мВт см-2. (65) Cronin et al (2014) Каналородопсин экспрессированный с промотором AAV2/8BP2 и 4xGRM6 стимулировали у rd1 мыши с пределом чувствительности в ON-BC = 1 × 1016 фотонов см−2 с−1 ~5 мВт см-2. (66) Berry et al. (2017) SNAG-MGluR2 экспрессированный с промотором AAV2-hSyn стимулировали при 445/50 нм у rd1 мыши с пределом чувствительности в RGC = 1 × 1014 фотонов см−2 с−1 ~0.5 мВт см-2.
(17) De Silva et al. (2017) экспрессировали с помощью AAV2/8 (Y733F) и CMV энхансера CMV/CBA промотора, стимулированных при 480/20 нм у мыши rd1 с пределом чувствительности к меланопсину в RGC = 1,20 × 1012 фотонов см−2 с−1 ~0,5 мкВт см-2.
Фиг. 8a-8e. Зависимая от интенсивности кинетика световой реакции MW-опсина. (a-c) Зависимость интенсивности света (в секундах) от Tau ON (a), Tau OFF (b) и времени до пика (T-пик) (c) в сетчатке rd1, экспрессирующей MW-опсин, n = 111 клеток, N = 3 сетчатки. Все клетки относятся к отсортированным единицам. Значения средние, ошибки - СОС. Длина волны: λ = 535 нм. (d, e) Средний отклик популяции RGC с СОС в сером цвете (вверху) и усредненный растровый график за 5 световых вспышек продолжительностью 1 секунда (внизу) для rd1, экспрессирующих MW-опсин (d; λ = 510 нм; n = 117 клеток) и wt (е, белый свет; n = 50 клеток).
Фиг. 18a-18c. Обнаружение контраста в выделенной сетчатке мыши rd1 экспрессирующей MW-опсин. MEA-регистрация откликов на шаги от темной до полной тоновой шкалы различной интенсивности на примере изолированной сетчатки от экспрессирующей MW-опсин мыши rd1 (в среднем по 14 каналам) (а). (b, c) Нормализованное изменение частоты пульсаций RGC в отклик на изменения контраста для мышей rd1, экспрессирующих MW-опсин (N = 2 сетчатки) (b) и wt мышей (N = 2 сетчатки) (c) 100% света = 25 мкВт см-2.
Фиг. 19a-19e. Световые отклики in vivo в V1 мыши rd1, экспрессирующей MW-опсин. (а) Схематическое изображение мыши с фиксированной головой на колесе для бега. Стимулы отображаются на стандартном мониторе компьютера, расположенном в пределах поля зрения одного глаза. (b) Реакция на импульс света 500 мс. Вверху, репрезентативный визуально вызванный потенциал из слоя 4 V1 (в среднем 20 откликов, заштрихованная область представляет собой среднее значение ± СОС). Внизу, тепловая карта откликов отдельных единиц от всех 16 электродов линейной электродной матрицы по всей глубине зрительной зоны коры головного мозга (в среднем 20 откликов). (c) Диаграмма рассеяния вызванной светом зависимости от базовой частоты пульсаций для 39 единиц у 3 мышей rd1, экспрессирующих MW-опсин. (d) PSTH (с интервалом 50 мс) типичного устройства в отклик на световую вспышку. (e) График процентного изменения пульсации нейронов после стимуляции в 39 единицах у 3 мышей.
Фиг. 20a-20d. Обнаружение контраста in vivo у экспрессирующей MW-опсин мыши rd1. (а) Иллюстрация записей зрительной зоне коры головного мозга у бодрствующей свободно бегущей мыши rd1, экспрессирующей MW-опсин. Рандомизированные контрастные изменения представлены на мониторе компьютера, расположенном в поле зрения животных. (b) Средняя частота пульсации в ответ на полные контрастные шаги (длительность 500 мс), записанные в слое 4 V1. На вставке показаны PSTH, излученные с 20 мс. 100% света = 115 мкВт см-2.
Фиг. 21a-21c. Временные свойства V1-откликов in vivo у мышей rd1, экспрессирующих MW-опсин. (a-c) Изменения в пульсации нейронов в зрительной зоне коры головного мозга, вызванные мерцающими стимулами полного поля 1, 2 и 4 Гц в течение 100 циклов.
MW-опсин восстанавливает врожденное избегание света
Наблюдая, что MW-опсин вызывает большие световые отклики при низкой интенсивности в выделенной сетчатке rd1, интактное животное использовали для оценки способности MW-опсина поддерживать визуальное поведение. Зрячие мыши врожденно избегают освещенных областей, механизм выживания, связанный с уклонением от захвата 35. Это поведение теряется после дегенерации фоторецепторов в модели мыши rd1 9,16. Чтобы определить, может ли это поведение быть восстановлено, мышей rd1 с MW-опсином в RGC тестировали в поведенческой коробке, состоящей из смежных светлых и темных отсеков (фиг. 4a). Фракцию времени, проведенного в каждом отсеке, регистрировали и сравнивали с мышами rd1, которых не лечили, и с мышами wt (фиг. 4, фиг. 9a-c, фиг. 11), как и долю успешного избегания для каждой когорты (фиг. 9а-с и фиг.11, таблица 1). Светлый отсек освещался белым светом низкой интенсивности, что эквивалентно освещению в помещении (100 мкВт/см-2). В то время как животные rd1, которых не лечили, не могут различить визуально между отсеками, они проводят около 40-50% времени в темном отсеке, что согласуется с установленным уклоном в пользу светлого отсека из-за знакомства с местом высвобождения (см. Способы) (фиг. 4b). Напротив, мыши rd1, экспрессирующие или родопсин, или MW-опсин, демонстрировали сильное предпочтение к темному отсеку, подобно животным с нормальным зрением (фиг. 4b и фиг. 9a). Затем, используя ту же поведенческую парадигму, белый свет был заменен синим (460 + 22 нм) или зеленым (534 + 25 нм) светом, а интенсивность была снижена до нижнего порога кривых выделенной сетчатки зависимости реакции от интенсивности для MW-опсина и родопсина (1 мкВт см-2; фиг. 3b). В условиях зеленого света животные, экспрессирующие MW-опсин и родопсин, демонстрировали избегание света (фиг. 4c, слева и фиг. 9b), однако, при синем свете только животные экспрессирующие родопсин демонстрировали избегание света (фиг. 4c, справа и фиг. 9c). Это проявление монохроматической чувствительности согласуется со спектром действия MW-опсина 36.
Фиг. 9a-9g. Избегание света и наученное поведение распознавания паттернов. (a-c) Доля успешного избегания светлого отсека (доля успешных испытаний на избегание) для rd1, экспрессирующих родопсин в RGC (синий; n = 6 мышей) или MW-опсин (зеленый; n = 5) и wt мышей (белый; n = 5 мышей) при освещении либо (а) белым светом (100 мкВт см-2), (b) зеленым светом 25 мкВт см-2 (535 нм) или (c) синим светом 25 мкВт см-2 (470 нм). Статистическую значимость оценивали с использованием двустороннего критерия хи-квадрат Пирсона и точного одностороннего критерия Фишера, когда это применимо (фиг. 11). Успех определяется как избегание больше среднего + S.D. контрольных необработанных мышей rd1 (см. Способы). (d) Схема эксперимента по распознаванию образов. Мышей адаптировали на день 1, и подвергали воздействию удара электрического тока в связи с определенным типом света (стимул A/B), случайным образом спаренным с любой камерой на 2-й и 3-й дни, и тестировали (время, проведенное в каждой камере) на 4-й день в отсутствие удара током с изменением структуры света, чтобы избежать смещения местоположения. (e-g) Доля успешной дискриминации модели в сочетании с ударом током (доля успешных испытаний на избегание) по сравнению с контрольной группой rd1, не получавшей лечения. (e) Горизонтальные против вертикальных параллельных линий. Различение параллельных статических (f) или движущихся (g) квадратов на расстоянии 1 против 6 см. Соответственно для e, f и g: rd1 родопсин (синий; n = 8 (e), 6 (f) мышей), rd1 MW-опсин (n = 17 (e), 11 (f), 6 (g) мышей) и wt (n = 5 (e), 6 (f), 9 (g) мышей). (25 мкВт см-2). Статистическую значимость оценивали с использованием двустороннего критерия хи-квадрат Пирсона и точного одностороннего критерия Фишера, когда это применимо (фиг. 11). Успех определяется как избегание больше среднего + S.D. По сравнению с контрольными необработанными мышами rd1.
MW-опсин поддерживает обнаружение временных световых паттернов
Заметив, что MW-опсин вызывает более быстрые световые отклики, чем родопсин в выделенной сетчатке rd1, был задан вопрос о том, приведет ли это к превосходной способности различать различные временные паттерны света. Для проверки способности животных отличать вспышку от постоянного света использовали визуально настроенную парадигму формирования страха. Мышей wt или мышей rd1, экспрессирующих либо MW-опсин, либо родопсин в RGC, помещали в поведенческий аппарат, состоящий из одного отсека, в котором ЖК-экран низкой интенсивности (100 мкВт см-2) переключался между постоянным светом и мигающим светом (2 Гц). У каждого животного постоянный свет или мигающий свет постоянно сочетались с легким ударом током стопы. Это выполняли для 1 испытания в день в течение 2 дней (фиг. 4d), и животных тестировали на 3-й день световыми сигналами, представленными в отсутствие удара током стопы, со временем замораживания, использованным для измерения ассоциации страха, как было сделано ранее 15,27,37. Время замораживания измеряли в течение 10 секунд после переключения временного светового паттерна. Измерения на животных, у которых визуальный сигнал и удар топом были в паре (парная группа), сравнивали с измерениями в когорте животных, у которых тренировочные удары током были рандомизированы (то есть не согласованы последовательно с одним из стимулов) (непарная группа). Время замораживания у необработанных мышей rd1 не различалось в парных и непарных условиях, что согласуется с ожидаемой неспособностью животных видеть визуальные сигналы (фиг. 4e, серый). Напротив, мыши rd1, экспрессирующие MW-опсин в RGC, показали большее замораживание в парных условиях, как это наблюдалось у животных (фиг. 4e, зеленый и белый). Поразительно, что мыши rd1, экспрессирующие родопсин в RGC, не отличались между парными и непарными условиями (фиг. 4e, синий). Это говорит о том, что, в отличие от слепых мышей, экспрессирующих MW-конопсин, мыши экспрессирующие родопсины не могут различать вспышки света при 2 Гц от постоянного света, что согласуется с кинетикой реакции на медленный свет, наблюдаемой в МЭА (фиг. 3e).
MW-опсин восстанавливает распознавание пространственного паттерна
Затем было определено, позволит ли MW-опсин в RGC мышам rd1 обнаруживать пространственные паттерны света. Была использована поведенческая камера с двумя смежными отсеками (фиг. 4f), каждый с ЖК-планшетом низкой интенсивности (iPad), установленным на стене. Каждый планшет отображал пару параллельных линий. В одном случае линии были ориентированы вертикально (||), а в другом - горизонтально (=). Для MW-опсина длина волны была центрирована на 535 нм (520-560), а для родопсина на 497 нм (480-520) (фиг. 9d). Сначала мышам давали время привыкать к отсекам с выключенными визуальными дисплеями (день 1). В течение двухдневного тренировочного периода удар током стопы сочетался с вертикальными или горизонтальными линиями. Отрицательный сигнал был назначен случайным образом и поддерживался последовательно для этого животного. На 4-й день местоположения стимулов были переключены, чтобы избежать смещения местоположения, и было проверено условное уклонение (фиг. 9d). Было обнаружено, что животные rd1 с MW-опсином в RGC показали избегание неприятного визуального сигнала, который был значительно выше, чем у необработанных контрольных животных rd1, и сходен с таковым у мышей wt (фиг. 4g и фиг. 9e). Напротив, животные rd1 с родопсином в RGC не отличались от необработанных контрольных животных rd1 и демонстрировали небольшое предпочтение неблагоприятного стимула, яркий пример смещения местоположения, наблюдаемого у слепых животных. Эти наблюдения показывают, что MW-опсин восстанавливает способность распознавать пространственные световые паттерны, а родопсин - нет.
Заметив, что MW-опсин поддерживает распознавание пространственных паттернов, был задан вопрос, могут ли мыши различать различия между линиями одинаковой ориентации, но разного расстояния, визуальная задача, принятая из тестов на остроту зрения у людей и животных 38,39. Параллельные вертикальные линии были разделены расстоянием 1 или 6 см. Как указано выше, удар током стопы случайным образом сочетался с одним из стимулов во время периода обучения на 2 и 3 дни, и воспоминание проверяли на 4 день в качестве меры избегания. Было обнаружено, что мыши rd1, экспрессирующие MW-опсин, способны различать два паттерна с предпочтением рабочих характеристик для неаверсивных стимулов, которое было сходным с таковым, наблюдаемым у мышей wt, тогда как животные, экспрессирующие родопсин были аналогичны необработанным мышам rd1 (фиг. 4h, фиг. 9f и фиг. 22). MW-опсин также поддерживал дифференциацию линий, когда параллельные линии находились в движении (1 см/с) (фиг. 4i и 9g).
Был задан вопрос, является ли скорость «обновления» MW-опсина достаточно быстрой, чтобы поддерживать распознавание паттерна линии, когда паттерн находится в движении. Чтобы проверить это, была выполнена та же самая задача дифференцирования близких линий, но теперь с параллельными линиями, движущимися со скоростью 5 см в секунду. Было обнаружено, что мыши rd1, экспрессирующие MW-опсин, проявляли предпочтение движущейся модели, которая была в паре с неверсивным стимулом, и работала так же, как и у мышей wt (фиг. 4i и фиг. 9g). Эти результаты показывают, что MW-опсин в RGC поддерживает распознавание как статических, так и движущихся пространственных паттернов при низкой интенсивности внутреннего освещения ЖК-экрана.
Фиг. 4a-4i. Избегание света и наученное зрительно-опосредованное поведение у мышей rd1, экспрессирующих MW-опсин или родопсин в RGC. (а) Схема светлой/темной коробки для испытания на избегание света. (b, c) Доля времени, проведенного в темном отсеке (доля избегания) для контроля rd1 (серый; n = 4 мыши), rd1, экспрессирующих родопсин в RGC (синий; n = 6 мышей) или MW-опсин (зеленый; n = 5) и wt мышей (белый; n = 5 мышей) при освещении либо (b) белым светом (100 мкВт см-2), (c) 25 мкВт см-2 синим светом (470 нм) (справа) или зеленым светом (535 нм) (слева). (d) Схема эксперимента по формированию страха замораживающей реакции. (е) Количественная оценка реакции страха на дискриминацию стимуляции во временном паттерне. Времени замораживания выше исходного уровня показано для случаев, когда переходы освещения от статической стимуляции к частоте 2 Гц (100 мкВт/см-2) были спарены или не связаны с электрическим током для контрольных мышей rd1, мышей экспрессирующих родопсин, MW-опсин и wt (n = 4, 6, 12, 10 парных, n = 7, 8, 7, 12 непарных). (f) Схема эксперимента по распознаванию паттерном. Мыши адаптировались в течения дня 1, а затем подвергались удару электрическим током в связи со специфическим паттерном света, проецируемым на ipad и случайным образом скомбинированным в любой камере (2 и 3 дни адаптации). На 4-й день проводили испытания на воспоминание (время, проведенное в каждой камере), при отсутствии удара током с изменением паттерна света, чтобы избежать смещения местоположения (см. фиг. 8d). (g-i) Наученное распознавание паттернов. Время, потраченное на то, чтобы избежать паттерна в сочетании с ударом током. (g) Горизонтальные и вертикальные параллельные полосы. (h) Различение параллельных статических (h) или движущихся (i) полос на расстоянии 1 против 6 см. Соответственно для g, h и i: контроль rd1 (n = 8,5,16 мышей), rd1 родопсин (синий; n = 8 мышей), rd1 MW-опсин (n = 17,11,6 мышей) и wt (n = 5,6,9 мышей). (25 мкВт см-2). (Обратите внимание, доля успеха для этих экспериментов показана на фиг. 9a-c). Интенсивность света = 25-100 мкВт см-2; Длина волны: = 535 нм (МВт-опсин), 510 нм (родопсин) или белый свет (МВт-опсин). n = количество мышей. Статистическая значимость оценивалась с помощью двустороннего критерия Cтьюдента с коррекцией Бонферрони: * р <0,01.
Фиг. 22a-22b. Расположение предпочтения в задаче дискриминации. (a) Иллюстрация арены, используемой в задачах распознавания, показывающая виртуальный разделитель, разделяющий каждый отсек пополам, чтобы определить соотношение времени, проведенного около центрального делителя между двумя камерами, и около экрана. (b) Отношение времени, проведенного в зоне, близкой к центральному разделителю, к зоне, ближайшей к экрану для отрицательных и неавверсивных сторон, показывает предпочтение для зоны, ближайшей к центральному разделителю. Значения являются средними; ошибки являются СОС.
MW-опсин подвергается адаптации к свету
Фундаментальной характеристикой зрения является способность различать объекты в широком диапазоне интенсивности окружающего света. Эта адаптация опосредуется несколькими различными механизмами в фоторецепторных клетках. Был задан вопрос о том, перейдет ли какой-либо аспект адаптации в RGC с MW-опсином. Сетчатки, экспрессирующие MW-опсин в RGC, вырезали, устанавливали на MEA и перфузировали 9 цис-ретиналем. Сетчатку сначала держали в полной темноте в течение 15 мин (адаптированной к темноте); затем была проведена серия коротких (1 с) вспышек зеленого света (535 + 25 нм) с большими интервалами (60 с) и в диапазоне интенсивностей. Затем свет адаптировали в течение 10 мин к умеренному уровню освещения в помещении (адаптированный к свету; белый свет при 100 мкВт/см-2) и серии импульсов света повторяли.
Была исследована кинетика световых откликов. Световой отклик быстро затухал, как показано выше, как для световой, так и для адаптированной к темноте сетчатки, за исключением одного случая: отклик на яркую вспышку в адаптированной к темноте сетчатке затухал примерно в 12 раз медленнее (3,14 + 0,63 с, n = 171, N = 3), чем в той же сетчатке в условиях адаптации к свету (фиг. 5а и фиг. 10а, b). Световые реакции, вызванные неповрежденными фоторецепторами, демонстрируют сходное поведение, и считается, что это играет роль в десенсибилизации к последующей стимуляции 40,41 и лежит в основе «остаточного изображения» у людей после яркой вспышки, которая временно затемняет зрение 42. Из-за своих необычных свойств этот отклик адаптированной к темноте сетчатки на самую яркую световую вспышку был исключен из анализа зависимости отклика от интенсивности.
Кривая зависимости отклика от интенсивности показала, что адаптированные к темноте сетчатки обладали высокой светочувствительностью, реагируя при ~0,5 мкВт/см-2, тогда как адаптированные к свету сетчатки были гораздо менее чувствительными, для отклика требовалось ~100 мкВт/см-2 (фиг. 5b, c и 10c, d). Эта адаптация сместила кривую интенсивности на ~3 порядка (780 + 82), N = 3) (фиг. 5b,c). Поразительной особенностью адаптации было то, что максимальный световой отклик был аналогичным в адаптированной к темноте и адаптированной к свету сетчатке (фиг. 5c), как показано ранее в нативных конусных фоторецепторах 43,44.
Наблюдая, что световой отклик, опосредованный MW-опсином в RGC, подвергается адаптации к свету в выделенной сетчатке, был задан вопрос, может ли это привести к визуально полезной адаптации к свету у поведенческого животного. MW-опсин-опосредованный световой отклик в RGC был исследован в контексте поведения избегания света. Перед тестированием мышей rd1, экспрессирующих MW-опсин в RGC, содержали в течение 1 часа либо в полной темноте (адаптирование к темноте), либо под освещением в помещении (белый свет, 1 мВт см-2 /535 нм, световой компонент, 50 мкВт см-2) (фиг. 5d). Затем животных немедленно тестировали в двухкамерной светло-темной коробке на поведение избегания света, когда в коробке имелось освещение зеленым светом (535 нм) при 1 мкВт см-2 (внутренний свет) или 100 мкВт см-2 (наружный свет). Адаптированные к свету MW-опсин-экспрессирующие мыши rd1 демонстрировали сильное избегание света, когда тестовый свет был ярче (535 нм, 100 мкВт см-2), чем уровень света, к которому они были адаптированы к свету (фиг. 5e). Избегание света было снижено, когда тестовый свет был более тусклым (535 нм, 1 мкВт см-2), чем уровень света, к которому мыши были адаптированы (фиг. 5e и фиг. 10e). Напротив, тусклый тестовый свет 1 мкВт/см-2 обеспечивает высокий уровень избегания света у адаптированных к темноте животных, что указывает на связанную с поведением адаптацию к свету.
Был задан вопрос, будет ли эффект адаптации к свету, связанный с поведением избегания света, также действовать для распознавания паттернов в задаче распознавания визуального изображения. Как указано выше (фиг. 4), мышей адаптировали в течение 3-дневного тренировочного периода путем сочетания легкого удара током стопы с одним из двух дисплеев с параллельными линиями с разным интервалом, представленным на экранах ЖКД в двух смежных камерах (фиг. 4h и 9d). Еще раз, мышей тестировали только визуальным стимулом в день 4, но на этот раз, непосредственно перед тестированием, они подвергались 1 часу либо темновой адаптации (без света), либо световой адаптации (белый свет) в течение 4 или 8 часов. Интенсивность паттернов линий во время воспоминания составляла либо 0,25 мкВт см-2 либо 10 мкВт см-2 после адаптации к свету. Было обнаружено, что мыши rd1, экспрессирующие MW-опсин в RGC, которые были адаптированы к темноте, были способны различать паттерны линий и избегать неприятного сигнала, независимо от того, был ли он представлен при низкой (0,25 мкВт см-2) или умеренной (10 мкВт см-2) интенсивности света в помещении (фиг. 5f и фиг. 10f). Напротив, адаптированные к свету животные добились успеха только с более яркими образцами испытательных линий и были идентичны по эффективности в группах, которые были адаптированы к свету в течение 1, 4 и 8 часов (фиг. 5f и 10g). Результаты показывают, что распознавание пространственных паттернов, опосредованное MW-опсином, является адаптивным в диапазоне интенсивностей естественного света.
MW-опсин восстанавливает новый объект исследования
Вышеприведенные эксперименты показывают, что MW-опсин обеспечивает распознавание образов в широком диапазоне интенсивностей света с использованием освещенных дисплеев. Вопрос заключался в том, как он будет работать в естественной среде, где окружающий случайный свет освещает трехмерные объекты. Чтобы решить эту проблему, в экспериментах использовалась арена открытого поля, которая обычно используется для проверки распознавания нового объекта и исследовательского поведения 62,63. Мыши естественным образом избегают открытых пространств и поддерживают близость к стенам своего окружения. Исследовательские экскурсии из этих безопасных мест могут быть мотивированы новыми стимулами. Хотя мыши используют несколько сенсорных модальностей во время исследования, было показано, что зрение имеет решающее значение для пространственной навигации64. Арена состояла из куба, содержащего два разных новых объекта. Мышь была расположена напротив стены арены, достаточно далеко от объектов, которые сами были достаточно далеко друг от друга, так что вероятность случайного столкновения была мала, независимо от того, шло ли животное вдоль стены или исследовало другой объект. Необработанные rd1, rd1, которым была проведена имитация внутриглазной инъекции, rd1, экспрессирующие родопсин или мыши rd1, экспрессирующие MW-опсин, а также животные wt были сняты на видео. Их движения отслеживались в течение 10 мин в первый раз, когда они были помещены на арену (фиг. 13a-d). Было обнаружено, что животные перемещаются в 1,57 раза дальше и движутся со сред скоростью в 1,55 раза быстрее, чем слепые животные rd1, что согласуется с известным визуальным компонентом исследовательского поведения. Поразительно, что, как и животные wt, животные rd1, экспрессирующие MW-опсин, путешествовали дальше (в 1,39 раза) и быстрее (в 1,37 раза), чем их необработанные однопометные особи rd1 (фиг. 13e, f), предполагая, что MW-опсин поддерживает нормальным новый объект исследования. Чтобы проанализировать это далее, эксперименты были сосредоточены на аспектах исследовательского поведения, которые, скорее всего, зависят от зрения на расстоянии; а именно на задержке в исследовании новых объектов, а также скорости и расстояния, пройденных на экскурсиях к объектам. Мыши, которым была проведена имитация внутриглазной инъекции, и мыши rd1, экспрессирующие родопсин, вели себя аналогично необработанным животным rd1, но мыши, экспрессирующие MW-опсин достигали первого и второго объектов в 3,88 и 3,62 раза быстрее, соответственно (фиг. 13g, h), двигаясь со скоростями, которые были в 2,1 раза и в 1,83 раза выше, к первому и второму объектам, соответственно (фиг. 13i, j), и выбирали более короткие пути, которые были в 0,69 раза и 0,64 раза соответственно короче до первого и второго объектов (фиг. 13k, l) по сравнению с необработанными мышами rd1. В каждой из этих мер мыши, экспрессирующие MW-опсин rd1, достигли уровней, которые были аналогичны уровням у животных wt (фиг. 13e-g). Эти результаты показывают, что MW-опсин в RGC обеспечивает ранее слепым животным натуралистическое видение объектов в окружающем свете.
Фиг. 5a-5f. Адаптация к свету в активности RGC и зрительно-опосредованное поведение, опосредованное MW-опсином. (a-c) MEA-записи в выделенной сетчатке светового отклика RGC, опосредованного MW-опсином в RGC сетчатки мыши rd1, показывают разницу в чувствительности с сетчаткой, адаптированной к темноте и свету. (a) Затухание светового отклика (Tau OFF) как функция интенсивности вспышки в условиях адаптации к темноте и свету (N = 3 сетчатки, n = 171 клеток). (b) Пример кривой зависимости отклика от интенсивности для репрезентативной сетчатки, сначала адаптированной к темноте (заполненные символы), а затем адаптированной к свету (открытые символы) (n = 57 ячеек). Адаптация к белому свету. Минимальное значение ChR2 от Bi et al. (2006)8 & Sengupta et al. (2016)13. (c) Средний (столбцы ошибок - СОС) нормализованный индекс световой реакции (LRI) при 3 интенсивностях вспышки в одной и той же сетчатке, сначала адаптированной к темноте, а затем адаптированной к свету (N = 3 сетчатки, n = 171 клеток). (d-f) Поведение показывает световую адаптацию в зрительно-опосредованных задачах. (d) Схема адаптации к темноте или свету до тестирования врожденного поведения избегания или наученного поведения распознавания паттернов. (e) Доля времени, проведенного в темном отсеке (доля избегания) при наружном освещении (100 мкВт см-2) или при внутреннем освещении (1 мкВт см-2) в течение 1 часа адаптации к темноте (n = 11 мышей) или адаптации к свету (белый свет; спектральный компонент 1 мВт см-2/535 нм; 50 мкВт см-2; n = 12,13 мыши). (f) Наученное распознавание паттернов параллельных полос, расположенных на расстоянии 1 против 6 см, отображается при низком (0,25 мкВт см-2) или внутреннем (10 мкВт см-2) уровне света в течение 1 часа адаптации к темноте (n = 8,8 мышей) или свету (белый свет; спектральный компонент 1 мВт см-2/535 нм; 50 мкВт см-2; n = 7,7 мышей). Пунктирная линия обозначает среднюю производительность необработанных контрольных мышей rd1. Интенсивность света 3,82×10-1 мВт см-2, длина волны: λ = 535 нм. Все клетки относятся к отсортированным единицам. Значения означают + СОС. Статистическую значимость оценивали с использованием U-критерия Манна-Уитни (* p<0,01). Двухсторонний критерий Cтьюдента с коррекцией Бонферрони: * р<0,05.
Фиг. 10a-10g. Адаптация к свету при удалении сетчатки и визуальное поведение мыши. (a-d) Репрезентативный след среднего отклика популяции RGC в сетчатке, экспрессирующей MW-опсин (n = 57). Реакция на световые вспышки 500 мс 3,82×101 мВт/см-2 (a, b) или 3,82×10-3 мВт см-2 (c, d) после адаптации к темноте (a, c) или свету (b, d). (e) Избегание светового отсека (доля успешных испытаний на избегание) при освещении в помещении (1 мкВт см-2) в течение 1 часа адаптации к темноте (n = 11 мышей) по сравнению с долей мышей с успешным избеганием при освещении в помещении (1 мкВт см-2; n = 12 мышей) и наружном освещении (100 мкВт см-2; n = 13 мышей) в течение 1 часа адаптации к свету (белый свет; спектральная составляющая 1 мВт см-2/535 нм; 50 мкВт см-2). (f) Доля успешного распознавания параллельных полос, расположенных на расстоянии 1 vs 6 см, отображаемых при низком (0,25 мкВт см-2) или внутреннем (10 мкВт см-2) уровне света после 1 часа, адаптация к темноте (n = 8 мышей при 0,25 мкВт см-2, 8 мышей при 10 мкВт см-2) или свету (n = 7 мышей при 0,25 мкВт см-2, 7 мышей при 10 мкВт см-2). (g) Наученное распознавание паттернов параллельных полос, расположенных на расстоянии 1 против 6 см, отображаемых при освещенности в помещении (10 мкВт см-2) через 1, 4 или 8 часов адаптации к свету (n = 7,4,4) по сравнению с неадаптированными контролями rd1.
Фиг. 11 (таблица 1). Статистическая значимость избегания света и наученного зрительно-опосредованного поведения. Коэффициенты успеха были рассчитаны для поведенческого избегания (фиг. 4, 5 и фиг. 9, 10). Для определения значимости различий между условиями была построена таблица попарных сопряженностей, и первоначально был проведен двусторонний тест хи-квадрат Пирсона. Чтобы исправить условия с малым n, был также проведен точный односторонний тест Фишера.
Ссылки
1. Tuo, J., Bojanowski, C.M. & Chan, C.-C. Genetic factors of age-related macular degeneration. Progress in retinal and eye research 23, 229-249 (2004).
2. Leveillard, T. & Sahel, J.A. Rod-derived cone viability factor for treating blinding diseases: from clinic to redox signaling. Sci Transl Med 2, 26ps16 (2010).
3. Bennett, J. Taking Stock of Retinal Gene Therapy: Looking Back and Moving Forward. Molecular Therapy 25, 1076-1094.
4. Daiger, S.P., Bowne, S.J. & Sullivan, L.S. Perspective on genes and mutations causing retinitis pigmentosa. Arch Ophthalmol 125, 151-158 (2007).
5. Ferrari, S., et al. Retinitis pigmentosa: genes and disease mechanisms. Curr Genomics 12, 238-249 (2011).
6. Mazzoni, F., Novelli, E. & Strettoi, E. Retinal ganglion cells survive and maintain normal dendritic morphology in a mouse model of inherited photoreceptor degeneration. J Neurosci 28, 14282-14292 (2008).
7. Haverkamp, S., et al. Synaptic plasticity in CNGA3(-/-) mice: cone bipolar cells react on the missing cone input and form ectopic synapses with rods. J Neurosci 26, 5248-5255 (2006).
8. Bi, A., et al. Ectopic expression of a microbial-type rhodopsin restores visual responses in mice with photoreceptor degeneration. Neuron 50, 23-33 (2006).
9. Busskamp, V., et al. Genetic reactivation of cone photoreceptors restores visual responses in retinitis pigmentosa. Science 329, 413-417 (2010).
10. Lagali, P.S., et al. Light-activated channels targeted to ON bipolar cells restore visual function in retinal degeneration. Nat Neurosci 11, 667-675 (2008).
11. Thyagarajan, S., et al. Visual function in mice with photoreceptor degeneration and transgenic expression of channelrhodopsin 2 in ganglion cells. J Neurosci 30, 8745-8758 (2010).
12. Zhang, Y., Ivanova, E., Bi, A. & Pan, Z.H. Ectopic expression of multiple microbial rhodopsins restores ON and OFF light responses in retinas with photoreceptor degeneration. J Neurosci 29, 9186-9196 (2009).
13. Sengupta, A., et al. Red-shifted channelrhodopsin stimulation restores light responses in blind mice, macaque retina, and human retina. EMBO Molecular Medicine 8, 1248-1264 (2016).
14. Cehajic-Kapetanovic, J., et al. Restoration of Vision with Ectopic Expression of Human Rod Opsin. Current biology : CB 25, 2111-2122 (2015).
15. Gaub, B.M., Berry, M.H., Holt, A.E., Isacoff, E.Y. & Flannery, J.G. Optogenetic Vision Restoration Using Rhodopsin for Enhanced Sensitivity. Mol Ther 23, 1562-1571 (2015).
16. Lin, B., Koizumi, A., Tanaka, N., Panda, S. & Masland, R.H. Restoration of visual function in retinal degeneration mice by ectopic expression of melanopsin. Proceedings of the National Academy of Sciences of the United States of America 105, 16009-16014 (2008).
17. De Silva, S.R., et al. Long-term restoration of visual function in end-stage retinal degeneration using subretinal human melanopsin gene therapy. Proc Natl Acad Sci U S A (2017).
18. Cepko, C. Neuroscience. Seeing the light of day. Science 329, 403-404 (2010).
19. Klapper, S.D., Swiersy, A., Bamberg, E. & Busskamp, V. Biophysical Properties of Optogenetic Tools and Their Application for Vision Restoration Approaches. Front Syst Neurosci 10, 74 (2016).
20. The Lasker, I.I.f.I.i.V.S. Restoring Vision to the Blind: The Lasker/IRRF Initiative for Innovation in Vision Science. Transl Vis Sci Technol 3, 1 (2014).
21. Vinores, S.A., et al. Blood-retinal barrier breakdown in retinitis pigmentosa: light and electron microscopic immunolocalization. Histol Histopathol 10, 913-923 (1995).
22. Kawamura, S. & Tachibanaki, S. Rod and cone photoreceptors: molecular basis of the difference in their physiology. Comp Biochem Physiol A Mol Integr Physiol 150, 369-377 (2008).
23. Korenbrot, J.I. Speed, sensitivity, and stability of the light response in rod and cone photoreceptors: facts and models. Prog Retin Eye Res 31, 442-466 (2012).
24. Masseck, O.A., et al. Vertebrate cone opsins enable sustained and highly sensitive rapid control of Gi/o signaling in anxiety circuitry. Neuron 81, 1263-1273 (2014).
25. Gutierrez, D.V., et al. Optogenetic control of motor coordination by Gi/o protein-coupled vertebrate rhodopsin in cerebellar Purkinje cells. J Biol Chem 286, 25848-25858 (2011).
26. Levitz, J., et al. Optical control of metabotropic glutamate receptors. Nat Neurosci 16, 507-516 (2013).
27. Friedmann, D., Hoagland, A., Berlin, S. & Isacoff, E.Y. A spinal opsin controls early neural activity and drives a behavioral light response. Current biology : CB 25, 69-74 (2015).
28. Fischer, R.M., et al. Co-expression of VAL- and TMT-opsins uncovers ancient photosensory interneurons and motorneurons in the vertebrate brain. PLoS Biol 11, e1001585 (2013).
29. Liegertova, M., et al. Corrigendum: Cubozoan genome illuminates functional diversification of opsins and photoreceptor evolution. Sci Rep 5, 14396 (2015).
30. Chen, M.H., Kuemmel, C., Birge, R.R. & Knox, B.E. Rapid release of retinal from a cone visual pigment following photoactivation. Biochemistry 51, 4117-4125 (2012).
31. Mark, M.D. & Herlitze, S. G-protein mediated gating of inward-rectifier K+ channels. Eur J Biochem 267, 5830-5836 (2000).
32. Shevtsova, Z., Malik, J.M., Michel, U., Bahr, M. & Kugler, S. Promoters and serotypes: targeting of adeno-associated virus vectors for gene transfer in the rat central nervous system in vitro and in vivo. Exp Physiol 90, 53-59 (2005).
33. Sancho-Pelluz, J., et al. Photoreceptor cell death mechanisms in inherited retinal degeneration. Molecular neurobiology 38, 253-269 (2008).
34. Schwartz, E.A. Responses of bipolar cells in the retina of the turtle. The Journal of physiology 236, 211-224 (1974).
35. Bourin, M. & Hascoet, M. The mouse light/dark box test. European journal of pharmacology 463, 55-65 (2003).
36. Merbs, S.L. & Nathans, J. Photobleaching difference absorption spectra of human cone pigments: quantitative analysis and comparison to other methods. Photochem Photobiol 56, 869-881 (1992).
37. Tochitsky, I., et al. Restoring visual function to blind mice with a photoswitch that exploits electrophysiological remodeling of retinal ganglion cells. Neuron 81, 800-813 (2014).
38. Bittner, A.K., Jeter, P. & Dagnelie, G. Grating Acuity and Contrast Tests for Clinical Trials of Severe Vision Loss. Optometry and vision science : official publication of the American Academy of Optometry 88, 1153-1163 (2011).
39. Wong, A.A. & Brown, R.E. Visual detection, pattern discrimination and visual acuity in 14 strains of mice. Genes, Brain and Behavior 5, 389-403 (2006).
40. Pepperberg, D.R. Bleaching desensitization: background and current challenges. Vision Res 43, 3011-3019 (2003).
41. Kang Derwent, J.J., Qtaishat, N.M. & Pepperberg, D.R. Excitation and desensitization of mouse rod photoreceptors in vivo following bright adapting light. The Journal of physiology 541, 201-218 (2002).
42. Di Lollo, V., Clark, C.D. & Hogben, J.H. Separating visible persistence from retinal afterimages. Percept Psychophys 44, 363-368 (1988).
43. Hurley, J.B. Shedding light on adaptation. J Gen Physiol 119, 125-128 (2002).
44. Normann, R.A. & Werblin, F.S. Control of retinal sensitivity. I. Light and dark adaptation of vertebrate rods and cones. J Gen Physiol 63, 37-61 (1974).
45. Doroudchi, M.M., et al. Virally delivered channelrhodopsin-2 safely and effectively restores visual function in multiple mouse models of blindness. Mol Ther 19, 1220-1229 (2011).
46. Caporale, N., et al. LiGluR restores visual responses in rodent models of inherited blindness. Mol Ther 19, 1212-1219 (2011).
47. Gaub, B.M., et al. Restoration of visual function by expression of a light-gated mammalian ion channel in retinal ganglion cells or ON-bipolar cells. Proc Natl Acad Sci U S A 111, E5574-5583 (2014).
48. Sommer, M.E., Hofmann, K.P. & Heck, M. Distinct loops in arrestin differentially regulate ligand binding within the GPCR opsin. Nat Commun 3, 995 (2012).
49. Polosukhina, A., et al. Photochemical restoration of visual responses in blind mice. Neuron 75, 271-282 (2012).
50. Holladay, J.T. Proper method for calculating average visual acuity. Journal of refractive surgery (Thorofare, N.J.: 1995) 13, 388-391 (1997).
51. Broichhagen, J., et al. Orthogonal Optical Control of a G Protein-Coupled Receptor with a SNAP-Tethered Photochromic Ligand. ACS Cent Sci 1, 383-393 (2015).
52. Levitz, J., Broichhagen, J., Leippe, P., Konrad, D., Trauner, D. and Isacoff, E.Y. Dual optical control and mechanistic insights into photoswitchable group II and III metabotropic glutamate receptors. Proc Natl Acad Sci U S A (2017).
53. Roska, B., Molnar, A. & Werblin, F.S. Parallel processing in retinal ganglion cells: how integration of space-time patterns of excitation and inhibition form the spiking output. Journal of neurophysiology 95, 3810-3822 (2006).
54. Leinonen H, Tanila H. Vision in laboratory rodents-Tools to measure it and implications for behavioral research. Behav Brain Res, (2017).
55. Prusky GT, West PW, Douglas RM. Behavioral assessment of visual acuity in mice and rats. Vision Res 40, 2201-2209 (2000).
56. Shi C, et al. Optimization of Optomotor Response-based Visual Function Assessment in Mice. Sci Rep 8, 9708 (2018).
57. Berson DM, Dunn FA, Takao M. Phototransduction by retinal ganglion cells that set the circadian clock. Science 295, 1070-1073 (2002).
58. Veit J, Hakim R, Jadi MP, Sejnowski TJ, Adesnik H. Cortical gamma band synchronization through somatostatin interneurons. Nat Neurosci 20, 951-959 (2017).
59. Brainard DH. The psychophysics toolbox. Spatial Vision 10, 433-436 (1997).
60. Hill DN, Mehta SB, Kleinfeld D. Quality Metrics to Accompany Spike Sorting of Extracellular Signals. Journal of Neuroscience 31, 8699-8705 (2011).
61. Berry M, et al. Restoration of Patterned Vision with an Engineered Photo-Activatable G Protein-Coupled Receptor. Nat Commun, (2017).
62. Antunes M, Biala G. The novel object recognition memory: neurobiology, test procedure, and its modifications. Cognitive Processing 13, 93-110 (2012).
63. Christmas AJ, Maxwell DR. A comparison of the effects of some benzodiazepines and other drugs on aggressive and exploratory behaviour in mice and rats. Neuropharmacology 9, 17-29 (1970).
64. Buhot MC, Dubayle D, Malleret G, Javerzat S, Segu L. Exploration, anxiety, and spatial memory in transgenic anophthalmic mice. Behavioral neuroscience 115, 455-467 (2001).
65. Cronin T, et al. Efficient transduction and optogenetic stimulation of retinal bipolar cells by a synthetic adeno-associated virus capsid and promoter. EMBO Molecular Medicine 6, 1175-1190 (2014).
66. Berry MH, et al. Restoration of patterned vision with an engineered photoactivatable G protein-coupled receptor. Nat Commun 8, 1862 (2017).
Хотя настоящее изобретение было описано со ссылкой на его конкретные варианты осуществления, специалистам в данной области техники должно быть понятно, что могут быть сделаны различные изменения и эквиваленты могут быть заменены без отклонения от истинной сущности и объема изобретения. Кроме того, может быть сделано много модификаций для адаптации конкретной ситуации, материала, состава вещества, способа, стадии или стадий способа к цели, сущности и объему настоящего изобретения. Предполагается, что все такие модификации находятся в пределах объема прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВИРИОНЫ АДЕНОАССОЦИИРОВАННОГО ВИРУСА С ВАРИАНТНЫМ КАПСИДОМ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2012 |
|
RU2611202C2 |
| ВИРИОНЫ АДЕНОАССОЦИИРОВАННОГО ВИРУСА С ВАРИАНТНЫМ КАПСИДОМ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2017 |
|
RU2742724C1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ И ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С RDH12 | 2017 |
|
RU2764920C2 |
| СВЕТОЧУВСТВИТЕЛЬНЫЙ ХИМЕРНЫЙ БЕЛОК GPCR | 2012 |
|
RU2637367C2 |
| КОМПОЗИЦИЯ И СПОСОБ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ, ОПОСРЕДОВАННОГО КОМПЛЕМЕНТОМ | 2016 |
|
RU2727411C2 |
| ВАКЦИНЫ ПРОТИВ FMDV НА ОСНОВЕ РЕКОМБИНАНТНОГО АДЕНОВИРУСНОГО ВЕКТОРА И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725495C2 |
| SYNP161, ПРОМОТОР ДЛЯ СПЕЦИФИЧЕСКОЙ ЭКСПРЕССИИ ГЕНОВ В ПАЛОЧКОВЫХ ФОТОРЕЦЕПТОРАХ | 2016 |
|
RU2758211C2 |
| СИСТЕМНАЯ ДОСТАВКА И РЕГУЛИРУЕМАЯ ЭКСПРЕССИЯ ПАРАКРИННЫХ ГЕНОВ ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ И ИНЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2642605C2 |
| SYNP198, ПРОМОТОР ДЛЯ СПЕЦИФИЧЕСКОЙ ЭКСПРЕССИИ ГЕНОВ В ГАНГЛИОНАРНЫХ КЛЕТКАХ СЕТЧАТКИ, ИЗБИРАТЕЛЬНЫХ В ОТНОШЕНИИ НАПРАВЛЕНИЯ | 2017 |
|
RU2766353C2 |
| КОНСТРУКЦИИ ДНК-АНТИТЕЛ ДЛЯ ПРИМЕНЕНИЯ ПРОТИВ БОЛЕЗНИ ЛАЙМА | 2017 |
|
RU2813829C2 |























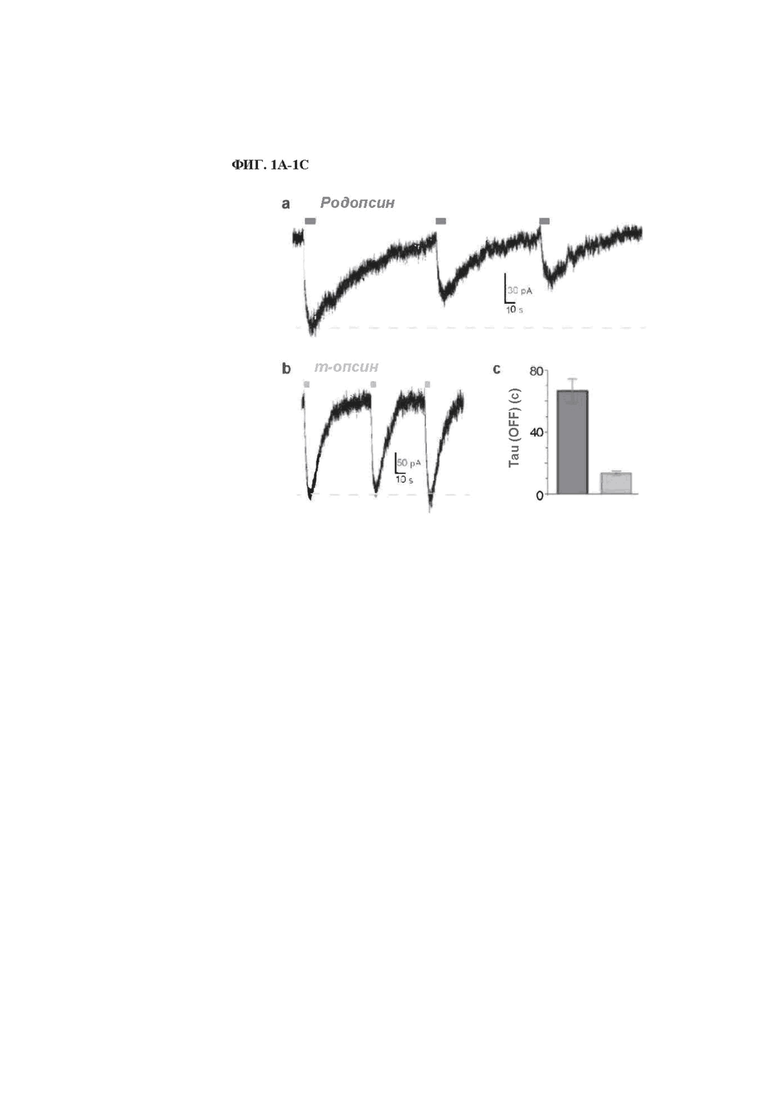
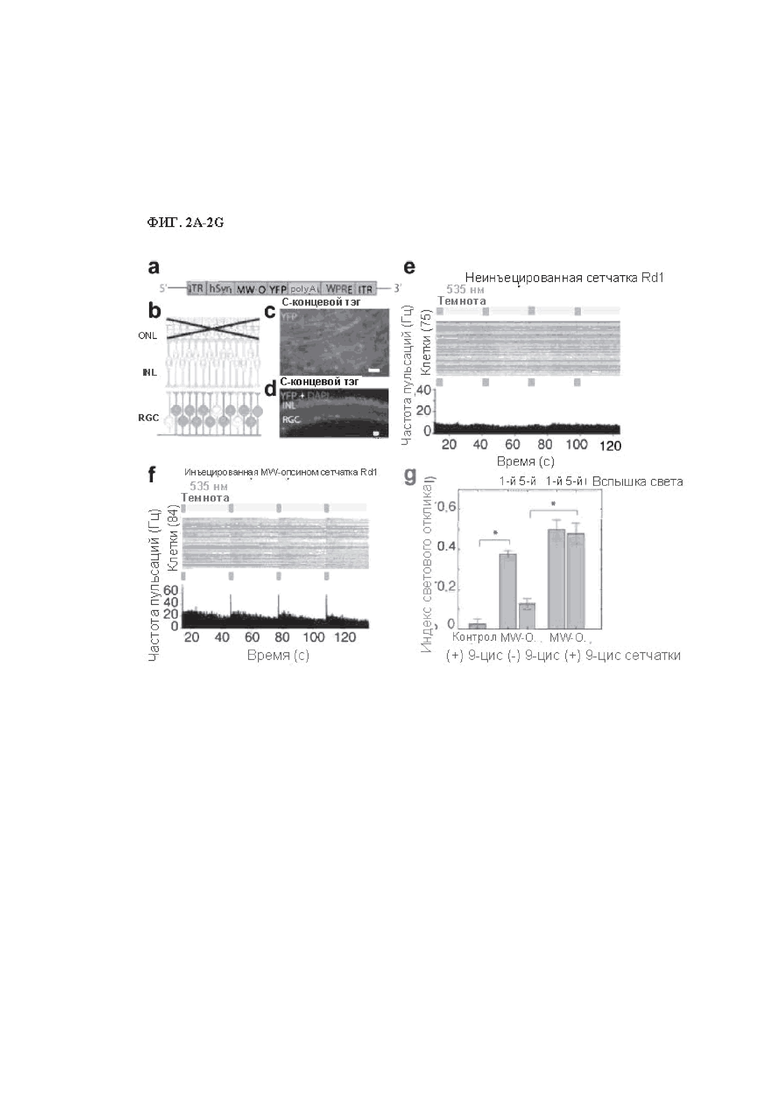
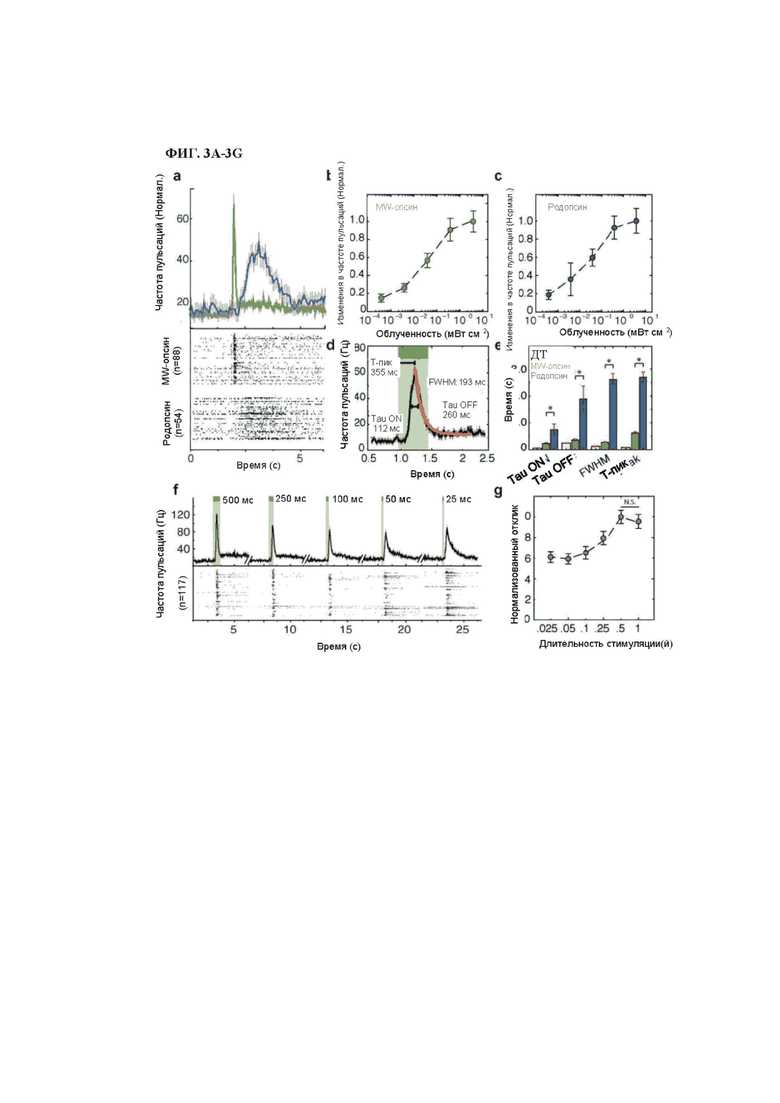
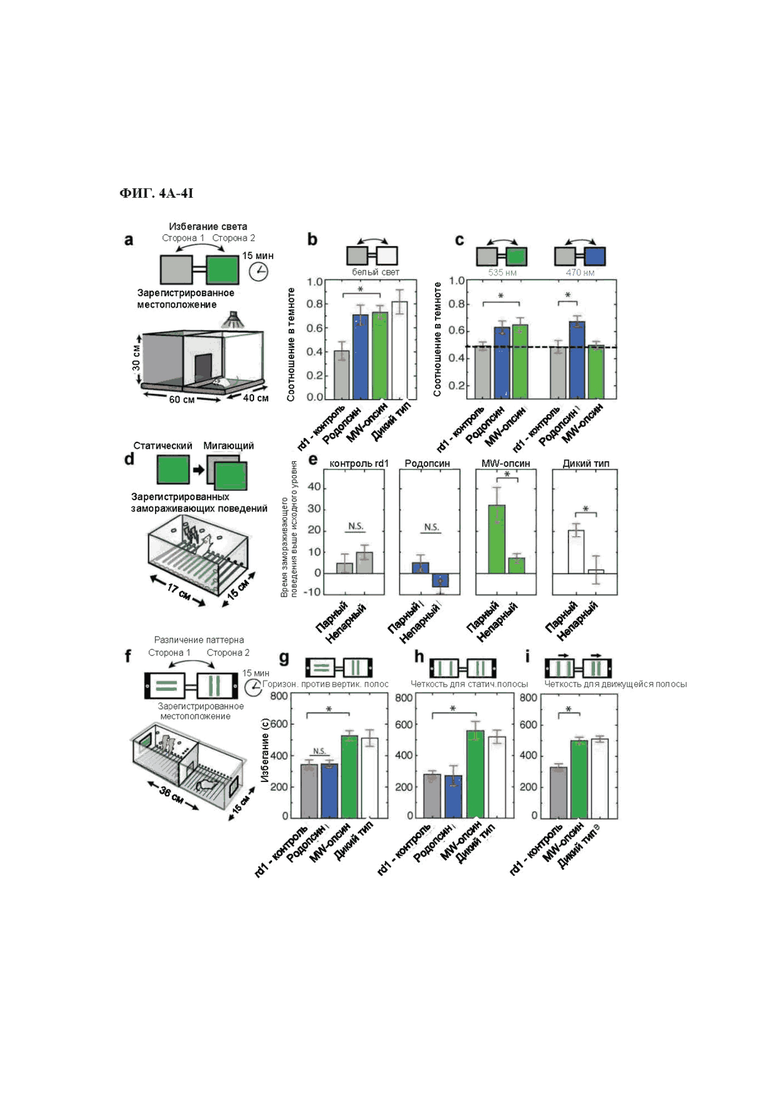
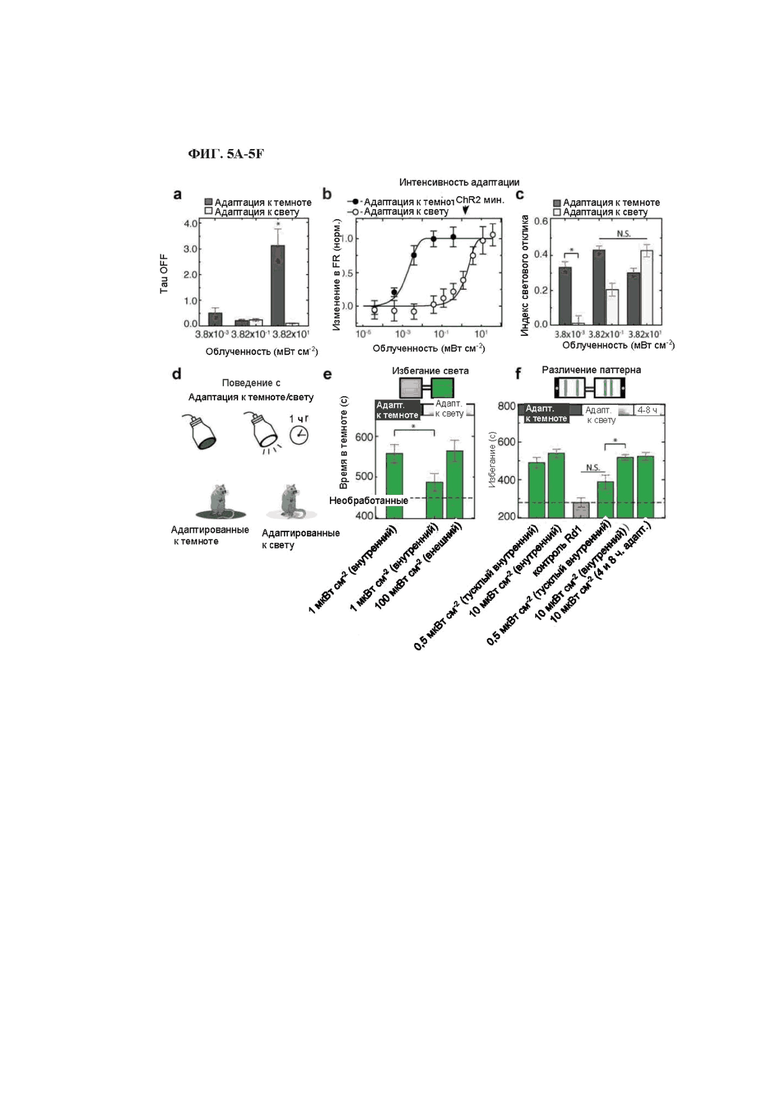
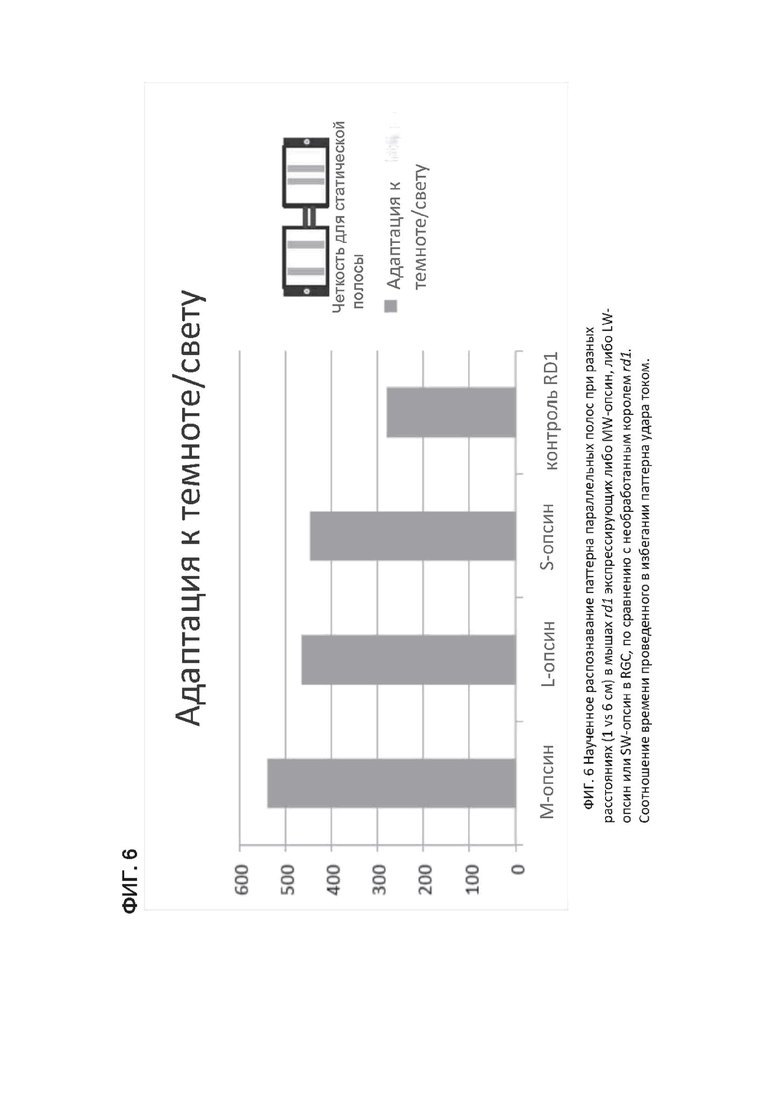



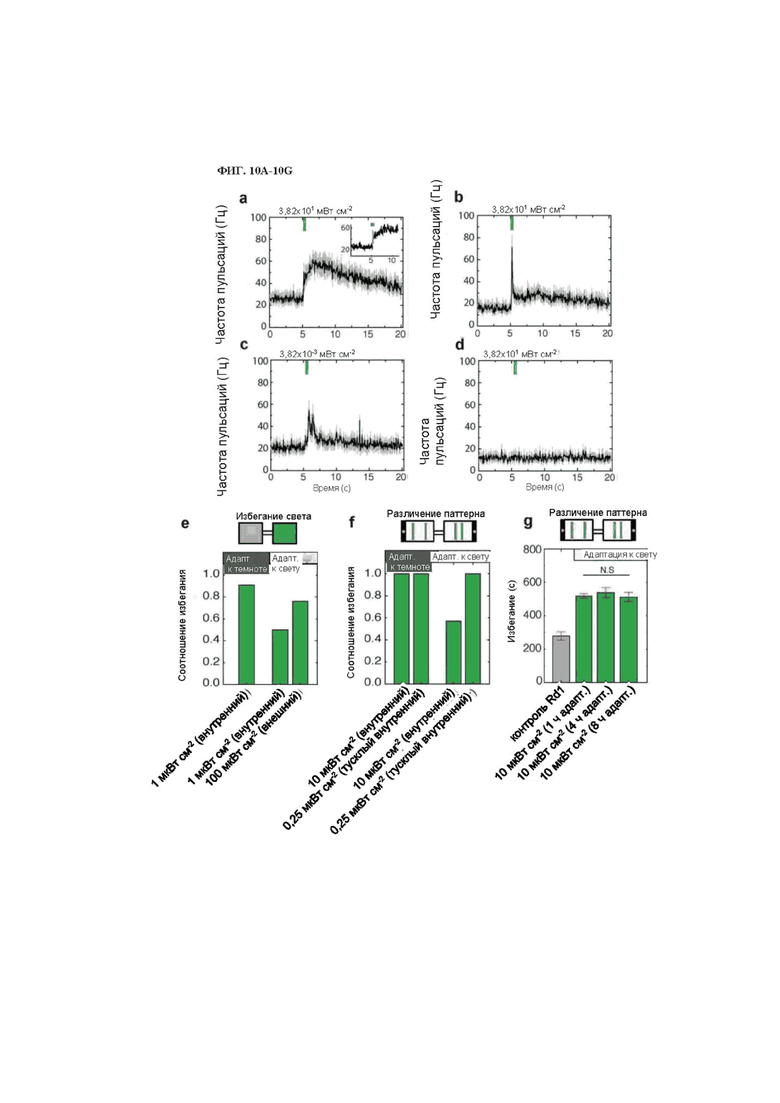




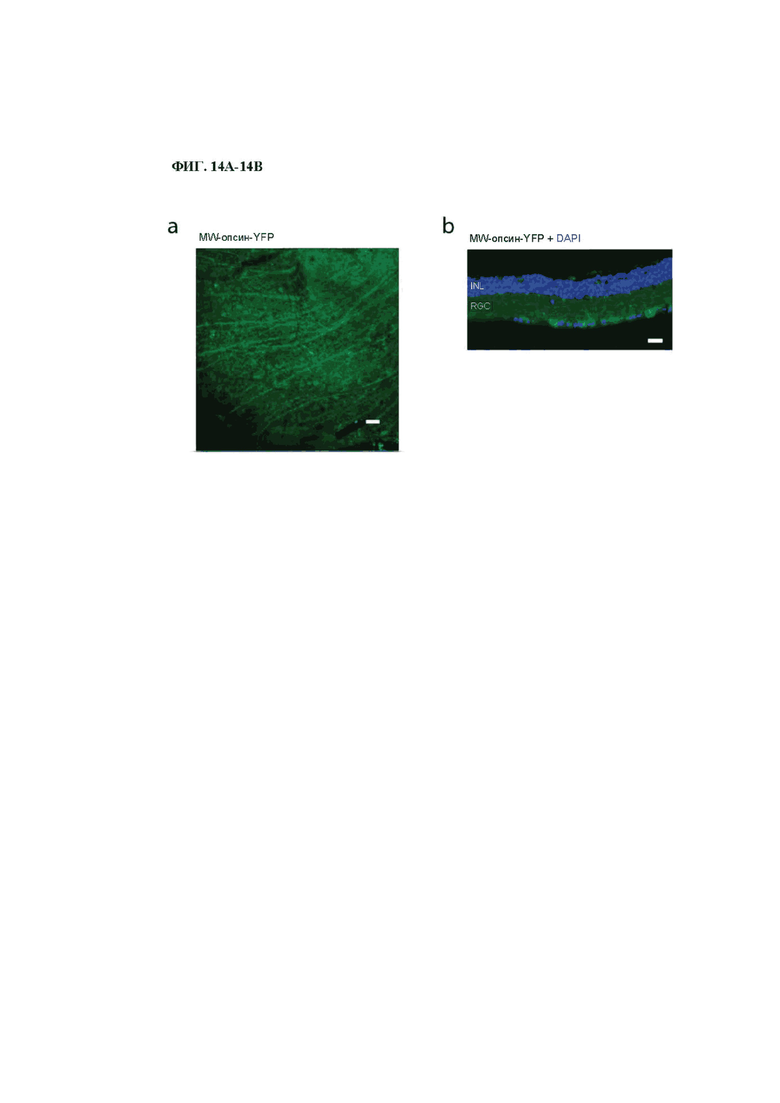
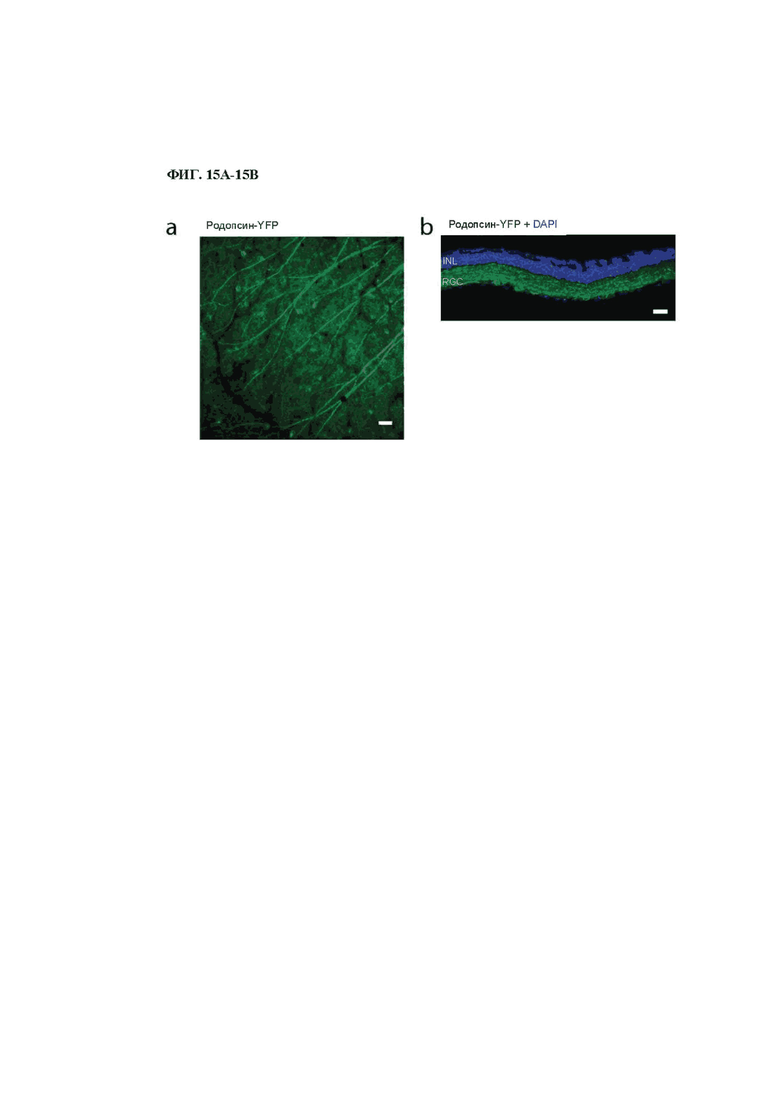



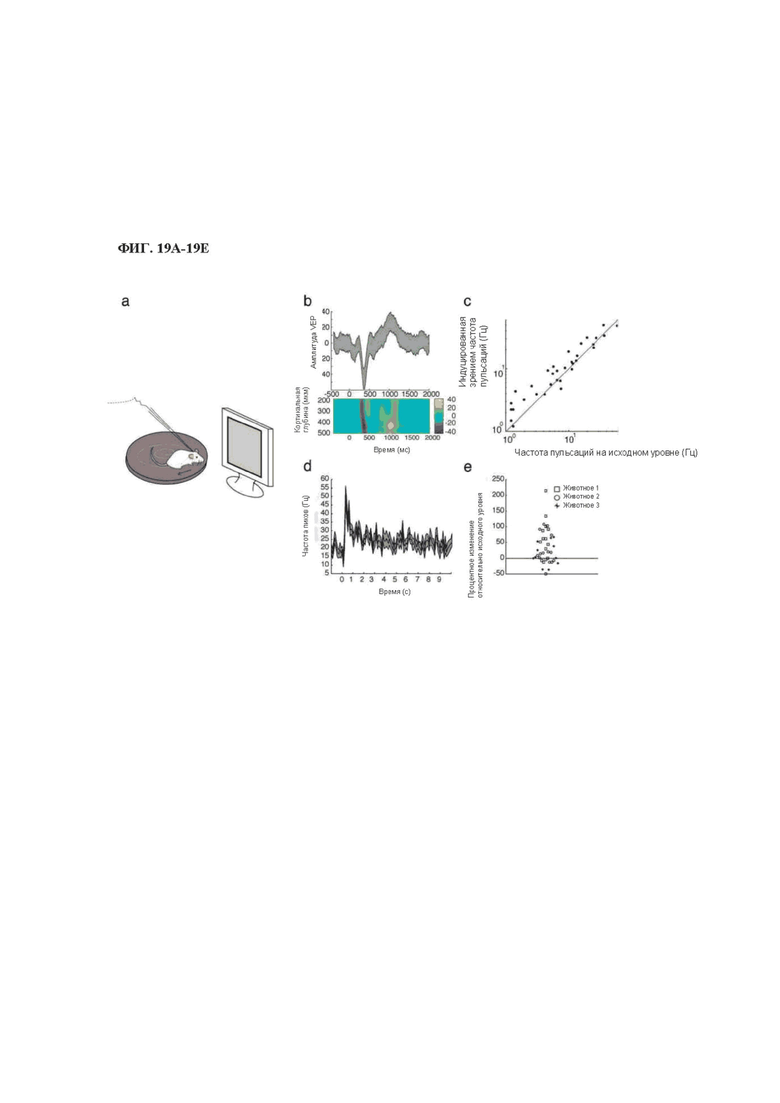
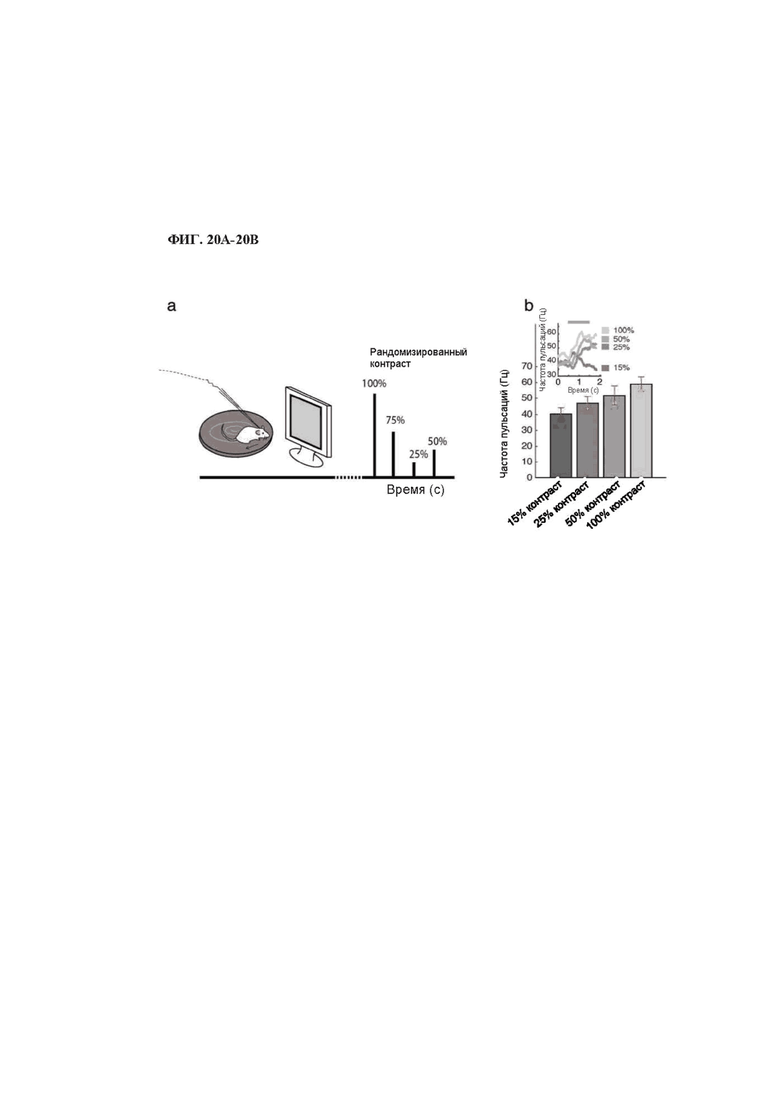
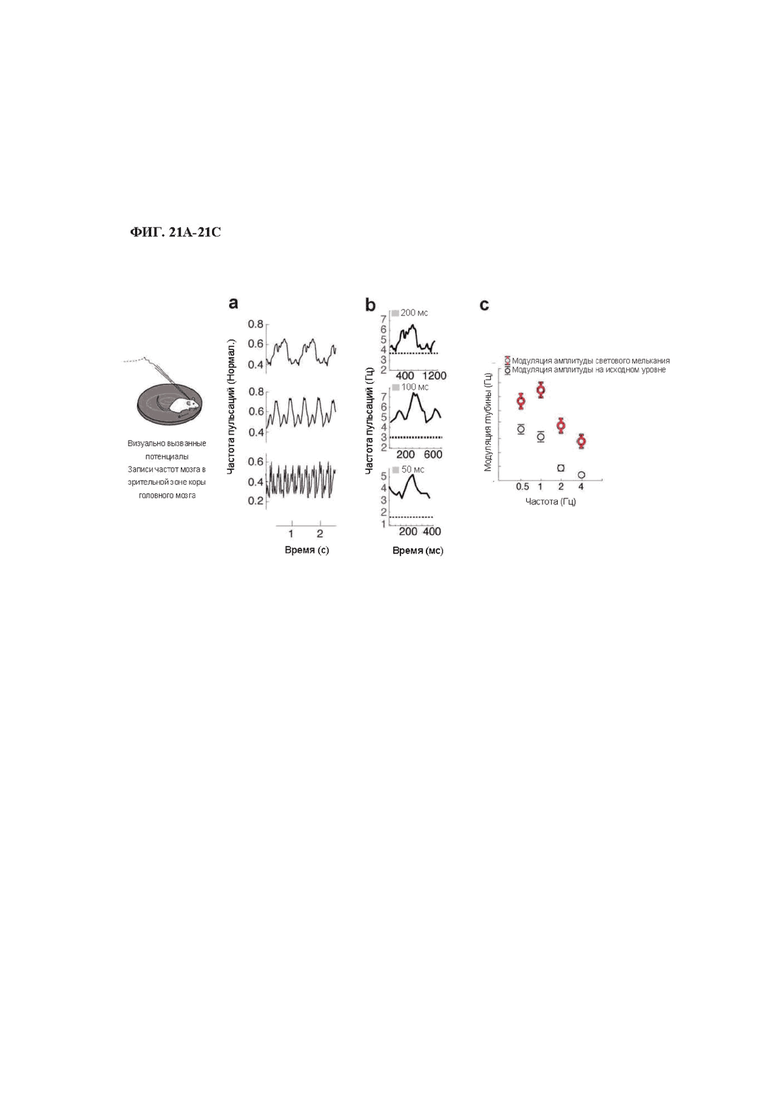
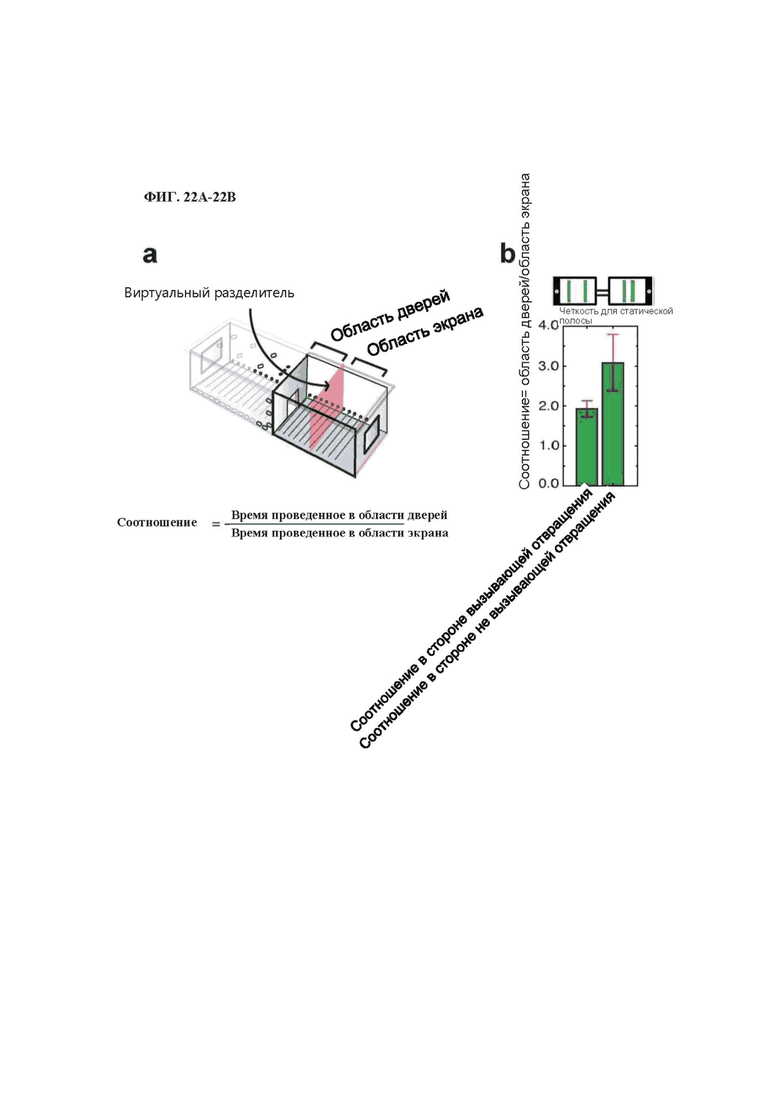
Изобретение относится к медицине, а именно к офтальмологии, и может быть использовано для восстановления или улучшения зрительной функции у индивидуума, имеющего дегенерацию сетчатки. Способ включает введение индивидууму по меньшей мере одного рекомбинантного вектора экспрессии, содержащего одно или несколько из: i) нуклеотидной последовательности, кодирующей MW-опсин; ii) нуклеотидной последовательности, кодирующей LW-опсин; и iii) нуклеотидной последовательности, кодирующей SW-опсин, где указанная нуклеотидная последовательность функционально связана с промотором, отличным от промотора опсина, и экспрессируется в клетке сетчатки у индивидуума, представляющей собой ганглиозную клетку сетчатки, амакриновую клетку, горизонтальную клетку или биполярную клетку. Способ обеспечивает восстановление или улучшение зрительной функции у индивидуума благодаря экспрессии указанной нуклеиновой кислоты в клетках сетчатки этого индивидуума. 21 з.п. ф-лы, 22 ил., 1 пр.
1. Способ восстановления или улучшения зрительной функции у индивидуума, имеющего дегенерацию сетчатки, причем способ включает введение индивидууму по меньшей мере одного рекомбинантного вектора экспрессии, содержащего одно или несколько из: i) нуклеотидной последовательности, кодирующей опсин средней длины волны (MW-опсин); ii) нуклеотидной последовательности, кодирующей длинноволновый опсин (LW-опсин); и iii) нуклеотидной последовательности, кодирующей коротковолновый опсин (SW-опсин), где нуклеотидная последовательность, кодирующая SW-опсин, нуклеотидная последовательность, кодирующая MW-опсин, или нуклеотидная последовательность, кодирующая LW-опсин, функционально связана с промотором, отличным от промотора опсина, и экспрессируется в клетке сетчатки у индивидуума, причем указанное введение обеспечивает восстановление или улучшение зрительной функции у индивидуума благодаря экспрессии указанной нуклеиновой кислоты в клетках сетчатки этого индивидуума, где клетка сетчатки представляет собой ганглиозную клетку сетчатки, амакриновую клетку, горизонтальную клетку или биполярную клетку.
2. Способ по п. 1, в котором MW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 85% аминокислотной последовательности, представленной в SEQ ID NO: 1; причем LW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 85% аминокислотной последовательности, представленной в SEQ ID NO: 4, и причем SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 85% аминокислотной последовательности, представленной в SEQ ID NO: 5.
3. Способ по п. 1, в котором рекомбинантный вектор экспрессии содержит нуклеотидную последовательность, кодирующую SW-опсин, при этом SW-опсин содержит аминокислотную последовательность, идентичную по меньшей мере на 87% аминокислотной последовательности SW-опсина человека, представленной в SEQ ID NO: 5, или идентичную по меньшей мере на 87% аминокислотной последовательности SW-опсина мыши, представленной в SEQ ID NO: 6.
4. Способ по любому из пп. 1-3, в котором экспрессия MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает структурированное зрение и распознавание изображения индивидуумом.
5. Способ по п. 4, в котором распознаваемое изображение представляет собой:
a) статическое изображение или паттерн или
b) движущееся изображение или паттерн.
6. Способ по любому из пп. 1-5, в котором экспрессия MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает распознавание изображения при интенсивности света от 10-4 Вт/см2 до 1 Вт/см2.
7. Способ по любому из пп. 1-6, в котором экспрессия MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает распознавание изображения при интенсивности света, которая по меньшей мере в 10 раз ниже, чем интенсивность света, необходимая для обеспечения распознавания изображения индивидуумом, экспрессирующим полипептид канального родопсина в клетке сетчатки.
8. Способ по любому из пп. 1-7, в котором экспрессия MW-опсина, и/или LW-опсина, и/или SW-опсина в клетке сетчатки обеспечивает кинетику, которая по меньшей мере в 2 раза быстрее, чем кинетика в клетке сетчатки вызванная полипептидом родопсина.
9. Способ по любому из пп. 1-8, в котором рекомбинантный вектор экспрессии представляет собой рекомбинантный вирусный вектор.
10. Способ по п. 9, в котором указанный рекомбинантный вирусный вектор представляет собой аденоассоциированный вирусный вектор, лентивирусный вектор, вектор вируса простого герпеса или ретровирусный вектор.
11. Способ по любому из пп. 1-10, в котором промотор представляет собой промотор синапсина, промотор CAG, промотор CMV, промотор grm6, промотор Pleiades, промотор ChAT, промотор V-glut, промотор GAD, промотор PV, промотор соматостатина (SST), нейропептидный Y (NPY) промотор, промотор VIP, промотор родопсинкиназы, промотор гена вителлиформной макулярной дистрофии 2 (VMD2) или промотор гена межфоторецепторного ретинол-связывающего белка (IRBP).
12. Способ по любому из пп. 1-11, в котором указанное введение осуществляется посредством внутриглазной инъекции, интравитреальной инъекции, субретинальной инъекции, или осуществляется с помощью периокулярного, внутриглазного, интравитреального, субконъюнктивального, ретробульбарного, склерального, субретинального или межкамерного пути введения.
13. Способ по любому из пп. 1-12, в котором индивидуум имеет глазное заболевание, выбранное из пигментного ретинита, макулярной дегенерации, ретиношизиса и врожденного амавроза Лебера, а также диабетической ретинопатии, или в котором у индивидуума имело место отслоение сетчатки или потеря фоторецептора вследствие травмы или повреждения головы.
14. Способ по любому из пп. 1-13, в котором по меньшей мере один рекомбинантный вектор экспрессии образует комплекс с наночастицей.
15. Способ по п. 1, отличающийся тем, что клетка сетчатки представляет собой ганглиозную клетку сетчатки.
16. Способ по п. 1, отличающийся тем, что по меньшей мере один рекомбинантный вектор экспрессии представляет собой рекомбинантный аденоассоциированный вирусный вектор.
17. Способ по п. 1, отличающийся тем, что у индивидуума имеется пигментный ретинит.
18. Способ по п. 16, отличающийся тем, что аденоассоциированный вирусный вектор представляет собой AAV2.
19. Способ по п. 1, отличающийся тем, что указанное введение осуществляют периокулярным, внутриглазным, интравитреальным, субконъюнктивальным, ретробульбарным, склеральным, субретинальным или межкамерным путем введения.
20. Способ по п. 1, отличающийся тем, что промотор представляет собой промотор синапсина.
21. Способ по п. 1, отличающийся тем, что промотор представляет собой промотор CAG.
22. Способ по п. 1, отличающийся тем, что промотор представляет собой промотор V-glut.
| WO 2017055421 A1, 06.04.2017 | |||
| US 2016015288 A1, 21.01.2016 | |||
| US 2014171376 A1, 19.06.2014 | |||
| ИВАНОВА М.Е | |||
| и др | |||
| Современные способы генетического лечения дистрофий сетчатки | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| GAUB B.M | |||
| et al | |||
| Optogenetic Vision Restoration Using Rhodopsin for Enhanced Sensitivity | |||
| Mol Ther | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
Авторы
Даты
2022-12-28—Публикация
2018-11-13—Подача