Область техники, к которой относится изобретение
Настоящее изобретение в целом относится к молекулам нуклеиновой кислоты, в отношении которых изменения ДНК или РНК или профилей экспрессии белка являются показателями появления, предрасположенности к появлению и/или развития неоплазмы. Конкретнее, настоящее изобретение относится к молекулам нуклеиновой кислоты, в отношении которых изменения ДНК или РНК или профилей экспрессии белка являются показателями появления и/или развития неоплазмы толстой кишки, такой как аденома или аденокарцинома. ДНК или профили экспрессии по настоящему изобретению полезны в ряде применений, в том числе, но без ограничения, случаях, относящихся к диагностике и/или мониторингу колоректальных неоплазм, таких как колоректальные аденокарциномы. Соответственно, в родственном аспекте настоящее изобретение относится к способу скрининга в отношении субъекта на появление, предрасположенность к появлению и/или развитие неоплазмы посредством скрининга на модуляцию ДНК или РНК или профиля экспрессии белка одной или более маркеров-молекул нуклеиновых кислот.
Уровень техники
Библиографические подробности публикаций, на которые ссылается автор в данном описании, собраны в алфавитном порядке в конце описания.
Ссылка в данном описании на любую предшествующую публикацию (или информацию из такой ссылки) или на любой известный материал не являются и не должны приниматься как подтверждение или признание или любая форма предположения, что предшествующая публикация (или информация из такой публикации) или известный материал образуют часть общего знания в сфере усилия, к которому относится данное описание.
Аденомы являются доброкачественными опухолями, или неоплазмами, эпителиального происхождения, которые образуются из железистой ткани или проявляют четко выраженные железистые структуры. Некоторые аденомы демонстрируют узнаваемые элементы ткани, такой как фиброзная ткань (фиброаденомы), и эпителиальную структуру, в то время как другие, такие как бронхиальные аденомы, вырабатывают активные соединения, которые могут дать начало клиническим синдромам.
Аденомы могут развиваться и стать инвазивными неоплазмами, и тогда их называют аденокарциномами. Соответственно, аденокарциномы определяются как злокачественные эпителиальные опухоли, возникающие из железистых структур, которые являются составными частями многих органов тела. Термин «аденокарцинома» также применим к опухолям, демонстрирующим особенности роста железы. Такие опухоли можно разбить на подклассы согласно веществам, которые они вырабатывают, например, секретирующие слизь и серозные аденокарциномы, или гистологическому расположению их клеток в структуры, например, папиллярные и фолликулярные аденокарциномы. Такие карциномы могут быть солидными или кистозными (цистаденокарциномы). Каждый орган может продуцировать опухоли, показывающие различные гистологические типы, например, яичник может продуцировать как слизеобразующие аденокарциномы, так и цистаденокарциномы.
Аденомы в различных органах ведут себя различно. Вообще, в целом возможность присутствия карциномы в аденоме (т.е. очага рака, развивающегося в доброкачественном патологическом изменении) составляет приблизительно 5%. Однако это связано с размером аденомы. Например, в толстой кишке (конкретно, в ободочной и прямой) в аденомах менее 1 см появление рака в пределах аденомы является редким. Такое развитие оценивается как 40-50% в аденомах, которые больше 4 см и показывают некоторые гистологические изменения, такие как изменение ворсинчатости, или дисплазию высокой степени. Аденомы с высокой степенью дисплазии имеют больший показатель появления карциномы. При любой данной колоректальной аденоме показатели уже наличия рака или появления рака в будущем включают размер (в особенности, более 9 мм), степень изменения морфологии от тубулярной к ворсинчатой, наличие дисплазии высокой степени и морфологическое изменение, описываемое как «зубчатая аденома». У любого данного индивидуума дополнительные особенности - старение, случаи колоректальной аденомы или рака в семье, мужской пол или множественность аденом, прогнозированный риск в отношении рака в органе - являются так называемыми факторами риска появления рака. За исключением наличия аденом и их размера ни одна из указанных особенностей объективно не определяется, и особенности иные, чем число и размер, являются предметом наблюдаемой ошибки и путаницы, когда встает вопрос о точном определении особенности. Поскольку такие факторы могут затруднить оценку и определение, их ценность как прогностических факторов имеющегося или будущего риска в отношении рака является неопределенной.
Как только развилась спорадическая аденома, возможность появления новой аденомы составляет приблизительно 30% в течение 26 месяцев.
Колоректальные аденомы представляют собой класс аденом, которые показывают возрастающее число случаев заболевания, особенно, в более богатых странах. Причины аденомы и развитие до аденокарциномы являются до сих пор предметом интенсивного исследования. На сегодняшний день предполагается, что кроме генетической предрасположенности роль в развитии такого состояния играют факторы окружающей среды (такие как питание). В большинстве исследований указывается, что к релевантным факторам окружающей среды относятся высокое содержание жира в пище, низкое содержание волокон, малое потребление овощей, курение, ожирение, гиподинамия и высокорафинированные углеводы.
Аденомы толстой кишки представляют собой локализованные участки диспластического эпителия, в которые сначала вовлекаются только одна или несколько крипт, и которые могут не выступать над поверхностью, но с возрастанием в размере, как правило, в результате дисбаланса пролиферации и/или апоптоза, они могут выступать. Аденомы можно классифицировать несколькими путями. Одним путем является их макроскопическая картина, и главные показатели включают степень протрузии: плоская бесчерешковая (т.е. выступает, но без явной ножки) или имеющая ножку (т.е. с явной ножкой). Другие макроскопические показатели включают фактический размер по наибольшему измерению и фактическое число в толстой/прямой кишке. В то время как малые аденомы (менее 5 или 10 мм) показывают ровную желтовато-коричневую поверхность, имеющие ножку и, в особенности, более крупные аденомы имеют склонность иметь красно-коричневую поверхность «булыжной мостовой» или дольковую поверхность. Более крупные бесчерешковые аденомы могут показывать более тонкую ворсинчатую поверхность. Другой набор показателей включает гистологическую классификацию; первичные показатели клинического значения включают степень дисплазии (низкая или высокая), присутствие или отсутствие очага инвазивного рака, степень изменения от образования тубулярной железы до образования ворсинчатой железы (поэтому с классификацией на тубулярные, ворсинчатые или тубулярноворсинчатые), наличие смешанного гиперпластического изменения и так называемых «зубчатых» аденом и их подгрупп. Аденомы могут располагаться в любом месте в толстой и/или прямой кишке, хотя они имеют склонность чаще находиться в прямой кишке и дистальном участке толстой кишки. Все такие показатели, за исключением числа и размера, являются относительно субъективными и предметом расхождения во мнениях между исследователями.
Различные описательные признаки аденом имеют значение не только для оценки неопластического статуса любой данной аденомы при обнаружении, но также для прогноза для личности будущего риска развития колоректальных аденом или рака. Такие особенности аденом или ряда аденом у индивидуума, которые указывают на повышенный будущий риск в отношении рака или появления новых аденом, включают размер самой крупной аденомы (в особенности, 10 мм или больше), степени изменения ворсинчатости (в особенности, по меньшей мере, 25% такое изменение и, в частности, 100% такое изменение), высокая степень дисплазии, число (3 или больше любого размера или гистологический статус) или наличие признаков «зубчатых» аденом. Ни один показатель, за исключением размера или числа, не является объективным, и все являются относительно субъективными и предметом расхождения во мнениях между исследователями. Такие показатели риска в отношении будущей неоплазии (далее «риска») являются жизненно важными на практике, поскольку они используются для определения скорости и необходимости в и частоты будущего эндоскопического наблюдения. Таким образом, более точная классификация риска может уменьшить рабочую нагрузку на колоноскопию, сделать ее более эффективной по стоимости и уменьшить опасность осложнений от процедур, не являющихся необходимыми.
Аденомы, как правило, являются бессимптомными, поэтому затруднительна их диагностика и лечение на стадии до того, когда у них могут развиться инвазивные свойства, и, таким образом, появляется рак. Технически невозможно прогнозировать наличие или отсутствие карциномы на основе макроскопической картины аденом, хотя более вероятно, что диапазон злокачественного изменения демонстрирует более крупные аденомы, а не более мелкие аденомы. Бесчерешковые аденомы демонстрируют большее число случаев злокачественности, чем аденомы того же размера с ножкой. Некоторые аденомы приводят к кровопотери, которую можно наблюдать или обнаружить в стуле; хотя иногда видимая глазу, она, когда происходит, часто является микроскопической или «скрытой». Более крупные аденомы имеют склонность к кровотечению большую, чем более мелкие аденомы. Однако, так как кровь в стуле, явная или скрытая, также может являться показателем неаденоматозных состояний, точный диагноз аденомы представляется затруднительным без применения высокоинвазивных процедур, таких как колоноскопия, в сочетании с отбором ткани либо удалением (т.е. полипэктомией), либо биопсией, и последующим гистопатологическим анализом.
Соответственно, существует непреходящая потребность в выяснении причин аденомы и разработке более информативных диагностических протоколов или вспомогательных средств для диагностики, которая дает одна право на прямую колоноскопию у людей с большей вероятностью наличия аденом. Такие аденомы могут быть опасными, запущенными или ни теми ни другими, в частности, нужны протоколы, которые дадут возможность быстрой, обычной и точной диагностики аденом. Кроме того, после колоноскопии может быть затруднительным иметь уверенность, что все аденомы удалены, в особенности, у личности, у которой было несколько аденом. Точный скрининг-тест может свести к минимуму необходимость предпринимать раннюю вторую колоноскопию для уверенности в том, что толстая кишка очищена от неоплазм. Соответственно, идентификация молекулярных маркеров для аденом могла бы обеспечить средства для понимания причины аденом и рака, улучшения диагностики аденом, в том числе, разработки скрининг-тестов, выяснения гистологической стадии аденомы, характеризации будущего риска для пациента в отношении колоректальной неоплазии на основании молекулярного статуса аденомы и облегчения лечения аденом.
До настоящего времени исследования фокусировались на идентификации генных мутаций, которые ведут к развитию колоректальных неоплазм. Однако в работе, ведущей к настоящему изобретению, определено, что изменения в ДНК или РНК, или профилях экспрессии белка генов, которые также экспрессируются у здоровых индивидуумов, являются показателями развития неоплазм толстой кишки, таких как аденомы и аденокарциномы. Также установлено, что в отношении неоплазм толстого кишечника диагностику можно сделать на основании скрининга одной или нескольких панелей таких различно экспрессируемых генов. В родственном аспекте еще также определяется, что к степени, до которой неопластическая ткань идентифицирована или способом по изобретению, или любым другим способом, настоящее изобретение также еще предоставляет средства характеризации такой ткани как аденомы или рака. В еще одном аспекте определяется, что пропорция таких генов характеризуется по экспрессии генов, которая происходит в контексте ненеопластической ткани, а не в контексте неопластической ткани, причем посредством этого облегчается разработка качественных анализов, которые не требуют относительного анализа, выполняемого против ненеопластического или нормального контрольного эталонного уровня. Соответственно, авторы идентифицируют панель генов, которая облегчает диагностику развития аденокарциномы и аденомы и/или мониторинг состояний, характеризующихся развитием таких типов неоплазм.
Раскрытие изобретения
В данном описании и последующей формуле изобретения, если контекст не требует иного, слово «включать» и такие вариации как «включает» и «включающий», следует понимать как означающие включение указанных чего-то целого или стадии или группы каких-то целых или стадий, но не исключение каких-либо других чего-то целого или стадии или группы каких-то целых или стадий.
Используемый в данном описании термин «получен из» следует принимать как указывающий, что определенное нечто целое или группа каких-то целых происходит от определенных видов, но необязательно получены непосредственно из определенного источника. Кроме того, используемый в данном описании формы единственного числа («а», «and» и «the») включают соответствующие множественные формы, если контекст явно не диктует иное.
Если нет иного определения, все технические и научные термины, используемые в данном описании, имеют те же значения, какие обычно понимаются специалистами в данной области техники, к которым обращено данное изобретение.
Описание предмета изобретения содержит информацию об аминокислотных и нуклеотидных последовательностях, полученной с использованием программы Patentln, версия 3.4, представленной в данном описании после библиографии. Каждая аминокислотная и нуклеотидная последовательность идентифицирована в списке последовательностей под числовым индикатором <210> с последующим идентификатором последовательности (например, <210>1, <210>2 и т.д.). Длина, тип последовательности (аминокислотная, ДНК и т.д.) и организм источник для каждой последовательности указаны с помощью информации, предоставленной в полях числовых индикаторов <211>, <212> и <213>, соответственно. Аминокислотные и нуклеотидные последовательности, упомянутые в описании, идентифицированы индикатором SEQ ID NO: с последующим идентификатором последовательности (например, SEQ ID NO: 1, SEQ ID NO: 2, и т.д.). Идентификатор последовательности, упомянутый в описании, коррелирует с информацией, предоставленной в поле числовых индикаторов <499> в списке последовательностей, которое следует за идентификатором последовательности (например, <400>1, <400>2 и т.д.). Иными словами, SEQ ID NO: 1, подробно описанная в описании, коррелирует с последовательностью, указанной как <400>1 в списке последовательностей.
Один аспект настоящего изобретения относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из




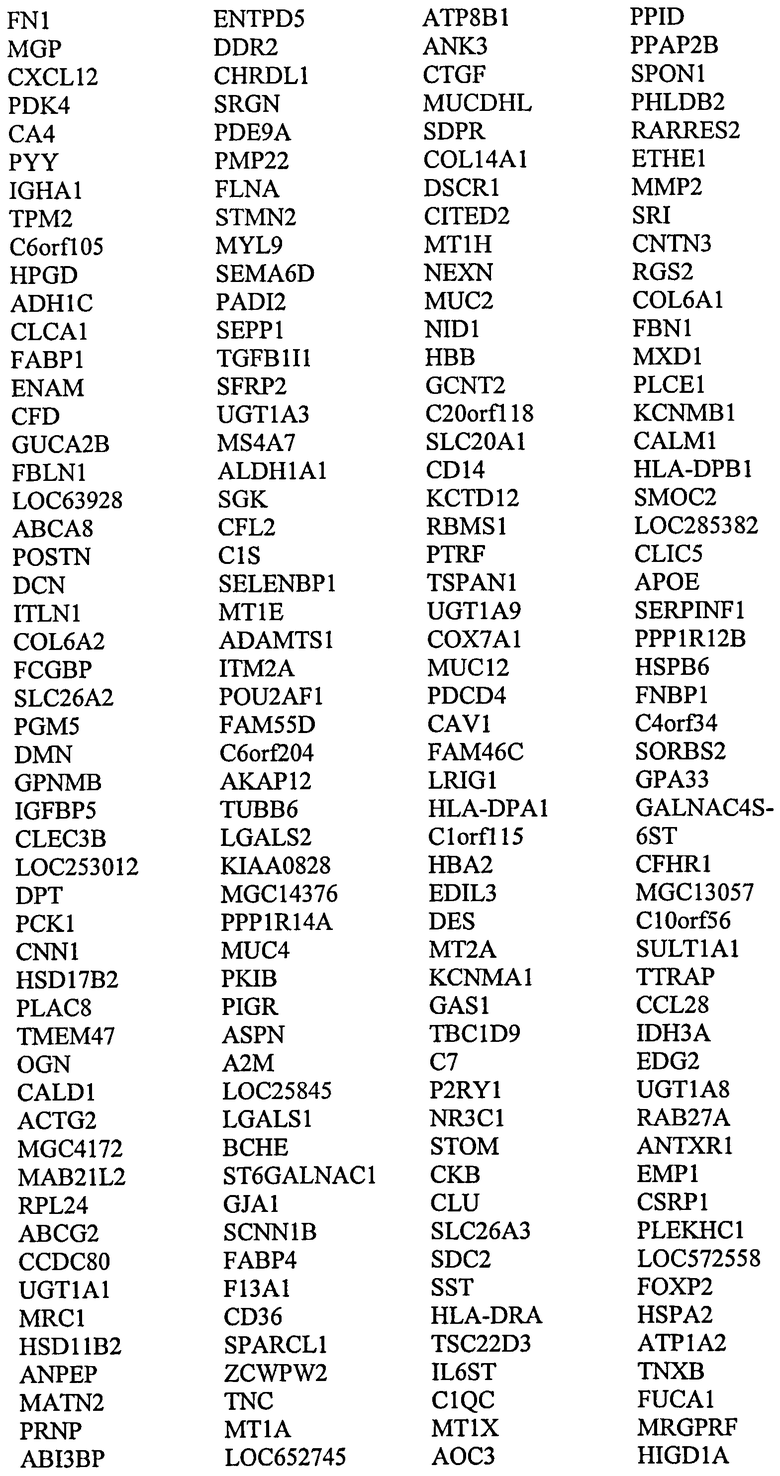

в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Другой аспект настоящего изобретения относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
2200026_at; и/или
(ii) CLCA4,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии гена или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В еще одном аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
214142_at; и/или
(ii) ZG16,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В еще одном аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
209301_at, 205950_s_at; и/или
(ii) СА2 СА1,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В еще одном аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
220834_at; и/или
(ii) MS4A12,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В еще одном аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
206784_at; и/или
(ii) AQP8,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В другом аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
203908_at, 206198_s_at, 205547_s_at, 207003_at, 206422_at, 209613_s_at, 207245_at; и/или
(ii) SLC4A4, CEACAM7, TAGLN, GUCA1B, GCG, ADH1B, UGT2B17,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В еще другом аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
203908_at, 206198_s_at, 205547_s_at, 207003_at, 206422_at, 209613_s_at, 207245_at; и/или
(ii) SLC4A4, CEACAM7, TAGLN, GUCA1B, GCG, ADH1B, UGT2B17,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В еще одном другом аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из

в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В еще одном еще другом аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из

в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В родственном аспекте настоящее изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из


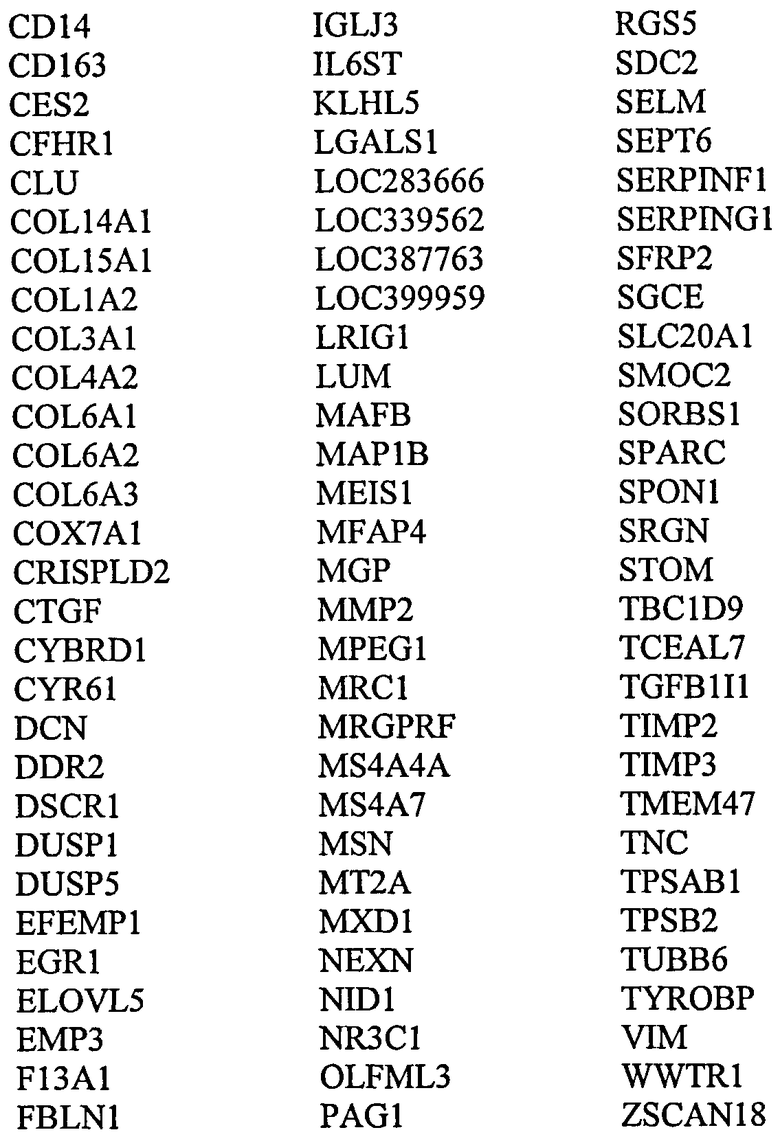
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем клетки аденомы толстой кишки или клетки, предрасположенной к появлению состояния аденомы.
В другом аспекте настоящее изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из


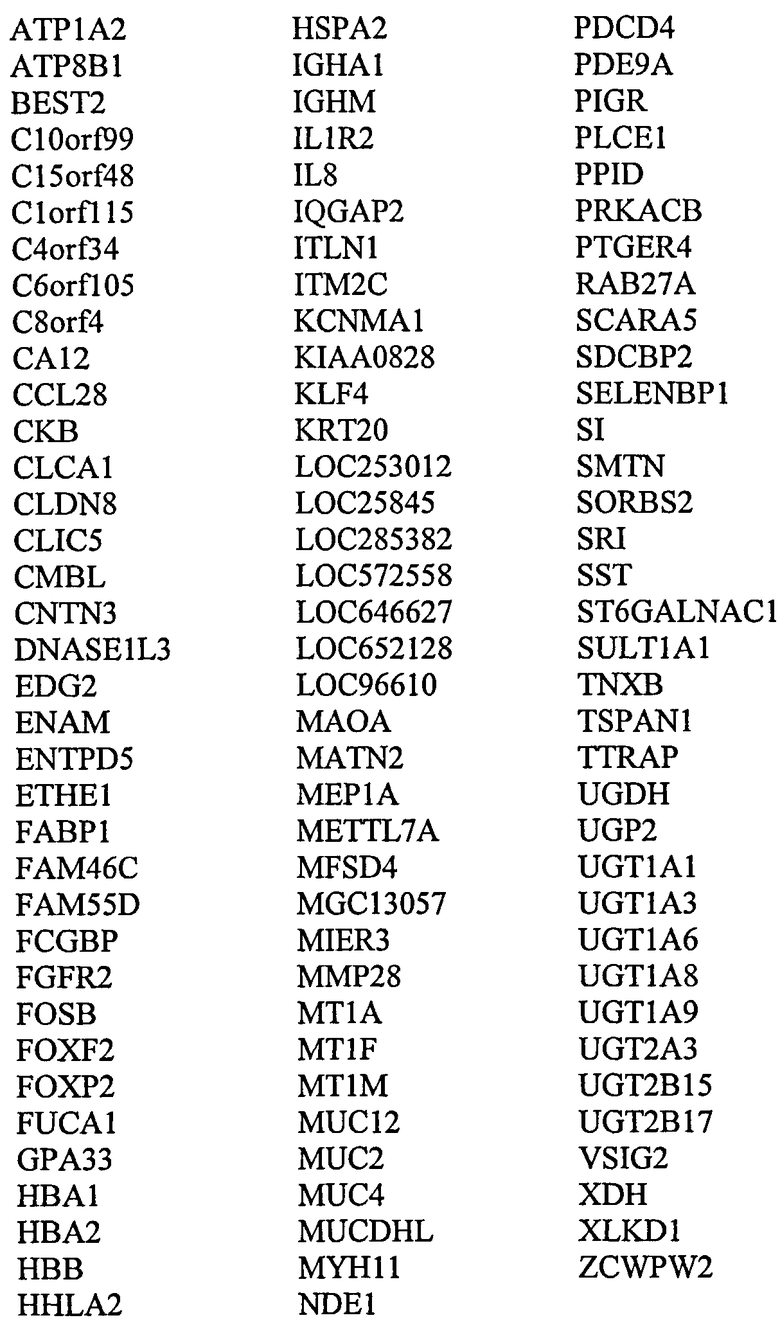
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем раковой клетки толстой кишки или клетки, предрасположенной к появлению состояния рака.
В еще одном аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
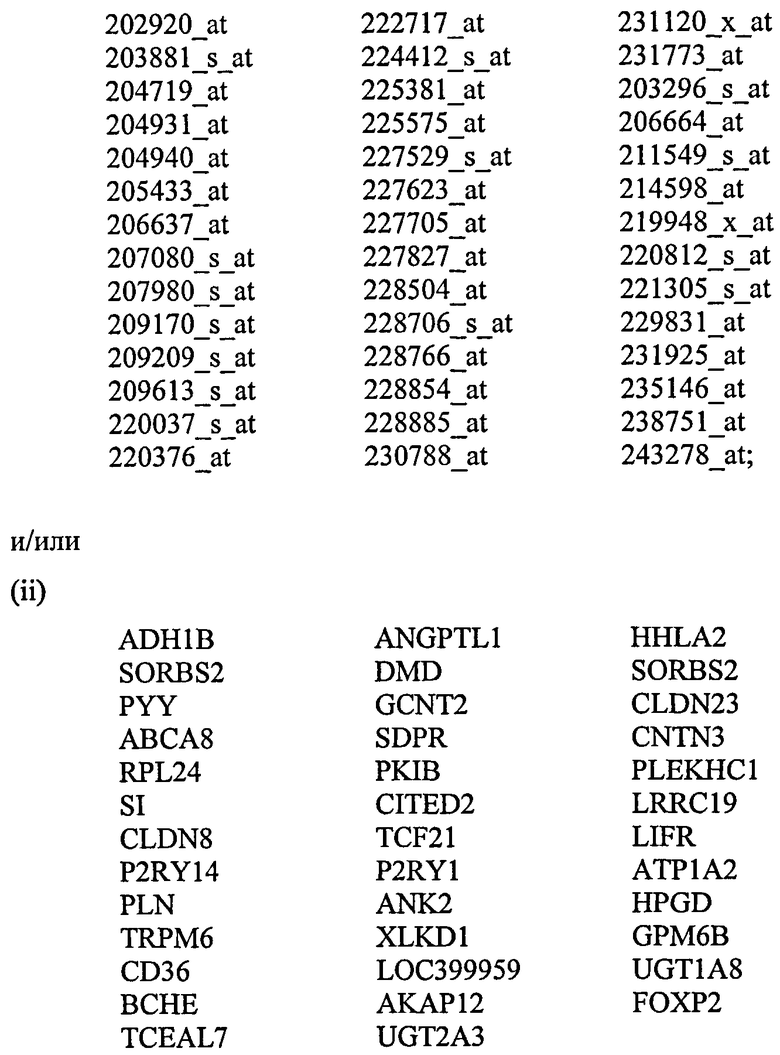
в биологическом образце от указанного индивидуума, где уровень экспрессии генов или транскриптов группы (i) и/или группы (ii), который, по существу, не выше фоновых уровней, является показателем неопластической клетки или клетки, предрасположенной к появлению неопластического состояния.
В другом аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
209209_s_at, 225381_at, 227529_s_at, 227623_at, 227705_at: и/или
(ii) AKAP12, LOC399959, PLEKHC1, TCEAL7,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii), который, по существу, не выше фоновых уровней, является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В еще одном другом аспекте изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из

в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii), который, по существу, не выше фоновых уровней, является показателем раковой клетки или клетки, предрасположенной к появлению состояния рака.
В одном другом аспекте изобретение относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из


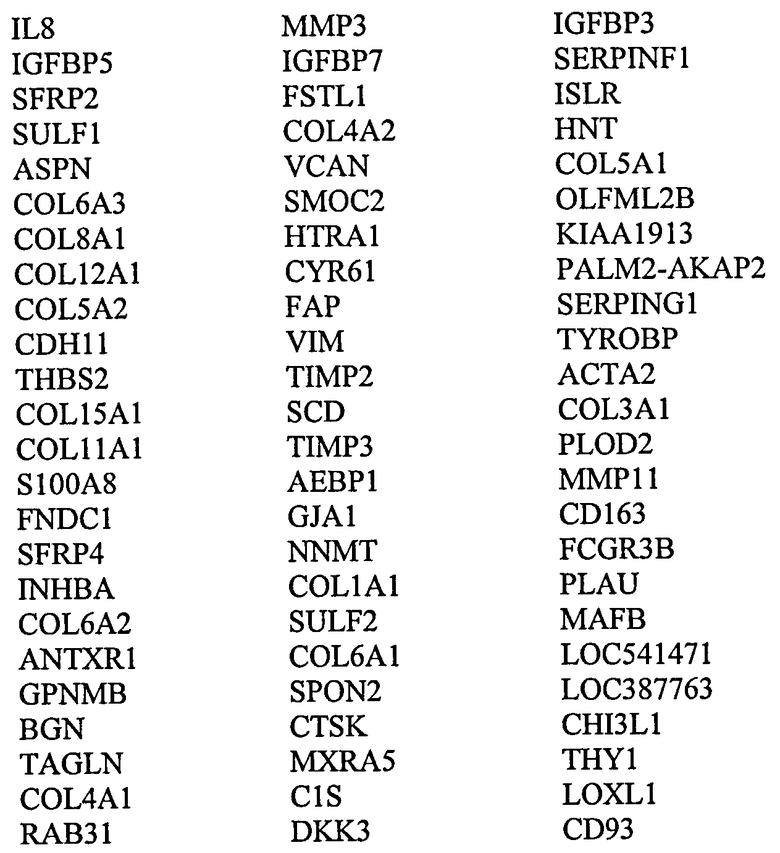
в указанной клетке или популяции клеток, где более низкий уровень экспрессии генов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинального рака является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В еще одном другом аспекте изобретение относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
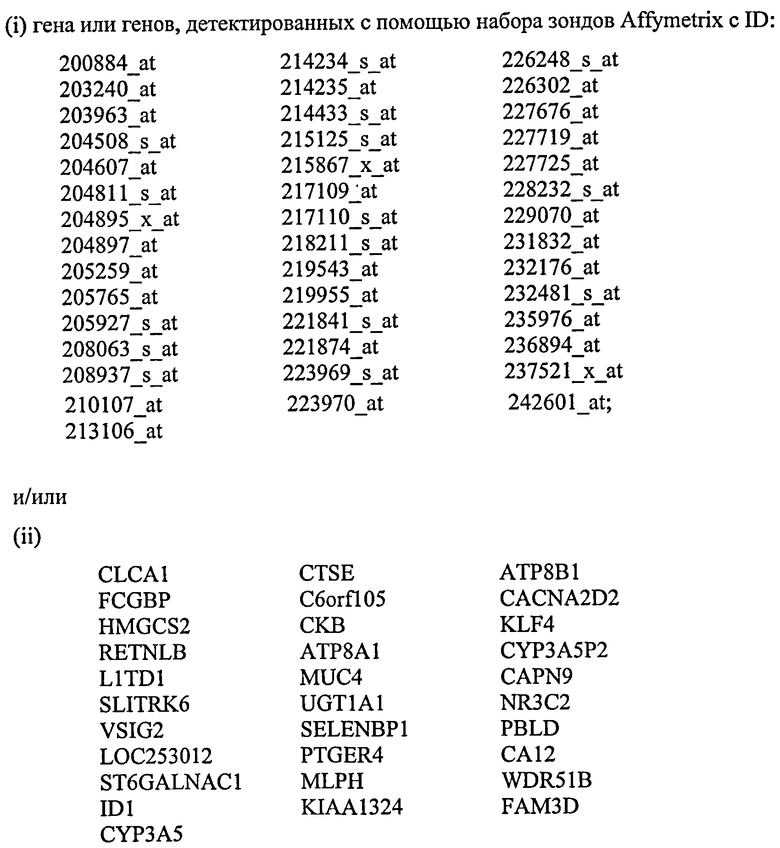
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинальной аденомы является показателем раковой клетки или клетки, предрасположенной к появлению состояния рака.
В еще одном аспекте изобретение относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
202404_s_at, 212464_s_at, 210809_s_at, 225681_at; и/или
(ii) COL1A2, FN1, POSTN, CTHRC1,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинального рака является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В еще одном другом аспекте изобретение относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
209875_s_at, 227140_at, 204475_at; и/или
(ii) SPP1, MMP1,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинального рака является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В еще одном аспекте настоящее изобретение относится к способу характеризации клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
202404_s_at, 212464_s_at, 210809_s_at, 225681_at;
и/или
(ii) COL1A2, FN1, POSTN, CTHRC1
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинального рака является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В еще одном аспекте изобретение относится к способу характеризации клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
210107_аt; и/или
(ii) CLCA1,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинальной аденомы является показателем рака или клетки, предрасположенной к появлению состояния рака.
В еще одном аспекте изобретение относится к способу характеризации клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
209875_s_at, 227140_at, 204475_at;
и/или
(ii) SPP1, MMP1
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинальной аденомы является показателем рака или клетки, предрасположенной к появлению состояния рака.
Другой аспект настоящего изобретения относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена или генов, детектированных с помощью набора зондов Affymetrix с ID:
235976_at, 236894_at, 237521; и/или
(ii) SLITRK6, L1TD1,
в биологическом образце от указанного индивидуума, где экспрессия генов или транскриптов группы (i) и/или группы (ii) на уровне, который, по существу, не выше фоновых уровней неопластической ткани, является показателем рака или клетки, предрасположенной к появлению рака состояния рака.
Родственный аспект настоящего изобретения относится к молекулярной матрице, которая включает совокупность
(i) молекул нуклеиновой кислоты, включающих нуклеотидную последовательность, соответствующую любому одному или нескольким неопластическим маркерным генам, описанным в данном описании ранее, или последовательность, показывающую, по меньшей мере, 80% идентичность к ним, или функциональных производных, фрагментов, вариантов или гомологов указанных молекул нуклеиновой кислоты; или
(ii) молекул нуклеиновой кислоты, включающих нуклеотидную последовательность, способную в условиях гибридизации средней строгости к гибридизации с любой одной или несколькими последовательностями из (i), или функциональных производных, фрагментов, вариантов или гомологов указанных молекул нуклеиновой кислоты; или
(iii) нуклеотидных зондов или олигонуклеотидов, включающих нуклеотидную последовательность, способную в условиях гибридизации средней строгости к гибридизации с любой одной или несколькими последовательностями из (i) или функциональными производными, фрагментами, вариантами или гомологами указанных молекул нуклеиновой кислоты; или
(iv) зондов, способных связываться с любым одним или несколькими белками, кодированными молекулами нуклеиновой кислоты из (i) или их производными, фрагментами или гомологами,
где уровень экспрессии указанных маркерных генов из (i) или белков из (iv) является показателем неопластического состояния клетки или субпопуляции клеток, полученных из толстой кишки.
Краткое описание фигур
Фигура 1 является графическим представлением бета-полипептида алкогольдегидрогеназы IB (класс I).
Фигура 2 является графическим представлением метилирования MAMDC2 и GPM6B в здоровых и неопластических тканях и клеточных линиях. Панель А показывает уровень метилирования гена MAMDC2, оцененного специфической ПЦР метилирования с использованием амплификации гена CAGE для нормализации для уровней исходной ДНК. Каждая точка представляет образец ткани индивидуума или клеточной линии. Образцы включают ДНК из 18 тканей колоректального рака, 12 колоректальных аденом, 22 соответствующих здоровых колоректальных тканей, 6 других здоровых тканей и клеточную линию и 6 клеточных линий рака ободочной кишки. Панель В показывает относительный уровень метилирования гена GPM6B, оцененный анализом COBRA. Уровни метилирования оцениваются от 0 (отсутствие расщепления рестриктазой) до 5 (полное расщепление рестриктазой). Каждая точка представляет образец одной ткани. Образцы включают 14 тканей колоректального рака, 11 колоректальных аденом и 22 соответствующие здоровые ткани.
Фигура 3 является схематическим представлением предсказанных вариантов РНК, полученных из hCG_1815491. Клоны кДНК, полученные из участка генетической карты 85793010 - 8562303 на человеческой хромосоме 16, используют для локализации последовательностей экзонов. Стрелки: наборы олигонуклеотидных праймеров создают для измерения ПЦР отдельных вариантов РНК. Праймеры, перекрывающие экзон-интронные стыки, показаны как распространяющиеся на последовательности интронов, которые не включаются в фактическую последовательность олигонуклеотидного праймера.
Осуществление изобретения
Настоящее изобретение прогнозировано частично на выяснении профилей экспрессии генов, которые характеризуют популяции клеток толстой кишки в смысле их неопластического состояния, и конкретнее, являются ли они злокачественными или находятся в состоянии злокачественного перерождения. Такое открытие теперь облегчает разработку простых способов скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки или характеризации популяций клеток, полученных из толстой кишки, на основании скрининга на отрицательную регуляцию экспрессии таких молекул относительно картин и уровней экспрессии контроля. С этой целью, кроме оценки уровней экспрессии подчиненных генов относительно нормальных или ненеопластических уровней, определяют, какая доля таких генов не экспрессирована в болезненном состоянии, причем посредством этого облегчается разработка простого качественного теста, основанного на потребности только в оценке относительно проверенных фоновых уровней.
Согласно настоящему изобретению определено, что гены, подробно описанные выше, модулируются в смысле различных изменений их уровней экспрессии в зависимости от того, является ли экспрессирующая указанный ген клетка неопластической или не является. Следует иметь в виду, что упоминание о «продукте экспрессии» гена или об «экспрессии гена» является упоминанием или о продукте транскрипции (таком как первичная РНК или мРНК) или о продукте трансляции, таком как белок. В этом отношении можно оценить изменения уровня экспрессии гена или скринингом в отношении уровня продукта экспрессии, который выработан (т.е. РНК или белка), или изменениями в белках хроматина, с которыми ген ассоциирован, например, присутствием гистона Н3, метилированного по лизину в позиции аминокислот за номерами 9 или 27 (репрессивная модификация), или изменениями в самой ДНК, которые действуют, отрицательно регулируя экспрессию, такими как изменения метилирования ДНК. Такие гены и продукты их экспрессии, являются ли они транскриптами РНК, изменениями в ДНК, которые действуют, отрицательно регулируя экспрессию, или кодированными белками, все вместе называются «неопластическими маркерами».
Соответственно, один аспект настоящего изобретения относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из

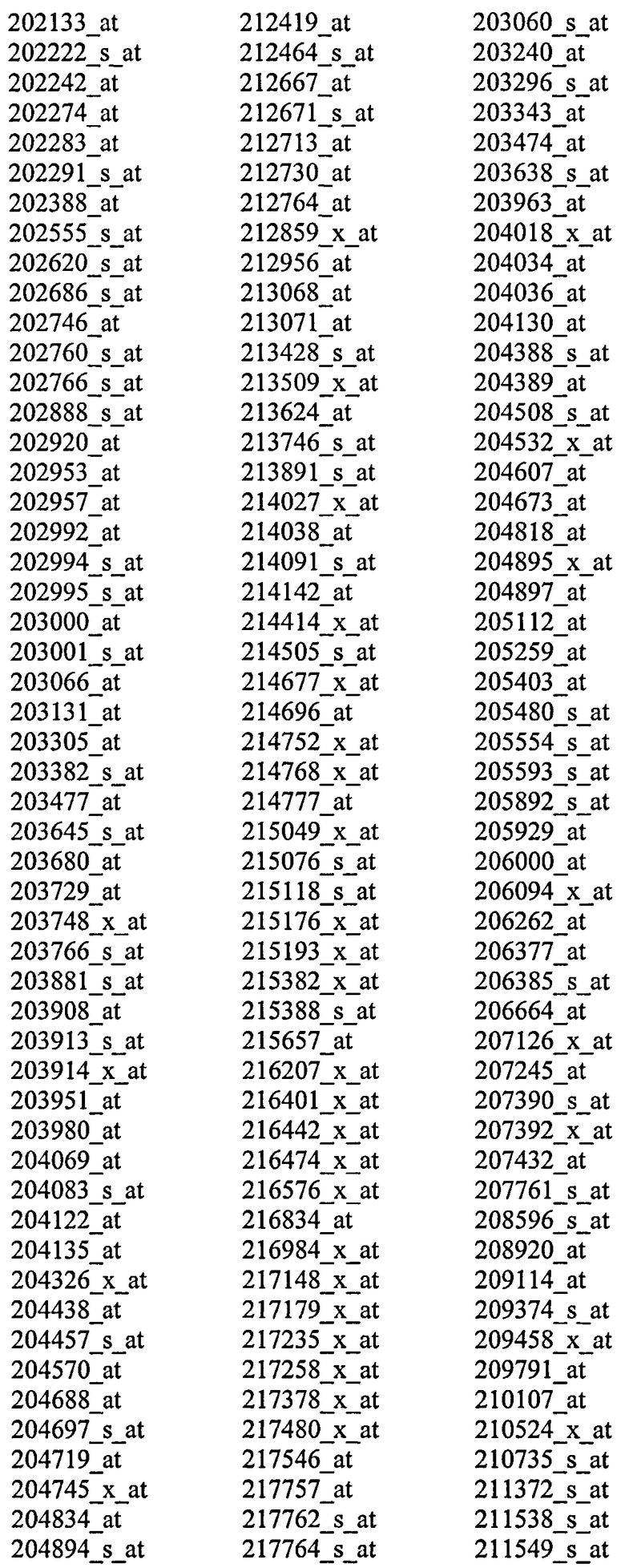





в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
В одном воплощении указанную экспрессию оценивают скринингом на изменения ДНК, которые оказывают воздействие на метилирование, в частности, гиперметилирование. В другом воплощении экспрессию оценивают по ассоциации ДНК с белками хроматина, содержащими репрессивные модификации, например, метилирование лизинов 9 или 27 гистона Н3.
Обозначение «толстая кишка» следует понимать как обозначение клетки, полученной из одного из шести анатомических участков толстой кишки, которые начинаются после конечного участка подвздошной кишки, представляющих собой
(i) слепую кишку;
(ii) восходящую ободочную кишку;
(iii) поперечную ободочную кишку;
(iv) нисходящую ободочную кишку;
(v) сигмовидную ободочную кишку и
(vi) прямую кишку.
Обозначение «неоплазма» следует понимать как обозначение повреждения, опухоли или другой инкапсулированной или некапсулированной массы или другой формы роста, которая включает неопластические клетки. Обозначение «неопластическая клетка» следует понимать как обозначение клетки, проявляющей анормальный рост. Термин «рост» следует понимать в его самом широком смысле, и он включает обращение к пролиферации. В этом отношении примером анормального роста клетки является нерегулируемая пролиферация клетки. Другим примером является отсутствие апоптоза в клетке, причем таким образом пролонгируется ее обычная продолжительность жизни. Неопластическая клетка может быть доброкачественной клеткой или злокачественной клеткой. В предпочтительном воплощении обсуждаемая неоплазма представляет собой аденому или аденокарциному. Без ограничения настоящего изобретения какой-либо теорией или способом действия, аденома обычно является доброкачественной опухолью эпителиального происхождения, которая или образована из эпителиальной ткани, или проявляет четко выраженные эпителиальные структуры. Такие структуры могут принимать вид желез. Популяция злокачественных клеток может заключаться в аденоме, так что происходит развитие доброкачественной аденомы в злокачественную аденокарциному.
Предпочтительно, указанная неопластическая клетка представляет собой аденому или аденокарциному, и даже предпочтительнее, колоректальную аденому или аденокарциному.
Каждый из генов и транскриптов, указанный выше в деталях в подразделах (i) и (ii), может быть хорошо известен специалистам в данной области техники, как и кодированные ими белки. Идентификация продуктов экспрессии таких генов и транскриптов как маркеров неоплазии происходит на основании анализа дифференциальной экспрессии с использованием генных чипов Affymetrix HGU133A или HGU133B. С этой целью каждый генный чип характеризуется набором приблизительно 45000 зондов, которые детектируют РНК, транскрибированную с генома. В среднем приблизительно 11 пар зондов детектируют перекрывающиеся или последовательные участки транскрипта РНК. Вообще, гены, РНК-транскрипты которых, описанные в данном описании, можно идентифицировать с помощью наборов зондов Affymetrix, являются хорошо известными и охарактеризованными генами. Однако в рамках, когда некоторые наборы зондов детектируют РНК-транскрипты, которые еще не определены, такие транскрипты указываются как «ген, гены или транскрипты, детектированные зондом Affymetrix х». В некоторых случаях ряд генов можно детектировать с помощью одного набора зондов. Однако следует иметь в виду, что это не рассматривается как ограничение того, каким образом можно определить уровень экспрессии рассматриваемого гена или транскрипта. В первом случае следует иметь в виду, что рассматриваемый ген или транскрипт также можно детектировать другими наборами зондов, которые могут присутствовать на генном чипе Affymetrix. Ссылка на один набор зондов включается просто как идентификатор генного транскрипта, представляющего интерес. Однако в условиях фактического скрининга в отношении транскрипта можно использовать зонд или набор зондов, направленные на любой участок транскрипта, а не только к 3-концевому участку транскрипта в 600 п.о., к которому обычно направлены зонды Affymetrix.
Следовательно, ссылку на каждый из генов и транскриптов, детализированных выше, и их транскрибированные и транслированные продукты экспрессии следует понимать как ссылку на все формы таких молекул и их фрагменты и варианты. Как будет понятно для специалистов в данной области техники, известно, что некоторые гены демонстрируют аллельную вариацию между индивидуумами. Соответственно, следует иметь в виду, что настоящее изобретение распространяется на такие варианты, которые, в условиях диагностических применений по настоящему изобретению достигают одинакового результата несмотря на тот факт, что могут существовать минорные генетические варианты между фактическими нуклеотидными последовательностями индивидуумов, или что у одного индивидуума могут иметься 2 или больше вариантов сплайсинга обсуждаемого гена. Поэтому следует иметь в виду, что настоящее изобретение распространяется на все формы РНК (напр., мРНК, первичный РНК-транскрипт, миРНК и т.д.), кДНК и пептидные изоформы, которые возникают из альтернативного сплайсинга или любой другой мутации, полиморфной или аллельной вариации. Также следует иметь в виду, что включены ссылки на любые субъединичные полипептиды, такие как предшествующие формы, которые могут быть образованы, существуют ли они как мономеры, мультимеры, слитые белки или другие комплексы.
С этой целью, в отношении генов, охваченных настоящим изобретением, в примере 6 описаны способы определения наличия таких вариантов и их характеризации. До пределов, в которых гены по настоящему изобретению описаны путем обращения к набору зондов Affymetrix, таблица 6 , приведенная в графической части, дает детали нуклеотидной последовательности, к которой направлен каждый зонд. На основании такой информации специалист может, осуществляя обычную процедуру, идентифицировать ген, в отношении которого данная последовательность образует часть. Типичный протокол осуществления этого также изложен в примере 6.
Следует иметь в виду, что «индивидуум», который является объектом испытания, может представлять собой любое млекопитающее - человека или млекопитающее, не являющееся человеком. Примеры млекопитающих, не относящихся к человеку, включают приматов, домашний скот (например, лошадей, крупный рогатый скот, овец, свиней, ослов), лабораторных подопытных животных (например, мышей, крыс, кроликов, морских свинок), домашних животных (например, собак, кошек) и содержащихся в неволе диких животных (например, оленей, лис). Предпочтительно, млекопитающее представляет собой человека.
Способ по настоящему изобретению основан на сравнении уровня неопластических маркеров биологического образца с контрольными уровнями таких маркеров. «Контрольный уровень» может представлять собой любой «нормальный уровень», который является уровнем маркера, экспрессируемого соответствующей клеткой толстой кишки или популяцией клеток, который не является неопластическим.
Нормальный (или «ненеопластический») уровень можно определить с использованием тканей, полученных от того же индивидуума, который является объектом проверки. Однако следует признать, что такой уровень может быть действительно инвазивным для рассматриваемого субъекта и поэтому, вероятно, в итоге более удобным для анализа результатов испытания относительно эталонного результата, который отражает отдельные или общие результаты, полученные для индивидуумов иных, чем пациент. Такая последняя форма анализа действительно является предпочтительным методом анализа, так как допускает создание наборов, которые требуют собирания, и анализ отдельного биологического образца, являющегося образцом для испытания, представляющим интерес. Эталонные результаты, которые предоставляют нормальный уровень, можно вычислить любым подходящим способом, который может быть хорошо известен специалисту в данной области техники. Например, можно оценить популяцию здоровых тканей' в отношении уровня неопластических маркеров по настоящему изобретению, причем посредством этого получают эталонную величину или интервал величин, относительно которых анализируют все будущие опытные образцы. Также следует иметь в виду, что нормальный уровень можно определить, исходя из субъектов определенной когорты, и использовать в отношении опытных образцов, полученных от указанной когорты. Соответственно, можно определить ряд эталонных величин или интервалов, которые соответствуют когортам, различающимся по таким характеристикам, как возраст, пол, расовая принадлежность или состояние здоровья. Указанный «нормальный уровень» может быть дискретным уровнем или интервалом уровней. Снижение уровня экспрессии генов субъекта относительно нормальных уровней является показателем того, что ткань является неопластической.
Без ограничения настоящего изобретения какой-либо теорией или типом действия, хотя каждый из генов или транскриптов, описанных в данном описании ранее, экспрессируется дифференциально - или один или в сочетании, как неопластические в сравнении с ненеопластическими клетками толстой кишки, и поэтому это является диагностикой наличия неоплазмы толстой кишки, обнаружено, что экспрессия некоторых таких генов демонстрирует особенно значимые уровни чувствительности, специфичности и положительную и отрицательную предсказательную ценность. Соответственно, в предпочтительном воплощении возможен скрининг в отношении оценки уровня экспрессии одного или нескольких таких генов. С этой целью, и без ограничения настоящего изобретения какой-либо теорией или типом действия, указанные далее маркеры определены как экспрессируемые в неопластической ткани на уровне в 3-11 раз меньше, чем в ненеопластической ткани, при оценке на основании метода, приведенного в данном описании в качестве примера.
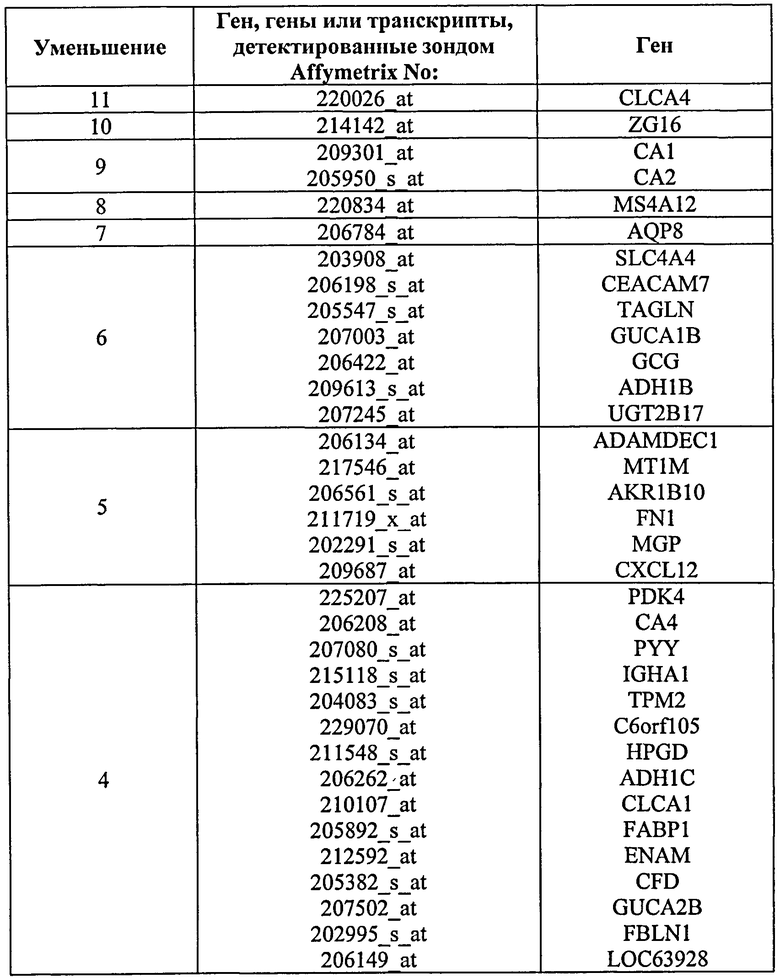
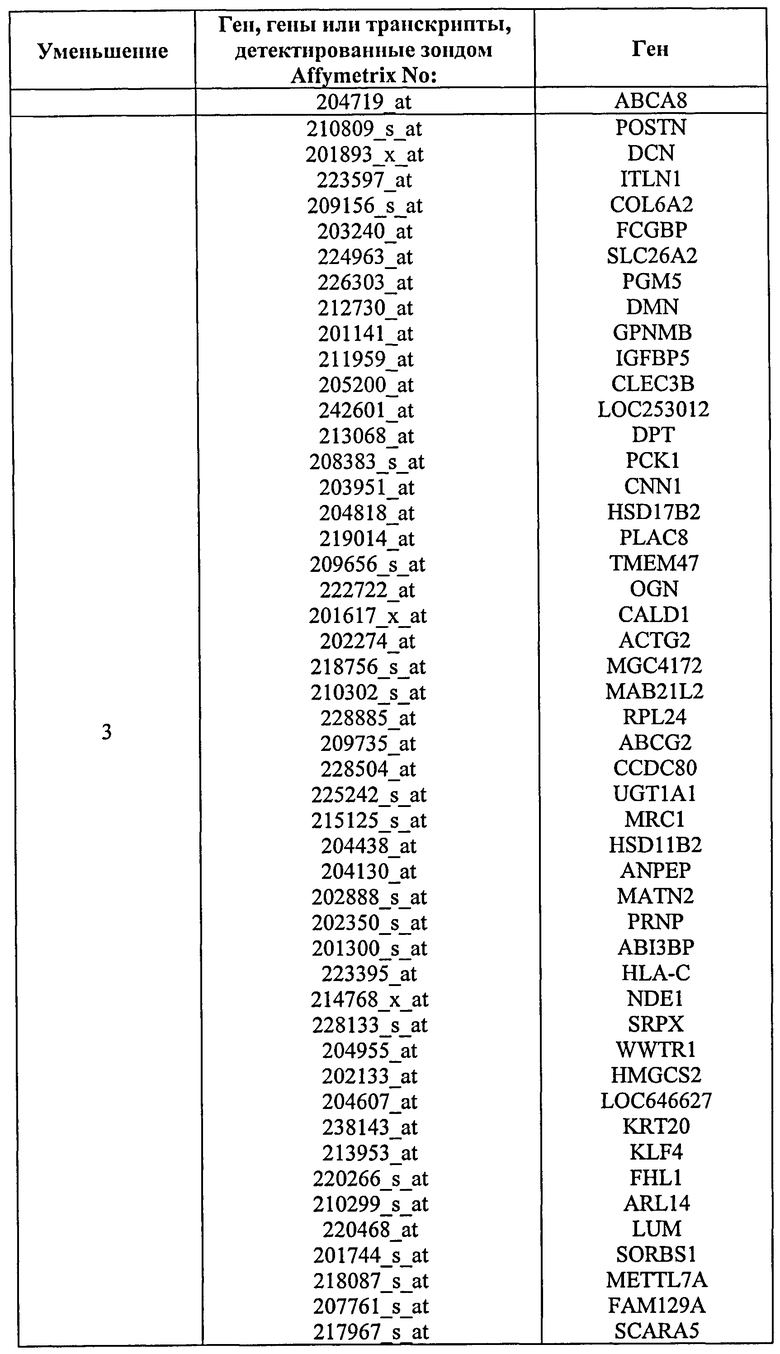

Поэтому конкретнее описывается способ скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
2200026_at; и/или
(ii)_CLCA4,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии гена или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
В другом воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
214142_at; и/или
(ii) ZG16,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
В еще одном воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
209301_at, 205950_s__at; и/или
(ii) CA2, СА1,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
В еще одном предпочтительном воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
220834_at; и/или
(ii) MS4A12,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
В еще одном воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
206784_at; и/или
(ii) AQP8,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
В другом воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
203908_at, 206198_s_at, 205547_s_at, 207003_at, 206422_at, 209613_s_at, 207245_at; и/или
(ii) SLC4A4, CEACAM7, TAGLN, GUCA1B, GCG, ADH1B, UGT2B17,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
В еще другом воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
206134_at, 217546_at, 206561_s_at, 211719_x_at, 202291_s_at, 209687_at; и/или
(ii) ADAMDEC1, MT1M, AKR1B10, FN1, MGP, CXCL12,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
В еще одном другом воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из

в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
В еще одном еще другом воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг в отношении уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
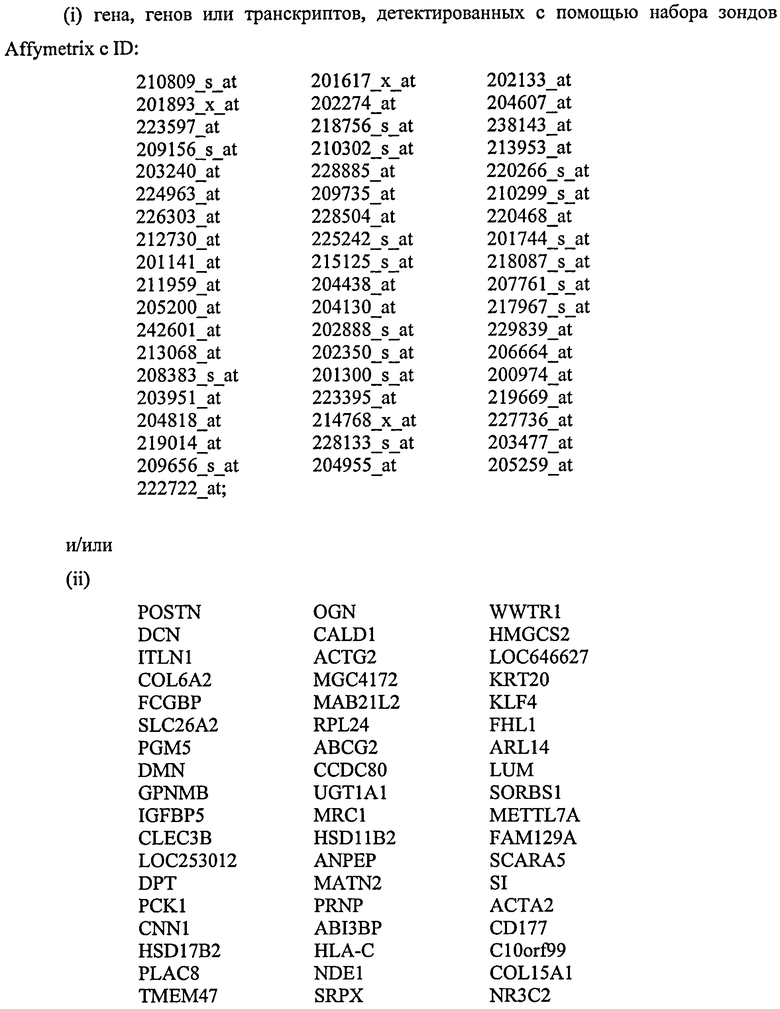
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
Предпочтительно, указанный контрольный уровень является ненеопластическим уровнем.
Согласно указанным аспектам настоящего изобретения указанная ткань толстой кишки предпочтительно является колоректальной тканью.
В одном воплощении указанную экспрессию оценивают скринингом в отношении ДНК, которые оказывают воздействие на метилирование, в частности, гиперметилирование. В другом воплощении экспрессию оценивают по ассоциации ДНК с белками хроматина, содержащими репрессивные модификации, например, метилирование лизинов 9 или 27 гистона Н3.
Способ детекции по настоящему изобретению можно выполнить на любом биологическом образце. Для такой цели обозначение «биологический образец» следует понимать как обозначение любого образца биологического материала, полученного от животного, такого как, но без ограничения, клеточный материал, биологические жидкости (напр., кровь), фекалии, образцы тканей (такие как образцы биопсии), образцы от операции или жидкость, которая вводилась в тело животного и затем удалялась (такая как, например, раствор, возвращенный после промывки клизмой). Биологический образец, который проверяют согласно способу по настоящему изобретению, можно испытывать непосредственно, или может потребоваться некоторая форма обработки перед испытанием, или может потребоваться изготовление срезов для испытания in situ качественных уровней экспрессии отдельных генов. С другой стороны, для клеточного образца может потребоваться предварительная иммобилизация перед испытанием. Далее, в случае, когда биологический образец находится не в жидкой форме (если такая форма требуется для испытания), может потребоваться добавление реагента, такого как буфер, для мобилизации образца.
В случае, когда продукт экспрессии гена неопластический маркер присутствует в биологическом образце, биологический образец можно испытать непосредственно, или все или некоторые материалы с нуклеиновыми кислотами можно выделить перед испытанием. В еще одном примере образец перед анализом можно частично очистить или обогатить иначе. Например, в случае, когда биологический образец включает весьма разнообразную популяцию клеток, может быть желательно обогащение в отношении субпопуляции, представляющей особый интерес. В объем настоящего изобретения входит предварительная обработка перед испытанием популяции-мишени клеток или молекул, полученных из нее, например, инактивация живого вируса или обработка в геле. Также следует иметь в виду, что биологический образец может являться свежесобранным или он может храниться (например, за счет замораживания) до испытания или иначе обрабатываться перед испытанием (например, подвергаться культивированию).
Выбор типа образца, наиболее подходящего для испытания согласно способу, раскрытому в данном описании, будет зависеть от характера ситуации. Предпочтительно, указанный образец представляет собой образец фекалий (стула), жидкость после клизмы, операционный материал, образец крови или ткани.
В родственном аспекте определяется, что маркеры, определенные в данном описании ранее, являются более показательными для развития аденомы в сравнении с развитием рака или наоборот. Это очень ценное открытие, так как оно позволяет более специфично характеризовать возможный характер неоплазмы, которая детектирована на основании способа по настоящему изобретению.
Соответственно, в родственном аспекте настоящее изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из


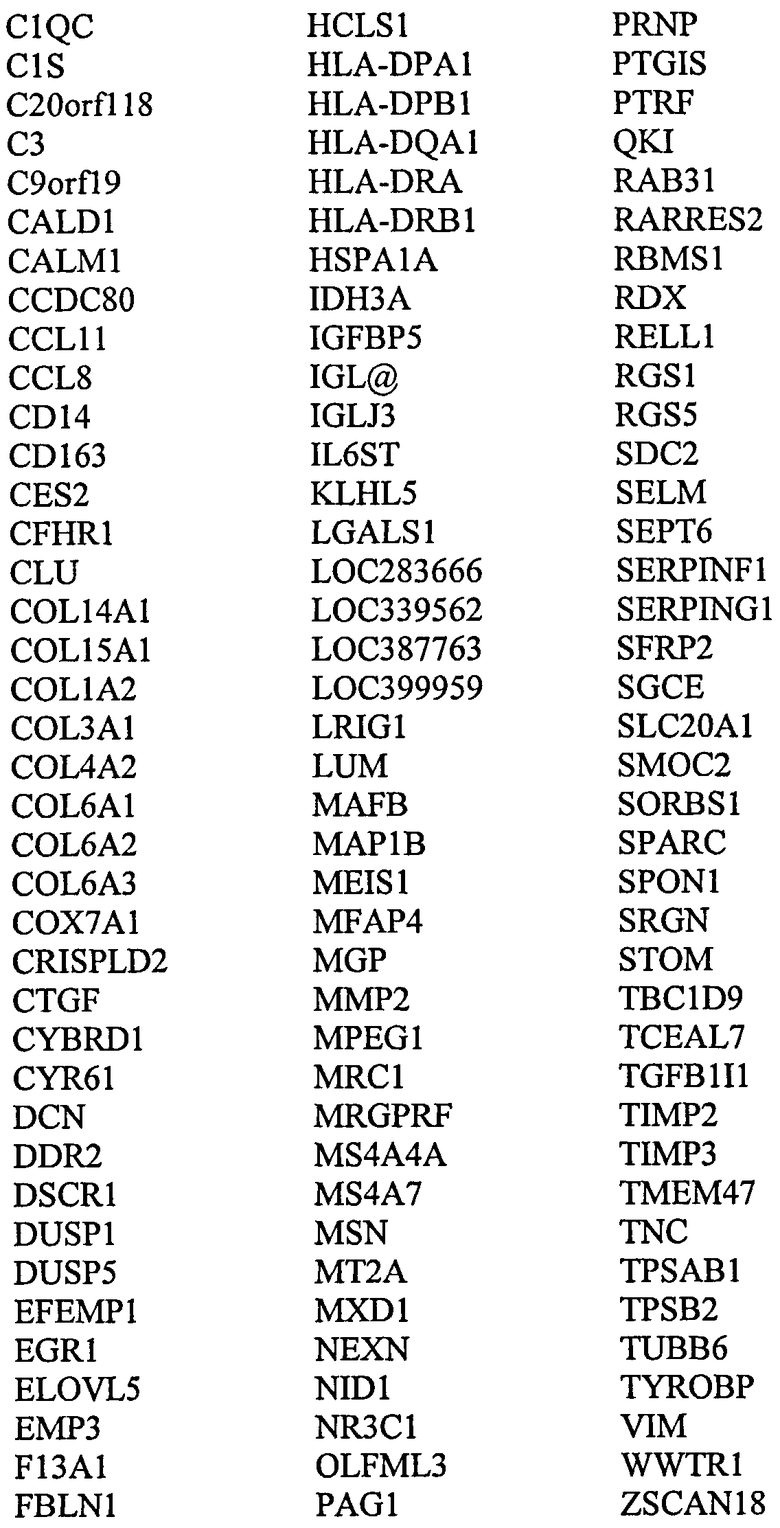
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В другом предпочтительном воплощении данного аспекта настоящее изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из

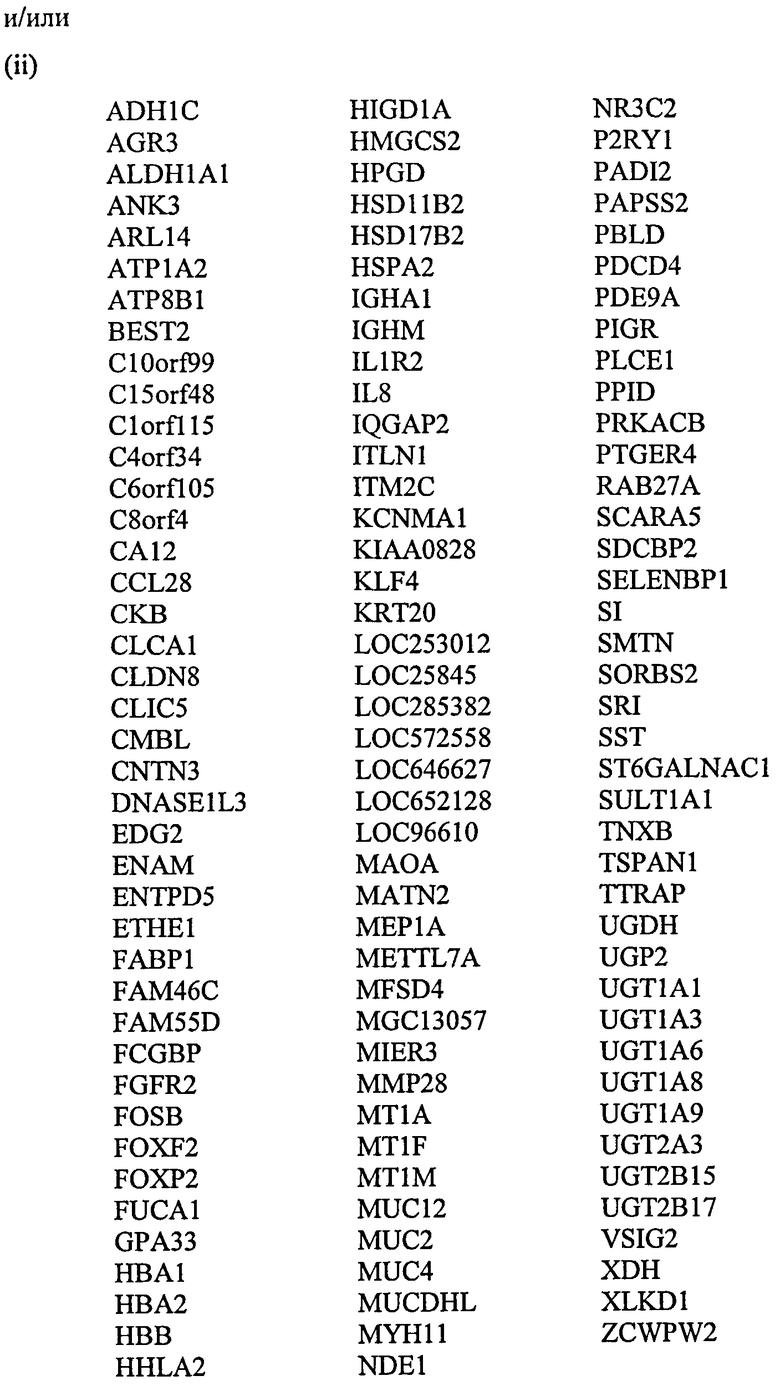
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем раковой клетки или клетки, предрасположенной к появлению состояния рака.
Согласно таким аспектам указанные контрольные уровни предпочтительно являются ненеопластическими уровнями, и указанная ткань толстой кишки представляет собой колоректальную ткань. Даже предпочтительнее, указанный биологический образец является образцом стула или образцом крови.
В одном воплощении указанную экспрессию оценивают скринингом в отношении ДНК, которые оказывают воздействие на метилирование, в частности, гиперметилирование. В другом воплощении экспрессию оценивают по ассоциации ДНК с белками хроматина, содержащими репрессивные модификации, например, метилирование лизинов 9 или 27 гистона Н3.
В родственном аспекте определяется, что субпопуляция маркеров по настоящему изобретению не только экспрессируется на уровнях более низких, чем нормальные уровни, но картина их экспрессии уникально характеризуется тем фактом, что уровни экспрессии выше, что фоновые контрольные уровни не детектируются в неопластической ткани. Следовательно, такое определение дает возможность разработки систем качественного скрининга, которые просто создаются для детектирования экспрессии с маркером относительно контрольного фонового уровня. Поэтому согласно данному аспекту настоящего изобретения указанный «контрольный уровень» является «фоновым уровнем».
Поэтому согласно данному аспекту изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг на уровень экспрессии одного или нескольких генов или транскриптов, выбранных из

в биологическом образце от указанного индивидуума, где уровень экспрессии генов или транскриптов группы (i) и/или группы (ii), который, по существу, не превышает вышеуказанные фоновые уровни, является показателем неопластической клетки или клетки, предрасположенной к появлению неопластического состояния.
В наиболее предпочтительном воплощении указанные гены или транскрипты выбирают из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
209613_s_at, 227827_at, 204719_at, 228504_at, 228885_at, 206664_at, 207080_s_at;
и/или
(ii) ADH1B, SORBS2, PYY, ABCA8, RPL24, SI.
Предпочтительно, указанная неоплазма представляет собой аденому или аденокарциному, и указанная гастроинтестинальная ткань представляет собой колоректальную ткань.
В еще одном воплощении определяется, что другая субпопуляция указанных маркеров более характеристична для развития аденомы, в то время как другие более характеристичны для развития рака. Соответственно, предлагается удобный способ получения качественно показательной информации в отношении характеристик неоплазмы субъекта.
Согласно такому воплощению, изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг на уровень экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
209209_s_at, 225381_at, 227529_s_at, 227623_at, 227705_at: и/или
(ii) AKAP12, LOC399959, PLEKHC1, TCEAL7,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii), который, по существу, не выше фоновых уровней, является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В еще одном предпочтительном воплощении изобретение относится к способу скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, причем указанный способ включает скрининг на уровень экспрессии одного или нескольких генов или транскриптов, выбранных из

в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii), который, по существу, не выше фоновых уровней, является показателем раковой клетки или клетки, предрасположенной к появлению состояния рака.
Предпочтительно, указанная ткань толстой кишки представляет собой колоректальную ткань.
Предпочтительнее, указанный биологический образец представляет собой образец стула или образец крови.
В одном воплощении указанную экспрессию оценивают скринингом в отношении ДНК, которые оказывают воздействие на метилирование, в частности, гиперметилирование. В другом воплощении экспрессию оценивают по ассоциации ДНК с белками хроматина, содержащими репрессивные модификации, например, метилирование лизинов 9 или 27 гистона Н3.
Как подробно описано ранее, настоящее изобретение создано для скрининга в отношении неопластической клетки или популяции клеток, которые располагаются в толстой кишке. Соответственно, обозначение «клетка или популяция клеток» следует понимать как обозначение отдельной клетки или группы клеток. Указанная группа клеток может представлять собой диффузную популяцию клеток, клеточную суспензию, инкапсулированную популяцию клеток или популяцию клеток, которая принимает форму ткани.
Обозначение «экспрессия» следует понимать как обозначение транскрипции и/или трансляции молекулы нуклеиновой кислоты. В этом отношении настоящее изобретение поясняется примерами, касающимися скрининга в отношении продуктов экспрессии неопластических маркеров, принимающих форму РНК-транскриптов (например, первичной РНК или мРНК). Обозначение «РНК» следует понимать как общее обозначение любой формы РНК, такой как первичная РНК или мРНК. Без ограничения настоящего изобретения каким-либо путем, модуляция транскрипции генов, ведущая к усиленному или ослабленному синтезу РНК, также будет коррелировать с трансляцией некоторых таких РНК-транскриптов (таких как мРНК) для получения белкового продукта. Соответственно, настоящее изобретение также распространяется на методологию детекции, которая направлена на скрининг в отношении модулированных уровней или картин белковых продуктов неопластических маркеров как индикатора неопластического состояния клетки или популяции клеток. Хотя один способ состоит в скрининге на РНК-транскрипты и/или соответствующий белковый продукт, следует иметь в виду, что настоящее изобретение не ограничивается в этом отношении и распространяется на скрининг в отношении любой формы продукта экспрессии неопластического маркера, такой как, например, первичный РНК-транскрипт.
Что касается скрининга в отношении отрицательной регуляции экспрессии маркера, специалистам в данной области техники должно быть хорошо известно, что изменения, которые можно обнаружить в уровне ДНК, являются показателями изменений активности экспрессии гена и, следовательно, изменений уровней экспрессии продукта. Такие изменения включают изменения метилирования ДНК и не только. Соответственно, ссылка в данном описании на «скрининг на уровень экспрессии» и сравнение таких «уровней экспрессии» для контроля «уровней экспрессии» следует понимать как обращение к факторам оценки ДНК, которые связаны с транскрипцией, таких как профили метилирования гена/ДНК.
Специалистам в данной области техники также должно быть хорошо известно, что изменения в структуре хроматина являются показателями изменений в экспрессии генов. Сайленсинг экспрессии генов часто ассоциируется с модификацией белков хроматина, метилированием лизинов в любой или в обеих позициях 9 и 27 гистона Н3, являющегося хорошо изученным примером, в то время как активный хроматин маркируется ацетилированием лизина-9 гистона Н3. Таким образом, ассоциацию генных последовательностей с хроматином, содержащим репрессивные или активные модификации, можно использовать для осуществления оценки уровня экспрессии гена.
Специалистам в данной области техники вполне по силам определить наиболее подходящий способ скрининга для любой данной ситуации. С этой целью гены, которых известны как кодирующие продукт экспрессии, который или секретирован клеткой или связан с мембраной, подробно описаны в таблице ниже. Следует признать, что скрининг а отношении неопластических маркеров, которые являются секретированными или мембранно-связанными, может обеспечить определенные преимущества с точки зрения создания диагностического продукта скрининга.
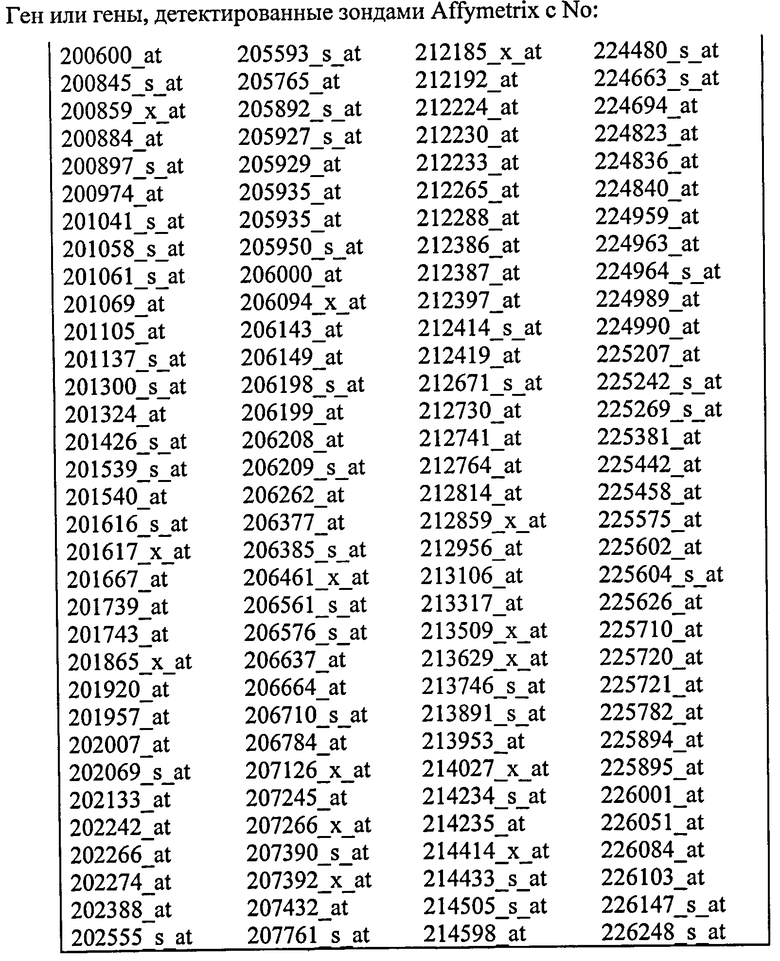

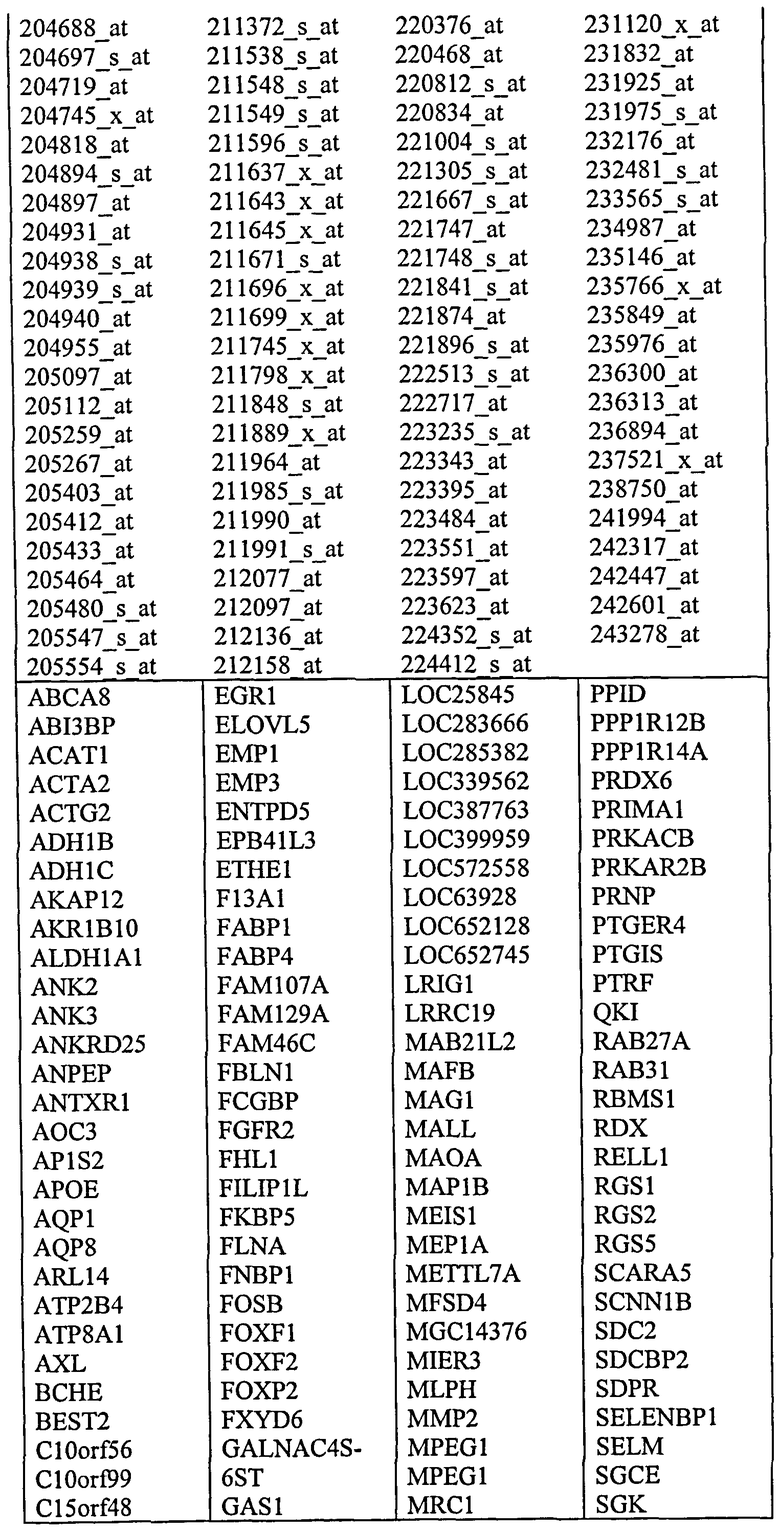
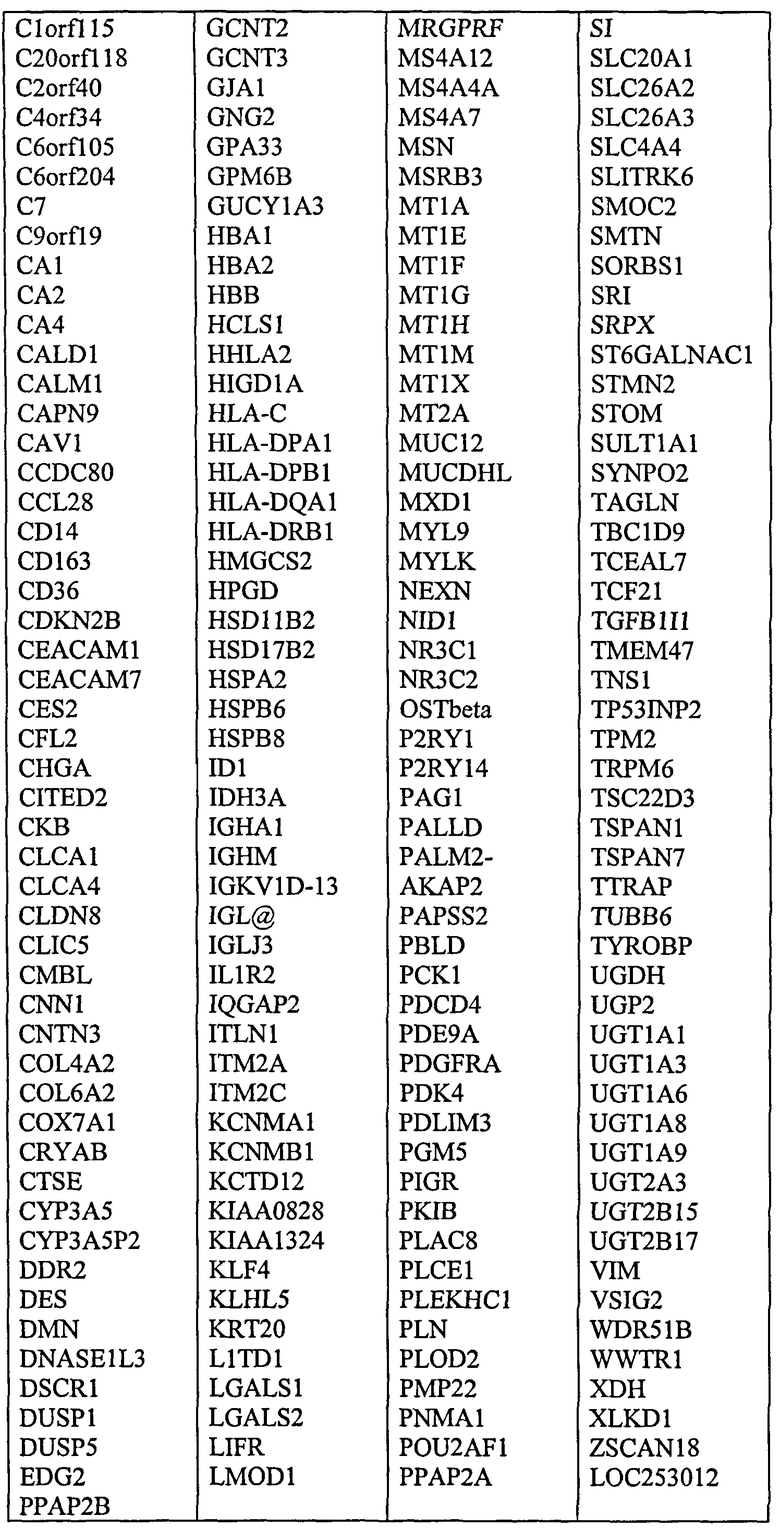
Обозначение «молекула нуклеиновой кислоты» следует понимать как обозначение как молекул дезоксирибонуклеиновой кислоты, так и молекул рибонуклеиновой кислоты и их фрагментов. Следовательно, настоящее изобретение распространяется непосредственно как на скрининг в отношении уровней мРНК в биологическом образце, так и на скрининг в отношении комплементарной кДНК, которая обратно транскрибирована из популяции мРНК, представляющей интерес. Специалистам в данной области техники вполне по силам создать методологию, направленную на скрининг в отношении ДНК или РНК. Как подробно описано выше, способ по настоящему изобретению также распространяется на скрининг в отношении белкового продукта, транслированный с мРНК субъекта или самой геномной ДНК.
В одном предпочтительном воплощении уровень экспрессии генов измеряют, обратившись к генам, которые кодируют белковый продукт, и, конкретнее, указанный уровень экспрессии измеряют по уровню белка. Соответственно, в пределах, в которых настоящее изобретение относится к скринингу в отношении маркеров, которые подробно описаны в предшествующей таблице, указанный скрининг, предпочтительно, направлен на кодированный белок.
В другом особенно предпочтительном воплощении указанную экспрессию генов оценивают по ассоциации ДНК с белками хроматина, содержащими репрессивные модификации, например, метилирование лизинов 9 или 27 гистона Н3.
Как подробно описано ранее, следует иметь в виду, что хотя настоящее изобретение поясняется примерами, касающимися детекции экспрессированных молекул нуклеиновой кислоты (например, мРНК), оно также охватывает способы детекции, основанные на скрининге в отношении белкового продукта генов субъекта. Также следует иметь в виду, что настоящее изобретение охватывает способы детекции, основанные на идентификации как белков, так и/или молекул нуклеиновой кислоты в одном или нескольких биологических образцах. Это может быть особенно существенно в той мере, что некоторые представляющие интерес маркеры могут соответствовать генам или генным фрагментам, которые не кодируют белковый продукт. Соответственно, в тех пределах, в каких это происходит, может не быть возможности испытать белок, и может отсутствовать возможность оценить маркер субъекта на основании транскрипции, профилей экспрессии или изменений геномной ДНК.
Термин «белок» следует понимать как охватывающий пептиды, полипептиды и белки (включая фрагменты белков). Белок может быть гликозилированным или негликозилированным и/или может содержать ряд других молекул, слитых, соединенных или иначе ассоциированных с белком, таких как аминокислоты, липиды, углеводы или другие пептиды, полипептиды или белки. Обозначение в данном описании «белок» включает белок, включающий последовательность аминокислот, а также белок, ассоциированный с другими молекулами, такими как аминокислоты, липиды, углеводы или другие пептиды, полипептиды или белки.
Белки, кодированные неопластическими маркерами по настоящему изобретению, могут находиться в мультимерной форме, означающей, что две или больше молекул ассоциированы друг с другом. Когда ассоциированы одинаковые молекулы, комплекс представляет собой гомомультимер. Примером гомомультимера является гомодимер. Когда, по меньшей мере, один маркерный белок ассоциирован с одним немаркерным белком, тогда комплекс представляет собой гетеромультимер, такой как гетеродимер.
Обозначение «фрагмент» следует понимать как обозначение белка молекулы нуклеиновой кислоты субъекта или белка. Это особенно релевантно в отношении скрининга в отношении модулированных уровней РНК в образце стула, так как РНК субъекта, возможно, претерпела разложение или иначе фрагментирована из-за среды в кишке. Поэтому может являться актуальной детекция фрагментов молекулы РНК субъекта, которые идентифицируются на основании применения подходящего специфического зонда.
Обозначение «появление» неоплазмы, такой как аденома или аденокарцинома, следует понимать как обозначение одной или нескольких клеток индивидуума, показывающих дисплазию. В этом отношении аденома или аденокарцинома могут быть хорошо развитыми в том смысле, что развилась масса диспластических клеток. С другой стороны, аденома или аденокарцинома могут находиться на очень ранней стадии, когда только относительно небольшое число делений аномальных клеток произошло на момент диагностики. Настоящее изобретение также распространяется на оценку предрасположенности индивидуума к развитию неоплазмы, такой как аденома или аденокарцинома. Без ограничения настоящего изобретения какой-либо теорией, измененные уровни неопластических маркеров могут являться показателями предрасположенности индивидуума к развитию неоплазмы, такому как будущее развитие аденомы или аденокарциномы или другой аденомы или аденокарциномы.
В еще одном родственном аспекте настоящего изобретения идентифицированы маркеры, которые дают возможность характеризации неопластической ткани толстой кишки с точки зрения того, является она аденомой или раком. Такая разработка теперь обеспечивает простое, но точное средство характеризации ткани с использованием иных средств, чем традиционные способы, которые используются в настоящее время.
Согласно такому аспекту настоящее изобретение относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из


в указанной клетке или популяции клеток, где более низкий уровень экспрессии генов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинального рака является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В другом аспекте изобретение относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из


в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинальной аденомы является показателем рака или клетки, предрасположенной к появлению состояния рака.
Предпочтительно, указанная гастроинтестинальная ткань является колоректальной тканью.
В одном воплощении указанную экспрессию оценивают скринингом в отношении ДНК, которые оказывают воздействие на метилирование, в частности, гиперметилирование. В другом воплощении экспрессию оценивают по ассоциации ДНК с белками хроматина, содержащими репрессивные модификации, например, метилирование лизинов 9 или 27 гистона Н3.
Определение «контрольный уровень аденомы» или «контрольный уровень рака» следует понимать как определение уровня указанной генной экспрессии в популяции гастроинтестинальных клеток аденомы или рака, соответственно. Как обсуждалось в данном описании ранее в отношении «нормальных уровней», уровень у субъекта может являться дискретным уровнем или интервалом уровней. Соответственно, следует иметь в виду, что определение «контрольный уровень аденомы» или «контрольный уровень рака», тем не менее, имеет соответствующее определение для «нормального уровня» в контексте экспрессии генов клетками неопластической популяции толстой кишки.
С точки зрения такого аспекта настоящего изобретения анализ для субъекта выполняют с популяцией неопластических клеток. Такие клетки можно получить любым способом, таким как извлечение неопластических клеток, которые собраны при промывке клизмой или из такого гастроинтестинального образца, как образец стула. С другой стороны, клетки субъекта можно получить биопсией или другим хирургическим методом.
Без какого-либо ограничения такого аспекта, некоторые из маркеров по такому аспекту настоящего изобретения определены как экспрессированные на особенно значимых уровнях ниже уровней неопластических клеток. Например, в 3-9 раз пониженные уровни экспрессии наблюдают в отношении указанных далее маркеров, которые являются показателями гастроинтестинальной аденомы, при оценке способом, приведенным в данном описании в качестве примера.
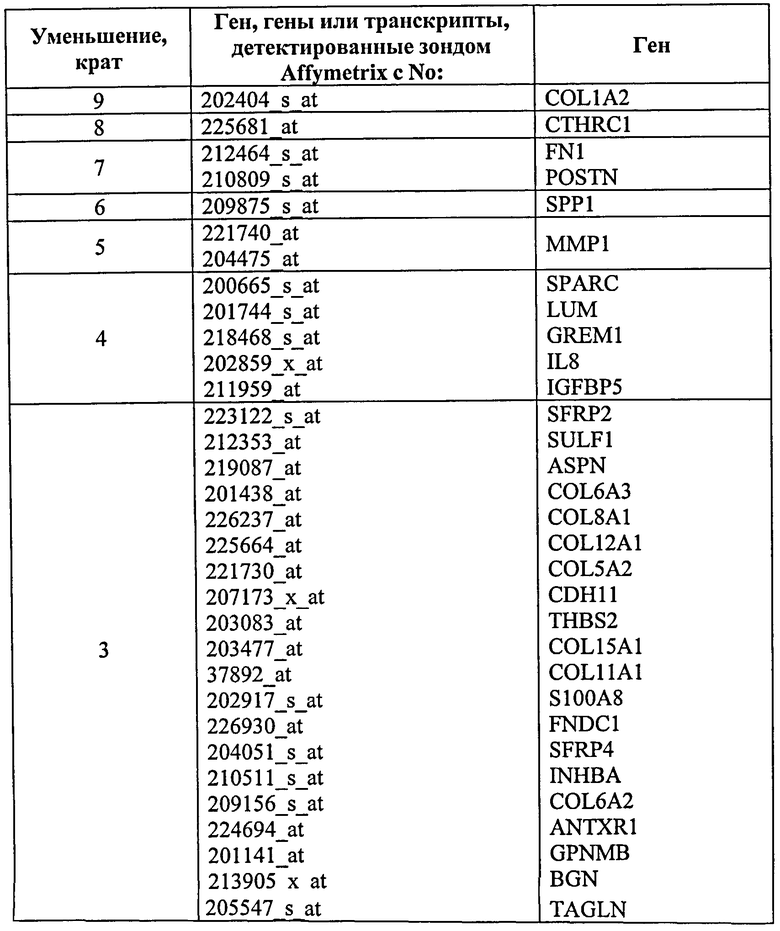
В другом примере в 3-5 раз пониженные уровни экспрессии наблюдают в отношении указанных далее маркеров, которые являются показателями гастроинтестинальных онкозаболеваний, при оценке способом, приведенным в данном описании в качестве примера.
Согласно такому воплощению изобретение относится к способу характеризации неопластической клетки или популяции клеток, полученных из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена или генов, детектированных с помощью набора зондов Affymetrix с ID:
202404_s_at, 212464_s_at, 210809_s_at, 225681_at; и/или
(ii) COL1A2, CTHRC1, FN1, POSTN,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинального рака является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В другом воплощении изобретение относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
209875_s_at, 227140_at, 204475_at; и/или
(ii) SPP1, MMP1,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинального рака является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
Предпочтительно, указанная гастроинтестинальная ткань является колоректальной тканью.
Еще предпочтительнее, указанный биологический образец является образцом ткани.
В другом предпочтительном воплощении изобретение относится к способу характеризации клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из

в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинального рака является показателем клетки аденомы или клетки, предрасположенной к появлению состояния аденомы.
В еще одном предпочтительном воплощении настоящее изобретение относится к способу характеризации клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
210107_at; и/или
(ii) CLCA1,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинальной аденомы является показателем рака или клетки, предрасположенной к появлению состояния рака.
В еще одном другом предпочтительном воплощении настоящее изобретение относится к способу характеризации клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
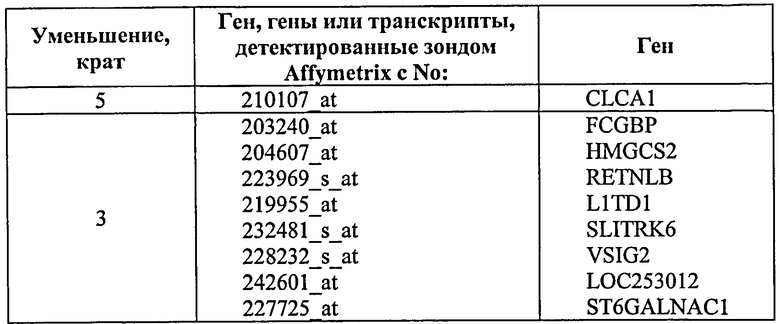
203240_at, 204607_at, 223969_s_at, 219955_at, 232481_s_at, 242601_at, 227725_at, 228232_s_at; и/или
(ii) FCGBP, HMGCS2, RETNLB, L1TD1, SLITRK6, VSIG2, LOC253012, ST6GALNAC1,
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольного уровня гастроинтестинальной аденомы является показателем рака или клетки, предрасположенной к появлению состояния рака.
Предпочтительно, указанная гастроинтестинальная ткань является колоректальной тканью.
Еще предпочтительнее, указанный биологический образец является образцом ткани.
В еще одном родственном аспекте определяется, что набор маркеров такого аспекта настоящего изобретения применим в качестве набора качественных маркеров характеризации неопластической ткани, в которой такие маркеры, если они не детектируются на уровнях, существенно превышающих фоновые уровни в неопластической ткани, являются показателями раковой ткани.
Согласно такому аспекту, настоящее изобретение относится к способу характеризации неопластической клетки или популяции клеток, которые получены из толстой кишки индивидуума, причем указанный способ включает оценку уровня экспрессии одного или нескольких генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью набора зондов Affymetrix с ID:
235976_at, 236894_at, 237521; и/или
(ii) SLITRK6, L1TD1,
в биологическом образце от указанного индивидуума, где экспрессия генов или транскриптов группы (i) и/или группы (ii) на уровне, который, по существу, не выше фоновых уровней неопластической ткани, является показателем рака или клетки, предрасположенной к появлению состояния рака.
Предпочтительно, указанная гастроинтестинальная ткань является колоректальной тканью.
Еще предпочтительнее, указанный биологический образец является образцом ткани.
В наиболее предпочтительном воплощении способы по настоящему изобретению относятся, предпочтительно, к скринингу в отношении белков, кодированных маркерами по настоящему изобретению, или изменений ДНК-метилирования геномной ДНК. В другом воплощении экспрессию оценивают по ассоциации ДНК с белками хроматина, содержащими репрессивные модификации, например, метилирование лизинов 9 или 27 гистона Н3.
Хотя предпочтительным способом является детекция продукта экспрессии или изменений ДНК неопластических маркеров с целью диагностики развития неоплазии или предрасположенности к этому, в некоторых обстоятельствах может быть желательна детекция обратных изменений в уровнях указанных маркеров, например, для мониторинга эффективности терапии или превентивного лечения, направленного на модуляцию неопластического состояния, такого как развитие аденомы или аденокарциномы. Например, когда ослабленная экспрессия маркеров субъекта указывает, что у индивидуума развилось состояние, характеризующееся развитием аденомы или аденокарциномы, например, скрининг на повышение уровней указанных маркеров после начала программы лечения можно использовать как показатель обратной или другой формы улучшения состояния отдельного субъекта.
Поэтому способ по настоящему изобретению применим как один из тестов или как постоянный контроль таких индивидуумов, которые, как предполагается, находятся в опасности развития неоплазии, или как контроль эффективности схем терапии или превентивного лечения, направленных на ингибирование или иное замедление развития неоплазии. В таких ситуациях картирование модуляции уровней экспрессии неопластических маркеров в любом одном или нескольких классах биологических образцов является ценным индикатором статуса индивидуума или эффективности схемы лечения или профилактики, которую в данном случае применяют. Соответственно, следует иметь в виду, что способ по настоящему изобретению распространяется на мониторинг возрастаний или снижений уровней экспрессии маркеров у индивидуума относительно ее нормального уровня (определенного в данном описании ранее), фоновых контрольных уровней, раковых уровней, уровней аденомы или относительно уровней экспрессии одного или нескольких ранних маркеров, определенных из биологического образца указанного индивидуума.
Оценку экспрессированных субъектом маркеров неоплазмы в биологическом образце можно осуществить любым подходящим способом, который может быть хорошо известен специалисту в данной области техники. С этой целью, как следует признать, проверяя или популяцию клеток (такую как в биопсии опухоли или популяция клеток, которая обогащена из исходной гетерогенной популяции) или срез ткани, можно использовать широкий ряд методов, таких как гибридизация in situ, оценка профилей экспрессии микроанализами, иммуноанализами и т.п. (описанных подробнее в данном описании далее), для детекции отсутствия или отрицательной регуляции уровня экспрессии одного или нескольких маркеров, представляющих интерес. Однако, что касается скрининга в отношении гетерогенной популяции клеток или жидкости организма, в которой обнаружены гетерогенные популяции клеток, такой как образец крови, отсутствие или снижение уровня экспрессии определенного маркера может не поддаваться детекции из-за неотъемлемой экспрессии маркера ненеопластическими клетками, которые присутствуют в образце. Иными словами, снижение уровня экспрессии подгруппы клеток может не поддаваться детекции. В такой ситуации более подходящим механизмом детекции снижения в неопластической субпопуляции уровней экспрессии одного или нескольких маркеров по настоящему изобретению является непрямой способ, такой как детекция эпигенетических изменений.
Без ограничения настоящего изобретения какой-либо теорией или способом действия, экспрессия генов в развитии регулируется процессами, которые изменяют доступность генов для экспрессии в клеточных линиях различной дифференцировки без какого-либо изменения в последовательности генов, и такие состояния могут быть унаследованы через деление клеток - процесс, называемый эпигенетическим наследованием. Эпигенетическое наследование определяется, комбинацией метилирования ДНК (модификация цитозина для получения 5-метилцитозина, 5meС) и модификациями хромосомных белков гистона, которые пакуют ДНК. Таким образом, метилирование ДНК в сайтах CpG и модификации, такие как деацетилирование гистона Н3 в лизине 9 и метилирование лизина 9 или 27, ассоциируются с инактивным хроматином и активной экспрессией генов. При раке часто обнаруживают, что такая эпигенетическая регуляция экспрессии генов разрушена (Esteller & Herman, 2000; Jones & Baylin, 2002). Часто обнаруживают, что гены, такие как супрессор опухоли или гены-супрессоры метастазирования, подвергаются сайленсингу метилированием ДНК, в то время как другие гены могут быть гипометилированными и экспрессируются несоответственно. Таким образом, гены, которые демонстрируют утрату экспрессии при раке, часто характеризуются метилированием промоторного или регуляторного участка гена.
Ряд способов доступен для детекции аберрантно метилированной ДНК специфического гена даже в присутствии большого избытка нормальной ДНК (Clark, 2007). Таким образом, утрату экспрессии гена, детекция которой в белке может быть затруднена, или уровень РНК, за исключением иммуногистохимии, обычно можно детектировать в образцах опухоли и в жидкостях организма больных раком по присутствию гиперметилированной ДНК промотора гена. Подобным образом, гиперметилирование ДНК можно использовать для детекции некоторых генов, экспрессию которых оценивают при раке. Эпигенетические изменения и изменения хроматина при раке также очевидны в измененной ассоциации модифицированных гистонов со специфическими генами (Esteller, 2007); например, репрессированные гены часто обнаруживают ассоциированными с гистоном 3, который является деацетилированным и метилированным в лизине 9. Использование антител, нацеленных на измененные гистоны, допускает изоляцию ДНК, ассоциированной с хроматином в определенных состояниях, и ее потенциальное применение в диагностике рака.
Другие способы детекции изменений уровней экспрессии генов, в частности, когда биологический образец субъекта не загрязнен большим количеством ненеопластических клеток, включают, но не ограничиваются перечисленным, способы, указанные далее.
(i) Детекция in vivo.
Молекулярную визуализацию можно использовать после введения формирующих изображение зондов или реагентов, способных раскрыть измененную экспрессию маркеров в интестинальных тканях.
Молекулярная визуализация (Moore et al., ВВА, 1402: 239-249, 1988; Weissleder et al., Nature Medicine, 6:351-355, 2000) является визуализацией in vivo экспрессии молекул, которая коррелирует с макропризнаками, визуализируемыми в настоящее время с использованием «классических» методов диагностической визуализации, таких как рентгенография, компьютерная томография (СТ), MRI, позитронная эмиссионная томография или эндоскопия.
(ii) Детекция отрицательной регуляции экспрессии РНК в клетках флуоресцентной гибридизацией in situ (FISH) или в экстрактах клеток такими технологиями, как количественная полимеразная цепная реакция с обратной транскриптазой (К-ОТ-ПЦР, QRTPCR) или оценка проточной цитометрией продуктов конкурентной ОТ-ПЦР (Wedemeyer et al., Clinical Chemistry, 48:9 1398-1405,2002).
(iii) Оценка профилей экспрессии РНК, например, матричными технологиями (Alon et al., Proc. Natl. Acad. Sci. USA: 96,6745-6750, June 1999).
«Микроматрица» представляет собой линейную или мультиразмерную матрицу предпочтительно из дискретных участков, причем каждый имеет определенную площадь, образованную на поверхности твердой подложки. Плотность дискретных участков на микроматрице определяется общим числом полинуклеотидов-мишеней, детектируемых на поверхности одного твердофазной подложки. В данном описании ДНК-микроматрица представляет собой матрицу олигонуклеотидных зондов, размещенных на чипе или других поверхностях, используемых для амплификации или клонирования полинуклеотидов-мишеней. Так как позиция каждой определенной группы зондов в матрице известна, можно определить идентичности полинуклеотидов-мишеней на основании их связывания с определенной позицией в микроматрице.
Последние разработки в технологии ДНК-микроматриц делают возможным проведение крупномасштабного анализа множества молекул-мишеней нуклеиновых кислот на одной твердофазной подложке. В патенте США № 5837832 (Chee et al.) и родственных заявках на патент описывается иммобилизация матрицы олигонуклеотидных зондов для гибридизации и детекции специфических нуклеотидных последовательностей в образце. Полинуклеотиды-мишени, представляющие интерес, выделяют из ткани, представляющей интерес, и гибридизуют с ДНК-чипом, и детектируют специфические последовательности на основании предпочтения полинуклеотидов-мишеней и степени гибридизации в местах расположения дискретных зондов. Одним важным применением матриц является анализ дифференциальной экспрессии генов, когда сравнивают профили экспрессии генов в различных клетках или тканях, обычно, ткани, представляющий интерес, и контрольной ткани, и идентифицируют любые различия в экспрессии генов среди соответствующих тканей. Такая информация применима для идентификации типов генов, экспрессированных в определенном типе ткани, и диагностике состояний на основании профиля экспрессии.
В одном примере РНК из образца, представляющего интерес, подвергают обратной транскрипции и получают меченую кДНК. См. патент США № 6410229 (Lockhart et al.). Затем кДНК гибридизируют с олигонуклеотидами кДНК известной последовательности, нанесенной на чип или другую поверхность, в известном порядке. В другом примере РНК выделяют из биологического образца и гибридизуют с чипом, на котором заякорены кДНК-зонды. Местоположение олигонуклеотида, с которым гибридизуется меченая кДНК, дает информацию о последовательности на кДНК, в то время как количество меченой гибридизованной РНК или кДНК дает оценку относительного представления РНК или мРНК, представляющей интерес. См. Schena et al., Science, 270: 467-470 (1995). Например, использование кДНК-матрицы для анализа картин экспрессии генов при раке человека описывают DeRisi et al. (Nature Genetics, 14: 457-460 (1996)).
В предпочтительном воплощении создают полинуклеотидные зонды, соответствующие нуклеиновым кислотам субъекта. Создают полинуклеотидные зонды, присоединенные к биочипу, по существу, комплементарные к нуклеиновым кислотам биологического образца, так что происходит специфическая гибридизация последовательности-мишени и зондов по настоящему изобретению. Такая комплементарность не обязательно полная, в ней может находиться любое число ошибочных спариваний оснований, которые будут препятствовать гибридизации между последовательностью-мишенью и одноцепочечными нуклеиновыми кислотами по настоящему изобретению. Ожидается, что общая гомология генов на уровне нуклеотидов, вероятно, будет составлять примерно 40% или более, вероятно, примерно 60% или более, и даже вероятнее, примерно 80% или более, и кроме того, будут соответствующие последовательности контигов в примерно 8-12 нуклеотидов или более длинные. Однако, если число мутаций настолько велико, что гибридизация не может происходить даже в наименее строгих условиях гибридизации, последовательность не является комплементарной последовательности-мишени. Таким образом, «по существу, комплементарные» в данном описании означает, что зонды являются достаточно комплементарными к последовательностям-мишеням для гибридизации в нормальных условиях реакции, в особенности, в условиях высокой строгости.
Полинуклеотидный зонд, как правило, является одноцепочечным, но может быть частично одно- и частично двухцепочечным. Число цепей зонда диктуется структурой, составом и свойствами последовательности-мишени. Вообще, олигонуклеотидные зонды по длине колеблются от примерно 6, 8, 10, 12, 15, 20, 30 до примерно 100 оснований, причем предпочтительна длина от примерно 10 до примерно 80 оснований, и длина от примерно 15 до примерно 40 оснований является особенно предпочтительной. Иными словами, как правило, полные гены редко используют в качестве зондов. В некоторых воплощениях можно использовать намного более длинные нуклеиновые кислоты.- до сотен оснований. Зонды являются достаточно специфическими для гибридизации с комплементарной матричной последовательностью в условиях, известных специалистам в данной области техники. Число ошибочных спариваний оснований между последовательностями зондов и комплементарными им матричными последовательностями (мишенями), с которыми они гибридизируют во время гибридизации, как правило, не превышает 15%, обычно не превышает 10%, и предпочтительно, не превышает 5%, при определении BLAST (установка по умолчанию).
Олигонуклеотидные зонды могут включать встречающиеся в природе гетероциклические основания, обычно обнаруживаемые в нуклеиновых кислотах (урацил, цитозин, тимин, аденин и гуанин), а также модифицированные основания и аналоги оснований. Любое модифицированное основание или аналог, совместимые с гибридизацией зонда с последовательностью-мишенью, применимы при практическом осуществлении изобретения. Сахарная или гликозидная часть зонда может включать дезоксирибозу, рибозу и/или модифицированные формы таких сахаров, такие как, например, 2'-О-алкилрибоза. В предпочтительном воплощении сахарная составляющая представляет собой 2'-дезоксирибозу; однако можно использовать любую сахарную составляющую, совместимую со способностью зонда гибридизоваться с последовательностью-мишенью.
В одном воплощении нуклеотидные звенья зонда соединяются фосфодиэфирным каркасом, что хорошо известно в технике. В других воплощениях межнуклеотидные связывающие группы могут включать любую группу, известную специалистам в данной области техники как совместимую со специфической гибридизацией зонда, включая, но не ограничиваясь указанным, фосфоротиоатную, метилфосфонатную, сульфаматную (например, патент США № 5470967) и полиамидную (т.е. пептидные нуклеиновые кислоты). Пептидные нуклеиновые кислоты описаны: Nielsen et al. (1991), Science, 254: 1497-1500; патент США № 5714331 и Nielsen (1999), Curr. Opin. Biotechnol., 10: 71-75.
В некоторых воплощениях зонд может представлять собой химерную молекулу, т.е. может включать более одного типа основания или сахарного звена, и/или связывающие группы в одном и том же праймере могут быть не одного типа. Зонд может включать группы, облегчающие гибридизацию с последовательностью-мишенью, какие известны в технике, например, интеркаляторы и/или агенты, связывающиеся с малыми бороздками. Вариации таких оснований, cахаров и межнуклеозидного каркаса, а также присутствие в зонде любой боковой группы будут совместимы со способностью зонда связываться с последовательностью-мишенью специфически в отношении последовательности. Большое число структурных модификаций возможно в пределах таких границ. Преимущественно зонды по настоящему изобретению могут иметь такие структурные характеристики, что они допускают амплификацию сигнала, причем такими структурными характеристиками обладают, например, разветвленные ДНК-зонды, такие, какие описаны в Urdea et al. (Nucleic Acids Symp. Ser., 24: 197-200 (1991)) или в Европейском патенте № ЕР-0225807. Более того, синтетические способы получения различных гетероциклических оснований, cахаров, нуклеозидов и нуклеотидов, которыми получают зонд, и получения олигонуклеотидов специфической предварительно установленной последовательности, широко разрабатываются и известны в технике. Предпочтительный способ синтеза олигонуклеотидов включает наставление согласно патенту США № 5419966.
Может быть создано несколько зондов для определенной нуклеиновой кислоты-мишени, в расчете на полиморфизм и/или вторичную структуру в нуклеиновой кислоте-мишени, избыточность данных и подобные обстоятельства. В некоторых воплощениях, когда используют более одного зонда на последовательность, используют или перекрывающиеся зонды или зонды к различным секциям одного гена-мишени. Иными словами, два, три, четыре или больше зондов используют для построения в избыточности для определенной мишени. Зонды могут быть перекрывающимися (т.е. иметь общую последовательность) или являются специфическими для определенных последовательностей гена. Когда необходимо по настоящему изобретению детектировать несколько полинуклеотидов-мишеней, каждый зонд или группу зондов, соответствующих определенному полинуклеотиду-мишени, помещают в отдельную зону микроматрицы.
Зонды могут находиться в растворе, например, в лунках или на поверхности микроматрицы, или присоединены к твердой подложке. Примеры материалов твердой подложки, которые можно использовать, включают пластик, керамику, металл, резину, гель и мембрану. Применимые типы твердых подложек включают пластины, гранулы, магнитный материал, микрогранулы, чипы для гибридизации, мембраны, кристаллы, керамические материалы и самособирающиеся монослои. Один из примеров включает двумерную или трехмерную матрицу, такую как гель или чип для гибридизации с несколькими сайтами связывания зондов (Pevzner et al., J. Biomol. Srtuc. & Dyn., 9: 399-410, 1991; Maskos and Southern, Nuc. Acids Res., 20: 1679-84, 1992). Чипы для гибридизации можно использовать для построения очень больших зондовых матриц, которые затем гибридизируют с нуклеиновой кислотой-мишенью. Анализ картины гибридизации чипа может помочь в идентификации нуклеотидной последовательности-мишени. Картины можно анализировать вручную или на компьютере, но ясно, что такое позиционное секвенирование гибридизации само ведет к компьютерному анализу и автоматизации. В другом примере можно использовать чип Affymetrix на твердофазной структурной подложке в сочетании с подходом на основании флуоресцентных гранул. В еще одном примере можно использовать кДНК-микроматрицу. В этом отношении олигонуклеотиды, описанные Lockkart et al. (т.е. зонды Affymetrix, синтезированные in situ на твердой фазе) являются особенно предпочтительными, т.е. предпочтительна фотолитография.
Как следует признать специалистам в данной области техники, нуклеиновые кислоты могут быть присоединены или иммобилизованы на твердой подложке самыми разными способами. Под «иммобилизованы» в данном описании понимается ассоциация или связывание между полинуклеотидным зондом и твердой подложкой, которая является достаточно устойчивой в условиях связывания, промывки, анализа и удаления. Связывание может быть ковалентным или нековалентным. Под «нековалентным связыванием» и его грамматическими эквивалентами в данном описании подразумеваются одно или несколько взаимодействий из числа электростатического, гидрофильного и гидрофобного. К нековалентному связыванию относят ковалентное присоединение молекулы, такой как стрептавидин, к подложке и нековалентное связывание биотинилированного зонда со стрептавидином. Под «ковалентным связыванием» и его грамматическими эквивалентами в данном описании подразумевается, что две сущности - твердая подложка и зонд соединены, по меньшей мере, одной связью, включая сигма-связи, пи-связи и координационные связи. Ковалентные связи могут образоваться непосредственно между зондом и твердой подложкой или могут образоваться с помощью перекрестно-сшиваемого агента или путем включения специфической реакционноспособной группы или в твердую подложку, или в зонд, или в обе молекулы. Иммобилизация также может включать комбинацию ковалентных и нековалентных взаимодействий.
Полинуклеотидные зонды могут присоединяться к твердой подложке путем ковалентного связывания, например, путем конъюгации с агентом сочетания, или путем ковалентного и нековалентного связывания, такого как электростатические взаимодействия, водородные связи или сочетание антитело-антиген, или путем их комбинаций. Типичные агенты сочетания включают биотин/авидин, биотин/стрептавидин, белок Staphylococcus aureus А/фрагмент Fc IgG и стрептавидин/химеры белка А (Т. Sano and C.R. Cantor, Bio. Technology, 9: 1378-81 (1991)), или комбинации таких агентов. Нуклеиновые кислоты могут быть присоединены к твердой подложке связями, легко разрушающимися под действием света, электростатическими связями, дисульфидными связями, пептидными связями, сложными диэфирными связями или. комбинацией связей таких типов. Матрица также может присоединяться к твердой подложке, селективно разъединяющимися связями, такими как 4,4'-диметокситритильная или ее производное. Производные, которые, как обнаружено, применимы, включают 3- или 4-[бис(4-метоксифенил)]метилбензойную кислоту, N-сукцинимидил-3(или 4)-[бис(4-метоксифенил)]метилбензойную кислоту, N-сукцинимидил-3(или 4)-[бис(4-метоксифенил)]гидроксиметилбензойную кислоту, N-сукцинимидил-3(или 4)-[бис(4-метоксифенил)]хлорметилбензойную кислоту и соли указанных кислот.
Вообще, зонды присоединяются к биочипу самыми разными путями, что будет понятно специалистам в данной области техники. Как описано в данном описании, нуклеиновые кислоты могут быть синтезированы или сначала с последующим присоединением к биочипу, или могут быть синтезированы непосредственно на биочипе.
Биочип включает подходящую твердую подложку. Под «носителем» или «твердой подложкой» или другими грамматическими эквивалентами в данном описании подразумевается любой материал, который можно модифицировать для содержания дискретных отдельных участков, подходящих для присоединения или ассоциации полинуклеотидных зондов, и поддается, по меньшей мере, одному способу детекции. Твердофазная подложка по настоящему изобретению может представлять собой любые твердые материалы и структуры, подходящие в качестве опоры для гибридизации и синтеза нуклеотидов. Предпочтительно твердофазная подложка включает, по меньшей мере, одну, по существу, жесткую поверхность, на которой могут быть иммобилизованы праймеры и осуществлено взаимодействие с обратной транскриптазой. Носители, с которыми элементы полинуклеотидной микроматрицы устойчиво ассоциируются, могут быть получены из различных материалов, включая пластики, керамические материалы, металлы, акриламид, целлюлозу, нитроцеллюлозу, стекло, полистирол, полиэтиленвинилацетат, полипропилен, полиметакрилат, полиэтилен, полиэтиленоксид, полисиликаты, поликарбонаты, тефлон, фторуглероды, нейлон, силиконовый каучук, полиангидриды, полигликолевую кислоту, полимолочную кислоту, полиортоэфиры, полипропилфумерат, коллаген, гликозаминогликаны и полиаминокислоты. Носители могут быть двумерными или трехмерными по форме, такими как гели, мембраны, тонкие пленки, стекла, пластины, цилиндры, гранулы, магнитные гранулы, оптические волокна, текстильные волокна и т.д. Предпочтительной формой матрицы является трехмерная матрица. Предпочтительная трехмерная матрица представляет собой собрание меченых гранул. Каждая меченая гранула имеет различные присоединенные к ней праймеры. Метки являются детектируемыми средствами, принимающими сигнал, такой как цвет (Luminex, Illumina) и электромагнитное поле (Pharmaseq), и сигналы на меченых гранулах даже могут быть детектированы дистанционно (например, с использованием оптических волокон). Размер твердой подложки может быть любым стандартным размером микроматрицы, применимым для ДНК-микроматричной технологии, и размер может быть приспособлен, чтобы подходить для определенной машины, используемой для проведения реакции по изобретению. Как правило, носители допускают оптическую детекцию и не являются заметно флуоресцирующими.
В одном воплощении поверхность биочипа и зонд могут быть дериватизированы химическими функциональными группами для последующего их присоединения. Так, например, биочип дериватизируют химической функциональной группой, в том числе, но без ограничения, аминогруппами, карбоксигруппами, оксогруппами и тиольными группами, причем аминогруппы являются особенно предпочтительными. Используя такие функциональные группы, можно присоединить зонды с использованием функциональных групп на зондах. Например, нуклеиновые кислоты, содержащие аминогруппы, можно присоединить к поверхностям, включающим аминогруппы, например, с использованием линкеров, известных в технике; например, в технике хорошо известны гомо- или гетеробифункциональные линкеры. Кроме того, в некоторых случаях можно использовать другие линкеры, такие как алкильные группы (в том числе, замещенные и гетероалкильные группы).
В таком воплощении олигонуклеотиды синтезируют так, как известно в технике, и затем присоединяют к поверхности твердой подложки. Как будет понятно специалистам в данной области техники, к твердой подложке можно присоединить или 5'- или 3'-конец, или присоединение может происходить через внутренний нуклеозид. В дополнительном воплощении иммобилизация на твердой подложке может быть очень сильной, но пока нековалентной. Например, можно получить биотинилированные олигонуклеотиды, которые связываются с поверхностями, ковалентно связанными с нанесенным стрептавидином, что приводит к присоединению.
Матрицы можно получить согласно любой принятой методологии, такой как предварительное формирование элементов полинуклеотидной микроматрицы и последующая устойчивая ассоциация их с поверхностью. С другой стороны, олигонуклеотиды можно синтезировать на поверхности, как известно в технике. Специалистам в данной области технике известен ряд различных конфигураций матриц и. способы их получения, и они раскрываются в WO 95/25116 и WO 95/35505 (фотолитографические методы), патент США № 5445934 (синтез in situ с помощью фотолитографии), патент США № 5384261 (синтез in situ с помощью механически направленных потоков) и патент США № 5700637 (синтез накалыванием, печатанием или сочетанием); все указанные работы включены в данное описание в качестве ссылок. В другом способе соединения ДНК с гранулами используют специфические лиганды, присоединенные к концу ДНК, соединяющиеся с лигандсвязывающими молекулами, присоединенными к гранулам. Возможные пары лигандсвязывающих партнеров включают биотин-авидин/стрептавидин или различные пары антитело/антиген, такие как дигоксигенин-антитела против дигоксигенина (Smith et al., Science, 258: 1122-1126 (1992)). Ковалентное химическое присоединение ДНК к подложке можно осуществить, используя агенты сочетания для соединения 5'-фосфатной группы ДНК с нанесенными микросферами через фосфоамидатную связь. Способы иммобилизации олигонуклеотидов на твердых носителях хорошо установлены. См. Pease et al., Proc. Natl. Acad. Sci. USA, 91(11): 5022-5026 (1994). Предпочтительный способ присоединения олигонуклеотидов к твердому носителю описан в Guo et al., Nucleic Acids Res., 22: 5456-5465 (1994). Иммобилизацию можно осуществить или синтезом ДНК in situ (Maskos and Southern, цит. выше) или ковалентным присоединением химически синтезированных олигонуклеотидов (Guo et al., цит. выше) в сочетании с обычными матричными технологиями.
Кроме твердофазной технологии, представленной биочипами-матрицами, экспрессию генов также можно определить количественно с использованием жидкофазных матриц. Одна такая система представляет собой кинетическую полимеразную цепную реакцию (ПЦР). Кинетическая ПЦР допускает одновременную амплификацию и определение количества специфических нуклеотидных последовательностей. Специфичность получают от синтетических олигонуклеотидных праймеров, созданных для преимущественного прилипания к одноцепочечным нуклеотидным последовательностям, включающим в себя участок-мишень. Такая пара олигонуклеотидных праймеров образует специфические нековалентно связанные комплексы на каждой цепи последовательности-мишени. Такие комплексы облегчают транскрипцию in vitro двухцепочечной ДНК в противоположных направлениях. Циклическая температурная обработка реакционной смеси создает непрерывный цикл связывания праймеров, транскрипции и повторного плавления нуклеиновой кислоты до отдельных цепей. Результатом является экспоненциальное возрастание продукта дцДНК-мишени. Такой продукт можно определить количественно в реальном времени или через использование интеркалярного красителя или зонда, специфического к последовательности. SYBR(r) Green 1 является примером интеркалярного красителя, который преимущественно связывается с дцДНК, что приводит к увеличению побочного продукта в сигнале флуоресценции. Зонды, специфические к последовательностям, такие, какие используются в технологии TaqMan, состоят из флуорохрома и молекулы-тушителя, ковалентно связанных с противоположными концами олигонуклеотида. Зонд создают для селективного связывания с последовательностью-мишенью ДНК между двумя праймерами. Когда цепи ДНК синтезируют во время реакции ПЦР, флуорохром отщепляется от зонда экзонуклеазной активностью полимеразы, что приводит к снятию тушения сигнала. Способ с передачей сигнала зондом может быть более специфичным, чем способ с интеркалярным красителем, но в каждом случае сила сигнала пропорциональна полученному продукту дцДНК. Каждый тип способа определения количества можно использовать в многолуночных жидкофазных матрицах, причем каждая лунка представляет праймеры и/или зонды, специфические к нуклеотидным последовательностям, представляющим интерес. При использовании препаратов тканей или клеточных линий с матричной РНК, матрица реакций зонд/праймер одновременно можно количественно определить экспрессию нескольких генных продуктов, представляющих интерес. См. Germer et al., Genome Res., 10: 258-266 (2000); Heid et al., Genome Res., 6: 986-994 (1996).
(iv) Измерение изменившихся уровней белка неопластического маркера в клеточных экстрактах, например, иммуноанализом.
Проверку белкового продукта экспрессии неопластического маркера в биологическом образце можно осуществить любым из ряда подходящих способов, которые хорошо известны специалистам в данной области техники. Примеры подходящих способов включают, но не ограничиваются перечисленным, скрининг в отношении антител в срезах тканей, образцах биопсии или образцах жидкостей организма.
В той мере, в какой используются способы диагностики на основе антител, присутствие маркерного белка можно определить рядом способов, таких как вестерн-блоттинг, ELISA или процедуры проточной цитометрии. Они, конечно, включают как односайтовые, так и двухсайтовые, или «сэндвич-», анализы неконкурентного типа, а также традиционные анализы конкурентного связывания. Такие анализы также включают прямое связывание меченого антитела с мишенью.
Сэндвич-анализы являются применимыми и обычно используемыми анализами. Существует ряд вариаций метода сэндвич-анализа, и подразумевается, что все они охватываются настоящим изобретением. Коротко, в типичном прямом анализе немеченые антитела иммобилизуют на твердом носителе, и испытываемый образец приводят в контакт со связанной молекулой. После подходящего периода инкубации в течение времени, достаточного для образования комплекса антитело-антиген, добавляют вторые антитела, специфические для антигена, меченные репортерной молекулой, способной вырабатывать детектируемый сигнал, и инкубируют в течение времени, достаточного для образования другого комплекса антитело-антиген-меченое антитело. Любое непрореагировавшее вещество вымывают, и присутствие антигена определяют, наблюдая за сигналом, производимым репортерной молекулой. Результаты могут быть или качественными по простому наблюдению видимого сигнала или количественными при сравнении с контрольным образцом. Вариации прямого анализа включают одновременный анализ, в котором два образца и меченые антитела добавляют к связанным антителам одновременно. Такие методы хорошо известны специалистам в данной области техники, в том числе, любые небольшие вариации, которые будут легко различимыми.
В типичном прямом сэндвич-анализе первые антитела со специфичностью к маркеру или его антигенным частям или ковалентно или пассивно связаны с твердой поверхностью. Твердая поверхность типично представляет собой стекло или полимер, причем наиболее обычно используемыми полимерами являются целлюлоза, полиакриламид, нейлон, полистирол, поливинилхлорид или полипропилен. Твердые подложки могут находиться в форме трубочек, гранул, кружочков тонких пластин или любой другой, поверхности, подходящей для проведения иммуноанализа. Способы связывания хорошо известны в технике и, как правило, включают перекрестное сшивание, ковалентное связывание или физическую адсорбцию, комплекс полимер-антитела промывают при подготовке для добавления испытываемого образца. Затем аликвоту испытываемого образца добавляют к твердофазному комплексу и инкубируют в течение достаточного времени (например, 2-40 минут) и в подходящих условиях (например, 25°С) для связывания любой субъединицы, присутствующей в антителе. После инкубации субъединицы антител на твердой фазе промывают и сушат и инкубируют со вторыми антителами, специфическими для части антигена. Вторые антитела соединяются с репортерной группой, которую используют как индикатор связывания вторых антител с антигеном.
Альтернативный способ включает иммобилизацию молекул-мишеней в биологическом образце и последующее воздействие на иммобилизованную мишень специфическими антителами, которые могут быть помечены репортерной группой или не мечены. В зависимости от количества мишени и силы сигнала репортерной группы связанную мишень можно детектировать посредством прямого мечения антителами. С другой стороны, на вторые меченые антитела, специфические к первым антителам, воздействуют комплексом мишень-первое антитело с образованием третичного комплекса мишень-первое антитело-второе антитело. Комплекс детектируют по сигналу, испускаемому репортерной группой.
«Репортерной группой» в настоящем описании обозначают молекулу, которая по своей химической природе обеспечивает аналитически идентифицируемый сигнал, который дает возможность детекции антигена, связанного с антителом. Детекция может быть или качественной или количественной. Наиболее обычными репортерными группами в анализе такого типа являются любые ферменты, молекулы, содержащие флуорофоры или радионуклеиды (т.е. радиоизотопы), и хемилюминесцентные молекулы.
В случае иммуноферментного анализа фермент конъюгируют со вторыми антителами, как правило, с помощью глутаральдегида или периодата. Однако, что легко выяснить, существует широкий ряд различных методов конъюгации, которые легко доступны специалистам. Обычно используемые ферменты включают, среди прочих, пероксидазу хрена, глюкозооксидазу, бета-галактозидазу и щелочную фосфатазу. Субстраты, используемые со специфическими ферментами, обычно выбирают для получения, после гидролиза соответствующим ферментом, поддающегося детекции изменения цвета. Также возможно использование флуорогенных субстратов, которые дают флуоресцентный продукт, а не хромогенных субстратов, указанных выше. Во всех случаях меченные ферментом антитела добавляют к комплексу первое антитело-гаптен, связывают, и затем избыток реагента вымывают. Затем к комплексу антитело-антиген-антитело добавляют раствор, содержащий соответствующий субстрат. Субстрат будет взаимодействовать с ферментом, связанным со вторыми антителами, образуя качественный видимый сигнал, который можно затем оценить количественно, как правило, спектрофотометрией, и получить показание количества антигена, который присутствует в образце. Применение «репортерной группы» также распространяется на агглютинацию клеток, таких как красные клетки крови, или ингибирование агглютинации на латексных гранулах и т.п.
С другой стороны, флуоресцентные соединения, такие как флуорецеин и родамин, можно химически соединить с антителами без изменения их связывающей способности. При активировании светом определенной длины волны меченные флуорохромом антитела поглощают световую энергию, вызывая в молекуле состояние возбуждения, с последующим испусканием света характерного цвета, визуально поддающегося детекции с помощью оптического микроскопа. Как в EIA, флуоресцентно меченые антитела связываются с комплексом первое антитело-гаптен. Затем после вымывания несвязанного реагента на оставшийся третичный комплекс воздействуют светом соответствующей длины волны, и наблюдаемая флуоресценция указывает на присутствие гаптена, представляющего интерес. Как иммунофлуоресценция, так и методы EIA хорошо упрочились в технике и особенно предпочтительны для способа по настоящему изобретению. Однако также можно использовать другие репортерные группы, такие как радиоизотопы, хемилюминесцентные или биолюминесцентные молекулы.
(v) Определение изменившейся экспрессии белковых неопластических маркеров на клеточной поверхности, например, иммуногистохимией.
(vi) Определение изменившейся экспрессии белков на основе подходящего функционального испытания, ферментного или иммунологического испытания в дополнение к испытаниям, подробно представленным выше в (i) и (v).
Специалист в данной области техники сможет определить самой обычной процедурой уместность применения данного способа к определенному типу биологического образца.
Не ограничивая настоящее изобретение каким-либо образом, и как подробно описано выше, уровни экспрессии генов можно измерить различными способами, известными в технике. Например, можно измерить продукты транскрипции или трансляции генов. Продукты транскрипции генов, т.е. РНК, можно определить, например, анализами с гибридизацией, анализами run-off, нозерн-блоттингом или другими методами, известными в технике.
Анализы с гибридизацией, как правило, включают использование олигонуклеотидных зондов, которые гибридизируют с продуктами транскрипции одноцепочечной РНК. Таким образом, олигонуклеотидные зонды комплементарны продукту экспрессии транскрибированной РНК. Типично, зонд, специфический к последовательности, может быть направлен на гибридизацию с РНК или кДНК. «Полинуклеотидный зонд», используемый в данном случае, может представлять собой ДНК-зонд или РНК-зонд, который гибридизирует с комплементарной последовательностью. Специалисту в данной области техники может быть известно, как создавать такой зонд с тем, чтобы происходила специфическая для последовательности гибридизация. Специалисту в данной области техники также будет известно, как количественно оценить специфическую для последовательности гибридизацию как количественную оценку экспрессии генов для гена, который транскрибируют для. получения специфической РНК.
Образец при гибридизации поддерживают в условиях, которые достаточны для специфической гибридизации полинуклеотидного зонда со специфическим продуктом экспрессии гена. Используемое в данном случае определение «специфическая гибридизация» указывает на почти точную гибридизацию (например, с несколькими, если не любыми, ошибочными спариваниями). Специфическую гибридизацию можно выполнить в условиях высокой строгости или условиях средней строгости. В одном воплощении условия гибридизации для специфической гибридизации являются весьма строгими. Например, некоторые условия высокой строгости можно использовать для того, чтобы отличить вполне комплементарные нуклеиновые кислоты от кислот меньшей комплементарности. «Условия высокой строгости», «условия умеренной строгости» и «условия низкой строгости» для гибридизации нуклеиновых кислот поясняются на сс. 2.10.1 - 2.10.16 и сс. 6.3.1 - 6.3.6 в Current Protocols in Molecular Biology (Ausubel F. et al., «Current Protocols in Molecular Biology», John Wiley & Sons (1998), включенная в данное описание в качестве ссылки). Точные условия, которые определяют строгость гибридизации, зависят не только от ионной силы (например, 0,2-крат. SSC, 0,1-крат. SSC), температуры (например, комнатная температура, 42°С, 68°С) и концентрации дестабилизаторов, таких как формамид, или денатурирующих агентов, таких как SDS, но также от таких факторов, как длина нуклеотидной последовательности, состав по основаниям, процент ошибочных спариваний между гибридизирующими последовательностями и частота появления групп такой последовательности в рамках других неидентичных последовательностей. Таким образом, эквивалентные условия можно определить путем изменения одного или нескольких таких параметров, пока сохраняется схожая степень идентичности или подобия между двумя молекулами нуклеиновых кислот. Типично используют такие условия, что последовательности, по меньшей мере, примерно на 60%, по меньшей мере, примерно на 70%, по меньшей мере, примерно на 80%, по меньшей мере, примерно на 90% или, по меньшей мере, примерно на 95% или более идентичны друг другу, оставаясь гибридизованными одна с другой. Изменяя условия гибридизации от уровня строгости, при котором гибридизация происходит, до уровня, при котором гибридизацию наблюдают впервые, можно определить условия, которые будут допускать данную последовательность к гибридизации (т.е. селективно) с наиболее комплементарными последовательностями в образце.
Примеры условий, которые описывают определение условий промывки в случае условий умеренной или низкой строгости, описаны в Kraus М. and Aaronson S., 1991, Methods Enzymol., 200: 546-556; и в Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons (1998). Промывка является стадией, условия которой обычно устанавливают такими, которые определяют минимальный уровень комплементарности гибридов. Как правило, начиная с самой низкой температуры, при которой происходит только гибридизация гомологов, каждый °С, на который уменьшают конечную температуру промывки (поддерживая концентрацию SSC постоянной), повышает на 1% максимальную процентную долю ошибочных спариваний среди последовательностей, которые гибридизируют. Как правило, удвоение концентрации SSC приводит к повышению Тm примерно на 17°С. С использованием таких указаний температуру промывки можно определить эмпирически для высокой, умеренной или низкой строгости, в зависимости от искомого уровня ошибочных спариваний. Например, промывка в условиях низкой строгости может включать промывку в растворе, содержащем 0,2-крат. SSC/0,1% SDS, в течение 10 минут при комнатной температуре; промывка в условиях умеренной строгости может включать промывку в предварительно подогретом (42 °С) растворе, содержащем 0,2-крат. SSC/0,1% SDS, в течение 15 минут при 42°С; и промывка в условиях высокой строгости может включать промывку в предварительно подогретом (68°С) растворе, содержащем 0,1-крат. SSC/0,1% SDS, в течение 15 минут при 68°С. Кроме того, как известно в технике, для получения желаемого результата промывки можно осуществлять повторно или последовательно. Эквивалентные условия можно определить, изменяя один или несколько параметров, приведенных в качестве примера, как известно в технике, сохраняя в то же время схожую степень комплементарности между молекулой нуклеиновой кислоты-мишени и используемым праймером или зондом (например, гибридизируемой последовательностью).
Родственный аспект настоящего изобретения относится к молекулярной матрице, включающей множество
(i) молекул нуклеиновых кислот, включающих нуклеотидную последовательность, соответствующую любому одному или нескольким неопластическим маркерным генам, описанным в данном описании ранее, или последовательность, показывающую, по меньшей мере, 80% идентичность к указанным генам, или функциональных производных, фрагментов, вариантов или гомологов указанных молекул нуклеиновых кислот; или
(ii) молекул нуклеиновых кислот, включающих нуклеотидную последовательность, способную к гибридизации с любой одной или несколькими последовательностями (i) в условиях средней строгости, или функциональных производных, фрагментов, вариантов или гомологов указанных молекул нуклеиновых кислот; или
(iii) нуклеотидных зондов или олигонуклеотидов, включающих нуклеотидную последовательность, способную к гибридизации с любой одной или - несколькими последовательностями (i) в условиях средней строгости, или функциональных производных, фрагментов, вариантов или гомологов указанных молекул нуклеиновых кислот; или
(iv) зондов, способных связываться с любым одним или несколькими белками, кодированными молекулами нуклеиновых кислот (i), или их функциональными производными, фрагментами, вариантами или гомологами,
где уровень экспрессии указанных маркерных генов из (i) или белков из (iv) является показателем неопластического состояния клетки или субпопуляции клеток, полученных из толстой кишки.
Предпочтительно, указанный процент идентичности составляет, по меньшей мере, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%.
Условия низкой строгости включают и охватывают от, по меньшей мере, примерно 1%, об./об., до, по меньшей мере, 15%, об./об., формамида и от, по меньшей мере, примерно 1 М до, по меньшей мере, 2 М соли для гибридизации, и от, по меньшей мере, примерно 1 М до, по меньшей мере, 2 М соли для промывки. При необходимости можно применить условия другой строгости, такой как средняя строгость, условия которой включают и охватывают от, по меньшей мере, примерно 16%, об./об., до, по меньшей мере, 30%, об./об., формамида и от, по меньшей мере, примерно 0,5 М до, по меньшей мере, 0,9 М соли для гибридизации, и от, по меньшей мере, примерно 0,5 М до, по меньшей мере, 0,9 М соли для промывки, или высокая строгость, условия которой включают и охватывают от, по меньшей мере, примерно 31%, об./об., до, по меньшей мере, 50%, об./об., формамида и от, по меньшей мере, примерно 0,01 М до, по меньшей мере, 0,15 М соли для гибридизации, и от, по меньшей мере, примерно 0,01 М до, по меньшей мере, 0,15 М соли для промывки. Как правило, промывку осуществляют при Тm = 69,3 ± 0,41 (G+C)%[19] = -12°С. Однако Тm двухцепочечной ДНК снижается на 1°С при каждом повышении на 1% числа ошибочных спариваний пар оснований (Bonner et al. (1973), J. Mol. Biol., 81: 123).
Предпочтительно, создают зонды субъекта, которые связываются с нуклеиновой кислотой или белком, на которые они направлены, с уровнем специфичности, который минимизирует число случаев неспецифической реактивности. Однако следует иметь в виду, что может не представляться возможным полное устранение потенциальной перекрестной реактивности или неспецифической реактивности, причем это является ограничением, присущим любой системе на основе зондов.
Что касается зондов, которые используют для детекции белков субъекта, то они могут принимать любую подходящую форму, включая антитела и аптамеры.
Библиотека или матрица полинуклеотидных или белковых зондов предоставляет глубокую и весьма ценную информацию. Далее, две или большее число матриц или профилей (информация, полученная от использования матрицы) таких последовательностей являются полезными инструментами для сравнения совокупности результатов испытаний с эталоном, таким как другой образец, или с хранящимся калибровочным стандартом. При использовании матрицы отдельные зонды типично иммобилизуют в отдельных местах и позволяют взаимодействовать в реакциях связывания. Праймеры, ассоциированные с собранными наборами маркеров, применимы или для получения библиотек последовательностей или прямого детектирования маркеров из других биологических образцов.
Библиотека (или матрица, когда имеют дело с физически разделенными нуклеиновыми кислотами, соответствующими, по меньшей мере, некоторым последовательностям в библиотеке) генных маркеров проявляет весьма нужные свойства. Такие свойства ассоциируются со специфическими состояниями и могут характеризоваться как регуляторные профили. Профиль в данном описании обозначает набор элементов, который дает диагностическую информацию о ткани, из которой первоначально получены маркеры. Профиль во многих случаях включает ряд пятен на матрице, полученной из депонированных последовательностей.
Характеристический профиль пациента, как правило, получают с использованием матрицы. Матричный профиль можно сравнить с одним или несколькими другими матричными профилями или другими эталонными профилями. Результаты сравнения могут дать ценную информацию относительно болезненных состояний, развивающегося состояния, восприимчивости к терапии и другую информацию о пациенте.
Другой аспект настоящего изобретения относится к диагностическому набору для оценки биологических образцов, включающему агент для детекции одного или нескольких неопластических маркеров, и реагенты, применимые для облегчения детекции агентом в первой классификации. Также могут быть включены другие средства, например, для получения биологического образца. Агент может представлять собой любой подходящий детектирующий фактор.
Настоящее изобретение описывается далее с помощью приведенных примеров, не являющихся ограничительными.
Пример 1
Методы и материалы Данные Affymetrix GeneChip
Информацию о профилях экспрессии генов и сопутствующую клиническую информацию приобрели у GeneLogic Inc. (Gaithersburg, MD, USA). Для каждой анализируемой ткани получают данные олигонуклеотидных матриц для наборов 44928 зондов (Affymetrix HGU133A & HGU133B, объединенные), идентификаторы экспериментальных и клинических данных и цифровой архив микроскопических изображений гистологических препаратов. Выполняют качественный контрольный анализ для удаления матриц, не соответствующих обязательным контрольным показателям качества, определенным изготовителем.
Уровни экспрессии транскриптов рассчитывали с использованием методов нормализации как Microarray Suite (MAS) 5.0 (Affymetrix), так и Robust Multichip Average (RMA) (Affymetrix. GeneChip expression data analysis fundamentals, Affymetrix, Santa Clara, CA, USA, 2001; Hubel et al., Bioinformatics, 18: 1585-1592; Irizarry et al., Nucleis Acids Research, 31, 2003). Нормализованные данные MAS используют для осуществления обычного стандартного контроля качества, и совокупность конечных данных нормализуют с использованием RMA для всех последующих анализов.
Одномерная дифференциальная экспрессия
Дифференциально экспрессированные генные транскрипты идентифицируют с использованием усредненного Т-критерия, осуществленного в библиотеке limma, пересланной по линии связи из хранилища Bioconductor R. (G.K. Smyth, Statistical Applications in Genetics and Molecular Biology, 3(1): Article 3, 2004; G.K. Smyth, Bioinformatics and Computational Biology Solutions using R and Bioconductor. Springer, New York, 2005). Оценки значимости (величины p) корректируют с использованием поправки Бонферрони для множественных сравнений.
Картины тканеспецифической экспрессии
Для построения фильтра для гипотетически «выключенной» экспрессии генов сначала оценивают средний уровень экспрессии для всех 44928 наборов зондов по всему ряду из 454 тканей. Для того, чтобы оценить вкл./выкл. порог экспрессии, упорядочивают 44928 средних величин, и вычисляют эквивалент величины экспрессии для 30-й процентили по набору данных. Такой произвольный порог выбирают, поскольку теоретически предсказано, что большинство транскриптов (и предположительно более 30%) в данном образце должны быть претерпевшими транскрипционный сайленсинг. Таким образом, такой порог представляет собой консервативную верхнюю границу для оценки сигнала как неспецифического или фонового.
Аннотации символов гена
Для того, чтобы картировать названия наборов зондов Affymetrix к официальным символам генов, используют метаданные, доступные от Bioconductor. Используют библиотеку Hgul33plus2, версия 1.16.0, которая собрана с использованием данных Entrez Gene, загруженных 15 марта 2007.
Оценки рабочих характеристик
Диагностическую полезность каждой таблицы маркеров, приведенной в данном описании, оценивают, включая чувствительность, специфичность, положительную прогностическую ценность, отрицательную прогностическую ценность, отношение правдоподобия положительной величины, отношение правдоподобия отрицательной величины. Такие оценки вычисляют с теми данными, которые используют для раскрытия маркеров, и поэтому оценки рабочих характеристик в будущих образцах тканей возможно будут завышенными. Для того, чтобы улучшить обобщаемость оценок, используют модифицированный метод «складного ножа» с повторным отбором образцов для вычисления менее смещенной величины для каждой характеристики.
Результаты
Ряд одномерных статистических критериев применяют к данным олигонуклеотидной матрицы Affymetrix для обнаружения человеческих генов, которые можно было бы использовать для того, чтобы отличить колоректальные неопластические ткани от ненеопластических тканей. Затем идентифицируют ряд генных транскриптов, которые, как оказывается, применимы для того, чтобы отличить колоректальные аденомы от колоректальных аденокарцином. Также идентифицируют подгруппу таких транскриптов, которая может иметь особую диагностическую полезность из-за белковых продуктов, или секретируемых или отраженных на клеточной поверхности эпителиальных клеток. Наконец, идентифицируют другую подгруппу транскриптов, экспрессированных специфически в неопластических тканях, и при уровнях ниже или почти равных фоновым уровням в неопластических тканях.
Гены, дифференциально экспрессированные в неопластических тканях
То, что из общего набора GeneChip в 44928 наборов зондов свыше 11000 наборов зондов дифференциально экспрессируются, определяют по усредненному t-критерию с использованием пакета limma в BioConductor (G.K. Smyth, 2004, цит. выше) с использованием консервативной поправки (Bonferroni) для множественных сравнений. Когда такой список фильтруют далее, включая только те наборы зондов, которые демонстрируют 2-кратное или большее изменение экспрессии между неопластическими и ненеопластическими тканями, находят, что 560 наборов зондов экспрессируются на более низком уровне в неопластических тканях по сравнению со здоровыми тканями.
Такие 560 наборов зондов аннотируют с использованием самых последних метаданных и пакетов аннотаций, доступных для чипов. Картируют 560 недоэкспрессированных наборов зондов по отношению к 434 символам генов.
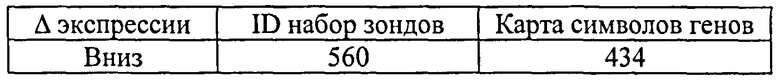
Гипотетические маркеры, специфические для колоректальной неоплазии Хотя картины дифференциальной экспрессии генов применимы для диагностических целей, к такому плану также обращаются для идентификации диагностических белков, сброшенных в просвет кишки неопластическим колоректальным эпителием. Для обнаружения белков-кандидатов список дифференциально экспрессированных транскриптов фильтруют с помощью критериев выбора, нацеленных на идентифицирующие маркеры, специфически «выключенных» в тканях колоректальной неоплазии. Для того, чтобы идентифицировать «выключенные» гены, создают критерии фильтрации для поиска генов с i) уровнями экспрессии ниже теоретического порога вкл/выкл и ii) нормальными сигналами, по меньшей мере, в 2 раза более высокими. Профиль экспрессии примера транскрипта, который является «выключенным» в неопластических тканях, показан на фигуре 1.
Пример 2
Наборы зондов, повышенные в отсутствие неоплазии в сравнении с неопластическими тканями
Анализ дифференциальной экспрессии применяют для идентификации претерпевших отрицательную регуляцию наборов зондов в данных GeneChip Affymetrix, измеряя концентрацию РНК в 454 колоректальных тканях, в том числе, 161 образца аденокарциномы, 29 образцов аденомы, 42 образца колита и 222 не пораженных болезнью тканей. С использованием консервативных поправок для множественной проверки гипотезы и порога 2-кратного абсолютного изменения определяют, что 560 наборов зондов обнаруживают пониженный уровень экспрессии в неопластических тканях относительно ненеопластических контролей. 560 этих наборов зондов были картированы к 434 предполагаемым символам генов на основании нуклеотидной последовательности транскриптов.
Проверка гипотезы/оценки достоверности
Уровни экспрессии указанных кандидатов измеряют в независимо полученных клинических образцах. Гибридизуют 526 наборов зондов с экстрактами РНК из 68 клинических образцов, в том числе, 19 образцов аденом, 19 аденокарцином и 30 контрольных здоровых тканей, с использованием созданного по индивидуальному проекту генного чипа на аденому («Adenoma Gene Chip»). Тридцать четыре (34) набора зондов не проверяют, так как они не были включены в индивидуальный проект.
Подтвердилось, что 459 из 526 наборов-мишеней зондов (или наборов зондов, непосредственно связанных с одним и тем же генным локусом-мишенью) подобным образом дифференциально экспрессируются (Р < 0,05) в таких независимо полученных тканях. Результаты анализа дифференциальной экспрессии таких 459 наборов зондов показаны в таблице 1, приведенной в графической части.
Затем проверяют 372 из 434 уникальных генных локусов, к которым представлены 560 наборов зондов для гибридизации. Остальные 62 символы гена не представляют в данных по проверке достоверности. Отмечают, что 328 или 372 символов генов представлены в данных по проверке достоверности, по меньшей мере, одним дифференциально экспрессирующимся набором зондов, и многие символы включают множество наборов зондов против участков во всем предполагаемом локусе. Полный список наборов зондов, которые связываются с локусами-мишенями, приводится в таблице 2, приведенной в графической части.
Выводы
Наборы зондов и символы, являющиеся кандидатами, приведенные в таблицах 1 и 2, приведенных в графической части, соответственно, дифференциально экспрессируются в неопластических колоректальных тканях на уровнях более низких по сравнению с ненеопластическими контрольными образцами.
Пример 3
Наборы зондов, демонстрирующие ненеопластический специфический профиль Во время анализа данных обнаружения получают новый профиль экспрессии среди неопластических и ненеопластических фенотипов. Предполагается, что подгруппа количественно дифференциально экспрессированных наборов зондов кроме того качественно экспрессирована дифференциально. Такие наборы зондов не показывают явной активности экспрессии генов в неопластических тканях, т.е. оказывается, что такие наборы зондов экспрессируются выше фоновых уровней только в ненеопластических тканях. Такое наблюдение и исходящая из этого гипотеза основаны на двух принципах:
1) большинство человеческих транскриптов, которые присутствуют на полногеномном генном чипе (например, U133), вероятно, не будут экспрессироваться в колоректальной слизистой; и
2) интенсивность связывания с микроматрицей для таких «выключенных» наборов зондов (к меченой кРНК) будет отражать технический фон способа анализа, т.е. неспецифическое связывание олигонуклеотидов.
Для получения списка ненеопластических специфических наборов зондов неопластическую интенсивность дифференциально экспрессированных наборов зондов сравнивают с гипотетическим порогом фонового сигнала от всех наборов зондов на чипе. Отмечается, что путем построения, все наборы зондов в пуле кандидатов, из которого выбирают транскрипты «включено», по меньшей мере, в два раз сверхэкспрессируются в здоровых тканях относительно больных тканей. Все вместе такие критерии приводят к подгруппе дифференциально экспрессированных видов транскриптов, которые специфически экспрессируются в ненеопластических тканях.
Такой анализ показывает, что 42 набора зондов, соответствующие приблизительно 41 генному локусу, показывают специфический профиль транскрипции экспрессии в отсутствие неоплазии.
Проверка достоверности/гипотезы
Конструкция созданного по индивидуальному проекту генного чипа препятствует проверке специфических для отсутствия неоплазии наборов зондов с использованием таких же принципов, какие используют для обнаружения. В частности, созданный по индивидуальному проекту генный чип (по конструкции) не содержит большого пула наборов зондов, прогнозированных для гибридизации гипотетически «выключенных»/«нетранскрибируемых» генных транскриптов. Это имеет место потому, что созданная по индивидуальному проекту конструкция генного чипа в сильной мере смещена в сторону дифференциально экспрессирующихся транскриптов в колоректальных неопластических тканях.
Обычная проверка дифференциальной экспрессии (limma) была поэтому применена к указанным наборам зондов-кандидатов в отношении специфически экспрессирующихся в неопластических тканях. Из 37 (из 42) наборов зондов на изготовленном по индивидуальному проекту генном чипе 33 набора зондов (или наборов зондов, которые связываются с одним и тем же локусом) дифференциально экспрессируются среди 38 неопластических тканей (аденома и рак) и ненеопластических контролей. Результаты таких экспериментов по проверке достоверности показаны в таблице 3, приведенной в графической части.
Также ставилась цель испытать наборы зондов, которые известны как гибридизующиеся с генными локусами, с которыми гибридизуются наборы зондов, заявленные в данной заявке. Из 41 предполагаемого генного локуса, на которые нацелены наборы зондов, 33 присутствуют в данных по достоверности. Все тридцать три (33) из таких 33 символов гена (100%) обнаруживают, по меньшей мере, один гибридизующийся набор зондов, который дифференциально экспрессируется в неопластических тканях. Результаты таких экспериментов, включая все наборы зондов, которые связываются с каждым локусом-мишенью по типу дифференциальной экспрессии, показаны в таблице 4, приведенной в графической части.
Пример 4
Материалы и методы для примеров 2 и 3
Данные по профилям экспрессии генов, измеренные в 454 образцах колоректальной ткани, в том числе, неопластической, здоровой и пораженной ненеопластическим заболеванием контрольной ткани, закупают у GeneLogic Inc. (Gaithersburg, MD, USA). Для каждого образца ткани получают данные по олигонуклеотидной микроматрице Affymetrix (Santa Clara, СА, USA), в сумме по 44928 наборам зондов (HGU133A & HGU133B, объединенные), экспериментальные и клинические дескрипторы и цифровой архив микроскопических изображений гистологических препаратов. Перед применением методов по изобретению к таким данным выполняют методы широкого качественного контроля, включая статистическое исследование, обзор историй болезни на непротиворечивость и гистопатологическую проверку случайной выборки матриц. Микроматрицы, которые не удовлетворяют приемлемым критериям качества, удаляют из анализа.
Проверка гипотезы
Кандидаты-биомаркеры транскрипции проверяют с использованием созданной по индивидуальному проекту олигонуклеотидной матрицы наборов 25-мерных олигонуклеотидных зондов, созданных для гибридизации с кандидатами-транскриптами РНК, идентифицированными во время обнаружения. Гипотезу дифференциальной экспрессии проверяют с использованием экстрактов РНК, полученных из независимо собранных клинических образцов, включающих 30 здоровых колоректальных тканей, 19 тканей колоректальной аденомы и 19 тканей колоректальной аденокарциномы. Подтверждают строгое соответствие каждого экстракта РНК критериям контроля качества.
Образцы колоректальной ткани
Все ткани, используемые для проверки гипотезы, были получены из банка тканей пациентов специализированного госпиталя 3-го уровня в центре Аделаиды, Австралия (Repatriation General Hospital и Flinders Medical Centre). Доступ к банку тканей для данного исследования санкционирован Research and Ethics Committee of Repatriation General Hospital и Ethics Committee of Flinders Medical Centre. Информированное согласие пациента получено для каждой исследуемой ткани.
После хирургического иссечения образцы помещают в стерильную емкость и собирают в операционной. Время от оперативного иссечения до сбора в операционной варьировало, но составляло не более 30 минут. Образцы размером приблизительно 125 мм3 (5×5×5 мм) берут из макроскопически здоровой ткани, а также в случае возможной патологии, определяемые обе участком толстой кишки, а также расстоянием - или проксимально или дистально от места патологии. Ткани помещают в криогенные емкости, затем сразу же погружают в жидкий азот и хранят при -150 °С до обработки.
Экстракция РНК
Экстракции РНК выполняют с использованием реагента Trisol (R) (Invitrogen, Carlsbad, СА, USA) по инструкциям изготовителя. Каждый образец гомогенизируют в 300 мкл реагента Trisol с использованием модифицированной дрели Dremel и стерилизованных съемных пестиков. К гомогенату добавляют еще 200 мкл реагента Trisol, и образцы инкубируют при комн.темп. в течение 10 минут. Затем добавляют 100 мкл хлороформа, образцы встряхивают при вращении в течение 15 секунд и инкубируют при комн.темп. еще в течение 3 минут. Водную фазу, содержащую целевую РНК, получают центрифугированием при 12000 об/мин в течение 15 мин, 40°С. Затем РНК осаждают, инкубируя образцы при комн.темп. в течение 10 минут с 250 мкл изопропанола. Преципитат очищенной РНК собирают центрифугированием при 12000 об/мин в течение 15 мин, 40°С, и супернатанты отбрасывают. Затем осадки промывают 1 мл 75% этанола, затем взбалтывают круговыми движениями и центрифугируют при 7500 об/мин в течение 8 мин, 40°С. Наконец, осадки сушат на воздухе в течение 5 мин и ресуспендируют в 80 мкл воды, не содержащей РНКазу. Для улучшения последующей растворимости образцы инкубируют при 55°С в течение 10 мин. Определяют количество РНК, измеряя оптическую плотность при А260/280 нм. Качество РНК оценивают электрофорезом в 1,2% агарозном геле с формальдегидом.
Обработка генного чипа
Для проверки гипотез, связанных с кандидатами-биомаркерами для колоректальной неоплазии, экстракты РНК оценивают с использованием, созданного по индивидуальному проекту авторами при сотрудничестве с Affymetrix (Santa Clara, СА, USA), генного чипа. Такие созданные по индивидуальному проекту генные чипы получают с использованием стандартного протокола Affymetrix, разработанного для матрицы HU Gene ST 1.0, описанной в (Affy:WTAssay).
Статистическая программа и обработка данных
Статистическую среду R и библиотеки BioConductor (BioConductor, www.bioconductor.org) (ВIOС) используют для большинства анализов. Для того, чтобы картировать идентификационные номера наборов зондов к символу гена на созданном по индивидуальному проекту генном чипе hgul33plus2, используют библиотеку, версия 2.2.0, которую собирают с использованием данных Entrez Gene, загруженную 18 апреля, 12:30:55,2008 (BIOC).
Проверка гипотезы дифференциально экспрессированных биомаркеров Для того, чтобы оценить дифференциальную экспрессию между классами тканей, используют критерий Стьюдента для равных значений между двумя образцами или робастный вариант, предоставляемый библиотекой limma (Smyth) (limma). Для смягчения влияния ложного обнаружения из-за множественной проверки гипотезы, применяют поправку Бонферрони к величинам Р в процессе обнаружения (MHT:Bonf). Для проверки гипотезы применяют несколько менее консервативную поправку множественной проверки гипотезы Benjamini & Hochberg, которая ставит целью регулирование степени ложного обнаружения решений (МНТ:ВН).
Обнаружение профилей тканеспецифической экспрессии генов Методы обнаружения с использованием данных по экспрессии генов часто используют для получения ряда кандидатов, многие из которых не подходят для коммерческих продуктов, поскольку они включают трудно уловимые различия в экспрессии генов, которые может быть трудно детектировать в лабораторной практике. Рере et al. отмечают, что «идеальный» биомаркер поддается детекции в опухолевой ткани, но не обнаруживается (вовсе) в неопухолевой ткани (Pepe:biomarker:development). Для того, чтобы сместить обнаружение в пользу кандидатов, которые удовлетворяют таким критериям, был разработан способ анализа, который имеет целью обогащение кандидатов в биомаркеры, качественная мера отсутствия или присутствия которых является диагностической для фенотипа, представляющего интерес. Такой способ предполагает попытку отобрать кандидатов, которые демонстрируют прототипный профиль «включенный» или «выключенный» относительно оценки фоновой/шумовой экспрессии по всему чипу. Предполагается, что такие РНК-транскрипты с большей вероятностью коррелируют с белками с диагностическим потенциалом, которые подвергаются трансляции ниже по ходу, или предсказывают имеющие место выше по ходу геномные изменения (например, статус метилирования), которые можно использовать для диагностики. Такое фокусирование скорее на качестве, чем на количестве, может упростить способ разработки продукта для таких биомаркеров.
Способ основан на предположении, что пул экстрагированных форм РНК в любой данной ткани (например, колоректальной слизистой оболочки) будет специфически связываться с относительно небольшой подгруппой всех наборов зондов на генном чипе, созданном для измерения всего генома. При таком предположении оценено, что большинство наборов зондов на полном генном чипе человека не показывает специфических сигналов высокой интенсивности.
Такое наблюдение используют для приближения к фоновому или «неспецифическому связыванию» на чипе, подбирая теоретический уровень, равный величине, например, самой низкой, 25% квантили ранжированных средних величин. Такая квантиль может быть произвольно установлена до некоторого более низкого уровня, который предоставляет разумное предположение, что сигналы не представляют связывание РНК выше фонового уровня. Наконец, такую оценку фона используют как порог для оценки наборов зондов «ВЫКЛ» в эксперименте для, скажем, образцов ненеопластических тканей.
Напротив, при дополнительной гибридизации наборы зондов, которые 1) экспрессированы выше такого теоретического порогового уровня и 2) при дифференциально более высоких уровнях в образцах опухолей, могут представлять собой опухолеспецифические кандидаты-биомаркеры. Отмечается, что в таком случае концепцию пороговых значений «кратного изменения» также можно удобно применить для того, чтобы дополнительно подчеркнуть концепцию абсолютного усиления экспрессии в предположительном наборе зондов «ВКЛ».
Что касается предположения о низком фоновом связывании для значительной фракции измеренных наборов зондов, такой способ используют только при большом объеме данных GeneLogic и обнаружения. Для того, чтобы построить фильтр для гипотетически «включенного» биомаркера в данных по обнаружению GeneLogic, оценивают средний уровень экспрессии для всех 44298 наборов зондов во всех 454 тканях. Затем среднее 44928 величин ранжируют, и вычисляют в наборе данных величину экспрессии, эквивалентную 25-ой процентили. Такой произвольный порог выбирают потому, что большинство транскриптов (и предположительно, более 25%) в данном образце будут проявлять низкую концентрацию, при которой происходит эффективный транскрипционный сайленсинг. Таким образом, такой порог представляет собой консервативную верхнюю границу, которую оценивают как неспецифическую, или фоновую, экспрессию.
Пример 5
Данные по метилированию ДНК
Анализы для детекции метилирования в промоторных участках восьми генов, претерпевших отрицательную регуляцию, показаны в таблице 5, приведенной в графической части. Способы обработки бисульфитом ДНК и анализы для определения уровней метилирования ДНК, включая MSP и COBRA, описаны в Clark et al. (2006).
В пяти анализах MSP используют пары праймеров, показанные в таблице 7, приведенной в графической части. Контрольную ПЦР для несмещенной амплификации гена CAGE используют для определения количества введенной ДНК для обеспечения стандарта для количественного определения уровня метилирования каждого гена. Для ПЦР реакционные смеси, 25 мкл, в Biorad iQ SyBr Green Super Mix содержат 5 нг обрабатываемых бисульфитом ДНК (1 нг для анализов клеточных линий и 6 нг для клинических образцов) и 200 нМ прямых и обратных праймеров. Условия циклов ПЦР:
95,0°С в течение 2 мин,
затем 50 циклов
95,0°С/15 с,
Темп. °С/30 с,
72,0°С/30 с,
где «Темп.» представляет собой температуру повторного отжига, оптимизированную для каждого гена.
Для гена DF предварительно проводят 3 цикла с использованием температуры плавления 95,0°С, с последующими 50 циклами с более низкой температурой плавления 84,0°С (для уменьшения неспецифической амплификации).
Получают стандартную кривую с использованием ДНК, метилированной метилазой M.SssI (100% метилирование), и ДНК, амплифицированной in vitro с использованием ДНК-полимеразы Рhi20 (метилирование 0%).
Анализы COBRA разрабатывают для трех генов, как показано в таблице 8, приведенной в графической части. ПЦР проводят так, как описано выше, в условиях циклов
95,0°С в течение 2 мин,
затем 50 циклов
95,0°С/15 с,
Темп. °С/30 с,
72,0°С/30 с.
После ПЦР 10 мкл продукта ПЦР расщепляют соответствующим ферментом (см. таблицу 8, приведенную в графической части), продукты расщепления анализируют электрофорезом в геле, и уровни метилирования определяют полуколичественно.
Состояние метилирования восьми генов определяют в четырех линиях клеток колоректального рака Сасо2, НСТ116, НТ29 и SW480, а также в ДНК нормальной крови и клеточной линии фибробластов в здоровых легких MRC5. Уровень метилирования суммирован в таблице 5, приведенной в графической части. Промоторные участки всех восьми генов показывают сильное метилирование в 2 или 3 из четырех испытываемых линий клеток колоректального рака. Все показывают утрату или низкий уровень метилирования в ДНК из ДНК нормальной крови и клеточной линии фибробластов MRC5, за исключением метилирования DF в MRC5.
Для двух из указанных генов MAMDC2 и GPM6B анализ расширяют до ряда из 12 образцов аденом, 18 образцов рака и 22 образцов соответствующих здоровых тканей (фигура 2, А и В).
Для MAMDC2 количественный анализ показывает, что 2 из 12 образцов аденом и 6 из 18 образцов рака показывают повышенное метилирование по сравнению с самым высоким уровнем, наблюдаемым в образцах здоровых тканей. Уровни метилирования гена GPM6B определяют полуколичественным анализом COBRA, оценивают по шкале от 0 до 5, основанной на визуальном осмотре продуктов расщепления рестриктазой. Очевидна четкая тенденция к усилению метилирования промоторов при развитии от здорового состояния к аденоме и к раку (фигура 2, часть В).
Такие данные для ряда примеров генов, подвергшихся отрицательной регуляции, показывают, что такая отрицательная регуляция в клеточных линиях колоректального рака и ткани первичной неоплазии может быть ассоциирована с метилированием ДНК, и что анализы метилирования ДНК можно использовать для того, чтобы различить здоровую и раковую ткани.
Пример 6
Идентификация генов нуклеотидной последовательности, представляющей интерес, которую определяют с помощью набора зондов Affymetrix
Проведение BLAST-анализа последовательности, представляющей интерес, с использованием интерактивных доступных онлайн программ Basic Local Alignement Search Tools [BLAST], например, NCBI/BLAST
http://blast.ncbi.nml.nih.gov/Blast.cgi
(a) Выбрать «Human» в BLAST ASSEMBLED GENOMES на веб-странице http://blast.ncbi.nml.nih.gov/Blast.cgi
(b) Оставить установку по умолчанию, т.е.
• База данных: Genome (all assemblies)
• Программа: megaBLAST: сравнивает близкородственные нуклеотидные последовательности
• Произвольные параметры: Expect: 0,01, Filter: по умолчанию, Descriptions: 100, Alignments: 100
(c) Копируйте/Вставьте последовательность в окно «BLAST»
(d) Откройте «Begin Search»
(e) Откройте «View Report»
Оценка результатов исследования открытого BLAST
При «BLAST-анализе» последовательности можно идентифицировать несколько значимых выравниваний последовательностей.
Идентификация номенклатуры генов в отношении идентифицированного соответствия последовательностей
(a) Открыть файл для одного из идентифицированных успешных вариантов (хитов)
(b) Новая страница будет схематически отображать позицию хита на одной хромосоме. Будет очевидно, какой ген является хитом.
(c) Вернитесь к последовательности «хита», щелкая по ссылке
(d) Найдите ген в предлагаемом окне «search». Это даст координаты нуклеотидов гена для гена.
Определение распространенности последовательности
(a) Откройте программу NCBI/BLAST (http://blast.ncbi.nml.nih.gov/Blast.cgi)
(b) Откройте «nucleotide Blast» под «basic BLAST»
(c) Копируйте/Вставьте интересующую последовательность в окно «Query Sequence»
(d) Откройте «Blast»
Оценка результатов поиска последовательности в nBLAST
(a) Тестирование nBLAST Sequence может привести к нескольким хитам Blast, из которых некоторые номера доступа приводятся в «Description».
(b) Эти хиты должны быть проанализированы.
Определение расположения последовательности в гене
База данных Ensemble является интерактивной базой данных, которая дает и сохраняет автоматическую аннотацию выбранных геномов эукариот (www.ensembl.orq/index.html)
Идентификация расположения последовательности в гене
(a) Установите «Search» для Homo Sapiens, тип «gene name» в предоставленном поле поиска Ensemble.org/index.html
(b) Откройте «Go»
(c) Щелкните по ссылке «vega protein_coding Gene: OTTHUMG000000144184» для получения отчета об аннотации
(d) Откройте «Gene DAS Report)) для поиска информации, касающейся альтернативной базы данных мест сплайсинга, введите «the gene name» в поле поиска
• Щелкните по «the gene entry))
• Прокрутите вниз до «evidences»
• Проанализируйте альтернативные сайты сплайсинга
• Щелкните по «Confirmed intron/exons» для получения списка координат для экзонов и интронов.
Альтернативный сплайсинг и/или транскрипция
База данных AceView дает проверенное и неизбыточное представление последовательностей для всех опубликованных последовательностей мРНК. База данных доступна через NCBI:
http://www.ncbi.nlm.nih.gov/IEB/Research/Acemblv/
Дополнительное исследование генных транскриптов мРНК
(a) Введите «gene name» в предоставленное поле «search»
(b) Щелкните по «Go»
(c) Следующая информация доступна от полученного ввода в AceView:
• Число клонов кДНК, из которых конструирован ген (т.е. полученный из экспериментальной работы, включающей выделение мРНК)
• мРНК, прогнозируемые как продуцированные геном
• Наличие неперекрывающихся альтернативных экзонов и проверенных альтернативных сайтов полиаденилирования
•Наличие усечений
• Возможность регулируемой альтернативной экспрессии
• Интроны, зарегистрированные как принимающие участие в альтернативном сплайсинге гена
(a) Классические мотивы сайта сплайсинга
Применение способа к LOC643911/hCG_1815491
(b) Материалы и методы
Экстракция РНК
Экстракцию РНК выполняют с использованием реагента Trisol (R) (Invitrogen, Carlsbad, СА, USA) по инструкциям изготовителя. Каждый образец гомогенизируют в 300 мкл реагента Trisol с использованием модифицированной дрели Dremel и стерилизованных съемных пестиков. К гомогенату добавляют еще 200 мкл реагента Trisol, и образцы инкубируют при комн. темп, в течение 10 минут. Затем добавляют 100 мкл хлороформа, образцы встряхивают при вращении в течение 15 секунд и инкубируют при комн.темп. еще в течение 3 минут. Водную фазу, содержащую целевую РНК, получают центрифугированием при 12000 об/мин в течение 15 мин, 40°С. Затем РНК осаждают, инкубируя образцы при комн. темп, в течение 10 минут с 250 мкл изопропанола. Преципитат очищенной РНК собирают центрифугированием при 12000 об/мин в течение 15 мин, 40°С, и супернатанты отбрасывают. Затем осадки промывают 1 мл 75% этанола, затем взбалтывают круговыми движениями и центрифугируют при 7500 об/мин в течение 8 мин, 40°С. Наконец, осадки сушат на воздухе в течение 5 мин и ресуспендируют в 80 мкл воды, не содержащей РНКазу. Для улучшения последующей растворимости образцы инкубируют при 55°С в течение 10 мин. Определяют количество РНК, измеряя оптическую плотность при А260/280 нм. Качество РНК оценивают электрофорезом в 1,2% агарозном геле в присутствии формальдегида.
Обработка генного чипа
Образцы РНК, которые анализируют на Human Exon 1.0 ST генный чип обрабатывают с использованием набора для мечения мишеней и контроля Affymetrix WT (часть # 900652), следуя протоколу, описанному в (Affymetrix 2007 P/N 701880 Rev.4). Коротко, кДНК первого цикла синтезируют из 100 нг рибосомной восстановленной РНК с использованием случайных гексамерных праймеров, меченных промоторной последовательностью Т7 и Superscript II (Invitrogen, Carlsbad, СА), за этим следует синтез двухцепочечной кДНК с помощью ДНК-полимеразы I. Затем синтезируют антисмысловую кРНК с использованием полимеразы Т7. Затем синтезируют смысловую кДНК второго цикла с использованием Superscript II, dNTP + dUTP и случайных гексамеров, и получают смысловую одноцепочечную кДНК, включающую урацил. Затем такую одноцепочечную содержащую урацил кДНК фрагментируют с использованием комбинации урацил-ДНК-гликозилаза (UDG) и апуриновой/апиримидиновой эндонуклеазы 1 (АРЕ 1). Наконец, ДНК метят биотином с использованием терминальной трансферазы (TdT) и реагента для мечения ДНК, запатентованного Affymetrix. Гибридизацию с матрицами осуществляют при 45°С в течение 16-18 часов.
Промывку и окрашивание гибридизованных генных чипов осуществляют с использованием Affymetrix Fluidics Station 450 и Affymetrix Scanner 3000, следуя рекомендованным протоколам.
Количественная ПЦР в реальном времени с использованием SYBR green
Количественную ПЦР в реальном времени выполняют на выделенной из клинических образцов РНК для амплификации и детекции различных транскриптов hCG_1815491.
Сначала синтезируют кДНК из 2 мкг полной РНК с использованием набора для обратной транскрипции Applied Biosystema High Capacity Reverse transcription (P/N 4368814). После синтеза реакционную смесь разбавляют 1:2 водой, и получают конечный объем 40 мкл, и 1 мкл такой разбавленной кДНК используют в последующих реакциях ПЦР.
ПЦР проводят в объеме 25 мкл с использованием основной смеси Promega 2х PCR (P/N М7502), 1,5 мкл 5 мкМ прямого праймера, 1,5 мкл 5мкМ обратного праймера, 7,875 мкл воды, 0,625 мкл разведения 1:3000 10000х исходного раствора чистого красителя SYBR green 1 (Invitrogen P/N S7567) и 1 мкл кДНК.
Условиями циклов амплификации являются 95° в течение 2 минут х 1 цикл, 95° в течение 15 секунд и 60° в течение 1 минуты х 40 циклов. Реакции амплификации выполняют в аппарате Corbett Research Rotor-Gene RG3000 или в аппарате Roche LightCycler 480 для ПЦР в реальном времени. Когда для амплификации используют аппарат Roche LightCycler 480, объем реакционной смеси уменьшают до 10 мкл, и реакцию выполняют в 384-луночном планшете, но соотношения между всеми компонентами остаются теми же. Конечные результаты получают с использованием метода DDCt, причем уровни экспрессии различных транскриптов hCG_1815491 вычисляют относительно уровня экспрессии эндогенного облигатного гена HPRT.
ПЦР с определением по «конечной точке» («End-point» ПЦР)
«End-point» ПЦР для различных транскриптов hCG_1815491 выполняют на РНК, выделенной из клинических образцов. Условия идентичны условиям, описанным выше для анализа с SYBR green, но краситель SYBR green заменяют водой. Реакции амплификации выполняют в термоячейке MJ Research РТС-200. Анализируют 2,5 мкл амплифицированного продукта в 2% агарозном Е-геле (Invitrogen) вместе с маркером-лесенкой размера ДНК в 100 пар оснований.
Результаты
Нуклеотидную структуру и уровни экспрессии транскриптов, родственных hCG_1815491, анализируют на основе идентификации диагностической полезности набора зондов Affymetrix 238021_s_at и 238022_at из анализа генного чипа.
Ген hCG_1815491 в настоящее время представлен в NCBI как единственная последовательность RefSeq ХМ_93911. Последовательность RefSeq hCG_1815491 основана на 89 поступлениях из GenBank из 83 клонов кДНК. До марта 2006 указанные клоны прогнозировались как представляющие два перекрывающихся гена LOC388279 и LOC650242 (последний также известен как LOC643911). В марте 2006 базу данных по геному человека фильтровали против реаранжировки клонов, выровняли вместе с геномом и образовали кластер минимальным неизбыточным путем. В результате LOC388279 и LOC650242 слились в одни ген, названный hCG_1815491 (более ранними названиями для hCG_1815491 являются LOC388279, LOC643911, LOC650242, ХМ_944116, AF275804, XMJ73688).
Установлено, что RefSequence, которая определяется геномными координатами
8579310-8562303 на человеческой хромосоме 16, как определяет стандарт контигов NCBI NT_010498.15 | Hsl6_10655, по NCBI 36 генома от марта 2006 охватывает hCG_1815491. Полученные из такого гена 10 предсказанных вариантов РНК выровняли с геномной нуклеотидной последовательностью, находящейся в участке карты 8579310-8562303. Такой анализ с выравниванием показал наличие, по меньшей мере, 6 экзонов, некоторые из которых претерпели альтернативный сплайсинг. Идентифицированные экзоны находятся в противоречии со всего 4 экзонами, определенными в NCBI hCG_1815491 RefSeq ХМ_93911. Два других предполагаемых экзона также идентифицированы в RefSequence путем проверки включенных наборов зондов на Affymetrix Genechip HuGene Exon 1.0, которые нацелены на нуклеотидные последовательности, включенные в RefSequence. Идентифицированную и расширенную экзон-интранную структуру hCG_1815491 используют для создания специфических олигонуклеотидных праймеров, которые позволяют измерить экспрессию вариантов РНК, полученных из RefSequence, с использованием методологии на основе ПЦР.
Таблицы
Обозначения наборов зондов включают как идентификационные номера (ID) набора зондов HG-133plus2, так и идентификационные номера зондов матрицы Human Gene LOST. Последние можно удобно картировать к идентификационным номерам (ID) кластера транскриптов с использованием файла с таблицей зондов Human Gene LOST, предоставленного Affymetrix
(http://www.affymetrix.com/Auth/analysis/downloads/na22/wtgene/HuGene-l 0-st-vl.probe.tab.zip). С использованием широко доступной программы, такой как NetAffx (предоставлена Affymetrix), ID кластера транскриптов можно также картировать к символам генов, местоположению на хромосоме и т.д.
Таблица 1
Показаны наборы зондов, экспрессированные на более высоких уровнях в ненеопластических тканях относительно неопластических контролей. TargetPS - id набора зондов Affymetrix HG-133plus2; Symbol - предполагаемый символ гена, соответствующий id набора зондов-мишени - несколько названий символов показывают возможность гибридизации набора зондов с несколькими генами-мишенями; Signif. FDR - приведенная величина р для проверки различия средних между РНК, экстрагированной из тканей неоплазии и из ненеопластических тканей. Приведение осуществляют с использованием поправки Benjamini & Hochberg для множественной проверки гипотезы (Benjamini and Hochberg, 1995); D.value50 - оценка параметра диагностической эффективности, соответствующая площади под кривой рабочей характеристики приемника ROC. Такой параметр дает подходящую оценку диагностической полезности и описан в Saunders, 2006; FC - изменение, крат, между средними уровнями экспрессии в отсутствие неоплазии по сравнению с неоплазией; Sens-Spec - оценка диагностической эффективности, соответствующая точке на кривой ROC, показывающей равную чувствительность и специфичность; CI (95) - 95% доверительный интервал оценок чувствительности и специфичности.
Таблица 2
Данные о множестве наборов зондов, соответствующих символам генов, заявленных в данной заявке, обнаруживающих различия концентрации ДНК между ненеопластическими тканями и неопластическими контролями. Symbol - символ гена; ValidPS_DOWN - ID наборов зондов Affymetrix ID, демонстрирующих статистически значимую сверхэкспрессию в ненеопластических экстрактах РНК относительно неопластических контролей. Signif. FDR - приведенная величина р для проверки различия средних между РНК, экстрагированной из тканей неоплазии и из ненеопластических тканей. Приведение осуществляют с использованием поправки Benjamini & Hochberg для множественной проверки гипотезы (Benjamini and Hochberg, 1995); D.value50 - оценка параметра диагностической эффективности, соответствующая площади под кривой рабочей характеристики приемника ROC. Такой параметр дает подходящую оценку диагностической полезности и описан в Saunders, 2006; FC - изменение, крат, между средними уровнями экспрессии в отсутствие неоплазии по сравнению с неоплазией; Sens-Spec - оценка диагностической эффективности, соответствующая точке на кривой ROC, показывающей равную чувствительность и специфичность; CI (95) - 95% доверительный интервал оценок чувствительности и специфичности.
Таблица 3
Наборы зондов, которые показывают качество (кроме количества) повышенного профиля в ненеопластических тканях относительно неопластических контролей. TargetPS - id набора зондов Affymetrix HG-133plus2; Simbol - предполагаемый символ гена, соответствующий id набора зондов-мишени - несколько названий символов показывают возможность гибридизации набора зондов с несколькими генами-мишенями; Signif. FDR - приведенная величина р для проверки различия средних между РНК, экстрагированной из тканей неоплазии и из ненеопластических тканей. Приведение осуществляют с использованием поправки Benjamini & Hochberg для множественной проверки гипотезы (Benjamini and Hochberg, 1995); D.value50 - оценка параметра диагностической эффективности, соответствующая площади под кривой рабочей характеристики приемника ROC. Такой параметр дает подходящую оценку диагностической полезности и описан в Saunders, 2006; FC - изменение, крат, между средними уровням экспрессии в отсутствие неоплазии по сравнению с неоплазией; Senc-Spec - оценка диагностической эффективности, соответствующая точке на кривой ROC, показывающей равную чувствительность и специфичность; CI (95) - 95% доверительный интервал оценок чувствительности и специфичности.
Таблица 4
Данные о множестве наборов зондов, соответствующих символам генов, заявленных в данной заявке, обнаруживающих качественные изменения концентрации ДНК в ненеопластических тканях по сравнению с неопластическими тканями. Simbol - символ гена; VaIidPS_DOWN - ID наборов зондов Affymetrix, демонстрирующих статистически значимую сверхэкспрессию в неопластических экстрактах РНК относительно ненеопластических контролей. Signif. FDR - приведенная величина р для проверки различия средних между РНК, экстрагированной из тканей неоплазии и из ненеопластических тканей. Приведение осуществляют с использованием поправки Benjamini & Hochberg для множественной проверки гипотезы (Benjamini and Hochberg, 1995); D.value50 - оценка параметра диагностической эффективности, соответствующая площади под кривой рабочей характеристики приемника ROC. Такой параметр дает подходящую оценку диагностической полезности и описан в Saunders, 2006; FC - изменение, крат, между средними уровнями экспрессии в отсутствие неоплазии по сравнению с неоплазией; Sens-Spec - оценка диагностической эффективности, соответствующая точке на кривой ROC, показывающей равную чувствительность и специфичность; CI (95) - 95% доверительный интервал оценок чувствительности и специфичности.
Специалистам в данной области техники будет понятно, что изобретение, описанное в данном описании, допускает вариации и модификации иные, чем описанные конкретно. Также следует иметь в виду, что изобретение включает все такие вариации и модификации. Изобретение также включает все стадии, особенности, композиции и соединения, упомянутые или указанные в данном описании, по отдельности или все вместе, и любую и все комбинации любых двух или большего числа указанных стадий или особенностей.
Библиография
Affymetrix. GeneChip expression data analysis fundamentals. Affymetrix, Santa Clara, CA USA, 2001.
Alon et al., Proc. Natl. Acad. Sci. USA: 96,6745-6750, June 1999
Ausubel, F. et al., "Current Protocols in Molecular Biology", John Wiley & Sons, (1998)
Bonner et al. (1973) J. Mol. Biol. 81:123
Clark et al. 2006, Nature Protocols 1:2353-2364
DeRisi, et al., Nature Genetics 14:457-460 (1996)
Germer et al., Genome Res. 10:258-266 (2000)
Guo et al., Nucleic Acids Res. 22:5456-5465 (1994)
Heid et al., Genome Res. 6:986-994 (1996)
Hubbell E.W., W. M. Liu, and R. Mei. Robust estimators for expression analysis. Bioinformatics, 18:1585-1592, 2002.
Irizarry R.W., В. M. Bolstad, F. Collin, L. M. Cope, B. Hobbs, and T. P. Speed. Summaries of affymetrix genechip probe level data. Nucleic Acid Research, 31,2003.
Kraus, M. and Aaronson, S., 1991. Methods Enzymol, 200:546-556
Maskos and Southern, Nuc. Acids Res. 20:1679-84,1992
Moore et al., BBA, 1402:239-249,1988
Nielsen (1999) Curr. Opin. Biotechnol. 10:71-75
Nielsen et al. (1991) Science 254: 1497-1500
Pease et al., Proc. Natl. Acad. Sci. USA9\(11):5022-5026 (1994)
Pevzner et al., J. Biomol. Struc. & Dyn. 9:399-410, 1991
Schena, et al. Science 270:467-470 (1995)
Smith et al., Science 258:1122-1126 (1992)
Smyth G.K. Bioinformatics and Computational Biology Solutions using R and Bioconductor. Springer, New York, 2005.
Smyth G.K. Linear models and empirical bayes methods for assessing differential expression in microarray experiments. Statistical Applications in Genetics and Molecular Biology, 3(l):Article 3,2004.
T. Sano and C. R. Cantor, Bio/Technology 9:1378-81 (1991) Urdea et al., Nucleic Acids Symp. Ser., 24:197-200 (1991) Wedemeyer et al., Clinical Chemistry 48:9 1398-1405,2002) Weissleder et al., Nature Medicine 6:351-355,2000
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕН MTS, МУТАЦИИ ДАННОГО ГЕНА И СПОСОБЫ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ С ИСПОЛЬЗОВАНИЕМ ПОСЛЕДОВАТЕЛЬНОСТИ ГЕНА MTS | 1995 |
|
RU2164419C2 |
| МУТАЦИИ ГЕНА МТS В ЗАРОДЫШЕВОЙ ЛИНИИ И СПОСОБ ВЫЯВЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ К ЗЛОКАЧЕСТВЕННЫМ ОПУХОЛЯМ В ГЕНЕ МТS | 1995 |
|
RU2161309C2 |
| СПОСОБ ОБНАРУЖЕНИЯ НЕОПЛАСТИЧЕСКИХ ЗАБОЛЕВАНИЙ ИСХОДЯ ИЗ СОЛЮБИЛИЗИРОВАННОГО ФИЗИОЛОГИЧЕСКОГО ОБРАЗЦА | 2004 |
|
RU2405158C2 |
| ГЕН, ВОВЛЕЧЕННЫЙ В ИММОРТАЛИЗАЦИЮ РАКОВОЙ КЛЕТКИ ЧЕЛОВЕКА, И ЕГО ПРИМЕНЕНИЕ | 2007 |
|
RU2449016C2 |
| СПОСОБ ИЗМЕРЕНИЯ РЕЗИСТЕНТНОСТИ ИЛИ ЧУВСТВИТЕЛЬНОСТИ К ДОЦЕТАКСЕЛУ | 2005 |
|
RU2403574C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ДИАГНОСТИКИ И МОНИТОРИНГА ГИПЕРТИРЕОЗА У ЖИВОТНЫХ СЕМЕЙСТВА КОШАЧЬИХ | 2012 |
|
RU2593952C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ НАРУШЕНИЙ ПОЧЕК У СОБАК | 2010 |
|
RU2546016C2 |
| КИНАЗА PIM-3 В КАЧЕСТВЕ МИШЕНИ ДЛЯ САХАРНОГО ДИАБЕТА ТИПА 2 | 2003 |
|
RU2316598C2 |
| СПОСОБЫ ПРОГНОЗИРОВАНИЯ РАКА ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ | 2016 |
|
RU2760577C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2013 |
|
RU2660349C2 |
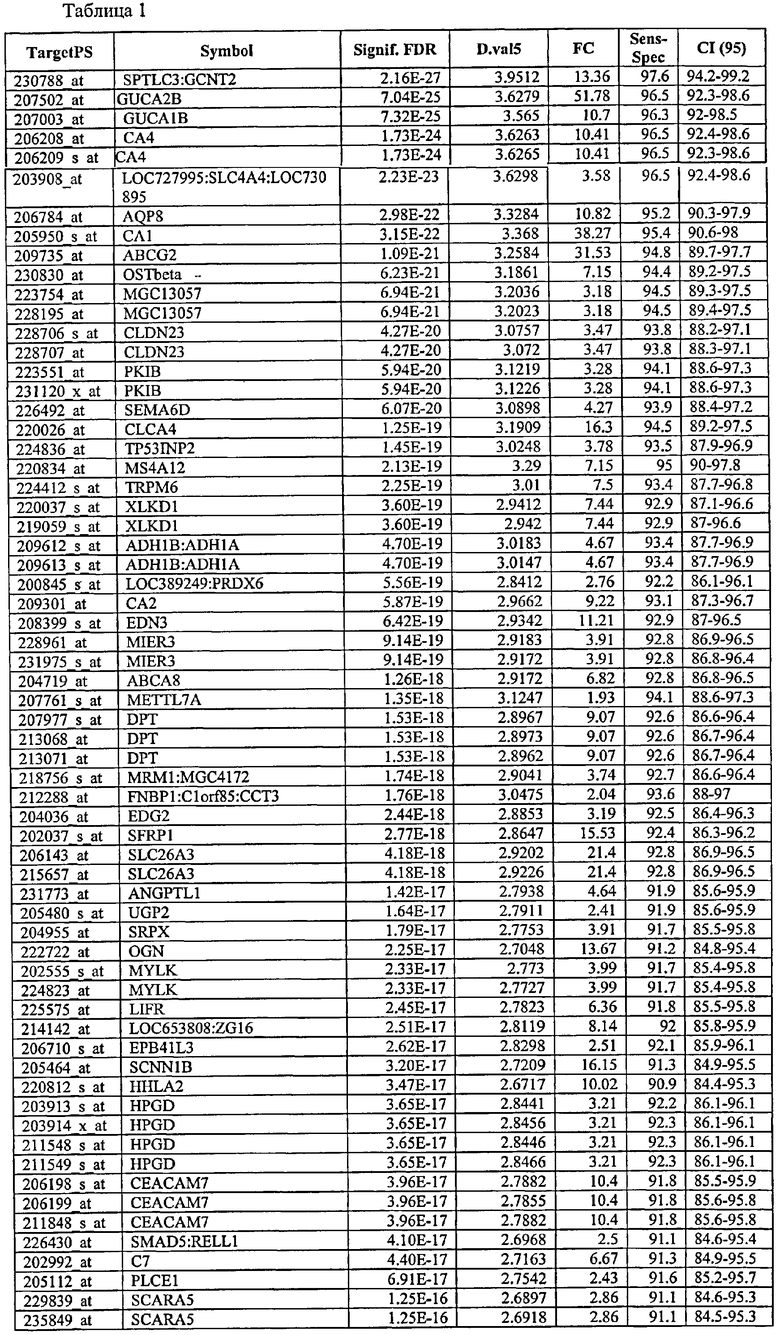
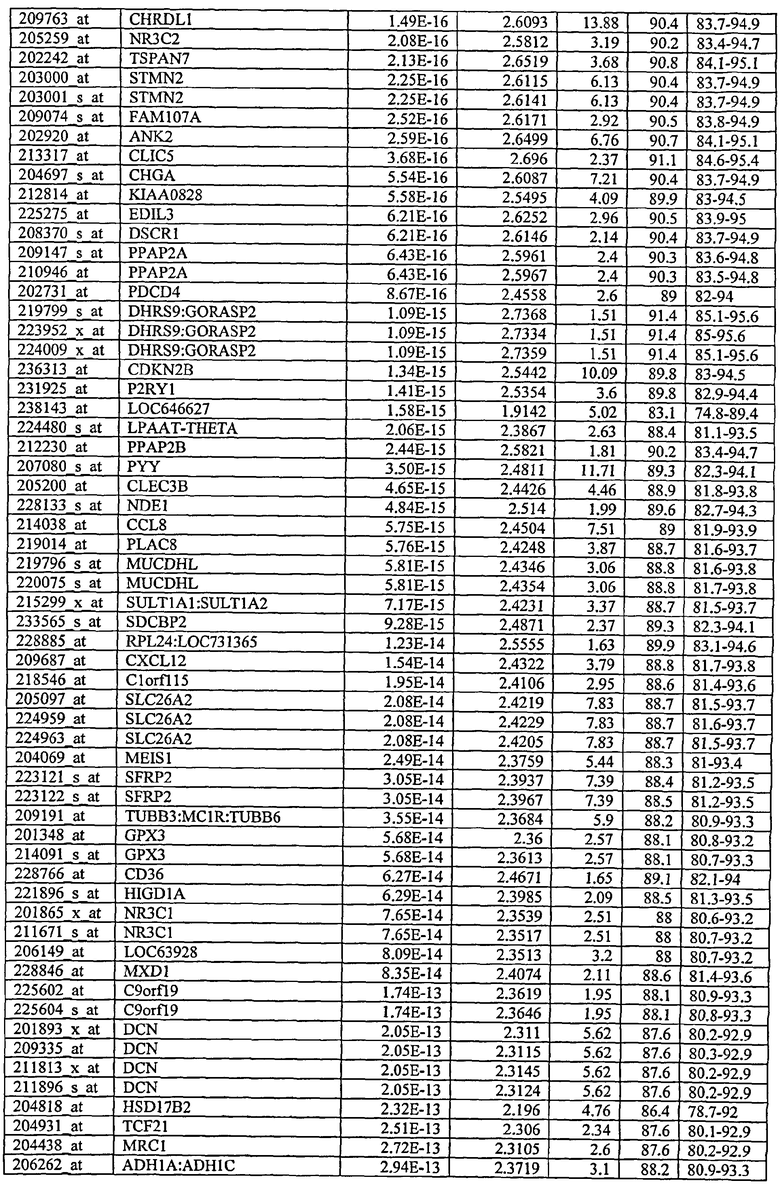
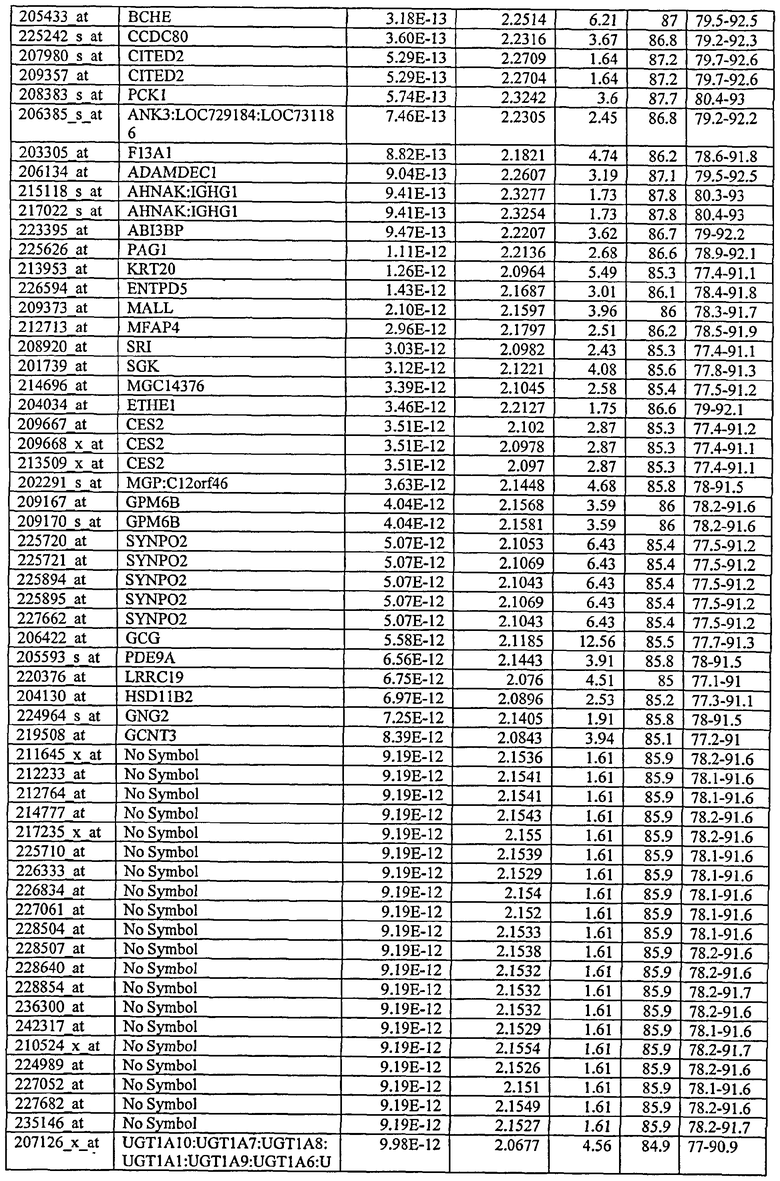
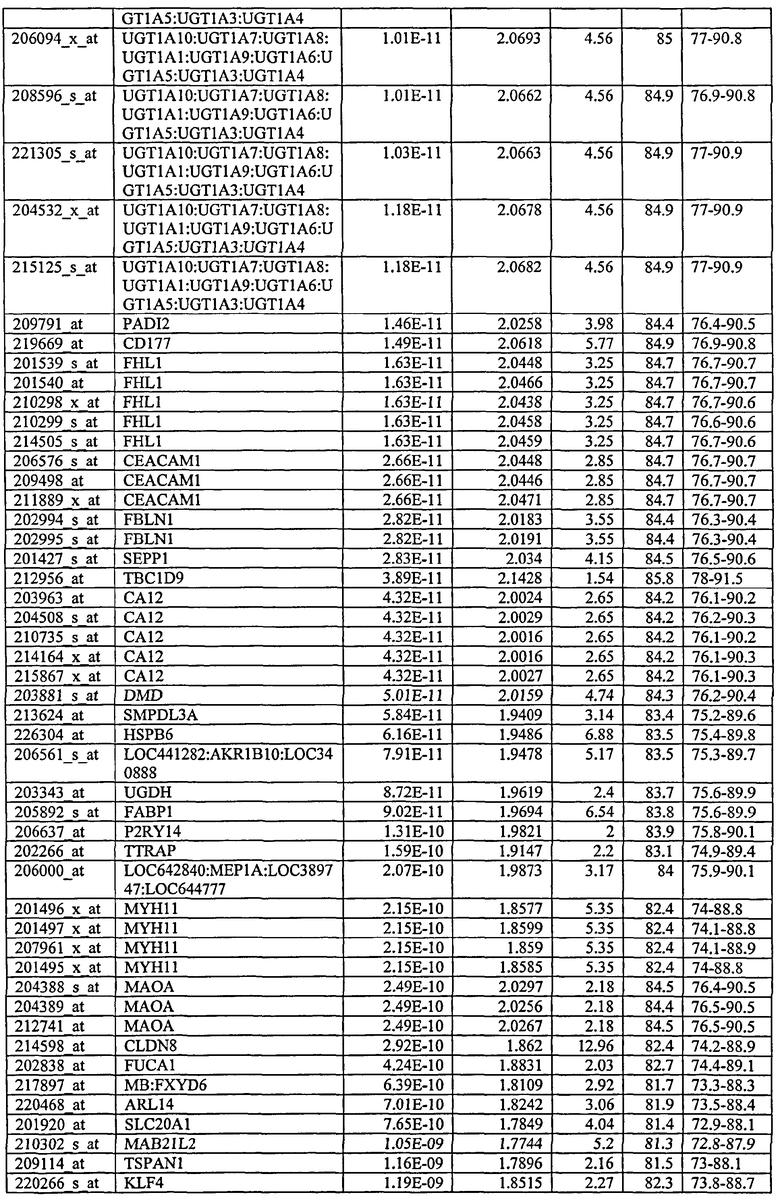
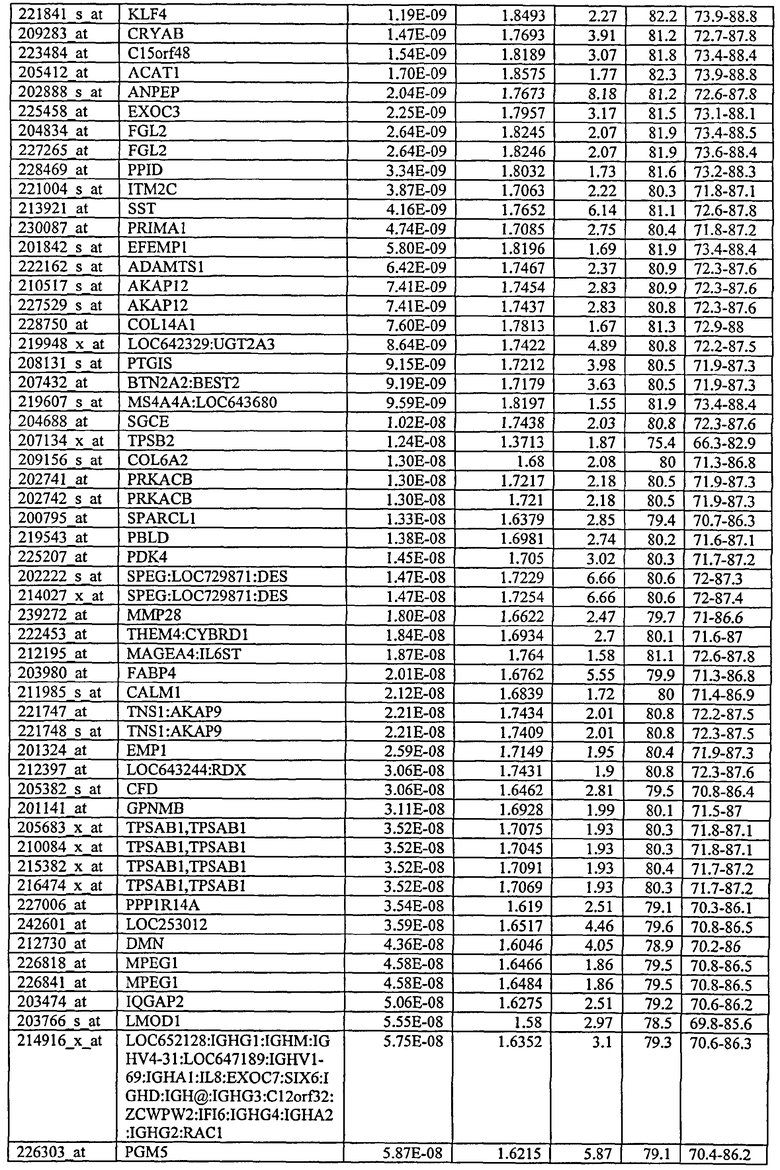
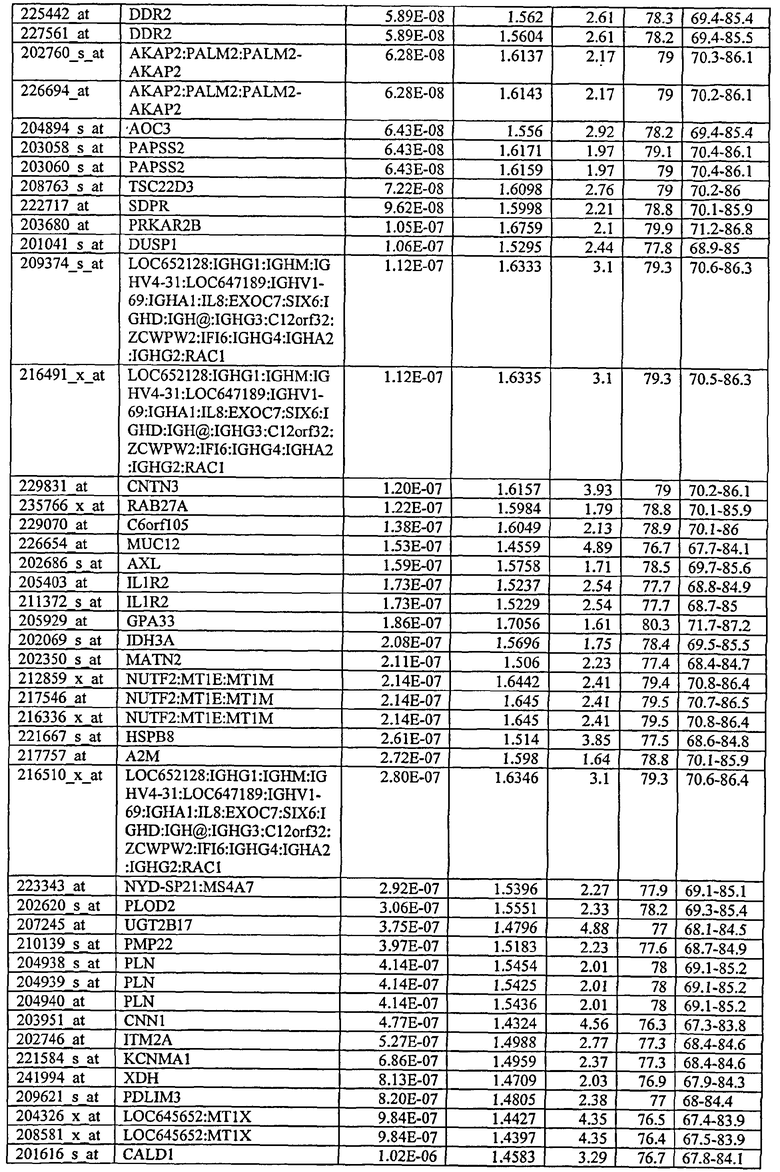
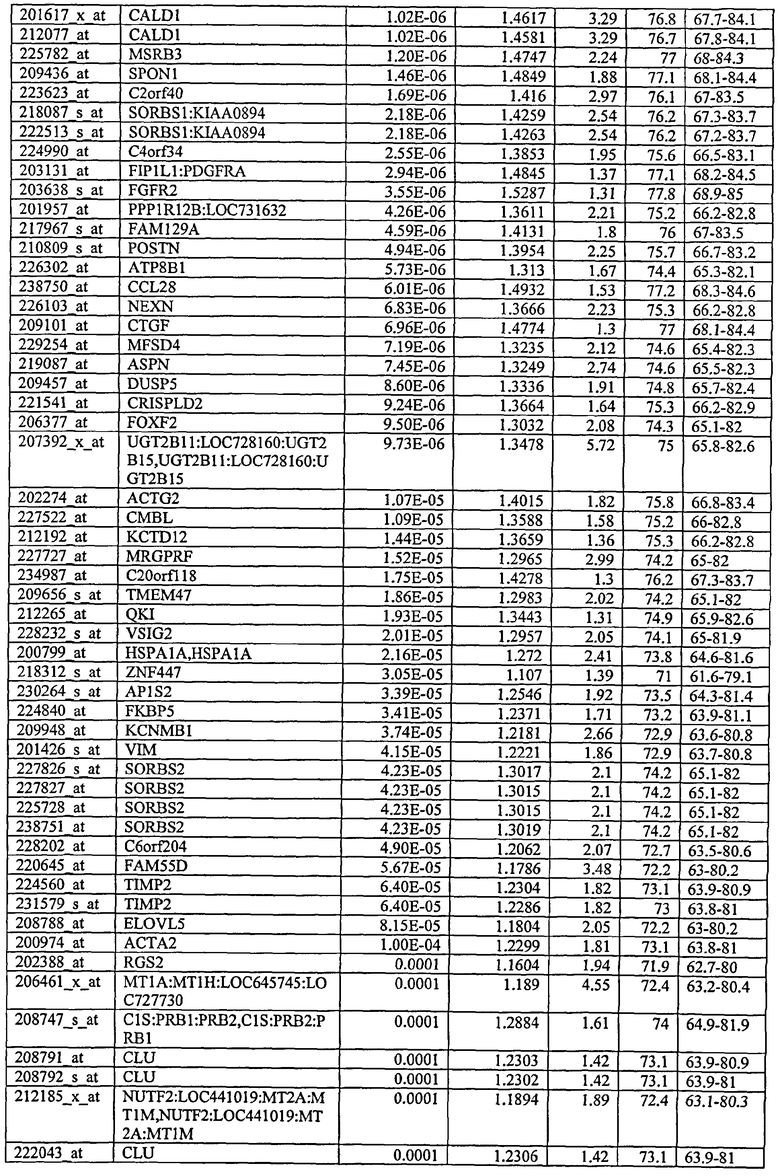
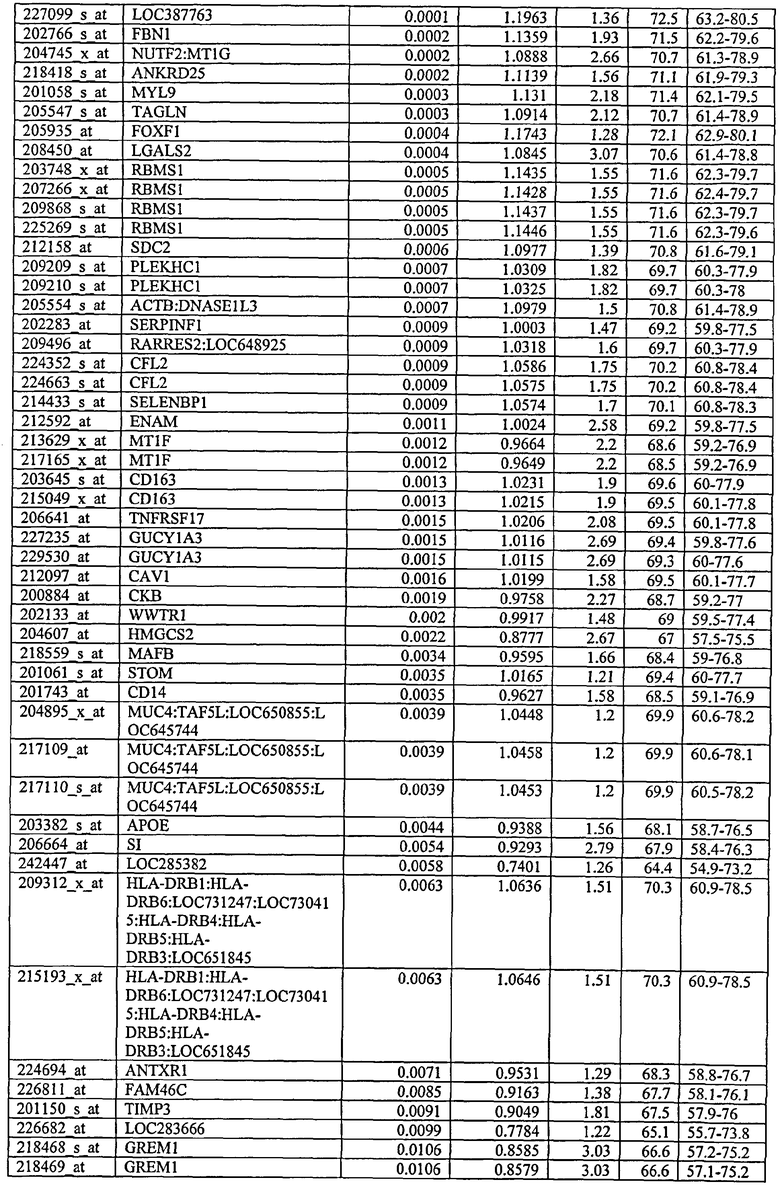
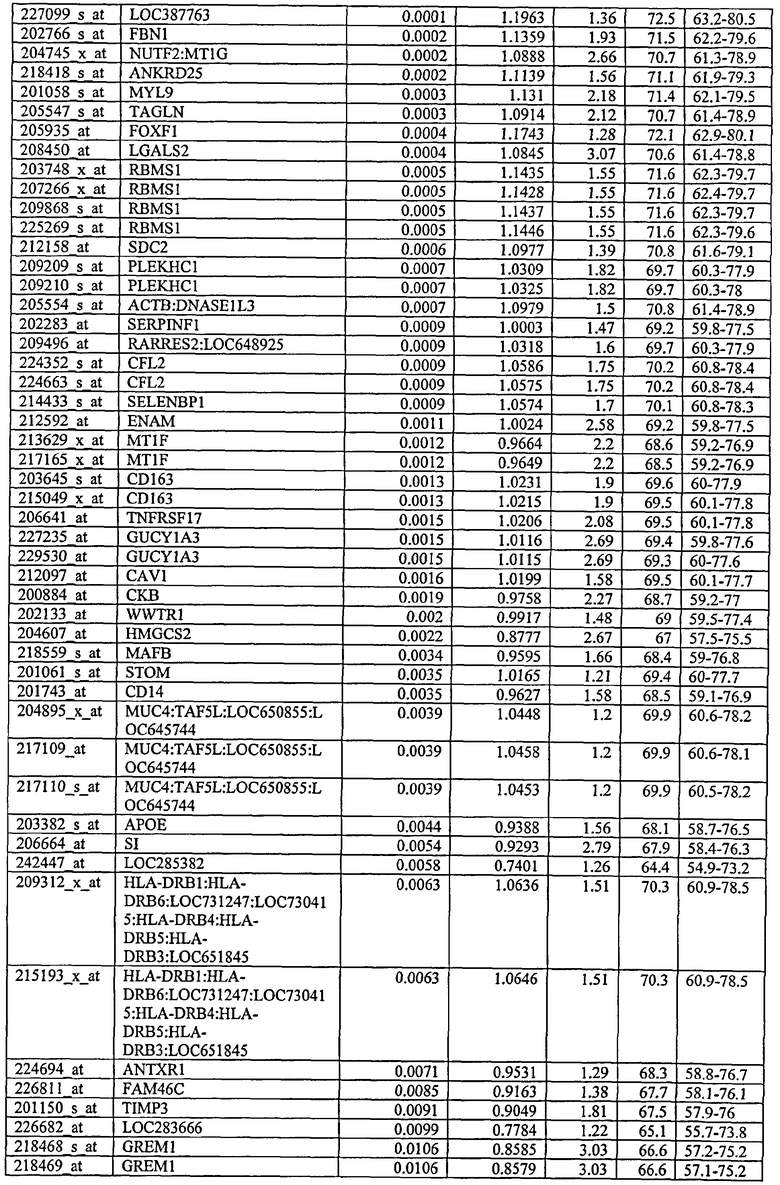
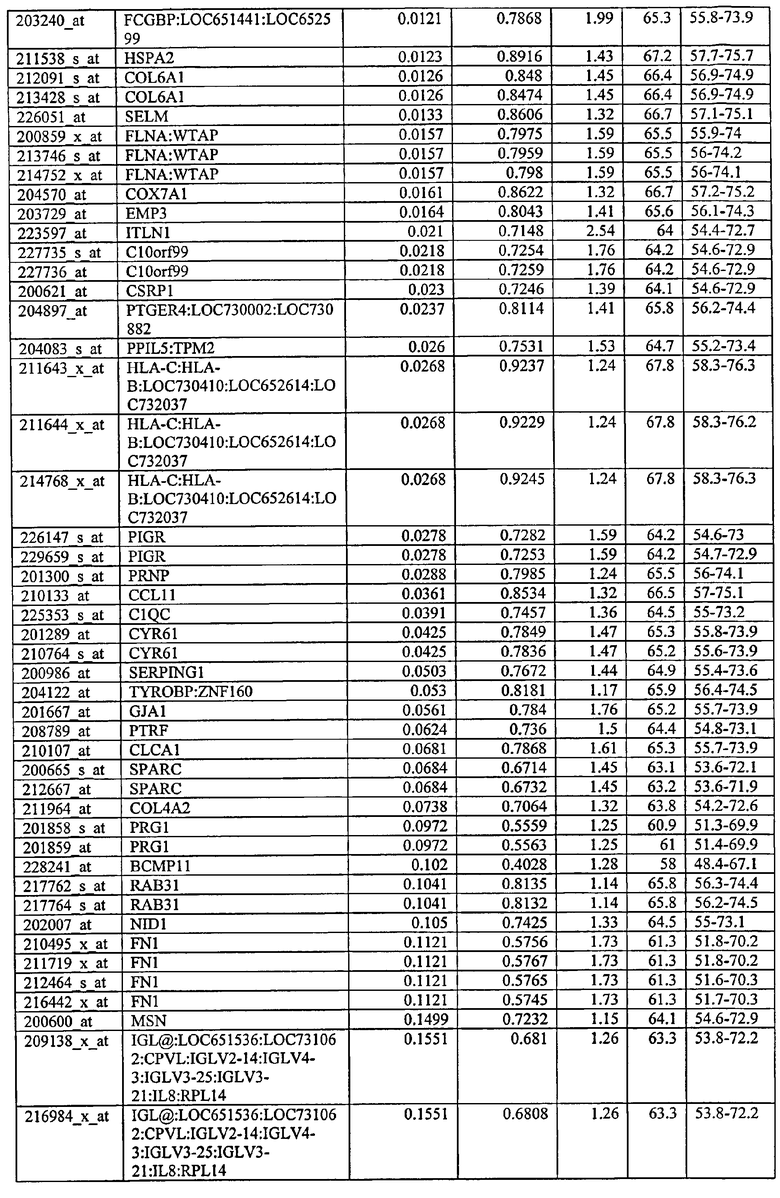
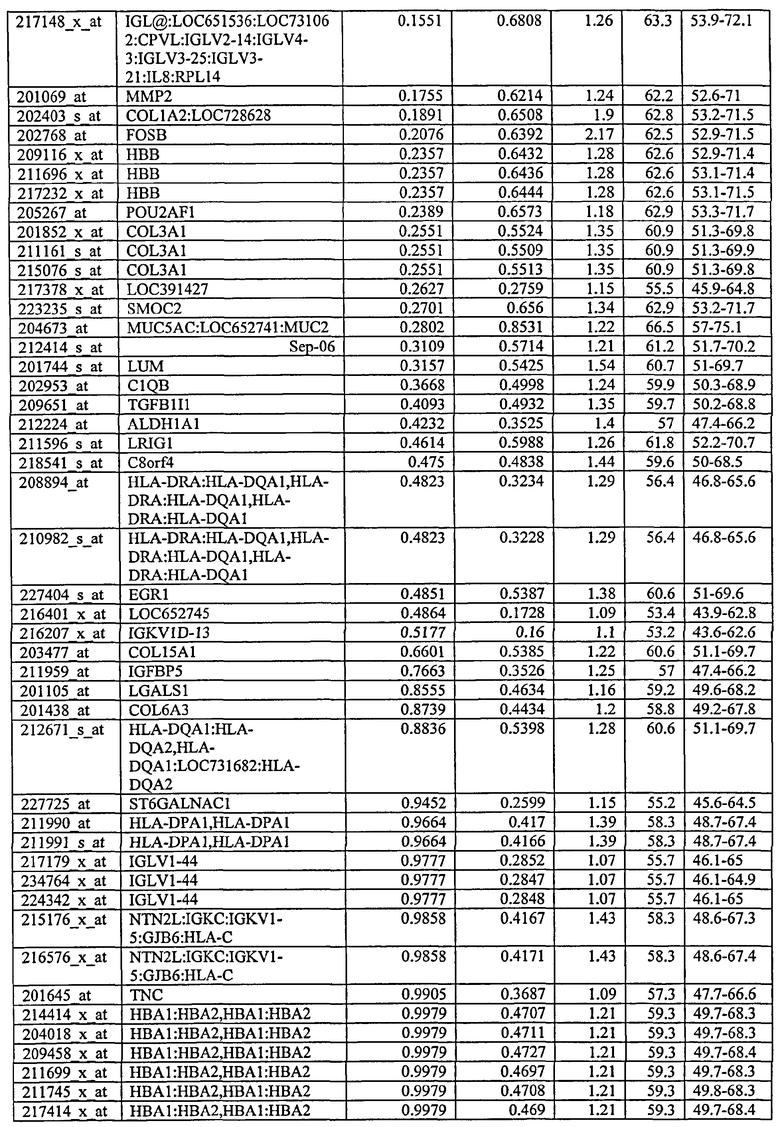
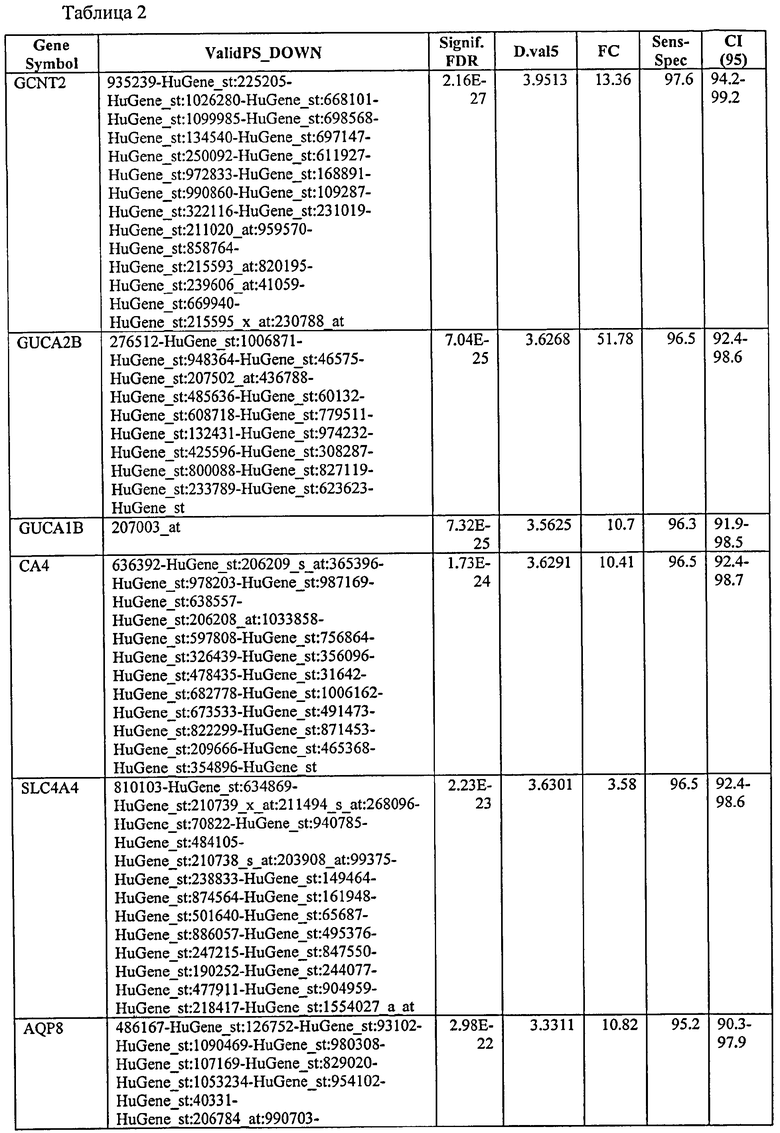
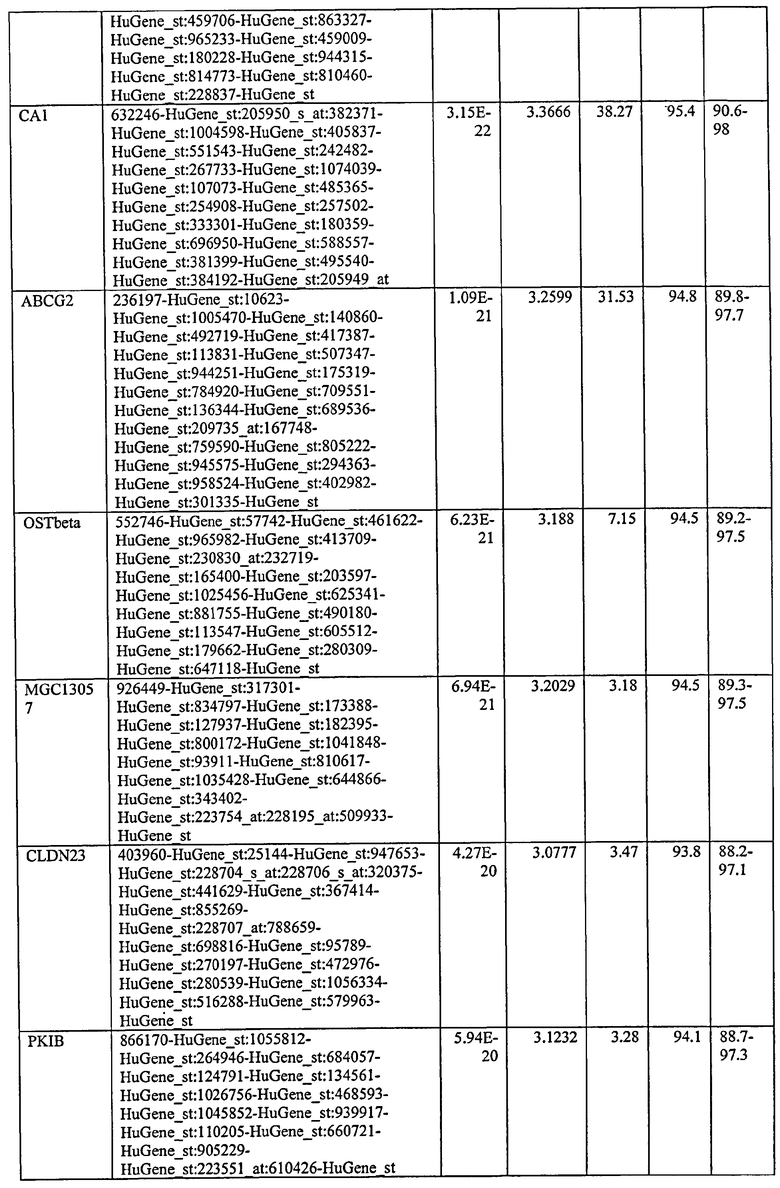
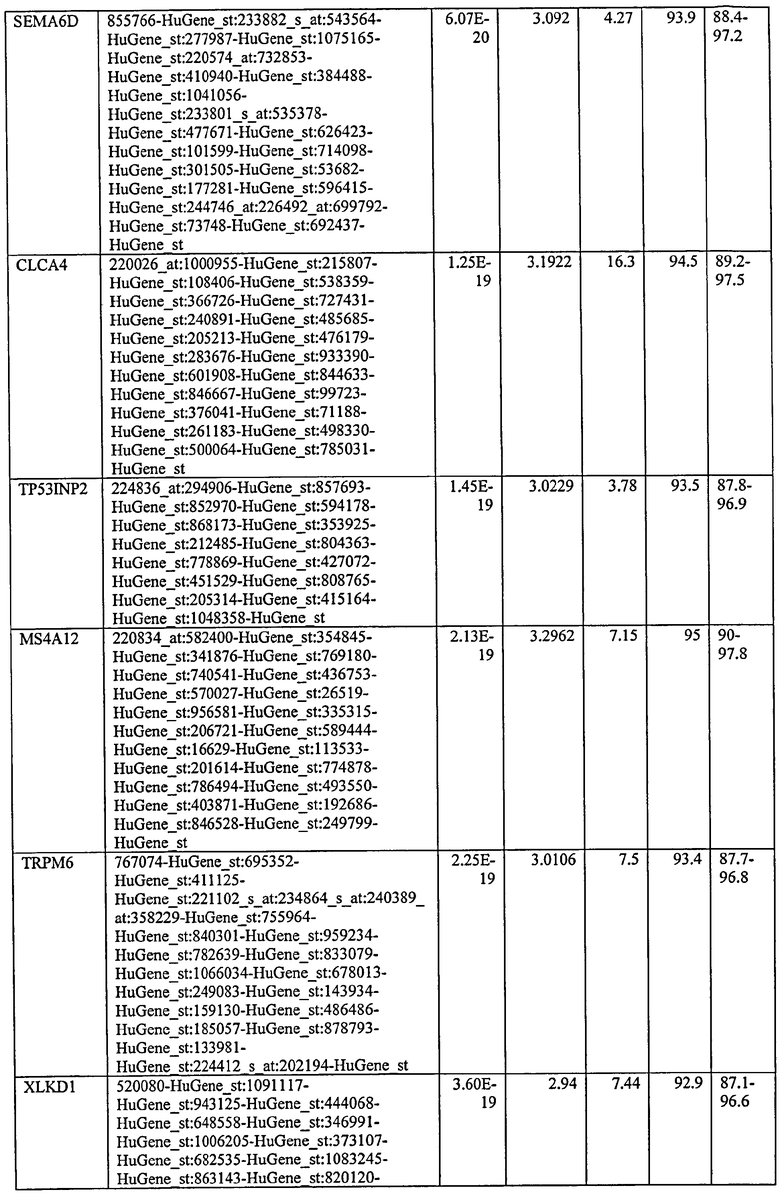
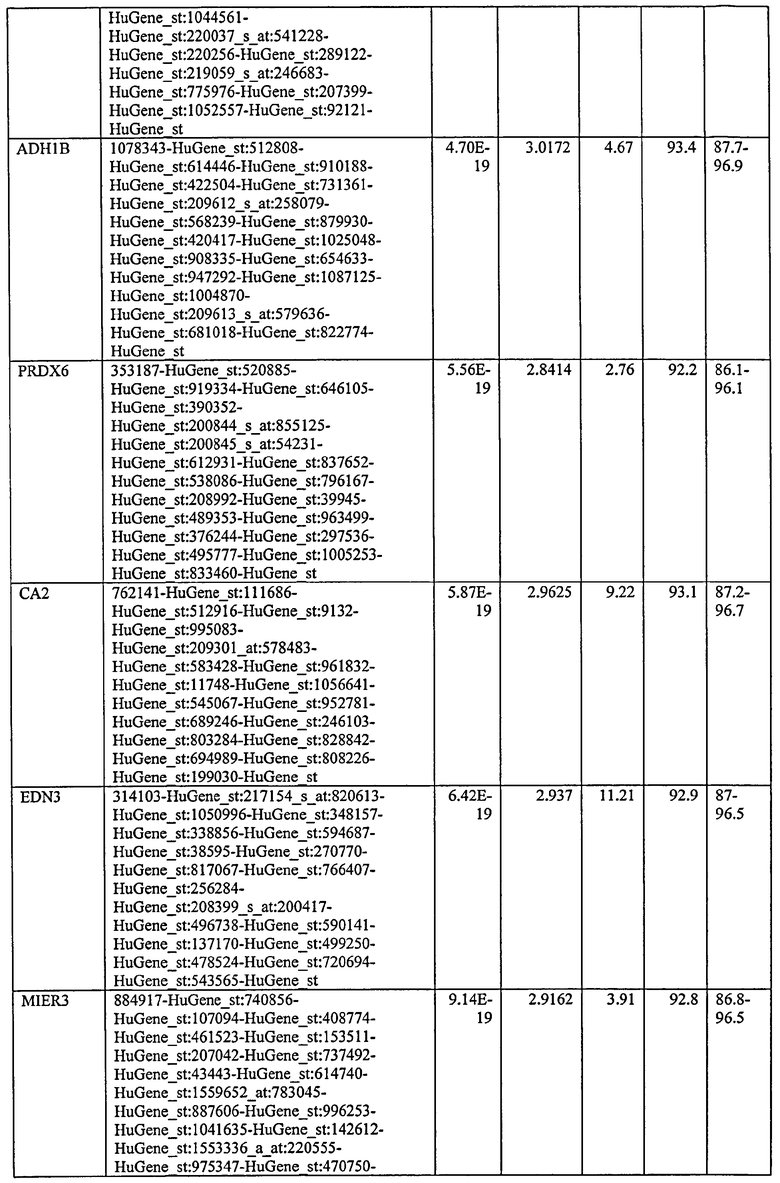
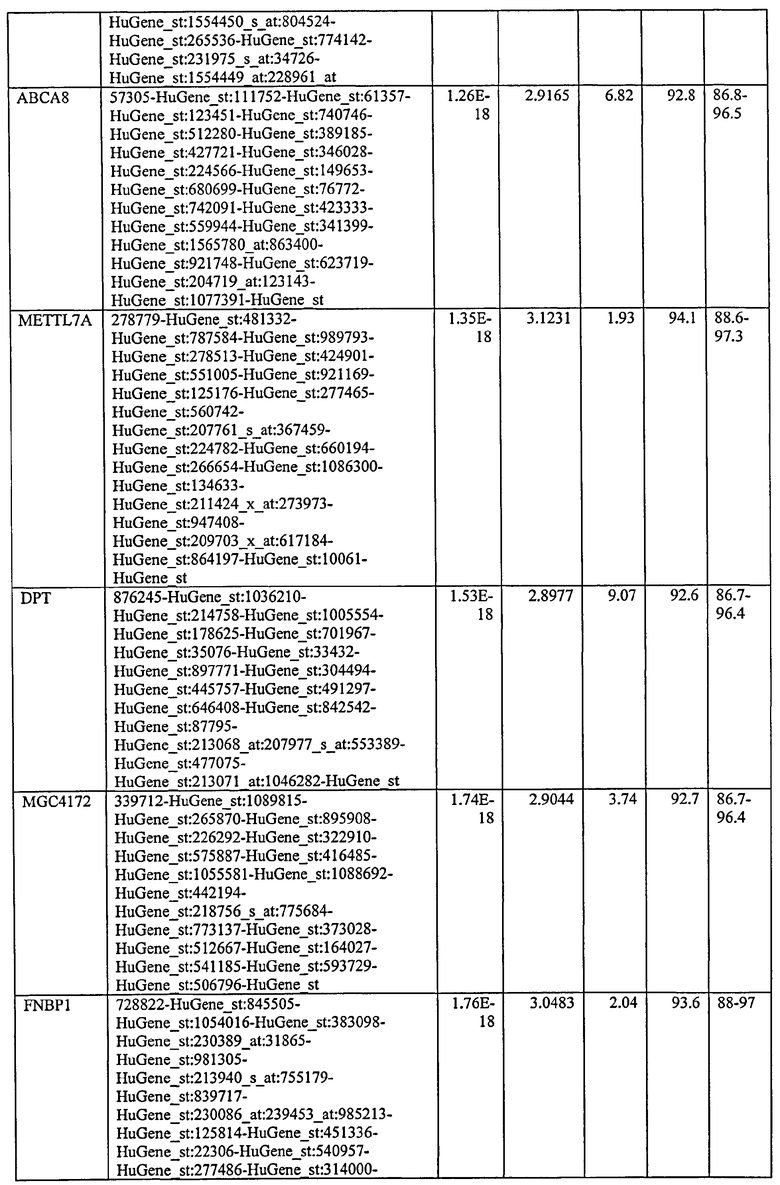
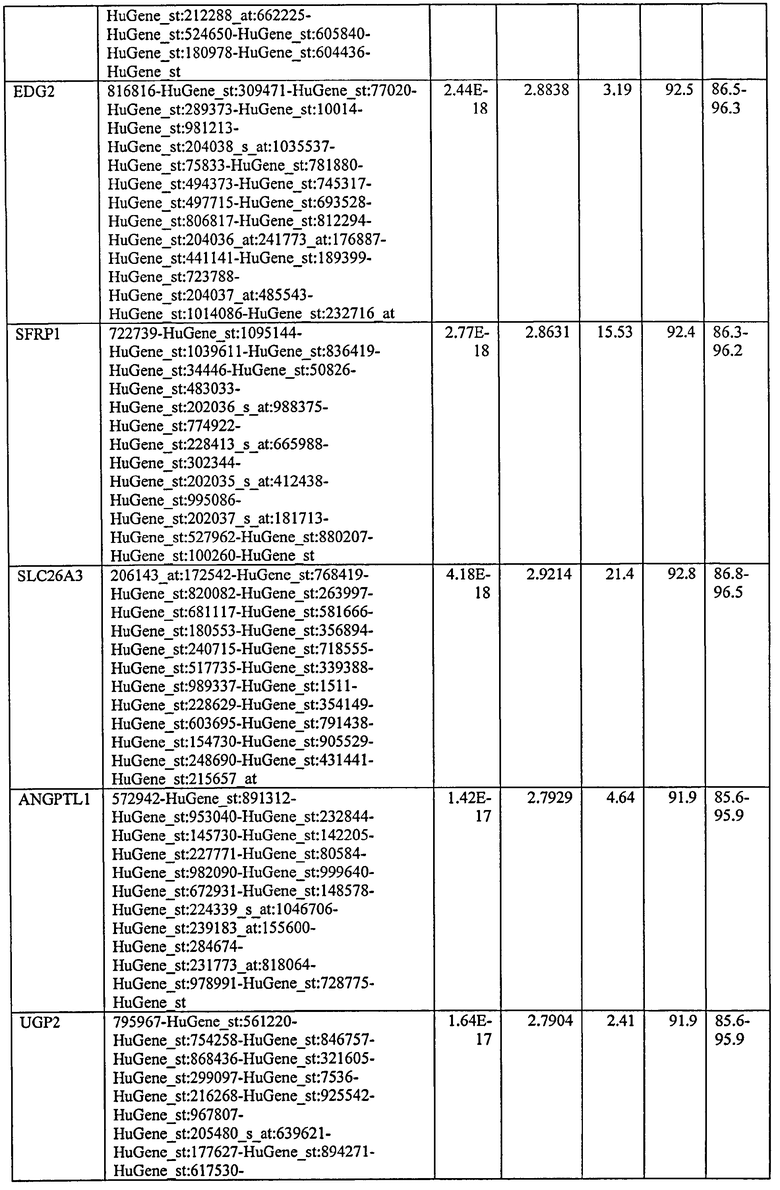
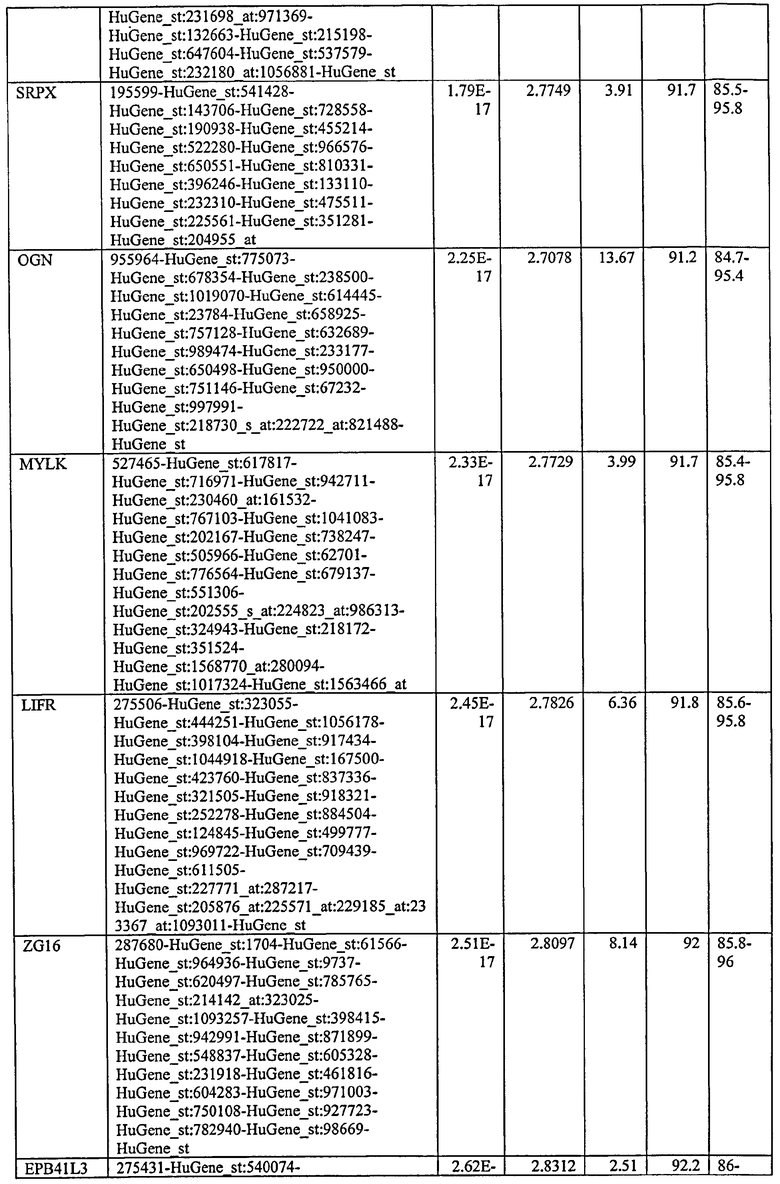
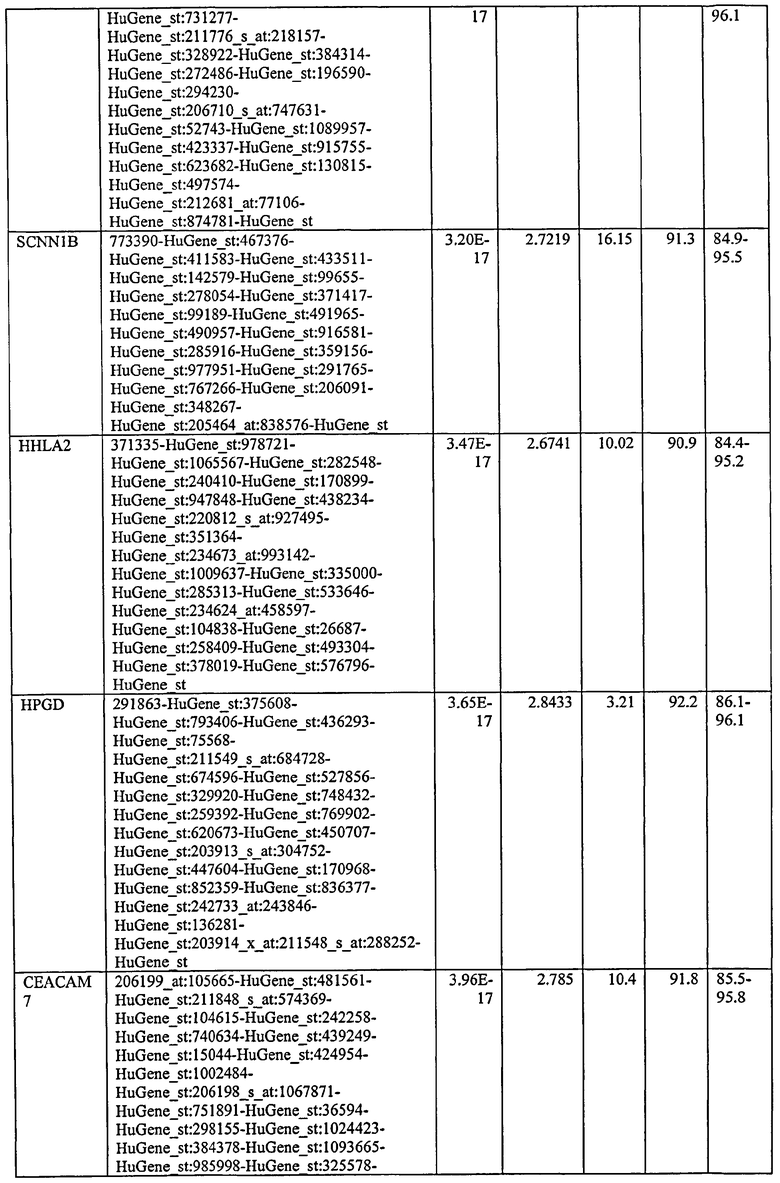
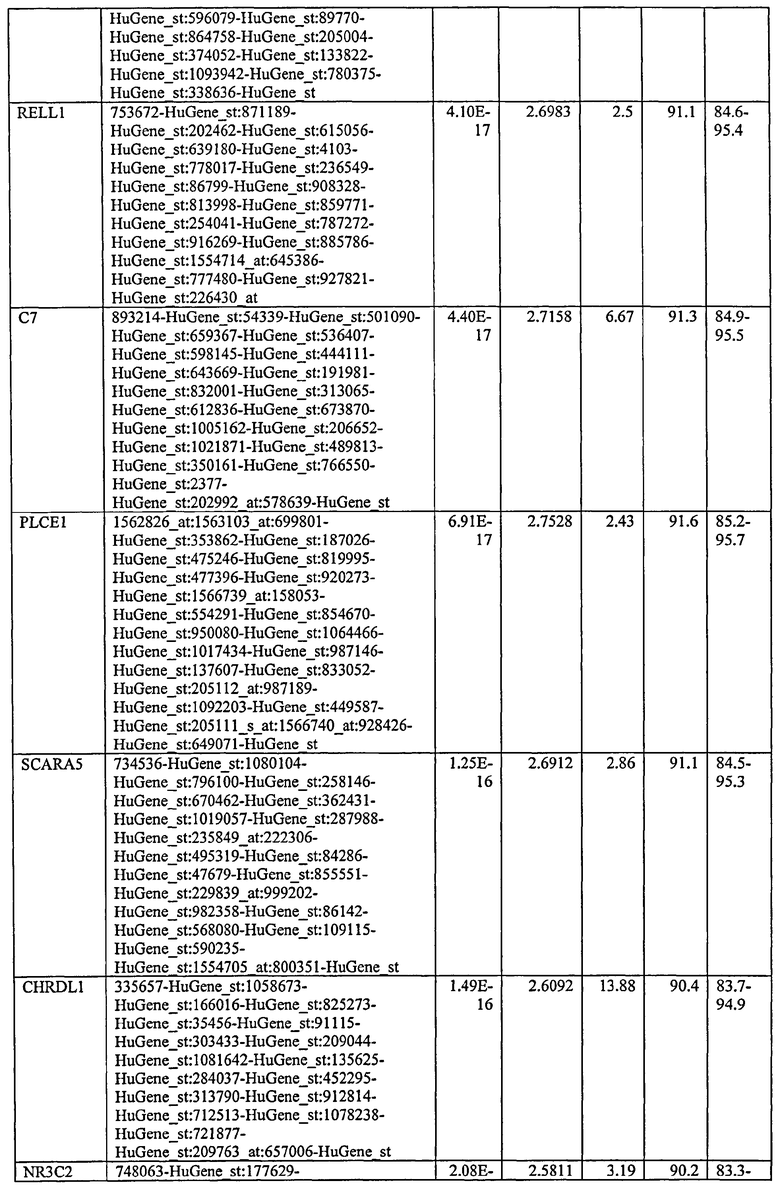
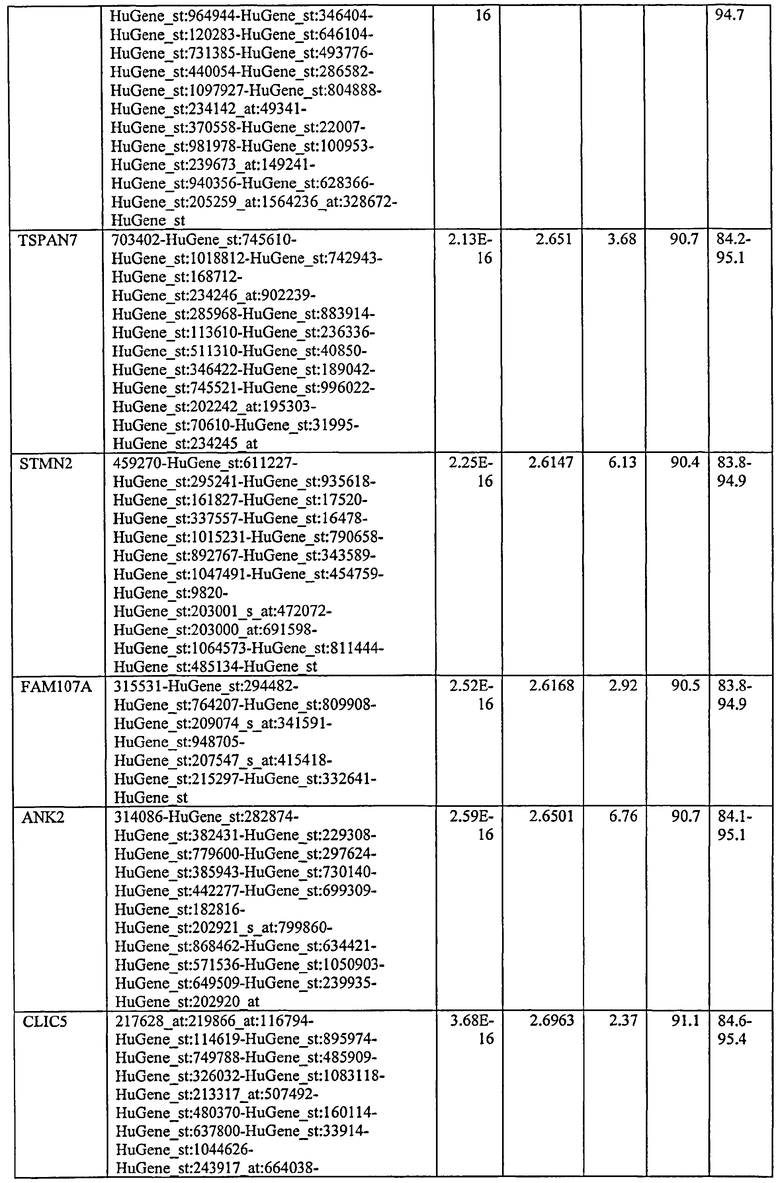
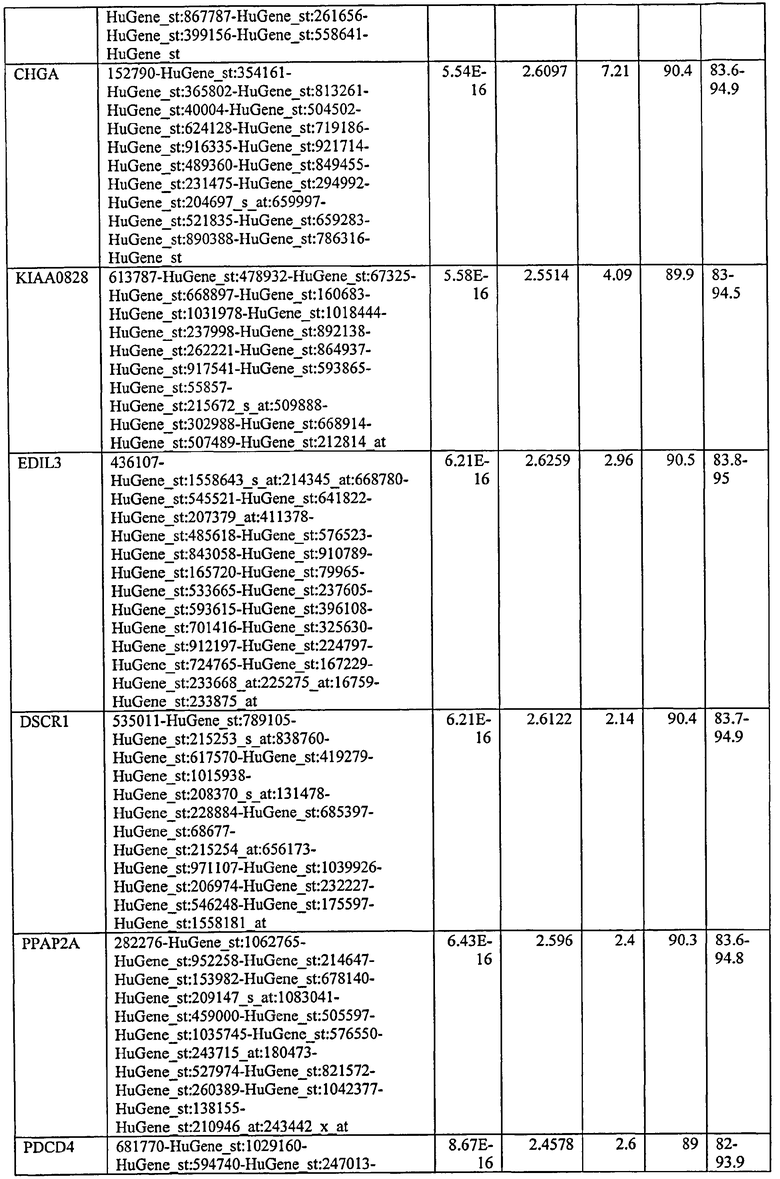
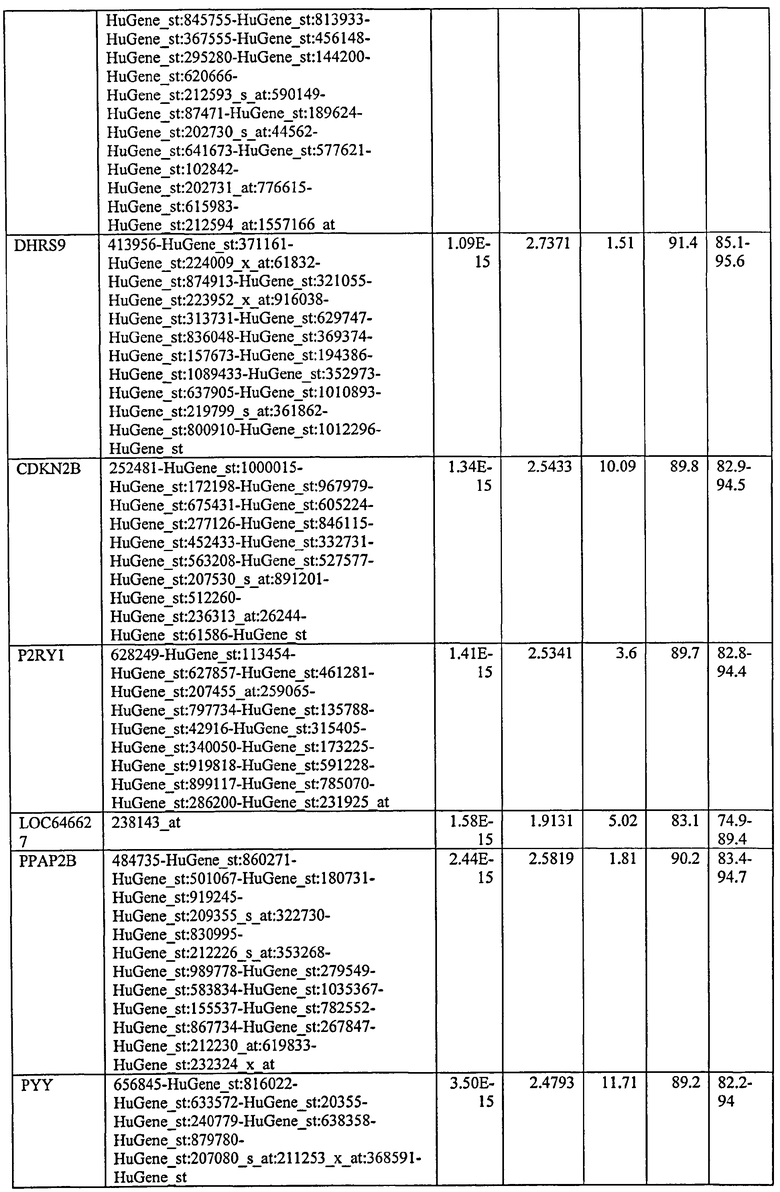
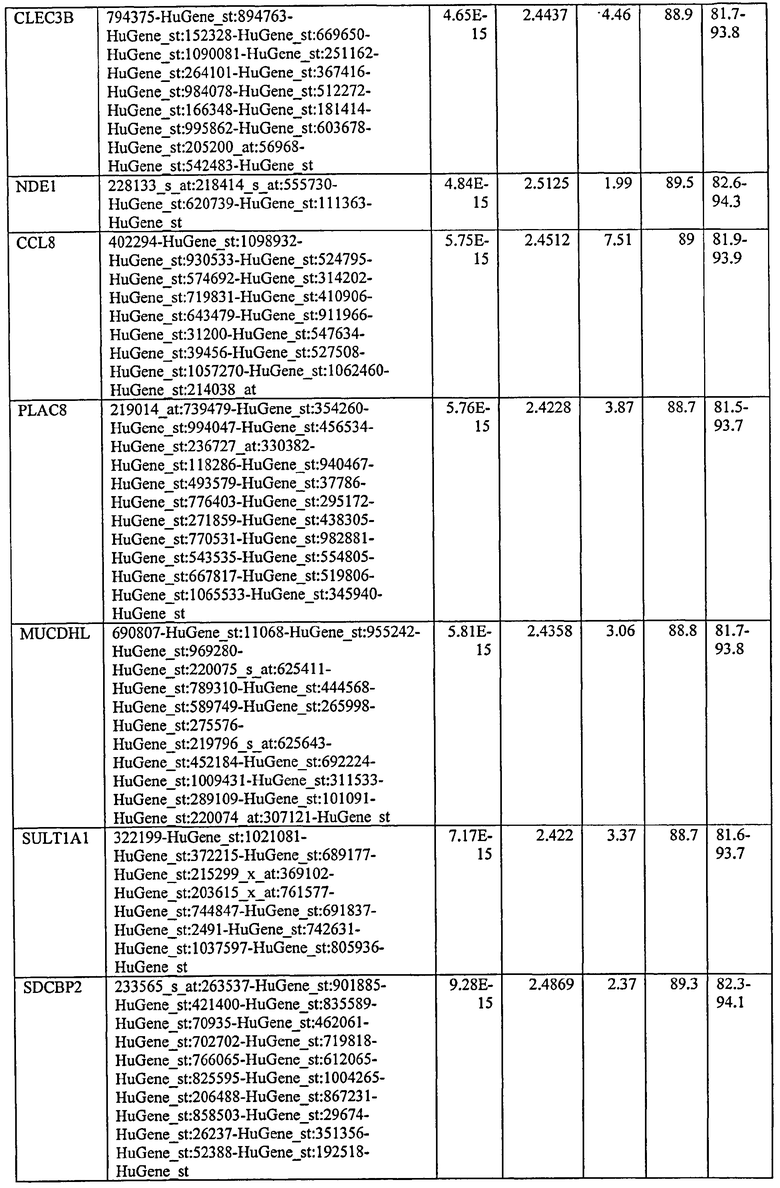
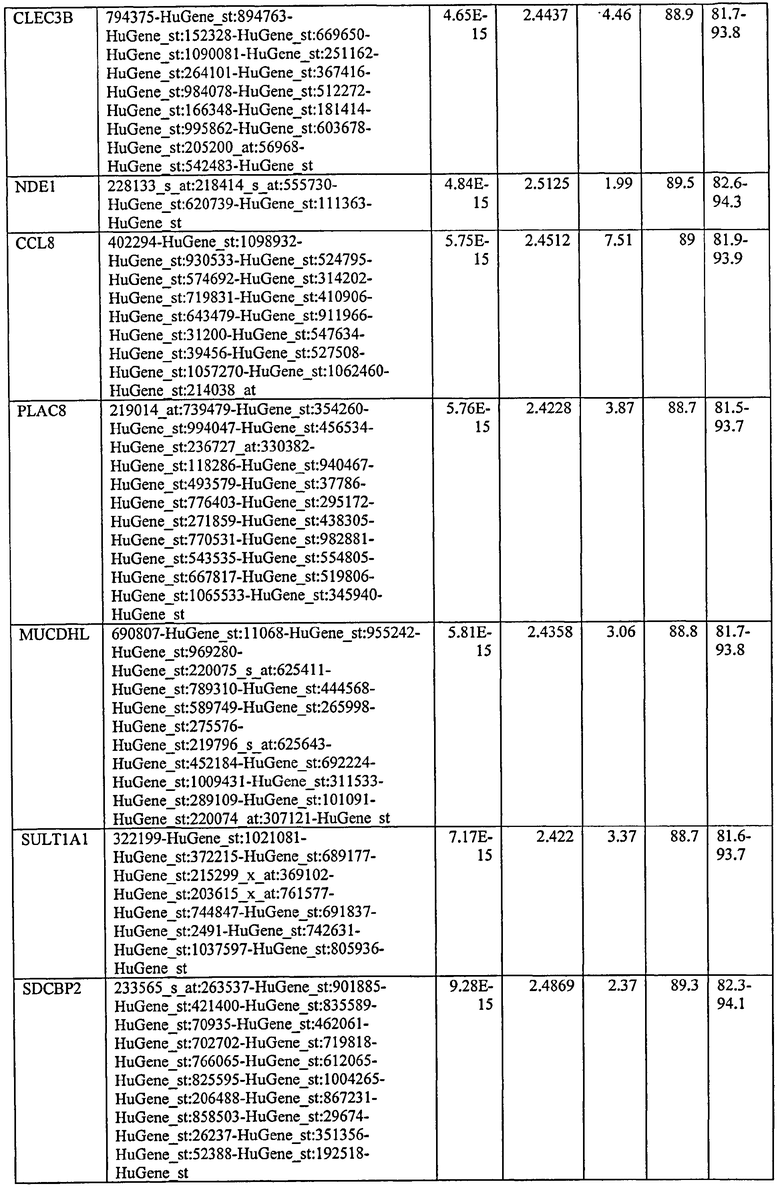
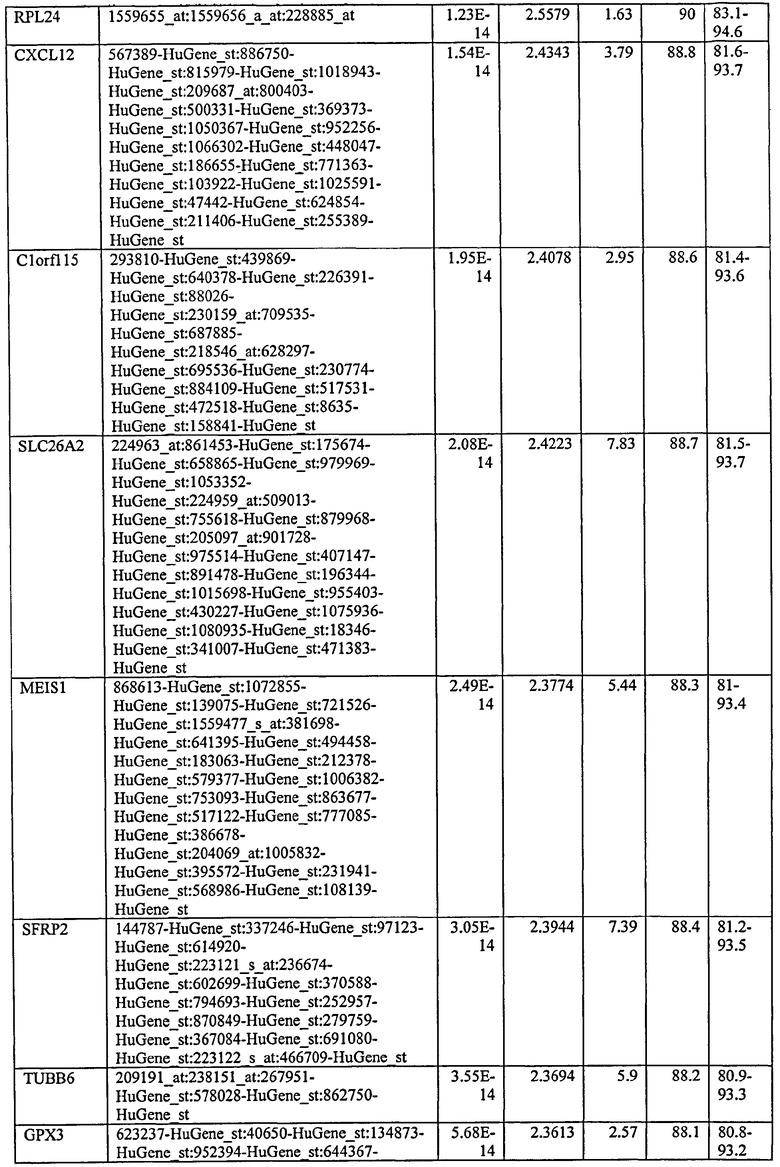
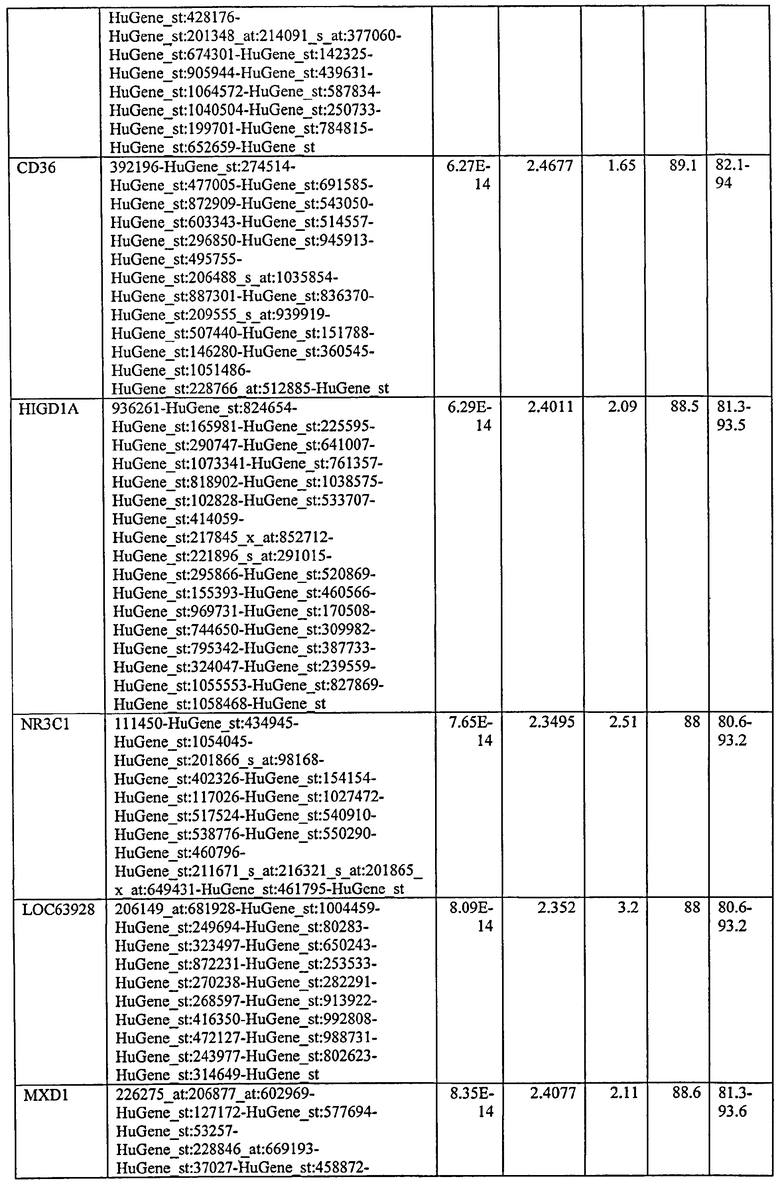
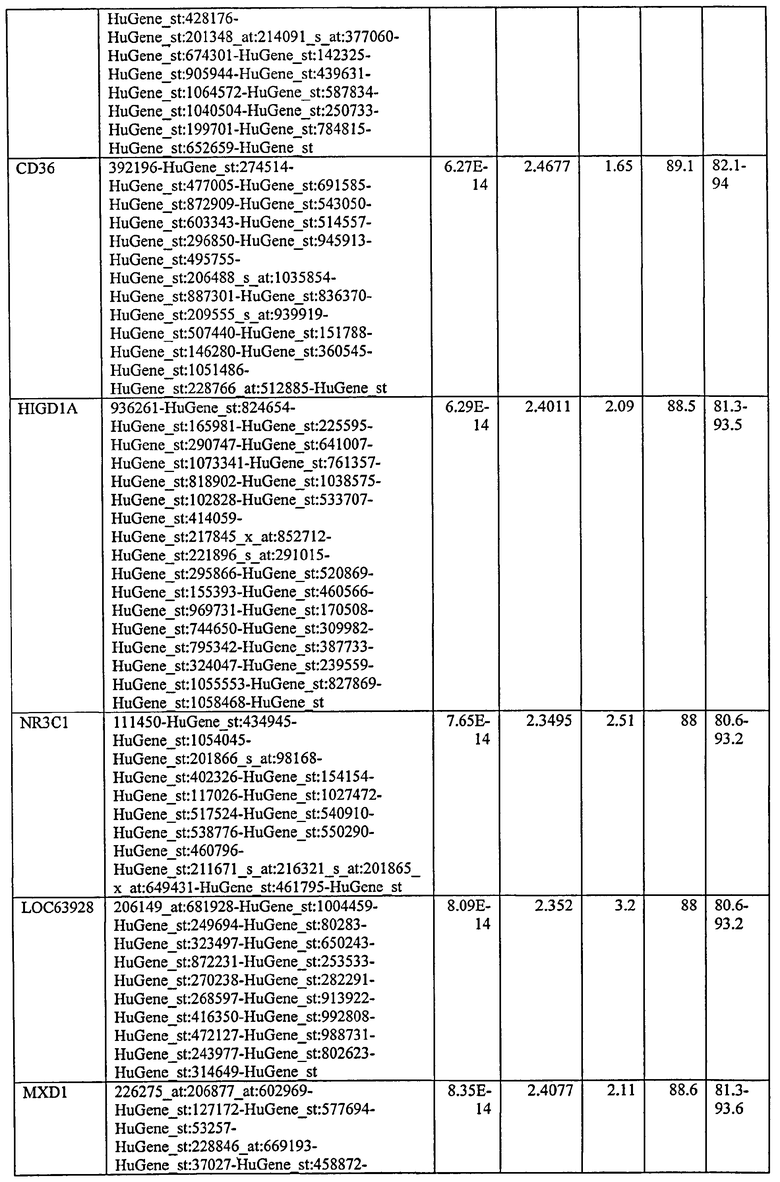
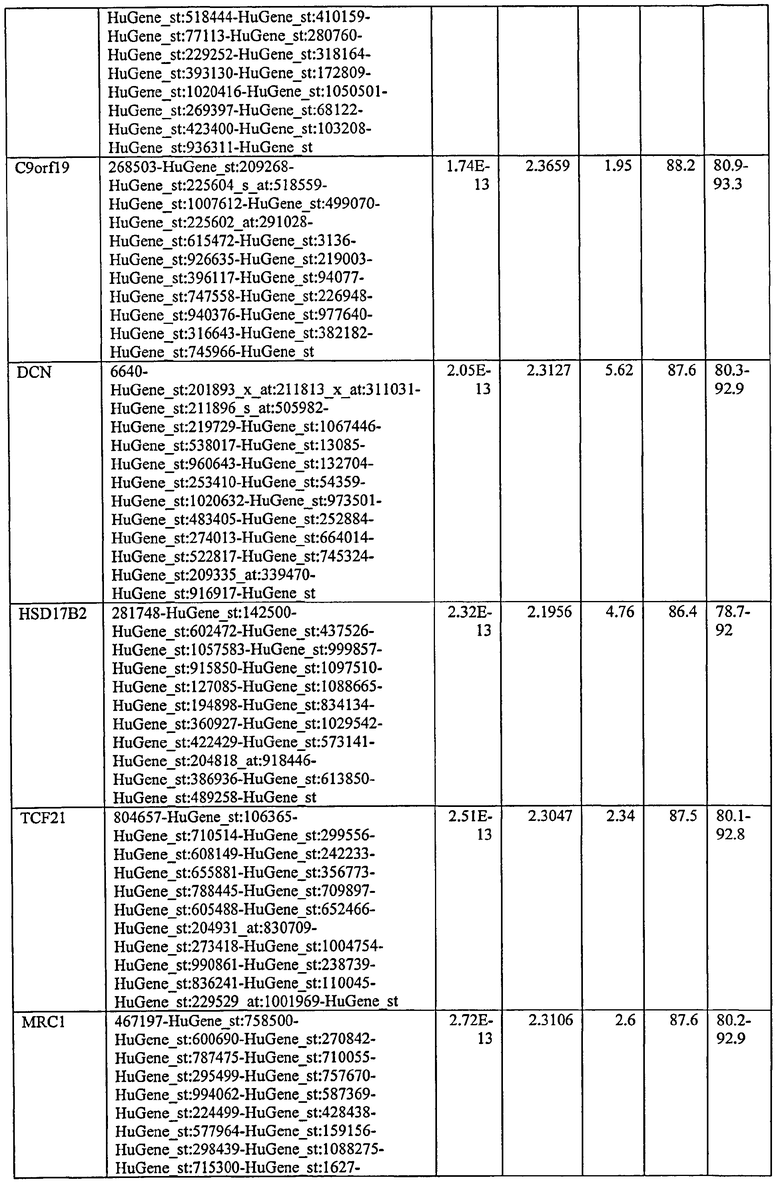
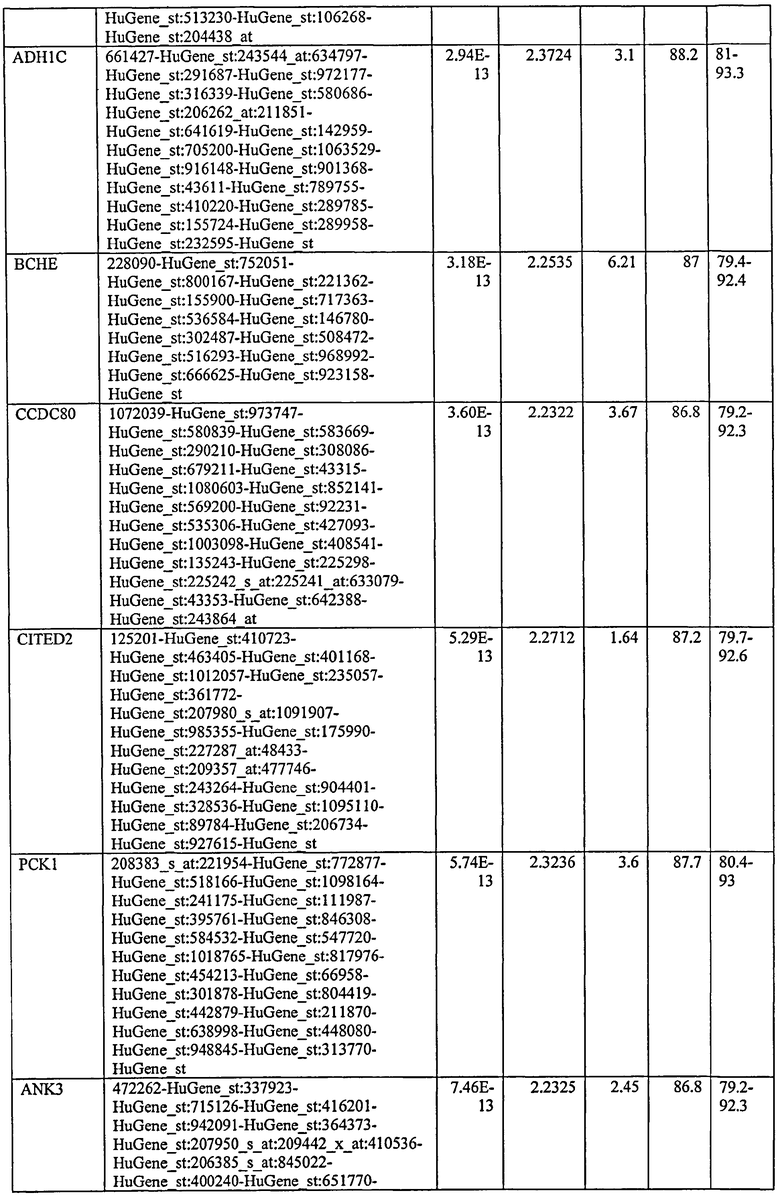
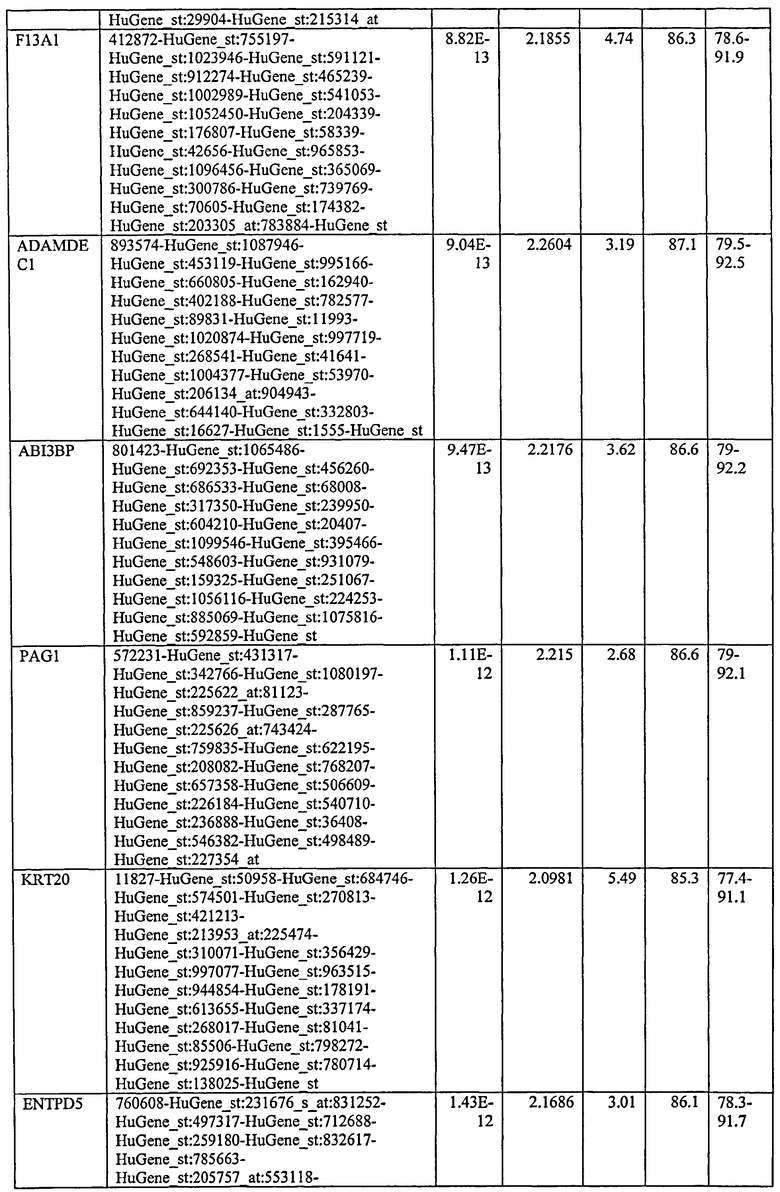
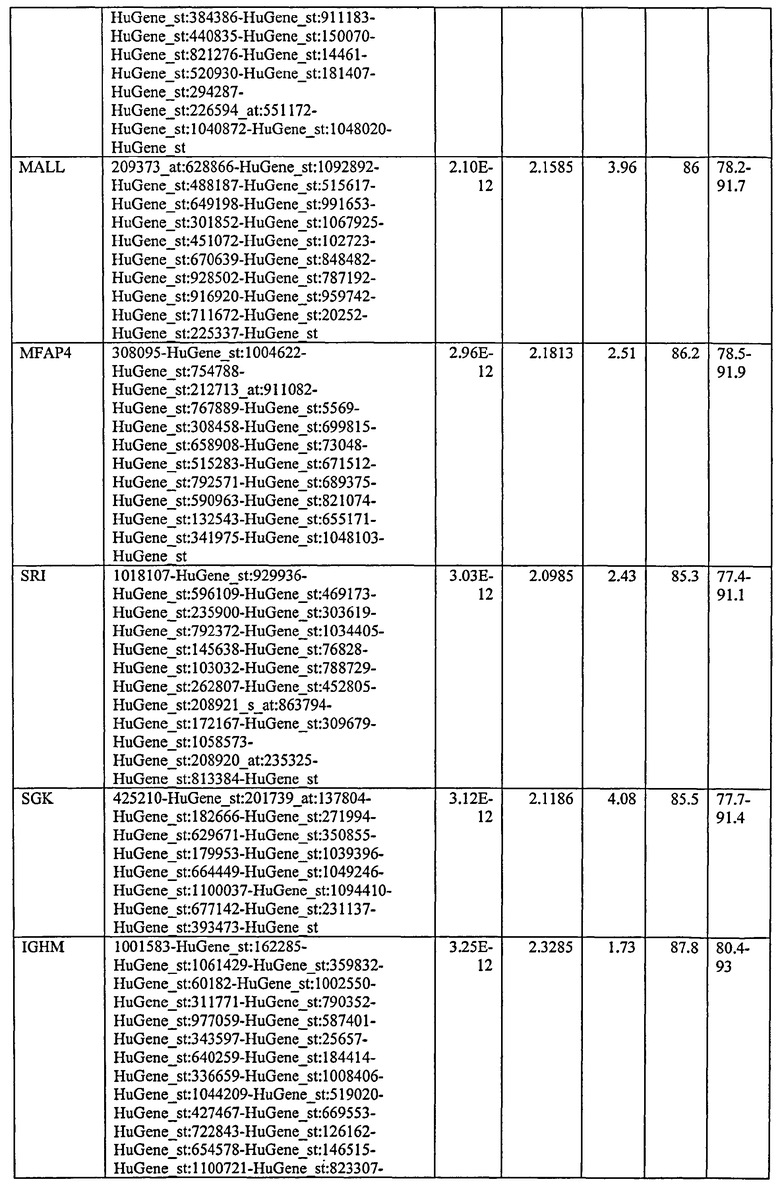
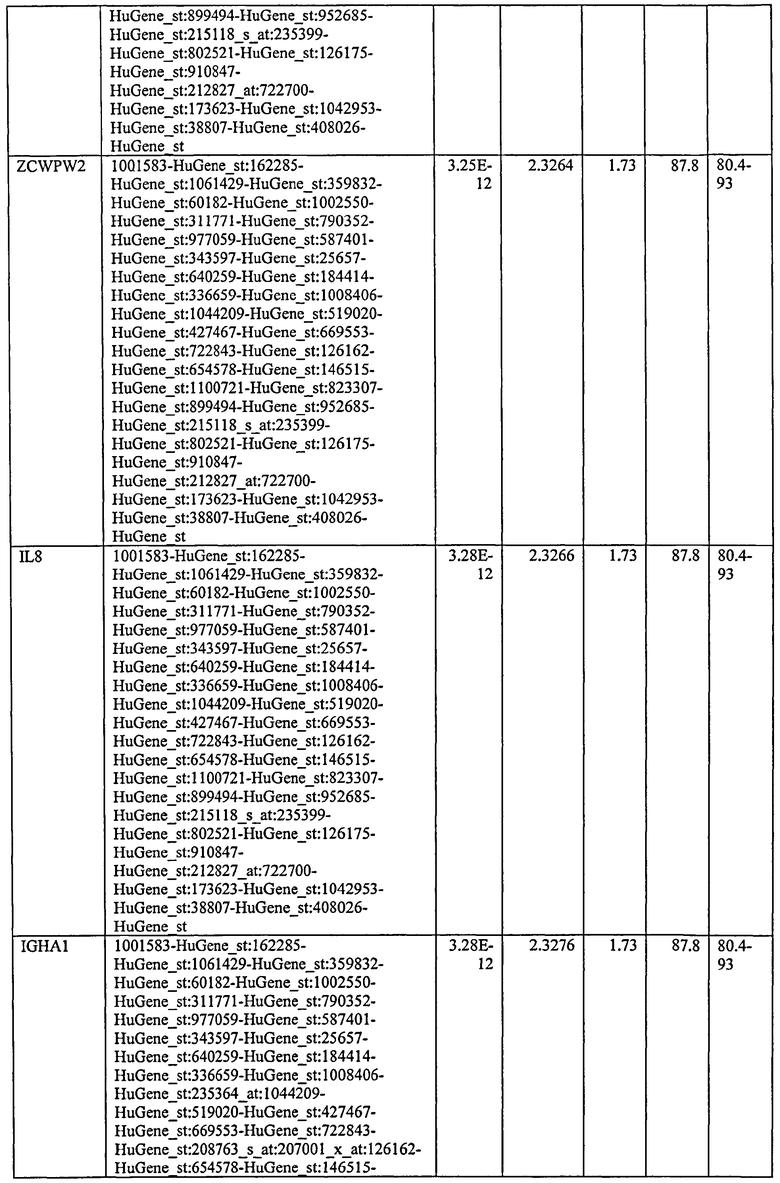
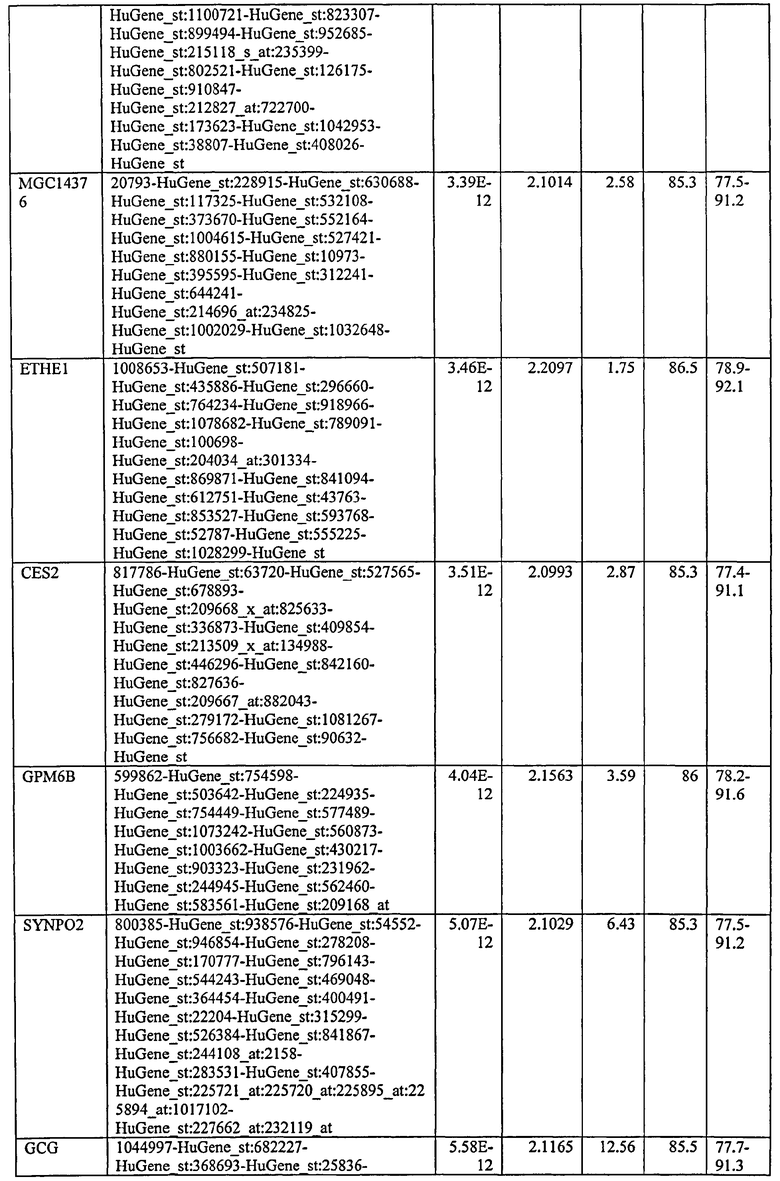
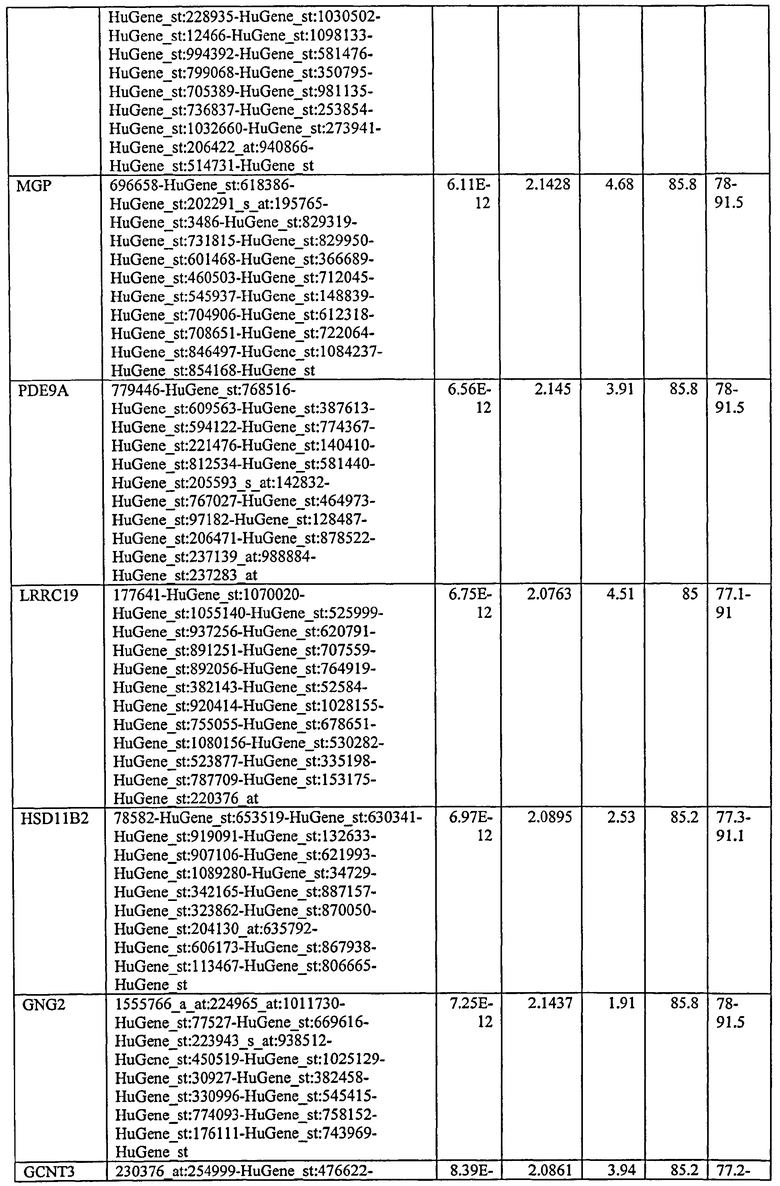
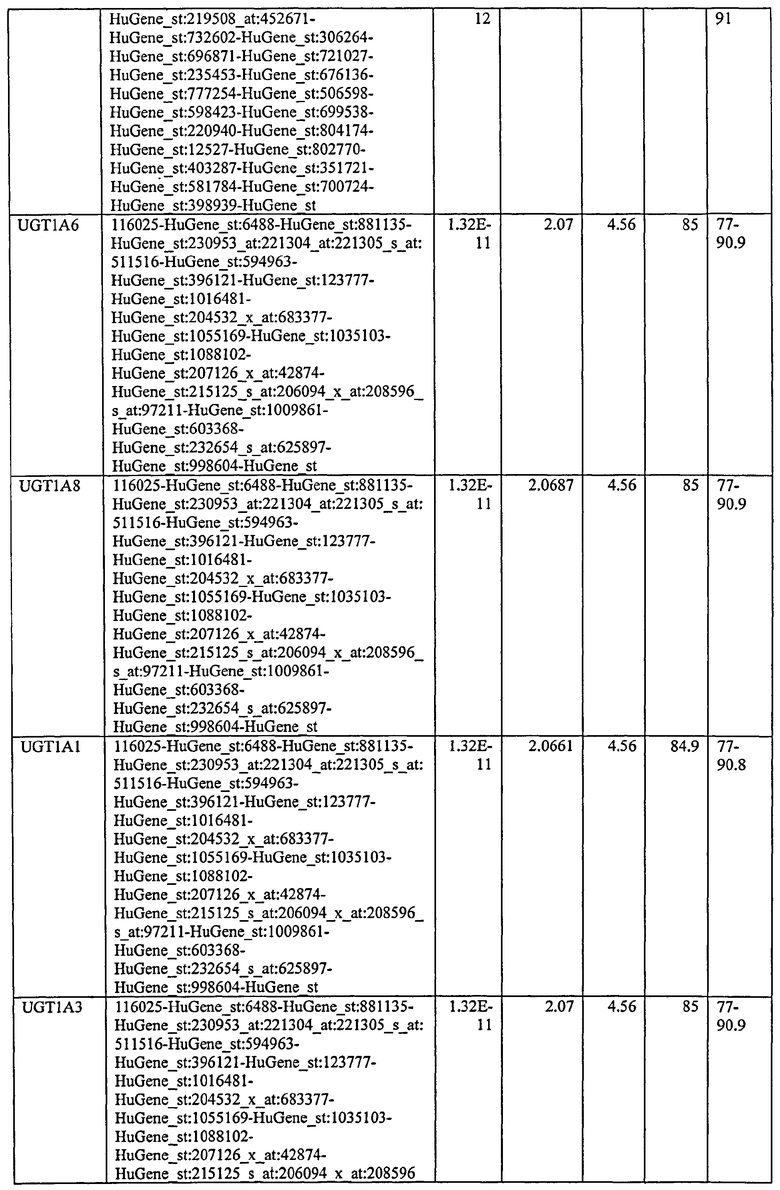
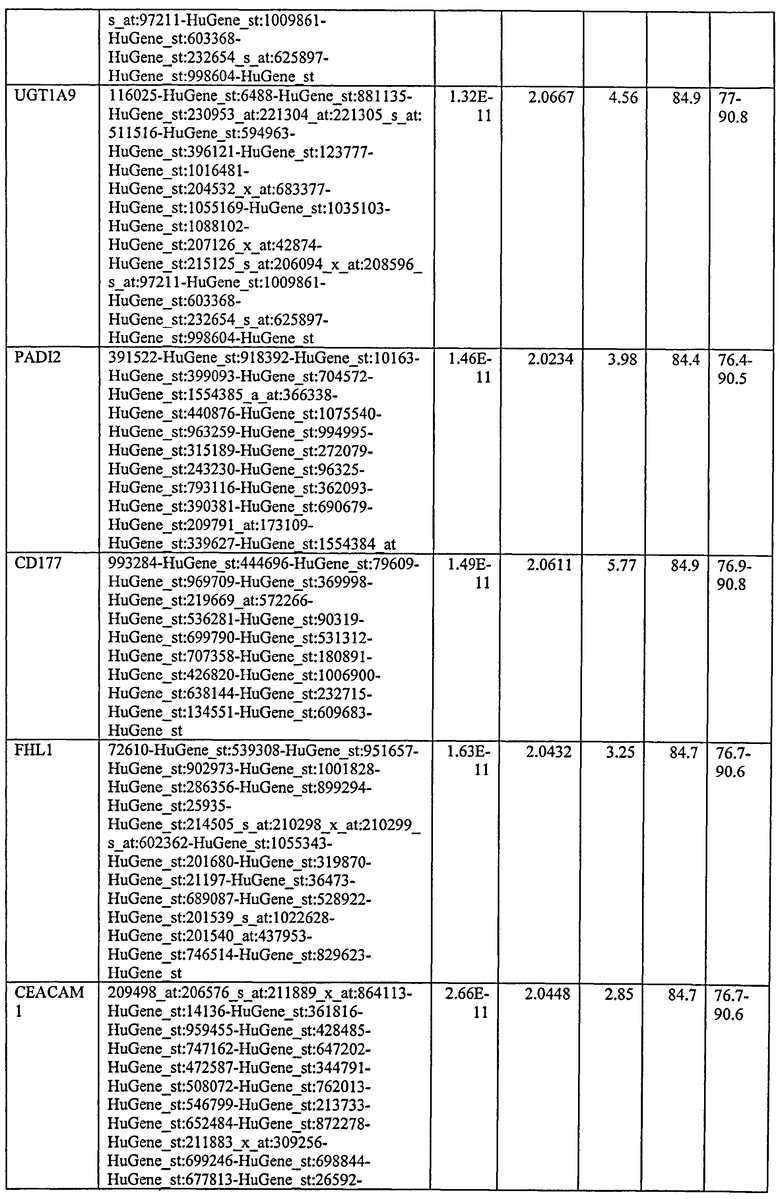
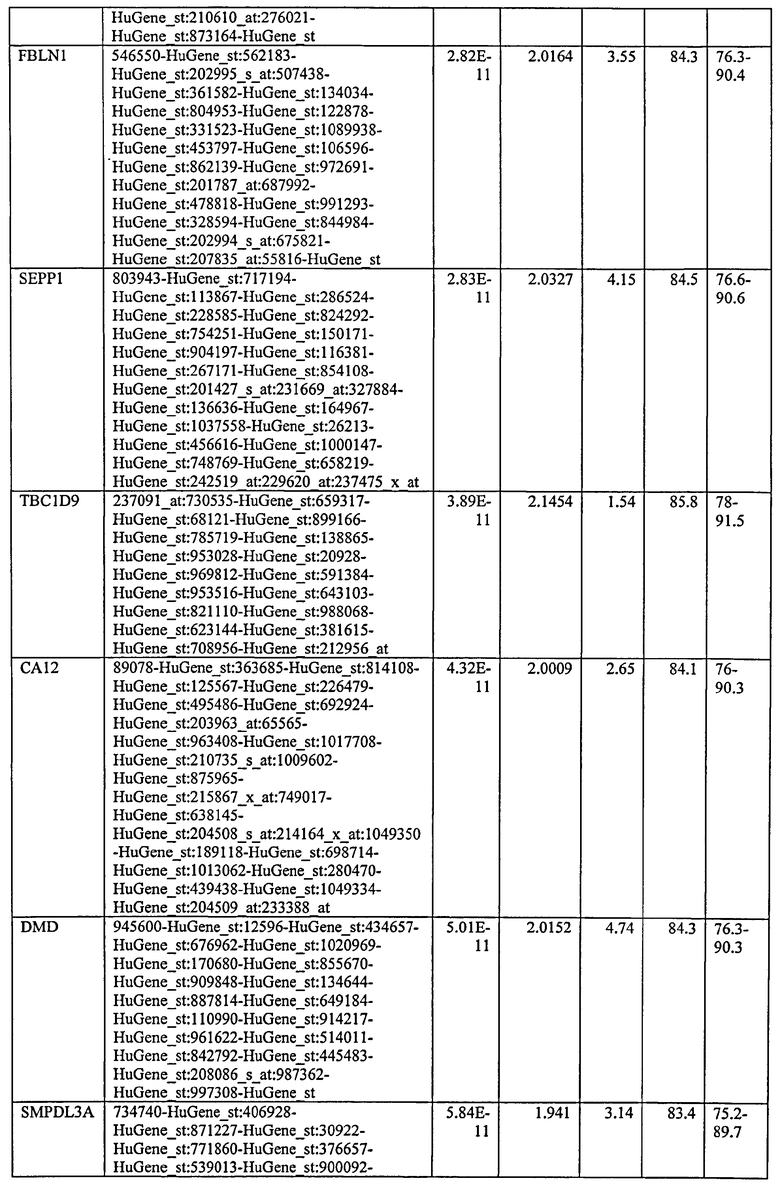
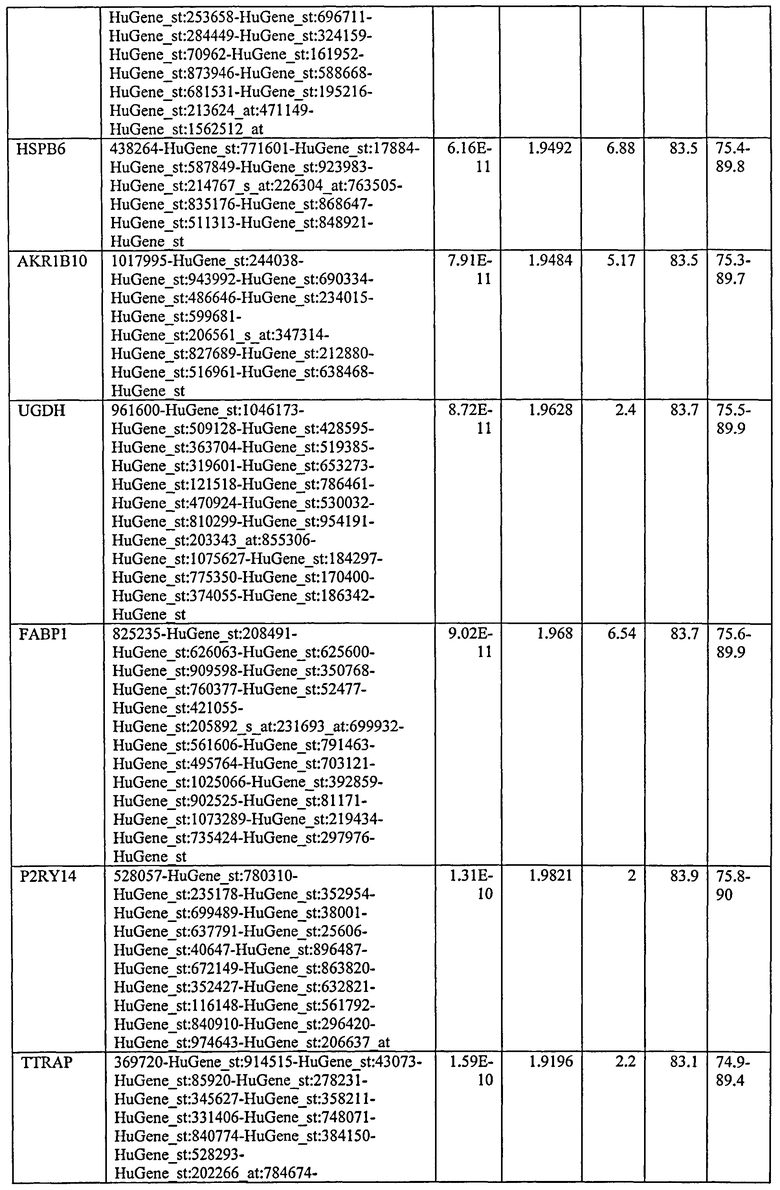
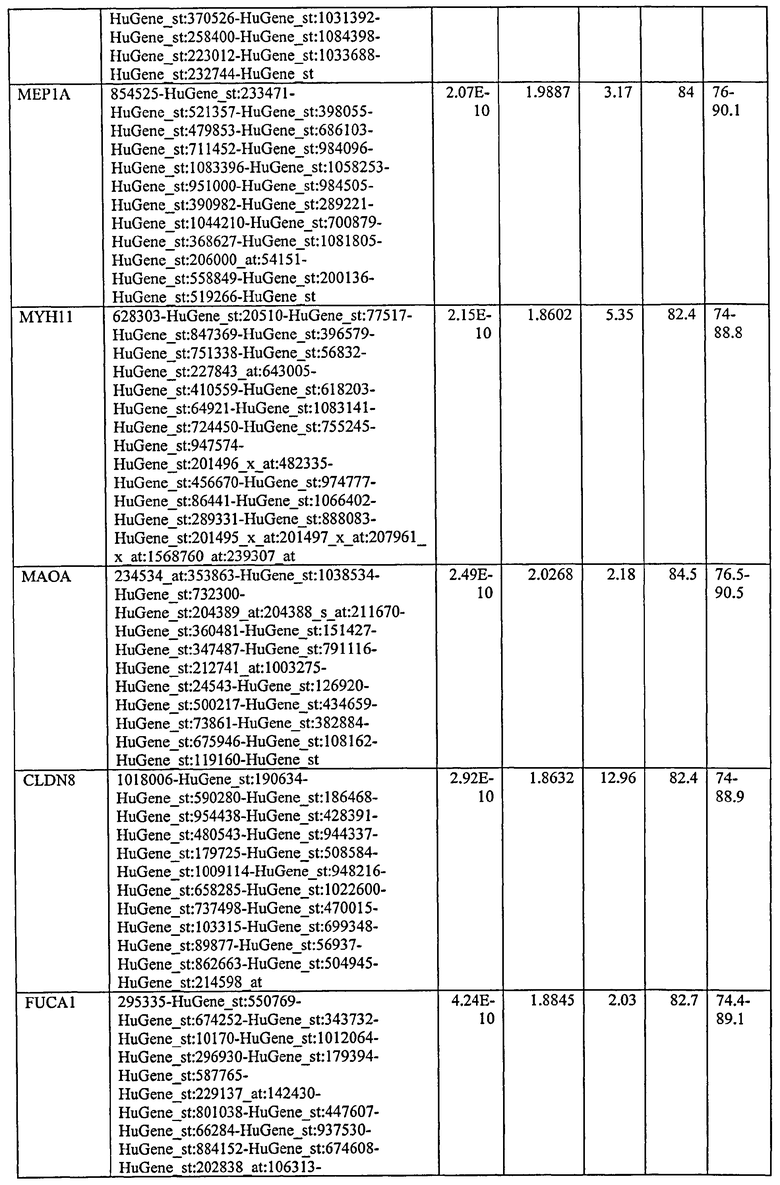
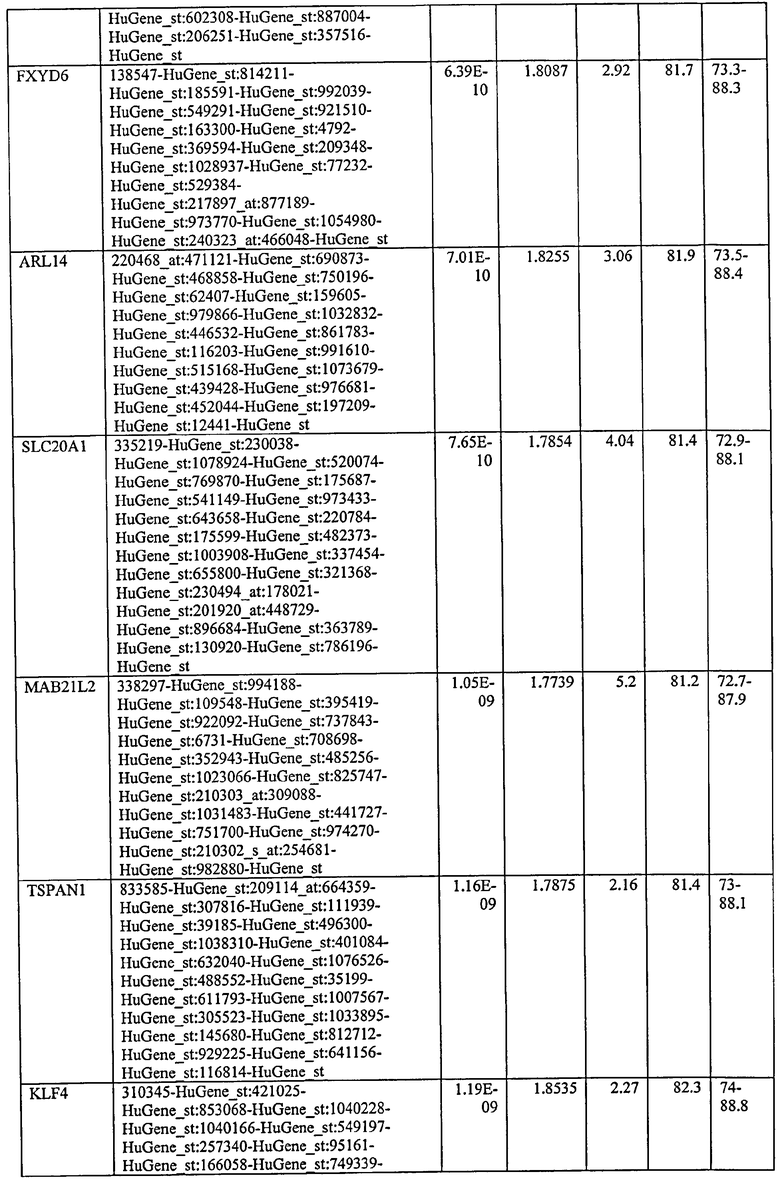
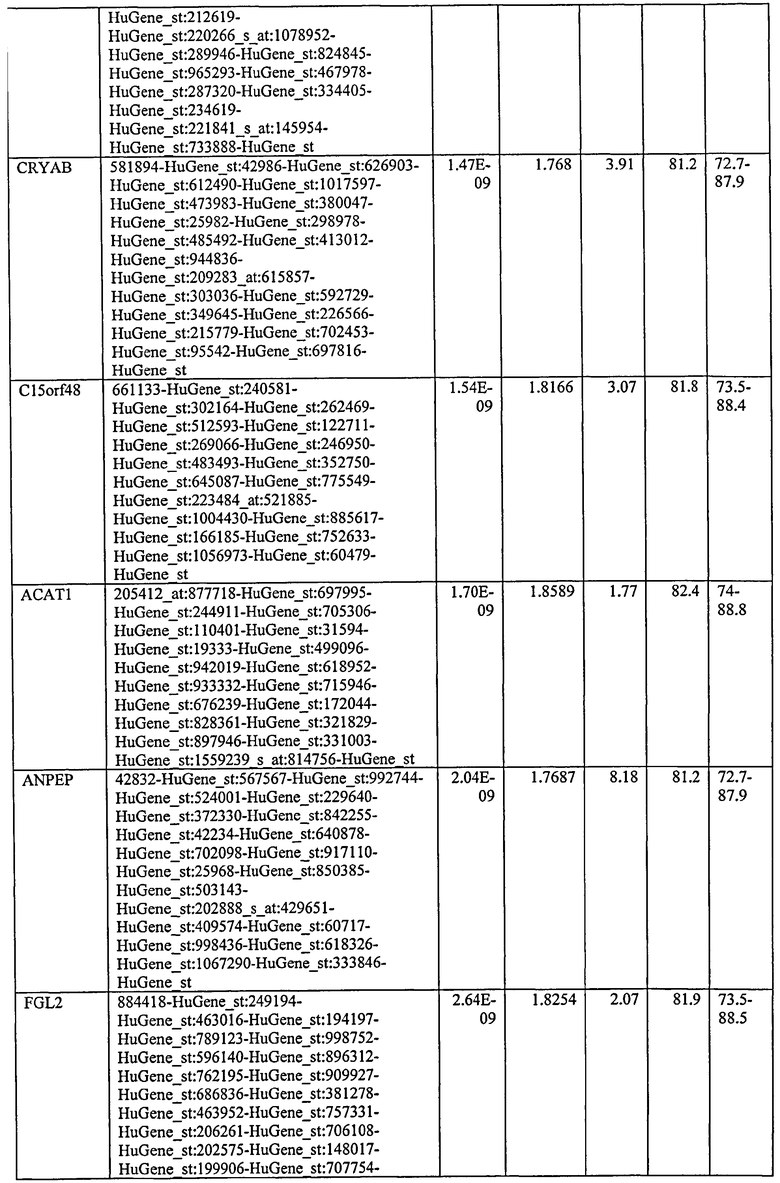
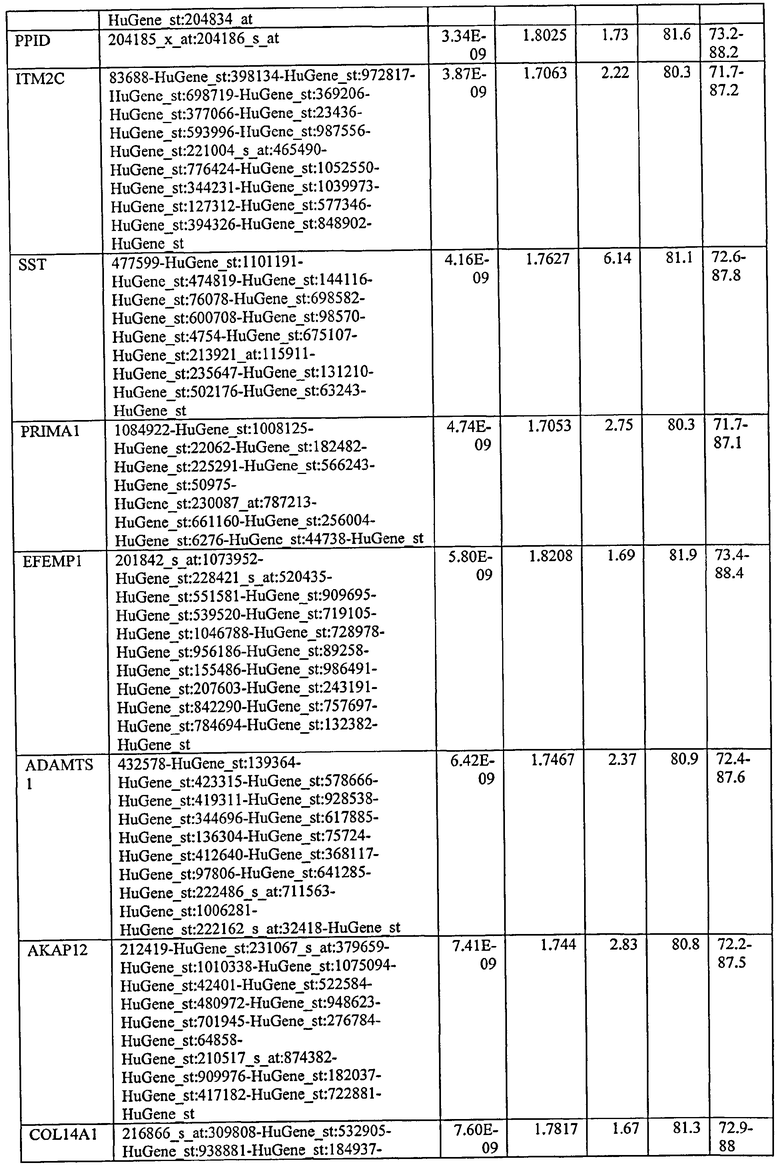
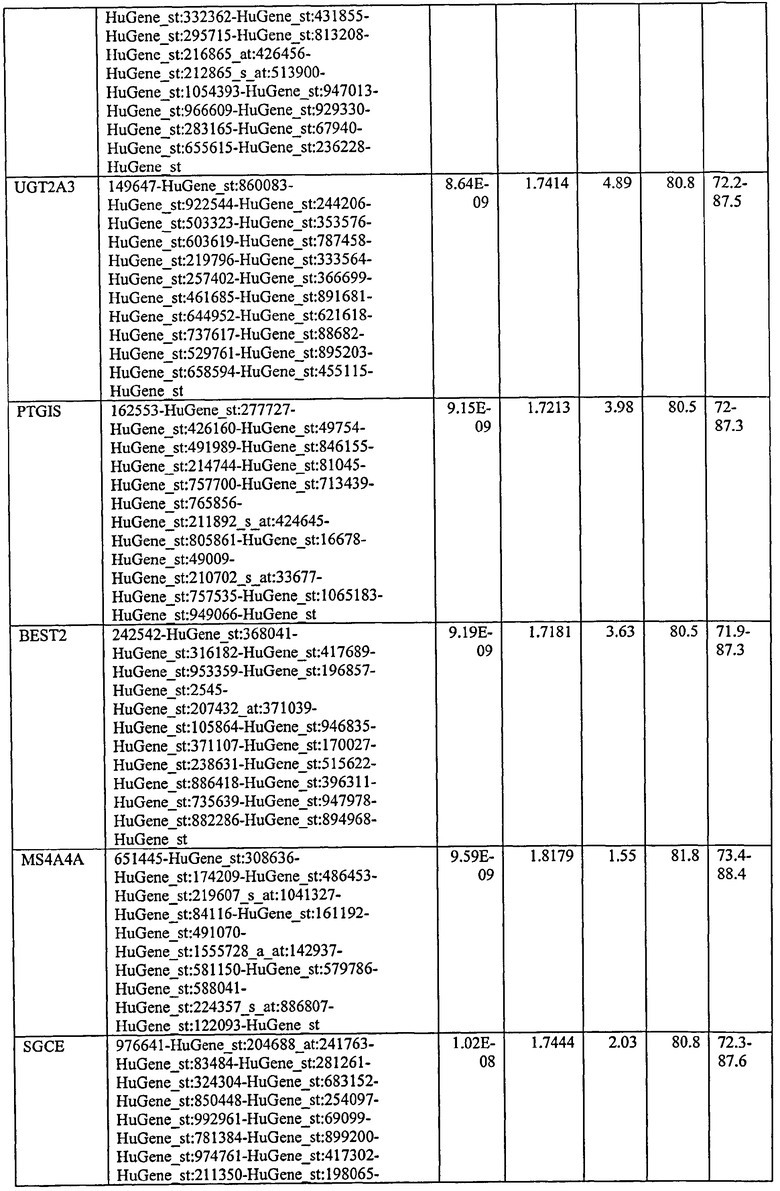
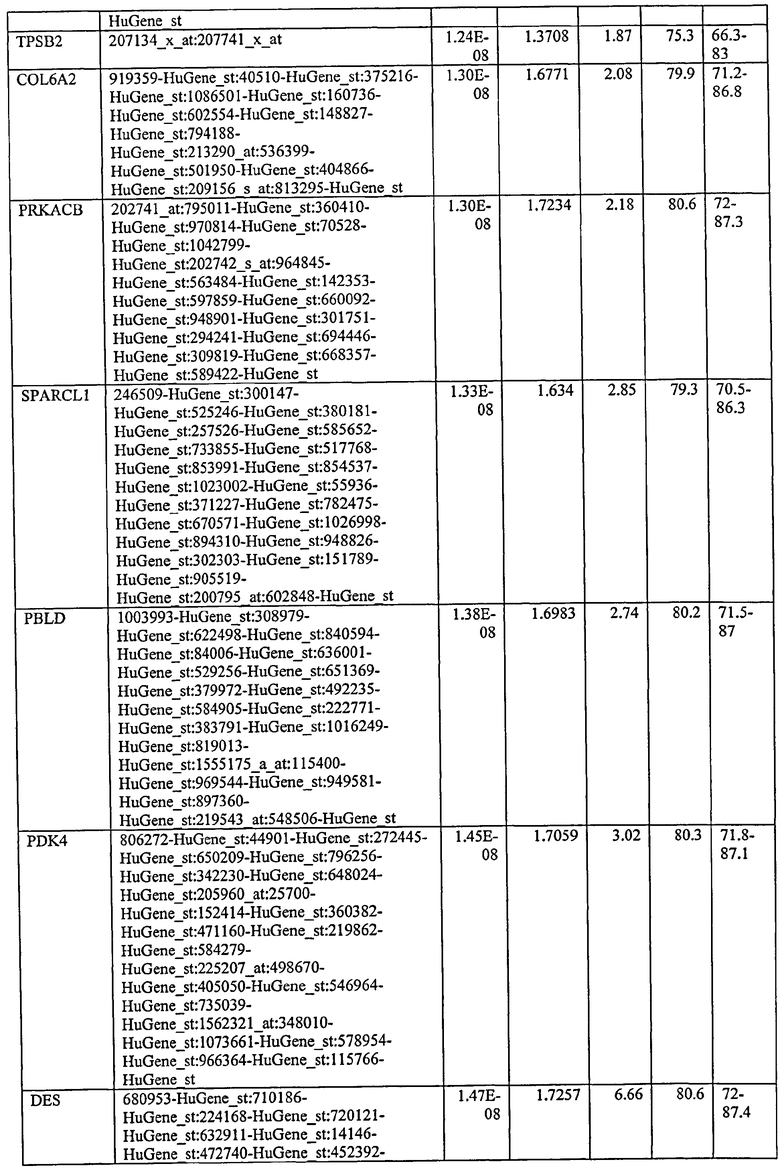
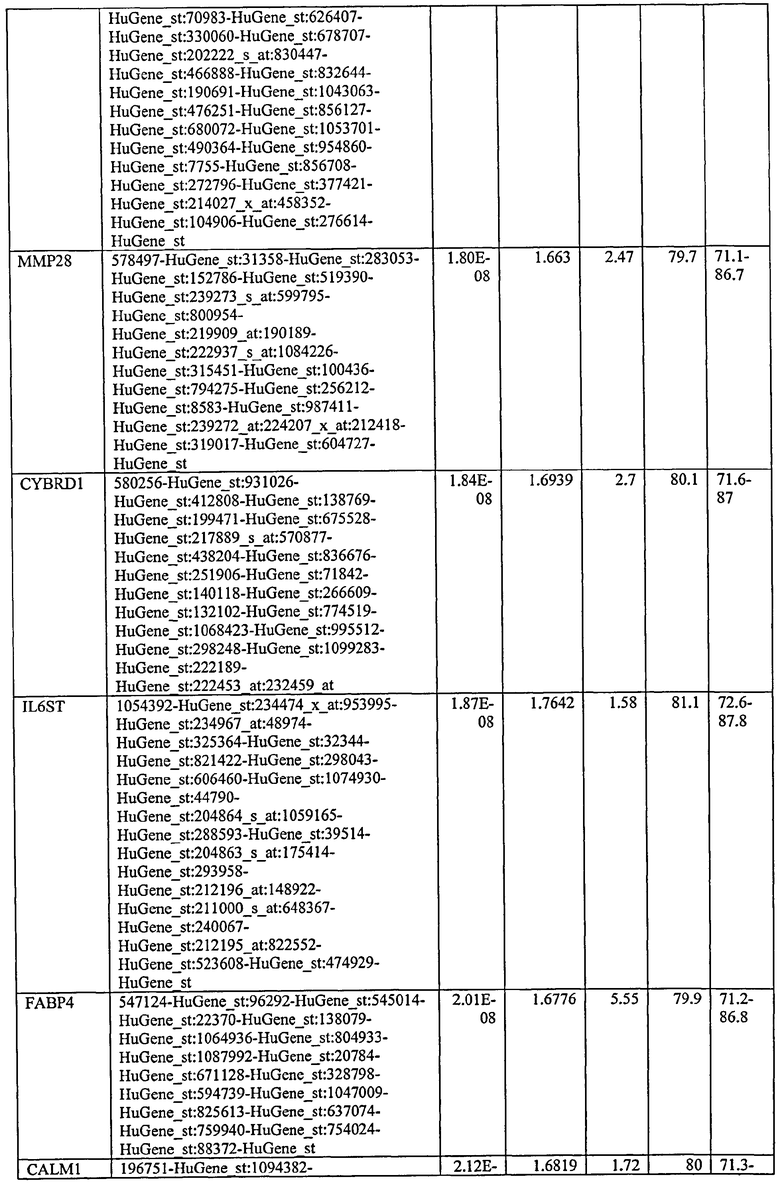
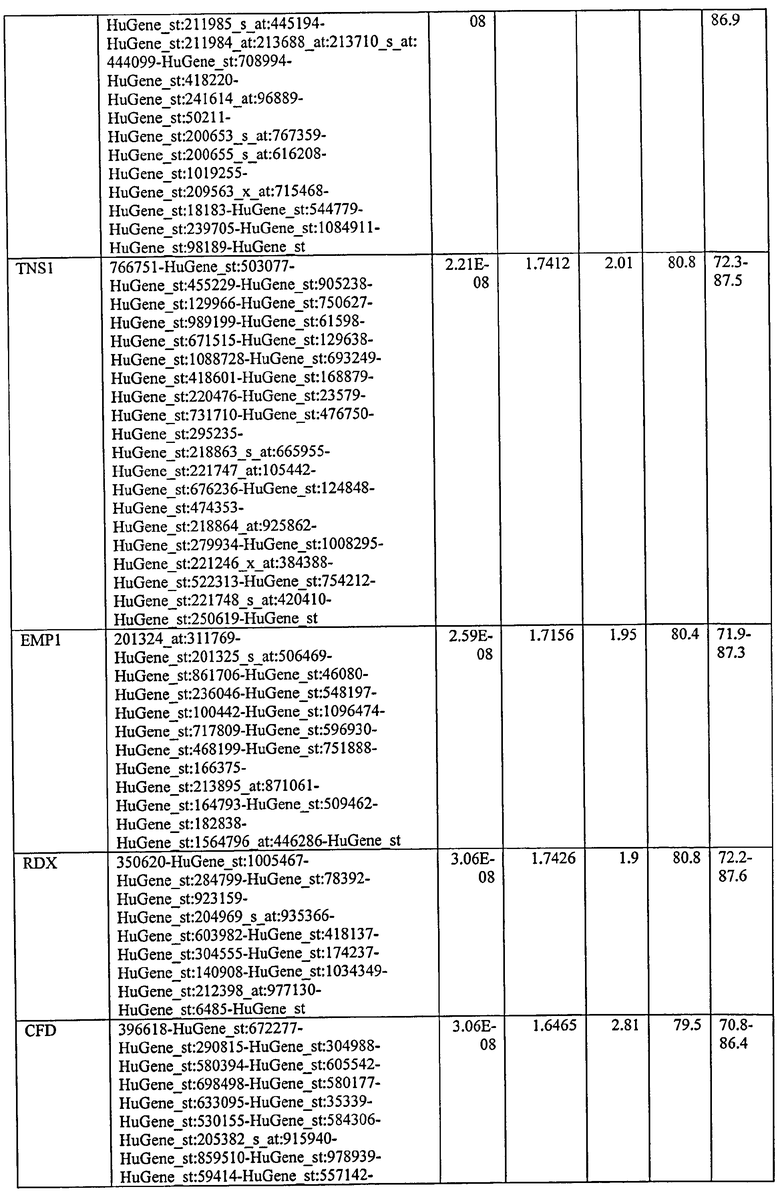
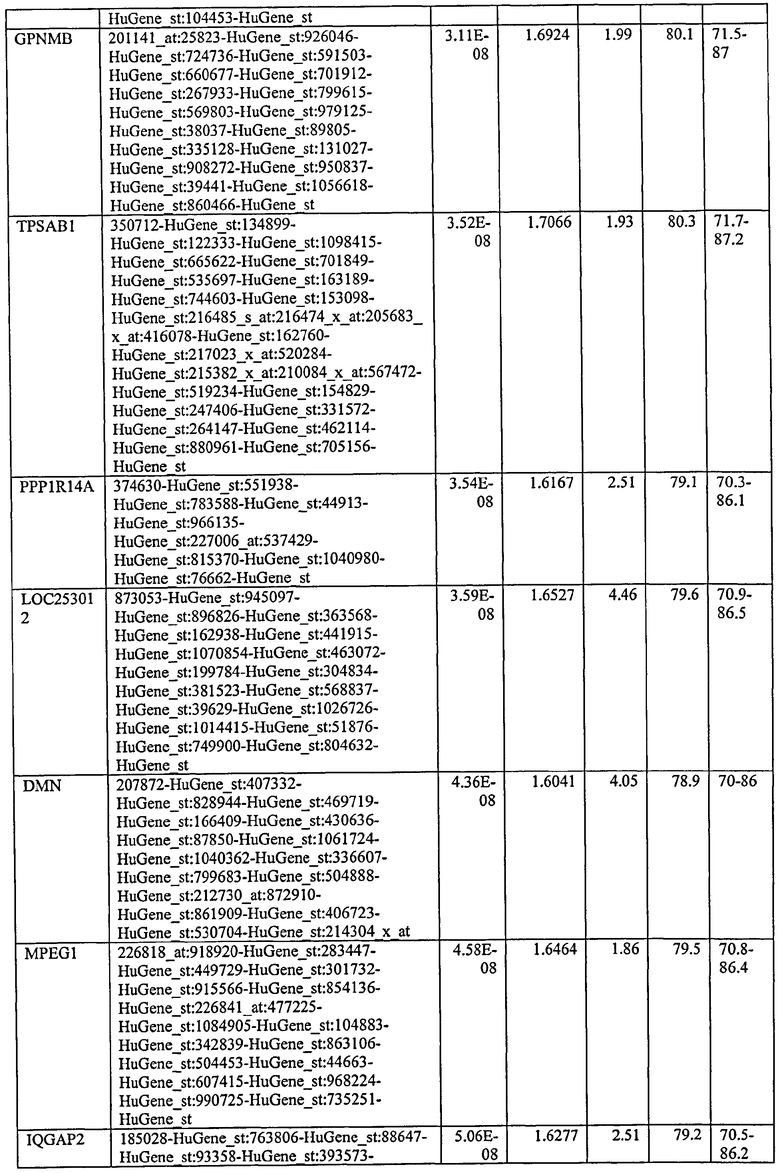
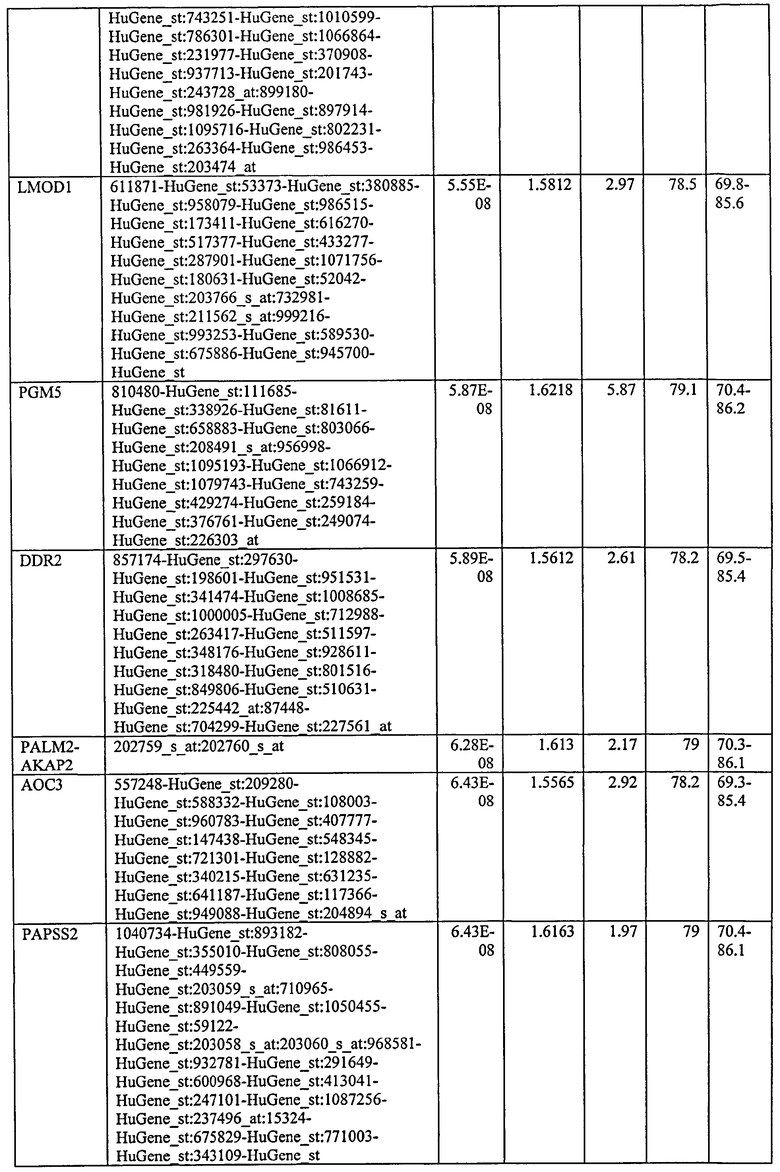
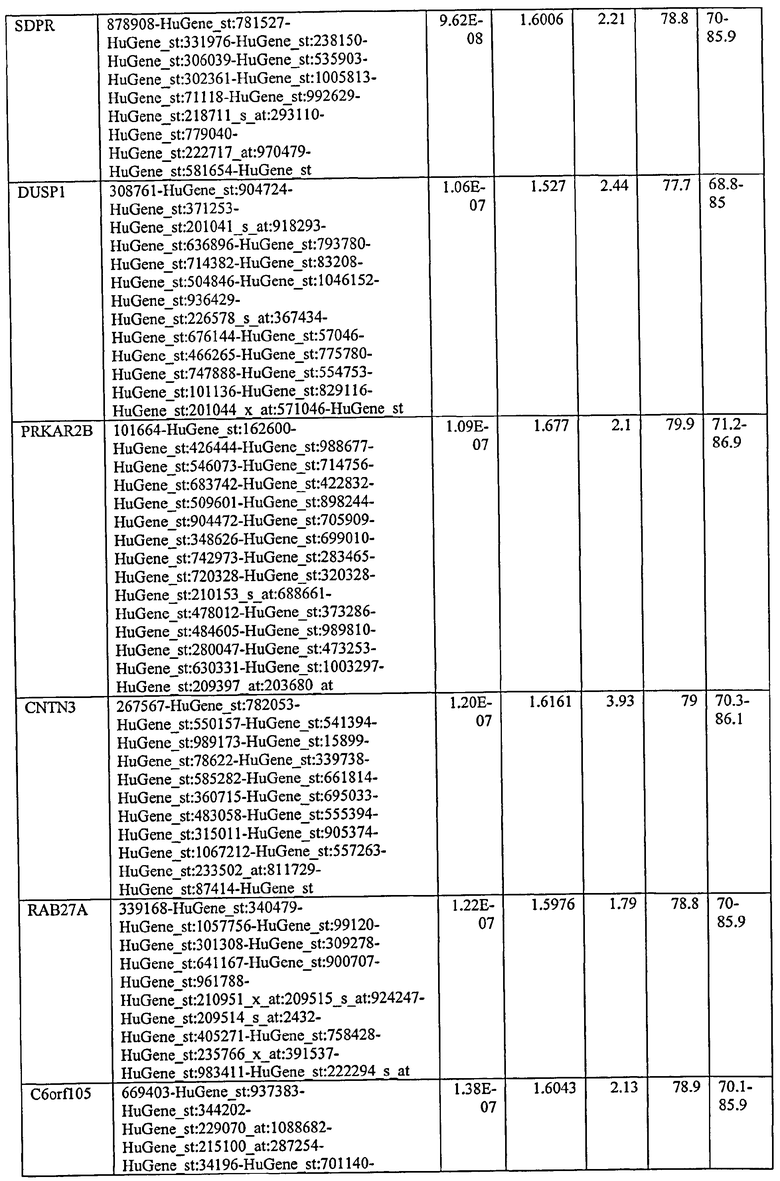
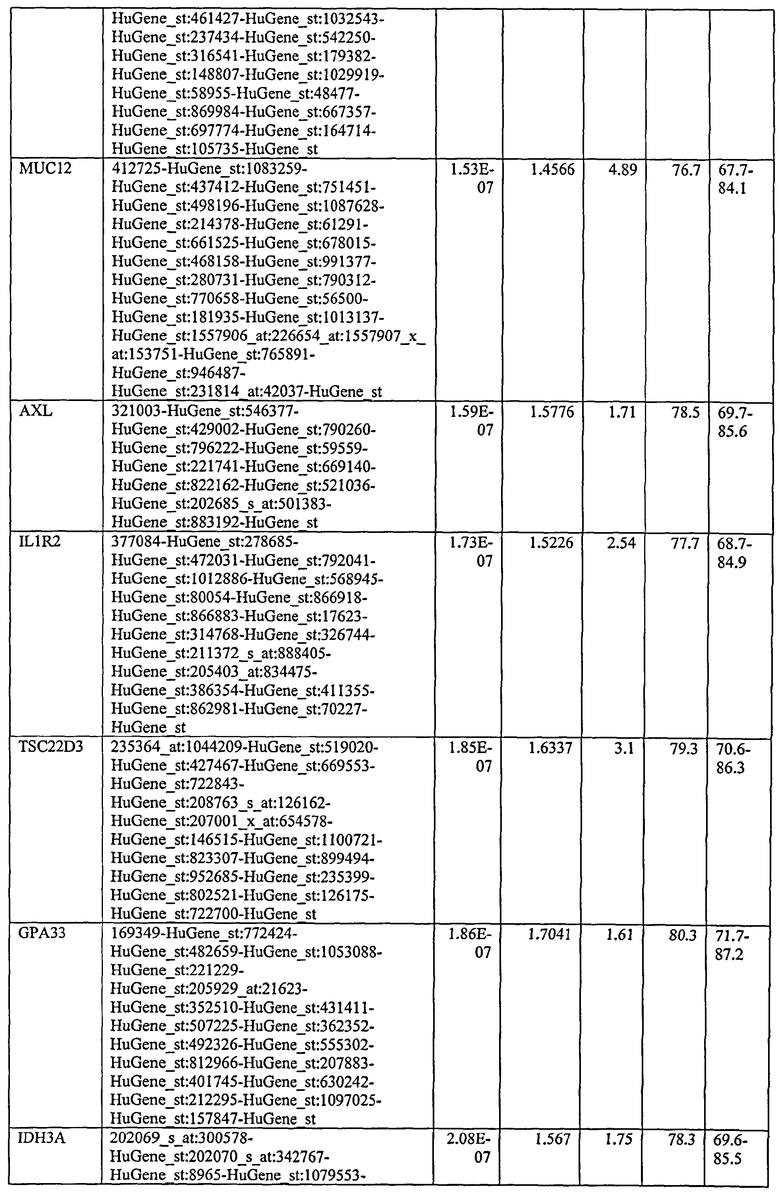
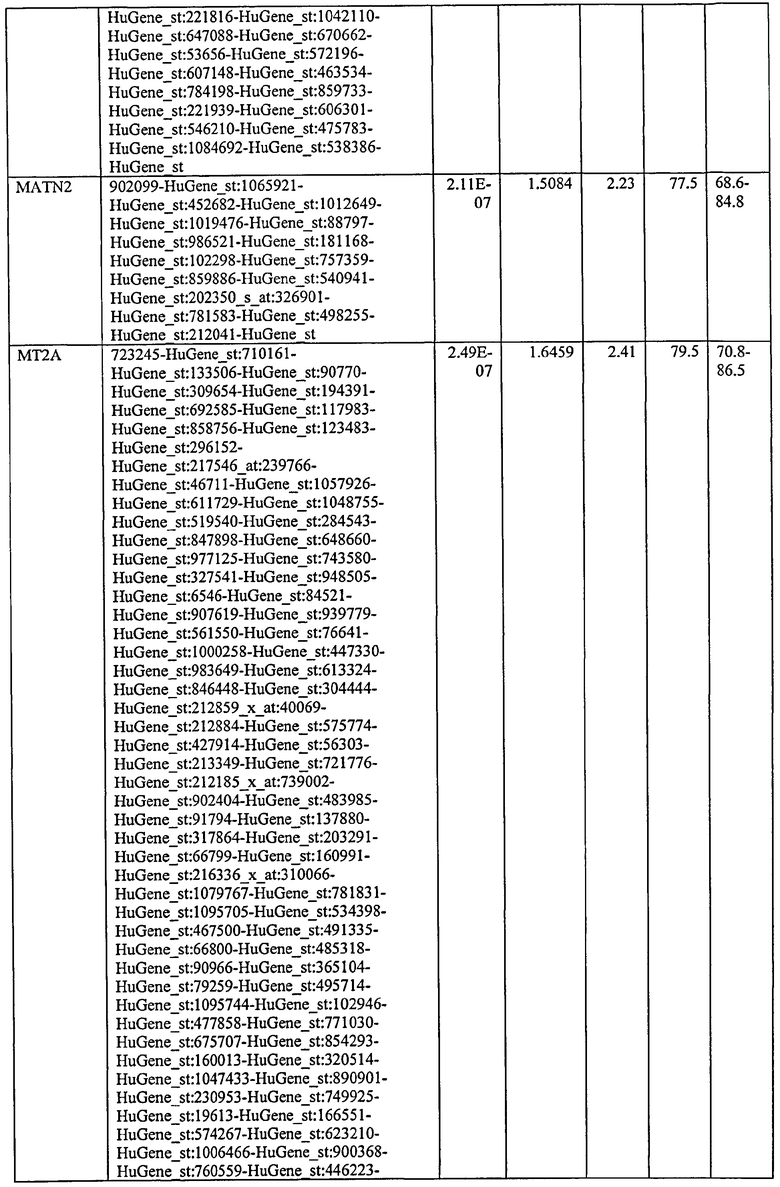
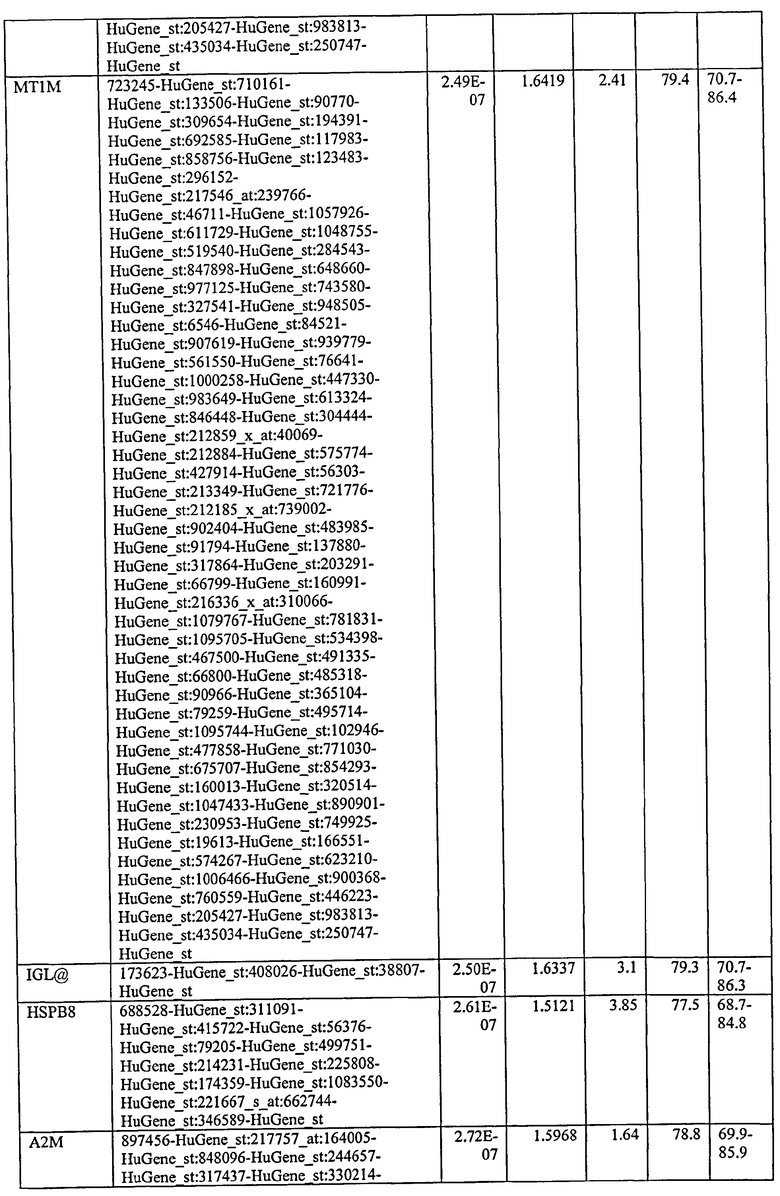
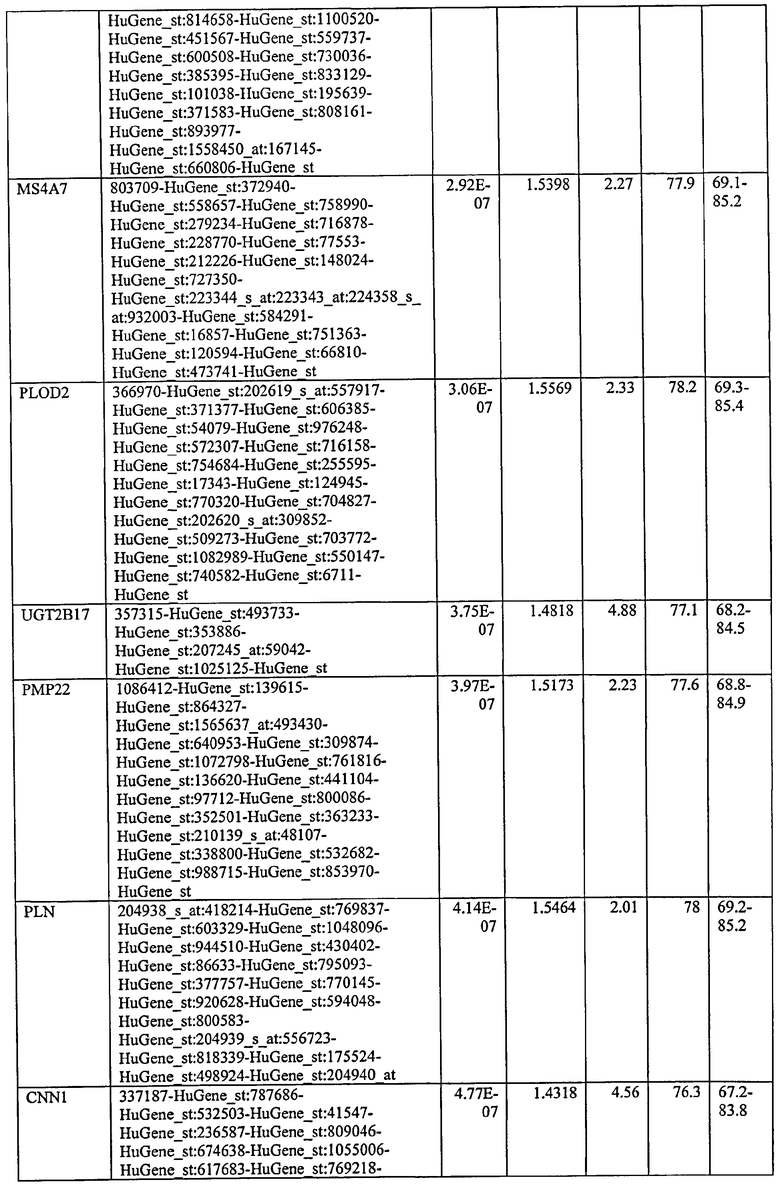
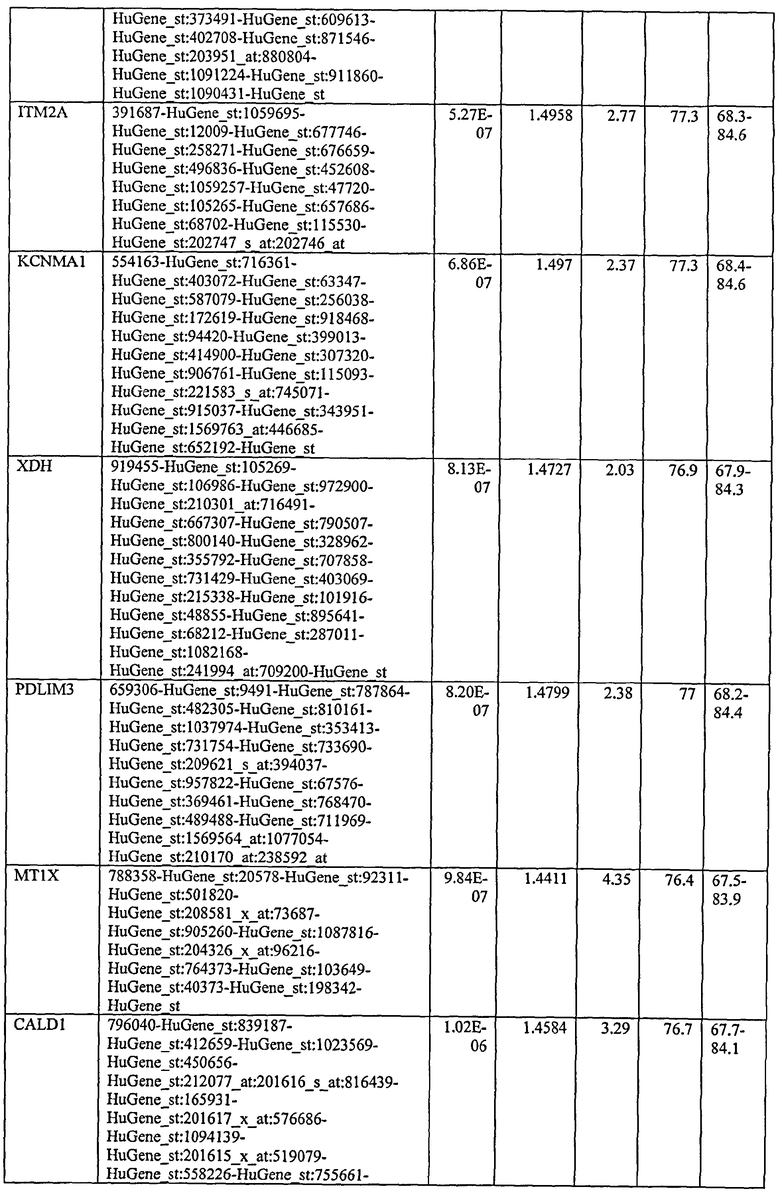
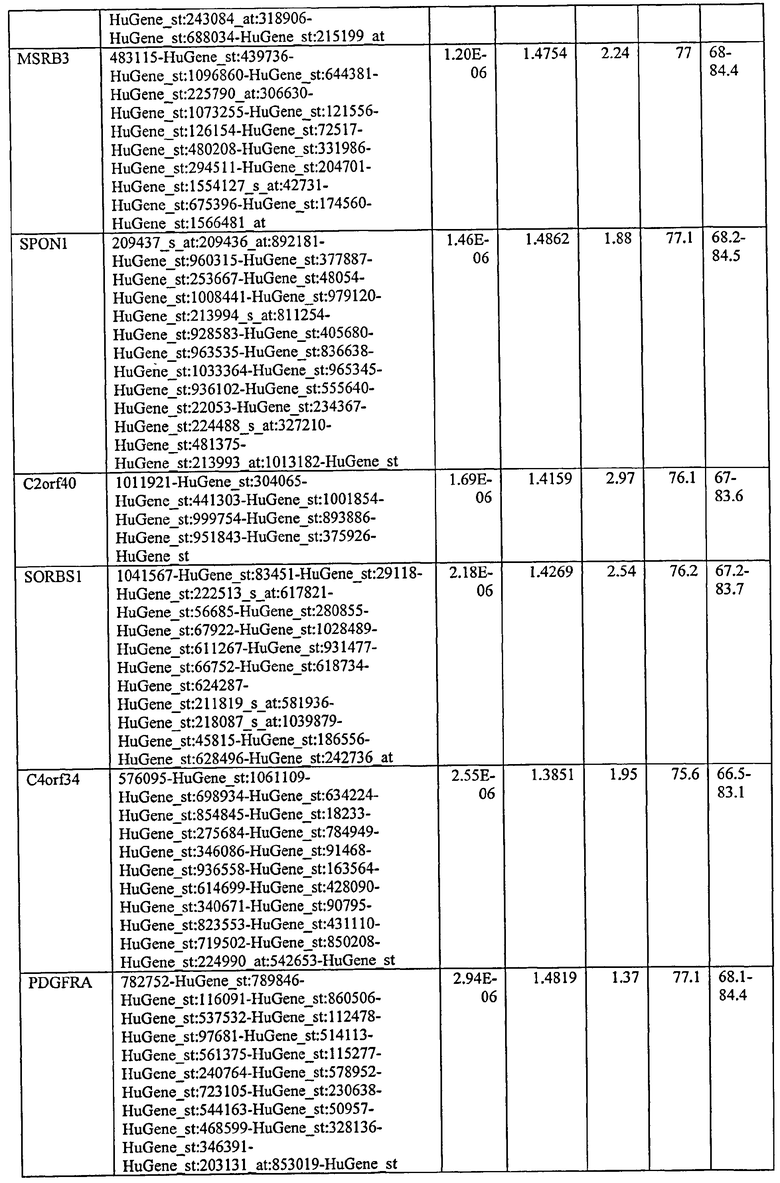
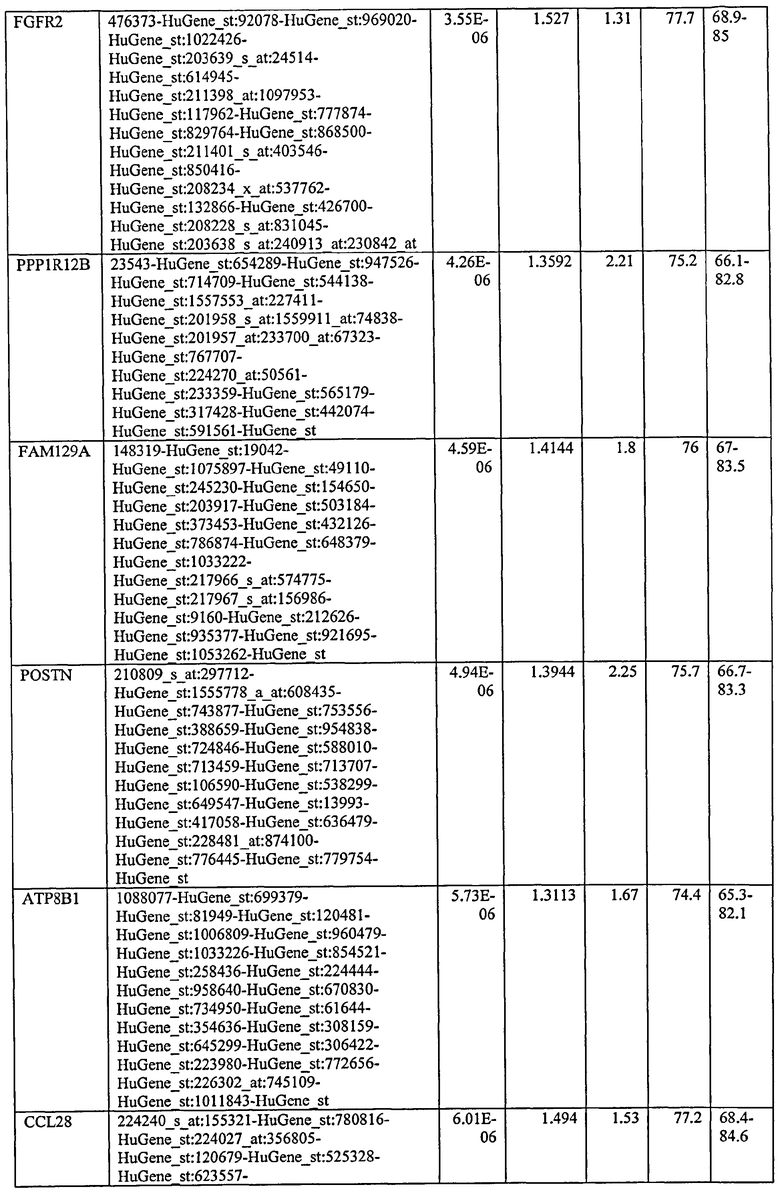
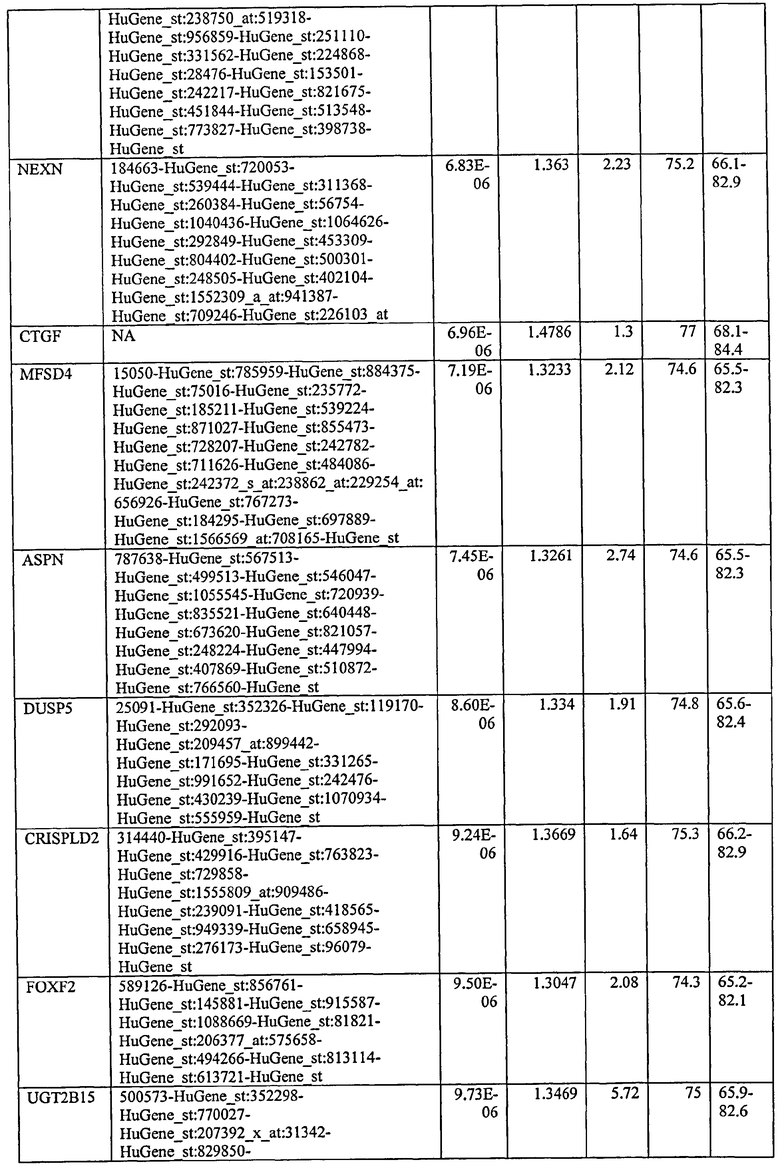
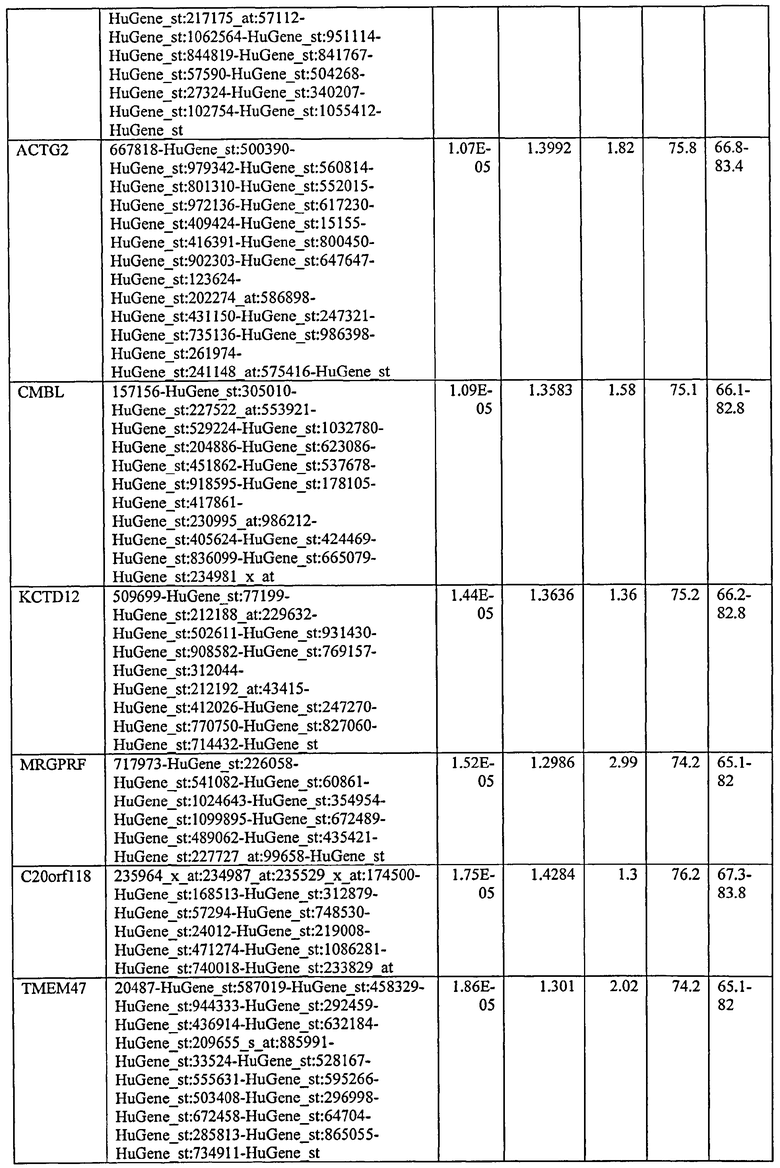
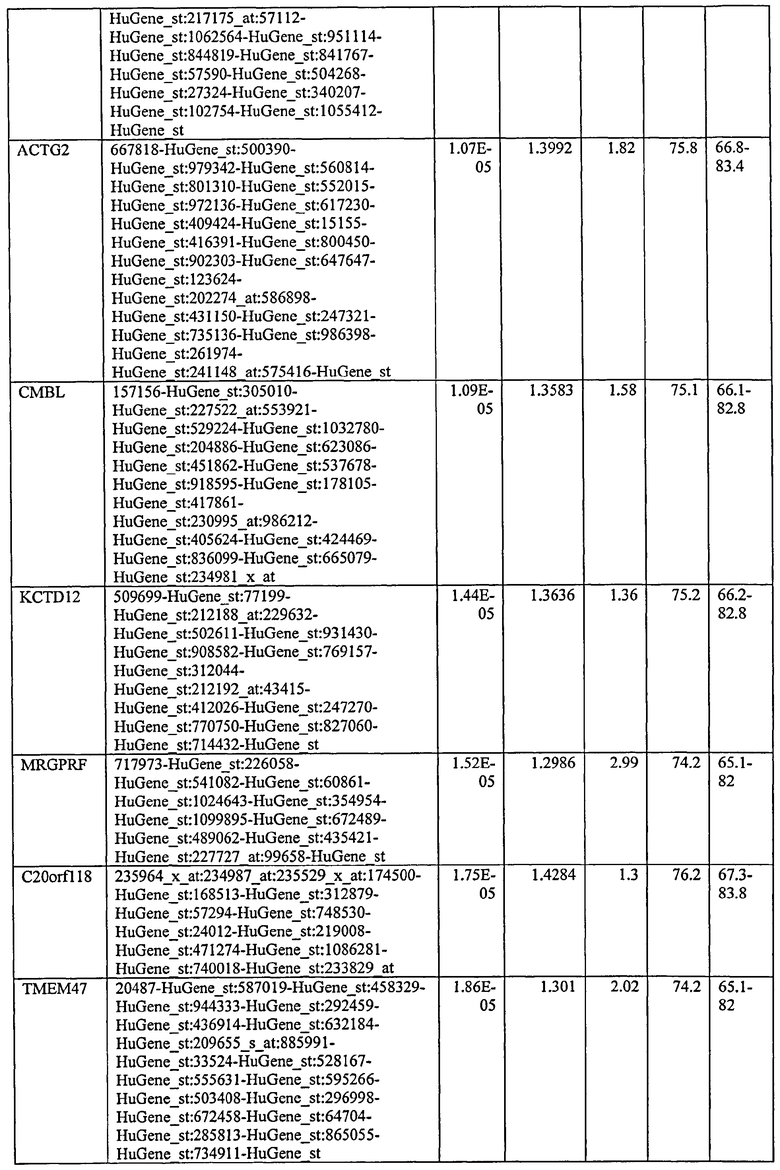
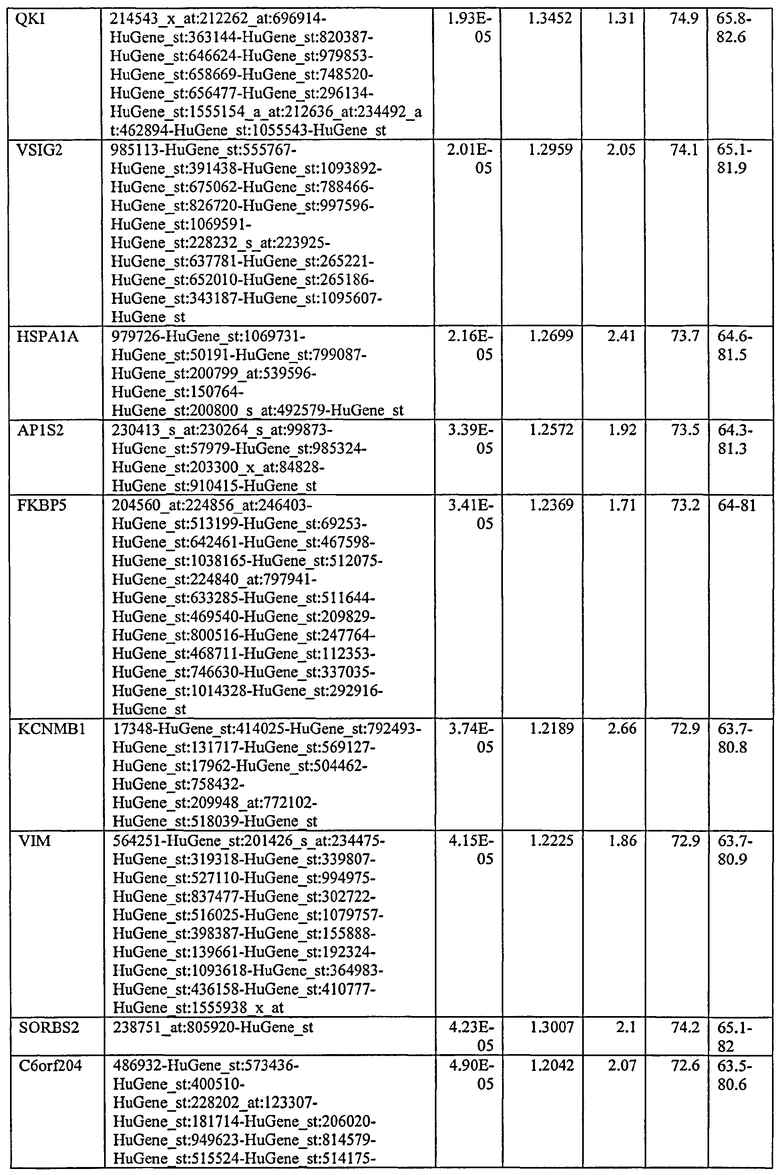
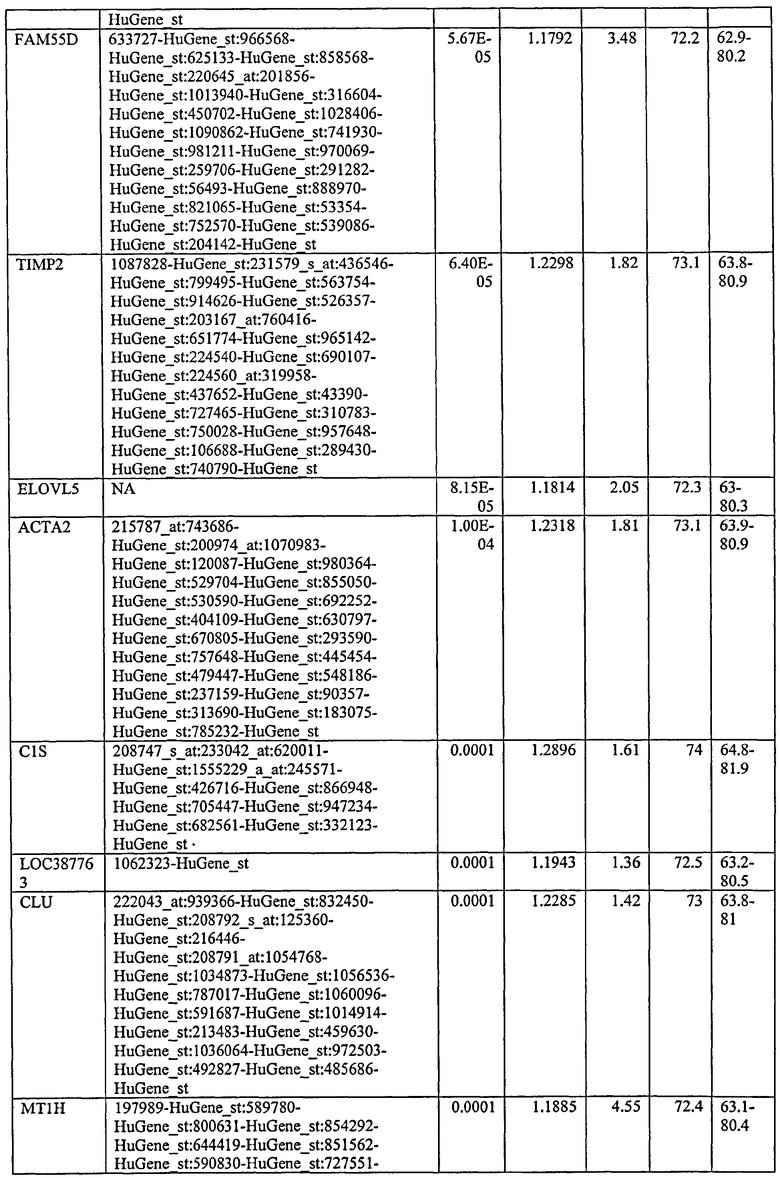
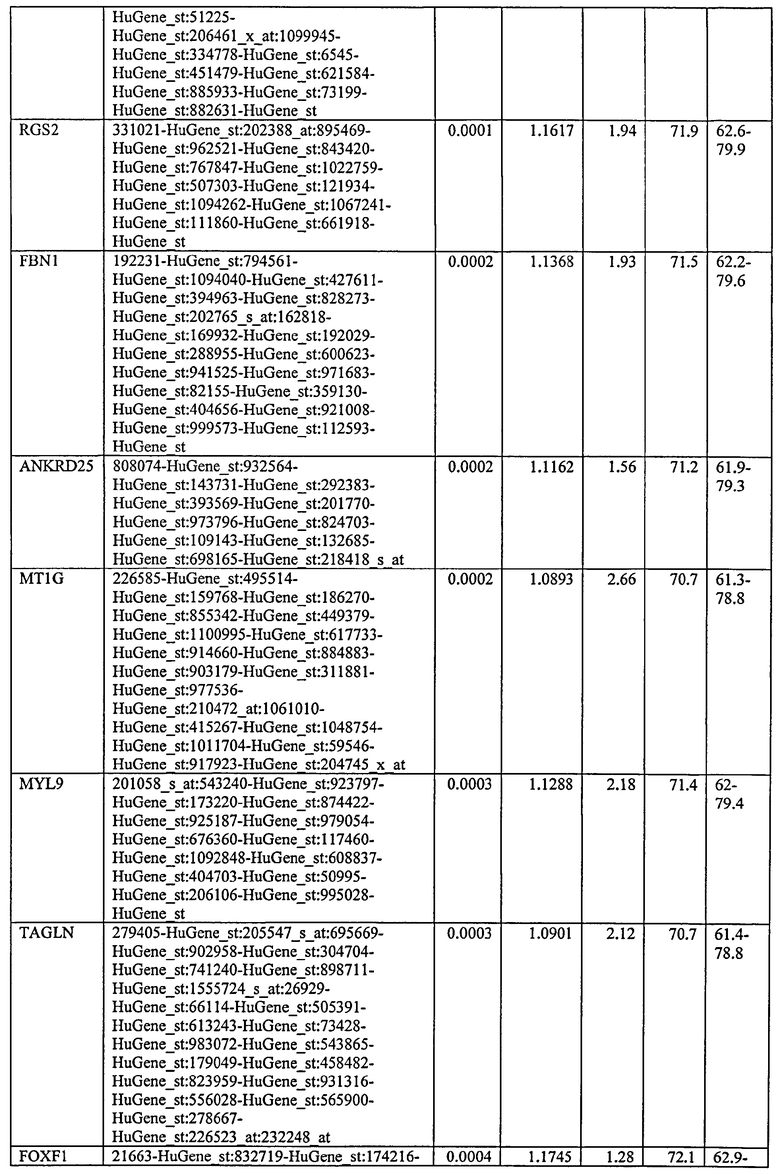
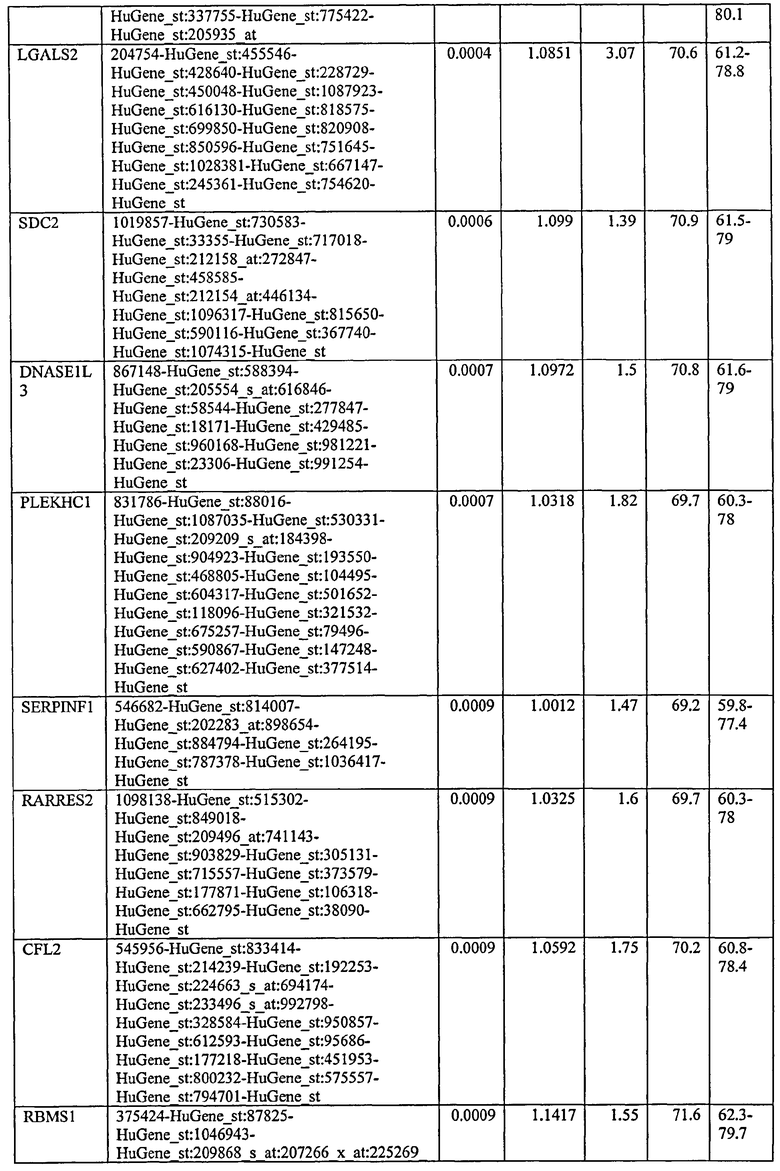
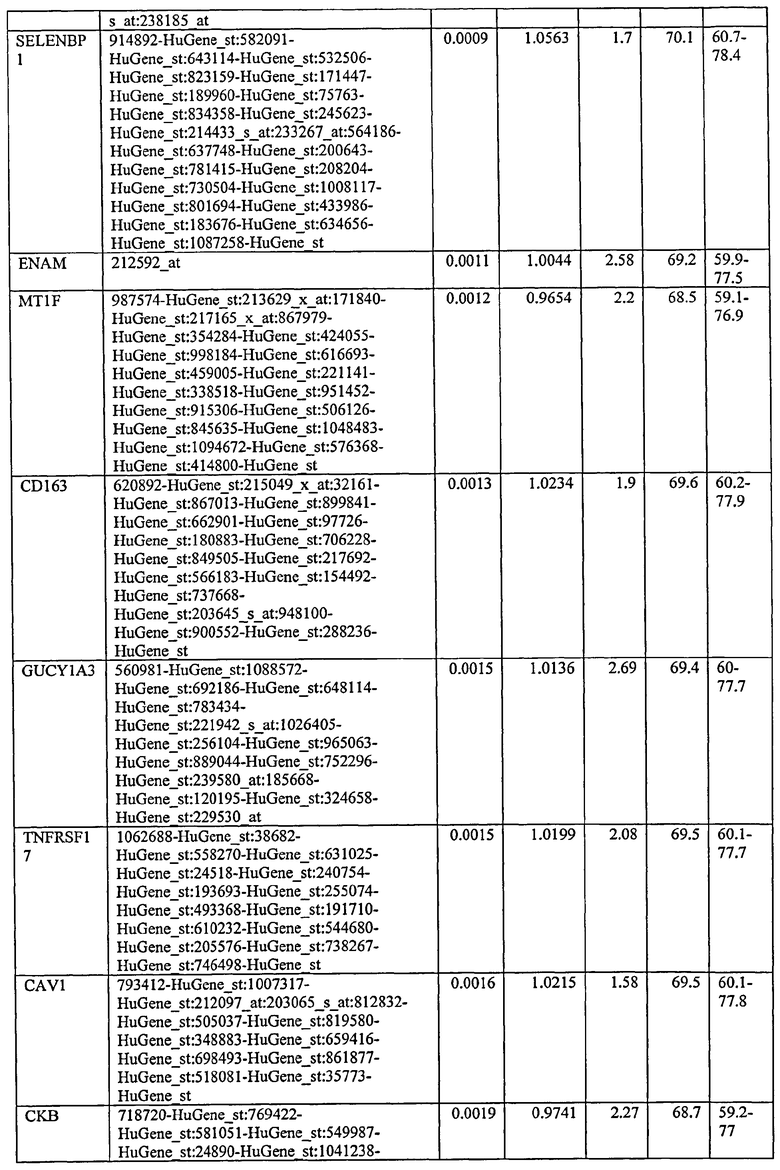
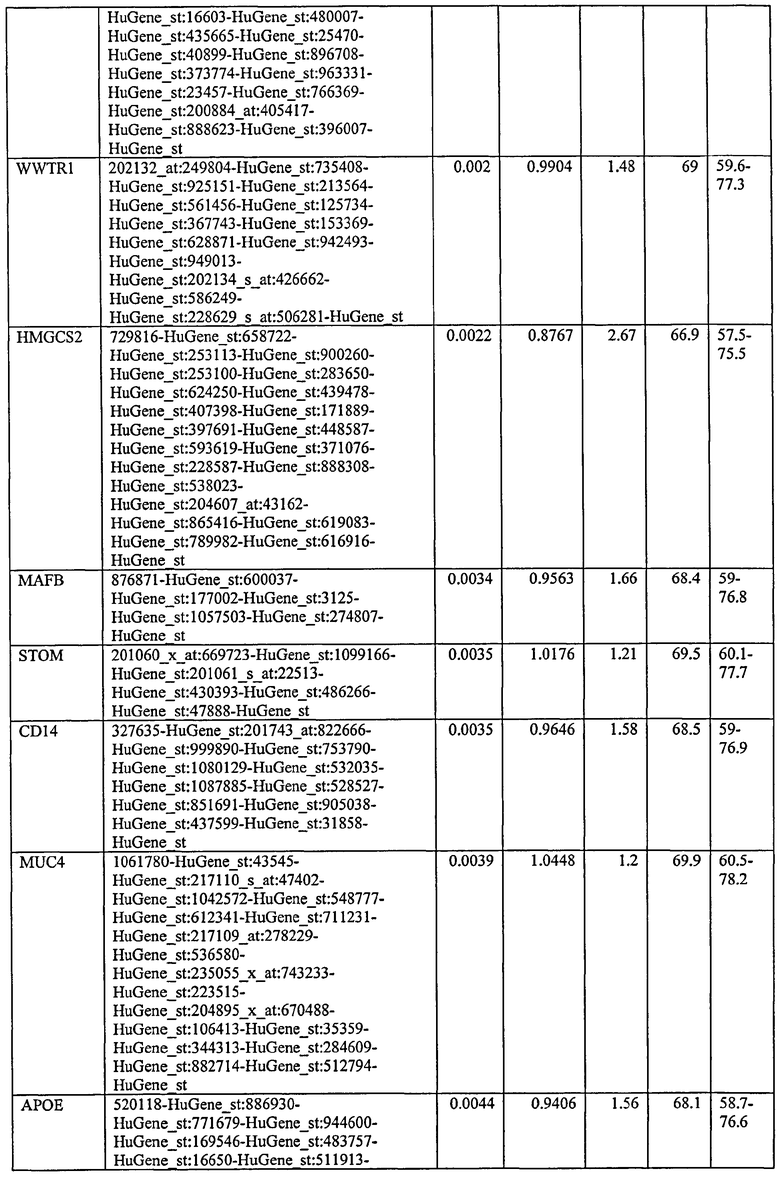
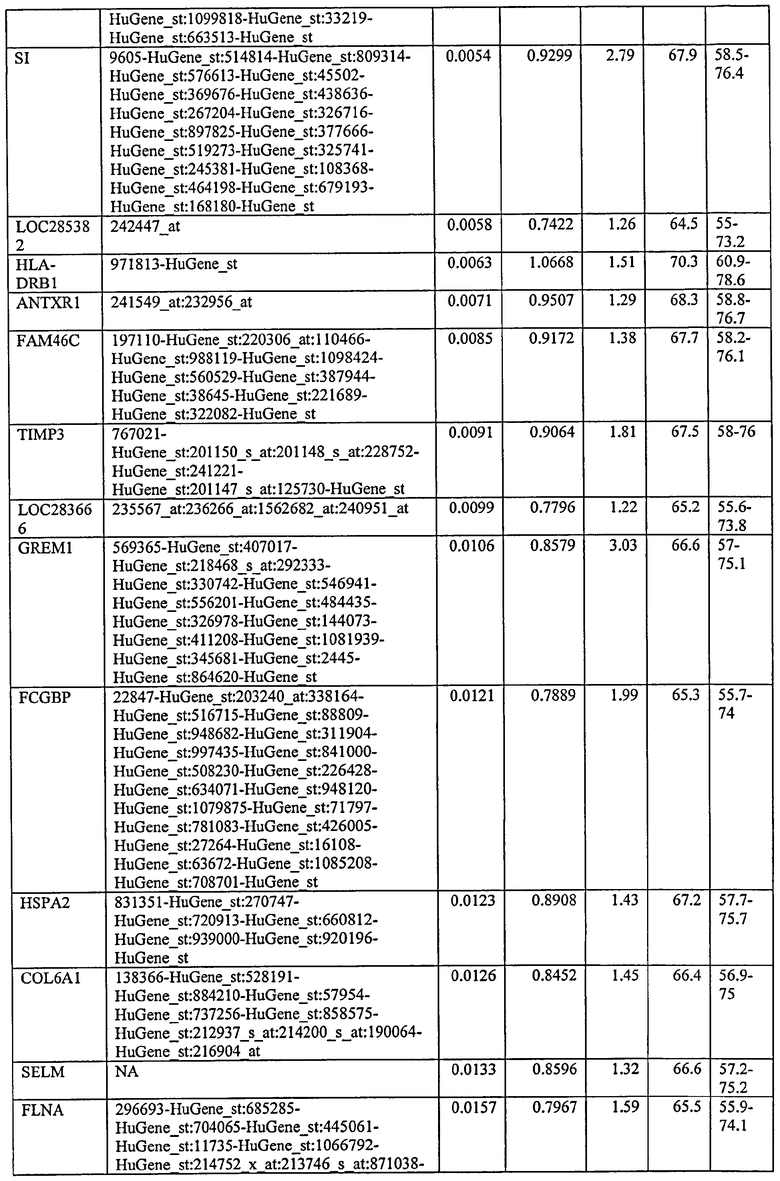
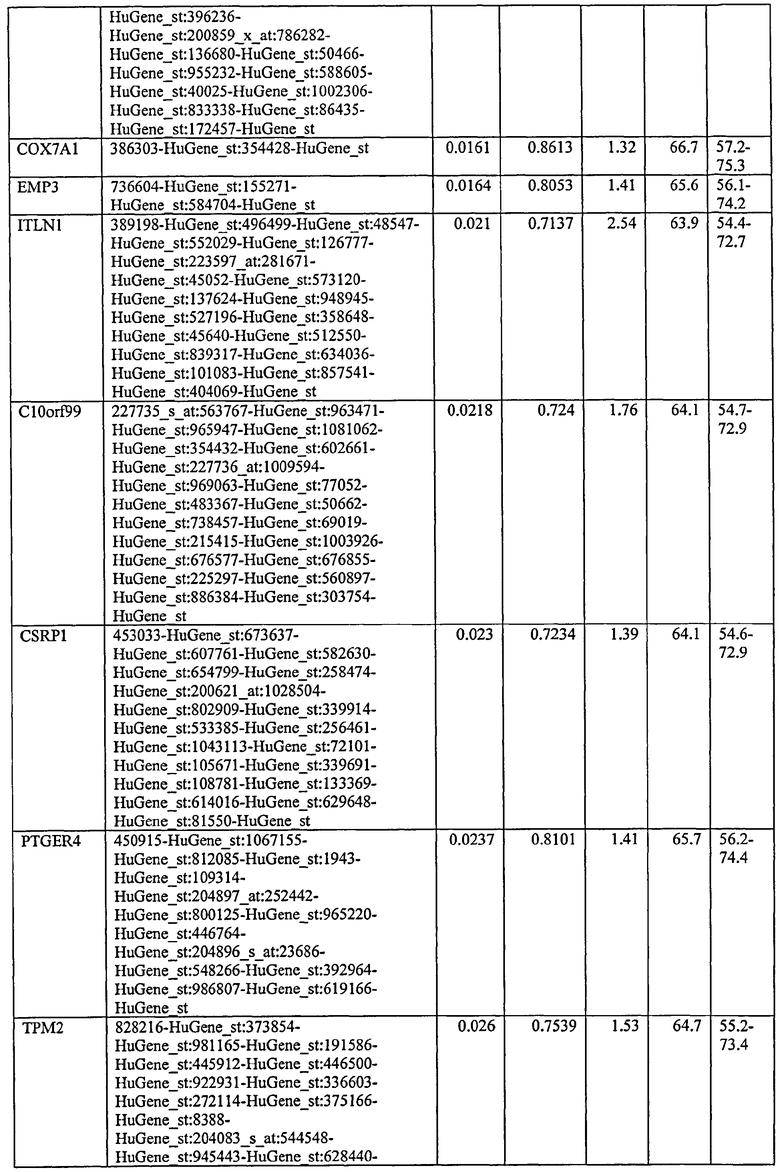
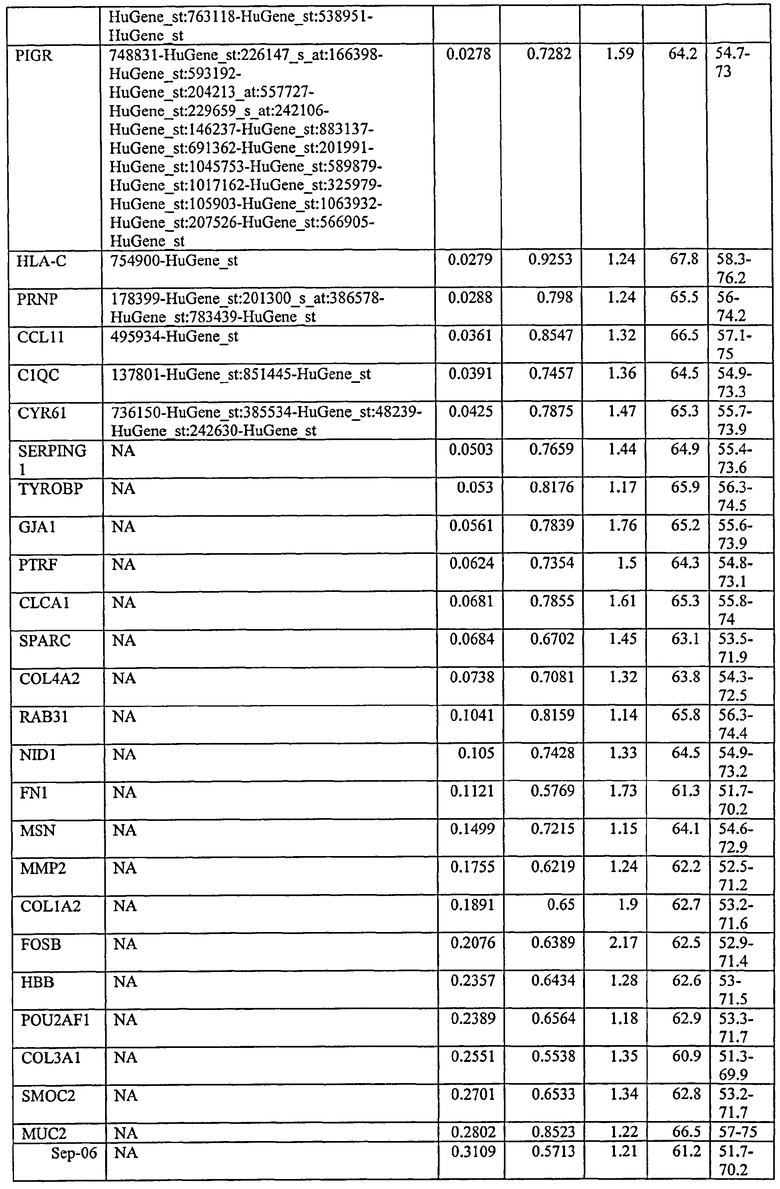
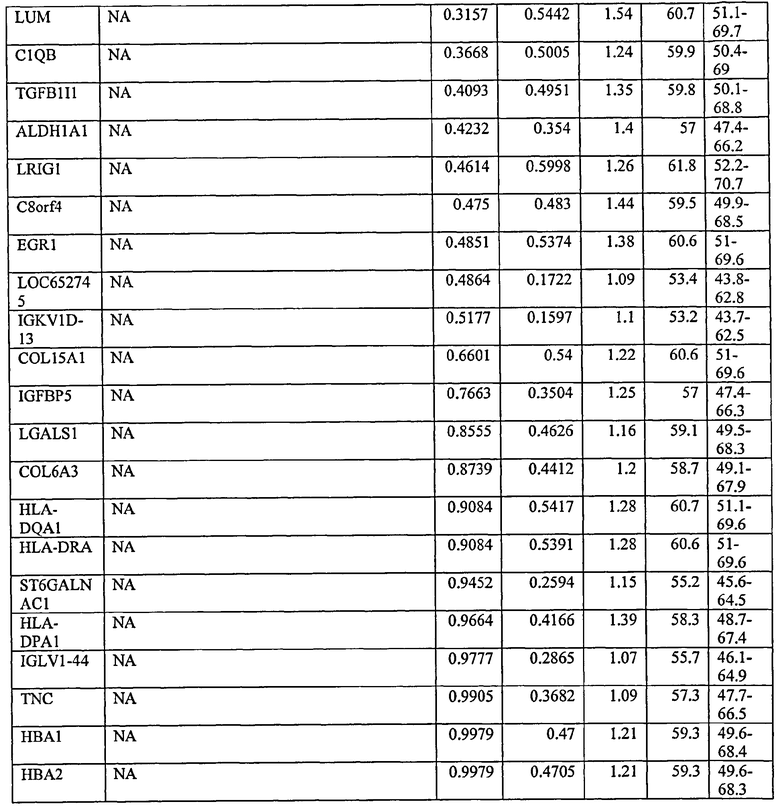
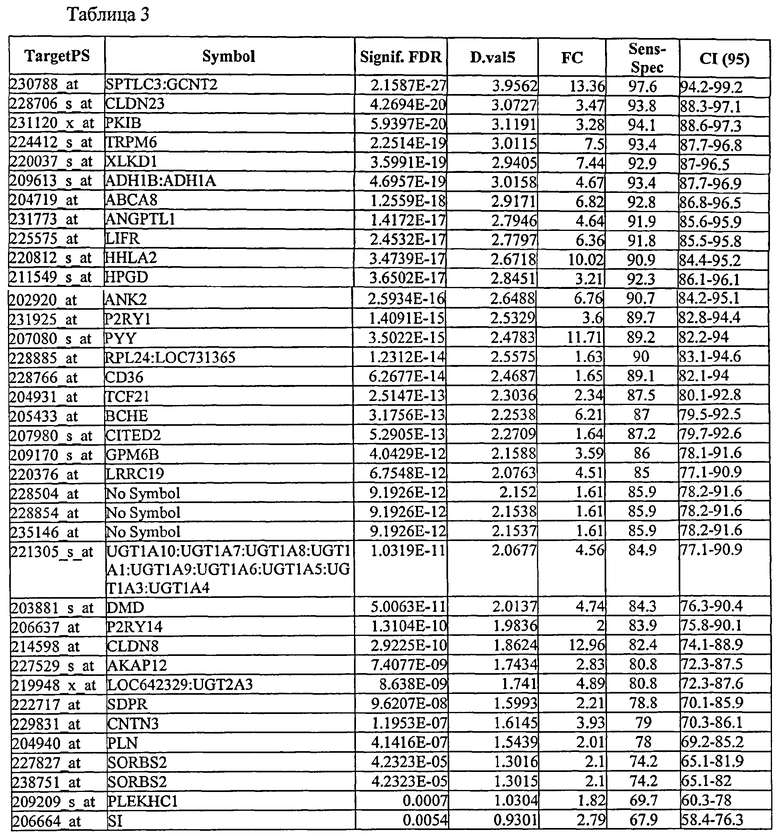
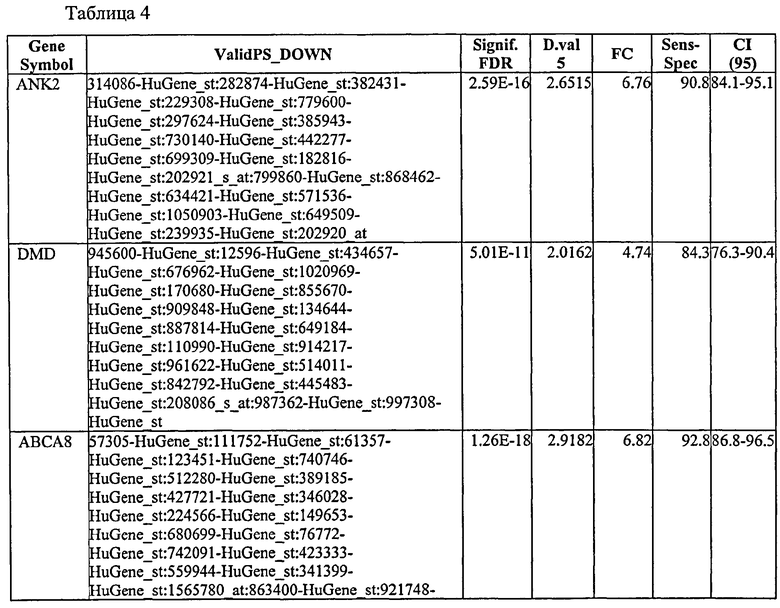
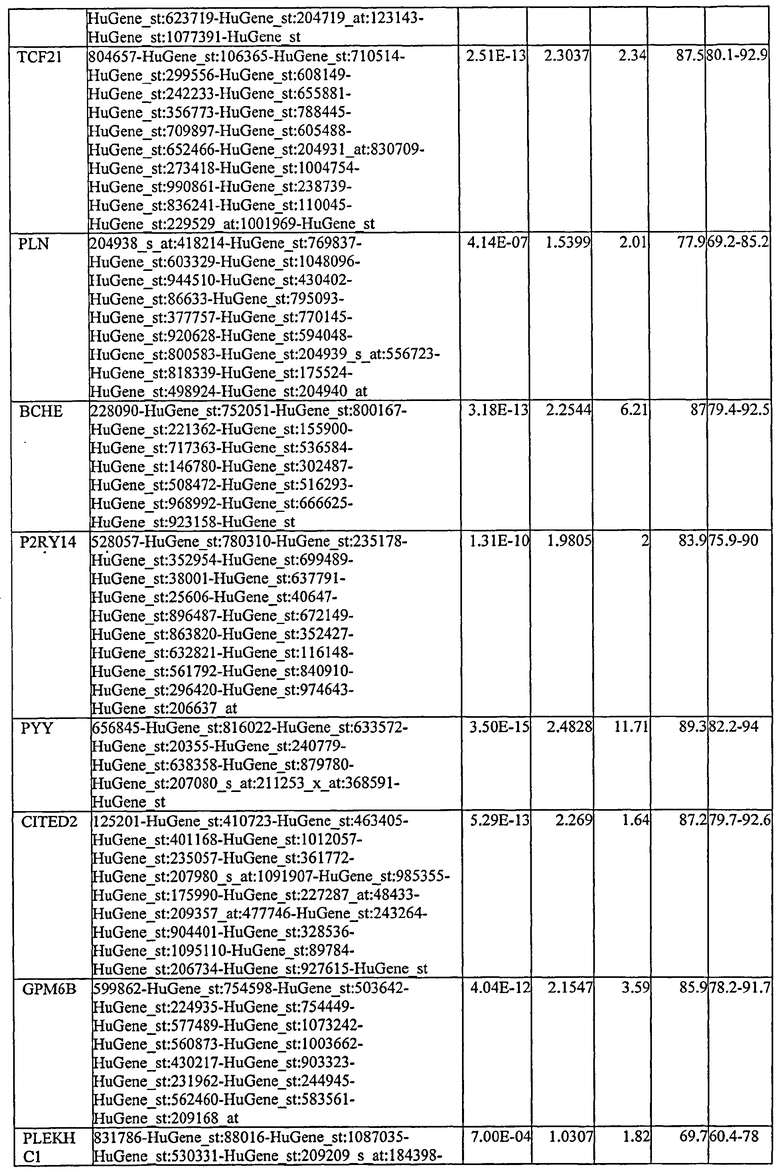
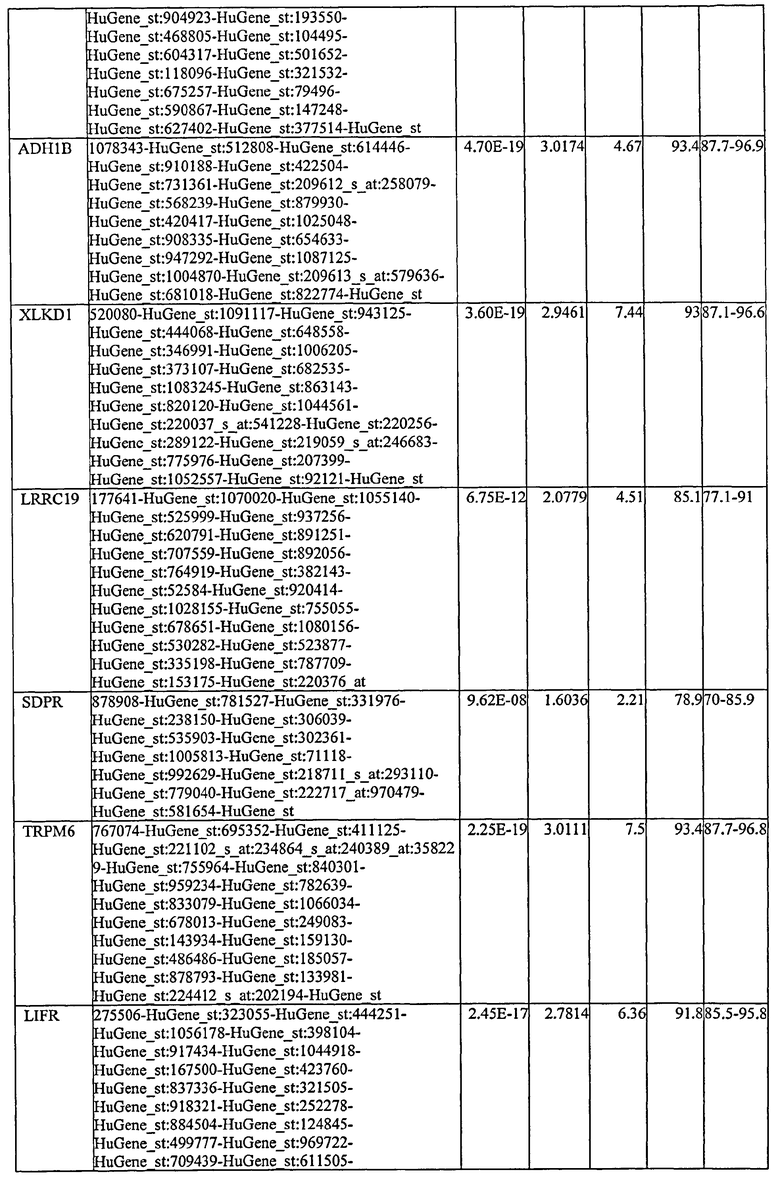
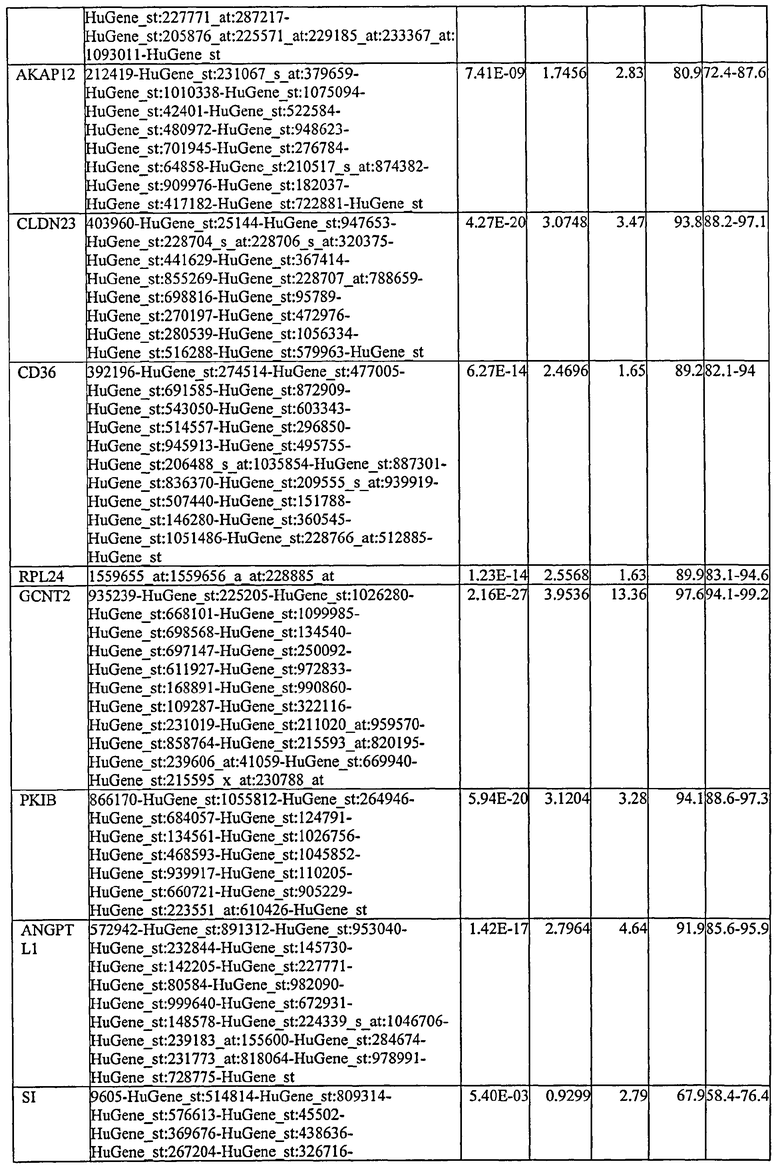
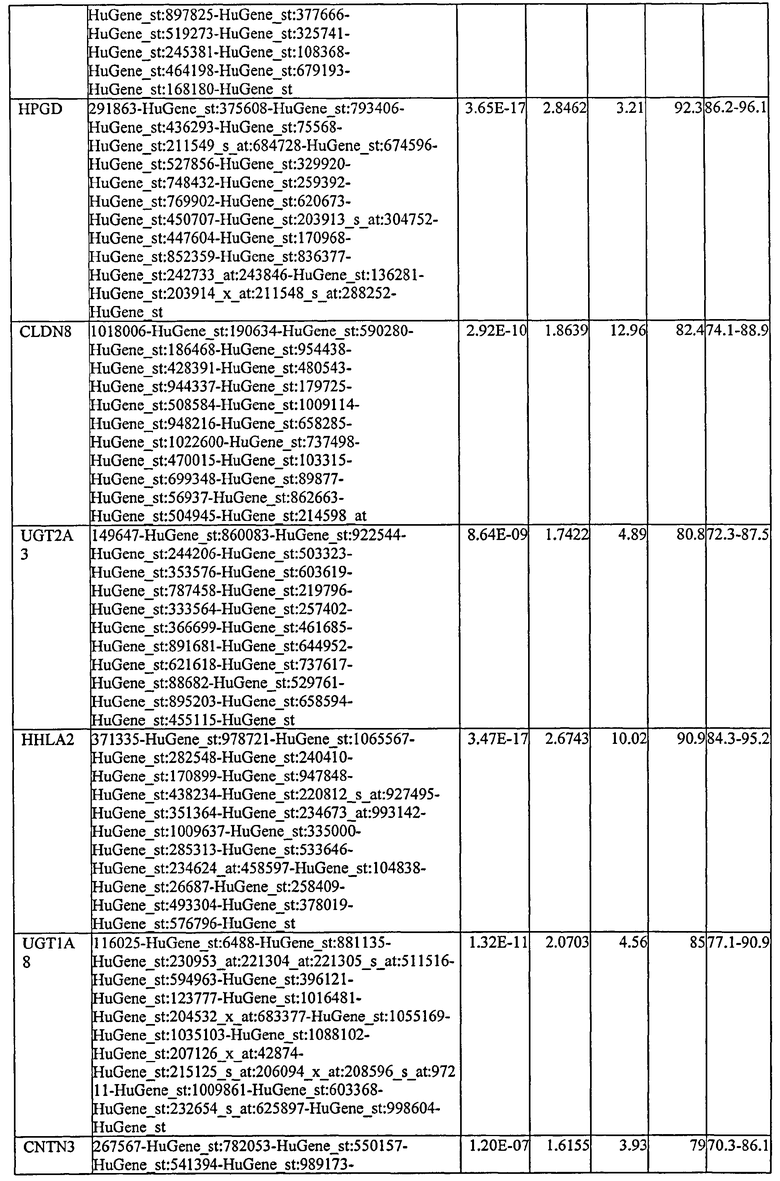

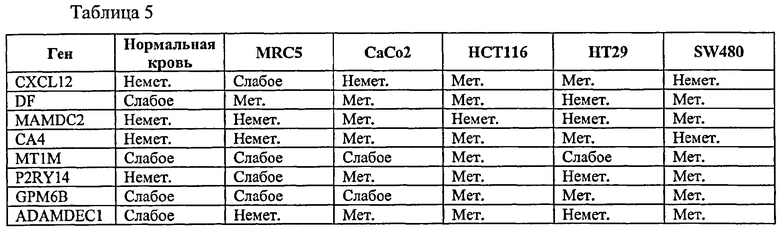
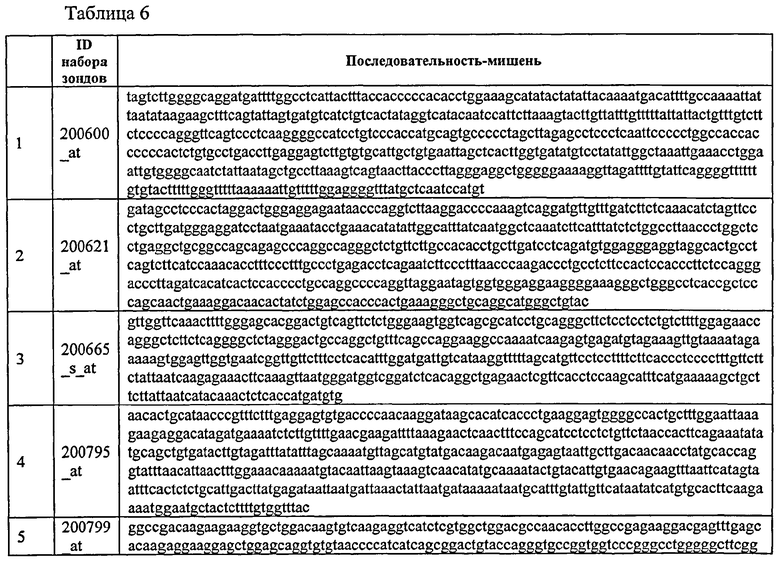



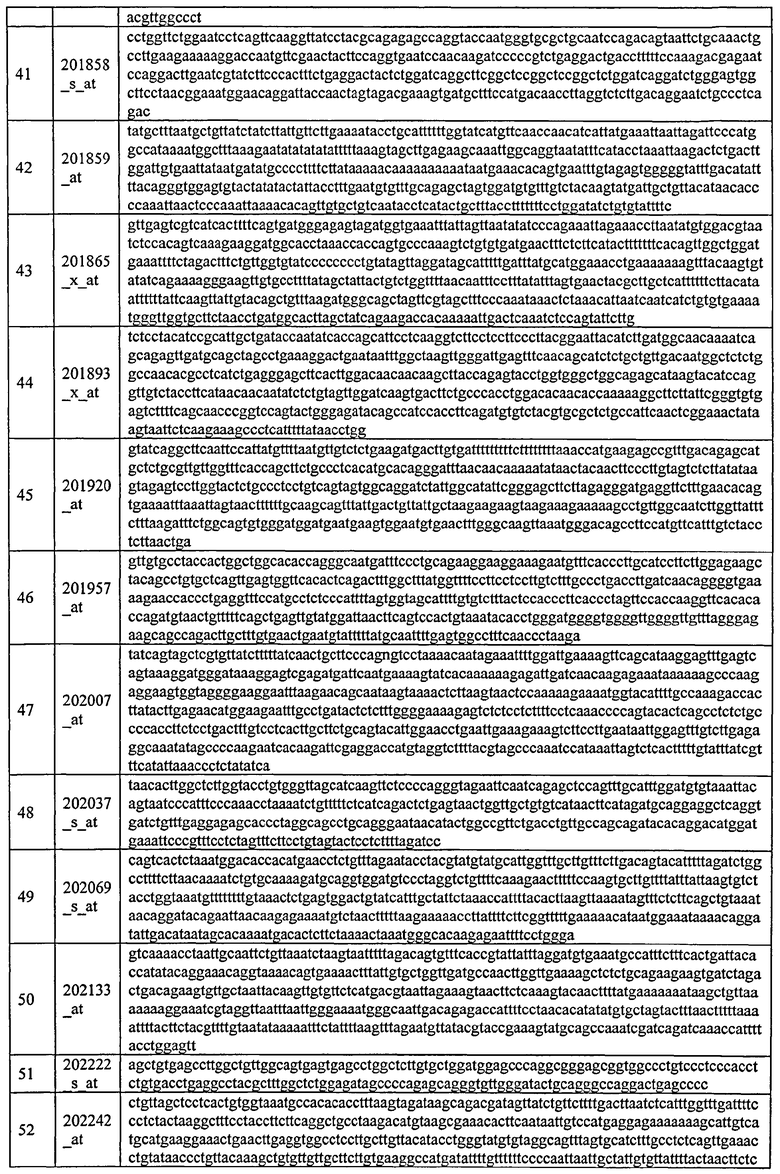


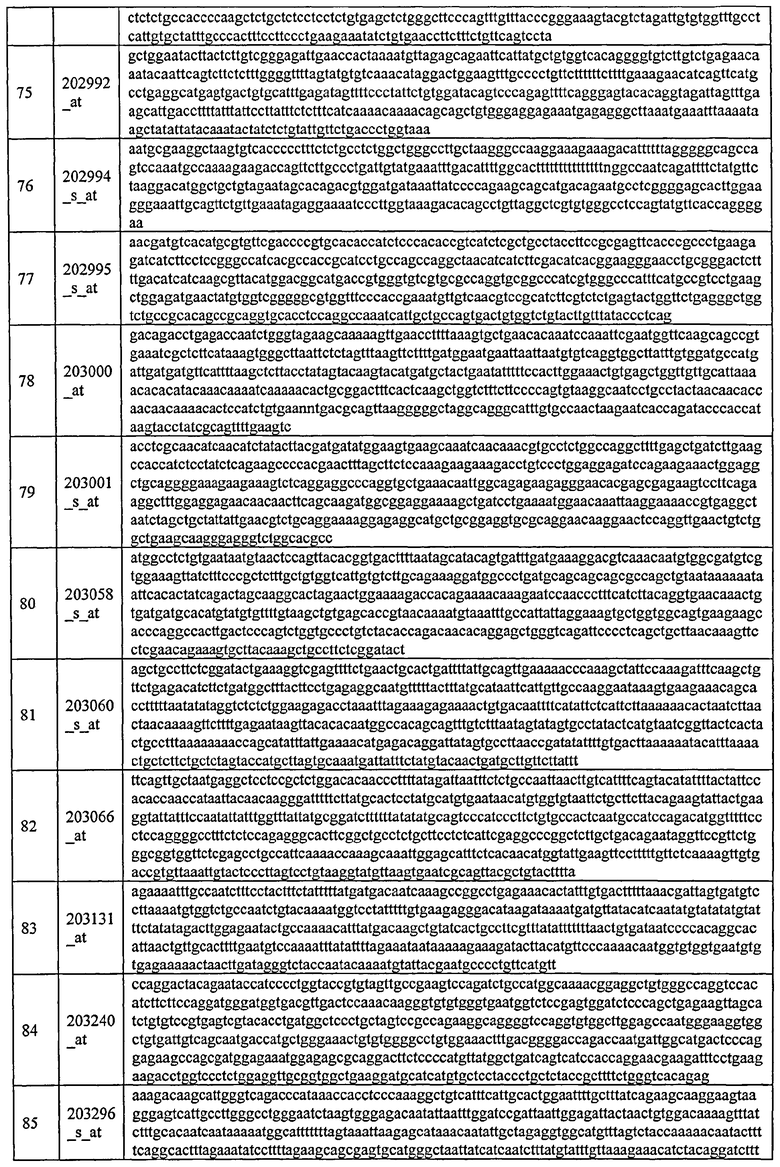
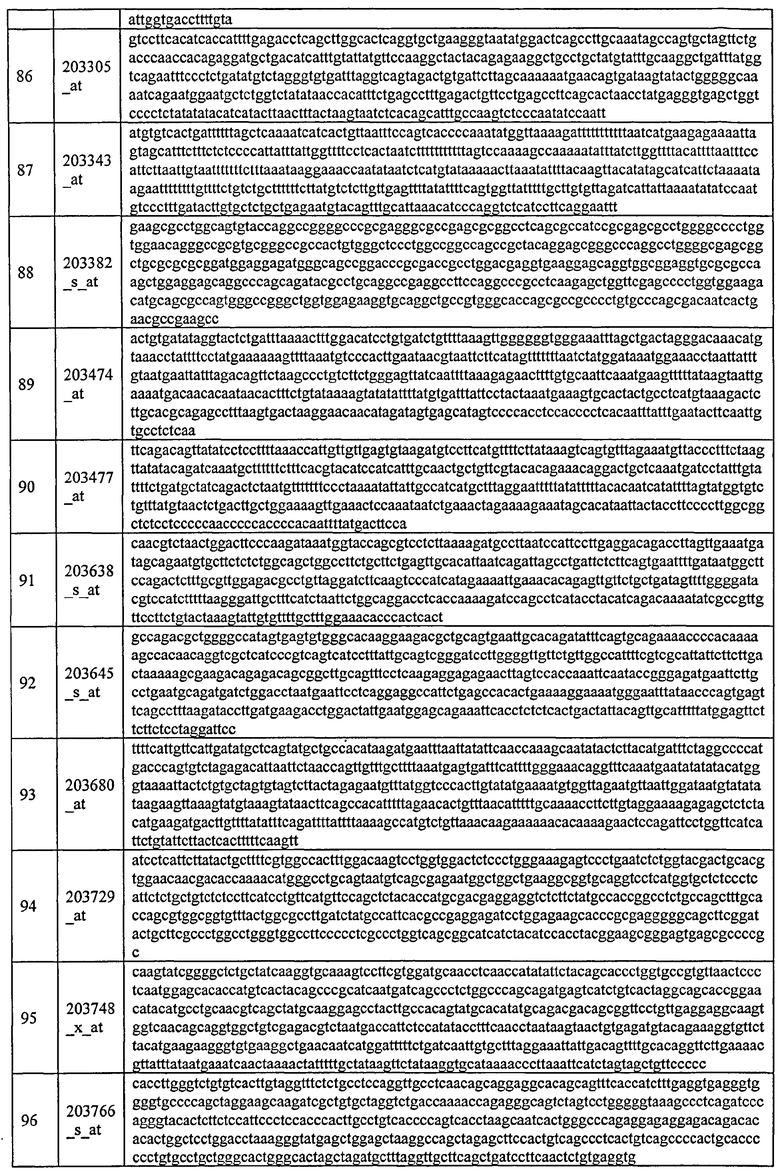


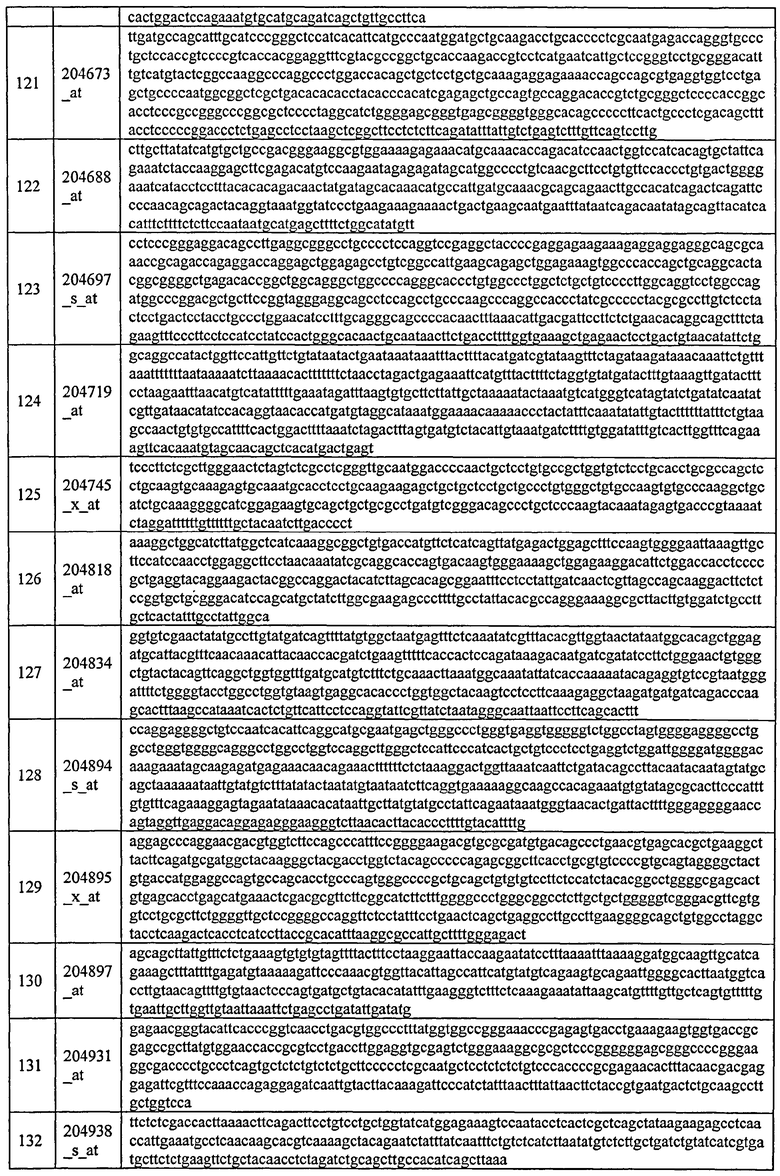
































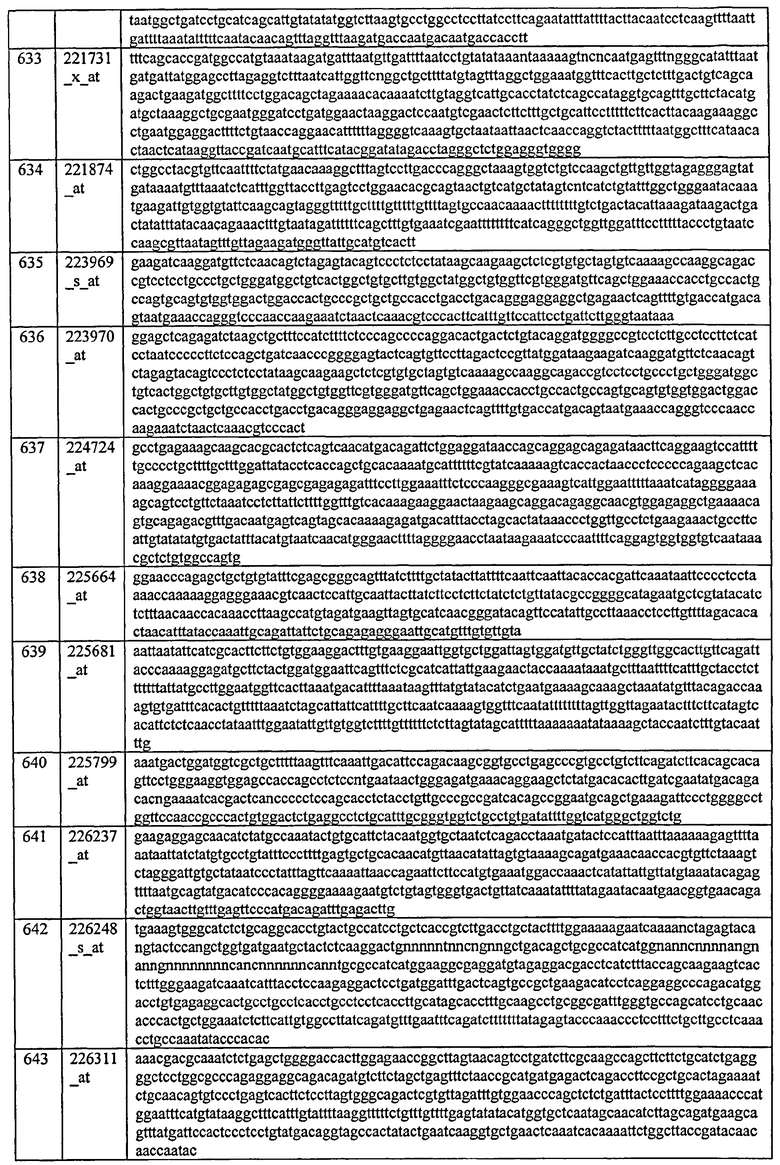


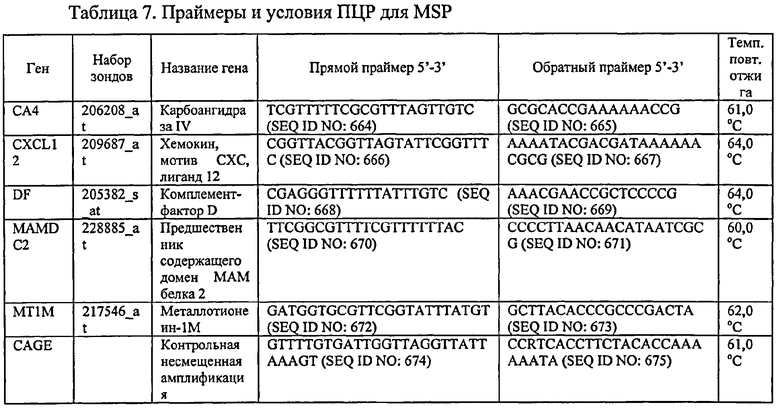






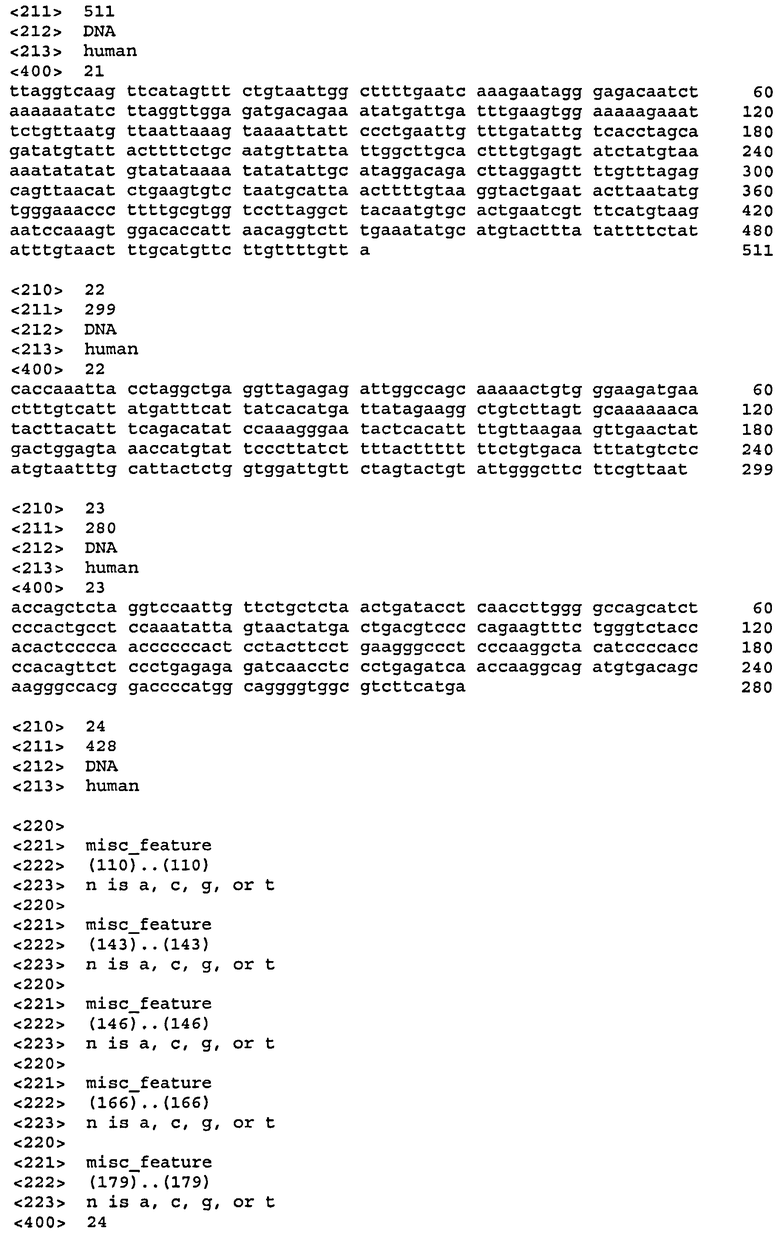









































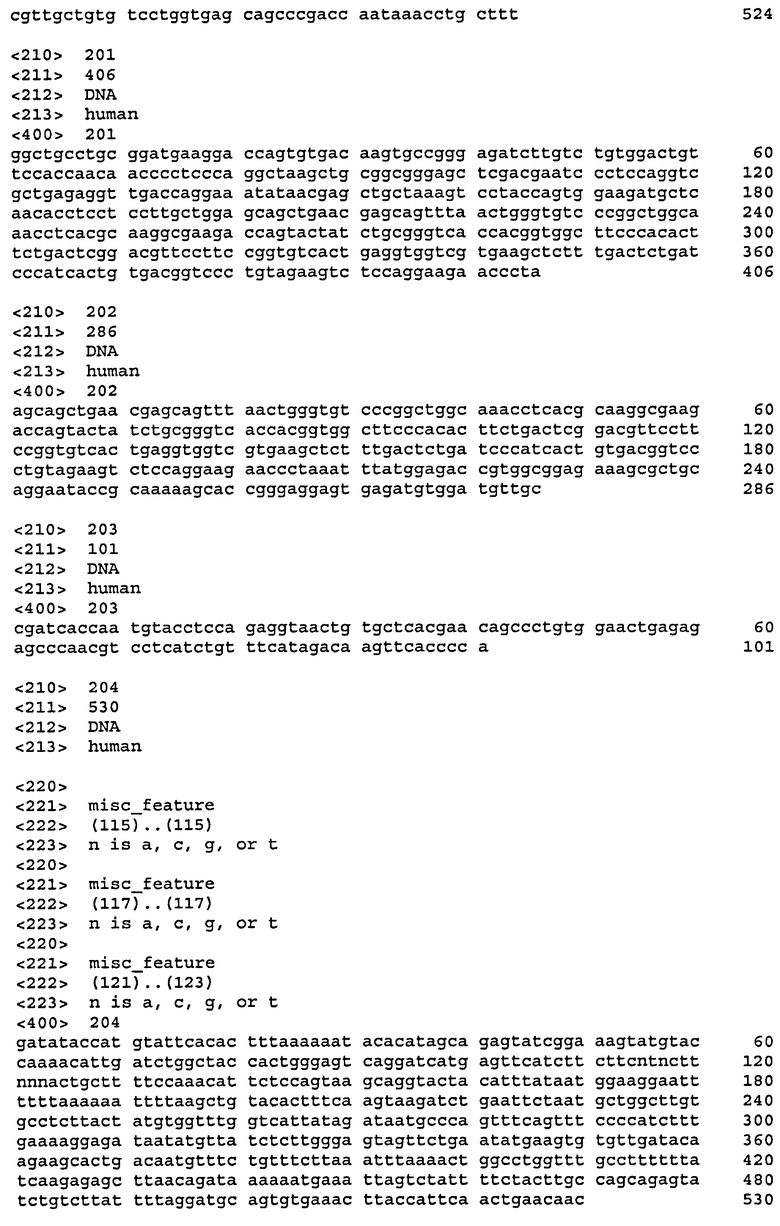






































































































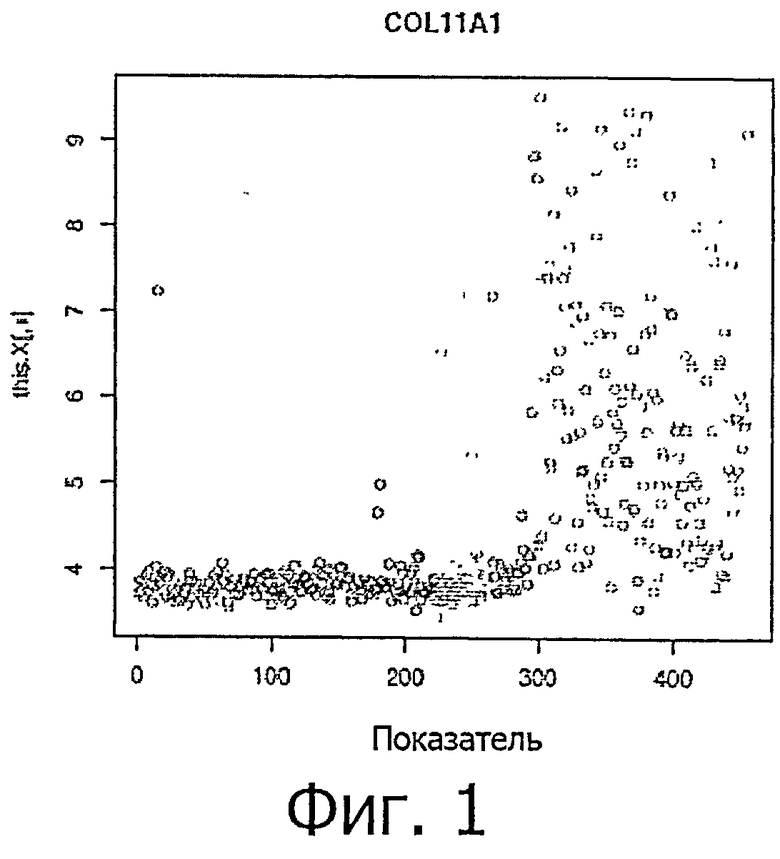
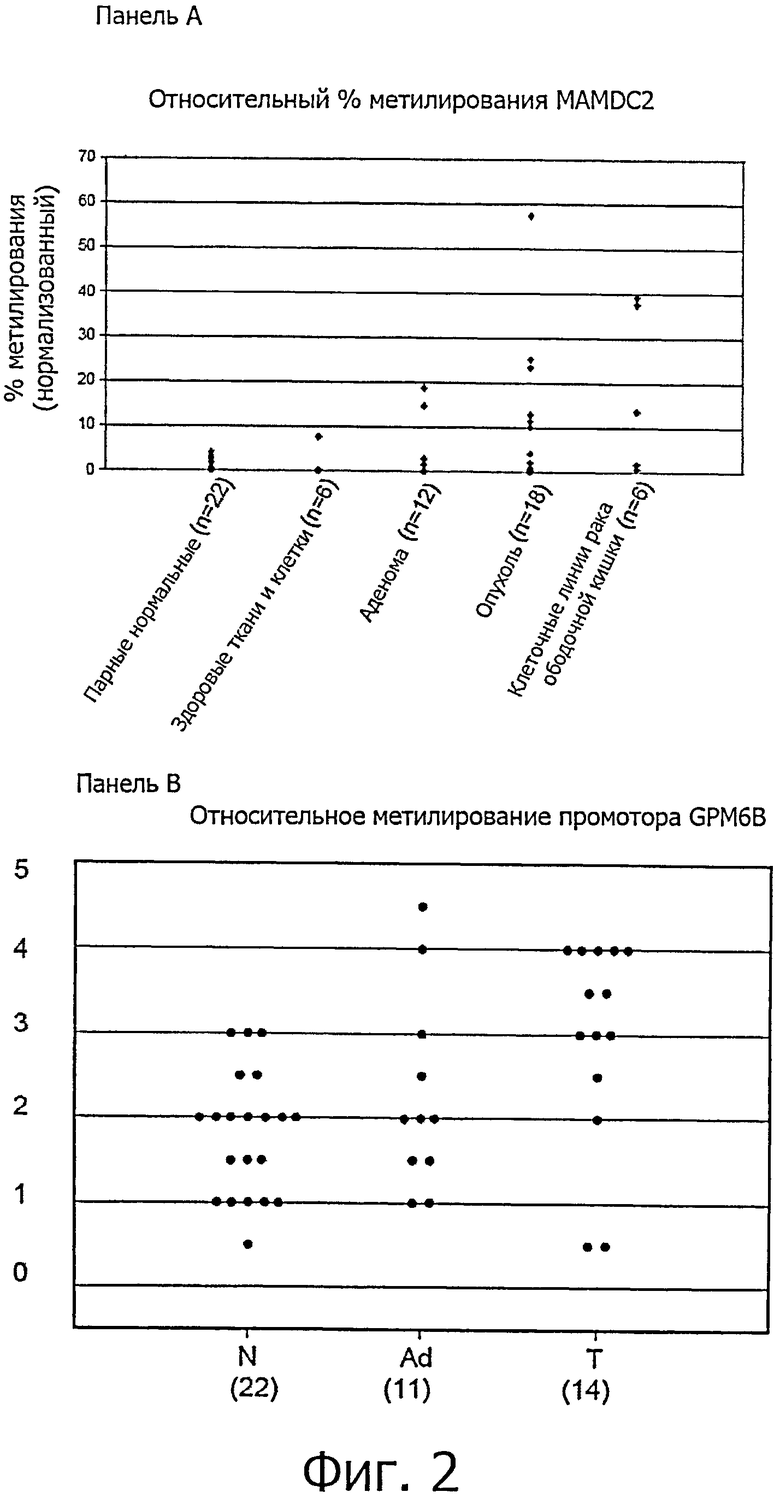
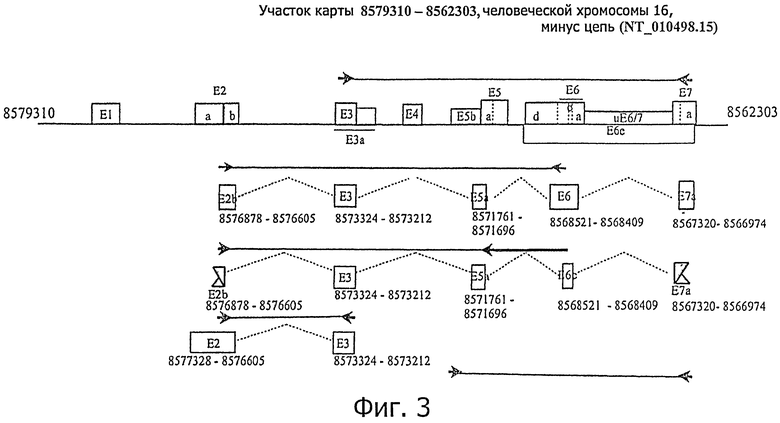
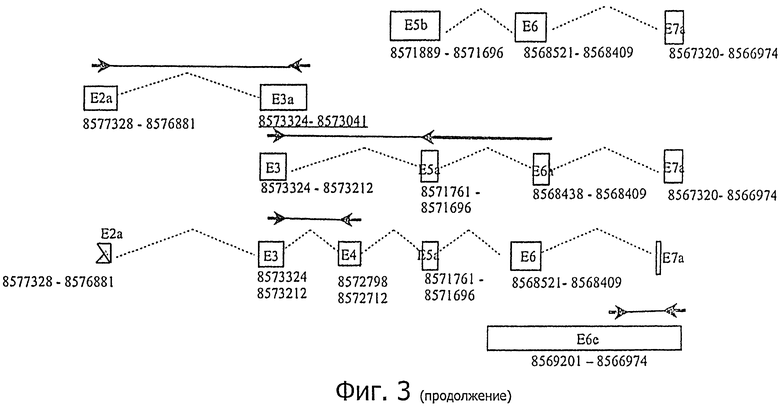
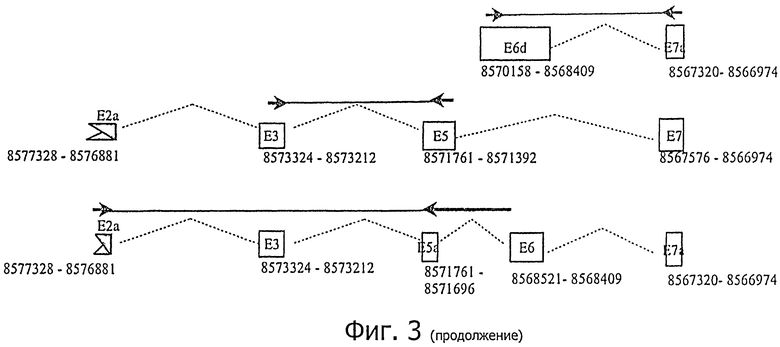
Изобретение относится к области биотехнологии. Предложен способ скрининга на появление, предрасположенность к появлению и/или развитие неоплазмы. Способ предусматривает скрининг в отношении модуляции ДНК или РНК или профиля экспрессии белка одного или нескольких маркеров молекул нуклеиновой кислоты. Изменения ДНК или РНК или профилей экспрессии белков являются показателями появления и/или развития неоплазмы толстой кишки, такой как аденома или аденокарцинома. Изобретение может быть использовано в медицине для диагностики или мониторинга колоректальных неоплазм, таких как колоректальные аденокарциномы. 2 н. и 11 з.п. ф-лы, 3 ил., 8 табл., 6 пр.
1. Способ скрининга на появление или предрасположенность к появлению неоплазмы толстой кишки у индивидуума, включающий оценку уровня экспрессии одного или более генов или транскриптов, выбранных из
(i) гена, генов или транскриптов, детектированных с помощью зонда или набора зондов, направленных на нуклеотидную последовательность:

(ii) SDC2
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
2. Способ мониторинга развития неоплазмы у индивидуума, включающий оценку уровня экспрессии одного или более генов или транскриптов, выбранных из:
(i) гена, генов или транскриптов, детектированных с помощью зонда или набора зондов, направленных на нуклеотидную последовательность:

(ii) SDC2
в биологическом образце от указанного индивидуума, где более низкий уровень экспрессии генов или транскриптов группы (i) и/или группы (ii) относительно контрольных уровней является показателем неопластической клетки толстой кишки или клетки, предрасположенной к появлению неопластического состояния.
3. Способ по п. 1, где указанная неопластическая клетка представляет собой аденому или аденокарциному.
4. Способ по п. 2, где указанная неопластическая клетка представляет собой аденому или аденокарциному.
5. Способ по п. 1, где указанный контрольный уровень представляет собой ненеопластический уровень.
6. Способ по п. 2, где указанный контрольный уровень представляет собой ненеопластический уровень.
7. Способ по п. 3, где указанный контрольный уровень представляет собой ненеопластический уровень.
8. Способ по п. 4, где указанный контрольный уровень представляет собой ненеопластический уровень
9. Способ по любому из пп. 1-8, где указанная клетка представляет собой колоректальную клетку.
10. Способ по любому из пп. 1-8, где указанный биологический образец представляет собой образец фекалий, промывного раствора после клизмы, операционного материала, биопсии ткани или крови.
11. Способ по любому из пп. 1-8, где указанный уровень экспрессии оценивают скринингом на отношения экспрессии мРНК, экспрессии белка, геномной ДНК или белков хроматина, с которыми указанный ген ассоциирован.
12. Способ по п. 11, где указанные изменения геномной ДНК представляют собой изменения метилирования ДНК.
13. Способ по любому из пп. 1-8, где указанный индивидуум представляет собой человека.
| WO 2005044990 A2, 19.05.2005 | |||
| УСТРОЙСТВО ДЛЯ ОФТАЛЬМОЛОГИЧЕСКИХ ОПЕРАЦИЙ | 1994 |
|
RU2068677C1 |
| WO 2005059160 A2, 30.06.2005 | |||
| СПОСОБ ОБНАРУЖЕНИЯ МЕТАСТАЗОВ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ В НЕБНЫХ МИНДАЛИНАХ | 2005 |
|
RU2293987C2 |
Авторы
Даты
2015-10-20—Публикация
2008-10-23—Подача