Область техники, к которой относится изобретение
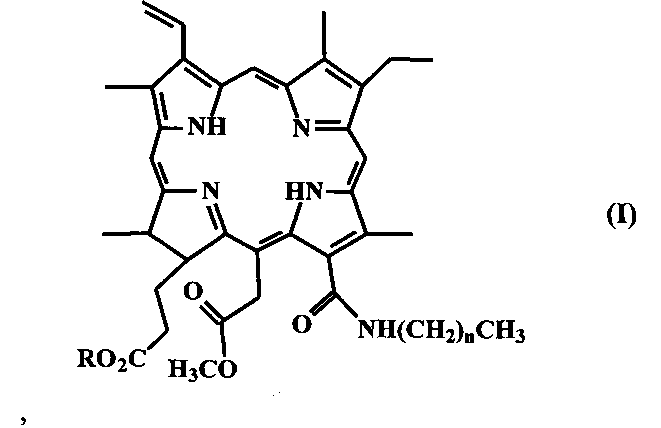
Изобретение относится к химии биологически активных соединений, а именно к способу получения группы производных хлорина e6 формулы (I):
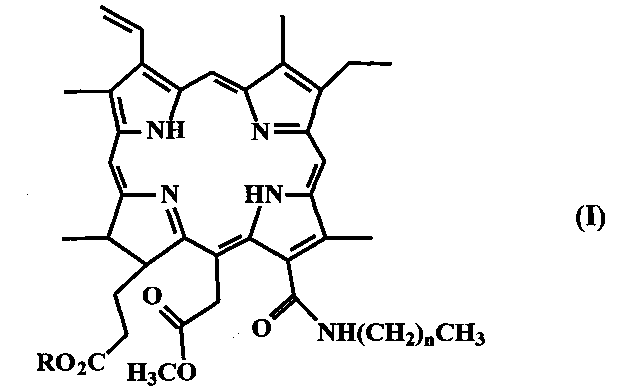
где n равно 3-11,
R представляет Н или CH3,
способных найти применение в качестве фотосенсибилизаторов (ФС) для фотодинамической терапии (ФДТ) рака и других новообразований.
Уровень техники
Известен способ получения производных хлорина e6, основанный на реакции феофорбида а формулы (II) с соответствующим амином, в результате которой происходит раскрытие экзоцикла феофорбида и образование соответствующего амида хлорина e6.
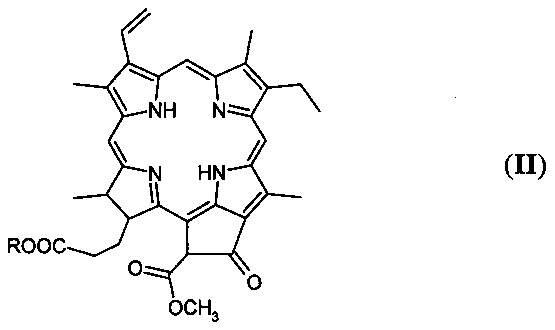
Так, например, в сообщении Dugin N.O., Zvialova M.G., Novokiv R.A., Timofeev V.P, Misharin A. Yu., Ponomarev G.V. «Facile Synthesis of 152-Carboxamides of MethylbPheophorbide a» (Macroheterocycles. Vol. 5. No. 2 (2012). Р. 146-148) описывается получение соединения общей формулы (I), где n принимает значение 15. Однако в данной статье раскрытие экзоциклического фрагмента проводилось на метиловом эфире феофорбида a (формула (II), где R=CH3), реакция протекала в тетрагидрофуране в течение длительного промежутка времени (от 14 до 72 часов), при этом данный продукт реакции охарактеризован как побочный.
Наиболее близким к описываемому способу аналогом является способ получения соединений формулы (III), где R представляет собой бутил, гексил и октил, описанный в публикации D.V. Belykh, E.A. Kopylov, I.V. Gruzdev, A.V. Kuchin «Opening of the Extra Ring in Pheophorbide a Methyl Ester by the Action of Amines as a One-Step Method for Introduction of Additional Fragments at the Periphery of Chlorin Macroring» (Russ. J. Org. Chem., 2010, Vol. 46, No. 4, Р. 584-592):
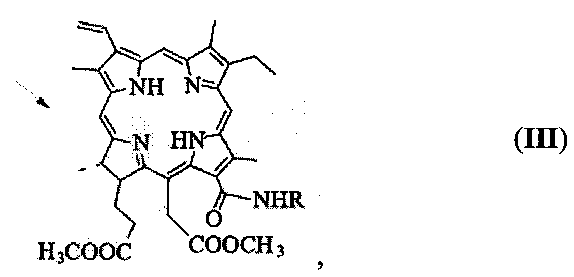
состоящий в перемешивании раствора 50 мг метилового эфира феофорбида а в смеси 0,5 мл первичного амина (бутил-, гексил- или октиламина) и 10 мл тетрагидрофурана при комнатной температуре в течение 24 часов, 10-кратном разбавлении реакционной смеси хлороформом с последующим прибавлением 1% раствора соляной кислоты для удаления избытка амина в виде соли, отделении органического слоя, промывании его водой до нейтрального значения pH с последующим высушиванием над сульфатом натрия, удалении хлороформа и хроматографировании на силикагеле с применением в качестве элюента смеси четыреххлористый углерод:ацетон (от 50:1 до 30:1). К недостаткам ближайшего аналога следует отнести длительность проведения реакции (до 24 часов) и выделение целевого продукта с невысоким выходом (около 30%).
Технический результат заявленного изобретения заключается в получении производных хлорина e6 формулы (I) с более высоким выходом за минимальное время для возможного применения полученных соединений в качестве ФС для ФДТ рака.
Раскрытие изобретения
В результате проведенных исследований авторы установили, что технический результат изобретения может быть достигнут созданием следующих объектов изобретения.
Первым объектом изобретения является способ получения соединений формулы (I)
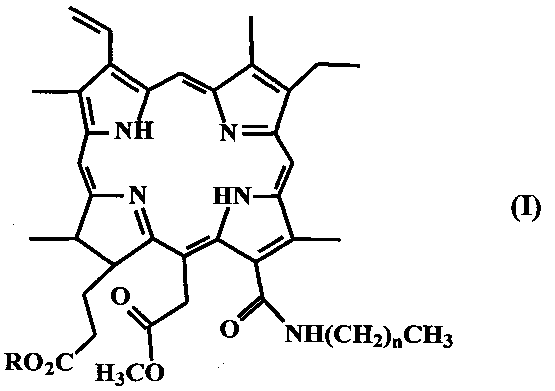
где n равно 3-11,
R представляет H или CH3,
заключающийся во взаимодействии феофорбида а или метилового эфира феофорбида а с первичным амином, при осуществлении которого:
а) феофорбид а или метиловый эфир феофорбида а, растворенный в органическом растворителе, выбранном из хлорированного алифатического углеводорода, обрабатывают 10-50-кратным по молям количеством (С4-С12)алкиламина при температуре 20-40°C до полного превращения исходного феофорбида а или метилового эфира феофорбида а;
б) полученную реакционную смесь объединяют с 1-3% водным раствором сильной фармацевтически приемлемой кислоты с образованием соли избыточного (С4-С12)алкиламина, которая переходит в водную фазу, которую отделяют;
в) органическую фазу промывают водой или водным раствором хлорида натрия, необязательно с добавлением гидрокарбоната натрия до нейтральной реакции промывных вод, осушают и хроматографируют в градиенте хлороформ:алифатический спирт, с получением раствора соединения формулы (I);
г) раствор соединения формулы (I) выпаривают при пониженном давлении, полученный твердый продукт, содержащий соединение формулы (I), подвергают очистке перекристаллизацией из смеси растворителей, выбранной из смеси хлороформ/петролейный эфир и ацетон/гептан, отфильтровывают и высушивают.
Предпочтительно в предлагаемом способе на стадии а) хлорированный алифатический углеводород выбран из группы, состоящей из хлороформа, хлористого метилена и дихлорэтана.
Также предпочтительно на стадии а) молярная концентрация феофорбида а или метилового эфира феофорбида а составляет не менее 50 ммоль/л.
Кроме того, предпочтительно на стадии в) алифатический спирт выбран из группы, состоящей из метанола, этанола, н-пропанола и изопропанола, и градиент хлороформ: алифатический спирт составляет от 400:1 до 30:1.
Далее предпочтительно феофорбид а или метиловый эфир феофорбида а обрабатывают 30-50-кратным количеством (С4-С12)алкиламина при температуре 35-40°C в хлороформе.
Другим объектом изобретения является способ получения соединений формулы (I),
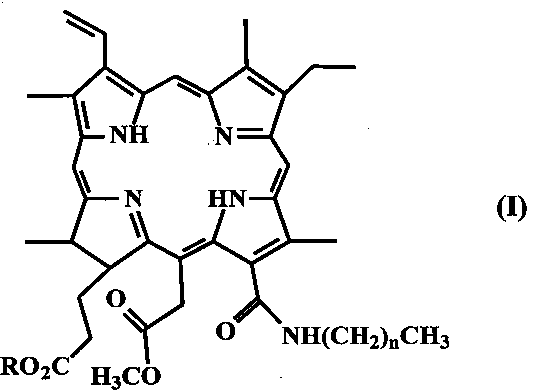
где n равно 3-11,
R представляет Н или СН3,
заключающийся во взаимодействии феофорбида а или метилового эфира феофорбида а с первичным амином, при осуществлении которого:
а) феофорбид а или метиловый эфир феофорбида а, растворенный в органическом растворителе, выбранном из хлорированного алифатического углеводорода, обрабатывают 10-20-кратным количеством (С4-С12)алкиламина при температуре 20-40°C в присутствии соединения, ускоряющего реакцию, выбранного из группы, состоящей из диметилформамида (ДМФА), триэтиламина, метилдиэтиламина и метил(ди-изопропил)амина до полного превращения исходного феофорбида а или метилового эфира феофорбида а;
б) полученную реакционную смесь объединяют с 1-3% водным раствором сильной физиологически приемлемой кислоты с образованием соли избыточного (С4-С12)алкиламина, которая переходит в водную фазу, которую отделяют;
в) органическую фазу промывают водой или водным раствором хлорида натрия, необязательно с добавлением гидрокарбоната щелочного металла до нейтральной реакции промывных вод, осушают и хроматографируют в градиенте хлороформ:алифатический спирт, с получением раствора соединения формулы (I);
г) раствор соединения формулы (I) выпаривают при пониженном давлении, полученный твердый продукт, содержащий соединение формулы (I), подвергают очистке перекристаллизацией из смеси растворителей, выбранной из смеси хлороформ/петролейный эфир и ацетон/гептан, отфильтровывают и высушивают.
Предпочтительно в другом предлагаемом способе на стадии а) хлорированный алифатический углеводород выбран из группы, состоящей из хлороформа, хлористого метилена и дихлорэтана, а кислота является хлористоводородной кислотой.
Также предпочтительно на стадии а) молярная концентрация феофорбида а или метилового эфира феофорбида а составляет не менее 50 ммоль/л.
Кроме того, предпочтительно при использовании на стадии а) ДМФА в качестве ускоряющего реакцию соединения он является сорастворителем и его содержание составляет не более 50 об.%.
Кроме того, также предпочтительно в качестве соединения, ускоряющего реакцию, применяют триэтиламин.
Дале предпочтительно на стадии в) алифатический спирт выбран из группы, состоящей из метанола, этанола, н-пропанола и изопропанола, и градиент хлороформ: алифатический спирт составляет от 400:1 до 30:1.
Осуществление изобретения
Достижение технического результата изобретения будет далее подтверждено примерами его предпочтительного осуществления.
Примеры 1-15. Получение соединений формулы (I)
Для получения соединений формулы (I) используют доступный в продаже феофорбид а (CAS RN 15664-29-6, Chemleader Biomedical Co. Ltd.).
Феофорбид а также можно получить из биомассы микроводоросли Spirulina platensis. Для этого из биомассы экстракцией слабощелочной водно-этанольной смесью удаляют примеси, после чего проводят деструкцию клеточных систем глубоким охлаждением жидким азотом, и затем биомассу повторно экстрагируют спиртсодержащим экстрагентом, удаляют магний из координационной сферы хлоринового макроцикла обработкой соляной кислотой и отделяют образующийся осадок феофитина а. Дальнейшие стадии (кислотный гидролиз и др.), приводящие к феофорбиду а или соединению формулы (II), где R=СН3, известны специалисту в данной области техники.
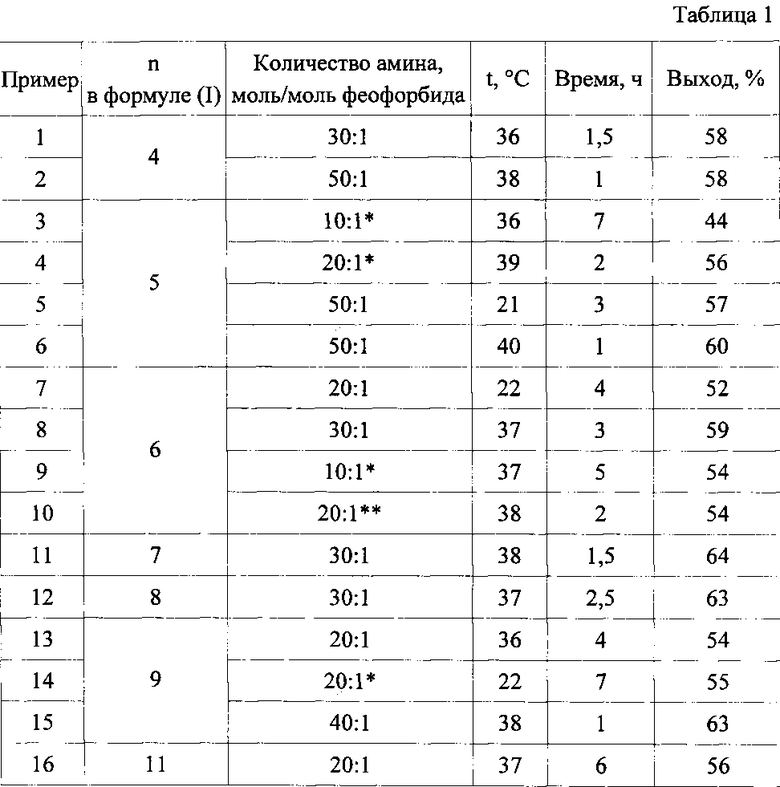
Реакцию размыкания экзоцикла феофорбида а под действием первичных неразветвленных алифатических аминов проводят в инертной атмосфере в темноте при температуре в интервале 20-40°C, для чего растворяют феофорбида а с получением раствора с концентрацией феофорбида а не менее 50 ммоль/л и при перемешивании в токе инертного газа, например аргона, добавляют 10-50 мольный избыток соответствующего первичного амина. В таблице 1 символом «*» обозначено использование ДМФА в качестве сорастворителя и ускоряющего реакцию соединения. Символами «**» обозначено добавление триэтиламина (Et3N) в количестве 5-10 моль/моль феофорбида а в качестве соединения, ускоряющего реакцию.
После завершения реакции реакционную смесь промывают разбавленным раствором хлористоводородной кислоты для удаления из смеси непрорегировавшего амина, экстрагируют хлороформом и промывают водой до нейтральной реакции среды, сушат и очищают методом колоночной хроматографии. Переосаждают из смеси ацетон-гексан или хлороформ-петролейный эфир.
Температурные режимы, избыток используемого амина, продолжительность реакции и выходы очищенных продуктов приведены в таблице 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФОТОСЕНСИБИЛИЗАТОРОВ НА ОСНОВЕ ЦИКЛОИМИДОВ ХЛОРИНА Р6 | 2016 |
|
RU2626234C1 |
| ПРОИЗВОДНЫЕ ХЛОРПИРИДИЛКАРБОНИЛА И ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ И СРЕДСТВО ДЛЯ БОРЬБЫ С ФИТОПАТОГЕННЫМИ ГРИБАМИ | 1996 |
|
RU2172314C2 |
| СПОСОБ ПОЛУЧЕНИЯ АМФИФИЛЬНЫХ СОЕДИНЕНИЙ ИМИДАЗОЛИНИЯ | 2016 |
|
RU2753541C2 |
| Способ получения производных морфина | 1978 |
|
SU856381A3 |
| СОЕДИНЕНИЕ ЦИКЛИЧЕСКОГО АМИНА | 2005 |
|
RU2379307C2 |
| СПОСОБ ПОЛУЧЕНИЯ (S)-3-[(1-ДИМЕТИЛАМИНО)ЭТИЛ]-ФЕНИЛ-N-ЭТИЛ-N-МЕТИЛ-КАРБАМАТА | 2005 |
|
RU2393148C2 |
| МЕТИЛОВЫЙ ЭФИР 4-ЙОД-2-[N-(N-АЛКИЛАМИНОКАРБОНИЛ)АМИНОСУЛЬФОНИЛ]-БЕНЗОЙНОЙ КИСЛОТЫ, ЕГО ПРОИЗВОДНЫЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1997 |
|
RU2309948C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕВОТИРОКСИНА И ЕГО СОЛЕЙ | 2015 |
|
RU2673540C2 |
| ЭКСТРАГЕНТ НА ОСНОВЕ ЧАСТИЧНО ФТОРИРОВАННОГО ТРИАЛКИЛАМИНА И СПОСОБ ИЗВЛЕЧЕНИЯ МЕТАЛЛОВ И КИСЛОТ ИЗ ВОДНО-СОЛЕВЫХ РАСТВОРОВ | 2017 |
|
RU2674371C1 |
| СПОСОБ ПОЛУЧЕНИЯ 5-(АЛЬФА-ГАЛОГЕНАЦЕТИЛ)-8-(ЗАМЕЩЕННЫЙ ОКСИ)-(1Н)-ХИНОЛИН-2-ОНОВ | 2004 |
|
RU2339621C2 |
Изобретение относится к вариантам способа получения соединений формулы (I) взаимодействием феофорбида а или метилового эфира феофорбида а с первичным амином. При этом феофорбид а или метиловый эфир феофорбида а, растворенный в органическом растворителе, выбранном из хлорированного алифатического углеводорода, обрабатывают 10-50-кратным по молям количеством (С4-С12)алкиламина при температуре 20-40°C до полного превращения исходного феофорбида а или метилового эфира феофорбида а; полученную реакционную смесь объединяют с 1-3% водным раствором сильной фармацевтически приемлемой кислоты с образованием соли избыточного (С4-С12)алкиламина, которая переходит в водную фазу, которую отделяют; органическую фазу промывают водой или водным раствором хлорида натрия, необязательно с добавлением гидрокарбоната натрия до нейтральной реакции промывных вод, осушают и хроматографируют в градиенте хлороформ : алифатический спирт, с получением раствора соединения формулы (I); раствор соединения формулы (I) выпаривают при пониженном давлении, полученный твердый продукт, содержащий соединение формулы (I), подвергают очистке перекристаллизацией из смеси растворителей, выбранной из смеси хлороформ/петролейный эфир и ацетон/гептан, отфильтровывают и высушивают. В формуле (I) n равно 3-11, R представляет Н или CH3. Способ позволяет получать продукт с высоким выходом за минимальное время. 2 н. и 9 з.п. ф-лы, 1 табл.
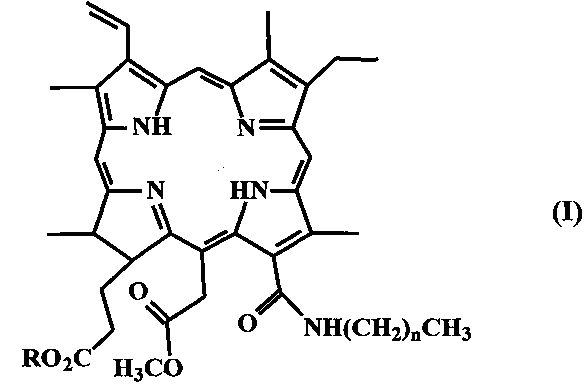
1. Способ получения соединений формулы (I)
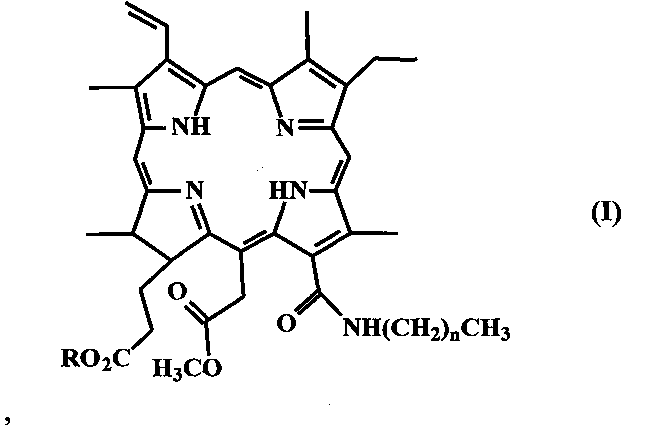
где n равно 3-11,
R представляет Н или CH3,
заключающийся во взаимодействии феофорбида а или метилового эфира феофорбида а с первичным амином, отличающийся тем, что:
а) феофорбид а или метиловый эфир феофорбида а, растворенный в органическом растворителе, выбранном из хлорированного алифатического углеводорода, обрабатывают 10-50-кратным по молям количеством (С4-С12)алкиламина при температуре 20-40°C до полного превращения исходного феофорбида а или метилового эфира феофорбида а;
б) полученную реакционную смесь объединяют с 1-3% водным раствором сильной фармацевтически приемлемой кислоты с образованием соли избыточного (С4-С12)алкиламина, которая переходит в водную фазу, которую отделяют;
в) органическую фазу промывают водой или водным раствором хлорида натрия, необязательно с добавлением гидрокарбоната натрия до нейтральной реакции промывных вод, осушают и хроматографируют в градиенте хлороформ : алифатический спирт, с получением раствора соединения формулы (I);
г) раствор соединения формулы (I) выпаривают при пониженном давлении, полученный твердый продукт, содержащий соединение формулы (I), подвергают очистке перекристаллизацией из смеси растворителей, выбранной из смеси хлороформ/петролейный эфир и ацетон/гептан, отфильтровывают и высушивают.
2. Способ по п. 1, отличающийся тем, что на стадии а) хлорированный алифатический углеводород выбран из группы, состоящей из хлороформа, хлористого метилена и дихлорэтана.
3. Способ по п. 1 или 2, отличающийся тем, что на стадии а) молярная концентрация феофорбида а или метилового эфира феофорбида а составляет не менее 50 ммоль/л.
4. Способ по п. 1 или 2, отличающийся тем, что на стадии в) алифатический спирт выбран из группы, состоящей из метанола, этанола, н-пропанола и изопропанола, и градиент хлороформ : алифатический спирт составляет от 400:1 до 30:1.
5. Способ по п. 1 или 2, отличающийся тем, что феофорбид а или метиловый эфир феофорбида а обрабатывают 30-50-кратным количеством (С4-С12) алкиламина при температуре 35-40°C в хлороформе.
6. Способ получения соединений формулы (I),
где n равно 3-11,
R представляет Н или СН3,
заключающийся во взаимодействии феофорбида а или метилового эфира феофорбида а с первичным амином, отличающийся тем, что
а) феофорбид а или метиловый эфир феофорбида а, растворенный в органическом растворителе, выбранном из хлорированного алифатического углеводорода, обрабатывают 10-20-кратным количеством (С4-С12)алкиламина при температуре 20-40°C в присутствии соединения, ускоряющего реакцию, выбранного из группы, состоящей из диметилформамида (ДМФА), триэтиламина, метилдиэтиламина и метил(ди-изопропил)амина до полного превращения исходного феофорбида а или метилового эфира феофорбида а;
б) полученную реакционную смесь объединяют с 1-3% водным раствором сильной физиологически приемлемой кислоты с образованием соли избыточного (С4-С12)алкиламина, которая переходит в водную фазу, которую отделяют;
в) органическую фазу промывают водой или водным раствором хлорида натрия, необязательно с добавлением гидрокарбоната щелочного металла до нейтральной реакции промывных вод, осушают и хроматографируют в градиенте хлороформ: алифатический спирт, с получением раствора соединения формулы (I);
г) раствор соединения формулы (I) выпаривают при пониженном давлении, полученный твердый продукт, содержащий соединение формулы (I), подвергают очистке перекристаллизацией из смеси растворителей, выбранной из смеси хлороформ/петролейный эфир и ацетон/гептан, отфильтровывают и высушивают.
7. Способ по п. 6, отличающийся тем, что на стадии а) хлорированный алифатический углеводород выбран из группы, состоящей из хлороформа, хлористого метилена и дихлорэтана, а кислота является хлористоводородной кислотой.
8. Способ по п. 6 или 7, отличающийся тем, что на стадии а) молярная концентрация феофорбида а или метилового эфира феофорбида а составляет не менее 50 ммоль/л.
9. Способ по п. 6 или 7, отличающийся тем, что при использовании на стадии а) ДМФА в качестве ускоряющего реакцию соединения он является сорастворителем и его содержание составляет не более 50 об.%.
10. Способ по п. 6 или 7, отличающийся тем, что в качестве соединения, ускоряющего реакцию, применяют триэтиламин.
11. Способ по п. 6 или 7, отличающийся тем, что на стадии в) алифатический спирт выбран из группы, состоящей из метанола, этанола, н-пропанола и изопропанола, и градиент хлороформ : алифатический спирт составляет от 400:1 до 30:1.
| D.V | |||
| BELYKH ET AL., Opening of the extra ring in pheophorbide alpha methyl ester by the action of amines as a one-step method for introduction of additional fragments at the periphery of chlorin macroring, Russian Journal of Organic Chemistry, 2010, vol.46(4), p.577-585 | |||
| WO2002098882 A1, 12.12.2002 | |||
| СПОСОБ СИНТЕЗА ДИ- И ТРИАМИНОХЛОРИНОВ | 2006 |
|
RU2304583C1 |
| N | |||
| O | |||
| DUGIN ET AL., | |||
Авторы
Даты
2015-10-20—Публикация
2014-06-10—Подача