Настоящее изобретение относится к способу получения 5-замещенных-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-аминов.
В патенте США 6005108 описаны некоторые замещенные 5,8-дизамещенные-[1,2,4]триазоло[1,5-с]пиримидин-2-аминные соединения и их применение в качестве промежуточных соединений для получения сульфонамидных гербицидов. 5,8-Диметокси[1,2,4]триазоло[1,5-с]пиримидин-2-амин является полезным промежуточным соединением для получения пеноксулама. В Monatsh. Chem. 1983, 114, 789 описано получение некоторых (амино)карбонотиоилкарбаматов с последующим их взаимодействием с гидроксиламином и последующей циклизацией в [1,2,4]триазоло[1,5-а]пиримидин-2-амины. В WO 2009/047514 A1 описано получение некоторых (амино)карбонотиоилкарбаматов с последующим их взаимодействием с гидроксиламином и последующей циклизацией в [1,2,4]триазоло[1,5-а]пиридиновые и [1,2,4]триазоло[1,5-с]пиримидиновые соединения. В US 6559101 В2 описано получение некоторых (амино)карбонотиоилкарбаматов с последующим их взаимодействием с гидроксиламином и последующей циклизацией в пиримидинзамещенные [1,2,4]триазоло[1,5-а] пиримидин-2-амины.
5,8-Диметокси[1,2,4]триазоло[1,5-с]пиримидин-2-амин получают из 2,4-дихлор-5-метоксипиримидина в многостадийном способе, который включает как гидразин, так и циангалогенид. Гидразин представляет серьезную опасность взрыва и является токсичным при проглатывании, вдыхании и адсорбции кожей. Он классифицируется как канцероген и имеет TLV 0,1 ч./млн в воздухе. Циангалогениды являются сильными раздражителями и очень ядовиты. Было бы выгодно получать 5-замещенные-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амины эффективно и с высоким выходом в производственном процессе, который позволит избежать использования гидразина и циангалогенида.
Настоящее изобретение относится к получению 5-замещенных-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-аминов из 2-замещенных-4-амино-5-метоксипиримидинов. Более конкретно, настоящее изобретение относится к способу получения 5-замещенных-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-аминов формулы (I):
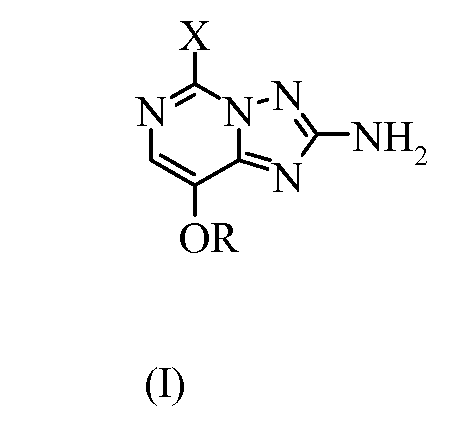
где
X представляет собой галоген или OR; и
R представляет собой C1-С4алкил;
который включает:
i) взаимодействие 2-замещенного-4-амино-5-алкоксипиримидина формулы:
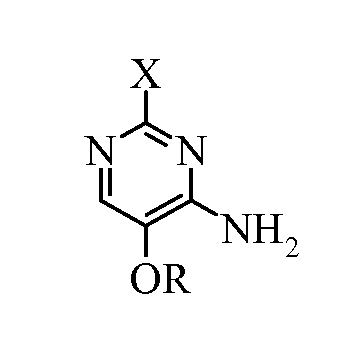
где X и R являются такими, как определено выше,
с изотиоцианатидокарбонатом формулы:
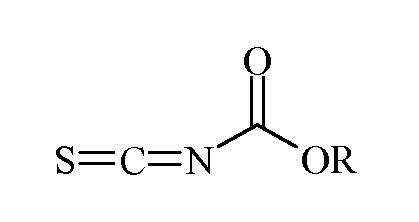
где R является таким, как определено выше,
в полярном апротонном растворителе с получением (пиримидиниламино)карбонотиоилкарбамата формулы:
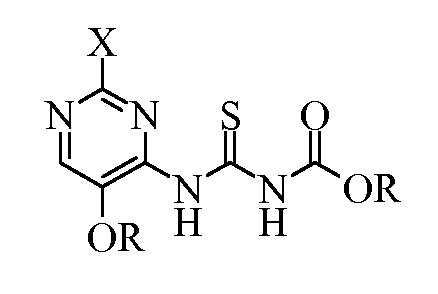
где X и R являются такими, как определено выше;
ii) приведение в контакт (пиримидиниламино)карбонотиоилкарбамата с гидроксиламином в присутствии основания с получением (пиримидиниламино)(гидроксиимино)метилкарбамата формулы:
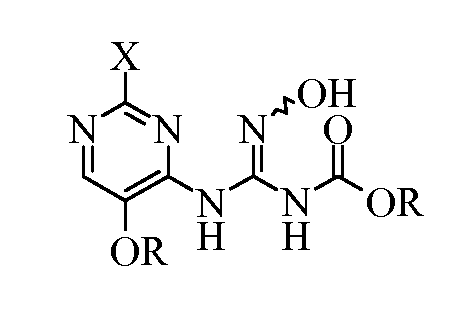
где X и R являются такими, как определено выше; и
iii) циклизацию (пиримидиниламино)(гидроксиимино)метилкарбамата нагреванием в инертном растворителе с получением 5-замещенного-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина.
В другом варианте осуществления изобретения 5-галоген-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амины могут быть преобразованы в соответствующие 5,8-диалкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амины заменой галогена алкоксидом щелочного металла в спиртовом растворителе.
Другой вариант осуществления изобретения включает (пиримидиниламино)карбонотиоилкарбамат формулы:
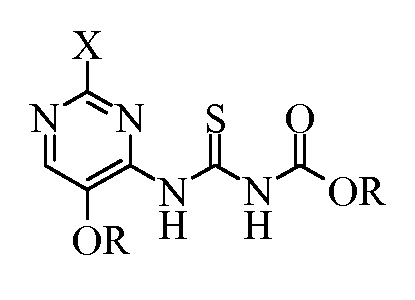
где
X представляет собой галоген или OR; и
R представляет собой C1-С4алкил.
Еще один вариант осуществления изобретения включает (пиримидиниламино)(гидроксиимино)метилкарбамат формулы:
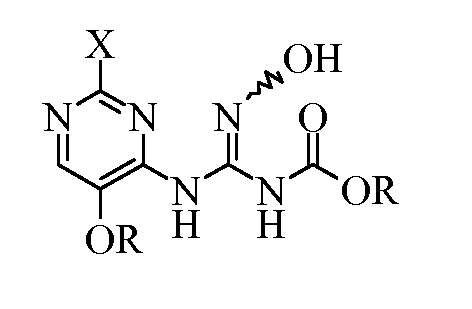
где
X представляет собой галоген или OR; и
R представляет собой C1-С4алкил.
Данное вещество может существовать в виде пары геометрических изомеров (E и Z), а также в различных таутомерных формах.
Дополнительный вариант осуществления изобретения включает 5-галоген-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амины формулы:
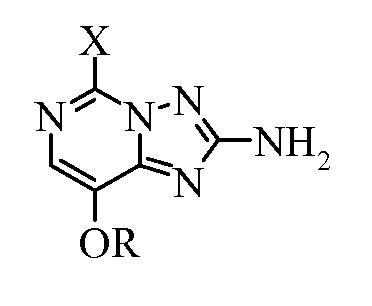
где
X представляет собой галоген; и
R представляет собой C1-С4алкил.
Термин алкил и производные термины, такие как алкокси, как используется в настоящем описании, относятся к группам с неразветвленной или разветвленной цепью. Конкретные алкильные группы представляют собой метил, этил, пропил, 1-метилэтил, бутил, 1,1-диметилэтил и 1-метилпропил. Метил и этил являются обычно предпочтительными. Термин галоген, как используется в настоящем описании, относится к фтору, хлору, брому и йоду. Группа хлора является обычно предпочтительной.
2-Замещенные-4-амино-5-алкоксипиримидиновые и алкилизотиоцианатидокарбонатные исходные вещества являются известными соединениями или могут быть получены способами, хорошо известными специалистам в данной области.
Настоящее изобретение относится к получению 5-замещенных-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-аминов из 2-замещенных-4-амино-5-метоксипиримидинов.
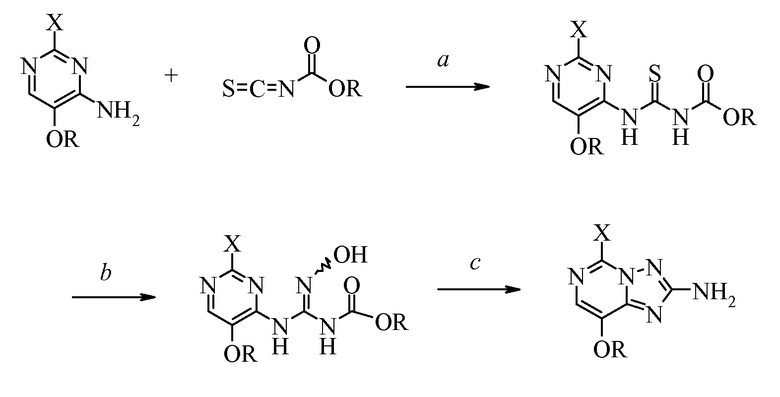
Первая стадия (а) настоящего изобретения касается преобразования 4-аминопиримидина, где
X представляет собой галоген или OR, и
R представляет собой С1-С4алкил,
в (пиримидиниламино)карбонотиоилкарбамат. Это достигается с помощью по меньшей мере одного эквивалента и, предпочтительно, избытка изотиоцианатидокарбоната в полярном апротонном растворителе, предпочтительно ацетонитриле или этилацетате. Также возможно проводить реакцию в присутствии дополнительных разбавителей при условии, что эти растворители не мешают протеканию желаемой реакции и химически инертны в отношении реагентов. Изотиоцианатидокарбонат добавляют при температуре от 0°C до комнатной температуры; смесь, как правило, нагревают до некоторой температуры в диапазоне от комнатной температуры до температуры кипения с обратным холодильником добавленного разбавителя, предпочтительно до температуры кипения с обратным холодильником. Продукт выделяют обычными способами, такими как фильтрование осажденного или кристаллизованного вещества.
В конкретной реакции аминопиримидин растворяют или суспендируют в этилацетате и затем обрабатывают соответствующим количеством изотиоцианатидокарбоната. После нагревания до температуры кипения с обратным холодильником реакционную смесь охлаждают до температуры, при которой целевое соединение осаждается, и отделяют фильтрованием и сушат. Необязательно, некоторая или большая часть растворителя может быть удалена перегонкой перед фильтрованием, для улучшения фильтрования кристаллов или снижения растворимости продукта в растворителе и, тем самым, улучшения выделения.
Вторая стадия (b) настоящего изобретения касается преобразования (пиримидиниламино)карбонотиоилкарбамата в его (пиримидиниламино)(гидроксиимино)метилкарбаматный эквивалент. Это достигается использованием по меньшей мере эквивалента гидроксиламина, предпочтительно в виде соли, и основания, такого как карбонат натрия или калия, гидроксид натрия или калия или триалкиламин. Карбонат натрия или гидроксид натрия являются предпочтительными вспомогательными основаниями. Обычно используют вплоть до 4 эквивалентов гидроксиламина и основания в этой реакции. Реакционную смесь разбавляют водой и полярным растворителем, предпочтительно этилацетатом или ацетонитрилом, и перемешивают при температуре от 0°C до 35°C, предпочтительно при комнатной температуре. Также возможно проводить реакцию в присутствии дополнительных разбавителей при условии, что эти разбавители не мешают протеканию желаемой реакции и химически инертны в отношении реагентов. Продукт необязательно охлаждают и выделяют обычными способами, такими как выделение фильтрованием и сушка, или флэш-хроматографией. Вещество может существовать в виде E/Z изомерной смеси и/или в различных таутомерных формах. Необязательно, вместо того чтобы выделять (пиримидиниламино)(гидроксиимино)метилкарбамат, реакция может быть продолжена в реакционной смеси при нагревании для осуществления циклизации в 5-замещенные-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амины и выделения в соответствии с подробным описанием ниже.
В конкретной реакции (пиримидиниламино)карбонотиоилкарбамат, гидроксиламин и основание растворяют в воде и либо в ацетонитриле, либо в этилацетате. Реакционную смесь перемешивают при комнатной температуре и затем либо нагревают для преобразования в 5-замещенный-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амин, либо фильтруют и перекристаллизовывают из ацетонитрила с выделением (пиримидиниламино)(гидроксиимино)метилкарбамата. Необязательно, некоторая или большая часть растворителя может быть удалена перегонкой перед фильтрованием для улучшения фильтрования кристаллов или снижения растворимости продукта в растворителе и тем самым улучшения выделения.
Третья стадия (с) настоящего изобретения касается преобразования необязательно выделенного (пиримидиниламино)(гидроксиимино)метилкарбамата в 5-замещенный-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амин при нагревании и в инертном растворителе. Часто предпочтительно преобразовывать (пиримидиниламино)(гидроксиимино)метилкарбамат в 5-замещенный-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амин без выделения. Это преобразование осуществляют нагреванием реакционной смеси. Продукт необязательно охлаждают и выделяют обычными методами, такими как выделение фильтрованием и сушка.
Другой вариант осуществления изобретения касается преобразования (d) 5-галоген-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина:
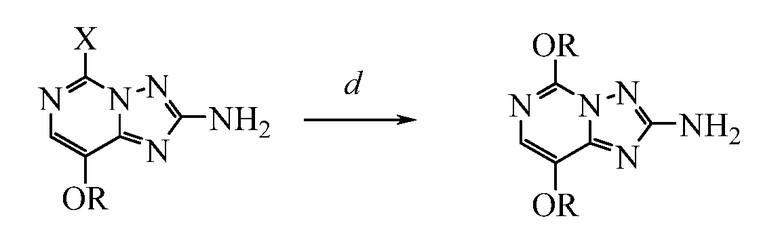
где
X представляет собой галоген; и
R представляет собой C1-С4алкил,
в его алкокси аналог, 5,8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амин, с использованием по меньшей мере одного эквивалента и предпочтительно избытка метоксида натрия или калия в спиртовом растворителе. Также возможно проводить реакцию в присутствии дополнительных разбавителей при условии, что эти разбавители не мешают протеканию желаемой реакции и химически инертны в отношении реагентов. Смесь перемешивают при некоторой температуре от 0°C до 50°C, предпочтительно при комнатой температуре. Продукт необязательно охлаждают и выделяют обычными методами, такими как выделение фильтрованием и сушка.
В конкретной реакции 5-хлор-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амин растворяют в ацетонитриле при комнатной температуре и обрабатывают 25% метоксидом натрия в метаноле. Полученную суспензию перемешивают при комнатной температуре несколько часов и затем фильтруют и сушат с получением 5-метокси-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина. Необязательно, некоторая или большая часть растворителя может быть удалена перегонкой перед фильтрованием, для улучшения фильтрования кристаллов или снижения растворимости продукта в растворителе и тем самым улучшения выделения.
Следующие примеры приведены для иллюстрации изобретения.
ПРИМЕРЫ
Все описанные реагенты были куплены и использовались без дополнительной очистки. Анализ ВЭЖХ проводили на приборе Perkin Elmer Series 200 с диодно-матричным ультрафиолетовым детектором. Использовали колонку Zorbax RX-C8 с различными соотношениями ацетонитрил-вода, модифицированную 0,1% фосфорную кислоту в качестве элюента при скорости потока 1 мл/мин и ультрафиолетовое детектирование при 220 нм. Спектры ядерного магнитного резонанса получали на спектрометре Bruker AC 300 NMR (300 МГц). Масс-спектральные данные получали с использованием точной масс-жидкостной хроматографии с электрораспылением-масс-спектрометрии (ESI/ЖХ/МС) в положительно ионном (PI) режиме и точной масс-жидкостной хроматографии с электрораспылением-масс-спектрометрии-масс-спектрометрии (ESI/ЖХ/МС/МС).
Пример 1. Получение этил[(2-хлор-5-метоксипиримидин-4-ил)амино]карбонотиоилкарбамата (2)
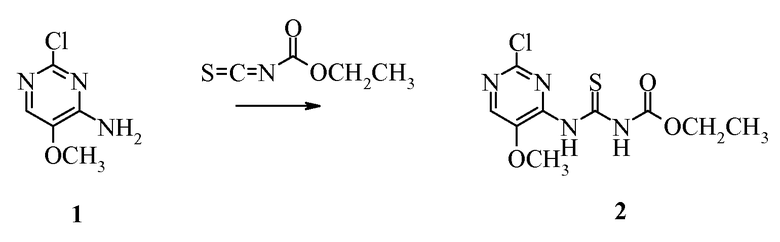
2-Хлор-5-метоксипиримидин-4-амин (1) (6,4 г, 0,040 моль) суспендировали в этилацетате (100 мл) и нагревали почти до температуры кипения с обратным холодильником. Добавляли сразу весь этилизотиоцианатидокарбонат (8,9 г, 1,7 экв.) и смесь кипятили с обратным холодильником в течение 10 часов. Полученную суспензию охлаждали до 15°C, твердый продукт выделяли фильтрованием и промывали осадок свежим этилацетатом с получением указанного в заголовке соединения несколькими порциями в виде твердого вещества (7,8 г, 67%): т.пл. 182°C;
1H ЯМР (ДМСО-d6): δ 11,97 (с, 1H), 11,72 (с, 1H), 8,50 (с, 1H), 4,22 (кв, 2H), 3,72 (с, 3H), 1,17 (т, 3H); 13C ЯМР (ДМСО-d6): 177,82, 153,58, 150,00, 149,01, 144,26, 142,63, 62,76, 57,56, 14,44; масс-спектр (точная масса): вычислено для C9H11ClN4O3S: 290,024039; найдено 290,0241.
Пример 2. Получение этил-(Z и E)-[(2-хлор-5-метоксипиримидин-4-ил)амино](гидроксиимино)метилкарбамата (3)
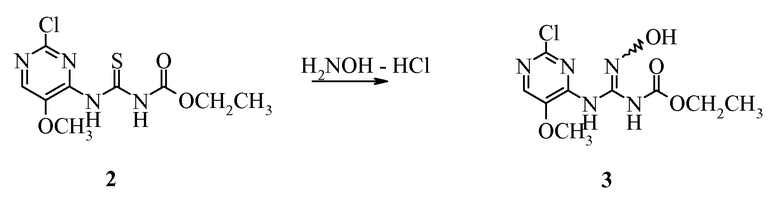
Объединяли гидрохлорид гидроксиламина (280 мг, 4 экв.) и бикарбонат натрия (335 мг, 4 экв.) и растворяли в воде (6 мл) при комнатной температуре. К полученному добавляли суспензию этил[(2-хлор-5-метоксипиримидин-4-ил)амино]карбонотиоилкарбамата (2; 290 мг, 1,0 ммоль) в ацетонитриле (15 мл). Полученную суспензию перемешивали при комнатной температуре в течение 1 часа и твердые частицы отделяли фильтрованием. Перекристаллизацией из ацетонитрила получали указанное в заголовке соединение в виде светло-желтого твердого вещества (170 мг, 59%): т.пл. 183-184°C (разл.);
1H ЯМР (ДМСО-d6) (смесь изомеров) δ 10,77 (с, 0,6H), 10,5 (с, 0,4H), 9,48 (с, 0,6H), 9,34 (с, 0,4H), 9,09 (с, 0,4H), 8,40 (с, 0,6H), 8,11 (с, 0,6H), 8,11 (с, 0,6H), 7,95 (с, 0,4H) 4,19-3,89 (м, 5H), 1,17-1,09 (м, 3H); 13C ЯМР (ДМСО-d6): δ: 154,4, 154,0, 149,9, 140,2, 140,0, 139,1, 138,6, 138,0, 61,2, 60,9, 57,3, 56,5, 14,8, 14,5; Масс-спектр (точная масса): вычислено для C9H12ClN5O4 289,05778; найдено 289,0577.
Пример 3. Получение 5-хлор-8-метокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина (4) без выделения (3)
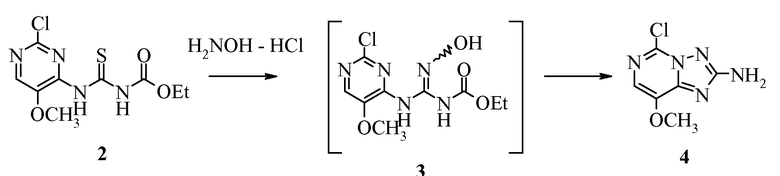
Объединяли этил[(2-хлор-5-метоксипиримидин-4-ил)амино]карбонотиоилкарбамат (2) (290 мг, 1,0 ммоль), гидрохлорид гидроксиламина (143 мг, 2 экв.) и бикарбонат натрия (170 мг, 2 экв.). Добавляли воду (5 мл) и ацетонитрил (5 мл) при комнатной температуре. Полученную суспензию перемешивали при комнатной температуре в течение ночи, затем обрабатывали 20 каплями насыщенного водного раствора карбоната натрия. Полученный раствор продували азотом и охлаждали, получая продукт в виде известкового осадка, который отделяли фильтрованием (в двух порциях), промывали водой и сушили с получением указанного в заголовке соединения в виде твердого вещества (139 мг, 68%): т.пл. 251°C;
1H ЯМР (ДМСО-d6) δ 7,73 (с, 1H), 3,98 (с 3H); 6,63 (с, 2H); 13С ЯМР (ДМСО-d6): 166,30, 148,14, 128,91, 124,67, 57,51; Масс-спектр (точная масса): вычислено для C6H6ClN5O 199,026087; найдено 199,0256.
Пример 4. Получение 5-хлор-8-метокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина (4) без выделения (3)
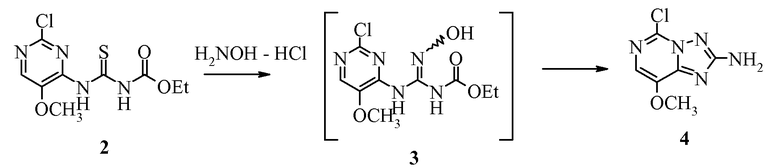
Гидрохлорид гидроксиламина (280 мг, 4 экв.) и бикарбонат натрия (210 мг, 2,5 экв.) объединяли в воде (5 мл) и перемешивали в течение 5 минут. Добавляли при комнатной температуре этил[(2-хлор-5-метоксипиримидин-4-ил)амино]карбонотиоилкарбамат (2) (290 мг, 1,0 ммоль), суспендированный в трет-бутаноле (15 мл). Реакцию перемешивали при комнатной температуре в течение 5 часов и затем обрабатывали 10 каплями насыщенного водного раствора карбоната натрия. Реакционную суспензию затем фильтровали и полученные твердые частицы промывали водой и сушили с получением указанного в заголовке соединения в виде серовато-белого твердого вещества (330 мг, 83%), которое было идентичным по ВЭЖХ удерживанию описанному выше 5-хлор-8-метокси[1,2,4]триазоло[1,5-с]пиримидин-2-амину (4).
Пример 5. Получение 5,8-диметокси[1,2,4]триазоло[1,5-с] пиримидин-2-амина (5)
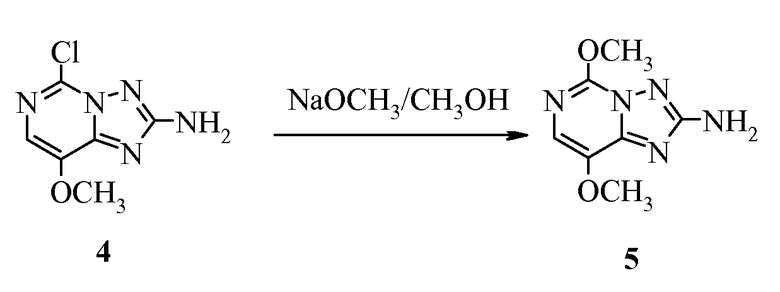
5-Хлор-8-метокси[1,2,4]триазоло[1,5-с]пиримидин-2-амин (4; 100 мг, 0,50 ммоль) суспендировали в ацетонитриле (5 мл) при комнатной температуре и обрабатывали 25% метоксидом натрия в метаноле (200 мг, 2 экв.). Полученную суспензию перемешивали при комнатной температуре в течение 1,5 часов и затем фильтровали. Твердые частицы промывали водой и сушили с получением указанного в заголовке соединения в виде вещества известкового цвета (87 мг, 88%), которое было идентичным по ВЭЖХ удерживанию подлинному 5,8-диметокси[1,2,4]триазоло[1,5-с]пиримидин-2-амину (5): т.пл. 185-186°C;
1H ЯМР (ДМСО-d6) 7,48 (с, 1H), 6,38 (ушир. с, 2H), 4,04 (с, 3H), 3,88 (с, 3H); EIMS m/z 195.
Пример 6. Получение этил[(2,5-диметоксипиримидин-4-ил)амино]карбонотиоилкарбамата
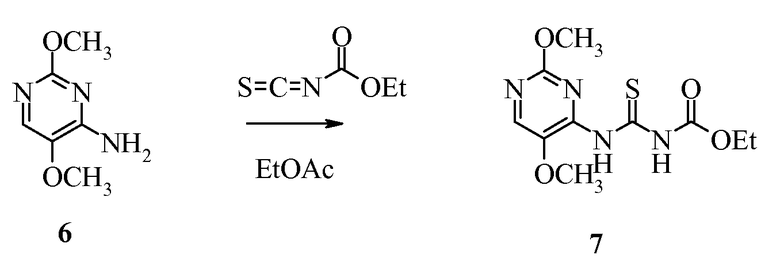
В 18 г этилацетата растворяли 2,5-диметоксипиримидин-4-амин (6) (3 г, 0,0193 моль). Добавляли этилизотиоцианатидокарбонат (2,77 г, 0,0208 моль) одной порцией. Раствор нагревали до 78°С и выдерживали при этой температуре в течение 11 ч. Добавляли дополнительные 1,4 г этилизотиоцианатидокарбоната и смесь нагревали в течение 2,5 ч. Смесь охлаждали до 22°C и фильтровали. Полученное твердое вещество промывали этилацетатом (20 мл) и сушили до постоянной массы в вытяжном шкафу с получением указанного в заголовке соединения в виде желтого твердого вещества (4,81 г, 89%):
13C ЯМР (ДМСО-d6, 100 МГц) δ 177,5, 158,4, 153,3, 149,5, 142,3, 139,5, 62,6, 57,6, 55,2, 14,4; HRMS (ESI), вычислено для C10H14N4O4S, 286,0736; найдено 286,0727.
Пример 7. Добавление гидроксиламина для получения соединения 8 и циклизация с образованием 5,8-диметокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина (5)
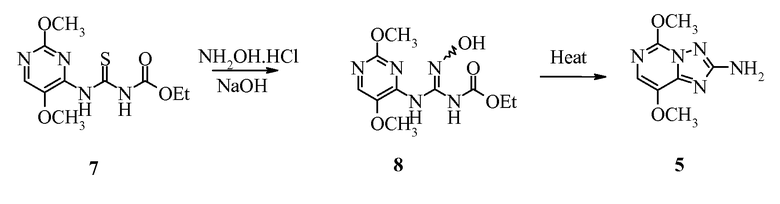
Этил[(2,5-диметоксипиримидин-4-ил)амино]карбонотиоилкарбамат (7; 4,30 г, 0,0154 моль) диспергировали в 24 г этилацетата. Затем к перемешиваемой суспензии добавляли гидрохлорид гидроксиламина (1,28 г, 0,0193 моль), воду (3,84 г) и 2М NaOH (12,61 г, 0,0252 моль). После добавления NaOH температура внутри поднялась до 26°C. Этил-(E/Z)-[(2-хлор-5-метоксипиримидин-4-ил)амино](гидроксиимино)метилкарбамат (8) не выделяли, но нагревали до 50°С для циклизации. Смесь охлаждали до комнатной температуры и перемешивали в течение ночи. Суспензию фильтровали при комнатной температуре, осадок промывали водой (3×8 г) и сушили до постоянной массы в вытяжном шкафу с получением указанного в заголовке соединения в виде рыжеватого твердого вещества (3,16 г, 105% выход по массе). Основной компонент имел время удерживания, идентичное подлинному 5,8-диметокси[1,2,4]триазоло[1,5-с]пиримидин-2-амину (5). В отдельном эксперименте этил-(E/Z)-[(2,5-диметоксипиримидин-4-ил)амино](гидроксиимино)метилкарбамат (8) выделяли хроматографией на силикагеле (хлороформ в качестве элюента) с получением белого твердого вещества (0,4 г, 13%), которое представляло собой ок. 77/23 смесь геометрических изомеров:
1H ЯМР (ДМСО-d6) (смесь изомеров) δ 10,65 (с, 1H), 10,34 (с, 0,3H), 9,56 (с, 1H), 8,98 (с, 0,3H), 8,94 (с, 0,3H), 8,20 (с, 1H), 8,00 (с, 1H), 7,82 (с, 0,3H), 4,25-3,90 (м, 2,6H), 3,88 (с, 3H), 3,81 (с, 0,9H), 3,78 (с, 3H), 3,22 (с, 0,9H), 1,20-1,15 (м, 3H); Масс-спектр (точная масса): вычислено для C9H12ClN5O4 289,0578; найдено 289,0571.
| название | год | авторы | номер документа |
|---|---|---|---|
| УЛУЧШЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ 2-АМИНО-5,8-ДИАЛКОКСИ[1,2,4]ТРИАЗОЛО[1,5-с]ПИРИМИДИНА ИЗ 4-АМИНО-2,5-ДИАЛКОКСИПИРИМИДИНА | 2013 |
|
RU2646603C2 |
| 5-АЛКОКСИ [1,2,4]ТРИАЗОЛО[1,5-C]ПИРИМИДИН-2(3H)-ТИОНОВЫЕ СОЕДИНЕНИЯ, 2,2'-ДИТИОБИС(5-АЛКОКСИ[1,2,4]ТРИАЗОЛО[1,5-C]ПИРИМИДИН), СПОСОБ ПОЛУЧЕНИЯ 2,2'-ДИТИОБИС(5-АЛКОКСИ[1,2,4]ТРИАЗОЛО[1,5-C]ПИРИМИДИНА) И 2-ХЛОРОСУЛЬФОНИЛ-5-АЛКОКСИ[1,2,4]ТРИАЗОЛО[1,5-C]ПИРИМИДИНОВЫХ СОЕДИНЕНИЙ | 1994 |
|
RU2131429C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-АМИНО-5,8-ДИМЕТОКСИ[1,2,4]ТРИАЗОЛО[1,5-c]ПИРИМИДИНА ИЗ 4-ХЛОР-2,5-ДИМЕТОКСИПИРИМИДИНА | 2013 |
|
RU2635352C2 |
| 1-ГИДРОКСИИМИНО-3-ФЕНИЛ-ПРОПАНЫ | 2011 |
|
RU2579114C9 |
| ПРОИЗВОДНЫЕ ФЕНИЛУКСУСНОЙ КИСЛОТЫ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ СРЕДСТВА | 1995 |
|
RU2165411C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛОПИРИМИДИНЫ И ЗАМЕЩЕННЫЕ ПУРИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ УБИКВИТИН-СПЕЦИФИЧЕСКОЙ ПРОЦЕССИРУЮЩЕЙ ПРОТЕАЗЫ 1 (USP1) | 2019 |
|
RU2833222C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛУКСУСНОЙ КИСЛОТЫ И СРЕДСТВО БОРЬБЫ ПРОТИВ НАСЕКОМЫХ И ПАУКООБРАЗНЫХ И ПРОТИВ ВРЕДОНОСНЫХ ГРИБОВ | 1995 |
|
RU2162075C2 |
| ФЕНОКСИМЕТИЛЬНЫЕ ПРОИЗВОДНЫЕ | 2016 |
|
RU2746481C1 |
| ПРОИЗВОДНЫЕ 2-(ФЕНИЛ ИЛИ ПИРИД-3-ИЛ)АМИНОПИРИМИДИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ БОГАТОЙ ЛЕЙЦИНОМ ПОВТОРНОЙ КИНАЗЫ 2 (LRRK2) ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА | 2012 |
|
RU2647849C2 |
| ЗАМЕЩЕННЫЕ АРИЛАЛКИЛТИОАЛКИЛТИОПИРИДИНЫ ДЛЯ БОРЬБЫ С БАКТЕРИЯМИ HELICOBACTER | 1995 |
|
RU2139286C1 |
Изобретение относится к способу получения 5-замещенных-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-аминов формулы (I):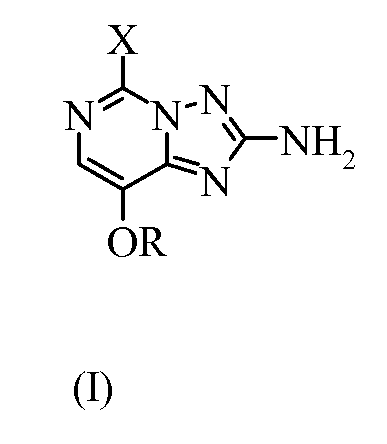 , где X представляет собой галоген или OR; и R представляет собой C1-С4алкил; который включает: i) взаимодействие 2-замещенного-4-амино-5-алкоксипиримидина формулы:
, где X представляет собой галоген или OR; и R представляет собой C1-С4алкил; который включает: i) взаимодействие 2-замещенного-4-амино-5-алкоксипиримидина формулы: 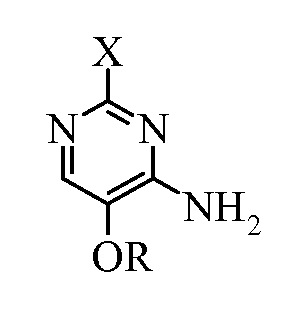 с изотиоцианатидокарбонатом формулы:
с изотиоцианатидокарбонатом формулы: 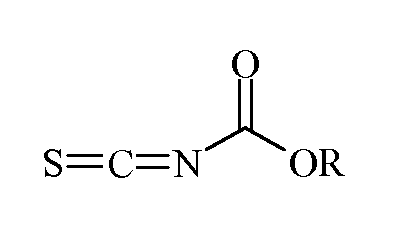 в полярном апротонном растворителе с получением (пиримидиниламино)карбонотиоилкарбамата формулы:
в полярном апротонном растворителе с получением (пиримидиниламино)карбонотиоилкарбамата формулы: 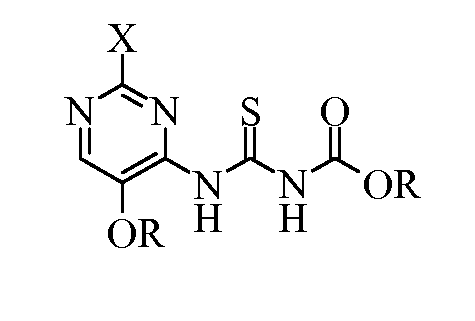 ; ii) приведение в контакт (пиримидиниламино)карбонотиоилкарбамата с гидроксиламином в присутствии основания с получением (пиримидиниламино)(гидроксиимино)метилкарбамата формулы:
; ii) приведение в контакт (пиримидиниламино)карбонотиоилкарбамата с гидроксиламином в присутствии основания с получением (пиримидиниламино)(гидроксиимино)метилкарбамата формулы: 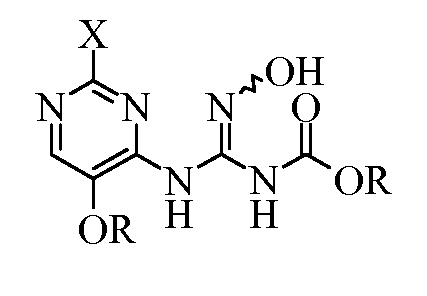 и iii) циклизацию (пиримидиниламино)(гидроксиимино)метилкарбамата нагреванием в инертном растворителе с получением 5-замещенного-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина. Изобретение относится также к способу получения 2-амино-5,8-алкокси[1,2,4]триазоло[1,5-с]пиримидинов формулы:
и iii) циклизацию (пиримидиниламино)(гидроксиимино)метилкарбамата нагреванием в инертном растворителе с получением 5-замещенного-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина. Изобретение относится также к способу получения 2-амино-5,8-алкокси[1,2,4]триазоло[1,5-с]пиримидинов формулы: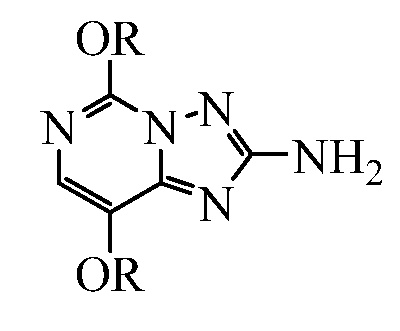 , где R представляет собой C1-С4алкил; который включает приведение в контакт 5-галоген-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина формулы:
, где R представляет собой C1-С4алкил; который включает приведение в контакт 5-галоген-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина формулы: 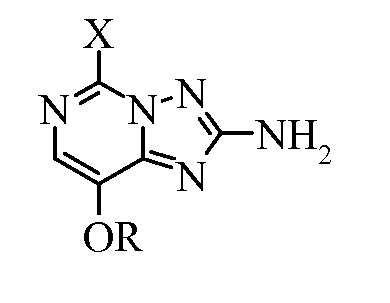 , где Х представляет собой галоген; и R представляет собой C1-С4алкил; с алкоксидом щелочного металла в спиртовом растворителе. Изобретение также относится к соединениям формул:
, где Х представляет собой галоген; и R представляет собой C1-С4алкил; с алкоксидом щелочного металла в спиртовом растворителе. Изобретение также относится к соединениям формул: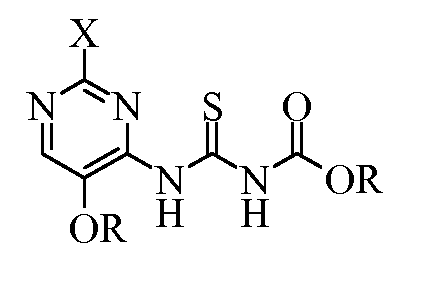 и
и 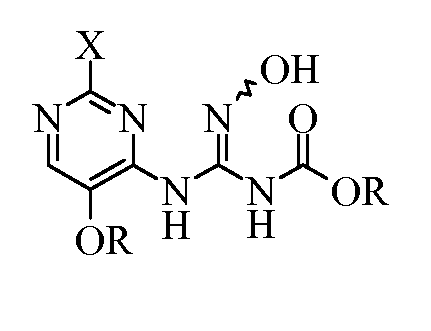 , где X представляет собой галоген или OR; и R представляет собой C1-С4алкил. Технический результат: получение 5-замещенных-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-аминов с высоким выходом без использования гидразина и циангалогенида. 4 н. и 2 з.п. ф-лы, 7 пр.
, где X представляет собой галоген или OR; и R представляет собой C1-С4алкил. Технический результат: получение 5-замещенных-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-аминов с высоким выходом без использования гидразина и циангалогенида. 4 н. и 2 з.п. ф-лы, 7 пр.
1. Способ получения 5-замещенных-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-аминов формулы (I):

где
X представляет собой галоген или OR; и
R представляет собой C1-С4алкил;
который включает:
i) взаимодействие 2-замещенного-4-амино-5-алкоксипиримидина формулы:

где X и R являются такими, как определено выше,
с изотиоцианатидокарбонатом формулы:

где R является таким, как определено выше,
в полярном апротонном растворителе с получением (пиримидиниламино)карбонотиоилкарбамата формулы:

где X и R являются такими, как определено выше;
ii) приведение в контакт (пиримидиниламино)карбонотиоилкарбамата с гидроксиламином в присутствии основания с получением (пиримидиниламино)(гидроксиимино)метилкарбамата формулы:

где X и R являются такими, как определено выше; и
iii) циклизацию (пиримидиниламино)(гидроксиимино)метилкарбамата нагреванием в инертном растворителе с получением 5-замещенного-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина.
2. Способ по п.1, в котором X и R, оба представляют собой OCH3.
3. Способ по п.1, в котором (пиримидиниламино)(гидроксиимино)метилкарбамат стадии ii) используют без выделения для получения 2-амино-5-замещенного-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина на стадии iii).
4. Способ получения 2-амино-5,8-алкокси[1,2,4]триазоло[1,5-с]пиримидинов формулы:

где
R представляет собой C1-С4алкил;
который включает приведение в контакт 5-галоген-8-алкокси[1,2,4]триазоло[1,5-с]пиримидин-2-амина формулы:

где
Х представляет собой галоген; и
R представляет собой C1-С4алкил;
с алкоксидом щелочного металла в спиртовом растворителе.
5. Соединение формулы:

где
X представляет собой галоген или OR; и
R представляет собой C1-С4алкил.
6. Соединение формулы:

где
X представляет собой галоген или OR; и
R представляет собой C1-С4алкил.
| СПОСОБ СВЕРТЫВАНИЯ ЗОЛЕЙ И ТОНКИХ СУСПЕНЗИЙ СУЛЬФИДОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 1924 |
|
SU1064A1 |
Авторы
Даты
2015-11-10—Публикация
2011-05-24—Подача