ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА СМЕЖНЫЕ ИЗОБРЕТЕНИЯ
Настоящая заявка истребует приоритет, заявленный в предварительных заявках на патент США №№ 61/171658 и 61/171649, поданных 22 апреля 2009 года, которые полностью включены в настоящий документ путем ссылки.
ИСПОЛЬЗОВАЛОСЬ ЛИ В ДАННОМ ИССЛЕДОВАНИИ ФЕДЕРАЛЬНОЕ ФИНАНСИРОВАНИЕ
Для исследований и разработки описанного ниже изобретения не привлекалось федеральное финансирование.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Конопля посевная (cannabis sativa) в течение многих лет используется в качестве болеутоляющего. Основным активным ингредиентом конопли посевной и агонистом каннабиноидных рецепторов является Δ9-тетрагидроканнабинол (Pertwee, Brit J Pharmacol, 2008, 153, 199-215). Было клонировано два рецептора, связанных с G-белками, - каннабиноидный рецептор типа 1 (CB1 Matsuda et al., Nature, 1990, 346, 561-4) и каннабиноидный рецептор типа 2 (CB2 Munro et al., Nature, 1993, 365, 61-5). Рецептор CB1 присутствует централизованно - в головном мозге (гипоталамус и центр удовольствия), а также на периферии - в печени, желудочно-кишечном тракте, поджелудочной железе, жировой ткани и скелетных мышцах (Di Marzo et al., Curr Opin Lipidol, 2007, 18, 129-140). Рецептор CB2 находится по существу в иммунных клетках, таких как моноциты (Pacher et al., Amer J Physiol, 2008, 294, H1133-H1134), а при определенных условиях - также в головном мозге (Benito et al., Brit J Pharmacol, 2008, 153, 277-285), скелетных мышцах (Cavuoto et al., Biochem Biophys Res Commun, 2007, 364, 105-110) и сердечной мышце (Hajrasouliha et al., Eur J Pharmacol, 2008, 579, 246-252). Множество фармакологических, анатомических и электрофизиологических данных, полученных с использованием синтетических агонистов, свидетельствует о том, что усиление передачи сигналов через каннабиноидные рецепторы CB1/CB2 обеспечивает аналгезию в ходе испытаний на острую ноцицепцию и подавляет гипералгезию в моделях хронической нейропатической и воспалительной боли (Cravatt et al., J Neurobiol, 2004, 61, 149-60; Guindon et al., Brit J Pharmacol, 2008, 153, 391-334).
Эффективность синтетических агонистов каннабиноидных рецепторов убедительно подтверждена документальными доказательствами. Более того, исследования с использованием антагонистов каннабиноидных рецепторов и нокаутных мышей также подтвердили важность системы эндоканнабиноидов как модулятора ноцицепции. Двумя основными эндоканнабиноидами являются анандамид (AEA) (Devane et al., Science, 1992, 258, 1946-9) и 2-арахидоноилглицерин (2-AG) (Mechoulam et al., Biochem Pharmacol, 1995, 50, 83-90; Sugiura et al., Biochem Biophys Res Commun, 1995, 215, 89-97). AEA гидролизуется гидролазой амида жирных кислот (FAAH), а 2-AG гидролизуется моноацилглицерин-липазой (MGL) (Piomelli, Nat Rev Neurosci, 2003, 4, 873-884). В моделях боли острого и воспалительного характера генетическое удаление FAAH вызывает повышение уровня эндогенного AEA, что ведет к аналгезии, обусловленной рецепторами CB1 (Lichtman et al., Pain, 2004, 109, 319-27). Это позволяет предположить, что естественной функцией эндоканнабиноидной системы является подавление боли (Cravatt et al., J Neurobiol, 2004, 61, 149-60). В отличие от конститутивного повышения уровней эндоканнабиноидов у нокаутных мышей с отсутствующим ферментом FAAH, применение специальных ингибиторов FAAH обеспечивает временное повышение уровней AEA, ведущее к антиноцицепции in vivo (Kathuria et al., Nat Med, 2003, 9, 76-81). Дальнейшее доказательство антиноцицептивного эффекта, обусловленного эндоканнабиноидами, демонстрируется выработкой AEA в околоводопроводном сером веществе после периферической болевой стимуляции (Walker et al., Proc Natl Cad Sci USA, 1999, 96, 12198-203) и, напротив, наступлением гипералгезии после ингибирования рецептора CB1 с помощью антисмысловой РНК в спинном мозге (Dogrul et al., Pain, 2002, 100, 203-9).
В отношении 2-AG, внутривенное введение 2-AG обеспечивает аналгезию в тестах отдергивания хвоста (Mechoulam et al., Biochem Pharmacol, 1995, 50, 83-90) и в тесте горячей пластинки (Lichtman et al., J Pharmacol Exp Ther, 2002, 302, 73-9). В отличие от этого было продемонстрировано, что применение одного только 2-AG не обеспечивает аналгезию в тесте горячей пластинки, но в сочетании с другими 2-моноацилглицеринами (например, 2-линолеоилглицерином и 2-пальмитоилглицерином) достигается выраженная аналгезия. Это явление получило название «эффект окружения» (Ben-Shabat et al., Eur J Pharmacol, 1998, 353, 23-31). Такие 2-моноацилглицерины «окружения» представляют собой эндогенные липиды, выделяемые совместно с 2-AG и потенцирующие сигнализацию эндоканнабиноидов, в частности, путем ингибирования разложения 2-AG, скорее всего, вследствие конкуренции за активный центр на MGL. Это говорит о том, что синтетические ингибиторы MGL должны иметь аналогичный эффект. Действительно, URB602, относительно слабый синтетический ингибитор MGL, продемонстрировал антиноцицептивный эффект на мышиной модели острого воспаления (Comelli et al., Brit J Pharmacol, 2007, 152, 787-794).
Хотя использование синтетических каннабиноидных агонистов убедительно продемонстрировало, что увеличение каннабиноидной сигнализации оказывает обезболивающее и противовоспалительное воздействие, оказалось трудно отделить положительные эффекты этих соединений от нежелательных побочных эффектов. Альтернативный подход заключается в повышении сигнализации системы эндоканнабиноидов путем повышения уровня 2-AG, наиболее часто встречающегося в центральной нервной системе (ЦНС) и желудочно-кишечном тракте эндоканнабиноида, которого можно добиться путем ингибирования MGL. Таким образом, ингибиторы MGL являются потенциально полезными для обезболивания, лечения воспалений и нарушений ЦНС (Di Marzo et al., Curr Pharm Des, 2000, 6, 1361-80; Jhaveri et al., Brit J Pharmacol, 2007, 152, 624-632; McCarberg Bill et al., Amer J Ther, 2007, 14, 475-83), а также для лечения глаукомы и болезненных состояний, возникающих вследствие повышенного внутриглазного давления (Njie, Ya Fatou; He, Fang; Qiao, Zhuanhong; Song, Zhao-Hui, Exp. Eye Res., 2008, 87(2):106-14).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соединению формулы (I)

Формула (I)
где
Y и Z независимо выбраны из группы a) или b) таким образом, что один из Y или Z выбран из группы a), а другой - из группы b).
Группа a) представляет собой
i) замещенный C6-10 арил;
ii) C3-8 циклоалкил, необязательно замещенный одним или двумя фтор-заместителями;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, пиримидинила, изоксазолила, бензотиенила, тиено[3,2-b]тиофен-2-ила, пиразолила, триазолила, тетразолила и [1,2,3]тиадиазолила;
где C6-10 арил замещен, а гетероарил необязательно замещен одним заместителем, выбранным из группы, состоящей из фтора, хлора, брома, C1-4алкила, C1-4алкокси, циано, C1-4алкилкарбониламино и трифторметила.
Группа b) представляет собой
i) C6-10 арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1H-пирроло[3,2-b]пиридин-5-ила, 1H-тиено[2,3-c]пиразол-5-ила, 1H-пирроло[2,3-b]пиридин-5-ила, 1H-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, хинолинила, хиназолинила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пирролила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1H-индолил;
iv) 2,3-дифенилиндолил;
v) дифенилимидазолил;
vi) 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-3-ил;
vii) 3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил;
viii) 1-(4-фторфенил)-1H-пирроло[3,2-b]пиридин-6-ил; или
ix) дифенил-1H-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем,
в котором C6-10 арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из брома, хлора, фтора, йода, C1-4алкила, C1-4алкокси и трифторметила, а также замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10 арила;
ii) гетероарила, выбранного из группы, состоящей из пиримидинила, тиенила, хинолинила, пиридинила, изоксазолила, тиазолила, бензимидазолила, пирролила, фуранила, пиримидинила и пиразолила; или
iii) 5,6-дигидро-4H-циклопентапиразол-2-ила;
при этом указанный гетероарил и 5,6-дигидро-4H-циклопентапиразол-2-ил необязательно замещены одним фенильным заместителем, указанный фенил необязательно замещен одним или двумя хлор-заместителями или трифторметилом;
и фенил, входящий в состав C6-10арила и гетероарила, необязательно независимо замещен одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкоксикарбониламино; C1-4алкила; цианометила; C1-4алкокси; от одного до трех фтор- или хлор-заместителей; трифторметила; трифторметокси; трифторметилтио; C1-4алкилкарбонила; C1-4алкоксикарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано)этиламинокарбонила; циано; карбокси; аминокарбонила; C1-4алкиламинокарбонила; ди(C1-4алкил)аминокарбонила; формила; нитро; брома; гидрокси; ди(C1-4алкил)аминосульфонила; C1-4алкилсульфонила; ди(C1-4алкил)аминосульфонила; морфолин-4-илсульфонила; -OCH2O-, присоединенного к соседним атомам углерода; и NRcRd; где Rc представляет собой водород или C1-6алкил, а Rd представляет собой водород, C1-6алкил, циано(C1-4)алкил, C3-8циклоалкил, C1-6алкилкарбонил, C1-6алкоксикарбонил, C3-8циклоалкилкарбонил, C3-8циклоалкил(C1-4)алкил, аминокарбонил, ди(C1-4алкил)аминокарбонил, C6-10арилкарбонил; ди(C1-4алкил)аминосульфонил и C1-4алкилсульфонил;
s равно 0, 1 или 2; при условии, что когда s равно 2, R1 независимо выбирается из группы, состоящей из фенила, C1-3алкила и C6-10арил(C1-3)алкила;
R1 представляет собой C6-10арил, C1-3алкил, бензилоксиметил, гидрокси(C1-3)алкил, аминокарбонил, карбокси, трифторметил, спироконденсированный циклопропил, 3-оксо или арил(C1-3)алкил; или (когда s равно 2 и R1 представляет собой C1-3алкил) заместители C1-3алкила берутся вместе с пиперазинильным кольцом с образованием 3,8-диазабицикло[3.2.1]октаниловой или 2,5-диазабицикло[2.2.2]октаниловой кольцевой системы;
и при условии, что соединение формулы (I) отлично от
соединения, в котором Y представляет собой 3-хлорбензотиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 2-цианофенил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой пиримидин-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил и s равно 1, а R1 представляет собой 3-фенил;
и его энантиомерам, диастереомерам, сольватам и фармацевтически приемлемым солям.
Настоящее изобретение дополнительно относится к соединению формулы (I)
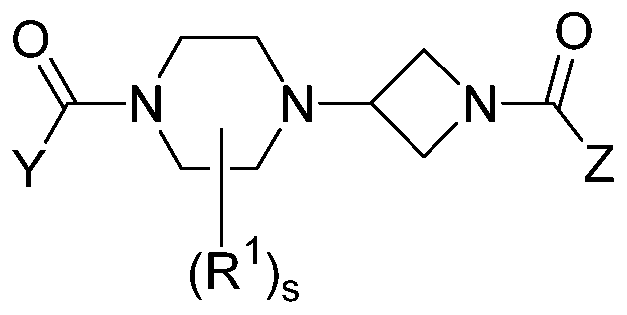
Формула (I)
где
Y и Z независимо выбраны из группы a) или b) таким образом, что один из Y или Z выбран из группы a), а другой - из группы b).
Группа a) представляет собой
i) замещенный C6-10 арил;
ii) C3-8 циклоалкил, необязательно замещенный одним или двумя фтор-заместителями;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, изоксазолила, бензотиенила, тиено[3,2-b]тиофен-2-ила, триазолила и [1,2,3]тиадиазолила;
в котором C6-10 арил замещен; а гетероарил необязательно замещен; один заместитель выбран из группы, состоящей из фтора, хлора, брома, C1-4алкила, циано и трифторметила.
Группа b) представляет собой
i) C6-10 арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1H-пирроло[3,2-b]пиридин-5-ила, 1H-тиено[2,3-c]пиразол-5-ила, 1H-пирроло[2,3-b]пиридин-5-ила, 1H-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, хиназолинила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пирролила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1H-индолил;
iv) 2,3 дифенилиндолил;
v) дифенилимидазолил;
vi) 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-3-ил;
vii) 3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил;
viii) 1-(4-фторфенил)-1H-пирроло[3,2-b]пиридин-6-ил; или
ix) дифенил-1H-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем;
в котором C6-10 арил, 2,3-дигидро-1H-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила, а также замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10 арила;
ii) гетероарила, выбранного из группы, состоящей из пиримидинила, тиенила, хинолинила, пиридинила, изоксазолила, тиазолила, бензимидазолила, пирролила, фуранила, пиримидинила и пиразолила; или
iii) 5,6-дигидро-4H-циклопентапиразол-2-ила;
в котором указанный гетероарил и 5,6-дигидро-4Н-циклопентапиразол-2-ил необязательно замещены одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкоксикарбониламино; C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителей, представляющих собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано) этиламинокарбонила; циано; карбокси; аминокарбонила; формила; нитро; брома; гидрокси; ди-(C1-4алкил)аминосульфонила; C1-4алкилсульфонила; -OCH2O-, присоединенного к соседним атомам углерода; и NRcRd; в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкил, C1-6алкилкарбонил, C1-6алкоксикарбонил и C1-4алкилсульфонил;
s равно 0 или 1;
R1 представляет собой C6-10арил, C1-3алкил или арил(C1-3)алкил;
и при условии, что соединение формулы (I) отлично от
соединения, в котором Y представляет собой 3-хлорбензотиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 2-цианофенил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой пиримидин-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, s равно 1, а R1 представляет собой 3-фенил;
и его энантиомерам, диастереомерам, сольватам и фармацевтически приемлемым солям.
Настоящее изобретение дополнительно относится к соединению формулы (I)

Формула (I)
где
Y и Z независимо выбраны из группы a) или b) таким образом, что один из Y или Z выбран из группы a), а другой - из группы b).
Группа a) представляет собой
i) замещенный C6-10 арил;
ii) C3-8 циклоалкил, необязательно замещенный одним или двумя фтор-заместителями;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, изоксазолила, тиено[3,2-b]тиофен-2-ил и[1,2,3]тиадиазолила;
в котором C6-10 арил, замещен; гетероарил необязательно замещен; один заместитель выбран из группы, состоящей из фтора, хлора, брома, C1-4алкила и трифторметила;
Группа b) представляет собой
i) C6-10 арил;
ii) гетероарил, выбранный из группы, состоящей из триазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1H-пирроло[3,2-b]пиридин-5-ила, 1H-тиено[2,3-c]пиразол-5-ила, 1H-пирроло[2,3-b]пиридин-5-ила, 1H-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, хиназолинила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1H-индолил;
iv) 2,3 дифенилиндолил;
v) дифенилимидазолил;
vi) 3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил; или
vii) дифенил-1H-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем;
в котором C6-10 арил, 2,3-дигидро-1H-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила, а также замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10 арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила, изоксазолила, бензимидазолила, фуранила, пиримидинила и пиразолила; или
iii) 5,6-дигидро-4H-циклопентапиразол-2-ила;
в котором указанный гетероарил и 5,6-дигидро-4Н-циклопентапиразол-2-ил необязательно замещены одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителей, представляющих собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано) этиламинокарбонила; циано; аминокарбонила; формила; нитро; брома; гидрокси; ди-(C1-4алкил)аминосульфонила; C1-4алкилсульфонила; -OCH2O-, присоединенного к соседним атомам углерода; NRcRd; в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкил, C1-6алкилкарбонил, C1-6алкоксикарбонил и C1-4алкилсульфонил;
s равно 0 или 1;
R1 представляет собой фенил или C1-3алкил;
и при условии, что соединение формулы (I) отлично от
соединения, в котором Y представляет собой 3-хлорбензотиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 2-цианофенил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой пиримидин-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, s равно 1, а R1 представляет собой 3-фенил;
и его энантиомерам, диастереомерам, сольватам и фармацевтически приемлемым солям.
Настоящее изобретение относится к соединению формулы (I)

Формула (I)
где
Y и Z независимо выбраны из группы a) или b) таким образом, что один из Y или Z выбран из группы a), а другой - из группы b).
Группа a) представляет собой
i) циклопропил, необязательно замещенный одним или двумя фтор-заместителями;
ii) трифторметил; или
iii) гетероарил, выбранный из группы, состоящей из триенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила и изоксазолила;
в котором C6-10 арил замещен; гетероарил необязательно замещен; один заместитель выбран из группы, состоящей из фтора, хлора, брома и трифторметила;
Группа b) представляет собой
i) C6-10 арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1H-пирроло[3,2-b]пиридин-5-ила, 1H-тиено[2,3-c]пиразол-5-ила, 1H-пирроло[2,3-b]пиридин-5-ила, хиназолинила, фуранила, тиенила, [1,3,4]оксадиазол-2-ила и бензимидазолила;
iii) 2,3-дигидро-1H-индолил;
iv) 2,3 дифенилиндолил;
v) дифенилимидазолил;
vi) 3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил; или
vii) дифенил-1H-пиразол-3-ил; в котором каждый фенил независимо замещен одним или двумя хлор-заместителями;
в котором C6-10 арил, 2,3-дигидро-1H-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила, а также замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10 арила;
ii) гетероарила, выбранного из группы, состоящей из пиримидинила, тиенила, хинолинила, пиридинила, пиримидинила и пиразолила; или
iii) 5,6-дигидро-4H-циклопентапиразол-2-ила;
в котором указанный гетероарил и 5,6-дигидро-4H-циклопентапиразол-2-ил необязательно замещены одним фенильным заместителем, а указанный фенил необязательно замещен одним или двумя хлор-заместителями или трифторметилом;
в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителей, включающих хлор или фтор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; формила; нитро; брома; гидрокси; ди-(C1-4алкил)аминосульфонила; C1-4алкилсульфонила; -OCH2O-, присоединенного к соседним атомам углерода; NRcRd; в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкоксикарбонил, и C1-4алкилсульфонил;
s равно 0 или 1;
R1 представляет собой фенил;
и при условии, что соединение формулы (I) отлично от
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, s равно 1, а R1 представляет собой 3-фенил;
и его энантиомерам, диастереомерам, сольватам и фармацевтически приемлемым солям.
Настоящее изобретение относится к соединению формулы (I),

Формула (I)
выбранному из группы, состоящей из:
соединения, в котором Y представляет собой фуран-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-5-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 2-метилтиазол-4-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 1-метил-1H-пиррол-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 5-бромфуран-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой тиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 5-метилтиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 5-бромтиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 5-хлортиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 3-бромтиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 4-бромтиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой тиено[3,2-b]тиофен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой бензотиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 3-метокситиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 4-бифенил, Z представляет собой тиазол-2-ил, s равно 1, а R1 представляет собой 3-фенил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-бифенил, s равно 1, а R1 представляет собой 2-метил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-бифенил, s равно 1, а R1представляет собой 2-фенил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-дифенил, s равно 1, а R1 представляет собой 3-метил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-бифенил, s равно 1, а R1 представляет собой 3-метил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-4-метилтиен-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(тиен-2-ил)-4-метилтиен-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-метилфенил)-4-метилтиен-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-трифторметилфенил)-4-метилтиен-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(тиен-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(тиен-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиридин-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиридин-3-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиридин-4-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(пиридин-3-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиримидин-5-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(пиримидин-5-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиримидин-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(пиримидин-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(2-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(2-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(4-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(6-бромпиридин-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(5-нитропиридин-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-нитропиридин-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-фторфенил)пиридин-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-фторфенил)-тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-фторфенил)-тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(2,4-дихлорфенил)-тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3,5-дихлорфенил)-тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-метоксифенил)-тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилтиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-цианофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-хлорфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-хлорфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3,5-дихлорфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилпиридин-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фтор-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-цианофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-бромфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 5-фенилпиридин-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-фтор-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(4-цианофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(4-бромфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3,4-дихлорфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-фтор-6-метилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-хлор-4-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(2,4-дифторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метоксифенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(бензо[1,3]диоксал-5-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(нафт-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-нитрофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-хинолин-5-ил-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-карбоксифенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-цианометилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метилсульфонилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-метилкарбонилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-формилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-гидроксифенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-хлор-3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-диметиламиносульфонилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4,5-дифтор-2-метоксифенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-нитрофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-формил-4-метоксифенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-аминокарбонилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-гидроксифенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метилсульфониламинофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трет-бутоксикарбониламинофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-изобутилоксифенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-(2-цианоэтил)аминокарбонилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-(2-цианоэтенил)фенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(2-метоксикарбонилэтенил)фенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(4-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(2,4-дифторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3-хлор-4-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3,4-дихлорфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-аминофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метилкарбониламинофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3-метилкарбониламинофенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3-метансульфонилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-метил-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метил-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фтор-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фтор-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метокси-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метокси-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-хлор-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-хлор-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-4-(3-хлор-4-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-4-(4-хлор-3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метил-4-(3-хлор-4-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метил-4-(4-хлор-3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метокси-4-(3-хлор-4-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метокси-4-(4-хлор-3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-хлор-4-(3-хлор-4-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-хлор-4-(4-хлор-3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 5-(4-метилфенил)-1H-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой 4-фторфенил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 2-фторфенил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой тиен-3-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой циклопропил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 3-фторфенил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой оксазол-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой [1,2,3]тиадиазол-4-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой изоксазол-5-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой фуразан-3-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 4-цианотиен-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой изотиазол-5-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой пиррол-3-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой 5-хлорфуран-2-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-трифторметилфенил)-бензоксазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилбензоксазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилбензоксазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилнафт-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-хлор-6-фенилбензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-хлор-6-фенилбензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой 2-метилкарбониламинотиазол-4-ил, Z представляет собой 4-бифенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-трифторметилфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-хлорфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-хлорфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенил-3-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4,5-трифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-1H-пирроло[2,3-b]пиридин-5-ил, а s равно 0;
соединения, в котором Y представляет собой циклопропил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метил-5-фенилбензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-фторфенил)-5-метилтиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-7-(3-трифторметилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(2,4-дифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(6-трифторметилпиридин-3-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фтор-6-(4-трифторметилфенил)-бензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметилфенил)-1H-бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-метил-5-(3-фторфенил)-тиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-7-(3-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 4-(3-трифторметилфенил)-фенил, Z представляет собой тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметоксифенил)-3-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-6-фториндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-фтор-4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(5-трифторметилтиен-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(6-метоксипиридин-3-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-метилпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой (2-метил-4-фенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-(4-фторфенил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-7-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3,4-дифторфенил)-бензоксазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой 5-хлорфуран-2-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметилфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-2,3-дигидро-1H-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фторфенил)-тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)-1-(3,4-дихлорфенил)-1H-пиразол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-метил-3-(3-трифторметилфенил)-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой оксазол-2-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-трифторметилфенил)-хиназолин-7-ил, а s равно 0;
соединения, в котором Y представляет собой 4-бромтиен-2-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-3-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 1-(4-фторфенил)-3-метилиндол-5-ил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(4-метоксифенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фтор-5-(4-трифторметилфенил)-бензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой оксазол-4-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-трифторметил-6-фенилбензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фторфенил)-5-метилтиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой изотиазол-5-ил, Z представляет собой 1-(4-трифторметилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-трифторметил-6-фенилбензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(4-фторфенил)-2,3-дигидро-1H-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(3-трифторметилфенил)-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-7-(4-фторфенил)-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-хлор-4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)-1-(2,4-дихлорфенил)-4-метил-1H-пиразол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-5-фторфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(6-метилпиридин-3-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дифторфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2-метоксипиридин-4-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фтор-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2-цианофенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-фторфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-7-фториндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 2,2-дифторциклопропил, Z представляет собой 4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-цианофенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой изотиазол-5-ил, Z представляет собой 3-метил-4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-метокси-4-цианофенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-хлор-5-трифторметилпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(2,4-дифторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой изоксазол-5-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2,3-дифенил-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(4-трифторметилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-фторпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилтиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3,5-дифторфенил)-пиразол-1-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(3-фторфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилбензотиазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(6-метилпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(пиридин-4-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-метилпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4-дифторфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-фенилхиназолин-7-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-фторфенил)-бензотиазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-фенилиндол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-цианофенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 1-(3,4-дифторфенил)-3-метилиндол-5-ил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(пиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 4-(5-трифторметилтиен-2-ил)-фенил, Z представляет собой тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-фенилиндазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 4-(5-трифторметилтиен-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(2,4-дифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой фуран-3-ил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенилбензоксазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(3-фторфенил)-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой 5-хлортиен-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-5-трифторметилфенил, а s равно 0;
соединения, в котором Y представляет собой изоксазол-3-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметилфенил)-3-метил-1H-тиено[2,3-c]пиразол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-фторпиримидин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-метил-3-(4-трифторметилфенил)-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-(2-фторпиридин-3-ил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-метил-(2-(4-фторфенил)-тиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-трифторметилфенил)-бензоксазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-3-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-1H-пирроло[3,2-b]пиридин-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилбензоксазол-7-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-метил-3-фенилиндол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-(4-метилфенил)-[1,3,4]оксадиазол-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фторфенил)-тиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-трифторметилфенил)-бензоксазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-цианофенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-фторфенил)-тиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой 4-(5-трифторметилтиен-2-ил)-фенил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой 4-(5-трифторметилтиен-2-ил)-фенил, Z представляет собой 1H-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенилиндазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1,5-дифенилпиразол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(пиридин-2-ил)-бензотиазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой 4-(3-трифторметилфенил)-фенил, Z представляет собой 1H-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-4-метоксифенил, а s равно 0;
соединения, в котором Y представляет собой оксазол-5-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(3-фторфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-аминокарбонилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фтор-3-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(2-хлорфенил)-бензоксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(пиримидин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-(5-метоксипиридин-3-ил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(6-метоксипиридин-3-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-аминокарбонилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3,4-дифторфенил)-бензоксазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4,5-дифенил-1H-имидазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(5-хлорпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(6-метилпиридин-3-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(2-цианофенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 7-(3-фторфенил)-1H-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(5-метилпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(2-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дифторфенил)-бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенилбензотиазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(пиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилбензоксазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-хлорфенил)-бензоксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(пиридин-3-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(2-фторфенил)-бензоксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-1H-бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(4-фторфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(5-метоксипиридин-3-ил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-метилпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 5-(4-хлорфенил)-1-(2,4-дихлорфенил)-4-метил-1H-пиразол-3-ил, а s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(4-метилпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-хлор-5-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(пиримидин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(2-фторфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-3-метил-1H-пиразоло[3,4-b]пиридин-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(4-фторфенил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-(2-метил-2H-пиразол-3-ил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дифторфенил)-2-метилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фтор-5-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилфуро[2,3-b]пиридин-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(тиазол-2-ил)-бензотиазол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(3,5-диметилизоксазол-4-ил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой 2-метил-4-(3-трифторметилфенил)-фенил, Z представляет собой тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-фторфенил)-фуро[2,3-b]пиридин-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-метил-2-(4-метилфенил)-2H-[1,2,3]триазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметилфенил)-2-метилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2-метилпиримидин-4-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 2-метилтиазол-4-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-метил-2-(4-хлорфенил)-2H-[1,2,3]триазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой 1-(3,4-дифторфенил)-3-метилиндол-5-ил, Z представляет собой 1H-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-хлорфенил)-бензоксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-хлор-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой оксазол-4-ил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(бензимидазол-1-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-индол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дихлорфенил)-3,5-диметил-1H-пиразол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-фторфенил)-индол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-2-метилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(3-фторфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенил-2-метилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-3-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-трифторметилфенил)-бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой циклобутил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой 2-фенилбензоксазол-6-ил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-метил-3-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой изотиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенилбензоксазол-7-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-хлорфенил)-бензоксазол-7-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(2,4-дифторфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фтор-3-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(2-метил-2H-пиразол-3-ил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой 3-фторфенил, а s равно 0;
соединения, в котором Y представляет собой 4-(3-трифторметилфенил)-фенил, Z представляет собой 1H-пиррол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(2-фторпиридин-3-ил)-1H-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-(4-метилфенил)-[1,2,3]триазол-1-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(пиридин-3-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(5-фторпиримидин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трифторметилпиразол-1-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(4-метоксифенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(пиридин-3-ил)-бензоксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(фуран-2-ил)-3H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метокси-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-фторфенил)-бензоксазол-7-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-3H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой 2,2-дифторциклопропил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-фторфенил)-бензоксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой 4-(3-трифторметилфенил)-фенил, Z представляет собой оксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-фенил-5-трифторметилфенил, а s равно 0;
соединения, в котором Y представляет собой 2-метил-4-(3-трифторметилфенил)-фенил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1,5-дифенил-1H-пиразол-3-ил, а s равно 0;
соединения, в котором Y представляет собой изоксазол-3-ил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-пиримидин-5-ил-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4-дифторфенил)-2-метилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-метокси-3-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-2-ил, s равно 1, а R1 представляет собой 3-фенилметил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-5-ил, Z представляет собой 4-(5-трифторметилтиен-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой 1H-[1,2,3]триазол-4-ил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4-дифторфенил)-бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 2-фенил-1H-бензимидазол-5-ил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(пиридин-4-ил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-фтор-5-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 2-фенилбензоксазол-6-ил, Z представляет собой тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой [1,2,3]тиадиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-1H-пирроло[3,2-b]пиридин-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(4-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3-фторфенил)-индол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фтор-5-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-фторфенил)-бензоксазол-7-ил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой оксазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-4-ил, s равно 1, а R1 представляет собой 3-фенилметил;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-3-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-4-ил, s равно 1, а R1 представляет собой 2-спироконденсированный циклопропил;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(2-фторфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-хлор-5-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-трифторметилфенил)-2-метилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-хлорфенил)-1H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-2-метилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой 1H-пиррол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бензимидазол-1-ил-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-фторфенил)-1H-бензимидазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-индол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-2-метилбензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1,5-дифенилпиразол-4-ил, а s равно 0;
соединения, в котором Y представляет собой 4-бензимидазол-1-ил-фенил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенил-1H-бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-[1,2,3]триазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-3,5-диметил-1H-пиразол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3-трифторметилпиразол-1-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-трифторметоксифенил)-1H-бензимидазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-3-ил, а s равно 0;
соединения, в котором Y представляет собой 4-бензимидазол-1-ил-фенил, Z представляет собой тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой бифенил-4-ил, s равно 1, а R1 представляет собой 2(R,S)-трифторметил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)-1H-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-индол-3-ил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-3-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиразол-4-ил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(6-трифторметилпиридин-3-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-хлорпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-трифторметилпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фтор-5-фенилбензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(4-фторфенил)-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(4-фторфенил)-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(3-фторфенил)-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-индол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трифторметилфенил)-тиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-хлор-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-3-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фенилтиазол-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(2-хлорфенил)-тиазол-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(2,4-дихлорфенил)-тиазол-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-(3-трифторметилфенил)-5,6-дигидро-4H-циклопентапиразол-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(3,4-дихлорфенил)-тиазол-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(3-трифторметилфенил)-тиазол-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(4-хлорфенил)-пиразол-1-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой 5-бромфуран-2-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой 5-фтортиен-2-ил, Z представляет собой 4-(3-трифторметилфенил)-фенил, а s равно 0;
соединения, в котором Y представляет собой 1-(4-трифторметилфенил)-индол-5-ил, Z представляет собой тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой 1-(4-трифторметилфенил)-индол-5-ил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой 1-(4-трифторметилфенил)-индол-5-ил, Z представляет собой 1H-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(4-трифторметилфенил)-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(3-трифторметилфенил)-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилбензофуран-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(3-трифторметилфенил)-бензофуран-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(4-трифторметилфенил)-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(3-трифторметилфенил)-1H-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-фенилбензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(4-трифторметилфенил)-индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-4-фториндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-6-фториндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-7-фториндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трифторметилфенил)-5-метилтиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-трифторметилфенил)-4-метилтиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-фторфенил)-4-метилтиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(3-трифторметилфенил)-4-метилтиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-7-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-трифторметилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенилиндазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-трифторметилтиен-2-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4-дифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2,4-дифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-3-хлориндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 1H-пиррол-2-ил, Z представляет собой 1-(3,4-дифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4,5-трифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-фторфенил)-3-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметоксифенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-трифторметоксифенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,5-дифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-фтор-4-хлорфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2,5-дифторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметоксифенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-циано-3-метилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-трифторметоксифенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метокси-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-метил-5-фенилфуран-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-трифторметил-5-фенилфуран-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-хлорфенил)-бензоксазол-7-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-хлорфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенилбензоксазол-5-ил и s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой 1H-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-хлорфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-5-трифторметилоксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-фторфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(пиридин-4-ил)-3H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(2-фторфенил)-1H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-хлорфенил)-3H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенил-3H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-фторфенил)-1H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-фторфенил)-1H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(2-хлорфенил)-1H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3,5-дихлорфенил)-тиазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-5-фенилфуран-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 5-фенил-2-трифторметилфуран-3-ил, а s равно 0;
соединения, в котором Y представляет собой циклопентил, Z представляет собой бифенил-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фуран-2-ил-3H-бензимидазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой пиримидин-2-ил, а s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-2-ил, s равно 1, а R1 представляет собой 2-фенил;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-4-ил, s равно 1, а R1 представляет собой 2-фенил;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенил-5-трифторметилоксазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой бифенил-4-ил, s равно 1, а R1 представляет собой 3-фенил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фтор-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метил-4-фенилфенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-трифторметилфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3-трифторметилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(5-хлорпиридин-2-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2-метилпиридин-4-ил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(1-фенилэтил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-(4-фторфенил)-пиразол-1-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метилиндол-1-ил)-фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-4-хлориндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-6-метилиндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-6-хлориндол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-циано-4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-аминокарбонил-4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметилфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-трифторметилфенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-циано-3-метилфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-трифторметоксифенил)-индазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 5-хлортиен-2-ил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 3-фторфенил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 5-хлорфуран-2-ил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой оксазол-2-ил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 5-фтортиен-2-ил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой оксазол-4-ил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой оксазол-5-ил, Z представляет собой 1-(4-фторфенил)-индол-5-ил, а s равно 0;
или его фармацевтически приемлемой соли.
В настоящем изобретении также, помимо прочего, предложена фармацевтическая композиция, включающая, состоящая из и (или) по существу состоящая из фармацевтически приемлемого носителя, фармацевтически приемлемого эксципиента и (или) фармацевтически приемлемого разбавителя, и соединение формулы (I) или его фармацевтически приемлемая соль.
В настоящей заявке также предложены технологии изготовления фармацевтической композиции, включающие, состоящие из и (или) по существу состоящие из смешивания соединения формулы (I) и фармацевтически приемлемого носителя, фармацевтически приемлемого эксципиента и (или) фармацевтически приемлемого разбавителя.
В настоящем изобретении также, помимо прочего, предложены способы лечения или облегчения расстройств, регулируемых MGL, у пациентов, включая человека или других млекопитающих, у которых заболевание, синдром или состояние зависят от модуляции фермента MGL (например, боль и заболевания, ведущие к возникновению такой боли, воспаления и нарушения ЦНС), с применением соединения формулы (I).
В настоящем изобретении также, помимо прочего, предложены способы получения рассматриваемых соединений и фармацевтических композиций, а также лекарственных препаратов, изготовленных на их основе.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В отношении замещающих групп термин «независимо» относится к ситуациям, что когда возможно наличие более одной замещающей группы, указанные заместители могут быть как одинаковыми, так и разными.
Термин «алкил», используемый самостоятельно или для обозначения заместителя, означает прямую или разветвленную углеродную цепь, включающую от 1 до 8 атомов углерода. Следовательно, указанные количества атомов углерода (например, C1-8) независимо обозначают количество атомов углерода в алкильном фрагменте или алкильной части более крупного алкилсодержащего заместителя. В группах заместителей, содержащих несколько алкильных групп, например, (C1-6алкил)2амино, C1-6алкильные группы диалкиламино могут быть одинаковыми или могут различаться.
Термин «алкокси» обозначает -O-алкильную группу, в которой термин «алкил» соответствует приведенному выше определению.
Термины «алкенил» и «алкинил» обозначают прямые и разветвленные углеродные цепи, включающие 2 или более атомов углерода, где алкениловая цепь содержит по меньшей мере одну двойную связь, а алкиниловая цепь содержит по меньшей мере одну тройную связь.
Термин «циклоалкил» обозначает насыщенное или частично насыщенное, моноциклическое или полициклическое углеводородное кольцо, включающее от 3 до 14 атомов углерода. Примеры таких колец включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и адамантил.
Термин «бензоконденсированный циклоалкил» обозначает 5-8-членное моноциклическое циклоалкильное кольцо, конденсированное с бензольным кольцом. Атомы углерода, образующие циклоалкильное кольцо, могут быть полностью или частично насыщенными.
Термин «гетероциклил» обозначает неароматическую моноциклическую или бициклическую кольцевую систему, включающую от 3 до 10 атомов и содержащую атомы углерода и от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из N, O и S. Определение термина «гетероциклил» также включает неароматическое циклическое кольцо, состоящее из 5-7 атомов, из которых 1-2 атома - атомы азота, или неароматическое циклическое кольцо, состоящее из 5-7 атомов, из которых атомы 0, 1 или 2 представляют собой атомы азота, а до 2 атомов представляют собой атомы кислорода или серы и по меньшей мере один атом должен быть атомом азота, кислорода или серы; где (необязательно) кольцо содержит от нуля до одной ненасыщенной связи и (необязательно, когда кольцо состоит из 6 или 7 атомов) оно содержит до 2 ненасыщенных связей. Атомы углерода, образующие гетероциклическое кольцо, могут быть полностью насыщенными или частично насыщенными. Определение термина «гетероциклил» также включает две 5-членные моноциклические гетероциклоалкильные группы, соединенные мостиковой связью с образованием бициклического кольца. Такие группы не считаются полностью ароматическими и не обозначаются как гетероарильные группы. В случае если гетероциклил является бициклическим, оба кольца гетероциклила и по меньшей мере одно из колец содержит член с гетероциклическим ядром. Примеры гетероциклических групп, помимо прочего, включают пирролинил (включая 2H-пиррол, 2-пирролинил или 3-пирролинил), пирролидинил, имидазолинил, имидазолидинил, пиразолинил, пиразолидинил, пиперидинил, морфолинил, тиоморфолинил и пиперазинил. Если не указано иное, гетероциклил присоединен к своей боковой группе на любом гетероатоме или атоме углерода с образованием стабильной структуры.
Термин «бензоконденсированный гетероциклил» обозначает 5-7-членное моноциклическое гетероциклическое кольцо, конденсированное с бензольным кольцом. Гетероциклическое кольцо содержит атомы углерода и от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из N, O и S. Атомы углерода, образующие гетероциклическое кольцо, могут быть полностью насыщенными или частично насыщенными. Если не указано иное, бензоконденсированное гетероциклическое кольцо присоединено к своей боковой группе на атоме углерода бензольного кольца.
Термин «арил» обозначает ненасыщенное ароматическое моноциклическое или бициклическое кольцо, включающее от 6 до 10 атомов углерода. Примеры арильных колец включают фенил и нафталенил.
Термин «гетероарил» обозначает ароматическую моноциклическую или бициклическую кольцевую систему, содержащую от 5 до 10 атомов-членов кольца и содержащую атомы углерода и от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из N, O и S. Определение термина «гетероарил» включает 5 или 6-членные ароматическое кольца, в которых кольцо состоит из атомов углерода и содержит по меньшей мере один гетероатом. Гетероатомы включают азот, кислород и серу. В случае 5-членных колец гетероарильное кольцо предпочтительно содержит один атом азота, кислорода или серы и, кроме того, до 3 дополнительных атомов водорода. В случае 6-членных колец гетероарильное кольцо предпочтительно содержит от 1 до 3 атомов азота. В случае когда 6-членное кольцо имеет 3 атома азота, чаще всего 2 атома азота являются смежными. Если гетероарил является бициклическим, в каждом кольце присутствует по меньшей мере один гетероатом. Примеры гетероарильных групп включают фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, оксадиазолил, триазолил, тиадиазолил, пиридинил, пиридазинил, пиримидинил и пиразинил. Если не указано иное, гетероарил присоединен к своей боковой группе на любом гетероатоме или атоме углерода с образованием стабильной структуры.
Если не указано иное, термин «бензоконденсированный гетероарил» обозначает 5-6-членное моноциклическое гетероарильное кольцо, конденсированное с бензольным кольцом. Гетероарильное кольцо содержит атомы углерода и от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из N, O и S. Примеры гетероарильных групп с необязательно конденсированными бензольными кольцами включают индолил, изоиндолил, индолинил, бензофурил, бензотиенил, индазолил, бензимидазолил, бензотиазолил, бензоксазолил, бензизоксазолил, бензотиадиазолил, бензотриазолил, хинолинил, изохинолинил и хиназолинил. Если не указано иное, бензоконденсированный гетероарил присоединен к своей боковой группе на любом гетероатоме или атоме углерода с образованием стабильной структуры.
Термин «галоген» или «гало» обозначает фтор, хлор, бром и йод.
Термин «формил» обозначает группу -C(=O)H.
Термин «оксо» обозначает группу (=O).
Если термин «алкил» или «арил», либо любой из образованных от этих корней префиксов появляется в названии заместителя (например, арилалкил, алкиламино), то подразумевается, что все оговоренные выше ограничения для терминов «алкил» и «арил» переносятся и на производные названия. Указание количества атомов углерода (например, C1-C6) относится независимо к количеству атомов углерода в алкильном фрагменте или алкильной части более крупного заместителя, в названии которого корень «алкил» используется в качестве префикса. Для алкильных и алкокси-заместителей указанное количество атомов углерода включает все независимые атомы-члены кольца, входящие в указанный диапазон. Например, C1-6 алкил включает по отдельности метил, этил, пропил, бутил, пентил и гексил, а также их подкомбинации (например, C1-2, C1-3, C1-4, C1-5, C2-6, C3-6, C4-6, C5-6, C2-5 и т.д.).
Как правило, в рамках используемой в описании настоящего изобретения стандартной номенклатуры первой указывается концевая часть описываемой боковой цепи, затем перечисляются следующие функциональные группы в направлении к точке присоединения заместителя. Так, например, описание заместителя C1-C6алкилкарбонила относится к группе следующей формулы:

Описанная ниже система нумерации используется для описания позиции R1 заместителей на пиперазинильном кольце формулы (I):

Термин «R» в стереоцентре означает, что стереоцентр имеет абсолютную R-конфигурацию согласно определению, принятому в отрасли. Аналогично, термин «S» означает, что стереоцентр имеет абсолютную S-конфигурацию. Используемые в настоящей заявке термины «*R» или «*S» в стереоцентре используются для обозначения того, что стереоцентр имеет абсолютную, но неизвестную конфигурацию. Используемый в настоящей заявке термин «RS» обозначает стереоцентр, существующий в форме смеси R- и S-конфигураций. Аналогичным образом, термины «*RS» или «*SR» обозначают стереоцентры, существующие в форме смеси R- и S-конфигураций и имеющие неизвестную конфигурацию относительно другого стереоцентра в молекуле.
Соединения, содержащие один стереоцентр без обозначения стереосвязи, представляют собой смесь 2 энантиомеров. Соединения, содержащие 2 стереоцентра без обозначения стереосвязи для обоих из них, представляют собой смесь 4 диастереомеров. Соединения с двумя стереоцентрами, оба из которых обозначены «RS» и имеют обозначения стереосвязи, представляют собой 2-компонентную смесь, обладающую соответствующими стереохимическими характеристиками, как показано в структурной формуле. Соединения с двумя стереоцентрами, оба из которых обозначены «*RS» и имеют обозначения стереосвязи, представляют собой 2-компонентную смесь с соответствующими неизвестными стереохимическими характеристиками. Необозначенные стереоцентры, указанные в структурной формуле без обозначения стереосвязей, представляют собой смесь R- и S-конфигураций. Для необозначенных стереоцентров, структурная формула которых приводится с обозначениями стереосвязей, абсолютные стереохимические характеристики соответствуют изображенной формуле.
Если не указано иное, предполагается, что определение какого-либо заместителя или переменной на определенной позиции в молекуле не зависит от соответствующих определений на других участках молекулы. При этом заместители и модели замещения, используемые в соединениях формулы (I), указанных в настоящем документе, могут выбираться средним специалистом отрасли для получения химически стабильных соединений, которые можно легко синтезировать с применением известных в отрасли технологий, а также способов, описанных в настоящей заявке.
Термин «пациент» обозначает животное, предпочтительно млекопитающее, наиболее предпочтительно человек, являющееся объектом лечения, наблюдения или эксперимента.
Термин «терапевтически эффективное количество» обозначает количество активного соединения или фармацевтической субстанции, включая соединение, предлагаемое в настоящем изобретении, которое вызывает биологическую или медицинскую реакцию в системе тканей (животного или человека), необходимую исследователю, ветеринару, врачу или другому клиницисту, включая облегчение или частичное облегчение симптомов заболевания, синдрома, состояния или расстройства, требующего лечения.
Термин «композиция» обозначает препарат, включающий указанные ингредиенты в терапевтически эффективных количествах, а также любой препарат, полученный (прямо или косвенно) из комбинаций указанных ингредиентов в указанных количествах.
Термин «ингибитор MGL» призван охватить соединение, взаимодействующее с MGL с целью существенно сократить или ликвидировать его каталитическую активность, тем самым повышая концентрацию его субстрата(ов). Термин «регулируемый MGL» используется для обозначения состояния, зависящего от модуляции фермента MGL, включая состояние, зависящее от ингибирования фермента MGL, например, боль и заболевания, ведущие к возникновению такой боли, воспаления и нарушения ЦНС.
Если не указано иное, используемый в настоящей заявке термин «зависеть» или «зависящий» (в отношении заболевания, синдрома, состояния или расстройства, зависящего от ингибирования MGL) включает снижение частоты и (или) снижение тяжести одного или нескольких симптомов или проявлений указанного заболевания, синдрома, состояния или расстройства, и (или) включает профилактику развития одного или нескольких симптомов или проявлений упомянутого заболевания, синдрома, состояния или расстройства либо развития заболевания, синдрома, состояния или расстройства.
Соединения формулы (I) полезны для применения в способах лечения, облегчения и (или) профилактики заболеваний, синдромов, состояний или расстройств, зависящих от ингибирования MGL. Такие способы включают, состоят из и (или) по существу состоят из назначения пациенту (включая животных, млекопитающих и человека), нуждающемуся в таком лечении, облегчении и (или) профилактике, терапевтически эффективного количества соединения формулы (I), указанного в настоящем документе, или его энантиомера, диастереомера, сольвата или фармацевтически приемлемой соли. В частности, соединения формулы (I), определенной в настоящей заявке, могут найти применение для лечения, облегчения и (или) предотвращения боли, болезней, синдромов, состояний или расстройств, вызывающих такую боль, воспаления и (или) расстройства центральной нервной системы. В частности, соединения формулы (I), указанные в настоящем документе, полезны при лечении, облегчении и (или) профилактике воспалительной боли, состояний повышенной чувствительности при воспалениях и (или) нейропатической боли. Такое лечение, облегчение и (или) профилактика включает назначение пациенту, требующему лечения, терапевтически эффективного количества соединения формулы (I), указанного в настоящем документе.
Примеры воспалительной боли включают боли, вызванные заболеванием, состоянием, синдромом, расстройством или болезненное состояние, в том числе воспалительные заболевания кишечника, висцеральную боль, мигрень, послеоперационные боли, остеоартроз, ревматоидный артрит, боли в спине, боль в пояснице, боли в суставах, боль в животе, боль в груди, схватки, заболевания опорно-двигательного аппарата, кожные заболевания, зубную боль, изжогу, ожог, солнечный ожог, укус змеи, укус ядовитой змеи, укус паука, укус насекомого, нейрогенный мочевой пузырь, интерстициальный цистит, инфекцию мочевыводящих путей, ринит, контактный дерматит или гиперчувствительность, зуд, экзема, фарингит, мукозит, энтерит, синдром раздраженной толстой кишки, холецистит, панкреатит, постмастэктомический болевой синдром, менструальные боли, эндометриоз, боль из-за физической травмы, головную боль, синусовую головную боль, головную боль от напряжения или арахноидит.
Одним из видов воспалительной боли является воспалительная гипералгезия или гиперчувствительность. Примеры воспалительной гипералгезии включают болезни, синдромы, состояния, расстройства или болевые состояния, включая воспаление, остеоартрит, ревматоидный артрит, боли в спине, суставах, брюшной области, костно-мышечные заболевания, заболевания кожи, послеоперационную боль, головные боли, зубную боль, ожоги, солнечные ожоги, укусы насекомых, нейрогенный мочевой пузырь, недержание мочи, интерстициальный цистит, инфекции мочевых путей, кашель, астму, хроническое обструктивное заболевание легких, ринит, контактный дерматит/аллергию, зуд, экзему, фарингит, энтерит, синдром раздраженной толстой кишки, воспалительные заболевания кишечника, включая болезнь Крона, язвенный колит, недержание мочи, доброкачественную простатическую гипертрофию, кашель, астму, ринит, повышенную чувствительность носа, зуд, контактные дерматиты и (или) кожную аллергию и хроническое обструктивное заболевание легких.
В одном варианте осуществления настоящее изобретение относится к способу лечения, облегчения и (или) профилактики висцеральной гипералгезии с повышенной висцеральной чувствительностью, включающему, состоящему из и (или) по существу состоящему из этапа назначения пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения, соли или сольвата формулы (I), указанных в настоящем документе. В дополнительном варианте осуществления настоящее изобретение направлено на способ лечения воспалительной соматической гипералгезии, при которой имеет место повышенная чувствительность к температурным, механическим и (или) химическим раздражителям, включающий назначение нуждающемуся в таком лечении млекопитающему терапевтически эффективной дозы соединения формулы (I) либо его энантиомера, диастереомера, сольвата или фармацевтически допустимой соли.
Дополнительный вариант осуществления настоящего изобретения относится к способу лечения, смягчения или предотвращения нейропатической боли. К примерам нейропатической боли относятся боль, вызванная заболеванием, синдромом, состоянием, расстройством, или болезненное состояние, в том числе рак, неврологические расстройства, операции спинного мозга и периферических нервов, опухоль головного мозга, черепно-мозговая травма (ЧМТ), травмы спинного мозга, синдром хронической боли, фибромиалгия, синдром хронической усталости, волчанка, саркоидоз, периферическая невропатия, двусторонняя периферическая невропатия, диабетическая нейропатия, центральная боль, невропатия, связанная с повреждением спинного мозга, инсульт, боковой амиотрофический склероз (БАС), болезнь Паркинсона, рассеянный склероз, воспаление седалищного нерва, невралгия нижнечелюстного сустава, периферический неврит, полиневрит, боль после ампутации, фантомная боль в конечностях, переломы костей, нейропатическая боль во рту, боли Шарко, комплексный регионарный болевой синдром I и II (КРБС I/II), радикулопатия, синдром Гийена-Барре, парестетический ишиас, синдром жжения во рту, неврит зрительного нерва, постфебрильный неврит, мигрирующий неврит, сегментарный неврит, неврит Гомбо, нейронит, шейно-плечевая невралгия, черепная невралгия, невралгия коленных суставов, языкоглоточная невралгия, мигренозная невралгия, идиопатическая невралгия, межреберная невралгия, невралгия молочных желез, невралгия Мортона, назоцилиарная невралгия, затылочная невралгия, постгерпетическая невралгия, каузалгия, красная невралгия, невралгия Сладера, невралгия крылонебного узла, надглазничная невралгия, невралгия тройничного нерва, вульводиния или невралгия Видиана.
Один вид нейропатической боли представляет собой нейропатическую холодовую аллодинию, которая характеризуется наличием связанного с нейропатией аллодинического состояния с повышенной чувствительностью к холодовым раздражителям. Примеры нейропатической холодовой аллодинии включают аллодинию вследствие заболевания, состояния, синдрома, расстройства или болевого состояния, включая невропатическую боль (невралгию), боль, возникающую после операции или травмы спинного или периферического нерва, травматические повреждения мозга (ТПМ), тригеминальную невралгию, постгерпетическую невралгию, каузалгию, периферическую невропатию, диабетическую невропатию, центральную боль, приступы, периферический неврит, полиневрит, комплексный регионарный болевой синдром I и II степени (КРБС I/II) и радикулопатию.
В другом варианте осуществления настоящее изобретение относится к способу лечения, облегчения и (или) профилактики нейропатической холодовой аллодинии с повышенной чувствительностью к холодовым раздражителям, включающему, состоящему из и (или) по существу состоящему из этапа назначения пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения формулы (I), указанного в настоящем документе, или его энантиомера, диастереомера, сольвата или фармацевтически приемлемой соли.
Дополнительный вариант осуществления настоящего изобретения относится к способу лечения, смягчения или предотвращения расстройств ЦНС. Примеры расстройств центральной нервной системы включают беспокойства, такие как социальное беспокойство, посттравматический стресс, фобии, социофобия, особые фобии, паническое расстройство, обсессивно-компульсивное расстройство, острый стресс, расстройство, тревожное расстройство, вызванное разлукой и генерализированное тревожное расстройство, а также депрессии, такие как большая депрессия, биполярное расстройство, зимняя депрессия, послеродовая депрессия, маниакально-депрессивный психоз и биполярная депрессия.
Настоящее изобретение включает фармацевтическую композицию, содержащую соединение формулы (I), где:
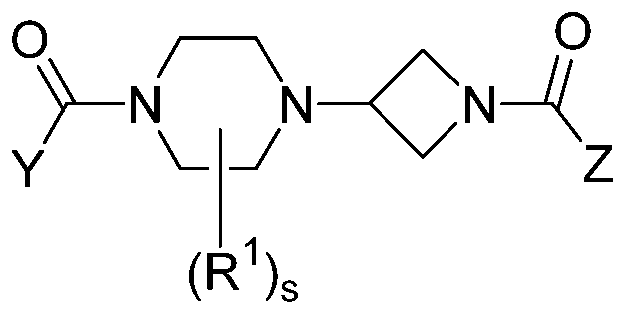
Формула (I)
где
a) Группа a) представляет собой
i) замещенный C6-10 арил;
ii) C3-8 циклоалкил, необязательно замещенный одним или двумя фтор-заместителями;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, изоксазолила, бензотиенила, тиено[3,2-b]тиофен-2-ила, триазолила и [1,2,3]тиадиазолила;
в котором C6-10 арил замещен; а гетероарил необязательно замещен; один заместитель выбран из группы, состоящей из фтора, хлора, брома, C1-4алкила, циано и трифторметила.
b) Группа a) представляет собой
i) замещенный C6-10 арил;
ii) C3-8 циклоалкил, необязательно замещенный одним или двумя фтор заместителями;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, изоксазолила, тиено[3,2-b]тиофен-2-ил и [1,2,3]тиадиазолила;
в котором C6-10 арил, замещен; гетероарил необязательно замещен; один заместитель выбран из группы, состоящей из фтора, хлора, брома, C1-4алкила и трифторметила;
c) Группа a) представляет собой
i) циклопропил, необязательно замещенный одним или двумя фтор-заместителями;
ii) трифторметил; или
iii) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила и изоксазолила;
в котором C6-10 арил замещен; гетероарил необязательно замещен; один заместитель выбран из группы, состоящей из фтора, хлора, брома и трифторметила.
d) Группа b) представляет собой
i) C6-10 арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1H-пирроло[3,2-b]пиридин-5-ила, 1H-тиено[2,3-c]пиразол-5-ила, 1H-пирроло[2,3-b]пиридин-5-ила, 1H-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, хиназолинила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пирролила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1H-индолил;
iv) 2,3 дифенилиндолил;
v) дифенилимидазолил;
vi) 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1H-индазол-3-ил;
vii) 3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил;
viii) 1-(4-фторфенил)-1H-пирроло[3,2-b]пиридин-6-ил; или
ix) дифенил-1H-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем;
в котором C6-10 арил, 2,3-дигидро-1H-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила, а также замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10 арила;
ii) гетероарила, выбранного из группы, состоящей из пиримидинила, тиенила, хинолинила, пиридинила, изоксазолила, тиазолила, бензимидазолила, пирролила, фуранила, пиримидинила и пиразолила; или
iii) 5,6-дигидро-4H-циклопентапиразол-2-ила;
в котором указанный гетероарил и 5,6-дигидро-4Н-циклопентапиразол-2-ил необязательно замещены одним фенильным заместителем, необязательно замещенным одним или двумя хлор заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкоксикарбониламино; C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителей, представляющих собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано) этиламинокарбонила; циано; карбокси; аминокарбонила; формила; нитро; брома; гидрокси; ди-(C1-4алкил)аминосульфонила; C1-4алкилсульфонила; -OCH2O-, присоединенного к соседним атомам углерода; и NRcRd, в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкил, C1-6алкилкарбонил, C1-6алкоксикарбонил и C1-4алкилсульфонил;
e) Группа b) представляет собой
i) C6-10 арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1H-пирроло[3,2-b]пиридин-5-ила, 1H-тиено[2,3-c]пиразол-5-ила, 1H-пирроло[2,3-b]пиридин-5-ила, 1H-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, хиназолинила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1H-индолил;
iv) 2,3 дифенилиндолил;
v) дифенилимидазолил;
vi) 3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил; или
vii) дифенил-1H-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем;
в котором C6-10 арил, 2,3-дигидро-1H-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила, а также замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10 арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила, изоксазолила, бензимидазолила, фуранила, пиримидинила и пиразолила; или
iii) 5,6-дигидро-4H-циклопентапиразол-2-ила;
в котором указанный гетероарил и 5,6-дигидро-4Н-циклопентапиразол-2-ил необязательно замещены одним фенильным заместителем, необязательно замещенным одним или двумя хлор-заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителей, представляющих собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано) этиламинокарбонила; циано; аминокарбонила; формила; нитро; брома; гидрокси; ди-(C1-4алкил)аминосульфонила; C1-4алкилсульфонила; -OCH2O-, присоединенного к соседним атомам углерода; NRcRd; в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкил, C1-6алкилкарбонил, C1-6алкоксикарбонил и C1-4алкилсульфонил;
f) Группа b) представляет собой
i) C6-10 арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1H-пирроло[3,2-b]пиридин-5-ила, 1H-тиено[2,3-c]пиразол-5-ила, 1H-пирроло[2,3-b]пиридин-5-ила, хиназолинила, фуранила, тиенила, [1,3,4]оксадиазол-2-ила и бензимидазолила;
iii) 2,3-дигидро-1H-индолил;
iv) 2,3 дифенилиндолил;
v) дифенилимидазолил;
vi) 3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил; или
vii) дифенил-1H-пиразол-3-ил; в котором каждый фенил независимо замещен одним или двумя хлор-заместителями;
в котором C6-10 арил, 2,3-дигидро-1H-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила, а также замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10 арила;
ii) гетероарила, выбранного из группы, состоящей из пиримидинила, тиенила, хинолинила, пиридинила, пиримидинила и пиразолила; или
iii) 5,6-дигидро-4H-циклопентапиразол-2-ила;
в котором указанный гетероарил и 5,6-дигидро-4Н-циклопентапиразол-2-ил необязательно замещены одним фенильным заместителем, необязательно замещенным одним или двумя хлор-заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителей, включающих хлор или фтор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; формила; нитро; брома; гидрокси; ди-(C1-4алкил)аминосульфонила; C1-4алкилсульфонила; -OCH2O-, присоединенного к соседним атомам углерода; NRcRd; в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкоксикарбонил, и C1-4алкилсульфонил;
g) s равно 0 или 1;
h) s равно 0;
i) R1 представляет собой C6-10арил, C1-3алкил или арил(C1-3)алкил;
j) R1 представляет собой фенил или C1-3алкил;
k) R1 представляет собой фенил;
и любое сочетание указанных выше вариантов осуществления a)-k), при условии что предполагается, что исключены комбинации, в которых будут объединены различные варианты осуществления с одинаковыми заместителями;
и при условии, что соединение формулы (I) отлично от
соединения, в котором Y представляет собой 3-хлорбензотиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 2-цианофенил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой пиримидин-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, s равно 1, а R1 представляет собой 3-фенил;
а также его энантиомеры, диастереомеры, сольваты и фармацевтически приемлемые соли.
Для использования в медицинских целях соли соединений формулы (I), указанных в настоящем документе, относятся к нетоксичным «фармацевтически приемлемым солям». Однако для получения соединений формулы (I), указанных в настоящем документе, или их фармацевтически приемлемых солей могут использоваться и другие соли. Соответствующие фармацевтически приемлемые соли соединений формулы (I), указанных в настоящем документе, включают кислотно-аддитивные соли, полученные, например, путем смешивания раствора соединения с раствором фармацевтически приемлемой кислоты, такой как соляная кислота, серная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, уксусная кислота, бензойная кислота, лимонная кислота, виннокаменная кислота, угольная кислота или фосфорная кислота. Кроме того, в случаях когда соединения формулы (I), указанные в настоящем документе, имеют кислотный фрагмент, его соответствующие фармацевтически приемлемые соли могут включать соли щелочных металлов, например соли натрия или калия; соли щелочноземельных металлов, например соли кальция или магния; а также соли, образованные соответствующими органическими лигандами, например четвертичные аммониевые соли. Таким образом, типичные примеры фармацевтически приемлемых солей включают в себя следующие соли: ацетаты, бензолсульфонаты, бензоаты, бикарбонаты, бисульфаты, битартраты, бораты, бромиды, кальция эдетаты, камсилаты, карбонаты, хлориды, клавуланаты, цитраты, дигидрохлориды, эдетаты, эдисилаты, эстолаты, эсилаты, фумараты, глуцептаты, глюконаты, глутаматы, гликоллиларсанилаты, гексилрезорцинаты, гидрабамины, гидробромиды, гидрохлориды, гидроксинафтоаты, йодиды, изотионаты, лактаты, лактобионаты, лаураты, малаты, малеаты, манделаты, мезилаты, метилбромиды, метилнитраты, метилсульфаты, мукаты, напсилаты, нитраты, N-метилглюкамина аммониевые соли, олеаты, памоаты (эмбонаты), пальмитаты, пантотенаты, фосфаты/дифосфаты, полигалактуронаты, салицилаты, стеараты, сульфаты, субацетаты, сукцинаты, таннаты, тартраты, теоклаты, тозилаты, триэтиодиды и валераты.
Типичные примеры кислот и оснований, которые можно использовать для получения фармацевтически приемлемых солей, включают кислоты, в том числе уксусную кислоту, 2,2-дихлоруксусную кислоту, ацилированные аминокислоты, адипиновую кислоту, альгиновую кислоту, аскорбиновую кислоту, L-аспарагиновую кислоту, бензолсульфоновую кислоту, бензойную кислоту, 4-ацетамидобензойную кислоту, (+)-камфорную кислоту, камфорсульфокислоту, (+)-(1S)-камфор-10-сульфокислоту, каприновую кислоту, капроновую кислоту, каприловую кислоту, коричную кислоту, лимонную кислоту, цикламовую кислоту, додецилсерную кислоту, этан-1,2-дисульфокислоту, этансульфокислоту, 2-гидроксиэтансульфокислоту, муравьиную кислоту, фумаровую кислоту, галактаровую кислоту, гентизиновую кислоту, глюкогептоновую кислоту, D-глюконовую кислоту, D-глюкороновую кислоту, L-глютаминовую кислоту, α-оксоглутаровую кислоту, гликолевую кислоту, гиппуровую кислоту, бромистоводородную кислоту, соляную кислоту, (+)-L-молочную кислоту, (±)-DL-молочную кислоту, лактобионовую кислоту, малеиновую кислоту, (-)-L-яблочную кислоту, малоновую кислоту, (±)-DL-миндальную кислоту, метансульфокислоту, нафталин-2-сульфокислоту, нафталин-1,5-дисульфокислоту, 1-гидрокси-2-нафтойную кислоту, никотиновую кислоту, азотную кислоту, олеиновую кислоту, оротовую кислоту, щавелевую кислоту, пальмитиновую кислоту, памовую кислоту, фосфорную кислоту, L-пироглютаминовую кислоту, салициловую кислоту, 4-аминосалициловую кислоту, себациновую кислоту, стеариновую кислоту, янтарную кислоту, серную кислоту, дубильную кислоту, (+)-L-виннокаменную кислоту, тиоциановую кислоту, п-толуолсульфокислоту и ундециленовую кислоту; а также основания, в том числе аммиак, L-аргинин, бенетамин, бензатин, гидроксид кальция, холин, динол, диэтаноламин, диэтиламин, 2-(диэтиламино)-этанол, этаноламин, этилендиамин, N-метилглюкамин, гидрабамин, 1H-имидазол, L-лизин, гидроксид магния, 4-(2-гидроксиэтил)-морфолин, пиперазин, гидроксид калия, 1-(2-гидроксиэтил)-пирролидин, вторичный амин, гидроксид натрия, триэтаноламин, трометамин и гидроксид цинка.
Варианты осуществления настоящего изобретения включают пролекарства соединений формулы (I), указанных в настоящем документе. В целом подобные пролекарства представляют собой функциональные производные соединений, составляющих предмет настоящего изобретения, которые in vivo легко превращаются в требуемое соединение. Таким образом, в вариантах осуществления настоящего изобретения, относящихся к способам лечения или профилактики, термин «применение» («прием», «назначение») охватывает лечение или профилактику различных заболеваний, состояний, синдромов и расстройств, упоминаемых в описании соединения, являющегося предметом настоящего изобретения, или соединения, не упоминаемого в настоящем описании, но преобразующегося в указанное соединение in vivo после его приема пациентом. Общепринятые процедуры отбора и приготовления соответствующих производных пролекарственных форм описаны, например, в работе Design of Prodrugs, Ed. H. Bundgaard, Elsevier, 1985.
В тех случаях, когда в определенных вариантах осуществления настоящего изобретения у соединений имеется два или более хиральных центров, они могут соответствующим образом существовать в форме энантиомеров. В тех случаях, когда соединения обладают двумя или более хиральными центрами, они дополнительно могут существовать в форме диастереомеров. Необходимо понимать, что все подобные изомеры и их смеси подпадают под действие настоящего изобретения. Кроме того, некоторые из кристаллических форм соединений настоящего изобретения могут существовать в виде полиморфов, и в таком качестве они подпадают под действие настоящего изобретения. Кроме того, некоторые из соединений могут образовывать сольваты с водой (то есть гидраты) или широко распространенными органическими растворителями, при этом такие сольваты также подпадают под действие настоящего изобретения. Специалисты в данной области понимают, что используемый в настоящей заявке термин «соединение» считается включающим сольватированные соединения формулы I.
В тех случаях, когда процессы получения соединений в соответствии с вариантами осуществления настоящего изобретения приводят к образованию смеси стереоизомеров, эти изомеры могут быть изолированы при помощи стандартных способов, таких как препаративная хроматография. Соединения могут быть получены в форме рацематов, либо отдельные энантиомеры могут быть получены в результате энантиоспецифического синтеза либо путем разделения. Например, соединения могут быть разделены на составляющие энантиомеры с использованием стандартных способов, таких как формирование диастереометрических пар путем образования солей с оптически активными кислотами, например, (-)-ди-п-толуоил-D-виннокаменная кислота и (или) (+)-ди-п-толуоил-L-виннокаменная кислота с последующей фракционной кристаллизацией и восстановлением свободного основания. Соединения могут также быть разделены с помощью образования диастереомерных эфиров или амидов с последующим хроматографическим разделением и удалением хирального партнера. В альтернативном варианте такие соединения могут быть разделены при помощи хиральной колонки для ВЭЖХ.
Один вариант осуществления настоящего изобретения относится к композиции (включая фармацевтическую композицию), включающей, состоящей из и (или) по существу состоящей из (+)-энантиомера соединения формулы (I), указанного в настоящем документе, где упомянутая композиция по существу не содержит (-)-изомера указанного соединения. В контексте настоящего документа термин «по существу не содержит» означает содержание (-)-изомера в концентрации менее приблизительно 25%, предпочтительно - менее приблизительно 10%, более предпочтительно - менее приблизительно 5%, еще более предпочтительно - менее приблизительно 2%, а еще более предпочтительно - менее приблизительно 1% при вычислении по следующей формуле:
 .
.
Другой вариант осуществления настоящего изобретения представляет собой композицию (включая фармацевтическую композицию), включающую, состоящую из и (или) по существу состоящую из (-)-энантиомера соединения формулы (I), указанного в настоящем документе, где указанная композиция практически не содержит (+)-изомера указанного соединения. В данном контексте «по существу отсутствует» означает менее 25%, предпочтительно - менее 10%, еще более предпочтительно - менее 5%, даже более предпочтительно - менее 2% и наиболее предпочтительно - менее 1% (+)-изомера, содержание которого рассчитывается по следующей формуле:
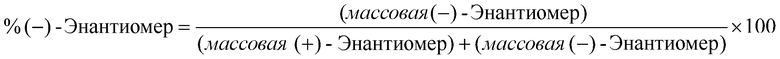 .
.
В ходе процессов получения соединений в соответствии с вариантами осуществления настоящего изобретения может возникнуть необходимость в защите чувствительных или реакционных групп на любой из рассматриваемых молекул. Для этих целей могут использоваться стандартные защитные группы, например, описанные в книгах Protective Groups in Organic Chemistry, Second Edition, J.F.W. McOmie, Plenum Press, 1973; T.W. Greene & P.G.M. Wuts, Protective Groups in Organic Synthesis, John Wiley & Sons, 1991 и T.W. Greene & P.G.M. Wuts, Protective Groups in Organic Synthesis, Third Edition, John Wiley & Sons, 1999. Введенные защитные группы могут быть впоследствии удалены на любой удобной для этого стадии с применением известных специалистам способов.
Хотя входящие в состав вариантов осуществления настоящего изобретения соединения (включая их фармацевтически приемлемые соли и фармацевтически приемлемые сольваты) могут вводиться пациенту отдельно, как правило, они будут вводиться в виде смеси с фармацевтически приемлемым носителем, эксципиентом или разбавителем, выбираемым с учетом предполагаемого способа введения и стандартной фармацевтической или ветеринарной практики. Следовательно, частные варианты осуществления настоящего изобретения относятся к фармацевтическим и ветеринарным композициям, включающим соединения формулы (I), указанные в настоящем документе, и по меньшей мере один фармацевтически приемлемый носитель, фармацевтически приемлемый эксципиент и (или) фармацевтически приемлемый разбавитель.
Например, в фармацевтических композициях в соответствии с вариантами осуществления настоящего изобретения соединения формулы (I), указанные в настоящем документе, могут быть смешаны с любым подходящим связывающим веществом (связывающими веществами), скользящим веществом (скользящими веществами), суспендирующим веществом (суспендирующими веществами), веществом (веществами) для нанесения оболочки, солюбилизирующим веществом (солюбилизирующими веществами), а также комбинациями указанных веществ.
Твердые пероральные лекарственные формы, такие как таблетки или капсулы, содержащие соединения, входящие в состав настоящего изобретения, могут вводиться по мере необходимости по меньшей мере в одной лекарственной форме за один раз. Описываемые соединения также могут вводиться в виде составов с замедленным высвобождением активного агента.
Дополнительные лекарственные формы для перорального применения, в которых могут применяться соединения в соответствии с настоящим изобретением, включают эликсиры, растворы, сиропы и суспензии. Каждая из таких форм необязательно может содержать вкусовые добавки и красители.
В другом варианте осуществления настоящего изобретения соединения формулы (I), указанные в настоящем документе, могут применяться в виде ингаляций (интратрахеальных или интраназальных) либо в форме суппозиториев или пессариев, а также могут наноситься местно в виде лосьонов, растворов, кремов, мазей или присыпок. Например, их можно включить в крем, включающий, состоящий из и (или) по существу состоящий из водной эмульсии полиэтиленгликолей или жидкого парафина. Их также можно включать в концентрации приблизительно от 1 до 10% по массе крема, в мазь, включающую, состоящую из и (или) по существу состоящую из белого воска или белой мягкой парафиновой основы с любыми необходимыми стабилизаторами и консервантами. К альтернативным способам введения относится чрескожное введение с помощью дермального или трансдермального пластыря.
Фармацевтический состав настоящего изобретения (а также входящих в его состав соединений по отдельности) можно вводить парентерально, например, интракавернозно, внутривенно, внутримышечно, подкожно, внутрикожно или интратекально. В таких случаях состав также включает по меньшей мере один подходящий носитель, один эксципиент и один растворитель.
При парентеральном введении фармацевтические составляющие настоящего изобретения лучше всего использовать в виде стерильного водного раствора, который может содержать другие вещества, например, достаточное количество солей и моносахаридов, чтобы раствор был изотоническим с кровью.
При буккальном или сублингвальном введении фармацевтические составляющие настоящего изобретения можно вводить в виде таблеток, изготавливать которые можно обычным способом.
Кроме того, как пример, фармацевтические композиции, содержащие в качестве активного ингредиента по меньшей мере одно из соединений формулы (I), указанных в настоящем документе, могут изготавливаться путем смешения данного соединения (соединений) с фармацевтически приемлемым носителем, фармацевтически приемлемым разбавителем и (или) фармацевтически приемлемым эксципиентом в соответствии с методиками составления композиций, принятыми в фармацевтической промышленности. Носитель, эксципиент и разбавитель могут принимать различные формы в зависимости от желаемого способа введения лекарства (например, перорального, парентерального и т.д.). Так, для жидких пероральных лекарственных форм, таких как суспензии, сиропы, эликсиры и растворы, приемлемые носители и растворители включают воду, гликоли, масла, спирты, вкусовые добавки, консерванты, стабилизаторы, красители и т.д. Для твердых пероральных лекарственных форм, таких как порошки, капсулы и таблетки, приемлемые носители, эксципиенты и разбавители включают крахмалы, сахара, разбавители, гранулообразующие агенты, лубриканты, связующие вещества, добавки для улучшения распадаемости таблеток и т.д. Твердые пероральные препараты также можно дополнительно покрывать такими веществами, как сахар или кишечнорастворимым покрытием, позволяющими модулировать основное место поглощения и распада. При парентеральном введении носитель, эксципиент и растворитель, как правило, включают стерильную воду; при этом для повышения растворимости и консервации состава могут добавляться и другие ингредиенты. Инъекции суспензий или растворов также можно получать с использованием водных носителей с такими добавками, как растворители и консерванты.
Терапевтически эффективное количество соединения формулы (I), указанного в настоящем документе, или фармацевтической композиции в соответствии с настоящим изобретением включает дозу в пределах от приблизительно 0,1 до приблизительно 3000 мг или любое конкретное количество или диапазон доз в указанных пределах, в частности, от приблизительно 1 до приблизительно 1000 мг, или любое конкретное количество или диапазон доз в указанных пределах, или, более конкретно, от приблизительно 10 до приблизительно 500 мг, или любое конкретное количество или диапазон доз в указанных пределах для активного ингредиента при режиме приема от приблизительно 1 до приблизительно 4 раз в день для среднего человека (массой 70 кг). Тем не менее, специалистам в данной области очевидно, что терапевтически эффективное количество соединения формулы (I), указанного в настоящем документе, будет варьироваться в зависимости от имеющихся заболеваний, синдромов, состояний и расстройств, для лечения которых используется данное соединение.
Для перорального применения фармацевтическая композиция предпочтительно предлагается в форме таблеток, содержащих приблизительно 0,01, приблизительно 10, приблизительно 50, приблизительно 100, приблизительно 150, приблизительно 200, приблизительно 250 и приблизительно 500 миллиграммов соединения формулы (I), указанного в настоящем документе.
Соединение формулы (I), указанное в настоящем документе, предпочтительно может применяться в однократной суточной дозировке либо общая суточная дозировка может быть разделена на два, три или четыре приема в день.
Оптимальные дозировки соединения формулы (I), указанного в настоящем документе, легко определяются специалистом и варьируются в зависимости от конкретного соединения, способа применения, концентрации препарата и стадии развития заболевания, синдрома, состояния или расстройства. Кроме того, на необходимость корректировки дозы для достижения соответствующего терапевтического уровня и желаемого терапевтического эффекта влияют факторы, связанные с конкретным пациентом, проходящим лечение, включая пол, возраст, массу тела, особенности диеты, а также время приема лекарственного препарата. Поэтому приведенные выше дозировки являются примерными для некоторого среднего случая. Несомненно, возможны индивидуальные обстоятельства, требующие применения более высоких или более низких диапазонов дозировки, которые также попадают в рамки настоящего изобретения.
Соединения формулы (I), указанные в настоящем документе, могут применяться в любых из вышеописанных композиций и схем приема либо в любых композициях и схемах приема, принятых в данной области, во всех случаях, когда для лечения пациента требуется применение соединения формулы (I), указанного в настоящем документе.
В качестве ингибиторов MGL соединения формулы (I), указанные в настоящем документе, полезны в способах лечения и профилактики заболеваний, синдромов, состояний или расстройств у пациентов (включая животных, млекопитающих и человека), у которых заболевание, синдром, состояние или расстройство зависит от модуляции фермента MGL. Такие способы включают, состоят из и (или) по существу состоят из назначения пациенту (включая животных, млекопитающих и человека), нуждающемуся в таком лечении или профилактике, терапевтически эффективного количества соединения, соли или сольвата формулы (I), указанных в настоящем документе. В частности, соединения формулы (I), указанные в настоящем документе, полезны для профилактики или лечения боли, заболеваний, синдромов, состояний или расстройств, вызывающих такую боль, либо для лечения воспалений или нарушений ЦНС.
Примеры воспалительной боли включают боль, вызванную заболеванием, состоянием, синдромом, расстройством или болезненным состоянием, в том числе воспалительными заболеваниями кишечника, висцеральную боль, мигрень, послеоперационную боль, остеоартрит, ревматоидный артрит, боль в спине, люмбаго, суставную боль, боль в животе, боль в груди, родовые схватки, мышечно-скелетные заболевания, кожные заболевания, зубную боль, нагноения, ожоги, солнечные ожоги, укусы змей, укусы ядовитых змей, укусы пауков, укусы насекомых, нейрогенный мочевой пузырь, интерстициальный цистит, инфекции мочевыводящих путей, ринит, контактный дерматит (повышенную чувствительность), зуд, экзему, фарингит, мукозит, энтерит, синдром раздраженного кишечника, холецистит, панкреатит, постмастэктомический болевой синдром, менструальную боль, эндометриозную боль, боль, вызванную физическими травмами, головную боль, синусовую головную боль, тензионную головную боль или арахноидит.
Примеры нарушений ЦНС включают тревожные состояния, например, социальное беспокойство, посттравматическое стрессовое расстройство, фобии, социофобия, особые фобии, панический синдром, обсессивно-компульсивное расстройство, острое стрессовое расстройство, тревожное расстройство, вызванное разлукой, генерализованное тревожное расстройство, а также депрессии, например, большая депрессия, биполярное аффективное расстройство, сезонное аффективное расстройство, послеродовая депрессия, маниакально-депрессивный психоз и биполярное расстройство.
ОБЩИЕ СПОСОБЫ СИНТЕЗА
Типичные примеры соединений настоящего изобретения могут быть синтезированы в соответствии с общими способами синтеза, описанными ниже и показанными на приведенных далее схемах и примерах. Поскольку схемы приводятся в качестве иллюстрации, настоящее изобретение не следует толковать как ограниченное химическими реакциями и условиями, описанными на схемах. Различные исходные вещества, указанные на схемах и используемые в примерах, имеются в продаже или могут быть получены способами, хорошо известными специалистам в данной области. Фрагменты соответствуют описанию, приведенному в настоящем документе.
В настоящем описании, в частности в схемах и примерах, используются следующие сокращения:
На схеме А показан путь синтеза соединений формулы (I)-A, где R1, s, Y и Z соответствуют определениям, приведенным в настоящем документе.
Схема A

Соединение формулы A1, в котором PG представляет собой обычную защитную аминогруппу, например, Boc, Fmoc, Cbz и тому подобные, имеется в продаже либо может быть получено известными способами, описанными в научной литературе. Соединение формулы A1 в присутствии ненуклеофильного основания, например, пиридина, обрабатывают трифторуксусным ангидридом для получения соединения формулы A2. При удалении защитной группы (PG) обычными способами получают соединение формулы A3. Соединение формулы A3 обрабатывают соединением формулы A4 в присутствии основания пространственно затрудненного амина, например, DIPEA, для получения соединения формулы A5. Обработка соединения формулы A5 1-хлорэтилхлорформиатом с последующим метанолизом позволяет получить соответствующий амин формулы A6. Аналогичным образом, если заместитель R1 соединения формулы A5 представляет собой гидрокси(C1-3)алкил, бензгидрильную группу удаляют путем гидрогенизации в присутствии палладиевого катализатора с получением амина формулы A6. Соединение формулы A6 соединяют с карбоновой кислотой формулы A7, где Q представляет собой гидрокси, в присутствии соответствующего связывающего агента, например, HATU, DCC, EDC, HBTU, PyBrOP и тому подобных, но необязательно в присутствии основания, например, DIPEA, с получением амида формулы A8. Аналогичным образом, для ацилирования соединения формулы А6 используют хлорангидрид формулы A7, где Q представляет собой хлор. В этом случае для получения амида формулы А8 добавляют ненуклеофильное основание, например, пиридин. Удаление трифторацетильной группы соединения формулы A8 осуществляют под действием карбоната калия или TEA в присутствии спиртового растворителя, например, метанола, с получением соединения формулы A9. Соединение формулы A9 ацилируют карбоновой кислотой или хлорангидридом формулы A10, где Q представляет собой гидрокси или хлорид соответственно. Соответствующие условия связывания при использовании соединения формулы A10 (где Q представляет собой OH) включают использование связывающего вещества, например, HATU, DCC, EDC, HBTU, PyBrOP и тому подобных, и основания, например, DIPEA, с получением соединения формулы (I)-A. При ацилировании путем добавления соответствующего хлорангидрида добавление ненуклеофильного основания, например, пиридина, позволяет получить соединение формулы (I)-A.
На схеме B показан альтернативный путь синтеза соединений формулы (I)-A, где R1, s, Y и Z соответствуют определениям, приведенным в настоящем документе.
Схема B

Соединение формулы A1, в котором PG представляет собой обычную защитную аминогруппу, например, Boc, Fmoc, Cbz и тому подобные, имеется в продаже либо может быть получено известными способами, описанными в научной литературе. Для получения соединения формулы B1 соединение формулы A1 ацилируют соединением формулы A10 с применением способов и реагентов, указанных выше в описании схемы A. После удаления защитной группы (PG) обычным способом соединение формулы B2 обрабатывают соединением формулы A4 в присутствии основания пространственно затрудненного амина, например, DIPEA, с применением способов, описанных на схеме А, для получения соединения формулы B3. Обработка соединения формулы B3 1-хлорэтилхлорформиатом с последующим метанолизом позволяет получить соответствующий амин формулы B4. Аналогичным образом, если заместитель R1 соединения формулы B3 представляет собой гидрокси(C1-3)алкил, бензгидрильную группу удаляют путем гидрогенизации в присутствии палладиевого катализатора с получением амина формулы B4. В результате реакции ацилирования с соединением формулы A7 с применением способов, описанных на схеме A, получают соответствующее соединение формулы (I)-A.
На схеме C показан альтернативный путь синтеза соединений формулы (I)-A, где R1, s, Y и Z соответствуют определениям, приведенным в настоящем документе.
Схема C
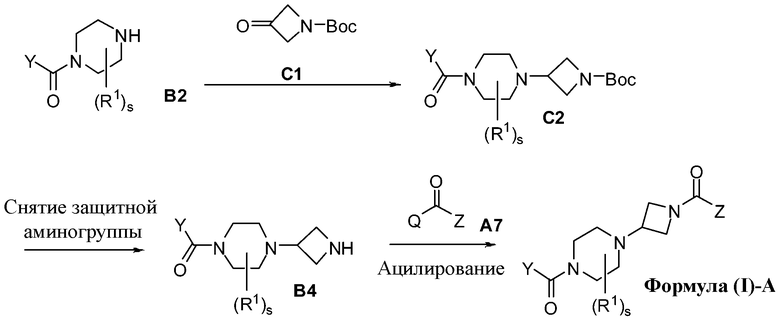
Соединение формулы B2 обрабатывают кетоном формулы C1 в присутствии декаборана или восстановителя, например, триацетоксиборогидрида натрия, с получением соединения формулы C2. В результате удаления Boc-защиты аминогруппы с помощью традиционных реагентов и методов получают соединение формулы B4. В результате связывания с соединением формулы А7, как описано в данном документе, образуется соединение формулы (I)-A.
На схеме D показан способ синтеза соединений формулы (I)-A, где R1, s, Y и Z соответствуют определению, приведенному в данном документе.
Схема D

Соединение формулы A1, в котором PG представляет собой обычную защитную аминогруппу, например, Boc, Fmoc, Cbz и тому подобные, имеется в продаже либо может быть получено известными способами, описанными в научной литературе. Соединение формулы A1 можно обработать соединением формулы A4 для получения соединения формулы D1. После удаления защитной группы PG традиционным способом соединение формулы D2 можно связать с соединением формулы A10 (где Q представляет собой OH) в присутствии связывающего агента, например HATU, DCC, EDC, HBTU, PyBrOP и т.п., необязательно в присутствии основания, например, DIPEA, для получения соединения формулы B3. При проведении ацилирования путем введения хлорида соответствующей кислоты, добавление ненуклеофильного основания, например, пиридина, позволяет получить соединение формулы B3. Удаление бензгидрильной группы описанным способом с последующим ацилированием соединением формулы A7 позволяет получить соединение формулы (I)-A.
Специалисту в данной области будет очевидно, что последовательности синтеза в схемах A, B, C и D можно изменить так, чтобы ацилирование соединением формулы A7 предшествовало удалению бензгидрильной группы с последующим ацилированием соединением формулы A10, и, таким образом, ввести группы Y и Z в обратном порядке.
На схеме E показан способ синтеза соединений формулы (I)-E, где R1, s и Y соответствуют определению, приведенному в данном документе, а Z представляет собой C6-10 арильное кольцо или гетероарильную группу, замещенную необязательно замещенной C6-10 арильной или гетероарильной группой, как указано в данном документе.
Схема E
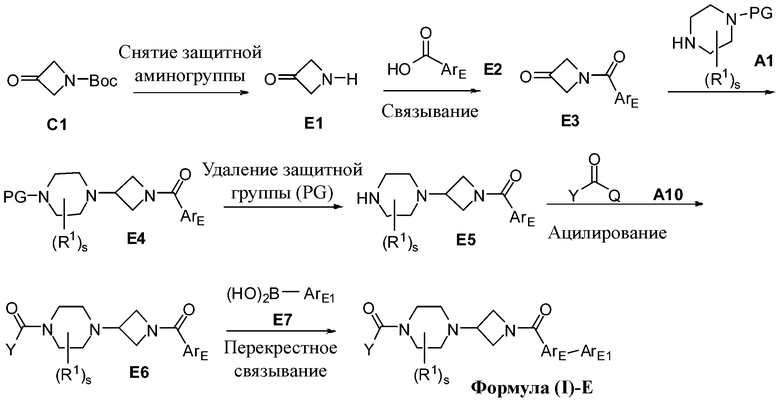
Удалить защиту соединения формулы C1 можно традиционными способами с получением соответствующего свободного амина формулы E1. В результате связывания с карбоновой кислотой формулы E2 (где ArE представляет собой C6-10-арил или гетероарильную группу, а указанное ArE замещено одним замещающим атомом брома, хлора или йода) в присутствии связывающего агента, например, HATU, DCC, EDC, HBTU, PyBrOP и т.п., необязательно в присутствии основания, например, DIPEA, образуется соединение формулы E3. Кетон формулы E3 может быть подвергнут восстановительному аминированию соединением формулы A1 в присутствии декаборана, триацетоксиборгидрида натрия и т.п. с образованием соединения формулы E4. После удаления защитной группы PG традиционным способом свободный амин формулы E5 можно ацилировать соединением формулы A10, как описано в данном документе, и получить соединение формулы E6. Замещенный заместитель ArE формулы E6 обрабатывают ArE1- бороновой кислотой или сложным эфиром (E7), замещенными соответствующим образом или замещенным соответствующим образом реагентом на основе триалкилолова, триалкилсиланом и т.п. (где ArE1 представляет собой необязательно замещенный C6-10арил или гетероарил, указанный в настоящем документе), в ходе одной из множества реакций связывания (например, реакции Сузуки, Стилле и Хияма), хорошо известных специалистам в данной области, в присутствии соответствующего катализатора, а также в присутствии основания, например, карбоната цезия, бикарбоната натрия, фторида натрия и тому подобных, с получением соединения формулы (I)-E.
На схеме F показан способ синтеза соединений формулы (I)-F, где R1, s и Y соответствуют определению, приведенному в данном документе, а Z представляет собой необязательно замещенную C6-10арил(C1-6)алкильную или C6-10арил(C2-6)алкенильную группу, где L представляет собой (C1-6)алкил или (C2-6)алкенил, соответственно.
Схема F

Соединение формулы B4 можно связать с имеющимся в продаже соединением формулы F2 (где ArF представляет собой необязательно замещенный заместитель C6-10арил согласно определению, приведенному в настоящем документе) в присутствии связывающего агента, например, HATU, DCC, EDC, HBTU, PyBrOP и т.п., необязательно в присутствии основания, например, DIPEA, с получением соединения формулы (I)-F.
На схеме G показан способ синтеза соединений формулы (I)-G и формулы (I)-G1, где R1, s и Y соответствуют определению, приведенному в настоящем документе, а Z представляет собой либо необязательно замещенный C6-10арил (ArG), замещенный фенил(C2-6)алкинилом (формула (I)-G), либо необязательно замещенный C6-10арил, замещенный фенил(C1-6)алкилом.
Схема G
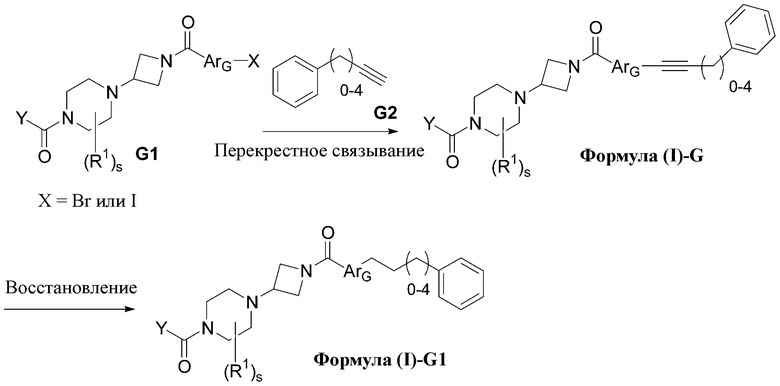
Соединение формулы G1 можно получить в соответствии со способами, описанными в данном документе, где ArG представляет собой C6-10арил, а X представляет собой заместитель, выбранный из брома или йода. X-замещенное кольцо ArG можно перекрестно связать с соединением формулы G2 в присутствии палладиевого катализатора, йодида меди и основания, например триэтиламина, и получить соединение формулы (I)-G. Алкинильную функциональность соединения формулы (I)-G можно понизить до соответствующей алкильной группы путем катализированного гидрирования переходного металла, например палладия на угле, гидроксида палладия (II) или платины, в водородной газовой среде, с получением соединения формулы (I)-G1.
На схеме H показан способ синтеза соединений формул (I)-H, H1, H2 и H3, где R1, s и Y соответствуют определению, приведенному в настоящем документе, а Z представляет собой аннелированный с бензольным кольцом гетероциклил, в котором гетероциклильная часть содержит атом азота и в котором атом азота является необязательно замещенным. Только в качестве иллюстрации была выбрана 1,2,3,4-тетрагидроизохинолинильная группа, представляющая собой аннелированный с бензольным кольцом гетероциклил настоящего изобретения.
Схема H
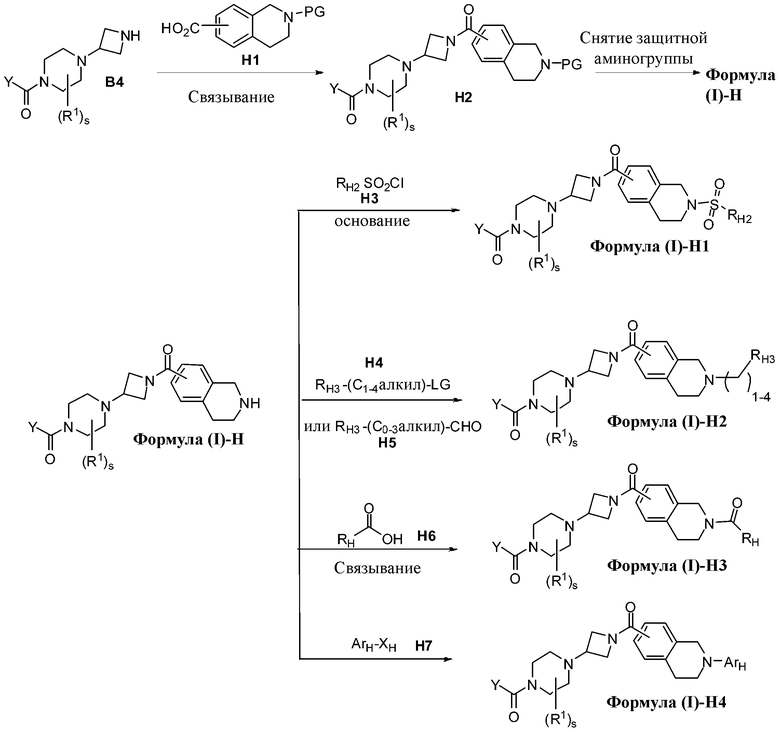
Соединение формулы B4 можно связать с замещенным карбоновой кислотой гетероциклилом, аннелированным с бензольным кольцом, формулы H1 (где PG представляет собой традиционную защитную аминогруппу), с получением соединения формулы H2. При снятии защитных аминогрупп с соединения формулы H2 образуется соответствующий амин формулы (I)-H, который можно получить различными способами синтеза для образования дополнительных соединений настоящего изобретения. Например, соединение формулы (I)-H можно обработать соответствующим образом замещенным сульфонилхлоридом формулы H3 в присутствии органического основания с образованием соединения формулы (I)-H1 (где RH2 представляет собой фенил или C1-6алкил. Кроме того, соединение формулы (I)-H2 можно получить алкилированием аминогруппы соединения формулы (I)-H с помощью алкилирующего агента формулы H4 (где RH3 представляет собой фенил или C1-6алкилкарбонил) в присутствии основания. LG в соединении формулы H4 представляет собой обычную уходящую группу, например, бромид, йодид, тозилат, мезилат и т.д. Соединение формулы (I)-H2 можно также получить путем восстановительного аминирования соединением формулы H5 в присутствии восстановителя, например, триацетоксиборгидрида натрия. Соединение формулы (I)-H3 можно получить в результате реакции связывания пептида между соединением формулы (I)-H и соответствующим образом замещенной карбоновой кислотой формулы H6 (где RH представляет собой необязательно замещенный циклогексил, C1-6алкил или фенил, согласно определению, приведенному в настоящем документе) в присутствии подходящего связывающего агента. Наконец, соединения формулы (I)-H4 настоящего изобретения, где ArH представляет собой пиримидин или соответствующим образом замещенную фенильную группу, можно получить путем обработки соединения формулы (I)-H соединением формулы H7 (где XH представляет собой группу, например, хлор, бром или йод, а ArH соответствует определению, приведенному в настоящем документе) в присутствии катализатора на основе переходного металла, например ацетата палладия, подходящего лиганда фосфина, например BINAP, и основания, например трет-бутоксида калия.
На схеме I показан способ синтеза соединений формулы (I)-I, где R1, s и Y соответствуют определению, приведенному в настоящем документе, а Z представляет собой C6-10арил, замещенный C6-10арил(C1-4)алкокси, как указано в настоящем документе. Только в качестве иллюстрации Z-C6-10арильное кольцо показано в виде фенильной группы.
Схема I

Имеющееся в продаже соединение формулы I1 можно преобразовать в соединение формулы I2 под воздействием хлорирующего агента, например оксалилхлорида, тионилхлорида и т.д. Соединение формулы B4 можно ацилировать соединением формулы I2 с получением соединения формулы I3. Удаление ацетильной группы из соединения формулы I3 путем гидролиза в присутствии нуклеофильного основания, например, гидроксида лития, позволяет получить соответствующее соединение формулы I4. В результате алкилирования соединением формулы I5 (где ArI представляет собой необязательно замещенную C6-10арильную группу, а XI представляет собой I, Br, Cl или тозилат) образуется соединение формулы (I)-I. Аналогичным образом для получения соединения формулы (I)-I можно использовать реакции Мицунобу с участием соединения формулы I6 (где XI представляет собой гидрокси).
На схеме J показан способ синтеза соединений формулы (I)-J, где R1, s и Y соответствуют определениям, приведенным в настоящем документе, а Z представляет собой C6-10арил, замещенный C6-10арил(C1-4)алкилтио, как указано в настоящем документе. Только в качестве иллюстрации Z C6-10арильное кольцо показано в виде фенильной группы.
Схема J
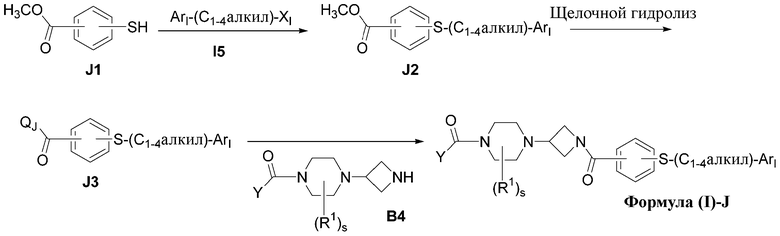
Соединение формулы J1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение формулы J1 можно алкилировать соединением формулы I5 (где XI представляет собой I, Br, Cl или тозилат) с получением соединения формулы J2. В результате щелочного гидролиза соединения формулы J2 образуется соединение формулы J3 (где QJ представляет собой гидрокси), которое можно связать с соединением формулы B4, либо можно сначала преобразовать карбоновую кислоту в соответствующий хлорангидрид формулы J3 (где QJ представляет собой хлор), а затем алкилировать соединение формулы B4 и получить соединение формулы (I)-J.
На схеме K показан способ синтеза соединений формулы (I)-K, где R1, s и Y соответствуют определениям, приведенным в данном документе, а Z представляет собой необязательно замещенный C6-10арил, дополнительно замещенный фенилокси-группой, и где фенилокси-группа необязательно замещена C1-4алкилом, трифторметилом или одним-двумя хлор-заместителями, как указано в настоящем документе. Только в качестве иллюстрации Z C6-10арильное кольцо показано в виде фенильной группы.
Схема K

Соединение формулы K1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение формулы K1 или его необязательно замещенную производную можно связать с арилбороновой кислотой формулы K2 (где ArK представляет собой фенил, необязательно замещенный C1-4алкилом, трифторметилом или одним-двумя хлор-заместителями), в присутствии катализатора на основе меди, например, иодида меди или ацетата меди (II), подходящих лигандов, например, пиридина, 1,10-фенантролина, этилендиамина и т.п., и органического основания, например, триэтиламина, с образованием соединения формулы K3. В другом варианте осуществления настоящего изобретения соединения формулы K3 можно получить путем ароматического нуклеофильного замещения соответствующим образом замещенной производной метилгалобензоата, где предпочтительным галогеновым заместителем является фтор, на ArK-OH, где ArK соответствует приведенному ранее определению, в присутствии основания. Щелочной гидролиз с последующей необязательной обработкой подходящим хлорирующим агентом позволяет получить соединение формулы K4, где QK представляет собой гидрокси или хлор. В результате ацилирования соединения формулы B4 соединением формулы K4 образуется соединение формулы (I)-K.
На схеме L показан способ синтеза соединений формулы (I)-L, где R1, s и Y соответствуют определениям, приведенным в настоящем документе, а Z представляет собой необязательно замещенный C6-10арил, замещенный фенилтио-группой, где фенилтио-группа необязательно замещена C1-4алкилом, трифторметилом или одним-двумя хлор-заместителями, как указано в настоящем документе. Только в качестве иллюстрации Z C6-10арильное кольцо показано в виде фенильной группы.
Схема L

Соединение формулы L1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Арилбромид формулы L1 или его необязательно замещенную производную можно перекрестно связать с соединением формулы L2 (где ArL представляет собой фенил, необязательно замещенный C1-4алкилом, трифторметилом или одним-двумя хлор-заместителями), в присутствии катализатора на основе палладия, например, тетракис(трифенилфосфин) палладия, подходящих лигандов, например трифенилфосфина, и основания, например трет-бутоксида калия, с образованием соединения формулы L3. В результате щелочного гидролиза сложного метилового эфира образуется соединение формулы L4. Соединение формулы B4 можно связать с соединением формулы L4 в присутствии подходящего связывающего пептиды агента, например DCC, EDC, HBTU, PyBrOP и т.п., с образованием соединения формулы (I)-L.
На схеме M показан способ синтеза соединений формулы (I)-M, где R1, s и Y соответствуют определениям, приведенным в настоящем документе, а Z представляет собой C6-10арил, замещенный фенилсульфонилом. Только в качестве иллюстрации Z C6-10арильное кольцо показано в виде фенильной группы.
Схема M
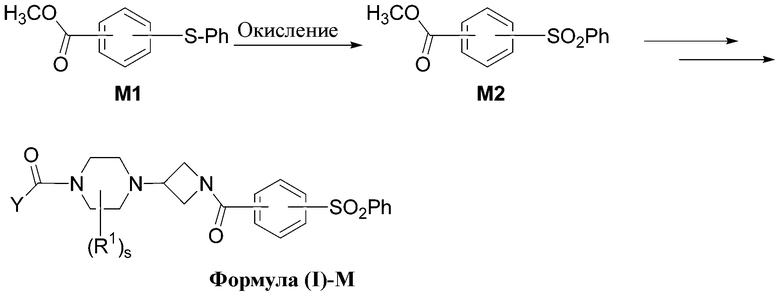
Соединение формулы M1 можно получить способами, описанными на схеме L. Окисление тиоэфирной группы может произойти под воздействием соответствующего окислителя, например mCPBA, перекиси водорода и т.п., с образованием соединения формулы M2. После щелочного гидролиза с последующим пептидным связыванием с соединением формулы B4 можно получить соединение формулы (I)-M.
На схеме N показан способ синтеза соединений формулы (I)-N, где R1, s и Y соответствуют определениям, приведенным в настоящем документе, а Z представляет собой C6-10арил, замещенный 5-8-членным гетероциклилокси, в котором атом азота необязательно замещен фенилкарбонилом, C1-4алкилкарбонилом или C1-4алкоксикарбонилом. Только в качестве иллюстрации Z-C6-10арильное кольцо показано в виде фенильной группы.
Схема N
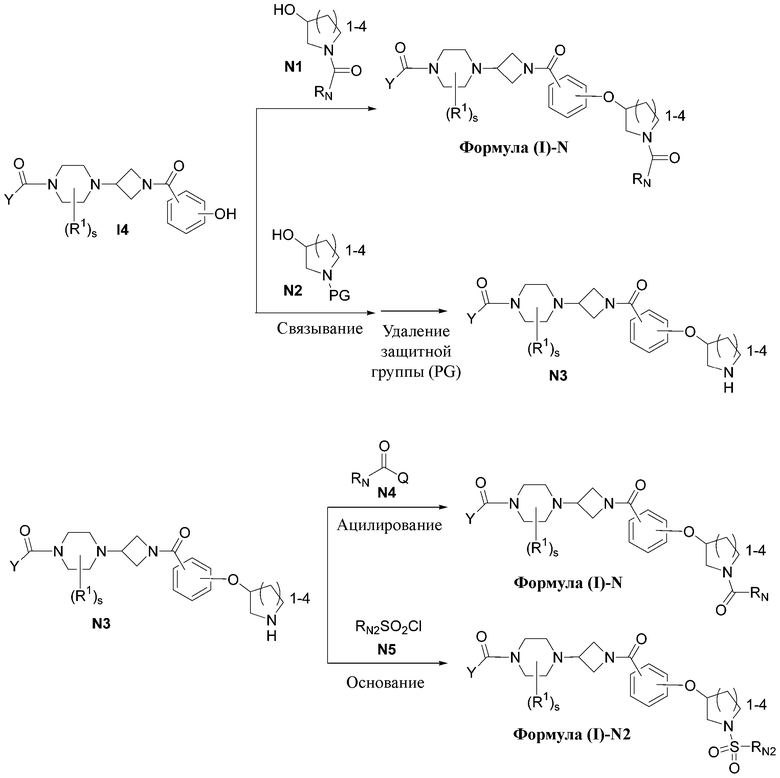
Соединение формулы I4 можно связать с соединением формулы N1 (где RN представляет собой фенил, C1-4алкил, C1-4алкокси, C1-4алкиламино, C1-4диалкиламино или N-содержащий гетероциклил, присоединенный через атом азота) в условиях реакции Мицунобу в апротонном органическом растворителе, например, THF, с образованием соединения формулы (I)-N. Связывание по реакции Мицунобу можно также осуществить между соединением формулы I4 и соединением формулы N2, где PG представляет собой традиционную защитную аминогруппу, например, Boc, Fmoc, Cbz и т.п. Затем традиционными способами удаляют защитную группу (PG), в результате чего образуется соединение формулы N3, которое можно дериватизировать с помощью различных способов синтеза для получения дополнительных соединений настоящего изобретения. Например, соединение формулы N3 можно связать с карбоновой кислотой (Q представляет собой гидрокси, RN представляет собой фенил или C1-4алкил), хлорангидридом (Q представляет собой хлорид, RN представляет собой фенил или C1-4алкил), хлорформиатом (Q представляет собой хлорид, RN представляет собой C1-4алкокси) или карбамоилхлоридом (Q представляет собой хлорид, RN представляет собой C1-4алкиламино, C1-4диалкиламино или N-содержащий гетероциклил, присоединенный через атом азота), либо соединением формулы N4, как указано в настоящем документе, с образованием соединения формулы (I)-N. Кроме того, соединение формулы N3 можно ввести в реакцию с сульфамоилхлоридом формулы N5, где RN2 представляет собой C1-4алкиламино, C1-4диалкиламино или N-содержащий гетероциклил, присоединенный через атом азота, с образованием соединения формулы (I)-N2.
На схеме O показан способ синтеза соединений формулы (I)-O, где R1, s и Y соответствуют определениям, приведенным в настоящем документе, а Z представляет собой необязательно замещенный C6-10арил, дополнительно замещенный RO, где RO представляет собой (1-R2)-пирролидин-3-ил-окси, C1-4алкил или C6-10арил(C1-4)алкил. Только в качестве иллюстрации Z-C6-10арильное кольцо показано в виде фенильной группы.
Схема O
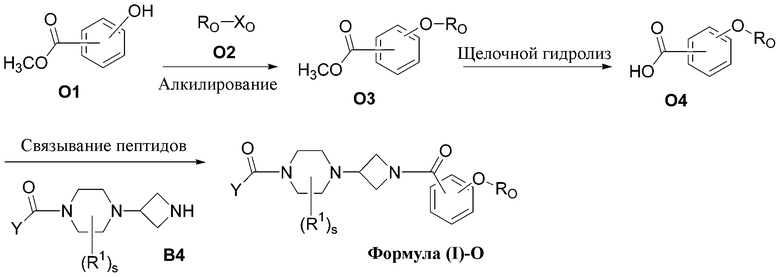
Соединение формулы O1 можно связать с соединением формулы O2 (где XO представляет собой гидрокси) в условиях реакции Мицунобу с образованием соединения формулы O3. Алкилирование можно также провести путем реакции нуклеофильного замещения с соединением формулы O2 (где XO представляет собой I, Br, Cl или тозилат) в присутствии основания с образованием соединения формулы O3. В результате щелочного гидролиза сложного метилового эфира в соединении формулы O3 образуется соответствующая карбоновая кислота формулы O4. Соединение формулы O4 можно связать с соединением формулы B4, как описано в настоящем документе, и получить соединение формулы (I)-O. Кроме того, с соединения формулы O3, где RO представляет собой (1-R2)-пирролидин-3-ил-окси, а R2 представляет собой традиционную защитную аминогруппу, можно снять защиту и дополнительно дериватизировать его по азоту пирролидина, как описано в настоящем документе, преобразовать полученное соединение в соединение формулы О4, связать его с соединением формулы В4 и получить, таким образом, соединение формулы (I)-O.
На схеме P показан способ синтеза соединений формулы (I)-P, где R1, s и Y соответствуют определениям, приведенным в настоящем документе, а Z представляет собой C6-10арил, замещенный фенил-(Q)-C1-6алкилом, в котором Q представляет собой O, S или NH, а фенил из фенил-(Q)-C1-6алкила необязательно независимо замещен одним-двумя заместителями, выбранными из брома, хлора, фтора, йода, C1-4алкила, C1-4алкокси и трифторметила.
Схема P
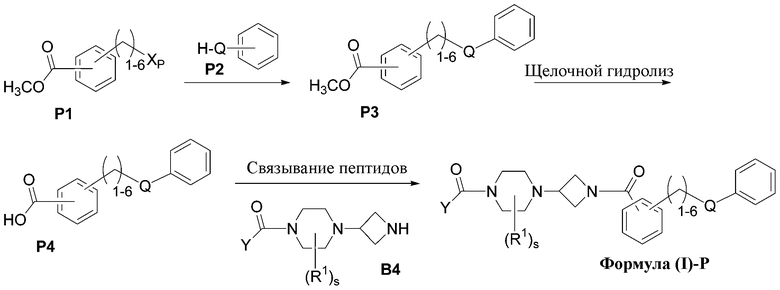
Соединение формулы P1 (где XP представляет собой гидрокси, хлор или бром) можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение формулы P1 может быть подвергнуто алкилированию реакцией Мицунобу или реакцией нуклеофильного замещения с соединением формулы P2 для получения соединения формулы P3. В результате щелочного гидролиза сложного метилового эфира из соединения формулы Р3 образуется соответствующая карбоновая кислота формулы P4. Соединение формулы P4 можно связать с соединением формулы B4, как описано в настоящем документе, с образованием соединения формулы (I)-P.
На схеме Q показано получение некоторых полезных промежуточных соединений формулы A7 (Q представляет собой гидрокси), где Z является гетероарилом, замещенным необязательно замещенной арильной группой (ArQ). Только в качестве иллюстрации гетероарильное кольцо представлено индолом.
Схема Q

Соединение формулы Q1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение Q1 можно обработать арилйодидом формулы Q2 в присутствии йодида меди, транс-N, N'-диметилциклогексан-1,2-диамина и фосфата калия с образованием соединения формулы Q3. Последующий щелочной гидролиз позволяет получить полезные промежуточные соединения на основе карбоновой кислоты формулы Q4.
На схеме R показано получение некоторых полезных промежуточных соединений формулы A7 (Q представляет собой гидрокси), где Z является бензимидазолилом или бензоксазолилом и где Z замещен необязательно замещенным арилом или гетероарильной группой (ArR), или ArR(C1-4)алкилом.
Схема R

Соединение формулы R1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение R1 можно обработать арил- или гетероарилзамещенной карбоновой кислотой формулы R2 в присутствии связывающего агента, например, DCC, и затрудненного основания, например, DMAP, в апротонном органическом растворе, с образованием соединения формулы R3. Катализированное кислотой замыкание кольца в соединении формулы R3 приводит к образованию замещенного бензимидазола или бензоксазола формулы R4 или R6, соответственно. Последующий щелочной гидролиз позволяет получить полезные промежуточные соединения на основе карбоновой кислоты формулы R5 или R7.
На схеме S показано получение некоторых полезных промежуточных соединений формулы A7 (Q представляет собой гидрокси), где Z является необязательно замещенной бензотиенильной группой, а RS представляет собой подходящие заместители в соответствии с формулой (I).
Схема S
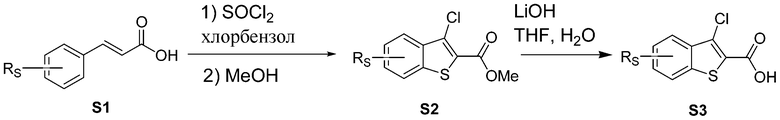
Соединение формулы S1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение формулы S1 можно обработать тионилхлоридом в апротонном органическом растворителе, а затем обработать метанолом, в результате чего образуется соединение формулы S2. Последующий щелочной гидролиз позволяет получить полезные промежуточные соединения на основе карбоновой кислоты формулы S3. Специалистам в данной области известно, что в результате циклизации таких асимметрично замещенных соединений формулы S1 тионилхлоридом можно получить смеси позиционных изомеров. Затем эти изомеры можно выделить и изолировать с помощью обычной хроматографии, известной специалистам в данной области.
На схеме T показано получение некоторых полезных промежуточных соединений формулы A7 (Q представляет собой гидрокси), где Z является C6-10арилом (ArT), замещенным необязательно замещенной C6-10арилметиловой группой.
Схема T

Соединение формулы T1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение формулы T1 можно обработать подходящим образом замещенным органометаллическим реагентом, например хлоридом ArT1-метилцинка формулы T2 в присутствии катализатора на основе палладия с образованием соединения формулы T3. Последующий щелочной гидролиз позволяет получить полезные промежуточные соединения на основе карбоновой кислоты формулы T4.
На схеме U показано получение некоторых полезных промежуточных соединений формулы A7 (Q представляет собой гидрокси), где Z является бензотиенильной группой, замещенной фтор-заместителем и необязательно замещенной C6-10арилом или гетероарильной группой (ArE1).
Схема U

Соединение формулы U1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение формулы U1 можно перекрестно связать с бороновой кислотой или сложным эфиром (E7) в присутствии катализатора на основе палладия и в присутствии подходящего основания, например, карбоната калия, с образованием соединения формулы U2. В результате щелочного гидролиза образуется соответствующая карбоновая кислота U3, которую можно обработать N-фторбензолсульфонимидом в присутствии органометаллического основания, например н-бутиллития, с образованием фторированного соединения формулы U4.
На схеме V показано получение некоторых полезных промежуточных соединений формул V6, V8 и V10 (Q представляет собой гидрокси), где Z является бензимидазолильной группой, замещенной ArV группой (в которой ArV представляет собой необязательно замещенный арильный или гетероарильный заместитель в соответствии с формулой (I)), и необязательно замещенной метил- или оксогруппой на второй позиции.
Схема V

Соединение формулы V1 можно приобрести либо в готовом виде, либо получить известными способами, описанными в научной литературе. Соединение формулы V1 можно обработать соединением формулы V2 с образованием соединения формулы V3. Аминогруппу можно сократить путем воздействия на нее хлоридом олова в спиртовом растворе или путем гидрирования, катализированного палладием, с образованием диамина формулы V4. В результате обработки триметилортоформиатом образуется бензимидазол формулы V5, который можно подвергнуть щелочному гидролизу для получения соединения формулы V6.
Соединение формулы V4 можно обработать триметилортоацетатом, а затем подвергнуть щелочному гидролизу для получения соответствующего 2-метил-замещенного бензимидазола, V8. Аналогичным образом, соединение формулы V4 можно обработать 1,1'-карбонилдиимидазолом в DMF, а затем подвергнуть щелочному гидролизу для получения соответствующего 2-оксозамещенного бензимидазола, V10.
Пример 1

A. трет-Бутиловый эфир 4-(2,2,2-трифторацетил)-пиперазин-1-карбоновой кислоты, 1c. В раствор трет-бутилового эфира пиперазин-1-карбоновой кислоты (1a, 10 г, 53,69 ммоль) и пиридина (8,7 мл, 107,57 ммоль) в CH2Cl2 (100 мл) покапельно ввели соединение 1b (10,5 мл, 75,54 ммоль) при температуре 0°C. Смесь перемешивали при температуре 0°C в течение 2 часов. К смеси добавили 2Н HCl (60 мл). Органический слой высушили над MgSO4, профильтровали и сконцентрировали. Полученное соединение 1c использовали в следующей реакции без дополнительной очистки. МС m/z (MH+-Boc) 183,1, (MH+-C4H9) 227,1; 1H ЯМР (300 МГц, CDCl3): δ 3,45-3,7 (м, 8H), 1,5 (с, 9H).
B. 2,2,2-Трифтор-1-пиперазин-1-ил-этанон, 1d. В раствор соединения 1c (15,15 г, 53,69 ммоль) в CH2Cl2 (60 мл) ввели трифторуксусную кислоту (18 мл) при комнатной температуре. Смесь перемешивали 18 часов при комнатной температуре. Растворитель удалили выпариванием. К остатку добавили эфир (100 мл). Твердое вещество белого цвета собрали фильтрованием, промыли эфиром и высушили в вакууме. Полученное соединение 1d использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 183,1.
C. 1-[4-(1-Бензгидрилазетидин-3-ил)-пиперазин-1-ил]-2,2,2-трифторэтанон, 1f. В раствор соединения 1d (6 г, 32,94 ммоль) и соединения 1e (12,5 г, 39,38 ммоль) в CH3CN (60 мл) ввели DIPEA (12 мл, 68,89 ммоль) при комнатной температуре. Смесь нагревали с обратным холодильником в течение 2 часов. Растворитель удалили выпариванием, а остаток разделили между CH2Cl2 и водным раствором NaHCO3. Органический слой промыли водным раствором NaHCO3 (2 раза), а затем экстрагировали 1Н HCl (2 раза). Водный слой охладили, после чего довели уровень рН до основного (рН=10) с помощью 1Н NaOH. Смесь экстрагировали CH2Cl2 (2 раза). Органический слой высушили над MgSO4 и сконцентрировали. Соединение 1f очистили хроматографией на обращенной фазе. МС m/z (M+H+) 404,2.
D. 1-(4-Азетидин-3-ил-пиперазин-1-ил)-2,2,2-трифторэтанон, 1g. В раствор соединения 1f (2,11 г, 5,23 ммоль) в CH2Cl2 (60 мл) ввели 1-хлорэтилхлорформиат (2,0 мл, 18,35 ммоль) при температуре 0°C в атмосфере N2. Смесь перемешивали при температуре 0°C в течение 90 минут, а затем добавили в нее MeOH (4 мл). Смесь нагревали с обратным холодильником в течение 1 часа. После охлаждения к смеси добавили Et2O (50 мл). Полученное твердое вещество собрали фильтрованием и высушили. Полученное соединение 1g использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 238,1.
E. 1-{4-[1-(4-Циклогексилбензоил)-азетидин-3-ил]-пиперазин-1-ил}-2,2,2-трифторэтанон, 1i. В раствор соединения 1g (2,5 г, 10,54 ммоль) и HATU (4 г, 10,52 ммоль) в DMF (25 мл) ввели DIPEA (5 мл, 28,70 ммоль). Смесь перемешивали при комнатной температуре в течение 30 минут, а затем соединение 1h (2 г, 9,79 ммоль) добавили к смеси. Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. В реакционную смесь добавили воду (40 мл). Смесь экстрагировали с помощью EtOAc (2x20 мл). Органический слой высушили над MgSO4, отфильтровали и сконцентрировали. Полученное соединение 1i очистили хроматографией на обращенной фазе. МС m/z (M+H+) 424,2.
Е. (4-Циклогексилфенил)-(3-пиперазин-1-ил-азетидин-1-ил)-метанон, 1j. В раствор соединения 1i (0,95 г, 2,24 ммоль) в CH3OH (16 мл) и H2O (4 мл) ввели K2CO3 (0,8 г, 5,79 ммоль). Смесь перемешивали при комнатной температуре в течение 1 часа. Смесь профильтровали и удалили растворитель выпариванием. Полученное соединение 1j использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 328,2.
G. 1-{1-[(4-Циклогексилфенил)карбонил]азетидин-3-ил}-4-(фенилкарбонил)пиперазин, соединение 1. В раствор соединения 1j (0,08 г, 0,24 ммоль) и HATU (0,093 г, 0,24 ммоль) в DMF (3 мл) ввели DIPEA (0,1 мл). Смесь перемешивали при комнатной температуре в течение 30 минут, а затем добавили к смеси соединение 1k (0,03 г, 0,25 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. К смеси добавили воду (6 мл). Смесь экстрагировали с помощью EtOAc (2x6 мл). Органический слой высушили над MgSO4, отфильтровали и сконцентрировали. Полученное соединение 1 очистили хроматографией на обращенной фазе. 1H ЯМР (300 МГц, CD3OD): δ 7,58 (д, 2H), 7,44-7,53 (м, 5H), 7,34 (д, 2H), 4,6 (м, 1H), 4,42 (м, 2H), 4,27 (м, 1H), 3,85 (м, 5H), 3,05 (м, 4H), 2,57 (м, 1H), 1,85 (м, 5H), 1,45 (м, 5H). МС m/z (M+H+) 432,3.
Следуя процедуре, описанной выше для примера 1, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (300 МГц, CD3OD): δ 7,71 (д, 1H), 7,59 (д, 2H), 7,34 (д, 2H), 7,13 (д, 1H), 6,62 (дд, 1H), 4,62 (м, 1H), 4,52 (м, 1H), 4,42 (м, 1H), 4,31 (м, 1H), 4,05 (м, 4H), 3,98(м, 1H), 3,18 (м, 4H), 2,58 (м, 1H), 1,84 (м, 5H), 1,24-1,52 (м, 5H)
МС m/z (M+H+) 422,2
МС m/z (M+H+) 436,2
МС m/z (M+H+) 433,2
1H ЯМР (300 МГц, CD3OD): δ 7,65 (м, 4H), 7,56 (д, 2H), 7,25-7,46 (м, 8H), 4,58 (м, 1H), 4,49 (м, 1H), 4,35 (м, 1H), 4,26 (м, 1H), 3,92 (м, 1H), 3,78 (м, 4H), 3,09 (м, 4H)
МС m/z (M+H+) 426,1
1H ЯМР (300 МГц, CD3OD): δ 7,66 (м, 4H), 7,62 (д, 1H), 7,56 (д, 2H), 7,38 (т, 2H), 7,30 (м, 1H), 7,03 (д, 1H), 6,51 (дд, 1H), 4,56 (м, 1H), 4,44 (м, 1H), 4,33 (м, 1H), 4,22 (м, 1H), 3,95 (м, 4H), 3,81 (м, 1H), 3,01 (м, 4H)
МС m/z (M+H+) 416,2
1H ЯМР (300 МГц, CD3OD): δ 8,97 (с, 1H), 8,14 (с, 1H), 7,66 (м, 4H), 7,56 (д, 2H), 7,37 (т, 2H), 7,30 (м, 1H), 4,60 (м, 1H), 4,49 (м, 1H), 4,37 (м, 1H), 4,27 (м, 1H), 4,08 (м, 4H), 3,95 (м, 1H), 3,14 (м, 4H)
МС m/z (M+H+) 433,2
1H ЯМР (300 МГц, CD3OD): δ 9,08 (с, 1H), 8,11 (с, 1H), 7,66 (м, 4H), 7,56 (д, 2H), 7,38 (т, 2H), 7,30 (м, 1H), 4,54 (м, 1H), 4,39 (м, 1H), 4,31 (м, 1H), 4,17 (м, 1H), 3,84 (м, 4H), 3,73 (м, 1H), 2,92 (м, 4H)
МС m/z (M+H+) 433,2
1H ЯМР (300 МГц, CD3OD): δ 7,88 (д, 1H), 7,78 (д, 1H), 7,66 (м, 4H), 7,57 (д, 2H), 7,38 (т, 2H), 7,30 (м, 1H), 4,62 (м, 3H), 4,48 (м, 1H), 4,37 (м, 1H), 4,26 (м, 1H), 3,91 (м, 3H), 3,13 (м, 4H)
МС m/z (M+H+) 433,2
МС m/z (M+H+) 447,1
МС m/z (M+H+) 429,3
1H ЯМР (300 МГц, CD3OD): δ 7,76 (м, 4H), 7,66 (д, 2H), 7,47 (т, 2H), 7,39 (м, 1H), 7,11 (д, 1H), 6,64 (д, 1H), 4,66 (м, 1H), 4,57 (м, 1H), 4,44 (м, 1H), 4,34 (м, 1H), 3,91-4,10 (м, 5H), 3,17 (м, 4H)
МС m/z (M+H+) 494,1/496,0
1H ЯМР (300 МГц, CD3OD): δ 7,75 (м, 4H), 7,61-7,72 (м, 3H), 7,34-7,52 (м, 4H), 7,14 (т, 1H), 4,65 (м, 1H), 4,52 (м, 1H), 4,42 (м, 1H), 4,29 (м, 1H), 3,96 (м, 4H), 3,90 (м, 1H), 3,07 (м, 4H)
МС m/z (M+H+) 432,1 (рассчитано для C25H25N3O2S 431,56)
МС m/z (M+H+) 446,1
МС m/z (M+H+) 510,1/512,1
МС m/z (M+H+) 466,1/467,1
МС m/z (M+H+) 510,0/512,1
МС m/z (M+H+) 510,0/512,1
МС m/z (M+H+) 488,1
МС m/z (M+H+) 482,1
МС m/z (M+H+) 462,1
МС m/z (M+H+) 442,22/444,19
МС m/z (M+H+) 465,0/467,1
МС m/z (M+H+) 458,1/460,0
МС m/z (M+H+) 469,04/471,04
МС m/z (M+H+) 462,11/464,11
МС m/z (M+H+) 500
МС m/z (M+H+) 474
МС m/z (M+H+) 507
МС m/z (M+H+) 507
Пример 1a

H. Метил 1-(4-фторфенил)-индол-5-карбоксилат, 1m. Смесь метил индол-5-карбоксилата 1j (0,5 г, 2,85 ммоль), 1-бром-4-фторбензола 1k (2 мл, 18,21 ммоль), CuI (0,544 г, 2,85 ммоль) и K2CO3 (0,591 г, 4,28 ммоль) нагревали в микроволновой печи при температуре 220°C в течение 2,5 часов. Реакционную смесь разбавили CH2Cl2 и профильтровали. Раствор сконцентрировали, а остаток очистили колоночной флэш-хроматографией (силикагель, 15% EtOAc/гептан) и получили соединение 1m (0,58 г).
I. 1-(4-Фторфенил)-индол-5-карбоновая кислота, 1n. Смесь метил 1-(4-фторфенил)-индол-5-карбоксилата 1m (0,58 г, 2,15 ммоль) и LiOH·H2O (0,36 г, 8,6 ммоль) в THF (15 мл) и H2O (10 мл) перемешивали при комнатной температуре в течение 5 суток. Водный 10%-ный раствор HCl добавили в реакционную смесь для доведения уровня pH до 3~4. Полученную смесь экстрагировали с помощью EtOAc (2x). Органический раствор промыли водным NaCl, высушили над Na2SO4 и сконцентрировали, получив в результате соединение 1n (0,5 г).
J. 1-(4-Фторфенил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 487. Названное соединение 487 было получено способом, описанным в примере 1, с использованием промежуточного соединения 1n из примера 1a и промежуточного соединения 1g из примера 1 в качестве исходных материалов. 1H ЯМР (400 МГц, CD3OD): δ 8,00 (д, J=1,2 Гц, 1H), 7,88 (д, J=3 Гц, 1H), 7,55 (м, 2H), 7,46 (м, 3H), 7,34 (д, J=3 Гц, 1H), 7,27-7,21 (м, 2H), 6,74 (д, J=3 Гц, 1H), 4,52 (уш.с, 1H), 4,43-4,20 (м, 4H), 4,14 (м, 1H), 3,95-3,80 (м, 2H), 3,25 (м, 1H), 2,60-2,40 (м, 4H). МС m/z (M+H+) 490.
Следуя процедуре, описанной выше для примера 1a, стадии H и I, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:
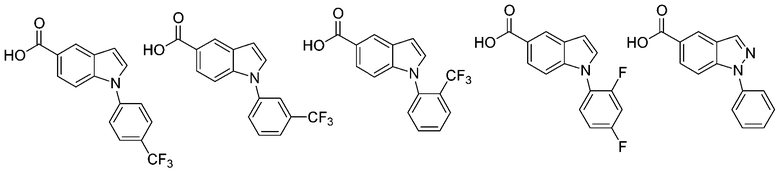
Следуя процедуре, описанной выше для примера 1a, стадия J, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (400 МГц, CD3OD): δ 7,99 (с, 1H), 7,55-7,21 (м, 12H), 6,73 (с, 1H), 4,37 (уш.с, 1H), 4,25 (м, 2H), 4,10 (уш.с, 1H), 3,90 (уш.с, 1H), 3,75 (уш.с, 1H), 3,48 (уш.с, 2H), 3,24 (м, 1H), 2,50-2,20 (м, 4H).
МС m/z (M+H+) 483
МС m/z (M+H+) 466
МС m/z (M+H+) 501
МС m/z (M+H+) 540
МС m/z (M+H+) 540
1H ЯМР (400 МГц, CD3OD): δ 8,00 (с, 1H), 7,88 (д, J=3 Гц, 1H), 7,81 (д, J=8,6 Гц, 2H), 7,64 (д, J=8,6 Гц, 2H), 7,59 (с, 2H), 7,54 (д, J=3 Гц, 1H), 7,41 (д, J=3,5 Гц, 1H), 6,79 (д, J=3,5 Гц, 1H), 4,53 (уш.с, 1H), 4,43 (м, 2H), 4,28 (м, 2H), 4,14 (уш.с, 1H), 3,86 (м, 2H), 3,26 (м, 1H), 2,50 (м, 4H).
МС m/z (M+H+) 540
МС m/z (M+H+) 490
МС m/z (M+H+) 540
МС m/z (M+H+) 473
1H ЯМР (400 МГц, CD3OD): δ 8,27 (с, 1H), 8,11 (с, 1H), 7,88 (д, J=3 Гц, 1H), 7,77 (м, 2H), 7,72 (д, J=8 Гц, 2H), 7,56 (м, 3H), 7,41 (т, J=8 Гц, 1H), 4,53 (уш.с, 1H), 4,44-4,28 (м, 4H), 4,15 (м, 1H), 3,86 (м, 2H), 3,28 (м, 1H), 2,50 (м, 4H). MC m/z 490 (M+H+)
МС m/z (M+H+) 473
МС m/z (M+H+) 508
1H ЯМР (CDCl3, 400 МГц): δ 8,79 (д, J=2,0 Гц, 1H), 7,93-8,09 (м, 2H), 7,39-7,64 (м, 2H), 7,18-7,34 (м, 2H), 6,98-7,16 (м, 2H), 6,76 (д, J=3,1 Гц, 1H), 4,20-4,51 (м, 3H), 4,13 (д, J=3,9 Гц, 1H), 3,92 (уш.с, 3H), 3,67-3,84 (м, 1H), 3,18-3,32 (м, 1H), 2,49 (уш.с, 4H).
МС m/z (M+H+) 508
МС m/z (M+H+) 490
Следуя процедуре, описанной выше для примера 1a, стадии H и I, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 1a, стадия J, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 467
МС m/z (M+H+) 485
1H ЯМР (CDCl3, 400 МГц): δ 8,83 (д, J=8,6 Гц, 1H), 8,73 (д, J=4,7 Гц, 2H), 8,33 (д, J=3,9 Гц, 1H), 7,80-8,02 (м, 2H), 7,64 (дд, J=8,8, 1,8 Гц, 1H), 7,54 (д, J=3,1 Гц, 1H), 7,10 (т, J=4,9 Гц, 1H), 6,75 (д, J=3,5 Гц, 1H), 4,03-4,72 (м, 6H), 3,86 (м, 2H), 3,08-3,37 (м, 1H), 2,31-2,68 (м, 3H).
МС m/z (M+H+) 474
МС m/z (M+H+) 474
МС m/z (M+H+) 492
МС m/z (M+H+) 492
Пример 1b

K. Метил 1-(3,4-дифторфенил)-индол-5-карбоксилат, 1p. Смесь метилиндол-5-карбоксилата 1j (2 г, 11,4 ммоль), 1-йод-3,4-дифторбензола 1o (1,5 мл, 12,5 ммоль), CuI (0,22 г, 1,14 ммоль), транс-N,N'-диметилциклогексан-1,2-диамина (0,54 мл, 3,43 ммоль) и K3PO4 (6,06 г, 28,5 ммоль) в толуоле (12 мл) подогревали при температуре 110°C в течение 7 часов. Реакционную смесь разбавили CH2Cl2 и профильтровали. Раствор сконцентрировали, и остаток очистили колоночной флэш-хроматографией (силикагель, 20% EtOAc/гептан), получив в результате соединение 1p (3,0 г).
L. 1-(3,4-Дифторфенил)-индол-5-карбоновая кислота, 1q. Смесь метил 1-(3,4-дифторфенил)-индол-5-карбоксилата 1p (3,0 г, 10,4 ммоль) и LiOH (1,0 г, 41,8 ммоль) в THF (120 мл) и H2O (60 мл) перемешивали при комнатной температуре в течение 5 суток. Водный 10%-ный раствор HCl добавили в реакционную смесь для доведения уровня pH до 3~4. Полученную смесь экстрагировали с помощью EtOAc (2x). Органический раствор промыли водным раствором NaCl, высушили над Na2SO4 и сконцентрировали, получив в результате соединение 1q (2,85 г).
М. 1-(3,4-Дифторфенил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 1362. Названное соединение 1362 получили в соответствии с примером 1 с использованием промежуточного соединения 1q из примера 1b и промежуточного соединения 1g из примера 1 в качестве исходных материалов. 1H ЯМР (CDCl3, 400 МГц): δ 7,99 (д, J=1,6 Гц, 1H), 7,88 (д, J=3,1 Гц, 1H), 7,44-7,64 (м, 3H), 7,18-7,44 (м, 4H), 6,75 (д, 1H), 4,47-4,63 (м, 1H), 4,19-4,47 (м, 4H), 4,07-4,19 (м, 1H), 3,89 (уш.с, 2H), 3,18-3,33 (м, 1H), 2,50 (т, J=5,1 Гц, 4H). МС m/z (M+H+) 508.
Следуя процедуре, описанной выше для примера 1b, стадии K и L, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:



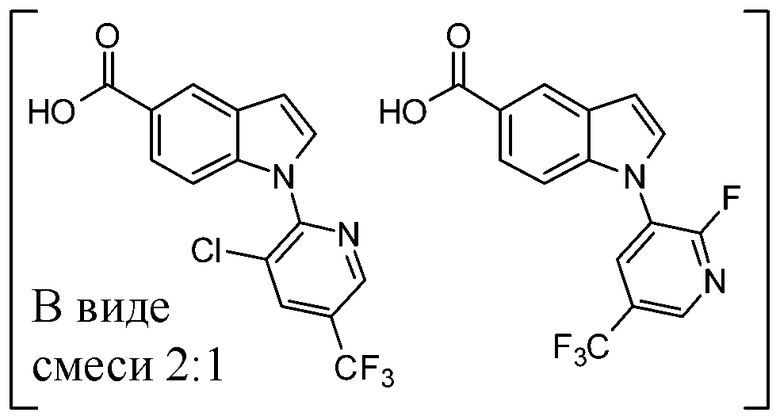
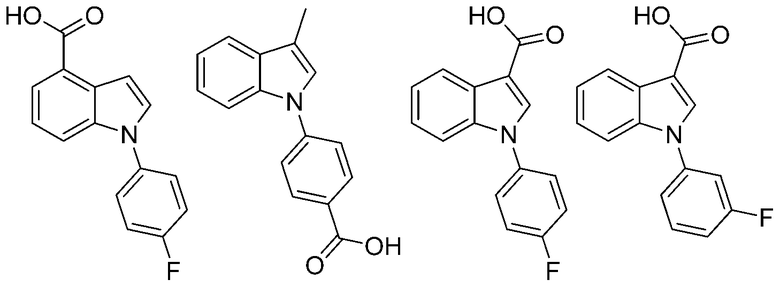
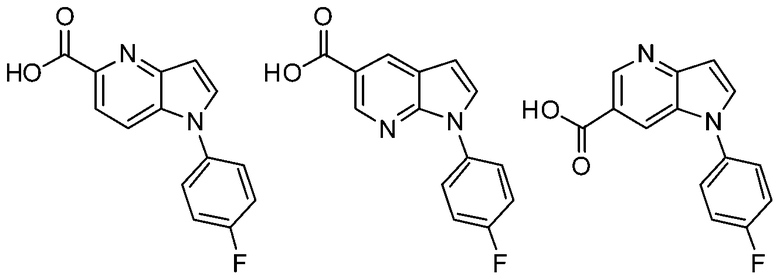
Следуя процедуре, описанной выше для примера 1b, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (CDCl3, 400 МГц): δ 8,79 (д, J=2,0 Гц, 1H), 8,00 (дд, J=11,5, 1,8 Гц, 2H), 7,44-7,65 (м, 2H), 7,18-7,42 (м, 4H), 6,75 (д, J=3,5 Гц, 1H), 4,20-4,46 (м, 3H), 4,13 (уш.с, 1H), 3,93 (уш.с, 3H), 3,67-3,85 (м, 1H), 3,17-3,36 (м, 1H), 2,49 (уш.с, 4H)
MC m/z 508 (M+H+)
1H ЯМР (CDCl3, 400 МГц): δ 9,42-9,61 (м, 1H), 7,99 (с, 1H), 7,54-7,64 (м, 1H), 7,45-7,54 (м, 1H), 7,15-7,43 (м, 4H), 6,93 (с, 1H), 6,75 (д, J=3,1 Гц, 1H), 6,52 (уш.с, 1H), 6,18-6,31 (м, 1H), 4,19-4,42 (м, 3H), 4,08-4,19 (м, 1H), 3,90 (уш.с, 4H), 3,24 (с, 1H), 2,34-2,56 (м, 4H)
MC m/z 490 (M+H+)
МС m/z (M+H+) 466,1
МС m/z (M+H+) 480,1
МС m/z (M+H+) 473,2
МС m/z (M+H+) 456,3
МС m/z (M+H+) 473,0
МС m/z (M+H+) 503,2
MS m/z (M+H+) 485,4
МС m/z (M+H+) 487,3
МС m/z (M+H+) 469,3
МС m/z (M+H+) 523,2
МС m/z (M+H+) 541,3
МС m/z (M+H+) 503,0
МС m/z (M+H+) 474,1
МС m/z (M+H+) 487,0
МС m/z (M+H+) 534,1
МС m/z (M+H+) 484,0
МС m/z (M+H+) 473,2
МС m/z (M+H+) 455,2
МС m/z (M+H+) 509,0
МС m/z (M+H+) 487,3
МС m/z (M+H+) 487,2
МС m/z (M+H+) 488,0
МС m/z (M+H+) 541,0
МС m/z (M+H+) 491,0
МС m/z (M+H+) 487,1
1H ЯМР (400 МГц, CDCl3): δ 9,06 (с, 1H), 8,4 (с, 1H), 7,9-7,68 (м, 8H), 7,4 (ар, 1H), 4,97 (м, 2H), 4,45 (м, 2H), 4,16 (уш.с, 1H)
МС m/z (M+H+) 508,0
1H ЯМР (400 МГц, CDCl3): δ 7,91 (м, 1H), 7,81 (м, 4H), 7,70 (м, 2H), 7,60 (м, 2H), 7,30 (м, 1H), 6,75 (м, 1H), 5,01-4,84 (м, 2H), 4,37 (м, 2H), 4,09 (уш.м, 1H)
МС m/z (M+H+) 540,2
МС m/z (M+H+) 522,2
1H ЯМР (400 МГц, CDCl3): δ 8,44 (с, 1H), 7,94 (с, 1H), 7,80 (м, 2H), 7,69 (м, 2H), 7,59 (м, 2H), 7,49 (м, 2H), 6,77 (м,1H), 4,65-4,15 (уш.м, 3H), 3,81 (уш.м, 4H), 3,0 (уш.м, 4H)
МС m/z (M+H+) 540,2
МС m/z (M+H+) 504,1
1H ЯМР (400 МГц, CDCl3): δ 7,92 (д, 1H), 7,78 (д, 1H), 7,69 (м, 1H), 7,42 (м, 3H), 7,21 (м, 6H), 4,94 (м, 1H), 4,40 (дд, 1H), 4,25 (дд, 1H), 4,0 (уш.м, 1H), 3,85 (уш.м, 3H), 3,15 (уш.м, 3H), 2,3 (с, 3H)
МС m/z (M+H+) 504,1
МС m/z (M+H+) 522,1
1H ЯМР (400 МГц, CDCl3): δ 8,0 (с, 1H), 7,86 (с, 1H), 7,80 (с, 1H), 7,62-7,42 (м, 3H), 7,36 (м, 3H), 5,05 (м, 1H), 4,5 (м, 1H), 4,35 (м, 1H), 4,08 (уш.м, 1H), 3,94 (уш.м, 4H), 3,24 (м, 3H)
МС m/z (M+H+) 522,2
МС m/z (M+H+) 465,1
Пример 1c
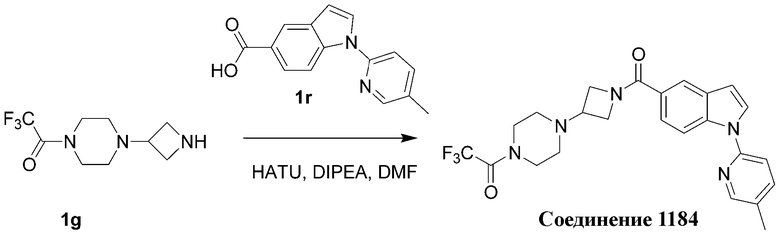
N. 1-(5-Метилпиридин-2-ил)-5-({3-[4-(трифторацетил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 1184. Названное соединение 1184 было получено способом, описанным в примере 1, с использованием промежуточного соединения 1r из примера 1b и промежуточного соединения 1g из примера 1 в качестве исходных материалов. МС m/z (M+H+) 472,1.
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 492,1
МС m/z (M+H+) 472,1
МС m/z (M+H+) 500,1
МС m/z (M+H+) 475,2
Пример 1d

О. Метил 2-фенил-бензооксазол-6-карбоксилат, 1u. Смесь метил 4-амино-3-гидроксибензоата 1s (0,3 г, 1,8 ммоль) и бензоилхлорида 1t (0,23 мл, 2,0 ммоль) в диоксане (2,5 мл) нагревали при температуре 210°C в микроволновой печи в течение 15 минут. Реакционную смесь разбавили CH2Cl2 и промыли водным раствором NaHCO3. Органический раствор высушили над Na2SO4, сконцентрировали и очистили колоночной флэш-хроматографией (силикагель, 20% EtOAc/гептан), получив в результате соединение 1u (0,39 г).
Р. 2-Фенилбензооксазол-6-карбоновая кислота, 1v. Смесь метил 2-фенилбензооксазол-6-карбоксилата 1u (0,37 г, 1,46 ммоль) и LiOH (0,10 г, 4,2 ммоль) в THF (4 мл), MeOH (4 мл) и H2O (4 мл) перемешивали при комнатной температуре в течение 6 часов. Для установления pH раствора на уровне 3~4 к смеси добавили 1Н раствора HCl. Полученную смесь экстрагировали с помощью EtOAc (2x). Органический раствор промыли водным раствором NaCl, высушили над Na2SO4 и сконцентрировали, получив в результате соединение 1t (0,34 г).
Следуя процедуре, описанной выше для примера 1d, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 1, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 474
МС m/z (M+H+) 542
МС m/z (M+H+) 542
Пример 1e
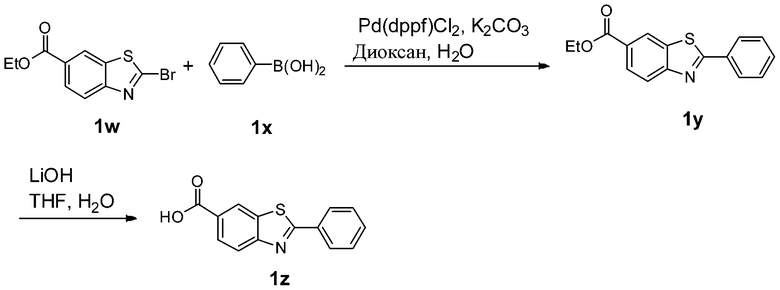
Q. Этил 2-фенилбензотиазол-6-карбоксилат, 1y. Смесь этил 2-бромбензотиазол-6-карбоксилата, 1w (300 мг, 1,05 ммоль), фенилбороновой кислоты 1x (192 мг, 1,57 ммоль), K2CO3 (188 мг, 1,36 ммоль) и Pd(dppf)Cl2·CH2Cl2 (43 мг, 0,05 ммоль) в диоксане (2 мл) и H2O (0,4 мл) нагревали при температуре 120°C в микроволновой печи в течение 25 минут. Реакционную смесь разбавили CH2Cl2, промыли H2O, высушили над Na2SO4 и сконцентрировали. В результате очистки колоночной флэш-хроматографией (силикагель, 15% EtOAc/гептан) было получено соединение 1y (220 мг).
R. 2-Фенилбензотиазол-6-карбоновая кислота, 1z. Этил 2-фенилбензотиазол-6-карбоксилат 1y (220 мг, 0,78 ммоль) перемешивали с LiOH (74 мг, 3,1 ммоль) в THF (4 мл) и H2O (4 мл) в течение 16 часов. Для установления pH раствора на уровне 3~4 к смеси добавили 1H раствора HCl. Полученную смесь экстрагировали с помощью EtOAc (2x). Органический раствор промыли водным раствором NaCl, высушили над Na2SO4 и сконцентрировали, получив в результате соединение 1z (200 мг).
Следуя процедуре, описанной выше для примера 1e, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, было получено следующее промежуточное соединение:

Следуя процедуре, описанной выше для примера 1, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 483
1H ЯМР (400 МГц, CD3OD): δ 8,25 (с, 1H), 8,12-8,06 (м, 3H), 7,88 (д, J=3 Гц, 1H), 7,74 (д, J=8 Гц, 1H), 7,53 (м, 4H), 4,53 (уш.с, 1H), 4,4-4,26 (м, 4H), 4,15 (м, 1H), 3,86 (м, 2H), 3,27 (м, 1H), 2,50 (м, 4H)
МС m/z (M+H+) 490
MC m/z 490 (M+H+)
Пример 1f

Q. Метил 1-(5-хлорпиридин-2-ил)-1H-индол-5-карбоксилат, 1bb. Смесь соединений 1j (1,14 ммоль, 200 мг), 1aa (1,14 ммоль, 150 мг), K2CO3 (2,28 ммоль, 315 мг) и NMP (1,5 мл) нагревали при температуре 200°C в микроволновом реакторе в течение 2 часов. Смесь влили в воду (50 мл) и экстрагировали с помощью EtOAc. Органический слой промыли солевым раствором, высушили над Na2SO4 и сконцентрировали в вакууме. Очистку производили колоночной флэш-хроматографией (силикагель, 15% EtOAc/гептан) с образованием 290 мг соединения 1bb (290 мг).
R. (5-Хлорпиридин-2-ил)-1H-индол-5-карбоновая кислота, 1cc. Смесь соединения 1bb (0,942 ммоль, 270 мг), LiOH (3,77 ммоль, 90 мг), THF (3 мл), MeOH (3 мл) и H2O (3 мл) перемешивали при комнатной температуре в течение ночи. Реакционную смесь подкислили 1Н водного раствора HCl до уровня pH=5. Твердый осадок отфильтровали, промыли EtOAc и высушили в вакууме, получив в результате 202 мг соединения 1cc.
Следуя процедуре, описанной выше для примера 1, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (CDCl3) δ 8,52 (д, J=2,2 Гц, 1H), 8,21 (д, J=8,6 Гц, 1H), 7,96 (с, 1H), 7,88 (д, J=3,2 Гц, 1H), 7,81 (дд, J=8,6, 2,4 Гц, 1H), 7,70 (д, J=3,4 Гц, 1H), 7,60 (д, J=8,8 Гц, 1H), 7,54 (д, J=2,9 Гц, 1H), 7,44 (д, J=8,6 Гц, 1H), 6,77 (д, J=3,4 Гц, 1H), 4,51 (уш.с, 1H), 4,19-4,47 (м, 4H), 4,12 (кв, J=7,1 Гц, 2H), 3,74-3,95 (м, 2H), 3,25 (т, J=5,6 Гц, 1H), 2,49 (уш.с, 4H)
МС m/z (M+H+) 508,0
МС m/z (M+H+) 501,0
1H ЯМР (CDCl3) δ 8,79 (с, 1H), 8,49 (с, 1H), 8,21 (д, J=8,6 Гц, 1H), 7,95 (с, 1H), 8,00 (с, 1H), 7,78 (д, J=8,6 Гц, 1H), 7,68 (д, J=2,9 Гц, 1H), 7,59 (д, J=8,6 Гц, 1H), 7,42 (д, J=8,6 Гц, 1H), 6,75 (д, J=2,9 Гц, 1H), 4,31-4,47 (м, 1H), 4,16-4,31 (м, 1H), 4,11 (к, J=7,0 Гц, 1H), 3,84-4,04 (м, 3H), 3,80 (уш.с, 1H), 3,18-3,31 (м, 1H), 2,47 (уш.с, 3H), 2,40 (уш.с, 1H)
МС m/z (M+H+) 507,0
Пример 2

A. [4-(1-Бензгидрилазетидин-3-ил)-пиперазин-1-ил]-фенилметанон, 2b. Названное соединение 2b было получено способом, описанным в примере 1, с заменой соединения 1d на соединение 2a на стадии C. Полученное соединение 2b очистили колоночной флэш-хроматографией. МС m/z (M+H+) 412,2.
B. (4-Азетидин-3-ил-пиперазин-1-ил)-фенилметанон, 2c. Названное соединение 2c было получено способом, описанным в примере 1, с заменой соединения 1f на соединение 2b на стадии D. Полученное соединение 2c использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 246,1.
C. 1-{1-[(4-Бромфенил)карбонил]азетидин-3-ил}-4-(фенилкарбонил)пиперазин, соединение 27. Названное соединение 27 было получено способом, описанным в примере 1, с заменой соединения 1g на соединение 2c и соединения 1h на соединение 2d на стадии E. Полученное соединение 27 очистили хроматографией на обращенной фазе. МС m/z (M+H+) 428,1/430,0.
Следуя процедуре, описанной выше для примера 2, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 415,2
МС m/z (M+H+) 419,2
ЖХ/МС m/z (M+H+) 421,2
МС m/z (M+H+) 393,2
ЖХ/МС m/z (M+H+) 442,2
ЖХ/МС m/z (M+H+) 444,1
ЖХ/МС m/z (M+H+) 456,1
ЖХ/МС m/z (M+H+) 456,1
ЖХ/МС m/z (M+H+) 460,2
ЖХ/МС m/z (M+H+) 486,3
ЖХ/МС m/z (M+H+) 500,3
1H ЯМР (300 МГц, CD3OD): δ 7,73 (д, 1H), 7,65 (м, 4H), 7,50 (м, 2H), 7,35-7,46 (м, 5H), 4,55 (м, 2H), 4,35 (м, 2H), 4,01 (м, 1H), 3,80 (м, 4H), 3,17 (м, 4H); ЖХ/МС m/z (M+H+) 494,1 (рассчитано для C27H25Cl2N3O2, 494,43)
1H ЯМР (300 МГц, CD3OD): δ 7,45-7,56 (м, 7H), 7,41 (т, 2H), 7,22 (м, 3H), 6,80 (д, 2H), 4,27-4,75 (м, 4H), 4,07 (м, 1H), 3,88 (м, 4H), 3,34 (с, 3H), 3,25 (м, 4H), ЖХ/МС m/z (M+H+) 455,3 (рассчитано для C28H30N4O2, 454,58)
1H ЯМР (300 МГц, CD3OD): δ 7,45-7,57 (м, 7H), 6,73 (д, 2H), 4,28-4,73 (м, 4H), 4,12 (м, 1H), 3,89 (м, 4H), 3,30 (м, 8H), 1,80 (м, 4H), 1,54 (м, 4H); ЖХ/МС m/z (M+H+) 447,3 (рассчитано для C27H34N4O2, 446,6)
ЖХ/МС m/z (M+H+) 431,1
1H ЯМР (400 МГц, MeOD): δ 7,86-7,95 (м, 1H), 7,73-7,79 (м, 1H), 7,62-7,68 (м, 2H), 7,53-7,59 (м, 2H), 7,47-7,52 (м, 2H), 7,41-7,47 (м, 2H), 7,33-7,41 (м, 4H), 7,21-7,33 (м, 2H), 5,67 (уш.с, 1H), 4,51-4,62 (м, 2H), 4,19-4,38 (м, 1H), 4,01-4,12 (м, 1H), 3,71-3,81 (м, 1H), 3,54-3,67 (м, 1H), 3,32 (м, 1H), 2,98-3,12 (м, 2H), 2,79-2,90 (м, 1H), 2,44-2,56 (м, 1H);
МС m/z (M+H+) 509,2 (рассчитано для C30H28N4O2S, 508,65)
1H ЯМР (400 МГц, MeOD): δ 7,67-7,75 (м, 2H), 7,59-7,67 (м, 4H), 7,53-7,58 (м, 2H), 7,40-7,53 (м, 9H), 7,31-7,40 (м, 2H), 5,73 (уш.с, 1H), 4,34-4,57 (м, 1H), 4,23-4,34 (м, 1H), 4,02-4,18 (м, 2H), 3,69-3,88 (м, 1H), 3,55-3,68 (м, 1H), 3,35-3,46 (м, 2H), 3,07 (м, 1H), 2,81-2,93 (м, 1H), 2,43-2,63 (м, 1H);
MC m/z (M+) 502,2 (рассчитано для C33H31N3O2, 502,23)
МС m/z (M+H+) 447,29 (рассчитано для C25H26N4O2S, 446,58)
МС m/z (M+H+) 463,2 (рассчитано для C25H26N4O3S, 462,57)
МС m/z (M+H+) 461,0 (рассчитано для C26H28N4O2S, 460,60)
МС m/z (M+H+) 466,3 (рассчитано для C28H27N5O2, 465,56)
МС m/z (M+H+) 368,2 (рассчитано для C21H22FN3O2, 367,43)
МС m/z (M+H+) 453,3 (рассчитано для C28H28N4O2, 452,56)
МС m/z (M+H+) 455,3 (рассчитано для C28H30N4O2, 454,58)
МС m/z (M+H+) 433,3 (рассчитано для C26H32N4O2, 432,57)
МС m/z (M+H+) 421,2 (рассчитано для C25H32N4O2, 420,56)
МС m/z (M+H+) 443,3 (рассчитано для C27H30N4O2, 442,57)
МС m/z (M+H+) 467,2 (рассчитано для C29H30N4O2, 466,59)
МС m/z (M+H+) 509,1 (рассчитано для C28H27F3N4O2, 508,55)
МС m/z (M+H+) 441,2 (рассчитано для C27H28N4O2, 440,55)
МС m/z (M+H+) 459,2 (рассчитано для C27H27FN4O2, 458,54)
МС m/z (M+H+) 469,2 (рассчитано для C29H32N4O2, 468,60)
МС m/z (M+H+) 456,221
МС m/z (M+H+) 442,3
МС m/z (M+H+) 442,3
МС m/z (M+H+) 434,161
МС m/z (M+H+) 458,1
МС m/z (M+H+) 414,151
МС m/z (M+H+) 394,205
МС m/z (M+H+) 506,086
МС m/z (M+H+) 408,221
МС m/z (M+H+) 396,167
МС m/z (M+H+) 415,136
МС m/z (M+H+) 428,157
МС m/z (M+H+) 475,2
МС m/z (M+H+) 484,0
МС m/z (M+H+) 455,1
МС m/z (M+H+) 457,1
МС m/z (M+H+) 491,1
МС m/z (M+H+) 415,2
МС m/z (M+H+) 435,1
МС m/z (M+H+) 436,0
МС m/z (M+H+) 516,1
МС m/z (M+H+) 502,0
МС m/z (M+H+) 509,1
МС m/z (M+H+) 523,1
МС m/z (M+H+) 523,3
МС m/z (M+H+) 523,2
МС m/z (M+H+) 509,0
Пример 3

A. (4-Бензилфенил)-пиперазин-1-ил-метанон, 3b. В раствор соединения 1a (1 г, 5,36 ммоль), соединения 3a (1,14 г, 5,36 ммоль) и DIPEA (1,38 г, 10,7 ммоль) в ацетонитриле (20 мл) ввели HBTU (2,64 г, 7,0 ммоль). Реакционную смесь перемешивали в течение 18 часов, и за это время растворитель удалили при пониженном давлении, а полученное соединение очистили методом ВЭЖХ на обращенной фазе. По окончании лиофилизации оставшееся твердое вещество растворили в DCM (20 мл) и медленно ввели трифторуксусную кислоту (15 мл). После перемешивания при комнатной температуре в течение 2 часов растворители были удалены, а остаток разделили между 1Н водного раствора NaOH и CHCl3. Органический слой отделили, высушили (MgSO4), отфильтровали и сконцентрировали, получив, таким образом, соединение 3b (1,21 г).
B. [4-(1-Бензгидрилазетидин-3-ил)-пиперазин-1-ил]-4-бензилфенилметанон, 3c. Названное соединение 3c было получено способом, описанным в примере 1, с заменой соединения 1d на соединение 3b на стадии C.
C. (4-Азетидин-3-ил-пиперазин-1-ил)-4-бензилфенилметанон, 3d. Названное соединение 3d было получено способом, описанным в примере 1, с заменой соединения 1f на соединение 3c на стадии D.
D. 1-[(4-Бензилфенил)карбонил]-4-[1-(фенилкарбонил)азетидин-3-ил]пиперазин, соединение 61. Соединение 3d было преобразовано в названное соединение 61 способом, описанным в примере 2, при использовании соединения 3d вместо соединения 2c, бензойной кислоты (соединение 1k) вместо соединения 2d и HBTU вместо HATU на стадии D. 1H ЯМР (400 МГц, MeOD): δ 7,64 (д, J=1,7 Гц, 2H), 7,51-7,58 (м, 1H); 7,48 (уш.с, 2H), 7,38 (с, 2H), 7,33 (д, J=8,1 Гц, 2H), 7,25 (уш.с, 2H), 7,20 (д, J=7,3 Гц, 3H), 4,51-4,64 (м, 1H), 4,33-4,51 (м, 2H), 4,20-4,33 (м, 1H), 4,01 (с, 2H), 3,86-3,96 (м, 2H), 3,69-3,86 (м, 3H), 3,07 (уш.с, 4H); МС m/z (M+H+) 440,2 (рассчитано для C28H29N3O2, 439,56).
Следуя процедуре, описанной выше для примера 3, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 433,1
МС m/z (M+H+) 433,2
МС m/z (M+H+) 444,1
МС m/z (M+H+) 433,2
МС m/z (M+H+) 414,0
МС m/z (M+H+) 434,0
МС m/z (M+H+) 413,0
МС m/z (M+H+) 428,1
МС m/z (M+H+) 417,0
МС m/z (M+H+) 481,1
МС m/z (M+H+) 462,1
МС m/z (M+H+) 461,0
МС m/z (M+H+) 481,0
МС m/z (M+H+) 481,0
МС m/z (M+H+) 466,1
МС m/z (M+H+) 482,2
МС m/z (M+H+) 501,0
МС m/z (M+H+) 483,0
МС m/z (M+H+) 483,0
МС m/z (M+H+) 509,0
МС m/z (M+H+) 509,0
Пример 4

A. трет-Бутиловый эфир 3-(4-бензоилпиперазин-1-ил)-азетидин-1-карбоновой кислоты, 4b. В раствор 1-Boc-азетидин-3-она (соединение 4a) и соединения 2a в CH3OH ввели декаборан при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Растворитель удалили при пониженном давлении и полученное соединение 4b использовали в последующей реакции без дополнительной очистки. МС m/z (M+H+) 346,2.
B. (4-Азетидин-3-ил-пиперазин-1-ил)-фенил-метанон, 2c. Названное соединение 2c было получено способом, описанным в примере 1, с заменой соединения 1c на соединение 4b на стадии B. Полученное соединение 2c использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 246,1.
C. 1-{1-[(4-Метил-2-фенил-1,3-тиазол-5-ил)карбонил]азетидин-3-ил}-4-(фенилкарбонил)пиперазин, соединение 62. Названное соединение 62 было получено способом, описанным в примере 1, с заменой соединения 1g на соединение 2c и соединения 1h на соединение 4c на стадии E. Полученное соединение 62 очистили хроматографией на обращенной фазе. МС m/z (M+H+) 447,1.
Следуя процедуре, описанной выше для примера 4, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
ЖХ/МС m/z (M+H+) 453,1
ЖХ/МС m/z (M+H+) 461,2
ЖХ/МС m/z (M+H+) 515,1
ЖХ/МС m/z (M+H+) 432,1
ЖХ/МС m/z (M+H+) 432,1
ЖХ/МС m/z (M+H+) 427,2
ЖХ/МС m/z (M+H+) 427,2
ЖХ/МС m/z (M+H+) 427,2
ЖХ/МС m/z (M+H+) 427,2
1H ЯМР (300 МГц, CD3OD): δ 7,81 (д, 1H), 7,64-7,77 (м, 3H), 7,59 (т, 1H), 7,42-7,54 (м, 7H), 7,36 (д, 1H), 4,70 (м, 1H), 4,58 (м, 1H), 4,47 (м, 1H), 4,35 (м, 1H), 4,04 (м, 1H), 3,86 (м, 4H), 3,19 (м, 4H); ЖХ/МС m/z (M+H+) 494,2 (рассчитано для C28H26F3N3O2, 493,53)
ЖХ/МС m/z (M+H+) 494,2
ЖХ/МС m/z (M+H+) 494,2
1H ЯМР (300 МГц, CD3OD): δ 7,74-7,89 (м, 8H), 7,46-7,54 (м, 5H), 4,68 (м, 1H), 4,61 (м, 1H), 4,47 (м, 1H), 4,38 (м, 1H), 4,07 (м, 1H), 3,88 (м, 4H), 3,23 (м, 4H); ЖХ/МС m/z (M+H+) 494,2 (рассчитано для C28H26F3N3O2, 493,53)
ЖХ/МС m/z (M+H+) 451,0
1H ЯМР (300 МГц, DMSO-d6): δ 7,77-7,86 (м, 3H), 7,68-7,76 (м, 3H), 7,43-7,58 (м, 7H), 4,60 (м, 2H), 4,39 (м, 1H), 4,28 (м, 1H), 4,08 (м, 1H), 3,29-3,94 (м, 6H), 3,06 (м, 2H); ЖХ/МС m/z (M+H+) 460,0 (рассчитано для C27H26ClN3O2, 459,98)
ЖХ/МС m/z (M+H+) 460,0
1H ЯМР (300 МГц, DMSO-d6): δ 7,87 (д, 2H), 7,81 (д, 2H), 7,73 (д, 2H), 7,67 (т, 1H), 7,48 (м, 5H), 4,67 (м, 1H), 4,58 (т, 1H), 4,43 (м, 1H), 4,29 (т, 1H), 4,10 (м, 1H), 3,25-3,93 (м, 6H), 3,06 (м, 2H); ЖХ/MC m/z (M+H+) 494,1 (рассчитано для C27H25Cl2N3O2, 494,43)
ЖХ/МС m/z (M+H+) 427,2
ЖХ/МС m/z (M+H+) 444,1
ЖХ/МС m/z (M+H+) 451,2
1H ЯМР (300 МГц, CD3OD): δ 7,25-7,74 (м, 13H), 4,08-4,59 (м, 4H), 3,43-3,97 (м, 5H), 2,92 (м, 4H); ЖХ/МС m/z (M+H+) 504,0/506,1 (рассчитано для C27H26BrN3O2, 504,43)
МС m/z (M+H+) 477,2
MC m/z (M+H+) 392,3
ЖХ/МС m/z (M+H+) 412,21 (рассчитано для C23H26ClN3O2, 411,92)
ЖХ/МС m/z (M+H+) 456,15 (рассчитано для C23H26BrN3O2, 456,38)
ЖХ/МС m/z (M+H+) 446,23 (рассчитано для C24H26F3N3O2, 445,48)
ЖХ/МС m/z (M+H+) 412,18 (рассчитано для C23H26ClN3O2, 411,92)
ЖХ/МС m/z (M+H+) 412,21 (рассчитано для C23H26ClN3O2, 411,92)
ЖХ/МС m/z (M+H+) 446,16 (рассчитано для C23H25Cl2N3O2, 446,37)
ЖХ/МС m/z (M+H+) 422,2 (рассчитано для C24H27N3O4, 421,49)
ЖХ/МС m/z (M+H+) 476,20 (рассчитано для C24H24F3N3O2S, 475,54
ЖХ/МС m/z (M+H+) 514,18 (рассчитано для C25H25F6N3O2, 514,18)
ЖХ/МС m/z (M+H+) 428,27 (рассчитано для C29H27N3O2, 427,54)
ЖХ/МС m/z (M+H+) 470,29 (рассчитано для C29H31N3O3, 469,59)
ЖХ/МС m/z (M+H+) 414,21 (рассчитано для C22H24ClN3O3, 413,91)
ЖХ/МС m/z (M+H+) 488,32 (рассчитано для C31H41N3O2, 487,69)
ЖХ/МС m/z (M+H+) 458,18 (рассчитано для C23H26BrN3O2, 456,39)
ЖХ/МС m/z (M+H+) 464,26 (рассчитано для C23H24F3N3O4, 475,54)
ЖХ/МС m/z (M+H+) 497,23 (рассчитано для C26H32N4O4S, 496,21)
ЖХ/МС m/z (M+H+) 503,37 (рассчитано для C31H42N4O2, 502,71)
ЖХ/МС m/z (M+H+) 406,2 (рассчитано для C23H23N3O2S, 405,52)
ЖХ/МС m/z (M+H+) 410,29 (рассчитано для C23H24ClN3O2, 409,92)
ЖХ/МС m/z (M+H+) 456,16 (рассчитано для C23H24BrN3O2, 454,37)
ЖХ/МС m/z (M+H+) 426,32 (рассчитано для C27H27N3O2, 425,54)
ЖХ/МС m/z (M+H+) 432,38 (рассчитано для C27H33N3O2, 431,58)
ЖХ/МС m/z (M+H+) 508,31 (рассчитано для C31H29N4O3, 507,59)
ЖХ/МС m/z (M+H+) 460,35 (рассчитано для C28H33N3O3, 459,59)
1H ЯМР (300 МГц, MeOD): δ 7,55 (ар, 2H), 7,4 (м, 5H). 7,25 (ар, 2H), 4,5 (м, 2H), 4,3 (м, 2H), 4,1 (м, 3H), 3,7 (уш.м, 4H), 3,0 (уш.м, 4H), 2,7 (м, 4H), 1,7 (м, 2H), 1,5 (м, 2H), 1,4 (с, 9H).
ЖХ/МС m/z (M+H+) 533,33 (рассчитано для C31H40N4O4, 532,69)
ЖХ/МС m/z (M+H+) 519,35 (рассчитано для C30H38N4O4, 518,66)
1H ЯМР (400 МГц, CDCl3): δ 7,57 (д, J=8,8 Гц, 2H), 7,44 (д, J=8,8 Гц, 2H), 7,36-7,42 (м, 4H), 7,20 (с, 1H), 4,25-4,34 (м, 1H), 4,17-4,26 (м, 1H), 4,13 (с, 1H), 3,97-4,08 (м, 1H), 3,81-3,95 (м, 1H), 3,68-3,80 (м, 1H), 3,32-3,61 (м, 2H), 3,15-3,27 (м, 1H), 2,16-2,59 (м, 4H), 1,50 (с, 9H)
MC (m/z) (M+H+) 465,2
MC m/z (M+H+) 481,0
MC m/z (M+H+) 515,1
MC m/z (M+H+) 481,0
MC m/z (M+H+) 465,1
MC m/z (M+H+) 485,1
MC m/z (M+H+) 430,2
MC m/z (M+H+) 484,0
MC m/z (M+H+) 511,1
MC m/z (M+H+) 484,2
Пример 5
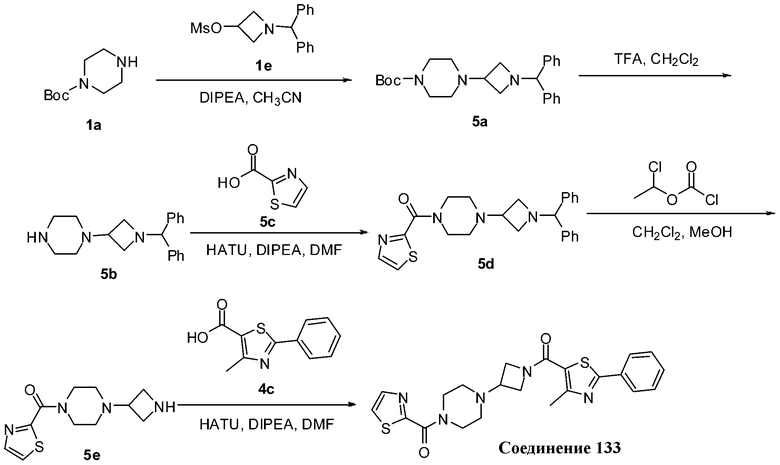
A. трет-Бутиловый эфир 4-(1-бензгидрилазетидин-3-ил)-пиперазин-1-карбоновой кислоты, 5a. Названное соединение 5a получили способом, описанным в примере 1, с заменой соединения 1d на соединение 1a на стадии В. Полученное соединение 5a использовали в следующей реакции без очистки. MC m/z (M+H+) 408,1.
B. 1-(1-Бензгидрилазетидин-3-ил)-пиперазин, 5b. Названное соединение 5b получили способом, описанным в примере 1, с заменой соединения 1c на соединение 5a на стадии B. Полученное соединение 5b использовали в следующей реакции без очистки. MC m/z (M+H+) 208,1.
C. [4-(1-Бензгидрилазетидин-3-ил)-пиперазин-1-ил]-тиазол-2-ил-метанон, 5d. Названное соединение 5d получили способом, описанным в примере 1, с заменой соединения 1g на соединение 5b и соединения 1h на соединение 5c на стадии E. Полученное соединение 5d очистили колоночной флэш-хроматографией. МС m/z (M+H+) 419,2.
D. (4-Азетидин-3-ил-пиперазин-1-ил)-тиазол-2-ил-метанон, 5e. Названное соединение 5e получили способом, описанным в примере 1, с заменой соединения 1f на соединение 5d на стадии D. Полученное соединение 5e использовали в следующей реакции без очистки. МС m/z (M+H+) 253,2.
E. 1-{1-[(4-Метил-2-фенил-1,3-тиазол-5-ил)карбонил]азетидин-3-ил}-4-1,3-тиазол-2-ил-карбонил)пиперазин, соединение 133. Названное соединение 133 было получено способом, описанным в примере 1, с заменой соединения 1g на соединение 5e и соединения 1h на соединение 4c на стадии E. Полученное соединение 133 очистили обращенно-фазовой хроматографией. 1Н ЯМР (300 МГц, CD3OD): δ 7,98 (м, 3H), 7,89 (д, 1H), 7,46-7,55 (м, 3H), 4,80 (м, 1H), 4,41-4,69 (м, 4H), 4,09 (м, 3H), 3,35 (м, 5H), 2,68 (с, 3H); ЖХ/МС m/z (M+H+) 454,2 (рассчитано для C22H23N5O2S2, 453,59).
Следуя процедуре, описанной выше для примера 5, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (300 МГц, CD3OD): δ 7,98 (с, 1H), 7,88 (с, 1H), 7,67 (м, 2H), 7,16 (м, 1H), 4,79 (м, 1H), 4,35-4,69 (м, 4H), 4,07 (м, 3H), 3,33 (м, 5H), 2,62 (с, 3H); ЖХ/МС m/z (M+H+) 460,0 (рассчитано для C20H21N5O2S3, 459,61)
1H ЯМР (300 МГц, CD3OD): δ 7,98 (д, 1H), 7,82-7,91 (м, 3H), 7,32 (д, 2H), 4,80 (м, 1H), 4,40-4,66 (м, 4H), 4,08 (м, 3H), 3,34 (м, 5H), 2,66 (с, 3H), 2,46 (с, 3H); ЖХ/МС m/z (M+H+) 468,1 (рассчитано для C23H25N5O2S2, 467,62)
1H ЯМР (300 МГц, CD3OD): δ 8,19 (д, 2H), 7,97 (д, 1H), 7,86 (д, 1H), 7,82 (д, 2H), 4,25-4,76 (м, 5H), 3,95 (м, 2H), 3,76 (м, 1H), 3,33 (м, 2H), 2,99 (м, 3H), 2,69 (с, 3H); ЖХ/МС m/z (M+H+) 522,2 (рассчитано для C23H22F3N5O2S2, 521,59)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,91 (т, 1H), 7,88 (д, 1H), 7,83 (дт, 1H), 7,54 (м, 2H), 7,47 (дд, 2H), 7,13 (дд, 1H), 4,30-4,79 (м, 5H), 4,02 (м, 3H), 3,24 (м, 5H); ЖХ/МС m/z (M+H+) 439,0 (рассчитано для C22H22N4O2S2, 438,57)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,89 (д, 1H), 7,75 (м, 4H), 7,51 (м, 2H), 7,14 (м, 1H), 4,28-4,82 (м, 5H), 4,02 (м, 3H), 3,25 (м, 5H); ЖХ/МС m/z (M+H+) 439,1 (рассчитано для C22H22N4O2S2, 438,57)
ЖХ/МС m/z (M+H+) 434,0
ЖХ/МС m/z (M+H+) 434,0
ЖХ/МС m/z (M+H+) 434,0
ЖХ/МС m/z (M+H+) 434,0
ЖХ/МС m/z (M+H+) 435,0
ЖХ/МС m/z (M+H+) 435,0
ЖХ/МС m/z (M+H+) 435,0
ЖХ/МС m/z (M+H+) 435,0
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,88 (д, 1H), 7,81 (д, 1H), 7,74 (д, 2H), 7,68 (т, 1H), 7,59 (т, 1H), 7,45 (д, 2H), 7,37 (д, 1H), 4,33-4,82 (м, 5H), 4,04 (м, 3H), 3,27 (м, 5H); ЖХ/МС m/z (M+H+) 501,0 (рассчитано для C25H23F3N4O2S, 500,55)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,88 (д, 1H), 7,81 (д, 1H), 7,73 (дт, 1H), 7,67 (д, 1H), 7,49-7,64 (м, 4H), 7,39 (д, 1H), 4,30-4,81 (м, 5H), 4,03 (м, 3H), 3,25 (м, 5H); ЖХ/МС m/z (M+H+) 501,0 (рассчитано для C25H23F3N4O2S, 500,55)
ЖХ/МС m/z (M+H+) 501,0
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,76-7,89 (м, 9H), 4,62-4,77 (м, 5H), 3,97 (м, 3H), 3,13 (м, 5H); ЖХ/MC m/z (M+H+) 501,0 (рассчитано для C25H23F3N4O2S, 500,55)
1H ЯМР (300 МГц, CD3OD): δ 8,34 (т, 1H), 8,21 (дт, 1H), 7,97 (д, 1H), 7,94 (дд, 1H), 7,87 (д, 1H), 7,72-7,82 (м, 2H), 7,54-7,67 (м, 2H), 4,26-4,68 (м, 6H), 3,84-4,06 (м, 3H), 3,13 (м, 4H); ЖХ/МС m/z (M+H+) 512,0/513,9 (рассчитано для C23H22BrN5O2S, 512,43)
ЖХ/МС m/z (M+H+) 479,0
ЖХ/МС m/z (M+H+) 479,0
ЖХ/МС m/z (M+H+) 452,0
ЖХ/МС m/z (M+H+) 458,0
ЖХ/МС m/z (M+H+) 458,0
ЖХ/МС m/z (M+H+) 507,9
1H ЯМР (300 МГц, CD3OD): δ 8,31 (с, 1H), 7,89 (м, 3H), 7,79 (д, 1H), 7,52 (т, 1H), 5,01 (м, 1H), 4,84 (м, 2H), 4,65 (м, 1H), 4,38 (дд, 1H), 4,26 (дд, 1H), 3,93 (м, 3H), 3,17 (м, 4H); ЖХ/МС m/z (M+H+) 507,9 (рассчитано для C21H19Cl2N5O2S2, 508,45)
ЖХ/МС m/z (M+H+) 470,0
ЖХ/МС m/z (M+H+) 440,0
1H ЯМР (300 МГц, DMSO-d6): δ 8,10 (д, 1H), 8,06 (д, 1H), 7,78-7,86 (м, 3H), 7,68-7,77 (м, 3H), 7,46-7,58 (м, 2H), 4,62 (м, 2H), 4,40 (м, 1H), 4,30 (м, 1H), 4,08 (м, 1H), 4,27-3,87 (м, 6H), 3,12 (м, 2H); ЖХ/МС m/z (M+H+) 458,1 (рассчитано для C25H23N5O2S, 457,56)
1H ЯМР (300 МГц, DMSO-d6): δ 8,10 (д, 1H), 8,06 (д, 1H), 7,78-7,86 (м, 3H), 7,68-7,77 (м, 3H), 7,46-7,58 (м, 2H), 4,61 (м, 2H), 4,37 (м, 1H), 4,29 (м, 1H), 4,05 (м, 1H), 4,30-3,84 (м, 6H), 3,08 (м, 2H); ЖХ/МС m/z (M+H+) 467,1 (рассчитано для C24H23ClN4O2S, 466,99)
1H ЯМР (300 МГц, CD3OD): δ 7,98 (д, 1H), 7,88 (д, 1H), 7,76 (м, 4H), 7,66 (м, 2H), 7,48 (м, 2H), 4,71 (м, 3H), 4,58 (м, 1H), 4,47 (м, 1H), 4,36 (м, 1H), 4,02 (м, 3H), 3,23 (м, 4H); ЖХ/МС m/z (M+H+) 467,1 (рассчитано для C24H23ClN4O2S, 466,99)
1H ЯМР (300 МГц, CD3OD): δ 7,88 (д, 1H), 7,78 (д, 1H), 7,68 (м, 4H), 7,55 (д, 2H), 7,39 (т, 1H), 4,57 (м, 3H), 4,45 (м, 1H), 4,35 (м, 1H), 4,23 (м, 1H), 3,91 (м, 2H), 3,81 (м, 1H), 3,03 (м, 4H); ЖХ/МС m/z (M+H+) 501,0 (рассчитано для C24H22Cl2N4O2S, 501,44)
ЖХ/МС m/z (M+H+) 434,1
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,37-7,67 (м, 8H), 4,66 (м, 3H), 4,53 (м, 1H), 4,42 (м, 1H), 4,30 (м, 1H), 3,98 (м, 2H), 3,85 (м, 1H), 3,07 (м, 4H); ЖХ/МС m/z (M+H+) 451,0 (рассчитано для C24H23FN4O2S, 450,54)
1H ЯМР (300 МГц, CD3OD): δ 7,98 (д, 1H), 7,77-7,92 (м, 9H), 4,63-4,79 (м, 3H), 4,57 (м, 1H), 4,46 (м, 1H), 4,35 (м, 1H), 3,90-4,13 (м, 3H), 3,19 (м, 4H); ЖХ/МС m/z (M+H+) 458,1 (рассчитано для C25H23N5O2S, 457,56)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,76 (м, 4H), 7,62 (дд, 4H), 4,67 (м, 3H), 4,51 (м, 1H), 4,44 (м, 1H), 4,30 (м, 1H), 3,98 (м, 2H), 3,88 (м, 1H), 3,10 (м, 4H); ЖХ/МС m/z (M+H+) 511,0/513,0 (рассчитано для C24H23BrN4O2S, 511,44)
ЖХ/МС m/z (M+H+) 434,1
1H ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,22 (с, 1H), 7,37-7,67 (м, 8H), 4,70 (м, 1H), 4,57 (м, 1H), 4,45 (м, 1H), 4,34 (м, 1H), 4,11 (м, 4H), 3,99 (м, 1H), 3,17 (м, 4H); ЖХ/МС m/z (M+H+) 451,0 (рассчитано для C24H23FN4O2S, 450,54)
ЖХ/МС m/z (M+H+) 458,1
1H ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,22 (с, 1H), 7,76 (м, 4H), 7,61 (дд, 4H), 4,68 (м, 1H), 4,57 (м, 1H), 4,46 (м, 1H), 4,36 (м, 1H), 4,15 (м, 4H), 4,04 (м, 1H), 3,22 (м, 4H); ЖХ/МС m/z (M+H+) 511,0/513,0 (рассчитано для C24H23BrN4O2S, 511,44)
МС m/z (M+H+) 439,2
МС m/z (M+H+) 515,2
МС m/z (M+H+) 381,1
МС m/z (M+H+) 467,2
МС m/z (M+H+) 480,1
ЖХ/МС m/z (M+H+) 436,2
МС m/z (M+H+) 463,2 (рассчитано для C25H26N4O3S, 462,57)
МС m/z (M+H+) 463,2 (рассчитано для C25H26N4O3S, 462,57)
МС m/z (M+H+) 509,0 (рассчитано для C30H28N4O2S, 508,65)
МС m/z (M+H+) 461,0 (рассчитано для C26H28N4O2S, 460,60)
МС m/z (M+H+) 446,9 (рассчитано для C25H26N4O2S, 446,58)
МС m/z (M+H+) 447,3 (рассчитано для C25H26N4O2S, 446,58)
1H ЯМР (300 МГЦ, CD3OD): δ 7,81-8,02 (м, 4H), 7,52 (д, 2H), 4,30-4,64 (м, 6H) 3,84-4,09 (м, 3H), 3,10-3,29 (м, 4H), 2,67 (с, 3H); ЖХ/МС m/z (M+H+) 488,1 (рассчитано для C22H22ClN5O2S2, 488,03)
1H ЯМР (300 МГц, CD3OD): δ 7,95-8,05 (м, 2H), 7,84-7,94 (м, 2H), 7,45-7,60 (м, 2H), 4,32-4,84 (м, 6H) 3,92-4,09 (м, 3H), 3,15-3,27 (м, 4H), 2,68 (с, 3H); ЖХ/МС m/z (M+H+) 488,1 (рассчитано для C22H22ClN5O2S2, 488,03)
1H ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,16-8,36 (м, 3H), 7,79-7,89 (м, 1H), 7,66-7,78 (м, 1H), 4,23-4,76 (м, 4H) 3,84-4,22 (м, 5H), 3,04-3,22 (м, 4H), 2,70 (с, 3H); ЖХ/МС m/z (M+H+) 522,2 (рассчитано для C23H22F2N5O2S2, 521,59)
МС m/z (M+H+) 476,1
МС m/z (M+H+) 499,1
МС m/z (M+H+) 516,2
МС m/z (M+H+) 448,0
МС m/z (M+H+) 552,0/554,0
МС m/z (M+H+) 452,1
МС m/z (M+H+) 466,0
МС m/z (M+H+) 615,0
МС m/z (M+H+) 479,1
МС m/z (M+H+) 469,1
МС m/z (M+H+) 499,1
МС m/z (M+H+) 472,1
МС m/z (M+H+) 490,0
МС m/z (M+H+) 442,0
МС m/z (M+H+) 491,1
МС m/z (M+H+) 424,0
МС m/z (M+H+) 465,1
МС m/z (M+H+) 450,1
МС m/z (M+H+) 460,2
МС m/z (M+H+) 469,0
МС m/z (M+H+) 519,0
МС m/z (M+H+) 491,4
МС m/z (M+H+) 438,3
МС m/z (M+H+) 469,4
МС m/z (M+H+) 473,2
МС m/z (M+H+) 413,3
МС m/z (M+H+) 426,3
МС m/z (M+H+) 427,2
МС m/z (M+H+) 399,3
МС m/z (M+H+) 454,4
МС m/z (M+H+) 439,2
МС m/z (M+H+) 497,1
МС m/z (M+H+) 413,3
МС m/z (M+H+) 455,3
МС m/z (M+H+) 427,2
МС m/z (M+H+) 399,1
МС m/z (M+H+) 413,3
МС m/z (M+H+) 443,2
МС m/z (M+H+) 539,4
МС m/z (M+H+) 517,3
МС m/z (M+H+) 515,4
МС m/z (M+H+) 461,1
МС m/z (M+H+) 534,2
МС m/z (M+H+) 500,1
МС m/z (M+H+) 516,2
МС m/z (M+H+) 587,3
МС m/z (M+H+) 575,2
МС m/z (M+H+) 475,0
МС m/z (M+H+) 560,2
МС m/z (M+H+) 550,0
МС m/z (M+H+) 584,1
МС m/z (M+H+) 547,3
МС m/z (M+H+) 515,2
МС m/z (M+H+) 607,3
МС m/z (M+H+) 456,1
МС m/z (M+H+) 442,2
МС m/z (M+H+) 442,2
МС m/z (M+H+) 456,1
МС m/z (M+H+) 476,1
МС m/z (M+H+) 584,1
МС m/z (M+H+) 447,1/449,1
МС m/z (M+H+) 447,1/449,1
МС m/z (M+H+) 427,2
МС m/z (M+H+) 520,2
МС m/z (M+H+) 458,3
МС m/z (M+H+) 450,1
МС m/z (M+H+) 584,1
МС m/z (M+H+) 472,2
МС m/z (M+H+) 601,0
МС m/z (M+H+) 456,1
МС m/z (M+H+) 529,0
МС m/z (M+H+) 429,1
МС m/z (M+H+) 428,1
МС m/z (M+H+) 469,2
МС m/z (M+H+) 458,3
МС m/z (M+H+) 455,1
МС m/z (M+H+) 533,1
МС m/z (M+H+) 506,2
МС m/z (M+H+) 561,0
МС m/z (M+H+) 455,1
МС m/z (M+H+) 548,2
МС m/z (M+H+) 485,1
МС m/z (M+H+) 475,1
МС m/z (M+H+) 490,0
МС m/z (M+H+) 431,3
МС m/z (M+H+) 459,1
МС m/z (M+H+) 535,2
МС m/z (M+H+) 470,1
МС m/z (M+H+) 452,2
МС m/z (M+H+) 518,1
МС m/z (M+H+) 526,0
МС m/z (M+H+) 574,0
МС m/z (M+H+) 544,0
МС m/z (M+H+) 504,1
МС m/z (M+H+) 542,2
МС m/z (M+H+) 473,0
1H ЯМР (300 МГц, CD3OD): δ 8,28 (с, 1H), 8,23 (д, 1H), 7,98 (д, 1H), 7,88 (д, 1H), 7,82 (д, 1H), 7,72 (т, 1H), 4,35-4,81 (м, 6H), 3,92-4,13 (м, 3H), 3,19-3,27 (м, 4H), 2,71 (с, 3H)
МС m/z (M+H+) 522,2
МС m/z (M+H+) 488,1
МС m/z (M+H+) 488,1
МС m/z (M+H+) 472,0
МС m/z (M+H+) 472,0
МС m/z (M+H+) 492,1
МС m/z (M+H+) 437,1
МС m/z (M+H+) 491,1
МС m/z (M+H+) 518,1
МС m/z (M+H+) 491,1
МС m/z (M+H+) 492,1
МС m/z (M+H+) 437,1
МС m/z (M+H+) 491,1
МС m/z (M+H+) 518,1
МС m/z (M+H+) 491,1
МС m/z (M+H+) 507,9/508,8
МС m/z (M+H+) 503/505
МС m/z (M+H+) 503/505
МС m/z (M+H+) 453/455
МС m/z (M+H+) 453/455
МС m/z (M+H+) 453/455
МС m/z (M+H+) 453/455
МС m/z (M+H+) 472,2
МС m/z (M+H+) 472,2
МС m/z (M+H+) 507,1
МС m/z (M+H+) 507,1
МС m/z (M+H+) 476,1
МС m/z (M+H+) 550,03
МС m/z (M+H+) 584,34
МС m/z (M+H+) 422,06
МС m/z (M+H+) 433,2
МС m/z (M+H+) 466,2
МС m/z (M+H+) 486,3
МС m/z (M+H+) 424
МС m/z (M+H+) 466,2
МС m/z (M+H+) 432,9
МС m/z (M+H+) 424
МС m/z (M+H+) 466
МС m/z (M+H+) 483,3
МС m/z (M+H+) 431,29
МС m/z (M+H+) 473,27
МС m/z (M+H+) 509,28
МС m/z (M+H+) 557,14
1H ЯМР (CDCl3): δ 9,02 (д, 1H), 8,31 (с, 1H), 8,22 (с, 1H), 8,12 (м, 1H), 7,77 (с, 1H), 7,69 (м, 1H), 7,50 (м, 5H), 7,35 (м, 1H), 5,91 (уш.м, 1H), 4,83 (м, 1H), 4,64 (м, 1H), 4,48-4,46 (м, 2H), 4,14 (м, 1H), 3,86 (м, 1H), 3,87 (м, 1H), 3,51 (м, 1H), 3,12 (т, 1H), 2,97 (м, 1H).
МС m/z (M+H+) 557,18
МС m/z (M+H+) 591,26
МС m/z (M+H+) 591,24
МС m/z (M+H+) 256
1H ЯМР (CDCl3): δ 7,99 (д, 1H), 7,88 (д, 1H), 7,71 (м, 2H), 7,52-7,32 (м, 4H), 4,75 (уш., 4H), 4,0 (уш.м, 3H), 3,22 (уш.м, 4H)
МС m/z (M+H+) 439,16
МС m/z (M+H+) 458,13
МС m/z (M+H+) 410,12
МС m/z (M+H+) 424,21
МС m/z (M+H+) 323,13
МС m/z (M+H+) 486
МС m/z (M+H+) 441,1
МС m/z (M+H+) 441,1
МС m/z (M+H+) 429,1
МС m/z (M+H+) 429,1
МС m/z (M+H+) 440,1
МС m/z (M+H+) 440,1
МС m/z (M+H+) 415
МС m/z (M+H+) 439,7, 440,3
МС m/z (M+H+) 428,8
МС m/z (M+H+) 440,1
МС m/z (M+H+) 444,1
МС m/z (M+H+) 415,2
МС m/z (M+H+) 428,8
1H ЯМР (CDCl3): δ 7,88 (д, 1H), 7,78 (д, 1H), 7,5 (м, 1H), 7,27 (м, 1H), 7,12 (м, 1H), 4,16 (уш.м, 1H), 4,32 (уш.м, 2H), 3,16 (м, 3H), 2,36 (с, 3H)
МС m/z (M+H+) 443,1
МС m/z (M+H+) 472,83
МС m/z (M+H+) 473,1
МС m/z (M+H+) 473,1
МС m/z (M+H+) 473,1
МС m/z (M+H+) 493,2
МС m/z (M+H+) 493,2
МС m/z (M+H+) 563,1
МС m/z (M+H+) 479,1
МС m/z (M+H+) 479,1
МС m/z (M+H+) 479,1
МС m/z (M+H+) 479,1
МС m/z (M+H+) 473,1
МС m/z (M+H+) 473,1
МС m/z (M+H+) 473,1
МС m/z (M+H+) 431
МС m/z (M+H+) 431
МС m/z (M+H+) 430,86
МС m/z (M+H+) 430,93
МС m/z (M+H+) 501,1
МС m/z (M+H+) 486,9
МС m/z (M+H+) 447,6
МС m/z (M+H+) 501,1
МС m/z (M+H+) 448
МС m/z (M+H+) 448
МС m/z (M+H+) 487
МС m/z (M+H+) 487
МС m/z (M+H+) 448,1
МС m/z (M+H+) 5,1
МС m/z (M+H+) 509,72
МС m/z (M+H+) 510
МС m/z (M+H+) 510
МС m/z (M+H+) 463,81
МС m/z (M+H+) 463,81
МС m/z (M+H+) 463,81
МС m/z (M+H+) 464,1
МС m/z (M+H+) 464,1
МС m/z (M+H+) 494,97
МС m/z (M+H+) 477,02
МС m/z (M+H+) 477,02
МС m/z (M+H+) 466,1
МС m/z (M+H+) 465,98
МС m/z (M+H+) 448,2
МС m/z (M+H+) 466
1H ЯМР (CDCl3): δ 7,38 (м, 2H), 7,19-6,84 (м, 5H), 6,88 (м, 1H), 6,56 (м, 1H), 6,13 (м, 1H), 4,67-4,21 (м, 3H), 4,12-3,90 (уш.д, 4H), 3,25 (уш.м, 3H)
МС m/z (M+H+) 461,2
МС m/z (M+H+) 465,2
МС m/z (M+H+) 465,1
МС m/z (M+H+) 447,1
МС m/z (M+H+) 477,1
МС m/z (M+H+) 477,1
МС m/z (M+H+) 477,1
МС m/z (M+H+) 458,2
МС m/z (M+H+) 458,1
МС m/z (M+H+) 485,1
МС m/z (M+H+) 440,2
МС m/z (M+H+) 543,1
МС m/z (M+H+) 440,2
МС m/z (M+H+) 543,1
МС m/z (M+H+) 525,2
МС m/z (M+H+) 543
МС m/z (M+H+) 465,1
МС m/z (M+H+) 465,1
МС m/z (M+H+) 465,1
МС m/z (M+H+) 428,3
МС m/z (M+H+) 495,1
МС m/z (M+H+) 472,8
МС m/z (M+H+) 472,8
МС m/z (M+H+) 465,1
МС m/z (M+H+) 488,1
МС m/z (M+H+) 490,1
МС m/z (M+H+) 475
МС m/z (M+H+) 471,1
МС m/z (M+H+) 476,1
МС m/z (M+H+) 509,0
Пример 6
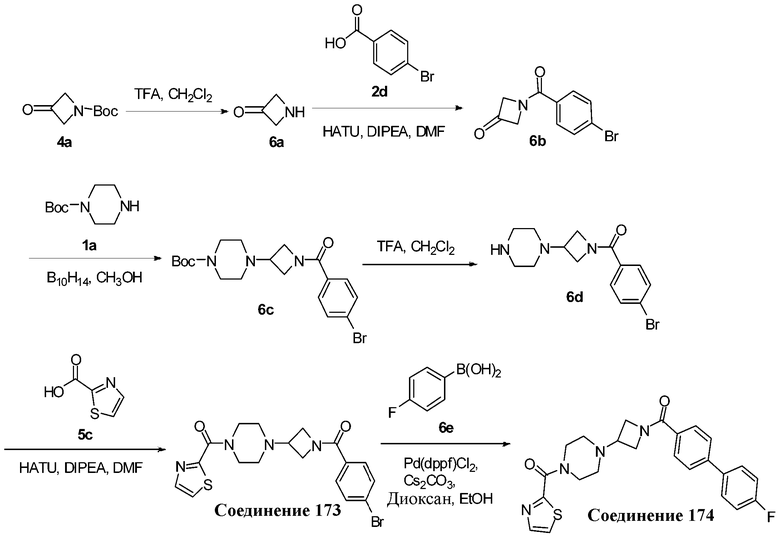
A. Азетидин-3-он, 6a. Названное соединение 6a было получено способом, описанным в примере 1, с заменой соединения 1c на соединение 4a на стадии B. Полученное соединение 6a использовали в следующей реакции без дополнительной очистки. МС m/z (M+H++CF3CO2H) 186,1.
B. 1-(4-Бромбензоил)-азетидин-3-он, 6b. Названное соединение 6b было получено способом, описанным в примере 1, с заменой соединения 1g на соединение 6a и соединения 1h на соединение 2d на стадии E. Полученное соединение 6b использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 419,2.
C. трет-Бутиловый эфир 4-[1-(4-бромбензоил)-азетидин-3-ил]-пиперазин-1-карбоновой кислоты, 6c. Названное соединение 6c было получено способом, описанным в примере 4, с заменой соединения 4a на соединение 6b и соединения 2a на соединение 1a на стадии А. Полученное соединение 6c очистили колоночной флэш-хроматографией. МС m/z (M+H+) 424,0, 426,1.
D. (4-Бромфенил)-(3-пиперазин-1-ил-азетидин-1-ил)-метанон, 6d. Названное соединение 6d было получено способом, описанным в примере 1, с заменой соединения 1c на соединение 6c на стадии B. Полученное соединение 6d использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 324,08/326,08.
E. 1-{1-[(4-Бромфенил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 173. Названное соединение 173 было получено способом, описанным в примере 1, с заменой соединения 1g на соединение 6d и соединения 1h на соединение 5c на стадии E. Полученное соединение 173 использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 435,0, 437,0.
F. 1-{1-[(4'-Фтордифенил-4-ил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 174. К суспензии соединения 173 (0,05 г, 0,115 ммоль), соединения 6e (0,0193 г, 0,14 ммоль) и Cs2CO3 (0,094 г, 0,288 ммоль) в диоксане (3 мл) и EtOH (1 мл) добавили Pd(dppf)Cl2 (0,0084 г, 0,0115 ммоль). Реакционную смесь перемешивали при 80°C в течение 3 часов. После охлаждения твердый осадок отделили путем фильтрации и промыли CH3OH. Полученный фильтрат сконцентрировали. Полученное соединение 174 очистили хроматографией на обращенной фазе. 1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,65-7,79 (м, 6H), 7,21 (т, 2H), 4,67 (м, 3H), 4,52 (м, 1H), 4,43 (м, 1H), 4,31 (м, 1H), 3,98 (м, 2H), 3,89 (м, 1H), 3,11 (м, 4H); МС m/z (M+H+) 451,2 (рассчитано для C24H23FN4O2S, 450,54).
Следуя процедуре, описанной выше для примера 6, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (300 МГц, CD3OD): δ 7,98 (д, 1H), 7,88 (д, 1H), 7,85 (д, 1H), 7,77 (м, 4H), 7,62 (м, 2H), 4,54-4,81 (м, 4H) 4,46 (м, 1H), 4,38 (м, 1H), 4,04 (м, 3H), 3,25 (м, 4H); ЖХ/МС m/z (M+H+) 501,0/503,1 (рассчитано для C24H22Cl2N4O2, 501,44)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,74 (м, 4H), 7,45 (м, 2H), 7,35 (т, 1H), 7,22 (д, 1H), 4,68 (м, 3H), 4,53 (м, 1H), 4,44 (м, 1H), 4,32 (м, 1H), 3,87-4,05 (м, 3H), 3,15 (м, 4H); ЖХ/МС m/z (M+H+) 447,1 (рассчитано для C25H26N4O2S, 446,58)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,76 (д, 2H), 7,46 (д, 2H), 7,30 (дд, 1H), 7,02 (тд, 1H), 6,94 (дд, 1H), 4,68 (м, 3H), 4,55 (м, 1H), 4,44 (м, 1H), 4,33 (м, 1H), 4,01 (м, 2H), 3,92 (м, 1H), 3,14 (м, 4H); ЖХ/МС m/z (M+H+) 465,1 (рассчитано для C25H25FN4O2S, 464,57)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,80 (дд, 1H), 7,76 (м, 4H), 7,64 (м, 1H), 7,36 (т, 1H), 4,68 (м, 3H), 4,52 (м, 1H), 4,45 (м, 1H), 4,32 (м, 1H), 3,89-4,06 (м, 3H), 3,16 (м, 4H); ЖХ/МС m/z (M+H+) 485,1 (рассчитано для C24H22ClFN4O2S, 484,98)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87(д, 1H), 7,77 (д, 2H), 7,65 (д, 2H), 7,55 (м, 1H), 7,10 (м, 2H), 4,65 (м, 3H), 4,50 (м, 1H), 4,42 (м, 1H), 4,30 (м, 1H), 3,97 (м, 2H), 3,86 (м, 1H), 3,07 (м, 4H); ЖХ/МС m/z (M+H+) 469,0 (рассчитано для C24H22F2N4O2S, 468,53)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,75 (м, 4H), 7,39 (т, 1H), 7,22 (д, 1H), 7,18 (т, 1H), 6,97 (дд, 1H), 4,67 (м, 3H), 4,51 (м, 1H), 4,43 (м, 1H), 4,32 (м, 1H), 3,96 (м, 3H), 3,86 (с, 3H), 3,15 (м, 4H); ЖХ/МС m/z (M+H+) 463,2 (рассчитано для C25H26N4O3S, 462,57)
1H ЯМР (300 МГц, CD3OD): δ 7,98 (д, 1H), 7,87 (д, 1H), 7,70 (м, 4H), 7,16 (м, 2H), 6,92 (д, 1H), 6,01 (с, 2H), 4,69 (м, 3H), 4,54 (м, 1H), 4,44 (м, 1H), 4,33 (м, 1H), 3,97 (м, 3H), 3,17 (м, 4H); ЖХ/МС m/z (M+H+) 477,1 (рассчитано для C25H24N4O4S, 476,56)
1H ЯМР (300 МГц, CD3OD): δ 7,79-8,01 (м, 11H), 7,50-7,56 (м, 2H), 4,60 (м, 1H), 4,49 (м, 1H), 4,37 (м, 1H), 4,27 (м, 1H), 4,08 (м, 4H), 3,95 (м, 1H), 3,14 (м, 4H); ЖХ/МС m/z (M+H+) 483,1 (рассчитано для C28H26N4O2S, 482,61)
1H ЯМР (300 МГц, CD3OD): δ 8,53 (т, 1H), 8,29 (м, 1H), 8,10 (м, 1H), 7,97 (д, 1H), 7,82-7,90 (м, 5H), 7,75 (т, 1H), 4,69 (м, 3H), 4,55 (м, 1H), 4,46 (м, 1H), 4,34 (м, 1H), 3,88-4,07 (м, 3H), 3,15 (м, 4H); ЖХ/МС m/z (M+H+) 478,2 (рассчитано для C24H23N5O4S, 477,55)
1H ЯМР (300 МГц, CD3OD): δ 9,14 (д, 1H), 8,80 (д, 1H), 8,24 (д, 1H), 8,13 (дд, 1H), 7,97 (д, 1H), 7,89 (м, 5H), 7,68 (м, 2H), 4,70 (м, 3H), 4,60 (м, 1H), 4,47 (м, 1H), 4,36 (м, 1H), 4,00 (м, 2H), 3,91 (м, 1H), 3,12 (м, 4H); ЖХ/МС m/z (M+H+) 484,2 (рассчитано для C27H25N5O2S, 483,6)
ЖХ/МС m/z (M+H+) 486,1
1H ЯМР (300 МГц, CD3OD): δ 7,94 (м, 2H), 7,80 (м, 4H), 7,70 (м, 2H), 7,45-7,53 (м, 5H), 4,66 (м, 1H), 4,52 (м, 1H), 4,44 (м, 1H), 4,31 (м, 1H), 3,95 (м, 1H), 3,84 (м, 4H), 3,10 (м, 4H); ЖХ/МС m/z (M+H+) 494,1 (рассчитано для C28H26F3N3O2, 493,53)
ЖХ/МС m/z (M+H+) 444,1
1H ЯМР (300 МГц, CD3OD): δ 7,73 (м, 4H), 7,48 (м, 5H), 7,36 (т, 1H), 7,19 (д, 1H), 7,14 (т, 1H), 6,94 (дд, 1H), 4,19-4,82 (м, 5H), 3,83 (м, 5H), 2,98 (м, 4H), 1,34 (д, 6H); ЖХ/МС m/z (M+H+) 484,2 (рассчитано для C30H33N3O3, 483,62)
ЖХ/МС m/z (M+H+) 510,1
ЖХ/МС m/z (M+H+) 445,2
ЖХ/МС m/z (M+H+) 474,1
ЖХ/МС m/z (M+H+) 484,2
ЖХ/МС m/z (M+H+) 480,1
ЖХ/МС m/z (M+H+) 525,3
1H ЯМР (300 МГц, CD3OD): δ 7,76 (м, 4H), 7,38-7,54 (м, 8H), 7,13 (м, 1H), 4,66 (м, 1H), 4,53 (м, 1H), 4,43 (м, 1H), 4,31 (м, 1H), 3,95 (м, 1H), 3,83 (м, 4H), 3,11 (м, 4H); ЖХ/МС m/z (M+H+) 444,1 (рассчитано для C27H26FN3O2, 443,53)
1H ЯМР (300 МГц, CD3OD): δ 7,77(д, 2H), 7,60 (д, 2H), 7,39-7,55 (м, 9H), 4,68 (м, 1H), 4,57 (м, 1H), 4,45 (м, 1H), 4,33 (м, 1H), 3,97 (м, 1H), 3,83 (м, 4H), 3,13 (м, 4H); ЖХ/МС m/z (M+H+) 510,1 (рассчитано для C28H26F3N3O3, 509,53)
ЖХ/МС m/z (M+H+) 440,2
ЖХ/МС m/z (M+H+) 484,2
ЖХ/МС m/z (M+H+) 484,2
ЖХ/МС m/z (M+H+) 474,3
ЖХ/МС m/z (M+H+) 486,3
ЖХ/МС m/z (M+H+) 462,1
ЖХ/МС m/z (M+H+) 474,3
ЖХ/МС m/z (M+H+) 462,1
1H ЯМР (300 МГц, CD3OD): δ 7,73 (дд, 4H), 7,33-7,54 (м, 8H), 7,23 (дт, 1H), 4,18-4,72 (м, 4H), 3,83 (м, 5H), 3,01 (м, 4H), 2,80 (с, 6H); ЖХ/МС m/z (M+H+) 548,3 (рассчитано для C29H33N5O4S, 547,68)
ЖХ/МС m/z (M+H+) 477,1
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,78 (м, 4H), 7,65 (м, 2H), 7,51 (т, 1H), 7,42 (д, 1H), 4,25-4,76 (м, 6H), 4,00 (с, 2H), 3,86-4,03 (м, 3H), 3,13 (м, 4H); ЖХ/МС m/z (M+H+) 472,2 (рассчитано для C26H25N5O2S, 471,59)
1H ЯМР (300 МГц, CD3OD): δ 8,22 (м, 1H), 7,95-8,07 (м, 3H), 7,71-7,90 (м, 6H), 4,31-4,81 (м, 6H), 4,03 (м, 3H), 3,21-3,36 (м, 4H), 3,19 (с, 3H); ЖХ/МС m/z (M+H+) 511,2 (рассчитано для C25H26N4O4S2, 510,64)
1H ЯМР (300 МГц, CD3OD): δ 8,11 (д, 2H), 7,97 (д, 1H), 7,76-7,91 (м, 7H), 4,70 (м, 3H), 4,55 (м, 1H), 4,45 (м, 1H), 4,34 (м, 1H), 3,98 (м, 3H), 3,16 (м, 4H), 2,65 (с, 3H); ЖХ/МС m/z (M+H+) 475,2 (рассчитано для C26H26N4O3S, 474,59)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,76 (м, 4H), 7,72 (м, 1H), 7,65 (м, 1H), 7,49 (м, 2H), 4,69 (м, 3H), 4,53 (м, 1H), 4,44 (м, 1H), 4,32 (м, 1H), 3,96 (м, 3H), 3,15 (м, 4H); ЖХ/МС m/z (M+H+) 461,2 (рассчитано для C25H24N4O3S, 460,56)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,86 (д, 1H), 7,69 (м, 4H), 7,52 (д, 2H), 6,88 (д, 2H), 4,66 (м, 3H), 4,51 (м, 1H), 4,42 (м, 1H), 4,29 (м, 1H), 3,98 (м, 2H), 3,86 (м, 1H), 3,09 (м, 4H); ЖХ/МС m/z (M+H+) 449,2 (рассчитано для C24H24N4O3S, 448,55)
1H ЯМР (300 МГц, CD3OD): δ 8,03 (д, 1H), 7,97 (д, 1H), 7,92 (дд, 1H), 7,86 (д, 1H), 7,80 (м, 4H), 7,73 (д, 1H), 4,62 (м, 3H), 4,45 (м, 2H), 4,28 (м, 1H), 3,96 (м, 2H), 3,82 (м, 1H), 3,03 (м, 4H); ЖХ/МС m/z (M+H+) 535,0 (рассчитано для C25H22ClF3N4O2S, 534,99)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,78-7,95 (м, 9H), 4,70 (м, 3H), 4,55 (м, 1H), 4,45 (м, 1H), 4,34 (м, 1H), 3,97 (м, 3H), 3,17 (м, 4H), 2,72 (с, 6H); ЖХ/МС m/z (M+H+) 540,2 (рассчитано для C26H29N5O4S2, 539,68)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,88 (д, 1H), 7,71 (д, 2H), 7,69 (д, 2H), 7,26 (дд, 1H), 7,08 (дд, 1H), 4,70 (м, 3H), 4,56 (м, 1H), 4,46 (м, 1H), 4,35 (м, 1H), 3,99 (м, 3H), 3,20 (м, 4H); ЖХ/МС m/z (M+H+) 499,2 (рассчитано для C25H24F2N4O3S, 498,56)
1H ЯМР (300 МГц, CD3OD): δ 8,36 (д, 2H), 7,78-7,99 (м, 8H), 4,67 (м, 3H), 4,52 (м, 1H), 4,44 (м, 1H), 4,31 (м, 1H), 3,98 (м, 2H), 3,99 (м, 1H), 3,12 (м, 4H); ЖХ/МС m/z (M+H+) 478,2 (рассчитано для C24H23N5O4S, 477,55)
1H ЯМР (300 МГц, CD3CN): δ 10,38 (с, 1H), 7,96 (д, 1H), 7,84-7,91 (м, 2H), 7,59-7,69 (м, 5H), 7,19 (д, 1H), 4,33-4,64 (м, 4H), 4,23 (м, 2H), 3,91 (с, 3H), 3,89 (м, 1H), 3,74 (м, 2H), 3,02 (м, 4H); ЖХ/МС m/z (M+H+) 491,2 (рассчитано для C26H26N4O4S, 490,59)
ЖХ/МС m/z (M+H+) 476,1
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,72 (м, 4H), 7,28 (т, 1H), 7,11 (д, 1H), 7,06 (т, 1H), 6,82 (дд, 1H), 4,64 (м, 3H), 4,49 (м, 1H), 4,40 (м, 1H), 4,28 (м, 1H), 3,96 (м, 2H), 3,81 (м, 1H), 3,03 (м, 4H); ЖХ/МС m/z (M+H+) 449,2 (рассчитано для C24H24N4O3S, 448,55)
1H ЯМР (300 МГц, CD3OD): δ 7,98 (д, 1H), 7,88 (д, 1H), 7,76 (м, 4H), 7,55 (т, 1H), 7,45 (м, 2H), 7,28 (м, 1H), 4,73 (м, 3H), 4,60 (м, 1H), 4,47 (м, 1H), 4,38 (м, 1H), 4,03 (м, 3H), 3,26 (м, 4H), 3,00 (с, 1H); ЖХ/МС m/z (M+H+) 526,2 (рассчитано для C25H27N5O4S2, 525,65)
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,80 (м, 1H), 7,75 (м, 4H), 7,37 (м, 2H), 7,30 (м, 1H), 4,69 (м, 3H), 4,52 (м, 1H), 4,44 (м, 1H), 4,31 (м, 1H), 3,85-4,07 (м, 3H), 3,13 (м, 4H), 1,53 (с, 9H); ЖХ/МС m/z (M+H+) 548,3 (рассчитано для C29H33N5O4S, 547,68)
1Н ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,75 (м, 4H), 7,37 (т, 1H), 7,21 (д, 1H), 7,17 (т, 1H), 6,96 (дд, 1H), 4,67 (м, 3H), 4,52 (м, 1H), 4,43 (м, 1H), 4,30 (м, 1H), 3,76-4,04 (м, 5H), 3,10 (м, 4H), 2,08 (м, 1H), 1,06 (д, 6H); ЖХ/МС m/z (M+H+) 505,2 (рассчитано для C28H32N4O3S: 504,66)
ЖХ/МС m/z (M+H+) 529,2
1Н ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 8,14 (с, 1H), 7,89 (м, 1H), 7,86 (д, 1H), 7,79 (м, 4H), 7,76 (м, 1H), 7,50-7,69 (м, 2H), 6,36 (д, 1H), 4,62 (м, 3H), 4,48 (м, 1H), 4,40 (м, 1H), 4,27 (м, 1H), 4,95 (м, 2H), 3,77 (м, 1H), 3,00 (м, 4H); ЖХ/МС m/z (M+H+) 484,2 (рассчитано для C27H25N5O2S: 483,6)
1Н ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,79 (м, 4H), 7,74 (м, 5H), 6,60 (д, 1H), 4,66 (м, 3H), 4,53 (м, 1H), 4,43 (м, 1H), 4,31 (м, 1H), 3,98 (м, 2H), 3,88 (м, 1H), 3,80 (с, 3H), 3,11 (м, 4H); ЖХ/МС m/z (M+H+) 517,2 (рассчитано для C28H28N4O4S: 516,62)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,22 (с, 1H), 7,74 (м, 4H), 7,69 (дд, 2H), 7,21 (т, 2H), 4,67 (м, 1H), 4,56 (м, 1H), 4,45 (м, 1H), 4,34 (м, 1H), 3,94-4,22 (м, 5H), 3,18 (м, 4H); ЖХ/МС m/z (M+H+) 451,2 (рассчитано для C24H23FN4O2S: 450,54)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,22 (с, 1H), 7,77 (д, 2H), 7,65 (д, 2H), 7,55 (м, 1H), 7,12 (м, 1H), 7,08 (д, 1H), 4,69 (м, 1H), 4,57 (м, 1H), 4,45 (м, 1H), 4,36 (м, 1H), 3,94-4,22 (м, 5H), 3,20 (м, 4H); ЖХ/МС m/z (M+H+) 469,1 (рассчитано для C24H22F2N4O2S: 468,53)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,22 (с, 1H), 7,79 (дд, 1H), 7,76 (м, 4H), 7,63 (м, 1H), 7,35 (т, 1H), 4,67 (м, 1H), 4,56 (м, 1H), 4,46 (м, 1H), 4,35 (м, 1H), 3,95-4,23 (м, 5H), 3,21 (м, 4H); ЖХ/МС m/z (M+H+) 485,1 (рассчитано для C24H22ClFN4O2S: 484,98)
1Н ЯМР (300 МГц, CD3OD): δ 8,96 (с, 1H), 8,12 (с, 1H), 7,75 (д, 1H), 7,67 (м, 4H), 7,52 (м, 2H), 4,57 (м, 1H), 4,50 (м, 1H), 4,37 (м, 1H), 4,27 (м, 1H), 3,88-4,15 (м, 5H), 3,13 (м, 4H); ЖХ/МС m/z (M+H+) 501,1 (рассчитано для C24H22Cl2N4O2S: 501,44)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,23 (с, 1H), 7,94 (м, 2H), 7,80 (м, 4H), 7,70 (м, 2H), 4,67 (м, 2H), 4,45 (м, 2H), 4,01-4,29 (м, 5H), 3,30 (м, 4H); ЖХ/МС m/z (M+H+) 501,1 (рассчитано для C25H23F3N4O2S: 500,55)
1Н ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,79 (м, 4H), 7,75 (д, 1H), 7,63 (м, 2H), 7,38 (д, 1H), 4,52-4,80 (м, 4H), 4,45 (м, 1H), 4,38 (м, 1H), 3,89-4,10 (м, 3H), 3,17 (м, 4H); ЖХ/МС m/z (M+H+) 448,0 (рассчитано для C24H25N5O2S: 447,56)
ЖХ/МС m/z (M+H+) 504,0
1Н ЯМР (300 МГц, DMSO-d6): δ 8,21 (с, 1H), 8,10 (д, 1H), 7,97 (д, 1H), 7,89 (д, 2H), 7,79 (м, 3H), 7,48 (м, 4H), 4,62 (м, 2H), 4,40 (м, 1H), 4,30 (м, 1H), 4,10 (м, 1H), 3,86 (м, 4H), 3,55 (м, 2H), 3,06 (м, 2H); ЖХ/МС m/z (M+H+) 528,0 (рассчитано для C28H25ClF3N3O2: 527,98)
ЖХ/МС m/z (M+H+) 483,3
1Н ЯМР (300 МГц, DMSO-d6): δ 8,10 (д, 1H), 8,06 (д, 1H), 8,00 (м, 1H), 7,75 (д, 2H), 7,70 (д, 2H), 7,57 (дт, 1H), 7,34-7,46 (м, 2H), 4,61 (м, 2H), 4,37 (м, 1H), 4,29 (м, 1H), 4,05 (м, 1H), 3,35-3,82 (м, 6H), 3,09 (м, 2H), 2,07 (с, 3H); ЖХ/МС m/z (M+H+) 490,2 (рассчитано для C26H27N5O3S: 489,6)
ЖХ/МС m/z (MH+) 490,2
ЖХ/МС m/z (M+H+) 511,2
1Н ЯМР (300 МГц, DMSO-d6): δ 8,01-8,14 (м, 4H), 7,88 (д, 2H), 7,67-7,83 (м, 4H), 4,60 (м, 2H), 4,39 (м, 1H), 4,28 (м, 1H), 4,06 (м, 2H), 3,22-3,85 (м, 5H), 3,10 (м, 2H); ЖХ/МС m/z (M+H+) 501,1 (рассчитано для C25H23F3N4O2S: 500,55)
1Н ЯМР (300 МГц, CD3OD): δ 7,85-7,94 (м, 2H), 7,40-7,73 (м, 10H), 4,42 (м, 1H), 4,26 (м, 2H), 4,16 (м, 1H), 3,61-3,96 (м, 5H), 2,99 (м, 4H), 2,47 (с, 3H); ЖХ/МС m/z (M+H+) 508,2 (рассчитано для C29H28F3N3O2: 507,56)
1Н ЯМР (300 МГц, CD3OD): δ 7,85-8,01 (м, 4H), 7,54-7,72 (м, 4H), 7,45 (д, 1H), 4,69 (м, 2H), 4,44 (м, 1H), 4,29 (м, 2H), 4,20 (м, 1H), 3,99 (м, 2H), 3,90 (м, 1H), 3,10 (м, 4H), 2,49 (с, 3H); ЖХ/МС m/z (M+H+) 515,1 (рассчитано для C26H25F3N4O2S: 514,57)
1Н ЯМР (300 МГц, CD3OD): δ 9,04 (с, 1H), 8,21 (с, 1H), 7,89 (м, 2H), 7,51-7,72 (м, 4H), 7,45 (д, 1H), 3,87-4,54 (м, 9H) 3,14 (м, 4H), 2,48 (с, 3H); ЖХ/МС m/z (M+H+) 515,1 (рассчитано для C26H25F3N4O2S: 514,57)
1Н ЯМР (300 МГц, CD3OD): δ 7,98 (д, 1H), 7,88 (д, 1H), 7,54-7,77 (м, 6H), 7,36 (д, 1H), 4,64-4,80 (м, 3H), 4,59 (м,H), 4,48 (м, 1H), 4,38 (м, 1H), 3,92-4,12 (м, 3H), 3,27 (м, 4H), 2,30 (с, 3H); ЖХ/МС m/z (M+H+) 515,1 (рассчитано для C26H25F3N4O2S: 514,57)
1Н ЯМР (300 МГц, CD3OD): δ 9,07 (с, 1H), 8,22 (с, 1H), 7,49-7,78 (м, 6H), 7,34 (д, 1H), 4,66 (м, 1H), 4,39-4,58 (м, 2H), 4,33 (м, 1H), 3,87-4,20 (м, 5H), 3,14 (м, 4H), 2,31 (с, 3H); ЖХ/МС m/z (M+H+) 515,1 (рассчитано для C26H25F3N4O2S: 514,57)
1Н ЯМР (300 МГц, CD3OD): δ 7,44-7,75 (м, 11H), 7,34 (д, 1H), 4,64 (м, 1H), 4,34-4,55 (м, 2H), 4,29 (м, 1H), 3,66-3,97(м, 5H), 3,03 (м, 4H), 2,30 (с, 3H); ЖХ/МС m/z (M+H+) 508,2 (рассчитано для C29H28F3N3O2: 507,56)
1Н ЯМР (300 МГц, CD3OD): δ 7,91-8,05 (м, 3H), 7,87 (д, 1H), 7,56-7,80 (м, 5H), 4,60-4,77 (м, 2H), 4,38-4,51 (м, 2H), 4,24-4,38 (м, 2H), 3,84-4,09 (м, 3H), 3,10 (м, 4H); ЖХ/МС m/z (M+H+) 519,2 (рассчитано для C25H22F4N4O2S: 518,54)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,20 (с, 1H), 7,95 (м, 2H), 7,55-7,80 (м, 5H), 4,38-4,51 (м, 2H), 4,25-4,38 (м, 2H), 3,86-4,19 (м, 5H), 3,08 (м, 4H); ЖХ/МС m/z (M+H+) 519,2 (рассчитано для C25H22F4N4O2S: 518,54)
1Н ЯМР (300 МГц, CD3OD): δ 7,90-8,01 (м, 2H), 7,56-7,80 (м, 5H), 7,42-7,56 (м, 5H), 4,35-4,50 (м, 2H), 4,20-4,35 (м, 2H), 3,66-3,98 (м, 5H), 3,00 (м, 4H); ЖХ/МС m/z (M+H+) 512,1 (рассчитано для C28H25F4N3O2: 511,52)
1Н ЯМР (300 МГц, CD3OD): δ 7,79 (д, 1H), 7,88 (д, 1H), 7,71-7,82 (м, 2H), 7,56-7,69 (м, 2H), 7,45 (д, 1H), 7,39 (д, 1H), 7,34 (дд, 1H), 4,61-4,78 (м, 3H), 4,57 (м, 1H), 4,46 (м, 1H), 4,34 (м, 1H), 3,87-4,06 (м, 3H), 3,89 (с, 3H), 3,17 (м, 4H); ЖХ/МС m/z (M+H+) 531,2 (рассчитано для C26H25F3N4O3S: 530,57)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,22 (с, 1H), 7,71-7,81 (м, 2H), 7,55-7,69 (м, 2H), 7,45 (д, 1H), 7,38 (с, 1H), 7,33 (дд, 3H), 4,70 (м, 1H), 4,58 (м, 1H), 4,47 (м, 1H), 4,36 (м, 1H), 3,94-4,25 (м, 5H), 3,89 (с, 3H), 3,21 (м, 4H); ЖХ/МС m/z (M+H+) 531,2 (рассчитано для C26H25F3N4O3S: 530,57)
1Н ЯМР (300 МГц, CD3OD): δ 7,72-7,84 (м, 2H), 7,56-7,71 (м, 2H), 7,27-7,56 (м, 8H), 4,66 (м, 1H), 4,37-4,59 (м, 2H), 4,32 (м, 1H), 3,66-4,03 (м, 8H), 3,08 (м, 4H); ЖХ/МС m/z (M+H+) 524,3 (рассчитано для C29H28F3N3O3: 523,56)
1Н ЯМР (300 МГц, CD3OD): δ 7,90-8,03 (м, 3H), 7,82-7,90 (м, 2H), 7,62-7,79 (м, 3H), 7,57 (д, 1H), 4,62-4,78 (м, 2H), 4,41-4,54 (м, 1H), 4,20-4,40 (м, 3H), 3,90-4,10 (м, 3H), 3,02-3,24 (м, 4H); ЖХ/МС m/z (M+H+) 535,0 (рассчитано для C25H22ClF3N4O2S: 534,99)
1Н ЯМР (300 МГц, CD3OD): δ 9,05 (с, 1H), 8,20 (с, 1H), 7,90-8,02 (м, 2H), 7,85 (с, 1H), 7,63-7,81 (м, 3H), 7,56 (д, 1H), 4,40-4,54 (м, 1H), 4,17-4,38 (м, 3H), 3,85-4,17 (м, 5H), 2,98-3,15 (м, 4H); ЖХ/МС m/z (M+H+) 535,0 (рассчитано для C25H22ClF3N4O2S: 534,99)
1Н ЯМР (300 МГц, CD3OD): δ 7,87-7,97 (м, 2H), 7,84 (д, 1H), 7,64-7,79 (м, 3H), 7,55 (д, 1H), 7,41-7,52 (м, 5H), 4,41 (дд, 1H), 4,21-4,34 (м, 2H), 4,17 (дд, 1H), 3,65-3,99 (м, 5H), 2,94 (м, 4H); ЖХ/МС m/z (M+H+) 528,2 (рассчитано для C28H25ClF3N3O2: 527,98)
1Н ЯМР (300 МГц, CD3OD): δ 9,05 (с, 1H), 8,19 (д, 1H), 7,75 (дд, 1H), 7,55-7,66 (м, 2H), 7,51 (дд, 1H), 7,27-7,45 (м, 2H), 4,42 (дд, 1H), 4,21-4,34 (м, 2H), 3,95-4,21 (м, 5H), 3,88 (м, 1H), 2,94-3,15 (м, 4H), 2,46 (с, 3H); ЖХ/МС m/z (M+H+) 499,0 (рассчитано для C25H24ClFN4O2S: 499,01)
1Н ЯМР (300 МГц, CD3OD): δ 9,05 (с, 1H), 8,19 (д, 1H), 7,98 (д, 1H), 7,88 (дд, 1H), 7,71 (д, 1H), 7,63 (м, 1H), 7,57 (дд, 1H), 7,45 (д, 1H), 4,44 (дд, 1H), 4,23-4,35 (м, 2H), 3,85-4,23 (м, 6H), 2,96-3,19 (м, 4H), 2,48 (с, 3H); ЖХ/МС m/z (M+H+) 549,2 (рассчитано для C26H24ClF3N4O2S: 549,02)
1Н ЯМР (300 МГц, CD3OD): δ 7,75 (дд, 1H), 7,28-7,65 (м, 10H), 4,38 (дд, 1H), 4,16-4,29 (м, 2H), 4,10(м, 1H), 3,60-3,95 (м, 5H), 2,91 (м, 4H), 2,45 (с, 3H); ЖХ/МС m/z (M+H+) 492,1 (рассчитано для C28H27ClFN3O2: 492,00)
1Н ЯМР (300 МГц, CD3OD): δ 7,97 (м, 1H), 7,87 (дд, 1H), 7,71 (д, 1H), 7,62 (м, 1H), 7,56 (м, 1H), 7,38-7,52 (м, 6H), 4,39 (дд, 1H), 4,16-4,28 (м, 2H), 4,11 (м, 1H), 3,63-3,93 (м, 5H), 2,91 (м, 4H), 2,47 (с, 3H); ЖХ/МС m/z (M+H+) 542,1 (рассчитано для C29H27ClF3N3O2: 542,01)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,20 (с, 1H), 7,49-7,67 (м, 2H), 7,44 (дд, 1H), 7,20-7,37 (м, 3H), 4,63 (м, 1H), 4,37-4,56 (м, 2H), 4,31 (м, 1H), 3,84-4,19 (м, 5H), 3,12 (м, 4H), 2,30 (с, 3H); ЖХ/МС m/z (M+H+) 499,0 (рассчитано для C25H24ClFN4O2S: 499,01)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,20 (с, 1H), 7,66-7,76 (м, 2H), 7,51-7,65 (м, 3H), 7,36 (д, 1H), 4,63 (м, 1H), 4,37-4,56 (м, 2H), 4,29 (м, 1H), 3,84-4,21 (м, 5H), 3,09 (м, 4H), 2,30 (с, 3H); ЖХ/МС m/z (M+H+) 549,2 (рассчитано для C26H24ClF3N4O2S: 549,02)
1Н ЯМР (300 МГц, CD3OD): δ 7,59 (м, 1H), 7,40-7,57 (м, 7H), 7,23-7,39 (м, 3H), 4,65 (м, 1H), 4,37-4,58 (м, 2H), 4,32 (м, 1H), 3,67-4,05 (м, 5H), 3,11 (м, 4H), 2,30 (с, 3H); ЖХ/МС m/z (M+H+) 492,1 (рассчитано для C28H27ClFN3O2: 492,00)
1Н ЯМР (300 МГц, CD3OD): δ 7,70-7,80 (м, 3H), 7,42-7,68 (м, 7H), 7,35 (д, 1H), 4,63 (м, 1H), 4,34-4,55 (м, 2H), 4,28 (м, 1H), 3,67-3,98 (м, 5H), 3,02 (м, 4H), 2,30 (с, 3H); ЖХ/МС m/z (M+H+) 542,1 (рассчитано для C29H27ClF3N3O2: 542,01)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,20 (с, 1H), 7,61 (д, 1H), 7,20-7,50 (м, 5H), 4,67 (м, 1H), 4,55 (м, 1H), 4,43 (м, 1H), 4,31 (м, 1H), 3,90-4,25 (м, 5H), 3,90 (с, 3H), 3,11 (м, 4H); ЖХ/МС m/z (M+H+) 515,1 (рассчитано для C25H24ClFN4O3S: 515,01)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,17 (с, 1H), 7,88 (с, 1H), 7,74 (дд, 1H), 7,66 (д, 1H), 7,45 (д, 1H), 7,38 (м, 1H), 7,33 (дд, 1H), 4,65 (м, 1H), 4,33-4,56 (м, 2H), 4,26 (м, 1H), 3,89-4,12 (м, 5H), 3,89 (с, 3H), 2,97 (м, 4H); ЖХ/МС m/z (M+H+) 565,0 (рассчитано для C26H24ClF3N4O3S: 565,02)
1Н ЯМР (300 МГц, CD3OD): δ 7,61 (дд, 1H), 7,38-7,57 (м, 7H), 7,35 (д, 1H), 7,23-7,33 (м, 2H), 4,65 (м, 1H) 4,36-4,57 (м, 2H), 4,30 (м, 1H), 3,88 (с, 3H), 3,67-3,97 (м, 5H), 3,05 (м, 4H); ЖХ/МС m/z (M+H+) 508,0 (рассчитано для C28H27ClFN3O3: 508,00)
1Н ЯМР (300 МГц, CD3OD): δ 7,88 (д, 1H), 7,74 (дд, 1H), 7,66 (д, 1H), 7,42-7,57 (м, 6H), 7,38 (м, 1H), 7,32 (дд, 1H), 4,58-4,69 (м, 1H), 4,36-4,58 (м, 2H), 4,20-4,33 (м, 1H), 3,89 (с, 3H), 3,60-4,04 (м, 5H), 3,03 (м, 4H); ЖХ/МС m/z (M+H+) 558,2 (рассчитано для C29H27ClF3N3O3: 558,01)
1Н ЯМР (300 МГц, CD3OD): δ 9,05 (с, 1H), 8,18 (с, 1H), 7,77-7,83 (м, 2H), 7,68 (дд, 1H), 7,58-7,67 (м, 1H), 7,53 (д, 1H), 7,36 (т, 1H), 4,42 (дд, 1H), 4,22-4,35 (м, 2H), 4,18 (дд, 1H), 3,80-4,13 (м, 5H), 2,90-3,11 (м, 4H); ЖХ/МС m/z (M+H+) 519,0 (рассчитано для C24H21Cl2FN4O2S: 519,43)
1Н ЯМР (300 МГц, CD3OD): δ 9,05 (с, 1H), 8,18 (с, 1H), 8,01 (м, 1H), 7,81-7,98 (м, 2H), 7,74 (д, 2H), 7,56 (д, 1H), 4,36-4,49 (дд, 1H), 4,22-4,35 (м, 2H), 4,19 (дд, 1H), 3,80-4,13 (м, 5H), 2,90-3,11 (м, 4H); ЖХ/МС m/z (M+H+) 569,0 (рассчитано для C25H21Cl2F3N4O2S: 569,44)
1Н ЯМР (300 МГц, CD3OD): δ 7,77-7,84 (м, 2H), 7,58-7,71 (м, 2H), 7,42-7,57 (м, 6H), 7,36 (т, 1H), 4,42 (дд, 1H) 4,13-4,34 (м, 3H), 3,62-4,01 (м, 5H), 2,98 (м, 4H); ЖХ/МС m/z (M+H+) 512,1 (рассчитано для C27H24Cl2FN3O2: 512,42)
1Н ЯМР (300 МГц, CD3OD): δ 8,01 (д, 1H), 7,90 (дд, 1H), 7,85 (д, 1H), 7,74 (д, 2H), 7,56 (д, 1H), 7,41-7,53 (м, 5H), 4,43 (дд, 1H), 4,14-4,35 (м, 3H), 3,63-4,04 (м, 5H), 2,99 (м, 4H); ЖХ/МС m/z (M+H+) 562,0 (рассчитано для C28H24Cl2F3N3O2: 562,42)
1Н ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,22 (с, 1H), 7,30-7,71 (м, 8H), 3,92-4,57 (м, 9H) 3,11-3,29 (м, 4H), 2,46 (с, 3H); ЖХ/МС m/z (M+H+) 447,1 (рассчитано для C25H26N4O2S: 446,58)
МС m/z (M+H+) 518,9
МС m/z (M+H+) 434,9
Пример 7

A. 2,2,2-Трифтор-1-[4-(тиазол-2-карбонил)-пиперазин-1-ил]-этанон, 7a. К раствору соединения 1d (5 г, 0,027 моль) в DMF (50 мл) и DIPEA (19,5 мл, 0,11 моль) было добавлено соединение 5c (3,3 г, 0,0255 моль) и HATU (12,6 г, 0,033 моль). Реакция протекала при перемешивании в течение 4 часов, затем реакционную смесь вылили в воду и экстрагировали с помощью EtOAc. Органическую часть промыли водой и солевым раствором и высушили над MgSO4. Растворитель выпарили в вакууме. Остаток пропустили через силикагелевую колонку (30-10%: EtOAc/гептан) с получением соединения 7a (3,8 г). МС m/z (M+H+) 294,1.
B. Пиперазин-1-ил-тиазол-2-ил-метанон, 7b. Раствор соединения 7a (3,8 г, 0,013 моль) и K2CO3 (3,5 г, 0,026 моль) в MeOH (40 мл) и воде (10 мл) перемешивали в течение 4 часов. Твердый осадок отделили путем фильтрации, растворитель выпарили под действием вакуума и получили соединение 7b (6,12 г). МС m/z (M+H+) 198,1.
C. трет-Бутиловый эфир 3-[4-(тиазол-2-карбонил)-пиперазин-1-ил]-азетидин-1-карбоновой кислоты, 7c. Раствор соединения 7b (6,1 г, 0,031 моль) и соединения 4a (5,1 г, 0,03 моль) в MeOH (30 мл) перемешивали в течение 15 минут. Затем к раствору добавили декаборан (1 г, 0,008 моль). Реакция протекала при перемешивании в течение 18 часов. Растворитель выпарили в вакууме. Остаток использовали в следующей стадии без дополнительной очистки. МС m/z (M+H+) 353,1.
D. (4-Азетидин-3-ил-пиперазин-1-ил)-тиазол-2-ил-метанон, 5e. К раствору соединения 7c в CH2Cl2 (100 мл) была добавлена TFA (30 мл). Реакция протекала при перемешивании в течение 3,5 часов, после чего растворитель выпаривали в вакууме. Остаток очистили препаративной ВЭЖХ на обращенной фазе и получили соединение 5e (5,15 г). МС m/z (M+H+) 253,1.
E. 1-{1-[3-(4-Хлорфенил)пропаноил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 269. К раствору соединения 5e (150 мг, 0,52 ммоль) в DMF (5 мл) и DIPEA (0,40 мл, 2,2 ммоль) прибавляли соединение 7d (125 мг, 0,067 ммоль) и HATU (0,25 г, 0,067 ммоль). Реакция протекала при перемешивании в течение 4 часов, затем реакционную смесь вылили в воду и экстрагировали с использованием EtOAc. Объединенные экстракты концентрировали под действием вакуума. Полученный остаток очистили ВЭЖХ на обращенной фазе и получили соединение 269 (20,2 мг). ЖХ/МС m/z (M+H+) 419,15 (рассчитано для C20H23ClN4O2S: 418,95).
Следуя процедуре, описанной выше для примера 7, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
ЖХ/МС m/z (M+2H+) 465,05 (рассчитано для C20H23BrN4O2S, 463,40)
ЖХ/МС m/z (M+H+) 453,15 (рассчитано для C21H23F3N4O2S: 452,50)
ЖХ/МС m/z (M+H+) 419,17 (рассчитано для C20H23ClN4O2S: 418,95)
1Н ЯМР (300 МГц, MeOD): δ 8,0 (д, 1H), 7,9 (д, 2H), 4,7 (уш.м, 2H), 4,4 (м, 2H), 4,3-4,1 (м, 2H), 4,0 (уш.м, 2H), 3,25 (м, 5H), 3,0 (м, 2H), 2,5 (м, 2H)
ЖХ/МС m/z (M+H+) 419,16 (рассчитано для C20H23ClN4O2S: 418,95)
1Н ЯМР (300 МГц, MeOD): δ 8 (д, 1H), 7,9 (д, 1H), 7,4 (ар, 2H), 7,2 (м, 1H), 4,75 (м, 2H), 4,5-4,1 (м, 5H), 4,0 (м, 3H), 3,2 (м, 5H), 2,4 (м, 3H)
ЖХ/МС m/z (M+2H+) 455,10 (рассчитано для C20H22Cl2N4O2S: 453,39)
ЖХ/МС m/z (M+H+) 421,19 (рассчитано для C20H22F2N4O2S: 420,48)
ЖХ/МС m/z (M+H+) 399,23 (рассчитано для C21H26N4O2S: 398,53)
ЖХ/МС m/z (M+H+) 415,23 (рассчитано для C21H26N4O3S: 414,53)
ЖХ/МС m/z (M+H+) 521,14 (рассчитано для C22H22F6N4O2S: 520,50)
ЖХ/МС m/z (M+H+) 435,22 (рассчитано для C24H26N4O2S: 434,56)
ЖХ/МС m/z (M+H+) 477,20 (рассчитано для C26H28N4O3S: 476,60)
1H ЯМР (300 МГц, MeOD) δ 8,0 (ар, 1H), 7,9 (ар, 1H), 7,4 (м, 2H), 7,2 (м, 1H), 4,4 (дд, 1H), 4,3-4,2 (м, 2H), 4,1 (м, 1H), 3,9 (м, 1H), 3,3 (м, 3H), 3,2 (м, 4H), 3,0 (уш.с, 1H), 2,9 (м, 2H), 2,5 (м, 2H)
ЖХ/МС m/z (M+2H+) 455,10 (рассчитано для C20H22Cl2N4O2S: 453,39)
1Н ЯМР (300 МГц, MeOD): δ 7,9 (ар, 1H), 7,7 (ар, 1H), 7,13 (ар, 1H), 7,0 (ар, 1H), 6,9 (ар, 1H), 4,2-4,1 (м, 2H), 4,1-4,0 (м, 1H), 3,9, (уш.с, 1H), 3,8 (м, 1H), 3,2 (м, 2H), 3,11 (м, 4H), 2,7 (т, 2H), 2,3 (т, 2H), 1,5 (с, 4H), 1,1 (дд, 12H),
ЖХ/МС m/z (M+H+) 495,24 (рассчитано для C28H38N4O2S: 494,70)
ЖХ/МС m/z (M+H+) 483,18 (рассчитано для C21H21F3N4O2S2: 482,55)
ЖХ/МС m/z (M+H+) 421,12 (рассчитано для C19H21ClN4O3S: 420,92)
ЖХ/МС m/z (M+H+) 421,12 (рассчитано для C19H21ClN4O3S: 420,92)
ЖХ/МС m/z (M+2H+) 465,07 (рассчитано для C20H23BrN4O2S: 463,40)
ЖХ/МС m/z (M+H+) 479,29 (рассчитано для C25H30N6O2S: 478,62)
ЖХ/МС m/z (M+2H+) 457,13 (рассчитано для C19H20Cl2N4O3S: 455,37)
ЖХ/МС m/z (M+H+) 471,16 (рассчитано для C20H21F3N4O4S: 470,47)
1H ЯМР (300 МГц, MeOD) δ 8,0 (д, 1H), 7,9 (д, 1H), 7,4 (м, 4H), 4,7 (уш.с, 2H), 4,4-4,1 (м, 3H), 4,1-3,9 (м, 3H), 3,8 (м, 1H), 3,1 (м, 3H), 3,0 (т, 2H), 2,5 (т, 2H), 2,1 м, 1H), 0,5 (м, 4H)
ЖХ/МС m/z (M+H+) 504,20 (рассчитано для C23H29N5O4S2: 503,65)
1Н ЯМР (300 МГц, MeOD): δ 8,0 (д, 1H), 7,9 (д, 1H), 7,5 (м, 4H), 4,4 (уш.м, 2H), 4,25-4,0 (м, 4H), 3,8 (м, 1H), 3,4 (д, 2H), 3,2 (с, м, 3H), 3,1 (уш.с, 3H), 3,0 (т, 2H), 2,5 (т, 2H), 1,7 (м, 5H), 1,1 (м, 5H)
ЖХ/МС m/z (M+H+) 510,32 (рассчитано для C28H39N5O2S: 509,72)
ЖХ/МС m/z (M+H+) 471,18 (рассчитано для C20H21F3N4O2S2: 470,54)
ЖХ/МС m/z (M+H+) 413,20 (рассчитано для C20H20N4O2S2: 412,54)
ЖХ/МС m/z (M+H+) 429,27 (рассчитано для C22H28N4O3S: 428,56)
ЖХ/МС m/z (M+H+) 417,0 (рассчитано для C20H21ClN4O2S: 416,93)
ЖХ/МС m/z (M+H+) 462,9 (рассчитано для C20H21BrN4O2S: 461,38)
ЖХ/МС m/z (M+H+) 433,29 (рассчитано для C24H24N4O2S: 432,55)
Пример 8

A. Бензиловый эфир 4-(1-бензгидрил-азетидин-3-ил)-пиперазин-1-карбоновой кислоты, 8b. К раствору соединения 8a (1,4 г, 6,3 ммоль) и соединения 1e (2 г, 6,3 ммоль) в CH3CN (30 мл) добавили DIPEA (1,5 мл, 8,1 ммоль) при комнатной температуре. Смесь нагревали в колбе с обратным холодильником в течение 18 часов. Растворитель удалили при пониженном давлении. Остаток разделили на водную фазу и фазу, растворимую в CHCl3. Органический слой высушили над K2CO3, профильтровали и сконцентрировали для получения неочищенного соединения 8b (2,65 г). МС m/z (M+H+) 442.
B. Бензиловый эфир 4-азетидин-3-ил-пиперазин-1-карбоновой кислоты, 8c. К раствору соединения 8b (3,4 г, 7,7 ммоль) в CH2Cl2 добавили 1-хлорэтилхлорформиат (2,5 мл, 23,1 ммоль) при температуре 0°C в атмосфере N2. Реакционную смесь извлекли из сосуда со льдом и перемешивали в течение 2 часов. Органическую фазу сконцентрировали при пониженном давлении и к полученному остатку добавили MeOH. Реакционную смесь нагревали в колбе с обратным холодильником в течение 2 часов и удалили растворитель при пониженном давлении. Остаток разделили на фазу, растворимую в хлороформе, и фазу, растворимую в водной HCl (1 Н). Водный слой отделили, привели к основности с помощью водного NaOH (3 Н) и экстрагировали с помощью хлороформа. Затем органический слой высушили (K2CO3), профильтровали и сконцентрировали для получения соединения 8c (2,65 г). МС m/z (M+H+) 276.
C. Бензиловый эфир 4-[1-(дифенил-4-карбонил)-азетидин-3-ил]-пиперазин-1-карбоновой кислоты, 8e. К раствору соединения 8c (2,6 г, 9,4 ммоль), соединения 8d (1,87 г, 9,4 ммоль) и DIPEA (2,43 г, 18,9 ммоль) в ацетонитриле добавили HBTU (4,6 г, 12,3 ммоль). Реакционную смесь перемешивали в течение 18 часов, и за это время растворитель удалили при пониженном давлении, а полученное соединение очистили путем обращенно-фазовой ВЭЖХ. Путем лиофилизации получили соединение 8e (1,74 г). МС m/z (M+H+) 456,2.
D. бифенил-4-ил-(3-пиперазин-1-ил-азетидин-1-ил)-метанон, 8f. Смесь соединения 8e (1,7 г, 2,9 ммоль) и 10% палладия на углероде (300 мг) гидрогенизировали (0,34 МПа (50 фунт/кв. дюйм), газ водород) в аппарате Парра в течение 18 часов. Катализатор удалили путем фильтрования, растворитель концентрировали при пониженном давлении для получения неочищенного соединения 8f (1,5 г). МС m/z (M+H+) 322.
E. 1-[1-(Дифенил-4-ил-карбонил)азетидин-3-ил]-4-[(4-фторфенил)-карбонил]пиперазин, соединение 299. К раствору соединения 8f (100 мг, 0,3 ммоль), соединения 8g (44 мг, 0,31 ммоль) и DIPEA (80 мг, 0,6 ммоль) в диметилформамиде добавили HBTU (141 мг, 0,37 ммоль). После перемешивания в течение 18 часов реакционную смесь очистили препаративной обращенно-фазовой ВЭЖХ для получения соединения 299. 1Н ЯМР (400 МГц, MeOD): δ 7,93-8,03 (м, 1H), 7,61-7,71 (м, 4H), 7,54-7,61 (м, 2H), 7,43-7,50 (м, 2H), 7,35-7,43 (м, 2H), 7,27-7,35 (м, 1H), 7,07-7,20 (м, 2H), 4,55-4,67 (м, 1H), 4,43-4,53 (м, 1H), 4,32-4,43 (м, 1H), 4,19-4,32 (м, 1H), 3,89-4,00 (м, 1H), 3,66-3,89 (м, 4H), 3,08 (уш.с, 4H); МС m/z (M+H+) 444,2 (рассчитано для C27H26FN3O2: 443,53).
Следуя процедуре, описанной выше для примера 8, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 444,2 (рассчитано для C27H26FN3O2: 443,53)
МС m/z (M+H+) 432,1 (рассчитано для C25H25N3O2S: 431,56)
МС m/z (M+2H+) 416,2 (рассчитано для C25H26N4O2: 414,51)
МС m/z (M+H+) 390,23 (рассчитано для C24H27N3O2: 389,5)
МС m/z (M+H+) 444,2 (рассчитано для C27H26FN3O2: 443,53)
МС m/z (M+H+) 417,2 (рассчитано для C24H24N4O3: 416,48)
МС m/z (M+H+) 434,1 (рассчитано для C23H23N5O2S: 433,54)
МС m/z (M+H+) 417,2 (рассчитано для C24H24N4O3: 416,48)
МС m/z (M+H+) 418,2 (рассчитано для C23H23N5O3: 417,47)
МС m/z (M+H+) 457,2 (рассчитано для C26H24N4O2S: 456,57)
1Н ЯМР (400 МГц, MeOD): δ 8,44 (с, 1H), 7,65 (с, 4H), 7,53-7,58 (м, 2H), 7,47 (д, J=1,71 Гц, 1H), 7,34-7,40 (м, 2H), 7,26-7,32 (м, 1H), 4,49-4,60 (м, 1H), 4,37-4,49 (м, 1H), 4,27-4,37 (м, 1H), 4,15-4,27 (м, 1H), 3,72-3,88 (м, 5H), 2,92-3,02 (м, 4H);
МС m/z (M+H+) 433,2 (рассчитано для C24H24N4O2S: 432,55)
1Н ЯМР (400 МГц, MeOD): δ 7,66 (с, 4H), 7,56-7,59 (м, 1H), 7,54-7,56 (м, 1H), 7,35-7,41 (м, 2H), 7,26-7,33 (м, 1H), 7,08-7,15 (м, 1H), 6,64-6,75 (м, 1H), 6,24-6,31 (м, 1H), 4,54-4,64 (м, 1H), 4,43-4,51 (м, 1H), 4,32-4,41 (м, 1H), 4,20-4,28 (м, 1H), 3,85-3,97 (м, 5H), 3,06 (уш.с, 4H);
МС m/z (M+H+) 415,2 (рассчитано для C25H26N4O2: 414,51)
1Н ЯМР (400 МГц, MeOD): δ 7,66 (с, 4H), 7,54-7,59 (м, 2H), 7,38 (д, J=7,58 Гц, 2H), 7,26-7,33 (м, 1H), 7,05 (д, J=3,67 Гц, 1H), 6,42 (д, J=3,42 Гц, 1H), 4,50-4,63 (м, 1H), 4,40-4,48 (м, 1H), 4,28-4,39 (м, 1H), 4,17-4,28 (м, 1H), 3,87-3,97 (м, 4H), 3,78-3,87 (м, 1H), 2,97-3,07 (м, 4H);
МС m/z (M+H+) 450,1 (рассчитано для C25H24ClN3O3: 449,94)
МС m/z (M+H+) 490,2
МС m/z (M+H+) 428,0
МС m/z (M+H+) 418,2
МС m/z (M+H+) 431,3
МС m/z (M+H+) 485,0
МС m/z (M+H+) 417,1
МС m/z (M+H+) 417,0
МС m/z (M+H+) 417,0
МС m/z (M+H+) 426,0
МС m/z (M+H+) 416,2
МС m/z (M+H+) 416,2
МС m/z (M+H+) 404,2
МС m/z (M+H+) 465,3
МС m/z (M+H+) 481,0
МС m/z (M+H+) 483,1
МС m/z (M+H+) 499,4
МС m/z (M+H+) 485,0
МС m/z (M+H+) 560,0/562,0
МС m/z (M+H+) 576,0/578,0
МС m/z (M+H+) 518,2
МС m/z (M+H+) 485,1
МС m/z (M+H+) 519,2
МС m/z (M+H+) 485,2
МС m/z (M+H+) 535,2
МС m/z (M+H+) 485,1
МС m/z (M+H+) 494,2
МС m/z (M+H+) 458,3
МС m/z (M+H+) 516,3
МС m/z (M+H+) 523,2
МС m/z (M+H+) 501,2
МС m/z (M+H+) 507,1
МС m/z (M+H+) 474,1
МС m/z (M+H+) 488,1
МС m/z (M+H+) 507,1
МС m/z (M+H+) 474,1
МС m/z (M+H+) 474,1
Пример 9

A. трет-Бутиловый эфир 4-(тиазол-2-карбонил)-пиперазин-1-карбоновой кислоты, 9a. К раствору соединения 5c (2,0 г, 15,50 ммоль), соединения 1a (3,2 г, 17,20 ммоль) и Et3N (8,6 мл, 61,2 ммоль) в CH2Cl2 (100 мл) добавили HATU (6,5 г, 17,1 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Затем смесь разбавили CH2Cl2 и промыли водным раствором NaHCO3. Органическую фазу высушили над Na2SO4, профильтровали и сконцентрировали. Путем очистки колоночной флэш-хроматографией (силикагель, 30% EtOAc/гептан) получили соединение 9a (4,0 г).
B. Соль пиперазин-1-ил-тиазол-2-ил-метанон трифторуксусной кислоты, 9b. К раствору соединения 9a (3,5 г, 11,78 ммоль) в CH2Cl2 (40 мл) добавили TFA (10 мл). Реакционную смесь перемешивали 2 часа при комнатной температуре. Затем смесь сконцентрировали для получения соединения 9b, которое использовали для следующей реакции без дополнительной очистки.
C. трет-Бутиловый эфир 3-[4-(тиазол-2-карбонил)-пиперазин-1-ил]-азетидин-1-карбоновой кислоты, 7c. К раствору соединения 9b (11,78 ммоль) и соединения 4a (2,2 г, 12,87 ммоль) в 1,2-DCE (35 мл) и уксусной кислоты (2 мл) добавили Na(OAc)3BH (2,75 г, 12,97 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 5 часов. К реакционной смеси добавили водный раствор NaHCO3. Полученную смесь экстрагировали с помощью CH2Cl2. Органический слой высушили над Na2SO4 и сконцентрировали. Путем очистки с использованием колоночной флэш-хроматографии (силикагель, 80% EtOAc/гептан) получили соединение 7c (3,78 г).
D. (4-Азетидин-3-ил-пиперазин-1-ил)-тиазол-2-ил-метанон, 5e. К раствору соединения 7c (1,2 г, 3,41 ммоль) в CH2Cl2 (12 мл) добавили TFA (3 мл). Реакционную смесь перемешивали при комнатной температуре в течение 4,5 часов, затем смесь сконцентрировали, а к полученному остатку добавили водный раствор NaHCO3. Смесь экстрагировали с помощью 2% MeOH/CH2Cl2 (3x). Органический раствор высушили над Na2SO4 и сконцентрировали для получения соединения 5e, которое использовали в следующей реакции без дополнительной очистки.
D. 1-{1-[(5-Бромнафталин-2-ил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 313. К раствору соединения 5e (63 мг, 0,25 ммоль), соединения 9c (95 мг, 0,38 ммоль) и Et3N (0,14 мл, 1,01 ммоль) в CH2Cl2 (3 мл) добавили HATU (143 мг, 0,38 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов, затем разбавили диэтиловым эфиром и промыли водным раствором NaHCO3 и водным раствором NaCl. Органический слой высушили над Na2SO4 и сконцентрировали. Путем очистки с использованием колоночной флэш-хроматографии (силикагель, 3% MeOH/CH2Cl2) получили соединение 313. 1Н ЯМР (400 МГц, CD3OD): δ 8,28 (д, J=9 Гц, 1H), 8,14 (д, J=1,6 Гц, 1H), 7,88-7,85 (м, 3H), 7,81 (д, J=8,4 Гц, 1H), 7,54 (д, J=3 Гц, 1H), 7,39 (т, J=7,8 Гц, 1H), 4,53 (уш.с, 1H), 4,45 (уш.с, 1H), 4,34 (м, 2H), 4,26 (м, 1H), 4,16 (м, 1H), 3,95-3,80 (м, 2H), 3,28 (м, 1H), 2,60-2,40 (м, 4H). МС m/z (M+H+) 485/487.
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CD3OD): δ 8,40 (д, J=7,8 Гц, 1H), 7,95 (с, 1H), 7,88 (д, J=3 Гц, 1H), 7,83-7,80 (м, 2H), 7,69 (д, J=8 Гц, 1H), 7,55 (д, J=3 Гц, 1H), 4,53 (м, 1H), 4,45-4,25 (м, 4H), 4,16 (м, 1H), 3,95-3,80 (м, 2H), 3,27 (м, 1H), 2,60-2,40 (м, 4H).
МС m/z (M+H+) 542
МС m/z (M+H+) 475/477
1Н ЯМР (400 МГц, CD3OD): δ 8,13 (с, 1H), 7,98 (д, J=8,6 Гц, 1H), 7,89 (д, J=3 Гц, 1H), 7,75 (с, 1H), 7,65 (д, J=8,6 Гц, 1H), 7,56 (д, J=3 Гц, 1H), 4,62-4,40 (м, 4H), 4,31 (м, 1H), 4,16 (м, 1H), 3,35 (м, 1H), 2,60-2,40 (м, 4H).
МС m/z (M+H+) 481
1Н ЯМР (400 МГц, CD3OD): δ 8,26 (м, 2H), 8,00 (с, 1H), 7,88 (д, J=3 Гц, 1H), 7,76 (д, J=8,6 Гц, 1H), 7,63 (д, J=8,6 Гц, 1H), 7,60-7,52 (м, 4H), 4,60-4,40 (м, 2H), 4,38 (м, 1H), 4,28 (м, 2H), 4,15 (м, 1H), 3,86 (м, 2H), 3,27 (м, 1H), 2,50 (м, 4H).
МС m/z (M+H+) 474
1Н ЯМР (400 МГц, CD3OD): δ 8,28 (м, 2H), 7,92 (с, 1H), 7,88 (д, J=3,2 Гц, 1H), 7,79 (д, J=8 Гц, 1H), 7,66 (д, J=8 Гц, 1H), 4,60-4,20 (м, 5H), 4,15 (м, 1H), 3,86 (м, 2H), 3,28 (м, 1H), 2,50 (м, 4H).
МС m/z (M+H+) 474
1 Н ЯМР (CDCl3): δ 7,44-7,39 (м, 7H), 7,13 (д, J=0,02, 1H), 4,59 (с, 2H), 4,27 (м, 2H), 4,15 (м, 1H), 4,06 (м, 1H), 3,90 (м, 1H), 3,74 (м, 1H), 3,65 (м, 2H), 3,46 (м, 2H), 3,22 (м, 1H), 2,85 (м, 2H), 2,27-2,23 (м, 4H), 1,49 (с, 9H)
МС m/z 405,0 (M-Boc), 449,0 (M-Bu-t), 527 (M+Na), 1009,2 (2M+H)
МС m/z (M+H+) 511,8, 513,8, 514,8
1Н ЯМР (CDCl3): δ 7,42-7,38 (м, 5H), 7,33-7,29 (м, 3H), 7,26 (м, 3H), 6,78 (д, J=0,01, 1H), 4,41 (м, 1H), 4,24 (м, 2H), 4,13 (с, 2H), 4,03 (м, 1H), 3,92-3,74 (м, 2H), 3,47 (м, 2H), 3,24 (м, 1H), 2,42-2,29 (м, 4H)
МС m/z (M+H+) 446,6
МС m/z (M+H+) 432,4, 434,4
МС m/z (M+H+) 493,0
МС m/z (M+H+) 615,0
МС m/z (M+H+) 465,1
МС m/z (M+H+) 491,1
МС m/z (M+H+) 499,2
МС m/z (M+H+) 479,1
МС m/z (M+H+) 460,0
МС m/z (M+H+) 497,1
МС m/z (M+H+) 450,1
МС m/z (M+H+) 462,3
МС m/z (M+H+) 462,3
МС m/z (M+H+) 486,1
МС m/z (M+H+) 412,1
1Н ЯМР (400 МГц, CD3OD): δ 7,99 (д, 1H), 7,89 (д, 1H), 7,57 (с, 1H), 7,52 (д, J=8,1 Гц, 1H), 7,03 (д, J=8,1 Гц, 1H), 4,28-4,90 (м, 6H), 4,01-4,22 (м, 3H), 3,73 (т, J=8,2 Гц, 2H), 3,37 (уш.с, 4H), 3,19 (т, J=8,2 Гц, 2H)
МС m/z (M+H+) 398,1
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,2 Гц, 1H), 7,50-7,57 (м, 2H), 7,42-7,48 (м, 2H), 7,38 (д, J=3,2 Гц, 1H), 7,33 (д, J=7,3 Гц, 1H), 7,18-7,26 (м, 3H), 6,99 (д, J=3,2 Гц, 1H), 4,05-4,63 (м, 6H), 3,75-3,99 (м, 2H), 3,22-3,32 (м, 1H), 2,37-2,62 (м, 4H)
МС m/z (M+H+) 490,1
МС m/z (M+) 440,0, (M+2+) 442,0
MC m/z 482 (M+H+)
1Н ЯМР (CDCl3,400 МГц): δ 7,98 (с, 1H), 7,88 (д, J=3,1 Гц, 1H), 7,47-7,58 (м, 2H), 7,38-7,47 (м, 3H), 7,16-7,26 (м, 2H), 7,12 (с, 1H), 4,47-4,64 (м, 1H), 4,38 (уш.с, 4H), 4,07-4,19 (м, 1H), 3,74-3,97 (м, 2H), 3,17-3,33 (м, 1H), 2,50 (т, J=4,9 Гц, 4H), 2,39 (с, 3H).
MC m/z 504 (M+H+)
MC m/z 508 (M+H+)
MC m/z 486 (M+H+)
MC m/z 486 (M+H+)
MC m/z 526 (M+H+)
1Н ЯМР (CDCl3,400 МГц): δ 8,27 (с, 1H), 8,12 (с, 1H), 7,88 (уш.с, 1H), 7,67-7,85 (м, 2H), 7,42-7,67 (м, 3H), 7,36 (кв., J=8,7 Гц, 1H), 4,49-4,62 (м, 1H), 4,20-4,48 (м, 4H), 4,05-4,20 (м, 1H), 3,84 (уш.с, 2H), 3,20-3,38 (м, 1H), 2,51 (м, 4H).
MC m/z 509 (M+H+)
MC m/z 509 (M+H+)
MC m/z 526 (M+H+)
MC m/z 510 (M+H+)
MC m/z 510 (M+H+)
MC m/z 504 (M+H+)
MC m/z 556 (M+H+)
MC m/z 556 (M+H+)
MC m/z 508 (M+H+)
MC m/z 570 (M+H+)
MC m/z 491 (M+H+)
MC m/z 523 (M+H+)
MC m/z 508 (M+H+)
MC m/z 491 (M+H+)
МС m/z (M+H+) 455, 457
МС m/z (M+H+) 468, 470
МС m/z (M+H+) 488, 490
МС m/z (M+H+) 455, 457
МС m/z (M+H+) 475, 477
МС m/z (M+H+) 490
МС m/z (M+H+) 490
МС m/z (M+H+) 490
МС m/z (M+H+) 490
МС m/z (M+H+) 474,1
МС m/z (M+H+) 452,4
МС m/z (M+H+) 459,3
МС m/z (M+H+) 272
1Н ЯМР (400 МГц, CDCl3): δ 3,34-3,48 (м, 1H), 3,89 (уш.с, 3H), 4,08-4,66 (м, 8H), 7,55 (д, J=8,8 Гц, 1H), 7,62 (д, J=3,2 Гц, 1H), 7,66 (дд, J=8,8, 1,5 Гц, 1H), 7,89 (д, J=3,2 Гц, 1H), 8,04 (с, 1H), 8,09 (с, 2H)
МС m/z (M+H+) 397,2
1Н ЯМР (400 МГц, CDCl3): δ 2,92-3,16 (м, 4H), 3,76 (т, J=5,3 Гц, 1H), 4,06 (уш.с, 2H), 4,39 (уш.с, 1H), 4,49-4,93 (м, 5H), 7,23 (д, J=3,2 Гц, 1H), 7,30-7,38 (м, 2H), 7,44-7,54 (м, 2H), 7,60 (д, J=3,2 Гц, 1H), 7,89 (д, J=3,2 Гц, 1H), 7,97 (д, J=3,2 Гц, 1H), 8,63 (с, 1H), 9,12 (с, 1H)
МС m/z (M+H+) 491,2
1Н ЯМР (400 МГц, CDCl3): δ 3,75 (с, 1H), 4,11 (уш.с, 2H), 4,32-5,02 (м, 10H), 6,75 (д, J=3,6 Гц, 1H), 7,23 (д, J=8,9 Гц, 2H), 7,53 (д, J=3,7 Гц, 1H), 7,61 (д, J=3,2 Гц, 1H), 7,65 (м, J=9,0, 4,7 Гц, 2H), 7,89 (д, J=3,2 Гц, 1H), 8,33 (д, J=2,0 Гц, 1H), 8,60 (д, J=1,7 Гц, 1H)
МС m/z (M+H+) 491,2
1Н ЯМР (400 МГц, CDCl3): δ 3,83-4,34 (м, 9H), 4,41-4,70 (м, 2H), 5,14 (д, J=5,8 Гц, 2H), 6,90 (уш.с, 1H), 7,28 (д, J=8,2 Гц, 2H), 7,38-7,51 (м, 2H), 7,62 (д, J=3,2 Гц, 1H), 7,65 (д, J=2,9 Гц, 1H), 7,85 (д, J=8,6 Гц, 1H), 7,90 (д, J=3,2 Гц, 1H), 7,99 (д, J=8,6 Гц, 1H)
МС m/z (M+H+) 491,2
1Н ЯМР (400 МГц, CD3OD): δ 2,14 (дд, J=22,7, 10,5 Гц, 1H), 2,43 (дд, J=41,6, 11,7 Гц, 1H), 2,87-3,18 (м, 1H), 3,18-3,44 (м, 1,5H), 3,58-3,81 (м, 0,5H), 3,95-4,17 (м, 1H), 4,18-4,40 (м, 2H), 4,49 (м, 1,5H), 5,43 (д, J=26,4 Гц, 1H), 6,95 (уш.с, 0,5H), 7,33-7,43 (м, 1H), 7,43-7,51 (м, 2H), 7,66 (д, J=7,6 Гц, 2H), 7,70-7,80 (м, 4H), 7,88 (уш.с, 1H), 7,93-8,03 (м, 1H)
МС m/z (M+H+) 501,1
МС m/z (M+H+) 378
основной: 1-[3-хлор-5-(трифторметил)пиридин-2-ил]-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол
МС m/z (M+H+) 575,1
второстепенный: 1-[2-фтор-5-(трифторметил)пиридин-3-ил]-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол
МС m/z (M+H+) 559,0
МС m/z (M+H+)) 474,1
Пример 9b

1-{1-[(6-Бромнафталин-2-ил)карбонил]азетидин-3-ил}-4-(фенилкарбонил)пиперазин, соединение 118. Названное соединение было получено способом, описанным в примере 9 применительно к получению соединения 313, с заменой промежуточного соединения 9b в качестве исходного материала на коммерчески доступный N-бензоилпиперазин. МС 478/480 (M+H+).
Следуя процедуре, описанной выше для примера 9b, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 479/481
1Н ЯМР (400 МГц, CD3OD): δ7,74 (д, J=2 Гц, 1H), 7,71 (д, J=8,6 Гц, 1H), 7,43-7,36 (м, 6H), 4,28 (м, 2H), 4,20-4,00 (м, 2H), 4,00-3,70 (м, 2H), 3,48 (м, 2H), 3,24 (м, 1H), 2,58 (с, 3H), 2,50-2,20 (м, 4H).
МС m/z (M+H+) 454
МС m/z (M+H+) 467
МС m/z (M+H+) 421
МС m/z (M+H+) 497
МС m/z (M+H+) 474
МС m/z (M+H+) 484/486
1Н ЯМР (400 МГц, CD3OD): δ 8,00 (с, 1H), 7,81 (д, J=8,2 Гц, 2H), 7,63 (д, J=8,6 Гц, 2H), 7,58 (с, 2H), 7,40 (м, 6H), 6,78 (д, J=3,5 Гц, 1H), 4,37 (м, 1H), 4,30-4,20 (м, 2H), 4,11 (м, 1H), 3,60-3,40 (м, 2H), 3,24 (м, 1H), 2,50-2,20 (м, 4H).
МС m/z (M+H+) 533
МС m/z (M+H+) 500
1Н ЯМР (400 МГц, CD3OD): δ 7,98 (с, 1H), 7,56-7,37 (м, 13H), 6,73 (д, J=3,2 Гц, 1H), 4,37 (м, 1H), 4,29-4,20 (м, 2H), 4,10 (уш.с, 1H), 3,90 (уш.с, 1H), 3,74 (уш.с, 1H), 3,38 (м, 2H), 3,23 (м, 1H), 2,50-2,20 (м, 4H).
МС m/z (M+H+) 465
1Н ЯМР (400 МГц, CD3OD): δ 8,00 (с, 1H), 7,76 (с, 1H), 7,72-7,64 (м, 3H), 7,58-7,50 (м, 2H), 7,41 (м, 6H), 6,78 (д, J=3 Гц, 1H), 4,37 (м, 1H), 4,30-4,20 (м, 2H), 4,11 (м, 1H), 3,91 (уш.с, 1H), 3,75 (уш.с, 1H), 3,48 (м, 2H), 3,25 (м, 1H), 2,55-2,20 (м, 4H).
МС m/z (M+H+) 533
МС m/z (M+H+) 529
1Н ЯМР (400 МГц, CD3OD): δ 8,54 (с, 1H), 8,45 (д, J=8,2 Гц, 1H), 7,94 (д, J=1,2 Гц, 1H), 7,82 (м, 2H), 7,69 (м, 2H), 7,41 (м, 5H), 4,38 (м, 1H), 4,32-4,22 (м, 2H), 4,12 (м, 1H), 3,90 (уш.с, 1H), 3,76 (уш.с, 1H), 3,50 (уш.с, 2H), 3,27 (м, 1H), 2,50-2,20 (м, 4H).
МС m/z (M+H+) 535
МС m/z (M+H+) 467
MC m/z 484 (M+H+)
1Н ЯМР (CDCl3, 400 МГц): δ 7,99 (с, 1H), 7,53-7,63 (м, 1H), 7,45-7,53 (м, 1H), 7,16-7,45 (м, 9H), 6,74 (д, J=3,1 Гц, 1H), 4,37 (уш.с, 1H), 4,16-4,32 (м, 2H), 4,11 (уш.с, 1H), 3,83-4,00 (м, 1H), 3,65-3,83 (м, 1H), 3,48 (уш.с, 2H), 3,17-3,31 (м, 1H), 2,44 (уш.с, 4H)
MC m/z 501 (M+H+)
MC m/z 497 (M+H+)
MC m/z 501 (M+H+)
MC m/z 497 (M+H+)
MC m/z 479 (M+H+)
MC m/z 519 (M+H+)
MC m/z 549 (M+H+)
MC m/z 501 (M+H+)
MC m/z 517 (M+H+)
MC m/z 501 (M+H+)
MC m/z 502 (M+H+)
Пример 9c
Следуя процедуре, описанной выше для примера 1b, за исключением использования 1,10-фенантролина вместо транс-N, N'-диметилциклогексан-1,2-диамина в качестве лиганда на стадии K при замене соответствующих реактивов, исходных материалов и способов очистки, известных специалистам в данной области, получили следующее промежуточное соединение:

Следуя процедуре, описанной выше для примера 9, стадия D, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 511
МС m/z (M+H+) 511
МС m/z (M+H+) 504
Пример 9d

E. Метил 1-(4-цианфенил)-индол-5-карбоксилат (9d) получили в соответствии с описанием в примере 1a, стадия H.
F. 1-(4-Цианфенил)-индол-5-карбоновая кислота (9e) и 1-(4-карбамоил-фенил)-индол-5-карбоновая кислота (9f). Смесь метил 1-(4-цианфенил)-индол-5-карбоксилата, 9d (156 мг, 0,57 ммоль), LiOH (54 мг, 2,26 ммоль) в THF (4 мл) и H2O (2 мл) перемешивали при комнатной температуре в течение 4 дней. Водный 10%-ный раствор HCl добавили в реакционную смесь для доведения уровня pH до 3~4. Полученную смесь экстрагировали с помощью EtOAc (2x). Органический раствор промыли водным раствором NaCl, высушили над Na2SO4 и концентрировали Путем очистки с использованием колоночной флэш-хроматографии (силикагель, 4-8% MeOH/CH2Cl2) получили соединение 9e (75 мг), а затем соединение 9f (27 мг).
Следуя процедуре, описанной выше для примера 9d, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 497
МС m/z (M+H+) 515
МС m/z (M+H+) 497
МС m/z (M+H+) 497
МС m/z (M+H+) 497
МС m/z (M+H+) 497
МС m/z (M+H+) 515
Следуя процедуре, описанной выше для примера 9b, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 490
МС m/z (M+H+) 490
МС m/z (M+H+) 508
Пример 9e

G. Этил 1-(3-трифторметил-фенил)-1H-индазол-5-карбоксилат (9i) и этил-1-(3-трифторметил-фенил)-1H-индазол-5-карбоксилат (9j). Смесь этил 1H-индазол-5-карбоксилата, 9g (150 мг, 0,79 ммоль), 1-бром-3-трифторметилбензола, 9h (0,13 мл, 0,95 ммоль), CuI (22,5 мг, 0,12 ммоль), транс-N,N'-диметилциклогексан-1,2-диамина (0,056 мл, 0,36 ммоль) и K3PO4 (0,37 г, 1,74 ммоль) в толуоле (1,5 мл) нагревали при 110°C в течение 16 часов. Реакционную смесь разбавили CH2Cl2 и профильтровали. Раствор сконцентрировали, остаток очистили с помощью колоночной флэш-хроматографии (силикагель, 10% EtOAc/гептан) для получения соединения 9i (190 мг), а затем соединения 9j (37 мг).
H. 1-(3-Трифторметилфенил)-1H-индазол-5-карбоновая кислота (9k) и 1-(3-трифторметилфенил)-1H-индазол-5-карбоновая кислота (9l). Соединения 9k и 9l получили в соответствии с описанием в примере 1b, стадия L, из соединений 9i и 9j, соответственно.
Следуя процедуре, описанной выше для примера 9e, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 541
МС m/z (M+H+) 557
МС m/z (M+H+) 557
МС m/z (M+H+) 541
МС m/z (M+H+) 541
МС m/z (M+H+) 557
Следуя процедуре, описанной выше для примера 9b, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:
МС m/z (M+H+) 534
МС m/z (M+H+) 550
Пример 9f

I. Метил 1-(4-циан-3-фторфенил)-индол-5-карбоксилат (9m) получили в соответствии с описанием, данным в примере 9e, стадия H.
J. Метил 1-(4-циан-3-метоксифенил)-индол-5-карбоксилат (9n). Раствор 95 мг (0,32 ммоль) соединения 9m объединили с раствором 120 мг (0,87 ммоль) K2CO3 в 8 мл MeOH и нагревали при температуре 75°C в течение 5 часов. Смесь охладили, разбавили водой и экстрагировали с помощью CH2Cl2. Органический раствор сконцентрировали для получения 100 мг (100%) соединения 9n в виде белого твердого вещества.
K. 1-(4-Циан-3-метоксифенил)-индол-5-карбоновая кислота (93) и 1-(4-карбамоил-фенил)-индол-5-карбоновая кислота (9o). Смесь 100 мг (0,33 ммоль) соединения 9m и LiOH (31 мг, 1,3 ммоль) в THF (4 мл) и H2O (2 мл) перемешивали при комнатной температуре в течение 3 дней. Водный 10%-ный раствор HCl добавили в реакционную смесь для доведения уровня pH до 3~4. Полученную смесь экстрагировали с помощью EtOAc (2x). Органический раствор промыли водным раствором NaCl, высушили над Na2SO4 и сконцентрировали для получения 90 мг (94%) соединения 9o в виде белого твердого вещества.
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 527
МС m/z (M+H+) 520
Пример 9g

L. Этил 2-(тиазол-2-ил)бензо[d]тиазол-6-карбоксилат (9q). Смесь этил 2-бромбензотиазол-6-карбоксилата, 1w (150 мг, 0,53 ммоль), 2-трибутилстаннилтиазола, 9p (0,25 мл, 0,79 ммоль), и Pd(PPh3)4 (30 мг, 0,03 ммоль) в диоксане (2 мл) нагревали при температуре 130°C в течение 30 минут в микроволновой печи. Реакционную смесь разбавили CH2Cl2, затем промыли водным раствором NaHCO3, высушили над Na2SO4 и сконцентрировали. Путем очистки колоночной флэш-хроматографией (силикагель, 10% EtOAc/гептан) получили соединение 9q (130 мг).
M. 2-(Тиазол-2-ил)бензо[d]тиазол-6-карбоновая кислота (9r). Этил 2-фенил-бензотиазол-6-карбоксилат, 9q (130 мг, 0,45 ммоль), перемешивали с раствором LiOH (43 мг, 1,8 ммоль) в THF (4 мл) и H2O (2 мл) в течение 6 часов. Для установления pH раствора на уровне 3~4 к смеси добавили 1Н раствора HCl. Полученную смесь экстрагировали с помощью EtOAc (2x). Органический раствор промыли водным раствором NaCl, высушили над Na2SO4 и сконцентрировали для получения соединения 9r (110 мг).
Следуя процедуре, описанной выше для примера 9g, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:
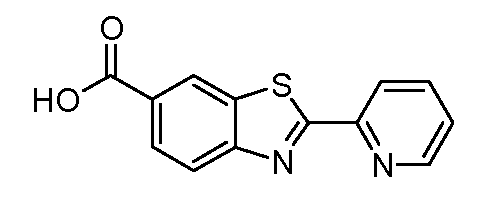
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 497
МС m/z (M+H+) 491
Пример 9h
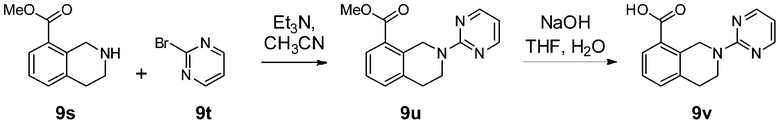
N. Метил 2-(пиримидин-2-ил)-1,2,3,4-тетрагидроизохинолин-8-карбоксилат (9u). Смесь метил-1,2,3,4-тетрагидроизохинолин-8-карбоксилата 9s (100 мг, 0,44 ммоль), 2-бромпиримидина 9t (77 мг, 0,48 ммоль) и Et3N (0,13 мл, 0,92 ммоль) в ацетонитриле (5 мл) перемешивали при комнатной температуре в течение ночи. Реакционную смесь обработали для получения соединения 9v (187 мг).
M. 2-(Пиримидин-2-ил)-1,2,3,4-тетрагидроизохинолин-8-карбоновая кислота (9v). Соединение 9u (187 мг, 0,44 ммоль) нагревали в колбе с обратным холодильником с 3Н водного NaOH (0,25 мл мг, 0,75 ммоль) в THF (6 мл) в течение ночи. К смеси добавили концентрированный раствор HCl для установления pH на уровне 3~4. Полученную смесь сконцентрировали для получения соединения 9v (350 мг) в виде соли трис-HCl.
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 490,1
Пример 9i
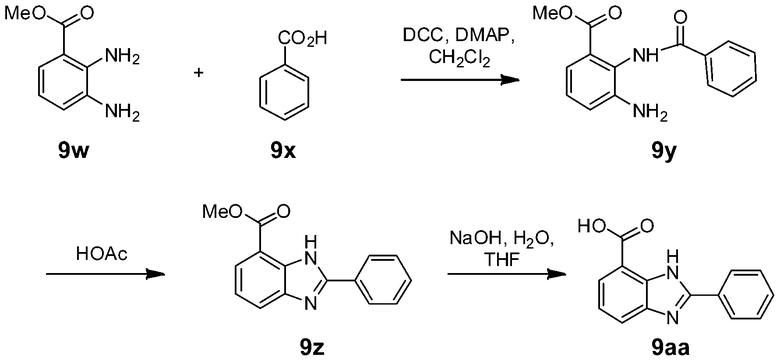
N. Метил 3-амин-2-бензоиламинобензоат (9y). К раствору 500 мг (3,0 ммоль) метил 2,3-диаминобензоата, 9w, и 730 мг (6,0 ммоль) бензойной кислоты, 9x, в 8 мл CH2Cl2 добавили 620 мг (3,0 ммоль) дициклогексилкарбодиимида (DCC) и 4 мг (0,033 ммоль) DMAP. Реакционную смесь перемешивали в течение ночи, затем отфильтровали осадок. Осадок очистили колоночной флэш-хроматографией (силикагель, 10-30% градиент EtOAc в гептане) для получения 220 мг (27%) метил 3-амин-2-бензоиламинобензоата, 9y. МС m/z (M+H+) 271,2
O. Метил 2-фенил-1H-бензо[d]имидазол-7-карбоксилат (9z). Раствор 810 мг (3,0 ммоль) метил 3-амино-2-бензоиламинобензоата, 9y, в 15 мл уксусной кислоты нагревали при температуре 125°C в течение 1,5 часов. Реакционную смесь охладили и вылили в лед/воду. Водный слой довели до щелочной реакции с помощью NaHCO3 и экстрагировали с помощью CH2Cl2. Органическую часть раствора высушили над Na2SO4 и выпарили с получением 540 мг (71%) метил 2-фенил-1H-бензо[d]имидазол-7-карбоксилата, 9z. МС m/z (M+H+) 253,2
P. Фенил-1H-бензо[d]имидазол-7-карбоновая кислота, 9aa. Смесь 540 мг (2,1 ммоль) метил 2-фенил-1H-бензо[d]имидазол-7-карбоксилата, 9z, и 3 мл (9 ммоль) 3Н водного NaOH в 8 мл THF нагревали в колбе с обратным холодильником в течение ночи. После охлаждения смесь вылили в ледяную воду и подкислили концентрированным раствором HCl. Полученный твердый осадок отфильтровали и высушили с получением 440 мг (86%) фенил-1H-бензо[d]имидазол-7-карбоновой кислоты, 9aa. МС m/z (M+H+) 238,9.
Следуя процедуре, описанной выше для примера 9i, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 500,3
МС m/z (M+H+) 484,3
МС m/z (M+H+) 484,3
МС m/z (M+H+) 500,3
МС m/z (M+H+) 466,3
МС m/z (M+H+) 507,2
МС m/z (M+H+) 463,2
МС m/z (M+H+) 473,2
МС m/z (M+H+) 474,3
МС m/z (M+H+) 463,3
МС m/z (M+H+) 463,3
МС m/z (M+H+) 491,2
МС m/z (M+H+) 491,2
МС m/z (M+H+) 491,2
МС m/z (M+H+) 507,2
МС m/z (M+H+) 507,2
МС m/z (M+H+) 487
МС m/z (M+H+) 505,2
МС m/z (M+H+) 505,2
МС m/z (M+H+) 521,2
МС m/z (M+H+) 488,2
Пример 9j

Q. Метил 2-(4-фторбензоиламино)-3-гидроксибензоат, 9dd. Раствор 1,0 г (4,9 ммоль) метил 2-амино-3-гидроксибензоата, 9bb, 1,03 г (7,4 ммоль) 4-фторбензойной кислоты, 9cc, 10 мл DMF и 2,9 мл (20,6 ммоль) TEA поместили в колбу и перемешивали в течение 10 минут. Затем добавили HATU (7,4 ммоль, 2,8 г), после чего реакционную смесь перемешивали в течение ночи. Реакционную смесь вылили в воду и экстрагировали с помощью EtOAc. Органическую фазу промыли водой и солевым раствором, растворитель выпарили для получения 1,2 г неочищенного соединения, метил 2-(4-фторбензоиламино)-3-гидроксибензоата, 9dd, который использовали далее без дополнительной очистки. МС m/z (M+H+) 290,1.
R. Метил 2-(4-фторфенил)бензо[d]оксазол-4-карбоксилат, 9ee. Метил 2-(4-фторбензоиламино)-3-гидроксибензоат, 9dd (7,4 ммоль, 1,2 г неочищенного продукта), и 1,3 г (7,5 ммоль) п-толуолсульфоновой кислоты в 10 мл ксилола нагревали в колбе с обратным холодильником в течение ночи. После охлаждения к смеси добавили насыщенный раствор NaHCO3, полученную смесь экстрагировали с помощью EtOAc. Органический растворитель выпарили для получения 1,1 г (55%) метил 2-(4-фторфенил)бензо[d]оксазол-4-карбоксилата, 9ee. МС m/z (M+H+) 272,0.
S. 2-(4-Фторфенил)-бензо[d]оксазол-4-карбоновая кислота, 9ff. Смесь 1,1 г (4,0 ммоль) метил 2-(4-фторфенил)бензо[d]оксазол-4-карбоксилата, 9ee, и 3,7 мл 3N водного NaOH в 10 мл THF нагревали в колбе с обратным холодильником в течение ночи. После охлаждения реакционную смесь вылили в воду и подкислили концентрированным раствором HCl. Полученный твердый осадок отфильтровали и высушили для получения 830 мг (79%) 2-(4-фторфенил)-бензо[d]оксазол-4-карбоновой кислоты, 9ff. МС m/z (M+H+) 258,1.
Следуя процедуре, описанной выше в примере 9j, заменив соответствующие вещества, исходные материалы и способы очистки, известные специалистам в данной области, получили следующие соединения, являющиеся предметом настоящего изобретения:
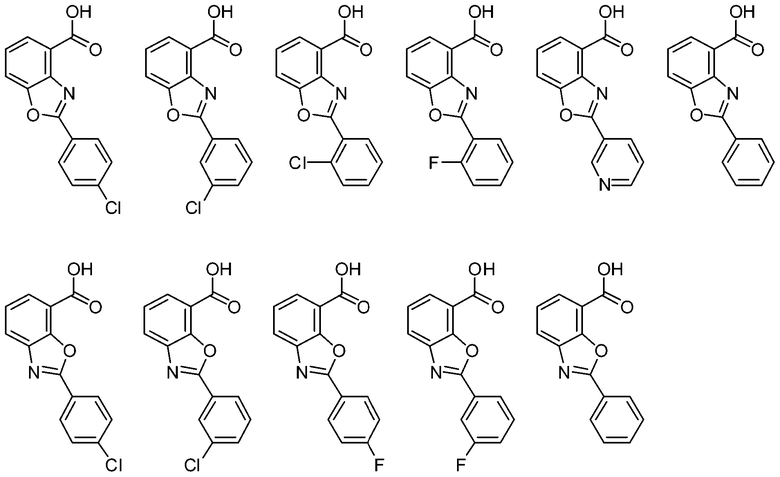
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 8,32 (м, 2H); 7,95 (м, 2H); 7,85 (м, 1H); 7,71-7,49 (м, 5H); 4,85-4,44 (уш.м, 3H); 4,15-3,91 (уш.м, 3H); 3,23 (уш.м, 3H)
МС м/z (M+H+) 474,2
МС м/z (M+H+) 492,1
МС м/z (M+H+) 492,1
МС м/z (M+H+) 507,9
1Н ЯМР (400 МГц, CDCl3): δ 9,05 (уш.с, 1H); 8,3 (д, 2H); 8,2 (м, 1H); 7,95 (д, 1H); 7,66 (т, 3H); 7,44 (т, 1H); 4,69-4,52 (м, 1H); 4,44 (м, 2H); 4,10 (уш.м, 2H); 3,20 (м, 4H).
МС м/z (M+H+) 507,9
МС м/z (M+H+) 474
МС м/z (M+H+) 492,2
МС м/z (M+H+) 492,2
МС м/z (M+H+) 508,2
МС м/z (M+H+) 508,2
МС м/z (M+H+) 508,9
МС м/z (M+H+) 474,2
МС м/z (M+H+) 475,1
Пример 10
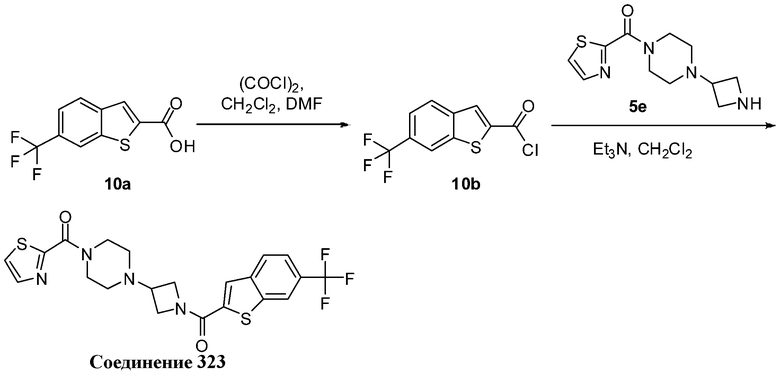
A. 6-Трифторметил-бензо[b]тиофен-2-карбонила хлорид, 10b. К соединению 10a (0,13 г, 0,53 ммоль) в CH2Cl2 (5 мл) при комнатной температуре добавили (COCl)2 (0,051 мл, 0,58 ммоль), а затем 2 капли DMF. Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Затем реакционную смесь сконцентрировали для получения соединения 10b, которое использовалось в следующей реакции без дополнительной очистки.
B. 1-(1,3-Тиазол-2-ил-карбонил)-4-(1-{[6-(трифторметил)-1-бензотиофен-2-ил]карбонил}азетидин-3-ил)пиперазин. К раствору соединения 5e (60 мг, 0,24 ммоль) и Et3N (0,08 мл, 0,58 ммоль) в CH2Cl2 (3 мл) при 0°C добавили раствор соединения 10b (0,53 ммоль) в CH2Cl2 (1 мл). Реакционную смесь медленно нагревали до комнатной температуры в течение 4,5 часов, разбавили CH2Cl2 и промыли водным раствором NaHCO3. Органический слой высушили над Na2SO4 и сконцентрировали. Путем очистки колоночной флэш-хроматографией (силикагель, 3% MeOH/CH2Cl2) получили соединение 323. 1Н ЯМР (400 МГц, CD3OD): δ 8,15 (с, 1H), 7,94 (д, J=8,6 Гц, 1H), 7,89 (д, J=3 Гц, 1H), 7,74 (с, 1H), 7,62 (д, J=8,6 Гц, 1H), 7,56 (д, J=3 Гц, 1H), 4,60 (м, 2H), 4,45 (м, 2H), 4,30 (м, 1H), 4,16 (м, 1H), 3,95-3,89 (м, 2H), 3,35 (м, 1H), 2,55 (уш.с, 4H). МС м/z (M+H+) 481.
Следуя процедуре, описанной выше для примера 10, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CD3OD): δ 8,13 (с, 1H), 8,01 (д, J=8 Гц, 1H), 7,88 (д, J=3 Гц, 1H), 7,73 (д, J=8 Гц, 1H), 7,55 (д, J=3 Гц, 1H), 4,53 (уш.с, 1H), 4,46 (уш.с, 1H), 4,31 (м, 2H), 4,22 (м, 1H), 4,16 (м, 1H), 3,33 (м, 1H), 2,60-2,40 (м, 4H).
МС м/z (M+H+) 515
1Н ЯМР (400 МГц, CD3OD): δ 8,15 (с, 1H), 7,94 (д, J=8,6 Гц, 1H), 7,73 (с, 1H), 7,62 (д, J=8,6 Гц, 1H), 7,42 (м, 5H), 4,58 (м, 1H), 4,42 (м, 1H), 4,28 (м, 1H), 4,12 (м, 1H), 3,93 (уш.с, 1H), 3,77 (уш.с, 1H), 3,51 (уш.с, 2H), 3,34 (м, 1H), 2,60-2,30 (м, 4H).
МС м/z (M+H+) 474
МС м/z (M+H+) 496
МС м/z (M+H+) 496
МС м/z (M+H+) 583,0
МС м/z (M+H+) 583,0
1Н ЯМР (400 МГц, CD3OD): δ 2,13 (д, J=13,2 Гц, 1H), 2,41 (д, J=47,2 Гц, 1H), 2,8-3,3 (м, 2,5H), 3,69 (д, J=13,7 Гц, 0,5H), 3,98-4,42 (м, 4H), 4,51 (т, J=13,4 Гц, 0,5H), 5,27-5,54 (м, 1H), 6,93 (уш.с, 0,5H), 7,83 (д, J=8,6 Гц, 1H), 7,88 (уш.с, 1H), 7,97 (т, J=6,8 Гц, 1H), 8,11 (д, J=8,8 Гц, 1H), 8,42 (с, 1H)
МС м/z (M+H+) 583,0
Пример 10а

С. Метил 3-хлор-5-фтор-6-трифторметил-бензо[b]тиофен-2-карбоксилат (10d) и метил 3-хлор-6-трифторметил-7-фтор-бензо[b]тиофен-2-карбоксилат (10e). Смесь 3-фтор-4-(трифторметил)-коричной кислоты, 10c (1,5 г, 6,4 ммоль), SOCl2 (2,33 мл, 32 ммоль), DMF (0,05 мл, 0,64 ммоль) и пиридина (0,05 мл, 0,64 ммоль) в хлорбензоле (5 мл) нагревали в колбе с обратным холодильником в течение 24 часов. Реакционную смесь охладили до комнатной температуры и сконцентрировали. Полученный остаток растворили в MeOH (50 мл) и перемешивали при комнатной температуре в течение 16 часов. Раствор сконцентрировали, разбавили CH2Cl2 и промыли H2O. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. Путем рекристаллизации гептанами с последующей колоночной флэш-хроматографией (силикагель, 2% EtOAc/гептан) получили соединения 10d (580 мг) и 10e (380 мг).
D. 3-Хлор-5-фтор-6-трифторметил-бензо[b]тиофен-2-карбоновая кислота, 10f. Метил 3-хлор-5-фтор-6-трифторметил-бензо[b]тиофен-2-карбоксилат, 10d (180 мг, 0,58 ммоль), перемешивали с раствором LiOH (55 мг, 2,3 ммоль) в THF (5 мл) и H2O (2,5 мл) в течение 4 часов. Для установления pH раствора на уровне 3~4 к смеси добавили 1Н раствора HCl. Полученную смесь экстрагировали с помощью EtOAc (2x). Органический раствор промыли водным раствором NaCl, высушили над Na2SO4 и сконцентрировали для получения соединения 10f (150 мг).
E. 3-Хлор-6-трифторметил-7-фтор-бензо[b]тиофен-2-карбоновая кислота, 10g. Соединение 10g получили из соединения 10e в результате процедуры, описанной выше для стадии D.
Следуя процедуре, описанной выше для примера 10, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС м/z (M+H+) 533
МС м/z (M+H+) 533
МС м/z (M+H+) 533
МС м/z (M+H+) 533
Пример 10b

F. 3-Хлор-5-трифторметил-6-фтор-бензо[b]тиофен-2-карбоновая кислота (10h) и 3-хлор-6-фтор-7-трифторметил-бензо[b]тиофен-2-карбоновая кислота (10i). Соединения 10h и 10i получены в соответствии с процедурой, описанной в примере 10a, с использованием 4-фтор-3-(трифторметил)-коричной кислоты вместо соединения 10c. Данные соединения получены в виде смеси ~2:1.
G. 3-Хлор-5-трифторметил-6-фтор-бензо[b]тиофен-2-карбонил хлорид (10j) и 3-хлор-6-фтор-7-трифторметил-бензо[b]тиофен-2-карбонил хлорид (10k). Соединения 10j и 10k получены в соответствии с процедурой, описанной в примере 10a, из соединений 10h и 10i. Данные соединения были получены в виде смеси ~2:1.
H. 1-(1-{[3-Хлор-6-фтор-5-(трифторметил)-1-бензотиофен-2-ил]карбонил}азетидин-3-ил)-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 901, и 1-(1-{[3-хлор-6-фтор-7-(трифторметил)-1-бензотиофен-2-ил]карбонил}азетидин-3-ил)-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 902. Соединения 901 и 902 получены в соответствии с процедурой, описанной в примере 10, из соединения 5e (соль бис-HCl) (0,31 ммоль, 150 мг), смеси соединений 10j и 10k (0,24 ммоль, 76 мг) и Et3N (1,44 ммоль, 0,2 мл) в 7 мл CH2Cl2. После обработки и очистки колоночной флэш-хроматографией (силикагель, 2% MeOH/CH2Cl2) получили 50 мг (39%) соединения 901, а затем 18 мг (14%) соединения 902. Соединение 901: МС м/z (M+H+) 533. Соединение 902: МС м/z (M+H+) 533.
Следуя процедуре, описанной выше для примера 10b, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС м/z (M+H+) 533
МС м/z (M+H+) 533
Пример 11

A. 1-{4-[1-(6-Бром-3-хлор-бензо[b]тиофен-2-карбонил)-азетидин-3-ил]-пиперазин-1-ил}-2,2,2-трифторэтанон, 11b. К раствору соединения 1g (0,19 г, 0,61 ммоль) и Et3N (0,51 мл, 3,67 ммоль) в CH2Cl2 (4 мл) при 0°C добавили раствор соединения 11a (полученное способом, аналогичным способу получения соединения 10b в примере 10) (0,69 ммоль) в CH2Cl2 (2 мл). Реакционную смесь медленно нагревали до комнатной температуры в течение 18 часов. Реакционную смесь разбавили CH2Cl2 и промыли водным раствором NaHCO3. Органический слой высушили над Na2SO4 и сконцентрировали. После очистки колоночной флэш-хроматографией (силикагель, 3% MeOH/CH2Cl2) получили соединение 11b (0,3 г).
B. (6-Бром-3-хлорбензо[b]тиофен-2-ил)-(3-пиперазин-1-ил-азетидин-1-ил)-метанон, 11c. Раствор соединения 11b (0,3 г, 0,59 ммоль) в Et3N (1 мл) и метаноле (9 мл) перемешивали 3 дня при комнатной температуре. Затем раствор концентрировали, получив соединение 11c, которое использовали в следующей реакции без дополнительной очистки.
C. 1-{1-[(6-Бром-3-хлор-1-бензотиофен-2-ил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 326. К смеси соединения 11c (0,2 ммоль), соединения 5c (31 мг, 0,24 ммоль) и Et3N (0,08 мл, 0,58 ммоль) в CH2Cl2 (3 мл) при комнатной температуре добавили HATU (91 мг, 0,24 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Смесь разбавили диэтиловым эфиром, промыли водным раствором NaHCO3 и водным раствором NaCl, высушили над Na2SO4, отфильтровали и концентрировали. После очистки колоночной флэш-хроматографией (силикагель, 3% MeOH/CH2Cl2) получили соединение 326 (57 мг). 1Н ЯМР (400 МГц, CD3OD): δ 7,98 (с, 1H), 7,88 (д, J=3 Гц, 1H), 7,75 (д, J=8,6 Гц, 1H), 7,61 (д, J=8,6 Гц, 1H), 7,55 (д, J=3 Гц, 1H), 4,53 (уш.с, 1H), 4,44 (уш.с, 1H), 4,30 (уш.с, 2H), 4,21(уш.с, 1H), 4,13 (уш.с,1H), 3,89 (уш.с, 1H), 3,84 (уш.с, 1H), 3,31 (м, 1H), 2,60-2,40 (м, 4H). МС м/z (M+H+) 525/527/529.
Следуя процедуре, описанной выше для примера 11, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CD3OD): δ 8,05 (д, J=8,2 Гц, 1H), 7,89 (д, J=3 Гц, 1H), 7,85 (с, 1H), 7,72 (д, J=7,4 Гц, 1H), 7,55 (д, J=3 Гц, 1H), 7,51 (т, J=7,8 Гц, 1H), 4,60 (м, 2H), 4,45 (м, 2H), 4,31 (м, 1H), 4,17 (м, 1H), 3,95-3,80 (м, 2H), 3,35 (м, 1H), 2,56 (уш.с, 4H).
МС м/z (M+H+) 481
МС м/z (M+H+) 481
1Н ЯМР (400 МГц, CD3OD): δ 8,02 (д, J=8,2 Гц, 1H), 7,80 (с, 1H), 7,73 (д, J=7,4 Гц, 1H), 7,51 (т, J=8,2 Гц, 1H), 7,42 (м, 5H), 4,60 (м, 1H), 4,43 (м, 1H), 4,28 (м, 1H), 4,12 (м, 1H), 3,94 (уш.с, 1H), 3,76 (уш.с, 1H), 3,51 (уш.с, 2H), 3,33 (м, 1H), 2,60-2,30 (м, 4H).
МС м/z (M+H+) 474
1Н ЯМР (400 МГц, CD3OD): δ 8,05 (д, J=8 Гц, 1H), 7,84 (с, 1S), 7,71 (д, J=8 Гц, 1H), 7,50 (т, J=8 Гц, 1H), 7,42 (м, 5H), 4,59 (м, 1H), 4,42 (м, 1H), 4,29 (м, 1H), 4,13 (м, 1H), 3,92 (уш.с, 1H), 3,79 (уш.с, 1H), 3,51 (уш.с, 1H), 3,34 (м, 1H), 2,60-2,30 (м, 4H).
МС м/z (M+H+) 474
МС м/z (M+H+) 518/520/522
1Н ЯМР (400 МГц, CD3OD): δ 8,80 (с, 1H), 8,04 (с, 1H), 8,02 (д, J=8 Гц, 1H), 7,81 (с, 1H), 7,73 (д, J=7,6 Гц, 1H), 7,51 (т, J=7,6 Гц, 1H), 4,60 (м, 1H), 4,45 (м, 1H), 4,30 (м, 1H), 4,15 (м, 1H), 4,02 (уш.с, 1H), 3,95 (м, 2H), 3,82 (уш.с, 1H), 3,35 (м, 1H), 2,60-2,40 (м, 4H).
МС м/z (M+H+) 481
1Н ЯМР (400 МГц, CD3OD): δ 8,80 (с, 1H), 8,02 (с, 1H), 7,97 (с, 1H), 7,74 (м, 1H), 7,60 (м, 1H), 4,30 (м, 2H), 4,21 (уш.с, 1H), 4,12 (уш.с, 1H), 4,00 (уш.с, 1H), 3,92 (м, 2H), 3,81 (уш.с, 1H), 3,31 (м, 1H), 2,50-2,30 (м, 4H).
МС м/z (M+H+) 525/527/529
1Н ЯМР (400 МГц, CD3OD): δ 8,80 (с, 1H), 8,05 (д, J=8 Гц, 1H), 8,04 (с, 1H), 7,85 (м, 1H), 7,72 (д, J=8 Гц, 1H), 7,51 (т, J=7,6 Гц, 1H), 4,60 (м, 1H), 4,44 (м, 1H), 4,30 (м, 1H), 4,16 (м, 1H), 4,10-3,80 (м, 4H), 3,36 (м, 1H), 2,60-2,40 (м, 4H).
МС м/z (M+H+) 481
1Н ЯМР (400 МГц, CD3OD): δ 8,80 (д, J=2 Гц, 1H), 8,13 (т, J=0,8 Гц, 1H), 8,03 (д, J=2 Гц, 1H), 8,01 (д, J=8,6 Гц, 1H), 7,73 (дд, J=1,2 Гц, 8,6 Гц, 1H), 4,31 (м, 2H), 4,21 (м, 1H), 4,15 (м, 1H), 4,01 (м, 1H), 3,93 (м, 2H), 3,81 (м, 1H), 3,33 (м, 1H), 2,55-2,40 (м, 4H).
МС м/z (M+H+) 515
МС м/z (M+H+) 508
МС м/z (M+H+) 481
МС м/z (M+H+) 488
МС м/z (M+H+) 458
МС м/z (M+H+) 438
МС м/z (M+H+) 481
МС м/z (M+H+) 495
МС м/z (M+H+) 495
МС м/z (M+H+) 465
МС м/z (M+H+) 465
МС м/z (M+H+) 459
МС м/z (M+H+) 445
МС м/z (M+H+) 445
Пример 12
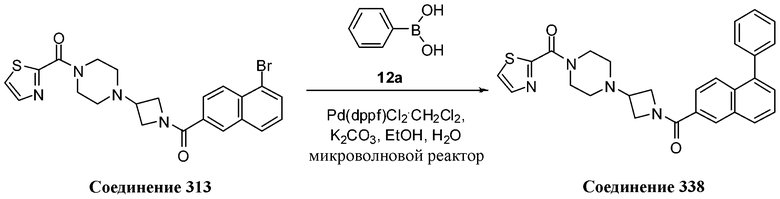
1-{1-[(5-Фенилнафталин-2-ил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 338. Смесь соединения 313 (48 мг, 0,1 ммоль), соединения 12a (24 мг, 0,2 ммоль), K2CO3 (27 мг, 0,2 ммоль) и Pd(dppf)Cl2·CH2Cl2 (4 мг, 0,005 ммоль) в EtOH (1 мл) и H2O (0,2 мл) нагревали в микроволновом реакторе при 130°C в течение 30 минут. Реакционную смесь охладили до комнатной температуры, разбавили CH2Cl2 и промыли H2O. Органический слой высушили над Na2SO4 и сконцентрировали. После очистки колоночной флэш-хроматографией (силикагель, 3% MeOH/CH2Cl2) получили соединение 338 (28 мг). 1Н ЯМР (400 МГц, CD3OD): δ 8,20 (д, J=1,6 Гц, 1H), 7,93 (т, J=9,6 Гц, 2H), 7,88 (д, J=3 Гц, 1H), 7,66-7,43 (м, 9H), 4,52 (уш.с, 1H), 4,50-4,20 (м, 4H), 4,16 (м, 1H), 3,88 (уш.с, 1H), 3,83 (уш.с, 1H), 3,28 (м, 1H), 2,60-2,40 (м, 4H). МС м/z (M+H+) 483.
Следуя процедуре, описанной выше для примера 12, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС м/z (M+H+) 476
МС м/z (M+H+) 477
МС м/z (M+H+) 550
1Н ЯМР (400 МГц, CD3OD): δ 8,05 (с, 1H), 7,88 (д, J=8,6 Гц, 1H), 7,70 (с, 1H), 7,66-7,62 (м, 3H), 7,49-7,36 (м, 8H), 4,58 (м, 1H), 4,42 (м, 1H), 4,28 (м, 1H), 4,11 (м, 1H), 3,92 (уш.с, 1H), 3,76 (уш.с, 1H), 3,49 (уш.с, 2H), 3,31 (м, 1H), 2,60-2,25 (м, 4H).
МС м/z (M+H+) 482
Пример 13

1-{1-[(3-Хлор-6-фенил-1-бензотиофен-2-ил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 343. Названное соединение получили способом, описанным в примере 12 для соединения 338, используя 1 эквивалент соединения 12a и заменив соединение 313 на соединение 326. Реакционную смесь нагревали в микроволновом реакторе при 120°C в течение 20 минут. 1Н ЯМР (400 МГц, CD3OD): δ 8,01 (д, J=1,2 Гц, 1H), 7,95 (д, J=8,6 Гц, 1H), 7,88 (д, J=3 Гц, 1H), 7,74 (д, J=8,6 Гц, 1H), 7,66 (д, J=8,2 Гц, 2H), 7,55 (д, J=3 Гц, 1H), 7,49 (м, 2H), 7,41 (м, 1H), 4,54 (уш.с, 1H), 4,46 (уш.с, 1H), 4,33 (м, 2H), 4,25 (м, 1H), 4,14 (м, 1H), 3,89 (уш.с, 1H), 3,84 (уш.с, 1H), 3,32 (м, 1H), 2,50 (м, 4H). МС м/z (M+H+) 523.
Следуя процедуре, описанной выше для примера 13, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС м/z (M+H+) 516 (M+H+).
МС м/z (M+H+) 523
МС м/z (M+H+) 550
МС м/z (M+H+) 514
МС м/z (M+H+) 528
Пример 14

1-(Фенилкарбонил)-4-{1-[(5-фенилтиофен-2-ил)карбонил]азетидин-3-ил}пиперазин, соединение 346. Смесь соединения 322 (40 мг), соединения 12a (16 мг), Pd(dppf)Cl2·CH2Cl2 (8 мг) и Na2CO3 (19 мг) в смеси диоксан (0,8 мл)/вода (0,2 мл) поместили в накрытую тару и нагревали при 80°C в течение 4 часов. Затем реакционную смесь разбавили EtOAc и водой. Органический слой концентрировали при пониженном давлении, остаток очищали колоночной флэш-хроматографией (силикагель, 5% MeOH/EtOAc), получив соединение 346 (17 мг). МС м/z (M+H+) 432,6.
Следуя процедуре, описанной выше для примера 14, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС м/z (M+H+) 500,0
МС м/z (M+H+) 530,0
МС м/z (M+H+) 598,0
МС м/z (M+H+) 598,0
МС м/z (M+H+) 570,1
МС м/z (M+H+) 457,0
МС м/z (M+H+) 457,0
МС м/z (M+H+) 507,0
МС м/z (M+H+) 466
МС м/z (M+H+) 483
МС м/z (M+H+) 473
МС м/z (M+H+) 541
МС м/z (M+H+) 471
МС м/z (M+H+) 521
МС м/z (M+H+) 504
МС м/z (M+H+) 504
МС м/z (M+H+) 554
МС м/z (M+H+) 521
МС м/z (M+H+) 471
МС м/z (M+H+) 521
МС м/z (M+H+) 490
МС м/z (M+H+) 471
Пример 14а
Следуя процедуре, описанной выше для примера 14, используя соединение 682 из примера 5 вместо соединения 322 и используя соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 7,93 (ар, 1H); 7,82 (ар, 1H); 7,76 (ар, 1H); 7,64 (м, 2H); 7,46 (м, 2H); 7,15 (м, 2H); 4,47-4,0 (уш.м, 6H); 3,82 (уш., 2H); 2,5 (с, 3H)
МС м/z (M+H+) 504,1
1Н ЯМР (400 МГц, CDCl3): δ 8,09-7,97 (м, 2H); 7,88 (ар, 1H); 7,82-7,72 (м, 2H); 7,42 (ар, 2H); 7,31 (м, 1H); 7,62 (уш.м, 1H); 4,48 (уш.м, 1H); 4,35 (уш.м, 2H); 3,96 (уш.м, 2H); 3,14 (м, 4H); 2,44 (с, 3H)
МС м/z (M+H+) 505,2
МС м/z (M+H+) 517,2
МС м/z (M+H+) 490,2
Пример 14b
Следуя процедуре, описанной выше для примера 14, используя соединение 792 из примера 5 вместо соединения 322 и используя соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения настоящего изобретения:
МС м/z (M+H+) 491,1
МС м/z (M+H+) 477,3
МС м/z (M+H+) 491,2
МС м/z (M+H+) 491,1
МС м/z (M+H+) 503,1
Пример 14c
Следуя процедуре, описанной выше для примера 14, используя соединение 864 из примера 5 вместо соединения 322 и используя соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения настоящего изобретения:
МС м/z (M+H+) 492,1
МС м/z (M+H+) 474,1
Пример 14d
Следуя процедуре, описанной выше для примера 14, используя соединение 315 из примера 5 вместо соединения 322 и используя соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения настоящего изобретения:
МС м/z (M+H+) 415,2
МС м/z (M+H+) 492,1
МС м/z (M+H+) 494,97
МС м/z (M+H+) 491,1
Пример 15
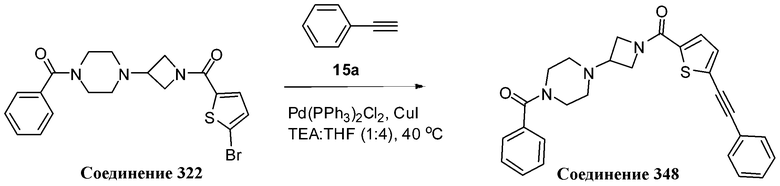
1-(Фенилкарбонил)-4-(1-{[5-(фенилэтинил)тиофен-2-ил]карбонил}азетидин-3-ил)пиперазин, соединение 348. К раствору соединения 322 (100 мг), соединения 15a (0,46 ммоль, 0,05 мл), CuI (4,4 мг) и Pd(PPh3)2Cl2 (16 мг) в THF (1 мл) добавили TEA (0,25 мл). Смесь нагревали при 40°C в течение 1 часа. Затем реакционную смесь разбавили EtOAc и водой. Органический слой концентрировали при пониженном давлении, остаток очищали колоночной флэш-хроматографией (силикагель, 5% MeOH/EtOAc), получив соединение 348 (75 мг). МС м/z (M+H+) 456,6.
Пример 16

1-(Фенилкарбонил)-4-(1-{[5-(2-фенилэтил)тиофен-2-ил]карбонил}азетидин-3-ил)пиперазин, соединение 349. К раствору соединения 348 (30 мг) в EtOH (20 мл) добавили 10% Pd/C (10 мг), после чего смесь подвергли гидрогенизации (0,31 МПа (45 фунтов/кв. дюйм) H2) в течение 1,5 часов. Реакционную смесь фильтровали, фильтрат концентрировали при пониженном давлении, получив соединение 349 (30 мг). МС м/z (M+H+) 460,6.
Пример 17

A. 6-({3-[4-(Фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидроизохинолин, 17a. К раствору соединения 319 (500 мг) в CH2Cl2 (6 мл) добавили TFA (4 мл) при комнатной температуре. Смесь перемешивали 1,5 часов, а затем концентрировали при пониженном давлении. Остаток разбавили CH2Cl2 и подщелочили 2Н водного раствора NaOH. Органический слой промыли водой и насыщенным раствором соли, высушили над безводным K2CO3, отфильтровывали, концентрировали, получив соединение 17a, которое использовали без дополнительной очистки.
B. 2-(Циклогексилкарбонил)-6-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидроизохинолин, соединение 350. Смесь соединения 17a (31 мг, 0,03 мл), HATU (100 мг) и TEA (0,11 мл) в DCM (1 мл) перемешивали при комнатной температуре в течение 5 часов. Реакционную смесь разбавляли DCM и водой. Органический слой концентрировали, остаток очистили колоночной флэш-хроматографией (силикагель, 8% MeOH/EtOAc), получив соединение 350 (65 мг). 1Н ЯМР (CDCl3): δ 7,47-7,39 (м, 7H), 7,17 (д, J=0,02, 1H), 4,74 (с, 1,2H), 4,48 (с, 0,8H), 4,25 (м, 2H), 4,10 (м, 2H), 3,92-3,71 (м, 4H), 3,43 (м, 2H), 3,19 (м, 1H), 2,93 (м, 1,2H), 2,86 (м, 0,8H), 2,55 (м, 1H), 2,42-2,24 (м, 4H), 1,83-1,57 (м, 8H), 1,26 (м, 2H). МС м/z (M+H+) 515,7.
Следуя процедуре, описанной выше для примера 17, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС м/z (M+H+) 503,7
МС м/z (M+H+) 509,6
МС м/z (M+H+) 463,6
МС м/z (M+H+) 583,7
МС м/z (M+H+) 475,2
МС м/z (M+H+) 461,2
МС м/z (M+H+) 516,2
Пример 17а

D. 6-{3-[4-(Тиазол-2-карбонил)-пиперазин-1-ил]-азетидин-1-карбонил}-3,4-дигидро-1H-изохинолин-2-карбоновой кислоты трет-бутиловый эфир, 17c. К раствору соединения 5e (651 мг, 2 ммоль), 2-трет-бутилового эфира 3,4-дигидро-1Н-изохинолин-2,6-дикарбоновой кислоты 17b (555 мг, 2 ммоль) и EDC (466 мг, 3 ммоль) в CH2Cl2 (20 мл) добавили Et3N (0,84 мл, 6 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Смесь экстрагировали CH2Cl2 и H2O после подкисления водного слоя до рН~6 1Н водного раствора HCl. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. Остаток очистили колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc) и получили 17c (826 мг). МС м/z (M+H+) 512,1.
Следуя процедуре, описанной выше для примера 17a, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:
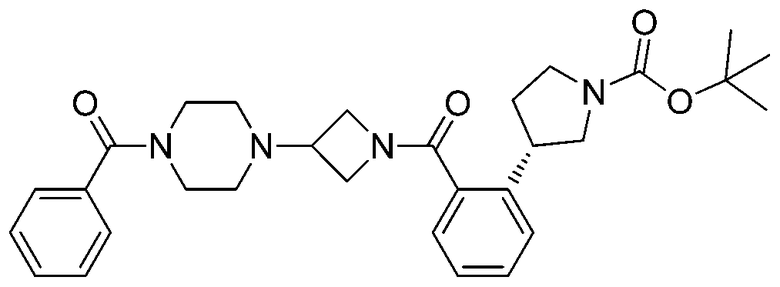
Следуя процедуре, описанной выше для примера 17a, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС м/z (M+H+) 533,4
МС м/z (M+H+) 540,1
МС м/z (M+H+) 512,2
Пример 17b

E. 6-({3-[4-(1,3-Тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидроизохинолин, соединение 916. К раствору соединения 17c (826 мг, 1,61 ммоль) в CH2Cl2 (5 мл) добавили трифторуксусную кислоту (1 мл) при комнатной температуре. Смесь перемешивали 18 часов при комнатной температуре. Смесь экстрагировали CH2Cl2 и H2O после подщелачивания водного слоя до рН~8 водным 1Н раствора NaOH. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. Остаток очищали колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc), получив соединение 916 (675 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,41 (с, 1H), 7,37 (д, J=8,03 Гц, 1H), 7,05 (д, J=8,3 Гц, 1H), 4,54 (уш.с, 1H), 4,44 (уш.с, 1H), 4,01-4,35 (м, 6H), 3,75-3,95 (м, 2H), 3,12-3,31 (м, 2H), 2,85 (т, J=5,8 Гц, 1H), 2,49 (уш.с, 4H). МС м/z (M+H+) 412,0.
Следуя процедуре, описанной выше для примера 17b, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Пример 18

2-Бензил-6-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидроизохинолин, соединение 355. К суспензии соединения 17a (100 мг) и K2CO3 (69 мг) в MeCN добавили соединение 18a (0,0353 мл) и перемешивали смесь при комнатной температуре в течение 30 минут. Реакционную смесь концентрировали, а остаток разбавляли EtOAc и водой. Органический слой концентрировали при пониженном давлении, остаток очищали колоночной флэш-хроматографией (силикагель, 8% MeOH/EtOAc), получив соединение 355 (85 мг). МС м/z (M+H+) 495,6.
Пример 19

N-трет-Бутил-6-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-3,4-дигидроизохинолин-2(1H)-карбоксамид, соединение 356. К раствору соединения 17a (75 мг) в DCM (1 мл) по каплям добавили соединение 19a (0,026 мл) при 0°C. Через 30 минут реакцию остановили DCM и водой при 0°C. Органические фракции сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 5% MeOH/EtOAc) с получением соединения 356 (60 мг). МС м/z (M+H+) 504,7.
Пример 20
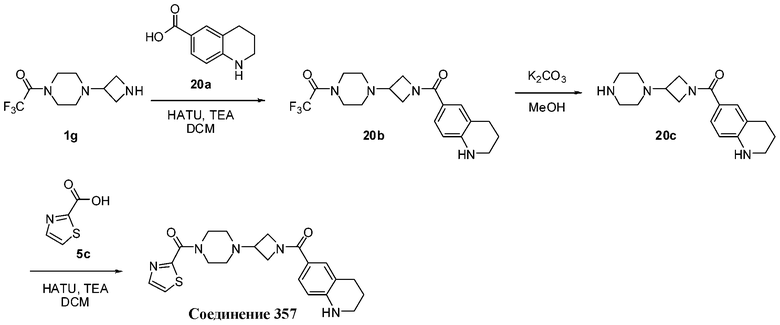
A. 6-({3-[4-(Трифторацетил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидрохинолин, 20b. К раствору соединения 1g (308 мг, 1 ммоль), соединения 20а (177 мг, 1 ммоль) и Et3N (0,42 мл, 3 ммоль) в CH2Cl2 (10 мл) при комнатной температуре добавили HATU (570 мг, 1,5 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Полученную смесь разбавили CH2Cl2 и промыли водным раствором NaHCO3. Органическую фазу сушили над Na2SO4, отфильтровывали и концентрировали при пониженном давлении. После очистки колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc+0,5% Et3N) получили соединение 20b (279 мг). ЖХ/МС м/z (M+H+) 397,0.
B. 6-([3-Пиперазин-1-ил]-азетидин-1-ил)карбонил-1,2,3,4-тетрагидрохинолин, 20c. К раствору соединения 20b (529 мг, 1,33 ммоль) в метаноле (10 мл) добавили K2CO3 (368 мг, 2,66 ммоль). Реакционную смесь перемешивали 30 минут при комнатной температуре. Полученную смесь отфильтровывали, концентрировали при пониженном давлении, и полученный остаток распределили между CH2Cl2 и H2O. Органическую фазу сушили над Na2SO4, отфильтровывали, концентрировали при пониженном давлении и получили соединение 20с (370 мг). ЖХ/МС м/z (M+H+) 301,0.
C. 6-(3-[4-(1,3-Тиазол-2-ил-карбонил)пиперазин-1-ил]-азетидин-1-ил)карбонил-1,2,3,4-тетрагидрохинолин, соединение 357. К раствору соединения 20c (370 мг, 1,23 ммоль), соединения 5c (160 мг, 1,24 ммоль) и Et3N (0,51 мл, 3,69 ммоль) в CH2Cl2 (10 мл) добавили HATU (703 мг, 1,85 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Полученную смесь разбавили CH2Cl2 и промыли водным раствором NaHCO3. Органическую фазу высушили над Na2SO4, отфильтровывали и концентрировали при пониженном давлении. Остаток очищали колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc+0,5% Et3N), получив соединение 357 (483 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,0 Гц, 1H), 7,53-7,58 (м, 1H), 7,33 (с, 1H), 7,24-7,30 (м, 1H), 6,39 (д, J=8,1 Гц, 1H), 3,97-4,66 (м, 6H), 3,86 (д, J=18,4 Гц, 2H), 3,35 (т, J=5,4 Гц, 2H), 3,16-3,26 (м, 1H), 2,77 (т, J=6,2 Гц, 2H), 2,39-2,59 (м, 4H), 1,94 (дт, J=11,8, 6,1 Гц, 2H); ЖХ/МС м/z (M+H+) 412,0.
Пример 21

6-(3-[4-(1,3-Тиазол-2-ил-карбонил)пиперазин-1-ил]-азетидин-1-ил)карбонил1-[3-(трифторметил)фенил]карбонил-1,2,3,4-тетрагидрохинолин, соединение 358. К раствору соединения 357 (30 мг, 0,073 ммоль) в CH2Cl2 (1 мл) при 0°C добавили соединение 1f (0,013 мл, 0,088 ммоль), а затем Et3N (0,03 мл, 0,22 ммоль). Реакционную смесь перемешивали при 0°C в течение 2 часов. Полученную смесь распределили между CH2Cl2 и H2O. Органическую фазу высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Остаток очищали колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc + 0,5% Et3N), получив соединение 358 (42 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,65 (д, J=7,8 Гц, 1H), 7,61 (с, 1H), 7,52-7,59 (м, 3H), 7,41-7,49 (м, 1H), 7,12 (дд, J=8,3, 1,8 Гц, 1H), 6,73 (д, J=7,8 Гц, 1H), 4,35-4,59 (м, 2H), 4,18-4,26 (м, 2H), 4,01-4,16 (м, 2H), 3,75-3,95 (м, 4H), 3,17-3,26 (м, 1H), 2,90 (т, J=6,6 Гц, 2H), 2,37-2,57 (м, 4H), 2,02-2,12 (м, 2H); ЖХ/МС m/z (M+H+) 584,0.
Следуя процедуре, описанной выше для примера 21, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,50 (с, 1H), 7,43-7,47 (м, 2H), 4,05-4,62 (м, 6H), 3,75-3,97 (м, 4H), 3,21-3,31 (м, 1H), 2,78 (т, J=6,6 Гц, 2H), 2,38-2,59 (м, 4H), 1,90-2,03 (м, 3H), 1,13-1,21 (м, 2H), 0,80-0,86 (м, 2H); ЖХ/МС m/z (M+H+) 480,0.
1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=3,0 Гц, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,50 (с, 1H), 7,44 (дд, J=8,2, 1,6 Гц, 1H), 7,28-7,33 (м, 1H), 4,04-4,62 (м, 6H), 3,73-3,96 (м, 4H), 3,21-3,30 (м, 1H), 2,72-2,82 (м, 3H), 2,40-2,59 (м, 4H), 1,98 (квин, J=6,6 Гц, 2H), 1,71-1,83 (м, 4H), 1,49-1,70 (м, 2H), 1,10-1,36 (м, 4H); ЖХ/МС m/z (M+H+) 522,2.
1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=3,0 Гц, 1H), 7,74 (д, J=8,6 Гц, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,51 (д, J=1,8 Гц, 1H), 7,40 (дд, J=8,6, 2,3 Гц, 1H), 4,03-4,61 (м, 6H), 3,78-3,96 (м, 4H), 3,21-3,29 (м, 1H), 2,95 (с, 3H), 2,89 (т, J=6,6 Гц, 2H), 2,40-2,59 (м, 4H), 1,97-2,08 (м, 2H); ЖХ/МС m/z (M+H+) 490,0.
1Н ЯМР (400 МГц, CDCl3): δ 8,79 (д, J=2,0 Гц, 1H), 8,02 (д, J=2,3 Гц, 1H), 7,73 (д, J=8,6 Гц, 1H), 7,49 (с, 1H), 7,39 (дд, J=8,7, 2,1 Гц, 1H), 3,72-4,37 (м, 10H), 3,19-3,30 (м, 1H), 2,94 (с, 3H), 2,87 (т, J=6,6 Гц, 2H), 2,33-2,56 (м, 4H), 1,96-2,04 (м, 2H); ЖХ/МС m/z (M+H+) 490,0.
1Н ЯМР (400 МГц, CDCl3): δ 7,73 (д, J=8,6 Гц, 1H), 7,49 (с, 1H), 7,35-7,44 (м, 6H), 4,00-4,36 (м, 4H), 3,64-3,97 (м, 4H), 3,48 (уш.с, 2H), 3,18-3,27 (м, 1H), 2,91-2,97 (м, 3H), 2,87 (т, J=6,6 Гц, 2H), 2,19-2,56 (м, 4H), 1,97-2,04 (м, 2H); ЖХ/МС m/z (M+H+) 483,0.
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,0 Гц, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,48 (с, 1H), 7,39-7,44 (м, 1H), 7,24-7,28 (м, 1H), 4,01-4,63 (м, 6H), 3,78-3,97 (м, 2H), 3,67-3,76 (м, 2H), 3,48 (квин, J=8,4 Гц, 1H), 3,20-3,30 (м, 1H), 2,76 (т, J=6,3 Гц, 2H), 2,34-2,60 (м, 6H), 2,08 (м, 2H), 1,83-2,02 (м, 4H); ЖХ/МС m/z (M+H+) 494,0.
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,52-7,61 (м, 4H), 7,49 (д, J=8,1 Гц, 2H), 7,12-7,18 (м, 1H), 6,75-6,85 (м, 1H), 4,00-4,60 (м, 6H), 3,76-3,95 (м, 4H), 3,18-3,27 (м, 1H), 2,90 (т, J=6,6 Гц, 2H), 2,37-2,57 (м, 4H), 2,02-2,12 (м, 2H); ЖХ/МС m/z (M+H+) 584,0
МС m/z (M+H+) 558,0
1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=3,3 Гц, 1H), 7,70-7,79 (м, 2H), 7,63-7,68 (м, 1H), 7,57-7,62 (м, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,50 (с, 1H), 7,45 (уш.с, 1H), 7,26 (с, 1H), 4,94 (уш.с, 1H), 4,48-4,66 (м, 2H), 4,44 (уш.с, 1H), 3,97-4,36 (м, 5H), 3,75-3,96 (м, 2H), 3,65 (уш.с, 1H), 3,19-3,33 (м, 1H), 2,85-3,12 (м, 2H), 2,37-2,62 (м, 4H). МС m/z (M+H+) 584,0
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,72 (д, J=7,6 Гц, 2H), 7,58 (д, J=7,6 Гц, 2H), 7,55 (д, J=3,3 Гц, 1H), 7,38-7,52 (м, 2H), 7,21-7,27 (м, 1H), 4,94 (уш.с, 1H), 4,48-4,65 (м, 2H), 4,43 (уш.с, 1H), 3,95-4,36 (м, 5H), 3,73-3,95 (м, 2H), 3,62 (уш.с, 1H), 3,19-3,32 (м, 1H), 2,85-3,10 (м, 2H), 2,38-2,59 (м, 4H). МС m/z (M+H+) 584,0
МС m/z (M+H+) 590,0
МС m/z (M+H+) 516,0
МС m/z (M+H+) 522,0
МС m/z (M+H+) 505
Пример 22

1-(Фенилсульфонил)-6-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидрохинолин, соединение 366. К раствору соединения 357 (60 мг, 0,015 ммоль) в пиридине (1 мл) добавили соединение 22a (0,023 мл, 0,017 ммоль). Реакционную смесь перемешивали 2 часа при комнатной температуре. Полученную смесь концентрировали при пониженном давлении, остаток очистили колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc + 0,5% Et3N), получив соединение 366 (66 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=3,3 Гц, 1H), 7,84 (д, J=8,3 Гц, 1H), 7,61-7,67 (м, 2H), 7,52-7,59 (м, 2H), 7,36-7,47 (м, 4H), 4,03-4,61 (м, 6H), 3,78-3,93 (м, 4H), 3,20-3,30 (м, 1H), 2,41-2,58 (м, 6H), 1,63-1,71 (м, 2H); ЖХ/МС m/z (M+H+) 552,0.
Следуя процедуре, описанной выше для примера 22, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 7,87-7,91 (м, 2H), 7,78-7,86 (м, 3H), 7,57-7,63 (м, 1H), 7,54-7,57 (м, 1H), 7,39-7,45 (м, 2H), 4,07-4,61 (м, 6H), 3,77-3,95 (м, 4H), 3,20-3,30 (м, 1H), 2,41-2,59 (м, 6H), 1,70 (квин, J=6,3 Гц, 2H); ЖХ/МС m/z (M+H+) 620,0.
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,0 Гц, 1H), 7,81 (д, J=8,3 Гц, 1H), 7,55 (д, J=3,0 Гц, 1H), 7,38-7,47 (м, 4H), 7,32-7,37 (м, 1H), 7,22-7,29 (м, 1H), 4,02-4,61 (м, 6H), 3,77-3,96 (м, 4H), 3,20-3,30 (м, 1H), 2,40-2,60 (м, 6H), 1,65-1,77 (м, 2H); ЖХ/МС m/z (M+H+) 570,0.
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,80-7,85 (м, 1H), 7,73-7,79 (м, 2H), 7,68-7,73 (м, 2H), 7,55 (д, J=3,3 Гц, 1H), 7,39-7,44 (м, 2H), 4,02-4,61 (м, 6H), 3,77-3,95 (м, 4H), 3,21-3,29 (м, 1H), 2,39-2,59 (м, 6H), 1,65-1,73 (м, 2H); ЖХ/МС m/z (M+H+) 620,0
МС m/z (M+H+) 552,0
МС m/z (M+H+) 619,8
МС m/z (M+H+) 558,0
Пример 23

1-Бензил-6-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидрохинолин, соединение 370. К раствору соединения 357 (30 мг, 0,0073 ммоль) в CH3CN (1 мл) добавили соединение 18a (0,01 мл, 0,0088 ммоль), а затем K2CO3 (20 мг, 0,015 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Полученную смесь распределили между CH2Cl2 и H2O. Органический раствор высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Остаток очищали колоночной флэш-хроматографией (силикагель, 1% MeOH/EtOAc + 0,5% Et3N), получив соединение 370 (14 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,54 (д, J=3,0 Гц, 1H), 7,38 (д, J=2,0 Гц, 1H), 7,30-7,36 (м, 2H), 7,19-7,30 (м, 4H), 6,44 (д, J=8,6 Гц, 1H), 4,54 (с, 2H), 3,97-4,52 (м, 6H), 3,77-3,96 (м, 2H), 3,40-3,47 (м, 2H), 3,15-3,24 (м, 1H), 2,83 (т, J=6,2 Гц, 2H), 2,38-2,59 (м, 4H), 1,98-2,05 (м, 2H); ЖХ/МС m/z (M+H+) 502,2.
Следуя процедуре, описанной выше для примера 23, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,0 Гц, 1H), 7,59 (д, J=8,3 Гц, 2H), 7,54 (д, J=3,0 Гц, 1H), 7,39 (с, 1H), 7,34 (д, J=8,1 Гц, 2H), 7,23-7,29 (м, 1H), 6,35 (д, J=8,6 Гц, 1H), 4,58 (с, 2H), 3,97-4,54 (м, 6H), 3,74-3,97 (м, 2H), 3,39-3,49 (м, 2H), 3,15-3,26 (м, 1H), 2,85 (т, J=6,1 Гц, 2H), 2,38-2,59 (м, 4H), 1,99-2,10 (м, 2H); ЖХ/МС m/z (M+H+) 570,0.
МС m/z (M+H+) 570,0.
МС m/z (M+H+) 570,0.
Пример 23а

2-Бензил-6-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидроизохинолин, соединение 680. Раствор соединения 916 (50 мг, 0,121 ммоль) и бензальдегида 23a (0,014 мл, 0,134 ммоль) в CH2Cl2 (2 мл) перемешивали при комнатной температуре в течение 30 минут. Затем добавили триацетоксиборогидрид натрия (38,6 мг, 0,182 ммоль) и перемешивали смесь в течение ночи. К полученной смеси добавили CH2Cl2 и H2O; pH водного слоя довели до ~8, добавляя 1Н водного раствора NaOH. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. Остаток очистили колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc), получив соединение 680 (38,6 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=3,2 Гц, 1H), 7,55 (д, J=3,2 Гц, 1H), 7,32-7,44 (м, 6H), 7,3 (д, J=8,1 Гц, 1H), 7,02 (д, J=8,1 Гц, 1H), 4,33-4,63 (м, 2H), 3,99-4,34 (м, 4H), 3,75-3,98 (м, 2H), 3,70 (с, 2H), 3,65 (с, 2H), 3,16-3,30 (м, 1H), 2,93 (т, J=5,7 Гц, 2H), 2,76 (т, J=5,7 Гц, 2H), 2,37-2,60 (м, 4H). МС m/z (M+H+) 502,0.
Следуя процедуре, описанной выше для примера 23a, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 502,3
Пример 24

1-Фенил-6-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидрохинолин, соединение 372. В сухой сосуд Шленка добавили смесь соединения l1 (30 мг, 0,0073 ммоль), ацетат палладия (II) (1 мг, 0,00037 ммоль), BINAP (3 мг, 0,00044 ммоль) и KOtBu (12 мг, 0,01 ммоль). Из сосуда, снабженного резиновой пробкой с тефлоновым покрытием, удалили воздух и заполнили его аргоном. Бромбензол (14 мг, 0,0088 ммоль) и толуол (0,8 мл) добавили к реакционной смеси с помощью шприца. Реакционную смесь нагревали при 110°C в течение 21 часа. Полученную смесь разбавили CH2Cl2 и последовательно промыли насыщенным водным NH4Cl и H2O. Органическую фазу высушили над Na2SO4, профильтровали и сконцентрировали. Остаток очистили препаративной ТСХ (силикагель, 2% MeOH/EtOAc + 0,5% Et3N), получив соединение 372 (1,3 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,55 (д, J=3,0 Гц, 1H), 7,36-7,45 (м, 3H), 7,14-7,26 (м, 4H), 6,55 (д, J=8,6 Гц, 1H), 3,98-4,64 (м, 6H), 3,74-3,96 (м, 2H), 3,61-3,72 (м, 2H), 3,16-3,27 (м, 1H), 2,88 (т, J=6,3 Гц, 2H), 2,37-2,61 (м, 4H), 2,05-2,13 (м, 2H); ЖХ/МС m/z (M+H+) 488,0.
Следуя процедуре, описанной выше для примера 24, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=3,3 Гц, 1H), 7,60 (д, J=8,3 Гц, 2H), 7,55 (д, J=3,0 Гц, 1H), 7,46 (с, 1H), 7,33 (д, J=8,3 Гц, 2H), 7,24 (дд, J=8,7, 2,1 Гц, 1H), 6,84 (д, J=8,6 Гц, 1H), 4,01-4,62 (м, 6H), 3,75-3,98 (м, 2H), 3,64-3,73 (м, 2H), 3,18-3,30 (м, 1H), 2,87 (т, J=6,3 Гц, 2H), 2,36-2,62 (м, 4H), 2,02-2,12 (м, 2H); ЖХ/МС m/z (M+H+) 556,0.
1Н ЯМР (400 МГц, CDCl3): δ 7,88 (д, J=3,0 Гц, 1H), 7,55 (д, J=3,0 Гц, 1H), 7,37-7,52 (м, 5H), 7,22 (дд, J=8,6, 2,0 Гц, 1H), 6,66 (д, J=8,6 Гц, 1H), 4,03-4,59 (м, 6H), 3,74-3,96 (м, 2H), 3,61-3,72 (м, 2H), 3,18-3,27 (м, 1H), 2,89 (т, J=6,3 Гц, 2H), 2,37-2,60 (м, 4H), 2,03-2,14 (м, 2H); ЖХ/МС m/z (M+H+) 556,0.
1Н ЯМР (400 МГц, CDCl3): δ 8,46 (д, J=4,8 Гц, 2H), 7,89 (д, J=3,0 Гц, 1H), 7,83 (д, J=8,6 Гц, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,50 (с, 1H), 7,41 (дд, J=8,6, 2,0 Гц, 1H), 6,75 (т, J=4,8 Гц, 1H), 4,06-4,61 (м, 6H), 3,99-4,06 (м, 2H), 3,77-3,96 (м, 2H), 3,18-3,29 (м, 1H), 2,83 (т, J=6,4 Гц, 2H), 2,39-2,59 (м, 4H), 1,99-2,07 (м, 2H); ЖХ/МС m/z (M+H+) 490,0.
МС m/z (M+H+) 488,1
МС m/z (M+H+) 490,0
МС m/z (M+H+) 489,0
МС m/z (M+H+) 490,1
Пример 25

A. Метиловый эфир 1-ацетил-6-бром-1,2,3,4-тетрагидрохинолин-2-карбоновой кислоты, 25b. К раствору соединения 25а (100 мг, 0,37 ммоль) в CH2Cl2 (5 мл) добавили ацетилхлорид (0,1 мл) и пиридин (0,1 мл). Реакционную смесь перемешивали 2 часа при комнатной температуре. Полученную смесь распределили между CH2Cl2 и H2O. Органическую фазу высушили над Na2SO4, отфильтровывали, сконцентрировали и получили соединение 25b (116 мг), которое использовали в следующей стадии без дополнительной очистки. ЖХ/МС m/z 312,0 (M+H+), 314,0 (M+2H+).
B. 1-Ацетил-6-бром-1,2,3,4-тетрагидрохинолин-2-карбоновая кислота, 25c. К раствору соединения 25b (116 мг, 0,37 ммоль) в THF/MeOH/H2O (2/2/2 мл) добавили LiOH (62 мг, 1,48 ммоль). Реакционную смесь перемешивали 3 часа при комнатной температуре. Полученную смесь концентрировали при пониженном давлении, распределяли между CH2Cl2 и H2O; доводили рН водной фазы до 5, добавляя 2Н HCl (водный). Органическую фазу высушили над Na2SO4, отфильтровали, сконцентрировали при пониженном давлении и получили соединение 25c, которое использовали в следующей стадии без дополнительной очистки. ЖХ/МС m/z 298,0 (M+H+), 300,0 (M+2H+).
C. 1-Ацетил-6-бром-2-({3-[4-(трифторацетил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидрохинолин, 25d. К раствору соединения 1g (228 мг, 0,74 ммоль), соединения 25c (22 мг, 0,74 ммоль) и Et3N (0,3 мл, 2,22 ммоль) в CH2Cl2 (7 мл) добавили HATU (338 мг, 0,89 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Полученную смесь разбавили CH2Cl2 и промыли водным раствором NaHCO3. Органическую фазу высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc + 0,5% Et3N), получив соединение 25d (265 мг). ЖХ/МС m/z (M+H+), 517,0 (M+2H+), 519,0.
D. 1-Ацетил-6-бром-2-({3-[пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидрохинолин, 25e. К раствору соединения 25d (261 мг, 0,505 ммоль) в MeOH (3 мл) добавили K2CO3 (140 мг, 1,01 ммоль). Реакционную смесь перемешивали 30 минут при комнатной температуре. Полученную смесь отфильтровали, фильтрат концентрировали при пониженном давлении, и полученный остаток распределили между CH2Cl2 и H2O. Органическую фазу высушили над Na2SO4, отфильтровывали, сконцентрировали при пониженном давлении и получили соединение 25e (158 мг). ЖХ/МС m/z (M+H+) 421,0, (M+2H+) 423,0.
E. 1-Ацетил-6-бром-2-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,2,3,4-тетрагидрохинолин, соединение 376. Названное соединение получили способом, аналогичным способу получения соединения 357, используя соединение 20c вместо соединения 25e. ЖХ/МС m/z (M+H+) 532,0, (M+2H+) 534,0.
Следуя процедуре, описанной выше для примера 25, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
ЖХ/МС m/z (M+H+) 532,0, (M+2H+) 534,0.
ЖХ/МС m/z (M+H+) 525,0, (M+2H+) 527,0.
Пример 26

A. трет-Бутил 3-(4-бензоилпиперазин-1-ил)-азетидин-1-карбоксилат, 4b. К раствору соединения 2а (5 г) и соединения 4а (6,75 г) в 1,2-дихлорэтане (50 мл) добавили уксусную кислоту (1,0 мл) и молекулярные сита 4Å. Полученную смесь перемешивали в течение 2 часов, добавив за это время NaBH(OAc)3 (11 г) в три приема. Смесь перемешивали 18 часов, вылили в 2Н KОН (водный, 50 мл), а затем экстрагировали EtOAc (3 раза). Объединенные органические экстракты высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией (5% MeOH/CH2Cl2), получив соединение 4b (11,6 г).
B. 3-(4-Бензоилпиперазин-1-ил)-азетидина гидрохлорид 2c. К раствору соединения 4b (5,1 г) в CH2Cl2 (20 мл) добавили TFA (10 мл). Полученную смесь перемешивали при комнатной температуре в течение 4 часов. Растворитель удалили при пониженном давлении. Полученный остаток растворили в CH2Cl2 (5 мл) и добавили к смеси 4M HCl в диоксане (3,67 мл). Полученный осадок отфильтровали, промыли эфиром, высушили при пониженном давлении и получили соединение 2c в виде гидрохлорида (4,0 г).
C. 4-Ацетоксибензоилхлорид, 26b. К раствору соединения 26a (200 мг, 1,11 ммоль) в THF (5 мл) добавили по каплям оксалилхлорид (97 мкл, 1,11 ммоль) при 0°C, а затем добавили 2 капли DMF. Полученную смесь перемешивали при 0°C в течение 3 часов, после чего нагревали до комнатной температуры в течение 18 часов. Растворители упарили при пониженном давлении и полученный остаток, неочищенное соединение 26b, сушили 2 часа при пониженном давлении, а затем использовали в следующей реакции без дальнейшей очистки.
D. 4-({3-[4-(Фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)фенилацетат (26c). К смеси солянокислой соли соединения 2c (373 мг, 1,33 ммоль), Et3N (0,5 мл) и CH2Cl2 (5 мл) добавили раствор соединения 26b в CH2Cl2 (1 мл). Полученную смесь перемешивали при комнатной температуре в течение 4 часов. Растворитель упарили при пониженном давлении, остаток растворили в CH2Cl2 (1 мл), а затем очистили колоночной флэш-хроматографией (силикагель, 5% MeOH/CH2Cl2), получив соединение 26c (442 мг).
E. 4-({3-[4-(Фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)фенол, 26d. Смесь соединения 26c (420 мг, 1,03 ммоль) и LiOH (100 мг, 4,0 ммоль) в смеси растворителей THF/MeOH/H2O (2/2/2 мл) перемешивали 4 часа при комнатной температуре, а затем подкислили до pH 5 добавлением 2Н HCl (водный). Смесь экстрагировали EtOAc (3 раза). Объединенные экстракты сушили над Na2SO4, отфильтровали и упарили при пониженном давлении. Полученный остаток (неочищенное соединение 26d) сушили 18 часов при пониженном давлении и использовали в следующей реакции без дальнейшей очистки.
F. 1-[1-({4-[(3,4-Дихлорбензил)окси]фенил}карбонил)азетидин-3-ил]-4-(фенилкарбонил)пиперазин, соединение 379. Смесь соединения 26d (70 мг, 0,191 ммоль), K2CO3 (53 мг, 0,382 ммоль), соединения 26e (68 мг, 0,287 ммоль) и DMF (3 мл) перемешивали при комнатной температуре в течение 18 часов. К реакционной смеси добавили воду и смесь экстрагировали EtOAc (3 раза). Объединенные органические экстракты сушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Полученный остаток очищали колоночной флэш-хроматографией, элюируя с помощью 5%MeOH/CH2Cl2, и получили соединение 379 (83 мг). 1Н ЯМР (CDCl3): δ 7,59-7,64 (д, J=8,8 Гц, 2H), 7,53 (д, J=2,0 Гц, 1H), 7,455 (д, J=8,0 Гц, 1H), 7,37-7,44 (м, 5H), 7,23-7,28 (м, 2H), 6,955 (д, J=8,84 Гц, 2H), 5,05 (с, 2H), 4,31 (уш.с, 1H), 4,11-4,27 (м, 2H), 4,00-4,10 (м, 1H), 3,91 (уш.с, 1H), 3,64-3,82 (м, 1H), 3,48 (уш.с, 2H), 3,18-3,27 (м, 1H), 2,42 (уш.с, 4H). МС m/z (M+H+) 524,0.
Следуя процедуре, описанной выше для примера 26, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (CDCl3): δ 7,80-7,88 (м, 4H), 7,59-7,64 (м, J=8,8 Гц, 2H), 7,45-7,53 (м, 3H), 7,36-7,43 (м, 5H), 7,00 (д, J=8,8 Гц, 2H), 5,22 (с, 2H), 4,24-4,32 (м, 1H), 4,08-4,24 (м, 2H), 4,03 (уш.с, 1H), 3,60-3,79 (м, 1H), 3,31-3,52 (м, 2H), 3,10-3,22 (м, 1H), 2,38 (уш.с, 4H).
МС m/z (M+H+) 506,2
1Н ЯМР (CDCl3): δ 7,625 (д, J=8,4 Гц, 2H), 7,44 (дд, J=8,0, 2,1 Гц, 2H), 7,37-7,41 (м, 5H), 7,23 (т, J=8,1, 1H), 6,97(д, J=8,8 Гц, 2H), 5,18 (с, 2H), 4,26-4,36 (м, 1H), 4,12-4,26 (м, 2H), 4,07 (уш.с, 1H), 3,88 (уш.с, 1H), 3,74 (уш.с, 1H), 3,47 (уш.с, 2H), 3,14-3,27 (м, 1H), 2,41 (уш.с, 3H), 2,22 (с, 1H).
МС m/z (M+H+) 524,0
МС m/z (M+H+) 474,2
МС m/z (M+H+) 524,2
МС m/z (M+H+) 490,2
МС m/z (M+H+) 524,1
МС m/z (M+H+) 481,2
МС m/z (M+H+) 504,2
МС m/z (M+H+) 488,2
МС m/z (M+H+) 556,2
МС m/z (M+H+) 540,2
МС m/z (M+H+) 490,2
МС m/z (M+H+) 508,2
МС m/z (M+H+) 540,2
МС m/z (M+H+) 605,2
МС m/z (M+H+) 542,2
МС m/z (M+H+) 457,2
Пример 27
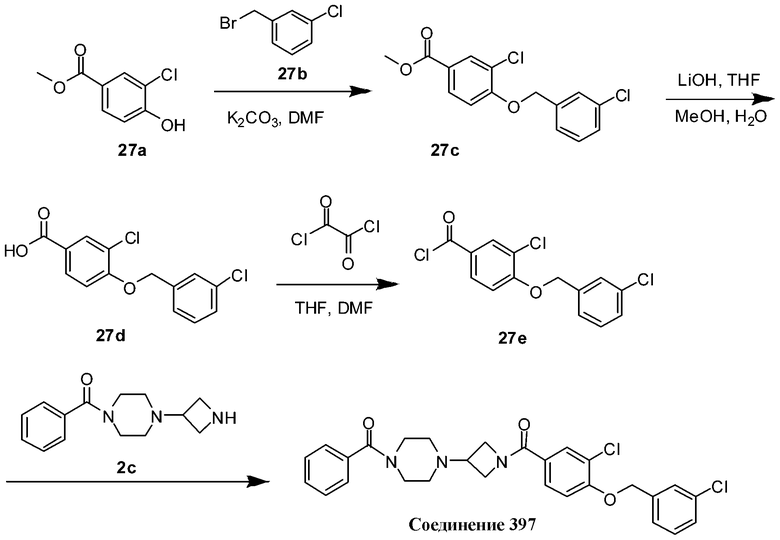
A. Метил 4-(3-хлорбензилокси)-3-хлорбензоат, 27c. Смесь соединения 27а (500 мг, 2,7 ммоль), соединения 27b (0,53 мл, 4,03 ммоль) и K2CO3 (745 мг, 5,4 ммоль) в DMF перемешивали 18 часов при комнатной температуре. К реакционной смеси добавили воду и смесь экстрагировали EtOAc (3 раза). Объединенные органические экстракты сушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Полученный остаток очищали колоночной флэш-хроматографией на силикагеле, элюируя смесью 30% EtOAc/гексан, и получили соединение 27c (662 мг).
B. 4-(3-Хлорбензилокси)-3-хлорбензойная кислота, 27d. Смесь соединения 27c (662 мг, 2,0 ммоль) и LiOH (192 мг, 8 ммоль) в смеси растворителей THF/MeOH/H2O (3/3/3 мл) перемешивали при комнатной температуре в течение 4 часов, а затем подкислили раствором 15% лимонной кислоты в H2O. Смесь экстрагировали EtOAc (3 раза) и объединенные экстракты промыли последовательно водой и насыщенным раствором соли. Экстракты сушили над Na2SO4, отфильтровали и упарили при пониженном давлении. Полученное неочищенное соединение 3b сушили при пониженном давлении в течение 18 часов и использовали в следующей реакции без дальнейшей очистки.
C. 4-(3-Хлорбензилокси)-3-хлорбензоилхлорид, 27e. К раствору соединения 27d (67 мг, 0,33 ммоль) в THF (2 мл) добавили по каплям оксалилхлорид (43 мкл, 0,50 ммоль) при 0°C, а затем добавили 2 капли DMF. Полученную смесь перемешивали при 0° C в течение 3 часов, а затем нагревали до комнатной температуры в течение 18 часов. Растворитель удалили при пониженном давлении. Полученный остаток неочищенного соединения 27e сушили при пониженном давлении в течение 2 часов и использовали в последующей реакции без дальнейшей очистки.
D. 1-[1-({3-Хлор-4-[(3-хлорбензил)окси]фенил}карбонил)азетидин-3-ил]-4-(фенилкарбонил)пиперазин, соединение 397. К смеси соединения 2c (84 мг, 0,30 ммоль), Et3N (0,5 мл) и CH2Cl2 (2,5 мл) добавили раствор соединения 27e в CH2Cl2 (1 мл). Полученную смесь перемешивали при комнатной температуре в течение 4 часов. Растворитель удалили при пониженном давлении. Полученный остаток растворили в CH2Cl2 (1 мл), нанесли на колонку с силикагелем и очистили колоночной флэш-хроматографией, элюируя смесью 5% MeOH/CH2Cl2, и получили соединение 397 (32 мг). 1Н ЯМР (CDCl3): δ 7,695 (д, 1H, J=2,0 Гц), 7,515 (дд, 1H, J1=2,0 Гц, J2=8,6 Гц), 7,44 (с, 1H), 7,38-7,43 (м, 5H), 7,30-7,35 (м, 3H), 6,91-6,97 (д, 1H, J=8,6 Гц), 5,15 (с, 2H), 4,26-4,37 (м, 1H), 4,15-4,26 (м, 2H), 3,84-3,98 (м, 1H), 3,68-3,82 (м, 1H), 3,48 (уш.с, 2H), 3,18-3,29 (м, 1H), 2,56-2,16 (м, 4H). МС m/z (M+H+) 524,0.
Следуя процедуре, описанной выше для примера 27, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (CDCl3): δ 8,64 (д, J=5,8 Гц, 2H), 7,2 (д, J=2,0 Гц, 1H), 7,53 (дд, J1=2,1, 8,4 Гц, 1H), 7,36-7,45 (м, 7H), 6,88-6,95 (д, J=8,6 Гц, 1H), 5,19 (с, 2H), 4,27-4,37 (м, 1H), 4,11-4,27 (м, 2H), 3,99-4,08 (м, 1H), 3,81-3,96 (м, 1H), 3,73 (уш.с, 1H), 3,48 (уш.с, 2H), 3,17-3,30 (м, 1H), 2,41 (уш.с, 4H), МС m/z (M+H+) 498,0
1Н ЯМР (CDCl3): δ 7,70 (д, J=2,0 Гц, 1H), 7,56 (с, 1H), 7,53 (дд, J=8,6, 2,0 Гц, 1H), 7,48 (д, J=8,2 Гц, 1H), 7,37-7,44 (м, 5H), 7,28-7,32 (м, 1H), 6,93 (д, J=8,2 Гц, 1H), 5,14 (с, 2H), 4,28-4,37 (м, 1H), 4,12-4,27 (м, 2H), 4,05 (уш.с, 1H), 3,91 (уш.с, 1H), 3,74 (уш.с, 1H), 3,49 (уш.с, 2H), 3,16-3,27 (м, 1H), 2,42 (уш.с, 4H).
МС m/z (M+H+) 558,0
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,53-7,57 (м, 2H), 7,41-7,48 (м, 2H), 7,39 (дд, J=8,5, 1,1 Гц, 1H), 7,25-7,30 (м, 1H), 6,97 (т, J=8,3 Гц, 1H), 5,12 (с, 2H), 4,52 (уш.д, J=33,8 Гц, 1H), 4,37-4,47 (м, 1H), 4,32 (д, J=6,8 Гц, 1H), 4,15-4,28 (м, 2H), 4,07 (д, J=8,3 Гц, 1H), 3,85 (д, J=17,4 Гц, 2H), 3,20-3,28 (м, 1H), 2,48 (т, J=4,8 Гц, 4H).
МС m/z (M+H+) 549,0.
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,71 (д, J=2,0 Гц, 1H), 7,50-7,57 (м, 2H), 7,45 (с, 1H), 7,30-7,35 (м, 3H), 6,95 (д, J=8,6 Гц, 1H), 5,17 (с, 2H), 4,43 (уш.с, 1H), 4,28-4,38 (м, 1H), 4,17-4,28 (м, 1H), 4,03-4,15 (м, 2H), 3,85 (д, J=19,5 Гц, 2H), 3,19-3,29 (м, 1H), 2,48 (м, 4H).
МС m/z (M+H+) 531,0
1Н ЯМР (CDCl3): δ 8,71 (с, 1H), 8,61 (д, J=3,5 Гц, 1H), 7,88 (д, J=3,0 Гц), 1H), 7,84 (д, J=7,8 Гц, 1H), 7,72 (д, J=2,3 Гц, 1H), 7,56 (д, J=2,0 Гц, 1H), 7,55 (д, J=3,6 Гц, 1H), 7,36 (дд, J=7,8, 4,8 Гц, 1H), 7,00 (д, J=8,6 Гц, 1H), 5,21 (с, 2H), 4,52 (уш.с, 1H), 4,43 (уш.с, 1H), 4,32 (м, 1H), 4,16-4,29 (м, 2Н), 4,03-4,16 (м, 1H), 3,76-3,95 (м, 2Н), 3,20-3,30 (м, 1H), 2,57-2,36 (м, 4H).
МС m/z (M+H+) 498,0.
1Н ЯМР (CDCl3): δ 8,63 (д, J=5,8 Гц, 2H), 7,88 (д, J=3,0 Гц, 1H), 7,63 (д, J=8,8 Гц, 2H), 7,55 (д, J=3,3 Гц, 1H), 7,36 (д, J=6,1 Гц, 2H), 6,96 (д, J=8,84 Гц, 2H), 5,14 (с, 2H), 4,52 (уш.с, 1H), 4,43 (уш.с, 1H), 4,36-4,29 (м, 1H), 4,16-4,29 (м, 2H), 4,04-4,16 (м, 1H), 3,75-3,93 (м, 2H), 3,18-3,28 (м, 1H), 2,37-2,58 (м, 4H).
МС m/z (M+H+) 464,0
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,0 Гц, 1H), 7,71 (д, J=2,0 Гц, 1H), 7,51-7,58 (м, 3H), 7,47 (дд, J=8,3, 4,0 Гц, 1H), 7,30 (дд, J=8,1, 2,0 Гц, 1H), 6,94 (д, J=8,6 Гц, 1H), 5,14 (с, 2H), 4,52 (уш.с, 1H), 4,37 (уш.с, 1H), 4,29-4,37 (м, 1H), 4,22 (уш.с, 2H), 4,01-4,14 (м, 1H), 3,88 (уш.с, 2H), 3,19-3,32 (м, 1H), 2,40-2,55 (м, 4H)
МС m/z (M+H+) 564,6, 566,8
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,50 (д, J=7,8 Гц, 1H), 7,47 (с, 1H), 7,43-7,46 (м, 1H), 7,40 (дд, J=8,6, 1,3 Гц, 1H), 7,28 (д, J=2,3 Гц, 1H), 7,25 (д, J=7,8 Гц, 1H), 7,00 (т, J=8,3 Гц, 1H), 5,28 (с, 2H), 4,49 (д, J=33,2 Гц, 2H), 4,31-4,39 (м, 1H), 4,22 (уш.с, 2H), 4,03-4,16 (м, 1H), 3,88 (уш.с, 2H), 3,19-3,31 (м, 1H), 2,40-2,58 (м, 4H).
МС m/z (M+H+) 549,0
1Н ЯМР (CDCl3): δ 8,59 (д, J=4,5 Гц, 1H), 7,76 (дд, J=1,5, 7,6 Гц, 1H), 7,73 (д, J=2,0 Гц, 1H), 7,61 (д, J=7,8 Гц, 1H), 7,50 (дд, J=8,6, 2,0 Гц, 1H), 7,37-7,44 (м, 5H), 7,25 (дд, J=6,9, 5,2 Гц, 1H), 7,00 (д, J=8,6 Гц, 1H), 5,28-5,35 (м, 2H), 4,27-4,37 (м, 1H), 4,12-4,27 (м, 2H), 3,99-4,12 (м, 1H), 3,89 (уш.с, 1H), 3,74 (уш.с, 1H), 3,47 (уш.с, 2H), 3,17-3,27 (м, 1H), 2,42 (уш.с, 3H), 2,27 (уш.с, 1H).
1Н ЯМР (CDCl3): δ 8,54 (уш.с, 1H), 8,49 (уш.с, 1H), 7,62-7,68 (м, 1H), 7,53 (д, J=8,6 Гц, 2H), 7,37-7,44 (м, 5H), 7,29 (д, J=9,1 Гц, 2H), 7,23 (дд, J=7,8, 4,8 Гц, 1H), 4,17-4,32 (м, 2H), 4,09-4,17 (м, 3H), 4,00-4,08 (м, 1H), 3,89 (уш.с, 1H), 3,74 (уш.с, 1H), 3,47 (уш.с, 2H), 3,15-3,28 (м, 1H), 2,41 (уш.с, 3H), 2,17 (уш.с, 1H)
МС m/z (M+H+) 498,0
МС m/z (M+H+) 491,2
МС m/z (M+H+) 491,2
МС m/z (M+H+) 508,2
МС m/z (M+H+) 542,1
МС m/z (M+H+) 542,1
МС m/z (M+H+) 616,1
МС m/z (M+H+) 496,0
МС m/z (M+H+) 507,0
МС m/z (M+H+) 535,0
МС m/z (M+H+) 497,0
МС m/z (M+H+) 503,0
МС m/z (M+H+) 514,0
МС m/z (M+H+) 543,8
МС m/z (M+H+) 497,0
МС m/z (M+H+) 503,0
МС m/z (M+H+) 514,0
МС m/z (M+H+) 542,0
Пример 27а

E. Метил 4-((5-хлорпиридин-3-ил)метокси)бензойной кислоты, 27b. К охлажденному на ледяной бане раствору метил 4-гидроксибензойной кислоты 29а (2,35 ммоль, 358 мг), (5-хлорпиридин-3-ил)метанола 27а (1,57 ммоль, 225 мг) и Ph3P (2,35 ммоль, 616 мг) в 8 мл THF добавили DIAD (2,35 ммоль, 0,45 мл). Смесь перемешивали 1 час при 0°С и в течение ночи при комнатной температуре. Реакционную смесь разбавили водой, неочищенный продукт очистили колоночной флэш-хроматографией (силикагель, смесь 20% EtOAc/гексан), получив 27b (300 мг, 68%).
F. 4-((5-Хлорпиридин-3-ил)метокси)бензойная кислота, 27c. Соединение 27b (1,22 ммоль, 340 мг) смешали с LiOH (4,9 ммоль, 118 мг) в 3 мл THF, 3 мл MeOH и 3 мл воды. Смесь перемешивали 4 часа при комнатной температуре, добавили к ней 15% водный раствор лимонной кислоты, а затем экстрагировали EtOAc. Экстракты промыли водой и насыщенным раствором соли, высушили над Na2SO4, упарили в вакууме, получив 288 мг соединения 27c.
Следуя процедуре, описанной выше для примера 1 или примера 27, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 491,0
МС m/z (M+H+) 498,0
МС m/z (M+H+) 498,0
Пример 27b
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 482,0
МС m/z (M+H+) 488,0
МС m/z (M+H+) 499,0
МС m/z (M+H+) 535,0
Пример 28

A. Метил 4-(3-хлорбензилсульфанил)бензойной кислоты, 28b. Названное соединение 28c было получено способом, описанным в примере 27, с заменой соединения 27a на соединение 28a на стадии A.
B. 4-(3-Хлорбензилсульфанил)бензойная кислота, 28c. Названное соединение 28c было получено способом, описанным в примере 27, с заменой соединения 27c на соединение 28b на стадии B.
C. 4-(3-Хлорбензилсульфанил)бензоилхлорид, 28d. Названное соединение 28d было получено способом, описанным в примере 27, с заменой соединения 27d на соединение 28c на стадии C.
D. 1-[1-({4-[(3-Хлорбензил)сульфанил]фенил}карбонил)азетидин-3-ил]-4-(фенилкарбонил)пиперазин, соединение 410. Названное соединение 410 было получено способом, описанным в примере 27, с заменой соединения 27e на соединение 28d на стадии D. 1Н ЯМР (CDCl3): δ 7,52 (д, J=8,6 Гц, 2H), 7,37-7,44 (м, 5H), 7,24-7,29 (м, 3H), 7,18-7,24 (м, 3H), 4,18-4,33 (м, 2H), 4,09-4,17 (м, 3H), 4,01-4,08 (м, 1H), 3,92 (уш.с, 1H), 3,74 (уш.с, 1H), 3,35-3,63 (м, 2Н), 3,17-3,29 (м, 1H), 2,20-2,50 (м, 4Н); MC m/z (M+H+) 506,0.
Следуя процедуре, описанной выше для примера 28, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (CDCl3): δ 7,52 (д, J=8,3 Гц, 2H), 7,38-7,43 (м, 5H), 7,29 (д, J=8,6 Гц, 2H), 7,27 (д, J=7,1 Гц, 1H), 7,2 (д, J=7,4 Гц, 1H), 7,11 (к, J=7,8 Гц, 1H), 4,24-4,38 (м, 4H), 4,22 (уш.с, 1H), 4,12-4,21 (м, 1H), 4,02-4,12 (м, 1H), 3,91 (уш.с, 1H), 3,77 (уш.с, 1H), 3,47 (с, 2H), 3,15-3,29 (м, 1H), 2,44 (уш.с, 4H).
МС m/z (M+H+) 540,0
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,49-7,57 (м, 3H), 7,25-7,30 (м, 3H), 7,18-7,25 (м, 3H), 4,51 (уш.с, 2H), 4,21-4,34 (м, 2H), 4,03-4,21 (м, 4H), 3,72-3,94 (м, 2H), 3,18-3,29 (м, 1H), 2,35-2,59 (м, 4H).
МС m/z (M+H+) 513,0
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,0 Гц, 1H), 7,50-7,57 (м, 3H), 7,38 (дд, J=7,8, 1,5 Гц, 1H), 7,26-7,33 (м, 3H), 7,22 (дд, J=7,7, 1,4 Гц, 1H), 7,11 (т, J=7,8 Гц, 1H), 4,44 (уш.д, J=32,6 Гц, 2H), 4,22-4,35 (м, 4H), 4,15-4,22 (м, 1H), 4,04-4,15 (м, 1H), 3,85 (д, J=17,4 Гц, 2H), 3,19-3,29 (м, 1H), 2,37-2,56 (м, 4H).
МС m/z (M+H+) 547,0.
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,54 (д, J=3,3 Гц, 2H), 7,51-7,53 (м, 1H), 7,40 (д, J=2,0 Гц, 1H), 7,36 (д, J=8,3 Гц, 1H), 7,24-7,29 (м, 3H), 7,13-7,17 (м, 1H), 4,48-4,59 (м, 1H), 4,35-4,48 (м, 1H), 4,20-4,34 (м, 2H), 4,13-4,20 (м, 1H), 4,01-4,13 (м, 4H), 3,79-3,94 (м, 2H), 3,19-3,29 (м, 1H), 2,37-2,57 (м, 4H).
МС m/z (M+H+) 547,0.
1Н ЯМР (CDCl3): δ 7,87 (д, J=3,3 Гц, 1H), 7,55 (д, J=3,3 Гц, 1H), 7,53 (д, J=8,6 Гц, 2H), 7,27-7,29 (м, 2H), 7,24-7,27 (м, 4H), 4,51 (уш.с, 1H), 4,35-4,47 (м, 1H), 4,20-4,33 (м, 2H), 4,02-4,20 (м, 4H), 3,76-3,93 (м, 2H), 3,18-3,28 (м, 1H), 2,38-2,54 (м, 4H).
МС m/z (M+H+) 513,0
1Н ЯМР (CDCl3): δ 8,55 (с, 1H), 8,48 (с, 1H), 7,82-7,93 (м, 1H), 7,65 (уш.с, 1H), 7,47-7,60 (м, 3H), 7,18-7,36 (м, 3H), 4,44 (д, J=33,9 Гц, 2H), 4,03-4,32 (м, 5H), 3,86 (уш.с, 2H), 3,23 (уш.с, 1H), 2,47 (уш.с, 4H)
МС m/z (M+H+) 540,1
МС m/z (M+H+) 506,2
МС m/z (M+H+) 473,0
МС m/z (M+H+) 540,0
МС m/z (M+H+) 547,0
МС m/z (M+H+) 531,8
Пример 28а
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 532,0
Пример 29

A. Метил 4-(3-трифторметил-фенокси)-бензоат, 29c. К раствору соединения 29a (400 мг, 2,63 ммоль) и соединения 29b (1,0 г, 5,26 ммоль) в CH2Cl2 (24 мл) добавили Cu(OAc)2 (714 мг, 3,94 ммоль), сита 4Å (400 мг, порошок, активированный) и пиридин (2 мл) и Et3N (2 мл). Полученную реакционную смесь перемешивали при комнатной температуре в течение 2 дней. К смеси добавили воду и отфильтровали. Фильтрат экстрагировали с помощью EtOAc (3 раза), объединенные органические фазы высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией на силикагеле, элюируя с помощью 20% EtOAc/гексана, и получили соединение 29c (470 мг).
B. 4-(3-Трифторметилфенокси)-бензойная кислота, 29d. Смесь соединения 29c (577 мг, 1,95 ммоль) с LiOH (187 мг, 7,80 ммоль) в THF/MeOH/H2O (4/4/4 мл) перемешивали в течение 4 часов. Добавили 15% раствор лимонной кислоты (20 мл), затем смесь экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором, высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Остаток - соединение 29d - высушивали при пониженном давлении в течение 18 часов и использовали без очистки.
C. 4-(3-Трифторметилфенокси)-бензоилхлорид, 29e. К раствору соединения 29d (100 мг, 0,35 ммоль) в THF (2 мл) добавили по каплям оксалилдихлорид (46 мкл, 0,53 ммоль) при 0°C с последующим добавлением 2 капель DMF. Полученную смесь перемешивали при 0°C в течение 3 часов и оставили нагреваться до комнатной температуры в течение ночи. Растворитель удалили при пониженном давлении; остаток - соединение 29e - высушивали при пониженном давлении в течение 2 часов и затем использовали в следующей стадии без дополнительной очистки.
D. 1-(Фенилкарбонил)-4-[1-({4-[3-(трифторметил)фенокси]фенил}карбонил)азетидин-3-ил]пиперазин, соединение 419. К смеси соединения 2c (80 мг, 0,32 ммоль), Et3N (0,5 мл) и CH2Cl2 (2,5 мл) добавили раствор соединения 29e в CH2Cl2 (1 мл). Полученную смесь перемешивали при комнатной температуре в течение 4 часов. Растворитель удалили при пониженном давлении, полученный остаток растворили в CH2Cl2 (1 мл), загруженном непосредственно в колонку с силикагелем, очистили колоночной флэш-хроматографией на силикагеле, элюируя с помощью 5% MeOH/CH2Cl2, и получили соединение 419 (53 мг). 1Н ЯМР (CDCl3): δ 7,65 (д, J=8,6 Гц, 2H), 7,45-7,53 (м, 1H), 7,41 (уш.с, 6H), 7,25-7,34 (м, 1H), 7,17-7,25 (м, 1H), 7,01 (д, J=7,3 Гц, 2H), 4,17-4,38 (м, 3H), 4,11 (уш.с, 1H), 3,92 (уш.с, 1H), 3,78 (уш.с, 1H), 3,49 (уш.с, 2H), 3,19-3,32 (м, 1H), 2,45 (уш.с, 4H). МС m/z (M+H+) 510,0.
Следуя процедуре, описанной выше для примера 29, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,0 Гц, 1H), 7,64 (д, J=8,6 Гц, 2H), 7,55 (д, J=3,0 Гц, 1H), 7,33 (д, J=8,8 Гц, 2H), 6,98 (д, J=8,8 Гц, 4H), 4,52 (уш.с, 1H), 4,38-4,48 (уш.с, 1H), 4,15-4,37 (м, 3H), 4,10 (уш.с, 1H), 3,88 (уш.с, 1H), 3,82 (уш.с, 1H), 3,19-3,31 (м, 1H), 2,35-2,60 (м, 4H).
МС m/z (M+H+) 483,1
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,65 (тт, J1=2 Гц, J2=8,8 Гц, 2H), 7,545 (д, J=3,3 Гц, 1H), 7,26-7,30 (м, 1H), 7,14 (дт, J=8,1, 1,0 Гц, 1H), 6,98-7,06 (м, 3H), 6,93-6,95 (м, 1H), 6,91-6,95 (м, 1H), 4,56 (уш.с, 1H), 4,43 (уш.с, 1H), 4,17-4,38 (м, 3H), 4,04-4,16 (м, 1H), 3,75-3,96 (м, 2H), 3,20-3,31 (м, 1H), 2,39-2,60 (м, 4H).
МС m/z (M+H+) 483,0
1Н ЯМР (CDCl3): δ 7,65 (д, J=8,6 Гц, 2H), 7,37-7,46 (м, 6H), 7,12 (д, J=2,8 Гц, 1H), 7,00 (д, J=8,8 Гц, 2H), 6,89 (дд, J=8,8, 2,8 Гц, 1H), 4,16-4,37 (м, 3H), 4,10 (уш.с, 1H), 3,92 (уш.с, 1H), 3,68-3,84 (м, 1H), 3,46 (с, 2H), 3,19-3,30 (м, 1H), 2,44 (уш.с, 4H).
МС m/z (M+H+) 510,0
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,66 (д, J=8,8 Гц, 2H), 7,55 (д, J=3,3 Гц, 1H), 7,42 (д, J=8,8 Гц, 1H), 7,13 (д, J=2,8 Гц, 1H), 7,0 (д, J=8,6 Гц, 2H), 6,90 (дд, J=8,8, 2,8 Гц, 1H), 4,53 (уш.с, 1H), 4,44 (уш.с, 1H), 4,17-4,38 (м, 3H), 4,11 (дд, J=9,0, 4,7 Гц, 1H), 3,88 (уш.с, 1H), 3,83 (уш.с, 1H), 3,20-3,32 (м, 1H), 2,50 (т, J=4,7 Гц, 4H).
МС m/z (M+H+) 517,0
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,67 (д, J=8,6 Гц, 2H), 7,55 (д, J=3,0 Гц, 1H), 7,49 (т, J=8,0 Гц, 1H), 7,41 (д, J=7,8 Гц, 1H), 7,21 (д, J=8,1 Гц, 1H), 7,03 (д, J=8,6 Гц, 2H), 4,53 (уш.с, 1H), 4,44 (уш.с, 1H), 4,17-4,38 (м, 3H), 4,16-4,05 (м, 1H), 3,86 (д, J=19,2 Гц, 2H), 3,20-3,33 (м, 1H), 2,37-2,60 (м, 4H).
МС m/z (M+H+) 517,0
МС m/z (M+H+) 476,2
МС m/z (M+H+) 476,2
МС m/z (M+H+) 500,8
Пример 29а
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 485,8
Пример 30
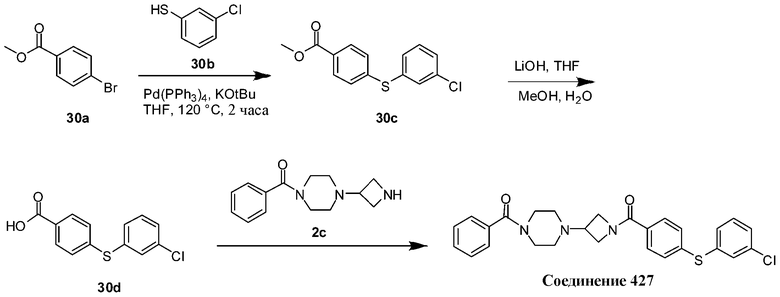
A. Метил 4-(3-хлорфенилсульфанил)-бензоат, 30c. Смесь соединения 30a (400 мг, 1,86 ммоль), соединения 30b (321 мг, 2,23 ммоль), Pd(PPh3)4 (215 мг, 0,186 ммоль), KOtBu (2,23 мл, 2,23 ммоль, 1-молярный раствор в THF) и THF (3,5 мл) нагревали в микроволновом реакторе при 130°C в течение 2 часов, а затем вылили в воду (50 мл). Смесь экстрагировали EtOAc (3 раза). Объединенные органические экстракты высушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией на силикагеле, элюируя с помощью 5% EtOAc/гексана, и получили соединение 30c (220 мг).
B. 4-(3-Хлорфенилсульфанил)бензойная кислота, 30d. Смесь соединения 30c (320 мг, 1,15 ммоль) и LiOH (110 мг, 4,59 ммоль) в THF/MeOH/H2O (3/3/3 мл) перемешивали в течение 4 часов. Добавили 15% водный раствор лимонной кислоты (10 мл). Затем смесь экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором, отфильтровали, высушили над Na2SO4 и сконцентрировали при пониженном давлении. Полученный остаток (соединение 30d, 290 мг) высушивали при пониженном давлении в течение 18 часов и использовали без дополнительной очистки.
C. 4-(1-{[4-(3-Хлорфенилсульфанил)фенил]карбонил}азетидин-3-ил)-1-(фенилкарбонил)-пиперазин, соединение 427. Смесь соединения 30d (60 мг, 0,23 ммоль), соединения 2c (83 мг, 0,29 ммоль) и HATU (129 мг, 0,34 ммоль) в Et3N и DMF (1 мл/3 мл) перемешивали в течение 18 часов, а затем вылили в воду (10 мл). Затем смесь экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором (2 раза), высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Полученный остаток очистили на силикагеле, элюируя 5% MeOH/CH2Cl2, и получили соединение 427 (33 мг). МС m/z (M+H+) 492,1.
Следуя процедуре, описанной выше для примера 30, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 499,1
МС m/z (M+H+) 499,1
МС m/z (M+H+) 526,2
МС m/z (M+H+) 533,1
МС m/z (M+H+) 533,1
Пример 30а
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 483,8
МС m/z (M+H+) 517,9
Пример 31
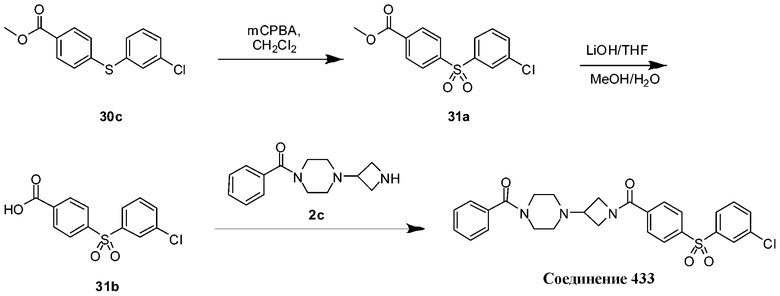
A. Метиловый эфир 4-(3-хлорбензолсульфонил)-бензойной кислоты, 31a.
К раствору соединения 30c (200 мг, 0,72 ммоль) в CH2Cl2 (5 мл) добавили mCPBA (320 мг, 1,43 ммоль) при 0°C. Через 2 часа смесь вылили в раствор 2Н KOH (20 мл) и экстрагировали EtOAc (3 раза). Объединенные органические экстракты высушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией на силикагеле, элюируя с помощью 5% EtOAc/гексана, и получили соединение 31a (138 мг).
B. 4-(3-Хлорбензолсульфонил)-бензойная кислота, 31b. Смесь соединения 31a (138 мг, 0,44 ммоль) и LiOH (42 мг, 1,77 ммоль) в THF/MeOH/H2O (2/2/2 мл) перемешивали в течение 4 часов. Добавили 15% раствор лимонной кислоты (10 мл). Затем смесь экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором, высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Полученный остаток - соединение 31b (130 мг) - высушивали при пониженном давлении в течение 18 часов и использовали без дополнительной очистки.
C. 1-[1-({4-[(3-Хлорфенил)сульфонил]фенил}карбонил)азетидин-3-ил]-4-(фенилкарбонил)пиперазин, соединение 433. Смесь соединения 31b (40 мг, 0,14 ммоль), соединения 2c (49 мг, 0,18 ммоль) и HATU (80 мг, 0,20 ммоль) в Et3N (1 мл) и DMF (2 мл) перемешивали в течение 18 часов, а затем вылили в воду (10 мл). Затем смесь экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором (2 раза), высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией на силикагеле, элюируя с помощью 5% MeOH/CH2Cl2, и получили соединение 428 (29 мг). МС m/z (M+H+) 524,1.
Следуя процедуре, описанной выше для примера 31, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 558,0
МС m/z (M+H+) 530,8
МС m/z (M+H+) 564,8
МС m/z (M+H+) 578,8
МС m/z (M+H+) 564,6
Пример 31а
Следуя процедуре, описанной выше для примера 31, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 31, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (CDCl3): δ 7,80-7,97 (м, 4H), 7,63-7,73 (м, 1H), 7,56 (дд, J=5,7, 2,4 Гц, 2H), 7,18 (д, J=8,1 Гц, 2H), 4,34-4,60 (м, 3H), 4,20-4,33 (м, 2H), 4,03-4,20 (м, 2H), 3,86 (уш.с, 2H), 3,15-3,32 (м, 1H), 2,37-2,60 (м, 4H).
МС m/z (M+H+) 578,8
МС m/z (M+H+) 572,0
1Н ЯМР (CDCl3): δ 7,88 (д, J=3,3 Гц, 1H), 7,65-7,77 (м, 4H), 7,52-7,65 (м, 2H), 7,35-7,52 (м, 2H), 7,24 (с, 1H), 4,39 (с, 4H), 4,17-4,33 (м, 2H), 4,12 (кв, J=7,1 Гц, 2H), 3,86 (уш.с, 2H), 3,19-3,34 (м, 1H), 2,38-2,59 (м, 4H).
МС m/z (M+H+) 578,8
МС m/z (M+H+) 578,6
Пример 31b
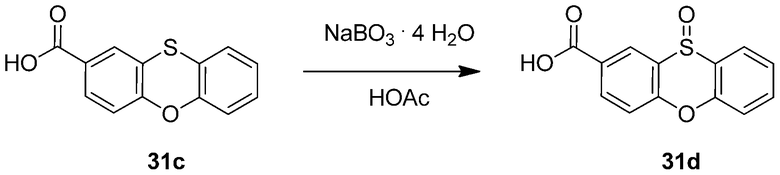
D. 10-Оксидфеноксатиин-2-карбоновая кислота, 31d. Смесь феноксатиин-2-карбоновой кислоты 31c (0,41 ммоль, 100 мг) и натрия пербората тетрагидрата (0,82 ммоль, 126 мг) в 3 мл HOAc перемешивали в течение 6 дней при комнатной температуре. ТСХ показала 90% превращение в соед. 31d. Добавили воду, полученный осадок отфильтровали и высушили, получив 65 мг соединение 31d 90% чистоты.
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 495,1
Пример 31c
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 516,8
МС m/z (M+H+) 550,5
МС m/z (M+H+) 563,8
Пример 32

трет-Бутил (3S)-3-[4-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)фенокси]пирролидин-1-карбоксилат, соединение 434. К раствору соединения 26d (100 мг, 0,273 ммоль) и (R)-N-Boc-3-гидроксипролина в THF добавили DIAD при 0°C. Полученную реакционную смесь перемешивали в течение 18 часов. После разбавления водой и экстрагирования с помощью EtOAc (3 раза) объединенные органические фазы высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Полученный остаток очистили колоночной флэш-хроматографией на силикагеле, используя 5% MeOH/CH2Cl2, и получили соединение 434 (95 мг). 1Н ЯМР (CDCl3): δ 7,52 (д, J=8,6 Гц, 2H), 7,37-7,44 (м, 5H), 7,24-7,29 (м, 3H), 7,18-7,24 (м, 3H), 4,18-4,33 (м, 2H), 4,09-4,17 (м, 3H), 4,01-4,08 (м, 1H), 3,92 (уш.с, 1H), 3,74 (уш.с, 1H), 3,35-3,63 (м, 2Н), 3,17-3,29 (м, 1H), 2,20-2,50 (м, 4Н); MC m/z (M+H+) 506,0.
Следуя процедуре, описанной выше для примера 32, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (CDCl3): δ 7,58 (д, J=8,8 Гц, 2H), 7,36-7,44 (м, 5H), 6,88 (д, J=8,8 Гц, 2H), 4,26-4,38 (м, 2H), 4,25-4,12 (м, 2H), 4,07 (уш.с, 1H), 3,82-3,99 (м, 1H), 3,48 (уш.с, 2H), 3,15-3,26 (м, 1H), 2,17-2,54 (м, 4H), 1,93-2,03 (м, 1H), 1,75-1,89 (м, 2H), 1,46-1,63 (м, 2H), 1,31-1,46 (м, 3H), 1,21-1,31 (м, 2H).
МС m/z (M+H+) 448,0
МС m/z (M+H+) 434,2
МС m/z (M+H+) 549,3
МС m/z (M+H+) 535,3
Пример 33
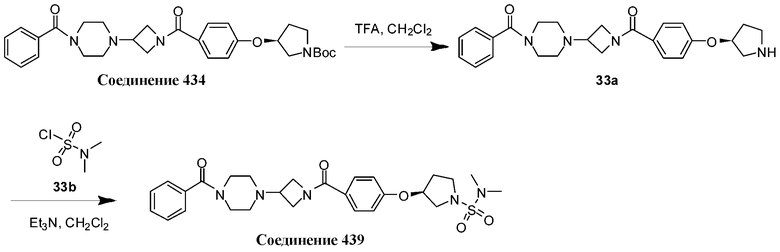
A. (3S)-3-[4-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)фенокси]пирролидин, 33a. К раствору соединения 434 (87,7 мг, 0,164 ммоль) в CH2Cl2 (1 мл) добавили TFA (0,5 мл). Полученную смесь перемешивали при комнатной температуре в течение 4 часов. Реакционную смесь сконцентрировали при пониженном давлении с получением соединения 33a, которое использовали без дополнительной очистки.
B. (3S)-N,N-диметил-3-[4-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)фенокси]пирролидин-1-сульфонамид, соединение 439. Раствор соединения 33a (0,164 ммоль) и Et3N (0,5 мл) в CH2Cl2 (2 мл) обработали N,N-диметилсульфамоилхлоридом (26 мкл, 0,246 ммоль) при комнатной температуре. Полученную смесь перемешивали в течение 3 часов, затем растворитель удалили при пониженном давлении. Полученный остаток загрузили непосредственно в колонку с силикагелем, очистили колоночной флэш-хроматографией на силикагеле, элюируя с помощью 5% MeOH/CH2Cl2, и получили соединение 439 (51,5 мг). 1Н ЯМР (CDCl3): δ 7,61 (д, J=8,21 Гц, 2H), 7,36-7,46 (м, 5H), 6,86 (д, J=8,6 Гц, 2H), 4,98 (м, 1H), 4,31 (уш.с, 1H), 4,11-4,26 (м, 2H), 4,05 (уш.с, 1H), 3,87-3,96 (м, 1H), 3,84 (м, 1H), 3,70-3,79 (м, 1H), 3,66 (дд, J=11,4, 4,8 Гц, 1H), 3,39-3,58 (м, 4H), 3,21-3,26 (м, 1H), 2,82 (с, 6H), 2,42 (уш.с, 4H), 2,19-2,29 (м, 2H); МС m/z (M+H+) 542,0.
Следуя процедуре, описанной выше для примера 33, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 553,3
МС m/z (M+H+) 491,3
МС m/z (M+H+) 539,3
МС m/z (M+H+) 545,3
МС m/z (M+H+) 539,3
МС m/z (M+H+) 519,3
МС m/z (M+H+) 506,3
МС m/z (M+H+) 568,3
МС m/z (M+H+) 532,3
МС m/z (M+H+) 548,3
Пример 34

A. трет-Бутил 3-(2-иод-4-метоксикарбонил-фенокси)-пирролидин-1-карбоксилат, 34b. К раствору соединения 34a (500 мг, 1,8 ммоль), соединения 32a (504 мг, 2,7 ммоль) и PPh3 (707 мг, 2,7 ммоль) в THF (10 мл) добавили DIAD (0,52 мл, 2,7 ммоль) при 0°C. Полученную смесь перемешивали при 0°C в течение 1 часа, а затем нагревали до комнатной температуры и перемешивали в течение 18 часов. Смесь вылили в воду и экстрагировали с помощью EtOAc (3 раза). Объединенные органические экстракты высушили над Na2SO4, отфильтровали и концентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией, элюируя с помощью 50% EtOAc/гексана, и получили соединение 34b (704 мг).
B. Метил 3-иод-4-[1-(пиролидин-1-карбонил)-пирролидин-3-ил-окси]-бензоат, 34d. К раствору соединения 34b (210 мг, 0,47 ммоль) в CH2Cl2 (3 мл) добавили TFA (1,5 мл) при комнатной температуре. Полученную смесь перемешивали при комнатной температуре в течение 4 часов. Растворитель удалили при пониженном давлении. Полученный остаток высушивали при пониженном давлении в течение 2 часов. К остатку добавили CH2Cl2 (3 мл) и Et3N (1 мл) с последующим добавлением соединения 34c (77 мкл, 0,7 ммоль). Полученную смесь перемешивали в течение 2 часов, затем вылили в воду (50 мл) и экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией, элюируя с помощью 80% EtOAc/гексана, и получили соединение 34d (180 мг).
C. 3-Йод-4-[1-(пирролидин-1-карбонил)-пирролидин-3-ил-окси]-бензойная кислота, 34e. Смесь соединения 34d (180 мг, 0,41 ммоль), LiOH (39 мг, 1,62 ммоль), THF (3 мл), MeOH (3 мл) и H2O (3 мл) перемешивали при комнатной температуре в течение 4 часов. Смесь подкислили 15% водным раствором лимонной кислоты и экстрагировали EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором, высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Полученный остаток высушивали при пониженном давлении в течение 2 часов с получением соединения 34e (166 мг).
D. 3-Йод-4-[1-(пирролидин-1-карбонил)-пирролидин-3-ил-окси]-бензоилхлорид, 34f. К раствору соединения 34e (166 мг, 0,39 ммоль) в THF (4 мл) добавили по каплям оксалилхлорид (43 мкл, 0,50 ммоль) при 0°C, а затем добавили 2 капли DMF. Полученную смесь перемешивали при 0°C в течение 3 часов, нагревали до комнатной температуры и перемешивали в течение 18 часов. Растворитель удалили при пониженном давлении. Полученный остаток - соединение 34f - высушивали при пониженном давлении в течение 2 часов и использовали в следующей стадии без дополнительной очистки.
E. 1-{1-[(3-Йод-4-{[(3S)-1-(пирролидин-1-ил-карбонил)пирролидин-3-ил]окси}фенил)карбонил]азетидин-3-ил}-4-(фенилкарбонил)пиперазин, соединение 450. К смеси соединения 2c (61 мг, 0,25 ммоль), Et3N (0,5 мл) и CH2Cl2 (2,5 мл) добавили раствор соединения 34f в CH2Cl2 (1 мл). Полученную смесь перемешивали при комнатной температуре в течение 2 часов. Растворитель удалили при пониженном давлении. Остаток растворили в CH2Cl2 (1 мл), загруженном непосредственно в колонку с силикагелем, и очистили колоночной флэш-хроматографией, элюируя с помощью 5% MeOH/CH2Cl2, получив соединение 451 (56 мг). 1Н ЯМР (CDCl3): δ 8,06 (д, J=2,3 Гц, 1H), 7,60 (дд, J=8,5, 2,1 Гц, 1H), 7,34-7,48 (м, 5H), 6,80 (д, J=8,6 Гц, 1H), 5,01 (уш.с, 1H), 3,66-4,36 (м, 8H), 3,28-3,64 (м, 8H), 3,12-3,27 (м, 1H), 2,05-2,56 (м, 6H), 1,55-1,97 (м, 4H).
Следуя процедуре, описанной выше для примера 34, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 632,2
МС m/z (M+H+) 665,2
Пример 35

A. Метил 4-[(3-хлорфенокси)метил]бензоат, 35c. К смеси соединения 35a (300 мг, 1,31 ммоль) и K2CO3 (400 мг, 2,88 ммоль) в DMF (1 мл) добавили соединение 35b (251 мг, 2,0 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 6 часов. Смесь вылили в воду (50 мл) и экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором, высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Полученный остаток очистили колоночной флэш-хроматографией на силикагеле, элюируя с помощью 20% EtOAc/гексана, и получили соединение 35c (340 мг).
B. 4-[(3-Хлорфенокси)метил]бензойная кислота, 35d. Смесь соединения 35c (340 мг, 1,18 ммоль) и LiOH (114 мг, 4,74 ммоль) в THF/MeOH/H2O (3/3/3 мл) перемешивали в течение 4 часов. Добавили 15% раствор лимонной кислоты (10 мл). Затем смесь экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором, высушили над Na2SO4 и сконцентрировали при пониженном давлении. Полученный остаток - соединение 35d (230 мг) - высушивали при пониженном давлении в течение 18 часов и использовали без дополнительной очистки.
C. 1-[1-({4-[(3-Хлорфенокси)метил]фенил}карбонил)азетидин-3-ил]-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 453. Смесь соединения 35d (77 мг, 0,29 ммоль), соединения 5e (108 мг, 0,38 ммоль) и HATU (165 мг, 0,44 ммоль) в Et3N (1 мл) и DMF (3 мл) перемешивали в течение 18 часов, а затем вылили в воду (10 мл). Затем смесь экстрагировали с помощью EtOAc (3 раза). Объединенные органические фазы промыли солевым раствором (2 раза), высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении. Полученный остаток очистили колоночной флэш-хроматографией, элюируя с помощью 5% MeOH/CH2Cl2, и получили соединение 453 (67 мг). МС m/z (M+H+) 497,1. 1Н ЯМР (CD3OD): δ 7,95 (д, J=2,0 Гц, 1H), 7,8 (д, J=2,0 Гц, 1H), 7,65 (д, J=8,1 Гц, 2H), 7,51 (д, J=8,1 Гц, 2H), 7,25 (т, J=8,0 Гц, 1H), 7,02 (с, 1H), 6,90-6,98 (м, 2H), 5,15 (с, 2H), 4,32-4,45 (м, 2H), 4,15-4,25 (м, 2H), 4,00-4,10 (м, 1H), 3,70-3,82 (уш.с, 2H), 2,47 (уш.с, 4H).
Следуя процедуре, описанной выше для примера 35, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 513,1
МС m/z (M+H+) 496,1
МС m/z (M+H+) 490,0
МС m/z (M+H+) 497,0
Пример 35а
Следуя процедуре, описанной выше для примера 35, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:
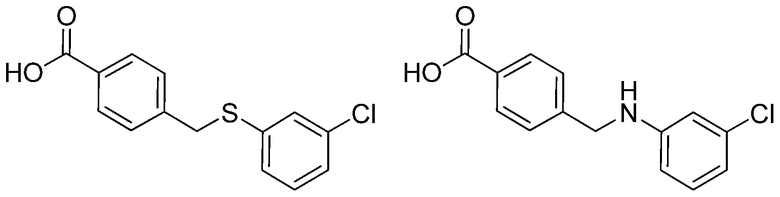
Следуя процедуре, описанной выше для примера 35 или примера 1, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 506,0
МС m/z (M+H+) 489,0
МС m/z (M+H+) 513,0
МС m/z (M+H+) 496,0
Пример 35b
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 498,0
МС m/z (M+H+) 481,0
Пример 36

1-(Фенилкарбонил)-4-{1-[(2-пирролидин-3-ил-фенил)карбонил]азетидин-3-ил}пиперазин, соединение 456. К раствору соединения 111 (300 мг, 0,58 ммоль) в 1,4-диоксане (10 мл) добавили 6Н HCl (3 мл). После перемешивания в течение 4 часов растворитель выпарили в вакууме. Остаток распределили между EtOAc и 3Н NaOH, органическую фазу отделили и высушили над MgSO4. Смесь профильтровали, фильтрат сконцентрировали при пониженном давлении, остаток очистили обращенно-фазовой ВЭЖХ с получением соединения 456 (52,3 мг). ЖХ/МС m/z (M+H+) 419,36 (рассчитано для C25H30N4O4, 418,54).
Пример 37
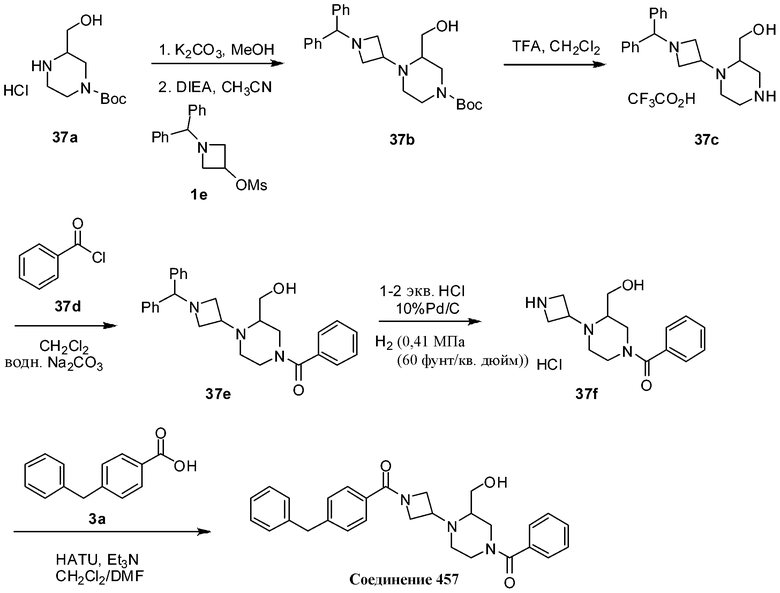
A. трет-Бутил 4-[1-(дифенилметил)азетидин-3-ил]-3-(гидроксиметил)пиперазин-1-карбоксилат, 37b. Соединение 37a (811 мг, 3,21 ммоль) добавили к одной части для перемешивания суспензии безводного K2CO3 (1,07 г, 7,9 ммоль) в MeOH (4 мл). Смесь перемешивали в течение 1,5 часов при комнатной температуре, затем удалили MeOH при пониженном давлении до почти сухого состояния. Полученную белую суспензию растерли в порошок с CH2Cl2 (40 мл) и профильтровали через пористую стеклянную воронку средней пористости. Сухой остаток промыли дополнительным количеством CH2Cl2, объединенные фильтраты сконцентрировали и высушили при пониженном давлении с получением соединения 37a (733 мг) в виде белого твердого вещества - свободного основания соли 37a и HCl.
Вещество суспендировали в CH3CN (8 мл) с соединением 1e (1,07 г, 3,37 ммоль). Добавили диизопропилэтиламин (1,23 мл, 7,06 ммоль) и нагревали смесь при 60°C в течение 14 часов. Добавили EtOAc (100 мл) и промыли органическую фазу водой (20 мл) и солевым раствором (20 мл), высушили над Na2SO4, отфильтровали и сконцентрировали при пониженном давлении с получением сырого остатка (1,42 г) в виде бледно-оранжевой пены. Вещество очистили жидкостной хроматографией среднего давления (ЖХСД), используя систему ISCO CombiFlash (силикагель, 10-50% EtOAc/гексан) с получением соединения 37b (979 мг) в виде белой пены. 1Н ЯМР (400 МГц, CDCl3): δ 7,39 (д, J=8,1 Гц, 4H), 7,23-7,33 (м, 4H), 7,14-7,23 (м, 2H), 4,34 (с, 1H), 3,28-3,58 (м, 8H), 2,76-2,95 (м, 2H), 2,26-2,75 (м, 4H), 2,20 (дт, J=12,3, 4,9 Гц, 1H), 1,44 (с, 9H); ЖХ/МС m/z (M+H+) 438,5, (M+Na+) 460,5.
B. {1-[1-(Дифенилметил)азетидин-3-ил]-пиперазин-2-ил}метанол, 37c. Соединение 37b (450 мг, 1,03 ммоль) растворили в CH2Cl2 (6 мл) и TFA (3 мл) и перемешивали при 20°C в течение 2,5 часов. Реакционную смесь сконцентрировали при пониженном давлении до сухого состояния с получением TFA-соли соединения 37c в виде оранжевой пены. Соединение 37c использовали в следующей стадии без дополнительной очистки. МС m/z (M+H+) 338,2.
C. {1-[1-(Дифенилметил)азетидин-3-ил]-4-(фенилкарбонил)пиперазин-2-ил}метанол, 37e. Соединение 37c (1,03 ммоль) растворили в CH2Cl2 (5 мл) и охладили при 0°C в емкости с ледяной водой. Добавили 10%-ный водный раствор Na2CO3 (5 мл) и добавили по каплям раствор соединения 37d (143 мкл, 1,23 ммоль), растворенного в CH2Cl2 (1 мл). Полученную смесь оставили до повышения ее температуры до 20°C, а затем интенсивно перемешивали в течение 62 часов. К реакционной смеси добавили CH2Cl2 (10 мл), затем водную фазу экстрагировали с помощью CH2Cl2 (2×20 мл). Объединенные органические фазы промыли солевым раствором, высушили над Na2SO4, отфильтровали и сконцентрировали с получением соединения 37e (465 мг) в виде белой пены. Соединение 37e использовали в следующей стадии без дополнительной очистки. 1Н ЯМР (400 МГц, CDCl3): δ 7,39 (м, 9H), 7,22-7,32 (м, 4H), 7,14-7,23 (м, 2H), 4,35 (с, 1H), 4,07 (уш.с, 1H), 3,30-3,71 (комплекс, 8H), 2,2-3,0 (комплекс, 6H); ЖХ/МС m/z (M+H+) 442,2.
D. [1-Азетидин-3-ил-4-(фенилкарбонил)пиперазин-2-ил]метанол, 37f. Соединение 37e (450 мг, 1,02 ммоль) поместили в 500 мл реактор Парра и растворили в абсолютном EtOH (6 мл). Добавили 12 Н концентрированного HCl (95 мкл, 1,14 ммоль), емкость продули N2. Добавили 10% Pd/C (264 мг) и встряхивали смесь при 0,41 МПа (60 фунт/кв. дюйм) H2 в течение 14 часов. Затем добавили дополнительное количество 10% Pd/C (430 мг) и снова встряхивали при 0,41 МПа (60 фунт/кв. дюйм) H2 в течение еще 5 часов. Смесь профильтровали через диатомитовую прокладку, сухой остаток тщательно промыли с помощью MeOH. Фильтрат сконцентрировали при пониженном давлении до сухого состояния с получением первичного соединения 37f в виде вязкой маслянистой жидкости (428 мг), которое использовали в следующей стадии без дополнительной очистки. ЖХ/МС m/z (M+H+) 276,3.
E. [1-{1-[(4-Бензилфенил)карбонил]азетидин-3-ил}-4-(фенилкарбонил)пиперазин-2-ил]метанол, соединение 457. Соединение 3a (142 мг, 0,67 ммоль) и HATU (256 мг, 0,67 ммоль) суспендировали в CH2Cl2 (1 мл) и DMF (0,2 мл). Добавили Et3N (195 мкл, 1,4 ммоль) и перемешивали раствор в течение 15 минут при 20°C. Первичное соединение 37f (214 мг, приблизительно 0,56 ммоль) растворили в смеси 1:1 CH2Cl2/DMF (3 мл) и добавили по частям к раствору соединения 3a, после чего смесь перемешивали в течение 64 часов. Органический раствор разбавили EtOAc (50 мл) и промыли последовательно водой (3×10 мл) и солевым раствором (10 мл). Органическую фазу высушили над Na2SO4, отфильтровали, фильтрат сконцентрировали при пониженном давлении с получением желтой маслянистой жидкости (310 мг). Первичное масло очистили при помощи ЖХСД (картридж Silicycle SiO2 4 г, 15-80% ацетон/гексан) с получением соединения 457 в виде белой пены (104 мг). 1Н ЯМР (400 МГц, CDCl3) δ 7,53 (д, J=7,8 Гц, 2H), 7,42 (уш.с, 5H), 7,11-7,37 (м, 7H), 4,26 (м, 5H), 4,00 (с, 2H), 3,71-3,89 (м, 1H), 3,54-3,71 (м, 3H), 3,25-3,54 (м, 3H), 2,92 (уш.с, 1H), 2,64 (уш.с, 1H), 2,41 (уш.с, 1H); ЖХ/МС m/z (M+H+) 470,5.
Следуя процедуре, описанной выше для примера 37, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 7,65-7,73 (м, 2H), 7,61 (дд, J=11,6, 8,1 Гц, 4H), 7,33-7,50 (м, 10H), 3,96-4,49 (м, 5H), 3,76-3,91 (м, 1H), 3,63 (м, 3H), 3,32-3,53 (м, 1H), 2,95 (уш.с, 1H), 2,64 (уш.с, 1H), 2,45 (уш.с, 1H)
ЖХ/МС m/z (M+H+) 456,5
1Н ЯМР (400 МГц, CDCl3): δ 7,55 (д, J=8,1 Гц, 2H), 7,35-7,46 (м, 5H), 7,10-7,34 (м, 7H), 4,82 (уш.с, 1H), 4,01 (с, 2H), 3,72-4,40 (м, 5H), 3,52 (уш.с, 1H), 3,16 (уш.с, 1H), 2,54-3,04 (м, 2H), 1,93-2,30 (м, 4H)
ЖХ/МС m/z (M+H+) 470,5
1Н ЯМР (400 МГц, CDCl3): δ 7,67-7,75 (д, J=8,3 Гц, 2H), 7,55-7,67 (м, 4H), 7,34-7,52 (м, 8H), 3,39-4,96 (м, 9H), 3,20 (квин, 1H), 2,51-3,05 (м, 3H), 2,22 (уш.с, 1H), 2,04 (уш.с, 1H)
ЖХ/МС m/z (M+H+) 456,5
Пример 38

4,4,4-Трифтор-N-[4-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)фенил]бутанамид, соединение 497. Смесь соединения 495 (65 мг, получено в соответствии с примером 9), 4,4,4-трифторбутановой кислоты (30 мг), HATU (116 мг) и TEA (0,12 мл) в DCM (1,5 мл) перемешивали при комнатной температуре в течение 5 часов. Реакционную смесь разбавили DCM и водой. Стандартное выполнение с последующей хроматографией привели к получению соединения 497 (71 мг). МС m/z (M+H+) 489,5.
Следуя процедуре, описанной выше для примера 38, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 483,6
МС m/z (M+H+) 475,6
МС m/z (M+H+) 463,6+
МС m/z (M+H+) 469,2
Пример 39

A. N-(Нафталин-2-илметил)-4-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)анилин, соединение 495. Соединение 496 растворили в CH2Cl2 и TFA и перемешали при 20°C. Реакционную смесь сконцентрировали при пониженном давлении до сухого состояния с получением соединения 495, которое использовали в следующей реакции без дальнейшей очистки. МС m/z (M+H+) 365.
B. N-(Нафталин-2-илметил)-4-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)анилин, соединение 491. Смесь соединения 495 (100 мг, 0,27 ммоль), соединения 39a (75 мг, 0,48 ммоль) и AcOH (0,5 мл) в 1,2-дихлорэтане (3 мл) перемешивали в течение 1 часа, а затем добавили NaBH(OAc)3 (136 мг, 0,64 ммоль). Полученную смесь перемешивали в течение ночи, после чего вылили в 2Н водного раствора KOH (20 мл) и экстрагировали с помощью EtOAc. Объединенные фазы высушили над Na2SO4 и сконцентрировали при пониженном давлении. Остаток очистили колоночной флэш-хроматографией, элюируя с помощью 5% MeOH/CH2Cl2, и получили 33,2 мг соединения 491. 1Н ЯМР (400 МГц, CDCl3): δ 7,75-7,85 (м, 4H), 7,43-7,53 (м, 5H), 7,35-7,42 (м, 5H), 6,61 (д, J=8,8 Гц, 2H), 4,64 (уш.с, 1H), 4,51 (с, 2H), 4,27 (уш.с, 1H), 4,08-4,35 (м, 3H), 4,02 (с,1H), 3,89 (с, 1H), 3,71 (уш.с, 1H), 3,34-3,55 (м, 2H), 3,10-3,22 (м, 1H), 2,13-2,49 (м, 3H); МС m/z (M+H+) 505,3.
Следуя процедуре, описанной выше для примера 39, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС (m/z) (M+H+) 489,2
МС (m/z) (M+H+) 523,2
МС (m/z) (M+H+) 541,2
Пример 40

1-(1,3-Тиазол-4-ил-карбонил)-4-(1-{[(1RS,2RS)-2-{4-[(трифторметил)сульфанил]фенил}циклопропил]карбонил}азетидин-3-ил)пиперазин, соединение 645 (рацемическое, транс). Триметилсульфоксония йодид 40a (1,15 ммоль, 253 мг) и гидрид натрия (60% дисперсия в минеральном масле, 1,1 ммоль, 44 мг) соединили в 3 мл высушенного DMSO и перемешивали 20 минут при комнатной температуре. К смеси добавили соединение 648, полученное в примере 5, и перемешивали ее при комнатной температуре в течение 15 минут, затем нагревали при 50°C в течение ночи. После охлаждения смесь распределили между EtOAc и водой, органический слой отделили и сконцентрировали с получением первичного продукта, который очистили препаративной обращенно-фазовой хроматографией с получением 9,1 мг(2%) соединения 645 в виде моно-соли TFA. МС m/z (M+H+) 497,2.
Следуя процедуре, описанной выше для примера 40, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, было получено следующее соединение, составляющее предмет настоящего изобретения:
МС m/z (M+H+) 431,1
Пример 41
Данная страница оставлена пустой намеренно
Пример 42

A. Метил 4-(4-(трифторметил)бензил)бензоат, 42b. Через смесь метил 4-бромбензоата 42a (9,3 ммоль, 2,0 г), 2 мл THF и 4-трифторметилбензилцинкхлорида (0,5 M в THF, 46,5 ммоль, 93 мл) в течение 5 минут пропускали аргон. Добавили Pd(dffp)Cl2·CH2Cl2(0,5 моль, 409 мг), реакционную трубку запечатали и нагревали при 70°C в течение 16 часов. Смесь охладили и профильтровали через целит. К фильтрату добавили воду, полученный осадок отфильтровали. Органический раствор высушили над MgSO4 и сконцентрировали. Полученный продукт очистили флэш-хроматографией (силикагель, 0-10% EtOAc в гептане) и получили 1,5 г (55%) метил 4-(4-(трифторметил)бензил)бензоата, 42b.
B. 4-(4-(Трифторметил)бензил)бензойная кислота, 42c. Следуя процедуре, описанной для примера 9i, стадия P, метил 4-(4-(трифторметил)бензил)бензоат 42b (1,5 г, 5,1 ммоль) преобразовали в 1,31 г (92%) метил 4-(4-(трифторметил)бензил)бензойной кислоты, 42c. МС m/z (M+H+) 279,1.
Следуя процедуре, описанной выше для примера 42, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:
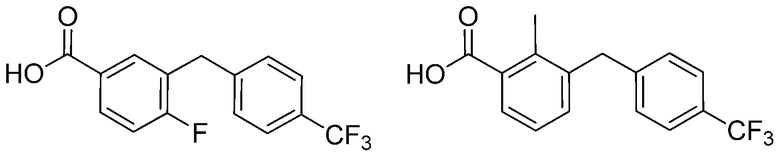
Промежуточные соединения были получены одним из альтернативных способов:

C. Метил 4-(4-(трифторметил)бензил)бензоат, 42b. Смесь метилового эфира 4-бромметил-бензойной кислоты 42d (1,0 г, 4,37 ммоль), 4-трифторфенилборной кислоты 42e (0,995 г, 5,24 ммоль) и Pd(PPh3)4 (50 мг, 0,044 ммоль) в диоксане (15 мл) перемешивали при комнатной температуре в течение 1 минуты, затем добавили 4 мл 2 М водного раствора Na2CO3. Полученный раствор нагревали при 90°C в течение 5 часов, затем охладили до комнатной температуры. К реакционной смеси добавили EtOAc и воду. Органические продукты сконцентрировали и очистили флэш-хроматографией (силикагель, 5% EtOAc/гексан) с получением метил 4-(4-(трифторметил)бензил)бензоата, 42b.
Следуя процедуре, описанной выше для примера 2, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 9,23 (с, 1H), 8,44 (с, 1H), 8,0-7,8 (м, 2H), 7,76-7,63 (м, 2H), 7,5 (д, 1H), 7,44-7,32 (м, 3H), 4,9-4,7 (м, 3H), 4,3-4,2 (м, 2H), 4,19-4,04 (м, 3H)
МС m/z (M+H+) 515,1
1Н ЯМР (400 МГц, CDCl3): δ 8,12 (м, 2H), 7,68 (м, 2H), 7,5 (м, 2H), 7,4 (м, 4H), 4,85 (уш.с, 2H), 4,47-4,26 (уш.м, 3H), 3,52 (уш.с, 4H), 3,02 (уш.с, 2H).
МС m/z (M+H+) 495,1
МС m/z (M+H+) 533,1
МС m/z (M+H+) 529,2
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 526,1
1Н ЯМР (400 МГц, CDCl3): δ 7,89 (с, 1H), 7,78 (с, 1H), 7,50 (м, 5H), 7,82 (м, 2H), 7,12 (т, 1H), 4,69 (уш.м, 2H), 4,48 (уш.м, 2H), 4,32 (уш.м, 2H), 4,0 (с, уш.м, 5H), 3,5 (уш.м, с, 2H)
МС m/z (M+H+) 533,1
МС m/z (M+H+) 529,2
МС m/z (M+H+) 529,2
МС m/z (M+H+) 511,2
МС m/z (M+H+) 529,2
МС m/z (M+H+) 529,2
MC m/z 515 (M+H+)
МС m/z (M+H+) 515
МС m/z (M+H+) 515
МС m/z (M+H+) 515
МС m/z (M+H+) 508
МС m/z (M+H+) 508
Пример 43

A. Метил 3-(4-фторбензоил)-1H-индол-6-карбоксилат, 43c. Раствор 4-фторбензоилхлорида 43b (2 ммоль, 0,24 мл) в 8 мл DCE по каплям добавили к ледяному раствору метил-1H-индол-6-карбоксилата 43a (1,43 ммоль, 250 мг) и диэтилалюминийхлорида (1 М в гексане, 1,86 ммоль, 1,86 мл) в 8 мл DCE. После выстаивания 2 часа при 0°C смесь нагрели до комнатной температуры и перемешивали в течение ночи. К смеси добавили pH 7-буффер, полученный осадок отфильтровали и промыли CH2Cl2 с получением 162 мг (38%) метил 3-(4-фторбензоил)-1H-индол-6-карбоксилата 43c. МС m/z (M+H+) 298,0.
B. 3-(4-Фторбензоил)-1H-индол-6-карбоновая кислота, 43d. Следуя процедуре, описанной для примера 9i, стадия P, получили 110 мг (72%) 3-(4-фторбензоил)-1H-индол-6-карбоновой кислоты.
Следуя процедуре, описанной выше для примера 43, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 518,2
МС m/z (M+H+) 542,1
МС m/z (M+H+) 535,0
МС m/z (M+H+) 501,0
Пример 44

A. Метил 4-(пиридин-2-ил-окси)-бензоат, 44b. Смесь 29a (433 мг, 2,85 ммоль), 44a (300 мг, 1,90 ммоль), Cu(biPy)2BF4 (88 мг, 0,19 ммоль), K3PO4 (805 мг, 3,80 ммоль) и DMF (1,5 мл) нагревали при 140°C в течение 1 часа. Через 0,5 часа смесь вылили в воду (60 мл) и экстрагировали с помощью EtOAc. Объединенные фазы промыли солевым раствором, высушили над Na2SO4 и сконцентрировали. Первичный продукт очистили колоночной флэш-хроматографией (силикагель, 20% EtOAc/гексан) с получением 298 мг 44b.
B. 4-(Пиридин-2-ил-окси)-бензойная кислота, 44c. Смесь 44b (430 мг, 1,87 ммоль), LiOH (180 мг, 7,5 ммоль), THF (3 мл), MeOH (3 мл) и H2O (3 мл) перемешивали при комнатной температуре в течение 4 часов. Затем реакционную смесь подкислили 15% лимонной кислотой (10 мл). Смесь экстрагировали с помощью EtOAc. Органический слой промыли солевым раствором, высушили над Na2SO4 и сконцентрировали с получением 44c (350 мг).
C. 1-(1-{[4-(Пиридин-2-ил-окси)фенил]карбонил}азетидин-3-ил)-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 913. Смесь соединений 44c (60 мг, 0,28 ммоль), 5e (105 мг, 0,36 ммоль), HATU (159 мг, 0,42 ммоль), Et3N (1 мл) и DMF (3 мл) перемешивали при комнатной температуре в течение ночи, а затем вылили в воду (10 мл). Смесь экстрагировали с помощью EtOAc. Экстракты промыли солевым раствором, высушили над Na2SO4 и сконцентрировали. Остаток очистили колоночной флэш-хроматографией (силикагель, 7% MeOH/CH2Cl2) с получением 98 мг соединения 913. МС m/z (M+H+) 450,0.
Следуя процедуре, описанной выше для примера 44, стадии A и B, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения.

Следуя процедуре, описанной выше для примера 44, стадия C, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
МС m/z (M+H+) 443,0
МС m/z (M+H+) 545,0
МС m/z (M+H+) 497,0
МС m/z (M+H+) 443,0
МС m/z (M+H+) 500,8
МС m/z (M+H+) 551,8
МС m/z (M+H+) 450,0
МС m/z (M+H+) 480,0
МС m/z (M+H+) 522,8
МС m/z (M+H+) 461,0
МС m/z (M+H+) 477,0
МС m/z (M+H+) 477,0
МС m/z (M+H+) 504,0
МС m/z (M+H+) 511,0
МС m/z (M+H+) 529,8
МС m/z (M+H+) 529,8
МС m/z (M+H+) 468,0
МС m/z (M+H+) 484,0
МС m/z (M+H+) 484,0
МС m/z (M+H+) 468,0
МС m/z (M+H+) 518,0
Пример 44а
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 503,0
МС m/z (M+H+) 435,0
МС m/z (M+H+) 512,8
МС m/z (M+H+) 536,8
Пример 44b
Следуя процедуре, описанной выше для примера 1, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
МС m/z (M+H+) 450,0
МС m/z (M+H+) 484,0
МС m/z (M+H+) 468,0
МС m/z (M+H+) 518,0
МС m/z (M+H+) 551,8
Пример 45

A. Метил 6-(3-хлорфенокси)-никотинат, 5c. Смесь соединений 45a (200 мг, 0,926 ммоль), 45b (178 мг, 1,39 ммоль), Cu(biPy)2BF4 (43 мг, 0,09 ммоль), K3PO4 (392 мг, 1,85 ммоль) и DMF (1,0 мл) нагревали при 140°C в течение 1 часа. Затем реакционную смесь вылили в воду (30 мл) и экстрагировали с помощью EtOAc. Экстракты промыли солевым раствором, высушили над Na2SO4 и сконцентрировали. Первичный продукт очистили колоночной флэш-хроматографией (силикагель, 20% EtOAc /гексан) с получением 202 мг 45c.
B. 6-(3-Хлорфенокси)-никотиновая кислота, 5d. Смесь 45c (202 мг, 0,766 ммоль), LiOH (74 мг, 3,06 ммоль), THF (2 мл), MeOH (2 мл) и H2O (2 мл) перемешивали при комнатной температуре в течение 4 часов. Реакционную смесь подкислили 15% лимонной кислотой (10 мл), а затем экстрагировали с помощью EtOAc. Экстракты промыли солевым раствором, высушили над Na2SO4 и сконцентрировали, получив 177 мг соединение 45d.
C. 1-(1-{[6-(3-Хлорфенокси)пиридин-3-ил]карбонил}азетидин-3-ил)-4-(фенилкарбонил)пиперазин, соединение 519. Смесь соединений 45d (60 мг, 0,24 ммоль), 2c (101 мг, 0,36 ммоль), HATU (137 мг, 0,36 ммоль), Et3N (0,5 мл) и DMF (3 мл) перемешивали при комнатной температуре в течение ночи. Смесь влили в воду (30 мл) и экстрагировали с помощью EtOAc. Экстракты промыли солевым раствором, высушили над Na2SO4 и сконцентрировали. Полученный остаток очистили колоночной флэш-хроматографией (силикагель, 5% MeOH/CH2Cl2), получив 50 мг соединения 519. 1Н ЯМР (CDCl3): δ 8,35-8,49 (м, 1H), 8,06 (дд, J=8,5, 2,1 Гц, 1H), 7,32-7,49 (м, 6H), 7,14-7,27 (м, 2H), 6,94-7,11 (м, 2H), 4,24 (уш.с, 1H), 4,15 (уш.с, 2H), 4,00-4,14 (м, 2H), 3,65-3,94 (м, 2H), 3,37-3,60 (м, 2H), 3,16-3,33 (м, 1H), 2,44 (уш.с, 4H). МС m/z (M+H+) 477,0.
Следуя процедуре, описанной выше для примера 45, стадии A и B, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения.

Следуя процедуре, описанной выше для примера 45, стадия C, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
МС m/z (M+H+) 511,0
МС m/z (M+H+) 477,0
МС m/z (M+H+) 484,0
МС m/z (M+H+) 518,0
МС m/z (M+H+) 484,0
МС m/z (M+H+) 536,0
Пример 45а
Следуя процедуре, описанной выше для примера 1, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
МС m/z (M+H+) 504,0
МС m/z (M+H+) 518,0
МС m/z (M+H+) 484,0
Пример 46
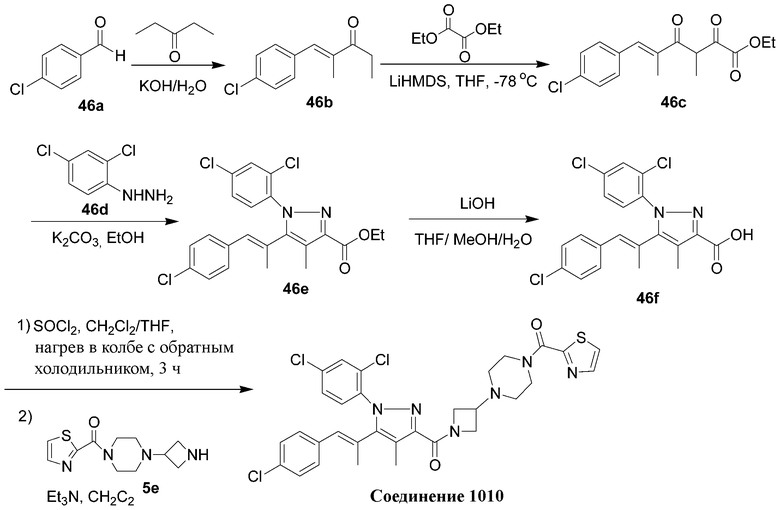
A. 1-(4-Хлорфенил)-2-метилпентен-1-3-он, 46b. К раствору 4-хлорбензальдегида 46a (99,6 ммоль, 14 г) в воде (44 мл) добавили KOH (44,6 ммоль, 2,5 г). Смесь нагревали при 65°C в течение 10 минут и по каплям добавляли 3-пентанон (99,6 ммоль, 8,58 г). После нагревания в колбе с обратным холодильником в течение 8 часов реакционную смесь охладили до комнатной температуры и перемешивали в течение ночи. Затем добавили 260 мл 1Н водного HCl и полученную смесь экстрагировали с помощью EtOAc. Органический слой высушили над Na2SO4 и сконцентрировали. Полученный продукт очистили колоночной флэш-хроматографией (силикагель, 5% EtOAc/гептан), получив 8,59 г соединения 46b.
B. Этил 6-(4-хлорофенил)-3,5-диметил-2,4-диоксогексен-5-ат, 46c. В раствор LiHMDS (1Н раствора в THF, 5,48 ммоль, 5,17 мл) в THF (16 мл) при температуре -78°C по каплям добавили раствор 46b (4,98 ммоль, 1,04 г) в THF (2,5 мл). После перемешивания при температуре -78°C в течение 1 часа смесь обработали раствором диэтилоксалата (4,98 ммоль, 0,73 г) в THF (2,5 мл). После перемешивания при температуре -78°C в течение 1 часа смесь нагрели до комнатной температуры и перемешивали в течение ночи. Растворитель испарили, а полученный продукт поместили в EtOAc и промыли в 1Н HCl и соляном растворе. Органический слой высушили над Na2SO4 и сконцентрировали, получив 1,5 г соединение 46c.
С. 5-[2-(4-Хлорофенил)-1-метилвинил]-1-(2,4-дихлорофенил)-4-метил-1H-пиразол-3-карбоксилат, 46e. Смесь 46c (15,6 ммоль, 4,82 г), 2,4-дихлорфенилгидразина 46d (17,2 ммоль, 3,67 г), K2CO3 (17,2 ммоль, 2,37 г) и EtOH (137 мл) перемешивали при температуре 70°C в течение ночи. Выпавший твердый осадок отфильтровали и промыли в EtOH. Фильтраты сконцентрировали и очистили колоночной флэш-хроматографией (силикагель, 5% EtOAc/гептан), получив 2,25 г соединение 46e.
D. 5-[2-(4-Хлорофенил)-1-метилвинил]-1-(2,4-дихлорофенил)-4-метил-1H-пиразол-3-карбоновая кислота, 46f. Смесь соединения 46e (3,34 ммоль, 1,5 г), LiOH (13,3 ммоль, 319 мг), THF (7 мл), MeOH (7 мл) и H2O (37 мл) перемешивали при комнатной температуре в течение 4 часов. Смесь подкислили 1Н HCl до pH=5 и экстрагировали с помощью EtOAc. Органический слой высушили над Na2SO4 и сконцентрировали, получив соединение 46f (202 мг).
E. 5-[2-(4-Хлорфенил)-1-метилвинил]-1-(2,4-дихлорфенил)-4-метил-1H-пиразол-3-карбоновая кислота, соединение 1010. К раствору 46f (0,138 ммоль, 60 мг) в CH2Cl2 и THF добавили SOCl2 (2Н раствора в THF, 0,414 ммоль, 0,212 мл). После нагревания в колбе с обратным холодильником в течение 4 часов смесь сконцентрировали и высушили в вакууме в течение 1 часа. В другую колбу добавили 5e (0,18 ммоль, 52 мг), CH2Cl2 (3 мл) и диизопропилэтиламин (0,69 ммоль, 0,12 мл). К этому раствору добавили полученный продукт из реакции SOCl2, растворенный в CH2Cl2 (1 мл). После перемешивания при комнатной температуре в течение 1 часа смесь разбавили CH2Cl2 (15 мл), промыли водным раствором 3Н NaOH (30 мл) и соляным раствором (30 мл), высушили над Na2SO4 и сконцентрировали. Первичный продукт очистили колоночной флэш-хроматографией (силикагель, 4% MeOH/CH2Cl2) с получением 74 мг соединения 1010. 1Н ЯМР (CDCl3): δ 7,87 (д, J=3,5 Гц, 1H), 7,55 (т, J=2,3 Гц, 2H), 7,33-7,36 (м, 2H), 7,30 (д, J=8,6 Гц, 2H), 7,13 (д, J=8,6 Гц, 2H), 6,41 (с, 1H), 4,49-4,62 (м, 2H), 4,41 (дд, J=10,4, 5,3 Гц, 2H), 4,22 (дд, J=10,0, 7,2 Гц, 1H), 4,04-4,10 (м, 1H), 3,87 (уш.с, 1H), 3,82 (уш.с, 1H), 3,18-3,26 (м, 1H), 2,41-2,58 (м, 4H), 2,39 (с, 3H), 1,88 (с, 3H). МС m/z (M+H+) 657,0.
Следуя процедуре, описанной выше для примера 46 (стадии A-D или B-D), и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения.

Следуя процедуре, описанной выше для примера 46 (стадия E) или для примера 1, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
МС m/z (M+H+) 639,2
МС m/z (M+H+) 669,0
МС m/z (M+H+) 651,2
МС m/z (M+H+) 671,0
МС m/z (M+H+) 651,2
МС m/z (M+H+) 645,2
МС m/z (M+H+) 627,2
МС m/z (M+H+) 669,1
МС m/z (M+H+) 545,2
Пример 46а
Следуя процедуре, описанной выше для примера 1c, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 642,9
МС m/z (M+H+) 654,0
МС m/z (M+H+) 654,1
МС m/z (M+H+) 530,2
Пример 47
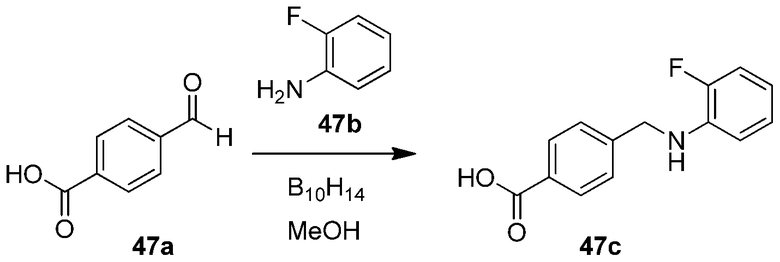
4-(((2-Фторфенил)амино)метил)бензойная кислота, 47c. Смесь 4-формилбензойной кислоты 47a (3,33 ммоль, 500 мг), 2-фтороанилина 47b (3,33 ммоль, 370 мг) и декаборана (1 ммоль, 122 мг) в 8 мл MeOH перемешивали при комнатной температуре в течение 15 минут. Полученную смесь сконцентрировали и очистили с помощью препаративной хроматографии на обращенной фазе, получив 0,81 г (99%) соединения 47c.
Следуя процедуре, описанной выше для примера 47, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения.

Следуя процедуре, описанной выше для примера 1 или примера 9, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
МС m/z (M+H+) 473,1
МС m/z (M+H+) 520,2
МС m/z (M+H+) 483,2
МС m/z (M+H+) 473,1
МС m/z (M+H+) 491,0
МС m/z (M+H+) 581,0
МС m/z (M+H+) 509,2
МС m/z (M+H+) 480,3
Пример 48
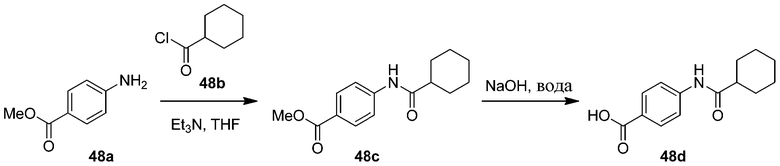
4-(Циклогексанкарбоксамидо)бензойная кислота, 48d. Смесь 4-аминобензойной кислоты 48a (1,98 ммоль, 300 мг), циклогексанкарбонилхлорида 48b (1,98 ммоль, 291 мг) и Et3N (2,52 ммоль, 0,43 мл) в 6 мл THF перемешивали при комнатной температуре в течение ночи. 1Н водного раствора NaOH (7,9 ммоль, 7,9 мл) добавили к смеси (содержащей метил 4-(циклогексанкарбоксамидо)бензоат (48c). Реакционную смесь перемешивали при комнатной температуре в течение 5 часов. THF удалили ротационным выпариванием, затем для выделения продукта добавили 1Н водного HCl и отфильтровали, получив 480 мг (92%) соединения 48d.
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, было получено следующее соединение, составляющее предмет настоящего изобретения.
МС m/z (M+H+) 482,1
Пример 49

2-(4,4-Дифторпиперидин-1-ил)бензо[d]тиазол-6-карбоновая кислота, 49d. Смесь 2-бромэтилбензо[d]тиазол-6-карбоксилата, 49a (1,75 ммоль, 500 мг), 4,4-дифторпиперидина, 49b (1,92 ммоль, 303 мг), и Cs2CO3 (5,24 ммоль, 1,71 г) в 15 мл CH3CN нагревали в колбе с обратным холодильником в течение ночи. Суспензию охладили до комнатной температуры и к смеси добавили 15 мл воды (содержащую этил 2-(4,4-дифторпиперидин-1-ил)бензо[d]тиазол-6-карбоксилат, 49c). Реакционную смесь нагревали при 60°C в течение 18 часов. После охлаждения смесь подкислили с помощью 3Н водной HCl и образовавшийся осадок отфильтровали, получив 575 мг (99%) соединения 49d. МС m/z (M+H+) 299,1.
Следуя процедуре, описанной выше для примера 9, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, было получено следующее соединение, составляющее предмет настоящего изобретения.
МС m/z (M+H+) 533,2
Пример 50

3-Хлор-1-(4-фторфенил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 1365. К раствору соединения 487 (0,2 ммоль, 100 мг) в CCl4 (4 мл) и CH2Cl2 (4 мл) добавили NCS (0,25 ммоль, 33 мг). Реакционную смесь перемешивали при комнатной температуре в течение 4 часов. Затем ее разбавили CH2Cl2 и промыли 1Н водного NaOH и H2O, высушили над Na2SO4 и сконцентрировали. После очистки колоночной флэш-хроматографией (силикагель, 3% MeOH/CH2Cl2) получили 51 мг соединения 1365. МС m/z (M+H+) 524.
Пример 51

A. 1-(3-Циано-4-фторфенил)-индол-5-карбоновая кислота (51a) и 1-(3-карбамоил-4-фторфенил)-индол-5-карбоновая кислота (51b). Промежуточные соединения 51a и 51b были подготовлены согласно примеру 9e и получены в пропорции ~1:1.
B. 2-Фтор-5-[5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол-1-ил]бензонитрил, соединение 1417, и 2-фтор-5-[5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол-1-ил]бензамид, соединение 1418. Соединения 1417 и 1418 получены в соответствии с процедурой, описанной в примере 9, из соединения 5a (соль бис-HCl) (0,22 ммоль, 72 мг), смеси ~1:1 соединений 51a и 51b (0,19 ммоль, 54 мг), HATU (0,22 ммоль, 85 мг) и Et3N (1,11 ммоль, 0,15 мл) в 4 мл CH2Cl2. После отработки и очистки колоночной флэш-хроматографией (силикагель, 3-4% MeOH/CH2Cl2) получили 28 мг (59%) соединения 1417 с последующим образованием 15 мг (31%) соединения 1418. Соединение 1417: МС m/z (M+H+) 515. Соединение 1418: МС m/z (M+H+) 533.
Пример 52

A. Метил 5-фенилбензо[b]тиофен-2-карбоксилат, 52b. Смесь соединения 52a (542,3 мг, 2 ммоль), фенилбороновой кислоты 1x (268,2 мг, 2,2 ммоль), Pd(dppf)Cl2·CH2Cl2 (98 мг, 0,12 ммоль) и K2CO3 (414,6 мг, 3 ммоль) в смеси диоксан (4 мл)/вода (1 мл) поместили в накрытую тару и нагревали при температуре 80°C в течение ночи. Затем реакционную смесь разбавили EtOAc и водой. Органический слой сконцентрировали при пониженном давлении и очистили колоночной флэш-хроматографией (силикагель, 2-10% EtOAc/гептан), получив соединение 52b (510 мг). МС m/z (M+H+) 269,1.
B. 5-Фенилбензо[b]тиофен-2-карбоновая кислота, 52c. Раствор соединения 52b (510 мг, 1,9 ммоль) и LiOH·H2O (319 мг, 7,6 ммоль) в THF/H2O (10/10 мл) перемешивали при комнатной температуре в течение ночи. Образовавшуюся смесь сконцентрировали и разбавили водой. Слой воды подкислили 1Н водной HCl до pH~4 и экстрагировали с помощью CH2Cl2. Органический раствор высушили над Na2SO4 и сконцентрировали, получив соединение 52c (479 мг), которое использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 255,0.
С. 3-Фтор-5-фенилбензо[b]тиофен-2-карбоновая кислота, 52d. К раствору соединения 52c (507 мг, 1,99 ммоль) в THF (8 мл) при -70°C добавили н-бутиллитий (1,6 M в гексане, 2,62 мл, 4,19 ммоль). Смесь перемешивали при температуре -70°C в течение 1 часа, затем постепенно добавили раствор N-фторбензолсульфонимида (817,3 мг, 2,59 ммоль) в THF (2 мл). Реакционной смеси дали нагреться до комнатной температуры и перемешивали в течение ночи. Полученную смесь экстрагировали с помощью EtOAc из разбавленной водной HCl. Органический раствор промыли водой и соляным раствором, высушили над Na2SO4 и сконцентрировали. Остаток растерли из CH2Cl2, отфильтровали и высушили выпавший осадок, получив соединение 52d (391,9 мг). МС m/z (M+H+) 273,0.
D. 3-Фтор-5-фенилбензо[b]тиофен-2-карбонилхлорид, 52e. К раствору соединения 52d (136,2 мг, 0,5 ммоль) в CH2Cl2 (5 мл) при комнатной температуре добавили (COCl)2 (0,064 мл, 0,75 ммоль) с последующим образованием DMF (0,01 мл, 0,125 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Затем реакционную смесь сконцентрировали для получения соединения 52e (светло-розовый порошок), которое использовали в следующей реакции без дополнительной очистки.
E. 1-{1-[(3-Фтор-5-фенил-1-бензотиофен-2-ил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 1315. К раствору соединения 5e (42,7 мг, 0,131 ммоль) и Et3N (0,07 мл, 0,5 ммоль) в CH2Cl2 (2 мл) при 0°C постепенно добавили раствор соединения 52e (36,3 мг, 0,125 ммоль) в CH2Cl2 (1 мл). Реакционную смесь перемешивали при температуре 0°C в течение 2 часов, разбавили CH2Cl2 и промыли водным раствором NaHCO3. Органический слой высушили над Na2SO4 и сконцентрировали. Остаток очистили колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc), получив соединение 1315 (16,7 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,98 (д, J=1,2 Гц, 1H), 7,89 (д, J=3,2 Гц, 1H), 7,80-7,86 (м, 1H), 7,73 (дд, J=8,6, 1,7 Гц, 1H), 7,62-7,68 (м, 2H), 7,55 (д, J=3,2 Гц, 1H), 7,46-7,53 (м, 2H), 7,37-7,44 (м, 1H), 4,22-4,67 (м, 5H), 4,05-4,20 (м, 1H), 3,77-4,01 (м, 2H), 3,25-3,37 (м, 1H), 2,42-2,68 (м, 4H). МС m/z (M+H+) 507,0.
Следуя процедуре, описанной выше для примера 52, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 575,1.
МС m/z (M+H+) 575,1.
Пример 53

A. 1-трет-Бутил 6-метил-3-(4-фторфенил)-1H-индол-1,6-дикарбоксилат, 53c. Смесь соединения 53a (1,00 г, 2,49 ммоль), 4-фторфенилбороновой кислоты 53b (523 мг, 3,74 ммоль), Pd(OAc)2 (44,8 мг, 0,2 ммоль), 2-дициклогексилфосфино-2',6'-диметоксидифенила (SPhos, 204,7 мг, 0,5 ммоль) и K3PO4 (1,06 г, 4,99 ммоль) в толуоле (5 мл) поместили в накрытую тару и нагревали до 90°C в N2 в течение 3 часов. Затем реакционную смесь разбавили EtOAc и водой. Органический слой промыли в соляном растворе, сконцентрировали при пониженном давлении и очистили колоночной флэш-хроматографией (силикагель, 2-10% EtOAc/гептан), получив соединение 53c в виде светло-желтого твердого вещества, которое затем перекристаллизовали из гептана, получив твердое вещество белого цвета (707 мг). МС m/z (M+H+) 370,2.
B. Метил 3-(4-фторфенил)-1H-индол-6-карбоксилат, 53d. К раствору соединения 53c (705 мг, 1,91 ммоль) в CH2Cl2 (4 мл) при комнатной температуре добавили трифторуксусную кислоту (1,5 мл). Смесь перемешивали при комнатной температуре в течение 2 часов. Полученную смесь сконцентрировали, получив соединение 53d (603,3 мг) в виде твердого вещества белого цвета. МС m/z (M+H+) 270,1.
C. 3-(4-Фторфенил)-1H-индол-6-карбоновая кислота, 53e. Раствор соединения 53d (303 мг, 0,79 ммоль) и LiOH·H2O (132,7 мг, 3,16 ммоль) в THF/H2O (10 мл/10 мл) перемешивали при 45°C в течение 5 часов. Образовавшуюся смесь сконцентрировали и разбавили водой. Слой воды подкислили 1Н водной HCl до pH~4 и экстрагировали с помощью CH2Cl2. Органический раствор высушили над Na2SO4 и сконцентрировали, получив соединение 53e (249 мг), которое использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 256,0.
D. 3-(4-Фторфенил)-6-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 1317. К смеси соединения 5e (42,9 мг, 0,132 ммоль), соединения 53e (30,6 мг, 0,12 ммоль) и Et3N (0,084 мл, 0,6 ммоль) в CH2Cl2 (1 мл) при комнатной температуре добавили HATU (70 мг, 0,168 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Смесь разбавили CH2Cl2 и H2O, промыли водным раствором NaHCO3 и соляным раствором, высушили над Na2SO4, отфильтровали и сконцентрировали. Остаток очистили колоночной флэш-хроматографией (силикагель, 2-4% MeOH/EtOAc), получив соединение 1317 (45,4 мг). 1Н ЯМР (400 МГц, CDCl3): δ 8,56 (уш.с, 1H), 7,83-7,94 (м, 3H), 7,57-7,65 (м, 2H), 7,55 (д, J=3,2 Гц, 1H), 7,46 (д, J=2,4 Гц, 1H), 7,40-7,45 (м, 1H), 7,13-7,20 (м, 2H), 4,07-4,66 (м, 6H), 3,76-4,01 (м, 2H), 3,21-3,36 (м, 1H), 2,38-2,64 (м, 4H). МС m/z (M+H+) 490,2.
Следуя процедуре, описанной выше для примера 53, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 53, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 472,2.
МС m/z (M+H+) 490,2.
Пример 53а

E. Метил 3-(4-фторфенил)-1-метил-1H-индол-6-карбоксилат, 53f. К раствору соединения 53d (300 мг, 0,78 ммоль) в DMF (3 мл) добавили NaH (60% в минеральном масле (68,9 мг, 1,72 ммоль) при 0°C. Смесь перемешивали при температуре 0°C в течение 30 минут, затем добавили CH3I (0,053 мл, 0,86 ммоль) и продолжили перемешивать при 0°C в течение еще одного часа. Полученную смесь разбавили EtOAc и водой. Органический слой промыли в соляном растворе и сконцентрировали. Остаток перекристаллизовали из гептана, отфильтровали и промыли выпавший осадок, получив соединение 53f (265 мг) в форме светло-желтого твердого вещества. МС m/z (M+H+) 284,1.
F. 3-(4-Фторфенил)-1-метил-1H-индол-6-карбоновая кислота, 53g. Раствор соединения 53f (264 мг, 0,93 ммоль) и LiOH·H2O (156,4 мг, 3,73 ммоль) в THF/H2O (10 мл/10 мл) перемешивали при 45°C в течение 5 часов. Образовавшуюся смесь сконцентрировали и разбавили водой. Слой воды подкислили 1Н водной HCl до pH~4 и экстрагировали с помощью CH2Cl2. Органический раствор высушили над Na2SO4 и сконцентрировали, получив соединение 53g (252 мг), которое использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 270,1.
Следуя процедуре, описанной выше для примера 53a, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, было получено следующее промежуточное соединение:
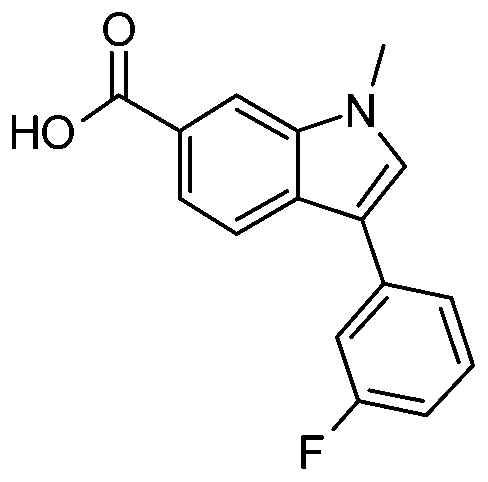
Следуя процедуре, описанной выше для примера 53, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=2,9 Гц, 1H), 7,79-7,87 (м, 2H), 7,51-7,63 (м, 3H), 7,39 (д, J=8,3 Гц, 1H), 7,31 (с, 1H), 7,15 (т, J=8,7 Гц, 2H), 4,21-4,67 (м, 5H), 4,08-4,21 (м, 1H), 3,89 (с, 3H), 3,77-3,98 (м, 2H), 3,19-3,35 (м, 1H), 2,36-2,65 (м, 4H)
МС m/z (M+H+) 504,1
МС m/z (M+H+) 504,1
Пример 54

A. Этил 1-метил-3-фенил-1H-индазол-5-карбоксилат, 54b. Смесь соединения 54a (300 мг, 0,91 ммоль), фенилбороновой кислоты 1x (133 мг, 1,09 ммоль), Pd(dppf)Cl2·CH2Cl2 (40 мг, 0,055 ммоль) и K2CO3 (251,2 мг, 1,82 ммоль) в смеси толуол (2 мл)/вода (0,4 мл) поместили в накрытую тару и нагревали при температуре 90°C в течение ночи. Затем реакционную смесь разбавили EtOAc и водой. Органический слой сконцентрировали при пониженном давлении и очистили колоночной флэш-хроматографией (силикагель, 2-10% EtOAc/гептаны), получив соединение 54b (231 мг). МС m/z (M+H+) 281,1.
B. 1-Метил-3-фенил-1H-индазол-5-карбоновая кислота, 54c. Раствор соединения 54b (230 мг, 0,58 ммоль) и LiOH·H2O (98 мг, 2,33 ммоль) в THF/H2O (10/10 мл) перемешивали при температуре 45°C в течение 8 часов. Образовавшуюся смесь сконцентрировали и разбавили водой. Слой воды подкислили 1Н водной HCl до pH~4 и экстрагировали с помощью CH2Cl2. Органический раствор высушили над Na2SO4 и сконцентрировали, получив соединение 54c (206 мг), которое использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 253,1.
C. 1-Метил-3-фенил-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индазол, соединение 1137. К смеси соединений 5e (42,9 мг, 0,132 ммоль), 54c (30,3 мг, 0,12 ммоль) и Et3N (0,084 мл, 0,6 ммоль) в CH2Cl2 (1 мл) при комнатной температуре добавили HATU (70 мг, 0,168 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Смесь разбавили CH2Cl2 и H2O, промыли водным раствором NaHCO3 и соляным раствором, высушили над Na2SO4, отфильтровали и сконцентрировали. Остаток очистили колоночной флэш-хроматографией (силикагель, 2-4% MeOH/EtOAc), получив соединение 1137 (48,1 мг). 1Н ЯМР (400 МГц, CDCl3): δ 8,32 (с, 1H), 7,94 (д, J=7,3 Гц, 2H), 7,88 (д, J=3,2 Гц, 1H), 7,74 (д, J=9,5 Гц, 1H), 7,49-7,58 (м, 3H), 7,39-7,48 (м, 2H), 4,16 (с, 3H), 4,09-4,62 (м, 6H), 3,86 (м, 2H), 3,21-3,33 (м, 1H), 2,39-2,63 (м, 4H). МС m/z (M+H+) 487,2.
Следуя процедуре, описанной выше для примера 54, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 54, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 505,2
МС m/z (M+H+) 505,2
МС m/z (M+H+) 485
МС m/z (M+H+) 553
МС m/z (M+H+) 478
МС m/z (M+H+) 546
Пример 55

A. Метил 2,3-дигидро-1H-индол-5-карбоксилат, 55a. К раствору метил 1H-индол-5-карбоксилата 1j (2 г, 11,4 ммоль) в безводной уксусной кислоте (15 мл) при температуре 0°C медленно добавляли цианоборогидрид натрия (1,08 г, 17,2 ммоль). Смесь дали нагреться и затем перемешивали при комнатной температуре в течение 2 часов. К образовавшейся смеси при температуре 0°C добавили воду, с помощью 1Н водного NaOH pH раствора был повышен до ~12. Смесь экстрагировали с помощью CH2Cl2, органический слой промыли в соляном растворе и высушили над Na2SO4. Раствор сконцентрировали и очистили колоночной флэш-хроматографией (силикагель, 15% EtOAc/гептан), получив соединение 55a (1,79 г). МС m/z (M+H+) 178,1.
B. Метил 1-(4-фторфенил)-2,3-дигидро-1H-индол-5-карбоксилат (55b) и 1-(4-фторфенил)-2,3-дигидро-1H-индол-5-карбоновая кислота (55c). Смесь соединения 55a (500 мг, 2,82 ммоль), 1-бром-4-фторбензола 1k (0,31 мл, 2,82 ммоль), Pd2(dba)3 (129 мг, 0,14 ммоль), BINAP (132 мг, 0,21 ммоль) и трет-бутоксида натрия (325 мг, 3,39 ммоль) в толуоле (25 мл) поместили в накрытую тару и нагревали при температуре 80°C в течение ночи. Затем реакционную смесь разбавили EtOAc и водой. С помощью 1Н водного NaOH основность слоя воды была повышена до pH~8. Органический слой сконцентрировали при пониженном давлении и очистили колоночной флэш-хроматографией (силикагель, 5-30% EtOAc/гептан), получив соединение 55b (145 мг), МС m/z (M+H+) 272,1, и соединение 55c (232 мг), МС m/z (M+H+) 258,0.
C. 1-(4-Фторфенил)-2,3-дигидро-1H-индол-5-карбоновая кислота, 55d. Раствор соединения 55b (144 мг, 0,53 ммоль) и LiOH·H2O (89,1 мг, 2,12 ммоль) в THF/H2O (5 мл/5 мл) перемешивали при температуре 45°C в течение ночи. Образовавшуюся смесь сконцентрировали и разбавили водой. Слой воды подкислили 1Н водной HCl до pH~4 и экстрагировали с помощью CH2Cl2. Органический раствор высушили над Na2SO4 и сконцентрировали, получив соединение 55d (138 мг), которое использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 258,0.
D. 1-(4-Фторфенил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-2,3-дигидро-1H-индол, соединение 885. К смеси соединений 5e (42,9 мг, 0,132 ммоль), 55d (30,9 мг, 0,12 ммоль) и Et3N (0,084 мл, 0,6 ммоль) в CH2Cl2 (1 мл) добавили HATU при комнатной температуре (70 мг, 0,168 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Смесь разбавили CH2Cl2 и промыли H2O, водным раствором NaHCO3 и солевым раствором, а затем высушили над Na2SO4, отфильтровали и сконцентрировали. Остаток очистили колоночной флэш-хроматографией (силикагель, 2-4% MeOH/EtOAc), получив соединение 885 (44,4 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=3,2 Гц, 1H), 7,55 (д, J=3,2 Гц, 1H), 7,51 (д, J=1,2 Гц, 1H), 7,38 (дд, J=8,3, 1,7 Гц, 1H), 7,16-7,25 (м, 2H), 7,03-7,12 (м, 2H), 6,88 (д, J=8,3 Гц, 1H), 4,05-4,67 (м, 6H), 3,99 (т, J=8,6 Гц, 2H), 3,76-3,94 (м, 2H), 3,20-3,30 (м, 1H), 3,16 (т, J=8,6 Гц, 2H), 2,37-2,64 (м, 4H); МС m/z (M+H+) 492,1.
Следуя процедуре, описанной выше для примера 55, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, было получено следующее промежуточное соединение:

Следуя процедуре, описанной выше для примера 55, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 492,1
МС m/z (M+H+) 492,1
МС m/z (M+H+) 474,1
Пример 55а

E. Метил 1-бензил-2,3-дигидро-1H-индол-5-карбоксилат, 55e. Раствор метил 2,3-дигидро-1H-индол-5-карбоксилата соли гидрохлорида 55a (88,6 мг, 0,42 ммоль) и бензальдегида 23a (0,060 мл, 0,55 ммоль) в CH2Cl2 (4 мл) перемешивали при комнатной температуре в течение 30 минут. Затем к смеси добавили триацетоксиборогидрид натрия (159 мг, 0,75 ммоль) и перемешивали еще в течение 2 часов. К образовавшейся смеси при температуре 0°C добавили воду, с помощью 1Н водного NaOH pH раствора был повышен до ~8. Смесь экстрагировали с помощью CH2Cl2, органический слой промыли в соляном растворе и высушили над Na2SO4. Раствор сконцентрировали и очистили колоночной флэш-хроматографией (силикагель, 10-25% EtOAc/гептаны), получив 55e (81,3 мг). МС m/z (M+H+) 268,0.
F. 1-Бензил-2,3-дигидро-1H-индол-5-карбоновая кислота, 55f. Раствор соединение 55e (80,2 мг, 0,3 ммоль) и LiOH·H2O (50,4 мг, 1,2 ммоль) в THF/H2O (1,2/1,2 мл) перемешивали при комнатной температуре в течение ночи. Образовавшуюся смесь сконцентрировали и разбавили водой. Слой воды подкислили 1Н водного HCl до pH ~4 и экстрагировали с помощью CH2Cl2. Органический раствор высушили над Na2SO4 и сконцентрировали, получив соединение 55f (60 мг), которое использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 254,1.
G. 1-Бензил-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-2,3-дигидро-1H-индол, соединение 994. К раствору соединений 5e (89,5 мг, 0,261 ммоль), 55f (60 мг, 0,237 ммоль) и EDC (68,1 мг, 0,356 ммоль) в CH2Cl2 (5 мл) добавили Et3N (0,1 мл, 0,711 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Смесь разбавили CH2Cl2 и H2O. С помощью 1Н водной HCl слой воды подкислили до pH ~6. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. Остаток очистили хроматографией на обращенной фазе, получив соединение 994 в виде трифторуксусной соли (40,4 мг). 1Н ЯМР (400 МГц, CD3OD): δ 7,98 (д, J=3,2 Гц, 1H), 7,89 (д, J=3,2 Гц, 1H), 7,36-7,44 (м, 2H), 7,29-7,36 (м, 4H), 7,22-7,29 (м, 1H), 6,52 (д, J=8,3 Гц, 1H), 4,39-4,91 (м, 6H), 4,38 (с, 2H), 3,99-4,23 (м, 3H), 3,48 (т, J=8,6 Гц, 2H), 3,42 (уш.с, 4H), 3,01 (т, J=8,6 Гц, 2H). МС m/z (M+H+) 488,1.
Следуя процедуре, описанной выше для примера 55а, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 55a, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 556,0
МС m/z (M+H+) 556,0
Пример 55b
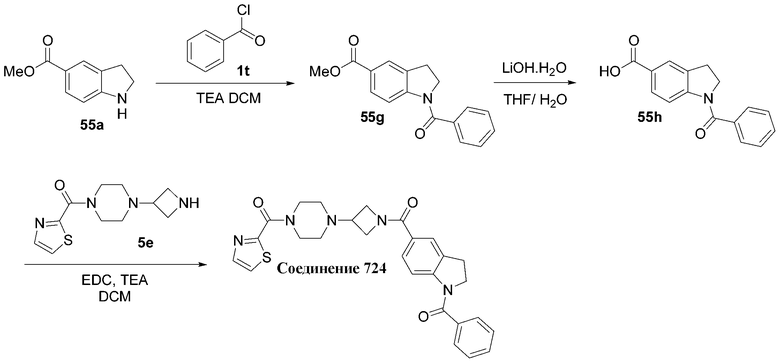
H. Метиловый эфир 1-бензоил-2,3-дигидро-1H-индол-5-карбоновой кислоты, 55g. К раствору гидрохлорида метил 2,3-дигидро-1H-индол-5-карбоксилата 55a (64,1 мг, 0,3 ммоль) и хлористого бензоила 1t (0,042 мл, 0,36 ммоль) в CH2Cl2 (1 мл) добавили Et3N (0,13 мл, 0,9 ммоль) при температуре 0°C. Реакционную смесь перемешивали при 0°C в течение 2 часов. Полученную смесь разделили с помощью CH2Cl2 и H2O. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. В результате очистки остатка колоночной флэш-хроматографией (силикагель, 10-20% EtOAc/гептаны) получили соединение 55g (88 мг). МС m/z (M+H+) 282,0.
I. 1-Бензоил-2,3-дигидро-1H-индол-5-карбоновая кислота, 55h. Раствор соединения 55g (87 мг, 0,31 ммоль) и LiOH·H2O (52 мг, 1,24 ммоль) в THF/H2O (2/2 мл) перемешивали при комнатной температуре в течение ночи. Образовавшуюся смесь сконцентрировали и разбавили водой. Слой воды подкислили 1Н водного HCl до pH ~6 и экстрагировали с помощью CH2Cl2. Органический раствор высушили над Na2SO4 и сконцентрировали, получив соединение 55h (82 мг), которое использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 268,0.
J. 1-(Фенилкарбонил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-2,3-дигидро-1H-индол, соединение 724. К раствору соединений 5e (115,9 мг, 0,34 ммоль), 55h (82 мг, 0,31 ммоль) и EDC (87,9 мг, 0,46 ммоль) в CH2Cl2 (5 мл) добавили Et3N (0,13 мл, 0,92 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Смесь разбавили CH2Cl2 и H2O. С помощью 1Н водной HCl слой воды подкислили до pH ~6. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. Остаток очистили колоночной флэш-хроматографией (силикагель, 2% MeOH/EtOAc), получив соединение 724 (64,4 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=3,2 Гц, 1H), 7,31-7,63 (м, 9H), 4,38-4,63 (м, 2H), 4,03-4,37 (м, 6H), 3,74-3,96 (м, 2H), 3,20-3,29 (м, 1H), 3,16 (т, J=8,3 Гц, 2H), 2,38-2,61 (м, 4H). МС m/z (M+H+) 502,0.
Следуя процедуре, описанной выше для примера 55b, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, было получено следующее промежуточное соединение:

Следуя процедуре, описанной выше для примера 55b, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, было получено следующее соединение, составляющее предмет настоящего изобретения:
МС m/z (M+H+) 466,0
Пример 56
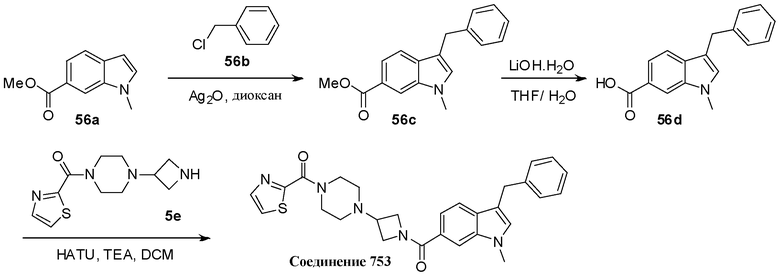
A. Метил 3-бензил-1-метил-1H-индол-6-карбоксилат, 56c. К раствору соединения 56a (500 мг, 2,64 ммоль) и бензилхлорида 56b (0,33 мл, 2,91 ммоль) в диоксане (5 мл) добавили оксид серебра (673,6 мг, 2,91 ммоль). Смесь перемешивали при температуре 80°C в течение ночи. Конечную смесь отфильтровали через целит и промыли с помощью EtOAc. Фильтрат сконцентрировали и очистили колоночной флэш-хроматографией (силикагель, 20-60% CH2Cl2/гептаны), получив соединение 56c (168 мг). МС m/z (M+H+) 280,2.
B. 3-Бензил-1-метил-1H-индол-6-карбоновая кислота, 56d. Раствор соединения 56c (168 мг, 0,60 ммоль) и LiOH·H2O (101 мг, 2,41 ммоль) в THF/H2O (3/3 мл) перемешивали при комнатной температуре в течение 6 часов. Конечную смесь сконцентрировали, остаток экстрагировали с помощью CH2Cl2, H2O, слой воды подкислили 1Н HCl (водный) до pH~4. Органический раствор высушили над Na2SO4 сконцентрировали, получив соединение 56d (172,2 мг), которое использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 266,2.
C. 3-Бензил-1-метил-6-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 753. К смеси соединения 5e (71,6 мг, 0,22 ммоль), соединения 56d (53,1 мг, 0,2 ммоль) и Et3N (0,14 мл, 1,0 ммоль) в CH2Cl2 (1 мл) при комнатной температуре добавили HATU (106,5 мг, 0,28 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Смесь разбавили CH2Cl2 и H2O, промыли водным раствором NaHCO3 и соляным раствором, высушили над Na2SO4, отфильтровали и сконцентрировали. В результате очистки остатка колоночной флэш-хроматографией (силикагель, 2-4% MeOH/EtOAc) получили соединение 753 (20,8 мг). 1Н ЯМР (400 МГц, CDCl3): δ 7,89 (д, J=2,4 Гц, 1H), 7,74 (с, 1H), 7,55 (д, J=2,7 Гц, 1H), 7,49 (д, J=8,3 Гц, 1H), 7,15-7,35 (м, 6H), 6,89 (с, 1H), 4,06-4,60 (м, 8H), 3,79-3,98 (м, 2H), 3,78 (с, 3H), 3,17-3,31 (м, 1H), 2,35-2,64 (м, 4H). МС m/z (M+H+) 500,3.
Следуя процедуре, описанной выше для примера 56, и заменив соответствующие реагенты, исходные вещества и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 56, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 518,1
МС m/z (M+H+) 518,1
МС m/z (M+H+) 500,1
m/z (M+H+) 518,2
Пример 57

5-({3-[4-(1,3-Тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,3,3-трис[3-(трифторметил)бензил]-1,3-дигидро-2H-индол-2-он, соединение 1430. К раствору соединения 918 (из примера 9) (25 мг, 0,061 ммоль) и K2CO3 (16,9 мг, 0,122 ммоль) в DMF (0,8 мл) добавили 3-трифторметилбензила бромид (20,4 мг, 0,085 ммоль). Смесь перемешивали при комнатной температуре в течение ночи. Полученную смесь экстрагировали с помощью EtOAc и H2O. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. Остаток очистили обращенно-фазовой хроматографией, получив соединение 1430 в виде трифторуксусной соли (3,6 мг), МС m/z (M+H+) 885,9.
Следуя процедуре, описанной выше для примера 57, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 682,0
МС m/z (M+H+) 728,0
Пример 58

5-({3-[4-(1,3-Тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 911, и 1-(2,3-дигидро-1H-индол-5-ил-карбонил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 988. К раствору соединения 5e (300 мг, 0,92 ммоль), смеси гидрохлорида 2,3-дигидро-1H-индол-5-карбоновой кислоты 58a (101 мг, 0,51 ммоль) и гидрохлорида 1H-индол-5-карбоновой кислоты 58b (100 мг, 0,51 ммоль) и EDC (265 мг, 1,38 ммоль) в CH2Cl2 (10 мл) добавили Et3N (0,39 мл, 2,77 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Полученную смесь экстрагировали с помощью CH2Cl2 и промыли H2O. Органическую часть раствора высушили над Na2SO4 и сконцентрировали. Остаток очистили обращенно-фазовой хроматографией, получив соединение 911 в виде трифторуксусной соли (89,4 мг) и соединение 988 в виде трифторуксусной соли (13,8 мг).
Соединение 911: 1Н ЯМР (400 МГц, CD3OD): δ 10,93 (уш.с, 1H), 7,98 (д, J=3,2 Гц, 1H), 7,95 (с, 1H), 7,89 (д, J=3,2 Гц, 1H), 7,47 (с, 2H), 7,36 (д, J=3,2 Гц, 1H), 6,57 (д, J=2,9 Гц, 1H), 4,25-4,84 (м, 6H), 3,91-4,15 (м, 4H), 2,80 (уш.с, 4H). МС m/z (M+H+) 396,0. Соединение 988: 1Н ЯМР (400 МГц, CD3OD): δ 7,98 (д, J=3,2 Гц, 1H), 7,88 (д, J=3,2 Гц, 1H), 7,85 (д, J=1,0 Гц, 1H), 7,58 (с, 1H), 7,27-7,56 (м, 5H), 6,56 (д, J=3,2 Гц, 1H), 4,29-4,89 (м, 6H), 4,20 (т, J=8,3 Гц, 2H), 3,96-4,15 (м, 3H), 3,32-3,43 (м, 4H), 3,17 (т, J=8,3 Гц, 2H). МС m/z (M+H+) 541,0.
Пример 59

A. 3-Метил-[1,1'-дифенил]-4-карбоновая кислота, 59b. Названное соединение 59b получили способом, описанным в примере 6 (стадия F), при использовании 4-бром-2-метилбензойной кислоты (59a) вместо соединения 173 и фенилборной кислоты 1x вместо соединения 6e. Полученное соединение 59b очистили хроматографией на обращенной фазе. МС m/z (M+H+) 213,1.
B. 1-{1-[(3-Метилдифенил-4-ил)карбонил]азетидин-3-ил}-4-(фенилкарбонил)пиперазин, соединение 619. Названное соединение 619 получили способом, описанным в примере 9, с заменой соединения 59b на соединение 9c и с заменой соединения 2c на соединение 5e. Полученное соединение 619 очистили хроматографией на обращенной фазе. МС m/z (M+H+) 440,1.
Следуя процедуре, описанной выше для примера 59, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:


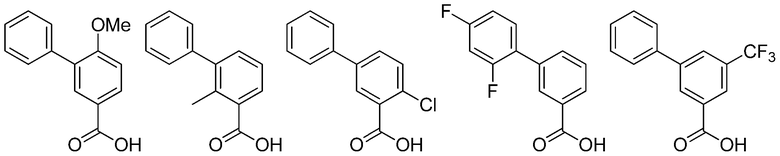

Следуя процедуре, описанной выше для примера 59, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 440,2
МС m/z (M+H+) 444,1
МС m/z (M+H+) 456,1
МС m/z (M+H+) 460,2
МС m/z (M+H+) 495,3
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,33-7,66 (м, 8H), 4,62-4,76 (м, 2H), 4,38-4,51 (м, 1H), 4,13-4,35 (м, 3H), 3,84-4,07 (м, 3H), 3,02-3,19 (м, 4H), 2,47 (с, 1H)
МС m/z (M+H+) 447,1
1H ЯМР (300 МГц, CD3OD): δ 7,98 (д, 1H), 7,88 (д, 1H), 7,59 (с, 1H), 7,54 (дд, 1H), 7,27-7,49 (м, 6H), 4,61-4,78 (м, 3H), 4,39-4,61 (м, 2H), 4,33 (M, 1H), 3,88-4,11 (м, 3H), 3,10-3,26 (м, 4H), 2,30 (с, 3H)
МС m/z (M+H+) 447,1
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,36-7,73 (м, 8H), 4,23-4,76 (м, 6H), 3,85-4,07 (м, 3H), 3,04-3,20 (м, 4H)
МС m/z (M+H+) 451,2
МС m/z (M+H+) 463,2
МС m/z (M+H+) 467,1
МС m/z (M+H+) 447,1
1H ЯМР (300 МГц, CD3OD): δ 9,06 (с, 1H), 8,22 (д, 1H), 7,38-7,71 (м, 8H), 4,28-4,53 (м, 4H), 3,94-4,25 (м, 5H), 3,16-3,27 (м, 4H)
МС m/z (M+H+) 451,1
МС m/z (M+H+) 463,2
МС m/z (M+H+) 467,1
МС m/z (M+H+) 501,0
МС m/z (M+H+) 501,0
МС m/z (M+H+) 563,0
МС m/z (M+H+) 463,0
МС m/z (M+H+) 501,0
МС m/z (M+H+) 451,0
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,87 (д, 1H), 7,80 (д, 1H), 7,66-7,75 (м, 2H), 7,50-7,64 (м, 2H), 7,05-7,16 (д, 1H), 4,24-4,75 (м, 6H), 3,83-4,06 (м, 3H), 3,02-3,18 (м, 4H)
МС m/z (M+H+) 469,0
МС m/z (M+H+) 501,0
МС m/z (M+H+) 451,0
МС m/z (M+H+) 469,0
МС m/z (M+H+) 451,0
МС m/z (M+H+) 467,0
МС m/z (M+H+) 463,0
МС m/z (M+H+) 447,0
МС m/z (M+H+) 451,0
МС m/z (M+H+) 467,0
МС m/z (M+H+) 463,0
МС m/z (M+H+) 447,0
МС m/z (M+H+) 451,0
МС m/z (M+H+) 451,0
1H ЯМР (300 МГц, CD3OD): δ 8,12 (с, 1H), 8,07 (с, 1H), 7,96 (д, 1H), 7,92 (с, 1H), 7,86 (д, 1H), 7,67-7,74 (м, 2H), 7,42-7,57 (м, 3H), 4,57-4,74 (м, 3H), 4,38-4,55 (м, 2H), 4,33 (м, 1H), 3,91-4,02 (м, 2H), 3,85 (м, 1H), 3,01-3,13 (м, 4H)
МС m/z (M+H+) 501,0
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,88 (д, 1H), 7,64-7,74 (м, 3H), 7,56-7,63 (дт, 1H), 7,35-7,53 (м, 4H), 4,31-4,83 (м, 6H), 3,94-4,10 (м, 3H), 3,19-3,27 (м, 4H)
МС m/z (M+H+) 451,0
МС m/z (M+H+) 501,0
МС m/z (M+H+) 451,0
1H ЯМР (400 МГц, CDCl3): δ 8,56 (д, 1H), 7,92 (д, 1H), 7,78-7,56 (м, 5H), 7,46 (м, 1H), 4,45 (м, 1H), 4,41-4,19 (м, 3H), 3,94 (уш.с, 5H), 3,12 (уш.с, 4H), 2,5 (с, 3H)
МС m/z (M+H+) 515,2
МС m/z (M+H+) 489
МС m/z (M+H+) 507,1
Пример 59а
Следуя процедуре, описанной выше для примера 2, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 515,12
МС m/z (M+H+) 507,05
МС m/z (M+H+) 515,2
МС m/z (M+H+) 507,1
МС m/z (M+H+) 489,2
Пример 60
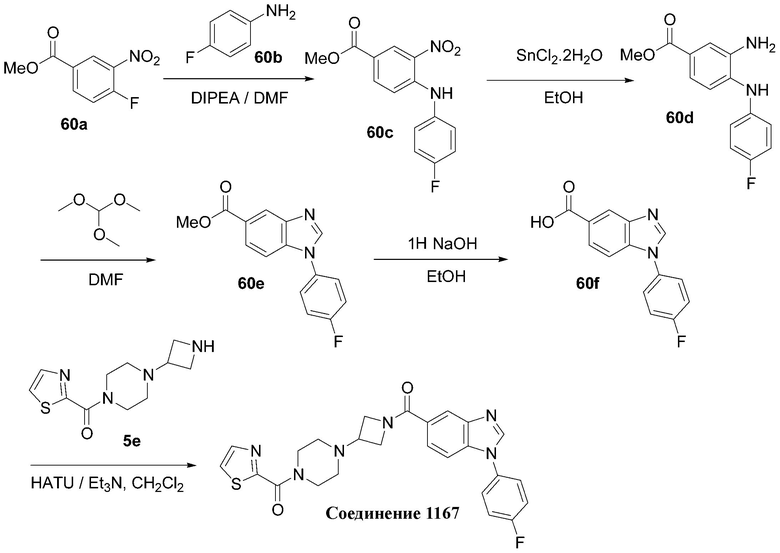
A. Метил 4-((4-фторфенил)амино)-3-нитробензоат, 60c. Смесь метил 4-фтор-3-нитробензоата 60a (1 г, 5,02 ммоль), 4-фторанилина 60b (4,34 мл, 5,02 ммоль) и DIPEA (1,04 мл, 6,03 ммоль) в DMF (10 мл) перемешивали при комнатной температуре в течение 2 часов. В смесь добавили воду. Образовавшийся осадок отфильтровали, промыли водой и высушили. Полученный продукт 60c использовали в следующей реакции без очистки.
B. Метил 3-амино-4-((4-фторфенил)амино)бензоат, 60d. Смесь соединения 60c (1,4 г, 4,8 ммоль) и SnCl2·2H2O (4,9 г, 21,7 ммоль) в EtOH (50 мл) перемешивали при температуре 80°C. Через 4 часа смесь охладили до комнатной температуры и постепенно добавили к насыщенному водному раствору NaHCO3. Выпавший осадок отфильтровали и промыли H2O. Выпавший осадок измельчили с EtOAc, фильтрат сконцентрировали. Полученный продукт 60d использовали в следующей реакции без очистки. МС m/z (M+H+) 261,1.
C. Метил 1-(4-фторфенил)-1H-бензо[d]имидазол-5-карбоксилат, 60e. Смесь 60d (0,18 г, 0,693 ммоль) и триметилортоформиат (0,7 мл, 6,39 ммоль) в DMF (2 мл) нагревали в колбе с обратным холодильником в течение 5 часов, а затем охладили до комнатной температуры. В смесь добавили воду. Образовавшийся осадок отфильтровали, промыли водой и высушили. Полученное соединение 60e использовали в следующей реакции без очистки. МС m/z (M+H+) 271,1.
D. 1-(4-Фторфенил)-1H-бензо[d]имидазол-5-карбоновая кислота, 60f. В раствор 60e (0,18 г, 0,666 ммоль) в EtOH (10 мл) добавили 1Н водного NaOH (2,5 мл, 2,5 ммоль). Смесь перемешивали при комнатной температуре в течение 4 дней. Растворитель испарили и добавили 1Н водной HCl с последующим экстрагированием с помощью EtOAc. Органический слой высушили над MgSO4 и сконцентрировали. Полученное соединение 60f использовали в следующей реакции без очистки. МС m/z (M+H+) 257,1.
E. 1-(4-Фторфенил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-бензимидазол, соединение 1167. К раствору соединения 5e (0,058 г, 0,178 ммоль) и HATU (0,081 г, 0,214 ммоль) в CH2Cl2 (3 мл) добавили Et3N (0,099 мл, 0,713 ммоль). Смесь перемешивали при комнатной температуре в течение 30 минут, а затем добавили 60f (0,050 г, 0,196 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Добавили воду (6 мл), после чего смесь экстрагировали с помощью EtOAc. Органический слой высушили над MgSO4 и сконцентрировали. Полученное соединение 1167 очистили препаративной хроматографией на обращенной фазе. МС m/z (M+H+) 491,2.
Следуя процедуре, описанной выше для примера 60, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения.

Следуя процедуре, описанной выше для примера 60, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
МС m/z (M+H+) 509,2
1H ЯМР (300 МГц, CD3OD): δ 8,82 (с, 1H), 8,14 (с, 1H), 7,96-8,03 (м, 3H), 7,86-7,95 (м, 3H), 7,76-7,85 (м, 2H), 7,08 (д, 1H), 4,36-4,86 (м, 6H), 3,97-4,16 (м, 3H), 3,32-3,42 (м, 4H)
МС m/z (M+H+) 541,2
МС m/z (M+H+) 479,1
МС m/z (M+H+) 493,2
МС m/z (M+H+) 515,2
МС m/z (M+H+) 473,2
МС m/z (M+H+) 491,2
МС m/z (M+H+) 509,1
МС m/z (M+H+) 541,2
МС m/z (M+H+) 493,2
МС m/z (M+H+) 515,2
МС m/z (M+H+) 473
Пример 60а
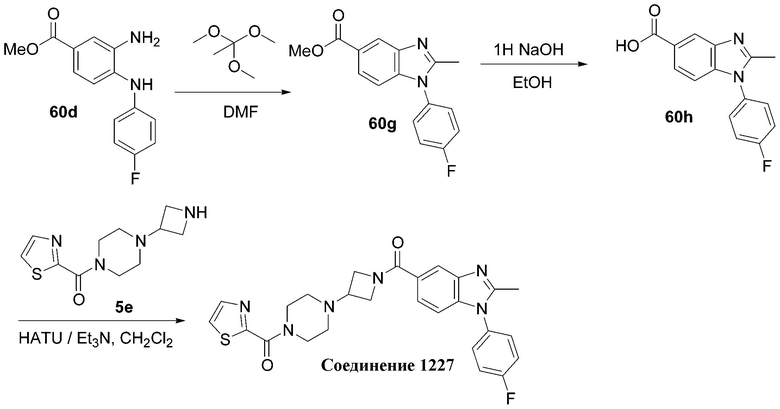
F. Метил 2-метил-1-(4-фторфенил)-1H-бензо[d]имидазол-5-карбоксилат, 60g. Названное соединение 60g было получено способом, описанным в примере 60, с заменой триметилортоацетат на триметилортоформиат на стадии C. Полученное соединение 60g использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 285,1.
G. 2-Метил-1-(4-фторфенил)-1H-бензо[d]имидазол-5-карбоксилат, 60h. Названное соединение 60h было получено способом, описанным в примере 60, с заменой соединения 60e на соединение 60g на стадии D. Полученное соединение 60h использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 271,2.
H. Соединение 1227. Названное соединение 1227 было получено способом, описанным в примере 60, с заменой соединения 60f на соединение 60h на стадии E. Полученное соединение 1227 очистили препаративной хроматографией на обращенной фазе. МС m/z (M+H+) 505,2.
Следуя процедуре, описанной выше для примера 60a, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения.

Следуя процедуре, описанной выше для примера 60a, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
МС m/z (M+H+) 487,2
МС m/z (M+H+) 523,2
МС m/z (M+H+) 555,2
МС m/z (M+H+) 493,2
МС m/z (M+H+) 507,2
МС m/z (M+H+) 529,2
МС m/z (M+H+) 505,2
МС m/z (M+H+) 487,2
МС m/z (M+H+) 523,2
МС m/z (M+H+) 555,2
МС m/z (M+H+) 493,2
МС m/z (M+H+) 507,1
МС m/z (M+H+) 529,2
МС m/z (M+H+) 480
Пример 60b

I. Метил 1-(4-фторфенил)-2-оксо-2,3-дигидро-1H-бензо[d]мидазол-5-карбоксилат, 60i. Смесь 60d (0,20 г, 0,826 ммоль) и 1,1'-карбонилдиимидазола (0,535 г, 3,3 ммоль) в DMF (8 мл) нагревали при температуре 90°C в течение 2 часов. Растворитель удалили, остаток измельчили в воде (15 мл). Образовавшийся осадок собрали фильтрованием и промыли водой несколько раз. Полученное соединение 60i использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 287,1.
J. 1-(4-Фторфенил)-2-оксо-2,3-дигидро-1H-бензо[d]мидазол-5-карбоксилат, 60j. Названное соединение 60j было получено способом, описанным в примере 60, с заменой соединения 60e на соединение 60i на стадии D. Полученное соединение 60j использовали в следующей реакции без дополнительной очистки. МС m/z (M+H+) 273,1.
K. 1-(4-Фторфенил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1,3-дигидро-2H-бензимидазол-2-он, соединение 934. Названное соединение 934 было получено способом, описанным в примере 60, с заменой соединения 60f на соединение 60j на стадии E. Полученное соединение 934 очистили препаративной хроматографией на обращенной фазе. МС m/z (M+H+) 507,1.
Следуя процедуре, описанной выше для примера 60b, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения.

Следуя процедуре, описанной выше для примера 60b, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения.
1H ЯМР (300 МГц, CD3OD): δ 7,97 (д, 1H), 7,88 (д, 1H), 7,56-7,66 (м, 2H), 7,46-7,55 (м, 4H), 7,42 (дд, 1H), 7,08 (д, 1H), 4,26-4,81 (м, 6H), 3,93-4,10 (м, 3H), 3,18-3,27 (м, 4H)
МС m/z (M+H+) 489,1
МС m/z (M+H+) 531,0
МС m/z (M+H+) 525,1
МС m/z (M+H+) 557,0
МС m/z (M+H+) 495,1
МС m/z (M+H+) 509,1
МС m/z (M+H+) 489,1
МС m/z (M+H+) 507,1
МС m/z (M+H+) 525,2
МС m/z (M+H+) 557,2
МС m/z (M+H+) 495,2
МС m/z (M+H+) 509,2
МС m/z (M+H+) 531,2
Пример 61

A. 3-Фтор-6-трифторметил-бензо[b]тиофен-2-карбоновая кислота, 61a. Раствор 6-трифторметил-бензо[b]тиофен-2-карбоновой кислоты 10a (2,031 ммоль, 0,50 г) в THF (8 мл) обработали при температуре -70°C 1,6-молярным раствором н-бутиллития в гексане (4,26 ммоль, 2,66 мл). Через 1 час при температуре -70°C постепенно добавили N-фторбензолсульфонимид (2,64 ммоль, 0,833 г) в THF (2 мл), и реакционную смесь нагрели до комнатной температуры. Через 1 час смесь экстрагировали с помощью EtOAc из разбавленной водной HCl. Органический слой промыли водой и соляным раствором, а затем сконцентрировали. Остаток измельчили с CH2Cl2. Осадок недостаточно белого цвета отфильтровали и собрали для приготовления 61a.
B. 3-Фтор-6-трифторметил-бензо[b]тиофен-2-карбонилхлорид, 61b. Названное соединение 61b было получено способом, описанным в примере 10, с заменой соединения 10a на соединение 61a на стадии A.
С. 1-(1-{[3-Фтор-6-(трифторметил)-1-бензтиофен-2-ил]карбонил}азетидин-3-ил)-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 895. Названное соединение 895 было получено способом, описанным в примере 10, с заменой соединения 10b на соединение 61b на стадии B. МС m/z (M+H+) 499.
Следуя процедуре, описанной выше для примера 61, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 499
МС m/z (M+H+) 492
Пример 62

A. 1-трет-Бутил 6-метил-3-фенил-1H-индол-1,6-дикарбоксилат, 62b. Смесь 1-трет-бутил 6-метил-3-йод-1H-индол-1,6-дикарбоксилата 62a (5,02 ммоль, 2,016 г), фенилбороновой кислоты 1x (7,53 ммоль, 0,92 г), Pd(OAc)2 (0,402 ммоль, 90 мг), Sphos (0,904 ммоль, 0,37 г) и K3PO4 (10,1 ммоль, 2,13 г) в толуоле (10 мл) в герметичном реакционном сосуде перемешивали при комнатной температуре в течение 2 минут, а затем нагревали до 90°C в атмосфере N2 в течение 4 часов. Реакционная смесь была погашена с помощью EtOAc и воды. Органический слой сконцентрировали и очистили колоночной флэш-хроматографией (силикагель, 8% EtOAc/гексаны). Полученное соединение в виде светло-желтого твердого вещества промыли в небольшом количестве гексанов, получив соединение 62b в виде твердого вещества белого цвета.
B. Метил 3-фенил-1Н-индол-6-карбоксилата трифторацетат, 62с. К раствору 1-трет-бутил-6-метил-3-фенил-1Н-индол-1,6-дикарбоксилата (соединение 62b, 4,04 ммоль, 1,42 г) в CH2Cl2 (8 мл) добавили 6 мл TFA. Полученный раствор перемешивали в течение 3 часов. Затем смесь сконцентрировали и промыли гексаном, получив соединение 62с.
C. Метил 1-метил-3-фенил-1Н-индол-6-карбоксилат, 62d. NaH (60%-ная дисперсия в минеральном масле, 4,52 ммоль, 186 мг) порциями добавляли к раствору метил 3-фенил-1Н-индол-6-карбоксилата TFA, 62с (2,07 ммоль, 757 мг), в DMF при температуре 0°C и перемешивали в течение 20 минут. Затем к смеси добавляли йодистый метил (2,28 ммоль, 0,14 мл) и в течение часа выдерживали полученную реакционную смесь при температуре 0°C. Затем добавили воду и экстрагировали полученную смесь этилацетатом. Органические фракции сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 15% этилацетат/гексаны), получив соединение 62d.
D. 1-Метил-3-фенил-1Н-индол-6-карбоновая кислота, 62е. Названное соединение 62е было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 62d на стадии B.
E. 1-Метил-3-фенил-6-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 1132. Названное соединение 1132 было получено способом, описанным в примере 9, с заменой соединения 9c на соединение 62d на стадии D. МС m/z (M+H+) 486.
Следуя процедуре, описанной выше для примера 62, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 62, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 536
МС m/z (M+H+) 554
МС m/z (M+H+) 554
МС m/z (M+H+) 554
МС m/z (M+H+) 554
МС m/z (M+H+) 486
МС m/z (M+H+) 547
МС m/z (M+H+) 479
Пример 62а

F. 1-трет-Бутил 6-метил-3-(3-(трифторметил)фенил)-1H-индол-1,6-дикарбоксилат, 62g. Названное соединение 62g было получено способом, описанным в примере 62, с заменой соединения 1x на соединение 62f на стадии A.
G. Метил 3-(3-(трифторметил)фенил)-1H-индол-6-карбоксилата трифторацетат, 62h. Названное соединение 62h было получено способом, описанным в примере 62, с заменой соединения 62b на соединение 62g на стадии B.
H. 3-(3-(Трифторметил)фенил)-1H-индол-6-карбоновая кислота, 62i. Названное соединение было получено способом, описанным в примере 62, с заменой соединения 62e на соединение 62h на стадии D.
E. 6-({3-[4-(1,3-Тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-3-[3-(трифторметил)фенил]-1H-индол, соединение 1341. Названное соединение 1341 было получено способом, описанным в примере 9, с заменой соединения 9c на соединение 62i на стадии D. МС m/z (M+H+) 540.
Следуя процедуре, описанной выше для примера 62a, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, было получено следующее промежуточное соединение:
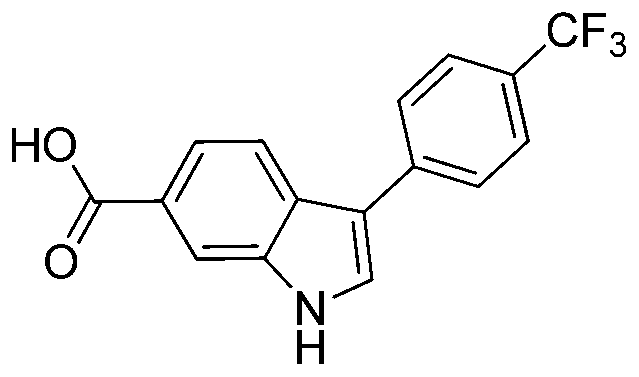
Следуя процедуре, описанной выше для примера 62a, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 533
МС m/z (M+H+) 533
МС m/z (M+H+) 540
МС m/z (M+H+) 540
МС m/z (M+H+) 540
Пример 63

A. Метил 4-(гидрокси(4-(трифторметил)фенил)метил)бензоат, 63c. К раствору метил 4-йодбензоата, 63a (8 ммоль, 2,1 г), в 10 мл сухого THF по каплям добавили i-пропилмагнийхлорид (2M в THF, 8,4 ммоль, 4,2 мл). Реакцию проводили в атмосфере N2 при температуре -20°C. Раствор перемешивали в течение 30 минут. Затем полученный реактив Гриньяра в THF постепенно добавили к раствору 4-трифторметилбензальдегида (8 ммоль, 1,1 мл) в THF (20 мл) при температуре -40°C. Через 20 минут реакционную смесь постепенно нагрели до комнатной температуры. Протекание реакции остановили насыщенным водным раствором NH4Cl и готовое соединение экстрагировали с помощью этилацетата. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 15% этилацетат/гексаны), получив соединение 63с в виде белого твердого остатка.
B. 4-Метил 4-(фтор(4-(трифторметил)фенил)метил)бензоат, 63d. К раствору соединения 63c (0,97 ммоль, 300 мг) в CH2Cl2 по каплям добавили DAST (1,015 ммоль, 0,133 мл). Реакция проводилась при температуре -78°C в атмосфере N2. Реакционную смесь выдержали 30 минут при температуре -78°C, а затем остановили реакцию водным раствором NaHCO3 при низкой температуре. В реакционную смесь ввели дополнительное количество CH2Cl2, а затем органический раствор сконцентрировали. Полученное соединение очистили с помощью колоночной флэш-хроматографии (силикагель, 10% этилацетат/гексаны), получив соединение 63d.
C. 4-(Фтор(4-(трифторметил)фенил)метил)бензойная кислота, 63e. Названное соединение было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 63d на стадии В.
D. 1-{1-[(4-{Фтор[4-(трифторметил)фенил]метил}фенил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 982. Названное соединение 982 было получено способом, описанным в примере 9, с заменой соединения 9c на соединение 63e на стадии D. МС m/z (M+H+) 533.
Пример 64

A. Метил 4-(2-фенил-1,3-дитиолан-2-ил)бензоат, 64b. Метил 4-бензилбензоат, 64a (2,08 ммоль, 0,50 г) и BF3.(OAc)2 (5,2 ммоль, 0,73 мл) растворили в сухом CH2Cl2 в атмосфере N2. К смеси добавили этан-1,2-дитиол (3,95 ммоль, 0,333 мл) и оставили раствор перемешиваться в течение ночи. Полученную реакционную смесь разделили между CH2Cl2 и водой. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 10% этилацетат/гексаны), получив соединение 64b.
B. Метил 4-(дифтор(фенил)метил)бензоат, 64c. Реагенты Selectfluor (1,07 ммоль, 381 мг) и HF-пиридин (1,5 мл, HF:пиридин = 70:30% по массе) растворили в CH2Cl2 (4 мл) в полиэтиленовой бутылке и охладили до 0°C. Раствор соединения 64b (0,512 ммоль, 162 мг) в CH2Cl2 (2 мл) постепенно добавили к реактивам и полученную смесь перемешивали в течение 45 минут при комнатной температуре. Когда результаты ТСХ показали, что соединение 64b полностью прореагировало, реакционную смесь разбавили CH2Cl2. Объединенные органические фракции высушили над безводным Na2SO4 и сконцентрировали. Полученный продукт очистили с использованием колоночной флэш-хроматографии (силикагель, 5% этилацетат/гексаны), получив соединение 64c в виде прозрачного масла.
C. 4-(Дифтор(фенил)метил)бензойная кислота, 64d. Названное соединение 64d было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 64c на стадии B.
D. 1-[1-({4-[Дифтор(фенил)метил]фенил}карбонил)азетидин-3-ил]-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 986. Названное соединение 986 было получено способом, описанным в примере 9, с заменой соединения 9с на соединение 64d на стадии D. МС m/z (M+H+) 483.
Пример 65

A. Метил 3-циклопропил-6-фторбензо[b]тиофен-2-карбоксилат, 65c. Смесь метил 3-хлор-6-фторбензо[b]тиофен-2-карбоксилата 65a (0,613 ммоль, 150 мг), циклопропилборной кислоты 65b (0,92 ммоль, 79 мг), Pd(OAc)2 (0,09 ммоль, 20 мг), SPhos (0,215 ммоль, 88мг) и K3PO4 (1,23 ммоль, 0,26 г) в толуоле (2 мл) выдерживали в герметичном реакционном сосуде в течение 3 часов при температуре 100°C. Затем реакционную смесь разбавили этилацетатом и водой. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 10% этилацетат/гексаны), получив соединение 65с.
B. 3-Циклопропил-6-фторбензо[b]тиофен-2-карбоновая кислота, 65d. Названное соединение 65d было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 65c на стадии B.
C. 3-Циклопропил-6-фторбензо[b]тиофен-2-карбонилхлорид, 65e. Названное соединение 65e было получено способом, описанным в примере 10, с заменой соединения 10a на соединение 65d на стадии А.
D. 1-{1-[(3-Циклопропил-6-фтор-1-бензотиофен-2-ил)карбонил]азетидин-3-ил}-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 714. Названное соединение 714 было получено способом, описанным в примере 10, с заменой соединения 10b на соединение 65e на стадии B. МС m/z (M+H+) 471.
Следуя процедуре, описанной выше для примера 65, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:
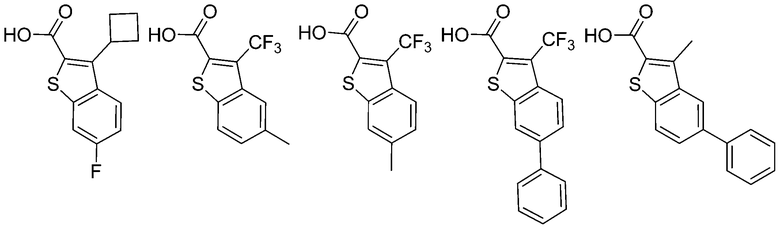
Следуя процедуре, описанной выше для примера 65, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 485
МС m/z (M+H+) 464
МС m/z (M+H+) 478
ЯМР (CDCl3) δ 7,96 (д, J=1,2 Гц, 1H), 7,84-7,93 (м, 2H), 7,62-7,74 (м, 3H), 7,55 (д, J=3,2 Гц, 1H), 7,49 (м, 2H), 7,34-7,44 (м, 1H), 4,12-4,47 (м, 6H), 3,87 (м, 2H), 3,19-3,35 (м, 1H), 2,69 (с, 3H), 2,50 (м, 4H)
МС m/z (M+H+) 503
Пример 66

A. Метил 4-тиоморфолинхиназолин-7-карбоксилат, 66c. Раствор метил 4-хлорхиназолин-7-карбоксилата 66a (1,01 ммоль, 225 мг) и тиоморфолина 66b (2,02 ммоль, 208 мг) в MeOH (1,6 мл) кипятили с обратным холодильником в течение ночи. После очистки соединение 66c было выделено в количестве 30 мг.
B. 4-Тиоморфолинхиназолин-7-карбоновая кислота, 66d. Названное соединение 66d было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 66с на стадии B.
C. 7-({3-[4-(1,3-Тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-4-тиоморфолин-4-ил-хиназолин, соединение 951. Названное соединение 951 было получено способом, описанным в примере 9, с заменой соединения 9с на соединение 66d на стадии D. МС m/z (M+H+) 510.
Пример 67

A. 1-(5-Хлор-2-фторфенил)-2,2,2-трифторэтанон, 67c. К раствору LDA (2,0 M в THF/гептан/этилбензол, 25,3 ммоль, 12,6 мл) в сухом THF постепенно добавили 1-фтор-4-хлорбензол 67a (23,0 ммоль, 2,45 мл). Реакцию проводили при температуре -78°C. Смесь перемешивали в течение 1 часа при температуре -78°C, а затем добавили этилтрифторацетат 67b (25,3 ммоль, 3,02 мл). Реакционную смесь оставили на ночь прогреваться до комнатной температуры, а затем реакцию остановили насыщенным водным раствором NH4Cl. Смесь экстрагировали с помощью EtOAc. Органические экстракты сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 15% этилацетат/гексаны), получив смесь соединения 67c с регио-изомерным побочным продуктом, 1-(5-фтор-2-хлорфенил)-2,2,2-трифторэтаноном, в соотношении 5:1 (67c - основное соединение).
B. Метил 5-хлор-3-(трифторметил)бензо[b]тиофен-2-карбоксилат, 67e. Раствор соединения 67c (6,62 ммоль; 1,5 г), метил 2-меркаптоацетата 67d (6,62 ммоль, 0,6 мл) и Et3N (8,6 ммоль, 1,2 мл) в ацетонитриле (12 мл) выдержали в течение 4 часов при температуре 75°C. Затем реакционную смесь разбавили этилацетатом и водой. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 10% этилацетат/гексаны), получив соединение 67e.
C. 5-Хлор-3-трифторметилбензо[b]тиофен-2-карбоновая кислота, 67f. Названное соединение 67f было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 67e на стадии B.
D. 5-Хлор-3-трифторметил-бензо[b]тиофен-2-карбонилхлорид, 67g. Названное соединение 65e было получено способом, описанным в примере 10, с заменой соединения 10a на соединение 67f на стадии A.
E. 1-(1-{[5-Хлор-3-(трифторметил)-1-бензотиофен-2-ил]карбонил}азетидин-3-ил)-4-(1,3-тиазол-2-ил-карбонил)пиперазин. Названное соединение 896 было получено способом, описанным в примере 10, с заменой соединения 10b на соединение 67g на стадии B. МС m/z (M+H+) 515.
Следуя процедуре, описанной выше для примера 67, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 515
МС m/z (M+H+) 508
Пример 67а

F. 1-(4-Хлор-2-фторфенил)-2,2,2-трифторэтанон, 67i. К раствору н-бутиллития (1,6 M в гексане, 4,68 ммоль, 2,93 мл) в сухом THF постепенно добавили 4-хлор-2-фтор-1-йодбензол 67h (3,9 ммоль, 1,0 г). Реакцию проводили при температуре -78°C в атмосфере N2. Реакционную смесь перемешивали в течение 1 часа при температуре -78°C, а затем добавили этилтрифторацетат 67b (0,51 мл, 4,29 ммоль). Реакционную смесь оставили на ночь прогреваться до комнатной температуры, а затем реакцию остановили насыщенным водным раствором NH4Cl. Смесь экстрагировали с помощью EtOAc. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 15% этилацетат/гексаны), получив соединение 67i.
G. Метил 6-хлор-3-(трифторметил)бензо[b]тиофен-2-карбоксилат, 67j. Названное соединение 67j было получено способом, описанным в примере 67, с заменой соединения 67c на соединение 67i на стадии B.
Следуя процедуре, описанной выше для примера 67 на стадиях C-E, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 515
МС m/z (M+H+) 515
МС m/z (M+H+) 508
Пример 67b

H. Метил 6-хлор-3-(трифторметил)бензо[b]тиофен-2-карбоксилат, 67l. Названное соединение 67l было получено способом, описанным в примере 67, с заменой соединения 67c на соединение 67k, Et3N на NaH и CH3CN на THF и DMSO на стадии B.
Следуя процедуре, описанной выше для примера 67 на стадии C-E, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (CDCl3): δ 8,41 (ар, 1H), 8,22 (ар, 1H), 7,98 (м, 1H), 7,65 (м, 1H), 7,48, (м, 1H), 3,83 (уш.м, 5H), 3,0 1(уш.м, 4H), 2,5 (с, 3H)
МС m/z (M+H+) 477,0
МС m/z (M+H+) 488
1H ЯМР (CDCl3, 400 МГц): δ 8,11 (с, 1H), 7,83-7,95 (м, 2H), 7,65 (д, J=8,6 Гц, 1H), 7,55 (д, J=3,1 Гц, 1H), 3,99-4,67 (м, 6H), 3,87 (уш.с, 2H), 3,16-3,41 (м, 1H), 2,66 (с, 3H), 2,50 (уш.с, 4H).
МС m/z (M+H+) 495
1H ЯМР (CDCl3,400 МГц): δ 8,79 (с, 1H), 8,10 (с, 1H), 8,03 (с, 1H), 7,89 (д, J=8 Гц, 1H), 7,65 (д, J=8 Гц, 1H), 3,80-4,40 (м, 8H), 3,28 (м, 1H), 2,66 (с, 3H), 2,49 (уш.с, 4H).
МС m/z (M+H+) 495
1H ЯМР (400 МГц, CDCl3): δ 8,33 (д, 1H), 8,09 (д, 1H), 7,72 (д, 1H), 6,95 (с, 1H), 6,67 (с, 1H), 6,23 (дд, 1H), 4,59 (уш.м, 3H), 4,26 (м, 1H), 3,40 (м, 3H), 2,68 (с, 3H)
МС m/z (M+H+) 477,1
Пример 68

A. Метил 3-гидрокси-6-трифторметилбензо[b]тиофен-2-карбоксилат, 68b. К раствору метил 2-фтор-4-трифторметилбензоата 68a (2,25 ммоль, 0,50 г) и метил 2-меркаптоацетата 67d (2,25 ммоль, 0,21 мл) в DMF (3 мл) при температуре 0°C добавили LiOH (4,5 ммоль, 0,11 г). Смесь перемешивали при 0°C в течение 30 минут, а затем нагрели до комнатной температуры и перемешивали в течение 1 часа. Затем добавили воду и конечный раствор подкислили 1Н водного раствора HCl. Полученный осадок профильтровали, промыли водой и высушили, получив соединение 68b.
B. Метил 3-метокси-6-трифторметилбензо[b]тиофен-2-карбоксилат, 68c. Смесь соединения 68b (0,543 ммоль, 150 мг), диметилсульфата (0,608 ммоль, 0,058 мл) и бикарбоната натрия (0,57 ммоль, 48 мг) в ацетоне кипятили с обратным холодильником в течение ночи. Затем реакционную смесь охладили и профильтровали. Фильтрат сконцентрировали и остаток разделили между этилацетатом и водой. Органический раствор сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 10% этилацетат/гексаны), получив соединение 68c.
C. 3-Метокси-6-трифторметилбензо[b]тиофен-2-карбоновая кислота, 68d. Названное соединение 68d было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 68с на стадии B.
D. 3-Метокси-6-трифторметилбензо[b]тиофен-2-карбонилхлорид, 68e. Названное соединение 68е было получено способом, описанным в примере 10, с заменой соединения 10a на соединение 68d на стадии A.
E. 1-(1-{[3-Метокси-6-(трифторметил)-1-бензотиофен-2-ил]карбонил}азетидин-3-ил)-4-(1,3-тиазол-2-ил-карбонил)пиперазин, соединение 649. Названное соединение 649 было получено способом, описанным в примере 10, с заменой соединения 10b на соединение 68e на стадии B. 1H ЯМР (CDCl3): δ 8,05 (с, 1H), 7,83-7,96 (м, 2H), 7,62 (дд, J=8,4, 1,1 Гц, 1H), 7,55 (д, J=3,2 Гц, 1H), 4,55-4,45 (м, 2H), 4,24-4,37 (м, 2H), 4,11-4,24 (м, 2H), 4,07 (с, 3H), 3,88 (м, 2H), 3,29 (м, 1H), 2,50 (м, 4H). МС m/z (M+H+) 511.
Следуя процедуре, описанной выше для примера 68, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 511
Пример 68а
Следуя процедуре, описанной выше для примера 2, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 495,1
МС m/z (M+H+) 495,1
Пример 69

A. Метил 3-фтор-1H-индол-6-карбоксилат, 69a. Раствор метил 1H-индол-6-карбоксилата 1j (11,4 ммоль, 2,0 г) и N-фтор-2,4,6-триметилпиридинийтрифлата (14,8 ммоль, 4,3 г) в MeOH (100 мл) кипятили с обратным холодильником в течение 18 часов. Реакционную смесь сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель,15-20% этилацетат/гексаны), получив соединение 69a в виде серовато-белого твердого вещества.
B. Метил 3-фтор-1-(4-фторфенил)-1H-индол-6-карбоксилат, 69c. Смесь соединения 69a (0,264 ммоль, 51 мг), CuI (0,0264 ммоль, 5 мг) и K3PO4 (0,66 ммоль, 40 мг) поместили в закрытый реакционный сосуд, который затем промыли обратным потоком N2. Используя шприц, в смесь ввели 4-фторйодбензол 69b (0,264 ммоль, 0,0394 мл) и N,N'-диметилциклогексан-1,2-диамин (0,0792 ммоль, 0,0125 мл) с последующим добавлением толуола. Полученную смесь выдерживали при температуре 95°C в течение 6 часов. Далее реакционную смесь разбавили этилацетатом и водой. Реакционную смесь сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 20% этилацетат/гексаны), получив соединение 69c.
C. 3-Фтор-1-(4-фторфенил)-1H-индол-6-карбоновая кислота, 69d. Названное соединение 69d было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 69с на стадии B.
D. 3-Фтор-1-(4-фторфенил)-5-({3-[4-(фенилкарбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 574. Названное соединение 574 было получено способом, описанным в примере 9, с заменой соединения 9c на соединение 69d и соединения 5е на соединение 2с на стадии D. МС m/z (M+H+) 501.
Следуя процедуре, описанной выше для примера 69, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 490
Пример 70

A. Метил 4-фтор-1-триизопропилсиланил-1H-индол-5-карбоксилат, 70b. К раствору 4-фтор-1-триизопропилсиланил-1H-индол-5-карбоновой кислоты 70a (8,08 ммоль, 2,71 г), полученной способом, описанным в работе Eur. J. Org. Chem. 2006, 2956, в сухом CH2Cl2 (20 мл) добавили оксалилхлорид (9,69 ммоль, 0,82 мл) с последующим введением DMF (0,81 ммоль, 0,063 мл). Реакционную смесь перемешивали при комнатной температуре в течение 30 минут, а затем сконцентрировали. Полученный остаток растворили в CH2Cl2 (20 мл) и охладили до 0°C. Затем добавили Et3N (40,4 ммоль, 5,6 мл) и постепенно добавили MeOH. Реакционную смесь перемешивали в течение 30 минут при температуре 0°C, а затем сконцентрировали. Остаток разделили между этилацетатом и водой. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 5% этилацетат/гексаны), получив соединение 70b.
B. Метил 4-фтор-1H-индол-5-карбоксилат, 70c. К раствору соединения 70b (7,9 ммоль, 2,76 г) в THF при температуре 0°C добавили TBAF (1M раствора в THF, 15,8 ммоль, 15,8 мл). Реакционную смесь выдерживали при комнатной температуре 10 мин, а затем разбавляли EtOAc и промывали солевым раствором, насыщенным раствором NaHCO3 и водой. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 35% этилацетат/гексаны), получив соединение 70c.
C. Метил 4-фтор-1-(4-фторфенил)-1H-индол-5-карбоксилат, 70d. Названное соединение 70d было получено способом, описанным в примере 69, с заменой соединения 69a на соединение 70c на стадии B.
D. 4-Фтор-1-(4-фторфенил)-1H-индол-5-карбоновая кислота, 70e. Названное соединение 70е было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 70d на стадии B.
E. 4-Фтор-1-(4-фторфенил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 1348. Названное соединение 1348 было получено способом, описанным в примере 9, с заменой соединения 9c на соединение 70e на стадии D. 1H ЯМР (CDCl3): δ 7,87 (д, J=3,2 Гц, 1H), 7,54 (д, J=3,2 Гц, 1H), 7,36-7,47 (м, 3H), 7,30 (д, J=3,2 Гц, 1H), 7,19-7,27 (м, 3H), 6,81 (д, J=3,2 Гц, 1H), 4,52-4,43 (м, 2H), 4,28 (дд, J=9,9, 7,7 Гц, 1H), 4,16-4,24 (м, 1H), 4,05-4,16 (м, 2H), 3,75-3,95 (м, 2H), 3,27 (м, 1H), 2,38-2,58 (м, 4H). МС m/z (M+H+) 508.
Следуя процедуре, описанной выше для примера 70, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, было получено следующее промежуточное соединение:

Следуя процедуре, описанной выше для примера 70, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 508
МС m/z (M+H+) 508
МС m/z (M+H+) 501
МС m/z (M+H+) 501
Пример 70а
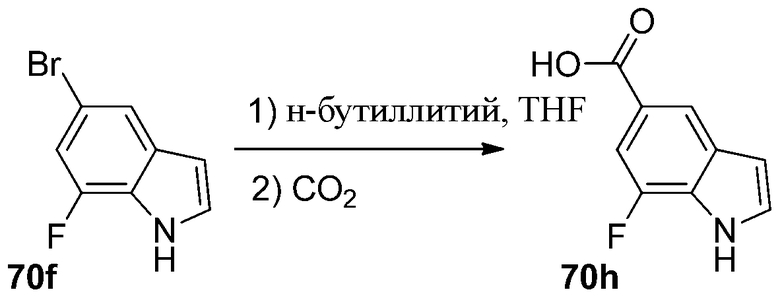
F. 7-Фтор-1H-индол-5-карбоновая кислота, 70h. К раствору 5-бром-7-фториндола 70f (1,71 ммоль, 365 мг) в THF добавили н-бутиллитий (1,6 M раствора в гексане, 5,2 ммоль, 3,2 мл). Реакцию проводили при температуре -60°C. Раствор выдержали 4 часа при температуре -60°C и затем вылили в емкость с большим количеством только что измельченного сухого льда. В смесь добавили воду и подкислили среду до pH=4. Органическую фазу сконцентрировали, остаток очистили с использованием колоночной флэш-хроматографии (силикагель, 35% этилацетат/гексаны), получив соединение 70h.
Следуя процедуре, описанной выше для примера 70, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, было получено следующее промежуточное соединение:

Следуя процедуре, описанной выше для примера 70, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (CDCl3): δ 7,88 (д, J=3,2 Гц, 1H), 7,76 (д, J=1,2 Гц, 1H), 7,55 (д, J=3,2 Гц, 1H), 7,42 (м, 2H), 7,22-7,31 (м, 2H), 7,12-7,22 (м, 2H), 6,69-6,81 (м, 1H), 4,53-4,27 (м, 5H), 4,12 (м, 1H), 3,89-3,83 (м, 2H), 3,26 (м, 1H), 2,50 (м, 4H)
МС m/z (M+H+) 508
МС m/z (M+H+) 508
Пример 70b

G. Метил 7-метил-1H-индол-5-карбоксилат, 70k. Названное соединение было получено способом, описанным в примере 65, с заменой соединения 65a на соединение 70i и соединения 65b на соединение 70j на стадии А.
Следуя процедуре, описанной выше для примера 70, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, было получено следующее промежуточное соединение:

Следуя процедуре, описанной выше для примера 70, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (CDCl3): δ 7,88 (д, J=2,4 Гц, 1H), 7,81 (с, 1H), 7,54 (д, J=2,4 Гц, 1H), 7,36 (м, 2H), 7,28 (S, 1H), 7,10-7,21 (м, 3H), 6,67 (д, J=2,4 Гц, 1H), 4,55-4,26 (м, 5H), 4,12 (м, 1H), 3,89 (м, 2H), 3,25 (м, 1H), 2,50 (м, 4H), 2,02 (с, 3H)
МС m/z (M+H+) 504
МС m/z (M+H+) 504
Пример 70с
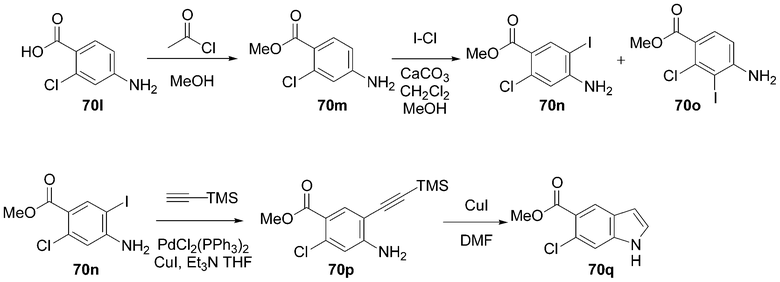
H. Метил 4-амино-2-хлорбензоат, 70m. Ацетилхлорид (35,2 ммоль; 2,5 мл) добавили по каплям к перемешиваемому раствору 4-амино-2-хлорбензойной кислоты 70l (12,9 ммоль, 2,22 г) в метаноле (50 мл). Смесь кипятили с обратным холодильником в течение 18 часов, затем охладили и сконцентрировали под вакуумом. Полученный остаток поместили в этилацетат, промыли насыщенным водным раствором NaHCO3 и насыщенным солевым раствором, затем высушили и сконцентрировали под вакуумом. Полученное соединение очистили с использованием колоночной флэш-хроматографии (силикагель, 30% этилацетат/гексаны), получив соединение 70m.
I. Метил 4-амино-2-хлор-5-йодбензоат, 70n. К суспензии соединения 70m (1,18 г; 6,38 ммоль) и CaCO3 (12,8 ммоль, 1,28 г) в MeOH (13 мл) при комнатной температуре по каплям добавили раствор монохлорида йода (6,70 ммоль, 1,09 г) в CH2Cl2 (6 мл). Полученную реакционную смесь перемешивали в течение полутора часов при комнатной температуре. Затем смесь сконцентрировали и разделили между этилацетатом и водой. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 20-25% этилацетат/гексаны), получив метил-4-амино-2-хлор-5-йодбензоат 70n в качестве главного соединения и метил-4-амино-2-хлор-3-йодбензоат 70o в качестве побочного соединения.
J. Метил 4-амино-2-хлор-5-((триметилсилил)этинил)бензоат, 70p. К смеси соединения 70n (0,642 ммоль, 200 мг), CuI (0,064 ммоль, 12,2 мг) и Pd(PPh3)2Cl2 (0,064 ммоль, 45мг) в THF (2 мл) добавили этинилтриметилсилан (0,963 ммоль, 95 мг), а затем ввели Et3N (7,19 ммоль, 1 мл). Реакцию проводили в атмосфере N2. Полученную реакционную смесь перемешивали в течение полутора часов при комнатной температуре, а затем разделили между этилацетатом и водой. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 15% этилацетат/гексаны), получив соединение 70p.
K. Метил 6-хлор-1H-индол-5-карбоксилат, 70q. Смесь соединения 70p (0,532 ммоль, 150 мг) и CuI (0,32 ммоль, 60 мг) в DMF (1,5 мл) выдерживали в течение 5 часов при температуре 110°C, а затем охладили до комнатной температуры. Реакцию остановили водой и провели экстракцию этилацетатом. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 15% этилацетат/гексаны), получив соединение 70q.
Следуя процедуре, описанной выше для примера 70c и примера 70, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:
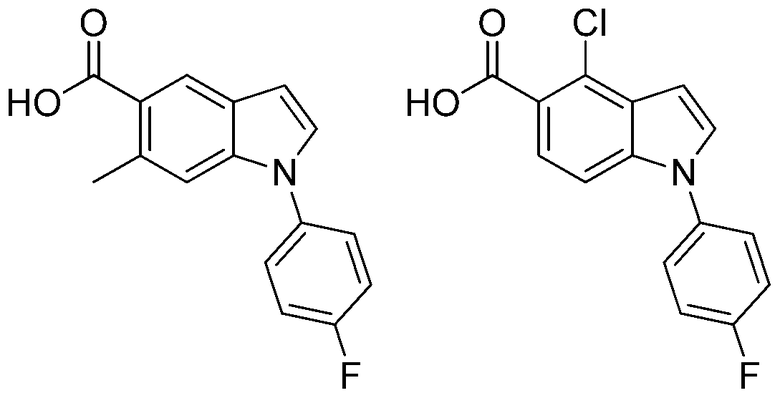
Следуя процедуре, описанной выше для примера 70, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 525
МС m/z (M+H+) 504
1H ЯМР (CDCl3): δ 7,87 (д, J=3,2 Гц, 1H), 7,54 (д, J=3,2 Гц, 1H), 7,40-7,46 (м, 2H), 7,34-7,39 (м, 2H), 7,19-7,29 (м, 3H), 6,83 (д, J=3,2 Гц, 1H), 4,52 (м, 1H), 4,35-4,48 (м, 1H), 4,30 (дд, J=9,9, 7,5 Гц, 1H), 4,08-4,18 (м, 1H), 3,75-4,05 (м, 4H), 3,23-3,33 (м, 1H), 2,37-2,57 (м, 4H)
МС m/z (M+H+) 525.
Пример 71

A. Метил 1-(2,2-дифторэтил)-1H-индол-5-карбоксилат, 71b. К суспензии NaH (60%-ная дисперсия в минеральном масле, 1,48 ммоль, 59 мг) в DMF (2 мл) постепенно добавили раствор метилового эфира 1H-индол-5-карбоновой кислоты, 1j (1,14 ммоль, 200 мг), в DMF (1 мл) при температуре 0°C. Полученный раствор перемешивали при 0°C в течение 20 минут, а затем добавили 1,1-дифтор-2-йодэтан 71a (1,37 ммоль, 263 мг). Смесь нагрели до комнатной температуры и перемешивали в течение 2 часов. Реакцию остановили водой и провели экстракцию этилацетатом. Органический слой сконцентрировали и очистили с использованием колоночной флэш-хроматографии (силикагель, 20% этилацетат/гексаны), получив соединение 71b.
B. 1-(2,2-Дифторэтил)-1H-индол-5-карбоновая кислота, 71c. Названное соединение 71c было получено способом, описанным в примере 29, с заменой соединения 29c на соединение 71b на стадии B.
C. 1-(2,2-Дифторэтил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индол, соединение 711. Названное соединение 711 было получено способом, описанным в примере 9, с заменой соединения 9с на соединение 71c на стадии D. 1H ЯМР (CDCl3): δ 7,94 (с, 1H), 7,88 (д, J=2,9 Гц, 1H), 7,59 (д, J=8,6 Гц, 1H), 7,54 (д, J=2,9 Гц, 1H), 7,36 (д, J=8,6 Гц, 1H), 7,17 (д, J=2,9 Гц, 1H), 6,63 (д, J=2,9 Гц, 1H), 6,01 (м, 1H), 4,51-4,24 (м, 7H), 4,12 (м, 1H), 3,85(м, 2H), 3,24 (м, 1H), 2,49 (м, 4H). МС m/z (M+H+) 460.
Следуя процедуре, описанной выше для примера 71, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

Следуя процедуре, описанной выше для примера 71, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
МС m/z (M+H+) 460
МС m/z (M+H+) 543
МС m/z (M+H+) 543
МС m/z (M+H+) 507
МС m/z (M+H+) 487
МС m/z (M+H+) 487
МС m/z (M+H+) 487
Пример 72

A. Этил 1-(4-фторбензил)-1H-индазол-5-карбоксилат, 72c, и этил 2-(4-фторбензил)-2H-индазол-5-карбоксилат, 72d. Этил 1H-индазол-5-карбоксилат 72a (0,79 ммоль, 150 мг) и Cs2CO3 (0,96 ммоль, 312 мг) смешали с 2 мл DMF, получив прозрачный красно-коричневый раствор. В раствор по каплям добавили чистый 1-(бромметил)-4-фторбензол 72b (0,87 ммоль, 0,11 мл) и смесь оставили на ночь перемешиваться при комнатной температуре. Затем добавили этилацетат, органический слой промыли водой и насыщенным солевым раствором. Органический раствор высушили над Na2SO4 и сконцентрировали, получив 260 мг твердого вещества оранжевого цвета. Полученный продукт очистили с использованием колоночной флэш-хроматографии (силикагель, 15-50% этилацетат/гексаны), получив 133 мг (57%) соединения 72c в виде твердого вещества оранжевого цвета и 67 мг (28%) соединения 72d в виде твердого вещества белого цвета.
Соединение 72c: 1H ЯМР (400 МГц, CDCl3): δ 1,41 (т, J=7,1 Гц, 3H), 4,40 (к, J=7,1 Гц, 2H), 5,58 (с, 2H), 6,99 (т, J=8,7 Гц, 2H), 7,19 (дд, J=8,8, 5,3 Гц, 2H), 7,36 (дт, J=8,9, 0,8 Гц, 1H), 8,04 (дд, J=8,9, 1,5 Гц, 1H), 8,15 (д, J=0,9 Гц, 1H), 8,53 (дд, J=1,5, 0,8 Гц, 1H). МС m/z (M+H+) 299,1.
Соединение 72d: 1H ЯМР (400 МГц, CDCl3): δ 1,41 (т, J=7,1 Гц, 3H), 4,39 (к, J=7,1 Гц, 2H), 5,59 (с, 2H), 7,07 (т, J=8,7 Гц, 2H), 7,27-7,34 (м, 2H), 7,72 (дт, J=9,1, 0,9 Гц, 1H), 7,92 (дд, J=9,1, 1,6 Гц, 1H), 8,02-8,06 (м, 1H), 8,48 (дд, J=1,5, 0,9 Гц, 1H). МС m/z (M+H+) 299,1.
B. 1-(4-Фторбензил)-1H-индазол-5-карбоксилат, 72e. К перемешиваемому раствору соединения 72c (0,43 ммоль, 128 мг) в 2,5 мл THF и 0,5 мл MeOH добавили 3Н водного раствора NaOH (2,62 ммоль, 0,87 мл) и 0,5 мл воды. Смесь оставили на ночь перемешиваться при комнатной температуре, а затем сконцентрировали под вакуумом. Полученный желтый остаток растворили в 10 мл воды и подкислили водным раствором HCl до pH 2-3. Получившийся осадок отфильтровали под вакуумом на бумажном фильтре и промыли водой. Оставшийся материал просушили под высоким вакуумом, получив 108 мг (93%) соединения 72e в виде бледно-желтого твердого вещества. 1H ЯМР (400 МГц, CDCl3): δ 1,41 (т, J=7,1 Гц, 3H), 4,39 (к, J=7,1 Гц, 2H), 5,59 (с, 2H), 7,07 (т, J=8,7 Гц, 2H), 7,27-7,34 (м, 2H), 7,72 (дт, J=9,1, 0,9 Гц, 1H), 7,92 (дд, J=9,1, 1,6 Гц, 1H), 8,02-8,06 (м, 1H), 8,48 (дд, J=1,5, 0,9 Гц, 1H). МС m/z (M+H+) 271,2.
C. 1-(4-Фторбензил)-5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индазол, соединение 1029. Названное соединение 1029 было получено способом, описанным в примере 9, с заменой соединения 9c на соединение 72e и HATU на HBTU на стадии D. 1H ЯМР (400 МГц, CDCl3): δ 1,41 (т, J=7,1 Гц, 3H), 4,39 (к, J=7,1 Гц, 2H), 5,59 (с, 2H), 7,07 (т, J=8,7 Гц, 2H), 7,27-7,34 (м, 2H), 7,72 (дт, J=9,1, 0,9 Гц, 1H), 7,92 (дд, J=9,1, 1,6 Гц, 1H), 8,02-8,06 (м, 1H), 8,48 (дд, J=1,5, 0,9 Гц, 1H). МС m/z (M+H+) 505,2.
Следуя процедуре, описанной выше для примера 72, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие промежуточные соединения:

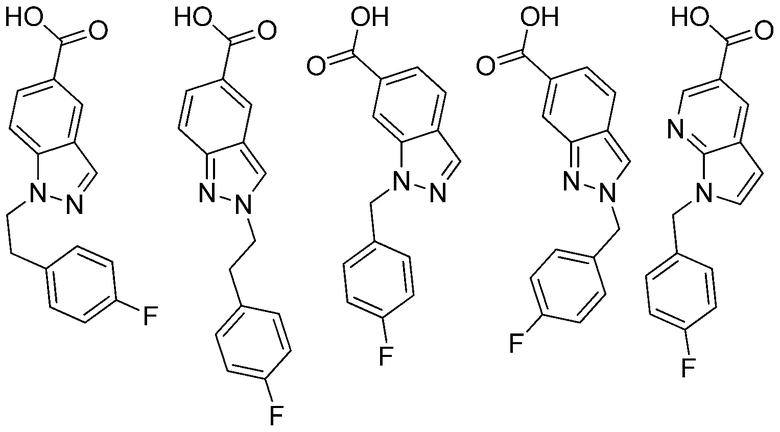
Следуя процедуре, описанной выше для примера 72, и заменив соответствующие реагенты, исходные соединения и способы очистки, известные специалистам в данной области, были получены следующие соединения, составляющие предмет настоящего изобретения:
1H ЯМР (400 МГц, CD3OD): δ 3,19-3,30 (м, 4H), 4,05 (д, J=5,6 Гц, 3H), 4,25-4,88 (м, 6H), 5,66 (с, 2H), 7,09 (т, J=8,4 Гц, 2H), 7,33-7,43 (м, 2H), 7,57 (д, J=9,0 Гц, 1H), 7,69 (д, J=9,0 Гц, 1H), 7,88 (м, J=2,9 Гц, 1H), 7,97 (д, J=2,7 Гц, 1H), 8,12 (с, 1H), 8,49 (с, 1H)
МС m/z (M+H+) 505,2
1H ЯМР (400 МГц, CD3OD): δ 3,24 (уш.с, 4H), 3,89-4,12 (м, 3H), 4,25-4,85 (м, 6H), 5,78 (с, 2H), 7,37 (м, J=8,1 Гц, 2H), 7,60 (м, J=8,1 Гц, 2H), 7,66 (д, J=8,8 Гц, 1H), 7,72 (дд, J=8,8, 1,5 Гц, 1H), 7,88 (д, J=3,0 Гц, 1H), 7,97 (д, J=3,3 Гц, 1H), 8,18 (с, 1H), 8,23 (с, 1H)
МС m/z (M+H+) 555,2
1H ЯМР (400 МГц, CD3OD): δ 3,18-3,41 (м, 4H), 3,92-4,18 (м, 3H), 4,27-4,86 (м, 6H), 5,79 (с, 2H), 7,47 (д, J=8,1 Гц, 2H), 7,58 (дд, J=9,1, 1,5 Гц, 1H), 7,66 (д, J=8,1 Гц, 2H), 7,70 (д, 1H), 7,88 (д, J=3,0 Гц, 1H), 7,97 (д, J=3,0 Гц, 1H), 8,14 (с, 1H), 8,56 (с, 1H)
МС m/z (M+H+) 555,2
1H ЯМР (400 МГц, CD3OD): δ 3,25 (уш.с, 4H), 3,89-4,13 (м, 3H), 4,22-4,82 (м, 6H), 5,78 (с, 2H), 7,40-7,54 (м, 3H), 7,58 (м, J=7,3 Гц, 1H), 7,69 (м, J=8,6 Гц, 1H), 7,73 (д, J=8,8 Гц, 1H), 7,88 (д, J=3,3 Гц, 1H), 7,97 (д, J=3,3 Гц, 1H), 8,18 (с, 1H), 8,24 (с, 1H)
МС m/z (M+H+) 555,2
1H ЯМР (400 МГц, CD3OD): δ 3,30 (уш.с, 4H), 4,04 (д, J=6,8 Гц, 3H), 4,29-4,84 (м, 6H), 5,78 (с, 2H), 7,58 (т, J=7,1 Гц, 3H), 7,64 (уш.с, 2H), 7,70 (д, J=9,1 Гц, 1H), 7,88 (д, J=3,0 Гц, 1H), 7,97 (д, J=3,0 Гц, 1H), 8,14 (с, 1H), 8,56 (с, 1H)
МС m/z (M+H+) 555,2
1H ЯМР (400 МГц, ацетон-d6): δ 2,01 (д, J=7,1 Гц, 3H), 3,35 (уш.с, 4H), 4,07 (уш.с, 2H), 4,11-4,19 (м, 1H), 4,25-4,53 (м, 2H), 6 4,60 (уш.с, 1H), 4,68-4,96 (м, 3H), 6,07 (к, J=7,1 Гц, 1H), 7,24 (д, J=7,1 Гц, 1H), 7,30 (т, J=7,3 Гц, 2H), 7,33-7,39 (м, 2H), 7,58-7,68 (м, 2H), 7,92 (д, J=3,3 Гц, 1H), 7,98 (д, J=3,0 Гц, 1H), 8,12 (с, 1H), 8,18 (с, 1H)
МС m/z (M+H+) 501,1
1H ЯМР (400 МГц, CD3OD): δ 2,04 (д, J=7,1 Гц, 3H), 3,20 (уш.с, 4H), 3,91-4,05 (м, 3H), 4,25-4,63 (м, 4H), 4,72 (уш.с, 2 4H), 5,94 (к, J=6,9 Гц, 1H), 7,25-7,39 (м, 5H), 7,57 (дд, J=9,0, 1,4 Гц, 1H), 7,69 (д, J=9,1 Гц, 1H), 7,88 (д, J=3,0 Гц, 1H), 7,97 (д, J=3,3 Гц, 1H), 8,12 (с, 1H), 8,51 (с, 1H)
МС m/z (M+H+) 501,3
1H ЯМР (400 МГц, CDCl3): δ 3,49 (уш.с, 4H), 4,12 (уш.с, 2H), 4,23-4,33 (м, 1H), 4,34-5,17 (м, 6H), 5,56 (с, 2H), 6,61 (д, J=3,5 Гц, 1H), 7,08 (т, J=8,7 Гц, 2H), 7,38 (дд, J=8,6, 5,6 Гц, 2H), 7,63 (д, J=3,5 Гц, 1H), 7,93 (д, J=3,3 Гц, 1H), 7,99 (д, J=3,3 Гц, 1H), 8,27 (д, J=1,8 Гц, 1H), 8,61 (д, J=1,8 Гц, 1H)
МС m/z (M+H+) 505,2
1H ЯМР (400 МГц, ацетон-d6): δ 3,24 (т, J=7,2 Гц, 2H), 3,40 (уш.с, 4H), 4,09 (уш.с, 2H), 4,16-4,23 (м, 1H), 4,31-4,65 (м, 4H), 6 4,69 (т, J=7,2 Гц, 2H), 4,85 (уш.с, 2H), 6,96 (т, J=8,8 Гц, 2H), 7,19 (дд, J=8,3, 5,6 Гц, 2H), 7,49 (д, J=8,8 Гц, 1H), 7,62 (дд, J=8,8, 1,3 Гц, 1H), 7,93 (д, J=3,0 Гц, 1H), 8,00 (д, J=3,0 Гц, 1H), 8,09 (с, 1H), 8,12 (с, 1H)
МС m/z (M+H+) 519,2
1H ЯМР (400 МГц, ацетон-d6): δ 3,35 (т, J=7,1 Гц, 2H), 3,38 - 3,43 (м, 4H), 4,09 (уш.с, 2H), 4,12-4,20 (м, 1H), 4,31-4,69 (м, 4 6H), 4,74 (т, J=7,2 Гц, 2H), 4,84 (уш.с, 2H), 7,01 (т, J=8,7 Гц, 2H), 7,21 (дд, J=8,3, 5,6 Гц, 2H), 7,55 (дд, J=9,1, 1,5 Гц, 1H), 7,66 (д, J=9,1 Гц, 1H), 7,93 (д, J=3,0 Гц, 1H), 8,00 (д, J=3,3 Гц, 1H), 8,03 (с, 1H), 8,23 (с, 1H)
МС m/z (M+H+) 519,2
1H ЯМР (400 МГц, ацетон-d6): δ 3,14-3,23 (м, 4H), 3,91-4,00 (м, 1H), 4,01-4,12 (м, 2H), 4,26-4,56 (м, 3H), 4,57-4,92 (м, 3 6H), 5,74 (с, 2H), 7,09 (т, J=8,8 Гц, 2H), 7,37-7,46 (м, 3H), 7,84 (д, J=8,3 Гц, 1H), 7,89-7,95 (м, 2H), 7,99 (д, J=3,0 Гц, 1H), 8,12 (с, 1H)
МС m/z (M+H+) 505,2
1H ЯМР (400 МГц, ацетон-d6): δ 3,21-3,30 (м, 4H), 3,94-4,15 (м, 3H), 4,28-4,52 (м, 2H), 4,52-4,68 (м, 1H), 4,68-4,93 (м, 3 6H), 5,72 (с, 2H), 7,15 (т, J=8,8 Гц, 2H), 7,34 (дд, J=8,6, 1,3 Гц, 1H), 7,45-7,52 (м, 2H), 7,75 (д, J=8,6 Гц, 1H), 7,91 (с, 1H), 7,92 (д, J=3,3 Гц, 1H), 7,99 (д, J=3,3 Гц, 1H), 8,42 (с, 1H)
МС m/z (M+H+) 505,2
Пример 72а

D. Метил 1-(4-цианобензил)-1H-индазол-5-карбоксилат, 72f. Названное соединение 72f было получено способом, описанным в примере 72, с заменой соединения 72a на метил 1H-индазол-5-карбоксилат и соединения 72b на 4-(бромметил)бензонитрил. 1H ЯМР (400 МГц, CDCl3): δ 3,95 (с, 3H), 5,67 (с, 2H), 7,26 (д, J=8,2 Гц, 2H), 7,33 (д, J=8,9 Гц, 1H), 7,61 (д, J=8,3 Гц, 2H), 8,06 (дд, J=8,9, 1,4 Гц, 1H), 8,18 (с, 1H), 8,55 (с, 1H). (M+H+) 292,2.
E. 1-(4-Цианобензил)-1H-индазол-5-карбоновая кислота, 72g и 1-(4-карбамоилбензил)-1H-индазол-5-карбоновая кислота, 72h. К перемешиваемому раствору соединения 72f (0,35 ммоль, 102 мг) в 2 мл THF и 0,5 мл MeOH добавили 3Н водного раствора NaOH (2,45 ммоль, 0,82 мл). Смесь оставили на ночь перемешиваться при комнатной температуре, а затем сконцентрировали под вакуумом. Полученный остаток желтого цвета растворили в 15 мл воды и подкислили водным раствором HCl до pH 1-2. Получившийся осадок отфильтровали под вакуумом на бумажном фильтре и промыли водой. Оставшийся материал просушили под высоким вакуумом, получив 87 мг смеси 3:1 соединений 72g и 72h (по результатам ЖХ/МС) в виде твердого вещества серовато-белого цвета.
Соединение 72g (с меньшей полярностью): МС m/z (M+H+) 278,1. Соединение 72h (с большей полярностью): МС m/z (M+H+) 296.
F. 4-{[5-({3-[4-(1,3-Тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индазол-1-ил]метил}бензонитрил, соединение 1045, и 4-{[5-({3-[4-(1,3-тиазол-2-ил-карбонил)пиперазин-1-ил]азетидин-1-ил}карбонил)-1H-индазол-1-ил]метил}бензамид, соединение 1044. Искомые соединения 1045 и 1044 были получены способом, описанным в примере 9, с заменой соединения 9c на смесь соединений 72g и 72h, синтезированных на стадии Е, а также с заменой HATU на HBTU на стадии D. Полученные соединения разделили методом препаративной обращенно-фазовой хроматографии, получив 64 мг соединения 1045 (с меньшей полярностью) и 6,4 мг соединения 1044 (с большей полярностью).
Соединение 1045: 1H ЯМР (400 МГц, ацетон-d6): δ 3,24-3,49 (м, 4H), 4,00-4,11 (м, 2H), 4,11-4,20 (м, 1H), 4,26-4,96 (м, 6H), 5,85 (с, 2H), 7,45 (д, J=8,3 Гц, 2H), 7,66-7,72 (м, 2H), 7,74 (д, J=8,3 Гц, 2H), 7,92 (д, J=3,3 Гц, 1H), 7,99 (д, J=3,0 Гц, 1H), 8,16 (с, 1H), 8,20 (с, 1H).
Соединение 1044: 1H ЯМР (400 МГц, ацетон-d6): δ 3,14 (уш.с, 4H), 3,87-3,96 (м, 1H), 3,96-4,08 (м, 2H), 4,35 (уш.с, 2H), 4,47-4,85 (м, 4H), 5,78 (с, 2H), 7,35 (д, J=8,3 Гц, 2H), 7,66 (с, J=8,8 Гц, 1H), 7,70 (д, J=8,6, 1,5 Гц, 1H), 7,88 (д, J=8,1 Гц, 2H), 7,91 (д, J=3,3 Гц, 1H), 7,98 (д, J=3,3 Гц, 1H), 8,16 (с, 1H), 8,18 (с, 1H)
Биологические исследования
Способы исследования in vitro
Пример 1
Анализ активности фермента MGL
Все представленные исследования проводились в 384-луночных черных полипропиленовых микропланшетах для полимеразной цепной реакции (ПЦР) производства компании Abgene суммарным объемом 30 мкл. Субстрат 4-метилумбеллиферилбутират (4MU-B, Sigma) и либо очищенный мутантный фермент MGL (mut-MGLL 11-313 L179S L186S), либо очищенный исходный фермент MGL (wt-MGLL 6H-11-313) по отдельности растворили в 20 ммоль буферного раствора (pH=7,0) 1,4-пиперазиндиэтансульфоновой кислоты (PIPES), содержащего 150 ммоль NaCl и 0,001% полисорбата 20 (Tween 20). Соединения формулы (I) предварительно поместили (по 50 нл) в планшет для анализа, используя систему Cartesian Hummingbird, и затем добавили 4MU-B (25 мкл 1,2X раствора до конечной концентрации 10 мкМ) и затем фермент (5 мкл 6X раствора до конечной концентрации 5 нМ) для инициирования реакции. Концентрация конечного продукта находилась в диапазоне от 17 до 0,0003 мкМ. Было зафиксировано изменение спектра флюоресценции, обусловленное расщеплением 4MU-B. Длины волн возбуждения и эмиссии составили 335 и 440 нм, соответственно, при ширине полосы 10 нм (спектрометр Safire2, Tecan). Исследование проводили при температуре 37°C в течение 5 минут.
Значения IC50 для соединений формулы (I) определяли с помощью Excel по результатам подгонки уравнения к концентрационной зависимости дробной активности в зависимости от концентрации ингибитора.
Биологические данные
пример
Пример 2
Исследование накопления 2-AG
Для измерения накопления 2-AG вследствие ингибирования MGL 1 грамм ткани мозга крысы гомогенизировали на гомогенизаторе Polytron (компании Brinkmann, PT300) в 10 мл буферного раствора HEPES (20 ммоль, pH=7,4), содержащего 125 ммоль NaCl, 1 ммоль ЭДТА, 5 ммоль KCl и 20 ммоль глюкозы. Соединения формулы (I) (10 мкМ) предварительно инкубировали в среде гомогената мозговой ткани крысы (50 мг). После 15-минутной инкубации при температуре 37°C добавили CaCl2 (до конечной концентрации 10 ммоль) и продолжили инкубацию еще 15 минут при температуре 37°C с общим объемом смеси 5 мл. Протекание реакций останавливали добавлением 6 мл раствора для экстракции органическими растворителями, содержащего хлороформ и метанол в соотношении 2:1 Накопленный 2-AG в органической фазе измерялся по методу ВЭЖХ/МС согласно следующему уравнению:
процент содержания в несущей среде = (аккумуляция 2-AG в присутствии соединения/аккумуляция 2-AG в несущей среде)×100.
Биологические данные
пример
Пример 3
Исследование мутантного фермента MGL методом ThermoFluor®
Метод исследования ThermoFluor (TF) представляет собой анализ связывания, проводимый с помощью 384-луночного планшета и определяющий термостойкость белков1,2. Эксперименты проводились с использованием инструментов, поставляемых Johnson & Johnson Pharmaceutical Research & Development, LLC. Краска TF, использованная во всех экспериментах, представляла собой 1,8-ANS (Invitrogen: A-47). TF-исследования фермента MGL проводили при следующих конечных условиях: 0,07 мг/мл мутантного фермента MGL, 100 мкМ ANS, 200 мМ NaCl, 0,001% Tween-20 в 50 мМ PIPES (pH=7,0).
На пластинах для скрининга соединения содержались 100%-ные растворы DMSO в одной концентрации. Для последующих концентрационных исследований соединения помещали в лунки планшета (компания Greiner Bio-one: 781280), в последовательных разведениях в 100% DMSO, используя 11 колонок лунок для каждой из серии исследований. Столбцы 12 и 24 использовались как DMSO-контроль и не содержали соединения. Как в однократных, так и во многократных экспериментах определения зависимости от концентрации аликвоты соединения (46 нл) автоматически распределяли непосредственно в черный 384-луночный планшет для исследований (Abgene: TF-0384/k) с помощью робота для распределения жидкостей Hummingbird. Затем туда же поместили растворы белка и красителя, в результате чего конечный исследуемый объем составил 3 мкл. Растворы, предназначенные для анализа, были покрыты 1 мкл силиконового масла (Fluka, тип DC 200: 85411) для предотвращения испарения.
Планшеты для анализа, снабженные штрихкодом, автоматически подавались в термоблок ПЦР-типа с регулируемой температурой и нагревались от 40 до 90°C со скоростью 1 градус в минуту для всех экспериментов. Флюоресценцию измеряли с помощью непрерывного источника ультрафиолетового излучения (Hamamatsu LC6), подаваемого через оптоволокно и пропускаемого через полосовой фильтр (380-400 нм; граница пропускания >6 ОП). Флуоресцентные эмиссии всей 384-луночной пластины определялись путем измерения интенсивности света с использованием ПЗС-камеры (Sensys, Roper Scientific) с применением фильтров для обнаружения 500±25 нм, что позволяло одновременно и независимо считывать все 384 лунки. Для каждого значения температуры получали один снимок с временем экспозиции 20 с, в данной области исследуемого планшета и подставляли ее в стандартное уравнение, получая величину Tm 1.
1. Pantoliano, M. W., Petrella, E. C., Kwasnoski, J. D., Lobanov, V. S., Myslik, J., Graf, E., Carver, T., Asel, E., Springer, B. A., Lane, P. и Salemme, F. R. (2001) J Biomol Screen 6, 429-40.
2. Matulis, D., Kranz, J. K., Salemme, F. R. и Todd, M. (2005) J. Biochemistry 44, 5258-66.
Значения Kd для соединений формулы (I) определили из результатов подгонки уравнения к концентрационной зависимости дробной активности в зависимости от величины Tm. В некоторых экспериментах для измерения концентраций исходных растворов веществ в 100% DMSO использовался метод количественной ЯМР-спектроскопии (кЯМР), а значения qKd были определены с использованием того же способа подгонки уравнения.
Биологические данные
Способы исследования in vivo
Пример 4
Измерение вызванной реагентом CFA гиперчувствительности крыс к тепловому воздействию
Каждая крыса была помещена в камеру для проведения исследований на теплую стеклянную поверхность и оставлена приблизительно на 10 минут для привыкания к новым условиям. Затем на подошвенную поверхность каждой из задних лапок крыс по очереди подействовали сквозь стекло тепловым раздражителем (лучом света). Тепловое воздействие автоматически прекращалось фотоэлектрическим реле, если лапка двигалась или если завершался период воздействия (20 с теплового облучения при ~5 амп). Для каждой из крыс был зафиксирован начальный (естественный) период ответа на термический раздражитель, после чего животным был введен полный адъювант Фрейнда (CFA). По прошествии 24 часов после введения CFA период ответа животных на термический раздражитель снова был измерен и сравнен с начальным. Анализ продолжали только для крыс, у которых имело место минимум 25%-ное сокращение латентного периода реакции (то есть имела место гипералгезия). Сразу по завершении оценки продолжительности латентного периода после введения CFA крысам перорально вводили указанное исследуемое лекарственное вещество или несущую среду. Затем, по прошествии определенных промежутков времени (обычно 30, 60, 120, 180 и 300 мин) оценивали латентный период реакции (отдергивания лапы) после прекращения введения указанного вещества.
Степень обращения гиперчувствительности (%R) рассчитывалась одним из двух способов: 1) на основе средних показателей по группе животных или 2) на основе показателей, полученных для отдельных животных. Более конкретно:
Способ 1. Для всех соединений в каждый конкретный момент времени величину %R гиперчувствительности вычисляли на основе средних показателей по группе животных, используя следующую формулу:
% обращения = [(реакция группы после введения соединения - реакция группы после введения CFA)/(начальная реакция группы - реакция после введения CFA)]×100
Представлены результаты для максимального процентного обращения для каждого соединения в конкретный момент времени.
Способ 2. Для ряда соединений величину %R гиперчувствительности вычисляли отдельно для каждого животного, используя следующую формулу:
% обращения = [(индивидуальная реакция после введения соединения - индивидуальная реакция после введения CFA)/(начальная индивидуальная реакция - индивидуальная реакция после введения CFA)]×100.
Результаты представлены в виде средних величин максимального процентного обращения, рассчитанного для каждого индивидуального животного.
Биологические данные: влияние CFA на гиперчувствительность к тепловому воздействию
(мг/кг, перорально)
Пример 5
Индуцированная CFA гиперчувствительность к надавливанию на лапу
Перед проведением эксперимента крыс приучали к будущей процедуре дважды в день на протяжении двух дней. Эксперимент заключался в размещении левой задней лапы животного на платформе с тефлоновым (политетрафторэтиленовым) покрытием и надавливании на нее с линейно растущим усилием (скорость увеличения давления - 1,67 кПа/с (12,5 мм рт.ст./с)) между третьей и четвертой плюсневой костью с тыльной стороны инструментом с куполовидным наконечником (радиусом 0,7 мм), измеряя аналгезию с помощью специального прибора (компания Stoelting, Чикаго, штат Иллинойс), известного как аппарат Рэндалла-Селитто. Эксперимент автоматически завершался при отдергивании задней лапы. В этот момент регистрировалась величина конечного усилия (в граммах). Перед введением полного адъюванта Фрейнда (CFA) для каждого животного также фиксировали начальный (базовый) порог реакции на механический раздражитель. Через 40 часов после введения CFA снова определяли порог реакции животного на механический раздражитель и сравнивали его с начальным значением. Реакцией считалось отдергивание лапы, попытка отдернуть лапу или подача голоса. Анализ продолжали только для крыс, у которых имело место минимум 25%-ное сокращение порога реакции (то есть имело место гипералгезия). Сразу по завершении оценки порога реакции после введения CFA крысам вводили указанное соединение или несущую среду. Пороги реакции (заключающейся в отдергивании лапы) после прекращения введения соединения оценивали спустя 1 час. Изменение порога реакции (отдергивания лапы) пересчитывали в процент изменения гиперчувствительности, используя следующую формулу:
% обращения = [(реакция после введения соединения - реакция до введения соединения)/(начальная реакция - реакция до введения соединения)]×100.
Биологические данные: индуцированная CFA гиперчувствительность к надавливанию на лапу
Пример 6
Модель индуцирования нейропатической боли посредством хронического компрессионного повреждения нерва (CCI): тест на гиперчувствительность с использованием холодного ацетона
Для оценки способности анализируемых соединений изменять вызванную CCI гиперчувствительность к холоду проводили эксперимент с крысами-самцами линии Sprague-Dawley (225-450 г). Вокруг левого седалищного нерва под ингаляционной анестезией делали не тугую перевязку с помощью 4 швов хромированного кетгута, как описано в работе Bennett et. al. (Bennett GJ, Xie YK. Pain 1988, 33(1): 87-107). Через 14-35 дней после операции CCI экспериментальное животное помещали в приподнятую клетку для наблюдения с проволочным дном, после чего с интервалом примерно в 5 минут пять раз на подошвенную часть лапы с помощью многодозового шприца наносили по 0,05 мл ацетона. Положительной реакцией считалось резкое отдергивание или поднятие лапы. Для каждого животного фиксировали количество положительных реакций на 5 доз ацетона. После определения начальной реакции указанным способом вводили исследуемое соединение в указанной несущей среде (см. таблицу 6). Через 1-4 часа после введения соединения снова определяли количество отдергиваний лапы. Результаты фиксировали в виде процента уменьшения реакции, который вычисляли для каждого животного по формуле: [1-(количество отдергиваний после введения исследуемого соединения/количество отдергиваний до введения соединения)]×100, после чего находили среднее между показателями всех животных, получивших соединение.
Биологические данные: индуцированная CCI гиперчувствительность к холоду
Пример 7
Модель индуцирования нейропатической боли посредством лигирования спинномозгового нерва (SNL): эксперимент с тактильной аллодинией
Для исследований с лигированием пятого (L5) корешка спинномозгового нерва проводили анестезию с помощью ингаляции изофлурана. Со спинной области таза срезали шерсть и выполняли 2-сантиметровый разрез кожи слева от срединной линии над спинной частью корешков L4-S2 спинномозгового нерва с последующим отделением параспинальных мышц от остистого отростка. Затем аккуратно удаляли поперечный отросток корешка L6 и открывали корешок L5 спинномозгового нерва. После этого туго лигировали левый корешок L5 спинномозгового нерва с помощью шелковой нити 6-0; на мышцу накладывали шов из викрила 4-0, а разрез кожи затягивали с помощью скоб для соединения краев раны. После операции подкожно вводили физраствор (5 мл).
Через 4 недели после лигирования проводили поведенческий тест. После начальной оценки чувствительности по методу фон Фрея для проверки наличия механической аллодинии крысам с SNL (L5) перорально вводили указанную несущую среду или соединение. Тактильную аллодинию определяли через 30, 60, 100, 180 и 300 мин после введения вещества, фиксируя усилие, при котором происходило отдергивание лапы, ипсилатерально по отношению к области лигирования, в ответ на стимулирование различными нитями фон Фрея (0,4, 0,6, 1,0, 2,0, 4, 6, 8 и 15 г, компания Stoelting, город Вуд-Дейл, штат Иллинойс). Начиная с нитей средней плотности (2,0 г), нити прикладывали к середине подошвенной области задней лапы примерно на 5 секунд для определения порога реакции. В случае резкого отдергивания лапы продолжали использовать менее жесткие нити, а при отсутствии реакции - более плотные. После определения начального порога реакции порог фиксировали еще четыре раза. 50% порогов отдергивания лапы были интерполированы по методу Диксона, описанному в обзоре Efficient analysis of experimental observations, Annu. Rev. Pharmacol. Toxicol. 20:441-462(1980) с модификацией, описанной в работе Chaplan et. al., Quantitative assessment of tactile allodynia in the rat paw, J. Neurosci. Methods. 53(1):55-63 (1994), а если порог реакции выходил за нижний или верхний предел диапазона оценки, то указывались значения для нитей 15,0 или 0,25 г, соответственно. Результаты оценки порога реакции по методу нитей фон Фрея были приведены как пороги отдергивания лапы в граммах. Данные были нормированы, а результаты представлены в виде % MPE (максимально возможный эффект) соединения, который вычисляется по следующей формуле:
Биологические данные: лигирование спинномозгового нерва - тактильная аллодиния
Приведенное выше техническое описание содержит сведения о принципах, лежащих в основе настоящего изобретения, и иллюстрирующие его примеры, однако необходимо понимать, что практическое применение изобретения распространяется на все обычные вариации, адаптации и (или) модификации в соответствии с приведенными ниже пунктами формулы и их аналогами.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЗЕТИДИНИЛДИАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ МОНОАЦИЛГЛИЦЕРИН-ЛИПАЗЫ | 2010 |
|
RU2549547C2 |
| ГЕТЕРОАРОМАТИЧЕСКИЕ И АРОМАТИЧЕСКИЕ ПИПЕРАЗИНИЛАЗЕТИДИНИЛАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ МОНОАЦИЛГЛИЦЕРИНЛИПАЗЫ | 2010 |
|
RU2558141C2 |
| ПИРАЗИНЫ ДЛЯ ИСПОЛЬЗОВАНИЯ В КАЧЕСТВЕ МОДУЛЯТОРОВ ДЕЛЬТА-ОПИОИДНЫХ РЕЦЕПТОРОВ | 2010 |
|
RU2543484C2 |
| ИНГИБИТОРЫ ФЕРМЕНТА ДИАЦИЛГЛИЦЕРИН О-АЦИЛТРАНСФЕРАЗЫ ТИПА 1 | 2008 |
|
RU2497816C2 |
| ХИНОКСАЛИНЫ И АЗАХИНОКСАЛИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРА CRTH | 2011 |
|
RU2589709C2 |
| ПИРИМИДИНОВЫЕ СОЕДИНЕНИЯ ДЛЯ ИСПОЛЬЗОВАНИЯ В КАЧЕСТВЕ МОДУЛЯТОРОВ ДЕЛЬТА-ОПИОИДНЫХ РЕЦЕПТОРОВ | 2010 |
|
RU2568434C2 |
| ПРОИЗВОДНЫЕ АЗАСПИРОАЛКАНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ МЕТАЛЛОПРОТЕАЗ | 2004 |
|
RU2379303C2 |
| АЗААДАМАНТАНОВЫЕ ПРОИЗВОДНЫЕ И СПОСОБЫ ПРИМЕНЕНИЯ | 2007 |
|
RU2450002C2 |
| ПРОИЗВОДНЫЕ БЕТА-КАРБОЛИНА, ОБЛАДАЮЩИЕ ДЕЙСТВИЕМ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ, СПОСОБ ИНГИБИРОВАНИЯ ДЕЙСТВИЯ ФОСФОДИЭСТЕРАЗЫ (ВАРИАНТЫ) И СПОСОБ УВЕЛИЧЕНИЯ КОНЦЕНТРАЦИИ ЦГМФ | 2001 |
|
RU2271358C2 |
| БОРСОДЕРЖАЩИЕ МАЛЫЕ МОЛЕКУЛЫ В КАЧЕСТВЕ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СРЕДСТВ | 2007 |
|
RU2508113C2 |
Изобретение относится к соединениям формулы (I), где Y и Z независимо выбраны из группы а) или b) таким образом, что один из Y или Z выбран из группы а), а другой - из группы b); группа а) представляет собой i) замещенный C6-10арил; ii) C3-8циклоалкил, необязательно замещенный одним или двумя заместителями, представляющими собой фтор; iii) трифторметил; или iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, пиримидинила, изоксазолила, бензотиенила, тиено[3,2-b]тиофен-2-ила, пиразолила, триазолила и [1,2,3]тиадиазолила; где C6-10арил замещен, а гетероарил необязательно замещен одним заместителем, выбранным из группы, состоящей из фтора, хлора, брома, C1-4алкила, C1-4алкокси и C1-4алкилкарбониламино; группа b) представляет собой i) C6-10арил; ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1Н-пирроло[3,2-b]пиридин-5-ила, 1Н-тиено[2,3-c]пиразол-5-ила, 1Н-пирроло[2,3-b]пиридин-5-ила, 1Н-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пирролила, пиразолила и бензимидазолила; iii) 2,3-дигидро-1Н-индолил; vi) 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1Н-индазол-3-ил; или ix) дифенил-1Н-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя заместителями, представляющими собой хлор, и в котором указанный пиразолил необязательно замещен одним заместителем, представляющим собой метил; где C6-10арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из брома, хлора, фтора, йода, C1-4алкила, C1-4алкокси и трифторметила; а также где C6-10арил и гетероарил замещены одним дополнительным заместителем, выбранным из группы, состоящей из i) С6-10арила; ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила, изоксазолила, бензимидазолила, пирролила, фуранила и пиразолила; где указанный гетероарил необязательно замещен одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом; и где фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителями, представляющими собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано)этиламинокарбонила; циано; карбокси; аминокарбонила; формила; нитро; брома; гидрокси; и NRcRd, в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкил, ди(C1-4алкил)аминосульфонил и C1-4алкилсульфонил; s равно 0, 1 или 2; R1 представляет собой C6-10арил, C1-3алкил; или его фармацевтически приемлемым солям. Соединения формулы (I) используются для изготовления фармацевтической композиции, обладающей ингибирующей активностью в отношении моноацилглицеринлипазы (MGL), содержащей терапевтически эффективное количество соединения формулы (I) и по меньшей мере один фармацевтически приемлемый носитель, фармацевтически приемлемый эксципиент и фармацевтически приемлемый разбавитель. Технический результат - соединения, предназначенные для лечения воспалительной боли. 7 н. и 13 з.п. ф-лы, 7 табл., 131 пр.

Формула (I)
1. Соединение формулы (I)

где
Y и Z независимо выбраны из группы а) или b) таким образом, что один из Y или Z выбран из группы а), а другой - из группы b);
группа а) представляет собой
i) замещенный C6-10арил;
ii) C3-8циклоалкил, необязательно замещенный одним или двумя заместителями, представляющими собой фтор;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, пиримидинила, изоксазолила, бензотиенила, тиено[3,2-b]тиофен-2-ила, пиразолила, триазолила и [1,2,3]тиадиазолила;
где C6-10арил замещен, а гетероарил необязательно замещен одним заместителем, выбранным из группы, состоящей из фтора, хлора, брома, C1-4алкила, C1-4алкокси и C1-4алкилкарбониламино;
группа b) представляет собой
i) C6-10арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1Н-пирроло[3,2-b]пиридин-5-ила, 1Н-тиено[2,3-c]пиразол-5-ила, 1Н-пирроло[2,3-b]пиридин-5-ила, 1Н-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пирролила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1Н-индолил;
vi) 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1Н-индазол-3-ил;
или
ix) дифенил-1Н-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя заместителями, представляющими собой хлор, и в котором указанный пиразолил необязательно замещен одним заместителем, представляющим собой метил;
где C6-10арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из брома, хлора, фтора, йода, C1-4алкила, C1-4алкокси и трифторметила; а также где C6-10арил и гетероарил замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) С6-10арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила, изоксазолила, бензимидазолила, пирролила, фуранила и пиразолила;
где указанный гетероарил необязательно замещен одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
и где фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителями, представляющими собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано)этиламинокарбонила; циано; карбокси; аминокарбонила; формила; нитро; брома; гидрокси; и NRcRd, в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкил, ди(C1-4алкил)аминосульфонил и C1-4алкилсульфонил;
s равно 0, 1 или 2; R1 представляет собой C6-10арил, C1-3алкил;
и при условии, что соединение формулы (I) отлично от
соединения, в котором Y представляет собой 3-хлорбензотиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 2-цианофенил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой пиримидин-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, s равно 1, a R1 представляет собой 3-фенил;
а также его фармацевтически приемлемые соли.
2. Соединение по п. 1, где
группа а) представляет собой
i) замещенный C6-10арил;
ii) C3-8циклоалкил, необязательно замещенный одним или двумя заместителями, представляющими собой фтор;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, изоксазолила, бензотиенила, тиено[3,2-b]тиофен-2-ила, триазолила и [1,2,3]тиадиазолила;
где C6-10арил замещен, а гетероарил необязательно замещен одним заместителем, выбранным из группы, состоящей из фтора, хлора, брома и C1-4алкила.
3. Соединение по п. 2, где
группа а) представляет собой
i) замещенный C6-10арил;
ii) C3-8циклоалкил, необязательно замещенный одним или двумя заместителями, представляющими собой фтор;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, изоксазолила, тиено[3,2-b]тиофен-2-ил и [1,2,3]тиадиазолила;
где C6-10арил замещен, а гетероарил необязательно замещен одним заместителем, выбранным из группы, состоящей из фтора, хлора, брома и C1-4алкила.
4. Соединение по п. 3, где
группа а) представляет собой
i) циклопропил, необязательно замещенный одним или двумя заместителями, представляющими собой фтор;
ii) трифторметил; или
iii) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила и изоксазолила;
в котором C6-10арил замещен, а гетероарил необязательно замещен одним заместителем, выбранным из группы, состоящей из фтора, хлора и брома.
5. Соединение по п. 1, где
группа b) представляет собой
i) C6-10арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1Н-пирроло[3,2-b]пиридин-5-ила, 1Н-тиено[2,3-c]пиразол-5-ила, 1Н-пирроло[2,3-b]пиридин-5-ила, 1Н-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пирролила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1Н-индолил;
vi) 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1Н-индазол-3-ил;
или
ix) дифенил-1Н-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем,
в котором C6-10арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила, а C6-10арил и гетероарил замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила, изоксазолила, бензимидазолила, пирролила, фуранила и пиразолила;
в котором указанный гетероарил необязательно замещен одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; C1-4алкокси; от одного до трех заместителями, представляющими собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано)этиламинокарбонила; циано; карбокси; аминокарбонила; формила; нитро; брома; гидрокси; и NRcRd, где Rc представляет собой водород или C1-6алкил и где Rd представляет собой водород, C1-6алкил и C1-4алкилсульфонил.
6. Соединение по п. 5, где
группа b) представляет собой
i) C6-10арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1Н-пирроло[3,2-b]пиридин-5-ила, 1Н-тиено[2,3-c]пиразол-5-ила, 1Н-пирроло[2,3-b]пиридин-5-ила, 1Н-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1Н-индолил;
или
vii) дифенил-1Н-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем;
в котором C6-10арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила,
а C6-10арил и гетероарил замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила, изоксазолила, бензимидазолила, фуранила и пиразолила;
в котором указанный гетероарил необязательно замещен одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; C1-4алкокси; от одного до трех заместителями, представляющими собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано)этиламинокарбонила; циано; аминокарбонила; формила; нитро; брома; гидрокси; и NRcRd, где Rc представляет собой водород или C1-6алкил и где Rd представляет собой водород, C1-6алкил и C1-4алкилсульфонил.
7. Соединение по п. 6, где
группа b) представляет собой
i) C6-10арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1Н-пирроло[3,2-b]пиридин-5-ила, 1Н-тиено[2,3-c]пиразол-5-ила, 1Н-пирроло[2,3-b]пиридин-5-ила, фуранила, тиенила, [1,3,4]оксадиазол-2-ила и бензимидазолила;
iii) 2,3-дигидро-1H-индолил; или
vii) дифенил-1Н-пиразол-3-ил; в котором каждый фенил независимо замещен одним или двумя хлор-заместителями;
в котором C6-10арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила;
а C6-10арил и гетероарил замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила и пиразолила;
в котором указанный гетероарил необязательно замещен одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; C1-4алкокси; от одного до трех заместителями, представляющими собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4) алкенила; циано; формила; нитро; брома; гидрокси; NRcRd, где Rc представляет собой водород или C1-6алкил и где Rd представляет собой водород и C1-4алкилсульфонил.
8. Соединение по п. 1, где s равно 0 или 1.
9. Соединение по п. 8, где s равно 0.
10. Соединение по п. 1, где R1 представляет собой фенил или C1-3алкил.
11. Соединение по п. 10, где R1 представляет собой фенил.
12. Соединение формулы (I)

где
Y и Z независимо выбраны из группы а) или b) таким образом, что один из Y или Z выбран из группы а), а другой - из группы b);
группа а) представляет собой
i) замещенный C6-10арил;
ii) C3-8циклоалкил, необязательно замещенный одним или двумя фтор-заместителями;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, изоксазолила, бензотиенила, тиено[3,2-b]тиофен-2-ила, триазолила и [1,2,3]тиадиазолила;
в котором C6-10арил замещен, а гетероарил необязательно замещен одним заместителем выбранным из группы, состоящей из фтора, хлора, брома и C1-4алкила;
группа b) представляет собой
i) C6-10арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1Н-пирроло[3,2-b]пиридин-5-ила, 1Н-тиено[2,3-c]пиразол-5-ила, 1Н-пирроло[2,3-b]пиридин-5-ила, 1Н-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пирролила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1Н-индолил;
vi) 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1Н-индазол-3-ил;
или
ix) дифенил-1Н-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем,
в котором C6-10арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила;
а C6-10арил и гетероарил замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила, изоксазолила, бензимидазолила, пирролила, фуранила и пиразолила;
в котором указанный гетероарил необязательно замещен одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителей, представляющих собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано)этиламинокарбонила; циано; карбокси; аминокарбонила; формила; нитро; брома; гидрокси; и NRcRd, в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкил и C1-4алкилсульфонил;
s равно 0 или 1;
R1 представляет собой C6-10арил или C1-3алкил;
и при условии, что соединение формулы (I) отлично от соединения, в котором Y представляет собой 3-хлорбензотиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 2-цианофенил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0; соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой пиримидин-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, s равно 1, a R1 представляет собой 3-фенил;
а также его фармацевтически приемлемые соли.
13. Соединение формулы (I)

где
Y и Z независимо выбраны из группы а) или b) таким образом, что один из Y или Z выбран из группы а), а другой - из группы b);
группа а) представляет собой
i) замещенный C6-10арил;
ii) C3-8циклоалкил, необязательно замещенный одним или двумя фтор-заместителями;
iii) трифторметил; или
iv) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила, изоксазолила, тиено[3,2-b]тиофен-2-ил и [1,2,3]тиадиазолила;
в котором C6-10арил замещен, гетероарил необязательно замещен одним заместителем выбранным из группы, состоящей из фтора, хлора, брома и C1-4алкила;
группа b) представляет собой
i) C6-10арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, пиридинила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1Н-пирроло[3,2-b]пиридин-5-ила, 1Н-тиено[2,3-c]пиразол-5-ила, 1Н-пирроло[2,3-b]пиридин-5-ила, 1Н-пиразоло[3,4-b]пиридин-5-ила, фуро[2,3-b]пиридин-2-ила, фуранила, [1,2,3]триазолила, тиенила, оксазолила, [1,3,4]оксадиазол-2-ила, пиразолила и бензимидазолила;
iii) 2,3-дигидро-1Н-индолил;
или
vii) дифенил-1Н-пиразол-3-ил; в котором каждый фенил необязательно замещен одним или двумя хлор-заместителями; при этом указанный пиразолил необязательно замещен одним метильным заместителем;
в котором C6-10арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила;
а C6-10арил и гетероарил замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила, изоксазолила, бензимидазолила, фуранила и пиразолила;
в котором указанный гетероарил необязательно замещен одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
и в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителями, представляющими собой фтор или хлор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; (2-циано)этиламинокарбонила; циано; аминокарбонила; формила; нитро; брома; гидрокси; NRcRd, в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород, C1-6алкил и C1-4алкилсульфонил;
s равно 0 или 1;
R1 представляет собой фенил или C1-3алкил;
и при условии, что соединение формулы (I) отлично от соединения, в котором Y представляет собой 3-хлорбензотиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 2-цианофенил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой пиримидин-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, s равно 1, a R1 представляет собой 3-фенил;
а также его фармацевтически приемлемые соли.
14. Соединение формулы (I)
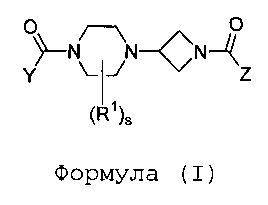
где
Y и Z независимо выбраны из группы а) или b) таким образом, что один из Y или Z выбран из группы а), а другой - из группы b);
группа а) представляет собой
i) циклопропил, необязательно замещенный одним или двумя фтор-заместителями;
ii) трифторметил; или
iii) гетероарил, выбранный из группы, состоящей из тиенила, фуранила, тиазолила, изотиазолила, оксазолила, пирролила и изоксазолила;
в котором C6-10арил замещен, а гетероарил необязательно замещен одним заместителем, выбранным из группы, состоящей из фтора, хлора или брома;
группа b) представляет собой
i) C6-10арил;
ii) гетероарил, выбранный из группы, состоящей из тиазолила, индолила, индазолила, бензоксазолила, бензотиазолила, бензофуранила, бензотиенила, 1Н-пирроло[3,2-b]пиридин-5-ила, 1Н-тиено[2,3-c]пиразол-5-ила, 1Н-пирроло[2,3-b]пиридин-5-ила, фуранила, тиенила, [1,3,4]оксадиазол-2-ила и бензимидазолила;
iii) 2,3-дигидро-1Н-индолил;
или
vii) дифенил-1Н-пиразол-3-ил, в котором каждый фенил независимо замещен одним или двумя хлор-заместителями;
в котором C6-10арил, 2,3-дигидро-1Н-индолил и гетероарил из группы b) необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из хлора, фтора, C1-4алкила, C1-4алкокси и трифторметила;
а C6-10арил и гетероарил замещены одним дополнительным заместителем, выбранным из группы, состоящей из
i) C6-10арила;
ii) гетероарила, выбранного из группы, состоящей из тиенила, хинолинила, пиридинила и пиразолила;
в котором указанный гетероарил необязательно замещен одним фенильным заместителем, при этом указанный фенильный заместитель необязательно замещен одним или двумя хлорными заместителями или трифторметилом;
в котором фенил C6-10арила и гетероарил необязательно независимо замещены одним или двумя заместителями, выбранными из группы, состоящей из C1-4алкила; цианометила; C1-4алкокси; от одного до трех заместителями, включающими хлор или фтор; трифторметила; трифторметокси; C1-4алкилкарбонила; C1-4алкоксикарбонил(C2-4)алкенила; циано(C2-4)алкенила; формила; нитро; брома; гидрокси; NRcRd, в котором Rc представляет собой водород или C1-6алкил и в котором Rd представляет собой водород и C1-4алкилсульфонил;
s равно 0 или 1;
R1 представляет собой фенил;
и при условии, что соединение формулы (I) отлично от
соединения, в котором Y представляет собой 3-хлортиен-2-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой 5-метилизоксазол-3-ил, Z представляет собой 4-бифенил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)оксазол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-пиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(2-фторпиридин-3-ил)-1Н-бензимидазол-2-ил и s равно 0
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, s равно 1, a R1 представляет собой 3-фенил;
а также его фармацевтически приемлемые соли.
15. Соединение формулы (I)

выбранное из группы, состоящей из:
соединения, в котором Y представляет собой фуран-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-5-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 2-метилтиазол-4-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 1-метил-1Н-пиррол-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 5-бромфуран-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой тиен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 5-метилтиен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 5-бромтиен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 5-хлортиен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 3-бромтиен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 4-бромтиен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой тиено[3,2-b]тиофен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой бензотиен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 3-метокситиен-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-бифенил, s равно 1, a R1 представляет собой 2-метил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-бифенил, s равно 1, a R1 представляет собой 2-фенил;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(тиен-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(тиен-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиридин-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиридин-3-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиридин-4-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(пиридин-3-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(пиримидин-5-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(пиримидин-5-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(2-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(2-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(4-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(6-бромпиридин-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(5-нитропиридин-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-нитропиридин-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-фторфенил)пиридин-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-фторфенил)тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-фторфенил)тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(2,4-дихлорфенил)тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3,5-дихлорфенил)тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-метоксифенил)тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилтиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-цианофенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-хлорфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-хлорфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3,5-дихлорфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилпиридин-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фтор-4-фенилфенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-цианофенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-бромфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 5-фенилпиридин-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фтор-4-фенилфенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(4-цианофенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(4-бромфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3,4-дихлорфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-фтор-2-метилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-хлор-4-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(2,4-дифторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метоксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(бензо[1,3]диоксал-5-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(нафт-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-нитрофенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-хинолин-5-ил-фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-карбоксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-цианометилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метилсульфонилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-метилкарбонилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-формилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-гидроксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-хлор-3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4,5-дифтор-2-метоксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-нитрофенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-формил-4-метоксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-аминокарбонилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-гидроксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-изобутилоксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(4-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(2,4-дифторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3-хлор-4-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3,4-дихлорфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-аминофенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-метил-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метил-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фтор-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-фтор-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-метокси-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метокси-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-хлор-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-хлор-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метил-4-(3-хлор-4-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-метил-4-(4-хлор-3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-4-(3-хлор-4-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-4-(4-хлор-3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метокси-4-(3-хлор-4-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метокси-4-(4-хлор-3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-хлор-4-(3-хлор-4-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-хлор-4-(4-хлор-3-трифторметилфенил)фенил, а s равно 0;
соединения, в котором Y представляет собой 4-фторфенил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 2-фторфенил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой тиен-3-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой циклопропил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 3-фторфенил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой оксазол-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой [1,2,3]тиадиазол-4-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой изоксазол-5-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой изотиазол-5-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой пиррол-3-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой 5-хлорфуран-2-ил, Z представляет собой 4-бифенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенил-3-метилиндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4,5-трифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-1Н-пирроло[2,3-b]пиридин-5-ил, a s равно 0;
соединения, в котором Y представляет собой циклопропил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-фторфенил)-5-метилтиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-7-(3-трифторметилфенил)индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(2,4-дифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(6-трифторметилпиридин-3-ил)индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фтор-6-(4-трифторметилфенил)бензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметилфенил)-1Н-бензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-метил-5-(3-фторфенил)тиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-7-(3-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 4-(3-трифторметилфенил)фенил, Z представляет собой тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметоксифенил)-3-метилиндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-6-фториндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(5-трифторметилтиен-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(6-метоксипиридин-3-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-метилпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой (2-метил-4-фенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-(4-фторфенил)-1Н-индол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-7-метилиндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3,4-дифторфенил)бензоксазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой 5-хлорфуран-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметилфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-2,3-дигидро-1Н-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фторфенил)тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)-1-(3,4-дихлорфенил)-1Н-пиразол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-метил-3-(3-трифторметилфенил)индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой оксазол-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой 4-бромтиен-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-3-метилиндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 1-(4-фторфенил)-3-метилиндол-5-ил, Z представляет собой тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(4-метоксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фтор-5-(4-трифторметилфенил)бензотиен-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой оксазол-4-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-трифторметил-6-фенилбензотиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фторфенил)-5-метилтиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой изотиазол-5-ил, Z представляет собой 1-(4-трифторметилфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-трифторметил-6-фенилбензотиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(4-фторфенил)-2,3-дигидро-1Н-индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(3-трифторметилфенил)индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-7-(4-фторфенил)индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)-1-(2,4-дихлорфенил)-4-метил-1Н-пиразол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-5-фторфенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(6-метилпиридин-3-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дифторфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2-метоксипиридин-4-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2-цианофенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-фторфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-7-фториндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 2,2-дифторциклопропил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-цианофенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой изотиазол-5-ил, Z представляет собой 3-метил-4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-хлор-5-трифторметилпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(2,4-дифторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой изоксазол-5-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2,3-дифенил-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-фторпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилтиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3,5-дифторфенил)пиразол-1-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(3-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилбензотиазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(6-метилпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(пиридин-4-ил)-индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-метилпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4-дифторфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-фторфенил)бензотиазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-фенилиндол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-цианофенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 1-(3,4-дифторфенил)-3-метилиндол-5-ил, Z представляет собой тиазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(пиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 4-(5-трифторметилтиен-2-ил)фенил, Z представляет собой тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-фенилиндазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 4-(5-трифторметилтиен-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(2,4-дифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой фуран-3-ил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенилбензоксазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(3-фторфенил)индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой 5-хлортиен-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-5-трифторметилфенил, a s равно 0;
соединения, в котором Y представляет собой изоксазол-3-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметилфенил)-3-метил-1Н-тиено[2,3-с]пиразол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-фторпиримидин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-метил-3-(4-трифторметилфенил)индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-(2-фторпиридин-3-ил)-1Н-индол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-метил-(2-(4-фторфенил)тиазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-трифторметилфенил)бензоксазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-3-метилиндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-1Н-пирроло[3,2-b]пиридин-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилбензоксазол-7-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-метил-3-фенилиндол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-(4-метилфенил)-[1,3,4]оксадиазол-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фторфенил)тиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-трифторметилфенил)бензоксазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-цианофенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-фторфенил)тиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой 4-(5-трифторметилтиен-2-ил)фенил, Z представляет собой тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой 4-(5-трифторметилтиен-2-ил)фенил, Z представляет собой 1Н-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенилиндазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1,5-дифенилпиразол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(пиридин-2-ил)бензотиазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой 4-(3-трифторметилфенил)фенил, Z представляет собой 1Н-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)бензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой оксазол-5-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(3-фторфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-аминокарбонилфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фтор-3-фенилфенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(2-хлорфенил)бензоксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(пиримидин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-(5-метоксипиридин-3-ил)-1Н-индол-2-ил, а s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(6-метоксипиридин-3-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-аминокарбонилфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3,4-дифторфенил)бензоксазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4,5-дифенил-1Н-имидазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(5-хлорпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(6-метилпиридин-3-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(2-цианофенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 7-(3-фторфенил)-1Н-индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(2-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дифторфенил)бензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенилбензотиазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(пиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенилбензоксазол-6-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-хлорфенил)бензоксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(пиридин-3-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(2-фторфенил)бензоксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-1Н-бензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(4-фторфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(5-метоксипиридин-3-ил)-1Н-индол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-метилпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 5-(4-хлорфенил)-1-(2,4-дихлорфенил)-4-метил-1Н-пиразол-3-ил, a s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(4-метилпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(2-фторфенил)-4-метилтиазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-3-метил-1Н-пиразоло[3,4-b]пиридин-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(4-фторфенил)-1Н-индол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дифторфенил)-2-метилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-фтор-дифенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилфуро[2,3-b]пиридин-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(тиазол-2-ил)-бензотиазол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(3,5-диметилизоксазол-4-ил)-1Н-индол-2-ил, a s равно 0;
соединения, в котором Y представляет собой 3-метил-4-(3-трифторметилфенил)фенил, Z представляет собой тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-фторфенил)-фуро[2,3-b]пиридин-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-метил-2-(4-метилфенил)-2Н-[1,2,3]триазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметилфенил)-2-метилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2-метилпиримидин-4-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 2-метилтиазол-4-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-метил-2-(4-хлорфенил)-2Н-[1,2,3]триазол-4-ил, а s равно 0;
соединения, в котором Y представляет собой 1-(3,4-дифторфенил)-3-метилиндол-5-ил, Z представляет собой 1Н-пиррол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-хлорфенил)бензоксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой оксазол-4-ил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(бензимидазол-1-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)индол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4-дихлорфенил)-3,5-диметил-1Н-пиразол-4-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-фторфенил)индол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-2-метилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(3-фторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенил-2-метилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-трифторметилфенил)бензимидазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой циклобутил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой 2-фенилбензоксазол-6-ил, Z представляет собой тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-метил-3-фенилфенил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой изотиазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенилбензоксазол-7-ил и s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-хлорфенил)бензоксазол-7-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(2,4-дифторфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фтор-3-фенилфенил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой 3-фторфенил, a s равно 0;
соединения, в котором Y представляет собой 4-(3-трифторметилфенил)фенил, Z представляет собой 1Н-пиррол-3-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 6-(2-фторпиридин-3-ил)-1Н-индол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-(4-метилфенил)-[1,2,3]триазол-1-ил)-фенил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(пиридин-3-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(5-фторпиримидин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трифторметилпиразол-1-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(4-метоксифенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(пиридин-3-ил)бензоксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(фуран-2-ил)-3Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-фторфенил)бензоксазол-7-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-3Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой 2,2-дифторциклопропил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(4-фторфенил)бензоксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой 4-(3-трифторметилфенил)фенил, Z представляет собой оксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-фенил-5-трифторметилфенил, a s равно 0;
соединения, в котором Y представляет собой 3-метил-4-(3-трифторметилфенил)фенил, Z представляет собой тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1,5-дифенил-1Н-пиразол-3-ил, a s равно 0;
соединения, в котором Y представляет собой изоксазол-3-ил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-пиримидин-5-ил-индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4-дифторфенил)-2-метилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1Н-индазол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-5-ил, Z представляет собой 4-(5-трифторметилтиен-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой 1Н-[1,2,3]триазол-4-ил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4-дифторфенил)бензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 2-фенил-1Н-бензимидазол-5-ил, Z представляет собой тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(пиридин-4-ил)-4-метилтиазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 5-фтор-дифенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)бензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 2-фенилбензоксазол-6-ил, Z представляет собой тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой [1,2,3]тиадиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-1Н-пирроло[3,2-b]пиридин-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(4-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3-фторфенил)индол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-фтор-дифенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-фторфенил)бензоксазол-7-ил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой оксазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-3-фенилфенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(2-фторфенил)-4-метилтиазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-трифторметилфенил)-2-метилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-хлорфенил)-1Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-2-метилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой 1Н-пиррол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-бензимидазол-1-ил-фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-фторфенил)-1Н-бензимидазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)-индол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-фенил-2-метилбензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1,5-дифенилпиразол-4-ил, a s равно 0;
соединения, в котором Y представляет собой 4-бензимидазол-1-ил-фенил, Z представляет собой тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенил-1Н-бензимидазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-[1,2,3] триазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-3,5-диметил-1Н-пиразол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 4-(3-трифторметилпиразол-1-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-трифторметоксифенил)-1Н-бензимидазол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1Н-индазол-3-ил, a s равно 0;
соединения, в котором Y представляет собой 4-бензимидазол-1-ил-фенил, Z представляет собой тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-хлорфенил)-1Н-пиррол-2-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-индол-3-ил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1Н-индазол-3-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиразол-4-ил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(2,4-дихлорфенил)-4,5,6,7-тетрагидро-1Н-индазол-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(6-трифторметилпиридин-3-ил)индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-хлорпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(5-трифторметилпиридин-2-ил)индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фтор-5-фенилбензотиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-фенил-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(4-фторфенил)-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(4-фторфенил)индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(3-фторфенил)-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)индол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трифторметилфенил)тиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-3-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-фенилтиазол-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-(4-хлорфенил)-4,5,6,7-тетрагидроиндазол-2-ил)-фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(2-хлорфенил)-тиазол-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(2,4-дихлорфенил)-тиазол-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(3,4-дихлорфенил)-тиазол-2-ил)фенил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(3-трифторметилфенил)-тиазол-2-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(4-(4-хлорфенил)-пиразол-1-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой 5-бромфуран-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой 5-фтортиен-2-ил, Z представляет собой 4-(3-трифторметилфенил)фенил, a s равно 0;
соединения, в котором Y представляет собой 1-(4-трифторметилфенил)индол-5-ил, Z представляет собой тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой 1-(4-трифторметилфенил)индол-5-ил, Z представляет собой тиазол-2-ил, a s равно 0;
соединения, в котором Y представляет собой 1-(4-трифторметилфенил)индол-5-ил, Z представляет собой 1Н-пиррол-2-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(4-трифторметилфенил)-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-(3-трифторметилфенил)-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-фенилбензофуран-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(3-трифторметилфенил)бензофуран-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(4-трифторметилфенил)-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 3-(3-трифторметилфенил)-1Н-индол-6-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 3-метил-5-фенилбензотиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-метил-3-(4-трифторметилфенил)индол-6-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-4-фториндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-6-фториндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-7-фториндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-трифторметилфенил)-5-метилтиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-трифторметилфенил)-4-метилтиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(4-фторфенил)-4-метилтиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 5-(3-трифторметилфенил)-4-метилтиен-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-7-метилиндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметилфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметилфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-трифторметилфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенилиндазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-трифторметилтиен-2-ил)-фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3,4-дифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2,4-дифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-3-хлориндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 1Н-пиррол-2-ил, Z представляет собой 1-(3,4-дифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,4,5-трифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-фторфенил)-3-метилиндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-трифторметоксифенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(4-трифторметоксифенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3,5-дифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-фтор-4-хлорфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2,5-дифторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметоксифенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-трифторметоксифенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-метил-5-фенилфуран-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-трифторметил-5-фенилфуран-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-хлорфенил)бензоксазол-7-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-хлорфенил)-4-метилтиазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенилбензоксазол-5-ил и s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой 1Н-пиррол-2-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-хлорфенил)-4-метилтиазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-фенил-5-трифторметилоксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-фторфенил)-4-метилтиазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(пиридин-4-ил)-3Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(2-фторфенил)-1Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-хлорфенил)-3Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенил-3Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-фторфенил)-1Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-фенил-5-трифторметилпиразол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(4-фторфенил)-1Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(2-хлорфенил)-1Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3,5-дихлорфенил)тиазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-метил-5-фенилфуран-3-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 5-фенил-2-трифторметилфуран-3-ил, a s равно 0;
соединения, в котором Y представляет собой циклопентил, Z представляет собой бифенил-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фуран-2-ил-3Н-бензимидазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой пиримидин-2-ил, a s равно 0;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-2-ил, s равно 1, a R1 представляет собой 2-фенил;
соединения, в котором Y представляет собой бифенил-4-ил, Z представляет собой тиазол-4-ил, s равно 1, a R1 представляет собой 2-фенил;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-фенил-5-трифторметилоксазол-4-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-трифторметилфенил)-4-метилтиазол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 1-(3-трифторметилфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой трифторметил, Z представляет собой 1-(5-хлорпиридин-2-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(2-метилпиридин-4-ил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(5-(4-фторфенил)-пиразол-1-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 4-(3-метилиндол-1-ил)фенил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-4-хлориндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-6-метилиндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(4-фторфенил)-6-хлориндол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-циано-4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-аминокарбонил-4-фторфенил)индол-5-ил, а s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 1-(3-трифторметилфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-2-ил, Z представляет собой 2-(3-трифторметилфенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой тиазол-4-ил, Z представляет собой 2-(3-трифторметоксифенил)индазол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 5-хлортиен-2-ил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 3-фторфенил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 5-хлорфуран-2-ил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой оксазол-2-ил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой 5-фтортиен-2-ил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой оксазол-4-ил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
соединения, в котором Y представляет собой оксазол-5-ил, Z представляет собой 1-(4-фторфенил)индол-5-ил, a s равно 0;
или его фармацевтически приемлемой соли.
16. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении моноацилглицеринлипазы (MGL), содержащая терапевтически эффективное количество соединения по п. 1 или 15 и по меньшей мере один из фармацевтически приемлемого носителя, фармацевтически приемлемого эксципиента и фармацевтически приемлемого разбавителя.
17. Фармацевтическая композиция по п. 16, где композиция представлена в виде твердой дозированной формы для перорального введения.
18. Фармацевтическая композиция по п. 16, где композиция представляется собой сироп, эликсир или суспензию.
19. Способ лечения воспалительной боли у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества соединения по п. 1 или 15.
20. Способ по п. 19, где воспалительная боль связана с воспалительным заболеванием кишечника, висцеральной болью, мигренью, послеоперационными болями, остеоартрозом, ревматоидным артритом, болями в спине, в пояснице, в суставах, в животе, в груди, родовыми схватками, заболеванием опорно-двигательного аппарата, кожным заболеванием, зубной болью, ожогом, солнечным ожогом, укусом ядовитой змеи, паука или насекомого, нейрогенным мочевым пузырем, интерстициальным циститом, инфекцией мочевыводящих путей, ринитом, контактным дерматитом/гиперчувствительностью, зудом, экземой, фарингитом, мукозитом, энтеритом, синдромом раздраженной толстой кишки, холециститом, панкреатитом, болевым синдромом после мастэктомии, менструальными болями, эндометриозом, болями по причине физической травмы, головной болью, синусовой головной болью, головной болью напряжения или арахноидитом.
| FR 2915199 A1, 24.10.2008 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| 3-АЗЕТИДИНИЛАЛКИЛПИПЕРИДИНЫ ИЛИ ПИРРОЛИДИНЫ В КАЧЕСТВЕ АНТАГОНИСТОВ ТАХИКИНИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 1996 |
|
RU2158264C2 |
Авторы
Даты
2015-11-20—Публикация
2010-04-22—Подача