Область техники
Данное изобретение относится к композиции реактивов, которую используют для количественного измерения лития в водном растворе, таком как биологические образцы и образцы жидкости из окружающей среды, к способу и устройству для определения количества ионов лития с использованием композиции реактивов.
Уровень техники
Известно, что литийсодержащие лекарственные средства эффективны при эмоциональной стабилизации и антидепрессивной терапии, так что их используют широко в качестве стабилизирующих эмоции и антидепрессивных лекарственных средств. Таблетки карбоната лития (для перорального введения) в целом прописывают в качестве стабилизатора эмоций, а также лекарственного средства для биполярного расстройства (циркуляторного психоза) или антидепрессивного лекарственного средства.
Однако когда такое литийсодержащее лекарственное средство вводят пациентам, необходимо контролировать или корректировать концентрацию лития в сыворотке в пределах надлежащего диапазона. Фактически карбонат лития (Li2CO3) имеет такую характеристику, что эффект от его введения проявляется только когда концентрация лития в крови достигает почти «уровня отравления литием». Другими словами, когда вводят лекарственное средство, мониторинг терапевтического лекарственного средства (TDM) является обязательным, чтобы осуществлять мониторинг концентрации лития в крови, поскольку терапевтический диапазон очень близок к токсическому уровню.
На практике необходимо контролировать или ограничивать концентрацию лития в образце крови пациента в пределах ограниченного диапазона обычно от 0,6 до 1,2 мг-экв./л. Фактически, когда концентрация лития в сыворотке ниже чем 0,6 мг-экв./л, антидепрессивный эффект не ожидается. Напротив, чрезмерное введение при концентрации в плазме выше 1,5 мг-экв./л ведет к отравлению литием. Передозировка ведет к фатальному случаю с симптомами отравления, которые включают тремор, алалию, нистагм, почечную недостаточность и конвульсии. Следовательно, когда наблюдают признаки потенциально опасных симптомов отравления литием, лечение таким литийсодержащим лекарственным средством следует останавливать и повторно измерять концентрацию в плазме с тем, чтобы получить необходимые измерения и облегчать отравление литием.
Таким образом, соль лития представляет собой эффективное лекарство при лечении пациентов с депрессией, но передозировка ведет к серьезным проблемам. Следовательно, когда вводят литийсодержащее антидепрессивное лекарственное средство, необходимо осуществлять мониторинг концентрации лития в сыворотке и обеспечить, чтобы концентрация всегда находилась в ограниченном диапазоне от 0,6 до 1,2 мг-экв./л. Следовательно, при лечении пациентов с депрессией необходимо количественное измерение лития в сыворотке.
Разработано несколько жидких композиций реактивов, которые делают возможным колориметрическое определение лития в клиническом лабораторном тесте.
В патентном документе 1 раскрыта композиция реактивов, которую используют для того, чтобы измерять концентрацию лития в биологическом образце посредством использования основного цвета тела cryptideinofa.
В патентном документе 2 раскрыт аналитический реактив, который вступает в реакцию с ионом лития, содержащий макроциклическое соединение, которое имеет пирроловое кольцо и восемь атомов брома (Br), комбинированных в β-положении пирролового кольца.
В непатентном документе 1 раскрыто, что ион лития можно определить соединением, в котором все водороды, связанные с углеродами тетрафенилпорфирина, заменяют на фтор.
Список литературы известного уровня техники
Патентный документ 1 JP-A1-7-113807.
Патентный документ 2 ЕР 1283986-B1.
Непатентный документ 1 Analytical Chemistry Vol.51, №.9, pp. 803-807 (2002); K. Koyanagi et al., «Synthesis of F28 tetraphenylporphyrin and its use for separation and detection».
Сущность изобретения
Проблемы, подлежащие решению с помощью изобретения
Недостатками известных композиций реактивов для определения лития является то, что они представляют собой ядовитые композиции, что лекарственные вещества дорого стоят или не поставляются стабильно и что большинство лекарственных веществ не растворяется в воде или, даже если растворимы, деактивируются в воде, так что цветная реакция протекает очень медленно.
Указанный выше непатентный документ 1 разработан для того, чтобы решить указанные выше проблемы, и делает возможным использование методики с окрашиванием. Способ по этому непатентному документу 1, однако, требует операции разведения образца, поскольку чувствительность слишком высока, а описание литиевой композиции реактивов требует диапазона выше pH 11, поэтому ее легко ухудшает CO2 из воздуха и, таким образом, измеряемые данные не стабильны. Кроме того, при практическом использовании не доступны иные концентрированные водные растворы, кроме растворов гидроксида натрия и гидроксида калия, для диапазона выше pH 11, так что сложно поддерживать постоянную концентрацию. Эти концентрированные водные растворы представляют собой опасные вещества, с которыми сложно обращаться, так что их использования следует избегать. Для их хранения необходимы специальные контейнеры и при обращении с ними необходимо крупномасштабное специальное оборудование или установка. Следовательно, эту технологию сложно применять для мониторинга на месте и для РОСТ (исследование по месту лечения).
Композиция реактивов для измерения количества лития, раскрытая в патентном документе 1, полностью отличается от настоящего изобретения и ее можно использовать только при pH 12. Как указано выше, на практике в диапазоне выше pH 11 нет концентрированного водного раствора, отличного от раствора гидроксида натрия и гидроксида калия, которые представляют собой опасные вещества, с которыми сложно обращаться, и для их добавления требуется крупномасштабное специальное оборудование или установка.
В документе Koyanagi et al. из непатентного документа 1 говорится о том, что ион лития можно отделять и обнаруживать с использованием F28 тетрафенилпорфирина. Однако экстрагирование с использованием масляного ядовитого хлороформа необходимо для того, чтобы осуществлять отделение и обнаружение иона лития. Фактически прямое определение лития в водном растворе без сложной предварительной обработки было невозможно.
Таким образом, имела место такая проблема, что быстрое и количественное измерение иона лития в сыворотке было невозможно. Фактически обнаружение иона лития в водном растворе с использованием F28 тетрафенилпорфирина не является простым, так что количественное измерение иона лития с использованием этого соединения не реализовано до сих пор.
Это изобретение выполнено для того, чтобы решить эту проблему, и предоставляет композицию реактивов, используемую при количественном измерении лития (концентрации) в водном растворе, таком как биологические образцы и образцы жидкости из окружающей среды, и способ определения и устройство с использованием композиции реактивов для определения количества иона лития. Это изобретение позволяет измерять концентрацию лития быстро или незамедлительно с использованием стандартного колориметра. Данное изобретение предусматривает также литиевую композицию реактивов, которую можно использовать для скрининга посредством визуального наблюдения, и способ и устройство для использования композиции реактивов для того, чтобы измерять ион лития.
Средства решения проблем
Объектом данного изобретения является композиция реактивов для определения лития (далее «композиция реактивов для определения лития»), которая отличается тем, что она содержит соединение, которое имеет структуру, представленную формулой (I):
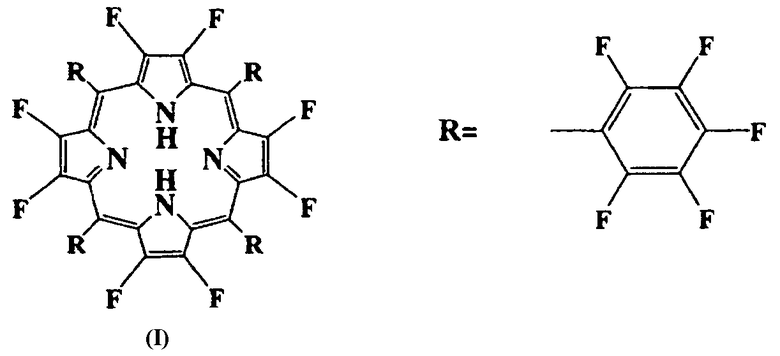 ,
,
в которой все водороды, связанные с углеродами тетрафенилпорфирина, заменяют на фтор, водорастворимый органический растворитель и модификатор pH.
Литий в водном растворе, таком как биологический образец и образец из окружающей среды, вызывает окраску с композицией реактивов в соответствии с настоящим изобретением, в частности, с приведенным выше соединением, в котором все водороды, связанные с углеродами тетрафенилпорфирина, заменяют на фтор, которое выполняет функцию хелатирующего реактива (проявитель окраски).
Изменение окраски с желтой на красную посредством реакции окрашивания, которую наблюдают между соединением F28 тетрафенилпорфирина и ионами лития, сложно осуществить. Однако требуется точно определять количество лития в сыворотке в диапазоне от 0,6 мг/дл до 2,0 мг/дл (от 0,9 мМ до 3 мМ). Авторы изобретения обнаружили, что количество лития в сыворотке можно точно определить, устанавливая концентрацию соединения F28 тетрафенилпорфирина в диапазоне от 0,1 до 1,0 г/л, предпочтительно 0,5 г/л в одном из вариантов осуществления данного изобретения.
Модификатор pH используют предпочтительно в настоящем изобретении. Действительно, в кислой части ниже pH 5,0, соединение F28 тетрафенилпорфирина, которое представляет собой проявитель окраски (хелатирующий реактив) в соответствии с данным изобретением, не связывается с ионом лития, так что изменение окраски не наблюдают и сложно определять количество лития. В диапазоне между pH 5 и pH 7 конкретная реакция протекает между проявителем окраски и ионом лития, но скорость реакции окрашивания низка. В диапазоне между pH 8 и pH 11, проявитель окраски быстро вступает в реакцию с ионом лития и может протекать образование стабильного окрашивающего комплекса. В щелочной части выше pH 11, тон окраски хелатирующего реактива и сформированного окрашивающего комплекса становится нестабильным во времени. Это может быть обусловлено абсорбцией диоксида углерода из воздуха, так что pH колеблется. Следовательно, необходимо использовать модификатор pH или pH буфер, который может сохранять pH литиевой композиции реактивов в соответствии с настоящим изобретением в диапазоне от pH 7 до pH 12, предпочтительно от pH 8 до pH 11.
Модификатор pH можно выбирать из щелочного агента, приемлемого в медицине, включая гидроксид натрия, гидроксид калия и аммиак, кислого средства, приемлемого в медицине, включая уксусную кислоту, фосфорную кислоту, лимонную кислоту, угольную кислоту, дикарбоновую кислоту, щавелевую кислоту, соляную кислоту, азотную кислоту и их соли. Модификатор pH может представлять собой pH буфер и его можно выбирать из лимонной кислоты, угольной кислоты, дикарбоновой кислоты, фосфорной кислоты, янтарной кислоты, фталевой кислоты, хлорида аммония, гидроксида натрия, гидроксида калия, MES в виде буфера Гуда, бис-трис, ADA, PIPES, ACES, MOPSO, BES, MOPS, TES, HEPES, DIPSO, TAPSO, POPSO, HEPPSO, EPPS, трицина, бицина, TAPS, CHES, CAPSO, CAPS и их солей.
Композиция реактивов для определения лития в соответствии с настоящим изобретением делает возможной специфическую реакцию окраски для лития в диапазоне от pH 5 до pH 12 посредством включения модификатора pH.
Обязательно растворитель (полярный растворитель), используемый в этом изобретении, представляет собой органический растворитель, который совместим с водой. Растворитель может представлять собой раствор, состоящий преимущественно из органического растворителя или водного раствора, в который добавляют органический растворитель, при условии, что растворитель можно смешивать единообразно с водным раствором, таким как сыворотка, плазма крови и элюат, которых представляет собой тестовый образец. Фактически, поскольку тестовый образец подлежит измерению в форме водного раствора, когда концентрацию лития в образце определяют посредством автоматизированного анализатора общего назначения и посредством спектрофотометра ультрафиолетового и видимого света, желательно, чтобы композиция реактивов находилась в форме водного раствора.
Органический растворитель предпочтительно выбирают из диметилсульфоксида (ДМСО), диметилформамида (ДМФ) и диметилацетамида (ДМА).
В данных продуктах подходящий стабилизатор вводят в композицию реактивов в соответствии с данным изобретением. В одном из вариантов осуществления поверхностно-активное вещество используют в качестве стабилизатора. Поверхностно-активное вещество улучшает диспергируемость соединения F28 тетрафенилпорфирина и препятствует образованию суспензий, образующихся в образце во время реакции развития окраски. Следовательно, стабилизатор используют для того, чтобы обеспечить такой эффект.
Стабилизатор может представлять собой неионное поверхностно-активное вещество или анионное поверхностно-активное вещество. Неионное поверхностно-активное вещество может представлять собой сложный сорбитановый эфир жирной кислоты, неполный сложный эфир пентаэритрита и жирной кислоты, сложный моноэфир пропиленгликоля и жирной кислоты, сложный моноэфир глицерина и жирной кислоты, полиоксиэтиленалкиловый эфир, полиоксиэтиленалкилфениловый эфир, полиоксиэтилен полиоксипропиленгликоль, неполный сложный эфир полиоксиэтилена и жирной кислоты, неполный сложный эфир полиоксиэтиленсорбита и жирной кислоты, сложный эфир полиоксиэтилена и жирной кислоты, диэтаноламид жирной кислоты, этаноламид жирной кислоты, полиоксиэтиленамид жирной кислоты, полиоксиэтилен октилфениловый эфир (Triton X-100®), п-нонилфеноксиполиглицидол или их соли. Предпочтительные неионные поверхностно-активные вещества представляют собой полиоксиэтилен октилфениловый эфир (Triton X-l00®) и п-нонилфеноксиполиглицидол.
Анионное поверхностно-активное вещество в качестве стабилизатора может представлять собой соль алкилсульфатного сложного эфира, сульфатную соль полиоксиэтиленалкилового эфира, сульфатную соль полиоксиэтиленфенилового эфира, алкилбензолсульфонат и алкансульфонат. Типичное анионное поверхностно-активное вещество выбирают из додецилсульфата натрия, додецилбензолсульфоната натрия и полиоксиэтиленалкилфенилового эфира сульфата натрия.
Композиция реактивов согласно настоящему изобретению может содержать больше, чем один маскирующий реактив во избежание искажения, обусловленного другими ионами, нежели литий, которые могут присутствовать в образце, чтобы подавлять окисление композиции реактивов и улучшать стабильность хранения. Маскирующий реактив может быть не обязателен, если имеет место незначительное количество ионов, отличных от лития.
Маскирующий реактив, который можно добавлять в литиевую композицию реактивов в соответствии с настоящим изобретением, может быть выбран из триэтаноламина, этилендиамина, N,N,N′,N′-тетракис(2-пиридилметилэтилендиамина (TPEN), пиридина, 2,2-дипиридина, пропилендиамина, диметилентриамина, диметилентриамин-N,N,N′,N′′,N′′-пентауксусной кислоты (DTPA), триметилентетрамина, триметилентетрамин-N,N,N′,N′′,N′′′,N′′′-гексауксусной кислоты (TTHA), 1,10-фенантролина, этилендиаминтетрауксусной кислоты (ЭДТА), O,O′-бис(2-аминофенил) этиленгликоль-N,N′,N′-тетрауксусной кислоты (BAPTA), N,N-бис(2-гидроксиэтил)глицина (бицина), транс-1,2-диаминоциклогексан-N,N,N′,N′-тетрауксусной кислоты (CyDTA), O,O′-бис(2-аминоэтил)этиленгликоль-N,N,N′,N′-тетрауксусной кислоты (EGTA), N-(2-гидроксил)иминодиуксусной кислоты (HIDA), иминодиуксусной кислоты (IDA), нитрилтриуксусной кислоты (NTA), нитрилтриметилфосфоната (NTPO) и их солей. Предпочтительно используют триэтаноламин.
Литиевая композиция реактивов в соответствии с данным изобретением может содержать антисептики для того, чтобы предотвращать разложение, обусловленное микроорганизмами. Антисептики конкретно не ограничены и могут представлять собой азид натрия и Procline®. Количество антисептиков конкретно не ограничено и может представлять собой концентрацию, используемую обычно в качестве антисептика. Например, в случае азида натрия, количество антисептиков составляет приблизительно 0,1% по массе реакционного раствора. Антисептики обычно предусмотрены для продуктов, которые хранят в течение длительного времени.
Для того чтобы гарантировать длительное хранение, литиевую композицию реактивов в соответствии с настоящим изобретением можно хранить отдельно в форме набора для измерения литиевого реактива, который содержит два отдельных реактива, которые смешивают непосредственно перед измерением для того, чтобы реализовать литиевую композицию реактивов по п. 1. Например, первый реактив содержит стабилизатор и модификатор pH или pH буфер, тогда как второй реактив содержит соединение тетрафенилпорфирина, смешиваемый с водой органический растворитель, стабилизатор и модификатор pH или pH буфер.
При данном использовании литиевую композицию реактивов в соответствии с настоящим изобретением приводят в контакт с тестовым образцом сыворотки и/или плазмы крови для того, чтобы вызвать окрашивание литиевого комплекса, который измеряют в единицах поглощения и спектра с тем, чтобы определять количество лития в образце по сравнению с эталонными концентрациями стандартного образца, концентрации лития в которых известны.
На практике в окрашивании литиевого комплекса и в его спектре чувствительность измеряют предпочтительно при длине волны 550 нм или вблизи от длины волны от 530 нм до 560 нм, или чувствительность измеряют при длине волны 570 нм или вблизи от длины волны от 565 нм до 650 нм для того, чтобы вычислять концентрацию лития. В этом случае чувствительность понимают как поглощение или разность поглощения в спектрофотометре ультрафиолетового и видимого света.
В измерительном устройстве измеряют окрашивание, поглощение или спектр литиевого комплекса, генерируемого из литиевой композиции реактивов в соответствии с настоящим изобретением, которую приводили в контакт с тестовым образцом сыворотки и плазмы крови, или чувствительность при длине волны 550 нм или вблизи от длины волны от 530 нм до 560 нм или чувствительность при длине волны 570 нм или вблизи от длины волны от 565 нм до 650 нм измеряют для того, чтобы вычислять количественное значение лития.
Преимущества изобретения
Композиция реактивов для определения лития в соответствии с настоящим изобретением и способ и устройство для измерения ионов лития позволяют легко определять или измерять концентрацию лития в водном растворе, таком как образец из окружающей среды и биологический образец. В литиевой композиции реактивов, определяемой в пунктах формулы изобретения с 1 до 13, калибровочная кривая концентрации лития является линейной в практическом диапазоне от 0,6 до 1,2 мг-экв./л, так что концентрацию можно вычислять с помощью простой операции по числовым значениям колориметра и спектрофотометра ультрафиолетового и видимого света. Следовательно, концентрацию лития в образце сыворотки или биологическом образце можно определять быстро и количественно с помощью обычного спектрофотометра. Получаемые данные можно использовать в качестве контрольного показателя, например, при TDM лечении. Или количественное определение большего числа образцов можно осуществлять за короткое время посредством автоматического анализатора для клинической химии.
В настоящем изобретении литиевую композицию реактивов корректируют до диапазона pH от pH 5 до pH 12 с тем, чтобы сделать возможным измерение посредством спектрометрии. В кислом диапазоне ниже pH 5 хелатирующий реактив в соответствии с настоящим изобретением (F28 тетрафенилпорфирин лития) не связывается с ионами гелия, так что изменение окраски, которое зависит от концентрации лития, не наблюдают. Напротив, в щелочной части выше pH 12 тон окраски хелатирующего реактива и образованного окрашивающего комплекса не стабилен. Стабильность тона окраски становится плохой из-за абсорбции диоксида углерода из воздуха, которая вызывает колебания pH. В диапазоне pH от pH 5 до pH 7, специфичное окрашивание хелатирующего реактива можно наблюдать, поскольку хелатирующий реактив связывается с ионами лития, но скорость окрашивания слишком низка. Следовательно, диапазон pH от pH 8 до pH 11 является предпочтительным, поскольку в диапазоне pH от pH 8 до pH 11 хелатирующий реактив связывается с ионом лития быстро и реакция развития окраски является специфичной и стабильной.
Металлический комплекс тетрафенилпорфирина обладает типичным конкретным спектральным диапазоном около от 380 нм до 460 нм, который называют «полосой Соре», в которой получают максимальную чувствительность. Этот диапазон можно выбирать в качестве измерительного диапазона длин волн. Однако чувствительность в этом диапазоне слишком высока для концентрации лития, имеющей клиническую значимость в образце сыворотки, так что необходима операция разведения, что ведет к увеличению сложных операций и дополнительным блокам для разведения, которые увеличивают размер измерительного блока.
В настоящем изобретении длину волны 550 нм или ближайший диапазон от 530 нм до 560 нм, в котором чувствительность ниже в несколько раз, чем в полосе Соре, используют в качестве измерительного диапазона длин волн. Выбирая этот диапазон, оптимальную чувствительность получают для концентрации образца, подлежащей тестированию, и сложная операция разведения и блок разведения могут быть устранены. Кроме того, калибровочная кривая в соответствии с настоящим изобретением имеет более высокую линейность, чем таковая в случае полосы Соре, так что концентрацию можно легко вычислять по измеряемым значениям, получаемым с помощью колориметра малого размера или спектрофотометра ультрафиолетового и видимого света. Кроме того, изменение тона окраски с желтого на красный является очень резким в настоящем изобретении, об уровне концентрации можно судить с помощью визуального наблюдения или невооруженным глазом.
Если полосу Соре используют в качестве длины волны фотометрии, имеет место такая другая проблема, что на количественное значение лития влияют другие органические вещества и окрашенные компоненты, такие как нитрат-ион, креатинин, билирубин, биливердин и гемолиз гемоглобина. Это влияние или проблему можно уменьшить в настоящем изобретении, и концентрацию лития можно определять с высокой воспроизводимостью.
В стандартном способе измерения лития требуется крупномасштабный специализированный аппарат. В этом изобретении концентрацию лития можно определять с помощью маленького портативного колориметра, и его можно сконструировать в виде набора для РОСТ.
Краткое описание чертежей
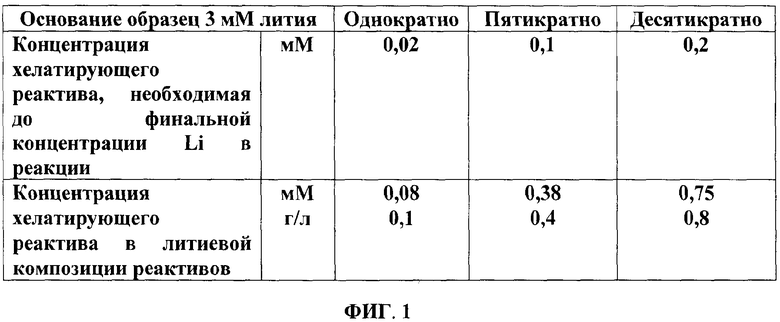
Фиг. 1 - таблица для вычисления оптимальной концентрации F28 тетрапорфирина в соответствии с данным изобретением.
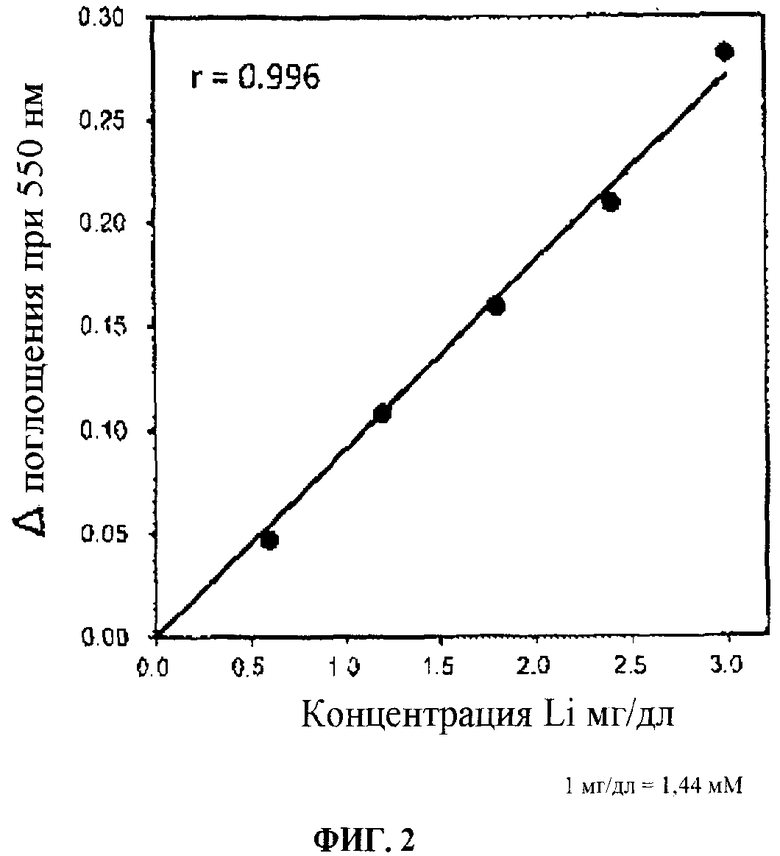
Фиг. 2 - графики спектрофотометра ультрафиолетового и видимого света, получаемые в результате примера 1 в соответствии с данным изобретением.
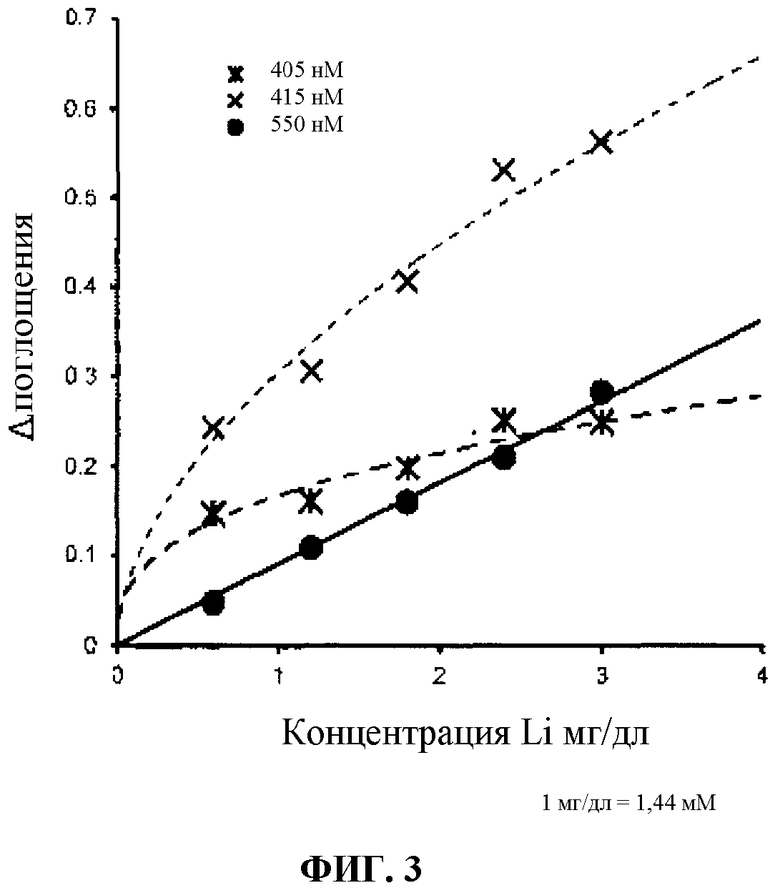
Фиг. 3 - график калибровочной кривой при различных длинах волн в примере 1 в соответствии с данным изобретением.
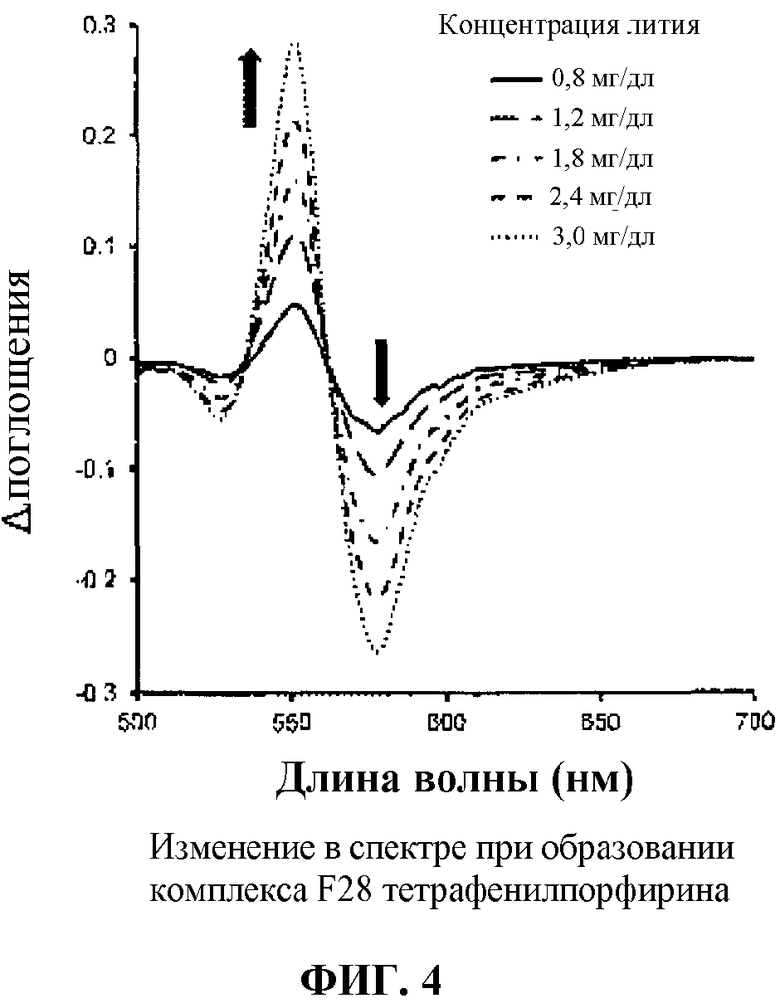
Фиг. 4 - графики, показывающие изменение спектра (реакции окраски), когда формируют F28 тетрафенилпорфирин-литиевый комплекс в примере 1 в соответствии с данным изобретением.
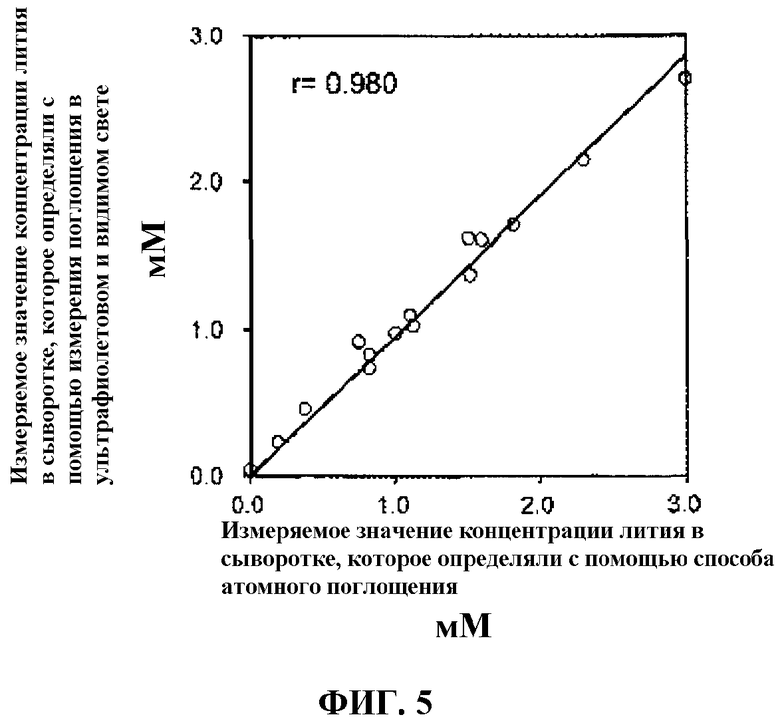
Фиг. 5 - график, показывающий корреляцию между измеряемыми значениями образцов сыворотки в примере 1 в соответствии с данным изобретением и измеряемыми значениями, получаемыми с помощью способа атомного поглощения (стандартный способ).
Фиг. 6 - таблица 1 показывает сравнение с измеряемыми значениями, получаемыми с использованием автоматизированного анализатора, в котором использовали контрольные образцы сыворотки.
Фиг. 7 - таблица 2 показывает, как обнаруживать литий посредством визуального наблюдения в этом изобретении.
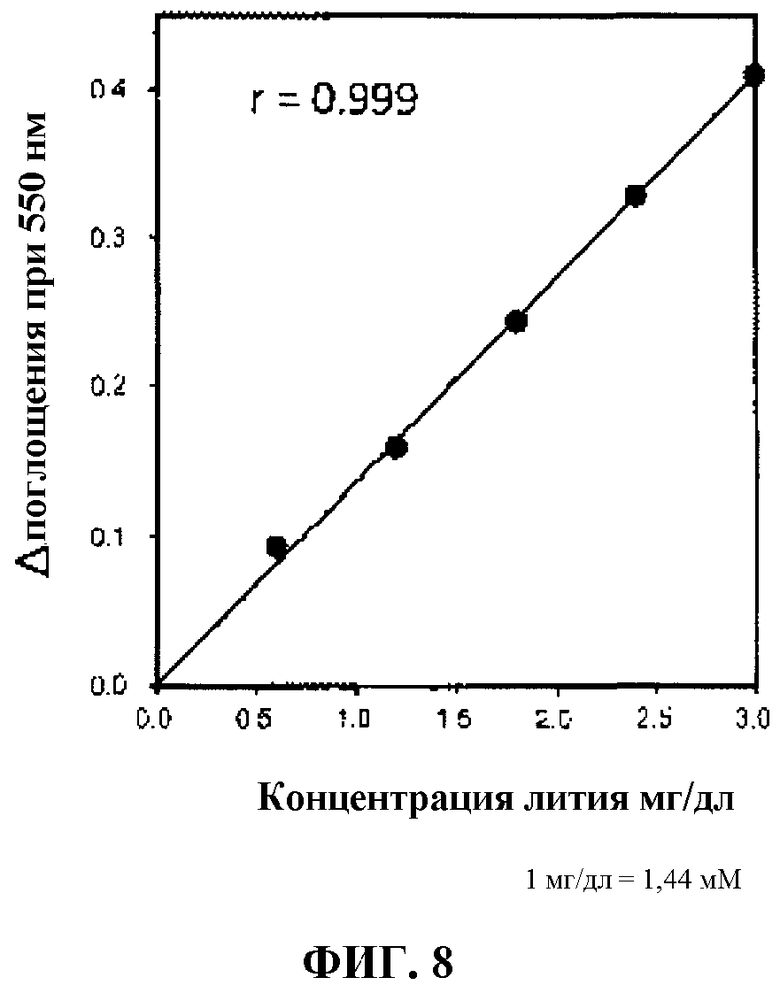
Фиг. 8 - график спектра поглощения в примере 1 в соответствии с данным изобретением.
Фиг. 9 - таблица 3 показывает измеряемые значения, получаемые с помощью различных органических растворителей в соответствии с данным изобретением.
Фиг. 10 - таблица 4 показывает измеряемые значения, получаемые с помощью различных стабилизаторов в соответствии с данным изобретением.
Фиг. 11 - таблица 5 показывает измеряемые значения, получаемые с помощью различных маскирующих реактивов в соответствии с данным изобретением.
Вариант осуществления изобретения
Авторы изобретения изучали композиции реактивов, которые можно использовать для измерения концентрации лития в сыворотке и плазме крови количественно и более просто, и сосредоточились на соединении, представленном общей формулой (I):
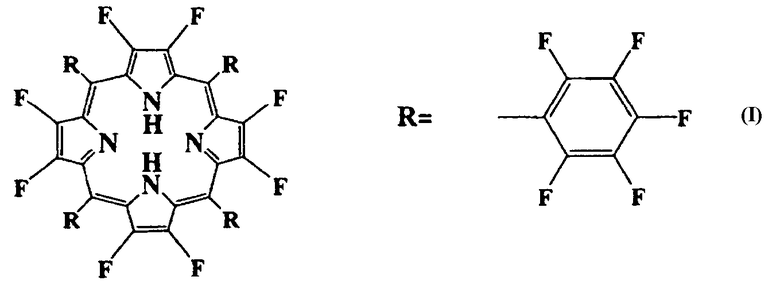 ,
,
в которой все атомы водорода, связанные с углеродами кольца тетрафенилпорфирина, заменяют на атомы фтора (общее число фторов равно 28) в макроциклическом соединении, раскрытом в непатентном документе 1, и выполнили настоящее изобретение. Приведенное выше соединение в настоящем документе называют «F28 тетрафенилпорфирин».
Патентные документы 2 и 3 раскрывают схожие композиции реактивов для определения содержания лития, которые содержат макроциклическое соединение, которое имеет пирроловые кольца, в которых восемь атомов брома (Br) связаны с β-положением пирролового кольца, чтобы предоставить аналитический реактив, который может вступать в реакцию с ионами лития. Однако это соединение с трудом вступает в реакцию с литием, если pH не находится в щелочной части выше pH 11.
В случае F28 тетрафенилпорфирина в соответствии с настоящим изобретением реакция протекает в диапазоне от pH 5 до pH 12. В настоящем изобретении F28 тетрафенилпорфирин используют в качестве хелатирующего реактива и используют для того, чтобы количественно определять ионы лития в водной системе.
Далее приведено более подробное объяснение литиевой композиции реактивов в соответствии с настоящим изобретением с использованием примеров.
ПРИМЕРЫ
Пример 1 (Образец 1)
В этом примере 1 сначала получали первый реактив в качестве pH буферного раствора и второй реактив в качестве раствора окрашивающего реактива. Затем два реактива из первого и второго реактивов смешивали непосредственно перед измерительной операцией для того, чтобы получать литиевую композицию реактивов в соответствии с настоящим изобретением. Несмотря на то, что эти два реактива можно хранить в форме смеси, но целесообразно хранить их отдельно и смешивать вместе непосредственно перед измерительной операцией для того, чтобы избежать порчи реактивов в течение длительного времени хранения.
Далее подробно объясняют, как получать композицию реактивов в соответствии с настоящим изобретением.
Для начала получают первый реактив (pH буферный раствор). Далее приведена композиция первого реактива.
(1) Первый реактив (в качестве стабилизатора и буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (дисперсант: неионное поверхностно-активное вещество): TritonX-100® 1,0% по массе (полиоксиэтилен октилфениловый эфир).
Маскирующий реактив: 10 мМ триэтаноламина.
В смесь приведенных выше компонентов, добавляли хлорид аммония 7% по массе для того, чтобы регулировать pH до 10. Затем общий объем увеличивали до 1 литра с использованием очищенной воды и хранили в обычном перемешиваемом контейнере. Если доля TritonX-100® (полиоксиэтилен октилфениловый эфир) составляет ниже чем 1,0% по массе, в некоторых случаях может возникать мутность. Напротив, если используют избыток стабилизатора, будет происходить образование пены в реакционном сосуде. Такая мутность или пенообразование может влиять на воспроизводимость измерения, так что диапазон в диапазоне от 0,1 до 5,0% по массе является предпочтительным и более предпочтительным является 1,0% по массе.
В этом примере маскирующим реактивом является 10 мМ триэтаноламина. Если количество маскирующего реактива мало, удовлетворительный маскирующий эффект не будет достигнут в таких образцах, которые содержат избыток посторонних ионов, отличных от лития. Напротив, избыток маскирующего реактива будет маскировать сам ион лития, что ведет к причине ошибок в измерении. Следовательно, диапазон от 1,0 до 100 мМ является предпочтительным и 10 мМ является более предпочтительным.
Второй реактив (раствор развивающего окраску реактива) получают следующим образом. (2) Второй реактив (в качестве раствора развивающего окраску реактива):
Хелатирующий реактив: 0,5 г/л F28 тетрафенилпорфирин.
Органический растворитель: 20% по массе диметилсульфоксида (ДМСО).
Стабилизатор (дисперсант: неионное поверхностно-активное вещество): 1,0% по массе TritonX-100® (полиоксиэтилен октилфениловый эфир).
Маскирующий реактив: 10 мМ триэтаноламина.
В смесь приведенных выше компонентов 0,05 M (моль/л) MOPS (буфер Гуда) добавляли для того, чтобы регулировать pH до 7,0. Затем общий объем увеличивали до 1 литра с использованием очищенной воды и получаемый раствор хранили в обычном перемешиваемом контейнере.
В примере 1 реакция окрашивания с соединением F28 тетрафенилпорфирина является трудной. Однако в практическом клиническом лабораторном тесте для измерения концентрации лития в сыворотке требуется точность в диапазоне концентраций лития от 0,6 мМ до 3 мМ. Автор изобретения обнаружил, что точное измерение можно осуществлять посредством выбора концентрации соединения F28 тетрафенилпорфирина от 0,1 до 1,0 г/л, предпочтительно 0,5 г/л.
В диапазоне концентраций лития от 0,6 мМ до 3 мМ измерение лития можно осуществлять благоприятно, задавая концентрацию соединения F28 тетрафенилпорфирина в конечной композиции реактивов от 0,1 до 1,0 г/л, предпочтительно 0,5 г/л. Если концентрация ниже, чем приведенный выше предел, реакция между F28 тетрафенилпорфирином и ионом лития не протекает в достаточной мере. Напротив, если концентрация превышает приведенный выше предел, будет возникать другая проблема увеличения поглощения пустой пробы с соединением F28 тетрафенилпорфирина. Следовательно, предпочтительно используют концентрацию 0,5 г/л.
Более подробно, реакция между F28 тетрафенилпорфирином и ионом лития представляет собой реакцию с равным молярным соотношением 1:1 для того, чтобы формировать хелатный комплекс. Когда тестовый образец, содержащий 3 мМ лития, вступает в реакцию с композицией реактивов в соответствии с настоящим изобретением в условиях примера 1, концентрация лития в реакционной системе становится 0,02 мМ. Следовательно, концентрация соединения F28 тетрапорфирина должна существовать при концентрации выше чем 0,02 мМ для того, чтобы реакция протекала в достаточной мере (ни слишком много, ни слишком мало).
В комплексообразующей реакции (реакция развития окраски) между хелатирующим реактивом и ионами металла обычно необходимо использовать хелатирующий реактив (F28 тетрапорфирин) в количестве от одного моля до десяти молей на один моль реагента или субъекта, подлежащего тестированию (литий). Как показано на фиг. 1, на которой представлены оптимальные концентрации F28 тетрапорфирина, композицию реактивов получают таким образом, чтобы концентрация F28 тетрапорфирина в течение времени реакции становилась от равномолярной до десятикратно превышающей. На практике предпочтительно использовать концентрацию хелатирующего реактива в композиции реактивов 0,5 г/л (пятикратно) вместо 0,1 г/л (та же величина) с тем, чтобы делать возможным использования в более широких условиях измерения, поскольку параметры доз в измерительной реакции добавленного количества композиции реактивов и количества образца, подлежащего тестированию, зависят от измерительного аппарата и желаемых порогов и варьируют. Например, в случае измерительного аппарата, измерительная точность которого не так высока, количество образца можно увеличивать от двух раз до пяти раз по отношению к таковому в примере 1. Для того чтобы подготовиться к таким случаям, целесообразно использовать концентрацию 0,5 г/л (5 раз) композиции реактивов, которая представляет собой достаточное количество реактива для реакции. Чрезмерное количество, превышающее десятикратное, не имеет преимущества, поскольку увеличенное количество реактива может не давать значительного преимущества в кинетике реакции развития окраски, а скорее усиливать проблему подъема уровня пустой пробы.
Необходимо удовлетворять условия реакции в молярном соотношении между хелатирующим реактивом и литием. Например, когда концентрация хелатирующего реактива (F28 тетрапорфирин) во втором реактиве составляет 1,0 г/л, количество второго реактива, который добавляют в реакцию, можно снижать до половины. Или, когда количество образца снижают до половины, количество хелатирующего реактива можно снижать до половины.
В примере 1 концентрация F28 тетрафенилпорфирина составляет 0,5 г/л. Оптимальная концентрация F28 тетрафенилпорфирина составляет от 0,1 до 1,0 г/л, что удовлетворяет условия реакции в молях и снижает до минимума уровень пустой пробы.
Количество диметилсульфоксида (ДМСО) составляет от 5 до 30% по массе. Когда это количество меньше, дисперсия F28 тетрафенилпорфирина в растворе становится плохой. Напротив, если избыточное количество диметилсульфоксида ведет к увеличению органического растворителя в композиции реактивов. Следовательно, предпочтительное количество составляет 20% по массе.
F28 тетрафенилпорфирин, используемый в этом примере 1, имеет структуру, представленную следующей формулой (I):
 ,
,
в которой все водороды, связанные с углеродами тетрафенилпорфирина, заменяют на атомы фтора.
(3) Далее объясняют, как получать калибровочную кривую литиевой композиции реактивов, получаемой смешиванием первого реактива со вторым реактивом, для образцов, в которых концентрации лития известны.
В примере 1 720 мкл первого реактива (буферный раствор) и 240 мкл второго реактива (раствор окрашивающего реактива) добавляли к 6 мкл образца. В этом случае первый реактив имеет буферную емкость при pH 10. После смешивания первого и второго реактивов и образца, получаемая смесь тестовой жидкости имеет pH приблизительно 10.
Таким образом, когда F28 тетрафенилпорфирин в соответствии с настоящим изобретением используют в качестве хелатирующего реактива, реакцию развития окраски можно осуществлять в диапазоне pH от pH 5 до pH 10. Фактически, настоящее изобретение предусматривает реактив для измерения лития, который обладает сильным pH буферным действием в диапазоне ниже pH 10, так что можно снижать колебания pH, обусловленные абсорбцией CO2 из воздуха. И, таким образом, можно избегать нежелательного эффекта, оказываемого на измеряемые значения, и возможно хранить измерительные реактивы в контейнерах общего назначения.
Возможно смешивать первый реактив со вторым реактивом непосредственно перед использованием и добавлять получаемую смесь к тому же объему образца. В этом случае, 940 мкл смеси жидкостей можно добавлять к 6 мкл образца.
Тестовый образец добавляли в получаемую смесь с pH 10 для того, чтобы провести реакцию при температуре окружающей среды в течение 10 минут, и затем измеряли поглощение на 550 нм посредством спектрофотометра ультрафиолетового и видимого света (HITACHI, тип U-3900), пустая проба является тестовым образцом. На фиг. 2 представлен результат, который представляет собой зависимость между поглощением и концентрацией Li (мг/л). На фиг. 4 представлен график, показывающий изменение в спектре в диапазоне видимого света при формировании F28 тетрафенилпорфирин-литиевого комплекса.
Для металлического комплекса тетрафенилпорфирина максимальную чувствительность получают при диапазоне длин волн так называемой полосы Соре (приблизительно от 380 нм до 460 нм). Однако в настоящем изобретении этот диапазон полосы Соре не используют, но используют длину волны 550 нм или в близлежащем диапазоне от 530 нм до 560 нм, так что в настоящем изобретении не требуются сложные операции разведения и средства для разведения или вспомогательные установки.
На фиг. 3 представлены графики калибровочных кривых при различных длинах волн, которые показывают, что наилучшую линейность в калибровочной кривой можно получать, когда длину волны 550 нм или в близлежащем диапазоне от 530 нм до 560 нм используют, чем в случаях, когда используют длины волн так называемой полосы Соре. Следовательно, точную концентрацию можно вычислять легко с помощью простого колориметра или спектрофотометра. Кроме того, изменение окраски с желтой на красную происходит очень резко, так что уровень концентрации можно обнаруживать легко невооруженным глазом. В общепринятом способе аппарат большого масштаба для исключительно использования необходим для того, чтобы измерять концентрацию лития, тогда как в настоящем изобретении концентрацию лития можно измерять легко с помощью портативного колориметра или спектрофотометра ультрафиолетового и видимого света, которые используют широко. Настоящее изобретение можно сконструировать в форме набора для РОСТ.
На графике на фиг. 3 линию (•) получали при длине волны 550 нм, которую использовали в примере 1, тогда как другие две кривые получали при длинах волн 405 нм (*) и 415 нм (×), которые соответствуют длинам волн полосы Соре, когда повторяли ту же процедуру, как в примере 1. Однако в случае 405 нм (*) и 415 нм (×) измерение осуществляли после того, как образцы разводили в 5 раз, поскольку чувствительность была слишком высока. На фиг. 3 показано, что калибровочную кривую, которая имеет хорошую линейность, можно получать для длины волны 550 нм из примера 1, но калибровочные кривые для длин волн 405 нм и 415 нм не являются линейными.
На фиг. 4 представлены изменения в спектре, когда формируют F28 тетрафенилпорфирин-литиевого комплекса. Фиг. 4 четко подтверждает, что поглощение будет возрастать линейно с увеличением концентрации лития с 6 мг/дл до 1,2 мг/дл, 1,8 мг/дл, 2,4 мг/дл и 3,0 мг/дл. Пик поглощения 415 нм (полоса Соре), который типичен для порфирин-металлического комплекса, и пик поглощения 550 нм (показанный на фиг. 4) возрастает, и пик поглощения 570 нм (также показанный на фиг. 4) снижается пропорционально концентрации лития. Следовательно, разность поглощения можно вычислять в этих пиках поглощения. В настоящем изобретении длину волны 550 нм предпочтительно используют в качестве длины волны фотометрических измерений по причине хорошей линейности калибровочной кривой.
Возможно выбирать диапазон длин волн от 540 нм до 560 нм в качестве диапазона фотометрических измерений вместо длины волны 550 нм, используемой в примере 1. Фактически, некоторое измерительное оборудование может не иметь фотометрического фильтра для 550 нм. В таком случае длину волны фотометрических измерений можно выбирать из диапазона длин волн вблизи, такую как 540 нм или 560 нм, где чувствительность также высока. Длину волны 570 нм также можно использовать в качестве длины волны фотометрических измерений, поскольку снижение чувствительности поглощения при 570 нм также является количественным, как показано на фиг. 4. Следовательно, разность поглощения (Δ поглощения) при 570 нм также можно вычислять, опираясь на реактив в качестве пустой пробы.
В таком редком случае, когда некоторые загрязнители, которые вмешиваются при длине волны 550 нм, получают в образце пациента и при длине волны 550 нм получают ошибочные данные, можно выбирать длину волны 570 нм или вблизи от 565 нм до 650 нм в качестве длины волны фотометрических измерений для того, чтобы избежать такой проблемы, и вычислять концентрацию лития по снижению чувствительности в виде разности поглощения.
Далее объясняют экспериментальные данные из примера 1, которые показывают, что концентрацию лития можно измерять с высокой точностью с использованием литиевой композиции реактивов в соответствии с настоящим изобретением.
Результаты эксперимента с помощью спектрофотометра ультрафиолетового и видимого света (HITACHI, модель U-3900)
На фиг. 2 представлен результат эксперимента, который измеряли посредством спектрофотометра ультрафиолетового и видимого света (HITACHI, модель U-3900). Ось абсцисс представляет собой известные концентрации ионов лития (концентрация Li, мг/дл), и ось ординат представляет собой разность поглощения, измеряемую посредством спектрофотометра ультрафиолетового и видимого света при длине волны 550 нм.
На фиг. 2 показано, что получают хорошую линейность зависимости между поглощением и концентрацией лития.
Корреляционный тест между способом атомного поглощения (стандартный способ) и способом в соответствии с данным изобретением для образца сыворотки
На фиг. 5 представлен график, показывающий корреляцию измеряемых значений между измерительным способом из примера 1 в соответствии с данным изобретением и стандартным способом атомного поглощения (стандартный способ), который осуществляют для того же образца сыворотки. Измеряемые значения, которые получают стандартным способом атомного поглощения (стандартный способ), наносят на график по оси абсцисс (X), тогда как измеряемые значения в соответствии с данным изобретением наносят на график по оси ординат (Y). Линия регрессии, представленная на фиг. 5, показывает хорошую корреляцию больше чем 95%. Этот результат показывает, что литий в образце сыворотки можно определять количественно посредством измерения поглощения в ультрафиолетовом и видимом свете с использованием композиции реактивов в соответствии с настоящим изобретением.
Сравнение измеряемых значений, которое осуществляли с помощью автоматического анализа для контрольных образцов сыворотки
Концентрацию лития измеряли для следующих контрольных образцов сыворотки, в которых концентрация лития оценена:
Precinorm U (Roche);
Precipath U (Roche);
Pathonorm H (SERO AS);
Auto norm (SERO AS)
с использованием биохимического автоматизированного анализатора (HITACHI, модель H-7700) при длине волны фотометрических измерений 546 нм (которая представляет собой длину волны, заданную в этом анализаторе и близкую к 550 нм) посредством способа 1 конечной точки.
Параметры устройства:
Реактив: 0,24 мл.
Образец: 0,005 мл.
Длина волны фотометрии (основная/второстепенная): 546 нм/700 нм.
Время измерения: 10 минут.
Температура: 37°C.
1 конечная точка: увеличивающий способ.
Результаты, представленные в таблице 1 на фиг. 6, доказывают тот факт, что измеряемые значения, получаемые посредством настоящего изобретения, совпадают с гарантированными значениями в приведенных выше условиях, так что подтверждено, что концентрацию лития в сыворотке можно измерять удовлетворительно посредством автоматизированного анализатора для клинических тестов.
Обнаружение лития посредством визуального наблюдения
В таблице 2 на фиг. 7 представлены результаты визуального наблюдения для жидкостей тестовых образцов. В этом тесте 920 мкл раствора окрашивающего реактива, который представлял собой смесь первого реактива и второго реактива в соответствии с настоящим изобретением, добавляли к 8 мкл тестового образца и проводили реакцию с получаемой смесью в течение 10 минут при температуре окружающей среды перед выполнением визуального наблюдения. Развивающиеся окраски сравнивали со шкалой тонов окраски, которую получали с использованием контрольных сывороток в форме растворов со стандартными концентрациями лития при различных уровнях концентрации лития.
Четкое изменение окраски с желтой на красную подтверждали при соответствующих уровнях концентрации, и изменение окраски контрольных сывороток совпадает со шкалой окрасок контрольных сывороток. Этот факт доказывал или подтверждал, что концентрацию лития в сыворотке можно определять быстро и легко в соответствии с настоящим изобретением без использования специального оборудования.
Как изложено выше, это подтверждает, что концентрацию лития можно измерять с высокой точностью, используя литиевый реактив из примера 1 в соответствии с настоящим изобретением.
Пример 2
Процедуру из примера 1 повторяли, но первый реактив в литиевой композиции реактивов изменяли посредством добавления 0,1 M (моль/л) MOPS для того, чтобы регулировать pH до 8,0 и посредством добавления чистой воды до общего объема 1 литр. А именно, смесь первого реактива, второго реактива и реактива корректировали приблизительно до pH=8 во время измерения.
(1) Первый реактив (в качестве стабилизатора и буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (диспергирующее неионное поверхностно-активное вещество): Triton X-l00® полиоксиэтилен октилфениловый эфир: 1,0% по массе.
Маскирующее средство: триэтаноламин: 10 мМ.
0,1 M MOPS добавляли в приведенную выше смесь для того, чтобы регулировать pH смеси до pH 8. Затем общий объем увеличивали до 1 литра с использованием очищенной воды и получаемый раствор хранили в перемешиваемом контейнере общего назначения.
(2) Второй реактив (в качестве раствора окрашивающего реактива):
Хелатирующий реактив: F28 тетрафенилпорфирин: 0,5 г/л.
Органический растворитель: диметилсульфоксид (ДМСО): 20% по массе.
Стабилизатор (дисперсант, неионное поверхностно-активное вещество): TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующее средство: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов 0,05 M MOPS (буфер) добавляли для того, чтобы регулировать pH до pH 7,0, и добавляли очищенную воду до общего объема 1 литр, который хранили в контейнере общего назначения.
Аналогичным образом, как в примере 1, 720 мкл первого реактива (буферный раствор) и 240 мкл второго реактива (раствор окрашивающего реактива) добавляли к 6 мкл тестового образца в то время, когда измеряли концентрацию лития. После реакцию продолжали в течение 10 минут при температуре окружающей среды, измеряли поглощение при длине волны 550 нм посредством спектрофотометра ультрафиолетового и видимого света (HITACHI тип U-3900).
Экспериментальный результат в спектрофотометре ультрафиолетового и видимого света (HITACHI тип U-3900)
На фиг. 8 представлен график экспериментальных результатов спектрофотометра ультрафиолетового и видимого света (HITACHI, тип U-3900). Абсцисса (X) представляет собой известные концентрации ионов лития (концентрация Li, мг/дл), а по ординате (Y) отложены различия в поглощении на 550 нм в спектрофотометре ультрафиолетового и видимого света.
На фиг. 8 показано, что разность поглощения зависимо пропорциональна концентрации лития для композиции реактивов, полученной при pH 8 или в условиях измерения при pH 8, и что также получают хорошую линейность калибровочной кривой при pH 8.
Однако в условиях измерения при pH 8 кинетика реакции немного замедляется и количественно стабилизируется приблизительно за 10-20 минут. В случае pH 10 реакция завершается в пределах 10 минут. Следовательно, в буферной системе в диапазоне от pH 5 до pH 10 литиевой композиции реактивов по данному изобретению нет необходимости на всякий случай использовать буферную систему с pH выше 11 на основе крепкого раствора гидроксида, такого как гидроксид натрия и гидроксид калия, и, таким образом, операция по манипуляции становится проще. Диапазон pH можно задавать согласно желаемым потребностям, и его корректируют предпочтительно до pH 10, при котором кинетика реакции является быстрой, и достаточную буферную способность можно сохранять при использовании буфера Гуда, системы хлорида аммония и системы угольной кислоты. С практической точки зрения, целесообразно осуществлять это с использованием буферной системы с pH 10 из примера 1, в которой реакция развивается правильно.
Таким образом, в литиевой композиции реактивов в соответствии с данным изобретением необходимо использовать pH буфер, который выполняет функцию модификатора pH для регулирования pH до диапазона от 7 до 12, или pH буфер в качестве модификатора pH. Более желательно, предпочтительно использовать модификатор pH или pH буфер, который корректирует pH от pH 8 до pH 11, и более предпочтительно использовать модификатор pH или pH буфер, который корректирует pH около pH 10.
Пример 3
Далее объяснен выбор органического растворителя. В изобретении важно, что растворитель представляет собой органический растворитель, который смешивается с водой, поскольку реакционные растворы, подлежащие измерению, представляют собой водные растворы, такие как сыворотка. Растворитель может представлять собой жидкость, преимущественно состоящую из органического растворителя, или водный раствор, содержащий органический растворитель, при условии, что компоненты в композиции реактивов стабилизированы в виде водного раствора. В частности, когда концентрацию лития в образце измеряют посредством автоматизированного анализатора общего назначения и посредством спектрофотометра ультрафиолетового и видимого света, желательно использовать в основном водный раствор, содержащий органический растворитель.
Другие органические растворители, которые можно смешивать с водой, нежели примеры 1, 2, объяснены в примере 3. В примере 3 повторяли ту же процедуру, как в примере 1, но органический растворитель второго реактива диметилсульфоксид (ДМСО) (20% по массе) в литиевой композиции реактивов заменяли на диметилформамид (ДМФ) (20% по массе).
(1) Первый реактив (в качестве буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (дисперсант: неионное поверхностно-активное вещество): TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 7% по массе хлорида аммония для того, чтобы регулировать pH до pH 10, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
(2) Второй реактив (в качестве раствора окрашивающего реактива):
Хелатирующий реактив: F28 тетрафенилпорфирин: 0,5 г/л.
Органический растворитель: Диметилформамид (ДМФ): 20% по массе.
Стабилизатор (диспергирующее средство: неионное поверхностно-активное вещество) TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов 0,05 M MOPS (буфер) добавляли для того, чтобы регулировать pH до pH 7,0, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
Пример 4
В качестве органического растворителя, который смешивается с водой, диметилсульфоксид (ДМСО) (20% по массе) использовали в примере 1 и диметилформамид (ДМФ) (20% по массе) использовали в примере 2.
В этом примере 4 композицию реактивов для определения лития получали с использованием диметилацетамида (ДМА) (20% по массе) в качестве органического растворителя, который смешивается с водой, и концентрацию лития измеряли посредством композиции реактивов для определения лития.
(1) Первый реактив (в качестве буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (дисперсант: неионное поверхностно-активное вещество): TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 7% по массе хлорида аммония для того, чтобы регулировать pH до pH 10, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
(2) Второй реактив (в качестве раствора окрашивающего реактива):
Хелатирующий реактив: F28 тетрафенилпорфирин: 0,5 г/л.
Органический растворитель: диметилацетамид (ДМА): 20% по массе.
Стабилизатор (диспергирующее средство: неионное поверхностно-активное вещество) TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 0,05 M MOPS (буфер) для того, чтобы регулировать pH до pH 7,0, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
На фиг. 9 представлены результаты сравнения лития, обнаруженного в контрольном образце сыворотки, в котором концентрацию лития измеряли посредством той же процедуры, как в примере 1, но органический растворитель изменяли с диметилсульфоксида (ДМСО) из примера 1 на диметилформамид (ДМФ) в примере 3 и диметилацетамид (ДМА) в примере 4. В [таблице 3] на фиг. 9 представлены результаты сравнения между стандартным измерительным способом и измерительным способом в соответствии с настоящим изобретением.
В таблице 3 на фиг. 9 представлено «Сравнение различных органических растворителей», которое показывает следующие результаты: измеряемое значение, которое получали с использованием диметилформамида (ДМФ) (20% по массе) в качестве органического растворителя, который смешивается с водой, в примере 1 составляло 0,83 мМ (ммоль/л); измеряемое значение, которое получали с использованием диметилформамида (ДМФ) (20% по массе) в качестве органического растворителя, который смешивается с водой, в примере 3 составляло 0,82 мМ (ммоль/л); и измеряемое значение, которое получали с использованием диметилацетамида (ДМА) (20% по массе) в качестве органического растворителя, который смешивается с водой, в примере 4 составляло 0,81 мМ (ммоль/л). Эти значения совпадают более чем на 95% с измеряемым значением, которое получали посредством спектрофотометрии атомного поглощения 0,82 мМ (ммоль/л). Следовательно, возможно определять количественно и точно концентрацию лития в водных образцах, таких как сыворотка, посредством диспергирования F28 тетрафенилпорфирина однородно в этих органических растворителях для того, чтобы получать жидкую композицию реактивов в соответствии с настоящим изобретением.
Пример 5
В этом примере 5 приведено объяснение выбора стабилизатора для литиевой композиции реактивов в соответствии с настоящим изобретением.
Использование стабилизаторов для литиевых композиций реактивов в примерах с 5 до 7 в целом аналогично примеру 1, но стабилизатор заменяли на только неионное поверхностно-активное вещество (пример 5), анионное поверхностно-активное вещество (пример 6) и как неионное поверхностно-активное вещество, так и анионное поверхностно-активное вещество (пример 7), соответственно.
В следующем примере 5 литиевая композиция реактивов содержит только неионное поверхностно-активное вещество (TritonX-100®) (полиоксиэтилен октилфениловый эфир) в качестве стабилизатора. Другие компоненты в литиевой композиции реактивов являются такими же, как в примере 1.
Пример 5
(1) Первый реактив (в качестве буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (дисперсант: неионное поверхностно-активное вещество): TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 7% по массе хлорида аммония для того, чтобы регулировать pH до pH 10, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
(2) Второй реактив (в качестве раствора окрашивающего реактива):
Хелатирующий реактив: F28 тетрафенилпорфирин: 0,5 г/л.
Органический растворитель: диметилсульфоксид (ДМСО): 20% по массе.
Стабилизатор (диспергирующее средство: неионное поверхностно-активное вещество) TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 0,05 M MOPS (буфер) для того, чтобы регулировать pH до pH 7,0, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
Пример 6
В примере 6 композиция содержит только анионное поверхностно-активное вещество (додецилсульфат натрия (Wako Junyaku)).
(1) Первый реактив (в качестве буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (дисперсант: только анионное поверхностно-активное вещество): додецилсульфат натрия (Wako Junyaku) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 7% по массе хлорида аммония для того, чтобы регулировать pH до pH 10, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
(2) Второй реактив (в качестве раствора окрашивающего реактива):
Хелатирующий реактив: F28 тетрафенилпорфирин: 0,5 г/л.
Органический растворитель: диметилсульфоксид (ДМСО): 20% по массе.
Стабилизатор (диспергирующее средство: только анионное поверхностно-активное вещество) (додецилсульфат натрия (Wako Junyaku)) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 0,05 M MOPS (буфер) для того, чтобы регулировать pH до pH 7,0. Затем общий объем увеличивали до 1 литра с использованием очищенной воды и получаемый раствор хранили в перемешиваемом контейнере общего назначения.
Пример 7
В примере 7 композиция содержит как анионное поверхностно-активное вещество, так и неионное поверхностно-активное вещество в качестве стабилизатора в литиевой композиции реактивов.
(1) Первый реактив (в качестве буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (дисперсант: неионное поверхностно-активное вещество и анионное поверхностно-активное вещество):
(a) неионное поверхностно-активное вещество: TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе;
(b) анионное поверхностно-активное вещество: додецилсульфат натрия (Wako Junyaku) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 7% по массе хлорида аммония для того, чтобы регулировать pH до pH 10. Затем общий объем увеличивали до 1 литра с использованием очищенной воды и получаемый раствор хранили в перемешиваемом контейнере общего назначения.
(2) Второй реактив (в качестве раствора окрашивающего реактива):
Хелатирующий реактив: F28 тетрафенилпорфирин: 0,5 г/л.
Органический растворитель: диметилсульфоксид (ДМСО): 20% по массе.
Стабилизатор (диспергирующее средство: неионное поверхностно-активное вещество и анионное поверхностно-активное вещество):
(a) неионное поверхностно-активное вещество: TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе;
(b) анионное поверхностно-активное вещество: додецилсульфат натрия (Wako Junyaku) 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов добавляли 0,05 M MOPS (буфер) для того, чтобы регулировать pH до pH 7,0. Затем общий объем увеличивали до 1 литра с использованием очищенной воды и получаемый раствор хранили в перемешиваемом контейнере общего назначения.
Концентрацию лития в контрольном образце сыворотки определяли количественно посредством той же процедуры, как в примере 1, с использованием литиевых композиций реактивов, которые получали в примере 5, примере 6 и примере 7. Результаты сведены в [таблице 4] на фиг. 10 «Сравнение измеряемых значений для различных стабилизаторов».
На фиг. 10 показано, что измеряемые значения совпадают более чем на 95% среди измеряемого значения для только неионного поверхностно-активного вещества (0,82 мМ), измеряемого значения для только анионного поверхностно-активного вещества (0,82 мМ) и измеряемого значения для двух поверхностно-активных веществ (0,83 мМ).
Этот результат показывает, что почти те же измеряемые значения можно получать независимо от типа используемого поверхностно-активного вещества или их комбинации. Следовательно, можно использовать комбинацию поверхностно-активных веществ для образца, в котором беспокоятся за суспензию или мутность.
Далее приведено объяснение выбора маскирующего реактива для литиевой композиции реактивов. В указанных выше примерах триэтаноламин использовали в качестве маскирующего реактива для литиевой композиции реактивов, но также можно использовать этилендиаминтетрауксусную кислоту (ЭДТА).
В примере 5 показан случай литиевой композиции реактивов, содержащей триэтаноламин в качестве маскирующего реактива, в примере 8 показан случай отдельно этилендиаминтетрауксусной кислоты (ЭДТА) и в примере 9 показан случай, содержащий оба маскирующих реактива.
Пример 8
В примере 8 использовали только этилендиаминтетрауксусную кислоту калия (ЭДТА, 2K) в качестве маскирующего реактива.
(1) Первый реактив (в качестве буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (дисперсант: неионное поверхностно-активное вещество): TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующий реактив: этилендиаминтетрауксусная кислота (ЭДТА 2K) (Dojin Chemical) 10 мМ.
В смесь приведенных выше компонентов добавляли 7% по массе хлорида аммония для того, чтобы регулировать pH до pH 10, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
(2) Второй реактив (в качестве раствора окрашивающего реактива):
Хелатирующий реактив: F28 тетрафенилпорфирин: 0,5 г/л.
Органический растворитель: диметилсульфоксид (ДМСО): 20% по массе.
Стабилизатор: TritonX-100® (полиоксиэтилен октилфениловый эфир): 1,0% по массе.
Маскирующий реактив: этилендиаминтетрауксусная кислота (ЭДТА 2K) (Dojin Chemical): 10 мМ.
В смесь приведенных выше компонентов добавляли 0,05 M MOPS (буфер) для того, чтобы регулировать pH до pH 7,0. Затем общий объем увеличивали до 1 литра с использованием очищенной воды и получаемый раствор хранили в перемешиваемом контейнере общего назначения.
Пример 9
В примере 9 как триэтаноламин, так и этилендиаминтетрауксусную кислоту (ЭДТА 2K) используют в комбинации в качестве маскирующего реактива.
(1) Первый реактив (в качестве буферного раствора):
Хелатирующий реактив: нет.
Органический растворитель: нет.
Стабилизатор (дисперсант: неионное поверхностно-активное вещество): TritonX-100® (полиоксиэтилен октилфениловый эфир): 1,0% по массе.
Маскирующий реактив: триэтаноламин 10 мМ.
В смесь приведенных выше компонентов, 7% по массе хлорида аммония добавляли для того, чтобы регулировать pH до pH 10, добавляли очищенную воду до общего объема 1 литр и хранили в контейнере общего назначения.
(2) Второй реактив (в качестве раствора окрашивающего реактива):
Хелатирующий реактив: F28 тетрафенилпорфирин: 0,5 г/л.
Органический растворитель: диметилсульфоксид (ДМСО): 20% по массе.
Стабилизатор: TritonX-100® (полиоксиэтилен октилфениловый эфир) 1,0% по массе.
Маскирующий реактив:
триэтаноламин: 10 мМ;
этилендиаминтетрауксусная кислота (ЭДТА 2K) (Dojin Chemical): 0,1 мМ.
В смесь приведенных выше компонентов добавляли 0,05 M MOPS (буфер) для того, чтобы регулировать pH до pH 7,0. Затем общий объем увеличивали до 1 литра с использованием очищенной воды и получаемый раствор хранили в перемешиваемом контейнере общего назначения.
Концентрацию лития в контрольном образце сыворотки определяли количественно посредством той же процедуры, как в примере 1, с использованием литиевых композиций реактивов, которые получали в примере 8 и примере 9. Результаты сведены в [таблице 5] на фиг. 11 «Сравнение измеряемых значений для различных маскирующих средств».
На фиг. 11 показано, что измеряемые значения совпадают более чем на 95% для измеряемого значения для только триэтаноламина (0,83 мМ), измеряемого значения для только этилендиаминтетрауксусной кислоты (ЭДТА) (0,83 мМ) и измеряемого значения для использования их комбинации (0,82 мМ).
Этот результат показывает, что почти те же измеряемые значения можно получать, независимо от типа используемого маскирующего средства или их комбинации. Следовательно, подходящее маскирующее средство(а) можно использовать для того, чтобы предотвращать разложение реактива, обусловленное следовыми ионами металлов, которые могут содержаться в исходном реактиве. Маскирующее средство можно использовать для тестового образца, содержащего избыточные ионные включения.
Как изложено в приведенных выше примерах в соответствии с данным изобретением, концентрацию лития в водном растворе, таком как образец из окружающей среды и биологический образец, можно определять посредством удобного колориметра и о ней можно судить незамедлительно посредством визуального наблюдения.
Объем данного изобретения не ограничен примерами, но его определяет формула изобретения. Детали в примерах можно заменять, изменять и модифицировать при условии, что характеристика данного изобретения не ухудшена. Например, в примерах 1-9 композицию реактивов для определения концентрации лития делят на два реактива первый и второй реактивы отдельно для того, чтобы хранить композицию реактивов в течение длительного времени. Однако если измерение осуществляют в пределах короткого периода, первый реактив и второй реактив можно смешивать в начале и получаемую смесь использовать в измерении.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ КЛОБЕТАЗОЛА В ВИДЕ НАНОЭМУЛЬСИИ МАСЛО В ВОДЕ | 2018 |
|
RU2759901C2 |
| РЕАКТИВ И НАБОР РЕАКТИВОВ ДЛЯ АНАЛИЗА НЕЗРЕЛЫХ ЛЕЙКОЦИТОВ | 2008 |
|
RU2435164C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2589842C2 |
| ПЛЕНКООБРАЗУЮЩАЯ КОМПОЗИЦИЯ СО СПОСОБНОСТЬЮ К РАСТЕКАНИЮ | 2007 |
|
RU2517960C2 |
| БОРИНОВЫЕ КОМПОЗИЦИИ | 2010 |
|
RU2521248C2 |
| КОМПОЗИЦИЯ ДЛЯ ОПРЕДЕЛЕНИЯ ИОНОВ НАТРИЯ (ВАРИАНТЫ) | 1991 |
|
RU2081411C1 |
| ФОСФАТ ЛИТИЯ-ЖЕЛЕЗА СО СТРУКТУРОЙ ОЛИВИНА И СПОСОБ ЕГО АНАЛИЗА | 2009 |
|
RU2484009C2 |
| ПОЛУЧЕНИЕ НАНОСТРУКТУРИРОВАННЫХ СМЕШАННЫХ ОКСИДОВ ЛИТИЯ И ЦИРКОНИЯ ПОСРЕДСТВОМ СПРЕЙ-ПИРОЛИЗА | 2020 |
|
RU2825204C1 |
| РЕАКТИВ ДЛЯ ИЗМЕРЕНИЯ ТРОМБОЦИТОВ, НАБОР РЕАКТИВОВ ДЛЯ ИЗМЕРЕНИЯ ТРОМБОЦИТОВ И СПОСОБ ИЗМЕРЕНИЯ ТРОМБОЦИТОВ | 2009 |
|
RU2445628C1 |
| КОМПОЗИЦИЯ ВОДНОЙ СУСПЕНЗИИ, ВКЛЮЧАЮЩАЯ НАНОЧАСТИЦЫ МАКРОЛИДНЫХ АНТИБИОТИКОВ | 2014 |
|
RU2707748C2 |





Группа изобретений относится к медицине и описывает композицию реактивов для измерения количества лития в биологических образцах, отличающуюся тем, что указанная композиция реактивов для измерения количества лития представляет собой водный раствор, содержащий соединение, которое имеет структуру, представленную формулой (I), смешиваемый с водой органический растворитель, выбранный из диметилсульфоксида (DMSO), диметилформамида (DMF) и диметилацетамида (DMA), и модификатор pH для доведения pH до значения в диапазоне от pH 5 до pH 12, концентрация соединения формулы (I) составляет от 0,1 до 1,0 г/л. Описан также набор реактивов для определения количества лития в биологических образцах, а также способ определения количества ионов лития в биологических образцах. Группа изобретений позволяет измерять количество ионов лития быстро или незамедлительно с использованием стандартного колориметра. 3 н. и 10 з.п. ф-лы, 9 пр., 11 ил.
1. Композиция реактивов для измерения количества лития в биологических образцах, отличающаяся тем, что указанная композиция реактивов для измерения количества лития представляет собой водный раствор, содержащий соединение, которое имеет структуру, представленную формулой (I):
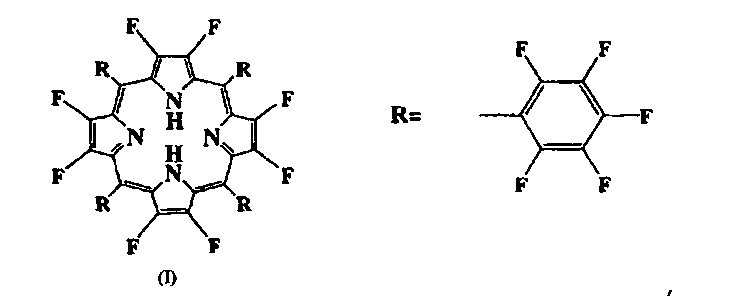
в которой все водороды, связанные с углеродами тетрафенилпорфирина, заменяют на атомы фтора, смешиваемый с водой органический растворитель, выбранный из диметилсульфоксида (DMSO), диметилформамида (DMF) и диметилацетамида (DMA), и модификатор pH для доведения pH до значения в диапазоне от pH 5 до pH 12, концентрация соединения формулы (I) составляет от 0,1 до 1,0 г/л.
2. Композиция реактивов по п. 1, в которой указанный модификатор pH выбирают из кислот, включающих соляную кислоту, азотную кислоту, уксусную кислоту, фосфорную кислоту, лимонную кислоту, угольную кислоту, дикарбоновую кислоту, щавелевую кислоту и их соли, щелочного средства, включая гидроксид натрия, гидроксид калия, аммиак и их соли.
3. Композиция реактивов по п. 1, в которой указанный модификатор pH представляет собой pH буфер.
4. Композиция реактивов по п. 3, в которой указанный pH буфер выбирают из лимонной кислоты, угольной кислоты, дикарбоновой кислоты, фосфорной кислоты, янтарной кислоты, фталевой кислоты, хлорида аммония, гидроксида натрия, гидроксида калия, MES в виде буфера Гуда, Bis-Tris, ADA, PIPES, ACES, MOPSO, BES, MOPS, TES, HEPES, DIPSO, TAPSO, POPSO, HEPPSO, EPPS, трицина, бицина, TAPS, CHES, CAPSO, CAPS и их солей.
5. Композиция реактивов по любому из пп. 1-4, в которой композиция реактивов развивает реакцию окраски для лития в диапазоне от pH 5 до pH 11.
6. Композиция реактивов по п. 1, которая дополнительно содержит стабилизатор.
7. Композиция реактивов по п. 1, в которой указанный стабилизатор представляет собой неионное поверхностно-активное вещество и/или анионное поверхностно-активное вещество.
8. Композиция реактивов по п. 7, в которой указанное неионное поверхностно-активное вещество выбирают из сложных эфиров сорбитана и жирной кислоты, неполных сложных эфиров пентаэритрита и жирной кислоты, сложных эфиров пропиленгликоля и жирной кислоты, сложного моноэфира глицерина и жирной кислоты, полиоксиэтиленалкилового эфира, полиоксиэтиленалкилфенилового эфира, полиоксиэтиленполиоксипропиленгликоля, неполных сложных эфиров полиоксиэтилена и жирной кислоты, неполных сложных эфиров полиоксиэтиленсорбита и жирной кислоты, сложных эфиров полиоксиэтилена и жирной кислоты, диэтаноламида жирной кислоты, моноэтаноламида жирной кислоты, полиоксиэтиленамида жирной кислоты, полиоксиэтилен октилфенилового эфира (TritonX-100®), п-нонилфеноксиполиглицидола и их солей.
9. Композиция реактивов по п. 7, в которой указанное анионное поверхностно-активное вещество представляет собой соль алкилсульфатного сложного эфира, включая додецилсульфат натрия, сульфатную соль полиоксиэтиленалкилового эфира, включая полиоксиэтиленалкилфенилового эфира сульфат натрия, алкилбензолсульфонатные соли, включая додецилбензолсульфонат натрия, и алкансульфонат.
10. Композиция реактивов по п. 1, которая дополнительно содержит маскирующий реактив.
11. Композиция реактивов по п. 10, в которой указанный маскирующий реактив выбирают из триэтаноламина, этилендиамина, N,N,N′,N′-тетракис(2-пиридилметил)этилендиамина (TPEN), пиридина, 2,2-дипиридина, пропилендиамина, диэтилентриамина, диэтилентриамин-N,N,N′,N″,N″-пентаацетата (DTPA), триэтилентетрамина, триэтилентетрамин-N,N,N′,N′,N″,N″-гексаацетата (ТТНА), 1,10-фенантролина, этилендиаминтетраацетата (ЭДТА), O,O′-бис(2-аминофенил)этиленгликоль-N,N,N′,N′-тетраацетата (ВАРТА), N,N-бис(гидроксиэтил)глицина (бицин), транс-1,2-диаминоциклогексан-N,N,N′,N″-тетраацетата (CyDTA), O,O′-бис(2-аминоэтил)этиленгликоль-N,N′,N′-тетраацетата (EGTA), N-(2-гидроксил)иминодиацетата (HIDA), иминодиуксусной кислоты (IDA), нитрилтриуксусной кислоты (NTA), нитрило трис-метилфосфоната (NTPO) и их солей.
12. Набор реактивов для определения количества лития в биологических образцах композицией литиевых реактивов в форме водного раствора, содержащий соединение, которое имеет структуру, представленную формулой (I):
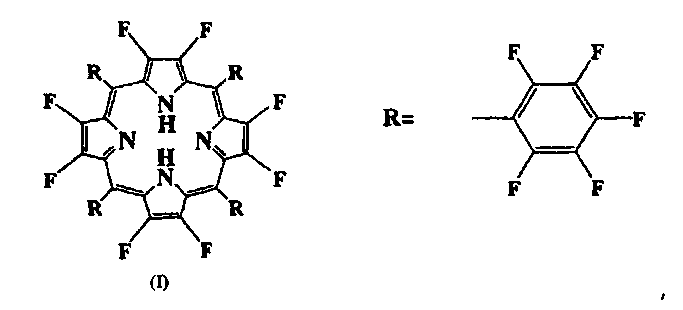
в которой все водороды, связанные с углеродами тетрафенилпорфирина, заменяют на атомы фтора, смешиваемый с водой органический растворитель, выбранный из диметилсульфоксида (DMSO), диметилформамида (DMF) и диметилацетамида (DMA) и модификатор pH для доведения pH до значения в диапазоне от pH 5 до pH 12, концентрация соединения формулы (I) составляет от 0,1 до 1,0 г/л,
в котором композицию реактивов для определения лития хранят в форме двух отдельных реактивов, включающих первый реактив, включающий модификатор pH, стабилизатор, маскирующий реагент и воду, и второй реактив, включающий соединение формулы (I), смешиваемый с водой органический растворитель, другой модификатор pH, стабилизатор, маскирующий реактив и воду, и указанные первый и второй реагенты смешивают непосредственно перед измерением для того, чтобы формировать литиевую композицию реактивов.
13. Способ определения количества ионов лития в биологических образцах, отличающийся тем, что биологический образец приводят в контакт с композицией реактивов в форме водного раствора, содержащего соединение, которое имеет структуру, представленную формулой (I):
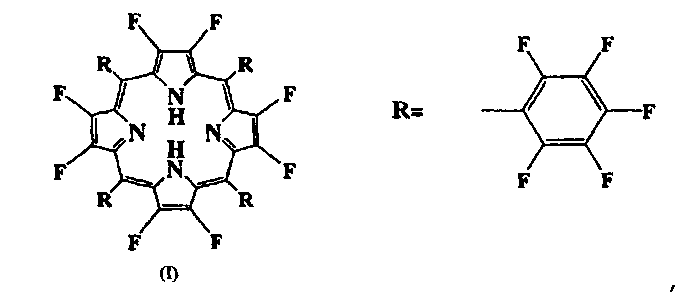
в которой все водороды, связанные с углеродами тетрафенилпорфирина, заменяют на атомы фтора, концентрация соединения формулы (I) составляет от 0,1 до 1,0 г/л, смешиваемый с водой органический растворитель, выбранный из диметилсульфоксида (DMSO), диметилформамида (DMF) и диметилацетамида (DMA), и модификатор pH для корректировки pH до диапазона от pH 5 до pH 12, и измеряют окраску получаемого литиевого комплекса в спектре при длине волны 550 нм, или вблизи от диапазона длин волн от 530 нм до 560 нм или при длине волны 570 нм или вблизи от диапазона длин волн от 565 нм до 650 нм, чтобы вычислить количество лития.
| K | |||
| Koyanagi et al | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Дезинтегратор | 1922 |
|
SU803A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2015-12-20—Публикация
2012-04-25—Подача