Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения смешанных оксидов лития и циркония посредством спрей-пиролиза в пламени, к смешанным оксидам, получаемым данным способом, и к их применению в литий-ионных аккумуляторных батареях.
Уровень техники
Вторичные литий-ионные аккумуляторные батареи являются одним из наиболее важных типов аккумуляторных батарей, используемых в настоящее время. Вторичные литий-ионные аккумуляторные батареи, как правило, состоят из анода, полученного из углеродного материала или сплава лития и металла, катода, полученного из оксида лития и металла, жидкого электролита, в котором соль лития растворена в органическом растворителе и сепаратора, обеспечивающего прохождение ионов лития между положительным и отрицательным электродом во время процессов заряда и разряда.
В стремлении разработать вторичные аккумуляторные батареи с улучшенной искробезопасностью и плотностью энергии в последнее время значительно продвинулось использование твердых электролитов вместо жидких. Такие полностью твердотельные вторичные литий-ионные аккумуляторные батареи должны иметь хорошую ионную проводимость на границе между материалом для активного электрода и электролитом, чтобы иметь требуемые характеристики нагрузки. Эта высокая ионная проводимость может быть достигнута посредством покрытия поверхности материала для активного электрода некоторыми соединениями, содержащими литий, такими как LiTi2(PO4)3, как описано в документе JP 4982866 В2.
Смешанные оксиды, содержащие литий, находят различные варианты применения как в твердотельных, так и в жидких литий-ионных аккумуляторных батареях.
Одной из общих проблем материалов катода литий-ионных аккумуляторных батарей является их быстрое старение и, следовательно, потеря характеристик в циклическом режиме работы. Известно, что покрытие или легирование частиц смешанного оксида лития и переходного металла некоторыми оксидами металлов может подавлять нежелательные реакции электролита с материалами электрода и, следовательно, улучшать длительную стабильность литиевых аккумуляторных батарей.
Среди других оксидов металлов для этой цели сообщалось о смешанных оксидах, содержащих цирконий.
В документе US 2017179544 А раскрыто получение материалов для литиевых положительных электродов, легированных смешанными оксидами металлов на основе циркония. Так, в примере 1, Li7La3Zr2Al0,07O12,0105 получали посредством смешивания солей металлов и спекания смеси при 1200°С в течение 10 часов с последующим сухим смешиванием со смешанным оксидом лития и переходного металла Li(Li10/75Ni18/75Co9/75Mn38/75)O2 и последующим нагреванием при 900°С в течение 20 часов с образованием материала для литиевого положительного электрода. Из этой процедуры получения видно, что в этом примере можно использовать только спеченные частицы Li7La3Zr2Al0,07O12,0105 большого размера.
Применение таких относительно больших частиц оксида металла, содержащих цирконий, зачастую приводит к неоднородному распределению и крупным агломерированным частицам оксида металла на поверхности ядра катодного материала, и, в результате чего, наблюдается минимальное улучшение характеристик при циклическом режиме работы или их отсутствие по сравнению с нелегированными или непокрытыми катодными материалами.
В Ceramic transactions (1997), 85, рр. 55-66, описано получение порошка Li2ZrO3 с первичными частицами размером менее 20 нм и площадью поверхности по методу БЭТ 10-14 м2/г в процессе горения, начиная с водных растворов предшественников в виде нитратов циркония и лития. К такому водному раствору предшественников металлов в качестве топлива добавляют мочевину и лимонную кислоту. Нагрев полученной смеси приводит к полному испарению воды и последующему сгоранию предшественников металлов и топлива. Несмотря на получение частиц оксида металла относительно небольшого размера, этот способ вряд ли применим в промышленности, особенно для непрерывного получения больших количеств соответствующего смешанного оксида лития и циркония.
Спрей-пиролиз является известным способом получения относительно небольших частиц оксида металла.
Спрей-пиролиз и спрей-пиролиз в пламени являются общепризнанными способами получения простых оксидов металлов, а также сложных смешанных оксидов металлов. При спрей-пиролизе соединения металлов в виде мелких капель вводятся в высокотемпературную зону, где они окисляются и/или гидролизуются с образованием оксидов металлов. Особой формой этого способа является спрей-пиролиз в пламени, при котором капли подаются в пламя, образующееся при воспламенении горючего газа и кислородсодержащего газа.
В IN2010K000216 описан способ спрей-пиролиза для синтеза наноструктурированного порошка цирконата лития с применением растворов предшественников на водной основе. Таким образом, в примерах данной заявки на патент показано применение водных растворов нитрата циркония или оксинитрата циркония, нитрата лития и мочевины или глицина для получения цирконата лития с площадью поверхности по методу БЭТ 6-10 м2/г и трамбовочной плотностью не более 1020 г/л.
Проблема и решение
В цитируемом документе предшествующего уровня техники описано получение смешанных оксидов лития и циркония посредством спрей-пиролиза. Однако сообщается, что полученные продукты имеют относительно большие значения трамбовочной плотности и относительно низкую площадь поверхности по методу БЭТ, что предполагает относительно большой совокупный размер таких частиц.
Задача, решаемая настоящим изобретением, заключается в предоставлении улучшенного способа промышленного получения смешанных оксидов лития и циркония, пригодных для применения в литий-ионных аккумуляторных батареях, особенно в качестве покрытия или легирующего материала для электродов литий-ионных аккумуляторных батарей, в частности катодов, и в качестве добавок к электролитам литий-ионных аккумуляторных батарей.
В частности, данный способ должен предоставить получение частиц оксида металла с относительно небольшим размером частиц, высокой площадью поверхности по методу БЭТ и низкой трамбовочной плотностью.
В ходе тщательных экспериментов было неожиданно обнаружено, что смешанные оксиды лития и циркония с требуемыми свойствами частиц могут быть получены посредством способа спрей-пиролиза в пламени при использовании специальной комбинации предшественников металлов и растворителей.
Способ получения смешанного оксида
В настоящем изобретении предусмотрен способ получения смешанного оксида лития и циркония посредством спрей-пиролиза в пламени и необязательной дополнительной термической обработки, характеризующийся тем, что в способе применяют по меньшей мере один раствор предшественников металлов, содержащий:
- карбоксилат лития и карбоксилат циркония, где каждый из данных карбоксилатов металлов содержит от 5 до 20 атомов углерода, и
- растворитель, содержащий менее 5% по массе воды.
Термин «смешанный оксид лития и циркония» в контексте настоящего изобретения обозначает химическое соединение или смесь химических соединений, содержащих атомы лития (Li), циркония (Zr) и кислорода (О).
Во время процесса спрей-пиролиза в пламени раствор соединений металлов (предшественников металлов) в виде мелких капель вводят в пламя, которое образуется при воспламенении горючего газа и кислородсодержащего газа, где используемые предшественники металлов окисляются и/или гидролизуются с получением соответствующих оксидов металлов.
В результате данной реакции сначала образуются высокодисперсные первичные частицы оксида металла примерно сферической формы, которые в дальнейшем в ходе реакции объединяются с образованием агрегатов. Затем агрегаты могут соединяться в агломераты. В отличие от агломератов, которые, как правило, можно относительно легко разделить на агрегаты путем подведения энергии, агрегаты распадаются дальше, если вообще распадаются, только за счет интенсивного подведения энергии.
Полученные оксиды металлов называются «высокодисперсными» или «полученными пирогенным способом» оксидами металлов.
Способ спрей-пиролиза в пламени в целом описан в документе WO 2015173114 А1 и других источниках.
Спрей-пиролиз в пламени предпочтительно включает следующие стадии, на которых:
а) по меньшей мере один раствор предшественников металлов распыляют с получением аэрозоля посредством распыляющего газа,
b) аэрозоль вводят в реакцию в реакционном пространстве реактора с пламенем, полученным воспламенением смеси горючего газа и кислородсодержащего газа, с получением реакционного потока,
c) реакционный поток охлаждают и
d) твердый оксид металла затем удаляют из реакционного потока.
Примерами подходящих горючих газов являются водород, метан, этан, природный газ и/или монооксид углерода. Особенно предпочтительно использовать водород. Горючий газ используется, в частности, для вариантов осуществления, где требуется высокая кристалличность получаемых оксидов металлов.
Кислородсодержащий газ обычно представляет собой воздух или воздух, обогащенный кислородом. Кислородсодержащий газ используется, в частности, для вариантов осуществления, где, например, требуется высокая площадь поверхности по методу БЭТ получаемого оксида металла. Общее количество кислорода обычно выбирают таким, чтобы его было достаточно, по крайней мере, для полной конверсии горючего газа и предшественников металлов.
Для получения аэрозоля выпаренный раствор, содержащий предшественники металлов, может быть смешан с распыляющим газом, таким как азот, воздух и/или другие газы. Полученные мелкие капли аэрозоля предпочтительно характеризуются средним размером капель 1-120 мкм, особенно предпочтительно 30-100 мкм. Капли обычно получают с использованием форсунок из одного или нескольких материалов. Чтобы увеличить растворимость предшественников металлов и достичь подходящей вязкости для распыления раствора, раствор можно нагреть.
Предшественники металлов, используемые в способе по настоящему изобретению, включают по меньшей мере один карбоксилат лития и по меньшей мере один карбоксилат циркония, каждый из которых содержит от 5 до 20 атомов углерода.
Карбоксилаты лития и циркония, используемые в способе в соответствии с настоящим изобретением, могут независимо друг от друга представлять собой линейные, разветвленные или циклические пентаноат (С5), гексаноат (С6), гептаноат (С7), октаноат (С8), нонаноат (С9), деканоат (D10), ундеканоат (С11), додеканоат (С12), тридеканоат (С13), тетрадеканоат (С14), пентадеканоат (С15), гексадеканоат (С16), гептадеканоат (С17), октадеканоат (С18), нонадеканоат (С19), икозаноат (С20) лития и/или циркония и их смеси.
Наиболее предпочтительно используют 2-этилгексаноат циркония (С8) и неодеканоат лития (С10).
Растворитель, применяемый в способе по настоящему изобретению, предпочтительно выбран из группы, состоящей из спирта, простого эфира, сложного эфира, карбоновых кислот, необязательно галогенированного углеводорода и их смесей.
Спирт может быть выбран из группы, состоящей из метанола, этанола, н-пропанола, изопропанола, н-бутанола, втор-бутанола, трет-бутанола, н-пентанола, н-гексанола, циклогексанола, н-октанола, 2-этилгексанола, н-деканола, неодеканола и их смесей.
Сложный эфир может представлять собой алкиловый эфир карбоновой кислоты, такой как этилацетат.
Карбоновая кислота предпочтительно содержит 1-20 атомов углерода и предпочтительно выбрана из группы, состоящей из уксусной кислоты, линейной, разветвленной или циклической пропионовой кислоты (С3), бутановой кислоты (С4), пентановой кислоты (С5), гексановой кислоты (С6), гептановой кислоты (С7), октановой кислоты (С8), нонановой кислоты (С9), декановой кислоты (С10), ундекановой кислоты (С11), додекановой кислоты (С12), тридекановой кислоты (С13), тетрадекановой кислоты (С14), пентадекановой кислоты (С15), гексадекановой кислоты (С16), гептадекановой кислоты (С17), октадекановой кислоты (С18), нонадекановой кислоты (С19), икозановой кислоты (С20) и их смесей.
Углеводороды могут быть линейными, разветвленными, циклическими алифатическими, ароматическими или смешанными алифатическими/ароматическими. Их подходящие примеры включают бензол, толуол, нафту и уайт-спирит.
Примеры галогенированных углеводородов включают хлороформ (CHCl3), дихлорметан (CH2Cl2), тетрахлорид углерода (CCl4).
Наиболее предпочтительно смесь углеводорода и карбоновой кислоты, например нафты и 2-этилгексановой кислоты, используется в качестве растворителя.
Растворитель, применяемый в настоящем изобретении, содержит менее 5 по массе воды, предпочтительно менее 3% по массе воды, более предпочтительно менее 2% по массе воды, еще более предпочтительно менее 1% по массе воды, еще более предпочтительно менее 0,5% по массе воды.
Наиболее предпочтительно растворитель по сути не содержит воды, т.е. содержание воды в растворителе составляет менее 0,1% по массе, более предпочтительно менее 500 ppm, еще более предпочтительно менее 200 ppm.
Общее содержание металлов в растворе предшественников металлов предпочтительно составляет 1% - 30% по массе, более предпочтительно 2% - 20% по массе, еще более предпочтительно 3% - 15% по массе. Под «общим содержанием металлов» понимают общую массовую долю всех металлов, содержащихся в предшественниках металлов, в используемом растворе предшественников металлов.
Смесь растворителей, используемая в способе по настоящему изобретению, может дополнительно содержать хелатирующее средство, т.е. соединение, способное образовывать две или более координационных связи с ионами металла. Примерами таких хелатирующих средств являются, например, диамины, такие как этилендиамин, этилендиаминтетрауксусная кислота (EDTA), 1,3-дикарбонильные соединения, такие как ацетилацетон и алкилацетилацетат. Наиболее предпочтительно в качестве такого хелатирующего средства используют ацетилацетон.
Было замечено, что в присутствии таких хелатирующих средств, предшественники циркония могут показывать лучшую растворимость и не осаждаться после относительно длительного времени хранения.
Применение специальной комбинации карбоксилатов металлов и растворителя с пониженным содержанием воды в соответствии с настоящим изобретением позволяет обеспечить хорошую растворимость предшественников металлов и достичь требуемых свойств частиц оксида металла, таких как малый размер частиц, высокая площадь поверхности по методу БЭТ и низкая трамбовочная плотность.
Способ в соответствии с настоящим изобретением включает необязательную дополнительную термическую обработку смешанного оксида, полученного способом спрей-пиролиза в пламени.
Данную дополнительную термическую обработку предпочтительно осуществляют при температуре 500°С - 1200°С, более предпочтительно при 550°С - 1150°С, даже более предпочтительно при 600°С - 1100°С, еще более предпочтительно при 650°С - 1050°С.
Термическая обработка в соответствии со способом по настоящему изобретению позволяет получить термически обработанный смешанный оксид с требуемыми свойствами, особенно с требуемыми химическими фазами, кристаллической структурой и т.д. Таким образом, термически необработанный смешанный оксид лития и циркония, полученный непосредственно способом спрей-пиролиза в пламени, может содержать смесь ZrO2, Li2O, Li2ZrO3 и других химических соединений. Термическая обработка этой смеси при температуре приблизительно 600°С - 800°С позволяет дополнительно образовать фазы Li2ZrO3 и Li4Zr3O8, так что это последнее соединение становится доминирующей химической фазой, присутствующей в термически обработанном смешанном оксиде.
Смешанный оксид
Смешанный оксид, полученный с помощью способа в соответствии с настоящим изобретением, предпочтительно характеризуется площадью поверхности по методу БЭТ 0,1 м2/г - 100 м2/г.
Термически необработанный смешанный оксид, т.е. продукт, полученный с помощью способа по настоящему изобретению, где не применялась дополнительная термическая обработка, предпочтительно характеризуется площадью поверхности по методу БЭТ 5 м2/г - 100 м2/г, более предпочтительно 7 м2/г-70 м2/г, наиболее предпочтительно 15-50 м2/г.
Термически обработанный смешанный оксид, т.е. продукт, полученный с помощью способа в соответствии с настоящим изобретением, где была использована дополнительная термическая обработка, предпочтительно характеризуется площадью поверхности по методу БЭТ менее 20 м2/г, более предпочтительно 0,1 м2/г - 10 м2/г, более предпочтительно 0,2 м2/г - 5 м2/г, наиболее предпочтительно 0,3-3 м2/г.
Площадь поверхности по методу БЭТ может быть определена согласно DIN 9277:2014 путем адсорбции азота согласно методу Брунауэра-Эммета-Теллера.
Смешанный оксид, полученный с помощью способа в соответствии с настоящим изобретением, обычно находится в форме агрегированных первичных частиц со среднечисловым диаметром первичных частиц 5-100 нм, предпочтительно 7-70 нм, более предпочтительно 10-50 нм, как определено с помощью просвечивающей электронной микроскопии (ТЕМ). Этот среднечисловой диаметр может быть определен путем вычисления среднего размера по меньшей мере 500 частиц, анализируемых с применением ТЕМ.
Среднечисловой диаметр частиц смешанного оксида (агрегированного и агломерированного) d50 обычно составляет приблизительно 0,05 мкм 2 мкм, более предпочтительно 0,05 мкм - 1 мкм, еще более предпочтительно 0,05 мкм - 0,5 мкм. Данный среднечисловой диаметр может быть определен в подходящей дисперсии, например, в водной дисперсии методом статического светорассеяния (SLS).
Агломераты и частично агрегаты могут быть разрушены, например, посредством измельчения или обработкой ультразвуком частиц для получения частиц с меньшим размером частиц и более узким распределением частиц по размерам.
Предпочтительно средний диаметр частиц d50 смешанного оксида составляет 10-150 нм, более предпочтительно 20-130 нм, еще более предпочтительно 30-120 нм, как определено посредством статического светорассеяния (SLS) после 300 с обработки ультразвуком при 25°С для смеси, состоящей из 5% по массе частиц и 95% по массе 0,5 г/л раствора пирофосфата натрия в воде.
Интервал (d90-d10)/d50 частиц диоксида циркония и/или смешанного оксида, содержащего цирконий, предпочтительно составляет 0,4-1,2, более предпочтительно 0,5-1,1, еще более предпочтительно 0,6-1,0, как определено посредством статического светорассеяния (SLS) после 300 с обработки ультразвуком при 25°С для смеси, состоящей из 5% по массе частиц и 95% по массе 0,5 г/л раствора пирофосфата натрия в воде.
Таким образом, смешанный оксид, полученный с помощью способа по настоящему изобретению, предпочтительно характеризуется относительно небольшим размером частиц и узким распределением частиц по размерам. Это помогает достичь качественного легирования оксидами металлов и/или покрытия материалов для активных электродов литий-ионных аккумуляторных батарей.
Значения d в виде d10, d50 и d90 обычно применяются для характеристики кумулятивного распределения частиц по диаметру для данного образца.
Например, диаметр d10 представляет собой диаметр, при котором 10% объема образца составляют частицы размером меньше чем d10, d50 представляет собой диаметр, при котором 50% объема образца составляют частицы размером меньше чем d50. d50 также известен как «объемный медианный диаметр», поскольку он делит образец поровну по объему; d90 представляет собой диаметр, при котором 90% объема образца составляют частицы размером меньше чем d90.
Смешанный оксид, полученный с помощью способа в соответствии с настоящим изобретением, предпочтительно характеризуется трамбовочной плотностью 20 г/л - 1000 г/л.
Термически необработанный смешанный оксид, полученный способом в соответствии с настоящим изобретением, предпочтительно имеет трамбовочную плотность 20 г/л - 300 г/л, более предпочтительно 30 г/л - 270 г/л, еще более предпочтительно 40 г/л - 250 г/л, еще более предпочтительно 50 г/л - 200 г/л.
Термически обработанный смешанный оксид, полученный с помощью способа в соответствии с настоящим изобретением, предпочтительно характеризуется трамбовочной плотностью 200 г/л - 800 г/л, более предпочтительно 250 г/л - 750 г/л, еще более предпочтительно 300 г/л - 700 г/л.
Трамбовочная плотность порошкообразного или крупнозернистого гранулированного материала можно определить согласно DIN ISO 787-11:1995 «General methods of test for pigments and extenders - Part 11: Determination of tamped volume and apparent density after tamping». Определение включает измерение кажущейся плотности слоя после встряхивания и трамбования.
Смешанный оксид, полученный с помощью способа по настоящему изобретению, предпочтительно является гидрофильным по своей природе, то есть его не подвергают дополнительной обработке какими-либо гидрофобными реагентами, такими как силаны, после его синтеза посредством способа спрей-пиролиза в пламени. Полученные таким образом частицы, как правило, характеризуются чистотой по меньшей мере 96% по массе, предпочтительно по меньшей мере 98% по массе, более предпочтительно по меньшей мере 99% по массе, где 100% чистота означает, что смешанный оксид содержит только указанные металлы и кислород. Смешанный оксид может содержать соединения гафния в форме диоксида гафния. Доля диоксида гафния может составлять от 1 до 4% по массе в пересчете на ZrO2. Содержание хлорида предпочтительно составляет менее 0,5% по массе, более предпочтительно менее 0,1% по массе в пересчете на массу порошка смешанного оксида. Доля углерода предпочтительно составляет менее 2% по массе, более предпочтительно 0,005% - 1%) по массе, еще более предпочтительно 0,01% - 0,5% по массе в пересчете на массу порошка смешанного оксида.
Смешанный оксид предпочтительно представляет собой соединение общей формулы
LiaZrbO0,5a+2b, где
0,5 ≤ а ≤ 12, предпочтительно 2,0 ≤ а ≤ 8;
1,0 ≤ b ≤ 4,0, предпочтительно 1,0 ≤ b ≤ 2,0.
Предпочтительно композиция смешанного оксида в соответствии с настоящим изобретением соответствует одной из формул: Li2ZrO3, Li4Zr2O6, Li4ZrO4, Li4Zr3O8, Li6Zr3O9, Li8ZrO6, наиболее предпочтительно Li2ZrO3.
В настоящем изобретении также предусмотрен смешанный оксид лития и циркония, где
- смешанный оксид находится в виде агрегированных первичных частиц,
- характеризуется площадью поверхности по методу БЭТ 15-50 м2/г,
- среднечисловым диаметром частиц d50=0,05-1 мкм,
как определено посредством статического светорассеяния (SLS), и
- трамбовочной плотностью 50-200 г/л.
Такой смешанный оксид может быть получен с помощью способа по настоящему изобретению, где не применяется дополнительная термическая обработка.
В настоящем изобретении также предусмотрен смешанный оксид лития и циркония, где
- смешанный оксид находится в виде агрегированных первичных частиц,
- характеризуется площадью поверхности по методу БЭТ менее 20 м2/г, предпочтительно 0,1-20 м2/г,
- среднечисловым диаметром частиц d50=1-50 мкм, как определено посредством статического светорассеяния (SLS), и
- трамбовочной плотностью 200-800 г/л.
Такой смешанный оксид может быть получен с помощью способа в соответствии с настоящим изобретением, где применяется дополнительная термическая обработка.
В настоящем изобретении дополнительно предусмотрен смешанный оксид, получаемый с помощью способа в соответствии с настоящим изобретением.
Применение смешанного оксида в литий-ионных аккумуляторных батареях
В настоящем изобретении дополнительно предусмотрено применение смешанного оксида в соответствии с настоящим изобретением или смешанного оксида, получаемого способом в соответствии с настоящим изобретением, в литий-ионных аккумуляторных батареях, в частности, в качестве покрытия или легирующего материала для электродов литий-ионных аккумуляторных батарей, особенно катодов, или в качестве добавки к жидкому, гелеобразному или твердотельному электролиту литий-ионных аккумуляторных батарей.
В настоящем изобретении дополнительно предусмотрена литий-ионная аккумуляторная батарея, содержащая смешанный оксид в соответствии с настоящим изобретением или смешанный оксид, получаемый с помощью способа по настоящему изобретению.
Литий-ионная аккумуляторная батарея в соответствии с настоящим изобретением, помимо активного положительного электрода (катода), может содержать анод, сепаратор и электролит, содержащий соединение, содержащее литий.
Положительный электрод литий-ионной аккумуляторной батареи (катод), как правило, включает токоприемник и слой материала для активного катода, образованный на токоприемнике.
Токоприемник может представлять собой алюминиевую фольгу, медную фольгу, никелевую фольгу, фольгу из нержавеющей стали, титановую фольгу, полимерную подложку, покрытую токопроводящим металлом, или их комбинацию.
Материалы для активного положительного электрода могут включать материалы, способные к обратимому интеркалированию/деинтеркалированию ионов лития, и они хорошо известны из уровня техники. Такие материалы для активного положительного электрода могут включать оксиды переходных металлов, такие как смешанные оксиды, содержащие Ni, Со, Mn, V или другие переходные металлы, и необязательно литий. Смешанные оксиды лития и переходных металлов, предпочтительно применяемые в качестве материалов для активного положительного электрода, выбраны из группы, состоящей из оксида лития и кобальта, оксида лития и марганца, оксидов лития, никеля и кобальта, оксидов лития, никеля, марганца и кобальта, оксидов лития, никеля, кобальта и алюминия, оксидов лития, никеля и марганца или их смеси. Смешанный оксид лития и переходного металла предпочтительно характеризуется общей формулой LiMO2, где М представляет собой по меньшей мере один переходный металл, выбранный из никеля, кобальта, марганца; более предпочтительно М=Со или NixMnyCoz, где 0,3 ≤ х ≤ 0,9, 0 ≤ у ≤ 0,45, 0 ≤ z ≤ 0,4.
Анод литий-ионной аккумуляторной батареи может содержать любой подходящий материал, обычно применяемый во вторичных литий-ионных аккумуляторных батареях, который способен к обратимому интеркалированию/деинтеркалированию ионов лития. Типичными их примерами являются углеродсодержащие материалы, включая кристаллический углерод, такой как природный или искусственный графит в форме пластинчатого, хлопьевидного, сферического или волокнистого графита; аморфный углерод, такой как мягкая сажа, твердый углерод, карбид мезофазного пека, обожженный кокс и т.п. или их смеси. Кроме того, в качестве активных анодных материалов можно использовать металлический литий или материалы конверсионного типа (например, Si или Sn).
Электролит литий-ионной аккумуляторной батареи может быть в жидкой, гелеобразной или твердой форме.
Жидкий электролит литий-ионной аккумуляторной батареи может содержать любой подходящий органический растворитель, обычно используемый в литий-ионных аккумуляторных батареях, такой как безводный этиленкарбонат (ЕС), диметилкарбонат (DMC), пропиленкарбонат, метилэтилкарбонат, диэтилкарбонат, гамма-бутиролактон, диметоксиэтан, фторэти лен карбонат, винилэтиленкарбонат или их смесь.
Гелеобразные электролиты включают образующие гели полимеры.
Твердый электролит литий-ионной аккумуляторной батареи может содержать оксиды, например, оксиды, сульфиды, фосфаты металлического лития или твердые полимеры.
Жидкий или гелеобразный электролит литий-ионной аккумуляторной батареи, как правило, содержит соль лития. Примеры таких солей лития включают гексафторфосфат лития (LiPF6), бис-2-(трифторметилсульфонил)имид лития (LiTFSI), перхлорат лития (LiClO4), тетрафторборат лития (LiBF4), Li2SiF6, трифлат лития, нитрат лития LiN(SO2CF2CF3)2, бис(оксалат)борат, литий-циклодифторметан-1,1-бис(сульфонил)имид, литий-циклогексафторпропан-1,1-бис(сульфонил)имид и их смеси.
Литий-ионная аккумуляторная батарея, особенно батарея с жидким или гелеобразным электролитом, также может содержать сепаратор, который предотвращает непосредственный контакт между двумя электродами, который может привести к внутреннему короткому замыканию.
Материал сепаратора может содержать полиолефиновую смолу, фторированную полиолефиновую смолу, полиэфирную смолу, полиакрилонитрильную смолу, целлюлозную смолу, нетканый материал или их смесь. Предпочтительно данный материал содержит полиолефиновую смолу, такую как полимер на основе полиэтилена или полипропилена, фторированную смолу, такую как полимер в виде поливинилиденфторида или политетрафторэтилен, полиэфирную смолу, такую как полиэтилентерефталат и полибутилентерефталат, полиакрилонитрильную смолу, целлюлозную смолу, нетканый материал или их смесь.
Краткое описание графических материалов
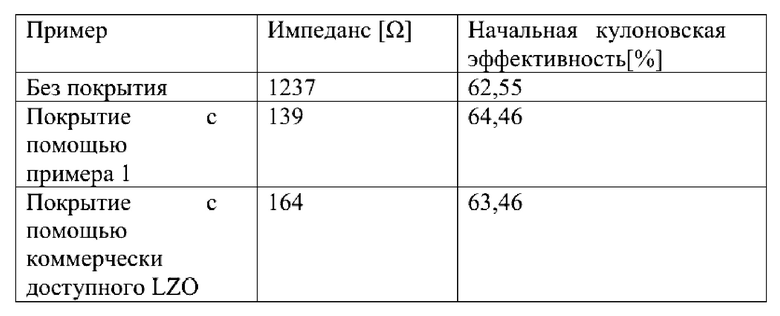
Фиг. 1А и 1В представляют собой полученные с помощью ТЕМ изображения частиц смешанного оксида Li-Zr, полученных, как описано в примере 1.
На фиг. 2 показано изображение картирования Zr (белого цвета) с помощью SEM-EDX на NMC, покрытом LZO, полученном с применением LZO, полученного, как описано в примере 1.
На фиг. 3 показано изображение картирования Zr (белого цвета) с помощью SEM-EDX на NMC, покрытом LZO, полученном с применением LZO, полученного, как описано в сравнительном примере 1.
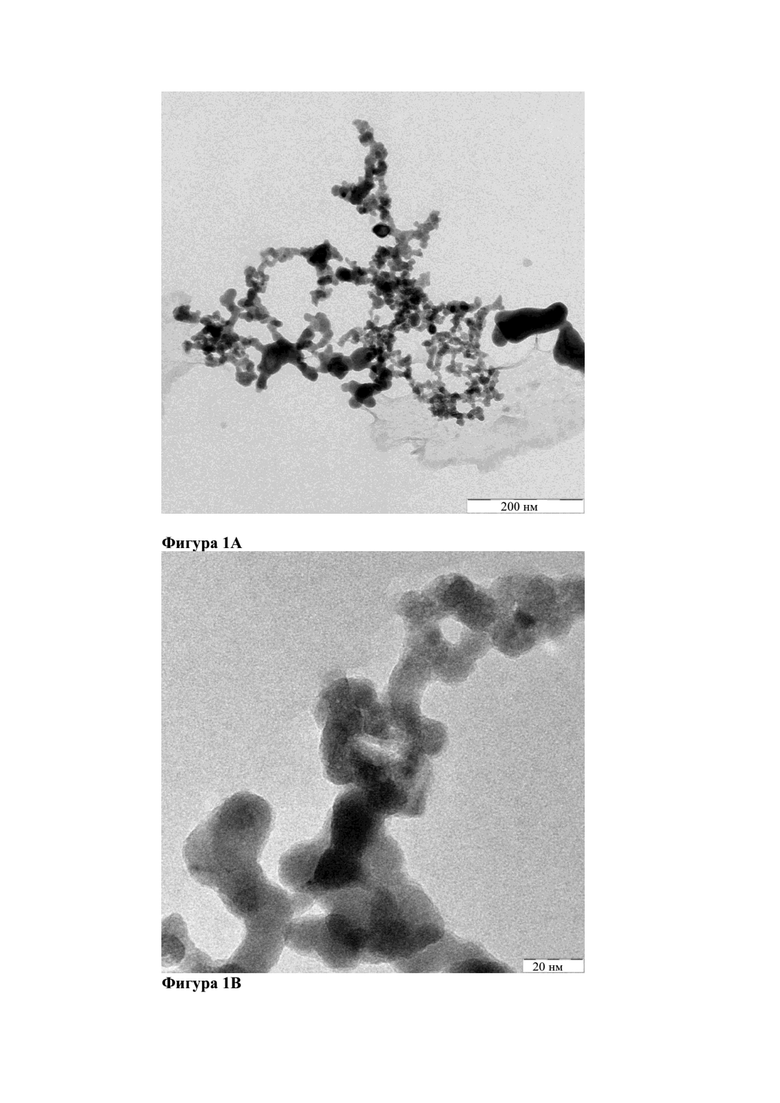
На фиг. 4 показаны результаты статистического анализа распределения площади Zr на изображениях картирования SEM-EDX для NMC, покрытого LZO, полученного с применением LZO, полученного, как описано в сравнительном примере 1 и примере 1.
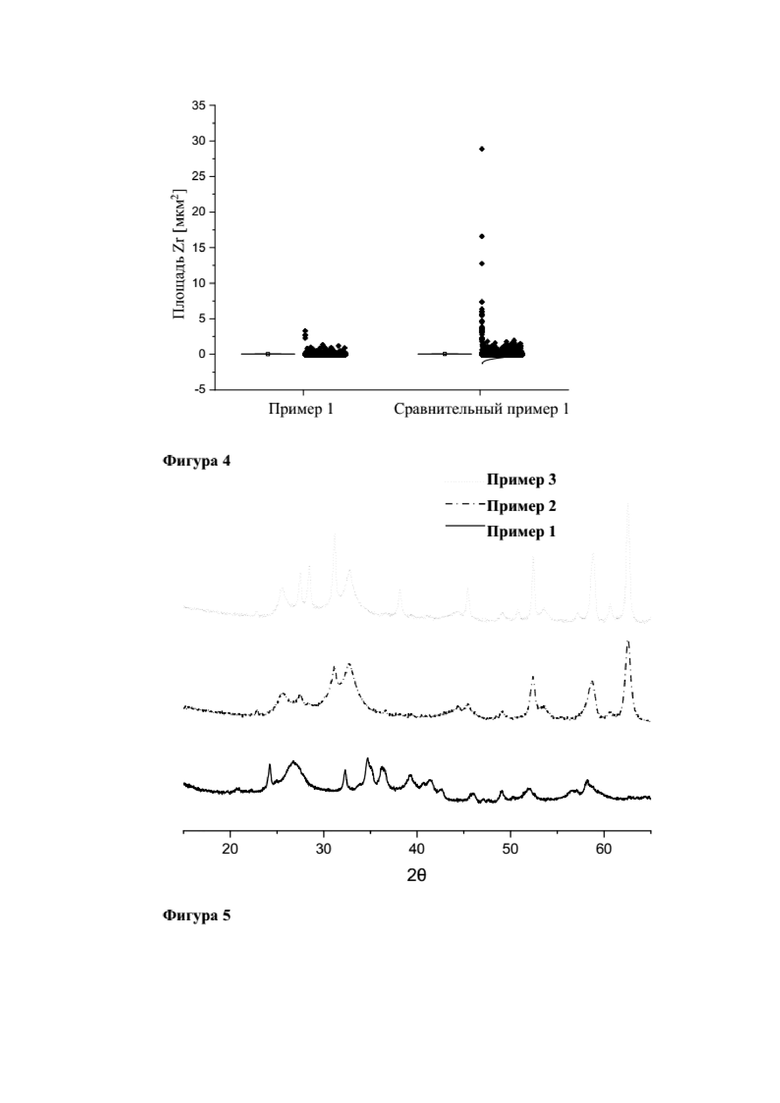
На фиг. 5 показаны рентгеновские дифрактограммы смешанного оксида Li-Zr (LZO) в соответствии с настоящим изобретением, полученного, как описано в примерах 1-3.
Примеры
Коммерчески доступный порошок смешанного оксида лития, никеля, марганца и кобальта NMC (7-1,5-1,5) (тип PLB-H7) с площадью поверхности по методу БЭТ 0,30-0,60 м2/г, средним диаметром частиц d50=10,6±2 мкм (определенным методом статического лазерного рассеяния) был предоставлен Linyi Gelon LIB Co.
Коммерчески доступный порошок оксида лития и циркония LZO (тип 2004PR) с площадью поверхности по методу БЭТ менее 1 м2/г, средним диаметром частиц d50=19,3±2 мкм (определенным методом статического лазерного рассеяния) был предоставлен Sigma Aldrich.
Сравнительный пример 1
(Смешанный оксид Li-Zr из водных предшественников в виде нитратов)
8,54 кг водного раствора, содержащего 630 г LiNO3 и 1733 г Zr(NO3)4 (содержание металла: 24 мас. %) получали при интенсивном перемешивании до растворения всего твердого содержимого. Данный раствор представляет собой теоретическую композицию Li2ZrO3.
Аэрозоль из 2,5 кг/ч потока данного раствора и 15 нм3/ч потока воздуха образовывали через форсунку для двух компонентов и распыляли в трубчатый реактор с горящим пламенем. Горючие газы пламени состоят из 13 нм3/ч водорода и 75 нм3/ч воздуха. Кроме того, применяли 25 нм3/ч вторичного воздуха. После реактора реакционные газы охлаждали и фильтровали.
Свойства частиц показаны в таблице 1.
Получение порошка NMC, покрытого смешанным оксидом Li-Zr из сравнительного примера 1
Порошок NMC (99 г) смешивали с 1,0 г (1 мас. %) высокодисперсного порошка из сравнительного примера 1 в лабораторном смесителе высокой интенсивности (смеситель Somakon MP-GL со смесительной установкой объемом 0,5 л) сначала в течение 1 мин. при 500 об./мин. (удельная электрическая мощность: 350 Вт/кг NMC) для однородного смешивания двух порошков. Затем интенсивность перемешивания увеличивали до 2000 об./мин. (удельная электрическая мощность: 800 Вт/кг NMC, скорость вращения смесительного приспособления в смесительной установке: 10 м/с) и перемешивание продолжали в течение 5 мин. до обеспечения сухого покрытия частиц NMC высокодисперсным порошком из сравнительного примера 1.
Сравнительный пример 2
(Смешанный оксид Li-Zr из этанольных растворов предшественников в виде нитратов)
8,32 кг этанольного раствора, содержащего 450 г LiNO3 и 1238 г Zr(NO3)4 (содержание металла: 24 мас. %) получали при интенсивном перемешивании до растворения всего твердого содержимого. Данный раствор представляет собой теоретическую композицию Li2ZrO3.
Аэрозоль из 2,5 кг/ч потока данного раствора и 15 нм3/ч потока воздуха образовывали через форсунку для двух компонентов и распыляли в трубчатый реактор с горящим пламенем. Горючие газы пламени состоят из 6,8 нм3/ч водорода и 75 нм3/ч воздуха. Кроме того, применяли 25 нм3/ч вторичного воздуха. После реактора реакционные газы охлаждали и фильтровали.
Свойства частиц показаны в таблице 1.
Пример 1
7,94 кг раствора, содержащего 2725 г коммерчески доступного раствора (Borchers® Deca Lithium2), содержащего 2 мас. % лития в форме неодеканоата лития, и 2984 г коммерчески доступного раствора (Octa Solingen® Zirconium 12), содержащего 12 мас. % Zr в форме этилгексаноата циркония и 2231 г 2-этилгексановой кислоты, смешивали с получением прозрачного раствора. Данный раствор представляет собой теоретическую композицию Li2ZrO3.
Аэрозоль из 2,5 кг/ч потока данного раствора и 15 нм3/ч потока воздуха образовывали через форсунку для двух компонентов и распыляли в трубчатый реактор с горящим пламенем. Горючие газы пламени состоят из 4 нм3/ч водорода и 75 нм3/ч воздуха. Кроме того, применяли 25 нм3/ч вторичного воздуха. После реактора реакционные газы охлаждали и фильтровали.
Свойства частиц показаны в таблице 1. Полученные с помощью ТЕМ изображения частиц показаны на фиг. 1А и 1В.
Анализ с помощью XRD (фиг. 5) показал, что основной фазой продукта все еще является структура ZrO2.
Пример 2
(Прокаленный смешанный оксид Li-Zr)
Смешанный оксид, полученный в примере 1, прокаливали при 700°С в течение 6 ч во вращающейся печи. Анализ с помощью XRD (фиг. 5) показал, что основной фазой продукта является тетрагональная структура оксида лития и циркония (Li4Zr3O8).
Пример 3
(Прокаленный смешанный оксид Li-Zr)
Смешанный оксид, полученный в примере 1, прокаливали при 750°С в течение 6 ч во вращающейся печи. Анализ с помощью XRD (фиг. 5) показал, что основной фазой продукта является моноклинная структура оксида лития и циркония (Li2ZrO3) и тетрагональная структура оксида лития и циркония (Li4Zr3O8).
Получение порошка NMC, покрытого смешанным оксидом Li-Zr из примера 1
Порошок NMC (99 г) смешивали с 1,0 г (1 мас. %) высокодисперсного порошка из примера 1 в лабораторном смесителе высокой интенсивности (смеситель Somakon MP-GL со смесительной установкой объемом 0,5 л) сначала в течение 1 мин. при 500 об./мин. (удельная электрическая мощность: 350 Вт/кг NMC) для однородного смешивания двух порошков. Затем интенсивность перемешивания увеличивали до 2000 об./мин. (удельная электрическая мощность: 800 Вт/кг NMC, скорость вращения смесительного приспособления в смесительной установке: 10 м/с) и перемешивание продолжали в течение 5 мин. до обеспечения сухого покрытия частиц NMC высокодисперсным порошком из примера 1.
Анализ смешанных оксидов лития и переходных металлов, подвергнутых сухому покрытию с помощью Li2ZrO3, посредством SEM-EDX
На фиг. 2 показано картирование Zr (белого цвета) с помощью SEM-EDX на покрытых Li2ZrO3 (LZO) NMC, полученных с применением высокодисперсного нано-LZO (пример 1), на фиг. 3 показаны результаты анализа NMC, покрытых высокодисперсным крупным LLZO (сравнительный пример 1). Оси на фиг. 2 и 3 показывают: ось х = диаметр частиц; левая ось у = объем в %, правая ось у = суммарный объем в %. Смешанный оксид NMC, подвергнутый сухому покрытию высокодисперсным нано-LZO (пример 1), демонстрирует полное и однородное покрытие всех частиц NMC с помощью LZO (фиг. 2). Не было обнаружено более крупных агломератов LZO, что свидетельствует о хорошей диспергируемости наноструктурированного высокодисперсного нано-LZO. Кроме того, не было обнаружено каких-либо свободных неприкрепленных частиц LZO рядом с частицами NMC, что указывает на сильную адгезию между покрытием и подложкой (NMC). Напротив, на фиг. 3 показано, что только мелкие частицы LZO из высокодисперсного грубого LZO прикреплены к поверхности частиц NMC. Более крупные частицы LZO не диспергированы и, следовательно, не прикреплены, они расположены рядом с частицами NMC. В результате частицы NMC не полностью покрыты оксидом циркония.
На фиг. 4 показаны результаты статистического анализа фиг. 2 и фиг. 3. Распределение площади Zr (белого цвета) мкм2 в картировании SEM-EDX дополнительно анализировали посредством коробчатого графика нормального распределения и показывает четкое различие диспергируемости Zr (белого цвета) между примером 1 на фиг. 2 и сравнительным примером 1 на фиг. 3.
Сборка и характеристики твердотельных литий-металлических аккумуляторных батарей
Три набора полностью твердотельных металлических аккумуляторных батарей NMC_Li6SP5Cl_Li, которые были собраны с использованием высокодисперсного нано-LZO (пример 1) и коммерчески доступного LZO от Sigma Aldrich. Композитный катод с применением NMC, покрытого LZO, получали с массовым соотношением NMC:Li6SP5Cl:углерод = 60:35:5 в качестве катода. В качестве анода используется сплав Li-In.
Исходный импеданс анализировали посредством спектроскопии электрохимического импеданса (EIS), и результаты показаны в таблице 2. В таблице 2 также показана начальная кулонов некая эффективность полностью твердотельных аккумуляторных батарей.

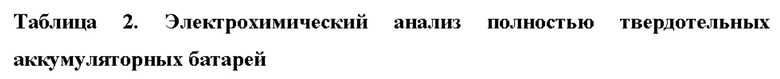

Изобретение может быть использовано при изготовлении покрытий или легирующих материалов для электродов литиевых аккумуляторных батарей, а также добавок к жидким, гелеобразным или твердотельным электролитам литий-ионных аккумуляторных батарей. Смешанный оксид лития и циркония получают спрей-пиролизом в пламени, используя по меньшей мере один раствор предшественников металлов, включающий карбоксилаты лития и циркония, содержащие 5-20 атомов углерода, и растворитель, содержащий менее 5 масс. % воды и выбранный из спирта, простого эфира, сложного эфира, карбоновых кислот, необязательно галогенированного углеводорода и их смесей. Раствор предшественников металлов может также содержать хелатирующее средство, выбранное из диаминов и 1,3-дикарбонильных соединений. По меньшей мере один раствор указанных предшественников металлов распыляют посредством распыляющего газа. Полученный аэрозоль вводят в реакционное пространство реактора, где он реагирует с пламенем, полученным воспламенением смеси горючего и кислородсодержащего газов. Затем реакционный поток охлаждают, удаляют из него твердый продукт, представляющий собой смешанный оксид общей формулы LiaZrbO0,5a+2b, где 0,5 ≤ а ≤ 12; 1,0 ≤ b ≤ 4,0. После стадии спрей-пиролиза в пламени можно дополнительно провести термическую обработку при 500-1200°С. Полученный смешанный оксид лития и циркония находится в виде агрегированных первичных частиц, характеризуется площадью поверхности по БЭТ 15-50 м2/г или менее 20 м2/г, среднечисловым диаметром частиц d50=0,05-1 мкм или d50=1-50 мкм, определенным посредством статического светорассеяния (SLS) и трамбовочной плотностью 50-200 г/л или 200-800 г/л. 5 н. и 5 з.п. ф-лы, 5 ил., 2 табл., 3 пр.
1. Способ получения смешанного оксида лития и циркония посредством спрей-пиролиза в пламени и необязательной дополнительной термической обработки, отличающийся тем, что в способе применяют по меньшей мере один раствор предшественников металлов, содержащий
- карбоксилат лития и карбоксилат циркония, при этом каждый из данных карбоксилатов металлов содержит от 5 до 20 атомов углерода, и
- растворитель, содержащий менее 5% воды по массе,
и тем, что смешанный оксид представляет собой соединение общей формулы LiaZrbO0,5a+2b, где
0,5 ≤ а ≤ 12,
1,0 ≤ b ≤ 4,0.
2. Способ по п. 1, отличающийся тем, что спрей-пиролиз в пламени включает следующие стадии, на которых:
a) по меньшей мере один раствор предшественников металлов распыляют с получением аэрозоля посредством распыляющего газа,
b) аэрозоль вводят в реакцию в реакционном пространстве реактора с пламенем, полученным воспламенением смеси горючего газа и кислородсодержащего газа, с получением реакционного потока,
c) реакционный поток охлаждают и
d) твердый оксид металла затем удаляют из реакционного потока.
3. Способ по п. 1 или 2, отличающийся тем, что карбоксилаты лития и циркония независимо друг от друга представляют собой карбоксилаты, выбранные из группы, состоящей из линейных, разветвленных или циклических пентаноата (С5), гексаноата (С6), гептаноата (С7), октаноата (С8), нонаноата (С9), деканоата (D10), ундеканоата (С11), додеканоата (С12), тридеканоата (С13), тетрадеканоата (С14), пентадеканоата (С15), гексадеканоата (С16), гептадеканоата (С17), октадеканоата (С18), нонадеканоата (С19), икозаноата (С20) лития и/или циркония и их смесей.
4. Способ по любому из пп. 1-3, отличающийся тем, что растворитель выбран из группы, состоящей из спирта, простого эфира, сложного эфира, карбоновых кислот, необязательно галогенированного углеводорода и их смесей.
5. Способ по любому из пп. 1-4, отличающийся тем, что раствор предшественников металлов содержит хелатирующее средство, выбранное из группы, состоящей из диаминов и 1,3-дикарбонильных соединений.
6. Способ по любому из пп. 1-5, отличающийся тем, что дополнительную термическую обработку проводят при температуре 500°С - 1200°С.
7. Смешанный оксид лития и циркония, где
смешанный оксид
находится в виде агрегированных первичных частиц,
характеризуется площадью поверхности по методу БЭТ 15-50 м2/г,
среднечисловым диаметром частиц d50=0,05-1 мкм, как определено посредством статического светорассеяния (SLS),
трамбовочной плотностью 50-200 г/л, и
где смешанный оксид получают с помощью способа по п. 1.
8. Смешанный оксид лития и циркония, где
смешанный оксид
находится в виде агрегированных первичных частиц,
характеризуется площадью поверхности по методу БЭТ менее 20 м2/г,
среднечисловым диаметром частиц d50=1-50 мкм, как определено посредством статического светорассеяния (SLS),
трамбовочной плотностью 200-800 г/л, и
где смешанный оксид получают с помощью способа по п. 1.
9. Применение смешанного оксида по п. 7 или 8 в качестве покрытия или легирующего материала для электродов литиевых аккумуляторных батарей или в качестве добавки к жидким, гелеобразным или твердотельным электролитам литий-ионных аккумуляторных батарей.
10. Литий-ионная аккумуляторная батарея, содержащая смешанный оксид по п. 7 или 8.
| EONGYU Y.I | |||
| et al | |||
| Flame made nanoparticles permit processing of dense, flexible, Li+ conducting ceramic electrolyte thin films of cubic-Li7La3Zr2O12 (c-LLZO), J | |||
| of Mater | |||
| Chem | |||
| A, 2016, v | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ сопряжения брусьев в срубах | 1921 |
|
SU33A1 |
| Ветряной двигатель со складными перьями или лопастями | 1929 |
|
SU12947A1 |
| СПОСОБ ОЧИСТКИ ПРОПИЛЕНОКСИДА | 2013 |
|
RU2639872C2 |
| НОСОК ДЛЯ ЗАЩИТЫ ОТ ВРОСШЕГО НОГТЯ (ВАРИАНТЫ) | 2024 |
|
RU2826750C1 |
| RU 2008101421 А, 20.07.2009 | |||
| СПОСОБ ПРИМЕНЕНИЯ ТИТАНОВОГО КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ МАТЕРИАЛОВ, СОДЕРЖАЩИХ КАРБАМАТНЫЕ ФУНКЦИОНАЛЬНЫЕ ГРУППЫ | 2015 |
|
RU2690164C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ МЕТАЛЛОВ | 2011 |
|
RU2486130C1 |
Авторы
Даты
2024-08-21—Публикация
2020-09-10—Подача