Изобретение относится к молекулярной биологии, в частности к способам выделения микроРНК из биологических жидкостей, и предназначено для выделения различных типов микроРНК из различных экзосомосодержащих биологических материалов для оценки отдельных фракций экзосом.
Экзосомы - маленькие, 20-100 нм, сферические пузырьки, формируемые клеткой для межклеточных взаимодействий. В экзосомах содержатся комплексы белков и микроРНК, которые представляют ценность как диагностические маркеры, а также могут использоваться для формирования иммунного ответа в онкологии. Однако для эффективного использования экзосом необходимо получение чистой фракции.
Экзосомы стабильны в биологических жидкостях, крови, моче, слюне, асците или культуральной жидкости в случае культивирования. Это делает доступной не инвазивную диагностику экзосом опухолевого происхождения в плазме крови и моче.
Экзосомы активно выделяются клетками иммунной системы - дендритные клетки и В-лимфоциты, клетками нервной ткани, секреторных тканей и особенно опухолевыми клетками [ K.Denzer et al. 2000, Huber et al. 005, P.Wwearsch 2009]. В случае дендритных клеток выделяются экзосомы содержащие маленькие (8-12 аминокислот) презентованные полипептиды в комплексе антигеном МНС I, присоединяющиеся к соответствующим рецепторам на CD8 цитотоксических Т-лимфоцитах, NK-клетках, а также в комплексе с МНС II, содержащие большие (12-16 аминокислот) презентированные полипептиды, к соответствующим рецепторам на CD4 цитотоксических Т-лимфоцитах. Экзосомы, выделяющиеся опухолевыми клетками, могут нарушать формирование противоопухолевогоответа цитотоксических Т-клеток за счет конкуренции с экзосомами дендритных клеток или макрофагов, учитывая, что концентрация экзосом увеличивается в плазме/сыворотке крови примерно в 50 раз при развитом раке [Taylor et al. 2008, Iero 2008].
Экзосомы содержат антигены МНС I и МНС II комплекса гистосовместимости, Rab-белки ряд интегринов, а также антигены и наборы микроРНК, определяемые тканевой принадлежностью и индивидуальными особенностями типа клеток. Так в экзосомах из мочи человека обнаружено присутствие 295 белков [ Pisitkun et al. 2004]. Около 50 белков встречаются регулярно во всех экзосомах [Gonzales et al., 2009]. В случае опухолей тканеспецифический набор белков и опухолевоспецифический набор микроРНК может использоваться для ранней диагностики или обоснования схемы лечения [Baj-Krzyworzeka et а1. 2007].
Для изучения специфических опухолевых экзосом необходимо их дифференцировать. Концентрация конкретных микроРНК является в таком случае критерием отбора экзосом из конкретных клеток.
Известен способ выделения экзосом из биологических жидкостей (см. ссылку http://tsitologiya.cytspb.rssi.ru/54 5/shtam ms.pdf сети Интернет), где собирают культуральную конденсированную среду (КС), проводят последовательное центрифугирование в режиме 2000 и 10000g, далее полученную КС объемом 500 мл концентрируют с помощью ультрафильтрации (Центрикон плюс-70, 100 кДа, Millipore) до конечного объема 10 мл. В дальнейшем для выделения экзосом из полученных препаратов концентрированной КС применяют ультрацентрифугирование на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 ч. После центрифугирования надосадочную жидкость собирают в отдельную пробирку и исследуют методом лазерной корреляционной спектроскопии (ЛКС) для проверки удаления из нее частиц экзосомального размера, осадок растворяют в максимальном объеме фосфатно-солевого буфера (PBS) и повторно центрифугируют при тех же условиях. Полученный осадок растворяют в 100 мкл воды (MiliQ) или PBS, разбивают на аликвоты, которые замораживают при -80 °С для дальнейших протеомных исследований.
Известный метод не позволяет разделить экзосомы на различные фракции, относящиеся к различным тканям, а следовательно, и осуществить оценку уровня микроРНК в выделенных образцах.
Техническим эффектом заявленного способа является возможность выделения отдельных типов микроРНК из биологических жидкостей, содержащих экзосомы, в частности, возможность выделения отдельных типов, например, тканеспецифичных и опухолевоспецифичных микроРНК в дальнейшем позволит создавать вакцины, основанные на экзосомах из опухолевых клеток.
Вышеприведенный технический результат достигается тем, что в способе выделения отдельных типов микроРНК из биологических жидкостей, содержащих экзосомы, включающем последовательное центрифугирование в режиме 2000 и 10000g, ультрафильтрацию полученной надосадочной жидкости на цетрифужном концентраторе Центрикон плюс-70, 100 кДа, Millipore до конечного объема 10 мл, ультрацентрифугирование на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 часов, растворение полученного осадка в фосфатно-солевом буфере, повторное центрифугирование при тех же условиях, и растворение полученного осадка в 100 мкл воды, согласно настоящему изобретению, далее полученный раствор подвергают электрофорезу в свободном потоке в бункерах для анодной и катодной стабилизации на приборе FFE System с последующим сбором отдельных фракций при следующих условиях: общее время проведения электрофореза 5 минут, подаваемое напряжение 900 В и ток 34 мА, образец и маркер вводят при скорости потока 2,5 мл/ч и 280 мл/ч соответственно, пробег проводят в режиме циклического интервала FF-ZE при 85 мл/ч и фракционированный образец элюируют при 320 мл/ч, для анодной стабилизации используют следующий буфер: 1,5 М тиомочевины + 6 M мочевины + 100 мМ H2SО4 +25 мМ 2-пиридин-пропанол +мМ 2-пиридин-этанол. Среда для разделения имеет следующий состав: 1,8 M тиомочевины + 6 M мочевины + 55 мМ MOPS + 55 мМ 2-пиридин-пропанол; для катодной стабилизации используют следующий буфер: 1,8 M тиомочевины + 76 M мочевины + 180 мМ NaOH + 25 мМ Трис + 35 мМ МОПС + 280 мМ EPPS, далее отдельные фракции повторно ультрацентрифугируют на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 ч, затем проводят выделение микроРНК из каждой отдельной фракции, а именно, в каждую из отдельных фракций добавляют 5 мкМ протеиназы К, инкубируют при 56°С в течение 1 ч, далее наносят на колонку Exiqon, после чего проводят центрифугирование при 2000g, затем колонку промывают 3 раза промывочным буфером, после каждого промывания проводят центрифугирование при 2000g на центрифуге eppendorf 5104, потом на колонку наносится 20 мкл безнуклеазной воды, далее колонку оставляют на 10 мин при комнатной температуре, а затем центрифугируют при 3000g, после чего проводят реакцию обратной транскрипции при помощи обратной транскриптазы (Exiqon), а именно, к 8 мкл образца добавляют 8 мкл реагента и инкубируют в течение 1 ч при температуре 60°С, после чего реакцию останавливают нагреванием до 95°С в течение 5 мин.
Далее, с целью выявления отдельных типов микроРНК проводят полимеразную цепную реакцию с детекцией в реальном времени на приборе 7500 Applied Biosystems спраймерами на отдельные типы, например, тканеспецифичных и опухолевоспецифичных микроРНК, а именно: miR-141, miR-200a, miR-200c, miR-203, miR-205, miR-214, miR-17-3р, miR-106a, miR-146, miR-155, miR-191, miR-192, miR-301a, miR-326, miR-331-3р, miR-432, miR-438, miR-574-3р, miR-625*, miR-92a, miR-584, miR-517c, miR-378, miR-520f, miR-142-5p, miR-451, miR-518d, miR-29a, miR-650, miR-151, miR-19b, miR-29c.
Затем при помощи программы GenEx qPCR software, вычисляют количество каждой из исследуемых микроРНК, выделенной из каждой фракции, после чего полученные данные сводят в таблицу для сравнения профилей экспрессии микроРНК в образцах из разных тканей.
Пример исследования
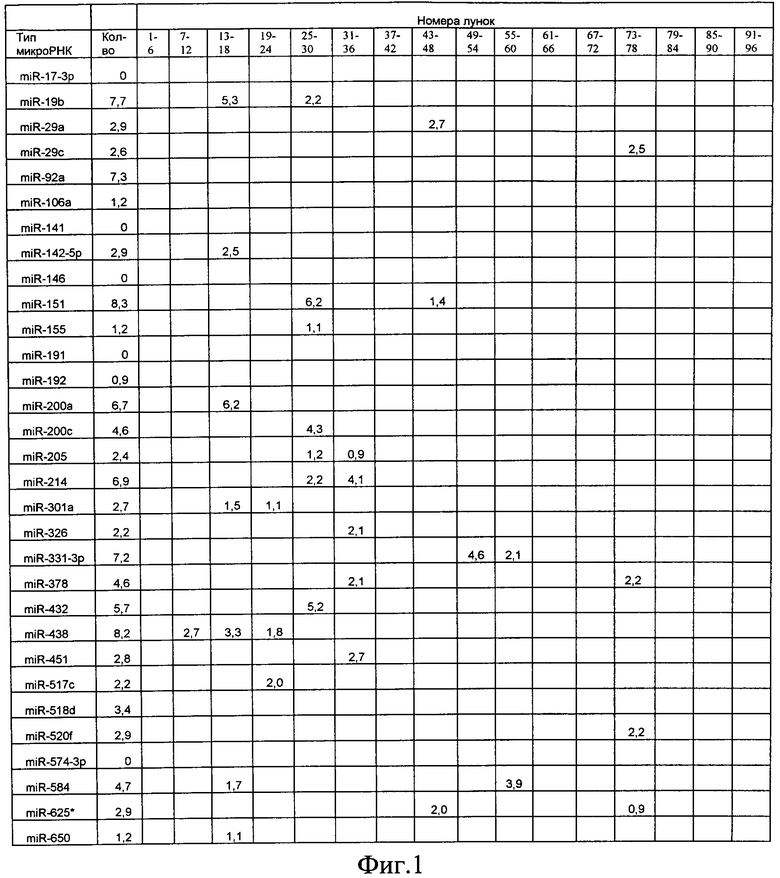
600 мл мочи, взятой у здорового донора подвергают последовательному центрифугированию в режиме 2000 и 10000g, далее полученную надосадочную жидкость объемом 500 мл концентрируют с помощью ультрафильтрации (Центрикон плюс-70, 100 кДа, Millipore) до конечного объема 10 мл. В дальнейшем для выделения экзосом применяют ультрацентрифугирование на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 ч. После центрифугирования надосадочную жидкость собирают в отдельную пробирку и исследуют методом лазерной корреляционной спектроскопии (ЛКС) для проверки удаления из нее частиц экзосомального размера, осадок растворяют в максимальном объеме фосфатно-солевого буфера (PBS) и повторно центрифугируют при тех же условиях. Полученный осадок растворяют в 100 мкл воды (MiliQ) или PBS, далее исследуемый образец подвергают электрофорезу в свободном потоке в специальных буферах на приборе FFE system (FFE Service GmbH) при следующих условиях: общее время проведения электрофореза 5 мин, подаваемое напряжение 900 В и ток 34 мА. Образец и маркер были введены при скорости потока 2,5 мл/ч и 280 мл/ч соответственно. Пробег проводили в режиме циклического интервала FF-ZE при 85 мл/ч и фракционированный образец элюируют при 320 мл/ч. Для анодной стабилизации используют следующий буфер: 1,5 М тиомочевины + 6 M мочевины + 100 мМ H2SO4+25 мМ 2-пиридин-пропанол + 300 мМ 2-пиридин-этанол. Среда для разделения имеет следующий состав: 1,8 M тиомочевины + 6 M мочевины + 55 мМ MOPS + 55 мМ 2-пиридин-пропанол; для катодной стабилизации используют следующий буфер: 1,8 M тиомочевины + 76 M мочевины + 180 мМ NaOH + 25 мМ Трис + 35 мМ МОПС + 280 мМ EPPS, с последующим сбором отдельных фракций, концентрированием образцов из отдельных лунок при помощи повторного ультрацентрифугирования на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 ч.. Затем проводят выделение микроРНК по следующей методике: в образец добавляют 5 мкМ протеиназы К, инкубируют при 56°С в течение 1 часа, затем используют колонки Exiqon, для очистки микроРНК - образец наносят на колонку, после чего проводят центрифугирование при 2000g на центрифуге eppendorf 5104, затем колонку 3 раза промывают промывочным буфером, после каждого промывания проводят центрифугирование при 2000g на центрифуге eppendorf 5104, потом на колонку наносится 20 мкл безнуклеазной воды. Колонку оставляют на 10 мин при комнатной температуре, а потом центрифугируют при 3000g на центрифуге eppendorf 5104, после чего проводят реакцию обратной транскрипции при помощи обратной транскриптазы (Exiqon), для этого к 8 мкл образца добавляют 8 мкл реагента и инкубируют в течение 1 ч при температуре 60°С, после чего реакцию останавливают нагреванием до 95°С в течение 5 мин. Затем проводят полимеразную цепную реакцию с детекцией в реальном времени на приборе 7500 Applied Biosystems, с праймерами на следующие микроРНК: miR-141, miR-200a, miR-200c, miR-203, miR-205, miR-214, miR-17-3р, miR-106a, miR-146, miR-155, miR-191, miR-192, miR-301a, miR-326, miR-331-Зр, miR-432, miR-438, miR-574-3р, miR-625*, miR-92a, miR-584, miR-517c, miR-378, miR-520f, miR-142-5p, miR-451, miR-518d, miR-29a, miR-650, miR-151, miR-19b, miR-29c результаты анализируют при помощи программы GenEx qPCR software и оформляют в виде таблицы 1 (см. фиг.1 - Распределение микроРНК, выделенной из 500 мл мочи здорового донора по лункам. Концентрация представлена как log с основанием 2 копий микроРНК в микролитре).
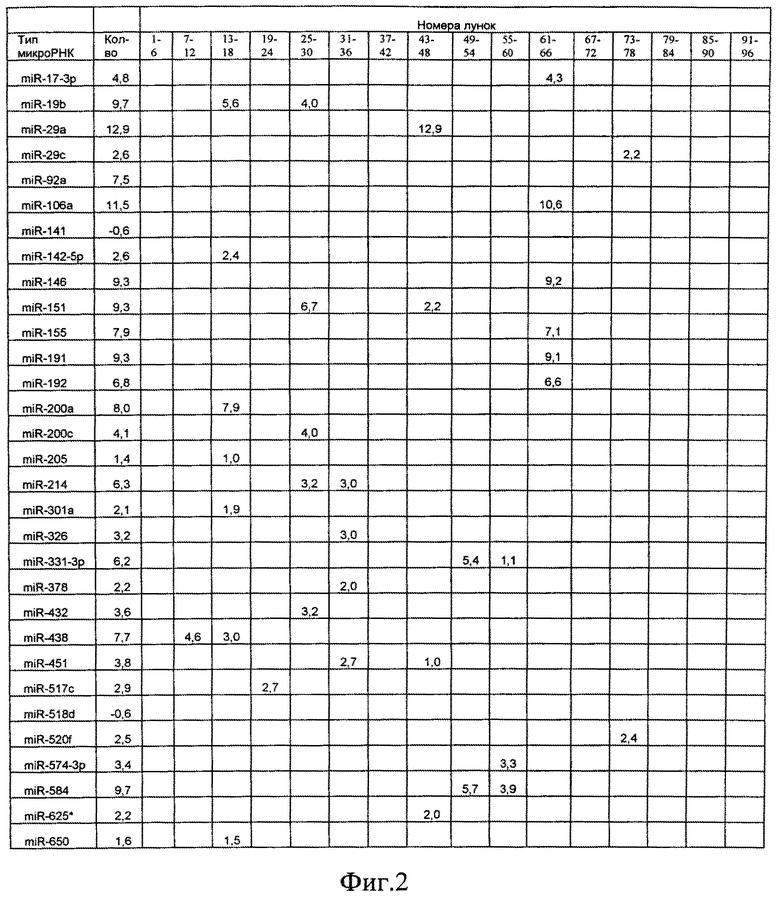
Затем 600 мл мочи, взятой у пациента с раком молочной железы, подвергают последовательному центрифугированию в режиме 2000 и 10000g, далее полученную надосадочную жидкость объемом 500 мл концентрируют с помощью ультрафильтрации (Центрикон плюс-70, 100 кДа, Millipore) до конечного объема 10 мл. В дальнейшем для выделения экзосом применяют ультрацентрифугирование на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 ч. После центрифугирования надосадочную жидкость собирают в отдельную пробирку и исследуют методом лазерной корреляционной спектроскопии (ЛКС) для проверки удаления из нее частиц экзосомального размера, осадок растворяют в максимальном объеме фосфатно-солевого буфера (PBS) и повторно центрифугируют при тех же условиях. Полученный осадок растворяют в 100 мкл воды (MiliQ) или PBS, далее исследуемый образец подвергают электрофорезу в свободном потоке в специальных буферах на приборе FFE system (FFE Service GmbH) при следующих условиях: общее время проведения электрофореза 5 минут, подаваемое напряжение 900 В и ток 34 мА. Образец и маркер были введены при скорости потока 2,5 мл/ч и 280 мл/ч соответственно. Пробег проводили в режиме циклического интервала FF-ZE при 85 мл/ч и фракционированный образец элюируют при 320 мл/ч. Для анодной стабилизации используют следующий буфер: 1,5М тиомочевины + 6 M мочевины + 100 мМ H2SO4+25 мМ 2-пиридин-пропанол + 300 мМ 2-пиридин-этанол. Среда для разделения имеет следующий состав: 1,8 M тиомочевины + 6 M мочевины + 55 мМ MOPS + 55 мМ 2-пиридин-пропанол; для катодной стабилизации используют следующий буфер: 1,8 M тиомочевины + 76 M мочевины +180 мМ NaOH + 25 мМ Трис + 35 мМ МОПС + 280 мМ EPPS, с последующим сбором отдельных фракций, концентрированием образцов из отдельных лунок при помощи повторного ультрацентрифугирования на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 ч. Затем проводят выделение микроРНК по следующей методике: в образец добавляют 5 мкМ протеиназы К, инкубируют при 56°С в течение 1 часа, затем используют колонки Exiqon, для очистки микроРНК - образец наносят на колонку, после чего проводят центрифугирование при 2000g на центрифуге eppendorf 5104, затем колонку 3 раза промывают промывочным буфером фирмы Exiqon, после каждого промывания проводят центрифугирование при 2000g на центрифуге eppendorf 5104, потом на колонку наносится 20 мкл безнуклеазной воды. Колонку оставляют на 10 минут при комнатной температуре, а потом центрифугируют при 3000g на центрифуге eppendorf 5104, после чего проводят реакцию обратной транскрипции при помощи обратной транскриптазы (Exiqon), для этого к 8 мкл образца добавляют 8 мкл реагента и инкубируют в течение 1 часа при температуре 60°С, после чего реакцию останавливают нагреванием до 95°С в течение 5 мин. Затем проводят полимеразную цепную реакцию с детекцией в реальном времени на приборе 7500 Applied Biosystems, с праймерами на следующие микроРНК: miR-141, miR-200a, miR-200c, miR-203, miR-205, miR-214, miR-17-Зр, miR-106a, miR-146, miR-155, miR-191, miR-192, miR-301a, miR-326, miR-331-Зр, miR-432, miR-438, miR-574-Зр, miR-625*, miR-92a, miR-584, miR-517c, miR-378, miR-520f, miR-142-5p, miR-451, miR-518d, miR-29a, miR-650, miR-151, miR-19b, miR-29c, результаты анализируют при помощи компьютерной программы GenEx qPCR software и оформляют в виде таблицы 2 (см. фиг.2 - Распределение микроРНК, выделенной из 500 мл мочи пациента с аденокарциномой легких по лункам. Концентрация представлена как log с основанием 2 копий микроРНК в микролитре).
Как видно из таблиц 1 и 2 в лунках 61-66 микроРНК miR-17-Зр, miR-106а, miR-146, miR-155, miR-191, miR-192 наблюдаются только у пациента с аденокарциномой легких и не выявляется у здорового донора, что указывает на то, что в эти лунки попадают только экзосомы из опухолевых клеток аденокарциномы легких, следовательно, заявленным способом возможно выделять чистые фракции отдельных типов микроРНК, в том числе тканеспецифичных и опухолевоспецифичных микроРНК, из биологических жидкостей, содержащих экзосомы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выделения свободных и экзосомальных микроРНК из слюны | 2018 |
|
RU2729423C2 |
| Способ диагностики гепатоцеллюлярной карциномы с помощью определения коэффициента развития гепатоцеллюлярной карциномы на основании изменений уровней экспрессии микроРНК в плазме крови и слюне человека | 2020 |
|
RU2760937C1 |
| Способ снижения уровней экспрессии генов LRNN3, GRAP, VAMP5 | 2021 |
|
RU2759806C1 |
| Способ диагностики меланомы с помощью экзосомальных микроРНК | 2020 |
|
RU2769927C2 |
| Способ загрузки экзосом малыми некодирующими РНК | 2020 |
|
RU2748767C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭКЗОСОМ ИЗ КРОВИ | 2014 |
|
RU2556825C1 |
| СПОСОБ ИММУНОТЕРАПИИ РАКОВЫХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2707281C1 |
| Способ подавления метастазирования опухолей | 2018 |
|
RU2678569C1 |
| СПОСОБ ДИАГНОСТИКИ И МОНИТОРИНГА ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ С ИСПОЛЬЗОВАНИЕМ ЭКЗОСОМ КРОВИ | 2014 |
|
RU2571507C1 |
| ВНЕКЛЕТОЧНЫЕ ВЕЗИКУЛЫ ДЛЯ ИНГАЛЯЦИИ | 2019 |
|
RU2799315C2 |
Изобретение относится к биотехнологии, в частности к способу выделения микроРНК из биологических жидкостей, содержащих экзосомы. Способ включает последовательное центрифугирование, ультрафильтрацию и ультрацентрифугирование культуральной конденсированной среды. Растворяют полученный осадок в фосфатно-солевом буфере и повторно центрифугируют. Растворяют полученный осадок в воде. Подвергают полученный раствор электрофорезу в свободном потоке на приборе FFE System. Проводят ультрацентрифугирование каждой из полученных фракций. Очищают каждую фракцию от клеточных стенок экзосом посредством фильтрации и центрифугирования. Проводят реакцию обратной транскрипции при помощи обратной транскриптазы. Останавливают реакцию нагреванием до 95°С в течение 5 минут. Предложенное изобретение позволяет выделить микроРНК из биологических жидкостей, содержащих экзосомы, с высоким выходом. 2 ил., 1 пр.
Способ выделения отдельных типов микроРНК из биологических жидкостей, содержащих экзосомы, включающий последовательное центрифугирование в режиме 2000 и 10000g, ультрафильтрацию полученной надосадочной жидкости на цетрифужном концентраторе Центрикон плюс-70, 100 кДа, Millipore до конечного объема 10 мл и ультрацентрифугирование на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 ч, далее полученный осадок растворяют в фосфатно-солевом буфере и повторно центрифугируют при тех же условиях, затем полученный осадок растворяют в 100 мкл воды, отличающийся тем, что далее полученный раствор подвергают электрофорезу в свободном потоке в бункерах для анодной и катодной стабилизации на приборе FFE System с последующим сбором отдельных фракций при следующих условиях: общее время проведения электрофореза 5 мин, подаваемое напряжение 900 В и ток 34 мА, образец и маркер вводят при скорости потока 2,5 мл/ч и 280 мл/ч соответственно, пробег проводят в режиме циклического интервала FF-ZE при 85 мл/ч и фракционированный образец элюируют при 320 мл/ч, для анодной стабилизации используют следующий буфер: 1,5 М тиомочевины + 6 M мочевины +100 мМ H2SO4 +25 мМ 2-пиридин-пропанол + 300 мМ 2-пиридин-этанол; среда для разделения имеет следующий состав: 1,8 M тиомочевины + 6 M мочевины + 55 мМ MOPS + 55 мМ 2-пиридин-пропанол; для катодной стабилизации используют следующий буфер: 1,8 M тиомочевины + 76 M мочевины + 180 мМ NaOH + 25 мМ Трис + 35 мМ МОПС + 280 мМ EPPS, далее отдельные фракции повторно ультрацентрифугируют на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000g в течение 2 ч, затем проводят выделение микроРНК из каждой отдельной фракции, а именно в каждую из отдельных фракций добавляют 5 мкМ протеиназы К, инкубируют при 56°С в течение 1 ч, далее наносят на колонку Exiqon, после чего проводят центрифугирование при 2000g, затем колонку промывают 3 раза промывочным буфером, после каждого промывания проводят центрифугирование при 2000g на центрифуге eppendorf 5104, потом на колонку наносится 20 мкл безнуклеазной воды, далее колонку оставляют на 10 мин при комнатной температуре, а затем центрифугируют при 3000g, после чего проводят реакцию обратной транскрипции при помощи обратной транскриптазы (Exiqon), а именно к 8 мкл образца добавляют 8 мкл реагента и инкубируют в течение 1 ч при температуре 60°С, после чего реакцию останавливают нагреванием до 95°в течение 5 мин.
| US 20120164648 A1, 28.06.2012 | |||
| WO 2011029903 A1, 17.03.2011 | |||
| BAJ-KRZYWORZEKA M | |||
| ET AL., Tumour-derived microvesicles modulate biological activity of human monocytes, Immunol Lett, 2007, v.113, no.2, p | |||
| Аппарат, предназначенный для летания | 0 |
|
SU76A1 |
| ВИРУСНЫЕ ВЕКТОРЫ С ЗАВИСИМОЙ ОТ УСЛОВИЙ РЕПЛИКАЦИЕЙ И ИХ ПРИМЕНЕНИЕ | 2001 |
|
RU2301260C2 |
Авторы
Даты
2015-04-20—Публикация
2013-12-16—Подача