Изобретение относится к области медицины, а именно к клинической лабораторной диагностике, и может быть использовано для оценки качества определения D-димера в плазме крови в условиях клинико-диагностической лаборатории.
Главной проблемой в определении D-димера в плазме крови является полное отсутствие стандартизации как на этапе производства лабораторного оборудования, так и на этапе производства реагентов, калибраторов тест-систем, контрольных материалов. Более того, даже единицы, в которых выражают концентрацию этого аналита, существуют двух типов: DDU и FEU, что также усложняет трактовку результатов определения D-димера врачами-лаборантами и клиницистами [Adam S.S., Key N.S., Greenberg С.S. D-dimer antigen: current concepts and future prospects, (англ.) // Blood. - 2009. - T. 113. - №13. - С. 2878-2887]. В дальнейшем мы будем придерживаться единиц DDU, как это рекомендует Федеральная Система Внешней Оценки Качества (ФСВОК) лабораторных исследований Российской Федерации.
Для того чтобы оценить масштаб проблемы несогласованности результатов лабораторного определения D-димера в нашей стране и за рубежом приведем результаты обоих циклов ФСВОК за 2013 год. В межлабораторном сравнении в России приняли участие 100 лабораторий (цикл 1 и 2), коэффициент межлабораторной вариации составил в первом цикле 84,27%, а во втором цикле - 77,33%. Во втором цикле при целевом значении по D-димеру 1.2 мг/л диапазон допустимых значений (целевое значение +- 1,64 s) составил от 0,34 до 4,27 нг/мл. Для сравнения при определении глюкозы коэффициент межлабораторной вариации составил 7,8%, то есть в десять раз меньше.
Важность правильного определения D-димера определяется также и тем, что при отсутствии стандартизованного контрольного материала каждый производитель реактивов для лабораторий предлагает каждой лаборатории набирать свой уровень нормальных значений, что является абсолютно неприемлемым для подавляющего большинства, если не всех лабораторий России, вследствие трудоемкости такой работы и ее высокой стоимости. Проблема эта не решена и Европейских странах и США [Frauke Bergmann, Nadine Pingel, Andreas Czwalinna and Matthias Koch. D-Dimer in normal pregnancy: determination of reference values for three commercially available assays. Clin Chem Lab Med 2014 www.degruvter.com/dg/viewarticle/j$002fcclm.ahead-of-print$002fcclm-2014-0054$002fcclm-2014-0054.xml; jsessionid=4B436D6A2ED57A968121ECAAOECEFA5E71.
Как и для других нестандартизированных тестов фирмы-производители оборудования и реактивов рекомендуют использовать референсные значения (границы нормы) исходя из значений, приведенных в инструкциях к наборам реактивов (то есть по результатам исследования показателя в здоровой популяции самой фирмой) или набирать свою контрольную группу здоровых лиц в лаборатории, выполняющей данное исследование (анализ). Однако такие исследования D-димера подавляющее большинство лабораторий не проводят, так как не имеют финансовых возможностей (стоимость 1 набора реактивов превышает 20 тысяч рублей в 2014 г.), а также не имеют организационных возможностей набирать кровь здоровых доноров, в том числе беременных женщин, концентрация D-димера у которых возрастает по мере приближения к родам. Таким образом, участие каждой лаборатории в системе внешней оценки качества определения D-димера крайне важно. С другой стороны в последние годы и по настоящее время такой контроль проводится только 2 раза в год, что не позволяет оперативно реагировать при получении новых наборов реагентов как одного производителя, так и при переходе лабораторией на использование коммерческих реактивов определения D-димера других производителей.
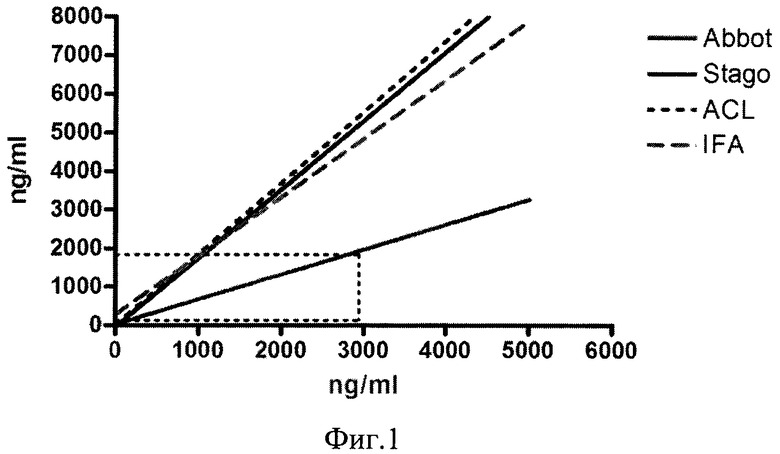
Известен способ оценки качества лабораторных исследований в рамках ФСВОК (Федеральная Система Внешней Оценки Качества лабораторных исследований Российской Федерации), состоящий в том, что с целью оценки качества определения D-димера используют контрольный материал двух уровней, проводят определение показателя дважды с каждым контрольным материалом и полученные результаты отправляют для статистической обработки в г. Москву, Центр ФСВОК РФ. Эксперты, сравнивая представленные результаты всеми участниками (лабораториями), указывают целевое значение для низкого и высокого уровня контрольного материала, среднее значение каждого образца лаборатории, смещение, диапазон допустимых значений. В результате делается вывод о качестве лабораторного исследования (фиг. 1) [http://www.fsvok.ru].
Недостатками данного способа являются: проведение тестирования только 2 раза в год, получение ответов через 1-3 месяца после проведения анализа (неоперативность), отсутствие механизма внесения изменений в результаты анализа лаборатории.
Наиболее близким к предлагаемому является способ «Оценка качества лабораторных исследований» (Хоровская Л.А., Эммануэль В.Л., Каллнер Α., Патент РФ на Изобретение №2304282 C1, опубликованный 10.08.2007 г. в бюл. №22), состоящий в том, что проводится также межлабораторное сравнение результатов анализа пациентов с низкими и высокими значениями аналита с последующим внесением изменений в калибровку приборов (рекалибровка) [Хоровская Л.А. Внутренний контроль качества и процедуры рекалибровки с использованием биоматериала пациента. Пособие для врачей / Под ред. А. Каллнера и В.Л. Эммануэля.. - СПб. - Изд-во СПбГМУ, 2007. - 67 с.].
Недостатками данного способа являются следующие: используется не стандартизованный контрольный материал, а замороженная сыворотка пациентов, возможно являющаяся потенциально инфицированной, требующей специальных условий для транспортировки. Используется межлабораторное сравнение в одном регионе, а в качестве референсного метода используют одну из лабораторий участниц, выбор которой в качестве эталона авторы никак не объясняют. Затем по результатам сравнения тестирования проводят рекалибровку других приборов, приводя их в соответствие с эталонной (референсной). Таким образом, разработанный авторами способ не подходит для определения такого не стандартизованного показателя как D-димер, возможно может ухудшить качество анализа в одной конкретно взятой лаборатории. Кроме того, использование данного метода технически сложно и мало применимо в рутинной практике при проверке качества каждого нового набора реагентов для определения D-димера, так как требует затраты более 14 тестов из исследуемого набора, который содержит обычно 96 лунок для анализа в случае техники иммуноферментного анализа (ИФА) или 100 тестов в составе автоматизированных методов. С учетом обычной калибровки (2 раза по 6 тестов) и постановки двух-трехуровневого контроля это приводит к удорожанию одного анализа на 17-20 процентов, что при средней стоимости анализа на D-димер в России 800-900 рублей (цены 2013-14 гг.) составляет не менее 180-200 рублей.
Технический результат, достигаемый изобретением, заключается в повышении точности и улучшении стандартизованности определения D-димера при одновременной простоте и доступности для широкого практического применения, возможности использовать ручные методы определения аналита без набора референсных значений для групп здоровых лиц разного возраста и пола (для установления верхней границы нормы).
Заявленный технический результат достигается тем, что в способе оценки качества определения D-димера в плазме крови в условиях клинико-диагностической лаборатории, включающем исследование контрольных материалов и сопоставление результатов исследования с целевыми значениями, согласно изобретению, для сопоставления результатов исследования выбирают референсный метод, наиболее точно совпадающий с целевыми значениями в системе Федеральной системы внешней оценки качества клинических лабораторных исследований или доступной международной системе внешней оценки качества лабораторных исследований, исследуют не менее двух раз концентрацию D-димера в двух уровнях аттестованных контрольных материалов с использованием оцениваемого метода и выбранного референсного, определяют коэффициент сопоставимости оцениваемого и выбранного референсного методов по следующей формуле:
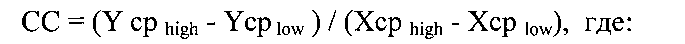
СС - коэффициент сопоставимости;
Ycphigh - среднее значение D-димера высокого уровня в контрольном материале, полученное оцениваемым методом;
Ycplow - среднее значение D-димера низкого уровня в контрольном материале, полученное оцениваемым методом;
Xcphigh - среднее значение D-димера высокого уровня в контрольном материале, полученное референсным методом;
Хcplow - среднее значение D-димера низкого уровня в контрольном материале, полученное референсным методом, затем результаты исследования, полученные оцениваемым методом, умножают на коэффициент сопоставимости, сравнивают с результатами, полученными выбранным референсным методом, и оценивают качество определения D-димера в плазме крови.
В качестве референсного метода нами был выбран метод определения D-димера на анализаторах фирмы «Sysmex», хотя возможно использование и других методов исследования в качестве референсного метода. Наш выбор был обусловлен широкой известностью и распространненостью оборудования «Sysmex» в клинико-диагностических лабораториях всего мира и России, высокими аналитическими характеристиками реактивов и оборудования указанной фирмы, огромным массивом данных по определению D-димера у здоровых и больных, а также беременных женщин в научной зарубежной и российской периодике (Воробьева Н.М., Добровольский А.Б., Титаева Е.В., Панченко Е.П. Тромбоэмболические осложнения и диагностическая значимость Д-димера при сердечнососудистых заболеваниях: ретроспективное исследование 1000 пациентов. Кардиологический вестник 2011. - №2. - С. 10-16). В то же время необходимо иметь в виду, что такая аппаратура и реактивы имеют высокую стоимость и не доступны многим лечебным учреждениям России, которые используют ручные методы определения D-димера.
При выборе контрольного материала авторы руководствовались следующим.
По результатам исследования авторы сделали вывод о необходимости использования контрольного материала, подходящего для всех используемых в настоящее время методов определения D-димера, то есть полученного с использованием материала из плазмы крови человека. Как показали исследования, большинство контрольных материалов производителей реактивов для определения D-димера представляют собой фрагменты антигена (молекулы) D-димера, а не нативную молекулу. Такой прием повышает стабильность контрольного материала и специфичность определения аналита, но не позволяет использовать такой материал в других тест-системах. В результате сравнений контрольных материалов разных производителей нами было обнаружено, что аттестованные контрольные материалы фирмы «Bio-Rad» имеют несколько уровней концентрации аналита от низкого до высокого, открываются на всех автоматических анализаторах известных производителей (США, Япония, Германия, Дания), имеющих разрешения к использованию в медицинских учреждениях России - МЗ РФ и методом иммуноферментного анализа.
Был проведен анализ определения D-димера в плазме крови здоровых доноров и пациентов, находящихся на лечении. Произведена оценка контрольных аттестованных материалов на D-димер производства фирм «Instrumentation Laboratory» (США), «Siemens» (Германия), «Abbott» (США), «Radiometer» (Копенгаген, Дания), «Bio-Rad» (США) с использованием автоматических анализаторов соответственно «ICL Elite Pro», «Sysmex CS-2000i», «Axsym, Abbott» (США), «AQT90 Flex», a также иммуноферментного анализа на 96-луночных планшетах фирмы «Technozym» (Австрия) с использованием анализатора фирмы «BioTek» (США), и термошейкера PST-60 HL («Biosan», Латвия).
На базе проведенного исследования был разработан способ оценки качества определения D-димера в плазме крови в условиях клинико-диагностической лаборатории, позволяющий получить результаты исследования, соответствующие выбранному референсному методу, что повышает точность оценки и улучшает стандартизованность определения D-димера.
Целесообразно производить рекалибровку (умножать на коэффициент сопоставимости) результатов определения D-димера в плазме крови пациента, полученные оцениваемым методом исследования, при значительном отклонении (более CV теста, около 10%) коэффициента сопоставимости от значения 1.0.
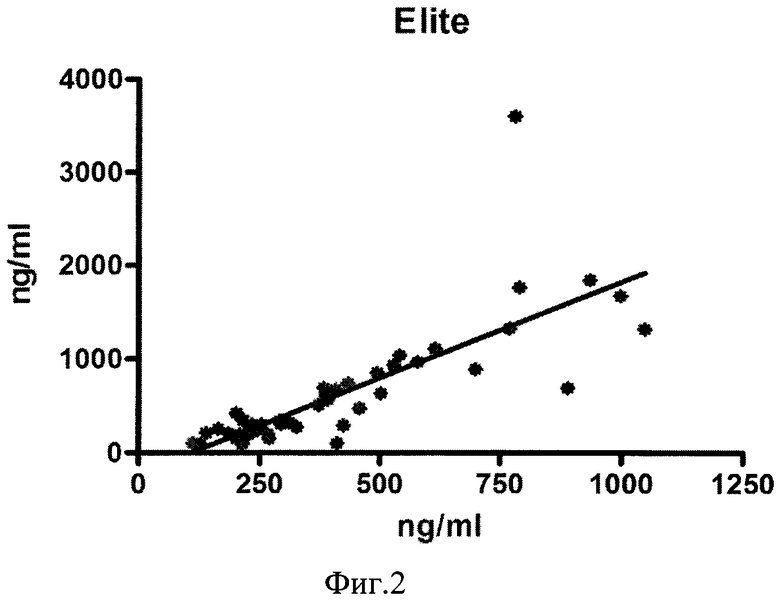
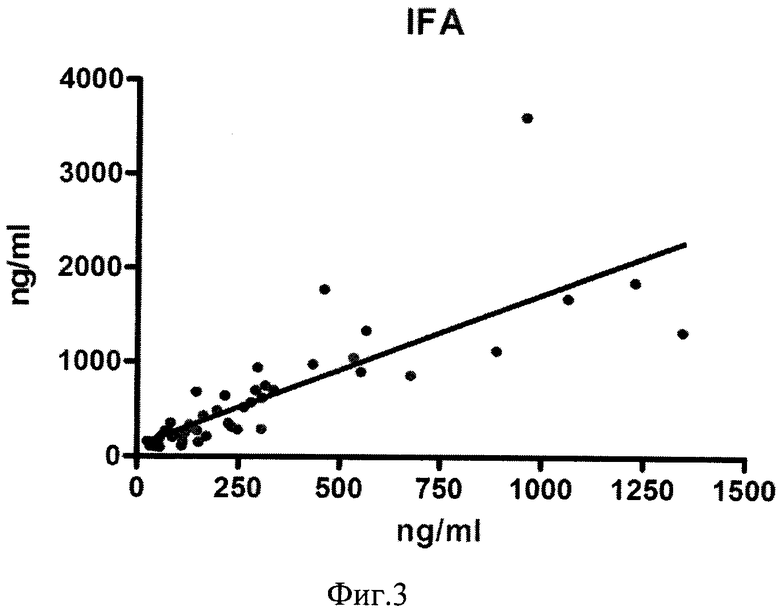
Сущность способа иллюстрируется фиг. 1-3: на фиг. 1 представлены графики сопоставимости методов определения D-димера по универсальному контрольному материалу Bio-Rad, США (по оси абсцисс), по оси ординатат - показания анализатора «Sysmex CS-2000i» (Япония); на фиг. 2 сопоставимость методов определения D-димера у 70 пациентов на анализаторах ICL (по оси абсцисс), по оси ординатат - показания анализатора «Sysmex CS-2000i» (Япония); на фиг. 3 - сопоставимость методов определения D-димера у 70 пациентов на иммуноферментном анализаторе IFA (по оси абсцисс), по оси ординат - показания автоматического анализатора «Sysmex CS-2000i» (Япония).
Способ осуществляют, например, следующим образом.
Пример 1 (фиг. 2)
Измеряли концентрацию D-димера в контрольной сыворотке производства фирмы «Bio-Rad» «D-dimer Control, Level 1,2,3 Lot 13780» второго уровня (Level 2, 13782, exp 31.03.2016) на автоматическом коагулометре «ACL Elite/PRO» фирмы IL (США), реактивы «HemosIL D-dimer». Получили значение 750 и 764 нг/мл. Среднее составляет 757 нг/мл. Процедуру повторили для контрольной сыворотки третьего уровня (Level 3, Level 13783 exp 31.03.2016). Получили значение 1445 и 1423 нг/мл. Среднее значение определения аналита составляет 1434 нг/мл.
Измеряли концентрацию D-димера в тех же образцах контрольных сывороток на автоматическом анализаторе фирмы «Sysmex CS-2000i» (Япония) с использованием рекомендованных реактивов «Siemens/Sismex Series D-dimer» (выбранный референсный метод). Получили значение 1380 и 1410 нг/мл. Среднее составляет 1395 нг/мл. Процедуру повторили для контрольной сыворотки третьего уровня. Получили значение 2630 и 2660 нг/мл. Среднее значение определения составляет 2645 нг/мл. Провели расчет по разработанной формуле
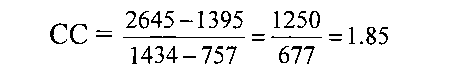
Таким образом, значения определения D-димера существенно отличаются при определении на этих двух приборах. Полученный коэффициент сопоставимости (рекалибровки) составил 1,85.
Этот коэффициент использовали для определения концентрации D-димера в крови у пациентов.
В плазме крови пациента Г. (от 10.02.2014 г.) концентрация содержания D-димера при измерении на анализаторе «ACL Elite/PRO» составила 201,5 нг/мл. При умножении на коэффициент сопоставимости получено значение 372,8 нг/мл. Реальное измерение на анализаторе «Sysmex CS-2000i» (Япония) дало значение 420 нг/мл (отклонение значений аналита составляет 11% по сравнению с 52% до процедуры рекалибровки).
В плазме крови пациента Е. (от 14.02.2014 г.) концентрация D-димера при измерении на анализаторе «ACL Elite/PRO» составила 494 нг/мл. При умножении на поправочный коэффициент получено значение 914 нг/мл. Реальное измерение на анализаторе «Sysmex CS-2000i» дало значение 855 нг/мл (отклонение значений аналита составляет 9,4% по сравнению с 58% до процедуры рекалибровки).
Пример 2 (фиг. 3)
Измеряли концентрацию D-димера в контрольной сыворотке производства фирмы «Bio-Rad» «D-dimer Control, Level 1,2,3 Lot 13780» второго уровня (Level 2, 13782, exp 31.03.2016) на иммуноферментном анализаторе фирмы «BioTek» (США), и термошейкера PST-60 HL (Biosan) на 96-луночных планшетах фирмы «Technozym» Австрия. Получили значение 732 и 736 нг/мл. Среднее значение определения составляет 734 нг/мл. Провели анализ для контрольной сыворотки третьего уровня (Level 3, Level 13783 exp 31.03.2016). Получили значение 1542 нг/мл и 1566 нг/мл. Среднее значение составляет 1554 нг/мл.
Измеряли концентрацию D-димера в тех же образцах контрольных сывороток на автоматическом анализаторе фирмы «Sysmex CS-2000i» (Япония) с использованием рекомендованных реактивов «Siemens/Sismex Series D-dimer». Получили значение 1380 и 1410 нг/мл. Среднее составляет 1395 нг/мл. Процедуру повторили для контрольной сыворотки третьего уровня. Получили значение 2630 нг/мл и 2660 нг/мл. Среднее значение составило 2645 нг/мл.
Провели расчет по разработанной формуле
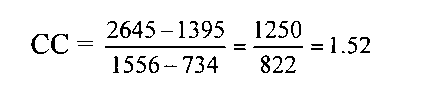
Таким образом, значения определения D-димера существенно отличаются при определении на этих двух приборах. Полученный коэффициент сопоставимости (рекалибровки) составил 1,52.
Этот коэффициент использовали для определения концентрации D-димера в плазме крови у пациентов.
В плазме крови пациента Г. (от 05.03.2014 г.) значение содержания D-димера при измерении на иммуноферментном анализаторе составило 1230 нг/мл. При умножении на поправочный коэффициент получено значение 1869,6 нг/мл. Реальное измерение на анализаторе «Sysmex CS-2000i» дало значение 1845 нг/мл (отклонение значений аналита составляет менее 2% по сравнению с 44% до процедуры рекалибровки).
В плазме крови пациента Е. (от 05.03.2014 г.) значение содержания D-димера при измерении на иммуноферментном анализаторе составило 553.5 нг/мл. При умножении на коэффициент сопоставимости получено значение 841.3 нг/мл. Реальное измерение на приборе Siemens дало значение 890 нг/мл (отклонение значений аналита составляет менее 6% по сравнению с 48% до процедуры рекалибровки).
Предложенный способ был успешно апробирован в параллельном исследовании D-димера в контрольных материалах и плазме крови пациентов в 2013-2014 г. с использованием сертифицированного оборудования и реактивов, имеющих все необходимые разрешения МЗ РФ. Результаты измерений содержания D-димера у пациентов обрабатывали методами вариационной статистики, включавшими расчеты ковариаций и дисперсий измеряемых признаков.
В табл. представлены коэффициенты сопоставимости (рекалибровки) для анализаторов разных фирм-производителей по сравнению с выбранным референсным методом Sysmex (Япония).
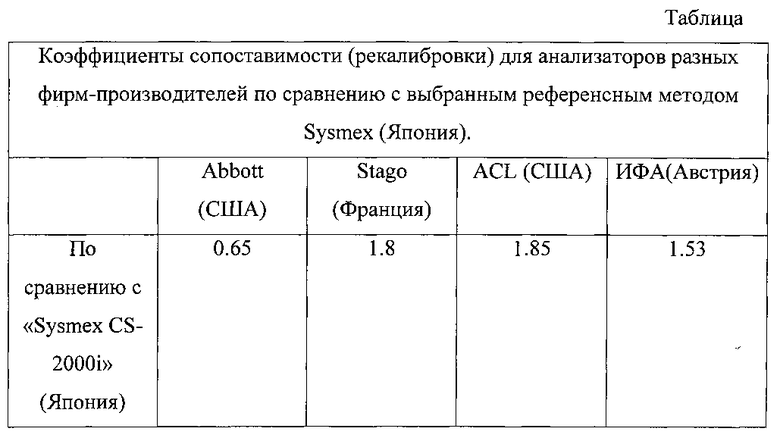
Результаты нашей работы проверили в масштабном исследовании определения D-димера в крови у пациентов (n=70) на трех анализаторах («ICL Elite Pro» (США), «Sysmex CS-2000i» (Япония) и «Technozym» Австрия). Рекалибровка определения D-димера по базе пациентов (n=70) дает сходные результаты с моделированием по контрольным материалам с использованием коэффициента сопоставимости, если показания анализатора «ICL Elite Pro» не превышают 1500 ng/ml (рекомендуемый фирмой без разведения образцов пациентов)
Разброс значений составляет: В=2.046±0.2412.
Рекалибровка определения D-димера по базе пациентов (n=70) дает сходные результаты с моделированием по контрольным материалам с использованием коэффициента сопоставимости, если показания иммуноферментного анализатора, реактивы «Technozym» Австрия (IFA на рисунке), не превышают 1500 ng/ml (рекомендуемый фирмой без разведения образцов пациентов).
Разброс значений составляет: В=1.603±0.1764.
Предлагаемый способ позволяет повысить точность оценки качества определения D-димера и улучшить стандартизованность определения D-димера. Способ обладает простотой и доступностью для широкого практического применения, дает возможность использовать ручные методы определения аналита без набора референсных значений для групп здоровых лиц разного возраста и пола (для установления верхней границы нормы).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЛЕТАЛЬНОГО ИСХОДА У РЕАНИМАЦИОННЫХ ПАЦИЕНТОВ КАРДИОХИРУРГИЧЕСКОГО ПРОФИЛЯ | 2016 |
|
RU2626674C1 |
| Способ диагностики воспалительных поражений верхних отделов ЖКТ | 2018 |
|
RU2672600C1 |
| СПОСОБ ОЦЕНКИ КАЧЕСТВА КЛИНИЧЕСКИХ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ | 2006 |
|
RU2304282C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ТРОМБИНЕМИИ ПРИ ЭНДОПРОТЕЗИРОВАНИИ КРУПНЫХ СУСТАВОВ | 2009 |
|
RU2423697C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТРОМБОЭМБОЛИЧЕСКИХ ОСЛОЖНЕНИЙ | 2016 |
|
RU2621298C1 |
| ДИАГНОСТИКА ТРОМБОЭМБОЛИЧЕСКИХ ЗАБОЛЕВАНИЙ ВЕН ПУТЕМ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ D-ДИМЕРОВ И РАСТВОРИМОГО ФИБРИНА | 2007 |
|
RU2475760C2 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ СВЕРТЫВАЕМОСТИ КРОВИ У БЕРЕМЕННЫХ ВО 2-3 ТРИМЕСТРЕ | 2014 |
|
RU2543653C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ГИПЕРКОАГУЛЯЦИИ И АКТИВАЦИИ ВНУТРИСОСУДИСТОГО СВЕРТЫВАНИЯ У БОЛЬНЫХ ОСТРЫМ ЛИМФОБЛАСТНЫМ ЛЕЙКОЗОМ ПРИ МАНИФЕСТАЦИИ ЗАБОЛЕВАНИЯ | 2012 |
|
RU2497127C1 |
| Способ оценки плазменного гемостаза | 2023 |
|
RU2816538C1 |
| Способ прогнозирования развития тромбоэмболии легочной артерии у онкологических больных с флеботромбозом нижних конечностей | 2016 |
|
RU2664448C2 |
Изобретение относится к клинической лабораторной диагностике и представляет собой способ оценки качества определения D-димера в плазме крови в условиях клинико-диагностической лаборатории, включающий исследование контрольных материалов и сопоставление результатов исследования с целевыми значениями, отличающийся тем, что выбирают референсный метод, наиболее точно совпадающий с целевыми значениями, исследуют не менее двух раз концентрацию D-димера в двух уровнях аттестованных контрольных материалов с использованием оцениваемого метода и выбранного референсного, определяют коэффициент сопоставимости оцениваемого и выбранного референсного методов по следующей формуле:
CC=(Yср high-Ycp low)/(Xcр high-Xcр low),
затем результаты исследования, полученные оцениваемым методом, умножают на коэффициент сопоставимости, сравнивают с результатами, полученными выбранным референсным методом, и оценивают качество определения D-димера в плазме крови. Изобретение позволяет повысить точность оценки качества определения определения D-димера и улучшить стандартизованность определения D-димера. 2 пр., 1 табл., 3 ил.
Способ оценки качества определения D-димера в плазме крови в условиях клинико-диагностической лаборатории, включающий исследование контрольных материалов и сопоставление результатов исследования с целевыми значениями, отличающийся тем, что для сопоставления результатов исследования выбирают референсный метод, наиболее точно совпадающий с целевыми значениями в системе Федеральной системы внешней оценки качества клинических лабораторных исследований или доступной международной системе внешней оценки качества лабораторных исследований, исследуют не менее двух раз концентрацию D-димера в двух уровнях аттестованных контрольных материалов с использованием оцениваемого метода и выбранного референсного, определяют коэффициент сопоставимости оцениваемого и выбранного референсного методов по следующей формуле:
CC=(Yср high-Ycp low)/(Xcр high-Xcр low), где:
CC - коэффициент сопоставимости;
Ycp high - среднее значение D-димера высокого уровня в контрольном материале, полученное оцениваемым методом;
Ycp low - среднее значение D-димера низкого уровня в контрольном материале, полученное оцениваемым методом;
Хcр high - среднее значение D-димера высокого уровня в контрольном материале, полученное референсным методом;
Хcр low - среднее значение D-димера низкого уровня в контрольном материале, полученное референсным методом,
затем результаты исследования, полученные оцениваемым методом, умножают на коэффициент сопоставимости, сравнивают с результатами, полученными выбранным референсным методом, и оценивают качество определения D-димера в плазме крови.
| MOJCA STEGNAR, MOJCA BOZIC / Determination of D-dimer by different quantitative assays - A harmonization exercise / Biochemia Medica / 2008, Vol.18, No.2, pp 216-223 | |||
| СПОСОБ ОЦЕНКИ КАЧЕСТВА КЛИНИЧЕСКИХ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ | 2006 |
|
RU2304282C1 |
| акад | |||
| И.П | |||
| Павлова | |||
Авторы
Даты
2015-12-27—Публикация
2014-09-15—Подача