Область техники
Настоящее изобретение относится к области биотехнологии и медицины и, в частности, к новому применению PRDX2 и/или PRDX6. А именно данное изобретение относится к применению PRDX2 и/или PRDX6 в лечении или предупреждении заболеваний, старения или повреждений, вызванных увеличением ROS (reactive oxygen species - активных форм кислорода).
Предшествующий уровень техники
При использовании кислорода клетки продуцируют свободные радикалы, например активные формы кислорода (ROS) и активные формы азота (RNS). В организмах людей каждая клетка продуцирует 2.5×1011 молекул ROS в сутки, и человеческий организм может продуцировать 40×1021 ROS в сутки. ROS не только обеспечивают и поставляют поддерживающую жизнь энергию, а также способствуют устранению бактерий и патогенов, токсинов и "отходов" из человеческого организма. ROS также служат в качестве инициатора и регулятора различных метаболических путей и сигнальных каналов внутри организма людей, таких как JNK/SAPK, P38MAPK, IKK/NF-KB, P13K, Akt, CD40/CD40L, PKC, и т.д., активируют и регулируют различные транскрипционные факторы (например, АР-1, Nrf2, NF-KB, p53, ATF-1, HIF, HSP, SIFT-1, MST/FOXO и т.д.), влияют на транскрипцию in vivo и экспрессию различных генов, и принимают участие в воспалении, иммунизации, репродукции, развитии, метаболизме, клеточном росте, пролиферации, клеточной регенерации, восстановлении и других изменениях в важных жизненных процессах. ROS усиливают и поддерживают метаболизм в клетках, тканях и организме, таким образом поддерживая и обеспечивая нормальные клеточные активности.
Свободные радикалы в человеческом организме образуются в двух аспектах. Во-первых, они образуются в различных метаболических реакциях в человеческом организме. Во-вторых, они возникают из экзогенных свободных радикалов, образующихся в результате расщепления ковалентных связей вследствие высокой температуры, излучения, фотолиза, химических веществ в окружающей среде, образующихся в результате таких процессов, как курение, употребление алкоголя, загрязнение, лекарства, заболевания и т.д.
Внутри человеческого организма существует динамическая антиоксидантная система, включающая, например, супероксиддисмутазу (SOD), каталазу (CAT), глутатионпероксидазу (GSH-Px), которые могут своевременно и быстро удалять избыток ROS внутри организма. В нормальных физиологических условиях окислительно-антиоксидантная система внутри организмов людей поддерживает гомеостаз, таким образом, обеспечивая нормальные реакции окислительного стресса и предупреждая повреждения человеческого организма за счет ROS. Только тогда, когда ROS образуются чрезмерно, и экспрессия антиоксидантных ферментов недостаточна, баланс между окислением и антиокислением утрачивается, и ROS не способны удаляться своевременно и накапливаются в организме, таким образом приводя в результате к клеточным и тканевым повреждениям (т.е. окислительный стресс) и риску для здоровья человека.
ROS могут прямо или опосредованно окислять или повреждать ДНК, белки и липиды. ROS могут вызывать мутацию генов, денатурацию белков и перекисное окисление липидов, которые рассматривают как основные факторы риска, приводящие к старению человека и различным значимым заболеваниям, таким как бесплодие, катаракта, рак, сердечно-сосудистые заболевания, старческая деменция/нейродегенеративные заболевания (такие как болезнь Альцгеймера, болезнь Паркинсона), сахарный диабет, воспаления (такие как остеоартрит, ревматоидный артрит, бронхит и т.д.), инфекции, реперфузионные повреждения миокарда при ишемии, трансплантации органов, атеросклероз и т.д.
В настоящее время существует множество "лекарств для антиокисления". Тем не менее, существует несколько лекарств, которые в самом деле эффективны в регуляции баланса окисление-антиокисление.
Краткое описание изобретения
Одна из задач настоящего изобретения заключается в том, чтобы предложить новое применение белка PRDX2 и/или белка PRDX6 в лечении или предупреждении повреждений, старения или заболеваний вследствие увеличения количества активных форм кислорода (ROS).
Еще одна задача настоящего изобретения заключается в том, чтобы предложить композицию, включающую фармацевтическую композицию и косметическую композицию, которая содержит белок PRDX2 и/или белок PRDX6 в качестве активного вещества.
Также предполагается, что в настоящем изобретении предложен способ улучшения качества спермы или лечения вызванного астеноспермией мужского бесплодия.
В первом аспекте настоящего изобретения предложено применение оксидоредуктазы перекиси водорода в приготовлении фармацевтической композиции для лечения или предупреждения повреждениий, старения или заболеваний, возникающих в результате увеличения активных форм кислорода (ROS), где оксидоредуктаза перекиси водорода содержит белок PRDX2 и/или белок PRDX6.
В предпочтительном воплощении повреждение, старение или заболевания, возникающие в результате увеличения количества ROS, включают один или более чем один тип, выбранный из группы, состоящей из:
(1) Повреждений, старения или заболеваний, возникающих в результате увеличения количества ROS, вызванных облучением или радиацией;
(2) Повреждений, старения или заболеваний, возникающих в результате увеличения количества ROS, вызванного гипергликемией (такие как сахарный диабет);
(3) Различных тканевых повреждений, вызванных курением;
(4) Различных тканевых повреждений, вызванных употреблением алкоголя;
(5) Других заболеваний, вызванных увеличением количества ROS, где заболевание выбрано из группы, состоящей из атеросклероза, гипертензии, рака, остеоартрита, ревматоидного артрита, легочного фиброза, эпилепсии или нейродегенеративных заболеваний (например, болезни Альцгеймера, болезни Паркинсона);
(6) Повреждений, возникающих в результате процесса клеточной криоконсервации - размораживания;
(7) Реперфузионного повреждения при ишемии;
(8) Асептического некроза головки бедренной кости или пролежней;
(9) Повреждений или заболеваний, вызванных увеличением количества ROS вследствие введения лекарственного средства, например химиотерапевтического лекарственного средства или фосфорорганических пестицидов;
(10) Кожных проблем (например, морщин, складок и ожогов и т.д.);
(11) Диабетического осложнения (например, педопатии (гангрены), заболевания глаз, заболевания почек, энцефалопатии и т.д.).
В предпочтительном воплощении фармацевтическую композицию используют в качестве:
(1) агента, защищающего клетки, агента, защищающего органы, или агента, защищающего ткани;
(2) лекарственного средства для улучшения качества спермы у пациента, страдающего от астеноспермии, или лечения мужского бесплодия; и в предпочтительном воплощении сперма находится на зрелой стадии;
(3) лекарственного средства или косметического средства против старения, заживления рубцов, против морщин, удаления морщин, осветления веснушек, отбеливания, для защиты от солнца или предупреждения рака кожи;
(4) лекарственного средства для лечения ожогов, областей обваривания или повреждения роговицы;
(5) лекарственного средства для ускорения процесса заживления ран (таких как порезы, раны и т.д.); или
(6) лекарственного или медицинского продукта для защиты тканей или клеток от окислительных повреждений или в качестве антиоксиданта.
В предпочтительном воплощении защитный агент представляет собой агент-криопротектор.
В предпочтительном воплощении защитный агент используют для приготовления жидкости для консервации клеток, жидкости для консервации органов, или жидкости для консервации тканей, и, предпочтительно, для приготовления жидкости для консервации трансплантируемых органов.
В предпочтительном воплощении клетка представляет собой клетку животного (предпочтительно клетку млекопитающего, такую как человеческая клетка), где клетка включает спермий, яйцо или клетки различных тканей.
В предпочтительном воплощении ткань включает различные органы или ткани животного, предпочтительно млекопитающего, такого как человек.
В предпочтительном воплощении белок PRDX2 включает белок PRDX2 млекопитающего или его активные фрагменты или производные; и белки PRDX6 включают белок PRDX6 млекопитающего или его активные фрагменты или производные.
В предпочтительном воплощении белок PRDX2 включает человеческий белок PRDX2 или его активные фрагменты или производные; и белок PRDX6 содержит человеческий белок PRDX6 или его активные фрагменты или производные.
В предпочтительном воплощении белок PRDX2 или белок PRDX6 является рекомбинантным.
В предпочтительном воплощении белок PRDX2 включает белок, аминокислотная последовательность которого представлена в SEQ ID NO:4, или фрагмент, представленный в позициях с 6 по 164 в SEQ ID NO:4, или его слитой белок, образованный с экспрессионной последовательностью.
Белок PRDX6 включает белок, аминокислотная последовательность которого представлена в SEQ ID NO:2, или фрагмент, представленный в позициях с 5 по 169 в SEQ ID NO:2, или его слитой белок, образованный с экспрессионной последовательностью.
Во втором аспекте настоящего изобретения предложена композиция, содержащая (а) белок PRDX2 и/или белок PRDX6; и (б) фармацевтически, косметически или алиментарно приемлемый носитель.
В предпочтительном воплощении белок PRDX2 включает белок PRDX2 млекопитающего или его активные фрагменты или производные; и белки PRDX6 включают белок PRDX6 млекопитающего или его активные фрагменты или производные.
В предпочтительном воплощении белок PRDX2 включает человеческий белок PRDX2 или его активные фрагменты или производные; и белок PRDX6 включает человеческий белок PRDX6 или его активные фрагменты или производные.
В предпочтительном воплощении белок PRDX2 или белок PRDX6 является рекомбинантным.
В предпочтительном воплощении композиция представляет собой фармацевтическую, пищевую, медицинскую, косметическую или дополнительную композицию.
В предпочтительном воплощении композиция дозируется для инъекции, мази, спрея, эмульсии, крема, пасты (включающей крем), геля, капель, пластыря или маски.
В предпочтительном воплощении косметическое средство включает перорально вводимое косметическое средство (такое как косметическое средство против воспаления в ротовой полости), спрей, лосьон, гигиеническую губную помаду, солнцезащитное средство, дневной крем, ночной крем, тоник или маску.
В третьем аспекте настоящего изобретения предложен способ лечения или профилактики повреждения, старения или заболевания, возникающего в результате увеличения количества ROS, при котором осуществляют следующие стадии: введение (1) белка PRDX2 и/или белка PRDX6, или (2) композиции в соответствии со вторым аспектом настоящего изобретения субъекту, нуждающемуся в лечении или предупреждении.
В предпочтительном воплощении способ имеет одно или более чем одно из следующих действий:
(1) улучшает качество спермы пациентов, страдающих от астеноспермии;
(2) против старения, заживление рубцов, против морщин, сглаживающее морщины, осветляющее веснушки, отбеливающее, предупреждающее солнечные ожоги или действие, предупреждающее рак кожи;
(3) лечение ожогов или областей обваривания или повреждения роговицы;
(4) ускорение заживления ран (например, порезов, ран и т.д.);
(5) защита тканей или клеток от окислительных повреждений;
(6) лечение или предупреждение осложнений сахарного диабета, таких как патология ног (гангрена), заболевания глаз, заболевания почек, энцефалопатия и т.д.
В предпочтительном воплощении способ имеет следующее действие(я):
(1) увеличение вероятности оплодотворения у пациента, страдающего от астеноспермии; или
(2) защита зрелых сперматозоидов.
В предпочтительном воплощении способ дополнительно обеспечивает одно или более чем одно из следующих действий:
(1) ослабление астенопии, усиление и улучшение зрения, или предупреждение прогрессирующей утраты зрения;
(2) устойчивость к солнечным ожогам и повреждениям вследствие перекисного окисления липидов, увеличение клеточного потенциала к захвату кислородных радикалов, уменьшение различий оттенка лица, лечение миопии, амблиопии, пресбиопии, глаукомы или помутнения волокон стекловидного тела;
(3) ингибирование образования свободных радикалов в стекловидном теле, ускорение клиренса и выведения свободных радикалов, предупреждение гликирования и окисления белков в стекловидном теле, защита групп SH растворимых белков от повреждений, восстановление нерастворимых белков в растворимые белки, предупреждение помутнения хрусталика или лечение или предупреждение образования и развития прогрессирующей катаракты;
(4) лечение старческой катаракты, диабетической катаракты, травматической катаракты, радиационной катаракты, поздней катаракты, или лечение помутнения хрусталика на начальной стадии, стадии распространения и зрелой стадии.
В предпочтительном воплощении окислительное повреждение включает одно или более чем одно из следующих повреждений:
(1) повреждения, вызванные радиационной терапией или химиотерапией;
(2) повреждение, вызванное курением или употреблением спиртных напитков;
(3) ишемические повреждения при реперфузии;
(4) повреждение, вызванное гипергликемией вследствие сахарного диабета.
В четвертом аспекте настоящего изобретения предложен способ улучшения качества спермы или лечения мужского бесплодия, при котором осуществляют введение (1) белка PRDX2 и/или белка PRDX6, или (2) композиции в соответствии со вторым аспектом настоящего изобретения пациенту, страдающему от астеноспермии.
В пятом аспекте настоящего изобретения предложен способ получения композиции в соответствии со вторым аспектом настоящего изобретения, при котором осуществляют смешивание белка PRDX2 и/или белка PRDX6 с фармацевтически, косметически или алиментарно- приемлемым носителем или эксципиентом, таким образом, образуя композицию в соответствии со вторым аспектом настоящего изобретения.
В шестом аспекте настоящего изобретения предложено применение белка Prx-6 в приготовлении лекарственного средства для лечения повреждений роговицы.
В предпочтительном воплощении белок Prx-6 представляет собой человеческий белок Prx-6.
В предпочтительном воплощении белок Prx-6 является рекомбинантным.
В предпочтительном воплощении белок Prx-6 содержит белок, аминокислотная последовательность которого представлена в SEQ ID NO:2, или его слитой белок, образованный с экспрессионной последовательностью.
В седьмом аспекте настоящего изобретения предложена фармацевтическая композиция для лечения повреждений роговицы, где фармацевтическая композиция содержит белок Prx-6 и фармацевтически приемлемый носитель, и фармацевтическая композиция представляет собой офтальмологический препарат.
В предпочтительном воплощении белок Prx-6 представляет собой человеческий белок Prx-6.
В предпочтительном воплощении белок Prx-6 представляет собой рекомбинантный белок.
В предпочтительном воплощении офтальмологический препарат представляет собой глазные капли, офтальмологический гель или офтальмологическую мазь.
В восьмом аспекте настоящего изобретения предложен способ лечения повреждений роговицы, при котором осуществляют следующие стадии: капельный или иной способ нанесения белка Prx-6 или фармацевтической композиции в соответствии с седьмым аспектом настоящего изобретения в конъюнктивальный мешок субъекта, нуждающегося в лечении.
В предпочтительном воплощении лечение включает ингибирование реваскуляризации роговицы, восстановление эпителиальных клеток поврежденной роговицы, уменьшение отека роговицы, восстановление степени прозрачности роговицы и зрения, захват антиоксидантных радикалов и ускорение восстановления пораженных воспалением тканей.
От предварительных экспериментов на клетках к экспериментам на животных автор изобретения убедился в том, что белки PRDX играют важную роль в захвате активной формы кислорода и корректировки трансдукции сигнала, зависимого от активной формы кислорода. Белок PRDX является многообещающим и эффективным антиоксидантом, который в качестве лекарственного ингредиента является эффективным для лечения и предупреждения заболеваний или неблагоприятных изменений, вызванных увеличением уровня ROS.
Понятно, что в настоящем изобретении каждое из технических свойств, специфическим образом описанных выше и ниже (таких как в Примерах), может быть комбинировано друг с другом, таким образом составляя новые или предпочтительные технические решения, которые нет необходимости уточнять здесь повторно.
Краткое описание графических материалов
На Фиг.1 показана амплификация путем ПЦР гена Prx-6. Полоса 1: контроль; Полоса 2: Prx-6; М: Маркер.
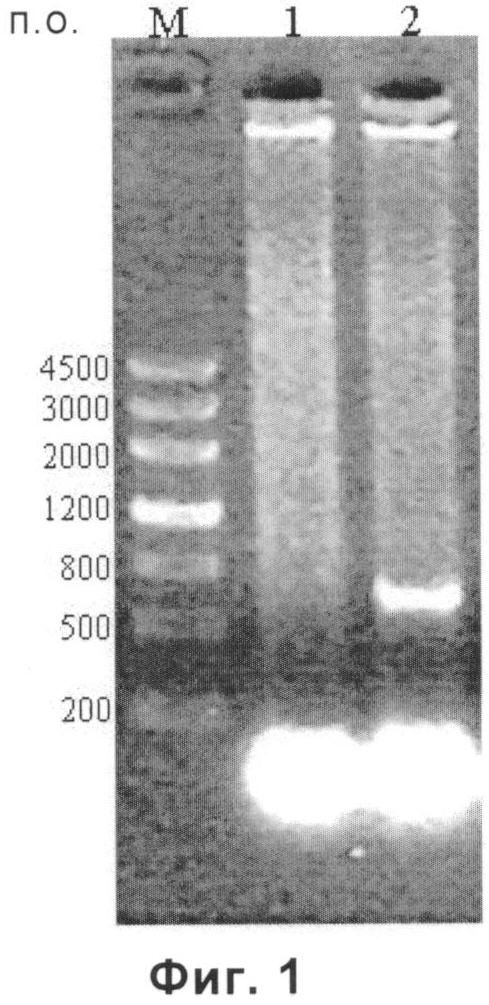
На Фиг.2 показана очистка путем аффинной хроматографии белка Prx-6. Пик 1: белковые примеси; пик 2: белок Prx-6.
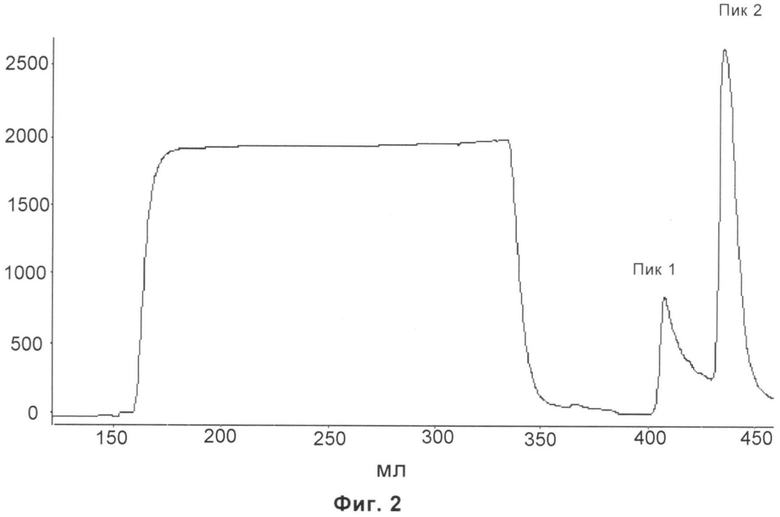
На Фиг.3 показан профиль очистки белка PRDX6 при помощи 12% SDS-PAGE (электрофорез в полиакриламидном геле с додецилсульфатом натрия). Полоса 1: Маркер (Fermentas); Полоса 2: белок PRDX6, очищенный при помощи аффинной хроматографии и обессоливания; Полоса 3: пик 1; Полоса 4: прошедший белок из образца; Полоса 5: супернатант бактериального лизата (т.е. нанесенный образец).
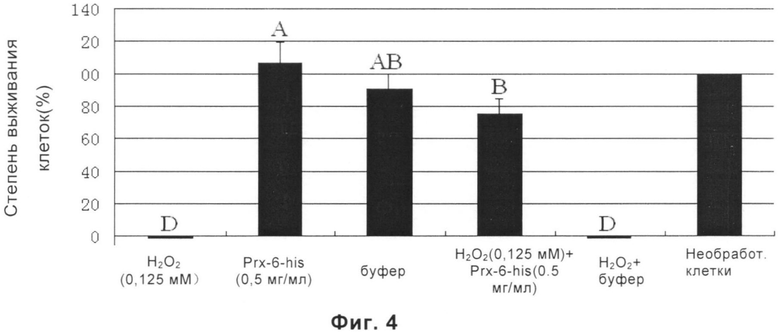
На Фиг.4 проиллюстрировано защитное действие рекомбинантного белка PRDX6 на клетки HEF против окисления (Р<0,05).
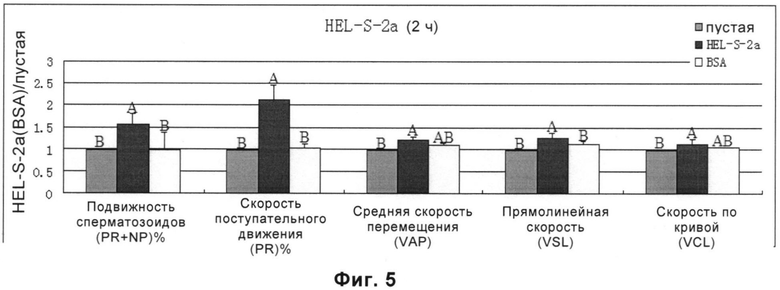
На Фиг.5 проиллюстрировано защитное действие белка PRDX2 (т.е. HEL-S-2a) на ослабленные сперматозоиды.
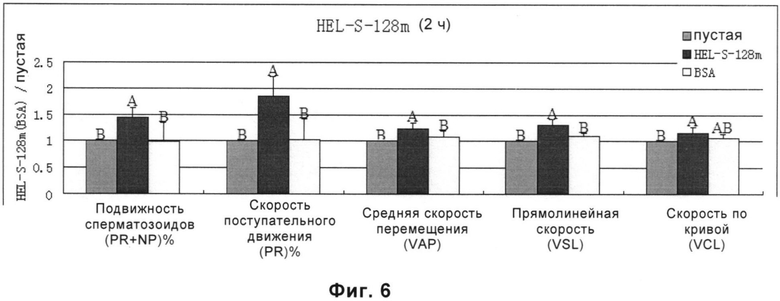
На Фиг.6 проиллюстрировано защитное действие белка PRDX6 (т.е. HEL-S-128m) на ослабленные сперматозоиды.
На каждой из вышеупомянутых фигур любые две группы, обозначенные одной и той же буквой, не обладают значимыми различиями в статистическом анализе. Например, отсутствует значимое различие между группой А и группой АВ. Любые две группы без любой общей буквы имеют значимое различие в статистическом анализе. Например, существует значимое различие между группой А и группой В или между группой А и группой D.
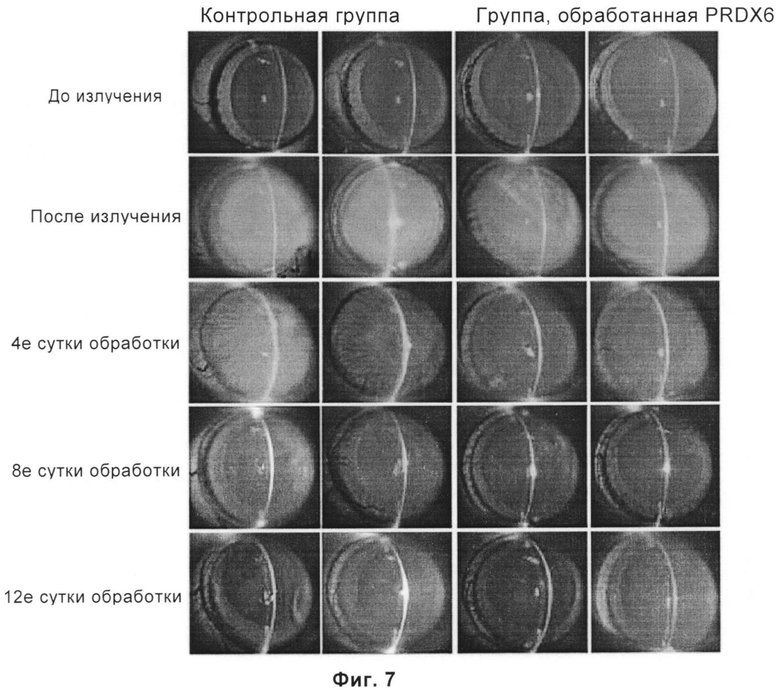
На Фиг.7 приведены результаты исследования рекомбинантного белка Prx-6 в лечении повреждений роговицы крыс при микроскопии с использованием щелевой лампы. Изображения слева направо: контрольная группа (2 крысы); и группа Prx-6 (2 крысы). Изображения сверху вниз: перед УФ излучением; после УФ излучения; 4 суток лечения; 8 суток лечения; 12 суток лечения.
Подробное описание изобретения
Посредством всестороннего и интенсивного исследования автор изобретения неожиданно обнаружил, что белки PRDX6 и PRDX2 могут быть использованы для приготовления фармацевтической композиции для лечения или предупреждения заболеваний, вызванных увеличением уровня ROS. Лекарственное средство, содержащее белок PRDX6 и/или белок PRDX2 в качестве активного вещества, может использоваться не только для того, чтобы защитить такие клетки, как HEF, но также применяться для лечения или предупреждения различных заболеваний, вызванных увеличением уровня ROS, или облегчения симптомов, вызванных увеличением уровня ROS. Настоящее изобретение выполнено на основе данного открытия.
Белок PRDX6
Использованные здесь термины "белок PRDX6", "белок Prx-6", "HEL-S-128m" могут использоваться взаимозаменяемо и все относятся к белку или полипептиду, имеющему аминокислотную последовательность человеческого PRDX6. Они могут содержать или не содержать стартовый метионин. Понятно, что эти термины охватывают как человеческие (источник) белки, так и гомологи или гомологичные белки у других млекопитающих (таких как собаки, крупный рогатый скот, овцы, обезьяны, грызуны (например мыши)), имеющие те же самые функции. Кроме того, термины относятся к белку PRDX6 дикого типа или мутантному белку PRDX6.
Регистрационный номер в GenBank последовательности кДНК гена человеческого PRDX6 составляет NM_004905.2, как представлено в SEQ ID NO:1. Регистрационный номер в GenBank аминокислотной последовательности человеческого белка PRDX6 составляет NP_004896.1, как представлено в SEQ ID NO:2.
Понятно, что поскольку нуклеотидная и аминокислотная последовательности PRDX6 известны, данный белок может быть получен при помощи обычной в области техники технологии рекомбинантной ДНК.
Особенно предпочтительный белок представляет собой аналоги белка PRDX6, т.е. белки, гомологичные PRDX6 у других млекопитающих (таких как крупный рогатый скот, овцы, кролики, собаки, обезьяны, крысы и т.д.). Кодирующие последовательности гомологичных белков у других видов могут быть получены с использованием способов гибридизации или амплификации в соответствии с последовательностью PRDX6. Затем гомологичные белки могут быть получены с использованием обычных рекомбинантных способов.
Белки по настоящему изобретению могут представлять собой рекомбинантный полипептид, природный полипептид, синтетический полипептид и, предпочтительно, рекомбинантный полипептид. В зависимости от хозяина, используемого в протоколе рекомбинантного получения, полипептиды по настоящему изобретению могут быть гликозилированными или негликозилированными. Полипептиды по изобретению могут включать или не включать остаток стартового метионина.
Изобретение также включает активные фрагменты человеческого белка PRDX6, его производные и аналоги. Используемые здесь термины "активный фрагмент", "производное" и "аналог" относятся к полипептиду, который, по существу, сохраняет ту же самую биологическую функцию или биологическую активность природного человеческого белка PRDX6 по настоящему изобретению. Активный фрагмент, производная и аналог здесь могут представлять собой (1) полипептид с одним или более чем одним замещенным консервативным или неконсервативным аминокислотным остатком (предпочтительно консервативным(и) аминокислотным(и) остатком(остатками)), где такой замещенный аминокислотный остаток может быть кодирован или не кодирован генетическим кодом, или (2) полипептид с группой заместителем в одном или более чем одном аминокислотном остатке, или (3) полипептид, образующийся в результате слияния зрелого полипептида и другого соединения (такого как соединение, которое удлиняет период полувыведения полипептидов, например полиэтиленгликоль), или (4) полипептид, который образуется путем слияния дополнительной аминокислотной последовательности с указанной полипептидной последовательностью (такой как лидирующая последовательность или секреторная последовательность, или последовательность, используемая для его очистки, или протеиногенная последовательность, или слитой белок образуется с фрагментами антигена IgG). В соответствии с изложенным здесь эти фрагменты, производные и аналоги находятся в пределах знаний специалиста в данной области техники.
В настоящем изобретении "человеческий полипептид PRDX6" относится к полипептиду, имеющему последовательность SEQ ID NO:2 и активность человеческого PRDX6. Он также включает варианты SEQ ID NO:2, которые обладают той же самой функцией, как человеческий PRDX6. Эти варианты включают (но не ограничиваются) делецию, вставку и/или замену нескольких (обычно 1-50, предпочтительно 1-30, более предпочтительно 1-20, наиболее предпочтительно 1-10) аминокислот, и добавление одной или более чем одной (обычно 20 или меньше, предпочтительно 10 или меньше, более предпочтительно 5 или меньше) аминокислот на С-конце и/или N-конце. Например, в настоящей области техники функция белка не будет изменена при замене аминокислот, обладающих приблизительными или похожими свойствами. Опять же в качестве примера в настоящей области техники функция белка не будет изменена при добавлении одной или нескольких аминокислот по С-концу и/или N-концу. Он также включает активные фрагменты или активные производные человеческого белка PRDX6. Предпочтительный активный фрагмент представляет собой полипептид, аминокислотная последовательность которого представлена в позициях 5-169 в SEQ ID NO:2.
Белок PRDX2
Используемые здесь термины "белок PRDX2", "Prx-2 белок", "HEL-S-2a" могут быть использованы взаимозаменяемо и все относятся к белку или полипептиду, имеющему аминокислотную последовательность человеческого PRDX2. Они могут содержать или не содержать стартовый метионин. Понятно, что эти термины включают человеческие (источник) белки, и гомологи или гомологичные белки других млекопитающих (таких как собаки, крупный рогатый скот, овцы, обезьяны, грызуны (например мышь)), имеющие те же самые функции. Кроме того, условия включают дикий тип и мутантный белок PRDX2.
Регистрационный номер в GenBank последовательности кДНК гена человеческого PRDX2 составляет NM_005809.4, как представлено в SEQ ID NO:3. Регистрационный номер в GenBank аминокислотной последовательности человеческого белка PRDX2 составляет NP_005800.3, как представлено в SEQ ID NO:4.
Понятно, что поскольку нуклеотидная и аминокислотная последовательности PRDX2 известны, данный белок может быть получен при помощи обычной в области техники технологии рекомбинантной ДНК.
Особенно предпочтительный белок представляет собой аналоги белка PRDX2, т.е. белки, гомологичные PRDX2 у других млекопитающих (таких как крупный рогатый скот, овцы, кролики, собаки, обезьяны, крысы и т.д.). Кодирующие последовательности гомологичных белков у других видов могут быть получены с использованием способов гибридизации или амплификации в соответствии с последовательностью PRDX2. Затем гомологичные белки могут быть получены с использованием обычных рекомбинантных способов.
Белки по настоящему изобретению могут представлять собой рекомбинантный полипептид, природный полипептид, синтетический полипептид и, предпочтительно, рекомбинантный полипептид. В зависимости от организма хозяина, используемого в протоколе рекомбинантного получения, полипептиды по настоящему изобретению могут быть гликозилированными или негликозилированными. Полипептиды по изобретению могут включать или не включать остаток стартового метионина.
Изобретение также включает активные фрагменты человеческого белка PRDX2, его производные и аналоги. Используемые здесь термины "активный фрагмент", "производное" и "аналог" относятся к полипептиду, который, по существу, сохраняет ту же самую биологическую функцию или биологическую активность природного человеческого белка PRDX2 по настоящему изобретению. Активный фрагмент, производная и аналог здесь могут представлять собой (1) полипептид с одним или более чем одним замещенным консервативным или неконсервативным аминокислотным остатком (предпочтительно консервативным аминокислотным остатком), и такой замещенный аминокислотный остаток может быть кодирован или не кодирован генетическим кодом, или (2) полипептид с группой заместителем в одном или более чем одном аминокислотном остатке, или (3) полипептид, образующийся в результате слияния зрелого полипептида и другого соединения (такого соединения, которое удлиняет период полувыведения полипептидов, например полиэтиленгликоль), или (4) полипептид, который образуется путем слияния дополнительной аминокислотной последовательности в указанном полипептиде (такой как лидирующая последовательность или секреторная последовательность, или последовательность, используемая для очистки указанного полипептида, или протеиногенная последовательность, или слитой белок образуется с фрагментами антигена IgG). В соответствии с изложенным здесь эти фрагменты, производные и аналоги находятся в пределах знаний специалиста в данной области техники.
В настоящем изобретении "человеческий полипептид PRDX2" относится к полипептиду, имеющему последовательность SEQ ID NO:4 и активность человеческого PRDX2. Он также включает варианты SEQ ID NO:4, которые обладают той же самой функцией, что и человеческий PRDX4. Эти варианты включают (но не ограничиваются) делецию, вставку и/или замену нескольких (обычно 1-50, предпочтительно 1-30, более предпочтительно 1-20, наиболее предпочтительно 1-10) аминокислот, и добавление одной или нескольких (обычно 20 или меньше, предпочтительно 10 или меньше, более предпочтительно 5 или меньше) аминокислот на С-конце и/или N-конце. Например, в настоящей области техники функция белка не будет изменена при замене аминокислот, обладающих приблизительными или похожими свойствами. Опять же в качестве примера, в настоящей области техники функция белка не будет изменена при добавлении одной или нескольких аминокислот по С-концу и/или N-концу. Он также включает активные фрагменты или активные производные человеческого белка PRDX2. Предпочтительный активный фрагмент представляет собой полипептид, аминокислотная последовательность которого представлена в позициях 6-164 в SEQ ID NO:4.
Заболевания, старение или повреждение, вызванное увеличением уровня ROS PRDX2 и/или PRDX6 по настоящему изобретению, могут быть использованы для лечения или предупреждения заболеваний, старения или повреждения, вызванного увеличением уровня ROS, где заболевания, старение или повреждение, вызванное увеличением ROS, могут представлять собой любые известные заболевания, старение или повреждение, вызванные увеличением уровня активных форм кислорода, и предпочтительно они включают (но не ограничены): 1) повреждения, старение или заболевание, возникающие в результате увеличения уровня ROS, вызванного путем излучения или радиации, включающей космическое излучение, излучение, продуцируемое радиоактивными элементами земли, ультрафиолетовое излучение, рентгеновское излучение, излучение, возникающее в результате сварки, излучение компьютеров, телевизоров, мобильных телефонов и других источников электрического излучения или радиотерапии опухолей, такие как повреждения роговицы, повреждение кожи, повреждение тканей, включающих повреждение различных тканей; 2) повреждение, старение или заболевания, возникающие в результате увеличения ROS, вызванные гипергликемией (такие как сахарный диабет), такие как инсулинорезистентность, повреждение β клеток поджелудочной железы, повреждение почек и т.д.; 3) различные повреждения тканей, вызванные курением, например повреждение легкого (такие как бронхит, повреждение поджелудочной железы, повреждение печени); 4) различные повреждения тканей, вызванные употреблением спиртных напитков, таких как алкогольное заболевание печени, повреждение поджелудочной железы; 5) другие заболевания, вызванные увеличением уровня ROS, например атеросклероз, гипертензия, рак, остеоартрит, ревматоидный артрит, легочный фиброз, эпилепсия или нейродегенеративные заболевания, такие как болезнь Альцгеймера, болезнь Паркинсона; 6) Повреждение, возникающее в результате процесса восстановления после криоконсервации клеток, где клетка включает сперматозоиды человека или животного, яйца, или клетки любой другой ткани; 7) ишемическое повреждение после реперфузии, включающее без ограничения ишемическое повреждение в результате реперфузии во время трансплантации органа, углубление микроциркуляции во время шока, облегчение спазма коронарной артерии, CPR (сердечно-легочная реанимация) сердца и мозга после внезапной остановки сердца, коронарное шунтирование, РТСА (Percutaneous transluminal coronary angioplasty чрескожная транслюминальная коронарная ангиопластика), постхирургия реваскуляризационной хирургии, такая как тромболитическая терапия, операция на сердце по сердечно-легочному шунтированию, трансплантация органа и трансплантация оторванной конечности и т.д.; 8) асептический некроз головки бедренной кости; 9) пролежни, вызванные длительным постельным режимом; 10) заболевания, вызванные увеличением уровня ROS, или заболевания, вызванные использованием лекарственного средства, такие как перекисное повреждение, вызванное вследствие использования химиотерапевтического лекарственного средства, вызванное вследствие отравления фосфорорганическими пестицидами, или вызванные вследствие приема токсичных наркотиков для самоубийства, и т.д.; 11. дерматологические проблемы, включающие без ограничения морщины, пятна и ожоги и т.д.; 12. осложнения сахарного диабета, например патология ног (гангрена), болезни глаз, болезнь почек, энцефалопатия и т.д.
Фармацевтическая композиция и способы введения
Фармацевтическая композиция по настоящему изобретению содержит безопасное эффективное количество белка PRDX6 и/или белка PRDX2, и фармакологически приемлемый эксципиент или носитель. Используемый здесь термин "безопасное эффективное количество" означает, что количество белка эффективно для значимого улучшения состояния заболевания, не вызывая серьезные побочные действия. Как правило, фармацевтическая композиция включает 0,1 нг - 2000 мг белка PRDX6 и/или белка PRDX2 за дозу, предпочтительно, включает 1-200 мг из белка PRDX6 и/или белка PRDX2 на дозу. Предпочтительно, "доза" представляет собой капсулу, таблетку или флакон глазных капель.
"Фармацевтически приемлемый носитель" обозначает один или более чем один совместимый твердый или заполненный жидкостью материал или гель, который подходит для использования людьми, обладающий достаточной чистотой и достаточно низкой токсичностью. "Совместимый" означает, что каждый компонент композиции могут быть смешан с белком по настоящему изобретению, не уменьшая эффективность композиции. Некоторые фармацевтически приемлемые носители представляют собой целлюлозу и ее производные (такие как натриевая карбоксиметилцеллюлоза, натриевая этилцеллюлоза, ацетат целлюлозы и т.д.), желатин, тальк, твердая смазка (такая как стеариновая кислота, стеарат магния), сульфат кальция, растительные масла (такие как соевое масло, кунжутное масло, арахисовое масло, оливковое масло и т.д.), полиолы (такие как пропиленгликоль, глицерин, маннит, сорбит и т.п.), эмульгаторы (таких как Tween®), увлажнители (например, лаурилсульфат натрия), красители, корригенты, стабилизаторы, антиоксиданты, консерванты, апирогенную воду и т.д.
Отсутствует конкретное ограничение на способы введения белка PRDX6 и/или белка PRDX2 или его фармацевтической композиции. Примеры способов введения включают (без ограничения): пероральное, ректальное, парентеральное (внутривенный, внутримышечный или подкожный) и местное введение (такое как пластыри).
Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В этих твердых лекарственных формах действующее начало смешивают по меньшей мере с одним обычным инертным эксципиентом (или носителем), такими как цитрат натрия или дикальция фосфат, или смешивали со следующими ингредиентами: (а) наполнителями или компатибилизаторами, такими как крахмал, лактоза, сахароза, и силикат; (б) связующими веществами, например гидроксиметилцеллюлозой, поливинилпирролидоном, сахарозой и аравийской камедью; (в) увлажнителями, например, глицерином; (г) разрыхлителями, такими как агар, картофельный крахмал или крахмал тапиоки, альгиновая кислота, некоторые сложные силикаты, и карбонат натрия; (д) агентами для длительного высвобождения, такими как парафин; (е) ускорителями абсорбции, такими как четвертичные аммониевые соединения; (ж) увлажнителями, такими как цетиловый спирт и глицерилмоностеарат; (з) адсорбентами, например каолином; и (и) смазывающими веществами, например тальком, стеаратом кальция, стеаратом магния, твердыми полиэтиленгликолями, натрий лаурилсульфатом или их комбинацией. Лекарственную форму в виде капсул, таблеток и пилюль могут также включать буферные агенты.
Твердые лекарственные формы, такие как таблетки, леденцы, капсулы, пилюли и гранулы, могут быть приготовлены с покрытиями и материалами оболочки, такими как искусственные оболочки и другие материалы, известные в области техники. Они могут содержать замутнители, и активное вещество из таких композиций может быть высвобождаться пролонгированно в определенной части пищеварительного тракта. Примерами внедряемых композиций, которые могут быть использованы, являются полимерные и восковые вещества. При необходимости вышеприведенные активные вещества могут также образовывать микроинкапсулированную форму с одним или более чем одним из перечисленных выше эксципиентов.
Жидкие лекарственные формы для перорального введения включают фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы или тинктуры. Помимо действующего начала жидкие лекарственные формы могут содержать инертные разбавители, обычно используемые в области техники, таких как вода или другие растворители, солюбилизаторы и эмульгаторы, например этанол, изопропиловый спирт, этилкарбонат, этилацетат, пропандиол, 1,3-бутиленгликоль, диметилформамид и масла, особенно хлопковое масло, арахисовое масло, масло проростков кукурузы, оливковое масло, касторовое масло и кунжутное масло, или их смеси.
В дополнение к таким инертным разбавителям композиции могут также содержать вспомогательные добавки, такие как увлажнители, эмульгаторы и суспендирующие агенты, подсластители, корригенты и специи.
В дополнение к действующему началу суспензии могут содержать суспендирующие агенты, например этоксилированные изостеариловые спирты, полиоксиэтиленсорбит и сложные эфиры сорбита, микрокристаллическую целлюлозу, алюминий метанол, агар или их смеси.
Композиция для парентеральной инъекции может включать физиологически приемлемые стерильные водные или неводные растворы, дисперсии, суспензии или эмульсии, и стерильные порошки, которые могут быть перерастворены в стерильных инъецируемых растворах или дисперсиях. Подходящие водные и неводные носители, разбавители, растворители и эксципиенты включают воду, этанол, полиолы и любую подходящую их смесь.
Лекарственные формы белка PRDX6 и/или белка PRDX2 для местного введения включают мази, порошки, пластыри, спреи, суппозитории и ингаляции. Активное вещество при необходимости смешивают в стерильных условиях с физиологически приемлемым носителем и любым консервантом, буфером или пропеллентом.
Белок по настоящему изобретению может быть введен индивидуально или вводиться в смеси с другими фармацевтически приемлемыми соединениями или белком.
При использовании фармацевтической композиции безопасное эффективное количество активного вещества вводят млекопитающему (например, человеку), нуждающемуся в таком лечении, где введенная доза представляет собой дозу, которую рассматривают как фармацевтически эффективную. Суточная доза, вводимая человеку массой 60 кг, обычно составляет 0,5 нг - 2000 мг, предпочтительно 2-50 мг. Безусловно, конкретная доза зависит от факторов, таких как путь введения, состояние здоровья человека, и находится в пределах знаний специалиста в данной области техники.
Предпочтительно в настоящем изобретении предложена фармацевтическая композиция, которая содержит безопасное эффективное количество белка PRDX6 и/или белка PRDX2 по настоящему изобретению, и фармацевтически приемлемые носители или эксципиенты. Эти носители или эксципиенты включают (но не ограничиваются): физиологический раствор, буфер, глюкозу, вода, глицерин, этанол, полоксамер, карбомер или их комбинации. Например, белок по настоящему изобретению может быть приготовлен в нетоксичной, инертной, фармацевтически приемлемой водной среде носителя, где рН обычно составляет приблизительно 5-8, предпочтительно рН составляет приблизительно 6-8, наиболее предпочтительно рН составляет приблизительно 6,8-7,6, хотя значение рН может варьировать в зависимости от свойства получаемого вещества и заболевания, которое необходимо вылечить.
Приготовленная композиция может быть введена обычными путями, включающими (без ограничения) местный, пероральный, внутримышечный и внутривенный пути введения или субконъюнктивальную инъекцию и т.д.
Лекарственная форма должна соответствовать способу введения. (1) Фармацевтические композиции по изобретению могут быть приготовлены в виде инъекций, например, приготовлены при помощи обычного способа с физиологическим или водным раствором, содержащим глюкозу и другие вспомогательные агенты. (2) Фармацевтические композиции, такие как мази, капли, спреи, капсулы, таблетки и т.п. могут быть приготовлены при помощи обычных способов. (3) Фармацевтические композиции, такие как инъекции, растворы, таблетки и капсулы, которые должны быть приготовлены в стерильных условиях. (4) Суппозиторий может быть приготовлен, например, в соответствии со следующим определенным способом: 1) смешивание подходящего количества этанола с β-CD в пасте, и добавление белка PRDX6, PRDX2, и измельчение до образования включения в течение 45 минут для дальнейшего использования. 2) растворение полусинтетического фермента жирной кислоты (тип 36) путем нагревания и поддержания при 38°С, и добавление включения основного активного вещества, полное смешивание при поддержании температуры. 3) гомогенную смесь выливают и дают сформироваться путем охлаждения. 4) приготовленные суппозитории должны быть введены в женский половой тракт перед половым актом, таким образом повышая вероятность успешного возникновения беременности у пациентов, страдающих от астеноспермии.
Доза активного вещества представляет собой терапевтически эффективное количество, например, от приблизительно 1 мкг/кг массы организма до приблизительно 10 мг/кг массы организма в сутки. Фармацевтическая композиция по настоящему изобретению также может быть приготовлена в виде глазных капель, глазной мази, или гелей, предпочтительно в стерильных условиях. Вводимое количество активного вещества представляет собой терапевтически эффективное количество, например, от приблизительно 10 мкг/кг массы организма до приблизительно 10 мг/кг массы организма в сутки. Безусловно, что конкретная доза зависит от факторов, таких как путь введения, состояние здоровья пациента, которые находятся в компетенции специалиста в данной области техники.
Клеточный криопротектор по настоящему изобретению
В предпочтительном воплощении в настоящем изобретении предложена композиция криопротектора сперматозоидов, которая содержит 0,1 мг/мл - 100 мг/мл рекомбинантного белка PRDX6 и/или белка PRDX2; и некоторые обычные компоненты криопротектора спермы, например хлорид калия, хлорид натрия, сульфат магния, дигидрофосфат натрия, бикарбонат натрия, глюкозу, яичный желток, альбумин, глицин, сахарозу, глицерин.
Кроме того, белки PRDX2 и PRDX6 могут быть введены индивидуально или вводиться вместе. Кроме того, белок по настоящему изобретению может быть использован с другим криопротектором спермы.
Лечение астенозооспермии
В предпочтительном воплощении настоящего изобретения предложена фармацевтическая композиция для лечения астеноспермии, которая содержит 1-100 мг действующего начала, которое представляет собой рекомбинантный белок PRDX2 и/или белок PRDX6; и фармацевтически приемлемые носители или эксципиенты. Такие носители включают (но не ограничиваются)солевой буферный раствор, декстрозу, воду, глицерин, Tween 80, β-CD и их комбинации.
Кроме того, белок PRDX2 и белок PRDX6 могут быть введены индивидуально или в комбинации. Кроме того, белок в настоящем изобретении может быть использован вместе с другими терапевтическими агентами для лечения астеноспермии.
Например, функция фармацевтической композиции по настоящему изобретению включает (но не ограничивается): (1) увеличение вероятности оплодотворения пациентов, страдающих от астеноспермии; (2) защиту сперматид на зрелой стадии.
Лечение повреждения роговицы
В предпочтительном воплощении настоящего изобретения предложена фармацевтическая композиция для лечения повреждения роговицы. Она включает капание или нанесение белка по настоящему изобретению в конъюнктивальный мешочек непосредственно в дозе каждый раз 0,05-0,2 мг. Кроме того, белки PRDX2 и PRDX6 могут быть введены индивидуально или вводиться вместе. Кроме того, белок по настоящему изобретению может быть использован с другими терапевтическими агентами для лечения повреждения роговицы.
В частности, фармацевтическая композиция обладает одной или более чем одной из следующих функций: (1) ослабление астенопии, усиление и улучшение зрения или предупреждение прогрессирующей утраты зрения; (2) противодействие легким повреждениям и повреждениям вследствие перекисного окисления липидов, увеличение клеточного потенциала к захвату кислородных радикалов, уменьшение различий оттенка, эффективное лечение миопии, амблиопии, пресбиопии, глаукомы или помутнения волокон стекловидного тела; (3) ингибирование образования свободных радикалов в стекловидном теле, ускорение клиренса и экскреции свободных радикалов, предупреждение гликирования и окисления белков в стекловидном теле, защита групп SH растворимых белков от повреждение, восстановление нерастворимых белков в растворимые белки, предупреждение помутнения хрусталика, или контроль образования и развития прогрессирующей катаракты, таким образом, эффективное лечение старческой катаракты, диабетической катаракты, травматической катаракты, радиационной катаракты, поздней катаракты или лечение помутнения хрусталика на незрелой стадии, стадии распространения и зрелой стадии.
Лечение ожогов и областей обваривания
В предпочтительном воплощении настоящего изобретения предложена фармацевтическая композиция для лечения ожогов и областей обваривания. Можно наносить белок по настоящему изобретению на поверхность ожогов и областей обваривания в количестве 0,1-0,5 мг/см2 поверхности раны. Кроме того, белок PRDX2 и белок PRDX6 может быть введен которым индивидуально или вводиться вместе. Кроме того, белок по настоящему изобретению может быть использован с другими терапевтическими агентами для лечения ожогов и областей обваривания.
Косметическая композиция
В настоящем изобретении предложена косметическая композиция, которая содержит белок PRDX2 и/или белок PRDX6 в качестве действующего начала. Композиция содержит эффективное количество белка PRDX2 и/или белка PRDX6, и косметически приемлемые носители или эксципиенты.
Косметическая композиция, которая содержит белок PRDX2 и/или белок PRDX6 в качестве активного вещества по настоящему изобретению, может содержать любое количество белка PRDX2 и/или белка PRDX6, подходящее для косметической композиции. Как правило, содержание белка PRDX2 и/или белка PRDX6 может составлять 0,1-30%, предпочтительно 1-15%, более предпочтительно 3-8% от общей массы косметической композиции.
В изобретении носители и эксципиенты для приготовления косметических композиций могут представлять собой любые обычные носители или эксципиенты, известные специалистам в данной области техники. Выбор конкретного носителя или эксципиента зависит от типа приготавливаемого косметического средства.
Косметическая композиция по настоящему изобретению может быть приготовлена при помощи способов, известных специалистам в данной области техники. Например, белок PRDX2 и/или белок PRDX6 может быть смешан в любом типе (тип масло-в-воде и/или масло-в-воде) косметических кремов (таких как крем, увлажняющий крем, бальзам, кольдкрем, тональный крем), косметических средств (таких как губная помада, румяна, карандаш для бровей, рассыпчатые тени для век, тушь, подводка для глаз, лак для ногтей, маска и т.д.), порошкообразных косметических средств (таких как рассыпчатая пудра, компактная пудра, тальковая пудра), парфюмерии (таких как духи, одеколон, цветочные духи, хинная вода, кондиционер, лосьон, средство после бритья и т.д.), лечебной косметики (такой как агенты для ухода за кожей (традиционная китайская терапия), косметических средств против прыщей, косметических средств против веснушек, косметических средств против рубцов и старения, косметических средств для похудения, отбеливающая косметика), солнцезащитных косметических средств, кремы для бритья и т.д. с использованием способов, известных специалистам в данной области техники.
Косметическая композиция по настоящему изобретению обладает действием против старения, заживляющим шрамы, против рубцов, разглаживающим морщины, удаляющим веснушки, отбеливающим, защищающим от солнца или предотвращающим рак кожи. Настоящее изобретение также позволяет применять композицию в общем уходе за кожей, в косметическом лечении некоторых морщин, родимых пятен и ожогов.
Главное преимущество настоящего изобретения заключается в том, что человеческие белки PRDX2 и/или PRDX6 обладают следующими действиями:
(1) защита сперматозоидов во время процесса замораживания и оживления сперматозоидов. Например, скорость восстановления спермы и скорость проникновения сперматозоидов (SPA) значимо улучшается тогда, когда рекомбинантный человеческий белок PRDX2 и/или белок PRDX6 добавлены в традиционный криопротектор. (2) улучшение качества сперматозоидов у пациентов, страдающих от астенозооспермии. Например, увеличивается общее количество активных сперматозоидов, и качество сперматозоидов и степень оплодотворения значимо улучшаются после добавления рекомбинантного человеческого белка PRDX2 и/или белка PRDX6 во время обработки спермы in vitro во вспомогательной репродуктивной технологии. (3) различные действия, такие как противодействие старению, заживление шрамов, предупреждение морщин, разглаживание морщин, удаление веснушек, отбеливание, защита от солнца, предупреждение рака кожи; (4) лечение ожога, областей обваривания и повреждений роговицы; (5) содействие заживлению ран; (6) защита тканей и клеток от окислительного повреждения.
Настоящее изобретение далее будет проиллюстрировано при помощи конкретных примеров. Понятно, что эти примеры приведены только для иллюстрации изобретения, а не для того, чтобы ограничить объем изобретения. Экспериментальные способы без особых условий, описанных в следующих примерах, в общем осуществляют в обычных условиях, например в условиях, описанных в Sambrook et al, Molecular Cloning: A Laboratory Manual (New York: Cold Spring Harbor Laboratory Press, 1989), или в соответствии с указаниями производителя. Если не указано иное, то части и проценты рассчитаны по массе. Исходные материалы или реактивы, используемые в изобретении, имеются в продаже.
Пример 1. Конструирование экспрессирующегося вектора pET32b(+)/PRDX6 и pET32b(+)/PRDX2
1.1. Конструирование экспрессирующегося вектора pET32b(+)/PRDX6
Пару специфических праймеров конструировали и синтезировали на основе генной последовательности, кодирующей зрелый белок PRDX6,
Прямой праймер: 5′-tatccatatgcccggaggtctgcttc-3′ (как представлено в SEQ ID NO:5);
Обратный праймер: 5′-ttactcgagaggctggggtgtgtagcg-3′ (как представлено в SEQ ID NO:6);
Сайт действия фермента представлял собой NdeI и XhoI соответственно.
Амплификацию путем RT-PCR (reverse transcription polymerase chain reaction - полимеразная цепная реакция с обратной транскрипцией) осуществляли с использованием мРНК человеческого эпидидимиса, выделенной при помощи обычного способа (или библиотеки кДНК человеческого эпидидимиса, приготовленной в лаборатории) в качестве матрицы. Результаты представлены на Фиг.1. Определили амплифицированный фрагмент 688 п.о., согласующийся с теоретической длиной.
Амплифицированный фрагмент отделяли (искомый фрагмент выделяли из агарозных гелей при помощи набора для экстракции из гелей) и расщепляли при помощи двух ферментов NdeI и XhoI. Затем расщепленный в результате фрагментативного расщепления фрагмент лигировали в экспрессирующий вектор pET32b (+) (имеющийся в продаже от Novagen), расщепленный до линейной формы при помощи NdeI и XhoI. Затем вектор переносили в обычный Е.coli TOP10F′ (имеющийся в продаже от Invitrogen). Положительные клоны подвергали скринингу при помощи ПЦР амплификации колонии и затем секвенировали для дополнительного подтверждения правильности последовательности и экспрессии рамки считывания, таким образом получая рекомбинантную экспрессирующуюся плазмиду pET32b(+)/PRDX6.
Белок PRDX6, экспрессирующийся экспрессирующимся вектором, представлял собой слитой белок PRDX6-His, где восемь аминокислот LEHHHHHH добавлены по C-концу для облегчения выделения и очистки.
1.2. Конструирование экспрессирующегося вектора pET32b(+)/PRDX2
Способ конструирования похож на способ в 1.1, где различие заключалось в том, что использовали следующую пару праймеров:
Прямой праймер: 5′-TATCCATATGGCCTCCGGTAACGCGC-3′ (как представлено в SEQ ID NO:7);
Обратный праймер: 5′-TTACTCGAGATTGTGTTTGGAGAAATATTC-3′ (как представлено в SEQ ID NO:8);
Сайт действия фермента представлял собой NdeI и XhoI соответственно. Получали рекомбинантную экспрессирующуюся плазмиду pET32b(+)/PRDX2.
Пример 2. Экспрессия белка PRDX6 и белка PRDX2
2.1. Экспрессия белка PRDX6
Плазмиду pET32b(+)/PRDX6 использовали для трансформации Е.coli Origami В (DE3) (приобретенной в Novagen). Положительные клоны инокулировали в среде LB (Луриа-Бертани), содержащей 100 мкг/мл ампициллина, и выращивали при встряхивании в течение ночи при 37°С.
На следующие сутки ее переносили в среду LB, содержащую 100 мкг/мл ампициллина (1:100), и выращивали при встряхивании при 37°С. После того как плотность бактерий достигала OD600=0,6-0,8, IPTG (изопропил-бета-D-1-тиогалактопиранозид) добавляли до конечной концентрации 0,4 мМ для того, чтобы вызвать экспрессию требуемого белка PRDX6. Через 3-4 часа бактерии собирали путем центрифугирования.
2.2. Экспрессия белка PRDX2
Экспрессию белка PRDX2 осуществляли с использованием того же самого способа, как в 2.1, где различие заключалось в том, что белок PRDX2 использовали для замены белка PRDX6.
Пример 3. Очистка белка PRDX6 и белка PRDX2
3.1. Очистка белка PRDX6
Бактерии, собранные путем центрифугирования, ресуспендировали в буфере А (20 мМ фосфатный буфер, 150 мМ NaCl, pH 7,2), и разрушали при помощи ультразвука в водяной бане и затем центрифугировали при низкой температуре (4°С) при 20000 g в течение 15 мин. Супернатант отбирали в качестве образцов для очистки.
После того как никелевую аффинную колонку уравновешивали с буфером А, образец наносили на колонку. Затем буфер А, содержащий 50 мМ имидазола, использовали для промывания колонки для удаления примесей белковой природы (пик 1) (смотри Фиг.2). Желаемый белок элюировали буфером А, содержащим 300 мМ имидазола (пик 2) (см. Фиг.2).
Наконец, элюированный белок переносили в буфер А с использованием обессоливающей колонки G-25 для удаления имидазола и обнаруживали при помощи SDS-PAGE электрофореза.
После анализа чистота полученного белка PRDX6 составила больше чем 95%, а молекулярная масса составила приблизительно 26,1 кДа. (см. Фиг.3)
3.2. Очистка белка PRDX2
Белок PRDX2 очищали с использованием того же самого способа 3.1, где различие заключалось в том, что белок PRDX2 использовали вместо белка PRDX6.
Пример 4. Антиоксидантная активность белка PRDX6 (эксперимент окислительного повреждения клеток HEF)
Клетки HEF представляли собой обычные человеческие эмбриональные фибробласты (Zavada et. al., Nature New Biology, 240:124-125 (1972); или US 7811817).
Клетки реактивировали культуральной средой (высокий уровень глюкозы DMEM +5% FBS (фетальная бычья сыворотка), приобретенной в Invitrogen), и выращивали в течение 48 ч.
Когда клетки вырастали до 90% конфлюэнтности, белок PRDX6 (PRDX6-His слитой белок), полученный в Примере 3, добавляли в культуральную систему в соответствии со следующим экспериментальным способом, и затем добавляли H2O2(пероксид водорода). Через 30 мин клеточную жизнеспособность определяли при помощи способа МТТ (3-{4,5-диметилтиазол-2-ил}-2,5-дифенилтетразолий бромид).
Схема эксперимента:
Фактор 1: уровень H2O2 (1 мМ, 0,5 мМ, 0,25 мМ, 0,125 мМ и 0 мМ).
Фактор 2: уровень PRDX6-His (0,5 мг/мл, 0,25 мг/мл, 0,125 мг/мл и 0 мг/мл).
Концентрация H2O2 и PRDX6-His в каждой экспериментальной группе представлена в таблице 1.
Результаты представлены в таблице 1 и Фиг.4.
Группа, в отношении которой использовали H2O2 (0,125 мМ): H2O2, оказывала сильное токсическое действие на клетки. Степень выживания клеток составили лишь 2,47%, когда концентрация H2O2 составила 0,125 мМ. Получающийся в результате вред был больше, когда концентрация H2O2 увеличивалась.
Группа, в отношении которой использовали буфер (20 мМ фосфатный буфер, 150 мМ NaCl, pH 7,2, содержащий 0,5 мг/мл 6×His экспрессирующую концевую последовательность): когда использовали только указанный буфер, тогда степень выживания значительно уменьшалась по сравнению с группой, которой вводили белок PRDX6-HJS (0,5 мг/мл).
Группа, в отношении которой использовали H2O2+PRDX6-His: принимая каждую группу в качестве примера, где концентрация H2O2 составила 0,125 мМ, добавляли белок PRDX6 (0,25 мг/мл, и 0,5 мг/мл), соответственно. Среди них белок 0,25 мг/мл может привести к тому, что клетки HEF до некоторой степени устойчивы к вреду, вызываемому 0,125 мМ H2O2; и 0,5 мг/мл PRDX6 может значительно увеличить степень выживания от приблизительно 2,5% до 65%.
Группа, в отношении которой использовали H2O2 + буфер (тот же самый, как предшествующий): указано, что буфер, содержащий 6×His экспрессирующую концевую последовательность, может не играть защитную роль.
Вышеприведенные результаты демонстрируют, что степень выживания клеток может в значительной степени быть увеличена тогда, когда в системе имеется белок PRDX6-His. Белок PRDX6-His может противостоять повреждению вследствие перекисного окисления со стороны H2O2.
Пример 5. Защита белка PRDX2 и белка PRDX6 на сперме пациентов, страдающих от астенозооспермии
Стадии:
1. Образец спермы отбирали, скорость поступательного движения сперматозоидов (PR)% определяли после разжижения, и отбирали образцы спермы с (PR)% меньше, чем 32% (астенозооспермия).
2. Подвергали флотации в культуральном растворе BWW в течение 1 ч.
3. Сперматозоиды трижды промывали культуральным раствором BWW.
4. Указанные сперматозоиды разделяли на три группы:
Группа - отрицательный контроль (сперматозоиды разбавляли в BWW + буфер (20 мМ фосфатный буфер, 150 мМ NaCl, pH 7,2));
Группа BSA (сперматозоиды разбавляли в BWW + 300 мкг/мл бычьего сывороточного альбумина (BSA, приобретен в Amresco)); и
Белковая группа (сперматозоиды разбавляли в BWW + 300 мкг/мл белка).
5. Параметры движения спермы определяли после инкубирования в течение 2 ч и 4 ч соответственно.
Результаты:
(1) Для образцов спермы, скорость поступательного движения сперматозоидов в которых (PR)% составляла меньше чем 32%, после 2 ч инкубации скорость движения, скорость поступательного движения сперматозоидов, средняя скорость перемещения, прямолинейная скорость и скорость по кривой сперматозоидов в группе с белком HEL-S-2a (т.е. белок PRDX2) были значимо выше, чем в контрольной группе. Скорость движения, скорость поступательного движения сперматозоидов и прямолинейная скорость сперматозоидов в группе с белком HEL-S-2a были значимо выше, чем в группе с BSA. Результаты статистического анализа представлены на Фиг.5.
(2) Для образцов спермы, скорость поступательного движения сперматозоидов в которых (PR)% составляла меньше чем 32%, после 2 ч инкубации скорость движения, скорость поступательного движения сперматозоидов, средняя скорость перемещения, прямолинейная скорость и скорость по кривой сперматозоидов в группе с белком HEL-S-128m (т.е. белок PRDX6) были значимо выше, чем в контрольной группе. Скорость движения, процент подвижных сперматозоидов, средняя скорость перемещения и прямолинейная скорость сперматозоидов в группе с белком HEL-S-128m были значимо выше, чем в группе с BSA. Результаты статистического анализа представлены на Фиг.6.
В способе обработки спермы во вспомогательной репродуктивной технологии in vitro добавление рекомбинантного человеческого белка PRDX2 и белка PRDX6 по настоящему изобретению может увеличить количество подвижных обработанных сперматозоидов, и улучшить качество обработанных сперматозоидов, таким образом, повышая вероятность успешного оплодотворения.
Пример 6. Описание приготовления суппозиториев для лечения бесплодия и способ приготовления
Способ приготовления суппозитория, ингредиенты и их дозы представлены в таблице 2:
1. Подходящее количество этанола добавляли в β-CD при перемешивании, таким образом получая пасту, и белок добавляли и измельчали с образованием включения в течение 45 мин для дальнейшего использования.
2. Полусинтетический фермент жирной кислоты (тип 36) растворяли путем нагревания и выдерживали при 38°С, добавляли включение основного активного вещества, полностью смешивали при поддержании температуры.
3. Гомогенную смесь выливали и охлаждали для формирования в пленку.
Пример 7. Описание приготовления криопротекторов спермы и их защитное действие
7.1. Описание приготовления криопротекторов спермы
В каждых 100 мл криопротектора спермы содержались:
белок PRDX6 500 мг, белок PRDX2 500 мг, KCl 0,54 ммоль/л,
NaCl 10,0 ммоль/л, MgSO4 0,05 ммоль/л, NaH2PO4 0,03 ммоль/л,
NaHCO3 10 ммоль/л, глюкоза 205,4 ммоль/л, глицин 13,0 ммоль/л,
сахароза 5,0 ммоль/л, HEPES 2,5 ммоль/л, глицерин 14% (об/об).
Основную композицию готовили с бидистиллированной водой, доводили рН до 7,4, и фильтровали для удаления бактерий через 0,22 мкм стерильный фильтр.
7.2. Сравнение защитного действия криопротекторов спермы по настоящему изобретению с действием имеющихся в продаже продуктов.
7.2.1. Материалы
Образцы спермы предоставлены 20 здоровыми, находящимися в браке и в возрасте от 30 до 35 лет добровольцами, имеющими детей. Добровольцев включали в настоящее исследование после урологического исследования и проверки спермы на нормальность.
7.2.2. Способы
Больше чем 2 мл спермы собирали у каждого добровольца и разделяли на 3 части.
Одна из них предназначалась для проверки предварительно замороженной спермы на нормальность и определение SPA;
Оставшиеся 2 части замораживали с криопротектором в соответствии с Примером 7 по настоящему изобретению и имеющимся в продаже продуктом соответственно и размораживали через 6 месяцев. Проводили проверку спермы на нормальность и определение SPA.
7.2.3 Результаты представлены в таблице 3.
Криопротектор по настоящему изобретению значимо превосходит имеющийся в продаже криопротектор в отношении скорости восстановления спермы и скорости проникновения сперматозоидов (SPA) (P<0,01).
Пример 8. Терапевтический эффект активных фрагментов
Пример 5 и 7 повторяли, где различие заключалось в том, что активный фрагмент Prx-6, располагающийся в позициях с 5 по 169 в SEQ ID NO:2, использовали вместо полноразмерного белка Prx-6, представленного в SEQ ID NO:2, и активный фрагмент Prx-2, представленный в позициях с 6 по 164 в SEQ ID NO:4, использовали вместо полноразмерного белка Prx-2, представленного в SEQ ID NO:4.
Результаты продемонстрировали, что вышеприведенные фрагменты оказывают защитное действие на сперматозоиды у пациентов, страдающих от астенозооспермии, и могут значимо улучшить качество обработанных сперматозоидов, таким образом повышая вероятность оплодотворения, причем терапевтическое действие эквивалентно терапевтическому действию полноразмерного Prx-6 и Prx-2. Вышеприведенные фрагменты также могут служить в качестве криопротекторов спермы и значимо улучшать скорость восстановления спермы и скорость проникновения сперматозоидов.
Пример 9. Терапевтическое действие белка Prx-6 на повреждения роговицы
9.1. Животный источник: 6-недельные крысы SD, приобретенные в Experimental Animal Center of Yantai Yuhuangding Hospital.
9.2. Лекарственные средства: экспериментальная группа: белок Prx-6, полученный в Примере 3; контрольная группа: нормальный физиологический раствор.
9.3. Приготовление модели повреждения роговицы
5% хлоралгидрат (7 мл/кг массы организма) инъецировали в энтероцель. Глазные капли тропикамидум и неосинефрин использовали в качестве мидриатического средства после анестезии каждые 2 мин и по 1 капле каждый раз. После 20 мин мидриатический агент на роговице и конъюнктиве осторожно отбирали ватным тампоном после мидриаз. Крысу подвергали излучению 300 нм УФ-лампой и фиксировали в соответствии с относительной позиционной высотой УФ-лампы, и излучение измеряли при помощи детектора УФ излучения, контролируемого при 1×103 мкВт/см2. Общая суточная доза излучения составила 9 кДж/м2, в течение 3 последовательных суток, таким образом, получая модель повреждения роговицы у крыс. Микроскоп с щелевой лампой использовали в исследованиях.
9.4. Способ обработки
Эксперименты включали контрольную группу (которой капали нормальный физиологический раствор), группу, обрабатываемую белком Prx-6 (капали 2 мг/мл белка Prx-6). Через двое суток после повреждения роговицы начинали обработку, 4 раза в сутки и каждый раз капая по 2 капли (приблизительно 30 мкл) в глаз крысы.
9.5. Результат эксперимента
Через двое суток после УФ излучения на роговице крыс образовывался отек, и прозрачность очевидно уменьшалась. На четвертые сутки обработки наблюдалась значительная реваскуляризация в роговице в контрольной группе и имелся сильный воспалительный ответ, тогда как лишь небольшая реваскуляризация в роговице отмечена в группе, обрабатываемой белком Prx-6, и отек значительно уменьшался; на восьмые сутки обработки отек в роговице в контрольной группе слегка уменьшился и прозрачность частично восстановилась, тогда как прозрачность роговицы в группе, которую обрабатывали белком Prx-6, по большей части восстановилась; на двенадцатые сутки обработки прозрачность роговицы в контрольной группе восстановилась не полностью, тогда как роговица крыс в группе, обработанной белком Prx-6, почти полностью восстановилась, и отек устранился (Фиг.7) (замечание: слева направо изображения: контрольная группа(2 крысы); группа, обработанная Prx-6 (2 крысы)).
Пример 10. Анализ активности PRDX2 и PRDX6
Перекись водорода обладает сильным поглощением при длине волны 240 нм, которое пропорционально концентрации (А240 нм × 22,94 = концентрация перекиси водорода мМ). И PRDX6, и PRDX2 способны разрушать перекись водорода, таким образом, что поглощение (А240 нм) реакционного раствора уменьшается с течением времени реакции.
Протокол эксперимента: 10 мМ перекись водорода готовили с буфером (20 мМ фосфатный буфер, 150 мМ NaCl, pH 7,2). 500 мкл отбирали и добавляли 10 мкл белка (количественно определенного при помощи способа ВСА (бицинхониновая кислота)), и приводили во взаимодействие при 25°С в течение 20 мин. Количество потребленной перекиси водорода рассчитывали путем измерения разницы в поглощении до и после реакции, таким образом, для расчета количества перекиси водорода (нмоль), потребленной на 1 мкг белка в течение 1 мин, т.е. нмоль/мин/мкг, таким образом, оценивая активность PRDX6 или PRDX2.
Результаты экспериментов PRDX6 представлены в таблице 4 и продемонстрируют, что активность PRDX6 по настоящему изобретению достигла больше чем 1 нмоль/мин/мкг.
трация белка
ствия А240, нм
ствия А240, нм
Результаты для PRDX6 также продемонстрировали, что активность PRDX2 может достигать значений больших чем 1 нмоль/мин/мкг.
Все литературные источники, приведенные в настоящей заявке на изобретение, указаны здесь в виде ссылок, таким образом, как если бы они были включены путем ссылки индивидуально. Дополнительно, понятно, что после прочтения вышеприведенного описания специалист в данной области техники может произвести множество изменений и модификаций, и эти эквиваленты также находятся в объеме изобретения, определяемом его формулой.





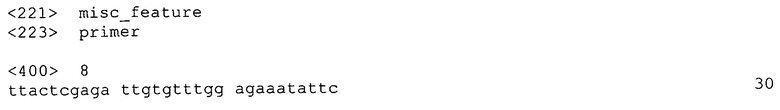
Изобретение относится к биотехнологии и представляет собой применение оксидоредуктазы перекиси водорода для получения фармацевтической композиции для улучшения качества спермы или лечения мужского бесплодия, где оксидоредуктаза перекиси водорода представляет собой белок PRDX2. Изобретение относится также к композиции для улучшения качества спермы или лечения мужского бесплодия, содержащей белок PRDX2 и фармацевтически приемлемый носитель. Изобретение позволяет эффективно улучшить качество спермы или эффетивно лечить мужское бесплодие пациента, страдающего от астеноспермии. 3 н. и 11 з.п. ф-лы, 7 ил., 4 табл., 10 пр.
1. Применение оксидоредуктазы перекиси водорода для получения фармацевтической композиции для улучшения качества спермы или лечения мужского бесплодия, где оксидоредуктаза перекиси водорода представляет собой белок PRDX2.
2. Применение по п. 1, где фармацевтическую композицию применяют в качестве криопротектора сперматозоидов.
3. Применение по п. 1, где белок PRDX2 представляет собой белок PRDX2 млекопитающего или его активные фрагменты или производные.
4. Применение по п. 1, где белок PRDX2 включает белок, аминокислотная последовательность которого представлена SEQ ID NO: 4, или фрагмент, представленный SEQ ID NO: 4 в позициях с 6 по 164, или его слитой белок, образованный с экспрессионной последовательностью.
5. Композиция для улучшения качества спермы или лечения мужского бесплодия, содержащая
(а) белок PRDX2; и
(б) фармацевтически приемлемый носитель.
6. Композиция по п. 5, где белок PRDX2 представляет собой белок PRDX2 млекопитающего или его активные фрагменты или производные.
7. Композиция по п. 6, где белок PRDX2 включает белок, аминокислотная последовательность которого представлена SEQ ID NO: 4, или фрагмент, представленный SEQ ID NO: 4 в позициях с 6 по 164, или его слитой белок, образованный с экспрессионной последовательностью.
8. Композиция по п. 5, где композиция дополнительно содержит белок PRDX6.
9. Композиция по п. 8, где белок PRDX6 представляет собой белок PRDX6 млекопитающего или его активные фрагменты или производные.
10. Композиция по п.9, где белок PRDX6 включает белок, аминокислотная последовательность которого представлена SEQ ID NO: 2, или фрагмент, представленный SEQ ID NO: 2 в позициях с 5 по 169, или его слитой белок, образованный с экспрессионной последовательностью.
11. Композиция по любому из пп. 5-10, где композиция представляет собой фармацевтическую или медицинскую композицию.
12. Композиция по любому из пп. 5-11, где композиция представляет собой криопротектор сперматозоидов.
13. Композиция по п. 12, где в каждых 100 мл криопротектора сперматозоидов криопротектор спермы включает:
белок PRDX6 500 мг, белок PRDX2 500 мг, KCl 0,54 ммоль/л,
NaCl 10,0 ммоль/л, MgSO4 0,05 ммоль/л, NaH2PO4 0,03 ммоль/л,
NаНСО3 10 ммоль/л, глюкоза 205,4 ммоль/л, глицин 13,0 ммоль/л,
сахароза 5,0 ммоль/л, HEPES 2,5 ммоль/л, глицерин 14% (об/об);
и криопротектор сперматозоидов готовят с бидистиллированной водой, доводят pH до 7,4 и фильтруют для удаления бактерий через 0,22 мкм стерильный фильтр.
14. Способ улучшения качества спермы или лечения мужского бесплодия, при котором осуществляют введение (1) белка PRDX2 и, возможно, белка PRDX6, или (2) композиции по п.5 пациенту, страдающему от астеноспермии.
| Транспортный рефрижератор для пищевых продуктов | 1988 |
|
SU1566182A1 |
| LI J | |||
| et.al | |||
| Systematic mapping and functional analysis of a family of human epididymal secretory sperm-located proteins, Mol Cell Proteomics | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| КАЛИНИНА E.B | |||
| и др | |||
| Участие тио-,перокси- и глутаредоксинов в клеточных | |||
Авторы
Даты
2016-01-27—Публикация
2012-05-23—Подача