ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение связано с новыми производными человеческого фактора VII свертывания крови, полипептидами фактора VII, а также полинуклеотидными конструкциями, кодирующими такие полипептиды, векторами и хозяйскими клетками, содержащими и экспрессирующими эти полинуклеотиды, фармацевтическими композициями, содержащими производные фактора VII, применениями и способами лечения.
ОСНОВА СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Свертывание крови представляет собой процесс, состоящий из комплексного взаимодействия различных компонентов (или факторов) крови, которые в конечном счете способствуют образованию фибринового сгустка. Обычно компоненты крови, которые участвуют в том, что принято называть "каскадом" свертывания, представляют собой ферментативно неактивные протеины (проферменты или зимогены), которые превращаются в протеолитические ферменты под действием активатора (который, в свою очередь, является фактором свертывания). Факторы свертывания, которые подверглись такому превращению, обычно называют "активными факторами", и для их обозначения обычно добавляют букву "a" к названию фактора свертывания (например, фактор VIIa).
Инициация гемостатического процесса опосредована образованием комплекса между тканевым фактором, экспонированным в результате повреждения сосудистой стенки, и фактором VIIa. Затем под действием этого комплекса происходит превращение факторов IX и X в их активные формы. Фактор Xa способствует превращению ограниченных количеств протромбина в тромбин на клетках, несущих тканевый фактор. Тромбин активирует тромбоциты и факторы V и VIII, превращая их в факторы Va и VIIIa, оба из которых являются кофакторами в дальнейшем процессе, ведущем к полному тромбиновому взрыву. Такой процесс включает в себя выработку фактора Xa под действием фактора IXa (в комплексе с фактором VIIIa) и возникает он на поверхности активированных тромбоцитов. В заключение тромбин способствует превращению фибириногена в фибрин, что приводит к образованию фибринового сгустка.
Фактор VII представляет собой следовой гликопротеин плазмы, который циркулирует в крови в виде одноцепочечного зимогена. Этот зимоген является каталитически неактивным. Одноцепочечный фактор VII может быть превращен в двухцепочечный фактор VIIa под действием фактора Xa, фактора XIIa, фактора IXa, фактора VIIa или тромбина in vitro. Фактор Xa, по-видимому, является основным физиологическим активатором фактора VII. Превращение зимогенного фактора VII в активированную двухцепочечную молекулу происходит при расщеплении внутренней пептидной связи Arg152-Ile153.
Зачастую бывает необходимо стимулировать или селективно блокировать у субъекта каскад свертывания крови. Фактор VIIa используется для осуществления контроля нарушений, связанных с кровотечением, которые вызваны рядом причин, таких как дефициты факторов свертывания (например, при гемофилии A и B или дефиците факторов свертывания XI или VII) или ингибиторы факторов свертывания. Фактор VIIa используется также для контролирования избыточного кровотечения, возникающего у субъекта с нормально функционирующим каскадом свертывания (отсутствие дефицитов факторов свертывания или ингибиторов какого бы то ни было из факторов свертывания крови). Такое кровотечение может, например, быть вызвано дефектом функционирования тромбоцитов, тромбоцитопенией или болезнью фон Виллебранда. Кровотечение представляет собой серьезную проблему в связи с хирургическими вмешательствами и иными формами повреждения тканей.
Европейский патент No. 200,421 (ZymoGenetics) связан с нуклеотидной последовательностью, кодирующей человеческий фактор VII, и рекомбинантной экспрессией фактора VII в клетках млекопитающих.
Публикация Dickinson et al. (Proc. Natl. Acad. Sci. USA 93,14379-14384,1996) связана с полипептидами фактора VII, в которых Lys157, Val158, Glu296, Met298, Asp334, Ser336 или Lys337 индивидуально заменена на Ala. Публикация Iwanaga et al. (Thromb. Haemost (supplement august 1999), 466, abstract 1474) связана с вариантами фактора VIIa, в котором имеет место делеция остатков 316-320 или в котором остатки 311-322 заменены соответствующими остатками из трипсина.
Антикоагулянты, такие как гепарин, кумарин, производные кумарина, производные индандиона или другие агенты, могут быть использованы для селективного блокирования каскада свертывания у пациента, например, в процессе почечного диализа или при лечении тромбоза глубоких вен, диссеминированного внутрисосудистого свертывания (DIC), а также при других медицинских нарушениях. Например, лечение гепарином или экстракорпоральная обработка цитратным ионом (Патент США No. 4,500,309) могут быть использованы при диализе для предотвращения свертывания в процессе проведения лечения. Гепарин также используется для предупреждения тромбоза глубоких вен у больных, подвергающихся оперативному вмешательству.
Однако лечение гепарином и другими антикоагулянтами может вызвать нежелательные побочные эффекты. Доступные антикоагулянты обычно проявляют свое действие во всем организме, а не специфически в сайте образования сгустка. Гепарин, например, может вызвать тяжелое кровотечение. Кроме того, имея время полужизни приблизительно 80 минут, гепарин быстро выводится из крови, что вызывает необходимость частых введений. Поскольку гепарин действует как кофактор для антитромбина III (AT III), а AT III быстро истощается при лечении DIC, зачастую трудно установить правильную дозу гепарина, необходимую для непрерывного мониторинга AT III и уровней гепарина. Гепарин также является неэффективным при экстремальном истощении AT III. Кроме того, длительное применение гепарина может также усилить агрегацию тромбоцитов и уменьшить число тромбоцитов, он также участвует в развитии остеопороза. Производные индандиона могут также вызывать токсические побочные эффекты.
Вдобавок к антикоагулянтам, кратко описанным выше, было обнаружено, что целый ряд природно образующихся белков обладает противосвертывающей активностью. Например, Reutelingsperger (U. S. Pat. No. 4,736,018) выделил антикоагулянтные белки из аорты быка и пуповинных артерий человека. В публикации Maki et al. (U. S. Pat. No. 4,732,891) описаны антикоагулянтные белки, полученные из плаценты человека. Кроме того, AT III был предложен в качестве лечебного антикоагулянта (Schipper et al., Lancet 1 (8069): 854-856 (1978); Jordan, U. S. Pat. No. 4,386,025; Bock et al., U. S. Pat. No. 4,517,294).
Приблизительно у 30% или более пациентов, подвергнутых ангиопластике, эндартерэктомии или обходному сосудистому шунту, тромбоз и/или пролиферация клеток гладких мышц в интиме вызывают ре-окклюзию сосуда и, как следствие этого, невозможность реконструктивной хирургии. Такое закрытие сосуда вследствие операции известно под названием рестеноза. Происхождение явления рестеноза связывают с комплексным взаимодействием биологических процессов, включая отложение тромбоцитов и тромбообразование, высвобождение хемотаксических и митогенных факторов, а также миграцию и пролиферацию клеток гладкой мускулатуры сосудов в интиме расширенного артериального сегмента.
Ингибирование аккумуляции тромбоцитов в сайтах механического повреждения может ограничивать скорость рестеноза у человека. В то время как в сайтах острого сосудистого повреждения происходит накопление тромбоцитов, выработка тромбина в этих сайтах может быть ответственна за активацию тромбоцитов и их последующее накопление.
Международная заявка No. WO 92/15686 связана с инактивированным фактором VIIa, полинуклеиновой кислотой и с линиями клеток млекопитающих, продуцирующих инактивированный фактор VIIa, а также с композициями, содержащими инактивированный фактор VIIa, для ингибирования свертывания крови.
Международная заявка No. WO 94/27631 связана со способами ингибирования рестеноза сосудов, активности тканевого фактора и отложения тромбоцитов.
Международная заявка No. WO 96/12800 связана со способом лечения острого закрытия коронарной артерии, включающим в себя введение пациенту композиции, которая содержит инактивированный фактор VIIa в сочетании с тканевым активатором плазминогена или стрептокиназой.
Большинство белков, поступающих в круг кровообращения, из организма млекопитающих быстро выводится почками. Эту проблему можно частично обойти путем введения большого количества белка или же путем повторных введений. Однако более высокие дозы белка могут вызвать образование антител, которые могут связывать и инактивировать белок и/или облегчать клиренс белка из организма пациента. Повторное введение белка в терапевтических целях в основном неэффективно и может оказаться опасным, так как это может вызвать аллергическую реакцию.
Различные попытки разрешить проблемы, связанные с белковой терапией, включают в себя микроинкапсулирование, липосомные системы доставки, введение слитых белков и химическую модификацию. Наиболее многообещающим из них на сегодняшний день является модификация терапевтического белка путем ковалентного прикрепления полимеров полиалкиленоксида, в частности, полиэтиленгликолей (ПЭГ). Например, в патенте США No. 4,179,337 описано применение ПЭГ или пропиленгликоля, связанного с белками, для обеспечения физиологически активной неиммуногенной водорастворимой полипептидной композиции. У Nucci et al. описано несколько белков, которые были модифицированы путем добавления ПЭГ, включая аденозиндезаминазу, L-аспарагиназу, интерферон-альфа-2b (IFN-α2b), супероксиддисмутазу, стрептокиназу, тканевый активатор плазминогена (tPA), урокиназу, уриказу, гемоглобин, интерлейкины, интерфероны, TGF-бета, EGF и другие факторы роста (Nucci et al., 1991, Adv. Drug Delivery Rev. 4: 133-151). Результатом таких попыток стало некоторое удлинение времени полужизни этих белков и уменьшение иммуногенности этих белков.
Обычно ПЭГилирование белков включает в себя активацию ПЭГ функциональными группами, которые будут реагировать с лизиновыми остатками на поверхности белка. Если белок полностью модифицирован, активность белка обычно утрачивается. Модификационные процедуры, которые дают возможность частичного ПЭГилирования белка, обычно приводят к потере активности приблизительно только на 50% и существенному увеличению времени его полужизни в сыворотке, так что суммарная эффективная доза белка уменьшается.
Современное развитие методов ПЭГилирования белков связано с использованием активированных ПЭГ-реагентов, которые взаимодействуют с тиоловыми группами белков, что приводит в результате к ковалентному связыванию ПЭГ с цистеином, который встроен вместо природно образующегося лизина в белке. У Shaw et al. (Патент США No. 5,166,322) описаны специфические варианты IL-3, которые содержат цистеин, встроенный в специфические сайты внутри природно образующейся аминокислотной последовательности. Затем сульфгидрильные реактивные соединения (например, активированный полиэтиленгликоль) прикрепляются к указанным цистеинам в результате реакции с конкретным вариантом IL-3. У Katre et al. (Патент США No. 5,206,344) описаны специфические варианты IL-2, которые содержат цистеин, встроенный в специфические сайты внутри природно образующейся аминокислотной последовательности. В дальнейшем конкретный вариант IL-2 реагирует с активированным полиэтиленгликолевым реагентом, прикрепляя этот фрагмент к цистеину.
В данной области техники все еще существует потребность в улучшенных полипептидах фактора VII, имеющих пролонгированную прокоагулянтную или антикоагулянтную активность. В частности, существует потребность в полипептидах фактора VII, которые имели бы увеличенное время полужизни в сыворотке без нежелательных побочных эффектов, таких как системная активация системы свертывания и кровотечения, соответственно, ассоциированные с традиционной терапией, и которые можно было бы вводить в относительно низких дозах, с тем, чтобы избежать введения более массивных доз белка.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение связано с новыми полипептидами фактора VII свертывания крови, имеющими такую же самую или повышенную активность по сравнению с фактором VIIa дикого типа и с производными фактора VII, имеющими повышенные времена полужизни в сыворотке.
Были идентифицированы области в молекуле фактора VIIa, в которых могут быть произведены изменения в первичной структуре, а также другие модификации, которые не вызывают изменения или снижения биологической активности фактора VIIa. Области внутри структуры фактора VIIa, которые были идентифицированы как неучаствующие в связывании с тканевым фактором или с фактором X, включая аминокислоты в положениях 247-260, а также от 393 до 406 положений в последовательности SEQ ID NO: 1. В частности, аминокислоты в положениях Q250, R396 и P406 последовательности SEQ ID NO: 1 были изучены с точки зрения включения цистеина (Cys). Включение цистеиновых остатков сопровождалось конъюгацией с химической группой, например, полиэтиленгликолем (ПЭГ), с тем, чтобы увеличить время полужизни производного фактора VII в циркуляции. Цистеин вводили в C-концевую последовательность SEQ ID NO: 1 (обозначается как 407C), что сопровождалось конъюгацией с полиэтиленгликолем. Кроме того, такое добавление цистеина в C-концевую последовательность SEQ ID NO: 1 не сопровождается снижением протеолитической активности полипептидов фактора VIIa. Указанные производные фактора VII, например полипептид фактора VII, конъюгированный с молекулой ПЭГ, являются терапевтически применимыми в ситуациях, когда желательно пролонгированное действие полипептидов фактора VII, например, в ситуациях, когда повторное введение или же введение большего количества полипептида фактора VII является нежелательным или проблематичным. Кроме того, полипептиды фактора VIIa согласно изобретению со встроенными аминокислотами (например, остатком цистеина), способными конъюгировать с химической группой в положениях молекулы фактора VIIa, которые не влияют на протеолитическую активность, могут быть использованы для встраивания любой функциональной группы конъюгата фактора VII.
В первом аспекте, настоящее изобретение связано с полипептидом фактора VII, содержащим аминокислотную последовательность SEQ ID NO: 1 или ее варианты, где аминокислота заменена другой аминокислотой, где другая аминокислота способна конъюгировать с химической группой и где полипептид фактора VII по существу имеет такую же или более высокую активность по сравнению с активностью рекомбинантного человеческого фактора VIIa дикого типа.
Во втором аспекте, настоящее изобретение связано с полипептидом фактора VII, содержащим аминокислотную последовательность SEQ ID NO: 1 или ее варианты, где аминокислота, соответствующая аминокислоте в положении, выбранном из 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой. Следует понимать, что любая аминокислота в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, может быть заменена другой аминокислотой без существенного снижения активности полипептида фактора VII.
В третьем аспекте, настоящее изобретение связано с полипептидом фактора VII, содержащим аминокислотную последовательность SEQ ID NO: 1 или ее варианты, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой. Следует понимать, что первая буква в обозначениях R396, Q250 и P406 представляет собой аминокислоту, встречающуюся в указанном положении в природном варианте последовательности SEQ ID NO: 1.
В другом аспекте, изобретение связано с полипептидом фактора VII, содержащим аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота способна к конъюгации с химической группой, встроенной внутри последовательности SEQ ID NO: 1 или ее варианта в положении, где полипептид фактора VII обладает по существу такой же или более высокой активностью по сравнению с активностью рекомбинантного человеческого фактора VIIa дикого типа. Подразумевается, что аминокислота может быть встроена внутрь последовательности SEQ ID NO: 1 и без замены какой-либо аминокислоты. Вставка аминокислоты может быть осуществлена в том же положении внутри последовательности SEQ ID NO: 1, где в дальнейшем будет произведена аминокислотная замена. Таким образом, в одном из воплощений, за вставкой будет следовать аминокислотная замена, или наоборот.
В другом аспекте, изобретение связано с полипептидом фактора VII, содержащим аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота способна к конъюгации с химической группой, добавленной к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта.
Термин "аминокислота", используемый в настоящем описании, означает одну или более аминокислот. Подразумевается, что аминокислота, заменяющая аминокислоту в полипептиде фактора VII или встроенная в этот полипептид, или же добавленная к полипептиду фактора VII, способна к конъюгации с любой химической группой, которая будет способствовать повышению истинной молекулярной массы полипептида фактора VII. Такая конъюгация с химической группой включает в себя, но не ограничивается ковалентным прикреплением полиэтиленгликоля (ПЭГ), монометокси-полиэтиленгликоля, декстрана, поли-(N-винилпирролидон)полиэтиленгликоля, гомополимеров пропиленгликоля, сополимера полипропиленоксида/этиленоксида, полипропиленгликоля, полиоксиэтилированных полиолов (например, глицерина) и поливинилового спирта, коломиновых кислот или других полимеров на основе углеводов, аминокислотных полимеров и биотиновых производных.
Предпочтительной химической группой является биосовместимый, нетоксичный, неиммуногенный и водорастворимый полимер. Предпочтительно химической группой является любой водорастворимый полимер в любых пропорциях.
Такая аминокислотная замена, вставка или добавка и конъюгирование с химической группой происходит без существенного снижения прокоагулянтной активности активированной формы производного фактора VII по сравнению с активностью рекомбинантного человеческого фактора VIIa дикого типа.
Используемый здесь термин "полипептид фактора VII" означает любой протеин, содержащий аминокислотную последовательность 1-406 нативного человеческого фактора VII (SEQ ID NO: 1) или его вариантов. Сюда включены, не ограничиваясь ими, человеческий фактор VII, человеческий фактор VIIa и их варианты.
Используемый здесь термин "фактор VII", или "FVII", означает продукт, состоящий из неактивированной формы (фактор VII). Используемый здесь термин "фактор VIIa", или "FVIIa", означает продукт, состоящий из активированной формы (фактор VIIa). Сюда включены белки, которые имеют аминокислотную последовательность 1-406 нативного человеческого фактора VII или фактора Factor VIIa. Сюда включаются также и белки со слегка модифицированной аминокислотной последовательностью, например, модифицированным N-концом, включая N-концевые аминокислотные делеции или добавки, такие, что образующиеся белки в существенной степени сохраняют активность фактора VIIa. В рамках приведенного выше определения, термин "фактор VII" или "фактор VIIa" также включает в себя природные аллельные варианты, которые могут существовать и возникать у того или иного индивидуума. Могут варьировать также степень и локализация гликозилирования или других посттрансляционных модификаций, в зависимости от того, какие выбраны хозяйские клетки, а также от природы клеточного окружения клеток-хозяев.
Под используемыми здесь терминами "вариант" или " варианты" подразумевается человеческий фактор VII, имеющий последовательность SEQ ID NO: 1, где одна или более аминокислот родительского белка заменены другой аминокислотой и/или где одна или более аминокислот родительского белка подвергнуты делеции и/или где одна или более аминокислот вставлены в родительский белок и/или одна или более аминокислот добавлены к родительскому белку. Такая добавка может иметь место либо на N-конце, либо на C-конце родительского белка, либо на них обоих.
Под термином "по существу такая же или более высокая активность по сравнению с активностью рекомбинантного человеческого фактора VIIa дикого типа" здесь подразумевается активность, составляющая более чем 70% активности рекомбинантного человеческого фактора VIIa дикого типа. В одном воплощении, указанная активность составляет более чем 80% активности рекомбинантного человеческого фактора VIIa дикого типа. В другом воплощении, указанная активность составляет более чем 90% активности рекомбинантного человеческого фактора VIIa дикого типа. Еще в одном воплощении, указанная активность составляет более чем 100% активности рекомбинантного человеческого фактора VIIa дикого типа. Еще в одном воплощении, эта активность составляет более чем 120% активности рекомбинантного человеческого фактора VIIa дикого типа. В другом воплощении, эта активность составляет более чем 200% активности рекомбинантного человеческого фактора VIIa дикого типа. В другом воплощении, эта активность составляет более чем 400% активности рекомбинантного человеческого фактора VIIa дикого типа.
Под термином "производное фактора VII" здесь подразумевается полипептид фактора VII, имеющий последовательность SEQ ID NO: 1 или ее вариант, где одна или более аминокислот родительского белка химически модифицированы, например, путем алкилирования, ПЭГилирования, ацилирования, образования сложного эфира или образования амида и пр. Это включает в себя, не ограничиваясь этим, ПЭГилированный человеческий фактор VIIa, цистеин-ПЭГилированный человеческий фактор VIIa и его варианты.
Под термином "ПЭГилированный человеческий фактор VIIa" подразумевается фактор VIIa, имеющий молекулу полиэтиленгликоля, конъюгированную с аминокислотой полипептида человеческого фактора VIIa.
Под термином "цистеин-ПЭГилированный человеческий фактор VIIa" подразумевается фактор VIIa, имеющий молекулу полиэтиленгликоля, конъюгированную с сульфгидрильной группой цистеина, встроенного в человеческий фактор VIIa.
Под термином "другая аминокислота" подразумевается одна или более аминокислот, которые отличны от той аминокислоты, которая в природе встречается в данном положении. Это подразумевает, не ограничиваясь ими, аминокислоты, которые могут быть кодированы полинуклеотидом. Предпочтительно другая аминокислота представляет собой природную L-форму и может кодироваться полинуклеотидом. Специфическим примером может служить L-цистеин (Cys).
Под термином "активность" здесь подразумевается способность полипептида фактора VII превращать его субстрат, фактор X, в активный фактор Xa. Активность полипептида фактора VII может быть измерена путем "анализа протеолиза in Vitro" (см. Пример 6).
Под термином "полиэтиленгликоль", или "PEG", подразумевается соединение полиэтиленгликоля или его производное, в присутствии или в отсутствие связывающих агентов, связывающих или активирующих фрагментов (например, в присутствии тиола, трифлата, трезилата, азирдина, оксирана или предпочтительно в присутствии малеимидного фрагмента). Соединения, такие как малеимидо-монометокси-ПЭГ, являются примерами активированных соединений полиэтиленгликоля согласно изобретению.
В другом аспекте, настоящее изобретение связано с производным фактора VII, содержащим полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее варианты, где аминокислота заменена другой аминокислотой, где указанная другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII с 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
Под термином "химическая группа" здесь подразумевается одна или более химических групп.
В другом аспекте, данное изобретение связано с производным фактора VII, содержащим полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее варианты, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII с 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, данное изобретение связано с производным фактора VII, содержащим полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, данное изобретение связано с производным фактора VII, содержащим полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота встроена в последовательность SEQ ID NO: 1 или ее вариант и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
Еще в одном аспекте, изобретение связано с производным фактора VII, содержащим полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, изобретение связано с композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, изобретение связано с композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100,000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, изобретение связано с композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100,000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, изобретение связано с композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота вставлена в последовательность SEQ ID NO: 1 или ее вариант, и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, изобретение связано с композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, изобретение связано с фармацевтической композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, изобретение связано с фармацевтической композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, изобретение связано с фармацевтической композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, изобретение связано с фармацевтической композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота вставлена в последовательность SEQ ID NO: 1 или ее вариант, и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, изобретение связано с фармацевтической композицией, содержащей производное фактора VII, содержащее полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта, и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, изобретение связано с полипептидом инактивированного фактора VII, где полипептид фактора VII дополнительно модифицирован в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX. В одном воплощении, полипептид инактивированного фактора VII модифицирован в своем каталитическом центре ингибитором сериновой протеиназы. В другом воплощении, полипептид инактивированного фактора VII модифицирован в своем каталитическом центре галометилкетоновым пептидом, выбранным из группы, состоящей из Phe-Phe-Arg-хлорметилкетона, Phe-Phe-Arg-хлорметилкетона, D-Phe-Phe-Arg-хлорметилкетона, D-Phe-Phe-Arg-хлорметилкетона, Phe-Pro-Arg-хлорметилкетона, D-Phe-Pro-Arg-хлорметилкетона, Phe-Pro-Arg-хлорметилкетона, D-Phe-Pro-Arg- хлорметилкетона, L-Glu-Gly-Arg-хлорметилкетона и D-Glu-Gly-Arg- хлорметилкетона, Dansyl-Phe-Phe-Arg-хлорметилкетона, Dansyl-Phe-Phe-Arg-хлорметилкетона, Dansyl-D-Phe-Phe-Arg-хлорметилкетона, Dansyl-D-Phe-Phe-Arg-хлорметилкетона, Dansyl-Phe-Pro-Arg-хлорметилкетона, Dansyl-D-Phe-Pro-Arg-хлорметилкетона, Dansyl-Phe-Pro-Arg-хлорметилкетона, Dansyl-D-Phe-Pro-Arg-хлорметилкетона, Dansyl-L-Glu-Gly-Arg-хлорметилкетона и Dansyl-D-Glu-Gly-Arg-хлорметилкетона.
Термин "полипептид инактивированного фактора VII", используемый в данном описании, означает полипептид фактора VII, не способный активировать плазменный фактор X или IX.
В другом аспекте, изобретение связано с производным инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, изобретение связано с производным инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота может быть конъюгирована с химической группой и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа и имеет модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, изобретение связано с производным инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, изобретение связано с производным инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, изобретение связано с производным инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, которая способна конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа и имеет модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, изобретение связано с производным инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, которая способна конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, настоящее изобретение связано с композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, настоящее изобретение связано с композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа и имеет модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, настоящее изобретение связано с композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, настоящее изобретение связано с композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, настоящее изобретение связано с композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, которая способна конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или вариант этой последовательности в положении, где полипептид фактора VII имеет по существу такую же активность или повышенную активность по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, настоящее изобретение связано с композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, которая способна конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или варианта этой последовательности, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон.
В другом аспекте, настоящее изобретение связано с композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, изобретение связано с фармацевтической композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, настоящее изобретение связано с фармацевтической композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, настоящее изобретение связано с фармацевтической композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, настоящее изобретение связано с фармацевтической композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, которая способна конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или вариант этой последовательности в положении, где полипептид фактора VII имеет по существу такую же активность или повышенную активность по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и имеющий модификацию в своем каталитическом центре, причем эта модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, настоящее изобретение связано с фармацевтической композицией, содержащей производное инактивированного фактора VII, где полипептид инактивированного фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, которая способна конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или варианта этой последовательности, и имеющий модификацию в своем каталитическом центре, причем эта модификация ингибирует способность полипептида фактора VII активировать плазменный фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу инактивированного полипептида фактора VII в 300 Дальтон приблизительно до 100000 Дальтон; и, необязательно, фармацевтически приемлемый носитель.
В другом аспекте, настоящее изобретение связано с полинуклеотидной конструкцией, кодирующей полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII имеет по существу такую же активность или повышенную активность по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, настоящее изобретение связано с полинуклеотидной конструкцией, кодирующей полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом аспекте, настоящее изобретение связано с полинуклеотидной конструкцией, кодирующей полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом аспекте, данное изобретение связано с полинуклеотидной конструкцией, кодирующей полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII имеет по существу такую же активность или повышенную активность по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, данное изобретение связано с полинуклеотидной конструкцией, кодирующей полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту.
В одном из аспектов полинуклеотидная конструкция представляет собой вектор.
Термин "полинуклеотид" означает одно- или двухцепочечный полимер дезоксирибонуклеотидных или рибонуклеотидных оснований, считываемых от 5'-конца к 3'-концу. Полинуклеотиды включают в себя РНК и ДНК и могут быть выделены из природных источников, синтезированы in vitro или же получены из комбинации природных и искусственных молекул. Длина полинуклеотидной молекулы дана здесь в нуклеотидах (обозначено "nt") или в парах нуклеотиднов (обозначено "п.н."). Термин "нуклеотиды" используется здесь в случаях, когда это позволяет контекст, для обозначения одно- или двухцепочечных молекул. Когда этот термин применяется к двухцепочечным молекулам, он используется для обозначения полной длины, и будет подразумеваться, что он эквивалентен термину "пар нуклеотидов". Специалистам в данной области будет очевидно, что две цепи двухцепочечного полинуклеотида могут слегка отличаться по длине и что его концы могут быть смещены в результате энзиматического расщепления; таким образом, могут не все нуклеотиды внутри двухцепочечной полинуклеотидной молекулы быть спарены. Обычно такие неспаренные концы в длину не превышают 20 нуклеотидов.
Термин "вектор", как использовано в настоящем описании, означает по сути любую нуклеиновую кислоту, способную к амплификации в хозяйской клетке. Таким образом, вектор может быть автономно реплицирующимся вектором, т. е. вектором, который существует как внехромосомное образование, репликация которого не зависит от репликации хромосомы, например плазмидой. Альтернативно, вектор может быть таким, чтобы он, будучи введенным в хозяйскую клетку, интегрировался в хозяйский геном и реплицировался вместе с хромосомой (хромосомами), в которую он интегрирован. Выбор вектора чаще всего будет зависеть от хозяйской клетки, в которую его собираются внедрить. Векторы включают в себя, не ограничиваясь при этом плазмидными векторами, фаговые векторы, вирусные или космидные векторы. Обычно векторы содержат ориджин репликации и по меньшей мере один селектируемый ген, т.е. ген, который кодирует продукт, который легко определяется или же присутствие которого является существенным для клеточного роста.
В дальнейшем аспекте, настоящее изобретение связано с эукариотической клеткой-хозяином, содержащей полинуклеотидную конструкцию, содержащую последовательность, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где указанная другая аминокислота способна конъюгировать с химической группой и где полипептид фактора VII имеет по существу такую же активность или повышенную активность по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В дальнейшем аспекте, настоящее изобретение связано с эукариотической клеткой-хозяином, содержащей полинуклеотидную конструкцию, содержащую последовательность, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В дальнейшем аспекте, настоящее изобретение связано с эукариотической клеткой-хозяином, содержащей полинуклеотидную конструкцию, содержащую последовательность, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В дальнейшем аспекте, настоящее изобретение связано с эукариотической клеткой-хозяином, содержащей полинуклеотидную конструкцию, содержащую последовательность, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена внутри последовательности SEQ ID NO: 1 или ее варианта в положении, где полинуклеотид фактора VII имеет по существу такую же активность или повышенную активность по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В дальнейшем аспекте, настоящее изобретение связано с эукариотической клеткой-хозяином, содержащей полинуклеотидную конструкцию, содержащую последовательность, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта.
Здесь под термином "эукариотическая клетка-хозяин" подразумевается любая клетка, включая гибридные клетки, в которой может быть экспрессирована гетерологичная ДНК. Обычно хозяйские клетки включают в себя, не ограничиваясь ими, клетки насекомых, дрожжевые клетки, клетки млекопитающих, включая клетки человека, такие как клетки BHK, CHO, HEK и COS. На самом деле культивируемыми хозяйскими клетками согласно настоящему изобретению предпочтительно являются клетки млекопитающих, более предпочтительно - установившиеся линии клеток млекопитающих, включая, но не ограничиваясь ими, линии клеток CHO (например, ATCC CCL 61), COS-1 (например, ATCC CRL 1650), почек (новорожденного) хомячка (BHK) и HEK293 (например, ATCC CRL 1573; Graham et al., J. Gen. Virol. 36: 59-72,1977).
Предпочтительной линией клеток BHK является линия клеток tk-ts13 BHK (Waechter and Baserga, Proc. Natl. Acad. Sci. USA 79: 1106-1110,1982), далее в настоящем описании обозначаемая как клетки BHK 570. Линия клеток BHK 570 может быть получена из Американской коллекции клеточных культур, 12301 Parklawn Dr., Rockville, MD 20852, под регистрационным номером ATCC CRL 10314. Линия клеток tk-ts13 BHK также доступна в ATCC под регистрационным номером CRL 1632.
Другие подходящие клеточные линии включают в себя, не ограничиваясь ими, Rat Hep I (крысиная гепатома; ATCC CRL 1600), Rat Hep II (крысиная гепатома; ATCC CRL 1548), TCMK (ATCC CCL 139), легкое человека (ATCC HB 8065), NCTC 1469 (ATCC CCL 9.1) и клетки DUKX (Urlaub and Chasin, Proc. Natal. Acad. Sci. USA 77: 4216-4220,1980). Подходящими также являются клетки 3T3, клетки Namalwa, клетки миелом и слияние миеломных клеток с другими клетками. В одном из воплощений, эукариотические хозяйские клетки происходят от млекопитающего. В другом воплощении, эукариотические хозяйские клетки выбраны из группы, состоящей из клеток CHO, клеток BHK или клеток HEK.
В другом аспекте, данное изобретение связано с трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, данное изобретение связано с трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом аспекте, данное изобретение связано с трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом аспекте, данное изобретение связано с трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, данное изобретение связано с трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту.
В другом аспекте, данное изобретение связано с трансгенным растением, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, данное изобретение связано с трансгенным растением, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом аспекте, данное изобретение связано с трансгенным растением, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом аспекте, данное изобретение связано с трансгенным растением, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, данное изобретение связано с трансгенным растением, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование в соответствующей питательной среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и получение полипептида фактора VII из культуральной среды.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование в соответствующей питательной среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и получение полипептида фактора VII из культуральной среды.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование в соответствующей питательной среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и получение полипептида фактора VII из культуральной среды.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование в соответствующей питательной среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и получение полипептида фактора VII из культуральной среды.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование в соответствующей питательной среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и получение полипептида фактора VII из культуральной среды.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и получение полипептида фактора VII из культуральной среды.
В другом аспекте, данное изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту.
В другом аспекте, изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование клетки трансгенного растения, экспрессирующей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и получение полипептида фактора VII из трансгенного растения.
В другом аспекте, изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование клетки трансгенного растения, экспрессирующей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и восстановление полипептида фактора VII из трансгенного растения.
В другом аспекте, изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование клетки трансгенного растения, экспрессирующей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и восстановление полипептида фактора VII из трансгенного растения.
В другом воплощении, изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование клетки трансгенного растения, экспрессирующей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и восстановление полипептида фактора VII из трансгенного растения.
В другом воплощении, изобретение связано со способом продуцирования полипептида фактора VII, где указанный способ включает в себя культивирование клетки трансгенного растения, экспрессирующей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту, и восстановление полипептида фактора VII из трансгенного растения.
Еще в одном воплощении, изобретение связано со способом продуцирования производного фактора VII, включающим в себя следующие стадии:
а) продуцирование полипептида фактора VII;
б) конъюгирование полипептида фактора VII с химической группой;
в) нанесение производного фактора VII на катионообменную хроматографическую или гель-фильтрационную колонку; и
г) элюирование производного фактора VII.
Еще в одном воплощении, изобретение связано со способом продуцирования инактивированного производного фактора VII, включающим в себя следующие стадии:
а) продуцирование полипептида фактора VII;
б) модифицирование полипептида фактора VII в его каталитическом центре ингибитором сериновой протеиназы;
в) конъюгирование инактивированного полипептида фактора VII с химической группой;
г) нанесение инактивированного производного фактора VII на катионообменную хроматографическую или гель-фильтрационную колонку; и
д) элюирование инактивированного производного фактора VII.
В одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование в соответствующей ростовой среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и восстановление полипептида фактора VII из культуральной среды.
В другом воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование в соответствующей ростовой среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и восстановление полипептида фактора VII из культуральной среды.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование в соответствующей ростовой среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и восстановление полипептида фактора VII из культуральной среды.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование в соответствующей ростовой среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и восстановление полипептида фактора VII из культуральной среды.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование в соответствующей ростовой среде эукариотической хозяйской клетки, содержащей полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности ID NO: 1 или ее варианту, в условиях, в которых возможен синтез белка на основе полинуклеотидной конструкции, и восстановление полипептида фактора VII из культуральной среды.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способна конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя восстановление полипептида фактора VII из молока, продуцируемого трансгенным животным, экспрессирующим полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование клетки трансгенного растения, экспрессирующего полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и восстановление полипептида фактора VII из трансгенного растения.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование клетки трансгенного растения, экспрессирующего полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и восстановление полипептида фактора VII из трансгенного растения.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование клетки трансгенного растения, экспрессирующего полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и восстановление полипептида фактора VII из трансгенного растения.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование клетки трансгенного растения, экспрессирующего полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и восстановление полипептида фактора VII из трансгенного растения.
Еще в одном воплощении согласно изобретению, способ продуцирования полипептида фактора VII включает в себя культивирование клетки трансгенного растения, экспрессирующего полинуклеотидную конструкцию, кодирующую полипептид фактора VII, содержащий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту, и восстановление полипептида фактора VII из трансгенного растения.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
Под применяемым здесь термином "лечение" подразумевается введение эффективного количества терапевтически активного соединения согласно изобретению с целью предотвращения любых симптомов заболевания или предотвращения развития заболевания, или с целью курирования или облегчения таких симптомов или уже развившихся болезненных состояний. Таким образом, термин "лечение" включает в себя также и профилактическое лечение.
Под термином "усиление нормальной системы гемостаза" подразумевается усиление способности вырабатывать тромбин.
Применяемый здесь термин "нарушения, связанные с кровотечением" отражает любой дефект, врожденный, приобретенный или индуцированный, клеточной или молекулярной природы, который проявляется в виде кровотечений. Примерами могут служить дефициты факторов свертывания (например, гемофилия A и B или дефицит факторов свертывания XI или VII), ингибиторы факторов свертывания, дефективная функция тромбоцитов, тромбоцитопения или заболевание фон Виллебранда.
Подразумевается, что термин "эпизоды кровотечения" включает в себя неконтролируемое и избыточное кровотечение, которое представляет собой основную проблему как в связи с хирургическими воздействиями, так и с иными формами повреждения тканей. Неконтролируемое и избыточное кровотечение может возникать у субъектов, имеющих нормальную систему свертывания, а также у субъектов, имеющих нарушения, связанные со свертыванием крови и с кровотечениями. Дефициты факторов свертывания (например, гемофилия A и B или дефицит факторов свертывания XI или VII), ингибиторы факторов свертывания могут быть причиной нарушений, связанных с кровотечениями. Избыточные кровотечения также могут возникать у субъектов, имеющих нормальную систему свертывания, а также у субъектов с нормально функционирующим каскадом свертывания крови (отсутствие дефицитов факторов свертывания или ингибиторов, действующих против любого из факторов свертывания), и могут быть вызваны дефектной функцией тромбоцитов, тромбоцитопенией или заболеванием фон Виллебранда. В таких случаях кровотечения могут быть сходными с такими кровотечениями, которые вызваны гемофилией, потому что гемостатическая система, как и в случае гемофилии, лишена необходимых свертывающих "соединений" или же имеет аномальные свертывающие "соединения" (такие как тромбоциты или белок фактора фон Виллебранда), что и является причиной основных кровотечений. У субъектов, переживших обширное повреждение ткани, ассоциированное с хирургическим воздействием или с обширной травмой, нормальный гемостатический механизм может быть подавлен потребностью организма в немедленном гемостазировании, и в ответ на это у них, несмотря на нормальный механизм гемостазирования, может развиться кровотечение. Достижение удовлетворительного гемостазирования также является проблемой в тех случаях, когда кровотечения возникают в органах, таких как мозг, глаза и область внутреннего уха, где возможности гемостазирования хирургическим путем ограничены. Точно такая же проблема может возникнуть в процессе отбора биопсийного материала из различных органов (печень, легкое, опухолевая ткань, желудочно-кишечный тракт), а также при лапароскопической хирургии. Общим моментом во всех перечисленных ситуациях является трудность, связанная с обеспечением гемостаза с помощью хирургической техники (швы, зажимы и т.д.), что также относится к случаям, когда имеют место диффузные кровотечения (геморрагический гастрит и профузное маточное кровотечение). Острые и профузные кровотечения могут возникать также и у субъектов при антикоагуляционной терапии, у которых дефектный гемостаз индуцирован данной терапией. Такие субъекты могут нуждаться в хирургическом вмешательстве в случаях, когда бывает нужно быстро подавить антикоагулянтное действие. Радикальная заднелобковая простатэктомия является обычно предпринимаемой процедурой у субъектов с локализованным раком предстательной железы. Такая операция часто осложняется значительными, а иногда и массивными кровопотерями. Значительные кровопотери в процессе простатэктомии главным образом связаны с осложненной анатомической ситуацией, с различными густоваскуляризованными участками, которые не так легко поддаются кровоостанавливающим манипуляциям при хирургическом вмешательстве и которые могут привести к диффузному кровотечению из обширной области. Другой ситуацией, которая может вызвать проблемы в случае неудовлетворительного гемостаза, является ситуация, когда субъекты с нормальным гемостатическим механизмом подвергаются антикоагуляционной терапии с целью предотвращения тромбоэмболического заболевания. Такая терапия может включать в себя гепарин, другие формы протеогликанов, варфарин или другие формы антагонистов витамина K, также как и аспирин и другие ингибиторы агрегации тромбоцитов.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота вставлена в последовательность SEQ ID NO: 1 или ее вариант, и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту, и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
В одном из воплощений согласно изобретению, кровотечение ассоциировано с гемофилией A или B. В другом воплощении, кровотечение ассоциировано с гемофилией с приобретенными ингибиторами. В другом воплощении, кровотечение ассоциировано с тромбоцитопенией. В другом воплощении, кровотечение ассоциировано с заболеванием фон Виллебранда. В другом воплощении, кровотечение ассоциировано с тяжелым повреждением ткани. В другом воплощении, кровотечение ассоциировано с тяжелой травмой. В другом воплощении, кровотечение ассоциировано с хирургией. В другом воплощении, кровотечение ассоциировано с лапароскопической хирургией. В другом воплощении, кровотечение ассоциировано с геморрагическим гастритом. В другом воплощении, кровотечение ассоциировано с профузным маточным кровотечением. В другом воплощении, кровотечение ассоциировано с органами с ограниченными возможностями для механического гемостаза. В другом воплощении, кровотечение имеет место в мозге, в области внутреннего уха и глазах. В другом воплощении, кровотечение ассоциировано с процессом взятия биопсии. В другом воплощении, кровотечение ассоциировано с антикоагуляционной терапией.
Под используемым здесь термином "субъект" подразумевается любое животное, в частности, млекопитающие, и этот термин, в случае необходимости, может использоваться наряду с термином "пациент".
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота вставлена в последовательность SEQ ID NO: 1 или ее вариант, и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
Еще в одном аспекте, данное изобретение связано с применением производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианту и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, для получения лекарственного средства для лечения эпизодических кровотечений или для усиления нормальной системы гемостаза.
В другом аспекте, настоящее изобретение связано со способом лечения у субъекта эпизодических кровотечений или связанных с кровотечениями заболеваний или со способом усиления нормальной системы гемостаза, где указанный способ включает в себя введение субъекту, в случае необходимости, терапевтически или профилактически эффективное количество производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, настоящее изобретение связано со способом лечения у субъекта эпизодических кровотечений или связанных с кровотечениями заболеваний или со способом усиления нормальной системы гемостаза, где указанный способ включает в себя введение субъекту, в случае необходимости, терапевтически или профилактически эффективное количество производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, настоящее изобретение связано со способом лечения у субъекта эпизодических кровотечений или связанных с кровотечениями заболеваний или со способом усиления нормальной системы гемостаза, где указанный способ включает в себя введение субъекту, в случае необходимости, терапевтически или профилактически эффективное количество производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, где эта другая аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, настоящее изобретение связано со способом лечения у субъекта эпизодических кровотечений или связанных с кровотечениями заболеваний или со способом усиления нормальной системы гемостаза, где указанный способ включает в себя введение субъекту, в случае необходимости, терапевтически или профилактически эффективное количество производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота вставлена в последовательность SEQ ID NO: 1 или ее вариант, и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом аспекте, настоящее изобретение связано со способом лечения у субъекта эпизодических кровотечений или связанных с кровотечениями заболеваний или со способом усиления нормальной системы гемостаза, где указанный способ включает в себя введение субъекту, в случае необходимости, терапевтически или профилактически эффективное количество производного фактора VII, включающего в себя полипептид фактора VII, имеющий аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта и где аминокислота конъюгирована с химической группой, которая увеличивает истинную молекулярную массу полипептида фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, и где производное фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В дальнейшем аспекте, настоящее изобретение связано с применением производного инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, для получения лекарственного средства для ингибирования у пациента тромбообразования.
В дальнейшем аспекте, настоящее изобретение связано с применением производного инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой, и где полипептид фактора VII, обладающий по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, для получения лекарственного средства для ингибирования у пациента тромбообразования.
В дальнейшем аспекте, настоящее изобретение связано с применением производного инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, для получения лекарственного средства для ингибирования у пациента тромбообразования.
В дальнейшем аспекте, настоящее изобретение связано с применением производного инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, для получения лекарственного средства для ингибирования у пациента тромбообразования.
В дальнейшем аспекте, настоящее изобретение связано с применением производного инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII имеет такую же самую активность или повышенную активность по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, для получения лекарственного средства для ингибирования у пациента тромбообразования.
В дальнейшем аспекте, настоящее изобретение связано с применением производного инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон, для получения лекарственного средства для ингибирования у пациента тромбообразования.
В дальнейшем аспекте, настоящее изобретение связано со способом ингибирования тромбообразования у пациента, включающим в себя местное введение на участке сосуда, чувствительном у пациента к тромбообразованию, терапевтически эффективной дозы композиции, включающей в себя производное инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон.
В дальнейшем аспекте, настоящее изобретение связано со способом ингибирования тромбообразования у пациента, включающим в себя местное введение на участке сосуда, чувствительном к тромбообразованию у пациента, терапевтически эффективной дозы композиции, включающей в себя производное инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота заменена другой аминокислотой, где эта другая аминокислота способна конъюгировать с химической группой и где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон.
В дальнейшем аспекте, настоящее изобретение связано со способом ингибирования тромбообразования у пациента, включающим в себя местное введение на участке сосуда, чувствительном у пациента к тромбообразованию, терапевтически эффективной дозы композиции, включающей в себя производное инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте в положении, выбранном из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон.
В дальнейшем аспекте, настоящее изобретение связано со способом ингибирования тромбообразования у пациента, включающим в себя местное введение на участке сосуда, чувствительном у пациента к тромбообразованию, терапевтически эффективной дозы композиции, включающей в себя производное инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, соответствующая аминокислоте, выбранной из R396, Q250 или P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон.
В дальнейшем аспекте, настоящее изобретение связано со способом ингибирования тромбообразования у пациента, включающим в себя местное введение на участке сосуда, чувствительном у пациента к тромбообразованию, терапевтически эффективной дозы композиции, включающей в себя производное инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, вставлена в последовательность a SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же самой активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон.
В дальнейшем аспекте, настоящее изобретение связано со способом ингибирования тромбообразования у пациента, включающим в себя местное введение на участке сосуда, чувствительном у пациента к тромбообразованию, терапевтически эффективной дозы композиции, включающей в себя производное инактивированного фактора VII, где полипептид инактивированного фактора VII, включающий в себя аминокислотную последовательность SEQ ID NO: 1 или ее вариант, где аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта, и имеющий модификацию в своем каталитическом центре, причем указанная модификация ингибирует способность полипептида фактора VII активировать плазматический фактор X или IX, дополнительно конъюгирован с химической группой, которая увеличивает истинную молекулярную массу полипептида инактивированного фактора VII примерно в 300 Дальтон приблизительно до 100000 Дальтон.
В одном из воплощений согласно изобретению, химическая группа является по существу нейтральной.
Здесь термин "нейтральный" относится к биосовместимой химической группе, и подразумевается, что она является нетоксичной, неиммуногенной и водорастворимой. Химические группы, будучи в рамках этого определения по существу нейтральными, включают в себя, не ограничиваясь ими, полиэтиленгликоль (ПЭГ), монометокси-полиэтиленгликоль, декстран, поли-(N-винилпирролидон)полиэтиленгликоль, гомополимеры пропиленгликоля, сополимеры полипропиленоксид/этиленоксида, полипропиленгликоль, полиоксиэтилированные полиолы (например, глицерин) и поливиниловый спирт, коломиновые кислоты или иные полимеры на основе углеводов, полимеры аминокислот и биотиновые производные.
В другом аспекте согласно изобретению, химическая группа является водорастворимой.
В другом аспекте согласно изобретению, химическая группа имеет молекулярную массу приблизительно от 1000 Дальтон до 80000 Дальтон.
В другом аспекте согласно изобретению, химическая группа имеет молекулярную массу приблизительно от 5000 Дальтон до 60000 Дальтон.
В другом аспекте согласно изобретению, химическая группа имеет молекулярную массу приблизительно от 10000 Дальтон до 40000 Дальтон.
В другом аспекте согласно изобретению, химическая группа имеет молекулярную массу приблизительно от 500 Дальтон до 20000 Дальтон.
В другом аспекте согласно изобретению, химическая группа имеет молекулярную массу приблизительно от 500 Дальтон до 5000 Дальтон.
В другом аспекте согласно изобретению, химическая группа имеет молекулярную массу приблизительно от 750 Дальтон до 5000 Дальтон.
В дальнейшем аспекте согласно изобретению, химическая группа представляет собой полиэтиленгликоль.
В дальнейшем аспекте согласно изобретению, химическая группа выбрана из одной-семи молекул полиэтиленгликоля.
В предпочтительном воплощении согласно изобретению, химическая группа представляет собой одну молекулу полиэтиленгликоля.
В другом воплощении согласно изобретению, химическая группа представляет собой монометоксиполиэтиленгликоль.
В другом воплощении согласно изобретению, химическая группа представляет собой декстран.
В другом воплощении согласно изобретению, химическая группа представляет собой поли-(N-винилпирролидон)полиэтиленгликоль.
В другом воплощении согласно изобретению, химическая группа представляет собой гомополимеры пропиленгликоля.
В другом воплощении согласно изобретению, химическая группа представляет собой полипропиленоксид.
В другом воплощении согласно изобретению, химическая группа представляет собой полипропиленгликоль.
В другом воплощении согласно изобретению, химическая группа представляет собой полиоксиэтилированный полиол.
В другом воплощении согласно изобретению, химическая группа представляет собой поливиниловый спирт.
В другом воплощении согласно изобретению, химическая группа представляет собой коломиновую кислоту.
В другом воплощении согласно изобретению, химическая группа представляет собой полимер на основе углевода.
В другом воплощении согласно изобретению, химическая группа представляет собой полимер из аминокислот.
В другом воплощении согласно изобретению, химическая группа представляет собой биотиновое производное.
В другом воплощении согласно изобретению, химическая группа конъюгирована со свободной сульфгидрильной группой, присутствующей на аминокислоте, заменяющей аминокислоту в полипептиде, включенной в полипептид или добавленной к полипептиду.
В другом воплощении согласно изобретению, химическая группа конъюгирована с цистеином.
В другом воплощении согласно изобретению, заменяющая, включенная или добавленная аминокислота способна конъюгировать с химической группой.
В другом воплощении согласно изобретению, аминокислота, способная конъюгировать с химической группой, является аминокислотой со свободной сульфгидрильной группой.
В другом воплощении согласно изобретению, аминокислотой, способной конъюгировать с химической группой, является цистеин.
В другом воплощении согласно изобретению, заменяющая, включенная или добавленная аминокислота является аминокислотой со свободной сульфгидрильной группой, такой как цистеин.
В другом воплощении, аминокислота полипептида фактора VII вставлена в положение, выбранное из положений 247-260, 393-405 или 406 последовательности SEQ ID NO: 1.
В другом воплощении, аминокислота полипептида фактора VII, соответствующая положению R396 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом воплощении, аминокислота полипептида фактора VII, соответствующая положению Q250 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом воплощении, аминокислота полипептида фактора VII, соответствующая положению P406 последовательности SEQ ID NO: 1, заменена другой аминокислотой.
В другом воплощении, связанном с полипептидом фактора VII, добавочная аминокислота, способная конъюгировать с химической группой, вставлена в последовательность SEQ ID NO: 1 или ее вариант в положении, где полипептид фактора VII обладает по существу такой же активностью или повышенной активностью по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом воплощении, связанном с полипептидом фактора VII, другая аминокислота, способная конъюгировать с химической группой, добавлена к N- или C-концу последовательности SEQ ID NO: 1 или ее варианта.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота добавлена к C-концу последовательности SEQ ID NO: 1.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота добавлена к N-концу последовательности SEQ ID NO: 1.
В другом воплощении, связанном с полипептидом фактора VII, к нему добавлен цистеин.
В другом воплощении, связанном с полипептидом фактора VII, в него включен цистеин.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, выбранная из группы, состоящей из K157, V158, E296, M298, L305, D334, S336, K337 и F374 последовательности SEQ ID NO: 1, заменена другой аминокислотой, которая повышает активность по сравнению с рекомбинантным человеческим фактором VIIa дикого типа.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая K157 последовательности SEQ ID NO: 1, заменена аминокислотой, независимо выбранной из G, V, S, T, N, Q, D и E.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая V158 последовательности SEQ ID NO: 1, заменена аминокислотой, независимо выбранной из S, T, N, Q, D и E.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая V158 последовательности SEQ ID NO: 1, заменена аминокислотой, независимо выбранной из T и D.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая E296 последовательности SEQ ID NO: 1, заменена аминокислотой, независимо выбранной из R, K и V.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая E296 последовательности SEQ ID NO: 1, заменена аминокислотой V.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая M298 последовательности SEQ ID NO: 1, заменена аминокислотой, независимо выбранной из R, K, Q и N.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая M298 последовательности SEQ ID NO: 1, заменена аминокислотой Q.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая L305 последовательности SEQ ID NO: 1, заменена аминокислотой, независимо выбранной из A, V, L, I, M, F, W, P, G, S, T, C, Y, N, E, K, R, H, D и Q.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая L305 последовательности SEQ ID NO: 1, заменена аминокислотой V.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая D334 последовательности SEQ ID NO: 1, заменена аминокислотой E.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая S336 последовательности SEQ ID NO: 1, заменена аминокислотой G.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая K337 последовательности SEQ ID NO: 1, заменена аминокислотой, независимо выбранной из A, G, V, S, T, N, Q, D и E.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая K337 последовательности SEQ ID NO: 1, заменена аминокислотой A.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая F374 последовательности SEQ ID NO: 1, заменена аминокислотой, независимо выбранной из A, V, L, I, M, F, W, P, G, S, T, C, Y, N, E, K, R, H, D и Q.
В другом воплощении, связанном с полипептидом фактора VII, аминокислота, соответствующая F374 последовательности SEQ ID NO: 1, заменена аминокислотой P.
В другом воплощении согласно изобретению, полипептид фактора VII представляет собой человеческий фактор VII.
В другом воплощении согласно изобретению, полипептид фактора VII представляет собой человеческий фактор VIIa.
В настоящем описании аминокислоты представлены с помощью аббревиатур, как показано в Таблице 1, принятых Комиссией по Биохимическим Номенклатурам (CBN) IUPAC-IUB. Подразумевается, что аминокислота и ей подобное [соединение], имеющие изомеры, представленные по названию или с помощью следующих аббревиатур, если не указано иначе, находятся в природной L-форме. Кроме того, левый и правый концы аминокислотной последовательности пептида, если не указано иначе, представляют собой, соответственно, его N- и C-концы.
Аббревиатуры, которыми обозначены аминокислоты
Настоящее изобретение связано, как указано выше, также и со способом получения полипептидов человеческого фактора VII. Полипептиды человеческого фактора VII предпочтительно продуцируются с помощью технологии рекомбинантной ДНК. С этой целью ДНК-последовательности, кодирующие человеческий фактор VII, могут быть выделены путем получения библиотеки геномной или кДНК и скрининга ДНК-последовательностей, полностью или частично кодирующих этот белок, с помощью синтетических олигонуклеотидных проб, в соответствии со стандартными технологиями (ср. Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, New York, 1989). В целях, связанных с настоящим изобретением, предпочтительно, чтобы последовательность ДНК, кодирующая этот белок, имела человеческую природу, т. е. чтобы она была получена из библиотеки кДНК или ДНК генома человека.
Последовательности ДНК, кодирующие полипептиды человеческого фактора VII, могут быть получены также и синтетическим путем с помощью отработанных стандартных методов, например, фосфоамидитного метода, описанного Beaucage and Caruthers, Tetrahedron Letters 22 (1981), 1859-1869, или метода, описанного Matthes et al., EMBO Journal 3 (1984), 801-805. В соответствии с фосфоамидитным методом, олигонуклеотиды синтезируются, например, в автоматическом ДНК-синтезаторе, очищаются, подвергаются отжигу, лигируются и клонируются в соответствующие векторы.
Последовательности ДНК могут быть получены также и с помощью полимеразной цепной реакции с использованием специфических праймеров, например, как описано в патенте США 4,683,202, Saiki et al., Science 239 (1988), 487-491, или Sambrook et al., выше.
Последовательности ДНК, кодирующие полипептиды человеческого фактора VII, обычно включают в рекомбинантный вектор, который может быть любым вектором, удобным с точки зрения технологии рекомбинантной ДНК, и выбор вектора обычно зависит от хозяйской клетки, в которую его предполагается ввести. Таким образом, вектор может быть автономно реплицирующимся вектором, т.е. вектором, который существует как внехромосомный объект, репликация которого не зависит от хромосомной репликации, например, плазмидой. Альтернативно, вектор может быть таким, который при введении в хозяйскую клетку интегрируется в геном хозяйской клетки и реплицируется вместе с хромосомой (хромосомами), в которую он был интегрирован.
Такой вектор предпочтительно является экспрессирующим вектором, в котором последовательность ДНК, кодирующая полипептиды человеческого фактора VII, оперативно связана с добавочными сегментами, необходимыми для транскрипции ДНК. Обычно экспрессирующий вектор получают из плазмидной ДНК или вирусной ДНК, или же он может содержать элементы и того, и другого. Термин "оперативно связанный" указывает, что сегменты арранжированы таким образом, что они функционируют согласованно в соответствии с намеченными целями, например, в области промотора инициируется транскрипция ДНК, которая происходит вдоль всей цепи последовательности ДНК, кодирующей полипептид.
Промотором может быть любая последовательность ДНК, которая обладает транскрипционной активностью в выбранной хозяйской клетке и которая может быть получена из генов, кодирующих либо гомологичные, либо гетерологичные белки для данной хозяйской клетки.
Примерами подходящих промоторов для направления транскрипции ДНК, кодирующей полипептид человеческого фактора VII, являются промотор SV40 (Subramani et al., Mol. Cell Biol. 1 (1981), 854-864), промотор MT-1 (ген металлотинеина) (Palmiter et al., Science 222 (1983), 809-814), промотор CMV (Boshart et al., Cell 41: 521-530,1985) или главный поздний промотор аденовируса 2 (Kaufman and Sharp, Mol. Cell Biol, 2: 1304-1319, 1982).
Примером подходящего промотора для применения в клетках насекомых является промотор полиэдрина (патент США 4,745,051; Vasuvedan et al., FEBS Lett. 311, (1992) 7-11), промотор P10 (J. M. Vlak et al., J. Gen. Virology 69,1988, pp. 765-776), промотор основного белка вируса полиэдроза Autographa californica (Европейский патент 397 485), промотор немедленного раннего гена 1 бакуловируса (патент США 5,155,037; патент США 5,162,222) или промотор отложенного-раннего гена бакуловируса 39K (патент США 5,155,037; патент США 5,162,222).
Примеры подходящих промоторов для применения в клетках дрожжей в качестве хозяйских клеток включают в себя промоторы из гликолитических генов дрожжей (Hitzeman et al., J. Biol. Chem. 255 (1980), 12073-12080; Alber and Kawasaki, J. Mol. Appl. Gen. 1 (1982), 419-434) или генов алкогольдегидрогеназы (Young et al., in Genetic Engineering of Microorganisms for Chemicals (Hollaender et al, eds.), Plenum Press, New York, 1982), или промоторы TPI1 (патент США 4,599,311) или ADH2-4c (Russell et al., Nature 304 (1983), 652-654).
Примерами подходящих промоторов для применения в хозяйских клетках нитевидных грибов являются, например, промотор ADH3 (McKnight et al., The EMBO J. 4 (1985), 2093-2099) или промотор tpiA. Примерами остальных подходящих промоторов являются промоторы, полученные из гена, кодирующего TAKA-амилазу A. oryzae, аспартильную протеиназу Rhizomucor miehei, нейтральную α-амилазу A. niger, кислотостабильную α-амилазу A. niger, глюкоамилазу (gluA) A. niger или A. awamori, липазу Rhizomucor miehei, щелочную протеиназу A. oryzae, триозофосфатизомеразу A. oryzae или ацетамидазу A. nidulans. Предпочтительными являются промоторы TAKA-амилазы и gluA. Подходящими промоторами являются промоторы, указанные, например, в Европейских патентах EP 238 023 и EP 383 779.
ДНК-последовательности, кодирующие полипептиды человеческого фактора VII, могут быть также, если это необходимо, оперативно связаны с подходящим терминатором, таким как терминатор гормона роста человека (Palmiter et al., Science 222,1983, pp. 809-814) или терминатор TPI1 (Alber and Kawasaki, J. Mol. Appl. Gen. 1,1982, pp. 419-434), или терминатор ADH3 (McKnight et al., The EMBO J. 4,1985, pp. 2093-2099). Вектор может также содержать набор сайтов сплайсинга РНК, локализованных вниз по течению от промотора и вверх по течению от сайта встраивания как таковой последовательности фактора VII. Предпочтительные сайты сплайсинга РНК могут быть получены из аденовирусных и/или иммуноглобулиновых генов. В экспрессирующих векторах также содержится сигнал полиаденилирования, локализованный вниз по течению от инсерционного сайта. Особенно предпочтительные сигналы полиаденилирования включают в себя ранний или поздний сигналы полиаденилирования из SV40 (Kaufman and Sharp, ibid.), сигнал полиаденилирования из области 5 Elb аденовируса, терминатор гормона роста человека (DeNoto et al. Nuc. Acids Res. 9: 3719-3730,1981) или сигнал полиаденилирования из гена фактора VII человека или бычьего гена фактора VII. Векторы экспрессии могут также включать в себя некодирующую вирусную лидерную последовательность, такую как трехсторонняя (tripartite) лидерная последовательность аденовируса 2, локализованная между промотором и сайтами сплайсинга РНК; и энхансерную последовательность, такую как энхансер SV40.
Рекомбинантный вектор может, кроме того, включать в себя последовательность ДНК, позволяющую вектору реплицироваться в конкретно требуемой хозяйской клетке. Примером такой последовательности (когда хозяйская клетка представляет собой клетку млекопитающего) является ориджин репликации SV40.
Когда клеткой-хозяином является дрожжевая клетка, подходящими последовательностями, дающими возможность вектору реплицироваться, являются гены репликации REP 1-3 и ориджин репликации дрожжевой плазмиды 2μ.
Вектор может включать в себя также селектируемый маркер, например ген, продукт которого восполняет дефект в хозяйской клетке, такой как ген, кодирующий дигидрофолатредуктазу (DHFR), или ген TPI Schizosaccharomyces pombe (описанный P. R. Russell, Gene 40, 1985, pp. 125-130), или ген, обеспечивающий лекарственную резистентность, например резистентность к ампициллину, канамицину, тетрациклину, хлорамфениколу, неомицину, гидромицину или метотрексату. В случае нитевидных грибов селективные маркеры включают в себя amdS, pyrG, argB, niaD или sC.
Для того чтобы к хозяйских клетках направить полипептиды человеческого фактора VII согласно изобретению по секреторному пути, нужно обеспечить рекомбинантный вектор секреторной сигнальной последовательностью (называемой также лидерной последовательностью, препропоследовательностью или препоследовательностью). Секреторная сигнальная последовательность связана с последовательностью ДНК, кодирующей полипептиды человеческого фактора VII в правильной рамке считывания. Секреторные сигнальные последовательности обычно расположены 5'-концом к последовательности ДНК, кодирующей пептид. Секреторная сигнальная последовательность может, таким образом, быть нормально ассоциирована с белком или может быть из гена, кодирующего другой секреторный белок.
В случае секреции из дрожжевых клеток секреторная сигнальная последовательность может кодировать любой сигнальный пептид, который обеспечивает эффективную направленность экспрессированных полипептидов человеческого фактора VII в клетке по секреторному пути. Сигнальный пептид может быть природным сигнальным пептидом или его функциональной частью, или он может быть синтетическим пептидом. Было установлено, что подходящими сигнальными пептидами являются α-факторный сигнальный пептид (ср. патент США 4,870,008), сигнальный пептид амилазы слюны мыши (ср. O. Hagenbuchle et al., Nature 289,1981, pp. 643-646), модифицированный карбоксипептидазный сигнальный пептид (ср. L. A. Valls et al., Cell 48, 1987, pp. 887-897), дрожжевой сигнальный пептид BAR1 (ср. WO 87/02670) или сигнальный пептид аспартильной протеиназы 3 (YAP3) (ср. M. Egel-Mitani et al., Yeast 6, 1990, pp. 127-137).
Для эффективной секреции в дрожжах последовательность, кодирующая лидерный пептид, также может быть вставлена ниже по течению от сигнальной последовательности и выше по течению от последовательности ДНК, кодирующей полипептиды человеческого фактора VII. Функция лидерного пептида состоит в том, чтобы направить экспрессированный пептид из эндоплазматического ретикулума в аппарат Гольджи, а затем - в секреторную везикулу, с тем, чтобы он был секретирован в культуральную среду (т. е. в экспортировании полипептидов человеческого фактора VII через клеточную стенку или по меньшей мере через клеточную мембрану в периплазматическое пространство дрожжевой клетки). Лидерный пептид может быть лидерным пептидом дрожжевого альфа-фактора (применение которого описано, например, в патенте США 4,546,082, патенте США 4,870,008, и в европейских патентах EP 16 201, EP 123 294, EP 123 544 и EP 163 529). Альтернативно, лидерный пептид может быть синтетическим лидерным пептидом, т.е. таким лидерным пептидом, который не обнаружен в природе. Синтетические лидерные пептиды могут быть, например, сконструированы, как описано в международных заявках WO 89/02463 или WO 92/11378.
Для применения в нитевидных грибах сигнальный пептид может быть получен, соответственно, из гена, кодирующего амилазу или глюкоамилазу Aspergillus sp., из гена, кодирующего липазу или протеиназу Rhizomucor miehei или липазу Humicola lanuginosa. Предпочтительно, если сигнальный пептид получен из гена, кодирующего TAKA-амилазу A. oryzae, нейтральную альфа-амилазу A. niger, кислотостабильную амилазу A. niger или глюкоамилазу A. niger. Приемлемые сигнальные пептиды описаны, например, в EP 238 023 и EP 215 594.
Для применения в клетках насекомых сигнальный пептид может быть, соответственно, получен из гена насекомого (ср. WO 90/05783), такой, например, как сигнальный пептид предшественной формы адипокинетического гормона чешуекрылых Manduca sexta (ср. патент США 5,023,328).
Методики, используемые для лигирования последовательностей ДНК, кодирующих полипептиды человеческого фактора VII, промоторную и - необязательно - терминаторную и/или секреторную сигнальную последовательность, соответственно, и для встраивания их в подходящие векторы, содержащие информацию, необходимую для репликации, хорошо известны специалистам в данной области (см., например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor, New York, 1989).
Методы трансфицирования клеток млекопитающих и экспрессирования последовательностей ДНК, встроенных в клетки, описаны, например, у Kaufman and Sharp, J. Mol. Biol. 159 (1982), 601-621; Southern and Berg, J. Mol. Appl. Genet. 1 (1982), 327-341; Loyter et al., Proc. Natl. Acad. Sci. USA 79 (1982), 422-426; Wigler et al., Cell 14 (1978), 725; Corsaro and Pearson, Somatic Cell Genetics 7 (1981), 603, Graham and van der Eb, Virology 52 (1973), 456; and Neumann et al., EMBO J. 1 (1982), 841-45.
Селективные маркеры могут быть введены в клетку в составе отдельной плазмиды, одновременно с представляющим интерес геном, или же они могут быть введены в клетку в составе одной и той же плазмиды. Если в составе одной и той же плазмиды селективный маркер и представляющий интерес ген могут находиться под контролем одного и того же промотора, то при таком расположении генов образуется двухцистронный мессенджер. Конструкции такого типа известны специалистам в данной области (например, Levinson and Simonsen, патент США No. 4,713,339). Может оказаться также успешным добавление в смесь, которая вводится в клетки, дополнительной ДНК, известной как "ДНК-носитель".
После того как ДНК будет захвачена клетками, последние растут в подходящей среде для роста клеток, обычно 1-2 дня, прежде чем начнется экспрессия представляющего интерес гена. Под используемым здесь термином "подходящая среда для роста клеток" подразумевается среда, содержащая питательные элементы и другие компоненты, необходимые для роста клеток и экспрессии представляющих интерес полипептидов человеческого фактора VII. Такая среда обычно включает в себя источник углерода, источник азота, основные аминокислоты, основные сахара, витамины, соли, фосфолипиды, белки и ростовые факторы. Для продуцирования гамма-карбоксилированных белков среда должна содержать витамин K, предпочтительно в концентрации приблизительно от 0.1 мкг/мл примерно до 5 мкг/мл. Затем производят подбор лекарственного средства для отбора роста клеток, которые стабильно экспрессируют селективный маркер. Для клеток, которые были трансфицированы амплифицируемым селективным маркером, концентрация лекарственного средства может быть повышена с целью отбора большего числа копий клонированных последовательностей, таким образом увеличивая уровни экспрессии. Затем клоны стабильно трансфицированных клеток подвергаются скринингу на предмет экспрессии представляющего интерес полипептида человеческого фактора VII.
Хозяйская клетка, в которую введены последовательности ДНК, кодирующие полипептиды человеческого фактора VII, может представлять собой любую клетку, которая способна продуцировать посттрансляционно модифицированные полипептиды человеческого фактора VII, включая дрожжевые клетки, клетки грибов и клетки высших эукариот.
Примерами линий клеток млекопитающих для использования в настоящем изобретении являются клеточные линии COS-1 (ATCC CRL 1650), клетки почки хомячка (BHK) и линия клеток 293 (ATCC CRL 1573; Graham et al., J. Gen. Virol 36: 59-72, 1977). Предпочтительной линией BHK является разновидность tk-ts13 линии клеток BHK (Waechter and Baserga, Proc. Natl. Acad. Sci. USA 79: 1106-1110, 1982, включена в настоящее описание в виде ссылки), обозначаемая здесь далее как клетки BHK 570. Линия клеток BHK 570 депонирована в Американской Коллекции Типовых Культур, 12301 Parklawn Dr., Rockville, Md. 20852, под идентификационным номером ATCC CRL 10314. Линия tk-ts13 клеток BHK доступна также и под идентификационным номером ATCC CRL 1632. Кроме этого в рамках настоящего изобретения может быть использован также и ряд других клеточных линий, включая клетки Rat Hep I (гепатома крысы; ATCC CRL 1600), Rat Hep II (гепатома крысы; ATCC CRL 1548), TCMK (ATCC CCL 139), клетки легкого человека (ATCC HB 8065), NCTC 1469 (ATCC CCL 9.1), CHO (ATCC CCL 61) и клетки DUKX (Urlaub and Chasin, Proc. Natl. Acad. Sci. USA 77: 4216-4220,1980).
Примеры подходящих дрожжевых клеток включают в себя клетки Saccharomyces spp. или Schizosaccharomyces spp., в частности, штаммы Saccharomyces cerevisiae или Saccharomyces kluyveri. Способы трансформации дрожжевых клеток с помощью гетерологичной ДНК и получения из них гетерологичных полипептидов описаны, например, в патентах США 4,599,311, US 4,931,373, US 4,870,008, 5,037,743 и US 4,845,075, все из которых включены в настоящее описание в виде ссылки. Трансформированные клетки отбирались путем фенотипирования, определяемого с помощью избирательного маркера, обычно по резистентности к лекарственному средству или по способности расти в отсутствие какого-нибудь конкретного питательного элемента, например лейцина. Предпочтительным вектором для использования в дрожжевых клетках является вектор POT1, описанный в патенте США 4,931,373. Последовательностям ДНК, кодирующим полипептиды человеческого фактора VII, может предшествовать сигнальная последовательность и - необязательно - лидерная последовательность, например, как описано выше. Кроме того, примерами подходящих дрожжевых клеток являются штаммы Kluyveromyces, такие как K. lactis, Hansenula, например H. polymorpha, или Pichia например P. pastoris (см. Gleeson et al., J. Gen. Microbiol. 132,1986, pp. 3459-3465; US 4,882,279).
Примерами других грибковых клеток являются клетки нитевидных грибов, например, Aspergillus spp., Neurospora spp., Fusarium spp. или Trichoderma spp., в частности штаммы A. oryzae, A. nidulans или A. niger. Использование Aspergillus spp. для экспрессии белков описано, например, в EP 272 277, EP 238 023, EP 184 438. Трансформация F. oxysporum может быть произведена, например, в соответствии с методикой, описанной Malardier et al., 1989, Gene 78: 147-156. Трансформация Trichoderma spp. может быть осуществлена, например, как описано в EP 244 234.
Когда в качестве хозяйских клеток используются нитевидные грибы, они могут быть трансформированы с помощью конструкции ДНК согласно изобретению, обычно путем интеграции конструкции ДНК в хозяйскую хромосому, с получением рекомбинантных клеток-хозяев. Такая интеграция обычно считается успешной, поскольку сохранение стабильности такой ДНК-последовательности в этой клетке более вероятно. Интеграция в хозяйскую хромосому может быть произведена согласно общепринятым методам, например, путем гомологичной или гетерологичной рекомбинации.
Трансформация клеток насекомых и продукция в них гетерологичных полипептидов может быть предпринята, как описано в патентах US 4,745,051; US 4,879,236; US 5,155,037; 5,162,222; EP 397,485, все из которых включены в настоящее описание в виде ссылки. Линиями клеток насекомых, используемыми в качестве хозяев, могут быть клеточные линии Lepidoptera, такие как клетки Spodoptera frugiperda или клетки Trichoplusia ni (см. патент США 5,077,214). Подходящими условиями культивирования могут быть условия, описанные, например, в международных заявках WO 89/01029 или WO 89/01028, или же в любой из перечисленных выше ссылок.
Затем описанные выше трансформированные или трансфицированные клетки культивируют в подходящей питательной среде, в условиях, допускающих экспрессию полипептида человеческого фактора VII, после чего полученный полипептид, полностью или частично, может быть извлечен из культуральной среды. Среда, используемая для культивирования клеток, может представлять собой любую удобную для использования среду, подходящую для роста хозяйских клеток, такую как минимальная или комплексная среда, содержащая соответствующие добавки. Подходящие среды можно приобрести в готовом виде или же приготовить самим, в соответствии с опубликованной рецептурой (например, в каталогах Американской Коллекции Типовых Культур). Продуцируемый клетками полипептид человеческого фактора VII может быть затем извлечен из культуральной среды с помощью общепринятых приемов, включая отделение хозяйских клеток от среды путем центрифугирования или фильтрования, преципитацию водорастворимых белковых компонентов супернатанта или фильтрата с помощью соли, например сульфата аммония, очистку с помощью различных хроматографических методов, например ионообменной хроматографии, гель-фильтрационной хроматографии, аффинной хроматографии и т.п., в зависимости от типа представляющего интерес полипептида.
Для получения полипептидов рекомбинантного человеческого фактора VII используется клонированная последовательность ДНК фактора VII дикого типа. Такая последовательность может быть модифицирована таким образом, чтобы кодировать требуемый вариант фактора VII. Полноразмерные нуклеотидная и аминокислотная последовательности человеческого фактора VII известны. См. Патент США No. 4,784,950, который включен в настоящее описание в виде ссылки и где описано клонирование и экспрессия рекомбинантного человеческого фактора VII. Последовательность бычьего фактора VII описана в публикации Takeya et al., J. Biol. Chem, 263: 14868-14872 (1988), которая включена в настоящее описание в виде ссылки.
Аминокислотные изменения могут быть произведены различными способами. Модификация последовательности ДНК может быть осуществлена путем сайт-специфического мутагенеза. Технология сайт-специфического мутагенеза хорошо известна в данной области и описана, например, у Zoller and Smith (DNA 3: 479-488,1984). Таким образом, используя нуклеотидную и аминокислотную последовательности фактора VII, можно по выбору внести изменения.
Последовательности ДНК для применения в рамках настоящего изобретения должны обычно кодировать препропептид на амино-конце протеина фактора VII для получения корректного посттрансляционного процессинга (например, гамма-карбоксилирования остатков глутаминовой кислоты) и секретирования из хозяйских клеток. Препропептид может быть препропептидом фактора VII или другого витамин K-зависимого белка плазмы, такого как фактор IX, фактор X, протромбин, протеин C или протеин S. Как должно быть очевидно специалистам в данной области, дополнительные модификации в аминокислотной последовательности фактора VII могут быть произведены в том случае, если эти модификации не вызовут существенного ухудшения способности белка функционировать в качестве фактора свертывания. Например, фактор VII в каталитической триаде может быть также модифицирован в сайте активационного расщепления, с тем, чтобы вызвать ингибирование превращения зимогена фактора VII в его активированную двухцепочечную форму, как в общем виде описано в патенте США No. 5,288,629, включенном в настоящее описание в виде ссылки.
В рамках настоящего изобретения для продукции полипептида человеческого фактора можно использовать технологию трансгенного животного. Предпочтительным является продуцирование белков в молочных железах, используя в качестве хозяина самку млекопитающего. Экспрессия в молочной железе и последующая секреция требуемого белка в молоко позволяет обойти многие трудности, связанные с выделением белков из других источников. Молоко легко поддается сбору, доступно в больших количествах, и его легко охарактеризовать биохимически. Более того, основные молочные белки представлены в молоке в больших концентрациях (обычно приблизительно от 1 до 15 г/л). С коммерческой точки зрения явно предпочтительнее использовать в качестве хозяина представителей такого вида, который отличается высоким уровнем продукции молока. Несмотря на то, что могут быть использованы и более мелкие животные, такие как мыши и крысы (и они даже являются предпочтительными на стадии принципиальной отработки), в рамках настоящего изобретения предпочтительно использование млекопитающих из разряда крупных домашних животных, включая, но не ограничиваясь ими, свиней, коз, овец и крупного рогатого скота. Овца является особенно предпочтительной в силу таких факторов, как предыстория трансгенности у этого вида, выход молока, стоимость и легкодоступное оборудование для сбора овечьего молока. См. публикацию WIPO под номером WO 88/00239 для сравнения факторов, влияющих на выбор вида хозяина. Обычно требуется разведение таких пород домашних животных, которых выращивают для производства молока, таких, например, как восточная овца East Friesland sheep, или же для выведения молочной породы путем разведения трансгенной линии на будущее.
В любом случае следует использовать животных с подтвержденным статусом здоровья.
Для получения экспрессии в молочной железе используется транскрипционный промотор из гена молочного белка. Гены молочных белков включают в себя гены, кодирующие казеины (см. патент США No. 5,304,489, включенный в настоящее описание в виде ссылки), бета-лактоглобулин, альфа-лактальбумин и кислый белок сыворотки. Предпочтительным является промотор бета-лактоглобулина (BLG). В случае овечьего гена бета-лактоглобулина обычно следует использовать область по меньшей мере из 406 п.н., проксимальных по отношению к 5'-фланкирующей последовательности гена, несмотря на то, что предпочтительна более крупная 5'-фланкирующая последовательность, вплоть до 5 т.п.н., такая как сегмент ДНК приблизительно в 4.25 т.п.н., охватывающий 5'-фланкирующий промотор и некодирующую часть гена бета-лактоглобулина. См. Whitelaw et al., Biochem J. 286: 31-39 (1992). Сходные фрагменты ДНК-промотора из других видов также являются приемлемыми.
Другие области гена бета-лактоглобулина также могут быть встроены в конструкции затем, чтобы дать возможность экспрессироваться другим геномным областям гена. В данной области считается общепринятым, что конструкции, лишенные интронов, например, отличаются слабой экспрессией по сравнению с конструкцией, которая содержит такие последовательности ДНК (см. Brinster et al., Proc. Natl. Acad. Sci. USA 85: 836-840 (1988); Palmiter et al., Proc. Nafl. Acad. Sci. USA 88: 478-482 (1991); Whitelaw et al., Transgenic Res. 1: 3-13 (1991); WO 89/01343; и WO 91/02318; каждая из этих публикаций считается включенной в настоящее описание в виде ссылки). В этом отношении обычно предпочтительно, когда это возможно, использовать геномные последовательности, содержащие все или некоторые из нативных интронов гена, кодирующего представляющий интерес белок или полипептид, так что дополнительное включение по меньшей мере некоторых интронов, например, из бета-лактоглобулинового гена является предпочтительным. Одной из таких областей является сегмент ДНК, который обеспечивает сплайсинг интрона и полиаденилирование РНК из 3'-некодирующей области овечьего бета-лактоглобулинового гена. При замене природных 3'-некодирующих последовательностей гена этот сегмент овечьего бета-лактоглобулинового гена может как усиливать, так и стабилизировать уровни экспрессии представляющего интерес белка или полипептида. В рамках остальных воплощений, область, окружающая инициирующий ATG последовательности, кодирующей полипептид человеческого фактора VII, заменена соответствующими последовательностями из гена специфичного молочного белка. Такая замена дает возможность предполагаемому тканеспецифическому инициирующему окружению усиливать экспрессию. Удобно заменить полную препропоследовательность полипептида человеческого фактора VII и 5'-некодирующие последовательности таковыми, например, гена BLG несмотря на то, что в этом случае будут заменены меньшие области.
Для экспрессии полипептида человеческого фактора VII у трансгенных животных сегмент ДНК, кодирующий полипептид человеческого фактора VII, оперативно связан с дополнительными ДНК-сегментами, необходимыми для его экспрессии с получением экспрессирующих единиц. Такие дополнительные сегменты включают в себя указанный выше промотор, а также последовательности, которые обеспечивают терминацию транскрипции и полиаденилирование мРНК. Экспрессирующие единицы, кроме того, будут включать в себя сегмент ДНК, кодирующий секреторную сигнальную последовательность, оперативно связанную с сегментом, кодирующим полипептид человеческого фактора VII. Секреторная сигнальная последовательность может быть нативной секреторной сигнальной последовательностью полипептида человеческого фактора VII или же может быть таковой другого белка, такого как молочный белок. См., например, публикацию von Heinje, Nuc. Acids Res. 14: 4683-4690 (1986); and Meade et al., U. S. Pat. No. 4,873,316, которая включена в настоящее описание в виде ссылки.
Конструкцию экспрессирующих единиц для применения в трансгенных животных удобно осуществлять путем встраивания последовательности, кодирующей полипептид человеческого фактора VII, в плазмидный или фаговый вектор, содержащий дополнительные сегменты ДНК, хотя экспрессирующая единица может быть сконструирована по существу с помощью любой лигирующей последовательности. В частности, удобно получить вектор, содержащий сегмент ДНК, кодирующий молочный белок, и заменить кодирующую последовательность молочного белка таковой полипептида человеческого фактора VII, создав таким образом слитый ген, который включает в себя контролирующие экспрессию последовательности гена молочного белка. В любом случае клонирование экспрессирующих единиц в плазмидах или других векторах облегчает амплификацию полипептида человеческого фактора VII. Амплификацию удобно производить в бактериальных клетках-хозяевах (например, в клетках E. coli), тогда векторы, как правило, будут включать в себя ориджин репликации и селектируемый маркер, функциональный в бактериальных клетках-хозяевах.
Затем экспрессирующая единица встраивается в оплодотворенные яйца (включая ранние эмбриональные стадии) выбранных видов хозяев. Введение гетерологичной ДНК может быть произведено одним из нескольких способов, включая микроинъекции (см., например, патент США No. 4,873,191), ретровирусные инфекции (Jaenisch, Science 240: 1468-1474 (1988)) или сайт-направленную интеграцию с использованием эмбриональных стволовых клеток (ES) (см. обзор Bradley et al., Bio/Technology 10: 534-539 (1992)). Затем яйца имплантировали в яйцеводы или матки псевдобеременных самок, предоставляя им возможность развиваться. Потомок, несущий в своей зародышевой линии встроенную ДНК, может, по Менделю, провести эту ДНК через свое потомство и положить начало развитию стада трансгенных животных. Обычно используемые процедуры для получения трансгенных животных хорошо известны специалистам в данной области. См., например, Hogan et al., Manipulating the Mouse Embryo: A Laboratory Manual, Cold Spring Harbor Laboratory, 1986; Simons et al., Bio/Technology 6: 179-183 (1988); Wall et al., Biol. Reprod. 32: 645-651 (1985); Buhler et al., Bio/Technology 8: 140-143 (1990); Ebert et al., Bio/Technology 9: 835-838 (1991); Krimpenfort et al., Bio/Technology 9: 844-847 (1991); Wall et al., J. Cell. Biochem. 49: 113-120 (1992); патенты США No. 4,873,191 и 4,873,316; публикации международных патентных заявок WO 88/00239, WO 90/05188, WO 92/11757 и заявки Великобритании GB 87/00458, которые включены в настоящее описание в виде ссылки. Технологии включения чужеродных последовательностей ДНК в животное и в стволовые клетки животного первоначально были отработаны на мышах. См., например, Gordon et al., Proc. Natl. Acad. Sci. USA 77: 7380-7384 (1980); Gordon and Ruddle, Science 214: 1244-1246 (1981); Palmiter and Brinster, Cell 41: 343-345 (1985); and Brinster et al., Proc. Natl. Acad. Sci. USA 82: 4438-4442 (1985). Эти технологии впоследствии были адаптированы для применения на более крупных животных, включая разные виды домашнего скота (см., например, публикации международных заявок WO 88/00239, WO 90/05188 и WO 92/11757; а также Simons et al., Bio/Technology 6: 179-183 (1988). Суммируя, следует отметить, что, согласно установленным технологиям, в наиболее эффективном из использующихся на сегодняшний день путей генерации трансгенных мышей или крупного рогатого скота, порядка нескольких сотен линейных молекул представляющей интерес ДНК приходится инъецировать в один из пронуклеусов оплодотворенного яйца. Можно использовать также инъекцию ДНК в цитоплазму зиготы. Можно использовать также продуцирование в трансгенных растениях. Экспрессия может быть генерализованной или направленной на конкретный орган, такой как клубень. См., например, Hiatt, Nature 344: 469-479 (1990); Edelbaum et al., J. Interferon Res. 12: 449-453 (1992); Sijmons et al., Bio/Technology 8: 217-221 (1990); и публикацию европейского патента EP 255,378.
Фактор VII, продуцируемый согласно настоящему изобретению, может быть очищен с помощью метода аффинной хроматографии или же на колонке с антителом против фактора VII. Предпочтительно, чтобы иммуноадсорбционная колонка содержала высокоспецифичное моноклональное антитело. Применение кальций-зависимых моноклональных антител, как описано в публикациях Wakabayashi et al., J. Biol. Chem, 261: 11097-11108, (1986) и Thim et al., Biochem. 27: 7785-7793, (1988), включенных в настоящее описание в виде ссылки, является особенно предпочтительным. Дополнительная очистка может быть предпринята с помощью обычно применяемых химических процедур для очистки, таких, например, как высокоэффективная жидкостная хроматография. Другие способы очистки, включая преципитацию цитратом бария, известны в данной области и могут быть применены для очистки фактора VII, описанного выше (в общем см. Scopes, R., Protein Purification, Springer-Verlag, N. Y., 1982). Для фармацевтических целей существенно чистый фактор VII, гомогенный по меньшей мере на 90 - 95%, является предпочтительным, а наиболее предпочтительной является степень гомогенности порядка 98 - 99% и выше. Частично или до полной гомогенности очищенный, в зависимости от потребностей, фактор VII может затем быть использован в терапевтических целях.
Превращение одноцепочечного фактора VII в активный двухцепочечный фактор VIIa может быть достигнуто с использованием фактора XIIa, как описано Hedner and Kisiel (1983, J. Clin. Invest. 71: 1836-1841), или с использованием других протеиназ, имеющих трипсиноподобную специфичность (Kisiel and Fujikawa, Behring Inst. Mitt. 73: 29-42, 1983). Альтернативно фактор VII может быть аутоактивирован путем пропускания его через ионообменную хроматографическую колонку, такую как моно-Q.RTM (Pharmacia Fire Chemicals) и прочие (Bjoern et al., 1986, Research Disclosures 269: 564-565). Молекулы фактора VII согласно настоящему изобретению и фармацевтические композиции согласно изобретению являются особенно полезными для введения человеку при лечении различных состояний, связанных с внутрисосудистым свертыванием.
Данное изобретение также обеспечивает подходящие подходы для отбора предпочтительных полипептидов фактора VIIa и производных фактора VIIa согласно изобретению. Эти подходы могут быть эффективными при предварительном тестировании in vitro.
Так, в Примере 5 в настоящем описании раскрыт простой тест (названный "гидролизный анализ In Vitro") на активность полипептидов фактора VIIa согласно изобретению. В соответствии с этим, полипептидами фактора VIIa, которые представляют особый интерес, являются такие полипептиды, в которых отношение между активностью варианта и активностью нативного человеческого фактора VII, как показано на Фиг. 1, составляет порядка 1.0 или выше при тестировании с помощью описанного выше "гидролизного анализа In Vitro".
Активность полипептидов может быть оценена также с помощью физиологического субстрата, такого как фактор X ("анализ протеолиза In Vitro") (см. Пример 6), примерно в концентрации 100-1000 нМ, где после добавления соответствующего хромогенного субстрата (например, S-2765) определяют уровень образовавшегося фактора Xa. Более того, анализ активности может проводиться при физиологической температуре.
Способность прокоагулянтных полипептидов фактора VIIa вырабатывать тромбин также может быть измерена с помощью анализа, включающего в себя все релевантные факторы свертывания и ингибиторы при физиологических концентрациях (за минусом фактора VIII в условиях моделирования гемофилии A) и активированные тромбоциты (как описано на странице 543 в публикации Monroe et al. (1997) Brit. J. Haematol. 99, 542-547, которая включена в настоящее описание в виде ссылки).
Производные прокоагулянтного фактора VII согласно настоящему изобретению могут быть использованы для контроля заболеваний, которые связаны с кровотечениями и которые могут быть обусловлены несколькими причинами, такими как дефициты фактора свертывания (например, гемофилии A и B или дефицит факторов свертывания XI или VII), или ингибиторами факторов свертывания, или же они могут быть использованы для контроля избыточного кровотечения, возникающего у субъектов с нормально функционирующим каскадом свертывания крови (в отсутствие дефицитов факторов свертывания или ингибиторов любого из факторов свертывания). Кровотечения могут быть вызваны дефектом функции тромбоцитов, тромбоцитопенией или заболеванием фон Виллебранда. Они могут наблюдаться также и у таких субъектов, у которых под действием различных стимулов индуцируется повышенная фибринолитическая активность.
У субъектов, которые пережили обширное поражение ткани в связи с операцией или обширной травмой, механизм гемостаза в условиях, когда организм испытывает огромную потребность в немедленном гемостазировании, может подавляться, и в результате, вместо нормального механизма гемостазирования, могут развиться кровотечения. Достижение удовлетворительного гемостазирования также является проблемой в тех случаях, когда кровотечения возникают в таких органах, как мозг, глаза и область внутреннего уха, а кроме того, могут возникать проблемы в случаях диффузных кровотечений (геморрагический гастрит и профузное маточное кровотечение), когда бывает трудно идентифицировать источник кровотечения. Такая же проблема может возникать в процессе взятия биопсийных проб из разных органов (из печени, легких, опухолевой ткани, желудочно-кишечного тракта), а также и при лапароскопической хирургии. Эти ситуации создают трудности, связанные с обеспечением гемостаза с помощью хирургических приемов (швы, зажимы и пр.). Острые и профузные кровотечения могут возникать также и при антикоагулянтной терапии у субъектов, у которых дефективный гемостаз индуцирован в результате проводимой терапии. Такие субъекты могут нуждаться в оперативных вмешательствах в случае, когда нужно немедленно противостоять антикоагулянтному эффекту. Другой ситуацией, которая может вызвать проблемы в случае неудовлетворительного гемостаза, является ситуация, когда у субъектов с нормальным механизмом гемостаза проводят антикоагулянтную терапию для предупреждения тромбоэмболического заболевания. Такая терапия может включать в себя гепарин, другие формы протеогликанов, варфарин или другие формы антагонистов витамина K, а также аспирин и другие ингибиторы агрегации тромбоцитов.
Системная активация каскада свертывания может привести к диссеминированному внутрисосудистому свертыванию (ДВС-синдром). Такие осложнения, однако, не возникали у субъектов, которых лечили большими дозами рекомбинантного фактора VIIa, потому что локализованный гемостатический процесс такого типа, индуцируемый образованием комплекса между фактором VIIa и тканевым фактором (TF), экспонированным в сайте повреждения сосудистой стенки. Таким образом, производные прокоагулянтного фактора VII согласно настоящему изобретению могут быть использованы также и в своей активной форме для контроля таких избыточных кровотечений, ассоциированных с нормальным механизмом гемостаза.
Для лечения в связи с преднамеренными вмешательствами производные прокоагулянтного фактора VII согласно настоящему изобретению, как правило, должны назначаться приблизительно в течение 24 часов перед вмешательством, а также в течение 7 или более дней после него. Введение фактора свертывания можно производить различными путями, как описано в настоящей заявке.
Доза производных фактора VII варьирует приблизительно от 0.05 мг до 500 мг в день, предпочтительно приблизительно от 1 мг до 200 мг в день, и еще более предпочтительно приблизительно от 10 мг примерно до 175 мг в день для пациента весом 70 кг в качестве загрузочной и поддерживающей доз, в зависимости от тяжести состояния.
Фармацевтические композиции первоначально были предназначены для парентерального введения для профилактического и/или терапевтического лечения. Предпочтительно фармацевтические композиции вводятся парентерально, например внутривенно, подкожно или внутримышечно, или же они могут быть введены путем непрерывной или пульсационной инфузии. Композиции для парентерального введения включают в себя производное фактора VII согласно изобретению предпочтительно в комбинации с фармацевтически приемлемым носителем, в котором оно растворено, предпочтительно с водным носителем. Могут быть использованы различные водные носители, такие как вода, забуференная вода, 0.4% соляной раствор, 0.3% глицин и т.п. Производные фактора VII согласно изобретению могут быть также составлены в липосомные препараты для доставки или нацеливания на сайты повреждения. Липосомные препараты в общем описаны, например, в патентах США 4,837,028, 4,501,728 и 4,975,282. Композиции могут подвергаться стерилизации с использованием обычных, хорошо известных способов стерилизации. Результирующие водные растворы могут быть расфасованы для применения [в жидком виде] или же отфильтрованы в асептических условиях и лиофилизированы, а перед употреблением будут объединяться со стерильным водным раствором. Эти композиции могут содержать фармацевтически приемлемые дополнительные вещества, если нужно приблизить их к физиологическим условиям, такие, например, как вещества для доведения рН и забуферивающие агенты, как вещества для установления тоничности раствора, такие, например, как ацетат натрия, лактат натрия, хлорид натрия, хлорид калия, хлорид кальция и т.д.
Концентрация производного фактора VII в этих композициях может широко варьировать, например, приблизительно менее чем от 0.5% по весу, обычно приблизительно по меньшей мере от 1% по весу, вплоть до 15 или 20% по весу, и будет отбираться прежде всего по объемам жидкости, по вязкости и т.д., в соответствии с конкретно выбранным способом введения.
Таким образом, типичная фармацевтическая композиция для внутривенного введения может быть составлена таким образом, что в ней будет содержаться вплоть до 250 мл стерильного раствора Рингера и 10 мг полипептида фактора VII. Актуальными способами получения парентерально вводимых композиций являются способы, хорошо известные или очевидные для специалистов в данной области и более подробно описанные, например, в Remington's Pharmaceutical Sciences, 18th ed., Mack Publishing Company, Easton, PA (1990).
Композиции, содержащие производные фактора VII согласно настоящему изобретению, могут быть введены в профилактических и/или терапевтических лечебных целях. При терапевтических применениях композиции вводят, как уже было сказано выше, субъекту, уже страдающему заболеванием, в количестве, достаточном для курирования, облегчения или остановки заболевания и его осложнений. Количество, адекватное тому, чтобы эти цели были достигнуты, определяется как "терапевтически эффективное количество". Специалистам в данной области должно быть очевидно, что количества, эффективные для достижения этой цели, будут зависеть от тяжести заболевания или повреждения, а также от веса тела и общего состояния конкретного субъекта. Однако обычно эффективное количество варьирует приблизительно от 0.05 мг примерно вплоть до 500 мг производного фактора VII в день для субъекта весом 70 кг, причем наиболее часто употребляемые дозы составляют приблизительно от 1.0 мг примерно до 200 мг производного фактора VII в день.
Следует иметь в виду, что материалы согласно данному изобретению могут быть использованы в случаях серьезных заболеваний или состояний при серьезных повреждениях, таких как ситуации, когда существует реальная или потенциальная угроза для жизни. В таких случаях, с точки зрения минимизации посторонних веществ и обычно отсутствия иммуногенности у производных человеческого фактора VII в отношении человеческого организма, возможно, а может быть, и необходимо, чтобы лечащий врач назначил заведомо избыточное количество вариантов композиций фактора VII.
При профилактическом применении композиции, содержащие производное фактора VII согласно настоящему изобретению, вводятся субъекту, подверженному заболеванию или в случае, когда существует риск получить повреждение, для усиления свертывающей способности его собственного организма. Такое количество определяется как "профилактически эффективная доза". При профилактических применениях также точные количества будут зависеть от состояния здоровья и от веса тела конкретного субъекта, при этом обычные дозы колеблются приблизительно от 0.05 мг примерно до 500 мг в день, причем наиболее часто употребляемые дозы составляют приблизительно от 1.0 мг примерно до 200 мг в день для субъекта весом 70 кг.
Однократное или многократные введения композиций могут быть осуществлены в дозах, уровень которых, так же, как и путь введения, определяется лечащим врачом. Для амбулаторных больных, нуждающихся в ежедневных поддерживающих дозах, производные фактора VII могут вводиться путем непрерывных инфузий с использованием, например, системы портативного насоса.
Локальная доставка производного фактора VII согласно настоящему изобретению, такая, например, как местная аппликация, может быть выполнена, например, с помощью спрея, перфузии, двухбаллонных катетеров, стентов, встроенных в сосудистые трансплантаты или стенты, гидрогелей, используемых для покрытия из баллонных катетеров, или другими хорошо известными способами. В любом случае фармацевтические композиции должны обеспечивать количество производного фактора VI, достаточное для эффективного лечения конкретного субъекта.
Полипептиды инактивированного фактора VII согласно настоящему изобретению способны связываться с тканевым фактором на клеточной поверхности. Например, DEGR-фактор VIIa связывается с клеточной поверхности с таким же самым или большим сродством, чем фактор VIIa дикого типа. DEGR-фактор VIIa, однако, не обладает ферментативной активностью, хотя он и связывается с тканевым фактором и действует в качестве конкурентного антагониста в отношении фактора VIIa дикого типа, ингибируя таким образом последующие этапы внешного пути свертывания, приводящего к выработке тромбина.
Производные инактивированного фактора VII применимы, в частности, для введения человеку при лечении различных состояний, включая внутрисосудистое свертывание. Например, несмотря на то, что тромбоз глубоких вен и легочную эмболию можно лечить с помощью традиционно применяемых антикоагулянтов, описанные здесь производные инактивированного фактора VII могут быть использованы для предупреждения возникновения тромбоэмболических осложнений у пациентов, входящих в группу высокого риска, таких как пациенты, подвергающиеся хирургическому вмешательству, или пациенты с застойной сердечной недостаточностью. Кроме того, производные инактивированного фактора VII могут действовать в качестве антагонистов индукции свертывания, опосредованной тканевым фактором, таким образом блокируя продукцию тромбина и последующее отложение фибрина. Как таковые, производные инактивированного фактора VII могут быть использованы для ингибирования активности тканевого фактора, в результате приводя, например, к ингибированию свертывания крови, тромбозов и отложения тромбоцитов.
Производные инактивированного фактора VII могут быть полезны, в частности, при лечении гиперплазии интимы, рестеноза в результате острого сосудистого повреждения, тромбоза глубоких вен, артериального тромбоза, постхирургического тромбоза, трансплантационного шунтирования коронарной артерии (аортокоронарный шунт)(CABG), чрескожной (трансдермальной) коронарной ангиопластике (чрескожной катетерной коронаропластике) (PTCA), инсульте, раке, опухолевом метастазировании, ангиогенезе, ишемии/реперфузии, ревматоидном артрите, тромболизе, артериосклерозе и рестенозе после ангиопластики, при острых и хронических показаниях, таких как воспаление, септический шок, септицемии, гипотензии, респираторном дистресс-синдроме у взрослых (ARDS), диссеминированной внутрисосудистой коагулопатии (DIC), легочной эмболии, отложении тромбоцитов, инфаркте миокарда или профилактическом лечении млекопитающих с атеросклеротическими сосудами при наличии риска, связанного с тромбозами. Острые сосудистые поражения представляют собой такие поражения, которые появляются быстро (т. e. в период, насчитывающий от дней до месяцев), в противоположность хроническим сосудистым поражениям (например, атеросклероз), которые развиваются в течение всей жизни. Острые сосудистые поражения часто возникают в результате хирургических процедур, таких как сосудистое реконструирование, при котором используется такая технология ангиопластики, как эндартерэктомия, атерэктомия, установление сосудистого имплантата или им подобные. Гиперплазия может возникать также и как запоздалая реакция, например, в ответ на установление трансплантата или пересадку органов. Поскольку производные инактивированного фактора VII являются более селективными, чем гепарин, обычно связывая только тканевый фактор, который экспонирован в сайтах повреждения, а также поскольку производные инактивированного фактора VII не разрушают другие белки свертывания, представляется, что последние будут более эффективными и менее рискованными с точки зрения возникновения возможных осложнений, связанных с кровотечениями, чем гепарин, в профилактическом применении для предотвращения тромбоза глубоких вен.
Производные инактивированного фактора VII, которые поддерживают связывание тканевого фактора, ингибируют накопление тромбоцитов в сайте сосудистого поражения путем блокирования производства тромбина и последующего отложения фибрина.
Благодаря способности DEGR-фактора VII блокировать выработку тромбина и ограничивать отложение тромбоцитов в сайтах острого сосудистого поражения, производные инактивированного фактора VII, которые поддерживают активность связывания тканевого фактора, но лишены ферментативной активности фактора VIIa, могут быть использованы для ингибирования рестеноза сосудов.
Композиции, содержащие производные инактивированного фактора VII, когда они составлены в фармацевтические композиции, находят применение, в частности, в способах лечения больных, где их можно давать больным, страдающим от различных болезненных состояний, для лечения состояний, связанных со свертыванием. Такие производные инактивированного фактора VII, способные связывать тканевый фактор, но имеющие существенно подавленную способность к каталитической активации других факторов в каскаде свертывания, могут иметь продолжительное время полужизни в плазме и, таким образом, соответственно, более продолжительный период антикоагуляционной активности по сравнению с другими антикоагулянтами. Среди медицинских показаний для применения этих композиций можно указать такие, которые обычно лечат антикоагулянтами, такими, например, как тромбоз глубоких вен, легочная эмболия, инсульт, диссеминированное внутрисосудистое свертывание (DIC), отложение фибрина в легких и почках, ассоциированное с грам-негативной эндотоксемией и инфарктом миокарда. Эти композиции могут быть использованы для ингибирования сосудистого рестеноза, возникающего в результате механического повреждения сосудов, такого как повреждение, вызванное баллонной ангиопластикой, эндартерэктомией, восстановительной атерэктомией, установлением стента, лазерной терапией или rotablation, или вторично возникающего в ответ на сосудистые трансплантаты, стенты, трансплантационное шунтирование или пересадку органов. Таким образом, эти композиции могут быть использованы для ингибирования отложения тромбоцитов и ассоциированных нарушений. Таким образом, способ ингибирования свертывания, сосудистого рестеноза или отложения тромбоцитов включает в себя, например, введение пациенту композиции, содержащей производные инактивированного фактора VII, такие как те, которые содержат по меньшей мере одну аминокислотную замену в каталитической триаде из Ser344, Asp242 и His193, в количестве, достаточном для эффективного ингибирования свертывания, рестеноза сосудов или отложения тромбоцитов. Эти способы также находят свое применение при лечении острого закрытия у субъекта коронарной артерии (например, при остром инфаркте миокарда), которое включает в себя введение производных инактивированного фактора VII, которые включают в себя DEGR-фактор VII и FFR-фактор VII, в сочетании с тканевым активатором плазминогена или стрептокиназой, и могут ускорить индуцированный тканевым активатором плазминогена тромболиз. Производные инактивированного фактора VII назначают до введения тромболитического агента, такого как тканевый активатор плазминогена, в сочетании с ним или же вскоре после него.
Композиции производных инактивированного фактора VII найдут также существенное применение в профилактике кардиогенной эмболии и в лечении тромботических инсультов. В связи с их низкой потенциальной способностью вызывать осложнения, связанные с кровотечениями, и в связи с их селективностью производные фактора VII могут назначаться жертвам инсульта в целях предотвращения распространения окклюзивного артериального тромбоза. Количество вводимых производных фактора VII будет варьировать от пациента к пациенту, в зависимости от природы и степени тяжести инсульта, но обычно дозы будут варьировать в интервале значений, предлагаемых ниже.
Производные инактивированного фактора VII и содержащие их композиции могут быть использованы также и для ингибирования вредных явлений, ассоциированных с ишемической реперфузией. Тяжелая ишемия ткани, органа или конечности может возникать в результате снижения кровотока и может быть ассоциирована с травмой, хирургическими манипуляциями или пониженным кровяным давлением. Одним из осложнений, ассоциированных с тяжелой ишемией, является повышение уровня тканевого фактора в артериальной системе. Эта повышенная экспрессия тканевого фактора, вероятнее всего, стимулирует прокоагулянтный ответ, прежде всего в сосудистом ложе капилляров. Вслед за реперфузией ишемической ткани может образоваться тромб, который может быть либо окклюзивным, либо неокклюзивным. Образование тромбов в сосудистом русле и отложение тромбоцитов вдоль тромба приводит к образованию вторичных ишемических явлений в данной ткани. Образование тромбов и присутствие тромбоцитов вызывает затем образование и высвобождение множества биореактивных факторов, включая такие, которые образуются в процессе свертывания крови, такие как тромбин и фактор X, а также факторы, высвобождаемые из активированных тромбоцитов. Эти факторы, в свою очередь, могут индуцировать образование дополнительных факторов со стороны низлежащих эндотелиальных клеток и клеток гладкой мускулатуры, или же со стороны прилежащих мононуклеарных клеток таких факторов, как TNF-альфа и IL-1. Эти факторы, в свою очередь, могут затем вызвать активацию эндотелиальных клеток, приводящую к повышению уровня различных адгезивных молекул, ассоциированных со связыванием моноцитов и нейтрофилов. Связывание и трансмиграция моноцитов и нейтрофилов, высвобождение этими клетками биологически активных соединений, включая образование свободных радикалов кислорода, может обострить уровень активации и повреждения эндотелиальных клеток. В конце концов, если каскад явлений происходит бесконтрольно, это может привести к системным осложнениям и потенциально - к стимуляции недостаточности многих органов. Путем блокирования согласно изобретению тканевого фактора в результате введения специфического ингибитора связывания тканевого фактора/фактора VII (например, FFR-FVIIa) и, таким образом, блокирования инициации внешнего пути свертывания крови можно предотвратить инициацию каскада явлений, таким образом избегая или минимизируя вредные явления, ассоциированные с ишемией/реперфузией.
Доза производных инактивированного фактора VII, необходимая для предотвращения тромбоза глубоких вен, приблизительно колеблется от 50 мкг до 500 мг в день, чаще от 1 мг до 200 мг в день, и более предпочтительно - приблизительно от 10 до 175 мг в день для пациента весом 70 кг, и введение должно начинаться по меньшей мере приблизительно за 6 часов до оперативного вмешательства и продолжаться по меньшей мере до тех пор, пока больной не будет переведен на амбулаторный режим. Доза производных инактивированного фактора VII, необходимая для лечения рестеноза, у разных пациентов будет варьировать, но обычно она колеблется в пределах, предлагаемых выше.
Композиции, содержащие производные инактивированного фактора VII, обычно должны будут вводиться приблизительно в пределах 24 часов до оперативного вмешательства, а также по меньшей мере в течение 7 и более дней после него. Введение может осуществляться различными путями, как будет дополнительно описано далее. Композиции, содержащие производные инактивированного фактора VII, могут вводиться также системно или локально для установления сосудистых трансплантатов (например, путем покрытия синтетических или модифицированных природных трансплантатов артериальных сосудов) в местах анастомоза, хирургической эндартерэктомии (обычно эндартерэктомии сонной артерии), экстракорпорального шунтирования и т.д.
При лечении установленного тромбоза глубоких вен и/или легочной эмболии доза производных фактора VII колеблется приблизительно от 50 мкг до 500 мг в день, чаще от 1 мг до 200 мг в день, и более предпочтительно - приблизительно от 10 до 175 мг в день для пациента весом 70 кг в качестве нагрузочной и поддерживающей доз, в зависимости от массы пациента и тяжести состояния. В силу того, что вероятность осложнения кровотечениями при инфузиях мала, производными инактивированного фактора VII можно заменить или снизить дозу гепарина в процессе операции или после операции по поводу тромбоэктомии или эмболэктомии.
В случаях острой бактериемии, эндотоксемии или DIC пациенту вводят нагрузочные дозы производного фактора VII, составляющие по меньшей мере примерно от 50 мкг до 500 мг в день, чаще от 1 мг до 200 мг в день, и более предпочтительно - приблизительно от 10 до 175 мг в день для пациента весом 70 кг, при этом поддерживающие дозы составляют от 50 мкг до 500 мг в день, чаще от 1 мг до 200 мг в день для пациента весом 70 кг.
Предпочтительно, чтобы производное фактора VII предпочтительно имело время полужизни (t1/2), превосходящее время полужизни неконъюгированного фактора VII, из которого оно было получено. Предпочтительно, чтобы время полужизни производного фактора VII было увеличено по меньшей мере в 1.5- 2 раза, более предпочтительно - приблизительно в 2- 3 раза, еще более предпочтительно - приблизительно в 5-10 раз, оптимально приблизительно в 100 раз, обычно приблизительно в 6 раз по сравнению со временем полужизни немодифицированного родительского фактора VII.
Общепринятые способы прикрепления полиэтиленгликоля к белкам описаны в патенте США No. 4,179,337, опубликованном 18 декабря 1979 (включен в настоящее описание путем ссылки на описание способов прикрепления полиэтиленгликоля к белкам). Кроме того, другие способы прикрепления полиэтиленгликоля описаны в патенте США No. 5,122,614, опубликованном 16 июня 1992, также включенном в настоящее описание ссылкой на описание способов прикрепления полиэтиленгликоля к белкам. Вероятно, ПЭГ-малеимидо представляет собой наиболее применимый реагент для ПЭГилирования цистеина, однако для специфической модификации цистеина доступны и другие химические вещества.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Настоящее изобретение описано далее более подробно в примерах, со ссылкой на прилагаемые чертежи.
На Фиг. 1 показана структура корректно процессированного человеческого фактора VII свертывания крови, аминокислоты от 1 до 406, с гамма-карбоксилированными остатками Glu (γ) и гликозилированием (*). Стрелка у аминокислотного остатка 152 указывает на сайт, где одноцепочечный фактор VII расщепляется, превращаясь в активированный двухцепочечный фактор VII (FVIIa).
Фиг. 2. Конструкция плазмид для экспрессии полипептидов рекомбинантного человеческого фактора VII. Плазмида pLN174 экспрессирует человеческий фактор VII со связанным пропептидом, в природе ассоциированным с фактором VII.
Далее настоящее изобретение иллюстрируется последующими примерами, которые, однако, приведены не для ограничения объема охраны настоящего изобретения. Признаки, представленные в приведенном выше описании и в последующих примерах, могут, порознь или в любой комбинации друг с другом, послужить основой для реализации изобретения в виде различных его возможных вариантов.
ПРИМЕРЫ
В последующих примерах используется следующая терминология для аминокислотных замен. Первая буква означает аминокислоту, природно присутствующую в положении последовательности SEQ ID NO: 1. Последующий номер означает положение в последовательности SEQ ID NO: 1. Вторая буква означает другую аминокислоту, заменяющую природную аминокислоту. Примером может служить R396C, где аргинин в положении 396 последовательности SEQ ID NO: 1 заменен на цистеин. В другом примере, V158T/M298Q, валин в положении 158 последовательности SEQ ID NO: 1 заменен на треонин, а метионин в положении 298 последовательности SEQ ID NO: 1 заменен на глутамин в одном и том же полипептиде фактора VII.
Пример 1
Конструкция ДНК, кодирующая FVII-(R396C), FVII-(Q250C), FVII-(P406C), FVII-(407C), FVII-(V158T/M298Q), FVII-(L305V/M306D/D309S), FVII-(K337A), FVII-(L305V) и FVII- (F374P)
Конструкции ДНК, кодирующие FVII-(R396C), FVII-(Q250C), FVII-(P406C), FVII-(407C) (один дополнительный C-концевой цистеин), FVII-(M298Q), FVII-(L305V/M306D/D309S), FVII- (K337A), FVII-(L305V) и FVII-(F374P), были получены методом сайт-направленного мутагенеза с помощью суперскрученной, двухцепочечной ДНК-вектора со вставкой человеческого фактора FVII (pLN174) и двух синтетических праймеров, содержащих требуемую мутацию. Были использованы следующие праймеры:

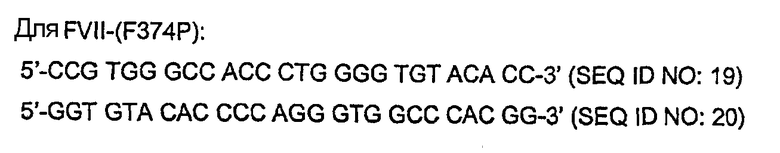
Олигопептидные праймеры, каждый из которых комплементарен противоположной цепи инсерционного вектора, удлиняли в процессе циклической смены температур с помощью ДНК-полимеразы Pfu. При включении праймеров вырабатывалась мутированная плазмида, содержащая смещенные ники. После температурной циклической реакции продукт обрабатывали с помощью Dpnl, которая является специфической в отношении метилированной и полуметилированной ДНК, для расщепления родительской ДНК-матрицы и отбора синтезированных ДНК, содержащих мутацию.
Процедуры получения конструкции ДНК с помощью полимеразной цепной реакции с использованием специфических праймеров хорошо известны специалистам в данной области (ср. PCR Protocols, 1990, Academic ress, San Diego, California, USA).
Пример 2
Получение FVII-(R396C)
Клетки BHK трансфицировали в основном, как было описано ранее (Thim et al. (1988) Biochemistry 27, 7785-7793; Persson and Nielsen (1996) FEBS Lett. 385, 241-243) для получения экспрессии варианта FVII-(R396C). Полипептид фактора VII подвергали очистке следующим образом.
Кондиционированную среду загружали в 25-миллилитровую колонку Q Sepharose Fast Flow (Pharmacia Biotech) после добавления 5 мМ EDTA, 0.1% Triton X-100 и 10 мМ Tris, доведения pH до 8,0 и доведения проводимости до 10-11 мСм/см путем добавления воды. Элюирование белка выполняли в градиенте от 10 мМ Tris, 50 мМ NaCl, 0,1% Triton X-100, pH 8,0 до 10 мМ Tris, 50 мМ NaCl, 25 мМ CaCl2, 0.1% Triton X-100, pH 7,5. Фракции, содержащие FVII-(R396C), собирали и наносили на 25-мл колонку, содержащую моноклональное антитело F1A2 (Novo Nordisk, Bagsvaerd, Denmark), связанное с CNBr-активированной Сефарозой 4B (Pharmacia Biotech). Колонку уравновешивали 50 мМ Hepes, pH 7,5, содержащим 10 мМ CaCl2, 100 мМ NaCl и 0,02% Triton X-100. После промывания уравновешивающим буфером и уравновешивающим буфером, содержащим 2 M NaCl, связанный материал элюировали уравновешивающим буфером, содержащим 10 мМ ЭДТА вместо CaCl2. Перед употреблением или хранением добавляли избыток CaCl2 по сравнению с ЭДТА, или FVII-(R396C) переносили в Ca2+-содержащий буфер. Выход продукта на каждой стадии контролировали путем измерения уровня фактора VII в методе ELISA, а очищенный белок подвергали анализу методом SDS-PAGE.
Пример 3
Получение FVII-(M298Q)
Клетки BHK трансфицировали в основном, как было описано ранее (Thim et al. (1988) Biochemistry 27, 7785-7793; Persson and Nielsen (1996) FEBS Lett. 385, 241-243) для получения экспрессии варианта FVII-(V158T/M298Q). Полипептид фактора VII подвергали очистке следующим образом:
Кондиционированную среду загружали в 25-миллилитровую колонку Q Sepharose Fast Flow (Pharmacia Biotech) после добавления 5 мМ ЭДТА, 0,1% Triton X-100 и 10 мМ Tris, доведения pH до 8,0 и доведения проводимости до 10-11 мСм/см путем добавления воды. Элюирование белка выполняли в градиенте от 10 мМ Tris, 50 мМ NaCl, 0,1% Triton X-100, pH 8,0 до 10 мМ Tris, 1 M NaCl, 5 мМ CaCl2, 0,1% Triton X-100, pH 7,5. Фракции, содержащие FVII-(V158T/M298Q), собирали, добавляли 10 мМ CaCl2 и наносили на 25-мл колонку, содержащую моноклональное антитело F1A2 (Novo Nordisk, Bagsvaerd, Denmark), связанное с CNBr-активированной Сефарозой 4B (Pharmacia Biotech). Колонку уравновешивали 50 мМ Hepes, pH 7.5, содержащим 10 мМ CaCl2, 100 мМ NaCl и 0,02% Triton X-100. После промывания уравновешивающим буфером и уравновешивающим буфером, содержащим 2 M NaCl, связанный материал элюировали уравновешивающим буфером, содержащим 10 мМ ЭДТА вместо CaCl2. Перед употреблением или хранением добавляли избыток CaCl2 по сравнению с ЭДТА, или FVII-(V158T/M298Q) переносили в Ca2+-содержащий буфер. Выход продукта на каждой стадии контролировали путем измерения уровня фактора VII в методе ELISA, а очищенный белок подвергали анализу методом SDS-PAGE.
Пример 4
Получение FVII-(L305V/M306D/D309S)
Клетки BHK трансфицировали в основном, как было описано ранее (Thim et al. (1988) Biochemistry 27, 7785-7793; Persson and Nielsen (1996) FEBS Lett. 385, 241-243) для получения экспрессии варианта FVII-(L305V/M306D/D309S). Полипептид фактора VII подвергали очистке следующим образом:
Кондиционированную среду загружали в 25-миллилитровую колонку Q Sepharose Fast Flow (Pharmacia Biotech) после добавления 5 мМ ЭДТА, 0,1% Triton X-100 и 10 мМ Tris, доведения pH до 8,0 и доведения проводимости до 10-11 мСм/см путем добавления воды. Элюирование белка выполняли в градиенте от 10 мМ Tris, 50 мМ NaCl, 0,1% Triton X-100, pH 8,0 до 10 мМ Tris, 1 M NaCl, 5 мМ CaCl2, 0,1% Triton X-100, pH 7,5. Фракции, содержащие FVII-(L305V/M306D/D309S), собирали, добавляли 10 мМ CaCl2 и наносили на 25-мл колонку, содержащую моноклональное антитело F1A2 (Novo Nordisk, Bagsvaerd, Denmark), связанное с CNBr-активированной Сефарозой 4B (Pharmacia Biotech). Колонку уравновешивали 50 мМ Hepes, pH 7.5, содержащим 10 мМ CaCl2, 100 мМ NaCl и 0,02% Triton X-100. После промывания уравновешивающим буфером и уравновешивающим буфером, содержащим 2 M NaCl, связанный материал элюировали уравновешивающим буфером, содержащим 10 мМ ЭДТА вместо CaCl2. Перед употреблением или хранением добавляли избыток CaCl2 по сравнению с ЭДТА, или FVII-(L305V/M306D/D309S) переносили в Ca2+-содержащий буфер. Выход продукта на каждой стадии контролировали путем измерения уровня фактора VII в методе ELISA, а очищенный белок подвергали анализу методом SDS-PAGE.
Пример 5
Анализ гидролиза In Vitro
Нативный (дикого типа) фактор VIIa и вариант фактора VIIa (оба далее будут обозначаться как "фактор VIIa") параллельно изучали путем прямого сравнения их специфических активностей. Анализ проводили в микротитрационном планшете (MaxiSorp, Nunc, Denmark). Хромогенный субстрат D-Ile-Pro-Arg-пара-нитроанилид (S-2288, Chromogenix, Sweden), конечная концентрация которого составляла 1 мМ, добавляли к фактору VIIa (конечная концентрация 100 нМ) в 50 мМ Hepes, pH 7.4, содержащем 0.1 M NaCl, 5 мМ CaC12 и 1 мг/мл бычьего сывороточного альбумина. Поглощение при 405 нм непрерывно изучали в устройстве для считывания планшетов SpectraMaxTM340 (Molecular Devices, USA). Поглощение, развиваемое в течение 20-минутной инкубации, после вычитания из этого значения поглощения в контрольной лунке, не содержащей фермента, использовали для вычисления отношения между активностями варианта фактора VIIa и фактора VIIa дикого типа:
Отношение=(A405 нм вариант фактора VIIa)/(A405 нм фактор VIIa дикого типа).
Пример 6
Анализ протеолиза In Vitro
Нативный (дикого типа) фактор VIIa и вариант фактора VIIa (оба далее будут обозначаться как "фактор VIIa") параллельно изучали путем прямого сравнения их специфических активностей. Анализ проводили в микротитрационном планшете (MaxiSorp, Nunc, Denmark). Фактор VIIa (10 нМ) и фактор X (0.8 мкМ) in 100 мкл 50 мМ Hepes, pH 7.4, содержащего 0.1 M NaCl, 5 мМ CaC12 и 1 мг/мл бычьего сывороточного альбумина, инкубировали в течение 15 минут. Затем расщепление фактора X останавливали путем добавления 50 мкл 50 мМ Hepes, pH 7.4, содержащего 0.1 M NaCl, 20 мМ ЭДТА и 1 мг/мл бычьего сывороточного альбумина. Количество вырабатываемого фактора Xa измеряли путем добавления хромогенного субстрата Z-D-Arg-Gly-Arg-пара-нитроанилид (S-2765, Chromogenix, Sweden), конечная концентрация которого составляла 0,5 мМ. Поглощение при 405 нм непрерывно изучали в устройстве для считывания планшетов SpectraMaxTM 340 (Molecular Devices, USA). Поглощение, развиваемое в течение 10-минутной инкубации, после вычитания из этого значения поглощения в контрольной лунке, не содержащей FVIIa, использовали для вычисления отношения между протеолитическими активностями варианта фактора VIIa и фактора VIIa дикого типа:
Отношение=(A405 нм вариант фактора VIIa)/(A405 нм фактор VIIa дикого типа).
Пример 7
Относительные активности полипептидов FVIIa, измеренные в пробах, описанных в примерах 5 и 6
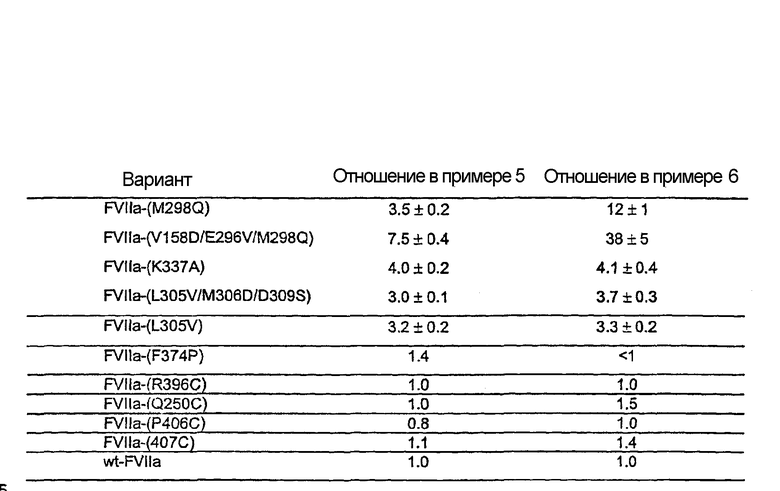
Пример 8
ПЭГ-конъюгирование вариантов факторов FVII-(R396C), FVII-(Q250C), FVII-(P406C), FVII-(407C)
Варианты фактора VIIa, как описано в примере 1, со свободной тиоловой группой, встроенной в любое из указанных положений (250, 396, 406 или 407 (последнее положение добавлено к C-концевому положению)), вводили в реакцию с 5-кратным молярным избытком ПЭГ-винилсульфона или ПЭГ-малеимида (альтернативно может быть использовано любое другое реактивное в отношении сульфгидрильной группы производное ПЭГ) в водном буфере в течение трех часов для проведения реакции до ее фактического завершения. Молекулярная масса ПЭГ-производного составляет по меньшей мере 10000. Полученные в результате ПЭГ-FVIIa тестировали на амидолитическую и протеолитическую активность, как описано в примерах 5 и 6, и в случаях, если выявлялась остаточная активность человеческого фактора FVIIa дикого типа или если Cys был встроен в вариант фактора FVIIa с повышенной активностью, активность после реакции с производным ПЭГ должна оставаться выше, чем активность человеческого фактора FVIIa дикого типа. ПЭГ-конъюгированный FVIIa отделяли от непрореагировавшего варианта FVIIa и свободного производного ПЭГ с помощью хроматографии, такой как гель-фильтрация на колонке Superdex-200 и т.п.
ПЭГ-конъюгирование белков у оснований цистеина хорошо известно специалистам в данной области и описано в нескольких публикациях, включая публикацию Goodson, R. J. & Katre, N. V. (1990) Bio/Technology 8,343 and Kogan, T. P. (1992) Synthetic Comm. 22, 2417.
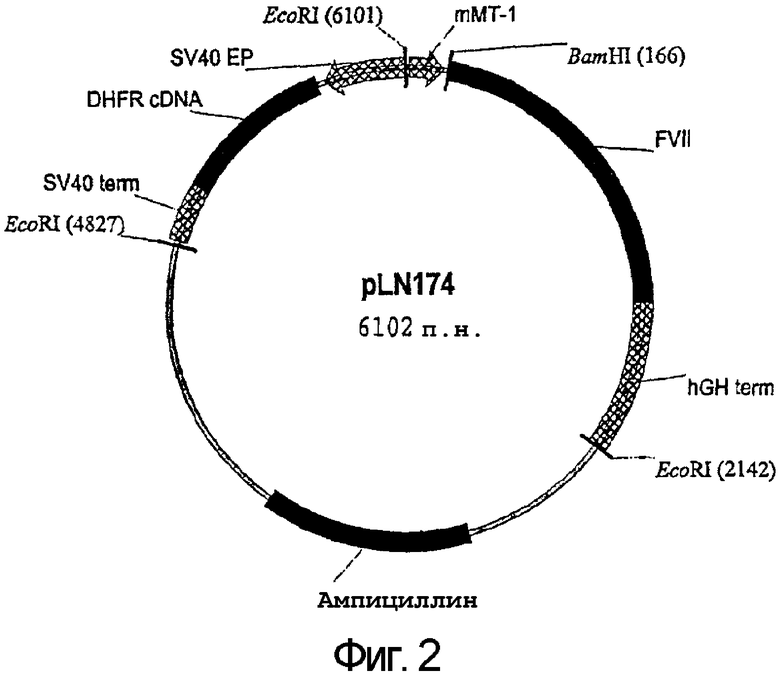
Изобретение относится к области биотехнологии и может быть использовано для получения фактора VII свертывания крови человека. Получают производные полипептида фактора VII с аминокислотными заменами Q250C, R396C и Р406С или с цистеином присоединенным к С-концу нативной последовательности фактора VII. Производные получают с использованием трансгенных технологий в эукариотических клетках-хозяевах млекопитающих. Изобретение позволяет получать производные фактора VII с сохраненной активностью коагуляционного фактора VII человека и с повышенной способностью конъюгировать с ПЭГ, по сравнению с природной формой полипептида. 7 н. и 13 з.п. ф-лы, 2 ил.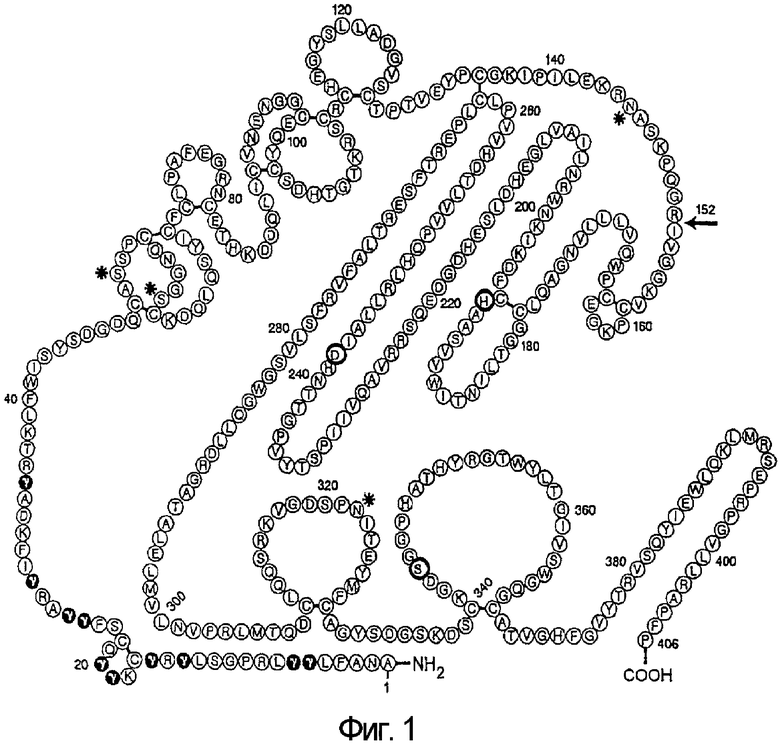
a) продуцирования полипептида фактора VII свертывания крови способом по п.19;
b) конъюгирование полипептида фактора VII свертывания крови с химической группой;
c) нанесение производного фактора VII свертывания крови на колонку катионообменной хроматографии или гель-фильтрационную колонку; и
d) элюирование производного фактора VII свертывания крови.
| WO 9747651, 18.12.1997 | |||
| WO 9612800, 02.05.1996 | |||
| WO 9832466, 03.07.1998 | |||
| WO 9913063, 18.03.1999 | |||
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКА, ОБЛАДАЮЩЕГО ОПОСРЕДОВАННОЙ ФАКТОРОМ VII АКТИВНОСТЬЮ В СВЕРТЫВАНИИ КРОВИ | 1986 |
|
RU2122583C1 |
Авторы
Даты
2008-11-20—Публикация
2002-03-21—Подача