ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способу получения молочной кислоты, при котором культивируют микроорганизм, обладающий способностью молочнокислого брожения, и отделяют молочную кислоту, произведенную в полученной ферментационной среде, и способу получения полимолочной кислоты из молочной кислоты, полученной указанным способом. Настоящее изобретение также относится к молочной кислоте и полимолочной кислоте, полученным этими способами.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Молочная кислота широко используется в пищевых целях, для фармацевтических препаратов и т.п., и также широко применяется в промышленности в качестве мономерного материала для получения полимолочной кислоты, которая является биоразлагаемой пластмассой, так что ее потребление увеличивается. Как известно, молочная кислота вырабатывается при ферментации микроорганизмов, которые преобразуют углеводсодержащие субстраты на основе глюкозы в молочную кислоту.
Чтобы получить молочную кислоту в качестве сырья для полимолочной кислоты, требуется высокопродуктивный способ получения молочной кислоты, поскольку необходимо большое количество молочной кислоты. Для повышения продуктивности по молочной кислоте необходимы высокий выход относительно потребления сахара при микробной ферментации, а также высокая скорость образования молочной кислоты в единицу времени на единицу объема, и в Патентном документе 1 раскрыт способ повышения продуктивности при помощи устройства для культивирования с использованием пористой мембраны.
Полимолочную кислоту можно производить путем полимеризации с раскрытием кольца лактида, который представляет собой циклический димер молочной кислоты, или способом прямой полимеризации исходного сырья в виде молочной кислоты. В лактидном способе молочную кислоту сначала олигомеризуют и затем деполимеризуют, отделяя полученный лактид, который затем подвергают полимеризации с раскрытием цикла в присутствии катализатора. В этом способе процесс полимеризации является сложным и, следовательно, требует больших трудозатрат и расходов. Поскольку в этом процессе примеси в исходном сырье молочной кислоты можно удалять путем процесса отделения лактида, можно использовать молочную кислоту относительно низкого качества. Однако, поскольку примеси в исходном сырье молочной кислоты, такие как неорганические ионы, вызывают уменьшение выхода лактида, который следует отделять, исходное сырье в виде молочной кислоты должно быть относительно свободным от примесей. С другой стороны, в прямом способе полимеризации исходное сырье в виде молочной кислоты подвергается прямой дегидратационной поликонденсации в присутствии катализатора. В этом способе можно ожидать упрощение процесса по сравнению с лактидным способом, однако примеси, которые ингибируют полимеризацию, следует предварительно удалить из исходного сырья в виде молочной кислоты, чтобы обеспечить высококачественное исходное сырье в виде молочной кислоты. Таким образом, эффективность очистки молочной кислоты влияет на повышение продуктивности по лактиду и полимолочной кислоте.
Производство молочной кислоты путем микробной ферментации проводят при добавлении щелочного агента к культуральной среде для поддержания оптимального pH для микробной ферментации, и примеры щелочного агента, который добавляется к культуральной среде, включают гидроксид кальция. В случаях, где использовали гидроксид кальция, молочная кислота, произведенная путем микробной ферментации, присутствует в культуральной среде в виде лактата кальция. Добавляя кислотный агент (например, серную кислоту) к культуральной среде после завершения культивирования, можно получить раствор свободной молочной кислоты, однако соль кальция (например, сульфат кальция) образуется в качестве примеси.
В качестве способа отделения молочной кислоты путем удаления одновременно произведенной соли кальция, в случаях, когда выпадает нерастворимая соль кальция, такая как сульфат кальция, применяется способ фильтрации через качественную фильтровальную бумагу или подобное, однако небольшие количества растворенной в растворе соли кальция не могут быть удалены и остаются в растворе, содержащем молочную кислоту. Поэтому в случаях, когда этот фильтрат, содержащий молочную кислоту, например, концентрируют на более поздней стадии очистки, соли кальция и другие растворимые неорганические соли осаждают из раствора, содержащего свободную молочную кислоту, что являлось проблематичным. Известно, что если содержащий молочную кислоту раствор, из которого не были в достаточной степени удалены неорганические ионы, нагревают в процессе, таком как дистилляция, неорганические ионы способствуют рацемизации и олигомеризации молочной кислоты.
Примеры способа удаления небольших количеств неорганических ионов из раствора, содержащего молочную кислоту, включают способы, использующие ионообменные смолы (например, см. Патентный документ 2). Однако, для поддержания осуществления ионного обмена ионообменной смолой, ионообменную смолу необходимо периодически восстанавливать. Кроме того, так как регенерацию ионообменной смолы выполняют путем использования больших количеств водного раствора гидроксида натрия и водного раствора соляной кислоты, большое количество отработанной жидкости высвобождается во время регенерации, так что требуются большие затраты для утилизации отработанной жидкости, что является проблематичным. Также повторная регенерация ионообменной смолы приводит к уменьшению скорости регенерации ионообменной смолы, а также к ослаблению проведения ионного обмена, приводя к уменьшению скорости удаления неорганических кислот, что является проблематичным.
Кроме того, также известны способы удаления небольших количеств компонентов неорганических ионов, такие как способ удаления кальциевых компонентов из раствора, содержащего молочную кислоту, с использованием электродиализатора с биполярной мембраной (например, см. Патентный документ 3). Однако биполярная мембрана, используемая в этих способах, является дорогостоящей, и эффективность удаления неорганических солей, таких как соли кальция, не обязательно была высокой, что является проблематичным.
Также были раскрыты способы удаления неорганических солей из раствора, содержащего молочную кислоту, с использованием нанофильтрационной мембраны (например, см. Патентные документы 4-6). Однако стадия восстановления молочной кислоты путем дистилляции, эффект дистилляции на выход молочной кислоты и возможность применения полученной молочной кислоты для получения полимолочной кислоты в промышленном масштабе путем прямой полимеризации не был раскрыт.
Также, в Патентных документах 7-10, был раскрыт факт того, что количество специфических примесей должно быть меньше определенных уровней для получения высокомолекулярной полимолочной кислоты, однако не были раскрыты воздействия примесей на термостабильность, механическую прочность и оттенок, которые являются важными факторами пригодности полимолочных кислот для химической переработки.
ДОКУМЕНТЫ УРОВНЯ ТЕХНИКИ
Патентные документы
[Патентный документ 1] WO2007/097260
[Патентный документ 2] Japanese Translated PCT Patent Application Laid-open No. 2001-506274
[Патентный документ 3] JP 2005-270025 A
[Патентный документ 4] US 5503750
[Патентный документ 5] US 5681728
[Патентный документ 6] US 2004/0033573
[Патентный документ 7] JP 6-279577 A
[Патентный документ 8] JP 7-133344 A
[Патентный документ 9] JP 8-188642 A
[Патентный документ 10] JP 9-31170 A
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ЗАДАЧИ, РЕШАЕМЫЕ ИЗОБРЕТЕНИЕМ
Одной из задач настоящего изобретения является предоставление способа получения молочной кислоты с высокой продуктивностью, которую можно применять для получения полимолочной кислоты в промышленном масштабе путем прямой полимеризации и можно применять для высокопродуктивного синтеза лактида; и способов получения лактида и полимолочной кислоты с использованием молочной кислоты. Также настоящее изобретение ставит задачу получения полимолочной кислоты, обладающей превосходной термостабильностью, механической прочностью и цветом, и получения молочной кислоты, в которой количество специфических примесей не превышает определенное количество, а также лактида и полимолочной кислоты, полученных с использованием молочной кислоты в качестве исходного сырья.
СРЕДСТВА ДЛЯ РЕШЕНИЯ ЗАДАЧ
Авторы настоящего изобретения проводили интенсивные исследования, чтобы решить вышеупомянутые задачи, и обнаружили, что культивирование микроорганизма, обладающего способностью продуцировать молочную кислоту в устройстве для непрерывного культивирования с использованием пористой мембраны, дает возможность получать молочную кислоту в фильтрате с высоким выходом и высокой продуктивностью, и путем направления полученного фильтрата на стадию нанофильтрации и стадию дистилляции можно получать молочную кислоту, которая применима для прямой полимеризации и делает возможным высокопродуктивный синтез лактида. Также авторы настоящего изобретения обнаружили, что при использовании молочной кислоты, в которой количество специфических примесей не превышает определенные уровни, в качестве исходного сырья для полимолочной кислоты, можно с высоким выходом получить лактид, обладающий превосходным цветом, и полимолочную кислоту, обладающую превосходной термостабильностью, механической прочностью и цветом, создав таким образом настоящее изобретение.
То есть, настоящее изобретение включает следующие объекты от (1) до (15).
(1) Способ получения молочной кислоты, включающий нижеследующие Стадии от (A) до (C):
(A) стадия непрерывной ферментации, где ферментационную культуральную среду микроорганизма, обладающего способностью молочнокислого брожения, фильтруют через пористую мембрану, обладающую средним размером пор не менее 0,01 мкм и меньше чем 1 мкм с разностью трансмембранного давления в интервале от 0,1 до 20 кПа, и фильтрат собирают, при сохранении неотфильтрованной жидкости в культуральной среде, или возвращении неотфильтрованной жидкости в культуральную среду, и добавлении исходного сырья к культуральной среде;
(B) стадия фильтрования фильтрата, полученного на Стадии (A), через нанофильтрационную мембрану; и
(C) стадия дистилляции фильтрата, полученного на Стадии (B), под давлением не меньше чем 1 Па и не больше атмосферного давления, при не меньше чем 25°C и не больше чем 200°C, для извлечения молочной кислоты.
(2) Способ получения молочной кислоты в соответствии с (1), где pH фильтрата, полученного на Стадии (A), доводят до не менее чем 2 и не более чем 4,5, после чего фильтрат предоставляют для Стадии (B).
(3) Способ получения молочной кислоты в соответствии с (1) или (2), где Стадия (A) является стадией непрерывной ферментации в присутствии соли кальция, и раствор, содержащий молочную кислоту, полученный после Стадии (D), в котором кальциевый компонент в фильтрате, полученном на Стадии (A), удаляют в качестве нерастворимого сульфата, направляют на Стадию (B).
(4) Способ получения молочной кислоты в соответствии с любым из (1)-(3), где соотношение скорости проникновения сульфата магния относительно скорости проникновения лимонной кислоты через нанофильтрационную мембрану составляет не меньше чем 3 при рабочем давлении 0,5 МПа, температуре сырьевой жидкости 25°C и концентрации в сырьевой жидкости 1000 м.д. (ppm, миллионные доли).
(5) Способ получения молочной кислоты в соответствии с любым из (1)-(4), где скорость проникновения сульфата магния через нанофильтрационную мембрану составляет не больше чем 1,5% при рабочем давлении 0,5 МПа, температуре сырьевой жидкости 25°C и концентрация в сырьевой жидкости 1000 м.д.
(6) Способ получения молочной кислоты в соответствии с любым из (1)-(5), где мембранный материал нанофильтрационной мембраны включает полиамид.
(7) Способ получения молочной кислоты в соответствии с (6), где полиамид включает поперечносшитый пиперазинполиамид в качестве главного компонента и дополнительно включает образующий компонент, представленный химической формулой 1:
Химическая Формула 1
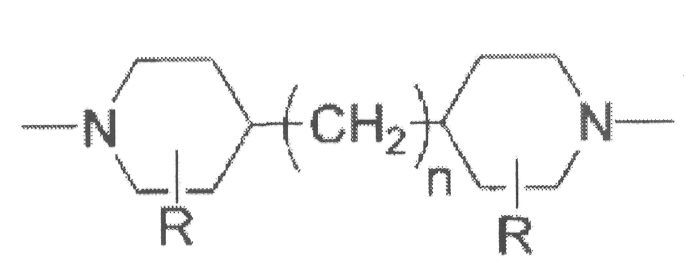
(где R представляет -H или -CH3; и n представляет целое число от 0 до 3).
(8) Способ получения лактида, где молочная кислота, полученная способом в соответствии с любым из (1)-(7), используется в качестве исходного сырья.
(9) Способ получения полимолочной кислоты, где полимеризуют лактид, полученный способом в соответствии с (8).
(10) Способ получения полимолочной кислоты, где молочную кислоту, полученную способом в соответствии с любым из (1)-(7), полимеризируют путем прямой дегидратационной поликонденсации.
(11) Молочная кислота, 90%-ый водный раствор которой содержит метанол в концентрации не больше чем 70 м.д., пировиноградную кислоту в концентрации не больше чем 500 м.д., фурфураль в концентрации не больше чем 15 м.д., 5-гидроксиметилфурфураль в концентрации не больше чем 15 м.д., метиллактат в концентрации не больше чем 600 м.д., уксусную кислоту в концентрации не больше чем 500 м.д. и 2-гидроксимасляную кислоту в концентрации не больше чем 500 м.д.
(12) Молочная кислота в соответствии с (11), обладающая оптической чистотой не меньше чем 90%.
(13) Лактид, полученный при использовании молочной кислоты в соответствии с (11) или (12) в качестве исходного сырья.
(14) Полимолочная кислота, полученная при использовании молочной кислоты в соответствии с (11) или (12) или лактида в соответствии с (13) в качестве исходного сырья.
(15) Полимолочная кислота, полученная путем прямой дегидратационной поликонденсации молочной кислоты в соответствии с (11) или (12) в качестве исходного сырья.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
В соответствии с настоящим изобретением можно производить высококачественную молочную кислоту и можно улучшить продуктивность по полимолочной кислоте, которая является биоразлагаемой пластмассой общего назначения. Кроме того, при использовании молочной кислоты, в которой количество специфических примесей не превышает определенное количество, в качестве исходного сырья для полимолочной кислоты можно получать полимолочную кислоту, обладающую превосходной термостабильностью, механической прочностью и цветом.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 представляет собой схематическую диаграмму, демонстрирующую вариант осуществления устройства для непрерывного культивирования, используемого в настоящем изобретении.
Фиг. 2 представляет собой диаграмму, демонстрирующую концентрацию накопленной молочной кислоты и скорость продуцирования молочной кислоты во время непрерывного культивирования, проводимого в Примере 1 по настоящему изобретению.
Фиг. 3 представляет собой схематическую диаграмму, демонстрирующую вариант осуществления устройства для нанофильтрационного мембранного разделения, используемого в настоящем изобретении.
Фиг. 4 представляет собой схематическую диаграмму, демонстрирующую вариант осуществления поперечного разреза ячейки, в которую помещали нанофильтрационную мембрану, в устройстве для нанофильтрационного мембранного разделения, используемого в настоящем изобретении.
ЛУЧШИЙ СПОСОБ ВЫПОЛНЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение будет теперь описано более подробно.
Способ Получения Молочной Кислоты
Способ получения молочной кислоты по настоящему изобретению включает Стадии (A)-(C) ниже:
(A) Стадия непрерывного культивирования, где культуральную среду для ферментации микроорганизма, обладающего способностью молочнокислой ферментации, фильтруют через пористую мембрану, обладающую средним размером пор не меньше чем 0,01 мкм и меньше чем 1 мкм с разностью трансмембранного давления в интервале от 0,1 до 20 кПа, и фильтрат собирают, при сохранении неотфильтрованной жидкости в культуральной среде или возвращении неотфильтрованной жидкости в культуральную среду, и добавлении сырья для ферментации к культуральной среде;
(B) Стадия фильтрования фильтрата, полученного на Стадии (A), через нанофильтрационную мембрану; и
(C) Стадия дистилляции раствора, полученного на Стадии (B) при давлении не меньше чем 1 Па и не больше чем атмосферное давление, при не меньше чем 25°C и не больше чем 200°C, для извлечения молочной кислоты.
Теперь будет описан микроорганизм, обладающий способностью молочнокислого брожения, который используется на Стадии (A). Микроорганизм, обладающий способностью молочнокислого брожения, не ограничен, при условии, что он может продуцировать молочную кислоту, и предпочтительно может использоваться молочнокислая бактерия или микроорганизм, которому была искусственно придана способность молочнокислого брожения или чья способность молочнокислого брожения была увеличена.
Молочнокислую бактерию можно определить здесь как прокариотический микроорганизм, который производит молочную кислоту с выходом не меньше чем 50% относительно потребляемой глюкозы. Предпочтительные примеры молочнокислой бактерии включают таковые, которые принадлежат роду Lactobacillus, роду Pediococcus, роду Tetragenococcus, роду Carnobacterium, роду Vagococcus, роду Leuconostoc, роду Oenococcus, роду Atopobium, роду Streptococcus, роду Enterococcus, роду Lactococcus, роду Sporolactobacillus и роду Bacillus. Путем отбора среди них, молочнокислой бактерии, демонстрирующей высокий выход молочной кислоты относительно сахарного потребления, бактерию можно предпочтительно использовать при получении молочной кислоты. Кроме того, путем отбора молочнокислой бактерии, демонстрирующей высокий выход L-молочной кислоты или D-молочной кислоты относительно потребления сахара, бактерию предпочтительно можно использовать при получении молочной кислоты, обладающей высокой оптической чистотой.
Примеры молочнокислой бактерии, демонстрирующей высокий выход L-молочной кислоты по отношению к потреблению сахара, включают Lactobacillus yamanashiensis, Lactobacillus animalis, Lactobacillus agilis, Lactobacillus aviaries, Lactobacillus casei, Lactobacillus delbruekii, Lactobacillus paracasei, Lactobacillus rhamnosus, Lactobacillus ruminis, Lactobacillus salivarius, Lactobacillus sharpeae, Pediococcus dextrinicus и Lactococcus lactis, которую можно выбрать и использовать для получения L-молочной кислоты.
Примеры молочнокислой бактерии, демонстрирующей высокий выход D-молочной кислоты по отношению к потреблению сахара, включают Sporolactobacillus laebolacticus, Sporolactobacillus inulinus, Lactobacillus bulgaricus, Lactobacillus casei, Lactobacillus delbruekii и Lactococcus lactis, которую можно выбрать и использовать для получения D-молочной кислоты.
Примеры микроорганизма, которому была искусственно придана способность молочнокислого брожения или чья способность молочнокислого брожения была увеличена, включают микроорганизмы, полученные известным химическим мутагенезом, и микроорганизмы, которым был введен ген лактатдегидрогеназы (который может в дальнейшем упоминаться как LDH), чтобы придать или увеличить способность ферментации молочной кислоты. Предпочтительные примеры этого включают рекомбинантные микроорганизмы, в которые LDH был включен внутриклеточно, чтобы увеличить способность молочнокислого брожения.
Предпочтительные примеры хозяина рекомбинантных микроорганизмов включают прокариотические клетки, такие как E. coli и молочнокислые бактерии; и эукариотические клетки, такие как дрожжи; и хозяином наиболее предпочтительно являются дрожжи. Дрожжи предпочтительно принадлежат роду Saccharomyces, и дрожжи более предпочтительно представляют собой Saccharomyces cerevisiae.
Ген LDH, используемый в настоящем изобретении, не ограничен, при условии, что он кодирует белок, обладающий активностью преобразования восстановленного никотинамидадениндинуклеотида (НАДН) и пировиноградной кислоты до окисленного никотинамидадениндинуклеотида (НАД+) и молочной кислоты. Например, можно использовать ген L-LDH, полученный из молочнокислой бактерии, показывающей высокий выход L-молочной кислоты относительно потребления сахара, или ген D-LDH, полученный из молочнокислой бактерии, показывающей высокий выход D-молочной кислоты относительно потребления сахара. Кроме того, предпочтительные примеры гена L-LDH включают гены, полученные из эукариотов, таких как корова, человек и лягушка, и ген L-LDH, более предпочтительно полученный из Xenopus laevis. Примеры микроорганизмов, в которые вводят ген L-LDH, полученный из лягушки, включают рекомбинантные дрожжи, раскрытые в JP 2008-029329 A.
Примеры гена LDH, используемого в настоящем изобретении, также включают варианты, полученные благодаря генетическому полиморфизмам и мутагенезу. Термин «генетический полиморфизм» означает частичную модификацию последовательности оснований гена благодаря естественной мутации, произошедший в гене. Термин «мутагенез» означает искусственное введение мутации в ген. Примеры способа мутагенеза включают способ, использующий набор для направленного мутагенеза (Mutan-K (произведенный TAKARA BIO INC.)), и способ, использующий набор для случайного мутагенеза (BD Diversify PCR Random Mutagenesis (произведенный CLONTECH)). LDH, используемый в настоящем изобретении, может содержать делецию(и) и/или вставку(ки) в части его последовательности оснований, при условии, что он кодирует белок, обладающий активностью преобразования НАДН и пировиноградный кислоты в НАД+ и молочную кислоту.
Теперь будет описана пористая мембрана, используемая на Стадии (A). Пористая мембрана, используемая в качестве разделяющей мембраны, предпочтительно является менее склонной к засорению микроорганизмом, обладающим способностью молочнокислого брожения, и обладает свойством устойчиво поддерживать осуществление фильтрации в течение долгого времени. Поэтому для пористой мембраны, используемой в настоящем изобретении, важно иметь средний размер пор не меньше чем 0,01 мкм и меньше чем 1 мкм. Пористая мембрана по настоящему изобретению обладает рабочими характеристиками разделения и проницаемости, подходящими для свойств и использования обрабатываемой жидкости, и, с учетом параметров забивки, проницаемости и устойчивости к загрязнениям, которая оказывает воздействие на рабочие характеристики разделения, пористая мембрана предпочтительно представляет собой мембрану, обладающую пористым слоем смолы. В качестве пористой мембраны, обладающей пористым слоем смолы, предпочтительна мембрана с наличием пористого слоя смолы на поверхности пористого материала подложки, слоя, который действует в качестве разделяющего функционального слоя. Пористый материал подложки поддерживает пористый слой смолы, чтобы усилить пористую мембрану.
Пористый материал подложки состоит из органического материала, неорганического материала и/или подобного, и предпочтительно используется органическое волокно. Предпочтительные примеры пористого материала подложки включают тканые материалы и нетканые материалы, подготовленные с использованием органических волокон, таких как целлюлозные волокна, триацетатцеллюлозные волокна, полиэфирные волокна, полипропиленовые волокна и полиэтиленовые волокна, среди которых предпочтительно используются нетканые материалы, так как их плотность можно относительно легко контролировать, они могут быть просты в изготовлении и не являются дорогостоящими.
Органическая полимерная мембрана может соответственно использоваться в качестве пористого слоя смолы, который действует как разделяющий функциональный слой, как упомянуто выше. Примеры материала органической полимерной мембраны включают полиэтиленовые смолы, полипропиленовые смолы, поливинилхлоридные смолы, поливинилидендифторидные смолы, полисульфоновые смолы, полиэфирсульфоновые смолы, полиакрилонитриловые смолы, полиолефиновые смолы, целлюлозные смолы и триацетилцеллюлозные смолы, и материал может представлять собой смесь смол, содержащих эти смолы в качестве основных компонентов. Здесь, основной компонент означает, что компонент содержится в количестве не меньше чем 50% по массе, предпочтительно не меньше чем 60% по массе. Среди них наиболее предпочтительные примеры материала пористой мембраны включают материалы, которые могут быть легко образованы растворами и являются превосходными по физической прочности и химической устойчивости, такие как поливинилхлоридные смолы, поливинилидендифторидные смолы, полисульфоновые смолы, полиэфирсульфоновые смолы, полиакрилонитриловые смолы, полиолефиновые смолы, среди которых наиболее предпочтительно используются поливинилидендифторидные смолы и смолы, содержащие их в качестве главных компонентов.
Здесь, в качестве поливинилидендифторидной смолы, предпочтительно используется гомополимер винилиденфторида, и, помимо гомополимера винилиденфторида, также предпочтительно используется сополимер с виниловыми мономерами, способными к сополимеризации с винилиденфторидом. Примеры виниловых мономеров, способных к сополимеризации с винилиденфторидом, включают тетрафторэтилен, гексафторпропилен и фтортрихлорэтан.
Примеры полиолефиновых смол включают полиэтилен, полипропилен, хлорированный полиэтилен и хлорированный полипропилен, и предпочтительно используется хлорированный полиэтилен.
Теперь будет представлен краткий обзор способа подготовки используемой в настоящем изобретении пористой мембраны. Во-первых, на поверхности вышеупомянутого пористого материала-подложки образуется покрытие начального раствора, содержащего вышеупомянутую смолу и растворитель, при пропитывании начальным раствором пористого материала подложки. После этого только покрытая поверхность пористого материала подложки, обладающего покрытием, приводится в соприкосновение с коагуляционной баней, содержащей осадитель для сгущения смолы, формируя пористый слой смолы на поверхности пористого материала подложки. Осадитель может также содержаться в начальном растворе. Температуру начального раствора обычно предпочтительно выбирают в интервале от 15 до 120°C с учетом пленкообразующих свойств.
К начальному раствору можно добавлять порообразующее вещество. Порообразующее вещество экстрагируется при погружении в коагуляционную ванну, чтобы сделать слой смолы пористым. Добавление порообразующего вещества позволяет регулировать средний размер пор. Порообразующее вещество предпочтительно обладает высокой растворимостью в коагуляционной ванне. Примеры порообразующего вещества, которое можно использовать, включают неорганические соли, такие как хлорид кальция и карбонат кальция. Дополнительные примеры порообразующего вещества, которое может использоваться, включают полиоксиалкилены, такие как полиэтиленгликоль и полипропиленгликоль; водорастворимые макромолекулярные соединения, такие как поливиниловый спирт, поливинилбутираль и полиакриловая кислота; и глицерин.
Растворитель растворяет смолу. Это действует на смолу и порообразующее вещество для стимулирования образования ими пористого слоя смолы. Примеры растворителей, которые можно использовать, включают N-метилпирролидидон (NMP), N,N- диметилацетамид (DMAc), N,N-диметилформамид (ДМФА), диметилсульфоксид (ДМСО), ацетон и метилэтилкетон. Среди них могут предпочтительно использоваться NMP, DMAc, ДМФА и ДМСО, в которых смолы показывают высокую растворимость.
Кроме того, к начальному раствору также можно добавлять осадитель. Осадитель представляет собой жидкость, которая не растворяет смолу. Осадитель обладает действием регулирования скорости коагуляции смолы, чтобы регулировать размеры пор. Примеры осадителя, который может использоваться, включают воду и спирты, такие как метанол и этанол. Среди них вода и метанол являются предпочтительными с точки зрения стоимости. Осадитель может также представлять смесь вышеуказанных веществ.
Как упомянуто выше, пористая мембрана, используемая в настоящем изобретении, предпочтительно является пористой мембраной, образованной пористым материалом подложки и пористым слоем смолы. Пористый материал подложки может быть либо пропитан слоем пористой смолы, либо не пропитан слоем пористой смолы, который выбирают в зависимости от использования. Среднюю толщину пористого материала подложки предпочтительно выбирают в интервале от 50 мкм до 3000 мкм. В случаях, где пористая мембрана представляет собой половолоконную мембрану, внутренний диаметр полого волокна предпочтительно выбирают в интервале от 200 мкм до 5000 мкм, и толщину мембраны предпочтительно выбирают в интервале от 20 мкм до 2000 мкм. Ткань или трикотаж, произведенные путем образования органического волокна или неорганического волокна в цилиндрическую форму, могут содержаться в полом волокне.
Пористая мембрана, используемая в настоящем изобретении, может быть превращена в элемент разделяющей мембраны путем комбинации с подложкой. Форма элемента разделяющей мембраны, обладающего пористой мембраной, не ограничена, и элемент разделяющей мембраны, где поддерживающая пластина используется в качестве подложки и пористая мембрана, используемая в настоящем изобретении, помещается, по крайней мере, на одну сторону поддерживающей пластины, является одним предпочтительным вариантом осуществления элемента разделяющей мембраны, имеющего пористую мембрану, используемую в настоящем изобретении. В случаях, когда трудно обеспечивать большую область мембраны в этом варианте осуществления, размещение пористых мембран с обеих сторон поддерживающей пластины для увеличения проницаемости также является предпочтительным вариантом осуществления.
Средний размер пор пористой мембраны, используемой в настоящем изобретении, составляет не меньше чем 0,01 мкм и меньше чем 1 мкм. Со средним размером пор пористой мембраны в пределах этого диапазона можно достичь высоких блокирующих характеристик, которые не позволяют клеткам просачиваться и отстаиваться, и высокой проницаемости, а также с меньшей вероятностью произойдет засорение, так чтобы проницаемость можно было бы поддерживать с высокой точностью и воспроизводимостью в течение долгого времени. Средний размер пор пористой мембраны предпочтительно не превышает 0,4 мкм, и процесс можно более предпочтительно выполнять при среднем размером пор меньше чем 0,2 мкм. В случаях, где средний размер пор является слишком маленьким, проницаемость может уменьшиться, поэтому средний размер пор составляет в настоящем изобретении не меньше чем 0,01 мкм, предпочтительно не меньше чем 0,02, более предпочтительно не меньше чем 0,04 мкм. Здесь, средний размер пор может быть определен путем измерения диаметров всех пор, которые можно наблюдать в пределах области 9,2 мкм × 10,4 мкм в сканирующий электронный микроскоп при увеличении 10000x, и усреднения измеренных значений.
Далее, стандартное отклонение среднего размера пор составляет предпочтительно не больше чем 0,1 мкм. Кроме того, в случаях, где стандартное отклонение среднего размера пор является небольшим, то есть в случаях, где размеры пор однородны, с большей вероятностью будет получен однородный фильтрат, и, следовательно, возможно более простое управление процессом ферментации, так что стандартное отклонение среднего размера пор предпочтительно является как можно меньшим.
Стандартное отклонение σ среднего размера пор вычисляют в соответствии с Уравнением 1, ниже, где N представляет число пор, наблюдаемых в пределах вышеупомянутой области 9,2 мкм × 10,4 мкм, Xk представляет соответствующие измеренные диаметры, и X(ave) представляет среднее размеров пор.
Уравнение 1
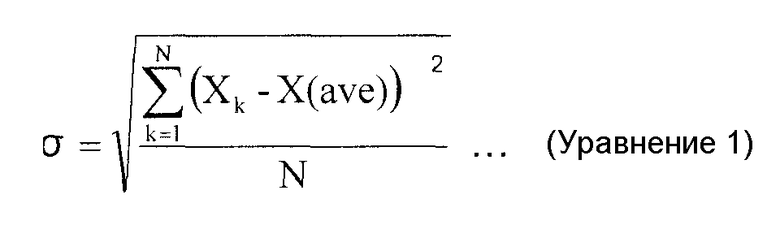
Для пористой мембраны, используемой в настоящем изобретении, проницаемость по отношению к культуральной среде является одним из ее важных свойств. В качестве показателя проницаемости перед использованием может применяться коэффициент проницаемости чистой воды для пористой мембраны. В настоящем изобретении коэффициент проницаемости чистой воды для пористой мембраны составляет предпочтительно не меньше чем 2×10-9 м3/м2/с/Па в случае, когда величину проникновения определяют с использованием очищенной воды при температуре 25°C, подготовленной путем фильтрации через обратноосмотическую мембрану, с главной высотой 1 м, и в случаях, где коэффициент проницаемости чистой воды для пористой мембраны составляет от 2×10-9 м3/м2/с/Па до 6×10-7 м3/м2/с/Па, можно достичь величины проникновения, которая фактически является достаточной.
Шероховатость поверхности мембраны, используемой в настоящем изобретении, является фактором, который воздействует на засорение разделяющей мембраны, и, предпочтительно, в случаях, где шероховатость мембранной поверхности составляет не больше чем 0,1 мкм, коэффициент отделения и мембранное сопротивление разделяющей мембраны могут быть соответственно подавлены, и, следовательно, можно выполнять непрерывную ферментацию при более низкой разнице трансмембранного давления. Следовательно, поскольку можно подавить засорение для обеспечения устойчивой непрерывной ферментации, шероховатость мембранной поверхности предпочтительно должна быть как можно меньше.
Кроме того, в случаях, где шероховатость мембранной поверхности является небольшой, сдвигающая сила, возникающая на мембранной поверхности во время фильтрации микроорганизма, как можно ожидать, будет небольшой, и, следовательно, разрушение микроорганизма может быть подавлено, и засорение пористой мембраны может быть подавлено. Поэтому предполагается, что устойчивая фильтрация возможна в течение продолжительного времени.
Здесь, шероховатость мембранной поверхности можно определить с использованием следующего атомно-силового микроскопа (AFM) при следующих условиях.
Устройство
Атомно-силовой микроскоп (Nanoscope IIIa, произведенный Digital Instruments)
Условия
Исследование: Консоль SiN (произведенная Digital Instruments)
Способ сканирования: Контактный способ (измерение в воздухе)
Способ подводного выявления (подводное измерение)
Область сканирования: 10 мкм × 10 мкм, 25 мкм × 25 мкм (измерение в воздухе)
5 мкм × 5 мкм, 10 мкм × 10 мкм (подводное измерение)
Разрешение сканирования: 512×512
Подготовка образцов
После выполнения измерения мембранный образец вымачивали в этаноле при комнатной температуре в течение 15 минут и затем вымачивали в воде после обратного осмоса в течение 24 часов, с последующими промывкой и высушиванием на воздухе.
Шероховатость мембранной поверхности (drough) вычисляют в соответствии со следующим Уравнением 2 с использованием вышеупомянутого AFM, на основании высот соответствующих пунктов в направлении оси Z.
Уравнение 2
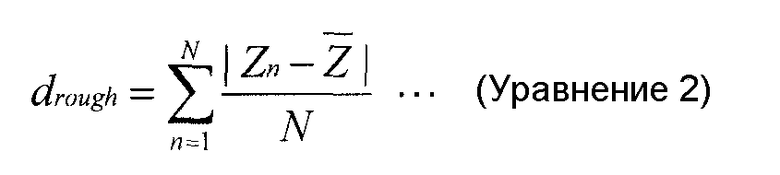
d rough: Шероховатость поверхности (мкм)
Z n: Высота в направлении оси Z (мкм)
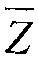 : Средняя высота (мкм) в сканированной области
: Средняя высота (мкм) в сканированной области
N: Число измеренных образцов
Различие трансмембранного давления во время фильтрации микроорганизма через пористую мембрану на Стадии (A) по настоящему изобретению может быть таким, при котором мембрана не быстро забивается микроорганизмом и компонентами среды, и важно выполнять фильтрацию при разности трансмембранного давления в интервале от 0,1 до 20 кПа. Разность трансмембранного давления предпочтительно находится в интервале от 0,1 до 10 кПа, более предпочтительно в интервале от 0,1 до 5 кПа, еще более предпочтительно в интервале от 0,1 до 2 кПа. В случаях, когда разность трансмембранного давления находится не в пределах вышеописанного диапазона, засорение микроорганизмом и компонентами среды может происходить быстро, и величина проникновения может уменьшаться, вызывая проблему во время процесса непрерывной ферментации.
В терминах движущей силы фильтрации можно применять сифон, использующий разницу в уровнях жидкости (различие в гидравлическом напоре) между ферментационной культуральной средой и фильтратом пористой мембраны, для получения различия в трансмембранном давлении в пористой мембране. Также, в качестве движущей силы фильтрации, с фильтрационной стороны пористой мембраны можно поместить отсасывающий насос, или со стороны ферментационной культуральной среды пористой мембраны можно поместить нагнетательный насос. Разницу трансмембранного давления можно контролировать путем изменения различия уровней жидкостей между ферментационной культуральной средой и фильтратом от пористой мембраны. Также, в случаях, где насос используется для получения разницы трансмембранного давления, разницей трансмембранного давления можно управлять при помощи давления всасывания, и кроме того, разницей трансмембранного давления можно управлять давлением газа или жидкости, которая используется для наведения давления со стороны ферментационной культуральной среды. В случаях, где осуществляется такой контроль за давлением, разница между давлением со стороны ферментационной культуральной среды и давлением с фильтрационной стороны пористой мембраны соответствует трансмембранной разнице давления, и может использоваться для контролирования разницы трансмембранного давления.
Устройство для непрерывной ферментации, используемое на Стадии (A), не ограничено, при условии удовлетворения вышеупомянутых условий, и предпочтительные примеры этого включают примеры, раскрытые в Фиг. 1 и Фиг. 2 в W02007/097260. Кроме того, пористый мембранный элемент для фильтрации ферментационной культуральной среды не ограничен, при условии удовлетворения вышеупомянутых условий, и предпочтительные примеры этого включают примеры, раскрытые в фиг. 3 и фиг. 4 в W02007/097260.
Исходное сырье для ферментации, используемое в настоящем изобретении, не ограничено при условии, что оно стимулирует рост культивируемого микроорганизма, обладающего способностью молочнокислого брожения, для обеспечения удовлетворительного получения представляющей интерес молочной кислоты. Предпочтительные примеры исходного сырья для ферментации включают обычные жидкие среды, содержащие источники углерода, источники азота, неорганические соли и, в соответствующих случаях, органические питательные микроэлементы, такие как аминокислоты и витамины, когда необходимо. Примеры источников углерода включают сахар, такой как глюкоза, сахароза, фруктоза, галактоза и лактоза; растворы гидролизованного крахмала, содержащие такие сахара; патоку сладкого картофеля; патоку сахарной свеклы; высококачественную патоку; а также органические кислоты, такие как уксусная кислота; спирты, такие как этанол; и глицерин. Примеры источников азота включают газообразный аммиак, нашатырный спирт, соли аммония, мочевину и соли азотной кислоты; и другие используемые дополнительные источники органического азота, такие как жмых, жидкости на основе гидролизата сои, гидролизаты казеина, прочие аминокислоты, витамины, жидкие кукурузные экстракты, дрожжи или дрожжевые экстракты, мясные экстракты, пептиды, такие как пептоны, и клетки различных ферментируемых микроорганизмов и гидролизатов этого. Примеры неорганических солей, которые могут быть добавлены в соответствующих случаях, включают соли фосфорной кислоты, соли магния, соли кальция, соли железа и соли марганца. В случаях, где используемый в настоящем изобретении микроорганизм, обладающий способностью молочнокислого брожения, требует специфических питательных веществ для своего роста, питательные вещества можно добавлять в качестве препаратов или естественных продуктов, их содержащих. Можно также при необходимости добавлять противовспенивающее вещество. В настоящем изобретении культуральная среда означает жидкость, полученную в результате роста микроорганизма, обладающего способностью молочнокислого брожения в исходном сырье для ферментации, и композиция добавляемого также сырья для ферментации может быть отлична в соответствующих случаях от композиции сырья для ферментации, используемого в начале культивирования, так что продуктивность молочной кислоты увеличивается.
В процессе непрерывного культивирования на Стадии (A), культивирование клеток, выращиваемых в замкнутом объеме, или культивирование с подпиткой можно выполнять в начальной фазе культивирования, чтобы увеличить концентрацию микроорганизма, после чего начинать непрерывное культивирование (извлечение), или клетки можно засевать в высокой концентрации и подвергать непрерывному культивированию с начала культивирования. Можно начинать снабжение средой исходного сырья и извлечение культуры в соответствующие моменты времени. Выбор времени начала снабжения средой исходного сырья и выбор времени начала извлечения культуры не обязательно являются одним и тем же. Снабжение средой исходного сырья и извлечение культуры могут выполняться либо непрерывно, либо периодически. Необходимые для роста клеток питательные вещества, как описано выше, могут добавляться к среде исходного сырья, чтобы обеспечить непрерывный рост клеток. Концентрация микроорганизма в культуральной среде предпочтительно поддерживается высокой в интервале, который не вызывает высокой скорости гибели микроорганизма благодаря окружению культуральной среды, которая является неподходящий для роста микроорганизма, в плане достижения эффективной производительности. Например, поддерживая концентрацию не меньше чем 5 г/л в пересчете на сухую массу, можно получить хорошую экономическую эффективность.
Далее, при необходимости микроорганизм может быть удален из ферментера. Например, поскольку в случаях, где концентрация микроорганизма в ферментере слишком высока и происходит, вероятно, засорение пористой мембраны, можно проводить удаление во избежание засорения. Кроме того, поскольку производительные характеристики для молочной кислоты могут изменяться в зависимости от концентрации микроорганизма в ферментере, удаление микроорганизма можно проводить при использовании производительных характеристик в качестве индикатора, для поддержания производительной характеристики.
Процесс непрерывного культивирования путем предоставления возможности роста свежих клеток, обладающих способностью молочнокислого брожения, обычно выполняют предпочтительно в отдельном ферментере с учетом контроля культуры. Однако число ферментеров не ограничено при условии выполнения непрерывного культивирования для получения продукта, при обеспечении возможности роста клеток. Можно применять множество ферментеров, например, из-за небольшой производительности каждого ферментера. В этом случае высокую продуктивность по продукту ферментации можно получить даже путем непрерывной культуры, используя множество ферментеров, соединенных параллельно или последовательно посредством трубок.
Теперь будет описана фильтрация через нанофильтрационную мембрану на Стадии (B).
Нанофильтрационную мембрану, используемую в настоящем изобретении, также называют нанофильтром (нанофильтрационной мембраной, NF-мембраной), и обычно определяют как «мембрана, которая дает возможность проникновения одновалентных ионов, но блокирует двухвалентные ионы». Мембрана, как полагают, обладает микропустотами, имеющими размеры приблизительно в несколько нанометров, и используется, главным образом, для блокировки мелких частиц, молекул, ионов и солей в воде.
Термин «фильтрация с использованием нанофильтрационной мембраны» означает, что фильтрат со Стадии (A) фильтруют через нанофильтрационную мембрану, чтобы заблокировать или отделить неорганические соли, растворенные или осажденные в качестве твердых частиц, позволяя раствору молочной кислоты проникать в качестве фильтрата. Здесь, неорганические соли включают любую форму неорганических солей, содержащихся в культуральной среде, таких как и растворенные в фильтрате Стадии (A), и как осажденные или преципитированные в фильтрате Стадии (A).
На Стадии (В) предпочтительно доведение pH фильтрата Стадии (A) до не меньше чем 2,0 и не больше чем 4,5. Известно, что вещества, ионизированные в растворе, с большей вероятностью будут удалены или заблокированы нанофильтрационной мембраной, чем неионизированные вещества. Поэтому, доводя pH фильтрата со Стадии (A) до не больше чем 4,5, соотношение молочной кислоты, диссоциированной в молочнокислые ионы, в фильтрате становится небольшим, и это дает возможность более эффективного проникновения молочной кислоты. Кроме того, в случаях, где pH составляет меньше чем 2,0, нанофильтрация может нарушаться. Также, поскольку pKa молочной кислоты составляет 3,86, в случаях, где pH не превышает 3,86, молочная кислота, которая не была диссоциирована на молочнокислые ионы и водородные ионы, содержится в фильтрате со Стадии (A) в большем количестве, так что молочной кислоте можно позволить эффективно проникать через нанофильтрационную мембрану, что является более предпочтительным. Регулирование pH фильтрата со Стадии (A) можно выполнять либо во время проведения микробной ферментации, либо после Стадии (A). Также pH можно доводить путем добавления неорганической или органической кислоты в случаях, где pH фильтрата нужно сделать более кислым, или путем добавления щелочного вещества, такого как гидроксид кальция, или водного раствора аммиака в случаях, где pH нужно сделать более щелочным.
Фильтрат со Стадии (A) для применения с нанофильтрационной мембраной на Стадии (B) предпочтительно подготавливают путем добавления щелочного вещества к культуральной среде на Стадии (A), чтобы поддерживать оптимальный pH для микробной ферментации, и пропускания полученной культуральной среды через пористую мембрану. Микроорганизм обычно культивируют при pH 4-8, температуре от 20 до 40°C. Щелочное вещество, которое добавляется, не ограничено, и предпочтительно добавляют основную соль кальция.
В случаях, когда Стадия (A) является стадией непрерывной ферментации в присутствии соли кальция, Стадия (D), в которой кальциевый компонент в фильтрате на Стадии (A) удаляют как нерастворимый сульфат, может вводиться перед Стадией (B). Конкретнее, например, Стадию (D) выполняют, добавляя серную кислоту к фильтрату Стадии (A) и преципитируя/фильтруя кальциевый компонент в фильтрате Стадии (A) в качестве сульфата кальция, который является нерастворимым сульфатом. Давая возможность фильтрату (отделенной жидкости, содержащей молочную кислоту) пройти через нанофильтрационную мембрану со Стадии (B), кальциевый компонент можно более эффективно удалять или блокировать. Примеры основных солей кальция включают гидроксид кальция, карбонат кальция, фосфат кальция, оксид кальция и ацетат кальция, и основные соли кальция предпочтительно являются гидроксидом кальция. В случаях, где кальциевый компонент в фильтрате Стадии (A) преципитируют/фильтруют в качестве нерастворимого сульфата, если число эквивалентов серной кислоты, добавленных к культуральной среде, превышает число эквивалентов кальция (число эквивалентов серной кислоты > число эквивалентов кальция), избыток серной кислоты частично проникает через нанофильтрационную мембрану. Если это следует за выдержкой фильтрата со Стадии (B) в условиях при нагревании, таких как концентрация или дистилляция, проникшая серная кислота может действовать как катализатор для стимулирования олигомеризации молочной кислоты, приводящей к уменьшению выхода при дистилляции. Поэтому в случаях, где кальциевый компонент в фильтрате со Стадии (A) преципитируется/фильтруется в качестве нерастворимого сульфата, число эквивалентов добавленной серной кислоты предпочтительно составляет не больше, чем число эквивалентов кальциевого компонента в фильтрате со Стадии (A). В случаях, где число эквивалентов добавленной серной кислоты доводят на основе pH, pH предпочтительно составляет не меньше чем 2,0, поскольку в этом случае число эквивалентов серной кислоты не превышает числа эквивалентов кальциевого компонента.
В качестве стадии, предшествующей вышеупомянутой Стадии (D), можно вводить Стадию (E), в которой органические кислоты, отличные от молочной кислоты, удаляют из фильтрата со Стадии (A) при удалении кристаллов лактата кальция. Конкретнее, pH доводят добавлением основного кальция к фильтрату со Стадии (A), и получающийся фильтрат фильтруют через нанофильтрационную мембрану, эквивалентную таковой, используемой на Стадии (B), собирая, таким образом, водный раствор, содержащий лактат кальция, со стороны подачи и удаляя органические кислоты, включая уксусную кислоту, со стороны фильтрата.
На Стадии (E) pH фильтрата со Стадии (A) доводят предпочтительно до не меньше чем 6 и не больше чем 11. Поскольку нанофильтрационные мембраны обладают свойствами, при которых вещества, ионизированные (диссоциированные) в растворе будут блокированы с большей вероятностью, чем неионизированные (недиссоциированные) вещества, то при доведении pH культуральной среды до не меньше чем 6, соотношение молочной кислоты, диссоциированной в ионы в культуральной среде (диссоциированная молочная кислота/недиссоциированная молочная кислота), становится выше, чем соотношение уксусной кислоты, диссоциированной на ионы (диссоциированная уксусная кислота/недиссоциированная уксусная кислота). В этом случае водный раствор, содержащий лактат кальция, можно эффективно собирать со стороны подачи, а органические кислоты, за исключением молочной кислоты, можно эффективно отделять со стороны фильтрата. Кроме того, в случаях, где pH культуральной среды превышает 11, имеет место неблагоприятное воздействие на срок действия нанофильтрационной мембраны, что не является предпочтительным.
На Стадии (E) органические кислоты, за исключением молочной кислоты, отделенной со стороны фильтрата нанофильтрационной мембраны, являются органическими кислотами, полученными из фильтрата со Стадии (A) или из исходного сырья для ферментации, и уксусную кислоту предпочтительно отделяют в настоящем изобретении.
Примеры основного кальция, предпочтительно добавляемого на Стадии (E) для доведения pH фильтрата со Стадии (A), включают гидроксид кальция, карбонат кальция, фосфат кальция, оксид кальция и ацетат кальция в формах твердых частиц и водных растворов, и основным кальцием предпочтительно является гидроксид кальция. В случаях, где добавляют водный раствор, концентрация основного кальция не ограничена, и основной кальций, который следует добавить, может быть в форме жидкого раствора, обладающего концентрацией, превышающей насыщающую растворимость.
Примеры способа оценки степени удаления, блокирования и фильтрации неорганических солей, растворенных или осажденных как твердые частицы нанофильтрационной мембраной, используемой в настоящем изобретении, включают способ оценки, рассчитывающий скорость удаления (скорость блокирования) неорганических ионов, однако способ не ограничен этим. Скорость блокирования (скорость удаления) неорганической соли можно вычислить в соответствии с Уравнением 3 путем измерения концентрации неорганической соли, содержащейся в жидкости исходного сырья (культуральная среда) (концентрация неорганической соли в жидкости исходного сырья), и концентрации неорганической соли, содержащейся в фильтрате (растворе молочной кислоты) (концентрация неорганической соли в фильтрате), путем анализа, представленного ионной хроматографией.
Скорость удаления неорганической соли (%) = (1-(концентрация неорганической соли в фильтрате/концентрация неорганической соли в жидкости исходного сырья))×100.. (Уравнение 3)
Эффективность мембранного разделения нанофильтрационной мембраны, используемой в Стадии (B), не ограничена, и отношение скорости проникновения сульфата магния относительно скорости проникновения лимонной кислоты через нанофильтрационную мембрану предпочтительно составляет не меньше чем 3 при рабочем давлении 0,5 МПа, температуре жидкости исходного сырья 25°C и концентрации в жидкости исходного сырья 1000 м.д. В случаях, где отношение скорости проникновения сульфата магния относительно скорости проникновения лимонной кислоты через нанофильтрационную мембрану при вышеупомянутых условиях составляет не меньше чем 3, можно удалить неорганические соли, содержащиеся в фильтрате Стадии (A), и молочной кислоте можно позволить проникать эффективно, что является предпочтительным. Здесь, скорость проникновения сульфата магния можно рассчитать в соответствии с Уравнением 4 путем определения концентрации сульфата магния, содержащегося в жидкости исходного сырья (концентрация сульфата магния в жидкости исходного сырья), и концентрации сульфата магния, содержавшего в фильтрате (концентрация сульфата магния в фильтрате) путем анализа, представленного ионной хроматографией. Точно так же скорость проникновения лимонной кислоты может быть вычислена путем замены концентрации сульфата магния в Уравнении 4 концентрацией лимонной кислоты и определения концентрации лимонной кислоты, содержащейся в жидкости исходного сырья (концентрация лимонной кислоты в жидкости исходного сырья), и концентрации лимонной кислоты, содержащейся в фильтрате (концентрация лимонной кислоты в фильтрате) путем анализа, представленного высокоэффективной жидкостной хроматографии.
Скорость проникновения сульфата магния (%) = (концентрация сульфата магния в фильтрате)/(концентрация сульфата магния в жидкости исходного сырья)×100.. (Уравнение 4)
Кроме того, скорость проникновения сульфата магния предпочтительно не превышает 1,5% при рабочем давлении 0,5 МПа, температуре жидкости исходного сырья 25°C и концентрации в жидкости исходного сырья 1000 м.д. В случаях, где скорость проникновения сульфата магния через нанофильтрационную мембрану превышает 1,5% при вышеупомянутых условиях, концентрация раствора молочной кислоты, прошедшей через нанофильтрационную мембрану, может вызвать осаждение неорганических солей, и процесс дистилляции, вероятно, вызовет рацемизацию и олигомеризацию благодаря воздействию проникших неорганических солей, и может уменьшить выход при дистилляции. Более предпочтительно, скорость проникновения сульфата магния через нанофильтрационную мембрану составляет не больше чем 1,0%.
Кроме того, предпочтительно используются нанофильтрационные мембраны, обладающие скоростью удаления хлорида натрия (500 мг/л) не меньше чем 45%. С точки зрения эффективности проникновения нанофильтрационной мембраны предпочтительно используется нанофильтрационная мембрана, для которой проточная скорость проникновения хлорида натрия (500 мг/л) на единицу области мембраны (м3/м2/день) при давлении фильтрации 0,3 МПа составляет не меньше чем 0,5 и не больше чем 0,8. Проточная скорость проникновения на единицу области мембраны (мембранный поток проникновения) можно оценить вычислением в соответствии с Уравнением 5 путем определения количества проникшей жидкости, времени сбора проникшей жидкости и мембранной области.
Мембранный поток проникновения (м3/м2/день) = количество прошедшей жидкости/мембранная область/время сбора.. (Уравнение 5)
Примеры материала нанофильтрационной мембраны, который может использоваться в настоящем изобретении, включают макромолекулярные материалы, такие как полимеры ацетатцеллюлозы, полиамиды, полиэфиры, полиимиды и виниловые полимеры. Мембрана не ограничена мембраной, образуемой только одним из материалов, и может представлять собой мембрану, включающую множественные мембранные материалы. С точки зрения структуры мембран, мембрана может являться либо асимметричной мембраной, которая имеет плотный слой, по крайней мере, на одной стороне мембраны и микропоры, имеющие размеры пор, которые постепенно увеличиваются в направлении от плотного слоя к внутренней части мембраны или другой стороне мембраны, либо композитной мембраной, которая имеет очень тонкий функциональный слой, сформированный другим материалом на плотном слое асимметричной мембраны. Примеры композитной мембраны, которая может использоваться, включают сложную мембрану, описанную в JP 62-201606 A, которая обладает нанофильтром, состоящим из полиамидного функционального слоя на мембране подложки, включающей полисульфон в качестве мембранного материала.
Среди них предпочтительна композитная мембрана, имеющая состоящий из полиамида функциональный слой, поскольку она обладает устойчивостью к высокому давлению, высокой проницаемостью и высокой эффективностью удаления раствора, что делает ее мембраной с высоким потенциалом. Для поддержания износоустойчивости против рабочего давления, высокой проницаемости и высокой эффективности блокирования, подходящей является мембрана, обладающая структурой, в которой полиамид используется в качестве функционального слоя, который поддерживается подложкой, включающей пористую мембрану и нетканый материал. Кроме того, в качестве полиамидной полупроницаемой мембраны, подходящей является композитная нанофильтрационная мембрана, имеющая, на подложке, функциональный слой поперечносшитого полиамида, полученного реакцией поликонденсации между полифункциональным амином и полифункциональным кислотным галогенидом.
В нанофильтрационной мембране, обладающей состоящим из полиамидов функциональным слоем, предпочтительные примеры компонента карбоксильных кислот мономеров, составляющих полиамид, включают ароматические карбоксильные кислоты, такие как тримезиновая кислота, бензофенонтетракарбоновая кислота, тримеллитовая кислота, пиромеллитовая кислота, изофталевая кислота, терефталевая кислота, нафталиндикарбоновая кислота, дифенилкарбоксильная кислота и пиридинкарбоновая кислота. Ввиду растворимости пленкообразующих растворителей тримезиновая кислота, изофталевая кислота и терефталевая кислота и их смеси являются более предпочтительными.
Предпочтительные примеры аминового компонента мономеров, составляющих полиамид, включают первичные диамины, имеющие ароматическое кольцо, такие как м-фенилендиамин, п- фенилендиамин, бензидин, метилен-бис-дианилин, 4,4'-диаминобифениловый эфир, дианизидин, 3,3',4-триаминобифениловый эфир, 3,3',4,4'-тетрааминобифениловый эфир, 3,3'-диоксибензидин, 1,8-нафталиндиамин, м(п)-монометилфенилендиамин, 3,3'-монометиламино-4,4'-диаминобифениловый эфир, 4,N,N'-(4- аминобензоил)-п(м)-фенилендиамин-2,2'-бис(4-аминофенилбензимидазол), 2,2'-бис(4-аминофенилбензооксазол) и 2,2'-бис(4-минофенилбензотиазол); и вторичные диамины, такие как пиперазин, пиперидин и их производные. Среди них предпочтительно используется нанофильтрационная мембрана, имеющая функциональный слой, состоящий из поперечносшитого полиамида, включающего пиперазин или пиперидин в качестве мономеров, поскольку она обладает устойчивостью к высокой температуре и химической устойчивостью в дополнение к сопротивлению давления и износоустойчивости. Полиамид более предпочтительно содержит в качестве главного компонента поперечносшитый пиперазинполиамид или поперечносшитый пиперидинполиамид и дополнительно содержит образующие компоненты, представленные химической Формулой (1), еще более предпочтительно содержит поперечносшитый пиперазинполиамид в качестве главного компонента и дополнительно содержит образующий компонент, представленный химической Формулой (1). Кроме того, в химической Формуле (1) предпочтительно n=3. Примеры нанофильтрационной мембраны, обладающей состоящим из полиамида функциональным слоем, содержащим поперечносшитый пиперазинполиамид в качестве главного компонента и дополнительно содержащим образующий компонент, представленный химической Формулой (1), включают описанную в JP 62-201606 A, и конкретные примеры включают UTC60, произведенную TORAY INDUSTRIES, INC., которая является поперечносшитой пиперазинполиамидной полупроницаемой мембраной, имеющей функциональный слой, состоящий из полиамида, содержащего поперечносшитый пиперазинполиамид в качестве главного компонента и дополнительно содержащего образующий компонент, представленный химической Формулой (1), где n=3.
Нанофильтрационная мембрана обычно используется в качестве спирально закрученного мембранного элемента, и нанофильтрационная мембрана, используемая в настоящем изобретении, также предпочтительно используется в качестве спирально закрученного мембранного элемента. Конкретные предпочтительные примеры элемента нанофильтрационной мембраны включают GEsepa, которая представляет собой ацетатцеллюлозную нанофильтрационную мембрану, произведенная GE Osmonics; NF99 и NF99HF, которые являются нанофильтрационными мембранами, обладающими функциональным слоем, состоящим из полиамида, произведенного Alfa-Laval; NF-45, NF-90, NF-200 и NF-400, которые являются нанофильтрационными мембранами, обладающими функциональным слоем, состоящим из поперечносшитого пиперазинполиамида, произведенными корпорацией Filmtec; и SU-210, SU-220, SU-600 и SU-610, которые являются нанофильтрационными мембранными модулями, произведенными TORAY INDUSTRIES, INC., обладающими UTC60, произведенной тем же изготовителем, которая обладает функциональным слоем, состоящим из полиамида, содержащего поперечносшитый пиперазинполиамид в качестве главного компонента и также содержащего образующий компонент, представленный химической Формулой (1). Элемент нанофильтрационной мембраны более предпочтительно представляет собой NF99 или NF99HF, которые являются нанофильтрационными мембранами, обладающими функциональным слоем, состоящим из полиамида, произведенного Alfa-Laval; NF-45, NF-90, NF-200 или NF-400, которые являются нанофильтрационными мембранами, обладающими функциональным слоем, состоящим из поперечносшитого пиперазинполиамида, произведенными корпорацией Filmtec; или SU-210, SU-220, SU-600 или SU-610, которые являются нанофильтрационными мембранными модулями, произведенными TORAY INDUSTRIES, INC., обладающими UTC60, произведенной тем же изготовителем, которая обладает функциональным слоем, состоящим из полиамида, содержащего поперечносшитый пиперазинполиамид в качестве главного компонента и также содержащего образующий компонент, представленный химической Формулой (1). Еще более предпочтительным является элемент нанофильтрационной мембраны SU-210, SU-220, SU-600 или SU-610, которые являются нанофильтрационными мембранными модулями, произведенными TORAY INDUSTRIES, INC., обладающими UTC60, произведенной тем же изготовителем, которая обладает функциональным слоем, состоящим из полиамида, содержащего поперечносшитый пиперазинполиамид в качестве главного компонента и также содержащего образующий компонент, представленный химической Формулой (1).
Фильтрацию через нанофильтрационную мембрану на Стадии (B) можно выполнять под давлением, и фильтрационное давление предпочтительно находится в интервале от 0,1 МПа до 8 МПа. В случаях, где фильтрационное давление составляет меньше чем 0,1 МПа, можно уменьшить скорость мембранного проникновения, в то время как в случаях, где фильтрационное давление составляет больше чем 8 МПа, мембрана может быть повреждена. В случаях, где мембрана используется при фильтрационном давлении в интервале от 0,5 МПа до 7 МПа, поток мембранного проникновения является высоким, так что раствору молочной кислоты можно предоставлять возможность эффективного проникновения, и возможность повреждения мембраны является небольшой, что является более предпочтительным. Мембрана особенно предпочтительно используется при фильтрационном давлении в интервале от 1 МПа до 6 МПа.
Концентрация молочной кислоты на Стадии (B) не ограничена, и в случаях, где концентрация является высокой, концентрация молочной кислоты, содержащейся в фильтрате на Стадии (B), также является высокой, так что можно сократить отрезок времени, требуемый для концентрации, что является предпочтительным ввиду сокращения стоимости.
Концентрации неорганических солей на Стадии (B) не ограничены и могут быть не меньшими, чем насыщающая растворимость. Таким образом, в случаях, где концентрация неорганической соли не превышает насыщающую растворимость, неорганическую соль растворяют в культуральной среде, а в случаях, где концентрация неорганической соли не меньше чем насыщающая растворимость, неорганическая соль частично осаждается. Однако на Стадии (B) как неорганические соли, растворенные в фильтрате со Стадии (A), так и неорганические соли, осажденные или преципитированные в фильтрате Стадии (A), можно удалить или блокировать, так что молочную кислоту можно фильтровать без ограничения концентрациями неорганических солей.
Проницаемость молочной кислоты через нанофильтрационную мембрану после отделения молочной кислоты, содержащейся в фильтрате Стадии (A) вышеупомянутого способа, можно оценить путем расчета скорости проникновения молочной кислоты. Скорость проникновения молочной кислоты можно вычислить в соответствии с Уравнением 6 путем измерения концентрации молочной кислоты, содержащейся в жидкости исходного сырья (культуральная среда) (концентрация молочной кислоты в жидкости исходного сырья), и концентрации молочной кислоты, содержащейся в фильтрате (растворе, содержащем молочную кислоту) (концентрация молочной кислоты в фильтрате), путем анализа, представленного высокоэффективной жидкостной хроматографией.
Скорость проникновения молочной кислоты (%) = (концентрация молочной кислоты в фильтрате/концентрация молочной кислоты в жидкости исходного сырья) × 100.. (Уравнение 6)
В способе получения молочной кислоты по настоящему изобретению фильтрат со Стадии (B) дополнительно подвергается дистилляции на Стадии (C) для получения молочной кислоты с высокой чистотой. Стадию дистилляции выполняют при уменьшенном давлении не меньше 1 Па и не больше чем атмосферное давление (нормальное давление, приблизительно 101 кПа). В случаях, где стадию выполняют при уменьшенном давлении не меньше чем 10 Па и не больше чем 30 кПа, температура дистилляции может быть ниже, что является более предпочтительным. Температура дистилляции в случаях, где стадию выполняют при уменьшенном давлении, не является меньшей, чем 20°C и не превышает 200°C, но в случаях, где дистилляцию выполняют при температуре не меньше чем 180°C, рацемизация молочной кислоты может быть вызвана влиянием примесей. Поэтому дистилляцию молочной кислоты можно предпочтительно выполнять при температуре не меньше чем 50°C и не больше чем 180°C, более предпочтительно не меньше чем 60°C и не больше чем 150°C.
Прежде чем подвергнуть Стадии (C) фильтрат со Стадии (B) можно один раз сконцентрировать, используя концентратор, такой как испаритель, или фильтрат со Стадии (B) можно также подвергнуть Стадии (F), где концентрацию молочной кислоты увеличивают фильтрацией через обратноосмотическую мембрану. В плане уменьшения энергии для концентрации, для увеличения концентрации молочной кислоты путем фильтрации через обратноосмотическую мембрану предпочтительно используется Стадия (F). Обратноосмотическая мембрана здесь означает фильтр для удаления ионов и/или молекул с низкой молекулярной массой, использующий в качестве движущей силы разницу давлений, большую, чем осмотическое давление обрабатываемой жидкости, и примеры этого, которые можно использовать, включают целлюлозные мембраны, такие как изготовленные из ацетата целлюлозы, и мембраны, подготовленные путем поликонденсации многофункционального аминного соединения и многофункционального кислого галогенида для предоставления разделяющего функционального слоя, изготовленного из полиамида на микропористой мембране подложки. Для того чтобы уменьшить грязь, то есть загрязнение, на поверхности обратноосмостической мембраны, можно также предпочтительно использовать слабозагрязняющуюся обратноосмостическую мембрану, которая служит, главным образом, для обработки сточных вод, обратноосмостическая мембрана, которую подготавливают, покрывая разделяющую поверхность изготовленного из полиамида функционального слоя водным раствором соединения, обладающего, по крайней мере, одной реактивной группой, реагирующей с группой кислого галогенида, давая возможность, таким образом, группам кислого галогенида, остающимся на поверхности разделяющего функционального слоя, создавать ковалентные связи с реактивными группами. Поскольку большинство двухвалентных ионов кальция было удалено на Стадии (B) по настоящему изобретению, устойчивые мембранные концентрации можно осуществить без образования солевых отложений на поверхности обратноосмотической мембраны.
Примеры обратноосмотической мембраны, предпочтительно используемой в настоящем изобретении, включают сложные мембраны, имеющие полимер ацетатцеллюлозы в качестве функционального слоя (в дальнейшем называемые ацетатцеллюлозными обратноосмотическими мембранами), и сложные мембраны, имеющие полиамидный функциональный слой (в дальнейшем называемые полиамидными обратноосмотическими мембранами). Здесь, примеры ацетатцеллюлозного полимера включают полимеры, подготовленные с целлюлозными эфирами органических кислот, такие как ацетат целлюлозы, диацетат целлюлозы, триацетат целлюлозы, пропионат целлюлозы и бутират целлюлозы, которые можно использовать исключительно в качестве смеси или в качестве смешанного эфира. Примеры полиамида включают линейные полимеры и поперечносшитые полимеры, образуемые алифатическими и/или ароматическими диаминовыми мономерами.
Примеры формы мембраны, которая может использоваться как соответствующая, включают плоскую мембрану, спирально скрученную мембрану и половолоконную мембрану.
Специфические примеры обратноосмостической мембраны, использованной в настоящем изобретении, включают модули полиамидной обратноосмостической мембраны, произведенные TORAY INDUSTRIES, INC., такие как модули типа низкого давления SU-710, SU-720, SU-720F, SU-710L, SU-720L, SU-720LF, SU-720R, SU-710P и SU-720P, а также модули типа высокого давления SU-810, SU-820, SU-820L и SU-820FA, содержащие UTC70 в качестве обратноосмостической мембраны; ацетатцеллюлозные обратноосмостической мембраны, произведенные тем же самым изготовителем, SC-L100R, SC-L200R, SC-1100, SC-1200, SC-2100, SC-2200, SC-3100, SC-3200, SC-8100 и SC-8200; NTR-759HR, NTR-729HF, NTR-70SWC, ES10-D, ES20-D, ES20-U, ES15-D, ES15-U и LF10-D, произведенные Корпорацией Nitto Denko; RO98pHt, RO99, HR98PP и CE4040C-30D, произведенные Alfa-Laval; GE Sepa, произведенные GE; и BW30-4040, TW30-4040, XLE-4040, LP-4040, LE-4040, SW30-4040 и SW30HRLE-404, произведенные Корпорацией FilmTec.
Молочная Кислота
Настоящие изобретатели обнаружили, что молочная кислота, полученная вышеупомянутым способом получения молочной кислоты, содержит только небольшие количества примесей, и, следовательно, качество молочной кислоты является достаточно высоким для использования при получении полимолочной кислоты путем прямой полимеризации. Кроме того, настоящие изобретатели определили диапазоны содержания примесей, с которыми можно получить высококачественный лактид (исходное сырье для полимолочной кислоты) и полимолочную кислоту, завершая тем самым настоящее изобретение. Первая особенность молочной кислоты по настоящему изобретению состоит в том, что молочная кислота содержит, в качестве примеси в 90%-ом водном растворе молочной кислоты, метанол в концентрации не больше чем 70 м.д., предпочтительно не больше чем 65 м.д., более предпочтительно, не больше чем 50 м.д., еще более предпочтительно, не больше чем 30 м.д. Содержание метанола в 90%-ом водном растворе молочной кислоты можно определить при помощи газовой хроматографии (GC). В случаях, где молочная кислоты содержит, в 90% водном растворе молочной кислоты, метанол больше чем 70 м.д., полимолочная кислота, полученная прямой дегидратационной поликонденсацией молочной кислоты, обладает низкой средневесовой молекулярной массой и низкой механической прочностью, что не является предпочтительным. Кроме того, в случаях, где использовалась молочная кислота, обладающая содержанием метанола больше чем 70 м.д., синтетический выход лактида уменьшался, что не является предпочтительным.
Вторая особенность молочной кислоты по настоящему изобретению состоит в том, что молочная кислота содержит, в качестве примеси в 90%-ом водном растворе молочной кислоты, пировиноградную кислоту в концентрации не больше чем 500 м.д., предпочтительно не больше чем 400 м.д., более предпочтительно, не больше чем 300 м.д. Содержание пировиноградной кислоты в 90%-ом водном растворе молочной кислоты можно определить высокоэффективной жидкостной хроматографией (ВЭЖХ). В случаях, где молочная кислота содержит, в 90%-ом водном растворе молочной кислоты, пировиноградную кислоту больше чем 500 м.д., у полимолочной кислоты, произведенной путем полимеризации молочной кислоты, получается нежелательный цвет. Цвет полимолочной кислоты можно оценить на основании степени окрашивания, и, в качестве индикатора степени окрашивания, можно использовать число цветовых единиц APHA. Число цветовых единиц APHA (число цвета Hazen) представляет собой значение, вычисленное в соответствии со способом измерения JISK0071-1 (установленный 20 октября 1998). Также в случаях, где использовалась молочная кислота, обладающая содержанием пировиноградной кислоты больше чем 500 м.д., синтетический выход лактида уменьшался, и число цветовых единиц APHA увеличивалось, что не является предпочтительным.
Третья особенность молочной кислоты по настоящему изобретению состоит в том, что молочная кислота содержит, в качестве примеси в 90%-ом водном растворе молочной кислоты, фурфураль при концентрации не больше чем 15 м.д., предпочтительно не больше чем 10 м.д., более предпочтительно не больше чем 5 м.д. Содержание фурфураля в 90%-ом водном растворе молочной кислоты можно определить высокоэффективной жидкостной хроматографией (ВЭЖХ). В случаях, где молочная кислоты имеет содержание фурфураля, в 90%-ом водном растворе молочной кислоты, больше чем 10 м.д., у полимолочной кислоты, произведенной полимеризацией молочной кислоты, получается нежелательный цвет и термостабильность. Термостабильность полимолочной кислоты можно оценить на основании тепловой скорости потери массы. Также в случаях, где использовалась молочная кислота, содержащая фурфураль больше чем 15 м.д., у полученного лактида происходит увеличение числа цветовых единиц APHA, что не является предпочтительным.
Четвертой особенностью молочной кислоты по настоящему изобретению является то, что молочная кислота содержит, в качестве примеси в 90%-ом водном растворе молочной кислоты, 5-гидроксиметилфурфураль при концентрации не больше чем 15 м.д., предпочтительно не больше чем 10 м.д., более предпочтительно не больше чем 5 м.д. Содержание 5-гидроксиметилфурфураля в 90%-ом водном растворе молочной кислоты может быть измерено высокоэффективной жидкостной хроматографией (ВЭЖХ). Полимолочная кислота, полученная полимеризацией молочной кислоты, обладающей содержанием, в 90%-ом водном растворе молочной кислоты, 5-гидроксиметилфурфураля больше чем 10 м.д., обладает нежелательным цветом и термостабильностью. Также в случаях, где использовалась молочная кислота, имеющая содержание 5-гидроксиметилфурфураля больше чем 15 м.д., у полученного лактида происходит увеличение числа цветовых единиц APHA, что не является предпочтительным.
Пятой особенностью молочной кислоты по настоящему изобретению является то, что молочная кислота содержит, в качестве примеси в 90%-ом водном растворе молочной кислоты, метиллактат в концентрации не больше чем 600 м.д., предпочтительно не больше чем 400 м.д., более предпочтительно не больше чем 100 м.д. Содержание метиллактата в 90%-ом водном растворе молочной кислоты можно определить газовой хроматографией (GC). В случаях, где молочная кислота содержит, в 90%-ом водном растворе молочной кислоты, метиллактата больше чем 600 м.д., полимолочная кислота, полученная прямой дегидратационной поликонденсацией молочной кислоты, обладает низкой средневесовой молекулярной массой и низкой механической прочностью, что не является предпочтительным. Кроме того, в случаях, где использовалась молочная кислота, имеющая содержание метиллактата больше чем 600 м.д., в полученном лактиде происходит увеличение числа цветовых единиц APHA, что не является предпочтительным.
Шестой особенностью молочной кислоты по настоящему изобретению является то, что молочная кислота содержит, в качестве примеси в 90%-ом водном растворе молочной кислоты, уксусную кислоту в концентрации не больше чем 500 м.д., предпочтительно не больше чем 400 м.д., более предпочтительно не больше чем 300 м.д. Содержание уксусной кислоты в 90%-ом водном растворе молочной кислоты можно определить путем высокоэффективной жидкостной хроматографии (ВЭЖХ). Полимолочная кислота, полученная полимеризацией молочной кислоты, имеющей содержание, в 90%-ом водном растворе молочной кислоты, уксусной кислоты больше чем 500 м.д., обладает нежелательной термостабильностью. Также, в случаях, где использовалась молочная кислота, имеющая содержание уксусной кислоты больше чем 500 м.д., синтетический выход лактида уменьшается, что не является предпочтительным.
Седьмой особенностью молочной кислоты по настоящему изобретению является то, что молочная кислота содержит, в качестве примеси в 90%-ом водном растворе молочной кислоты, 2-гидроксимасляную кислоту в концентрации не больше чем 500 м.д., предпочтительно не больше чем 300 м.д., более предпочтительно не больше чем 200 м.д. Содержание 2-гидроксимасляной кислоты в 90%-ом водном растворе молочной кислоты можно определить высокоэффективной жидкостной хроматографией (ВЭЖХ). Полимолочная кислота, полученная полимеризацией молочной кислоты, содержащая, в 90%-ом водном растворе молочной кислоты, 2-гидроксимасляную кислоту больше чем 500 м.д., имеет нежелательную термостабильность. Кроме того, в случаях, где использовалась молочная кислота, имеющая содержание 2-гидроксимасляной кислоты больше чем 500 м.д., синтетический выход лактида уменьшается, что не является предпочтительным.
Молочная кислота по настоящему изобретению может представлять собой либо одну из (L)-формы или (D)-формы, либо смесь из (L)-формы и (D)-формы. В случаях, где молочная кислота представляет собой смесь, оптическая чистота, которая указывает на содержание изомеров (L)-формы или (D)-формы, составляет предпочтительно не меньше чем 90%, поскольку точка плавления полученной полимолочной кислоты в этом случае является высокой. Оптическая чистота составляет более предпочтительно не меньше чем 95%, еще более предпочтительно не меньше чем 99%, наиболее предпочтительно не меньше чем 99,9%.
В настоящее изобретение также включены лактид, произведенный при использовании молочной кислоты по настоящему изобретению в качестве исходного сырья, и способ получения лактида; и полимолочная кислота, произведенная при использовании молочной кислоты по настоящему изобретению в качестве исходного сырья, и способ получения полимолочной кислоты.
Лактид
Лактид по настоящему изобретению включает L,L-лактид, D,D-лактид и D,L-лактид, которые состоят из L-молочной кислоты и/или D-молочной кислоты. Лактид предпочтительно является L,L-лактидом или D,D-лактидом.
Способ получения лактида не ограничен, и можно предпочтительно использовать общепринятый способ, при котором молочную кислоту нагревают при уменьшенном давлении для получения олигомеров молочной кислоты, которые затем деполимеризуют путем нагревания в присутствии катализатора при уменьшенном давлении, чтобы вызвать трансформирование в лактид. Катализатор, используемый для деполимеризации олигомеров молочной кислоты, не ограничен и обычно является катализатором с на основе металла, выбранного из металлов Группы IA, Группы IIIA, Группы IVA, Группы IIB, Группы IVB и Группы VA в периодической таблице, или содержащим такой металл соединением.
Примеры катализатора на основе металла, относящегося к Группе IA, включают гидроксиды щелочных металлов (например, гидроксид натрия, гидроксид калия и гидроксид лития), соли щелочных металлов со слабыми кислотами (например, лактат натрия, ацетат натрия, карбонат натрия, октилат натрия, стеарат натрия, лактат калия, ацетат калия, карбонат калия и октилат калия) и алкоксиды щелочных металлов (например, натрийметоксид, калийметоксид, натрийэтилат и калийэтилат).
Примеры катализатора на основе металла, относящимся к Группе IIIA, включают алюминийэтилат, алюминийизопропилат, окись алюминия и хлорид алюминия.
Примеры катализатора на основе металла, относящегося к Группе IVA, включают оловоорганические катализаторы (лактат олова, тартрат олова, дикаприлат олова, дилаурат олова, дипальмитат олова, дистеарат олова, диолеат олова, α-нафтоат олова, β-нафтоат олова и октилат олова), а также оловянную пудру, оксид олова и галогениды олова.
Примеры катализатора на основе металла, относящегося к Группе IIB, включают порошок цинка, галогениды цинка, оксид цинка и цинкорганические соединения.
Примеры катализатора на основе металла, относящегося к Группе IVB, включают соединения титана, такие как тетрапропилтитанат; и соединения циркония, такие как изопропилат циркония.
Примеры катализатора на основе металла, относящегося к Группе VA, включают соединения сурьмы, такие как триоксид сурьмы; и соединения висмута, такие как оксид висмута(III).
Среди них катализатор, содержащий олово или соединение олова, является предпочтительным ввиду активности, и особенно предпочтительным является октилат олова.
Количество катализатора, который нужно использовать, составляет приблизительно от 0,01 до 20% по массе, предпочтительно приблизительно от 0,05 до 15% по массе, более предпочтительно приблизительно от 0,1 до 10% по массе, по отношению к олигомерам молочной кислоты.
Реакция деполимеризации может быть выполнена с использованием обычного сосуда для вертикальных реакций, или может быть выполнена с использованием устройства молекулярной дистилляции. Примеры устройства молекулярной дистилляции включают устройства типа вертикального перегонного куба, типа нисходящей пленки и центрифужного типа. Устройства типа нисходящей пленки и центрифужного типа представляют собой устройства непрерывного процесса и широко используются в промышленности. Устройство молекулярной дистилляции центробежного типа использует способ, в котором пленка испаряемого вещества распределяется по горячей поверхности с использованием центробежных сил, а устройство молекулярной дистилляции типа нисходящей пленки использует способ, при котором испаряемому веществу предоставляется возможность стекать вниз по горячей поверхности для образования тонкой пленки выпаренного вещества.
Температуру деполимеризации устанавливают от 160 до 300°C, предпочтительно от 180 до 260°C, более предпочтительно от 190 до 250°C. В случаях, где температура составляет ниже, чем 160°C, дистилляция лактида является затруднительной, и требуется значительно более высокая степень вакуума. С другой стороны, в случаях, где температура составляет выше, чем 300°C, вероятно, имеют место рацемизация и окрашивание.
Давление внутри деполимеризационного устройства не превышает давление пара лактида при температуре деполимеризации и обычно составляет приблизительно 1-50 торр. Более низкое давление предпочтительно, поскольку в этом случае нагревающаяся температура может быть низкой. Конкретнее, давление составляет предпочтительно 1-20 торр, более предпочтительно 1-10 торр, еще более предпочтительно 1-5 торр.
Время нахождения в деполимеризационном устройстве предпочтительно является настолько коротким, насколько возможно ввиду предотвращения рацемизации, и обычно составляет не больше чем 1 час. Использование устройства молекулярной дистилляции предпочтительно, поскольку в этом случае время может составлять не больше чем 10 минут, предпочтительно не больше чем 3 минуты, более предпочтительно не больше чем 1 минута.
Лактид, произведенный способом получения лактида, может быть удален за пределы системы реакции деполимеризации в качестве пара и собран. Сбор лактида можно просто выполнить, используя конденсатор, присоединенный к деполимеризационному устройству.
Полимолочная Кислота
Полимолочная кислота по настоящему изобретению включает гомополимер единиц L-молочной кислоты или D-молочной кислоты; блоксополимер полимолочной кислоты, образованный сегментом, состоящим из единиц поли-L-молочной кислоты, и сегментом, состоящим из единиц поли-D-молочной кислоты; и сополимер с мономерами, отличными от молочной кислоты. В случаях, где полимолочная кислота представляет собой сополимер, примеры мономерных единиц, отличных от молочной кислоты, включают соединения гликоля, такие как этиленгликоль, пропиленгликоль, бутандиол, гептандиол, гександиол, октандиол, нонандиол, декандиол, 1,4-циклогександиметанол, неопентилгликоль, глицерин, пентаэритритол, бисфенол A, полиэтиленгликоль, полипропиленгликоль и политетраметиленгликоль; двухосновные кислоты, такие как щавелевая кислота, адипиновая кислота, себациновая кислота, азелаиновая кислота, додекандиовая кислота, малоновая кислота, глутаровая кислота, циклогександикарбоновая кислота, терефталевая кислота, изофталевая кислота, фталевая кислота, нафталиндикарбоновая кислота, бис(п-карбоксифенил)метан, антрацендикарбоновая кислота, дифениловый эфир дикарбоновой кислоты, натрийсульфоизофталевая кислота и тетрабутилфосфонийизофталевая кислота; гидроксикарбоновые кислоты, такие как гликолевая кислота, гидроксипропионовая кислота, гидроксимасляная кислота, гидроксивалериановая кислота, гидроксикапроновая кислота и гидроксибензойная кислота; и лактоны, такие как капролактон, валеролактон, пропиолактон, ундекалактон и 1,5-оксепан-2-он. Степень сополимеризации вышеописанных других компонентов сополимеризации составляет предпочтительно от 0 до 30 мол.%, более предпочтительно от 0 до 10 мол.% относительно полных мономерных компонентов.
Способ получения полимолочной кислоты не ограничен, и можно использовать обычный способ получения полимолочной кислоты. Конкретные примеры известного способа включают лактидный способ, состоящий из двух стадий, где лактид, который является циклическим димером, сначала производится с использованием молочной кислоты в качестве исходного сырья, после чего выполняется полимеризация с раскрытием кольца; и прямой способ полимеризации, состоящий из единственной стадии, где исходное сырье подвергается прямой дегидратационной поликонденсации в растворителе. Любой из этих способов может использоваться.
В лактидном способе и прямом способе полимеризации продолжительность времени, требуемого для полимеризации, можно сократить при использовании катализатора для реакции полимеризации. Примеры катализатора включают металлы, такие как олово, цинк, свинец, титан, висмут, цирконий, германий, сурьма и алюминий, и производные этого. Производные предпочтительно представляют собой металлические алкоксиды, карбоксилаты, карбонаты, оксиды и галогениды. Конкретные примеры включают хлорид олова, ацетат олова, октилат олова, хлорид цинка, оксид свинца, карбонат свинца, хлорид титана, алкоксититан, оксид германия и оксид циркония. Среди них предпочтительны соединения олова, и более предпочтительными являются ацетат олова и октилат олова.
Реакцию полимеризации можно проводить в присутствии вышеупомянутого катализатора обычно при температуре от 100 до 200°C, хотя температура изменяется в зависимости от типа катализатора. Кроме того, для удаления воды, произведенной путем реакции полимеризации, реакцию полимеризации предпочтительно выполняют при уменьшенном давлении, и давление предпочтительно составляет не больше чем 7 кПа, более предпочтительно не больше чем 1,5 кПа.
Для реакции полимеризации соединение, имеющее две или несколько гидроксильных групп или аминогрупп в молекуле, может использоваться в качестве инициатора полимеризации. Примеры соединения, используемого в качестве инициатора полимеризации, которое имеет две или несколько гидроксильных групп или аминогрупп в молекуле, включают полиолы, такие как этиленгликоль, пропиленгликоль, бутандиол, гександиол, октандиол, неопентилгликоль, диэтиленгликоль, триэтиленгликоль, полиэтиленгликоль, полипропиленгликоль, глицерин, триметилолпропан, пентаэритритол, дипентаэритритол, трипентаэритритол, сорбитол, поли(виниловый спирт), поли(гидроксиэтилметакрилат) и поли(гидроксипропилметакрилат); и поливалентные амины, такие как этилендиамин, пропилендиамин, бутандиамин, гександиамин, диэтилентриамин и меламин; среди которых более предпочтительны полиолы.
Количество добавляемого инициатора полимеризации не ограничено и составляет предпочтительно от 0,001 до 5 частей по массе, более предпочтительно от 0,01 до 3 частей по массе относительно 100 частей по массе используемого исходного сырья (L-молочная кислота, D-молочная кислота, L,L-лактид или D,D-лактид).
В случаях, где полимолочная кислота производится прямым способом полимеризации, используемая в качестве исходного сырья молочная кислота должна быть очень чистой, и молочную кислоту по настоящему изобретению можно адекватно применять в прямом способе полимеризации. Растворитель, используемый для прямого способа полимеризации, не ограничен, при условии, что он не оказывает неблагоприятного воздействия на полимеризацию, и может представлять собой воду или органический растворитель. Примеры органического растворителя включают ароматические углеводороды. Примеры ароматических углеводородов включают толуол, ксилол, нафталин, хлорбензол и дифениловый эфир. В случаях, где полимолочную кислоту производят прямым способом полимеризации, полимеризацию проводят путем удаления воды, произведенной при реакции полимеризации, за пределы системы. Способом удаления за пределы системы предпочтительно является полимеризация при уменьшенном давлении, и давление составляет предпочтительно не больше чем 7 кПа, более предпочтительно не больше чем 1,5 кПа.
Полимолочная кислота по настоящему изобретению характеризуются средневесовой молекулярной массой не меньше чем 120000, скоростью тепловой потери массы меньше чем 6,5% под атмосферой азота при постоянной температуре 200°C с временем нагревания 20 минут, и числом цветовых единиц APHA не больше чем 15. В случаях, где средняя молекулярная масса полимолочной кислоты составляет не меньше чем 120000, предпочтительно не меньше чем 140000, полимолочная кислота обладает превосходной механической прочностью; в случаях, где скорость тепловой потери массы составляет меньше чем 6,5%, предпочтительно не больше чем 6,0%, полимолочная кислота обладает превосходной термостабильностью; и в случаях, где APHA составляет не больше чем 15, предпочтительно не больше чем 10, полимолочная кислота обладает превосходным цветом; так что полимолочная кислота по настоящему изобретению, которая удовлетворяет этим физическим свойствам, является подходящей для различных применений, таких как волокна, пленки и формованные изделия.
ПРИМЕРЫ
Настоящее изобретение теперь будет описано более подробно, однако настоящее изобретение не ограничено Примерами, приведенными ниже.
В настоящем изобретении в качестве микроорганизма, обладающего способностью ферментации L-молочной кислоты, использовался Saccharomyces cerevisiae, в хромосому которого был введен ген L-лактатдегидрогеназы (ген L-LDH), полученный из Xenopus laevis, обладающий последовательностью оснований, приведенной в SEQ ID NO:1.
Справочный Пример 1: Подготовка штамма дрожжей, обладающего способностью ферментации L-молочной кислоты
Штамм, производный от штамма B3, описанного в JP 2008-029329 A, использовался в качестве штамма дрожжей, обладающего способностью ферментации L-молочной кислоты. Способ получения описан ниже.
В штамме B3 ген L-LDH, приведенный в SEQ ID NO:1, был встроен в локус SED1. Для встраивания в локус SED1 был выполнен ПЦР, используя pTRS102, описанную в JP 2008-029329, в качестве матрицы для амплификации, и олигонуклеотиды (SEQ ID NO:2 и 3) в качестве набора праймеров, для амплификации ПЦР-фрагмента в 1,3 т.п.н., содержащего ген L-LDH, полученного из Xenopus laevis, и последовательность терминатора TDH3. Здесь, SEQ ID NO:2 была разработана таким образом, что была добавлена последовательность, соответствующая 60 п.н.-последовательности выше инициирующего кодона гена SED1.
Затем при помощи ПЦР с использованием плазмиды pRS423 в качестве матрицы для амплификации и олигонуклеотидов (SEQ ID NO:4 и 5) в качестве набора праймеров был амплифицирован ПЦР-фрагмент приблизительно 1,3 т.п.н., содержащий ген HIS3, который является селективным маркером дрожжей. Здесь, SEQ ID NO:5 была разработана таким образом, что была добавлена последовательность, соответствующая 60 п.н.-последовательности, расположенной ниже от терминирующего кодона гена SED1.
Каждый фрагмент ДНК разделяли путем электрофореза в 1%-ом агарозном геле и очищали в соответствии с обычном способом. ПЦР выполняли, используя смесь полученных двух типов фрагментов приблизительно в 1,3 т.п.н., в качестве матрицы для амплификации, и олигонуклеотиды (SEQ ID NO:2 и 5) в качестве набора праймеров для амплификации ПЦР-фрагмента приблизительно 2,6 т.п.н., в котором соединены ген L-LDH, полученный из Xenopus laevis, терминатор TDH3 и ген HIS3, и последовательности, соответствующие 60 п.н.-последовательностям выше и ниже гена SED1, были добавлены к 5'-концу и 3'-концу, соответственно.
Вышеупомянутый фрагмент ДНК разделяли путем электрофореза в 1%-ом агарозном геле и очищали в соответствии с обычным способом. Штамм B3 был трансформирован фрагментом ДНК и выращивался на среде без гистидина для отбора трансформантов, у которых ген L-LDH, полученный из Xenopus laevis, был введен в хромосому ниже промотора гена SED1.
Подтверждение факта, что полученный таким образом трансформант представляет собой дрожжи, имеющие ген L-LDH из Xenopus laevis, введенный в хромосому ниже промотора гена SED1, было выполнено следующим образом. Была подготовлена геномная ДНК трансформанта с использованием набора для экстрагирования геномной ДНК Dr. GenTLE (произведенный TAKARA BIO INC.), и затем выполняли ПЦР, используя готовую геномную ДНК в качестве матрицы для амплификации и олигонуклеотиды (SEQ ID NO:6 и 7) в качестве набора праймеров для подтверждения получения амплифицированного фрагмента ДНК приблизительно в 2,9 т.п.н. В нетрансформированном штамме путем вышеупомянутого ПЦР получается амплифицированный фрагмент ДНК приблизительно 1,4 т.п.н. Трансформант, обладающий полученным из Xenopus laevis геном L-LDH, введенным в хромосому ниже промотора гена SED1, в дальнейшем упоминается как штамм B4.
Затем штамм дрожжей SW015, описанный в JP 2008-48726 A, несущий чувствительную к температуре мутацию в гене pdc5, скрестили со штаммом B4, полученным как описано выше, чтобы получить диплоидные клетки. Диплоидные клетки культивировали в среде для формирования асков для того, чтобы дать возможность аскам сформироваться. Аски растаскивали с использованием микроманипулятора для получения соответствующих гаплоидных клеток, которые затем проверяли на ауксотрофность. Среди полученных гаплоидных клеток был отобран штамм, несущий ген L-LDH из Xenopus laevis, который вставлен в локусы PDC1, SED1 и TDH3, и чувствительную к температуре мутацию в гене PDC5 (отсутствие жизнеспособности при 34°C), и были отобраны соответствующее типы спаривания MATa и MATα. Среди полученных штаммов дрожжей штамм, обладающий типом спаривания MATa, был обозначен как штамм SU014-8A, а штамм, обладающий типом спаривания MATα, обозначен как штамм SU014-3B.
Затем была восстановлена ауксотрофность по лизину штамма SU014-8A. Используя геномную ДНК BY4741, произведенную Корпорацией Funakoshi, в качестве матрицы и олигонуклеотиды (SEQ ID NO:8 и 9) в качестве набора праймеров, был выполнен ПЦР, чтобы амплифицировать ПЦР-фрагмент приблизительно в 2 т.п.н., соответствующий первой половине гена LYS2. Вышеупомянутый ПЦР-фрагмент разделяли путем электрофореза в 1%-ом агарозном геле и очищали в соответствии с обычным способом. Штамм SU014-8A трансформировали ПЦР-фрагментом для нейтрализации амбер-мутации в гене LYS2. При культивировании полученного в результате в среде без лизина отбирали трансформант, обладающий восстановленной способностью синтезировать лизин.
Подтверждение факта, что таким образом полученный трансформант представляет собой дрожжи, в которых была нейтрализована амбер-мутация в гене LYS2, выполняли следующим образом. Во-первых, полученный трансформант скрещивали со штаммом 20GY77, имеющим ген LYS2 дикого типа, чтобы получить диплоидные клетки. Диплоидные клетки культивировали в среде для формирования асков для того, чтобы дать возможность аскам сформироваться. Аски растаскивали с использованием микроманипулятора для получения соответствующих гаплоидных клеток, которые затем проверяли на ауксотрофность. Было подтверждено, что все полученные гаплоидные клетки обладали способностью синтезировать лизин. В случаях, где способность синтезировать лизин была восстановлена без нейтрализации мутации в LYS2, клетки, которые не обладали способностью синтезировать лизин, образуются среди гаплоидных клеток, полученных, как описано выше. Штамм, полученный восстановлением способности штамма SU014-8A синтезировать лизин, в дальнейшем упоминается как HI001.
После этого была восстановлена ауксотрофность по лейцину штамма SU014-3B. Используя pRS425 в качестве матрицы и олигонуклеотиды (SEQ ID NO: 10 и 11) в качестве набора праймеров, был выполнен ПЦР, чтобы амплифицировать ПЦР-фрагмент гена LEU2 приблизительно в 2 т.п.н. Вышеупомянутый ПЦР-фрагмент разделяли путем электрофореза в 1%-ом агарозном геле и очищали в соответствии с обычным способом. Штамм SU014-3B трансформировали ПЦР-фрагментом для нейтрализации мутации гена LEU2. Путем культивирования полученного в результате в среде без лейцина отбирали трансформант, обладающий восстановленной способностью синтезировать лейцин.
Подтверждение факта, что таким образом полученный трансформант представляет собой дрожжи, в которых была нейтрализована мутация в гене LEU2, было выполнено следующим образом. Во-первых, полученный трансформант был скрещен со штаммом 20GY7, имеющим ген LEU2 дикого типа, чтобы получить диплоидные клетки. Диплоидные клетки культивировали в среде для формирования асков для того, чтобы дать возможность аскам сформироваться. Аски растаскивали с использованием микроманипулятора для получения соответствующих гаплоидных клеток, которые были затем проверены на ауксотрофность. Было подтверждено, что все полученные гаплоидные клетки обладали способностью синтезировать лейцин. В случаях, где способность синтезировать лейцин была восстановлена без нейтрализации мутации в LEU2, клетки, которые не обладали способностью синтезировать лизин, образуются среди гаплоидных клеток, полученных, как описано выше. Штамм, полученный восстановлением способности штамма SU014-3B синтезировать лизин, в дальнейшем упоминается как HI002.
Затем, таким образом полученные штамм HI001 и штамм HI002 скрещивали друг с другом, чтобы получить диплоидный прототрофный штамм, который не обладает ауксотрофностью. Полученный штамм в дальнейшем упоминается как штамм HI003.
Уровень молочной кислоты был подтвержден путем определения количества молочной кислоты при помощи ВЭЖХ при следующих условиях.
Колонка: Shim-Pack SPR-H (произведенная Корпорацией Shimadzu)
Мобильная фаза: 5 мМ п-толуолсульфоновая кислота (скорость потока: 0,8 мл/мин)
Раствор для реакции: 5 мМ п-толуолсульфоновая кислота, 20 мМ бис-Трис, 0,1 мМ ЭДТК 2Na (скорость потока: 0,8 мл/мин)
Способ детектирования: электропроводность
Температура: 45°C
Измерение оптической чистоты L-молочной кислоты или D-молочной кислоты выполняли с использованием ВЭЖХ при следующих условиях.
Колонка: TSK-gel Enantio LI (произведенная Корпорацией Tosoh)
Мобильная фаза: 1 мМ водный раствор сульфата меди
Скорость потока: 1,0 мл/мин
Способ детектирования: ультрафиолет 254 нм
Температура: 30°C
Оптическую чистоту молочной кислоты расчитывали путем следующего уравнения.
Оптическая чистота (%) = 100 × (L-D) или (D-L)/(L+D)
(где L представляет концентрацию L-молочной кислоты, и D представляет концентрацию D-молочной кислоты).
Справочный Пример 2: Получение L-молочной кислоты путем периодического культивирования
Используя штамм HI003, подготовленный в Справочном примере 1, и среду исходного сырья с сахаром (70 г/л Yutosei (произведенный MUSO Co., Ltd.)), был выполнена проверка периодического культивирования. Среду автоклавировали (121°C, 15 минут) перед использованием. Оценку концентрации молочной кислоты, которая является продуктом, проводили с использованием ВЭЖХ, описанной в Справочном примере 1, и концентрацию глюкозы определяли с использованием Glucose Test Wako С (произведенный Wako Pure Chemical Industries, Ltd.). Эксплуатационные режимы устройства периодического культивирования Справочного примера 2 представляли собой, как показано ниже:
Объем ферментера (количество среды для ферментации молочной кислоты), 2 (л); температурное регулирование, 32 (°C); объем вентиляции для ферментера, 0,1 (л/мин); скорость перемешивания для ферментера, 200 (оборотов в минуту); регулирование pH, доведение до pH 5 при помощи 1Н гидроксида кальция.
Во-первых, штамм HI003 культивировали в 5 мл среды исходного сырья с сахаром в пробирке в течение ночи с встряхиванием (предварительная предкультура). Средой с предварительной предкультурой инокулировали 100 мл новой среды исходного сырья с сахаром и подвергли культивированию во фляге Sakaguchi на 500 мл в течение 24 часов с встряхиванием (предварительная культура). Выполняли температурное регулирование и регулирование pH, и проводили ферментационное культивирование. В результате периодического культивирования в течение 50 часов концентрация накопленной молочной кислоты составляла 45-49 г/л, и оптическая чистота составляла 99,9% для L-молочной кислоты.
Справочный Пример 3: Процесс непрерывной ферментации
Используя штамм HI003, подготовленный в Справочном примере 1, проводили непрерывную ферментацию молочной кислоты с использованием устройства для культивирования, показанного на фиг. 1. Удаление фильтрата из емкости для мембранного разделения проводили, используя насос Masterflex. В качестве среды использовали среду исходного сырья с сахаром (70 г/л Yutosei (произведенную MUSO Co., Ltd.), 1,5 г/л сульфата аммония). Перед использованием эту среду исходного сырья с сахаром автоклавировали при температуре 121°C в течение 15 минут при высоком давлении (2 атм). В качестве участника пористого мембранного элемента использовали формованное изделие, изготовленное из нержавеющей стали и полисульфоновой смолы, и в качестве пористой мембраны использовали половолоконную мембрану, подготовленную способом, описанным в Справочном примере 13 в W02007/097260. Эксплуатационные режимы были следующие.
Объем реактора для культивирования: 20 (л)
Объем культуральной среды в реакторе для культивирования: 15 (л)
Использованная пористая мембрана: фильтрационная мембрана PVDF
Область эффективной фильтрации элемента мембранного разделения: 2800 см2
Температурное регулирование: 32 (°C)
Объем вентиляции для реактора для культивирования: воздух, 1 (л/мин)
Скорость перемешивания реактора для культивирования: 800 (оборотов в минуту)
Регулирование pH: доведение до pH 5 при помощи 5Н гидроксида кальция
Стерилизация: 121°C, 0,2 МПа, 20 мин, для всего реактора для культивирования, включая элемент пористой мембраны, и использованной среды
Скорость удаления культуральной среды: 0,16 м3/м2/д
Удаление культуральной среды при помощи насоса Masterflex начинали через 50 часов после начала культивирования, и культивирование продолжалось до 500 часов после начала культивирования. Результаты измерения концентрации молочной кислоты, которая является продуктом, и скорости продуцирования молочной кислоты показаны на фиг. 2. Концентрацию молочной кислоты определяли способом, приведенном в Справочном примере 1, и скорость продуцирования молочной кислоты вычисляли, используя Уравнение 7, ниже.
Скорость продуцирования молочной кислоты (г/л/час)
= концентрация молочной кислоты, накопленной в удаленной жидкости (г/л) × скорость удаления ферментационной жидкости (л/час)/эксплуатационный объем жидкости устройства (л).. (Уравнение 7)
В результате разница трансмембранного давления не превышала 1 кПа, и был возможен устойчивый процесс, без вызывания засорения мембраны. Средняя скорость продуцирования молочной кислоты в течение периода времени от 50 часов до 500 часов после начала культивирования составляла 6 г/л/час. Молочная кислота, полученная из фильтрата пористой мембраны в течение периода времени от 400 часов до 500 часов после начала культивирования, использовалась в последующих примерах (концентрация молочной кислоты: 52 г/л, оптическая чистота L-молочной кислота: 99,9%).
Справочный Пример 4: Оценка проницаемости сульфата магния через нанофильтрационную мембрану
К 10 л ультрачистой воды добавляли 10 г сульфата магния (произведенного Wako Pure Chemical Industries, Ltd.), и образующуюся смесь перемешивали при 25°C в течение 1 часа, чтобы подготовить водный раствор с 1000 м.д. сульфата магния. Затем 10 л готового водного раствора сульфата магния подавали в резервуар для сырьевой жидкости 13 устройства для мембранной фильтрации, показанного на фиг. 3. В качестве 90φ нанофильтрационной мембраны, обозначенной символом 19 на фиг. 4, нанофильтрационная мембрана из поперечносшитого пиперазинполиамида «UTC60» (нанофильтрационная мембрана 1, произведенная TORAY INDUSTRIES, INC.), нанофильтрационная мембрана из поперечносшитого пиперазинполиамида «NF-400» (нанофильтрационная мембрана 2, произведенная Корпорацией Filmtec), полиамидная нанофильтрационная мембрана «NF99» (нанофильтрационная мембрана 3, произведенная Alfa-Laval) или ацетатцеллюлозная нанофильтрационная мембрана «GEsepa» (нанофильтрационная мембрана 4, произведенная GE Osmonics) были помещены в ячейку, изготовленную из нержавеющей стали (SUS316). Температуру сырьевой жидкости доводили до 25°C, и давление насоса высокого давления 15 доводили до 0,5 МПа, чтобы собрать фильтрат 16. Концентрации сульфата магния, содержащегося в сырьевой жидкости в резервуаре 13 и фильтрате 16, анализировали путем ионной хроматографии (произведенной Корпораций Dionex) при следующих условиях, рассчитывая таким образом скорость проникновения сульфата магния.
Анион: колонка (AS4A-SC (произведенная Корпорацией Dionex)), элюент (1,8 мМ карбонат натрия/1,7 мМ двууглекислый натрий), температура (35°C).
Катион: колонка (CS12A (произведенная Корпорацией Dionex)), элюент (20 мМ метансульфоновая кислота), температура (35°C).
Результаты приведены в таблице 1.
(%)
Справочный Пример 5: Оценка проницаемости лимонной кислоты через нанофильтрационную мембрану
К 10 л ультрачистой воды добавляли 10 г лимонной кислоты (произведенный Wako Pure Chemical Industries, Ltd.), и образующуюся смесь перемешивали при 25°C в течение 1 часа, чтобы подготовить водный раствор с 1000 м.д. лимонной кислоты. Затем, фильтрат от нанофильтрационных мембран 1-4 собирали при тех же условиях, что и в Справочном примере 3. Концентрации лимонной кислоты, содержащейся в сырьевой жидкости в резервуаре 13 и фильтрате 16, анализировали высокоэффективной жидкостной хроматографией (произведенной Корпорацией Shimadzu) при следующих условиях, рассчитывая таким образом скорость проникновения лимонной кислоты и скорость проникновения лимонной кислоты/скорость проникновения сульфата магния.
Колонка: Shim-Pack SPR-H (произведенная Корпорацией Shimadzu); мобильная фаза: 5 мМ п-толуолсульфоновой кислоты (скорость потока: 0,8 мл/мин); реакционный раствор: 5 мМ п-толуолсульфоновой кислота, 20 мМ бис-Трис, 0,1 мМ ЭДТК 2Na (скорость потока: 0,8 мл/мин); способ детектирования: электропроводность; температура: 45°C.
Результаты показаны в таблице 2.
(Имя изготовителя)
сырьевой
жидкости
(м.д.)
(%)
скорость проникновения сульфата магния
Справочные Примеры 6-12: Проверка проникновения молочной кислоты ферментационной культуральной среды через нанофильтрационную мембрану
Из культуральной среды (2 л), полученной, как в Справочном примере 2, клетки удаляли центрифугированием, и затем добавляли по каплям концентрированную серную кислоту (произведенную Wako Pure Chemical Industries, Ltd.) к культуральной среде до pH 1,9 (Справочный пример 6), 2,0 (Справочный пример 7), 2,2 (Справочный пример 8), 2,6 (Справочные примеры 9-11) или 4,0 (Справочный пример 12), с последующим перемешиванием образующейся смеси в течение 1 часа при 25°C, преобразуя таким образом лактат кальция в культуральной среде в молочную кислоту и сульфат кальция. Затем осажденный сульфат кальция отделяли фильтрованием преципитата с использованием качественной фильтровальной бумаги No.2 (произведенной ADVANTEC) путем фильтрования с отсасыванием, и собирали 2 л фильтрата.
Затем 2 л каждого фильтрата, полученного, как описано выше, вливали в резервуар для сырьевой жидкости 13 устройства для мембранной фильтрации, показанного на фиг. 3. В качестве 90φ нанофильтрационной мембраны, обозначенной символом 19 на фиг. 4, каждую из нанофильтрационных мембран 1-4 помещали в ячейку, сделанную из нержавеющей стали (SUS316). В каждом случае давление насоса 15 для высокого давления доводили до 4 МПа, чтобы собрать фильтрат 16. Концентрации ионов сульфата и ионов кальция, содержащиеся в сырьевой жидкости в резервуаре 13 и фильтрате 16, анализировали ионной хроматографией (произведенной Корпорацией Dionex) при тех же условиях, что и в Справочном примере 4, и концентрацию молочной кислоты анализировали путем высокоэффективной жидкостной хроматографии (произведенной Корпорацией Shimadzu) при тех же условиях, что и Справочном примере 1. Результаты показаны в таблице 3.
Как показано в таблице 3, было обнаружено, что сульфат кальция удалялся с высокой эффективностью при всех pH. Также было показано, что скорость проникновения молочной кислоты и поток проникновения через мембрану были самыми высокими для нанофильтрационной мембраны 1.
Примеры 1-5: Примеры получения молочной кислоты
К 200 л фильтрата пористой мембраны, который был получен в Справочном примере 3, добавляли по каплям концентрированную серную кислоту (произведенную Wako Pure Chemical Industries, Ltd.) до pH 1,9 (Пример 1), 2,0 (Пример 2), 2,2 (Пример 3), 2,6 (Пример 4) или 4,0 (Пример 5), с последующим перемешиванием образующейся смеси в течение 1 часа при 25°C, преобразуя таким образом лактат кальция в культуральной среде в молочную кислоту и сульфат кальция. Затем преципитированный сульфат кальция отделяли фильтрованием с отсасыванием, используя качественную фильтровальную бумагу, путем фильтрации всасывания, и собирали 200 л каждого из фильтратов.
Затем 200 л каждого фильтрата, полученного в вышеупомянутых Примерах, вливали в резервуар для сырьевой жидкости 13 устройства для мембранной фильтрации, показанного на фиг.3. 4-Дюймовый нанофильтрационный модуль 2 («UTC60», произведенный TORAY INDUSTRIES, INC.) нанофильтрационной мембраны 1, который продемонстрировал самые высокие скорости проникновения молочной кислоты в Справочных примерах 6-12, помещали в специальный резервуар, и процесс проводили путем регулирования давления в насосе высокого давления 15 до 4 МПа, чтобы собрать фильтрат для каждого pH. Концентрации ионов серной кислоты и ионов кальция, содержащихся в сырьевой жидкости в резервуаре 13 и фильтрате 16, анализировали ионной хроматографией (произведенной Корпорацией Dionex) при тех же условиях, что и в Справочном примере 4, и концентрацию молочной кислоты анализировали путем высокоэффективной жидкостной хроматографии (произведенной Корпорацией Shimadzu) при тех же условиях, что и в Справочном примере 1. В результате этого было показано, что сульфат кальция удалялся с высокой эффективностью при всех pH, как в Справочных примерах 6-12.
После этого 100 л каждого из фильтратов нанофильтрационной мембраны концентрировали путем дистилляции воды с использованием выпарного устройства мгновенного действия (произведенного TOKYO RIKAKIKAI) при уменьшенном давлении (50 гПа). В это время осаждение сульфата кальция не наблюдалось.
После этого дистилляцию проводили при уменьшенном давлении 133 Па при 130°C. Для подтверждения рацемизации дистиллированной молочной кислоты путем высокоэффективной жидкостной хроматографии определяли оптическую чистоту до и после дистилляции. Результаты приведены в таблице 4.
Полученную очищенную молочную кислоту использовали для проверки прямой полимеризации в примере 6 и проверки синтеза лактида в примере 7, и молочную кислоту перед дистилляцией использовали для проверки прямой полимеризации в Сравнительном примере 2 и проверки синтеза лактида в Сравнительном примере 3.
Сравнительный Пример 1: Пример получения молочной кислоты
К 200 л мембранного фильтрата, полученного как в Справочном примере 3, добавляли по каплям концентрированную серную кислоту (произведенную Wako Pure Chemical Industries, Ltd.) до pH 2,0, после чего образующуюся смесь перемешивали в течение 1 часа при 25°C, преобразуя таким образом лактат кальция в культуральной среде в молочную кислоту и сульфат кальция. Затем преципитированный сульфат кальция отделяли фильтрованием преципитатов, с использованием качественной фильтровальной бумаги, фильтрацией всасывания, и собирали 200 л фильтрата. Концентрацию сульфата кальция, содержащегося в фильтрате, анализировали ионной хроматографией, и было показано, что концентрация составляет 549 мг/л. Таким образом, было показано, что сульфат кальция не был в достаточной степени удален.
После этого 100 л фильтрата концентрировали дистилляцией воды с использованием выпарного устройства мгновенного действия при уменьшенном давлении (50 гПа), и это вызвало осаждение сульфата кальция, который не был удален вышеописанной качественной фильтровальной бумагой. Затем дистилляцию проводили при уменьшенном давлении 133 Па при 130°C. Для подтверждения рацемизации дистиллированной молочной кислоты, оптическую чистоту молочной кислоты определяли до и после дистилляции, путем высокоэффективной жидкостной хроматографии при тех же условиях, что и в Справочном примере 1. В результате наблюдалось уменьшение в оптической чистоте. Кроме того, в дистилляционном остатке наблюдали частично олигомеризованную молочную кислоту, и дистилляционный выход уменьшился до 30%. Эти результаты показаны в таблице 4, вместе с результатами очистки через нанофильтрационную мембрану.
Пример 6: Проверка прямой полимеризации для молочной кислоты
В реакционном резервуаре, имеющем мешалку, 150 г молочной кислоты, полученной в примере 2, нагревали при 800 Па при 160°C в течение 3,5 часов, чтобы получить олигомеры. Затем 0,12 г ацетата олова(II) (произведенного Kanto Chemical Co., Ltd.) и 0,33 г метансульфоновой кислоты (произведенный Wako Pure Chemical Industries, Ltd.) добавляли к олигомерам, и образующуюся смесь нагревали при 500 Па при 180°C в течение 7 часов, чтобы получить преполимер. Преполимер затем кристаллизовали путем нагревания в печи при 120°C в течение 2 часов. Полученный преполимер растирали в порошок, используя молотковую мельницу, и просеивали через решето, для получения порошкообразной массы, обладающей средним размером частицы 0,1 мм. В твердофазной стадии полимеризации брали 150 г преполимера и помещали в печь, с которой был связан масляный ротационный насос, выполняя таким образом вакуумную термообработку. Давление было установлено в 50 Па, и нагревающаяся температура была установлена: 140°C в течение 10 часов; 150°C в течение 10 часов; и 160°C в течение 20 часов. Полученная полимолочная кислота была подвергнута анализу средневесовой молекулярной массы при помощи GPC (произведенной Корпорацией Tosoh), анализу точки плавления при помощи DSC (произведенной SII NanoTechnology Inc.) и анализу скорости тепловой потери массы при помощи TG (произведенный SII NanoTechnology Inc.).
Анализ средневесовой молекулярной массы полимолочной кислоты
Средневесовая молекулярная масса (Mw) полимолочной кислоты, произведенной путем полимеризации, представляет собой значение средневесовой молекулярной массы в отношении стандартного полиметилметакрилата, определенное гельпроникающей хроматографией (GPC). Определение GPC проводили с использованием HLC8320GPC (произведенного Корпорацией Tosoh) в качестве системы GPC и двух последовательных колонок TSK-GEL SuperHM-M (произведенных Корпорацией Tosoh). Детектирование выполняли, используя дифференциальный рефрактометр. В плане условий для определения, скорость потока составляла 0,35 мл/мин, в качестве растворителя использовался гексафторизопропиловый спирт и впрыскивалось 0,02 мл раствора с концентрацией образца 1 мг/мл.
Анализ точки плавления полимолочной кислоты
Точка плавления полимолочной кислоты, произведенной путем полимеризации, представляет собой значение, определенное при помощи дифференциального сканирующего калориметра DSC7020 (произведенного SII NanoTechnology Inc.), и определение выполняли при помощи 10 мг образца, в атмосфере азота при скорости нагревания 20°C/мин.
Анализ скорости тепловой потери массы полимолочной кислоты
Скорость тепловой потери массы полимолочной кислоты, произведенной путем полимеризации, определяли с использованием термогравиметрического дифференциального теплового анализатора TG/DTA7200 (произведенного SII NanoTechnology Inc.). Определение выполняли при помощи 10 мг образца, в атмосфере азота при постоянной температуре 200°C в течение времени нагрева 20 минут.
Анализ степени окрашивания полимолочной кислоты
В 9,5 г хлороформа расторяли 0,5 г полимолочной кислоты, произведенной путем полимеризации, и степень окрашивания анализировали, используя колориметр (произведенный NIPPON DENSHOKU INDUSTRIES CO., LTD.), в качестве числа единиц окрашивания APHA.
Полимолочная кислота, полученная путем прямой полимеризации молочной кислоты, обладала средневесовой молекулярной массой 155000, точкой плавления 165°C, скоростью тепловой потери массы 5% и степенью окрашивания APHA 10.
Сравнительный Пример 2: Проверка прямой полимеризации молочной кислоты
Молочную кислоту перед дистилляцией в примере 2 концентрировали при помощи ротационного испарителя до 90% по массе, чтобы получить 150 г концентрированной молочной кислоты. Прямую полимеризацию проводили при тех же условиях, что и в примере 6. Полимолочная кислота, полученная путем прямой полимеризации, обладала средневесовой молекулярной массой 85000, точкой плавления 160°C, скоростью тепловой потери массы 15% и степенью окрашивания APHA 50. Таким образом, качество молочной кислоты было ниже по сравнению с качеством молочной кислоты, полученной в примере 6, для всех пунктов оценки.
Пример 7: Проверка синтеза лактида
В реакционном резервуаре, имеющем мешалку, 150 г молочной кислоты, полученной в примере 2, концентрировали путем нагревания при атмосферном давлении при 135°C в течение 30 минут. Затем, при уменьшенном давлении (4500-6500 Па), температуру жидкости поэтапно увеличивали до 135°C (20 минут), 150°C (20 минут) и 160°C (20 минут), чтобы получить олигомеры. После этого к олигомерам добавляли 0,75 г октилата олова(II) (Nacalai Tesque) и выполняли простую дистилляцию при уменьшенном давлении (1000-2000 Па) при 200°C в течение 2 часов, чтобы дистиллировать лактид. Во избежание засорения труб температуру конденсатора установили в 110°C. Фракцию лактида получили в количестве 92,3 г. Выход лактида составлял 85,4% по отношению к начальной L-молочной кислоте.
Анализ химической чистоты лактида
Химическую чистоту синтезированного лактида (соотношение LL-лактида в восстановленном лактиде) анализировали при помощи газовой хроматографии GC2010 (произведенной Корпорацией Shimadzu). В качестве колонки использовали капиллярную колонку RT BDEXM (произведенную RESTEK), и условия определения представляли собой: скорость потока газа-носителя (He), 69,2 мл/мин; температура испарительной камеры, 230°C; температура колонки, 150°C; температура детектора (FID), 230°C; и отношение разделения, 50. По соотношениям областей пиков LL-лактида, DD-лактида и DL-лактида расчитывали химическую чистоту LL-лактида.
Анализ степени окрашивания лактида
6 г синтезированного лактида полностью растворили в 20 г ацетона, и степень окрашивания анализировали, используя колориметр (произведенный NIPPON DENSHOKU INDUSTRIES CO., LTD.), как число единиц окрашивания APHA.
В результате полученный лактид обладал химической чистотой 96,2% и степенью окрашивания APHA 2.
Сравнительный Пример 3: Проверка на синтез лактида
Молочную кислоту перед дистилляцией в примере 2 концентрировали при помощи ротационного испарителя до 90% по массе, чтобы получить 150 г концентрированной молочной кислоты. Лактид синтезировали при тех же условиях, что и в примере 7. Лактид был получен в количестве 79,1 г при выходе 73,2% и имел химическую чистоту 93,1% и степень окрашивания APHA 12. Таким образом, как выход, так и качество молочной кислоты были хуже, чем таковые для молочной кислоты, полученной в примере 7.
Пример 8: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
В реакционный резервуар, имеющий мешалку, помещали 50 г лактида, полученного в примере 7, и 0,05 г стеарилового спирта, и атмосферу в системе заменяли азотом, после чего нагревали образующуюся смесь до 190°C до растворения лактида. Затем к этому добавляли 0,025 г октилата олова(II), и полимеризацию выполняли при 190°C в течение 2 часов. У полученной полимолочной кислоты анализировали ее средневесовую молекулярную массу, точку плавления, скорость тепловой потери массы и степень окрашивания способами, описанными в примере 6. Средневесовая молекулярная масса составляла 135000; точка плавления составляла 165°C; скорость тепловой потери массы составляла 5,1%; и степень окрашивания составляла APHA 5.
Сравнительный Пример 4: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида в соответствии с той же процедурой, что и в примере 8, за исключением того, что использовали 50 г лактида, полученного в Сравнительном примере 3. Полученная полимолочная кислота обладала средневесовой молекулярной массой 109000, точкой плавления 162°C, скоростью потери массы 6,3% и степенью окрашивания APHA 11. Таким образом, качество полимолочной кислоты было хуже, чем качество полимолочной кислоты, полученной в примере 8, для всех пунктов оценки.
Пример 9: Анализ примесей в молочной кислоте
Три литра фильтрата, полученного таким же образом, что и в примере 3, фильтровали через нанофильтрационный мембранный модуль SU-610 (произведенный TORAY INDUSTRIES, INC.) при рабочем давлении 2,0 МПа, чтобы удалить примеси. Водный раствор молочной кислоты, который прошел через нанофильтрационный мембранный модуль, концентрировали с использованием модуля обратноосмотической мембраны SU-810 (произведенный TORAY INDUSTRIES, INC.), а также концентрировали дистилляцией воды с использованием ротационного испарителя (произведенного TOKYO RIKAKIKAI) при уменьшенном давлении (50 гПа), получая таким образом 80%-ый водный раствор молочной кислоты. После этого проводили дистилляцию при уменьшенном давлении 133 Па при 133°C, чтобы получить 500 г молочной кислоты.
Анализ примесей в молочной кислоте
К молочной кислоте, полученной, как описано выше, добавляли очищенную воду для подготовки 90%-го водного раствора молочной кислоты. Содержащиеся примеси анализировали путем ВЭЖХ (высокоэффективная жидкостная хроматография) или GC (газовая хроматография) при следующих условиях. Результаты анализа приведены в таблице 5.
Анализ уксусной кислоты, пировиноградной кислоты и 2-гидроксимасляной кислоты при помощи ВЭЖХ
Колонка: Shim-Pack SPR-H (произведенная Корпорацией Shimadzu); мобильная фаза: 5 мМ п-толуолсульфоновая кислота (скорость потока: 0,8 мл/мин); реакционный раствор: 5 мМ п-толуолсульфоновая кислота, 20 мМ бис-Трис, 0,1 мМ ЭДТК 2Na (скорость потока: 0,8 мл/мин); способ детектирования: электропроводность; температура: 45°C.
Анализ фурфураля и HMF при помощи ВЭЖХ
Колонка: Synergie HydroRP (произведенная Phenomenex, Inc.); мобильная фаза: 5%-ый водный раствор ацетонитрила (скорость потока 1,0 мл/мин); способ детектирования: УФ (283 нм); температура: 40°C.
Анализ метанола и метиллактата при помощи способа GC
Колонка: DB-5 (0,25 мм × 30 м., произведенная J&W); температура колонки: от 50°C до 250°C (8°C/мин); температура входного отверстия: 250°C; газ-носитель: гелий; давление носителя: 65 кПа.
Как показано в таблице 5, концентрации всех примесей, за исключением уксусной кислоты и пировиноградной кислоты, составляли 0 м.д. (ниже предела чувствительности).
Пример 10: Проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
В реакционном резервуаре, имеющем мешалку, 150 г 90%-го водного раствора молочной кислоты из примера 9 нагревали при 800 Па при 160°C в течение 3,5 часов, чтобы получить олигомеры. Затем к олигомерам добавляли 0,12 г ацетата олова(II) (произведенного Kanto Chemical Co., Ltd.) и 0,33 г метансульфоновой кислоты (произведенной Wako Pure Chemical Industries, Ltd.), и образующуюся смесь нагревали при 500 Па при 180°C в течение 7 часов, чтобы получить преполимер. Преполимер затем кристаллизовали путем нагревания в печи при 120°C в течение 2 часов. Полученные преполимеры измельчали с использованием молотковой мельницы и просеивали через сито, чтобы получить измельченную массу, обладающую средним размером частиц 0,1 мм. На твердофазной стадии полимеризации брали 150 г преполимера и помещали в печь, с которой был связан масляный ротационный насос, выполняя таким образом вакуумную термообработку. Давление устанавливали в 50 Па, и нагревающую температуру устанавливали в: 140°C в течение 10 часов; 150°C в течение 10 часов; и 160°C в течение 20 часов. Средневесовую молекулярную массу, точку плавления, скорость тепловой потери массы и степень окрашивания полученной полимолочной кислоты анализировали способами, описанными в примере 6.
Пример 11: Анализ примесей в молочной кислоте, проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, как в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 30 м.д. метанола, 100 м.д. муравьиной кислоты, 200 м.д. пировиноградной кислоты, 100 м.д. 2-гидроксимасляной кислоты, 3 м.д. фурфураля, 2 м.д. 5-гидроксиметилфурфураля и 100 м.д. метилалактата.
Пример 12: Анализ примесей в молочной кислоте, проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, что и в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 5: Анализ примесей в молочной кислоте и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, что и в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 100 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 6: Анализ примесей в молочной кислоте, проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, что и в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 600 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 7: Анализ примесей в молочной кислоте, проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, что и в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 25 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 8: Анализ примесей в молочной кислоте, проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, что и в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 25 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 9: Анализ примесей в молочной кислоте, проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, что и в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 650 м.д. метиллактата.
Сравнительный Пример 10: Анализ примесей в молочной кислоте, проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, что и в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 70 м.д. метанола, 750 м.д. 2-гидроксимасляной кислоты и 500 м.д. метиллактата.
Сравнительный Пример 11: Анализ примесей в молочной кислоте, проверка прямой полимеризации молочной кислоты и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации и анализировали таким же образом, что и в примере 10, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 600 м.д. уксусной кислоты и 300 м.д. пировиноградной кислоты.
Средневесовые молекулярные массы, точки плавления, скорости тепловой потери массы и степени окрашивания APHA полимолочных кислот, полученных в примерах 10-12 и Сравнительных примерах 5-11, приведены в таблице 6. В примерах 10-12 были получены полимолочные кислоты, обладающие превосходными физическими свойствами по средневесовой молекулярной массе, скорости тепловой потери массы и степени окрашивания. Однако в Сравнительном примере 5 средневесовая молекулярная масса была небольшая, и следовательно механическая прочность была низкой, и скорость тепловой потери массы была высокой, и следовательно термостабильность была низкой; в Сравнительных примерах 6-9 скорость тепловой потери массы была высокой, и степень окрашивания была высокой; и в Сравнительных примерах 10 и 11 скорость тепловой потери массы была высокой. Из этих результатов ясно, что в случаях, где количества примесей в молочной кислоте составляют не более чем предопределенные значения, можно получить полимолочную кислоту, обладающую превосходной термостабильностью, механической прочностью и цветом.
Пример 13: Анализ примесей в молочной кислоте и оценка физических свойств лактида
В реакционном резервуаре, имеющем мешалку, 150 г молочной кислоты, полученной в примере 9, концентрировали при нагревании при 135°C при атмосферном давлении в течение 30 минут. Затем, при уменьшенном давлении (4500-6500 Па), температуру жидкости ступенчато увеличивали до 135°C (20 минут), 150°C (20 минут) и 160°C (20 минут), чтобы получить олигомеры. После этого к олигомерам добавляли 0,75 г октилата олова(II) (Nacalai Tesque), и проводили простую дистилляцию при уменьшенном давлении (1000-2000 Па) при 200°C в течение 2 часов, чтобы дистиллировать лактид. Чтобы избежать засорения труб, температуру конденсатора устанавливали 110°C. Фракция лактида была получена в количестве 93,3 г. Выход лактид составил 87,2% по отношению к начальной L-молочной кислоте.
Пример 14: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 30 м.д. метанола, 100 м.д. муравьиной кислоты, 200 м.д. пировиноградной кислоты, 100 м.д. 2-гидроксимасляной кислоты, 3 м.д. фурфураля, 2 м.д. 5-гидроксиметилфурфураля и 100 м.д. метиллактата.
Пример 15: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 12: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 100 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 13: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 600 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 14: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 25 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 15: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 25 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 350 м.д. метиллактата.
Сравнительный Пример 16: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 65 м.д. метанола, 100 м.д. муравьиной кислоты, 300 м.д. уксусной кислоты, 300 м.д. пировиноградной кислоты, 150 м.д. 2-гидроксимасляной кислоты, 5 м.д. фурфураля, 5 м.д. 5-гидроксиметилфурфураля и 650 м.д. метиллактата.
Сравнительный Пример 17: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 70 м.д. метанола, 750 м.д. 2-гидроксимасляной кислоты и 500 м.д. метиллактата.
Сравнительный Пример 18: Анализ примесей в молочной кислоте и оценка физических свойств лактида
Лактид синтезировали таким же образом, что и в примере 13, за исключением того, что использовали 150 г водного раствора молочной кислоты, который подготавливали путем добавления соответствующих компонентов, наряду с примесями, содержащимися в 90%-ом водном растворе молочной кислоты, полученном в примере 9, к молочной кислоте, полученной в примере 9, таким образом, чтобы их концентрации были доведены до 600 м.д. уксусной кислоты и 300 м.д. пировиноградной кислоты.
Выход и степени окрашивания APHA лактидов, полученных в примерах 13-15 и Сравнительных примерах 12-18 приведены в таблице 6. В примерах 13-15 были получены превосходные результаты по выходу лактида и степени окрашивания. Однако, в Сравнительных примерах 12-18, выход составлял меньше чем 80%; и в Сравнительных примерах 13-15, где содержалось большое количество пировиноградной кислоты, фурфураля и т.п., степень окрашивания была высокой. Из этих результатов было обнаружено, что в случаях, где количества примесей в молочной кислоте составляют не больше чем предопределенные значения, можно получить лактид, демонстрирующий высокий выход и низкую степень окрашивания.
Пример 16: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
В реакционный резервуар, имеющий мешалку, добавляли 50 г лактида, полученного в примере 13, и 0,05 г стеарилового спирта, и атмосферу в системе заменяли азотом, с последующим нагреванием образующейся смеси до 190°C до растворения лактида. Затем добавляли 0,025 г октилата олова(II) в качестве катализатора, и выполняли полимеризацию при 190°C в течение 2 часов. Полученную полимолочную кислоту анализировали по ее средневесовой молекулярной массе, точке плавления, скорости тепловой потери массы и степени окрашивания при помощи способов, описанных в примере 6.
Пример 17: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 14.
Пример 18: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 15.
Сравнительный Пример 19: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 12.
Сравнительный Пример 20: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 13.
Сравнительный Пример 21: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 14.
Сравнительный Пример 22: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 15.
Сравнительный Пример 23: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 16.
Сравнительный Пример 24: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 17.
Сравнительный Пример 25: Получение полимолочной кислоты путем полимеризации с использованием лактида в качестве исходного сырья и оценка физических свойств полимолочной кислоты
Полимолочную кислоту производили путем полимеризации лактида и анализировали в соответствии с той же процедурой, что и в примере 16, за исключением того, что было использовано 50 г лактида, полученного в примере 18.
Средневесовые молекулярные массы, точки плавления, скорости тепловой потери массы и степени окрашивания APHA полимолочных кислот, полученных в примерах 16-18 и Сравнительных примерах 19-25, приведены в таблице 6. В примерах 16-18 были получены полимолочные кислоты, обладающие превосходными физическими свойствами по средневесовой молекулярной массе, скорости тепловой потери массы и степени окрашивания. Однако, в Сравнительных примерах 19 и 20, средневесовая молекулярная масса была небольшой. Также, в Сравнительных примерах 20-22, скорость потери массы была высокой и степень окрашивания была высокой; и в Сравнительных примерах 23-25 скорость потери массы была высокой.
ПРИМЕНИМОСТЬ В ПРОИЗВОДСТВЕННЫХ УСЛОВИЯХ
Молочную кислоту, полученную способом по настоящему изобретению для получения молочной кислоты, можно соответственно использовать для продуктов питания и фармацевтических препаратов, и в качестве мономерного материала для полимолочной кислоты, которая является разлагаемой микроорганизмами пластмассой общего назначения. Кроме того, полимолочная кислота, полученная при использовании молочной кислоты в качестве сырьевого материала, обладает превосходной термостабильностью, механической прочностью и цветом, так что полимолочная кислота является подходящей для различных применений, таких как волокна, пленки и формованные изделия.
ОПИСАНИЕ СИМВОЛОВ
1. Ферментационный реактор
2. Резервуар для мембранного разделения
3. Элемент разделяющей мембраны
4. Устройство, подающее газ
5. Мешалка
6. Контрольное устройство гидравлической разности напора
7. Насос, подающий культуральную среду
8. Насос, подающий раствор для регулирования pH
9. Устройство, детектирующее/контролирующее pH
10. Насос для циркуляции ферментационной жидкости
11. Датчик уровня
12. Температурный регулятор
13. Резервуар для сырьевой жидкости
14. Ячейка, оборудованная нанофильтрационной мембранной или обратноосмотической мембраной
15. Насос высокого давления
16. Поток мембранного фильтрата
17. Поток мембранного концентрата
18. Поток культуральной среды, подаваемой насосом высокого давления
19. Нанофильтрационная мембрана
20. Поддерживающая пластина
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ МОЛОЧНОЙ КИСЛОТЫ И ЕЕ ПРИМЕНЕНИЕ | 2009 |
|
RU2650802C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОЛОЧНОЙ КИСЛОТЫ И ПОЛИМОЛОЧНОЙ КИСЛОТЫ | 2014 |
|
RU2675823C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОЛОЧНОЙ КИСЛОТЫ | 2013 |
|
RU2643147C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХИМИЧЕСКОГО ВЕЩЕСТВА | 2013 |
|
RU2595386C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХИМИЧЕСКОГО ВЕЩЕСТВА | 2013 |
|
RU2595388C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХИМИЧЕСКОГО ПРОДУКТА И АППАРАТ ДЛЯ НЕПРЕРЫВНОЙ ФЕРМЕНТАЦИИ | 2009 |
|
RU2513694C2 |
| СПОСОБ ПОЛУЧЕНИЯ САХАРНОГО РАСТВОРА | 2009 |
|
RU2516792C2 |
| ПОЛИПЕПТИД, ОБЛАДАЮЩИЙ АКТИВНОСТЬЮ D-ЛАКТАТДЕГИДРОГЕНАЗЫ, ПОЛИНУКЛЕОТИД, КОДИРУЮЩИЙ ЭТОТ ПОЛИПЕПТИД, И СПОСОБ ПОЛУЧЕНИЯ D-МОЛОЧНОЙ КИСЛОТЫ | 2010 |
|
RU2553563C2 |
| СПОСОБ ПРОИЗВОДСТВА МОЛОЧНОЙ КИСЛОТЫ | 2015 |
|
RU2695229C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИГИДРОКСИКАРБОНОВОЙ КИСЛОТЫ | 2011 |
|
RU2575709C2 |



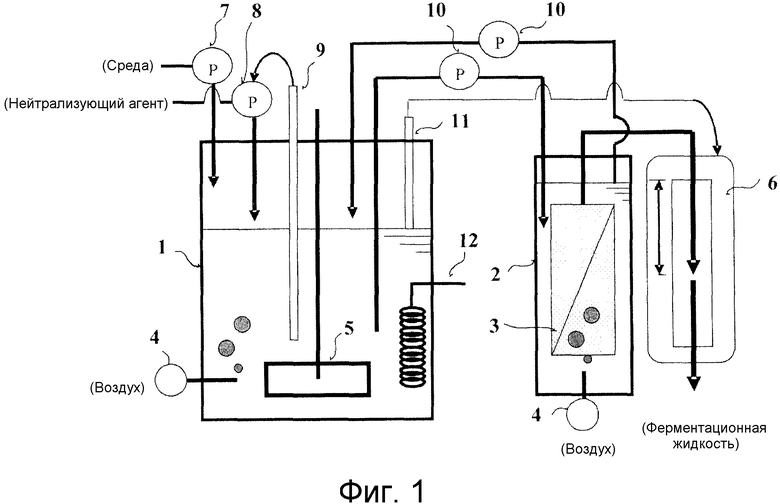
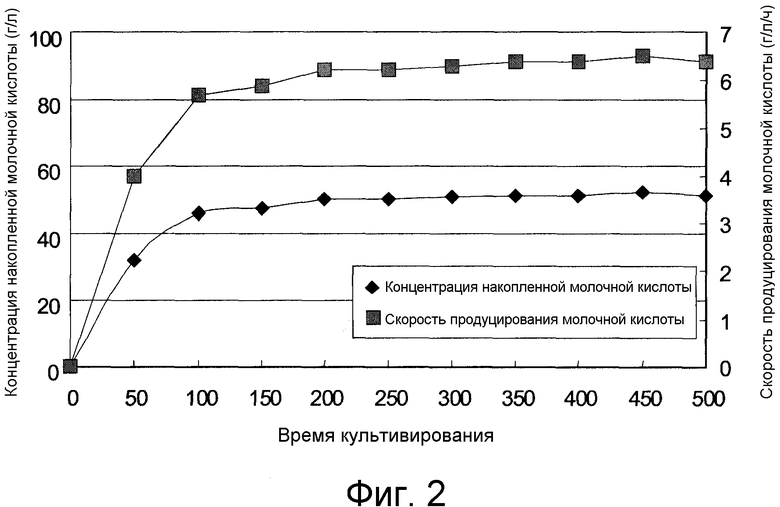
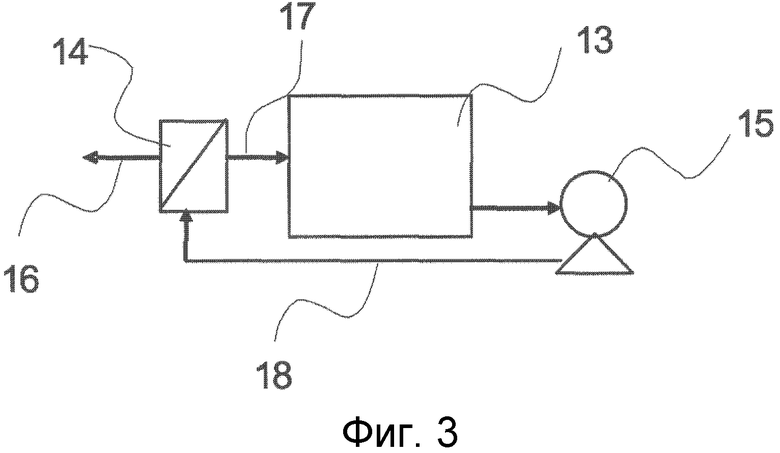
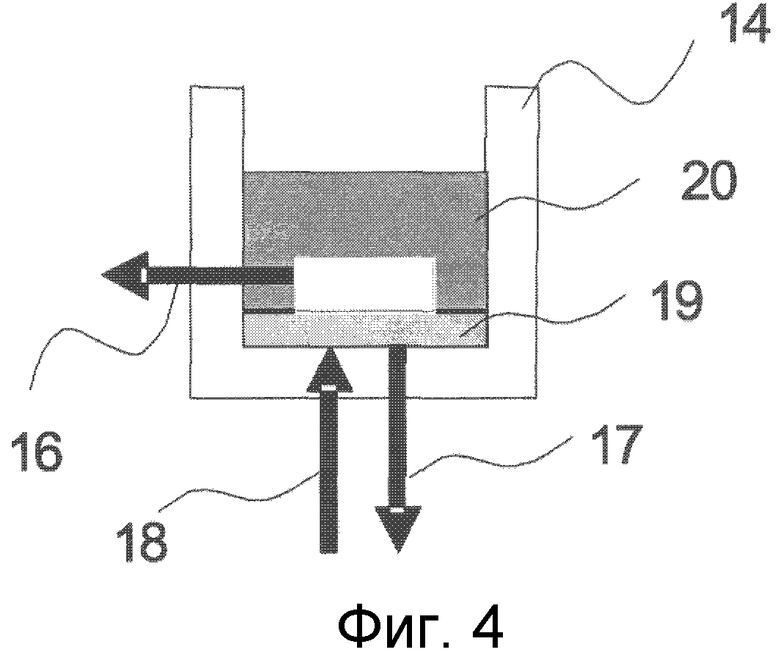
Группа изобретений относится к биотехнологии. Предложены способы получения молочной кислоты, получения лактида и получения полимолочной кислоты. Осуществляют непрерывную ферментацию микроорганизма, обладающего способностью молочнокислого брожения. Затем ферментационную среду фильтруют через мембрану со средним размером пор от 0,01 мкм до 1 мкм при разности трансмембранного давления от 0,1 до 20 кПа. Фильтрат собирают при сохранении неотфильтрованной жидкости в культуральной среде или возвращении неотфильтрованной жидкости в культуральную среду и добавлении сырья для ферментации к культуральной среде. Полученный фильтрат фильтруют через нанофильтрационную мембрану. Осуществляют дистилляцию полученного фильтрата при давлении от 10 Па до 30 кПа и температуре от 25°C до 200°C для извлечения молочной кислоты. Молочную кислоту, полученную указанным способом, каталитически превращают в лактид либо в полимолочную кислоту путем прямой дегидратационной поликонденсации. Изобретения позволяют получать молочную кислоту с оптической чистотой до 99% и выходом до 60-92% и получать полимолочную кислоту с улучшенными термостабильностью, механической прочностью и цветом. 3 н. и 7 з.п. ф-лы, 4 ил., 6 табл., 25 пр.
1. Способ получения молочной кислоты, включающий приведенные ниже стадии (А)-(С):
(A) стадия непрерывного культивирования, где ферментационную культуральную среду микроорганизма, обладающего способностью молочнокислого брожения, фильтруют через пористую мембрану, имеющую средний размер пор не меньше чем 0,01 мкм и меньше чем 1 мкм, с разностью трансмембранного давления в интервале от 0,1 до 20 кПа, и фильтрат собирают при сохранении неотфильтрованной жидкости в культуральной среде или возвращении неотфильтрованной жидкости в культуральную среду и добавлении сырья для ферментации к культуральной среде;
(B) стадия фильтрования фильтрата, полученного на стадии (А), через нанофильтрационную мембрану; и
(C) стадия дистилляции фильтрата, полученного на стадии (В), под давлением не меньше чем 10 Па и не больше чем 30 кПа, при не меньше чем 50°C и не больше чем 180°C для извлечения молочной кислоты.
2. Способ получения молочной кислоты по п.1, где pH фильтрата, полученного на указанной стадии (А), доводят до не меньше чем 2 и не больше чем 4,5 с последующим направлением фильтрата на указанную стадию (В).
3. Способ получения молочной кислоты по п.1, где указанная стадия (А) представляет собой стадию непрерывной ферментации в присутствии соли кальция, включающий после стадии (А) дополнительную стадию (D), на которой кальциевый компонент в фильтрате, полученном на стадии (А), удаляют в виде нерастворимого сульфата, и раствор, содержащий молочную кислоту, полученный после стадии (D), направляют на указанную стадию (В).
4. Способ получения молочной кислоты по п.1, где на стадии (В) отношение скорости проникновения сульфата магния относительно скорости проникновения лимонной кислоты через указанную нанофильтрационную мембрану составляет не меньше чем 3 при рабочем давлении 0,5 МПа, температуре сырьевой жидкости 25°C и концентрации в сырьевой жидкости 1000 м.д.
5. Способ получения молочной кислоты по п.1, где на стадии (В) скорость проникновения сульфата магния через указанную нанофильтрационную мембрану составляет не больше чем 1,5% при рабочем давлении 0,5 МПа, температуре сырьевой жидкости 25°C и концентрации в сырьевой жидкости 1000 м.д.
6. Способ получения молочной кислоты по п.1, где мембранный материал указанной нанофильтрационной мембраны включает полиамид.
7. Способ получения молочной кислоты по п.6, где указанный полиамид включает поперечносшитый пиперазинполиамид в качестве основного компонента и дополнительно включает образующий компонент, представленный химической формулой 1:
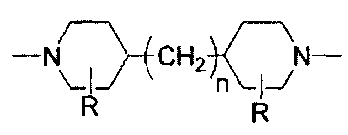
где R представляет -Н или -СН3 и n представляет целое число от 0 до 3.
8. Способ получения лактида, включающий следующие стадии:
(A) стадия непрерывного культивирования, где ферментационную культуральную среду микроорганизма, обладающего способностью молочнокислого брожения, фильтруют через пористую мембрану, имеющую средний размер пор не меньше чем 0,01 мкм и меньше чем 1 мкм, с разностью трансмембранного давления в интервале от 0,1 до 20 кПа, и фильтрат собирают при сохранении неотфильтрованной жидкости в культуральной среде или возвращении неотфильтрованной жидкости в культуральную среду и добавлении сырья для ферментации к культуральной среде;
(B) стадия фильтрования фильтрата, полученного на стадии (А), через нанофильтрационную мембрану;
(C) стадия дистилляции фильтрата, полученного на стадии (В), под давлением не меньше чем 10 Па и не больше чем 30 кПа, при не меньше чем 50°C и не больше чем 180°C с получением молочной кислоты; и
последующая стадия получения лактида, где молочную кислоту, полученную на стадии (С), используют в качестве исходного сырья.
9. Способ получения полимолочной кислоты, включающий следующие стадии:
(А) стадия непрерывного культивирования, где ферментационную культуральную среду микроорганизма, обладающего способностью молочнокислого брожения, фильтруют через пористую мембрану, имеющую средний размер пор не меньше чем 0,01 мкм и меньше чем 1 мкм, с разностью трансмембранного давления в интервале от 0,1 до 20 кПа, и фильтрат собирают при сохранении неотфильтрованной жидкости в культуральной среде или возвращении неотфильтрованной жидкости в культуральную среду и добавлении сырья для ферментации к культуральной среде;
(B) стадия фильтрования фильтрата, полученного на стадии (А), через нанофильтрационную мембрану;
(C) стадия дистилляции фильтрата, полученного на стадии (В), под давлением не меньше чем 10 Па и не больше чем 30 кПа, при не меньше чем 50°C и не больше чем 180°C с получением молочной кислоты;
с последующим получением лактида из молочной кислоты, полученной на стадии (С), и его полимеризацией с получением полимолочной кислоты.
10. Способ получения полимолочной кислоты, включающий следующие стадии:
(A) стадия непрерывного культивирования, где ферментационную культуральную среду микроорганизма, обладающего способностью молочнокислого брожения, фильтруют через пористую мембрану, имеющую средний размер пор не меньше чем 0,01 мкм и меньше чем 1 мкм, с разностью трансмембранного давления в интервале от 0,1 до 20 кПа, и фильтрат собирают при сохранении неотфильтрованной жидкости в культуральной среде или возвращении неотфильтрованной жидкости в культуральную среду и добавлении сырья для ферментации к культуральной среде;
(B) стадия фильтрования фильтрата, полученного на стадии (А), через нанофильтрационную мембрану;
(C) стадия дистилляции фильтрата, полученного на стадии (В), под давлением не меньше чем 10 Па и не больше чем 30 кПа, при не меньше чем 50°C и не больше чем 180°C с получением молочной кислоты; и
последующая стадия получения полимолочной кислоты, где молочную кислоту, полученную на стадии (С), полимеризируют путем прямой дегидратационной поликонденсации.
| WO 2007097260 A1, 30.08.2007 | |||
| ГИДРОСТАТИЧЕСКИЙ ПОДШИПНИК | 0 |
|
SU192555A1 |
| US 6489508 B1, 03.12.2002 | |||
| JP 2003335850 A, 28.11.2003 | |||
| WO 2006001034 A2, 05.01.2006 | |||
| ZHANG WANG-XI ET AL | |||
| "Synthesis and Properties of High Molecular Weight Poly(Lactic Acid) and its Resultant Fibers", Chinese Journal of Polymer Science, 2008, v.26, No.4, p.425-432 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЛАКТИДА | 2005 |
|
RU2301230C2 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2016-02-10—Публикация
2009-12-25—Подача