Изобретение относится к пространственно-затрудненным фенолам, а именно к терпенофенолам, и более точно к функциональным производным изоборнилфенола.
Группа соединений представлена формулой (I)
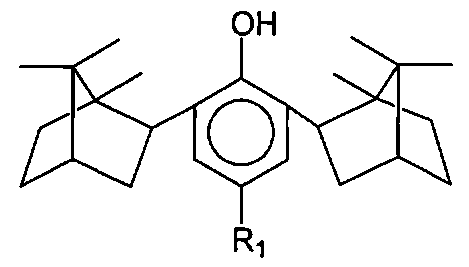
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1′R, 2′S, 4′S) или (1S, 2R, 4R, 1′S, 2′R, 4′R) и (1R, 2S, 4S, 1′R, 2′S, 4′S),
R1 представляет собой группу общей формулы II -(CH2)nNX2, где X - алкильный радикал С1-С8, линейный или разветвленный, циклогексил-, морфолин-, пиперидин-, бензил-, сальсолидина, сальсолина, N-бензил-1-фенилэтиламина,
n=1-10.
Группа соединений представлена формулой (I)
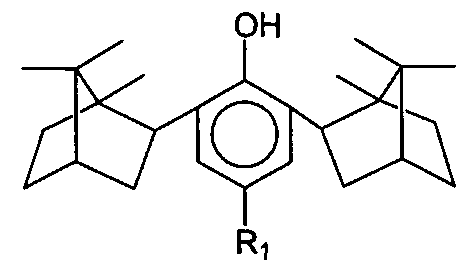
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1′R, 2′S, 4′S) или (1S, 2R, 4R, 1′S, 2′R, 4′R) и (1R, 2S, 4S, 1′R, 2′S, 4′S),
R1 представляет собой группу общей формулы II -(CH2)nNHX, где X - алкильный радикал С1-С8, линейный или разветвленный, циклогексил-, морфолин-, пиперидин-, бензил,
n=1-10.
Группа соединений представлена формулой (I)
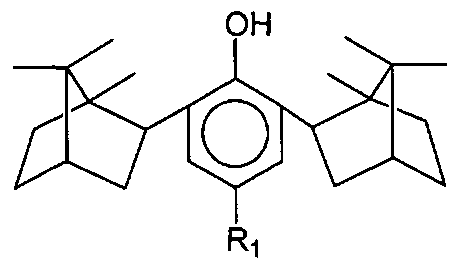
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1′R, 2′S, 4′S) или (1S, 2R, 4R, 1′S, 2′R, 4′R) и (1R, 2S, 4S, 1′R, 2′S, 4′S),
R1 представляет собой группу общей формулы III -(CH2)nY, где Y - ОН-группа; Hal; SH,
n=1-10.
Группа соединений представлена формулой (I)
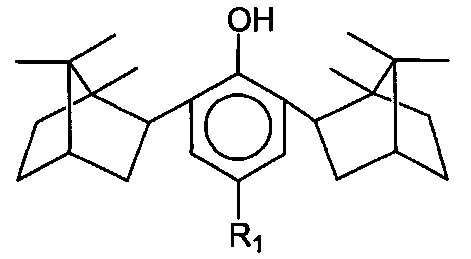
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1′R, 2′S, 4′S) или (1S, 2R, 4R, 1′S, 2′R, 4′R) и (1R, 2S, 4S, 1′R, 2′S, 4′S),
R1 - формильная группа,
n=1-10.
Одним из самых важных путей использования фенолов является производство антиоксидантов. В настоящее время в мире сложился устойчивый рынок различных по значению и химической структуре антиоксидантов, в котором фенольные антиокислители занимают определенную нишу. Терпенофенольные соединения, к группе которых относятся заявляемые соединения, являются физиологически активными веществами широкого спектра действия с низкой токсичностью [Кузаков Е.В., Шмидт Э.Н. ХПС. 2000 (3), 198; Cirri М., Mura P., Corvi Mora P. Int. J. Pharm. 2007, 30, 84; RU №2347561]. Для изоборнилфенолов и их производных характерны гемореологические и антиагрегантные эффекты [RU №2347561, опубл. 27.02.2009. Бюл. №6; №2351321, опубл. 10.042009. Бюл. №10; №2406488, 20.12.2010; №2406487, 20.12.2010], а также противовоспалительная активность [И.Ю. Чукичева, И.В. Федорова, Е.В. Буравлев, А.Е. Лумпов, Ю.Б. Вихарев, Л.В. Аникина, В.В. Гришко, А.В. Кучин. Химия природ. соедин. 402 (2010); Е.V. Buravlev, I.Yu. Chukicheva, К.Yu. Suponitsky, Yu.В. Vikharev, V.V. Grishko, A.V. Kutchin, Lett. Org. Chem. 8. 301 (2011)].
Одним из наиболее перспективных и практически важных направлений в настоящее время является синтез гибридных антиоксидантов, молекулы которых содержат различные реакционные центры, способные ингибировать процесс окисления по различным механизмам, тем самым расширяя спектр применимости фенольных антиоксидантов и увеличивая их эффективность. Кроме того, введение функциональных групп в молекулу фенола позволяет в дальнейшем сочетать антиоксидантные свойства с адресной доставкой и способностью к структурным взаимодействиям с биосистемой. К числу таких гибридных антиоксидантов относятся ИХФАНы [Никифоров Г.А., Белостоцкая И.С., Вольева В.Б., Комиссарова Н.Л., Горбунов Д.Б. В сб. "Биоантиоксиданты", Научный вестник мед. акад. Тюмень. 2003. С. 50-51; Molotchkina Е.М., Ozerova I.В., Burlakova E.B. Free Radical Biology and Medicine. 2002. V. 33. Issue 2S1. №610, p. S229-S230; E.Б. Бурлакова. Рос. хим. ж. (Ж. рос. хим. об-ва им. Д.И. Менделеева). 2007. Т. LI. №1. С. 3-12; Перевозкина М.Г., Сторожок Н.М., Борисенко В.Е. Вестник Тюменского государственного университета. 2006. №3. С. 58-66]. Из числа технических антиоксидантов и стабилизаторов, содержащих функциональные группы, можно отметить используемые в промышленности Anox, Irganox 1076, Агидол-3 и т.п.
Целью изобретения является получение производных 2,6-диизоборнилфенола. Заявляемые соединения являются промежуточными соединениями для дальнейшей функционализации 2,6-диизоборнилфенола (галогенсодержащих, аминных, амидных, сложноэфирных, фенолокислот и так далее), кроме того, возможна трансформация одной функциональной группы в другую.
Известно о получении 3,5-диизоборнил-4-оксибензальдегида [Казаринова Н.Ф., Новицкая Л.П. Определение стабилизаторов и некоторых продуктов их превращения методом хроматографии // Пластические массы. 1975. 3. 76-77]. Однако в качестве характеристик указанного производного авторы приводят только значение Rf.
Иных прототипов для описываемых в изобретении функциональных производных 2,6-диизоборнилфенола нами не выявлено.
Заявляемые соединения синтезированы по типовым методикам аминометилирования по Манниху, бромометилирования, окисления и восстановления. Структура полученных соединений подтверждена методами ИК- и ЯМР-спектроскопии. ИК-спектры записывали на ИК-Фурье-спектрометре Shimadzu IR Prestige 21 в таблетках с KBr. Спектры ЯМР 1Н и 13C регистрировали на приборе «Bruker Avance II 300» (рабочая частота 300 и 75 МГц) в CDCl3. Производные 2,6-диизоборнилфенола с различной конфигурацией терпенового фрагмента получены на основе чистых изомеров 2,6-диизоборнилфенола, в которых изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1′R, 2′S, 4′S) или (1S, 2R, 4R, 1′S, 2′R, 4′R) и (1R, 2S, 4S, 1′R, 2′S, 4′S).
Пример 1. 4-Гидрокси-3-{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гепт-2-ил}-5-{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гепт-2-ил}бензальдегид, бесцветный порошок, т.пл. 233-235°C. Соединение получено на основе мезо-формы 2,6-диизоборнил-4-метилфенола по известной методике [V.V. Ershov, A.A. Volodkin, G.A. Nikiforov, К.М. Dyumaev. Sterically hindered phenols. Bromination of 2,6-dialkyl-p-cresols and 2,6-dialkyl-4-(bromomethyl)phenols // Russian Chemical Bulletin. 1962. Volume 11. No. 10. P. 1744-1747].
ИК-спектр (табл. KBr), v/см-1: 3595 (v, ОН), 2951, 2875, 1452, 1381, 1369 (Me, СН2), 1662 (C=O). Спектр ЯМР 1H (CDCl3, 300 МГц, δ, м.д., J/Гц): 0.88 (с, 6Н, Ме-10, Ме-10′); 0.90 (с, 6Н, Ме-9, Ме-9′); 0.93 (с, 6Н, Ме-8, Ме-8′); 1.40-1.48, 1.63-1.71 (оба м, по 4Н, Н-3, Н-3′, Н-4, Н-4′, СН2-5, СН2-5′); 1.90-1.94 (м, 4Н, СН2-6, СН2-6′); 2.27-2.38 (м, 2Н, Н-3, Н-3′); 3.02 (т, 2Н, J=9.0 Гц, Н-2, Н-2′); 5.49 (с, 1Н, ОН); 7.75 (с, 2Н, Н-14, Н-16); 9.87 (с, 1H, СНО). Спектр ЯМР l3C (CDCl3, 75 МГц, δ, м.д.): 12.63 (С-10, С-10′); 20.23 (С-9, С-9′); 21.32 (С-8, С-8′); 27.50 (С-5, С-5′); 34.06 (С-3, С-3′); 40.04 (С-6, С-6′); 45.36 (С-4, С-4′); 46.06 (С-2, С-2′); 48.38 (С-1, С-1′); 50.10 (С-7, С-7′); 128.11 (С-14, С-16); 128.59 (С-15); 129.49 (С-11, С-13); 159.86 (С-12); 191.67 (СНО).
Аналогично на основе рацемической формы 2,6-диизоборнил-4-метилфенола получен рацемат 3,5-диизоборнил-4-оксибензальдегида (4-гидрокси-3,5-ди{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гепт-2-ил}бензальдегид и 4-гидрокси-3,5-ди{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гепт-2-ил}бензальдегид), бесцветный порошок, т.пл. 189-191°C (возм. разл.).
Спектр ЯМР 1H (CDCl3, 300 МГц, δ, м.д., J/Гц): 0.78 (с, 6Н, Ме-10, Ме-10′); 0.89 (с, 6Н, Ме-9, Ме-9′); 0.93 (с, 6Н, Ме-8, Ме-8′); 1.41-1.52, 1.63-1.79 (оба м, по 4Н, Н-3, Н-3′, Н-4, Н-4′, СН2-5, СН2-5′); 1.94-1.98 (м, 4Н, СН2-6, СН2-6′); 2.31-2.39 (м, 2Н, Н-3, Н-3′); 3.09 (т, 2Н, J=8.6 Гц, Н-2, Н-2′); 5.43 (с, 1Н, ОН); 7.75 (с, 2Н, Н-14, Н-16); 9.87 (с, 1Н, СНО). Спектр ЯМР 13C (CDCl3, 75 МГц, δ, м.д.): 12.51 (С-10, С-10′); 20.36 (С-9, С-9′); 21.35 (С-8, С-8′); 27.54 (С-5, С-5′); 34.50 (С-3, С-3′); 40.21 (С-6, С-6′); 45.47 (С-4, С-4′); 46.15 (С-2, С-2′); 48.38 (С-1, С-1′); 49.82 (С-7, С-7′); 128.07 (С-14, С-16); 128.49 (С-15); 129.57 (С-11, С-13); 159.58 (С-12); 191.65 (СНО).
Пример 2. Третичные аминометильные производные получены по реакции Манниха [Н.А. Ниязов, В.П. Тимофеев, В.Д. Сурков, Н.В. Любимов. Способ получения 2-(N,N-диметиламинометил)фенола. Пат. док. RU 2144529 C1, заявл. 18.03.1998, опубл. 20.01.2000; Ki-Whan Chi, Yoon Soo Ann, Kwang Taeg Shim, Tae Ho Park, Jeong Soo Ahn. One-pot synthesis of Mannich base using hydroxy aromatic rings and secondary amines // Bull. Korean Chem. Soc. 1999. Vol. 20. No. 8. P. 973-976] исходя из мезо-формы 2,6-диизоборнилфенола.
4-(диметиламино)метил-2-{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гепт-2-ил}-6-{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гепт-2-ил}фенол. Белый порошок. Тпл=134-136°C. ИК-спектр (табл. с KBr), v/см-1: 3620 (ОН), 2960, 2888, 1462, 1392, 1372 (Me, СН2), 1200 (С-N).
Спектр ЯМР 1H (CDCl3, 300 МГц, δ, м.д., J/Гц): 0.80 (с, 6Н, Me-10, Me-10′); 0.84 (с, 6Н, Ме-9, Ме-9′); 0.89 (с, 6Н, Ме-8, Ме-8′); 1.33-1.45 (м, 4Н, Н-6, Н-6′); 1.55-1.67 (м, 4Н, Н-3, Н-3′); 1.85-1.88 (м, 4Н, Н-5, Н-5′); 2.18 (с, 6Н, Ме-18, Ме-18′); 2.28-2.32 (м, 2Н, Н-4, Н-4′); 3.01 (т, 2Н, Н-2, Н-2′, J=9 Гц); 3.41 (с, 2Н, СН2-17); 7.05 (с, 2Н, Н-14 и Н-16). Спектр ЯМР 13C (CDCl3,75 МГц, δ, м.д.): 12.49 (С-10, С-10′); 20.13 (С-9, С-9′); 21.41 (С-8, С-8′); 27.55 (С-5, С-5′); 33.93 (С-3, С-3′); 39.97 (С-6, С-6′); 44.55 (С-18, С-18′); 45.46 (С-2, С-2′); 46.05 (С-4, С-4′); 48.12 (С-7, С-7′); 49.94 (С-1, С-1′); 64.31 (С-17); 126.75 (С-14, С-16); 127.31 (С-11, С-13); 128.21 (С-15).
4-(диэтиламино)метил-2-{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гепт-2-ил}-6-{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гепт-2-ил}фенол. Порошок желтого цвета. Тпл=128-130°C. ИК-спектр (табл. с KBr), v/см-1: 3620 (ОН), 2964, 2880, 1468, 1392, 1380 (Me, СН2), 1200 (C-N).
Спектр ЯМР 1H (CDCl3, 300 МГц, δ, м.д., J/Гц): 0.84 (с, 6Н, Me-10, Me-10′); 0.88 (с, 6Н, Ме-9, Ме-9′); 0.93 (с, 6Н, Ме-8, Ме-8′); 1.05 (т, 6Н, Ме-19, Ме-19′, J=7 Гц); 1.38-1.50 (м, 4Н, Н-6, Н-6′); 1.58-1.74 (м, 4Н, Н-3, Н-3′); 1.91-1.98 (м, 4Н, Н-5, Н-5′); 2.28-2.35 (м, 2Н, Н-4, Н-4′); 3.03 (т, 2Н, Н-2, Н-2′, J=9 Гц); 3.58 (с, 2Н, СН2-17); 4.78 (с, 1H, ОН); 7.13 (с, 2Н, Н-14 и Н-16). Спектр ЯМР 13C (CDCl3, 75 МГц, δ, м.д.): 12.14 (С-19, С-19′); 12.57 (С-10, С-10′); 20.16 (С-9, С-9′); 21.50 (С-8, С-8′); 27.62 (С-5, С-5′); 34.08 (С-3, С-3′); 40.08 (С-6, С-6′); 45.49 (С-2, С-2′); 46.14 (С-4, С-4′); 46.44 (С-18, С-18′); 48.16 (С-7, С-7′); 49.93 (С-1, С-1′); 57.42 (С-17); 126.07 (С-14, С-16); 127.93 (С-11, С-13).
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПРОИЗВОДНЫЕ 2,6-ДИИЗОБОРНИЛФЕНОЛА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2516699C2 |
| 2,6-ДИИЗОБОРНИЛФЕНОЛЫ | 2011 |
|
RU2502719C2 |
| ТЕТРА-(МЕЗО-АРИЛ)-ПОРФИРИН С ДИИЗОБОРНИЛФЕНОЛЬНЫМИ ЗАМЕСТИТЕЛЯМИ В МАКРОЦИКЛЕ | 2012 |
|
RU2496761C1 |
| N-БОРНИЛ- И N-ФЕНХИЛКАРБОКСАМИДЫ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ ОРТОПОКСВИРУСОВ | 2022 |
|
RU2800448C1 |
| Хиральные комплексы цинка с терпеновыми производными этилендиамина | 2022 |
|
RU2785281C1 |
| Кумарины с бициклическими монотерпеновыми заместителями | 2019 |
|
RU2707103C1 |
| Хиральные S-монотерпенилцистеины | 2018 |
|
RU2689381C1 |
| Способ получения хиральных S-монотерпенилцистеинов | 2018 |
|
RU2675238C1 |
| Средство с комплексным фармакологическим эффектом для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней (варианты) | 2019 |
|
RU2757874C1 |
| ПРОИЗВОДНЫЕ БЕНЗОКСАЗОЛОНА, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2024512C1 |
Изобретение относится к новым пространственно-затрудненным фенолам, которые являются промежуточными соединениями для дальнейшей функционализации 2,6-диизоборнилфенола,
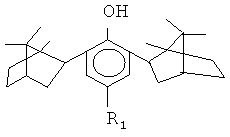
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1'R, 2'S, 4'S),
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1'S, 2'R, 4'R) и (1R, 2S, 4S 1'R, 2'S, 4'S),
R1 представляет собой формильную группу или группу общей формулы II -(CH2)nNX2, где X - алкильный радикал С1-С8, линейный или разветвленный, циклогексил-, морфолин-, пиперидин-, бензил-, сальсолидина, сальсолина, N-бензил-1-фенилэтиламина, n=1-10. 2 н.п. ф-лы, 2 пр.
1. Группа соединений, представленная формулой (I)

где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1'R, 2'S, 4'S),
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1'S, 2'R, 4'R) и (1R, 2S, 4S 1'R, 2'S, 4'S),
R1 представляет собой группу общей формулы II -(CH2)nNX2, где X - алкильный радикал С1-С8, линейный или разветвленный, циклогексил-, морфолин-, пиперидин-, бензил-, сальсолидина, сальсолина, N-бензил-1-фенилэтиламина,
n=1-10.
2. Группа соединений, представленная формулой (I)
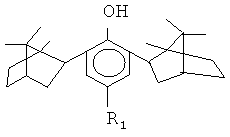
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1'R, 2'S, 4'S),
где изоборнильные фрагменты имеют конфигурацию (1S, 2R, 4R, 1'S, 2'R, 4'R) и (1R, 2S, 4S, 1'R, 2'S, 4'S),
R1 - формильная группа.
| Способ реконструкции жесткой армировкиВЕРТиКАльНОгО СТВОлА | 1979 |
|
SU827797A1 |
| СПОСОБ ИНГИБИРОВАНИЯ ТЕРМОПОЛИМЕРИЗАЦИИ ПРИ ПЕРЕРАБОТКЕ ЖИДКИХ ПРОДУКТОВ ПИРОЛИЗА | 2008 |
|
RU2375342C2 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Казаринова Н.Ф | |||
| и др., Определение стабилизаторов и некоторых продуктов их превращения хроматографически | |||
| Пластические массы, 1975, N3, 76-77 | |||
| M.B Plotnikov et al, Antithrombogenic and antiplatelet activity of ortho-isobornyl phenol derivative | |||
| Bulletin of Experimental Biology and Medicine, 2008, | |||
Авторы
Даты
2016-02-20—Публикация
2011-07-06—Подача