Изобретение относится к медицине, конкретно к фармакологии, и касается средств для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней.
Производные c бицикло[2.2.1]гептановой структурой, к которым относятся камфора и ее производные, изоборнилфенолы, обладают физиологическими свойствами и находят применение в медицине [О.И. Киселев, Химиопрепараты и химиотерапия гриппа, Росток, Санкт Петербург, 2012, 272 с.; М. Д. Машковский, Лекарственные средства, 16-е изд., Новая Волна, Москва, 2012, 1216 с. M. Cirri, P. Mura, P. Corvi Mora, Int. J. Pharm., 2007, 340, 84].
Известно, что 2,6-диизоборнил-4-метилфенол (2,6-ди(1,7,7-триметилбицикло[2.2.1]гептан-экзо-2-ил)-4-метилфенол) обладает широким спектром фармакологической активности: антирадикальной, антиоксидантной, нейропротекторной, противоишемической, ретинопротекторной и другими видами действия [Патенты РФ № 2347561; 2351321; 2406488; 2406487; Морфология. 2011. Т. 140. № 6. С.43-47; Neuroscience and Behavioral Physiology. 2012. Vol. 42. No. 9. Р. 1019-1023; Бюллетень экспериментальной биологии и медицины. 2014. Т. 157. № 2. С. 173-176; Медицинские науки. Фундаментальные исследования. 2014. № 7. С. 790-794; Key Engineering Materials. 2016. Vol. 683. Р. 469; Бюллетень экспериментальной биологии и медицины. 2018. Т. 165. № 5. С. 601-604].
Задачей изобретения является исследование фармакологической активности структурных изомеров: 2-{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-6-{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенола − мезо-форма и 2,6-ди{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}фенол и 2,6-ди{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенола – рацемическая форма.
Изобретение представлено в вариантах.
Технический результат состоит в расширении арсенала средств для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней, а также в усилении фармакологической активности за счет стереоспецифичности действия индивидуальных стереоизомеров, что обеспечивает повышение эффективности лечения заболеваний.
Технический результат достигается тем, что средство для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней (по первому варианту) выделено из смеси диастереомеров 2,6-ди(1,7,7-триметилбицикло[2.2.1]гептан-экзо-2-ил)-4-метилфенола в виде мезо-формы − 2-{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-6-{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол с химической чистотой более 98%.
Технический результат достигается тем, что средство для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней (по второму варианту) выделено из смеси диастереомеров 2,6-ди(1,7,7-триметилбицикло[2.2.1]гептан-экзо-2-ил)-4-метилфенола в виде рацемической формы – 2,6-ди{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол и 2,6-ди{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол с химической чистотой более 98%.
Научно обосновано, что заявленные средства обладают антирадикальной, гемореологической, антитромбоцитарной и антитромбогенной активностью, увеличивают мозговой кровоток, а также обладают нейропротекторной активностью.
Механизм действия биологически активных веществ обычно заключается в их соединении со специфическими рецепторами. Каждый рецептор обладает характерной пространственной структурой участка, взаимодействующего с биологически активным веществом, и их структуры должны соответствовать друг другу по принципу ключ-замок. Поэтому у большинства лекарственных препаратов существует тесная взаимосвязь между пространственной структурой и фармакологической активностью, то есть стереоспецифичность действия. Различное фармакологическое воздействие форм изомеров, а также различная степень их действия и наличие побочных эффектов необходимо учитывать при создании нового лекарственного средства.
Введение терпенового заместителя в ароматическое ядро фенолов осуществляется с использованием реакции алкилирования Фриделя-Крафтса при взаимодействии 4-метилфенола с камфеном [Патент РФ № 2485090]. Применение в качестве алкилирующего агента бициклического монотерпена камфена, независимо от его оптической чистоты, приводит к образованию смеси стереоизомеров 2,6-диизоборнил-4-метилфенола. Индивидуальные диастереомеры мезо- и рац-формы с de >97% получены в результате дополнительного разделения путем кристаллизации [Патент РФ № 2502719].
Нами разработаны условия для выделения из смеси диастереомеров 2,6- диизоборнил-4-метилфенола мезо-формы − 2-{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-6-{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол (далее мезо-2,6-диизоборнил-4-метилфенол или мезо-1) с химической чистотой более 98% и рацемической формы – 2,6-ди{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол и 2,6-ди{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол (далее рац-2,6-диизоборнил-4-метилфенол или рац-2) с химической чистотой более 98%.
Фармакологические свойства полученных индивидуальных структурных изомеров 2,6-диизоборнил-4-метилфенола в литературе не описаны и не следуют явным образом из известного уровня техники. Авторами изобретения проведены научно-исследовательские и экспериментальные работы и осуществлена оценка комплекса фармакологических свойств и эффектов каждого соединения, выделенного из смеси диастереомеров 2,6-ди(1,7,7-триметилбицикло[2.2.1]гептан-экзо-2-ил)-4-метилфенола.
Нами выполнена оценка токсичности соединений мезо-1 и рац-2 на белых беспородных мышах. Острую токсичность образцов в каждой дозе исследовали на 10 беспородных мышах (5 самок и 5 самцов массой 18−22 г). Животных наблюдали в течение 14 суток, в течение первых суток - наблюдение постоянное. Для определения показателя острой токсичности LD50 использовали пробит-анализ по методу Литчфилда-Вилкоксона. Средняя смертельная доза (LD50) для соединений мезо-1 и рац-2 при введении в желудок не выявлена: введение этих соединений в дозе 5 г/кг не вызывало летального исхода ни у одного животного, что позволило отнести изученные вещества к 4-му классу опасности [ГОСТ 12.1.007–76, Система стандартов безопасности труда (ССБТ). Вредные вещества. Классификация и общие требования безопасности. Вредные вещества. Классификация и общие требования безопасности, 1977].
Антирадикальную активность изомеров мезо-1 и рац-2 оценивали по их способности взаимодействовать с DPPH. В видимой области спектра DPPH в органических растворителях имеет максимум поглощения в диапазоне длин волн 515-520 нм, который прогрессивно уменьшается и исчезает при переходе соединения в нерадикальную форму. Кинетическую кривую изменения оптической плотности контрольной и опытных проб записывали на спектрофотометре «Varian Cary 50» (США) сразу после смешивания раствора DPPH (0.25 ммоль) с растворителем (контрольная проба) или раствором исследуемого соединения (0.25 ммоль) (опытные пробы) в соотношении 1:1 по объему. Таким образом, конечные концентрации DPPH и исследуемого вещества в пробах составляли 0.125 ммоль. В качестве растворителя использовали этанол. Для количественной оценки антирадикальной активности применили показатель эффективного времени (ET50%) - время, за которое происходит уменьшение исходной оптической плотности на 50%.
В результате сравнительного исследования антирадикальной активности в тесте DPPH индивидуальных изомеров мезо-1 и рац-2 установлено, что ET50% (мезо-1) = 5.88±0.46, ET50% (рац-2) = 9.42±0.54.
Эксперименты по изучению гемореологических свойств мезо-2,6-диизоборнил-4-метилфенол и рац-2,6-диизоборнил-4-метилфенол проводили на 25 крысах-самцах Вистар массой 250−300 г. Животные были разделены на группы: 5 животных получили внутрижелудочно крахмальную слизь (контроль), 5 животных получили внутрижелудочно пентоксифиллин (400 мг/кг, группа Pph); 5 животных получили внутрижелудочно мезо-2,6-диизоборнил-4-метилфенол (100 мг/кг, группа мезо-1) и 5 животных получили внутрижелудочно рац-2,6-диизоборнил-4-метилфенол (100 мг/кг, группа рац-2). Соединения и эквиобъемное количество крахмальной слизи (1 мл) вводили внутрижелудочно через зонд за один час до забора крови. Влияние соединений на вязкость крови оценивали с использованием модели гипервязкости крови in vitro. Кровь забирали из общей сонной артерии под эфирным наркозом. В качестве стабилизатора использовали 3.8% раствор цитрата натрия в соотношении с кровью 1:9. Вязкость крови измеряли на ротационном вискозиметре АКР-2 в диапазоне скоростей сдвига от 5 с−1 до 300 с-1 до и после инкубации образцов при температуре 20.0±0.4 °С в течение 60 минут.
Спонтанную агрегацию эритроцитов исследовали с помощью модифицированного метода [Габриэлян Э.С., Акопов С.Э. Клетки крови и кровообращение. Ереван: Айастан, 1985. 399 с.; Плотников М.Б., Алиев О.И., Маслов М.Ю. и др. Эксперим. и клинич. фармакология. 1999. № 6. С. 45–47]. Для установления интенсивности фотометрического сигнала использовали микроколориметр МКМФ-1, с графической регистрацией на графопостроителе Н306. Критерием агрегационной активности эритроцитов служил полупериод агрегации Т1/2 – время, за которое величина фотометрического сигнала снижается в два раза.
Эксперименты по изучению антитромбоцитарной активности проводили на крысах-самцах Вистар массой 250−280 г. Животные были разделены на группы: 5 животных получили внутрижелудочно крахмальную слизь (контроль), 5 животных получили внутрижелудочно пентоксифиллин (400 мг/кг, группа Pph); 5 животных получили внутрижелудочно мезо-2,6-диизоборнил4-метилфенол (100 мг/кг, группа мезо-1), 5 животных получили внутрижелудочно рац-2,6-диизоборнил-4-метилфенол (100 мг/кг, группа рац-2). Препараты и эквиобъемное количество крахмальной слизи (1 мл) вводили внутрижелудочно через зонд за один час до забора крови. Кровь забирали из общей сонной артерии под эфирным наркозом. В качестве стабилизатора использовали 3.8% раствор цитрата натрия в соотношении с кровью 1 : 9.
Получение богатой (БТП) и бедной (БеТП) тромбоцитами плазмы и подсчет числа тромбоцитов проводили по стандартному методу [Баркаган З.С., Момот А.П. Основные методы лабораторной диагностики нарушений системы гемостаза. – Барнаул, 1998. С. 10–11]. Из проб крови получали плазмы БТП и БеТП соответственно на центрифуге РС-6 при 400 g и 1800 g. В полученной БТП подсчитывали количество тромбоцитов микроскопическим методом при фазовом контрасте в камере Горяева. Агрегацию тромбоцитов в богатой тромбоцитами плазме (БТП) определяли нефелометрическим методом [Born G.V.R. Aggregation of blood platelets by adenosine diphosphate and its reversal // Nature. 1962. Vol. 194, № 4832. P. 927–929].
Так как в норме число тромбоцитов в крови у крысы колеблется в широких пределах − от 430 000 до 1 млн в 1 мм3 − после определения числа тромбоцитов в БТП проводили стандартизацию числа тромбоцитов, для чего БПТ разводили необходимым количеством БеТП до 400±30 тыс. тромбоцитов в 1 мм3 в пробе [Закревская А.Л. Тромбоциты крыс как модель исследования ингибиторов агрегации // Патологическое функционирование системы гемостаза. Л., 1990. С. 46–54; Западнюк И.П., Западнюк В.И., Захария Е.А. Лабораторные животные. – Киев, 1974. 303 с.]. Агрегацию тромбоцитов оценивали в стандартизованной плазме на приборе АТ-02, агрегатограммы регистрировали с помощью самописца Reсorder 2210.
После добавления индуктора агрегации (АДФ в конечной концентрации 4⋅10-6 М) регистрировали изменение уровня оптической плотности БТП. В качестве критерия агрегационной активности тромбоцитов использовали показатель степени агрегации (в %), характеризуемый изменением оптической плотности БТП после добавления в кювету индуктора агрегации. При этом за 100% принимали величину оптической плотности БеТП, а за 0% − величину оптической плотности БТП.
Эксперименты по изучению антитромбогенной активности фенолов мезо-1 и рац-2 проводили на 20 крысах-самцах Вистар массой 220‒240 г. Животные были разделены на группы: 5 животных получили внутрижелудочно крахмальную слизь (контроль), 5 животных получили внутрижелудочно пентоксифиллин (400 мг/кг, группа (Pph); 5 животных получили внутрижелудочно мезо-2,6-диизоборнил-4-метилфенол (100 мг/кг, группа мезо-1), 5 животных получили внутрижелудочно рац-2,6-диизоборнил-4-метилфенол (100 мг/кг, группа рац-2). Соединения и эквиобъемное количество крахмальной слизи (1 мл) вводили внутрижелудочно через зонд в течение трех суток. На третьи сутки эксперимента – через 1 час после последнего введения животных наркотизировали (тиопентал натрия в дозе 60 мг/кг внутрибрюшинно), выделяли левую общую сонную артерию и воспроизводили модель внутрисосудистого тромбоза [Максименко А.В., Тищенко Е.Г. Антиоксидантная биотерапия для защиты сосудистой производными супероксиддисмутазы и каталазы // Цитология. 1999. Т. 41, № 9. С. 821–822]. На отпрепарированную сонную артерию накладывали манжеточные датчики и регистрировали величину кровотока по сосуду с помощью электромагнитного расходомера крови MFV-1100 (Nihon Kohden, Япония). Затем под сонную артерию подкладывали полоску фильтровальной бумаги и полоску полиэтиленовой пленки. Сверху на эту артерию накладывали полоску фильтровальной бумаги, на которую наносили 1 каплю 10% раствора FeCl2. Измеряли величину кровотока в артерии, время от момента нанесения хлорида железа на левую сонную артерию до полной остановки кровотока в ней (время образования тромба). Кроме того, производили расчет снижения кровотока относительно исходной величины кровотока в процентах. Массу тромба оценивали гравиметрическим методом.
Статистическую обработку проводили с помощью пакета программного обеспечения «Statistica 6.0». Рассчитывали среднее значение, стандартную ошибку, для выявления межгрупповых различий использовали t-критерий Стьюдента.
Результаты исследований гемореологической активности соединений мезо-1 и рац-2 представлены в примерах 1, 2 и таблицах 1, 2.
Пример 1. Инкубирование крови в течение 60 мин при температуре 20.0±0.4 °С приводило к значимому повышению вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 30, 17, 26, 27 и 13% соответственно (табл. 1, контроль).
У опытных крыс в группе, получавшей пентоксифиллин, вязкость крови до инкубации была достоверно ниже, чем в контроле при скоростях сдвига 5, 10 и 50 с-1 на 10%, 19% и 4% соответственно. Инкубирование крови крыс этой группы в течение 60 мин при температуре 20.0±0.4 °С приводило к повышению вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 8, 11, 12, 9 и 8% соответственно. После инкубации вязкость крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1, 300 с-1 была ниже, чем в контроле на 26, 20, 18, 18 и 8% соответственно (табл. 1). Таким образом, на модели гипервязкости крови in vitro пентоксифиллин ограничивает возрастание вязкости крови в широком диапазоне скоростей сдвига.
У опытных крыс, получавших препарат мезо-1, до инкубации вязкость крови была ниже, чем в контроле при скоростях сдвига 5 с-1, 10 с-1 и 50 с-1 на 12%, 11% и 7% соответственно. Инкубирование крови крыс этой группы в течение 60 мин при температуре 20.0±0.4 °С приводило к повышению вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 8, 9, 8, 7 и 4% соответственно. После инкубирования вязкость крови была ниже, чем в контроле при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 28, 17, 21, 19 и 8% соответственно (табл. 1). Таким образом, на модели гипервязкости крови in vitro мезо-2,6-диизоборнил-4-метилфенол ограничивает возрастание вязкости крови в широком диапазоне скоростей сдвига. Выраженность гемореологической активности мезо-2,6-диизоборнил-4-метилфенола несколько превосходит таковую у прототипа − пентоксифиллина.
У опытных крыс в группе, получавшей препарат рац-2,6-диизоборнил-4-метилфенол, исходные значения вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1 были ниже на 14, 11 и 7% соответственно, чем в контроле. Инкубирование крови крыс этой группы в течение 60 мин при температуре 20.0±0.4 °С приводило к повышению вязкости крови во всем диапазоне исследуемых скоростей сдвига на 17, 12, 12, 13 и 9%. После инкубирования вязкость крови крыс этой группы была ниже, чем в контроле при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 22, 15, 18, 15 и 4% соответственно (табл. 1). Таким образом, на модели гипервязкости крови in vitro рац-2,6-диизоборнил-4-метилфенол ограничивает возрастание вязкости крови в широком диапазоне скоростей сдвига. Выраженность гемореологической активности рац-2 сопоставима с таковой у прототипа − пентоксифиллина.
Пример 2. Полупериод агрегации эритроцитов у крыс контрольной группы составил 20.7±2.1 с. Инкубирование крови в течение 60 мин при температуре 20.0±0.4 °С приводило к уменьшению полупериода агрегации эритроцитов на 35% (табл. 2, контроль). Таким образом, на модели гипервязкости крови in vitro в контрольной группе установлено уменьшение полупериода агрегации эритроцитов, что свидетельствовало об усилении агрегации эритроцитов.
Инкубирование крови у крыс, получавших пентоксифиллин или препараты мезо-1 и рац-2, в течение 60 мин при температуре 20.0±0.4 °С не вызывало значимых сдвигов в значении полупериода агрегации эритроцитов (табл. 2). Значение полупериода агрегации эритроцитов по сравнению с показателем контрольной группы после инкубации представлено в таблице 2. Анализ полученных данных показывает, что на модели гипервязкости крови in vitro наиболее значимо предотвращает усиление агрегации эритроцитов пентоксифиллин. Выраженность гемореологической активности диастереомеров мезо-2,6-диизоборнил-4-метилфенола и рац-2,6-диизоборнил-4-метилфенола сопоставима с таковой у прототипа – пентоксифиллина.
Таблица 1. Влияние внутривенной 10-минутной инфузии винпоцетина (4 мг/кг, Vinp) и подкожного введения масленого раствора мезо-2,6-диизоборнил-4-метилфенола (100 мг/кг, мезо-1) и рац-2,6-диизоборнил-4-метилфенола (100 мг/кг, рац-2) на динамику мозгового кровотока (МК, мл/мин) и системного артериального давления (САД, мм рт.ст.)

Примечание: × – р < 0.05 по сравнению с исходными значениями;
* – р < 0.05 по сравнению с группой контроля.
Таблица 2. Влияние однократного внутрижелудочного введения пентоксифиллина (400 мг/кг, Pph), мезо-2,6-диизоборнил-4-метилфенола (100 мг/кг, мезо-1), рац-2,6-диизоборнил-4-метилфенола (100 мг/кг, рац-2) на агрегацию эритроцитов до (1) и через 1 ч после инкубации при комнатной температуре (20.0±0.4 °С) (2)

Примечание: × − р < 0.05 по сравнению с исходными значениями;
* – р < 0.05 по сравнению с группой контроля.
Результаты исследований антитромбоцитарной активности изомеров мезо-1 и рац-2 представлены в примере 3 и таблице 3.
Пример 3. В контрольной группе животных амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизованной плазме составила 27±1% (табл. 3, контроль).
После однократного внутрижелудочного введения пентоксифиллина в дозе 400 мг/кг амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизированной плазме составила 18±1%, что на 33% ниже показателя у крыс контрольной группы (табл. 3, Pph). Таким образом, пентоксифиллин в дозе 400 мг/кг внутрижелудочно однократно обладает выраженной антиагрегантной активностью.
После однократного внутрижелудочного введения рац-2,6-диизоборнил-4-метилфенола (100 мг/кг, рац-2) в дозе 100 мг/кг амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизованной плазме составила 17±1% (табл. 3, рац-2). Амплитуда агрегации тромбоцитов была на 37% ниже, чем в контроле и была близка к значению показателя у крыс, получавших пентоксифиллин. Тем самым рац-2,6-диизоборнил-4-метилфенол показывает выраженную антиагрегантную активность.
После однократного внутрижелудочного введения мезо-2,6-диизоборнил-4-метилфенола в дозе 100 мг/кг амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизованной плазме составила 16±1% (табл. 3, мезо-1). Амплитуда агрегации тромбоцитов была на 41% ниже, чем в контроле и была близка к значению показателя у крыс в группе, получавших прототип – пентоксифиллин. Таким образом, мезо-2,6-диизоборнил-4-метилфенол обнаруживает выраженную антиагрегантную активность.
Таблица 3. Влияние введения препаратов на АДФ-индуцированную агрегацию тромбоцитов* и на снижение кровотока в сонной артерии в течение 90 минут и массу тромба через сутки после аппликации хлорида железа**

Примечание: * − однократного внутрижелудочного введения пентоксифиллина (400 мг/кг, Pph), мезо-2,6-изоборнил-4-метилфенола (100 мг/кг, мезо-1), рац-2,6-изоборнил-4-метилфенола (100 мг/кг, рац-2); ** − трехкратное внутрижелудочное введение указанных препаратов; × – р < 0.05 по сравнению с группой контроля.
Результаты исследований антитромбогенной активности изомеров мезо-1 и рац-2 представлены в примере 4 и таблице 3.
Пример 4. В контрольной группе животных исходная величина кровотока в сонной артерии составляла 5.3±0.5 мл/мин. После аппликации железа хлорида на поверхность сонной артерии у всех животных происходило полное прекращение кровотока по сосуду. Среднее время полной остановки кровотока до нуля составило 20±2 минуты. Масса тромба, определяемая через сутки после аппликации хлорида железа, составила 1.2±0.2 мг (табл. 3, контроль).
У опытных крыс в группе, получавшей пентоксифиллин, исходное значение величины кровотока составляло 6.5±0.5 мл/мин, что достоверно на 22% превосходило показатель контрольной группы. К концу периода наблюдения (90 мин с момента аппликации хлорида железа) происходило снижение кровотока в сонной артерии на 34±9%. На следующие сутки в просвете сонной артерии не выявлено тромбов ни у одного животного (табл. 3, Pph).
Таким образом, пентоксифиллин в дозе 400 мг/кг внутрижелудочно вызывает повышение кровотока по сравнению с группой контрольных животных и обладает выраженной антитромбогенной активностью.
У опытных крыс, получавших мезо-2,6-изоборнил-4-метилфенол, исходное значение величины кровотока составляло 7.5±0.8 мл/мин, что было на 42% выше, чем показатель контрольной группы. К концу периода наблюдения (90 мин с момента аппликации хлорида железа) происходило снижение кровотока в сонной артерии на 11±10%. На следующие сутки в просвете сонной артерии не выявлено тромбов ни у одного животного (табл. 3, группа мезо-1).
Таким образом, мезо-2,6-изоборнил-4-метилфенол в дозе 100 мг/кг внутрижелудочно способствует повышению кровотока по сравнению с группой контрольных животных и обладает выраженной антитромбогенной активностью.
У опытных крыс группы, получавших рац-2,6-изоборнил-4-метилфенол, исходное значение величины кровотока составляла 7.1±0.6 мл/мин, что было на 34% выше, чем показатель контрольной группы. К концу периода наблюдения (90 мин с момента аппликации хлорида железа) происходило снижение кровотока в сонной артерии на 13±8%. Через сутки у двух животных из пяти были обнаружены тромбы в просвете сонной артерии. Средняя масса тромба составила 0.02±0.02 мг, что было на 98% ниже, чем в контроле (табл. 3, группа рац-2).
Таким образом, рац-2,6-изоборнил-4-метилфенол в дозе 100 мг/кг внутрижелудочно обеспечивает повышение кровотока по сравнению с группой контрольных животных и обладает выраженной антитромбогенной активностью.
Изомеры мезо-2,6-изоборнил-4-метилфенол и рац-2,6-изоборнил-4-метилфенол могут быть использованы для лечения больных с сердечно-сосудистыми заболеваниями для уменьшения повышенной вязкости крови, спонтанной агрегации эритроцитов, а также снижения агрегационной способности тромбоцитов и внутрисосудистого тромбообразования.
Эксперименты по изучению влияния однократного парентерального введения винпоцетина, мезо-2,6-диизоборнил-4-метилфенола и рац-2,6-диизоборнил-4-метилфенола на динамику мозгового кровотока и системного артериального давления проводили на 36 крысах-самцах Вистар массой 320−380 г. Животные были разделены на 4 групп: 10 животным подкожно вводили 1 мл миндального масла (контроль), 6 животным проводили 10-минутную внутривенную инфузию винпоцетина (5 мг/кг) (Vinp); 10 животным подкожно вводили мезо-2,6-диизоборнил-4-метилфенол (100 мг/кг) в виде раствора в 1 мл миндального масла (мезо-1) и 10 животным подкожно вводили рац-2,6-диизоборнил-4-метилфенол (100 мг/кг) в виде раствора в 1 мл миндального масла (рац-1).
Для проведения эксперимента животных наркотизировали (тиопентал натрия в дозе 100 мг/кг внутрибрюшинно) и в отпрепарированную правую бедренную артерию имплантировали катетер для измерения системного артериального давления. Системное артериальное давление регистрировали с помощью датчика полиграфа «Салют», сигнал которого усиливали рН-метром рН-340, с непрерывной записью на самописце КСП-4. Отпрепарировывали левую общую сонную артерию и перевязывали наружную сонную артерию. На общую сонную артерию накладывали манжеточный датчик и регистрировали величину мозгового кровотока с помощью электромагнитного расходомера крови MFV-1100 (Nihon Kohden, Япония).
Эксперименты по изучению влияния курсового внутрижелудочного введения винпоцетина, мезо-2,6-диизоборнил-4-метилфенола и рац-2,6-диизоборнил-4-метилфенола на мозговой кровоток проводили на 20 крысах-самцах Вистар массой 220−240 г. Животные были разделены на 4 группы: 5 животных получили внутрижелудочно крахмальную слизь (контроль), 5 животных получили внутрижелудочно винпоцетин (45 мг/кг) (Vinp); 5 животных получили внутрижелудочно мезо-2,6-диизоборнил-4-метилфенол (100 мг/кг) (мезо-1) и 5 животных получили внутрижелудочно рац-2,6-диизоборнил-4-метилфенол (100 мг/кг) (рац-2).
Препараты и эквиобъемное количество крахмальной слизи (1 мл) вводили внутрижелудочно через зонд ежедневно однократно в течение 3-х суток. На третьи сутки эксперимента через 1 час после последнего введения животных наркотизировали (тиопентал натрия в дозе 100 мг/кг внутрибрюшинно), выделяли левую общую сонную артерию и перевязывали наружную сонную артерию. На общую сонную артерию накладывали манжеточный датчик и регистрировали величину мозгового кровотока с помощью электромагнитного расходомера крови MFV-1100 (Nihon Kohden, Япония).
Статистическую обработку проводили с помощью пакета программного обеспечения «Statistica 6.0». Рассчитывали среднее значение, стандартную ошибку, для выявления межгрупповых различий использовали t-критерий Стьюдента.
Результаты исследований влияния винпоцетина и мезо-2,6-диизоборнил-4-метилфенола и рац-2,6-диизоборнил-4-метилфенола на мозговой кровоток представлены в примерах 5 и 6, таблице 4.
Пример 5. В контрольной группе величина мозгового кровотока в течение 1 часа была стабильной; в последующие 30 мин наблюдения отмечена незначительная тенденция к снижению мозгового кровотока. Со стороны системного артериального давления наблюдалась тенденция к снижению в течение опыта, что, очевидно, отражает условия эксперимента (наличие операционной травмы и использование наркоза) (табл. 4, контроль).
Исходное значение мозгового кровотока у крыс в группе, получавших винпоцетин (Vinp) составило 7.5±0.2 мл/мин. К 5-10 мин внутривенной инфузии винпоцетина мозговой кровоток слабо возрастал (на 4–5%) и через 5 мин после окончания инфузии (15 мин) значительно увеличивался и сохранялся на повышенном уровне (на 15–31%) до конца эксперимента. Данные изменения носили статистически достоверный характер, как по сравнению с исходным значением, так и по отношению к показателю контрольной группы (табл. 4, группа Vinp).
Исходное значение системного артериального давления у крыс группы Vinp составило 114±3 мм рт.ст. К 5 и 10 минуте инфузии отмечена выраженная гипотензивная реакция системного артериального давления, через 5 мин после окончания инфузии (на 15 минуте опыта) показатель оставался сниженным на 11%. Эти изменения носили статистически значимый характер по сравнению с контролем. С 30 по 90 мин эксперимента системное артериальное давление находилось на уровне значений этого показателя в контрольной группе (табл. 4).
Таким образом, внутривенная инфузия винпоцетина в дозе 4 мг/кг вызывает значимое повышение мозгового кровотока и выраженное транзиторное снижение САД во время инфузии и временно сохраняется после ее завершения.
Исходное значение мозгового кровотока у крыс в группе мезо-1 составило 7.7±0.3 мл/мин. Начиная с 5 мин после введения мезо-2,6-диизоборнил-4-метилфенола и до конца наблюдения, отмечен рост мозгового кровотока со стабилизацией на повышенном, по сравнению с исходным, уровне в период наблюдения с 45 до 90 мин опыта. В период с 60 по 90 мин значения мозгового кровотока у крыс группы мезо-1 достоверно превосходили значения этого показателя в контрольной группе (табл. 4, мезо-1).
Исходное значение системного артериального давления у крыс в группе мезо-1 составило 111±3 мм рт.ст. В течение всего периода наблюдения достоверных изменений показателя не выявлено.
Таким образом, подкожное введение масляного раствора мезо-2,6-диизоборнил-4-метилфенола в дозе 100 мг/кг повышает мозговой кровоток, не вызывая снижение системного артериального давления.
Исходное значение мозгового кровотока у крыс в группе рац-2 составило 7.5±0.3 мл/мин. Начиная с 5 мин после введения рац-2,6-диизоборнил-4-метилфенола и до конца наблюдения, отмечен рост мозгового кровотока со стабилизацией на повышенном, по сравнению с исходным, уровне в период с 45 до 90 мин опыта. В период с 60 по 90 мин значения мозгового кровотока у крыс группы рац-2 достоверно превосходили значения этого показателя в контрольной группе (табл. 4, рац-2).
Исходное значение системного артериального давления у крыс в группе рац-2 составило 113±3 мм рт.ст. В течение всего периода наблюдения достоверных изменений показателя не выявлено.
Таблица 4. Влияние внутривенной 10-минутной инфузии винпоцетина (4 мг/кг, Vinp) и подкожного введения масленого раствора мезо-2,6-диизоборнил-4-метилфенола (100 мг/кг, мезо-1) и рац-2,6-диизоборнил-4-метилфенола (100 мг/кг, рац-2) на динамику мозгового кровотока (МК, мл/мин) и системного артериального давления (САД, мм рт.ст.)

Примечание: × – р < 0.05 по сравнению с исходными значениями; * – р < 0.05 по сравнению с группой контроля.
Таким образом, подкожное введение масляного раствора рац-2,6-диизоборнил-4-метилфенола в дозе 100 мг/кг повышает мозговой кровоток, не вызывая снижение системного артериального давления.
Пример 6. У крыс в контрольной группе после курсового внутрижелудочного введения крахмальной слизи значение мозгового кровотока составляло 5.0±0.5 мл/мин.
У крыс в группе, получавших винпоцетин, после курсового внутрижелудочного введения винпоцетина в дозе 45 мг/кг значение мозгового кровотока составляли 7.1±0.5 мл/мин, что достоверно на 42% превосходило показатель контрольной группы. Таким образом, трехкратное внутрижелудочное введение винпоцетина в дозе 45 мг/кг вызывает значимое увеличение мозгового кровотока.
У крыс в группе, получавших мезо-2,6-диизоборнил-4-метилфенол, после курсового внутрижелудочного введения данного препарата в дозе 100 мг/кг значение мозгового кровотока составляли 7.0±0.5 мл/мин, что было на 40% выше, чем показатель контрольной группы. Таким образом, трехкратное внутрижелудочное введение мезо-2,6-диизоборнил-4-метилфенола в дозе 100 мг/кг вызывает значимое увеличение мозгового кровотока; эффект по выраженности не уступает эффекту винпоцетину.
У крыс в группе, получавших рац-2,6-диизоборнил-4-метилфенол, после курсового внутрижелудочного введения данного препарата в дозе 100 мг/кг значение мозгового кровотока составляли 6.8±0.5 мл/мин, что было на 36% выше, чем показатель контрольной группы. Таким образом, трехкратное внутрижелудочное введение рац-2,6-диизоборнил-4-метилфенола в дозе 100 мг/кг вызывает значимое увеличение мозгового кровотока; эффект по выраженности не уступает эффекту винпоцетину.
Изомеры мезо-2,6-диизоборнил-4-метилфенол и рац-2,6-диизоборнил-4-метилфенол могут быть использованы для лечения нарушений мозгового кровообращения у больных с сосудистыми заболеваниями головного мозга.
Эксперименты по оценке нейропротекторных эффектов проводили на 96 беспородных крысах-самках массой 200–230 г с использованием модели тотальной транзиторной ишемии головного мозга. Модель тотальной транзиторной ишемии головного мозга воспроизводили по методу W.A. Pulsineli [Pulsinelli W.A., Brierley J.B. A new model of bilateral hemispheric ischemia in the unanesthetized rat // Stroke. 1979. Vol. 10, № 3. P. 267–272] в нашей модификации. За 1 сутки до моделирования тотальной транзиторной ишемии головного мозга у наркотизированных крыс (этаминал-натрий 60 мг/кг внутрибрюшинно) производили термокоагуляцию обеих вертебральных артерий на уровне первого шейного позвонка. Через 24 ч под эфирным наркозом на обе общие сонные артерии накладывали окклюдеры на 30 мин. Состоятельность модели оценивали по побледнению видимой части сосудистой оболочки глаза, расширению зрачков, развитию гипервентиляции. В случае развития апноэ использовали искусственную вентиляцию легких (аппарат АИД–2). Реперфузию проводили снятием окклюдеров, после чего рану ушивали. Крысы контрольной группы получали внутрижелудочно 1 мл 1%-ой крахмальной слизи, животные опытных групп – мезо-2,6-диизоборнил-4-метилфенол в дозе 100 мг/кг в 1 мл крахмальной слизи один раз в сутки в течение 7 дней (группа мезо-1) и рац-2,6-диизоборнил-4-метилфенол в дозе 100 мг/кг в 1 мл крахмальной слизи один раз в сутки в течение 7 дней (группа рац-2). Первое введение осуществляли через 1 час после создания модели ишемии.
Оценку функционального состояния высшей нервной деятельности на 1-е, 3-и, 5-е и 7-е сутки после создания модели тотальной транзиторной ишемии головного мозга проводили по шкале Stroke-index [McGraw C.P. Experimental cerebral infarction effects of pentobarbital in Mongolian gerbils // Arch. Neurol. 1977. Vol. 34, № 6. P. 334–336] в нашей модификации по следующим показателям: спонтанная двигательная активность (нормальная, повышенная или сниженная, отсутствие), расстройства походки (скованность, шаткость, замедленность движений, нарушение ориентации), рефлексы отдергивания хвоста, обеих передних и задних лап, реакция на звук, тремор, судороги, тонус мышц туловища и конечностей (нормальный, повышенный, отсутствие), признаки птоза (отсутствие, односторонний, двусторонний). Каждый показатель оценивали в баллах: 0 баллов – норма; 1 балл – умеренно выраженные изменения; 2 балла – резко выраженные изменения.
Неврологический дефицит животного оценивали суммой баллов по всем показателям. Кроме того, в каждой группе крыс определяли долю животных с тяжелыми неврологическими расстройствами (6 баллов и более), с нарушениями средней тяжести (3–5 баллов) и с легкими изменениями (до 2 баллов). Выживаемость животных регистрировали на 1-е, 3-и, 5-е и 7-е сутки после тотальной транзиторной ишемии головного мозга.
По завершению экспериментов эвтаназию животных вызывали передозировкой эфирного наркоза.
Статистическую обработку результатов проводили стандартными методами с применением t-критерия Стъюдента и критерия χ2 с помощью пакета программ Statistica for Windows 6.0.
Результаты исследований нейропротекторной активности мезо-2,6-диизоборнил-4-метилфенола и рац-2,6-диизоборнил-4-метилфенола представлены в примере 7, таблицах 5−7.
Пример 7. В контрольной группе в течение первых суток после эпизода тотальной транзиторной ишемии головного мозга погибло 36% животных. К третьим суткам эксперимента в контрольной группе погибло 43% животных (табл. 5).
У животных контрольной группы неврологический дефицит в первые сутки после эпизода тотальной транзиторной ишемии головного мозга составил 7.0±0.8 балла, к третьим суткам – 4.8±0.5 балла, к пятым суткам – 5.2±0.8 балла и к седьмым суткам – 3.5±0.6 балла (табл. 6).
Таблица 5. Влияние курсового (7 суток) внутрижелудочного введения мезо-2,6-диизоборнил-4-метилфенола (100 мг/кг) и рац-2,6-диизоборнил-4-метилфенол (100 мг/кг) на смертность животных (%) после тотальной транзиторной ишемии головного мозга

Примечание: * – р < 0.05 по сравнению с группой контроля.
Таблица 6. Влияние курсового (7 суток) внутрижелудочного введения мезо-2,6-диизоборнил-4-метилфенола (100 мг/кг) и рац-2,6-диизоборнил-4-метилфенол (100 мг/кг) на средний балл неврологического дефицита крыс после тотальной ишемии головного мозга

Примечание: × − р < 0.05 по сравнению с группой контроля.
В первые сутки количество животных с тяжелой степенью неврологического дефицита (более 6 баллов) составило 70%, со средней степенью (3–5 баллов) – 20%, с легкой степенью (менее 2 баллов) – 10%. К третьим суткам количество животных с тяжелой степенью неврологического дефицита снизилось до 43.3%, а со средней и легкой степенью повысилась соответственно до 36.7 и 20.0%. К пятым суткам эксперимента в контрольной группе количество животных с тяжелой степенью неврологического дефицита составило 40.0%, средней – 33.3%, а с легкой степенью возросло до 26.7%. К седьмым суткам наблюдения количество животных с тяжелой степенью неврологического дефицита продолжало снижаться и составило 20.0%, со средней степенью не изменилось, а с легкой степенью увеличилось до 46.7% (табл. 7).
Таблица 7. Влияние курсового введения 4-метил-2,6-диизоборнилфенола на выраженность неврологического дефицита у крыс после тотальной ишемии головного мозга (% от общего числа животных в группе)
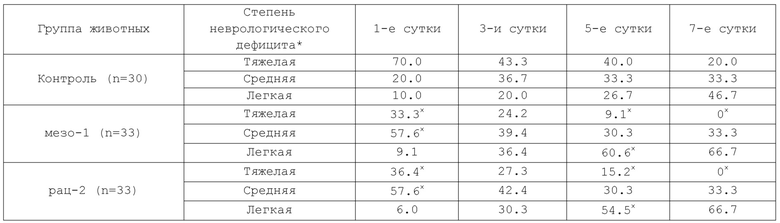
Примечание: * − тяжелая степень неврологического дефицита (более 6 баллов), средняя степень (3–5 баллов), легкая степень (менее 2 баллов); × − р < 0.05 по сравнению с группой контроля.
В первые сутки после эпизода тотальной транзиторной ишемии головного мозга в группе крыс, получавших мезо-2,6-диизоборнил-4-метилфенол (мезо-1), погибло 9% животных, что было в 4 раза ниже контрольного показателя. К третьим суткам эксперимента в опытной группе погибло 15% животных, что было достоверно ниже контроля (р<0.05) (табл. 5).
У животных опытной группы неврологический дефицит в первые сутки после эпизода тотальной транзиторной ишемии головного мозга составил 5.9±0.6 балла, к третьим суткам – 4.0±0.5 балла, к пятым – 2.6±0.5 балла, к седьмым суткам – 1.9±0.5 балла (табл. 6). Достоверность между контрольной и опытной группами выявились к 5-м и 7-м суткам.
К первым суткам количество опытных животных с тяжелой степенью неврологического дефицита (более 6 баллов) составило 33.3%, со средней степенью (3–5 баллов) – 57.6%, с легкой степенью (менее 2 баллов) – 9.1% (табл. 7). К третьим суткам в опытной группе количество животных с тяжелой степенью неврологического дефицита снизилось до 24.2%, средней – 39.4% и значительно возросло число крыс с легкой степенью (36.4%). К пятым суткам эксперимента прогрессивно снижалось количество крыс с тяжелой и средней степенью неврологического дефицита до 9.1 и 30.3% соответственно, а с легкой степенью увеличилось до 60.6%. К седьмым суткам наблюдения в опытной группе тяжелого неврологического дефицита не выявлено не у одного животного, со средней степенью возросло незначительно до 33.3%, а количество крыс с легкой степенью составило 66.7%. По показателю степени неврологического дефицита основные различия между контрольной и опытной группами наблюдались на 1-е, 5-е и 7-е сутки после эпизода тотальной транзиторной ишемии головного мозга.
Таким образом, внутрижелудочное введение мезо-2,6-диизоборнил-4-метилфенола в дозе 100 мг/кг в течение 7 суток крысам, перенесшим тотальную транзиторную ишемию головного мозга, приводит к повышению выживаемости животных, уменьшению среднего балла неврологического дефицита, возрастанию числа животных со средней и легкой степенью неврологического дефицита и снижению числа животных с тяжелой степенью неврологического дефицита.
В первые сутки после эпизода тотальной транзиторной ишемии головного мозга в группе крыс, получавших рац-2,6-диизоборнил-4-метилфенол (рац-2), погибло 11% животных, что было в 3 раза ниже контрольного показателя. К третьим суткам эксперимента в опытной группе погибло 21% животных, что было достоверно ниже контроля (р<0.05) (табл. 5).
У животных опытной группы неврологический дефицит в первые сутки после эпизода тотальной транзиторной ишемии головного мозга составил 6.0±0.8 балла, к третьим суткам – 4.1±0.4 балла, к пятым – 2.7±0.4 балла, к седьмым суткам – 2.0±0.3 балла (табл. 6). Достоверность между контрольной и опытной группами выявились к 5-м и 7-м суткам.
К первым суткам количество опытных животных с тяжелой степенью неврологического дефицита (более 6 баллов) составило 36.4%, со средней степенью (3–5 баллов) – 57.6%, с легкой степенью (менее 2 баллов) – 6.0% (табл. 7). К третьим суткам в опытной группе количество животных с тяжелой степенью неврологического дефицита снизилось до 27.3%, средней – 42.4% и значительно возросло число крыс с легкой степенью (30.3%). К пятым суткам эксперимента прогрессивно снижалось количество крыс с тяжелой и средней степенью неврологического дефицита до 15.2 и 30.3% соответственно, а с легкой степенью увеличилось до 54.5%. К седьмым суткам наблюдения в опытной группе тяжелого неврологического дефицита не выявлено не у одного животного, со средней степенью возросло незначительно до 33.3%, а количество крыс с легкой степенью составило 66.7%. По показателю степени неврологического дефицита основные различия между контрольной и опытной группами наблюдались на 1-е, 5-е и 7-е сутки после эпизода тотальной транзиторной ишемии головного мозга.
Таким образом, внутрижелудочное введение рац-2,6-диизоборнил-4-метилфенола в дозе 100 мг/кг в течение 7 суток крысам, перенесшим тотальную транзиторную ишемию головного мозга, приводит к повышению выживаемости животных, уменьшению среднего балла неврологического дефицита, возрастанию числа животных со средней и легкой степенью неврологического дефицита и снижению числа животных с тяжелой степенью неврологического дефицита.
Изомеры мезо-2,6-диизоборнил-4-метилфенол и рац-2,6-диизоборнил-4-метилфенол могут быть использованы для лечения последствий цереброваскулярных болезней.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, ослабляющее постинфарктное ремоделирование миокарда | 2020 |
|
RU2740895C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2555335C9 |
| Средство, увеличивающее мозговой кровоток | 2016 |
|
RU2655810C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НЕЙРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2018 |
|
RU2701739C1 |
| СРЕДСТВО, УЛУЧШАЮЩЕЕ РЕОЛОГИЧЕСКИЕ СВОЙСТВА КРОВИ | 2013 |
|
RU2546297C1 |
| СРЕДСТВО, УВЕЛИЧИВАЮЩЕЕ МОЗГОВОЙ КРОВОТОК | 2007 |
|
RU2351321C1 |
| НЕЙРОПРОТЕКТОРНОЕ СРЕДСТВО | 2009 |
|
RU2406488C1 |
| СРЕДСТВА, ОБЛАДАЮЩИЕ ГЕМОРЕОЛОГИЧЕСКОЙ, АНТИАГРЕГАНТНОЙ И АНТИТРОМБОГЕННОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2347561C2 |
| 2,6-ДИИЗОБОРНИЛФЕНОЛЫ | 2011 |
|
RU2502719C2 |
| ПРОТИВОИШЕМИЧЕСКОЕ СРЕДСТВО | 2012 |
|
RU2499593C1 |
Изобретение относится к фармакологии и касается применения мезо- и рацемической формы 2,6-ди(1,7,7-триметилбицикло[2.2.1]гептан-экзо-2-ил)-4-метилфенола в качестве средств для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней. Мезо-форма представляет собой 2-{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-6-{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол, рацемическая форма - 2,6-ди{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол и 2,6-ди{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол. Технический результат состоит в расширении арсенала средств для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней, а также в усилении фармакологической активности за счет стереоспецифичности действия изомеров и за счет наличия у них комплекса фармакологических свойств (антирадикальной, гемореологической, антитромбоцитарной, антитромбогенной и нейропротекторной активности, увеличения мозгового кровотока), что также обеспечивает повышение эффективности лечения указанных заболеваний. 2 н.п. ф-лы, 7 табл., 7 пр.
1. Применение мезо-формы 2,6-ди(1,7,7-триметилбицикло[2.2.1]гептан-экзо-2-ил)-4-метилфенола − 2-{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-6-{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенола в качестве средства для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней.
2. Применение рацемической формы 2,6-ди(1,7,7-триметилбицикло[2.2.1]гептан-экзо-2-ил)-4-метилфенола – 2,6-ди{(1S,2R,4R)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол и 2,6-ди{(1R,2S,4S)-1,7,7-триметилбицикло[2.2.1]гептан-2-ил}-4-метилфенол в качестве средства для лечения сердечно-сосудистых заболеваний, коррекции нарушений мозгового кровообращения, лечения последствий цереброваскулярных болезней.
| 2,6-ДИИЗОБОРНИЛФЕНОЛЫ | 2011 |
|
RU2502719C2 |
| СУКРУШЕВА О.В | |||
| Функциональные производные терпенофенолов | |||
| Автореферат диссертации на соискание учёной степени кандидата химических наук | |||
| Сыктывкар, 2016, 23 с. | |||
| ЧУКИЧЕВА И.Ю | |||
| Закономерности алкилирования фенолов монотерпеноидами и направленный синтез терпенофенолов | |||
| Автореферат диссертации на соискание учёной степени | |||
Авторы
Даты
2021-10-22—Публикация
2019-10-30—Подача