Область техники, к которой относится изобретение
В целом, настоящее изобретение относится к применениям глицирретиновой кислоты, глицирризиновой кислоты и родственных им соединений для предотвращения и/или лечения фиброза легких и заболеваний легких, связанных с фиброзом легких.
Уровень техники
Легочный фиброз (ЛФ) представляет собой бессимптомно развивающееся состояние, которое характеризуется постепенным замещением нормальных клеток паренхимы на фиброзные (волокнистые), соединительные, матриксные макромолекулы (например, коллагены, фибронектины и протеогдиканы) на поверхности и внутри легких, как правило, в местах травмы или инфекции. Избыточное образование фиброзной ткани в результате активации и пролиферации фибробластов разрушает нормальную структуру легких и их функцию. Например, накопление фиброзной ткани приводит к утолщению альвеолярных перегородок, уменьшает объем воздушного пространства и вызывает повреждения эпителия или даже альвеолярный коллапс. В результате, пациенты, страдающие от легочного фиброза испытывают различную степень одышки при физических нагрузках, а на поздних стадиях - ортопноэ, цианоз и респираторную недостаточность1. Медиана выживаемости при фиброзе легких составляет около 2-3 лет, и приблизительно 65% больных умирают в течение 5 лет после постановки диагноза.
Лучевая (irradiation или IR) терапия, являющаяся наиболее распространенным методом лечения опухоли или рака, может вызвать повреждение легких и в конечном итоге привести к IR-индуцированной пневмопатии, включая легочный фиброз1. Риск IR-индуцированной пневмопатии дополнительно увеличивается при одновременном введении цитотоксических химиотерапевтических агентов. ИК-индуцированная пневмопатия не только оказывает разрушительное воздействие на качество жизни пациента, но иногда может быть даже более опасной для жизни, чем первичные опухоль или рак1. Таким образом, риск IR-индуцированной пневмопатии, такой как фиброз легких, стал основным фактором, ограничивающим дозу излучения, и иногда он даже не позволяет использовать лучевую терапию.
В настоящее время нет ни одного способа лечения легочного фиброза. В то время как противовоспалительные средства или средства, защищающие легкие, могут в некоторой степени облегчить симптомы легочного фиброза или улучшить жизнь пациента, они не могут остановить прогрессирование заболевания. Обычные лекарственные препараты для легочного фиброза включают амифостин, целебрекс и дексаметазон. Хотя амифостин и дает определенный цитопротекторный эффект от IR-индуцированного повреждения легких2, его необходимо вводить пациентам за 30 минут до повреждения легких, и, таким образом, он не может предотвратить или вылечить случайное повреждение легких. Сведения об эффективности целебрекса, широко используемого противовоспалительного средства, для лечения пневмонита или легочного фиброза отсутствуют.Дексаметазон является стероидным противовоспалительным препаратом и может вызывать серьезные побочные эффекты при длительном использовании. Кроме того, авторы настоящего изобретения обнаружили, что дексаметазон может привести к ухудшению легочного фиброза, приводя к легочной недостаточности или даже более ранней смерти по сравнению с контрольными группами, не получавшими лечения. Таким образом, остро необходимы терапевтические агенты с улучшенной эффективностью и безопасностью.
Традиционная китайская медицина практикуется китайским народом в течение 2-3 тысячелетий. Она касается различных патологий, а также диагностики, лечения и профилактики заболеваний. Китайские лекарственные вещества записаны в различных фармакопеях. Одной из классических ссылок для лекарственных трав является работа Ben Cao Gang Mu, написанная Li Shizhen в конце 14-го века. Эта книга описывает около 2500 трав и других продуктов, включая животных и минералы.
Лакричник обыкновенный (Glycyrrhiza glabra) имеет давнюю и разнообразную историю лекарственного применения в странах Восточной Азии. Его корень используется в качестве терапевтического средства для лечения дерматитов и язвенной болезни (пептической язвы). Глицирризиновая кислота (также известная как Глицирризин) (GLA) является природным соединением, которое может быть выделено из корня видов Glycyrrhiza, в том числе из лакричника обыкновенного (Glycyrrhiza glabra). GLA широко используется в качестве ароматизатора в Соединенных Штатах Америки и Европе, и была одобрена Государственным управлением по контролю за качеством медикаментов и продуктов питания Китая для лечения хронического гепатита и цирроза печени. Глицирретиновая кислота (GA), пентациклическое тритерпеноидное производное, составляющее функциональный фрагмент глицирризиновой кислоты (GLA), использовалась для лечения воспалений, язвенной болезни и инфекции. Однако ранее не отмечалось, что GA, GLA и родственные им соединения играют какую-либо роль в лечении легочного фиброза.
Краткое раскрытие изобретения
Настоящее изобретение относится к новым применениям глицирретиновой кислоты (GA), глицирризиновой кислоты (GLA) и родственных им соединений для предотвращения и/или лечения легочного фиброза и заболеваний легких, связанных с легочным фиброзом. Способ по изобретению включает введение пациенту, нуждающемуся в таком лечении, эффективного количества одного или нескольких соединений и композиций по настоящему изобретению. Также описываются терапевтические применения пролекарств, метаболитов, производных (например, кислот, сложных эфиров, простых эфиров и амидов), а также солей глицирретиновой (GA) и глицирризиновой (GLA) кислот.
В одном варианте осуществления изобретения соединения и фармацевтические композиции по настоящему изобретению могут быть использованы для лечения или ослабления легочного фиброза, включая, но, не ограничиваясь, индуцированный излучением легочный фиброз и идиопатический легочный фиброз.
Настоящее изобретение также относится к терапевтическим или фармацевтическим композициям, содержащим соединения по настоящему изобретению в форме, которая может быть объединена с фармацевтически приемлемым носителем. В предпочтительных вариантах осуществления изобретения композиции готовят в форме, приспособленной для доставки в легкие. Настоящее изобретение также относится к пищевым добавкам и диетическим продуктам или составам напитков, содержащим соединения по изобретению.
Краткое описание фигур
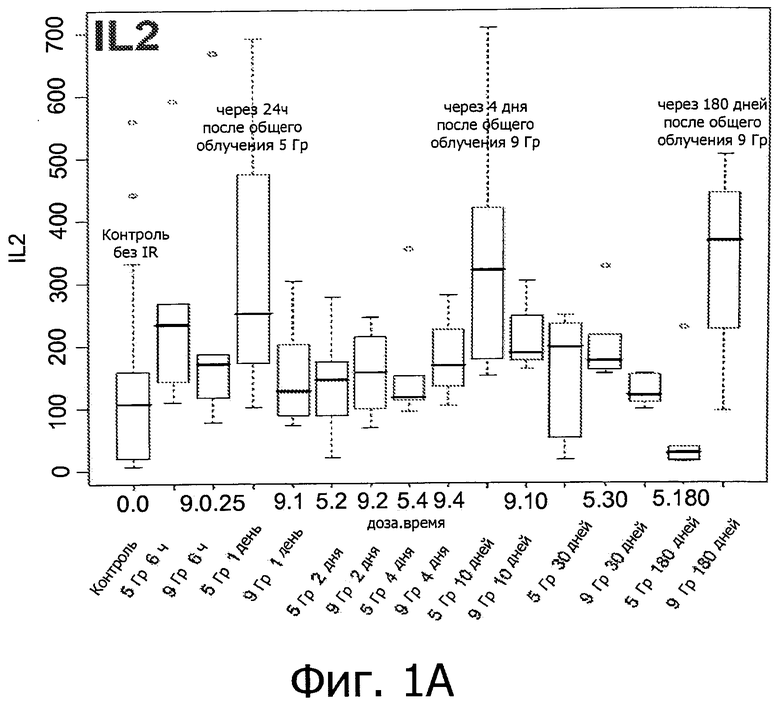
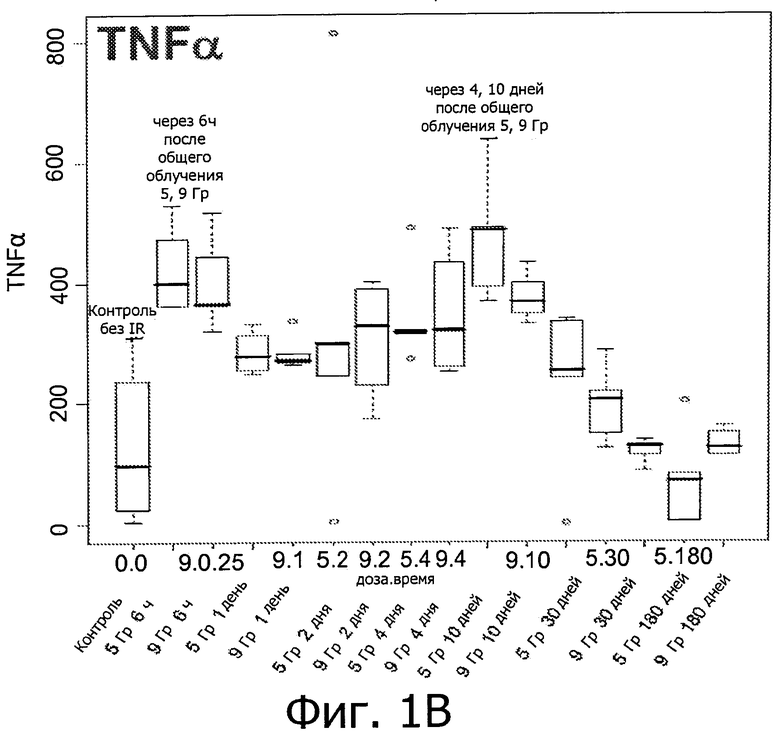
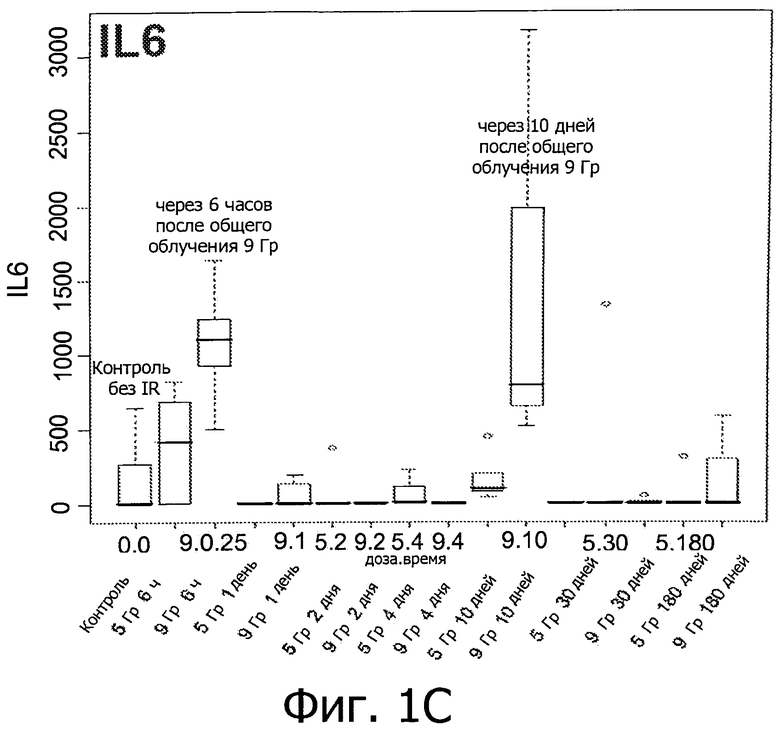
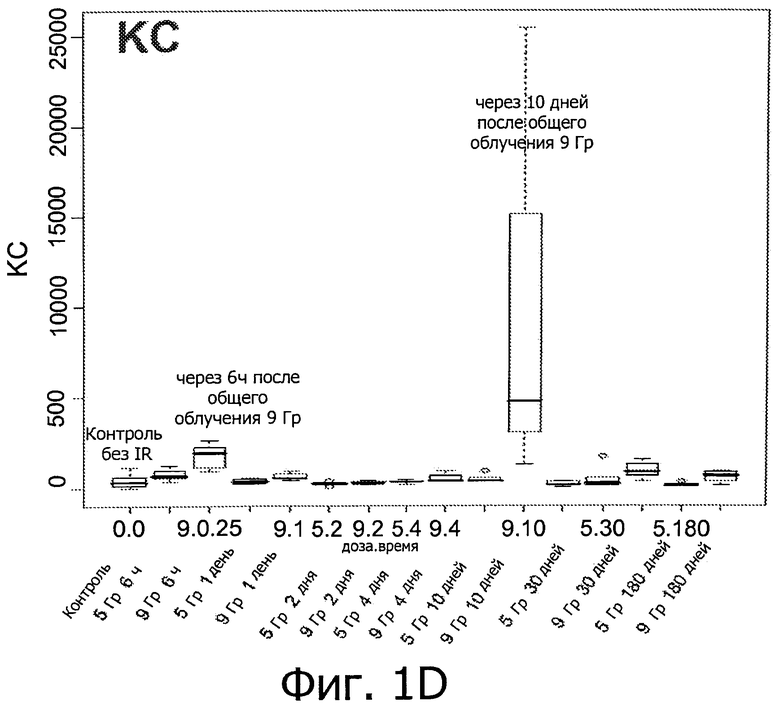
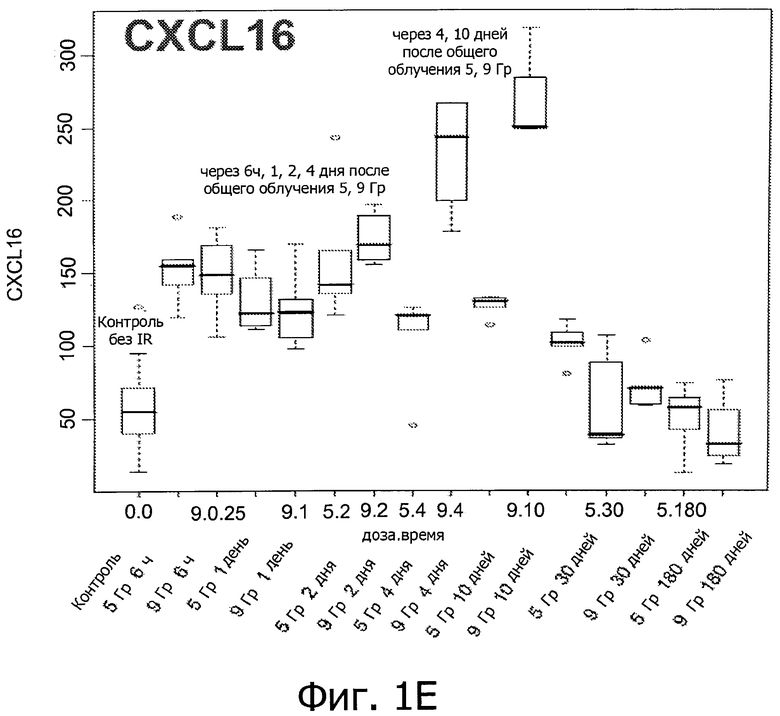
Фиг.1 иллюстрирует возникновение воспалительных реакций в результате облучения. (А)-(Е) отображают изменение уровней воспалительных медиаторов (IM) у мышей, подверженных IR (облучению) при дозе 0, 5 или 9 Гр.
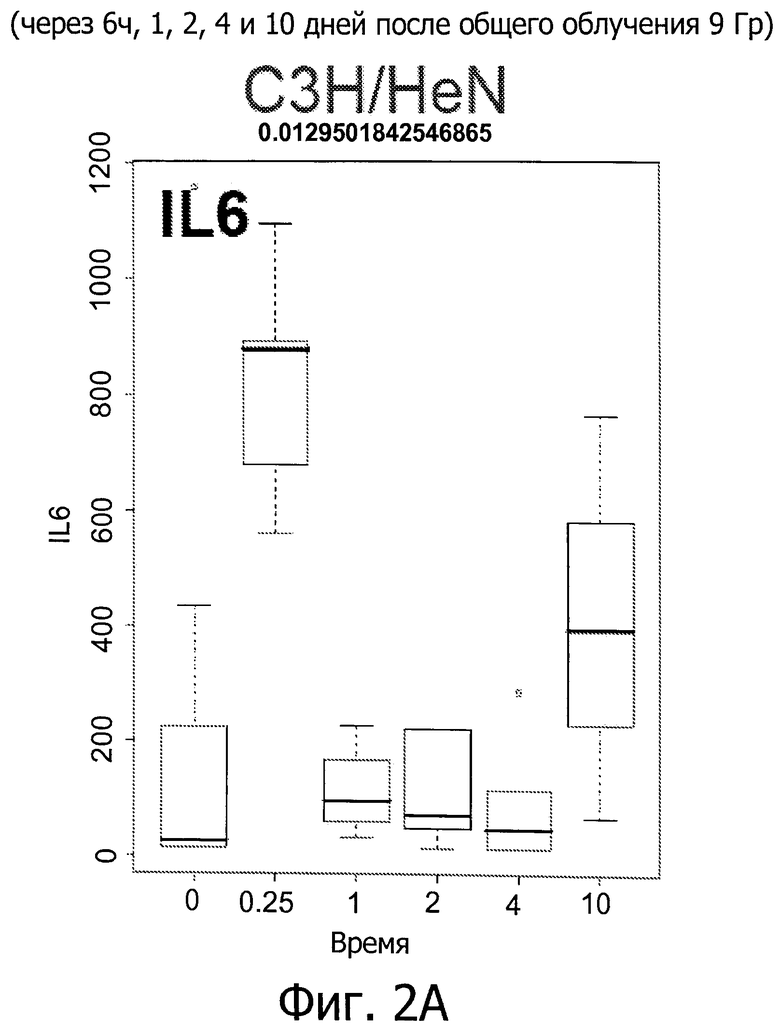
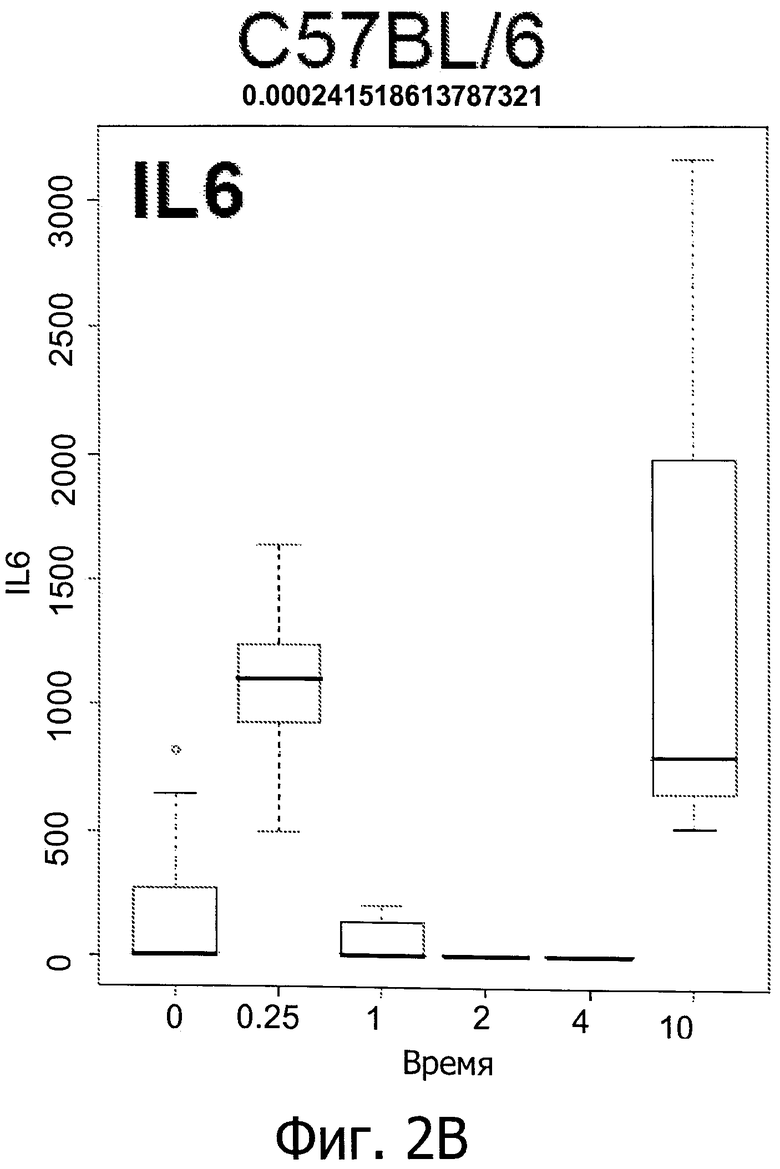
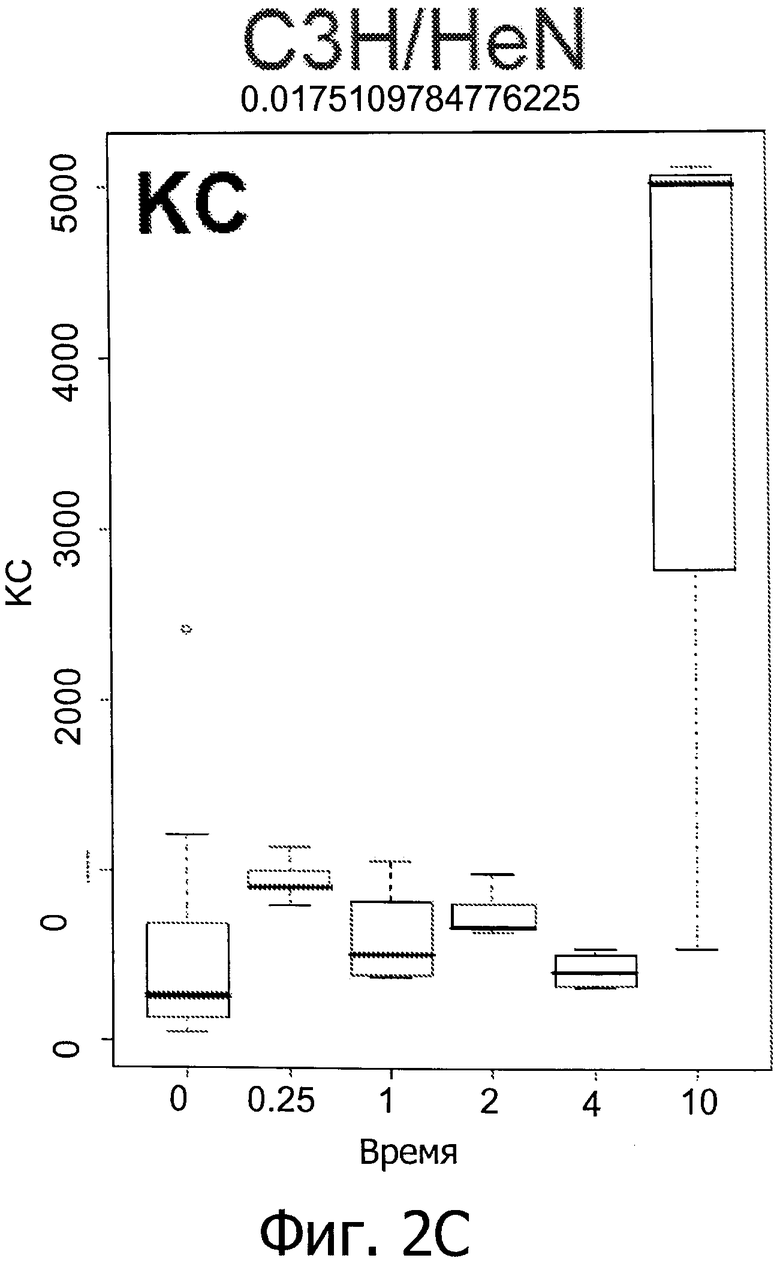
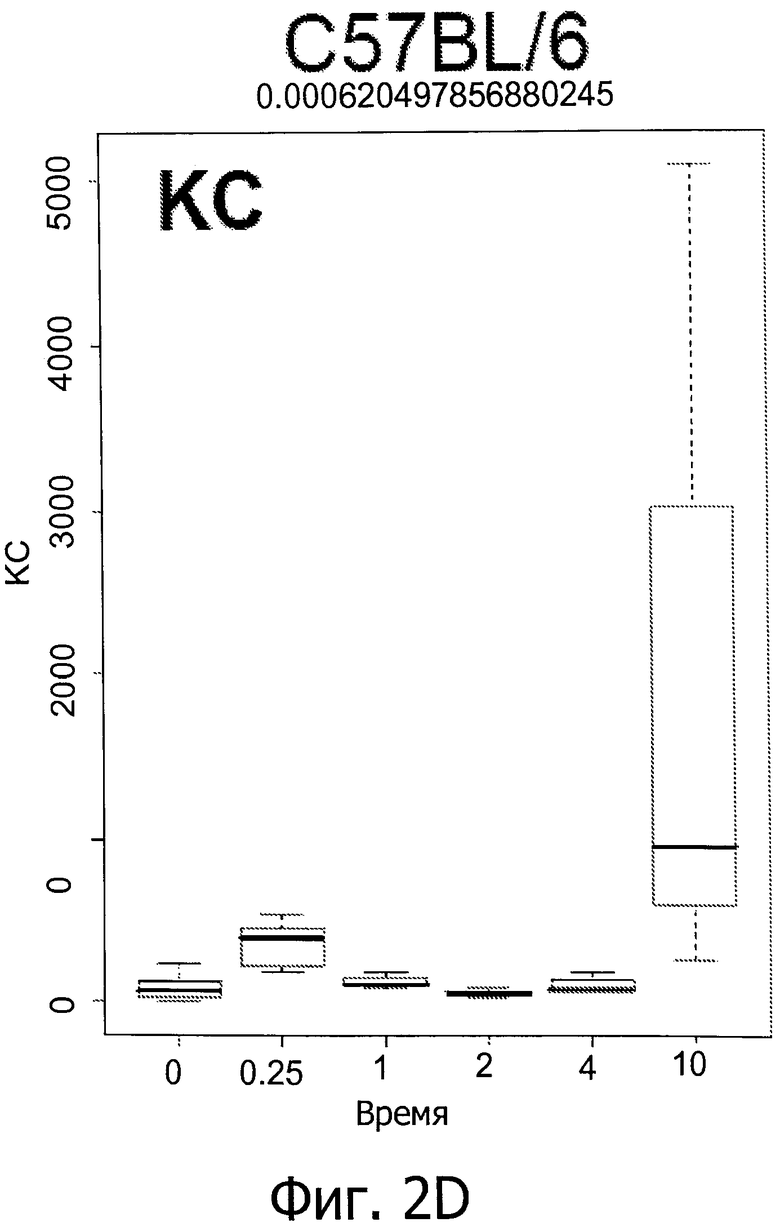
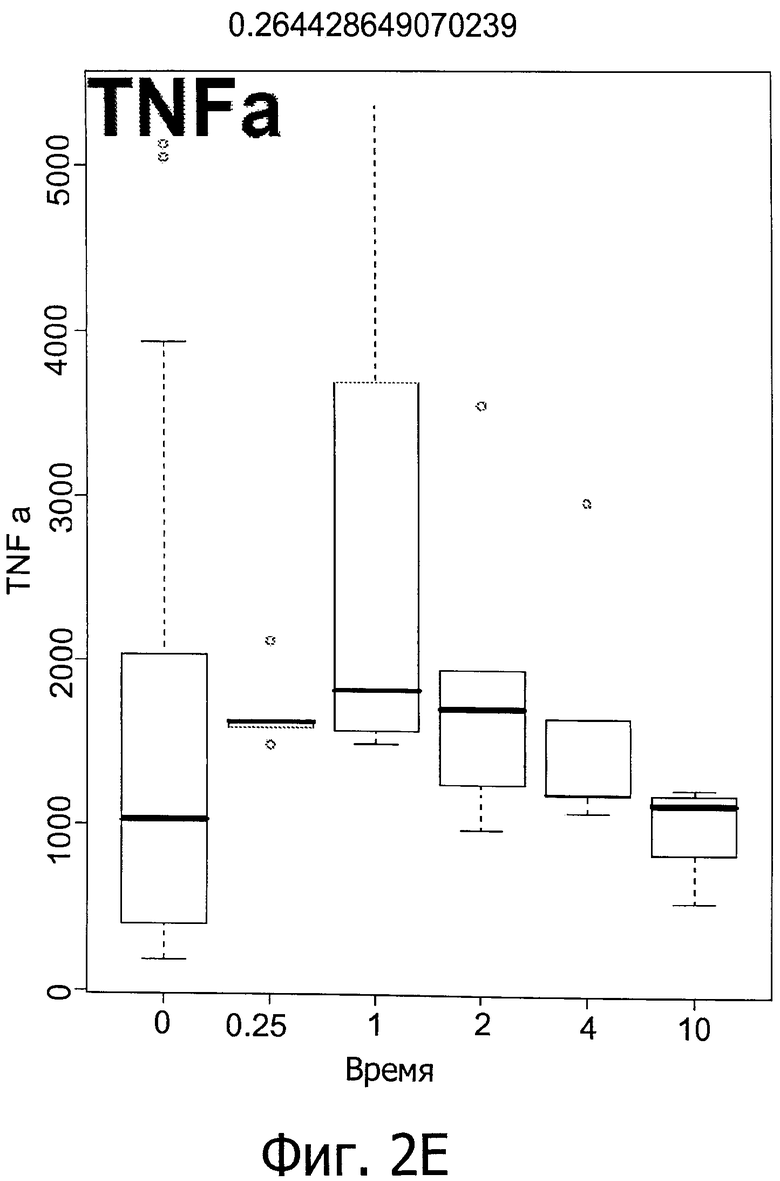
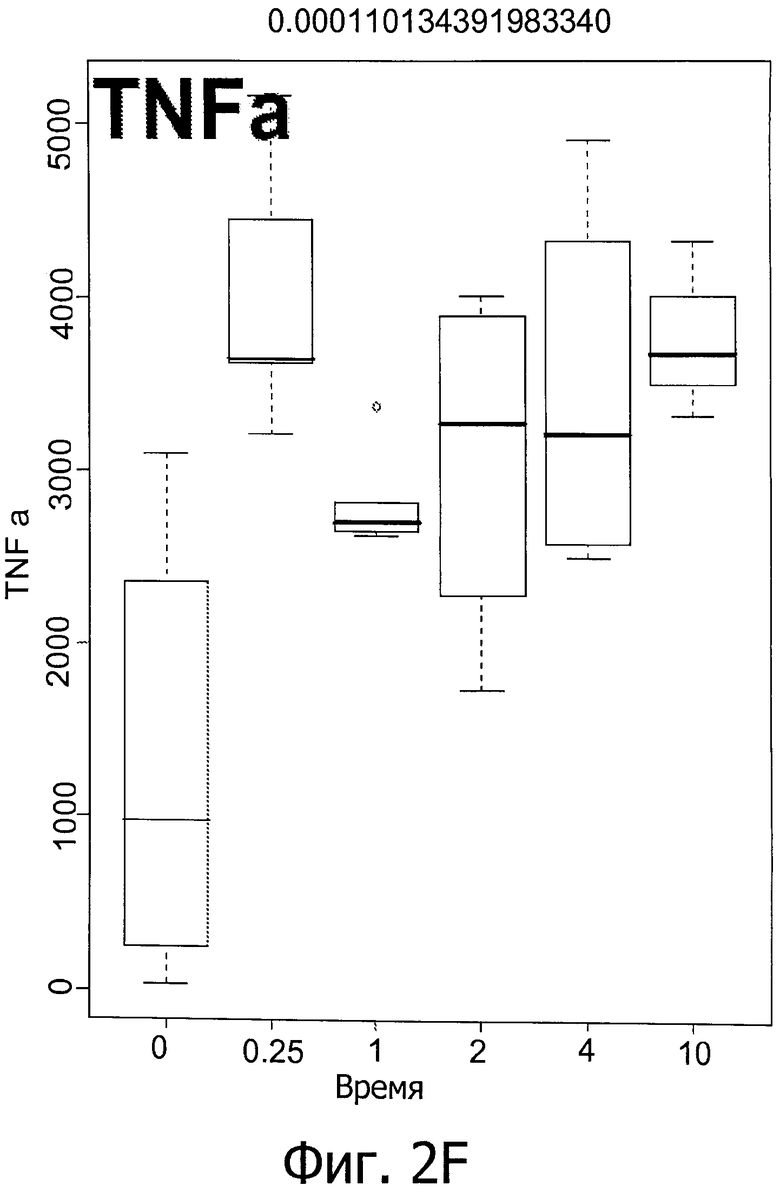
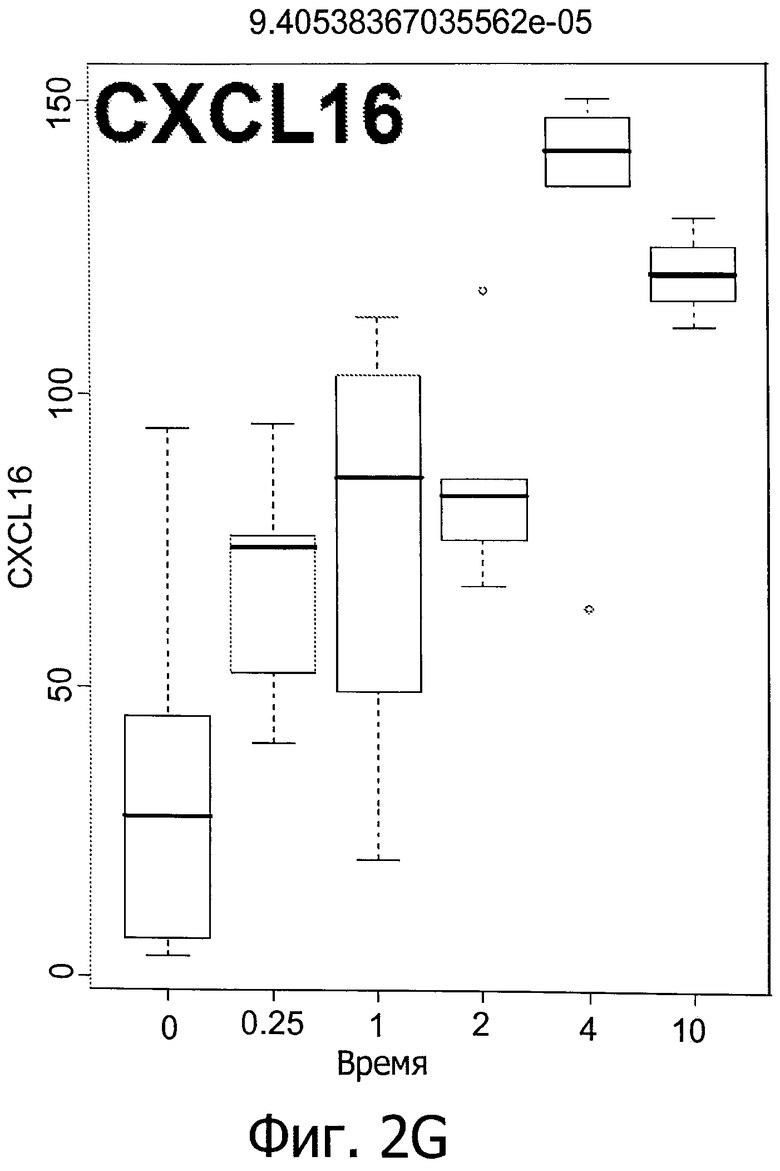
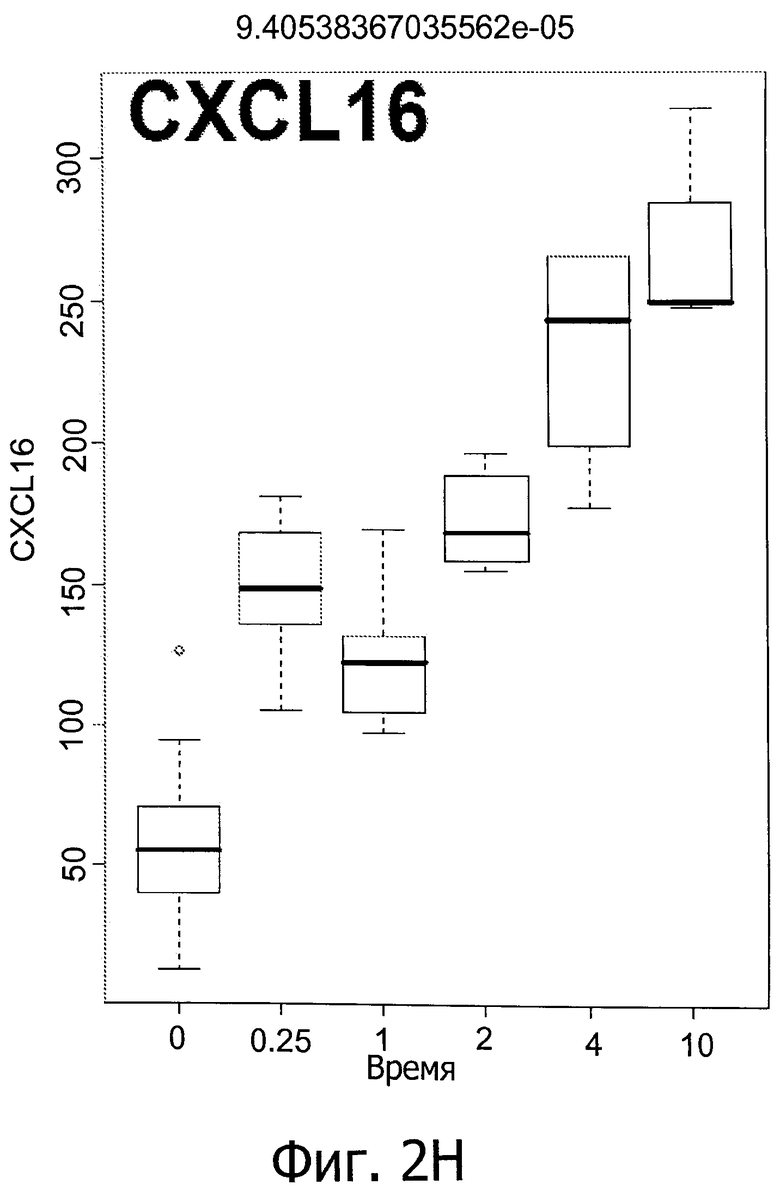
Фиг.2 показывает колебание в уровнях IM у мышей линии C57BL/6 и C3H/NeH с повреждением головного мозга, вызванным IR (облучением) (6 часов и 1, 2, 4 и 10 дней после облучения при дозе 9 Гр).
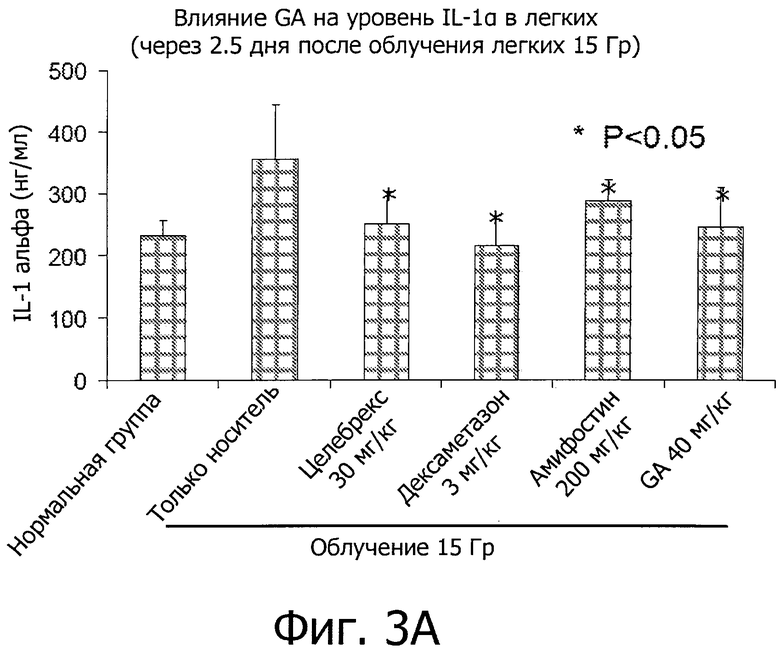
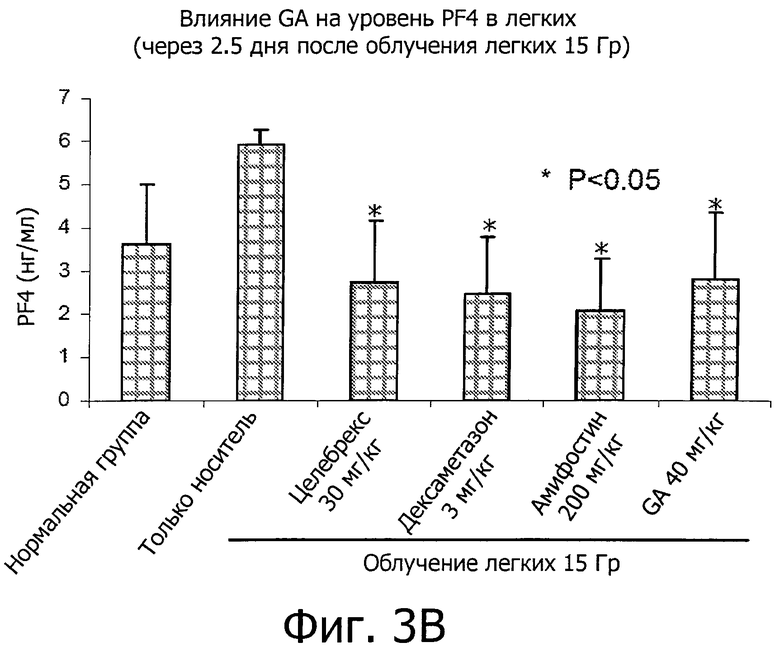
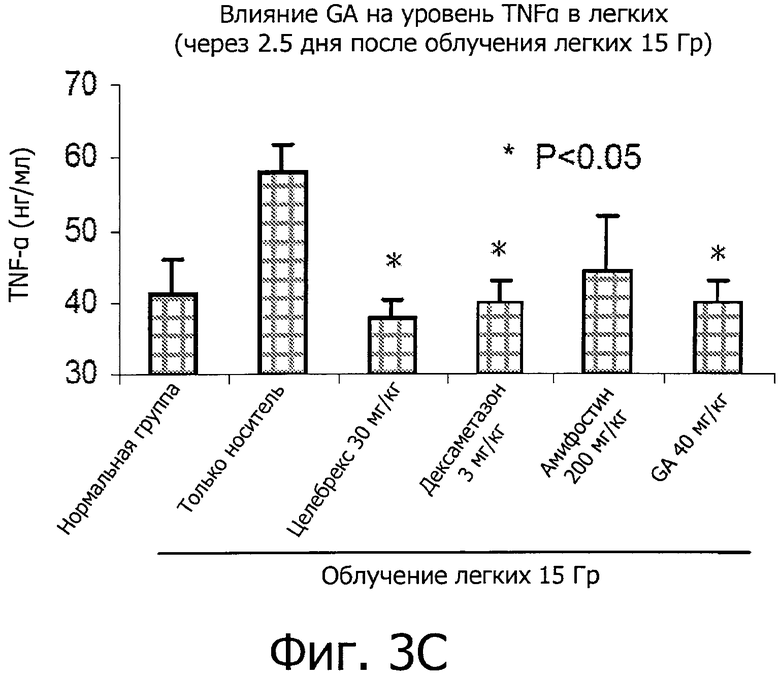
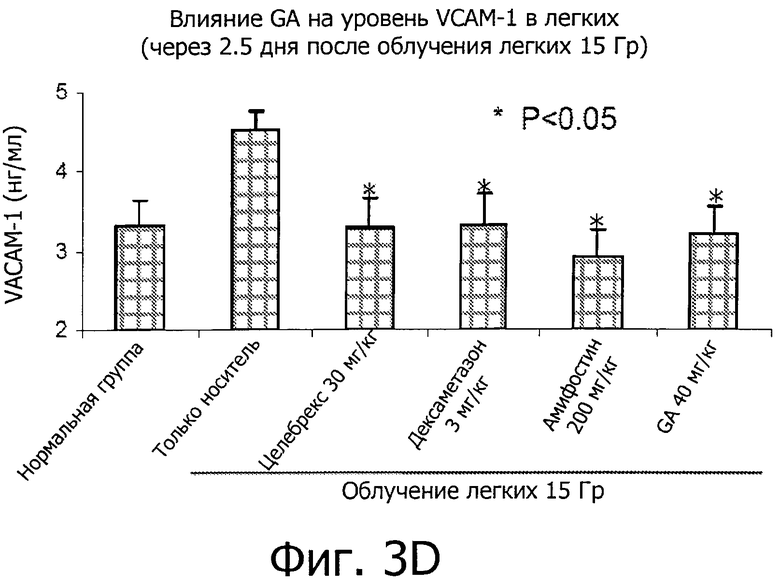
Фиг.3 иллюстрирует ингибирующие эффекты глицирретиновой кислоты (GA) на вызванное облучением (IR) воспаление во время острой фазы IR-вызванного пневмонита.
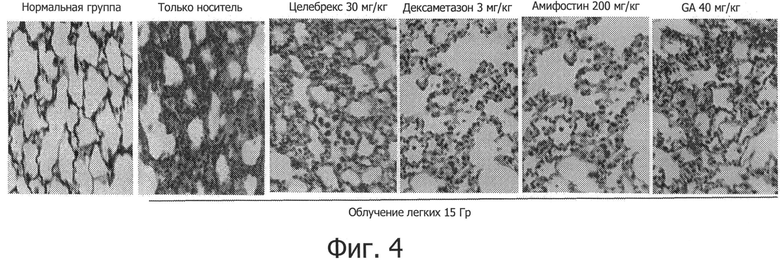
Фиг.4 показывает, что GA понижает воспалительную клеточную инфильтрацию и экссудацию плазмы в интерстициальном пространстве во время острой фазы IR-вызванного пневмонита (2,5 дня после подтверждения торакальному облучению при дозе 15 Гй).
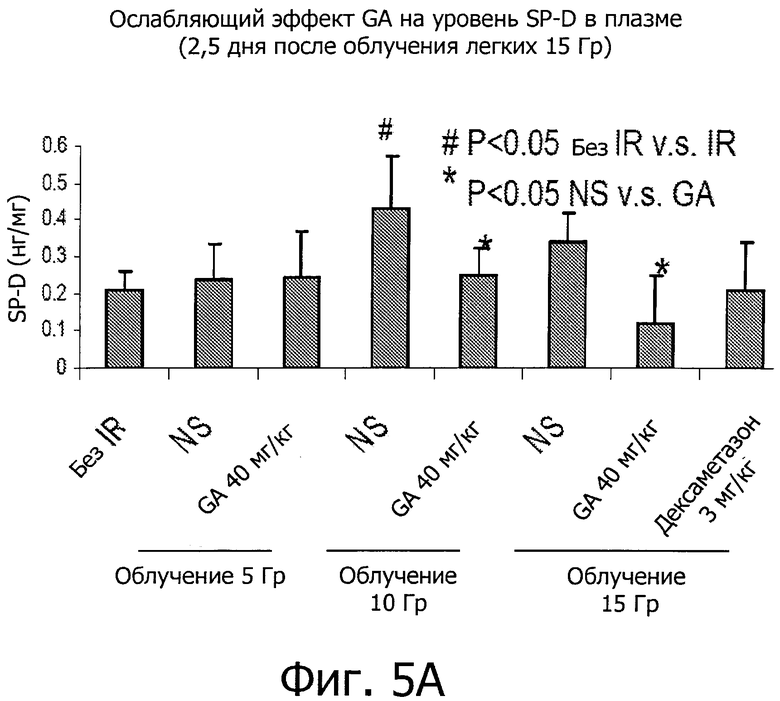
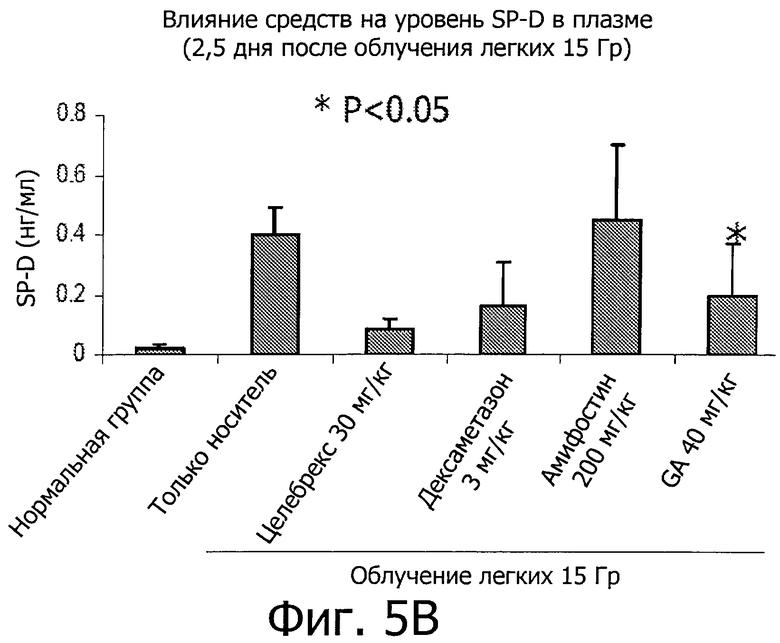
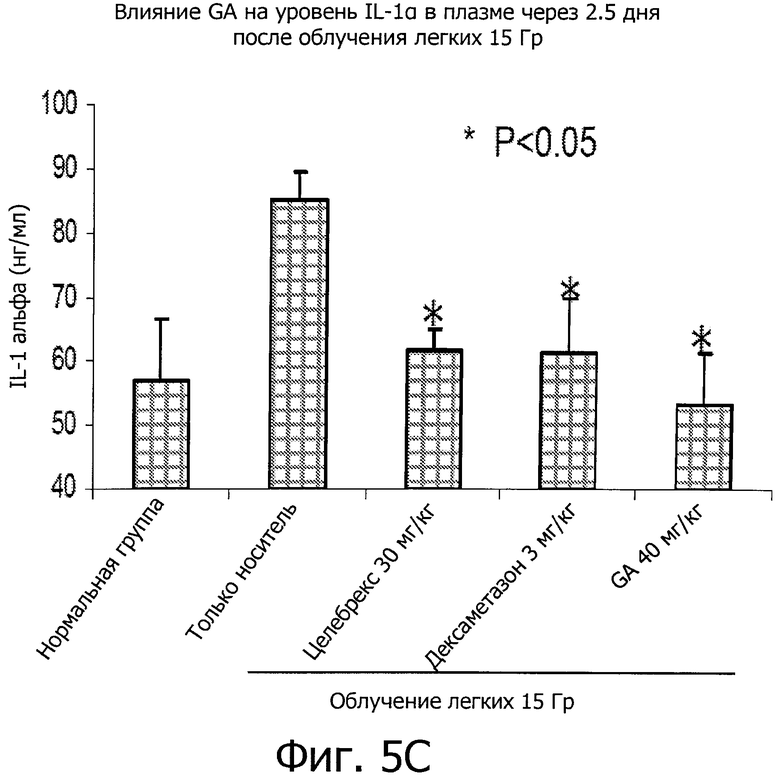
Фиг.5 показывает, что GA понижает уровни SP-D и ILα в плазме во время острой фазы IR-вызванного пневмонита.
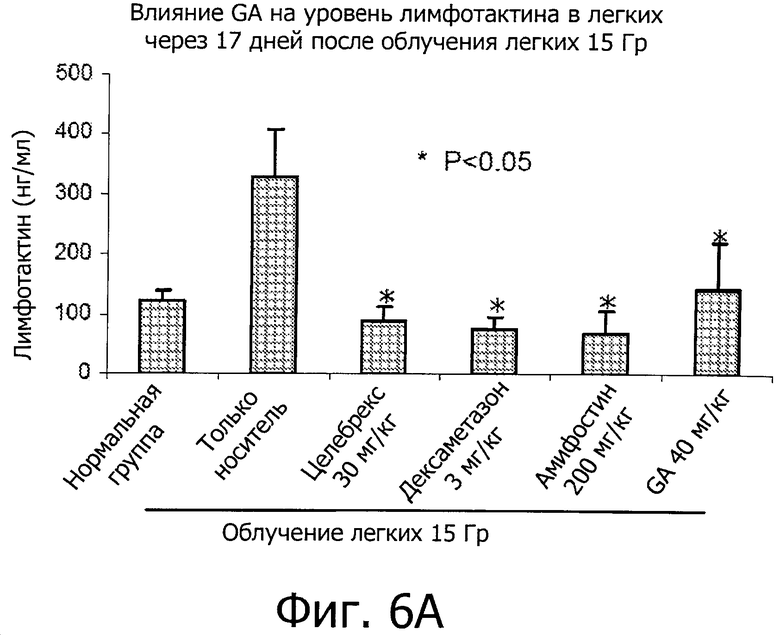
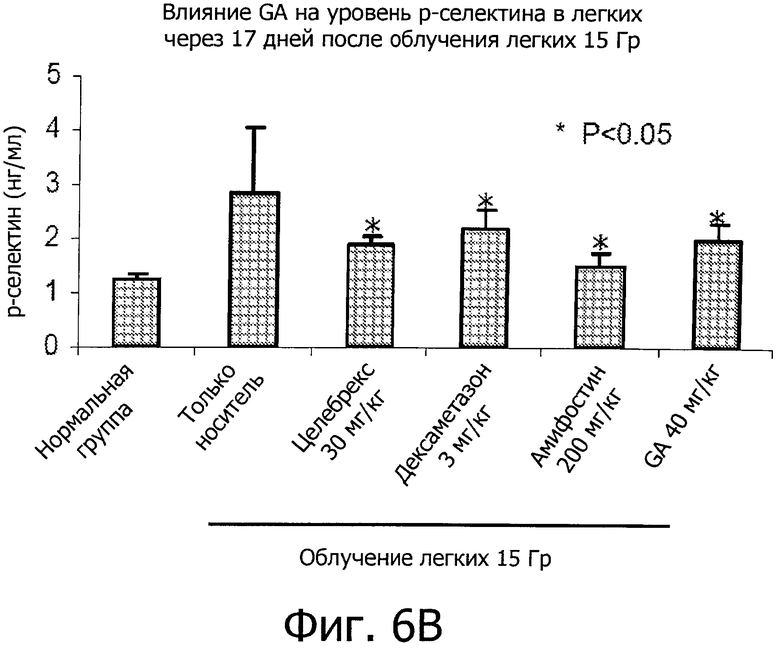
Фиг.6 показывает, что GA понижает уровни воспалительных медиаторов во время подострой фазы IR-вызванного пневмонита (17 дней после IR).
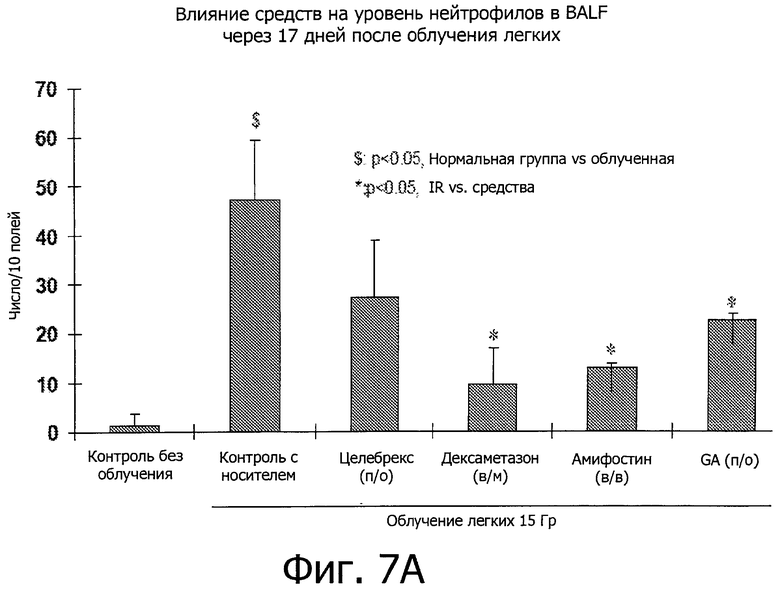
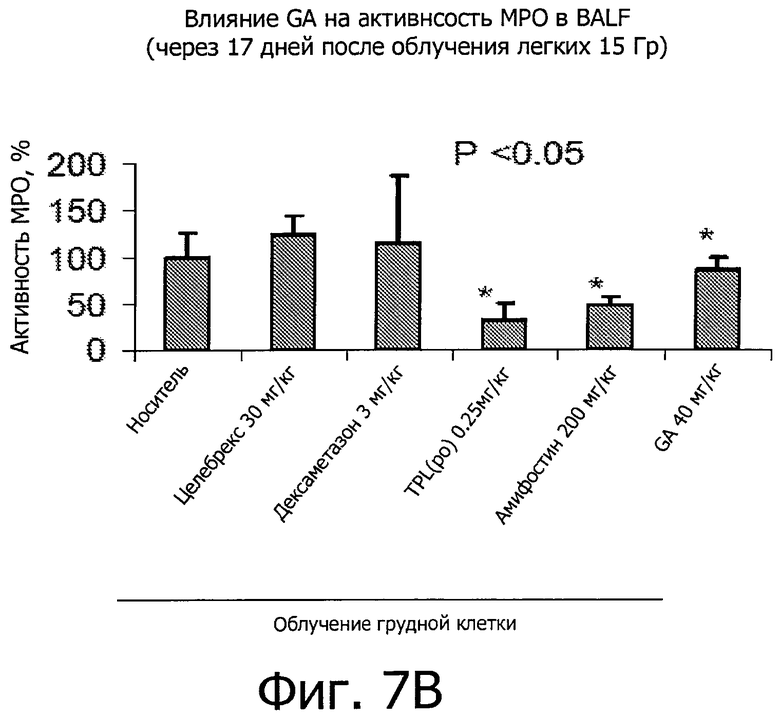
Фиг.7 показывает, что GA понижает число нейтрофилов и активность миелопероксидазы (МРО) в жидкости бронхоальвеолярного лаважа (BALF) во время подострой фазы IR-вызванного пневмонита (17 дней после IR при дозе 15 Гр).
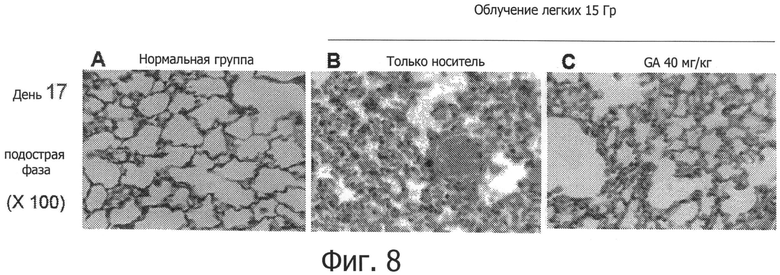
Фиг.8 показывает, что GA ослабляет подострую фазу IR-вызванного пневмонита (17 дней после подтверждения IR при дозе 15 Гр).
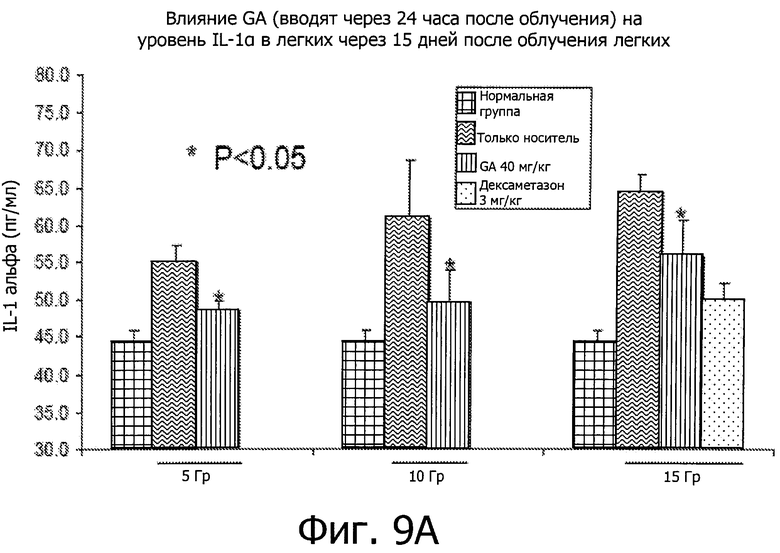
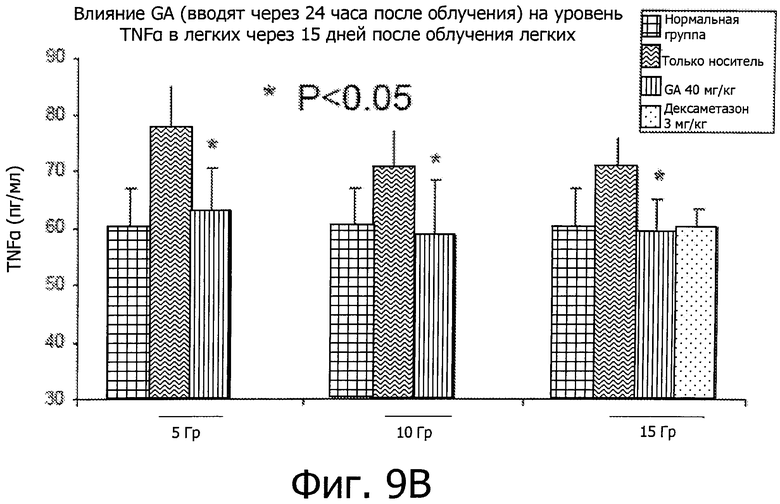
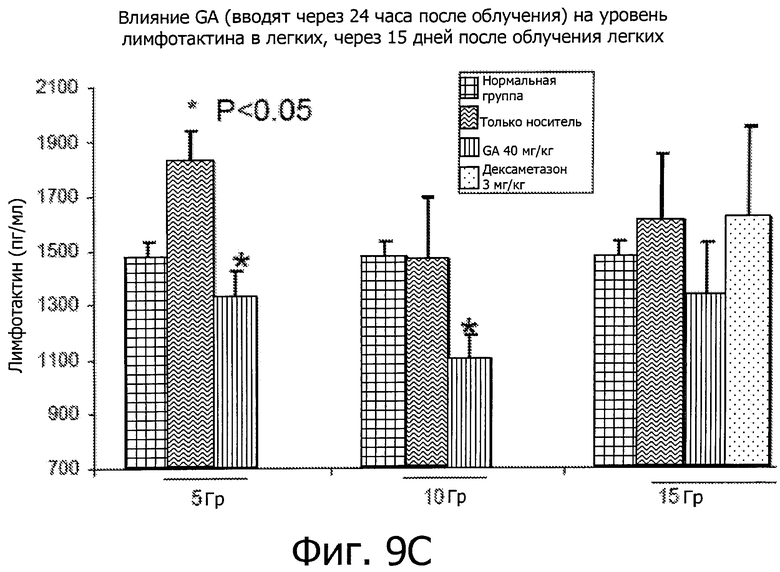
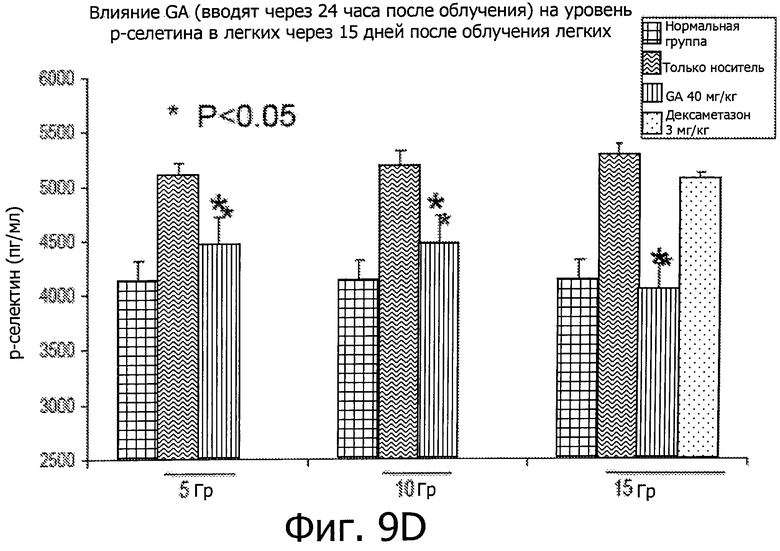
Фиг.9 показывает, что GA ингибирует воспалительные реакции во время подострой фазы IR-вызванного пневмонита. GA вводили мышам через 24 часа после IR при дозе 15 Гр.
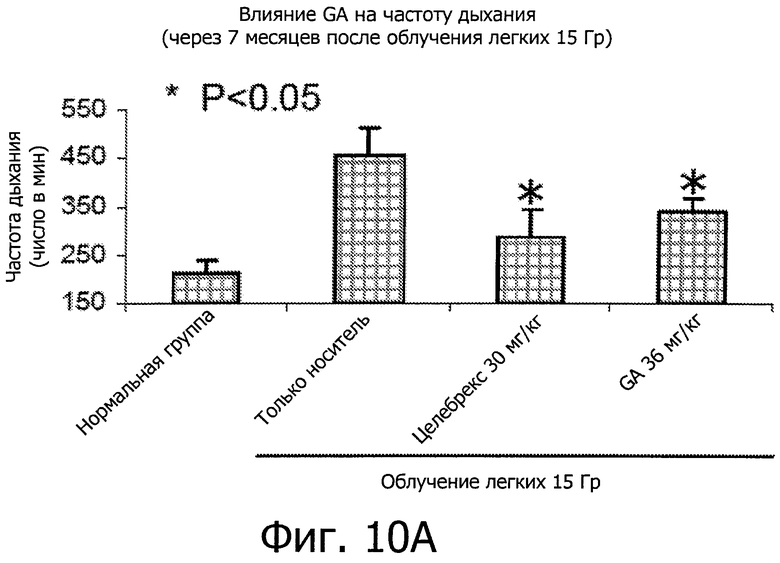
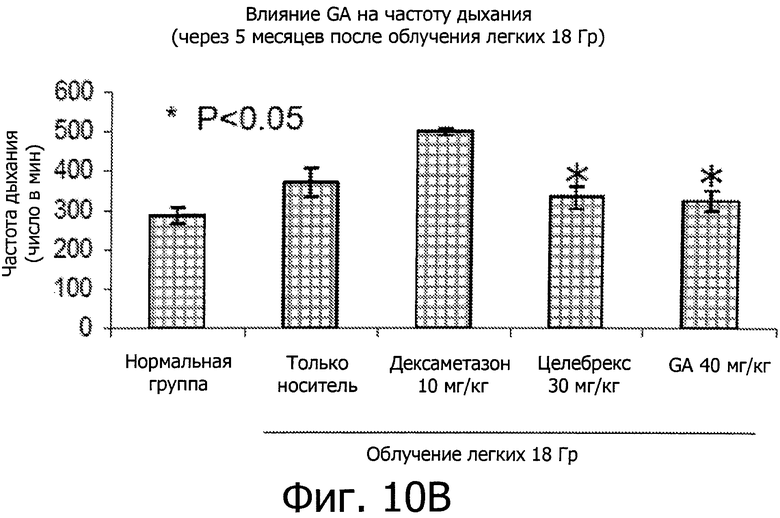
Фиг.10 показывает, что GA сокращает частоту дыхания у мышей с легочным фиброзом, вызванным IR. (А) показывает снижение частоты дыхания через 7 месяцев после IR при дозе 15 Гр. (В) показывает снижение частоты дыхания через 5 месяцев после IR при дозе 18 Гр.
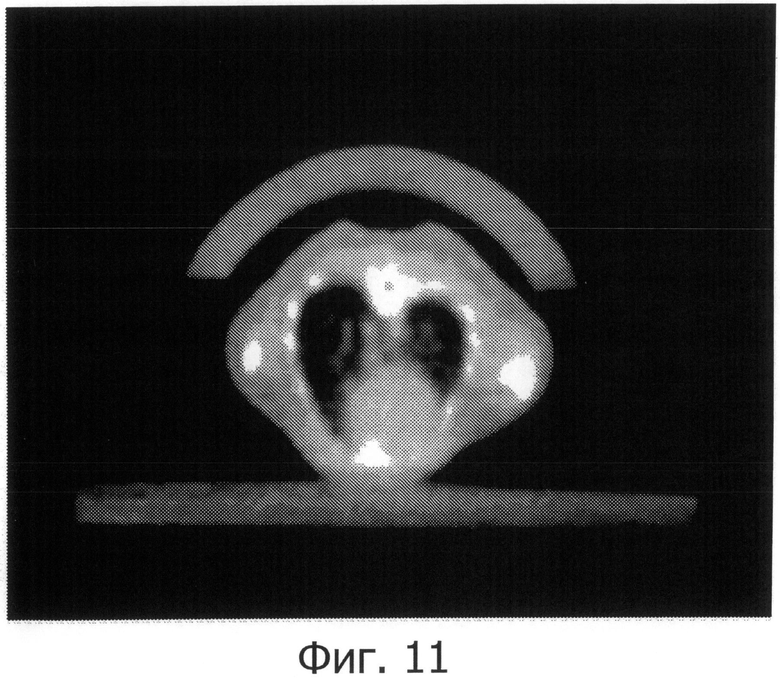
Фиг.11 изображает легкое мыши методом конусно-лучевой компьютерной томографии (КЛКТ).
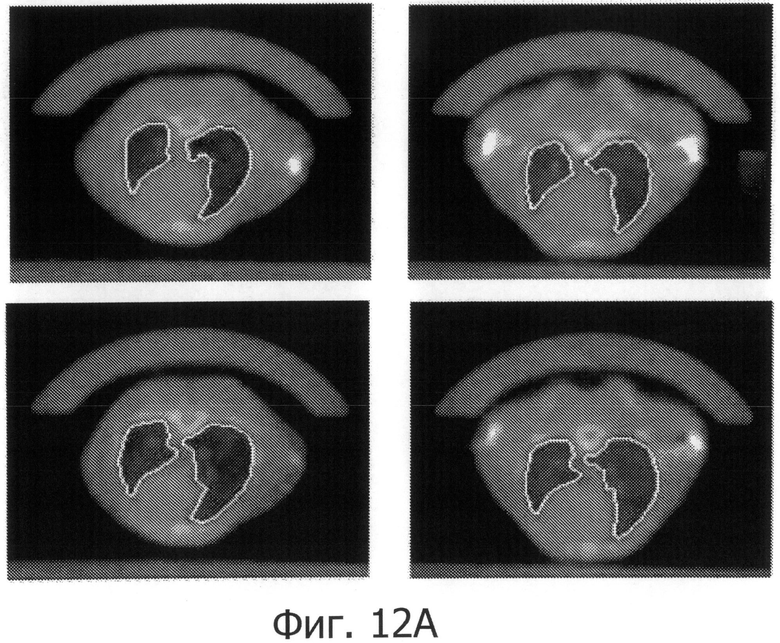
Фиг.12 показывает изображения легких мышей, полученные методом КЛКТ.
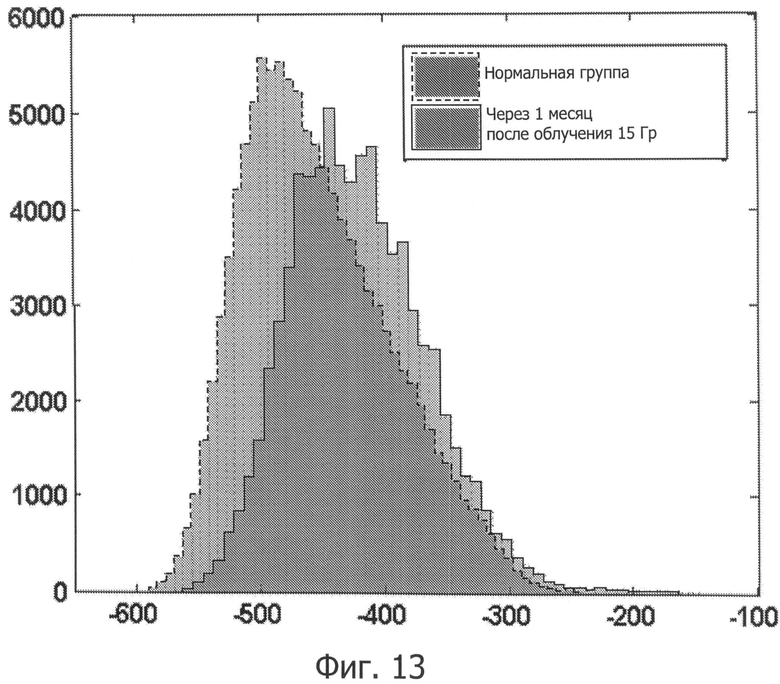
Фиг.13 показывает увеличение плотности легкого в результате IR. Плотность легкого мыши нормальной контрольной группы (не подвергаемой IR) представлена пунктирной линией. Плотность легкого мыши через месяц после торакального IR при дозе 15 Гр показана сплошными линиями.
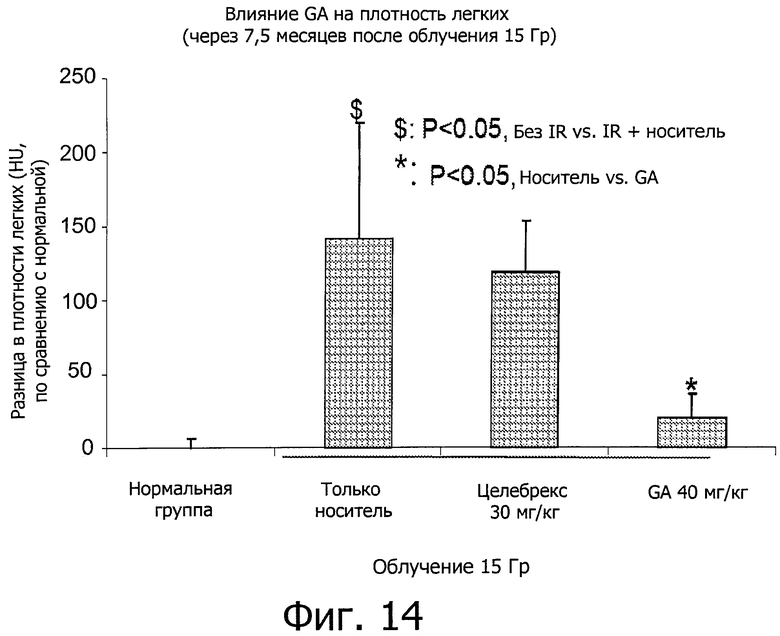
Фиг.14 показывает, что GA понижает плотность легкого у мышей с IR-вызванным легочным фиброзом через 7,5 месяцев после IR при дозе 15 Гр.
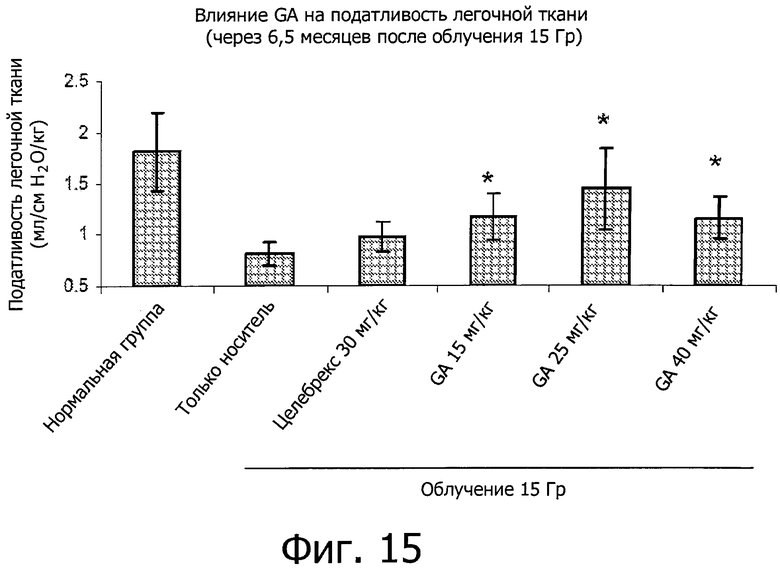
Фиг.15 показывает влияния GA на податливость легочной ткани через 6,5 месяцев после IR при дозе 15 Гр.
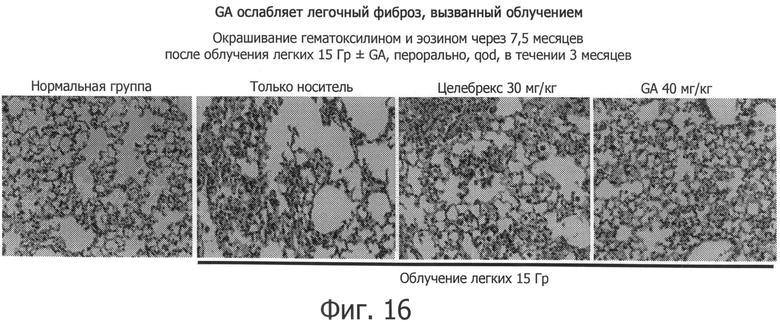
Фиг.16 показывает, что GA ослабляет легочный фиброз, вызванный IR.
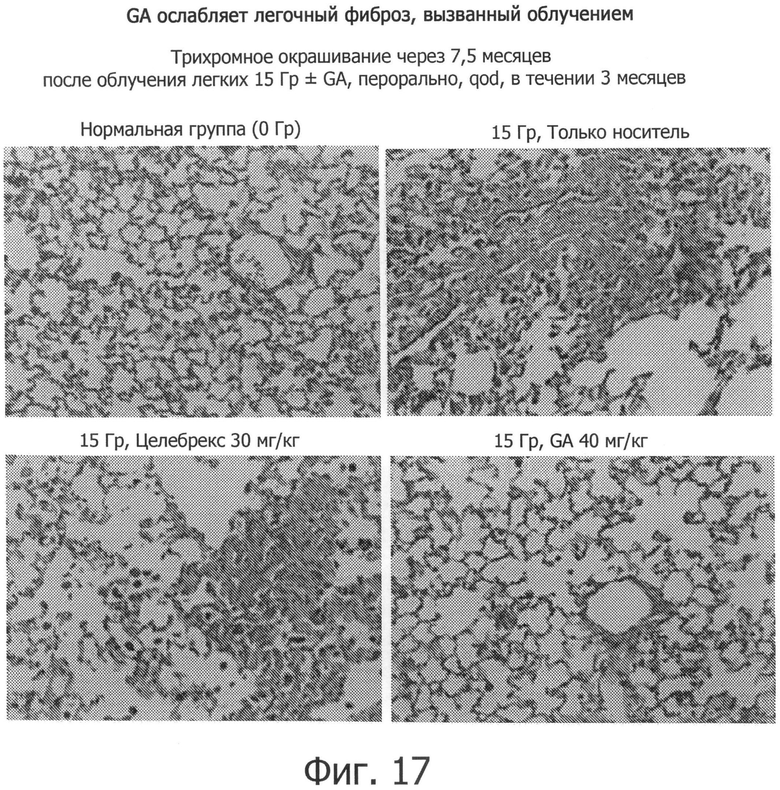
Фиг.17 показывает, что GA ослабляет фиброз легких, вызванный IR.
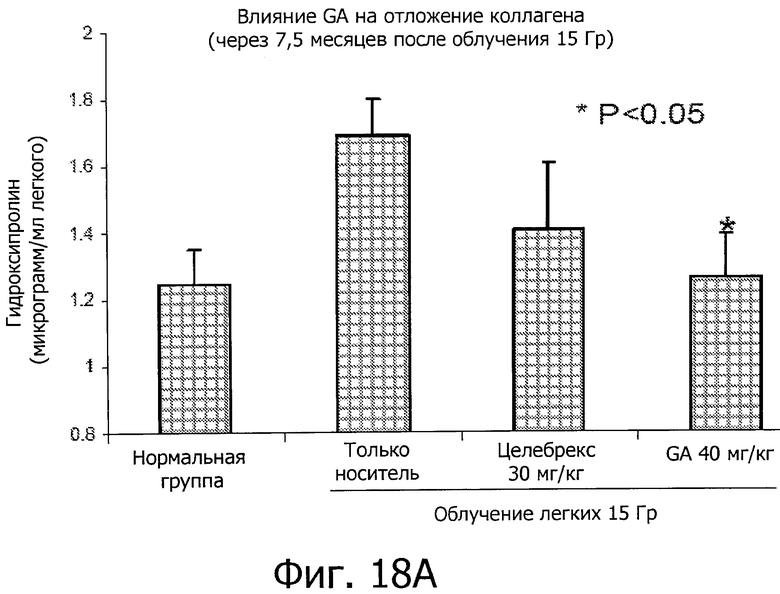
Фиг.18 показывает, что GA понижает отложения коллагена у мышей с легочным фиброзом, вызванным IR.
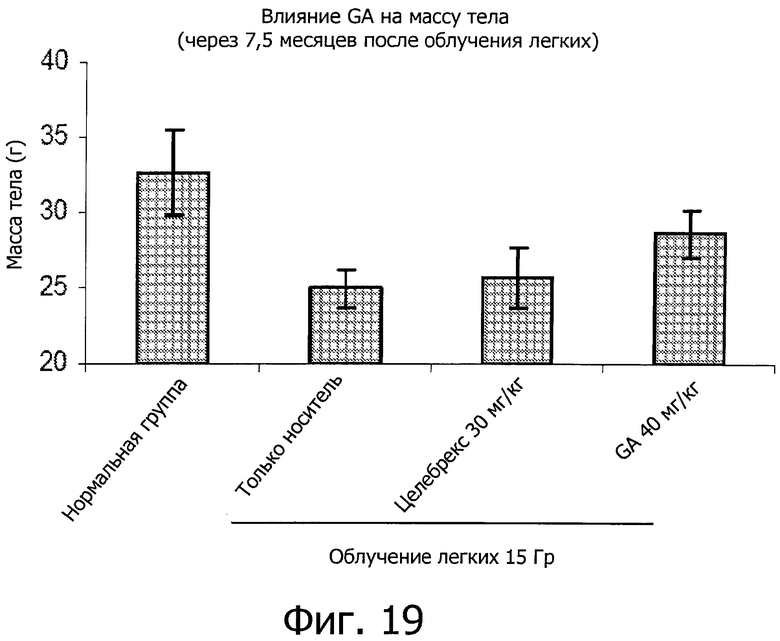
Фиг.19 показывает, что GA увеличивает вес тела мышей с легочным фиброзом, вызванным IR.
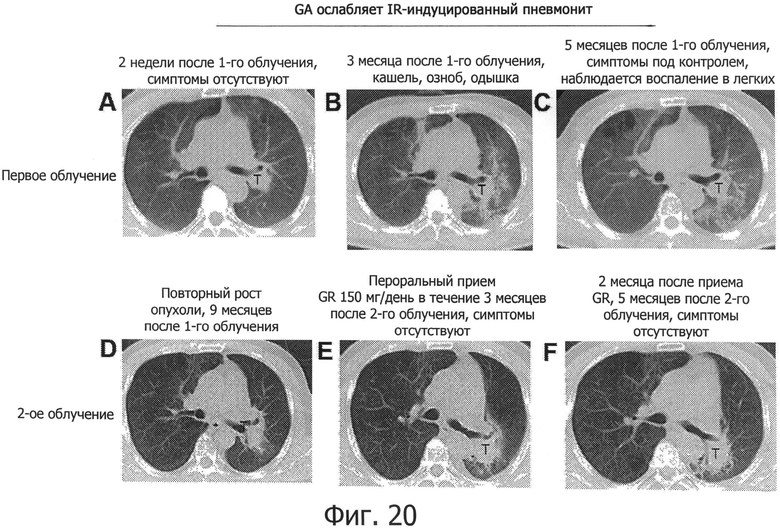
Фиг.20 показывает, что глицирризиновая кислота (GLA) ослабляет пневмонит у раковых пациентов, которые получали лучевую терапию.
Подробное описание изобретения
Настоящее изобретение относится к новым применениям глицирретиновой кислоты (GA), глицирризиновой кислоты (GLA) и родственных им соединений для предотвращения и/или лечения легочного фиброза, в частности легочного фиброза, вызванного облучением. Также описываются терапевтические применения пролекарств, метаболитов, производных (например, кислот, сложных эфиров и простых эфиров) и солей глицирретиновой кислоты (GA) и глицирризиновой кислоты (GLA).
В одном варианте осуществления способ по изобретению включает введение субъекту, нуждающемуся в таком лечении, эффективного количества соединений и композиций по настоящему изобретению. Настоящее изобретение также может быть использовано для лечения заболеваний легких, связанных с легочным фиброзом.
Настоящее изобретение также предназначено для терапевтических или фармацевтических композиций, содержащих соединение по изобретению в форме, которая может быть соединена с фармацевтически приемлемым носителем. В предпочтительных вариантах осуществления композиции по изобретению выполнены в форме, пригодной для доставки в легкие.
Соединения
Настоящее изобретение относится к терапевтическим применениям глицирретиновой кислоты (GA), глицирризиновой кислоты (GLA) и родственных им соединений. Также описываются терапевтические применения пролекарств, метаболитов, производных (например, кислот, сложных эфиров и простых эфиров) и солей глицирретиновой кислоты (GA) и глицирризиновой кислоты (GLA).
Было обнаружено, что GA и GLA эффективно подавляют воспаление легких, облегчают симптомы повреждения легких, улучшает функцию легких и обращают прогрессирующее отложение волокнистых тканей в легких. В частности, GA ослабляет легочные воспалительные реакции и значительно снижает уровни специфичных для легких медиаторов воспаления (например, IL-1, PF-4, SP-D, IL1α, TNFα, лимфотактина, р-селектина, 1-селектина, sTNF-R1 и VACAM-1) во время острой и подострой стадий пневмонита. Кроме того, GA способствует сохранению целостности альвеолярно-капиллярного барьера, о чем свидетельствует снижение экссудации плазмы и инфильтрации воспалительных клеток у субъектов, получавших GA. Дополнительно, GA значительно облегчает симптомы легочного фиброза, улучшает морфологию легочной ткани и подавляет избыточное отложение коллагена в легких.
В одном варианте осуществления настоящее изобретение относится к глицирретиновой кислоте (GA) (МВ:470,68), имеющей следующую структуру (Структура А):
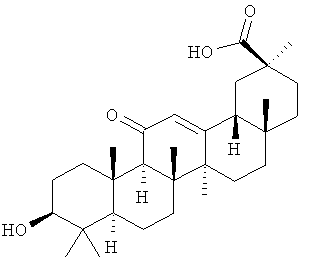
В другом варианте осуществления настоящее изобретение относится к глицирризиновой кислоте (GLA) (MB: 822,93), тритерпеноидному сапонин гликозиду глицирретиновой кислоты, имеющему следующую структуру (Структура В):
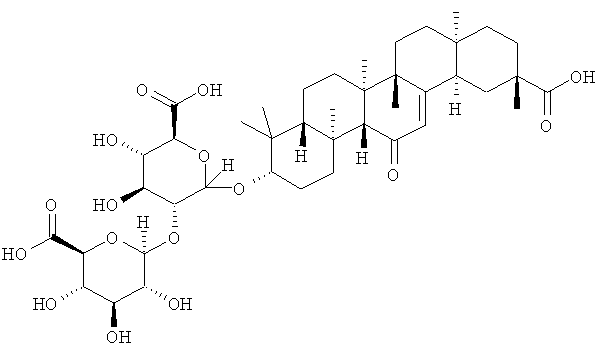
Глицирризиновая кислота может быть выделена из корня лакричника обыкновенного (Glycyrrhiza glabrd) или других видов солодки (Glycyrrhiza).
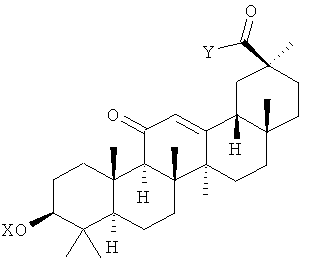
В некоторых вариантах осуществления настоящее изобретение относится к сложноэфирной, эфирной и/или амидной формам глицирретиновой кислоты (GA), представленным следующей структурой (Структура С):
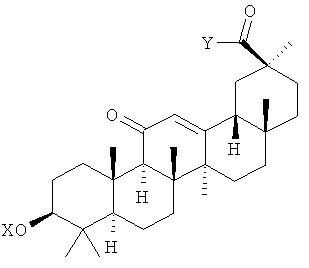 ,
,
где
X представляет собой любую группу, образующую эфирную или сложноэфирную связь с гидроксильным радикалом; и
Y представляет собой любую группу, которая образует сложноэфирную или амидную связь с карбоксильной группой.
В некоторых вариантах осуществления настоящее изобретение относится к сложноэфирной и/или амидной формам глицирризиновой кислоты (GLA), представленной следующей структурой (Структура D):
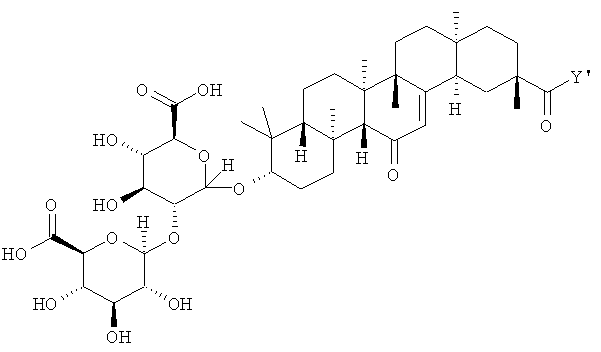
где Y' представляет собой любую группу, образующую сложноэфирную или амидную связь с карбоксильной группой.
В некоторых вариантах осуществления изобретения Х может быть алкилом, замещенным алкилом (например, галогеналкилом и гидроксиалкилом), алкенилом, замещенным алкенилом, -СООН, ацилом, алкилкарбонилом, бензилом, циклическим алкилом или циклическим алкенилом.
В некоторых вариантах осуществления изобретения Х может быть органической или неорганической кислотной группой, включающей, но без ограничения, уксусную кислоту, карбоновую кислоту, аспарагиновую кислоту, муравьиную кислоту, лимонную кислоту, бензойную кислоту, гиппуровую кислоту, яблочную кислоту, муциновую кислоту, фосфорную кислоту, серную кислоту, глюконовую кислоту, малеиновую кислоту, янтарную кислоту, винную кислоту и молочную кислоту.
В некоторых вариантах осуществления изобретения Х может быть углеводной группой, в которой моносахарид, дисахарид, олигосахарид или его производное теряет -Н в гидроксильной группе и, соответственно, образует радикал. Подходящие углеводные группы могут быть получены, например, из глюкозы, фруктозы и сахарозы.
В некоторых вариантах осуществления изобретения, Y и Y' могут независимо означать-NH2, алкиламино или алкокси.
«Алкил» означает линейный насыщенный моновалентный радикал, содержащий от одного до шестнадцати атомов углерода, или разветвленный насыщенный моновалентный радикал, содержащий от трех до шестнадцати атомов углерода. Алкил может включать углеводородные радикалы, содержащие от одного до четырех или от одного до трех атомов углерода, которые могут быть линейными. Примеры включают метил, этил, пропил, 2-пропил, н-бутил, изо-бутил, трет-бутил, пентил и тому подобное. «Алкенил» означает линейный или разветвленный C2-C16 углеводородный радикал, содержащий одну или несколько углерод-углеродных двойных связей. Примеры включают пропиленил, бутен-1-ил, изобутенил, пентен-1-ил, 2,2-метилбутен-1-ил, 3-метилбутен-1-ил, гексан-1-ил, гептен-1-ил, октен-1-ил и тому подобное. «Ацил» означает радикал -C(O)R, в котором R представляет собой водород, алкил или циклоалкил, или гетероциклоалкил. Примеры включают формил, ацетил, этилкарбонил и тому подобное.
«Карбоксил» означает радикал -CO(O)H.
«Карбалкокси» означает радикал -C(O)R, в котором R представляет собой, например, водород, алкил или циклоалкил, гетероциклоалкил, галоген или галогеналкил. «Галоген» означает фтор, хлор, бром или иод, например бром и хлор. «Галогеналкил» означает алкил, замещенный одним или несколькими одинаковыми или различными атомами галогена, например -CH2Cl, -CH2Br, -CF3, -CH2CH2Cl, -CH2CCl3 и тому подобное.
«Амино» означает радикал -NH2.
«Алкиламино» означает радикал -NHR или -NR2, в которых каждый R независимо представляет собой алкильную группу. Примеры включают метиламино, (1-метилэтил)амино, диметиламино, метилэтиламино, ди(1-метилэтил)амино и тому подобное.
«Гидрокси» означает радикал -ОН.
«Гидроксиалкил» означает алкильный радикал, как определено в настоящем изобретении, замещенный одной или более, предпочтительно одной, двумя или тремя гидроксильными группами. Иллюстративные примеры включают (но не ограничиваются указанным) гидроксиметил, 2-гидроксиэтил, 2-гидроксипропил, 3-гидроксипропил, 1-(гидроксиметил)-2-метилпропил, 2-гидроксибутил, 3-гидроксибутил, 4-гидроксибутил, 2,3-дигидроксипропил, 2-гидрокси-1-гидроксиметилэтил, 2,3-дигидроксибутил, 3,4-дигидроксибутил и 2-(гидроксиметил)-3-гидроксипропил, предпочтительно 2-гидроксиэтил, 2,3-дигидроксипропил и 1-(гидроксиметил)-2-гидроксиэтил.
«Алкокси» означает радикал -ORa, где Ra представляет собой алкильную группу или замещенную алкильную группу.
Примеры алкокси групп включают метокси, этокси, пропокси и тому подобное.
В одном варианте осуществления настоящее изобретение относится к ацетоксолону (C32H48O5, CAS No.6277-14-1) - ацетильному производному глицирризиновой кислоты.
Настоящее изобретение также относится к солевым формам GA, GLA и родственных им соединений, включающих (но не ограничивающихся указанным), аммонийные соли, натриевые соли и калиевые соли.
Настоящее изобретение также относится к применениям пролекарств и метаболитов соединений. Термин «пролекарство», как использовано в настоящем изобретении, относится к метаболическому предшественнику соединения по настоящему изобретению или к его фармацевтически приемлемой форме. В общем, пролекарства включают в себя функциональные производные соединения, которые могут быть неактивными при введении субъекту, но легко превращаются в активный метаболит in vivo.
Обычные процедуры для выбора и получения подходящих пролекарств описаны, например, в "Design of Prodrugs", под редакцией Н. Bundgaard, Elsevier, 1985. Пролекарство по настоящему изобретению предпочтительно усиливает желательные характеристики соединения по настоящему изобретению, включая растворимость, биодоступность и стабильность, но, не ограничиваясь только ими. Таким образом, соединения, используемые в способах по изобретению могут, при желании, вводиться в форме пролекарства. Пролекарства соединений, используемые в настоящем изобретении, могут быть получены путем модификации функциональных групп, присутствующих в соединении, таким образом, чтобы модифицирующие группы отщеплялись либо в ходе обычных манипуляций, либо in vivo, с образованием основного соединения.
Термин "метаболит" относится к фармакологически активному продукту, включая, например, активный промежуточный или конечный продукт, полученному путем in vivo метаболизма соединения по настоящему изобретению у субъекта. Метаболит может получаться вследствие, например, анаболических и/или катаболических превращений вводимого соединения в организме субъекта, включающих окисление, восстановление, гидролиз, амидирование, дезамидирование, эстерификацию, деэстерификацию, ферментативное расщепление и тому подобное, но не ограничивающихся только этим.
Метаболиты, как правило, определяют путем приготовления меченого изотопом (например, 14C или 3H) соединения по настоящему изобретению, введением его парентерально в детектируемой дозе (например, в дозе более чем примерно 0,5 мг/кг) животному, такому как крыса, мышь, морская свинка, обезьяна или человек, выжиданием достаточного времени для того, чтобы произошел обмен веществ (обычно от около 30 секунд до 30 часов), и выделение продуктов преобразования соединения из мочи, крови или других биологических образцов. Эти продукты легко выделить, так как они помечены изотопами (другие выделяют за счет использования антител, способных связывать эпитопы, выживающие в процессе метаболизма). Структура метаболитов может быть определена обычным образом, например с помощью MS, LC/MS или ЯМР-анализов. В целом, анализ метаболитов осуществляется в соответствии с методами, хорошо известными специалистам в области исследований метаболизма препаратов.
Настоящее изобретение дополнительно относится к выделенным энантиомерным соединениям. Изолированные энантиомерные формы соединений по изобретению являются по существу свободными друг от друга (т.е. имеет место энантиомерный избыток). Иными словами, "R" формы соединений по существу свободны от "S" форм соединений и присутствуют, таким образом, в энантиомерном избытке относительно "S" форм. Точно так же, "S" формы соединений по существу свободны от "R" форм соединений и присутствуют, таким образом, в энантиомерном избытке относительно "R" форм. В одном варианте осуществления изобретения выделенные энантиомерные соединения присутствуют по крайней мере в примерно 80%-ом энантиомерном избытке. В предпочтительном варианте осуществления изобретения соединения присутствуют в по меньшей мере около 90% энантиомерном избытке. В более предпочтительном варианте осуществления изобретения соединения присутствуют в по меньшей мере около 95% энантиомерном избытке. В еще более предпочтительном варианте осуществления изобретения соединения присутствуют в по меньшей мере около 97,5% энантиомерном избытке. В наиболее предпочтительном варианте осуществления изобретения соединения присутствуют в по меньшей мере около 99% энантиомерном избытке.
В одном варианте осуществления соединения настоящего изобретения имеют ту же самую хиральную структуру, какая показана в любой из структур А-D.
Профилактика и/или Лечение Легочного Фиброза
Настоящее изобретение относится к способам предотвращения и/или лечения легочного фиброза, в частности легочного фиброза, вызванного облучением. Способы по настоящему изобретению также могут быть использованы для того, чтобы предотвращать, лечить или ослаблять заболевания легких, связанные с легочным фиброзом.
В одном варианте осуществления способ по изобретению включает введение субъекту, нуждающемуся в таком лечении, эффективного количества соединений и композиций по настоящему изобретению. Предпочтительно соединения и композиции по настоящему изобретению получают в форме, подходящей для введения в легкие.
Термин "легочный фиброз" или "фиброз легких", используемый в настоящем изобретении, относится к атипичному образованию или накоплению фиброзной, соединительной или рубцовой ткани и/или матриксных макромолекул (например, коллагена, фибронектина, протеогликана) на поверхности и/или внутри легких. Симптомы легочного фиброза включают одышку, сухой кашель, повышенную частоту дыхания, пониженную эластичность легких, увеличенную плотность легких, дискомфорт в груди и быструю потерю веса. Легочный фиброз не охватывает фиброзные состояния, которые развиваются в органах, отличных от легких, такие как фиброзные состояния, развивающиеся в печени.
Термин "лечение" или любая его вариация (например, лечить, лечение, лечебная терапия и т.д.), используемые в настоящем изобретении, включают ослабление или облегчение симптомов заболевания или состояния, снижение, подавление, замедление, ослабление, или влияние на прогрессирование, степень тяжести и/или масштаб состояния, но не ограничиваются только этим. В одном варианте осуществления изобретения лечение относится к снижению, подавлению, замедлению, ослаблению или влиянию на прогрессирование, степень тяжести и/или масштаб атипичного образования или накопления фиброзной, соединительной или рубцовой ткани и/или матриксных макромолекул (например, коллагена, фибронектина и протеогликана) на поверхности или внутри легких.
Термин "предотвращение" или любая его вариация (например, предотвращать, предотвращение и профилактика и т.д.), используемые в настоящем изобретении, включают задержку появления симптомов, предотвращение рецидивов заболевания, увеличение задержки между симптоматическими эпизодами или их комбинации, но не ограничиваются только этим. Профилактика, как этот термин используется в настоящем изобретении, не требует абсолютного отсутствия симптомов.
Заболевания легких, связанные с легочным фиброзом, включают осложнения легочного фиброза, заболевания легких, которые могут развиться при легочном фиброзе, а также заболевания легких, которые проистекают из легочного фиброза. Симптомы и осложнения легочных заболеваний включают гипоксемию, диспноэ, ортопноэ, цианоз, легочную гипертензию, легочное сердце и дисфункцию легких, но не ограничиваются только этим. Легочные состояния, которые могут развиться в легочные заболевания включают (но не ограничиваются указанным) повреждения легких (например, облучением, химическими веществами, лекарственной терапией, биологическим повреждением или загрязнением), инфекции легких (например, вирусные, бактериальные, грибковые и паразитарные инфекции), интерстициальные легочные заболевания, повреждения легких, вызванные паразитарными инфекциями и пневмонит.
«Пневмонит», как этот термин используется в настоящем изобретении, относится к своему обычному значению, которое представляет собой воспаление легочной ткани.
Термин «эффективное количество», как он используется в настоящем изобретении, относится к количеству, которое способно предотвратить, ослабить или лечить легочный фиброз. Например, эффективное количество представляет собой количество, способное к ослаблению одного или нескольких симптомов легочного фиброза. В некоторых вариантах осуществления изобретения эффективное количество обеспечивает по крайней мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 100% сокращение в частоте дыхания, понижение в плотности легких, увеличение по массе тела и/или увеличение в эластичности легочной ткани по сравнению с субъектами с легочным фиброзом, не получающих лечение.
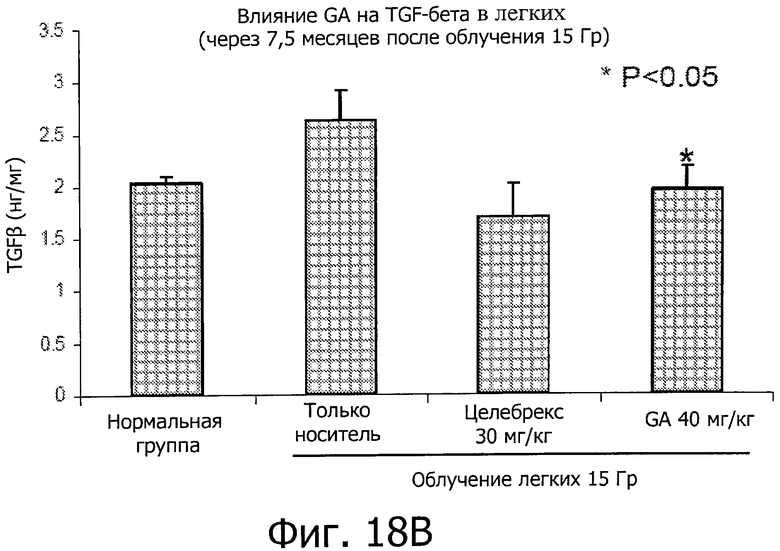
В конкретном варианте осуществления изобретения эффективное количество обеспечивает по крайней мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 100% сокращение в атипичном накоплении фиброзных тканей (например, коллагена, фибронектина и протеогликанов) в легких по сравнению с субъектами с легочным фиброзом, не получающих лечение. Например, эффективное количество обеспечивает по крайней мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 100% сокращение в содержании коллагена, фибронектина, протеогликана и/или гидроксипролина в легких по сравнению с субъектами с легочным фиброзом, не получающих лечение. В другом примере эффективное количество обеспечивает по крайней мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 100% сокращение в профиброзных медиаторах, таких как TGFp в тканях легкого, по сравнению с субъектами с легочным фиброзом, не получающих лечение.
Кроме того, поскольку легочный фиброз во многих случаях возникает из воспалительных реакций в ответ на легочное повреждение или инфекцию, эффективное количество способно снизить уровень одного или нескольких легочных медиаторов воспаления в ткани легкого. Иллюстративные примеры легочных медиаторов воспаления включают SP-D, IL1α, TNFα, IL6, PF4, Р-селектин, L-селектин, VCAM-1, лимфотактин и простагландин Е (PGE), но не ограничиваются этим. В некоторых вариантах осуществления изобретения эффективное количество обеспечивает по крайней мере 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 60%, 70%, 80%, 90% или 100% сокращение в уровнях одного или нескольких медиаторов воспаления по сравнению с субъектами с легочным фиброзом, не получающими лечение.
Термин "субъект", как он используется в настоящем изобретении, описывает организм, включая млекопитающих, таких как приматы, которым может быть предоставлено лечение с помощью композиций по настоящему изобретению. Виды млекопитающих, которые могут получить пользу от описанных способов лечения включают обезьян, шимпанзе, орангутангов, людей, мартышек; и домашних животных, таких как собаки, кошки, лошади, крупный рогатый скот, свиней, овец, коз, кур, мышей, крыс, морских свинок и хомяков, но не ограничиваются только ими.
Выражение "субъект, нуждающийся в таком лечении", как оно используется в настоящем изобретении, относится к субъекту, который находится в группе риска, имеет симптомы или диагноз легочного фиброза и/или легочных заболеваний, связанных с легочным фиброзом. В одном варианте осуществления настоящее изобретение включает диагностику легочного фиброза у субъекта, в ходе которой соединения и композиции по настоящему изобретению вводят субъекту, которому имеет диагноз или симптомы легочного фиброза.
Идентификация субъектов, которые имеют легочный фиброз, находится в пределах знаний и способностей квалифицированного специалиста в данной области знаний. К примеру, квалифицированный врач в данной области может с использованием физических проверок, таких как тест легочной функции и тестовые упражнения, легко заметить видимые симптомы легочного фиброза. Кроме того, сочетание медицинских методов, таких как рентген грудной клетки, компьютерная томография высокого разрешения (КТВР) и хирургическая биопсия легких, может быть использовано, чтобы определить патологические изменения тканей легких, вызванных легочным фиброзом.
В другом варианте осуществления соединения и композиции по настоящему изобретению вводят субъекту, который не имеет видимых симптомов легочного фиброза, но в отношении которого была установлена предрасположенность к развитию легочного фиброза (в дальнейшем такой пациент называется "пациент в группе риска"). Например, "пациенты группы риска" включают субъектов, у которых были повреждения легких (например, облучением, химическими веществами, лекарственной терапией, биологическим повреждением и загрязнением), легочная инфекция (например, вирусная, бактериальная, грибковая и паразитарная инфекция), а также такие заболевания, как пневмонит и интерстициальное заболевание легких. В одном варианте осуществления изобретения до введения соединений и композиций по настоящему изобретению проводят оценку пациента, чтобы определить риск развития у него фиброза легких. В еще одном варианте осуществления изобретения субъектом является больной раком, который получил или получает лучевую терапию.
В одном варианте осуществления изобретения соединения и фармацевтические композиции по настоящему изобретению могут быть использованы для предотвращения, лечения или ослабления легочного фиброза, включая индуцированный излучением фиброз легких, идиопатический легочный фиброз и кистозный фиброз легких, но не ограничиваясь только этим.
В одном варианте осуществления настоящее изобретение может быть использовано для предотвращения, лечения или ослабления повреждения легких, вызванного облучением, и/или лучевой пневмопатии, включая пневмонит и легочный фиброз. В одном варианте осуществления настоящее изобретение может быть использовано для предотвращения, лечения или ослабления легочного фиброза, вызванного лучевой терапией опухоли или лечением рака. В другом варианте осуществления настоящее изобретение может быть использовано для предотвращения, лечения или ослабления легочного фиброза, являющегося следствием случайного повреждения легких, вызванного облучением или ядерными инцидентами.
В одном варианте осуществления настоящее изобретение может быть использовано для предотвращения, лечения или ослабления легочного фиброза, вызванного торакальным облучением. В некоторых вариантах осуществления настоящее изобретение может быть использовано для предотвращения, лечения или ослабления легочного фиброза, вызванного облучением в дозах по крайней мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 80, 85, 90, 95, 100, 120 или 150 Гр. Кроме того, настоящее изобретение может быть использовано для предотвращения, лечения или ослабления легочного фиброза, вызванного радиацией в дозах по крайней мере 0,1, 0,3, 0,5, 0,7, 0,9, 1,0, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,7, 3,0, 3,2, 3,5 или 4,0 Гр в день.
В одном из вариантов осуществления соединения и фармацевтические композиции по настоящему изобретению могут быть использованы для предотвращения, лечения или ослабления легочного фиброза, вызванного облучением (в том числе лучевой терапией), загрязняющими веществами, токсинами, травмой, курением, аутоиммунными заболеваниями, такие как ревматоидный артрит, лекарственной терапией (например, амиодароном, блеомицином, бусульфаном, метотрексатом и нитрофурантоином), асбестом и инфекцией (например, вирусной, бактериальной, грибковой и паразитарной инфекцией).
В одном варианте осуществления соединения и фармацевтические композиции по настоящему изобретению могут быть использованы для предотвращения, лечения или облегчения заболевания, развивающегося в легочный фиброз, включая интерстициальное заболевание легких, острый и/или хронический пневмонит, хроническое обструктивное заболевание легких (ХОБЛ), астму, силикоз, повреждение легких и пневмонию.
В одном варианте осуществления соединения и фармацевтические композиции по настоящему изобретению могут быть использованы для предотвращения, лечения или ослабления фиброзных заболеваний или состояний, которые развиваются в коже, сердце, кишечнике и/или забрюшинном пространстве. В одном варианте осуществления настоящее изобретение исключает лечение фиброза печени.
Хотя в экспериментальных моделях настоящего изобретения легочный фиброз вызывали с помощью облучения грудной клетки, специалисту понятно, что терапевтические преимущества настоящего изобретения выходят за пределы IR-индуцированного легочного фиброза.
В еще одном варианте осуществления настоящее изобретение не охватывает лечение воспаления тканей, отличных от легочных тканей. В одном варианте осуществления настоящее изобретение не охватывает лечение воспалительных состояний печени и кожи. В другом варианте осуществления настоящее изобретение не включает лечение одного или нескольких воспалительных состояний и заболеваний, включающих гепатит, цирроз печени, гипертонию и нелегочный отек. В другом варианте осуществления настоящее изобретение не охватывает лечения вирусной (например, гриппа А, вируса простого герпеса, атипичной пневмонии (ОРС) и/или ВИЧ), бактериальной (например, стафилококк) или грибковой инфекций, которые не развиваются в легочный фиброз. В другом варианте осуществления настоящее изобретение не охватывает лечение дерматита, язвенной болезни или ревматоидного артрита. В другом варианте осуществления настоящее изобретение не охватывает лечение респираторных заболеваний, которые не приводят к развитию фиброза легких.
Терапевтические композиции и составы
Настоящее изобретение также относится к терапевтическим или фармацевтическим композициям, содержащим соединение по изобретению в форме, которая может быть скомбинирована с фармацевтически приемлемым носителем. В связи с этим, соединение по изобретению может быть изолированным или по существу чистым. Настоящее изобретение также включает пищевые добавки и диетическое питание или составы напитков, содержащие соединение по изобретению.
Термин «носитель» относится к разбавителю, адьюванту, наполнителю или средству доставки, с которым вводят соединение по изобретению. Такие фармацевтические носители могут быть стерильными жидкостями, такими как вода и масла, включая масла из нефтяных масел, такие как минеральное масло, растительные масла, такие как арахисовое масло, соевое масло и кунжутное масло, животные масла или масла синтетического происхождения. Солевые растворы и водные растворы декстрозы и глицерина также могут быть использованы в качестве жидких носителей, особенно в случае растворов для инъекций. Особенно предпочтительные фармацевтические носители для лечения или облегчения воспалительных процессов в центральной нервной системе представляют собой носители, которые могут проникать через гематоэнцефалический барьер. В соответствии с использованием в настоящем изобретении носители не включают естественные растительные материалы в том виде, как он существует в природе.
Подходящие фармацевтические наполнители включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропиленгликоль, воду, этанол и тому подобное. Терапевтическая композиция, при желании, может также содержать небольшие количества увлажняющих или эмульгирующих агентов или агентов буферизации рН. Эти композиции могут иметь форму растворов, суспензий, эмульсий, таблеток, капсул, порошков, составов с замедленным высвобождением и тому подобного. Композиция может быть составлена с использованием традиционных связующих веществ и носителей, таких как триглицериды. Примеры подходящих фармацевтических носителей описаны в «Remington's Pharmaceutical Sciences» за авторством E.W. Martin. Такие композиции содержат терапевтически эффективное количество терапевтической композиции вместе с подходящим количеством носителя, чтобы получить форму, подходящую для введения пациенту. Состав композиции должен соответствовать способу введения.
В предпочтительных вариантах осуществления изобретения композиции готовят в форме, адаптированной для доставки в легкие. Например, при ингаляционной доставке жидкая фармацевтическая композиция может быть лиофилизирована до использования, где лиофилизированную композицию измельчают для получения тонко измельченного сухого порошка, состоящего из частиц с размерами в пределах указанного выше желаемого диапазона. С другой стороны, например, для получения формы сухого порошка жидкой фармацевтической композиции может быть использована распылительная сушка, и этот процесс осуществляется в условиях, которые приводят к по существу аморфному тонко измельченному сухому порошку, состоящему из частиц с размерами в пределах желаемого диапазона. Для способов получения сухих порошковых форм фармацевтических композиций см., например, WO 96/32149, WO 97/41833, WO 98/29096 и патенты США. №№5976574, 5985248, 6001336 и 6875749, которые включены в настоящее описание посредством ссылки. Кроме того, сухая порошковая форма фармацевтической композиции может быть получена и использована как водный или неводный раствор или суспензия в дозированных ингаляторах.
Кроме того, фармацевтически эффективное количество сухой порошковой формы композиции может быть приготовлено в виде аэрозоля или другого препарата, подходящего для легочной ингаляции. Количество сухой порошковой формы композиции, помещаемое в устройство доставки, должно быть достаточным для обеспечения доставки фармацевтически эффективного количества композиции субъекту при ингаляции. Устройство доставки обеспечивает введение в одной или нескольких дробных дозах за счет легочной ингаляции фармацевтически эффективного количества композиции в легкие пациента. Аэрозольным пропеллентом может быть любой традиционный материал, применяемый для этой цели.
При использовании в контексте фармацевтических композиций, пригодных для доставки в легкие, указанные термины имеют следующие значения. Под "водной" подразумевается композиция, полученная с водой, содержащая воду или растворенная в воде, включая смеси, где вода является преобладающим веществом в смеси. Под «неводной» подразумевается композиция, полученная с, содержащая или растворенная в веществе, отличном от воды и смеси, в которой вода не является преобладающим веществом. Под «раствором» подразумевается гомогенный препарат из двух или более веществ, которые могут быть твердыми веществами, жидкостями, газами или их различными комбинациями. Под "суспензией" подразумевается смесь веществ, таких что одно или несколько нерастворимых веществ однородно диспергированы в другом преобладающем веществе.
Для целей настоящего изобретения термины "твердое вещество" и "сухой порошок" используют взаимозаменяемо там, где это касается фармацевтических композиций. Под "твердой" или "сухой порошковой" формой фармацевтической композиции подразумевают композицию, которая была высушена до тонкодисперсного порошка с содержанием влаги ниже около 10% по весу, как правило, ниже примерно около 5% по весу и предпочтительно ниже примерно 3% по весу. Указанная сухая порошковая форма композиции состоит из частиц, содержащих пептиды по настоящему изобретению. Предпочтительно средний диаметр частиц составляет менее чем около 90,0 мкм, более предпочтительно менее чем около 70,0 мкм, более предпочтительно менее чем около 50,0 мкм, еще более предпочтительно менее чем около 30,0 мкм, более предпочтительно менее чем около 10,0 мкм, более предпочтительно менее чем около 7,0 мкм, еще более предпочтительно в диапазоне от 0,1 до 5,0 мкм, наиболее предпочтительно в диапазоне от приблизительно 1,0 до приблизительно 5,0 мкм.
Для уменьшения адгезии сухого порошка на стенках устройства доставки, из которого аэрозоль распределяют, к фармацевтической композиции может быть добавлено поверхностно-активное вещество. Подходящие поверхностно-активные вещества для этого предполагаемого использования, включают сорбитан триолеат, соевый лецитин и олеиновую кислоту, но не ограничиваются только ими. Устройства, подходящие для ингаляционной доставки сухой порошковой формы композиции в виде неводной суспензии, являются коммерчески доступными. Примеры таких устройств включают в себя ингалятор с контролем дозы Вентолин (Glaxo Inc., Research Triangle Park, N.C.), и ингалятор Интал (Fisons, Corp., Bedford, Mass.). Смотри также аэрозольные устройства доставки, раскрытые в патентах США №№5522378; 5775320; 5934272; и 5960792, которые включены в настоящее описание посредством ссылки.
В еще одном варианте осуществления изобретения фармацевтическая композиция может быть доставляться с помощью системы с контролируемым высвобождением. В одном варианте осуществления изобретения может быть использован насос (смотри Langer, supra; Sefton, 1987, CRC Crit. Ref. Biomed. Eng. 14:201; Buchwald et al., 1980, Surgery 88:507; и Saudek et al., 1989, N. Engl. J. Med. 321:574). В другом варианте осуществления изобретения могут быть использованы полимерные материалы (смотри Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Fla. (1974); Controlled Drug Bioavailability, Drug Product Design and Performance, Smolen and Ball (eds.), Wiley, New York (1984); Ranger and Peppas, J. Macromol. Sci. Rev. Macromol. Chem. 23:61 (1983); смотри также Levy et al., 1985, Science 228:190; During et al., 1989, Ann. Neurol. 25:351; Howard et al., 1989, J. Neurosurg. 71:105). В еще одном варианте осуществления система контролируемого высвобождения может быть размещена в непосредственной близости от цели композиции, а именно легкого, таким образом, требуется только часть от обычной системной дозы (смотри, например, Goodson, в Medical Applications of Controlled Release, supra, vol. 2, pp.115- 138 (1984).
В одном варианте осуществления изобретения композицию готовят в соответствии с обычными процедурами в виде фармацевтической композиции, адаптированной для местного инъекционного введения человеку. Как правило, композиции для местного инъекционного введения представляют собой растворы в стерильном изотоническом водном буфере. В случае необходимости композиция может также включать солюбилизирующий агент и местный анестетик, такой как лидокаин, чтобы облегчить боль в месте инъекции. Как правило, компоненты поставляются либо отдельно или смешанными в стандартной лекарственной форме, например в виде сухого лиофилизированного порошка или безводного концентрата в герметично закрытом контейнере, таком как ампула или саше с указанием количества активного вещества. В случае, когда композицию вводят путем инъекций, ампулы со стерильной водой для инъекций или физиологическим раствором могут поставляться таким образом, чтобы ингредиенты могли быть смешаны перед введением.
Терапевтические или фармацевтические композиции по изобретению могут быть изготовлены в виде нейтральной или солевой форм. Фармацевтически приемлемые соли включают соли, образованные со свободными аминогруппами, такими как группы, полученные из соляной, фосфорной, уксусной, щавелевой, винной кислот и т.д., и соли образованные со свободными карбоксильными группами, такими как полученные из натрия, калия, аммония, кальция, гидроксидов железа, изопропиламина, триэтиламина, 2-этиламиноэтанола, гистидина, прокаина и т.д.
Настоящее изобретение также предусматривает модификацию соединения, так чтобы оно было более стабильным после введения субъекту, то есть, чтобы после введения соединения оно имело более длительный период эффективности по сравнению с немодифицированным соединением. Такие модификации хорошо известны специалистам в данной области, например микрокапсулирование и т.д.
Изобретение также относится к фармацевтической упаковке или набору, включающим один или несколько контейнеров, заполненных одним или несколькими ингредиентами фармацевтической композицией по изобретению, например соединением, носителем.
Соединения по настоящему изобретению могут быть также приготовлены в соответствии с традиционной китайской медицинской практикой. Композиция и дозировка состава, которые являются эффективными в лечении конкретного заболевания, состояния или расстройства, будут определяться природой заболевания, состояния или расстройства посредством стандартных клинических методов.
В традиционной китайской медицине рецептурные количества могут быть легко превращены в любую форму лекарственного препарата, пригодного для введения людям или животным. Подходящие формы включают, например, настойки, отвары и сухие экстракты. Они могут быть приняты перорально, введены с помощью инъекцию в вену или слизистые оболочки. Активный ингредиент также может быть помещен в капсулы, порошки, паллеты, пастилки, суппозитории, растворы для приема внутрь, пастеризованные желудочно-кишечные суспензионные инъекции, инъекции малого или большого количества, замороженные порошковые инъекции, пастеризованное порошковые инъекции и тому подобное. Все вышеупомянутые способы известны специалистам в данной области техники, описаны в книгах и широко используются специалистами в области фитотерапии.
Настойки готовят путем суспендирования трав в алкогольный раствор, такой как, например, вино или ликер. После периода суспендирования жидкость (спиртовой раствор) можно принимать, например, два или три раза в день по одной чайной ложке каждый раз.
Отвар является распространенной формой растительного препарата. Отвар традиционно готовится в глиняном горшке, но также может быть приготовлен в стеклянных, эмалированных контейнерах или контейнерах из нержавеющей стали. Состав может быть замочен на некоторое время в воде, а затем доведен до кипения и проварен на медленном огне, пока количество воды не уменьшится, например, наполовину.
Экстракт представляет собой концентрированный препарат из необходимых ингредиентов лекарственных трав. Как правило, основные ингредиенты извлекаются из трав путем суспендирования трав в соответствующем выбранном растворителе, как правило, в воде, смеси этанол/вода, метаноле, бутаноле, изо-бутаноле, ацетоне, гексане, петролейном эфире или других органических растворителях. Процесс экстракции может быть дополнительно оснащен средствами мацерации, перколяции, повторной перколяции, противоточной экстракции, турбо-экстракции или диоксид-углеродной сверхкритической (температура/давление) экстракцией. После фильтрации, чтобы избавиться от растительного мусора, экстракционный раствор может быть дополнительно выпарен и таким образом сконцентрирован с получением мягкого экстракта (extractum spissum) и/или, в конечном итоге, высушенного экстракта (extracum siccum) с помощью распылительной сушки, сушки в вакуумной печи, сушки в псевдоожиженном слое или лиофилизации. Мягкий экстракт или высушенный экстракт могут быть дополнительно растворены в подходящей жидкости до требуемой концентрации для введения или переработки в форму, такую как драже, капсулы, инъекции и т.д.
Пути Введения
Соединения и композиции по настоящему изобретению могут быть введены субъекту, которого лечат, с использованием стандартных маршрутов, включая пероральное, ингаляционное или парентеральное введение, включая внутривенное, подкожное, местное, трансдермальное, внутрикожное, трансмукозальное, внутрибрюшинное, внутримышечное, интракапсулярноее, внутриглазничное, внутрисердечное, транстрахеальноее, подкожное введение, под кутикулу, внутрисуставное, субкапсулярное, субарахноидальное, интраспинальное введение, эпидуральную и интрастернальную инъекцию, инфузию и электропорацию, а также совместное введение в качестве компонента любого медицинского устройства или объекта, который должен быть помещен (временно или постоянно) в этого субъекта.
В предпочтительных вариантах осуществления соединения и композиции по данному изобретению вводят любым путем, подходящим для легочной доставки. Легочное введение требует высвобождения биологически активного вещества из средства доставки в полость рта субъекта во время вдоха. Для целей настоящего изобретения фармацевтические композиции можно вводить путем ингаляции аэрозоля или другого подходящего препарата, который получают из водного или неводного раствора или суспензионной формы или твердой или сухой порошковой формы фармацевтической композиции, в зависимости от используемого устройства доставки. Легочная ингаляция приводит к нанесению вдыхаемой композиции на альвеолы легких субъекта. После осаждения соединения или композиции могут быть поглощены, пассивно или активно, через слои эпителия альвеол и капиллярного эпителия в кровь.
Количество терапевтической или фармацевтической композиции по изобретению, которое является эффективным в лечении конкретного заболевания, состояния или расстройства, будет зависеть от способа введения и тяжести заболевания, состояния или расстройства, и должно определяться в соответствии с клиническим опытом лечащего врача и обстоятельств в отношении каждого пациента. Обычно доза находится в диапазоне от около 0,001 мг/кг до около 3 г/кг.Например, подходящие единичные дозы могут составлять от около 0,01 до около 3 г, от около 0,01 до около 1 г, от около 0,01 до около 500 мг, от около 0,01 до около 400 мг, от около 0,01 до около 300 мг, от около 0,01 до около 200 мг, от около 0,01 до около 100 мг, от около 0,01 до около 50 мг, от около 0,01 до около 30 мг, от около 0,01 до около 20 мг, от около 0,01 до около 10 мг, от около 0,01 до около 5 мг, от около 0,01 до около 3 мг, от около 0,01 до около 1 мг или от около 0,01 до около 0,5 мг. Такая единичная доза может быть введена более чем один раз в день, например два или три раза в день.
Количество активного ингредиента, который может быть объединен с материалами-носителями для получения одной дозированной формы будет меняться в зависимости, например, от типа состояния и субъекта, подлежащего лечению. Обычно терапевтическая композиция содержит от примерно 5% до примерно 95% активного ингредиента (масс./масс.). Более конкретно, терапевтическая композиция содержит от около 20% (масс./масс.) до около 80%, или от около 30% до около 70% активного ингредиента (масс./масс.).
После того как произошло улучшение состояния больного, в случае необходимости вводится поддерживающая доза. Впоследствии дозу или частоту приема, или и то, и другое, можно уменьшить в зависимости от симптомов до уровня, при котором улучшение состояния сохраняется. Когда симптомы облегчены до желаемого уровня лечение следует прекратить. Пациенты могут, однако, требовать периодического лечения на долгосрочной основе, в случае каких-либо рецидивных симптомов заболевания.
В дополнение к сказанному, для выявления оптимальных диапазонов доз могут необязательно быть использованы анализы in vitro. Точная доза, которую необходимо использовать в составе, также будет зависеть от способа введения и тяжести заболевания, состояния или расстройства, и должна быть определена в соответствии с клиническим опытом лечащего врача и обстоятельств каждого пациента. Эффективные дозы могут быть экстраполированы из кривых доза-ответ, полученных из тестовых систем на моделях in vitro или животной модели.
Ниже приведены примеры, которые иллюстрируют методики для реализации настоящего изобретения. Эти примеры не должны рассматриваться как ограничение изобретения.
Пример 1 - индуцирование воспалительных реакций посредством IR
Вкратце, предрасположенных к фиброзу мышей линии C57BL/6 подвергали воздействию IR (излучения) при дозе 0, 5 или 9 Гр. Как показано на фиг.1, IR индуцирует первую стадию воспалительной реакции через 6 часов после воздействия, вторую стадия - через 4-10 дней после воздействия, и третью стадию - через 180 дней после воздействия (только IL2) (фиг.1, первый прямоугольник: контроль нормальной группы). Фиг.2 показывает рост уровней IM у мышей линии C57BL/6 и C3H/NeH с IR-индуцированного мозгового повреждения (МП) через 6 часов, 1, 2, 4 и 10 дней после воздействия при 9 Гр. Это означает, что IR вызывает воспалительные реакции, и уровни медиаторов воспаления могут быть использованы для мониторинга IR-индуцированного повреждения легких.
Пример 2 - модуляция воспалительных реакций во время острой фазы пневмонита, вызванного IR
Данный пример показывает, что GA подавляет рост воспалительных реакций во время острой фазы IR-индуцированного пневмонита, которые возникают в течение 48 часов после воздействия на мышей IR (облучением). Вкратце, мыши линии C57BL/6, предрасположенные к фиброзу получали одну дозу торакального IR в 15 Гр с мощностью дозы в 1,9 Гр/мин. Через шесть часов после воздействия IR мышей разделили на следующие группы лечения: 1) нормальная (получили дозу в 0 Гр, без обработки); 2) обработанные носителем; 3) GA-обработанные (30-40 мг/кг/q.o.d (т.е. через день) (дозировка GA, используемая в данном случае, была получена исходя из эффективной доза для человека (3-4 мг/кг), которая, как правило, в 6-10 раз ниже, чем у мышей), 4) пролеченные дексаметазоном (Положительная контрольная группа 1) (Dex, 3 мг/кг, в/м или п/о, через день); 5) пролеченные амифостином (Положительная контрольная группа 2) (Ami, 200 мг/кг/внутривенно, за 0,5 часа до облучения) и 6) пролеченные целебрексом (Положительная контрольная группа 3) (30 мг/кг, перорально, через день).
Мышей умерщвляли через 2,5 дня после воздействия IR и готовили свежий гомогенат ткани легкого с использованием буфера для лизиса, смешанного со смесью ингибитора протеназы. После того, как концентрацию белка доводили до 1 мг/мл, свежий гомогенат легкого добавляли в планшеты ELISA при концентрации 100 мкл/лунку. Уровни медиаторов воспаления измеряли с помощью ELISA.
Как показано на фиг.3, воздействие IR вызывает рост уровней медиаторов воспаления (IM), включая IL1α, TNFα, PF4 и VCAM-1. GA эффективно снижала уровни IM по сравнению с мышами, обработанных носителем (фиг.2, P<0,05). Степень ингибирования GA была сравнима со степенью ингибирования целебрексом, дексаметазоном и амифостином.
Пример 3 - подавление экссудации плазмы и инфильтрации воспалительных клеток во время острой фазы IR-индуцированного пневмонита
Данный пример показывает, что GA подавляет IR-индуцированную экссудацию плазмы и инфильтрацию воспалительных клеток во время острой фазы IR-индуцированного пневмонита. Вкратце, предрасположенные к фиброзу мыши линии C57BL/6 получали одну дозу торакального IR в 15 Гр с мощностью дозы в 1,9 Гр/мин и были обработаны, как описано в примере 2. Мышей умерщвляли через 2,5 дня после воздействия IR и легочные ткани были собраны и проанализированы на морфологические изменения.
Как показано на фиг.4, обработанные носителем легкие были наполнены инфильтратными воспалительными клетками и экссудатами плазмы по сравнению с нормальными, не подвергавшимися воздействию IR, легкими. GA значительно подавляла экссудацию плазмы и инфильтрацию воспалительных клеток внутри интерстициального пространства. Целебрекс, Дексаметазон и Амифостин также производили подобный эффект лечения.
Пример 4 - снижение в плазме уровней SP-D и IL1a во время острой фазы IR-индуцированного пневмонита
Данный пример показывает, что GA уменьшила в плазме уровни SP-D и IL1α.. IR повреждает эпителий легких и эндотелиальные клетки и вызывает дисфункцию плотных соединений, повышенную клеточную проницаемость и потерю целостности альвеолярно-капиллярного барьера. В результате, SP-D и IL1α аномально попадают в кровь из воспаленной легочной ткани, что приводит к повышенным уровням в плазме SP-D и IL1α.
В данном примере предрасположенные к фиброзу мыши линии C57BL/6 получали одну дозу торакального IR в 15 Гр с мощностью дозы в 1,9 Гр/мин и обрабатывались, как описано в примере 2. Мышей умерщвляли через 2,5 дня после воздействия IR и измеряли уровни в плазме SP-D и IL1α. Фиг.5A показывает, что воздействие IR приводит к зависимому от дозы увеличению уровней SP-D в плазме. В частности, SP-D в плазме не увеличивалось при воздействии IR в 5 Гр, но увеличилось при 10 Гр и 15 Гр. Как показано на фиг.5А-В, GA эффективно уменьшила в плазме уровни SP-D (Р<0,05). Кроме того, фиг.5С показывает, что GA эффективно уменьшила в плазме уровни IL1α (Р<0,05).
Пример 5 - влияние GA на подострую фазу IR-индуцированного пневмонита
Данный пример показывает, что GA эффективно модулирует подострую фазу IR-индуцированного пневмонита, которая развивается примерно через 2-4 недели после воздействия IR на мышей. Вкратце, предрасположенные к фиброзу мыши линии C57BL/6 получали торакальное IR и обрабатывались, как описано в примере 2. Мышей умерщвляли через 17 дней после воздействия IR и легочные ткани собирали. Делали анализы жидкости бронхоальвеолярного лаважа (BALF).
Результаты показали, что GA снизила уровни лимфотактина и p-селектина, двух ключевых медиаторов воспаления, участвующих в легочном иммунном ответе и врожденном иммунитете (фиг.6A и B, Р<0,05). Кроме того, GA снизила уровень нейтрофилов, проникающих в жидкость бронхоальвеолярного лаважа (фиг.7А, Р<0,05). GA также снизило активность миелопероксидазы (МРО) в (BALF) (фиг.7B, Р<0,05). Фиг.8A-C также показывают подавление инфильтрации нейтрофилов в интерстициальной (межклеточной) жидкости (фиг.8A-C).
Кроме того, отмечено, что рост медиаторов воспаления во время подострой фазы не имеет зависимости от дозы. IR воздействие при дозе 5 Гр может вызвать воспалительные реакции. Авторы настоящего изобретения также отметили, что воздействие IR с дозой выше чем 5 Гр может вызвать легочный фиброз. Чем больше доза, тем быстрее это может повлиять на развитие фиброза. Авторы настоящего изобретения обнаружили, что у мышей, получивших IR при дозе 7,5 Гр развился фиброз легких и они умерли от легочной недостаточности через 1,5 года после воздействия IR.
Введение GA через 24 часа после воздействия IR может эффективно блокировать рост воспалительных реакций. Фиг.9 показывает, что GA значительно снизила уровни ключевых медиаторов воспаления, включая IL1α, TNFα, лимфотактин и p-селектин, у мышей, подверженных торакальному IR при дозах 5, 10 и 15 Гр соответственно.
Пример 6 - ослабляющий эффект GA на IR-индуцированный легочный фиброз
Данный пример показывает, что GA улучшает функцию легких и ослабляет IR-индуцированный фиброз легких. У мышей, подверженных торакальному IR, развивался фиброз легких через 6 месяцев после воздействия IR (облучения) в 18 Гр, через 8 месяцев после воздействия IR в 15 Гр и через 10 месяцев после воздействия IR в 12,5 Гр. Чтобы оценки эффективности GA в отношении фиброза легких и функции легких, у мышей определяли частоту дыхания, плотность легких и растяжимость легких.
Чтобы оценить улучшение дыхательной функции мышей, подвергнутых воздействию торакального IR при дозе 15 Гр, обрабатывали GA (30-40 мг/кг) q.o.d (через день) или два раза в неделю в течение 3 месяцев. Частоту дыхания мышей измеряли с помощью Гарвардского дыхательного аппарата для грызунов, соединенного с плетизмографом под давлением. Как показано на фиг.10A-B, воздействие IR значительно увеличило частоту дыхания мышей, а лечение GA вызвало эффективное снижение частоты дыхания (P<0,05).
Для оценки влияния GA на плотность легких выполнили конусно-лучевую КТ (КЛКТ) легких мыши. КЛКТ обеспечивает полное 3D 650×650×428 сканирование (т.е. 428 срезов) легких с изотропным разрешение 270 мкм (центральный срез показан на фиг.11) в течение 30 секунд. Сканер обеспечивает КТ плотность чувствительность ~5 HU3, и, таким образом, можно различить изменения в плотности легких.
Данные КЛКТ были дополнительно проанализированы с использованием программного обеспечения MATLAB. Легкие были автоматически сегментированы (фиг.12A) и для каждого мышиного легкого было создано 3D-изображение (фиг.12B). Чтобы уменьшить влияние сердечных движений на среднее значение плотности легких, границы легких для анализа не использовались. Была создана гистограмма интенсивности воксела (плотность легочной ткани) для каждой мыши (фиг.13).
Таблица 1 показывает среднее значение и стандартное отклонение (SD) плотности легкого. Воздействие IR (облучения) при 18 Гр постепенно увеличивало плотность легких от нормальной плотности -454+60 HU (шкала Хаунсфилда) вплоть до -364+45 HU в год. Как показано на фиг.14, GA значительно сократило аномальное увеличение плотности легких (P<0,05). Уменьшение плотности легкого за счет GA является более мощным, чем в случае использования Целебрекса.
Чтобы оценить влияние GA на растяжимость легких мышей анестезировали и их трахеи хирургически извлекали и рассекали. 1 см трубка из нержавеющей стали 18 размера вставляли в трахею и закрепляли с помощью хирургических швов. Частоту дыхания и объем вдоха мышей измеряли с помощью Гарвардского дыхательного аппарата для грызунов. Средняя частота дыхания составляла 150 вдохов в минуту, а объем вдоха был скорректирован в соответствии с весом (0,01 мл на грамм веса тела). Затем мышей помещали в плетизмограф для измерений давление-объем. Как показано на фиг.15, лечение GA значительно и в целом эффективно повышала растяжимость легких, сниженную за счет воздействия IR (P<0,05).
Пример 7 - ослабление фиброзных состояний
Данный пример показывает, что GA меняет в обратную сторону патологическую альтерацию ткани легких, улучшает морфологию легких и подавляет отложение коллагена при IR-индуцированном фиброзе. Вкратце, мышей, получавших GA (40 мг/кг/q.o.d (через день)) в течение 3 месяцев, умерщвляли через 7 месяцев после воздействия IR (облучения) при дозе 15 Гр, и образцы легочной ткани окрашивали, используя вещество для окрашивания гематоксилин и эозин (H&E). Как показано на фиг.16, обработанные носителем легкие продемонстрировали нарушение нормальной структуры легких, включая утолщение альвеолярных перегородок и повышение уровней фибробластов. Для сравнения, GA-обработанные легкие показывали почти нормальную морфологию (фиг.16).
Чтобы оценить, насколько GA снижает ненормальное отложение коллагена в легких, образец легочной ткани окрашивали коллаген-связывающим красителем треххромный синий. На фиг.17 показано, что GA уменьшает отложение коллагена, вызванное воздействием IR, и улучшает морфологию легких.
Сокращение отложения коллагена был дополнительно проанализировано путем измерения уровней гидроксипролина, ключевого компонента коллагена. Фиг.18A показывает, что GA уменьшила уровни гидроксипролина в легких по сравнению с IR + контроль (чистый носитель) (P<0,05). Фиг.18B показывает, что GA снизила уровень TGFβ, про-фиброзного фактора.
Пример 8 - низкая токсичность
Данный пример показывает, что долговременное использование GA вызывает мало побочных эффектов, основываясь на наблюдениях активности, морфологии шерсти и массы тела (МТ) обработанных мышей. В частности, через 7,5 месяцев после воздействия IR при дозе 15 Гр, мыши, обработанные носителем, потеряли 6-7 граммов веса тела, в то время как в случае GA- или целебрекс-обработанных мышей наблюдаются менее серьезные потери МТ (фиг.19). Ни одна мышь не умерла во время лечения GA.
Пример 9 - влияние GA на эндокринную систему
Химическая структура GA схожа со структурой кортизола. Таким образом, данный пример исследует влияние долговременного применения GA на образование кортизола и появление побочных эффектов. Уровни в плазме ACTH (адренокортикотропный гормон) - гормона, высвобождающего кортизол, - были измерены с помощью ELISA через 6, 7, и 10 недель после лечения GA (40 мг/кг, qod (через день), перорально). Результаты (данные не приведены) показали, что хотя GA и уменьшала уровни АСТН на 60% на 6 неделе, уровни АСТН быстро вернулись к нормальному уровню через 7-10 недель. Для сравнения, лечение дексаметазоном вызвало 10-50- кратное снижение в уровнях АСТН на протяжении всех 7-10 недель.
Кроме того, уровни гормона роста (GH) в плазме измеряли с помощью ELISA через 6, 7 и 10 недель после лечения GA. Результаты показали, что как GA, так и дексаметазон увеличили уровень GH в плазме. Было отмечено, что воздействие IR нетипично снижает уровень гормона роста и, таким образом, GA-индуцированное увеличение уровня GH является полезным для восстановления пациента4.
Пример 10 - влияние лечения GLA на IR-индуцированный пневмонит
В сотрудничестве с онкологами-радиологами в First Affiliated Hospital при Fujian Medical School в Китае, таблетки GLA (полученные Minophagen Co. из Японии и доступные в аптеках в Китае) вводили пациентке, которая проходила второй курс IR-лечения рака легких. В ходе первого курса IR-лечения у пациентки развился тяжелый IR-индуцированный пневмонит через три месяца после лечения IR и выявились симптомы повреждения легких, включая лихорадку, кашель и затрудненное дыхание. Для контроля прогрессирования пневмонита она получила лечение дексаметазоном. В связи с возобновлением роста опухоли через 9 месяцев после ее первого лечения IR она прошла второй курс IR-лечения с предупреждением, что IR может ухудшить пневмонит.
В целях снижения IR-индуцированного повреждения легких GLA вводили в дозе по 150 мг в день (эквивалент GA около 85 мг в день), начиная с даты 2-го IR-лечения в течение 3 месяцев. Результат был крайне удивительным. Пациентка, пневмонит которой, как ожидалось, должен был ухудшиться, не имела каких-либо симптомов пневмонита или фиброза во время курса лечения GLA. Сравнение результатов КТ, взятые после 1-го и 2-го курсов IR-лечения также показали, что GLA значительно снизила плотность легких у пациента (фиг.20).
Следует понимать, что примеры и варианты осуществления настоящего изобретения, описанные в настоящем документе, предназначены только для иллюстративных целей, и что различные модификации или изменения будут очевидны квалифицированным специалистам в данной области техники в свете настоящего раскрытия. Такие модификации и изменения должны быть включены в концепцию и раскрытие данной заявки и должны подпадать под объем прилагаемой формулы изобретения.
Все ссылки, включая публикации, патентные заявки и патенты, приведенные в настоящем документе, включены в данное описание посредством ссылок в той же степени, как если бы каждая ссылка была индивидуально и конкретно указана, как включенная посредством ссылки и ее содержание было изложено в настоящем документе полностью.
В настоящем изобретении термин в единственном числе охватывает также и множественное число, если явно не указано иное и если это не противоречит контексту.
Использование в настоящем документе диапазонов значений предназначено только в качестве метода сокращения текста. Следует понимать, что такие диапазоны подразумевают индивидуальное указание на каждое отдельное значение, входящее в данный диапазон, если в явном виде не указано иное, и каждое такое отдельное значение считается включенным в описание, как если бы оно было индивидуально приведено в настоящем документе.
Все способы, описанные в настоящем изобретении, могут быть выполнены в любом подходящем порядке, если в настоящем документе не указано иное и если это не противоречит контексту.
Все примеры или иллюстративные термины (например, "такой как"), представленные в настоящем изобретении, предназначены только для лучшего разъяснения настоящего изобретения и не являются ограничением объема изобретения, если явно не указано иное. Никакой термин в описании не должен быть истолкован как указание, что какой-либо элемент имеет определяющее значение для практики настоящего изобретения, если это не оговорено в явном виде.
Описание в настоящем документе любого аспекта или варианта осуществления изобретения, использующее такие термины, как "содержащий", "имеющий" или "включающий" со ссылкой на какой-либо элемент или элементы, включает также и тот вариант изобретения, в котором используются термины "состоит из", "состоит в основном из" или "по существу содержит только" этот конкретный элемент или элементы, если явно не указано иное и если это не противоречит контексту (например, композиция, описанная в настоящем изобретении как содержащая определенный элемент, понимается также и как композиция, состоящая из этого элемента, если не указано иное и если это не противоречит контексту).
Источники информации
1. Tsoutsou, P.G. & Koukourakis, M.I. Radiation pneumonitis and fibrosis: mechanisms underlying its pathogenesis and implications for future research. Int J Radiat Oncol Biol Phys 66, 1281-1293 (2006).
2. Choi, N.C. Radioprotective effect of amifostine in radiation pneumonitis. Semin Oncol 30, 10-17(2003).
3. Ning, R., Tang, X., Conover, D. & Yu, R. Flat panel detector-based cone beam computed tomography with a circle-plus-two-arcs data acquisition orbit: preliminary phantom study. Medical Physics 30, 1694-1705 (2003).
4. Vazquez et al., Protective effect of enriched diet plus growth hormone administration on radiation-induced intestinal injury and on its evolutionary pattern in the rat, Digestive Diseases and Sciences, 44 (11) 2350-2058 (1999).

Группа изобретений относится к медицине, а именно к пульмонологии, и предназначена для предотвращения и/или лечения легочного повреждения, вызванного облучением. Для предотвращения, лечения или ослабления вызванного облучением легочного повреждения, в частности легочного фиброза, вводят субъекту, получающему дозу излучения и нуждающемуся в таком предотвращении, ослаблении или лечении, эффективное количество выделенного или по существу чистого соединения или его соли. Указанное соединение выбирают из группы, состоящей из глицирретиновой кислоты (GA), глицирризиновой кислоты (GLA), сложноэфирной, эфирной и/или амидной форм глицирретиновой кислоты (GA) и сложноэфирной и/или амидной форм глицирризиновой кислоты (GLA). Использование группы изобретений обеспечивает возможность предотвращения, лечения или ослабления вызванного облучением легочного повреждения, в частности легочного фиброза. 2 н. и 16 з.п. ф-лы, 44 ил., 1 табл., 10 пр.
1. Способ предотвращения, лечения или ослабления вызванного облучением легочного фиброза, включающий введение субъекту, получающему дозу излучения и нуждающемуся в таком предотвращении, ослаблении или лечении, эффективного количества выделенного или по существу чистого соединения или его соли, где указанное соединение выбрано из группы, состоящей из:
(A) глицирретиновой кислоты (GA);
(B) глицирризиновой кислоты (GLA);
(C) сложноэфирной, эфирной и/или амидной форм глицирретиновой кислоты (GA), представленной следующей структурой (Структурой С):
 ;
;
и
(D) сложноэфирной и/или амидной форм глицирризиновой кислоты (GLA), представленной следующей структурой (Структурой D):
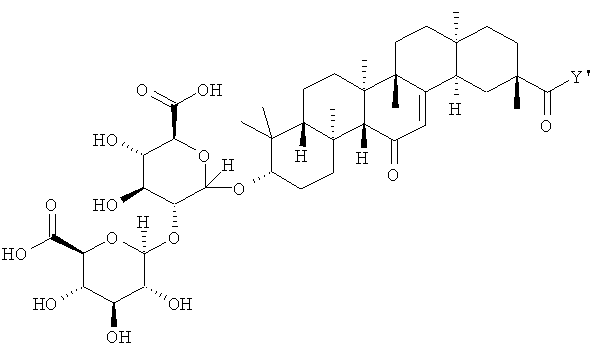 ;
;
где
X представляет собой любую группу, образующую эфирную или сложноэфирную связь с гидроксильным радикалом; и
Y и Y' каждый независимо представляет собой любую группу, образующую сложноэфирную или амидную связь с карбоксильной группой.
2. Способ по п. 1, в котором субъект представляет собой человека.
3. Способ по п. 1, в котором соединение представляет собой глицирретиновую кислоту (GA) или ее соль.
4. Способ по п. 1, в котором соединение представляет собой глицирризиновую кислоту (GLA) или ее соль.
5. Способ по п. 1, в котором Х выбран из группы, состоящей из
a) алкила, замещенного алкила, алкенила, замещенного алкенила, -COOH, ацила, алкилкарбонила, бензила, циклического алкила и циклического алкенила;
b) кислотной группы, выбранной из группы, состоящей из группы уксусной кислоты, карбоновой кислоты, аспарагиновой кислоты, муравьиной кислоты, лимонной кислоты, бензойной кислоты, гиппуровой кислоты, яблочной кислоты, муциновой кислоты, фосфорной кислоты, серной кислоты, глюконовой кислоты, малеиновой кислоты, янтарной кислоты, винной кислоты и молочной кислоты; и
c) углеводной группы.
6. Способ по п. 1, в котором каждый из Y и Y' представляет собой -NH2, алкиламино или алкокси.
7. Способ по п. 1, в котором субъект получает лучевую терапию для лечения рака.
8. Способ п. 1, в котором субъект случайно подвергается облучению.
9. Способ по п. 1, в котором снижается уровень медиатора воспаления в легочной ткани субъекта, где указанный медиатор воспаления выбран из группы, состоящей из SP-D, IL1α, TNFα, IL6, PF4, P-селектина, L-селектина, VCAM-1, лимфотактина и простагландина Е (PGE).
10. Способ по п. 1, в котором снижается содержание коллагена, фибронектина, протеогликана и/или гидроксипролина в легочной ткани субъекта.
11. Способ по п. 1, в котором снижается уровень TGFβ в ткани легкого субъекта.
12. Способ по п. 1, в котором снижается частота дыхания субъекта, снижается плотность легкого субъекта и/или увеличивается податливость легочной ткани субъекта.
13. Способ по п. 1, в котором соединение вводят до, во время или после того, как субъект получает дозу облучения.
14. Способ по п. 1, в котором субъект получает дозу облучения по крайней мере 1 Гр.
15. Способ предотвращения, лечения или ослабления вызванного облучением легочного повреждения, включающий введение субъекту, который получает дозу облучения и нуждается в таком предотвращении, ослаблении или лечении, эффективного количества выделенного или по существу чистого соединения или его соли, где указанное соединение выбрано из группы, состоящей из:
(A) глицирретиновой кислоты (GA);
(B) глицирризиновой кислоты (GLA);
(C) сложноэфирной, эфирной и/или амидной форм глицирретиновой кислоты (GA), представленной следующей структурой (Структура С):
 ; и
; и
(D) сложноэфирной и/или амидной форм глицирризиновой кислоты (GLA), представленной следующей структурой (Структура D):
 ;
;
где
X представляет собой любую группу, образующую эфирную или сложноэфирную связь с гидроксильным радикалом; и
Y и Y' каждый независимо представляет собой любую группу, образующую сложноэфирную или амидную связь с карбоксильной группой.
16. Способ по п. 15, в котором соединение представляет собой глицирретиновую кислоту (GA) или ее соль.
17. Способ по п. 15, в котором соединение представляет собой глицирризиновую кислоту (GLA) или ее соль.
18. Способ по п. 15, в котором субъект получает дозу облучения по крайней мере 1 Гр.
| Пулевой перфоратор последовательного действия | 1960 |
|
SU132156A1 |
| JP 2008222682 A, 25.09.2008 | |||
| US 4933169 A, 12.06.1990 | |||
| US 2009076032 A1, 19.03.2009 | |||
| XIAO-HUA LV et al | |||
| "Interventional Effect of Glycyrrhizin on Hydroxyproline, Hyaluronic Acid, and Laminin in Pulmonary Fibrosis Model Rats" | |||
| China Pharmacy, 2008, p.25 | |||
| MENEGAZZI M et al | |||
| "Glycyrrhizin attenuates the development of | |||
Авторы
Даты
2016-02-20—Публикация
2010-08-25—Подача