ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0001] Данное изобретение относится к многоцелевой, основанной на пострецепторном механизме фармацевтической композиции, изготовленной из исходных материалов гинзенозида Rg1 и Rb1, глицирризиновой кислоты и циклического аденозинмонофосфата жужуба (сАМР жужуба) для лечения депрессии. В частности, данное изобретение относится к фармацевтическому препарату для перорального применения или лечебному питанию для лечения депрессии, которые имеют определенные функции и компоненты, очевидные лечебные эффекты и высокую безопасность при длительном употреблении и которые лишены побочных эффектов, таких как тяжелая рвота.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002] Депрессия является распространенным заболеванием. Согласно статистике около 25% женщин населения земного шара испытывало депрессию в своей жизни и около 10% мужчин испытывало депрессию (ссылка на Modern Psychology, написанную Ch'un-Hsing Chang). Всемирная Организация Здравоохранения (ВОЗ) опубликовала "Заболеваемость депрессией в мире составляет приблизительно 11%. В настоящее время в мире насчитывается приблизительно 340 миллионов пациентов с психологической депрессией, и число растет. Исследование обнаружило, что депрессия будет расти, чтобы стать вторым по значению распространенным заболеванием в мире с настоящего времени на последующие 20 лет".
[0003] В настоящее время основные антидепрессивные лекарственные средства представляют собой прозак, паксил, золофт и т.д., которые относятся к селективным ингибиторам обратного захвата серотонина (SSRI), ингибиторам обратного захвата серотонина, норэпинефрина (SNRI) и ингибиторам обратного захвата норэпинефрина и допамина (NDRI), ингибирующим поглощение нейротрансмиттеров, таких как 5-гидрокситриптамин (5-НТ), норэпинефрин (NE) и допамин (DA). Механизм, посредством которого данные антидепрессивные лекарственные препараты функционируют, состоит в увеличении уровня нейротрансмиттеров 5-НТ человека для снижения и облегчения симптомов депрессии.
[0004] Однако продаваемые антидепрессивные лекарственные препараты имеют различные побочные эффекты с различной степенью тяжести, такие как повышенная интенсивность суицида, головная боль, головокружение, вертиго, бессонница, гиперсомния, шум в ушах, жажда, отвращение к пище, орексия, повышенная масса тела, повышенное давление крови, расстройство желудка, регургитация с тошнотой, рвота, диспепсия, диарея, запор, боль в ногах, кожная сыпь, озноб, судороги, гипергидроз, отек, половое влечение и импотенция и т.д. В последние годы лекарственные препараты для депрессии, такие как прозак и т.д., стали серьезной социальной проблемой. В 2004 году Управление по контролю качества пищевых продуктов и лекарственных средств (FDA) США дополнительно потребовало от фармацевтических компаний пересмотреть инструкции по медицинскому применению для четкого указания побочных эффектов и предостережения в инструкциях 32 важнейших антидепрессивных лекарственных препаратов на рынке и акцентировало внимание врачей и медицинских сестер на том, что данные лекарственные препараты могут повышать интенсивность суицида у детей и подростков. В 1996 году даже было обнаружено, что среди 32 антидепрессантов паксил является опасным и с 2001 был неоднократно отозван с рынка. В июне 2004 Генеральный прокурор штата Нью-Йорк обвинил компанию GlaxoSmithKline, Великобритания, в сокрытии обманным путем отчета об исследовании связи между паксилом и "повышенным риском суицидального поведения и тенденциями у подростков". В свете современного положения поиск нового поколения лекарственных препаратов с меньшими побочными эффектами и более ясно выраженными/сильными антидепрессивными качествами стал центром внимания всего фармацевтического мира.
[0005] В последние годы ученые в фармакологии сделали новый прорыв в исследовании механизма патогенеза депрессии, они обнаружили, что в дополнение к ингибированию обратного захвата нейротрансмиттеров, таких как 5-НТ, NE и DA, как стратегии для лечения депрессии, регуляция пострецепторного механизма также могла быть адаптирована для лечения депрессии. Кроме того, с тех пор как появилось лекарственное средство, регулирующее пострецепторный механизм, ролипрам (Rolipram), пострецепторный механизм стал горячей точкой исследования лечения депрессии в фармакологии. Ролипрам является ингибитором фосфодиэстеразы 4 (PDE4, пер., ФДЭ-4) и в клинических испытаниях было показано, что он обладает заметной антидепрессивной функцией; однако, поскольку ролипрам вызывает тяжелую рвоту, дальнейшее изучение ролипрама было полностью остановлено. Несмотря на эту неудачу, ролипрам открыл совершенно новое мышление "пострецепторного механизма в отношении антидепрессивного лекарственного средства".
[0006] Поэтому предпринята попытка авторами заявки рассмотреть вышеизложенную ситуацию, обнаруженную в известном уровне техники.
КРАТКОЕ ИЗЛОЖЕНИЕ ИЗОБРЕТЕНИЯ
[0007] Для преодоления недостаточности данной технологии целью данного изобретения является обеспечение многоцелевого фармацевтического препарата для перорального применения или лечебного питания, основанных на пострецепторном механизме действия, в виде изготовленных из исходных материалов гинзенозида Rg1 и Rb1, глицирризиновой кислоты и сАМР жужуба для лечения депрессии. В частности, обеспечивают новые технологические схемы, приводящие к определенным функциям и компонентам, очевидному лечебному действию и высокой безопасности при длительном применении без побочных эффектов, таких как тяжелая рвота и т.д.
[0008] Разрешающая схема фармацевтического препарата данного изобретения является результатом, предпринятым заявителем в соответствии с патологическими и фармакологическими теориями современной медицины для лечения депрессии. В частности, данное изобретение объединяет прогресс новейших исследований по антидепрессивным лекарственным средствам и пострецепторные механизмы путем применения стимулирующего действия гинзенозида на аденилатциклазу (АС) и сильного ингибирующего действия глицирризиновой кислоты (и глицирретиновой кислоты) на фосфодиэстеразу сАМР (CAPD). Антидепрессивная функция данного изобретения была подтверждена во множестве экспериментов на животных. Гинзенозид и глицирризиновая кислота (и глицирретиновая кислота) (пер., глицирретовая кислота) при соединении действуют синергетически для дополнительного роста применения и активности сАМР. Образовавшаяся концентрация и активность сАМР может (1) повышать синтез и высвобождение нейротрансмиттера (пер., нейромедиатора), такого как норэпинефрин и т.д., (2) повышать экспрессию нейротрофического фактора головного мозга (BDNF) и (3) ингибировать гиперактивность гипоталамо-гипофизарно-надпочечниковой оси (НРА) и секрецию глюкокортикоида для достижения существенной антидепрессивной функции. Кроме того, сАМР жужуба также может повышать уровень сАМР в человеке для индукции антидепрессивной функции. Следовое количество сАМР жужуба (приблизительно одну десятитысячную) из жужуба экстрагируют и очищают в виде экстракта жужуба, имеющего 1% сАМР жужуба для выполнения антиэкспериментальной функции депрессии в экспериментах на животных. Результат показывает, что экстракт жужуба, содержащий 1% сАМР жужуба, имеет существенную антиэкспериментальную функцию депрессии. Однако обычный экстракт жужуба (например, жужуба, экстрагированный в воде при нагревании, но концентрация в нем сАМР жужуба далее не повышается), хотя содержащий следовое количество сАМР жужуба не обладает заметной антиэкспериментальной функцией депрессии. С целью дополнительного повышения антидепрессивного эффекта данного изобретения, в котором сАМР жужуба, гинзенозид и глицирризиновую кислоту дополнительно объединяют для совместного действия. Женьшень, солодка и жужуба являются обычно используемым сырьем для фармацевтической промышленности и пищевыми продуктами в китайской медицине и были использованы в диетическом питательном лечебном питании в течение нескольких тысяч лет. В этой тысячелетней клинической истории и истории питания безопасность и эффективность комплексного использования женьшеня, солодки и жужуба были полностью доказаны. Исследование изобретателя и экспериментальные результаты показывают, что если данные три вида фармацевтического сырья только стандартно настаиваются и экстрагируются по отдельности для получения экстракта, то экстракт не обладает существенным антидепрессивным эффектом по сравнению с экстрактом современного антидепрессивного лекарственного средства для лечения депрессии. Причина в том, что в данном изобретении концентрации эффективных компонентов (таких как гинзенозид Rg1 и Rb1 и сАМР жужуба и т.д.) экстракта дополнительно повышают очисткой (такой как хроматография), и исходные материалы (такие как глицирризиновая кислота и глицирретиновая кислота и т.д.) добавляют к экстракту для получения лекарственного средства для лечения депрессии. Эксперименты на животных демонстрируют, что произведенное таким образом лекарственное средство имеет в значительной степени превосходящую антидепрессивную функцию по сравнению с предшествующими антидепрессивными лекарственными средствами. Дебрис (остатки) данных трех видов фармацевтического сырья после экстракции, хроматографии и очистки также собирают и анализируют высокоэффективной жидкостной хроматографией (ВЭЖХ) (HPLC). Хотя дебрис содержит следовое количество гинзенозида Rg1 и Rb1, глицирризиновой кислоты и сАМР жужуба, данный дебрис не обладает существенной антидепрессивной функцией по результатам экспериментов на животных. Важно, чтобы прием женьшеня, солодки и жужуба не произвел бы побочных эффектов, таких как тяжелая рвота и т.д.. Таким образом, автор изобретения представляет фармацевтический препарат для перорального применения или лечебное питание, произведенные из исходных материалов, в том числе гинзенозида Rg1 и Rb1, глицирризиновой кислоты и сАМР жужуба, с многоцелевым и пострецепторным механизмом для лечения депрессии. В частности, в дополнение к экстракции при нагревании в растворителе (таком как вода и этанол и т.д.) экстракт дополнительно очищают для повышения концентраций исходных материалов (гинзенозида Rg1 и Rb1 и сАМР жужуба) и к ним добавляют глицирризиновую кислоту и глицирретиновую кислоту. Новую технологическую схему создают для получения определенных функций и компонентов, очевидного лечебного действия, высокой безопасности при длительном применении и без стимулирования побочных эффектов, таких как тяжелая рвота и т.д., для преодоления недостаточности доступных в настоящее время антидепрессантов.
[0009] Сравнения мишени для антидепрессивного лекарственного средства и механизма действия фармацевтической композиции данного изобретения и ролипрама обеспечивают, как указано ниже.
2. Фосфорилирование синапсина и усиление высвобождения норэпинефрина; и
3. Ингибирование фосфодиэстеразы, снижение деградации сАМР и повышение использования сАМР для генерирования «downstream»-функции.
2. Фосфорилирование синапсина и усиление высвобождения норэпинефрина;
3. Ингибирование фосфодиэстеразы, снижение деградации сАМР и повышение использования сАМР для обнаружения функции;
4. Запуск АС, повышение концентрации и активности сАМР;
5. Повышение АТР для активации синтеза сАМР;
6. Активация бензолпропионовой кислоты гемоэнцефалическим барьером, активация синтеза NE и DA, и down-регуляция гипоталамо-гипофизарно-надпочечниковой системы (НРА axis); и
7. up-Регуляция экспрессии BDNF (пер., нейротрофического фактора головного мозга) и нейротрофина (NT-3) непосредственно в клетках головного мозга при анти-стрессовой реакции.
[0010] Различия между фармацевтической композицией данного изобретения и антидепрессивным лекарственным средством с пострецепторным механизмом (ролипрам) состоят в том, что антидепрессивная реакция достигается многоцелевым и пострецепторным механизмом и избегается побочный эффект, индуцированный ролипрамом (такой как тяжелая рвота).
[0011] Коэффициент преобразования глицирризиновой кислоты в глицирретиновую кислоту в человеческом теле составляет почти 100%, и глицирретиновая кислота вследствие своей более высокой липорастворимости, чем у глицирризиновой кислоты, может проникать в головной мозг через гемоэнцефалический барьер. Таким образом, ингибирование глицирризиновой кислотой CAPD (пер., фосфодиэстеразы сАМР) происходит путем трансформации глицирризиновой кислоты в глицирретиновую кислоту в теле. Таким образом, глицирризиновая кислота или глицирретиновая кислота могут быть исходным материалом для изготовления фармацевтической композиции данного изобретения.
[0012] В соответствии с одним аспектом данного изобретения обеспечивают фармацевтическую композицию с многоцелевым пострецепторным механизмом для лечения депрессии. Фармацевтическая композиция включает в себя: гинзенозид Rg1 и Rb1, производное глицирризиновой кислоты, будучи выбранным из группы, состоящей из глицирризиновой кислоты, глицирретиновой кислоты и их комбинации и сАМР жужуба.
[0013] Предпочтительно фармацевтическая композиция включает в себя 2~26 мас. частей гинзенозида, 3~48 мас. производного глицирризиновой кислоты и 0,002~0,5 мас. частей сАМР жужуба.
[0014] Предпочтительно фармацевтическая композиция включает в себя 4~13 мас. частей гинзенозида, 5~16 мас. частей производного глицирризиновой кислоты и 0,01~0,1 мас.частей сАМР жужуба.
[0015] Предпочтительно гинзенозид экстрагируют из женьшеня, производное глицирризиновой кислоты экстрагируют из солодки и сАМР жужуба экстрагируют из жужуба.
[0016] Предпочтительно жужуба экстрагируют для получения первичного экстракта, имеющего первичную концентрацию сАМР жужуба, первичный экстракт дополнительно экстрагируют для получения вторичного экстракта, имеющего вторичную концентрацию сАМР жужуба, вторичная концентрация сАМР жужуба является выше, чем первичная концентрация сАМР жужуба, и вторичный экстракт представляет собой исходный материал в фармацевтической композиции.
[0017] В соответствии с другим аспектом данного изобретения обеспечивают многоцелевую фармацевтическую композицию с пострецепторным действием для лечения депрессии. Фармацевтическая композиция включает в себя гинзенозид и производное глицирризиновой кислоты, будучи выбранным из группы, состоящей из глицирризиновой кислоты, глицирретиновой кислоты и их комбинации.
[0018] Предпочтительно гинзенозид включает в себя Rg1 и Rb1.
[0019] Предпочтительно фармацевтическая композиция включает в себя 2~26 мас. частей гинзенозида и 3~48 мас. частей производного глицирризиновой кислоты.
[0020] Предпочтительно фармацевтическая композиция включает в себя 4~13 мас. частей гинзенозида и 5~16 мас. частей производного глицирризиновой кислоты.
[0021] Предпочтительно гинзенозид очищают из женьшеня и производное глицирризиновой кислоты очищают из солодки.
[0022] Предпочтительно фармацевтическая композиция включает в себя, по меньшей мере, один фармакологически приемлемый носитель и добавку.
[0023] Предпочтительно фармацевтическая композиция имеет лекарственную форму, будучи одной, выбранной из группы, состоящей из таблетки, капсулы, порошка, драже, пудры, раствора, микрокапсулы, суспензии, эмульсии, частицы, капельного средства и шарика.
[0024] Предпочтительно фармацевтическую композицию производят в виде одной из лечебного питания и пищевой добавки.
[0025] В соответствии с другим аспектом данного изобретения обеспечивают способ получения фармацевтической композиции с многоцелевым пострецепторным механизмом для лечения депрессии. Фармацевтическая композиция включает в себя сАМР жужуба в виде исходного материала. Способ получения включает в себя стадии: (а) экстрагирования жужуба для получения первичного экстракта, имеющего первичную концентрацию сАМР жужуба; и (b) очистки первичного экстракта для получения вторичного экстракта, имеющего вторичную концентрацию сАМР жужуба, где вторичная концентрация сАМР жужуба является выше, чем первичная концентрация сАМР жужуба.
[0026] Предпочтительно стадию (b) проводят хроматографированием первичного экстракта с использованием макропористой смолы связанной с альдегидной группой (со связанной альдегидной группой).
[0027] Предпочтительно макропористая смола представляет собой OU-2.
[0028] Предпочтительно первичный экстракт дополнительно подвергают хроматографированию на макропористой смоле МЕ-2, связанной с альдегидной группой.
[0029] Фармацевтический препарат для перорального применения для лечения депрессии, описанный в описании и формуле данного изобретения, является основным содержанием цели данного изобретения. После опубликования данного изобретения любой специалист в данной области сможет продолжить нормальное повышение/снижение или заменить на другие эффективные компоненты медицины на основе лекарственных трав (такие как онджисапонин, сайкосапонин и кумарин солодки и т.д.), имеющие эффекты/функции, идентичные вышеуказанному лекарственному средству в соответствии с теорией китайской медицины или родственной теорией современной фармакологии. Замещение указанного нормального повышения/снижения медицины на основе лекарственных трав, имеющих аналогичный механизм, другим идентичным ингибитором CAPD, активатором АС или соответствующими эффективными компонентами относится к нормальным видам деятельности обычного специалиста в данной области. Таким образом, замещения находятся в области защиты данного изобретения.
[0030] Вышеуказанные цели и преимущества данного изобретения станут полностью очевидны обычному специалисту в данной области техники после рассмотрения нижеследующих подробных описаний и приводимых рисунков.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
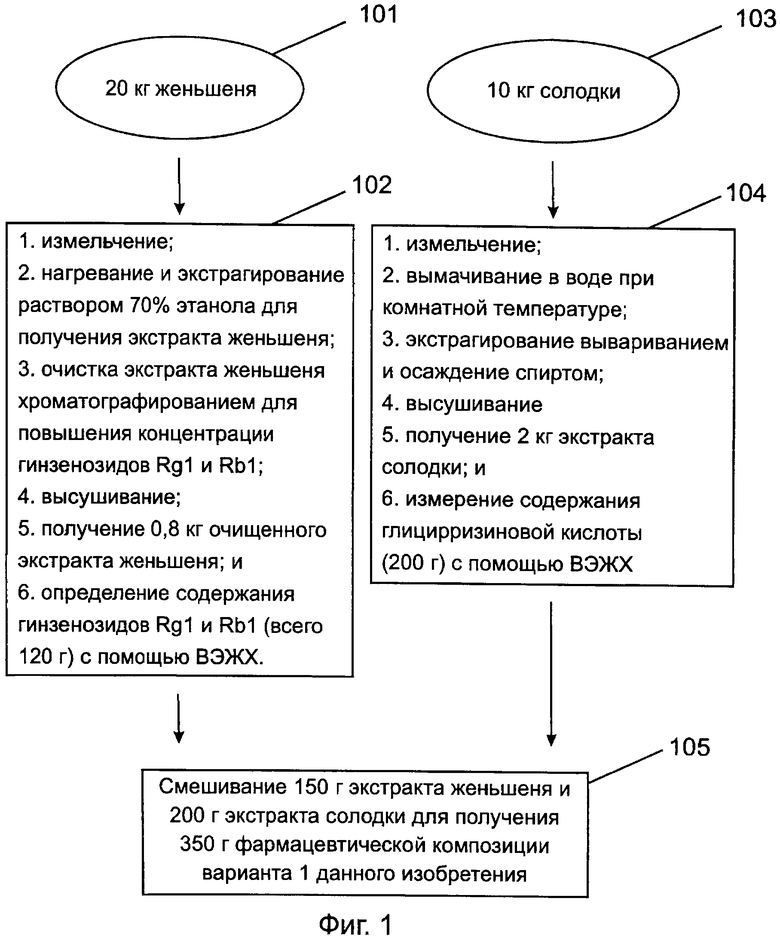
[0031] Фигура 1 представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с первым предпочтительным вариантом данного изобретения;
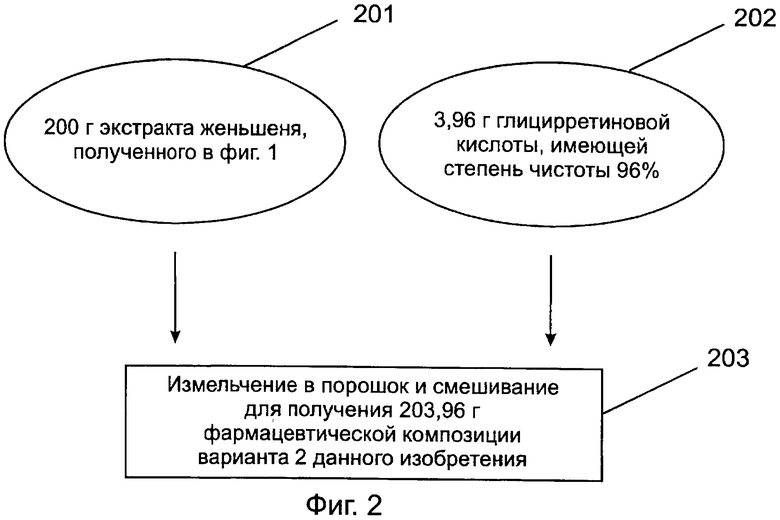
[0032] Фигура 2 представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии со вторым предпочтительным вариантом данного изобретения;
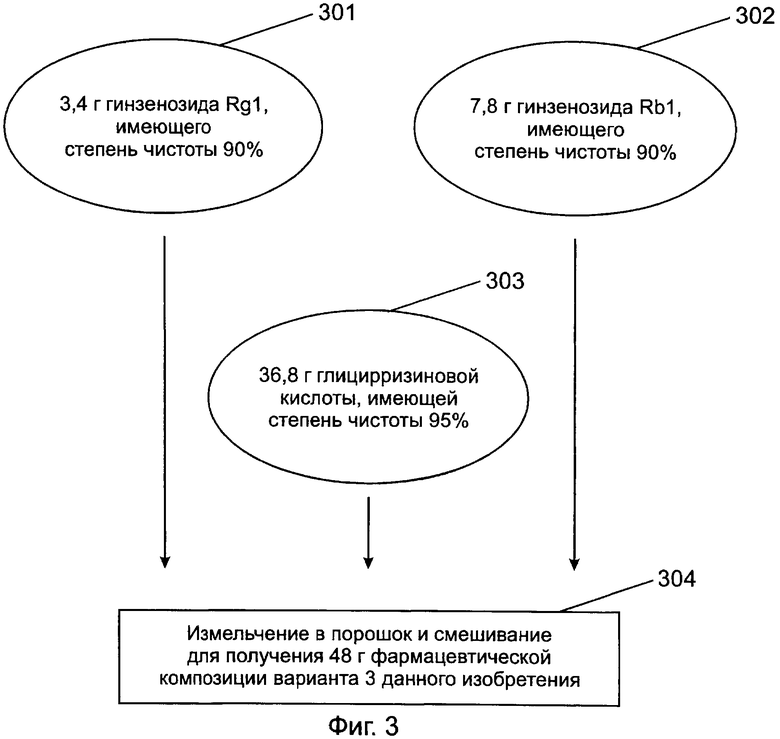
[0033] Фигура 3 представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с третьим предпочтительным вариантом данного изобретения;
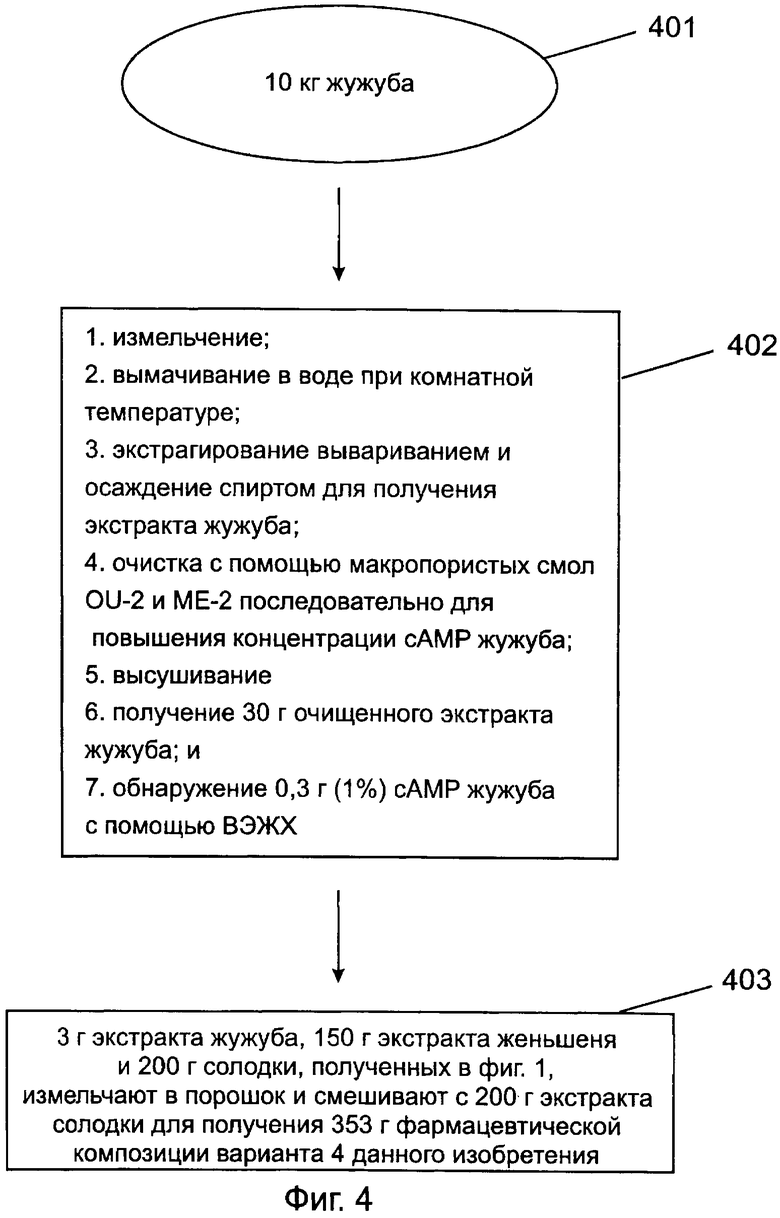
[0034] Фигура 4 представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с четвертым предпочтительным вариантом данного изобретения;
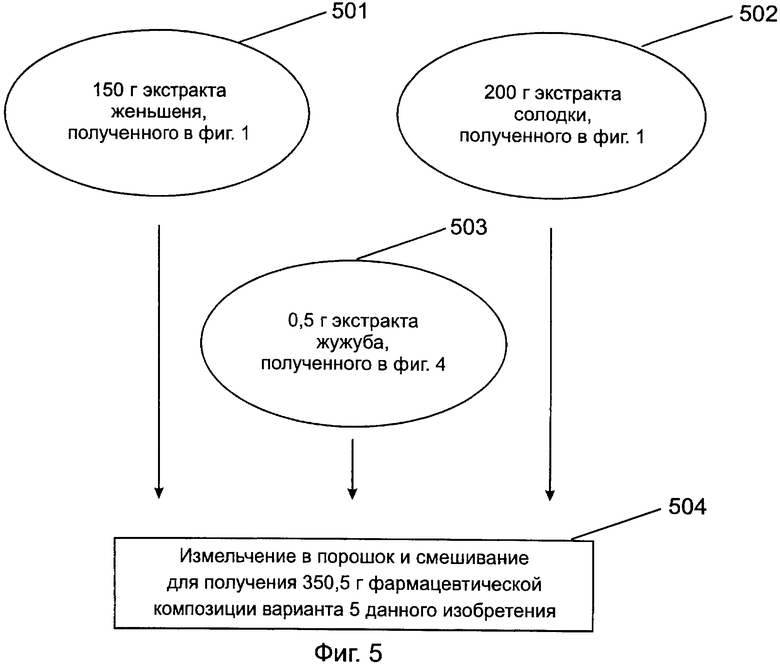
[0035] Фигура 5 представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с пятым предпочтительным вариантом данного изобретения; и
[0036] Фигура 6 представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с шестым предпочтительным вариантом данного изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО ВАРИАНТА
[0037] Данное изобретение теперь будет описано более конкретно со ссылкой на последующие варианты. Нужно отметить, что последующие описания предпочтительных вариантов данного изобретения представлены здесь только в целях иллюстрации и описания; не предполагается, что они будут исчерпывающими или будут ограничены точной раскрытой формой.
[0038] Для выполнения цели данного изобретения технологические схемы данного изобретения являются конкретно обеспеченными, как изложено ниже.
[0039] В данном изобретении раскрывают фармацевтическую композицию с многоцелевым и пострецепторным механизмом для лечения депрессии и фармацевтическую композицию изготавливают, в том числе, с помощью сырьевых материалов гинзенозида Rg1 и Rb1 и глицирризиновой кислоты (или глицирретиновой кислоты).
Пример 1:
[0040] Фармацевтическую композицию данного изобретения с многоцелевым и пострецепторным механизмом для лечения депрессии изготавливают, в том числе из исходных материалов гинзенозида Rg1 и Rb1 и глицирризиновой кислоты (или глицирретиновой кислоты).
Пример 2:
[0041] Фармацевтическую композицию данного изобретения изготавливают из исходных материалов, имеющих всего 2~26 мас. частей гинзенозида Rg1 и Rb1 и 3~48 мас. частей глицирризиновой кислоты (или глицирретиновой кислоты).
Пример 3:
[0042] Фармацевтическую композицию данного изобретения изготавливают в том числе из исходных материалов, имеющих всего 4~13 мас. частей гинзенозида Rg1 и Rb1 и 5~16 мас. частей глицирризиновой кислоты (или глицирретиновой кислоты).
Пример 4:
[0043] Фармацевтическую композицию данного изобретения с многоцелевым и пострецепторным механизмом для лечения депрессии изготавливают в том числе из исходных материалов гинзенозида Rg1 и Rb1, глицирризиновой кислоты (или глицирретиновой кислоты) и сАМР жужуба.
Пример 5:
[0044] Фармацевтическую композицию данного изобретения изготавливают в том числе из исходных материалов, имеющих всего 2~26 мас. частей гинзенозидов Rg1 и Rb1, 3~48 мас. частей глицирризиновой кислоты (или глицирретиновой кислоты) и 0,002~0,5 мас. частей сАМР жужуба.
Пример 6:
[0045] Фармацевтическую композицию данного изобретения изготавливают в том числе из исходных материалов, имеющих всего 4~13 мас.частей гинзенозида Rg1 и Rb1, 5~16 мас. частей глицирризиновой кислоты (или глицирретиновой кислоты) и 0,01~0,1 мас. частей сАМР жужуба.
Пример 7:
[0046] Фармацевтическая композиция данного изобретения может включать в себя фармакологически приемлемые носители или добавки. Фармацевтическая композиция может быть изготовлена в виде лекарственной формы, и лекарственная форма выбрана из одной из форм таблетки, капсулы, порошка, драже, пудры, раствора, микрокапсулы, суспензии, эмульсии, частицы, капельного средства, шарика и фармакологической фармацевтической лекарственной формы для перорального применения.
Пример 8:
[0047] Фармацевтическая композиция данного изобретения может быть изготовлена в виде лекарственных средств, лечебного питания и пищевых добавок для лечения депрессии.
[0048] Для достижения цели данного изобретения способы получения фармацевтической композиции описывают, как изложено ниже.
Способ 1:
[0049] Фармацевтическую композицию данного изобретения с многоцелевым и пострецепторным механизмом для лечения депрессии изготавливают из одного экстракта, имеющего гинзенозид Rg1 и Rb1, экстрагированного из женьшеня, и другого экстракта, имеющего глицирризиновую кислоту, экстрагированную из солодки, в виде исходных материалов. Кроме того, вышеуказанную фармацевтическую композицию изготавливают путем прямого использования подготовленных исходных материалов, имеющих гинзенозид Rg1 и Rb1 и глицирризиновую кислоту (или глицирретиновую кислоту).
Способ 2:
[0050] Фармацевтическую композицию данного изобретения изготавливают из исходных материалов, имеющих всего 2~26 мас. частей гинзенозида Rg1 и Rb1 и 3~48 мас. частей глицирризиновой кислоты (или глицирретиновой кислоты).
Способ 3:
[0051] Фармацевтическую композицию данного изобретения изготавливают в том числе из исходных материалов, имеющих всего 4~13 мас. частей гинзенозида Rg1 и Rb1 и 5~16 мас. частей глицирризиновой кислоты (или глицирретиновой кислоты).
Способ 4:
[0052] Фармацевтическую композицию данного изобретения с многоцелевым и пострецепторным механизмом для лечения депрессии изготавливают из одного экстракта, имеющего гинзенозид Rg1 и Rb1, экстрагированные из женьшеня, еще одного экстракта, имеющего глицирризиновую кислоту, экстрагированную из солодки, и другого экстракта, имеющего сАМР жужуба, экстрагированный из жужуба, в виде исходных материалов. Кроме того, вышеуказанную фармацевтическую композицию изготавливают путем прямого использования подготовленных исходных материалов, имеющих гинзенозид Rg1 и Rb1, глицирризиновую кислоту (или глицирретиновую кислоту) и сАМР жужуба.
Способ 5:
[0053] Фармацевтическую композицию данного изобретения изготавливают из исходных материалов, имеющих всего 2~26 мас. частей гинзенозида Rg1 и Rb1, 3~48 мас. частей глицирризиновой кислоты (или глицирретиновой кислоты) и 0,002~0,5 мас. частей сАМР жужуба.
Способ 6:
[0054] Фармацевтическую композицию данного изобретения изготавливают из исходных материалов, имеющих всего 4~13 мас. частей гинзенозида Rg1 и Rb1, 5~16 глицирризиновой кислоты (или глицирретиновой кислоты) и 0.01~0.1 мас. частей сАМР жужуба.
Способ 7:
[0055] Фармацевтическая композиция данного изобретения может включать в себя фармакологически приемлемые носители или добавки. Фармацевтическая композиция может быть изготовлена в виде лекарственной формы, и лекарственная форма выбрана из одной из форм таблетки, капсулы, порошка, драже, пудры, раствора, микрокапсулы, суспензии, эмульсии, частицы, капельного средства, шарика и фармакологической фармацевтической лекарственной формы для перорального применения.
Способ 8:
[0056] Фармацевтическая композиция данного изобретения может быть изготовлена из исходных материалов, описанных в данном изобретении в соответствии с фармацевтическими стандартами Надлежащей практики организации производства (GMP) в отношении лечебного питания.
ПРЕДПОЧТИТЕЛЬНЫЙ ВАРИАНТ ИЗОБРЕТЕНИЯ
[0057] Данное изобретение дополнительно иллюстрируют, как изложено ниже, комбинированием фигур и предпочтительных вариантов изобретения.
Вариант 1:
[0058] Пожалуйста, обратитесь к фиг.1, которая представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с первым предпочтительным вариантом данного изобретения. На фиг.1, после измельчения 20 кг женьшеня (стадия 101), разрушенный женьшень нагревают для экстрагирования раствором этанола 70% концентрации. Экстрагированный женьшень отделяют и колоночной хроматографией очищают и высушивают и получают 0,8 кг экстракта женьшеня, имеющего 120 г гинзенозида Rg1 и Rb1 (стадия 102). Затем после измельчения 10 кг солодки (стадия 103) измельченную солодку вымачивают при комнатной температуре в течение 12 часов.
Вымоченную солодку экстрагируют вывариванием и осаждением спиртом, концентрируют и высушивают и получают 2 кг экстракта солодки, имеющего 200 г глицирризиновой кислоты (стадия 104). После этого 150 г полученного экстракта женьшеня и 200 г полученного экстракта солодки измельчают в порошок и смешивают и получают 350 г фармацевтической композиции (содержащей 22,5 г гинзенозида Rg1 и Rb1 и 20 г глицирризиновой кислоты) варианта 1 данного изобретения (стадия 105).
Вариант 2:
[0059] Пожалуйста, обратитесь к фиг.2, которая представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии со вторым предпочтительным вариантом данного изобретения. На фиг.2, после измельчения в порошок и смешивания 3,96 г полученной глицирретиновой кислоты, имеющей 96% чистоту (стадия 202), и 200 г экстракта женьшеня, полученного в варианте 1 (стадия 201), получают 203,96 г фармацевтической композиции (содержащей 30 г гинзенозида Rg1 и Rb1 и 3,8 г глицирретиновой кислоты) варианта 2 данного изобретения (стадия 203).
Вариант 3:
[0060] Пожалуйста, обратитесь к фиг.3, которая представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с третьим предпочтительным вариантом данного изобретения. На фиг.3, после измельчения в порошок и смешивания 3,4 г полученного гинзенозида Rg1, имеющего 90% чистоту (стадия 301), 7,8 г полученного гинзенозида Rb1, имеющего 90% чистоту (стадия 302), и 36,8 г глицирризиновой кислоты, имеющей 90% чистоту (стадия 303), получают 48 г фармацевтической композиции (содержащей 10 г гинзенозида Rg1 и Rb1 и 35 г глицирризиновой кислоты) варианта 3 данного изобретения (стадия 304).
Вариант 4:
[0061] Пожалуйста, обратитесь к фиг.4, которая представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с четвертым предпочтительным вариантом данного изобретения. На фиг.4, 10 кг жужуба (стадия 401) измельчают и вымачивают в воде при комнатной температуре. Затем вымоченный жужуба экстрагируют вывариванием и осаждением в спирте для получения экстракта жужуба, который дополнительно абсорбируют и разделяют последовательно на макропористых смолах OU-2 и МЕ-2 и высушивают. Получают тридцать (30) г экстракта жужуба, содержащего 0,3 г сАМР жужуба, которые являются сырьем для получения фармацевтической композиции данного изобретения (стадия 402).
[0062] Затем, после измельчения в порошок 150 г экстракта женьшеня и 200 г экстракта солодки, полученных в варианте 1, и смешивания с 3 г вышеуказанного экстракта жужуба, получают 353 г фармацевтической композиции (содержащей 22,5 г гинзенозида Rg1 и Rb1, 20 г глицирризиновой кислоты и 0,03 г сАМР жужуба) варианта 4 данного изобретения (стадия 403).
Вариант 5:
[0063] Пожалуйста, обратитесь к фиг.5, которая представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с пятым предпочтительным вариантом данного изобретения. На фиг.5, после измельчения в порошок 150 г экстракта женьшеня (стадия 501) и 200 г экстракта солодки (стадия 502), полученных в варианте 1 соответственно, и смешивания с 0,5 г экстракта жужуба, полученного в варианте 4 (стадия 503), получают 350,5 г фармацевтической композиции (содержащей 22,5 г гинзенозида Rg1 и Rb1, 20 г глицирризиновой кислоты и 0,005 г сАМР жужуба) варианта 5 данного изобретения (стадия 504).
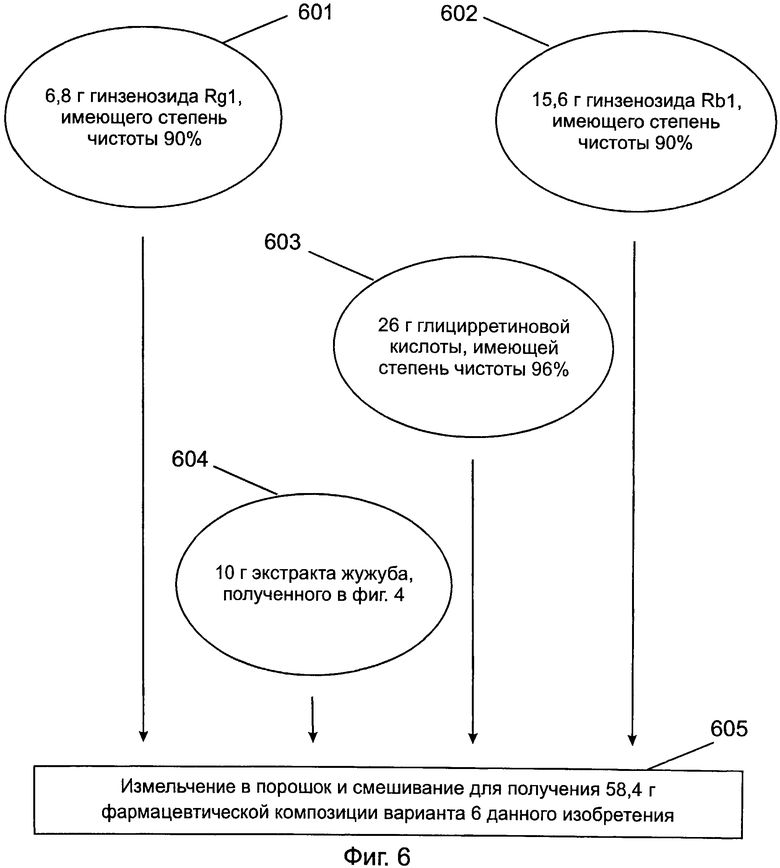
Вариант 6:
[0064] Пожалуйста, обратитесь к фиг.6, которая представляет собой блок-схему, показывающую способ получения фармацевтической композиции в соответствии с шестым предпочтительным вариантом данного изобретения. На фиг.6, после измельчения в порошок и смешивания 6,8 г полученного гинзенозида Rg1, имеющего 90% чистоту (стадия 601), 15,6 г полученного гинзенозида Rb1, имеющего 90% чистоту (стадия 602), 26 г глицирретиновой кислоты, имеющей 96% чистоту (стадия 603), и 10 г экстракта жужуба, полученного в варианте 4 (стадия 604), получают 58,4 г фармацевтической композиции (содержащей 20 г гинзенозида Rg1 и Rb1, 25 г глицирретиновой кислоты и 0,1 г сАМР жужуба) варианта 6 данного изобретения (стадия 605).
Эксперимент 1: Влияние варианта 1 в эксперименте подвешивания мыши за хвост
[0065] 1.1 Экспериментальные животные: мыши ICR, самцы, масса тела 22,0±2 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин.
[0066] 1.2 Экспериментальные лекарственные препараты: лекарственный препарат варианта 1 предоставлен компанией Beijing Wonner Biotech. Ltd. Co., и пароксетин (паксил) является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd.
[0067] 1.3 Экспериментальное оборудование: секундомер.
[0068] 1.4 Дизайны доз: 1. Высокая доза варианта 1 (80 мг/кг/день); 2. Средняя доза варианта 1 (40 мг/кг/день); и 3. Низкая доза варианта 1 (20 мг/кг/день).
[0069] 1.5 Экспериментальный метод и результат:
[0070] 1.5.1 Деление на группы и введение лекарственного средства: Мышей произвольно делят на группы и в каждой группе находится 10 мышей. 1. Высокая доза варианта 1 (80 мг/кг, перорально (P.O.), вводили в течение 7 дней); 2. Средняя доза варианта 1 (40 мг/кг, P.O., вводили в течение 7 дней); 3. Низкая доза варианта 1 (20 мг/кг, P.O., вводили в течение 7 дней); 4. Пароксетин (3 мг/кг, P.O., вводили в течение 7 дней); и 5. Физиологический раствор (P.O.). Через 1 час после последнего введения лекарственного средства выполняют эксперимент подвешивания мыши за хвост.
[0071] 1.5.2 Метод эксперимента: Хвост мыши (1 см до кончика хвоста) приклеивают липкой лентой к деревянной планке, на 5 см выше, чем платформа, и подвешивают на 6 минут. Регистрируют время неподвижности мыши в течение по меньшей мере 5 минут.
[0072] 1.5.3 Статистический расчет: Экспериментальные данные представляют в виде 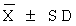 и результат эксперимента вычисляют в виде дисперсионного анализа (ANOVA) с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде дисперсионного анализа (ANOVA) с помощью пакета программ обработки статистических данных SPSS 11.5.
[0073] 1.5.4 Результат эксперимента: см. таблицу 1.
[0074] Вывод: В соответствии с вышеуказанным экспериментом может быть обнаружено, что все высокие и средние дозы варианта 1 данного изобретения и пароксетин все сокращают время неподвижности после подвешивания за хвост мыши, существенно отличающееся по сравнению с группой физиологического раствора (контроль). Таким образом, вариант 1 данного изобретения, как имеющий антиэкспериментальную функцию депрессии, может быть экстраполирован.
Эксперимент 2: Влияние варианта 1 в эксперименте Resetpine-индуцированного снижения температуры тела мышей
[0075] 2.1 Экспериментальные животные: мыши ICR, самцы, масса тела 22,0±2 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин.
[0076] 2.2 Экспериментальные лекарственные препараты: лекарственный препарат варианта 1 предоставлен компанией Beijing Wonner Biotech. Ltd. Co., пароксетин (паксил) является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd., и Resetpine является продуктом компании Guangdong BangMin Pharmaceutical Co., Ltd.
[0077] 2.3 Экспериментальное оборудование: Электронный термометр (модель: GM222) и секундомер.
[0078] 2.4 Структуры доз: 1. Высокая доза варианта 1 (80 мг/кг/день); 2. Средняя доза варианта 1 (40 мг/кг/день); и 3. Низкая доза варианта 1 (20 мг/кг/день).
[0079] 2.5 Экспериментальный метод и результат:
[0080] 2.5.1 Деление на группы и введение лекарственного средства: Мышей произвольно делят на группы, и в каждой группе находится 10 мышей. 1. Высокая доза варианта 1 (80 мг/кг, P.O., вводили в течение 7 дней); 2. Средняя доза варианта 1 (40 мг/кг, P.O., вводили в течение 7 дней); 3. Низкая доза варианта 1 (20 мг/кг, P.O., вводили в течение 7 дней); 4. Пароксетин (3 мг/кг, P.O., вводили в течение 7 дней); и 5. Физиологический раствор (P.O.).
[0081] 2.5.2 Экспериментальный метод: Через 1 час после последнего введения лекарственного средства на восьмой день определяют анальную температуру у мышей. Затем 2 мг Resetpine на килограмм массы тела дают интраперитонеальной инъекцией. Через 4 часа после инъецирования Resetpine еще раз определяют анальную температуру у мышей. Глубина и время введения термометра в анус мышей являются идентичными при каждом измерении температуры.
[0082] 2.5.3 Статистический расчет: Экспериментальные данные представляют в виде 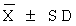 и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[0083] 2.5.4 Результат эксперимента: см. таблицу 2.
[0084] Вывод: В соответствии с вышеуказанным экспериментом может быть обнаружено, что высокая, средняя и низкая дозы варианта 1 данного изобретения и пароксетин все снижают пониженную температуру тела, индуцированную Resetpine, это означает, что те антиэкспериментальные функции депрессии данных фармацевтических препаратов могли быть связаны с их эффектами на содержание моноаминового нейротрансмиттера. Таким образом, вариант 1 данного изобретения, как имеющий антиэкспериментальную функцию депрессии, может быть экстраполирован.
Эксперимент 3: Влияние варианта 2 в эксперименте подвешивания мыши за хвост
[0085] 3.1 Экспериментальные животные: мыши ICR, самцы, масса тела 22,0±2 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин.
[0086] 3.2 Экспериментальные лекарственные препараты: лекарственный препарат варианта 2 предоставлен компанией Beijing Wonner Biotech. Ltd. Co., и пароксетин (паксил) является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd.
[0087] 3.3 Экспериментальное оборудование: секундомер.
[0088] 3.4 Дизайны доз: 1. Высокая доза варианта 2 (80 мг/кг/день); 2. Средняя доза варианта 2 (40 мг/кг/день); и 3. Низкая доза варианта 2 (20 мг/кг/день).
[0089] 3.5 Экспериментальный метод и результат:
[0090] 3.5.1 Деление на группы и введение лекарственного средства: Мышей произвольно делят на группы, и в каждой группе находится 10 мышей. 1. Высокая доза варианта 2 (80 мг/кг, перорально (P.O.), вводили в течение 7 дней); 2. Средняя доза варианта 2 (40 мг/кг, P.O., вводили в течение 7 дней); 3. Низкая доза варианта 2 (20 мг/кг, P.O., вводили в течение 7 дней); 4. Пароксетин (3 мг/кг, P.O., вводили в течение 7 дней); и 5. Физиологический раствор (P.O.). Через 1 час после последнего введения лекарственного средства выполняют эксперимент подвешивания мыши за хвост.
[0091] 3.5.2 Метод эксперимента: Хвост мыши (1 см до кончика хвоста) приклеивают липкой лентой к деревянной планке, на 5 см выше, чем платформа, и подвешивают на 6 минут. Регистрируют время неподвижности мыши в течение по меньшей мере 5 минут.
[0092] 3.5.3 Статистический расчет: Экспериментальные данные представляют в виде 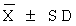 и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[0093] 3.5.4 Результат эксперимента: см. таблицу 3.
[0094] Вывод: В соответствии с вышеуказанным экспериментом может быть обнаружено, что средняя доза варианта 2 данного изобретения и пароксетин все сокращают время неподвижности после подвешивания за хвост мыши, существенно отличающееся по сравнению с группой физиологического раствора (контроль). Таким образом, вариант 2 данного изобретения, как имеющий антиэкспериментальную функцию депрессии, может быть экстраполирован.
Эксперимент 4: Влияние варианта 2 в эксперименте Resetpine-индуцированного снижения температуры тела мышей
[0095] 4.1 Экспериментальные животные: мыши ICR, самцы, масса тела 22,0±2 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин.
[0096] 4.2 Экспериментальные лекарственные препараты: лекарственный препарат варианта 2 предоставлен компанией Beijing Wonner Biotech. Ltd. Co., пароксетин (паксил) является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd. и Resetpine является продуктом компании Guangdong BangMin Pharmaceutical Co., Ltd.
[0097] 4.3 Экспериментальное оборудование: Электронный термометр (модель: GM222) и секундомер.
[0098] 4.4 Дизайны доз: 1. Высокая доза варианта 2 (80 мг/кг/день); 2. Средняя доза варианта 2 (40 мг/кг/день); и 3. Низкая доза варианта 2 (20 мг/кг/день).
[0099] 4.5 Экспериментальный метод и результат:
[00100] 4.5.1 Деление на группы и введение лекарственного средства: Мышей произвольно делят на группы, и в каждой группе находится 10 мышей. 1. Высокая доза варианта 2 (80 мг/кг, P.O., вводили в течение 7 дней); 2. Средняя доза варианта 2 (40 мг/кг, P.O., вводили в течение 7 дней); 3. Низкая доза варианта 2 (20 мг/кг, P.O., вводили в течение 7 дней); 4. Пароксетин (3 мг/кг, P.O., вводили в течение 7 дней); и 5. Физиологический раствор (P.O.).
[00101] 4.5.2 Экспериментальный метод: Через 1 час после последнего введения лекарственного средства на восьмой день определяют анальную температуру у мышей. Затем 2 мг Resetpine на килограмм массы тела дают интраперитонеальной инъекцией. Через 4 часа после инъецирования Resetpine еще раз определяют анальную температуру у мышей. Глубина и время введения термометра в анус мышей являются идентичными при каждом измерении температуры.
[00102] 4.5.3 Статистический расчет: Экспериментальные данные представляют в виде 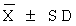 и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[00103] 4.5.4 Результат эксперимента: см. таблицу 4.
[00104] Вывод: В соответствии с вышеуказанным экспериментом может быть обнаружено, что средняя доза варианта 2 данного изобретения и парксетин все снижают пониженную температуру тела, индуцированную Resetpine, это означает, что антиэкспериментальные функции депрессии фармацевтических препаратов могли быть связаны с их эффектами на количество моноаминового нейротрансмиттера. Таким образом, вариант 2 данного изобретения, как имеющий антиэкспериментальную функцию депрессии, может быть экстраполирован.
Эксперимент 5: Влияние варианта 3 в эксперименте подвешивания мыши за хвост
[00105] 5.1 Экспериментальные животные: мыши ICR, самцы, масса тела 22,0±2 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин.
[00106] 5.2 Экспериментальные лекарственные препараты: лекарственный препарат варианта 3 предоставлен компанией Beijing Wonner Biotech. Ltd. Co., и пароксетин (паксил) является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd.
[00107] 5.3 Экспериментальное оборудование: секундомер.
[00108] 5.4 Дизайны доз: 1. Высокая доза варианта 3 (80 мг/кг/день); 2. Средняя доза варианта 3 (40 мг/кг/день); и 3. Низкая доза варианта 3 (20 мг/кг/день).
[00109] 5.5 Экспериментальный метод и результат:
[00110] 5.5.1 Деление на группы и введение лекарственного средства: Мышей произвольно делят на группы, и в каждой группе находится 10 мышей. 1. Высокая доза варианта 3 (80 мг/кг, P.O., вводили в течение 7 дней); 2. Средняя доза варианта 3 (40 мг/кг, P.O., вводили в течение 7 дней); 3. Низкая доза варианта 3 (20 мг/кг, P.O., вводили в течение 7 дней); 4. Пароксетин (3 мг/кг, P.O., вводили в течение 7 дней); и 5. Физиологический раствор (P.O.). Через 1 час после последнего введения лекарственного средства выполняют эксперимент подвешивания мыши за хвост.
[00111] 5.5.2 Метод эксперимента: Хвост мыши (1 см до кончика хвоста) приклеивают липкой лентой к деревянной планке, на 5 см выше, чем платформа, и подвешивают на 6 минут. Регистрируют время неподвижности мыши в течение по меньшей мере 5 минут.
[00112] 5.5.3 Статистический расчет: Экспериментальные данные представляют в виде 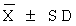 и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[00113] 5.5.4 Результат эксперимента: см. таблицу 5.
[00114] Вывод: В соответствии с вышеуказанным экспериментом может быть обнаружено, что высокие и средние дозы варианта 3 данного изобретения и пароксетин все могут сокращать время неподвижности после подвешивания за хвост мыши, существенно отличающееся от группы физиологического раствора (контроль). Таким образом, вариант 3 данного изобретения, как имеющий антиэкспериментальную функцию депрессии, может быть экстраполирован.
Эксперимент 6: Влияние варианта 3 в эксперименте Resetpine-индуцированного снижения температуры тела мышей
[00115] 6.1 Экспериментальные животные: мыши ICR, самцы, масса тела 22,0±2 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин.
[00116] 6.2 Экспериментальные лекарственные препараты: лекарственный препарат варианта 3 предоставлен компанией Beijing Wonner Biotech. Ltd. Co., пароксетин (паксил) является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd., и Resetpine является продуктом компании Guangdong BangMin Pharmaceutical Co., Ltd.
[00117] 6.3 Экспериментальное оборудование: Электронный термометр (модель: GM222) и секундомер.
[00118] 6.4 Дизайны доз: 1. Высокая доза варианта 3 (80 мг/кг/день); 2. Средняя доза варианта 3 (40 мг/кг/день); и 3. Низкая доза варианта 3 (20 мг/кг/день).
[00119] 6.5 Экспериментальный метод и результат:
[00120] 6.5.1 Деление на группы и введение лекарственного средства: Мышей произвольно делят на группы, и в каждой группе находится 10 мышей. 1. Высокая доза варианта 3 (80 мг/кг, P.O., вводили в течение 7 дней); 2. Средняя доза варианта 3 (40 мг/кг, P.O., вводили в течение 7 дней); 3. Низкая доза варианта 3 (20 мг/кг, P.O., вводили в течение 7 дней); 4. Пароксетин (3 мг/кг, P.O., вводили в течение 7 дней); и 5. Физиологический раствор (P.O.).
[00121] 6.5.2 Экспериментальный метод: Через 1 час после последнего введения лекарственного средства на восьмой день определяют анальную температуру у мышей. Затем 2 мг Resetpine на килограмм массы тела дают интраперитонеальной инъекцией. Через 4 часа после инъецирования Resetpine еще раз определяют анальную температуру у мышей. Глубина и время введения термометра в анус мышей являются идентичными при каждом измерении температуры.
[00122] 6.5.3 Статистический расчет: Экспериментальные данные представляют в виде 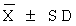 и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[00123] 6,5.4 Результат эксперимента: см. таблицу 6.
[00124] Вывод: В соответствии с вышеуказанным экспериментом может быть обнаружено, что высокая, средняя и низкая дозы варианта 3 данного изобретения и пароксетин все могут снижать пониженную температуру тела, индуцированную Resetpine, и это означает, что антиэкспериментальные функции депрессии фармацевтических препаратов могли быть связаны с их эффектами на количество моноаминового нейротрансмиттера. Таким образом, вариант 3 данного изобретения, как имеющий антиэкспериментальную функцию депрессии, может быть экстраполирован.
Эксперимент 7: Влияние варианта 4 в эксперименте поражения обонятельных луковиц у мышей
[00125] 7.1 Экспериментальные животные:
[00126] Модель поражения обонятельных луковиц: здоровые самцы крыс Wistar, вторичные, масса тела 330±20 г, приобретают у Beijing Vital River Experimental Animal Technology Ltd. Co. (номер сертификата качества: SCXK (JING) 2002-2003).
[00127] 7.2 Реагенты и лекарственные препараты: Лекарственный препарат Варианта 4 обеспечивается компанией Beijing Wonner Biotech Ltd. Co. (Lot: 060313), и пароксетин является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd. (Lot: 04050011). Вышеуказанные лекарственные препараты получают в 0,5% натрий-карбоксиметилцеллюлозе (CMC-Na) для введения в желудок. Бензилпенициллин натрия для инъекции представляет собой продукт North China Pharmaceutical Huasheng Co. Ltd. (Lot: S0511204), и стандарты норэпинефрин (NE) и 5-гидротриптамин (5-НТ) являются продуктами Sigma Co.. Другие реагенты являются поставленными.
[00128] 7.3 Оборудование: Самодельная камера для изучения поведения в открытом поле, ступенька через камеру, стереотаксический инструмент для крыс, высокоэффективная жидкостная хроматография (ВЭЖХ, HPLC) и 10-канальный помехоустойчивый счетчик для радиации (тип: DFM-96).
[00129] 7.4 Экспериментальные методы:
[00130] 7.4.1 Деление на группы и введение лекарственного средства: Крыс произвольно делят на 6 групп. 1. Ложная терапевтическая группа; 2. Модельная группа (контроль); 3. Высокая доза варианта 4 (60 мг/кг/день); 4. Средняя доза варианта 4 (30 мг/кг/день); 5. Низкая доза варианта 4 (15 мг/кг/день); и 6. Пароксетин (2 мг/кг/день). Тестируемые лекарственные средства и положительное лекарственное средство готовят с 0,5% CMC-Na для введения в желудок раз в день.
[00131] 7.4.2 Способ приготовления модели: Крыс анестезируют хлоралгидратом. После анестезии производят разрез по серединной линии родничка крысы от 1 см до лобного родничка до 1 см за лобным родничком и обнажают кости черепа. Открывают окна на черепе, имеющие диаметр 2 мм, от 8 мм перед лобным родничком и по 2 мм с двух сторон серединной линии. Специально изготовленный электрический паяльник вставляют перпендикулярно в череп на 2 секунды и разрушают обонятельную луковицу. Гемостатическую губку погружают в окна черепа и кожу зашивают. После терапии 40000 единиц бензилпенициллина натрия на килограмм массы тела, выполненной интраперитонеальной инъекцией в течение каждых четырех дней, дают тестируемое лекарственное средство постоянно в течение 24 дней.
[00132] 7.5 Показатели визуального наблюдения:
[00133] 7.5.1 Эксперимент поведения в камере открытое поле: Камеру для изучения поведения в открытом поле (1 м×1 м×0,4 м) конструируют с использованием светло-голубой фанеры и каркаса из алюминиевого сплава. Дно камеры делят на 25 квадратов (20 см×20 см для каждого квадрата), периметр представляет собой периферические квадраты (16 квадратов), а остальные представляют собой центральные квадраты (9 квадратов). Крысу помещают в центр центральных квадратов и число пересеченных крысой квадратов (число пересечений соседнего квадрата более чем тремя когтями) и число стоящих крыс (две передние конечности, оставляющие дно на более чем 1 см) подсчитывают/получают наблюдением в течение 3 минут.
[00134] 7.5.2 Эксперимент пассивного избегания (тест на перешагивание): Перегородку через камеру формируют между светлой камерой и темной камерой, и проход связывает светлую камеру и темную камеру для выхода и входа мыши. Решетку темной камеры соединяют с оборудованием для поражения электрическим током и там в промежутке устанавливают мобильную пластину. Если крыса входит в темную камеру, то крыса будет подвержена электрошоку. Во время обучения крысу помещают в светлую камеру и затем обратно в нору для адаптации в течение 5 минут. Затем пластину убирают и за крысой наблюдают в течение последующих 5 минут. Регистрируют время, когда крыса входит первый раз (электрошоковый латентный период), и это время является результатом изучения. Через 24 часа тест повторяют. Пластину удаляют и темную камеру подвергают воздействию электрическим током в течение 5 минут для установки времени, когда крыса входит в темную камеру первый раз. Это время представляет собой запись памяти.
[00135] 7.6 Статистический расчет: Экспериментальные данные представляют в виде 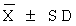 и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[00136] 7.7 Результаты экспериментов:
[00137] 7.7.1 Результат эксперимента поведения в камере открытое поле: см. таблицу 7.
[00138] 7.7.2 Результат теста перешагивания: см., таблицу 8.
[00139] Вывод: Результат эксперимента 7 демонстрирует, что высокая доза варианта 4 может заметно сокращать рост горизонтальных и вертикальных движений крыс, вызванных поражением обонятельных луковиц, и средняя доза варианта 4 также имеет заметное улучшенное действие на рост вертикального движения в модели поражения обонятельных луковиц у крыс. Кроме того, высокая и средняя дозы варианта 4 обладают заметными улучшенными эффектами на снижение функций обучения и памяти у крыс, вызываемые поражением обонятельных луковиц.
Эксперимент 8: Влияние варианта 4 в эксперименте непредсказуемых длительных стимулов у крыс
[00140] 8.1 Экспериментальные животные:
[00141] Модель непредсказуемых длительных стимулов: самцов крыс Health Wistar, вторичные, 240~270 г массы тела, приобретают у Beijing Vital River Experimental Animal Technology Ltd. Co. (Номер сертификата качества: SCXK (JING) 2002-2003).
[00142] 8.2 Реагенты и фармацевтические препараты: Фармацевтический препарат варианта 4 обеспечен Beijing Wonner Biotech Ltd. Co. (Lot: 060313) и пароксетин является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd. (Lot: 04050011). Вышеуказанные лекарственные препараты получают в 0,5% натрий-карбоксиметилцеллюлозе (CMC-Na) для введения в желудок. Бензилпенициллин натрия для инъекции представляет собой продукт North China Pharmaceutical Huasheng Co. Ltd. (Lot: S0511204), и стандарты норэпинефрин (NE) и 5-гидротриптамин (5-НТ) являются продуктами Sigma Co. Другие реагенты являются поставленными (купленными).
[00143] 8.3 Оборудование: Самодельная камера для изучения поведения в открытом поле, ступенька через камеру, стереотаксический инструмент для крыс, высокоэффективная жидкостная хроматография (ВЭЖХ, HPLC) и 10-канальный помехоустойчивый счетчик для радиации (тип: DFM-96).
[00144] 8.4 Методы эксперимента:
[00145] 8.4.1 Деление на группы и введение лекарственного средства: Крыс произвольно делят на 6 групп. 1. Ложная терапевтическая группа; 2. Модельная группа (контроль); 3. Высокая доза варианта 4 (60 мг/кг/день); 4. Средняя доза варианта 4 (30 мг/кг/день); 5. Низкая доза варианта 4 (15 мг/кг/день); и 6. Пароксетин (2 мг/кг/день). Тестируемые лекарственные средства и положительное лекарственное средство готовят с 0,5% CMC-Na для введения в желудок раз в день.
[00146] 8.4.2 Способ получения модели:
[00147] Модель непредсказуемых длительных стимулов: Крысы в контрольной группе едят и пьют нормально, и нет никаких выполненных стимулов. В других 5 группах одну крысу кормят в каждой клетке и крысу подвергают 24-дневным непредсказуемым стресс/стимулам, в том числе 24-часовая абсистенция 3 раза, 24-часов без питья 3 раза, 24-часовая влажная подстилка 3 раза (200 мл воды выливают в клетку крысы), освещение всю ночь 3 раза, плавание при 4°С в течение 5 минут 3 раза, нагревание при 45°С в духовке в течение 5 минут 3 раза, наложение зажимов на хвост крысы в течение 1 минуты 3 раза и 30-минутная высокоскоростное встряхивание в горизонтальном направлении 3 раза. Один стимул выполняют произвольно каждый день и всего 24 дня. Каждый стимул не может выполняться постоянно. Фармацевтический препарат подают в желудок крысы один раз в день и всего 24 дня.
[00148] 8.5 Показатели визуального наблюдения:
[00149] 8.5.1 Эксперимент изучения поведения в открытом поле: Такой же, как вышеуказанный.
[00150] 8.5.2 Эксперимент пассивного избегания: Такой же, как вышеуказанный.
[00151] 8.5.3 Плавание крыс в тесте принудительного плавания: Данный эксперимент продолжают в течение двух дней после последнего введения лекарственного средства. На первый день эксперимент выполняют предварительно в течение 15 минут. Температура воды в стеклянном резервуаре составляет 25°С, и глубина воды составляет 25 см. Через 24 часа формальный эксперимент продолжают. Через 1 час после введения лекарственного средства крысу помещают в резервуар и регистрируют время неподвижности крысы для последних 5 минут.
[00152] 8.5.4 Измерение массы тела: Сравнивают возрастающие значения до и после каждого эксперимента с животными.
[00153] 8.5.5 Объемный тест питья сахарозы: Сравнивают объемы поглощенной крысами сахарозы. Крысы в каждой группе пьют 1% сахарозу в течение 1 часа. Объемы питья определяют до стимула и после 3 недель стимула. После того как крыса находится в абсистенции и в воде в течение 14 часов, в клетку помещают 1% сахарозу и заменяют на обычную питьевую воду. Измеряют и регистрируют разницу веса бутылки до и после питья сахарозы крысой в течение 1 часа и высчитывают объем выпитой сахарозы для каждого момента времени. Сравнивают объем поглощенной сахарозы для каждого момента времени.
[00154] 8.5.6 ВЭЖХ-электрохимический тест: Измеряют количества норэпинефрина и 5-гидротриптамина в коре головного мозга крысы.
[00155] 8.6 Статистический расчет: Экспериментальные данные представляют в виде 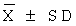 и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[00156] 8.7 Результаты эксперимента:
[00157] 8.7.1 Объемный тест питья сахарозы: см. таблицу 9.
[00158] 8.7.2 Результат увеличения массы тела крысы: см. таблицу 10.
[00159] 8.7.3 Время неподвижности крысы при принудительном плавании: см. таблицу 11.
[00160] 8.7.4 Результат эксперимента поведения в открытом поле: см. таблицу 12.
[00161] 8.7.5 Результат теста перешагивания: см. таблицу 13.
[00162] 8.7.6 Результат содержания NE и 5-НТ в коре головного мозга крысы: см. таблицу 14.
[00163] Вывод: Результаты эксперимента 8 показывают, как изложено ниже. Средняя и низкая дозы варианта 4 могут заметно повышать сниженный объем питья сахарозы и снижать массу тела в ответ на непредсказуемые длительные стресс/стимулы. Высокая, средняя и низкая дозы варианта 4 могут заметно повышать время неподвижности при принудительном плавании крыс. Высокая доза варианта 4 может заметно улучшать пониженные горизонтальные и вертикальные движения крыс, вызываемые непредсказуемыми длительными стресс/стимулами. Низкая доза варианта 4 также обладает заметной функцией улучшения пониженного вертикального движения крыс, вызываемого непредсказуемыми длительными стресс/стимулами. Низкая доза варианта 4 обладает функцией улучшения на сниженную способность к обучению крыс, вызываемую непредсказуемыми длительными стресс/стимулами. Высокая, средняя и низкая дозы варианта 4 все могут заметно повышать содержание NE и 5-НТ в коре головного мозга крысы.
Эксперимент 9: Влияние варианта 5 в эксперименте подвешивания мыши за хвост
[00164] 9.1 Экспериментальные лекарственные препараты: фармацевтический препарат варианта 5 предоставлен компанией Beijing Wonner Biotech. Ltd. Co. (опытный продукт накопления) и пароксетин является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd (Lot: 05070384). Вышеуказанные фармацевтические препараты готовят с физиологическим раствором для подачи в желудок.
[00165] 9.2 Экспериментальные животные: мыши ICR, самцы, масса тела 20,0±1 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин. Номер сертификата качества мышей представляет собой SCXK (JING) 2006-2008.
[00166] 9.3 Экспериментальное оборудование: Секундомер.
[00167] 9.4 Метод: Семьдесят (70) мышей произвольно делят на 5 групп: группа физиологический солевой раствор (NS), пароксетин (3 мг/кг/день), высокая доза варианта 5 (80 мг/кг/день), средняя доза варианта 5 (40 мг/кг/день) и низкая доза варианта 5 (20 мг/кг/день). Лекарственные препараты вводят в желудок мыши раз в день. Через 1 час после последнего введения лекарственного средства на восьмой день хвост мыши (1 см до кончика хвоста) приклеивают липкой лентой к горизонтальной опоре в открытой камере, и мышь находится в перевернутом висячем положении. Голова мыши находится приблизительно на 10 см ниже дна открытой камеры, и мышь находится в подвешенном состоянии в течение 6 минут. Регистрируют неподвижность мыши в течение последних 5 минут.
[00168] 9.5 Статистический расчет: Экспериментальные данные представляют в виде 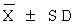 и результат эксперимента вычисляют в виде однонаправленного ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде однонаправленного ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[00169] 9.6 Результат эксперимента: Результат времени неподвижности в эксперименте подвешивания мыши за хвост: см. таблицу 15.
[00170] Вывод: Результат исследования демонстрирует, что высокая, средняя и низкая дозы варианта 5 и клинически эффективное антидепрессивное лекарственное средство, пароксетин все могут заметно снижать суммарное время неподвижности в эксперименте подвешивания мыши за хвост. Результат показывает, что вариант 5 данного изобретения имеет специфическую антиэкспериментальную депрессивную функцию.
Эксперимент 10: Влияние варианта 5 в эксперименте принудительного плавания мышей.
[00171] 10.1 Экспериментальные лекарственные препараты: фармацевтический препарат варианта 5 предоставлен компанией Beijing Wonner Biotech. Ltd. Co. (опытный продукт накопления), и пароксетин является продуктом компании Zhong Mei Tianjin Smith Kline phannaceuticals Co. Ltd (Lot: 05070384). Вышеуказанные фармацевтические препараты готовят с физиологическим раствором для подачи в желудок.
[00172] 10.2 Экспериментальные животные: мыши ICR, самцы, масса тела 20,0±1 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин. Номер сертификата качества мышей представляет собой SCXK (JING) 2006-2008.
[00173] 10.3 Экспериментальное оборудование: Секундомер.
[00174] 10.4 Метод эксперимента: Группы мышей и введение лекарственного средства являются такими же, как и в эксперименте с подвешиванием мыши за хвост. В каждой группе тестируемых мышей продолжают эксперимент через 1 час после введения лекарственного средства. Мышей учат плаванию в течение 15 минут перед экспериментом и на восьмой день. Эксперимент выполняют за 24 часа. Мышей помещают в стеклянный резервуар, имеющий глубину воды 10 см, диаметр 14 см при температуре воды 25°С. Регистрируют суммарное время неподвижности в течение последних 5 минут.
[00175] 10.5 Статистический расчет: Экспериментальные данные представляют в виде 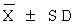 и результат эксперимента вычисляют в виде однонаправленного ANOVA
и результат эксперимента вычисляют в виде однонаправленного ANOVA
с помощью пакета программ обработки статистических данных SPSS 11.5.
[00176] 10.6 Результат эксперимента: Результат принудительного плавания мышей: см. таблицу 16.
[00177] Вывод: Результат эксперимента показывает, что высокая, средняя и низкая дозы варианта 5 и клинически эффективное антидепрессивное лекарственное средство пароксетин все могут заметно снижать суммарное время неподвижности мышей в тесте принудительного плавания. Результат показывает, что вариант 5 данного изобретения имеет специфическую антиэкспериментальную депрессивную функцию.
Эксперимент 11:
[00178] Девять (9) кг оставшегося дебриса женьшеня, 7 кг оставшегося дебриса солодки и 0,9 кг дебриса жужуба из процедур экстрагирования вариантов 1 и 4 собирают, высушивают, измельчают в порошок и хорошо перемешивают для получения смеси дебрисов, содержащей следовые количества гинзенозида Rg1 и Rb1, глицирризиновой кислоты и сАМР жужуба. Проводят контрольный эксперимент влияния дебриса в эксперименте подвешивания мыши за хвост.
[00179] 11.1 Экспериментальные животные: мыши ICR, самцы, масса тела 22,0±2 г, вторичные, предоставлены Научным департаментом экспериментальных животных Столичного медицинского университета, Пекин.
[00180] 11.2 Экспериментальные лекарственные препараты: Смесь дебрисов предоставлена компанией Beijing Wonner Biotech. Ltd. Со., и пароксетин (паксил) является продуктом компании Zhong Mei Tianjin Smith Kline pharmaceuticals Co. Ltd.
[00181] 11.3 Экспериментальное оборудование: Секундомер.
[00182] 11.4 Дизайны доз: 1. Высокая доза смеси дебрисов (160 мг/кг/день); 2. Средняя доза смеси дебрисов (80 мг/кг/день) и 3. Низкая доза смеси дебрисов (40 мг/кг/день).
[00183] 11.5 Экспериментальный метод и результат:
[00184] 11.5.1 Деление на группы и введение лекарственного средства: Мышей произвольным образом распределяют, по 10 мышей находится в каждой группе. 1. Высокая доза смеси дебрисов (160 мг/кг, P.O., вводят в течение 7 дней); 2. Средняя доза смеси дебрисов (80 мг/кг, P.O., вводят в течение 7 дней); 3. Низкая доза смеси дебрисов (40 мг/кг, P.O., вводят в течение 7 дней); 4. Пароксетин (3 мг/кг, P.O., вводят в течение 7 дней) и 5. Физиологический раствор (P.O.). Через 1 час после последнего введения лекарственного средства проводят эксперимент подвешивания мыши за хвост.
[00185] 11.5.2 Метод эксперимента: Хвост мыши (1 см до кончика хвоста) приклеивают липкой лентой к деревянной планке, на 5 см выше, чем платформа, и подвешивают на 6 минут. Регистрируют время неподвижности мыши в течение последних 5 минут.
[00186] 11.5.3 Статистический расчет: Экспериментальные данные
представляют в виде 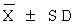 и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
и результат эксперимента вычисляют в виде ANOVA с помощью пакета программ обработки статистических данных SPSS 11.5.
[00187] 11.5.4 Результат эксперимента: см. таблицу 17.
[00188] Вывод: В соответствии с вышеприведенным экспериментом может быть обнаружено, что хотя высокая, средняя и низкая дозы смеси дебрисов могут сокращать время неподвижности подвешенной за хвост мыши, эти различия не имеют статистической значимости по сравнению с группой физиологического раствора (контроль). Таким образом, заключение, что смесь дебрисов может быть экстраполирована как лишенная антиэкспериментальной функции депрессии.
[00189] Область применения фармацевтической композиции для перорального применения данного изобретения для лечения депрессии состоит в том, что:
[00190] 1. Описанный фармацевтический препарат для перорального применения данного изобретения для лечения депрессии может включать в себя фармакологически приемлемые добавки;
[00191] 2. Описанный фармацевтический препарат для перорального применения данного изобретения для лечения депрессии может быть изготовлен в виде известных лекарственных форм, таких как порошок, капсула, таблетка и т.д.; и
[00192] 3. Описанный фармацевтический препарат для перорального применения данного изобретения для лечения депрессии может быть изготовлен в виде лечебного питания для лечения депрессии.
[00193] Тогда как изобретение было описано в контексте того, что, как полагают в настоящее время, является наиболее практичными и предпочтительными вариантами изобретения, нужно понимать, что изобретение не должно быть ограничено раскрытыми вариантами изобретения. Напротив, изобретение предназначено для покрытия различных модификаций и подобных композиций, включенных в рамки сущности и объема приложенной формулы изобретения, которые должны согласовываться с самой широкой интерпретацией, чтобы охватить все такие модификации и аналогичные структуры.
Изобретение относится к фармацевтической композиции, в частности к композиции (варианты) для лечения депрессии. Фармацевтическая композиция с многоцелевым пострецепторным механизмом для лечения депрессии, содержащая гинзенозиды Rg1 и Rb1; и производное глицирризиновой кислоты, будучи одним, выбранным из группы, состоящей из глицирризиновой кислоты, глицирретиновой кислоты и их комбинации, взятые в определенном количестве. Многоцелевая пострецепторная фармацевтическая композиция для лечения депрессии, содержащая гинзенозиды Rgl и Rbl; производное глицирризиновой кислоты, будучи одним, выбранным из группы, состоящей из глицирризиновой кислоты, глицирретиновой кислоты и их комбинации; и циклический аденозинмонофосфат жужуба (сАМР жужуба), взятые в определенном количестве. Вышеописанные фармацевтические композиции обладают существенной антидепрессивной эффективностью. 2 н.з. и 11 з.п. ф-лы, 17 табл., 6 ил., 8 пр.
1. Фармацевтическая композиция с многоцелевым пострецепторным механизмом для лечения депрессии, содержащая:
2~26 мас.ч. гинзенозидов Rg1 и Rb1; и
3~48 мас.ч. производного глицирризиновой кислоты, будучи одним, выбранным из группы, состоящей из глицирризиновой кислоты, глицирретиновой кислоты и их комбинации.
2. Фармацевтическая композиция по п.1, содержащая 4~13 мас.ч. гинзенозидов Rg1 и Rb1 и 5~16 мас.ч. производного глицирризиновой кислоты.
3. Фармацевтическая композиция по п.1, гинзенозиды Rg1 и Rb1 экстрагированы из женьшеня.
4. Фармацевтическая композиция по п.1, содержащая по меньшей мере один из фармакологически приемлемых носителей и добавку.
5. Фармацевтическая композиция по п.1, имеющая лекарственную форму, выбранную из группы, состоящей из таблетки, капсулы, порошка, драже, пудры, раствора, микрокапсулы, суспензии, эмульсии, частицы, капельного средства и шарика.
6. Фармацевтическая композиция по п.1, производимая в виде одного из лечебного питания и пищевой добавки.
7. Многоцелевая пострецепторная фармацевтическая композиция для лечения депрессии, содержащая:
2~26 мас.ч. гинзенозидов Rg1 и Rb1; и
3~48 мас.ч. производного глицирризиновой кислоты, будучи одним, выбранным из группы, состоящей из глицирризиновой кислоты, глицирретиновой кислоты и их комбинации; и
0,002~0,5 мас.ч. циклического аденозинмонофосфата жужуба (сАМР жужуба).
8. Фармацевтическая композиция по п.7, содержащая 4~13 мас.ч. гинзенозидов Rg1 и Rb1, 5~16 мас.ч. производного глицирризиновой кислоты и 0,01~0,1 мас.ч. сАМР жужуба.
9. Фармацевтическая композиция по п.7, где гинзенозиды Rg1 и Rb1 экстрагированы из женьшеня, производное глицерризиновой кислоты представляет собой экстракт солодки, содержащий глицирризиновую кислоту, и сАМР жужуба экстрагировано из жужуба.
10. Фармацевтическая композиция по п.7, где сАМР жужуба экстрагировано из жужуба для получения первичного экстракта, имеющего первичную концентрацию сАМР жужуба, первичный экстракт дополнительно экстрагируется для получения вторичного экстракта, имеющего вторичную концентрацию сАМР жужуба, причем вторичная концентрация сАМР жужуба выше, чем первичная концентрация сАМР жужуба, и вторичный экстракт является сырьем для фармацевтической композиции.
11. Фармацевтическая композиция по п.7, содержащая по меньшей мере один из фармакологически приемлемых носителей и добавку.
12. Фармацевтическая композиция по п.7, имеющая лекарственную форму, выбранную из группы, состоящей из таблетки, капсулы, порошка, драже, пудры, раствора, микрокапсулы, суспензии, эмульсии, частицы, капельного средства и шарика.
13. Фармацевтическая композиция по п.7, производимая в виде одного из лечебного питания и пищевой добавки.
| Устройство для разделения во времени запросов на запись и чтение данных | 1991 |
|
SU1836687A3 |
| Sarris J | |||
| Herbal medicines in the treatment of psychiatric disorders: a systematic review // Phytother | |||
| Res., 2007 Aug., 21 (8): 703-16 | |||
| CN 1948329 A, 18.04.2007 | |||
| Большова T.A | |||
| и др | |||
| Практическое руководство по хроматографическим методам анализа | |||
| - М., 1993, с.1-89. | |||
Авторы
Даты
2012-06-10—Публикация
2007-11-30—Подача