Изобретение относится к биотехнологии, в частности к промышленному способу получения биспецифических антител против CD3*CD19 формата «флексибоди» в клетках млекопитающих.
Биспецифические антитела (БАТ) против CD3*CD19 в настоящее время разрабатываются преимущественно для лечения злокачественных заболеваний В-клеток или истощения В-клеток, в том числе неходжкинской лимфомы (WO 2010037835, RU 2228202), В-клеточного лейкоза (RU 2008129080), детской острой лимфобластической лейкемии (WO 20100052013) и т.д.
Только в России ежегодно регистрируется более 20000 новых случаев неходжкинской лимфомы (НХЛ). Менее 5% пациентов выживает в течение 5 лет, при том, что заболеваемость неходжскинскими лимфомами в России составляет 4:100000 человек в год. Стандартом лечения НХЛ в России является сочетание Ритуксимаба и химиотерапевтических препаратов. Однако более 20% первично диагностированных пациентов и около 50% пациентов с рецидивирующей лимфомой перестают отвечать на терапию ритуксимабом, а у изначально отвечающих пациентов эффективность ритуксимаба падает при последующих курсах терапии в связи с развитием резистентности (Br. J. Haematol. 2011, v.155, 426-437).
Проведенные в настоящее время исследования (например, J Clin Oncol, 2011, 29: 2493-8; Cancer, 2010, 116: 5568-74; Science, 2008, 321: 974-7) дают все основания полагать, что лекарственные препараты на основе биспецифических антител против CD3*CD19 обещают стать более эффективными в лечении упомянутых выше заболеваний.
Повышенная эффективность объясняется тем, что БАТ выполняют функцию адаптеров, которые физически соединяют Т-клетки с опухолевыми клетками и запускают мощный сигнальный каскад рецепторного комплекса Т-клеток посредством связывания с инвариантным компонентом CD3 Т-клеточного рецептора. При этом второй (целевой) антиген-специфичный фрагмент узнает CD19. Т.е. БАТ может временно соединить Т-клетку и раковую клетку за счет одновременного связывания с CD3 и антигеном-мишенью. В этом случае происходят активация и пролиферация Т-клеток, образование цитолитического синапса с высвобождением цитотоксических гранул и секреции цитокинов. Направленный лизис раковых клеток включает в себя перфорацию мембраны клетки-мишени с участием перфорина и последующий апоптоз, индуцированный гранзимами. Следует отметить, что Т-клетки, активированные с помощью БАТ, распознают антигены на поверхности раковой клетки так же, как обычные моноспецифические антитела. Таким образом удается перенаправить цитотоксическую функцию Т-клеток против опухолевых клеток, причем активность БАТ наблюдается уже при относительно низких (пикомолярных) концентрациях. Связывание же БАТ только с Т-клеткой в отсутствии клетки-мишени не вызывает Т-клеточную активацию.
В настоящее время наиболее успешным в клинике БАТ является анти-CD19/анти-CD3 (CD19*CD3) препарат блинатумомаб (blinatumomab, МТ103; продукт фирмы Micromet), действие которого основано на мобилизации нестимулированных первичных Т-клеток против CD19+ клеток лимфомы. Блинатумомаб состоит из двух доменов: домена анти-CD19 scFv из гибридомы HD37 и домена анти-CD3 scFv из гибридомы TR66. Для получения антитела фрагмент ДНК VLCD19-VHCD19-VHCD3-VLCD3 экспрессируют в DHFR-отрицательных СНО клетках (патент RU 2228202).
Но блинатумомаб имеет относительно небольшие размеры и быстро элиминируется из кровотока. Поэтому для достижения стабильных концентраций препарата в крови используется непрерывное внутривенное введение препарата в течение 4-8 недель за один цикл, что достаточно тяжело для пациента. Для преодоления этих недостатков был предложен новый формат антител, называемый «флексибоди», технология создания которого подробно описана в патенте ЕР 1293514. Флексибоди состоит из двух пар вариабельных доменов VH и VL, которые размещены на одной полипептидной цепи и соединены линкерами, длина которых определяет возможность образования мультимерных структур: димеров, тримеров и тетрамеров. Наиболее перспективным представляется вариант, когда полученный полипептид представляет собой две нековалентно связанные молекулы биспецифического антитела. В этом случае флексибоди имеет молекулярную массу около 120 кДа и способно к дивалентному связыванию как с клеткой мишенью, так и с эффекторной Т-клеткой, что позволяет повысить терапевтический потенциал молекулы (Kratz F, Senter P, Kiprijanov S. Bispecific Antibodies and Immune Therapy Targeting в книге Drug Delivery in Oncology: From Basic Research to Cancer Therapy. Wiley, 2011) и увеличить время элиминирования из организма.
Такая молекула флексибоди имеет модульную структуру, в которой диабоди-модуль служит для димеризации одноцепочечной молекулы. Посредством спаривания комплементарных VH и VL доменов, находящихся на разных пептидных цепях, формируются функциональные Fv модули одинаковой специфичности, и получается стабильный нековалентный белковый димер.
Примеры биспецифических антител, известных из уровня техники (Blood, (ASH Annual Meeting Abstracts), 2009, 114:840), свидетельствуют о том, что эффективная терапевтическая концентрация препаратов, полученных на основе использования мультивалентных антител, существенно ниже по сравнению с классическими антительными противораковыми препаратами. Это способствует хорошей переносимости, возможности осуществления длительных курсов лечения и уменьшению риска побочных эффектов. Кроме того, объем и стоимость производства биспецифических антител ниже. Поэтому разработка нового метода получения таких антител позволит существенно сократить масштабы и расходы на производство препаратов на их основе и, что самое главное, сделать эти лекарства доступными для всех пациентов, нуждающихся в подобной терапии.
Известен способ получения биспецифических флексибоди против CD3*CD19 в клетках Е. Coli, штамм RV308 (патент ЕР 1293514), включающий следующие стадии: трансформация клеток плазмидами, содержащими целевые последовательности белка; культивирование в среде 2xYT, содержащей 50 мкг/мл ампициллина и 100 мМ глюкозу при 28 С до достижения значения оптической плотности 0,8 (при длине волны 600); после чего клетки центрифугируют, ресуспендируют в свежей среде и растят в присутствии ИПТГ при 20С в течение 18-20 часов. Для получения фракции растворимых перипластических белков бактериальный осадок отделяют, ресуспендируют в буфере, содержащем ЭДТА, HCl и сахарозу (рН 8,0). Указанную суспензию подвергают последовательным стадиям центрифугирования и диализа, и, наконец, концентрируют рекомбинантный продукт путем осаждения с сульфатом аммония, после чего проводят несколько стадий хроматографической очистки.
Однако данный способ недостаточно удобен для промышленного производства, поскольку разработан для получения небольших количеств антител, содержит большое число стадий. Кроме того при выделении белка, наработанного в E. Coli, требуется введение дополнительных этапов очистки из-за наличия больших количеств бактериальных эндотоксинов. В описании патента указана теоретическая возможность получения антител формата флексибоди в клетках млекопитающих, однако пример реализации такой возможности отсутствует.
Наиболее близким к заявленному способу является способ получения антитела против CD3*CD19 в клетках СНО, описанный в патенте RU 2228202 для получения антитела блинатомумаб. В данном способе антитело против CD19*CD3 получали из клеток яичника китайского хомячка (СНО), которые трансфецировали экспрессионным вектором (pEF-DHFR), кодирующим это антитело, а также дополнительно содержащим гексагистидиновую метку и FLAG-метку. Трансфекцию проводили при помощи электропорации. Затем клетки выращивали в бессывороточной среде в ферментере с системой полых волокон. Очистку супернатанта проводили с использованием последовательных стадий: аффинная хроматография на Ni-NTA-колонке, катионообменная хроматография, кобальтовая хелатная аффинная хроматография и на конечной стадии гель-фильтрация. Получали около 4 мг антитела на 1 л супернатанта. Столь низкие выходы (4 мг антитела на 1 л) негативно отражаются на себестоимости и сложности производства ГЛФ. К недостаткам прототипа также можно отнести наличие гексагистидиновой и FLAG-меток, которые являются дополнительными антигенными детерминантами, а следовательно, требуют подтверждения иммунной безопасности целевой молекулы.
Настоящее изобретение решает задачу конструирования плазмидной ДНК, содержащей последовательность биспецифического антитела против CD3*CD19 формата флексибоди и разработки способа промышленного получения биспецифических антител против CD3*CD19 формата флексибоди в клетках млекопитающих. Разработанный способ позволяет получить порядка 8-13 мг антитела на 1 л супернатанта, что примерно в 2-3 раза превышает выход прототипа.
Поставленная задача решается за счет конструирования рекомбинантной плазмидной ДНК pOG766 размером 10618 п.о., содержащей антитело Bis1, и рекомбинантной плазмидной ДНК pVS854 размером 10618 п.о., содержащей антитело Bis2, а также подбора оптимальных условий производственного процесса, позволяющих получать антитела в формате флексибоди в клетках млекопитающих со стабильно высоким выходом, достаточным для промышленного производства. Предлагаемый способ получения антител формата флексибоди против CD3*CD19 в клетках СНО также позволяет расширить арсенал способов получения таких антител.
Подробное описание изобретения
Для экспрессии в клетках СНО были сконструированы две последовательности антител Bis1 и Bis2 (Фиг.1 и Фиг.2). На основе указанных аминокислотных последовательностей была проведена оптимизация кодонного состава для экспрессии в СНО-клетках. Аналогичная работа была проведена для оптимизации последовательности блинатумомаба или МТ-103 (Фиг.3), который использовали в качестве контроля.
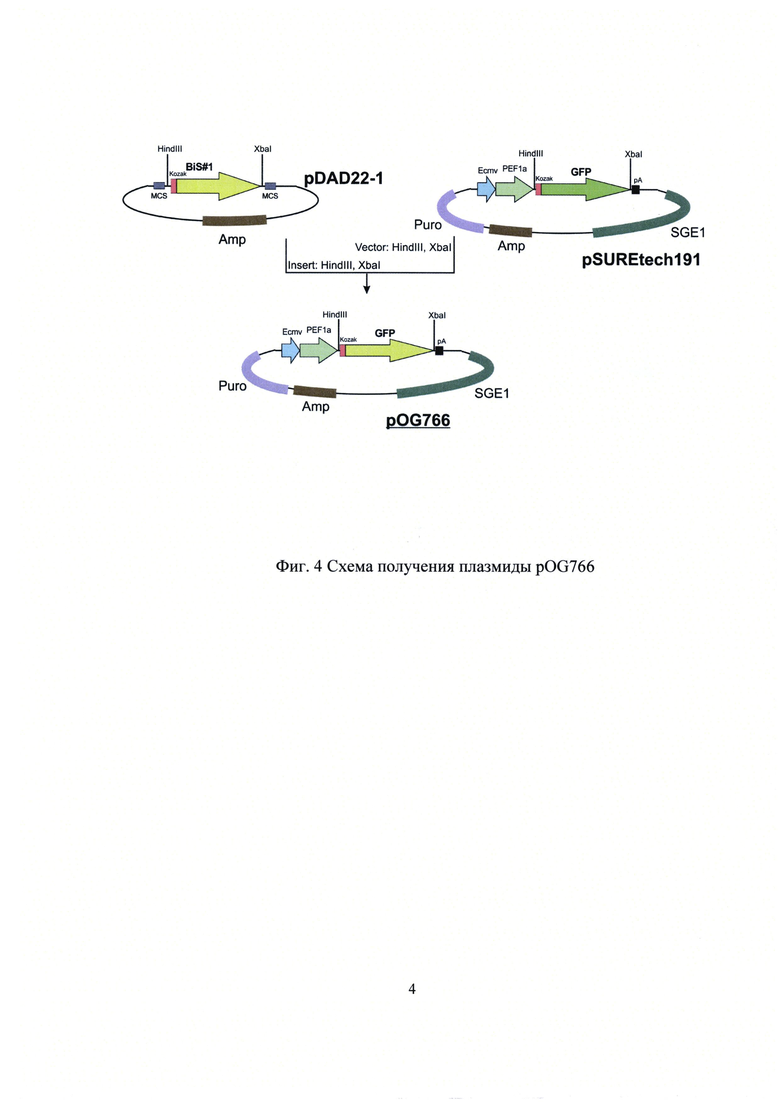
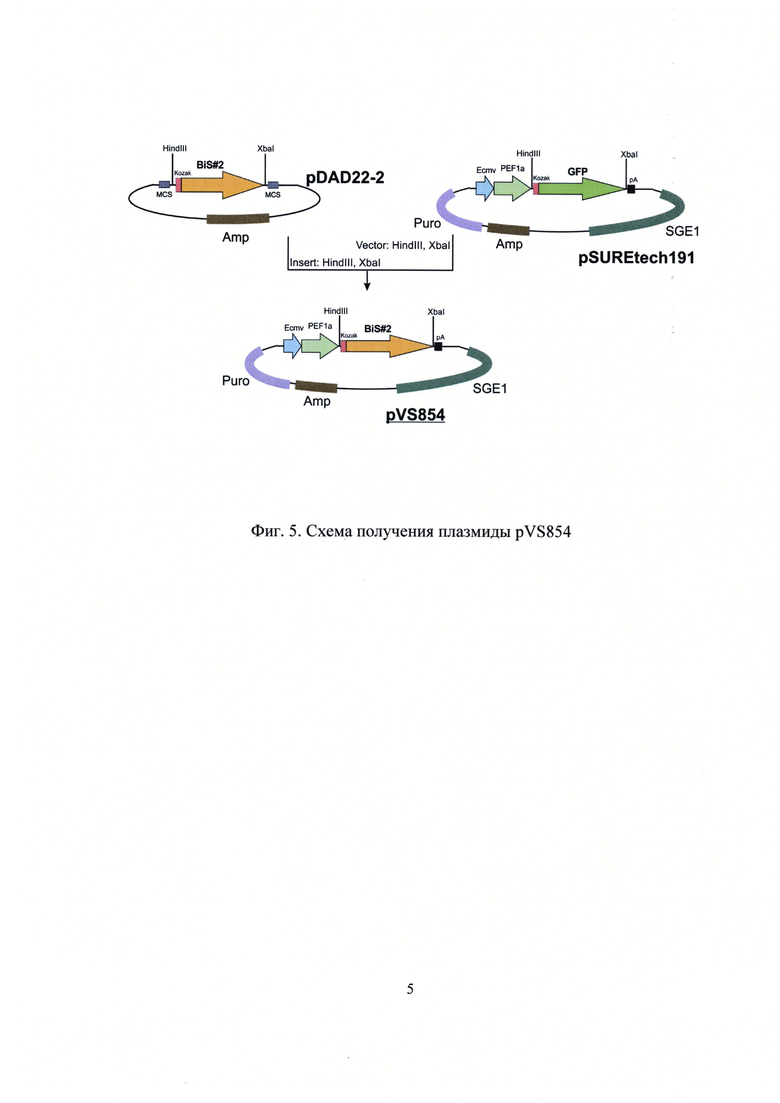
Векторы для трансфекции конструировали на основе коммерчески доступных плазмид pSUREtech191 (Selexis, Швейцария). Схемы конструирования приведены на Фиг.4 и Фиг.5.
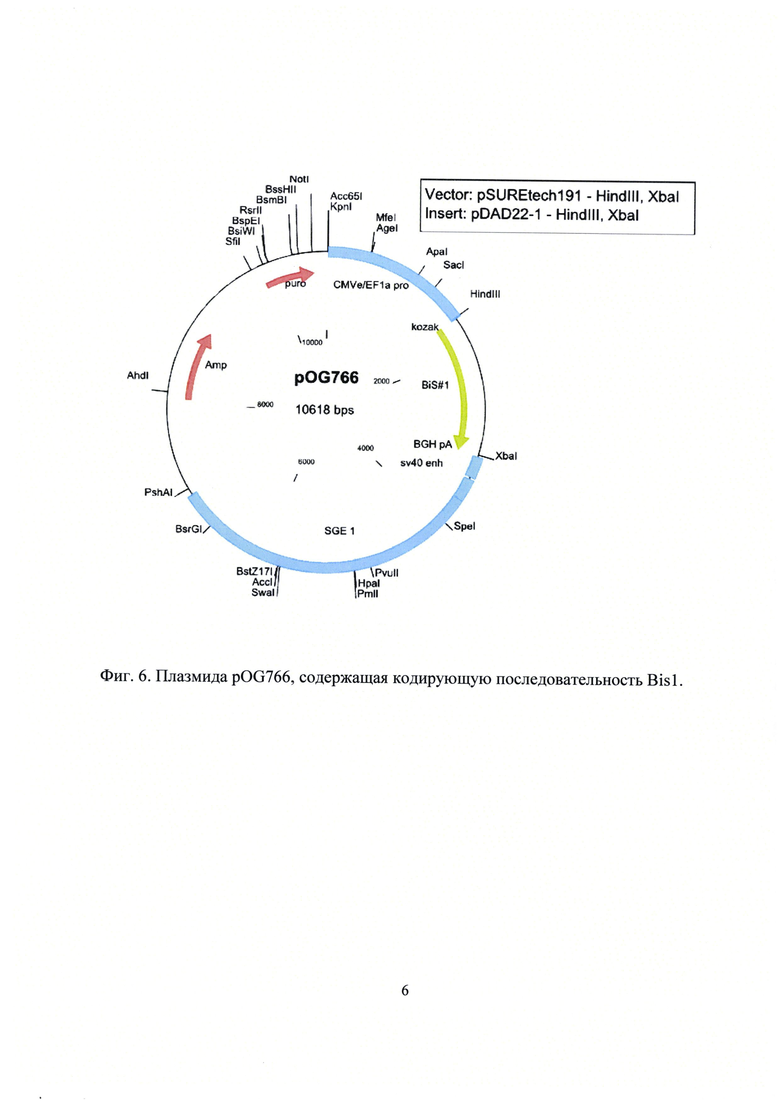
Плазмида pOG766 (Фиг.6), кодирующая полипептид Bis1, характеризуется следующими признаками:
- состоит из 10618 п.о.,
- имеет молекулярную массу 6,4 МДа,
- кодирует полипептид биспецифического антитела формата флексибоди против CD3*CD19, BiS1
- обеспечивает устойчивость клеток млекопитающих, трансфицированных указанной плазмидой, к пуромицину;
- содержит следующие элементы:
- CMVe/EFa pro - энхансер вируса CMV и промотор транскрипции гена фактора элонгации альфа,
- BGH pA - сигнал полиаденилирования бычьего гормона роста,
- sv40 enh - энхансер вируса SV40,
- SGE 1 - элемент прикрепления к ядерному матриксу,
- Amp - ген β-лактамазы,
- puro - ген устойчивости к пуромицину.
- содержит уникальные участки узнавания следующих эндонуклеаз рестрикции: KpnI (7 п.о.), AgeI (460 п.о.). SacI (1206 п.о.), HindIII (1590 п.о.), XbaI (3135 п.о.), SpeI (3932 п.о.), PvuII (4835 п.о.), AccI (5800 п.о.), BsrGI (6612 п.о.), AhdI (8138 п.о.), SfiI (9774 п.о.), BsiWI (9912 п.о.), NotI (10456 п.о.).
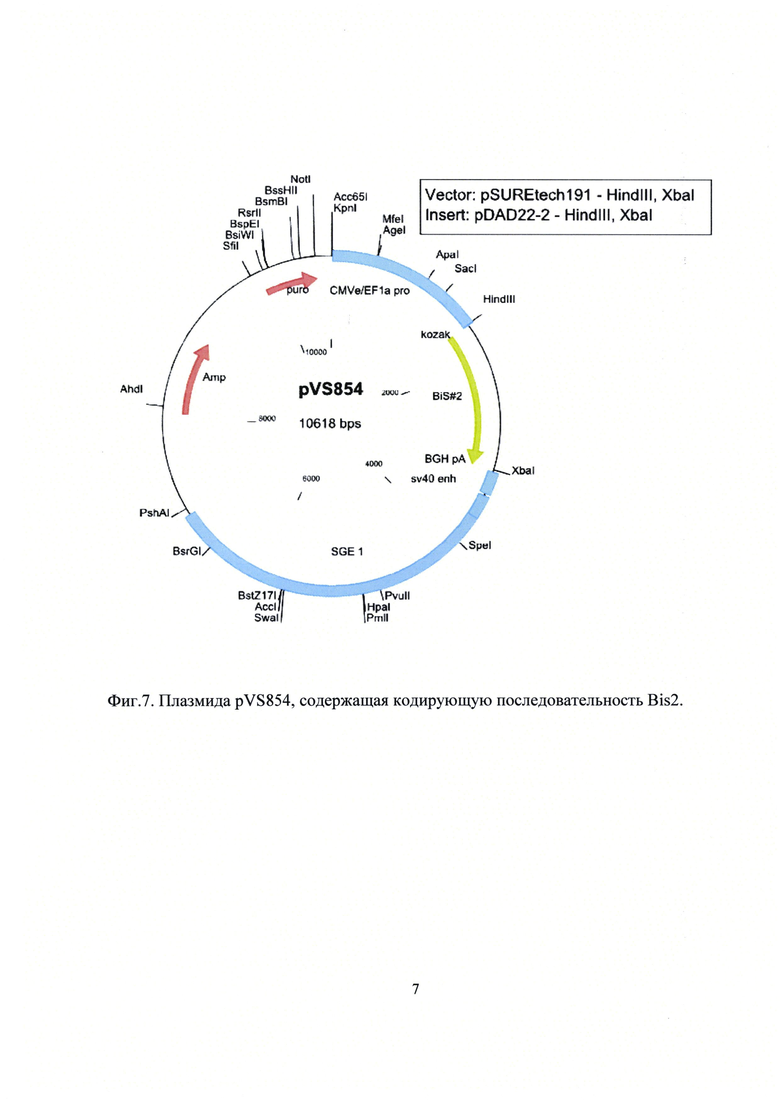
Плазмида pVS854 (фиг.7), кодирующая полипептид Bis2, характеризуется следующими признаками:
- состоит из 10618 п.о.,
- имеет молекулярную массу 6,4 МДа,
- кодирует полипептид биспецифического антитела формата флексибоди против CD3*CD19, BiS2,
- обеспечивает устойчивость клеток млекопитающих, трансфицированных указанной плазмидой, к пуромицину,
- содержит следующие элементы:
- CMVe/EFa pro - энхансер вируса CMV и промотор транскрипции гена фактора элонгации альфа,
- BGH pA - сигнал полиаденилирования бычьего гормона роста,
- sv40 enh - энхансер вируса SV40,
- SGE 1 - элемент прикрепления к ядерному матриксу,
- Amp - ген β-лактамазы,
- puro - ген устойчивости к пуромицину.
- содержит уникальные участки узнавания следующих эндонуклеаз рестрикции: KpnI (7 п.о.), AgeI (460 п.о.). SacI (1206 n.o.), HindIII (1590 n.o.), XbaI (3135 п.о.), SpeI (3932 п.о.), PvuII (4835 п.о.), AccI (5800 п.о.), BsrGI (6612 п.о.), AhdI (8138 п.о.), SfiI (9774 п.о.), BsiWI (9912 п.о.), NotI (10456 п.о.).
Трансфекцию проводили с использованием коммерчески доступного штамма СНО-М (Selexis). Выбор линии клеток обусловлен наличием оптимального профиля гликозилирования для синтеза человеческих белков, стабильностью, безопасностью и суспензионными условиями культивирования данной линии клеток, что является важнейшим параметром для производства терапевтических антител.
Заявители обнаружили, что в случае культивирования антител биореакторы позволяют достичь более высоких плотностей клеточных культур, чем при проведении процесса в шейкерных колбах, вероятно вследствие лучшего рН-статирования и оксигенации. Кроме того, выяснилось, что в данном случае использование перфузионного процесса культивации для получения продуцентов целевых белков Bis1 и Bis2, позволяет достичь существенно лучшей производительности, чем Batch процесс. На увеличение выхода белка в культурах продуцентов Bis1 и Bis2 также удалось повлиять за счет обогащения питательной среды оптимально сбалансированным набором фидерных добавок. В итоге помимо повышения продуктивности нам удалось достичь высокой технологичности процесса, в том числе обеспечить возможность линейного масштабирования, что является огромным преимуществом для промышленного производства.
При масштабировании процессов выделения и очистки целевого продукта была разработана схема, включающая аффинную стадию (CaptoL) с выходом продукта свыше 90%, катионообменную хроматографию на SP-сефарозе (выход более 80%), гель-фильтрацию на Сефакрил S300 (выход ~55%) и MonoQ (выход ~60%). Разработка и оптимизация данной схемы позволили выделить биспецифические антитела в количествах, достаточных для исследования их фармакокинетических и фармакологических свойств.
Описание чертежей
Фиг.1. Аминокислотная последовательность биспецифической конструкции
Bisi с ориентацией VL αCD19-L1-VH αCD19-L2-VH αCD3-L3-VL αCD3
Фиг.2. Аминокислотная последовательность биспецифической конструкции Bis2 с ориентацией VH αCD19-L1-VL αCD19-L2-VL αCD3-L3-VH αCD3
Фиг.3. Аминокислотная последовательность блинатумомаба (МТ103).
Фиг.4. Схема получения плазмиды pOG766, кодирующей антитело Bis12.
Фиг.5. Схема получения плазмиды pVS854, кодирующей антитело Bis2.
Фиг.6. Плазмида pOG766, содержащая кодирующую последовательность Bis1.
Фиг.7. Плазмида pVS854, содержащая кодирующую последовательность Bis2.
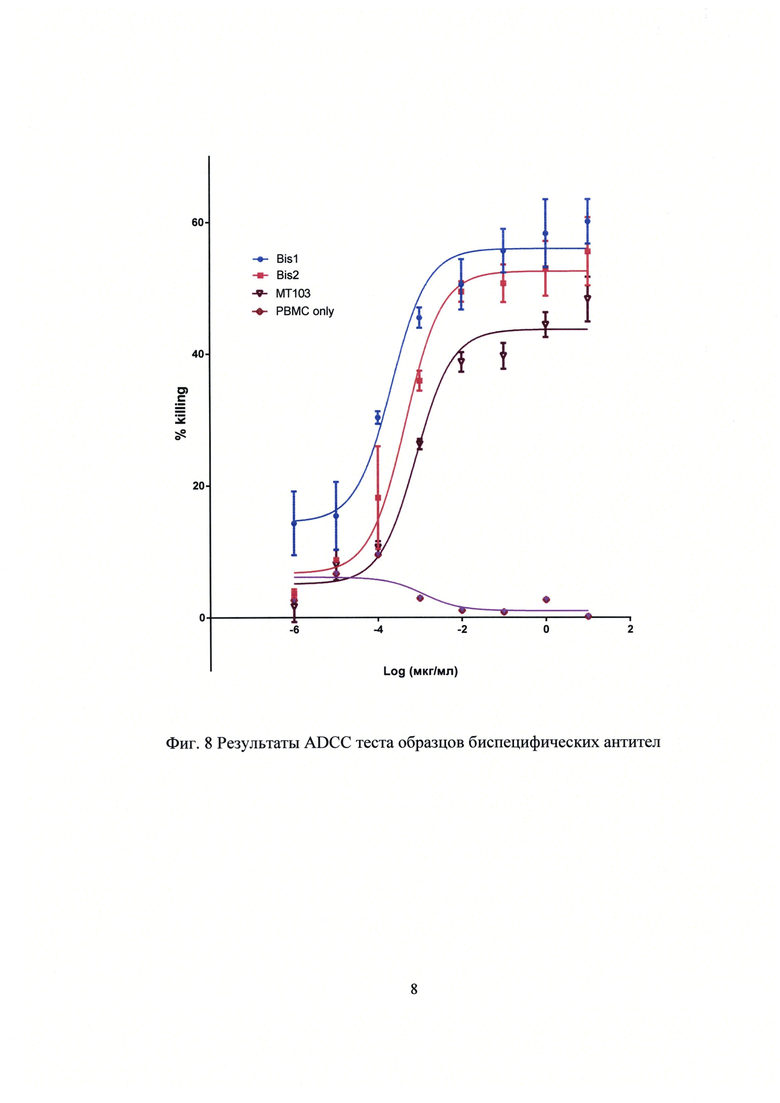
Фиг.8. Результаты сравнительного ADCC теста образцов биспецифических антител.
Описание последовательностей
SEQ ID №1 - аминокислотная последовательность антитела Bis1 против CD3*CD19 формата флексибоди с ориентацией VL αCD19-L1-VH αCD19-L2-VH αCD3-L3-VL αCD3
SEQ ID №2 - аминокислотная последовательность антитела Bis2 против CD3*CD19 формата флексибоди с ориентацией VH αCD19-L1-VL αCD19-L2-VL αCD3-L3-VH αCD3
SEQ ID №3 - оптимизированная нуклеотидная последовательность антитела Bis1 против CD3*CD19 формата флексибоди с ориентацией VL αCD19-L1-VH αCD19-L2-VL αCD3-L3-VH αCD3
SEQ ID №4 - оптимизированная нуклеотидная последовательность антитела Bis2 против CD3*CD19 формата флексибоди с ориентацией VH αCD19-L1-VL αCD19-L2-VL αCD3-L3-VH αCD3
Изобретение иллюстрируется приведенными ниже примерами.
Пример 1. Конструирование рекомбинантных плазмидных ДНК.
Для клонирования были выбраны коммерчески доступные вектора pSUREtech, содержащие генетический элемент SGE, способствующий усилению экспрессии в результате непосредственной близости целевого трансгена с высокоактивным ядерным транскрипционным комплексом.
Для удобства клонирования целевого гена в вектора pSUREtech на 5′ и 3′-концы последовательностей добавляли сайты рестрикции HindIII и XbaI, соответственно. На 5′-конце последовательности добавляли консенсус Kozak, на 3′-конце - 2 стоп-сигнала. На N-конце последовательности добавлен сигнальный пептид MGWSLILLFLVAVATRVLS. Плазмида pOG766 была получена в результате клонирования, в котором в качестве вектора использовалась pSUREtechl91, обработанная HindIII, XbaI; вставкой являлся фрагмент pDAD22-1 - HindIII, XbaI, содержащий кодирующую последовательность Bis1. Плазмида pVS854 была получена в результате клонирования, в котором в качестве вектора использовалась pSUREtechl91, обработанная HindIII, XbaI; вставкой являлся фрагмент pDAD22-2 - HindIII, XbaI, содержащий кодирующую последовательность Bis2. Схемы полученных экспрессионных векторов приведены на Фиг.6 и 7.
Полученные плазмиды были верифицированы рестрикционным картированием. После этого проводили последовательную двойную трансфекцию с последующей селекцией по резистентности к пуромицину с использованием стандартных методов.
Пример 2. Подбор оптимального способа культивирования.
Для выбора оптимального способа культивирования проводили сравнение продуктивности и ростовых характеристик культур клеток - продуцентов Bis1, Bis2 и МТ 103 в Batch-процессе и перфузионном процессе культивации.
Культивации проводились в шейкерных флаконах с рабочим объемом 50 мл, на базовой питательной среде SFM4 СНО; температура - 37°С, 5% СО2 в газовой фазе инкубатора.
Модельная перфузия осуществлялась ежедневным центрифугированием культур клеток (при 100 g), отъемом супернатанта и ресуспендированием клеток в таком же объеме свежей питательной среды.
Реализованы 6-дневные Batch культивирования и 12-дневные перфузионные культивирования. Эффективность процессов оценивали, учитывая:
- Количество клеток;
- Процент жизнеспособных клеток;
- Содержание целевых белков в культуральной жидкости методом ИФА.
Полученные в ходе экспериментов результаты представлены в Таблице 1, откуда видно, что применение перфузионного процесса позволило увеличить продуктивность в случае продуцентов МТ103 и Bis1 примерно в 5 раз, а в случае Bis2 - почти в 20 раз.
Пример 3. Изучение влияния фидерных добавок в базовую питательную среду на продуктивность клеточных культур в перфузионном процессе культивации.
Целью эксперимента было изучение влияния фидерных добавок Cell Boost на продуктивность культур клеток (продуценты Bis1, Bis2 и МТ 103) в перфузионном процессе культивации в среде SFM4 СНО.
В результате проведенной оптимизации продуктивности для целевых продуцентов наилучший результат был получен при использовании комбинации Cell Boost I (CB1) и Cell Boost 5 (CB5) в соотношении 1:1, с объемом добавки = 25% от объема питательной среды.
В Таблице 2 представлены сводные данные по отобранной комбинации CB1 и CB5 в соотношении 1:1, с объемом добавки 25% от объема питательной среды.
Культивация проводилась в шейкерных флаконах с рабочим объемом 50 мл, температура 37°С, 5% СО2 в газовой фазе инкубатора. Модельная перфузия осуществлялась:
- Ежедневным центрифугированием культур клеток (при 100 g);
- Отъемом супернатанта;
- Ресуспендированием клеток в таком же объеме свежей питательной среде.
Из Таблицы 2 видно, что обогащение питательной среды фидерными добавками привело к существенному (в 2-3 раза) увеличению выхода белка в культурах продуцентов Bis1 и Bis2. Однако тот же подход в случае продуцента МТ103 не дал никакого эффекта.
На основании проведенных экспериментов была разработана итоговая методика процесса культивирования, описанная в Примере 4.
Пример 4. Культивирование биспецифических антител против CD3*CD19 формата флексибоди в клетках СНО.
Этап 1 - Расконсервация культуры клеток
После размораживания ампулы с культурой клеток СНО-М продуцентом целевого белка (Bis1 или Bis2) осуществляется подсчет концентрации клеток и определяется их жизнеспособность. С целью наращивания клетки засеваются в культуральный флакон в ростовой среде SFM4CHO (HyClone).
Этап 2 - Получение посевного инокулума
После расконсервирования культуру-продуцент целевого белка (Bis1 или Bis2) пересевают до 100 мл объема среды SFM4CHO с плотностью культуры 5,1×106 кл/мл и жизнеспособностью 98%.
Этап 3 - Культивирование клеток в биореакторе Sartorius CultiBag 10L
Культуру, полученную на Этапе 2, пересевают в одноразовый биореактор Sartorius cultibag 10L perfusion с рабочим объемом 1 л, из них:
- 0,9 л ростовой среды SFM4CHO (Hyclone);
- 0,1 л клеточной суспензии;
- посевная концентрация клеток в реакторе 0,5×106 кл/мл, жизнеспособность 99%;
- температура культивирования 37°С;
- скорость качалки 16-25 кач./мин;
- угол наклона 6-8°;
- концентрация растворенного кислорода поддерживалась на уровне не менее 30% от насыщения путем обогащения подаваемой воздушной смеси кислородом и изменения параметров качания.
На 3-и сутки культивирования в биореакторе объем культуры клеток доводят до 5 л ростовой средой SFM4CHO, осуществляется подсчет концентрации клеток и определяется их жизнеспособность, которая должна быть выше 95%.
На 4-е сутки культивирования в биореакторе при жизнеспособности культуры выше 95% инициируется перфузия подобранной фидерной комбинацией СВ1-СВ5 с кратностью перфузии - 0,5 рабочего объема биореактора в сутки (2,5 л ростовой среды).
На 7-е сутки культивирования в биореакторе при жизнеспособности культуры выше 95% увеличивается кратность перфузии до 1 рабочего объема биореактора в сутки (5 л среды), температура культивирования снижается до 32°С;
До окончания культивирования (15-е сутки) кратность перфузии и состав питательной среды остаются неизменными.
Всего получено:
47,5 л перфузата с суммарным содержанием целевого белка Bis1=2117 мг.
36 л перфузата с суммарным содержанием 1134 мг Bis2.
Пример 5. Выделение и очистка биспецифического антитела против CD3*CD19 формата флексибоди.
Аффинная хроматография на Capto L (CV - 35 мл)
Буфер A: PBS, рН 7,2
Буфер В: PBS, 5% iso-Propanol, pH 7,2
Буфер С: 0,1 М Na-Citrate, pH 2,4
Колонка: HiScale 26/20
Перед нанесением культуральной жидкости сорбент уравновешивали 3-5 колоночными объемами (CV) буфера А. Все промывки осуществляли до выхода оптической плотности, проводимости и рН на базовые линии.
Перед нанесением на Capto L к исходной КЖ добавляли 5 М NaCl до концентрации 0,15 М и 0,5 М фосфат натрия, рН 7,4-7,6, до концентрации 0,02 М. Кондиционированную КЖ наносили на колонку со скоростью 170 см/ч. После нанесения сорбент промывали от не связавшихся белков буфером А (3-5 CV), буфером В (не менее 10 CV), затем буфером А (не менее 5 CV).
Фракцию, содержащую целевой белок, элюировали буфером С со скоростью 55 см/ч. В элюате измеряли рН (должен быть менее 3,0) и оставляли на 1 час при комнатной температуре для вирусной инактивации.
Регенерацию колонки осуществляли последовательными промывками 0,01 М NaOH (время контакта 15-30 минут), буфером А (до перехода рН в нейтральное значение) и консервировали 20% этанолом (3-4 CV).
Хроматография на SP-сефарозе (CV - 70 мл)
Буфер D: 0,04 М MES, 0,004 М EDTA, рН 5,5
Буфер Е: 0,02 М MES, 0,02 М NaCl, рН 5,8
Буфер F: 0,02 М MES, 0,02 М NaCl, 5% iso-Propanol, pH 5,8
Буфер G: 0,02 M MES, 0,5 M NaCl, pH 5,8
Колонка: ХК 50/20
Перед нанесением раствора белка колонки уравновешивали буфером Е. Элюат с предыдущей стадии после инкубации при комнатной температуре разводили буфером D в 3 раза и титровали 1 М раствором Tris до pH 5,8. Полученный раствор наносили на колонку со скоростью 60 см/ч. После нанесения колонку с SP-сефарозой промывали последовательно буферами Е (5 CV), F (10 CV) и E (5 CV).
Фракцию, содержащую целевой белок, элюировали буфером G со скоростью 15 см/ч. Регенерацию SP-сефарозы осуществляют последовательными промывками 2 М NaCl, водой, 0,5 M HCl, водой, 0,5 М NaOH, водой.
Гель-фильтрация на Sephacryl S300 (CV - 320 ml)
Буфер Н: PBS, pH 7.2
Колонка: HiPrep 26/60 (преднабитая)
Колонку предварительно уравновешивали буфером Н. Элюат с предыдущей стадии наносили частями (объем нанесения не более 15 мл) со скоростью 22 см/ч. Сбор основной фракции белка начинали через 160-163 мл после начала нанесения образца (в зависимости от высоты предыдущего пика олигомерных форм) и до падения значения оптической плотности до 30 mAu. Регенерацию колонки осуществляли последовательными промывками 0,5 М NaOH и водой.
Хроматография на Mono Q (CV - 1 мл)
Буфер I: 0,02 М Na-Phosphate, 0,02 М His, 1,8% Mannitol, 0,01% Tween 80, pH 7,3
Буфер J: 0,02 M Na-Phosphate, 0,02 M His, 1,8% Mannitol, 0,1% Triton X100, pH 7,3
Буфер K: 0,02 М Na-Phosphate, 0,02 M His, 1,8% Mannitol, 5% iso-Propanol, pH 7,3
Буфер L: 0,02 M Na-Phosphate, 0,02 M His, 1,8% Mannitol, 0,01% Tween 80, 0,5 M NaCl, pH 7,3
Колонка: HiTrap 5/50
Перед нанесением раствора белка колонку уравновешивали буфером I. Элюат с предыдущей стадии разводили буфером I в 3 раза. Наносили не более 15 мг по общему белку со скоростью 300 см/ч. После нанесения колонку с Mono Q промывали буфером I (10 CV), затем последовательно промывали буферами J, I, K по схеме (30 CV J, 10 CV I, 30 CV K, 10 CV I).
Фракцию, содержащую основную димерную форму целевого белка, элюировали градиентом со ступенью буфера L со скоростью 300 см/ч. Задавали градиент 0-100% буфера L за 60 CV, затем при достижении проводимости 16,75±0,05 mS/cm2 для BIS1 (14,55±0,05 mS/cm2 для BIS2) фиксировали соответствующее процентное содержание буфера L и собирали пик целевого белка с 35 mAu в начале и до 20% от максимума оптической плотности пика.
Регенерацию Mono Q осуществляют последовательными промывками 2 М NaCl, водой, 0,5М NaOH, водой, 0,1 M HCl, водой.
В результате проведения указанных стадий получали 582,7 мг Bis1 и 295,2 Bis2 из 47,5 л и 36 л супернатанта соответственно.
Пример 6. Изучение биологической активности биспецифических молекул в ADCC тесте
Для определения биологической активности полученных биспецифических антител был отработан и апробирован тест антитело-зависимой клеточно-опосредованной цитотоксичности (ADCC), позволяющий в условиях in vitro смоделировать процесс иммунной реакции, возникающий в живом организме. В результате этого анализа для антител определяется такой параметр, как концентрация активного вещества, при которой наблюдается половинный биологический эффект, что является качественной характеристикой антителоподобных структур, специфичных к рецепторам клеток
С целью изучения биологической активности биспецифических молекул Bis1, Bis2 и МТ103 использовали мононуклеарную фракцию крови человека.
Подготовка эффекторных РВМС клеток человека.
Для выделения мононуклеарной фракции из 50 мл донорской крови, проводили очистку от тромбоцитов и эритроцитов путем градиентного центрифугирования в фиколле 1,077. Клеточную массу разводили в 50 мл фосфатного буфера и наносили в пробирки по 10 мл, наслаивая на 5 мл предварительно нанесенного фиколла. После 20-минутного центрифугирования при 2500 об/мин отбирали фракцию клеток из моноцитарного кольца. Клетки дважды промывали средой RPMI1640 с 10% FBS с последующим осаждением в результате 5-минутного центрифугирования при 1600 об/мин при +4С. После ресуспендирования в 10 мл среды осадки каждой пробирки объединяли, затем подсчитывали количество РВМС.
Подготовка таргетных клеток RAji (CD19+).
Клетки растили в среде DMEM/F12 с 10% ЭТС и глютамином. Перед экспериментом подсчитывали концентрацию целевых клеток. При проведении анализа подготавливается соответствующее количество планшетов с таргетными клетками Raji, из расчета 15 тыс. клеток на лунку. Для этого клетки промывали дважды в PBS, с последующим ресуспендированием осадка в среде RPMI1640. После чего к клеткам добавляли краситель кальцеин AM с последующей 30-минутной инкубатцией в CO2 шейк-инкубаторе. Клетки отмывали от красителя с последующей сменой среды на среду с пробеницидом, предотвращающим выход метаболизированного красителя из клеток через транспортные системы.
Готовили 10-кратные разведения образцов биспецификов антител исходя из того, что конечная концентрация должна быть от 10 мкг/мл до 0,000001 мкг. В планшеты с таргетными клетками (Raji) вносили эффекторные клетки человека (РВМС) и разведенные образцы биспецификов. После 3-часового инкубирования в условии 5% CO2 в контрольные лунки (максимальное значение киллинга клеток) добавляли 20 мкл 9% водного раствора Тритона X100 и проводили анализ данных при помощи планшетного флюороскана (флюоресценцию 488 нм возб., 518 нм йен.).
Полученный результат, обсчитанный с помощью пакета GraphPad Prizm, также представлен на Фиг.8 и в Таблице 3.
На основе полученных данных видно, что образцы Bis1 и Bis2 достигают наибольшего максимума киллинга клеток (% max) и более активны (меньшее значение IC50) в сравнении с контрольной молекулой МТ103.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ОСНОВЕ ФЛЕКСИБОДИ ПРОТИВ CD3*CD19 ДЛЯ ЛЕЧЕНИЯ В-КЛЕТОЧНЫХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2568910C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА ПРОТИВ CD3*CD19 | 2015 |
|
RU2651776C2 |
| CD3-ЭПСИЛОН-СВЯЗЫВАЮЩИЙ ДОМЕН С МЕЖВИДОВОЙ СПЕЦИФИЧНОСТЬЮ | 2008 |
|
RU2561457C2 |
| PSCAXCD3, CD19XCD3, C-METXCD3, ЭНДОСИАЛИНXCD3, EPCAMXCD3, IGF-1RXCD3 ИЛИ FAP-АЛЬФАXCD3 БИСПЕЦИФИЧЕСКОЕ ОДНОЦЕПОЧЕЧНОЕ АНТИТЕЛО С МЕЖВИДОВОЙ СПЕЦИФИЧНОСТЬЮ | 2009 |
|
RU2547600C2 |
| PSMA×CD3 БИСПЕЦИФИЧЕСКОЕ ОДНОЦЕПОЧЕЧНОЕ АНТИТЕЛО С МЕЖВИДОВОЙ СПЕЦИФИЧНОСТЬЮ | 2009 |
|
RU2559531C2 |
| БИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ АГЕНТЫ С МЕЖВИДОВОЙ СПЕЦИФИЧНОСТЬЮ | 2008 |
|
RU2535992C2 |
| КОНСТРУКЦИИ АНТИТЕЛ И ХЕМОКИНОВ И ИХ ПРИМЕНЕНИЕ ПРИ ИММУНОЛОГИЧЕСКИХ НАРУШЕНИЯХ | 2001 |
|
RU2252786C2 |
| CD19XCD3-СПЕЦИФИЧЕСКИЕ ПОЛИПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ | 1999 |
|
RU2228202C2 |
| ОПРЕДЕЛЯЮЩИЕ КОМПЛЕМЕНТАРНОСТЬ УЧАСТКИ ДЛЯ СВЯЗЫВАНИЯ CD3 И СОДЕРЖАЩАЯ ИХ БИСПЕЦИФИЧЕСКАЯ АНТИГЕНСВЯЗЫВАЮЩАЯ МОЛЕКУЛА | 2019 |
|
RU2738802C1 |
| АНТИТЕЛО, НАЦЕЛИВАЮЩЕЕСЯ НА CD3, БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2808138C1 |












Изобретение относится к биотехнологии. Описан способ получения рекомбинантного моноклонального антитела против CD3*CD19 формата флексибоди. Конструируют рекомбинантную экспрессионную плазмидную ДНК, кодирующую биспецифическое антитело против CD3*CD19. Трансфецируют полученный ДНК штамм клеток CHO М и культивируют полученную линию клеток. Культивирование проводят в перфузионном режиме в присутствии фидерных добавок СВ1 и СВ5 в соотношении 1:1, с объемом добавки, составляющим 25% от объема питательной среды. Представлено моноклональное антитело против CD3*CD19 формата флексибоди, содержащее две нековалентно связанные полипептидные цепи с аминокислотной последовательностью SEQ ID №1 или две нековалентно связанные полипептидные цепи с аминокислотной последовательностью SEQ ID №2, полученное описанным способом. Также представлены рекомбинантная экспрессионная плазмидная ДНК pOG776, кодирующая полипептид с последовательностью биспецифического антитела формата флексибоди против CD3*CD19, имеющая размер 10618 п.о., и рекомбинантная экспрессионная плазмидная ДНК pOG854, кодирующая полипептид с последовательностью биспецифического антитела против CD3*CD19, имеющая размер 10618 п.о., с физической картой, представленной на фиг. 6. Изобретение позволяет достичь высокого выхода белка фармакопейного качества, пригодного для производства лекарственных препаратов. 4 н. и 2 з.п. ф-лы, 8 ил., 3 табл., 6 пр.
1. Способ получения рекомбинантного моноклонального антитела против CD3*CD19 формата флексибоди, включающий конструирование рекомбинантной экспрессионной плазмидной ДНК, кодирующей биспецифическое антитело против CD3*CD19, трансфекцию полученной ДНК штамма клеток CHO М и культивирование полученной линии клеток, характеризующийся тем, что культивирование проводят в перфузионном режиме в присутствии фидерных добавок СВ1 и СВ5 в соотношении 1:1, с объемом добавки, составляющим 25% от объема питательной среды.
2. Способ по п. 1, отличающийся тем, что в качестве плазмидной ДНК используют экспрессионную плазмиду pOG776, кодирующую полипептид с последовательностью биспецифического антитела формата флексибоди против CD3*CD19, имеющую размер 10618 п.о., с физической картой, представленной на фиг. 6, и состоящей из следующих элементов:
- оптимизированной последовательности, кодирующей полипептид биспецифического антитела формата флексибоди против CD3*CD19, SEQ ID №3,
- энхансера вируса CMV и промотора транскрипции гена фактора элонгации альфа, CMVe/EFa pro,
- сигнала полиаденилирования бычьего гормона роста, BGH рА,
- энхансера вируса SV40, sv40 enh,
- элемента прикрепления к ядерному матриксу, SGE 1,
- кассеты для экспрессии в клетках бактерий гена β-лактамазы, обеспечивающей устойчивость к ампицилину,
- кассеты, обеспечивающей устойчивость к пуромицину,
- уникальных участков узнавания следующих эндонуклеаз рестрикции:
KpnI (7 п.о.), AgeI (460 п.о.), SacI (1206 п.о.), HindIII (1590 п.о.), XbaI (3135 п.о.), SpeI (3932 п.о.), PvuII (4835 п.о.), AccI (5800 п.о.), BsrGI (6612 п.о.), AhdI (8138 п.о.), SfiI (9774 п.о.), BsiWI (9912 п.о.), NotI (10456 п.о.).
3. Способ по п. 1, отличающийся тем, что в качестве плазмидной ДНК используют экспрессионную плазмиду pOG854, кодирующую полипептид с последовательностью биспецифического антитела против CD3*CD19, имеющую размер 10618 п.о., с физической картой, представленной на фиг. 6, и состоящую из следующих элементов:
- оптимизированной последовательности, кодирующей полипептид биспецифического антитела формата флексибоди против CD3*CD19, SEQ ID №4,
- энхансера вируса CMV и промотора транскрипции гена фактора элонгации альфа, CMVe/EFa pro,
- сигнала полиаденилирования бычьего гормона роста, BGH рА,
- энхансера вируса SV40, sv40 enh,
- элемента прикрепления к ядерному матриксу, SGE 1,
- кассеты для экспрессии в клетках бактерий гена β-лактамазы, обеспечивающей устойчивость к ампицилину,
- кассеты, обеспечивающей устойчивость к пуромицину,
- уникальных участков узнавания следующих эндонуклеаз рестрикции:
KpnI (7 п.о.), AgeI (460 п.о.), SacI (1206 п.о.), HindIII (1590 п.о.), XbaI (3135 п.о.), SpeI (3932 п.о.), PvuII (4835 п.о.), AccI (5800 п.о.), BsrGI (6612 п.о.), AhdI (8138 п.о.), SfiI (9774 п.о.), BsiWI (9912 п.о.), NotI (10456 п.о.).
4. Моноклональное антитело против CD3*CD19 формата флексибоди, содержащее две нековалентно связанные полипептидные цепи с аминокислотной последовательностью SEQ ID №1 или две нековалентно связанные полипептидные цепи с аминокислотной последовательностью SEQ ID №2, полученное способом по любому из пп. 1-3.
5. Рекомбинантная экспрессионная плазмидная ДНК pOG776, кодирующая полипептид с последовательностью биспецифического антитела формата флексибоди против CD3*CD19, имеющая размер 10618 п.о., с физической картой, представленной на фиг. 6, и состоящая из следующих элементов:
- оптимизированной последовательности, кодирующей полипептид биспецифического антитела формата флексибоди против CD3*CD19, SEQ ID №3,
- энхансера вируса CMV и промотора транскрипции гена фактора элонгации альфа, CMVe/EFa pro,
- сигнала полиаденилирования бычьего гормона роста, BGH рА,
- энхансера вируса SV40, sv40 enh,
- элемента прикрепления к ядерному матриксу, SGE 1,
- кассеты для экспрессии в клетках бактерий гена β-лактамазы, обеспечивающей устойчивость к ампицилину,
- кассеты, обеспечивающей устойчивость к пуромицину,
- уникальных участков узнавания следующих эндонуклеаз рестрикции:
KpnI (7 п.о.), AgeI (460 п.о.), SacI (1206 п.о.), HindIII (1590 п.о.), XbaI (3135 п.о.), SpeI (3932 п.о.), PvuII (4835 п.о.), AccI (5800 п.о.), BsrGI (6612 п.о.), AhdI (8138 п.о.), SfiI (9774 п.о.), BsiWI (9912 п.о.), NotI (10456 п.о.).
6. Рекомбинантная экспрессионная плазмидная ДНК pOG854, кодирующая полипептид с последовательностью биспецифического антитела против CD3*CD19, имеющая размер 10618 п.о., с физической картой, представленной на фиг. 6, и состоящая из следующих элементов:
- оптимизированной последовательности, кодирующей полипептид биспецифического антитела формата флексибоди против CD3*CD19, SEQ ID №4,
- энхансера вируса CMV и промотора транскрипции гена фактора элонгации альфа, CMVe/EFa pro,
- сигнала полиаденилирования бычьего гормона роста, BGH рА,
- энхансера вируса SV40, sv40 enh,
- элемента прикрепления к ядерному матриксу, SGE 1,
- кассеты для экспрессии в клетках бактерий гена β-лактамазы, обеспечивающей устойчивость к ампицилину,
- кассеты, обеспечивающей устойчивость к пуромицину,
- уникальных участков узнавания следующих эндонуклеаз рестрикции:
KpnI (7 п.о.), AgeI (460 п.о.), SacI (1206 п.о.), HindIII (1590 п.о.), XbaI (3135 п.о.), SpeI (3932 п.о.), PvuII (4835 п.о.), AccI (5800 п.о.), BsrGI (6612 п.о.), AhdI (8138 п.о.), SfiI (9774 п.о.), BsiWI (9912 п.о.), NotI (10456 п.о.).
| Устройство для испытания клапанов | 1983 |
|
SU1293514A1 |
| CD19XCD3-СПЕЦИФИЧЕСКИЕ ПОЛИПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ | 1999 |
|
RU2228202C2 |
| Режущий аппарат газонокосилки | 1985 |
|
SU1400534A1 |
| WO 2011090762 A1, 28.07.2011. | |||
Авторы
Даты
2016-03-10—Публикация
2014-04-10—Подача