Изобретение относится к области иммунологии и биотехнологии, а также к созданию новых эффективных высокомолекулярных соединений, обладающих терапевтическими свойствами. Предложены варианты аминокислотных последовательностей определяющих комплементарность участков (CDR) антигенсвязывающих фрагментов белковой молекулы, специфичной к человеческому клеточному рецептору CD3. Указанные последовательности CDR, обеспечивающие связывание данных фрагментов с антигеном CD3, получили с помощью технологии фагового дисплея. Предложенные CDR могут быть использованы при конструировании различных антигенсвязывающих молекул, одной из неотъемлемых функций которых является специфическое взаимодействие с CD3-несущими клетками. При включении указанных CDR в состав антителоподобной молекулы, исходно связывающейся с рецептором CD 19, были также сконструированы биспецифические молекулы, которые специфично связываются с человеческими клеточными рецепторами CD3 и CD19. В одном из воплощений биспецифические молекулы состоят из двух полипептидных цепей, каждая из которых содержит вариабельный домен легкой цепи, специфичный к антигену CD3(VLCD3), вариабельный домен тяжелой цепи, специфичный к антигену CD19 (VHCD19), вариабельный домен легкой цепи, специфичный к антигену CD19 (VL CD19) и вариабельный домен тяжелой цепи, специфичный к антигену CD3 (VH CD3). Домены расположены в следующем порядке VL CD3 - VH CD19 - VL CD19 - VH CD3. Такое расположение вариабельных доменов в антиген-связывающей молекуле от N-конца к С-концу полипептида обеспечивает возможность одновременного связывания молекулы с двумя различными антигенами, что и определяет ее терапевтическую эффективность за счет селективного связывания с экстраклеточной частью человеческих рецепторов CD3 и CD19, экспрессируемых Т- и В-клетками, соответственно. При одновременном взаимодействии молекулы по изобретению с экстраклеточной частью рецепторов CD3 и CD19 происходит контакт Т- и В-клеток, что приводит к активации Т-клеток, образованию цитолитического синапса и высвобождению протеолитических ферментов, разрушающих CD19-позитивные клетки-мишени. Предложенная структура расположения антигенсвязывающих участков биспецифической молекулы позволяет сформировать молекулу, эффективно связывающую экстраклеточную частью рецепторов CD3 и CD19, экспрессируемых различными видами клеток. Подобная молекула активирует Т-клетки в ответ на взаимодействие с клетками-мишенями, экспрессирующими опухолевый антиген (CD19), что приводит к цитолизу последних. Группа изобретений позволяет на основе комбинации CDR, содержащейся в любом из предложенных четырнадцати антигенсвязывающих фрагментов, получить рекомбинантное моноклональное биспецифическое терапевтическое антитело, пригодное для создания лекарственного средства для лечения опухолевых заболеваний, в частности гематологических злокачественных заболеваний B-клеточной природы.
Сокращения и термины:
МКПК - Мононуклеарные клетки периферической крови
TDCC - Т-клеточно-зависимая цитотоксическая активность
БСАТ - биспецифическое антитело
MFI - mean fluorescence intensity, усредненная интенсивность флуоресценции
V - вариабельный домен
VL - вариабельный домен легкой цепи
VH - вариабельный домен тяжелой цепи
CDR - определяющий комплементарность участок
Fc-фрагмент - кристаллизующийся фрагмент иммуноглобулина (Fc, fragment crystallizable region, Fc region).
Антитело - молекула иммуноглобулина, для которого существует антиген.
Аффинность - термодинамическая характеристика, количественно описывающая силу взаимодействия антигена и антитела; определяется по закону действующих масс как отношение концентрации комплекса антиген - антитело к произведению концентраций компонентов.
Авидность - характеристика общей стабильности комплекса антигена и антитела; определяется аффинностью антитела к антигену, количеством антигенсвязывающих центров в молекуле антитела и особенностями пространственной структуры антигена, создающими стерические препятствия для создания комплекса. В отличие от аффинности, которая является термодинамическим параметром, количественно описывающим силу единственного взаимодействия антигена и антитела, авидность описывает силу кооперативных аффинных взаимодействий.
Антигенсвязывающий участок антитела - часть антитела, распознающая эпитоп. Имеет несколько названий: активный или антигенсвязывающий центр антител, антидетерминанта или паратоп.
Биспецифические антитела - молекулы иммуноглобулина, которые объединяют антиген-связывающие участки для двух различных антигенов в одной молекуле. Биспецифическое антитело в состоянии связывать два антигена одновременно.
Злокачественные заболевания В-клеточной природы означают в настоящем изобретении:
- В-клеточные опухоли из клеток предшественников В-лимФоцитов
В-лимфобластная лимфома/лейкоз из клеток-предшественников (В-клеточный острый лимфобластный лейкоз из клеток-предшественников)
- В-клеточные опухоли с фенотипом зрелых лимфоцитов
1. Хронический лимфоцитарный лейкоз / лимфоцитарная лимфома
2. В-клеточный пролимфоцитарный лейкоз
3. Лимфоплазмоцитарная лимфома
4. Селезеночная лимфома маргинальной зоны
5. Волосатоклеточный лейкоз
6. Миелома или плазмоцитома (солитарная и внекостная)
7. Экстранодальная В-клеточная лимфома маргинальной зоны лимфоидной ткани, ассоциированной со слизистыми оболочками (MALT-лимфома)
8. Нодальная В-клеточная лимфома маргинальной зоны (с или без моноцитоидными В-клетками)
9. Фолликулярная лимфома
10. Лимфома из клеток зоны мантии
11. Диффузная В-крупноклеточная лимфома
12. Медиастинальная В-крупноклеточная лимфома
13. Первичная лимфома серозных полостей
14. Лимфома/Лейкоз Беркитта
Истощение В-клеток - снижение числа клеток, экспрессирующих определенный антиген.
Комплементарность антитела - способность антитела к специфическому взаимодействию с антигеном. За редким исключением, антитело взаимодействуют только с тем антигеном, который индуцировал их образование и подходит к ним по пространственной структуре.
Определяющий комплементарность участок - гипервариабельный участок вариабельной цепи, образующий антигенсвязывающий центр молекулы антитела.
Опухолевые антигены - антигены, продуцируемые раковыми клетками и способные вызвать иммунный ответ организма. Являются результатом проявления измененного генома раковой клетки.
Острый лимфобластный лейкоз - злокачественное заболевание системы кроветворения, характеризующееся неконтролируемой пролиферацией незрелых лимфоидных клеток (лимфобластов).
В-клеточная лимфома - разновидность неходжкинских новообразований. Заболевание возникает на фоне бесконтрольного деления В-лимфоцитов, принимающих клетки и ткани организма за чужеродные.
Специфичность - способность антитела проявлять различную аффинность по отношению к различным антигенам.
Эпитоп, или антигенная детерминанта - часть макромолекулы антигена, небольшой участок молекулы антигена, который взаимодействует со специфичным к нему антителом. Этот участок распознается клетками или молекулами иммунной системы (антителами, В-лимфоцитами, Т-лимфоцитами).
CD3 (англ. Cluster of Differentiation 3) - мультипротеиновый комплекс на поверхности Т-лимфоцитов, у млекопитающих образован 4 субъеденицами: CD3γ, CD3δ и двумя CD3ε.
CD19, или В-лимфоцитарный антиген CD19 - белок, расположенный на поверхности В-лимфоцитов.
Все термины и сокращения, используемые в настоящей заявке, употребляются в том же значении, как это принято в данной области техники, и понятны специалистам. Приведенные выше определения даны для устранения каких-либо разночтений.
Описание чертежей.
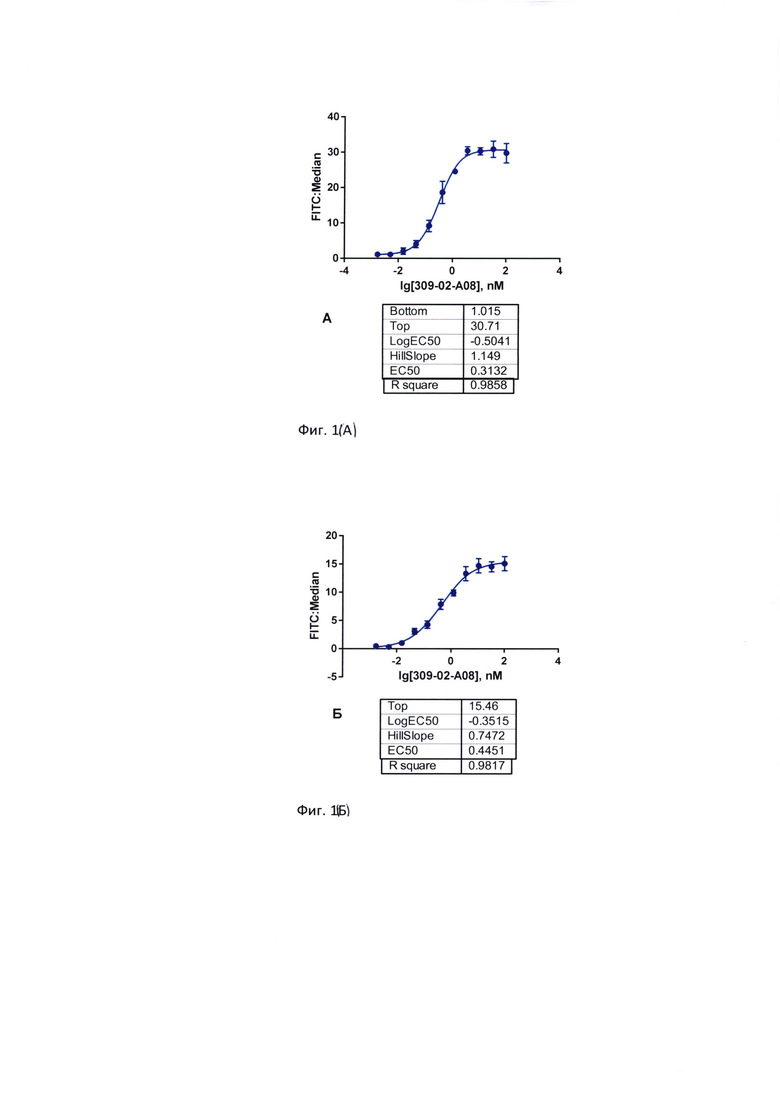
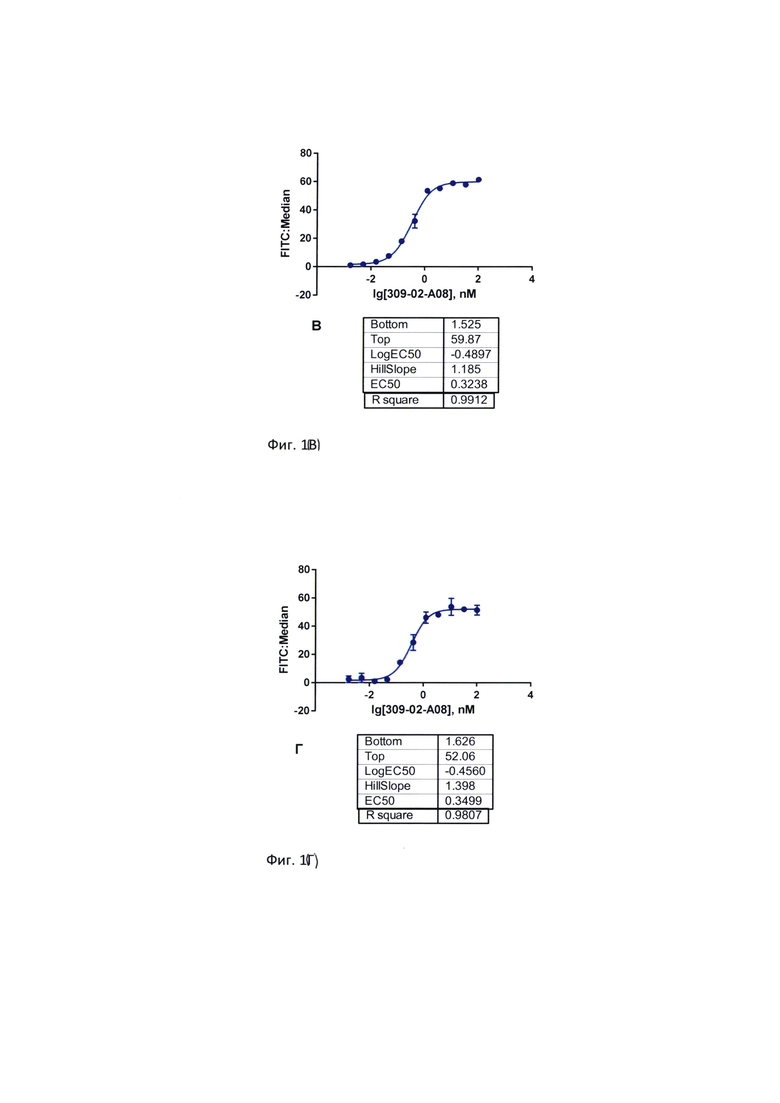
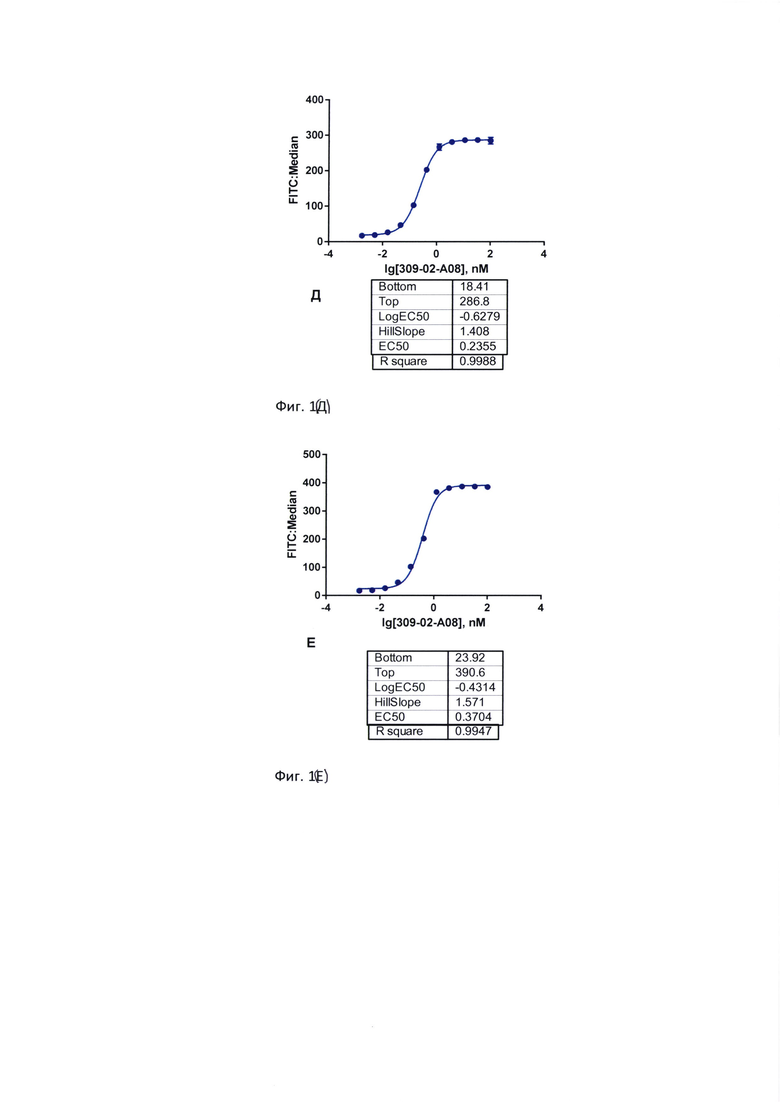
Фиг. 1. Эффективность связывания препарата БСАТ с человеческими CD19-позитивными клеточными линиями. А) клеточная линия Namalwa (АТСС® CRL-1432™); Б) клеточная линия Daudi (АТСС® CCL-213™); В) клеточная линия NALM6 (АТСС® CRL-3273™); Г) клеточная линия Ramos (АТСС® CRL-1596™); Д) клеточная линия Toledo (АТСС® CRL-2631™); Е) клеточная линия Raji (АТСС® CCL-86™).
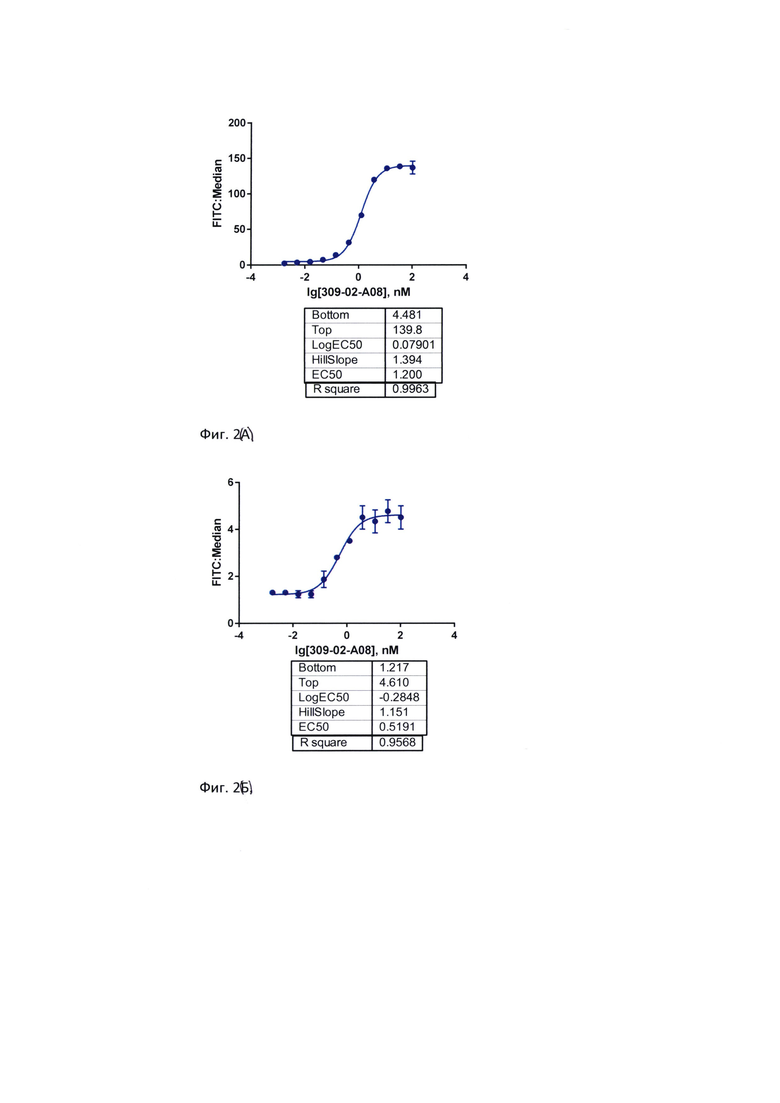
Фиг. 2. Эффективность связывания препарата БСАТ с CD3-позитивными клеточными линиями. А) клеточная линия HUT78 (АТСС® TIB-161™); Б) клеточная линия CCRF-CEM (АТСС® CCL-119™); В) клеточная линия Jurkat (АТСС® TIB-152™).
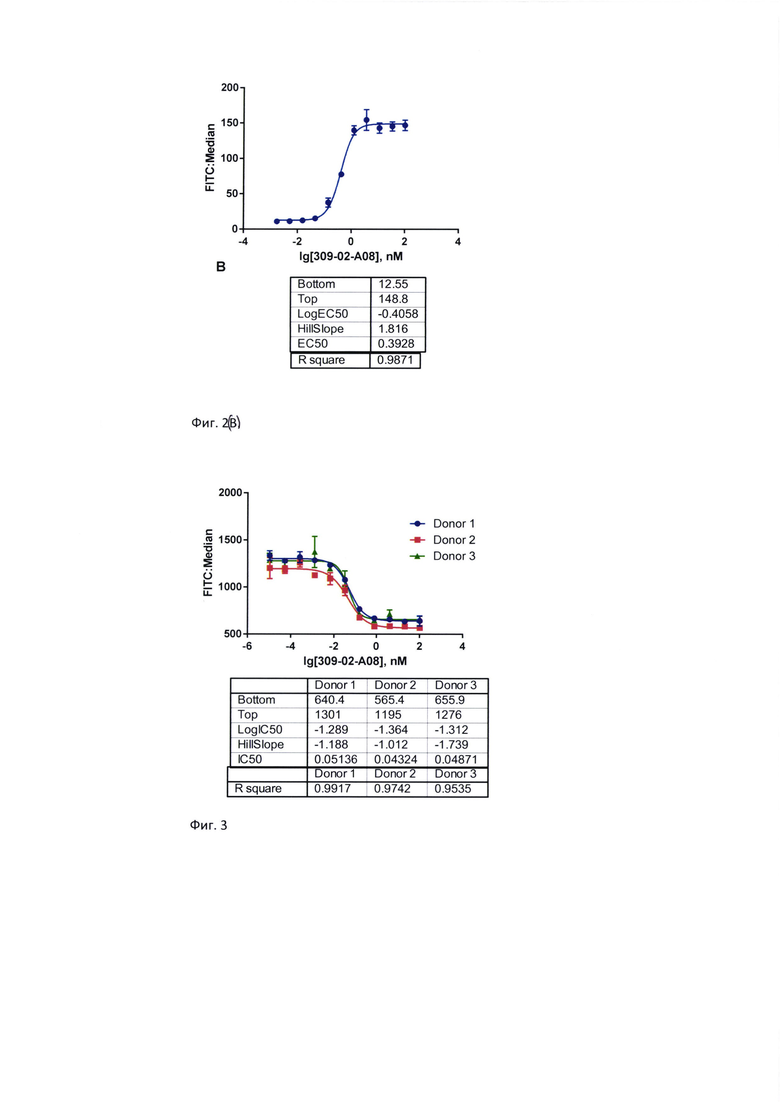
Фиг. 3. Взаимодействие CD19-позитивных РВМС условно здоровых доноров с конъюгированным с FITC антителом к экстраклеточной части человеческого рецептора CD 19 (клон HD37) (Millipore milli-mark, кат. № FCMAB184F) в присутствии препарата БСАТ в разных концентрациях.
Фиг. 4. Взаимодействие БСАТ с CD3-позитивными РВМС условно здоровых доноров.
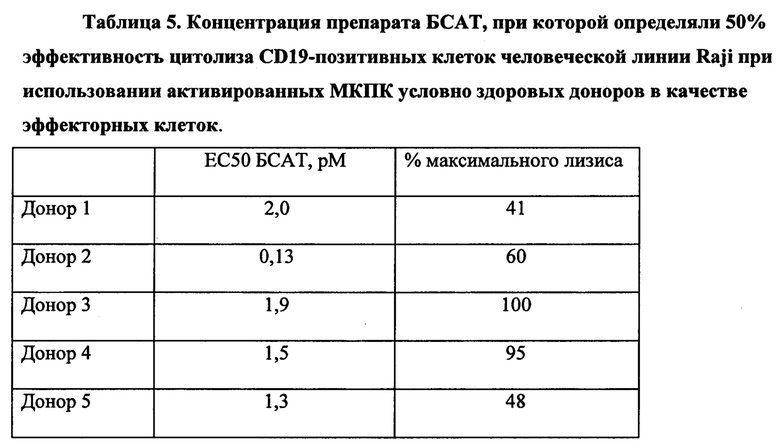
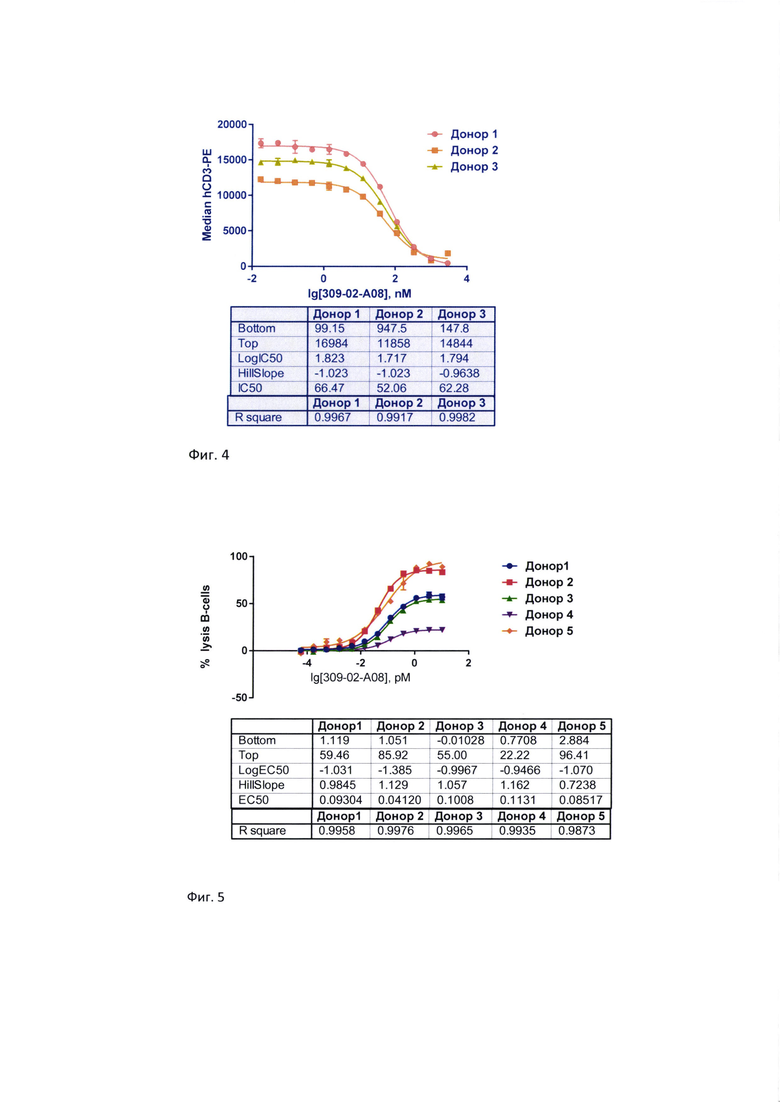
Фиг. 5. Эффективность цитолиза CD19-позитивных клеток человеческой линии Raji препаратом БСАТ при использовании в качестве эффекторных клеток активированных МКПК условно здоровых доноров.
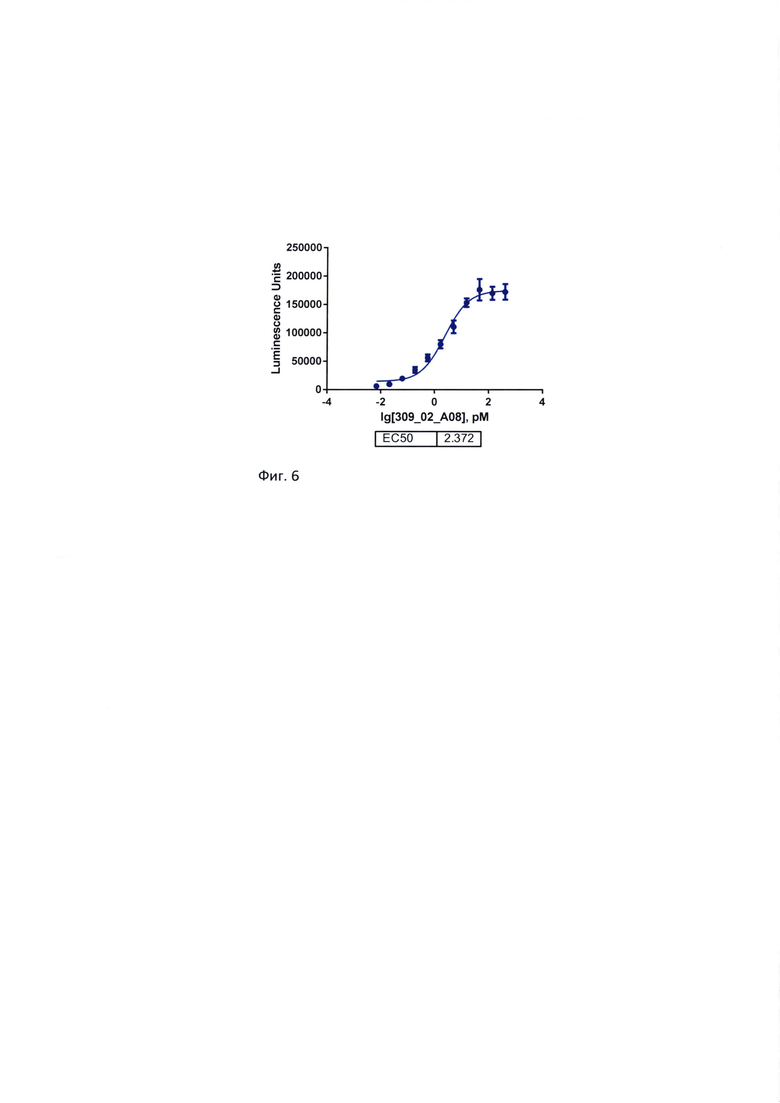
Фиг. 6. Способность БСАТ одновременно связывать CD3 и CD19 при использовании клеток человеческой линии Raji и эффекторных клеток коммерческой репортерной линии Jurkat-LUCIA-NFAT (Promega).
Фиг. 7. Оценка активности и специфичности биспецифических IgG-подобных молекул в ходе анализа активации клеток линии Jurkat. IgG-подобные молекулы титровали и оценивали их способность активировать транскрипцию NFAT в репортерных клетках линии Jurkat. Синими линиями обозначена активация эффекторных клеток (модифицированных путем генной инженерии клеток линии Jurkat) в присутствии клеток-мишеней (клеток линии Raji), красными линиями обозначена активация эффекторных клеток в отсутствие клеток-мишеней. Нумерация клонов справа налево и сверху вниз: 309_ 01_А02; 309_01_G04; 309_01_G12; 309_02_А08; 309_02_F01; 309_04_А04; 309_05_В08; контроль 1; контроль 2; 400_01_D06; 400_03_Н07; 410_01_С03; 410_01_С09; 418_01_С05; 418_03_Е12; 418_03_Н01; отрицательный контроль.
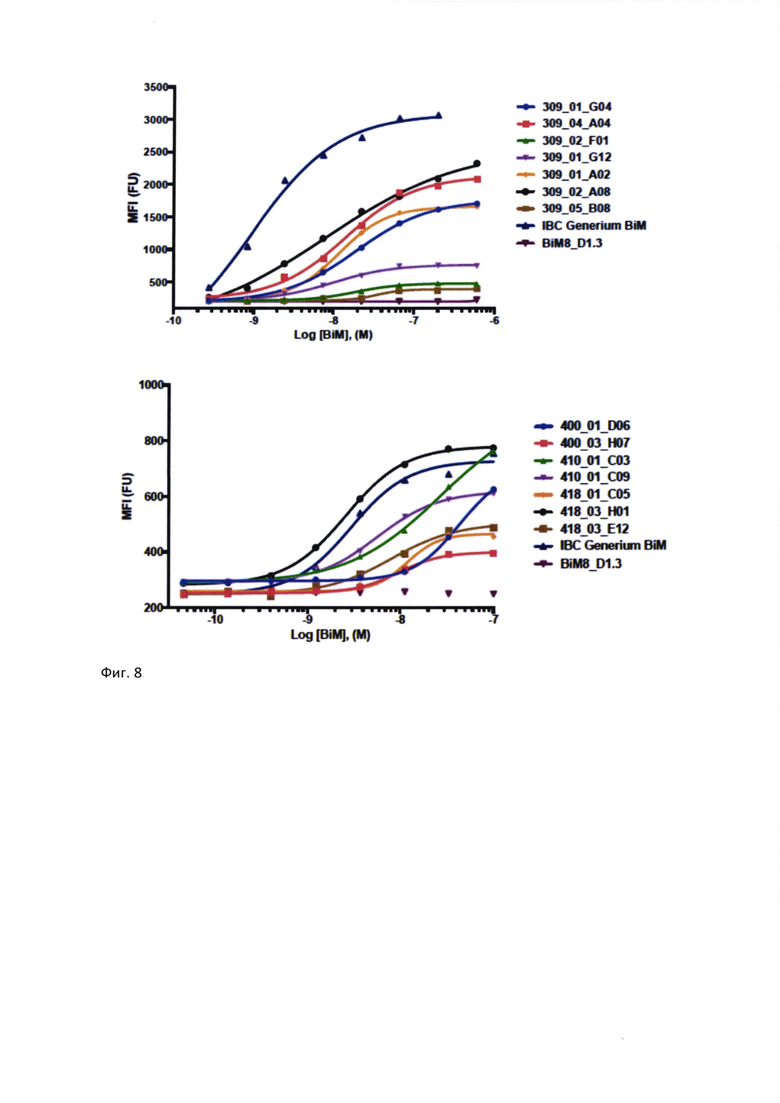
Фиг. 8. Анализ связывания IgG-подобных антител к CD3 с клетками линии Jurkat методом проточной цитометрии. По оси у представлена средняя интенсивность флуоресценции, по оси х - логарифм концентрации биспецифической IgG-подобной молекулы. Данные, полученные в независимых экспериментах, представлены отдельно (верхняя и нижняя панели). Обозначения: MFI (FU)- Средняя интенсивность флуоресценции (единицы флуоресценции). IBC Generium BiM - биспецифическая IgG-подобная молекула, положительный контроль и BiM - биспецифическая IgG-подобная молекула, отрицательный контроль
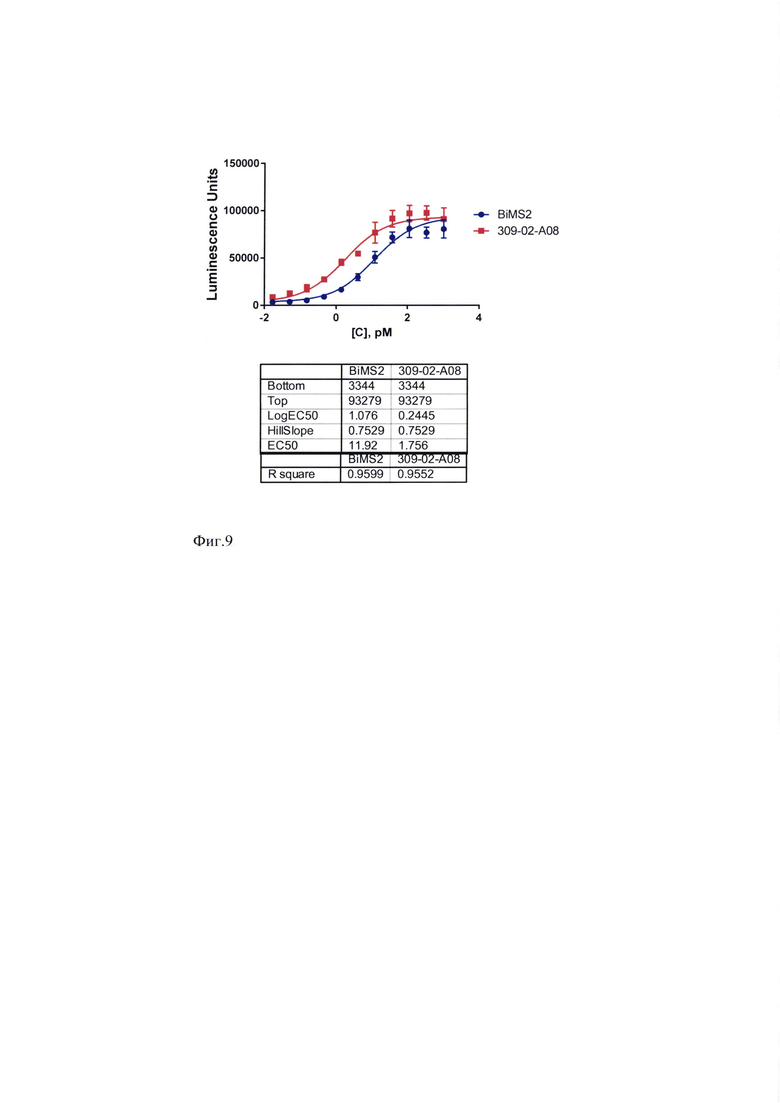
Фиг. 9. Сравнительная способность биспецифического антитела по изобретению 309-02-F08 и терапевтического антитела BIMSA2 одновременно связывать CD3 и CD19 с использованием клеток человеческой линии Raji и эффекторных клеток коммерческой репортерной линии Jurkat-LUCIA-NFAT (Promega).
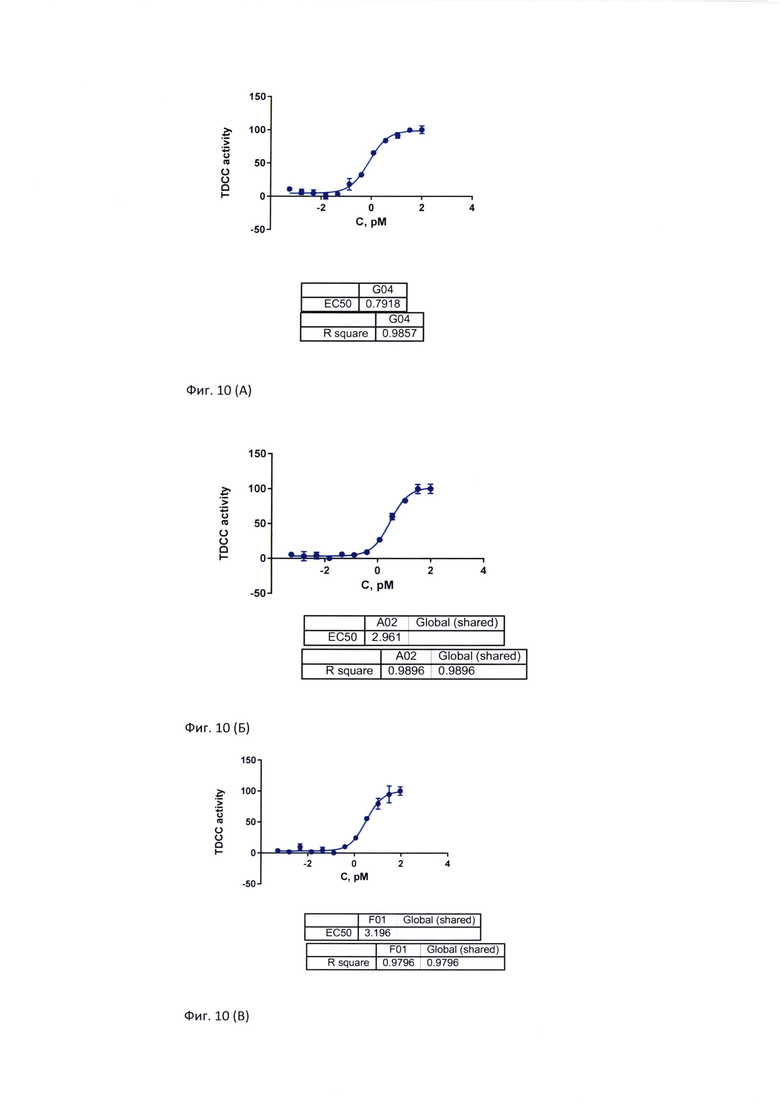
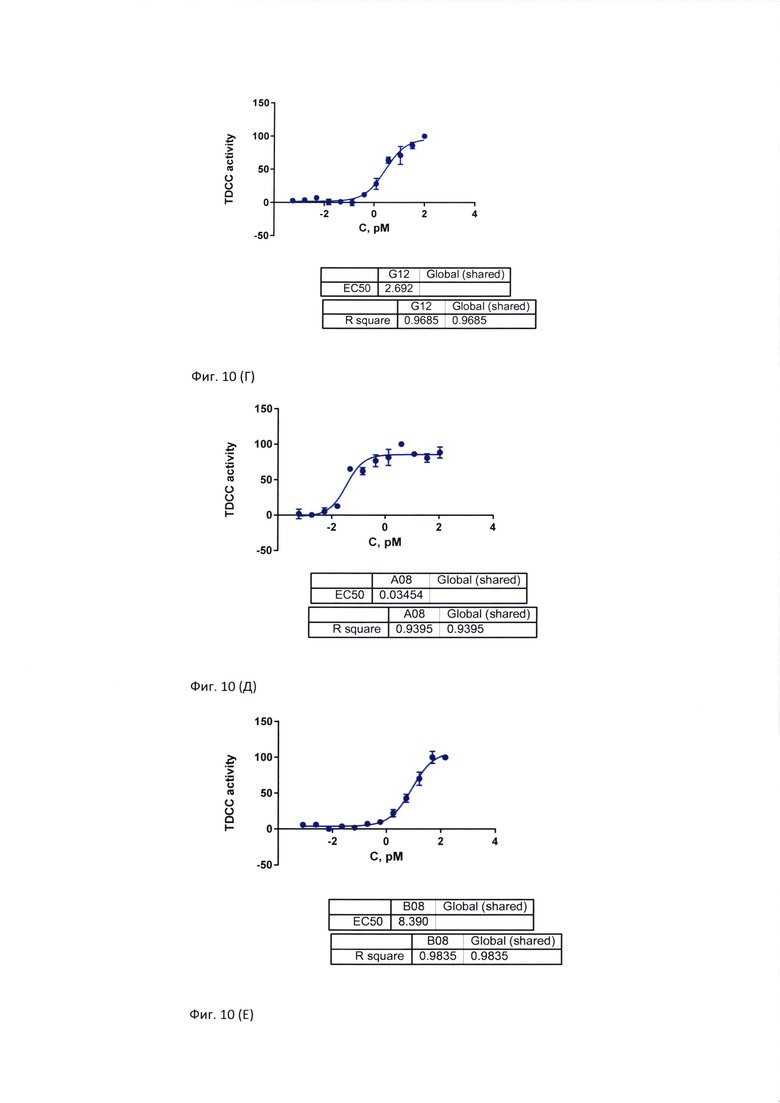
Фиг. 10, А-Е. Эффективность цитолиза CD19-позитивных клеток человеческой линии Raji препаратами различных вариантов БСАТ при использовании в качестве эффекторных клеток активированных МКПК условно здоровых доноров. А: клон 309_01_G04, Б: клон 309_01_А02, В: клон 309_02_F01, Г: клон 309_01_G12, Д: клон 309_02_А08, Е: клон 309_05_В08.
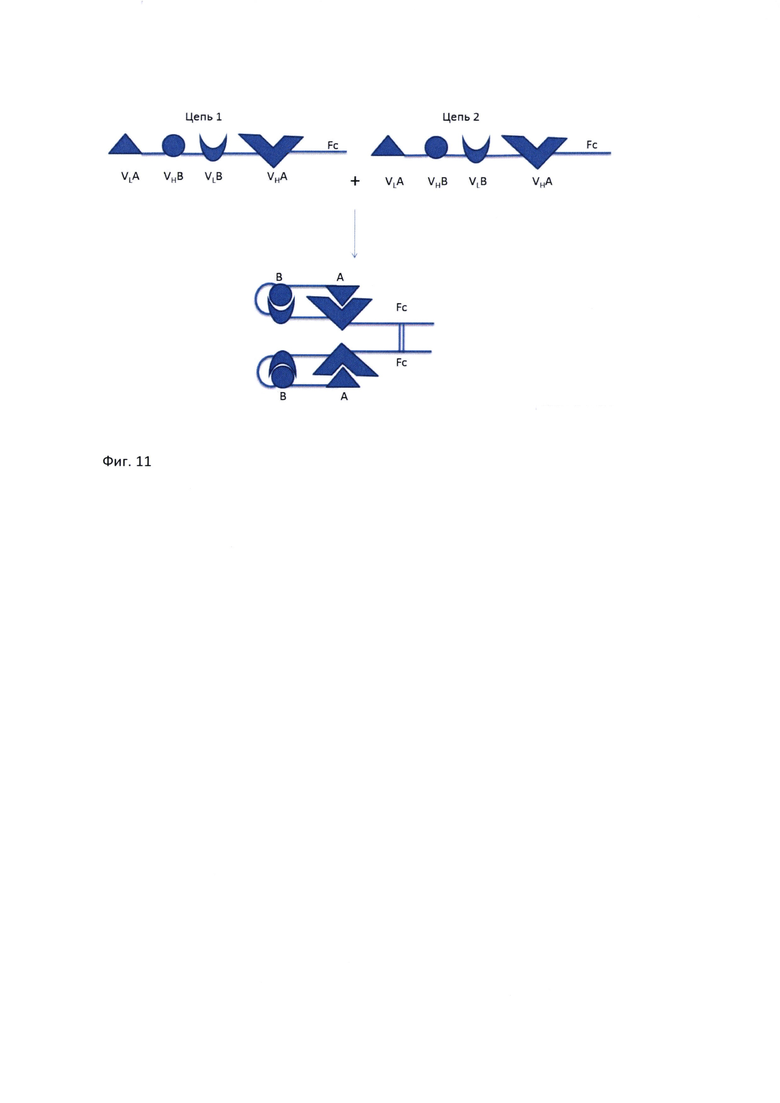
Фиг. 11. Схема возможного фолдинга БСАТ.
Антитела, или иммуноглобулины (Ig), - это растворимые гликопротеины крови и тканевой жидкости. Классические антитела представляют собой мультимерные белки, объединяющие две идентичные тяжелые (Н) цепи и две идентичные легкие (L) цепи. Н-цепи, в свою очередь, состоят из вариабельного домена (VH) и трех константных (СН1, СН2, СН3) доменов, а также шарнирного участка между СН1 и СН2 доменами. L-цепи состоят из вариабельного, VL, и константного, CL, доменов. Четыре цепи объединяются в молекулу посредством нековалентных и ковалентных (дисульфидных) связей. Комбинация антигенсвязывающих участков (CDR-Complementarity Determining Regions) вариабельного домена тяжелой цепи и вариабельного домена легкой цепи формирует участок связывания антигена, в то время как каркасные регионы вариабельных доменов (FR - Framework Regions) и константные домены антител непосредственно не участвуют в распознавании антигена. Вариабельные области, хотя и находятся на большом отдалении друг от друга в первичной структуре легкой цепи, при образовании трехмерной структуры оказываются расположенными в непосредственной близости друг к другу. В пространственной структуре вариабельных доменов гипервариабельные последовательности расположены в зоне изгибов полипептидной цепи, направленной навстречу соответствующим участкам V-домена другой цепи (т.е. CDR легкой и тяжелой цепей направлены навстречу друг другу). В результате взаимодействия вариабельного домена Н- и L-цепей формируется антигенсвязывающий участок (активный центр) иммуноглобулина. Пространственная структура этой полости, обусловленная строением гипервариабельных участков, определяет способность антител распознавать и связывать конкретные молекулы на основе пространственного соответствия (специфичность антител). Гипервариабельные участки V-доменов входят в состав активного центра не полностью - поверхность антигенсвязывающего участка захватывает только около 30% CDR. Специфически взаимодействуют с эпитопами антигена отдельные аминокислотные остатки в CDRh.
Минимизированной производной антигенсвязывающего фрагмента классических антител является одноцепочечная конструкция, в которой вариабельные домены тяжелой и легкой цепей соединены линкерной последовательностью (scFv). Участок связывания антигена имеет разную пространственную конфигурацию для каждой антигенной специфичности антитела. Когда антиген вступает в контакт с антителом, многочисленные простетические группы антигена как зеркальное изображение соответствуют таким же группам антитела, благодаря чему между антителом и антигеном осуществляется быстрое и плотное связывание. Если антитело высокоспецифично, сцепление между антителом и антигеном может происходить посредством сразу нескольких форм взаимодействия: гидрофобных связей; водородных связей; ионного притягивания; Ван-дер-Ваальсовых сил. Антитело, имеющее два вариабельных участка для прикрепления антигена, называют бивалентным. Биспецифическое антитело в состоянии связывать два различных антигена одновременно. В зависимости от практической задачи исследователи могут изменять размер антител, их специфичность, аффинность, валентность, уменьшать иммуногенность, оптимизировать фармакокинетические свойства и эффекторные функции. В дополнение к этому, антитела получают в виде рекомбинантных составных белков, включающих антитела другой специфичности, цитокины, белковые токсины и радиоизотопы, ферменты, флуоресцентные белки (см. Деев С.М., and Лебеденко Е.Н. "Современные технологии создания неприродных антител для клинического применения" Acta Naturae (русскоязычная версия), vol. 1, no. 1, 2009, pp. 32-50). Каждое антитело обладает уникальной специфичностью и высоким сродством, или аффинностью (KD 10-8-10-11 М) к своему антигену, которое обеспечивается комплементарностью антигенсвязывающего участка антитела определенному участку молекулы антигена (эпитопу). Различные антитела способны одновременно связывать один, два и более антигенов. Аффинность антител, применяемых для терапии в настоящее время, лежит в пределах наномолярных концентраций (от 10-8 до 10-10 М), которые являются оптимальными для большинства задач. Размер молекул терапевтического антитела является важным фактором, определяющим возможность их вывода через почки и, соответственно, быстроту выведения из организма. Время полувыведения белков через почки коррелирует с размером молекулы. Оптимальным поверхностным зарядом для терапевтических антител является интервал их изоэлектрических точек от 5 до 9. Увеличение как положительного, так и отрицательного заряда ухудшает связывание антитела с клетками-мишенями.
Свойства предложенных по изобретению 14 функциональных антител, способных к связыванию рецепторного комплекса CD3 на поверхности экспрессирующих его клеток, даны в таблице 1. Антитело «ОКТ3» включено в качестве стандартного контроля. Антитела содержат одну из комбинаций CDR, предложенных по изобретению, а также антигенсвязывающий фрагмент для рецептора CD19. В таблице представлена информация о характеризующих антитело последовательностях CDR3 легкой и тяжелой цепи, активности по данным анализа взаимодействия с клетками и индикаторе пригодности к промышленному производству, такому как продуктивность экспрессии. Последовательности всех антител характеризуются уникальными комбинациями последовательностей CDR3 тяжелой цепи и легкой цепи и способностью активировать клетки линии Jurkat (с репортерным геном, регулируемым ядерным фактором активированных Т-клеток (NFAT)) в ответ на взаимодействие с клетками-мишенями, экспрессирующими CD19. В отсутствие клеток-мишеней неспецифическая активация клеток линии Jurkat была низкой или не обнаруживалась (при концентрациях биспецифических JgG-подобных молекул ≥ 1 нМ). Данные об активности в отношении активации клеток линии Jurkat приведены в таблице 1. Связывание с нативным CD3 на поверхности клеток линии Jurkat измеряли путем проточной цитометрии.
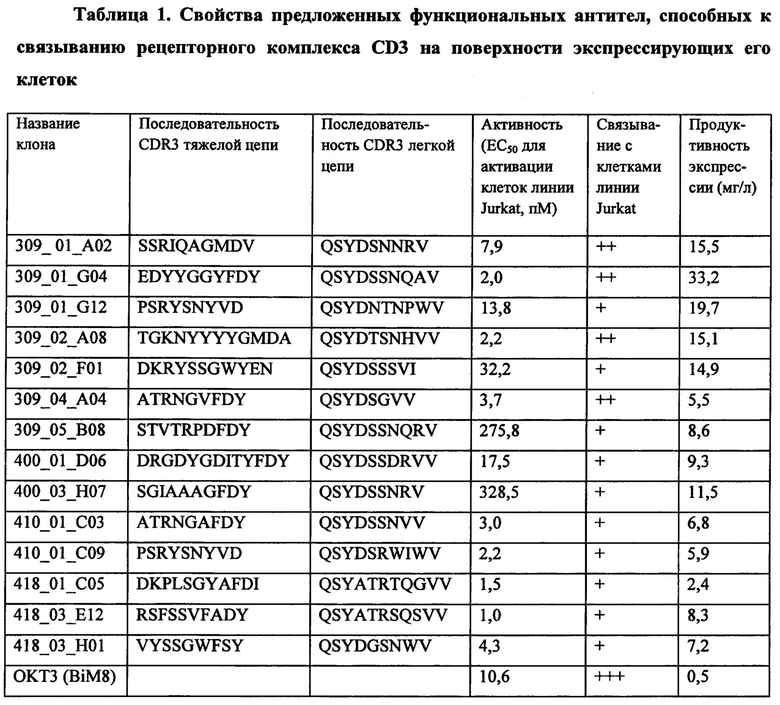
При одновременном взаимодействии биспецифической молекулы с экстраклеточной частью рецепторов CD3 и CD19 происходит контакт Т- и В-клеток, что приводит к активации Т-клеток, образованию цитолитического синапса и высвобождению протеолитических ферментов, разрушающих CD19-позитивные клетки-мишени. CD3-CD19 - направленные биспецифические антитела в настоящее время разрабатываются преимущественно для терапии злокачественных В-клеточных заболеваний или для истощения В-клеток, например, для терапии неходжкинской лимфомы, острого лимфобластного лейкоза и др. Биспецифические антитела (БСАТ) выполняют функцию адаптеров, которые физически соединяют Т-клетки с опухолевыми CD 19-позитивными клетками-мишенями и запускают их цитолиз. CD3 является пан-Т-клеточным рецептором, то есть он представлен на всех Т-лимфоцитах, поэтому при применении биспецифического антитела к опухолевым клеткам будут привлекаться различные субпопуляции Т-клеток. Рецептор CD19 устойчиво и равномерно экспрессируется только клетками В-лимфоцитарного ряда (в том числе и опухолевыми). CD19 практически нигде, кроме В-клеток, более не синтезируется и, соответственно, получаемая терапия специфична. БСАТ соединяет Т-клетку и раковую клетку за счет одновременного связывания с CD3 и с антигеном-мишенью. В этом случае происходит активация и пролиферация Т-клеток, образование цитолитического синапса с высвобождением цитотоксических гранул и секреция цитокинов. Направленный лизис раковых клеток включает в себя перфорацию мембраны клетки-мишени с участием перфорина и последующий апоптоз, индуцированный гранзимами. Связывание БСАТ только с Т-клеткой в отсутствие клетки-мишени не вызывает Т-клеточную активацию.
Примеры биспецифических антител, известных из уровня техники (Blood, (ASH Annual Meeting Abstracts), 2009, 114:840), свидетельствуют о том, что эффективная терапевтическая концентрация препаратов, полученных на основе использования мультивалентных антител, существенно ниже по сравнению с классическими антительными противораковыми препаратами. Это способствует хорошей переносимости, возможности осуществления длительных курсов лечения и уменьшению риска побочных эффектов.
В настоящее время известны различные полипептиды, специфичные в отношении CD19 и CD3, и их применение в качестве компонента лекарственного средства для истощения В-клеток и лечения В-клеточных заболеваний. Изобретение, раскрытое в RU 2228202, раскрывает одноцепочечный многофункциональный полипептид, специфичный в отношении С19 и CD3 антигенов формулы: VLCD19 - VHCD19 - VHCD3 - VLCDS, полинуклеотид, кодирующий этот полипептид, экспрессирующий вектор, штамм культуры клеток, способ получения полипептида, фармацевтическую композицию для лечения злокачественных заболеваний В-клеток, диагностическую композицию, способ выявления активаторов или ингибиторов Т-клеточной активации или стимуляции, способ приготовления фармацевтической композиции, предназначенной для лечения злокачественных заболеваний В-клеток, способ лечения злокачественных заболеваний В-клеток или истощения В-клеток и способ замедления развития патологического состояния. Из патента RU 2651776 известно рекомбинантное моноклональное биспецифическое антитело, включающее две соединенных дисульфидными связями цепи, каждая из которых состоит из следующих доменов: VL(CD3)-L1-VH(CD19)-L2-VL(CD19)-L3-VH(CD3)-H-CH2-CH3(IgG2), где VL (CD3) и VH(CD3). Антитело может быть использовано для лечения гематологических злокачественных заболеваний В-клеточной природы.
Известна также димерная антиген-связывающая молекула тандемного диатела для одновременного связывания с двумя различными антигенами, раскрытая в документе RU 2613368. Молекула состоит из двух идентичных полипептидных цепей.
В заявленном изобретении каждую полипептидную цепь биспецифической молекулы составляют первый домен VL CD3, являющийся вариабельным доменом легкой цепи, специфичным по отношению к CD3; второй домен VH CD19, являющийся вариабельным доменом тяжелой цепи, специфичным по отношению к CD19; третий домен VL CD19, являющийся вариабельным доменом легкой цепи, специфичным по отношению к CD19; и четвертый домен VH CD3, являющийся вариабельным доменом тяжелой цепи, специфичным по отношению к CD3. Указанные домены расположены в каждой из полипептидных цепей в следующем порядке: VLCD3-VHCD19-VLCD19-VHCD3 от N-конца к С-концу. Первый домен VLCD3 связан со вторым доменом VHCD19 посредством первого линкера L1, второй домен VHCD19 связан с третьим доменом VLCD19 посредством второго линкера L2, и третий домен VLCD19 связан с четвертым доменом VHCD3 посредством третьего линкера L3. Линкер L2 состоит из 15 или менее аминокислотных остатков. При формировании биспецифической молекулы первый домен VLCD3 первой полипептидной цепи оказывается связан с четвертым доменом VHCD3 первой полипептидной цепи с образованием антиген-связывающего сайта для CD3; второй домен VHCD19 первой полипептидной цепи связан с третьим доменом VLCD19 первой полипептидной цепи с образованием антиген-связывающего сайта для CD19 (Фиг. 11). На схеме для наглядности CD3-связывающий домен обозначен символом A, CD19-связывающий домен обозначен символом В. Добавление Fc-области к молекуле продлевает время ее пребывания в кровотоке за счет связывания с неонатальным рецептором FcRn, увеличивая, таким образом, период полувыведения лекарственного препарата (Hmila I., et al.. Mol. Immunol. England, 2008, Vol. 45, no. 14, pp. 3847-3856). Образование полной молекулы из двух цепей происходит в результате классического процесса фолдинга антител. В процессе формирования третичной структуры антитела между константными регионами тяжелых цепей образуются дисульфидные связи. Одна цепь является полностью функциональной. Димер является более стабильным по сравнению с мономером, и большая молекулярная масса позволяет ему дольше циркулировать в крови.
Термин "линкер", используемый в соответствии с настоящим изобретением, относится к пептидным линкерам. Длина и/или последовательность линкера влияет на стабильность и/или растворимость биспецифической молекулы. Линкер может повысить гибкость полученной связывающей молекулы и/или может улучшить связывание ее с антигеном-мишенью путем уменьшения стерических помех. Длина и последовательность линкера зависит от последовательности и длины связываемых последовательностей. Специалисту хорошо известны способы тестирования пригодности различных линкеров. Например, свойства связывающей молекулы можно легко протестировать путем анализа ее аффинности связывания при использовании различных типов линкеров. Стабильность полученной молекулы можно измерить способами, известными в данной области техники, такими как, например, высокоэффективная жидкостная храматография, разделяющая исследуемый белковый материал на фракции, в зависимости от молекулярной массы белка и гидродинамических характеристик.
Особенно предпочтительными являются линкеры, которые представляют собой пептиды, состоящие по меньшей мере на 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или 100% из небольших аминокислот, таких как глицин, серии и аланин. Особенно предпочтительными являются линкеры, состоящие только из молекул глицина и серина. Предпочтительно линкерные последовательности по изобретению состоят из 5-15 аминокислот. Более предпочтительно, чтобы линкеры LI, L2, L3 антитела против CD3*CD19 по изобретению были выбраны из следующих последовательностей:
LI : (XXS)k, где k=2-3, L2: (XXS)n, где n=4-5, L3: (XXS)m, где m=2-3, X=G.
В одном из воплощений в антителе по изобретению LI, L2, L3 могут быть представлены последовательностями, соответствующими SEQ ID NO: 17, SEQ ID NO: 18, SEQ ID NO: 19.
В одном из воплощений посредством короткого шарнирного участка каждая из указанных цепей присоединена к Fc-последовательности IgG2 человека. Биспецифическая молекула в отсутствие FC фрагмента и шарнирной области также связывается с CD3 и CD19 антигенами, вследствие малой молекулярной массы не взаимодействует с Fc-рецепторами и поэтому быстро выводится из кровотока.
Шарнирная область представляет собой последовательность, которая в природном иммуноглобулине связывает СН1 -домен с областью СН2-СН3 Fc-фрагмента. Шарнирная область, используемая в антителе по изобретению предпочтительно гомологична природной области иммуноглобулина и обычно включает цистеиновые остатки, связывающие две тяжелые цепи посредством дисульфидных связей, как в природных иммуноглобулинах. Типичные последовательности шарнирных областей иммуноглобулинов человека и мыши можно найти в ANTIBODY ENGINEERING, а PRACTICAL GUIDE, (Borrebaeck, ed., W.H. Freeman and Co., 1992). Подходящие шарнирные области по настоящему изобретению могут происходить от IgG1, IgG2, IgG3, IgG4 и других изотипов иммуноглобулинов. В представленном воплощении в конструкции антитела по изобретению использована шарнирная область IgG1 с последовательностью, представленной в SEQ ID NO: 15.
Fc фрагмент представляет собой концевую часть молекулы иммуноглобулина, которая взаимодействует с Fc-рецептором на поверхности клетки и с некоторыми белками системы комплемента. В зависимости от аминокислотной последовательности константной области тяжелых цепей иммуноглобулины подразделяют на классы: IgA, IgD, IgE, IgG и IgM, и некоторые из них могут быть дополнительно разделены на подклассы (изотипы), например, IgG1, IgG2, IgG3 и IgG4, IgA1 и IgA2. В соответствии с константными областями тяжелых цепей различные классы иммуноглобулинов называют [альфа], [дельта], [эпсилон], [гамма] и [мю], соответственно. Четыре изотипа человеческого IgG связывают различные рецепторы, такие как неонатальный Fc-рецептор, активирующие Fc-рецепторы гамма, FcgRI, FcgRJIa и FcgRIIIa, ингибирующий рецептор FcgRIIb и Clq с различной аффинностью, получая разные виды активности. Однако термин "Fc-последовательность" в рамках настоящего изобретения относится, в том числе, к Fc-последовательностям, модифицированным для изменения сродства к соответствующему рецептору. Антитело по настоящему изобретению содержит Fc-часть, чтобы продлить период полураспада. Такая Fc-последовательность имеет предпочтительно человеческое происхождение, более предпочтительно, представляет собой человеческую Fc- последовательность антитела IgG, более предпочтительно IgG2. В одном из предпочтительных воплощений последовательность соответствует SEQ ID NO: 16. При этом выбор Fc-последовательности типа IgG2 позволяет обеспечить снижение эффекторной нагрузки, обусловленной Fc-последовательностью и снизить таким образом направленную токсичность антитела по изобретению.
Таким образом, молекула, включающая предложенные по изобретению новые антиген-связывающие участки CD3 антигена, конструируется на основе единого каркаса, где вариабельные домены легкой и тяжелой цепей для связывания CD3 и CD19 антигенов соединены тремя линкерными участками в определенном порядке. Дополнительные функциональные свойства молекуле добавляет присоединение к ней Fc фрагмента посредством шарнирной области.
На основании предложенных CD3-антигенсвязывающих фрагментов авторы изобретения получили набор антител, имеющих различные последовательности вариабельных участков легкой и тяжелой цепи для связывания CD3, соединенных в биспецифическую молекулу согласно указанной выше единой схеме. Был получен ряд антителоподобных молекул, полные последовательности которых приведены в списке последовательностей, №№1-14. Последовательности CDR для связывания CD19 воссозданы на основании известного антитела HD37, являются общими для всех биспецифических антител и представляют собой для тяжелой цепи:
CDRH1: GYAFSSY
CDRH2: WIGQIWPGDGDTNYNGKFKG
CDRH3: RETTTVGRYYYAMDY
Для легкой цепи:
CDRL1: KASQSVDYDGDSYLN
CDRL2: DASNLVS
CDRL3: QQSTEDPWT
Последовательности CDR, обеспечивающие связывание молекулы с антигенами CD3, для каждого из антител приведены в таблице 2.
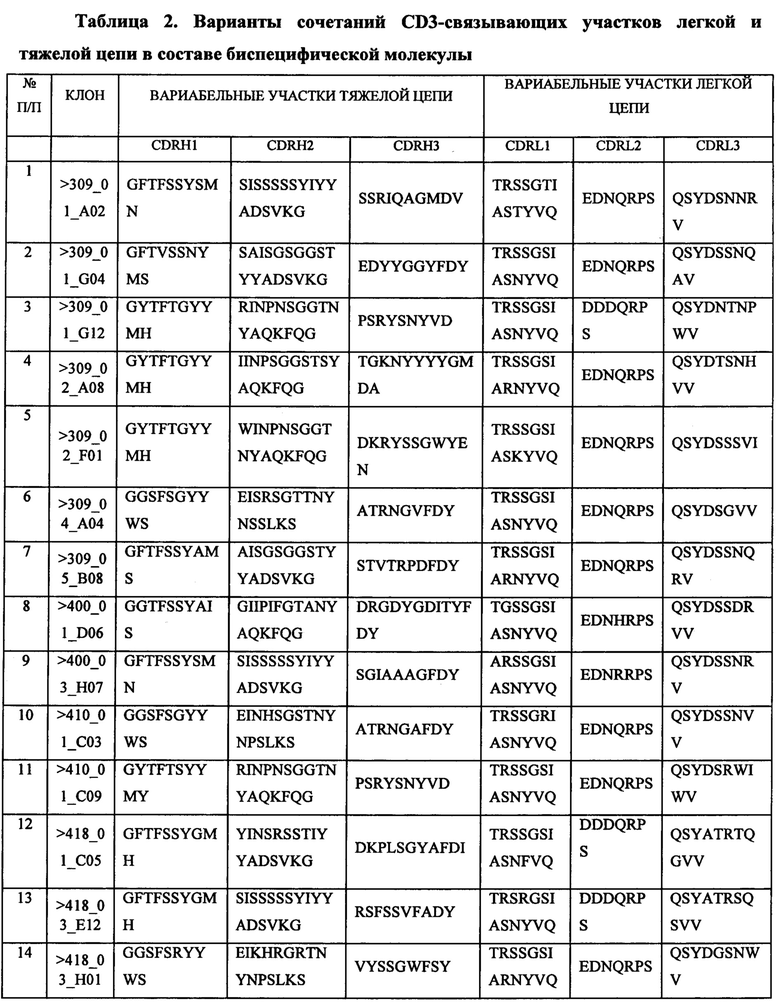
Активность и специфичность полученных антител подтверждена рядом примеров.
Функционально активные биспецифические IgG-подобные молекулы были подвергнуты скринингу на предмет связывания с эндогенным белком CD3, присутствующим на поверхности клеток линии Jurkat в составе Т-клеточного рецепторного комплекса. Сначала связывание с клетками линии Jurkat оценивали путем проточной цитометрии для одной концентрации биспецифических IgG-подобных молекул 100 нМ; все 14 биспецифических IgG-подобных молекул демонстрировали связывание с клетками. Для дальнейшего определения профиля связывания с клетками каждого клона биспецифические IgG-подобные молекулы-кандидаты титровали и оценивали зависимое от концентрации связывание с клетками линии Jurkat (результаты представлены на Фиг. 8). Эти эксперименты были проведены отдельно для двух независимых серий клонов антител к CD3. Для сравнения приведены данные для применявшихся в качестве положительных контролей двух биспецифических IgG-подобных молекул, содержащих ОКТ3 в роли связывающегося с CD3 фрагмента и HD37, связывающегося с CD19. В качестве негативного контроля использовали BiM8_D1.3, в котором одноцепочечный вариабельный фрагмент (scFv) антитела к CD3 замещен на одноцепочечный вариабельный фрагмент (scFv) антитела к лизоциму (D1.3). Все антитела к CD3 оказались способными связываться с нативным CD3 на поверхности клеток, хотя максимальные сигналы и активность существенно варьировались между клонами. Как и ожидалось, контрольный BiM_D1.3 не связывался с клетками ни в одной из исследованных концентраций.
Фиг. 9. демонстрирует сравнительную способность биспецифического антитела по изобретению и терапевтического антитела по патенту RU2651776 одновременно связывать CD3 и CD19 с использованием клеток человеческой линии Raji и эффекторных репортерных клеток.
Весь набор антител, имеющих заявленную структуру, был протестирован на цитолитическую активность в отношении CD19-позитивных клеток-мишеней в репортерном TDCC-тесте. Эффективность цитолиза CD19-позитивных клеток человеческой линии Raji препаратами различных вариантов предложенных БСАТ при использовании в качестве эффекторных клеток активированных МКПК условно здоровых доноров продемонстрирована на Фиг. 10.
Была подтверждена способность биспецифических антител вызывать активацию и пролиферацию CD3-позитивных клеток в ответ на контакт с CD19-позитивными клетками-мишенями и вызывать выброс провоспалительных цитокинов Т клетками.
Таким образом, приведенные данные показывают, что молекулы, созданные с использованием предложенных вариантов CDR, могут быть с высокой эффективностью продуцированы в культуре клеток, обладают функциональными свойствами, не уступающими известным биспецифическим CD3-CD19 направленным молекулам и, следовательно, могут быть использованы при разработке лекарственных препаратов, применяемых при лечении В-клеточных заболеваний.
Препарат на основе биспецифической молекулы, связывание которых с антигеном CD3 обеспечивается включением в состав указанной молекулы вариантов легкой и тяжелой цепи, содержащих CDR, перечисленные в таблице 2, может быть применен для терапии пре-В-клеточного отрицательного по филадельфийской хромосоме рецидивирующего или рефрактерного острого лимфобластного лейкоза. Механизм действия обеспечивается связыванием БСАТ с CD19-рецептором на поверхности В-лимфоцитов и с CD3-рецептором на поверхности эффекторных Т-лимфоцитов и инициирует активацию Т клеток, которая приводит к лизису CD19-позитивных В-клеток.
Для указанных антител была определена специфичность и эффективность взаимодействия с CD3- и CD19-позитивными человеческими клеточными линиями с использованием проточной цитометрии. Предложенные молекулы специфично связываются с CD3-позитивными клеточными линиями (Jurkat, HUT-78, CCRF-CEM) и CD19-позитивными клеточными линиями (Raji, NALM6, Daudi, Namalwa, Ramos и др.). Эксперименты in vitro доказывают, что молекулы по настоящему изобретению могут демонстрировать в 7 раз более высокую цитотоксическую активностью в сравнении с молекулами, обладающими альтернативной доменной структурой.
Подтверждением физиологической активности предложенной молекулы послужили следующие эксперименты: была определена концентрация препарата, при которой 50% CD3- и CD19- рецепторов находятся в комплексе с биспецифической молекулой с использованием МКПК условно здоровых доноров; определена Т-клеточно-опосредованная цитолитическая активность препарата в отношении CD19-позитивных клеток-мишеней опухолевых линий человека при использовании в качестве эффекторных клеток активированных МКПК условно здоровых доноров. Способность одновременно связывать CD3 и CD19 подтверждена с помощью клеток линии Raji и клеток коммерческой репортерной линии Jurkat-LUCIA-NFAT (Promega).
Примеры 1-4 показывают, что антитело по изобретению имеет высокое сродство к таргетным CD3- и CD19-позитивным человеческим клеточным линиям в субнаномолярном диапазоне. Концентрация, при которой выявляли 50% свободных CD3-рецепторов при инкубации с РВМС условно здоровых доноров, варьировала от 52,1 до 66,5 nM. Концентрация, при которой выявляли 50% свободных CD19-рецепторов, варьировала от 0,02 до 0,06 nM в зависимости от донора. Препарат БСАТ проявлял Т-опосредованную цитолитическую активность в отношении CD19-позитивных клеток-мишеней человеческой линии Raji при использовании в качестве эффекторных клеток МКПК условно здоровых доноров. ЕС50 варьировала от 1,3 рМ до 3,1 рМ, а процент максимального лизиса клеток-мишеней - от 41 до 100, в зависимости от донора. В репортерном тесте ЕС50 составила 2,3 рМ. Оба метода подтверждают одновременное связывание препарата 309_02_А08 по изобретению с CD3- и CD19- позитивными клетками.
Все молекулы по настоящему изобретению могут быть получены с использованием рутинных методов, применяемых в настоящее время для получения терапевтических белковых молекул с известной первичной структурой. Ген, кодирующий полипептидную цепь, имеющую любую из предложенных аминокислотных последовательностей, получают путем отжига перекрывающихся химически синтезированных олигонуклеотидов и затем клонируют в экспрессионный вектор рМТ1638. Полученный вектор рМТ1638 верифицируется рестрикционным картированием и секвенированием. После этого проводят трансфекцию с последующей селекцией по резистентности к пуромицину с использованием стандартных методов. Трансфекцию проводят с использованием коммерчески доступного штамма СНО-K1, адаптированного к суспензионному росту. Выбор линии клеток-продуцентов обусловлен необходимостью формирования оптимального профиля гликозилирования при синтезе человеческих белков, а также их стабильностью, безопасностью и возможностью применения суспензионных условий культивирования данной линии клеток, что является важнейшими параметрами для производства терапевтических антител. Культивирование продуцента проводится в режиме fed-batch с использованием питательной среды BalanCD СНО Growth A (Irvine Scientific) и нутриентной добавки BalanCD® СНО Feed 4 (Irvine Scientific) в течение 11 суток при температуре 37°С (1-6 сутки), 32°С (7-11 сутки) и 5% CO2 в газовой фазе инкубатора. После культивирования культуральная жидкость осветляется центрифугированием.
Для выделения и очистки целевого продукта из культуральной жидкости могут быть применены различные известные методы очистки антител. Может быть использована, например, схема, включающая аффинную стадию с использованием сорбента на основе протеина А и катионообменную хроматографию на сорбенте высокого разрешения, обеспечивающую эффективное разделение целевой формы белка и его олигомерных форм.
Пример 1. Определение специфичности и эффективности взаимодействия молекулы БСАТ с CD3- и CD19-позитивными клетками человека.
Клеточные суспензии CD19-позитивных клеточных линий (NALM6 (АТСС® CRL-3273™), Toledo (АТСС® CRL-2631™), Namalwa (АТСС® CRL-1432™), Daudi (АТСС® CCL-213™), Ramos (RA 1) (АТСС® CRL-1596™), Raji (АТСС® CCL-86™)) и CD3-позитивных клеточных линий (HuT78 (АТСС® TIB-161™), CCRF-CEM (АТСС® CCL-119™), Jurkat (АТСС® TIB-152™)) с концентрацией 2*106 клеток в мл вносили по 30 мкл в 96-луночный планшет с V-образным дном (Corning Inc, кат. №3894). Вносили в лунки с клетками по 30 мкл раствора БСАТ клон 309_02_А08 в последовательных 3-кратных разведениях от 200 nM до 0,003 nM (финальные концентрации от 100 nM до 0,0016 nM). Инкубировали 60 мин на льду. По окончанию инкубации дважды отмывали клетки FACS буфером, осаждая клетки центрифугированием при 1000 об/мин (4±2)°С. К осадку клеток добавляли по 30 мкл раствора антител к человеческому IgG, меченных FITC, (Donkey F(ab)2 Anti-Human IgG, Abcam, кат. № Ab102437) в разведении 1:200. Инкубировали 30 мин на льду в темноте с последующей трехкратной отмывкой FACS буфером. После отмывки клетки фиксировали, ресуспендируя клеточный осадок в каждой лунке в 150 мкл FIX-буфера (фосфатно-солевой буфер с 1% раствором формалина). Интенсивность флуоресценции клеток в FITC-канале измеряли на цитометре Canto II.
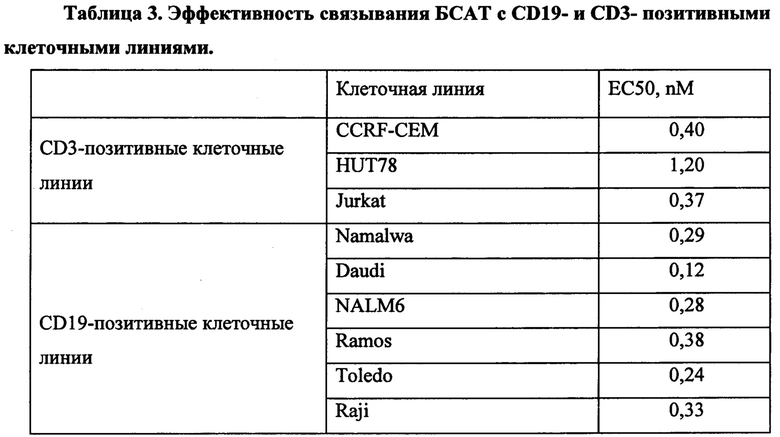
Показано, что БСАТ специфично связывается с CD19- и CD3- позитивными клеточными линиями с субнаномолярным аффинитетом. Результаты экспериментов продемонстрированы на фигурах 1 и 2 и в таблице 3.
Пример 2. Определение концентрации препарата БСАТ, при которой 50% CD3- и CD19- рецепторов находятся в комплексе с антителом, с использованием МКПК условно здоровых доноров
Выделение мононуклеарных клеток периферической крови (МКПК).
Кровь условно здоровых доноров стерильно отбирали в вакутейнеры с гепарином (Greiner Bio-One, кат. №455084). Кровь разбавляли равным объемом фосфатно-солевого буфера (ЭКО сервис, кат. № В-60201), наслаивали на градиент плотности фиколла (ρ=1,077 г/см3) («ПанЭко», кат. № Р052) и центрифугировали в течение 30 минут при 800 g при температуре (20±2)°С. Собирали МКПК на границе фаз и дважды отмывали клетки изотоническим фосфатно-солевым буферным раствором. Осадок клеток ресуспендировали в 15 мл среды ДМЕМ/Ф12 (Sigma, кат. № D8900-10L) с 10% фетальной бычьей сыворотки (GE Healthcare, кат. № SV30160) и инкубировали 4 часа в культуральном флаконе (SPL Life Sciences Со, кат. №70075) при температуре (37±2)°С для прикрепления моноцитов. По окончанию инкубации собирали неприкрепленные клетки, клеточную суспензию центрифугировали, осадок клеток ресуспендировали в FACS буфере с добавлением раствора Fc Blook в разведении 1:100 (BD Pharmingen™, кат. №564220) для ингибирования неспецифичного связывания Fc-рецепторов, экспонированных на мембране В-клеток. Приготовленную суспензию МКПК с концентрацией клеток 4*106/мл вносили по 50 мкл (2*105 клеток на лунку) в 96-луночный планшет с V-образным дном (Corning Inc, кат. №3894).
Связывание БСАТ с CD19-позитивными мононуклеарными клетками периферической крови условно здоровых доноров.
К клеткам добавляли по 50 мкл раствора БСАТ клон 309_02_А08 в последовательных 3-кратных разведениях в FACS буфере с добавлением Fc Block 1:100 от 200 nM до 0,003 nM (финальные концентрации - от 100 до 0,0016 nM). Инкубировали 60 минут при температуре (37±2)°С. По окончанию инкубации дважды отмывали клетки ледяным FACS буфером, осаждая клетки центрифугированием в течение 10 мин при 1300 об/мин и температуре (5±3)°С. После этого осадок клеток ресуспендировали в 100 мкл FACS буфера и добавляли антитела к экстраклеточной части человеческого рецептора CD19 (клон HD37), меченные FITC (Millipore milli-mark, кат. № FCMAB184F) в объеме 10 мкл, конечное разведение 1:150, инкубировали 30 минут при температуре (5±3)°C с последующей трехкратной отмывкой. Клетки фиксировали ресуспендированием в 250 мкл FIX-буфера (фосфатно-солевой буферный раствор с 1% раствором формалина). Интенсивность флуоресценции клеток в FITC-канале измеряли на цитометре Canto II. Для достоверности получаемых данных собирали не менее 50000 событий.
Связывание препарата БСАТ с CD3-позитивными мононуклеарными клетками периферической крови условно здоровых доноров
К клеткам добавляли по 50 мкл раствора БСАТ клон 309_02_А08 в последовательных 3-кратных разведениях в FACS буфере с добавлением Fc Block (1:100) от 8700 nM до 0,04 nM (финальные концентрации - от 2900 nM до 0,01 nM). Затем готовили раствор биотинилированного БСАТ с концентрацией 300 nM и вносили в лунки с клетками по 50 мкл (финальная концентрация препарата 100 nM). Инкубировали 60 минут при температуре (37±2)°С. По окончанию инкубации клетки дважды отмывали клетки ледяным FACS буфером, осаждая клетки центрифугированием в течение 10 мин при 1300 об/мин и температуре (5±3)°С. Осадок клеток ресуспендировали в 100 мкл FACS буфера и добавляли конъюгат PE-Streptavidin (BD Pharmingen, кат. №554061) в объеме 10 мкл (конечное разведение 1:200), инкубировали 30 минут при температуре (5±3)°C с последующей трехкратной отмывкой. Клетки фиксировали ресуспендированием в 250 мкл FIX-буфера (фосфатно-солевой буферный раствор с 1% раствором формалина). Интенсивность флуоресценции клеток в РЕ-канале измеряли на цитометре Canto II. Для достоверности получаемых данных собирали не менее 50000 событий.
Обработку данных проводили с помощью программного обеспечения FlowJo, Excel и GraphPad Prism 6.0 с использованием 4-х параметрической логистической функции дозозависимого ингибирования, и функции "constrain - shared value" для значений верхней и нижней асимптот и угла наклона сигмоидной кривой (hill slope). Определяли дозу полумаксимального ингибирования (IC50) и коэффициент достоверности аппроксимации функции (R2).
Результаты.
Концентрация БСАТ, при которой выявляли 50% свободных CD19-рецепторов, и соответственно, 50% CD19-рецепторов находились в комплексе с антителом, варьировала от 0,02 до 0,06 nM в зависимости от донора (фигура 3).
Концентрация БСАТ, при которой выявляли 50% свободных CD3-рецепторов, и соответственно, 50% CD3-рецепторов находились в комплексе с антителом, варьировала от 52,1 до 66,5 nM в зависимости от донора (фигура 4).
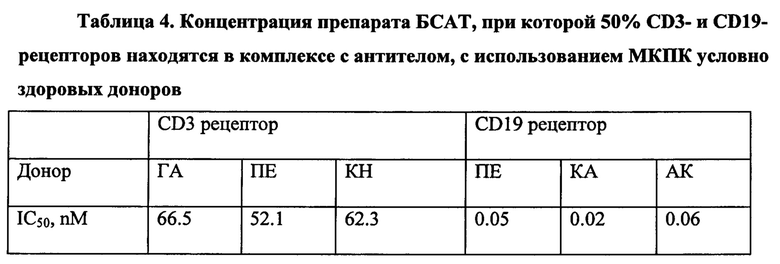
Пример 3. Определение Т-клеточно опосредованной цитолитической активности БСАТ в отношении CD19-позитивных клеток-мишеней опухолевых линий человека при использовании в качестве эффекторных клеток активированных МКПК условно здоровых доноров
Выделение и активация мононуклеарных клеток периферической крови (МКПК).
Выделяли МКПК условно здоровых доноров проводили, как описано в примере 2. К 5 мл суспензии РВМС с концентрацией 2*106 кл/мл в среде ДМЕМ/Ф12 (Sigma, кат. № D8900-10L) с 10% фетальной бычьей сыворотки (GE Healthcare, кат. № SV30160) добавляли IL-2 (Abcam, кат. № ab155694) до конечной концентрации 5 нг/мл и магнитные частицы Dynabeads с иммобилизованными на них антителами к человеческим рецепторам CD3 и CD28 для активации Т-лимфоцитов человека (Gibco, кат. №11131D) в объеме 65 мкл. Клетки инкубировали в течение 5-7 дней при температуре (37±2)°С в атмосфере (5,0±0,5)% СО2 с ежедневным подсчетом количества клеток, при необходимости добавляли среду ДМЕМ/Ф12 (Sigma, кат. № D8900-10L), содержащую 10% фетальной бычьей сыворотки (GE Healthcare, кат. № SV30160) и IL-2 в концентрации 5 нг/мл.
Постановка метода.
Клетки-мишени человеческой линии Raji (АТСС® CCL-86™) дважды отмывали от культуральной среды изотоническим фосфатно-солевым буферным раствором, осаждая клетки центрифугированием в течение 10 минут при 1300 об/мин и температуре (22±2)°С. Осадок клеток ресуспендировали в изотоническом фосфатно-солевом буферном растворе и добавляли 10 мкл 1 mM раствор кальцеина (Molecular Probes, кат. № С3100МР) из расчета 10 мкл раствора кальцеина на 1 млн клеток и инкубировали в течение 40 минут. По окончанию инкубации клетки трижды отмывали от свободного кальцеина изотоническим фосфатно-солевым буферным раствором. Доводили плотность клеточной суспензии до 2×105 клеток в мл средой ADCF-Mab (GE Healthcare Life Sciences, кат. № SH30349.02) и добавляли 1/100 объема 100Х раствора пробенецида (Sigma-Aldrich, кат. № P8761-25G).
Активированные IL-2/CD3/CD28 Т-клетки осаждали центрифугированием в течение 10 минут при 1300 об/мин и температуре (22±2)°С, однократно промывали изотоническим фосфатно-солевым буферным раствором. Осадок клеток ресуспендировали в среде ADCF-Mab и доводили клеточную суспензию до концентрации 4×106 клеток в мл.
Делали 12 последовательных 3-кратных разведения БСАТ клон 309_02_А08 от 100 до 0,0005 рМ и каждый раствор вносили в трипликатах по 50 мкл в лунки 96-луночного плоскодонного планшета (Corning Inc, кат. №3599). Затем в лунки планшета с препаратом вносили по 50 мкл активированных IL-2/CD3/CD28 Т-клеток и по 50 мкл клеток Raji (соотношение Т-клеток к клеткам Raji 10:1). В лунки планшета вносили также 1) клетки-мишени, меченные кальцеином (контроль спонтанного выхода кальцеина); 2) клетки-мишени, меченные кальцеином, с эффекторными клетками (лизис клеток, обусловленный цитолитической активностью эффекторных клеток без добавления препарата 309_02_А08); 3) клетки-мишени, меченные кальцеином, для последующей обработки раствором тритона X100 (Sigma-Aldrich, кат. № X100-1L). Инкубировали 3 часа при температуре (37±2)°С.
Через 3 часа в лунки с клетками Raji, меченными кальцеином, вносили по 20 мкл 10% раствора Тритона X100, для полного лизиса клеток (MFI_max) и инкубировали 1 час при температуре (37±2)°С.
По окончанию инкубации планшет центрифугировали 5 минут при 1300 об/мин и с помощью многоканальной пипетки аккуратно, чтобы не захватить клетки, переносили по 120 мкл супернатанта из каждой лунки в планшеты из непрозрачного белого пластика (Corning Inc, кат. №3912) для измерения флуоресценции. Флуоресценцию измеряли на планшетном спектрофотометре Tecan Infinite М200 при длине возбуждения 488 нм и эмиссии при 518 нм. Полученные данные экспортировали в программу Excel и рассчитывали эффективность лизиса в каждой экспериментальной лунке по формуле:
% специфичного лизиса = (MFIexp-MFI_min)/(MFI_max-MFI_min)*100%.
Дальнейшую обработку данных проводили с помощью программного обеспечения GraphPad Prism 6.0 с использованием 4-х параметрической логистической функции и функции "constrain - shared value" для значений верхней и нижней асимптот и угла наклона сигмоидной кривой (hill slope). Определяли полумаксимальную эффективную дозу (ЕС50) и коэффициент достоверности аппроксимации функции (R2).
Результаты.
Препарат БСАТ проявлял цитолитическую активность в отношении CD19-позитивных клеток-мишеней человеческой линии Raji при использовании в качестве эффекторных клеток МКПК условно здоровых доноров. ЕС50 варьировала от 1,3 рМ до 3,1 рМ, а процент максимального лизиса клеток-мишеней - от 41 до 100, в зависимости от донора. Результаты экспериментов представлены на фигуре 5.
Пример 4. Определение Т-клеточно опосредованной активности БСАТ с использованием клеток коммерческой репортерной линии Jurkat-LUCIA-NFAT (Promega) в качестве эффекторных клеток
Описание метода.
Клеточную линию Raji (ATCC®CCL-86™) культивировали согласно рекомендациям производителя. Клетки-мишени человеческой линии Raji (АТСС® CCL-86™) дважды отмывали от культуральной среды изотоническим фосфатно-солевым буферным раствором, осаждая клетки центрифугированием в течение 10 минут при 1300 об/мин и температуре (22±2)°С. Осадок клеток ресуспендировали в среде для выполнения теста (RPMI-1640 без фенолового красного (Lonza, кат № BE12918F) с 5% фетальной бычьей сыворотки (GE Healthcare, кат. № SV30160)). Готовили 5 мл клеточной суспензии с концентрацией 2×105 клеток в мл.
Клеточную линию Jurkat-Luc-NFAT (эффекторные клетки) (Promega, кат. №jktl-nfat) размораживали на водяной бане при температуре (37±2)°С. Содержимое ампулы переносили в центрифужную пробирку, содержащую 5 мл среды для выполнения теста, и центрифугировали 5 минут при 1000 об/мин. Осадок клеток ресуспендировали в среде для выполнения теста. Делали 5 мл клеточной суспензии с концентрацией 2,5×106 клеток/мл.
Готовили 11 последовательных 3-кратных разведений БСАТ клон 309_02_А08 от 1200 рМ до 0,02 рМ (финальные концентрации - от 400 до 0,007 рМ) в среде для выполнения теста.
В лунки А2-Н12, U-образного 96-луночного культурального планшета (Corning Inc, кат. №3799) вносили растворы препарата в трипликатах по 40 мкл, начиная с минимальной концентрации. В лунки А1-Н1 вносили по 40 мкл среды. Смешивали подготовленные суспензии клеток Raji и Jurkat-Luc-NFAT и вносили по 80 мкл во все лунки (А1-Н12) планшета. Планшет инкубировали 18 часов при температуре (37±2)°С.
По окончанию инкубации содержимое лунок планшета ресуспендировали и переносили по 40 мкл суспензии в лунки 96-луночного плоскодонного планшета из белого непрозрачного пластика (Corning Inc, кат. №3912). Затем в каждую лунку вносили по 25 мкл подогретого до комнатной температуры (20±5)°С субстрата QUANTI-Luc™ Lucia™ (Invivogen, кат. № rep-qlc1, rep-qlc2). Содержимое лунок аккуратно перемешивали. Интенсивность хемилюминесценции измеряли на планшетном спектрофотометре Tecan Infinite М200.
Полученные данные обрабатывали с использованием программного обеспечения GraphPad Prism 6.0. Зависимость уровня хемилюминесценции от десятичного логарифма концентрации препарата БСАТ аппроксимировали уравнением 4-параметрической логарифмической функции. Автоматически определяли ЕС50 и R2.
Результаты.
При совместном культивировании клеточной линии Raji с клетками Jurkat-Luc-NFAT в присутствии БСАТ наблюдали дозозависимое увеличение сигнала хемилюминесценции, ЕС50 составила 2,3 рМ. Результаты эксперимента представлены на Фиг. 6.
Пример 5. Оценка функциональной активности и специфичности биспецифических антител путем анализа активации клеток линии Jurkat
Активацию Т-клеток измеряли с использованием клеток линии Jurkat с репортерным геном, закупленных у компании Promega. Данные об активности (ЕС50) 14 биспецифических IgG-подобных антител к CD3 приведены в таблице 1, а полные кривые зависимости доза-ответ представлены на Фиг. 7. Исследуемые биспецифические IgG-подобные молекулы титровали и оценивали их способность индуцировать транскрипцию NFAT в эффекторных клетках линии Jurkat в присутствии или в отсутствие клеток-мишеней, экспрессирующих CD19 (т.е. оценивали мишень-зависимую и мишень-независимую активацию). Все биспецифические IgG-подобные молекулы демонстрировали высокую мишень-зависимую активность в этом анализе. Также приведены данные для применявшихся в качестве положительных контролен двух различных биспецифических IgG-подобных молекул, в которых ОКТ3 используется как связывающийся с CD3 фрагмент (коетроли 1 и 2). В качестве негативного контроля использовали BiM8_D1.3 (в котором одноцепочечный вариабельный фрагмент (scFv) антитела к CD3 замещен на аналогичный фрагмент антитела к лизоциму куриного яйца D1.3). Для этого анализа используются модифицированные путем генной инженерии клетки линии Jurkat, стабильно экспрессирующие репортерный ген люциферазы, регулируемый элементом ответа ядерного фактора активированных Т-клеток (NFAT). Совместное культивирование этих репортерных клеток с экспрессирующими CD19 клетками линии Raji в присутствии функциональных биспецифических антител к CD3/CD19 приводит к активации Т-клеточного рецепторного комплекса и увеличению активности люциферазы, обусловленному активацией элемента ответа NFAT.
Готовые к использованию после размораживания клетки линии GloResponse™ NFAT-Re-luc2 Jurkat (каталожный номер компании Promega CS176403) были разморожены в течение 2 минут на водяной бане при температуре 37°С и осторожно перенесены в предварительно нагретую среду для анализа RPMI 1640 (каталожный номер компании Gibco 22400) объемом 4 мл с добавлением 10% фетальной бычьей сыворотки (каталожный номер компании HyClone SH30070.03). По 25 мкл ресуспендированных клеток было помещено в каждую лунку белого 96-луночного планшета для анализа (каталожный номер компании Costar 3917), итоговое количество клеток линии Jurkat в каждой лунке составило 1×105. Суспензия клеток линии Raji была приготовлена в концентрации 2×106/мл в среде для анализа, и по 25 мкл суспензии было добавлено в лунки, содержащие репортерные клетки линии Jurkat (количество клеток линии Raji в каждой лунке составило 5×104). Было добавлено по 5,5 мкл исследуемой биспецифической IgG-подобной молекулы (или используемого в качестве контроля растворителя, если применимо), и образцы инкубировали при температуре 37°С в течение 5 часов (статический инкубатор, 5% CO2). По завершении инкубации планшеты для анализа были оставлены при комнатной температуре (21°С) на 15 минут, после чего в лунки было добавлено по 55 мкл реагента Bio-Glo (каталожный номер компании Promega G7940, реагент был растворен в соответствии с инструкцией производителя). Наконец, планшеты инкубировали в течение 5 минут (21°С), и измеряли люминесценцию при помощи прибора BMG Pherastar.
Низкий уровень мишень-независимой активации клеток линии Jurkat является многообещающим свойством всех клонов предложенных биспецифических IgG-подобных молекул.
Перечень последовательностей
Пискунов А.А., Аббасова С.Г., Морозов А.Н., Шустер А.М., Петер Славни, Даниел Гриффитс, Изабеле Касзинска, Джон МcCафферти, Михаел Дайсон
Определяющие комплементарность участки для связывания CD3 и содержащая их биспецифическая антигенсвязывающая молекула.
SEQ ID NO:1 (>309_01_A02)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAEVQLVESGG
GLVKPGGSLRLSCAASGFTFSSYSMNWVRQAPGKGLEWVSSISSSSSYIYYADSVKGRFTISRDN
AKNSLYLQMNSLRAEDTAVYYCARSSRIQAGMDVWGQGTLVTVSSGGGGSGGGGSGGGASN
FMLTQPHSVSESPGKTVTISCTRSSGTIASTYVQWYQQRPGSSPTTVIYEDNQRPSGVPDRFSGS
IDSSSNSASLTISGLKTEDAADYFCQSYDSNNRVFGGGTKVTVLGQPAAAGGGGSQVQLQQSG
AELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKGKAT
LTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVECPP
CPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPR
EEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSREE
MTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQ
GNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:2 (>309_01_G04)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAEVQLVESGG
GVVQPGRSLRLSCAASGFTVSSNYMSWVRQAPGKGLEWVSAISGSGGSTYYADSVKGRFTTSR
DNSKNTLYLQMNSLRAEDTAIYYCAKEDYYGGYFDYWGQGTMVTVSSGGGGSGGGGSGGGA
SNFMLTQPHSVSESPGKTVTISCTRSSGSIASNYVQWYQQRPGSSPTTVIYEDNQRPSGVPDRFS
GSIDSSSNSASLTISGLKTEDEADYYCQSYDSSNQAVFGGGTKVTVLGQPAAAGGGGSQVQLQ
QSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKG
KATLTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVE
CPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKT
KPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPS
REEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRW
QQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:3 (>309_01_G12)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAEVQLVQSGA
EVKKPGASVKVSCKASGYTFTGYYMHWVRQAPGQGLEWMGRINPNSGGTNYAQKFQGRVT
MTRDTSISTAYMELSRLRSDDAAVYYCARPSRYSNYVDWGQGTTVTVSSGGGGSGGGGSGGG
ASNFMLTQPHSVSESPGKTVTISCTRSSGSIASNYVQWYQQRPGSAPTTVIYDDDQRPSGVPDR
FSGSIDRSSNSASLTISGLKTEDEADYYCQSYDNTNPWVFGGGTKLTVLGQPAAAGGGGSQVQL
QQSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFK
GKATLTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAA
VECPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNA
KTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLP
PSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSR
WQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:4 (>309_02_A08)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAQVQLVQSGA
EVKKPGASVKVSCKASGYTFTGYYMHWVRQAPGQGLEWMGIINPSGGSTSYAQKFQGRVTM
TRDTSTSTVYMELSSLRSEDTAVYYCARTGKNYYYYGMDAWGQGTTVTVSSGGGGSGGGGSG
GGASNFMLTQPHSVSESPGKTVTISCTRSSGSIARNYVQWYQQRPGSSPTTVIYEDNQRPSGVP
DRFSASIDSSSNSASLTISGLQTEDEADYYCQSYDTSNHVVFGGGTKLTVLGQPAAAGGGGSQV
QLQQSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGK
FKGKATLTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASA
AVECPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHN
AKTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTL
PPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKS
RWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:5 (>309_02_F01)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAEVQLVQSGA
EVKKPGASVKVSCKASGYTFTGYYMHWVRQAPGQGLEWMGWINPNSGGTNYAQKFQGRVT
MTRDTSISTAYMELSSLRSEDTAVYYCARDKRYSSGWYENWGQGTLVTVSSGGGGSGGGGSG
GGASNFMLTQPHSVSESPGKTVTISCTRSSGSIASKYVQWYQQRPGSSPTTVIYEDNQRPSGVP
DRFSGSIDISSNSASLTISGLKTEDEADYFCQSYDSSSVIFGGGTKLTVLGQPAAAGGGGSQVQLQ
QSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKG
KATLTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVE
CPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKT
KPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPS
REEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRW
QQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:6 (>309_04_A04)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAQVQLQQWG
AGLLKPSETLSLTCAVYGGSFSGYYWSWIRQPPGKGLEWIGEISRSGTTNYNSSLKSRVTISVDTS
KNQFSLKLSSVTAADTAVYYCARATRNGVFDYWGQGTLVTVSSGGGGSGGGGSGGGASNFM
LTQPHSVSESPGKTVTISCTRSSGSIASNYVQWYQQRPGSAPSTVIYEDNQRPSGVPDRFSGSID
SSSNSASLTISGLKTEDEADYYCQSYDSGVVFGGGTKLTVLGQPAAAGGGGSQVQLQQSGAELV
RPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKGKATLTAD
ESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVECPPCPAP
PVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPREEQF
NSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSREEMTK
NQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQGNVF
SCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:7 (>309_05_B08)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAEVQLLESGGG
LVQPGGSLRLSCAASGFTFSSYAMSWVRQAPGKGLEWVSAISGSGGSTYYADSVKGRFTISRDN
SKNTLYLQMNSLRAEDTAVYYCAISTVTRPDFDYWGQGTLVTVSSGGGGSGGGGSGGGASNF
MLTQPHSVSESPGKTVTISCTRSSGSIARNYVQWYQQRPGSAPTTVIYEDNQRPSGVPDRFSGSI
DSSSNSASLTISGLKTEDEADYYCQSYDSSNQRVFGGGTKVTVLGQPAAAGGGGSQVQLQQSG
AELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKGKAT
LTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVECPP
CPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPR
EEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSREE
MTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQ
GNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:8 (>400_01_D06)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAQVQLVQSGA
EVKKPGSSVKVSCKASGGTFSSYAISWVRQAPGQGLEWMGGIIPIFGTANYAQKFQGRVTITAD
ESTSTAYMEVRSLRSDDTAVYYCVRDRGDYGDITYFDYWGQGTLVTVSSGGGGSGGGGSGGG
ASNFMLTQPHSVSESPGKTVTISCTGSSGSIASNYVQWYQQRPGSAPTIVIYEDNHRPSGVPDR
FSGSIDSSSNSASLTISGLKTEDEADYYCQSYDSSDRVVFGGGTKVTVLGQPAAAGGGGSQVQL
QQSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFK
GKATLTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAA
VECPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNA
KTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLP
PSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSR
WQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:9 (>400_03_H07)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAQVQLVESGG
GVVQPGRSLRLSCAASGFTFSSYSMNWVRQAPGKGLEWVSSISSSSSYIYYADSVKGRFTISRDN
AKNSLYLQMNSLRAEDTAVYYCARSGIAAAGFDYWGQGTLVTVSSGGGGSGGGGSGGGASN
FMLTQPHSVSESPGKTVTISCARSSGSIASNYVQWYQQRPGSSPTTVIYEDNRRPSGVPDRFSGS
FDSSSNSASLTISGLKTEDEADYYCQSYDSSNRVFGGGTKLTVLGQPAAAGGGGSQVQLQQSG
AELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKGKAT
LTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVECPP
CPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPR
EEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSREE
MTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQ
GNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:10 (>410_01_C03)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAQVQLQQWG
AGLLKPSETLSLTCAVYGGSFSGYYWSWIRQPPGKGLEWIGEINHSGSTNYNPSLKSRVTISVDTS
KNQFSLKLSSVTAADTAVYYCARATRNGAFDYWGQGTLVTVSSGGGGSGGGGSGGGASNFM
LTQPHSVSESPGKTVTISCTRSSGRIASNYVQWYQQRPGSSPTTVIYEDNQRPSGVPDRFSGSID
SSSNSASLTISGLKTEDEADYYCQSYDSSNVVFGGGTQLTVLGQPAAAGGGGSQVQLQQSGAE
LVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKGKATLT
ADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVECPPC
PAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPRE
EQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSREE
MTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQ
GNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:11 (>410_01_C09)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAEVQLVQSGA
EVKKPGASVKVSCKASGYTFTSYYMYWVRQAPGQGLEWMGRINPNSGGTNYAQKFQGRVT
MTRDTSISTAYMELSRLRSDDTAVYYCARPSRYSNYVDWGQGTLVTVSSGGGGSGGGGSGGG
ASNFMLTQPHSVSESPGKTVTISCTRSSGSIASNYVQWYQQRPGSSPTTVIYEDNQRPSGVPDR
FSGSIDSSSNSASLTISGLKTEDEADYYCQSYDSRWIWVSGGGTKVTVLGQPAAAGGGGSQVQL
QQSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFK
GKATLTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAA
VECPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNA
KTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLP
PSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSR
WQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:12 (>418_01_C05)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAEVQLVESGG
GVVQPGRSLRLSCAASGFTFSSYGMHWVRQAPGKGLEWVSYINSRSSTIYYADSVKGRFTISRD
NAKNSLYLQMNSLRDEDTAVYYCAKDKPLSGYAFDIWGQGTTVTVSSGGGGSGGGGSGGGAS
NFMLTQPHSVSESPGKTVTISCTRSSGSIASNFVQWYQQRPGRAPTIVIFDDDQRPSGVPDRFS
GSIDRSSDSASLSISGLKTEDEADYYCQSYATRTQGVVFGGGTKVTVLGQPAAAGGGGSQVQLQ
QSGAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKG
KATLTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVE
CPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKT
KPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPS
REEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRW
QQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:13 (>418_03_E12)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAQVQLVESGG
GVVQPGRSLRLSCAASGFTFSSYGMHWVRQAPGKGLEWVSSISSSSSYIYYADSVKGRFTISRDN
AKNSLYLQMNSLRADDTAVYYCARRSFSSVFADYWGQGTLVTVSSGGGGSGGGGSGGGASNF
MLTQPHSVSESPGKTVTISCTRSRGSIASNYVQWYQQRPGRAPTIVIFDDDQRPSGVPDRFSGSI
DRSSDSASLRISGLKTEDEADYYCQSYATRSQSVVFGGGTKLTVLGQPAAAGGGGSQVQLQQS
GAELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKGKA
TLTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVECP
PCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKP
REEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSRE
EMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQ
GNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:14 (>418_03_H01)
DIQLTQTPASLAVSLGQRATISCKASQSVDYDGDSYLNWYQQIPGQPPKLLIYDASNLVSGIPPRF
SGSGSGTDFTLNIHPVEKVDAATYHCQQSTEDPWTFGGGTKLEIKGGSGGAMAQVQLQQWG
AGLLKPSETLSLTCAVYGGSFSRYYWSWIRQSPGKGLEWIGEIKHRGRTNYNPSLKSRVTMSVDT
SKNQFSLQLRSVTAADTAVYYCARVYSSGWFSYWGQGTLVTVSSGGGGSGGGGSGGGASNF
MLTQPHSVSESPGKTVTISCTRSSGSIARNYVQWYQQRPGSAPTTVIYEDNQRPSGVPDRFSGSI
DSSSNSASLTISGLKTEDEADYYCQSYDGSNWVFGGGTKVTVLGQPAAAGGGGSQVQLQQSG
AELVRPGSSVKISCKASGYAFSSYWMNWVKQRPGQGLEWIGQIWPGDGDTNYNGKFKGKAT
LTADESSSTAYMQLSSLASEDSAVYFCARRETTTVGRYYYAMDYWGQGTSVTVSSASAAVECPP
CPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPR
EEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSREE
MTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQ
GNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO:15 (шарнирная область)
VECPPCP
SEQ ID NO:16 (Fc-фрагмент IgG2 человека)
APPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
SEQ ID NO: 17 (линкер 1)
GGSGGAMA
SEQ ID NO: 18 (линкер 2)
GGGGSGGGGSGGGAS
SEQ ID NO: 19 (линкер 3)
AAAGGGGS
| название | год | авторы | номер документа |
|---|---|---|---|
| БИСПЕЦИФИЧЕСКИЕ АСИММЕТРИЧНЫЕ ГЕТЕРОДИМЕРЫ, СОДЕРЖАЩИЕ АНТИ-CD3 КОНСТРУКЦИИ | 2013 |
|
RU2650868C2 |
| ТЕСТ-СИСТЕМА ДЛЯ АНАЛИЗА ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ АНТИТЕЛ ПРОТИВ PD-1 И АНТИТЕЛ ПРОТИВ PD-L1 | 2019 |
|
RU2731896C1 |
| НОВЫЕ БИСПЕЦИФИЧНЫЕ ПОЛИПЕПТИДНЫЕ КОМПЛЕКСЫ ПРОТИВ CD3/CD19 | 2018 |
|
RU2788127C2 |
| НОВЫЕ БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, ОБЛАДАЮЩИЕ СПОСОБНОСТЬЮ СПЕЦИФИЧЕСКИ СВЯЗЫВАТЬСЯ С CD40 И FAP | 2018 |
|
RU2766234C2 |
| CD19XCD3-СПЕЦИФИЧЕСКИЕ ПОЛИПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ | 1999 |
|
RU2228202C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2012 |
|
RU2650775C2 |
| УЛУЧШЕННЫЙ СИНТЕТИЧЕСКИЙ Т-КЛЕТОЧНЫЙ РЕЦЕПТОР И АНТИГЕННЫЙ РЕЦЕПТОР | 2021 |
|
RU2820497C1 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА ПРОТИВ CD3*CD19 | 2015 |
|
RU2651776C2 |
| Вирус-кодируемые регулируемые агенты, связывающие T-клетки (CATVERT) или NK-клетки (CATVERN), нацеленные на рак | 2020 |
|
RU2827779C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С CD3 | 2019 |
|
RU2810924C2 |

Изобретение относится к области иммунологии и биотехнологии. Предложена антигенсвязывающая молекула, способная связывать рецепторный комплекс CD3, содержащая вариабельные домены легкой и тяжелой цепи, охарактеризованные аминокислотными последовательностями определяющих комплементарность участков (CDR). Кроме того, рассмотрено применение биспецифической антигенсвязывающей молекулы, способной связывать CD3 и CD19, для создания лекарственного средства для лечения злокачественных заболеваний В-клеточной природы или истощения В-клеток, в частности для лечения гематологических злокачественных заболеваний В-клеточной природы, таких как острый лимфобластный лейкоз и В-клеточные лимфомы, включая их рефрактерные или рецидивирующие формы. Благодаря способности связывать CD3 и активировать Т-клетки антигенсвязывающая молекула по настоящему изобретению может быть использована при конструировании различных биспецифических терапевтических антител. 2 н. и 10 з.п. ф-лы, 11 ил., 5 табл., 5 пр.
1. Антигенсвязывающая молекула, способная связывать рецепторный комплекс CD3, содержащая по меньшей мере один антигенсвязывающий фрагмент, включающий вариабельный домен легкой цепи и вариабельный домен тяжелой цепи, отличающаяся тем, что аминокислотные последовательности определяющих комплементарность участков тяжелой цепи HCDR1, HCDR2 и HCDR3 и определяющих комплементарность участков легкой цепи LCDR1, LCDR2 и LCDR3 в составе указанной молекулы выбраны из одного из следующих вариантов сочетаний последовательностей для определяющих комплементарность участков:
а) GFTFSSYSMN, SISSSSSYIYYADSVKG, SSRIQAGMDV, TRSSGTIASTYVQ, EDNQRPS, QSYDSNNRV;
б) GFTVSSNYMS, SAISGSGGSTYYADSVKG, EDYYGGYFDY, TRSSGSIASNYVQ, EDNQRPS, QSYDSSNQAV;
в) GYTFTGYYMH, RINPNSGGTNYAQKFQG, PSRYSNYVD, TRSSGSIASNYVQ, DDDQRPS, QSYDNTNPWV;
г) GYTFTGYYMH, IINPSGGSTSYAQKFQG, TGKNYYYYGMDA, TRSSGSIARNYVQ, EDNQRPS, QSYDTSNHVV;
д) GYTFTGYYMH, WINPNSGGTNYAQKFQG, DKRYSSGWYEN, TRSSGSIASKYVQ, EDNQRPS, QSYDSSSVI;
е) GGSFSGYYWS, EISRSGTTNYNSSLKS, ATRNGVFDY, TRSSGSIASNYVQ, EDNQRPS, QSYDSGVV;
ж) GFTFSSYAMS, AISGSGGSTYYADSVKG, STVTRPDFDY, TRSSGSIARNYVQ, EDNQRPS, QSYDSSNQR;
з) GGTFSSYAIS, GIIPIFGTANYAQKFQ, DRGDYGDITYFDY, TGSSGSIASNYVQ, EDNHRPS, QSYDSSDRVV;
и) GFTFSSYSMN, SISSSSSYIYYADSVKG, SGIAAAGFDY, ARSSGSIASNYVQ, EDNRRPS, QSYDSSNRV;
к) GGSFSGYYWS, EINHSGSTNYNPSLKS, ATRNGAFDY, TRSSGRIASNYVQ, EDNQRPS, QSYDSSNVV;
л) GYTFTSYYMY, RINPNSGGTNYAQKFQG, PSRYSNYVD, TRSSGSIASNYVQ, EDNQRPS, QSYDSRWIWV;
м) GFTFSSYGMH, YINSRSSTIYYADSVKG, KPLSGYAFDI, TRSSGSIASNFVQ, DDDQRPS, QSYATRTQGVV;
н) GFTFSSYGMH, SISSSSSYIYYADSVKG, RSFSSVFADY, TRSRGSIASNYVQ, DDDQRPS, QSYATRSQSVV;
о) GGSFSRYYWS, EIKHRGRTNYNPSLKS, VYSSGWFSY, TRSSGSIARNYVQ, EDNQRPS, QSYDGSNWV.
2. Молекула по п. 1, которая моновалентно и специфически связывает CD3, расположенный на Т-лимфоцитах человека.
3. Молекула по любому из пп. 1, 2, которая является частью биспецифической антигенсвязывающей молекулы.
4. Молекула по любому из пп. 1-3, которая содержит вторую антигенсвязывающую полипептидную конструкцию, которая моновалентно и специфически связывает CD19, расположенный на В-лимфоцитах человека.
5. Молекула по любому из пп. 1-4, последовательность которой включает (а) первый домен, включающий антигенсвязывающий участок молекулы по любому из пп. 1-5, и (б) второй домен, содержащий антигенсвязывающий участок цепи иммуноглобулина или антитела, который специфически распознает антиген CD19 В-клеток человека, причем домены, формирующие антигенсвязывающие участки, расположены в следующем порядке: VLCD3-VHCD19-VHCD19-VLCD3.
6. Молекула по любому из пп. 1-5, которая дополнительно содержит Fc фрагмент.
7. Молекула по любому из пп. 1-6, которая способна индуцировать активацию Т-клеток в формате биспецифического антитела.
8. Молекула по любому из пп. 1-7, аминокислотная последовательность которой включает в себя последовательности, выбранные из списка SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:8, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14.
9. Применение молекулы по любому из пп. 4, 5, 8 для создания лекарственного средства для лечения злокачественных заболеваний В-клеточной природы или истощения В- клеток.
10. Применение по п. 9, где лекарственное средство включает молекулу по любому из пп. 4, 5, 8 в эффективном количестве, и необязательные нейтральные носители из круга традиционно применяющихся в композициях этого назначения.
11. Применение по п. 10, где злокачественное заболевание В-клеточной природы выбрано из острого лимфобластного лейкоза и В-клеточных лимфом.
12. Применение по п. 11, где заболевание проходит в рефрактерной или рецидивирующей форме.
Авторы
Даты
2020-12-17—Публикация
2019-08-21—Подача