В настоящем изобретении предложен новый FACS-анализ антитело-обусловленной цитотоксичности на основе трехмерного сфероида или агрегата, образованного клетками лимфомы и естественными клетками-киллерами. Указанный метод можно применять для осуществления функциональных анализов in vitro терапевтических иммуноглобулинов как индивидуально, так и в широкомасштабном формате.
Предпосылки создания изобретения
При проведении базового биологического исследования опухолей и при разработке противоопухолевых лекарственных средств часто применяют монослойные культуры созданных линий опухолевых клеток. Однако двухмерная, иными словами плоская, модель культуры не отражает в достаточной степени трехмерную (3D) архитектуру опухоли. Таким образом, специфические аспекты, связанные с развитием in vivo диффузионных градиентов растворимых веществ, можно изучать только с использованием трехмерной культуральной системы, например, такой как многоклеточная модель опухоли в виде сфероида или агрегата. Содержащие опухолевые клетки сфероиды или агрегаты имитируют несосудистые области опухоли, отличающиеся ограниченной поставкой питательных веществ из-за барьеров для диффузии, создаваемых многоклеточными слоями.
Однако широкое применение 3D-культур в исследовательских целях сдерживается сложностями, связанными с их созданием и обращением с ними. Поэтому разработан простой и быстрый способ создания индивидуальных сфероидов или агрегатов в суспензионной культуре в широкомасштабном формате. Индивидуальные сфероиды или агрегаты одинакового размера и с гомогенной сферической геометрией можно получать в индивидуальных лунках 96-луночного планшета в течение 24-часового периода культивирования. Это представляет собой стандартизованный формат культуры, хорошо приспособленный для обработки соединением и пригодный для сбора сфероидов для последующего анализа. Одинаковый размер и геометрия гарантируют получение практически идентичных диффузионных градиентов в каждом сфероиде или агрегате (Ivascu А. и Kubbies М., J. Biomol. Screening 11, 2006, сс.922-932). Известный протокол создания сфероидов предусматривает добавление экстракта мышиных базальных мембран (rBM), смеси внеклеточных матриксных белков, которые индуцируют уплотнение агрегата с образованием сфероида.
Inami K. с соавторами описали противоопухолевую активность моноклонального антител к C-ERC/мезотелину in vivo (Cancer Sci. 101, 2010, сс.969-974).
Краткое изложение сущности изобретения
При создании изобретения было установлено, что применение комбинации опухолевых клеток и естественных клеток-киллеров в виде трехмерного сфероида или агрегата позволяет, с одной стороны, сделать оценку иммуноглобулинов более приближенной к условиям in vivo, а с другой стороны, позволяет осуществлять с использованием настоящего изобретения широкомасштабный анализ.
Первым объектом настоящего изобретения является способ оценки in vitro эффекторной функции антитела, заключающийся в том, что осуществляют стадию, на которой инкубируют трехмерный сфероид или агрегат, содержащий опухолевые клетки и естественные клетки-киллеры, с иммуноглобулином.
Согласно одному из вариантов осуществления изобретения способ заключается в том, что осуществляют стадии, на которых:
а) метят опухолевые клетки-мишени первым флуоресцентным красителем,
б) смешивают естественные клетки-киллеры и опухолевые клетки-мишени,
в) добавляют примерно 104 клеток на 200 мкл в лунку многолуночного планшета,
г) центрифугируют многолуночный планшет и тем самым инициируют образование трехмерного клеточного сфероида,
д) добавляют иммуноглобулин в лунки многолуночного планшета,
е) инкубируют многолуночный планшет в течение промежутка времени, составляющего от примерно 20 до примерно 72 ч,
ж) метят мертвые клетки в лунках с помощью второго флуоресцентного красителя, и
з) анализируют клетки в лунках многолуночного планшета с помощью клеточного сортера с возбуждением флуоресценции (FACS) и тем самым оценивают эффекторную функцию антитела.
В одном из вариантов осуществления изобретения естественные клетки-киллеры представляют собой человеческие естественные клетки-киллеры и имеют чистоту 90% или более. В другом варианте осуществления изобретения естественные клетки-киллеры и опухолевые клетки-мишени смешивают в соотношении от 10:1 до 1:10. В следующем варианте осуществления изобретения соотношение составляет от 1:3 до 1:10. В другом варианте осуществления изобретения соотношение составляет от 1:2 до 1:4. В одном из вариантов осуществления изобретения центрифугирование осуществляют в течение 10 мин при 100-1000 об/мин. В следующем варианте осуществления изобретения центрифугирование осуществляют примерно при 1000 об/мин. В одном из вариантов осуществления изобретения второй флуоресцентный краситель представляет собой йодид пропидия (PI). В одном из вариантов осуществления изобретения продолжительность инкубации составляет от примерно 20 до примерно 28 ч.
В одном из вариантов осуществления изобретения опухолевые клетки представляют собой клетки лимфомы. В другом варианте осуществления изобретения клетку лимфомы выбирают из группы, включающей Raji-клетки, SU-DHL4-клетки и Z138-клетки. В другом варианте осуществления изобретения антитело добавляют так, чтобы конечная концентрация в лунке составляла от 100 до 0,001 мкг/мл. В следующем варианте осуществления изобретения антитело добавляют так, чтобы конечная концентрация в лунке составляла от 20 до 0,1 мкг/мл. В одном из вариантов осуществления изобретения антитело добавляют так, чтобы конечная концентрация в лунке составляла от 8 до 12 мкг/мл.
Следующим объектом изобретения является применение трехмерного сфероида или агрегата, содержащего опухолевые клетки и естественные клетки-киллеры, для широкомасштабного анализа комбинации множества антител и множества опухолевых клеток.
Следующим объектом изобретения является способ выявления in vitro антитела, которое обладает эффекторной функцией, заключающийся в том, что
а) получают по меньшей мере одно антитело,
б) метят опухолевые клетки-мишени первым флуоресцентным красителем,
в) смешивают естественные клетки-киллеры и опухолевые клетки-мишени,
г) добавляют примерно по 104 клеток на 200 мкл в лунки многолуночного планшета,
д) центрифугируют многолуночный планшет и тем самым инициируют образование трехмерного клеточного сфероида,
е) добавляют каждое из полученных антител в индивидуальную лунку многолуночного планшета,
ж) инкубируют многолуночный планшет в течение промежутка времени, составляющего от примерно 20 до примерно 72 ч,
з) метят мертвые клетки в каждой из подвергнутых инкубации лунок с помощью второго флуоресцентного красителя,
и) анализируют каждую лунку многолуночного планшета с помощью клеточного сортера с возбуждением флуоресценции и
к) выявляют антитело, при применении которого обнаружено наиболее высокое соотношение мертвых и жизнеспособных клеток или соотношение мертвых и жизнеспособных клеток, превышающее 1, в качестве антитела, обладающего эффекторной функцией.
Объектом настоящего изобретения является также набор, содержащий:
а) опухолевую клетку, меченную флуоресцентным красителем,
б) выделенные естественные клетки-киллеры,
в) 96-луночный многолуночный планшет и
г) йодид пропидия.
В одном из вариантов осуществления изобретения многолуночный планшет представляет собой 96-луночный многолуночный планшет.
Подробное описание изобретения
В настоящем изобретении предложена клеточная аналитическая технология, основанная на применении анализа совместно культивируемых сфероидов или агрегатов, где сфероиды или агрегаты содержат опухолевые клетки и естественные клетки-киллеры. Согласно одному из вариантов осуществления изобретения указанный анализ можно применять в качестве функционального анализа in vitro иммуноглобулинов как индивидуально, так и в широкомасштабном формате. Согласно одному из вариантов осуществления изобретения индивидуальный трехмерный сфероид или агрегат помещают в каждую лунку 96-луночного круглодонного многолуночного планшета, сенсибилизированную полиНЕМА (поли(гидроксиэтилметакриловая) кислота). Согласно другому варианту осуществления изобретения NK-клетки представляют собой здоровые диплоидные человеческие естественные клетки-киллеры (NK). Согласно одному из вариантов осуществления изобретения NK-клетки отобраны с помощью метода негативной селекции, т.е. таким образом, чтобы клетки не повреждались в процессе стадии селекции (см., например, Horgan K. и др., «Immunomagnetic purification of Т cell subpopulations», Curr. Prot. Immunol., глава 7, раздел 7.4, 2009, и Neurauter А.А. и др., Adv. Biochem. Eng. Biotechnol. 106, 2007, cc. 41-73). Установлено, что с использованием указанных NK-клеток можно точно рассчитывать процентное содержание жизнеспособных и мертвых клеток.
В области биологии опухолей большую часть экспериментов in vitro осуществляют с использованием монослойных культур, поскольку они просты и удобны в обращении. Однако хотя они представляют собой ценную модель при изучении различных функций, монослойные культуры не отражают соответствующим образом патобиологию опухоли, поскольку в них отсутствуют компоненты стромы, внеклеточного матрикса, и существуют фундаментальные геометрические различия между двухмерными (2D) культурами и трехмерными (3D) плотными (солидными) опухолями. Трехмерная организация клеток обеспечивает сложную сеть взаимодействий типа клетка-клетка и клетка-матрикс, относящихся, например, к распределению и функции гормонов, факторов роста и питательных веществ, которые влияют на дифференцировку, пролиферацию и выживание клеток.
Согласно одному из вариантов осуществления изобретения способ создания трехмерных сфероидов из агрегатов заключается в том, что добавляют в культуральную среду восстановленный матрикс базальной мембраны, полученный из мышиной опухоли Энгельбрета-Холма-Суорма (rBM, Matrigel™), белковый гель, содержащий компоненты внеклеточного матрикса, такие как коллагены, ламинин, фибронектин, энтактин (нидоген) и протеогликаны. Трехмерная архитектура позволяет совместно культивировать опухолевые клетки с фибробластами, иммунными и эндотелиальными клетками, что позволяет изучать результаты взаимодействия опухоль/строма in vitro (Friedrich J. и др., Int. J. Radiat. Biol. 83, 2007, cc. 849-871).
При использовании центрифуг (Sutherland R.M. и Durand R.E., Recent Results Cancer Res. 95, 1984, cc. 24-49) и технических средств, обеспечивающих круговое вращение (Moscona A., Exp.Cell Res. 22, 1961, сс.455-475), обработанные трипсином клетки помещают в сосуд для культивирования с магнитной мешалкой, что препятствует прикреплению клеток к субстрату и способствует адгезии по типу клетка-клетка. Согласно более современной методике сфероиды выращивают в висящей капле на перевернутом микропланшете (Kelm J.M. и др., Biotechnol. Bioeng. 83, 2003, сс.173-180). Однако применение всех этих методов ограничено либо продолжительным временем культивирования, либо образованием сфероидов неодинакового размера, либо сложностями, связанными с механической доступностью. Кроме того, в суспензионных культурах из многих линий опухолевых клеток плохо образуются трехмерные компактные сфероиды (Mueller-Klieser W., Crit. Rev. Oncol. Hematol. 36, 2000, cc. 123-139).
Для применения сфероидов или агрегатов в широкомасштабных исследованиях требуется стандартизованный протокол быстрого получения сфероидов одинакового размера со сходными диффузионными градиентами и физиологией клеток в многолуночном формате, который позволяет легко их использовать для последующих биохимических или клеточных анализов. Кроме того, указанный протокол должен быть пригоден для широкого разнообразия линий опухолевых клеток.
При создании изобретения было установлено, что поставленную задачу можно решать с помощью способов, предлагаемых в настоящем изобретении. Таким образом, одним из объектов изобретения является анализ, предназначенный для выявления эффекторной функции антитела, заключающийся в том, что
а) метят клетки (мишени) лимфомы зеленым флуорофором CMFDA (5-хлорметилфлуоресцеиндиацетат),
б) выделяют здоровые человеческие естественные клетки-киллеры (NK) из крови человека, чистота которых согласно одному из вариантов осуществления изобретения составляет более 90%,
в) смешивают NK и клетки лимфомы, представляющие собой мишени, в соотношении от 1:10 до 10:1,
г) добавляют примерно по 104 клеток на 200 мкл в некоторые или во все лунки многолуночного планшета,
д) центрифугируют многолуночный планшет,
е) добавляют представляющий интерес иммуноглобулин в лунки многолуночного планшета,
ж) инкубируют многолуночный планшет в течение промежутка времени, составляющего вплоть до 72 ч, согласно одному из вариантов осуществления изобретения в течение 20-72 ч,
з) добавляют в лунки йодид пропидия и
и) анализируют клетки в лунках многолуночного планшета с помощью FACS.
Было установлено, что при объединении клеток лимфомы и естественных клеток-киллеров можно проводить чувствительный анализ антитело-обусловленной клеточнозависимой цитотоксичности. Согласно одному из вариантов осуществления изобретения выявление эффекторной функции антитела представляет собой выявление или оценку антитело-обусловленной клеточнозависимой цитотоксичности антитела. Кроме того, преимуществом является также созданный трехмерный анализ опухоли и иммуноэффекторной функции клеток. Согласно одному из вариантов осуществления изобретения способы, предлагаемые в изобретении, представляют собой способы in vitro. Согласно другому варианту осуществления изобретения смешение опухолевых клеток и естественных клеток-киллеров приводит к образованию трехмерного сфероида.
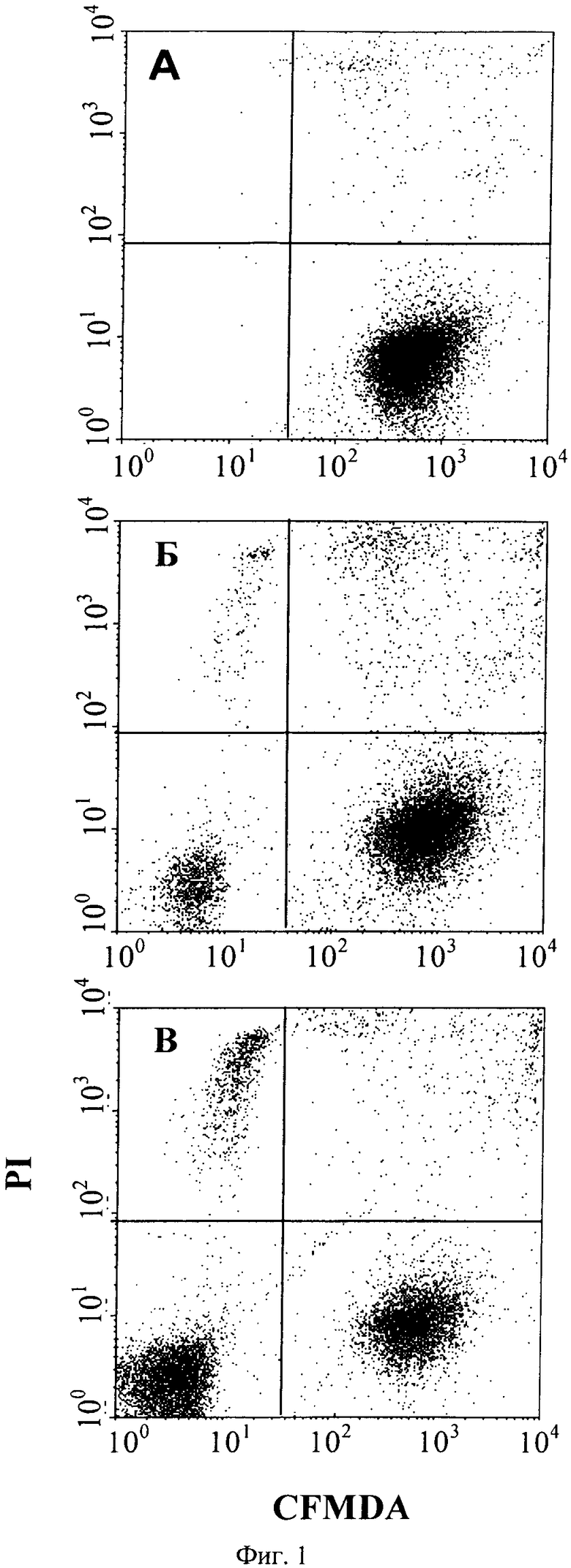
На фиг.1 и 2 показано распределение жизнеспособных и мертвых клеток, проанализированных с помощью FACS. На фиг.1 показано распределение жизнеспособных и мертвых Raji-клеток, меченных с помощью CMFDA, по данным FACS-анализа. Жизнеспособные Raji-клетки локализованы в нижнем правом секторе FACS-диаграммы. На фиг 16 и 1в показано распределение живых и мертвых клеток при совместном культивировании Raji-клеток и естественных клеток-киллеров без добавления антитела. Жизнеспособные естественные клетки-киллеры локализованы в нижнем левом секторе FACS-диаграммы, жизнеспособные Raji-клетки локализованы в нижнем правом секторе FACS-диаграммы, мертвые естественные клетки-киллеры локализованы в верхнем левом секторе FACS-диаграммы, а мертвые Raji-клетки локализованы в верхнем правом секторе FACS-диаграммы. Из фиг.1Б (соотношение Raji-клеток и NK-клеток 1:1) и 1В (соотношение Raji-клеток и NK-клеток 1:10) видно, что в отсутствии антитела и вне зависимости от соотношения Raji-клеток и естественных клеток-киллеров количество жизнеспособных и мертвых клеток лимфомы существенно не изменялось.
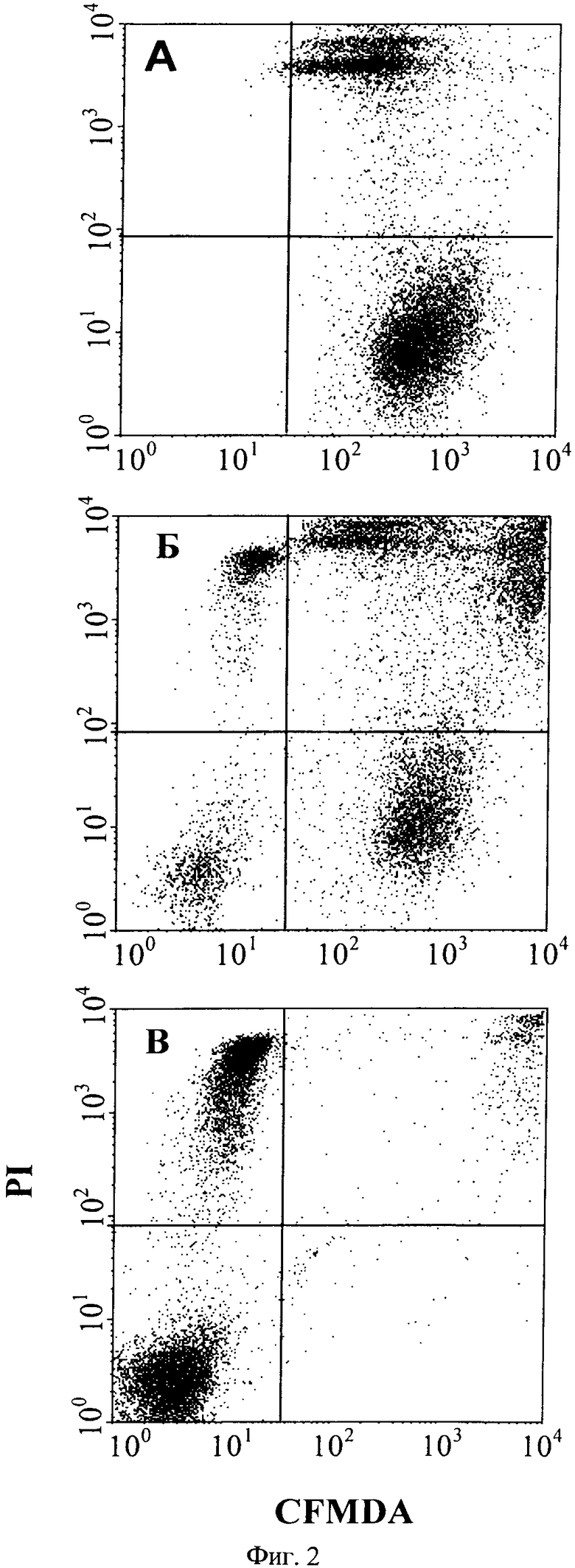
На фиг.2А показаны результаты FACS-анализа жизнеспособных и мертвых Raji-клеток после инкубации с антителом. При сравнении с FACS-диаграммой, представленной на фиг.1А, видно, что при инкубации Raji-клеток только с антителом фракция мертвых клеток повышалась в результате способности антитела вызывать непосредственную гибель клеток. В присутствии NK-клеток количество мертвых Raji-клеток возрастало еще больше в результате эффекторной ADCC-функции (верхние правые кластеры: фиг.2Б - соотношение Raji-клеток/МК-клеток 1:1, а фиг.2В - соотношение Raji-клеток/МК-клеток 1:10). Установлено, что путем добавления естественных клеток-киллеров можно повышать чувствительность анализа.
Согласно одному из вариантов осуществления изобретения при проведении анализа многолуночные планшеты центрифугируют в течение 10 мин при 1000 g. В процессе центрифугирования из всех клеток в каждой лунке образуется дебрис на дне лунки. Это гарантирует наличие одинакового количества клеток, которые участвуют в образовании индивидуального сфероида или агрегата в каждой лунке.
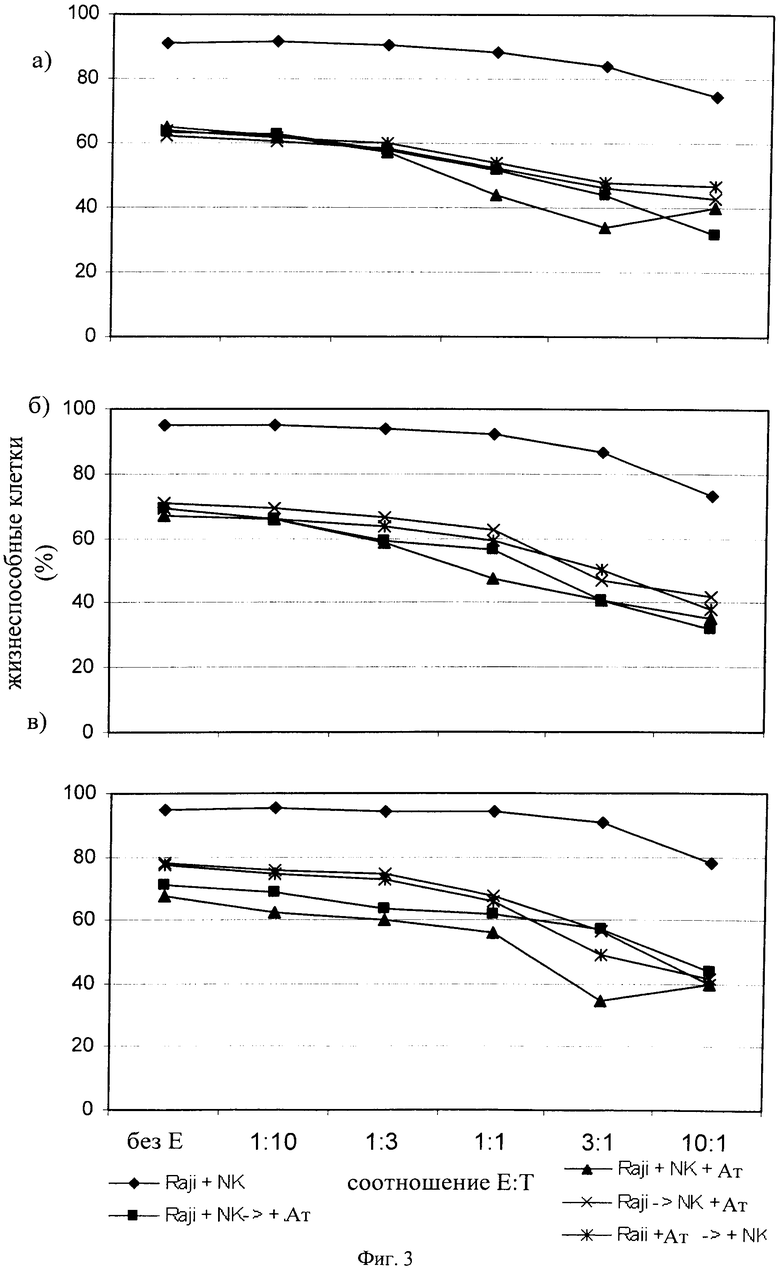
На фиг.3 показано воздействие последовательного введения индивидуальных компонентов, т.е. Raji-клеток, естественных клеток-киллеров и антитела на анализ. Установлено, что введение всех трех компонентов параллельно приводит к небольшому, но значимому повышению уровня гибели клеток. Однако согласно одному из вариантов осуществления изобретения для более точной имитации ситуации in vivo при осуществлении анализа трехмерный(ые) сфероид или агрегаты, содержащий(е) клетки лимфомы-NK, получали перед добавлением подлежащего тестированию антитела.
Анализ, предлагаемый в изобретении, можно осуществлять с использованием любой опухолевой клетки-мишени. Согласно одному из вариантов осуществления изобретения опухолевая клетка представляет собой клетку лимфомы. Согласно другому варианту осуществления изобретения клетку лимфомы выбирают из Raji-клетки, SU-DHL4-клетки и Z138-клетки.
Согласно одному из вариантов осуществления изобретения при применении в качестве опухолевых клеток растущих в прикрепленном состоянии опухолевых клеток карциномы или саркомы образование трехмерного сфероида осуществляли в присутствии жидкой восстановленной базальной мембраны (rMB). Согласно одному из вариантов осуществления изобретения используют rMB в концентрации 2,5 об.%. Согласно этому варианту осуществления изобретения все клетки включали в один конкретный сфероид, имеющий округлую геометрическую форму. Образование и уплотнение завершалось после культивирования в течение 24 ч. Таким образом, согласно одному из вариантов осуществления изобретения продолжительность инкубации составляла от 20 до 28 ч. Более низкие концентрации rMB не гарантировали включение всех клеток в сфероид, а более высокие концентрации ухудшали округлую геометрическую форму сфероидов. После осуществления стадии центрифугирования продолжительностью 10 мин все клетки в лунке оказывались включенными в один плоский дебрис. Через 3 ч становилась заметной некоторая степень уплотнения в присутствии rMB и без rMB. В отсутствие rMB не удалось обнаружить дополнительное уплотнение агрегатов через 6 и 24 ч. Согласно одному из вариантов осуществления изобретения опухолевая клетка представляет собой Raji-клетку и rMB отсутствует на всех стадиях способа.
Согласно одному из вариантов осуществления изобретения пять тысяч клеток центрифугировали в среде RPMI 1640, дополненной 10% FCS (фетальная телячья сыворотка) и 2,5 об.% rMB. Размер сфероида анализировали после культивирования в течение 24 ч. Все сфероиды имели правильную форму, отличающуюся однородным округлым геометрическим строением, и для них была характерна вариация размера в узком диапазоне.
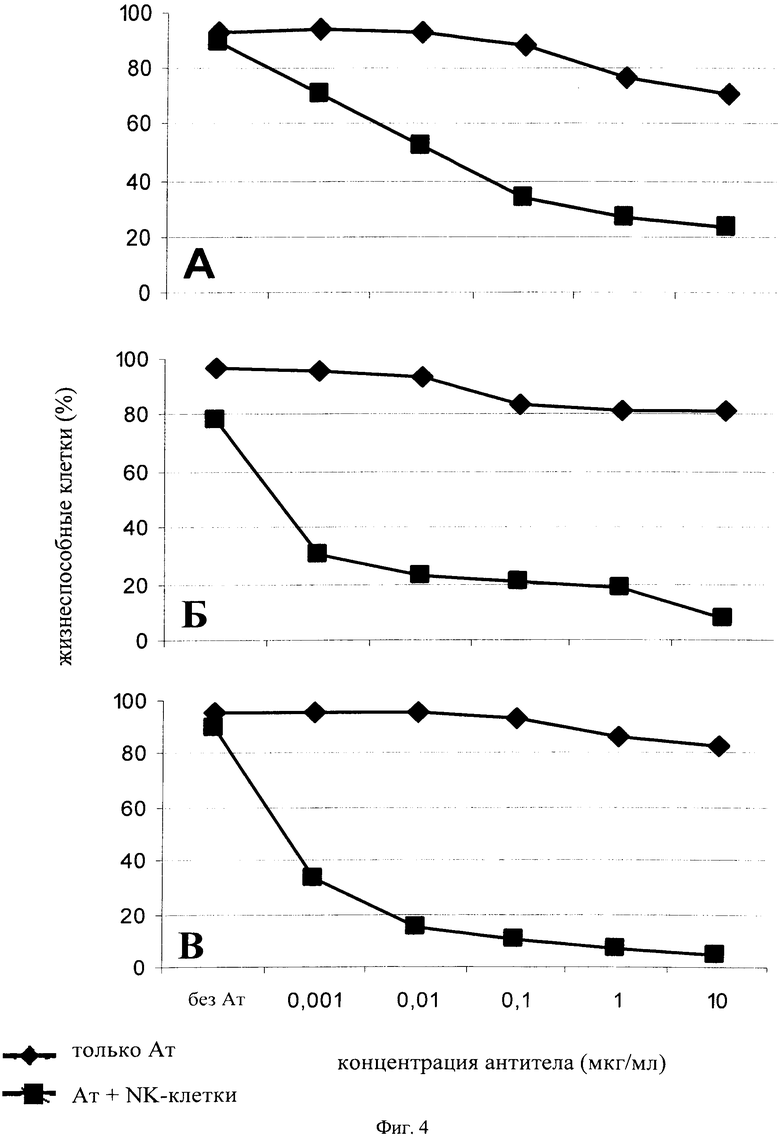
На фиг.4 показы результаты анализа, который осуществляли с использованием различных линий опухолевых клеток лимфомы (мишеней) и антитела в различных концентрациях. Установлено, что анализ, предлагаемый в изобретении, можно осуществлять с одинаковой эффективностью при применении различных клеточных линий лимфом. Продемонстрировано также, что анализ можно осуществлять с использованием антитела в концентрации от 10 до 0,1 мкг/мл. Таким образом, согласно одному из вариантов осуществления анализ, предлагаемый в изобретении, заключается в том, что вносят антитело к концентрации от 0,1 до 15 мкг/мл, в другом варианте осуществления изобретения в концентрации от 8 до 12 мкг/мл.
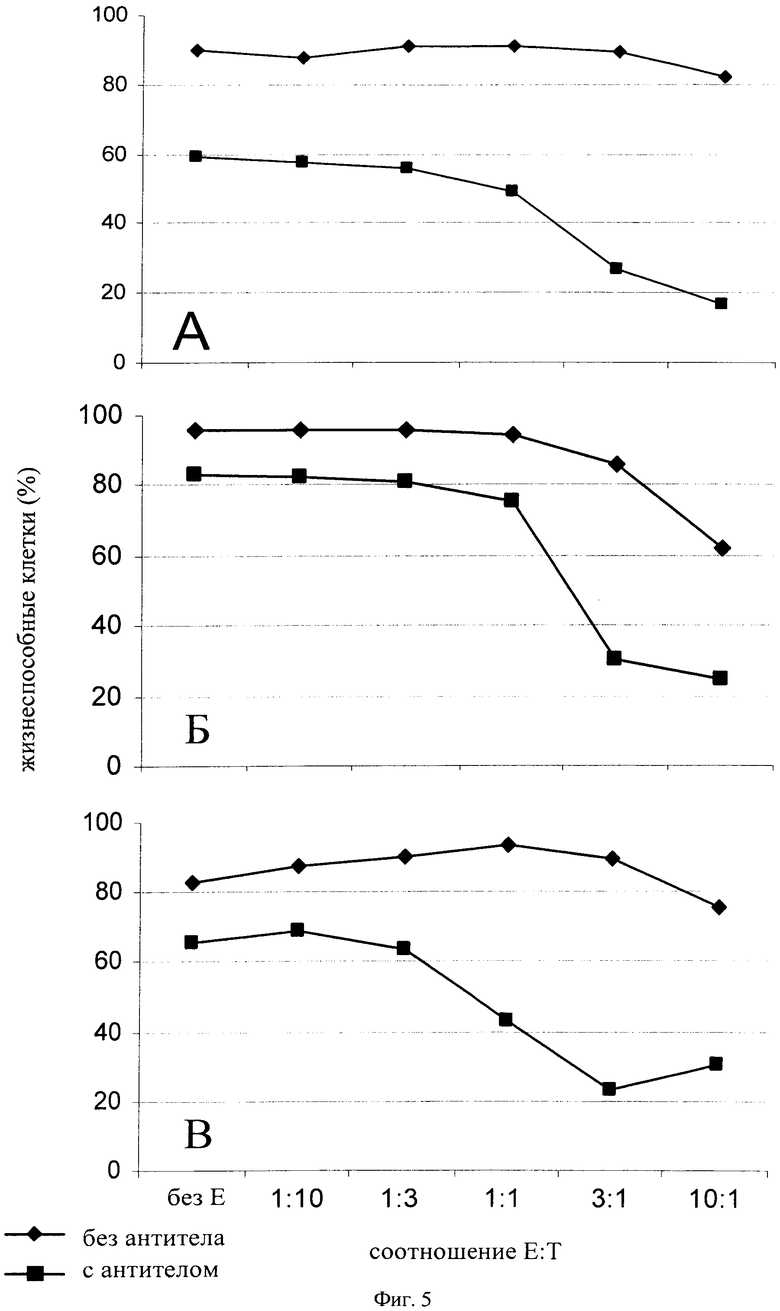
На фиг.5 представлены результаты, характеризующие чувствительность анализа, предлагаемого в изобретении, в зависимости от соотношения клеток лимфомы и естественных клеток-киллеров. Установлено, что при соотношении клеток лимфомы (мишени) и естественных клеток-киллеров от 1:1 до 1:10 проявляется эффекторная ADCC-функция NK-клеток. Таким образом, в одном из вариантов осуществления изобретения соотношение клеток лимфомы и естественных клеток-киллеров составляет от 1:1 до 1:10, в другом варианте осуществления изобретения от 1:3 до 1:10, в следующем варианте осуществления изобретения от 1:2 до 1:4.
При осуществлении анализа, предлагаемого в изобретении, можно получать индивидуальные трехмерные сфероиды или агрегаты, характеризующиеся узким диапазоном распределения размеров и однородной сферической геометрической формой, в индивидуальной лунке или параллельно в нескольких лунках многолуночного планшета в течение периода культивирования продолжительностью 24 ч. Установлено, что этот формат можно рассматривать в качестве стандартизованного формата культуры, который удобно использовать для манипуляции с соединениями и для сбора сфероидов для последующего анализа. Практически однородный размер и геометрия сфероидов или агрегатов гарантирует создание практически одинаковых диффузионных градиентов в каждом сфероиде. Таким образом, одним из объектов изобретения является автоматизированный или широкомасштабный анализ, включающий описанный выше анализ. Протокол создания сфероидов предусматривает добавление экстракта мышиной базальной мембраны (rMB), т.е. смеси внеклеточных матриксных белков, которые индуцируют уплотнение агрегата с образованием сфероида.
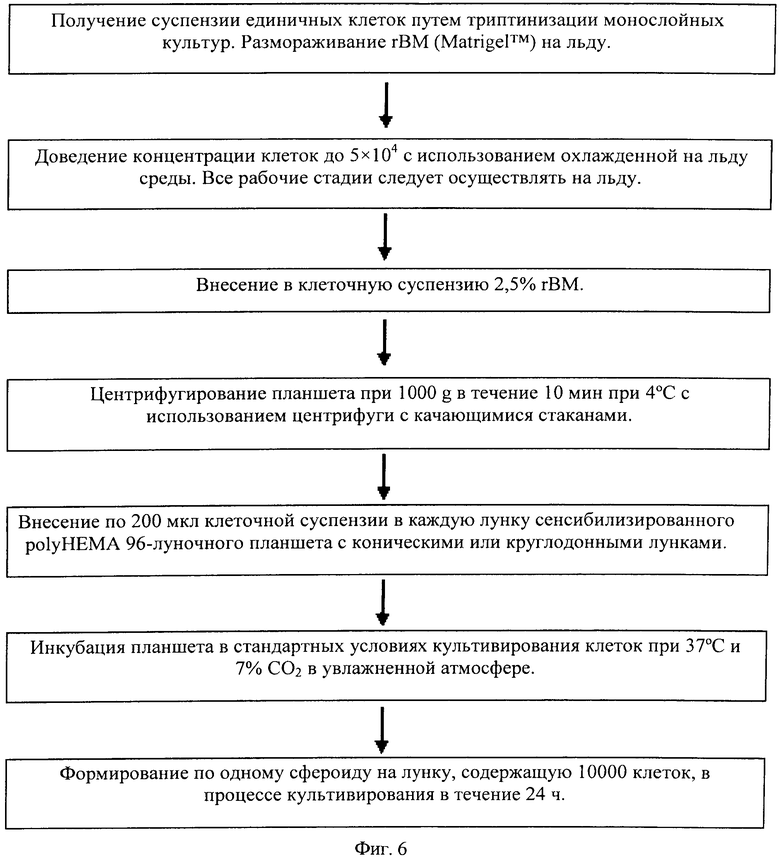
На фиг.6 представлена приведенная в качестве примера схема создания трехмерных сфероидов.
В настоящем описании представлен способ оценки in vitro эффекторной функции антитела, заключающийся в том, что инкубируют трехмерный сфероид или агрегат, содержащий опухолевые клетки и естественные клетки-киллеры, с антителом.
Согласно одному из вариантов осуществления изобретения способ заключается в том, что осуществляют стадии, на которых:
- смешивают естественные клетки-киллеры и опухолевые клетки,
- добавляют примерно по 104 клеток в 200 мкл в лунки многолуночного планшета,
- центрифугируют многолуночный планшет и тем самым индуцируют образование трехмерного сфероида или агрегата,
- добавляют иммуноглобулин в лунки многолуночного планшета,
- инкубируют многолуночный планшет в течение промежутка времени, составляющего от примерно 20 до примерно 72 ч, и
- анализируют клетки в лунках многолуночного планшета с помощью клеточного сортера с возбуждением флуоресценции и тем самым оценивают эффекторную функцию антитела.
Согласно другому варианту осуществления изобретения способ заключается в том, что в качестве первой стадии дополнительно осуществляют следующую стадию, на которой:
- метят опухолевые клетки с помощью первого флуоресцентного красителя.
Согласно другому варианту осуществления изобретения способ заключается в том, что осуществляют следующие дополнительные стадии, на которых:
- метят мертвые клетки с помощью второго флуоресцентного красителя и
- анализируют клетки в лунках многолуночного планшета с помощью клеточного сортера с возбуждением флуоресценции и тем самым оценивают эффекторную функцию антитела.
В одном из вариантов осуществления изобретения естественные клетки-киллеры представляют собой человеческие естественные клетки-киллеры. Согласно еще одному варианту осуществления изобретения естественные клетки-киллеры и опухолевые клетки смешивают в соотношении от 10:1 до 1:10. Согласно следующему варианту осуществления изобретения соотношение составляет от 1:2 до 1:4.
В одном из вариантов осуществления изобретения продолжительность инкубации составляет от примерно 20 до примерно 28 ч.
В одном из вариантов осуществления изобретения центрифугирование осуществляют при 1000 об/мин в течение 10 мин.
В одном из вариантов осуществления изобретения опухолевая клетка представляет собой клетку лимфомы. В другом варианте осуществления изобретения клетка лимфомы представляет собой Raji-клетку или SU-DHL4-клетку, или Z138-клетку.
В одном из вариантов осуществления изобретения антитело добавляют в концентрации от 15 до 0,1 мкг/мл. В другом варианте осуществления изобретения антитело добавляют в концентрации от 8 до 12 мкг/мл.
Следующим объектом изобретения является применение трехмерного сфероида или агрегата, содержащего опухолевые клетки и естественные клетки киллеры, для оценки эффекторной функции комбинации множества антител в отношении множества опухолевых клеток.
Следующим объектом изобретения является способ выявления in vitro антитела, обладающего эффекторной функцией, заключающийся в том, что осуществляют стадии, на которых
- смешивают естественные клетки-киллеры и опухолевые клетки,
- добавляют примерно по 104 клеток в 200 мкл в лунки многолуночного планшета,
- центрифугируют многолуночный планшет и тем самым индуцируют образованием трехмерного сфероида или агрегата,
- добавляют антитело в индивидуальную лунку многолуночного планшета,
- инкубируют многолуночный планшет в течение промежутка времени, составляющего от примерно 20 до примерно 72 ч, и
- выявляют антитело, при применении которого обнаружено определенное соотношение мертвых и жизнеспособных клеток, в качестве антитела, обладающего эффекторной функцией.
Согласно одному из вариантов осуществления изобретения способ заключается в том, что осуществляют дополнительно следующие первые стадии, на которых:
- получают по меньшей мере одно антитело и
- метят опухолевые клетки с помощью первого флуоресцентного красителя. Согласно другому варианту осуществления изобретения способ
заключается в том, что осуществляют следующие стадии, на которых:
- добавляют каждое из полученных антител в индивидуальную лунку многолуночного планшета, при этом в каждую лунку добавляют максимум одно антитело,
- метят мертвые клетки в каждой из подвергнутых инкубации лунок с помощью второго флуоресцентного красителя,
- анализируют клетки в каждой лунке многолуночного планшета с помощью клеточного сортера с возбуждением флуоресценции и
- выявляют антитело, при применении которого обнаружено самое высокое соотношение мертвых и жизнеспособных клеток, в качестве антитела, обладающего эффекторной функцией.
Анализ и способ, предлагаемые в изобретении, можно осуществлять, используя в качестве примера антитело к CD20, описанное в WO 2005/044859 (указанная заявка включена в настоящее описание в качестве ссылки). Это антитело выбрано только в качестве примера осуществления настоящего изобретения и не направлено на ограничение его объема. Объем изобретения определяется представленной ниже формулой изобретения.
Приведенные ниже примеры и чертежи даны с целью лучшего понимания настоящего изобретения, истинный объем которого представлен ниже в формуле изобретения. Как должно быть очевидно, в описанных процедурах могут быть сделаны модификации без отклонения от сущности изобретения.
Описание чертежей
На чертежах показано:
на фиг.1 - результаты, полученные с помощью FACS-анализа жизнеспособных и мертвых Raji-клеток и естественных клеток-киллеров (NK) в отсутствии антитела. Квадранты: нижний левый: жизнеспособные NK-клетки, верхний левый: мертвые NK-клетки, нижний правый: жизнеспособные Raji-клетки, верхний правый: мертвые Raji-клетки. Панель А: только Raji-клетки, панель Б: Raji-клетки и NK-клетки в соотношении 1:1, панель В: Raji-клетки и NK-клетки в соотношении 1:10;
на фиг.2 - результаты, полученные с помощью FACS-анализа жизнеспособных и мертвых Raji-клеток и естественных клеток-киллеров (NK) в присутствии внесенного антитела к CD20 (10 мкг/мл). Квадранты: нижний левый: жизнеспособные NK-клетки, верхний левый: мертвые NK-клетки, нижний правый: жизнеспособные Raji-клетки, верхний правый: мертвые Raji-клетки. Панель А: только Raji-клетки, панель Б: Raji-клетки и NK-клетки в соотношении 1:1, панель В: Raji-клетки и NK-клетки в соотношении 1:10;
на фиг.3 - данные об оптимизации совместного культивирования клеток лимфомы/сфероидов-агрегатов путем изменения схемы введения клетки лимфомы, NK-клетки и антитела. Клетки лимфомы: Raji-клетки;
на фиг.4 - проценты жизнеспособных клеток лимфомы в присутствии NK-клеток в качестве функции от концентрации антитела к CD20. Панель А: Raji-клетки, панель Б: SU-DHL4-клетки, панель В: Z138-клетки. Соотношение NK-клеток и клеток лимфомы (соотношение Е:Т) составляло 3:1;
на фиг.5 - проценты жизнеспособных клеток лимфомы в присутствии взятого в определенной концентрации антитела к CD20 в качестве функции от соотношения: эффекторные клетки (NK):клетки-мишени (клетка лимфомы). Панель А: Raji-клетки, панель Б: SU-DHL4-клетки, панель В: Z138-клетки. Концентрация антитела к CD20: 10 мкг/мл;
на фиг.6 - приведенная в качестве примера схема осуществления способа;
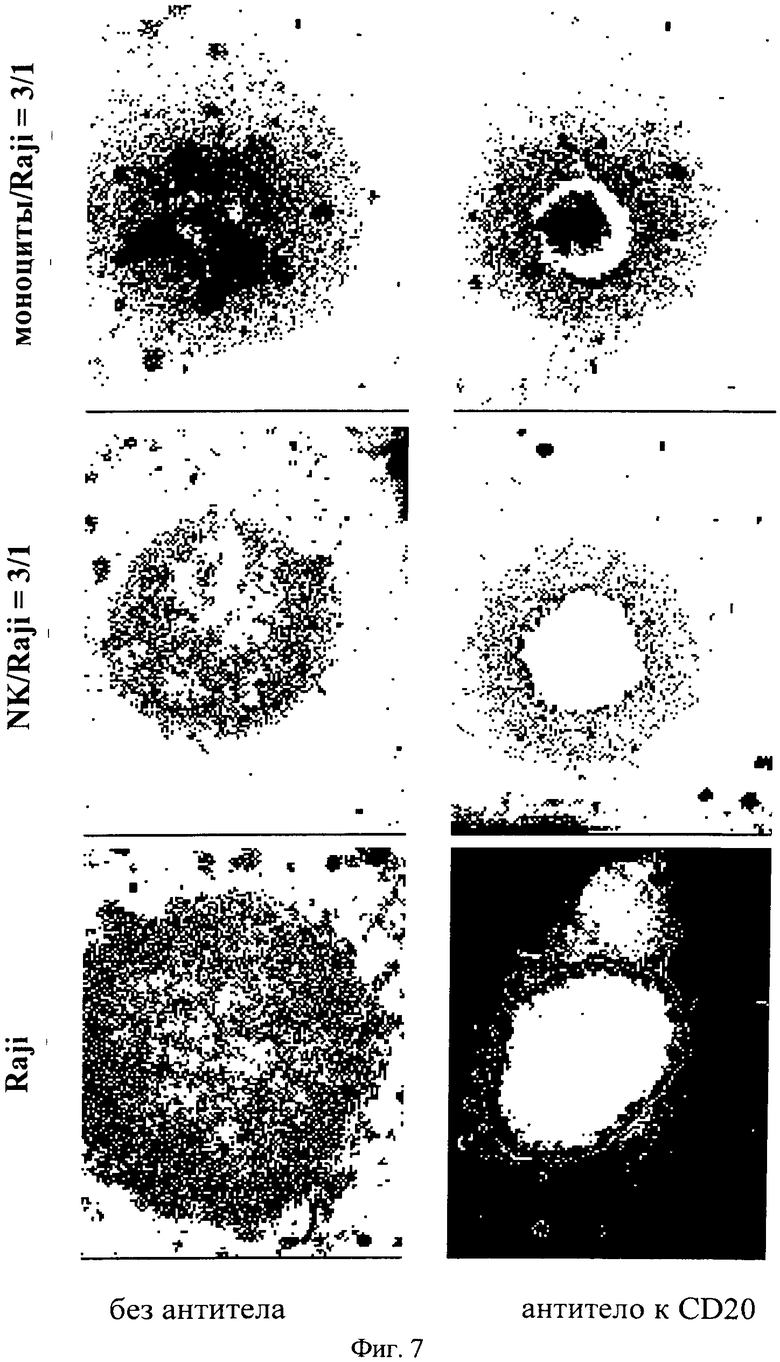
на фиг.7 - микроскопические изображения только Raji-клеток и Raji-клеток, совместно культивируемых с очищенными NK-клетками.
Пример 1
Материалы и методы
Клеточные линии:
Линии Raji-клеток, SU-DHL4-клеток и 2138-клеток получали из АТСС (Манассас, шт. Вирджиния, США), из DSMZ (Брауншвейг, Германия) и от проф. М. Dyer (Университет Лейцестера, Великобритания) соответственно. Raji-клетки и SU-DHL4-клетки культивировали в среде RPMI 1640 (фирма PAN Biotech, каталожный №Р04-18500), а Z138-клетки в среде DMEM (фирма PAN Biotech, каталожный №Р04-02500), дополненной 10% FCS (фирма Gibco, каталожный №10500-064) и Pen/Strep (фирма Roche, каталожный №11 074 440 001), при 37°С во влажной камере. В экспериментах по совместному культивированию с NK-клетками применяли клетки, находящиеся на экспоненциальной фазе роста, жизнеспособность которых составляла 90% или более.
Очистка NK-клеток
Образцы цельной крови получали из здоровых доноров в вакуумные пробирки типа Вакутайнер (фирма Becton Dickinson, каталожный №368484). РВМС получали с помощью препарата фиколл (фирма PAN Biotech, каталожный №Р04-60125). Для того, чтобы не повреждать NK-клетки, NK-клетки очищали с помощью набора для выделения NK-клеток путем негативной селекции (фирма Miltenyi, каталожный №130-092-657). В целом, метод состоял в следующем: выделенные с помощью фиколла РВМС ресуспендировали в MACS-буфере (ЗФР/0,5% БСА/2 мМ ЭДТК) из расчета 1×107 клеток/40 мкл. К клеткам добавляли 10 мкл смеси: NK-клетка - биотин - антитело и инкубировали в течение 10 мин при 4°C, после чего добавляли 30 мкл MACS-буфера. Затем к клеткам добавляли 20 мкл смеси NK-клетка - гранулы Microbead и инкубировали в течение 15 мин при 4°C. Добавляли 2 мл MACS-буфера и клетки центрифугировали в течение 10 мин при 300 g. Дебрис ресуспендировали в 500 мкл MACS-буфера и вносили в разделительную колонку, предварительно уравновешенную с помощью 500 мкл MACS-буфера. Колонку последовательно промывали трижды с помощью 500 мкл MACS-буфера и количество клеток определяли во всем элюате с помощью счетчика клеток типа CASY (фирма Scharfe System).
Чистоту препарата NK-клеток определяли путем окрашивания аликвот полученного с помощью MACS элюата. В целом, примерно 2x105 клеток ресуспендировали в 100 мкл RPMI 1640/10% FCS и окрашивали с использованием 10 мкл каждого из следующих антител: анти-CD56-PE и анти-CD3-ФИТЦ (фирма Becton Dickinson, каталожные №№555516 и 555339 соответственно) в течение 15 мин при 4°C. Затем добавляли 2 мл RPMI 1640/10% FCS к клеткам, которые центрифугировали в течение 5 мин при 400 g. Дебрис ресуспендировали в 0,5 мл RPMI 1640/10% FCS и процент CD56-позитивных, но CD3-негативных клеточных фракций в гейте (дискриминационном окне) клеток, дающих сигналы светорассеивания, характерные для лимфоцитов, анализировали с использованием устройства FACS Scan или FACS Canto II (фирма Becton Dickinson).
Очистка моноцитов
Образцы цельной крови получали из здоровых доноров в вакуумные пробирки типа Вакутайнер (фирма Becton Dickinson, каталожный №368484). РВМС получали с помощью препарата фиколл (фирма PAN Biotech, каталожный №Р04-60125). Для того, чтобы не повреждать моноциты, моноциты очищали с помощью набора для обогащения моноцитов путем негативной селекции (фирма Stem Cell Technologies, каталожный №19059).
Окрашивание клеток лимфомы с помощью CMFDA:
Лиофилизат CMFDA (фирма Invitrogen, каталожный №С7025) ресуспендировали в ДМСО с получением 10мМ маточного раствора. 1×106 клеток лимфомы инкубировали в течение 30 мин при 37°C в 1 мл полной среды, дополненной 1 мкМ CMFDA. Затем клетки пеллетировали, однократно отмывали в полной среде и окончательно ресуспендировали в полной среде, получая 1×106 клеток/мл.
Пример 2
Получение 3D-сфероидов/агрегатов из клеточных линий лимфом. Количество клеток лимфомы определяли с помощью устройства CASY (фирма Schärfe-Systems, Ройтлинген) и клеточную суспензию разводили в охлажденной на льду среде до концентрации 2,5×104 клеток/мл (5000 клеток на сфероид/агрегат) и 5×104 клеток/мл (10000 клеток на сфероид /агрегат). В каждую лунку 96-луночного планшета с круглым дном (фирма Corning Inc., Нью-Йорк, США) или коническим дном (фирма Nunc, Роскильд, Нидерланды) добавляли по 200 мкл клеточной суспензии. Для предотвращения прикрепления клеток планшеты предварительно сенсибилизировали с использованием 50 мкл 0,5% полиНЕМА (фирма Polysciences, Эппельхайм, Германия) в 95 об.% этанола и сушили при 37°C в течение трех дней. Образование сфероидов инициировали центрифугированием планшетов при 1000 g в течение 10 мин с помощью корзиночной центрифуги с качающимися стаканами типа Эппендорф 5810 (фирма Eppendorf AG, Гамбург, Германия). Планшеты инкубировали в стандартных для культивирования клеток условиях при 37°C и в атмосфере, содержащей 7% СО2, во влажных камерах.
Пример 3
Получение 3D-сфероидов/агрегатов из клеточных линий плотных опухолей
Монослои клеток отделяли с помощью аккутазы (фирма РАА Laboratories GmbH, Инсбрук, Австрия) для получения суспензии единичных клеток. Количество клеток определяли с помощью устройства CASY (фирма Scharfe-Systems, Ройтлинген) и клеточную суспензию разводили в охлажденной на льду среде до концентрации 2,5×104 клеток/мл (5000 клеток на сфероид/агрегат) и 5×104 клеток/мл (10000 клеток на сфероид /агрегат). rBM подвергали оттаиванию на льду в течение ночи и добавляли в клеточную суспензию в конечной концентрации 2,5 об.% с помощью охлажденных на льду наконечников пипеток. В каждую лунку 96-луночного планшета с круглым дном (фирма Corning Inc., Нью-Йорк, США) или коническим дном (фирма Nunc, Роскильд, Нидерланды) по 200 мкл клеточной суспензии. Для предотвращения прикрепления клеток планшеты предварительно сенсибилизировали с использованием 50 мкл 0,5% полиНЕМА (фирма Polysciences, Эппельхайм, Германия) в 95 об.% этанола и сушили при 37°C в течение трех дней. Образование сфероидов инициировали центрифугированием планшетов при 1000 g в течение 10 мин с помощью корзиночной центрифуги с качающимися стаканами типа Эппендорф 5810 (фирма Eppendorf AG, Гамбург, Германия). Планшеты инкубировали в стандартных для культивирования клеток условиях при 37°C и в атмосфере, содержащей 7% СО2, во влажных камерах.
Пример 4
Совместное культивирование сфероида/агрегата, содержащего клетки лимфомы/NK-клетки, и инкубация с антителом
Последовательность совместного культивирования клеток и добавления антитела можно варьировать. В приведенном в качестве примера эксперименте по совместному культивированию клетки лимфомы (меченные с помощью CMFDA) и NK-клетки смешивали в различных указанных соотношениях в 6-луночных планшетах. Например, соотношение Е:Т (соотношение NK-клеток и клеток лимфомы) 3:1 соответствовало смеси клеток 3+1 (например, 75% NK-клеток и 25% клеток лимфомы). По 200 мкл клеточной суспензии добавляли в индивидуальную лунку сенсибилизированного полиНЕМА 96-луночного планшете V-образным дном (фирма Nunc, каталожный №249662). Покрытие из полиНЕМА: 50 мкл 0,5% полиНЕМА в 95% этанола на лунку; сушка в течение 72 ч при 37°C (фирма Polysciences, каталожный №18894). Планшеты центрифугировали в течение 10 мин при 1000 g. Затем добавляли антитела в указанных выше концентрациях и клеточные агрегаты/сфероиды инкубировали при 37°C во влажной камере в атмосфере, содержащей 7% СО2. Микроскопические изображения только Raji-клеток и Raji-клеток, совместно культивированных с очищенными NK-клетками, представлены на фиг.7, наряду с изображениями совместно культивированных Raji-клеток и моноцитов для иллюстрации 3D-структуры, полученной при совместном культивировании опухолевых клеток с другими клетками иммунной системы, отличными от NK-клеток.
Пример 5
Анализ жизнеспособных клеток и мертвых клеток
Сфероиды/агрегаты получали с использованием 10000 клеток и инкубировали с антителом согласно методам, описанным в примерах 2 и 3.
Идентификацию жизнеспособных клеток лимфомы осуществляли следующим образом: объединяли индивидуальные агрегаты из индивидуальных лунок, в которых использовали идентичные экспериментальные условия, осуществляли их диссоциацию путем пипетирования и центрифугировали при 300 g в течение 10 мин. Индивидуальные сфероиды объединяли, однократно отмывали забуференным фосфатом физиологическим раствором (ЗФР), ресуспендировали в растворе аккутазы и инкубировали при 37°C. Каждые 5 мин сфероиды/агрегаты ресуспендировали путем пипетирования и диссоциацию завершали в течение 5-15 мин. Клетки отмывали полной средой, центрифугировали и клеточный дебрис ресуспендировали в полной среде и добавляли йодид пропидия в концентрации 1 мкг/мл (фирма Sigma, каталожный №Р4170). Анализ флуоресценции осуществляли с помощью FACS (фирма Becton Dickinson, устройство Canto II).
Данные о жизнеспособности клеток лимфомы представлены на фиг.16. В верхнем правом квадранте локализованы PI- и CMFDA-позитивные клетки, представляющие собой мертвые клетки лимфомы, а в нижнем правом квадранте PI- негативные, но CMFDA-позитивные клетки, представляющие собой фракцию жизнеспособных представляющих собой мишень опухолевых клеток лимфомы. В нижнем левом квадранте локализованы жизнеспособные NK-клетки, а мертвые NK-клетки локализованы в верхнем левом квадранте.
В альтернативном варианте осуществляли анализ апоптоза. Сфероиды/агрегаты получали с использованием 10000 клеток и инкубировали с антителом согласно методам, описанным в примерах 2 и 3. Для анализа апоптоза сфероиды/агрегаты переносили в 96-луночный планшет с коническим дном, однократно отмывали забуференным фосфатом физиологическим раствором (ЗФР), ресуспендировали в растворе аккутазы и инкубировали при 37°C. Каждые 5 мин сфероиды/агрегаты ресуспендировали путем пипетирования и диссоциацию завершали в течение 5-15 мин. Объединяли суспензии единичных клеток из 8 сфероидов/агрегатов и клетки окрашивали аннексином-V-fluos и йодидом пропидия в присутствии в качестве добавки 2 мМ CaCl2 (набор для окрашивания Annexin-V-fluos, фирма Roche Diagnostics GmbH, Маннгейм, Германия. Флуоресценцию 10000 клеток оценивали с помощью проточного цитометра (устройство FACS scan, фирма Becton Dickinson, Сан-Хосе, шт. Калифорния, США). Осуществляли статистическую обработку приведенных в квадранте точечных диаграмм, соответствующих количеству жизнеспособных клеток, локализованных в нижнем левом квадранте.
Для получения абсолютного количества мертвых и жизнеспособных клеток подсчитывали общее количество клеток, полученных после диссоциации сфероидов /агрегатова, с помощью камеры для подсчета клеток Фукса-Розенталя и умножали на процент жизнеспособных или мертвых клеток из таких же сфероидов/агрегатов по данным окрашивания с помощью аннексина-V-fluos/PI.
Группа изобретений относится к медицине, а именно к биотехнологии, и может быть использована для выявления in vitro антитела, обладающего эффекторной функцией. Для этого смешивают естественные клетки-киллеры и опухолевые клетки, добавляют примерно по 104 клеток на 200 мкл в лунки многолуночного планшета. Затем проводят центрифугирование многолуночного планшета и тем самым индукцируют образования трехмерного сфероида. Добавляют каждого из полученных антител в индивидуальную лунку многолуночного планшета и инкубируют в течение промежутка времени, составляющего от примерно 20 до примерно 72 ч. Анализируют клетки в лунках многолуночного планшета с помощью клеточного сортера с возбуждением флуоресценции и тем самым оценивают эффекторную функцию антитела. Выявляют антитела, обладающие эффекторной функцией, при применении которого обнаружено, что соотношение мертвых к жизнеспособным клеткам превышает 1. Группа изобретений относится также к применению трехмерного сфероида или агрегата, который содержит опухолевые клетки и естественные клетки-киллеры, для оценки эффекторной функции комбинации антител. 3 н. и 9 з.п. ф-лы, 7 ил., 5 пр.
1. Способ оценки in vitro эффекторной функции антитела, включающий инкубирование трехмерного сфероида или агрегата, который содержит опухолевые клетки и естественные клетки-киллеры, с антителом, для этого осуществляют следующие стадии, на которых:
а) смешивают естественные клетки-киллеры и опухолевые клетки,
б) добавляют примерно по 104 клеток на 200 мкл в лунки многолуночного планшета,
в) центрифугируют многолуночный планшет и тем самым индуцируют образование трехмерного сфероида или агрегата,
г) добавляют антитело в лунки многолуночного планшета,
д) инкубируют многолуночный планшет в течение промежутка времени, составляющего от примерно 20 до примерно 72 ч,
е) анализируют клетки в лунках многолуночного планшета с помощью клеточного сортера с возбуждением флуоресценции и тем самым оценивают эффекторную функцию антитела.
2. Способ по п. 1, отличающийся тем, что естественные клетки-киллеры представляют собой человеческие естественные клетки-киллеры.
3. Способ по одному из предыдущих пунктов, отличающийся тем, что естественные клетки-киллеры и опухолевые клетки смешивают в соотношении от 10:1 до 1:10.
4. Способ по п. 3, отличающийся тем, что соотношение составляет от 1:2 до 1:4.
5. Способ по п. 1, отличающийся тем, что продолжительность инкубации составляет от примерно 20 до примерно 28 ч.
6. Способ по п. 1 или 5, отличающийся тем, что центрифугирование осуществляют при 1000 об/мин в течение 10 мин.
7. Способ по п. 1 или 5, отличающийся тем, что опухолевая клетка представляет собой клетку лимфомы.
8. Способ по п. 7, отличающийся тем, что клетка лимфомы представляет собой Raji-клетку или SU-DHL4-клетку, или Z138-клетку.
9. Способ по п. 1 или 5, отличающийся тем, что антитело добавляют в концентрации от 15 до 0,1 мкг/мл.
10. Способ по п. 9, отличающийся тем, что антитело добавляют в концентрации от 8 до 12 мкг/мл.
11. Применение трехмерного сфероида или агрегата, который содержит опухолевые клетки и естественные клетки-киллеры, для оценки эффекторной функции комбинации антител с использованием опухолевых клеток.
12. Способ выявления in vitro антитела, обладающего эффекторной функцией, включающий:
а) смешивание естественных клеток-киллеров и опухолевых клеток,
б) добавление примерно по 104 клеток на 200 мкл в лунки многолуночного планшета,
в) центрифугирование многолуночного планшета и тем самым индукция образования трехмерного сфероида,
г) добавление каждого из полученных антител в индивидуальную лунку многолуночного планшета,
д) инкубация многолуночного планшета в течение промежутка времени, составляющего от примерно 20 до примерно 72 ч,
е) выявление антитела, при применении которого обнаружено, что соотношение мертвых к жизнеспособным клеткам превышает 1, в качестве антитела, обладающего эффекторной функцией.
Авторы
Даты
2016-03-20—Публикация
2011-02-04—Подача