Изобретение относится к медицине, в частности к фармакологии, а именно к лекарственным средствам для лечения и профилактики постменопаузального и инволюционного остеопороза.
Поиск и разработка новых лекарственных средств, предназначенных для лечения и профилактики заболеваний постменопаузального и инволюционного остеопороза, обусловлены широким распространением заболевания и особой тяжестью течения.
Известны фармакологические и парафармакологические средства для профилактики и лечения различных видов возрастного и эндокриннозависимого остеопороза.
Среди известных препаратов множество:
- монопрепаратов (кальций глюконат, глицерофосфат Ca, хлорид кальция). Однако эти препараты не имеют дополнительных соединений, а значит, они не так хорошо усваиваются;
- витаминно-минеральных препаратов, содержащих группу различных витаминов, микро- и макроэлементов (Нутримакс + Vision», «Компливит»). Эти препараты содержат недостаточное количество кальция и подходят только для профилактики, но не для лечения;
- гормонально активных композиций (Raloxifene, Кальцитонин, паратиреоидный гормон);
- комбинированных препаратов кальция (Натекаль, Кальций-D3 Никомед, Витрум Кальций + Витамин D3). По сравнению с другими препаратами они содержат кальций в небольших количествах;
- а также биологических активных добавок (БАД) к пище (OsteoPlus, ВИТАЛАЙН).
Среди последних ведущее место занимают половые гормоны (прежде всего эстрогены) и анаболические гормоны, предшественники и гормоноподобные аналоги, их предшественники, «синтетические» и растительные аналоги гормонов, агонисты рецепторов и ингибиторы факторов резорбции, например, подавляющие действие паратгормонома (Лесняк О.М. Аудит состояния проблемы остеопороза в Российской Федерации // Профилактическая медицина. 2011. Т. 2. С. 7-10).
Все известные средства для лечения инволюционного остеопороза и остеопении у мужчин и женщин пожилого возраста в большинстве случаев своими действиями направлены на увеличение поступления и усвоения кальция и сопутствующих минеральных компонентов, на увеличение синтетической активности остеобластов и подавление резорбции костной ткани остеокластами, обогащение межклеточного матрикса минералами и коллагеном путем насыщения организма избыточно повышенными количествами пластических материалов - природных компонентов костной ткани и участниками процессов биосинтеза, витамином Д, искусственными кальцийсвязывающими соединениями, активации ответственных за анаболическую направленность метаболизма гормонзависимых рецепторов.
В настоящее время используются все известные средства местного и системного воздействия и фактически происходит замещение синтетического потенциала организма за счет избыточного поступления активаторов и «строительного» материала в сочетании с «золотым стандартом терапии остеопороза» - гормональной заместительной терапией (Поворознюк В.В., Григорьева Н.В. Менопауза и остеопороз. Киев: Здоровье, 2004. 356 с.). Такой подход оправдывает себя при относительно коротких курсах лечения (WHO. FRAX® WHO fracture risk assessment tool: calculation tool. Accessed February 14, 2011).
Однако известные средства обладают недостаточно высокой эффективностью действия, поэтому для препятствия, торможения или временного обращения развития возрастного инволюционного остеопороза требуются не месячные или даже годовые курсы фармакологической и пищевой поддержки и коррекции остеогенеза, а пожизненные проведения антиостеопорозной терапии.
Из известных лекарственных средств в качестве прототипа выбрано средство Кальцемин (http://medprep.info/drug/medicament/895), предназначенное для регуляции фосфорно-кальциевого обмена. В состав кальцемина входит кальций (в виде цитрата или карбоната) 250 мг, витамин D3 50 ME, медь (в виде оксида меди) 0,5 мг, цинк (в виде оксида цинка) 2 мг, марганец (в виде сульфата марганца) 0,5 мг, бор (в виде бората натрия) 50 мкг, неактивные ингредиенты: мальтодекстрин, МКЦ, кросскармеллозный натрий, акация, кислота стеариновая, сои полисахарид, магния стеарат.
Техническим результатом настоящего изобретения является расширение арсенала лекарственных средств и повышение терапевтического эффекта лекарственного средства, за счет использования компонентов от природных конформеров, а также исключение побочного эффекта и рецидивов при использовании заявленного средства, предназначенного для лечения и профилактики постменопаузального и инволюционного остеопороза.
Указанный технический результат достигается за счет того, что в антиостеопорозное средство, представляющее собой фармакологический композит, содержащий микроэлементы в виде бората и соли марганца и витамин D3, согласно изобретению дополнительно введены природные конформеры янтарной или фумаровой кислоты в виде кислых и аммониевых солей кальция, магния и цинка в аквахилатной форме, микроэлементы в виде фторида и селената в качестве натриевых или калиевых солей, казеинат кальция, обогащенный глицином и моно-L-глутаминатом натрия при следующем соотношении компонентов в мг/доза:
Кроме того, средство может содержать вспомогательные вещества для формирования его пористости.
Кроме того, в качестве вспомогательного средства может быть использована микроцеллюлоза.
Кроме того, в качестве вспомогательного средства может быть использована стеариновая кислота или стеарат магния.
Кроме того, средство может быть выполнено в форме, приемлемой для перорального применения.
Кроме того, средство может быть выполнено в виде капсул.
Заявленное антиостеопорозное средство отличается от прототипа содержанием в композите кислых и аммониевых солей кальция, магния и цинка в аквахилатной форме янтарной или фумаровой кислоты (200-300 мг), казеината кальция, обогащенного глицином и моно-L-глутаминатом натрия (75-150 мг), а также микроэлементов фтора и селена в виде натриевых или кальциевых солей (5-10 мг) и отсутствием в его составе меди.
В связи с использованием производных солей от природного конформера янтарной кислоты ее сигнальная и субстратная функции, заключающиеся в активации ангиогенеза, активации экспрессии ферментных систем энергетического обмена, в активации экспрессии глюкозного переносчика, во влиянии на реакции гидроксилирования пролина, в участии в окислительных превращениях в митохондриях - основных аккумуляторах кальция во внутриклеточном матриксе с последующим его вовлечением в костеобразование, повышены в несколько раз по сравнению с солями синтетической янтарной кислоты, обладающей 10-кратной меньшей активностью по сравнению с аналогом природного конформера янтарной кислоты, используемого в заявленном средстве.
Подобранный качественный и количественный состав представленного композита найден экспериментально и является оптимальным.
Изобретение иллюстрируется следующими фигурами:
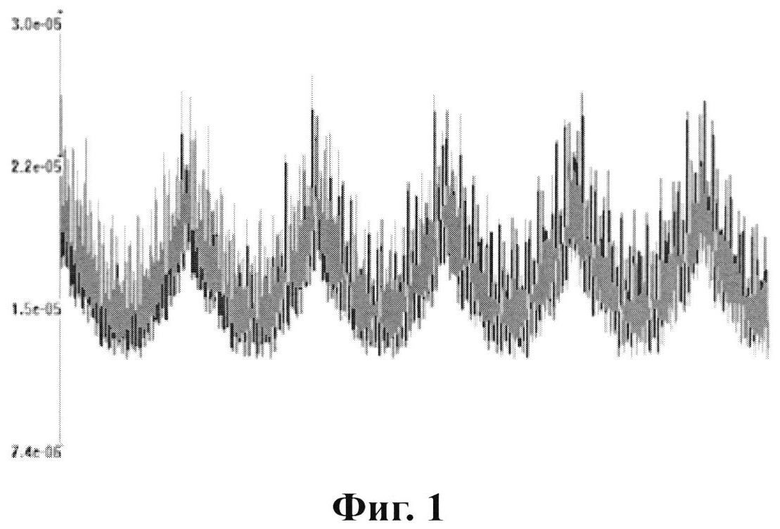
на фиг. 1 представлен автокорреляционный спектр по данным поляризационно-лазерно-радиоволновой спектроскопии обычной синтетической янтарной кислоты (производство ИжБиофарм);
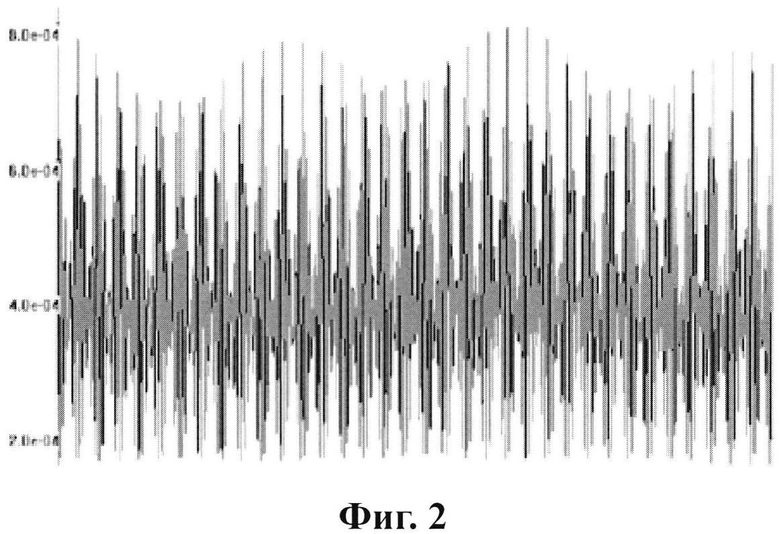
на фиг. 2 представлен автокорреляционный спектр по данным поляризационно-лазерно-радиоволновой спектроскопии янтарной кислоты, полученной из природного янтаря;
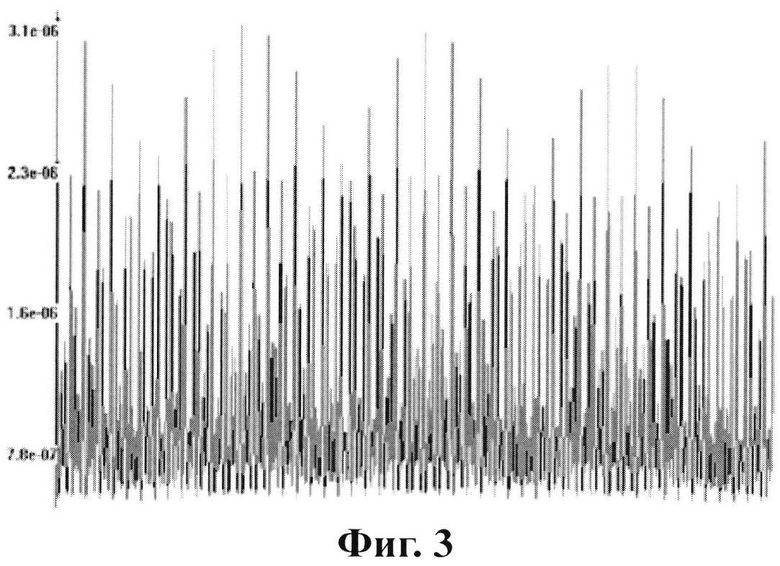
на фиг. 3 представлен автокорреляционный спектр по данным поляризационно-лазерно-радиоволновой спектроскопии синтетического аналога природной янтарной кислоты (производства ООО «ЭкоМедСервис», г. Тула), используемой в заявленной заявке на изобретение.
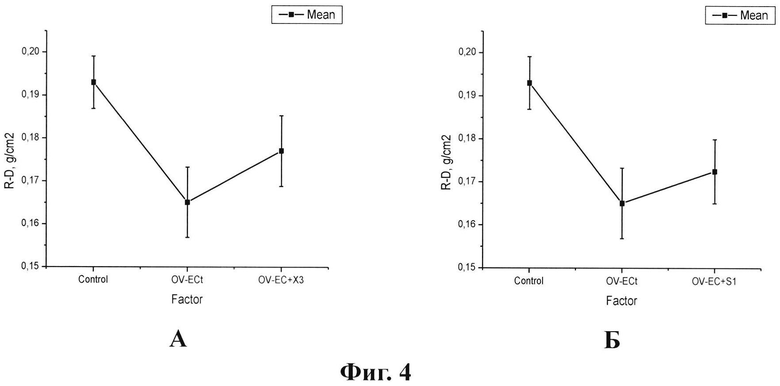
на фиг. 4 - графики сопоставления влияния курса препаратов на рентгеноденситометрическую плотность бедренной кости после овариоэктомии: А - заявленного антиостеопорозного средства (X3); Б - прототипа Кальцемин (S1).
Приведенные спектры автокорреляционной функции по данным поляризационно-лазерно-радиоволновой спектроскопии разных образцов, используемый авторами препарат янтарной кислоты (фиг. 3) близок по своему конформерному составу природной янтарной кислоте, полученной из природного янтаря (фиг. 2), что подчеркивает его преимущество в сравнении с другими формами янтарной кислоты (прежде всего синтетическими).
Использование кислых аквахелатных гидратных форм - цинка фумарата, кальция сукцината, магния сукцината обеспечивает сохранение природной конформерной конфигурации и существенно повышает проникающую способность и усвоение таких элементов, как кальций, цинк и магний, необходимых для нормального функционирования остеобластов.
В композит добавлен казеинат кальция как лекарственная основа для стабилизации компонентов, входящих в состав композита, а также для повышения усвоения органического кальция благодаря связи с природным белком, используемым при остеогенезе. Кроме того, казеинат является легко, но медленно ассимилируемым белком и дает достаточное количество незаменимых аминокислот, включая также пролин, которые не могут быть синтезированы самим организмом, Еще одно полезное свойство казеина заключается в том, что он дает чувство сытости.
Глицин добавлен в сигнальной дозе для легкой активации глициновых тормозных рецепторов с целью предотвращения возможной активации гормональных воздействий (со стороны катехоламинов и тиреоидных гормонов, которые могут активировать остеокластную деградацию костной такни за счет ускорения в них метаболизма).
Моноглутаминат натрия добавлен в дозе, которая никоим образом не может быть источником глутаматной эксайтотоксичности, но является необходимым компонентом воздействия на чувствительность гипоталамуса к активирующим и тормозным сигналам (показано Дильманом В.М. и др. еще в 1976 г.), источником α-кетоглутарата, абсолютно необходимого и лимитирующего участника процесса гидроксилирования пролина в оксипролин. Глутамат также является известным активатором сукцинатдегидргогеназы, что обеспечивает эффективное окисление эндогенной и экзогенной янтарной кислоты. Дополнительным и необходимым фактором остеобластообразования является использование в составе рецептуры витамина D3 (холекальциферола).
Биологические исследования
Исследованы острая токсичность на мышах, общая генотоксичность на мышах и специфическая активность на крысах.
Острая токсичность
При испытании разработанных авторами композиций оказалось, что выбранные композиции имеют малую токсичность, так как величина ЛД50 для мышей превысила 2,5 г/кг массы животного, что соответствует требованиям 4 класса опасности «вещества малоопасные» (ГОСТ 12.1.007-76 «Вредные вещества»).
Общая генотоксичность
Одновременно были выполнены тесты на генотоксичность по микроядерному тесту на мышах. После введения 3-кратной дозы препаратов ежедневно в течение 7 дней число микроядер в эритроидных клетках костного мозга мышей достигало 4-5 на 1000 эритроидных клеток при анализе у каждой особи не менее 2000 клеток, что находится на уровне интактной нормы. Позитивный контроль был выполнен при облучении животных в дозе 1,6 Грей. Эта доза вызывает легкую лучевую болезнь. После такого облучения число микроядер у разных особей из той же самой популяции мышей составляло от 25 до 60 клеток на 1000 эритроидных клеток костного мозга, что свидетельствует о высокой чувствительности к генотоксическим воздействиям использованной популяции животных и одновременно подтверждает отсутствие генотоксичности у созданных авторами лекарственных композиций.
Специфическая активность
Активность антиостеопорозного средства (композита) проверяли на 72 самках крыс с предварительной двусторонней овариоэктомией и дополнительными двукратными подкожными введениями (интервалом 4 дня) дексаметозона (0,5 мг/кг), усугубляющего течение остеопороза после двусторонней овариоэктомии. Кроме того, композит испытывали на старых крысах самках линии Вистар в возрасте 13-14 месяцев, у которых прекратился астральный цикл, о наличии фаз которого судили по влагалищному мазку.
Контроль состояния плотности костной ткани проводили неинвазивно с помощью рентгеноденситометрии на рентгеновском томографе в режиме сканирования.
Рентегноденситометрию выполняли методом двухэнергетической рентгеновской абсорбциометрии по окончанию кормления животных препаратом. Элементный анализ костной ткани бедра выполнен с помощью атомно-адсорбционной спектрометрии (спектрометр фирмы Varian) после гравиметрического исследования (лабораторные электронные весы ВЛКТ, замер с точностью до 0,5 мг), включавшего оценки влажного веса бедренных кости, сухого веса после высушивания (в термостате при температуре 95-102°C, поскольку при 104°C начинается испарение жиров кости), веса золы (полученной при сжигании костей в муфельной печени). Порядок исследования: сначала определяли влажный вес костей, затем вес высушенных костей, далее проводили озоление костей, сжигая их в муфельной печи, для анализа зольности и расчета степени минерализации. Полученную золу подготавливали к атомно-абсорбционной спектроскопии и пламенной фотометрии для определения элементного состава (K, Na, Ca, Mg, Zn) костной ткани (бедренной кости) с целью оценки фармакологических свойств разработанного препарата в сопоставлении с препаратом сравнения.
Свойства образцов препаратов оценивали по составу в начале и в конце эксперимента по ЯМР-спектрам (Брюккер, 600 МГц, ФРГ), органолептически и визуально при испытании степени рассыпчатости, слипания, изменению цвета и влажности.
С помощью метода H+-ЯМР-спектроскопии была идентифицирована и подтверждена структурная идентичность композиции каждого вида полученного порошка (аналитический ЯМР-спектрометр высокого разрешения на 600 МГ, фирмы Brukker, Германия). Расхождение не превышало 1,5% для каждого компонента от заданной прописи, что выше заложенных в проект ТУ требований. Посторонних примесей на уровне чувствительности ЯМР-спектрометра (1 ppm = 1 часть на миллион) не было обнаружено. Антиостеопорозное средство после ежедневного введения внутрь (15 мг/крысу, или 75 мг/кг) в течение 20 дней способствовало уменьшению остеопороза по сравнению с контрольными (овариоэктомированными самками и старыми самками пострепродуктивного периода) в среднем на 10-12% (табл. 1-3, рис. 2). Особенно высокая эффективность была показана на самках пострепродуктивного периода, у которых наряду с улучшением показателей плотности костной ткани было обнаружено возобновление в ряде случаев эстральной фазы цикла (по цитологии влагалищных мазков). Очевидно, в этом возрасте еще не происходит полной инволюции яичников, и восстановление гипоталамо-гипофизарной регуляции обеспечивает некоторую их активацию.


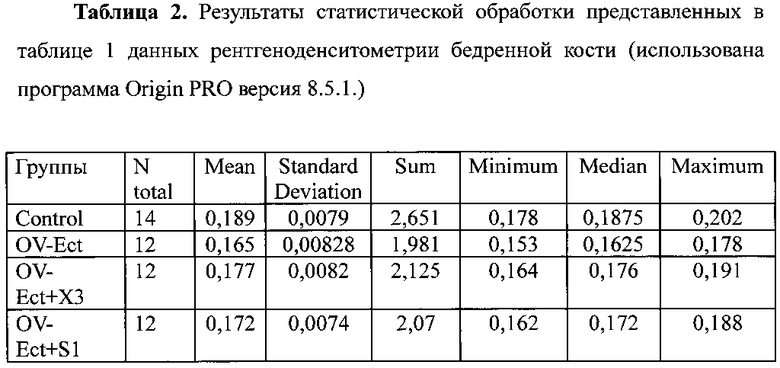

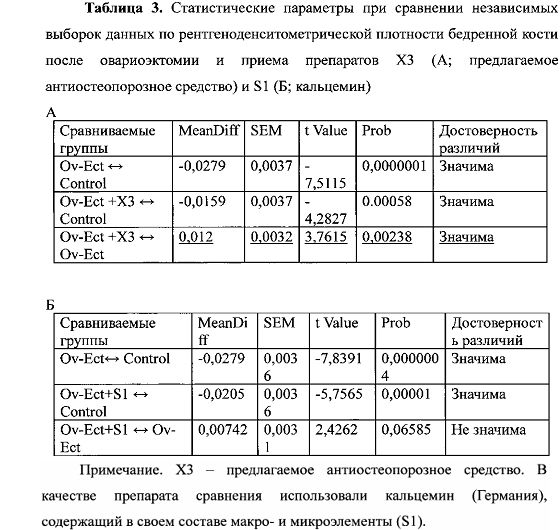
Из приведенных данных в таблицах и сопоставлении влияния курса препаратов на рентгеноденситометрическую плотность бедренной кости после овариоэктомии (фиг. 4, А - заявленного антиостеопорозного средства X3; Б - прототипа Кальцемин S1) видно, что эффективность предлагаемого антиостеопорозного средства (X3) достаточна для восстановления рентгеноденситометрически определяемой плотности костной ткани почти до нормального уровня на фоне овариоэктомии.
Таким образом, доказана специфическая антиостеопорозная активность предлагаемого антиостеопорозного средства.
Как показал экспертный анализ и первичный контроль специфической активности, предлагаемое антиостеопорозное средство может способствовать более эффективному лечению и профилактике возрастного и постменопаузального остеопороза. Биодоступность используемых в составе нового препарата кислых солей янтарной и фумаровой кислот увеличена за счет использования их природных конформеров и гидратных солей этих конформеров, обладающих повышенной проницаемостью и усвояемостью в отношении низких доз макро- и микроэлементов, что в свою очередь способствует более эффективному торможению развития остеопороза, влияя на соотношение активности остеокластов и остеобластов. Использование малых сигнальных доз компонентов и отсутствие перегрузки со стороны кальция и витамина D3 способствуют уменьшению возможных проявлений побочных эффектов лекарственной терапии. Таким образом, предлагаемый композит в составе технологии его длительного применения в конечном итоге обеспечит уменьшение осложнений (летальности) от переломов, социальных и экономических потерь от осложнений и последствий остеопороза, а также снижение финансовых затрат на профилактику и лечение пациентов соответствующего профиля.
Таким образом, новый композит показал высокие результаты и может быть рекомендован к внедрению в клиническую практику, тем самым расширяя арсенал лекарственных средств для лечения и профилактики инволюционного остеопороза и остеопении у мужчин и женщин пожилого возраста.
Изобретение относится к фармацевтической промышленности и представляет собой антиостеопорозное средство, содержащее микроэлементы в виде бората и соли марганца и витамин D3, отличающееся тем, что в средство дополнительно входят природные конформеры янтарной или фумаровой кислоты в виде кислых и аммониевых солей кальция, магния и цинка в аквахилатной форме, микроэлементы в виде фторида и селената в качестве натриевых или калиевых солей, казеинат кальция, обогащенный глицином и моно-L-глутаминатом натрия, причем компоненты средства находятся в определенном соотношении, в мг/дозу. Изобретение обеспечивает расширение арсенала лекарственных средств для лечения остеопороза, повышение терапевтического эффекта, а также позволяет исключить побочные эффекты и рецидивы. 5 з.п. ф-лы, 4 ил., 3 табл.
1. Антиостеопорозное средство, представляющее собой фармакологический композит, содержащий микроэлементы в виде бората и соли марганца и витамин D3, отличающийся тем, что в его состав дополнительно входят природные конформеры янтарной или фумаровой кислоты в виде кислых и аммониевых солей кальция, магния и цинка в аквахилатной форме, микроэлементы в виде фторида и селената в качестве натриевых или калиевых солей, казеинат кальция, обогащенный глицином и моно-L-глутаминатом натрия, при следующем соотношении компонентов в мг/доза:
2. Антиостеопорозное средство по п. 1, отличающееся тем, что оно содержит вспомогательные вещества для формирования пористости средства.
3. Антиостеопорозное средство по п. 2, отличающееся тем, что оно содержит в качестве вспомогательного вещества микроцеллюлозу.
4. Антиостеопорозное средство по п. 2, отличающееся тем, что оно содержит в качестве вспомогательного вещества стеариновую кислоту или стеарат магния.
5. Антиостеопорозное средство по п. 1, отличающееся тем, что оно выполнено в форме, приемлемой для перорального применения.
6. Антиостеопорозное средство по п. 5, отличающееся тем, что оно выполнено в виде капсул.
| Инструкция по медицинскому применению препарата Кальцемин, найдено в Интернет:http://grls.rosminzdrav.ru/InstrImgMZ.aspx?regNr=13141&page=1, дата регистрации 30.06.2009 | |||
| СРЕДСТВО И НАБОР ДЛЯ НОРМАЛИЗАЦИИ ФУНКЦИОНАЛЬНЫХ НАРУШЕНИЙ, ВОЗНИКАЮЩИХ В ПРЕДКЛИМАКТЕРИЧЕСКИЙ И КЛИМАКТЕРИЧЕСКИЙ ПЕРИОД | 2002 |
|
RU2220712C1 |
| WO 2014159886 A1, 02.10.2014 | |||
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОСТЕОПОРОЗА У ЖЕНЩИН В ПЕРИОД МЕНОПАУЗЫ | 2007 |
|
RU2379043C2 |
| WO 2012002918 A1, 05.01.2012. | |||
Авторы
Даты
2016-04-27—Публикация
2015-03-10—Подача