Изобретение относится к медицине, а более конкретно к офтальмологии, и может быть использовано для лечения и профилактики заболеваний роговой оболочки глаза, при лечении любых повреждений роговицы с явлениями воспаления и отека, а также в качестве протектора тканей глаза для защиты поверхности глаза от воздействия вредных факторов внешней среды, как лечебное и профилактическое средство при дистрофиях роговицы, в том числе при кератоконусе и как средство для коррекции амметропий слабой степени.
Наиболее близким по решению задачи является раствор для защиты роговицы от повреждений, описанный в патенте RU №2310440 от 29.05.2006, содержащий сбалансированный солевой раствор, водорастворимые гидроксиэтилцеллюлозу и хондроитин сульфат.
Недостатком указанного раствора является то, что он не обладает достаточным активным действием и защитным свойством на ткани переднего отрезка глаза (роговица и конъюнктива) из-за недостаточно длительного времени сохранения образуемой им пленки на поверхности глаза. Кроме того, активность всех гликозаминогликанов обладает дозозависимым защитным действием на ткани глаза и также зависит от времени их экспозиции на ткани, подлежащие защите. Быстрое выведение из полости глаз защитной пленки, образуемой известными растворами, снижает лечебный эффект хондроитин сульфата, находящегося в их составе.
Техническим результатом изобретения является увеличение времени высыхания композиции на поверхности тканей глаза за счет применения хондроитин сульфата в минимальных концентрациях в сочетании со смесью гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы, что улучшает реологические и вязкие свойства всего раствора, что позволяет создать на поверхности эпителия устойчивую защитную пленку, а также усилить получение противовоспалительного и противоотечного эффекта, ускорение процессов репарации ткани роговицы за счет пролонгированного направленного действия предлагаемой композиции.
Другим техническим результатом является затруднение выведения композиции с поверхности глаза и из полостей органа зрения через естественные пути оттока за счет увеличения усилия вязкого сдвига. Что также увеличивает экспозицию хондроитин сульфата на ткани глаза и его терапевтический эффект.
Еще одним техническим результатом является увеличение поверхностного напряжения защитной пленки на поверхности глаза, уменьшающего механические напряжения, способные вызвать эктазию при дистрофических заболеваниях роговицы или после хирургических операций на роговице.
Еще одним техническим результатом является увеличение способности раствора к созданию на поверхности роговицы оптически прозрачной зеркальной и ровной пленки, позволяющей временно корригировать амметропии слабой степени.
Технический результат, согласно изобретению, достигается тем, что в растворе для защиты роговицы от повреждений, включающем сульфатированный гликозаминогликан хондроитин сульфат, водорастворимое производное целлюлозы и сбалансированный солевой раствор, в качестве водорастворимых производных целлюлозы используют смесь гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы, а в качестве солевого раствора используют сбалансированный солевой раствор при следующем соотношении г/100,0 мл:
При этом соотношение количества гидроксипропилметилцелюллозы к количеству гидроксиэтилцелюллозы составляет от 3:7 до 7:3. Согласно изобретению, в качестве основного действующего вещества для получения раствора для защиты роговицы от повреждений применен хондроитин сульфат. Это вещество является сложным полисахаридом и относится к классу сульфатированных гликозаминогликанов.
Хондроитин сульфат входит в состав протеогликанов различных тканей глаза. Полисахариды, входящие в их состав, это линейные полимеры, построенные из разных дисахаридных субъединиц, образованных уроновыми кислотами (глюкуроновой, галактуроновой и идуроновой), N-ацетилгексозаминами (N-ацетилглюкозамин, N-ацетилгалактозамин) и нейтральными сахаридами (галактозой, маннозой и ксилозой). Именно эти полисахаридные цепи называются гликозаминогликанами. По меньшей мере, один из сахаров в дисахариде имеет отрицательно заряженную сульфатную группу.
Ткани глаза содержат такие сульфатированные гликозаминогликаны как кератансульфат, хондроитин-4- и хондроитин-6-сульфаты и незначительное количество дерматан сульфата. Биосинтез протеогликанов в тканях глаза, в частности роговицы, осуществляется главным образом активированными фибробластами (кератобластами) стромы роговицы, эпителием и в незначительной степени эндотелием.
Введение в состав раствора хондроитин сульфата обусловлено его способностью при экзогенном воздействии на роговицу влиять на активность кератобластов по синтезу эндогенных кератан сульфатов, которые укрепляют роговицу и ускоряют регенерацию. Т.е. другими словами хондроитин сульфат обладает свойством стимулировать процессы репарации эпителия и стромы роговицы, а также при введении в полость глаза он обладает способностью защищать эндотелий роговицы от повреждающего воздействия удаляемых хрусталиковых масс при удалении катарактально измененного хрусталика, тормозить процесс фиброзообразования и развития грануляций после оперативных вмешательств на тканях глаза. Однако в известных вязких композициях он недостаточно долго удерживается на поверхности тканей глаза, что уменьшает его экспозицию и значительно снижает терапевтический и протекторный эффект.
Кроме того, введение в композицию хондроитин сульфата обусловлено его влиянием на осмотическое давление в клетках эпителия роговицы, конъюнктивы, склеры и тканей передней камеры глаза, что особенно важно для профилактики отека тканей глаза при воспалительных заболеваниях глаза, так и после проведенных оперативных вмешательствах. Ингибируя макрофагальные клеточные рецепторы хондроитин сульфат, оказывает умеренное противовоспалительное действие. Однако, в известных композициях, из-за относительно быстрого вымывания раствора с поверхности тканей глаза вместе с вязким носителем хондроитин сульфат не проявляет своих лечебных свойств в полной мере.
Производные целлюлозы гидроксиэтилцеллюлоза и гидроксипропилметилцеллюлоза имеют, несмотря на свое большое химическое сходство, разную величину частиц в водяном или соляном растворе. Гидроксиэтилцеллюлоза имеет более короткие и компактные частицы со средним диаметром около 5 мкм. Раствор гидроксипропилметилцеллюлозы содержит более длинные молекулы, которые по своей длине могут превышать 100 мкм. А частицы хондроитинсульфата из всех компонентов композиции обладают наименьшими размерами. При смешении этих трех вязких компонентов в водном или соляном растворе они формируют сложную структуру, когда в сети из более длинных молекул гидроксипропилметилцеллюлозы располагаются более мелкие частицы гидроксиэтилцеллюлозы и хондроитин сульфата, такая многоуровневая архитектура приводит к образованию коллоидной системы, которая высыхает медленнее, чем каждый отдельный компонент вне этой системы. При попадании на поверхность тканей глаза композиция высыхает существенно медленнее, что является техническим результатом предлагаемого изобретения. Получаемая согласно предлагаемому изобретению коллоидная система более упруга и, попадая на поверхность глаза, обладает большим поверхностным натяжением, которое снижает механическое напряжение в роговице, и может использоваться для профилактики и лечения эктазий роговицы как первичного, так и вторичного генеза.
Более длительное и стабильное присутствие защитной пленки на поверхности глаза после применения раствора согласно предлагаемому изобретению выравнивает поверхность роговицы, что позволяет проводить временную коррекцию миопии слабой степени и астигматизма, в том числе неправильного.
Нами экспериментально установлено, что в отличие от других композиций сульфатированных гликозаминогликанов, применяемых в офтальмологии и офтальмохирургии, именно хондроитин сульфат, взятый в таких низких концентрациях, способен положительно влиять на репарацию тканей глаза, в частности роговой оболочки, не оказывая ингибирующего действия на пролиферацию эпителиальных клеток, и синтез ими коллагенов десцеметовой мембраны, что важно для гармоничной регенерации поврежденной роговицы и ее активной ремодуляции в нормальном состоянии.
В экспериментальных условиях наблюдали, что при применении одного хондроитин сульфата отмечали только ускорение роста эпителия без прямого положительного эффекта на фибробласты стромы роговицы.
Другие исследования применения дерматан сульфата и гиалуроновой кислоты не выявляли стимулирующего действия на пролиферацию и метаболизм эпителия и фибробластов стромы роговицы (Proc. Nat. Acad. Sci. S. Meier. Stimulation Extracellular Matrix Synthesis in Developing Cornea by Glycosaminoglycans).
При применении аналога изобретения отмечали стимуляцию стромальных фибробластов роговицы, но рост эпителия и синтез протеогликанов и коллагена клетками эпителия недостаточен для полноценной регенерации роговицы после повреждения.
Нашими исследованиями было показано, что положительный эффект хондроитин сульфата имеет не только дозозависимый эффект, но и зависит от времени его экспозиции на защищаемую роговицу. Время экспозиции зависит от двух параметров вязкой составляющей предлагаемого раствора гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы - от времени высыхания указанных компонентов и усилия сдвига, который характеризует способность вязких растворов к вымыванию через узкие отверстия. Хондроитин сульфат увеличивает способность растворов к выведению через малые отверстия, для чего он используется в производстве вискоэластиков - защитных растворов для хирургии катаракты, например, в составе вискоэластика Дисковиск, фирмы Алкон, США. Смесь гидроксипропилметилцелюллозы с гидроксиэтилцеллюлозой позволяет увеличить не только время высыхания, но и время выведения раствора из конъюнктивальной полости даже в присутствии хондроитин сульфата. Этот эффект подтвержден нами экспериментальным путем при регистрации времени высыхания раствора, состоящего из смеси гидроксипропилметилцеллюлозы и гидроксиэтилцелюллозы, в сравнении со временем высыхания отдельно гидроксипропилметилцеллюлозы и гидроксиэтилцелюллозы (таблица 1). Для измерения скорости высыхания растворов использовали микроаналитические весы Sartorius (Швейцария) в нормальных условиях.
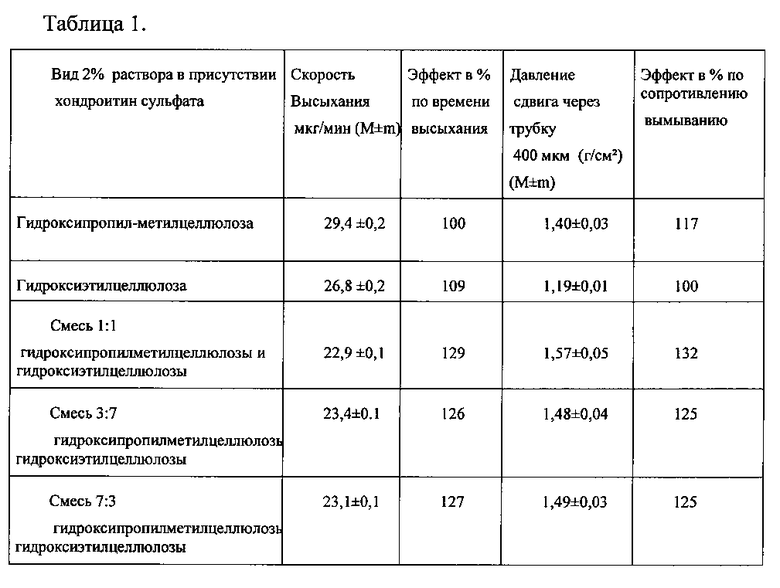
При этом усилие сдвига раствора при пропускании его через калиброванную 400 микронную трубку, которая имитирует слезоотводящие пути, через которые происходит эвакуация жидкости из конъюнктивальной полости, больше чем при пропускании через эту трубку отдельно гидроксипропилметилцеллюлозы или гидроксиэтилцелюллозы (таблица 2), что говорит о более трудном выведении раствора через естественные пути в виде слезных каналов. При этом гидроксипропилметилцеллюлоза, будучи так называемым дисперсивным вискоэластиком, труднее проходит через мелкие отверстия и быстрее высыхает на воздухе. Более когезивный вискоэластик демонстрирует меньшую скорость высыхания и с большей легкостью проникает через мелкое отверстие, что объясняется его пространственной структурой. Однако в растворе в виде смеси эти производные целлюлозы дают необычный эффект в виде уменьшения скорости высыхания и увеличения давления, требуемого для эластичного сдвига.
Предлагаемый раствор согласно изобретению содержит хондроитин сульфат в минимально необходимых и достаточных концентрациях от 0,0005 до 0,001 г, что является оптимальным для изменения свойств раствора, улучшения его реологических и вязких свойств, для получения тонкой, но стойкой к разрушению и высыханию защитной пленки на поверхности эпителия роговицы и конъюнктивы, что позволило получить надежный протективный эффект на эпителиальные клетки роговицы и другие ткани глаза, а также противовоспалительный, репарационный и противоотечный эффект.
Концентрация хондроитин сульфата менее 0,0005 г не оказывает влияния на изменения реологических и вязких свойств раствора, не удается получить тонкой защитной пленки, а также выраженного стимулирующего эффекта на процесс репарации эпителия и стромы роговицы, а концентрация 0,001 г может привести к обратному эффекту - снижению вязкости и реологических показателей.
В качестве вещества, придающего раствору вязкость и пролонгирующие свойства в растворе, применена смесь водорастворимых производных целлюлозы-гидроксиэтилцеллюлозы в концентрации 0,15 до 1,0 г на 100 мл раствора и гидроксипропилметилцеллюлозы в концентрации от 0,15 до 1,0 г на 100 мл раствора. При этом соотношение количества гидроксипропилметилцеллюлозы к количеству гидроксиэтилцеллюлозы составляет от 3:7 до 7:3. Именно в этом диапазоне суммарная величина вязкости смеси гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы превышает их среднеарифметическое значение, чем обеспечивается большая стойкость раствора к высыханию и вымыванию, что подтверждается примерами, показывающими клинический эффект раствора в эксперименте на животных. При соотношении менее 3:7 или более 7:3 пропадает эффект неаддитивности реологических свойств гидроксиэтилцеллюлозы и гидроксипропилметилцеллюлозы и величина вязкости раствора начинает представлять собой среднеарифметическую сумму вязкостей обоих водорастворимых производных целлюлозы.
В изобретении применена коммерческая гидроксиэтилцеллюлоза фармацевтическая фирмы Геркулес (Натросол 250 Pharm Бельгия) и гидроксипропилметилцеллюлоза фирмы Wolff Cellulosics, что, однако, не исключает использование водорастворимых производных других компаний, обладающих аналогичными характеристиками и свойствами.
Смесь гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы вводится в раствор с целью придания ему протективных вязкоэластических свойств. При этом их суммарная стойкость к высыханию в указанных диапазонах концентраций выше, а вымываемость через мелкие отверстия ниже, чем у каждого из этих водорастворимых производных целлюлозы по отдельности. Кроме того, вязкие растворы в указанной комбинации усиливают пролонгацию действия основного вещества раствора, а именно хондроитин сульфата.
Суммарная концентрация производных целлюлозы в растворе ниже 0,3 г на 100 мл раствора не придает раствору вязкости, а при концентрации выше 2,0 г на 100 мл раствора возникают трудности распределения основного вещества и других компонентов по всему объему раствора.
В качестве растворителя и стабилизатора компонентов раствора, согласно изобретению, использован сбалансированный солевой раствор, который в настоящее время является общепринятым в офтальмологической практике и офтальмохирургии.
Использование в качестве растворителя сбалансированного солевого раствора обусловлено несколькими обстоятельствами. Прежде всего, он содержит все минеральные компоненты, необходимые для поддержания изотоничности и осмолярности при добавлении других веществ, при нагревании без изменения рН получаемого раствора, а также обладает большой буферной емкостью, что особенно важно при его хранении для сохранения реологических свойств всего раствора.
В изобретении используют коммерческий сбалансированный солевой раствор фирмы Алкон (BSS Canada), что не исключает применения других растворов с аналогичными свойствами и характеристиками, также допустимо использование 0,9% раствора очищенной поваренной соли.
Краткая технология получения раствора.
50,0 мл сбалансированного солевого раствора нагревают до кипения и добавляют в него стерильный порошок субстанции 0,0005 г хондроитин сульфата, перемешивают и добавляют по 0,15 г гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы, перемешивают в течение 2 часов и доводят объем сбалансированного солевого раствора до 100,0 мл, отстаивают раствор в течение 24 часов, разливают во флаконы и стерилизуют автоклавированием в течение 10 минут при 120°C.
Приготовление раствора контролируется на каждой стадии его получения и включает основные методики оценки его характеристик, принятые для Гос. Фармакопеи XI издания.
Хондроитин сульфат определяли спектрофотометрически по окрашиванию 1,9-диметиленовым синим при длине волны 735 нм по методу Farndel.
Контроль остальных компонентов композиции делают по Гос Фармакопее XI издания.
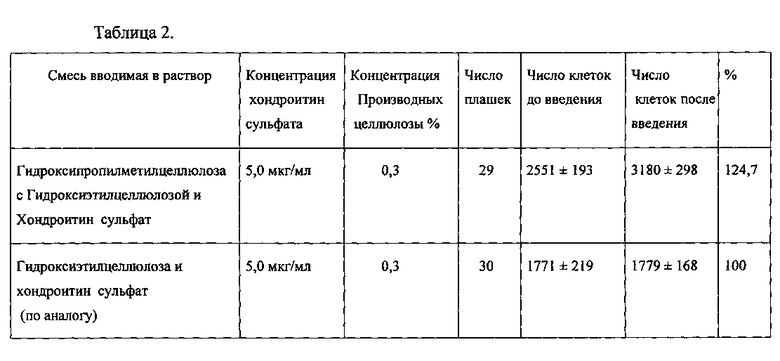
Стимулирующий эффект на синтез клетками эпителия и кератоцитов стромы роговой оболочки проводили на первичной культуре клеток, для чего в культуру клеток с обедненной средой вводили фармацевтическую субстанцию хондроитин сульфата в концентрации 5 мкг/мл и субстанцию аналога в концентрации 200 мкг/мл и с помощью радиоактивной метки отмечали ее включение через 24 часа
После инкубации.
Результаты этих исследований изложены в таблице 2.
Противовоспалительный и репарационный эффект предлагаемой композиции изучали на экспериментальных животных - кроликах породы Шиншилла, которым под местной анестезией 0,5% раствора дикаина наносили радиальные разрезы на 2/3 толщины роговицы и проводили инстилляции раствора в каждый оперированный глаз, контрольным животным закапывали раствор по прототипу.
На сроки 7, 14 и 21 день после операции животных выводили из эксперимента внутрисердечным введением высокой дозы тиопентала натрия, роговицы секторально вырезали и готовили гистологические срезы для световой микроскопии.
Гистоморфологические исследования проводили на микроскопе Opton Германия.
Изучение гистологических препаратов показало, что в опытных глазах процесс репарации протекал более гладко, без явлений отека и воспаления роговицы и окружающих тканей.
При использовании раствора для лечения и профилактики заболеваний и повреждений роговицы, согласно изобретению, ускоряются процессы заживления тканей, чем обеспечивается сокращение сроков лечения и реабилитации пациентов. Входящие в раствор компоненты обеспечивают патогенетически направленную терапию заболеваний и повреждений роговицы.
Для лучшего понимания сущности изобретение поясняется примерами конкретного исполнения.
Пример 1.
Исследование влияния предлагаемого раствора на получение тонкой защитной пленки на эпителии роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 7 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз, в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме. Время сохранения защитной пленки и темп ее выведения с передней поверхности глаза определяли с помощью теста "время разрыва слезной пленки" на поверхности глаза в сравнении с контрольным глазом куда закапывали раствор по прототипу.
Через 7 дней проводили тест "время разрыва слезной пленки" и гистоморфологические исследования, которые показали формирование тонкой защитной пленки на эпителии роговицы и конъюнктивы. Время разрыва слезной пленки в сравнении с контролем увеличивалось на 30%.
Раствор, согласно изобретению, применяется в качестве лечебно-профилактического средства для защиты роговицы с явлениями воспаления и отека, а также в качестве профилактического средства при «синдроме сухого глаза».
Пример 2.
Исследование влияния предлагаемого раствора на получение тонкой защитной пленки на эпителии роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 7 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз, в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 7 дней провели тест "время разрыва слезной пленки" и гистоморфологические исследования, которые показали формирование тонкой защитной пленки на эпителии роговицы и конъюнктивы. Время ее разрыва увеличивалось при применении предлагаемого раствора на 30%. Это объясняется тем, что на сохранение защитной пленки одновременно влияет и удлинение времени ее высыхания на поверхности, и затруднение выведения компонентов раствора из полости глаза.
Раствор, согласно изобретению, применяется в качестве лечебно-профилактического средства для защиты роговицы с явлениями воспаления и отека, а также в качестве профилактического средства при «синдроме сухого глаза».
Пример 3.
Исследование влияния предлагаемого раствора на репарацию роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 14 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз (опыт), в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 14 дней проводили тест "время разрыва слезной пленки" и гистоморфологические исследования, которые показали, что на роговице и конъюнктиве формируется защитная пленка. Время разрыва слезной пленки удвоилось. Эпителиальная пробка заполняет всю область разреза, десцеметова мембрана частично сформирована, процесс заживления идет несколько быстрее по сравнению с контрольным глазом. Строма роговицы в опытном глазу менее отечна.
Раствор применяется в качестве лечебно-профилактического средства для защиты роговицы, при хирургических вмешательствах и лазерных операциях на роговице, конъюнктиве и склере, а также при любых заболеваниях и повреждениях роговицы и окружающих тканях глаза с явлениями воспаления и отека.
Пример 4.
Исследование влияния предлагаемого раствора на репарацию роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 14 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз (опыт), в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 14 дней проводили тест "время разрыва слезной пленки" и гистоморфологические исследования. Результаты исследования показали, что на роговице и конъюнктиве формируется защитная пленка. Время разрыва слезной пленки увеличилось на 70%. Эпителиальная пробка заполняет всю область разреза, десцеметова мембрана частично сформирована, процесс заживления идет несколько быстрее по сравнению с контрольным глазом. Строма роговицы в опытном глазу менее отечна.
Раствор применяется в качестве лечебно-профилактического средства для защиты роговицы, при хирургических вмешательствах и лазерных операциях на роговице, конъюнктиве и склере, а также при любых заболеваниях и повреждениях роговицы и окружающих тканях глаза с явлениями воспаления и отека.
Пример 5.
Исследование влияния предлагаемого раствора на репарацию роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 7 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз, в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 21 день проводили тест "время разрыва слезной пленки" и гистоморфологические исследования. На роговице и конъюнктиве формируется защитная пленка. Время ее разрыва увеличилось на 30% в сравнении с контрольным глазом. Это свидетельствует о пролонгированном действии предлагаемого раствора, даже после его длительной отмены. Эпителиальная пробка узкая, десцеметова мембрана сформирована, процесс заживления практически закончен, роговица и рубец прозрачные по сравнению с контрольным глазом, в котором десцеметова мембрана сформировалась частично, роговичный надрез белесоватый и более широкий по сравнению с опытным глазом.
Пример 6.
Исследование влияния предлагаемого раствора на репарацию роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 7 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз, в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 21 день проводили тест "время разрыва слезной пленки" и гистоморфологические исследования. На роговице и конъюнктиве формируется защитная пленка. Время ее разрыва увеличилось на 30% в сравнении с контролем по прототипу. Эпителиальная пробка узкая, десцеметова мембрана сформирована, процесс заживления практически закончен, роговица и рубец прозрачные по сравнению с контрольным глазом, в котором десцеметова мембрана сформировалась частично, роговичный надрез белесоватый и более широкий по сравнению с опытным глазом.
Пример 7.
Исследование влияния предлагаемого раствора на репарацию роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 7 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз, в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 21 день проводили тест время разрыва слезной пленки и гистоморфологические исследования, которые показали, что на роговице и конъюнктиве формируется защитная пленка. Время ее разрыва увеличилось в сравнении с контролем, выполненным по прототипу на 30%. Эпителиальная пробка тонкая, десцеметова мембрана сформирована, процесс заживления практически закончен, роговица и рубец прозрачные по сравнению с контрольным глазом, в котором десцеметова мембрана сформировалась частично, роговичный надрез белесоватый и более широкий по сравнению с опытным глазом.
Пример 8.
Исследование влияния предлагаемого раствора на репарацию роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 7 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз, в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 21 день проводили тест время разрыва слезной пленки и гистоморфологические исследования, которые показали, что на роговице и конъюнктиве формируется защитная пленка. Время разрыв слезной пленки увеличилось на 30% в сравнении с контрольным глазом. Эпителиальная пробка узкая, десцеметова мембрана сформирована, процесс заживления практически закончен, роговица и рубец прозрачные по сравнению с контрольным глазом, в котором десцеметова мембрана сформировалась частично, роговичный надрез белесоватый и более широкий по сравнению с опытным глазом.
Пример 9.
Исследование влияния предлагаемого раствора на репарацию роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 14 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз (опыт), в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 14 дней проводили тест "время разрыва слезной пленки" и гистоморфологические исследования, которые показали, что на роговице и конъюнктиве формируется защитная пленка. Время разрыва слезной пленки увеличилось в два раза в сравнении с контролем. Эпителиальная пробка заполняет всю область разреза, десцеметова мембрана частично сформирована, процесс заживления идет несколько быстрее по сравнению с контрольным глазом. Строма роговицы в опытном глазу менее отечна.
Раствор применяется в качестве лечебно-профилактического средства для защиты роговицы, при хирургических вмешательствах и лазерных операциях на роговице, конъюнктиве и склере и а также при любых заболеваниях и повреждениях роговицы и окружающих тканей глаза с явлениями воспаления и отека.
Пример 10.
Исследование влияния предлагаемого раствора на репарацию роговицы проводили на кроликах породы Шиншилла массой 2,5-3,0 кг, которым под местной анестезией 1% раствора дикаина делали радиальные надрезы роговицы и после чего проводили инстилляции предлагаемого раствора при следующем соотношении г/100,0 мл:
Раствор инстиллировали в течение 14 дней 3 раза в день по 1-2 капли в каждый оперированный левый глаз (опыт), в правый (контрольный глаз) инстиллировали физиологический раствор по той же схеме.
Через 14 дней проводили тест "время разрыва слезной пленки" и гистоморфологические исследования, которые показали, что на роговице и конъюнктиве формируется защитная пленка. Время разрыва слезной пленки увеличилось в 2 раза в сравнении с контролем. Эпителиальная пробка заполняет всю область разреза, десцеметова мембрана частично сформирована, процесс заживления идет несколько быстрее по сравнению с контрольным глазом. Строма роговицы в опытном глазу.
Раствор применяется в качестве лечебно-профилактического и протективного средства при хирургических и лазерных операциях на роговице, при экстракции катаракты, при операциях на конъюнктиве и склере, а также при любых повреждениях роговицы и окружающих тканей глаза, требующих защиты эпителия роговой оболочки глаза и конъюнктивы, а также в качестве средства для предупреждения явлений воспаления и отека.
Примеры конкретного выполнения предлагаемого изобретения показывают увеличение эффективности предлагаемого раствора в сравнении с ранее известным на 30-100%. Это объясняется тем, что предлагаемый раствор при соблюдении заданных диапазонов концентраций компонентов приобретает оптимальное коллоидное состояние, которое для препятствование высыханию на поверхности глаза и его выведения из конъюнктивальной полости.
Пример 11. Пациент П. 34 года. Диагноз: кератоконус 2 стадии OS. Данные офтальмометрии до начала лечения: 49,9Д - 170 град
47.8 Д-80 град,
острота зрения без коррекции 0,3
Раствор в составе:
инстиллировали в течение 30 дней 3 раза в день по 1-2 капли.
Через 1 месяц после начала лечения офтальмометрия OS:
47,0 D - 165 град
45,6 D - 75 град
Отмечен регресс кератоконуса, острота зрения без коррекции = 0,5
Пример 12. Пациент М., 25 лет. Диагноз: миопия слабой степени, сложный миопический астигматизм. Острота зрения OU без коррекции 0,3.
Раствор в составе:
Раствор инстиллировали в течение 7 дней 3 раза в день по 1-2 капли в каждый глаз. Острота зрения OU 0,9-1,0.
Последние два примера демонстрируют эффективность особенных коллоидных свойств предлагаемого раствора при лечении начального кератоконуса и для коррекции амметропий слабой степени.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА И РАСТВОР ДЛЯ ЛЕЧЕНИЯ, ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ И ПОВРЕЖДЕНИЙ РОГОВИЦЫ | 2015 |
|
RU2585955C1 |
| РАСТВОР ДЛЯ ЗАЩИТЫ РОГОВИЦЫ ОТ ПОВРЕЖДЕНИЙ | 2006 |
|
RU2310440C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА И РАСТВОР ДЛЯ ЛЕЧЕНИЯ, ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ И ПОВРЕЖДЕНИЙ РОГОВИЦЫ | 2006 |
|
RU2336862C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ПАРОДОНТА | 2006 |
|
RU2304427C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ ПАРОДОНТА | 2021 |
|
RU2761303C1 |
| Способ хирургической коррекции пресбиопии у лиц среднего и пожилого возраста - тканесохранный ЛАСИК | 2020 |
|
RU2743218C1 |
| ГЛАЗНЫЕ КАПЛИ ДЛЯ ЛЕЧЕНИЯ СИНДРОМА СУХОГО ГЛАЗА | 2006 |
|
RU2302231C1 |
| СПОСОБ ЛЕЧЕНИЯ ТРАВМ РОГОВИЦЫ В ЭКСПЕРИМЕНТЕ | 1999 |
|
RU2180825C2 |
| ДРЕНАЖ ДЛЯ ОФТАЛЬМОЛОГИЧЕСКИХ ОПЕРАЦИЙ | 2015 |
|
RU2585728C1 |
| Способ лечения роговично-конъюнктивального ксероза | 2017 |
|
RU2652581C1 |
Изобретение относится к медицине, а именно к офтальмологии и офтальмохирургии, и предназначено для лечения и профилактики заболеваний роговой оболочки глаза, при лечении любых повреждений роговицы с явлениями воспаления и отека, а также в качестве протектора тканей глаза. Раствор включает сульфатированные гликозаминогликаны, в качестве которых используют хондроитин сульфат, водорастворимые производные целлюлозы и сбалансированный солевой раствор. В качестве водорастворимых производных целлюлозы используют смесь гидроксипропилметилцеллюлозы с гидроксиэтилцеллюлозой в пропорции от 3:7 до 7:3. Компоненты используют в заявленных соотношениях. Использование изобретения позволяет увеличить время высыхания композиции на поверхности тканей глаза за счет применения хондроитин сульфата в минимальных концентрациях в сочетании со смесью гидроксипропилметилцеллюлозы и гидроксиэтилцеллюлозы, что улучшает реологические и вязкие свойства всего раствора, что позволяет создать на поверхности эпителия устойчивую защитную пленку, а также усилить получение противовоспалительного и противоотечного эффекта и ускорить процессы репарации ткани роговицы. 2 табл., 12 пр.
Раствор - протектор роговицы, включающий сульфатированные гликозаминогликаны, в качестве которых используют хондроитин сульфат, водорастворимые производные целлюлозы и сбалансированный солевой раствор, отличающийся тем, что в качестве водорастворимых производных целлюлозы используют смесь гидроксипропилметилцеллюлозы с гидроксиэтилцеллюлозой в пропорции от 3:7 до 7:3 при следующем соотношении г/100,0 мл:
| РАСТВОР ДЛЯ ЗАЩИТЫ РОГОВИЦЫ ОТ ПОВРЕЖДЕНИЙ | 2006 |
|
RU2310440C1 |
| ОФТАЛЬМОЛОГИЧЕСКИЙ ПРЕПАРАТ В ВИДЕ ГЛАЗНЫХ КАПЕЛЬ, СОДЕРЖАЩИЙ РАЗВЕТВЛЕННЫЕ ПОЛИГЕКСАМЕТИЛЕНГУАНИДИНЫ | 2012 |
|
RU2510264C1 |
| WO 2006112029 A1, 26.10.2006 | |||
| CN 104083396 A, 08.10.2014 | |||
| EFTIMOV P et al | |||
| Effect of hydrophilic polymers on the wettability, static and dynamic, of solid substrate covered by confluent monolayer of air-damaged SIRC cells | |||
| Biotechnol Biotechnol Equip | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Поливное приспособление для паровозов | 1922 |
|
SU390A1 |
Авторы
Даты
2016-06-10—Публикация
2015-05-12—Подача