Изобретение относится к области ветеринарии и биотехнологии и касается получения вакцины для профилактики сибирской язвы и некробактериоза животных.
Известна вакцина для профилактики некробактериоза рогатого скота, содержащая в равных объемных соотношениях инактивированные формалином эндотоксин и экзотоксин, полученные из местных эпизоотических культур возбудителя некробактериоза, и адъювант на основе минерального масла и ланолина (Патент RU 1816348, A61K 39/00, 1995).
Однако известная вакцина не достаточно иммуногенна, так как требует двукратного введения и обеспечивает иммунитет только против некробактериоза в течение 3,5-4 мес. Кроме того, при получении вакцины осуществляют предварительный подбор местных штаммов для каждого конкретного хозяйства, что невозможно при промышленном производстве.
Известна вакцина для профилактики сибирской язвы и некробактериоза животных и способ получения ее, содержащая инактивированный формалином лейкоцидин-экзотоксин, полученный из производственного штамма Fusobacterium necrophorum "0-1" ВИЭВ, представляющий собой высокоочищенный белок с молекулярной массой 18-20 кДа и адсорбированный на гидроокиси алюминия, а также суспензию живых спор сибиреязвенного вакцинного штамма 55-ВНИИВВиМ в физиологическом растворе, глицерин и сапонин (Патент RU 2524430, МПК А61К 39/116, A61K 39/07, опубл. 27.07.2014, Бюл. №21).
Однако известная вакцина не обеспечивает создание достаточного иммунитета против сибирской язвы и некробактериоза.
Задачей изобретения является повышение эффективности вакцины против сибирской язвы и некробактериоза за счет увеличения сроков иммунитета животных и снижения реактогенности вакцины.
Технический результат изобретения достигается в вакцине против сибирской язвы и некробактериоза, содержащей инактивированный формалином лейкоцидин-экзотоксин, полученный из производственного штамма Fusobacterium necrophorum "0-1" ВИЭВ, представляющий собой высокоочищенный белок с молекулярной массой 18-20 кДа и адсорбированный на гидроокиси алюминия, а также суспензию живых спор сибиреязвенного вакцинного штамма 55-ВНИИВВиМ в физиологическом растворе, глицерин и сапонин, причем инактивированный формалином лейкоцидин-экзотоксин, полученный из производственного штамма Fusobacterium necrophorum "0-1" ВИЭВ, представляет собой высокоочищенный белок с молекулярной массой 18-20 кДа с содержанием 1,5-2,0 млрд. клеток Fusobacterium necrophorum "0-1" ВИЭВ в 1 см3, адсорбированный на гидроокиси алюминия, и дополнительно содержит натриевую соль сукцината хитозана при следующем соотношении компонентов, мас.%:


Технический результат изобретения достигается также в способе получения вакцины против сибирской язвы и некробактериоза путем культивирования штамма Fusobacterium necrophorum "0-1" ВИЭВ, инактивирования его формалином, отделения бактериальной массы от культуральной жидкости центрифугированием, выделением из культуральной жидкости экзотоксина-лейкоцидина, его очистки и концентрирование ультрафильтрацией на полых волокнах и адсорбцией на гидроокиси алюминия в гликолевом буфере, добавлением суспензии живых спор сибириязвенного вакцинного штамма 55-ВНИИВВиМ и сапонина, причем перед адсорбцией на гидроокиси алюминия к экзотоксину добавляют 1-10% инактивированной бактериальной массы штамма Fusobacterium necrophorum "0-1" ВИЭВ с содержанием 1,5-2,0 млрд. клеток в 1 см3, после чего последовательно добавляют натриевую соль сукцината хитозана и сапонин, а глицерин добавляют сразу после добавления сапонина.
Ассоциированную вакцину вводят однократно крупному рогатому скоту, овцам, козам, свиньям и северным оленям внутрикожно при помощи безыгольного инъектора в объеме 0,2-0,4 см3.
Вакцину против сибирской язвы и некробактериоза готовят следующим образом.
Пример 1. Для получения некробактериозного антигена - лейкоцидин-экзотоксина берут производственный штамм Fusobacterium necrophorum "0-1" ВИЭВ, культивируют, инактивируют формалином в конечной концентрации 0,4%, отделяют бакмассу от культуральной жидкости центрифугированием, из культуральной жидкости выделяют экзотоксин, подвергают его высокой очистке ультрафильтрацией на полых волокнах с размером пор 13-17 кДа и концентрируют до содержания белка (по Лоури) 5,5-7,0 мг % с молекулярной массой 18-20 кДа. Далее к полученному антигену - экзотоксину-лейкоцидину добавляют 1-10% инактивированной бактериальной массы штамма Fusobacterium necrophorum "0-1" ВИЭВ с содержанием 1,5 млрд. клеток в 1 см3, затем сорбируют на 12% гидроокисью алюминия в гликолевом буфере с pH 8,4, взятой в конечной концентрации 1,8%. После сорбции антигена на гидрате окиси алюминия проверяют нейтрализацию остаточного количества формалина. Далее к полученному антигену - экзотоксину-лейкоцидину добавляют инактивированную бактериальную массу штамма Fusobacterium necrophorum "0-1" ВИЭВ до содержания Fusobacterium necrophorum "0-1" ВИЭВ 1,5 млрд. клеток в 1 см3, затем сорбируют на 12% гидроокисью алюминия в гликолевом буфере с pH 8,4, взятой в конечной концентрации 1,0%. После сорбции антигена на гидрате окиси алюминия проверяют нейтрализацию остаточного количества формалина. К 77,55 г смеси инактивированного формалином экзотоксина-лейкоцидина и инактивированной бактериальной массы штамма Fusobacterium necrophorum "0-1" ВИЭВ добавляют 1,2 г суспензии живых спор сибиреязвенного вакцинного штамма 55-ВНИИВВиМ с исходной концентрацией спор 2,5×107 в 1 см3 физиологического раствора, а затем последовательно добавляют натриевую соль сукцината хитозана, сапонин и глицерин, взятых в конечной концентрации 1,0, 0,25 и 20,0%, соответственно, получая состав 1 при следующем соотношении компонентов, мас.%:


Вакцину эмульгируют в гомогенизаторе при 3500 об/мин в течение 15 мин.
Полученная вакцина представляет собой однородную эмульсию белого цвета.
Пример 2. Для получения некробактериозного антигена - лейкоцидин-экзотоксина берут производственный штамм Fusobacterium necrophorum "0-1" ВИЭВ, культивируют, инактивируют формалином в конечной концентрации 0,4%, отделяют бакмассу от культуральной жидкости центрифугированием, из культуральной жидкости выделяют экзотоксин, подвергают его высокой очистке ультрафильтрацией на полых волокнах с размером пор 13-17 кДа и концентрируют до содержания белка (по Лоури) 5,5-7,0 мг % с молекулярной массой 18-20 кДа. Далее к полученному антигену - экзотоксину-лейкоцидину добавляют 1-10% инактивированной бактериальной массы штамма Fusobacterium necrophorum "0-1" ВИЭВ с содержанием 2,0 млрд. клеток в 1 см3, затем сорбируют на 15% гидроокисью алюминия в гликолевом буфере с pH 8,6, взятой в конечной концентрации 3,0%. После сорбции антигена на гидрате окиси алюминия проверяют нейтрализацию остаточного количества формалина. Далее к полученному антигену - экзотоксину-лейкоцидину добавляют инактивированную бактериальной массы штамма Fusobacterium necrophorum "0-1" ВИЭВ до содержания Fusobacterium necrophorum "0-1" ВИЭВ 2,0 млрд. клеток в 1 см3, затем сорбируют на 15% гидроокисью алюминия в гликолевом буфере с pH 8,6, взятой в конечной концентрации 2,0%. После сорбции антигена на гидрате окиси алюминия проверяют нейтрализацию остаточного количества формалина. К 63,25 г смеси инактивированного формалином экзотоксина-лейкоцидина и инактивированной бактериальной массы штамма Fusobacterium necrophorum "0-1" ВИЭВ, добавляют 1,0 г суспензии живых спор сибиреязвенного вакцинного штамма 55-ВНИИВВиМ с исходной концентрацией спор 3,0×107 в 1 см3 физиологического раствора, а затем последовательно добавляют натриевую соль сукцината хитозана, сапонин и глицерин, взятых в конечной концентрации 5,0, 0,75 и 30,0%, соответственно, получая состав 2 при следующем соотношении компонентов, мас.%:

Вакцину эмульгируют в гомогенизаторе при 3500 об/мин в течение 15 мин.
Полученная вакцина представляет собой однородную эмульсию белого цвета.
Пример 3. Полученные по примерам 1-2 составы 1-2 применяют для профилактических и вынужденных прививок клинически здоровых животных однократно. Молодняк, не достигший 3-месячного возраста, прививать ассоциированной вакциной не разрешается. Вакцину вводят внутрикожно с помощью безыгольного инъектора в бесшерстный участок тела крупному рогатому скоту и свиньям по 0,4 см3 (2 раза по 0,2 см3) овцам, козам и северным оленям по 0,2 см3.
Устойчивость к заражению сибирской язвой и некробактериозом сохраняется до 1,5 года, что в 1,5 раза длительней, чем известная вакцина (полученная по прототипу) - что подтверждают данные таблицы.
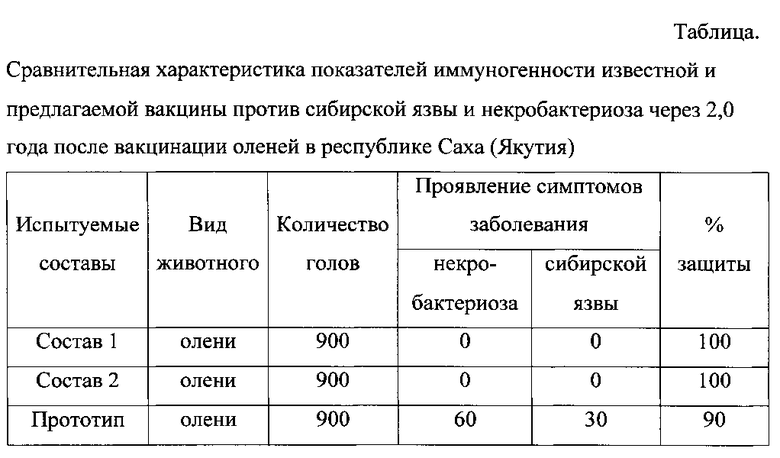
Кроме того, реактогенность в группе контрольных животных, получавших вакцину, полученную по прототипу, составила 5,2±1,6 см2, в то время как в опытных группах она была равна 0.
Таким образом, вакцина против некробактериоза является высокоэффективным препаратом, способным более длительно защитить животных от некробактериоза (более двух лет) и снизить реактогенность с 3,6-6,8 см до 0 см.
Предлагаемая ассоциированная вакцина против сибирской язвы и некробактериоза создает длительный иммунитет у привитых животных, при этом по иммуногенности она превосходит известную вакцину против сибирской язвы и некробактериоза. Вакцина безвредна и авирулентна для лабораторных и сельскохозяйственных животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ СИБИРСКОЙ ЯЗВЫ И НЕКРОБАКТЕРИОЗА ЖИВОТНЫХ И СПОСОБ ПОЛУЧЕНИЯ ЕЕ | 2013 |
|
RU2524430C1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ СИБИРСКОЙ ЯЗВЫ И НЕКРОБАКТЕРИОЗА ЖИВОТНЫХ | 2011 |
|
RU2480237C1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ СИБИРСКОЙ ЯЗВЫ И НЕКРОБАКТЕРИОЗА ЖИВОТНЫХ | 2001 |
|
RU2191599C1 |
| ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ НЕКРОБАКТЕРИОЗА ЖИВОТНЫХ И СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2015 |
|
RU2590596C1 |
| ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ НЕКРОБАКТЕРИОЗА ЖИВОТНЫХ И СПОСОБ ЕЁ ПОЛУЧЕНИЯ | 2015 |
|
RU2636454C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИПЕРИММУННОЙ СЫВОРОТКИ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ НЕКРОБАКТЕРИОЗА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 2015 |
|
RU2629861C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИПЕРИММУННОЙ СЫВОРОТКИ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ НЕКРОБАКТЕРИОЗА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 2015 |
|
RU2622746C2 |
| ДНК-конструкция, кодирующая модифицированный вариант протективного антигена Bacillus anthracis | 2015 |
|
RU2622085C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ НЕКРОБАКТЕРИОЗА ЖИВОТНЫХ | 1997 |
|
RU2109519C1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ СИБИРСКОЙ ЯЗВЫ И НЕКРОБАКТЕРИОЗА ЖИВОТНЫХ | 2002 |
|
RU2286174C2 |
Изобретение относится к области биотехнологии и микробиологии. Описана вакцина для профилактики сибирской язвы и некробактериоза животных. Вакцина содержит инактивированный формалином лейкоцидин-экзотоксин, адсорбированный на гидроокиси алюминия, а также суспензию живых спор сибиреязвенного вакцинного штамма 55-ВНИИВВиМ в физиологическом растворе. Вакцина также включает глицерин, сапонин и натриевую соль сукцината хитозана при определенных соотношениях компонентов. Кроме того, описан способ получения такой вакцины. Описанная вакцина обладает повышенной эффективностью за счет увеличения сроков иммунитета животных в вакцине против сибирской язвы и некробактериоза, Изобретение может быть использовано в ветеринарии. 2 н.п. ф-лы, 4 табл., 3 пр.
1. Вакцина против сибирской язвы и некробактериоза, содержащая инактивированный формалином лейкоцидин-экзотоксин, полученный из производственного штамма Fusobacterium necrophorum "0-1" ВИЭВ, представляющий собой высокоочищенный белок с молекулярной массой 18-20 кДа и адсорбированный на гидроокиси алюминия, а также суспензию живых спор сибиреязвенного вакцинного штамма 55-ВНИИВВиМ в физиологическом растворе, глицерин и сапонин, отличающаяся тем, что инактивированный формалином лейкоцидин-экзотоксин, полученный из производственного штамма Fusobacterium necrophorum "0-1" ВИЭВ, представляет собой высокоочищенный белок с молекулярной массой 18-20 кДа с содержанием 1,5-2,0 млрд. клеток Fusobacterium necrophorum "0-1" ВИЭВ в 1 см3, адсорбированный на гидроокиси алюминия, и дополнительно содержит натриевую соль сукцината хитозана при следующем соотношении компонентов, мас.%:

2. Способ получения вакцины против сибирской язвы и некробактериоза путем культивирования штамма Fusobacterium necrophorum "0-1" ВИЭВ, инактивирования его формалином, отделения бактериальной массы от культуральной жидкости центрифугированием, выделением из культуральной жидкости экзотоксина-лейкоцидина, его очистки и концентрирования ультрафильтрацией на полых волокнах и адсорбцией на гидроокиси алюминия в гликолевом буфере, добавлением суспензии живых спор сибириязвенного вакцинного штамма 55-ВНИИВВиМ, сапонина и глицерина, отличающийся тем, что к экзотоксину-лейкоцидину добавляют инактивированную бактериальную массу штамма Fusobacterium necrophorum "0-1" ВИЭВ с содержанием 1,5-2,0 млрд. клеток Fusobacterium necrophorum "0-1" ВИЭВ в 1 см3, а после добавления в реакционную смесь суспензии живых спор сибириязвенного вакцинного штамма 55-ВНИИВВиМ последовательно добавляют натриевую соль сукцината хитозана и сапонин, а глицерин добавляют сразу после добавления сапонина.
Авторы
Даты
2016-07-10—Публикация
2015-05-22—Подача