ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Переносчик желчных кислот из подвздошной кишки (IBAT) представляет собой основной механизм реабсорбции желчных кислот из GI (желудочно-кишечного) тракта. Частичное или полное блокирование этого механизма приводит к уменьшению концентрации желчных кислот в стенках тонкого кишечника, воротной вене, паренхиме печени, внутрипеченочных желчных протоках, внепеченочных желчных протоках, включая желчный пузырь.
Заболевания, при которых может оказаться полезным частичное или полное блокирование механизма IBAT, могут представлять собой такие заболевания, при которых имеется первичный патофизиологический дефект, вызывающий или сопровождающийся симптомами слишком высокой концентрации желчных кислот в сыворотке и перечисленных выше органах. В заявке WO 2008/058630 описан определенный эффект переноса желчных кислот из подвздошной кишки при лечении заболеваний печени, связанных с жировыми расстройствами.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к определенным ингибиторам IBAT в профилактике и/или лечении заболеваний печени.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретение относится к соединениям формулы (I), ингибирующим IBAT:
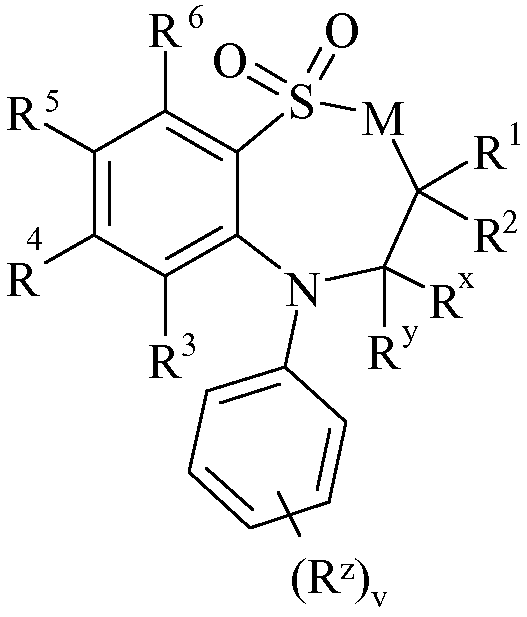
(I)
где:
M представляет собой CH2, NH
один из R1 и R2 выбран из водорода или C1-6-алкила, и другой выбран из C1-6-алкила;
Rx и Ry независимо выбраны из водорода, гидрокси, амино, меркапто, C1-6-алкила, C1-6-алкокси, N-(C1-6-алкил)амино, N,N-(C1-6-алкил)2амино, C1-6-алкил-S(O)a, где a принимает значения от 0 до 2;
RZ выбран из галогена, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, C1-6-алкила, C2-6-алкенила, C2-6-алкинила, C1-6-алканоила, C1-6-алканоилокси, N-(C1-6-алкил)амино, N,N-(C1-6-алкил)2амино, C1-6-алканоиламино, N-(C1-6-алкил)карбамоила, N,N-(C1-6-алкил)2карбамоила, C1-6-алкил-S(O)a, где a принимает значения от 0 до 2, C1-6-алкоксикарбонила, N-(C1-6-алкил)сульфамоила и N,N-(C1-6-алкил)2сульфамоила;
v принимает значения 0-5;
один из R4 и R5 представляет собой группу формулы (IA):
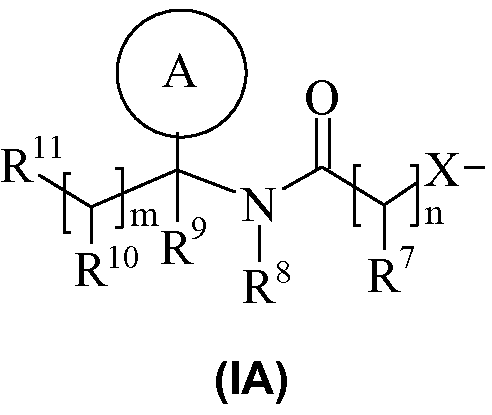
R3 и R6, и оставшийся из R4 и R5 независимо выбраны из водорода, галогена, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, C1-4-алкила, C2-4-алкенила, C2-4-алкинила, C1-4-алкокси, C1-4-алканоила, C1-4-алканоилокси, N-(C1-4-алкил)амино, N,N-(C1-4-алкил)2амино, C1-4-алканоиламино, N-(C1-4-алкил)карбамоила, N,N-(C1-4-алкил)2карбамоила, C1-4-алкил-S(O)a, где a принимает значения от 0 до 2, C1-4-алкоксикарбонила, N-(C1-4-алкил)сульфамоила и N,N-(C1-4-алкил)2сульфамоила; где R3 и R6, и оставшийся из R4 и R5 необязательно могут быть замещены по атому углерода одним или несколькими заместителями R16;
X представляет собой -O-, -N(Ra)-, -S(O)b- или -CH(Ra)-; где Ra представляет собой водород или C1-6-алкил, и b принимает значения 0-2;
цикл A представляет собой арил или гетероарил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из групп R17;
R7 представляет собой водород, C1-4-алкил, карбоциклил или гетероциклил; где R7 необязательно замещен одним или несколькими заместителями, выбранными из групп R16;
R8 представляет собой водород или C1-4-алкил;
R9 представляет собой водород или C1-4-алкил;
R10 представляет собой водород, C1-4-алкил, карбоциклил или гетероциклил; где R10 необязательно замещен одним или несколькими заместителями, выбранными из групп R19;
R11 представляет собой карбокси, сульфо, сульфино, фосфоно, -P(O)(ORc)(ORd), -P(O)(OH)(ORc), -P(O)(OH)(Rd) или -P(O)(ORc)(Rd), где Rc и Rd независимо выбраны из C1-6-алкила; или R11 представляет собой группу формулы (IB) или (IC):
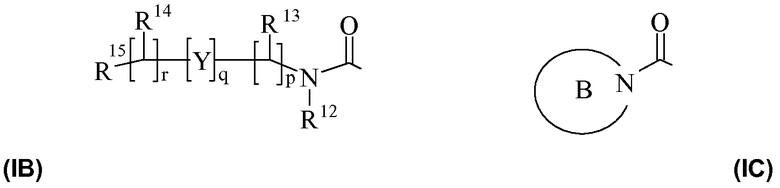
где:
Y представляет собой -N(Rn)-, -N(Rn)C(O)-, -N(Rn)C(O)(CRsRt)vN(Rn)C(O)-, -O- и -S(O)a-; где a принимает значения 0-2, v принимает значения 1-2, Rs и Rt независимо выбраны из водорода или C1-4-алкила, необязательно замещенного R26, и Rn представляет собой водород или C1-4-алкил;
R12 представляет собой водород или C1-4-алкил;
R13 и R14 независимо выбраны из водорода, C1-4-алкила, карбоциклила или гетероциклила; и если q означает 0, заместитель R14 может быть дополнительно выбран из гидроксигруппы, где R13 и R14 могут быть независимо необязательно замещены одним или несколькими заместителями, выбранными из групп R20;
R15 представляет собой карбокси, сульфо, сульфино, фосфоно, -P(O)(ORe)(ORf), -P(O)(OH)(ORe), -P(O)(OH)(Re) или -P(O)(ORe)(Rf), где Re и Rf независимо выбраны из C1-6-алкила;
p принимает значения 1-3; где R13 могут быть одинаковыми или различными;
q означает 0-1;
r означает 0-3; где R14 могут быть одинаковыми или различными;
m означает 0-2; где R10 могут быть одинаковыми или различными;
n означает 1-3; где R7 могут быть одинаковыми или различными;
цикл B представляет собой гетероциклический фрагмент, связанный с остальной частью молекулы через атом азота, замещенный по атому углерода одной группой, выбранной из R23 и необязательно дополнительно замещенный по атому углерода одним или несколькими фрагментами R24; и где, если указанный гетероциклил содержит фрагмент -NH-, этот атом азота может быть необязательно замещен группой, выбранной из R25;
R16, R17 и R18 независимо выбраны из галогена, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, C1-4-алкила, C2-4-алкенила, C2-4-алкинила, C1-4-алкокси, C1-4-алканоила, C1-4-алканоилокси, N-(C1-4-алкил)амино, N,N-(C1-4-алкил)2амино, C1-4-алканоиламино, N-(C1-4-алкил)карбамоила, N,N-(C1-4-алкил)2карбамоила, C1-4-алкил-S(O)a, где a принимает значения от 0 до 2, C1-4-алкоксикарбонила, N-(C1-4-алкил)сульфамоила и N,N-(C1-4-алкил)2сульфамоила; где R16, R17 и R18 могут быть независимо необязательно замещены по атому углерода одним или несколькими R21;
R19, R20, R24 и R26 независимо выбраны из галогена, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, C1-4-алкила, C2-4-алкенила, C2-4-алкинила, C1-4-алкокси, C1-4-алканоила, C1-4-алканоилокси, N-(C1-4-алкил)амино, N,N-(C1-4-алкил)2амино, C1-4-алканоиламино, N-(C1-4-алкил)карбамоила, N,N-(C1-4-алкил)2карбамоила, C1-4-алкил-S(O)a, где a принимает значения от 0 до 2, C1-4-алкоксикарбонила, N-(C1-4-алкил)сульфамоила, N,N-(C1-4-алкил)2сульфамоила, карбоциклила, гетероциклила, бензилоксикарбониламино, сульфо, сульфино, амидино, фосфоно, -P(O)(ORa)(ORb), -P(O)(OH)(ORa), -P(O)(OH)(Ra) или -P(O)(ORa)(Rb), где Ra и Rb независимо выбраны из C1-6-алкила; где R19, R20, R24 и R26 могут быть независимо необязательно замещены по атому углерода одним или несколькими R22;
R21 и R22 независимо выбраны из галогена, гидрокси, циано, карбамоила, уреидо, амино, нитро, карбокси, карбамоила, меркапто, сульфамоила, трифторметила, трифторметокси, метила, этила, метокси, этокси, винила, аллила, этинила, метоксикарбонила, формила, ацетила, формамидо, ацетиламино, ацетокси, метиламино, диметиламино, N-метилкарбамоила, N,N-диметилкарбамоила, метилтио, метилсульфинила, мезила, N-метилсульфамоила и N,N-диметилсульфамоила;
R23 представляет собой карбокси, сульфо, сульфино, фосфоно, -P(O)(ORg)(ORh), -P(O)(OH)(ORg), -P(O)(OH)(Rg) или -P(O)(ORg)(Rh), где Rg и Rh независимо выбраны из C1-6-алкила;
R25 выбран из C1-6-алкила, C1-6-алканоила, C1-6-алкилсульфонила, C1-6-алкоксикарбонила, карбамоила, N-(C1-6-алкил)карбамоила, N,N-(C1-6-алкил)2карбамоила, бензила, бензилоксикарбонила, бензоила и фенилсульфонила;
или их фармацевтически приемлемым солям, сольватам, сольватам этих солей или пролекарствам, для применения в профилактике или лечении заболевания печени.
Соединения, применяемые в настоящем изобретении, улучшают результаты тестов, связанных с деятельностью печени (содержание аминотрансферазы в сыворотке) и гистологию печени и значительно уменьшают содержание гидроксипролина и количество инфильтрующихся нейтрофилов и пролиферирующих гепатоцитов и холангиоцитов.
В литературе ингибиторы IBAT часто встречаются под различными наименованиями. Следует понимать, что, если в настоящей заявке упоминаются ингибиторы IBAT, этот термин также охватывает соединения, известные в литературе как: 1) ингибиторы подвздошного апикального натрий-созависимого переносчика желчных кислот (ASBT); ii) ингибиторы переносчика желчных кислот (BAT); iii) ингибиторы системы совместного переноса натрия/желчных кислот в подвздошной кишке; iv) ингибиторы апикального совместного переносчика натрия-желчных кислот; v) ингибиторы натрий-зависимого переноса желчных кислот в подвздошной кишке; vi) ингибиторы реабсорбции желчных кислот (BARI); и vii) ингибиторы переносчика натрия желчных кислот (SBAT); где они действуют за счет ингибирования IBAT.
В настоящем описании термин «алкил» включает алкильные группы как с линейной, так и с разветвленной цепью, но упоминания индивидуальных алкильных групп, например «пропила», конкретно указывают только на линейный вариант. Например, «C1-6-алкил» включает C1-4-алкил, C1-3-алкил, пропил, изопропил и трет-бутил. Однако упоминание индивидуальных алкильных групп, например «пропила», указывает только на линейный вариант, и упоминание индивидуальных алкильных групп с разветвленной цепью, например «изопропила», указывает только на вариант с разветвленной цепью. Аналогичная интерпретация применима к другим радикалам, например, «фенил-C1-6-алкил» мог бы включать фенил-C1-4-алкил, бензил, 1-фенилэтил и 2-фенилэтил. Термин «галоген» относится к фтору, хлору, брому и йоду.
Если необязательные заместители выбраны из «одной или нескольких групп», то следует понимать, что это определение включает все заместители, выбранные из одной из указанных групп, или заместители, выбранные из двух или нескольких из указанных групп.
«Гетероарил» представляет собой полностью ненасыщенный моно- или бициклический фрагмент, содержащий 3-12 атомов, причем по меньшей мере один из них выбран из азота, серы или кислорода, который, если не указано иначе, может быть связан с остальной частью молекулы через атом углерода или азота. Предпочтительно, термин «гетероарил» относится к полностью ненасыщенному моноциклическому фрагменту, содержащему 5 или 6 атомов, или бициклическому фрагменту, содержащему 9 или 10 атомов, причем по меньшей мере один из них выбран из азота, серы или кислорода, который, если не указано иначе, может быть связан с остальной частью молекулы через атом углерода или азота. В другом аспекте настоящего изобретения термин «гетероарил» относится к полностью ненасыщенному моноциклическому фрагменту, содержащему 5 или 6 атомов, или бициклическому фрагменту, содержащему 8, 9 или 10 атомов, причем по меньшей мере один из них выбран из азота, серы или кислорода, который, если не указано иначе, может быть связан с остальной частью молекулы через атом углерода или азота. Примерами и характерными представителями фрагментов, именуемых «гетероарилами», являются тиенил, изоксазолил, имидазолил, пирролил, тиадиазолил, изотиазолил, триазолил, пиранил, индолил, пиримидил, пиразинил, пиридазинил, пиридил и хинолил. Предпочтительно, термин «гетероарил» относится к тиенилу или индолилу.
Термин «арил» относится к полностью ненасыщенному моно- или бициклическому углеродному фрагменту, который включает 3-12 атомов. Предпочтительно «арил» представляет собой моноциклический фрагмент, содержащий 5 или 6 атомов, или бициклический фрагмент, содержащий 9 или 10 атомов. Характерные примеры «арила» включают фенил или нафтил. В честности «арил» представляет собой фенил.
«Гетероциклил» представляет собой насыщенный, частично насыщенный или ненасыщенный моно- или бициклический фрагмент, содержащий 3-12 атомов, причем по меньшей мере один из них выбран из азота, серы или кислорода, который, если не указано иначе, может быть связан с остальной частью молекулы через атомы углерода или азота, где группа -CH2- может быть необязательно заменена -C(O)-, или циклический атом серы может быть необязательно окислен с образованием S-оксида. Предпочтительно, «гетероциклил» представляет собой насыщенный, частично насыщенный или ненасыщенный моно- или бициклический фрагмент, содержащий 5 или 6 атомов, причем по меньшей мере один из них выбран из азота, серы или кислорода, который, если не указано иначе, может быть связан с остальной частью молекулы через атомы углерода или азота, где группа -CH2- может быть необязательно заменена -C(O)-, или циклический атом серы может быть необязательно окислен с образованием S-оксида(оксидов). Примерами и характерными представителями фрагментов, описываемых термином «гетероциклил», являются тиазолидинил, пирролидинил, пирролинил, 2-пирролидонил, 2,5-диоксопирролидинил, 2-бензоксазолинонил, 1,1-диоксотетрагидротиенил, 2,4-диоксоимидазолидинил, 2-оксо-1,3,4-(4-тиазолинил), 2-оксазолидинонил, 5,6-дигидроурацилил, 1,3-бензодиоксолил, 1,2,4-оксадиазолил, 2-азабицикло[2.2.1]гептил, 4-тиазолидонил, морфолино, 2-оксотетрагидрофуранил, тетрагидрофуранил, 2,3-дигидробензофуранил, бензотиенил, тетрагидропиранил, пиперидил, 1-оксо-1,3-дигидроизоиндолил, пиперазинил, тиоморфолино, 1,1-диоксотиоморфолино, тетрагидропиранил, 1,3-диоксоланил, гомопиперазинил, тиенил, изоксазолил, имидазолил, пирролил, тиадиазолил, изотиазолил, 1,2,4-триазолил, 1,3,4-триазолил, пиранил, индолил, пиримидинил, тиазолил, пиразинил, пиридазинил, пиридил, 4-пиридонил, хинолил и 1-изохинолонил.
«Карбоциклил» представляет собой насыщенный, частично насыщенный или ненасыщенный моно- или бициклический углеродный фрагмент, который содержит 3-12 атомов; в котором группа -CH2- может быть необязательно заменена -C(O)-. Предпочтительно, «карбоциклил» представляет собой моноциклический фрагмент, содержащий 5 или 6 атомов, или бициклический фрагмент, содержащий 9 или 10 атомов. Характерные примеры «карбоциклила» включают циклопропил, циклобутил, 1-оксоциклопентил, циклопентил, циклопентенил, циклогексил, циклогексенил, фенил, нафтил, тетралинил, инданил или 1-оксоинданил. В частности, «карбоциклил» представляет собой циклопропил, циклобутил, 1-оксоциклопентил, циклопентил, циклопентенил, циклогексил, циклогексенил, фенил или 1-оксоинданил.
Примером «C1-6-алканоилокси» и «C1-4-алканоилокси» является ацетоксигруппа. Примеры «C1-6-алкоксикарбонила» и «C1-4-алкоксикарбонила» включают метоксикарбонил, этоксикарбонил, н- и трет-бутоксикарбонил. Примеры «C1-6-алкокси» и «C1-4-алкокси» включают метокси, этокси и пропокси. Примеры «C1-6-алканоиламино» и «C1-4-алканоиламино» включают формамидо, ацетамидо и пропиониламино. Примеры «C1-6-алкил-S(O)a, где a принимает значения от 0 до 2» и «C1-4-алкил-S(O)a, где a принимает значения от 0 до 2» включают метилтио, этилтио, метилсульфинил, этилсульфинил, мезил и этилсульфонил. Примеры «C1-6-алканоила» и «C1-4-алканоила» включают C1-3-алканоил, пропионил и ацетил. Примеры «N-(C1-6-алкил)амино» и «N-(C1-4-алкил)амино» включают метиламино и этиламино. Примеры «N,N-(C1-6-алкил)2амино» и «N,N-(C1-4-алкил)2амино» включают ди-N-метиламино, ди-(N-этил)амино и N-этил-N-метиламино. Примерами «C2-6-алкенила» и «C2-4-алкенила» являются винил, аллил и 1-пропенил. Примерами «C2-6-алкинила» и «C2-4-алкинила» являются этинил, 1-пропинил и 2-пропинил. Примерами «N-(C1-6-алкил)сульфамоила» и «N-(C1-4-алкил)сульфамоила» являются N-(C1-3-алкил)сульфамоил, N-(метил)сульфамоил и N-(этил)сульфамоил. Примерами «N-(C1-6-алкил)2сульфамоила» и «N-(C1-4-алкил)2сульфамоила» являются N,N-(диметил)сульфамоил и N-(метил)-N-(этил)сульфамоил. Примерами «N-(C1-6-алкил)карбамоила» и «N-(C1-4-алкил)карбамоила» являются метиламинокарбонил и этиламинокарбонил. Примерами «N,N-(C1-6-алкил)2карбамоила» и «N,N-(C1-4-алкил)2карбамоила» являются диметиламинокарбонил и метилэтиламинокарбонил. Примерами «C1-6-алкоксикарбониламино» являются этоксикарбониламино и трет-бутоксикарбониламино. Примерами «N'-(C1-6-алкил)уреидо» являются N'-метилуреидо и N'-этилуреидо. Примерами «N-(C1-6-алкил)уреидо» являются N-метилуреидо и N-этилуреидо. Примерами «N',N'-(C1-6-алкил)2уреидо» являются N',N'-диметилуреидо и N'-метил-N'-этилуреидо. Примерами «N'-(C1-6-алкил)-N-(C1-6-алкил)уреидо» являются N'-метил-N-метилуреидо и N'-пропил-N-метилуреидо. Примерами «N',N'-(C1-6-алкил)2-N-(C1-6-алкил)уреидо» являются N',N'-диметил-N-метилуреидо и N'-метил-N'-этил-N-пропилуреидо.
Подходящая фармацевтически приемлемая соль соединения по настоящему изобретению является, например, кислотно-аддитивной солью соединения по настоящему изобретению, которое является главным образом основным, например, кислотно-аддитивной солью, образованной, например, неорганической или органической кислотой, например, хлористоводородной, бромистоводородной, серной, фосфорной, трифторуксусной, лимонной или малеиновой кислотой.
Кроме того, подходящая фармацевтически приемлемая соль соединения по настоящему изобретению, которое является главным образом кислотным, представляет собой соль щелочного металла, например, соль натрия или калия, соль щелочноземельного металла, например, соль кальция или магния, соль аммония или соль с органическим основанием, которое образует физиологически приемлемый катион, например, соль с метиламином, диметиламином, триметиламином, пиперидином, морфолином или трис-(2-гидроксиэтил)амином.
Соединения формулы (I) можно вводить в форме пролекарства, которое в организме человека или животного расщепляется с образованием соединения формулы (I). Примеры пролекарств включают гидролизуемые in vivo сложные эфиры и гидролизуемые in vivo амиды соединения формулы (I).
Гидролизуемый in vivo сложный эфир соединения формулы (I), содержащего карбокси- или гидроксигруппу, является, например, фармацевтически приемлемым эфиром, который гидролизуется в организме человека или животного с образованием исходной кислоты или спирта. Подходящие фармацевтически приемлемые сложные эфиры для карбоксисоединений включают C1-6-алкоксиметиловые эфиры, например, метоксиметиловый, C1-6-алканоилоксиметиловые эфиры, например, пивалоилоксиметиловый, фталидиловые эфиры, C3-8-циклоалкоксикарбонилокси-C1-6-алкиловые эфиры, например, 1-циклогексилкарбонилоксиэтиловый; 1,3-диоксолен-2-онилметиловые эфиры, например, 5-метил-1,3-диоксолен-2-онилметиловый; и C1-6-алкоксикарбонилоксиэтиловые эфиры, например, 1-метокси-карбонилоксиэтиловый, и такие эфиры могут быть образованы любой карбоксигруппой соединения по настоящему изобретению.
Гидролизуемые in vivo сложные эфиры соединения формулы (I), содержащего гидроксигруппу, включают неорганические сложные эфиры, например, фосфаты и α-ацилоксиалкиловые эфиры и родственные соединения, которые в результате гидролиза эфира in vivo распадаются с образованием исходного гидроксисоединения. Примеры α-ацилоксиалкиловых эфиров включают ацетоксиметокси и 2,2-диметилпропионилокси-метокси. Группы, образующие гидролизуемый in vivo сложный эфир с гидроксигруппами, включают алканоил, бензоил, фенилацетил и замещенные бензоил и фенилацетил, алкоксикарбонил (который образует алкилкарбонаты), диалкилкарбамоил и N-(диалкиламиноэтил)-N-алкилкарбамоил (который образует карбаматы), диалкиламиноацетил и карбоксиацетил. Примеры заместителей бензоильной группы включают морфолино- и пиперазиногруппы, связанные по циклическому атому азота через метиленовую группу с 3- или 4-положением бензоильного цикла.
Подходящими примерами гидролизуемых in vivo амидов соединения формулы (I), содержащих карбоксигруппу, являются, например, N-C1-6-алкил или N,N-ди-C1-6-алкиламиды, такие как N-метил, N-этил, N-пропил, N,N-диметил, N-этил-N-метил или N,N-диэтиламиды. Кроме того, следует понимать, что некоторые соединения формулы (I) могут существовать как в сольватированной, так и в несольватированной формах, например, в гидратированных формах. Следует понимать, что изобретение охватывает все эти сольватированные формы, которые обладают IBAT-ингибирующей активностью.
Ниже по тексту приведены предпочтительные значения R1, R2, R3, R4, R5 и R6. Эти конкретные значения могут использоваться во всех подходящих случаях в любых определениях, формуле изобретения или вариантах осуществления, описанных выше или ниже по тексту.
Предпочтительно, R1 и R2 независимо выбраны из C1-4-алкилов. Более предпочтительно, R1 и R2 независимо выбраны из этила или бутила. Более предпочтительно, R1 и R2 независимо выбраны из этила, пропила или бутила. В одном из аспектов настоящего изобретения оба заместителя R1 и R2 в частности являются бутилом. В другом аспекте настоящего изобретения оба заместителя R1 и R2 в частности являются пропилом. В еще одном аспекте изобретения один из R1 и R2 конкретно представляет собой этил, а другой - бутил.
Предпочтительно, Rx и Ry независимо выбраны из водорода или C1-6-алкила. Более предпочтительно, оба Rx и Ry являются атомами водорода. Предпочтительно, Rz выбран из галогена, амино, C1-6-алкила, C1-6-алкоксикарбониламино или N'-(C1-6-алкил)уреидо.
Более предпочтительно, Rz выбран из хлора, амино, трет-бутила, трет-бутоксикарбониламино или N'-(трет-бутил)уреидо.
Предпочтительно, v означает 0 или 1. В одном из аспектов настоящего изобретения более предпочтительно v принимает значение 0. В другом аспекте изобретения более предпочтительно v принимает значение 1.
В одном из аспектов настоящего изобретения R4 предпочтительно представляет собой группу формулы (IA) (которая показана выше). В другом аспекте настоящего изобретения R5 предпочтительно представляет собой группу формулы (IA) (которая показана выше).
R3 и R6 предпочтительно являются атомами водорода. Предпочтительно, оставшиеся R4 и R5, которые не являются группами формулы (IA), выбраны из галогена, C1-4-алкокси или C1-4-алкил-S(O)a, где a принимает значения от 0 до 2; где эти R4 или R5 могут быть необязательно замещены по атому углерода одним или несколькими R16; где R16 независимо выбран из гидрокси и N,N-(C1-4-алкил)2амино.
Более предпочтительно, оставшиеся R4 и R5, которые не являются группами формулы (IA), выбраны из брома, метокси, изопропокси, метилтио, этилтио, изопропилтио или мезила; где эти R4 или R5 могут быть необязательно замещены по атому углерода одним или несколькими R16; причем R16 независимо выбран из гидрокси и N,N-диметиламино.
В частности эти оставшиеся R4 и R5, которые не являются группами формулы (IA), выбраны из брома, метокси, изопропокси, метилтио, этилтио, изопропилтио, 2-гидроксиэтилтио, 2-(N,N-диметиламино)этилтио или мезила.
Более конкретно, эти оставшиеся R4 и R5, которые не являются группами формулы (IA), представляют собой метилтио. Предпочтительно, эти оставшиеся R4 и R5, которые не являются группами формулы (IA), выбраны из водорода, галогена, C1-4-алкокси или C1-4-алкил-S(O)a, где a принимает значения от 0 до 2; где эти R4 или R5 могут быть необязательно замещены по атому углерода одним или несколькими R16; причем R16 независимо выбран из гидрокси, карбокси и N,N-(C1-4-алкил)2амино.
Более предпочтительно, эти оставшиеся R4 и R5, которые не являются группами формулы (IA), выбраны из водорода, брома, метокси, изопропокси, метилтио, этилтио, изопропилтио или мезила; где эти R4 или R5 могут быть необязательно замещены по атому углерода одним или несколькими R16; причем R16 независимо выбран из гидрокси, карбокси и N,N-диметиламино.
В частности, эти оставшиеся R4 и R5, которые не являются группами формулы (IA), выбраны из водорода, брома, метокси, изопропокси, метилтио, карбоксиметилтио, этилтио, изопропилтио, 2-гидроксиэтилтио, 2-(N,N-диметиламино)этилтио или мезила. В другом аспекте настоящего изобретения, более предпочтительно, эти оставшиеся R4 и R5, которые не являются группами формулы (IA), выбраны из водорода, хлора, брома, метокси, изопропокси, метилтио, этилтио или изопропилтио; где эти R4 или R5 могут быть необязательно замещены по атому углерода одним или несколькими R16; причем R16 независимо выбран из гидрокси, карбокси и N,N-диметиламино.
В другом аспекте настоящего изобретения эти оставшиеся R4 и R5, которые не являются группами формулы (IA), конкретно выбраны из водорода, хлора, брома, метокси, изопропокси, метилтио, карбоксиметилтио, этилтио, изопропилтио, 2-гидроксиэтилтио или 2-(N,N-диметиламино)этилтио.
В другом аспекте настоящего изобретения, более конкретно, эти оставшиеся R4 и R5, которые не являются группами формулы (IA), представляют собой бром или хлор.
В другом аспекте настоящего изобретения, более конкретно, эти оставшиеся R4 и R5, которые не являются группами формулы (IA), представляют собой метокси.
В одном из аспектов настоящего изобретения цикл A предпочтительно представляет собой арил. В другом аспекте настоящего изобретения цикл A предпочтительно представляет собой гетероарил. Если цикл A представляет собой арил, предпочтительно цикл A представляет собой фенил. Если цикл A представляет собой гетероарил, предпочтительно цикл A представляет собой тиенил или индолил. Предпочтительно, цикл A представляет собой арил или гетероарил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из R17; где R17 выбран из галогена, гидрокси или C1-4-алкила; причем R17 может быть необязательно замещен по атому углерода одним или несколькими R21; где R21 выбран из галогена.
X предпочтительно представляет собой -O.
Более предпочтительно, цикл A представляет собой фенил, тиенил или индолил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из галогена, гидрокси или трифторметила. В частности, цикл A выбран из фенила, 4-гидроксифенила, тиен-2-ила, 4-трифторметилфенила, 3-гидроксифенила, 2-фторфенила, 2,3-дигидроксифенила или индол-3-ила. Более конкретно, цикл A представляет собой фенил.
В другом аспекте настоящего изобретения цикл A предпочтительно представляет собой арил или гетероарил; причем цикл A необязательно замещен одним или несколькими заместителями, выбранными из R17; где R17 выбран из галогена, гидрокси, C1-4-алкила или C1-4-алкокси; причем R17 может быть необязательно замещен по атому углерода одним или несколькими R21; где R21 выбран из галогена.
В другом аспекте настоящего изобретения цикл A более предпочтительно представляет собой фенил, тиенил или индолил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из галогена, гидрокси, метокси или трифторметила.
В другом аспекте настоящего изобретения цикл A в частности выбран из фенила, 4-гидроксифенила, 4-метоксифенила, тиен-2-ила, 4-трифторметилфенила, 3-гидроксифенила, 2-фторфенила, 2,3-дигидроксифенила или индол-3-ила.
В еще одном аспекте настоящего изобретения цикл A конкретно выбран из фенила, 4-гидроксифенила, 4-метоксифенила, тиен-2-ила, 4-трифторметилфенила, 3-гидроксифенила, 2-фторфенила, 4-фторфенила, 2,3-дигидроксифенила или индол-3-ила.
R7 предпочтительно представляет собой водород, C1-4-алкил или карбоциклил. Более предпочтительно, R7 представляет собой водород, метил или фенил. В частности, R7 представляет собой водород. В одном из аспектов настоящего изобретения R8 предпочтительно представляет собой водород. В другом аспекте настоящего изобретения R8 предпочтительно представляет собой C1-4-алкил. В другом аспекте настоящего изобретения R8 более предпочтительно представляет собой водород или метил. В одном из аспектов настоящего изобретения R9 предпочтительно представляет собой водород. В другом аспекте настоящего изобретения R9 предпочтительно представляет собой C1-4-алкил. В другом аспекте настоящего изобретения R9 более предпочтительно представляет собой водород или метил. R10 предпочтительно представляет собой водород.
В одном из аспектов настоящего изобретения R11 представляет собой карбокси, сульфо, сульфино, фосфоно, -P(O)(ORc)(ORd), -P(O)(OH)(ORc), -P(O)(OH)(Rd) или -P(O)(ORc)(Rd), где Rc и Rd независимо выбраны из C1-6-алкилов.
В другом аспекте настоящего изобретения R11 предпочтительно представляет собой группу формулы (IB) (которая изображена выше).
Предпочтительно, R11 представляет собой карбокси, -P(O)(OH)(ORc) или группу формулы (IB) (которая изображена выше). Более предпочтительно, R11 представляет собой карбокси, -P(O)(OH)(OEt) или группу формулы (IB) (которая изображена выше).
В другом аспекте настоящего изобретения R11 предпочтительно представляет собой карбокси, сульфо, -P(O)(OH)(ORc), где Rc выбран из C1-4-алкила или группы формулы (IB) (которая изображена выше).
Y предпочтительно представляет собой -NH- или -NHC(O)-.
Более предпочтительно, Y представляет собой -NHC(O)-.
В одном из аспектов настоящего изобретения R12 предпочтительно представляет собой водород. В другом аспекте настоящего изобретения R12 предпочтительно представляет собой C1-4-алкил. В следующем аспекте изобретения R12 более предпочтительно представляет собой водород или метил.
R13 предпочтительно представляет собой водород, C1-4-алкил или карбоциклил; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; где R20 представляет собой гидрокси. Более предпочтительно, R13 представляет собой водород, метил или фенил; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; где R20 представляет собой гидрокси. В частности, R13 представляет собой водород, гидроксиметил или фенил. Более конкретно, R13 представляет собой водород или гидроксиметил.
В другом аспекте настоящего изобретения R13 предпочтительно представляет собой водород, C1-4-алкил или карбоциклил; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; где R20 представляет собой гидрокси, карбокси, карбоциклил или амино; причем R20 может быть необязательно замещен по атому углерода одним или несколькими R22; где R22 представляет собой гидрокси.
В другом аспекте настоящего изобретения R13 более предпочтительно представляет собой водород, метил, этил, бутил или фенил; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; где R20 представляет собой гидрокси, карбокси, фенил или амино; причем R20 может быть необязательно замещен по атому углерода одним или несколькими R22; где R22 представляет собой гидрокси.
В следующем аспекте настоящего изобретения R13 конкретно представляет собой водород, гидроксиметил, 4-аминобутил, 2-карбоксиэтил, 4-гидроксибензил или фенил.
В следующем аспекте настоящего изобретения R13 предпочтительно представляет собой водород, C1-4-алкил или карбоциклил; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; где R20 представляет собой гидрокси, карбокси, карбоциклил, гетероциклил или амино; причем R20 может быть необязательно замещен по атому углерода одним или несколькими R22; где R22 представляет собой гидрокси.
В другом аспекте настоящего изобретения R13 более предпочтительно представляет собой водород, метил, этил, бутил или фенил; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; где R20 представляет собой гидрокси, карбокси, фенил, имидазолил или амино; причем R20 может быть необязательно замещен по атому углерода одним или несколькими R22; где R22 представляет собой гидрокси.
В еще одном аспекте настоящего изобретения R13 конкретно представляет собой водород, гидроксиметил, 4-аминобутил, 2-карбоксиэтил, 4-гидроксибензил, имидазол-5-илметил или фенил.
В следующем аспекте настоящего изобретения R13 предпочтительно представляет собой водород, C1-4-алкил, карбоциклил или R23; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; причем R20 представляет собой гидрокси, C1-4-алкил-S(O)a, где a равно 0, C1-4-алкокси, амино, карбоциклил, гетероциклил или меркапто; причем R20 может быть независимо необязательно замещен по атому углерода одним или несколькими R22; где R22 представляет собой гидрокси; и R23 представляет собой карбокси.
В еще одном аспекте настоящего изобретения R13 более предпочтительно представляет собой водород, метил, этил, бутил, фенил или R23; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; причем R20 представляет собой гидрокси, метилтио, метокси, амино, имидазолил или меркапто; причем R20 может быть независимо необязательно замещен по атому углерода одним или несколькими R22; где R22 представляет собой гидрокси; и R23 представляет собой карбокси.
В следующем аспекте настоящего изобретения R13 в частности представляет собой водород, карбокси, гидроксиметил, меркаптометил, метоксиметил, метилтиометил, 2-метилтиоэтил, 4-аминобутил, 4-гидроксибензил, имидазол-5-илметил или фенил.
В другом аспекте R13 более конкретно представляет собой метилтиометил, метилсульфинилметил или метилсульфонилметил.
R14 предпочтительно представляет собой водород.
В другом аспекте настоящего изобретения R14 предпочтительно выбран из водорода, C1-4-алкила или карбоциклила; где указанный C1-4-алкил или карбоциклил может быть необязательно замещен одним или несколькими заместителями, выбранными из R20; и R20 представляет собой гидрокси.
В следующем аспекте настоящего изобретения R14 более предпочтительно выбран из водорода, метила или фенила; где указанный метил или фенил может быть необязательно замещен одним или несколькими заместителями, выбранными из R20; и R20 представляет собой гидрокси.
В другом аспекте изобретения R14, в частности, представляет собой водород, фенил или гидроксиметил.
R15 в том числе представляет собой карбокси или сульфо.
В одном из аспектов изобретения R15 более конкретно представляет собой карбокси.
В другом аспекте настоящего изобретения R15 более конкретно представляет собой сульфогруппу.
R15 предпочтительно представляет собой карбокси, сульфо, -P(O)(ORe)(ORf), -P(O)(OH)(ORe), -P(O)(OH)(Re) или -P(O)(ORe)(Rf), где Re и Rf независимо выбраны из C1-4-алкила.
Более предпочтительно, R15 представляет собой карбокси, сульфо, -P(O)(ORe)(ORf), -P(O)(OH)(ORe), -P(O)(OH)(Re) или -P(O)(ORe)(Rf), где Re и Rf независимо выбраны из метила или этила.
R15 предпочтительно представляет собой карбокси, сульфо, -P(O)(OEt)(OEt), -P(O)(OH)(OEt), -P(O)(OH)(Me) или -P(O)(OEt)(Me).
R15 предпочтительно представляет собой карбокси, сульфо, фосфоно, -P(O)(ORe)(ORf), -P(O)(OH)(ORe), -P(O)(OH)(Re) или -P(O)(ORe)(Rf), где Re и Rf независимо выбраны из C1-4-алкила, или R15 представляет собой группу формулы (IC) (которая приведена выше).
Более предпочтительно, R15 представляет собой карбокси, сульфо, фосфоно, -P(O)(ORe)(ORf), -P(O)(OH)(ORe), -P(O)(OH)(Re) или -P(O)(ORe)(Rf), где Re и Rf независимо выбраны из метила или этила, или R15 представляет собой группу формулы (IC) (которая приведена выше).
R15 предпочтительно представляет собой карбокси, сульфо, фосфоно, -P(O)(OEt)(OEt), -P(O)(Ot-Bu)(Ot-Bu), -P(O)(OH)(OEt), -P(O)(OH)(Me) или -P(O)(OEt)(Me), или R15 представляет собой группу формулы (IC) (которая приведена выше).
В одном из аспектов настоящего изобретения R15 предпочтительно представляет собой карбокси.
В другом аспекте настоящего изобретения R15 предпочтительно представляет собой сульфо.
В следующем аспекте настоящего изобретения R15 предпочтительно представляет собой -P(O)(OH)(OEt).
В следующем аспекте настоящего изобретения R15 предпочтительно представляет собой -P(O)(OH)(Me).
В следующем аспекте настоящего изобретения R15 предпочтительно представляет собой -P(O)(OEt)(Me).
В одном из аспектов настоящего изобретения R24 предпочтительно представляет собой водород.
В другом аспекте настоящего изобретения R24 предпочтительно представляет собой C1-4-алкил.
R25 предпочтительно представляет собой водород.
R26 предпочтительно представляет собой карбокси.
Предпочтительно, p принимает значения 1 или 2; где R13 могут быть одинаковыми или различными. В одном из аспектов настоящего изобретения p более предпочтительно равно 1. В другом аспекте настоящего изобретения p, более предпочтительно, равно 2; причем R13 могут быть одинаковыми или различными. В следующем аспекте настоящего изобретения p, более предпочтительно, равно 3; причем R13 могут быть одинаковыми или различными.
В одном из аспектов настоящего изобретения q предпочтительно равно 0. В другом аспекте настоящего изобретения q предпочтительно равно 1.
В одном из аспектов настоящего изобретения r предпочтительно равно 0. В одном из аспектов настоящего изобретения r более предпочтительно равно 1. В другом аспекте настоящего изобретения r более предпочтительно равно 2; причем R14 могут быть одинаковыми или различными. В следующем аспекте настоящего изобретения r более предпочтительно равно 3; причем R14 могут быть одинаковыми или различными.
Предпочтительно m принимает значение 0. В другом аспекте настоящего изобретения m предпочтительно принимает значения 0 или 1.
Предпочтительно n равно 1. В другом аспекте изобретения n предпочтительно равно 1 или 2.
Предпочтительно z равно 1.
Группа формулы (IA), где R7 представляет собой водород, метил или фенил, n равно 1, цикл A представляет собой фенил, тиенил или индолил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из галогена, гидрокси или трифторметила, m равно 0, и R9 представляет собой карбокси, -P(O)(OH)(ORc) или группу формулы (IB).
Группа формулы (IA), где X представляет собой -O-.
Цикл A представляет собой фенил, тиенил или индолил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из галогена, гидрокси, метокси или трифторметила;
R7 представляет собой водород, метил или фенил;
R8 представляет собой водород или метил;
R9 представляет собой водород или метил;
R10 представляет собой водород;
m означает 0-2, где R10 могут быть одинаковыми или различными; и R11 представляет собой карбокси, -P(O)(OH)(OEt) или группу формулы (IB) (которая изображена в п.1 формулы изобретения); группа формулы (IB), где R10 представляет собой водород, гидроксиметил или фенил, p равно 1 или 2; где R10 могут быть одинаковыми или различными, и R11 представляет собой карбокси или сульфо.
Группа формулы (IB), в которой:
R12 представляет собой водород или метил;
R13 представляет собой водород, метил, этил, бутил, фенил или R23; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; R20 представляет собой гидрокси, метилтио, метокси, амино, имидазолил или меркапто; где R20 может быть независимо необязательно замещен по атому углерода одной или несколькими гидроксигруппами; R23 представляет собой карбокси; Y представляет собой -NH- или -NHC(O)-; R14 выбран из водорода, метила или фенила; где указанные метил или фенил могут быть необязательно замещены одним или несколькими заместителями, выбранными из гидрокси; R15 представляет собой карбокси, сульфо, фосфоно, -P(O)(ORe)(ORf), -P(O)(OH)(ORe), -P(O)(OH)(Re) или -P(O)(ORe)(Rf), где Re и Rf независимо выбраны из метила или этила, или R15 представляет собой группу формулы (IC) (которая приведена в п.1 формулы изобретения);
p означает 1-3, где R13 могут быть одинаковыми или различными;
q означает 0-1; и
r означает 0-3, где R14 могут быть одинаковыми или различными.
Группа формулы (IC), где
R24 представляет собой водород;
R25 представляет собой водород;
R26 представляет собой карбокси; и
z равно 1;
или его фармацевтически приемлемая соль, сольват, сольват этой соли или пролекарство.
Таким образом, в другом аспекте настоящее изобретение относится к соединению приведенной выше формулы (I), в котором:
R1 и R2 независимо выбраны из этила или бутила;
R3 и R6 представляют собой атомы водорода;
R4 выбран из галогена, C1-4-алкокси или C1-4-алкил-S(O)a, где a принимает значения от 0 до 2; где упомянутый R4 может быть необязательно замещен по атому углерода одним или несколькими R16; где R16 независимо выбран из гидрокси и N,N-(C1-4-алкил)2амино;
R5 представляет собой группу формулы (IA);
цикл A представляет собой арил или гетероарил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из R17; где
R17 выбран из галогена, гидрокси или C1-4-алкила; где R17 может быть необязательно замещен по атому углерода одним или несколькими R21; где
R21 выбран из галогена;
R7 представляет собой водород, C1-4-алкил или карбоциклил;
R11 представляет собой карбокси, -P(O)(OH)(ORc) или группу формулы (IB) (которая изображена выше);
R13 представляет собой водород, C1-4-алкил или карбоциклил; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; где
R20 представляет собой гидрокси;
R15 представляет собой карбокси или сульфо;
p означает 1 или 2; где заместители R13 могут быть одинаковыми или различными;
m равно 0; и
n равно 1;
или его фармацевтически приемлемой соли, сольвату, сольвату этой соли или пролекарству.
Таким образом, в еще одном аспекте настоящее изобретение относится к соединению приведенной выше формулы (I), где:
оба R1 и R2 являются бутилом, или один из R1 и R2 представляет собой этил, а другой представляет собой бутил;
R4 представляет собой метилтио;
R5 представляет собой группу формулы (IA) (которая показана выше);
R3 и R6 представляют собой атомы водорода;
цикл A представляет собой фенил;
R7 представляет собой водород;
R11 представляет собой группу формулы (IB) (которая показана выше);
R13 представляет собой водород или гидроксиметил;
R15 представляет собой карбокси или сульфо;
p равно 1 или 2, где R13 могут быть одинаковыми или различными;
m равно 0;
n равно 1;
или его фармацевтически приемлемой соли, сольвату, сольвату этой соли или пролекарству.
Таким образом, в еще одном аспекте настоящее изобретение относится к соединению приведенной выше формулы (I), где:
R1 и R2 независимо выбраны из этила или бутила;
R3 и R6 представляют собой атомы водорода;
R4 выбран из галогена, C1-4-алкокси или C1-4-алкил-S(O)a, где a принимает значения от 0 до 2; где упомянутый R4 может быть необязательно замещен по атому углерода одним или несколькими R16; где R16 независимо выбран из гидрокси и N,N-(C1-4-алкил)2амино;
R5 представляет собой группу формулы (IA);
цикл A представляет собой арил или гетероарил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из R17;
R7 представляет собой водород, C1-4-алкил или карбоциклил;
R8 представляет собой водород или метил;
R9 представляет собой водород или метил;
R11 представляет собой карбокси, -P(O)(OH)(ORc) или группу формулы (IB) (которая изображена выше);
X представляет собой -NH- или -NHC(O)-;
R12 представляет собой водород или метил;
R13 представляет собой водород, C1-4-алкил или карбоциклил; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20;
R14 представляет собой водород;
R15 представляет собой карбокси или сульфо;
R17 выбран из галогена, гидрокси, C1-4-алкила или C1-4-алкокси; где R17 может быть необязательно замещен по атому углерода одним или несколькими R21;
R20 представляет собой гидрокси, карбокси, карбоциклил или амино; где R20 может быть необязательно замещен по атому углерода одним или несколькими R22;
R21 выбран из галогена;
R22 представляет собой гидрокси;
p означает 1-3; где R13 могут быть одинаковыми или различными;
q означает 0-1;
r означает 0-3; где R14 могут быть одинаковыми или различными; и где, если q равно 1, r не равно 0;
m означает 0-2; и
n означает 1-3;
или его фармацевтически приемлемой соли, сольвату, сольвату этой соли или пролекарству.
Таким образом, в еще одном дополнительном аспекте настоящее изобретение относится к соединению приведенной выше формулы (I), где:
R1 и R2 независимо выбраны из C1-4-алкила;
оба Rx и Ry представляют собой атомы водорода;
Rz выбран из галогена, амино, C1-6-алкила, C1-6-алкоксикарбониламино или N'-(C1-6-алкил)уреидо;
v означает 0 или 1;
R3 и R6 представляют собой атомы водорода;
один из R4 и R5 представляет собой группу формулы (IA) (которая показана выше), и другой выбран из водорода, галогена, C1-4-алкокси или C1-4-алкил-S(O)a, где a принимает значения от 0 до 2; где этот R4 или R5 может быть необязательно замещен по атому углерода одним или несколькими R16; где R16 независимо выбран из гидрокси, карбокси и N,N-(C1-4-алкил)2амино;
X представляет собой -O-;
R7 представляет собой водород, метил или фенил;
R8 представляет собой водород или метил;
цикл A представляет собой арил или гетероарил; где цикл A необязательно замещен одним или несколькими заместителями, выбранными из R17; где R17 выбран из галогена, гидрокси, C1-4-алкила или C1-4-алкокси; где R17 может быть необязательно замещен по атому углерода одним или несколькими R21; где R21 выбран из галогена;
R9 представляет собой водород или метил;
R10 представляет собой водород;
R11 представляет собой карбокси, -P(O)(OH)(ORc), где Rc выбран из C1-4-алкила или группы формулы (IB) (которая изображена выше);
R12 представляет собой водород или метил;
Y представляет собой -NH- или -NHC(O)-;
R13 представляет собой водород, C1-4-алкил, карбоциклил или R23; где R13 необязательно замещен одним или несколькими заместителями, выбранными из R20; где R20 представляет собой гидрокси, C1-4-алкил-S(O)a, где a равно 0, C1-4-алкокси, амино, карбоциклил, гетероциклил или меркапто; где R20 может быть независимо необязательно замещен по атому углерода одним или несколькими R22; где R22 выбран из гидрокси; и R23 представляет собой карбокси;
R14 выбран из водорода, C1-4-алкила или карбоциклила; где указанные C1-4-алкил или карбоциклил могут быть необязательно замещены одним или несколькими заместителями, выбранными из R20; и R20 представляет собой гидрокси;
R15 представляет собой карбокси, сульфо, фосфоно, -P(O)(ORe)(ORf), -P(O)(OH)(ORe), -P(O)(OH)(Re) или -P(O)(ORe)(Rf), где Re и Rf независимо выбраны из C1-4-алкила, или R15 представляет собой группу формулы (IC) (которая приведена выше);
R24 представляет собой водород;
R25 представляет собой водород;
R26 представляет собой карбокси;
p означает 1-3; где R13 могут быть одинаковыми или различными;
q означает 0-1;
r означает 0-3; где R14 могут быть одинаковыми или различными;
m означает 0-2; где R10 могут быть одинаковыми или различными;
n означает 1-2; где R7 могут быть одинаковыми или различными;
z означает 0-1; где R25 могут быть одинаковыми или различными;
или его фармацевтически приемлемой соли, сольвату, сольвату этой соли или пролекарству.
В другом аспекте настоящего изобретения предпочтительные соединения по настоящему изобретению являются любыми соединениями из числа приведенных в примерах настоящей заявки, или их фармацевтически приемлемых солей, сольватов, сольватов этих солей или пролекарств.
В одном из аспектов настоящее изобретение относится к соединению формулы (II):
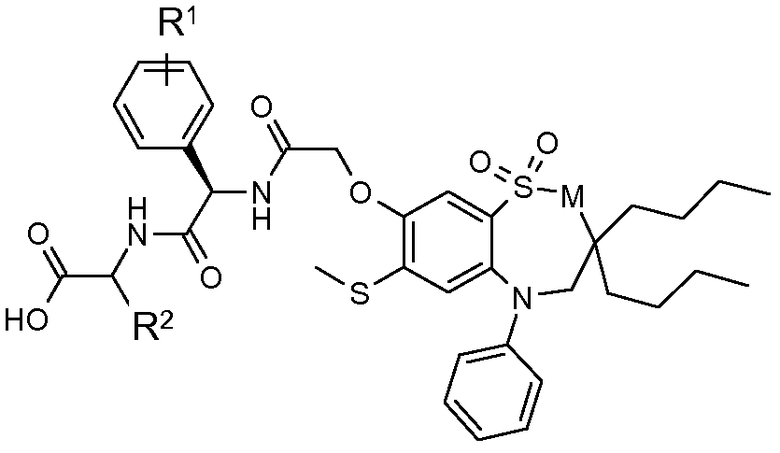
Формула II
где
M представляет собой CH2 или NH;
R1 представляет собой H или гидрокси;
R2 представляет собой H, CH3, -CH2CH3, -CH2CH2CH3, -CH2CH2CH2CH3, -CH(CH3)2, -CH2CH(CH3)2, -CH(CH3)CH2CH3, -CH2OH, -CH2OCH3, -CH(OH)CH3, -CH2SCH3 или -CH2CH2SCH3;
для применения в профилактике или лечении заболеваний печени.
Примерами веществ, подходящих для применения по настоящему изобретению, являются:
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-(карбоксиметил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N'-((S)-1-карбоксиэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((R)-1-карбокси-2-метилтиоэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((R)-1-карбокси-2-метилтиоэтил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-метилпропил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-(R)-гидроксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксибутил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксиэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N'-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксиэтил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-метилпропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин; и
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1'-фенил-1'-[N'-(карбоксиметил)карбамоил]метил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин.
Соединения формулы (I) или формулы (II) могут иметь хиральные центры и/или центры геометрической изомерии (E- и Z-изомеры), и необходимо понимать, что изобретение охватывает все оптические изомеры, диастереомеры и геометрические изомеры, которые обладают IBAT-ингибирующей активностью. Изобретение относится ко всем без исключения таутомерным формам соединений формулы (I) или формулы (II), которые обладают IBAT-ингибирующей активностью.
Кроме того, настоящее изобретение относится ко всем возможным изомерам соединений по настоящему изобретению, например, оптическим и/или геометрическим, чистым или в форме смеси, во всех соотношениях, указанных соединений формул (I) и (II) и конкретно упомянутых соединений этих формул, а также к возможным таутомерным формам.
В некоторых вариантах осуществления, соединения, описанные в настоящей заявке, содержат один или несколько хиральных центров. В этом случае все стереоизомеры предусмотрены настоящим изобретением. В различных вариантах осуществления, соединения, описанные в настоящей заявке, находятся в оптически активной или рацемической формах. Следует понимать, что соединения по настоящему изобретению охватывают рацемические, оптически активные, региоизомерные и стереоизомерные формы или их комбинации, которые обладают терапевтически полезными свойствами, описанными в заявке. Получение оптически активных форм осуществляется любым подходящим способом, в том числе, в качестве неограничивающих примеров, разделение рацемической формы путем перекристаллизации, синтез из оптически активных исходных веществ, хиральный синтез или хроматографическое разделение с использованием хиральной неподвижной фазы. В некоторых вариантах осуществления, в качестве терапевтического соединения, описанного в настоящем изобретении, применяются смеси одного или нескольких изомеров. В некоторых вариантах осуществления описанные в изобретении соединения содержат один или несколько хиральных центров. Эти соединения получают любыми подходящими способами, включая энантиоселективный синтез и/или разделение смеси энантиомеров и/или диастереомеров. Разделение соединений и их изомеров достигается любыми подходящими способами, в том числе, в качестве неограничивающих примеров, химическими методиками, методиками, основанными на ферментах, фракционной кристаллизацией, перегонкой, хроматографией и т.п.
Соединения могут существовать в форме свободной кислоты или свободного основания или фармацевтически приемлемой солевой форме. В некоторых вариантах осуществления описанные в заявке соединения находятся в несольватированной или сольватированной форме, причем сольватированные формы включают любой фрамацевтически приемлемый растворитель, например, воду, этанол и т.п.
Далее, настоящее изобретение относится к композиции, включающей по меньшей мере один ингибитор IBAT формулы (I) или формулы (II), для применения в профилактике и/или лечении заболеваний печени.
Одним из аспектов настоящего изобретения является применение соединения формулы (I) или формулы (II) для получения лекарственного препарата, предназначенного для лечения заболеваний печени.
Заболевания печени
Под заболеваниями печени в настоящей заявке понимают любые заболевания печени и связанных с ней органов, таких как воротная вена поджелудочной железы, паренхима печени, внутрипеченочные желчные протоки, внепеченочные желчные протоки и желчный пузырь, зависимые от желчных кислот (BA).
Переносчик желчных кислот из подвздошной кишки (IBAT) является основным механизмом реабсорбции желчных кислот из желудочно-кишечного тракта. Частичное или полное блокирование этого механизма приводит к понижению концентрации желчных кислот в стенке тонкого кишечника, воротной вене, паренхиме печени, внутрипеченочных желчных протоках, внепеченочных желчных протоках и в желчном пузыре. Заболевания, при которых можно получить пользу от частичного или полного блокирования механизма IBAT, могут представлять собой такие заболевания, при которых имеется в наличии первичное патофизиологическое нарушение, вызывающее или связанное с симптомом слишком высокой концентрации желчных кислот в сыворотке и перечисленных выше органах.
Один из аспектов настоящего изобретения относится к соединениям формулы (I) или формулы (II), которые определены выше, для применения в профилактике или лечении паренхимы печени; врожденного метаболического расстройства печени; синдрома Билера; первичного нарушения синтеза желчных кислот (BA), например, церебросухожильного ксантоматоза; вторичного нарушения, например, синдрома Зельвегера, неонатального гепатита, кистозного фиброза, печеночных симптомов, ALGS (синдрома Алажилля), PFIC (прогрессирующего семейного внутрипеченочого холестаза), аутоиммунного гепатита, первичного биллиарного цирроза (PBC), фиброза печени, неалкогольной жировой дистрофии печени, NAFLD/NASH, портальной гипертензии, общего холестаза, например, разлития желчи в результате действия лекарственных веществ или во время беременности, внутри- и вне печеночного холестаза, например, врожденных форм холестаза, таких как PFIC1, первичного склерозирующего холангита, желчных камней и холедохолитиаза, злокачественных заболеваний, которые вызывают сужение желчных протоков, симптомов (чесания, зуда), возникающих из-за холестаза/разлития желчи, панкреатита, хронических аутоиммунных заболеваний печени, ведущих к прогрессирующему холестазу, или зуда, вызванного холестатической болезнью печени.
Один из аспектов настоящего изобретения относится к соединениям формулы (I) или формулы (II), которые определены выше, для применения в профилактике или лечении расстройства печени или состояния, связанного с печенью, жировой дистрофии печени, стеатоза печени, неалкогольного стеатогепатита (NASH), алкогольного гепатита, острой жировой дистрофии печени, жировой дистрофии печени вследствие беременности, гепатита, вызванного лекарственными средствами, расстройств, связанных с избытком железа, фиброза печени, цирроза печени, гепатомы, вирусного гепатита и проблем, связанных с опухолями и новообразованиями печени, желчных путей и поджелудочной железы.
Комбинации с другими действующими веществами
Один из аспектов настоящего изобретения относится к комбинациям ингибитора IBAT формулы (I) или формулы (II), которые определены выше, по меньшей мере с одним другим терапевтически активным веществом. Это по меньшей мере одно другое терапевтически активное вещество может являться соединением, ингибирующим IBAT.
Инкретины и гормоны, продуцируемые L-клетками
Упомянутое по меньшей мере одно другое терапевтически активное вещество может представлять собой инкретин или гормон, продуцируемый L-клетками.
В одном из аспектов настоящего изобретения, по меньшей мере одно другое терапевтически активное вещество представляет собой L-клеточный эндокринный пептидный усилитель, например, усилитель, связанный с GLP-1. Примерами GLP-1 усилителя, применимого в соответствии с настоящим изобретением, являются GLP-1, усилитель секреции GLP-1, ингибитор разрушения GLP-1 или их комбинация.
В одном из аспектов настоящего изобретения L-клеточный эндокринный пептидный усилитель представляет собой усилитель, связанный с GLP-2, например, GLP-2, усилитель секреции GLP-2, ингибитор разрушения GLP-2 или их комбинацию.
В одном из аспектов настоящего изобретения L-клеточный эндокринный пептидный усилитель представляет собой усилитель PYY, например, усилитель оксинтомодулина.
Миметики инкретина
В одном из аспектов настоящего изобретения упомянутое по меньшей мере одно другое терапевтически активное вещество представляет собой миметик инкретина, например, эксенатид (Byetta®).
Один из аспектов настоящего изобретения относится к пероральной комбинации ингибитора IBAT формулы (I) или формулы (II), раскрытого в настоящем изобретении, и ингибитора DPP-IV.
Энтероэндокринные пептиды
В одном из аспектов настоящего изобретения упомянутое по меньшей мере одно другое терапевтически активное вещество представляет собой энтероэндокринный пептид, например, GLP-1 или аналог GLP-1, например, Taspoglutide® (Ipsen) или подобный.
Комбинированная терапия с применением ингибитора IBAT и ингибитора DPP-IV
В одном из аспектов настоящего изобретения упомянутое по меньшей мере одно другое терапевтически активное вещество представляет собой ингибитор DPP-IV.
Один из аспектов настоящего изобретения относится к комбинации ингибитора IBAT и метформина и/или ситаглипина (Janumet®); и/или ингибиторы DPP-IV, подходящие для применения в способах по настоящей заявке, включают, не ограничиваясь этим, (2S)-1-{2-[(3-гидрокси-1-адамантил)амино]ацетил}пирролидин-2-карбонитрил (вилдаглиптин), (3R)-3-амино-1-[9-(трифторметил)-1,4,7,8-тетразабицикло[4.3.0]нона-6,8-диен-4-ил]-4-(2,4,5-трифторфенил)бутан-1-он (ситаглиптин), (1S,3S,5S)-2-[(2S)-2-амино-2-(3-гидрокси-1-адамантил)ацетил]-2-азабицикло[3.1.0]гексан-3-карбонитрил (саксаглиптин) и 2-({6-[(3R)-3-аминопиперидин-1-ил]-3-метил-2,4-диоксо-3,4-дигидропиримидин-1-(2H)-ил}метил)бензонитрил (алоглиптин).
Модуляторы рецептора TGR5
В одном из аспектов настоящего изобретения упомянутое по меньшей мере одно другое терапевтически активное вещество представляет собой агонист TGR5. Модуляторы TGR5 (например, агонисты) включают, не ограничиваясь только ими, соединения, описанные в WO 2008/091540, WO 2008/067219 и заявке на патент США № 2008/0221161.
Тиазолидиндионы
В одном из вариантов осуществления настоящего изобретения упомянутое по меньшей мере одно другое терапевтически активное вещество представляет собой тиазолидиндион, например, розиглитазон (Avanda), пиоглитазон (Actos), троглитазон (Rezulin), MCC-555, ривоглитазон, циглитазон или подобные.
Комбинированная терапия с применением ингибитора IBAT, шунта желчных протоков и ингибитора DPP-IV
В одном из вариантов осуществления настоящего изобретения ингибитор IBAT формулы (I) или формулы (II), описанных в настоящей заявке, вводят в комбинации с ингибитором DPP-IV и/или шунтом желчных протоков. Примеры шунтов желчных протоков включают, не ограничиваясь этим, шунты, описанные в заявке WO 2007/0050628, содержание которой включено в настоящую заявку как ссылка.
В настоящей заявке термин «аддитивный эффект» описывает комбинированное действие двух (или нескольких) фармацевтически активных агентов, которое эквивалентно сумме действий каждого из агентов при его индивидуальном применении. Термин «синергетический эффект» относится к ситуации, в которой комбинированное действие двух (или нескольких) фармацевтически активных агентов превышает сумму действий каждого из агентов при индивидуальном применении. Считается, что любая подходящая комбинация ASBTI с одним или несколькими из упомянутых выше других активных ингредиентов и, необязательно, с одним или несколькими прочими фармакологически активными веществами, входит в объем способов, описанных в настоящем изобретении.
В некоторых вариантах осуществления конкретный выбор соединений зависит от диагноза, поставленного лечащим врачом, и его мнения о состоянии индивидуума и подходящей схеме лечения. Соединения необязательно вводят одновременно (например, одновременно, практически одновременно или в рамках одной и той же схемы лечения) или последовательно, в зависимости от природы заболевания, расстройства или состояния, состояния здоровья индивидуума и реального выбора применяемых соединений. В некоторых случаях определение порядка введения и числа повторных введений каждого терапевтического агента на протяжении схемы лечения, основывается на оценке подвергаемого лечению заболевания и состояния индивидуума.
В некоторых вариантах осуществления терапевтически эффективные дозировки меняются при использовании лекарственных препаратов в виде комбинаций. Способы экспериментального определения терапевтически эффективных дозировок лекарственных препаратов и других агентов для применения в схемах комбинированного лечения описаны в литературе.
В некоторых вариантах осуществления комбинированных схем лечения, описанных в настоящей заявке, дозировки совместно вводимых соединений меняются в зависимости от типа совместно вводимого лекарства, от конкретного применяемого препарата, от заболевания или состояния, подвергаемого лечению, и т.п. Кроме того, при совместном введении с одним или несколькими биологически активными агентами, соединения по настоящему изобретению необязательно вводят либо одновременно, либо последовательно с биологически активными агентами. В некоторых случаях, при последовательном введении, лечащий врач должен принять решение о подходящей последовательности введения терапевтического соединения по настоящему изобретению в комбинации с выбранным дополнительным терапевтическим агентом.
Несколько терапевтических агентов (по меньшей мере один из которых является терапевтическим соединением, описанным в настоящей заявке) необязательно вводят в любом порядке или даже одновременно. При одновременном введении несколько терапевтических агентов необязательно включают в состав одной объединенной лекарственной формы или в состав нескольких лекарственных форм (только в качестве примера: либо в состав одной пилюли, либо в состав двух отдельных пилюль). В некоторых случаях один из терапевтических агентов необязательно применяют в виде нескольких доз. В других случаях оба агента применяют в виде нескольких доз. Если введение осуществляется не одновременно, период времени между введением доз является любым подходящим периодом времени, например, от более нуля недель, до менее четырех недель. Кроме того, комбинированные способы лечения, композиции и составы не следует ограничивать применением только двух агентов; в изобретении предусматривается применение терапевтических комбинаций нескольких агентов (включая два или несколько соединений, описанных в настоящей заявке).
В некоторых вариантах осуществления схема введения, предназначенная для лечения, профилактики или облегчения состояния (состояний), для которых требуется улучшение, подвергается модификации с учетом ряда факторов. Эти факторы включают расстройство, от которого страдает субъект, а также возраст, массу тела, пол, рацион питания и медицинское состояние субъекта. Таким образом, в различных вариантах осуществления реально применяемая схема введения подвергается изменениям и отклоняется от схем введения, изложенных в настоящей заявке.
В некоторых вариантах осуществления фармацевтические агенты, которые входят в комбинированную терапию, описанную в настоящей заявке, включены в комбинированную дозированную форму или в отдельные дозированные формы, предназначенные для практически одновременного введения. В некоторых вариантах осуществления фармацевтические агенты, которые входят в комбинированную терапию, вводят последовательно с любым терапевтическим соединением, вводимым по схеме, требующей двухстадийного введения. В некоторых вариантах осуществления двухстадийная схема введения предусматривает последовательное введение действующих агентов или разнесенное по времени введение отдельных действующих агентов. В некоторых вариантах осуществления период времени между несколькими этапами введения меняется, в качестве неограничивающего примера, от нескольких минут до нескольких часов, в зависимости от свойств каждого из фармацевтических агентов, например, эффективности, растворимости, биодоступности, времени полужизни в плазме и кинетического профиля фармацевтического агента.
Кроме того, изобретение относится к ингибиторам IBAT, описанным в настоящей заявке, в комбинации по меньшей мере с одним препаратом, связывающим желчные кислоты, например, смолой, такой как холестирамин, холестипол и колесевелам.
Препараты, связывающие желчные кислоты (секвестранты желчных кислот, смолы)
В одном из вариантов осуществления изобретения ингибитор IBAT формулы (I) или формулы (II), которые определены выше, можно вводить в виде фармацевтического состава, включающего также по меньшей мере один секвестрант желчных кислот, где указанный состав предназначен для доставки секвестранта желчных кислот в толстый кишечник и ингибитора IBAT в тонкий кишечник.
Примерами подходящего секвестранта желчных кислот по настоящему изобретению являются холестирамин, который представляет собой гидрофильную полиакриловую анионообменную смолу, включающую фрагменты четвертичного аммония, которая, как известно, эффективно понижает уровень холестерина в крови. Холестирамин и различные композиции, включающие холестирамин, описаны, например, в патентах Великобритании №№ 929391 и 1286949; и патентах США №№ 3383281; 3308020; 3769399; 3846541; 3974272; 4172120; 4252790; 4340585; 4814354; 4874744; 4895723; 5695749; и 6066336. Холестирамин можно приобрести у Novopharm, USA Inc (Questrans Light), Upsher-Smith (PREVALITE (D)) и Apothecon. В настоящей заявке термин «холестирамин» включает любые подобные композиции, содержащие холестирамин или его фармацевтически приемлемые соли. Кроме того, они именуются QuestransTM. Questran Light Questrans Light (холестирамин) представляет собой неабсорбируемую анионную связывающую смолу, одобренную FDA для лечения гиперхолестеринемии.
Аминосодержащий полимер, включающий первый заместитель, связанный с первой аминогруппой полимера, который содержит гидрофобный алифатический фрагмент, а также второй заместитель, связанный со второй аминогруппой полимера, который содержит фрагмент алифатического четвертичного аммония, который описан в патентах США 5693675 и 5607669.
Соль алкилированного и поперечно-сшитого полимера, включающего продукт реакции (a) одного или нескольких поперечно-сшитых полимеров или их солей и сополимеров, содержащих повторяющееся звено, выбранное из группы, состоящей из: (NR-CH2-CH2)n (2) и (NR-CH2CH2-NR-CH2CH2-NR-CH2CHOH-CH2)n (3), где n означает положительное целое число и каждый из заместителей R независимо представляет собой H или C1-C8-алкильную группу; (b) по меньшей мере одного алифатического алкилирующего агента, где указанный продукт реакции отличается тем, что: (i) по меньшей мере некоторые из атомов азота указанных повторяющихся звеньев не вступили в реакцию с указанным алкилирующим агентом; (ii) менее 10 мольн. процентов атомов азота в указанных повторяющихся звеньях вступили в реакцию с указанным алкилирующим агентом с образованием четвертичных аммониевых звеньев; и (iii) имеется постоянный положительный заряд и один или несколько противоионов, например, колесевелам и колесевелама гидрохлорид.
Применимыми секвестрантами желчных кислот по настоящему изобретению являются смолы, например, холестирамин и холестипол. Одно из преимуществ комбинации соединения по настоящему изобретению с секвестрантами желчных кислот заключается в том, что дозировка секвестранта желчных кислот может быть меньше терапевтической дозы, применяемой для лечения холестеринемии при индивидуальной схеме введения, включающей только секвестрант желчных кислот. Благодаря уменьшению дозировки секвестраната желчных кислот можно было бы также избежать любых возможных побочных эффектов, вызванных плохой переносимостью терапевтических доз пациентом.
Другим подходящим секвестрантом желчных кислот является не растворимый в воде нетоксичный полимерный амин с молекулярной массой более 3000, обладающий способностью связывать по меньшей мере 30% имеющейся гликохолевой кислоты в течение 5 минут при взаимодействии с водным раствором указанной кислоты равной массы, имеющий полимерный скелет, устойчивый к пищеварительным ферментам и имеющий содержание воды более 65% после установления равновесия с воздухом при 100% относительной влажности, например, холестипол, описанный в USP 3383281.
В другом аспекте настоящего изобретения подходящий секвестрант желчных кислот является одним из препаратов, выбранных из холестирамина, холестипола или колесевелама.
Предпочтительный аспект настоящего изобретения заключается в применении в качестве секвестранта желчных кислот колесевелама.
Композиции по настоящему изобретению могут дополнительно включать статины, например, ингибитор HMG Co-A редуктазы или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство, в сочетании с фармацевтически приемлемым разбавителем или носителем.
Один из вариантов настоящего изобретения относится к комбинированному фармацевтическому составу для перорального приема, включающему ингибитор IBAT, т.е. соединение формулы (I) или формулы (II), которые определены выше, или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство, а также секвестрант желчных кислот или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство, где указанный состав предназначен для доставки секвестранта желчных кислот в толстый кишечник и ингибитора IBAT в тонкий кишечник.
Одним из вариантов осуществления настоящего изобретения является фармацевтический состав, включающий ядро, содержащее секвестрант желчных кислот для высвобождения в кишечнике, окруженное внешним слоем, содержащим ингибитор IBAT формулы (I) или формулы (II), который определен выше, предназначенный для немедленного высвобождения или замедленного высвобождения в дистальной области тощей кишки или проксимальной области подвздошной кишки.
Статины
В другом аспекте настоящего изобретения ингибитор IBAT, например, соединение формулы (I) или формулы (II), которое определено выше по тексту, или его фармацевтически приемлемая соль, сольват, сольват этой соли или пролекарство можно вводить в комбинации с ингибитором HMG Co-A редуктазы или его фармацевтически приемлемой солью, сольватом, сольватом этой соли или пролекарством. Подходящие ингибиторы HMG Co-A редуктазы, их фармацевтически приемлемые соли, сольваты, сольваты этих солей или пролекарства представляют собой статины, широко известные в технике. Конкретными статинами являются флувастатин, ловастатин, правастатин, симвастатин, аторвастатин, церивастатин, бервастатин, далвастатин, мевастатин и (E)-7-[4-(4-фторфенил-6-изопропил-2-[метил(метилсульфонил)амино]пиримидин-5-ил](3R,5S)-3,5-дигидроксигепт-6-еноевая кислота (розувастатин) или их фармацевтически приемлемые соли, сольваты, сольваты этих солей или пролекарства. Конкретным примером статина является аторвастатин или его фармацевтически приемлемая соль, сольват, сольват этой соли или пролекарство. Более конкретным примером статина является кальциевая соль аторвастатина. Другим конкретным примером статина является (E)-7-[4-(4-фторфенил-6-изопропил-2-[метил(метилсульфонил)амино]пиримидин-5-ил](3R,5S)-3,5-дигидроксигепт-6-еноевая кислота (розувастатин) или его фармацевтически приемлемая соль, сольват, сольват этой соли или пролекарство. Другим конкретным примером статина является кальциевая соль розувастатина и питавастатин (HMG Co-A редуктаза).
В дополнительном аспекте настоящего изобретения соединение формулы (I) или формулы (II), которое определено выше, или его фармацевтически приемлемая соль, сольват, сольват этой соли или пролекарство можно вводить в сочетании с ингибитором HMG Co-A редуктазы или его фармацевтически приемлемой солью, сольватом, сольватом этой соли или пролекарством, и/или секвестрантом желчных кислот, избегая, тем самым, возможного риска избыточного содержания желчных кислот в толстом кишечнике, вызванного ингибированием системы переноса желчных кислот из подвздошной кишки. Избыток желчных кислот в содержимом внутренних органов может вызывать диарею. Таким образом, настоящее изобретение относится также к лечению возможных побочных эффектов, таких как диарея, у пациентов при проведении терапии, включающей соединение формулы (I) или формулы (II), которые определены выше, или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство.
Ингибитор HMG Co-A редуктазы или его фармацевтически приемлемая соль, сольват, сольват этой соли или пролекарство, за счет своего действия будет уменьшать содержание эндогенного холестерина, который может являться исходным соединением для синтеза желчных кислот, и обеспечивать аддитивный эффект в комбинации с соединением формулы (I) или формулы (II), которое определено выше, или его фармацевтически приемлемой солью, сольватом, сольватом этой соли или пролекарством, по снижению содержания липидов.
В композицию по настоящему изобретению дополнительно могут входить:
агонисты PPAR альфа и/или гамма, или их фармацевтически приемлемые соли;
ингибиторы CETP (белка-переносчика эфиров холестерина), например, упомянутые и описанные в WO 00/38725 стр.7 строка 22 - страница 10 строка 17, где указанный фрагмент включен в настоящую заявку посредством ссылки;
антагонисты абсорбции холестерина, например, азетидиноны, такие как SCH 58235, а также соединения, описанные в патенте США 5767115, который включен в настоящую заявку с помощью ссылки;
ингибиторы MTP (микросомального белка переноса), например, описанные в работе Science, 282, 751-54, 1998, которая включена в настоящую заявку с помощью ссылки;
производные фиброевой кислоты; например, клофибрат, гемфиброзил, фенофибрат, ципрофибрат и безафибрат;
производные никотиновой кислоты, например, никотиновая кислота (ниацин), аципимокс и ницеритол;
фитостерины, например, станолы;
пробукол;
соединения, противодействующие ожирению, например, орлистат (EP 129748) и сибутрамин (GB 2184122 и US 4929629);
противогипертонические соединения, например, ингибитор ангиотензин-превращающего фермента (ACE), антагонист рецептора ангиотензина II, адреноблокатор, блокатор альфа-адренергических рецепторов, блокатор бета-адренергических рецепторов, смешанный блокатор альфа/бета адренергических рецепторов, стимулятор адренергических рецепторов, блокатор кальциевого канала, диуретик или сосудорасширяющее средство;
инсулин;
сульфонилмочевины, включая глибенкламид и/или толбутамид;
бигуаниды
В некоторых вариантах осуществления дополнительный терапевтический агент представляет собой бигуанид. В некоторых случаях бигуаниды понижают уровни глюкозы в крови и/или плазме. Примеры бигуанидов включают, не ограничиваясь этим, метформин, буформин, фенформин, прогуанил или подобные препараты;
акарбоза;
или фармацевтически приемлемые соли, сольваты, сольваты этих солей или пролекарства перечисленных препаратов, необязательно в сочетании с разбавителями или носителями, фармацевтически приемлемыми для теплокровных животных, например, человека.
Антагонисты ангиотензина II
Предпочтительные антагонисты ангиотензина II, их фармацевтически приемлемые соли, сольваты, сольваты этих солей или пролекарства для применения в комбинации с соединением формулы (I) включают, не ограничиваясь этим, такие соединения, как: кандесартан, кандесартан цилексетил, лозартан, валсартан, ирбесартан, тасосартан, телмисартан и эпросартан. Особенно предпочтительными антагонистами ангиотензина II или их фармацевтически приемлемыми производными для применения в настоящем изобретении являются кандесартан и кандесартан цилексетил.
Агонисты PPAR альфа и/или гамма, и/или дельта или их фармацевтически приемлемые соли
В другом аспекте настоящего изобретения ингибитор IBAT или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство можно вводить вместе с агонистом PPAR альфа и/или гамма, или его фармацевтически приемлемыми солями, сольватами, сольватами этих солей или пролекарствами. Подходящие агонисты PPAR альфа и/или гамма, их фармацевтически приемлемые соли, сольваты, сольваты этих солей или пролекарства хорошо известны в технике. Эти препараты включают соединения, описанные в WO 01/12187, WO 01/12612, WO 99/62870, WO 99/62872, WO 99/62871, WO 98/57941, WO 01/40170, J. Med. Chem., 1996, 39, 665, Expert Opinion on Therapeutic Patients, 10(5), 623-634 (в частности, соединения, описанные в патентных заявках, перечисленных на стр.634) и J. Med. Chem., 2000, 43, 527, где все указанные источники включены в настоящую заявку посредством ссылки. Конкретно, термин «агонисты PPAR альфа и/или гамма» относится к WY-14643, клофибрату, фенофибрату, безафибрату, GW 9578, троглитазону, пиоглитазону, росиглитазону, эглитазону, проглитазону, BRL-49634, KRP-297, JTT-501, SB 213068, GW 1929, GW 7845, GW 0207, L-796449, L-165041 и GW 2433.
В частности, термин «агонист PPAR альфа и/или гамма» относится к (S)-2-этокси-3-[4-(2-{4-метансульфонилоксифенил}этокси)фенил]пропановой кислоте и ее фармацевтически приемлемым солям.
Согласно одному из вариантов осуществления, соединения по настоящему изобретению применяются совместно с одним или несколькими антидиабетическими гипогликемически активными ингредиентами, ингибиторами абсорбции холестерина, агонистами PPAR дельта, фибратами, ингибиторами MTP, ингибиторами абсорбции желчных кислот, полимерными адсорбентами желчных кислот, индукторами рецептора LDL, ингибиторами ACAT, антиоксидантами, ингибиторами липопротеин липазы, ингибиторами АТФ-цитрат лиазы, ингибиторами сквален синтетазы, антагонистами липопротеина(ов), агонистами рецептора HM74A, ингибиторами липазы, инсулинами, сульфонилмочевинами, бигуанидами, меглитинидами, тиазолидиндионами, ингибиторами альфа-глюкозидазы, активными ингредиентами, которые воздействуют на АТФ-зависимый калиевый канал бета клеток, ингибиторами гликоген фосфорилазы, антагонистами рецептора глюкагона, активаторами глюкокиназы, ингибиторами глюконеогенеза, ингибиторами фруктоза-1,6-бифосфатазы, модуляторами переносчика глюкозы 4, ингибиторами глутамин-фруктоза-6-фосфат амидотрансферазы, ингибиторами дипептидилпептидазы IV, ингибиторами 11-бета-гидроксистероид дегидрогеназы 1, ингибиторами протеин тирозин фосфатазы 1B, модуляторами натрий-зависимого переносчика глюкозы 1 или 2, модуляторами GPR40, ингибиторами гормон-чувствительной липазы, ингибиторами ацетил-CoA карбоксилазы, ингибиторами фосфоенолпируват карбоксикиназы, ингибиторами гликоген синтазы киназы-3 бета, ингибиторами протеин киназы C бета, антагонистами рецептора эндотелина-A, ингибиторами I каппа B киназы, модуляторами глюкокортикоидного рецептора, агонистами CART, агонистами NPY, агонистами MC4, агонистами орексина, агонистами H3, агонистами TNF, агонистами CRF, антагонистами CRF BP, агонистами урокортина, агонистами бета 3, антагонистами рецептора CB1, агонистами MSH (меланоцит-стимулирующего гормона), агонистами CCK, ингибиторами обратного захвата серотонина, смесями серотонинергических и норадренергических соединений, агонистами 5HT, агонистами бомбезина, антагонистами галанина, гормонами роста, соединениями, способствующими выделению гормона роста, агонистами TRH, модуляторами разобщающего белка 2 или 3, агонистами лептина, агонистами DA (бромокриптином, допрексином), ингибиторами липазы/амилазы, модуляторами PPAR, модуляторами RXR, агонистами TR-бета или амфетаминами.
Один из аспектов настоящего изобретения относится к способу лечения заболевания печени, в котором описанный выше ингибитор IBAT формулы (I) или формулы (II) приводят в контакт с дистальной частью подвздошной кишки индивидуума, у которого имеется необходимость в таком лечении.
В одном из вариантов осуществления описанный выше ингибитор IBAT формулы (I) или формулы (II) вводят в комбинации со вторым терапевтическим агентом, выбранным из ингибитора DPP-IV, тиазолидиндиона или его аналога, или агониста TGR5.
В некоторых вариантах осуществления ингибиторы IBAT, описанные в настоящей заявке, объединяют или применяют в комбинации с одним или несколькими из следующих терапевтических агентов в любых сочетаниях: инсулином, миметиками инсулина, ингибиторами DPP-IV или модуляторами TGR5.
Другие действующие вещества, которые предполагается комбинировать с одним или несколькими ингибиторами IBAT по настоящему изобретению, можно выбрать из одного или нескольких из следующих веществ: урсодезоксихолевой кислоты; норурсодезоксихолевой кислоты; рифампицина и родственных производных рифампицина, которые описаны в US 3342810; антагонистов опиатов, таких как налоксон и налтрексон; антагонистов серотонина, например, антагонистов рецептора 5-HT3 и антагонистов 5-HT2, таких как тразодон, нефазодон, амоксапин, клозапин; антигистаминовых препаратов, таких как бромфенирамин, хлорфенирамина дименгидринат, дифенгидрамин, доксиламин, лоратидин, цетиризин; ингибиторов обратного захвата серотонина, таких как циталопрам, дапоксетин, эсциталопрам, флуоксетин, флувоксамин, линдалпин, пароксетин, сертралин, зимелидин; кортикостероидов, например, глюкокортикоидов и минералокортикоидов, например, выбранных из гидрокортизона (кортизола), кортизона и его ацетата, преднизона, преднизолона, метилпреднизолона, дексаметазона, бетаметазона, триамцинолона, беклометазона, флудрокортизона и его ацетата, дезоксикортикостерона и его ацетата (DOCA), альдостерона.
Примерами агонистов PPAR дельта являются GW-501516 (501516, GSK-516, GW-516, GW-1516; агонист рецептора, активируемого пероксисомными пролифераторами (PPAR)-дельта) и несколько других соединений, являющихся производными GW-501516, включая GI-262570, GW-0072, GW-7845 и GW-7647.
Согласно одному из вариантов осуществления, ингибитор IBAT может применяться в комбинации с одним или несколькими из таких препаратов, как атрелеутон, эпротиром, лосмапимод, эзетимиб (SCH58235), безафибрат, фенофибрат, вареспладиб, дарапладиб, ломитапид, имплитапид, росиглитазон, далцетрапиб, анацетрапиб, лоркасерин, дапаглифлозин, канаглифлозин, серглифлозин, ASP-1941, орлистат, пиоглитазон, соделглитазар, нетоглитазон, индеглитазар, навеглитазар, лобеглитазон, алеглитазар, бромокриптин, тезофеназин, моноамин, алоглиптин, вилдаглиптин, саксаглиптин, ситаглиптин, денаглиптин, гемиглиптин, линаглиптин, дутоглиптин, тенелиглиптин, LC-150444, ларопипрант, ниацин с продолжительным высвобождением, симвастатин эзетимиб, розувастатин фенофибрат, розувастатин эзетимиб и аторвастатин эзетимиб.
Могут применяться комбинации с тредаптивом, виторином и цертриадом.
Согласно одному из вариантов осуществления, ингибитор IBAT может быть скомбинирован с одним или несколькими из любых из упомянутых выше других соединений.
Согласно одному из вариантов осуществления, ингибиторы IBAT по настоящему изобретению комбинируют по меньшей мере с одним другим активным веществом, выбранным из ингибиторов дипептидил пептидазы-IV, агонистов PPAR γ, статинов и секвестрантов желчных кислот в любой комбинации.
Согласно одному из вариантов осуществления, ингибиторы IBAT по настоящему изобретению комбинируют с по меньшей мере одним ингибитором DPP-IV, по меньшей мере одним агонистом PPAR γ, например, ситаглиптином или пиоглитазоном.
Согласно другому варианту осуществления, ингибиторы IBAT по настоящему изобретению комбинируют с по меньшей мере одним ингибитором DPP-IV и по меньшей мере одним статином, например, ситаглиптином и симвастатином.
Другим действующим веществом, которое может быть скомбинировано с ингибиторами IBAT по настоящему изобретению, является урсодезоксихолевая кислота.
Согласно одному из вариантов осуществления, настоящее изобретение относится к композиции, включающей один или несколько ингибиторов IBAT по настоящему изобретению и холестирамин и/или колесевелам, и/или холестипол.
Согласно одному из вариантов осуществления, настоящее изобретение относится к композиции, включающей одно или несколько из соединений примеров 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 и 14, а также холестирамин и/или колесевелам, и/или холестипол.
Согласно другому варианту осуществления, настоящее изобретение относится к композиции, включающей 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1'-фенил-1'-[N'-(карбоксиметил)карбамоил]метил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин (пример 5) и холестирамин и/или колесевелам, и/или холестипол.
Согласно другому варианту осуществления, настоящее изобретение относится к композиции, включающей 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N((S)-1-карбокси-2-метилпропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадизепин (пример 13) и холестирамин, и/или колесевелам, и/или холестипол.
Согласно еще одному варианту осуществления, настоящее изобретение относится к композиции, включающей 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1'-фенил-1'-[N'-(карбоксиметил)карбамоил]метил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин (пример 14) и холестирамин, и/или колесевелам, и/или холестипол.
Носители и эксципиенты
Композиции по настоящему изобретению могут дополнительно включать фармацевтически приемлемый разбавитель или носитель.
Фармацевтические композиции можно получать способами, известными в технике, применяя один или несколько физиологически приемлемых носителей, в том числе, например, эксципиентов, и зависящими от выбранного пути введения.
В некоторых вариантах осуществления носитель включает фармацевтически приемлемый эксципиент, выбранный на основе совместимости с соединениями, описанными в настоящей заявке, например, любыми соединениями формул (I) и (II), и профилем высвобождения желаемой дозированной формы.
Типовые примеры носителей включают, например, связующие вещества, суспендирующие агенты, дезинтегрирующие агенты, наполнители, ПАВ, солюбилизаторы, стабилизаторы, смазывающие средства, смачивающие агенты, разбавители.
Фармацевтические композиции и носители описаны, например, в Remington: The Science and Practice of Pharmacy, Nineteenth Ed (Easton, Pa.: Mack Publishing Company, 1995); Hoover, John E., Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa. 1975; Liberman, H. A. and Lachman, L, Eds., Pharmaceutical Dosage Forms, Marcel Decker, New York, N.Y., 1980; and Pharmaceutical Dosage Forms and Drug Delivery Systems, Seventh Ed. (Lippincott Williams & Wilkins 1999).
Композиция может быть получена из смеси соединения формул (I) и (II) и, возможно, также других действующих соединений, упомянутых в настоящей заявке, с другими химическими компонентами, такими как носители, стабилизаторы, разбавители, диспергирующие агенты, суспендирующие агенты, загустители и/или эксципиенты. В некоторых вариантах осуществления терапевтически эффективные количества соединений, описанных в настоящей заявке, вводят в составе фармацевтических композиций индивидууму, у которого имеется заболевание, расстройство или состояние, которое необходимо лечить. В конкретных вариантах осуществления этот индивидуум является человеком. Соединения, описанные в настоящей заявке, применяются либо индивидуально, либо в комбинации с одним или несколькими дополнительными терапевтическими агентами. В некоторых вариантах осуществления фармацевтические составы, описанные в настоящей заявке, вводят индивидууму любым способом, включая один или несколько из таких способов введения, как, в качестве неограничивающих примеров, пероральный, парентеральный (например, внутривенный, подкожный, внутримышечный), интраназальный, буккальный, местный, ректальный или трансдермальный пути введения.
Фармацевтические композиции, описанные в настоящей заявке, получают в виде дозированных форм. В этом случае, в некоторых вариантах осуществления, дозированная форма по настоящему изобретению, подходящая для введения индивидууму, включает соединение, описанное в настоящей заявке. В некоторых вариантах осуществления подходящие дозированные формы включают, в качестве неограничивающего примера, водные дисперсии для перорального введения, жидкие препараты, гели, сиропы, эликсиры, кашицы, суспензии, твердые пероральные дозированные формы, аэрозоли, составы с регулируемым высвобождением, легкоплавкие составы, шипучие составы, лиофилизированные составы, таблетки, порошки, пилюли, драже, капсулы, составы с замедленным высвобождением, составы с продолжительным высвобождением, составы с пульсирующим высвобождением, составы, содержащие множество отдельных частиц и смеси составов с немедленным высвобождением и регулируемым высвобождением.
Твердые фармацевтические дозированные формы по настоящей заявке необязательно включают дополнительное терапевтическое соединение, указанное в заявке, и одну или несколько фармацевтически приемлемых добавок, таких как совместимый носитель, связующий компонент, наполнитель, суспендирующий агент, вкусоароматическое средство, подсластитель, дезинтегрирующий агент, диспергирующий агент, ПАВ, смазывающее средство, краситель, разбавитель, солюбилизатор, смачивающий агент, пластификатор, стабилизатор, средство для улучшения проникновения, увлажняющий агент, пеногаситель, антиоксидант, консервант, или одну или несколько комбинаций перечисленных добавок. В некоторых аспектах, применяя стандартные методики нанесения покрытий, например, описанные в Remington's Pharmaceutical Sciences, 20th edition (2000), получают пленочное покрытие, окружающее состав соединения формулы I-II. В одном из вариантов осуществления соединение, описанное в настоящей заявке, находится в форме частиц, и некоторые из этих частиц или все частицы соединения имеют покрытие. В некоторых вариантах осуществления некоторые или все частицы соединения по настоящему изобретению являются микроинкапсулированными. В некоторых вариантах осуществления, частицы соединения по настоящему изобретению не являются микроинкапсулированными и не имеют покрытия.
Способ лечения
Настоящее изобретение относится также к способу лечения и/или профилактики заболеваний печени у теплокровных животных, например, человека, у которого есть необходимость в таком лечении и/или профилактике, включающему введение индивидууму эффективного количества соединения или композиции по настоящему изобретению.
Способ лечения любого заболевания или состояния, описанного в настоящей заявке, у индивидуума при необходимости такого лечения, может включать введение указанному индивидууму фармацевтических композиций, содержащих по меньшей мере один ингибитор IBAT, описанный в настоящей заявке, или его фармацевтически приемлемую соль, фармацевтически приемлемый N-оксид, фармацевтически активный метаболит, фармацевтически приемлемое пролекарство или фармацевтически приемлемый сольват в терапевтически эффективных количествах.
Дозированные формы
Твердые фармацевтические дозированные формы могут необязательно включать дополнительные терапевтические соединения, а также одну или несколько фармацевтически приемлемых добавок, таких как совместимый носитель, связующее вещество, наполнитель, суспендирующее средство, вкусоароматическую добавку, подсластитель, дезинтегрирующее средство, диспергирующее средство, ПАВ, смазывающее средство, краситель, разбавитель, солюбилизатор, смачивающее средство, пластификатор, стабилизатор, средство для улучшения проникновения, увлажняющее средство, пеногаситель, антиоксидант, консервант, или одну или несколько комбинаций перечисленных добавок. В некоторых аспектах, применяя стандартные методики нанесения покрытий, например, описанные в Remington's Pharmaceutical Sciences, 20th edition (2000), получают пленочное покрытие, окружающее состав соединения формулы I-II. В одном из вариантов осуществления соединение, описанное в настоящей заявке, находится в форме частиц, и некоторые из этих частиц или все частицы соединения имеют покрытие. В некоторых вариантах осуществления некоторые или все частицы соединения по настоящему изобретению являются микроинкапсулированными. В некоторых вариантах осуществления, частицы соединения по настоящему изобретению не являются микроинкапсулированными и не имеют покрытия.
Ингибитор IBAT формул I и II может применяться в изготовлении лекарственных средств для профилактического и/или терапевтического лечения ожирения и/или диабета. Способ лечения любого из заболеваний или состояний, описанных в настоящей заявке, у индивидуума, которому необходимо такое лечение, включает введение индивидууму фармацевтической композиции, содержащей по меньшей мере один ингибитор IBAT, описанный в заявке, или его фармацевтически приемлемую соль, фармацевтически приемлемый N-оксид, фармацевтически активный метаболит, фармацевтически приемлемое пролекарство или фармацевтически приемлемый сольват, в терапевтически эффективных количествах.
В число дозированных форм входит матрица, которая обеспечивает регулируемое высвобождение действующего агента в дистальной части тощей кишки, проксимальной части подвздошной кишки, дистальной части подвздошной кишки и/или в толстой кишке. В некоторых вариантах осуществления дозированная форма включает полимер, который является pH-чувствительным (например, матрицу MMX.TM. фирмы Cosmo Pharmaceuticals) и обеспечивает регулируемое высвобождение действующего агента в подвздошной кишке и/или толстой кишке. Примеры таких pH-чувствительных полимеров, пригодных для регулируемого высвобождения, включают, не ограничиваясь этим, полиакриловые полимеры (например, анионные полимеры метакриловой кислоты и/или эфиров метакриловой кислоты, например полимеры Carbopol.RTM. (номер CAS 9063-87-0), которые включают кислотные группы (например, -COOH, SO3H) и разбухают при основных значениях pH в кишечнике (например, при pH около 7-8). В некоторых вариантах осуществления, дозированная форма, подходящая для регулируемого высвобождения в дистальной части подвздошной кишки, включает действующий агент в форме микрочастиц (например, тонкоизмельченный действующий агент). В некоторых вариантах осуществления, для доставки IBAT в дистальную часть подвздошной кишки подходит ядро из не разрушающегося ферментами поли(DL-лактид-гликолида) (PLGA). В некоторых вариантах осуществления дозированная форма, включающая IBAT, покрыта кишечным полимером (например, Eudragit.RTM. S-100, номер CAS 25086-15-1), ацетатом фталатом целлюлозы, поливинилацетатом фталатом, фталатом гидроксипропилметилцеллюлозы, анионными полимерами метакриловой кислоты, эфирами метакриловой кислоты или подобными веществами для доставки действующего вещества в конкретный участок подвздошной кишки и/или толстой кишки. В некоторых вариантах осуществления, для направленной доставки в подвздошную кишку подходят системы, активируемые бактериями. Примеры систем, активируемых микрофлорой, включают дозированные формы, содержащие пектин, галактоманнан и/или азо гидрогели и/или конъюгаты действующего агента с гликозидами (например, конъюгаты с D-галактозидом, бета-D-ксилопиранозидом и т.п.). Примеры ферментов желудочно-кишечной микрофлоры включают бактериальные гликозидазы, например, D-галактозидазу, бета-D-глюкозидазу, альфа-L-арабинофуранозидазу, бета-D-ксилопиранозидазу или подобные ферменты.
Частички лекарственного вещества с покрытием можно помещать в твердые желатиновые капсулы или смешивать с эксципиентами для получения таблеток, например, с наполнителями, связующими веществами, дезинтегрирующими средствами, смазывающими средствами и другими фармацевтически приемлемыми добавками, и подвергнуть прессованию с получением таблеток. Прессованные таблетки необязательно покрывают пленкообразующими агентами для получения гладкой поверхности таблеток и дополнительного улучшения механической стабильности таблетки при упаковке и транспортировке. Такое покрытие, которое может быть нанесено на таблетку, состоящую из нескольких частей, или на обычную таблетку, может дополнительно включать добавки, такие как средства против слипания, красители и пигменты, или другие добавки, предназначенные для улучшения внешнего вида таблеток.
Подходящими средствами для новых составов являются ингибиторы IBAT, например, описанные в обсуждавшихся выше документах, включенных в настоящую заявку посредством ссылок.
В качестве альтернативы ингибиторы IBAT могли бы представлять собой лекарственные препараты с низкой проникающей способностью, как определено в Biopharmaceutical Classification System (системе биофармацевтической классификации), предложенной FDA.
Комбинированная терапия по настоящему изобретению предпочтительно должна включать одновременное, раздельное или последовательное введение ингибитора IBAT и секвестранта желчных кислот. Ингибитор IBAT мог бы предпочтительно входить в состав для доставки в подвздошную кишку, и секвестрант желчных кислот мог бы предпочтительно входить в состав для высвобождения в толстой кишке.
Дозировка
Соединение формулы (I) или его фармацевтически приемлемая соль, сольват, сольват этой соли или пролекарство обычно следует вводить теплокровным животным в разовой дозе в диапазоне 5-5000 мг на квадратный метр поверхности тела животного, т.е. примерно 0,1-100 мг или 0,001-50 мг, что, как правило, обеспечивает терапевтически эффективную дозу. Дозированная лекарственная форма, например, таблетка или капсула, как правило, будет содержать, например, 1-250 мг действующего ингредиента. Предпочтительно применяется дневная доза в диапазоне 1-50 мг. В другом аспекте применяется дневная доза в диапазоне 0,02-20 мг. Однако дневную дозу необходимо варьировать в зависимости от пациента, конкретного пути введения и тяжести подвергаемого лечению заболевания. Соответственно, оптимальная дозировка может быть определена практикующим врачом, который осуществляет лечение того или иного конкретного пациента.
Величину дозы, требуемой для терапевтического или профилактического лечения, обязательно следует изменять в зависимости от пациента, конкретного пути введения и тяжести подвергаемого лечению заболевания. Предусматривается разовая доза в диапазоне, например, 1-100 мг, предпочтительно 1-50 мг. Дневную дозу можно вводить за один прием или делить на одну, две, три или более разовых доз.
Фармацевтический состав по настоящему изобретению с направленной доставкой в желудочно-кишечный тракт обеспечивает более слабое системное воздействие, что можно определить по площади под кривой зависимости концентрации лекарственного соединения или 7α-гидрокси-4-холестен-3-она (C4) в плазме от времени (AUC), при сохранении или даже увеличении терапевтического эффекта, что можно определить, например, по уменьшению уровня холестерина в сыворотке.
В комбинированной терапии, включающей ингибитор IBAT и секвестрант желчных кислот, предпочтительно применяются низкие дневные дозировки секвестранта желчных кислот, например, менее чем приблизительно 5 г смолы, и более предпочтительно менее 2 г. Дозированную форму с высвобождением секвестранта желчных кислот в толстом кишечнике можно создать с применением любого из описанных выше принципов получения составов с замедленным высвобождением.
В комбинированной терапии, включающей ингибитор IBAT и секвестрант желчных кислот, могут применяться низкие дневные дозировки секвестранта желчных кислот, например, менее чем 5 г смолы, и, более предпочтительно, менее 4, 3, 2 или менее 1 г. Подходящими диапазонами могут являться 0,1-5 г, 0,5-4 г, 1-3 г, 2-4 г, 2-3 г в день. Дозированную форму с высвобождением секвестранта желчных кислот в толстом кишечнике можно создать с применением любого из описанных выше принципов получения составов с замедленным высвобождением.
Таблетка может состоять из внутреннего ядра, содержащего 1-1000 мг, например, 200-800 мг, 10-400 мг, 10-200 мг или 20-80 мг секвестранта желчных кислот в составе с высвобождением в толстой кишке и внешнего тонкого слоя, включающего 1-100 мг, 5-50 мг, например, 1-20 мг ингибитора IBAT.
Дневную дозу ингибитора IBAT и/или секвестранта желчных кислот можно вводить в один прием или делить на две, три или несколько разовых доз.
Введение три раза в день 400 мг колесевелама в виде состава с высвобождением в толстом кишечнике должно обеспечить достаточное связывание желчных кислот в толстом кишечнике, если считать общий объем полости кишечника равным примерно 100 мл, что соответствует принятому при фармакокинетических расчетах объему тонкого кишечника от 250 до 300 мл. Общая рекомендованная дневная доза колесевелама для блокирования абсорбции желчных кислот во всем объеме кишечника человека составляет 3750 мг/день.
Наборы
Кроме того, настоящее изобретение относится к набору, включающему соединение или композицию по настоящему изобретению и, возможно, также инструкцию по применению.
Согласно другому аспекту, настоящее изобретение относится к набору, включающему ингибитор IBAT по настоящему изобретению, или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство, а также инструкцию по применению.
Согласно следующему аспекту, настоящее изобретение относится к набору, включающему ингибитор IBAT по настоящему изобретению, или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство, а также любое из упомянутых выше веществ для применения в комбинации, или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство.
Согласно еще одному аспекту, настоящее изобретение относится к набору, включающему: a) ингибитор IBAT по настоящему изобретению, или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство в составе первой дозированной лекарственной формы; b) любое из упомянутых выше веществ для применения в комбинации, или его фармацевтически приемлемую соль, сольват, сольват этой соли или пролекарство в составе второй дозированной лекарственной формы; c) контейнер, в котором находятся упомянутые первая и вторая дозированные формы.
Рассмотренные далее примеры предназначены для иллюстрации, и они никоим образом не ограничивают объем изобретения. Все упомянутые в заявке источники включены в заявку в полном объеме посредством ссылок.
Выражение «включающий» в настоящей заявке следует понимать, как включающий указанные позиции, но не ограниченный ими.
Пример 1
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-(карбоксиметил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 696,89. Это соединение получали, как описано в примере 2 WO 3022286.
Пример 2
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N'-((S)-1-карбоксиэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин, мол. масса 709,92.
Это соединение получали, как описано в примере 2 WO 03106482.
Пример 3
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 724,94.
Это соединение получали, как описано в примере 6 WO 3022286.
Пример 4
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((R)-1-карбокси-2-метилтиоэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 757,01.
Это соединение получали, как описано в примере 7 WO 3022286.
Пример 5
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 740,94.
Это соединение получали, как описано в примере 29 WO 3022286.
Пример 6
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((R)-1-карбокси-2-метилтиоэтил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 773,00.
Это соединение получали, как описано в примере 30 WO 3022286.
Пример 7
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-метилпропил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 738,97.
Это соединение получали, как описано в примере 15 WO 3022286.
Пример 8
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-(R)-гидроксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 756,94.
Это соединение получали, как описано в примере 26 WO 3022286.
Пример 9
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксибутил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 754,97.
Это соединение получали, как описано в примере 28 WO 3022286.
Пример 10
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксиэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 710,91.
Это соединение получали, как описано в примере 5 WO 3022286.
Пример 11
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N'-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин, мол. масса 739,95.
Это соединение получали, как описано в примере 1 WO 3022286.
Пример 12
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксиэтил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 726,91.
Это соединение получали, как описано в примере 11 WO 3022286.
Пример 13
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-метилпропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин, мол. масса 754,97.
Это соединение получали, как описано в примере 27 WO 3022286.
Пример 14
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1'-фенил-1'-[N'-(карбоксиметил)карбамоил]метил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин, мол. масса 695,90.
Это соединение получали, как описано в примере 43 WO 0250051.
Пример 15
Фармацевтический эффект: среднее ингибирующее действие (%)
Для соединений примеров 1-14 определяли средние значения IBAT-ингибирующего действия (%) при различных дозировках и средние значения IC50 (нМ), исследуя распределение 75Se гомотаурохолевой кислоты (75SeHCAT).
Система для тестирования
Животные
Вид: мышь; линия: ApoE нокаутированная; сублиния C57BL/6; пол: женский; общее количество животных: 70; диапазон массы тела 20-22 г; поставщик: Möllegaard's Breeding (Skensved, Denmark); способ идентификации: ID карты (штрих-код).
Акклиматизация: по меньшей мере одна неделя в отделе лаборатории животных ресурсов на фирме AstraZeneca; условия содержания: размещали по пять животных в клетке (Makrolon III, 7 дм2) в комнате с регулируемой температурой (22°C), относительной влажностью (от 40% до 60%) и циклом свет/темнота 12/12 часов; питание: неограниченный доступ к гранулам R3 (Lactamin, Vadstena, Sweden) во время проживания и в период проведения экспериментов; вода: неограниченный доступ к водопроводной воде во время проживания и в период проведения экспериментов.
Подстилка: подстилка из рассыпанных осиновых опилок (Tapvei, Finland).
Методика эксперимента
В 13:00 в день эксперимента животным осуществляли пероральное введение носителя (n=3) или соединения примера 14 (0,156 (n=3), 0,625 (n=3) или 2,5 мкмоль/кг (n=3)). Через 30 мин каждой мыши осуществляли пероральное введение следового количества 75SeHCAT (75Se гомотаурохолевой кислоты) (0,1 мКюри на 0,1 мл на мышь). Через 24 часа после введения 75SeHCAT, животных умерщвляли действием CO2. У животных удаляли желчный пузырь и весь кишечник, причем в течение 24 часов после введения 75SeHCAT, собирали все экскременты каждой мыши. С помощью счетчика гамма-излучения 1282 CompuGamma CS (Walla coy, Turku, Finland) по отдельности измеряли гамма-радиоактивность 75SeHCAT в экскрементах и в желчном пузыре-кишечнике. Стабильность и количество 75SeHCAT, введенной каждой мыши, контролировали с помощью дополнительной аликвоты 75SeHCAT, используя ту же методику эксперимента, что и для других тестируемых образцов в исследовании.
Анализ данных
Суммарное гамма-излучение экскрементов и желчного пузыря-кишечника считали показателем общего количества выделившейся 75SeHCAT, которое составляло в среднем примерно 85% от общего количества 75SeHCAT, введенного каждой мыши. Из выделившейся радиоактивности 75SeHCAT, процентная доля 75SeHCAT, обнаруженная в экскрементах, считалась выделением с экскрементами, в то время как 75SeHCAT, обнаруженная в желчном пузыре-кишечнике, рассматривалась, как удержанная в организме. Ингибирующее действие соединения примера 14 на абсорбцию 75SeHCAT в кишечнике вычисляли, исходя из данных по удержанию 75SeHCAT в организме и выделения с фекалиями, и ED50 соединения определяли, исходя из кривой зависимости эффекта от дозы.
Результаты
Среднее IBAT-ингибирующее действие (5) при дозировке 0,156 мкмоль/кг определяли для соединений примеров 1-14 и полученные значения приведены в таблице 1.
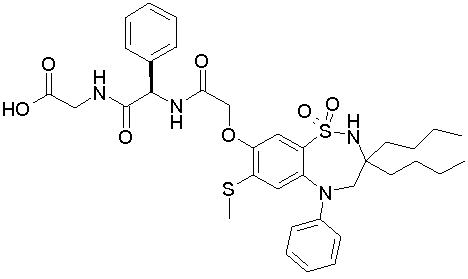
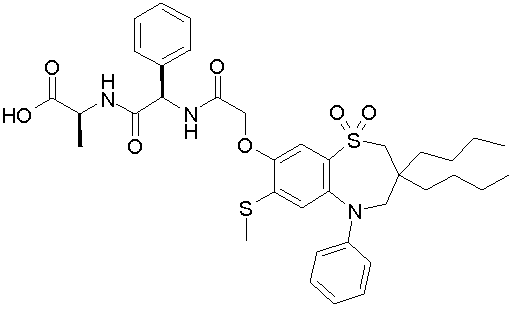
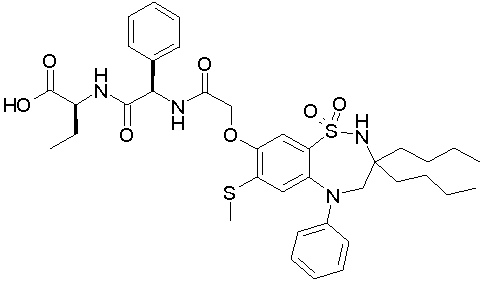
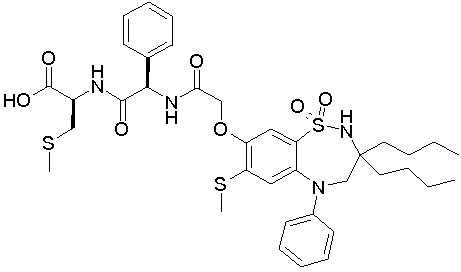
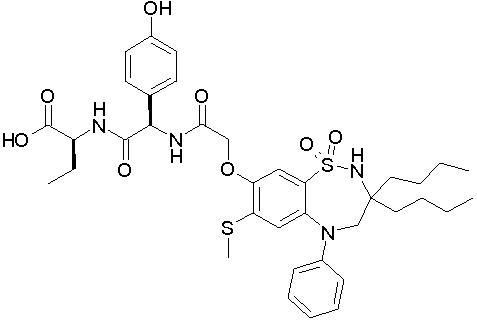
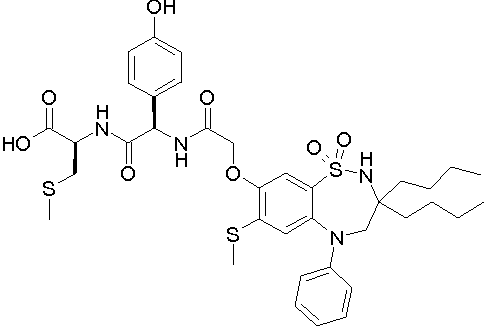
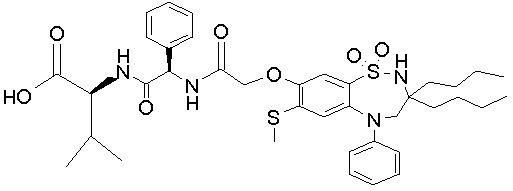
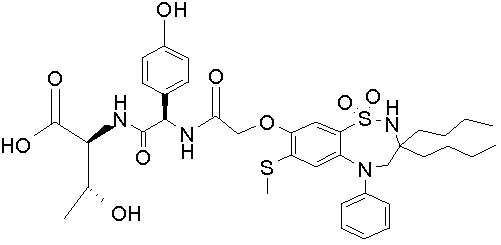
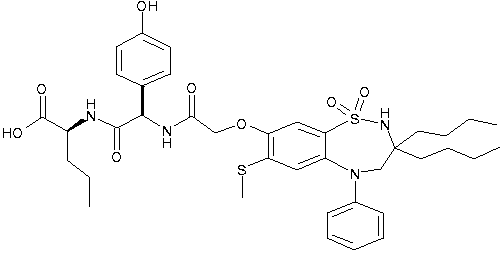
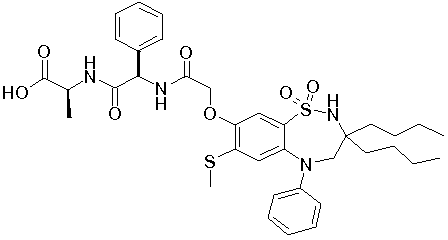
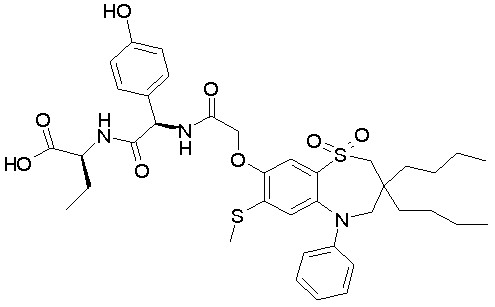
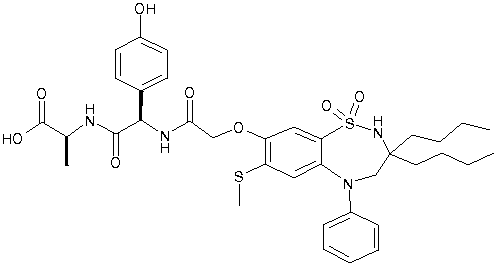
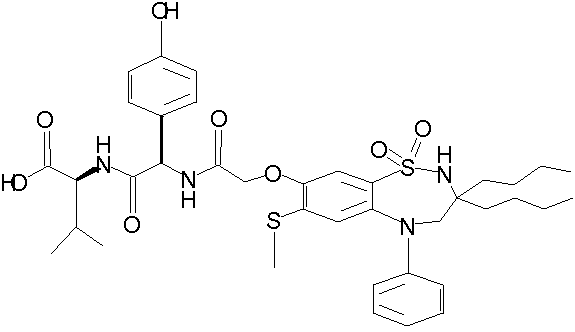
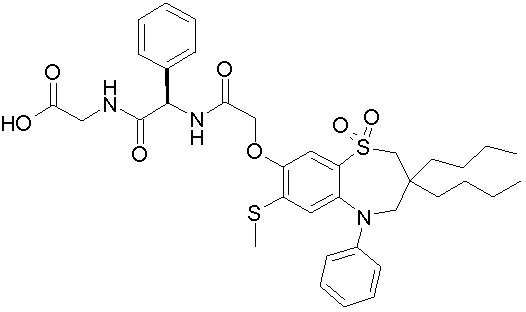
Пример 16
In vivo животная модель первичного склерозирующего холангита (PSC)
У генетически модифицированных мышей с направленным выключением гена мультилекарственной устойчивости Mdr2 (Abcb4), кодирующего канальцевую фосфолипидную флиппазу (мышей Mdr2-/-), самопроизвольно развивается склерозирующий холагнит с макроскопическими и микроскопическими особенностями первичного склерозирующего холангита человека. Поражение желчного протока у этих мышей связано с нарушением секреции фосфолипидов желчи, что приводит к повышению концентрации свободных, не включенных в мицеллы, желчных кислот, которое в свою очередь вызывает повреждение эпителиальных клеток (холангиоцитов) желчного протока, перихолангит, перидуктальный фиброз с пролиферацией желчного протока и, наконец, склерозирующий холангит. Анализ профиля экспрессии генов выявил примечательные сходства между Mdr2-/- и человеческим PSC. По аналогии с мышиной моделью Mdr2-/- склерозирующего холангита, дефекты белка мультилекарственной устойчивости MDR3/ABCB4 (человеческого ортолога белка грызунов Mdr2/Abcb4) играют важную роль в патогенезе различных холангиопатий у людей. Варианты MDR3 играют важную роль в качестве модификатора генов в патогенезе различных холангиопатий, например, PSC, первичного биллиарного цирроза (PBC) и идиопатической дуктопении в зрелом возрасте/биллиарного фиброза.
Мышам Mdr2-/- каждый день перорально вводили соединение примера 14 с помощью принудительного кормления в течение 2-4 недель, и контрольным животным аналогичным образом вводили носитель. Осуществляли исследование сыворотки печени, гистологии печени и фиброза. Соединение примера 14 улучшало результаты тестов печени, гистологию печени и ослабляло фиброз.
Пример 17
Получали состав для замедленного высвобождения ингибитора IBAT, имеющий следующий состав:
Соединение, ингибирующее IBAT, примера 14 растворяли в 99% этаноле совместно с этилцеллюлозой и гидроксипропилцеллюлозой. Полученную смесь затем распыляли на сферы нонпарель в установке с кипящим слоем. После этого гранулы высушивали и продували воздухом для удаления остатков этанола. Затем на лекарственные гранулы в установке с кипящим слоем распыляли дисперсию эудрагита L100-55 с добавкой триэтилцитрата. Затем полученными гранулами с покрытием после их высушивания и просеивания заполняли твердые желатиновые капсулы.
Пример 18
Получали состав для замедленного высвобождения ингибитора IBAT, имеющий следующий состав:
Ингибитор IBAT соединение примера 14 суспендировали в воде и распыляли на крупинки диоксида кремния заранее установленного размера в установке с кипящим слоем. Лекарственные гранулы высушивали в печи при температуре 40°C в течение 24 ч. После этого на гранулы наносили слой повидона K-25 из этанольного раствора в установке с кипящим слоем. После этого в установке с кипящим слоем наносили конечное покрытие из дисперсии эудрагита FS30D. Покрытие гранулы смешивали с микрокристаллической целлюлозой и стеарилфумаратом натрия в миксере и затем прессовали в таблетки.
Пример 19
Получали комбинированную таблетку ингибитор IBAT-колесевелам с немедленным высвобождением ингибитора IBAT и высвобождением секвестранта желчных кислот в толстой кишке, имеющую следующий состав:
Колесевелама гидрохлорид, микрокристаллическую целлюлозу и коллоидный диоксид кремния смешивали и гранулировали с гидроксипропилметилцеллюлозой, растворенной в воде. Гранулы высушивали, смешивали со стеаратом магния и прессовали в таблетки. Дисперсию эудрагита FS30D и воду смешивали в PlasACRYL T20 и распыляли на ядра таблеток, применяя подходящее устройство для нанесения. Суспензию покрытия, включающую ингибитор IBAT, готовили смешиванием ингибитора IBAT, гидроксипропилметилцеллюлозы и натрий кросскармелозы в воде, и распыляли ее на ядра таблеток со слоем для высвобождения в толстой кишке, применяя подходящее устройство для нанесения покрытия. На завершающем этапе раствор защитного покрытия, включающий гидроксипропилметилцеллюлозу и полиэтиленгликоль распыляли на таблетки, применяя подходящее устройство для нанесения покрытия.
Пример 20
Получали таблетки колесевелама с высвобождением в толстой кишке, имеющие следующий состав:
Колесевелама гидрохлорид, микрокристаллическую целлюлозу и коллоидный диоксид кремния смешивали и гранулировали с гидроксипропилметилцеллюлозой, растворенной в воде. Гранулы высушивали, смешивали со стеаратом магния и прессовали в таблетки. Амилозу, эудрагит 100, триэтилцитрат и глицерилмоностерат растворяли в подходящих растворителях и распыляли на ядра таблеток, используя подходящее устройство для нанесения покрытия.
Настоящее изобретение относится к применению соединений формулы II для лечения и/или профилактики заболевания печени, опосредованного IBAT, выбранного из синдрома Алажилля (ALGS), прогрессирующего семейного внутрипеченочого холестаза (PFIC), первичного биллиарного цирроза (РВС), первичного склерозирующего холангита (PSC), неалкогольного жирового стеатогепатита (NASH) и зуда, вызванного холестатической болезнью печени, а также к фармацевтической композиции на их основе и способу лечения указанных выше заболеваний. В общей формуле II М означает СН2 или NH; R1 означает Н или гидрокси; R2 представляет собой Н, СН3, -СН2СН3, -СН2СН2СН3, -СН2СН2СН2СН3, -СН(СН3)2, -СН2СН(СН3)2, -СН(СН3)СН2СН3, -СН2ОН, -СН2ОСН3, -СН(ОН)СН3, -CH2SCH3 или -CH2CH2SCH3. 3 н. и 8 з.п. ф-лы, 1 табл., 20 пр.
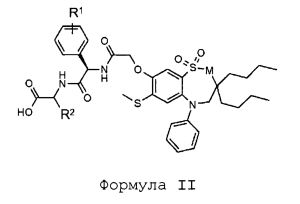
1. Применение соединения формулы (II)

где М означает СН2 или NH;
R1 означает Н или гидрокси;
R2 представляет собой Н, СН3, -СН2СН3, -СН2СН2СН3, -СН2СН2СН2СН3, -СН(СН3)2, -СН2СН(СН3)2, -СН(СН3)СН2СН3, -СН2ОН, -СН2ОСН3, -СН(ОН)СН3, -CH2SCH3 или -CH2CH2SCH3;
или его фармацевтически приемлемая соль для получения лекарственного средства для профилактики и/или лечения заболевания печени, опосредованного IBAT, где заболевание печени выбирают из группы, состоящей из синдрома Алажилля (ALGS), прогрессирующего семейного внутрипеченочого холестаза (PFIC), первичного биллиарного цирроза (РВС), первичного склерозирующего холангита (PSC), неалкогольного жирового стеатогепатита (NASH) и зуда, вызванного холестатической болезнью печени.
2. Применение соединения по п. 1, где соединение формулы II выбирают из группы, состоящей из:
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-(карбоксиметил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N′-((S)-1-карбоксиэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((R)-1-карбокси-2-метилтиоэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((R)-1-карбокси-2-метилтиоэтил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-метилпропил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-(R)-гидроксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксибутил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксиэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N′-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксиэтил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-метилпропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина; и
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1′-фенил-1′-[N′-(карбоксиметил)карбамоил]метил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепина
или его фармацевтически приемлемой соли.
3. Применение по п. 1 или 2, где соединение формулы II представляет собой 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин или его фармацевтически приемлемую соль.
4. Применение по п. 1 или 2, где соединение формулы II представляет собой 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1′-фенил-1′-[N′-(карбоксиметил)карбамоил]метил}-карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин
или его фармацевтически приемлемую соль.
5. Применение фармацевтической композиции, включающей соединение формулы (II):
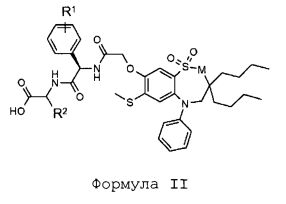
где М означает СН2 или NH;
R1 означает Н или гидрокси;
R2 представляет собой Н, СН3, -СН2СН3, -СН2СН2СН3, -СН2СН2СН2СН3, -СН(СН3)2, -СН2СН(СН3)2, -СН(СН3)СН2СН3, -СН2ОН, -СН2ОСН3, -СН(ОН)СН3, -CH2SCH3 или -CH2CH2SCH3;
или его фармацевтически приемлемую соль для получения лекарственного средства для профилактики и/или лечения заболевания печени, опосредованного IBAT, где заболевание печени выбирают из группы, состоящей из синдрома Алажилля (ALGS), прогрессирующего семейного внутрипеченочого холестаза (PFIC), первичного биллиарного цирроза (РВС), первичного склерозирующего холангита (PSC), неалкогольного жирового стеатогепатита (NASH) и зуда, вызванного холестатической болезнью печени.
6. Применение по п. 5, где соединение формулы II представляет собой 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}-карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин или его фармацевтически приемлемую соль.
7. Применение по п. 5, где соединение формулы II представляет собой 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1′-фенил-1′-[N′-(карбоксиметил)карбамоил]метил}-карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин или его фармацевтически приемлемую соль.
8. Способ лечения и/или профилактики заболевания печени, опосредованного IBAT, где заболевание печени выбирают из группы, состоящей из синдрома Алажилля (ALGS), прогрессирующего семейного внутрипеченочого холестаза (PFIC), первичного биллиарного цирроза (РВС), первичного склерозирующего холангита (PSC), неалкогольного жирового стеатогепатита (NASH) и зуда, вызванного холестатической болезнью печени, включающий введение субъекту, нуждающемуся в таком лечении, соединения формулы (II):
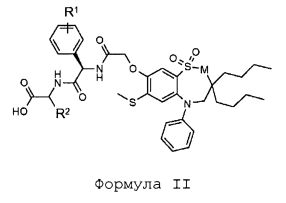
где М означает СН2 или NH;
R1 означает Н или гидрокси;
R2 представляет собой Н, СН3, -СН2СН3, -СН2СН2СН3, -СН2СН2СН2СН3, -СН(СН3)2, -СН2СН(СН3)2, -СН(СН3)СН2СН3, -СН2ОН, -СН2ОСН3, -СН(ОН)СН3, -CH2SCH3 или -CH2CH2SCH3;
или его фармацевтически приемлемую соль.
9. Способ по п. 8, где соединение формулы (II)
выбирают из группы, состоящей из:
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-(карбоксиметил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N′-((S)-1-карбоксиэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((R)-1-карбокси-2-метилтиоэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((R)-1-карбокси-2-метилтиоэтил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-метилпропил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-(R)-гидроксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксибутил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксиэтил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N′-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксиэтил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина;
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбокси-2-метилпропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепина; и
1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1′-фенил-1′-[N′-(карбоксиметил)карбамоил]метил}карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепина или его фармацевтически приемлемой соли.
10. Способ по п. 8 или 9, где соединение формулы II представляет собой 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-α-[N-((S)-1-карбоксипропил)карбамоил]-4-гидроксибензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,2,5-бензотиадиазепин или его фармацевтически приемлемую соль.
11. Способ по п. 8 или 9, где соединение формулы II представляет собой 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1′-фенил-1′-[N′-(карбоксиметил)карбамоил]метил}-карбамоилметокси)-2,3,4,5-тетрагидро-1,5-бензотиазепин
или его фармацевтически приемлемую соль.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Устройство для уплотнения строительных смесей | 1987 |
|
SU1535913A1 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАДИАЗЕПИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2002 |
|
RU2305681C2 |
Авторы
Даты
2016-07-10—Публикация
2011-11-08—Подача