Область техники, к которой относится изобретение
Настоящее изобретение, в целом, относится к катализаторам, полезным для конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси. Более конкретно, изобретение относится к катализаторам, полезным для дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, с высоким выходом и селективностью в акриловую кислоту, производные акриловой кислоты или их смеси, коротким временем пребывания, и без значительной конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в нежелательные побочные продукты, такие как, например, ацетальдегид, пропионовая кислота, уксусная кислота, 2,3-пентандион, диоксид углерода и монооксид углерода.
Уровень техники
Акриловая кислота, производные акриловой кислоты или их смеси имеют множество промышленных применений, как правило, потребляемых в виде полимеров. В свою очередь, эти полимеры широко используются в производстве, среди прочего, адгезивов, связующих веществ, покрытий, красок, полиролей, моющих средств, флокулянтов, диспергаторов, тиксотропных веществ, секвестрантов и суперабсорбирующих полимеров, которые используются в одноразовых абсорбирующих изделиях, в том числе подгузниках и гигиенических продуктах, например. Акриловую кислоту обычно получают из источников нефти. Например, акриловую кислоту уже давно получают путем каталитического окисления пропилена. Эти и другие способы получения акриловой кислоты из источников нефти, описаны в Kirk-Othmer Encyclopedia of Chemical Technology, Vol. 1, pgs. 342-369 (5th Ed., John Wiley & Sons, Inc., 2004). Акриловая кислота, полученная из нефти, способствует парниковым выбросам благодаря своему высокому содержанию углерода на основе нефти. Дополнительно, нефть является не возобновляемым материалом, так как сотни тысяч лет необходимы для природного образования и только короткое время для потребления. Поскольку нефтехимические ресурсы становятся все более скудными, дорогими и подчиняются правилам для выбросов CO2, существует растущий спрос на полученную из биологического сырья акриловую кислоту, производные акриловой кислоты или их смеси, которые могут служить в качестве альтернативы акриловой кислоте, производным акриловой кислоты или их смесям, полученным из нефти.
В течение последних 40-50 лет были сделаны многие попытки, чтобы получить акриловую кислоту, производные акриловой кислоты или их смеси, полученные из биологического сырья, из источников, отличных от нефти, таких как молочная кислота (также известная как 2-гидроксипропионовая кислота), 3-гидроксипропионовая кислота, глицерин, монооксид углерода и этиленоксид, диоксид углерода и этилен, и кротоновая кислота. Из этих источников, отличных от нефти, только молочную кислоту получают сегодня с высоким выходом из сахара (≥90% теоретического выхода, или эквивалентно ≥0,9 г молочной кислоты на грамм сахара) и чистотой, и экономикой, которые могли бы поддерживать получение акриловой кислоты при стоимости, конкурентной для акриловой кислоты, полученной из нефти. Как таковая, молочная кислота или лактат представляет собой реальную возможность служить в качестве сырья для акриловой кислоты, производных акриловой кислоты или их смесей, полученных из биологического сырья. Кроме того, 3-гидроксипропионовая кислота, как ожидается, будет производиться в коммерческих масштабах в течение нескольких лет, и в этом качестве, 3-гидропропионовая кислота представит еще одну реальную возможность служить в качестве сырья для акриловой кислоты, производных акриловой кислоты или их смесей, полученных из биологического сырья. Сульфатные соли; фосфатные соли; смеси сульфатных и фосфатных солей; основания; цеолиты или модифицированные цеолиты; оксиды металлов или модифицированные оксиды металлов; и сверхкритическая вода являются основными катализаторами, которые были использованы для дегидратации молочной кислоты или лактата в акриловую кислоту, производные акриловой кислоты или их смеси, в прошлом, с различной степенью успеха.
Например, в патенте США №4,786,756 (выдан в 1988 году), описывается дегидратация в паровой фазе молочной кислоты или лактата аммония в акриловую кислоту с помощью фосфата алюминия (AlPO4), который обрабатывают водным неорганическим основанием в качестве катализатора. В качестве примера, ′756 патент раскрывает максимальный выход акриловой кислоты 43,3%, когда молочную кислоту подают в реактор приблизительно при атмосферном давлении, и соответствующий выход 61,1%, когда лактат аммония подают в реактор. В обоих примерах, ацетальдегид был получен с выходами 34,7% и 11,9%, соответственно, и другие побочные продукты также присутствовали в больших количествах, такие как, пропионовая кислота, СО и CO2. Отсутствие обработки основанием вызвало повышенное количество побочных продуктов. Другим примером является Hong et al. (2011) Appl. Catal. A: General 396:194-200, который разработал и испытал композитные катализаторы, приготовленные с Са3(PO4)2 и Са2(P2O7) солями методом суспензионного смешивания. Катализатор с наиболее высоким выходом акриловой кислоты из метиллактата был 50%-50% (по массе) катализатор. Это дает выход 68% акриловой кислоты, приблизительно 5% метилакрилата и приблизительно 14% ацетальдегида при 390°С. Тот же катализатор приводит к 54% выходу акриловой кислоты, 14% выходу ацетальдегида и 14% выходу пропионовой кислоты из молочной кислоты.
Группа профессора Д. Миллера в Мичиганском государственном университете (MSU) опубликовала много работ по дегидратации молочной кислоты или сложных эфиров молочной кислоты в акриловую кислоту и 2,3-пентандион, такие как, Gunter et al. (1994) J. Catalysis 148:252-260; и Tam et al. (1999) Ind. Eng. Chem. Res. 38:3873-3877. Лучшие выходы акриловой кислоты, представленные группой, составляли приблизительно 33%, когда молочную кислоту дегидратировали при 350°С на более низкой площади поверхности и объеме пор кремнезема, пропитанного NaOH. В том же самом эксперименте, выход ацетальдегида составлял 14,7% и выход пропионовой кислоты составлял 4,1%. Примеры других катализаторов, проверенных группой, были Na2SO4, NaCl, Na3PO4, NaNO3, Na2SiO3, Na4P2O7, NaH2PO4, Na2HPO4, Na2HAsO4, NaC3H5O3, NaOH, CsCl, Cs2SO4, KOH, CsOH и LiOH. Во всех случаях, на которые ссылаются выше, катализаторы были испытаны в качестве отдельных компонентов, а не в виде смесей. Наконец, группа предположила, что выход в акриловую кислоту улучшается, а выход в побочные продукты подавляется, когда площадь поверхности на носителе из кремнезема является низкой, температура реакции является высокой, давление реакции является низким, и время пребывания реагентов в слое катализатора короткое.
И, наконец, китайская заявка на патент 200910054519.7 раскрывает применение ZSM-5 молекулярных сит, модифицированных с помощью водного раствора щелочи (например, NH3, NaOH и Na2CO3) или соли фосфорной кислоты (например, NaH2PO4, Na2HPO4, LiH2PO4, LaPO4 и т.д.). Лучший выход акриловой кислоты, который достигается при дегидратации молочной кислоты, составлял 83,9%, однако, данный выход получен при очень длительных сроках пребывания.
Таким образом, производство акриловой кислоты, производных акриловой кислоты или их смесей из молочной кислоты или лактата способами, такими как те, которые описаны в литературе, как отмечалось выше, показало: 1) выходы акриловой кислоты, производных акриловой кислоты или их смесей не превышают 70%; 2) низкие селективности получения акриловой кислоты, производных акриловой кислоты или их смесей, то есть, значительные количества нежелательных побочных продуктов, таких как, ацетальдегид, 2,3-пентандион, пропионовая кислота, СО и CO2; 3) длительное время пребывания в слоях катализатора; и 4) дезактивацию катализатора в короткое время в потоке (TOS). Побочные продукты могут осаждаться на катализатор, приводя в результате к загрязнению, и преждевременной и быстрой дезактивации катализатора. Кроме того, после осаждения, эти побочные продукты могут катализировать другие нежелательные реакции, такие как реакции полимеризации. Кроме осаждения на катализаторы, эти побочные продукты, даже если они присутствуют только в малых количествах, приводят к дополнительным затратам при обработке акриловой кислоты (если они присутствуют в выходящем потоке продукта реакции) в производстве суперабсорбирующих полимеров (SAP), например. Эти недостатки известных способов и катализаторов делают их коммерчески нежизнеспособными.
Таким образом, существует потребность в катализаторах и способах дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, с высоким выходом, селективностью и эффективностью (т.е. коротким временем пребывания) и высокой долговечностью катализаторов.
Сущность изобретения
Представлен катализатор для дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси. Катализатор содержит: (а) по меньшей мере, один анион конденсированного фосфата, выбранный из группы, состоящей из формул (I), (II) и (III)
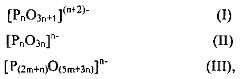
где n составляет, по меньшей мере, 2 и m составляет, по меньшей мере, 1, и (b) по меньшей мере, два различных катиона, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и, по меньшей мере, двух различных катионов составляет от приблизительно 0,7 до приблизительно 1,7. Анионы, определенные формулами (I), (II) и (III), также называют полифосфатами (или олигофосфатами), циклофосфатами и ультрафосфатами, соответственно.
В другом осуществлении настоящего изобретения представлен способ получения катализатора. Способ включает стадии, на которых смешивают и нагревают, по меньшей мере, два соединения, содержащие фосфор, при этом каждое указанное соединение описано одной из формул (IV)-(XXV), или любой из гидратированных форм указанных формул:
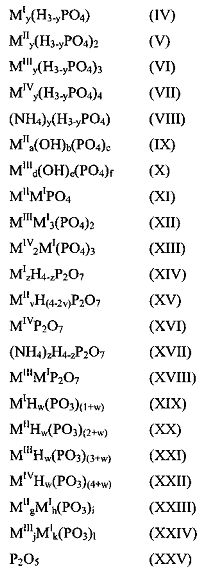
где MI представляет собой одновалентный катион; где MII представляет собой двухвалентный катион; где MIII представляет собой трехвалентный катион; где MIV представляет собой четырехвалентный катион; где y означает 0, 1, 2 или 3; где z означает 0, 1, 2, 3 или 4; где v означает 0, 1 или 2; где w означает 0 или любое положительное целое число; и где а, b, с, d, е, f, g, h, i, j, k и l означают любые положительные целые числа, таким образом, что удовлетворены уравнения: 2а=b+3с, 3d=е+3f, i=2g+h, и l=3j+k.
В еще одном осуществлении настоящего изобретения представлен способ получения катализатора. Способ включает стадии, на которых смешивают и нагревают: (а) по меньшей мере, одно соединение, содержащее фосфор, при этом каждое указанное соединение описано одной из формул (IV)-(XXV), или любой из гидратированных форм указанных формул:
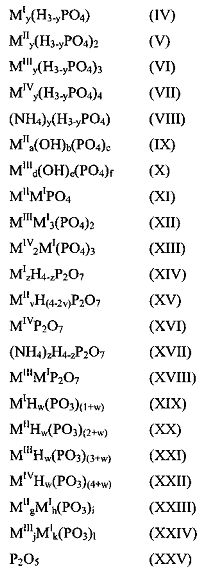
где MI представляет собой одновалентный катион; где MII представляет собой двухвалентный катион; где MIII представляет собой трехвалентный катион; где MIV представляет собой четырехвалентный катион; где y означает 0, 1, 2 или 3; где z означает 0, 1, 2, 3 или 4; где v означает 0, 1 или 2; где w означает 0 или любое положительное целое число; и где а, b, с, d, е, f, g, h, i, j, k и l означают любые положительные целые числа, таким образом, что удовлетворены уравнения: 2а=b+3с, 3d=е+3f, i=2g+h, и l=3j+k; и (b) по меньшей мере, одно соединение, не содержащее фосфор, выбранное из группы, состоящей из нитратных солей, карбонатных солей, ацетатных солей, оксидов металлов, хлоридных солей, сульфатных солей и гидроксидов металлов, при этом каждое указанное соединение описано одной из формул (XXVI)-(XL), или любой из гидратированных форм указанных формул:
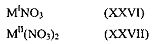
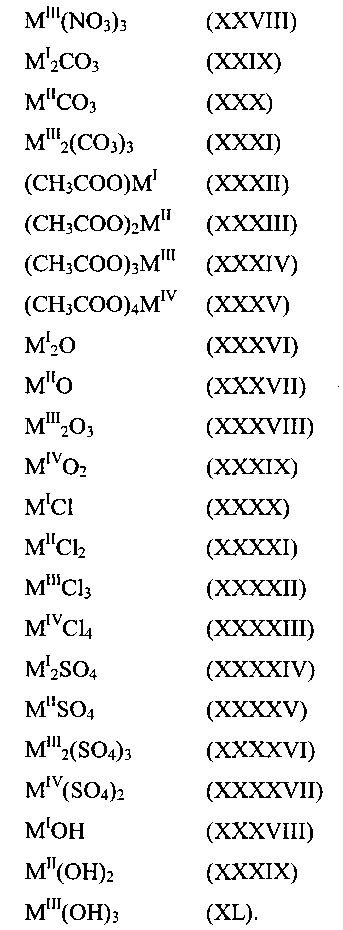
В другом осуществлении настоящего изобретения, представлен способ получения катализатора, включающий следующие стадии, на которых: (а) объединяют соединение, содержащее фосфор, нитратную соль, фосфорную кислоту и воду с образованием влажной смеси, при этом мольное соотношение фосфора и катионов, как в соединении, содержащем фосфор, так и в нитратной соли, составляет приблизительно 1; (b) прокаливают указанную влажную смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С с получением высушенного твердого вещества; и (с) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В еще одном осуществлении настоящего изобретения, представлен способ получения катализатора, включающий стадии, на которых: (а) объединяют Са2Р2О7 и KH2PO4 в мольном соотношении приблизительно 3:1 с образованием твердой смеси; и (b) прокаливают указанную твердую смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С, с получением указанного катализатора.
Дополнительные признаки настоящего изобретения станут очевидными специалистам в данной области техники после рассмотрения приведенного ниже подробного описания в сочетании с примерами.
Подробное описание изобретения
I Определения
Как используют в данной заявке, термин «монофосфат» или «ортофосфат» относится к любой соли, анионный фрагмент которой, [PO4]3-, состоит из четырех атомов кислорода, расположенных в почти правильной тетраэдрической матрице с приблизительно центральным атомом фосфора.
Как используют в данной заявке, термин «конденсированный фосфат» относится к любым солям, содержащим одну или несколько P-О-Р связей, образованных углом, общим с PO4 тетраэдром.
Как используют в данной заявке, термин «полифосфат» относится к любым конденсированным фосфатам, содержащим линейные Р-О-Р связи, образованные углом, общим с PO4 тетраэдром, приводя к образованию конечных цепей.
Как используют в данной заявке, термин «олигофосфат» относится к любым полифосфатам, содержащим пять или менее РО4 звеньев.
Как используют в данной заявке, термин «циклофосфат» относится к любому циклическому конденсированному фосфату, состоящему из двух или более имеющих общий угол РО4 тетраэдров.
Как используют в данной заявке, термин «ультрафосфат» относится к любому конденсированному фосфату, где, по меньшей мере, два РО4 тетраэдра анионного фрагмента имеют три общих угла с прилегающими углами.
Как используют в данной заявке, термин «катион» относится к любому атому или группе ковалентно-связанных атомов, имеющих положительный заряд.
Как используют в данной заявке, термин «анион» относится к любому атому или группе ковалентно-связанных атомов, имеющих отрицательный заряд.
Как используют в данной заявке, термин «одновалентный катион» относится к любому катиону с положительным зарядом +1.
Как используют в данной заявке, термин «многовалентный катион» относится к любому катиону с положительным зарядом равным или более, чем +2.
Как используют в данной заявке, термин «гетерополианион» относится к любому аниону с ковалентно связанным XOp и YOr полиэдром и включает X-O-Y и возможно X-О-Х и Y-O-Y связи, где X и Y представляют собой любые атомы и где риг представляют собой любые положительные целые числа.
Как используют в данной заявке, термин «гетерополифосфат» относится к любому гетерополианиону, где X представляет собой фосфор (P) и Y означает любой другой атом.
Как используют в данной заявке, термин «фосфатный аддукт» относится к любому соединению с одним или более фосфатными анионами, и одним или более нефосфатными анионами, не связанными ковалентно.
Как используют в данной заявке, термины «LA» относится к молочной кислоте, «АА» относится к акриловой кислоте, «АсН» относится к ацетальдегиду и «РА» относится к пропионовой кислоте.
Как используют в данной заявке, термин «разброс значений диаметра частиц» относится к статистическому представлению данной пробы частиц и равен (Dv,0,90-Dv,0,10)/Dv,0,50. Термин «медианный размер частиц» или Dv,0,50 относится к диаметру частицы, менее которого находятся 50% общего объема частиц. Дополнительно, Dv,0,10 относится к размеру частицы, отделяющему пробу частицы при 10% по объемной фракции и Dv,0,90, представляет собой размер частицы, отделяющий пробу частицы при 90% по объемной фракции.
Как используют в данной заявке, термин «конверсия» в % определяют как [скорость втекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин) - скорость вытекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)]/[скорость втекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)]*100. Для целей настоящего изобретения, термин «конверсия» означает мольная конверсия, если не указано иное.
Как используют в данной заявке, термин «выход» в % определен как [скорость вытекания продукта (моль/мин)/скорость втекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)]*100. Для целей настоящего изобретения, термин «выход» означает мольный выход, если не указано иное.
Как используют в данной заявке, термин «селективность» в % определен как [Выход/Конверсия]*100. Для целей настоящего изобретения, термин «селективность» означает мольнуюселективность, если не указано иное.
Как используют в данной заявке, термин «общая скорость вытекания» в моль/мин и для гидроксипропионовой кислоты определен как: (2/3)*[скорость вытекания С2 (моль/мин)]+[скорость вытекания С3 (моль/мин)]+(2/3)*[скорость вытекания ацетальдегида (моль/мин)]+(4/3)*[скорость вытекания С4 (моль/мин)]+[скорость вытекания гидроксипропионовой кислоты (моль/мин)]+[скорость вытекания виноградной кислоты (моль/мин)]+(2/3)*[скорость вытекания уксусной кислоты (моль/мин)]+[скорость вытекания 1,2-пропандиола (моль/мин)]+[скорость вытекания пропионовой кислоты (моль/мин)]+[скорость вытекания акриловой кислоты (моль/мин)]+(5/3)*[скорость вытекания 2,3-пентандиона (моль/мин)]+(1/3)*[скорость вытекания монооксида углерода (моль/мин)]+(1/3)*[скорость вытекания диоксида углерода (моль/мин)]. Если используют производное гидроксипропионовой кислоты вместо гидроксипропионовой кислоты, указанная выше формула должна быть скорректирована на количество атомов углерода в производном гидроксипропионовой кислоты.
Как используют в данной заявке, термин «С2» означает этан и этилен.
Как используют в данной заявке, термин «С3» означает пропан и пропилен.
Как используют в данной заявке, термин «С4» означает бутан и бутены.
Как используют в данной заявке, термин «общий мольный баланс» или «ТМВ» в % определен как [общая скорость вытекания (моль/мин)/скорость втекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)]*100.
Как используют в данной заявке, термин «выход акриловой кислоты скорректирован на ТМВ» определен как [выход акриловой кислоты/общий мольный баланс]*100, для учета слегка более высоких потоков в реакторе.
Как используют в данной заявке, термин «часовая объемная скорость газа» или «GHSV» в ч-1 определен как [Общая скорость потока газа (мл/мин)/объем слоя катализатора (мл)]/60. Общая скорость потока газа рассчитывается в условиях стандартной температуры и давления (STP; 0°С и 1 атм).
Как используют в данной заявке, термин «часовая объемная скорость жидкости» или «LHSV» в ч-1 определен как [Общая скорость потока жидкости (мл/мин)/объем слоя катализатора (мл)]/60.
II Катализаторы
Неожиданно было обнаружено, что смешанные конденсированные фосфатные катализаторы дегидратируют гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси в акриловую кислоту, производные акриловой кислоты или их смеси с высоким: 1) выходом и селективностью получения акриловой кислоты, производных акриловой кислоты или их смесей, то есть низким количеством побочных продуктов и немногими побочными продуктами; 2) эффективностью, т.е. производительностью за короткое время пребывания; и 3) долговечностью. Не желая быть связанными какой-либо теорией, заявители предполагают, что катализатор, который содержит, по меньшей мере, один анион конденсированного фосфата и два различных катиона, работает следующим образом: карбоксилатная группа гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, связывается с одним или несколькими катионами, которые в одном осуществлении являются многовалентными, через один или оба атома кислорода, удерживая молекулу на поверхности катализатора, дезактивируя ее от декарбонилирования, и активизируя связь C-OH для устранения. Затем полученный протонированный анион конденсированного фосфата дегидратирует гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси с согласованным протонированием гидроксильной группы, удалением протона из метальной группы, и устранением протонированной гидроксильной группы в качестве молекулы воды, образуя акриловую кислоту, производные акриловой кислоты или их смеси и повторно активизируя катализатор. Дополнительно, заявители считают, что когда гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси разбавляют водой, то некоторые конденсированные фосфатные соли в катализаторе можно гидролизировать до неконденсированных монофосфатов или коротких конденсированных фосфатов, которые могут быть преобразованы в жидком состоянии в надлежащих условиях температуры и давления, что способствует дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей.
В одном осуществлении, катализатор содержит: (а) по меньшей мере, один анион конденсированного фосфата, который выбирают из группы, состоящей из формул (I), (II) и (III)
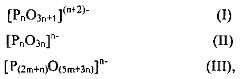
где n составляет, по меньшей мере, 2 и m составляет, по меньшей мере, 1, и (b) по меньшей мере, два различных катиона, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и, по меньшей мере, двух различных катионов составляет от приблизительно 0,7 до приблизительно 1,7.
Анионы, определенные формулами (I), (II) и (III) также называют полифосфатами (или олигофосфатами), циклофосфатами и ультрафосфатами, соответственно.
В другом осуществлении, катализатор содержит: (а) по меньшей мере, один анион конденсированного фосфата, который выбирают из группы, состоящей из формул (I) и (II)

где n составляет, по меньшей мере, 2, и (b) по меньшей мере, два различных катиона, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и, по меньшей мере, двух различных катионов составляет от приблизительно 0,7 до приблизительно 1,7.
Катионы могут быть одновалентными или многовалентными. В одном осуществлении, один катион является одновалентным и другой катион является многовалентным. В другом осуществлении, многовалентный катион выбирают из группы, состоящей из двухвалентных катионов, трехвалентных катионов, четырехвалентных катионов, пятивалентных катионов и их смесей. Неограничивающие примеры одновалентных катионов представляют собой Н+, Li+, Na+, K+, Rb+, Cs+, Ag+, Rb+, Tl+ и их смеси. В одном осуществлении, одновалентный катион выбирают из группы, состоящей из Li+, Na+, K+, Rb+, Cs+ и их смесей; в другом осуществлении, одновалентный катион представляет собой Na+ или K+; и в еще одном осуществлении, одновалентный катион представляет собой K+. Неограничивающие примеры многовалентных катионов представляют собой катионы щелочноземельных металлор (т.е., Be, Mg, Са, Sr, Ва и Ra), переходных металлов (например, Y, Ti, Zr, V, Nb, Cr, Mo, Mn, Re, Fe, Ru, Co, Rh, Ni, Pd, Pt, Cu, Ag и Au), легких металлов (например, Zn, Ga, Si, Ge, B, Al, In, Sb, Sn, Bi и Pb), лантанидов (например, La и Се) и актинидов (например, Ас и Th). В одном осуществлении, многовалентный катион выбирают из группы, состоящей из Ве2+, Mg2+, Са2+, Sr2+, Ва2+, Mn2+, Fe2+, Co2+, Ni2+, Cu2+, Zn2+, Cd2+, Sn2+, Pb2+, Ti3+, Cr3+, Mn3+, Fe3+, Al3+, Ga3+, Y3+, In3+, Sb3+, Bi3+, Si4+, Ti4+, V4+, Ge4+, Mo4+, Pt4+, V5+, Nb5+, Sb5+и их смесей. В одном осуществлении, многовалентный катион выбирают из группы, состоящей из Са2+, Ва2+, Cu2+, Mn2+, Mn3+ и их смесей; в другом осуществлении, многовалентный катион выбирают из группы, состоящей из Са2+, Ва2+, Mn3+ и их смесей; и в еще одном осуществлении, многовалентный катион представляет собой Ва2+.
Катализатор может включать катионы: (а) Н+, Li+, Na+, K+, Rb+, Cs+ или их смеси; и (b) Be2+, Mg2+, Ca2+, Sr2+, Ba2+, Mn2+, Fe2+, Со2+, Ni2+, Cu2+, Zn2+, Cd2+, Sn2+, Pb2+, Ti3+, Cr3+, Mn3+, Fe3+, Al3+, Ga3+, Y3+, In3+, Sb3+, Bi3+, Si4+, Ti4+, V4+, Ge4+, Mo4+, Pt4+, V5+, Nb5+, Sb5+ или их смеси. В одном осуществлении катализатор содержит Li+, Na+ или K+ в качестве одновалентного катиона, и Са2+, Ва2+ или Mn3+ в качестве многовалентного катиона; в другом осуществлении, катализатор содержит Na+ или K+ в качестве одновалентного катиона, и Ca2+ или Ba2+ в качестве многовалентного катиона; и в еще одном осуществлении, катализатор содержит K+ в качестве одновалентного катиона и Ba2+ в качестве многовалентного катиона.
В одном осуществлении, катализатор содержит Ba2-x-sK2xH2sP2O7 и (KPO3)n, где х и s превышают или равны 0 и менее чем приблизительно 0,5 и n представляет собой положительное целое число. В другом осуществлении, катализатор содержит Ca2 -x-sK2xH2sP2O7 и (KPO3)n, где х и s превышают или равны 0 и менее, чем приблизительно 0,5 и n представляет собой положительное целое число. В еще одном осуществлении, катализатор содержит Mn1-x-sK1+3xH3sP2O7 или Mn1-x-sK2+2xH2sP2O7 и (KPO3)n, где х и s превышают или равны 0 и менее, чем приблизительно 0,5 и n представляет собой положительное целое число. В другом осуществлении, катализатор содержит любую смесь Ba2-x-sK2xH2sP2O7, Ca2-x-sK2xH2sP2O7, Mn1-x-sK1+3xH3sP2O7 или Mn1-x-sK2+2xH2sP2O7; и (KPO3)n, где х и s превышают или равны 0 и менее, чем приблизительно 0,5 и n представляет собой положительное целое число.
В одном осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,7 до приблизительно 1,7; в другом осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,8 до приблизительно 1,3; и в еще одном осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет приблизительно 1.
В одном осуществлении, катализатор содержит: (а) по меньшей мере, два различных аниона конденсированного фосфата, которые выбирают из группы, состоящей из формул (I), (II) и (III)
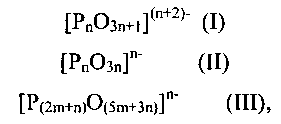
где n составляет, по меньшей мере, 2 и m составляет, по меньшей мере, 1, и (b) один катион, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и катиона составляет от приблизительно 0,5 до приблизительно 4,0. В другом осуществлении, мольное соотношение фосфора и катиона составляет от приблизительно t/2 до приблизительно t, где t является зарядом катиона.
Катализатор может включать инертный носитель, который выполнен из материала, содержащего силикаты, алюминаты, уголь, оксиды металлов и их смеси. В качестве альтернативы, носитель является инертным по отношению к реакционной смеси, которая, как ожидают, вступит в контакт с катализатором. В контексте реакций, четко описанных в данной заявке, в одном осуществлении носитель представляет собой кремнезем или двуокись циркония с низкой площадью поверхности. Если присутствует, носитель представляет собой количество от приблизительно 5 мас. % до приблизительно 98 мас. %, исходя из общей массы катализатора. Как правило, катализатор, который содержит инертный носитель, может быть выполнен с помощью одного из двух иллюстративных способов: пропитки или совместного осаждения. В способе пропитки, суспензию твердого инертного носителя обрабатывают раствором пре-катализатора, и полученный материал затем активизируют в условиях, которые преобразуют пре-катализатор в более активное состояние. В способе совместного осаждения, однородный раствор ингредиентов катализатора осаждают добавлением дополнительных ингредиентов.
III Способы получения катализатора
В одном осуществлении, способ получения катализатора включает стадии, на которых смешивают и нагревают, по меньшей мере, два различных соединения, содержащие фосфор, при этом каждое указанное соединение описано одной из формул (IV)-(XXV), или любой из гидратированных форм указанных формул:


где MI представляет собой одновалентный катион; где MII представляет собой двухвалентный катион; где MIII представляет собой трехвалентный катион; где MIV представляет собой четырехвалентный катион; где y означает 0, 1, 2 или 3; где z означает 0, 1, 2, 3 или 4; где v означает 0, 1 или 2; где w означает 0 или любое положительное целое число; и где а, b, с, d, е, f, g, h, i, j, k и l означают любые положительные целые числа, таким образом, что удовлетворены уравнения: 2а=b+3с, 3d=е+3f, i=2g+h, и l=3j+k.
В одном осуществлении, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (IV), где у равен I, и одного или более соединений, содержащих фосфор, формулы (V), где у равен 2. В другом осуществлении, катализатор получают смешиванием и нагреванием MIH2PO4 и MIIHPO4. В одном осуществлении, MI представляет собой K+ и MII представляет собой Ca2+, т.е. катализатор получают смешиванием и нагреванием KH2PO4 и CaHPO4; или MI представляет собой K и MII представляет собой Ba2+, т.е. катализатор получают смешиванием и нагреванием KH2PO4 и BaHPO4.
В одном осуществлении, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (IV), где у равен 1, одного или более соединений, содержащих фосфор, формулы (XV), где v равен 2. В другом осуществлении, катализатор получают смешиванием и нагреванием MIH2PO4 и 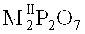
В другом осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,7 до приблизительно 1,7; в еще одном осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,8 до приблизительно 1,3; и в другом осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет приблизительно 1.
В другом осуществлении, способ получения катализатора включает стадии, на которых смешивают и нагревают (а) по меньшей мере, одно соединение, содержащее фосфор, при этом каждое указанное соединение описано одной из формул (IV)-(XXV), или любой из гидратированных форм указанных формул:


где y означает 0, 1, 2 или 3; где z означает 0, 1, 2, 3 или 4; где v означает 0, 1 или 2; где w означает 0 или любое положительное целое число; и где а, b, с, d, е, f, g, h, i, j, k и l означают любые положительные целые числа, таким образом, что уравнения: 2а=b+3с, 3d=е+3f, i=2g+h и l=3j+к удовлетворены, и (b) по меньшей мере, одно соединение, не содержащее фосфор, выбранное из группы, состоящей из нитратных солей, карбонатных солей, ацетатных солей, оксидов металлов, хлоридных солей, сульфатных солей и гидроксидов металлов, при этом каждое указанное соединение описано одной из формул (XXVI)-(XL), или любой из гидратированных форм указанных формул:
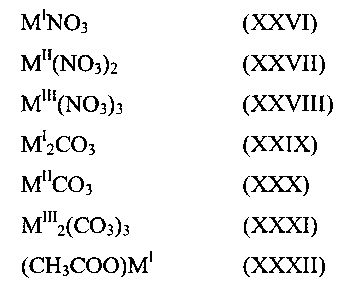
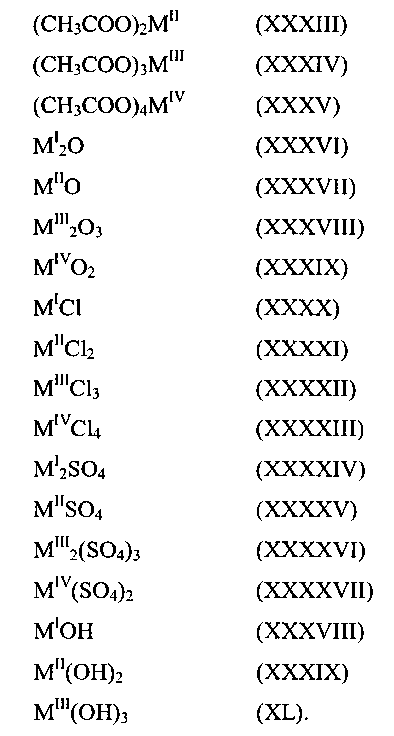
В другом осуществлении, соединения, не содержащие фосфор, могут быть выбраны из группы, состоящей из солей карбоновых кислот, галидных солей, ацетилацетонатов металлов и алкоксидов металлов.
В одном осуществлении настоящего изобретения, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,7 до приблизительно 1,7; в другом осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,8 до приблизительно 1,3; и в еще одном осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет приблизительно 1.
В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формул (IV)-(XXV) или их гидратированных форм, и одной или более нитратных солей формул (XXVI)-(XXVIII) или их гидратированных форм. В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (IV) и одной или более нитратных солей формулы (XXVII). В дополнительном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (IV), где y равен 2, соединения, содержащего фосфор, формулы (IV), где y равен 0 (т.е. фосфорной кислоты), и нитратной соли формулы (XXVII). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием K2HPO4, H3PO4 и Ba(NO3)2. В еще одном осуществлении, катализатор получают смешиванием и нагреванием K2HPO4, H3PO4 и Ca(NO3)2.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (IV) и одной или более нитратных солей формулы (XXVIII). В дополнительном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (IV), где y равен 2, соединения, содержащего фосфор, формулы (IV), где y равен 0 (т.е. фосфорной кислоты) и нитратной соли формулы (XXVIII). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием K2HPO4, H3PO4 и Mn(NO3)2·4H2O.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (V) и одной или более нитратных солей формулы (XXVI). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (V), где y равен 2, соединения, содержащего фосфор, формулы (V), где y равен 0 (т.е. фосфорной кислоты) и нитратной соли формулы (XXVI). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием BaHPO4, H3PO4 и KNO3. В другом осуществлении, катализатор получают смешиванием и нагреванием CaHPO4, H3PO4 и KNO3.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (V), одного или более соединений, содержащих фосфор, формулы (XV), и одной или более нитратных солей формулы (XXVI). В дополнительном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (V), где y равен 0 (т.е. фосфорной кислоты); соединения, содержащего фосфор, формулы (XV), где v равен 2; и нитратной соли формулы (XXVI). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием H3PO4, Ca2P2O7 и KNO3. В еще одном осуществлении, катализатор получают смешиванием и нагреванием H3PO4, Ba2P2O7 и KNO3.
В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (VI) и одной или более нитратных солей формулы (XXVI). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (VI), где y равен 3; соединения, содержащего фосфор, формулы (VI), где у равен 0 (т.е. фосфорной кислоты); и нитратной соли формулы (XXVI). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием MnPO4·qH2O, H3PO4 и KNO3.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (IV), одного или более соединений, содержащих фосфор, формулы (IX) и одной или более нитратных солей формулы (XXVII). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (IV), где y равен 2; соединения, содержащего фосфор, формулы (IV), где y равен 0 (т.е. фосфорной кислоты); соединения, содержащего фосфор, формулы (IX), где а равен 2, b равен 1, и с равен 1; и нитратной соли формулы (XXVII). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием K2HPO4, H3PO4, Cu2(ОН)PO4 и Ba(NO3)2.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (V), одного или более соединений, содержащих фосфор, формулы (IX) и одной или более нитратных солей формулы (XXVI). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (V), где y равен 3; соединения, содержащего фосфор, формулы (V), где y равен 0 (т.е. фосфорной кислоты); соединения, содержащего фосфор, формулы (IX), где а равен 2, b равен 1, и с равен 1; и нитратной соли формулы (XXVI). В еще одном осуществлении, катализатор получают смешиванием и нагреванием Ba3(PO4)2, H3PO4, Cu2(ОН)PO4 и KNO3.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IV)-(XXV) или любой гидратированной формы, и одной или более карбонатных солей, описанных одной из формул (XXIX)-(XXXI) или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IV)-(XXV) или любой гидратированной формы, и одной или более ацетатных солей, описанных одной из формул (XXXII)-(XXXV), любых других солей органической кислоты, или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IV)-(XXV) или любой гидратированной формы, и одного или более оксидов металлов, описанных одной из формул (XXXVI)-(XXXIX) или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IV)-(XXV) или любой гидратированной формы, и одной или более хлоридных солей, описанных одной из формул (ХХХХ)-(XXXXIII), любых других галидных солей, или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IV)-(XXV) или любой гидратированной формы, и одной или более сульфатных солей, описанных одной из формул (XXXXIV)-(XXXXVII) или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IV)-(XXV) или любой гидратированной формы, и одного или более гидроксидов, описанных одной из формул (XXXXVIII)-(XL) или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формул (IV)-(XXV), и двух или более соединений, не содержащих фосфор, формул (XXVI)-(XL) или их гидратированных форм.
В одном осуществлении, мольное соотношение фосфора и катионов (т.е. MI+MII+MIII+…) составляет от приблизительно 0,7 до приблизительно 1,7; в другом осуществлении, мольное соотношение фосфора и катионов (т.е. MI+MII+MIII+…) составляет от приблизительно 0,8 до приблизительно 1,3, и в еще одном осуществлении, мольное соотношение фосфора и катионов (т.е. MI+MII+MIII+…) составляет приблизительно 1. Например, в осуществлении, если катализатор содержит калий (K+) и барий (Ba2+), мольное соотношение фосфора и металлов (K+Ba) составляет от приблизительно 0,7 до приблизительно 1,7; и в другом осуществлении, мольное соотношение фосфора и металлов (K+Ba) составляет приблизительно 1.
Если катализатор содержит только два различных катиона, мольное соотношение между катионами, в одном осуществлении, составляет от приблизительно 1:50 до приблизительно 50:1; и в другом осуществлении, мольное соотношение между катионами составляет от приблизительно 1:4 до приблизительно 4:1. Например, если катализатор содержит калий (K+) и барий (Ba2+), мольное соотношение между ними (K:Ba), в одном осуществлении, составляет от приблизительно 1:4 до приблизительно 4:1. Также, если катализатор получают смешиванием и нагреванием K2HPO4, Ba(NO3)2 и H3PO4, калий и барий присутствуют, в другом осуществлении, в мольном соотношении, К:Ва, от приблизительно 2:3 до приблизительно 1:1.
В одном осуществлении, катализатор может включать инертный носитель, который выполнен из материала, содержащего силикаты, алюминаты, уголь, оксиды металлов и их смеси. В качестве альтернативы, носитель является инертным по отношению к реакционной смеси, которая как ожидается, контактирует с катализатором. В другом осуществлении, способ получения катализатора может дополнительно включать стадию, на которой смешивают инертный носитель с катализатором до, во время или после смешивания и нагревания соединений, содержащих фосфор, при этом инертный носитель включает силикаты, алюминаты, уголь, оксиды металлов и их смеси. В еще одном осуществлении, способ получения катализатора может дополнительно включать стадию, на которой смешивают инертный носитель с катализатором до, во время или после смешивания и нагревания соединений, содержащих фосфор, и соединений, не содержащих фосфор, при этом инертный носитель включает силикаты, алюминаты, уголь, оксиды металлов и их смеси.
Смешивание соединений, содержащих фосфор, или соединений, содержащих и не содержащих фосфор, катализатора может быть выполнено любым способом, известным специалистам в данной области техники, таким как, в качестве примера, а не ограничения: смешивание твердых веществ и совместное осаждение. В способе смешивания твердых веществ, различные компоненты физически смешивают вместе с необязательным измельчением с помощью любого способа, известного специалистам в данной области техники, такого как, в качестве примера, а не ограничения, сдвиг, растяжение, разминание, экструзия и другие. В способе совместного осаждения, водный раствор или суспензию из различных компонентов, включая одно или более фосфатных соединений, получают с последующей необязательной фильтрацией и нагреванием для удаления растворителей и летучих веществ (например, воды, азотной кислоты, диоксида углерода, аммиака или уксусной кислоты). Нагревание обычно осуществляется с помощью любого способа, известного специалистам в данной области техники, такого как, в качестве примера, а не ограничения, конвекция, теплопроводность, излучение, СВЧ-нагрев и другие.
В одном осуществлении настоящего изобретения, катализатор прокаливают. Прокаливание представляет собой процесс, который позволяет химическую реакцию и/или термическое разложение и/или фазовый переход и/или удаление летучих веществ. Процесс прокаливания осуществляется при помощи любого оборудования, известного специалистам в данной области техники, такого как, в качестве примера, а не ограничения, печи или реакторы различных конструкций, в том числе шахтные печи, вращающиеся печи, печи с обогреваемым подом и реакторы с псевдоожиженным слоем. Температура прокаливания, в одном осуществлении, составляет от приблизительно 200°С до приблизительно 1200°С; в другом осуществлении, температура прокаливания составляет от приблизительно 250°С до приблизительно 900°С; и в еще одном осуществлении, температура прокаливания составляет от приблизительно 300°С до 600°С. Время прокаливания, в одном осуществлении, составляет от приблизительно одного часа до приблизительно семидесяти двух часов.
В то время как многие способы и устройства известны специалистам в данной области техники для фракционирования частиц на дискретные размеры и определения распределения частиц по размерам, просеивание является одним из самых простых и наименее дорогих и распространенных способов. Альтернативный способ определения распределения частиц по размерам представляет собой рассеяние света. После прокаливания катализатор, в одном осуществлении, измельчают и просеивают, чтобы обеспечить более однородный продукт. Распределение частиц катализатора по размерам включает разброс значений диаметра частиц, который, в одном осуществлении, составляет менее, чем приблизительно 3; в другом осуществлении, распределение частиц катализатора по размерам включает разброс значений диаметра частиц, который составляет менее, чем приблизительно 2; и в еще одном осуществлении, распределение частиц катализатора по размерам включает разброс значений диаметра частиц, который составляет менее, чем приблизительно 1,5. В другом осуществлении настоящего изобретения, катализатор просеивают, чтобы медианный размер частиц составлял от приблизительно 50 мкм до приблизительно 500 мкм. В другом осуществлении настоящего изобретения, катализатор просеивают до медианного размера частиц от приблизительно 100 мкм до приблизительно 200 мкм.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют соединение, содержащее фосфор, нитратную соль, фосфорную кислоту и воду с образованием влажной смеси, при этом мольное соотношение фосфора и катионов, как в указанном соединении, содержащем фосфор, так и в указанной нитратной соли, составляет приблизительно 1, (b) прокаливают указанную влажную смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (с) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют MnPO4·qH2O, KNO3 и H3PO4, в мольном соотношении приблизительно 0,3:1:1, на безводной основе, и воду с получением влажной смеси, (b) прокаливают указанную влажную смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (с) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют Ca2P2O7, KNO3 и H3PO4, в мольном соотношении приблизительно 1,6:1:1, и воду с получением влажной смеси, (b) прокаливают указанную влажную смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (с) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют соединение, содержащее фосфор, нитратную соль, фосфорную кислоту и воду с получением влажной смеси, при этом мольное соотношение фосфора и катионов, как в соединении, содержащем фосфор, так и в нитратной соли, составляет приблизительно 1, (b) нагревают указанную влажную смесь до приблизительно 80°С при перемешивании почти до полного высушивания с образованием влажного твердого вещества, (с) прокаливают указанное влажное твердое вещество постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (d) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют Ba(NO3)2, K2HPO4 и H3PO4, в мольном соотношении приблизительно 3:1:4, и воду с получением влажной смеси, (b) нагревают указанную влажную смесь до приблизительно 80°С при перемешивании почти до полного высушивания с образованием влажного твердого вещества, (с) прокаливают указанное влажное твердое вещество постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (d) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют Mn(NO3)2·4H2O, K2HPO4 и H3PO4, в мольном соотношении приблизительно 1:1,5:2 и воду с получением влажной смеси, (b) нагревают указанную влажную смесь до приблизительно 80°С при перемешивании почти до полного высушивания с образованием влажного твердого вещества, (с) прокаливают указанное влажное твердое вещество постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (d) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют Ca2P2O7 и KH2PO4 в мольном соотношении приблизительно 3:1 с получением твердой смеси, и (b) прокаливают указанную твердую смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и при приблизительно от 450°С до приблизительно 550°С, с получением указанного катализатора.
После прокаливания и необязательного измельчения и просеивания, катализатор может быть использован для катализирования нескольких химических реакций. Неограничивающие примеры реакций представляют собой дегидратацию гидроксипропионовой кислоты в акриловую кислоту (как более подробно описано ниже), дегидратацию глицерина в акролеин, дегидратацию алифатических спиртов в алкены или олефины, дегидрогенизирование алифатических спиртов в эфиры, другие реакции дегидрогенизирования, гидролизы, алкилирования, деалкилирования, окисления, диспропорционирования, эстерификации, циклизации, изомеризации, конденсации, ароматизации, полимеризации, и другие реакции, которые могут быть очевидны специалистам в данной области техники.
IV. Способы получения акриловой кислоты, производных акриловой кислоты или их смесей
Представлен способ дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси. Способ включает стадию, на которой вводят в контакт поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, с катализатором, содержащим: (а) по меньшей мере, один анион конденсированного фосфата, который выбирают из группы, состоящей из формул (I), (II) и (III)
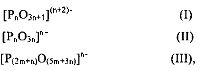
где n составляет, по меньшей мере, 2 и m составляет, по меньшей мере, 1, и (b) по меньшей мере, два различных катиона, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и, по меньшей мере, двух различных катионов составляет от приблизительно 0,7 до приблизительно 1,7, таким образом получая акриловую кислоту, производные акриловой кислоты или их смеси в результате контактирования указанного потока с катализатором.
Альтернативные катализаторы, содержащие анионы, выбранные из группы, состоящей из анионов, не содержащих фосфор, гетерополианионов и фосфатных аддуктов, и, по меньшей мере, два различных катиона, при этом катализатор, по существу, нейтрально заряжен, могут быть использованы для дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси. Неограничивающие примеры анионов, не содержащих фосфор, представляют собой арсенаты, конденсированные арсенаты, нитраты, сульфаты, ванадаты, ниобаты, танталаты, селенаты и другие, которые могут быть очевидны специалистам в данной области техники. Неограничивающие примеры гетерополианионов представляют собой гетерополифосфаты, такие как арсенатофосфаты, фосфоалюминаты, фосфобораты, фосфохроматы, фосфомолибдаты, фосфосиликаты, фосфосульфаты, фосфотангстаты и другие, которые могут быть очевидны специалистам в данной области техники. Неограничивающие примеры фосфатных аддуктов представляют собой аддукты фосфатных анионов с теллуровой кислотой, галиды, бораты, карбонаты, нитраты, сульфаты, хроматы, силикаты, оксалаты, их смеси, или другие, которые могут быть очевидными специалистам в данной области техники.
Гидроксипропионовая кислота может быть 3-гидроксипропионовой кислотой, 2-гидроксипропионовой кислотой (также называемой молочной кислотой) или их смесями. Производными гидроксипропионовой кислоты могут быть соли металлов или аммония гидроксипропионовой кислоты, алкильные сложные эфиры гидроксипропионовой кислоты, олигомеры гидроксипропионовой кислоты, циклические сложные диэфиры гидроксипропионовой кислоты, ангидрид гидроксипропионовой кислоты или их смесь. Неограничивающие примеры солей металлов гидроксипропионовой кислоты представляют собой натрий гидроксипропионат, калий гидроксипропионат и кальций гидроксипропионат. Неограничивающие примеры алкильных сложных эфиров гидроксипропионовой кислоты представляют собой метилгидроксипропионат, этилгидроксипропионат или их смеси. Неограничивающим примером циклических сложных диэфиров гидроксипропионовой кислоты является дилактид.
Производные акриловой кислоты могут быть солями металла или аммония акриловой кислоты, алкильными сложными эфирами акриловой кислоты, олигомерами акриловой кислоты или их смесями. Неограничивающие примеры солей металла акриловой кислоты представляют собой акрилат натрия, акрилат калия и акрилат кальция. Неограничивающие примеры алкильных сложных эфиров акриловой кислоты представляют собой метиллактат, этиллактат или их смеси.
Поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, может включать поток жидкости и инертный газ (т.е. газ в других случаях инертный к реакционной смеси в условиях способа), который может быть по отдельности или совместно подан в выпарной аппарат выше по потоку от реактора катализатора для того, чтобы поток стал газообразным. Поток жидкости может включать гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси и разбавитель. Неограничивающими примерами разбавителя являются вода, метанол, этанол, ацетон, С3-С8 линейные и разветвленные спирты, С5-С8 линейные и разветвленные алканы, этилацетат, нелетучие эфиры (в том числе дифениловый эфир) и их смеси. В одном осуществлении, разбавителем является вода. В определенных осуществлениях поток жидкости содержит водный раствор молочной кислоты или производных молочной кислоты, которые выбирают из группы, состоящей из лактида, олигомеров молочной кислоты, солей молочной кислоты и алкиллактатов. В одном осуществлении, поток жидкости содержит от приблизительно 2 мас. % до приблизительно 95 мас. % молочной кислоты или производных молочной кислоты, исходя из общей массы потока жидкости. В другом осуществлении, поток жидкости содержит от приблизительно 5 мас. % до приблизительно 50 мас. % молочной кислоты или производных молочной кислоты, исходя из общей массы потока жидкости. В другом осуществлении, поток жидкости содержит от приблизительно 10 мас. % до приблизительно 25 мас. % молочной кислоты или производных молочной кислоты, исходя из общей массы потока жидкости. В другом осуществлении, поток жидкости содержит приблизительно 20 мас. % молочной кислоты или производных молочной кислоты, исходя из общей массы потока жидкости. В другом осуществлении, поток жидкости содержит водный раствор молочной кислоты, а также производные молочной кислоты. В другом осуществлении, поток жидкости содержит менее, чем приблизительно 30 мас. % производных молочной кислоты, исходя из общей массы потока жидкости. В другом осуществлении, поток жидкости содержит менее, чем приблизительно 10 мас. % производных молочной кислоты, исходя из общей массы потока жидкости. В еще одном осуществлении, поток жидкости содержит менее, чем приблизительно 5 мас. % производных молочной кислоты, исходя из общей массы потока жидкости.
Инертный газ представляет собой газ, который в других случаях инертный по отношению к реакционной смеси в условиях способа. Неограничивающие примеры инертного газа представляют собой воздух, азот, гелий, аргон, диоксид углерода, монооксид углерода, пар и их смеси. В одном осуществлении, инертный газ представляет собой азот.
Поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, может находиться в виде газообразной смеси при контакте с катализатором. В одном осуществлении, концентрация гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, исходя из общего количества молей указанного потока (рассчитывается при условиях STP) составляет от приблизительно 0,5 мол.% до приблизительно 50 мол.%. В другом осуществлении, концентрация гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, исходя из общего количества молей указанного потока (рассчитывается при условиях STP) составляет от приблизительно 1 мол.% до приблизительно 10 мол.%. В другом осуществлении, концентрация гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, исходя из общего количества молей указанного потока (рассчитывается при условиях STP) составляет от приблизительно 1,5 мол.% до приблизительно 3,5 мол.%. В еще одном осуществлении, концентрация гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, исходя из общего количества молей указанного потока (рассчитывается при условиях STP) составляет приблизительно 2,5 мол.%. В одном осуществлении, температура, при которой указанный поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором, составляет от приблизительно 120°С до приблизительно 700°С. В другом осуществлении, температура, при которой указанный поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором, составляет от приблизительно 150°С до приблизительно 500°С. В другом осуществлении, температура, при которой указанный поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором, составляет от приблизительно 300°С до приблизительно 450°С. В еще одном осуществлении, температура, при которой указанный поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором, составляет от приблизительно 325°С до приблизительно 400°С. В одном осуществлении, поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором при GHSV от приблизительно 720 ч-1 до приблизительно 36000 ч-1. В другом осуществлении, поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором при GHSV от приблизительно 1800 ч-1 до приблизительно 7200 ч-1. В другом осуществлении, поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором при GHSV приблизительно 3600 ч-1.
В одном осуществлении, поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором при давлении от приблизительно 0 фунт./кв.дюйм изб. до приблизительно 550 фунт./кв.дюйм изб. В другом осуществлении, поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором при давлении приблизительно 360 фунт./кв.дюйм изб.
В одном осуществлении, поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором в реакторе, имеющем внутреннюю поверхность, содержащую материал, который выбирают из группы, состоящей из кварца, боросиликатного стекла, кремния, сплава Hastelloy, инконеля, искусственного сапфира, нержавеющей стали и их смесей. В другом осуществлении, поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором в реакторе, имеющем внутреннюю поверхность, содержащую материал, который выбирают из группы, состоящей из кварца или боросиликатного стекла. В другом осуществлении, поток, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, контактирует с катализатором в реакторе, имеющем внутреннюю поверхность, содержащую боросиликатное стекло.
В одном осуществлении, способ включает стадию, на которой вводят в контакт катализатор с газообразной смесью, содержащей гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, в условиях, достаточных для получения акриловой кислоты, производных акриловой кислоты или их смесей с выходом, по меньшей мере, 50%. В другом осуществлении, способ включает стадию, на которой вводят в контакт катализатор с газообразной смесью, содержащей гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, в условиях, достаточных для получения акриловой кислоты, производных акриловой кислоты или их смесей с выходом, по меньшей мере, приблизительно 70%. В другом осуществлении, способ включает стадию, на которой вводят в контакт катализатор с газообразной смесью, содержащей гидроксипропионовую кислоту, производные гидроксипропионовой кислоты, или их смеси, в условиях, достаточных для получения акриловой кислоты, производных акриловой кислоты или их смесей с выходом, по меньшей мере, приблизительно 80%. В другом осуществлении, условия способа достаточны для получения акриловой кислоты, производных акриловой кислоты или их смесей с селективностью, по меньшей мере, приблизительно 50%. В другом осуществлении, условия способа достаточны для получения акриловой кислоты, производных акриловой кислоты или их смесей с селективностью, по меньшей мере, приблизительно 70%. В другом осуществлении, условия способа достаточны для получения акриловой кислоты, производных акриловой кислоты или их смесей с селективностью, по меньшей мере, приблизительно 80%. В другом осуществлении, условия способа достаточны для получения акриловой кислоты, производных акриловой кислоты или их смесей с пропановой кислотой в качестве примеси, где селективность получения пропановой кислоты составляет менее, чем приблизительно 5%. В другом осуществлении, условия способа достаточны для получения акриловой кислоты, производных акриловой кислоты или их смесей с пропановой кислотой в качестве примеси, где селективность получения пропановой кислоты составляет менее, чем приблизительно 1%. В другом осуществлении, условия способа достаточны для получения акриловой кислоты, производных акриловой кислоты или их смесей с конверсией указанной гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей более, чем приблизительно 50%. В другом осуществлении, условия способа достаточны для получения акриловой кислоты, производных акриловой кислоты или их смесей с конверсией указанной гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей более, чем приблизительно 80%.
Среди преимуществ, присущих приведенным в данной заявке осуществлениям, является низкий выход побочных продуктов. В одном осуществлении, условия достаточны для получения пропановой кислоты с выходом менее, чем приблизительно 6% от молочной кислоты, присутствующей в газообразной смеси. В другом осуществлении, условия достаточны для получения пропановой кислоты с выходом менее, чем приблизительно 1% от молочной кислоты, присутствующей в газообразной смеси. В одном осуществлении, условия достаточны для получения каждого из уксусной кислоты, виноградной кислоты, 1,2-пропандиола и 2,3-пентандиола с выходом менее, чем приблизительно 2% от молочной кислоты, присутствующей в газообразном потоке. В другом осуществлении, условия достаточны для получения каждого из уксусной кислоты, виноградной кислоты, 1,2-пропандиола и 2,3-пентандиола с выходом менее, чем приблизительно 0,5% от молочной кислоты, присутствующей в газообразном потоке. В одном осуществлении, условия достаточны для получения ацетальдегида с выходом менее, чем приблизительно 8% от молочной кислоты, присутствующей в газообразной смеси. В другом осуществлении, условия достаточны для получения ацетальдегида с выходом менее, чем приблизительно 4% от молочной кислоты, присутствующей в газообразной смеси. В другом осуществлении, условия достаточны для получения ацетальдегида с выходом менее, чем приблизительно 3% от молочной кислоты, присутствующей в газообразной смеси. Эти выходы, как полагают, недостижимо низкие. Действительно, эти преимущества достижимы, как дополнительно свидетельствуют приведенные ниже Примеры.
Представлен способ дегидратации глицерина в акролеин. Способ включает стадию, на которой вводят в контакт поток, содержащий глицерин, с катализатором, содержащим: (а) по меньшей мере, один анион конденсированного фосфата, который выбирают из группы, состоящей из формул (I), (II) и (III)
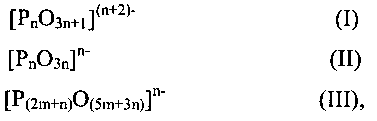
где n составляет, по меньшей мере, 2 и m составляет, по меньшей мере, I, и (b) по меньшей мере, два различных катиона, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и, по меньшей мере, двух различных катионов составляет от приблизительно 0,7 до приблизительно 1,7, таким образом получая акролеин в результате контактирования указанного глицерина с катализатором. Акролеин является промежуточным соединением, которое может быть преобразовано в акриловую кислоту с использованием условий, аналогичных используемым сегодня на второй стадии окисления в способе пропилена в акриловую кислоту.
V Примеры
Следующие примеры приведены для иллюстрации настоящего изобретения, но не предназначены для ограничения его объема. Примеры 1-7 описывают получение различных смешанных конденсированных фосфатных катализаторов в соответствии с различными осуществлениями, описанными выше. Примеры 8-12 описывают получение катализаторов не в соответствии с настоящим изобретением.
ПРИМЕР 1
Водный раствор нитрата бария, Ba(NO3)2 (85,36 мл 0,08 г/мл маточного раствора, 26 ммоль, 99,999%; Sigma - Aldrich Co., St. Louis, МО; каталог №202754), добавляли к твердому двухосновному фосфату калия, K2HPO4 (1,52 г, 8,7 ммоль, ≥98%; Sigma - Aldrich Co., St. Louis, МО; каталог № P 3786) при комнатной температуре. Фосфорную кислоту, H3PO4 (2,45 мл 85 мас. %, плотность = 1,684 г/мл, 36 ммоль; Acros Organics, Geel, Belgium; каталог №295700010), добавляли в суспензию, получая раствор, содержащий катионы калия (K+, MI) и бария (Ba2+, MII). Конечное значение pH суспензии составляло приблизительно 1,6. Суспензию, содержащую кислоту, затем медленно высушивали в стеклянном стакане при 80°С, используя нагревательную плиту с магнитным перемешиванием суспензии до испарения жидкости и почти полного высушивания материала. После выпаривания, материал переносили на разрушаемую керамику. Нагревание продолжали в печи с циркуляцией воздуха (N30/80 НА; Nabertherm GmbH, Lilienthal, Germany) при 50°C в течение 10 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), 120°С в течение 2 часов (0,5°С/мин линейное возрастание) для удаления остаточной воды с последующим прокаливанием при 450°С в течение 4 часов (2°С/мин линейное возрастание). После прокаливания материал оставляли внутри печи до самоохлаждения при температуре ниже 100°С перед тем, как вынуть его из печи. Наконец, катализатор измельчали и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм. Материал анализировали при помощи рентгеновской дифракции (XRD) и энергодисперсионной спектроскопии в сочетании со сканирующей электронной микроскопией (EDS/SEM), позволяя идентификацию σ-Ba2P2O7, α-Ba3P4O13, Ba(NO3)2 и KPO3 с некоторым включением K в Ba-содержащие фазы. Мольное соотношение фосфора (P) и катионов (MI и MII) в идентифицированных солях конденсированного фосфата составляло от приблизительно 1 до приблизительно 1,3.
ПРИМЕР 2
Твердый двухосновной фосфат калия, K2HPO4 (36,40 г, 209 ммоль, ≥98%; Sigma - Aldrich Co., St. Louis, МО; каталог № P 3786) быстро смешивали с водным раствором нитрата бария, Ba(NO3)2 (2050 мл 0,08 г/мл маточного раствора, 627 ммоль, 99,999%; Sigma - Aldrich Co., St. Louis, МО; каталог №202754) при комнатной температуре. Фосфорную кислоту, H3PO4 (58,7 мл 85 мас. %, плотность = 1,684 г/мл, 857 ммоль; Acros Organics, Geel, Belgium; каталог №295700010), добавляли в суспензию, получая раствор, содержащий катионы калия (K+, MI) и бария (Ba2+, MII). Конечное значение pH суспензии составляло приблизительно 1,6. Суспензию, содержащую кислоту, затем медленно высушивали в стеклянном стакане при 80°С, используя нагревательную плиту с магнитным перемешиванием суспензии до испарения жидкости и почти полного высушивания материала. Нагревание продолжали в печи с циркуляцией воздуха (G1530A, НР6890 GC; Agilent Corp., Santa Clara, CA) при 50°C в течение 5,3 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), с последующим охлаждением при 25°С. Материал прокаливали при 120°С в течение 2 часов (0,5°С/мин линейное возрастание) и еще при 450°С в течение 4 часов (2°С/мин линейное возрастание) в той же печи. После прокаливания, материал оставляли внутри печи до самоохлаждения при температуре ниже 25°С перед тем, как вынуть его из печи. Наконец, катализатор измельчали и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм. Материал анализировали при помощи XRD и EDS/SEM, позволяя идентификацию σ-Ba2P2O7, α-Ba3P4O13, Ba(NO3)2, KPO3 и некоторого аморфного материала с некоторым включением K в Ba-содержащих фазах. Мольное соотношение фосфора (P) и катионов (MI и MII) в идентифицированных солях конденсированного фосфата составляло от приблизительно 1 до приблизительно 1,3.
ПРИМЕР 3
Водный раствор нитрата калия, KNO3 (1,51 мл 1 г/мл маточного раствора, 14,9 ммоль, Sigma - Aldrich Co., St. Louis, МО; каталог №60415), добавляли к дифосфату кальция, Ca2P2O7 (5,93 г, 23,3 ммоль, Alfa Aesar, Ward Hill, MA; каталог №89836), при комнатной температуре. Фосфорную кислоту, H3PO4 (1,05 мл 85 мас. %, плотность = 1,684 г/мл, 15,3 ммоль, Acros Organics, Geel, Belgium; каталог №201140010), добавляли в суспензию, получая суспензию содержащую катионы калия (K+, MI) и кальция (Ca2+, MII). Материал нагревали в печи с циркуляцией воздуха (N30/80 НА; Nabertherm GmbH, Lilienthal, Germany) при 50°C в течение 2 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), 120°С в течение 2 часов (0,5°С/мин линейное возрастание) для удаления остаточной воды с последующим прокаливанием при 450°С в течение 4 часов (2°С/мин линейное возрастание). После прокаливания материал оставляли внутри печи до самоохлаждения при температуре ниже 100°С перед тем, как вынуть его из печи. Наконец, катализатор измельчали и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм. Материал анализировали при помощи XRD, позволяя идентификацию β-Ca2P2O7 и KPO3. Мольное соотношение фосфора (Р) и катионов (MI и MII) в этих солях конденсированного фосфата составляло приблизительно 1.
ПРИМЕР 4
Дифосфат кальция, Ca2P2O7 (5,93 г, 23,3 ммоль, Alfa Aesar, Ward Hill, MA; каталог №89836), и одноосновной монофосфат калия, KH2PO4 (1,08 г, 7,9 ммоль, Sigma-Aldrich Co., St. Louis, МО; каталог №60216), которые предварительно просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм, смешивали в стеклянной бутылке в раскаточной машине в течение 5 мин, получая твердую смесь содержащую катионы калия (K+, MI) и кальция (Са2+, MII). Материал нагревали в печи с циркуляцией воздуха (N30/80 НА; Nabertherm GmbH, Lilienthal, Germany) при 50°C в течение 2 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), 120°С в течение 2 часов (0,5°С/мин линейное возрастание) для удаления остаточной воды с последующим прокаливанием при 550°С в течение 4 часов (2°С/мин линейное возрастание). После прокаливания материал оставляли внутри печи до самоохлаждения при температуре ниже 100°С перед тем, как вынуть его из печи. Материал анализировали при помощи XRD, позволяя идентификацию β-Са2Р2О7 и KPO3. Мольное соотношение фосфора (Р) и катионов (MI и MII) в этих солях конденсированного фосфата составляло приблизительно 1.
ПРИМЕР 5
Водный раствор нитрата марганца(II), Mn(NO3)2·4H2O (14,25 мл 0,3 г/мл маточного раствора, 17,0 ммоль, Sigma-Aldrich Co., St. Louis, МО; каталог №63547), добавляли к двухосновному монофосфату калия, K2HPO4 (4,45 г, 25,5 ммоль, Sigma-Aldrich Co., St. Louis, МО; каталог №P3786), при комнатной температуре. Фосфорную кислоту, Н3РО4 (2,39 мл 85 мас. %, плотность = 1,684 г/мл, 34,9 ммоль, Acros Organics, Geel, Belgium; каталог №201140010), добавляли в суспензию, получая суспензию содержащую катионы калия (K+, MI) и марганца (Mn2+, MII). Материал нагревали в печи с циркуляцией воздуха (N30/80 НА; Nabertherm GmbH, Lilienthal, Germany) при 50°C в течение 2 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), 120°С в течение 2 часов (0,5°С/мин линейное возрастание) для удаления остаточной воды с последующим прокаливанием при 450°С в течение 4 часов (2°С/мин линейное возрастание). После прокаливания материал оставляли внутри печи до самоохлаждения при температуре ниже 100°С перед тем, как вынуть его из печи. Наконец, катализатор измельчали и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм. Материал анализировали при помощи XRD, позволяя идентификацию MnKP2O7 и KPO3; мольное соотношение фосфора (Р) и катионов (MI и MII) в этих солях конденсированного фосфата составляло приблизительно 1.
ПРИМЕР 6
Водный раствор нитрата калия, KNO3 (5,16 мл 1 г/мл маточного раствора, 51,1 ммоль, Sigma-Aldrich Co., St. Louis, МО; каталог №60415), добавляли к фосфату марганца(III), MnPO4·qH2O (2,58 г, 17,2 ммоль на безводной основе, Alfa Aesar, Ward Hill, MA; каталог №A17868), при комнатной температуре. Фосфорную кислоту, Н3РО4 (3,58 мл 85 мас. %, плотность = 1,684 г/мл, 52,4 ммоль, Acros Organics, Geel, Belgium; каталог №295700010), добавляли в суспензию, получая суспензию содержащую катионы калия (K+, MI) и марганца (Mn3+, MIII). Материал нагревали в печи с циркуляцией воздуха (N30/80 НА; Nabertherm GmbH, Lilienthal, Germany) при 50°C в течение 2 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), 120°С в течение 2 часов (0,5°С/мин линейное возрастание) для удаления остаточной воды с последующим прокаливанием при 550°С в течение 4 часов (2°С/мин линейное возрастание). После прокаливания, материал оставляли внутри печи до самоохлаждения при температуре ниже 100°С перед тем, как вынуть его из печи. Наконец, катализатор измельчали и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм. Материал анализировали при помощи XRD, позволяя идентификацию MnKP2O7 и KPO3. Мольное соотношение фосфора (Р) и катионов (MI и MII) в этих солях конденсированного фосфата составляло приблизительно 1.
ПРИМЕР 7
Получение Ва3(PO4)2: Фосфат натрия, Na3PO4 (85,68 г, 523 ммоль, Sigma-Aldrich Co., St. Louis, МО; каталог №342483), растворяли в 580 мл деионизированной воды и рН доводили до 7 концентрированным гидроксидом аммония. Нитрат бария, Ba(NO3)2 (121,07 г, 463 ммоль, Sigma-Aldrich Co., St. Louis, МО; каталог №202754), растворяли в 1220 мл деионизированной воды. Раствор Ba(NO)3)2 добавляли по каплям к раствору Na3PO4 при перемешивании и нагревании до 60°С, образуя белую суспензию во время добавления. Значение рН постоянно мониторили и концентрированный гидроксид аммония добавляли по каплям для поддержания рН 7. Нагревание и перемешивание при 60°С продолжали в течение 60 мин, в это время твердое вещество фильтровали и тщательно промывали деионизированной водой. Твердое вещество суспендировали в 2 л деионизированной воды и снова фильтровали и тщательно промывали деионизированной водой. В печи с вентиляцией, осадок на фильтре высушивали при 120°С в течение 5 часов (1°С/мин линейное возрастание), с последующим прокаливанием при 350°С в течение 4 часов(2°С/мин линейное возрастание) с получение Ba3(PO4)2 в виде белого твердого вещества.
Получение катализатора: Водный раствор нитрата калия, KNO3 (0,68 мл 1 г/мл маточного раствора, 6,8 ммоль, Sigma - Aldrich Co., St. Louis, МО; каталог №60415), добавляли к фосфату бария, Ba3(PO4)2 (4,07 г, 6,8 ммоль) как получено выше, при комнатной температуре. Гидроксид фосфат меди(II), Cu2(ОН)PO4 (3,23 г, 13,5 ммоль, Sigma - Aldrich Co., St. Louis, МО; каталог №344400), и фосфорную кислоту, H3PO4 (0,47 мл 85 мас. %, плотность = 1,684 г/мл, 6,9 ммоль, Acros Organics, Geel, Belgium; каталог №201140010), добавляли к суспензии, получая суспензию, содержащую катионы калия (K+, MI), бария (Ba2+, MII) и меди (Cu2+, MII). Материал нагревали в печи с циркуляцией воздуха (N30/80 НА; Nabertherm GmbH, Lilienthal, Germany) при 50°C в течение 2 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), 120°С в течение 2 часов (0,5°С/мин линейное возрастание) для удаления остаточной воды с последующим прокаливанием при 550°С в течение 4 часов (2°С/мин линейное возрастание). После прокаливания материал оставляли внутри печи до самоохлаждения при температуре ниже 100°С перед тем, как вынуть его из печи. Материал анализировали при помощи XRD, позволяя идентификацию α-Ba2P2O7, KPO3 и некоторого аморфного материала; мольное соотношение фосфора (P) и катионов (MI и MII) в этих солях конденсированного фосфата составляло приблизительно 1.
ПРИМЕР 8 (сравнительный)
Смешанный конденсированный фосфатный катализатор получали и использовали для целей сравнения. Водный раствор нитрата бария, Ba(NO3)2 (88,39 мл 0,08 г/мл маточного раствора, 27 ммоль, 99,999%; Sigma - Aldrich Co., St. Louis, МО; каталог №202754), добавляли к твердому двухосновному фосфату калия, K2HPO4 (1,57 г, 9,0 ммоль, ≥98%; Sigma - Aldrich Co., St. Louis, МО; каталог №P3786), при комнатной температуре. Фосфорную кислоту, H3PO4 (1,27 мл 85 мас. %, плотность = 1,684 г/мл, 19 ммоль; Acros Organics, Geel, Belgium; каталог №295700010), добавляли в суспензию, получая суспензию содержащую катионы калия (K+, MI) и бария (Ba2+, MII), так, что мольное соотношение фосфора (P) и катионов (MI и MII) составляло приблизительно 0,6. Суспензию, содержащую кислоту, затем медленно высушивали в стеклянном стакане при 80°С, используя нагревательную плиту при перемешивании суспензии до испарения жидкости и почти полного высушивания материала. После выпаривания, материал переносили на разрушаемую керамику. Нагревание продолжали в печи с циркуляцией воздуха (N30/80 НА; Nabertherm GmbH, Lilienthal, Germany) при 50°C в течение 2 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), 120°С в течение 2 часов (0,5°С/мин линейное возрастание) для удаления остаточной воды с последующим прокаливанием при 450°С в течение 4 часов (2°С/мин линейное возрастание). После прокаливания материал оставляли внутри печи до самоохлаждения при температуре ниже 100°С перед тем, как вынуть его из печи. Наконец, катализатор измельчали и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм.
ПРИМЕР 9 (сравнительный)
Смешанный конденсированный фосфатный катализатор получали и использовали для целей сравнения. Водный раствор нитрата бария, Ba(NO3)2 (88,39 мл 0,08 г/мл маточного раствора, 27 ммоль, 99,999%; Sigma - Aldrich Co., St Louis, МО; каталог №202754), добавляли к твердому двухосновному фосфату калия, K2HPO4 (1,57 г, 9,0 ммоль, ≥98%; Sigma - Aldrich Co., St Louis, МО; каталог № P 3786) при комнатной температуре. Фосфорную кислоту, H3PO4 (5,06 мл 85 мас. %, плотность = 1,684 г/мл, 74 ммоль; Acros Organics, Geel, Belgium; каталог №295700010), добавляли в суспензию, получая раствор, содержащий катионы калия (K+, MI) и бария (Ba2+, MII), так что мольное соотношение фосфора (P) и катионов (MI и MII) составляло приблизительно 1,8. Раствор, содержащий кислоту, затем медленно высушивали в стеклянном стакане при 80°С, используя нагревательную плиту при перемешивании суспензии до испарения жидкости и почти полного высушивания материала. После выпаривания, материал переносили на разрушаемую керамику. Нагревание продолжали в печи с циркуляцией воздуха (N30/80 НА; Nabertherm GmbH, Lilienthal, Germany) при 50°C в течение 2 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), 120°С в течение 2 часов (0,5°С/мин линейное возрастание) для удаления остаточной воды с последующим прокаливанием при 450°С в течение 4 часов (2°С/мин линейное возрастание). После прокаливания материал оставляли внутри печи до самоохлаждения при температуре ниже 100°С перед тем, как вынуть его из печи. Наконец, катализатор измельчали и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм.
ПРИМЕР 10 (сравнительный)
Барий монофосфатный катализатор, не в соответствии с настоящим изобретением, получали и использовали для целей сравнения. Кислый фосфат аммония, (NH4)2HPO4 (142,20 г, 1,08 моль; Aldrich, St Louis, МО; каталог №215996), растворяли в 1 л деионизированной воды. Водный гидроксид аммония, NH4OH (290 мл, 28-29%; EMD, Merck KGaA, Darmstadt, Germany; каталог № AX 1303) добавляли медленно и осторожно нагревали до растворения с образованием раствора фосфата аммония. В отдельном стакане, ацетат бария, (CH3COO)2Ba (285,43 г, 1,12 моль, Aldrich, St Louis, МО; каталог №243671), растворяли в 1 л деионизированной воды с образованием раствора ацетата бария. Раствор ацетата бария медленно добавляли к раствору фосфата аммония с образованием белого осадка. После перемешивания в течение 45 мин, белое твердое вещество фильтровали. Твердое вещество затем повторно суспендировали в 300 мл деионизированной воды, перемешивали в течение 10 мин, и снова фильтровали. Данный процесс повторяли дважды. Полученное в результате белое твердое вещество высушивали в печи с вентиляцией при 130°С всю ночь. Твердое вещество просеивали до размера от приблизительно 500 мкм до 710 мкм и прокаливали в кальцинаторе при 500°С в течение 4 часов (100°С/ч линейное возрастание). После прокаливания пробу катализатора просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм. Материал анализировали при помощи XRD, позволяя идентификацию Ba3(PO4)2.
ПРИМЕР 11 (сравнительный)
Барий дифосфатный катализатор, не в соответствии с настоящим изобретением, получали и использовали для целей сравнения. Пробу двухосновного фосфата бария, BaHPO4 (Sigma - Aldrich Co., St. Louis, МО; каталог №31139), прокаливали при 550°C в течение 12 ч, используя керамический тигель и линейное возрастание температуры 2°С/мин в термостате с гравитационной конвекцией. После прокаливания катализатор измельчали при помощи ступки и пестика и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм. Материал анализировали при помощи XRD, позволяя идентификацию α-Ba2P2O7.
ПРИМЕР 12 (сравнительный)
Барий тетрафосфатный катализатор, не в соответствии с настоящим изобретением, получали и использовали для целей сравнения. Двухосновной барий монофосфат, BaHPO4 (23,52 г, 100,8 ммоль, Sigma - Aldrich Co., St Louis, МО; каталог №31139) и двухосновной монофосфат аммония, (NH4)2HPO4 (4,44 г, 33,6 ммоль, Sigma - Aldrich Co., St. Louis, MO; каталог №379980) смешивали и измельчали совместно при помощи ступки и пестика. Твердое вещество затем прокаливали при 300°С в течение 14 ч, используя линейное возрастание температуры 2°С/мин в термостате с гравитационной конвекцией. После прокаливания катализатор измельчали снова при помощи ступки и пестика, с последующим прокаливанием при 500°С в течение 14 ч при помощи того же самого линейного возрастания температуры и печи, как ранее. Наконец, дополнительный раунд измельчения и прокаливания проводили при 750°С в течение 14 ч. Катализатор просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм. Материал анализировали при помощи XRD, позволяя идентификацию α-Ba3P4O13.
ПРИМЕР 13
Эксперимент проводили для определения активности катализатора в соответствии с настоящим изобретением. Конкретно, катализатор получали как описано в Примере 1 в течение 21,6 часов времени реакции в условиях, изложенных в разделе VI. Результаты приведены в таблице 2, ниже, где выход и селективность получения акриловой кислоты скорректированы на ТМВ.
VI Тестовые процедуры
XRD: Широкоугольные данные (WAXS) получали в дифрактометре STADI-P в режиме пропускания (Stoe & Cie GmbH, Darmstadt, Germany). Генератор работал при 40 кВ/40 мА, приводя в движение медную анодную с длинной тонкой фокусировкой Cu рентгеновскую трубку. Дифрактометр включает падающего пучка изогнутый монохроматор на кристалле германия, стандартную падающего пучка щелевую систему и чувствительный к положению сигнальной пластины детектор с угловым диапазоном приблизительно 124° 2θ. Данные получали в режиме пропускания. Пробы осторожно измельчали вручную с использованием ступки и пестика до тонкодисперсной консистенции, если возможно, перед загрузкой в стандартный держатель для проб для устройства. Кристаллические фазы идентифицировали с использованием наиболее современной базы данных порошковой дифракции (от ICDD) с использованием рутинных процедур Search/Match в Jade (Materials Data, Inc. v 9.4.2).
SEM/EDS: Сухие порошки диспергировали на двухстороннюю медную или угольную ленту, смонтированную на металлическую подложку электронного сканирующего микроскопа (SEM). Каждый образец покрывали Au/Pd в течение приблизительно 65-80 с, используя Gatan Alto 2500 Cryo камеру подготовки. SEM картирование формирования изображения и энергодисперсионной спектроскопии (EDS) производили с использованием либо Hitachi S-4700 FE-SEM или Hitachi S-5200 в линзах FE-SEM (Hitachi Ltd., Tokyo, Japan), оба оснащены EDS с Bruker XFlash 30 мм2 SDD детекторами (Quantax 2000 система с 5030 детектором; Bruker Corp., Billerica, MA). EDS картирование выполняли с использованием ускоряющего напряжения при 10 кВ в Методе аназиза зондового тока. Все карты генерировали при помощи программного обеспечения Bruker Esprit V 1.9 в Hypermap модуле.
Реактор - система А (0,2 мл масштабный реактор): Некоторые из данных конверсий проводили в системе текучего реактора с максимумом объема слоя катализатора приблизительно 0,2 мл. Система содержала регуляторы температур и потока масс и поставлялась с отдельными системами подачи жидкости и газа, которые смешивали перед достижением слоя катализатора. Система подачи газа состояла из молекулярного азота (N2) и гелия (He), которые добавляли как внутренний стандарт для анализа при помощи газового хроматографа (GC). Система подачи жидкости представляла собой водный раствор молочной кислоты (20 мас. % L-молочной кислоты) и ее подавали в верхнюю часть реактора, контролируя давление насоса до приблизительно 360 фунт./кв.дюйм изб. для преодоления какого-либо падения давления из слоя катализатора. Использовали реакторы из кварца или нержавеющей стали с аспектным соотношением (т.е. длина/диаметр) 75.
Были использованы различные слои катализатора и системы подачи газовых потоков, приводя к диапазону объемных скоростей (сообщается в разделе Результаты в данной заявке). Выходящий из реактора поток был также подключен к другой линии разбавления азота, которая разбавляла выходящий поток с коэффициентом два. Внутренний стандарт гелия нормализовал любые изменения в этом разбавлении для аналитических целей. Конденсированные продукты собирали с помощью системы отбора проб жидкости, охлажденной до температуры от 6,5°С до 10°С, в то время как газообразные продукты накапливали в воздушной прослойке виалы сбора. Накопленные в прослойке газообразные продукты анализировали с помощью клапанов отбора проб и онлайн газовой хроматографии (GC).
Систему подачи приводили в равновесие в течение 1 часа, после этого жидкую пробу отбирали в течение 2,7 часа и анализировали в конце эксперимента при помощи офлайн ВЭЖХ. В течение этого времени, газообразные продукты анализировали онлайн дважды при помощи GC и сообщали среднее значение. Жидкие продукты анализировали при помощи высокоэффективной жидкостной хроматографии (ВЭЖХ) на приборе Agilent 1200 Series (Agilent Technologies, Santa Clara, CA), Supelcogel-H колонка (4,6×250 мм; Supelco, St. Louis, МО), и диодно-матричного детектора и детектора с коэффициентом преломления (RI). Аналиты элюировали изократически, используя 0,005 М H2SO4 (водн.) как элюирующий буфер, в течение периода 30 мин и при потоке 0,2 мл/мин. Температуры колонки и RI детектора устанавливали на 30°С. Газообразные продукты анализировали при помощи системы газовой хроматографии Interscience Compact (GC) (Interscience BV, Breda, Netherlands) используя три детектора (один пламенно-ионизационный детектор - FID - и два термопроводящих - TCD - детектора «А» и «В», которые в данной заявке называются «TCD-А» и «TCD-В», соответственно). Газообразные продукты сообщали как среднее значение, данное двумя последовательными GC хроматограммами.
Колонка TCD-А была Rt-Q Bond (Restek Corp., Bellefonte, PA), имела 26 м в длину и I.D. 0,32 мм с толщиной пленки 10 мкм и использовали пре-колонку 2 м. Давление устанавливали на 150 кПа, расщепление потока 10 мл/мин. Температуру печи колонки устанавливали на 100°С с температурой желоба печи 50°С. Поток устанавливали на 5,0 мл/мин, газ-носитель - гелий. TCD-В колонка была Mol sieve MS5A (Restek Corp., Bellefonte, PA), имела длину 21 м и толщину пленки 10 мкм и использовали пре-колонку 2 м. Давление устанавливали на 200 кПа, расщепление потока 10 мл/мин. Температуру печи колонки устанавливали на 70°С с температурой желоба печи 50°С. Поток устанавливали на 2,0 мл/мин, газ-носитель - аргон. FID колонка была RTx-624 (Restek, Bellefonte, PA), имела длину 28 м и внутренний диаметр 0,25 мм с толщиной пленки 14 мм и использовали пре-колонку 2 м. Давление устанавливали на 100 кПа, расщепление потока 20 мл/мин. Температуру печи колонки устанавливали на 45°С с температурой желоба печи 50°С.
Реактор - система В (1,6 мл масштабный реактор): Некоторые из данных конверсии проводили в системе проточного реактора с уплотненным слоем с объемом слоя катализатора приблизительно 1,6 мл. Трубку длиной 13 дюймов (330 мм) из нержавеющей стали и оклеенную стеклом (SGE Analytical Science Pty Ltd., Ringwood, Australia) с 4,0 мм внутренним диаметром (ID) набивали стекловолокном (3 дюйма/76 мм длина слоя), с катализатором наверху (1,6 см3 объем слоя, 5 дюймов/127 мм длина слоя) с получением 2,55 см3 уплотненного слоя (8 дюймов/203 мм) и 1,6 см3 (5 дюймов/127 мм) свободного пространства в верхней части реактора. Трубку помещали внутрь алюминиевого блока и помещали в печь из глинистого железняка серия 3210 (Applied Test Systems, Butler, PA) таким образом, что верх уплотненного слоя выравнивали по верхней части алюминиевого блока. Реактор устанавливали в режим нисходящего потока и оснащали Knauer Smartline 100 насосом подачи (Berlin, Germany), Brooks 0254 регулятором газового потока (Hatfield, PA), Brooks регулятором давления всасывания и улавливающим резервуаром. Печь из глинистого железняка нагревали таким образом, что температуру стенок реактора поддерживали постоянной при приблизительно 350°С во время течения реакции. Реактор поставлялся отдельными системами подачи жидкости и газа, которые смешивались вместе перед достижением слоя катализатора. Система подачи газа состояла из молекулярного азота (N2) при приблизительно 360 фунт./кв.дюйм изб. при потоке 45 мл/мин. Система подачи жидкости представляла собой водный раствор молочной кислоты (20 мас. % L-молочной кислоты) и подана при 0,045 мл/мин (1,7 ч-1 LHSV), что дает время пребывания приблизительно 1 с (3600 ч-1 GHSV) в условиях STP. После протекания через реактор, газообразный поток охлаждали и жидкости собирали в улавливающий резервуар для анализа при помощи офлайн ВЭЖХ, используя систему Agilent 1100 (Santa Clara, СА), оснащенную диодно-матричным детектором (DAD) и колонкой Waters Atlantis Т3 (Каталог №186003748; Milford, MA) с использованием способов, известных специалистам в данной области техники. Газообразный поток анализировали онлайн при помощи GC, используя систему Agilent 7890 (Santa Clara, СА), оснащенную детектором FID и колонкой Varian CP-Para Bond Q (Каталог № CP 7351; Santa Clara, СА).
Система подачи реактора: раствор (113,6 г) полученной из биомассы молочной кислоты (88 мас. %, Purac Corp., Lincolnshire, IL) растворяли в дистиллированной воде (386,4 г) с получением раствора с ожидаемой концентрацией молочной кислоты 20 мас. %. Данный раствор нагревали при температуре от 95°С до 100°С в течение 12-30 часов. Полученную в результате смесь охлаждали и анализировали при помощи ВЭЖХ (описана выше) по сравнению с известными весовыми стандартами.
VII Результаты
В Таблице 1 ниже приведены параметры реакций с каждым катализатором, которые проводили в газовой фазе. Когда использовали 0,2 мл масштабный реактор, сообщенные выходы определяли через 222 мин (3 часа и 42 мин) времени реакции и использовали кварцевые реакторы, которые работали при 350°С. Когда использовали 1,6 мл масштабный реактор, использовали реактор из нержавеющей стали, покрытый с внутренней стороны эмалью, и сообщенные выходы определяли через от приблизительно 150 мин до приблизительно 650 мин. GHSV были следующими: 3490 ч-1 в Примере 1; 3535 ч-1 в Примерах 2, 10, 11 и 12; 3414 ч-1 в Примерах 3, 4 и 7; 3566 ч-1 в Примерах 5 и 6; и 3379 ч-1 в Примерах 8 и 9. В таблице, «N.D.» означает, что значение не было определено.
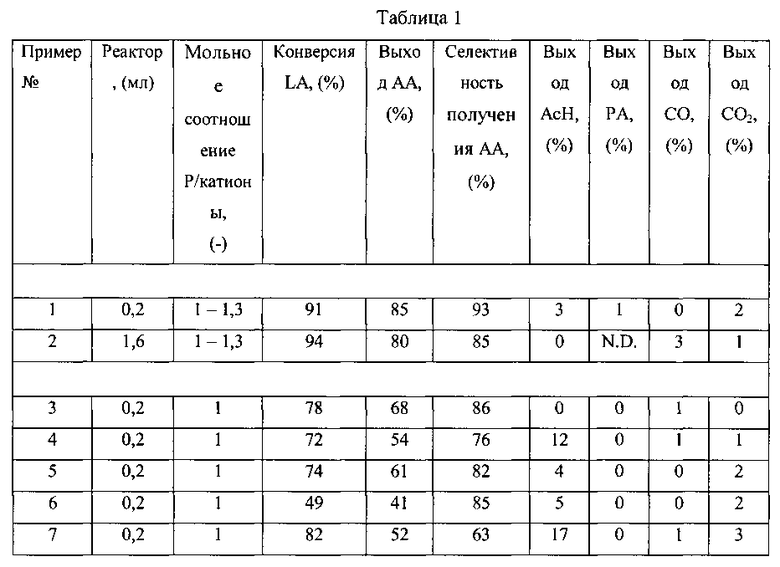
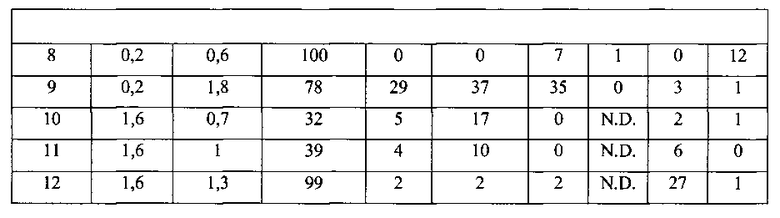
Результаты в Таблице 1 обеспечивают удобное сравнение конверсии молочной кислоты в акриловую кислоту с использованием катализаторов в соответствии с настоящим изобретением (т.е. Примеры 1-7) и не в соответствии с настоящим изобретением (т.е. Примеры 8-12). Среди прочего, в таких же или аналогичных условиях реакции, катализаторы в соответствии с настоящим изобретением приводят к значительно большей селективности для акриловой кислоты и значительно более низкой селективности для пропионовой кислоты, чем катализаторы не в соответствии с настоящим изобретением. Катализаторы в Примерах 8 и 9 имели более низкие селективности по сравнению с катализаторами в соответствии с настоящим изобретением, что демонстрирует, что присутствие определенных фосфатных анионов имеет важное значение для высокой селективности получения акриловой кислоты. Катализаторы в Примерах 10, 11 и 12 имели более низкую селективность, чем катализаторы в соответствии с настоящим изобретением, что демонстрирует, что присутствие двух различных металлов имеет важное значение для высокой селективности получения акриловой кислоты. Дополнительно, более низкие мольные соотношения фосфора (Р) и металлов (т.е. сравнительный Пример 8) способствуют декарбоксилированию (образование СО2), в то время как более высокие мольные соотношения (т.е. сравнительные Примеры 9 и 12), кажутся предпочтительными для декарбонилирования (образование СО).
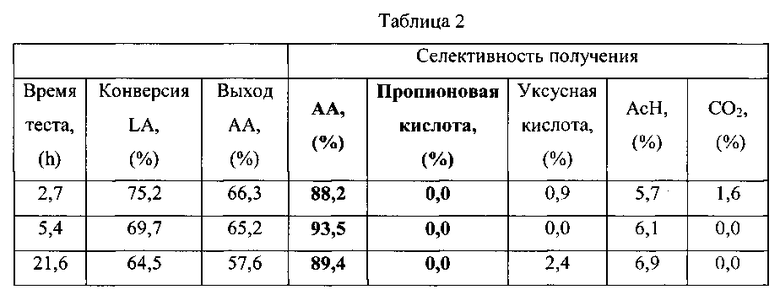
Результаты в Таблице 2 показывают, что катализатор стабилен в течение, по меньшей мере, 21,6 часа постольку поскольку катализатор, со временем, не кажется значительно или вредным образом измененным относительно выхода и селективности получения акриловой кислоты и аналогично не кажется вредным относительно селективности для нежелательных побочных продуктов, таких как пропионовая кислота, уксусная кислота, ацетальдегид и диоксид углерода.
Приведенное выше описание дано только для ясности понимания, и никаких ненужных ограничений не должно быть истолковано из него, так как модификации в объеме настоящего изобретения могут быть очевидными специалистам в данной области техники.
Размеры и значения, описанные в данной заявке, не следует понимать как строго ограниченные в точности приведенными численными значениями. Вместо этого, если не указано иное, каждый такой размер должен обозначать как приведенное значение, так и функционально эквивалентный диапазон, окружающий это значение. Например, размер, раскрытый как «40 мм» означает «приблизительно 40 мм».
Каждый документ, цитируемый в данной заявке, включая любые перекрестные ссылки или родственные патенты или заявки, настоящим включен в данную заявку путем ссылки во всей своей полноте, если специально не исключен или иным образом не ограничен. Цитирование любого документа не является признанием, что он является уровнем техники по отношению к любому изобретению, раскрытому или заявленному в данной заявке, или что только он, или в любой комбинации с любой другой ссылкой или ссылками, учит, предполагает или раскрывает любое такое изобретение. Кроме того, в той степени, в которой любое значение или определение термина в данной заявке противоречит любому значению или определению этого же термина в документе, включенном путем ссылки, значение или определение для этого термина в данной заявке превалирует.
В то время как конкретные осуществления настоящего изобретения были проиллюстрированы и описаны, специалистам в данной области техники будет очевидно, что различные другие изменения и модификации могут быть выполнены без отступления от сущности и объема настоящего изобретения. Поэтому прилагаемая формула изобретения предназначена для охвата всех таких изменений и модификаций, которые находятся в пределах объема настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИТИЧЕСКАЯ КОНВЕРСИЯ ГИДРОКСИПРОПИОНОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ В АКРИЛОВУЮ КИСЛОТУ И ЕЕ ПРОИЗВОДНЫЕ | 2013 |
|
RU2586327C2 |
| КАТАЛИЗАТОРЫ ДЛЯ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ | 2013 |
|
RU2586329C2 |
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ | 2013 |
|
RU2605206C2 |
| Катализатор для получения акриловой кислоты и ее производных на основе биологического сырья и способ его получения | 2014 |
|
RU2662229C2 |
| Полиакриловая кислота на основе полученной из биологического сырья акриловой кислоты и ее производных | 2013 |
|
RU2606124C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ | 2013 |
|
RU2587494C2 |
| ОЧИСТКА АКРИЛОВОЙ КИСЛОТЫ, ПОЛУЧЕННОЙ ИЗ БИОЛОГИЧЕСКОГО СЫРЬЯ, С ПОЛУЧЕНИЕМ СЫРОЙ И ЛЕДЯНОЙ АКРИЛОВОЙ КИСЛОТЫ | 2013 |
|
RU2599640C2 |
| Катализаторы для дегидратации гидроксипропионовой кислоты и ее производных | 2016 |
|
RU2694897C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ ИЗ ГИДРОКСИПРОПИОНОВОЙ КИСЛОТЫ | 2017 |
|
RU2719485C1 |
| КАТАЛИТИЧЕСКАЯ КОНВЕРСИЯ МОЛОЧНОЙ КИСЛОТЫ В АКРИЛОВУЮ КИСЛОТУ | 2013 |
|
RU2598380C2 |
Представлены катализаторы для дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси с высоким выходом и селективностью, коротким временем пребывания и без значительной конверсии в нежелательные побочные продукты, такие как, например, ацетальдегид, пропионовая кислота и уксусная кислота. Катализаторы представляют собой смешанные конденсированные фосфаты, содержащие (a) по меньшей мере один анион конденсированного фосфата формулы (I)

где n составляет по меньшей мере 2, и (b) по меньшей мере два различных катиона. При этом катализатор, по существу, нейтрально заряжен, и мольное соотношение фосфора и указанных по меньшей мере двух различных катионов составляет от 0,7 до 1,7. Катионы включают: (i) по меньшей мере, один одновалентный катион; и (ii) по меньшей мере один многовалентный катион, причем многовалентный катион выбран из группы, состоящей из Be2+, Mg2+, Са2+, Sr2+, Ва2+, Mn2+, Со2+, Ni2+, Cu2+, Zn2+, Cd2+, Sn2+, Pb2+, Ti3+, Cr3+, Mn3+, Al3+, Ga3+, Y3+, In3+, Sb3+, Bi3+, Si4+, Ti4+, V4+, Ge4+, Mo4+, Pt4+, V5+, Nb5+, Sb5+ и их смесей. Также представлены способы получения катализаторов. Первый способ включает стадии, на которых смешивают и нагревают по меньшей мере два различных соединения, содержащих фосфор, при этом каждое указанное соединение описывается одной из формул (IV) и (XV), или любой из гидратированных форм указанных формул


где MI представляет собой одновалентный катион; где MII представляет собой двухвалентный катион; где у означает 0, 1, 2 или 3; где v означает 0, 1 или 2. Второй способ включает стадии, на которых смешивают и нагревают (а) по меньшей мере одно соединение, содержащее фосфор, при этом каждое указанное соединение описывается одной из формул (IV)-(VI) и (XV), или любой из гидратированных форм указанных формул




где MI представляет собой одновалентный катион; где MII представляет собой двухвалентный катион; где MIII представляет собой трехвалентный катион; где у означает 0, 1, 2 или 3; где v означает 0, 1 или 2; и (b) по меньшей мере одно соединение, не содержащее фосфор, выбранное из группы, состоящей из нитратных солей, при этом каждое указанное соединение описывается одной из формул (XXVI)-(XXVII), или любой из гидратированных форм указанных формул


Третий способ включает стадии, на которых (a) объединяют Ca2P2O7 и KH2PO4 в мольном соотношении 3:1 с образованием твердой смеси, и (b) прокаливают указанную твердую смесь постадийно при 50°С, 80°С, 120°С и при от 450°С до 550°С, с получением указанного катализатора. 4 н. и 20 з.п. ф-лы, 2 табл., 13 пр.
1. Катализатор для конверсии гидроксипропионовой кислоты или ее производных в акриловую кислоту или ее производные, содержащий:
(a) по меньшей мере один анион конденсированного фосфата формулы (I)

где n составляет по меньшей мере 2, и
(b) по меньшей мере два различных катиона,
при этом катализатор, по существу, нейтрально заряжен, и дополнительно при этом мольное соотношение фосфора и указанных по меньшей мере двух различных катионов составляет от 0,7 до 1,7,
причем катионы включают:
(i) по меньшей мере один одновалентный катион; и
(ii) по меньшей мере один многовалентный катион, причем многовалентный
катион выбран из группы, состоящей из Be2+, Mg2+, Са2+, Sr2+, Ва2+, Mn2+, Со2+, Ni2+, Cu2+, Zn2+, Cd2+, Sn2+, Pb2+, Ti3+, Cr3+, Mn3+, Al3+, Ga3+, Y3+, In3+, Sb3+, Bi3+, Si4+, Ti4+, V4+, Ge4+, Mo4+, Pt4+, V5+, Nb5+, Sb5+ и их смесей.
2. Катализатор по п. 1, отличающийся тем, что указанный одновалентный катион выбран из группы, состоящей из Н+, Li+, Na+, K+, Rb+, Cs+ и их смесей.
3. Катализатор по п. 1, отличающийся тем, что указанный катализатор содержит:
(a) Ba2-x-sK2xH2sP2O7, или Са2-x-sK2xH2sP2O7, или Mn1-x-sK1+3xH3sP2O7, или Mn1-x-sK2+2xH2sP2O7; и
(b) (KPO3)n;
где x и s превышают или равны 0 и менее чем 0,5 и n представляет собой положительное целое число.
4. Катализатор по п. 1, отличающийся тем, что мольное соотношение фосфора и катионов в указанном катализаторе составляет от 0,8 до 1,3.
5. Катализатор по п. 1, отличающийся тем, что мольное соотношение фосфора и катионов в указанном катализаторе составляет 1.
6. Катализатор по п. 1, отличающийся тем, что указанные катионы включают:
(i) Н+, Li+, Na+, K+, Rb+, Cs+ или их смеси; и
(ii) Ве2+, Mg2+, Са2+, Sr2+, Ва2+, Mn2+, Со2+, Ni2+, Cu2+, Zn2+, Cd2+, Sn2+, Pb2+, Ti3+, Cr3+, Mn3+, Al3+, Ga3+, Y3+, In3+, Sb3+, Bi3+, Si4+, Ti4+, V4+, Ge4+, Mo4+, Pt4+, V5+, Nb5+, Sb5+ или их смеси.
7. Катализатор по n. 1, отличающийся тем, что указанный катализатор включает инертный носитель, который выполнен из материала, содержащего силикаты, алюминаты, уголь, оксиды металлов и их смеси.
8. Способ получения катализатора по п. 1, включающий стадии, на которых смешивают и нагревают по меньшей мере два различных соединения, содержащие фосфор, при этом каждое указанное соединение описывается одной из формул (IV) и (XV), или любой из гидратированных форм указанных формул


где MI представляет собой одновалентный катион; где MII представляет собой двухвалентный катион; где у означает 0, 1, 2 или 3; где v означает 0, 1 или 2.
9. Способ по п. 8, отличающийся тем, что мольное соотношение фосфора и катионов в указанном катализаторе составляет 1.
10. Способ по п. 8, отличающийся тем, что указанный катализатор прокаливают при температуре от 200°С до 1200°С.
11. Способ по п. 8, отличающийся тем, что указанные соединения, содержащие фосфор, включают соединение, содержащее фосфор, формулы (IV), где у равен 1, и соединение, содержащее фосфор, формулы (XV), где v равен 2.
12. Способ по п. 11, отличающийся тем, что указанные соединения, содержащие фосфор, включают:
(a) KH2PO4; и
(b) Ba2P2O7 или Ca2P2O7.
13. Способ по п. 8, отличающийся тем, что дополнительно включает стадию, на которой смешивают инертный носитель с указанными соединениями, содержащими фосфор, до, во время или после указанного смешивания и нагревания соединений, содержащих фосфор, при этом указанный инертный носитель содержит силикаты, алюминаты, уголь, оксиды металлов и их смеси.
14. Способ получения катализатора по п. 1, включающий стадии, на которых смешивают и нагревают:
(а) по меньшей мере одно соединение, содержащее фосфор, при этом каждое указанное соединение описывается одной из формул (IV)-(VI) и (XV), или любой из гидратированных форм указанных формул:




где MI представляет собой одновалентный катион; где MII представляет собой двухвалентный катион; где MIII представляет собой трехвалентный катион; где у означает 0, 1, 2 или 3; где v означает 0, 1 или 2; и
(b) по меньшей мере одно соединение, не содержащее фосфор, выбранное из группы, состоящей из нитратных солей, при этом каждое указанное соединение описывается одной из формул (XXVI)-(XXVII), или любой из гидратированных форм указанных формул:


15. Способ по п. 14, отличающийся тем, что мольное соотношение фосфора и катионов в указанном катализаторе составляет 1.
16. Способ по п. 14, отличающийся тем, что указанный катализатор прокаливают при температуре от 200°С до 1200°С.
17. Способ по п. 14, отличающийся тем, что указанные соединения, содержащие фосфор, включают:
(a) по меньшей мере, фосфат формулы (IV), где у равен 2; и
(b) H3PO4; и
при этом указанные нитратные соли включают, по меньшей мере, нитратную соль формулы (XXVII).
18. Способ по п. 17, отличающийся тем, что указанные соединения, содержащие фосфор, включают:
(a) K2HPO4; и
(b) H3PO4; и
при этом указанные нитратные соли включают Ba(NO3)2, Ca(NO3)2 или Mn(NO3)2·4H2O.
19. Способ по п. 14, отличающийся тем, что указанные соединения, содержащие фосфор, включают:
(a) по меньшей мере, фосфат формулы (XV), где v равен 2; и
(b) H3PO4;
и при этом указанные нитратные соли включают, по меньшей мере, нитратную соль формулы (XXVI).
20. Способ по п. 19, отличающийся тем, что указанные соединения, содержащие фосфор, включают:
(a) Ba2P2O7 или Ca2P2O7; и
(b) H3PO4;
и при этом указанные нитратные соли включают KNO3.
21. Способ по п. 14, отличающийся тем, что указанные соединения, содержащие фосфор, включают:
(a) по меньшей мере, фосфат формулы (VI), где у равен 3; и
(b) Н3РО4;
и при этом указанные нитратные соли включают по меньшей мере нитратную соль формулы (XXVI).
22. Способ по п. 21, отличающийся тем, что указанные соединения, содержащие фосфор, включают:
(a) MnPO4·qH2O; и
(b) Н3РО4;
и при этом указанные нитратные соли включают KNO3.
23. Способ по п. 14, отличающийся тем, что дополнительно включает стадию, на которой смешивают инертный носитель с указанными соединениями, содержащими фосфор, и указанными соединениями, не содержащими фосфор, при этом инертный носитель смешивают до, во время или после указанного смешивания и нагревания соединений, и причем указанный инертный носитель содержит силикаты, алюминаты, уголь, оксиды металлов и их смеси.
24. Способ получения катализатора, включающий стадии, на которых:
(a) объединяют Ca2P2O7 и KH2PO4 в мольном соотношении 3:1 с образованием твердой смеси, и
(b) прокаливают указанную твердую смесь постадийно при 50°С, 80°С, 120°С и при от 450°С до 550°С, с получением указанного катализатора.
| US 2859240 A1, 04.11.1958 | |||
| CN 101537362 A, 23.09.2009 | |||
| US 4729978 A1, 08.03.1988 | |||
| KR 2011022235 A, 07.03.2011 | |||
| CN 101176847 A, 14.05.2008. |
Авторы
Даты
2016-07-10—Публикация
2013-04-11—Подача