Область техники, к которой относится изобретение
Настоящее изобретение, в целом, относится к способам каталитической конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси. Более конкретно, настоящее изобретение относится к способам, полезным для дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, с высоким выходом и селективностью в акриловую кислоту, производные акриловой кислоты или их смеси, коротким временем пребывания, и без значительной конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в нежелательные побочные продукты, такие как, например, ацетальдегид, пропановая кислота, уксусная кислота, 2,3-пентандион, диоксид углерода и монооксид углерода.
Уровень техники
Акриловая кислота, производные акриловой кислоты или их смеси имеют множество промышленных применений, как правило, потребляемых в виде полимеров. В свою очередь, эти полимеры широко используются в производстве, среди прочего, адгезивов, связующих веществ, покрытий, красок, полиролей, моющих средств, флокулянтов, диспергаторов, тиксотропных веществ, секвестрантов и суперабсорбирующих полимеров, которые используются в одноразовых абсорбирующих изделиях, в том числе подгузниках и гигиенических продуктах, например. Акриловую кислоту обычно получают из источников нефти. Например, акриловую кислоту уже давно получают путем каталитического окисления пропилена. Эти и другие способы получения акриловой кислоты из источников нефти, описаны в Kirk-Othmer Encyclopedia of Chemical Technology, Vol. 1, pgs. 342-369 (5th Ed., John Wiley & Sons, Inc., 2004). Акриловая кислота, полученная из нефти, способствует парниковым выбросам благодаря своему высокому содержанию углерода на основе нефти. Дополнительно, нефть является не возобновляемым материалом, так как сотни тысяч лет необходимы для природного образования и только короткое время для потребления. Поскольку нефтехимические ресурсы становятся все более скудными, дорогими и подчиняются правилам для выбросов СО2, существует растущий спрос на полученную из биологического сырья акриловую кислоту, производные акриловой кислоты или их смеси, которые могут служить в качестве альтернативы акриловой кислоте, производным акриловой кислоты или их смесям, полученным из нефти.
В течение последних 40-50 лет были сделаны многие попытки, чтобы получить акриловую кислоту, производные акриловой кислоты или их смеси, полученные из биологического сырья, из источников, отличных от нефти, таких как молочная кислота (также известная как 2-гидроксипропионовая кислота), 3-гидроксипропионовая кислота, глицерин, монооксид углерода и этиленоксид, диоксид углерода и этилен, и кротоновая кислота. Из этих источников, отличных от нефти, только молочную кислоту получают сегодня с высоким выходом из сахара (≥90% теоретического выхода, или эквивалентно ≥0,9 г молочной кислоты на грамм сахара) и чистотой, и экономикой, которые могли бы поддерживать получение акриловой кислоты при стоимости, конкурентной для акриловой кислоты, полученной из нефти. Как таковая, молочная кислота или лактат представляет собой реальную возможность служить в качестве сырья для акриловой кислоты, производных акриловой кислоты или их смесей, полученных из биологического сырья. Кроме того, 3-гидроксипропионовая кислота, как ожидается, будет производиться в коммерческих масштабах в течение нескольких лет, и в этом качестве, 3-гидропропионовая кислота представит еще одну реальную возможность служить в качестве сырья для акриловой кислоты, производных акриловой кислоты или их смесей, полученных из биологического сырья. Сульфатные соли; фосфатные соли; смеси сульфатных и фосфатных солей; основания; цеолиты или модифицированные цеолиты; оксиды металлов или модифицированные оксиды металлов; и сверхкритическая вода являются основными катализаторами, которые были использованы для дегидратации молочной кислоты или лактата в акриловую кислоту, производные акриловой кислоты или их смеси, в прошлом, с различной степенью успеха.
Например, в патенте США №4,786,756 (выдан в 1988 году), изобретатели заявляют дегидратацию в паровой фазе молочной кислоты или лактата аммония в акриловую кислоту с помощью фосфата алюминия (AlPO4), который обрабатывают водным неорганическим основанием в качестве катализатора. В качестве примеров, ′756 патент раскрывает максимальный выход акриловой кислоты 43,3%, когда молочную кислоту подают в реактор приблизительно при атмосферном давлении, и соответствующий выход 61,1%, когда лактат аммония подают в реактор. В обоих примерах, ацетальдегид был получен с выходами 34,7% и 11,9%, соответственно, и другие побочные продукты также присутствовали в больших количествах, такие как, пропионовая кислота, СО и CO2. Отсутствие обработки основанием вызвало повышенное количество побочных продуктов. Другим примером является Hong et al. (2011) Appl. Catal. A: General 396:194-200, который разработал и испытал композитные катализаторы, приготовленные с Са3(PO4)2 и Са2(P2O7) солями методом суспензионного смешивания. Катализатор с наиболее высоким выходом акриловой кислоты из метил лактата был 50%-50% (по массе) катализатор. Это дает выход 68% акриловой кислоты, приблизительно 5% метилакрилата и приблизительно 14% ацетальдегида при 390°С. Тот же катализатор приводит к 54% выходу акриловой кислоты, 14% выходу ацетальдегида и 14% выходу пропионовой кислоты из молочной кислоты.
Группа профессора Д. Миллера в Мичиганском государственном университете (MSU) опубликовала много работ по дегидратации молочной кислоты или сложных эфиров молочной кислоты в акриловую кислоту и 2,3-пентандион, такие как, Gunter et al. (1994) J. Catalysis 148:252-260; и Tam et al. (1999) Ind. Eng. Chem. Res. 38:3873-3877. Лучшие выходы акриловой кислоты, представленные группой, составляли приблизительно 33%, когда молочную кислоту дегидратировали при 350°С на более низкой площади поверхности и объеме пор кремнезема, пропитанного NaOH. В том же самом эксперименте, выход ацетальдегида составлял 14,7% и выход пропионовой кислоты составлял 4,1%. Примеры других катализаторов, проверенных группой, были Na2SO4, NaCl, Na3PO4, NaNO3, Na2SiO3, Na4P2O7, NaH2PO4, Na2HPO4, Na2HAsO4, NaC3H5O3, NaOH, CsCl, Cs2SO4, KOH, CsOH и LiOH. Во всех случаях, на которые ссылаются выше, катализаторы были испытаны в качестве отдельных компонентов, а не в виде смесей. Наконец, группа предположила, что выход в акриловую кислоту улучшается, а выход в побочные продукты подавляется, когда площадь поверхности на носителе из кремнезема является низкой, температура реакции является высокой, давление реакции является низким, и время пребывания реагентов в слое катализатора короткое.
И, наконец, китайская заявка на патент 200910054519.7 раскрывает применение ZSM-5 молекулярных сит, модифицированных с помощью водного раствора щелочи (например, NH3, NaOH и Na2CO3) или соли фосфорной кислоты (например, NaH2PO4, Na2HPO4, LiH2PO4, LaPO4 и т.д.). Лучший выход акриловой кислоты, который достигается при дегидратации молочной кислоты, составлял 83,9%, однако, данный выход получен при очень длительных сроках пребывания.
Таким образом, производство акриловой кислоты, производных акриловой кислоты или их смесей из молочной кислоты или лактата способами, такими, как те, которые описаны в литературе, как отмечалось выше, приводит к: 1) выходам акриловой кислоты, производных акриловой кислоты или их смесей, не превышающим 70%; 2) низким селективностям получения акриловой кислоты, производных акриловой кислоты или их смесей, то есть, значительным количествам нежелательных побочных продуктов, таких как, ацетальдегид, 2,3-пентандион, пропионовая кислота, СО и СО2; 3) длительному времени пребывания в слоях катализатора; и 4) дезактивации катализатора в короткое время в потоке (TOS). Побочные продукты могут осаждаться на катализатор, приводя в результате к загрязнению, и преждевременной и быстрой дезактивации катализатора. Кроме того, после осаждения, эти побочные продукты могут катализировать другие нежелательные реакции, такие как реакции полимеризации. Кроме осаждения на катализаторы, эти побочные продукты, даже если они присутствуют только в малых количествах, приводят к дополнительным затратам при обработке акриловой кислоты (если они присутствуют в выходящем потоке продукта реакции) в производстве суперабсорбирующих полимеров (SAP), например. Эти недостатки известных способов и катализаторов делают их коммерчески нежизнеспособными.
Таким образом, существует потребность в способах дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, с высоким выходом, селективностью и эффективностью (т.е. коротким временем пребывания) и высокой долговечностью катализаторов.
Сущность изобретения
В одном осуществлении настоящего изобретения, представлен способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
a) получают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота находится в мономерной форме в указанном водном растворе;
b) объединяют указанный водный раствор с инертным газом с образованием смеси водного раствора/газа;
c) испаряют указанную смесь водного раствора/газа с получением газообразной смеси; и
d) дегидратируют указанную газообразную смесь путем контактирования указанной газообразной смеси с катализатором дегидратации под давлением по меньшей мере приблизительно 80 фунт/кв.дюйм изб., с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей.
В другом осуществлении настоящего изобретения, представлен способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
a) получают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота содержит олигомеры в указанном водном растворе;
b) нагревают указанный водный раствор при температуре от приблизительно 50°С до приблизительно 100°С с удалением указанных олигомеров указанной гидроксипропионовой кислоты и получением водного раствора мономерной гидроксипропионовой кислоты;
c) объединяют указанный водный раствор мономерной гидроксипропионовой кислоты с инертным газом с образованием смеси водного раствора/газа;
d) испаряют указанную смесь водного раствора/газа с получением газообразной смеси; и
e) дегидратируют указанную газообразную смесь путем контактирования указанной смеси с катализатором дегидратации, с получением указанной акриловой кислоты, производных акриловой кислоты и их смесей.
В еще одном осуществлении настоящего изобретения, представлен способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
a) получают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота находится в мономерной форме в указанном водном растворе;
b) объединяют указанный водный раствор с инертным газом с образованием смеси водного раствора/газа;
c) испаряют указанную смесь водного раствора/газа с получением газообразной смеси;
d) дегидратируют указанную газообразную смесь путем контактирования указанной смеси с катализатором дегидратации, с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей; и
е) охлаждают указанную акриловую кислоту, производные акриловой кислоты или их смеси при GHSV (часовая объемная скорость газа) более чем приблизительно 360 ч-1.
В одном осуществлении настоящего изобретения, представлен способ конверсии молочной кислоты в акриловую кислоту, включающий следующие стадии, на которых:
a) разбавляют приблизительно 88% водный раствор молочной кислоты водой с образованием приблизительно 20 мас. % водного раствора молочной кислоты;
b) нагревают приблизительно 20 мас. % указанный водный раствор молочной кислоты при температуре от приблизительно 95°С до приблизительно 100°С для удаления олигомеров указанной молочной кислоты, с получением водного раствора мономерной молочной кислоты, содержащего по меньшей мере 95 мас. % указанной молочной кислоты в мономерной форме, исходя из общего количества молочной кислоты;
c) объединяют указанный водный раствор мономерной молочной кислоты с азотом с образованием смеси водного раствора/газа;
d) испаряют указанную смесь водного раствора/газа в реакторе с внутренней поверхностью из боросиликатного стекла при GHSV приблизительно 7200 ч-1 при температуре от приблизительно 300°С до приблизительно 350°С с получением газообразной смеси, содержащей приблизительно 2,5 мол.% молочной кислоты и приблизительно 50 мол.% воды;
e) дегидратируют указанную газообразную смесь в реакторе с внутренней поверхностью из боросиликатного стекла при GHSV приблизительно 3600 ч-1 при температуре от приблизительно 350°С до приблизительно 425°С путем контактирования указанной смеси с катализатором дегидратации под давлением приблизительно 360 фунт/кв.дюйм изб., с получением указанной акриловой кислоты; и
f) охлаждают указанную акриловую кислоту с получением раствора акриловой кислоты при GHSV от приблизительно 360 ч-1 до приблизительно 36000 ч-1.
В другом осуществлении настоящего изобретения, представлен способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты и их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
а) получают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота находится в мономерной форме в указанном водном растворе, и причем содержание гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет от приблизительно 10 мас. % до приблизительно 25 мас. % указанного водного раствора;
b) объединяют указанный водный раствор с инертным газом с образованием смеси водного раствора/газа;
c) испаряют указанную смесь водного раствора/газа с получением газообразной смеси; и
d) дегидратируют указанную газообразную смесь путем контактирования указанной смеси с катализатором дегидратации с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей.
В еще одном осуществлении настоящего изобретения, представлен способ конверсии алкиллактатов в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
a) получают алкиллактаты или раствор, содержащий алкиллактаты и растворитель;
b) объединяют указанные алкиллактаты или указанный раствор, содержащий указанные алкиллактаты и указанный растворитель, с инертным газом с образованием смеси жидкость/газ;
c) испаряют указанную смесь жидкость/газ с получением газообразной смеси; и
d) дегидратируют указанную газообразную смесь путем контактирования указанной газообразной смеси с катализатором дегидратации под давлением по меньшей мере приблизительно 80 фунт/кв.дюйм изб., с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей.
Дополнительные признаки настоящего изобретения станут очевидными специалистам в данной области техники после обзора приведенного ниже подробного описания, в сочетании с примерами и формулой изобретения, которая прилагается.
Подробное описание изобретения
I Определения
Как используют в данной заявке, термин «конденсированный фосфат» относится к любым солям, содержащим одну или несколько Р-О-Р связей, образованных углом, общим с РО4 тетраэдром.
Как используют в данной заявке, термин «циклофосфат» относится к любому циклическому конденсированному фосфату, состоящему из двух или более имеющих общий угол РО4 тетраэдров.
Как используют в данной заявке, термин «монофосфат» или «ортофосфат» относится к любой соли, анионный фрагмент которой, [РО4]3-, состоит из четырех атомов кислорода, расположенных в почти правильной тетраэдрической матрице с приблизительно центральным атомом фосфора.
Как используют в данной заявке, термин «олигофосфат» относится к любым полифосфатам, содержащим пять или менее РО4 звеньев.
Как используют в данной заявке, термин «полифосфат» относится к любым конденсированным фосфатам, содержащим линейные Р-О-Р связи, образованные углом, общим с PO4 тетраэдром, приводя к образованию конечных цепей.
Как используют в данной заявке, термин «ультрафосфат» относится к любому конденсированному фосфату, где по меньшей мере два РО4 тетраэдра анионного фрагмента имеют три общих угла с прилегающими тетраэдрами.
Как используют в данной заявке, термин «катион» относится к любому атому или группе ковалентно-связанных атомов, имеющих положительный заряд.
Как используют в данной заявке, термин «одновалентный катион» относится к любому катиону с положительным зарядом +1.
Как используют в данной заявке, термин «многовалентный катион» относится к любому катиону с положительным зарядом равным или более чем +2.
Как используют в данной заявке, термин «анион» относится к любому атому или группе ковалентно-связанных атомов, имеющих отрицательный заряд.
Как используют в данной заявке, термин «гетерополианион» относится к любому аниону с ковалентно связанными ХОр и YOr полиэдром и включает X-O-Y и возможно Х-О-Х и Y-O-Y связи, где X и Y представляют собой любые атомы и где р и r представляют собой любые положительные целые числа.
Как используют в данной заявке, термин «гетерополифосфат» относится к любому гетерополианиону, где X представляет собой фосфор (Р) и Y означает любой другой атом.
Как используют в данной заявке, термин «фосфатный аддукт» относится к любому соединению с одним или более фосфатными анионами, и одним или более нефосфатными анионами, не связанными ковалентно.
Как используют в данной заявке, термины «LA» относится к молочной кислоте, «АА» относится к акриловой кислоте, «АсН» относится к ацетальдегиду и «РА» относится к пропионовой кислоте.
Как используют в данной заявке, термин «разброс значений диаметра частиц» относится к статистическому представлению данной пробы частиц и равен (Dν,0,90-Dν,0,10)/Dv,0,50. Термин «медианный размер частиц» или Dν,0,50 относится к диаметру частицы, менее которого находятся 50% общего объема частиц. Дополнительно, Dν,0,10 относится к размеру частицы, отделяющему пробу частицы при 10% по объемной фракции и Dν,0,90, представляет собой размер частицы, отделяющий пробу частицы при 90% по объемной фракции.
Как используют в данной заявке, термин «конверсия» в % определяют как [скорость втекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)-скорость вытекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)]/[скорость втекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)]*100. Для целей настоящего изобретения, термин «конверсия» означает мольную конверсию, если не указано иное.
Как используют в данной заявке, термин «выход» в % определен как [скорость вытекания продукта (моль/мин)/скорость втекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)]*100. Для целей настоящего изобретения, термин «выход» означает мольный выход, если не указано иное.
Как используют в данной заявке, термин «селективность» в % определен как [Выход/Конверсия]*100. Для целей настоящего изобретения, термин «селективность» означает мольную селективность, если не указано иное.
Как используют в данной заявке, термин «общая скорость вытекания» в моль/мин и для гидроксипропионовой кислоты определен как: (2/3)*[скорость вытекания С2 (моль/мин)]+[скорость вытекания С3 (моль/мин)]+(2/3)*[скорость вытекания ацетальдегида (моль/мин)]+(4/3)*[скорость вытекания С4 (моль/мин)]+[скорость вытекания гидроксипропионовой кислоты (моль/мин)]+[скорость вытекания виноградной кислоты (моль/мин)]+(2/3)*[скорость вытекания уксусной кислоты (моль/мин)]+[скорость вытекания 1,2-пропандиола (моль/мин)]+[скорость вытекания пропионовой кислоты (моль/мин)]+[скорость вытекания акриловой кислоты (моль/мин)]+(5/3)*[скорость вытекания 2,3-пентандиона (моль/мин)]+(1/3)*[скорость вытекания монооксида углерода (моль/мин)]+(1/3)*[скорость вытекания диоксида углерода (моль/мин)]. Если используют производное гидроксипропионовой кислоты вместо гидроксипропионовой кислоты, указанная выше формула должна быть скорректирована на количество атомов углерода в производном гидроксипропионовой кислоты.
Как используют в данной заявке, термин «С2» означает этан и этилен.
Как используют в данной заявке, термин «С3» означает пропан и пропилен.
Как используют в данной заявке, термин «С4» означает бутан и бутены.
Как используют в данной заявке, термин «общий мольный баланс» или «ТМВ» в % определен как [общая скорость вытекания (моль/мин)/скорость втекания гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей (моль/мин)]*100.
Как используют в данной заявке, термин «выход акриловой кислоты скорректирован на ТМВ» определен как [выход акриловой кислоты/общий мольный баланс]*100, для учета слегка более высоких потоков в реакторе.
Как используют в данной заявке, термин «часовая объемная скорость газа» или «GHSV» в ч-1 определен как [Общая скорость потока газа (мл/мин)/объем слоя катализатора (мл)]×60. Общая скорость потока газа рассчитывается в условиях стандартной температуры и давления (STP; 0°С и 1 атм).
Как используют в данной заявке, термин «часовая объемная скорость жидкости» или «LHSV» в ч-1 определен как [Общая скорость потока жидкости (мл/мин)/объем слоя катализатора (мл)]×60.
II Способ
Изобретателями было неожиданно обнаружено, что способ дегидратации гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей может привести к получению высоких выходов и селективности получения акриловой кислоты, производных акриловой кислоты или их смесей, если раствор гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей содержит гидроксипропионовую кислоту в мономерной форме, и его объединяют с инертным газом, и способ включает стадию испарения и стадию дегидратации. Дополнительно, стадия охлаждения с коротким временем пребывания, ниже по потоку стадии дегидратации, и проведение стадии дегидратации под давлением 80 фунт/кв.дюйм изб. или более, способствуют достижению высоких выходов и селективности получения акриловой кислоты, производных акриловой кислоты или их смесей.
Способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси в соответствии с настоящим изобретением включает следующие стадии, на которых: а) получают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота находится в мономерной форме в водном растворе; b) объединяют водный раствор с инертным газом с образованием смеси водного раствора/газа; с) испаряют смесь водного раствора/газа с получением газообразной смеси; и d) дегидратируют газообразную смесь путем контактирования смеси с катализатором дегидратации под давлением по меньшей мере приблизительно 80 фунт/кв.дюйм изб.
Гидроксипропионовая кислота может быть 3-гидроксипропионовой кислотой, 2-гидроксипропионовой кислотой (также называемой молочной кислотой), 2-метилгидроксипропионовой кислотой, или их смесями. Производными гидроксипропионовой кислоты могут быть соли металлов или аммония гидроксипропионовой кислоты, алкильные сложные эфиры гидроксипропионовой кислоты, алкильные сложные эфиры 2-метилгидроксипропионовой кислоты, циклические сложные диэфиры гидроксипропионовой кислоты, ангидрид гидроксипропионовой кислоты" или их смесь. Неограничивающие примеры солей металлов гидроксипропионовой кислоты представляют собой натрий гидроксипропионат, калий гидроксипропионат и кальций гидроксипропионат. Неограничивающие примеры алкильных сложных эфиров гидроксипропионовой кислоты представляют собой метилгидроксипропионат, этилгидроксипропионат, бутилгидроксипропионат, 2-этилгексилгидроксипропионат или их смеси. Неограничивающим примером циклических сложных диэфиров гидроксипропионовой кислоты является дилактид.
Гидроксипропионовая кислота может быть в мономерной форме или в виде олигомеров в водном растворе гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. В одном осуществлении, олигомеры гидроксипропионовой кислоты в водном растворе гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, составляют менее чем приблизительно 25 мас. %, исходя из общего количества гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. В другом осуществлении, олигомеры гидроксипропионовой кислоты в водном растворе гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, составляют менее чем приблизительно 10 мас. %, исходя из общего количества гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. В другом осуществлении, олигомеры гидроксипропионовой кислоты в водном растворе гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, составляют менее чем приблизительно 5 мас. %, исходя из общего количества гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. В еще одном осуществлении, гидроксипропионовая кислота находится в мономерной форме в водном растворе гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. Стадии способа удаления олигомеров из водного раствора могут быть очисткой или разбавлением водой и нагреванием. В одном осуществлении, стадия нагревания может включать нагревание водного раствора гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей при температуре от приблизительно 50°С до приблизительно 100°С, чтобы удалить олигомеры гидроксипропионовой кислоты. В другом осуществлении, стадия нагревания может включать нагревание водного раствора молочной кислоты при температуре от приблизительно 95°С до приблизительно 100°С, чтобы удалить олигомеры молочной кислоты и получить водный раствор мономерной молочной кислоты, содержащий по меньшей мере 95 мас. % молочной кислоты в мономерной форме, исходя из общего количества молочной кислоты. В другом осуществлении, приблизительно 88 мас. % водный раствор молочной кислоты (например, от Purac Corp., Lincolnshire, IL) разбавляют водой, с образованием приблизительно 20 мас. % водного раствора молочной кислоты, чтобы удалить сложноэфирные примеси, которые получают в результате реакции межмолекулярной конденсации. Эти сложные эфиры могут привести к потере продукта из-за их высокой точки кипения и олигомеризации на стадии испарения способа. Дополнительно, эти сложные эфиры могут привести к коксованию, дезактивации катализатора и закупориванию реактора. По мере того, как содержание воды уменьшается в водном растворе, потеря исходного материала для каталитической реакции, из-за потерь на стадии испарения, увеличивается.
В одном осуществлении, гидроксипропионовая кислота представляет собой молочную кислоту или 2-метилмолочную кислоту. В другом осуществлении, гидроксипропионовая кислота представляет собой молочную кислоту. Молочная кислота может быть L-молочной кислотой, D-молочной кислотой или их смесями. В одном осуществлении, производным гидроксипропионовой кислоты является метиллактат. Метиллактат может быть в чистом виде или в виде водного раствора.
Производные акриловой кислоты могут быть солями металлов или аммония акриловой кислоты, сложными алкильными эфирами акриловой кислоты, олигомерами акриловой кислоты или их смесями. Неограничивающими примерами солей металлов акриловой кислоты являются акрилат натрия, акрилат калия и акрилат кальция. Неограничивающими примерами сложных алкильных эфиров акриловой кислоты являются метилакрилат, этилакрилат, бутилакрилат, 2-этилгексилакрилат или их смеси.
В одном осуществлении, концентрация гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в водном растворе составляет от приблизительно 5 мас. % до приблизительно 50 мас. %. В другом осуществлении, концентрация гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в водном растворе составляет от приблизительно 10 мас. % до приблизительно 25 мас. %. В еще одном осуществлении, концентрация гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в водном растворе составляет приблизительно 20 мас. %.
Водный раствор может быть объединен с инертным газом с образованием смеси водного раствора/газа. Неограничивающими примерами инертного газа являются воздух, азот, гелий, аргон, диоксид углерода, монооксид углерода, пар и их смеси. Инертный газ может быть введен на стадии испарения отдельно или в сочетании с водным раствором. Водный раствор может быть введен с помощью простой трубки или посредством форсунок распыления. Неограничивающие примеры из форсунок распыления включают веерные форсунки, вихревые форсунки давления, пневматические форсунки, форсунки двухфазных жидкостей, поворотные форсунки и форсунки сверхкритического диоксида углерода. В одном осуществлении, капли водного раствора являются менее чем приблизительно 500 мкм в диаметре. В другом осуществлении, капли водного раствора являются менее чем приблизительно 200 мкм в диаметре. В еще одном осуществлении, капли водного раствора являются менее чем 100 мкм в диаметре.
На стадии испарения, смесь водного раствора/газа нагревают с получением газообразной смеси. В одном осуществлении, температура во время стадии испарения составляет от приблизительно 165°С до приблизительно 450°С. В другом осуществлении, температура во время стадии испарения составляет от приблизительно 250°С до приблизительно 375°С. В одном осуществлении, часовая объемная скорость газа (GHSV) на стадии испарения составляет от приблизительно 720 ч-1 до 3600 ч-1. В другом осуществлении, часовая объемная скорость газа (GHSV) на стадии испарения составляет приблизительно 7200 ч-1. Стадия испарения может быть выполнена при атмосферном давлении или при более высоком давлении. В одном осуществлении, стадию испарения выполняют под давлением от приблизительно 80 фунт/кв.дюйм изб. до приблизительно 550 фунт/кв.дюйм изб. В другом осуществлении, стадию испарения выполняют под давлением от приблизительно 300 фунт/кв.дюйм изб. до приблизительно 400 фунт/кв.дюйм изб. В еще одном осуществлении, стадию испарения выполняют под давлением от приблизительно 350 фунт/кв.дюйм изб. до приблизительно 375 фунт/кв.дюйм изб. В одном осуществлении, газообразная смесь содержит от приблизительно 0,5 мол.% до приблизительно 50 мол.% гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. В другом осуществлении, газообразная смесь содержит от приблизительно 1 мол.% до приблизительно 10 мол.% гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. В другом осуществлении, газообразная смесь содержит от приблизительно 1,5 мол.% до приблизительно 3,5 мол.% гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. В другом осуществлении, газообразная смесь содержит от приблизительно 2,5 мол.% гидроксипропионовой кислоты, производных гидроксипропионовой гидроксипропионовой кислоты или их смесей.
Стадия испарения может быть выполнена на различных видах оборудования, таком как, но не ограничиваясь приведенным, пластинчатый теплообменник, реактор пустого потока и проточный реактор неподвижного слоя. Независимо от типа реактора, в одном осуществлении, реактор имеет внутреннюю поверхность, содержащую материал, выбранный из группы, состоящей из кварца, боросиликатного стекла, кремния, сплава Hastelloy, инконеля, искусственного сапфира, нержавеющей стали и их смесей. В другом осуществлении, реактор имеет внутреннюю поверхность, содержащую материал, выбранный из группы, состоящей из кварца, боросиликатного стекла и их смесей. Стадия испарения может быть выполнена в реакторе с водным раствором, текущим вниз, или текущим вверх, или текущим горизонтально. В одном осуществлении, стадию испарения выполняют в реакторе с водным раствором, текущим вниз. Дополнительно, стадия испарения может быть выполнена периодически.
Газообразную смесь от стадии испарения преобразуют в акриловую кислоту, производные акриловой кислоты и их смесь при его контакте с катализатором дегидратации на стадии дегидратации. Катализатор дегидратации может быть выбран из группы, включающей сульфаты, фосфаты, оксиды металлов, алюминаты, силикаты, алюмосиликаты (например, цеолиты), арсенаты, нитраты, ванадаты, ниобаты, танталаты, селенаты, арсенатофосфаты, фосфоалюминаты, фосфобораты, фосфохроматы, фосфомолибдаты, фосфосиликаты, фосфосульфаты, фосфотангстаты и их смеси, а также другие, которые могут быть очевидны специалистам в данной области техники. Катализатор может содержать инертный носитель, который выполнен из материала, содержащего силикаты, алюминаты, уголь, оксиды металлов и их смеси. В одном осуществлении, стадию дегидратации выполняют в реакторе, где реактор имеет внутреннюю поверхность, содержащую материал, выбранный из группы, состоящей из кварца, боросиликатного стекла, кремния, сплава Hastelloy, инконеля, искусственного сапфира, нержавеющей стали, а также их смесей. В другом осуществлении, стадию дегидратации выполняют в реакторе, где реактор имеет внутреннюю поверхность, содержащую материал, выбранный из группы, состоящей из кварца, боросиликатного стекла, а также их смесей. В одном осуществлении, температура во время стадии дегидратации составляет от приблизительно 150°С до приблизительно 500°С. В другом осуществлении, температура во время стадии дегидратации составляет от приблизительно 300°С до приблизительно 450°С. В одном осуществлении, GHSV на стадии дегидратации составляет от приблизительно 720 ч-1 до приблизительно 36000 ч-1. В другом осуществлении, GHSV на стадии дегидратации составляет приблизительно 3600 ч-1. Стадия дегидратации может быть выполнена при более высоком давлении, чем атмосферное. В одном осуществлении, стадию дегидратации выполняют под давлением по меньшей мере приблизительно 80 фунт/кв.дюйм изб. В другом осуществлении, стадию дегидратации выполняют под давлением от приблизительно 80 фунт/кв.дюйм изб. до приблизительно 550 фунт/кв.дюйм изб. В другом осуществлении, стадию дегидратации выполняют под давлением от приблизительно 150 фунт/кв.дюйм изб. до приблизительно 500 фунт/кв.дюйм изб. В еще одном осуществлении, стадию дегидратации выполняют под давлением от приблизительно 300 фунт/кв.дюйм изб. до приблизительно 400 фунт/кв.дюйм изб. Стадия дегидратации может быть выполнена в реакторе с газообразной смесью, текущей вниз, текущей вверх или текущей горизонтально. В одном осуществлении, стадию дегидратации выполняют в реакторе с газообразной смесью, текущей вниз. Дополнительно, стадия дегидратации может быть выполнена периодически.
В одном осуществлении, стадии испарения и дегидратации объединены в одну стадию. В другом осуществлении, стадии испарения и дегидратации выполняют последовательно в одном реакторе. В еще одном осуществлении, стадии испарения и дегидратации выполняют последовательно в тандемном реакторе.
В одном осуществлении, селективность получения акриловой кислоты, производных акриловой кислоты и их смеси из гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет по меньшей мере приблизительно 50%. В другом осуществлении, селективность получения акриловой кислоты, производных акриловой кислоты и их смеси из гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет по меньшей мере приблизительно 80%. В одном осуществлении, селективность получения пропановой кислоты из гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет менее чем приблизительно 5%. В другом осуществлении, селективность получения пропановой кислоты из гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет менее чем приблизительно 1%. В одном осуществлении, конверсия гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, составляет более чем приблизительно 50%. В другом осуществлении, конверсия гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей, составляет более чем приблизительно 80%.
В другом осуществлении настоящего изобретения, обеспечен способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси. Способ включает следующие стадии, на которых: а) получают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом гидроксипропионовая кислота содержит олигомеры в водном растворе; b) нагревают водный раствор при температуре от приблизительно 50°С до приблизительно 100°С, с удалением олигомеров гидроксипропионовой кислоты и получением водного раствора мономерной гидроксипропионовой кислоты; с) объединяют водный раствор мономерной гидроксипропионовой кислоты с инертным газом с образованием смеси водного раствора/газа; d) испаряют смесь водного раствора/газа с получением газообразной смеси; и е) дегидратируют газообразную смесь путем контактирования смеси с катализатором дегидратации и получают акриловую кислоту, производные акриловой кислоты или их смеси.
В одном осуществлении, после стадии нагревания, концентрация олигомеров гидроксипропионовой кислоты в водном растворе мономерной гидроксипропионовой кислоты составляет менее чем приблизительно 20 мас. %, исходя из общего количества гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей. В другом осуществлении, после стадии нагревания, концентрация олигомеров гидроксипропионовой кислоты в водном растворе мономерной гидроксипропионовой кислоты составляет менее чем приблизительно 5 мас. %, исходя из общего количества гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей.
В другом осуществлении настоящего изобретения, обеспечен способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты и их смеси. Способ включает следующие стадии, на которых: а) получают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом гидроксипропионовая кислота находится в мономерной форме в водном растворе; b) объединяют водный раствор с инертным газом с образованием смеси водного раствора/газа; с) испаряют смесь водного раствора/газа с получением газообразной смеси; d) дегидратируют газообразную смесь путем контактирования смеси с катализатором дегидратации с получением акриловой кислоты и/или акрилатов; и е) охлаждают акриловую кислоту, производные акриловой кислоты и их смесь при GHSV более чем приблизительно 360 ч-1.
Поток акриловой кислоты, производных акриловой кислоты и их смеси, полученный на стадии дегидратации, охлаждают до получения водной композиции акриловой кислоты в качестве потока продукта. Время, необходимое для охлаждения потока акриловой кислоты, производных акриловой кислоты или их смесей необходимо контролировать, чтобы уменьшить разложение акриловой кислоты в этилен и полимеризацию. В одном осуществлении, GHSV акриловой кислоты, производных акриловой кислоты и их смеси на стадии охлаждения составляет более чем приблизительно 720 ч-1.
В другом осуществлении настоящего изобретения, обеспечен способ конверсии молочной кислоты в акриловую кислоту. Способ включает следующие стадии, на которых: а) разбавляют приблизительно 88 мас. % водный раствор молочной кислоты водой с образованием приблизительно 20 мас. % водного раствора молочной кислоты; b) нагревают приблизительно 20 мас. % водный раствор молочной кислоты при температуре от приблизительно 95°С до приблизительно 100°С, чтобы удалить олигомеры молочной кислоты, с получением раствора мономерной молочной кислоты, содержащего по меньшей мере приблизительно 95 мас. % молочной кислоты в мономерной форме, исходя из общего количества молочной кислоты; с) объединяют раствор мономерной молочной кислоты с азотом с образованием смеси водного раствора/газа; d) испаряют смесь водного раствора/газа в реакторе с внутренней поверхностью из боросиликатного стекла при GHSV приблизительно 7200 ч-1 при температуре от приблизительно 300°С до приблизительно 350°С, с получением газообразной смеси, содержащей приблизительно 2,5 мол.% молочной кислоты и приблизительно 50 мол.% воды; е) дегидратируют газообразную смесь в реакторе с внутренней поверхностью из боросиликатного стекла при GHSV приблизительно 3600 ч-1 при температуре от 350°С до приблизительно 425°С путем контактирования смеси с катализатором дегидратации под давлением приблизительно 360 фунт/кв.дюйм изб., с получением акриловой кислоты; и f) охлаждают акриловую кислоту при GHSV от приблизительно 360 ч-1 до приблизительно 36000 ч-1.
В другом осуществлении настоящего изобретения, обеспечен способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты и их смесей в акриловую кислоту, производные акриловой кислоты или их смеси. Способ включает следующие стадии, на которых: а) получают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом гидроксипропионовая кислота находится в мономерной форме в водном растворе, и причем содержание гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет от приблизительно 10 мас. % до приблизительно 25 мас. % водного раствора; b) объединяют водный раствор с инертным газом с образованием смеси водного раствора/газа; с) испаряют смесь водного раствора/газа с получением газообразной смеси; и d) дегидратируют газообразную смесь путем контактирования смеси с катализатором дегидратации с получением акриловой кислоты, производных акриловой кислоты или их смесей.
В другом осуществлении настоящего изобретения, обеспечен способ конверсии алкиллактатов в акриловую кислоту, производные акриловой кислоты или их смеси. Способ включает следующие стадии, на которых: а) получают алкиллактаты или раствор, содержащий алкиллактаты и растворитель; b) объединяют указанные алкиллактаты или указанный раствор, содержащий указанные алкиллактаты и указанный растворитель, с инертным газом с образованием смеси жидкость/газ; с) испаряют указанную смесь жидкость/газ с получением газообразной смеси; и d) дегидратируют указанную газообразную смесь путем контактирования указанной газообразной смеси с катализатором дегидратации под давлением по меньшей мере приблизительно 80 фунт/кв.дюйм изб., с получением акриловой кислоты, производных акриловой кислоты или их смесей.
В одном осуществлении, алкиллактаты выбирают из группы, состоящей из метиллактата, этиллактата, бутиллактата, 2-этилгексиллактата и их смесей. В другом осуществлении, растворитель выбирают из группы, состоящей из воды, метанола, этанола, бутанола, 2-этилгексанола, изобутанола, изооктилового спирта и их смесей.
III Катализаторы для конверсии гидроксипропионовой кислоты или ее производных в акриловую кислоту или ее производные
В одном осуществлении, катализатор содержит: (а) анионы моногидромонофосфата и дигидромонофосфата, которые описываются формулами (I) и (II):

и (b) по меньшей мере два различных катиона, где катализатор по существу нейтрально заряжен; и дополнительно, при этом мольное соотношение указанного аниона моногидромонофосфата и указанного аниона дигидромонофосфата в катализаторе составляет от приблизительно 0,1 до приблизительно 10. В другом осуществлении, мольное соотношение аниона моногидромонофосфата и аниона дигидромонофосфата составляет от приблизительно 0,2 до приблизительно 5. В еще одном осуществлении, мольное соотношение аниона моногидромонофосфата и аниона дигидромонофосфата составляет приблизительно 1.
В одном осуществлении настоящего изобретения катализатор содержит монофосфатные соли, описанные формулами (III) и (IV):
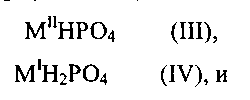
где MI представляет собой одновалентный катион и MII представляет собой двухвалентный катион. В другом осуществлении, мольное соотношение MIIHPO4 и MIH2PO4 составляет от приблизительно 0,1 до приблизительно 10. В другом осуществлении, мольное соотношение MIIHPO4 и MIH2PO4 составляет от приблизительно 0,2 до приблизительно 5. В еще одном осуществлении, мольное соотношение MIIHPO4 и MIH2PO4 составляет приблизительно 1.
В одном осуществлении настоящего изобретения, катализатор содержит монофосфатную соль, описанную формулой (V):

где MI представляет собой одновалентный катион и MII представляет собой двухвалентный катион; и где α составляет более чем приблизительно 0,2 и менее чем приблизительно 1,8. В другом осуществлении настоящего изобретения, α составляет приблизительно 1.
В другом осуществлении, анион моногидромонофосфата, описанный формулой (I), замещен одним или более фосфатными анионами, описанными формулой [H(1-β)Р(1+β)O(4+3β)]2(1+β)-, где β более или равен нулю и менее или равен 1.
В другом осуществлении, анион дигидромонофосфата, описанный формулой (II), замещен одним или более фосфатными анионами, описанными формулой [Н2(1-β)РО(4-β)]-, где β более или равен нулю и менее или равен 1.
В одном осуществлении, катализатор содержит: (а) по меньшей мере один анион конденсированного фосфата, который выбирают из группы, состоящей из формул (VI), (VII) и (VIII)
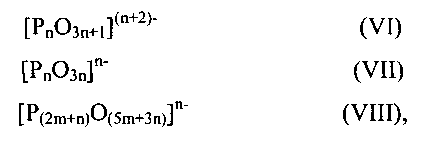
где n составляет по меньшей мере 2 и m составляет по меньшей мере 1,
и (b) по меньшей мере два различных катиона, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и по меньшей мере двух различных катионов составляет от приблизительно 0,7 до приблизительно 1,7.
Анионы, определенные формулами (VI), (VII) и (VIII) также называют полифосфатами (или олигофосфатами), циклофосфатами и ультрафосфатами, соответственно.
В другом осуществлении, катализатор содержит: (а) по меньшей мере один анион конденсированного фосфата, который выбирают из группы, состоящей из формул (VI) и (VII)
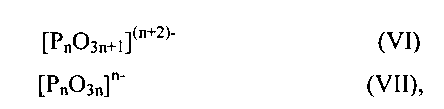
где n составляет по меньшей мере 2, и (b) по меньшей мере два различных катиона, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и по меньшей мере двух различных катионов составляет от приблизительно 0,7 до приблизительно 1,7.
В одном осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,7 до приблизительно 1,7; в другом осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,8 до приблизительно 1,3; и в еще одном осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет приблизительно 1.
В одном осуществлении, по меньшей мере два различных катиона содержат (а) по меньшей мере один одновалентный катион, и (b) по меньшей мере один многовалентный катион. В другом осуществлении, мольное соотношение одновалентных катионов и многовалентных катионов составляет от приблизительно 0,1 до приблизительно 10. В еще одном осуществлении, мольное соотношение одновалентных катионов и многовалентных катионов составляет от приблизительно 0,5 до приблизительно 5. В дополнительном осуществлении настоящего изобретения, мольное соотношение одновалентных катионов и многовалентных катионов составляет приблизительно 1.
В другом осуществлении, многовалентный катион выбирают из группы, состоящей из двухвалентных катионов, трехвалентных катионов, четырехвалентных катионов, пятивалентных катионов и их смесей. Неограничивающие примеры одновалентных катионов представляют собой Н+, Li+, Na+, К+, Rb+, Cs+, Ag+, Rb+, Tl+ и их смеси. В одном осуществлении, одновалентный катион выбирают из группы, состоящей из Li+, Na+, К+, Rb+, Cs+ и их смесей; в другом осуществлении, одновалентный катион представляет собой Na+ или К+; и в еще одном осуществлении, одновалентный катион представляет собой К+. Неограничивающие примеры многовалентных катионов представляют собой катионы щелочноземельных металлов (т.е., Be, Mg, Са, Sr, Ва и Ra), переходных металлов (например, Y, Ti, Zr, V, Nb, Сг, Mo, Mn, Re, Fe, Ru, Co, Rh, Ni, Pd, Pt, Cu, Ag и Au), легких металлов (например, Zn, Ga, Si, Ge, B, Al, In, Sb, Sn, Bi и Pb), лантанидов (например, La и Се) и актинидов (например, Ас и Th). В одном осуществлении, многовалентный катион выбирают из группы, состоящей из Ве2+, Mg2+, Са2+, Sr2+, Ва2+, Mn2+, Fe2+, Со2+, Ni2+, Cu2+, Zn2+, Cd2+, Sn2+, Pb2+, Ti3+, Cr3+, Mn3+, Fe3+, Al3+, Ga3+, Y3+, In3+, Sb3+, Bi3+, Si4+, Ti4+, V4+, Ge4+, Mo4+, Pt4+, V5+, Nb5+, Sb5+ и их смесей. В одном осуществлении, многовалентный катион выбирают из группы, состоящей из Са2+, Ва2+, Cu2+, Mn2+, Mn3+ и их смесей; в другом осуществлении, многовалентный катион выбирают из группы, состоящей из Са2+, Ва2+, Mn3+ и их смесей; и в еще одном осуществлении, многовалентный катион представляет собой Ва2+.
Катализатор может включать катионы: (а) Н+, Li+, Na+, К+, Rb+, Cs+ или их смеси; и (b) Ве2+, Mg2+, Са2+, Sr2+, Ва2+, Mn2+, Fe2+, Со2+, Ni2+, Cu2+, Zn2+, Cd2+, Sn2+, Pb2+, Ti3+, Cr3+, Mn3+, Fe3+, Al3+, Ga3+, Y3+, In3+, Sb3+, Bi3+, Si4+, Ti4+, V4+, Ge4+, Mo4+, Pt4+, V5+, Nb5+, Sb5+ или их смеси. В одном осуществлении катализатор содержит Li+, Na+или К+ в качестве одновалентного катиона, и Са2+, Ва2+или Mn3+ в качестве многовалентного катиона; в другом осуществлении, катализатор содержит Na+ или К+ в качестве одновалентного катиона, и Са2+ или Ва2+ в качестве многовалентного катиона; и в еще одном осуществлении, катализатор содержит К+ в качестве одновалентного катиона и Ва2+ в качестве многовалентного катиона.
В одном осуществлении, катализатор содержит Ba2-x-sK2xH2sP2O7 и (КРО3)n, где х и s превышают или равны 0 и менее чем приблизительно 0,5 и n представляет собой положительное целое число. В другом осуществлении, катализатор содержит Са2-х-sK2xH2sP2O7 и (КРО3)n, где х и s превышают или равны 0 и менее чем приблизительно 0,5 и n составляет по меньшей мере, 2. В еще одном осуществлении, катализатор содержит Mn1-x-sK1+3xH3sP2O7 или Mn1-x-sK2+2xH2sP2O7 и (KPO3)n, где х и s превышают или равны 0 и менее чем приблизительно 0,5 и n составляет по меньшей мере 2. В другом осуществлении, катализатор содержит любую смесь Ba2-x-sK2xH2sP2O7, Са2-х-sK2xH2sP2O7, Mn1-x-sK1+3xH3sP2O7 или Mn1-x-sK2+2xH2sP2O7; и (KPO3)n, где х и s превышают или равны 0 и менее чем приблизительно 0,5 и n составляет по меньшей мере 2.
В одном осуществлении, катализатор содержит: (а) по меньшей мере два различных аниона конденсированного фосфата, которые выбирают из группы, состоящей из формул (VI), (VII) и (VIII)
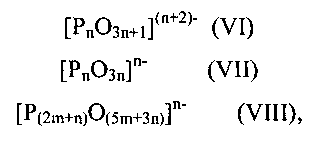
где n составляет по меньшей мере 2 и m составляет по меньшей мере 1,
и (b) один катион, при этом катализатор, по существу, нейтрально заряжен, и дополнительно, при этом мольное соотношение фосфора и катиона составляет от приблизительно 0,5 до приблизительно 4,0. В другом осуществлении, мольное соотношение фосфора и катиона составляет от приблизительно t/2 до приблизительно t, где t является зарядом катиона.
Катализатор может включать инертный носитель, который выполнен из материала, содержащего силикаты, алюминаты, уголь, оксиды металлов и их смеси. В качестве альтернативы, носитель является инертным по отношению к реакционной смеси, которая, как ожидают, вступит в контакт с катализатором. В контексте реакций, четко описанных в данной заявке, в одном осуществлении носитель представляет собой кремнезем или двуокись циркония с низкой площадью поверхности. Если присутствует, носитель представляет собой количество от приблизительно 5 мас. % до приблизительно 98 мас. %, исходя из общей массы катализатора. Как правило, катализатор, который содержит инертный носитель, может быть выполнен с помощью одного из двух иллюстративных способов: пропитки или совместного осаждения. В способе пропитки, суспензию твердого инертного носителя обрабатывают раствором пре-катализатора, и полученный материал затем активизируют в условиях, которые преобразуют пре-катализатор в более активное состояние. В способе совместного осаждения, однородный раствор ингредиентов катализатора осаждают добавлением дополнительных ингредиентов.
В другом осуществлении, катализатор может быть сульфатными солями; фосфатными солями; смесями сульфатных и фосфатных солей; основаниями; цеолитами или модифицированными цеолитами; оксидами металлов или модифицированными оксидами металлов; сверхкритической водой или их смесями.
IV Способы получения катализатора
В одном осуществлении, способ получения катализатора включает стадию, на которой смешивают по меньшей мере два различных соединения, содержащие фосфор, при этом каждое указанное соединение описано одной из формул (IX) - (XXX), или любой из гидратированных форм указанных формул:

где MI представляет собой одновалентный катион; где MII представляет собой двухвалентный катион; где MIII представляет собой трехвалентный катион; где MIV представляет собой четырехвалентный катион; где у означает 0, 1, 2 или 3; где z означает 0, 1, 2, 3 или 4; где v означает 0, 1 или 2; где w означает 0 или любое положительное целое число; и где а, b, с, d, е, f, g, h, i, j, k и l означают любые положительные целые числа, таким образом, что удовлетворены уравнения: 2а=b+3с, 3d=е+3f, i=2g+h, и l=3j+k. В другом осуществлении, способ получения катализатора включает стадию, на которой нагревают соединения, содержащие фосфор, после смешивания. В другом осуществлении, способ получения катализатора включает стадию, на которой вводят в контакт соединения, содержащие фосфор, после смешивания с газообразной смесью, содержащей воду.
В одном осуществлении, катализатор получают с помощью стадии, на которой смешивают одно или более соединений, содержащих фосфор, формулы (IX), где у равен 1, и одно или более соединений, содержащих фосфор, формулы (X), где у равен 2. В другом осуществлении, катализатор получают с помощью стадии, на которой смешивают MIH2PO4 и MIIHPO4. В одном осуществлении, MI представляет собой К+ и М представляет собой Са2+, т.е., катализатор получают смешиванием КН2РО4 и CaHPO4; или MI представляет собой К и MII представляет собой Ва2+, т.е., катализатор получают с помощью стадии, на которой смешивают КН2РО4 и BaHPO4.
В одном осуществлении, катализатор получают с помощью стадии, на которой смешивают одно или более соединений, содержащих фосфор, формулы (IX), где у равен 1, одно или более соединений, содержащих фосфор, формулы (XX), где v равен 2. В другом осуществлении, катализатор получают с помощью стадии, на которой смешивают MIH2PO4 и MII 2P2O7. В одном осуществлении, MI представляет собой К+ и MII представляет собой Са2+, т.е. катализатор получают смешиванием КН2РО4 и Ca2P2O7; или MI представляет собой К+ и MII представляет собой Ва2+, т.е. катализатор получают с помощью стадии, на которой смешивают KH2PO4 и Ba2P2O7.
В другом осуществлении, катализатор получают с помощью стадии, на которой смешивают одно или более соединений, содержащих фосфор, формулы (X), где указанный у равен 2, и одно или более соединений, содержащих фосфор, формулы (XXIV), где указанный w равен 0. В другом осуществлении, соединения, содержащие фосфор, представляют собой (КРО3)n и BaHPO4 или CaHPO4; где n является целым числом, большим чем 2.
В еще одном осуществлении, катализатор получают с помощью стадии, на которой смешивают одно или более соединений, содержащих фосфор, формулы (XX), где указанное v равно 2, и одно или более соединений, содержащих фосфор, формулы (XXIV), где указанное w равно 0. В другом осуществлении, соединения, содержащие фосфор, представляют собой (КРО3)n и Ba2P2O7 или Ca2P2O7; где n является целым числом, большим чем 2.
В другом осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,7 до приблизительно 1,7; в еще одном осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,8 до приблизительно 1,3; и в другом осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет приблизительно 1.
В другом осуществлении, способ получения катализатора включает стадию, на которой смешивают (а) по меньшей мере одно соединение, содержащее фосфор, при этом каждое указанное соединение описано одной из формул (IX)-(XXX), или любой из гидратированных форм указанных формул:

где y означает 0, 1, 2 или 3; где z означает 0, 1, 2, 3 или 4; где v означает 0, 1 или 2; где w означает 0 или любое положительное целое число; и где а, b, с, d, е, f, g, h, i, j, k и l означают любые положительные целые числа, таким образом, что уравнения: 2а=b+3с, 3d=е+3f, i=2g+h и l=3j+k удовлетворены, и (b) по меньшей мере одно соединение, не содержащее фосфор, выбранное из группы, состоящей из нитратных солей, карбонатных солей, ацетатных солей, оксидов металлов, хлоридных солей, сульфатных солей и гидроксидов металлов, при этом каждое указанное соединение описано одной из формул (XXVI)-(L), или любой из гидратированных форм указанных формул:

В другом осуществлении, соединения, не содержащие фосфор, могут быть выбраны из группы, состоящей из солей карбоновых кислот, галидных солей, ацетилацетонатов металлов и алкоксидов металлов.
В другом осуществлении, способ получения катализатора включает стадию, на которой вводят в контакт соединения, содержащие фосфор, и соединения, не содержащие фосфор, после смешивания, с газообразной смесью, содержащей воду.
В одном осуществлении настоящего изобретения, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,7 до приблизительно 1,7; в другом осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет от приблизительно 0,8 до приблизительно 1,3; и в еще одном осуществлении, мольное соотношение фосфора и катионов в катализаторе составляет приблизительно 1.
В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формул (IX)-(XXX) или их гидратированных форм, и одной или более нитратных солей формул (XXXI)-(XXXIII) или их гидратированных форм. В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (IX) и одной или более нитратных солей формулы (XXXII). В дополнительном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (IX), где y равен 2, соединения, содержащего фосфор, формулы (IX), где у равен 0 (т.е. фосфорной кислоты), и нитратной соли формулы (XXXII). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием К2НРО4, Н3РО4 и Ва(NO3)2. В еще одном осуществлении, катализатор получают смешиванием и нагреванием К2НРО4, H3PO4 и Са(NO3)2.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (IX) и одной или более нитратных солей формулы (XXXIII). В дополнительном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (IX), где у равен 2, соединения, содержащего фосфор, формулы (IX), где у равен 0 (т.е. фосфорной кислоты) и нитратной соли формулы (XXXIII). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием К2НРО4, Н3РО4 и Mn(NO3)2·4H2O.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (X) и одной или более нитратных солей формулы (XXXI). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (X), где y равен 2, соединения, содержащего фосфор, формулы (X), где y равен 0 (т.е. фосфорной кислоты) и нитратной соли формулы (XXXI). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием BaHPO4, Н3РО4 и KNO3. В другом осуществлении, катализатор получают смешиванием и нагреванием CaHPO4, Н3РО4 и KNO3.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (X), одного или более соединений, содержащих фосфор, формулы (XX), и одной или более нитратных солей формулы (XXXI). В дополнительном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (X), где у равен 0 (т.е. фосфорной кислоты); соединения, содержащего фосфор, формулы (XX), где v равен 2; и нитратной соли формулы (XXXI). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием H3PO4, Ca2P2O7 и KNO3. В еще одном осуществлении, катализатор получают смешиванием и нагреванием H3PO4, Ba2P2O7 и KNO3.
В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (XI) и одной или более нитратных солей формулы (XXXI). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (XI), где у равен 3; соединения, содержащего фосфор, формулы (XI), где у равен 0 (т.е. фосфорной кислоты); и нитратной соли формулы (XXXI). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием MnPO4·qH2O, Н3РО4 и KNO3.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (IX), одного или более соединений, содержащих фосфор, формулы (XIV) и одной или более нитратных солей формулы (XXXII). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (IX), где y равен 2; соединения, содержащего фосфор, формулы (IX), где y равен 0 (т.е. фосфорной кислоты); соединения, содержащего фосфор, формулы (XIV), где а равен 2, b равен 1, и с равен 1; и нитратной соли формулы (XXXII). В еще одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием К2НРО4, Н3РО4, Cu2(ОН)PO4 и Ba(NO3)2.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формулы (X), одного или более соединений, содержащих фосфор, формулы (XIV) и одной или более нитратных солей формулы (XXXI). В другом осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием соединения, содержащего фосфор, формулы (X), где y равен 3; соединения, содержащего фосфор, формулы (X), где y равен 0 (т.е. фосфорной кислоты); соединения, содержащего фосфор, формулы (XIV), где а равен 2, b равен 1, и с равен 1; и нитратной соли формулы (XXXI). В еще одном осуществлении, катализатор получают смешиванием и нагреванием Ва3(PO4)2, H3PO4, Cu2(ОН)PO4 и KNO3.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IX)-(XXX) или любой гидратированной формы, и одной или более карбонатных солей, описанных одной из формул (XXXIV)-(XXXVI) или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IX)-(XXX) или любой гидратированной формы, и одной или более ацетатных солей, описанных одной из формул (XXXVII)-(XL), любых других солей органической кислоты, или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IX)-(XXX) или любой гидратированной формы, и одного или более оксидов металлов, описанных одной из формул (XLI)-(XLIV) или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IX)-(XXX) или любой гидратированной формы, и одной или более хлоридных солей, описанных одной из формул (XLV)-(XLVIII), любых других галидных солей, или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IX)-(XXX) или любой гидратированной формы, и одной или более сульфатных солей, описанных одной из формул (XLIX)-(LII) или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, описанных одной из формул (IX)-(XXX) или любой гидратированной формы, и одного или более гидроксидов, описанных одной из формул (LIII)-(LV) или любой гидратированной формы.
В одном осуществлении настоящего изобретения, катализатор получают смешиванием и нагреванием одного или более соединений, содержащих фосфор, формул (IX)-(XXX), и двух или более соединений, не содержащих фосфор, формул (XXXI)-(LV) или их гидратированных форм.
В одном осуществлении настоящего изобретения, способ получения катализатора включает стадию, на которой вводят в контакт: (а) газообразную смесь, содержащую воду, с (b) смесью соединений, содержащих по меньшей мере один анион конденсированного фосфата, выбранный из группы, состоящей из формул (VI)-(VIII)
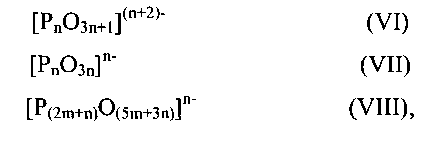
где n составляет по меньшей мере 2; где m составляет по меньшей мере 1; где, указанная смесь соединений, по существу, нейтрально заряжена; и дополнительно, где мольное соотношение фосфора и одновалентных и многовалентных катионов в катализаторе составляет от приблизительно 0,7 до приблизительно 1,7. В другом осуществлении, мольное соотношение фосфора и одновалентных и многовалентных катионов составляет приблизительно 1.
В еще одном осуществлении, катализатор получают с помощью стадии, на которой вводят в контакт: (а) газообразную смесь, содержащую воду, с (b) смесью соединений, содержащих соль конденсированного фосфата, выбранную из группы, состоящей из Ва2-x-sK2xH2sP2O7, Са2-х-sK2xH2sP2O7, Mn1-x-sK1+3xH3sP2O7, Mn1-x-sK2+2xH2sP2O7, а также их смесей; и (КРО3)n; где х и s являются большими или равными 0 и меньшими чем приблизительно 0,5 и n составляет по меньшей мере 2.
В одном осуществлении, мольное соотношение фосфора и катионов (т.е. MI+MII+MIII+…) составляет от приблизительно 0,7 до приблизительно 1,7; в другом осуществлении, мольное соотношение фосфора и катионов (т.е. MI+MII+MIII+…) составляет от приблизительно 0,8 до приблизительно 1,3, и в еще одном осуществлении, мольное соотношение фосфора и катионов (т.е. MI+MII+MIII+…) составляет приблизительно 1. Например, в осуществлении, если катализатор содержит калий (К+) и барий (Ва2+), мольное соотношение фосфора и металлов (К+Ва) составляет от приблизительно 0,7 до приблизительно 1,7; и в другом осуществлении, мольное соотношение фосфора и металлов (К+Ва) составляет приблизительно 1.
В одном осуществлении, катализатор может включать инертный носитель, который выполнен из материала, содержащего силикаты, алюминаты, уголь, оксиды металлов и их смеси. В качестве альтернативы, носитель является инертным по отношению к реакционной смеси, которая как ожидается, контактирует с катализатором. В другом осуществлении, способ получения катализатора может дополнительно включать стадию, на которой смешивают инертный носитель с катализатором до, во время или после смешивания и нагревания соединений, содержащих фосфор, при этом инертный носитель включает силикаты, алюминаты, уголь, оксиды металлов и их смеси. В еще одном осуществлении, способ получения катализатора может дополнительно включать стадию, на которой смешивают инертный носитель с катализатором до, во время или после смешивания и нагревания соединений, содержащих фосфор, и соединений, не содержащих фосфор, при этом инертный носитель включает силикаты, алюминаты, уголь, оксиды металлов и их смеси.
Смешивание соединений, содержащих фосфор, или соединений, содержащих и не содержащих фосфор, катализатора может быть выполнено любым способом, известным специалистам в данной области техники, таким как, в качестве примера, а не ограничения: смешивание твердых веществ и совместное осаждение. В способе смешивания твердых веществ, различные компоненты физически смешивают вместе с необязательным измельчением с помощью любого способа, известного специалистам в данной области техники, такого как, в качестве примера, а не ограничения, сдвиг, растяжение, разминание, экструзия и другие. В способе совместного осаждения, водный раствор или суспензию из различных компонентов, включая одно или более фосфатных соединений, получают с последующей необязательной фильтрацией и нагреванием для удаления растворителей и летучих веществ (например, воды, азотной кислоты, диоксида углерода, аммиака или уксусной кислоты). Нагревание обычно осуществляется с помощью любого способа, известного специалистам в данной области техники, такого как, в качестве примера, а не ограничения, конвекция, теплопроводность, излучение, СВЧ-нагрев и другие.
В одном осуществлении настоящего изобретения, катализатор прокаливают. Прокаливание представляет собой процесс, который позволяет химическую реакцию и/или термическое разложение и/или фазовый переход и/или удаление летучих веществ. Процесс прокаливания осуществляется при помощи любого оборудования, известного специалистам в данной области техники, такого как, в качестве примера, а не ограничения, печи или реакторы различных конструкций, в том числе шахтные печи, вращающиеся печи, печи с обогреваемым подом и реакторы с псевдоожиженным слоем. Температура прокаливания, в одном осуществлении, составляет от приблизительно 200°С до приблизительно 1200°С; в другом осуществлении, температура прокаливания составляет от приблизительно 250°С до приблизительно 900°С; и в еще одном осуществлении, температура прокаливания составляет от приблизительно 300°С до 600°С. Время прокаливания, в одном осуществлении, составляет от приблизительно одного часа до приблизительно семидесяти двух часов.
В то время как многие способы и устройства известны специалистам в данной области техники для фракционирования частиц на дискретные размеры и определения распределения частиц по размерам, просеивание является одним из самых простых и наименее дорогих и распространенных способов. Альтернативный способ определения распределения частиц по размерам представляет собой рассеяние света. После прокаливания катализатор, в одном осуществлении, измельчают и просеивают, чтобы обеспечить более однородный продукт. Распределение частиц катализатора по размерам включает разброс значений диаметра частиц, который, в одном осуществлении, составляет менее чем приблизительно 3; в другом осуществлении, распределение частиц катализатора по размерам включает разброс значений диаметра частиц, который составляет менее чем приблизительно 2; и в еще одном осуществлении, распределение частиц катализатора по размерам включает разброс значений диаметра частиц, который составляет менее чем приблизительно 1,5. В другом осуществлении настоящего изобретения, катализатор просеивают, чтобы медианный размер частиц составлял от приблизительно 50 мкм до приблизительно 500 мкм. В другом осуществлении настоящего изобретения, катализатор просеивают до медианного размера частиц от приблизительно 100 мкм до приблизительно 200 мкм.
В одном осуществлении настоящего изобретения, катализатор получают с помощью стадий, на которых объединяют BaHPO4 и КН2РО4 в мольном соотношении от приблизительно 3:2 до приблизительно 2:3 с образованием твердой смеси, и измельчают указанную твердую смесь с получением катализатора.
В другом осуществлении настоящего изобретения, катализатор получают с помощью стадий, на которых: (а) объединяют BaHPO4 и КН2РО4 в мольном соотношении от приблизительно 3:2 до приблизительно 2:3 с образованием твердой смеси; (b) измельчают указанную твердую смесь с получением смешанного порошка; (с) прокаливают указанный смешанный порошок при температуре приблизительно 550°С, с получением конденсированной фосфатной смеси; и (d) вводят в контакт указанную конденсированную фосфатную смесь с газообразной смесью, содержащей воду и молочную кислоту при температуре приблизительно 350°С и общем давлении приблизительно 25 бар, с получением указанного катализатора, и при этом парциальное давление воды в указанной газообразной смеси составляет приблизительно 12,5 бар.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют соединение, содержащее фосфор, нитратную соль, фосфорную кислоту и воду с образованием влажной смеси, при этом мольное соотношение фосфора и катионов, как в указанном соединении, содержащем фосфор, так и в указанной нитратной соли, составляет приблизительно 1, (b) прокаливают указанную влажную смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и от приблизительно 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (с) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют MnPO4·qH2O, KNO3 и Н3РО4, в мольном соотношении приблизительно 0,3:1:1, на безводной основе, и воду с получением влажной смеси, (b) прокаливают указанную влажную смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и от приблизительно 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (с) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют Ca2P2O7, KNO3 и H3PO4, в мольном соотношении приблизительно 1,6:1:1 и воду с получением влажной смеси, (b) прокаливают указанную влажную смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и от приблизительно 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (с) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют соединение, содержащее фосфор, нитратную соль, фосфорную кислоту и воду с получением влажной смеси, где мольное соотношение фосфора и катионов, как в соединении, содержащем фосфор, так и в нитратной соли, составляет приблизительно 1, (b) нагревают указанную влажную смесь до приблизительно 80°С при перемешивании почти до полного высушивания с образованием влажного твердого вещества, (с) прокаливают указанное влажное твердое вещество постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и от приблизительно 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (d) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют Ва(NO3)2, К2НРО4 и Н3РО4, в мольном соотношении приблизительно 3:1:4 и воду с получением влажной смеси, (b) нагревают указанную влажную смесь до приблизительно 80°С при перемешивании почти до полного высушивания с образованием влажного твердого вещества, (с) прокаливают указанное влажное твердое вещество постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и от приблизительно 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (d) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В еще одном осуществлении настоящего изобретения, катализатор получают с помощью стадий, на которых: (а) объединяют К2НРО4, Ва(NO3)2, Н3РО4 и воду, с образованием влажной смеси, при этом мольное соотношение Ba(NO3)2, К2НРО4 и Н3РО4 составляет приблизительно 3:1:4; (b) нагревают указанную влажную смесь до приблизительно 80°С при перемешивании почти до полного высушивания с образованием влажного твердого вещества, (с) прокаливают указанное влажное твердое вещество постадийно при температуре приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и от приблизительно 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (d) вводят в контакт указанное высушенное твердое вещество с газообразной смесью, содержащей воду и молочную кислоту, при температуре приблизительно 350°С и общем давлении приблизительно 25 бар, с получением указанного катализатора, и при этом парциальное давление воды в указанной газообразной смеси составляет приблизительно 12,5 бар.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют Mn(NO3)2·4H2O, К2НРО4 и Н3РО4, в мольном соотношении приблизительно 1:1,5:2 и воду с получением влажной смеси, (b) нагревают указанную влажную смесь до приблизительно 80°С при перемешивании почти до полного высушивания с образованием влажного твердого вещества, (с) прокаливают указанное влажное твердое вещество постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и от приблизительно 450°С до приблизительно 550°С с получением высушенного твердого вещества, и (d) измельчают и просеивают указанное высушенное твердое вещество до размера от приблизительно 100 мкм до приблизительно 200 мкм, с получением указанного катализатора.
В другом осуществлении, катализатор получают с помощью следующих стадий, на которых: (а) объединяют Ca2P2O7 и КН2РО4 в мольном соотношении приблизительно 3:1 с получением твердой смеси, и (b) прокаливают указанную твердую смесь постадийно при приблизительно 50°С, приблизительно 80°С, приблизительно 120°С и от приблизительно 450°С до приблизительно 550°С, с получением указанного катализатора.
После прокаливания и необязательного измельчения и просеивания, катализатор может быть использован для катализирования нескольких химических реакций. Неограничивающие примеры реакций представляют собой дегидратацию гидроксипропионовой кислоты в акриловую кислоту (как более подробно описано ниже), дегидратацию глицерина в акролеин, дегидратацию алифатических спиртов в алкены или олефины, дегидрогенизирование алифатических спиртов в эфиры, другие реакции дегидрогенизирования, гидролизы, алкилирования, деалкилирования, окисления, диспропорционирования, эстерификации, циклизации, изомеризации, конденсации, ароматизации, полимеризации, и другие реакции, которые могут быть очевидны специалистам в данной области техники.
V Примеры
Следующие примеры приведены для иллюстрации настоящего изобретения, но не предназначены для ограничения его объема.
ПРИМЕР 1
Твердый двухосновной фосфат калия, К2НРО4 (36,40 г, 209 ммоль, ≥98%; Sigma - Aldrich Co., St. Louis, МО; каталог №P3786) быстро смешивали с водным раствором нитрата бария, Ва(NO3)2 (2050 мл 0,08 г/мл маточного раствора, 627 ммоль, 99,999%; Sigma - Aldrich Co., St. Louis, МО; каталог №202754) при комнатной температуре. Фосфорную кислоту, Н3РО4 (58,7 мл 85 мас. %, плотность =1,684 г/мл, 857 ммоль; Acros Organics, Geel, Belgium; каталог №295700010), добавляли в суспензию, получая раствор, содержащий катионы калия (К+, MI) и бария (Ва2+, MII). Конечное значение рН суспензии составляло приблизительно 1,6. Суспензию, содержащую кислоту, затем медленно высушивали в стеклянном стакане при 80°С, используя нагревательную плиту с магнитным перемешиванием суспензии до испарения жидкости и почти полного высушивания материала. Нагревание продолжали в печи с циркуляцией воздуха (G1530A, НР6890 GC; Agilent Corp., Santa Clara, CA) при 50°C в течение 5,3 ч, затем при 80°С в течение 10 ч (0,5°С/мин линейное возрастание), с последующим охлаждением при 25°С. Материал прокаливали при 120°С в течение 2 часов (0,5°С/мин линейное возрастание) и еще при 450°С в течение 4 часов (2°С/мин линейное возрастание) в той же печи. После прокаливания материал оставляли внутри печи до самоохлаждения при температуре ниже 25°С перед тем, как вынуть его из печи. Наконец, катализатор измельчали и просеивали до размера от приблизительно 100 мкм до приблизительно 200 мкм.
ПРИМЕР 2
113,6 г 88 мас. % раствора L-молочной кислоты (Purac Corp., Lincolnshire, IL) разбавляли 386,4 г дистиллированной воды с получением раствора с ожидаемой концентрацией молочной кислоты 20 мас. %. Этот раствор нагревали до 95°С-100°С в течение 12-30 часов. Затем раствор охлаждали до комнатной температуры, и концентрации молочной кислоты и олигомеров молочной кислоты были измерены с помощью ВЭЖХ (Agilent 1100 система; Santa Clara, СА), снабженного детектором DAD и колонкой Waters Atlantis Т3 (каталог №186003748; Milford, MA) с использованием способов, хорошо известных специалистам в данной области техники. Раствор являлся, по существу, свободным от олигомеров.
ПРИМЕР 3
454 г 88 мас. % раствора L-молочной кислоты (Purac Corp., Lincolnshire, IL) разбавляли 1300 г воды. Разбавленный раствор нагревали до 95°С и выдерживали при этой температуре при перемешивании в течение приблизительно от 4 до 12 часов. Затем раствор охлаждали до комнатной температуры, и концентрации молочной кислоты и олигомеров молочной кислоты были измерены с помощью ВЭЖХ (Agilent 1100 система; Santa Clara, СА), снабженного детектором DAD и колонкой Waters Atlantis Т3 (каталог №186003748; Milford, MA) с использованием способов, хорошо известных специалистам в данной области техники. Раствор являлся, по существу, свободным от олигомеров. Наконец, раствор дополнительно разбавляли водой с получением 20 мас. % водного раствора L-молочной кислоты и являлся, по существу, свободным от олигомеров.
ПРИМЕР 4
Трубку длиной 13′′ (33 см) из нержавеющей стали и оклеенную стеклом (SGE Analytical Science Pty Ltd., Ringwood, Australia) с 4,0 мм внутренним диаметром (ID) набивали стекловолокном с длиной слоя 3′′ (7,6 см) и катализатором 5′′ (12,7 см) из Примера 1 (1,6 мл объем слоя) с получением 2,55 мл общего уплотненного слоя (8′′ или 20,3 см) и 1,6 мл (5′′ или 12,7 см) свободного пространства в верхней части реактора. Трубку помещали внутрь алюминиевого блока и помещали в печь из глинистого железняка серия 3210 (Applied Test Systems, Butler, PA) таким образом, что верх уплотненного слоя выравнивали по верхней части алюминиевого блока. Реактор устанавливали в режим нисходящего потока и оснащали Knauer Smartline 100 насосом подачи (Berlin, Germany), Brooks 0254 регулятором газового потока (Hatfield, РА), Brooks регулятором давления всасывания и улавливающим резервуаром. Печь из глинистого железняка нагревали таким образом, что температуру стенок реактора поддерживали постоянной при приблизительно 350°С во время течения реакции. Реактор поставлялся отдельными системами подачи жидкости и газа, которые смешивались вместе перед достижением слоя катализатора. Система подачи газа состояла из молекулярного азота при приблизительно 360 фунт/кв.дюйм изб. и при потоке 45 мл/мин. Система подачи жидкости представляла собой 20 мас. % водный раствор L-молочной кислоты, полученный, как в Примере 2, и поданный при 0,045 мл/мин (LHSV 1,7 ч-1), что дает время пребывания приблизительно 1 с (GHSV 3600 ч-1) в условиях STP. После протекания через реактор, газообразный поток охлаждали и жидкость собирали в улавливающий резервуар через 6 ч и 42 мин (402 мин в общем) для анализа при помощи офлайн ВЭЖХ (система Agilent 1100; Santa Clara, СА), оснащенной детектором DAD и колонкой Waters Atlantis Т3 (Каталог №186003748; Milford, MA) с использованием способов, хорошо известных специалистам в данной области техники. Газообразный поток анализировали онлайн с помощью GX (система Agilent 7890; Santa Clara, СА), оснащенной детектором FID и колонкой Varian CP-Para Bond Q (каталог №CP7351; Santa Clara, С А). Водный раствор акриловой кислоты содержал 14,8% акриловой кислоты и 1,5% молочной кислоты. Выход акриловой кислоты составил 80%, селективность составила 85% и конверсия молочной кислоты составила 94%.
ПРИМЕР 5
Реактор состоял из электрической печи из глинистого железняка (Applied Test systems, Butler, PA) с 8′′ (20,3 см) зоной подогрева с одним регулятором температуры, соединенным последовательно с другой электрической печью из глинистого железняка (Applied Test systems, Butler, PA) с 16′′ (40,6 см) зоной подогрева, содержащей два регулятора температуры и трубку реактора. Трубка реактора состояла из трубки, оклеенной боросиликатным стеклом 13′′ (33 см) (SGE Analytical Science Pty Ltd., Ringwood, Australia)) и трубки, оклеенной боросиликатным стеклом 23′′ (58,4 см), соединенных последовательно с помощью тройника Swagelok™, оснащенного внутренней термопарой и имеющего внутренний диаметр 9,5 мм. Голова колонки была оснащена 1/8′′ (3,2 мм) линией подачи азота из нержавеющей стали и 1/16′′ (1,6 мм) линией подачи жидкости из нержавеющей стали, оклеенной кварцевым стеклом, подключенной к ВЭЖХ насосу (Smartline 100, Knauer, Berlin, Germany), который соединен с резервуаром подачи молочной кислоты. Дно реактора было подключено к улавливающему резервуару с тефлоновым покрытием с использованием трубки 1/8′′ (3,2 мм) из нержавеющей стали, оклеенной кварцевым стеклом и тройников Swagelok™. Колонка реактора была набита пробкой из стекловаты, 13 г плавленого кварца, 16′′ (40,7 см) с катализатором Примера 1 (47 г и 28,8 мл, объем набитого слоя) и покрыта сверху 25 г плавленого кварца. Трубку реактора помещали в алюминиевый блок и помещали в реактор сверху в нисходящем потоке. Реактор предварительно нагревали до 375°С в течение ночи при 0,25 л/мин азота. Подача азота была увеличена до 0,85 л/мин в течение проведения эксперимента. Система подачи жидкости представляла собой 20 мас. % водный раствор L-молочной кислоты, полученный, как в Примере 3, и поданный при 0,845 мл/мин (LHSV 1,8 ч-1; 50,7 г/ч), что дает время пребывания приблизительно 1 с (GHSV 3600 ч-1) в условиях STP. Нагреватели из глинистого железняка были отрегулированы, чтобы дать внутреннюю температуру приблизительно 350°С. После протекания через реактор, газообразный поток охлаждали и жидкость собирали в улавливающий резервуар для анализа при помощи офлайн ВЭЖХ с использованием системы Agilent 1100 (Santa Clara, С А), оснащенной детектором DAD и колонкой Waters Atlantis ТЗ (Каталог №186003748; Milford, MA) с использованием способов, хорошо известных специалистам в данной области техники. Газообразный поток анализировали онлайн при помощи GC с использованием системы Agilent 7890 (Santa Clara, СА), оснащенной детектором FID и колонкой Varian CP-Para Bond Q (каталог № CP7351; Santa Clara, СА). Сырую реакционную смесь охлаждали и собирали в течение 159 ч, чтобы получить 748 г акриловой кислоты в виде сырой смеси с выходом 54%, 75% селективности получения акриловой кислоты и 69% конверсии молочной кислоты. Выход акриловой кислоты, с поправкой на потери во время стадии испарения, составил 61%, а ее селективность составила 89%. Водная концентрация акриловой кислоты составила 8,4 мас. %, и для молочной кислоты составила 6,3 мас. %.
ПРИМЕР 6
Эксперименты без присутствия катализатора дополнительно продемонстрировали влияние стабилизации подачи в реакторе из кварца. Все тестирования проводили с использованием 0,2 мл реактора. Пустые реакторы сравнили с теми, которые набиты аморфным кварцем (SiO2) (Sigma - Aldrich Co., St. Louis, МО) и Zirblast (Saint Gobain Zirpro, Le Pontet Cedex, France) как в реакторах из нержавеющей стали (SS) так и в реакторах из кварца. Результаты представлены в Таблице 1 ниже.
0,2 мл система реактора содержала регуляторы температур и потока масс и поставлялась с отдельными системами подачи жидкости и газа, которые смешивали перед достижением слоя катализатора. Система подачи газа состояла из молекулярного азота (N2) и гелия (Не), которые добавляли как внутренний стандарт для анализа при помощи газового хроматографа (GC). Система подачи жидкости представляла собой 20 мас. % водный раствор L-молочной кислоты, полученный как в 2, и поданный в верхнюю часть реактора, контролируя давление насоса до приблизительно 360 фунт/кв.дюйм изб. для преодоления какого-либо падения давления из слоя катализатора. Использовали реакторы из кварца или нержавеющей стали с аспектным соотношением (т.е. длина/диаметр) 75.
Были использованы различные слои катализатора и системы подачи газовых потоков, приводя к диапазону объемных скоростей (сообщается в данной заявке). Выходящий из реактора поток был также подключен к другой линии разбавления азота, которая разбавляла выходящий поток с коэффициентом два. Внутренний стандарт гелия нормализовал любые изменения в этом разбавлении для аналитических целей. Конденсированные продукты собирали с помощью системы отбора проб жидкости, охлажденной до температуры от 6,5°С до 10°С, в то время как газообразные продукты накапливали в воздушной прослойке виалы сбора. Накопленные в прослойке газообразные продукты анализировали с помощью клапанов отбора проб и онлайн газовой хроматографии (GC).
Систему подачи приводили в равновесие в течение 1 часа, после этого жидкую пробу отбирали в течение 2,7 часа и анализировали в конце эксперимента при помощи офлайн ВЭЖХ. В течение этого времени, газообразные продукты анализировали онлайн дважды при помощи GC и сообщали среднее значение. Жидкие продукты анализировали при помощи высокоэффективной жидкостной хроматографии (ВЭЖХ) на приборе Agilent 1200 Series (Agilent Technologies, Santa Clara, CA), Supelcogel-H колонка (4,6×250 мм; Supelco, St. Louis, МО), и диодно-матричного детектора и детектора с коэффициентом преломления (RI). Аналиты элюировали изократически, используя 0,005 М H2SO4 (водн.) как элюирующий буфер, в течение периода 30 мин и при потоке 0,2 мл/мин. Температуры колонки и RI детектора устанавливали на 30°С. Газообразные продукты анализировали при помощи системы газовой хроматографии Interscience Compact (GC) (Interscience BV, Breda, Netherlands) используя три детектора (один пламенно-ионизационный детектор - FID - и два термопроводящих - TCD-детектора «А» и «В», которые в данной заявке называются «TCD-А» и «TCD-B», соответственно). Газообразные продукты сообщали как среднее значение, данное двумя последовательными GC хроматограммами.
Колонка TCD-А была Rt-Q Bond (Restek Corp., Bellefonte, PA), имела 26 м в длину и I.D. 0,32 мм с толщиной пленки 10 мкм и использовали пре-колонку 2 м. Давление устанавливали на 150 кПа, расщепление потока 10 мл/мин. Температуру печи колонки устанавливали на 100°С с температурой желоба печи 50°С. Поток устанавливали на 5,0 мл/мин, газ-носитель - гелий. TCD-B колонка была Mol sieve MS5A (Restek Corp., Bellefonte, PA), имела длину 21 м и толщину пленки 10 мкм и использовали пре-колонку 2 м. Давление устанавливали на 200 кПа, расщепление потока 10 мл/мин. Температуру печи колонки устанавливали на 70°С с температурой желоба печи 50°С. Поток устанавливали на 2,0 мл/мин, газ-носитель - аргон. FID колонка была RTx-624 (Restek, Bellefonte, РА), имела длину 28 м и внутренний диаметр 0,25 мм с толщиной пленки 14 мм и использовали пре-колонку 2 м. Давление устанавливали на 100 кПа, расщепление потока 20 мл/мин. Температуру печи колонки устанавливали на 45°С с температурой желоба печи 50°С.
VI Результаты
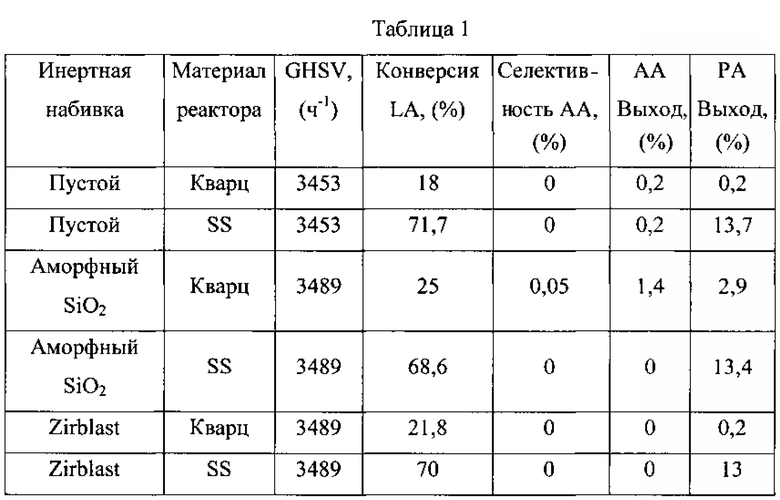
Результаты, представленные в Таблице 1, показывают, что при высоких объемных скоростях, наблюдалось очень небольшое количество побочных продуктов при использовании реакторов из кварца, с или без инертных набивок. Таким образом, было определено, что использование реакторов из кварца минимизировало две важные побочные реакции: олигомеризации молочной кислоты и восстановления в пропионовую кислоту. Это важно, чтобы оценить истинную активность катализаторов.
Приведенное выше описание дано только для ясности понимания, и никаких ненужных ограничений не должно быть истолковано из него, так как модификации в объеме настоящего изобретения могут быть очевидными специалистам в данной области техники.
Размеры и значения, описанные в данной заявке, не следует понимать как строго ограниченные в точности приведенными численными значениями. Вместо этого, если не указано иное, каждый такой размер должен обозначать как приведенное значение, так и функционально эквивалентный диапазон, окружающий это значение. Например, размер, раскрытый как «40 мм» означает «приблизительно 40 мм».
Каждый документ, цитируемый в данной заявке, включая любые перекрестные ссылки или родственные патенты или заявки, настоящим включен в данную заявку путем ссылки во всей своей полноте если специально не исключен или иным образом не ограничен. Цитирование любого документа не является признанием, что он является уровнем техники по отношению к любому изобретению, раскрытому или заявленному в данной заявке или что только он, или в любой комбинации с любой другой ссылкой или ссылками, учит, предполагает или раскрывает любое такое изобретение. Кроме того, в той степени, в которой любое значение или определение термина в данной заявке противоречит любому значению или определению этого же термина в документе, включенном путем ссылки, значение или определение для этого термина в данной заявке превалирует.
В то время как конкретные осуществления настоящего изобретения были проиллюстрированы и описаны, специалистам в данной области техники будет очевидно, что различные другие изменения и модификации могут быть выполнены без отступления от сущности и объема настоящего изобретения. Поэтому прилагаемая формула изобретения предназначена для охвата всех таких изменений и модификаций, которые находятся в пределах объема настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Катализатор для получения акриловой кислоты и ее производных на основе биологического сырья и способ его получения | 2014 |
|
RU2662229C2 |
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ | 2013 |
|
RU2587494C2 |
| ОЧИСТКА АКРИЛОВОЙ КИСЛОТЫ, ПОЛУЧЕННОЙ ИЗ БИОЛОГИЧЕСКОГО СЫРЬЯ, С ПОЛУЧЕНИЕМ СЫРОЙ И ЛЕДЯНОЙ АКРИЛОВОЙ КИСЛОТЫ | 2013 |
|
RU2599640C2 |
| КАТАЛИТИЧЕСКАЯ КОНВЕРСИЯ ГИДРОКСИПРОПИОНОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ В АКРИЛОВУЮ КИСЛОТУ И ЕЕ ПРОИЗВОДНЫЕ | 2013 |
|
RU2586327C2 |
| КАТАЛИЗАТОРЫ ДЛЯ КОНВЕРСИИ ГИДРОКСИПРОПИОНОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ В АКРИЛОВУЮ КИСЛОТУ ИЛИ ЕЕ ПРОИЗВОДНЫЕ | 2013 |
|
RU2591192C2 |
| Полиакриловая кислота на основе полученной из биологического сырья акриловой кислоты и ее производных | 2013 |
|
RU2606124C1 |
| КАТАЛИЗАТОРЫ ДЛЯ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ | 2013 |
|
RU2586329C2 |
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ ИЗ ГИДРОКСИПРОПИОНОВОЙ КИСЛОТЫ | 2017 |
|
RU2719485C1 |
| Катализаторы для дегидратации гидроксипропионовой кислоты и ее производных | 2016 |
|
RU2694897C1 |
| КАТАЛИЗАТОРЫ ДЛЯ ПОЛУЧЕНИЯ АКРИЛОВОЙ КИСЛОТЫ ИЗ МОЛОЧНОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ В ЖИДКОЙ ФАЗЕ | 2017 |
|
RU2715707C1 |
Изобретение относится к способам конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси. Например, способ включает следующие стадии, на которых: a. обеспечивают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота находится в мономерной форме в указанном водном растворе; b. объединяют указанный водный раствор с инертным газом с образованием смеси водного раствора/газа; c. испаряют указанную смесь водного раствора/газа с получением газообразной смеси; d. дегидратируют указанную газообразную смесь путем введения в контакт указанной газообразной смеси с катализатором дегидратации под давлением по меньшей мере 80 фунт/кв.дюйм изб. (0,55 МПа изб.) с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей. Представленные способы осуществляются с высоким выходом и селективностью и без значительной конверсии в нежелательные побочные продукты, такие как ацетальдегид, пропановая кислота и уксусная кислота. 6 н. и 28 з.п. ф-лы, 1 табл., 6 пр.
1. Способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
a. обеспечивают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота находится в мономерной форме в указанном водном растворе;
b. объединяют указанный водный раствор с инертным газом с образованием смеси водного раствора/газа;
c. испаряют указанную смесь водного раствора/газа с получением газообразной смеси; и
d. дегидратируют указанную газообразную смесь путем введения в контакт указанной газообразной смеси с катализатором дегидратации под давлением по меньшей мере 80 фунт/кв.дюйм изб. (0,55 МПа изб.) с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей.
2. Способ по п. 1, отличающийся тем, что давление составляет от 80 фунт/кв.дюйм изб. (0,55 МПа изб.)до 550 фунт/кв.дюйм изб. (3,79 МПа изб.).
3. Способ по п. 1, отличающийся тем, что давление составляет от 150 фунт/кв.дюйм изб. (1,03 МПа изб.) до 500 фунт/кв.дюйм изб (3,45 МПа изб.).
4. Способ по п. 1, отличающийся тем, что температура во время стадии испарения составляет от 165°С до 450°С.
5. Способ по п. 1, отличающийся тем, что температура во время стадии испарения составляет от 250°С до 375°С.
6. Способ по п. 1, отличающийся тем, что GHSV (часовая объемная скорость газа) на стадии испарения составляет от 720 ч-1 до 36000 ч-1.
7. Способ по п. 1, отличающийся тем, что температура во время стадии дегидратации составляет от 150°С до 500°С.
8. Способ по п. 1, отличающийся тем, что температура во время стадии дегидратации составляет от 300°С до 450°С.
9. Способ по п. 1, отличающийся тем, что GHSV на стадии дегидратации составляет от 720 ч-1 до 36000 ч-1.
10. Способ по п. 1, отличающийся тем, что GHSV на стадии дегидратации составляет 3600 ч-1.
11. Способ по п. 1, отличающийся тем, что содержание гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет от 5 мас. % до 50 мас. % указанного водного раствора.
12. Способ по п. 1, отличающийся тем, что содержание гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет от 10 мас. % до 25 мас. % указанного водного раствора.
13. Способ по п. 1, отличающийся тем, что инертный газ выбран из группы, состоящей из воздуха, азота, гелия, аргона, диоксида углерода, монооксида углерода, пара и их смесей.
14. Способ по п. 1, отличающийся тем, что газообразная смесь содержит от 1 мол. % до 10 мол. % указанной гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей.
15. Способ по п. 1, отличающийся тем, что указанную стадию испарения выполняют в реакторе, при этом указанный реактор имеет внутреннюю поверхность, содержащую материал, выбранный из группы, состоящей из кварца, боросиликатного стекла, кремния, сплава Hastelloy, инконеля, искусственного сапфира, нержавеющей стали и их смесей.
16. Способ по п. 1, отличающийся тем, что указанную стадию дегидратации выполняют в реакторе, при этом указанный реактор имеет внутреннюю поверхность, содержащую материал, выбранный из группы, состоящей из кварца, боросиликатного стекла, кремния, сплава Hastelloy, инконеля, искусственного сапфира, нержавеющей стали и их смесей.
17. Способ по п. 1, отличающийся тем, что указанная гидроксипропионовая кислота представляет собой молочную кислоту.
18. Способ по п. 17, отличающийся тем, что селективность получения акриловой кислоты из молочной кислоты составляет по меньшей мере 50%.
19. Способ по п. 17, отличающийся тем, что селективность получения акриловой кислоты из молочной кислоты составляет по меньшей мере 80%.
20. Способ по п. 17, отличающийся тем, что селективность получения пропановой кислоты из молочной кислоты составляет менее чем 5%.
21. Способ по п. 17, отличающийся тем, что селективность получения пропановой кислоты из молочной кислоты составляет менее чем 1%.
22. Способ по п. 17, отличающийся тем, что конверсия указанной молочной кислоты составляет более чем 50%.
23. Способ по п. 17, отличающийся тем, что конверсия указанной молочной кислоты составляет более чем 80%.
24. Способ по п. 1, отличающийся тем, что указанную стадию испарения выполняют под давлением от 80 фунт/кв.дюйм изб. (0,55 МПа изб.) до 550 фунт/кв.дюйм изб. (3,79 МПа изб.).
25. Способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
a. обеспечивают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота содержит олигомеры в указанном водном растворе;
b. нагревают указанный водный раствор при температуре от 50°С до 100°С с удалением указанных олигомеров указанной гидроксипропионовой кислоты и получением водного раствора мономерной гидроксипропионовой кислоты;
c. объединяют указанный водный раствор мономерной гидроксипропионовой кислоты с инертным газом с образованием смеси водного раствора/газа;
d. испаряют указанную смесь водного раствора/газа с получением газообразной смеси; и
e. дегидратируют указанную газообразную смесь путем введения в контакт указанной смеси с катализатором дегидратации с получением указанной акриловой кислоты, производных акриловой кислоты и их смесей.
26. Способ по п. 25, отличающийся тем, что после указанной стадии нагревания указанные олигомеры составляют менее чем 5 мас. %, исходя из общего количества гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей.
27. Способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
a. обеспечивают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота находится в мономерной форме в указанном водном растворе;
b. объединяют указанный водный раствор с инертным газом с образованием смеси водного раствора/газа;
c. испаряют указанную смесь водного раствора/газа с получением газообразной смеси;
d. дегидратируют указанную газообразную смесь путем введения в контакт указанной смеси с катализатором дегидратации с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей; и
e. охлаждают указанную акриловую кислоту, производные акриловой кислоты или их смеси при GHSV более чем 360 ч-1.
28. Способ по п. 27, отличающийся тем, что GHSV на стадии охлаждения составляет более чем 720 ч-1.
29. Способ конверсии молочной кислоты в акриловую кислоту, включающий следующие стадии, на которых:
a. разбавляют 88% водный раствор молочной кислоты водой с образованием 20 мас. % водного раствора молочной кислоты;
b. нагревают указанный 20 мас. % водный раствор молочной кислоты при температуре от 95°С до 100°С для удаления олигомеров указанной молочной кислоты с получением водного раствора мономерной молочной кислоты, содержащего по меньшей мере 95 мас. % указанной молочной кислоты в мономерной форме, исходя из общего количества молочной кислоты;
c. объединяют указанный водный раствор мономерной молочной кислоты с азотом с образованием смеси водного раствора/газа;
d. испаряют указанную смесь водного раствора/газа в реакторе с внутренней поверхностью из боросиликатного стекла при GHSV 7200 ч-1 при температуре от 300°С до 350°С с получением газообразной смеси, содержащей 2,5 мол. % молочной кислоты и 50 мол. % воды;
e. дегидратируют указанную газообразную смесь в реакторе с внутренней поверхностью из боросиликатного стекла при GHSV 3600 ч-1 при температуре от 350°С до 425°С путем введения в контакт указанной смеси с катализатором дегидратации под давлением 360 фунт/кв.дюйм изб. (2,48 МПа изб.) с получением указанной акриловой кислоты; и
f. охлаждают указанную акриловую кислоту с получением раствора акриловой кислоты при GHSV от 360 ч-1 до 36000 ч-1.
30. Способ конверсии гидроксипропионовой кислоты, производных гидроксипропионовой кислоты и их смесей в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
а. обеспечивают водный раствор, содержащий гидроксипропионовую кислоту, производные гидроксипропионовой кислоты или их смеси, при этом указанная гидроксипропионовая кислота находится в мономерной форме в указанном водном растворе, причем содержание гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет от 10 мас. % до 25 мас. % указанного водного раствора;
b. объединяют указанный водный раствор с инертным газом с образованием смеси водного раствора/газа;
c. испаряют указанную смесь водного раствора/газа с получением газообразной смеси; и
d. дегидратируют указанную газообразную смесь путем введения в контакт указанной смеси с катализатором дегидратации с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей.
31. Способ по п. 30, отличающийся тем, что содержание гидроксипропионовой кислоты, производных гидроксипропионовой кислоты или их смесей составляет 20 мас. % указанного водного раствора.
32. Способ конверсии алкиллактатов в акриловую кислоту, производные акриловой кислоты или их смеси, включающий следующие стадии, на которых:
a. обеспечивают алкиллактаты или раствор, содержащий алкиллактаты и растворитель;
b. объединяют указанные алкиллактаты или указанный раствор, содержащий указанные алкиллактаты и указанный растворитель, с инертным газом с образованием смеси жидкость/газ;
c. испаряют указанную смесь жидкость/газ с получением газообразной смеси; и
d. дегидратируют указанную газообразную смесь путем введения в контакт указанной газообразной смеси с катализатором дегидратации под давлением по меньшей мере 80 фунт/кв.дюйм изб. (0,55 МПа изб.) с получением указанной акриловой кислоты, производных акриловой кислоты или их смесей.
33. Способ по п. 32, отличающийся тем, что указанные алкиллактаты выбраны из группы, состоящей из метиллактата, этиллактата, бутиллактата, 2-этилгексиллактата и их смесей.
34. Способ по п. 32, отличающийся тем, что растворитель выбран из группы, состоящей из воды, метанола, этанола, бутанола, 2-этилгексанола, изобутанола, изооктилового спирта и их смесей.
| US 2859240 A, 04.11.1958 | |||
| CN 101537362 A, 23.09.2009 | |||
| WO 03082795 A2, 09.10.2003 | |||
| RU 2008137274 A, 27.03.2010. |
Авторы
Даты
2016-12-20—Публикация
2013-04-11—Подача