Изобретение относится к медицине, более точно к неврологии и эндокринологии, и может быть использовано для прогнозирования восстановления чувствительности кожных зон нижних конечностей при лечении пациентов, страдающих диабетической полиневропатией с болевым синдромом.
Диабетическая полиневропатия (ДПН) является частым осложнением сахарного диабета. Среди клинических форм ДПН наиболее часто встречается хроническая дистальная симметричная сенсорная и сенсомоторная полиневропатия, сопровождающаяся болевым синдромом. Боль при ДПН - это самый распространенный вариант нейропатического типа боли. В лечении ДПН особое место отводят нормализации уровня глюкозы в крови, а при лечении болевого синдрома широко используют антидепрессанты, например дулоксетин (симбалта) /Аль-Замиль М.Х. Эффективность Симбалты в лечении болевого синдрома у пациентов с диабетической полиневропатией. Практическая неврология и нейрореабилитация. 2008: (1) с. 16-18; 2. Detke M.., Goldstein D.., Lu Y.., Iyengar S.. Эффективность дулоксетина при лечении болей, связанных с диабетической нейропатией. Joint Antidepressant Group. Eli Lilly and Company, Indianapolis, IN, United States Источник: Diabetologia 46 (Suppl. 2): A315, 2003/. Кроме того, в лечении этой патологии используют лидокаин и мексилетин. Механизм действия основан на стабилизации мембран нейронов за счет блокады натриевых каналов лидокаин /Аль-Замиль М.Х. Сочетание фибулярного туннельного синдрома с дистальной симметричной полиневропатией нижних конечностей при сахарном диабете, клиническая неврология, 2011. - N 3. - С. 3-7; Аль-Замиль М.Х. Применение метода внутрикостной блокады в лечении нейропатической боли. Практическая неврология и нейрореабилитация, 2007 - N 4 - С 36-38.; Арсюхин Н.А. Внутрикостные блокады при лечении дистальной симметричной диабетической полинейропатии с болевым синдромом. Кандидатская диссертация. 2012. Москва. РУДН/.
Из патента РФ 2273028 известен способ прогнозирования диабетической периферической нейропатии у детей и подростков, включающий определение в периферической крови серологическим методом мозгового нейротрофического фактора. При величине исследуемого нейротрофина больше 9000 пг/мл диагностируют субклиническую стадию ДИН. Способ позволяет прогнозировать осложнение при сахарном диабете 1 типа у детей и подростков и своевременно начать профилактическое лечение. Однако, этот способ не предусматривает прогнозирование восстановления чувствительности при данной патологии с болевым синдромом.
Из патента РФ №2491925 известен способ прогнозирования эффективности лечения диабетической полиневропатии у больных сахарным диабетом 2 типа и дислипидемией. Для этого оценивают выраженность проявлений диабетической полинейропатии с учетом баллов нейропатического дисфункционального счета, определяют содержание тришлицеридов и гликозилированного гемоглобина в крови до лечения и на основании полученных данных выбирают стратегию лечения с последующим определением вероятности успешной коррекции диабетической полинейропатии по формуле. Разработанный метод позволяет выбрать эффективный способ лечения ДГШ и профилактировать развитие язвенных дефектов стоп, синдрома диабетической стопы, что способствует снижению риска инвалидизации пациента и потери им своего социального и трудового потенциала. Этот способ был выбран в качестве прототипа.
Недостатком этого способа является то, что этот способ не позволяет прогнозировать восстановление поверхностной чувствительности при лечении полиневропатий с болевым синдромом. Кроме того, способ является достаточно сложным, т.к. при его реализации необходимо определение триглицеридов и компьютерная обработка результатов.
Техническим результатом заявленного изобретения является прогнозирование возможности устранения такого грозного осложнения диабетической полинейропатии как нарушения поверхностной чувствительности в дистальных отделах нижних конечностях, а также возможность использования способа для прогноза течения дистальной полиневропатии при сахарном диабете 2 типа после регрессии болевого синдрома до умеренных величин. Кроме того, способ обеспечивает возможность его использования в амбулаторных условиях, или в условиях отсутствия доступа к лабораторным исследованиям, например в отдаленных районах, а также при отсутствии возможности квалифицированного исследования тактильной и температурной чувствительности.
Этот технический результат достигается тем, что в известном способе прогнозирования восстановления поверхностной чувствительности при лечении диабетической дистальной полиневропатии нижних конечностей с болевым синдромом, включающий специфическую антидиабетическую терапию и неврологическое исследование пациента до и после лечения с последующим вынесением суждения, в качестве неврологического исследования определяют степень выраженности болевого синдрома по визуальной аналоговой шкале (ВАШ) в баллах и при снижении после лечения степени выраженности болевого синдрома до 4 баллов и ниже прогнозируют после лечения достоверное восстановление тактильной болевой и температурной чувствительности в дистальных отделах нижних конечностей.
Степень выраженности болевого синдрома определяют по визуальной аналоговой шкале (ВАШ), русифицированного макгилловского болевого опросника и схеме тела.
В качестве медикаментозных средств лечения полиневропатий используют антидепрессанты, например дулоксетин.
В качестве медикаментозного средства при лечении полиневропатии используют внутрикостное введение лидокаина в губчатое вещество головки малоберцовой кости.
Степень выраженности болевого синдрома определяют по визуальной аналоговой шкале (ВАШ), русифицированного макгилловского болевого опросника и схеме тела.
Степень выраженности клинических сенсорных нарушений определяют по 5-балльной шкале, как указано при применении неврологического дисфункционального счета NDS.
1. Н.А. Белякова, Д.Г. Михайлова, И.Г. Цветкова, С.А. Горбачева, А.Л. Старцев. КЛИНИКО-ПСИХОЛОГИЧЕСКИЕ ОСОБЕННОСТИ БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ 2 ТИПА РАЗЛИЧНЫХ ВОЗРАСТНЫХ ГРУПП. Журнал «Профилактическая и клиническая медицина», 2010, №4, С. 32-36.
2. Caroline A. Abbott. Prevalence and Characteristics of Painful Diabetic Neuropathy in a Large Community-Based Diabetic Population in the U.K. Diabetes Care October 2011 vol. 34 no. 10 2220-2224.
Мы отдельно изучали нарушения каждого вида чувствительности по 5-балльной шкале (температурная, тактильная, болевая и вибрационная), после чего сравнивали эти нарушения между собой и с исходным уровнем. Далее для определения степени невропатии эти данные вводятся в таблицу определения DNS для расчета степени выраженности этой невропатии
Способ осуществляют следующим образом.
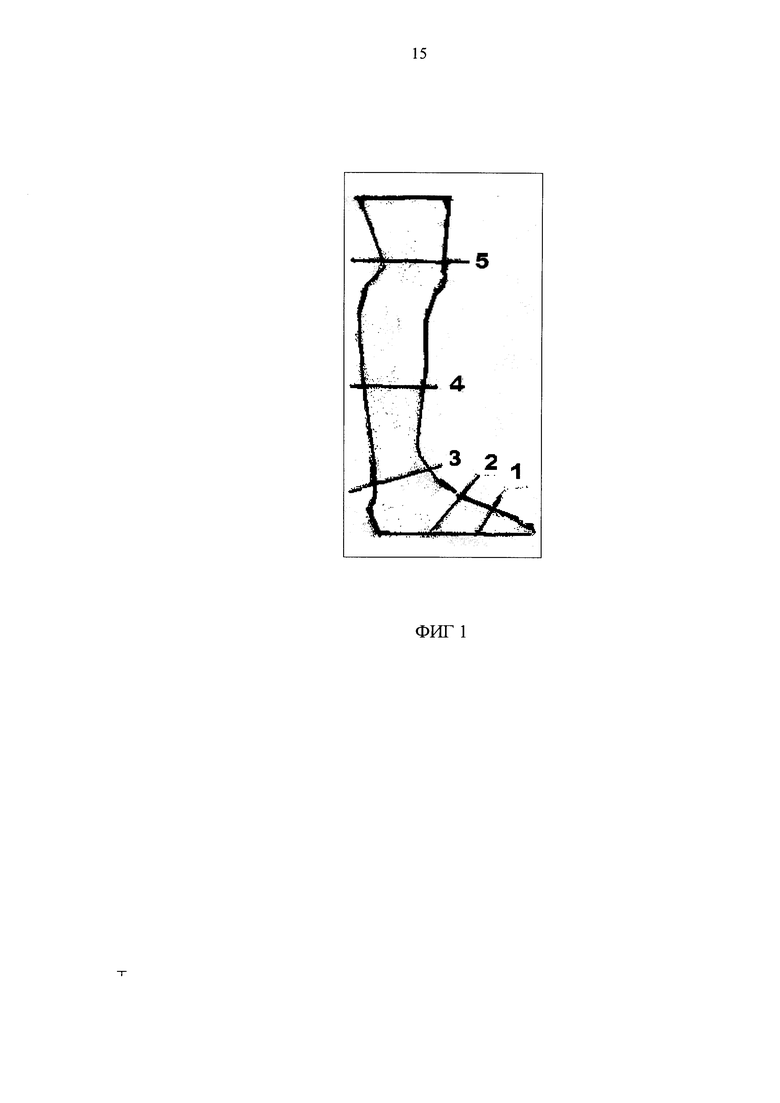
Исследование чувствительности проводилось от проксимального отдела нижней конечности до дистального. Начиналось исследование с участка кожи, где пациент хорошо различал соприкосновение монофиламента (Semmens-wienstien NCM серии 5,07, США), при исследовании тактильной чувствительности, четко отличал холодное от теплого при исследовании температурной чувствительности с помощью термометра «Thio-Therm» (NeueMedizintechnic GMBH, Германия) и отчетливо дифференцировал острый конец иглы от тупого при исследовании болевой чувствительности с помощью Нейротепса. Ошибки восприятия различий при исследовании каждой из этих чувствительностей принимались как признак нарушения исследованной чувствительности. Выраженность каждого из нарушений тактильной, температурной и болевой чувствительности определялась по 5-балльной шкале в зависимости от уровня начала сенсорного нарушения, отмеченного на исследованной конечности. Снижение чувствительности на уровне дистального отдела пальцев стопы соответствовало 1 баллу, на уровне середины стопы 2 баллам, на уровне голеностопного сустава 3 баллам, на уровне середины голени 4 баллам и на уровне коленного сустава 5-баллам. ФИГ. 1.
2. Вибрационная чувствительность проверялась с помощью градуированного камертона «Riedel-Siefert» (фирмы Kicher + Wilhelm, Германия) 128 Гц. Исследование проводилось на кончиках больших пальцев стоп и на медиальной поверхности пяточных костей. Выраженность вибрационной чувствительности определялась по 8-балльной шкале, отмеченной на кончиках камертона.
Определение выраженности болевого синдрома по ВАШ.
Степень выраженности болевого синдрома определяют по визуальной аналоговой шкале (ВАШ), русифицированного макгилловского болевого опросника и схеме тела, Аль-Замиль М.Х. Клинико-морфологические корреляции при поясничном остеохондрозе. Кандидатская диссертация. 2004. Москва РУДН. Арсюхин Н.А. Внутрикостные блокады при лечении дистальной симметричной диабетической полинейропатии с болевым синдромом. Кандидатская диссертация. 2012. Москва. РУДН/.
Клинические обследования проводились до лечения и сразу после окончания курса лечения (через месяц после начала лечения) и в отдаленном периоде (через 3 месяца после начала лечения).
Результаты клинических наблюдений при лечении пациентов дулоксетином.
Под наблюдением с 2004 по 2014 гг. в городских поликлиниках №11 УЗ ЮЗАО и №158 УЗ ЗАО г. Москвы, Эндокринологическом Центре УЗ ЮЗАО г. Москвы и в Клинике Мозга и Позвоночника г. Подольска находились 62 пациентов (Ж:38, М:24) с диагнозом Сахарный диабет (СД) 2 типа. Диагноз СД 2 типа был установлен эндокринологами на основании анамнеза, клинического осмотра и результатов лабораторных анализов как исследование гликемического профиля и определение уровня гликозилированного гемоглобина и инсулина.
В данную работу вошли пациенты с компенсированным сахарным диабетом. При этом уровень гликозилированного гемоглобина не превышал 7%. В исследование включены только пациенты с выраженным болевым синдромом в дистальных отделах нижних конечностей на фоне перенесенной дистальной полиневропатии нижних конечностей.
Из исследования были исключены пациенты с сопутствующими заболеваниями, которые могли стать патогенетическим фактором для развития ДПНК или причиной ухудшения течения ДПНК, такие как выраженная варикозная болезнь, выраженные отеки нижних конечностей, алкогольная болезнь, наследственные миопатии и полиневропатии, облитерирующий эндартериит, ревматическое поражение и подагра. Также были исключены пациенты с признаками диабетической стопы.
После недостаточной эффективности применения противовоспалительных препаратов пациенты прошли курс лечения препаратом дулоксетин в дозировке 60 мг/день в течение 3-х месяцев.
Результаты лечения
До лечения пациенты оценивали выраженность болевого синдрома по ВАШ от 7 до 10 баллов (в среднем 9,1±0,2 балла). После лечения болевой синдром достоверно регрессировал до 4,5±±0,6 балла (р<0,01). По результатам лечения мы распределили пациентов на 3 группы в зависимости от выраженности сохранившегося болевого синдрома после лечения. Для определения выраженности болевого синдрома мы принимали ВАШ. С помощью данного инструмента пациент сам выбирал из 10 баллов количество баллов, которые соответствуют его болевому синдрому. В первую группу вошли пациенты с выраженностью болевого синдрома после лечения 4 балла и ниже (n=32). Во вторую группу вошли пациенты с выраженностью болевого синдрома после лечения больше 4 балла и до 6 баллов баллов (n=16). Третья группа включала в себе пациентов с болевым синдромом между от 6 баллов и выше (n=14).
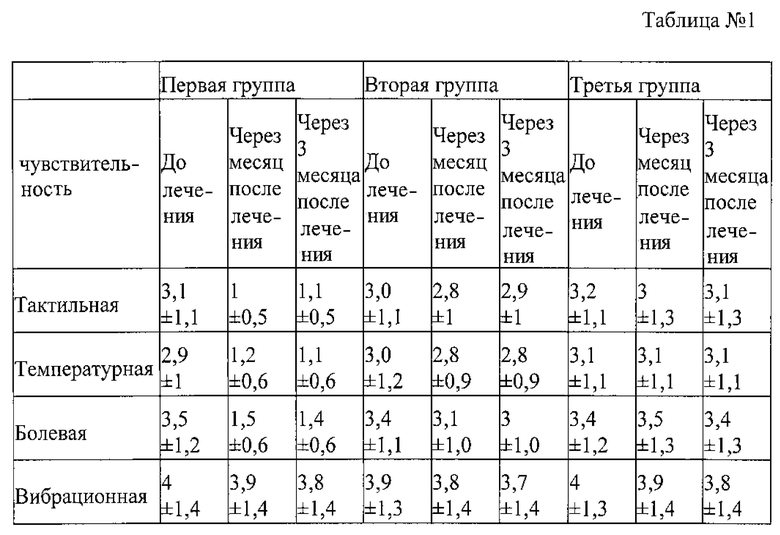
При исследовании температурной, болевой, тактильной и вибрационной чувствительности до и после лечения мы получили следующее результаты, которые продемонстрированы в таблице №1.
В первой группе отмечалось достоверное снижение зон тактильной, температурной и болевой чувствительности (p<0,01) и продолжало это снижение в отдаленном периоде через 2 месяца после окончания лечения (через 3 месяца после начала лечения) без существенной динамики (p>1), как указано в таблице №1.
Во второй и третей группах зоны сенсорной, температурной и болевой чувствительностей достоверно не изменились от тех зон до лечения (p>1). Таблица №1.
Таким образом, мы отмечаем достоверное уменьшение зоны снижения температурной, болевой и тактильной чувствительности после лечения на фоне снижения болевого синдрома до 4 балла и ниже по ВАШ. Однако в группе пациентов, у которых болевой синдром сохранился после лечения больше 4 балла по ВАШ, зоны тактильной, температурной и болевой чувствительностей остаются без существенного изменения.
Однако вибрационная чувствительность во всех группах сохранилась без существенной динамики после лечения (p>1). Результаты вибрационной чувствительности в трех группах указаны в таблице №1.
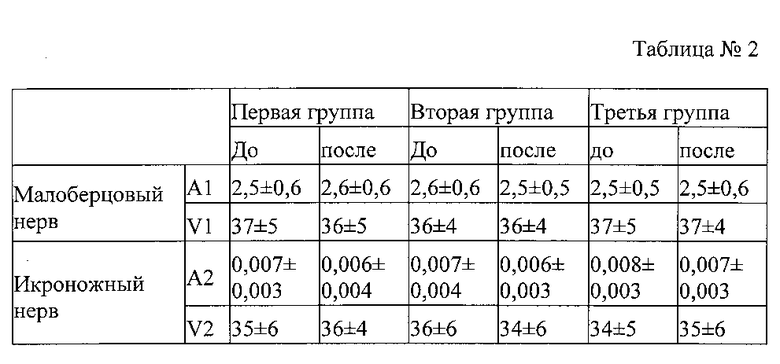
При электромиографическом исследовании малоберцовых и икроножных нервов до и после лечения существенного изменения скорость проведения импульсов по нервам и амплитуды M-ответа для моторных волокон и потенциала действия для сенсорных волокон не отмечается (p>1). Результаты полученных ЭМГ исследований указаны в таблице №2.
Выраженное снижение болевого синдрома в результате применения центральных аналгетиков, не обладающих антивоспалительным действием как дулоксетин, сопровождается уменьшением зоны снижения температурной, болевой и тактильной чувствительности, отмеченной до лечения. При этом вибрационная чувствительность и ЭМГ нарушений остаются без существенной динамики.
Результаты клинических наблюдений при лечении пациентов внутрикостным введением лидокаина в губчатое вещество головки малоберцовой кости
Материалы и методы: Под нашим наблюдением с 2004 по 2014 гг. в городских поликлиниках №11 УЗ ЮЗАО и №158 УЗ ЗАО г. Москвы, Эндокринологическом Центре УЗ ЮЗАО г. Москвы и в Клинике Мозга и Позвоночника г. Подольска находились 55 пациентов (Ж:42, М:13) с диагнозом СД 2 типа. Диагноз СД 2 типа был установлен эндокринологами на основании анамнеза, клинического осмотра и результатов лабораторных анализов, таких как исследование гликемического профиля и определение уровня гликозилированного гемоглобина и инсулина.
В данную работу вошли пациенты с компенсированным сахарным диабетом. При этом уровень гликозилированного гемоглобина не превышал 7%. В исследование включены только пациенты с выраженным болевым синдромом в дистальных отделах нижних конечностей на фоне перенесенной дистальной полиневропатии нижних конечностей.
Из исследования были исключены пациенты с сопутствующими заболеваниями, которые могли стать патогенетическим фактором для развития ДПНК или причиной ухудшения течения ДПНК, такие как выраженная варикозная болезнь, выраженные отеки нижних конечностей, алкогольная болезнь, наследственные миопатии и полиневропатии, облитерирующий эндартериит, ревматическое поражение и подагра. Также были исключены пациенты с признаками диабетической стопы.
Клиническое исследование
После недостаточной эффективности применения противовоспалительных препаратов и препаратов антиконвульсантов и антидепрессантов пациенты прошли курс лечения с введением 2% -2 мл лидокаина в губчатое вещество малоберцовой кости. Процедура проводилась 2 раза/неделю (5 процедур на курс лечения).
Результаты лечения. До лечения пациенты оценивали выраженность болевого синдрома по ВАШ от 8 до 10 баллов (в среднем 9,3±0,2 балла). После лечения болевой синдром достоверно регрессировал до 2,5±0,5 балла (р<0,01). У 44 пациентов болевой синдром после процедуры регрессировал до 4 балла и ниже (первая группа). У 6 пациентов болевой синдром выше 4 балла и до 6 балла (вторая группа) и у 5 пациентов от 6 баллов и выше (третья группа).
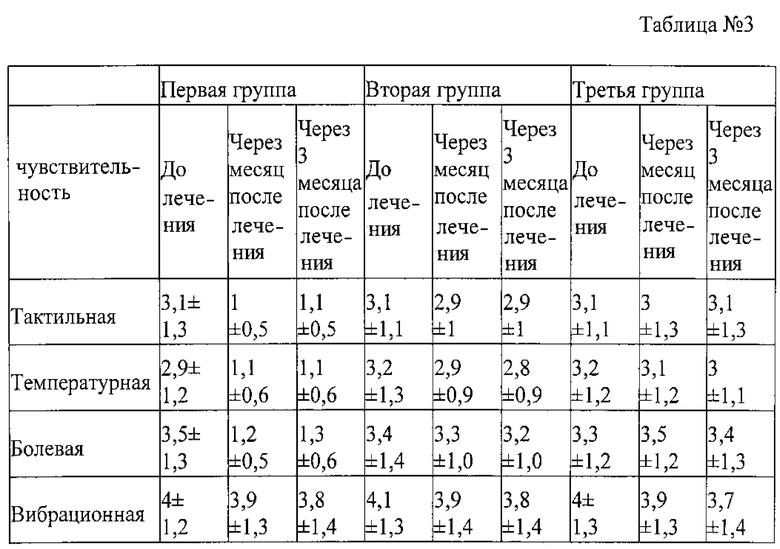
При исследовании зоны снижения чувствительности по 5-балльной шкале, как указано на фиг. 1, до и после лечения мы получили следующее результаты, которые продемонстрированы в следующей таблице №3.
В первой группе отмечалось достоверное снижение зон тактильной, температурной и болевой чувствительности (р<0,01) с сохранением данного результата в отдаленном периоде после лечения без существенной динамики (р>1). При этом вибрационная чувствительность достоверно оставалась без динамики (р>1).
Во второй и третьей группах зоны сенсорной, температурной и болевой чувствительностей достоверно не изменились от тех зон до лечения. Выраженность вибрационной чувствительности при этом сохранилась без достоверной динамики
Таким образом, мы отмечаем достоверное снижение зон снижения температурной, болевой и тактильной чувствительности после лечения на фоне снижения болевого синдрома до 4 балла и ниже по ВАШ с сохранением данного результата в отдаленном периоде. Однако в группе пациентов, у которых болевой синдром сохранился после лечения выше 4 баллов по ВАШ, зоны тактильной, температурной и болевой чувствительностей остаются без существенного изменения. Важно отметить, что вибрационная чувствительности во всех группах сохранилась без существенной динамики (р>1).
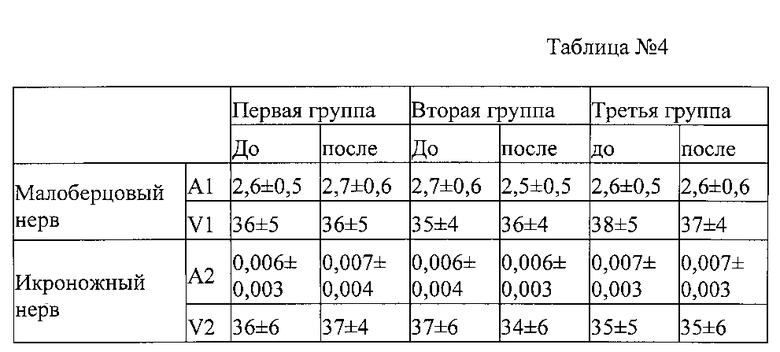
При электромиографическом исследовании малоберцовых и икроножных нервов до и после лечения существенного изменения скорость проведения импульсов по нервам и амплитуды M-ответа для моторных волокон и потенциала действия для сенсорных волокон не отмечается (p>1).
Выраженное снижение болевого синдрома в результате применения внутрикостного введения в губчатое вещество малоберцовой кости приводит к снижению зоны снижения температурной, болевой и тактильной чувствительности, отмеченной до лечения. При этом вибрационная чувствительность и ЭМГ нарушений остаются без существенной динамики.
Такой феномен может быть объяснен следующим образом.
При развитии повышенной болевой сенситизации в задних рогах спинного мозга как защитная реакция развивается сегментарное игнорирование поступления импульсов по медленным волокнам и в том числе поступающие по медленным волокнам поверхностной чувствительности. Игнорирование может быть в результате активации промежуточных нейронов (клетки обратного контроля) оказывающих тормозящий эффект на дендриты всех афферентов в измененном сегменте.
Этот феномен объясняет причину усиления зоны и выраженности снижения поверхностной чувствительности в остром периоде болевого синдрома и уменьшение выраженности и зоны гипестезии после снятия болевого синдрома препаратами, не оказывающими антивоспалительным действием. Теория входных ворот (авторы: Мелзака и Волла - 1976 г.) гласит, что поступление импульсов по быстрым волокнам возбуждает клетка ЖС (желатинозная субстанции), в то время как поступление импульсов по медленным волокнам тормозят эти клетки. Желатинозная субстанция в свою очередь тормозит поступление импульсов по болевым волокнам на уровне 5-ой пластинки заднего рога спинного мозга (V). Теория обратного контроля гласит, что повышенная и долгая импульсация по болевым волокнам способствуют возбуждения КОК (клетки обратного контроля), которые в свою очередь тормозят передачи импульсов от тонких чувствительных волокон к третьему сенсорному нейрону.
Таким образом, проведенные исследования наглядно показывают, что при лечении полиневропатий с болевым синдромом следует прогнозировать после лечения достоверное восстановление тактильной болевой и температурной чувствительности дистальных отделов нижних конечностей при снижении степени выраженности болевого синдрома, определяемого по ВАШ до 4 балла и ниже.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ДИАБЕТИЧЕСКИХ ДИСТАЛЬНЫХ СЕНСОМОТОРНЫХ ПОЛИНЕВРОПАТИЙ | 2015 |
|
RU2596714C2 |
| СПОСОБ ДИАГНОСТИКИ ДИСТАЛЬНОЙ ПОЛИНЕВРОПАТИИ ВЕРХНИХ КОНЕЧНОСТЕЙ ПРИ САХАРНОМ ДИАБЕТЕ 2 ТИПА | 2015 |
|
RU2593226C1 |
| СПОСОБ ЛЕЧЕНИЯ ДИАБЕТИЧЕСКОЙ ДИСТАЛЬНОЙ СИММЕТРИЧНОЙ СЕНСОМОТОРНОЙ ПОЛИНЕВРОПАТИИ НИЖНИХ КОНЕЧНОСТЕЙ | 2008 |
|
RU2358720C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕЙРОПАТИИ ЛУЧЕВОГО НЕРВА В СПИРАЛЬНОМ КАНАЛЕ | 2015 |
|
RU2595746C1 |
| СПОСОБ ЛЕЧЕНИЯ КАРПАЛЬНОГО СИНДРОМА | 2015 |
|
RU2595749C1 |
| Способ лечения невропатии локтевого нерва в кубитальном канале | 2015 |
|
RU2612496C1 |
| Способ лечения невропатии срединного нерва в карпальном канале | 2024 |
|
RU2837179C1 |
| Способ лечения болевой формы периферической диабетической полинейропатии нижних конечностей | 2024 |
|
RU2840092C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ДИСТАЛЬНЫМИ ДИАБЕТИЧЕСКИМИ ПОЛИНЕВРОПАТИЯМИ | 1999 |
|
RU2167681C1 |
| Способ диагностики диабетической периферической нейропатии | 2021 |
|
RU2751973C1 |
Изобретение относится к области медицины, а именно к неврологии и эндокринологии. Для прогнозирования восстановления поверхностной чувствительности при лечении диабетической дистальной полиневропатии нижних конечностей с болевым синдромом проводят специфическую антидиабетическую терапию и неврологическое исследование пациента до и после лечения. В качестве неврологического исследования определяют степень выраженности болевого синдрома по визуальной аналоговой шкале (ВАШ) в баллах. При снижении после лечения степени выраженности болевого синдрома до 4 баллов и ниже прогнозируют достоверное восстановление тактильной, болевой и температурной чувствительности в дистальных отделах нижних конечностей. Способ позволяет прогнозировать восстановление поверхностной чувствительности при лечении диабетической дистальной полиневропатии нижних конечностей с болевым синдромом в условиях отсутствия квалифицированных кадров и лабораторий. 1 ил., 4 табл.
Способ прогнозирования восстановления поверхностной чувствительности при лечении диабетической дистальной полиневропатии нижних конечностей с болевым синдромом, включающий специфическую антидиабетическую терапию и неврологическое исследование пациента до и после лечения с последующим вынесением суждения, отличающийся тем, что в качестве неврологического исследования определяют степень выраженности болевого синдрома по визуальной аналоговой шкале (ВАШ) в баллах и при снижении после лечения степени выраженности болевого синдрома до 4 баллов и ниже прогнозируют после лечения достоверное восстановление тактильной, болевой и температурной чувствительности в дистальных отделах нижних конечностей.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ ДИАБЕТИЧЕСКОЙ ПОЛИНЕЙРОПАТИИ У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ 2 ТИПА И ДИСЛИПИДЕМИЕЙ | 2011 |
|
RU2491925C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ДИАБЕТИЧЕСКОЙ ПЕРИФЕРИЧЕСКОЙ НЕЙРОПАТИИ У ДЕТЕЙ И ПОДРОСТКОВ | 2004 |
|
RU2273028C1 |
| МЕДВЕДЕВА Л.А | |||
| и др | |||
| Нейрометаболическая терапия диабетической невропатии, Журнал неврологии и психиатрии, N 7, 2006, с.71-73 | |||
| ПОПОВ К.М | |||
| Комплексное лечение больных с нейропатической формой синдрома диабетической стопы, Автореферат дисс | |||
| на соиск.учен.степени канд.мед.наук, Томск, 2012, с.6, | |||
Авторы
Даты
2016-08-10—Публикация
2015-01-16—Подача